Лекарства и БАД
226,00 грн
195,00 грн
Склад, форма випуску та упаковкаСпрей – 1 доза: діюча речовина: ксилометазоліну гідрохлорид – 140 мкг; допоміжні речовини: натрію гідрофосфат дигідрат – 280 мкг; натрію дигідрофосфат дигідрат - 280 мкг; динатрію едетат – 70 мкг; натрію хлорид – 1,02 мг; вода очищена – 139,0 мг. По 10 мл препарату у пластиковому флаконі, забезпеченому помповим дозуючим пристроєм з наконечником та захисним ковпачком із поліетилену. По 1 флакону разом з інструкцією із застосування поміщають у картонну пачку.Опис лікарської формиПрозора, безбарвна або трохи пофарбована рідина.Фармакотерапевтична групаПротиконгестивний засіб – альфа-адреноміметик.ФармакокінетикаПри місцевому застосуванні практично не абсорбується, концентрації у плазмі настільки малі, що їх неможливо визначити сучасними аналітичними методами.ФармакодинамікаКсилометазолін відноситься до групи місцевих судинозвужувальних засобів (деконгестантів) з альфа-адреноміметичною дією, викликає звуження кровоносних судин слизової оболонки носа, усуваючи, таким чином, набряк і гіперемію слизової оболонки носоглотки. Полегшує носове дихання та прохідність при ринітах. Ксимелін Еко не містить консервантів. У терапевтичних концентраціях не подразнює слизову оболонку, не викликає гіперемію. Дія настає через дві хвилини і продовжується протягом 12 годин. Дослідження in vitro показали, що ксилометазолін пригнічує інфекційну активність риновірусу людини, що викликає "застуду".Показання до застосуванняГострі респіраторні захворювання з явищами риніту (нежить), гострий алергічний риніт, поліноз, синусит, євстахііт, середній отит (для зменшення набряку слизової оболонки носоглотки). Підготовка хворого до діагностичних маніпуляцій у носових ходах.Протипоказання до застосуванняПідвищена чутливість до компонентів препарату, артеріальна гіпертензія, тахікардія, виражений атеросклероз, глаукома, атрофічний риніт, гіпертиреоз, хірургічні втручання на мозкові оболонки (в анамнезі), вагітність, дитячий вік до 2 років (для препарату Ксімелін Еко 35 м); дитячий вік до 10 років (для препарату Ксімелін Еко 140 мкг/доза). Не застосовувати препарат при терапії інгібіторами моноаміноксидази (МАО) або трициклічними антидепресантами, включаючи період 14 днів після їх відміни. З обережністю: цукровий діабет; феохромоцитома; захворювання серцево-судинної системи, у т.ч. ІХС, стенокардія ІІІ-ІV функціонального класу; порфірія; період грудного вигодовування; гіперплазія передміхурової залози; атеросклероз; при підвищеній чутливості до адренергічних препаратів, що супроводжується безсонням, запамороченням, аритмією, тремором, підвищенням артеріального тиску.Вагітність та лактаціяЗастосування препарату протипоказане під час вагітності. У період грудного вигодовування препарат повинен застосовуватися лише після ретельної оцінки співвідношення ризику та користі для матері та дитини під контролем лікаря. Не допускається перевищувати рекомендовану дозу.Побічна діяКласифікація частоти виникнення небажаних реакцій: дуже часто (≥1/10); часто (≥ 1/100, < 1/10); нечасто (≥ 1/1000, < 1/100); рідко (≥1/10000, <1/1000); дуже рідко (<1/10000). Порушення з боку імунної системи - Дуже рідко: реакції гіперчутливості (ангіоневротичний набряк, висип, свербіж). Порушення з боку нервової системи: - Часто: головний біль; Рідко: безсоння, депресія (при тривалому застосуванні у високих дозах); Дуже рідко: занепокоєння, втома, галюцинації та судоми (переважно у дітей). Порушення з боку органу зору - дуже рідко: порушення чіткості зорового сприйняття. Порушення з боку серця: - Рідко: відчуття серцебиття, підвищення артеріального тиску; Дуже рідко: тахікардія, аритмія. Порушення з боку дихальної системи, органів грудної клітки та середостіння - Часто: подразнення та/або сухість слизової оболонки носа, печіння, поколювання, чхання, гіперсекреція слизової оболонки носоглотки; Нечасто: закладеність носа (реактивна гіперемія) (особливо при частому та тривалому застосуванні), кровотеча з носа. Порушення з боку шлунково-кишкового тракту: - Часто: нудота; Рідко: блювання. Якщо будь-які вказані в інструкції побічні ефекти посилюються, або Ви помітили будь-які інші побічні ефекти, не вказані в інструкції, повідомте про це лікаря.Взаємодія з лікарськими засобамиЗастосування ксилометазоліну протипоказане пацієнтам, які отримують інгібітори МАО або трициклічні антидепресанти, включаючи період 14 днів після їх відміни. Одночасне застосування три- або тетрациклічних антидепресантів та симпатоміметичних препаратів може призвести до збільшення симпатоміметичного ефекту ксилометазоліну, тому такого поєднання рекомендується уникати.Спосіб застосування та дозиІнтраназально. Препарат Ксімелін Еко, 35 мкг/доза, спрей для дітей віком від 2 до 10 років: по 1 впорскування у кожний носовий хід; не слід застосовувати більше 3-х разів на добу. Препарат застосовується не більше 5 днів під наглядом дорослих. Препарат Ксімелін Еко, 140 мкг/доза, спрей для дорослих та дітей старше 10 років: по 1 впорскування у кожний носовий хід (при необхідності можна повторити); не слід застосовувати більше 3-х разів на добу. Препарат застосовується трохи більше 10 днів. Одне впорскування препарату Ксимелін Еко 35 мкг/доза містить близько 35 мкг ксилометазолу іну гідрохлориду; одне впорскування препарату Ксимелін Еко 140 мкг/доза містить близько 140 мкг ксилометазоліну гідрохлориду. Препарат у дітей слід застосовувати під наглядом дорослих. Застосовуйте препарат тільки згідно з тими показаннями, тим способом застосування і в дозах, які вказані в інструкції. Під час застосування препарату флакон слід тримати розпилювачем вгору.ПередозуванняКсилометазолін при місцевому введенні надмірної дози або при випадковому прийомі внутрішньо може викликати сильне запаморочення, посилений та нерівномірний пульс, підвищене потовиділення, різке зниження температури тіла, головний біль, сонливість, брадикардію, підвищення артеріального тиску, пригнічення дихання, кому та судно. Після підвищення артеріального тиску може спостерігатися його різке зниження. Відповідні підтримувальні заходи повинні вживатися за будь-яких підозр на передозування, у деяких випадках показано негайне симптоматичне лікування під наглядом лікаря. У разі тяжкого отруєння із зупинкою серця реанімаційні дії мають тривати не менше 1 години.Запобіжні заходи та особливі вказівкиНеприпустимо застосування в дітей віком до 2-х років. Не рекомендується застосовувати у безперервному режимі більше 10 днів. Не слід перевищувати рекомендовані дози, особливо у дітей та людей похилого віку. Тривале (більше 10 днів) або надмірне застосування препарату може спричинити набряк слизової оболонки або гіперсекрецію, спричинену підвищеною чутливістю клітин ("ефект рикошету"). Вплив на здатність до керування автотранспортом та управління механізмами Чи не описано.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаРозчин для місцевого застосування в олії 2% - 1 л. евкаліпта кулькового листя екстракт – 20 г. У флаконах темного скла 20 мл.Фармакотерапевтична групаПротимікробне.ФармакодинамікаПротимікробний засіб; активно щодо Staphylococcus spp.Показання до застосуванняХлорофіліпта розчин у маслі 2%: ерозії шийки матки. Хлорофіліпта розчин спиртової 1%: опіки; трофічні виразки; кишкове носійство стафілококів. Хлорофіліпта розчин спиртової 0,25%: септичні стани; пневмонія; перитоніт; емпієма; абсцес легень.Протипоказання до застосуванняПідвищена чутливість до компонентів препарату. При застосуванні внутрішньо – вік до 18 років, вагітність, період грудного вигодовування, захворювання печінки, черепно-мозкова травма, алкоголізм, захворювання головного мозку.Побічна діяАлергічні реакції (набряклість губ, слизової оболонки порожнини носа, зіва; шкірні висипання).Взаємодія з лікарськими засобамиПерекис водню. Слід враховувати, що за наявності в рані залишків перекису водню, Хлорофілліпт випадає в осад, тому після промивання рани перекисом водню залишки його слід вилучити стерильним 0,9% розчином натрію хлориду.Спосіб застосування та дозиХлорофіліпта розчин в олії 2% Місцево. При ерозії шийки матки - 2% масляний розчин для змащування каналу шийки матки і ерозії, змочування тампонів, що вводяться в піхву. Хлорофіліпту розчин спиртовий 1% Місцево, при лікуванні опіків та трофічних виразок – 1% спиртовий розчин розводять щодо 1:5 у 0,25% розчині прокаїну; 1% спиртовий розчин (15 мл розводять в 1 л води) – для спринцювання піхви. Всередину, при кишковому носійстві стафілококів - по 5 мл 1% спиртового розчину, розведених у 30 мл води, щодня 3 десь у день 40 хв до їжі. Клізми – 20 мл 1% спиртового розчину в 1 л води. Хлорофіліпта розчин спиртовий 0,25% В/в струминно (повільно), при септичних станах та пневмоніях - по 2 мл 0,25% розчину, розведеного в 38 мл стерильного 0,9% розчину NaCl, 4 рази на добу протягом 4-5 днів. В/в краплинно, у комплексній терапії гострих абсцесів легень - по 8-10 мл 0,25% розчину (розведених у 150 мл 0,9% розчину NaCl) 2 рази на день. Внутрішньопорожнинно, через дренажну трубку, при перитоніті та емпіємі - 0,25% спиртовий розчин у розведенні 0,25% розчином прокаїну у співвідношенні 1:20, протягом 5-6 днів (розчин готують їх tempore).ПередозуванняДо цього часу передозування при правильному застосуванні препарату не зареєстровано. Можливе посилення дозозалежних побічних ефектів.Запобіжні заходи та особливі вказівкиНезалежно від лікарської форми Хлорофіліпта, що призначається, чутливість до нього визначають шляхом прийому внутрішньо 0,25% спиртового розчину Хлорофіліпту. Перед застосуванням препарату визначають чутливість до Хлорофіліпту, для цього хворий випиває 25 крапель препарату, розчиненого в 1 ст. ложці води. За відсутності через 6-8 годин ознак алергії (набряк губ, слизових оболонок) Хлорофіліпт можна застосовувати.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаСпрей – 1 мл Активні речовини: ксилометазоліну гідрохлорид – 500 мкг; іпратропія бромід моногідрат – 600 мкг; Допоміжні речовини: динатрію едетату дигідрат, гліцерол 85%, хлористоводнева кислота концентрована (до pH 4.5), гідроксид натрію (до pH 4.5), вода очищена. 10 мл - флакони пластикові з помповим дозуючим пристроєм (1) - пачки картонні.Опис лікарської формиНазальний спрей у вигляді прозорої, безбарвної або злегка пофарбованої рідини.Фармакотерапевтична групаКомбінований препарат для місцевого застосування у ЛОР-практиці.ФармакокінетикаПри інтраназальному застосуванні ксилометазоліну гідрохлорид та іпратропію бромід мало абсорбуються і присутні в плазмі крові в незначних кількостях.ФармакодинамікаКсилометазолін – альфа-адреноміметик. Викликає звуження кровоносних судин слизової оболонки носа, усуваючи, таким чином, набряк і гіперемію слизової оболонки носоглотки. Полегшує носове дихання при ринітах. Іпратропія бромід має антихолінергічний ефект. При інтраназальному застосуванні зменшує секрецію залоз слизової оболонки порожнини носа. У терапевтичних дозах Ксімелін Екстра не подразнює слизову оболонку, не викликає гіперемію. Дія препарату настає через 5-10 хв і продовжується протягом 6-8 год.Показання до застосуваннясимптоматичне лікування набряку та гіперемії носової порожнини; гострі респіраторні захворювання із явищами риніту (нежить); гострий алергічний риніт; поліноз; синусит.Протипоказання до застосуванняартеріальна гіпертензія; тахікардія; виражений атеросклероз; глаукому; атрофічний риніт; тиреотоксикоз; хірургічні втручання на мозкові оболонки (в анамнезі); І триместр вагітності; вік до 18 років; - підвищена чутливість до компонентів препарату. З обережністю слід застосовувати препарат при цукровому діабеті, стенокардії III-IV функціонального класу, обструкції шийки сечового міхура, гіперплазії передміхурової залози, у хворих на муковісцидоз; у пацієнтів схильних до носових кровотеч, паралітичної непрохідності кишечника, запаморочення, тремору скелетної мускулатури, до порушень сну, аритмії, підвищення артеріального тиску.Вагітність та лактаціяПротипоказано застосування препарату у І триместрі вагітності. У II та III триместрах вагітності та в період лактації (грудного вигодовування) препарат слід застосовувати лише після ретельної оцінки очікуваної користі терапії для матері та можливого ризику для плода. Не допускати перевищення рекомендованої дози. Протипоказаний у дитячому та підлітковому віці до 18 років.Побічна діяПри частому та/або тривалому застосуванні: подразнення та/або сухість слизової оболонки носоглотки, печіння та поколювання в носі та горлі, набряк слизової оболонки носа, чхання, гіперсекреція залоз слизової оболонки порожнини носа, носові кровотечі, головний біль. Рідко: системні алергічні реакції, порушення зору, серцебиття, тахікардія, аритмія, біль голови, запаморочення, підвищення артеріального тиску, безсоння.Взаємодія з лікарськими засобамиПри одночасному застосуванні з інгібіторами МАО можливе підвищення артеріального тиску. При одночасному застосуванні з три- та тетрациклічними антидепресантами можливе посилення симпатоміметичного ефекту ксилометазоліну. При супутньому призначенні інших антихолінергічних препаратів можливе посилення антихолінергічного ефекту іпратропію броміду.Спосіб застосування та дозиПрепарат застосовують інтраназально. Дорослим старше 18 років - по 1 впорскування у кожний носовий хід 3 рази на добу. Препарат застосовується трохи більше 10 днів без консультації лікаря. Одне впорскування Ксимелін Екстра містить близько 70 мкг ксилометазоліну гідрохлориду та 84 мкг іпратропію броміду.ПередозуванняПісля інтраназального застосування Ксимеліну Екстра гостре передозування малоймовірне, т.к. всмоктування препарату дуже незначне. Симптоми: сухість у роті, порушення акомодації, тахікардія, біль голови, артеріальна гіпертензія. Лікування: відміна препарату, проведення симптоматичної терапії.Запобіжні заходи та особливі вказівкиПеред застосуванням препарату слід очистити носові ходи. Не слід застосовувати препарат протягом тривалого часу, наприклад, при хронічному риніті. Пацієнтів необхідно попередити про неприпустимість розпилення препарату Ксімелін Екстра у вічі або навколо очей. При попаданні препарату у вічі необхідно промити їх холодною водою. Якщо симптоми захворювання погіршуються або стан хворого не покращується протягом 3 днів прийому Ксімеліну Екстра, необхідно проконсультуватися з лікарем. Вплив на здатність до керування автотранспортом та управління механізмами Застосування препарату в терапевтичних дозах не впливає на здатність керувати транспортними засобами та працювати з механізмами. Передозування або потрапляння препарату в очі може впливати на здатність керувати транспортними засобами та іншими потенційно небезпечними видами діяльності.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. активна речовина: левоцетиризину дигідрохлорид 5,0 мг; допоміжні речовини: лактози моногідрат 63,50 мг, целюлоза мікрокристалічна 30,00 мг, кремнію діоксид колоїдний 0,50 мг, магнію стеарат 1,00 мг; Оболонка: опадрай Y-1-7000 3,00 мг (містить гіпромелозу 62,5%, титану діоксид (Е171) 31,25%, макрогол 400 6,25%). По 7 або 10 таблеток у блістері із ПВХ-алюмінієвої фольги. 1 або 2 блістери разом з інструкцією із застосування в картонній пачці.Опис лікарської формиОвальної форми таблетки, покриті плівковою оболонкою білого або майже білого кольору. На одному боці таблетки видавлено маркування "Y".Фармакотерапевтична групаПротиалергічний засіб - блокатор H1-гістамінових рецепторів.ФармакокінетикаФармакокінетичні параметри левоцетиризину змінюються лінійно та практично не відрізняються від фармакокінетики цетиризину. Всмоктування. Після прийому внутрішньо препарат швидко і повністю абсорбується із ШКТ. Їда не впливає на повноту абсорбції, хоча швидкість її зменшується. У дорослих після одноразового прийому препарату в терапевтичній дозі (5 мг) Cmax у плазмі становить 270 нг/мл і досягається через 0,9 год, після повторного прийому в дозі 5 мг – 308 нг/мл. Css досягається через 2 добу. Розподіл. Левоцетиризин на 90% зв'язується з білками плазми. Vd становить 0,4 л/кг. Біодоступність сягає 100%. Метаболізм. У невеликих кількостях ( Виведення. У дорослих T1/2 становить (7,9±1,9) год; у маленьких дітей T1/2 укорочений. У дорослих загальний кліренс становить 0,63 мл/хв/кг. Близько 85,4% прийнятої дози препарату виводиться нирками у незміненому вигляді шляхом клубочкової фільтрації та канальцевої секреції; близько 12,9% – через кишечник. У пацієнтів з нирковою недостатністю (Cl креатинінуФармакодинамікаЛевоцетиризин – активна речовина препарату Ксизал® – це R-енантіомер цетиризину, який відноситься до групи конкурентних антагоністів гістаміну та блокує H1-гістамінові рецептори. Левоцетиризин впливає на гістамінозалежну стадію алергічних реакцій, а також зменшує міграцію еозинофілів, проникність судин, обмежує вивільнення медіаторів запалення. Левоцетиризин попереджає розвиток і полегшує перебіг алергічних реакцій, має протиексудативну, протисвербіжну і практично не чинить антихолінергічну та антисеротонінову дію. У терапевтичних дозах мало викликає седативний ефект.Показання до застосуваннялікування таких симптомів цілорічного (персистуючого) та сезонного (інтермітуючого) алергічних ринітів та алергічного кон'юнктивіту, як свербіж, чхання, закладеність носа, ринорея, сльозотеча, гіперемія кон'юнктиви; поліноз (сінна лихоманка); кропив'янка; інші алергічні дерматози, що супроводжуються свербінням та висипаннями.Вагітність та лактаціяДоклінічні дослідження не виявили будь-які прямі або непрямі несприятливі ефекти левоцетиризину на плід, що розвивається, а також на розвиток в постнатальному періоді; перебіг вагітності та пологів також не змінювалося. Адекватних та строго контрольованих клінічних досліджень щодо безпеки застосування препарату під час вагітності не проводилося. Застосування препарату при вагітності протипоказане. Левоцетиризин виділяється з грудним молоком, тому за необхідності застосування препарату при лактації рекомендується припинити грудне вигодовування.Побічна діяПід час проведення клінічних досліджень в осіб чоловічої та жіночої статі 12–71 роки часто (≥1/100, З боку імунної системи: реакції гіперчутливості, включаючи анафілаксію. З боку метаболізму та розладу харчування: підвищення апетиту. З боку психіки: тривога, агресія, збудження, безсоння, галюцинації, депресія, суїцидальні думки. З боку нервової системи: судоми, тромбоз синусів твердої мозкової оболонки, парестезія, запаморочення, непритомність, тремор, дисгевзія. З боку слуху: вертиго. З боку органу зору: порушення зору, нечіткість зорового сприйняття, запальні прояви. З боку ССС: відчуття серцебиття, тахікардія, тромбоз яремної вени. З боку дихальної системи: задишка, посилення симптомів риніту. З боку травної системи: нудота, блювання. Гепатобіліарні розлади: гепатит. З боку нирок та сечовидільної системи: дизурія, затримка сечі. З боку шкіри та м'яких тканин: ангіоневротичний набряк, стійка лікарська еритема, висипання, свербіж, кропив'янка, гіпотрихоз, тріщини, фотосенсибілізація. З боку кістково-м'язової системи: біль у м'язах. Загальні розлади: периферичні набряки. Інше: збільшення маси тіла, зміна функціональних спроб печінки, перехресна реактивність. Якщо будь-які побічні ефекти, що зазначені в інструкції, посилюються або пацієнт помітив інші побічні ефекти, слід повідомити про це лікаря.Взаємодія з лікарськими засобамиВивчення взаємодії левоцетиризину з іншими лікарськими засобами не проводилося. При вивченні лікарської взаємодії рацемату цетиризину з феназоном, псевдоефедрином, циметидином, кетоконазолом, еритроміцином, азитроміцином, гліпізидом та діазепамом клінічно значимих небажаних взаємодій не виявлено. При одночасному призначенні з теофіліном (400 мг на добу) загальний кліренс цетиризину знижується на 16% (кінетика теофіліну не змінюється). У дослідженні при одночасному прийомі ритонавіру (600 мг 2 рази на день) та цетиризину (10 мг/добу) показано, що експозиція цетиризину збільшувалася на 40%, а експозиція ритонавіру злегка змінювалася (-10%). У ряді випадків при одночасному застосуванні левоцетиризину з алкоголем або лікарськими препаратами, які пригнічують ЦНС, можливе посилення їх впливу на ЦНС, хоча не доведено, що рацемат цетиризину потенціює ефект алкоголю.Спосіб застосування та дозиПрепарат приймають внутрішньо, проковтуючи повністю під час їжі або натще, запиваючи невеликою кількістю води. Дорослі та діти старше 6 років: добова доза становить 5 мг (1 таблетка) одноразово. Основним шляхом виведення левоцетиризину з організму є виведення нирками, тому при застосуванні препарату у пацієнтів похилого віку та з нирковою недостатністю доза повинна коригуватися залежно від ступеня ниркової недостатності, ґрунтуючись на оцінці кліренсу креатиніну (мл/хв). Пацієнтам з легким порушенням ниркової функції (кліренс креатиніну 50-79 мл/хв) корекції дози не потрібно. У пацієнтів із помірною нирковою недостатністю (кліренс креатиніну від 30 до 49 мл/хв) рекомендована доза 5 мг через день. У пацієнтів з тяжкою нирковою недостатністю (кліренс креатиніну менше 30 мл/хв) рекомендована доза 5 мг 1 раз на 3 дні. Пацієнтам з нирковою та печінковою недостатністю дозування здійснюється за наведеною вище схемою. Пацієнтам з порушенням функції печінки корекції режиму дозування не потрібно. Тривалість прийому препарату: При лікуванні сезонного (інтермітуючого) алергічного риніту (наявність симптомів менше 4 днів на тиждень або їх загальна тривалість менше 4-х тижнів); тривалість лікування залежить від тривалості симптоматики; лікування може бути припинено при зникненні симптомів та відновлено з появою симптомів. При лікуванні цілорічного (персистирующего) алергічного риніту (наявність симптомів більше 4-х днів на тиждень та їх загальна тривалість більше 4-х тижнів) лікування може тривати протягом усього періоду дії алергенів. Є клінічний досвід безперервного застосування препарату Ксизал у лікарській формі таблетки покриті плівковою оболонкою 5 мг у дорослих пацієнтів тривалістю до 6 місяців. Якщо ви приймаєте або недавно приймали інші препарати, повідомте про це лікаря. Якщо ви забули прийняти препарат Ксізал, не приймайте подвійну дозу для компенсації пропущеної, прийміть наступну дозу у звичайний час.ПередозуванняСимптоми: сонливість (у дорослих), збудження та занепокоєння, що змінюються сонливістю (у дітей). Промивання шлунка або призначення активованого вугілля, якщо після прийому препарату пройшло мало часу. Рекомендується проведення симптоматичної та підтримуючої терапії. Специфічного антидоту немає. Гемодіаліз неефективний.Запобіжні заходи та особливі вказівкиМетилпарагідроксибензоат і пропілпарагідроксибензоат, що входять до складу крапель для прийому внутрішньо, можуть бути причиною алергічних реакцій (можливо уповільненого типу). Вплив на здатність керувати транспортними засобами та працювати з механізмами. Левоцетиризин може призвести до підвищеної сонливості, отже препарат Ксизал може впливати на здатність керувати автомобілем або працювати з технікою. У період лікування необхідно утримуватися від занять потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. активна речовина: левоцетиризину дигідрохлорид 5,0 мг; допоміжні речовини: лактози моногідрат 63,50 мг, целюлоза мікрокристалічна 30,00 мг, кремнію діоксид колоїдний 0,50 мг, магнію стеарат 1,00 мг; Оболонка: опадрай Y-1-7000 3,00 мг (містить гіпромелозу 62,5%, титану діоксид (Е171) 31,25%, макрогол 400 6,25%). По 7 або 10 таблеток у блістері із ПВХ-алюмінієвої фольги. 1 або 2 блістери разом з інструкцією із застосування в картонній пачці.Опис лікарської формиОвальної форми таблетки, покриті плівковою оболонкою білого або майже білого кольору. На одному боці таблетки видавлено маркування "Y".Фармакотерапевтична групаПротиалергічний засіб - блокатор H1-гістамінових рецепторів.ФармакокінетикаФармакокінетичні параметри левоцетиризину змінюються лінійно та практично не відрізняються від фармакокінетики цетиризину. Всмоктування. Після прийому внутрішньо препарат швидко і повністю абсорбується із ШКТ. Їда не впливає на повноту абсорбції, хоча швидкість її зменшується. У дорослих після одноразового прийому препарату в терапевтичній дозі (5 мг) Cmax у плазмі становить 270 нг/мл і досягається через 0,9 год, після повторного прийому в дозі 5 мг – 308 нг/мл. Css досягається через 2 добу. Розподіл. Левоцетиризин на 90% зв'язується з білками плазми. Vd становить 0,4 л/кг. Біодоступність сягає 100%. Метаболізм. У невеликих кількостях ( Виведення. У дорослих T1/2 становить (7,9±1,9) год; у маленьких дітей T1/2 укорочений. У дорослих загальний кліренс становить 0,63 мл/хв/кг. Близько 85,4% прийнятої дози препарату виводиться нирками у незміненому вигляді шляхом клубочкової фільтрації та канальцевої секреції; близько 12,9% – через кишечник. У пацієнтів з нирковою недостатністю (Cl креатинінуФармакодинамікаЛевоцетиризин – активна речовина препарату Ксизал® – це R-енантіомер цетиризину, який відноситься до групи конкурентних антагоністів гістаміну та блокує H1-гістамінові рецептори. Левоцетиризин впливає на гістамінозалежну стадію алергічних реакцій, а також зменшує міграцію еозинофілів, проникність судин, обмежує вивільнення медіаторів запалення. Левоцетиризин попереджає розвиток і полегшує перебіг алергічних реакцій, має протиексудативну, протисвербіжну і практично не чинить антихолінергічну та антисеротонінову дію. У терапевтичних дозах мало викликає седативний ефект.Показання до застосуваннялікування таких симптомів цілорічного (персистуючого) та сезонного (інтермітуючого) алергічних ринітів та алергічного кон'юнктивіту, як свербіж, чхання, закладеність носа, ринорея, сльозотеча, гіперемія кон'юнктиви; поліноз (сінна лихоманка); кропив'янка; інші алергічні дерматози, що супроводжуються свербінням та висипаннями.Вагітність та лактаціяДоклінічні дослідження не виявили будь-які прямі або непрямі несприятливі ефекти левоцетиризину на плід, що розвивається, а також на розвиток в постнатальному періоді; перебіг вагітності та пологів також не змінювалося. Адекватних та строго контрольованих клінічних досліджень щодо безпеки застосування препарату під час вагітності не проводилося. Застосування препарату при вагітності протипоказане. Левоцетиризин виділяється з грудним молоком, тому за необхідності застосування препарату при лактації рекомендується припинити грудне вигодовування.Побічна діяПід час проведення клінічних досліджень в осіб чоловічої та жіночої статі 12–71 роки часто (≥1/100, З боку імунної системи: реакції гіперчутливості, включаючи анафілаксію. З боку метаболізму та розладу харчування: підвищення апетиту. З боку психіки: тривога, агресія, збудження, безсоння, галюцинації, депресія, суїцидальні думки. З боку нервової системи: судоми, тромбоз синусів твердої мозкової оболонки, парестезія, запаморочення, непритомність, тремор, дисгевзія. З боку слуху: вертиго. З боку органу зору: порушення зору, нечіткість зорового сприйняття, запальні прояви. З боку ССС: відчуття серцебиття, тахікардія, тромбоз яремної вени. З боку дихальної системи: задишка, посилення симптомів риніту. З боку травної системи: нудота, блювання. Гепатобіліарні розлади: гепатит. З боку нирок та сечовидільної системи: дизурія, затримка сечі. З боку шкіри та м'яких тканин: ангіоневротичний набряк, стійка лікарська еритема, висипання, свербіж, кропив'янка, гіпотрихоз, тріщини, фотосенсибілізація. З боку кістково-м'язової системи: біль у м'язах. Загальні розлади: периферичні набряки. Інше: збільшення маси тіла, зміна функціональних спроб печінки, перехресна реактивність. Якщо будь-які побічні ефекти, що зазначені в інструкції, посилюються або пацієнт помітив інші побічні ефекти, слід повідомити про це лікаря.Взаємодія з лікарськими засобамиВивчення взаємодії левоцетиризину з іншими лікарськими засобами не проводилося. При вивченні лікарської взаємодії рацемату цетиризину з феназоном, псевдоефедрином, циметидином, кетоконазолом, еритроміцином, азитроміцином, гліпізидом та діазепамом клінічно значимих небажаних взаємодій не виявлено. При одночасному призначенні з теофіліном (400 мг на добу) загальний кліренс цетиризину знижується на 16% (кінетика теофіліну не змінюється). У дослідженні при одночасному прийомі ритонавіру (600 мг 2 рази на день) та цетиризину (10 мг/добу) показано, що експозиція цетиризину збільшувалася на 40%, а експозиція ритонавіру злегка змінювалася (-10%). У ряді випадків при одночасному застосуванні левоцетиризину з алкоголем або лікарськими препаратами, які пригнічують ЦНС, можливе посилення їх впливу на ЦНС, хоча не доведено, що рацемат цетиризину потенціює ефект алкоголю.Спосіб застосування та дозиПрепарат приймають внутрішньо, проковтуючи повністю під час їжі або натще, запиваючи невеликою кількістю води. Дорослі та діти старше 6 років: добова доза становить 5 мг (1 таблетка) одноразово. Основним шляхом виведення левоцетиризину з організму є виведення нирками, тому при застосуванні препарату у пацієнтів похилого віку та з нирковою недостатністю доза повинна коригуватися залежно від ступеня ниркової недостатності, ґрунтуючись на оцінці кліренсу креатиніну (мл/хв). Пацієнтам з легким порушенням ниркової функції (кліренс креатиніну 50-79 мл/хв) корекції дози не потрібно. У пацієнтів із помірною нирковою недостатністю (кліренс креатиніну від 30 до 49 мл/хв) рекомендована доза 5 мг через день. У пацієнтів з тяжкою нирковою недостатністю (кліренс креатиніну менше 30 мл/хв) рекомендована доза 5 мг 1 раз на 3 дні. Пацієнтам з нирковою та печінковою недостатністю дозування здійснюється за наведеною вище схемою. Пацієнтам з порушенням функції печінки корекції режиму дозування не потрібно. Тривалість прийому препарату: При лікуванні сезонного (інтермітуючого) алергічного риніту (наявність симптомів менше 4 днів на тиждень або їх загальна тривалість менше 4-х тижнів); тривалість лікування залежить від тривалості симптоматики; лікування може бути припинено при зникненні симптомів та відновлено з появою симптомів. При лікуванні цілорічного (персистирующего) алергічного риніту (наявність симптомів більше 4-х днів на тиждень та їх загальна тривалість більше 4-х тижнів) лікування може тривати протягом усього періоду дії алергенів. Є клінічний досвід безперервного застосування препарату Ксизал у лікарській формі таблетки покриті плівковою оболонкою 5 мг у дорослих пацієнтів тривалістю до 6 місяців. Якщо ви приймаєте або недавно приймали інші препарати, повідомте про це лікаря. Якщо ви забули прийняти препарат Ксізал, не приймайте подвійну дозу для компенсації пропущеної, прийміть наступну дозу у звичайний час.ПередозуванняСимптоми: сонливість (у дорослих), збудження та занепокоєння, що змінюються сонливістю (у дітей). Промивання шлунка або призначення активованого вугілля, якщо після прийому препарату пройшло мало часу. Рекомендується проведення симптоматичної та підтримуючої терапії. Специфічного антидоту немає. Гемодіаліз неефективний.Запобіжні заходи та особливі вказівкиМетилпарагідроксибензоат і пропілпарагідроксибензоат, що входять до складу крапель для прийому внутрішньо, можуть бути причиною алергічних реакцій (можливо уповільненого типу). Вплив на здатність керувати транспортними засобами та працювати з механізмами. Левоцетиризин може призвести до підвищеної сонливості, отже препарат Ксизал може впливати на здатність керувати автомобілем або працювати з технікою. У період лікування необхідно утримуватися від занять потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. активна речовина: левоцетиризину дигідрохлорид 5,0 мг; допоміжні речовини: лактози моногідрат 63,50 мг, целюлоза мікрокристалічна 30,00 мг, кремнію діоксид колоїдний 0,50 мг, магнію стеарат 1,00 мг; Оболонка: опадрай Y-1-7000 3,00 мг (містить гіпромелозу 62,5%, титану діоксид (Е171) 31,25%, макрогол 400 6,25%). По 7 або 10 таблеток у блістері із ПВХ-алюмінієвої фольги. 1 або 2 блістери разом з інструкцією із застосування в картонній пачці.Опис лікарської формиОвальної форми таблетки, покриті плівковою оболонкою білого або майже білого кольору. На одному боці таблетки видавлено маркування "Y".Фармакотерапевтична групаПротиалергічний засіб - блокатор H1-гістамінових рецепторів.ФармакокінетикаФармакокінетичні параметри левоцетиризину змінюються лінійно та практично не відрізняються від фармакокінетики цетиризину. Всмоктування. Після прийому внутрішньо препарат швидко і повністю абсорбується із ШКТ. Їда не впливає на повноту абсорбції, хоча швидкість її зменшується. У дорослих після одноразового прийому препарату в терапевтичній дозі (5 мг) Cmax у плазмі становить 270 нг/мл і досягається через 0,9 год, після повторного прийому в дозі 5 мг – 308 нг/мл. Css досягається через 2 добу. Розподіл. Левоцетиризин на 90% зв'язується з білками плазми. Vd становить 0,4 л/кг. Біодоступність сягає 100%. Метаболізм. У невеликих кількостях ( Виведення. У дорослих T1/2 становить (7,9±1,9) год; у маленьких дітей T1/2 укорочений. У дорослих загальний кліренс становить 0,63 мл/хв/кг. Близько 85,4% прийнятої дози препарату виводиться нирками у незміненому вигляді шляхом клубочкової фільтрації та канальцевої секреції; близько 12,9% – через кишечник. У пацієнтів з нирковою недостатністю (Cl креатинінуФармакодинамікаЛевоцетиризин – активна речовина препарату Ксизал® – це R-енантіомер цетиризину, який відноситься до групи конкурентних антагоністів гістаміну та блокує H1-гістамінові рецептори. Левоцетиризин впливає на гістамінозалежну стадію алергічних реакцій, а також зменшує міграцію еозинофілів, проникність судин, обмежує вивільнення медіаторів запалення. Левоцетиризин попереджає розвиток і полегшує перебіг алергічних реакцій, має протиексудативну, протисвербіжну і практично не чинить антихолінергічну та антисеротонінову дію. У терапевтичних дозах мало викликає седативний ефект.Показання до застосуваннялікування таких симптомів цілорічного (персистуючого) та сезонного (інтермітуючого) алергічних ринітів та алергічного кон'юнктивіту, як свербіж, чхання, закладеність носа, ринорея, сльозотеча, гіперемія кон'юнктиви; поліноз (сінна лихоманка); кропив'янка; інші алергічні дерматози, що супроводжуються свербінням та висипаннями.Вагітність та лактаціяДоклінічні дослідження не виявили будь-які прямі або непрямі несприятливі ефекти левоцетиризину на плід, що розвивається, а також на розвиток в постнатальному періоді; перебіг вагітності та пологів також не змінювалося. Адекватних та строго контрольованих клінічних досліджень щодо безпеки застосування препарату під час вагітності не проводилося. Застосування препарату при вагітності протипоказане. Левоцетиризин виділяється з грудним молоком, тому за необхідності застосування препарату при лактації рекомендується припинити грудне вигодовування.Побічна діяПід час проведення клінічних досліджень в осіб чоловічої та жіночої статі 12–71 роки часто (≥1/100, З боку імунної системи: реакції гіперчутливості, включаючи анафілаксію. З боку метаболізму та розладу харчування: підвищення апетиту. З боку психіки: тривога, агресія, збудження, безсоння, галюцинації, депресія, суїцидальні думки. З боку нервової системи: судоми, тромбоз синусів твердої мозкової оболонки, парестезія, запаморочення, непритомність, тремор, дисгевзія. З боку слуху: вертиго. З боку органу зору: порушення зору, нечіткість зорового сприйняття, запальні прояви. З боку ССС: відчуття серцебиття, тахікардія, тромбоз яремної вени. З боку дихальної системи: задишка, посилення симптомів риніту. З боку травної системи: нудота, блювання. Гепатобіліарні розлади: гепатит. З боку нирок та сечовидільної системи: дизурія, затримка сечі. З боку шкіри та м'яких тканин: ангіоневротичний набряк, стійка лікарська еритема, висипання, свербіж, кропив'янка, гіпотрихоз, тріщини, фотосенсибілізація. З боку кістково-м'язової системи: біль у м'язах. Загальні розлади: периферичні набряки. Інше: збільшення маси тіла, зміна функціональних спроб печінки, перехресна реактивність. Якщо будь-які побічні ефекти, що зазначені в інструкції, посилюються або пацієнт помітив інші побічні ефекти, слід повідомити про це лікаря.Взаємодія з лікарськими засобамиВивчення взаємодії левоцетиризину з іншими лікарськими засобами не проводилося. При вивченні лікарської взаємодії рацемату цетиризину з феназоном, псевдоефедрином, циметидином, кетоконазолом, еритроміцином, азитроміцином, гліпізидом та діазепамом клінічно значимих небажаних взаємодій не виявлено. При одночасному призначенні з теофіліном (400 мг на добу) загальний кліренс цетиризину знижується на 16% (кінетика теофіліну не змінюється). У дослідженні при одночасному прийомі ритонавіру (600 мг 2 рази на день) та цетиризину (10 мг/добу) показано, що експозиція цетиризину збільшувалася на 40%, а експозиція ритонавіру злегка змінювалася (-10%). У ряді випадків при одночасному застосуванні левоцетиризину з алкоголем або лікарськими препаратами, які пригнічують ЦНС, можливе посилення їх впливу на ЦНС, хоча не доведено, що рацемат цетиризину потенціює ефект алкоголю.Спосіб застосування та дозиПрепарат приймають внутрішньо, проковтуючи повністю під час їжі або натще, запиваючи невеликою кількістю води. Дорослі та діти старше 6 років: добова доза становить 5 мг (1 таблетка) одноразово. Основним шляхом виведення левоцетиризину з організму є виведення нирками, тому при застосуванні препарату у пацієнтів похилого віку та з нирковою недостатністю доза повинна коригуватися залежно від ступеня ниркової недостатності, ґрунтуючись на оцінці кліренсу креатиніну (мл/хв). Пацієнтам з легким порушенням ниркової функції (кліренс креатиніну 50-79 мл/хв) корекції дози не потрібно. У пацієнтів із помірною нирковою недостатністю (кліренс креатиніну від 30 до 49 мл/хв) рекомендована доза 5 мг через день. У пацієнтів з тяжкою нирковою недостатністю (кліренс креатиніну менше 30 мл/хв) рекомендована доза 5 мг 1 раз на 3 дні. Пацієнтам з нирковою та печінковою недостатністю дозування здійснюється за наведеною вище схемою. Пацієнтам з порушенням функції печінки корекції режиму дозування не потрібно. Тривалість прийому препарату: При лікуванні сезонного (інтермітуючого) алергічного риніту (наявність симптомів менше 4 днів на тиждень або їх загальна тривалість менше 4-х тижнів); тривалість лікування залежить від тривалості симптоматики; лікування може бути припинено при зникненні симптомів та відновлено з появою симптомів. При лікуванні цілорічного (персистирующего) алергічного риніту (наявність симптомів більше 4-х днів на тиждень та їх загальна тривалість більше 4-х тижнів) лікування може тривати протягом усього періоду дії алергенів. Є клінічний досвід безперервного застосування препарату Ксизал у лікарській формі таблетки покриті плівковою оболонкою 5 мг у дорослих пацієнтів тривалістю до 6 місяців. Якщо ви приймаєте або недавно приймали інші препарати, повідомте про це лікаря. Якщо ви забули прийняти препарат Ксізал, не приймайте подвійну дозу для компенсації пропущеної, прийміть наступну дозу у звичайний час.ПередозуванняСимптоми: сонливість (у дорослих), збудження та занепокоєння, що змінюються сонливістю (у дітей). Промивання шлунка або призначення активованого вугілля, якщо після прийому препарату пройшло мало часу. Рекомендується проведення симптоматичної та підтримуючої терапії. Специфічного антидоту немає. Гемодіаліз неефективний.Запобіжні заходи та особливі вказівкиМетилпарагідроксибензоат і пропілпарагідроксибензоат, що входять до складу крапель для прийому внутрішньо, можуть бути причиною алергічних реакцій (можливо уповільненого типу). Вплив на здатність керувати транспортними засобами та працювати з механізмами. Левоцетиризин може призвести до підвищеної сонливості, отже препарат Ксизал може впливати на здатність керувати автомобілем або працювати з технікою. У період лікування необхідно утримуватися від занять потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаРозчин - 1 мл: активна речовина: левоцетиризину дигідрохлорид – 5 мг; допоміжні речовини: натрію ацетат 5,70 мг, оцтова кислота 0,53 мг, пропіленгліколь 350,00 мг, гліцерол 85 % 294,10 мг, метилпарагідроксибензоат 0,3375 мг, пропілпарагідроксибензоат 0,037 вода очищена до 1,00мл. По 10,0 мл розчину у флакони темного скла (тип III, Євр. Ф.) номінальною місткістю 15 мл, забезпечені крапельницею з поліетилену низької щільності, з кришкою, що нагвинчується, з білого поліпропілену з "захистом від дітей". По 20,0 мл розчину у флакони темного скла (тип III, Євр. Ф.) номінальною місткістю 20 мл, забезпечені крапельницею з поліетилену низької щільності, з кришкою, що нагвинчується, з білого поліпропілену з "захистом від дітей". По 1 флакон разом з інструкцією по застосуванню поміщають у картонну пачку.Опис лікарської формиПрактично безбарвний слабо опалесцентний розчин.Фармакотерапевтична групаПротиалергічний засіб - блокатор H1-гістамінових рецепторів.ФармакокінетикаФармакокінетичні параметри левоцетиризину змінюються лінійно та практично не відрізняються від фармакокінетики цетиризину. Всмоктування. Після прийому внутрішньо препарат швидко і повністю абсорбується із ШКТ. Їда не впливає на повноту абсорбції, хоча швидкість її зменшується. У дорослих після одноразового прийому препарату в терапевтичній дозі (5 мг) Cmax у плазмі становить 270 нг/мл і досягається через 0,9 год, після повторного прийому в дозі 5 мг – 308 нг/мл. Css досягається через 2 добу. Розподіл. Левоцетиризин на 90% зв'язується з білками плазми. Vd становить 0,4 л/кг. Біодоступність сягає 100%. Метаболізм. У невеликих кількостях ( Виведення. У дорослих T1/2 становить (7,9±1,9) год; у маленьких дітей T1/2 укорочений. У дорослих загальний кліренс становить 0,63 мл/хв/кг. Близько 85,4% прийнятої дози препарату виводиться нирками у незміненому вигляді шляхом клубочкової фільтрації та канальцевої секреції; близько 12,9% – через кишечник. У пацієнтів з нирковою недостатністю (Cl креатинінуФармакодинамікаЛевоцетиризин – активна речовина препарату Ксизал® – це R-енантіомер цетиризину, який відноситься до групи конкурентних антагоністів гістаміну та блокує H1-гістамінові рецептори. Левоцетиризин впливає на гістамінозалежну стадію алергічних реакцій, а також зменшує міграцію еозинофілів, проникність судин, обмежує вивільнення медіаторів запалення. Левоцетиризин попереджає розвиток і полегшує перебіг алергічних реакцій, має протиексудативну, протисвербіжну і практично не чинить антихолінергічну та антисеротонінову дію. У терапевтичних дозах мало викликає седативний ефект.Показання до застосуваннялікування таких симптомів цілорічного (персистуючого) та сезонного (інтермітуючого) алергічних ринітів та алергічного кон'юнктивіту, як свербіж, чхання, закладеність носа, ринорея, сльозотеча, гіперемія кон'юнктиви; поліноз (сінна лихоманка); кропив'янка; інші алергічні дерматози, що супроводжуються свербінням та висипаннями.Вагітність та лактаціяДоклінічні дослідження не виявили будь-які прямі або непрямі несприятливі ефекти левоцетиризину на плід, що розвивається, а також на розвиток в постнатальному періоді; перебіг вагітності та пологів також не змінювалося. Адекватних та строго контрольованих клінічних досліджень щодо безпеки застосування препарату під час вагітності не проводилося. Застосування препарату при вагітності протипоказане. Левоцетиризин виділяється з грудним молоком, тому за необхідності застосування препарату при лактації рекомендується припинити грудне вигодовування.Побічна діяПід час проведення клінічних досліджень в осіб чоловічої та жіночої статі 12–71 роки часто (≥1/100, З боку імунної системи: реакції гіперчутливості, включаючи анафілаксію. З боку метаболізму та розладу харчування: підвищення апетиту. З боку психіки: тривога, агресія, збудження, безсоння, галюцинації, депресія, суїцидальні думки. З боку нервової системи: судоми, тромбоз синусів твердої мозкової оболонки, парестезія, запаморочення, непритомність, тремор, дисгевзія. З боку слуху: вертиго. З боку органу зору: порушення зору, нечіткість зорового сприйняття, запальні прояви. З боку ССС: відчуття серцебиття, тахікардія, тромбоз яремної вени. З боку дихальної системи: задишка, посилення симптомів риніту. З боку травної системи: нудота, блювання. Гепатобіліарні розлади: гепатит. З боку нирок та сечовидільної системи: дизурія, затримка сечі. З боку шкіри та м'яких тканин: ангіоневротичний набряк, стійка лікарська еритема, висипання, свербіж, кропив'янка, гіпотрихоз, тріщини, фотосенсибілізація. З боку кістково-м'язової системи: біль у м'язах. Загальні розлади: периферичні набряки. Інше: збільшення маси тіла, зміна функціональних спроб печінки, перехресна реактивність. Якщо будь-які побічні ефекти, що зазначені в інструкції, посилюються або пацієнт помітив інші побічні ефекти, слід повідомити про це лікаря.Взаємодія з лікарськими засобамиВивчення взаємодії левоцетиризину з іншими лікарськими засобами не проводилося. При вивченні лікарської взаємодії рацемату цетиризину з феназоном, псевдоефедрином, циметидином, кетоконазолом, еритроміцином, азитроміцином, гліпізидом та діазепамом клінічно значимих небажаних взаємодій не виявлено. При одночасному призначенні з теофіліном (400 мг на добу) загальний кліренс цетиризину знижується на 16% (кінетика теофіліну не змінюється). У дослідженні при одночасному прийомі ритонавіру (600 мг 2 рази на день) та цетиризину (10 мг/добу) показано, що експозиція цетиризину збільшувалася на 40%, а експозиція ритонавіру злегка змінювалася (-10%). У ряді випадків при одночасному застосуванні левоцетиризину з алкоголем або лікарськими препаратами, які пригнічують ЦНС, можливе посилення їх впливу на ЦНС, хоча не доведено, що рацемат цетиризину потенціює ефект алкоголю.Спосіб застосування та дозиПрепарат приймають внутрішньо під час їди або натще. Для застосування препарату слід використовувати чайну ложку. При необхідності дозу можна розбавити в невеликій кількості води безпосередньо перед вживанням. Дорослі та діти старше 6 років: добова доза становить 5 мг (20 крапель) одноразово. Діти віком від 2 до 6 років: по 1,25 мг (5 крапель) 2 рази на день; добова доза – 2,5 мг (10 крапель). Оскільки левоцетиризин виводиться з організму нирками, при застосуванні препарату пацієнтам із нирковою недостатністю та пацієнтам похилого віку дозу слід коригувати залежно від величини кліренсу креатиніну (КК). Кліренс креатиніну (КК) для чоловіків можна розрахувати, виходячи з концентрації сироваткового креатиніну, за такою формулою: КК (мл/хв)=[140 - вік (роки)] × маса тіла (кг) / 72 × ККсиворот (мг/дл) КК для жінок можна розрахувати, помноживши отримане значення коефіцієнт 0,85. Ниркова недостатність КК (мл/хв) Режим дозування Норма ≥80 5 мг/добу Легка 50-79 5 мг/добу Середня 30-49 5 мг/добу × 1 раз на 2 дні Важка <30 5 мг на добу × 1 раз на 3 дні Термінальна стадія – пацієнти, які перебувають на діалізі < 10 Прийом препарату протипоказаний Пацієнтам з нирковою та печінковою недостатністю дозування здійснюється за таблицею, наведеною вище. Пацієнтам з порушенням функції печінки корекції режиму дозування не потрібно. Тривалість прийому препарату: При лікуванні сезонного (інтермітуючого) алергічного риніту (наявність симптомів менше 4 днів на тиждень або їх загальна тривалість менше 4-х тижнів) тривалість лікування залежить від характеру захворювання; лікування може бути припинено при зникненні симптомів та відновлено з появою симптомів. При лікуванні цілорічного (персистирующего) алергічного риніту (наявність симптомів більше 4-х днів на тиждень або їх загальна тривалість більше 4-х тижнів) лікування може тривати протягом усього періоду дії алергенів. Є клінічний досвід безперервного застосування у дорослих пацієнтів тривалістю до 6 місяців.ПередозуванняСимптоми: сонливість (у дорослих), збудження та занепокоєння, що змінюються сонливістю (у дітей). Промивання шлунка або призначення активованого вугілля, якщо після прийому препарату пройшло мало часу. Рекомендується проведення симптоматичної та підтримуючої терапії. Специфічного антидоту немає. Гемодіаліз неефективний.Запобіжні заходи та особливі вказівкиМетилпарагідроксибензоат і пропілпарагідроксибензоат, що входять до складу крапель для прийому внутрішньо, можуть бути причиною алергічних реакцій (можливо уповільненого типу). Вплив на здатність керувати транспортними засобами та працювати з механізмами. Левоцетиризин може призвести до підвищеної сонливості, отже препарат Ксизал може впливати на здатність керувати автомобілем або працювати з технікою. У період лікування необхідно утримуватися від занять потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови відпустки з аптекБез рецептаВідео на цю тему
10 469,00 грн
746,00 грн
Склад, форма випуску та упаковкаЛіофілізат - 1 фл. активна речовина: омалізумаб – 150 мг; допоміжні речовини: сахароза – 108.0 мг, L-гістидин – 1,3 мг, L-гістидину гідрохлориду моногідрат – 2,1 мг, полісорбат 20 – 0,4 мг; розчинник: вода для ін'єкцій – 2,0 мл. Ліофілізат для приготування розчину для підшкірного введення, 150 мг, у флаконі місткістю 6 мл з безбарвного скла, закупореному гумовою пробкою і алюмінієвою кришкою з пластиковим верхом. Розчинник – вода для ін'єкцій 2 мл у ампулі безбарвного скла гідролітичного класу I. Один флакон з ліофілізатом у комплекті з однією ампулою з розчинником та з інструкцією із застосування в картонній пачці.Опис лікарської формиЛіофілізат: білого або майже білого кольору. Розчинник: безбарвна прозора рідина.Фармакотерапевтична групаІнші засоби для системного застосування при обструктивних захворюваннях дихальних шляхів.ФармакокінетикаВсмоктування Після підшкірного введення у пацієнтів з астмою абсолютна біодоступність омалізумабу становить у середньому 62%. При застосуванні у дозах понад 0,5 мг/кг фармакокінетика омалізумабу має лінійний характер. Пацієнти з атопічною БА Після одноразового підшкірного введення у дорослих і підлітків з бронхіальної астми всмоктування омалізумабу відбувається повільно, пік концентрації в сироватці крові досягається в середньому через 7-8 днів. Після багаторазового введення омалізумабу площа під кривою "концентрація-час" (AUC) протягом періоду від 0 до 14 діб у рівноважному стані була у 6 разів вищою, ніж після введення одноразової дози. Пацієнти з ГІК Після одноразового підшкірного введення у дорослих та підлітків з ХІК всмоктування омалізумабу відбувається повільно, пік концентрації у сироватці крові досягається в середньому через 6-8 днів. При застосуванні омалізумабу у пацієнтів з ХІК у діапазоні доз від 75 мг до 600 мг у вигляді одноразової підшкірної ін'єкції фармакокінетика має лінійний характер. Мінімальна концентрація омалізумабу у сироватці крові збільшується пропорційно підвищенню дози при введенні 75 мг, 150 мг або 300 мг кожні 4 тижні. Розподіл In vitro омалізумаб з IgE утворює комплекс певного розміру. In vitro чи in vivo не спостерігалося утворення преципітуючих комплексів та комплексів, молекулярна вага яких перевищувала 1 млн. дальтон. У клінічних дослідженнях не виявлено специфічного накопичення омалізумабу у будь-яких органах та тканинах. Пацієнти з атопічною БА У пацієнтів з атопічною БА після підшкірного введення обсяг розподілу омалізумабу, що здається, становив 78±32 мл/кг. Пацієнти з ГІК На підставі популяційної фармакокінетичної моделі було показано, що розподіл омалізумабу у пацієнтів з ГІК був подібним до таких у пацієнтів з атопічною БА. Виведення Кліренс омалізумабу включає як власне кліренс IgG, так і кліренс шляхом специфічного зв'язування та утворення комплексів з лігандом-мішенню – вільним IgE сироватки крові. Печінкова елімінація IgG включає деградацію в ретикулоендотеліальній системі печінки та ендотеліальних клітинах печінки. Інтактний IgG також виводиться із жовчю. Пацієнти з атопічною БА У пацієнтів з бронхіальною астмою період напіввиведення омалізумабу з сироватки становив у середньому 26 днів, кліренс в середньому становив 2,4 ± 1,1 мл/кг/добу. Крім того, при збільшенні маси тіла вдвічі відзначалося приблизно дворазове збільшення кліренсу, що здається. Пацієнти з ГІК На підставі популяційної фармакокінетичної моделі у пацієнтів з ХІК період напіввиведення омалізумабу з сироватки крові при рівноважній концентрації становив у середньому 24 дні, кліренс при рівноважній концентрації в середньому становив 240 мл/добу (що відповідає 3,0 мл/кг/добу для пацієнта масою тіла 80 кг. Фармакокінетика в особливих клінічних випадках Вік, расова/етнічна приналежність, стать, маса тіла, індекс маси тіла, вихідна концентрація IgE, аутоімунні антитіла до FceRI-рецептора, одночасне застосування лікарських засобів. Пацієнти з атопічною БА У пацієнтів з бронхіальною астмою не потрібно корекції дози омалізумабу залежно від віку (6-76 років), расової або етнічної приналежності, статі та індексу маси тіла. Пацієнти з ГІК У пацієнтів з ХІК не потрібна корекція дози омалізумабу залежно від віку (12-75 років), расової або етнічної приналежності, статі пацієнта, маси тіла, індексу маси тіла, вихідної концентрації IgE, аутоімунних антитіл до FceRI-рецептора або одночасного застосування блокаторів Н2 -гістамінових рецепторів та антагоністів лейкотрієнових рецепторів Порушення функції нирок та печінки Фармакокінетичні та фармакодинамічні параметри омалізумабу у пацієнтів з атопічною астмою або ХІК та порушеннями функції нирок або печінки не вивчалися. Оскільки метаболізм препарату здійснюється переважно ретикулоендотеліальною системою, порушення функції печінки та нирок не впливають на нього. Незважаючи на те, що корекція дози омалізумабу не потрібна, препарат слід застосовувати з обережністю у пацієнтів цієї категорії.ФармакодинамікаОмалізумаб є гуманізованим моноклональним антитілом, отриманим на основі рекомбінантної ДНК, що селективно зв'язується з імуноглобуліном (IgE). Омалізумаб являє собою антитіло IgG1 каппа, що містить людську структурну основу з визначальними комплементарність ділянками мишачого антитіла, що зв'язують IgE. Пацієнти з атопічною бронхіальною астмою Омалізумаб зв'язується з IgE і запобігає його взаємодії з високоафінним FcɛRI-рецептором. Таким чином відбувається зниження кількості вільного IgE, який є пусковим фактором для каскаду алергічних реакцій. При застосуванні препарату у пацієнтів з атопічною бронхіальною астмою (БА) відзначається помітне зменшення кількості FcRRI-рецепторів на поверхні базофілів. У клінічних дослідженнях у пацієнтів з бронхіальною астмою концентрація вільного IgE у сироватці крові дозозалежно зменшувалася протягом 1 години після введення першої дози препарату Ксолар і зберігалася на досягнутому рівні в період між введенням наступних доз. При застосуванні в дозах, що рекомендуються, середнє зменшення концентрації вільного IgE в сироватці крові становило більше 96%. Загальна концентрація IgE (пов'язаного та незв'язаного) у сироватці крові збільшувалася після застосування першої дози внаслідок утворення комплексу омалізумаб-IgE, що характеризується більш повільною швидкістю виведення порівняно з вільним IgE. На 16 тижні після введення першої дози препарату середня концентрація загального IgE у сироватці крові була в 5 разів вищою порівняно з такою до лікування.Після відміни лікування препаратом обумовлене його дією збільшення концентрації загального IgE та зменшення концентрації вільного IgE були оборотними. Після повного виведення омалізумабу з організму не спостерігалося збільшення концентрації IgE у сироватці крові. Концентрація загального IgE залишалася підвищеною протягом 1 року після відміни препарату Ксолар. При застосуванні препарату Ксолар у пацієнтів з середньотяжкою та тяжкою атопічною бронхіальною астмою відзначалося достовірне зменшення частоти загострень бронхіальної астми (визначених як погіршення перебігу астми, що потребує застосування системних глюкокортикостероїдів (ГКС) або подвоєння вихідної дози інгаляційних глюкокортикостероїдів) та зниження потреб. При застосуванні препарату Ксолар протягом 16 тижнів на тлі поступового зменшення дози інгаляційних або пероральних кортикостероїдів також спостерігалося достовірне зменшення частоти загострень бронхіальної астми та зниження потреби в інгаляційних кортикостероїдах порівняно з плацебо. У пацієнтів з бронхіальною астмою та цілорічним алергічним ринітом, які отримували терапію кортикостероїдами, при застосуванні омалізумабу протягом 28 тижнів відзначалося зниження вираженості симптомів бронхіальної астми та цілорічного алергічного риніту, а також поліпшення параметрів легеневої функції. Зменшення частоти загострень бронхіальної астми та поліпшення якості життя пацієнтів (за сертифікованим опитувальником якості життя) на фоні терапії препаратом Ксолар зберігалося протягом тривалого часу порівняно з плацебо. При застосуванні препарату Ксолар у дітей віком від 6 до 12 років протягом 52 тижнів було відмічено зниження частоти загострень бронхіальної астми в порівнянні з групою пацієнтів, які отримували плацебо. В іншому дослідженні на фоні застосування препарату Ксолар протягом 28 тижнів у дітей віком 6-12 років було відзначено зменшення частоти та вираженості загострень бронхіальної астми,а також зниження дози інгаляційних кортикостероїдів до кінця 28 тижня терапії в порівнянні з групою застосування плацебо. Пацієнти з хронічною ідіопатичною кропивницею У деяких пацієнтів із хронічною ідіопатичною кропив'янкою (ГІК) із сироватки крові були виділені аутоімунні антитіла до IgE та FceRI-рецептора. Дані антитіла здатні до активації базофілів або опасистих клітин, що призводить до вивільнення гістаміну. Одна з гіпотез механізму дії омалізумабу у пацієнтів з ГІК полягає у зниженні концентрації вільного IgE у крові, а потім і у шкірі. В результаті зменшується передача сигналу за допомогою FcsRI-рецепторів і, отже, пригнічується активація клітин, що беруть участь у запальній реакції. Таким чином, частота виникнення та вираженість симптомів ГІК знижується. Крім того, вважається, що зниження концентрації циркулюючого IgE призводить до швидкої неспецифічної десенсибілізації опасистих клітин у шкірі, а FcsRI-рецептори за допомогою зворотного негативного зв'язку підтримують цю реакцію. У клінічних дослідженнях у пацієнтів з ГІК, так само як і у пацієнтів з атопічною астмою, застосування омалізумабу призводило до дозозалежного зниження концентрації вільного IgE та підвищення концентрації загального IgE. Максимальне зниження концентрації вільного IgE спостерігалося через 3 дні після підшкірного введення першої дози препарату Ксолар. Після повторного введення препарату 1 раз кожні 4 тижні концентрація вільного IgE у сироватці крові перед введенням чергової дози зберігалася на досягнутому рівні в період між 12 та 24 тижнями лікування. Концентрація загального IgE у сироватці крові підвищувалася після введення першої дози внаслідок утворення комплексу омалізумаб-IgE, що характеризується більш повільною швидкістю виведення порівняно з вільним IgE. Після повторного введення препарату 1 раз кожні 4 тижні у дозі від 75 мг до 300 мг, концентрація загального IgE у сироватці крові на 12 тижні від початку лікування була в 2-3 рази вищою порівняно з таким до лікування та зберігалася на досягнутому рівні в період між 12 та 24 тижнями лікування. Після відміни препарату Ксолар протягом 16 тижнів наступного спостереження концентрація загального IgE зменшувалася,а концентрація вільного IgE збільшувалася, наближаючись до вихідних значень. При застосуванні препарату Ксолар у дозах 150 та 300 мг кожні 4 тижні у пацієнтів з ГІК спостерігалися відтворювані та статистично значущі терапевтичні ефекти щодо зменшення тяжкості свербежу. Ефект досягав максимуму до 12 тижня лікування та зберігався протягом усього періоду спостереження. Крім того, препарат Ксолар у дозі 300 мг надавав відтворюваний і статистично значущий ефект щодо індексу активності кропив'янки (UAS), частки днів без ангіоневротичного набряку, тижневого індексу порушень сну та якості життя пацієнтів, що оцінюється за опитувальником Cu-Q2oL (опитувач для вивчення якості життя у пацієнтів із ХІК), а також індексом DLQI (Дерматологічний індекс якості життя).Показання до застосуванняЛікування персистуючої атопічної бронхіальної астми середньотяжкої та тяжкої течії, симптоми якої недостатньо контролюються застосуванням інгаляційних глюкокортикостероїдів у пацієнтів 6 років та старше. Препарат Ксолар слід застосовувати у пацієнтів з початковою концентрацією IgE та масою тіла, які відповідають наведеним у таблиці з підбору режиму дозування. Лікування хронічної ідіопатичної кропив'янки, резистентної до терапії блокаторами Н1-гістамінових рецепторів, у пацієнтів 12 років та старше.Протипоказання до застосуванняПідвищена чутливість до омалізумабу або до іншого компонента препарату. Дитячий вік до 6 років у пацієнтів з атопічною БА та до 12 років у пацієнтів з ГІК у зв'язку з відсутністю відповідних даних щодо ефективності та безпеки. З обережністю: Слід з обережністю застосовувати препарат у пацієнтів з порушеннями функції печінки та нирок, з аутоімунними захворюваннями або захворюваннями, пов'язаними з накопиченням імунних комплексів. При застосуванні препарату Ксолар, як і при застосуванні будь-яких інших препаратів, що містять протеїн, можуть виникати місцеві або системні алергічні реакції, включаючи анафілактичні реакції. Перед введенням препарату Ксолар необхідно заздалегідь приготувати відповідне реанімаційне обладнання та лікарські засоби, необхідні для усунення реакцій гіперчутливості. Необхідно обережно застосовувати препарат у пацієнтів з підвищеним ризиком розвитку гельмінтних інвазій (особливо в ендемічних районах).Вагітність та лактаціяСпеціальних досліджень із застосування омалізумабу у вагітних жінок не проводилося. В експериментальних дослідженнях не було виявлено прямого або непрямого негативного впливу препарату протягом вагітності, розвиток ембріона та плода, перебіг пологів та розвиток новонароджених. Відомо, що молекули IgG проникають через гематоплацентарний бар'єр. Застосування препарату під час вагітності можливе лише у випадку, якщо користь матері перевищує потенційний ризик для плода. Людський IgG виділяється із грудним молоком. Невідомо, чи виділяється омалізумаб із грудним молоком у людини. Не можна виключити ризик для новонароджених/немовлят, які перебувають на грудному вигодовуванні, тому омалізумаб не слід застосовувати під час грудного вигодовування. У разі необхідності застосування препарату грудне вигодовування слід припинити. Вплив на фертильність Відсутні дані про вплив омалізумабу на фертильність у людини. Дослідження продемонстрували відсутність порушення чоловічої та жіночої фертильності у тварин при застосуванні багаторазових доз, що перевищують 75 мг/кг.Побічна діяАтопічна БА Найчастішими небажаними явищами (НЯ) при застосуванні препарату Ксолар є головний біль, реакції в місці ін'єкції, включаючи біль, набряк, еритему та свербіж у місці введення препарату. Більшість НЯ були легким або помірним ступенем тяжкості. Для визначення частоти розвитку небажаних реакцій, виявлених у ході клінічних досліджень, були використані такі критерії: дуже часто (≥1/10), часто (>1/100, 1/1000, Інфекційні та паразитарні захворювання: нечасто – фарингіт; рідко – паразитарні інвазії. Порушення з боку імунної системи: рідко – анафілактичні реакції та інші алергічні стани, включаючи ангіоневротичний набряк, виникнення антитіл до омалізумабу. Порушення з боку нервової системи: часто – головний біль; нечасто – запаморочення, сонливість, парестезії, синкопальні стани. Порушення з боку судин: нечасто – постуральна гіпотензія, "припливи". Порушення з боку дихальної системи, органів грудної клітки та середостіння: нечасто – кашель, алергічний бронхоспазм; рідко – набряк гортані. Порушення з боку шлунково-кишкового тракту: нечасто – нудота, діарея, диспепсичні явища. Порушення з боку шкіри та підшкірних тканин: нечасто – кропив'янка, висипання, свербіж, фотосенсибілізація; рідко – ангіоневротичний набряк. Загальні розлади та порушення у місці введення: часто – реакції у місці ін'єкції, такі як біль, еритема, свербіж, набряклість; нечасто – збільшення маси тіла, почуття втоми, набряклість рук, грипоподібний стан. На тлі терапії препаратом Ксолар у постреєстраційному періоді у клінічній практиці відзначалися такі НЯ, частота яких невідома, у зв'язку з тим, що спонтанні повідомлення про НЯ надходять у добровільному порядку з популяції невизначеного розміру. Порушення з боку імунної системи: анафілаксія та анафілактоїдні реакції (відзначалися як при першому, так і при повторному застосуванні препарату в більшості випадків протягом 2-х годин після підшкірної ін'єкції, у деяких пацієнтів через 2 години після введення препарату Ксолар), сироваткова хвороба може включати підвищення температури тіла, лімфаденопатію. Порушення з боку шкіри та підшкірних тканин: алопеція. Порушення з боку крові та лімфатичної системи: тяжка ідіопатична тромбоцитопенія. Порушення з боку дихальної системи, органів грудної клітки та середостіння: алергічний гранулематозний васкуліт (синдром Чарга-Строс). Порушення з боку скелетно-м'язової та сполучної тканини: артралгія, міалгія, припухлість суглобів. У типових дослідженнях у дітей 6-12 років було відзначено такі НЯ: Порушення з боку нервової системи: дуже часто – головний біль. Порушення з боку шлунково-кишкового тракту: часто – біль у верхньому відділі живота. Загальні розлади та порушення у місці введення: дуже часто – підвищення температури тіла. ХІК Найчастішими НЯ при застосуванні препарату Ксолар у пацієнтів 12 років і старших є головний біль та назофарингіт. Наведені нижче НЯ відзначалися у >1% пацієнтів у всіх групах лікування та не менше ніж на 2% частіше у пацієнтів, які отримували препарат Ксолар у рекомендованих дозах (150 мг та 300 мг), порівняно з групою застосування плацебо. НЯ згруповані відповідно до класифікації органів та систем органів MedDRA, у межах кожної групи перераховані у порядку зменшення частоти народження. Для визначення частоти народження використані наступні критерії: дуже часто (≥1/10), часто (>1/100, 1/1000, Інфекційні та паразитарні захворювання: часто – назофарингіт, синусит, інфекції верхніх дихальних шляхів, включаючи вірусну етіологію, інфекції сечовивідних шляхів. Порушення з боку нервової системи: дуже часто – головний біль; часто - головний біль у ділянці придаткових пазух носа. Порушення з боку скелетно-м'язової та сполучної тканини: часто – артралгія, міалгія, біль у кінцівках, кістково-м'язовий біль. Загальні розлади та порушення у місці введення: часто – підвищення температури тіла, реакції у місці ін'єкції, такі як набряклість, еритема, біль, гематома, свербіж, кровотеча, кропив'янка. Анафілаксія У післяреєстраційному періоді частота анафілактичних реакцій при застосуванні препарату Ксолар склала приблизно 0,2% (з усіх випадків анафілактичних реакцій на 500000 пацієнто-років). Анафілактичні реакції в анамнезі, не пов'язані із застосуванням омалізумабу, можуть бути фактором ризику розвитку анафілактичної реакції на введення препарату Ксолар. Малігнізація Загальна частота розвитку новоутворень при застосуванні препарату Ксолар у клінічних дослідженнях була подібною до такої в загальній популяції. Частота розвитку злоякісних новоутворень у групі пацієнтів, які отримували препарат Ксолар, та у контрольній групі оцінювалася У дітей 6-12 років випадків розвитку злоякісних новоутворень у групі пацієнтів, які отримували Ксолар, зареєстровано не було. Тромбоемболічні ускладнення У контрольованих клінічних дослідженнях у пацієнтів, які отримували лікування препаратом Ксолар, відмічався розвиток тромбоемболічних ускладнень, включаючи інсульт, транзиторні ішемічні атаки, інфаркт міокарда, нестабільну стенокардію, смерть від серцево-судинних причин (у тому числі летальний результат з невстановлених причин). При аналізі основних факторів серцево-судинного ризику співвідношення ризиків склало 1,32. Гельмінтні інвазії Можлива участь IgE у імунній відповіді при розвитку гельмінтних інвазій. У плацебо-контрольованих дослідженнях у пацієнтів з алергічними захворюваннями та ризиком розвитку гельмінтних інвазій при застосуванні препарату Ксолар відзначалося невелике підвищення частоти виникнення гельмінтозів (проте перебіг, тяжкість захворювання та відповідь на терапію не змінювалися). Загальна частота розвитку гельмінтних інвазій у всіх клінічних дослідженнях була меншою за 1 з 1000 (дизайн досліджень не включав спеціальне вивчення частоти розвитку гельмінтних захворювань). Зміна кількості тромбоцитів крові При застосуванні препарату Ксолар у ході клінічних досліджень у декількох пацієнтів спостерігалося зниження кількості тромбоцитів нижче за норму, що не супроводжувалося кровотечею або зменшенням концентрації гемоглобіну. У ході клінічних досліджень не було виявлено постійне зменшення кількості тромбоцитів. Дані інших лабораторних досліджень Значних змін лабораторних показників у ході клінічних досліджень не виявлено.Взаємодія з лікарськими засобамиОскільки IgE може брати участь у формуванні імунної відповіді на деякі гельмінтні інвазії, препарат Ксолар може опосередковано знижувати ефективність лікарських засобів для лікування гельмінтних та інших паразитарних інвазій. Оскільки ферменти цитохрому Р450, механізми системи енергетичного викиду (ефлюксні насоси) та зв'язування з білками не відіграють ролі в кліренсі омалізумабу, ймовірність виникнення лікарської взаємодії з іншими препаратами мала. Спеціальних досліджень щодо взаємодії препарату Ксолар із лікарськими препаратами, включаючи вакцини, не проводилося. Взаємодія омалізумабу з лікарськими препаратами, що використовуються для лікування ХА або ХІК, є малоймовірною. Атопічна БА У клінічних дослідженнях препарат Ксолар широко застосовували в комбінації з інгаляційними та пероральними глюкокортикостероїдами, інгаляційними бета2-адреноміметиками короткої та тривалої дії, антагоністами лейкотрієнів, теофіліном та пероральними антигістамінними засобами. Вказані вище препарати не впливають на безпеку препарату Ксолар. В даний час дані щодо застосування препарату Ксолар у комбінації зі специфічною імунотерапією (гіпосенсибілізуючою терапією) обмежені. ХІК У клінічних дослідженнях препарат Ксолар застосовували у комбінації з антигістамінними засобами (блокаторами Н1- та Н2-гістамінових рецепторів), антагоністами лейкотрієнових рецепторів. Не виявлено впливу вищезгаданих препаратів на профіль безпеки препарату Ксолар. Внаслідок популяційного фармакокінетичного аналізу також не виявлено впливу блокаторів Н2-гістамінових рецепторів та антагоністів лейкотрієнових рецепторів на фармакокінетику омалізумабу. Застосування препарату Ксолар у комбінації з імунодепресивними засобами не вивчалось. Препарат Ксолар не слід змішувати з іншими лікарськими препаратами або розчинами, крім води для ін'єкцій.Спосіб застосування та дозиТільки для підшкірного введення! Препарат не можна вводити внутрішньовенно або внутрішньом'язово. Атопічна БА Дозу препарату Ксолар і періодичність введення визначають на підставі вихідної концентрації IgE (МО/мл), виміряної на початок лікування, а також маси тіла (кг). Залежно від початкової концентрації IgE (МО/мл) та маси тіла (кг), рекомендована доза препарату становить від 75 до 600 мг 1 раз на 2 або 4 тижні (див. табл. 3 та 4). Препарат Ксолар не слід застосовувати у пацієнтів з початковою концентрацією IgE та масою тіла, які не відповідають наведеним у таблиці щодо підбору режиму дозування. Визначення кількості флаконів, ін'єкцій та загальний обсяг розчину препарату Ксолар залежно від дози див. у таблиці 1. Таблиця 1. Кількість флаконів, кількість ін'єкцій та загальний обсяг розчину препарату залежно від дози Доза (мг) Кількість флаконів Кількість ін'єкцій Загальний об'єм розчину (мл) 75 1 1 0,6 150 1 1 1,2 225 2 2 1,8 300 2 2 2,4 375 3 3 3,0 450 3 3 3,6 525 3 4 4,2 600 4 4 4.8 Розрахунок обсягу препарату для кожної дози При розведенні одного флакона препарату Ксолар виходить 1,2 мл розчину для підшкірного введення. Алгоритм розрахунку дози однією ін'єкцію представлений нижче у таблиці 2. Таблиця 2. Алгоритм розрахунку обсягу розчину на одну підшкірну ін'єкцію в залежності від дози Доза (мг) Кількість ін'єкцій Об'єм розчину (мл) 75 одна ін'єкція 0,6 м 150 одна ін'єкція 1,2 225 перша ін'єкція 1,2 друга ін'єкція 0,6 300 перша ін'єкція 1,2 друга ін'єкція 1,2 375 перша ін'єкція 1,2 друга ін'єкція 1,2 третя ін'єкція 0,6 450 перша ін'єкція 1,2 друга ін'єкція 1,2 третя ін'єкція 1,2 525 перша ін'єкція 1,2 друга ін'єкція 1,2 третя ін'єкція 1,2 четверта ін'єкція 0,6 600 перша ін'єкція 1,2 друга ін'єкція 1,2 третя ін'єкція 1,2 четверта ін'єкція 1,2 Тривалість лікування, моніторинг та корекція дози Дози препарату Ксолар слід коригувати за значних змін маси тіла (див. Таблиці 3, 4). Схеми визначення дози див. у таблицях 3 та 4. Таблиця 3. Розрахунок дози препарату Ксолар (мг) для підшкірного введення кожні 4 тижні. Маса тіла (кг) Початкова концентрація IgE (МЕ/мл) >20-25 >25-30 >30-40 >40-50 >50-60 >60-70 >70-80 >80-90 >90-125 >125-150 >30-100 75 75 75 150 150 150 150 150 300 300 >100-200 150 150 150 300 300 300 300 300 450 600 >200-300 150 150 225 300 300 450 450 450 600 >300-400 225 225 300 450 450 450 600 600 >400-500 225 300 450 450 600 600 Застосовується 1 раз на 2 тижні >500-600 300 300 450 600 600 таблицю 4 >600-700 300 450 600 Таблиця 4 . Розрахунок дози препарату Ксолар (мг) для підшкірного введення кожні 2 тижні. Маса тіла (кг) Вихідна >20- >25- >30- >40- >50- >60- >70- >80- >90- >125- >150- концентрація 25 30 40 50 60 70 80 90 125 150 200 IgE (МЕ/мл) >30-100 Застосовується раз на 4 тижні 225 >100-200 таблицю 3 375 >200-300 375 525 >300-400 450 525 >400-500 375 375 525 600 >500-600 375 450 450 600 >600-700 225 375 450 450 525 >700-800 225 225 300 375 450 450 525 600 >800-900 225 225 300 375 450 525 600 >900-1000 225 300 375 450 525 600 >1000-1100 225 300 375 450 600 >1100-1200 300 300 450 525 600 Не застосовується >1200-1300 300 375 450 525 >1300-1500 300 375 525 600 При застосуванні препарату Ксолар протягом перших 16 тижнів у ході клінічних досліджень спостерігалося зменшення частоти розвитку загострень бронхіальної астми, зниження кількості випадків застосування невідкладної терапії, а також поліпшення симптомів захворювання. Оцінку ефективності терапії препаратом Ксолар слід проводити як мінімум 12 тижнів лікування препаратом. Препарат Ксолар призначений для тривалої терапії. Відміна препарату, як правило, призводить до відновлення підвищеної концентрації вільного IgE та розвитку відповідних симптомів. Концентрація загального IgE зростає під час лікування та залишається підвищеною протягом одного року після припинення терапії. Таким чином, концентрація IgE при повторному визначенні на фоні терапії препаратом Ксолар не може бути орієнтиром для добору дози препарату. Для підбору дози препарату після зупинення лікування на період менше 1 року слід орієнтуватися на концентрацію IgE у сироватці крові, встановлену до введення початкової дози препарату. Якщо лікування препаратом Ксолар було зупинено на 1 рік або більше для підбору дози препарату Ксолар, слід повторно визначити концентрацію IgE у сироватці крові. Хронічна ідіопатична кропив'янка Рекомендована доза препарату Ксолар становить 300 мг кожні 4 тижні як п/к ін'єкції. Лікарю слід періодично повторно оцінювати необхідність продовження терапії препаратом. Досвід тривалого застосування омалізумабу у клінічних дослідженнях у пацієнтів з ГІК обмежений. Застосування у дітей та підлітків Препарат Ксолар не рекомендований для застосування у пацієнтів з атопічною бронхіальної астмою у віці до 6 років та у пацієнтів з ГІК у віці до 12 років у зв'язку з відсутністю даних щодо ефективності та безпеки. Застосування у пацієнтів похилого віку Є обмежений досвід застосування препарату Ксолар у пацієнтів віком від 65 років. Однак даних, що свідчать про корекцію дози препарату у пацієнтів цього віку, немає. Правила приготування та введення розчину При приготуванні розчину для підшкірного введення препарату Ксолар слідуйте наведеним нижче інструкціям. За допомогою шприца з голкою 18 калібру з ампули набирають 1,4 мл води для ін'єкцій для приготування розчину. Встановивши флакон із препаратом вертикально, його проколюють голкою відповідно до правил асептики та вводять воду для ін'єкцій безпосередньо в суху речовину препарату. Зберігаючи флакон у вертикальному положенні для рівномірного просочування сухої речовини водою для ін'єкцій флакон обережно обертають (не струшуючи) протягом 1 хвилини. Для полегшення розчинення флакон обертають протягом 5-10 секунд приблизно кожні 5 хвилин до повного розчинення всіх твердих частинок. У деяких випадках для повного розчинення сухої речовини може знадобитися більше 20 хвилин. У такому разі повторюють вищезгадані дії до розчинення видимих гелеподібних частинок. Після повного розчинення сухої речовини в розчині повинно бути видимих гелеподібних частинок. Допустимо наявність невеликих бульбашок або піни по стінках флакона. Отриманий розчин повинен бути прозорим або злегка опалесцентним, безбарвним або світло-жовтим кольором. Не можна використовувати розчин при виявленні у ньому сторонніх частинок. Після вилучення голки переверніть флакон на 15 секунд для того, щоб дати можливість перетекти розчину у напрямку до пробки. Використовуючи новий шприц об'ємом 3 см, оснащений голкою 18 калібру з широким просвітом, введіть голку в флакон. Помістіть кінець голки в найнижчу точку розчину, що скупчився в пробці флакона, і наберіть розчин у шприц. Перед видаленням голки витягніть поршень повністю назад до кінця циліндра шприца, щоб видалити весь розчин з перевернутого флакона. Замініть голку 18 калібру на голку 25 калібру для підшкірного введення. - Випустіть зайве повітря, великі бульбашки та надлишок розчину, щоб отримати необхідну дозу (об'ємом 1,2 мл). Тонкий шар невеликих пухирців може залишатися зверху розчину у шприці. Оскільки розчин має певну в'язкість, тривалість ін'єкції може становити 5-10 секунд. Розчин препарату вводять підшкірно в ділянку дельтовидного м'яза або в передньолатеральну ділянку стегна, уникаючи ділянки висипань при кропив'янці. Препарат Ксолар не слід змішувати з іншими лікарськими препаратами або розчинами, крім води для ін'єкцій. Розчин слід використовувати одразу після приготування, оскільки препарат не містить антибактеріальних консервантів. У разі потреби допускається зберігання розчину протягом 8 годин при температурі від 2 до 8 °С та протягом 4 годин при 30 °С. Невикористані залишки препарату та відходи упаковки утилізують відповідно до місцевих вимог.ПередозуванняПро випадки передозування омалізумабом дотепер не повідомлялося. Максимальна доза препарату Ксолар, що переноситься, дотепер не визначена. При одноразовому внутрішньовенному введенні у дозі до 4000 мг не відмічено ознак дозолімітуючої токсичності. При введенні найвищої кумулятивної дози препарату – 44 000 мг протягом 20 тижнів не відзначалося розвитку будь-яких тяжких гострих НЯ.Запобіжні заходи та особливі вказівкиАлергічні реакції При застосуванні препарату Ксолар, як і при застосуванні будь-яких інших препаратів, що містять протеїн, можуть виникати місцеві або системні алергічні реакції, включаючи анафілактичні реакції. Перед введенням препарату Ксолар необхідно заздалегідь приготувати відповідне реанімаційне обладнання та лікарські засоби, необхідні для усунення реакцій гіперчутливості. Слід поінформувати пацієнтів про можливість розвитку анафілактичних реакцій та забезпечити відповідне медичне спостереження. У клінічних дослідженнях розвиток анафілаксії та анафілактоїдних реакцій відзначався при застосуванні як першої, так і повторних доз препарату Ксолар. Найчастіше виникнення таких реакцій відзначалося протягом 2 годин після введення препарату. Так само як при застосуванні інших гуманізованих моноклональних антитіл - похідних рекомбінантної ДНК, в окремих випадках можливе утворення антитіл до омалізумабу. Сироваткова хвороба У пацієнтів, які отримували терапію гуманізованими моноклональними антитілами, у тому числі омалізумабом, у поодиноких випадках спостерігався розвиток сироваткової хвороби та подібних до неї станів, що є проявом відстрочених алергічних реакцій 3 типу. Початок розвитку таких станів зазвичай спостерігався на 1-5 день після першої або наступних ін'єкцій, а також при тривалій терапії. Симптоми, що дозволяють запідозрити розвиток сироваткової хвороби, включають: артрит/артралгію, висип (кропив'янка або інші форми), лихоманку та лімфаденопатію. Як профілактика та лікування даної патології можливе застосування антигістамінних препаратів та глюкокортикостероїдів. Слід поінформувати пацієнта про можливість розвитку цього стану та попередити про необхідність звернення до лікаря у разі можливих симптомів. Синдром Чарга-Стросс та гіпереозинофіл'ний синдром У пацієнтів з бронхіальною астмою тяжкого ступеня в окремих випадках може розвиватися системний гіпереозинофільний синдром або алергічний еозинофільний гранулематозний васкуліт (синдром Чарга-Строс), для лікування яких зазвичай застосовують терапію системними глюкокортикостероїдами (ГКС). У поодиноких випадках у пацієнтів, які отримують протиастматичні лікарські препарати, у тому числі омалізумаб, може проявитися або розвинутись системна еозинофілія або васкуліт. Ці випадки зазвичай пов'язані зі зниженням дози пероральних кортикостероїдів. Лікарю слід виявляти настороженість до розвитку вираженої еозинофілії, васкулітного висипу, погіршення перебігу легеневих симптомів, патології придаткових пазух носа, ускладнень з боку серця та/або нефропатії у таких пацієнтів. У разі розвитку вищезазначених порушень тяжкого ступеня з боку імунної системи слід розглянути можливість відміни омалізумабу. загальні вказівки Препарат не слід застосовувати для лікування гострих нападів бронхіальної астми, гострого бронхоспазму або астматичного статусу. Не вивчалося застосування препарату Ксолар у пацієнтів із синдромом підвищеної концентрації IgE, з алергічним бронхолегеневим аспергільозом, для профілактики анафілактичних реакцій, при атопічному дерматиті, алергічному риніті або при харчовій алергії. Не вивчалося застосування препарату Ксолар у пацієнтів з порушеннями функції печінки та нирок, аутоімунними захворюваннями або захворюваннями, пов'язаними з накопиченням імунних комплексів. Слід бути обережними при застосуванні препарату у таких пацієнтів. Не слід різко скасовувати терапію системними або інгаляційними глюкокортикостероїдами після початку лікування препаратом Ксолар. Дозу зазначених препаратів, що застосовуються одночасно з препаратом Ксолар, поступово знижують під наглядом лікаря. Вміст сахарози в препараті не має клінічно значущого впливу на концентрацію глюкози у сироватці крові у пацієнтів з цукровим діабетом, тому корекція дози препарату Ксолар та гіпоглікемічних препаратів не потрібна. Вплив на здатність до керування автотранспортом та управління механізмами Пацієнтам, у яких на фоні застосування препарату Ксолар виникає запаморочення, підвищена стомлюваність, синкопальні стани або сонливість слід утриматися від керування транспортними засобами та механізмами.Умови зберіганняУ холодильнику +2+8 градусівУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковка«Ротокан»: екстракт ромашки рідкий, екстракт календули рідкий, екстракт деревію рідкий; екстракт евкаліпта прутовидного, ефірна олія евкаліпта, ефірна олія сосни, ефірна олія ялиці, ефірна олія розмарину, ефірна олія лаванди, ефірна олія м'яти, ефірна олія чайного дерева, ефірна олія коріандру, ефірна олія рожева, ефірна олія полину, гліцерин, твін-80 , бензалконію хлорид, вода очищена.ХарактеристикаСкладно-комбінований засіб природного походження є спрей на водній основі для місцевого застосування для профілактики та у складі комплексної терапії при інфекційно-запальних захворюваннях порожнини рота, горла та шкіри. Активний комплекс «РОТОКАН», що складається з екстрактів ромашки, календули та деревію, посилює та прискорює процеси регенерації слизових оболонок, нормалізує та покращує трофічні процеси, за рахунок засобів біологічно активних речовин, що входять до складу засобу.ІнструкціяЗасіб застосовується місцево шляхом зрошення слизових оболонок порожнини рота та носоглотки 1-2 натисканнями головки розпилювача до 8 разів на добу. У момент упорскування рекомендується затримати дихання. Після зрошення порожнини рота слід утриматися від їди протягом 15-30 хвилин. Утримувати засіб у ротовій порожнині 5-7 хвилин. Тривалість застосування 5-7 днів. При запаленнях і травмах шкірних покровів, слизових оболонок перед застосуванням з уражених ділянок за допомогою стерильних тампонів рекомендується видалити некротичний наліт, потім поверхню обробляють марлевою серветкою, змоченою в засобі, і залишають на 15-20 хвилин, процедуру проводять 2-6 разів на добу протягом 10 днів. Спрей застосовується для профілактики та як додатковий засіб до основного лікування при інфекційно-запальних захворюваннях порожнини рота, ЛОР-органів та шкірних покривів: при тонзилітах, фарингітах, ангінах, ларингітах різної етіології (у тому числі втрата голосу, хрип, втома голосових зв'язок) тощо; при стоматологічних захворюваннях: афтозному стоматиті, пародонтозі, виразково-некротичному гінгівостоматиті, після видалення зубних відкладень та вишкрібання патологічних ясенних кишень, інфекційних стоматитах (вірусні, бактеріальні, грибкові інфекції) тощо; при трофічних виразках, опіках, в'ялогранулюючих і довго не гояться ранах, пролежнях; після резекції мигдаликів та поліпів; для профілактики грипу та застудних захворювань.Протипоказання до застосуванняІндивідуальна нестерпність компонентів.Запобіжні заходи та особливі вказівкиПеред застосуванням рекомендується проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаКраплі - 1 мл: Діюча речовина: бетаксол 5 мг; Допоміжні речовини: бензалконію хлорид, гіпромелоза, натрію хлорид, натрію гідроксид, динатрію едетат, вода д/і. Краплі очні. 5 мл - флакон-крапельниці пластикові (1) - пачки картонні.Фармакотерапевтична групаПротиглаукомний препарат. Селективний бета1-адреноблокатор без внутрішньої симпатоміметичної активності. Не має мембраностабілізуючу (місцевоанестезуючу) дію. При місцевому застосуванні бетаксолол знижує внутрішньоочний тиск за рахунок зменшення продукції внутрішньоочної рідини. Настання гіпотензивної дії спостерігається через 30 хв після закапування, максимальний ефект розвивається через 2 години. Після одноразової інстиляції вплив на офтальмотонус зберігається протягом 12 годин. Бетаксолол (порівняно з іншими бета-адреноблокаторами) не викликає зниження кровотоку в зоровому нерві. Застосування очних крапель Ксонеф не призводить до виникнення міозу, спазму акомодації, гемералопії (на відміну міотиків).ФармакокінетикаБетаксолол високо ліпофілен, внаслідок чого добре проникає через рогівку у передню камеру ока. Cmax (1.17 мг/мл) у передній камері визначається через 20 хвилин після інстиляції. Проникає у системний кровотік. T1/2 із внутрішньоочної рідини близько 1 год. T1/2 із плазми крові 16-22 год. Виведення переважно через нирки.Показання до застосуванняЯк монотерапія: Для зниження внутрішньоочного тиску. У поєднанні з іншими препаратами при: Відкритокутової глаукоми; очної гіпертензії.Протипоказання до застосуванняСинусова брадикардія; AV-блокада II та III ступеня; виражена серцева недостатність; кардіогенний шок; артеріальна гіпотензія; дитячий вік до 18 років; - підвищена чутливість до компонентів препарату. З обережністю слід застосовувати препарат при тиреотоксикозі, міастенії, цукровому діабеті, синдромі Рейно, феохромоцитомі, бронхіальній астмі, хронічному обструктивному бронхіті. З обережністю призначають препарат пацієнтам із цукровим діабетом, оскільки бета-адреноблокатори можуть маскувати симптоми гострої гіпоглікемії. З обережністю препарат призначають пацієнтам з тиреотоксикозом, т.к. бета-адреноблокатори можуть маскувати симптоми тиреотоксикозу (наприклад, тахікардію). З обережністю слід призначати бета-адреноблокатори пацієнтам із вираженими порушеннями функції дихальної системи. Препарат слід призначати з обережністю пацієнтам із синдромом Рейно або феохромоцитомою.Вагітність та лактаціяДостатнього досвіду застосування препарату Ксонеф при вагітності та в період лактації немає. Застосування препарату при вагітності та в період лактації (грудного вигодовування) можливе лише в тому випадку, коли передбачувана користь для матері перевищує потенційний ризик для плода чи дитини. Дитячий вік віком до 18 років.Побічна діяЗ боку органу зору: часто – короткочасний дискомфорт в очах після закапування, сльозотеча; в окремих випадках – зниження чутливості рогівки, почервоніння очей, точковий кератит, світлобоязнь, анізокорія, фотофобія, свербіж, відчуття "сухості" очей, алергічні реакції. Системні побічні ефекти відзначаються рідко: З боку ЦНС: запаморочення, нудота, сонливість, безсоння, біль голови, депресія, посилення симптомів міастенії. З боку серцево-судинної системи: брадикардія, порушення серцевої провідності та серцева недостатність. З боку дихальної системи: диспное, бронхоспазм, бронхіальна астма, дихальна недостатність.Взаємодія з лікарськими засобамиПри одночасному застосуванні препарату Ксонеф та бета-адреноблокаторів для прийому внутрішньо підвищується ризик розвитку побічних ефектів (як місцевих, так і системних) внаслідок адитивного ефекту (тому пацієнти, які отримують цю комбінацію препаратів, повинні бути під медичним наглядом). При застосуванні препарату Ксонеф у поєднанні з препаратами, що виснажують запаси катехоламінів (такими як резерпін), може спостерігатися зниження артеріального тиску та брадикардія. При одночасному призначенні міорелаксантів та гіпоглікемічних засобів може спостерігатися посилення їхньої дії. При спільному застосуванні з симпатоміметиками - посилення їх судинозвужувального ефекту. Слід бути обережними при спільному застосуванні препарату Ксонеф та психотропних засобів внаслідок можливого посилення їх дії.Спосіб застосування та дозиПрепарат закопують у кон'юнктивальний мішок по 1-2 краплі 2 рази на добу. У деяких пацієнтів стабілізація внутрішньоочного тиску відбувається протягом декількох тижнів, тому рекомендується контролювати внутрішньоочний тиск протягом першого місяця лікування. При недостатній клінічній ефективності монотерапії призначають додаткову терапію.ПередозуванняПри надходженні в очі надмірної кількості препарату слід промити очі теплою водою. Симптоми: при передозуванні бета-адреноблокаторів можуть спостерігатися зниження артеріального тиску, брадикардія, гостра серцева недостатність. Лікування: проводять симптоматичну терапію.Запобіжні заходи та особливі вказівкиПеред плановою хірургічною операцією слід поступово відмінити бета-адреноблокатори за 48 год до загальної анестезії, т.к. під час проведення загальної анестезії можуть зменшити чутливість міокарда до симпатичної стимуляції. Пацієнти, у яких використовуються бета-адреноблокатори, можуть мати в анамнезі атопію або анафілактичні реакції. У разі розвитку повторних реакцій підвищеної чутливості такі пацієнти можуть бути не чутливі до звичайних доз епінефрину (адреналіну), необхідного для усунення анафілаксії. При закапуванні у вічі бета-адреноблокатори можуть всмоктуватися в системний кровотік. При цьому можуть бути такі ж побічні ефекти, як і при системному застосуванні. Описані випадки тяжких дихальних та серцево-судинних розладів, включаючи бронхоспазм з летальним кінцем у пацієнтів з бронхіальною астмою та смерть від серцевої недостатності. Ксонеф має мінімальний вплив на АТ та ЧСС. Однак слід дотримуватися обережності при призначенні препарату пацієнтам з AV-блокадою І ступеня та легкою та помірною серцевою недостатністю. Лікування препаратом Ксонеф слід негайно припинити з появою перших симптомів декомпенсації з боку серцево-судинної системи. Ксонеф містить консервант бензалконію хлорид, який може брати в облогу на м'яких контактних лінзах і надавати токсичну дію на тканині ока. Тому пацієнтам, які носять контактні лінзи, слід зняти їх перед застосуванням крапель і встановити не раніше ніж через 20 хв після закапування. Вплив на здатність до керування автотранспортом та управління механізмами: Якщо після застосування крапель у пацієнтів тимчасово знижується чіткість зору, до її відновлення не рекомендується керувати транспортними засобами та займатися видами діяльності, що потребують підвищеної уваги та реакції.Умови відпустки з аптекЗа рецептомВідео на цю тему
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
982,00 грн
893,00 грн
Склад, форма випуску та упаковкаКраплі - 1 мл: Активна речовина: убідекаренон – 30 мг; Допоміжні речовини: альфа-токоферолу ацетат 4,5 мг, аскорбіл пальмітат 1,0 мг, макрогол гліцерилгідроксистеарат (Кремофор RH-40) 105,0 мг, натрію бензоат 2,0 мг, лимонна кислота (харчова) 1,6 мг очищена до 1 мл. Краплі прийому внутрішньо 3%. По 15, 20, 25, 50, 60, 100 мл у флакони світлозахисного (помаранчевого) скла, забезпеченими поліетиленовими пробками-крапельницями і кришками, що нагвинчуються. Кожен флакон разом з інструкцією із застосування поміщають у пачки з картону.Опис лікарської формиПрозора рідина жовтувато-жовтогарячого кольору з легкою опалесценцією.Фармакотерапевтична групаКардіотонічне засіб неглікозидної структури.ФармакодинамікаУбідекаренон (коензим Q10, убихинон) - природна речовина, що є вітаміноподібним коферментом. Убідекаренон є ендогенним субстратом, бере участь у переносі електронів у транспортному ланцюжку окиснювально-відновлювальних процесів, у процесі обміну енергії, у реакції окисного фосфорилювання в дихальному ланцюзі мітохондрій клітин. Бере участь у процесах клітинного дихання, збільшуючи синтез аденозинтрифосфорної кислоти (АТФ). Чинить клінічно значущу антиоксидантну дію. Захищає ліпіди клітинних мембран від перекисного окиснення. Зменшує зону пошкодження міокарда в умовах ішемії та реперфузії. Убідекаренон перешкоджає подовженню QT інтервалу, покращує переносимість фізичного навантаження.За рахунок ендогенного синтезу 100% задоволення потреб організму в коензимі Q10 відбувається лише до 20-річного віку. Концентрація коензиму Q10 знижується у пацієнтів похилого віку, а також за різних захворювань як у дорослих, так і у дітей.Показання до застосуванняУ складі комплексної терапії: У дорослих: хронічна серцева недостатність, дилатаційна кардіоміопатія, ішемічна хвороба серця, у тому числі інфаркт міокарда (під час відновної терапії), аритмії, артеріальна гіпертензія. У дітей з 1 року: хронічна серцева недостатність, дилатаційна кардіоміопатія, аритмії, хронічний гастродуоденіт, хронічний пієлонефрит, метаболічна нефропатія, мігрень, нейро-циркуляторна дистонія, спадкові нейродегенеративні захворювання (мітохондріальний синдром, міопатії, м'язові дистрофії, захворювання, пов'язані з порушенням обмінних процесів (астенічний синдром, відновлювальний період після тяжких захворювань та хірургічних втручань). Період підготовки до проведення операцій на серці (аорто-коронарне шунтування, вроджені та набуті вади) у дорослих та дітей з 1 року за рекомендацією лікаря. Для покращення адаптації до підвищених фізичних навантажень у дорослих та дітей з 1 року. Для профілактики та поповнення недостатності коензиму Q10 у дорослих та дітей з 1 року.Протипоказання до застосуванняПідвищена чутливість до компонентів препарату. Дитячий вік до 1 року. З обережністю: При артеріальній гіпотензії.Вагітність та лактаціяПрепарат не рекомендується призначати вагітним і жінкам, що годують, у зв'язку з відсутністю достатнього досвіду клінічного застосування.Побічна діяМожливі алергічні реакції. Дуже рідко: нудота, діарея.Взаємодія з лікарськими засобамиОдночасне застосування гіполіпідемічних засобів (статини, фібрати), бета-адреноблокаторів (атенолол, метопролол, пропранолол), трициклічних антидепресантів може призводити до зниження концентрації убідекаренону в плазмі крові. Убідекаренон може знижувати дію варфарину. Убідекаренон може потенціювати дію дилтіазему, метопрололу, еналаприлу та нітратів.Спосіб застосування та дозиПрепарат Кудесан® слід приймати внутрішньо 1 раз на добу під час їди в першій половині дня, попередньо розчинивши в невеликій кількості кип'яченої води або іншому напої кімнатної температури. З метою профілактики та поповнення недостатності коензиму Q10 приймати: Діти 1-3 роки – по 2-4 краплі на день (3-6 мг). Діти 3-7 років – по 4-8 крапель на день (6-12 мг). Діти 7-12 років – по 8-12 крапель на день (12-18 мг). Діти старше 12 років та дорослі – по 12-24 крапель на день (18-30 мг). У комплексній терапії різних захворювань Кудесан® приймати в залежності від віку за всіма заявленими показаннями: Діти 1-3 роки – по 4-10 крапель на день (6-15 мг). Діти 3-7 років – по 10-16 крапель на день (15-24 мг). Діти 7-12 років – по 16-20 крапель на день (24-30 мг). Діти старше 12 років та дорослі – по 20-60 крапель на день (30-90 мг). Тривалість курсу застосування препарату Кудесан становить 2-3 місяці. Повторні курси – за рекомендацією лікаря.ПередозуванняНемає даних.Запобіжні заходи та особливі вказівкиВплив на здатність до керування автотранспортом та управління механізмами Немає даних.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаКраплі - 1 мл: Діюча речовина: убідекаренон – 30,0 мг; Допоміжні речовини: DL-альфа-токоферолу ацетат, аскорбіл пальмітат, макрогол гліцерилгідроксистеарат, натрію бензоат, лимонна кислота моногідрат, вода очищена. По 15, 20, 25, 50, 60, 100 мл у флакони темного скла, з гвинтовими кришками з поліетилену низького тиску та крапельницями з поліетилену високого тиску. На флакон наклеюють самоклеючу етикетку. По 1 флакону разом з інструкцією по застосуванню поміщають у картонну пачку.Опис лікарської формиПрозора рідина жовтувато-жовтогарячого кольору з легкою опалесценцією.Фармакотерапевтична групаКардіотонічне засіб неглікозидної структури.ФармакодинамікаУбідекаренон (коензим Q10, убихинон) - природна речовина, що є вітаміноподібним коферментом. Убідекаренон є ендогенним субстратом, бере участь у переносі електронів у транспортному ланцюжку окиснювально-відновлювальних процесів, у процесі обміну енергії, у реакції окисного фосфорилювання в дихальному ланцюзі мітохондрій клітин. Бере участь у процесах клітинного дихання, збільшуючи синтез аденозинтрифосфорної кислоти (АТФ). Чинить клінічно значущу антиоксидантну дію. Захищає ліпіди клітинних мембран від перекисного окиснення. Зменшує зону пошкодження міокарда в умовах ішемії та реперфузії. Убідекаренон перешкоджає подовженню QT інтервалу, покращує переносимість фізичного навантаження.За рахунок ендогенного синтезу 100% задоволення потреб організму в коензимі Q10 відбувається лише до 20-річного віку. Концентрація коензиму Q10 знижується у пацієнтів похилого віку, а також за різних захворювань як у дорослих, так і у дітей.РекомендуєтьсяУ складі комплексної терапії: дорослих: хронічна серцева недостатність, дилатаційна кардіоміопатія, ішемічна хвороба серця, у тому числі інфаркт міокарда (під час відновної терапії), аритмії, артеріальна гіпертензія. У дітей з 1 року: хронічна серцева недостатність, дилатаційна кардіоміопатія, аритмії, хронічний гастродуоденіт, хронічний пієлонефрит, метаболічна нефропатія, мігрень, нейро-циркуляторна дистонія, спадкові нейродегенеративні захворювання (мітохондріальний синдром, міопатії, м'язові дистрофії, захворювання, пов'язані з порушенням обмінних процесів (астенічний синдром, відновлювальний період після тяжких захворювань та хірургічних втручань). Період підготовки до проведення операцій на серці (аорто-коронарне шунтування, вроджені та набуті вади) у дорослих та дітей з 1 року за рекомендацією лікаря. Для покращення адаптації до підвищених фізичних навантажень у дорослих та дітей з 1 року. Для профілактики та поповнення недостатності коензиму Q10 у дорослих та дітей з 1 року.Протипоказання до застосуванняПідвищена чутливість до компонентів препарату. Дитячий вік до 1 року. З обережністю: при артеріальній гіпотензії.Вагітність та лактаціяПрепарат не рекомендується призначати вагітним і жінкам, що годують, у зв'язку з відсутністю достатнього досвіду клінічного застосування.Побічна діяМожливі алергічні реакції. Дуже рідко: нудота, діарея.Взаємодія з лікарськими засобамиОдночасне застосування гіполіпідемічних засобів (статини, фібрати), бета-адреноблокаторів (атенолол, метопролол, пропранолол), трициклічних антидепресантів може призводити до зниження концентрації убідекаренону в плазмі крові. Убідекаренон може знижувати дію варфарину. Убідекаренон може потенціювати дію дилтіазему, метопрололу, еналаприлу та нітратів.Спосіб застосування та дозиПрепарат "Кудесан® для дітей" слід приймати внутрішньо 1 раз на добу під час їди в першій половині дня. З метою профілактики та поповнення недостатності коензиму Q10 приймати відповідно до рекомендацій, викладених у таблиці 1. Таблиця 1 Вік Кількість таблеток, призначення в середньому Еквівалентний вміст коензиму Q10 3 роки - 7 років 1 таблетка 7,5 мг 7-12 років 1-2 таблетки 7,5-15 мг діти старше 12 років та дорослі 2-4 таблетки 15-30 мг У комплексній терапії різних захворювань препарат "Кудесан® для дітей" прийматиме залежно від віку за всіма заявленими показаннями відповідно до рекомендацій, викладених у таблиці 2. Таблиця 2 Вік Кількість таблеток, призначення в середньому Еквівалентний вміст коензиму Q10 3 роки - 7 років 2-3 таблетки 15-22,5 мг 7-12 років 3-4 таблетки 22,5-30 мг Дітям старше 12 років і дорослим для застосування в комплексній терапії захворювань рекомендовано прийом препарату "Кудесан®", краплі для внутрішнього прийому 3%. Тривалість курсу застосування препарату "Кудесан® для дітей" становить 2-3 місяці. Повторні курси – за рекомендацією лікаря.ПередозуванняНемає даних.Запобіжні заходи та особливі вказівкиВплив на здатність до керування автотранспортом та управління механізмами Немає даних.Умови відпустки з аптекБез рецептаВідео на цю тему
Упакування: упак. Виробник: Парафарм Завод-виробник: Парафарм(Росія). .
Упакування: упак. Виробник: Парафарм Завод-виробник: Парафарм(Росія). .
Склад, форма випуску та упаковкаТаблетки – 1 таб.:. Діюча речовина: тадалафілу 20,00 мг; допоміжні речовини: лактози моногідрат 249,00 мг, целюлоза мікрокристалічна 66,00 мг, гіпоролоза 3,50 мг, натрію лаурилсульфат 1,00, кроскармеллоза натрію 7,00 мг, магнію стеарат 3,50 мг; Плівкова оболонка: опадрай II 32К520009 жовтий 8,00 мг (лактози моногідрат 36%, гіпромелоза 26%, титану діоксид 15,5%, заліза оксид жовтий 8,5%, тріацетин 8,0%, тальк 6,0 Пігулки, покриті плівковою оболонкою, 20 мг. По 1 або 2 таблетки в блістер із ПВХ/ПВДХ/Аl. По 1 або 2 або 4 блістери разом з інструкцією із застосування в картонну пачку.Опис лікарської формиМигдалеподібні пігулки, покриті плівковою оболонкою, жовтого кольору, з гравіюванням "20" на одній стороні.Фармакотерапевтична групаЕректильна дисфункція Засіб лікування - ФДЕ5-інгібітор.ФармакокінетикаВсмоктування. Після прийому препарату тадалафіл швидко всмоктується. Середня максимальна концентрація (Сmах) у плазмі крові досягається в середньому через 2 години після прийому внутрішньо. Швидкість і ступінь всмоктування тадалафілу не залежать від часу їди, тому препарат Купид 36 можна застосовувати незалежно від часу їди. Час прийому (вранці або ввечері) не надавав клінічно значущого впливу на швидкість та ступінь всмоктування. Фармакокінетика тадалафілу у здорових осіб лінійна щодо часу та дози. У діапазоні доз від 2,5 до 20 мг площа під кривою "концентрація - час" (AUC) збільшується пропорційно дозі. Рівноважні концентрації у плазмі досягаються протягом 5 днів при прийомі препарату один раз на добу.Фармакокінетика тадалафілу у пацієнтів з порушенням ерекції аналогічна фармкокінетиці препарату у осіб без порушення ерекції. Розподіл. Середній обсяг розподілу становить близько 63 л, що свідчить про те, що тадалафіл розподіляється у тканинах організму. У терапевтичних концентраціях 94% тадалафілу у плазмі зв'язується з білками. Зв'язування з білками не змінюється за порушення функції нирок. У здорових осіб менше 0,0005% введеної дози виявлено у спермі. Метаболізм. Тадалафіл переважно метаболізується за участю ізоферменту CYP3A4 цитохрому Р450. Основним циркулюючим метаболітом є метилкатехолглюкуронід. Цей метаболіт принаймні у 13 000 разів менш активний щодо ФДЕ-5, ніж тадалафіл. Отже, концентрація цього метаболіту не є клінічно значущою. Виведення. У здорових осіб середній кліренс тадалафілу при внутрішньому прийомі становить 2,5 л/год, а середній Т1/2 - 17,5 ч. Тадалафіл виводиться переважно у вигляді неактивних метаболітів, в основному, через кишечник (близько 61% дози) і, меншою мірою, нирками (близько 36% дози). Особливі групи населення. Літні пацієнти. Здорові пацієнти похилого віку (65 років і більше) мали нижчий кліренс тадалафілу при прийомі внутрішньо, що виражалося у збільшенні площі під кривою "концентрація-час" на 25% порівняно зі здоровими особами віком від 19 до 45 років. Ця відмінність не є клінічно значущою і не потребує добору дози. Пацієнти з нирковою недостатністю. У осіб з нирковою недостатністю, включаючи пацієнтів, що перебувають на гемодіалізі, площа під кривою "концентрація-час" була більшою, ніж у інших здорових осіб. Пацієнти з печінковою недостатністю. Фармакокінетика тадалафілу у пацієнтів зі слабкою та середньотяжкою печінковою недостатністю можна порівняти з такою у здорових осіб. Щодо пацієнтів з тяжкою печінковою недостатністю (клас С за класифікацією Чайлд-П'ю) даних немає. Пацієнти із цукровим діабетом. У пацієнтів з цукровим діабетом на фоні застосування тадалафілу площа під кривою "концентрація - час" була меншою приблизно на 19%, ніж у здорових осіб. Ця відмінність не потребує підбору дози.ФармакодинамікаТадалафіл є оборотним селективним інгібітором специфічної фосфодіестерази 5 типу (ФДЕ-5) циклічного гуанозинмонофосфату (цГМФ). Коли сексуальне збудження викликає місцеве вивільнення оксиду азоту, пригнічення ФДЕ-5 тадалафілом призводить до підвищення концентрації цГМФ в печеристому тілі статевого члена. Наслідком цього є розслаблення гладких м'язів артерій та приплив крові до тканин статевого члена, що викликає ерекцію. Тадалафіл не має ефекту за відсутності сексуального збудження. Дослідження in vitro показали, що тадалафіл є селективним інгібітором ФДЕ-5. ФДЕ-5 є ферментом, виявленим у гладких м'язах печеристого тіла, у гладких м'язах судин внутрішніх органів, у скелетних м'язах, тромбоцитах, нирках, легенях та мозочку. Дія тадалафілу на ФДЕ-5 є більш активною, ніж на інші фосфодіестерази. Тадалафіл є в 10 000 разів більш потужним щодо ФДЕ-5, ніж щодо ФДЕ-1, ФДЕ-2, ФДЕ-4 та ФДЕ-7, які локалізуються в серці, головному мозку, кровоносних судинах, печінці, лейкоцитах, скелетних м'язах. та в інших органах. Тадалафіл у 10 000 разів активніше блокує ФДЕ-5, ніж ФДЕ-3 – фермент, який виявляється у серці та кровоносних судинах. Ця селективність щодо ФДЕ-5 у порівнянні з ФДЕ-3 має важливе значення, оскільки ФДЕ-3 є ферментом,беруть участь у скороченні серцевого м'яза. Крім того, тадалафіл приблизно в 700 разів активніше щодо ФДЕ-5, ніж щодо ФДЕ-6, виявленої в сітківці ока і є відповідальною за фотопередачу. Тадалафіл також виявляє дію у 9000 разів більш потужну щодо ФДЕ-5 порівняно з його впливом на ФДЕ-8, ФДЕ-9 та ФДЕ-10, та у 14 разів більш потужну щодо ФДЕ-5 порівняно з ФДЕ-11. Розподіл у тканинах та фізіологічні ефекти інгібування ФДЕ-8 – ФДЕ-11 дотепер не з'ясовані.і в 14 разів потужніша щодо ФДЕ-5 порівняно з ФДЕ-11. Розподіл у тканинах та фізіологічні ефекти інгібування ФДЕ-8 – ФДЕ-11 дотепер не з'ясовані.і в 14 разів потужніша щодо ФДЕ-5 порівняно з ФДЕ-11. Розподіл у тканинах та фізіологічні ефекти інгібування ФДЕ-8 – ФДЕ-11 дотепер не з'ясовані. Тадалафіл покращує ерекцію та підвищує можливість проведення повноцінного статевого акту. Препарат діє протягом 36 годин. Ефект виявляється через 16 хвилин після прийому препарату за наявності сексуального збудження. Тадалафіл у здорових осіб не викликає достовірної зміни систолічного артеріального та діастолічного артеріального тиску в порівнянні з плацебо у положенні лежачи (середнє максимальне зниження становить 1,6/0,8 мм рт. ст. відповідно) та у положенні стоячи (середнє максимальне зниження становить 0 ,2/4,6 мм рт.ст., відповідно). Тадалафіл не викликає достовірної зміни ЧСС. Тадалафіл не викликає змін розпізнавання кольорів (блакитний/зелений), що пояснюється його низькою спорідненістю з ФДЕ-6. Крім того, не спостерігається вплив тадалафілу на гостроту зору, електроретинограму, внутрішньоочний тиск та розмір зіниці. З метою оцінки впливу щоденного прийому тадалафілу на сперматогенез було проведено декілька досліджень. У жодному з досліджень не спостерігалося небажаного впливу на морфологію сперматозоїдів та їхню рухливість. В одному з досліджень було виявлено зниження середньої концентрації сперматозоїдів у порівнянні із плацебо. Зниження концентрації сперматозоїдів пов'язано з вищою частотою еякуляції. Крім того, не спостерігалося небажаного впливу на середню концентрацію статевих гормонів, тестостерону, лютеїнізуючого гормону та фолікулостимулюючого гормону при прийомі тадалафілу.Показання до застосуванняЕректильна дисфункція.Протипоказання до застосуванняПідвищена чутливість до тадалафілу або будь-якої речовини, що входить до складу препарату; у разі прийому препаратів, що містять будь-які органічні нітрати; вік до 18 років; тяжкий ступінь ниркової недостатності; одночасне застосування зі стимуляторами гуанілатциклази, такими як ріоцигуат; наявність протипоказань до сексуальної активності у пацієнтів із захворюваннями серцево-судинної системи: інфаркт міокарда протягом останніх 90 днів, нестабільна стенокардія, виникнення нападу стенокардії під час статевого акту, хронічна серцева недостатність II-IV класів за класифікацією NYHA, неконтрольовані аритмії, АТ менше 90/50 мм.рт.ст.), неконтрольована артеріальна гіпертензія, ішемічний інсульт протягом останніх 6 місяців; втрата зору внаслідок неартеріальної передньої ішемічної нейропатії зорового нерва (незалежно від зв'язку з прийомом інгібіторів ФДЕ-5); одночасний прийом доксазозину, а також лікарських засобів для лікування еректильної дисфункції; часто (більше 2 разів на тиждень) застосування у пацієнтів з хронічною нирковою недостатністю (кліренс креатиніну менше 30 мл/хв); дефіцит лактази, непереносимість лактози, глюкозо-галактозна мальабсорбція. З обережністю:. Оскільки немає даних щодо пацієнтів з тяжкою печінковою недостатністю (клас С за класифікацією Чайлд-П'ю), необхідно виявляти обережність при призначенні препарату Купід 36 цій групі пацієнтів. Необхідно виявляти обережність при призначенні препарату Купід 36 пацієнтам, які приймають альфа[1]-адреноблокатори, наприклад, доксазозин, оскільки одночасне застосування може призвести до симптоматичної гіпотензії у деяких пацієнтів. У дослідженні клінічної фармакології у 18 здорових добровольців, які приймали одноразову дозу тадалафілу, не спостерігалося симптоматичної гіпотензії при одночасному введенні тамсулозину, альфа[1А]-адреноблокатора. Слід враховувати потенційний ризик ускладнень при сексуальній активності у пацієнтів із серцево-судинними захворюваннями (інфаркт міокарда протягом останніх 90 днів; нестабільна стенокардія або стенокардія, що виникає під час статевого акту; серцева недостатність класу 2 та вище за NYHA, що розвинулася протягом останніх 6 місяців неконтрольовані порушення серцевого ритму, артеріальна гіпотензія (АТ менше 90/50 мм рт.ст.) або неконтрольована артеріальна гіпертензія; інсульт, перенесений протягом останніх 6 місяців. Купид 36 слід застосовувати з обережністю у пацієнтів з тяжкою нирковою недостатністю (КК менше 30 мл/хв), ХНН (КК менше 50 мл/хв), схильністю до приапізму (при серповидно-клітинній анемії, множинні мієломи або лейкемії) або у пацієнтів з анатомічною деформацією статевого члена (кутове викривлення, кавернозний фіброз або хвороби Пейроні)Вагітність та лактаціяПрепарат Купід 36 не призначений для застосування у жінок.Побічна діяПобічні реакції, що зустрічалися частіше, ніж у поодиноких випадках, перераховані відповідно до наступної градації: дуже часто (≥ 10%); часто (≥ 1%, < 10%); нечасто (≥0,1%, <1%); рідко (≥0,01%, <0,1%); дуже рідко ( Порушення імунної системи. Нечасто (≥0,1%, Порушення нервової системи. Дуже часто (≥10%): головний біль. Часто (≥1%, Рідко (≥0,01%, Порушення із боку органів зору. Нечасто (≥0,1%, Рідко (≥0,01%, Порушення з боку органу слуху та лабіринтні порушення. Рідко (≥0,01%, Порушення з боку серцево-судинної системи. Нечасто (≥ 0,1%, < 1%): відчуття серцебиття, тахікардія, зниження артеріального тиску (у пацієнтів, які вже приймали гіпотензивні засоби), підвищення артеріального тиску. Рідко (≥0,01%, <0,1%): інфаркт міокарда, шлуночкові порушення ритму3, нестабільна стенокардія3. Порушення з боку дихальної системи. Часто (≥1%, <10%): закладеність носа. Нечасто (≥ 0,1%, Рідко (≥0,01%, <0,1%): носова кровотеча. Порушення з боку шлунково-кишкового тракту. Часто (≥1%, <10%): диспепсія. Нечасто (≥ 0,1%, < 1%): біль у животі, гастроезофагеальний рефлюкс. Порушення з боку шкіри та підшкірних тканин. Нечасто (≥ 0,1%, < 1%): висипання на шкірі, гіпергідроз (підвищена пітливість). Рідко (≥0,01%, <0,1%): кропив'янка, синдром Стівенс-Джонсона3, ексфоліативний дерматит3. Порушення з боку скелетно-м'язової та сполучної тканини. Часто (≥ 1%, < 10%): біль у спині, міалгія. Порушення з боку статевих органів та молочної залози. Рідко (≥ 0,01%, < 0,1%): тривала ерекція, пріапізм3. Загальні розлади. Нечасто (≥ 0,1%, < 1%): біль у грудях1. Рідко (≥ 0,01%, < 0,1%): набряк особи3, раптова серцева смерть1,3. (1) Спостерігалися у пацієнтів, які раніше мали серцево-судинні фактори ризику. Однак неможливо точно визначити, чи пов'язані ці явища безпосередньо з цими факторами ризику, з тадалафілом, із сексуальним збудженням або з комбінацією цих чи інших факторів. (2) Про раптову втрату слуху було повідомлено у невеликій кількості випадків з постмаркетингових та клінічних досліджень при застосуванні всіх ФДЕ-5 інгібіторів, включаючи тадалафіл. (3) Побічні реакції, виявлені в ході постмаркетингових досліджень, що не спостерігалися в ході клінічних плацебо-контрольованих досліджень.Взаємодія з лікарськими засобамиВплив інших препаратів на тадалафіл. Тадалафіл в основному метаболізується за участю ферменту CYP3A4. Селективний інгібітор CYP3A4, кетоконазол у дозі 400 мг/добу збільшує експозицію одноразової дози тадалафілу (AUC) на 312% і Сmах - на 22%, а кетоконазол (200 мг/добу) збільшує експозицію одноразової дози тадалафілу (AUC) на 15% щодо AUC та величин Сmах тільки для одного тадалафілу. Ритонавір (200 мг 2 рази на добу), інгібітор ізоферментів CYP3A4, 2С9, 2С19 та 2D6 збільшує експозицію одноразової дози тадалафілу (AUC) на 124% без зміни Cmax. Незважаючи на те, що специфічні взаємодії не вивчалися, можна припустити, що інші інгібітори ВІЛ-протеази, як саквінавір, а також інгібітори ізоферменту CYP3A4, такі як еритроміцин та інтраконазол, підвищують активність тадалафілу. Селективний індуктор ізоферменту CYP3A4, рифампіцин (600 мг на добу), знижує експозицію одноразової дози тадалафілу (AUC) на 88% та Сmах на 46%, відносно AUC та величин Сmах тільки для одного тадалафілу. Можна припустити, що одночасне введення інших індукторів ізоферменту CYP3A4 також має знижувати концентрації тадалафілу у плазмі. Одночасний прийом антациду (магнію гідроксид/алюмінію гідроксид) та тадалафілу знижується швидкість всмоктування останнього без зміни площі під фармакокінетичною кривою для тадалафілу. Збільшення pH вмісту шлунка в результаті прийому блокатора гістамінових H2-рецепторів нізатидину не впливають на фармакокінетику тадалафілу. Безпека та ефективність комбінації тадалафілу з іншими видами лікування порушень ерекції не вивчалися, тому застосування таких комбінацій не рекомендується. Вплив тадалафілу на інші препарати. Тадалафіл посилює гіпотензивну дію нітратів. Це відбувається в результаті адитивної дії нітратів та тадалафілу на метаболізм оксиду азоту та цГМФ. Тому призначення препарату Купід 36 проти застосування нітратів протипоказане. Тадалафіл не має клінічно значущої дії на кліренс препаратів, метаболізм яких протікає за участю цитохрому Р450. Дослідження підтвердили, що тадалафіл не інгібує та не індукує ізоферменти CYP3A4, CYP1A2, CYP2D6, CYP2E1, CYP2C9, CYP2C19. Тадалафіл не має клінічно значущого впливу на фармакокінетику S- та R-варфарину. Тадалафіл не впливає на дію варфарину щодо протромбінового часу. Тадалафіл не збільшує тривалість кровотечі на фоні дії ацетилсаліцилової кислоти. Тадалафіл має системні судинорозширюючі властивості і може посилювати дію гіпотензивних препаратів, спрямовану на зниження артеріального тиску. Додатково для пацієнтів, які приймають кілька гіпотензивних засобів, у яких погано контролювалася артеріальна гіпертензія, спостерігалося дещо більше зниження артеріального тиску. Переважна більшість пацієнтів це зниження був пов'язані з гипотензивными симптомами. Пацієнтам, які отримують лікування гіпотензивними препаратами та приймають тадалафіл, повинні бути надані відповідні клінічні рекомендації. Не спостерігалося значне зниження артеріального тиску при застосуванні тадалафілу особами, які приймали селективний альфа[1А]-адреноблокатор тамсулозин. При застосуванні тадалафілу здоровими добровольцями, які приймали доксазозин (4-8 мг на добу), альфа[1]-адреноблокатор, спостерігалося посилення гіпотензивної дії доксазозину. Деякі пацієнти відчували симптоми, пов'язані зі зниженням артеріального тиску, включаючи непритомність. Тадалафіл не впливав на концентрацію алкоголю, так само як і алкоголь не впливав на концентрацію тадалафілу. При високих дозах алкоголю (0,7 г/кг) прийом тадалафілу не викликав статистично значущого зниження середньої величини артеріального тиску. У деяких пацієнтів спостерігалося постуральне запаморочення та ортостатична гіпотензія. При прийомі тадалафілу в поєднанні з нижчими дозами алкоголю (0,6 г/кг) зниження артеріального тиску не спостерігалося, а запаморочення виникало з тією ж частотою, що і при прийомі одного алкоголю. Тадалафіл не має клінічно значущої дії на фармакокінетику та фармакодинаміку теофіліну.Спосіб застосування та дозиВсередину (як мінімум за 16 хв до передбачуваної сексуальної активності). Рекомендована максимальна доза препарату Купід 36 становить 20 мг. Максимальна рекомендована частота прийому – 1 раз на добу. Пацієнти можуть робити спробу статевого акту у будь-який час протягом 36 годин після прийому препарату для того, щоб встановити оптимальний час відповіді на прийом препарату.ПередозуванняПри одноразовому призначенні здоровим особам тадалафілу в дозі до 500 мг та пацієнтам з еректильною дисфункцією – багаторазово до 100 мг на добу небажані ефекти були такі самі, що й при застосуванні нижчих доз. У разі передозування слід проводити стандартне симптоматичне лікування. При гемодіалізі тадалафілу практично не виводиться.Запобіжні заходи та особливі вказівкиСексуальна активність має потенційний ризик для пацієнтів із серцево-судинними захворюваннями. Тому лікування еректильної дисфункції, у тому числі з препаратом Купід 36, не слід проводити у чоловіків із такими захворюваннями серця, при яких сексуальна активність не рекомендована. Є повідомлення про виникнення приапізму при застосуванні інгібіторів ФДЕ-5, включаючи тадалафіл. Пацієнти повинні бути проінформовані про необхідність негайного звернення за медичною допомогою у разі виникнення ерекції, що триває 4 години та більше. Несвоєчасне лікування приапізму веде до пошкодження тканин статевого члена, внаслідок чого може настати довготривала втрата потенції. Безпека та ефективність комбінації препарату Купід 36 з іншими видами лікування порушень не вивчалися. Тому застосування таких комбінацій не рекомендується. Як і інші ФДЕ-5 інгібітори, тадалафіл має системні судинорозширюючі властивості, що може призводити до транзиторного зниження артеріального тиску. Перед призначенням препарату Купід 36 лікарі повинні ретельно розглянути питання, чи не будуть пацієнти з серцево-судинним захворюванням піддаватися небажаному впливу за рахунок таких судиннорозширювальних ефектів. Неартеріальна передня ішемічна оптична нейропатія (НАПІОН) є причиною порушення зору, включаючи повну втрату зору. Є рідкісні постмаркетингові повідомлення про випадки розвитку НАПІОН, за часом пов'язані з прийомом інгібіторів ФДЕ-5. В даний час неможливо визначити, чи існує прямий зв'язок між розвитком НАПІОН та прийомом інгібіторів ФДЕ-5 або іншими факторами. Лікарі повинні рекомендувати пацієнтам у разі раптової втрати зору припинити прийом тадалафілу та звернутися за медичною допомогою. Лікарі також повинні повідомити пацієнтам, що у людей, які перенесли НАПІОН, підвищений ризик повторного розвитку НАПІОН. Вплив на здатність до керування автотранспортом та управління механізмами. Незважаючи на те, що частота виникнення запаморочення на тлі плацебо і тадалафілу однакова, в період лікування необхідно дотримуватися обережності при керуванні автотранспортом та заняттями іншими потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Діюча речовина: тадалафілу 20,00 мг; допоміжні речовини: лактози моногідрат 249,00 мг, целюлоза мікрокристалічна 66,00 мг, гіпоролоза 3,50 мг, натрію лаурилсульфат 1,00, кроскармеллоза натрію 7,00 мг, магнію стеарат 3,50 мг; Плівкова оболонка: опадрай II 32К520009 жовтий 8,00 мг (лактози моногідрат 36%, гіпромелоза 26%, титану діоксид 15,5%, заліза оксид жовтий 8,5%, тріацетин 8,0%, тальк 6,0 Пігулки, покриті плівковою оболонкою, 20 мг. По 1 або 2 таблетки в блістер із ПВХ/ПВДХ/Аl. По 1 або 2 або 4 блістери разом з інструкцією із застосування в картонну пачку.Опис лікарської формиМигдалеподібні пігулки, покриті плівковою оболонкою, жовтого кольору, з гравіюванням "20" на одній стороні.Фармакотерапевтична групаЕректильна дисфункція Засіб лікування - ФДЕ5-інгібітор.ФармакокінетикаВсмоктування Після прийому препарату тадалафіл швидко всмоктується. Середня максимальна концентрація (Сmах) у плазмі крові досягається в середньому через 2 години після прийому внутрішньо. Швидкість і ступінь всмоктування тадалафілу не залежать від часу їди, тому препарат Купид 36 можна застосовувати незалежно від часу їди. Час прийому (вранці або ввечері) не надавав клінічно значущого впливу на швидкість та ступінь всмоктування. Фармакокінетика тадалафілу у здорових осіб лінійна щодо часу та дози. У діапазоні доз від 2,5 до 20 мг площа під кривою "концентрація - час" (AUC) збільшується пропорційно дозі. Рівноважні концентрації у плазмі досягаються протягом 5 днів при прийомі препарату один раз на добу.Фармакокінетика тадалафілу у пацієнтів з порушенням ерекції аналогічна фармкокінетиці препарату у осіб без порушення ерекції. Розподіл Середній обсяг розподілу становить близько 63 л, що свідчить про те, що тадалафіл розподіляється у тканинах організму. У терапевтичних концентраціях 94% тадалафілу у плазмі зв'язується з білками. Зв'язування з білками не змінюється за порушення функції нирок. У здорових осіб менше 0,0005% введеної дози виявлено у спермі. Метаболізм Тадалафіл переважно метаболізується за участю ізоферменту CYP3A4 цитохрому Р450. Основним циркулюючим метаболітом є метилкатехолглюкуронід. Цей метаболіт принаймні у 13 000 разів менш активний щодо ФДЕ-5, ніж тадалафіл. Отже, концентрація цього метаболіту не є клінічно значущою. Виведення У здорових осіб середній кліренс тадалафілу при внутрішньому прийомі становить 2,5 л/год, а середній Т1/2 - 17,5 ч. Тадалафіл виводиться переважно у вигляді неактивних метаболітів, в основному, через кишечник (близько 61% дози) і, меншою мірою, нирками (близько 36% дози). Особливі групи населення Літні пацієнти Здорові пацієнти похилого віку (65 років і більше) мали нижчий кліренс тадалафілу при прийомі внутрішньо, що виражалося у збільшенні площі під кривою "концентрація-час" на 25% порівняно зі здоровими особами віком від 19 до 45 років. Ця відмінність не є клінічно значущою і не потребує добору дози. Пацієнти з нирковою недостатністю У осіб з нирковою недостатністю, включаючи пацієнтів, що перебувають на гемодіалізі, площа під кривою "концентрація-час" була більшою, ніж у інших здорових осіб. Пацієнти з печінковою недостатністю Фармакокінетика тадалафілу у пацієнтів зі слабкою та середньотяжкою печінковою недостатністю можна порівняти з такою у здорових осіб. Щодо пацієнтів з тяжкою печінковою недостатністю (клас С за класифікацією Чайлд-П'ю) даних немає. Пацієнти з цукровим діабетом У пацієнтів з цукровим діабетом на фоні застосування тадалафілу площа під кривою "концентрація - час" була меншою приблизно на 19%, ніж у здорових осіб. Ця відмінність не потребує підбору дози.ФармакодинамікаТадалафіл є оборотним селективним інгібітором специфічної фосфодіестерази 5 типу (ФДЕ-5) циклічного гуанозинмонофосфату (цГМФ). Коли сексуальне збудження викликає місцеве вивільнення оксиду азоту, пригнічення ФДЕ-5 тадалафілом призводить до підвищення концентрації цГМФ в печеристому тілі статевого члена. Наслідком цього є розслаблення гладких м'язів артерій та приплив крові до тканин статевого члена, що викликає ерекцію. Тадалафіл не має ефекту за відсутності сексуального збудження. Дослідження in vitro показали, що тадалафіл є селективним інгібітором ФДЕ-5. ФДЕ-5 є ферментом, виявленим у гладких м'язах печеристого тіла, у гладких м'язах судин внутрішніх органів, у скелетних м'язах, тромбоцитах, нирках, легенях та мозочку. Дія тадалафілу на ФДЕ-5 є більш активною, ніж на інші фосфодіестерази. Тадалафіл є в 10 000 разів більш потужним щодо ФДЕ-5, ніж щодо ФДЕ-1, ФДЕ-2, ФДЕ-4 та ФДЕ-7, які локалізуються в серці, головному мозку, кровоносних судинах, печінці, лейкоцитах, скелетних м'язах. та в інших органах. Тадалафіл у 10 000 разів активніше блокує ФДЕ-5, ніж ФДЕ-3 – фермент, який виявляється у серці та кровоносних судинах. Ця селективність щодо ФДЕ-5 у порівнянні з ФДЕ-3 має важливе значення, оскільки ФДЕ-3 є ферментом,беруть участь у скороченні серцевого м'яза. Крім того, тадалафіл приблизно в 700 разів активніше щодо ФДЕ-5, ніж щодо ФДЕ-6, виявленої в сітківці ока і є відповідальною за фотопередачу. Тадалафіл також виявляє дію у 9000 разів більш потужну щодо ФДЕ-5 порівняно з його впливом на ФДЕ-8, ФДЕ-9 та ФДЕ-10, та у 14 разів більш потужну щодо ФДЕ-5 порівняно з ФДЕ-11. Розподіл у тканинах та фізіологічні ефекти інгібування ФДЕ-8 – ФДЕ-11 дотепер не з'ясовані.і в 14 разів потужніша щодо ФДЕ-5 порівняно з ФДЕ-11. Розподіл у тканинах та фізіологічні ефекти інгібування ФДЕ-8 – ФДЕ-11 дотепер не з'ясовані.і в 14 разів потужніша щодо ФДЕ-5 порівняно з ФДЕ-11. Розподіл у тканинах та фізіологічні ефекти інгібування ФДЕ-8 – ФДЕ-11 дотепер не з'ясовані. Тадалафіл покращує ерекцію та підвищує можливість проведення повноцінного статевого акту. Препарат діє протягом 36 годин. Ефект виявляється через 16 хвилин після прийому препарату за наявності сексуального збудження. Тадалафіл у здорових осіб не викликає достовірної зміни систолічного артеріального та діастолічного артеріального тиску в порівнянні з плацебо у положенні лежачи (середнє максимальне зниження становить 1,6/0,8 мм рт. ст. відповідно) та у положенні стоячи (середнє максимальне зниження становить 0 ,2/4,6 мм рт.ст., відповідно). Тадалафіл не викликає достовірної зміни ЧСС. Тадалафіл не викликає змін розпізнавання кольорів (блакитний/зелений), що пояснюється його низькою спорідненістю з ФДЕ-6. Крім того, не спостерігається вплив тадалафілу на гостроту зору, електроретинограму, внутрішньоочний тиск та розмір зіниці. З метою оцінки впливу щоденного прийому тадалафілу на сперматогенез було проведено декілька досліджень. У жодному з досліджень не спостерігалося небажаного впливу на морфологію сперматозоїдів та їхню рухливість. В одному з досліджень було виявлено зниження середньої концентрації сперматозоїдів у порівнянні із плацебо. Зниження концентрації сперматозоїдів пов'язано з вищою частотою еякуляції. Крім того, не спостерігалося небажаного впливу на середню концентрацію статевих гормонів, тестостерону, лютеїнізуючого гормону та фолікулостимулюючого гормону при прийомі тадалафілу.Показання до застосуванняЕректильна дисфункція.Протипоказання до застосуванняПідвищена чутливість до тадалафілу або будь-якої речовини, що входить до складу препарату; у разі прийому препаратів, що містять будь-які органічні нітрати; вік до 18 років; тяжкий ступінь ниркової недостатності; одночасне застосування зі стимуляторами гуанілатциклази, такими як ріоцигуат; наявність протипоказань до сексуальної активності у пацієнтів із захворюваннями серцево-судинної системи: інфаркт міокарда протягом останніх 90 днів, нестабільна стенокардія, виникнення нападу стенокардії під час статевого акту, хронічна серцева недостатність II-IV класів за класифікацією NYHA, неконтрольовані аритмії, АТ менше 90/50 мм.рт.ст.), неконтрольована артеріальна гіпертензія, ішемічний інсульт протягом останніх 6 місяців; втрата зору внаслідок неартеріальної передньої ішемічної нейропатії зорового нерва (незалежно від зв'язку з прийомом інгібіторів ФДЕ-5); одночасний прийом доксазозину, а також лікарських засобів для лікування еректильної дисфункції; часто (більше 2 разів на тиждень) застосування у пацієнтів з хронічною нирковою недостатністю (кліренс креатиніну менше 30 мл/хв); дефіцит лактази, непереносимість лактози, глюкозо-галактозна мальабсорбція. З обережністю: Оскільки немає даних щодо пацієнтів з тяжкою печінковою недостатністю (клас С за класифікацією Чайлд-П'ю), необхідно виявляти обережність при призначенні препарату Купід 36 цій групі пацієнтів. Необхідно виявляти обережність при призначенні препарату Купід 36 пацієнтам, які приймають альфа[1]-адреноблокатори, наприклад, доксазозин, оскільки одночасне застосування може призвести до симптоматичної гіпотензії у деяких пацієнтів. У дослідженні клінічної фармакології у 18 здорових добровольців, які приймали одноразову дозу тадалафілу, не спостерігалося симптоматичної гіпотензії при одночасному введенні тамсулозину, альфа[1А]-адреноблокатора. Слід враховувати потенційний ризик ускладнень при сексуальній активності у пацієнтів із серцево-судинними захворюваннями (інфаркт міокарда протягом останніх 90 днів; нестабільна стенокардія або стенокардія, що виникає під час статевого акту; серцева недостатність класу 2 та вище за NYHA, що розвинулася протягом останніх 6 місяців неконтрольовані порушення серцевого ритму, артеріальна гіпотензія (АТ менше 90/50 мм рт.ст.) або неконтрольована артеріальна гіпертензія; інсульт, перенесений протягом останніх 6 місяців. Купид 36 слід застосовувати з обережністю у пацієнтів з тяжкою нирковою недостатністю (КК менше 30 мл/хв), ХНН (КК менше 50 мл/хв), схильністю до приапізму (при серповидно-клітинній анемії, множинні мієломи або лейкемії) або у пацієнтів з анатомічною деформацією статевого члена (кутове викривлення, кавернозний фіброз або хвороби Пейроні)Вагітність та лактаціяПрепарат Купід 36 не призначений для застосування у жінок.Побічна діяПобічні реакції, що зустрічалися частіше, ніж у поодиноких випадках, перераховані відповідно до наступної градації: дуже часто (≥ 10%); часто (≥ 1%, < 10%); нечасто (≥0,1%, <1%); рідко (≥0,01%, <0,1%); дуже рідко ( Порушення з боку імунної системи: Нечасто (≥0,1%, Порушення нервової системи: Дуже часто (≥ 10%): головний біль; Часто (≥1%, Порушення з боку органів зору: Нечасто (≥0,1%, Порушення з боку органу слуху та лабіринтні порушення: Рідко (≥0,01%, Порушення серцево-судинної системи: Нечасто (≥ 0,1%, < 1%): відчуття серцебиття, тахікардія, зниження артеріального тиску (у пацієнтів, які вже приймали гіпотензивні засоби), підвищення артеріального тиску; Рідко (≥0,01%, <0,1%): інфаркт міокарда, шлуночкові порушення ритму3, нестабільна стенокардія3. Порушення дихальної системи: Часто (≥ 1%, < 10%): закладеність носа; Нечасто (≥ 0,1%, Порушення шлунково-кишкового тракту: Часто (≥ 1%, < 10 %): диспепсія; Нечасто (≥ 0,1%, < 1%): біль у животі, гастроезофагеальний рефлюкс. Порушення з боку шкіри та підшкірних тканин: Нечасто (≥ 0,1%, < 1%): висипання на шкірі, гіпергідроз (підвищена пітливість); Рідко (≥0,01%, <0,1%): кропив'янка, синдром Стівенс-Джонсона3, ексфоліативний дерматит3. Порушення з боку скелетно-м'язової та сполучної тканини: Часто (≥ 1%, < 10 %): біль у спині, міалгія. Порушення з боку статевих органів та молочної залози: Рідко (≥ 0,01%, < 0,1%): тривала ерекція, пріапізм3. Загальні розлади: Нечасто (≥ 0,1%, < 1%): біль у грудях1; Рідко (≥ 0,01%, < 0,1%): набряк особи3, раптова серцева смерть1,3. (1) Спостерігалися у пацієнтів, які раніше мали серцево-судинні фактори ризику. Однак неможливо точно визначити, чи пов'язані ці явища безпосередньо з цими факторами ризику, з тадалафілом, із сексуальним збудженням або з комбінацією цих чи інших факторів. (2) Про раптову втрату слуху було повідомлено у невеликій кількості випадків з постмаркетингових та клінічних досліджень при застосуванні всіх ФДЕ-5 інгібіторів, включаючи тадалафіл. (3) Побічні реакції, виявлені в ході постмаркетингових досліджень, що не спостерігалися в ході клінічних плацебо-контрольованих досліджень.Взаємодія з лікарськими засобамиВплив інших препаратів на тадалафіл Тадалафіл в основному метаболізується за участю ферменту CYP3A4. Селективний інгібітор CYP3A4, кетоконазол у дозі 400 мг/добу збільшує експозицію одноразової дози тадалафілу (AUC) на 312% і Сmах - на 22%, а кетоконазол (200 мг/добу) збільшує експозицію одноразової дози тадалафілу (AUC) на 15% щодо AUC та величин Сmах тільки для одного тадалафілу. Ритонавір (200 мг 2 рази на добу), інгібітор ізоферментів CYP3A4, 2С9, 2С19 та 2D6 збільшує експозицію одноразової дози тадалафілу (AUC) на 124% без зміни Cmax. Незважаючи на те, що специфічні взаємодії не вивчалися, можна припустити, що інші інгібітори ВІЛ-протеази, як саквінавір, а також інгібітори ізоферменту CYP3A4, такі як еритроміцин та інтраконазол, підвищують активність тадалафілу. Селективний індуктор ізоферменту CYP3A4, рифампіцин (600 мг на добу), знижує експозицію одноразової дози тадалафілу (AUC) на 88% та Сmах на 46%, відносно AUC та величин Сmах тільки для одного тадалафілу. Можна припустити, що одночасне введення інших індукторів ізоферменту CYP3A4 також має знижувати концентрації тадалафілу у плазмі. Одночасний прийом антациду (магнію гідроксид/алюмінію гідроксид) та тадалафілу знижується швидкість всмоктування останнього без зміни площі під фармакокінетичною кривою для тадалафілу. Збільшення pH вмісту шлунка в результаті прийому блокатора гістамінових H2-рецепторів нізатидину не впливають на фармакокінетику тадалафілу. Безпека та ефективність комбінації тадалафілу з іншими видами лікування порушень ерекції не вивчалися, тому застосування таких комбінацій не рекомендується. Вплив тадалафілу на інші препарати Тадалафіл посилює гіпотензивну дію нітратів. Це відбувається в результаті адитивної дії нітратів та тадалафілу на метаболізм оксиду азоту та цГМФ. Тому призначення препарату Купід 36 проти застосування нітратів протипоказане. Тадалафіл не має клінічно значущої дії на кліренс препаратів, метаболізм яких протікає за участю цитохрому Р450. Дослідження підтвердили, що тадалафіл не інгібує та не індукує ізоферменти CYP3A4, CYP1A2, CYP2D6, CYP2E1, CYP2C9, CYP2C19. Тадалафіл не має клінічно значущого впливу на фармакокінетику S- та R-варфарину. Тадалафіл не впливає на дію варфарину щодо протромбінового часу. Тадалафіл не збільшує тривалість кровотечі на фоні дії ацетилсаліцилової кислоти. Тадалафіл має системні судинорозширюючі властивості і може посилювати дію гіпотензивних препаратів, спрямовану на зниження артеріального тиску. Додатково для пацієнтів, які приймають кілька гіпотензивних засобів, у яких погано контролювалася артеріальна гіпертензія, спостерігалося дещо більше зниження артеріального тиску. Переважна більшість пацієнтів це зниження був пов'язані з гипотензивными симптомами. Пацієнтам, які отримують лікування гіпотензивними препаратами та приймають тадалафіл, повинні бути надані відповідні клінічні рекомендації. Не спостерігалося значне зниження артеріального тиску при застосуванні тадалафілу особами, які приймали селективний альфа[1А]-адреноблокатор тамсулозин. При застосуванні тадалафілу здоровими добровольцями, які приймали доксазозин (4-8 мг на добу), альфа[1]-адреноблокатор, спостерігалося посилення гіпотензивної дії доксазозину. Деякі пацієнти відчували симптоми, пов'язані зі зниженням артеріального тиску, включаючи непритомність. Тадалафіл не впливав на концентрацію алкоголю, так само як і алкоголь не впливав на концентрацію тадалафілу. При високих дозах алкоголю (0,7 г/кг) прийом тадалафілу не викликав статистично значущого зниження середньої величини артеріального тиску. У деяких пацієнтів спостерігалося постуральне запаморочення та ортостатична гіпотензія. При прийомі тадалафілу в поєднанні з нижчими дозами алкоголю (0,6 г/кг) зниження артеріального тиску не спостерігалося, а запаморочення виникало з тією ж частотою, що і при прийомі одного алкоголю. Тадалафіл не має клінічно значущої дії на фармакокінетику та фармакодинаміку теофіліну.Спосіб застосування та дозиВсередину (як мінімум за 16 хв до передбачуваної сексуальної активності). Рекомендована максимальна доза препарату Купід 36 становить 20 мг. Максимальна рекомендована частота прийому – 1 раз на добу. Пацієнти можуть робити спробу статевого акту у будь-який час протягом 36 годин після прийому препарату для того, щоб встановити оптимальний час відповіді на прийом препарату.ПередозуванняПри одноразовому призначенні здоровим особам тадалафілу в дозі до 500 мг та пацієнтам з еректильною дисфункцією – багаторазово до 100 мг на добу небажані ефекти були такі самі, що й при застосуванні нижчих доз. У разі передозування слід проводити стандартне симптоматичне лікування. При гемодіалізі тадалафілу практично не виводиться.Запобіжні заходи та особливі вказівкиСексуальна активність має потенційний ризик для пацієнтів із серцево-судинними захворюваннями. Тому лікування еректильної дисфункції, у тому числі з препаратом Купід 36, не слід проводити у чоловіків із такими захворюваннями серця, при яких сексуальна активність не рекомендована. Є повідомлення про виникнення приапізму при застосуванні інгібіторів ФДЕ-5, включаючи тадалафіл. Пацієнти повинні бути проінформовані про необхідність негайного звернення за медичною допомогою у разі виникнення ерекції, що триває 4 години та більше. Несвоєчасне лікування приапізму веде до пошкодження тканин статевого члена, внаслідок чого може настати довготривала втрата потенції. Безпека та ефективність комбінації препарату Купід 36 з іншими видами лікування порушень не вивчалися. Тому застосування таких комбінацій не рекомендується. Як і інші ФДЕ-5 інгібітори, тадалафіл має системні судинорозширюючі властивості, що може призводити до транзиторного зниження артеріального тиску. Перед призначенням препарату Купід 36 лікарі повинні ретельно розглянути питання, чи не будуть пацієнти з серцево-судинним захворюванням піддаватися небажаному впливу за рахунок таких судиннорозширювальних ефектів. Неартеріальна передня ішемічна оптична нейропатія (НАПІОН) є причиною порушення зору, включаючи повну втрату зору. Є рідкісні постмаркетингові повідомлення про випадки розвитку НАПІОН, за часом пов'язані з прийомом інгібіторів ФДЕ-5. В даний час неможливо визначити, чи існує прямий зв'язок між розвитком НАПІОН та прийомом інгібіторів ФДЕ-5 або іншими факторами. Лікарі повинні рекомендувати пацієнтам у разі раптової втрати зору припинити прийом тадалафілу та звернутися за медичною допомогою. Лікарі також повинні повідомити пацієнтам, що у людей, які перенесли НАПІОН, підвищений ризик повторного розвитку НАПІОН. Вплив на здатність до керування автотранспортом та управління механізмами Незважаючи на те, що частота виникнення запаморочення на тлі плацебо і тадалафілу однакова, в період лікування необхідно дотримуватися обережності при керуванні автотранспортом та заняттями іншими потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаЕвкаліпта прутовидного листя – 200 г, міді дволористої 2-водної (міді хлориду дигідрату) – 0,06 г, спирту етилового 95 % (етанолу) до отримання 1000 мл препарату. 100 мл – флакони темного скла (1) – пачки картонні.Опис лікарської формиПрозора рідина від зеленого до темно-зеленого кольору із характерним запахом. Можливе помутніння рідини та випадання осаду в процесі зберігання.Фармакотерапевтична групаПрепарат має широкий спектр протимікробної дії, у тому числі - по відношенню до антибіотикостійких штамів золотистого стафілококу; стимулює регенерацію ушкоджених тканин.Показання до застосуванняМісцево: у комплексному лікуванні опіків та трофічних виразок, ерозії шийки матки. Внутрішньо і місцево: для санації кишечника при стафілококоносійстві.Протипоказання до застосуванняПідвищена чутливість до компонентів препарату, вагітність, період грудного вигодовування, вік до 18 років. При застосуванні внутрішньо: захворювання печінки, алкоголізм, черепно-мозкова травма, захворювання головного мозку.Вагітність та лактаціяПротипоказано застосування препарату при вагітності та в період грудного вигодовування. Дитячий вік віком до 18 років.Побічна діяАлергічні реакції: набряклість губ, слизових оболонок, шкірні висипання. Якщо будь-які вказані в інструкції побічні дії посилюються, або Ви помітили будь-які інші побічні дії, не вказані в інструкції, повідомте про це лікаря.Взаємодія з лікарськими засобамиПри взаємодії препарату з перекисом водню випадає осад. Тому після обробки рани розчином перекису водню перед використанням Хлорофіллонг рану слід промити стерильним 0,9% розчином натрію хлориду.Спосіб застосування та дозиДля місцевого застосування: при лікуванні опіків та трофічних виразок препарат розводять у співвідношенні 1:5 у 0,25 % розчині новокаїну. Використовують як просочених розчином марлевих пов'язок. Курс лікування – 2-3 тижні. При лікуванні ерозії шийки матки попередньо осушують тампоном усі складки слизової оболонки піхви та піхвової частини шийки матки. Змащують канал шийки матки та ерозії нерозведеним препаратом. Курс лікування – 10 днів. Для спринцювання піхви використовують розчин, який отримується розведенням 15 мл (1 столової ложки) препарату в 1 л води. Курс лікування – 2 тижні. При стафілококовому ураженні кишечника приймають внутрішньо по 5 мл препарату, розведеного в 30 мл води, 3 рази на день за 40 хв перед їдою щодня. Препарат застосовують також місцево ректально у клізмі (по 20 мл препарату в 1 л води – доза для однієї клізми) 1 раз на 2 дні. Курс лікування складається із 10 процедур. Перед застосуванням препарат необхідно збовтувати.ПередозуванняДо цього часу випадків передозування не зареєстровано.Запобіжні заходи та особливі вказівкиДо лікування слід перевірити індивідуальну чутливість пацієнта до препарату. Для цього пацієнту дають випити 25 крапель препарату, розведених у 1 столовій ложці води. За відсутності через 6-8 годин алергічних реакцій (набряклості губ, слизових оболонок, шкірних висипань) можна призначити курсове лікування препаратом; за наявності алергічних реакцій препарат протипоказаний. Вміст абсолютного етилового спирту при прийомі препарату внутрішньо становить у максимальній разовій дозі – 5,19 г, у максимальній добовій дозі – 15,57 г. Вплив на здатність керувати транспортними засобами, механізмами: При застосуванні препарату внутрішньо необхідно утримуватися від керування транспортними засобами та заняттями іншими потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій, оскільки препарат містить етиловий спирт.Умови відпустки з аптекБез рецептаВідео на цю тему
1 961,00 грн
793,00 грн
Склад, форма випуску та упаковкаТаблетки, вкриті оболонкою - 1 табл. активні речовини: дипіридамол – 250 мг; допоміжні речовини: лактози; моногідрат; кукурудзяний крохмаль; желатин; крохмалю карбоксиметилового натрієвої солі (типу А); кремнію двоокис високодисперсний; магнію стеарат склад оболонки: гіпромелоза; тальк; макрогол 6000; титану двоокис; барвник хіноліновий жовтий (барвник Е104); симетикону емульсія у флаконах скляних по 100 шт.; у коробці 1 флакон.Опис лікарської формиТаблетки, вкриті оболонкою: плоскоциліндричні, жовті кольори.ХарактеристикаПохідне піримідину.Фармакотерапевтична групаКонкурентно інгібує аденозиндезаміназу, сприяючи накопиченню аденозину, що бере участь у регуляції коронарного кровотоку, а також здатності тромбоцитів до агрегації та адгезії. Блокує фосфодіестеразу та збільшує вміст у клітинах цАМФ. Як похідне піримідину, Курантил є індуктором інтерферону і має модулюючий вплив на функціональну активність системи інтерферону; підвищує неспецифічну противірусну резистентність до вірусних інфекцій.ФармакокінетикаШвидко всмоктується із шлунка (більша частина) та тонкого кишечника (незначна кількість). Майже повністю зв'язується із білками плазми. Cmax - протягом 1 години після прийому. Накопичується, насамперед, у серці та еритроцитах. Метаболізується печінкою шляхом зв'язування з глюкуроновою кислотою, виводиться із жовчю у вигляді моноглюкуроніду. Для пігулок T1/2 становить 10 год ± 2,2 год.ФармакодинамікаЗнижує опір коронарних артерій на рівні дрібних гілок та артеріол, збільшує кількість колатералей та колатеральний кровотік; підвищує концентрацію аденозину та синтез АТФ у міокарді, покращує його скоротливість, зменшує ОПСС, знижує АТ, гальмує агрегацію тромбоцитів (покращує мікроциркуляцію, попереджає артеріальний тромбоз), нормалізує венозний відтік; зменшує опір мозкових судин, коригує плацентарний кровотік; при загрозі прееклампсії попереджає дистрофічні зміни у плаценті, усуває гіпоксію тканин плода, сприяє накопиченню в них глікогену; має модулюючий вплив на функціональну активність системи інтерферону, підвищує неспецифічну противірусну резистентність до вірусних інфекцій.Показання до застосуванняпорушення мозкового кровообігу; профілактика та лікування тромбозів; профілактика тромбоемболії (закупорювання судини тромбом) після операції протезування клапанів серця; Хронічна серцева недостатність.Протипоказання до застосуваннягострий інфаркт міокарда; поширений атеросклероз; тяжка серцева недостатність; виражене зниження артеріального тиску; тяжкі порушення серцевого ритму; схильність до кровотеч; ниркова недостатність; Підвищена чутливість до препарату.Вагітність та лактаціяПри вагітності слід суворо визначити необхідність застосування препарату, особливо у ІІ та ІІІ третинах. Препарат протипоказаний для дітей і дітей до 12 років.Побічна діяголовний біль, серцебиття, почервоніння обличчя; неприємні відчуття у шлунку; алергічні шкірні реакції; зниження артеріального тиску при швидкому внутрішньовенному введенні.Взаємодія з лікарськими засобамиПослаблюють ефект похідні ксантину (наприклад, кава, чай); посилюють пероральні непрямі антикоагулянти (гепарин, тромболітики) або ацетилсаліцилова кислота (підвищується ризик розвитку геморагічних ускладнень). Підвищує гіпотензивну дію антигіпертензивних засобів, послаблює холінергічні властивості інгібіторів холінестерази. Посилюється антиагрегаційна дія при прийомі антибіотиків-цефалоспоринів (цефамандол, цефоперазон, цефотетан). Антациди зменшують максимальну концентрацію через зниження абсорбції.Спосіб застосування та дозиПрепарат приймають за 1 годину до їди. Для профілактики та лікування тромбозів призначається самостійно або у поєднанні з протизгортаючими засобами внутрішньо по 75 мг 3-6 разів на добу; добова доза становить 300-450 мг, за необхідності – до 600 мг. При серцевій недостатності призначають внутрішньо по 25-50 мг 3 рази на добу; при необхідності у тяжких випадках на початку лікування призначають по 75 мг 3 рази на добу, потім зменшують дозу; добова доза – 150-225 мг. Дітям добова доза становить 5-10 мг/кг/сут.Запобіжні заходи та особливі вказівкиСлід уникати вживання натуральної кави та чаю (можливе ослаблення ефекту).Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецепта. . .
281,00 грн
233,00 грн
Склад, форма випуску та упаковкаЕвкаліпта прутовидного листя – 200 г, міді дволористої 2-водної (міді хлориду дигідрату) – 0,06 г, спирту етилового 95 % (етанолу) до отримання 1000 мл препарату. 50 мл - флакони темного скла (1) - пачки картонні.Опис лікарської формиПрозора рідина від зеленого до темно-зеленого кольору із характерним запахом. Можливе помутніння рідини та випадання осаду в процесі зберігання.Фармакотерапевтична групаПрепарат має широкий спектр протимікробної дії, у тому числі - по відношенню до антибіотикостійких штамів золотистого стафілококу; стимулює регенерацію ушкоджених тканин.Показання до застосуванняМісцево: у комплексному лікуванні опіків та трофічних виразок, ерозії шийки матки. Внутрішньо і місцево: для санації кишечника при стафілококоносійстві.Протипоказання до застосуванняПідвищена чутливість до компонентів препарату, вагітність, період грудного вигодовування, вік до 18 років. При застосуванні внутрішньо: захворювання печінки, алкоголізм, черепно-мозкова травма, захворювання головного мозку.Вагітність та лактаціяПротипоказано застосування препарату при вагітності та в період грудного вигодовування. Дитячий вік віком до 18 років.Побічна діяАлергічні реакції: набряклість губ, слизових оболонок, шкірні висипання. Якщо будь-які вказані в інструкції побічні дії посилюються, або Ви помітили будь-які інші побічні дії, не вказані в інструкції, повідомте про це лікаря.Взаємодія з лікарськими засобамиПри взаємодії препарату з перекисом водню випадає осад. Тому після обробки рани розчином перекису водню перед використанням Хлорофіллонг рану слід промити стерильним 0,9% розчином натрію хлориду.Спосіб застосування та дозиДля місцевого застосування: при лікуванні опіків та трофічних виразок препарат розводять у співвідношенні 1:5 у 0,25 % розчині новокаїну. Використовують як просочених розчином марлевих пов'язок. Курс лікування – 2-3 тижні. При лікуванні ерозії шийки матки попередньо осушують тампоном усі складки слизової оболонки піхви та піхвової частини шийки матки. Змащують канал шийки матки та ерозії нерозведеним препаратом. Курс лікування – 10 днів. Для спринцювання піхви використовують розчин, який отримується розведенням 15 мл (1 столової ложки) препарату в 1 л води. Курс лікування – 2 тижні. При стафілококовому ураженні кишечника приймають внутрішньо по 5 мл препарату, розведеного в 30 мл води, 3 рази на день за 40 хв перед їдою щодня. Препарат застосовують також місцево ректально у клізмі (по 20 мл препарату в 1 л води – доза для однієї клізми) 1 раз на 2 дні. Курс лікування складається із 10 процедур. Перед застосуванням препарат необхідно збовтувати.ПередозуванняДо цього часу випадків передозування не зареєстровано.Запобіжні заходи та особливі вказівкиДо лікування слід перевірити індивідуальну чутливість пацієнта до препарату. Для цього пацієнту дають випити 25 крапель препарату, розведених у 1 столовій ложці води. За відсутності через 6-8 годин алергічних реакцій (набряклості губ, слизових оболонок, шкірних висипань) можна призначити курсове лікування препаратом; за наявності алергічних реакцій препарат протипоказаний. Вміст абсолютного етилового спирту при прийомі препарату внутрішньо становить у максимальній разовій дозі – 5,19 г, у максимальній добовій дозі – 15,57 г. Вплив на здатність керувати транспортними засобами, механізмами: При застосуванні препарату внутрішньо необхідно утримуватися від керування транспортними засобами та заняттями іншими потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій, оскільки препарат містить етиловий спирт.Умови зберіганняУ прохолодному місці +8+15 градусУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаСклад: Суміш глікоалколоїдів - соласонін (solasonine) та соламаргін (solamargine). Діючі речовини: ; глікозиди соласодину 0,001гр. Допоміжні речовини: саліцилова кислота 2,0гр; сечовина 1,0 гр.
Склад, форма випуску та упаковкаСупліддя хмелю звичайного.ХарактеристикаСедативна, протизапальна, болезаспокійлива, бактерицидна, антиалергічна, покращує травлення дія.Фармакотерапевтична групаКомплекс біологічно активних речовин (в т. ч. флавоноїдів, гормонів, вітамінів) обумовлює протизапальні, капіляроукріплюючі, гіпосенсибілізуючі та болезаспокійливі властивості. Крім того, галенові препарати шишок хмелю мають регенеративні, бактерицидні та фунгіцидні властивості. Антимікробна активність пояснюється наявністю гірких кислот гумулону та лупулону. Є дані про естрогенну активність екстракту з шишок хмелю.РекомендуєтьсяПри нервовій перевтомі, легких депресіях, неврозах, головному болі, запамороченні, безсонні, гастритах, хворобливих подразненнях сечового міхура, при циститах, уретритах, захворюваннях нирок, печінки та жовчного міхура, а також як засіб, що зміцнює серцево-судинну систему. міокарда); При туберкульозі, грипі; При порушенні обміну речовин, розладах кишок; Як загальнозміцнюючий, що посилює секреторну та рухову функцію шлунка засіб; При паралічі, подагрі, ревматизмі, нефритах (як ванн);Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність, годування груддю.Вагітність та лактаціяПротипоказаний під час вагітності.Побічна діяПісля прийому внутрішньо: нудота, блювання, біль у животі, головний біль, відчуття втоми (при передозуванні).Спосіб застосування та дозиПриймати дорослим по 1/2 склянки 3 десь у день під час їжі. 1 столову ложку (5 г) подрібненої рослинної сировини (гранул) або 2 фільтр-пакети (по 2 г) або 3 фільтр-пакети (по 1,5 г) або 2 брикети (по 2,5 г) або 1 брикет (по 5 г) залити 1 склянкою окропу (200 мл), настояти 15 хвилин, процідити. Тривалість прийому – 1 місяць.Запобіжні заходи та особливі вказівкиПеред застосуванням проконсультуйтеся зі спеціалістом.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаКомплекс цинку з гідролізатом молочного білка 4,8 мг, комплекс марганцю з гідролізатом молочного білка 0,8 мг, комплекс хрому з гідролізатом молочного білка 20 мкг, шипшина. Пігулки 60 шт.ХарактеристикаАнтиоксидантна дія. Ранозагоювальна дія. Поліпшення обміну речовин. Поліпшення стану волосся та шкіри. Поліпшення ментальної концентрації та пам'яті. Поліпшення обміну холестерину. Сприяє збільшенню щільності кісткових тканин.Властивості компонентівЦинк бере участь у освіті інсуліну; Хром допомагає клітинам отримати у достатній кількості глюкозу; Марганець необхідний для забезпечення основних нейрохімічних процесів у ЦНС, бере участь у нормальній роботі підшлункової залози;РекомендуєтьсяПідвищений рівень цукру на крові; Поганий стан волосся та шкіри; Зайва вага; Переломи; Підвищена потяг до солодкого; Високі розумові навантаження; Стрес; Порушення пам'яті; Підвищений рівень холестерину; Втома; Хронічна втома; Незагойні рани, виразки;Протипоказання до застосуванняВагітність; індивідуальна непереносимість компонентів препарату; Період лактації;Вагітність та лактаціяПротипоказаний під час вагітності.Спосіб застосування та дозиДорослим – 1 табл 2 рази на день (1 місяць).Запобіжні заходи та особливі вказівкиПеред застосуванням проконсультуйтеся зі спеціалістом.Умови відпустки з аптекБез рецептаВідео на цю тему




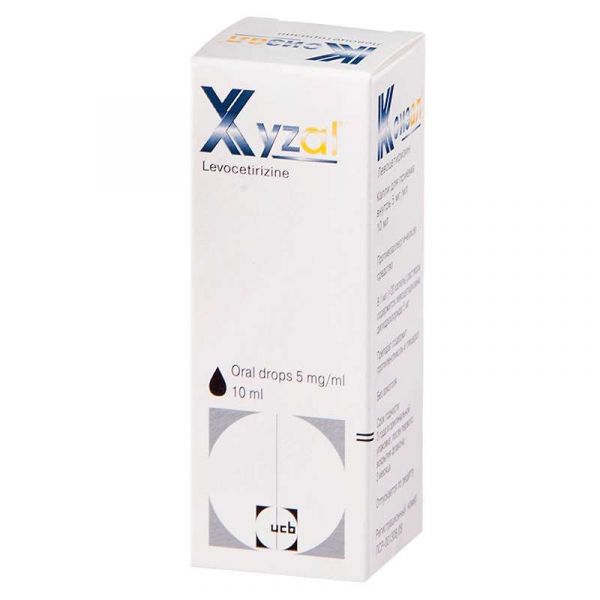






![Хлорофиллонг 50мл раствор для приема внутрь и местного применения [спиртовой] тульская фф Хлорофиллонг 50мл раствор для приема внутрь и местного применения [спиртовой] тульская фф](https://e-med.com.ua/files/resized/products/hlorofillong_50ml_rastvor_dlya_priema_vnutr_i_mestnogo_primeneniya_spirtovoy_tul_skaya_ff.600x800.jpg)