Лекарства и БАД
184,00 грн
144,00 грн
Склад, форма випуску та упаковкаРозчин - ;1 фл.: Активні речовини: ацетон 4,9%, борна кислота 0,8%, резорцинол 7,8%. допоміжні речовини: фенол. 25 мл – флакони темного скла (1) – пачки картонні.Фармакотерапевтична групаМає антисептичну та протигрибкову дію.Клінічна фармакологіяАнтисептик для зовнішнього застосування.Показання до застосуванняГнійничкові та грибкові захворювання шкіри; поверхневі рани; ерозії; тріщини; садна шкіри.Протипоказання до застосуванняПідвищена чутливість до компонентів препарату.Побічна діяКороткочасне відчуття печіння та болю, яке проходить самостійно і не вимагає відміни препарату.Спосіб застосування та дозиЗовнішньо. Розчин наносять за допомогою ватного тампона або пензлика на уражені ділянки шкіри 2-4 рази на день. Після підсихання рідини на оброблену ділянку можна наносити мазі та пасти.Запобіжні заходи та особливі вказівкиНе слід наносити препарат великі ділянки шкіри, т.к. фенол, що входить до складу розчину, проникає в кров і може спричинити токсичні явища (запаморочення, слабкість). Препарат має своєрідний запах і червоний колір і може забруднити білизну.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаГранули гомеопатичні - 100 г. активні компоненти: Fucus vesiculosus (Fucus) (фукус везикулозус (фукус)) С3 – 0,17 г; Graphites (графітес) C6-0,17г; Hydrastis canadensis (Hydrastis) (гідрастис канаденсіс (гідрастис)) C3-0,17г; Phytolacca americana (Phytolacca) (фітолакка американа (фітолакка)) C3 – 0,17г; Carbo vegetabilis (карбо вегетабіліс) C6-0,17г; Prunus spinosa (прунус спиноза) C3 – 0,17г; допоміжні компоненти: цукрові гранули - 100 г. Гранули гомеопатичні.
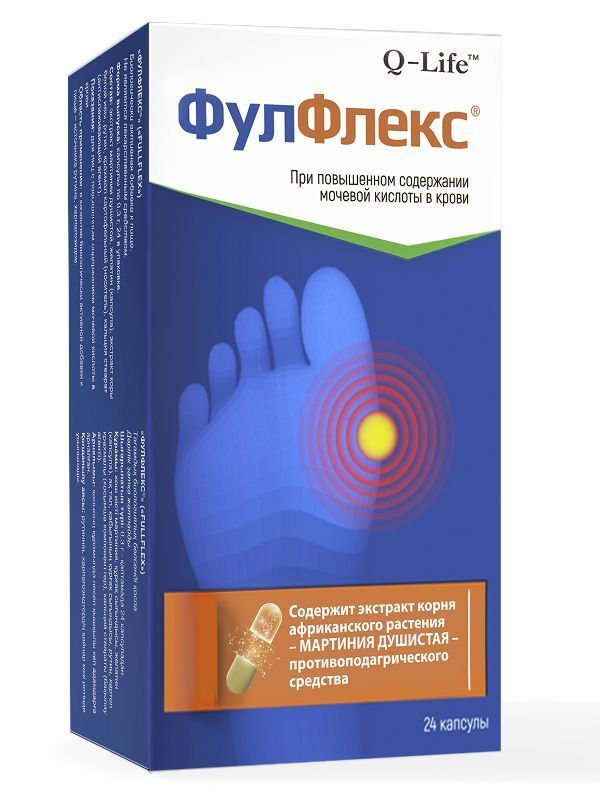
Склад, форма випуску та упаковкаЕкстракт мартинії запашної, желатин (капсула), екстракт кори білої верби, рутин, крохмаль картопляний (носій), стеарат кальцію (антистежуючий агент).ХарактеристикаКапсули «Фулфлекс» рекомендуються як біологічно активна добавка до їжі – джерела рутину, харпагозидів для осіб з підвищеним вмістом сечової кислоти в крові.РекомендуєтьсяДля осіб із підвищеним вмістом сечової кислоти в крові.Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність, годування груддю.Спосіб застосування та дозиДорослим та дітям старше 14 років по 1 капсулі 1 раз на день під час їжі. Тривалість прийому 1 місяць. За потреби прийом можна повторити.Запобіжні заходи та особливі вказівкиПеред застосуванням слід проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
1 845,00 грн
1 804,00 грн
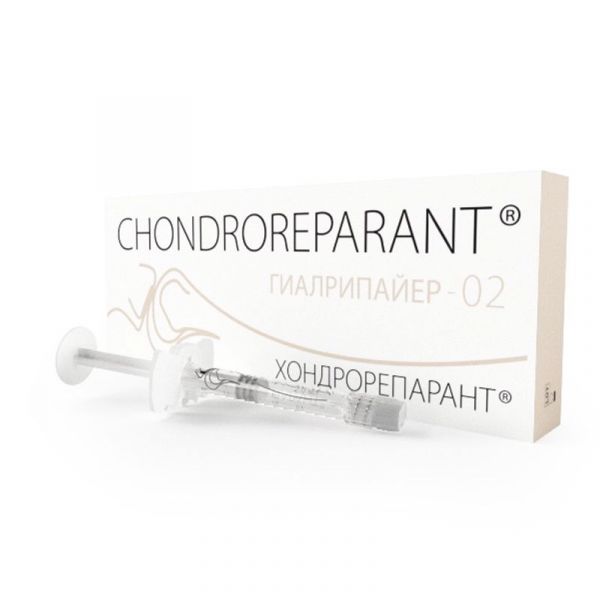
Склад, форма випуску та упаковкаРідина - 1 фл./шприц: активні речовини: гіалуронат натрію та сополімер гіалуронової кислоти з аскорбілфосфатом магнію - 15 мг/мл; L-пролін – 3 мг/мл; L-лізину гідрохлорид – 3 мг/мл; гліцин – 3 мг/мл; допоміжні речовини: хлорид натрію; фосфатний буфер; вода для ін'єкцій.Опис лікарської формиПрозора, безбарвна, злегка гелеподібна речовина.ХарактеристикаПрепарат стимулює синтез волокон колагену та еластину, забезпечує адресну доставку активних речовин та сприяє їх тривалому утриманню у шкірі. Цистеїн та глутатіон – потужні антиоксиданти. Цистеїн входить до складу альфа-кератину – основного білка шкіри, бере участь у формуванні епідермального бар'єру. Глутатіон має цитопротективну дію, гальмуючи апоптоз клітин.ФармакодинамікаХондрорепаративний. Стан метаболізму суглобів, в'язкоеластичні та захисні властивості синовіальної рідини багато в чому визначаються концентрацією в ній гіалуронової кислоти, специфічного протеоглікану, зосередженого в хрящі, синовіальних оболонках та інших сполучнотканинних структурах організму. Дія гелевого матеріалу ГІАЛРІПАЙЄР-02 (хондрорепарант) заснована на біологічній стимуляції процесів природного метаболізму, за допомогою чого покращується фізіологічний та реологічний статус синовіальної рідини. Гелевий матеріал ГІАЛРІПАЙЄР-02 (хондрорепарант) сприяє уповільненню руйнування суглобового хряща у комплексі з процесами відновлення гомеостазу синовіальної рідини. Гелевий матеріал ГІАЛРІПАЙЄР-02 (хондрорепарант) дозволяє відновлювати ефективну концентрацію гіалуронової кислоти в матриксі, що призводить до стимуляції фібробластів та хондроцитів. Проміжні продукти деградації гіалуронової кислоти мають ангіогенну, імуностимулюючу та протизапальну дію. Гелевий матеріал ГІАЛРІПАЙЄР-02 (хондрорепарант), будучи біоактивною композицією модифікованої гіалуронової кислоти з аскорбіновою кислотою та амінокислотами, що беруть участь у синтезі колагену, дозволяє здійснювати спрямовану доставку активних речовин безпосередньо до зони пошкоджених сполучнотканин. Структурна модифікація гіалуронової кислоти (полімерна зшивка) в гелевому матеріалі ГІАЛРИПАЙЕР-02 (хондрорепарант) визначає пролонговану реконструктивну дію на пошкоджені внаслідок травм або дегенеративно-дистрофічних процесів хрящові, зв'язувальні та сполучнотканинні структури сустав. При внутрішньосуглобовому введенні продукти катаболізму гелевого матеріалу ГІАЛРІПАЙЄР-02 (хондрорепарант), звільнені амінокислоти, в т.ч. незамінна - лізин, разом з вітаміном С створюють фізіологічно сприятливе середовище для посилення метаболічної активності клітин та запускають синтез основних компонентів міжклітинного матриксу хрящових та сполучнотканинних структур. Вітамін С, що входить до складу матеріалу, бере участь у метаболічних перетвореннях гліцину, проліну і лізину. Гідроксилювання проліну необхідно для стабілізації потрійної спіралі колагену, а гідроксилювання лізину дуже важливо для подальшого утворення ковалентних зв'язків між молекулами колагену при формуванні колагенових фібрил. Цей процес є визначальним для стабілізації міжклітинної речовини всіх видів сполучної тканини.ІнструкціяУ порожнину суглоба. Обсяг введення матеріалу та підбір ін'єкційної голки визначається лікарем індивідуально, залежно від анатомо-фізіологічних характеристик та стану суглоба. За наявності випоту у суглобі рекомендується попередня евакуація зайвого обсягу синовіальної рідини. Залежно від розміру суглоба необхідно вводити в порожнину суглоба до 2 мл гелю матеріалу ГІАЛРИПАЙЕР-02 (хондрорепарант) 1 раз на 14 днів протягом 6-8 тижнів. Повторний курс проводиться через 6-12 місяців. Одночасно можна проводити лікування кількох суглобів. Лікування гелевим матеріалом ГІАЛРІПАЙЄР-02 (хондрорепарант) впливає тільки на суглоб, в який вводиться матеріал, системний ефект ГІАЛРІПАЙЄР-02 (хондрорепарант) не має. Шприц, голка та залишок невикористаного матеріалу після виконання процедури підлягають негайній утилізації. Увага! Для ефективного результату лікування дуже важливо правильно виконати ін'єкцію. Введення гелевого матеріалу ГІАЛРІПАЙЄР-02 (хондрорепарант) можуть виконувати лише фахівці, які мають на це дозвіл відповідно до місцевого законодавства. ТОВ «Лабораторія ТОСКАНІ» не несе відповідальності за наслідки неправильного використання гелевого матеріалу ГІАЛРІПАЙЄР-02 (хондрорепарант).Показання до застосуванняУ складі комплексної терапії при наступних захворюваннях та станах: лікування остеоартрозу І–ІІІ стадії колінного, тазостегнового та інших синовіальних суглобів дегенеративно-дистрофічного або травматичного походження; необхідність поліпшення в'язкоеластичних та захисних властивостей синовіальної рідини суглобів; дегенеративно-дистрофічні стани зв'язкового апарату, сполучнотканинних та хрящових структур; артрити на стадії ремісії. для профілактики дегенеративно-дистрофічних захворювань опорно-рухового апарату; у період реабілітації після перенесених травм та оперативних втручань.Протипоказання до застосуванняпідвищена чутливість до компонентів матеріалу; наявність в анамнезі аутоімунних захворювань або проведення аутоімунної терапії; прийом антикоагулянтів; важка форма запалення чи інфікування суглоба; наявність ознак активного захворювання шкіри або шкірної інфекції у безпосередній близькості від місця введення; вагітність; період лактації.Побічна діяВнутрішньосуглобове введення гелевого матеріалу ГІАЛРІПАЙЄР-02 (хондрорепарант) відрізняється гарною переносимістю. У поодиноких випадках можливі локальні вторинні явища - біль, відчуття тепла, поява внутрішньосуглобової ексудації; дуже рідко – алергічні реакції. Про небажані явища слід повідомляти місцеві представники ТОВ «Лабораторія ТОСКАНІ».Взаємодія з лікарськими засобамиВведення у поєднанні з іншими лікарськими препаратами та виробами не досліджено.Запобіжні заходи та особливі вказівкиНеобхідно дотримуватися загальних запобіжних заходів для внутрішньосуглобових ін'єкцій. Не слід вводити гелевий матеріал ГІАЛРІПАЙЄР-02 (хондрорепарант) за наявності інфікованих ран, саден у ділянці суглоба, вираженого запалення, значного внутрішньосуглобового випоту, венозного та лімфатичного стазу на боці ураженого суглоба. При обробці шкіри перед проведенням внутрішньосуглобової ін'єкції не можна використовувати дезінфектанти, що містять четвертинні амонієві солі. Перед введенням необхідно нагріти матеріал до кімнатної температури. Гелевий матеріал ГІАЛРІПАЙЄР-02 (хондрорепарант) повинен акуратно вводитися в порожнину суглоба. Після ін'єкції гелевого матеріалу ГІАЛРІПАЙЄР-02 (хондрорепарант) пацієнту рекомендується дотримуватися щадного режиму та уникати зайвого навантаження на суглоб протягом декількох днів. Під час курсу введення гелевого матеріалу ГІАЛРІПАЙЄР-02 (хондрорепарант) не допускається введення в порожнину ураженого суглоба анестетиків та інших фармакологічних препаратів. Не застосовувати виріб із пошкодженою упаковкою. Вплив на здатність до керування автотранспортом та управління механізмамиУмови відпустки з аптекЗа рецептомВідео на цю тему
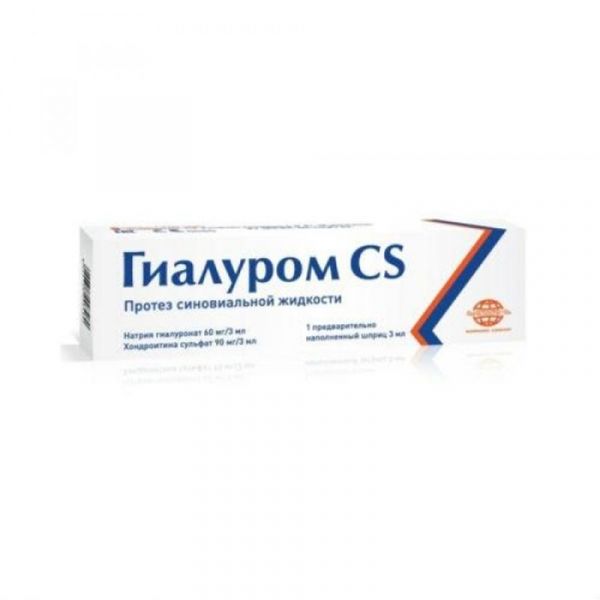
Склад, форма випуску та упаковка1 попередньо наповнений шприц Гіалуром CS містить: Гіалуронат натрію 60,00 мг Хондроїтин сульфат натрію 90,00 мг Натрію хлорид 10,50 мг Допоміжні речовини Вода для ін'єкцій до 3,00 млОпис лікарської формиГіалуром CS прозорий в'язкий розчин від безбарвного до коричневого кольору в одноразових скляних шприцах гідролітичного класу I, оснащених системою фіксації голки типу Луєр Лок, в комплекті з голкою із тригранним лазерним заточуванням. Сфера застосування: хірургія, травматологія, ортопедія, ревматологія.ХарактеристикаГіалуром CS – протез синовіальної рідини, стерильний, прозорий в'язкоеластичний розчин, до складу якого входять гіалуронат натрію 60 мг/3 мл та хондроїтин сульфат натрію 90 мг/3 мл. Гіалуронова кислота є основним компонентом синовіальної рідини, визначаючи її в'язкоеластичні властивості. Вона формує на всій внутрішній поверхні суглоба шар, що покриває, який захищає хрящ і синовіальну оболонку від механічних пошкоджень, а також від вільних радикалів і факторів запалення. Хондроїтину сульфат є одним з природних глікозаміногліканів (ГАГ), що складається з альтернативного цукру D-глюкуронової кислоти та N-ацетил-D-галактозаміну. Хондроїтину сульфат отримують у вигляді натрієвої солі з трахей великої рогатої худоби та використовують для приготування активних фармацевтичних субстанцій. Хондроїтину сульфат є стимулятором регенерації тканин, сприяє утриманню води та відновленню амортизуючих функцій у хрящових тканинах. Сприяє синтезу та захисту колагену, який є структурною основою всіх сполучних тканин, а також збільшує вироблення гіалуронової кислоти в синовіальних клітинах, що сприятливо впливає на підтримку в'язкості синовіальної рідини. Використання хондроїтину сульфату разом з гіалуронатом натрію сприяє уповільненню деградації та стимулює регенерацію хряща.Клінічна фармакологіяГіалуром CS призначений для внутрішньосуглобового введення. Розчин не слід вводити поза порожниною суглоба, а також пацієнтам з інфекціями або захворюваннями шкіри в області ін'єкції. Внутрішньосуглобова ін'єкція повинна вводитися фахівцями, що пройшли навчання техніки внутрішньосуглобового введення та проводитися в асептичних умовах у лікувальних закладах. Можливе застосування місцевих анестетиків перед проведенням внутрішньосуглобової ін'єкції, наприклад, підшкірне введення лідокаїну. Необхідно належним чином продезінфікувати місце ін'єкції (застосовують розчин спирту 70% або інші засоби дезінфікування). Не повинні бути використані дезинфікуючі засоби, що містять солі четвертинного амонію (наприклад, хлорид бензалконію), так як можлива реакція преципітації. Перед введенням Гіалуром CS слід видалити рідину з порожнини суглоба. Рекомендується проведення артроцентезу перед введенням розчину. Після видалення захисного ковпачка з наконечника шприца приєднайте до шприца стерильну голку. Зазвичай для колінного суглоба використовують голку розміром 0,8х40 мм (21G), для інших суглобів рекомендуємо використовувати голку необхідного розміру (від 17G до 22G) залежно від суглоба. Гіалуром CS вводять у суглоб обсягом залежно від розміру суглоба. Порожнина суглоба має бути перевантажена. Кожен наповнений шприц призначений для одноразового використання. Вміст шприца слід використовувати негайно після відкриття. Невикористаний повністю розчин не підлягає зберіганню та не повинен бути повторно стерилізований. Після ін'єкції Гіалурому CS, пацієнту рекомендується дотримуватися щадного режиму та уникати зайвого або тривалого навантаження на суглоби (наприклад, біг чи гра в теніс) протягом 48 годин.Показання до застосуванняГіалуром СS застосовується: для симптоматичного лікування остеоартриту легкого, середнього або тяжкого ступеня; при болю та обмеженні рухливості, спричинених дегенеративно-дистрофічними або посттравматичними змінами колінного, тазостегнового та інших синовіальних суглобів; для полегшення болю після проведення артроскопії (застосування можливе не раніше ніж через 1 тиждень після втручання).Протипоказання до застосуваннявстановлена підвищена чутливість до компонентів даного медичного виробу; наявність активних запальних чи інфекційних процесів у суглобі; наявність ознак активного захворювання шкіри або шкірної інфекції в області передбачуваної ін'єкції; застосування у пацієнтів із встановленим діагнозом аутоімунного захворювання або проходять курс імунотерапії; застосування при вагітності або під час лактації; вік до 18 років.Побічна діяМожливе виникнення помірної хворобливості та набряку в області ін'єкції. Вищевказані симптоми носять минущий характер і зазвичай зникають через 72 год.Запобіжні заходи та особливі вказівкиПеред використанням необхідно перевірити дату закінчення терміну придатності та цілісність упаковки. Не використовувати після закінчення терміну придатності, вказаного на упаковці. Використання відкритої та/або пошкодженої стерильної упаковки не допускається. Використані для ін'єкції голки та шприци не повинні використовуватися повторно. Повторна стерилізація заборонена.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаРозчин для внутрішньосуглобового введення Гіалуро 1,5% розчин натрію гіалуронату по 2 мл в одноразових попередньо наповнених шприцах з прозорого скла з голкою для ін'єкцій. Вміст попередньо наповненого шприца 2 мл становить 30 мг гіалуронату натрію, 18 мг натрію хлориду і вода для ін'єкцій, достатня до досягнення об'єму препарату 2 мл.Опис лікарської формиРозчин для внутрішньосуглобового введення Гіалуро випускається у вигляді попередньо наповнених шприців одноразового використання, які містять 2 мл стерильного, в'язкоеластичного розчину гіалуронату натрію. Кожен мл розчину «ГІАЛУРОМ» містить 15 мг гіалуронату натрію, 9 мг натрію хлориду і воду для ін'єкційних розчинів. Розмір упаковки: 1 або 3 попередньо наповнені шприці в пачці з картону.ХарактеристикаРозчин для внутрішньосуглобового введення ГІАЛУРОМ - 1,5% розчин натрію гіалуронату в одноразових шприцах по 2 мл є стерильний, в'язкоеластичний розчин гіалуронату натрію. Гіалуронат натрію отримано внаслідок бактеріальної ферментації. Гіалуронат натрію ГІАЛУРОМ являє собою полісахарид ідентичний людському, складається з повторюваних дисахаридних ланок N-ацетилглікозаміну та глюкуронату натрію, з молекулярною масою, що перевищує 2400000 Да. Натрію гіалуронат присутній повсюдно в організмі людини і присутній у великих концентраціях у тканинах, таких як склоподібне тіло, синовіальній рідині, пуповині та дермі. У синовіальній рідині гіалуронат натрію виступає як мастило та поглинач удару, що сприяє нормальному руху без болю. При захворюванні на тип артриту,в'язкопружність синовіальної рідини знижується, так що значно збільшує механічне навантаження на суглоб і посилюється руйнування суглобового хряща, проявляється обмеженням та болями при русі в суглобах. Змащувальна та амортизуюча дія цього препарату пом'якшують болі та покращують рухливість суглоба при внутрішньосуглобовому застосуванні.Показання до застосуванняРозчин ГІАЛУРОМ застосовується як в'язкоеластична добавка для заміщення синовіальної рідини при болях, спричинених дегенеративними захворюваннями синовіальних суглобів, такі як остеоартрит або остеоартроз. За своєю дією препарат ГІАЛУРОМ служить мастилом та механічною підтримкою для хворого суглоба. Розчин Гіалуро вводиться в суглоби людини: при болях та обмеженій рухливості, викликаних дегенеративно-дистрофічними та травматичними змінами колінного, тазостегнового та інших синовіальних суглобів; для тимчасового заміщення та заповнення синовіальної рідини; при лікуванні пацієнтів, які ведуть активний спосіб життя та регулярно навантажують уражений суглоб.Протипоказання до застосуванняіндивідуальна непереносимість (в т.ч. гіперчутливість в анамнезі) компонентів розчину ГІАЛУРОМ; наявність інфікованих ран, садна в ділянці суглоба; інфекційні захворювання суглобів; відомі системні порушення згортання крові. Гіалур може містити сліди бактеріальних білків і протипоказаний пацієнтам з відповідною гіперчутливістю.Побічна діяГіалуронат натрію відрізняється чудовою переносимістю. Можлива поява місцевих вторинних явищ, таких як болі, відчуття тепла, почервоніння та опухання можуть спостерігатися на суглобі, в який введений препарат (накладення льоду на суглоб протягом п'яти - десяти хвилин знімуть усі подібні явища). Вкрай рідко можуть спостерігатися алергічні реакції. При внутрішньосуглобовому введенні існують мінімальні ризики, пов'язані з інфекцією та кровотечею.Спосіб застосування та дозиІн'єкції ГІАЛУРОМ виробляються лікарями-фахівцями. Розчин Гіалуро призначений тільки для внутрішньосуглобового застосування. Не застосовують внутрішньовенно. Введення гіалуронату натрію здійснюється за кімнатної температури. Введений обсяг залежить від розміру суглоба, але не перевищує 2 мл колінний суглоб та інші великі суглоби, або 1 мл для маленьких суглобів. Лікар є відповідальним за встановленням застосовного обсягу і повинен переконатися, що суглоб не перевантажений. Розчин Гіалуро вводиться всередину порожнини суглоба один раз на тиждень протягом 3-х тижнів поспіль. Можливе одночасне лікування кількох суглобів. Повторний цикл лікування не можна проводити раніше ніж через 6 місяців, для того самого суглоба. Перед застосуванням препарату Гіалуром, накопичення рідини в суглобі повинні бути видалені шляхом висмоктування шприцом. Розчин Гіалуро випускається у вигляді попередньо наповненого шприца, вміст якого не потрібно розбавляти. Препарат є стерильним і слід використовувати відразу після відкриття упаковки. Препарат призначений лише для одноразового використання. Гіалур повинен акуратно вводитися в порожнину суглоба, ретельно дотримуючись схеми введення. Введення є асептичною процедурою, тому дотримуйтесь відповідних запобіжних заходів. Готовий шприц витягується зі стерильного футляра, ковпачок знімається, після чого надягається стерильна голка, яка фіксується невеликим поворотом. Перед введенням необхідно видалити повітря зі шприца.Запобіжні заходи та особливі вказівкиПотрібно дотримуватися схеми введення та правила асептики та антисептики при внутрішньосуглобовому введенні. Ін'єкції гіалуронату натрію повинні проводитись виключно дипломованими та сертифікованими лікарями відповідного профілю. Не використовувати натрію гіалуронат у надмірній кількості, ретельно спостерігати за пацієнтами. Не перевантажувати міжсуглобовий простір. Якщо біль посилюється під час введення, процедура має бути зупинена. Перед застосуванням розчину Гіалуром пацієнти повинні бути ретельно обстежені для виявлення ознак гострого запалення, і лікар повинен визначити можливість і схему лікування таких пацієнтів зазначеним препаратом. Як і після будь-якої іншої інвазивної процедури на суглобі, після ін'єкції гіалуронату натрію, пацієнту рекомендується дотримуватись щадного режиму та уникати зайвого навантаження на суглоб протягом декількох днів. Пацієнтам із хворобливими наслідками після внутрішньосуглобового введення гіалуронату натрію слід негайно звернутися до лікаря. До сьогоднішнього дня немає достатніх даних, щоб рекомендувати використання цього препарату в дітей віком і підлітків. Не слід використовувати Гіалуро одночасно або в суміші з іншими препаратами, призначеними для внутрішньосуглобового застосування.Умови відпустки з аптекБез рецептаВідео на цю тему
3 552,00 грн
3 513,00 грн
Склад, форма випуску та упаковкаШприц - 2 мл: Гіалуронат натрію С14Н20NNaO11 CAS [9067-32-7] 40,00 мг; Фармасал - Натрію хлорид NaCl CAS [7647-14-5] 14,00 мг; Натрію дигідрофосфат моногідрат NaH2PO4 х H2O CAS [10049-21-5] 0,11 мг; Динатрію фосфат додекагідрат Na2HPO4 x 12H2O CAS [10039-32-4] 1,22 мг; Маннітол (перлітол ПФ) C6H14O6 CAS [69-65-8] 10,00 мг; Гідроксид натрію NaOH CAS [1310-73-2], хлористоводнева кислота HCl CAS [7647-01-0] до pH 7,2÷7,5%; Вода ін'єкцій H2O до 2,00 мл. Гіалуром Тендон – стерильний розчин у попередньо наповнених одноразових скляних шприцах гідролітичного класу I, що містить гіалуронат натрію 40 мг/2 мл. 1 попередньо наповнений шприц в осередковій полімерній упаковці разом з інструкцією із застосування в пачці з картону.Опис лікарської формиГіалуром Тендон – стерильний, в'язкоеластичний прозорий безбарвний розчин гіалуронату натрію високого ступеня очищення. Гіалуронат натрію отримано шляхом бактеріальної ферментації, що не містить тваринного білка. Стерилізований вологою парою. Гіалуром Тендон призначений для навколосухожильного та внутрішньосуглобового введення.ХарактеристикаГіалуром Тендон - це стерильний, в'язкоеластичний, прозорий, безбарвний розчин гіалуронату натрію, поміщений в одноразовий шприц з безбарвного скла гідролітичного класу I, силіконізований і оснащений еластомерним ковпачком, штоком поршня і фланцем для управління. Градуювання шприца відсутнє, воно не потрібне, оскільки вміст одного шприца використовується одноразово і призначений лише для одного пацієнта. Гіалуром Тендон має динамічну в'язкість в діапазоні 35-65 Па?с, осмоляльність становить 270-350 мОсмол/кг, щільність розчину - 1,005-1,025 г/см3. Сфера застосування: хірургія, травматологія, ортопедія, ревматологія.Показання до застосуванняБолі та обмеження рухів при різних захворюваннях сухожилля (хронічні тендинопатії). Болі та обмеження рухливості внаслідок первинного або вторинного остеоартриту, посттравматичних змін або інших захворювань суглобів.Протипоказання до застосуванняГіалуром Тендон не слід використовувати: пацієнтам із встановленою гіперчутливістю до будь-якого з його компонентів; пацієнтам із встановленою гіперчутливістю до білків грампозитивних бактерій; пацієнтам з ознаками активного захворювання шкіри або шкірної інфекції в області передбачуваної ін'єкції; пацієнтам, які отримували інший ін'єкційний препарат в області або у безпосередній близькості до місця передбачуваної ін'єкції; за наявності активних запальних або інфекційних процесів у суглобі; за наявності системних порушень згортання крові; при вагітності або під час лактації; віком до 18 років.Побічна діяПісля навколосухожильного введення розчину Гіалуром Тендон можлива поява місцевих реакцій, таких як біль, відчуття жару, синець, почервоніння або припухлість. Можливе виникнення помірної хворобливості та набряку після внутрішньосуглобової ін'єкції гіалуронату натрію. Існують мінімальні ризики, пов'язані з процедурою внутрішньосуглобової ін'єкції, в основному, інфекції та кровотечі.Взаємодія з лікарськими засобамиВ даний час відсутня інформація про несумісність Гіалуром Тендон з іншими лікарськими засобами, які застосовуються для лікування захворювань сухожилля або суглобів.Спосіб застосування та дозиГіалуром Тендон повинен вводитися тільки лікарями, навченими технікою введення в навколосухожильне місце і місце прикріплення сухожилля або в порожнину суглоба, і повинно проводитися в асептичних умовах в лікувальних закладах. Для навколосухожильного введення: Гіалуром Тендон вводять в область ураженого сухожилля або місце прикріплення сухожилля один раз на тиждень, курс становить 2 ін'єкції. Одночасно можна лікувати кілька сухожиль. При необхідності можуть застосовуватися повторні курси лікування. Для внутрішньосуглобового введення: Вводять Гіалуром Тендон у уражений суглоб раз на тиждень, курс становить 1-3 ін'єкції. Одночасно можна лікувати кілька суглобів. Курс лікування можна повторити, за потреби. За наявності випоту в порожнині суглоба, рекомендується зменшити його шляхом аспірації, після чого рекомендується відпочинок, застосування пакету з льодом та/або внутрішньосуглобової ін'єкції кортикостероїдів за необхідності. Лікування Гіалуром Тендон можна почати через два-три дні. Для навколосухожильного введення: Візьміть шприц, відкрутіть захисний ковпачок, прикріпіть голку відповідного розміру (наприклад, 25-27 G) та зафіксуйте легким обертанням. Для внутрішньосуглобового введення: Візьміть шприц, відкрутіть захисний ковпачок, прикріпіть голку відповідного розміру (наприклад, 18-25 G) та зафіксуйте легким обертанням. Остаточний вибір голки для будь-якої процедури визначається лікарем. Є кілька факторів, які необхідно враховувати при виборі розміру (калібру) та довжини голки, які будуть використовуватися для навколосухожильного або внутрішньосуглобового введення, у тому числі анатомія області введення, відстань між шкірою та сухожиллям та характеристики пацієнта (вага, вік). Перед введенням слід видалити бульбашки повітря, якщо вони є. Вміст шприца Гіалуром Тендон є стерильним.Запобіжні заходи та особливі вказівкиСлід з обережністю застосовувати Гіалуром Тендон для лікування пацієнтів з відомою гіперчутливістю до будь-якого компонента препарату. Необхідно дотримуватися загальних запобіжних заходів при введенні ін'єкції в навколосухожильний простір або в порожнину суглоба. Гіалуром Тендон слід вводити точно в навколосухожильний простір або в область ураженого сухожилля, за необхідності використовуючи діагностичну візуалізацію, наприклад, ультразвукове дослідження або томографічні знімки. Слід уникати влучення голки в кровоносні судини та нерви! Гіалуром Тендон – стерильний, в'язкоеластичний прозорий безбарвний розчин гіалуронату натрію високого ступеня очищення. Гіалуронат натрію отримано шляхом бактеріальної ферментації, що не містить тваринного білка. Стерилізований вологою парою. Гіалуром Тендон призначений для навколосухожильного та внутрішньосуглобового введення. Процедуру слід уникати у пацієнтів з відомими системними порушеннями згортання крові або у пацієнтів з вазовагальною реакцією та непритомністю в анамнезі. Не рекомендується застосовувати Гіалуром Тендон у дітей, вагітних та жінок, що годують у зв'язку з недостатністю даних про клінічне застосування гіалуронату натрію у даних груп пацієнтів. Пацієнти, які пережили будь-які ускладнення протягом декількох днів після ін'єкції, повинні негайно звернутися до лікаря. Необхідно належним чином продезінфікувати місце ін'єкції (застосовують розчин спирту 70% або інші засоби дезінфікування). Не повинні бути використані дезінфікуючі засоби, що містять солі четвертинного амонію, оскільки можлива реакція преципітації. Перед використанням необхідно перевірити цілісність упакування. Використання відкритої та/або пошкодженої стерильної упаковки не допускається. Шприц призначений лише для одноразового застосування, його слід використовувати негайно після розкриття упаковки. Використані голки та шприци з розчином не підлягають зберіганню та повторній стерилізації, не повинні бути використані повторно.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаКапсули - 1 капс. Діюча речовина: рацекадотрил – 100 мг; Допоміжні речовини: лактози моногідрат – 41 мг, крохмаль кукурудзяний прежелатинізований – 78 мг, магнію стеарат – 4 мг, кремнію діоксид колоїдний – 2 мг; Тверда желатинова капсула: барвник заліза оксид жовтий (Е 172) – 0,10 %, титану діоксид (Е 171) – 2,0 %, желатин – до 100 %. По 10 капсул у блістери з ПВХ/ПВДХ/Ал фольги. По 1,2 блістера в картонну пачку разом з інструкцією із застосування.Опис лікарської формиТверді желатинові капсули №2 світло-жовтого кольору. Вміст капсул – білий порошок з характерним запахом.Фармакотерапевтична групаПротидіарейний засіб.ФармакокінетикаВсмоктування Після внутрішнього прийому рацекадотрил швидко абсорбується. Час до початку інгібування енкефалінази плазми становить 30 хв. Прийом їжі не впливає на біодоступність рацекадотрилу, але після їди активність препарату проявляється із затримкою приблизно на півтори години. Розподіл У плазмі крові, після застосування рацекадотрилу, міченого радіоактивним ізотопом 14С, вміст радіовуглецю був у багато разів вищий, ніж у клітинах крові, і в 3 рази вищий, ніж у цільній крові. Таким чином, препарат незначно зв'язується із клітинами крові. Радіовуглець помірно розподіляється в інших тканинах організму, про що свідчить обсяг його розподілу в плазмі в розмірі 66,4 кг. 90% активного метаболіту рацекадотрилу (тіорфан) ((RS)-N-(1-оксо-2-(меркаптометил)-3-фенілпропіл) гліцину), зв'язується з білками плазми, переважно альбуміном. Фармакокінетичні властивості рацекадотрилу не змінюються внаслідок прийому повторних доз, а також при призначенні пацієнтам похилого віку. Тривалість та ефективність дії рацекадотрилу залежать від дози препарату. У дорослих час до пікового інгібування енкефалінази плазми становить приблизно 2 години і відповідає 75% інгібуванню при прийомі дози 100 мг. Час пригнічення енкефалінази плазми становить приблизно 8 годин. Метаболізм Біологічний період напіввиведення рацекадотрилу, виміряний як час пригнічення енкефалінази плазми, становить приблизно 3 години. Рацекадотрил швидко гідролізується до тіорфану, активного метаболіту, який у свою чергу трансформується в неактивні метаболіти. Прийом повторних доз рацекадотрилу не призводить до накопичення в організмі. Дані, отримані в результаті досліджень in vitro, показують, що рацекадотрил/тіорфан і чотири основні неактивні метаболіти не інгібують ізоформи ферменту CYP (3А4, 2D6, 2С9, 1А2 та 2С19) у ступені, який може бути клінічно значущим. Дані, отримані в результаті досліджень in vitro, показують, що рацекадотрил/тіорфан і чотири основні неактивні метаболіти не індукують ізоформи ферменту CYP (ЗА, 2А6, 2В6, 2С9/2С19, 1А, 2Е1) і кон'юговані ферменти уридинглюкуроноз яка може бути клінічно значущою. Рацекадотрил не впливає на білкове зв'язування таких активних речовин, як толбутамід, варфарин, ніфлумова кислота, дигоксин або фенітоїн. У пацієнтів з печінковою недостатністю (клас В за класифікацією Чайлд-П'ю) кінетичний профіль активного метаболіту рацекадотрилу продемонстрував подібні показники Тmах (час досягнення максимальної концентрації в крові) та Т1/2 (період напіввиведення) та нижчі показники Сmах (максимальна концентрація в крові) (-65 %) та AUC (площа під кривою "концентрація-час") (-29 %) порівняно з цими показниками у здорових людей. У пацієнтів з тяжкою нирковою недостатністю (кліренс креатиніну 11-39 мл/хв) кінетичний профіль активного метаболіту рацекадотрилу продемонстрував нижчий показник Сmах (-49%) та більш високий показник AUC (+16%) та Т1/2 порівняно зі здоровими добровольцями (Кліренс креатиніну >70 мл/хв.). Схах досягається через 2 години 30 хв після застосування. Не спостерігалося кумуляції при повторному прийомі кожні 8 годин протягом 7 днів. Виведення Рацекадотрил виводиться з організму у формі активних та неактивних метаболітів переважно через нирки, і набагато меншою мірою – з калом. Виведення через легені – незначне.ФармакодинамікаРацекадотрил є проліками, які гідролізуються до свого активного метаболіту - тіорфану, що є інгібітором енкефалінази, поверхневої пептидази (розташованої на клітинній мембрані), локалізованої в різних тканинах, особливо в епітелії тонкого кишечника. Цей фермент відповідає одночасно за гідроліз екзогенних пептидів та за розщеплення ендогенних пептидів, таких як енкефаліни. В результаті рацекадотрил захищає ендогенні енкефаліни, які виявляють фізіологічну активність на рівні травного тракту, пролонгуючи їхню антисекреторну дію. Рацекадотрил є кишковою антисекреторною речовиною. Воно зменшує кишкову гіперсекрецію води та електролітів, що викликається ентеротоксином холери або запаленням, і не впливає на базальну секрецію кишківника. Рацекадотрил чинить швидку протидіарейну дію, не змінюючи час проходження кишкового вмісту через кишечник. Рацекадотрил не викликає здуття живота. У клінічних дослідженнях частота виникнення вторинних запорів прийому рацекадотрилу була порівнянна з плацебо.Показання до застосуванняСимптоматичне лікування гострої діареї у дорослих.Протипоказання до застосуванняГіперчутливість до діючої речовини або до будь-якого іншого компонента препарату. Вроджена непереносимість галактози, недостатність лактази, синдром глюкозо-галактозної мальабсорбції (у зв'язку з тим, що препарат містить лактозу). Вагітність та період грудного вигодовування. Дитячий вік до 18 років (через високий вміст діючої речовини).Вагітність та лактаціяВагітність Достатніх даних про застосування рацекадотрилу вагітними відсутні. У ході досліджень на тваринах не виявлено прямих або непрямих несприятливих ефектів щодо вагітності, ембріонального розвитку, пологів або післяпологового розвитку. Однак через відсутність клінічних даних не слід застосовувати препарат Гідрасек під час вагітності. Період грудного вигодовування У зв'язку з відсутністю інформації про екскрецію рацекадотрилу до грудного молока не слід застосовувати препарат Гідрасек під час грудного вигодовування.Побічна діяПовідомлення про наступні небажані реакції були відзначені при прийомі рацекадотрилу частіше, ніж при прийомі плацебо або отримані в період постмаркетингового застосування: Порушення з боку нервової системи Часто (≥ 1/100, Порушення з боку шкіри та підшкірних тканин Нечасто (≥ 1/1000, Частота невідома (для оцінки частоти випадків наявних даних недостатньо): поліморфна еритема, набряк язика, набряк обличчя, набряк губ, набряк повік, ангіоневротичний набряк, кропив'янка, вузлувата еритема, папульозний висип, пруриго, свербіж шкіри, токсичний дерматит.Взаємодія з лікарськими засобамиВ даний час даних про взаємодію з іншими препаратами відсутні. Лоперамід або ніфуроксазид не впливає на кінетику рацекадотрилу при сумісному застосуванні цих препаратів.Спосіб застосування та дозиДля прийому всередину. Першу капсулу на початку лікування приймають незалежно від доби. Далі – одну капсулу тричі на день перед їдою. Лікування необхідно продовжувати до нормалізації випорожнення (появи нормального калу до двох разів), але не більше 7 днів. Не рекомендується застосовувати рацекадотрил тривалий час. Особливі групи пацієнтів Пацієнти похилого віку: корекція дози препарату для пацієнтів похилого віку не потрібна.ПередозуванняВ даний час відомі поодинокі випадки передозування без побічних ефектів. У дорослих прийом одноразової дози препарату більше 2 г, еквівалентної 20-кратної терапевтичної дози, несприятливих ефектів не викликав.Запобіжні заходи та особливі вказівкиЗастосування препарату Гідрасек не звільняє від проведення пероральної регідратації у випадках, коли вона необхідна. Наявність кров'яних або гнійних виділень у стільці і висока температура можуть бути симптомами інвазивної бактеріальної інфекції, що стала причиною діареї, або іншого серйозного захворювання, що є підставою для етіотропної терапії (наприклад, із застосуванням антибіотиків) або подальшого дослідження. Монотерапія рацекадотрилом за даних станів протипоказана. Як додаткову терапію гострої бактеріальної діареї рацекадотрил може застосовуватися спільно з антибіотиками. У зв'язку з недостатністю даних не рекомендується застосовувати рацекадотрил при антибіотик-асоційованій діареї та хронічній діареї. У зв'язку з недостатністю даних рацекадотрил слід застосовувати з обережністю пацієнтам з нирковою та печінковою недостатністю. Біодоступність рацекадотрилу може бути знижена при багаторазовому блюванні. Вплив на здатність до керування автотранспортом та управління механізмами Застосування препарату Гідрасек не впливає або незначно впливає на здатність до керування автомобілем та механізмами.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
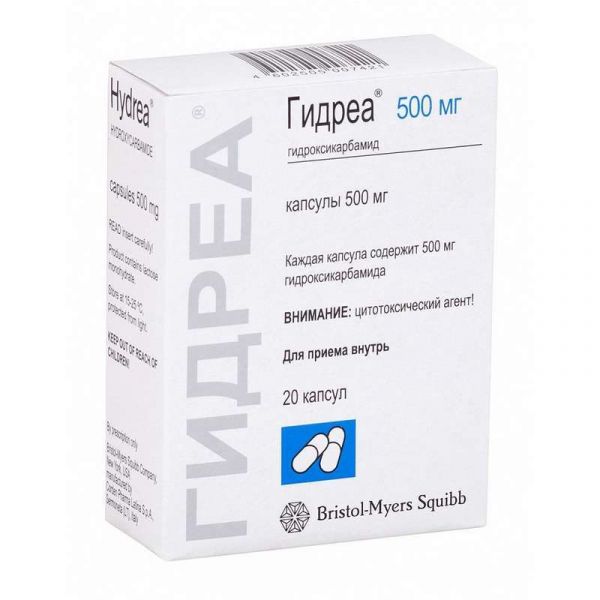
Склад, форма випуску та упаковкаКапсули - 1 капс. активна речовина: гідроксикарбамід 500 мг; допоміжні речовини: лимонна кислота 12,8 мг, лактози моногідрат 42,2 мг, гідрофосфат натрію 36,0 мг, магнію стеарат 9,0 мг; склад оболонки капсули: желатин 93,743 мг, титану діоксид 2,016 мг, барвник заліза оксид червоний 0,115 мг, барвник заліза оксид жовтий 0,110 мг, барвник індигокармін FD&C синій 2 0,017 мг; склад чорнила для напису: шеллак, заліза оксид чорний, N-бутиловий спирт, вода очищена, пропіленгліколь, промисловий метильований спирт, ізопропіловий спирт. По 10 капсул у блістер з алюмінієвої фольги/ПВХ/ПВДХ. По 2 блістери разом із інструкцією із застосування в картонну пачку.Опис лікарської формиКапсули – тверді желатинові, непрозорі, розміром №0. Кришечка: зелена матова. Корпус: блідо-рожевий матовий. На капсулі є напис чорного кольору "BMS 303". капсули: порошок або ущільнена маса білого кольору.Фармакотерапевтична групаПротипухлинний засіб - антиметаболіт.ФармакокінетикаПісля прийому внутрішньо швидко всмоктується із шлунково-кишкового тракту. Максимальні концентрації препарату в плазмі досягаються протягом 2 годин після прийому. Даних щодо впливу їжі на всмоктування препарату немає. Швидко розподіляється по тканинах організму, проникає через гематоенцефалічний бар'єр. У спинномозковій рідині визначається 10-20%, в асцитичній рідині – 15-50% від концентрації у плазмі крові. Гідроксикарбамід накопичується в лейкоцитах та еритроцитах. Період напіввиведення – 3-4 години. Частково метаболізується у печінці. 80% гідроксимочевини протягом 12 годин виводиться із сечею, при цьому 50% у незміненому вигляді та у невеликих кількостях у вигляді сечовини. Препарат також виводиться через дихальні шляхи у вигляді вуглецю діоксиду. Через 24 години у плазмі не визначається. Пацієнти з порушенням функції нирок Оскільки гідроксимочевина виводиться переважно через нирки, потрібне зниження дози при призначенні препарату таким пацієнтам.ФармакодинамікаГідроксикарбамід є фазоспецифічним цитостатичним препаратом (антиметаболіт, за деякими даними - алкілуючої дії), що діє у фазі S клітинного циклу. Блокує зростання клітин в інтерфазі G1-S, що істотно для променевої терапії, що проводиться одночасно, оскільки з'являється синергічна чутливість пухлинних клітин у фазі G1 на опромінення. Підсилюючи дію інгібітору РНК-редуктази - рибонуклеозиддифосфатредуктази, викликає пригнічення синтезу ДНК. Препарат не впливає на синтез РНК та білка.Показання до застосуваннярезистентний хронічний мієлолейкоз; істинна поліцитемія (еритремія) із високим ризиком тромбоемболічних ускладнень; есенціальна тромбоцитемія із високим ризиком тромбоемболічних ускладнень; остеомієлофіброз; меланома; злоякісні пухлини голови та шиї (за винятком раку губи) у комбінації з променевою терапією; рак шийки матки у комбінації з променевою терапією.Протипоказання до застосуванняПідвищена чутливість до гідроксикарбаміду або будь-якої іншої допоміжної речовини, що входить до складу препарату; вагітність та період грудного вигодовування; лейкопенія нижче 2500/мкл, тромбоцитопенію нижче 100000/мкл; дитячий вік (безпека та ефективність застосування не встановлена). З обережністю: Печінкова та/або ниркова недостатність; тяжка анемія (має бути компенсована перед початком лікування), пацієнти після перенесеної радіотерапії або хіміотерапії (можливість мієлосупресії, загострення променевої еритеми); дефіцит лактази, непереносимість лактози, глюкозо-галактозна мальабсорбція.Вагітність та лактаціяПрепарат не слід приймати під час вагітності. Під час терапії слід попередити пацієнтку про необхідність надійної контрацепції. Якщо вагітність настала під час лікування, необхідно попередити пацієнтку про можливість ризику для плода. Препарат проникає у грудне молоко. Слід припинити грудне вигодовування на період лікування або скасувати терапію, попередньо оцінивши важливість її проведення для матері.Побічна діяУмовні позначення небажаних явищ (НЯ): "дуже часто" (≥ 1/10), "часто" (≥1/100, Інфекції: частота невідома – гангрена. З боку органів кровотворення: частота невідома – пригнічення функції кісткового мозку (лейкопенія, анемія, тромбоцитопенія). З боку органів травлення: частота невідома - гепатотоксичність, панкреатит, іноді з летальним кінцем (у ВІЛ-інфікованих пацієнтів, які одночасно отримують антиретровірусну терапію, зокрема диданозин та ставудін); стоматит, анорексія, нудота, блювання, діарея, запор, мукозит, диспепсія, подразнення слизової оболонки шлунка, виразка слизової оболонки шлунково-кишкового тракту; підвищення активності "печінкових" ферментів та концентрації білірубіну в плазмі, холестаз, гепатит. З боку шкіри та шкірних придатків: частота невідома - шкірний васкуліт, макульозно-папульозні висипання, еритема обличчя та периферична еритема, виразки на шкірі, дерматоміозитоподібні зміни шкіри, ексфоліація шкіри, гіперпігментація, еритема, атрофія шкіри та нігтів, шкірні токсичні васкуліти (включаючи васкулітні виразки та гангрену); рідко – алопеція, рак шкіри. З боку нервової системи: частота невідома – запаморочення, сонливість, дезорієнтація; головний біль, галюцинації, судоми, периферична нейропатія (у ВІЛ-інфікованих пацієнтів, які одночасно отримують антиретровірусну терапію, зокрема диданозин та ставудін), підвищена стомлюваність. З боку респіраторної системи: частота невідома – фіброз легень, дифузна інфільтрація легень, задишка. З боку сечовидільної системи: частота невідома – збільшення вмісту сечової кислоти у сироватці крові, підвищення вмісту азоту сечовини та креатиніну у плазмі крові, затримка сечі, інтерстиціальний нефрит; рідко – дизурія. Інше: частота невідома – озноб, лихоманка, загальне нездужання, підвищення ШОЕ, шкірні алергічні реакції, астенія, азооспермія, олігоспермія, синдром лізису пухлини; рідко – дифузна інфільтрація легень, задишка. Випадки розвитку панкреатиту та гепатотоксичності (з можливим смертельним наслідком), а також важкої периферичної нейропатії відмічені у хворих на ВІЛ, які приймали гідроксикарбамід спільно з антиретровірусними препаратами, зокрема диданозин у комбінації зі ставудином або без нього. Побічні явища, що спостерігаються при одночасному застосуванні гідроксикарбаміду та променевої терапії, такі ж, як і при монотерапії препаратом, головним чином пригнічення функції кісткового мозку (лейкопенія, анемія) та подразнення слизової оболонки шлунка. Прийом гідроксикарбаміду може посилювати деякі побічні ефекти, що спостерігаються при променевій терапії, такі як дискомфорт у шлунку та мукозит.Взаємодія з лікарськими засобамиПри одночасному застосуванні препарату з іншими мієлосупресивними препаратами або променевою терапією рівень пригнічення функції кісткового мозку або розвиток інших побічних ефектів може зростати. У дослідженнях in vitro зазначено, що при одночасному застосуванні препарату Гідреа® та цитарабіну підвищується цитотоксичний ефект останнього. Якщо в ході комбінованої терапії відзначаються тяжкі диспепсія, нудота, блювання або анорексія, їх зазвичай можна усунути перериванням прийому препарату Гідреа®. Болючість і дискомфорт слизових оболонок у місці опромінення (мукозит) можна полегшити застосуванням місцевих анестетиків та прийомом анальгезирующих препаратів внутрішньо. При тяжкому мукозиті терапію препаратом Гідреа® тимчасово припиняють; у дуже тяжких випадках призупиняють також променеву терапію. Препарат може збільшувати вміст сечової кислоти в сироватці крові, тому може знадобитися коригування дози препаратів, що підвищують виведення сечової кислоти з організму. Урикозуричні засоби збільшують ризик розвитку нефропатії. Відзначено випадки появи хибнопозитивних результатів аналізів при визначенні сечовини, сечової кислоти та молочної кислоти внаслідок взаємодії гідроксикарбаміду та ферментів (уреази, урикази, лактатдегідрогенази). Підвищений ризик розвитку вакциноасоційованих інфекцій зі смертельними наслідками можливий при сумісному застосуванні Гідреа® та живих вакцин. Застосування живих вакцин не рекомендовано у пацієнтів із зниженим імунітетом.Спосіб застосування та дозиПри виборі режиму та доз у кожному індивідуальному випадку слід керуватися даними спеціальної літератури. Препарат застосовують внутрішньо. При утрудненні ковтання капсулу можна розкрити, висипати вміст у склянку води та негайно випити. При цьому деякі водонерозчинні допоміжні речовини залишаються на поверхні розчину. Під час лікування препаратом слід приймати досить велику кількість рідини. Резистентний хронічний мієлолейкоз Безперервна терапія. Від 20 до 30 мг/кг щодня раз на день. Оцінку ефективності препарату проводять після 6 тижнів лікування. При прийнятному клінічному відповіді лікування можна продовжувати необмежено довго. Лікування слід призупинити, якщо вміст лейкоцитів – менше 2,5х109/л або вміст тромбоцитів – менше 100х109/л. Через 3 дні повторно проводять аналіз крові. Лікування відновлюють тоді, коли вміст лейкоцитів та еритроцитів підвищується до прийнятного. Зазвичай відновлення вмісту лейкоцитів та еритроцитів відбувається досить швидко, інакше при спільному застосуванні препарату з променевою терапією остання може бути також припинена. Розвиток анемії, навіть тяжкої, не вимагає переривання курсу лікування за умови адекватної терапії (трансфузія еритроцитарної маси). Істинна поліцитемія (еритремія) з високим ризиком тромбоемболічних ускладнень Лікування починають із добової дози 15-20 мг/кг. Дозу встановлюють індивідуально, прагнучи підтримувати гематокрит нижче 45%, а кількість тромбоцитів – нижче 400х109/л. У більшості хворих вдається досягти цих показників, постійно застосовуючи гідроксикарбамід у добовій дозі від 500 до 1000 мг. Лікування продовжують доти, доки зберігається можливість адекватно контролювати кількість тромбоцитів та/або лейкоцитів або до появи резистентності чи непереносимості препарату. Есенційна тромбоцитемія з високим ризиком тромбоемболічних ускладнень Зазвичай призначають препарат Гідреа у початковій добовій дозі 15 мг/кг; потім підбирають таку дозу, яка підтримує кількість тромбоцитів на рівні нижче 600х109/л, не призводячи до зменшення кількості лейкоцитів нижче 4х109/л. Лікування продовжують доти, доки зберігається можливість адекватно контролювати кількість тромбоцитів та/або лейкоцитів або до появи резистентності чи непереносимості препарату. Остеомієлофіброз Зазвичай призначають препарат Гідреа у початковій добовій дозі 15 мг/кг; потім підбирають таку дозу, яка підтримує кількість лейкоцитів не нижче 4х109/л та кількість тромбоцитів не нижче 100х109/л. Меланома, солідні пухлини Переривчаста терапія: 80 мг/кг один раз на день кожні три дні (6-7 доз) Безперервна терапія: 20-30 мг/кг щодня раз на день протягом 3-х тижнів. Злоякісні пухлини голови та шиї (за винятком раку губи) у комбінації з променевою терапією, рак шийки матки у комбінації з променевою терапією 80 мг/кг один раз на день, кожні три дні у комбінації з променевою терапією. Лікування препаратом починають не менше ніж за 7 днів до початку променевої терапії та продовжують під час променевої терапії. Після променевої терапії препарат продовжують приймати протягом необмеженого часу при суворому спостереженні за хворим та за відсутності у нього незвичайних чи тяжких токсичних реакцій. Пацієнти з порушенням функції печінки Вказівки щодо зміни доз цієї групи пацієнтів відсутні. Слід проводити ретельний моніторинг показників крові у пацієнтів із порушенням функції печінки. Пацієнти з порушенням функції нирок Оскільки гідроксимочевина виводиться переважно через нирки, потрібне зниження дози при застосуванні препарату таким пацієнтам. Хворим із нирковою недостатністю (кліренс креатиніну менше 60 мл/хв) препарат зазвичай призначається у дозі 15 мг/кг. Хворим у термінальній стадії ниркової недостатності препарат призначається у дозі 15 мг/кг двічі, з інтервалом у 7 днів між прийомами: перший раз – після закінчення 4-годинного сеансу гемодіалізу, другий раз – перед проведенням сеансу гемодіалізу. Літні пацієнти Оскільки у пацієнтів похилого віку ймовірність розвитку побічних ефектів при застосуванні препарату Гідреа® вища, ніж у пацієнтів молодого віку, рекомендована доза для пацієнтів цієї групи не повинна перевищувати 60 мг/кг на добу.ПередозуванняСимптоми. При застосуванні препарату в дозах, що у кілька разів перевищували рекомендовані, у хворих розвивалися ознаки гострої дерматологічної токсичності: болючість, фіолетова еритема, набряк з подальшим лущенням долонь рук та стоп ніг, інтенсивна генералізована гіперпігментація шкіри та стоматит. Лікування. Специфічний антидот не відомий. Лікування симптоматичне.Запобіжні заходи та особливі вказівкиЛікування препаратом слід проводити лише під наглядом лікаря, який має досвід застосування протипухлинної терапії. Перед кожним курсом та періодично під час лікування препаратом необхідно контролювати функції кісткового мозку, нирок та печінки. Визначення гемоглобіну, лейкоцитів та тромбоцитів має проводитися не рідше 1 разу на тиждень протягом усього періоду лікування препаратом. Лікування призначають тільки у тому випадку, якщо вміст лейкоцитів перевищує 2500/мкл, а тромбоцитів – 100000/мкл. Якщо в ході лікування виявлено, що вміст лейкоцитів – менше 2500/мкл або тромбоцитів – менше 100000/мкл, лікування слід призупинити доти, доки вміст їх не відновиться до норми. Тяжка форма анемії повинна бути компенсована до початку лікування препаратом. Під час лікування препаратом може розвинутись мієлосупресія, головним чином лейкопенія. Тромбоцитопенія і анемія розвиваються рідше і дуже рідко - без попередньої лейкопенії. Мієлосупресія найбільш ймовірна у хворих після нещодавньої попередньої променевої терапії або хіміотерапії іншими препаратами. Після нещодавньої променевої або хіміотерапії препарат повинен застосовуватися з обережністю через можливе загострення пострадіаційної еритеми та посилення виразності побічних ефектів (аплазія кісткового мозку, диспепсія та ульцерація шлунково-кишкового тракту). При виникненні тяжких побічних явищ з боку органів травлення (таких як нудота, блювання, анорексія) зазвичай припиняють терапію препаратом Гідреа. При болю та дискомфорті при розвитку мукозиту в області опромінення зазвичай призначають місцеві анестетики та анальгетики для вживання. У тяжких випадках терапію препаратом тимчасово припиняють, а у дуже тяжких випадках – тимчасово скасовують супутню променеву терапію. На ранніх стадіях лікування препаратом часто спостерігається помірний мегалобластичний еритропоез. Морфологічні зміни нагадують перніціозну анемію, однак вони не пов'язані з дефіцитом вітаміну В12 або фолієвої кислоти. У зв'язку з тим, що макроцитоз може маскувати дефіцит фолієвої кислоти, рекомендується регулярне визначення фолієвої кислоти у сироватці крові. Гідроксикарбамід може також уповільнювати кліренс заліза плазми та знижувати швидкість утилізації заліза еритроцитами, проте це не впливає на час життя еритроцитів. Випадки розвитку панкреатиту та гепатотоксичності (з можливим смертельним наслідком) відзначені у ВІЛ-інфікованих пацієнтів, які приймали гідроксикарбамід спільно з антиретровірусними препаратами, зокрема диданозин (зі ставудином та без нього). У зв'язку із цим слід уникати спільного призначення цих препаратів. Також випадки розвитку периферичної нейропатії, іноді тяжкі, спостерігалися у ВІЛ-інфікованих пацієнтів, які приймали гідроксикарбамід спільно з антиретровірусними препаратами, включаючи диданозин (зі ставудином та без нього). Під час лікування хворі повинні вживати достатньо рідини. Можливе зниження дози препарату при порушеннях функції нирок. Препарат слід застосовувати з обережністю у хворих при порушеній функції нирок та печінки. Під час лікування препаратом у хворих з мієлопроліферативними захворюваннями спостерігалися шкірні токсичні васкуліти, включаючи васкулітні виразки та гангрену. Найчастіше повідомлялося про токсичні васкуліти у пацієнтів, які отримували або отримували в минулому інтерферон. При прогресуванні васкулітних виразок прийом препарату слід припинити. При тривалому застосуванні препарату Гідреа у пацієнтів з мієлопроліферативними захворюваннями, такими як істинна поліцитемія та тромбоцитемія, відмічені випадки вторинних лейкозів. При цьому невідомо, що причина розвитку вторинного лейкозу: прийом гідроксикарбаміду або основне захворювання. При тривалому застосуванні препарату Гідреа спостерігалися також випадки раку шкіри. Слід попередити пацієнтів про необхідність захищати шкіру від сонячного світла та проводити самоконтроль стану шкіри. Під час планових відвідувань лікаря слід контролювати стан шкірних покривів пацієнта з метою виявлення можливих злоякісних змін. Азооспермія або олігоспермія, іноді оборотна, спостерігалася у пацієнтів чоловічої статі. У зв'язку з цим пацієнтів слід повідомити про можливість консервації сперми перед початком терапії. У зв'язку з можливою генотоксичністю препарату Гідреа® пацієнти чоловічої статі, які приймають препарат Гідреа®, повинні бути поінформовані про необхідність надійної контрацепції під час лікування та щонайменше протягом 1 року після закінчення терапії. При вакцинації живими вірусними вакцинами одночасно з терапією препаратом Гідреа® можлива активація реплікації вірусу вакцини та/або збільшення розвитку побічних реакцій через придушення захисних механізмів організму, спричинене прийомом препарату Гідреа®. Вакцинація живими вакцинами під час прийому препарату Гідреа може призвести до розвитку важких інфекцій. Можливе також зниження імунної відповіді на введення вакцин. Слід уникати введення живих вакцин у період терапії препаратом Гідреа® та проконсультуватися у спеціаліста. Препарат Гідреа® має цитотоксичну дію, тому слід бути обережним при розтині капсул і уникати попадання порошку капсул на шкіру, слизові оболонки або вдихання препарату. Якщо вміст капсули випадково розсипаний, слід негайно зібрати порошок серветкою в поліетиленовий пакет, зав'язати його та викинути. Застосування у педіатрії. Безпека та ефективність застосування у дітей не встановлена. Оскільки у пацієнтів похилого віку ймовірність розвитку побічних ефектів при застосуванні препарату Гідреа® вища, ніж у пацієнтів молодого віку, може знадобитися застосування препарату у зниженій дозі. Вплив на здатність до керування автотранспортом та управління механізмами Досліджень щодо вивчення впливу препарату на здатність до керування автотранспортом та управління механізмами не проводилося. У зв'язку з тим, що гідроксикарбамід може викликати запаморочення та інші небажані явища з боку нервової системи, у період лікування препаратом здатність до концентрації уваги може погіршуватись.Умови відпустки з аптекЗа рецептомВідео на цю тему
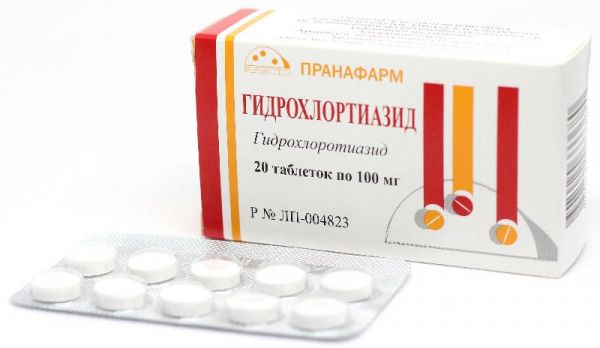
Склад, форма випуску та упаковкаПігулки - 1 таб. Активні речовини: гідрохлортіазид 100мг; Допоміжні речовини: лактози моногідрат, повідон, целюлоза, крохмаль кукурудзяний, магнію стеарат. У упаковці 20 штук.ФармакокінетикаНа 60-80% всмоктується із ШКТ. На 40% зв'язується з білками крові, де через 2-5 годин визначається його максимальна концентрація. Період напіввиведення – 6-15 год. Більшість (95%) у незміненому вигляді виводиться нирками.ФармакодинамікаТіазидний діуретик (салуретик) середньої сили та тривалості дії. Має слабший діуретичний ефект порівняно з фуросемідом. Зменшує реабсорбцію натрію, хлору та води з первинної сечі в кров у проксизмальній частині канальців. Виводить K+, Mg2+, гідрокарбонатів та фосфатів, затримує Ca2+. Сечогінний ефект починає проявлятися через 2 години, максимум – через 4 години, тривалість діуретичної дії становить 10-12 годин. За рахунок розширення артеріол та зменшення ОЦК знижує тиск. Гіпертензивна дія проявляється через 4 дні. При нецукровому діабеті знижує об'єм сечі, одночасно збільшуючи її концентрацію.ІнструкціяТаблетки приймаються внутрішньо після їди.Показання до застосуванняЛікування гіпертензії – монотерапія або комбінація з іншими гіпеотензивними препаратами. Набряки різного генезу (при нефротичному синдромі, гострій та хронічній нирковій недостатності, ХСН, передменструальному синдромі, при лікуванні кортикостероїдами та при токсикозах вагітних). Нефрогенний нецукровий діабет (контроль поліурії).Протипоказання до застосуванняТяжкі форми цукрового діабету; підвищена чутливість до препарату або сульфонамідів; тяжка ниркова недостатність; анурія; хвороба Аддісона; подагра.Вагітність та лактаціяПротипоказаний дітям до 2 років та у першому триместрі вагітності.Побічна діяЗниження рівня калію, магнію, підвищення кальцію в крові проявляється спрагою та сухістю в роті, нудотою, судомами у м'язах, порушенням серцевого ритму, змінами психіки, вираженою втомою; гіпонатріємія, яка проявляється сплутаністю свідомості, уповільнення процесу мислення, підвищеною збудливістю, конвульсіями та м'язовими судомами; підвищення рівня цукру в крові та поява його в сечі. Тіазиди знижують толерантність до глюкози, тому латентний цукровий діабет проявляється; підвищення ліпідів та сечової кислоти в крові (при тривалому застосуванні високих доз); холецистит, холестатична жовтяниця, запалення слинних залоз, запор; аритмії та ортостатична гіпотензія; запаморочення, біль голови, порушення зору (розпливчастість), парестезії; кропив'янка, пурпура, синдром Стівенса-Джонсона, некротичний васкуліт, анафілактичний шок; інтерстиціальний нефрит із порушенням функції нирок; зниження потенції.Взаємодія з лікарськими засобамиНепрямі антикоагулянти, НПЗЗ, Клофібрат посилюють діуретичний ефект. Прийом вазодилататорів, бета-адреноблокаторів, трициклічних антидепресантів, діазепаму, барбітуратів та етанолу посилює гіпотензивний ефект діуретиків. Індометацин та інші НПЗЗ знижують гіпотензивний ефект. Холестирамін зменшує дію тіазидних діуретиків, оскільки гальмує їхнє всмоктування. При одночасному застосуванні із серцевими глікозидами підвищується ризик їх токсичності (підвищена збудливість шлуночків), що пов'язано з гіпокаліємією та гіпомагніємією. Застосування аміодарону та діуретиків підвищує ризик появи аритмій, що пов'язано з гіпокаліємією. При сумісному застосуванні з кортикостероїдами виникає ризик розвитку гіпокаліємії. Тіазидні діуретики послаблюють дію гіпоглікемічних препаратів та норадреналіну зменшують ефект пероральних контрацептивів, посилюють нейротоксичність саліцилатів та збільшують чутливість до тубокурарину. Прийом метилдопи та діуретика може спричинити гемоліз.Спосіб застосування та дозиЯк антигіпертензивний засіб: ЦД 25-50 мг. Гідрохлортіазид застосовується як засіб для монотерапії або у комбінації з іншими антигіпертензивними засобами (інгібіторами АПФ, вазодилататорами, бета-адреноблокаторами, симпатолітиками). Збільшення дози до 100 мг пропорційно веде до збільшення діурезу, зниження артеріального тиску та втрати натрію. Якщо доза – більше 100 мг, зростання діурезу та зниження АТ дуже незначні, проте зростає втрата електролітів K+ та Mg2+. Доцільним є збільшення дози до 200 мг, оскільки посилення діурезу не відзначається. Гіпотензивна дія проявляється через 3-4 дні, а для стійкого ефекту іноді потрібні 3-4 тижні. Якщо гідрохлортіазид комбінується з іншими гіпотензивними засобами, дозу іншого препарату іноді доводиться знижувати, щоб уникнути надмірного зниження тиску. Набряковий синдром: 25-100 мг вранці (можна поділити на 2 прийоми до 11 години дня). Іноді у тяжких випадках спочатку лікування призначається до 200 мг на добу. Через 3 дні роблять перерву на 5 днів. Для підтримуючої терапії 25-50 мг – двічі на тиждень. При такому уривчастому курсі лікування побічні явища розвиваються рідше. Нефрогенний нецукровий діабет: 25 мг на добу, поступово збільшуючи до 50-150 мг, розділивши на 2 прийоми. При досягненні ефекту (зменшення поліурії та спраги) доза знижується. Передменструальний синдром: 25 мг із моменту прояву симптомів до настання менструації. Для дітей дози обчислюються, виходячи з ваги дитини. Педіатрична доза – 1-2 мг/кг ваги 1 раз на добу. Для зниження внутрішньоочного тиску інструкція застосування Гідрохлортіазиду передбачає призначення 25 мг 1 раз на 3-6 днів.ПередозуванняПроявляється адинамією, тахікардією та аритмією, запорами, сонливістю, сухістю у роті зниженням артеріального тиску, зменшенням добового діурезу. Специфічного антидоту немає, симптоматичне лікування: промивання шлунка, прийом сорбентів, інфузія розчинів електролітів.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
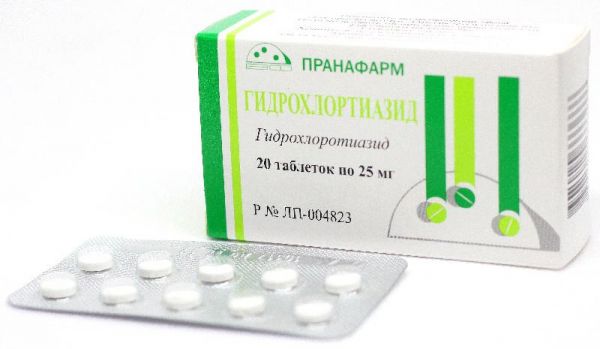
Склад, форма випуску та упаковкаПігулки - 1 таб. Активні речовини: гідрохлортіазид 25 мг; Допоміжні речовини: лактози моногідрат, повідон, целюлоза, крохмаль кукурудзяний, магнію стеарат. У упаковці 20 штук.ФармакокінетикаНа 60-80% всмоктується із ШКТ. На 40% зв'язується з білками крові, де через 2-5 годин визначається його максимальна концентрація. Період напіввиведення – 6-15 год. Більшість (95%) у незміненому вигляді виводиться нирками.ФармакодинамікаТіазидний діуретик (салуретик) середньої сили та тривалості дії. Має слабший діуретичний ефект порівняно з фуросемідом. Зменшує реабсорбцію натрію, хлору та води з первинної сечі в кров у проксизмальній частині канальців. Виводить K+, Mg2+, гідрокарбонатів та фосфатів, затримує Ca2+. Сечогінний ефект починає проявлятися через 2 години, максимум – через 4 години, тривалість діуретичної дії становить 10-12 годин. За рахунок розширення артеріол та зменшення ОЦК знижує тиск. Гіпертензивна дія проявляється через 4 дні. При нецукровому діабеті знижує об'єм сечі, одночасно збільшуючи її концентрацію.ІнструкціяТаблетки приймаються внутрішньо після їди.Показання до застосуванняЛікування гіпертензії – монотерапія або комбінація з іншими гіпеотензивними препаратами. Набряки різного генезу (при нефротичному синдромі, гострій та хронічній нирковій недостатності, ХСН, передменструальному синдромі, при лікуванні кортикостероїдами та при токсикозах вагітних). Нефрогенний нецукровий діабет (контроль поліурії).Протипоказання до застосуванняТяжкі форми цукрового діабету; підвищена чутливість до препарату або сульфонамідів; тяжка ниркова недостатність; анурія; хвороба Аддісона; подагра.Вагітність та лактаціяПротипоказаний дітям до 2 років та у першому триместрі вагітності.Побічна діяЗниження рівня калію, магнію, підвищення кальцію в крові проявляється спрагою та сухістю в роті, нудотою, судомами у м'язах, порушенням серцевого ритму, змінами психіки, вираженою втомою; гіпонатріємія, яка проявляється сплутаністю свідомості, уповільнення процесу мислення, підвищеною збудливістю, конвульсіями та м'язовими судомами; підвищення рівня цукру в крові та поява його в сечі. Тіазиди знижують толерантність до глюкози, тому латентний цукровий діабет проявляється; підвищення ліпідів та сечової кислоти в крові (при тривалому застосуванні високих доз); холецистит, холестатична жовтяниця, запалення слинних залоз, запор; аритмії та ортостатична гіпотензія; запаморочення, біль голови, порушення зору (розпливчастість), парестезії; кропив'янка, пурпура, синдром Стівенса-Джонсона, некротичний васкуліт, анафілактичний шок; інтерстиціальний нефрит із порушенням функції нирок; зниження потенції.Взаємодія з лікарськими засобамиНепрямі антикоагулянти, НПЗЗ, Клофібрат посилюють діуретичний ефект. Прийом вазодилататорів, бета-адреноблокаторів, трициклічних антидепресантів, діазепаму, барбітуратів та етанолу посилює гіпотензивний ефект діуретиків. Індометацин та інші НПЗЗ знижують гіпотензивний ефект. Холестирамін зменшує дію тіазидних діуретиків, оскільки гальмує їхнє всмоктування. При одночасному застосуванні із серцевими глікозидами підвищується ризик їх токсичності (підвищена збудливість шлуночків), що пов'язано з гіпокаліємією та гіпомагніємією. Застосування аміодарону та діуретиків підвищує ризик появи аритмій, що пов'язано з гіпокаліємією. При сумісному застосуванні з кортикостероїдами виникає ризик розвитку гіпокаліємії. Тіазидні діуретики послаблюють дію гіпоглікемічних препаратів та норадреналіну зменшують ефект пероральних контрацептивів, посилюють нейротоксичність саліцилатів та збільшують чутливість до тубокурарину. Прийом метилдопи та діуретика може спричинити гемоліз.Спосіб застосування та дозиЯк антигіпертензивний засіб: ЦД 25-50 мг. Гідрохлортіазид застосовується як засіб для монотерапії або у комбінації з іншими антигіпертензивними засобами (інгібіторами АПФ, вазодилататорами, бета-адреноблокаторами, симпатолітиками). Збільшення дози до 100 мг пропорційно веде до збільшення діурезу, зниження артеріального тиску та втрати натрію. Якщо доза – більше 100 мг, зростання діурезу та зниження АТ дуже незначні, проте зростає втрата електролітів K+ та Mg2+. Доцільним є збільшення дози до 200 мг, оскільки посилення діурезу не відзначається. Гіпотензивна дія проявляється через 3-4 дні, а для стійкого ефекту іноді потрібні 3-4 тижні. Якщо гідрохлортіазид комбінується з іншими гіпотензивними засобами, дозу іншого препарату іноді доводиться знижувати, щоб уникнути надмірного зниження тиску. Набряковий синдром: 25-100 мг вранці (можна поділити на 2 прийоми до 11 години дня). Іноді у тяжких випадках спочатку лікування призначається до 200 мг на добу. Через 3 дні роблять перерву на 5 днів. Для підтримуючої терапії 25-50 мг – двічі на тиждень. При такому уривчастому курсі лікування побічні явища розвиваються рідше. Нефрогенний нецукровий діабет: 25 мг на добу, поступово збільшуючи до 50-150 мг, розділивши на 2 прийоми. При досягненні ефекту (зменшення поліурії та спраги) доза знижується. Передменструальний синдром: 25 мг із моменту прояву симптомів до настання менструації. Для дітей дози обчислюються, виходячи з ваги дитини. Педіатрична доза – 1-2 мг/кг ваги 1 раз на добу. Для зниження внутрішньоочного тиску інструкція застосування Гідрохлортіазиду передбачає призначення 25 мг 1 раз на 3-6 днів.ПередозуванняПроявляється адинамією, тахікардією та аритмією, запорами, сонливістю, сухістю у роті зниженням артеріального тиску, зменшенням добового діурезу. Специфічного антидоту немає, симптоматичне лікування: промивання шлунка, прийом сорбентів, інфузія розчинів електролітів.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. речовини: гідрохлортіазид - 25,0 мг, каптоприл - 50,0 мг; Допоміжні речовини: лактози моногідрат (цукор молочний) – 169,0 мг, целюлоза мікрокристалічна – 100,0 мг, крохмаль кукурудзяний – 40,0 мг, кроскармелоза натрію – 12,0 мг, магнію стеарат – 4,0 мг. Пігулки 25 мг + 50 мг. По 7, 10, 30 таблеток у контурне осередкове пакування з плівки полівінілхлоридної та фольги алюмінієвої друкованої лакованої. По 10, 20, 28, 30, 40, 50 або 100 таблеток у банки з поліетилентерефталату для лікарських засобів, закупорені кришками нагвинчувані з контролем першого розтину або системою «натиснути-повернути» з поліпропілену або поліетилену або банки поліпропілен натягуються з контролем першого розтину з поліетилену або банки поліпропіленові для лікарських засобів, закупорені кришками, що натягуються з контролем першого розтину з поліетилену високого тиску. Одну банку або 1, 2, 3, 4, 5 або 10 контурних осередкових упаковок разом з інструкцією із застосування поміщають у картонну упаковку (пачку).Опис лікарської формиКруглі плоскоциліндричні таблетки з ризиком з одного боку та фасками з двох сторін, білого або білого з бежевим відтінком кольору, з характерним запахом, допускається незначна мармуровістьФармакотерапевтична групаГіпотензивний комбінований засіб (ангіотензинперетворюючого ферменту (АПФ) інгібітор + діуретик).ФармакокінетикаКаптоприл Абсорбція – швидка, становить близько 60-70 % від прийнятої дози. Їда знижує біодоступність на 30-40%. Максимальна концентрація у плазмі крові відзначається через 1 годину після прийому внутрішньо. Зв'язується з білками плазми крові - 25-30%, переважно з альбуміном. Менше 0,002% від прийнятої дози каптоприлу секретується з грудним молоком, що не проникає через гематоенцефалічний бар'єр. Метаболізується в печінці з утворенням дисульфідного димеру каптоприлу та каптоприл-цистеїнсульфіду. Метаболіти фармакологічно неактивні. Період напіввиведення (Т1/2) каптоприлу становить близько 2-3 год. Близько 95% виводиться нирками протягом першої доби, їх 40-50% у незміненому вигляді, решта - як метаболітів. Через 4 години після одноразового прийому внутрішньо в сечі міститься близько 38% незміненого каптоприлу та 28% у вигляді метаболітів, через 6год – тільки у вигляді метаболітів; у добовій сечі – 38 % незміненого каптоприлу та 62 % – у вигляді метаболітів. Внаслідок накопичення каптоприлу та його метаболітів у нирках може виникнути порушення їх функції. Період напіввиведення при нирковій недостатності – 3,5-32 години. Кумулює при хронічній нирковій недостатності. Тому пацієнтам з порушенням функції нирок дозу препарату слід зменшити або збільшити інтервал між прийомом доз. Гідрохлоротіазид Після прийому внутрішньо абсорбція та біодоступність гідрохлортіазиду становить близько 70%. Зв'язок із білками плазми крові – 60-80 %. При прийомі внутрішньо 12,5 мг гідрохлортіазиду максимальна плазмова концентрація досягається через 1,5-4 години і становить 70 нг/мл, а при прийомі внутрішньо 25 мг гідрохлортіазиду максимальна плазмова концентрація досягається через 2-5 годин і становить 142 нг/мл . У терапевтичному діапазоні доз середня величина площі під кривою «концентрація - час» (AUC) зростає прямо пропорційно дозу, при призначенні 1 раз на добу кумуляція незначна. Проникає через гематоплацентарний бар'єр та у грудне молоко. Т1/2 – 5-15 год. Гідрохлортіазид незначно метаболізується у печінці. Гідрохлортіазид виводиться практично повністю (більше 95%) нирками у незміненому вигляді. 50-70% прийнятої внутрішньо дози виводиться протягом 24 годин.ФармакодинамікаГідрохлортіазид + Каптоприл – комбінований препарат, який має антигіпертензивну та діуретичну дію. Каптоприл – інгібітор ангіотензинперетворюючого ферменту (АПФ), зменшує утворення ангіотензину II з ангіотензину I, зменшує виділення альдостерону, знижує загальний периферичний судинний опір (ОПСС), артеріальний тиск (АТ), пост- та переднавантаження. Розширює артерії більшою мірою, ніж вени. Підсилює коронарний та нирковий кровообіг. При тривалому застосуванні зменшується гіпертрофія міокарда та стінок артерій резистивного типу. Каптоприл покращує кровопостачання ішемізованого міокарда; знижує агрегацію тромбоцитів. Гідрохлортіазид – тіазидний діуретик середньої сили, що знижує реабсорбцію іонів натрію на рівні кортикального сегмента петлі Генле. Чи не впливає на кислотно-основний стан. Знижує АТ за рахунок зміни реактивності судинної стінки, зниження пресорного впливу ендогенних судинозвужувальних речовин (адреналіну, норадреналіну) та посилення депресорного впливу на вегетативні ганглії (менше за рахунок зменшення об'єму циркулюючої крові (ОЦК)). Посилює антигіпертензивний ефект каптоприлу. Діуретичний ефект відзначається через 2 години та досягає максимуму через 4 години після прийому внутрішньо. Дія зберігається протягом 6-12 годин. Ефективність та безпека застосування каптоприлу у дітей не встановлено. У літературі описано обмежений досвід застосування каптоприлу у дітей. Діти, особливо новонароджені, можуть бути більш схильними до розвитку гемодинамічних побічних ефектів. Відзначалися випадки розвитку надмірного, тривалого та непередбачуваного підвищення артеріального тиску, а також пов'язаних з ним ускладнень, включаючи олігурію та судоми.Показання до застосуванняАртеріальна гіпертензія.Протипоказання до застосуванняПідвищена чутливість до каптоприлу або інших інгібіторів АПФ, тіазидних діуретиків та інших похідних сульфаніламіду (можливі перехресні алергічні реакції), будь-якого компонента препарату; ангіоневротичний набряк спадковий або ідіопатичний, у тому числі і в анамнезі на фоні прийому інгібіторів АПФ; аортальний стеноз; мітральний стеноз; гіпертрофічна обструктивна кардіоміопатія; двосторонній стеноз ниркових артерій; стеноз ниркової артерії єдиної нирки; стан після трансплантації нирки (в анамнезі); хронічна серцева недостатність; кардіогенний шок, гіпотензія, тахікардія; тяжка печінкова недостатність (прекома або кома); тяжка ниркова недостатність (креатинін сироватки крові більше 1,8 мг/100 мл або кліренс креатиніну (КК) менше 20-30 мл/хв, анурія); первинний гіперальдостеронізм;вагітність, період грудного вигодовування, вік до 18 років (ефективність та безпека не встановлена), одночасне застосування з аліскіреном та аліскіренсодержащими препаратами у пацієнтів з цукровим діабетом або порушення функції нирок (швидкість клубочкової фільтрації (СКФ) менше 60 мл/хв/1,73) м2), непереносимість лактози, дефіцит лактази та синдром глюкозо-галактозної мальабсорбції. З обережністю Помірна ниркова недостатність (КК 30-60 мл/хв), протеїнурія (більше 1 г/добу), порушення функції печінки, прогресуючі захворювання печінки, гіпокаліємія (що не коригується лікарськими засобами); гіпонатріємія, гіповолемія, гіперкальціємія, подагра, гіперурикемія, системні захворювання сполучної тканини та інші імунні захворювання (в т.ч. системний червоний вовчак, склеродермія, вузликовий періартеріїт); літній вік (старше 65 років), одночасне застосування лікарських засобів, що пригнічують захисні реакції організму (глюкокортикостероїди (ГКС), цитостатики, імунодепресанти), алопуринол, прокаїнамід, хірургічне втручання/загальна анестезія, застосування у пацієнтів з негрозою наприклад, AN69®), десенсибілізуюча терапія,одночасне застосування калійзберігаючих діуретиків, препаратів калію і замінників харчових солей, що містять калій, препаратів літію, гостра міопія і вторинна закритокутова глаукома.Вагітність та лактаціяЗастосування препарату Гідрохлоротіазид+Каптоприл під час вагітності протипоказане. Епідеміологічні дані, що свідчать про ризик тератогенності після впливу інгібіторів АПФ у І триместрі вагітності, не були переконливими, проте деяке збільшення ризику не може бути виключено. Якщо застосування інгібітору АПФ вважається за необхідне, пацієнтки, які планують вагітність, повинні бути переведені на альтернативну гіпотензивну терапію з доведеним профілем безпеки застосування під час вагітності. Відомо, що тривала дія інгібіторів АПФ на плід у II та III триместрах вагітності може призводити до порушення його розвитку (зниження функції нирок, олігогідрамніону, уповільнення осифікації кісток черепа) та розвитку ускладнень у новонародженого (ниркова недостатність, артеріальна гіпотензія, гіперкалієм). Якщо пацієнтка отримувала препарат Гідрохлортіазид+Каптоприл під час ІІ або ІІІ триместру вагітності, рекомендується провести ультразвукове обстеження плода для оцінки стану кісток черепа та функції нирок. Застосування гідрохлортіазиду при вагітності не рекомендується, оскільки може погіршити перфузію плаценти та викликати жовтяницю плода/новонародженого, тромбоцитопенію, порушення водно-електролітного балансу та, можливо, інші небажані реакції, що спостерігалися у дорослих. Застосування інгібіторів АПФ під час вагітності може спричинити порушення розвитку (включаючи артеріальну гіпотензію, неонатальну гіпоплазію кісток черепа, анурію, оборотну або необоротну ниркову недостатність) та смерть плода. При діагностуванні вагітності застосування препарату Гідрохлортіазид+Каптоприл слід припинити якнайшвидше. Каптоприл і гідрохлортіазид після прийому внутрішньо жінкою, що годує, виявляються в грудному молоці. У зв'язку з ризиком розвитку серйозних побічних реакцій у дитини, що викликаються обома діючими речовинами, слід припинити грудне вигодовування або відмінити терапію препаратом Гідрохлортіазид+Каптоприл у матері на період грудного вигодовування.Побічна діяЧастота побічних ефектів викладена відповідно до класифікації Всесвітньої організації охорони здоров'я: часто – ≥ 1/100 – З боку серцево-судинної системи: нечасто – біль у грудях, стенокардія, «припливи» крові до шкіри обличчя, тахікардія або тахіаритмія, відчуття серцебиття, периферичні набряки, виражене зниження артеріального тиску (в т.ч. ортостатичний) з симптомами запаморочення, відчуття слабкості , синдром Рейно, інфаркт міокарда, непритомність; дуже рідко – зупинка серця, кардіогенний шок. З боку дихальної системи: часто – сухий непродуктивний кашель, задишка; дуже рідко – бронхоспазм, еозинофільний пневмоніт, синусит, риніт, ларингіт, набряк легенів. Алергічні реакції: часто - свербіж шкіри, з висипаннями або без них, іноді супроводжується лихоманкою і артралгією, висипання на шкірі, алопеція; нечасто – судинний набряк шкіри та підшкірної клітковини; рідко – ангіоневротичний набряк кишківника; дуже рідко – кропив'янка, синдром Стівенса-Джонсона, мультиформна еритема, фоточутливість, еритродермія, оборотні пемфігоїдні реакції, ексфоліативний дерматит, а також токсичний епідермальний некроліз (синдром Лайєлла), алергічний альвеоліт, еноніно, губ, слизових оболонок (у тому числі з летальним результатом), респіраторний дистрес-синдром (включаючи пневмоніт та некардіогенний набряк легені). З боку центральної та периферичної нервової системи: часто – сонливість, запаморочення, безсоння; рідко – біль голови, атаксія, парестезія; дуже рідко – сплутаність свідомості, депресія, порушення мозкового кровообігу, включаючи інсульт та синкопе, нечіткість зору. З боку системи кровотворення: дуже рідко – анемія, включаючи апластичну та гемолітичну форми, зниження гематокриту, тромбоцитопенію, лейкопенію, нейтропенію (аж до розвитку панцитопенії та агранулоцитозу – особливо на тлі одночасного прийому аллопуринолу, прокаїнаміду, а також, підвищення титру антиядерних антитіл, аутоімунні захворювання. З боку травної системи: часто - оборотне і зазвичай самостійне порушення почуття смаку, нудота, блювання, запор або діарея, відчуття дискомфорту в області шлунка, диспепсія, біль у животі, сухість слизової оболонки порожнини рота; рідко – стоматит, афтозний стоматит, анорексія; дуже рідко – глосит, виразка шлунка, панкреатит, гіперплазія ясен, порушення функції печінки та холестазу (включаючи жовтяницю), підвищення активності «печінкових» трансаміназ, гепатит (включаючи некроз), гіпербілірубінемію. З боку опорно-рухового апарату: дуже рідко – міалгія, артралгія, міастенія. З боку сечовидільної системи: нечасто – порушення функції нирок (включаючи ниркову недостатність), поліурію, олігоурію, прискорене сечовипускання, нефротичний синдром. З боку репродуктивної системи: дуже часто – імпотенція, гінекомастія. Інші: нечасто – біль у грудях, підвищена стомлюваність, погане самопочуття. Лабораторні показники: часто – еозинофілія; дуже рідко – протеїнурія, гіперкаліємія, гіпонатріємія (у тому числі симптоматична), підвищення концентрації азоту сечовини, білірубіну та креатиніну в крові, зниження гематокриту, гемоглобіну, лейкоцитів, тромбоцитів. З боку обміну речовин: дуже рідко – гіперглікемія; гіперурикемія (до загострення подагри). Лікування тіазидами може порушувати толерантність до глюкози, і цукровий діабет, що латентнопротікає, може маніфестувати. При застосуванні високих доз можуть збільшуватися концентрації ліпідів у сироватці крові. Порушення водно-електролітного балансу: гіпокаліємія, гіпомагніємія, гіперкальціємія та гіпохлоремічний алкалоз: сухість слизової оболонки порожнини рота, почуття спраги, нерегулярний ритм серця, зміни в настрої або психіці, судоми та болі в м'язах, нудота, блювота; . Гіпохлоремічний алкалоз може викликати печінкову енцефалопатію або печінкову кому. Гіпонатріємія: сплутаність свідомості, конвульсії, летаргія, уповільнення процесу мислення, підвищена втома, збудливість, м'язові судоми. При застосуванні інгібіторів АПФ, у тому числі каптоприлу, пацієнтами, які отримують внутрішньовенно препарат золота (натрію ауротіомалат), був описаний симптомокомплекс, що включає гіперемію шкіри обличчя, нудоту, блювання, артеріальну гіпотензію.Взаємодія з лікарськими засобамиКаптоприл Одночасне застосування протипоказане. Аліскірен У пацієнтів з цукровим діабетом або порушеннями функції нирок (ШКФ менше 60 мл/хв/1,73 м2) зростає ризик гіперкаліємії, погіршення функції нирок та підвищення частоти серцево-судинної захворюваності та смертності. Одночасне застосування не рекомендується. Аліскірен У пацієнтів, які не мають цукрового діабету або порушення функції нирок, можливе підвищення ризику гіперкаліємії, погіршення функції нирок та підвищення частоти серцево-судинної захворюваності та смертності. Подвійна блокада РААС У літературі повідомлялося, що у пацієнтів із встановленим атеросклеро- тичним захворюванням, серцевою недостатністю або цукровим діабетом з ураженням органів-мішеней, одночасна терапія інгібітором АПФ та антагоністами рецепторів до ангіотензину II (APAII) пов'язана з більш високою частотою розвитку артеріальної гіпо та погіршення функції нирок (включаючи гостру ниркову недостатність) порівняно із застосуванням лише одного препарату, що впливає на РААС. Подвійна блокада (наприклад, при поєднанні інгібітору АПФ з АРАII) повинна бути обмежена окремими випадками з ретельним моніторингом функції нирок, вмісту калію та АТ. У пацієнтів, які приймають діуретичні засоби, каптоприл може потенціювати антигіпертензивну дію. Подібну дію надають також суворе обмеження надходження кухонної солі в організм (безсольові дієти), гемодіаліз. Зазвичай надмірне зниження артеріального тиску відбувається протягом 1-ї години після прийому першої дози каптоприлу. Вазодилататори (наприклад, нітрогліцерин) у поєднанні з каптоприлом слід застосовувати у найнижчих ефективних дозах через ризик надмірного зниження АТ. Зменшує виведення хінідину. норепінефрину, епінефрину та протиподагричних препаратів. Слід бути обережними при одночасному призначенні каптоприлу (без або з діуретиком) та лікарських препаратів, що впливають на симпатичну нервову систему (наприклад, гангліоблокатори, альфаадреноблокатори). При одночасному застосуванні каптоприлу та нестероїдних протизапальних препаратів (НПЗП) може спостерігатися зниження антигіпертензивної дії, особливо при артеріальній гіпертензії, що супроводжується низьким вмістом реніну. У пацієнтів з факторами ризику (літні пацієнти, пацієнти з гіповолемією, які приймають діуретики, з порушенням функції нирок), одночасне застосування нестероїдних протизапальних засобів (включаючи інгібітори циклооксигенази-2 (ЦОГ-2)) та інгібітори АПФ, включаючи каптоприл, може призводити до погіршення функції. , аж до гострої ниркової недостатності Зазвичай порушення функції нирок у разі бувають оборотними. Слід періодично контролювати функцію нирок у пацієнтів, які приймають каптоприл та нестероїдні протизапальні засоби. При терапії каптоприлом калійзберігаючі діуретики (наприклад, тріамтерен, амілорид, спіронолактон та його похідне - еплеренон), препарати калію, калієві добавки, замінники солі (містять великі кількості калію) слід призначати тільки при доведеній гіпокаліємії, т.к. їх одночасне застосування збільшує ризик розвитку гіперкаліємії. При одночасному застосуванні інгібіторів АПФ (особливо у поєднанні з діуретиками) та солей літію можливе збільшення концентрації літію у плазмі крові, і, отже, токсичності препаратів літію. Слід періодично визначати концентрацію літію у плазмі крові. При призначенні каптоприлу на фоні прийому алопуринолу або прокаїнаміду підвищує ризик розвитку нейтропенії та/або синдрому Стівенса-Джонсона. Застосування каптоприлу у пацієнтів, які приймають імунодепресанти (наприклад, циклофосфацин або азатіоприн), збільшує ризик розвитку гематологічних порушень. Інгібітори АПФ, включаючи каптоприл, можуть потенціювати гіпоглікемічний ефект інсуліну та гіпоглікемічних засобів для прийому внутрішньо, наприклад, похідних сульфонілсечовини, що може вимагати зниження дози гіпоглікемічних препаратів при одночасному застосуванні з каптоприлом. Симпатоміметики можуть зменшити антигіпертензивний ефект каптоприлу. Підвищує концентрацію дигоксину у плазмі крові на 15-20%. Збільшує біодоступність пропранололу. Циметидин, сповільнюючи метаболізм у печінці, підвищує концентрацію каптоприлу у плазмі крові. При одночасному застосуванні з тіазидними діуретиками, вазодилататорами (міноксидил), верапамілом, бета-адреноблокаторами, трициклічними антидепресантами або етанолом посилюється антигіпертензивний ефект. Естрамустін Одночасне застосування може призвести до підвищення ризику побічних ефектів, таких як ангіоневротичний набряк. Баклофен Посилює антигіпертензивний ефект інгібіторів АПФ. Слід ретельно контролювати АТ і, у разі потреби, дозування гіпотензивних препаратів. Гліптини (лінагліптин, саксагліптин, ситагліптин, віллдагліптин) Спільне застосування з інгібіторами АПФ може підвищувати ризик розвитку ангіоневротичного набряку внаслідок пригнічення активності дипептидилпептидази IV (ДПП-IV) гліптинами. Препарати золота При застосуванні інгібіторів АПФ, у тому числі каптоприлу, пацієнтами, які отримують внутрішньовенно препарат золота (натрію ауротіомалат), був описаний симптомокомплекс, що включає гіперемію шкіри обличчя, нудоту, блювання, артеріальну гіпотензію. Трициклічні антидепресанти, антипсихотичні засоби (нейролептики) та засоби для загальної анестезії Одночасне застосування з інгібіторами АПФ може призводити до посилення антигіпертензивної дії. Гідрохлоротіазид З тіазидними діуретиками такі лікарські засоби, як етанол, барбітурати та наркотичні засоби можуть потенціювати ризик розвитку ортостатичної гіпотензії. Гіпоглікемічні засоби (для прийому внутрішньо та інсулін) – може знадобитися корекція дози гіпоглікемічних засобів. Інші гіпотензивні засоби – адитивний ефект. Колестирамін і колестипол – у присутності аніонообмінних смол всмоктування гідрохлортіазиду порушується. Колестирамін і колестипол у разовій дозі пов'язують гідрохлортіазид і зменшують його всмоктування у шлунково-кишковому тракті на 85% та 43% відповідно. Кортикостероїди, АКТГ (адренокортикотропний гормон) або гліцирризинова кислота (міститься в корені солодки) – виражене зниження вмісту електролітів, зокрема ризик гіпокаліємії. Пресорні аміни (наприклад, епінефрін, норепінефрін) – зниження вираженості відповіді приймання пресорних амінів. Міорелаксанти недеполяризуючого типу дії (наприклад, тубокурарин) – посилення ефекту міорелаксантів. Літій – діуретики знижують нирковий кліренс літію та підвищують ризик розвитку токсичної дії літію; одночасне застосування не рекомендується. Нестероїдні протизапальні засоби (включаючи інгібітори ЦОГ-2) – можуть знижувати діуретичний, натрійуретичний та антигіпертензивний ефект діуретиків. У деяких пацієнтів з порушенням функції нирок (наприклад, літні пацієнти або пацієнти з зневодненням, у тому числі приймаючі діуретики), які отримують терапію НПЗП, включаючи інгібітори ЦОГ-2, лікування APAII або інгібіторами АПФ, може викликати подальше погіршення функції нирок, включаючи розвиток гострої нирки. ниркової недостатності. Ці ефекти оборотні. Одночасне застосування цих препаратів має проводитися з обережністю у пацієнтів із порушенням функції нирок. У зв'язку з впливом на метаболізм кальцію, їх прийом може спотворювати результати дослідження функції паращитовидних залоз. Лікарські препарати, що застосовуються для лікування подагри (пробенецид, сульфінпіразон та алопуринол): може знадобитися корекція дози урикозуричних препаратів, оскільки гідрохлортіазид може спричинити підвищення концентрації сечової кислоти у сироватці крові. Тіазидні діуретики можуть збільшити частоту розвитку реакцій гіперчутливості на алопуринол. Антихолінергічні препарати (наприклад, атропін, біпериден): збільшують біодоступність тіазидних діуретиків за рахунок зниження моторики шлунково-кишкового тракту та швидкості спорожнення шлунка. Цитостатичні препарати, наприклад, циклофосфамід, метотрексат: збільшується мієлопригнічуюча дія за рахунок уповільнення виведення з організму. Саліцилати – при прийомі високих доз саліцилатів гідрохлортіазид може посилювати їхню токсичну дію на центральну нервову систему. Метилдоп: описані окремі випадки гемолітичної анемії при одночасному застосуванні гідрохлортіазиду та метилдопи. Одночасне застосування циклоспорину збільшує ризик розвитку гіперурикемії та загострення перебігу подагри. Серцеві глікозиди: гіпокаліємія та гіпомагніємія, спричинені застосуванням тіазидних діуретиків, збільшує ризик розвитку аритмій при лікуванні серцевими глікозидами. Солі кальцію – тіазидні діуретики можуть збільшувати вміст кальцію у сироватці крові внаслідок зниження його екскреції. При необхідності застосування препаратів кальцію дозу підбирають під контролем вмісту кальцію у сироватці крові. Вітамін D – підвищує ризик розвитку гіперкальціємії. Вплив на результати лабораторних досліджень – завдяки впливу на екскрецію кальцію тіазиди можуть спотворювати результати досліджень функції паращитовидних залоз. Карбамазепін – збільшує ризик симптоматичної гіпонатріємії. Необхідно контролювати вміст натрію у сироватці крові. Йодмісткі контрастні речовини – при дегідратації, викликаної прийомом діуретиків, підвищується ризик розвитку гострої ниркової недостатності, особливо при введенні високих доз препаратів, що містять йод. Перед введенням подібних засобів пацієнту має бути проведена регідратація. Амфотерицин (для внутрішньовенного введення), проносні засоби стимулюючої дії – гідрохлортіазид може посилювати порушення водно-електролітного балансу, особливо гіпокаліємію. Лікарські препарати, що інтенсивно зв'язуються з білками, посилюють діуретичний ефект. Може знадобитися корекція дози антикоагулянтів для прийому внутрішньо, пробенециду та сульфінпіразону, оскільки гідрохлортіазид може пригнічувати їхню дію.Спосіб застосування та дозиВсередину, незалежно від часу їди, по 1 таблетці 1 раз на добу. Таблетки слід ковтати повністю, не розжовуючи, запиваючи невеликою кількістю рідини.ПередозуванняСимптоми: виражене зниження АТ, шок, ступор, брадикардія, порушення водно-електролітного балансу, ниркова недостатність, летаргія (яка може прогресувати в кому протягом кількох годин), що не супроводжується порушенням водно-електролітного балансу і викликає лише незначне пригнічення функції дихання та серця. Можуть відзначатися подразнення слизової оболонки шлунка та підвищення скоротливої активності шлунково-кишкового тракту. Лікування: промивання шлунка, введення адсорбентів та натрію сульфату протягом 30 хвилин після прийому, 0,9 % розчин натрію хлориду або інших плазмозамінних розчинів, гемодіаліз. При брадикардії або виражених вагусних реакцій – запровадження атропіну. Можливо розглянуто застосування штучного водія ритму. Перитонеальний діаліз є неефективним для виведення каптоприлу з організму.Запобіжні заходи та особливі вказівкиНа початку лікування може спостерігатися надмірне зниження артеріального тиску, особливо у пацієнтів із хронічною серцевою недостатністю, тяжкою формою артеріальної гіпертензії (в т.ч. ниркового генезу) та/або нирковою недостатністю. Перед початком лікування необхідно компенсувати дефіцит іонів натрію та ОЦК (зменшити дозу призначених раніше діуретиків або, в окремих випадках, повністю їх скасувати), а також визначити показники функції нирок. Необхідний регулярний контроль вмісту в плазмі крові іонів калію та кальцію (особливо у пацієнтів, які отримують лікування препаратами наперстянки, глюкокортикостероїдами, що часто користуються проносними, а також у літніх пацієнтів), глюкози, сечової кислоти, ліпідів (холестерину та тригліцеридів) креатиніну, активності "печінкових" ферментів. Особливо ретельний контроль за рівнем артеріального тиску та лабораторними показниками необхідний у таких випадках: у пацієнтів з нирковою недостатністю; пацієнтів з артеріальною гіпертензією тяжкого перебігу (в т.ч. ниркового генезу); у пацієнтів похилого віку (старше 65 років); у пацієнтів з порушеннями водно-електролітного балансу та декомпенсованої ХСН; а також одержують одночасно алопуринол, солі літію, прокаїнамід та лікарські засоби, що знижують імунітет. При прийомі інгібіторів АПФ відзначається характерний непродуктивний кашель, що припиняється після відміни терапії інгібіторами АПФ. У деяких пацієнтів із захворюваннями нирок, особливо з тяжким стенозом ниркових артерій, спостерігається збільшення концентрації азоту сечовини та креатиніну у сироватці крові після зниження артеріального тиску. Це явище зазвичай оборотне, і спостерігається зниження концентрації азоту сечовини та креатиніну у сироватці крові у разі відміни препарату. Може знадобитися зниження дози препарату Гідрохлортіазид + Каптоприл та/або відміни діуретика. У деяких випадках на фоні застосування інгібіторів АПФ спостерігається підвищення вмісту калію у сироватці крові. Ризик розвитку гіперкаліємії при застосуванні інгібіторів АПФ підвищений у пацієнтів з порушенням функції нирок та цукровим діабетом, а також приймають калійзберігаючі діуретики, препарати калію та інших препаратів, що спричиняють збільшення вмісту калію в крові (наприклад, гепарин). Слід уникати одночасного застосування калійзберігаючих діуретиків та препаратів калію. Крім того, при застосуванні інгібіторів АПФ одночасно з тіазидними діуретиками не виключено ризик розвитку гіпокаліємії, тому в таких випадках слід проводити регулярний контроль вмісту калію в крові під час терапії. Слід бути обережними при прийомі інгібіторів АПФ пацієнтами з мітральним/аортальним стенозом/гіпертрофічною обструктивною кардіоміопатією, у разі кардіогенного шоку та гемодинамічно значущої обструкції – прийом не рекомендований. Не рекомендується застосування подвійної блокади РААС, викликаної одночасним застосуванням інгібіторів АПФ та APAII або аліскірену та аліскіренсодержащих препаратів, оскільки вона асоціювалася з підвищеною частотою розвитку побічних ефектів, таких як артеріальна гіпотензія, гіперкаліємія, зниження функції нирок (включаючи гостру). Якщо одночасне застосування інгібіторів АПФ та АРАII (подвійна блокада РААС) необхідне, то лікування має проводитися під контролем лікаря та при здійсненні постійного контролю функції нирок, вмісту електролітів у крові, а також АТ. Не рекомендується одночасне застосування інгібіторів АПФ та АРАІІ у пацієнтів з діабетичною нефропатією. При проведенні гемодіалізу у пацієнтів, які отримують інгібітори АПФ, слід уникати застосування діалізних мембран з високою проникністю (наприклад, AN®69), оскільки в таких випадках підвищується ризик розвитку анафілактоїдних реакцій. Анафілактоїдні реакції відзначалися також у пацієнтів, яким проводилася процедура видалення ліпопротеїнів низької щільності (аферез) шляхом абсорбції за допомогою декстрану сульфату. Слід розглянути питання застосування або гіпотензивних препаратів іншого класу, або іншого типу діалізних мембран. У разі розвитку ангіоневротичного набряку препарат скасовують та здійснюють ретельне медичне спостереження до повного зникнення симптомів. Ангіоневротичний набряк гортані може призвести до смерті. Якщо набряк локалізується на обличчі, спеціального лікування зазвичай не потрібно (для зменшення виразності симптомів можуть бути застосовані антигістамінні препарати), у тому випадку, якщо набряк поширюється на язик, горлянку і є загроза розвитку обструкції дихальних шляхів, слід негайно ввести епінефрин (адреналін) ) підшкірно (0,3-0,5 мл у розведенні 1:1000). У поодиноких випадках у пацієнтів після прийому інгібіторів АПФ відзначався ангіоневротичний набряк кишечника, який супроводжувався болями в черевній порожнині (з нудотою та блюванням або без них).Іноді - при нормальних значеннях активності С-1-естерази та без попереднього набряку особи. Набряк кишечника слід включити до спектру диференціальної діагностики пацієнтів зі скаргами на біль у животі при прийомі інгібіторів АПФ. У представників негроїдної раси випадки розвитку ангіоневротичного набряку відзначалися з більшою частотою порівняно з представниками європеоїдної раси. У двох пацієнтів, які проходять процедуру десенсибілізації отрутою перетинчастокрилих, на фоні прийому каптоприлу відмічені життєзагрозливі анафілактоїдні реакції. При тимчасовому відміні інгібітору АПФ вдалося уникнути анафілактоїдних реакцій. Слід бути обережними при проведенні десенсибілізуючої терапії у пацієнтів, які приймають інгібітори АПФ. У пацієнтів з цукровим діабетом, які отримують гіпоглікемічні препарати для внутрішнього застосування та інсулін, слід ретельно контролювати рівень глікемії, особливо протягом першого місяця терапії інгібіторами АПФ. При проведенні великих хірургічних втручань або при застосуванні засобів для загальної анестезії, які мають антигіпертензивний ефект, у пацієнтів, які приймають інгібітори АПФ, може спостерігатися надмірне зниження артеріального тиску. У таких випадках можна збільшити ОЦК. У поодиноких випадках при прийомі інгібіторів АПФ відзначається синдром, що починається з появи холестатичної жовтяниці, яка переходить у фульмінантний гепатонекроз, іноді з летальним кінцем. Механізм розвитку цього синдрому невідомий. Якщо у пацієнта, який отримує терапію інгібіторами АПФ, розвивається жовтяниця або відзначається тимчасове підвищення активності «печінкових» трансаміназ, слід припинити лікування інгібіторами АПФ та встановити спостереження за пацієнтом. У пацієнтів, які приймають інгібітори АПФ, спостерігалися нейтропенія/агранулоцитоз, тромбоцитопенія та анемія. У пацієнтів з нормальною функцією нирок та без інших порушень, нейтропенія зустрічається рідко. Препарат Гідрохлортіазид + Каптоприл слід застосовувати з обережністю у пацієнтів з аутоімунними захворюваннями сполучної тканини, у пацієнтів, які приймають імуносупресори, алопуринол та прокаїнамід, особливо за наявності наявного раніше порушення функції нирок. У зв'язку з тим, що більшість летальних випадків нейтропенії на тлі інгібіторів АПФ розвивалися у таких пацієнтів, слід контролювати у них кількість лейкоцитів крові перед початком лікування, у перші 3 місяці – кожні 2 тижні, потім – кожні 2 місяці. У всіх пацієнтів слід щомісяця контролювати кількість лейкоцитів у крові у перші 3 місяці після початку терапії, потім – кожні 2 місяці. Якщо кількість лейкоцитів нижче 4000/мкл, показано повторне проведення загального аналізу крові, нижче 1000/мкл – прийом препарату припиняють, продовжуючи спостереження за пацієнтом. Зазвичай відновлення числа нейтрофілів відбувається протягом 2-х тижнів після відміни каптоприлу. У 13% випадків нейтропенії відзначали летальний кінець. Практично у всіх випадках летальний результат спостерігався у пацієнтів із захворюваннями сполучної тканини, нирковою або серцевою недостатністю, на фоні прийому імуносупресорів або при поєднанні обох зазначених факторів. При застосуванні інгібіторів АПФ може відзначатись протеїнурія, в основному у пацієнтів з порушенням функції нирок, а також при застосуванні високих доз препаратів. У більшості випадків протеїнурія при прийомі препарату каптоприл зникала або ступінь її вираженості зменшувалась протягом 6 місяців незалежно від того, припинявся прийом препарату чи ні. Показники функції нирок (концентрації азоту сечовини та креатиніну) у пацієнтів із протеїнурією майже завжди були в межах норми. У пацієнтів із захворюваннями нирок слід визначати вміст білка в сечі перед початком лікування та періодично протягом курсу терапії. При прийомі тіазидних діуретиків було виявлено випадки розвитку агранулоцитозу та пригнічення функції кісткового мозку. Гідрохлортіазид може викликати ідіосинкразічну реакцію, що призводить до розвитку гострої міопії та гострого нападу вторинної глаукоми. Симптоми включають: раптове зниження гостроти зору або біль в очах, які проявляються, як правило, протягом декількох годин або тижнів від початку терапії гідрохлортіазидом. За відсутності лікування гостра глаукома може призвести до стійкої втрати зору. Лікування: якнайшвидше припинити прийом гідрохлортіазиду. Якщо внутрішньоочний тиск залишається неконтрольованим, може знадобитися невідкладне медикаментозне лікування або хірургічне втручання. Факторами ризику гострої глаукоми є: алергічна реакція на сульфонаміди або пеніцилін в анамнезі. У всіх пацієнтів, які приймають тіазидні діуретики, слід виявляти клінічні ознаки порушення водно-електролітного балансу (гіпонатріємія, гіпохлоремічний алкалоз, гіпокаліємія). Особливо важливо визначати вміст електролітів у сироватці крові та сечі при сильному блюванні або при введенні інфузійних розчинів. Ознаками порушень водно-електролітного балансу можуть бути сухість слизової оболонки порожнини рота, спрага, слабкість, летаргія, сплутаність свідомості, занепокоєння, болі або судоми в м'язах, м'язова слабкість, надмірне зниження артеріального тиску, олігоурія, тахікардія, нудота. Гіпокаліємія може спровокувати або посилити кардіотоксичну дію серцевих глікозидів. У пацієнтів з набряками при спекотній погоді може спостерігатись гіпонатріємія, спричинена збільшенням ОЦК. Слід обмежити споживання рідини.У випадках життєзагрозливої гіпонатріємії призначають прийом кухонної солі. Під час терапії тіазидними діуретиками можуть спостерігатися гіперурикемія або загострення перебігу подагри; може також проявитися цукровий діабет, що латентно протікає. Тіазидні діуретики можуть викликати зниження концентрації пов'язаного йоду у сироватці крові без ознак порушення функції щитовидної залози. На фоні прийому тіазидних діуретиків знижується рівень виведення кальцію; відзначалися випадки патологічних змін паращитовидних залоз, що супроводжуються гіперкальціємією та гіпофосфатемією. Перед дослідженням функції паращитовидних залоз слід припинити прийом тіазидних діуретиків. На фоні прийому тіазидних діуретиків відзначалося підвищення екскреції магнію, що може призводити до гіпомагніємії. Препарат може викликати хибнопозитивну реакцію при аналізі сечі на ацетон та спотворювати результати тесту з бентиромідом. При появі лихоманки, збільшення лімфатичних вузлів та/або ознак ларингіту та/або фарингіту необхідно негайно визначити кількість лейкоцитів. Спортсменів слід поінформувати, що препарат містить гідрохлоротіазид, який може давати хибнопозитивні результати при проведенні допінг-контролю. Вплив на здатність керувати транспортними засобами та заняття іншими потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій На тлі прийому препарату слід дотримуватися обережності при керуванні транспортними засобами, роботі з механізмами та зайняттям інших потенційно небезпечних видів діяльності, що потребують підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаВодорості фукус сушені харчові подрібнені.ХарактеристикаЄ додатковим джерелом природного йоду, мікро- та макроелементів, амінокислот, полісахароз та волокон. Містить до 18% фукоїдану. Використовується для профілактики йодної недостатності, підвищення гостроти зору, захисту населення, що проживає на територіях з підвищеним радіаційним фоном. Фукус має антиатеросклеротичну, протизапальну, протимікробну, ранозагоювальну та ендоекологічну дію на організм. Він підвищує активність ферментів, що беруть участь у перетворенні холестерину на жовчні кислоти, перешкоджає відкладенню холестерину в стінках судин без порушення його біосинтезу, дозволяючи виключити негативні наслідки цього процесу. Фукус ефективний при запальних захворюваннях сечостатевої системи, при дисбактеріозі – пригнічує ріст патогенної мікрофлори. Компоненти водорості стимулюють регенеративні процеси, сприяючи грануляції тканин, епітелізації та рубцювання ран та виразок. Поєднання антиоксидантної дії біологічно активних компонентів водорості з ентеросорбційним ефектом альгінової кислоти забезпечує радіопротекторну та детоксикувальну дію, включаючи виведення з організму важких металів, у тому числі свинцю, ртуті та радіонуклідів. Фукус має також антикоагулянтну дію, сприяє нормалізації судинної проникності. Містить йод 300-800 мкг у рекомендованій добовій дозі (1/2 чайної ложки – 1 г) – 30-80% від норми добового споживання з урахуванням часткової засвоюваності йоду згідно з ТР ТС 022/2011. Порошок дрібнодисперсний, світло-коричневого кольору.ІнструкціяДля профілактики достатньо використовувати по 1 ч. л. до 3-х р. в день. Можна сушені трави розжовувати, запиваючи водою, або додавати до улюблених страв, попередньо подрібнивши. Для зовнішнього застосування водорості наполягають на протязі. 30 хвилин.РекомендуєтьсяРекомендується як біологічно активна добавка до їжі - додаткового джерела йоду.Протипоказання до застосуванняІндивідуальна непереносимість компонентів продукту, підвищена чутливість до йоду, при яких протипоказані препарати йоду.Запобіжні заходи та особливі вказівкиБіологічно активна добавка до їжі. Чи не є лікарським засобом. Перед застосуванням рекомендується проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
754,00 грн
686,00 грн
Склад, форма випуску та упаковкаWater, Vitis vinifera (Grape seed) oil, Emulsifying wax, Harpogophytum procumbens (Devil's Claw) root extract, Propylen glycol, Ricinus communis oil, Linum usitassimum (Linceed) oil, Syringa vulgaris flower/ Glycerine, Cyclopentasiloxane, Panthenol, Camphor, Horse chestnut seed extract, Benzyl alcohol, Ethylhexylglicerin, Sodium carbomer, Sodium polyacrylate, Phenoxyethanol, Methyl paraben, Ethyl paraben, Propyl paraben, Ecopylus Butylhydroxytoluol, Propylgallate, Citric acid.ХарактеристикаОснова крему забезпечує гарний розподіл на шкірі, швидке вбирання та ефективне проникнення діючих речовин. Властивості компонентів допомагають справлятися з проявами запального характеру при загостренні недуги, сприяють зниженню м'язової напруги та покращенню рухливості та гнучкості у суглобах. Екстракти мартинії запашної, бузку, кінського каштану, що входять до оригінального складу, забезпечують посилення циркуляції рідини в тканинах, надають тонізуючу дію, сприяють зниженню набряклості. Д-пантенол, вітамін Е, лляна олія активно насичують епідерміс поживними речовинами, вирівнюють та покращують рельєф шкіри. Камфора при місцевому застосуванні має відволікаючу дію, знімає неприємні відчуття.ІнструкціяНаносити регулярно тонким шаром м'якими, що масажують рухами до повного вбирання.РекомендуєтьсяМістить екстракт кореня африканської рослини Мартінія запашна - протиподагричний засіб.Протипоказання до застосуванняІндивідуальна нестерпність компонентів.Запобіжні заходи та особливі вказівкиПеред застосуванням слід проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
299,00 грн
251,00 грн
Склад, форма випуску та упаковкаПігулки - 1 таб. активні речовини: лізиноприлу дигідрат 21,8 мг (еквівалентно лізиноприлу 20 мг), гідрохлортіазид 12,5 мг; маннітол 40 мг, кальцію фосфату дигідрат 114 мг, крохмаль кукурудзяний 31 мг, крохмаль прежелатинізований 4 мг, магнію стеарат 1,5 мг. Пігулки, 12,5 мг +20 мг. По 14 таблеток у блістер із ПВХ-алюмінієвої фольги. По 2 блістери в картонній пачці разом із інструкцією із застосування.Опис лікарської формиКруглі, двоопуклі таблетки білого кольору, з ризиком на одній стороні.Фармакотерапевтична групаГіпотензивний засіб комбінований (діуретик+АПФ інгібітор).ФармакокінетикаГідрохлоротіазид Всмоктування та розподіл Гідрохлортіазид неповно, проте досить швидко всмоктується із шлунково-кишкового тракту (ЖКТ). Після прийому внутрішньо в дозі 100 мг максимальна концентрація гідрохлортіазиду в плазмі досягається через 1,5-2,5 год. На максимумі діуретичної активності (приблизно через 4 год після прийому) концентрація гідрохлортіазиду в плазмі становить 2 мкг/мл. Зв'язок із білками плазми становить 40%. Гідрохлортіазид проникає через плацентарний бар'єр і грудне молоко, не проникає через гематоенцефалічний бар'єр. Метаболізм Гідрохлоротіазид в організмі людини не метаболізується. Виведення Первинний шлях виведення – нирками (фільтрація та секреція) у незміненому вигляді. Приблизно 61% прийнятої внутрішньо дози виводиться протягом 24 годин. У пацієнтів з нормальною нирковою функцією період напіввиведення становить від 5,6 до 14,8 години (в середньому 6,4 години). Фармакокінетика в спеціальних групах пацієнтів Порушення функції нирок У пацієнтів з помірною нирковою недостатністю період напіввиведення гідрохлортіазиду становить у середньому 11,5 год, а у пацієнтів з кліренсом креатиніну (КК) менше 30 мл/хв – 20,7 год. Лізіноприл Абсорбція Абсорбція лізиноприлу становить у середньому 25-30% при значній міжіндивідуальній варіабельності (6-60%). Їда не впливає на всмоктування лізиноприлу. Час досягнення максимальної концентрації у плазмі крові (ТСmах) становить приблизно 7 год; у пацієнтів з ГІМ ТСmах становить 8-10 год. Розподіл У незміненому вигляді потрапляє до системного кровообігу. Лізиноприл не зв'язується з білками плазми (за винятком циркулюючого АПФ). Проникність через гематоенцефалічний та плацентарний бар'єр низька. Метаболізм Лізиноприл не піддається метаболізму. Виведення Лізиноприл виводиться нирками у незміненому вигляді. Фракція, пов'язана з АПФ, виводиться повільно. Кліренс лізиноприлу у здорових добровольців становить приблизно 50 мл/хв. Після багаторазового прийому ефективний період напіввиведення лізиноприлу становить 12,6 год. Фармакокінетика в особливих клінічних випадках Хронічна серцева недостатність У пацієнтів із ХСН абсолютна біодоступність лізиноприлу знижується приблизно на 16%; однак AUC (площа під кривою "концентрація-час") збільшується в середньому на 125% порівняно зі здоровими добровольцями. Порушення функції нирок У пацієнтів з нирковою недостатністю спостерігається підвищена концентрація лізиноприлу в плазмі крові, відзначається збільшення ТСmах та збільшення періоду напіввиведення. Порушення функції нирок призводить до збільшення AUC та періоду напіввиведення лізиноприлу, але ці зміни стають клінічно значущими лише тоді, коли швидкість клубочкової фільтрації (СКФ) знижується нижче 30 мл/хв/1,73 м2 площі поверхні тіла. При легкій та помірній нирковій недостатності (КК від 31 до 80 мл/хв) середнє значення AUC збільшується на 13%, у той час як при тяжкій нирковій недостатності (КК від 5 до 30 мл/хв) спостерігається збільшення середнього значення AUC у 4, 5 разів. Порушення функції печінки У пацієнтів з цирозом печінки біодоступність лізиноприлу знижена приблизно на 30%, проте експозиція препарату (AUC) збільшується на 50% порівняно зі здоровими добровольцями через зниження кліренсу. Літній вік У пацієнтів похилого віку (старше 65 років) концентрація лізиноприлу в плазмі крові та AUC у 2 рази вища, ніж у пацієнтів молодого віку.ФармакодинамікаГіпотензивний комбінований засіб. Має гіпотензивну та діуретичну дію. Гідрохлоротіазид Механізм дії тіазидних діуретиків (тіазидів) не повністю вивчений. Тіазиди блокують реабсорбцію іонів натрію та хлору на початку ниркових канальців. Таким чином, вони збільшують екскрецію натрію та хлору і, отже, виведення води з організму. Внаслідок сечогінної дії гідрохлортіазиду зменшується об'єм циркулюючої рідини, внаслідок чого збільшується активність реніну та вміст альдостерону у плазмі крові. Це призводить до збільшення екскреції іонів калію із сечею та зниження вмісту калію в крові (гіпокаліємії). Гідрохлортіазид також збільшує екскрецію іонів магнію та знижує екскрецію іонів кальцію із сечею. Тіазидні діуретики знижують екскрецію сечової кислоти нирками та збільшують її вміст у крові. Тіазидні діуретики також зменшують активність карбоангідрази шляхом посилення виведення іонів бікарбонату. Але ця дія зазвичай проявляється слабо і не впливає на рН сечі. У максимальних терапевтичних дозах діуретичний/натрійуретичний ефект усіх тіазидних діуретиків приблизно однаковий. Натріурез і діурез наступають протягом 2 годин і досягають максимуму через 4 год. Тривалість діуретичної дії гідрохлортіазиду становить від 6 до 12 год. Гідрохлортіазид має антигіпертензивну дію. На нормальний артеріальний тиск (АТ) тіазидні діуретики не впливають. Лізіноприл Лізиноприл - інгібітор ангіотензинперетворюючого ферменту (АПФ). Зменшує утворення ангіотензину ІІ з ангіотензину І. Зниження вмісту ангіотензину ІІ веде до прямого зменшення виділення альдостерону. Зменшує деградацію брадикініну та збільшує синтез простагландинів. Знижує загальний периферичний судинний опір, артеріальний тиск, переднавантаження, тиск у легеневих капілярах, викликає збільшення хвилинного об'єму крові та підвищує толерантність міокарда до навантажень у пацієнтів з хронічною серцевою недостатністю (ХСН). Розширює артерії більшою мірою, ніж вени. Деякі ефекти пояснюються впливом на тканинну ренін-ангіотензинову систему. При тривалому застосуванні зменшується гіпертрофія міокарда та стінок артерій резистивного типу. Покращує кровопостачання ішемізованого міокарда. Початок антигіпертензивної дії - через 1 годину. Максимальний ефект спостерігається через 6-7 годин і зберігається протягом 24 годин. Тривалість ефекту також залежить від величини дози. При артеріальній гіпертензії ефект відзначається у перші дні після початку лікування, стабільна дія розвивається через 1-2 місяці. При різкій відміні лізиноприлу не спостерігається вираженого підвищення артеріального тиску. Інгібітори АПФ подовжують тривалість життя у пацієнтів із ХСН, уповільнюють прогресування дисфункції лівого шлуночка у пацієнтів, які перенесли інфаркт міокарда, без клінічних проявів серцевої недостатності. Оцінка ефективності та безпеки лізиноприлу (до 10 мг на добу) проводилася у пацієнтів із гострим інфарктом міокарда (ГІМ). Лізиноприл, призначений у перші 24 години після ГІМ, протягом 6 тижнів призводив до статистично значущого зниження загальної смертності на 11%. Крім зниження артеріального тиску лізиноприл зменшує альбумінурію. Прийом 10-20 мг лізиноприлу 1 раз на добу протягом 12 місяців у пацієнтів з артеріальною гіпертензією та цукровим діабетом 2 типу з початковою стадією нефропатії, що проявляється як мікроальбумінурія, знижував систолічний/діастолічний артеріальний тиск на 13/10 мм рт. ст., а екскрецію альбуміну із сечею на 40%. У пацієнтів із гіперглікемією сприяє нормалізації функції пошкодженого гломерулярного ендотелію. Лізиноприл не впливає на концентрацію глюкози в крові у пацієнтів із цукровим діабетом і не призводить до почастішання випадків гіпоглікемії.Показання до застосуванняАртеріальна гіпертензія (у пацієнтів, яким показано комбіновану терапію).Протипоказання до застосуванняПідвищена чутливість до гідрохлортіазиду, інших похідних сульфонаміду, лізиноприлу, інших інгібіторів АПФ та/або будь-якої з допоміжних речовин препарату; ангіоневротичний набряк в анамнезі, у тому числі на фоні застосування інгібіторів АПФ; спадковий або ідіопатичний ангіоневротичний набряк; тяжка ниркова недостатність (КК менше 30 мл/хв); анурія; тяжка печінкова недостатність або печінкова енцефалопатія (ризик розвитку печінкової коми); рефрактерна гіпокаліємія, гіпонатріємія, гіперкальціємія; одночасне застосування з аліскіреном та препаратами, що містять аліскірен, у пацієнтів з цукровим діабетом або помірним, або тяжким порушенням функції нирок (СКФ одночасне застосування з антагоністами рецепторів ангіотензину II (АРА II) у пацієнтів з діабетичною нефропатією; вагітність; період грудного вигодовування; дитячий вік до 18 років. Обережно: артеріальна гіпотензія, двосторонній стеноз ниркових артерій або стеноз артерії єдиної нирки; реноваскулярна гіпертензія; порушення функції нирок легкого та помірного ступеня тяжкості; стан після трансплантації нирки; аортальний стеноз, мітральний стеноз, гіпертрофічна обструктивна кардіоміопатія; хронічна серцева недостатність; ішемічна хвороба серця чи цереброваскулярні захворювання; системні захворювання сполучної тканини (системний червоний вовчак, склеродермія та ін.), пригнічення кістковомозкового кровотворення, імуносупресивна терапія, одночасне застосування алопуринолу або прокаїнаміду, або комбінація зазначених ускладнюючих факторів (ризик розвитку нейтропенії та агранулоцит); порушення функції печінки легкого та помірного ступеня тяжкості, що прогресують захворювання печінки; цукровий діабет;гіперкаліємія; одночасне застосування з калійзберігаючими діуретиками, препаратами калію, калійвмісними замінниками харчової солі; одночасне застосування з препаратами літію; обтяжений алергологічний анамнез; одночасне проведення десенсибілізації алергеном з отрути перетинчастокрилих; одночасне проведення процедури аферезу ліпопротеїнів низької щільності (ЛПНЩ-аферезу) з використанням декстран сульфату; гемодіаліз із використанням високопроточних мембран (таких як AN69®); стани, що супроводжуються зниженням обсягу циркулюючої крові (ОЦК) (у тому числі при терапії діуретиками, дотриманні дієти з обмеженням кухонної солі, діалізі, діареї або блювоті); застосування під час великих хірургічних втручань або проведення загальної анестезії; гіпокаліємія; гіпонатріємія; гіперкальціємія; збільшення інтервалу QT на ЕКГ;одночасне застосування лікарських засобів, які можуть викликати поліморфну шлуночкову тахікардію типу "пірует" або збільшувати тривалість інтервалу QT на ЕКГ; одночасне застосування лікарських засобів, здатних викликати гіпокаліємію, серцевих глікозидів; алергічні реакції на пеніцилін в анамнезі; гіперпаратиреоз; гіперурикемія, подагра; застосування у пацієнтів негроїдної раси; застосування у пацієнтів похилого віку (старше 65 років).застосування у пацієнтів негроїдної раси; застосування у пацієнтів похилого віку (старше 65 років).застосування у пацієнтів негроїдної раси; застосування у пацієнтів похилого віку (старше 65 років).Вагітність та лактаціяЗастосування препарату під час вагітності та у період грудного вигодовування протипоказане. Гідрохлоротіазид Вагітність Існує обмежений досвід застосування гідрохлортіазиду під час вагітності (особливо у першому триместрі). Доклінічні дані щодо безпеки недостатні. Гідрохлортіазид проникає через плацентарний бар'єр і визначається пуповинної крові. З урахуванням механізму фармакологічної дії гідрохлортіазиду, його застосування у другому та третьому триместрах вагітності може порушувати фетоплацентарну перфузію та призводити до розвитку у плода та новонародженого таких ускладнень, як жовтяниця, порушення водно-електролітного балансу та тромбоцитопенія. Описано випадки розвитку тромбоцитопенії у новонароджених, матері яких отримували тіазидні діуретики. Застосування гідрохлортіазиду під час вагітності протипоказане. Гідрохлортіазид не можна застосовувати для лікування гестозів ІІ половини вагітності (набряків, артеріальної гіпертензії або прееклампсії), т.к. він збільшує ризик зниження ОЦК та плацентарної гіпоперфузії, але не надає сприятливого впливу протягом зазначених ускладнень вагітності. Діуретики не запобігають розвитку гестозів. Період грудного вигодовування Гідрохлортіазид проникає в материнське молоко, у зв'язку з чим його застосування у період грудного вигодовування протипоказане. Якщо застосування гідрохлортіазиду в період грудного вигодовування є абсолютно необхідним, слід припинити грудне вигодовування. Лізіноприл Вагітність Застосування лізиноприлу під час вагітності у жінок, які планують вагітність, а також у жінок із збереженим репродуктивним потенціалом, які не застосовують надійні методи контрацепції, протипоказано. При встановленні вагітності прийом препарату слід припинити якомога раніше. Лізиноприл проникає крізь плаценту. Даних про негативні впливи лізиноприлу на плід у разі застосування під час першого триместру вагітності немає. Прийом інгібіторів АПФ у II та III триместрі вагітності надає несприятливий вплив на плід (можливі виражене зниження артеріального тиску, ниркова недостатність, гіперкаліємія, гіпоплазія кісток черепа, внутрішньоутробна смерть). За новонародженими та грудними дітьми, які зазнали внутрішньоутробного впливу інгібіторів АПФ, рекомендується вести ретельне спостереження для своєчасного виявлення вираженого зниження АТ,олігурії, гіперкаліємії. Якщо з II триместру вагітності мало місце внутрішньоутробна дія інгібіторів АПФ, рекомендується проведення ультразвукового дослідження (УЗД) нирок та кісток черепа. Період грудного вигодовування Немає даних про проникнення лізиноприлу у грудне молоко. На період лікування лізиноприлом необхідно припинити грудне вигодовування.Побічна діяЧастота виникнення небажаних реакцій визначалася відповідно до класифікації Всесвітньої Організації Охорони Здоров'я: дуже часто (≥ 1/10); часто (≥ 1/100 та Порушення з боку крові та лімфатичної системи: рідко – пригнічення кістковомозкового кровотворення, лейкопенія, нейтропенія, агранулоцитоз, тромбоцитопенія, анемія, гемолітична анемія, лімфаденопатія. Порушення з боку імунної системи: рідко – аутоімунні захворювання. Порушення з боку ендокринної системи: рідко – синдром неадекватної секреції антидіуретичного гормону. Порушення з боку обміну речовин та харчування: дуже рідко – гіпоглікемія. Порушення психіки: нечасто – зміна настрою, порушення сну, галюцинації; рідко – психічний розлад, сплутаність свідомості, сонливість; частота невідома – депресія. Порушення з боку нервової системи: часто – запаморочення, головний біль; нечасто – вертиго, парестезія, дизгевзія, порушення нюху; частота невідома - непритомність. Порушення з боку серця: нечасто – інфаркт міокарда (внаслідок вираженого зниження артеріального тиску у груп пацієнтів підвищеного ризику), тахікардія, прискорене серцебиття, біль у грудях. Порушення з боку судин: часто – виражене зниження артеріального тиску, ортостатична гіпотензія; нечасто – гостре порушення мозкового кровообігу (внаслідок вираженого зниження АТ у груп пацієнтів підвищеного ризику), синдром Рейно. Порушення з боку дихальної системи, органів грудної клітки та середостіння: часто – кашель; нечасто – риніт; дуже рідко – бронхоспазм, задишка, алергічний альвеоліт/еозинофільна пневмонія, синусит. Порушення з боку шлунково-кишкового тракту: часто – діарея, блювання; нечасто – біль у животі, нудота, диспепсія; рідко – сухість слизової оболонки порожнини рота; дуже рідко – панкреатит, інтестинальний ангіоневротичний набряк, анорексія. Порушення з боку печінки та жовчовивідних шляхів: дуже рідко – печінкова недостатність, гепатит, жовтяниця (гепатоцелюлярна або холестатична). Порушення з боку шкіри та підшкірних тканин: нечасто - шкірний висип, свербіж шкіри; рідко - кропив'янка, псоріаз, алопеція, ангіоневротичний набряк обличчя, кінцівок, губ, язика, надгортанника та/або гортані; дуже рідко – токсичний епідермальний некроліз (синдром Лайєлла), синдром Стівенса-Джонсона, багатоформна еритема, вульгарна пухирчатка, псевдолімфома шкіри, підвищене потовиділення (гіпергідроз). Повідомлялося про симптомокомплекс, який може включати один або кілька з наступних симптомів - лихоманка, васкуліт, міалгія, артралгія/артрит, позитивна реакція на антинуклеарні антитіла (АНА), збільшення швидкості осідання еритроцитів (ШОЕ), еозинофілія та я інші зміни з боку шкіри. Порушення з боку скелетно-м'язової та сполучної тканини: рідко – м'язові судоми, біль у спині, біль у кінцівках. Порушення з боку нирок та сечовивідних шляхів: часто – порушення функції нирок; рідко – гостра ниркова недостатність, уремія; дуже рідко – анурія, олігурія, протеїнурія. Порушення з боку статевих органів та молочної залози: нечасто – імпотенція; рідко – гінекомастія, сексуальна дисфункція. Загальні розлади: нечасто – підвищена стомлюваність, астенія. Лабораторні та інструментальні дані: нечасто – гіперкаліємія, підвищення концентрації сечовини у крові, підвищення концентрації креатиніну в крові, підвищення активності “печінкових” трансаміназ; рідко – зниження гемоглобіну, зниження гематокриту, гіпербілірубінемія, гіпонатріємія.Взаємодія з лікарськими засобамиГідрохлоротіазид Нерекомендовані поєднання лікарських засобів Препарати літію При одночасному застосуванні гідрохлортіазиду та препаратів літію знижується нирковий кліренс літію, що може призвести до підвищення концентрації літію у плазмі крові та збільшення його токсичності. При необхідності одночасного застосування гідрохлортіазиду слід ретельно підбирати дозу препаратів літію, регулярно контролювати концентрацію літію у плазмі крові та відповідним чином підбирати дозу препарату. Поєднання лікарських засобів, що вимагають особливої уваги Препарати, здатні викликати поліморфну шлуночкову тахікардію типу "пірует" Слід з особливою обережністю застосовувати гідрохлортіазид одночасно з такими препаратами, як: антиаритмічні лікарські препарати ІА класу (хінідин, гідрохінідин, дизопірамід, прокаїнамід); антиаритмічні лікарські препарати ІІІ класу (дофетилід, ібутилід, бретилія тозилат), соталол, дронедарон, аміодарон; інші (неантіаритмічні) лікарські засоби, такі як: нейролептики: фенотіазини (хлорпромазин, ціамемазин, левомепромазин, тіоридазин, трифлуоперазин, флуфеназин), бензаміди (амісульприд, сультоприд, сульприд, тіаприд), бутирофенони (дроперидол, галоперидол); пімозід, сертиндол; антидепресанти: трициклічні антидепресанти, селективні інгібітори зворотного захоплення серотоніну (циталопрам, есциталопрам); антибактеріальні засоби: фторхінолони (левофлоксацин, моксифлоксацин, спарфлоксацин, ципрофлоксацин); макроліди (еритроміцин при внутрішньовенному введенні, азитроміцин, кларитроміцин, рокситроміцин, спіраміцин), ко-тримоксазол; протигрибкові засоби: азоли (воріконазол, ітраконазол, кетоконазол, флуконазол); протималярійні засоби (хінін, хлорохін, мефлохін, галофантрин, лумефантрін); протипротозойні засоби (пентамідин при парентеральному введенні); антиангінальні засоби (ранолазин, беприділ); протипухлинні засоби (вандетаніб, миш'яку триоксид, оксаліплатин, такролімус); протиблювотні засоби (домперидон, ондансетрон); засоби, що впливають на моторику ШКТ (цизаприд); антигістамінні засоби (астемізол; терфенадин; мізоластин); інші лікарські засоби (анагрелід, вазопресин, дифеманілу метилсульфат, кетансерин, пробукол, пропофол, севофлуран, терліпресин, теродилін, цилостазол); у зв'язку із збільшенням ризику шлуночкових аритмій, особливо поліморфної шлуночкової тахікардії типу "пірует" (фактор ризику – гіпокаліємія). Слід визначити вміст калію в плазмі крові та, при необхідності, коригувати його до початку комбінованої терапії гідрохлортіазидом із зазначеними вище препаратами. Необхідний контроль клінічного стану пацієнта, вмісту електролітів плазми крові та показників ЕКГ. У пацієнтів з гіпокаліємією необхідно застосовувати препарати, що не викликають поліморфної шлуночкової тахікардії типу "пірует". Лікарські засоби, здатні збільшувати тривалість інтервалу QT Одночасне застосування гідрохлортіазиду з лікарськими препаратами, здатними збільшувати тривалість інтервалу QT, має ґрунтуватися на ретельній оцінці для кожного пацієнта співвідношення очікуваної користі та потенційного ризику (можливе збільшення ризику розвитку поліморфної шлуночкової тахікардії типу "пірует"). При застосуванні таких комбінацій необхідно регулярно реєструвати ЕКГ (для виявлення подовження інтервалу QT), а також контролювати вміст калію в крові. Препарати, здатні викликати гіпокаліємію: амфотерицин В (при внутрішньовенному введенні), глюко- та мінералокортикостероїди (при системному застосуванні), тетракозактид (АКТГ), гліциризинова кислота (карбеноксолон, препарати, що містять корінь солодки), проносні засоби, Збільшення ризику розвитку гіпокаліємії при одночасному застосуванні з гідрохлортіазидом (адитивний ефект). Необхідний регулярний контроль вмісту калію у плазмі крові, за необхідності – його корекція. На тлі терапії гідрохлортіазидом рекомендується застосовувати проносні засоби, що не стимулюють моторику кишечника. Серцеві глікозиди Гіпокаліємія та гіпомагніємія, зумовлені дією тіазидних діуретиків, посилюють токсичність серцевих глікозидів. При одночасному застосуванні гідрохлортіазиду та серцевих глікозидів слід регулярно контролювати концентрацію калію в плазмі крові, показники ЕКГ та, за необхідності, коригувати терапію. Поєднання лікарських препаратів, які потребують уваги Інші гіпотензивні препарати Потенціювання антигіпертензивної дії гідрохлоротіазиду (адитивний ефект). Може виникнути необхідність корекції дози одночасно застосовуваних гіпотензивних препаратів. Рекомендується припинити прийом гідрохлортіазиду за 2-3 дні до початку терапії інгібіторами АПФ для запобігання розвитку симптоматичної артеріальної гіпотензії. Якщо це неможливо, слід зменшити початкову дозу інгібіторів АПФ. Етанол, барбітурати, антипсихотичні засоби (нейролептики), антидепресанти, анксіолітики, наркотичні анальгетики та засоби для загальної анестезії Можливе посилення антигіпертензивної дії гідрохлортіазиду та потенціювання ортостатичної гіпотензії (адитивний ефект). Недеполяризуючі міорелаксанти (наприклад, тубокурарин) Можливе посилення ефекту недеполяризуючих міорелаксантів. Адреноміметики (пресорні аміни) Гідрохлоротіазид може знижувати ефект адреноміметиків, таких як епінефрин (адреналін) та норепінефрин (норадреналін). Нестероїдні протизапальні препарати (НПЗН), включаючи селективні інгібітори циклооксигенази-2 (ЦОГ-2) та високі дози ацетилсаліцилової кислоти (>3 г/добу) НПЗЗ можуть знижувати діуретичну та антигіпертензивну дії гідрохлортіазиду. При одночасному застосуванні існує ризик розвитку гострої ниркової недостатності внаслідок зниження швидкості клубочкової фільтрації. Гідрохлортіазид може посилювати токсичну дію високих доз саліцилатів на центральну нервову систему. Пероральні гіпоглікемічні засоби та інсулін Тіазидні діуретики впливають на толерантність до глюкози (можливий розвиток гіперглікемії) та знижують ефективність гіпоглікемічних засобів (може знадобитися корекція дози гіпоглікемічних засобів). Слід з обережністю спільно застосовувати гідрохлортіазид та метформін у зв'язку з ризиком розвитку лактоацидозу на фоні порушення функції нирок, спричиненого гідрохлортіазидом. Бета-адреноблокатори, діазоксид Одночасне застосування тіазидних діуретиків (включаючи гідрохлортіазид), з бета-адреноблокаторами або діазоксидом може збільшити ризик розвитку гіперглікемії. Лікарські препарати, що застосовуються для лікування подагри (пробенецид, сульфінпіразон, алопуринол) Може знадобитися корекція дози урикозуричних лікарських засобів, оскільки гідрохлортіазид збільшує концентрацію сечової кислоти у сироватці крові. Тіазидні діуретики можуть збільшити частоту розвитку реакцій гіперчутливості до алопуринолу. Амантадін Тіазидні діуретики (включаючи гідрохлортіазид) можуть знижувати кліренс амантадину, призводити до підвищення концентрації амантадину в плазмі та збільшувати ризик його небажаних ефектів. Антихолінергічні препарати (холіноблокатори) Антихолінергічні препарати (наприклад, атропін, біпериден) збільшують біодоступність тіазидних діуретиків за рахунок зниження моторики шлунково-кишкового тракту та швидкості спорожнення шлунка. Цитотоксичні (протипухлинні) препарати Тіазидні діуретики зменшують ниркову екскрецію цитотоксичних лікарських засобів (наприклад, циклофосфаміду та метотрексату) та потенціюють їхню мієлосупресивну дію. Метилдопа Описано випадки гемолітичної анемії при одночасному застосуванні гідрохлортіазиду та метилдопи. Карбамазепін Ризик розвитку симптоматичної гіпонатріємії. При одночасному застосуванні гідрохлортіазиду та карбамазепіну необхідне спостереження за станом пацієнта та контроль вмісту натрію у плазмі крові. Циклоспорин При одночасному застосуванні тіазидних діуретиків та циклоспорину збільшується ризик розвитку гіперурикемії та загострення подагри. Пероральні антикоагулянти Тіазидні діуретики можуть зменшувати ефект пероральних антикоагулянтів. Йодмісткі контрастні речовини Зневоднення організму на фоні прийому тіазидних діуретиків збільшує ризик розвитку гострої ниркової недостатності, особливо при застосуванні високих доз йодовмісних контрастних речовин. Перед застосуванням йодовмісних контрастних речовин необхідно компенсувати втрату рідини. Препарати кальцію При одночасному застосуванні можливе підвищення вмісту кальцію в крові та розвиток гіперкальціємії внаслідок зниження виведення іонів кальцію нирками. Якщо необхідне одночасне призначення кальцієвмісних лікарських засобів, слід контролювати вміст кальцію в плазмі крові і коригувати дозу препаратів кальцію. Аніонні обмінні смоли (колестирамін та колестипол) Аніонні обмінні смоли зменшують абсорбцію гідрохлортіазиду. Одноразові дози колестираміну та колестиполу зменшують всмоктування гідрохлортіазиду у ШКТ на 85% та 43% відповідно. Лізіноприл Подвійна блокадаренін-ангіотензин-альдостеронова система (РААС) У пацієнтів з атеросклеротичним захворюванням, серцевою недостатністю або цукровим діабетом з ураженням органів-мішеней, одночасна терапія інгібітором АПФ та АРА II пов'язана з вищою частотою розвитку артеріальної гіпотензії, непритомності, гіперкаліємії та погіршення функції нирок (включаючи гостру по лише одного препарату, що впливає на РААС. Подвійна блокада (наприклад, при поєднанні інгібітору АПФ з АРА II) повинна бути обмежена окремими випадками з ретельним моніторингом функції нирок, вміст калію та регулярним контролем АТ. Одночасне застосування інгібіторів АПФ з лікарськими засобами, що містять аліскірен, протипоказане у пацієнтів з цукровим діабетом та/або з помірною або тяжкою нирковою недостатністю (ШКФ менше 60 мл/хв/1,73 м2 площі поверхні тіла) та не рекомендується у інших пацієнтів. Одночасне застосування інгібіторів АПФ з АРА II протипоказане у пацієнтів з діабетичною нефропатією та не рекомендується у інших пацієнтів. Калійзберігаючі діуретики, препарати калію, замінники харчової солі та інші лікарські препарати, що здатні збільшувати вміст калію в сироватці крові. При одночасному застосуванні лізиноприлу з калійзберігаючими діуретиками (спіронолактон, тріамтерен, амілорид, еплеренон), препаратами калію або калійвмісними замінниками харчової кухонної солі та іншими лікарськими препаратами, здатними збільшувати вміст калію в сироватці крові (включаючи антагоністи, препарати, що містять котримоксазол (триметоприм + сульфаметоксазол), підвищується ризик розвитку гіперкаліємії (особливо у пацієнтів з порушеннями функції нирок). Тому ці комбінації призначають з обережністю, під контролем вмісту калію в плазмі та функції нирок. У літніх пацієнтів і пацієнтів з порушенням функції нирок одночасний прийом інгібіторів АПФ з сульфаметоксазолом/триметопримом супроводжувався тяжкою гіперкаліємією, яка, як вважається, була викликана триметопримом, тому лізиноприл слід застосовувати з обережністю з препаратами, що містять тріметоприм. Калійнесберігаючі діуретики При одночасному застосуванні лізиноприлу з калійнезберігаючими діуретиками гіпокаліємія, спричинена їх застосуванням, може бути зменшена. Інші гіпотензивні лікарські засоби При одночасному застосуванні з вазодилататорами, бета-адреноблокаторами, блокаторами "повільних" кальцієвих каналів, діуретиками та іншими гіпотензивними лікарськими засобами посилюється вираженість антигіпертензивної дії лізиноприлу. Препарати літію При одночасному застосуванні лізиноприлу з препаратами літію виведення літію з організму сповільнюється (ризик посилення кардіотоксичної та нейротоксичної дії літію). Одночасне застосування лізиноприлу із препаратами літію не рекомендується. У разі необхідності застосування цієї комбінації слід регулярно контролювати концентрацію літію у плазмі крові. НПЗЗ, включаючи селективні інгібітори ЦОГ-2, та високі дози ацетилсаліцилової кислоти (> 3 г/добу) Нестероїдні протизапальні засоби (в тому числі селективні інгібітори ЦОГ-2) та ацетилсаліцилова кислота в дозах більше 3 г/добу, знижують антигіпертензивний ефект лізиноприлу. У деяких пацієнтів з порушеною функцією нирок (наприклад, у літніх пацієнтів або пацієнтів з зневодненням, у тому числі хворих на діуретики), які отримують терапію НПЗП (у тому числі селективними інгібіторами ЦОГ-2), одночасне застосування інгібіторів АПФ або АРА II може спричинити подальше погіршення здоров'я. функції нирок, включаючи розвиток гострої ниркової недостатності, та гіперкаліємію. Ці ефекти зазвичай оборотні. Одночасне застосування інгібіторів АПФ та нестероїдних протизапальних засобів має проводитися з обережністю (особливо у літніх пацієнтів та у пацієнтів з порушеною функцією нирок). Пацієнти повинні мати адекватну кількість рідини. Рекомендується ретельно контролювати функцію нирок як на початку, так і в процесі лікування. Не протипоказано застосування лізиноприлу в комбінації з ацетилсаліциловою кислотою як антиагрегантний засіб. Гіпоглікемічні лікарські засоби Одночасний прийом лізиноприлу та інсуліну, а також пероральних гіпоглікемічних засобів може призводити до розвитку гіпоглікемії. Найбільший ризик розвитку спостерігається протягом перших тижнів сумісного застосування, а також у пацієнтів із порушенням функції нирок. Трициклічні антидепресанти/нейролептики/засоби для загальної анестезії/наркотичні засоби При одночасному застосуванні з трициклічними антидепресантами, нейролептиками, засобами загальної анестезії, барбітуратами, міорелаксантами спостерігається посилення антигіпертензивної дії лізиноприлу. Альфа- та бета-адреноміметики Альфа- та бета-адреноміметики (симпатоміметики), такі як епінефрин (адреналін), ізопротеренол, добутамін, допамін, можуть знижувати антигіпертензивний ефект лізиноприлу. Баклофен Посилює антигіпертензивний ефект інгібіторів АПФ. Слід ретельно контролювати артеріальний тиск і, у разі потреби, коригувати дозу ангігіпертензивних препаратів. Етанол При одночасному застосуванні етанолу посилює антигіпертензивну дію лізиноприлу. Естрогени Естрогени послаблюють антигіпертензивний ефект лізиноприлу через затримку рідини. Алопуринол, прокаїнамід, цитостатики, імунодепресанти, глюкокортикостероїди (ГКС) (при системному застосуванні) Спільне застосування інгібіторів АПФ з алопуринолом, прокаїнамідом, цитостатиками збільшує ризик розвитку нейтропенії/агранулоцитозу. Препарати золота При одночасному застосуванні лізиноприлу та препаратів золота внутрішньовенно (натрію ауротіомалат) описаний симптомокомплекс, що включає гіперемію обличчя, нудоту, блювання та зниження артеріального тиску. Селективні інгібітори зворотного захоплення серотоніну Спільне застосування лізиноприлу із селективними інгібіторами зворотного захоплення серотоніну може призводити до вираженої гіпонатріємії. Інгібітори mTOR (mammalian Target of Rapamycin - мета рапаміцину в клітинах ссавців) (наприклад, темсіролімус, сиролімус, еверолімус) У пацієнтів, які приймають одночасно інгібітори АПФ та інгібітори mTOR (темсіролімус, сиролімус, еверолімус), спостерігалося збільшення частоти розвитку ангіоневротичного набряку. Інгібітори дипептидилпептидази N типу (ДПП-IV) (гліптини), наприклад, ситагліптин, саксагліптин, віллдагліптин, лінагліптин У пацієнтів, які приймали інгібітори АПФ та інгібітори дипептидилпептидази IV типу (гліптини), спостерігалося збільшення частоти розвитку ангіоневротичного набряку. Естрамустін Збільшення частоти розвитку ангіоневротичного набряку при одночасному застосуванні з інгібіторами АПФ. Інгібітори нейтральної ендопептидази (НЕП) Повідомлялося про підвищений ризик розвитку ангіоневротичного набряку при одночасному застосуванні інгібіторів АПФ та рацекадотрилу (інгібітор енкефалінази). При одночасному застосуванні інгібіторів АПФ з лікарськими препаратами, що містять сакубітрил (інгібітор неприлізину), зростає ризик розвитку ангіоневротичного набряку, через що одночасне застосування зазначених препаратів протипоказане. Інгібітори АПФ слід призначати не раніше ніж через 36 годин після відміни препаратів, що містять сакубітрил. Протипоказано призначення препаратів, що містять сакубітрил, пацієнтам, які отримують інгібітори АПФ, а також протягом 36 годин після відміни інгібіторів АПФ. Тканинні активатори плазміногену В обсерваційних дослідженнях виявлено підвищену частоту розвитку ангіоневротичного набряку у пацієнтів, які приймали інгібітори АПФ після застосування алтеплази для тромболітичної терапії ішемічного інсульту. Фармакокінетичні взаємодії Антациди та колестірамін знижують всмоктування лізиноприлу в ШКТ.Спосіб застосування та дозиВнутрішньо, по 1 таблетці Гідрохлортіазид+Лізіноприл-Акріхін 1 раз на день, незалежно від їди. Максимальна добова доза – 2 таблетки 1 раз на день (25 мг гідрохлортіазиду/40 мг лізиноприлу). Якщо потрібна зміна дози однієї з діючих речовин у складі комбінованого препарату (наприклад, у зв'язку з новодіагностованим захворюванням, зміною стану пацієнта або лікарською взаємодією), необхідний індивідуальний підбір доз окремих компонентів. Порушення функції нирок У хворих з кліренсом креатиніну від 30 і менше 80 мл/хв препарат можна застосовувати лише після підбору дози окремих компонентів препарату. Застосування препарату при КК Порушення функції печінки Корекція дози не потрібна. Літній вік Корекція дози не потрібна.ПередозуванняГідрохлоротіазид Симптоми Найчастішими проявами передозування гідрохлортіазиду є збільшення діурезу, що супроводжується гострою втратою рідини (дегідратацією) та електролітними порушеннями (гіпокаліємія, гіпонатріємія, гіпохлоремія). Передозування гідрохлортіазиду може виявлятися такими симптомами: з боку серцево-судинної системи: тахікардія; зниження артеріального тиску; шок; з боку нервової системи: слабкість, сплутаність свідомості, запаморочення та спазми литкових м'язів, парестезія, порушення свідомості, втома; з боку шлунково-кишкового тракту: нудота, блювання, спрага; з боку нирок та сечовивідних шляхів: поліурія, олігурія або анурія (через гемоконцентрацію); лабораторні показники: гіпокаліємія, гіпонатріємія, гіпохлоремія, алкалоз, підвищений вміст азоту сечовини у крові (особливо у пацієнтів із нирковою недостатністю). Лікування При передозуванні проводиться симптоматична та підтримуюча терапія. Якщо препарат був прийнятий нещодавно, для виведення гідрохлортіазиду показано індукцію блювоти або промивання шлунка. Абсорбцію гідрохлортіазиду можна зменшити прийомом внутрішньо активованого вугілля. У разі зниження АТ або шоку слід заповнити ОЦК запровадженням плазмозамінних рідин та дефіцит електролітів (калій, натрій). При дихальних порушеннях показано інгаляцію кисню або штучну вентиляцію легень. Слід контролювати водно-електролітний баланс (особливо вміст калію у сироватці крові) та функцію нирок до їх нормалізації. Специфічного антидоту немає. Гідрохлортіазид виводиться при гемодіалізі, проте ступінь його виведення не встановлено. Лізіноприл Симптоми Дані про передозування у людини обмежені. Симптоми, пов'язані з передозуванням інгібіторами АПФ, можуть включати артеріальну гіпотензію, циркуляторний колапс, сухість слизової оболонки порожнини рота, сонливість, затримку сечовипускання, запор, порушення водно-електролітного балансу, ниркову недостатність, почастішання дихання. запаморочення, стан тривоги та кашель. Лікування Промивання шлунка, застосування ентеросорбентів (прийом активованого вугілля), симптоматична терапія. При розвитку артеріальної гіпотензії слід покласти пацієнта на спину та підняти ноги. Для лікування передозування показано внутрішньовенне введення 0,9% натрію хлориду. Необхідний контроль АТ, показників водноелектролітного балансу. Брадикардія може бути зменшена внутрішньовенним введенням атропіну. У разі розвитку стійкої до лікування брадикардії слід розглянути можливість встановлення електрокардіостимулятора. Лізиноприл може бути видалений із системного кровотоку за допомогою гемодіалізу. Під час діалізу слід уникати застосування високопроточних поліакрилонітрилових мембран (ризик розвитку анафілактоїдних реакцій).Запобіжні заходи та особливі вказівкиГідрохлоротіазид Порушення функції нирок У пацієнтів з порушенням функції нирок гідрохлортіазид може спричинити азотемію. При нирковій недостатності можлива кумуляція гідрохлортіазиду. У пацієнтів із зниженою функцією нирок потрібен періодичний контроль КК. При прогресуванні порушення функції нирок та/або настання олігурії (анурії) гідрохлортіазид слід відмінити. Порушення функції печінки При застосуванні тіазидних діуретиків у пацієнтів з порушенням функції печінки можливий розвиток печінкової енцефалопатії. Пацієнтам з тяжкою печінковою недостатністю або печінковою енцефалопатією застосування тіазидів протипоказане. У пацієнтів з печінковою недостатністю легкого та помірного ступеня тяжкості та/або прогресуючими захворюваннями печінки гідрохлортіазид слід застосовувати з обережністю, оскільки навіть невелика зміна водноелектролітного балансу та накопичення амонію у сироватці крові може спричинити печінкову кому. У разі появи симптомів енцефалопатії прийом діуретиків слід негайно припинити. Водно-електролітний баланс та метаболічні порушення Тіазидні діуретики (включаючи гідрохлортіазид) можуть викликати зменшення ОЦК (гіповолемію) та порушення водно-електролітного балансу (в т.ч. гіпокаліємію, гіпонатріємію, гіпохлоремічний алкалоз). Клінічними симптомами порушень водно-електролітного балансу є сухість у роті, спрага, слабкість, млявість, стомлюваність, сонливість, занепокоєння, м'язовий біль або судоми, м'язова слабкість, виражене зниження АТ, олігурія, тахікардія, аритмія та порушення з боку шлунково-кишкового тракту. та блювання). У пацієнтів, які отримують терапію гідрохлортіазидом (особливо при тривалому курсовому лікуванні), слід виявляти клінічні симптоми порушень водно-електролітного балансу регулярно контролювати вміст електролітів у крові. Натрій Всі діуретичні препарати можуть викликати гіпонатріємію, що іноді призводить до тяжких ускладнень. Гіпонатріємія та гіповолемія можуть призводити до зневоднення та ортостатичної гіпотензії. Супутнє зниження іонів хлору може призводити до вторинного компенсаторного метаболічного алкалозу, проте частота та ступінь виразності цього ефекту незначні. Рекомендується визначити вміст іонів натрію в плазмі крові до початку лікування та регулярно контролювати цей показник на фоні прийому гідрохлортіазиду. Калій При застосуванні тезових та тіазидоподібних діуретиків існує ризик різкого зниження вмісту калію у плазмі крові та розвитку гіпокаліємії (концентрація калію менше 3,4 ммоль/л). Гіпокаліємія підвищує ризик розвитку порушень серцевого ритму (в т.ч. тяжких аритмій) та посилює токсичну дію серцевих глікозидів. Крім того, гіпоглікемія (так само, як і брадикардія) є станом, що сприяє розвитку поліморфної шлуночкової тахікардії типу "пірует", яка може призводити до летального результату. Гіпокаліємія представляє найбільшу небезпеку для наступних груп пацієнтів: особи похилого віку, пацієнти, що одночасно отримують терапію антиаритмічними та неантіаритмічними препаратами, які можуть викликати поліморфну шлуночкову тахікардію типу "пірует" або збільшувати тривалість інтервалу QT на ЕКГ, пацієнти з порушеннями хронічної серцевої недостатністю. Крім того, до групи підвищеного ризику належать пацієнти із збільшеним інтервалом QT. При цьому немає значення, викликане це збільшення вродженими причинами або дією лікарських засобів. У всіх описаних вище випадках необхідно уникати ризику розвитку гіпокаліємії та регулярно контролювати вміст калію у плазмі крові. Перший вимір вмісту іонів калію в крові необхідно провести протягом першого тижня від початку лікування. З появою гіпокаліємії має бути призначене відповідне лікування. Гіпокаліємію можна коригувати застосуванням калійвмісних препаратів або прийомом харчових продуктів, багатих калієм (сухофрукти, фрукти, овочі). Кальцій Тіазидні діуретики можуть зменшувати виведення іонів кальцію нирками, призводячи до незначного та тимчасового підвищення вмісту кальцію в плазмі. У деяких пацієнтів при тривалому застосуванні тіазидних діуретиків спостерігалися патологічні зміни паращитовидних залоз з гіперкальціємією та гіперфосфатемією, але без типових ускладнень гіперпаратиреозу (нефролітіаз, зниження мінеральної щільності кісткової тканини, виразкова хвороба). Виражена гіперкальціємія може бути проявом раніше не діагностованого гіперпаратиреозу. Через вплив на метаболізм кальцію тіазиди можуть впливати на лабораторні показники функції паращитовидних залоз. Слід припинити прийом тіазидних діуретиків (включно з гідрохлортіазидом) перед дослідженням функції паращитовидних залоз. Магній Встановлено, що тіазиди збільшують виведення магнію нирками, що може призвести до гіпомагніємії. Клінічне значення гіпомагніємії залишається незрозумілим. Глюкоза Лікування тіазидними діуретиками може порушувати толерантність до глюкози. При застосуванні гідрохлортіазиду у пацієнтів з маніфестним або латентним цукровим діабетом необхідно регулярно контролювати концентрацію глюкози в крові. Може знадобитися корекція дози гіпоглікемічних лікарських засобів. Сечова кислота У пацієнтів з подагрою може збільшуватись частота виникнення нападів або загострюватися перебіг подагри. Необхідний ретельний контроль за пацієнтами з подагрою та порушенням метаболізму сечової кислоти (гіперурикемією). Ліпіди При застосуванні гідрохлортіазиду може збільшуватися концентрація холестерину та тригліцеридів у плазмі крові. Гостра міопія/вторинна глаукома. Гідрохлортіазид може викликати ідіосинкразічну реакцію, що призводить до розвитку гострої міопії та гострого нападу вторинної глаукоми. Симптоми включають: раптове зниження гостроти зору або біль в очах, які проявляються, як правило, протягом декількох годин або тижнів від початку терапії гідрохлортіазидом. За відсутності лікування гостра глаукома може призвести до незворотної втрати зору. З появою симптомів необхідно якнайшвидше припинити прийом гідрохлортіазиду. Якщо внутрішньоочний тиск залишається неконтрольованим, може знадобитися невідкладне медикаментозне лікування або хірургічне втручання. Факторами ризику гострої глаукоми є: алергічна реакція на сульфонаміди або пеніцилін в анамнезі. Порушення з боку імунної системи Є повідомлення про те, що тіазидні діуретики (в т.ч. гідрохлортіазид) можуть викликати загострення або прогресування системного червоного вовчаку, а також вовчаковоподібні реакції. У пацієнтів, які отримують тіазидні діуретики, реакції підвищеної чутливості можуть спостерігатися навіть за відсутності вказівок на наявність в анамнезі алергічних реакцій або бронхіальної астми. Фоточутливість Існує інформація про випадки розвитку реакцій фоточутливості при прийомі тіазидних діуретиків. У разі появи фоточутливості на фоні прийому гідрохлортіазиду слід припинити лікування. Якщо продовження прийому діуретика необхідне, слід захищати шкірні покриви від впливу сонячних променів або штучних ультрафіолетових променів. Інше У пацієнтів з вираженим атеросклерозом церебральних і коронарних артерій слід особливо обережно застосовувати гідрохлортіазид. Тіазидні діуретики можуть знижувати кількість йоду, пов'язаного з білками плазми, без прояву ознак порушення функції щитовидної залози. Лізіноприл Симптоматична артеріальна гіпотензія Найчастіше виражене зниження артеріального тиску виникає при зниженні ОЦК, викликаної терапією діуретиками, зменшенням кухонної солі в їжі, діалізом, діареєю або блюванням. У пацієнтів з ХСН та за наявності ниркової недостатності або без неї можливе виражене зниження артеріального тиску. Воно найчастіше виявляється у пацієнтів з тяжкою стадією ХСН, як наслідок застосування великих доз діуретиків, гіпонатріємії або порушеної функції нирок. У таких пацієнтів лікування слід розпочати під суворим медичним наглядом (з обережністю проводити підбір дози препарату та діуретиків). Ті ж рекомендації стосуються і пацієнтів з ішемічною хворобою серця, цереброваскулярною недостатністю, у яких різке зниження артеріального тиску може призвести до інфаркту міокарда або інсульту. Транзиторна гіпотензія не є протипоказанням для прийому наступної дози препарату. При застосуванні лізиноприлу, у деяких пацієнтів з ХСН, але з нормальним або зниженим артеріальним тиском, може спостерігатися зниження артеріального тиску, що, як правило, не є причиною припинення лікування. До початку лікування лізиноприлом, по можливості, слід заповнити ОЦК та/або нормалізувати вміст натрію у сироватці крові, проводити ретельний моніторинг стану пацієнтів, які перебувають у групі підвищеного ризику розвитку симптоматичної гіпотензії на початку лікування та при корекції дози. У разі розвитку артеріальної гіпотензії пацієнта слід покласти на спину і, при необхідності, провести внутрішньовенну інфузію фізіологічного розчину. У разі стенозу ниркових артерій (особливо при двосторонньому стенозі або за наявності стенозу артерії єдиної нирки), а також при недостатності кровообігу внаслідок нестачі натрію та/іл рідини застосування лізиноприлу може призвести до порушення функції нирок, гострої ниркової недостатності, яка зазвичай виявляється незворотній навіть після відміни препарату. Артеріальна гіпотензія при ГІМ При ГІМ застосування лізиноприлу протипоказано при кардіогенному шоці та вираженій артеріальній гіпотензії (систолічний артеріальний тиск менше 100 мм рт.ст.), т.к. у таких пацієнтів застосування вазодилататора може суттєво погіршити показники гемодинаміки. У пацієнтів з низьким систолі АТ (>100 мм рт.ст. і При ГІМ лікування лізиноприлом не слід починати у пацієнтів з ознаками ниркової дисфункції, які визначалися як концентрація креатину у сироватці крові, що перевищує 177 мкмоль/л, та/або протеїнурія, що перевищує 500 мг/24 год. У разі розвитку порушення функції нирок під час терапії лізиноприлом (концентрація креатиніну в сироватці крові, що перевищує 265 мкмоль/л або в 2 рази перевищує відповідне значення до початку лікування), лікар повинен розглянути доцільність відміни лізиноприлу. Мітральний стеноз/аортальний стеноз/гіпертрофічна обструктивна кардіоміопатія Лізиноприл, як і інші інгібітори АПФ, повинен з обережністю застосовуватися у пацієнтів з обструкцією тракту лівого шлуночка, що виносить (аортальний стеноз, гіпертрофічна обструктивна кардіоміопатія), а також у пацієнтів з мітральним стенозом. Порушення функції нирок У пацієнтів з порушенням функції нирок (КК менше 80 мл/хв) початкова доза лізиноприлу повинна бути змінена відповідно до КК (див. розділ "Спосіб застосування та дози"). Регулярний контроль вмісту калію та концентрації креатиніну в плазмі є обов'язковою тактикою лікування таких пацієнтів. У пацієнтів із ХСН артеріальна гіпотензія може призвести до погіршення функції нирок. У таких пацієнтів відзначалися випадки гострої ниркової недостатності, звичайно оборотної. У деяких пацієнтів із двостороннім стенозом ниркових артерій або зі стенозом артерії єдиної нирки, які отримували інгібітори АПФ, спостерігалося збільшення концентрації сечовини та креатиніну у сироватці крові, як правило, оборотне при припиненні лікування. Це особливо можливо у пацієнтів з нирковою недостатністю. У разі супутньої вазоренальної артеріальної гіпертензії існує підвищений ризик розвитку тяжкої гіпотензії та ниркової недостатності. У таких пацієнтів лікування слід розпочинати під ретельним медичним наглядом з низьких доз та обережно титрувати дозу. Оскільки лікування діуретиками може сприяти розвитку вищезазначених станів, діуретик слід відмінити, при цьому функцію нирок слід контролювати протягом перших тижнів терапії лізиноприлом. У деяких пацієнтів з артеріальною гіпертензією без вираженої попередньої вазоренальної гіпертензії відзначалося збільшення концентрації сечовини та креатиніну у сироватці крові, зазвичай незначне та транзиторне, особливо у тих випадках, коли лізиноприл застосовувався одночасно з діуретиком. Це особливо можливо у пацієнтів з попередньою нирковою недостатністю. Може знадобитися зниження дози та/або скасування діуретика та/або лізиноприлу. Трансплантація нирки Досвід застосування лізиноприлу у пацієнтів, які недавно перенесли трансплантацію нирки, відсутній. Реакції гіперчутливості/ангіоневротичний набряк Ангіоневротичний набряк обличчя, кінцівок, губ, язика, надгортанника та/або гортані відмічався рідко у пацієнтів, які лікувалися інгібіторами АПФ, включаючи лізиноприл. Ангіоневротичний набряк може виникнути будь-якої миті під час лікування. У таких випадках слід негайно відмінити препарат, призначити відповідне лікування та забезпечити медичний нагляд до повної регресії симптомів. Навіть у випадках набряку язика, що не супроводжується дихальною недостатністю, пацієнтам може знадобитися тривале спостереження, оскільки лікування антигістамінними препаратами та кортикостероїдами може бути недостатньо. Ангіоневротичний набряк, що супроводжується набряком гортані, може призвести до смерті. Набряк мови, голосових складок або гортані може призвести до обструкції дихальних шляхів. При появі таких симптомів потрібна невідкладна терапія: введення епінефрину (0,3-0,5 мл розчину епінефрину (адреналіну) 1:1000 підшкірно, введення глюкокортикоїдів, антигістамінних препаратів) та/або забезпечення вільної прохідності дихальних шляхів. Пацієнт повинен перебувати під медичним наглядом до повного та стійкого зникнення симптомів. У поодиноких випадках на тлі терапії інгібіторами АПФ розвивається інтестинальний набряк (ангіоневротичний набряк кишечника). При цьому у пацієнтів відзначається біль у животі як ізольований симптом або у поєднанні з нудотою та блюванням, у деяких випадках без попереднього ангіоневротичного набряку обличчя та при нормальному рівні С1-естерази. Діагноз встановлюється за допомогою комп'ютерної томографії черевної порожнини, УЗД або хірургічного втручання. Симптоми зникали після припинення інгібіторів АПФ. Можливість розвитку інтестинального набряку необхідно враховувати під час проведення диференціальної діагностики болю у животі у пацієнтів, які приймають інгібітори АПФ. Пацієнти, що мають в анамнезі ангіоневротичний набряк, не пов'язаний з прийомом інгібіторів АПФ, можуть бути схильними до ризику розвитку ангіоневротичного набряку на тлі терапії інгібіторами АПФ. У пацієнтів негроїдної раси, які приймали інгібітори АПФ, ангіоневротичний набряк спостерігався частіше, ніж у інших рас. Збільшення ризику розвитку ангіоневротичного набряку спостерігалося у пацієнтів, які одночасно приймають інгібітори АПФ та такі лікарські засоби, як інгібітори mTOR (темсиролімус, сиролімус, еверолімус), інгібітори дипептидилпептидази IV типу (ситагліптин, саксагліптин, відаценіда , сакубітрил) та тканинні активатори плазміногену Анафілактоїдні реакції під час проведення десенсибілізації алергеном з отрути перетинчастокрилих У пацієнтів, які приймають інгібітори АПФ при проведенні десенсибілізації отрутою гіменоптери (перетинчастокрилих), вкрай рідко можлива поява загрозливого життя анафілактоїдної реакції. Необхідно тимчасово припинити лікування інгібітором АПФ перед початком курсу десенсибілізації. Анафілактоїдні реакції під час проведення аферезу ліпопротеїнів низької щільності (ЛПНЩ-аферезу) У пацієнтів, які приймають інгібітори АПФ, можливий розвиток анафілактоїдних реакцій при проведенні ЛПНЩ-аферезу з використанням декстрану сульфату. Розвиток цих реакцій можна запобігти, якщо тимчасово скасовувати інгібітор АПФ до початку кожної процедури ЛПНГ-аферезу. Гемодіаліз з використанням високопроточних мембран Можливе виникнення анафілактоїдних реакцій при одночасному проведенні гемодіалізу з використанням високопроточних мембран (в т.ч. AN69®). Необхідно розглянути можливість застосування іншого типу мембрани для діалізу чи іншого гіпотензивного засобу. Порушення функції печінки У поодиноких випадках на фоні прийому інгібіторів АПФ спостерігався синдром розвитку холестатичної жовтяниці з переходом у фульмінантний некроз печінки, іноді з летальним кінцем. Механізм розвитку цього синдрому незрозумілий. При появі жовтяниці або значного підвищення активності печінкових ферментів на фоні прийому інгібіторів АПФ слід припинити прийом препарату, пацієнт повинен перебувати під відповідним медичним наглядом. Нейтропенія/агранулоцитоз/тромбоцитопенія/анемія На фоні прийому інгібіторів АПФ можуть виникати нейтропенія/агранулоцитоз, тромбоцитопенія та анемія. У пацієнтів з нормальною функцією нирок та за відсутності інших обтяжливих факторів нейтропенія розвивається рідко. Нейтропенія та агранулоцитоз є оборотними та зникають після відміни інгібітору АПФ. Лізиноприл слід застосовувати з особливою обережністю у пацієнтів із системними захворюваннями сполучної тканини, на фоні прийому імунодепресантів, алопуринолу або прокаїнаміду, особливо у пацієнтів з порушеною функцією нирок. У деяких пацієнтів виникали важкі інфекції, у ряді випадків стійкі до інтенсивної антибіотикотерапії. При застосуванні лізиноприлу у таких пацієнтів рекомендується періодичний контроль вмісту лейкоцитів у крові (аналіз крові з підрахунком лейкоцитарної формули). Пацієнти повинні бути попереджені про необхідність повідомляти лікаря про будь-які ознаки інфекційних захворювань (наприклад, біль у горлі, гарячка). Етнічні відмінності Слід враховувати, що у пацієнтів негроїдної раси ризик розвитку ангіоневротичного набряку є вищим. Як і інші інгібітори АПФ, лізиноприл менш ефективний щодо зниження артеріального тиску у пацієнтів негроїдної раси. Даний ефект пов'язаний з вираженим переважанням низькоренінового статусу у пацієнтів негроїдної раси з артеріальною гіпертензією. Хірургічні втручання/загальна анестезія Перед хірургічним втручанням (включаючи стоматологічну хірургію) слід інформувати лікаря/анестезіолога про застосування інгібітора АПФ. При великих хірургічних втручаннях, а також при застосуванні інших засобів, що викликають зниження артеріального тиску, лізиноприл, блокуючи утворення ангіотензину II, може викликати виражене непрогнозоване зниження артеріального тиску. У разі розвитку артеріальної гіпотензії слід здійснювати її корекцію збільшенням ОЦК. Кашель При застосуванні інгібіторів АПФ відзначали сухий тривалий кашель, який зникає після припинення лікування інгібітором АПФ. При диференціальному діагнозі кашлю треба враховувати і кашель, спричинений інгібітором АПФ. Гіперкаліємія Гіперкаліємія може розвинутись на фоні терапії інгібіторами АПФ, включаючи лізиноприл. Факторами ризику гіперкаліємії є ниркова недостатність, літній вік (старше 65 років), цукровий діабет, деякі супутні стани (дегідратація, зниження ОЦК, гостра серцева недостатність у стадії декомпенсації, метаболічний ацидоз), одночасне застосування калійзберігаючих діуретиків (таких як спірно триамтерен або амілорид), а також препаратів калію, калій, що містять замінників харчової солі та інших лікарських засобів, що сприяють підвищенню вмісту калію в плазмі крові (наприклад, гепарину). Застосування харчових добавок/препаратів калію, калійзберігаючих діуретиків, замінників харчових солей, що містять калій, може призвести до значного підвищення вмісту калію в крові, особливо у пацієнтів зі зниженою функцією нирок. Гіперкаліємія може призвести до серйозних, іноді фатальних порушень серцевого ритму. При необхідності одночасного застосування лізиноприлу і перерахованих вище калійвмісних або підвищують вміст калію в плазмі крові лікарських засобів слід дотримуватися обережності і регулярно контролювати вміст калію в сироватці крові. Цукровий діабет При застосуванні лізиноприлу у пацієнтів з цукровим діабетом, які отримують пероральні гіпоглікемічні засоби або інсулін, протягом першого місяця лікування необхідно регулярно контролювати концентрацію глюкози в крові. Препарати літію Як правило, одночасне застосування препаратів літію та лізиноприлу не рекомендується. Етанол У період лікування рекомендується вживати алкогольні напої, т.к. етанол посилює антигіпертензивну дію інгібіторів АПФ. Подвійна блокад аренін-ангіотензин-альдостеронової системи (РААС) Повідомлялося про випадки артеріальної гіпотензії, непритомність, інсульт, гіперкаліємію та порушення функції нирок (включаючи гостру ниркову недостатність) у сприйнятливих пацієнтів, особливо при одночасному застосуванні кількох лікарських препаратів, що впливають на РААС. Одночасне застосування інгібіторів АПФ з лікарськими засобами, що містять аліскірен, протипоказане у пацієнтів з цукровим діабетом та/або з помірною або тяжкою нирковою недостатністю (ШКФ менше 60 мл/хв/1,73 м2 площі поверхні тіла) та не рекомендується у інших пацієнтів. Одночасне застосування інгібіторів АПФ з антагоністами рецепторів ангіотензину II протипоказане у пацієнтів з діабетичною нефропатією та не рекомендується в інших пацієнтів. У випадках, коли одночасне призначення двох лікарських засобів, що впливають на РААС, є необхідним, їх застосування має проводитися під контролем лікаря з особливою обережністю та з регулярним контролем функції нирок, показників АТ та вмісту електролітів у плазмі крові. Комбінована терапія При гострому інфаркті міокарда показано застосування стандартної терапії (тромболітики, ацетилсаліцилова кислота як антиагрегантний засіб, бета-адреноблокатори). Лізиноприл можна застосовувати спільно з внутрішньовенним введенням або із застосуванням терапевтичних трансдермальних систем нітрогліцерину. Літній вік У пацієнтів похилого віку застосування стандартних доз лізиноприлу призводить до більш високої концентрації лізиноприлу у плазмі. Тому потрібна особлива обережність щодо дози, незважаючи на те, що відмінностей в антигіпертензивній дії лізиноприлу у літніх та молодих пацієнтів не виявлено. Вплив на здатність до керування автотранспортом та управління механізмами У період лікування слід утриматися від керування транспортними засобами та механізмами та занять потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій, оскільки можливе запаморочення, особливо на початку курсу лікування.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаЦиклометикон, ізопропілміристат, на водній основі, не містить традиційних пестицидів. Розчин 100мл.Фармакотерапевтична групаФулл маркс надає фізичний вплив на вошей, призводячи до їх дегідратації (зневоднення) та смерті. На відміну від опірності вошей деяким пестицидам, які використовуються в інших засобах, в даний час не виявлено механізми опірності головних вошей ефекту зневоднення!.ІнструкціяРозчесати сухе волосся звичайною гребінцем, щоб звільнити сплутане волосся. Струсити пляшечку з розчином, нанести розчин на сухе волосся і втерти так, щоб шкіра голови і волосся по всій довжині були покриті розчином. Залишити засіб на волоссі на 10 хвилин. Кожен курс обробки потребує приблизно 50 мл розчину. Для довгого/густого волосся може знадобитися більша кількість розчину.РекомендуєтьсяГоловні воші.Протипоказання до застосуванняІндивідуальна нестерпність компонентів.Вагітність та лактаціяДля дітей старших за п'ять років.Запобіжні заходи та особливі вказівкиЯкщо розчин проти головних вошей потрапив на шкіру (крім шкіри голови) або у вічі, змити теплою водою. Однак при підвищеній чутливості до препарату припиніть його використання та зверніться за консультацією до лікаря або фармацевта.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаКрем – 1 г: кислота саліцилова, калій йодистий, цинку окис, метиловий та пропіловий ефіри параоксибензойної кислоти, екстракт трави чистотілу, екстракт кори дуба. Туба 30 гХарактеристикаКрем Фундізол ефективний засіб при грибкових ураженнях нігтів, грибкових та бактеріальних ураженнях шкіри, що "вросли нігті". Розм'якшує та видаляє пошкоджену частину нігтьової пластинки та поверхневих уражений шар пошкодженого грибком епідермісу. Пом'якшує шкіру стоп, загоює шкірні тріщини. Усуває неприємний запах ніг. Не викликає подразнення шкіри. "Підсушує" шкірні висипання. Запобігає надмірній пітливості стоп.ІнструкціяПри грибкових ураженнях нігтів крем наносять на шкіру та нігті 2 рази на день товстим шаром та залишають на 4-6 годин під компресним папером, фіксуючи лейкопластирем. Для пом'якшення ороговілих ділянок шкіри та запобігання зараженню грибковою інфекцією 2-3 рази на день тонким шаром масажними рухами нанесіть крем на шкіру стоп (рук), міжпальцеві проміжки, здорові нігтьові пластинки.Протипоказання до застосуванняІндивідуальна непереносимість компонентів продукту, вагітність та годування груддю.Запобіжні заходи та особливі вказівкиПеред застосуванням рекомендується проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
288,00 грн
261,00 грн
Склад, форма випуску та упаковкаПігулки - 1 таб. активні речовини: калію лозартан 50 мг; гідрохлортіазид 12,5 мг; допоміжні речовини: лактоза 111,55 мг, мікрокристалічна целюлоза 37,2 мг, крохмаль прежелатинізований 35 мг, магнію стеарат 3,75 мг; оболонка: опадрай зелений [гіпролоза, гіпромелоза, титану діоксид, барвник хіноліновий жовтий] 7,8 мг. Пігулки, покриті плівковою оболонкою, 12,5 мг + 50 мг. По 14 таблеток у блістер із ПВХ-алюмінієвої фольги. По 2 або 6 блістерів у картонній пачці разом із інструкцією із застосування.Опис лікарської формиДовгасті двоопуклі таблетки, вкриті оболонкою жовтого або жовтого із зеленуватим відтінком кольору.Фармакотерапевтична групаГіпотензивний комбінований засіб (діуретик + ангіотензину II рецепторів антагоніст).ФармакокінетикаГідрохлоротіазид Гідрохлортіазид не піддається метаболізму, але швидко виводиться нирками. При підтримці концентрації гідрохлортіазиду в плазмі крові протягом як мінімум 24 годин період напіввиведення варіював від 5,6 до 14,8 годин. Не менше 61% прийнятої внутрішньо дози виводиться у незміненому вигляді протягом 24 годин. проникає через гематоенцефалічний бар'єр. Лозартан Всмоктування При прийомі внутрішньо лозартан добре всмоктується та піддається метаболізму при «первинному проходженні» через печінку з утворенням активного карбоксильованого метаболіту та неактивних метаболітів. Системна біодоступність лозартану у таблетованій формі становить приблизно 33%. Середні Сmax лозартану та його активного метаболіту досягаються через 1 годину та через 3-4 години відповідно. При прийомі лозартану в процесі звичайного їди клінічно значущого впливу на профіль концентрації лозартану в плазмі виявлено не було. Розподіл Лозартан та його активний метаболіт пов'язуються з білками плазми крові (переважно з альбуміном) не менше ніж на 99%. Об'єм розподілу лозартану становить 34 л. Дослідження на щурах показали, що лозартан практично не проникає через гематоенцефалічний бар'єр. Метаболізм Приблизно 14% дози лозартану при внутрішньовенному введенні або прийомі внутрішньо перетворюється на його активний метаболіт. Після прийому внутрішньо або внутрішньовенного введення, міченого радіоактивним вуглецем лозартану (14С лозартану) радіоактивність циркулюючої плазми крові, перш за все, обумовлена наявністю в ній лозартану та його активного метаболіту. Низька ефективність перетворення лозартану на його активний метаболіт спостерігалася приблизно у 1% пацієнтів, які брали участь у дослідженні. Крім активного метаболіту утворюються біологічно неактивні метаболіти, у тому числі два основних метаболіти, що утворюються в результаті гідроксилювання бічного бутилового ланцюга, і один другорядний N-2-тетразол-глюкуронід. Виведення Плазмовий кліренс лозартану та його активного метаболіту становить близько 600 мл/хв та 50 мл/хв відповідно. Нирковий кліренс лозартану та його активного метаболіту становить приблизно 74 мл/хв та 26 мл/хв відповідно. При прийомі лозартану внутрішньо приблизно 4% дози виводиться нирками у незміненому вигляді та близько 6% дози виводиться нирками у вигляді активного метаболіту. Лозартан та його активний метаболіт мають лінійну фармакокінетику при прийомі внутрішньо лозартану у дозах до 200 мг. Після прийому внутрішньо плазмові концентрації лозартану та його активного метаболіту знижуються поліекспоненційно з кінцевим періодом напіввиведення приблизно 2 та 6-9 годин відповідно. При режимі дозування препарату 100 мг 1 раз на добу немає значного накопичення в плазмі крові ні лозартану, ні його активного метаболіту. Виведення лозартану та його метаболітів здійснюється нирками та через кишечник з жовчю. Після прийому внутрішньо 14С лозартану у чоловіків близько 35% радіоактивності виявляється у сечі та 58% у калі. Після внутрішньовенного введення 14С лозартану у чоловіків приблизно 43% радіоактивності виявляється у сечі та 50% у калі. Фармакокінетика у спеціальних груп пацієнтів Лозартан - гідрохлортіазид Літні пацієнти Концентрації лозартану та його активного метаболіту в плазмі крові та швидкість всмоктування гідрохлортіазиду у літніх пацієнтів з артеріальною гіпертензією значуще не відрізняються від цих показників у молодих пацієнтів з артеріальною гіпертензією. Лозартан Підлога Значення концентрації лозартану в плазмі крові у жінок з артеріальною гіпертензією в 2 рази перевищували відповідні значення у чоловіків з гіпертензією. Концентрації активного метаболіту у чоловіків та жінок не відрізнялися. Ця явна фармакокінетична відмінність, проте, не має клінічного значення. Пацієнти з порушенням функції печінки При прийомі лозартану внутрішньо пацієнтами з легким та помірним алкогольним цирозом печінки концентрації лозартану та його активного метаболіту у плазмі крові виявилися відповідно у 5 та 1,7 рази вищими, ніж у молодих здорових добровольців чоловічої статі. Пацієнти з порушенням функції нирок Концентрації лозартану в плазмі у пацієнтів з кліренсом креатиніну (КК) вище 10 мл/хв не відрізнялися від таких у пацієнтів з незміненою функцією нирок. Площа під кривою "концентрація-час" (AUC) лозартану у пацієнтів, які перебувають на гемодіалізі, була приблизно в 2 рази більша в порівнянні з AUC лозартану у пацієнтів з нормальною нирковою функцією. Концентрації активного метаболіту в плазмі не змінювалися у пацієнтів з порушенням функції нирок або пацієнтів, які перебували на гемодіалізі. Лозартан та його активний метаболіт не виводяться за допомогою процедури гемодіалізу.ФармакодинамікаГідрохлоротіазид Механізм антигіпертензивної дії тіазид невідомий. Тіазиди зазвичай не впливають на нормальний рівень артеріального тиску. Гідрохлортіазид є діуретиком та гіпотензивним засобом. Він впливає на реабсорбцію електролітів у дистальних канальцях нирок. Гідрохлортіазид приблизно однаково збільшує екскрецію іонів натрію і хлору. Натрійурез може супроводжуватися невеликою втратою іонів калію та бікарбонату. При внутрішньому прийомі діуретичний ефект розвивається протягом 2 годин, досягає максимуму в середньому через 4 години і триває від 6 до 12 годин. Лозартан Ангіотензин II є потужним вазоконстриктором, головним активним гормоном ренін-ангіотензин-альдостеронової системи (РААС), а також вирішальною ланкою при розвитку артеріальної гіпертензії (АГ). Ангіотензин II зв'язується з AT1-рецепторами, що знаходяться в багатьох тканинах (у гладком'язових тканинах судин, надниркових залозах, нирках і серці), і виконує кілька важливих біологічних функцій, включаючи вазоконстрикцію та вивільнення альдостерону. Крім цього, ангіотензин II стимулює розростання гладких клітин. АТ2-рецептори - другий тип рецепторів, з якими зв'язується ангіотензин II, але його роль у регуляції функції серцево-судинної системи невідома. Лозартан селективний антагоніст AT1-рецепторів ангіотензину II, високоефективний при внутрішньому прийомі. Лозартан та його фармакологічно активний карбоксильований метаболіт (Е-3174) як in vitro, так і in vivo блокують усі фізіологічні ефекти ангіотензину II незалежно від його джерела чи шляху синтезу. На відміну від деяких пептидних антагоністів ангіотензину II лозартан не має властивостей агоніста. Лозартан вибірково зв'язується з AT1-рецепторами і не зв'язується, і не блокує рецептори інших гормонів та іонних каналів, що відіграють важливу роль у регуляції функції серцево-судинної системи. Крім того, лозартан не інгібує ангіотензинперетворюючий фермент (АПФ, кініназа II), що відповідає за руйнування брадикініну. Отже, ефекти, які безпосередньо не пов'язані з блокадою AT1-рецепторів, такі як посилення брадикінін-опосередкованих ефектів або розвиток набряків (лозартан 1,7%, плацебо 1,9%), не мають відношення до дії лозартану. Препарат Гідрохлортіазид+Лозартан-Акріхін Компоненти препарату Гідрохлортіазид+Лозартан-Акріхін мають адитивну антигіпертензивну дію, знижуючи рівень артеріального тиску (АТ) більшою мірою, ніж кожен із компонентів окремо. Вважається, що цей ефект зумовлений взаємодоповнювальною дією обох компонентів. Внаслідок діуретичного ефекту гідрохлортіазид підвищує активність реніну плазми крові (АРП), стимулює секрецію альдостерону, збільшує концентрацію ангіотензину II та знижує вміст калію у сироватці крові. Прийом лозартану блокує всі фізіологічні ефекти ангіотензину II і внаслідок придушення ефектів альдостерону може сприяти зниженню втрати калію, пов'язаного з прийомом діуретика. Лозартан має помірний і минущий урикозуричний ефект. Гідрохлортіазид викликає невелике підвищення концентрації сечової кислоти у крові. Комбінація лозартану та гідрохлортіазиду сприяє зменшенню вираженості гіперурикемії, спричиненої діуретиком. Препарат Гідрохлортіазид+Лозартан-Акріхін є комбінованим препаратом лозартану та гідрохлортіазиду. У пацієнтів з артеріальною гіпертензією та гіпертрофією лівого шлуночка лозартан, у тому числі в комбінації з гідрохлоротіазидом, зменшує ризик серцево-судинної захворюваності та смертності, що було доведено за допомогою оцінки комбінованої частоти розвитку інсульту та інфаркту міокарда, а також показника серцевості. цієї категорії хворих. Гідрохлоротіазид Механізм антигіпертензивної дії тіазид невідомий. Зазвичай, тіазиди не впливають на нормальні значення АТ. Гідрохлортіазид є діуретичним та гіпотензивним засобом. Він впливає на механізм реабсорбції електролітів у дистальних звивистих ниркових канальцях. Гідрохлортіазид збільшує екскрецію натрію та хлориду приблизно в еквівалентних кількостях. Натрійурез може супроводжуватися деякою втратою іонів калію та бікарбонату. Після прийому внутрішньо діурез починається протягом 2 год, досягає максимуму протягом приблизно 4 год і триває приблизно 6-12 год. Лозартан Лозартан пригнічує підвищення систолічного та діастолічного артеріального тиску (АТ) при інфузії ангіотензину ІІ. У момент досягнення максимальної концентрації лозартану в плазмі крові (Сmax) після прийому лозартану в дозі 100 мг вищевказаний ефект ангіотензину II пригнічується приблизно на 85%, а через 24 години після одноразового та багаторазового прийому на 26-39%. У період прийому лозартану усунення негативного зворотного зв'язку, що полягає у придушенні ангіотензином II секреції реніну, веде до збільшення АРП. Збільшення АРП призводить до збільшення концентрації ангіотензину ІІ у плазмі крові. При тривалому (6-тижневому) лікуванні пацієнтів з артеріальною гіпертензією лозартаном у дозі 100 мг на добу спостерігалося 2-3-кратне збільшення концентрації ангіотензину II у плазмі крові в момент досягнення Сmax лозартану. У деяких пацієнтів спостерігалося ще більше збільшення концентрації ангіотензину II, особливо при невеликій тривалості лікування (2 тижні). Незважаючи на це, у процесі лікування антигіпертензивний ефект та зниження концентрації альдостерону у плазмі крові виявлялися через 2 та 6 тижнів терапії, що вказує на ефективну блокаду рецепторів ангіотензину ІІ.Після відміни лозартану АРП та концентрації ангіотензину II знижувалися протягом 3 діб до значень, що спостерігалися до початку прийому лозартану. Вплив препарату Гідрохлортіазид+Лозартан-Акріхін на АРП та концентрацію ангіотензину II був подібним до спостеріганих ефектів при прийомі лозартану в дозі 50 мг. Оскільки лозартан є специфічним антагоністом AT1-рецепторів ангіотензину II, він не пригнічує АПФ (кініназу II) — фермент, який інактивує брадикінін. Дослідження, в якому порівнювалися ефекти лозартану в дозах 20 мг та 100 мг з ефектами інгібітору АПФ за впливом на ангіотензин I, ангіотензин II та брадикінін, показало, що лозартан блокує ефекти ангіотензину I та ангіотензину II, не впливаючи на ефект. Це зумовлено специфічним механізмом дії лозартану. Інгібітор АПФ блокував реакції на ангіотензин I і підвищував вираженість ефектів, зумовлених дією брадикініну, не впливаючи на вираженість відповіді на ангіотензин II, що демонструє фармакодинамічну різницю між лозартаном та інгібіторами АПФ. Концентрації лозартану та його активного метаболіту у плазмі крові, а також антигіпертензивний ефект лозартану зростають із збільшенням дози препарату. Оскільки лозартан та його активний метаболіт є антагоністами рецепторів ангіотензину II (АРА II), вони обидва роблять внесок у антигіпертензивний ефект. У дослідженні з одноразовим прийомом лозартану в дозі 100 мг, до якого включалися здорові добровольці (чоловіки), прийом препарату внутрішньо в умовах високо- та малосольової дієти не впливав на швидкість клубочкової фільтрації (СКФ), ефективний нирковий плазмоток та фільтраційну фракцію. Лозартан мав натрійуретіческій ефект, який був більш виражений при малосольової дієті і, мабуть, не був пов'язаний з придушенням ранньої реабсорбції натрію в проксимальних ниркових канальцях. Лозартан також викликав минуще збільшення виділення сечової кислоти нирками. У пацієнтів з АГ, протеїнурією (не менше 2 г/24 год), без цукрового діабету та приймаючих лозартан протягом 8 тижнів у дозі 50 мг з поступовим збільшенням до 100 мг, спостерігалося достовірне зниження протеїнурії (на 42%), фракційної екскреції альбуміну. та імуноглобулінів (IgG). У цих пацієнтів лозартан стабілізував ШКФ та зменшував фільтраційну фракцію. У жінок у постменопаузальному періоді з АГ, які приймали лозартан у дозі 50 мг протягом 4 тижнів, не було виявлено впливу терапії на нирковий та системний рівень простагландинів. Лозартан не впливає на вегетативні рефлекси і не має тривалого ефекту щодо концентрації норадреналіну в плазмі крові. У пацієнтів з артеріальною гіпертензією лозартан у дозах до 150 мг на добу не викликав клінічно значущих змін концентрації тригліцеридів натще, загального холестерину та холестерину ліпопротеїнів високої щільності. У тих же дозах лозартан не впливав на концентрацію глюкози в крові натще. Загалом лозартан викликав зниження концентрації сечової кислоти в сироватці крові (зазвичай менше 0,4 мг/дл), що зберігалося при тривалому лікуванні. У контрольованих клінічних дослідженнях за участю пацієнтів з артеріальною гіпертензією випадків відміни препарату у зв'язку зі збільшенням концентрації креатиніну або вмісту калію в сироватці крові не зареєстровано. У 12-тижневому паралельному дослідженні, яке включали пацієнтів з лівошлуночковою недостатністю (II-IV функціонального класу за класифікацією NYHA), більшість з яких приймали діуретики та/або серцеві глікозиди, порівнювали ефекти лозартану в дозах 2,5, 10, 25 і 5 мг/добу з плацебо. У дозах 25 та 50 мг на добу препарат виявляв позитивні гемодинамічні та нейрогормональні ефекти, які зберігалися протягом усього дослідження. Гемодинамічні ефекти включали збільшення серцевого індексу та зниження тиску заклинювання у легеневих капілярах, а також зниження загального периферичного судинного опору, середнього системного АТ та частоти серцевих скорочень. Частота виникнення гіпотензії у цих пацієнтів залежала від дози препарату.Нейрогормональні ефекти включали зниження концентрації альдостерону та норадреналіну в крові.Показання до застосуванняАртеріальна гіпертензія (пацієнтам, яким показано комбіновану терапію). Зниження ризику асоційованої серцево-судинної захворюваності та смертності у пацієнтів з артеріальною гіпертензією та гіпертрофією лівого шлуночка, що проявляється сукупним зниженням частоти серцево-судинної смертності, частоти інсульту та інфаркту міокарда.Протипоказання до застосуванняПідвищена чутливість до будь-якого з компонентів препарату; Підвищена чутливість до інших похідних сульфонаміду; Анурія; Тяжкі порушення функції нирок (кліренс креатиніну менше 30 мл/хв); Тяжкі порушення функції печінки; Рефрактерна гіпокаліємія, гіпонатріємія, гіперкальціємія; Одночасне застосування з аліскіреном та препаратами, що містять аліскірен, у пацієнтів з цукровим діабетом та/або помірними або тяжкими порушеннями функції нирок (швидкість клубочкової фільтрації (СКФ) менше 60 мл/хв/1,73 м2 площі поверхні тіла); Одночасне застосування з інгібіторами АПФ у пацієнтів з діабетичною нефропатією; Вагітність та період грудного вигодовування; Дитячий вік до 18 років (ефективність та безпека застосування не встановлені); Рідкісна спадкова непереносимість галактози, дефіцит лактази, синдром глюкозо-галактозної мальабсорбції (препарат містить лактозу). З обережністю Двосторонній стеноз ниркових артерій чи стеноз артерії єдиної нирки; гіперкаліємія; стани після трансплантації нирки (відсутня досвід застосування); аортальний чи мітральний стеноз; гіпертрофічна обструктивна кардіоміопатія; хронічна серцева недостатність із супутнім тяжким порушенням функції нирок; тяжка серцева недостатність (IV функціонального класу за класифікацією NYHA); хронічна серцева недостатність з загрозливими для життя аритміями; ішемічна хвороба серця; цереброваскулярні захворювання; первинний гіперальдостеронізм; ангіоневротичний набряк в анамнезі; артеріальна гіпотензія; порушення функції печінки; порушення функції нирок; порушення водно-електролітного балансу; пацієнтам зі зниженим обсягом циркулюючої крові (наприклад,які отримують лікування великими дозами діуретиків) у зв'язку з можливістю виникнення симптоматичної артеріальної гіпотензії; гіпокаліємія; гіпонатріємія; гіперкальціємія; одночасне застосування лікарських засобів, які можуть викликати поліморфну шлуночкову тахікардію типу «пірует» або збільшувати тривалість інтервалу QT на ЕКГ; одночасне застосування лікарських засобів, здатних викликати гіпокаліємію, серцевих глікозидів; алергічні реакції на пеніцилін в анамнезі; гіперпаратиреоз; гіперурикемія; подагра, немеланомний рак шкіри в анамнезі.одночасне застосування лікарських засобів, здатних викликати гіпокаліємію, серцевих глікозидів; алергічні реакції на пеніцилін в анамнезі; гіперпаратиреоз; гіперурикемія; подагра, немеланомний рак шкіри в анамнезі.одночасне застосування лікарських засобів, здатних викликати гіпокаліємію, серцевих глікозидів; алергічні реакції на пеніцилін в анамнезі; гіперпаратиреоз; гіперурикемія; подагра, немеланомний рак шкіри в анамнезі.Вагітність та лактаціяЗастосування препарату Гідрохлортіазид+Лозартан-Акріхін при вагітності та в період грудного вигодовування протипоказане. Гідрохлоротіазид Вагітність Існує обмежений досвід застосування гідрохлортіазиду під час вагітності (особливо у першому триместрі). Доклінічні дані щодо безпеки недостатні. Гідрохлортіазид проникає через плацентарний бар'єр і визначається пуповинної крові. З урахуванням механізму фармакологічної дії гідрохлортіазиду, його застосування у другому та третьому триместрах вагітності може порушувати фетоплацентарну перфузію та призводити до розвитку у плода та новонародженого таких ускладнень, як жовтяниця, порушення водно-електролітного балансу та тромбоцитопенія. Описано випадки розвитку тромбоцитопенії у новонароджених, матері яких отримували тіазидні діуретики. Застосування гідрохлортіазиду під час вагітності протипоказане. Гідрохлортіазид не можна застосовувати для лікування гестозів ІІ половини вагітності (набряків, артеріальної гіпертензії або прееклампсії), т.к. він збільшує ризик зниження обсягу циркулюючої крові та плацентарної гіпоперфузії, але не надає сприятливого впливу протягом зазначених ускладнень вагітності. Діуретики не запобігають розвитку гестозів. Період грудного вигодовування Гідрохлортіазид проникає в материнське молоко, у зв'язку з чим його застосування у період грудного вигодовування протипоказане. Якщо застосування гідрохлортіазиду в період лактації є абсолютно необхідним, слід припинити грудне вигодовування. Лозартан Вагітність Лозартан протипоказаний під час вагітності. Терапію лозартаном не можна розпочинати під час вагітності. Якщо пацієнткам, які планують вагітність, продовження терапії лозартаном вважається за необхідне, слід замінити лозартан на альтернативні гіпотензивні засоби, які мають встановлений профіль безпеки при застосуванні під час вагітності. Хоча немає досвіду застосування лозартану у вагітних, доклінічні дослідження на тваринах показали, що прийом лозартану призводить до розвитку серйозних ембріональних та неонатальних ушкоджень та загибелі плода чи потомства. Вважається, що механізм даних явищ обумовлений впливом на РААС. Ниркова перфузія у плода, що залежить від розвитку РААС, з'являється у другому триместрі, тому ризик для плода зростає, якщо лозартан застосовується у другому або третьому триместрі вагітності.Застосування лікарських засобів, що впливають на РААС, у другому та третьому триместрі вагітності знижує функцію нирок плода та збільшує захворюваність та смертність плода та новонароджених. Розвиток олігогідрамніону може бути асоційований з гіпоплазією легких плода та деформаціями скелета. Можливі небажані явища у новонароджених включають гіпоплазію кісток черепа, анурію, артеріальну гіпотензію, ниркову недостатність та летальний кінець. Зазначені вище небажані наслідки зазвичай обумовлені застосуванням лікарських засобів, що впливають на РААС, у другому та третьому триместрі вагітності. Більшість епідеміологічних досліджень щодо вивчення розвитку аномалій плода після застосування гіпотензивних лікарських засобів у першому триместрі вагітності не виявили відмінностей між лікарськими засобами, що впливають на РААС,та іншими гіпотензивними засобами. При призначенні гіпотензивної терапії вагітним важливо оптимізувати можливі наслідки для матері та плода. Якщо неможливо підібрати альтернативну терапію замість терапії лікарськими засобами, що впливають на РААС, необхідно проінформувати пацієнтку про можливий ризик терапії для плода. Необхідне проведення періодичних ультразвукових досліджень з метою оцінки інтраамніотичного простору. При виявленні олігогідрамніону необхідно припинити прийом лозартану, якщо він не є життєво необхідним для матері. Залежно від тижня вагітності потрібне проведення відповідних тестів плода. Пацієнтки та лікарі повинні знати, що олігогідрамніон може не виявлятися до появи незворотних ушкоджень плода. Необхідно ретельне спостереження за новонародженими,чиї матері приймали лозартан під час вагітності з метою контролю артеріальної гіпотензії, олігурії та гіперкаліємії. Період грудного вигодовування Лозартан протипоказаний у період грудного вигодовування. Невідомо, чи виділяється лозартан із грудним молоком. Так як багато лікарських засобів виділяються з грудним молоком і існує ризик розвитку можливих несприятливих ефектів у дитини, яка перебуває на грудному вигодовуванні, слід прийняти рішення про припинення грудного вигодовування або про відміну препарату з урахуванням необхідності його прийому для матері.Побічна діяЧастота виникнення небажаних реакцій визначалася відповідно до класифікації Всесвітньої Організації Охорони Здоров'я: дуже часто (≥ 1/10); часто (≥ 1/100 та У клінічних дослідженнях з гідрохлортіазидом/лозартаном не спостерігалося небажаних явищ, специфічних для комбінованого препарату. Небажані явища обмежувалися тими, про які повідомлялося раніше при застосуванні гідрохлортіазиду та лозартану у монотерапії. Системно-органний клас Небажана реакція Гідрохло ротіазид+ Лозартан Гідрохлор-ротіазид Лозартан Порушення з боку крові та лімфатичної системи: анемія пурпура Шенлейн-Геноха екхімози гемолітична анемія тромбоцитопенія агранулоцитоз апластична анемія лейкопенія пурпура нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто частота невідома Алергічні реакції анафілактичні реакції ангіоневротичний набряк, включаючи набряк гортані та глотки, що викликає обструкцію дихальних шляхів, та/або набряк особи, губ, глотки та/або язика; у деяких пацієнтів ангіоневротичний набряк також відзначався в анамнезі при лікуванні іншими препаратами, включаючи інгібітори АПФ. ангіоневротичний набряк гортані, глотки, язика, обличчя, губ, слизових оболонок (у тому числі з летальним результатом) кропив'янка синдром Стівенса-Джонсона мультиформна еритема еритродермія рідко дуже рідко дуже рідко дуже рідко дуже рідко дуже рідко дуже рідко дуже рідко дуже рідко дуже рідко рідко рідко рідко рідко Порушення з боку метаболізму та харчування втрата апетиту гіперглікемія гіперурикемія порушення водно-електролітного балансу (зокрема гіпокаліємія та гіпонатріємія, гіпомагніємія та гіпохлоремія, а також гіперкальціємія) лікування тіазидами може знижувати толерантність до глюкози, і латентно протікає цукровий діабет може маніфестувати нечасто нечасто нечасто нечасто нечасто дуже рідко Порушення з боку центральної нервової системи головний біль запаморочення безсоння занепокоєння парестезія периферична нейропатія тремор мігрень непритомність тривога тривожний розлад (надмірний, неконтрольований і часто ірраціональний занепокоєння про повсякденні події) панічний розлад сплутаність свідомості депресія сонливість порушення сну часто нечасто нечасто часто часто часто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто Порушення з боку органу зору порушення зору відчуття сухості та печіння/почуття поколювання в очах кон'юнктивіт гостра міопія гостра закритокутова глаукома рідко дуже рідко рідко частота невідома частота невідома нечасто нечасто нечасто нечасто Порушення з боку органу слуху та лабіринтні порушення вертиго шум у вухах нечасто нечасто Порушення з боку дихальної системи закладеність носа кашель інфекції верхніх дихальних шляхів (підвищена температура тіла, біль у горлі, синусопатія, синусит, фарингіт) фарингіт ларингіт диспное бронхіт риніт носова кровотеча дискомфорт у глотковій області не часто часто часто часто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто Порушення з боку серцево-судинної системи некротизуючий ангіїт (васкуліт, шкірний васкуліт) виражене зниження артеріального тиску при надмірному зниженні АТ) васкуліт не часто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто Порушення з боку травної системи Порушення з боку шкіри та підшкірної клітковини Порушення з боку опорно-рухового апарату Порушення з боку сечостатевої системи Загальні порушення Лабораторні показники нудота діарея блювота запор диспептичні явища біль в животі сухість слизової оболонки порожнини рота » крові до шкіри обличчя шкірний свербіж висип підвищене потовиділення алопеція дерматит судоми в м'язах міалгія біль у спині, в ногах артралгія біль у руках, у плечі,колене артрит фибромиалгия скованность мышечная слабость припухлость суставов скелетно – мышечная боль рабдомиолиз нарушение функции почек почечная недостаточность интерстициальный нефрит глюкозурия никтурия учащенное мочеиспускание инфекции мочевыводящих путей ослабление либидо импотенция повышение температуры тела астения повышенная утомляемость анорексия отек лица отеки лихорадка гриппоподобные симптомы недомогание гиперкалиемия повышение активности «печеночных» трансаміназ зниження гематокриту та гемоглобіну гіпоглікемія підвищення концентрації сечовини та креатинінуанорексія набряк особи набряки лихоманка грипоподібні симптоми нездужання гіперкаліємія підвищення активності «печінкових» трансаміназ зниження гематокриту та гемоглобіну гіпоглікемія підвищення концентрації сечовини та креатинінуанорексія набряк особи набряки лихоманка грипоподібні симптоми нездужання гіперкаліємія підвищення активності «печінкових» трансаміназ зниження гематокриту та гемоглобіну гіпоглікемія підвищення концентрації сечовини та креатиніну рідко * рідко * рідко * нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто часто часто нечасто нечасто часто часто нечасто нечасто нечасто нечасто нечасто частота невідома частота невідома нечасто нечасто нечасто нечасто нечасто нечасто нечасто часто часто часто нечасто нечасто нечасто нечасто нечасто нечасто нечасто часто невідома частота невідома часто дуже рідко часто часто нечасто *-небажані явища спостерігалися при постмаркетинговому застосуванні гідрохлортіазиду/лозартану.Взаємодія з лікарськими засобамиГідрохлоротіазид Нерекомендовані поєднання лікарських засобів Препарати літію При одночасному застосуванні гідрохлортіазиду та препаратів літію знижується нирковий кліренс літію, що може призвести до підвищення концентрації літію у плазмі крові та збільшення його токсичності. При необхідності одночасного застосування гідрохлортіазиду слід ретельно підбирати дозу препаратів літію, регулярно контролювати концентрацію літію у плазмі крові та відповідним чином підбирати дозу препарату. Поєднання лікарських засобів, що вимагають особливої уваги Препарати, здатні викликати поліморфну шлуночкову тахікардію типу «пірует» Слід з особливою обережністю застосовувати гідрохлортіазид одночасно з такими препаратами, як: антиаритмічні лікарські препарати ІА класу (хінідин, гідрохінідин, дизопірамід, прокаїнамід); антиаритмічні лікарські препарати ІІІ класу (дофетилід, ібутилід, бретилія тозилат), соталол, дронедарон, аміодарон; інші (неантіаритмічні) лікарські засоби, такі як: нейролептики: фенотіазиниСпосіб застосування та дозиПрепарат Гідрохлортіазид+Лозартан-Акріхін приймається внутрішньо незалежно від їди. Препарат можна приймати у комбінації з іншими гіпотензивними засобами. Артеріальна гіпертензія Зазвичай початкова та підтримуюча доза -1 таблетка препарату Гідрохлортіазид+Лозартан-Акріхін 1 раз на добу. У пацієнтів без адекватної терапевтичної відповіді на прийом 1 таблетки препарату (містить 50 мг лозартану +12, 5 мг гідрохлортіазиду) 1 раз на добу протягом 2 – 4 тижнів, доза препарату може бути збільшена до 2 таблеток препарату 1 раз на добу. Максимальна доза – 2 таблетки (50 мг + 12,5 мг) 1 раз на добу. Як правило, антигіпертензивний ефект досягається протягом трьох тижнів після початку терапії. Зниження ризику серцево-судинної захворюваності та смертності у пацієнтів з артеріальною гіпертензією та гіпертрофією лівого шлуночка Зазвичай початкова доза 50 мг лозартану 1 раз на добу. Пацієнтам, у яких не вдається досягти цільових значень рівня АТ на фоні прийому лозартану 50 мг на добу, потрібен підбір терапії шляхом комбінації лозартану з низькими дозами гідрохлортіазиду (12,5 мг). У разі потреби потрібно збільшити дозу лозартану до 100 мг/кг у поєднанні з гідрохлортіазидом у дозі 12,5 мг/добу, надалі – збільшити дозу до 2 таблеток препарату Гідрохлортіазид + Лозартан – Акріхін (50 мг + 12,5 мг) 1 раз. на добу.ПередозуванняГідрохлоротіазид Симптоми Найчастішими проявами передозування гідрохлортіазидом є збільшення діурезу, що супроводжується гострою втратою рідини (дегідратацією) та електролітними порушеннями (гіпокаліємія, гіпонатріємія, гіпохлоремія). Передозування гідрохлортіазидом може виявлятися такими симптомами: з боку серцево-судинної системи: тахікардія; зниження артеріального тиску; шок; з боку нервової системи: слабкість, сплутаність свідомості, запаморочення та спазми литкових м'язів, парестезія, порушення свідомості, втома; з боку шлунково-кишкового тракту: нудота, блювання, спрага; з боку нирок та сечовивідних шляхів: поліурія, олігурія або анурія (через гемоконцентрацію). лабораторні показники: гіпоглікемія, гіпонатріємія, гіпохлоремія, алкалоз, підвищений вміст азоту сечовини у крові (особливо у пацієнтів із нирковою недостатністю). Лікування При передозуванні проводиться симптоматична та підтримуюча терапія. Якщо препарат був прийнятий нещодавно, для виведення гідрохлортіазиду показано індукцію блювоти або промивання шлунка. Абсорбцію гідрохлортіазиду можна зменшити прийомом внутрішньо активованого вугілля. У разі зниження АТ або шоку слід заповнити об'єм циркулюючої крові запровадженням плазмозамінних рідин та дефіцит електролітів (калій, натрій). При дихальних порушеннях показано інгаляцію кисню або штучну вентиляцію легень. Слід контролювати водно-електролітний баланс (особливо вміст калію у сироватці крові) та функцію нирок до їх нормалізації. Специфічного антидоту немає. Гідрохлортіазид виводиться при гемодіалізі, проте ступінь його виведення не встановлено. Лозартан Симптоми Відомості про передозування лозартану обмежені. Найбільш ймовірне прояв передозування - виражене зниження артеріального тиску та тахікардія; брадикардія може виникнути внаслідок парасимпатичної (вагусної) стимуляції. Лікування Симптоматична терапія. У разі розвитку симптоматичної артеріальної гіпотензії показано підтримуючу терапію. Лозартан та його активний метаболіт не виводяться за допомогою гемодіалізу.Запобіжні заходи та особливі вказівкиГідрохлоротіазид Артеріальна гіпотензія та порушення водно-електролітного балансу При застосуванні гіпотензивних засобів у деяких пацієнтів може розвинутись симптоматична артеріальна гіпотензія. Пацієнти повинні спостерігатися з метою своєчасного виявлення клінічних ознак порушення водно-електролітного балансу, наприклад, зневоднення, гіпонатріємії, гіпохлоремічного алкалозу, гіпомагніємії або гіпокаліємії, які можуть розвинутись на тлі супутньої діареї або блювання. У таких пацієнтів потрібний регулярний контроль вмісту електролітів сироватки крові. У пацієнтів з набряками може спостерігатися дилюційна гіпонатріємія у спеку. Метаболічні та ендокринні ефекти Терапія тіазидами може порушувати толерантність до глюкози. У ряді випадків може знадобитися корекція дози гіпоглікемічних засобів, у тому числі інсуліну. Тіазиди можуть знижувати виведення кальцію нирками та викликати короткочасне та незначне підвищення вмісту кальцію сироватки крові. Виражена гіперкальціємія може свідчити про прихований гіперпаратиреоз. У зв'язку з впливом тіазидів на метаболізм кальцію їх прийом може спотворювати результати дослідження функції паращитовидних залоз, тому перед дослідженням функції паращитовидних залоз тіазидний діуретик повинен бути скасований. Підвищення концентрації холестерину та тригліцеридів у крові також може бути пов'язане з терапією тіазидними діуретиками. У деяких пацієнтів прийом тіазидних діуретиків може призводити до гіперурикемії та/або розвитку подагри. Оскільки лозартан зменшує концентрацію сечової кислоти, його одночасне застосування з гідрохлортіазидом знижує вираженість гіперурикемії, спричиненої діуретиком. Порушення функції печінки Тіазиди слід застосовувати з обережністю у пацієнтів з порушеннями функції печінки або прогресуючим захворюванням печінки, оскільки це може призвести до розвитку внутрішньопечінкового холестазу, а незначні зміни водно-електролітного балансу можуть спровокувати розвиток печінкової коми. Препарат Гідрохлортіазид+Лозартан-Акріхін протипоказаний пацієнтам із тяжкими порушеннями функції печінки. Гостра міопія та вторинна закритокутова глаукома Гідрохлортіазид, похідний сульфонаміду, може викликати ідіосинкратичну реакцію у вигляді гострої транзиторної міопії та гострої закритокутової глаукоми. Симптомами цих порушень є несподіване зниження гостроти зору або біль в очах, які в типових випадках виникають протягом декількох годин до декількох тижнів після початку застосування препарату. Якщо не проводиться терапія, гостра глаукома може призвести до втрати зору. Основне лікування полягає в якнайшвидшому відміні гідрохлортіазиду. Необхідно мати на увазі, що якщо внутрішньоочний тиск залишається неконтрольованим, може знадобитися невідкладне консервативне або хірургічне лікування. До факторів ризику розвитку гострої глаукоми можна віднести відомості про алергію до сульфонамідів або пеніциліну в анамнезі. Немеланомний рак шкіри (НМРК) В епідеміологічних дослідженнях спостерігався підвищений ризик раку шкіри (базальноклітинної карциноми і плоскоклітинної карциноми) у зв'язку зі збільшенням сумарної (накопиченої) дози гідрохлортіазиду. Можливим механізмом розвитку НМРК є фотосенсибілізуюча дія гідрохлортіазиду. Пацієнти, які приймають гідрохлортіазид, повинні бути обізнані про ризик розвитку НМРК. Таким пацієнтам слід рекомендувати дотримуватись профілактичних заходів, таких як обмеження впливу сонячного світла та штучних UVA променів. Пацієнти повинні регулярно оглядати свої шкірні покриви з метою виявлення будь-яких нових підозрілих поразок та негайно повідомляти про них лікаря. У пацієнтів із НМРК в анамнезі рекомендується переглянути доцільність застосування гідрохлортіазиду. Інші ефекти У пацієнтів, які приймають тіазидні діуретики, реакції гіперчутливості можуть виникати навіть за відсутності в анамнезі алергічних реакцій або бронхіальної астми. Повідомлялося про рецидиви або посилення тяжкості перебігу системного червоного вовчаку у пацієнтів, які приймали тіазидні діуретики. Особливі групи пацієнтів Раса Аналіз даних всієї популяції пацієнтів, включених у дослідження LIFE щодо вивчення впливу лозартану на зниження частоти розвитку первинної кінцевої точки у пацієнтів з АГ та гіпертрофією лівого шлуночка (n = 9193), показав, що здатність лозартану порівняно з атенололом знижувати на 13,0% ризик розвитку серцево-судинних ускладнень (р = 0,021) не поширюється на пацієнтів негроїдної раси, хоча обидва режими терапії ефективно знижували рівень АТ у цих пацієнтів. Однак у цьому дослідженні пацієнти негроїдної раси, які отримували атенолол, мали менший ризик розвитку первинної кінцевої точки (серцево-судинна смертність, інсульт та інфаркт міокарда) порівняно з пацієнтами тієї ж раси, які приймали лозартан (р = 0,03). Діти та підлітки Ефективність та безпека застосування препарату Гідрохлортіазид+Лозартан-Акріхін у дітей та підлітків до 18 років не встановлені. Якщо у новонароджених, чиї матері приймали препарат Гідрохлортіазид+Лозартан-Акріхін під час вагітності, спостерігається розвиток олігурії або артеріальної гіпотензії, необхідно проведення симптоматичної терапії, спрямованої на підтримання артеріального тиску та ниркової перфузії. Може знадобитися переливання крові або проведення діалізу для запобігання розвитку артеріальної гіпотензії та/або підтримання функції нирок. Пацієнти похилого віку Клінічні дослідження не виявили жодних особливостей щодо безпеки та ефективності препарату Гідрохлортіазид+Лозартан-Акріхін у пацієнтів похилого віку (старше 65 років). Лозартан Артеріальна гіпотензія та зниження об'єму циркулюючої крові (ОЦК) У пацієнтів зі зниженим ОЦК або вмістом натрію в крові, що розвинулися через інтенсивну терапію діуретиками, дієти з обмеженням кухонної солі, діареї або блювання, може розвиватися симптоматична артеріальна гіпотензія, особливо після прийому першої дози препарату Гідрохлортіазид+Лозартан-Акрихін. Корекцію таких станів необхідно проводити до призначення препарату Гідрохлортіазид+Лозартан-Акріхін. Порушення водно-електролітного балансу Порушення водно-електролітного балансу характерне для пацієнтів з нирковою недостатністю з цукровим діабетом або без цукрового діабету, тому необхідно ретельне спостереження за даними пацієнтами. Необхідний ретельний контроль вмісту калію в крові або КК, особливо у пацієнтів із серцевою недостатністю та КК 30-50 мл/хв. Під час лікування препаратом Гідрохлортіазид+Лозартан-Акріхін не рекомендується приймати калійзберігаючі діуретики, препарати калію або замінники харчової солі, що містять калій. Аортальний або мітральний стеноз, гіпертрофічна обструктивна кардіоміопатія Як і всі лікарські засоби, що мають вазодилатуючу дію, АРА II повинні призначатися з обережністю пацієнтам з аортальним або мітральним стенозом або гіпертрофічною обструктивною кардіоміопатією. Ішемічна хвороба серця та цереброваскулярні захворювання Як і всі лікарські засоби, що мають вазодилатуючу дію, АРА II повинні призначатися з обережністю пацієнтам з ішемічною хворобою серця або цереброваскулярними захворюваннями, оскільки надмірне зниження артеріального тиску у цієї групи пацієнтів може призвести до розвитку інфаркту міокарда або інсульту. Хронічна серцева недостатність (ХСП) Як і при застосуванні інших лікарських засобів, що впливають на РААС, у пацієнтів з ХСН та з або без порушення функції нирок існує ризик розвитку тяжкої артеріальної гіпотензії або гострої ниркової недостатності. Первинний гіперальдостеронізм Оскільки у пацієнтів з первинним гіперальдостеронізмом, як правило, не спостерігається позитивної відповіді на терапію гіпотензивними засобами, що діють шляхом інгібування РААС, застосування препарату Гідрохлортіазид+Лозартан-Акріхін не рекомендується у цієї групи пацієнтів. Порушення функції печінки Дані фармакокінетичних досліджень вказують на те, що концентрація лозартану в плазмі крові у пацієнтів з цирозом печінки значно збільшується, тому пацієнтам з легким або помірним порушенням функції печінки в анамнезі препарат Гідрохлортіазид+Лозартан-Акріхін слід призначати з обережністю. Відсутня досвід застосування лозартану у пацієнтів з тяжкими порушеннями функції печінки (більше 9 балів за шкалою Чайлд-П'ю), тому препарат Гідрохлортіазид+Лозартан-Акріхін не повинен застосовуватись у цієї групи пацієнтів. Порушення функції нирок Внаслідок інгібування РААС у деяких схильних пацієнтів спостерігалися зміни функції нирок, включаючи розвиток ниркової недостатності. Ці зміни ниркової функції можуть повертатися до норми після припинення лікування. Деякі лікарські засоби, що впливають на РААС, можуть збільшувати концентрацію сечовини у крові та сироваткового креатиніну у пацієнтів із двостороннім стенозом ниркових артерій або стенозом ниркової артерії єдиної нирки. Повідомлялося про виникнення подібних ефектів прийому лозартану. Подібні порушення функції нирок можуть бути оборотними після відміни терапії. Лозартан повинен застосовуватися обережно у пацієнтів з двостороннім стенозом ниркових артерій або стенозом ниркової артерії єдиної нирки. Збільшення концентрації калію у сироватці крові Одночасне застосування інших препаратів, які здатні збільшувати вміст калію в сироватці, може призвести до розвитку гіперкаліємії (див. Взаємодія з іншими лікарськими засобами). Лозартан-гідрохлортіазид Реакції гіперчутливості У пацієнтів з ангіоневротичним набряком в анамнезі (набряк обличчя, губ, глотки/гортані та/або язика) необхідний контроль застосування препарату. Порушення функції нирок та печінки Препарат Гідрохлортіазид+Лозартан-Акріхін протипоказаний для застосування у пацієнтів з тяжкими порушеннями функції печінки та тяжкими порушеннями функції нирок (КК не більше 30 мл/хв). Ембріотоксичність Застосування лікарських засобів, що впливають на РААС, у другому та третьому триместрі вагітності знижує функцію нирок плода та збільшує захворюваність та смертність плода та новонароджених. Розвиток олігогідрамніону може бути асоційований з гіпоплазією легких плода та деформаціями скелета. Можливі небажані явища у новонароджених включають гіпоплазію кісток черепа, анурію, артеріальну гіпотензію, ниркову недостатність та летальний кінець. При діагностуванні вагітності препарат Гідрохлортіазид+Лозартан-Акріхін має бути одразу відмінено. Вплив на здатність до керування автотранспортом та управління механізмами Не проводилося досліджень для оцінки впливу на здатність керувати транспортними засобами та працювати з механізмами. При керуванні транспортними засобами або роботі з механізмами слід бути обережними через можливість розвитку запаморочення, слабкості та інших можливих небажаних реакцій.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
289,00 грн
242,00 грн
Склад, форма випуску та упаковкаПігулки - 1 таб. активні речовини: калію лозартан 50 мг; гідрохлортіазид 12,5 мг; допоміжні речовини: лактоза 111,55 мг, мікрокристалічна целюлоза 37,2 мг, крохмаль прежелатинізований 35 мг, магнію стеарат 3,75 мг; оболонка: опадрай зелений [гіпролоза, гіпромелоза, титану діоксид, барвник хіноліновий жовтий] 7,8 мг. Пігулки, покриті плівковою оболонкою, 12,5 мг + 50 мг. По 14 таблеток у блістер із ПВХ-алюмінієвої фольги. По 2 або 6 блістерів у картонній пачці разом із інструкцією із застосування.Опис лікарської формиДовгасті двоопуклі таблетки, вкриті оболонкою жовтого або жовтого із зеленуватим відтінком кольору.Фармакотерапевтична групаГіпотензивний комбінований засіб (діуретик + ангіотензину II рецепторів антагоніст).ФармакокінетикаГідрохлоротіазид Гідрохлортіазид не піддається метаболізму, але швидко виводиться нирками. При підтримці концентрації гідрохлортіазиду в плазмі крові протягом як мінімум 24 годин період напіввиведення варіював від 5,6 до 14,8 годин. Не менше 61% прийнятої внутрішньо дози виводиться у незміненому вигляді протягом 24 годин. проникає через гематоенцефалічний бар'єр. Лозартан Всмоктування При прийомі внутрішньо лозартан добре всмоктується та піддається метаболізму при «первинному проходженні» через печінку з утворенням активного карбоксильованого метаболіту та неактивних метаболітів. Системна біодоступність лозартану у таблетованій формі становить приблизно 33%. Середні Сmax лозартану та його активного метаболіту досягаються через 1 годину та через 3-4 години відповідно. При прийомі лозартану в процесі звичайного їди клінічно значущого впливу на профіль концентрації лозартану в плазмі виявлено не було. Розподіл Лозартан та його активний метаболіт пов'язуються з білками плазми крові (переважно з альбуміном) не менше ніж на 99%. Об'єм розподілу лозартану становить 34 л. Дослідження на щурах показали, що лозартан практично не проникає через гематоенцефалічний бар'єр. Метаболізм Приблизно 14% дози лозартану при внутрішньовенному введенні або прийомі внутрішньо перетворюється на його активний метаболіт. Після прийому внутрішньо або внутрішньовенного введення, міченого радіоактивним вуглецем лозартану (14С лозартану) радіоактивність циркулюючої плазми крові, перш за все, обумовлена наявністю в ній лозартану та його активного метаболіту. Низька ефективність перетворення лозартану на його активний метаболіт спостерігалася приблизно у 1% пацієнтів, які брали участь у дослідженні. Крім активного метаболіту утворюються біологічно неактивні метаболіти, у тому числі два основних метаболіти, що утворюються в результаті гідроксилювання бічного бутилового ланцюга, і один другорядний N-2-тетразол-глюкуронід. Виведення Плазмовий кліренс лозартану та його активного метаболіту становить близько 600 мл/хв та 50 мл/хв відповідно. Нирковий кліренс лозартану та його активного метаболіту становить приблизно 74 мл/хв та 26 мл/хв відповідно. При прийомі лозартану внутрішньо приблизно 4% дози виводиться нирками у незміненому вигляді та близько 6% дози виводиться нирками у вигляді активного метаболіту. Лозартан та його активний метаболіт мають лінійну фармакокінетику при прийомі внутрішньо лозартану у дозах до 200 мг. Після прийому внутрішньо плазмові концентрації лозартану та його активного метаболіту знижуються поліекспоненційно з кінцевим періодом напіввиведення приблизно 2 та 6-9 годин відповідно. При режимі дозування препарату 100 мг 1 раз на добу немає значного накопичення в плазмі крові ні лозартану, ні його активного метаболіту. Виведення лозартану та його метаболітів здійснюється нирками та через кишечник з жовчю. Після прийому внутрішньо 14С лозартану у чоловіків близько 35% радіоактивності виявляється у сечі та 58% у калі. Після внутрішньовенного введення 14С лозартану у чоловіків приблизно 43% радіоактивності виявляється у сечі та 50% у калі. Фармакокінетика у спеціальних груп пацієнтів Лозартан - гідрохлортіазид Літні пацієнти Концентрації лозартану та його активного метаболіту в плазмі крові та швидкість всмоктування гідрохлортіазиду у літніх пацієнтів з артеріальною гіпертензією значуще не відрізняються від цих показників у молодих пацієнтів з артеріальною гіпертензією. Лозартан Підлога Значення концентрації лозартану в плазмі крові у жінок з артеріальною гіпертензією в 2 рази перевищували відповідні значення у чоловіків з гіпертензією. Концентрації активного метаболіту у чоловіків та жінок не відрізнялися. Ця явна фармакокінетична відмінність, проте, не має клінічного значення. Пацієнти з порушенням функції печінки При прийомі лозартану внутрішньо пацієнтами з легким та помірним алкогольним цирозом печінки концентрації лозартану та його активного метаболіту у плазмі крові виявилися відповідно у 5 та 1,7 рази вищими, ніж у молодих здорових добровольців чоловічої статі. Пацієнти з порушенням функції нирок Концентрації лозартану в плазмі у пацієнтів з кліренсом креатиніну (КК) вище 10 мл/хв не відрізнялися від таких у пацієнтів з незміненою функцією нирок. Площа під кривою "концентрація-час" (AUC) лозартану у пацієнтів, які перебувають на гемодіалізі, була приблизно в 2 рази більша в порівнянні з AUC лозартану у пацієнтів з нормальною нирковою функцією. Концентрації активного метаболіту в плазмі не змінювалися у пацієнтів з порушенням функції нирок або пацієнтів, які перебували на гемодіалізі. Лозартан та його активний метаболіт не виводяться за допомогою процедури гемодіалізу.ФармакодинамікаГідрохлоротіазид Механізм антигіпертензивної дії тіазид невідомий. Тіазиди зазвичай не впливають на нормальний рівень артеріального тиску. Гідрохлортіазид є діуретиком та гіпотензивним засобом. Він впливає на реабсорбцію електролітів у дистальних канальцях нирок. Гідрохлортіазид приблизно однаково збільшує екскрецію іонів натрію і хлору. Натрійурез може супроводжуватися невеликою втратою іонів калію та бікарбонату. При внутрішньому прийомі діуретичний ефект розвивається протягом 2 годин, досягає максимуму в середньому через 4 години і триває від 6 до 12 годин. Лозартан Ангіотензин II є потужним вазоконстриктором, головним активним гормоном ренін-ангіотензин-альдостеронової системи (РААС), а також вирішальною ланкою при розвитку артеріальної гіпертензії (АГ). Ангіотензин II зв'язується з AT1-рецепторами, що знаходяться в багатьох тканинах (у гладком'язових тканинах судин, надниркових залозах, нирках і серці), і виконує кілька важливих біологічних функцій, включаючи вазоконстрикцію та вивільнення альдостерону. Крім цього, ангіотензин II стимулює розростання гладких клітин. АТ2-рецептори - другий тип рецепторів, з якими зв'язується ангіотензин II, але його роль у регуляції функції серцево-судинної системи невідома. Лозартан селективний антагоніст AT1-рецепторів ангіотензину II, високоефективний при внутрішньому прийомі. Лозартан та його фармакологічно активний карбоксильований метаболіт (Е-3174) як in vitro, так і in vivo блокують усі фізіологічні ефекти ангіотензину II незалежно від його джерела чи шляху синтезу. На відміну від деяких пептидних антагоністів ангіотензину II лозартан не має властивостей агоніста. Лозартан вибірково зв'язується з AT1-рецепторами і не зв'язується, і не блокує рецептори інших гормонів та іонних каналів, що відіграють важливу роль у регуляції функції серцево-судинної системи. Крім того, лозартан не інгібує ангіотензинперетворюючий фермент (АПФ, кініназа II), що відповідає за руйнування брадикініну. Отже, ефекти, які безпосередньо не пов'язані з блокадою AT1-рецепторів, такі як посилення брадикінін-опосередкованих ефектів або розвиток набряків (лозартан 1,7%, плацебо 1,9%), не мають відношення до дії лозартану. Препарат Гідрохлортіазид+Лозартан-Акріхін Компоненти препарату Гідрохлортіазид+Лозартан-Акріхін мають адитивну антигіпертензивну дію, знижуючи рівень артеріального тиску (АТ) більшою мірою, ніж кожен із компонентів окремо. Вважається, що цей ефект зумовлений взаємодоповнювальною дією обох компонентів. Внаслідок діуретичного ефекту гідрохлортіазид підвищує активність реніну плазми крові (АРП), стимулює секрецію альдостерону, збільшує концентрацію ангіотензину II та знижує вміст калію у сироватці крові. Прийом лозартану блокує всі фізіологічні ефекти ангіотензину II і внаслідок придушення ефектів альдостерону може сприяти зниженню втрати калію, пов'язаного з прийомом діуретика. Лозартан має помірний і минущий урикозуричний ефект. Гідрохлортіазид викликає невелике підвищення концентрації сечової кислоти у крові. Комбінація лозартану та гідрохлортіазиду сприяє зменшенню вираженості гіперурикемії, спричиненої діуретиком. Препарат Гідрохлортіазид+Лозартан-Акріхін є комбінованим препаратом лозартану та гідрохлортіазиду. У пацієнтів з артеріальною гіпертензією та гіпертрофією лівого шлуночка лозартан, у тому числі в комбінації з гідрохлоротіазидом, зменшує ризик серцево-судинної захворюваності та смертності, що було доведено за допомогою оцінки комбінованої частоти розвитку інсульту та інфаркту міокарда, а також показника серцевості. цієї категорії хворих. Гідрохлоротіазид Механізм антигіпертензивної дії тіазид невідомий. Зазвичай, тіазиди не впливають на нормальні значення АТ. Гідрохлортіазид є діуретичним та гіпотензивним засобом. Він впливає на механізм реабсорбції електролітів у дистальних звивистих ниркових канальцях. Гідрохлортіазид збільшує екскрецію натрію та хлориду приблизно в еквівалентних кількостях. Натрійурез може супроводжуватися деякою втратою іонів калію та бікарбонату. Після прийому внутрішньо діурез починається протягом 2 год, досягає максимуму протягом приблизно 4 год і триває приблизно 6-12 год. Лозартан Лозартан пригнічує підвищення систолічного та діастолічного артеріального тиску (АТ) при інфузії ангіотензину ІІ. У момент досягнення максимальної концентрації лозартану в плазмі крові (Сmax) після прийому лозартану в дозі 100 мг вищевказаний ефект ангіотензину II пригнічується приблизно на 85%, а через 24 години після одноразового та багаторазового прийому на 26-39%. У період прийому лозартану усунення негативного зворотного зв'язку, що полягає у придушенні ангіотензином II секреції реніну, веде до збільшення АРП. Збільшення АРП призводить до збільшення концентрації ангіотензину ІІ у плазмі крові. При тривалому (6-тижневому) лікуванні пацієнтів з артеріальною гіпертензією лозартаном у дозі 100 мг на добу спостерігалося 2-3-кратне збільшення концентрації ангіотензину II у плазмі крові в момент досягнення Сmax лозартану. У деяких пацієнтів спостерігалося ще більше збільшення концентрації ангіотензину II, особливо при невеликій тривалості лікування (2 тижні). Незважаючи на це, у процесі лікування антигіпертензивний ефект та зниження концентрації альдостерону у плазмі крові виявлялися через 2 та 6 тижнів терапії, що вказує на ефективну блокаду рецепторів ангіотензину ІІ.Після відміни лозартану АРП та концентрації ангіотензину II знижувалися протягом 3 діб до значень, що спостерігалися до початку прийому лозартану. Вплив препарату Гідрохлортіазид+Лозартан-Акріхін на АРП та концентрацію ангіотензину II був подібним до спостеріганих ефектів при прийомі лозартану в дозі 50 мг. Оскільки лозартан є специфічним антагоністом AT1-рецепторів ангіотензину II, він не пригнічує АПФ (кініназу II) — фермент, який інактивує брадикінін. Дослідження, в якому порівнювалися ефекти лозартану в дозах 20 мг та 100 мг з ефектами інгібітору АПФ за впливом на ангіотензин I, ангіотензин II та брадикінін, показало, що лозартан блокує ефекти ангіотензину I та ангіотензину II, не впливаючи на ефект. Це зумовлено специфічним механізмом дії лозартану. Інгібітор АПФ блокував реакції на ангіотензин I і підвищував вираженість ефектів, зумовлених дією брадикініну, не впливаючи на вираженість відповіді на ангіотензин II, що демонструє фармакодинамічну різницю між лозартаном та інгібіторами АПФ. Концентрації лозартану та його активного метаболіту у плазмі крові, а також антигіпертензивний ефект лозартану зростають із збільшенням дози препарату. Оскільки лозартан та його активний метаболіт є антагоністами рецепторів ангіотензину II (АРА II), вони обидва роблять внесок у антигіпертензивний ефект. У дослідженні з одноразовим прийомом лозартану в дозі 100 мг, до якого включалися здорові добровольці (чоловіки), прийом препарату внутрішньо в умовах високо- та малосольової дієти не впливав на швидкість клубочкової фільтрації (СКФ), ефективний нирковий плазмоток та фільтраційну фракцію. Лозартан мав натрійуретіческій ефект, який був більш виражений при малосольової дієті і, мабуть, не був пов'язаний з придушенням ранньої реабсорбції натрію в проксимальних ниркових канальцях. Лозартан також викликав минуще збільшення виділення сечової кислоти нирками. У пацієнтів з АГ, протеїнурією (не менше 2 г/24 год), без цукрового діабету та приймаючих лозартан протягом 8 тижнів у дозі 50 мг з поступовим збільшенням до 100 мг, спостерігалося достовірне зниження протеїнурії (на 42%), фракційної екскреції альбуміну. та імуноглобулінів (IgG). У цих пацієнтів лозартан стабілізував ШКФ та зменшував фільтраційну фракцію. У жінок у постменопаузальному періоді з АГ, які приймали лозартан у дозі 50 мг протягом 4 тижнів, не було виявлено впливу терапії на нирковий та системний рівень простагландинів. Лозартан не впливає на вегетативні рефлекси і не має тривалого ефекту щодо концентрації норадреналіну в плазмі крові. У пацієнтів з артеріальною гіпертензією лозартан у дозах до 150 мг на добу не викликав клінічно значущих змін концентрації тригліцеридів натще, загального холестерину та холестерину ліпопротеїнів високої щільності. У тих же дозах лозартан не впливав на концентрацію глюкози в крові натще. Загалом лозартан викликав зниження концентрації сечової кислоти в сироватці крові (зазвичай менше 0,4 мг/дл), що зберігалося при тривалому лікуванні. У контрольованих клінічних дослідженнях за участю пацієнтів з артеріальною гіпертензією випадків відміни препарату у зв'язку зі збільшенням концентрації креатиніну або вмісту калію в сироватці крові не зареєстровано. У 12-тижневому паралельному дослідженні, яке включали пацієнтів з лівошлуночковою недостатністю (II-IV функціонального класу за класифікацією NYHA), більшість з яких приймали діуретики та/або серцеві глікозиди, порівнювали ефекти лозартану в дозах 2,5, 10, 25 і 5 мг/добу з плацебо. У дозах 25 та 50 мг на добу препарат виявляв позитивні гемодинамічні та нейрогормональні ефекти, які зберігалися протягом усього дослідження. Гемодинамічні ефекти включали збільшення серцевого індексу та зниження тиску заклинювання у легеневих капілярах, а також зниження загального периферичного судинного опору, середнього системного АТ та частоти серцевих скорочень. Частота виникнення гіпотензії у цих пацієнтів залежала від дози препарату.Нейрогормональні ефекти включали зниження концентрації альдостерону та норадреналіну в крові.Показання до застосуванняАртеріальна гіпертензія (пацієнтам, яким показано комбіновану терапію). Зниження ризику асоційованої серцево-судинної захворюваності та смертності у пацієнтів з артеріальною гіпертензією та гіпертрофією лівого шлуночка, що проявляється сукупним зниженням частоти серцево-судинної смертності, частоти інсульту та інфаркту міокарда.Протипоказання до застосуванняПідвищена чутливість до будь-якого з компонентів препарату; Підвищена чутливість до інших похідних сульфонаміду; Анурія; Тяжкі порушення функції нирок (кліренс креатиніну менше 30 мл/хв); Тяжкі порушення функції печінки; Рефрактерна гіпокаліємія, гіпонатріємія, гіперкальціємія; Одночасне застосування з аліскіреном та препаратами, що містять аліскірен, у пацієнтів з цукровим діабетом та/або помірними або тяжкими порушеннями функції нирок (швидкість клубочкової фільтрації (СКФ) менше 60 мл/хв/1,73 м2 площі поверхні тіла); Одночасне застосування з інгібіторами АПФ у пацієнтів з діабетичною нефропатією; Вагітність та період грудного вигодовування; Дитячий вік до 18 років (ефективність та безпека застосування не встановлені); Рідкісна спадкова непереносимість галактози, дефіцит лактази, синдром глюкозо-галактозної мальабсорбції (препарат містить лактозу). З обережністю Двосторонній стеноз ниркових артерій чи стеноз артерії єдиної нирки; гіперкаліємія; стани після трансплантації нирки (відсутня досвід застосування); аортальний чи мітральний стеноз; гіпертрофічна обструктивна кардіоміопатія; хронічна серцева недостатність із супутнім тяжким порушенням функції нирок; тяжка серцева недостатність (IV функціонального класу за класифікацією NYHA); хронічна серцева недостатність з загрозливими для життя аритміями; ішемічна хвороба серця; цереброваскулярні захворювання; первинний гіперальдостеронізм; ангіоневротичний набряк в анамнезі; артеріальна гіпотензія; порушення функції печінки; порушення функції нирок; порушення водно-електролітного балансу; пацієнтам зі зниженим обсягом циркулюючої крові (наприклад,які отримують лікування великими дозами діуретиків) у зв'язку з можливістю виникнення симптоматичної артеріальної гіпотензії; гіпокаліємія; гіпонатріємія; гіперкальціємія; одночасне застосування лікарських засобів, які можуть викликати поліморфну шлуночкову тахікардію типу «пірует» або збільшувати тривалість інтервалу QT на ЕКГ; одночасне застосування лікарських засобів, здатних викликати гіпокаліємію, серцевих глікозидів; алергічні реакції на пеніцилін в анамнезі; гіперпаратиреоз; гіперурикемія; подагра, немеланомний рак шкіри в анамнезі.одночасне застосування лікарських засобів, здатних викликати гіпокаліємію, серцевих глікозидів; алергічні реакції на пеніцилін в анамнезі; гіперпаратиреоз; гіперурикемія; подагра, немеланомний рак шкіри в анамнезі.одночасне застосування лікарських засобів, здатних викликати гіпокаліємію, серцевих глікозидів; алергічні реакції на пеніцилін в анамнезі; гіперпаратиреоз; гіперурикемія; подагра, немеланомний рак шкіри в анамнезі.Вагітність та лактаціяЗастосування препарату Гідрохлортіазид+Лозартан-Акріхін при вагітності та в період грудного вигодовування протипоказане. Гідрохлоротіазид Вагітність Існує обмежений досвід застосування гідрохлортіазиду під час вагітності (особливо у першому триместрі). Доклінічні дані щодо безпеки недостатні. Гідрохлортіазид проникає через плацентарний бар'єр і визначається пуповинної крові. З урахуванням механізму фармакологічної дії гідрохлортіазиду, його застосування у другому та третьому триместрах вагітності може порушувати фетоплацентарну перфузію та призводити до розвитку у плода та новонародженого таких ускладнень, як жовтяниця, порушення водно-електролітного балансу та тромбоцитопенія. Описано випадки розвитку тромбоцитопенії у новонароджених, матері яких отримували тіазидні діуретики. Застосування гідрохлортіазиду під час вагітності протипоказане. Гідрохлортіазид не можна застосовувати для лікування гестозів ІІ половини вагітності (набряків, артеріальної гіпертензії або прееклампсії), т.к. він збільшує ризик зниження обсягу циркулюючої крові та плацентарної гіпоперфузії, але не надає сприятливого впливу протягом зазначених ускладнень вагітності. Діуретики не запобігають розвитку гестозів. Період грудного вигодовування Гідрохлортіазид проникає в материнське молоко, у зв'язку з чим його застосування у період грудного вигодовування протипоказане. Якщо застосування гідрохлортіазиду в період лактації є абсолютно необхідним, слід припинити грудне вигодовування. Лозартан Вагітність Лозартан протипоказаний під час вагітності. Терапію лозартаном не можна розпочинати під час вагітності. Якщо пацієнткам, які планують вагітність, продовження терапії лозартаном вважається за необхідне, слід замінити лозартан на альтернативні гіпотензивні засоби, які мають встановлений профіль безпеки при застосуванні під час вагітності. Хоча немає досвіду застосування лозартану у вагітних, доклінічні дослідження на тваринах показали, що прийом лозартану призводить до розвитку серйозних ембріональних та неонатальних ушкоджень та загибелі плода чи потомства. Вважається, що механізм даних явищ обумовлений впливом на РААС. Ниркова перфузія у плода, що залежить від розвитку РААС, з'являється у другому триместрі, тому ризик для плода зростає, якщо лозартан застосовується у другому або третьому триместрі вагітності.Застосування лікарських засобів, що впливають на РААС, у другому та третьому триместрі вагітності знижує функцію нирок плода та збільшує захворюваність та смертність плода та новонароджених. Розвиток олігогідрамніону може бути асоційований з гіпоплазією легких плода та деформаціями скелета. Можливі небажані явища у новонароджених включають гіпоплазію кісток черепа, анурію, артеріальну гіпотензію, ниркову недостатність та летальний кінець. Зазначені вище небажані наслідки зазвичай обумовлені застосуванням лікарських засобів, що впливають на РААС, у другому та третьому триместрі вагітності. Більшість епідеміологічних досліджень щодо вивчення розвитку аномалій плода після застосування гіпотензивних лікарських засобів у першому триместрі вагітності не виявили відмінностей між лікарськими засобами, що впливають на РААС,та іншими гіпотензивними засобами. При призначенні гіпотензивної терапії вагітним важливо оптимізувати можливі наслідки для матері та плода. Якщо неможливо підібрати альтернативну терапію замість терапії лікарськими засобами, що впливають на РААС, необхідно проінформувати пацієнтку про можливий ризик терапії для плода. Необхідне проведення періодичних ультразвукових досліджень з метою оцінки інтраамніотичного простору. При виявленні олігогідрамніону необхідно припинити прийом лозартану, якщо він не є життєво необхідним для матері. Залежно від тижня вагітності потрібне проведення відповідних тестів плода. Пацієнтки та лікарі повинні знати, що олігогідрамніон може не виявлятися до появи незворотних ушкоджень плода. Необхідно ретельне спостереження за новонародженими,чиї матері приймали лозартан під час вагітності з метою контролю артеріальної гіпотензії, олігурії та гіперкаліємії. Період грудного вигодовування Лозартан протипоказаний у період грудного вигодовування. Невідомо, чи виділяється лозартан із грудним молоком. Так як багато лікарських засобів виділяються з грудним молоком і існує ризик розвитку можливих несприятливих ефектів у дитини, яка перебуває на грудному вигодовуванні, слід прийняти рішення про припинення грудного вигодовування або про відміну препарату з урахуванням необхідності його прийому для матері.Побічна діяЧастота виникнення небажаних реакцій визначалася відповідно до класифікації Всесвітньої Організації Охорони Здоров'я: дуже часто (≥ 1/10); часто (≥ 1/100 та У клінічних дослідженнях з гідрохлортіазидом/лозартаном не спостерігалося небажаних явищ, специфічних для комбінованого препарату. Небажані явища обмежувалися тими, про які повідомлялося раніше при застосуванні гідрохлортіазиду та лозартану у монотерапії. Системно-органний клас Небажана реакція Гідрохло ротіазид+ Лозартан Гідрохлор-ротіазид Лозартан Порушення з боку крові та лімфатичної системи: анемія пурпура Шенлейн-Геноха екхімози гемолітична анемія тромбоцитопенія агранулоцитоз апластична анемія лейкопенія пурпура нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто частота невідома Алергічні реакції анафілактичні реакції ангіоневротичний набряк, включаючи набряк гортані та глотки, що викликає обструкцію дихальних шляхів, та/або набряк особи, губ, глотки та/або язика; у деяких пацієнтів ангіоневротичний набряк також відзначався в анамнезі при лікуванні іншими препаратами, включаючи інгібітори АПФ. ангіоневротичний набряк гортані, глотки, язика, обличчя, губ, слизових оболонок (у тому числі з летальним результатом) кропив'янка синдром Стівенса-Джонсона мультиформна еритема еритродермія рідко дуже рідко дуже рідко дуже рідко дуже рідко дуже рідко дуже рідко дуже рідко дуже рідко дуже рідко рідко рідко рідко рідко Порушення з боку метаболізму та харчування втрата апетиту гіперглікемія гіперурикемія порушення водно-електролітного балансу (зокрема гіпокаліємія та гіпонатріємія, гіпомагніємія та гіпохлоремія, а також гіперкальціємія) лікування тіазидами може знижувати толерантність до глюкози, і латентно протікає цукровий діабет може маніфестувати нечасто нечасто нечасто нечасто нечасто дуже рідко Порушення з боку центральної нервової системи головний біль запаморочення безсоння занепокоєння парестезія периферична нейропатія тремор мігрень непритомність тривога тривожний розлад (надмірний, неконтрольований і часто ірраціональний занепокоєння про повсякденні події) панічний розлад сплутаність свідомості депресія сонливість порушення сну часто нечасто нечасто часто часто часто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто Порушення з боку органу зору порушення зору відчуття сухості та печіння/почуття поколювання в очах кон'юнктивіт гостра міопія гостра закритокутова глаукома рідко дуже рідко рідко частота невідома частота невідома нечасто нечасто нечасто нечасто Порушення з боку органу слуху та лабіринтні порушення вертиго шум у вухах нечасто нечасто Порушення з боку дихальної системи закладеність носа кашель інфекції верхніх дихальних шляхів (підвищена температура тіла, біль у горлі, синусопатія, синусит, фарингіт) фарингіт ларингіт диспное бронхіт риніт носова кровотеча дискомфорт у глотковій області не часто часто часто часто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто Порушення з боку серцево-судинної системи некротизуючий ангіїт (васкуліт, шкірний васкуліт) виражене зниження артеріального тиску при надмірному зниженні АТ) васкуліт не часто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто Порушення з боку травної системи Порушення з боку шкіри та підшкірної клітковини Порушення з боку опорно-рухового апарату Порушення з боку сечостатевої системи Загальні порушення Лабораторні показники нудота діарея блювота запор диспептичні явища біль в животі сухість слизової оболонки порожнини рота » крові до шкіри обличчя шкірний свербіж висип підвищене потовиділення алопеція дерматит судоми в м'язах міалгія біль у спині, в ногах артралгія біль у руках, у плечі,колене артрит фибромиалгия скованность мышечная слабость припухлость суставов скелетно – мышечная боль рабдомиолиз нарушение функции почек почечная недостаточность интерстициальный нефрит глюкозурия никтурия учащенное мочеиспускание инфекции мочевыводящих путей ослабление либидо импотенция повышение температуры тела астения повышенная утомляемость анорексия отек лица отеки лихорадка гриппоподобные симптомы недомогание гиперкалиемия повышение активности «печеночных» трансаміназ зниження гематокриту та гемоглобіну гіпоглікемія підвищення концентрації сечовини та креатинінуанорексія набряк особи набряки лихоманка грипоподібні симптоми нездужання гіперкаліємія підвищення активності «печінкових» трансаміназ зниження гематокриту та гемоглобіну гіпоглікемія підвищення концентрації сечовини та креатинінуанорексія набряк особи набряки лихоманка грипоподібні симптоми нездужання гіперкаліємія підвищення активності «печінкових» трансаміназ зниження гематокриту та гемоглобіну гіпоглікемія підвищення концентрації сечовини та креатиніну рідко * рідко * рідко * нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто часто часто нечасто нечасто часто часто нечасто нечасто нечасто нечасто нечасто частота невідома частота невідома нечасто нечасто нечасто нечасто нечасто нечасто нечасто часто часто часто нечасто нечасто нечасто нечасто нечасто нечасто нечасто часто невідома частота невідома часто дуже рідко часто часто нечасто *-небажані явища спостерігалися при постмаркетинговому застосуванні гідрохлортіазиду/лозартану.Взаємодія з лікарськими засобамиГідрохлоротіазид Нерекомендовані поєднання лікарських засобів Препарати літію При одночасному застосуванні гідрохлортіазиду та препаратів літію знижується нирковий кліренс літію, що може призвести до підвищення концентрації літію у плазмі крові та збільшення його токсичності. При необхідності одночасного застосування гідрохлортіазиду слід ретельно підбирати дозу препаратів літію, регулярно контролювати концентрацію літію у плазмі крові та відповідним чином підбирати дозу препарату. Поєднання лікарських засобів, що вимагають особливої уваги Препарати, здатні викликати поліморфну шлуночкову тахікардію типу «пірует» Слід з особливою обережністю застосовувати гідрохлортіазид одночасно з такими препаратами, як: антиаритмічні лікарські препарати ІА класу (хінідин, гідрохінідин, дизопірамід, прокаїнамід); антиаритмічні лікарські препарати ІІІ класу (дофетилід, ібутилід, бретилія тозилат), соталол, дронедарон, аміодарон; інші (неантіаритмічні) лікарські засоби, такі як: нейролептики: фенотіазиниСпосіб застосування та дозиПрепарат Гідрохлортіазид+Лозартан-Акріхін приймається внутрішньо незалежно від їди. Препарат можна приймати у комбінації з іншими гіпотензивними засобами. Артеріальна гіпертензія Зазвичай початкова та підтримуюча доза -1 таблетка препарату Гідрохлортіазид+Лозартан-Акріхін 1 раз на добу. У пацієнтів без адекватної терапевтичної відповіді на прийом 1 таблетки препарату (містить 50 мг лозартану +12, 5 мг гідрохлортіазиду) 1 раз на добу протягом 2 – 4 тижнів, доза препарату може бути збільшена до 2 таблеток препарату 1 раз на добу. Максимальна доза – 2 таблетки (50 мг + 12,5 мг) 1 раз на добу. Як правило, антигіпертензивний ефект досягається протягом трьох тижнів після початку терапії. Зниження ризику серцево-судинної захворюваності та смертності у пацієнтів з артеріальною гіпертензією та гіпертрофією лівого шлуночка Зазвичай початкова доза 50 мг лозартану 1 раз на добу. Пацієнтам, у яких не вдається досягти цільових значень рівня АТ на фоні прийому лозартану 50 мг на добу, потрібен підбір терапії шляхом комбінації лозартану з низькими дозами гідрохлортіазиду (12,5 мг). У разі потреби потрібно збільшити дозу лозартану до 100 мг/кг у поєднанні з гідрохлортіазидом у дозі 12,5 мг/добу, надалі – збільшити дозу до 2 таблеток препарату Гідрохлортіазид + Лозартан – Акріхін (50 мг + 12,5 мг) 1 раз. на добу.ПередозуванняГідрохлоротіазид Симптоми Найчастішими проявами передозування гідрохлортіазидом є збільшення діурезу, що супроводжується гострою втратою рідини (дегідратацією) та електролітними порушеннями (гіпокаліємія, гіпонатріємія, гіпохлоремія). Передозування гідрохлортіазидом може виявлятися такими симптомами: з боку серцево-судинної системи: тахікардія; зниження артеріального тиску; шок; з боку нервової системи: слабкість, сплутаність свідомості, запаморочення та спазми литкових м'язів, парестезія, порушення свідомості, втома; з боку шлунково-кишкового тракту: нудота, блювання, спрага; з боку нирок та сечовивідних шляхів: поліурія, олігурія або анурія (через гемоконцентрацію). лабораторні показники: гіпоглікемія, гіпонатріємія, гіпохлоремія, алкалоз, підвищений вміст азоту сечовини у крові (особливо у пацієнтів із нирковою недостатністю). Лікування При передозуванні проводиться симптоматична та підтримуюча терапія. Якщо препарат був прийнятий нещодавно, для виведення гідрохлортіазиду показано індукцію блювоти або промивання шлунка. Абсорбцію гідрохлортіазиду можна зменшити прийомом внутрішньо активованого вугілля. У разі зниження АТ або шоку слід заповнити об'єм циркулюючої крові запровадженням плазмозамінних рідин та дефіцит електролітів (калій, натрій). При дихальних порушеннях показано інгаляцію кисню або штучну вентиляцію легень. Слід контролювати водно-електролітний баланс (особливо вміст калію у сироватці крові) та функцію нирок до їх нормалізації. Специфічного антидоту немає. Гідрохлортіазид виводиться при гемодіалізі, проте ступінь його виведення не встановлено. Лозартан Симптоми Відомості про передозування лозартану обмежені. Найбільш ймовірне прояв передозування - виражене зниження артеріального тиску та тахікардія; брадикардія може виникнути внаслідок парасимпатичної (вагусної) стимуляції. Лікування Симптоматична терапія. У разі розвитку симптоматичної артеріальної гіпотензії показано підтримуючу терапію. Лозартан та його активний метаболіт не виводяться за допомогою гемодіалізу.Запобіжні заходи та особливі вказівкиГідрохлоротіазид Артеріальна гіпотензія та порушення водно-електролітного балансу При застосуванні гіпотензивних засобів у деяких пацієнтів може розвинутись симптоматична артеріальна гіпотензія. Пацієнти повинні спостерігатися з метою своєчасного виявлення клінічних ознак порушення водно-електролітного балансу, наприклад, зневоднення, гіпонатріємії, гіпохлоремічного алкалозу, гіпомагніємії або гіпокаліємії, які можуть розвинутись на тлі супутньої діареї або блювання. У таких пацієнтів потрібний регулярний контроль вмісту електролітів сироватки крові. У пацієнтів з набряками може спостерігатися дилюційна гіпонатріємія у спеку. Метаболічні та ендокринні ефекти Терапія тіазидами може порушувати толерантність до глюкози. У ряді випадків може знадобитися корекція дози гіпоглікемічних засобів, у тому числі інсуліну. Тіазиди можуть знижувати виведення кальцію нирками та викликати короткочасне та незначне підвищення вмісту кальцію сироватки крові. Виражена гіперкальціємія може свідчити про прихований гіперпаратиреоз. У зв'язку з впливом тіазидів на метаболізм кальцію їх прийом може спотворювати результати дослідження функції паращитовидних залоз, тому перед дослідженням функції паращитовидних залоз тіазидний діуретик повинен бути скасований. Підвищення концентрації холестерину та тригліцеридів у крові також може бути пов'язане з терапією тіазидними діуретиками. У деяких пацієнтів прийом тіазидних діуретиків може призводити до гіперурикемії та/або розвитку подагри. Оскільки лозартан зменшує концентрацію сечової кислоти, його одночасне застосування з гідрохлортіазидом знижує вираженість гіперурикемії, спричиненої діуретиком. Порушення функції печінки Тіазиди слід застосовувати з обережністю у пацієнтів з порушеннями функції печінки або прогресуючим захворюванням печінки, оскільки це може призвести до розвитку внутрішньопечінкового холестазу, а незначні зміни водно-електролітного балансу можуть спровокувати розвиток печінкової коми. Препарат Гідрохлортіазид+Лозартан-Акріхін протипоказаний пацієнтам із тяжкими порушеннями функції печінки. Гостра міопія та вторинна закритокутова глаукома Гідрохлортіазид, похідний сульфонаміду, може викликати ідіосинкратичну реакцію у вигляді гострої транзиторної міопії та гострої закритокутової глаукоми. Симптомами цих порушень є несподіване зниження гостроти зору або біль в очах, які в типових випадках виникають протягом декількох годин до декількох тижнів після початку застосування препарату. Якщо не проводиться терапія, гостра глаукома може призвести до втрати зору. Основне лікування полягає в якнайшвидшому відміні гідрохлортіазиду. Необхідно мати на увазі, що якщо внутрішньоочний тиск залишається неконтрольованим, може знадобитися невідкладне консервативне або хірургічне лікування. До факторів ризику розвитку гострої глаукоми можна віднести відомості про алергію до сульфонамідів або пеніциліну в анамнезі. Немеланомний рак шкіри (НМРК) В епідеміологічних дослідженнях спостерігався підвищений ризик раку шкіри (базальноклітинної карциноми і плоскоклітинної карциноми) у зв'язку зі збільшенням сумарної (накопиченої) дози гідрохлортіазиду. Можливим механізмом розвитку НМРК є фотосенсибілізуюча дія гідрохлортіазиду. Пацієнти, які приймають гідрохлортіазид, повинні бути обізнані про ризик розвитку НМРК. Таким пацієнтам слід рекомендувати дотримуватись профілактичних заходів, таких як обмеження впливу сонячного світла та штучних UVA променів. Пацієнти повинні регулярно оглядати свої шкірні покриви з метою виявлення будь-яких нових підозрілих поразок та негайно повідомляти про них лікаря. У пацієнтів із НМРК в анамнезі рекомендується переглянути доцільність застосування гідрохлортіазиду. Інші ефекти У пацієнтів, які приймають тіазидні діуретики, реакції гіперчутливості можуть виникати навіть за відсутності в анамнезі алергічних реакцій або бронхіальної астми. Повідомлялося про рецидиви або посилення тяжкості перебігу системного червоного вовчаку у пацієнтів, які приймали тіазидні діуретики. Особливі групи пацієнтів Раса Аналіз даних всієї популяції пацієнтів, включених у дослідження LIFE щодо вивчення впливу лозартану на зниження частоти розвитку первинної кінцевої точки у пацієнтів з АГ та гіпертрофією лівого шлуночка (n = 9193), показав, що здатність лозартану порівняно з атенололом знижувати на 13,0% ризик розвитку серцево-судинних ускладнень (р = 0,021) не поширюється на пацієнтів негроїдної раси, хоча обидва режими терапії ефективно знижували рівень АТ у цих пацієнтів. Однак у цьому дослідженні пацієнти негроїдної раси, які отримували атенолол, мали менший ризик розвитку первинної кінцевої точки (серцево-судинна смертність, інсульт та інфаркт міокарда) порівняно з пацієнтами тієї ж раси, які приймали лозартан (р = 0,03). Діти та підлітки Ефективність та безпека застосування препарату Гідрохлортіазид+Лозартан-Акріхін у дітей та підлітків до 18 років не встановлені. Якщо у новонароджених, чиї матері приймали препарат Гідрохлортіазид+Лозартан-Акріхін під час вагітності, спостерігається розвиток олігурії або артеріальної гіпотензії, необхідно проведення симптоматичної терапії, спрямованої на підтримання артеріального тиску та ниркової перфузії. Може знадобитися переливання крові або проведення діалізу для запобігання розвитку артеріальної гіпотензії та/або підтримання функції нирок. Пацієнти похилого віку Клінічні дослідження не виявили жодних особливостей щодо безпеки та ефективності препарату Гідрохлортіазид+Лозартан-Акріхін у пацієнтів похилого віку (старше 65 років). Лозартан Артеріальна гіпотензія та зниження об'єму циркулюючої крові (ОЦК) У пацієнтів зі зниженим ОЦК або вмістом натрію в крові, що розвинулися через інтенсивну терапію діуретиками, дієти з обмеженням кухонної солі, діареї або блювання, може розвиватися симптоматична артеріальна гіпотензія, особливо після прийому першої дози препарату Гідрохлортіазид+Лозартан-Акрихін. Корекцію таких станів необхідно проводити до призначення препарату Гідрохлортіазид+Лозартан-Акріхін. Порушення водно-електролітного балансу Порушення водно-електролітного балансу характерне для пацієнтів з нирковою недостатністю з цукровим діабетом або без цукрового діабету, тому необхідно ретельне спостереження за даними пацієнтами. Необхідний ретельний контроль вмісту калію в крові або КК, особливо у пацієнтів із серцевою недостатністю та КК 30-50 мл/хв. Під час лікування препаратом Гідрохлортіазид+Лозартан-Акріхін не рекомендується приймати калійзберігаючі діуретики, препарати калію або замінники харчової солі, що містять калій. Аортальний або мітральний стеноз, гіпертрофічна обструктивна кардіоміопатія Як і всі лікарські засоби, що мають вазодилатуючу дію, АРА II повинні призначатися з обережністю пацієнтам з аортальним або мітральним стенозом або гіпертрофічною обструктивною кардіоміопатією. Ішемічна хвороба серця та цереброваскулярні захворювання Як і всі лікарські засоби, що мають вазодилатуючу дію, АРА II повинні призначатися з обережністю пацієнтам з ішемічною хворобою серця або цереброваскулярними захворюваннями, оскільки надмірне зниження артеріального тиску у цієї групи пацієнтів може призвести до розвитку інфаркту міокарда або інсульту. Хронічна серцева недостатність (ХСП) Як і при застосуванні інших лікарських засобів, що впливають на РААС, у пацієнтів з ХСН та з або без порушення функції нирок існує ризик розвитку тяжкої артеріальної гіпотензії або гострої ниркової недостатності. Первинний гіперальдостеронізм Оскільки у пацієнтів з первинним гіперальдостеронізмом, як правило, не спостерігається позитивної відповіді на терапію гіпотензивними засобами, що діють шляхом інгібування РААС, застосування препарату Гідрохлортіазид+Лозартан-Акріхін не рекомендується у цієї групи пацієнтів. Порушення функції печінки Дані фармакокінетичних досліджень вказують на те, що концентрація лозартану в плазмі крові у пацієнтів з цирозом печінки значно збільшується, тому пацієнтам з легким або помірним порушенням функції печінки в анамнезі препарат Гідрохлортіазид+Лозартан-Акріхін слід призначати з обережністю. Відсутня досвід застосування лозартану у пацієнтів з тяжкими порушеннями функції печінки (більше 9 балів за шкалою Чайлд-П'ю), тому препарат Гідрохлортіазид+Лозартан-Акріхін не повинен застосовуватись у цієї групи пацієнтів. Порушення функції нирок Внаслідок інгібування РААС у деяких схильних пацієнтів спостерігалися зміни функції нирок, включаючи розвиток ниркової недостатності. Ці зміни ниркової функції можуть повертатися до норми після припинення лікування. Деякі лікарські засоби, що впливають на РААС, можуть збільшувати концентрацію сечовини у крові та сироваткового креатиніну у пацієнтів із двостороннім стенозом ниркових артерій або стенозом ниркової артерії єдиної нирки. Повідомлялося про виникнення подібних ефектів прийому лозартану. Подібні порушення функції нирок можуть бути оборотними після відміни терапії. Лозартан повинен застосовуватися обережно у пацієнтів з двостороннім стенозом ниркових артерій або стенозом ниркової артерії єдиної нирки. Збільшення концентрації калію у сироватці крові Одночасне застосування інших препаратів, які здатні збільшувати вміст калію в сироватці, може призвести до розвитку гіперкаліємії (див. Взаємодія з іншими лікарськими засобами). Лозартан-гідрохлортіазид Реакції гіперчутливості У пацієнтів з ангіоневротичним набряком в анамнезі (набряк обличчя, губ, глотки/гортані та/або язика) необхідний контроль застосування препарату. Порушення функції нирок та печінки Препарат Гідрохлортіазид+Лозартан-Акріхін протипоказаний для застосування у пацієнтів з тяжкими порушеннями функції печінки та тяжкими порушеннями функції нирок (КК не більше 30 мл/хв). Ембріотоксичність Застосування лікарських засобів, що впливають на РААС, у другому та третьому триместрі вагітності знижує функцію нирок плода та збільшує захворюваність та смертність плода та новонароджених. Розвиток олігогідрамніону може бути асоційований з гіпоплазією легких плода та деформаціями скелета. Можливі небажані явища у новонароджених включають гіпоплазію кісток черепа, анурію, артеріальну гіпотензію, ниркову недостатність та летальний кінець. При діагностуванні вагітності препарат Гідрохлортіазид+Лозартан-Акріхін має бути одразу відмінено. Вплив на здатність до керування автотранспортом та управління механізмами Не проводилося досліджень для оцінки впливу на здатність керувати транспортними засобами та працювати з механізмами. При керуванні транспортними засобами або роботі з механізмами слід бути обережними через можливість розвитку запаморочення, слабкості та інших можливих небажаних реакцій.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
336,00 грн
293,00 грн
Склад, форма випуску та упаковкаПігулки - 1 таб. активні речовини: калію лозартан 50 мг; гідрохлортіазид 12,5 мг; допоміжні речовини: лактоза 111,55 мг, мікрокристалічна целюлоза 37,2 мг, крохмаль прежелатинізований 35 мг, магнію стеарат 3,75 мг; оболонка: опадрай зелений [гіпролоза, гіпромелоза, титану діоксид, барвник хіноліновий жовтий] 7,8 мг. Пігулки, покриті плівковою оболонкою, 12,5 мг + 50 мг. По 14 таблеток у блістер із ПВХ-алюмінієвої фольги. По 2 або 6 блістерів у картонній пачці разом із інструкцією із застосування.Опис лікарської формиДовгасті двоопуклі таблетки, вкриті оболонкою жовтого або жовтого із зеленуватим відтінком кольору.Фармакотерапевтична групаГіпотензивний комбінований засіб (діуретик + ангіотензину II рецепторів антагоніст).ФармакокінетикаГідрохлоротіазид Гідрохлортіазид не піддається метаболізму, але швидко виводиться нирками. При підтримці концентрації гідрохлортіазиду в плазмі крові протягом як мінімум 24 годин період напіввиведення варіював від 5,6 до 14,8 годин. Не менше 61% прийнятої внутрішньо дози виводиться у незміненому вигляді протягом 24 годин. проникає через гематоенцефалічний бар'єр. Лозартан Всмоктування При прийомі внутрішньо лозартан добре всмоктується та піддається метаболізму при «первинному проходженні» через печінку з утворенням активного карбоксильованого метаболіту та неактивних метаболітів. Системна біодоступність лозартану у таблетованій формі становить приблизно 33%. Середні Сmax лозартану та його активного метаболіту досягаються через 1 годину та через 3-4 години відповідно. При прийомі лозартану в процесі звичайного їди клінічно значущого впливу на профіль концентрації лозартану в плазмі виявлено не було. Розподіл Лозартан та його активний метаболіт пов'язуються з білками плазми крові (переважно з альбуміном) не менше ніж на 99%. Об'єм розподілу лозартану становить 34 л. Дослідження на щурах показали, що лозартан практично не проникає через гематоенцефалічний бар'єр. Метаболізм Приблизно 14% дози лозартану при внутрішньовенному введенні або прийомі внутрішньо перетворюється на його активний метаболіт. Після прийому внутрішньо або внутрішньовенного введення, міченого радіоактивним вуглецем лозартану (14С лозартану) радіоактивність циркулюючої плазми крові, перш за все, обумовлена наявністю в ній лозартану та його активного метаболіту. Низька ефективність перетворення лозартану на його активний метаболіт спостерігалася приблизно у 1% пацієнтів, які брали участь у дослідженні. Крім активного метаболіту утворюються біологічно неактивні метаболіти, у тому числі два основних метаболіти, що утворюються в результаті гідроксилювання бічного бутилового ланцюга, і один другорядний N-2-тетразол-глюкуронід. Виведення Плазмовий кліренс лозартану та його активного метаболіту становить близько 600 мл/хв та 50 мл/хв відповідно. Нирковий кліренс лозартану та його активного метаболіту становить приблизно 74 мл/хв та 26 мл/хв відповідно. При прийомі лозартану внутрішньо приблизно 4% дози виводиться нирками у незміненому вигляді та близько 6% дози виводиться нирками у вигляді активного метаболіту. Лозартан та його активний метаболіт мають лінійну фармакокінетику при прийомі внутрішньо лозартану у дозах до 200 мг. Після прийому внутрішньо плазмові концентрації лозартану та його активного метаболіту знижуються поліекспоненційно з кінцевим періодом напіввиведення приблизно 2 та 6-9 годин відповідно. При режимі дозування препарату 100 мг 1 раз на добу немає значного накопичення в плазмі крові ні лозартану, ні його активного метаболіту. Виведення лозартану та його метаболітів здійснюється нирками та через кишечник з жовчю. Після прийому внутрішньо 14С лозартану у чоловіків близько 35% радіоактивності виявляється у сечі та 58% у калі. Після внутрішньовенного введення 14С лозартану у чоловіків приблизно 43% радіоактивності виявляється у сечі та 50% у калі. Фармакокінетика у спеціальних груп пацієнтів Лозартан - гідрохлортіазид Літні пацієнти Концентрації лозартану та його активного метаболіту в плазмі крові та швидкість всмоктування гідрохлортіазиду у літніх пацієнтів з артеріальною гіпертензією значуще не відрізняються від цих показників у молодих пацієнтів з артеріальною гіпертензією. Лозартан Підлога Значення концентрації лозартану в плазмі крові у жінок з артеріальною гіпертензією в 2 рази перевищували відповідні значення у чоловіків з гіпертензією. Концентрації активного метаболіту у чоловіків та жінок не відрізнялися. Ця явна фармакокінетична відмінність, проте, не має клінічного значення. Пацієнти з порушенням функції печінки При прийомі лозартану внутрішньо пацієнтами з легким та помірним алкогольним цирозом печінки концентрації лозартану та його активного метаболіту у плазмі крові виявилися відповідно у 5 та 1,7 рази вищими, ніж у молодих здорових добровольців чоловічої статі. Пацієнти з порушенням функції нирок Концентрації лозартану в плазмі у пацієнтів з кліренсом креатиніну (КК) вище 10 мл/хв не відрізнялися від таких у пацієнтів з незміненою функцією нирок. Площа під кривою "концентрація-час" (AUC) лозартану у пацієнтів, які перебувають на гемодіалізі, була приблизно в 2 рази більша в порівнянні з AUC лозартану у пацієнтів з нормальною нирковою функцією. Концентрації активного метаболіту в плазмі не змінювалися у пацієнтів з порушенням функції нирок або пацієнтів, які перебували на гемодіалізі. Лозартан та його активний метаболіт не виводяться за допомогою процедури гемодіалізу.ФармакодинамікаГідрохлоротіазид Механізм антигіпертензивної дії тіазид невідомий. Тіазиди зазвичай не впливають на нормальний рівень артеріального тиску. Гідрохлортіазид є діуретиком та гіпотензивним засобом. Він впливає на реабсорбцію електролітів у дистальних канальцях нирок. Гідрохлортіазид приблизно однаково збільшує екскрецію іонів натрію і хлору. Натрійурез може супроводжуватися невеликою втратою іонів калію та бікарбонату. При внутрішньому прийомі діуретичний ефект розвивається протягом 2 годин, досягає максимуму в середньому через 4 години і триває від 6 до 12 годин. Лозартан Ангіотензин II є потужним вазоконстриктором, головним активним гормоном ренін-ангіотензин-альдостеронової системи (РААС), а також вирішальною ланкою при розвитку артеріальної гіпертензії (АГ). Ангіотензин II зв'язується з AT1-рецепторами, що знаходяться в багатьох тканинах (у гладком'язових тканинах судин, надниркових залозах, нирках і серці), і виконує кілька важливих біологічних функцій, включаючи вазоконстрикцію та вивільнення альдостерону. Крім цього, ангіотензин II стимулює розростання гладких клітин. АТ2-рецептори - другий тип рецепторів, з якими зв'язується ангіотензин II, але його роль у регуляції функції серцево-судинної системи невідома. Лозартан селективний антагоніст AT1-рецепторів ангіотензину II, високоефективний при внутрішньому прийомі. Лозартан та його фармакологічно активний карбоксильований метаболіт (Е-3174) як in vitro, так і in vivo блокують усі фізіологічні ефекти ангіотензину II незалежно від його джерела чи шляху синтезу. На відміну від деяких пептидних антагоністів ангіотензину II лозартан не має властивостей агоніста. Лозартан вибірково зв'язується з AT1-рецепторами і не зв'язується, і не блокує рецептори інших гормонів та іонних каналів, що відіграють важливу роль у регуляції функції серцево-судинної системи. Крім того, лозартан не інгібує ангіотензинперетворюючий фермент (АПФ, кініназа II), що відповідає за руйнування брадикініну. Отже, ефекти, які безпосередньо не пов'язані з блокадою AT1-рецепторів, такі як посилення брадикінін-опосередкованих ефектів або розвиток набряків (лозартан 1,7%, плацебо 1,9%), не мають відношення до дії лозартану. Препарат Гідрохлортіазид+Лозартан-Акріхін Компоненти препарату Гідрохлортіазид+Лозартан-Акріхін мають адитивну антигіпертензивну дію, знижуючи рівень артеріального тиску (АТ) більшою мірою, ніж кожен із компонентів окремо. Вважається, що цей ефект зумовлений взаємодоповнювальною дією обох компонентів. Внаслідок діуретичного ефекту гідрохлортіазид підвищує активність реніну плазми крові (АРП), стимулює секрецію альдостерону, збільшує концентрацію ангіотензину II та знижує вміст калію у сироватці крові. Прийом лозартану блокує всі фізіологічні ефекти ангіотензину II і внаслідок придушення ефектів альдостерону може сприяти зниженню втрати калію, пов'язаного з прийомом діуретика. Лозартан має помірний і минущий урикозуричний ефект. Гідрохлортіазид викликає невелике підвищення концентрації сечової кислоти у крові. Комбінація лозартану та гідрохлортіазиду сприяє зменшенню вираженості гіперурикемії, спричиненої діуретиком. Препарат Гідрохлортіазид+Лозартан-Акріхін є комбінованим препаратом лозартану та гідрохлортіазиду. У пацієнтів з артеріальною гіпертензією та гіпертрофією лівого шлуночка лозартан, у тому числі в комбінації з гідрохлоротіазидом, зменшує ризик серцево-судинної захворюваності та смертності, що було доведено за допомогою оцінки комбінованої частоти розвитку інсульту та інфаркту міокарда, а також показника серцевості. цієї категорії хворих. Гідрохлоротіазид Механізм антигіпертензивної дії тіазид невідомий. Зазвичай, тіазиди не впливають на нормальні значення АТ. Гідрохлортіазид є діуретичним та гіпотензивним засобом. Він впливає на механізм реабсорбції електролітів у дистальних звивистих ниркових канальцях. Гідрохлортіазид збільшує екскрецію натрію та хлориду приблизно в еквівалентних кількостях. Натрійурез може супроводжуватися деякою втратою іонів калію та бікарбонату. Після прийому внутрішньо діурез починається протягом 2 год, досягає максимуму протягом приблизно 4 год і триває приблизно 6-12 год. Лозартан Лозартан пригнічує підвищення систолічного та діастолічного артеріального тиску (АТ) при інфузії ангіотензину ІІ. У момент досягнення максимальної концентрації лозартану в плазмі крові (Сmax) після прийому лозартану в дозі 100 мг вищевказаний ефект ангіотензину II пригнічується приблизно на 85%, а через 24 години після одноразового та багаторазового прийому на 26-39%. У період прийому лозартану усунення негативного зворотного зв'язку, що полягає у придушенні ангіотензином II секреції реніну, веде до збільшення АРП. Збільшення АРП призводить до збільшення концентрації ангіотензину ІІ у плазмі крові. При тривалому (6-тижневому) лікуванні пацієнтів з артеріальною гіпертензією лозартаном у дозі 100 мг на добу спостерігалося 2-3-кратне збільшення концентрації ангіотензину II у плазмі крові в момент досягнення Сmax лозартану. У деяких пацієнтів спостерігалося ще більше збільшення концентрації ангіотензину II, особливо при невеликій тривалості лікування (2 тижні). Незважаючи на це, у процесі лікування антигіпертензивний ефект та зниження концентрації альдостерону у плазмі крові виявлялися через 2 та 6 тижнів терапії, що вказує на ефективну блокаду рецепторів ангіотензину ІІ.Після відміни лозартану АРП та концентрації ангіотензину II знижувалися протягом 3 діб до значень, що спостерігалися до початку прийому лозартану. Вплив препарату Гідрохлортіазид+Лозартан-Акріхін на АРП та концентрацію ангіотензину II був подібним до спостеріганих ефектів при прийомі лозартану в дозі 50 мг. Оскільки лозартан є специфічним антагоністом AT1-рецепторів ангіотензину II, він не пригнічує АПФ (кініназу II) — фермент, який інактивує брадикінін. Дослідження, в якому порівнювалися ефекти лозартану в дозах 20 мг та 100 мг з ефектами інгібітору АПФ за впливом на ангіотензин I, ангіотензин II та брадикінін, показало, що лозартан блокує ефекти ангіотензину I та ангіотензину II, не впливаючи на ефект. Це зумовлено специфічним механізмом дії лозартану. Інгібітор АПФ блокував реакції на ангіотензин I і підвищував вираженість ефектів, зумовлених дією брадикініну, не впливаючи на вираженість відповіді на ангіотензин II, що демонструє фармакодинамічну різницю між лозартаном та інгібіторами АПФ. Концентрації лозартану та його активного метаболіту у плазмі крові, а також антигіпертензивний ефект лозартану зростають із збільшенням дози препарату. Оскільки лозартан та його активний метаболіт є антагоністами рецепторів ангіотензину II (АРА II), вони обидва роблять внесок у антигіпертензивний ефект. У дослідженні з одноразовим прийомом лозартану в дозі 100 мг, до якого включалися здорові добровольці (чоловіки), прийом препарату внутрішньо в умовах високо- та малосольової дієти не впливав на швидкість клубочкової фільтрації (СКФ), ефективний нирковий плазмоток та фільтраційну фракцію. Лозартан мав натрійуретіческій ефект, який був більш виражений при малосольової дієті і, мабуть, не був пов'язаний з придушенням ранньої реабсорбції натрію в проксимальних ниркових канальцях. Лозартан також викликав минуще збільшення виділення сечової кислоти нирками. У пацієнтів з АГ, протеїнурією (не менше 2 г/24 год), без цукрового діабету та приймаючих лозартан протягом 8 тижнів у дозі 50 мг з поступовим збільшенням до 100 мг, спостерігалося достовірне зниження протеїнурії (на 42%), фракційної екскреції альбуміну. та імуноглобулінів (IgG). У цих пацієнтів лозартан стабілізував ШКФ та зменшував фільтраційну фракцію. У жінок у постменопаузальному періоді з АГ, які приймали лозартан у дозі 50 мг протягом 4 тижнів, не було виявлено впливу терапії на нирковий та системний рівень простагландинів. Лозартан не впливає на вегетативні рефлекси і не має тривалого ефекту щодо концентрації норадреналіну в плазмі крові. У пацієнтів з артеріальною гіпертензією лозартан у дозах до 150 мг на добу не викликав клінічно значущих змін концентрації тригліцеридів натще, загального холестерину та холестерину ліпопротеїнів високої щільності. У тих же дозах лозартан не впливав на концентрацію глюкози в крові натще. Загалом лозартан викликав зниження концентрації сечової кислоти в сироватці крові (зазвичай менше 0,4 мг/дл), що зберігалося при тривалому лікуванні. У контрольованих клінічних дослідженнях за участю пацієнтів з артеріальною гіпертензією випадків відміни препарату у зв'язку зі збільшенням концентрації креатиніну або вмісту калію в сироватці крові не зареєстровано. У 12-тижневому паралельному дослідженні, яке включали пацієнтів з лівошлуночковою недостатністю (II-IV функціонального класу за класифікацією NYHA), більшість з яких приймали діуретики та/або серцеві глікозиди, порівнювали ефекти лозартану в дозах 2,5, 10, 25 і 5 мг/добу з плацебо. У дозах 25 та 50 мг на добу препарат виявляв позитивні гемодинамічні та нейрогормональні ефекти, які зберігалися протягом усього дослідження. Гемодинамічні ефекти включали збільшення серцевого індексу та зниження тиску заклинювання у легеневих капілярах, а також зниження загального периферичного судинного опору, середнього системного АТ та частоти серцевих скорочень. Частота виникнення гіпотензії у цих пацієнтів залежала від дози препарату.Нейрогормональні ефекти включали зниження концентрації альдостерону та норадреналіну в крові.Показання до застосуванняАртеріальна гіпертензія (пацієнтам, яким показано комбіновану терапію). Зниження ризику асоційованої серцево-судинної захворюваності та смертності у пацієнтів з артеріальною гіпертензією та гіпертрофією лівого шлуночка, що проявляється сукупним зниженням частоти серцево-судинної смертності, частоти інсульту та інфаркту міокарда.Протипоказання до застосуванняПідвищена чутливість до будь-якого з компонентів препарату; Підвищена чутливість до інших похідних сульфонаміду; Анурія; Тяжкі порушення функції нирок (кліренс креатиніну менше 30 мл/хв); Тяжкі порушення функції печінки; Рефрактерна гіпокаліємія, гіпонатріємія, гіперкальціємія; Одночасне застосування з аліскіреном та препаратами, що містять аліскірен, у пацієнтів з цукровим діабетом та/або помірними або тяжкими порушеннями функції нирок (швидкість клубочкової фільтрації (СКФ) менше 60 мл/хв/1,73 м2 площі поверхні тіла); Одночасне застосування з інгібіторами АПФ у пацієнтів з діабетичною нефропатією; Вагітність та період грудного вигодовування; Дитячий вік до 18 років (ефективність та безпека застосування не встановлені); Рідкісна спадкова непереносимість галактози, дефіцит лактази, синдром глюкозо-галактозної мальабсорбції (препарат містить лактозу). З обережністю Двосторонній стеноз ниркових артерій чи стеноз артерії єдиної нирки; гіперкаліємія; стани після трансплантації нирки (відсутня досвід застосування); аортальний чи мітральний стеноз; гіпертрофічна обструктивна кардіоміопатія; хронічна серцева недостатність із супутнім тяжким порушенням функції нирок; тяжка серцева недостатність (IV функціонального класу за класифікацією NYHA); хронічна серцева недостатність з загрозливими для життя аритміями; ішемічна хвороба серця; цереброваскулярні захворювання; первинний гіперальдостеронізм; ангіоневротичний набряк в анамнезі; артеріальна гіпотензія; порушення функції печінки; порушення функції нирок; порушення водно-електролітного балансу; пацієнтам зі зниженим обсягом циркулюючої крові (наприклад,які отримують лікування великими дозами діуретиків) у зв'язку з можливістю виникнення симптоматичної артеріальної гіпотензії; гіпокаліємія; гіпонатріємія; гіперкальціємія; одночасне застосування лікарських засобів, які можуть викликати поліморфну шлуночкову тахікардію типу «пірует» або збільшувати тривалість інтервалу QT на ЕКГ; одночасне застосування лікарських засобів, здатних викликати гіпокаліємію, серцевих глікозидів; алергічні реакції на пеніцилін в анамнезі; гіперпаратиреоз; гіперурикемія; подагра, немеланомний рак шкіри в анамнезі.одночасне застосування лікарських засобів, здатних викликати гіпокаліємію, серцевих глікозидів; алергічні реакції на пеніцилін в анамнезі; гіперпаратиреоз; гіперурикемія; подагра, немеланомний рак шкіри в анамнезі.одночасне застосування лікарських засобів, здатних викликати гіпокаліємію, серцевих глікозидів; алергічні реакції на пеніцилін в анамнезі; гіперпаратиреоз; гіперурикемія; подагра, немеланомний рак шкіри в анамнезі.Вагітність та лактаціяЗастосування препарату Гідрохлортіазид+Лозартан-Акріхін при вагітності та в період грудного вигодовування протипоказане. Гідрохлоротіазид Вагітність Існує обмежений досвід застосування гідрохлортіазиду під час вагітності (особливо у першому триместрі). Доклінічні дані щодо безпеки недостатні. Гідрохлортіазид проникає через плацентарний бар'єр і визначається пуповинної крові. З урахуванням механізму фармакологічної дії гідрохлортіазиду, його застосування у другому та третьому триместрах вагітності може порушувати фетоплацентарну перфузію та призводити до розвитку у плода та новонародженого таких ускладнень, як жовтяниця, порушення водно-електролітного балансу та тромбоцитопенія. Описано випадки розвитку тромбоцитопенії у новонароджених, матері яких отримували тіазидні діуретики. Застосування гідрохлортіазиду під час вагітності протипоказане. Гідрохлортіазид не можна застосовувати для лікування гестозів ІІ половини вагітності (набряків, артеріальної гіпертензії або прееклампсії), т.к. він збільшує ризик зниження обсягу циркулюючої крові та плацентарної гіпоперфузії, але не надає сприятливого впливу протягом зазначених ускладнень вагітності. Діуретики не запобігають розвитку гестозів. Період грудного вигодовування Гідрохлортіазид проникає в материнське молоко, у зв'язку з чим його застосування у період грудного вигодовування протипоказане. Якщо застосування гідрохлортіазиду в період лактації є абсолютно необхідним, слід припинити грудне вигодовування. Лозартан Вагітність Лозартан протипоказаний під час вагітності. Терапію лозартаном не можна розпочинати під час вагітності. Якщо пацієнткам, які планують вагітність, продовження терапії лозартаном вважається за необхідне, слід замінити лозартан на альтернативні гіпотензивні засоби, які мають встановлений профіль безпеки при застосуванні під час вагітності. Хоча немає досвіду застосування лозартану у вагітних, доклінічні дослідження на тваринах показали, що прийом лозартану призводить до розвитку серйозних ембріональних та неонатальних ушкоджень та загибелі плода чи потомства. Вважається, що механізм даних явищ обумовлений впливом на РААС. Ниркова перфузія у плода, що залежить від розвитку РААС, з'являється у другому триместрі, тому ризик для плода зростає, якщо лозартан застосовується у другому або третьому триместрі вагітності.Застосування лікарських засобів, що впливають на РААС, у другому та третьому триместрі вагітності знижує функцію нирок плода та збільшує захворюваність та смертність плода та новонароджених. Розвиток олігогідрамніону може бути асоційований з гіпоплазією легких плода та деформаціями скелета. Можливі небажані явища у новонароджених включають гіпоплазію кісток черепа, анурію, артеріальну гіпотензію, ниркову недостатність та летальний кінець. Зазначені вище небажані наслідки зазвичай обумовлені застосуванням лікарських засобів, що впливають на РААС, у другому та третьому триместрі вагітності. Більшість епідеміологічних досліджень щодо вивчення розвитку аномалій плода після застосування гіпотензивних лікарських засобів у першому триместрі вагітності не виявили відмінностей між лікарськими засобами, що впливають на РААС,та іншими гіпотензивними засобами. При призначенні гіпотензивної терапії вагітним важливо оптимізувати можливі наслідки для матері та плода. Якщо неможливо підібрати альтернативну терапію замість терапії лікарськими засобами, що впливають на РААС, необхідно проінформувати пацієнтку про можливий ризик терапії для плода. Необхідне проведення періодичних ультразвукових досліджень з метою оцінки інтраамніотичного простору. При виявленні олігогідрамніону необхідно припинити прийом лозартану, якщо він не є життєво необхідним для матері. Залежно від тижня вагітності потрібне проведення відповідних тестів плода. Пацієнтки та лікарі повинні знати, що олігогідрамніон може не виявлятися до появи незворотних ушкоджень плода. Необхідно ретельне спостереження за новонародженими,чиї матері приймали лозартан під час вагітності з метою контролю артеріальної гіпотензії, олігурії та гіперкаліємії. Період грудного вигодовування Лозартан протипоказаний у період грудного вигодовування. Невідомо, чи виділяється лозартан із грудним молоком. Так як багато лікарських засобів виділяються з грудним молоком і існує ризик розвитку можливих несприятливих ефектів у дитини, яка перебуває на грудному вигодовуванні, слід прийняти рішення про припинення грудного вигодовування або про відміну препарату з урахуванням необхідності його прийому для матері.Побічна діяЧастота виникнення небажаних реакцій визначалася відповідно до класифікації Всесвітньої Організації Охорони Здоров'я: дуже часто (≥ 1/10); часто (≥ 1/100 та У клінічних дослідженнях з гідрохлортіазидом/лозартаном не спостерігалося небажаних явищ, специфічних для комбінованого препарату. Небажані явища обмежувалися тими, про які повідомлялося раніше при застосуванні гідрохлортіазиду та лозартану у монотерапії. Системно-органний клас Небажана реакція Гідрохло ротіазид+ Лозартан Гідрохлор-ротіазид Лозартан Порушення з боку крові та лімфатичної системи: анемія пурпура Шенлейн-Геноха екхімози гемолітична анемія тромбоцитопенія агранулоцитоз апластична анемія лейкопенія пурпура нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто частота невідома Алергічні реакції анафілактичні реакції ангіоневротичний набряк, включаючи набряк гортані та глотки, що викликає обструкцію дихальних шляхів, та/або набряк особи, губ, глотки та/або язика; у деяких пацієнтів ангіоневротичний набряк також відзначався в анамнезі при лікуванні іншими препаратами, включаючи інгібітори АПФ. ангіоневротичний набряк гортані, глотки, язика, обличчя, губ, слизових оболонок (у тому числі з летальним результатом) кропив'янка синдром Стівенса-Джонсона мультиформна еритема еритродермія рідко дуже рідко дуже рідко дуже рідко дуже рідко дуже рідко дуже рідко дуже рідко дуже рідко дуже рідко рідко рідко рідко рідко Порушення з боку метаболізму та харчування втрата апетиту гіперглікемія гіперурикемія порушення водно-електролітного балансу (зокрема гіпокаліємія та гіпонатріємія, гіпомагніємія та гіпохлоремія, а також гіперкальціємія) лікування тіазидами може знижувати толерантність до глюкози, і латентно протікає цукровий діабет може маніфестувати нечасто нечасто нечасто нечасто нечасто дуже рідко Порушення з боку центральної нервової системи головний біль запаморочення безсоння занепокоєння парестезія периферична нейропатія тремор мігрень непритомність тривога тривожний розлад (надмірний, неконтрольований і часто ірраціональний занепокоєння про повсякденні події) панічний розлад сплутаність свідомості депресія сонливість порушення сну часто нечасто нечасто часто часто часто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто Порушення з боку органу зору порушення зору відчуття сухості та печіння/почуття поколювання в очах кон'юнктивіт гостра міопія гостра закритокутова глаукома рідко дуже рідко рідко частота невідома частота невідома нечасто нечасто нечасто нечасто Порушення з боку органу слуху та лабіринтні порушення вертиго шум у вухах нечасто нечасто Порушення з боку дихальної системи закладеність носа кашель інфекції верхніх дихальних шляхів (підвищена температура тіла, біль у горлі, синусопатія, синусит, фарингіт) фарингіт ларингіт диспное бронхіт риніт носова кровотеча дискомфорт у глотковій області не часто часто часто часто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто Порушення з боку серцево-судинної системи некротизуючий ангіїт (васкуліт, шкірний васкуліт) виражене зниження артеріального тиску при надмірному зниженні АТ) васкуліт не часто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто Порушення з боку травної системи Порушення з боку шкіри та підшкірної клітковини Порушення з боку опорно-рухового апарату Порушення з боку сечостатевої системи Загальні порушення Лабораторні показники нудота діарея блювота запор диспептичні явища біль в животі сухість слизової оболонки порожнини рота » крові до шкіри обличчя шкірний свербіж висип підвищене потовиділення алопеція дерматит судоми в м'язах міалгія біль у спині, в ногах артралгія біль у руках, у плечі,колене артрит фибромиалгия скованность мышечная слабость припухлость суставов скелетно – мышечная боль рабдомиолиз нарушение функции почек почечная недостаточность интерстициальный нефрит глюкозурия никтурия учащенное мочеиспускание инфекции мочевыводящих путей ослабление либидо импотенция повышение температуры тела астения повышенная утомляемость анорексия отек лица отеки лихорадка гриппоподобные симптомы недомогание гиперкалиемия повышение активности «печеночных» трансаміназ зниження гематокриту та гемоглобіну гіпоглікемія підвищення концентрації сечовини та креатинінуанорексія набряк особи набряки лихоманка грипоподібні симптоми нездужання гіперкаліємія підвищення активності «печінкових» трансаміназ зниження гематокриту та гемоглобіну гіпоглікемія підвищення концентрації сечовини та креатинінуанорексія набряк особи набряки лихоманка грипоподібні симптоми нездужання гіперкаліємія підвищення активності «печінкових» трансаміназ зниження гематокриту та гемоглобіну гіпоглікемія підвищення концентрації сечовини та креатиніну рідко * рідко * рідко * нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто нечасто часто часто нечасто нечасто часто часто нечасто нечасто нечасто нечасто нечасто частота невідома частота невідома нечасто нечасто нечасто нечасто нечасто нечасто нечасто часто часто часто нечасто нечасто нечасто нечасто нечасто нечасто нечасто часто невідома частота невідома часто дуже рідко часто часто нечасто *-небажані явища спостерігалися при постмаркетинговому застосуванні гідрохлортіазиду/лозартану.Взаємодія з лікарськими засобамиГідрохлоротіазид Нерекомендовані поєднання лікарських засобів Препарати літію При одночасному застосуванні гідрохлортіазиду та препаратів літію знижується нирковий кліренс літію, що може призвести до підвищення концентрації літію у плазмі крові та збільшення його токсичності. При необхідності одночасного застосування гідрохлортіазиду слід ретельно підбирати дозу препаратів літію, регулярно контролювати концентрацію літію у плазмі крові та відповідним чином підбирати дозу препарату. Поєднання лікарських засобів, що вимагають особливої уваги Препарати, здатні викликати поліморфну шлуночкову тахікардію типу «пірует» Слід з особливою обережністю застосовувати гідрохлортіазид одночасно з такими препаратами, як: антиаритмічні лікарські препарати ІА класу (хінідин, гідрохінідин, дизопірамід, прокаїнамід); антиаритмічні лікарські препарати ІІІ класу (дофетилід, ібутилід, бретилія тозилат), соталол, дронедарон, аміодарон; інші (неантіаритмічні) лікарські засоби, такі як: нейролептики: фенотіазиниСпосіб застосування та дозиПрепарат Гідрохлортіазид+Лозартан-Акріхін приймається внутрішньо незалежно від їди. Препарат можна приймати у комбінації з іншими гіпотензивними засобами. Артеріальна гіпертензія Зазвичай початкова та підтримуюча доза -1 таблетка препарату Гідрохлортіазид+Лозартан-Акріхін 1 раз на добу. У пацієнтів без адекватної терапевтичної відповіді на прийом 1 таблетки препарату (містить 50 мг лозартану +12, 5 мг гідрохлортіазиду) 1 раз на добу протягом 2 – 4 тижнів, доза препарату може бути збільшена до 2 таблеток препарату 1 раз на добу. Максимальна доза – 2 таблетки (50 мг + 12,5 мг) 1 раз на добу. Як правило, антигіпертензивний ефект досягається протягом трьох тижнів після початку терапії. Зниження ризику серцево-судинної захворюваності та смертності у пацієнтів з артеріальною гіпертензією та гіпертрофією лівого шлуночка Зазвичай початкова доза 50 мг лозартану 1 раз на добу. Пацієнтам, у яких не вдається досягти цільових значень рівня АТ на фоні прийому лозартану 50 мг на добу, потрібен підбір терапії шляхом комбінації лозартану з низькими дозами гідрохлортіазиду (12,5 мг). У разі потреби потрібно збільшити дозу лозартану до 100 мг/кг у поєднанні з гідрохлортіазидом у дозі 12,5 мг/добу, надалі – збільшити дозу до 2 таблеток препарату Гідрохлортіазид + Лозартан – Акріхін (50 мг + 12,5 мг) 1 раз. на добу.ПередозуванняГідрохлоротіазид Симптоми Найчастішими проявами передозування гідрохлортіазидом є збільшення діурезу, що супроводжується гострою втратою рідини (дегідратацією) та електролітними порушеннями (гіпокаліємія, гіпонатріємія, гіпохлоремія). Передозування гідрохлортіазидом може виявлятися такими симптомами: з боку серцево-судинної системи: тахікардія; зниження артеріального тиску; шок; з боку нервової системи: слабкість, сплутаність свідомості, запаморочення та спазми литкових м'язів, парестезія, порушення свідомості, втома; з боку шлунково-кишкового тракту: нудота, блювання, спрага; з боку нирок та сечовивідних шляхів: поліурія, олігурія або анурія (через гемоконцентрацію). лабораторні показники: гіпоглікемія, гіпонатріємія, гіпохлоремія, алкалоз, підвищений вміст азоту сечовини у крові (особливо у пацієнтів із нирковою недостатністю). Лікування При передозуванні проводиться симптоматична та підтримуюча терапія. Якщо препарат був прийнятий нещодавно, для виведення гідрохлортіазиду показано індукцію блювоти або промивання шлунка. Абсорбцію гідрохлортіазиду можна зменшити прийомом внутрішньо активованого вугілля. У разі зниження АТ або шоку слід заповнити об'єм циркулюючої крові запровадженням плазмозамінних рідин та дефіцит електролітів (калій, натрій). При дихальних порушеннях показано інгаляцію кисню або штучну вентиляцію легень. Слід контролювати водно-електролітний баланс (особливо вміст калію у сироватці крові) та функцію нирок до їх нормалізації. Специфічного антидоту немає. Гідрохлортіазид виводиться при гемодіалізі, проте ступінь його виведення не встановлено. Лозартан Симптоми Відомості про передозування лозартану обмежені. Найбільш ймовірне прояв передозування - виражене зниження артеріального тиску та тахікардія; брадикардія може виникнути внаслідок парасимпатичної (вагусної) стимуляції. Лікування Симптоматична терапія. У разі розвитку симптоматичної артеріальної гіпотензії показано підтримуючу терапію. Лозартан та його активний метаболіт не виводяться за допомогою гемодіалізу.Запобіжні заходи та особливі вказівкиГідрохлоротіазид Артеріальна гіпотензія та порушення водно-електролітного балансу При застосуванні гіпотензивних засобів у деяких пацієнтів може розвинутись симптоматична артеріальна гіпотензія. Пацієнти повинні спостерігатися з метою своєчасного виявлення клінічних ознак порушення водно-електролітного балансу, наприклад, зневоднення, гіпонатріємії, гіпохлоремічного алкалозу, гіпомагніємії або гіпокаліємії, які можуть розвинутись на тлі супутньої діареї або блювання. У таких пацієнтів потрібний регулярний контроль вмісту електролітів сироватки крові. У пацієнтів з набряками може спостерігатися дилюційна гіпонатріємія у спеку. Метаболічні та ендокринні ефекти Терапія тіазидами може порушувати толерантність до глюкози. У ряді випадків може знадобитися корекція дози гіпоглікемічних засобів, у тому числі інсуліну. Тіазиди можуть знижувати виведення кальцію нирками та викликати короткочасне та незначне підвищення вмісту кальцію сироватки крові. Виражена гіперкальціємія може свідчити про прихований гіперпаратиреоз. У зв'язку з впливом тіазидів на метаболізм кальцію їх прийом може спотворювати результати дослідження функції паращитовидних залоз, тому перед дослідженням функції паращитовидних залоз тіазидний діуретик повинен бути скасований. Підвищення концентрації холестерину та тригліцеридів у крові також може бути пов'язане з терапією тіазидними діуретиками. У деяких пацієнтів прийом тіазидних діуретиків може призводити до гіперурикемії та/або розвитку подагри. Оскільки лозартан зменшує концентрацію сечової кислоти, його одночасне застосування з гідрохлортіазидом знижує вираженість гіперурикемії, спричиненої діуретиком. Порушення функції печінки Тіазиди слід застосовувати з обережністю у пацієнтів з порушеннями функції печінки або прогресуючим захворюванням печінки, оскільки це може призвести до розвитку внутрішньопечінкового холестазу, а незначні зміни водно-електролітного балансу можуть спровокувати розвиток печінкової коми. Препарат Гідрохлортіазид+Лозартан-Акріхін протипоказаний пацієнтам із тяжкими порушеннями функції печінки. Гостра міопія та вторинна закритокутова глаукома Гідрохлортіазид, похідний сульфонаміду, може викликати ідіосинкратичну реакцію у вигляді гострої транзиторної міопії та гострої закритокутової глаукоми. Симптомами цих порушень є несподіване зниження гостроти зору або біль в очах, які в типових випадках виникають протягом декількох годин до декількох тижнів після початку застосування препарату. Якщо не проводиться терапія, гостра глаукома може призвести до втрати зору. Основне лікування полягає в якнайшвидшому відміні гідрохлортіазиду. Необхідно мати на увазі, що якщо внутрішньоочний тиск залишається неконтрольованим, може знадобитися невідкладне консервативне або хірургічне лікування. До факторів ризику розвитку гострої глаукоми можна віднести відомості про алергію до сульфонамідів або пеніциліну в анамнезі. Немеланомний рак шкіри (НМРК) В епідеміологічних дослідженнях спостерігався підвищений ризик раку шкіри (базальноклітинної карциноми і плоскоклітинної карциноми) у зв'язку зі збільшенням сумарної (накопиченої) дози гідрохлортіазиду. Можливим механізмом розвитку НМРК є фотосенсибілізуюча дія гідрохлортіазиду. Пацієнти, які приймають гідрохлортіазид, повинні бути обізнані про ризик розвитку НМРК. Таким пацієнтам слід рекомендувати дотримуватись профілактичних заходів, таких як обмеження впливу сонячного світла та штучних UVA променів. Пацієнти повинні регулярно оглядати свої шкірні покриви з метою виявлення будь-яких нових підозрілих поразок та негайно повідомляти про них лікаря. У пацієнтів із НМРК в анамнезі рекомендується переглянути доцільність застосування гідрохлортіазиду. Інші ефекти У пацієнтів, які приймають тіазидні діуретики, реакції гіперчутливості можуть виникати навіть за відсутності в анамнезі алергічних реакцій або бронхіальної астми. Повідомлялося про рецидиви або посилення тяжкості перебігу системного червоного вовчаку у пацієнтів, які приймали тіазидні діуретики. Особливі групи пацієнтів Раса Аналіз даних всієї популяції пацієнтів, включених у дослідження LIFE щодо вивчення впливу лозартану на зниження частоти розвитку первинної кінцевої точки у пацієнтів з АГ та гіпертрофією лівого шлуночка (n = 9193), показав, що здатність лозартану порівняно з атенололом знижувати на 13,0% ризик розвитку серцево-судинних ускладнень (р = 0,021) не поширюється на пацієнтів негроїдної раси, хоча обидва режими терапії ефективно знижували рівень АТ у цих пацієнтів. Однак у цьому дослідженні пацієнти негроїдної раси, які отримували атенолол, мали менший ризик розвитку первинної кінцевої точки (серцево-судинна смертність, інсульт та інфаркт міокарда) порівняно з пацієнтами тієї ж раси, які приймали лозартан (р = 0,03). Діти та підлітки Ефективність та безпека застосування препарату Гідрохлортіазид+Лозартан-Акріхін у дітей та підлітків до 18 років не встановлені. Якщо у новонароджених, чиї матері приймали препарат Гідрохлортіазид+Лозартан-Акріхін під час вагітності, спостерігається розвиток олігурії або артеріальної гіпотензії, необхідно проведення симптоматичної терапії, спрямованої на підтримання артеріального тиску та ниркової перфузії. Може знадобитися переливання крові або проведення діалізу для запобігання розвитку артеріальної гіпотензії та/або підтримання функції нирок. Пацієнти похилого віку Клінічні дослідження не виявили жодних особливостей щодо безпеки та ефективності препарату Гідрохлортіазид+Лозартан-Акріхін у пацієнтів похилого віку (старше 65 років). Лозартан Артеріальна гіпотензія та зниження об'єму циркулюючої крові (ОЦК) У пацієнтів зі зниженим ОЦК або вмістом натрію в крові, що розвинулися через інтенсивну терапію діуретиками, дієти з обмеженням кухонної солі, діареї або блювання, може розвиватися симптоматична артеріальна гіпотензія, особливо після прийому першої дози препарату Гідрохлортіазид+Лозартан-Акрихін. Корекцію таких станів необхідно проводити до призначення препарату Гідрохлортіазид+Лозартан-Акріхін. Порушення водно-електролітного балансу Порушення водно-електролітного балансу характерне для пацієнтів з нирковою недостатністю з цукровим діабетом або без цукрового діабету, тому необхідно ретельне спостереження за даними пацієнтами. Необхідний ретельний контроль вмісту калію в крові або КК, особливо у пацієнтів із серцевою недостатністю та КК 30-50 мл/хв. Під час лікування препаратом Гідрохлортіазид+Лозартан-Акріхін не рекомендується приймати калійзберігаючі діуретики, препарати калію або замінники харчової солі, що містять калій. Аортальний або мітральний стеноз, гіпертрофічна обструктивна кардіоміопатія Як і всі лікарські засоби, що мають вазодилатуючу дію, АРА II повинні призначатися з обережністю пацієнтам з аортальним або мітральним стенозом або гіпертрофічною обструктивною кардіоміопатією. Ішемічна хвороба серця та цереброваскулярні захворювання Як і всі лікарські засоби, що мають вазодилатуючу дію, АРА II повинні призначатися з обережністю пацієнтам з ішемічною хворобою серця або цереброваскулярними захворюваннями, оскільки надмірне зниження артеріального тиску у цієї групи пацієнтів може призвести до розвитку інфаркту міокарда або інсульту. Хронічна серцева недостатність (ХСП) Як і при застосуванні інших лікарських засобів, що впливають на РААС, у пацієнтів з ХСН та з або без порушення функції нирок існує ризик розвитку тяжкої артеріальної гіпотензії або гострої ниркової недостатності. Первинний гіперальдостеронізм Оскільки у пацієнтів з первинним гіперальдостеронізмом, як правило, не спостерігається позитивної відповіді на терапію гіпотензивними засобами, що діють шляхом інгібування РААС, застосування препарату Гідрохлортіазид+Лозартан-Акріхін не рекомендується у цієї групи пацієнтів. Порушення функції печінки Дані фармакокінетичних досліджень вказують на те, що концентрація лозартану в плазмі крові у пацієнтів з цирозом печінки значно збільшується, тому пацієнтам з легким або помірним порушенням функції печінки в анамнезі препарат Гідрохлортіазид+Лозартан-Акріхін слід призначати з обережністю. Відсутня досвід застосування лозартану у пацієнтів з тяжкими порушеннями функції печінки (більше 9 балів за шкалою Чайлд-П'ю), тому препарат Гідрохлортіазид+Лозартан-Акріхін не повинен застосовуватись у цієї групи пацієнтів. Порушення функції нирок Внаслідок інгібування РААС у деяких схильних пацієнтів спостерігалися зміни функції нирок, включаючи розвиток ниркової недостатності. Ці зміни ниркової функції можуть повертатися до норми після припинення лікування. Деякі лікарські засоби, що впливають на РААС, можуть збільшувати концентрацію сечовини у крові та сироваткового креатиніну у пацієнтів із двостороннім стенозом ниркових артерій або стенозом ниркової артерії єдиної нирки. Повідомлялося про виникнення подібних ефектів прийому лозартану. Подібні порушення функції нирок можуть бути оборотними після відміни терапії. Лозартан повинен застосовуватися обережно у пацієнтів з двостороннім стенозом ниркових артерій або стенозом ниркової артерії єдиної нирки. Збільшення концентрації калію у сироватці крові Одночасне застосування інших препаратів, які здатні збільшувати вміст калію в сироватці, може призвести до розвитку гіперкаліємії (див. Взаємодія з іншими лікарськими засобами). Лозартан-гідрохлортіазид Реакції гіперчутливості У пацієнтів з ангіоневротичним набряком в анамнезі (набряк обличчя, губ, глотки/гортані та/або язика) необхідний контроль застосування препарату. Порушення функції нирок та печінки Препарат Гідрохлортіазид+Лозартан-Акріхін протипоказаний для застосування у пацієнтів з тяжкими порушеннями функції печінки та тяжкими порушеннями функції нирок (КК не більше 30 мл/хв). Ембріотоксичність Застосування лікарських засобів, що впливають на РААС, у другому та третьому триместрі вагітності знижує функцію нирок плода та збільшує захворюваність та смертність плода та новонароджених. Розвиток олігогідрамніону може бути асоційований з гіпоплазією легких плода та деформаціями скелета. Можливі небажані явища у новонароджених включають гіпоплазію кісток черепа, анурію, артеріальну гіпотензію, ниркову недостатність та летальний кінець. При діагностуванні вагітності препарат Гідрохлортіазид+Лозартан-Акріхін має бути одразу відмінено. Вплив на здатність до керування автотранспортом та управління механізмами Не проводилося досліджень для оцінки впливу на здатність керувати транспортними засобами та працювати з механізмами. При керуванні транспортними засобами або роботі з механізмами слід бути обережними через можливість розвитку запаморочення, слабкості та інших можливих небажаних реакцій.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептом
Склад, форма випуску та упаковкаПігулки - 1 таб. Активні речовини: гідрохлортіазид 100мг; Допоміжні речовини: лактози моногідрат, повідон, целюлоза, крохмаль кукурудзяний, магнію стеарат. У упаковці 20 штук.ФармакокінетикаНа 60-80% всмоктується із ШКТ. На 40% зв'язується з білками крові, де через 2-5 годин визначається його максимальна концентрація. Період напіввиведення – 6-15 год. Більшість (95%) у незміненому вигляді виводиться нирками.ФармакодинамікаТіазидний діуретик (салуретик) середньої сили та тривалості дії. Має слабший діуретичний ефект порівняно з фуросемідом. Зменшує реабсорбцію натрію, хлору та води з первинної сечі в кров у проксизмальній частині канальців. Виводить K+, Mg2+, гідрокарбонатів та фосфатів, затримує Ca2+. Сечогінний ефект починає проявлятися через 2 години, максимум – через 4 години, тривалість діуретичної дії становить 10-12 годин. За рахунок розширення артеріол та зменшення ОЦК знижує тиск. Гіпертензивна дія проявляється через 4 дні. При нецукровому діабеті знижує об'єм сечі, одночасно збільшуючи її концентрацію.Показання до застосуванняЛікування гіпертензії – монотерапія або комбінація з іншими гіпеотензивними препаратами. Набряки різного генезу (при нефротичному синдромі, гострій та хронічній нирковій недостатності, ХСН, передменструальному синдромі, при лікуванні кортикостероїдами та при токсикозах вагітних). Нефрогенний нецукровий діабет (контроль поліурії).Протипоказання до застосуванняТяжкі форми цукрового діабету; підвищена чутливість до препарату або сульфонамідів; тяжка ниркова недостатність; анурія; хвороба Аддісона; подагра.Вагітність та лактаціяПротипоказаний дітям до 2 років та у першому триместрі вагітності.Побічна діяЗниження рівня калію, магнію, підвищення кальцію в крові проявляється спрагою та сухістю в роті, нудотою, судомами у м'язах, порушенням серцевого ритму, змінами психіки, вираженою втомою; гіпонатріємія, яка проявляється сплутаністю свідомості, уповільнення процесу мислення, підвищеною збудливістю, конвульсіями та м'язовими судомами; підвищення рівня цукру в крові та поява його в сечі. Тіазиди знижують толерантність до глюкози, тому латентний цукровий діабет проявляється; підвищення ліпідів та сечової кислоти в крові (при тривалому застосуванні високих доз); холецистит, холестатична жовтяниця, запалення слинних залоз, запор; аритмії та ортостатична гіпотензія; запаморочення, біль голови, порушення зору (розпливчастість), парестезії; кропив'янка, пурпура, синдром Стівенса-Джонсона, некротичний васкуліт, анафілактичний шок; інтерстиціальний нефрит із порушенням функції нирок; зниження потенції.Взаємодія з лікарськими засобамиНепрямі антикоагулянти, НПЗЗ, Клофібрат посилюють діуретичний ефект. Прийом вазодилататорів, бета-адреноблокаторів, трициклічних антидепресантів, діазепаму, барбітуратів та етанолу посилює гіпотензивний ефект діуретиків. Індометацин та інші НПЗЗ знижують гіпотензивний ефект. Холестирамін зменшує дію тіазидних діуретиків, оскільки гальмує їхнє всмоктування. При одночасному застосуванні із серцевими глікозидами підвищується ризик їх токсичності (підвищена збудливість шлуночків), що пов'язано з гіпокаліємією та гіпомагніємією. Застосування аміодарону та діуретиків підвищує ризик появи аритмій, що пов'язано з гіпокаліємією. При сумісному застосуванні з кортикостероїдами виникає ризик розвитку гіпокаліємії. Тіазидні діуретики послаблюють дію гіпоглікемічних препаратів та норадреналіну зменшують ефект пероральних контрацептивів, посилюють нейротоксичність саліцилатів та збільшують чутливість до тубокурарину. Прийом метилдопи та діуретика може спричинити гемоліз.Спосіб застосування та дозиЯк антигіпертензивний засіб: ЦД 25-50 мг. Гідрохлортіазид застосовується як засіб для монотерапії або у комбінації з іншими антигіпертензивними засобами (інгібіторами АПФ, вазодилататорами, бета-адреноблокаторами, симпатолітиками). Збільшення дози до 100 мг пропорційно веде до збільшення діурезу, зниження артеріального тиску та втрати натрію. Якщо доза – більше 100 мг, зростання діурезу та зниження АТ дуже незначні, проте зростає втрата електролітів K+ та Mg2+. Доцільним є збільшення дози до 200 мг, оскільки посилення діурезу не відзначається. Гіпотензивна дія проявляється через 3-4 дні, а для стійкого ефекту іноді потрібні 3-4 тижні. Якщо гідрохлортіазид комбінується з іншими гіпотензивними засобами, дозу іншого препарату іноді доводиться знижувати, щоб уникнути надмірного зниження тиску. Набряковий синдром: 25-100 мг вранці (можна поділити на 2 прийоми до 11 години дня). Іноді у тяжких випадках спочатку лікування призначається до 200 мг на добу. Через 3 дні роблять перерву на 5 днів. Для підтримуючої терапії 25-50 мг – двічі на тиждень. При такому уривчастому курсі лікування побічні явища розвиваються рідше. Нефрогенний нецукровий діабет: 25 мг на добу, поступово збільшуючи до 50-150 мг, розділивши на 2 прийоми. При досягненні ефекту (зменшення поліурії та спраги) доза знижується. Передменструальний синдром: 25 мг із моменту прояву симптомів до настання менструації. Для дітей дози обчислюються, виходячи з ваги дитини. Педіатрична доза – 1-2 мг/кг ваги 1 раз на добу. Для зниження внутрішньоочного тиску інструкція застосування Гідрохлортіазиду передбачає призначення 25 мг 1 раз на 3-6 днів. Таблетки приймаються внутрішньо після їди.ПередозуванняПроявляється адинамією, тахікардією та аритмією, запорами, сонливістю, сухістю у роті зниженням артеріального тиску, зменшенням добового діурезу. Специфічного антидоту немає, симптоматичне лікування: промивання шлунка, прийом сорбентів, інфузія розчинів електролітів.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Діючі речовини: гідрохлортіазид – 25 мг; Допоміжні речовини: лактози моногідрат – 70 мг, целюлоза мікрокристалічна – 20 мг, крохмаль картопляний – 13.7 мг, магнію стеарат – 1.3 мг. 7 чи 10 шт. - Упаковки осередкові контурні (1,2,3,4,5) - Пачки картонні.Опис лікарської формиТаблетки білого або майже білого з жовтуватим кольором, круглі, плоскоциліндричні, без ризику, з фаскою; допускається легка мармуровість.Фармакотерапевтична групаДіуретичний засіб.ФармакокінетикаПісля прийому внутрішньо 60-80% дози абсорбується із ШКТ. Час досягнення Cmax у плазмі – 1.5-3 год. Гідрохлортіазид накопичується в еритроцитах. У фазі виведення його концентрація в еритроцитах у 3-9 разів більша, ніж у плазмі. Зв'язування з білками плазми – 40-70%. Vd у термінальній фазі виведення становить 3-6 л/кг (що еквівалентно 210-420 л при масі тіла 70 кг). Гідрохлортіазид метаболізується дуже мало. Його єдиним виявленим у слідових кількостях метаболітом є 2-аміно-4-хлоро-М-бензендісульфонамід. Виведення гідрохлортіазиду з плазми має двофазний характер: T1/2 у початковій фазі становить 2 год, у термінальній фазі – близько 10 год. У пацієнтів із нормальною функцією нирок виведення здійснюється майже виключно нирками. Загалом 50-75% прийнятої внутрішньо дози виводиться із сечею у незміненому вигляді. У пацієнтів похилого віку та при порушеннях функції нирок кліренс гідрохлортіазиду суттєво знижується, що призводить до значного збільшення його концентрації у плазмі крові. Зниження кліренсу, що спостерігається у літніх хворих, мабуть, пов'язане з погіршенням функції нирок. У хворих на цироз печінки змін фармакокінетики гідрохлортіазиду не відзначається.ФармакодинамікаТіазидний діуретик. Порушує реабсорбцію іонів натрію, хлору та води в дистальних канальцях нефрону. Збільшує виведення іонів калію, магнію, бікарбонату; затримує в організмі іони кальцію. Діуретичний ефект настає через 2 години, досягає максимуму через 4 години і триває до 12 годин. Сприяє зниженню підвищеного АТ. Крім того, зменшує поліурію у хворих з нецукровим діабетом (механізм дії остаточно не з'ясований). У ряді випадків знижує внутрішньоочний тиск при глаукомі.Показання до застосуванняАртеріальна гіпертензія (як монотерапія або у складі комбінованої терапії), набряковий синдром різного генезу (хронічна серцева недостатність, нефротичний синдром, передменструальний синдром, гострий гломерулонефрит, хронічна ниркова недостатність, портальна гіпертензія, затримка рідини при ожирінні, лікування кортикостероїд при нецукровому діабеті, глаукоми (субкомпенсовані форми), профілактика утворення кальцій-фосфатних конкрементів у сечовивідних шляхах при гіперкальціурії.Протипоказання до застосуванняНиркова недостатність тяжкого ступеня, анурія, тяжка печінкова недостатність або печінкова енцефалопатія (ризик розвитку печінкової коми), тяжкі форми подагри та цукрового діабету, рефрактерна гіпокаліємія, гіперкальціємія, гіпонатріємія, недостатність функції кори надниркових залоз (хвороба Аддісона); І триместр вагітності, період грудного вигодовування; дитячий вік до 3 років (для жорсткої лікарської форми); підвищена чутливість до сульфонамідів.Вагітність та лактаціяПротипоказано застосування в І триместрі вагітності та в період грудного вигодовування. З обережністю застосовувати у ІІ та ІІІ триместрах вагітності. Гідрохлортіазид виділяється із грудним молоком.Побічна діяЗ боку травної системи: нудота, блювання, діарея; рідко – панкреатит. Серцево-судинна система: ортостатична гіпотензія, тахікардія. З боку обміну речовин: гіпокаліємія, гіпомагніємія, гіпонатріємія, гіпохлоремічний алкалоз, гіперурикемія, гіперкальціємія. З боку ендокринної системи: гіперглікемія. З боку системи кровотворення: рідко – нейтропенія, тромбоцитопенія. З боку органу зору: рідко – порушення зору. З боку ЦНС та периферичної нервової системи: слабкість, стомлюваність, запаморочення, парестезії. Алергічні реакції: рідко – алергічні дерматити.Взаємодія з лікарськими засобамиПри одночасному застосуванні антигіпертензивних засобів, що недеполяризують міорелаксантів, їх дія посилюється. При одночасному застосуванні барбітуратів, діазепаму, етанолу підвищується ризик розвитку ортостатичної гіпотензії. При одночасному застосуванні з кортикостероїдами виникає ризик розвитку гіпокаліємії, а також ортостатичної гіпотензії. При одночасному застосуванні з інгібіторами АПФ (в т.ч. каптоприлом, еналаприлом) посилюється антигіпертензивна дія. Можлива виражена артеріальна гіпотензія, особливо після прийому першої дози гідрохлортіазиду, мабуть, за рахунок гіповолемії, що призводить до посилення транзиторного гіпотензивного ефекту інгібітора АПФ. Підвищується ризик порушення функції нирок. Не виключається розвиток гіпокаліємії. При одночасному застосуванні пероральних гіпоглікемічних препаратів знижується їхня ефективність. При одночасному застосуванні препаратів кальцію та/або вітаміну D у високих дозах можлива гіперкальціємія та ризик розвитку метаболічного ацидозу внаслідок уповільнення виведення кальцію із сечею під впливом тіазидних діуретиків. При одночасному застосуванні з алопуринолом підвищується ризик розвитку алергічних реакцій, особливо у пацієнтів із порушеннями функції нирок. При одночасному застосуванні з дигоксином можливе підвищення ризику глікозидної інтоксикації. При одночасному застосуванні з індометацином, піроксикамом, напроксеном, фенілбутазоном можливе зменшення гіпотензивного ефекту. При одночасному застосуванні з ірбесартаном можливий розвиток адитивного гіпотензивного ефекту. При одночасному застосуванні з карбамазепіном є повідомлення розвитку гіпонатріємії. При одночасному застосуванні з колестиполом, колестираміном зменшується абсорбція та діуретичний ефект гідрохлортіазиду. При одночасному застосуванні з літієм карбонатом можливе підвищення концентрації в крові солей літію до токсичного рівня. При одночасному застосуванні з орлістатом зменшується ефективність гідрохлортіазиду, що може призвести до значного підвищення артеріального тиску та розвитку гіпертонічного кризу. При одночасному застосуванні з соталолом можлива гіпокаліємія та розвиток шлуночкової аритмії типу "пірует".Спосіб застосування та дозиПриймають усередину. Схема застосування залежить від показань, клінічної ситуації, супутніх захворювань. Для дорослих разова доза становить 12,5-100 мг 1 раз на добу. Для дітей старше 3 років доза становить 1-2 мг/кг/добу або 30-60 мг/м2 поверхні тіла 1 раз на добу.Запобіжні заходи та особливі вказівкиЗ обережністю застосовують у пацієнтів з подагрою та цукровим діабетом, зі збільшенням тривалості інтервалу QT на ЕКГ, при одночасному застосуванні з препаратами, які здатні викликати поліморфну шлуночкову тахікардію типу "пірует" або збільшувати тривалість інтервалу QT на ЕКГ; одночасно з препаратами літію, здатними викликати гіпокаліємію, із серцевими глікозидами; при алергічних реакціях на пеніцилін в анамнезі; при системному червоному вовчаку; при ІХС, вираженому атеросклерозі коронарних або церебральних артерій, хронічній серцевій недостатності; при немеланомному ракі шкіри в анамнезі; у пацієнтів похилого віку; у II та III триместрах вагітності; у дітей віком від 3 до 18 років. У хворих з нирковою недостатністю необхідний систематичний контроль концентрації у плазмі електролітів та КК. При появі ознак дефіциту калію, а також при одночасному застосуванні серцевих глікозидів, кортикостероїдів та АКТГ показано призначення препаратів калію або калійзберігаючих діуретиків. При тривалому застосуванні слід дотримуватися дієти, багатої на калій. Не рекомендується одночасне застосування діуретиків з НПЗЗ.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Активні речовини: гідрохлортіазид 25 мг; Допоміжні речовини: лактози моногідрат, повідон, целюлоза, крохмаль кукурудзяний, магнію стеарат. У упаковці 20 штук.ФармакокінетикаНа 60-80% всмоктується із ШКТ. На 40% зв'язується з білками крові, де через 2-5 годин визначається його максимальна концентрація. Період напіввиведення – 6-15 год. Більшість (95%) у незміненому вигляді виводиться нирками.ФармакодинамікаТіазидний діуретик (салуретик) середньої сили та тривалості дії. Має слабший діуретичний ефект порівняно з фуросемідом. Зменшує реабсорбцію натрію, хлору та води з первинної сечі в кров у проксизмальній частині канальців. Виводить K+, Mg2+, гідрокарбонатів та фосфатів, затримує Ca2+. Сечогінний ефект починає проявлятися через 2 години, максимум – через 4 години, тривалість діуретичної дії становить 10-12 годин. За рахунок розширення артеріол та зменшення ОЦК знижує тиск. Гіпертензивна дія проявляється через 4 дні. При нецукровому діабеті знижує об'єм сечі, одночасно збільшуючи її концентрацію.Показання до застосуванняЛікування гіпертензії – монотерапія або комбінація з іншими гіпеотензивними препаратами. Набряки різного генезу (при нефротичному синдромі, гострій та хронічній нирковій недостатності, ХСН, передменструальному синдромі, при лікуванні кортикостероїдами та при токсикозах вагітних). Нефрогенний нецукровий діабет (контроль поліурії).Протипоказання до застосуванняТяжкі форми цукрового діабету; підвищена чутливість до препарату або сульфонамідів; тяжка ниркова недостатність; анурія; хвороба Аддісона; подагра.Вагітність та лактаціяПротипоказаний дітям до 2 років та у першому триместрі вагітності.Побічна діяЗниження рівня калію, магнію, підвищення кальцію в крові проявляється спрагою та сухістю в роті, нудотою, судомами у м'язах, порушенням серцевого ритму, змінами психіки, вираженою втомою; гіпонатріємія, яка проявляється сплутаністю свідомості, уповільнення процесу мислення, підвищеною збудливістю, конвульсіями та м'язовими судомами; підвищення рівня цукру в крові та поява його в сечі. Тіазиди знижують толерантність до глюкози, тому латентний цукровий діабет проявляється; підвищення ліпідів та сечової кислоти в крові (при тривалому застосуванні високих доз); холецистит, холестатична жовтяниця, запалення слинних залоз, запор; аритмії та ортостатична гіпотензія; запаморочення, біль голови, порушення зору (розпливчастість), парестезії; кропив'янка, пурпура, синдром Стівенса-Джонсона, некротичний васкуліт, анафілактичний шок; інтерстиціальний нефрит із порушенням функції нирок; зниження потенції.Взаємодія з лікарськими засобамиНепрямі антикоагулянти, НПЗЗ, Клофібрат посилюють діуретичний ефект. Прийом вазодилататорів, бета-адреноблокаторів, трициклічних антидепресантів, діазепаму, барбітуратів та етанолу посилює гіпотензивний ефект діуретиків. Індометацин та інші НПЗЗ знижують гіпотензивний ефект. Холестирамін зменшує дію тіазидних діуретиків, оскільки гальмує їхнє всмоктування. При одночасному застосуванні із серцевими глікозидами підвищується ризик їх токсичності (підвищена збудливість шлуночків), що пов'язано з гіпокаліємією та гіпомагніємією. Застосування аміодарону та діуретиків підвищує ризик появи аритмій, що пов'язано з гіпокаліємією. При сумісному застосуванні з кортикостероїдами виникає ризик розвитку гіпокаліємії. Тіазидні діуретики послаблюють дію гіпоглікемічних препаратів та норадреналіну зменшують ефект пероральних контрацептивів, посилюють нейротоксичність саліцилатів та збільшують чутливість до тубокурарину. Прийом метилдопи та діуретика може спричинити гемоліз.Спосіб застосування та дозиЯк антигіпертензивний засіб: ЦД 25-50 мг. Гідрохлортіазид застосовується як засіб для монотерапії або у комбінації з іншими антигіпертензивними засобами (інгібіторами АПФ, вазодилататорами, бета-адреноблокаторами, симпатолітиками). Збільшення дози до 100 мг пропорційно веде до збільшення діурезу, зниження артеріального тиску та втрати натрію. Якщо доза – більше 100 мг, зростання діурезу та зниження АТ дуже незначні, проте зростає втрата електролітів K+ та Mg2+. Доцільним є збільшення дози до 200 мг, оскільки посилення діурезу не відзначається. Гіпотензивна дія проявляється через 3-4 дні, а для стійкого ефекту іноді потрібні 3-4 тижні. Якщо гідрохлортіазид комбінується з іншими гіпотензивними засобами, дозу іншого препарату іноді доводиться знижувати, щоб уникнути надмірного зниження тиску. Набряковий синдром: 25-100 мг вранці (можна поділити на 2 прийоми до 11 години дня). Іноді у тяжких випадках спочатку лікування призначається до 200 мг на добу. Через 3 дні роблять перерву на 5 днів. Для підтримуючої терапії 25-50 мг – двічі на тиждень. При такому уривчастому курсі лікування побічні явища розвиваються рідше. Нефрогенний нецукровий діабет: 25 мг на добу, поступово збільшуючи до 50-150 мг, розділивши на 2 прийоми. При досягненні ефекту (зменшення поліурії та спраги) доза знижується. Передменструальний синдром: 25 мг із моменту прояву симптомів до настання менструації. Для дітей дози обчислюються, виходячи з ваги дитини. Педіатрична доза – 1-2 мг/кг ваги 1 раз на добу. Для зниження внутрішньоочного тиску інструкція застосування Гідрохлортіазиду передбачає призначення 25 мг 1 раз на 3-6 днів. Таблетки приймаються внутрішньо після їди.ПередозуванняПроявляється адинамією, тахікардією та аритмією, запорами, сонливістю, сухістю у роті зниженням артеріального тиску, зменшенням добового діурезу. Специфічного антидоту немає, симптоматичне лікування: промивання шлунка, прийом сорбентів, інфузія розчинів електролітів.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаТаблетки – 1 таб.:. Діюча речовина: Гідрохлортіазид 25; допоміжні речовини: лактози моногідрат 70 мг; целюлоза мікрокристалічна 20 мг; крохмаль картопляний 13,7 мг; стеарат магнію 1,3 мг. По 7 таблеток у контурне осередкове пакування з плівки полівінілхлоридної та фольги алюмінієвої друкованої. 2, 3, 4 контурні коміркові упаковки разом з інструкцією по застосуванню поміщають в пачку з картону. По 10 таблеток у контурне осередкове впакування з плівки полівінілхлоридної та фольги алюмінієвої друкованої. 1, 2, 3, 4, 5 контурні коміркові упаковки разом з інструкцією із застосування поміщають у пачку з картону.Опис лікарської формиТаблетки 25 мг - круглі, плоскоциліндричні, без ризику, з фаскою, білого або майже білого з жовтуватим відтінком кольору. Допускається наявність легкої мармуровості.Фармакотерапевтична групаДіуретичний засіб.ФармакокінетикаВсмоктування та розподіл. Гідрохлортіазид неповно, проте досить швидко всмоктується із шлунково-кишкового тракту. Після прийому внутрішньо в дозі 100 мг максимальна концентрація гідрохлортіазиду в плазмі досягається через 1,5-2,5 години. На максимумі діуретичної активності (приблизно через 4 години після прийому) концентрація гідрохлортіазиду у плазмі становить 2 мкг/мл. Зв'язок із білками плазми становить 40%. Гідрохлортіазид проникає через плацентарний бар'єр та екскретується у грудне молоко, але не проникає через гематоенцефалічний бар'єр. Метаболізм. Гідрохлоротіазид в організмі людини не метаболізується. Виведення. Первинний шлях виведення через нирки (фільтрація та секреція) у незмінному вигляді. Приблизно 61% прийнятої дози виводиться протягом 24 годин. У пацієнтів з нормальною нирковою функцією період напіввиведення становить від 5,6 до 14,8 години (в середньому 6,4 години). Фармакокінетика в спеціальних групах пацієнтів. Порушення функції нирок. У пацієнтів з помірною нирковою недостатністю період напіввиведення гідрохлортіазиду становить у середньому 11,5 години, а у пацієнтів з кліренсом креатиніну менше 30 мл/хв – 20,7 години.ФармакодинамікаМеханізм дії тіазидних діуретиків (тіазидів) не повністю вивчений. Тіазиди блокують реабсорбцію іонів натрію та хлору на початку ниркових канальців. Таким чином, вони збільшують екскрецію натрію та хлору і, отже, виведення води з організму. Внаслідок сечогінної дії гідрохлортіазиду зменшується об'єм циркулюючої рідини, внаслідок чого збільшується активність реніну та вміст альдостерону у плазмі крові. Це призводить до збільшення екскреції іонів калію із сечею та зниження вмісту калію в крові (гіпокаліємії). Гідрохлортіазид також збільшує екскрецію іонів магнію та знижує екскреції іонів кальцію із сечею. Тіазидні діуретики знижують екскрецію сечової кислоти нирками та збільшують її вміст у крові. Тіазидні діуретики також зменшують активність карбоангідрази шляхом посилення виведення іонів бікарбонату. Але ця дія зазвичай проявляється слабо і не впливає на рН сечі. У максимальних терапевтичних дозах діуретичний/натрійуретичний ефект усіх тіазидних діуретиків приблизно однаковий. Натріурез та діурез наступають протягом 2 годин і досягають свого максимуму приблизно через 4 години. Тривалість діуретичної дії гідрохлортіазиду становить від 6 до 12 годин. Гідрохлортіазид має антигіпертензивну дію. На нормальний артеріальний тиск тіазидні діуретики не впливають.Показання до застосуванняАртеріальна гіпертензія (застосовується як у монотерапії, так і у комбінації з іншими гіпотензивними засобами). Набряковий синдром різного генезу (хронічна серцева недостатність, нефротичний синдром, передменструальний синдром, гострий гломерулонефрит, хронічна ниркова недостатність, портальна гіпертензія, лікування кортикостероїдами). Зменшення симптоматичної поліурії при нефрогенному нецукровому діабеті. Профілактика утворення кальцій-фосфатних конкрементів у сечостатевому тракті при гіперкальціурії.Протипоказання до застосуванняПідвищена чутливість до гідрохлортіазиду, інших похідних сульфонаміду або будь-якої з допоміжних речовин. Анурія. Тяжка ниркова недостатність (кліренс креатиніну менше 30 мл/хв). Тяжка печінкова недостатність або печінкова енцефалопатія (ризик розвитку печінкової коми). Важкоконтрольований цукровий діабет. Рефрактерна гіпокаліємія, гіпонатріємія, гіперкальціємія. Недостатність кори надниркових залоз (зокрема. хвороба Аддісона). Вагітність (I триместр) та період грудного вигодовування. Дитячий вік до 3 років (тверда лікарська форма). Рідкісна спадкова непереносимість галактози, дефіцит лактази, синдром глюкозо-галактозної мальабсорбції (препарат містить лактози моногідрат). З обережністю. Порушення функції нирок. Порушення функції печінки легкого та помірного ступеня тяжкості, що прогресують захворювання печінки. Гіпокаліємія. Гіпонатріємія. Гіперкальціємія. Збільшення тривалості інтервалу QT на ЕКГ. Одночасне застосування лікарських препаратів, які можуть викликати поліморфну шлуночкову тахікардію типу «пірует» або збільшувати тривалість інтервалу QT на ЕКГ. Одночасне застосування препаратів літію, лікарських засобів, здатних викликати гіпокаліємію, серцевих глікозидів. Алергічні реакції на пеніцилін в анамнезі. Гіперпаратиреоз. Цукровий діабет. Гіперурикемія, подагра. Системна червона вовчанка. Ішемічна хвороба серця, виражений атеросклероз коронарних чи церебральних артерій. Хронічна серцева недостатність. Літній вік. Вагітність (другий та третій триместр). Дитячий вік (від 3 до 18 років).Вагітність та лактаціяВагітність. Існує обмежений досвід застосування гідрохлортіазиду під час вагітності (особливо у першому триместрі). Доклінічні дані щодо безпеки недостатні. Гідрохлортіазид проникає через плацентарний бар'єр і визначається пуповинної крові. З урахуванням механізму фармакологічної дії гідрохлортіазиду, його застосування у другому та третьому триместрах вагітності може порушувати фетоплацентарну перфузію та призводити до розвитку у плода та новонародженого таких ускладнень, як жовтяниця, порушення водно-електролітного балансу та тромбоцитопенія. Описано випадки розвитку тромбоцитопенії у новонароджених, матері яких отримували тіазидні діуретики. Застосування гідрохлортіазиду у першому триместрі вагітності протипоказане. У другому та третьому триместрах вагітності гідрохлортіазид може застосовуватися лише у разі безумовної необхідності, коли користь для матері перевищує потенційний ризик для плода та/або дитини. Гідрохлортіазид не можна застосовувати для лікування гестозів ІІ половини вагітності (набряків, артеріальної гіпертензії або прееклампсії), т.к. він збільшує ризик зниження обсягу циркулюючої крові та плацентарної гіпоперфузії, але не надає сприятливого впливу протягом зазначених ускладнень вагітності. Діуретики не запобігають розвитку гестозів. Період грудного вигодовування. Гідрохлортіазид проникає в материнське молоко, у зв'язку з чим його застосування у період грудного вигодовування протипоказане. Якщо застосування гідрохлортіазиду в період лактації є абсолютно необхідним, слід припинити грудне вигодовування.Побічна діяДля опису частоти небажаних реакцій використовувалася наступна градація частоти розвитку небажаних реакцій: часто ≥ 1/100 до Частота розвитку побічних реакцій наведена відповідно до класифікації Всесвітньої організації охорони здоров'я. Порушення з боку крові та лімфатичної системи дуже рідко: лейкопенія, агранулоцитоз, тромбоцитопенія, гемолітична анемія, апластична анемія. Порушення з боку імунної системи частота невідома: кропив'янка, пурпура, лихоманка, некротизуючий ангіїт (васкуліт та шкірний васкуліт), синдром Стівенса-Джонсона, анафілактичні реакції аж до шоку; загострення течії системного червоного вовчаку. Порушення з боку нервової системи не часто: непритомність (зазвичай при застосуванні у високих дозах); рідко: біль голови, запаморочення, вертиго, парестезія; частота невідома: сонливість, сплутаність свідомості. Порушення з боку органу зору рідко: минуща нечіткість зору; частота невідома: гостра міопія, гострий напад глаукоми, ксантопсія. Порушення серця: нечасто: брадикардія. Порушення з боку судин не часто: ортостатична гіпотензія. Порушення з боку дихальної системи, органів грудної клітки та середостіння: нечасто: інтерстиційна пневмонія; дуже рідко: респіраторний дистрес-синдром (включаючи пневмоніт та некардіогенний набряк легень). Порушення з боку шлунково-кишкового тракту: часто: втрата апетиту, анорексія, дискомфорт у шлунку, біль у верхніх відділах живота, діарея, нудота, блювання, запор; рідко: панкреатит; частота невідома: сіаладеніт. Порушення з боку печінки та жовчовивідних шляхів рідко: жовтяниця (внутрішньопечінкова холестатична жовтяниця); Нечасто: холецистит. Порушення з боку шкіри та підшкірних тканин нечасто: шкірний висип, свербіж шкіри, фотосенсибілізація; частота невідома: алопеція. Порушення з боку скелетно-м'язової та сполучної тканини рідко: судоми, м'язова слабкість (особливо при застосуванні у високих дозах). Порушення з боку нирок та сечовивідних шляхів частота невідома: порушення функції нирок, інтерстиціальний нефрит, ниркова недостатність. Порушення з боку статевих органів та молочної залози частота невідома: зниження потенції. Порушення з боку обміну речовин і харчування дуже часто: гіпонатріємія, гіпокаліємія, гіпомагніємія, гіпохлоремічний алкалоз, гіперкальціємія: часто: гіперурикемія (в т.ч. з розвитком нападу подагри), маніфестація цукрового діабету, що протікає латентно; частота невідома: гіперглікемія та глюкозурія у пацієнтів із цукровим діабетом, зниження толерантності до глюкози; підвищення концентрації холестерину або тригліцеридів у сироватці крові (зазвичай при застосуванні у високих дозах). Загальні розлади та порушення у місці введення дуже часто: втома, спрага (зазвичай при застосуванні у високих дозах).Взаємодія з лікарськими засобамиНерекомендовані поєднання лікарських засобів. Препарати літію. При одночасному застосуванні гідрохлортіазиду та препаратів літію знижується нирковий кліренс літію, що може призвести до підвищення концентрації літію у плазмі крові та збільшення його токсичності. При необхідності одночасного застосування гідрохлортіазиду слід ретельно підбирати дозу препаратів літію, регулярно контролювати концентрацію літію у плазмі крові та відповідним чином підбирати дозу препарату. Поєднання лікарських засобів, що вимагають особливої уваги. Препарати, здатні викликати поліморфну шлуночкову тахікардію типу "пірует". Слід особливо обережно застосовувати гідрохлортіазид одночасно з такими препаратами, як:. антиаритмічні лікарські препарати ІА класу (хінідин, гідрохінідин, дизопірамід, прокаїнамід); антиаритмічні лікарські препарати ІІІ класу (дофетилід, ібутилід, бретилія тозилат), соталол, дронедарон, аміодарон; інші (неантіаритмічні) лікарські засоби, такі як: нейролептики: фенотіазини (хлорпромазин, ціамемазин, левомепромазин, тіоридазин, трифлуоперазин, флуфеназин), бензаміди (амісульприд, сультоприд, сульприд, тіаприд), бутирофенони (дроперидол, галоперидол); пімозід, сертиндол; антидепресанти: трициклічні антидепресанти, селективні інгібітори зворотного захоплення серотоніну (циталопрам, есциталопрам); антибактеріальні засоби: фторхінолони (левофлоксацин, моксифлоксацин, спрафлоксацин, ципрофлоксацин); макроліди (еритроміцин при внутрішньовенному введенні, азитроміцин, кларитроміцин, рокситроміцин, спіраміцин), ко-тримоксазол; протигрибкові засоби: азоли (воріконазол, ітраконазол, кетококоназол, флуконазол); протималярійні засоби (хінін, хлорохін, мефлохін, галофантрин, лумефантрін); протипротозойні засоби (пентамідин при парентеральному введенні); антиангінальні засоби (ранолазин, беприділ); протипухлинні засоби (вандетаніб, миш'яку триоксид, оксаліплатин, такролімус); протиблювотні засоби (домперидон, ондансетрон); засоби, що впливають на моторику шлунково-кишкового тракту (цизапрід); антигістамінні засоби (астемізол, терфенадин, мізоластин); інші лікарські засоби (анагрелід, вазопресин, дифеманілу метилсульфат, кетансерин, пробукол, пропофол, севофлуран, терліпресин, теродилін, цилостазол); у зв'язку із збільшенням ризику шлуночкових аритмій, особливо поліморфної шлуночкової тахікардії типу "пірует" (фактор ризику – гіпокаліємія). Слід визначити вміст калію в плазмі крові та, при необхідності, коригувати його до початку комбінованої терапії гідрохлортіазидом із зазначеними вище препаратами. Необхідний контроль клінічного стану пацієнта, вмісту електролітів плазми крові та показників ЕКГ. У пацієнтів з гіпокаліємією необхідно застосовувати препарати, що викликають поліморфну шлуночкову тахікардію типу "пірует". Лікарські засоби, здатні підвищувати тривалість інтервалу QT. Одночасне застосування гідрохлортіазиду з лікарськими препаратами, здатними збільшувати тривалість інтервалу QT, має ґрунтуватися на ретельній оцінці для кожного пацієнта співвідношення очікуваної користі та потенційного ризику (можливе збільшення ризику розвитку поліморфної шлуночкової тахікардії типу "пірует"). При застосуванні таких комбінацій необхідно регулярно реєструвати ЕКГ (для виявлення подовження інтервалу QT), а також контролювати вміст калію в крові. Препарати, здатні викликати гіпокаліємію: амфотерицин В (при внутрішньовенному введенні), глюко- та мінералокортикостероїди (при системному застосуванні), тетракозактид (АКТГ), гліциризинова кислота (карбеноксолон, препарати, що містять корінь солодки), проносні засоби, Збільшення ризику розвитку гіпокаліємії при одночасному застосуванні з гідрохлортіазидом (адитивний ефект). Необхідний регулярний контроль вмісту калію у плазмі крові, за необхідності – його корекція. На тлі терапії гідрохлортіазидом рекомендується застосовувати проносні засоби, що не стимулюють моторику кишечника. Серцеві глікозиди. Гіпокаліємія та гіпомагніємія, зумовлені дією тіазидних діуретиків, посилюють токсичність серцевих глікозидів. При одночасному застосуванні гідрохлортіазиду та серцевих глікозидів слід регулярно контролювати концентрацію калію в плазмі крові, показники ЕКГ та, за необхідності, коригувати терапію. Поєднання лікарських засобів, що потребують уваги. Інші гіпотензивні препарати. Потенціювання антигіпертензивної дії гідрохлоротіазиду (адитивний ефект). Може виникнути потреба у корекції дози одночасно призначених гіпотензивних препаратів. Рекомендується припинити прийом гідрохлортіазиду за 2-3 дні до початку терапії інгібіторами ангіотензинперетворюючого ферменту (АПФ) для запобігання розвитку симптоматичної артеріальної гіпотензії. Якщо це неможливо, слід зменшити початкову дозу інгібіторів АПФ. Етанол, барбітурати, антипсихотичні засоби (нейролептики), антидепресанти, анксіолітики, наркотичні анальгетики та засоби для загальної анестезії. Можливе посилення антигіпертензивної дії гідрохлортіазиду та потенціювання ортостатичної гіпотензії (адитивний ефект). Теофілін. Теофілін посилює дію діуретиків. Недеполяризуючі міорелаксанти (наприклад, тубокурарин). Можливе посилення ефекту недеполяризуючих міорелаксантів. Адреноміметики (пресорні аміни). Гідрохлоротіазид може знижувати ефект адреноміметиків, таких як епінефрин (адреналін) та норепінефрин (норадреналін). Нестероїдні протизапальні препарати (НПЗЗ), включаючи селективні інгібітори циклооксигенази-2 (ЦОГ-2) та високі дози ацетилсаліцилової кислоти (≥3 г/добу). НПЗЗ можуть знижувати діуретичну та антигіпертензивну дії гідрохлортіазиду. При одночасному застосуванні існує ризик розвитку гострої ниркової недостатності внаслідок зниження швидкості клубочкової фільтрації. Гідрохлортіазид може посилювати токсичну дію високих доз саліцилатів на центральну нервову систему. Гіпоглікемічні засоби для внутрішнього прийому та інсулін. Тіазидні діуретики впливають на толерантність до глюкози (можливий розвиток гіперглікемії) та знижують ефективність гіпоглікемічних засобів (може знадобитися корекція дози гіпоглікемічних засобів). Слід з обережністю спільно застосовувати гідрохлортіазид та метформін у зв'язку з ризиком розвитку лактоацидозу на фоні порушення функції нирок, спричиненого гідрохлортіазидом. Бета-адреноблокатори, діазоксид. Одночасне застосування тіазидних діуретиків (включаючи гідрохлортіазид), з бета-адреноблокаторами або діазоксидом може збільшити ризик розвитку гіперглікемії. Лікарські препарати, що застосовуються для лікування подагри (пробенецид, сульфінпupазон, алопуринол). Може знадобитися корекція дози урикозуричних лікарських засобів, оскільки гідрохлортіазид збільшує концентрацію сечової кислоти у сироватці крові. Тіазидні діуретики можуть збільшити частоту розвитку реакцій гіперчутливості до алопуринолу. Амантадін. Тіазидні діуретики (включаючи гідрохлортіазид) можуть знижувати кліренс амантадину, призводити до підвищення концентрації амантадину в плазмі та збільшувати ризик його небажаних ефектів. Флуконазол. При багаторазовому одночасному застосуванні з гідрохлортіазидом максимальна концентрація флуконазолу у плазмі збільшується на 40%. Корекція дози флуконазолу не потрібна, проте цю взаємодію слід брати до уваги. Антихолінергічні препарати (холіноблокатори). Антихолінергічні препарати (наприклад, атропін, біпериден) збільшують біодоступність тіазидних діуретиків за рахунок зниження моторики шлунково-кишкового тракту та швидкості спорожнення шлунка. Цитотоксичні (протипухлинні) препарати. Тіазидні діуретики зменшують ниркову екскрецію цитотоксичних лікарських засобів (наприклад, циклофосфаміду та метотрексату) та потенціюють їхню мієлосупресивну дію. Метилдоп. Описано випадки гемолітичної анемії при одночасному застосуванні гідрохлортіазиду та метилдопи. Карбамазепін. Ризик розвитку симптоматичної гіпонатріємії. При одночасному застосуванні гідрохлортіазиду та карбамазепіну необхідне спостереження за станом пацієнта та контроль вмісту натрію у плазмі крові. Циклоспорин. При одночасному застосуванні тіазидних діуретиків та циклоспорину збільшується ризик розвитку гіперурикемії та загострення подагри. Пероральні антикоагулянти. Тіазидні діуретики можуть зменшувати ефект пероральних антикоагулянтів. Йодомісткі контрастні речовини. Зневоднення організму на фоні прийому тіазидних діуретиків збільшує ризик розвитку гострої ниркової недостатності, особливо при застосуванні високих доз йодовмісних контрастних речовин. Перед застосуванням йодовмісних контрастних речовин необхідно компенсувати втрату рідини. Препарати кальцію. При одночасному застосуванні можливе підвищення вмісту кальцію в крові та розвитку гіперкальціємії внаслідок зниження виведення іонів кальцію нирками. Якщо необхідно одночасне призначення кальцієвмісних лікарських засобів, слід контролювати вміст кальцію в плазмі крові і коригувати дозу препаратів кальцію. Аніонні обмінні смоли (колестирамін та колестипол). Аніонні обмінні смоли зменшують абсорбцію гідрохлортіазиду. Одноразові дози колестираміну та колестиполу зменшують всмоктування гідрохлортіазиду у шлунково-кишковому тракті на 85% та 43% відповідно.Спосіб застосування та дозиВсередину. Таблетки слід приймати після їди. Дозування гідрохлортіазиду має бути підібрано індивідуально. Рекомендується приймати препарат у мінімальній ефективній дозі. Для забезпечення зазначених режимів дозування за необхідності застосування гідрохлортіазиду в разовій дозі 12,5 мг слід призначати препарати інших виробників у лікарській формі «таблетки 25 мг» із ризиком. Дорослі. Артеріальна гіпертензія. Звичайна початкова доза гідрохлортіазиду становить 25-50 мг 1 раз на добу, у вигляді монотерапії або комбінації з іншими гіпотензивними засобами. У деяких пацієнтів антигіпертензивний ефект досягається при застосуванні гідрохлортіазиду у початковій дозі 12,5 мг 1 раз на добу (як у вигляді монотерапії, так і у комбінації з іншими лікарськими засобами). Необхідно застосовувати максимально ефективну дозу препарату. Максимальна добова доза гідрохлортіазиду на лікування артеріальної гіпертензії становить 100 мг на добу. Якщо гідрохлортіазид застосовується в комбінації з іншими гіпотензивними препаратами, може виникнути потреба знизити дозу іншого препарату, щоб запобігти надмірному зниженню артеріального тиску (АТ). Антигіпертензивна дія гідрохлоротіазиду проявляється протягом 3-4 днів, однак для досягнення оптимального ефекту може знадобитися до 3-4 тижнів. Після закінчення лікування антигіпертензивний ефект зберігається протягом одного тижня. Набряковий синдром різного генезу. Звичайною початковою дозою гідрохлортіазиду при лікуванні набряків різного генезу є 25-100 мг 1 раз на день щодня. Деякі пацієнти відповідають на прийом гідрохлортіазиду через день або 1 раз на 3-5 днів. Залежно від клінічної відповіді, доза препарату може бути знижена до 25-50 мг 1 раз на добу щодня або 1 раз на 2-5 днів. У деяких випадках на початку лікування може знадобитися прийом гідрохлортіазиду у максимальній (для даного показання до застосування) дозі 200 мг на добу. При передменструальному синдромі нормальна доза становить 25 мг на добу і застосовується від моменту появи симптомів до початку менструації. Зменшення симптоматичної поліурії при нефрогенному нецукровому діабеті. Рекомендована добова доза гідрохлортіазиду – 50-150 мг на добу (у кілька прийомів). Профілактика утворення кальцій-фосфатних конкрементів у сечостатевому тракті при гіперкальціурії. Застосування гідрохлортіазиду показано при кальціурії понад 8 ммоль/добу. Початкова доза гідрохлортіазиду, що рекомендується, – 25 мг 1 раз на добу. Надалі показано збільшення до максимальної (для цього показання до застосування) дози 50 мг на добу. Діти. Дози встановлюються, виходячи з маси тіла дитини. Дітям старше 3 років – по 1-2 мг/кг/добу або 30-60 мг/м2 поверхні тіла 1 раз на добу. Загальна добова доза для дітей віком 3-12 років становить 37,5-100 мг (максимальна добова доза для дітей – 100 мг на добу). Після 3-5 днів лікування рекомендується зробити перерву на 3-5 днів. Як підтримуючу терапію у зазначеній дозі призначають 2 рази на тиждень. При застосуванні переривчастого курсу лікування з прийомом через 1-3 дні або протягом 2-3 днів з подальшою перервою зниження ефективності виражене меншою мірою, і побічні ефекти розвиваються рідше.ПередозуванняСимптоми. Найчастішими проявами передозування гідрохлортіазидом є збільшення діурезу, що супроводжується гострою втратою рідини (дегідратацією) та електролітними порушеннями (гіпокаліємія, гіпонатріємія, гіпохлоремія). Передозування гідрохлортіазидом може виявлятися такими симптомами: з боку серцево-судинної системи: тахікардія; зниження артеріального тиску; шок; з боку нервової системи: слабкість, сплутаність свідомості, запаморочення та спазми литкових м'язів, парестезія, порушення свідомості, втома; з боку шлунково-кишкового тракту: нудота, блювання, спрага; з боку нирок та сечовивідних шляхів: поліурія, олігурія або анурія (через гемоконцентрацію). Лабораторні показники: гіпокаліємія, гіпонатріємія, гіпохлоремія, алкалоз, підвищений вміст азоту сечовини у крові (особливо у пацієнтів із нирковою недостатністю). Лікування. При передозуванні проводиться симптоматична та підтримуюча терапія. Якщо препарат був прийнятий нещодавно, для виведення гідрохлортіазиду показано індукцію блювоти або промивання шлунка. Абсорбцію гідрохлортіазиду можна зменшити прийомом внутрішньо активованого вугілля. У разі зниження АТ або шоку слід заповнити об'єм циркулюючої крові запровадженням плазмозамінних рідин та дефіцит електролітів (калій, натрій). При дихальних порушеннях показано інгаляцію кисню або штучну вентиляцію легень. Слід контролювати водно-електролітний баланс (особливо вміст калію у сироватці крові) та функцію нирок до їх нормалізації. Специфічного антидоту немає. Гідрохлортіазид виводиться при гемодіалізі, проте ступінь його виведення не встановлено.Запобіжні заходи та особливі вказівкиПорушення функції нирок. У пацієнтів з порушеннями функції нирок гідрохлортіазид може спричинити азотемію. При нирковій недостатності можлива кумуляція гідрохлортіазиду. У пацієнтів зі зниженою нирковою функцією необхідний періодичний контроль кліренсу креатиніну. При прогресуванні порушення функції нирок та/або настання олігонурії (анурії) гідрохлортіазид слід відмінити. Порушення функції печінки. При застосуванні тіазидних діуретиків у пацієнтів з порушеннями функції печінки можливий розвиток печінкової енцефалопатії. Пацієнтам з тяжкою печінковою недостатністю або печінковою енцефалопатією застосування тіазидів протипоказане. У пацієнтів з печінковою недостатністю легкого та помірного ступеня тяжкості та/або прогресуючими захворюваннями печінки гідрохлортіазид слід застосовувати з обережністю, оскільки навіть невелика зміна водноелектролітного балансу та накопичення амонію у сироватці крові може спричинити печінкову кому. У разі прояву симптомів енцефалопатії прийом діуретиків слід негайно припинити. Водно-електролітний баланс та метаболічні порушення. Тіазидні діуретики (включаючи гідрохлортіазид) можуть спричинити зменшення об'єму циркулюючої рідини (гіповолемію) та порушення водно-електролітного балансу (в т.ч. гіпокаліємію, гіпонатріємію, гіпохлоремічний алкалоз). Клінічними симптомами порушень водноелектролітного балансу є сухість у роті, спрага, слабкість, млявість, стомлюваність, сонливість, занепокоєння, м'язовий біль або судоми, м'язова слабкість, виражене зниження артеріального тиску, олігурія, тахікардія, аритмія та порушення з боку шлунка як нудота та блювота). У пацієнтів, які отримують терапію гідрохлортіазидом (особливо при тривалому курсовому лікуванні), слід виявляти клінічні симптоми порушень водноелектролітного балансу, регулярно контролювати вміст електролітів у крові. Натрій. Всі діуретичні препарати можуть викликати гіпонатріємію, що іноді призводить до тяжких ускладнень. Гіпонатріємія та гіповолемія можуть призводити до зневоднення та ортостатичної гіпотензії. Супутнє зниження іонів хлору може призводити до вторинного компенсаторного метаболічного алкалозу, проте частота та ступінь виразності цього ефекту незначні. Рекомендується визначити вміст іонів натрію в плазмі крові до початку лікування та регулярно контролювати цей показник на фоні прийому гідрохлортіазиду. Калій. При застосуванні тіазидних та тіазидоподібних діуретиків існує ризик різкого зниження вмісту калію в плазмі та розвитку гіпокаліємії (концентрація калію менше 3,4 ммоль/л). Гіпокаліємія підвищує ризик розвитку порушень серцевого ритму (в т.ч. тяжких аритмій) та посилює токсичну дію серцевих глікозидів. Крім того, гіпокаліємія (так само, як і брадикардія) є станом, що сприяє розвитку поліморфної шлуночкової тахікардії типу "пірует", яка може призводити до летального результату. Гіпокаліємія представляє найбільшу небезпеку для наступних груп пацієнтів: особи похилого віку, пацієнти, що одночасно одержують терапію антиаритмічними та неантіаритмічними препаратами, які можуть викликати поліморфну шлуночкову тахікардію типу "пірует" або збільшувати тривалість інтервалу QT на ЕКГ, хвороби хронічної серцевої недостатністю. Крім того, до групи підвищеного ризику належать пацієнти із збільшеним інтервалом QT. При цьому немає значення, викликане це збільшення вродженими причинами або дією лікарських засобів. У всіх описаних вище випадках необхідно уникати ризику розвитку гіпокаліємії та регулярно контролювати вміст калію у плазмі крові. Перший вимір вмісту іонів калію в крові необхідно провести протягом першого тижня від початку лікування. З появою гіпокаліємії має бути призначене відповідне лікування. Гіпокаліємію можна коригувати застосуванням калійвмісних препаратів або прийомом харчових продуктів, багатих калієм (сухофрукти, фрукти, овочі). Кальцій. Тіазидні діуретики можуть зменшувати виведення іонів кальцію нирками, призводячи до незначного та тимчасового підвищення вмісту кальцію в плазмі. У деяких пацієнтів при тривалому застосуванні тіазидних діуретиків спостерігалися патологічні зміни паращитовидних залоз з гіперкальціємією та гіперфосфатемією, але без типових ускладнень гіперпаратиреозу (нефролітіаз, зниження мінеральної щільності кісткової тканини, виразкова хвороба). Виражена гіперкальціємія може бути проявом раніше не діагностованого гіперпаратиреозу. Через вплив на метаболізм кальцію тіазиди можуть впливати на лабораторні показники функції паращитовидних залоз. Слід припинити прийом тіазидних діуретиків (включно з гідрохлортіазидом) перед дослідженням функції паращитовидних залоз. Магній. Встановлено, що тіазиди збільшують виведення магнію нирками, що може призвести до гіпомагніємії. Клінічне значення гіпомагніємії залишається незрозумілим. Глюкоза. Лікування тіазидними діуретиками може порушувати толерантність до глюкози. При застосуванні гідрохлортіазиду у пацієнтів з маніфестним або латентним цукровим діабетом необхідно регулярно контролювати концентрацію глюкози в крові. Може знадобитися корекція дози гіпоглікемічних лікарських засобів. Сечова кислота. У пацієнтів з подагрою може збільшуватись частота виникнення нападів або загострюватися перебіг подагри. Необхідний ретельний контроль за пацієнтами з подагрою та порушенням метаболізму сечової кислоти (гіперурикемією). Ліпіди. При застосуванні гідрохлортіазиду може збільшуватися концентрація холестерину та тригліцеридів плазми. Гостра міопія/вторинна закрита глаукома. Гідрохлортіазид може викликати ідіосинкразічну реакцію, що призводить до розвитку гострої міопії та гострого нападу вторинної глаукоми. Симптоми включають раптове зниження гостроти зору або біль в очах, які проявляються, як правило, протягом декількох годин або тижнів від початку терапії гідрохлортіазидом. За відсутності лікування гостра глаукома може призвести до незворотної втрати зору. При прояві симптомів необхідно якнайшвидше припинити прийом гідрохлортіазиду. Якщо внутрішньоочний тиск залишається неконтрольованим, може знадобитися невідкладне медикаментозне лікування або хірургічне втручання. Факторами ризику гострої глаукоми є: алергічна реакція на сульфонаміди або пеніцилін в анамнезі. Порушення імунної системи. Є повідомлення про те, що тіазидні діуретики (в т.ч. гідрохлортіазид) можуть викликати загострення або прогресування системного червоного вовчаку, а також вовчаковоподібні реакції. У пацієнтів, які отримують тіазидні діуретики, реакції підвищеної чутливості можуть спостерігатися навіть за відсутності вказівок на наявність в анамнезі алергічних реакцій або бронхіальної астми. Фоточутливість. Існує інформація про випадки розвитку реакцій фоточутливості при прийомі тіазидних діуретиків. У разі появи фоточутливості на фоні прийому гідрохлортіазиду слід припинити лікування. Якщо продовження прийому діуретика необхідне, слід захищати шкірні покриви від впливу сонячних променів або штучних ультрафіолетових променів. Алкоголь. У період лікування гідрохлортіазидом не рекомендується вживати алкогольних напоїв, т.к. етанол посилює антигіпертензивну дію тіазидних діуретиків. Спортсмени. Гідрохлортіазид може давати позитивний результат під час проведення допінг-контролю у спортсменів. Інше. У пацієнтів з вираженим атеросклерозом церебральних і коронарних артерій слід особливо обережно застосовувати гідрохлортіазид. Тіазидні діуретики можуть знижувати кількість йоду, пов'язаного з білками плазми, без прояву ознак порушення функції щитовидної залози. Вплив на здатність до керування автотранспортом та управління механізмами. Спеціальні клінічні дослідження з оцінки впливу гідрохлортіазиду на здатність керувати транспортними засобами та працювати з технікою не проводились. Слід пам'ятати можливість прояву сонливості і запаморочення прийому препарату. Тому необхідно бути обережними при виконанні робіт, що вимагають підвищеної уваги і при керуванні транспортними засобами, особливо на початку лікування, при підвищенні дози гідрохлортіазиду.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему