Лекарства и БАД
Склад, форма випуску та упаковкаМазь - 100 г: Активна речовина: індометацин – 10,0 г; Допоміжні речовини: диметилсульфоксид – 10,0 г, макрогол-1500 – 45,0 г, макрогол-400 – 25,0 г, гліцерол – 10,0 г. Мазь для зовнішнього застосування 10%. По 40 г у туби алюмінієві. По 10, 15, 20, 25, 30 або 40 г у банки темного скла типу БТС зі скломаси з кришками, що натягуються. На банку наклеюють етикетку самоклеючу. Кожну тубу або банку разом з інструкцією із застосування поміщають у картонну упаковку (пачку).Опис лікарської формиМазь від світло-жовтого до темно-жовтого із зеленуватим відтінком кольору із запахом диметилсульфоксиду.Фармакотерапевтична групаНестероїдний протизапальний препарат.ФармакокінетикаВсмоктується через шкіру, при багаторазовому застосуванні накопичується в тканинах, м'язах, в суглобах і в синовіальній рідині. При зовнішньому застосуванні клінічно незначна кількість індометацину може потрапляти у системний кровотік, звідки виводиться нирками у вигляді метаболітів та у незначній кількості у незміненому вигляді, а також частково через шлунково-кишковий тракт.ФармакодинамікаВиявляє протизапальну, аналгетичну, протинабрякову дію, пов'язану з неселективним інгібуванням циклооксигенази-1 (ЦОГ1) та циклооксигенази-2 (ЦОГ2), що регулюють синтез протизапальних простагландинів. Усуває біль, зменшує набряк, еритему, ранкову скутість та припухлість суглобів, сприяє збільшенню обсягу рухів.Показання до застосуванняЗапальні та дегенеративні захворювання опорно-рухового апарату: суглобовий синдром при загостренні подагри, ревматоїдний артрит, ювенільний хронічний артрит, анкілозуючий спондиліт (хвороба Бехтерева), остеохондроз з корінцевим синдромом, остеоартроз різної лочок, М'язові болі ревматичного та неревматичного походження, навколосуглобові захворювання: тендиніт, бурсит, тендобурсит, тендовагініт. Посттравматичне запалення м'яких тканин та структур опорно-рухового апарату: пошкодження та розриви зв'язок, забиття.Протипоказання до застосуванняПідвищена чутливість до індометацину, інших нестероїдних протизапальних засобів, або інших компонентів лікарського препарату (в т. ч. димексид). Повне або неповне поєднання бронхіальної астми, рецидивуючого поліпозу носа та приносових пазух та непереносимості ацетилсаліцилової кислоти або інших нестероїдних протизапальних засобів (в т.ч. в анамнезі). Порушення цілісності шкірних покровів у місці передбачуваного нанесення препарату. Вагітність III триместр та період грудного вигодовування. Дитячий вік віком до 6 років. З обережністю Алергічні захворювання та реакції, порушення функції печінки та нирок (у разі нанесення на великі ділянки поверхні шкіри), ерозивно-виразкові ураження шлунково-кишкового тракту, порушення згортання крові (в т. ч. гемофілія, подовження часу кровотечі, схильність до кровотеч), супутнє застосування НПЗЗ, печінкова порфірія (загострення), літній вік, дитячий вік від 6 до 12 років, вагітність І-ІІ триместри.Вагітність та лактаціяПротипоказано застосування у III триместрі вагітності та в період грудного вигодовування.Побічна діяІноді може виникнути свербіж та гіперемія шкіри, печіння, висипання, лущення, сухість шкіри. Рідко розвивається локальний набряк і везикульозний висип, а в окремих випадках - ангіоневротичний набряк і задишка. При застосуванні на великій площі поверхні шкіри можуть наступити системні реакції, переважно шлунково-кишкові порушення (відсутність апетиту, нудота, блювання, діарея, біль у животі, кровотечі та ульцерації). У поодиноких випадках – загострення псоріазу.Взаємодія з лікарськими засобамиМазь може посилювати дію препаратів, що спричиняють фотосенсибілізацію. Клінічно значущої взаємодії з іншими лікарськими засобами за вказаним способом застосування не описано.Спосіб застосування та дозиЗовнішньо. Дорослим та дітям з 12 років мазь втирають легкими рухами, тонким шаром у шкіру над хворобливою зоною по 4-5 см 3-4 рази на день. Дітям з 6 до 12 років застосовують по 2-2,5 см 2-3 десь у день. Інтервал між нанесенням мазі має бути не менше ніж 6 годин. Курс лікування – 7-10 днів. Загальна кількість мазі для дорослих на добу не повинна перевищувати 15 см, що видавлюються з туби, для дітей – 7,5 см. Не рекомендується використовувати оклюзійні пов'язки.ПередозуванняВкрай низька системна абсорбція активних компонентів препарату при зовнішньому застосуванні робить передозування практично неможливим. Явлення передозування (переважно з боку шлунково-кишкового тракту) не виключаються тільки при тривалому застосуванні на великій площі поверхні шкіри. При попаданні препарату всередину, спостерігаються печіння в слизовій оболонці ротової порожнини, слиновиділення, нудота, блювання, в цьому випадку слід проводити промивання ротової порожнини та шлунка, прийом активованого вугілля, при необхідності симптоматичне лікування.Запобіжні заходи та особливі вказівкиПрепарат слід наносити лише на непошкоджені та неінфіковані ділянки шкіри. Не допускати попадання в очі, в ротову порожнину, на слизові оболонки або відкриті рани, тому що в цьому випадку спостерігається локальне роздратування - сльозотеча, почервоніння, печіння, біль до зменшення чи зникнення скарг). З появою висипки лікування необхідно негайно припинити. При тривалому лікуванні (більше 10 днів) рекомендується провести лабораторний контроль вмісту лейкоцитів та тромбоцитів. Вплив на здатність до керування автотранспортом та управління механізмами Немає даних про порушення здатності керувати автомобілем і займатися іншими потенційно небезпечними видами діяльності, що вимагають швидкості психомоторних реакцій та підвищеної концентрації уваги.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаРозчин – 1 фл. (7 мл): Активна речовина: холін альфосцерат – 600 мг; Допоміжні речовини: метилпарагідроксибензоат – 8,0 мг; пропілпарагідроксибензоат – 2,4 мг; натрію сахаринат – 3,0 мг; ароматизатор апельсиновий – 29,0 мг; вода очищена – до 7 мл. По 7 мл розчину у флакони коричневого скла (тип III, Євр.Ф.) закупорені поліетиленовими ковпачками з контролем першого розтину. По 10 флаконів разом з інструкцією із застосування в пачку з картону.Опис лікарської формиПрозорий безбарвний розчин.Фармакотерапевтична групаНоотропний засіб.ФармакокінетикаАбсорбція прийому внутрішньо - 88%; легко проникає через гематоенцефалічний бар'єр, накопичується переважно в мозку (концентрація в мозку досягає 45% рівня в крові), легенів та печінки; 85% екскретується легкими у вигляді діоксиду вуглецю, решта (15%) виводиться нирками та через кишечник. Не впливає на репродуктивний цикл, не має тератогенної та мутагенної дії.ФармакодинамікаПокращує передачу нервових імпульсів у холінергічних нейронах; позитивно впливає на пластичність нейрональних мембран та на функцію рецепторів. Покращує церебральний кровотік, посилює метаболічні процеси у головному мозку, активує структури ретикулярної формації головного мозку та відновлює свідомість при травматичному ураженні головного мозку. Має профілактичну та коригуючу дію на такі патогенетичні фактори інволюційного психоорганічного синдрому, як зміна фосфоліпідного складу мембран нейронів та зниження холінергічної активності. Експериментальні дослідження показали, що Гліатилін стимулює дозозалежне виділення ацетилхоліну у фізіологічних умовах нейротрансмісії. При попаданні в організм розщеплюється під впливом ферментів на холін та гліцерофосфат. Гліатилін, з одного боку, будучи донором холіну, збільшує синтез ацетилхоліну і позитивно впливає на нейротрансмісію, з іншого - гліцерофосфат бере участь у синтезі фосфатидилхоліну (мембранного фосфоліпіду), в результаті і те й інше надає позитивний вплив на мембранну ефун. покращує синаптичну трансмісію. Таким чином, фармакодинамічні дослідження показали, що Гліатилін діє на синаптичну, у т.ч. холінергічну нейротрансмісію; пластичність нейронної мембрани; функцію рецепторів.Показання до застосуваннягострий період ЧМТ з переважно стовбуровим рівнем ураження (порушення свідомості, коматозний стан, осередкова півкульна симптоматика, симптоми ураження стовбура мозку); ішемічний (гострий та відновлювальний період) та геморагічний інсульт (відновлювальний період); дегенеративні та інволюційні психоорганічні синдроми та наслідки цереброваскулярної недостатності, такі як первинні та вторинні порушення мнестичних функцій, що характеризуються порушеннями пам'яті, сплутаністю свідомості, дезорієнтацією, зниженням мотивації, ініціативності, здатності до концентрації уваги; зміни в емоційній та поведінковій сфері: емоційна лабільність, підвищена дратівливість, зниження інтересу, стареча псевдомеланхолія; мультиінфарктна деменція.Протипоказання до застосуванняПідвищена чутливість до компонентів препарату.Вагітність та лактаціяПротипоказано при вагітності та лактації.Побічна діяНудота (як наслідок допамінергічної активації) у цьому випадку слід знизити дозу препарату. Можливі алергічні реакції. Як правило, препарат добре переноситься навіть при тривалому застосуванні.Взаємодія з лікарськими засобамиЛікарська взаємодія не встановлена.Спосіб застосування та дозиДо їжі, запиваючи водою, по 1 флакону 600 мг (7 мл) 2 рази на добу. Тривалість терапії становить 3-6 місяців.ПередозуванняСимптоми: нудота. У разі появи цього симптому рекомендується знизити дозу препарату.Запобіжні заходи та особливі вказівкиВплив на здатність до керування автотранспортом та управління механізмами Слід бути обережними при керуванні транспортними засобами або заняттями іншими видами діяльності, що вимагають підвищеної концентрації уваги та/або швидкості психомоторних реакцій.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаГліцин; холекальциферол; фітоменадіон; піридоксину гідрохлорид; харчові волокна (камедь акації, фруктоолігосахариди); антислежуючий агент: діоксид кремнію аморфний; носій: стеаринова кислота; антислежуючий агент: тальк; ароматизатор натуральний апельсиновий (носія: мальтодекстрин, модифікований крохмаль); антислежуючий агент: стеарат магнію.Характеристика«Глірикум + Вітамін D3» – збалансований комплекс, діючі речовини якого-амінокислота гліцин, а також вітаміни В6, D3 та К1 – сприяють активізації мозкових функцій, зміцненню пам'яті та уваги, підвищенню працездатності головного мозку.Властивості компонентівГліцин: - підтримує нормальну роботу головного мозку; допомагає покращувати концентрацію уваги та пам'ять; впливає зменшення психоемоційного напруги; дозволяє підвищити соціальну адаптацію; полегшує засинання та нормалізує сон; сприяє полегшенню вегетосудинних розладів (у тому числі при клімаксі); має антиоксидантну та антитоксичну дію. Вітамін В6: необхідний засвоєння деяких незамінних для мозку амінокислот; сприяє збереженню пам'яті в зрілому та похилому віці; позитивно впливає на захищеність мозку від алкоголю та нікотину; потрібен підтримки у нормі роботи нервової системи. Вітамін D3: має нейропротекторну дію; перешкоджає дегенерації нейронів; впливає збереження еластичності капілярів мозку; сприяє зміцненню імунітету. Вітамін К1: виявляє антигеморагічний ефект, сприяє попередженню кровотеч головного мозку; бере участь у засвоєнні вітаміну D3; впливає підвищення згортання крові.РекомендуєтьсяРекомендується як біологічно активна добавка до їжі - додаткового джерела вітамінів В6, D3, К1, джерела гліцину.Протипоказання до застосуванняІндивідуальна нестерпність компонентів.Спосіб застосування та дозиДорослим, по 1 таблетці на день під час їжі, слід розсмоктати в роті, не розжовувати. Тривалість прийому – 1 місяць.Запобіжні заходи та особливі вказівкиПеред застосуванням проконсультуйтеся зі спеціалістом.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаНосій: декстрози моногідрат; глюкозаміну гідрохлорид; колаген гідролізований; хондроїтину сульфат натрію; аскорбінова кислота; регулятор кислотності: лимонна кислота (Е330); ароматизатор харчовий натуральний: ананасовий (декстроза, мальтодекстрин, гуміарабік, натуральні ароматичні субстанції, ароматичні речовини); антистежувальний агент: діоксид кремнію аморфний (Е551); гіалуронат натрію; кверцетин; підсолоджувач: стевіозид (Е960); марганцю сульфат. Порошок у саші (стиках) по 10 г. Опис лікарської формиПорошок у саші.
Склад, форма випуску та упаковкаМазь - 1 г: Активна речовина: 100 мг індометацину. Допоміжні речовини: вазелін білий, віск бджолиний, диметилсульфоксид, кремнію діоксид колоїдний, олія лавандова, ланолін безводний. 40 г - туби алюмінієві (1) - картонні пачки.Опис лікарської формиМазь для зовнішнього вживання 10%.Фармакотерапевтична групаНПЗЗ, похідне індолоцтової кислоти. Чинить протизапальну, аналгетичну та жарознижувальну дію. Механізм дії пов'язаний з пригніченням ферменту ЦОГ, що призводить до пригнічення синтезу простагландинів з арахідонової кислоти.ФармакокінетикаПісля прийому внутрішньо індометацин швидко всмоктується із ШКТ. Cmax у плазмі досягається через 2 год. Метаболізується у печінці. Піддається кишково-печінковій рециркуляції. Індометацин визначається у плазмі крові у вигляді незміненої речовини та незв'язаних метаболітів – дезметильного, десбензоїльного, дезметил-дезбензоїльного. T1/2 становить близько 4.5 год. Виводиться із сечею - 60% як незміненої речовини і метаболітів, і з калом - 33% переважно як метаболітів.ФармакодинамікаПригнічує агрегацію тромбоцитів. При введенні всередину і парентерально сприяє ослабленню больового синдрому, особливо болів у суглобах у спокої та при русі, зменшенню ранкової скутості та припухлості суглобів, збільшенню обсягу рухів. Протизапальний ефект розвивається до кінця першого тижня лікування. При місцевому застосуванні усуває біль, зменшує набряк та еритему. При зовнішньому застосуванні, крім того, сприяє зменшенню ранкової скутості, збільшення обсягу рухів.Показання до застосуванняДля системного застосування: суглобовий синдром (в т.ч. ревматоїдний артрит, остеоартрит, анкілозуючий спондиліт, подагра), болі в хребті, невралгії, міалгії, травматичне запалення м'яких тканин та суглобів, ревматизм, дифузні хвороби сполучної тканини. Як допоміжний засіб при інфекційно-запальних захворюваннях ЛОР-органів, аднекситі, простатиті, циститі. Для місцевого застосування: профілактика запального процесу при хірургічних втручаннях з приводу катаракти та на передньому сегменті ока, інгібування міозу під час операції. Для зовнішнього застосування: суглобовий синдром (в т.ч. ревматоїдний артрит, остеоартрит, анкілозуючий спондиліт, подагра), біль у хребті, невралгії, міалгії, травматичне запалення м'яких тканин та суглобів.Протипоказання до застосуванняПідвищена чутливість до індометацину, ерозивно-виразкові ураження шлунково-кишкового тракту у фазі загострення, "аспіринова тріада", порушення кровотворення, виражені порушення функції печінки та/або нирок, тяжкі форми хронічної серцевої недостатності, артеріальної гіпертензії, панкреатиту, III триместр вагітності, дитячий вік років; для ректального застосування: проктит, недавня кровотеча із прямої кишки.Вагітність та лактаціяІндометацин протипоказаний у III триместрі вагітності. У I та II триместрах вагітності, а також у період лактації (грудного вигодовування) застосування не рекомендується. Індометацин у невеликих кількостях виділяється із грудним молоком. Застосування у дітей Протипоказаний дітям віком до 14 років.Побічна діяЗ боку травної системи: нудота, анорексія, блювання, біль та неприємні відчуття в животі, запор або діарея, ерозивно-виразкові ураження, кровотечі та перфорації ШКТ; рідко – стриктури кишечника, стоматит, гастрит, метеоризм, кровотеча із сигмовидної кишки або з дивертикулу, жовтяниця, гепатит. З боку ЦНС та периферичної нервової системи: запаморочення, головний біль, депресія, відчуття втоми; рідко – тривога, непритомність, сонливість, судоми, периферична невропатія, м'язова слабкість, мимовільні м'язові рухи, порушення сну, психічні розлади (деперсоналізація, психотичні епізоди), парестезії, дизартрія, паркінсонізм. З боку серцево-судинної системи: набряки, підвищення артеріального тиску, тахікардія, біль у грудній клітці, аритмія, пальпітація, артеріальна гіпотензія, застійна серцева недостатність, гематурія. Алергічні реакції: рідко - свербіж, кропив'янка, ангіїт, вузлувата еритема, шкірні висипання, ексфоліативний дерматит, синдром Стівенса-Джонсона, багатоформна еритема, токсичний епідермальний некроліз, випадання волосся, гострий респіраторний дистрес, різке падіння, різке падіння , бронхіальна астма, набряк легенів З боку системи кровотворення: рідко – лейкопенія, петехії або екхімози, пурпура, апластична та гемолітична анемія, тромбоцитопенія, синдром ДВЗ. З боку органів чуття: рідко – порушення чіткості зорового сприйняття, диплопія, орбітальний та періорбітальний біль, тиніт, порушення слуху, глухота. З боку сечовидільної системи: рідко – протеїнурія, нефротичний синдром, інтерстиціальний нефрит, порушення ниркової недостатності. З боку обміну речовин: рідко – гіперглікемія, глюкозурія, гіперкаліємія. Інші: рідко – вагінальна кровотеча, припливи, підвищене потовиділення, носова кровотеча, збільшення та напруженість молочних залоз, гінекомастія. Місцеві реакції: у місці внутрішньом'язового введення в окремих випадках - утворення інфільтрату, абсцесу; при ректальному застосуванні можливе подразнення слизової оболонки прямої кишки, тенезми, загострення хронічного коліту. При зовнішньому застосуванні: свербіж, почервоніння, висипи в місці аплікації.Взаємодія з лікарськими засобамиПри одночасному застосуванні індометацин може зменшувати ефекти салуретиків, бета-адреноблокаторів; посилювати ефекти непрямих антикоагулянтів. При одночасному застосуванні індометацину та дифлунізалу існує небезпека виникнення сильної кровотечі із ШКТ. При одночасному застосуванні з пробенецидом можливе підвищення концентрації індометацину у плазмі крові. Індометацин може зменшувати канальцеву секрецію метотрексату, що призводить до підвищення його токсичності. При одночасному застосуванні з НПЗЗ підвищується токсичність циклоспорину. Індометацин у дозі по 50 мг 3 рази на добу підвищує концентрацію літію в плазмі крові та зменшує кліренс літію з організму у пацієнтів із психічними захворюваннями. При одночасному застосуванні індометацину з дигоксином можливе підвищення концентрації дигоксину в плазмі та збільшення Т1/2 дигоксину.Спосіб застосування та дозиВстановлюють індивідуально з урахуванням тяжкості перебігу захворювання. Для дорослих прийому внутрішньо початкова доза - по 25 мг 2-3 рази/сут. При недостатній вираженості клінічного ефекту збільшують дозу до 50 мг 3 рази на добу. Лікарські форми пролонгованої дії застосовують 1-2 рази на добу. Максимальна доза: 200 мг. При досягненні ефекту лікування продовжують протягом 4 тижнів у тій самій або зменшеній дозі. При тривалому застосуванні добова доза не повинна перевищувати 75 мг. Приймають після їди. Для лікування гострих станів або усунення загострення хронічного процесу вводять внутрішньом'язово по 60 мг 1-2 рази на добу. Тривалість внутрішньом'язового введення - 7-14 днів. Потім індометацин застосовують внутрішньо або ректально по 50-100 мг 2 рази на добу, при цьому максимальна добова доза не повинна перевищувати 200 мг. Для підтримуючого лікування застосовують ректально по 50-100 мг 1 раз на добу на ніч. Для місцевого застосування в офтальмології доза частоти та тривалості застосування визначаються індивідуально. Зовнішньо застосовують 2 рази на добу.Запобіжні заходи та особливі вказівкиЗ обережністю застосовують у пацієнтів похилого віку, а також при захворюваннях печінки, нирок, шлунково-кишкового тракту в анамнезі, при диспептичних симптомах у момент застосування, артеріальної гіпертензії, серцевої недостатності, одразу після серйозних хірургічних втручань, при паркінсонізмі, епілепсії. При вказівках в анамнезі на алергічні реакції до НПЗЗ застосовують лише у невідкладних випадках. У період лікування необхідний систематичний контроль за функцією печінки та нирок, картиною периферичної крові. Не рекомендується одночасне застосування з ацетилсаліцилової кислотою та іншими НПЗЗ. Не слід застосовувати індометацин одночасно з дифлунізалом. При одночасному застосуванні індометацину з препаратами літію слід на увазі можливість появи симптомів токсичної дії літію. При місцевому застосуванні не слід наносити на ранову поверхню шкіри, а також уникати попадання в очі або слизові оболонки. Вплив на здатність до керування автотранспортом та управління механізмами У період лікування слід утримуватися від потенційно небезпечних видів діяльності, пов'язаних із необхідністю концентрації уваги та підвищеної швидкості психомоторних реакцій.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
191,00 грн
152,00 грн
Склад, форма випуску та упаковкаПігулки - 1 таб. Активна речовина: 25 мг індометацину. Допоміжні речовини: лактоза, крохмаль пшеничний, желатин, тальк, магнію стеарат, целюлоза мікрокристалічна, еудражит (L-12.5% і S-12.5%), титану діоксид, макрогол 6000, макрогол 400, лак сіток2 , ізопропанол, вода очищена. 30 шт. - блістери (1) - пачки картонні.Опис лікарської формиТаблетки, покриті кишковорозчинною оболонкою світло-коричневого кольору, круглі, двоопуклі.Фармакотерапевтична групаНПЗЗ, похідне індолоцтової кислоти. Чинить протизапальну, аналгетичну та жарознижувальну дію. Механізм дії пов'язаний з пригніченням ферменту ЦОГ, що призводить до пригнічення синтезу простагландинів з арахідонової кислоти.ФармакокінетикаПісля прийому внутрішньо індометацин швидко всмоктується із ШКТ. Cmax у плазмі досягається через 2 год. Метаболізується у печінці. Піддається кишково-печінковій рециркуляції. Індометацин визначається у плазмі крові у вигляді незміненої речовини та незв'язаних метаболітів – дезметильного, десбензоїльного, дезметил-дезбензоїльного. T1/2 становить близько 4.5 год. Виводиться із сечею - 60% як незміненої речовини і метаболітів, і з калом - 33% переважно як метаболітів.ФармакодинамікаПригнічує агрегацію тромбоцитів. При введенні всередину і парентерально сприяє ослабленню больового синдрому, особливо болів у суглобах у спокої та при русі, зменшенню ранкової скутості та припухлості суглобів, збільшенню обсягу рухів. Протизапальний ефект розвивається до кінця першого тижня лікування. При місцевому застосуванні усуває біль, зменшує набряк та еритему. При зовнішньому застосуванні, крім того, сприяє зменшенню ранкової скутості, збільшення обсягу рухів.Показання до застосуванняДля системного застосування: суглобовий синдром (в т.ч. ревматоїдний артрит, остеоартрит, анкілозуючий спондиліт, подагра), болі в хребті, невралгії, міалгії, травматичне запалення м'яких тканин та суглобів, ревматизм, дифузні хвороби сполучної тканини. Як допоміжний засіб при інфекційно-запальних захворюваннях ЛОР-органів, аднекситі, простатиті, циститі. Для місцевого застосування: профілактика запального процесу при хірургічних втручаннях з приводу катаракти та на передньому сегменті ока, інгібування міозу під час операції. Для зовнішнього застосування: суглобовий синдром (в т.ч. ревматоїдний артрит, остеоартрит, анкілозуючий спондиліт, подагра), біль у хребті, невралгії, міалгії, травматичне запалення м'яких тканин та суглобів.Протипоказання до застосуванняПідвищена чутливість до індометацину, ерозивно-виразкові ураження шлунково-кишкового тракту у фазі загострення, "аспіринова тріада", порушення кровотворення, виражені порушення функції печінки та/або нирок, тяжкі форми хронічної серцевої недостатності, артеріальної гіпертензії, панкреатиту, III триместр вагітності, дитячий вік років; для ректального застосування: проктит, недавня кровотеча із прямої кишки.Вагітність та лактаціяІндометацин протипоказаний у III триместрі вагітності. У I та II триместрах вагітності, а також у період лактації (грудного вигодовування) застосування не рекомендується. Індометацин у невеликих кількостях виділяється із грудним молоком. Застосування у дітей Протипоказаний дітям віком до 14 років.Побічна діяЗ боку травної системи: нудота, анорексія, блювання, біль та неприємні відчуття в животі, запор або діарея, ерозивно-виразкові ураження, кровотечі та перфорації ШКТ; рідко – стриктури кишечника, стоматит, гастрит, метеоризм, кровотеча із сигмовидної кишки або з дивертикулу, жовтяниця, гепатит. З боку ЦНС та периферичної нервової системи: запаморочення, головний біль, депресія, відчуття втоми; рідко – тривога, непритомність, сонливість, судоми, периферична невропатія, м'язова слабкість, мимовільні м'язові рухи, порушення сну, психічні розлади (деперсоналізація, психотичні епізоди), парестезії, дизартрія, паркінсонізм. З боку серцево-судинної системи: набряки, підвищення артеріального тиску, тахікардія, біль у грудній клітці, аритмія, пальпітація, артеріальна гіпотензія, застійна серцева недостатність, гематурія. Алергічні реакції: рідко - свербіж, кропив'янка, ангіїт, вузлувата еритема, шкірні висипання, ексфоліативний дерматит, синдром Стівенса-Джонсона, багатоформна еритема, токсичний епідермальний некроліз, випадання волосся, гострий респіраторний дистрес, різке падіння, різке падіння , бронхіальна астма, набряк легенів З боку системи кровотворення: рідко – лейкопенія, петехії або екхімози, пурпура, апластична та гемолітична анемія, тромбоцитопенія, синдром ДВЗ. З боку органів чуття: рідко – порушення чіткості зорового сприйняття, диплопія, орбітальний та періорбітальний біль, тиніт, порушення слуху, глухота. З боку сечовидільної системи: рідко – протеїнурія, нефротичний синдром, інтерстиціальний нефрит, порушення ниркової недостатності. З боку обміну речовин: рідко – гіперглікемія, глюкозурія, гіперкаліємія. Інші: рідко – вагінальна кровотеча, припливи, підвищене потовиділення, носова кровотеча, збільшення та напруженість молочних залоз, гінекомастія. Місцеві реакції: у місці внутрішньом'язового введення в окремих випадках - утворення інфільтрату, абсцесу; при ректальному застосуванні можливе подразнення слизової оболонки прямої кишки, тенезми, загострення хронічного коліту. При зовнішньому застосуванні: свербіж, почервоніння, висипи в місці аплікації.Взаємодія з лікарськими засобамиПри одночасному застосуванні індометацин може зменшувати ефекти салуретиків, бета-адреноблокаторів; посилювати ефекти непрямих антикоагулянтів. При одночасному застосуванні індометацину та дифлунізалу існує небезпека виникнення сильної кровотечі із ШКТ. При одночасному застосуванні з пробенецидом можливе підвищення концентрації індометацину у плазмі крові. Індометацин може зменшувати канальцеву секрецію метотрексату, що призводить до підвищення його токсичності. При одночасному застосуванні з НПЗЗ підвищується токсичність циклоспорину. Індометацин у дозі по 50 мг 3 рази на добу підвищує концентрацію літію в плазмі крові та зменшує кліренс літію з організму у пацієнтів із психічними захворюваннями. При одночасному застосуванні індометацину з дигоксином можливе підвищення концентрації дигоксину в плазмі та збільшення Т1/2 дигоксину.Спосіб застосування та дозиВстановлюють індивідуально з урахуванням тяжкості перебігу захворювання. Для дорослих прийому внутрішньо початкова доза - по 25 мг 2-3 рази/сут. При недостатній вираженості клінічного ефекту збільшують дозу до 50 мг 3 рази на добу. Лікарські форми пролонгованої дії застосовують 1-2 рази на добу. Максимальна доза: 200 мг. При досягненні ефекту лікування продовжують протягом 4 тижнів у тій самій або зменшеній дозі. При тривалому застосуванні добова доза не повинна перевищувати 75 мг. Приймають після їди. Для лікування гострих станів або усунення загострення хронічного процесу вводять внутрішньом'язово по 60 мг 1-2 рази на добу. Тривалість внутрішньом'язового введення - 7-14 днів. Потім індометацин застосовують внутрішньо або ректально по 50-100 мг 2 рази на добу, при цьому максимальна добова доза не повинна перевищувати 200 мг. Для підтримуючого лікування застосовують ректально по 50-100 мг 1 раз на добу на ніч. Для місцевого застосування в офтальмології доза частоти та тривалості застосування визначаються індивідуально. Зовнішньо застосовують 2 рази на добу.Запобіжні заходи та особливі вказівкиЗ обережністю застосовують у пацієнтів похилого віку, а також при захворюваннях печінки, нирок, шлунково-кишкового тракту в анамнезі, при диспептичних симптомах у момент застосування, артеріальної гіпертензії, серцевої недостатності, одразу після серйозних хірургічних втручань, при паркінсонізмі, епілепсії. При вказівках в анамнезі на алергічні реакції до НПЗЗ застосовують лише у невідкладних випадках. У період лікування необхідний систематичний контроль за функцією печінки та нирок, картиною периферичної крові. Не рекомендується одночасне застосування з ацетилсаліцилової кислотою та іншими НПЗЗ. Не слід застосовувати індометацин одночасно з дифлунізалом. При одночасному застосуванні індометацину з препаратами літію слід на увазі можливість появи симптомів токсичної дії літію. При місцевому застосуванні не слід наносити на ранову поверхню шкіри, а також уникати попадання в очі або слизові оболонки. Вплив на здатність до керування автотранспортом та управління механізмами У період лікування слід утримуватися від потенційно небезпечних видів діяльності, пов'язаних із необхідністю концентрації уваги та підвищеної швидкості психомоторних реакцій.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
185,00 грн
152,00 грн
Склад, форма випуску та упаковкаПігулки - 1 таб. Активна речовина індометацин 25 мг. Допоміжні речовини: лактоза, крохмаль пшеничний, желатин, тальк, магнію стеарат, целюлоза мікрокристалічна, еудражит (L-12.5% і S-12.5%), титану діоксид, макрогол 6000, макрогол 400, лак сіток2 , ізопропанол, вода очищена. 30 шт. - блістери (1) - пачки картонні.Опис лікарської формиТаблетки, покриті кишковорозчинною оболонкою світло-коричневого кольору, круглі, двоопуклі.Фармакотерапевтична групаНПЗЗ, похідне індолоцтової кислоти. Чинить протизапальну, аналгетичну та жарознижувальну дію. Механізм дії пов'язаний з пригніченням ферменту ЦОГ, що призводить до пригнічення синтезу простагландинів з арахідонової кислоти.ФармакокінетикаПісля прийому внутрішньо індометацин швидко всмоктується із ШКТ. Cmax у плазмі досягається через 2 год. Метаболізується у печінці. Піддається кишково-печінковій рециркуляції. Індометацин визначається у плазмі крові у вигляді незміненої речовини та незв'язаних метаболітів – дезметильного, десбензоїльного, дезметил-дезбензоїльного. T1/2 становить близько 4.5 год. Виводиться із сечею - 60% як незміненої речовини і метаболітів, і з калом - 33% переважно як метаболітів.ФармакодинамікаПригнічує агрегацію тромбоцитів. При введенні всередину і парентерально сприяє ослабленню больового синдрому, особливо болів у суглобах у спокої та при русі, зменшенню ранкової скутості та припухлості суглобів, збільшенню обсягу рухів. Протизапальний ефект розвивається до кінця першого тижня лікування. При місцевому застосуванні усуває біль, зменшує набряк та еритему. При зовнішньому застосуванні, крім того, сприяє зменшенню ранкової скутості, збільшення обсягу рухів.Показання до застосуванняДля системного застосування: суглобовий синдром (в т.ч. ревматоїдний артрит, остеоартрит, анкілозуючий спондиліт, подагра), болі в хребті, невралгії, міалгії, травматичне запалення м'яких тканин та суглобів, ревматизм, дифузні хвороби сполучної тканини. Як допоміжний засіб при інфекційно-запальних захворюваннях ЛОР-органів, аднекситі, простатиті, циститі. Для місцевого застосування: профілактика запального процесу при хірургічних втручаннях з приводу катаракти та на передньому сегменті ока, інгібування міозу під час операції. Для зовнішнього застосування: суглобовий синдром (в т.ч. ревматоїдний артрит, остеоартрит, анкілозуючий спондиліт, подагра), біль у хребті, невралгії, міалгії, травматичне запалення м'яких тканин та суглобів.Протипоказання до застосуванняПідвищена чутливість до індометацину, ерозивно-виразкові ураження шлунково-кишкового тракту у фазі загострення, "аспіринова тріада", порушення кровотворення, виражені порушення функції печінки та/або нирок, тяжкі форми хронічної серцевої недостатності, артеріальної гіпертензії, панкреатиту, III триместр вагітності, дитячий вік років; для ректального застосування: проктит, недавня кровотеча із прямої кишки.Вагітність та лактаціяІндометацин протипоказаний у III триместрі вагітності. У I та II триместрах вагітності, а також у період лактації (грудного вигодовування) застосування не рекомендується. Індометацин у невеликих кількостях виділяється із грудним молоком. Застосування у дітей Протипоказаний дітям віком до 14 років.Побічна діяЗ боку травної системи: нудота, анорексія, блювання, біль та неприємні відчуття в животі, запор або діарея, ерозивно-виразкові ураження, кровотечі та перфорації ШКТ; рідко – стриктури кишечника, стоматит, гастрит, метеоризм, кровотеча із сигмовидної кишки або з дивертикулу, жовтяниця, гепатит. З боку ЦНС та периферичної нервової системи: запаморочення, головний біль, депресія, відчуття втоми; рідко – тривога, непритомність, сонливість, судоми, периферична невропатія, м'язова слабкість, мимовільні м'язові рухи, порушення сну, психічні розлади (деперсоналізація, психотичні епізоди), парестезії, дизартрія, паркінсонізм. З боку серцево-судинної системи: набряки, підвищення артеріального тиску, тахікардія, біль у грудній клітці, аритмія, пальпітація, артеріальна гіпотензія, застійна серцева недостатність, гематурія. Алергічні реакції: рідко - свербіж, кропив'янка, ангіїт, вузлувата еритема, шкірні висипання, ексфоліативний дерматит, синдром Стівенса-Джонсона, багатоформна еритема, токсичний епідермальний некроліз, випадання волосся, гострий респіраторний дистрес, різке падіння, різке падіння , бронхіальна астма, набряк легенів З боку системи кровотворення: рідко – лейкопенія, петехії або екхімози, пурпура, апластична та гемолітична анемія, тромбоцитопенія, синдром ДВЗ. З боку органів чуття: рідко – порушення чіткості зорового сприйняття, диплопія, орбітальний та періорбітальний біль, тиніт, порушення слуху, глухота. З боку сечовидільної системи: рідко – протеїнурія, нефротичний синдром, інтерстиціальний нефрит, порушення ниркової недостатності. З боку обміну речовин: рідко – гіперглікемія, глюкозурія, гіперкаліємія. Інші: рідко – вагінальна кровотеча, припливи, підвищене потовиділення, носова кровотеча, збільшення та напруженість молочних залоз, гінекомастія. Місцеві реакції: у місці внутрішньом'язового введення в окремих випадках - утворення інфільтрату, абсцесу; при ректальному застосуванні можливе подразнення слизової оболонки прямої кишки, тенезми, загострення хронічного коліту. При зовнішньому застосуванні: свербіж, почервоніння, висипи в місці аплікації.Взаємодія з лікарськими засобамиПри одночасному застосуванні індометацин може зменшувати ефекти салуретиків, бета-адреноблокаторів; посилювати ефекти непрямих антикоагулянтів. При одночасному застосуванні індометацину та дифлунізалу існує небезпека виникнення сильної кровотечі із ШКТ. При одночасному застосуванні з пробенецидом можливе підвищення концентрації індометацину у плазмі крові. Індометацин може зменшувати канальцеву секрецію метотрексату, що призводить до підвищення його токсичності. При одночасному застосуванні з НПЗЗ підвищується токсичність циклоспорину. Індометацин у дозі по 50 мг 3 рази на добу підвищує концентрацію літію в плазмі крові та зменшує кліренс літію з організму у пацієнтів із психічними захворюваннями. При одночасному застосуванні індометацину з дигоксином можливе підвищення концентрації дигоксину в плазмі та збільшення Т1/2 дигоксину.Спосіб застосування та дозиВстановлюють індивідуально з урахуванням тяжкості перебігу захворювання. Для дорослих прийому внутрішньо початкова доза - по 25 мг 2-3 рази/сут. При недостатній вираженості клінічного ефекту збільшують дозу до 50 мг 3 рази на добу. Лікарські форми пролонгованої дії застосовують 1-2 рази на добу. Максимальна доза: 200 мг. При досягненні ефекту лікування продовжують протягом 4 тижнів у тій самій або зменшеній дозі. При тривалому застосуванні добова доза не повинна перевищувати 75 мг. Приймають після їди. Для лікування гострих станів або усунення загострення хронічного процесу вводять внутрішньом'язово по 60 мг 1-2 рази на добу. Тривалість внутрішньом'язового введення - 7-14 днів. Потім індометацин застосовують внутрішньо або ректально по 50-100 мг 2 рази на добу, при цьому максимальна добова доза не повинна перевищувати 200 мг. Для підтримуючого лікування застосовують ректально по 50-100 мг 1 раз на добу на ніч. Для місцевого застосування в офтальмології доза частоти та тривалості застосування визначаються індивідуально. Зовнішньо застосовують 2 рази на добу.Запобіжні заходи та особливі вказівкиЗ обережністю застосовують у пацієнтів похилого віку, а також при захворюваннях печінки, нирок, шлунково-кишкового тракту в анамнезі, при диспептичних симптомах у момент застосування, артеріальної гіпертензії, серцевої недостатності, одразу після серйозних хірургічних втручань, при паркінсонізмі, епілепсії. При вказівках в анамнезі на алергічні реакції до НПЗЗ застосовують лише у невідкладних випадках. У період лікування необхідний систематичний контроль за функцією печінки та нирок, картиною периферичної крові. Не рекомендується одночасне застосування з ацетилсаліцилової кислотою та іншими НПЗЗ. Не слід застосовувати індометацин одночасно з дифлунізалом. При одночасному застосуванні індометацину з препаратами літію слід на увазі можливість появи симптомів токсичної дії літію. При місцевому застосуванні не слід наносити на ранову поверхню шкіри, а також уникати попадання в очі або слизові оболонки. Вплив на здатність до керування автотранспортом та управління механізмами У період лікування слід утримуватися від потенційно небезпечних видів діяльності, пов'язаних із необхідністю концентрації уваги та підвищеної швидкості психомоторних реакцій.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
311,00 грн
262,00 грн
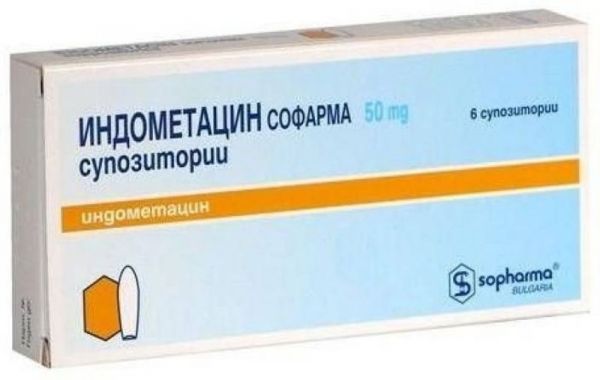
Склад, форма випуску та упаковкаСупозиторії – 1 супп.: Діюча речовина: індометацин – 50,0 мг; допоміжні речовини: крохмаль кукурудзяний, жир твердий Супозиторії ректальні, 50 мг. По 5 супозиторіїв у контурній комірковій упаковці (блістер) із білої ПВХ/ПЕ плівки. По 2 блістери з інструкцією щодо застосування препарату у картонній пачці.Інформація від виробникаТермін придатності до 3 років. Не застосовувати після закінчення терміну придатності, вказаного на упаковці.Опис лікарської формиЖовтуватого кольору супозиторії торпедоподібної форми з заглибленням у підставі.ФармакокінетикаАбсорбція – швидка. Біодоступність при ректальному шляху введення – 80-90%. Зв'язок з білками плазми – 90 %, період напіввиведення – 4,5 год. Не видаляється при діалізі. Проникає у грудне молоко.ФармакодинамікаІндометацин має протизапальну, аналгетичну, жарознижувальну та антиагрегантну дію. Пригнічує активність протизапальних факторів, знижує агрегацію тромбоцитів. Пригнічуючи циклооксигеназу I та II, порушує метаболізм арахідонової кислоти, зменшує кількість простагландинів як в осередку запалення, так і у здорових тканинах, пригнічує ексудативну та проліферативну фази запалення. Усуває або зменшує больовий синдром ревматичного та неревматичного характеру (у т. ч. при болях у суглобах у спокої та при русі), зменшує ранкову скутість та припухлість суглобів, сприяє збільшенню обсягу рухів; при запальних процесах, що виникають після операцій та травм, швидко полегшує як спонтанний біль, так і біль під час руху, зменшує запальний набряк на місці рани).Показання до застосуванняГострі та хронічні болі при запальних та дегенеративних захворюваннях опорно-рухового апарату: ревматоїдний артрит, ювенільний хронічний артрит, анкілозуючий хронічний спондиліт (хвороба Бехтерева), подагричний артрит. псоріатичний артрит, хвороба Рейтера; ревматичні ураження м'яких тканин: тендиніти, бурсити, тендобурсити, тендовагініти; дископатії, неврити, плексити, радикулоневрити; дисменорея. Препарат призначений для симптоматичної терапії, зменшення болю та запалення на момент застосування, на прогресування захворювання не впливає.Протипоказання до застосуваннягіперчутливість до індометацину або будь-якої з допоміжних речовин препарату; повне або неповне поєднання бронхіальної астми, рецидивуючого поліпозу носа та приносових пазух та непереносимості ацетилсаліцилової кислоти або інших нестероїдних протизапальних препаратів (в т. ч. в анамнезі), кропив'янки або риніту; виразкова хвороба шлунка та 12-палої кишки, запальні захворювання кишечника (виразковий коліт, хвороба Крона), кровотечі (в т. ч. внутрішньочерепна, з органів шлунково-кишкового тракту); вроджені вади серця (важка коарктація аорти, атрезія легеневої артерії, важкий зошит Фалло); період після аортокоронарного шунтування; тяжка серцева недостатність; ниркова недостатність (кліренс креатиніну менше 30 мл/хв); печінкова недостатність, активне захворювання печінки, порушення згортання крові (у т. ч. гемофілія, збільшення часу кровотечі, схильність до кровотеч); порушення кровотворення (лейкопенія та анемія); підтверджена гіперкаліємія; вагітність, період грудного вигодовування; дитячий вік (до 15 років). З обережністю Ішемічна хвороба серця, цереброваскулярні захворювання, хронічна серцева недостатність, дисліпідемія, гіперліпідемія, цукровий діабет, тромбоцитопенія, захворювання периферичних артерій, артеріальна гіпертензія, куріння, хронічна ниркова недостатність (кліренс креатиніну 30-60 мл/хв) , виразкове ураження ШКТ в анамнезі, наявність інфекції Helicobacter pylori, тривале застосування нестероїдних протизапальних засобів, часте вживання алкоголю, тяжкі соматичні захворювання; супутня терапія наступними препаратами: антикоагулянти (в т. ч. варфарин), антиагреганти (в т. ч. ацетилсаліцилова кислота, клопідогрел), глюкокортикостероїди для внутрішнього застосування (в т. ч. преднізолон), селективні інгібі. ч. циталопрам, флуоксетин, пароксетин, сертралін);психічні розлади, епілепсія, паркінсонізм, депресія, літній вік.Вагітність та лактаціяВагітність Індометацин протипоказаний під час вагітності. Грудне годування Індометацин проникає у грудне молоко. За необхідності лікування препаратів грудне вигодовування слід припинити.Побічна діяМожливі побічні ефекти при застосуванні препарату Індометацин 100 Берлін-Хемі наведені відповідно до частоти виникнення: дуже часто (≥ 1/10), часто ≥ 1700, < 1/0), нечасто (≥ 1/1000, < 1/100), рідко (≥ 1/10000, < 1/1000), дуже рідко (< 1/10000), частота невідома (за наявними даними частота не може бути встановлена). Необхідно зазначити, що перелічені побічні дії препарату переважно варіюють залежно від дози та індивідуальних особливостей пацієнтів. Порушення з боку шлунково-кишкового тракту Дуже часто: нудота, блювання, діарея. Часто: крововиливи та виразки шлунково-кишкового тракту; НПЗП-гастропатія, біль у животі, печія, зниження апетиту, виразковий стоматит. Нечасто: кривава блювота, мелена. Дуже рідко: запори. При тривалому застосуванні в більших дозах - виразка слизової оболонки шлунково-кишкового тракту. Порушення з боку печінки та жовчовивідних шляхів Часто: підвищення активності «печінкових» трансаміназ (АЛТ, АСТ), минуще підвищення концентрації білірубіну в плазмі крові. Рідко: токсичний гепатит, із жовтяницею або без неї. Дуже рідко: фульмінантний гепатит. Порушення з боку нервової системи Дуже часто: головний біль. Часто: запаморочення, сонливість, надмірна стомлюваність, дратівливість, депресія. Нечасто: периферична нейропатія, збудження, безсоння. Порушення з боку органу зору Нечасто: диплопія, помутніння рогівки, нечіткість зорового сприйняття, кон'юктивіт. Порушення з боку органу слуху Часто: шум у вухах. Дуже рідко: тимчасове порушення слуху. Порушення з боку серця Дуже рідко: тахіаритмія, набряковий синдром, розвиток (погіршення) хронічної серцевої недостатності. Порушення з боку судин Дуже рідко: підвищення артеріального тиску. Порушення з боку нирок та сечовивідних шляхів Дуже рідко: порушення функції нирок, нефротичний синдром, протеїнурія, гематурія, інтерстиціальний нефрит, некроз сосочків. Порушення з боку крові та лімфатичної системи Дуже рідко: кровотеча (шлунково-кишкова, ясенна, маткова, гемороїдальна), лейкопенія, тромбоцитопенія, агранулоцитоз, анемія (у тому числі гемолітична та апластична), еозинофілія, тромбоцитопенічна пурпура. Порушення з боку імунної системи Часто: свербіж шкіри, висипання на шкірі. Рідко: кропив'янка, бронхоспазм, астматичні напади. Дуже рідко: бульозні висипання, почервоніння шкіри, екзема, ексфоліативний дерматит, пурпура алергічного типу, синдром Стівенса-Джонсона; у поодиноких випадках – фотосенсибілізація, токсичний епідермальний некроліз (синдром Лайєлла), вузлувата еритема, анафілактичний шок. Лабораторні показники Дуже рідко: агранулоцитоз, лейкопенія, тромбоцитопенія, гіперглікемія, глюкозурія, гіперкаліємія. Загальні розлади та порушення у місці введення Частота невідома: подразнення, тяжкість в аноректальній ділянці, загострення геморою. Інші Частота невідома: асептичний менінгіт (частіше у пацієнтів з аутоімунними захворюваннями), посилене потовиділення, апластична анемія, аутоімунна гемолітична анемія.Взаємодія з лікарськими засобамиІндометанін підвищує концентрацію в плазмі крові дигоксину, метотрексату та препаратів літію, що може призвести до посилення їхньої токсичності. Одночасне застосування з парацетамолом збільшує ризик розвитку нефротоксичних ефектів. Етанол, колхіцин, глюкокортикостероїди та кортикотропін підвищують ризик розвитку кровотеч у ШКТ. Підсилює гіпоглікемічну дію інсуліну та гіпоглікемічних засобів для прийому внутрішньо; посилює дію непрямих антикоагулянтів, антиагрегантів, тромболітиків (алтеплази, стрептокінази та урокінази) – виникає ризик розвитку кровотеч. Знижує ефект діуретиків, на фоні застосування калійзберігаючих діуретиків зростає ризик гіперкаліємії: знижує ефективність урикозуричних та гіпотензивних лікарських засобів (в т.ч. бета-адреноблокаторів); посилює побічні ефекти метотрексату, ацетилсаліцилової кислоти, глюкокортикостероїдів, інших нестероїдних протизапальних засобів. Циклоспорин та препарати золота підвищують нефротоксичність (очевидно, за рахунок придушення синтезу простагландинів у нирках). Цефамандол, цефаперазон, цефотетан, вальпроєва кислота,Плікаміцин підвищують частоту розвитку гіпопротромбінемій та небезпеку кровотеч. Антациди та колестірамін знижують абсорбцію індометацину. Підсилює токсичність зидовудину (за рахунок інгібування метаболізму); у новонароджених підвищує ризик розвитку токсичних ефектів аміноглікозидів (тк. знижує нирковий кліренс та підвищує концентрацію у крові). Мієлотоксичні лікарські засоби посилюють прояви гематотоксичності індометацину.Спосіб застосування та дозиРектально. Дорослі та діти старше 15 років: по 100 мг (1 супозиторій) один раз на добу. Максимальна добова доза – 200 мг. Доза вище 150-200 мг збільшує ризик побічних дій. Тривалість лікування: не більше ніж 7 днів. Побічні дії можна зменшити, використовуючи мінімальну ефективну дозу в якомога коротший період часу застосування.ПередозуванняСимптоми: нудота, блювання, сильний біль голови, запаморочення, порушення пам'яті, дезорієнтація. У важких випадках парестезії, оніміння кінцівок, судоми. Лікування: швидке виведення препарату з організму, симптоматична терапія. Гемодіаліз неефективний.Запобіжні заходи та особливі вказівкиПід час лікування необхідний контроль картини периферичної крові та функціонального стану печінки та нирок. При необхідності визначення 17-кетостероїдів препарат слід відмінити за 48 годин до дослідження. Для попередження та зменшення диспептичних явищ слід застосовувати антацидні лікарські засоби. Не слід застосовувати препарат одночасно з іншими нестероїдними протизапальними засобами. Препарат може змінювати властивості тромбоцитів, проте не замінює профілактичної дії ацетилсаліцилової кислоти при серцево-судинних захворюваннях. Застосування препарату може негативно впливати на жіночу фертильність та не рекомендується жінкам, які планують вагітність. Умови зберігання За температури не вище 25°С. Зберігати у недоступному для дітей місці! Вплив на здатність до керування транспортними засобами та механізмами У період лікування індометацином необхідно утримуватися від керування автотранспортом та занять потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаСупозиторії – 1 супп.: Активна речовина: індометацин – 50 мг або 100 мг; Допоміжна речовина: Жирних кислот гліцериди (жир твердий, Вітепсол Н15) - 0,95 г або 1,0 г.Фармакотерапевтична групаНестероїдний протизапальний препарат.ФармакокінетикаАбсорбція – швидка. Біодоступність при ректальному шляху введення – 80-90%. Максимальна концентрація індометацину у крові досягається через 45-60 хв після введення препарату. Максимальна концентрація індометацину становить 1,56-2,81 мкг/мл. Зв'язок із білками плазми – 90%. Метаболізується в основному в печінці. Період напіввиведення індометацину – 4-9 годин (показник може варіювати залежно від вираженості системного метаболізму, кишково-печінкової рециркуляції). 70% виводиться нирками, причому 30% у незміненому вигляді, і через кишечник у вигляді метаболітів – 30%. Не видаляється при діалізі. Проникає у грудне молоко.ФармакодинамікаІндометацин має аналгетичну, протизапальну, жарознижувальну дію. НПЗП, похідне індолоцтової кислоти. Механізм дії пов'язаний з невибірковим пригніченням циклооксигенази-1 та циклооксигенази-2, що призводить до пригнічення синтезу простагландинів із арахідонової кислоти. Пригнічує агрегацію тромбоцитів. При ревматичних захворюваннях протизапальні та аналгетичні властивості викликають ослаблення таких симптомів як, біль у стані спокою і при русі, ранкова скутість, припухлість суглобів, покращує функціональну здатність суглобів. Чинить аналгетичну дію при помірному болю неревматичного характеру. При запальних процесах, що виникають після операцій та травм, швидко полегшує як спонтанний біль, так і біль під час руху, зменшує запальний набряк у рані.Показання до застосуванняЗапальні та дегенеративні захворювання опорно-рухового апарату: ревматоїдний, псоріатичний, ювенільний хронічний артрит, анкілозуючий спондиліт (хвороба Бехтерева), подагричний артрит. Больовий синдром: головний і зубний біль, люмбаго, ішіас, невралгія, міалгія, після травм та оперативних втручань, що супроводжується запаленням м'яких тканин та суглобів, бурсит та тендиніт, дисменорея. Як допоміжний засіб при запальних процесах у малому тазі, зокрема. аднекситі, простатиті, циститі, інфекційно-запальних захворюваннях ЛОР-органів з вираженим больовим синдромом (у складі комплексної терапії): фарингіт, тонзиліт, отит. Препарат призначений для симптоматичної терапії, зменшення болю та запалення на момент використання, на прогресування захворювання не впливає.Протипоказання до застосуванняГіперчутливість. Повне або неповне поєднання бронхіальної астми, рецидивуючого поліпозу носа або приносових пазух та непереносимості ацетилсаліцилової кислоти та інших нестероїдних протизапальних засобів (в т.ч. в анамнезі). Ерозивно-виразкові зміни слизової оболонки шлунка або 12-палої кишки, активна шлунково-кишкова кровотеча, у т.ч. ректальна, цереброваскулярна або інша кровотеча. Запальні захворювання кишок (хвороба Крона, виразковий коліт) у фазі загострення. Гемофілія та інші порушення згортання. Печінкова недостатність. Виражена ниркова недостатність (кліренс креатиніну менше 30 мл/хв), прогресуючі захворювання нирок, підтверджена гіперкаліємія. Період після проведеного аортокоронарного шунтування. Вагітність. Період грудного вигодовування. Дитячий вік віком до 14 років. Захворювання зорового нерва, порушення колірного зору. Проктит, геморой. З обережністю Ішемічна хвороба серця, цереброваскулярні захворювання, хронічна серцева недостатність, дисліпідемія, гіперліпідемія, цукровий діабет, захворювання печінки та нирок, виразкове ураження шлунково-кишкового тракту в анамнезі, тромбоцитопенія, цироз печінки з портальною гіпертензією, гіпербілірубінем втручань, куріння, хронічна ниркова недостатність (кліренс креатиніну 30-60 мл/хв), у хворих з епілепсією, паркінсонізмом, депресією, психічними розладами, порушеннями зору та слуху. Наявність інфекції Helicobacter pylori, літній вік, тривале застосування нестероїдних протизапальних засобів, часте вживання алкоголю, тяжкі соматичні захворювання; супутня терапія наступними препаратами: антикоагулянти (наприклад, варфарин), антиагреганти (наприклад, ацетилсаліцилова кислота, клопідогрел), пероральні глюкокортикостероїди (наприклад, преднізолон), селективні інгібітори зворотного захоплення серотоніну (наприклад, циталопрам, флуоксетин, пароксетин, сертралін).Вагітність та лактаціяПротипоказано при вагітності. На час лікування слід припинити грудне вигодовування.Побічна діяЧасто – 1-10%; нечасто - 0,1-1%; рідко - 0,01-0,1%; дуже рідко - менше 0,01%, включаючи окремі випадки. З боку травної системи: часто – НПЗЗ-гастропатія, біль та неприємні відчуття у животі, нудота, блювання, печія, зниження апетиту, діарея. Нечасто при тривалому застосуванні у великих дозах – виразка слизової оболонки шлунково-кишкового тракту. Рідко - порушення функції печінки (підвищення активності "печінкових" трансаміназ, гіпербілірубінемія). При тривалому застосуванні можливі нервові системи: головний біль, запаморочення, безсоння, збудження, дратівливість, надмірна стомлюваність, сонливість, депресія, периферична невропатія; з боку органів чуття: рідко – порушення смаку, зниження слуху, шум у вухах, диплопія, нечіткість зорового сприйняття, помутніння рогівки, кон'юнктивіт; у схильних пацієнтів – виникнення набряків, підвищення артеріального тиску. З боку серцево-судинної системи: дуже рідко розвиток (погіршення) явищ хронічної серцевої недостатності, тахіаритмія. З боку сечовидільної системи: рідко – порушення функції нирок, протеїнурія, гематурія, інтерстиціальний нефрит, нефротичний синдром, некроз сосочків. З боку органів кровотворення та системи гемостазу: нечасто – кровотеча (шлунково-кишкова, ясенна, маткова, гемороїдальна), рідко – анемія (в т.ч. гемолітична та апластична), лейкопенія, тромбоцитопенія, агранулоцитоз; дуже рідко – еозинофілія, тромбоцитопенічна пурпура. Алергічні реакції: рідко – шкірний висип, свербіж, кропив'янка, ангіоневротичний набряк, бронхоспазм; у поодиноких випадках – фотосенсибілізація, токсичний епідермальний некроліз (синдром Лайєлла), вузлувата еритема, анафілактичний шок. Лабораторні показники: рідко – гіперглікемія, клюкозурія, гіперкаліємія. Місцеві реакції: нечасто – печіння, свербіж, тяжкість в аноректальній ділянці, загострення геморою. Інші: рідко – посилення потовиділення, асептичний менінгіт (частіше у пацієнтів з аутоімунними захворюваннями).Взаємодія з лікарськими засобамиСпільне застосування з парацетамолом збільшує ризик розвитку нефротоксичних ефектів. Етанол, колхіцин, глюкокортикостероїди та кортикотропін – підвищують ризик розвитку кровотеч у шлунково-кишковому тракті. Збільшує концентрацію в плазмі препаратів літію, метотрексату та дигоксину, що може призвести до їх токсичності. Підсилює гіпоглікемічну дію інсуліну та пероральних гіпоглікемічних лікарських засобів; посилює дію непрямих антикоагулянтів, антиагрегантів, тромболітиків (алтепази, стрептокінази та урокінази) – підвищується ризик розвитку кровотеч. Знижує ефект діуретиків, на фоні застосування калійзберігаючих діуретиків зростає ризик гіперкаліємії; знижує ефективність урикозуричних та гіпотензивних лікарських засобів (в т.ч. бета-адреноблокаторів); посилює побічні ефекти мінералокортикостероїдів, глюкокортикоїдів, ацетилсаліцилової кислоти, естрогенів, ін. НПЗЗ. Циклоспорин, препарати золота підвищують нефротоксичність індометацину. Цефамандол, цефоперазон, цефотетан, вальпроєва кислота, плікаміцин підвищують частоту розвитку гіпопротромбінемій та небезпеку кровотеч. Потенціює токсичну дію зидовудину (за рахунок інгібування метаболізму). Мієлотоксичні лікарські засоби посилюють прояви гематотоксичності препарату.Спосіб застосування та дозиПрепарат застосовують ректально. Супозиторій звільнити від контурної упаковки і після спорожнення кишечника ввести загостреним кінцем, по можливості глибоко в пряму кишку. Дорослим призначають супозиторії по 50 мг 1-3 рази на добу або супозиторії по 100 мг – 1 раз на добу перед сном. Під час нападу подагри – 200 мг на добу (як доповнення до прийому внутрішньо). Максимальна добова доза становить 200 мг. Доза, що підтримує 50-100 мг 1 раз на добу, на ніч. Тривалість курсу лікування встановлюють індивідуально. Дітям старше 14 років – по 1,5-2,5 мг/кг на добу.ПередозуванняПри ректальному застосуванні індометацин зустрічається дуже рідко. Можливі симптоми: нудота, блювання, сильний біль голови, запаморочення, порушення пам'яті, дезорієнтація. У важких випадках парестезії, оніміння кінцівок, судоми. Лікування: симптоматична терапія, форсований діурез. Гемодіаліз неефективний.Запобіжні заходи та особливі вказівкиДля зниження ризику розвитку небажаних явищ з боку шлунково-кишкового тракту слід використовувати найменшу ефективну дозу максимально можливим коротким курсом. При появі ознак ураження печінки (свербіж шкіри, пожовтіння шкірних покривів, нудота, блювання, біль у животі, потемніння сечі) слід припинити прийом препарату і звернутися до лікаря. Не рекомендується одночасне застосування з ацетилсаліцилової кислотою та іншими нестероїдними протизапальними засобами. Застосування препарату може негативно впливати на жіночу фертильність та не рекомендується жінкам, які планують вагітність. Після 2-х тижнів застосування препарату необхідний контроль клітинного складу периферичної крові та функціонального стану печінки та нирок. При необхідності визначення 17-кетостероїдів препарат слід відмінити за 48 годин до дослідження. У період лікування необхідно утриматися від водіння автотранспорту та занять потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаСупозиторії – 1 супп.: Діюча речовина: індометацин – 50 мг (100 мг); Допоміжні речовини: жир твердий (Вітепсол Н 15) – 1,30 г (1,30 г), жир твердий (Вітепсол W 35) – 0,65 г (0,60 г). По 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 супозиторіїв у контурній комірковій упаковці з двошарової плівки або плівки з полімерних матеріалів ПВХ/ПЕ або з плівки ПВХ/ПЕ білої комбінованої або плівки полівінілхлорид. По 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 контурних осередкових упаковок разом з інструкцією з медичного застосування препарату поміщають у картонну пачку.Опис лікарської формиСупозиторії торпедоподібної форми з гладкою поверхнею від білого до світло-жовтого кольору, без запаху. Поверхня зрізу має бути гладкою та однорідною.Фармакотерапевтична групаНестероїдний протизапальний препарат.ФармакокінетикаАбсорбція – швидка. Біодоступність при ректальному шляху введення – 80-90%. Зв'язок з білками плазми – 90 %, період напіввиведення – 4,5 год. Не видаляється при діалізі. Проникає у грудне молоко.ФармакодинамікаІндометацин має протизапальну, аналгетичну, жарознижувальну та антиагрегантну дію. Пригнічує активність протизапальних факторів, знижує агрегацію тромбоцитів. Пригнічуючи циклооксигеназу II типу, порушує метаболізм арахідонової кислоти, зменшує кількість простагландинів як в осередку запалення, так і у здорових тканинах, пригнічує ексудативну та проліферативну фази запалення. Усуває або зменшує больовий синдром ревматичного та неревматичного характеру (у т.ч. при болях у суглобах у спокої та при русі, зменшує ранкову скутість та припухлість суглобів, сприяє збільшенню обсягу рухів; при запальних процесах, що виникають після операцій та травм, швидко полегшує як спонтанний біль, і біль під час руху, зменшує запальний набряк дома рани).Показання до застосуванняГострі та хронічні болі при запальних та дегенеративних захворюваннях опорно-рухового апарату: ревматоїдний артрит; ювенільний хронічний артрит; анкілозуючий спондиліт (хвороба Бехтерєва); подагричний артрит; псоріатичний артрит; хвороба Рейтера. Ревматичні ураження м'яких тканин: тендиніти, бурсити, тендобурсити, тендовагініти. Дископатії, неврити, плексити, радикулоневрити. Дисменорея. Препарат призначений для симптоматичної терапії, зменшення болю та запалення на момент використання, на прогресування захворювання не впливає.Протипоказання до застосуванняГіперчутливість до індометацину або будь-якої з допоміжних речовин препарату. Повне або неповне поєднання бронхіальної астми, рецидивуючого поліпозу носа та приносових пазух та непереносимості ацетилсаліцилової кислоти або ін. нестероїдних протизапальних препаратів (в т.ч. в анамнезі), кропив'янки або риніту. Виразкова хвороба шлунка та 12-палої кишки, запальні захворювання кишечника (виразковий коліт, хвороба Крона), кровотечі (в т.ч. внутрішньочерепна, з органів шлунково-кишкового тракту (ЖКТ)). Вроджені вади серця (важка коарктація аорти, атрезія легеневої артерії, важкий зошит Фалло), період після аортокоронарного шунтування. Тяжка серцева недостатність. Ниркова недостатність (КК менше 30 мл/хв), активне захворювання печінки. Печінкова недостатність. Порушення згортання крові (в т.ч. гемофілія, подовження часу кровотечі, схильність до кровотеч). Порушення кровотворення (лейкопенія, анемія). Підтверджена гіперкаліємія. Вагітність та грудне вигодовування. Дитячий вік (до 15 років). З обережністю: ішемічна хвороба серця, цереброваскулярні захворювання, хронічна серцева недостатність, дисліпідемія, гіперліпідемія, цукровий діабет, тромбоцитопенія, захворювання периферичних артерій, артеріальна гіпертензія, куріння, хронічна ниркова недостатність (КК 36-60 мл/хв) , гіпербілірубінемія, виразкове ураження ШКТ в анамнезі, наявність інфекції Helicobacter pylori, тривале використання нестероїдних протизапальних засобів, часте вживання алкоголю, тяжкі соматичні захворювання, супутня терапія такими препаратами: антикоагулянти (в т.ч. варфарин) , клопідогрел), пероральні глюкокортикостероїди (в т.ч. преднізолон), селективні інгібітори зворотного захоплення серотоніну (в т.ч. циталопрам, флуоксетин, пароксетин, сертралін);психічні розлади, епілепсія, паркінсонізм, депресія, літній вік.Вагітність та лактаціяВагітність Індометацин не застосовується під час вагітності. Грудне годування Індометацин виділяється із грудним молоком. При необхідності лікування препаратом грудне вигодовування необхідно припинити.Побічна діяЗ боку травної системи - НПЗП-гастропатія, нудота, печія, зниження апетиту, біль у животі, крововиливи та виразки, блювання (в т.ч. і кров'я), діарея, запори, мелена, виразковий стоматит, підвищення активності "печінкових трансаміназ" (АЛТ, АСТ), минуще підвищення білірубіну; рідко токсичний гепатит з або без жовтяниці; дуже рідко – фульмінантний гепатит. При тривалому застосуванні у великих дозах – виразка слизової оболонки шлунково-кишкового тракту. З боку нервової системи – головний біль, запаморочення, безсоння, психомоторне збудження, дратівливість, надмірна втома, сонливість, депресія, периферична невропатія. З боку органів чуття – диплопія, нечіткість зорового сприйняття, зниження слуху, шум у вухах, порушення смаку, помутніння рогівки, кон'юнктивіт. З боку серцево-судинної системи – тахіаритмія, набряковий синдром, підвищення артеріального тиску, розвиток (погіршення) хронічної серцевої недостатності. З боку сечовидільної системи – порушення функції нирок, нефротоксичний синдром, протеїнурія, гематурія, інтерстиціальний нефрит, некроз сосочків. З боку органів кровотворення та системи гемостазу – кровотечі (шлунково-кишкова, ясенна, маткова, гемороїдальна), лейкопенія, тромбоцитопенія, агранулоцитоз, анемія (в т.ч. гемолітична та апластична), еозинофілія, тромбоцито. Алергічні реакції - зазвичай свербіж шкіри, висипання на шкірі; рідко – кропив'янка, бронхоспазм, астматичні напади, ангіоневротичний набряк; дуже рідко – бульозні висипання, почервоніння шкіри, екзема, ексфоліативний дерматит, пурпура алергічного типу, синдром Стівенса-Джонсона, у поодиноких випадках – фотосенсибілізація, токсичний епідермальний некроліз (синдром Лайєлла), вузлувата еритема, я. Лабораторні показники – агранулоцитоз, лейкопенія, тромбоцитопенія, гіперглікемія, глюкозурія, гіперкаліємія. Місцеві реакції - подразнення, тяжкість в аноректальній ділянці, загострення геморою. Інші – асептичний менінгіт (частіше у пацієнтів з аутоімунними захворюваннями), посилення потовиділення, апластична анемія, аутоімуна гемолітична анемія.Взаємодія з лікарськими засобамиПідвищує концентрацію в плазмі дигоксину, метотрексату та препаратів Li+, що може призвести до посилення їхньої токсичності. Спільне застосування з парацетамолом підвищує ризик розвитку нефротоксичних ефектів. Етанол, колхіцин, глюкокортикостероїди та кортикотропін підвищують ризик розвитку кровотеч із ШКТ. Підсилює гіпоглікемічну дію інсуліну та пероральних гіпоглікемічних лікарських засобів; посилює дію непрямих антикоагулянтів, антиагрегантів, тромболітиків (алтеплази, стрептокінази та урокінази) – виникає ризик кровотеч. Знижує ефект діуретиків, на фоні застосування калійзберігаючих діуретиків зростає ризик гіперкаліємії; знижує ефективність урикозуричних та гіпотензивних лікарських засобів (в т.ч. бета-адреноблокаторів); посилює побічні ефекти метотрексату, глюкокортикостероїдів, інших нестероїдних протизапальних засобів. Циклоспорин та препарати золота підвищують нефротоксичність (очевидно, за рахунок придушення синтезу простагландинів у нирках). Цефамандол, цефоперазон, цефотетан, вальпроєва кислота, плікаміцин підвищують частоту розвитку гіпопротромбінемій та небезпеку кровотеч. Антациди та колестірамін знижують абсорбцію індометацину. Підсилює токсичність зидовудину (за рахунок інгібування метаболізму); у новонароджених підвищує ризик розвитку токсичних ефектів аміноглікозидів (оскільки знижує нирковий кліренс і підвищує концентрацію в крові). Мієлотоксичні лікарські засоби посилюють прояви гемотоксичності препарату.Спосіб застосування та дозиРектально. Дорослі та діти старше 15 років: супозиторії по 50 мг двічі на добу або 100 мг один раз на добу. Максимальна добова доза – 200 мг. Доза вище 150-200 мг збільшує ризик побічних дій. Тривалість лікування: не більше ніж 7 днів. Побічні дії можна зменшити, використовуючи мінімальну ефективну дозу на більш короткий період часу.ПередозуванняСимптоми: нудота, блювання, сильний біль голови, запаморочення, порушення пам'яті, дезорієнтація. У важких випадках парестезії, оніміння кінцівок, судоми. Лікування: швидке виведення препарату з організму, симптоматична терапія. Гемодіаліз неефективний.Запобіжні заходи та особливі вказівкиПід час лікування необхідний контроль картини периферичної крові та функціонального стану печінки та нирок. При необхідності визначення 17-кетостероїдів препарат слід відмінити за 48 годин до дослідження. Для запобігання та зменшення диспепсичних явищ слід використовувати антацидні лікарські засоби. Не слід застосовувати препарат одночасно з іншими нестероїдними протизапальними засобами. Препарат може змінювати властивості тромбоцитів, проте не замінює профілактичної дії ацетилсаліцилової кислоти при серцево-судинних захворюваннях. Застосування препарату може негативно впливати на жіночу фертильність та не рекомендується жінкам, які планують вагітність. Вплив на здатність до керування автотранспортом та управління механізмами У період лікування індометацином необхідно утримуватися від керування автотранспортом та занять потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
Дозування: 50 мг Фасування: N6 Форма випуску: супозиторії Діюча речовина: Індометацин. . .
278,00 грн
229,00 грн
Склад, форма випуску та упаковкаГліцин, магнію цитрат, аскорбінова кислота; тіаміну гідрохлорид, піридоксину гідрохлорид, ціанокобаламін, орбіт; діоксид кремнію аморфний, тальк; стеаринова кислота; стеарат магнію.ХарактеристикаДля нормального функціонування нервової системи недостатньо лише тих засобів, які задіяні у процесах, що забезпечують вищу нервову діяльність. Важливим доповненням до них є органічні сполуки та макроелементи, здатні стимулювати її функції, благотворно впливати на емоції, настрій, поведінку та життєвий тонус, сприйняття та запам'ятовування, водночас покращуючи харчування головного мозку. Необхідний ефект може бути досягнутий при комплексному застосуванні цих речовин, завдяки чому вони здатні доповнювати та посилювати дію один одного. «Глірикум + Вітаміни B» — збалансований комплекс, додаткове джерело амінокислоти гліцину, яка бере участь у роботі мозку, а також вітамінів групи, С і магнію, що впливають на функціональний стан нервової системи, що сприяють збереженню і правильній роботі нервових клітин, постачанню їх енергією.Властивості компонентівГЛІЦИН сприяє покращенню концентрації уваги та пам'яті, підвищення швидкості реакції, розумової працездатності, зниження дратівливості, нормалізації засинання та сну; допомагає протистояти стресам; не викликає сонливості та звикання. ВІТАМІН В1 необхідний для захисту оболонок нервових клітин; потрібно передачі імпульсу в нейронах; підтримує живлення головного мозку; підвищує життєву активність, беручи участь у перетворенні їжі на енергію. ВІТАМІН В6 необхідний для засвоєння нервовими клітинами глюкози; впливає на поліпшення настрою та пам'яті, включаючись у синтез «гормону щастя» — серотоніну; покращує всмоктування магнію, що забезпечує передачу нервових імпульсів. Вітамін В12 впливає формування оболонки нервових волокон (мієліну); захищає від руйнування відростки нейронів; дозволяє зберігати бадьорість, зміцнює загальний тонус організму; стабілізує нервову систему. Вітамін С є фактором захисту організму від наслідків стресу; підтримує роботу нейротрансмітерів у головному мозку; бере участь у перетворенні триптофану в серотонін; грає важливу роль обміні тирозину, у тому числі синтезується адреналін. МАГНІЙ бере участь у передачі нервових імпульсів; надає заспокійливу дію на нервову систему; зменшує нервово-м'язову збудливість; включається до процесів розподілу енергії в нервових клітинах.РекомендуєтьсяРекомендується як біологічно активна добавка до їжі - додаткового джерела гліцину, вітамінів С, В1, В6, В12, що містить магній.Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність, годування груддю.Спосіб застосування та дозиДорослим, по 1 таблетці 2 десь у день під час їжі. Таблетку слід розсмоктати у роті. Тривалість прийому – 1 місяць.Запобіжні заходи та особливі вказівкиПеред застосуванням рекомендується проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаСупозиторії – 1 суп.: діюча речовина: індометацин – 50 мг; допоміжні речовини: твердий жир (тип І), твердий жир (тип ІІ). По 6 супозиторіїв у стрипі. По 1 стрипу у картонній пачці.Опис лікарської формиСупозиторії торпедоподібної форми з гладкою поверхнею від білого до світло-жовтого кольору без запаху. Поверхня зрізу має бути гладкою та однорідною.Фармакотерапевтична групаНестероїдні протизапальні засоби. Похідні оцтової кислоти та споріднені сполуки.ФармакокінетикаПри ректальному застосуванні 80-90% дози швидко всмоктується. Максимальна концентрація у плазмі досягається протягом 1-2 годин. Розподіл: розподіляється по всіх тканинах та органах. Проникає через плацентарний та гематоенцефалічний бар'єр. Проникає через синовіальну мембрану суглоб, при цьому його концентрація в синовіальній рідині підвищується. З білками плазми зв'язується 90-98% і здатний витісняти інші лікарські засоби та посилити їх терапевтичний ефект при одночасному застосуванні. Метаболізм: метаболізується в печінці за допомогою окиснення та кон'югації. Висновок: період напіввиведення індометацину варіюється між 2,6 та 11,2 годинами або в середньому 5,8 години. 60-75% виводиться нирками, з них 10-20% у незміненому вигляді, а решта виділяється з жовчю і калом. Проникає у грудне молоко.ФармакодинамікаІндометацин - похідне індолоцтової кислоти і відноситься до групи нестероїдних протизапальних лікарських засобів (НПЗЗ). Має виражену протизапальну дію, значно перевищує дію фенілбутазоном та ацетилсаліцилової кислоти. Його аналгетичну активність відповідає аналгетичній активності метамізолу. Має жарознижувальну дію. Індометацин виявляє сильну пригнічуючу дію на синтез простагландинів шляхом інгібування циклооксигенази. Крім цього, зменшує і агрегацію тромбоцитів, і ліпоксигеназну активність в області запалення, відповідно, і лейкотрієни; також зменшує вивільнення ендогенних пірогенів, інактивує лізосомні ферменти, пригнічує активність нейтральних протеаз. Значення мають його інші ефекти,такі як декупелювання окисного фосфорилювання та пригнічення зворотного захоплення катехоламінів, посилення обміну норадреналіну та відома гангліоблокуюча дія.Показання до застосуванняЕфективність короткочасного симптоматичного лікування індометацином встановлена стосовно наступних станів: гострого та хронічного болю при запальних та дегенеративних захворюваннях опорно-рухового апарату: ревматоїдний артрит гострий та у стадії загострення; хронічний анкілозуючий спондилоартрит (хвороба Бехтерева); напад подагри та подагричний артрит; захворювання навколосуглобових тканин тендиніт, бурсит (гостре хворобливе плече), тендобурсит, тендовагініти, больовий синдром та запалення після травм (у тому числі у спортсменів) та оперативних втручань дископатії, плексит, радикулоневрит; дисменорея. Слід обережно оцінити потенційну користь та ризик застосування індометацину та інші варіанти лікування, перш ніж ухвалити рішення щодо застосування індометацину. Необхідно використовувати найнижчу ефективну дозу за найкоротший період часу відповідно до індивідуальної мети лікування пацієнта.Протипоказання до застосуванняПідвищена чутливість до активної або будь-якої з допоміжних речовин препарату. Підвищена чутливість до ацетилсаліцилової кислоти або інших нестероїдних протизапальних засобів з клінічним проявом астматичного нападу, кропив'янки або риніту, ангіоневротичний набряк. Дані в анамнезі шлунково-кишкові кровотечі або перфорації, які були спричинені застосуванням лікарських засобів групи нестероїдних протизапальних засобів у минулому. Активна або рецидивна виразка або кровотеча (два або більше випадків підтверджених виразок або кровотеч), виразковий коліт та/або ентероколіт. Одночасне застосування інших нестероїдних протизапальних засобів, включаючи специфічні інгібітори циклооксигенази-2 через підвищений ризик виникнення побічних ефектів. Тяжка серцева недостатність. Тяжка печінкова та ниркова недостатність. Геморої, анальні нориці та тріщини, проктити та інші хвороби прямої кишки та анусу. Кровотечі із гемороїдальних вузлів. Перед- та постопераційний біль при операції аортокоронарного обхідного шунтування.Вагітність та лактаціяВагітність. Препарат протипоказаний під час вагітності. Годування груддю. У ході лікування слід припинити годування груддю, тому що індометацин у невеликих кількостях проникає у грудне молоко. Безпека застосування у дітей не встановлена. Препарат не застосовувати для лікування дітей віком до 14 років.Побічна діяНайчастішими побічними ефектами є шлунково-кишкові розлади. Можлива поява виразкової хвороби, перфорації або кровотечі зі шлунково-кишкового тракту (іноді з летальним наслідком) переважно у пацієнтів похилого віку. З боку крові та лімфатичної системи: лейкопенія, нейтропенія, тромбоцитопенія, агранулоцитоз, анемія (включаючи гемолітичну та апластичну), пригнічення функції кісткового мозку, ДВЗ. З боку імунної системи: дуже рідко – бронхоспазм, астматичні напади, анафілактичні або анафілактоїдні реакції у алергічних пацієнтів, лихоманка, васкуліт, анафілактичний шок, набряк легенів, мозку. З боку обміну речовин: підвищення рівня сечовини, збільшення маси тіла, підвищення рівня печінкових ферментів, підвищений потовиділення, прискорення хрящової дегенерації, затримка рідин, гіперглікемія, глюкозурія, гіперкаліємія. З боку дихальної системи: носова кровотеча, легенева субтропічна еозинофілія, задишка, гострий респіраторний дистрес. З боку нервової системи: збудження, судоми, м'язова слабкість, мимовільні м'язові рухи, психічні розлади, посилення епілепсії та паркінсонізму, порушення свідомості, кома, дизартрія, асептичний менінгіт, галюцинації, страх, запаморочення, головний біль, вертиго, сонність , тривожність, слабкість, порушення концентрації, мережевні порушення, включаючи парестезії, дезорієнтація, безсоння, дратівливість, периферична невропатія, розлад пам'яті, психотичні реакції, непритомність, деперсоналізація. З боку органу зору: неврит зорового нерва, відкладення на рогівці та пошкодження сітківки, у тому числі жовтої плями, кон'юнктивіт, біль у навколоочній ділянці, диплопія, нечіткість зору. З боку органів слуху та лабіринту: дуже рідко – порушення слуху, шум у вухах, глухота. З боку серця: тахікардія, стенокардія, пальпітація, аритмії, набряки, дуже рідко – серцева недостатність, пов'язана з прийомом НПЗЗ. Застосування індометацину (особливо у високих дозах та тривалому застосуванні) можна пов'язати зі слабким підвищеним ризиком інфаркту міокарда або інсульту. З боку судин: артеріальна гіпертензія, гіпотензія, тромботична мікроангіопатія. З боку шлунково-кишкового тракту: анорексія, порушення смаку, гастроентерит, ерозивно-виразкові ураження, кровотечі та перфорації ШКТ, проктит, стриктури кишечника, гастрит, кровотеча з сигмовидної кишки або з дивертикулу, регіональний ілеїт, холестаз, диспепсія, запор, біль у животі, метеоризм, мелена, криваве блювання, виразковий стоматит, загострення виразкового коліту (хвороба Крона), загострення існуючої виразки. З боку печінки та жовчовивідних шляхів: токсичний гепатит з або без жовтяниці, дуже рідко – фульмінантний гепатит. З боку шкіри та підшкірних тканин: випадання волосся, загострення псоріазу, екземи, свербіж з або без висипань, кропив'янка, петехії, екхімози, дуже рідко – ангіоневротичний набряк, ексфоліативний дерматит, пурпура, вузлувата еритема, мультиформна ер Джонсона та токсичний епідермальний некроліз. З боку нирок та сечостатевої системи: порушення функції нирок, набряки, вагінальна кровотеча, збільшення та нагрубання молочних залоз, гінекомастія, протеїнурія, гематурія, нефротичний синдром, інтерстиціальний нефрит, гостра ниркова недостатність, папілярний некроз. Загальні розлади та порушення у місці введення: місцеве роздратування, місцева кровотеча та загострення геморою, свербіж в аноректальній ділянці, тенезми. Лабораторні та інструментальні дані: підвищення рівня амінотрансфераз у сироватці крові (ALAT, ASAT), минуще підвищення білірубіну.Взаємодія з лікарськими засобамиСлід уникати застосування двох або більше нестероїдних протизапальних засобів у зв'язку з підвищеним ризиком виникнення побічних ефектів. При одночасному застосуванні з антибактеріальними засобами може підвищуватися ризик виникнення судом, з ципрофлоксацином – ризик шкірних реакцій та нейротоксичність. Одночасне застосування зальцитабіну та індометацину викликає зміни у їхній факмакодинаміці. Одночасне застосування зидовудину та індометацину підвищує ризик гематологічної токсичності. Ризик прояву токсичності індометацину підвищується при застосуванні з ритонавіром. Слід бути обережними при одночасному застосуванні з циклофосфамідом у зв'язку з виникненням водної інтоксикації. Слід обережно застосовувати одночасно з антидепресантами (селективними інгібіторами зворотного захоплення серотоніну) через підвищення ризику кровотеч. Дія похідних сульфонілсечовини може посилюватись нестероїдними протизапальними засобами. У поодиноких випадках одночасне застосування з метформіном може спричинити метаболічний ацидоз. З обережністю слід застосовувати одночасно з протиепілептичними препаратами через посилення дії фенітоїну. Одночасне застосування з галоперидолом посилює сонливість. Слід уникати одночасного прийому з тріамтереном через виникнення зворотної ниркової недостатності. При одночасному застосуванні з бензодіазепінами підвищується ризик виникнення запаморочення. При одночасному застосуванні з дермопресином посилюється дія останнього. Слід уникати прийому нестероїдних протизапальних засобів протягом 8-12 діб після застосування міфепрістону. Індометацин здатний знижувати швидкість виведення баклофену і, таким чином, підвищувати рівень його токсичної дії. Для пацієнтів при одночасному застосуванні індометацину та Муромонаб-CD3 підвищується ризик розвитку психозу та енцефалопатії. Індометацин здатний спотворювати результати лабораторних аналізів: викликати підвищення рівня одного або більше печінкових ферментів; препарат може бути причиною отримання помилково негативних результатів при спробі пригнічення дексаметазону. Одночасне застосування нестероїдних протизапальних засобів та інгібіторів ЦОГ-2 підвищує ризик розвитку «анальгезуючого» нефропатії та папілярного некрозу нирок. Тому необхідно уникати їхнього одночасного застосування. При одночасному прийомі з судинно-розширювальними засобами підвищується ризик кровотеч. Інші нестероїдні протизапальні засоби: одночасне застосування індометацину з іншими нестероїдними протизапальними засобами підвищує ризик шлунково-кишкових ускладнень. Дифлунізал: підвищує рівень індометацину у плазмі та знижує його нирковий кліренс. Можливе виникнення летальних шлунково-кишкових кровотеч. Ця комбінація не рекомендується. Дигоксин: індометацин може підвищувати концентрацію дигоксину в плазмі, що потребує корекції дози та відстеження рівня дигоксину. Солі літію індометацин подовжує та потенціює дію солей літію та підвищує літієву токсичність. Імуносупресори: одночасне застосування індометацину та імуносупресорів, таких як метотрексат та циклоспорин, веде до посилення їх токсичності. Такролімус: одночасне застосування з такролімусом підвищує нефротоксичність індометацину. Діуретики: НПЗЗ знижує терапевтичну ефективність діуретиків. Можливе підвищення ризику виникнення гіперкаліємії при сумісному застосуванні з калійзберігаючими діуретиками та зменшення функції нирок при комбінованому застосуванні з тіазидними діуретиками. Діуретики можуть посилювати нефротоксичність індометацину. Пробенецид: уповільнює виведення та підвищує токсичність індометацину. Антигіпертензивні засоби: індометацин може послаблювати гіпотензивну дію інгібіторів АПФ та β-блокаторів при одночасному застосуванні. Кортикостероїди: підвищує ризик шлунково-кишкових ульцерацій та кровотеч. Антикоагулянти НПЗЗ можуть посилити дію антикоагулянтів при комбінованому застосуванні. Підвищується ризик ульцерацій та кровотеч. Необхідно контролювати час кровотечі та протромбінового часу. Індометацин конкурентно взаємодіє з кумариновими антикоагулянтами в місцях зв'язування з білками плазми крові, в результаті підвищується їх концентрація в плазмі крові. У разі їх одночасного застосування індометацин призначають у найменшій можливій дозі та оцінюється можливість додавання протективних агентів. Антиагреганти та селективні інгібітори зворотного захоплення серотоніну (SSRIs): підвищений ризик шлунково-кишкової кровотечі. Хінолонові антибактеріальні засоби: з обережністю використовувати пацієнтам, які приймають хінолонові антибактеріальні лікарські препарати. Протидіабетичні засоби: індометацин не змінює терапевтичну ефективність пероральних протидіабетичних засобів та інсуліну, незважаючи на те, що є спостереження про гіпо- або гіперглікемізуючу дію при їх одночасному застосуванні. Пентоксифілін: одночасне застосування з пентоксифіліном підвищує рівень розвитку кровотеч. Бісфосфонати: одночасне застосування з бісфосфонатами підвищує біодоступність індометацину. Зідовідин: одночасне призначення з зидовидином підвищує мієлотоксичність індометацину.Спосіб застосування та дозиДорослі: звичайна доза – 50 мг (1 супозиторій) 2 рази на добу або по 100 мг (2 супозиторії) один раз на добу. Максимальна добова доза становить 200 мг. При застосуванні добової дози, що перевищує 150-200 мг, збільшується ризик побічних дій. Пацієнти похилого віку рекомендується приймати найнижчу ефективну дозу протягом якомога коротшого часу, оскільки існує ризик виникнення побічних дій. Пацієнти необхідно стежити, оскільки можливе виникнення кровотечі із шлунково-кишкового тракту. Тривалість лікування має перевищувати 7 днів. Спосіб застосування Індометацин Софарма, супозиторії застосовувати ректально. Частоту появи побічних дій можна зменшити, застосовуючи для усунення симптомів мінімальну ефективну дозу протягом короткого часу.ПередозуванняСимптоми: нудота, блювання, сильний головний біль, запаморочення, порушення пам'яті та дезорієнтація. У складніших випадках спостерігаються парестезії та судоми. Лікування: симптоматичне та підтримуюче. Неможливо вивести індометацин із організму за допомогою гемодіалізу.Запобіжні заходи та особливі вказівкиПобічна дія можна зменшити, використовуючи для усунення симптомів найнижчу ефективну дозу протягом найбільш короткого часу. Слід з обережністю застосовувати препарат пацієнтам з порушеннями функції нирок, печінки чи серця, або станами, схильними до затримки рідини в організмі, оскільки індометацин спричиняє ослаблення функції нирок та застій рідини. У пацієнтів із системним червоним вовчаком та захворюваннями сполучної тканини можливе підвищення ризику розвитку вірусного менінгіту. Слід бути обережним при застосуванні препарату пацієнтам після хірургічних втручань, оскільки тривалість кровотеч у них може бути збільшена. В окремих випадках застосування індометацину може маскувати прояви інфекційно-запального процесу, а також слід бути обережними при застосуванні живих вакцин. Пацієнтам, які тривалий час застосовують препарат, слід періодично проводити дослідження крові, функції печінки або шлунка, щоб якомога раніше виявити будь-яку небажану дію. Слід обережно застосовувати препарат пацієнтам з аномаліями сигмовидної кишки. Пацієнтам зі зниженим кровотоком, у яких ниркові простагландини відіграють важливу роль у підтримці ниркової перфузії, НПЗЗ можуть спровокувати виражену ниркову декомпенсацію. До групи ризику виникнення подібної реакції входять пацієнти з нирковою або печінковою дисфункцією, хворі на цукровий діабет, пацієнти похилого віку, пацієнти зі зниженим об'ємом міжклітинної рідини, застійною серцевою недостатністю, сепсисом, а також особи, які одночасно приймають нефротоксичні препарати. Таким пацієнтам необхідно контролювати функцію нирок під час прийому препарату. Слід бути обережним, застосовуючи препарат хворим на бронхіальну астму, у зв'язку з можливістю виникнення бронхоспазму. Слід уникати одночасного застосування індометацину з іншими лікарськими засобами групи НПЗЗ, включаючи селективні інгібітори ЦОГ-2. Шлунково-кишкові крововиливи, ульцерації та перфорації, включаючи ті, що мають летальний кінець, спостерігаються при застосуванні всіх нестероїдних протизапальних засобів у будь-який час у ході лікування, за наявності або без попереджувальних симптомів або даних про попередні серйозні інциденти з боку шлунково-кишкового тракту. Ризик появи побічних дій з боку шлунково-кишкового тракту вищий при застосуванні високих доз НПЗЗ у пацієнтів з виразковою хворобою в анамнезі, особливо ускладненою крововиливом або перфорацією, та у пацієнтів похилого віку. У таких пацієнтів лікування НПЗЗ слід розпочинати з низької можливої дози, беручи до уваги необхідність застосування протективних лікарських засобів (наприклад, мізопростолу або інгібіторів протонної помпи). Цей підхід рекомендується і у випадках одночасного застосування низьких доз ацетилсаліцилової кислоти або інших лікарських засобів, які збільшують ризик шлунково-кишкових ускладнень (кортикостероїди, антикоагулянти, антиагреганти, селективні інгібітори зворотного захоплення серотоніну). Особлива обережність необхідна при лікуванні пацієнтів із захворюваннями шлунково-кишкового тракту, такими як хвороба Крона, які можуть загостритись при застосуванні нестероїдних протизапальних засобів. Збільшення ризику ускладнень з боку шлунково-кишкового тракту існує у пацієнтів, які зловживають алкоголем, у курців, тому у цієї групи пацієнтів лікування необхідно проводити з особливою обережністю. Пацієнтам з даними в анамнезі шлунково-кишкові порушення (переважно хворим похилого віку) слід порадити повідомляти про незвичайні абдомінальні симптоми (особливо про шлунково-кишкові кровотечі), особливо на початку лікування. При появі ульцерацій та кровотеч із шлунково-кишкового тракту лікування індометацином слід зупинити. Необхідно забезпечити належний нагляд та увагу пацієнтам з даними в анамнезі гіпертензію та/або від легкої до помірної застійної серцевої недостатності, оскільки є повідомлення про набряки та затримку рідини, пов'язаних із лікуванням НПЗЗ. Клінічні дослідження та епідеміологічні дані показують, що застосування деяких нестероїдних протизапальних засобів (особливо у високих дозах та при тривалому застосуванні) можуть бути пов'язані зі слабким підвищенням ризику артеріальних тромботичних подій (наприклад, інфаркт міокарда або інсульт). Немає достатньої кількості даних, щоб унеможливити такий ризик для індометацину. Пацієнтів з неконтрольованою гіпертензією, застійною серцевою недостатністю, встановленою ішемічною хворобою серця, захворюванням периферичних артерій та/або судинно-мозковою хворобою слід лікувати індометацином тільки після ретельної оцінки ситуації, яка необхідна для початку тривалого лікування пацієнтів з факторами ризику розвитку серцево-судин. , гіпертензія, гіперліпідемія, цукровий діабет, куріння) Застосовується з обережністю пацієнтам із проявами гіперчутливості до харчових продуктів та лікарських препаратів, хворим на алергічні захворювання – сінна лихоманка, бронхіальна астма, назальний поліпоз. Індометацин застосовується з обережністю пацієнтам із нирковими захворюваннями через можливе ураження нирок. Застосовується з обережністю хворим на психічні порушення, депресію, епілепсію, паркінсонізм, оскільки може призвести до погіршення основного захворювання. Необхідно призначати з обережністю пацієнтам з анамнезом порушення коагуляції, оскільки лікарський препарат пригнічує біосинтез простагландинів та впливає на функцію тромбоцитів. Лікування індометацином, як і іншими лікарськими препаратами групи НПЗП, при тривалому застосуванні може викликати зміни функції печінки, що потребує періодичного контролю печінкових ферментів. Серйозні шкірні реакції, з летальним результатом включно, дуже рідко спостерігаються при застосуванні нестероїдних протизапальних засобів і стосуються випадків ексфоліативного дерматиту, синдрому Стівенса-Джонсона, токсичний епідермальний некроліз. Найвищий ризик появи зазначених реакцій – на початку лікування (у перший місяць). Застосування лікарського препарату слід припинити з появою перших шкірних чи інших ознак гіперчутливості. Внаслідок своєї протизапальної дії препарат може маскувати симптоми гострого запалення, що вимагає виключення наявності бактеріальної інфекції при його призначенні. Жінки репродуктивного віку мають ризик зворотного придушення фертильності при застосуванні препарату. При застосуванні лікарських препаратів із групи НПЗЗ існує ризик розвитку гіперкаліємії, особливо у пацієнтів віком від 65 років, пацієнтів з нирковою недостатністю, пацієнтів, які лікуються β-блокаторами, інгібіторами АПФ та калійзберігаючих діуретиків. У таких пацієнтів необхідно контролювати рівень калію у сироватці крові. Здатність впливати на швидкість реакції при керуванні автотранспортом чи іншими механізмами Індометацин Софарма може викликати побічні дії (шум у вухах, запаморочення, сонливість, порушення слуху та зору), які можуть порушити активну увагу та рефлекси та діяти на здатність керувати транспортними засобами та працювати з машинами.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаГель - 1 г: Активні речовини: індометацин 30мг, троксерутин 20мг. Допоміжні речовини: карбомер – 23 мг, макрогол 400 – 524.5 мг, натрію бензоат – 2.5 мг, пропіленгліколь – 100 мг, етанол 96% – 300 мг. 45 г – туби алюмінієві (1) – пачки картонні.Опис лікарської формиГель для зовнішнього застосування від жовтого до жовто-коричневого кольору з легкою опалесценцією.Фармакотерапевтична групаІндовазин® гель є комбінованим лікарським препаратом, до складу якого входять індометацин і троксерутин. Індометацин має виражену протизапальну, аналгетичну та протинабрякову дію. Це призводить до зняття болю, зменшення набряку та скорочення часу відновлення пошкоджених тканин. Основний механізм дії пов'язаний з придушенням синтезу простагландинів за допомогою оборотної блокади ЦОГ-1 та ЦОГ-2. Троксерутин (тригідроксіетилрутинозід) являє собою біофлавоноїд. Він відноситься до ангіопротекторних засобів. Зменшує проникність капілярів та виявляє венотонізуючу дію. Блокує венодилатуючу дію гістаміну, брадикініну та ацетилхоліну. Діє протизапально на околовенозну тканину, зменшує ламкість капілярів і має деяку антиагрегантну дію. Зменшує набряклість, покращує трофіку при патологічних змінах, пов'язаних із венозною недостатністю. При нанесенні на шкіру Індовазин® гель пригнічує запальну набряклу реакцію, знімає біль і температуру в осередках запалення, що знаходяться на поверхні та в глибині, досягаючи розташованих там кровоносних судин. Виявляє венотонізуючу та капіляропротекторну дію.ФармакокінетикаВикористовувана мазева основа забезпечує розчинність та вивільнення індометацину та троксерутину. Гелева лікарська форма, в яку включені індометацин та троксерутин, добре всмоктується з поверхні шкіри та забезпечує терапевтичну дію препарату. При нанесенні на шкіру в підшкірній клітковині та навколосуглобових тканинах створюються концентрації, близькі до терапевтичних. Проникнення активних компонентів препарату в системний кровотік клінічно незначне.Клінічна фармакологіяПрепарат із протизапальною та ангіопротекторною дією для зовнішнього застосування.Показання до застосуванняУ комплексній терапії хронічної венозної недостатності нижніх кінцівок (варикозне розширення вен) – для зняття набряку, почуття тяжкості та болю в ногах; поверхневий тромбофлебіт, флебіт, післяфлебітні стани; ревматичне ураження м'яких тканин: тендовагініт, бурсит, фіброзит, періартрит; при набряках після хірургічних втручань, контузіях, вивихах, розтягуваннях.Протипоказання до застосуванняпорушення цілісності шкірних покровів; ІІІ триместр вагітності; період лактації (грудного вигодовування); дитячий вік до 14 років (відсутній клінічний досвід застосування); підвищена чутливість до компонентів препарату та нестероїдних протизапальних засобів. З обережністю: одночасний прийом препарату з іншими нестероїдними протизапальними засобами, бронхіальна астма, алергічний риніт, поліпи слизової оболонки носа.Вагітність та лактаціяКлінічний досвід, що доводить безпеку препарату при застосуванні при вагітності та під час годування груддю, відсутній. Його застосування можливе лише у випадку, якщо очікувана користь перевищує потенційний ризик для плода. Застосування у дітей Протипоказаний у дитячому віці до 14 років.Побічна діяПереносимість препарату зазвичай хороша. Місцеві реакції: можлива поява симптомів підвищеної чутливості з боку шкіри – контактний дерматит, свербіж, почервоніння, висипання, почуття тепла та печіння в місці нанесення.Взаємодія з лікарськими засобамиМазь може посилювати дію препаратів, що спричиняють фотосенсибілізацію. Клінічно значущої взаємодії з іншими лікарськими засобами не описано.Спосіб застосування та дозиПрепарат призначений для зовнішнього застосування. 4-5 см гелю наносять 3-4 рази на добу тонким шаром на уражену ділянку легкими рухами, що втирають. Загальна добова кількість не повинна перевищувати 20 см. Тривалість лікування не повинна перевищувати 10 днів.ПередозуванняНемає відомостей про випадки передозування під час місцевого застосування. При випадковому проковтуванні великих кількостей можливе відчуття печіння в роті, слиновиділення, нудота, блювання. Лікування: промивання ротової порожнини та шлунка, при необхідності – симптоматичне лікування.Запобіжні заходи та особливі вказівкиНе наноситься на відкриті рани, слизові оболонки, в ротову порожнину, очі. При попаданні в очі, на слизові оболонки або відкриті ранові поверхні спостерігається місцеве подразнення - сльозогінність, почервоніння, печіння, біль. Необхідні заходи - промивання ураженої ділянки багатою дистильованою водою або фізіологічним розчином до зникнення або зменшення скарг. Індовазин® гель містить натрію бензоат і пропіленгліколь як допоміжні речовини, які можуть мати подразнюючу дію на шкіру. Вплив на здатність до керування автотранспортом та управління механізмами Не впливає на швидкість психомоторних реакцій при керуванні та роботі з механізмами.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
800,00 грн
756,00 грн
Склад, форма випуску та упаковкаРозчин для внутрішньом'язового введення – 1 мл: активна речовина: хондроїтину сульфат натрію – 100 мг (у перерахунку на суху речовину); допоміжні речовини: натрію дисульфіт – 2 мг; метилпарагідроксибензоат - 0,5 мг; 1 М розчин гідроксиду натрію - до рН 6-7,5; вода для ін'єкцій – до 1 мл. Розчин для внутрішньом'язового введення 100 мг/мл. По 1 або 2 мл у ампулі нейтрального скла або скла з класом опору гідролізу HGA1 (I гідролітичний). 5 амп. поміщають у контурну осередкову упаковку (з плівки ПВХ або з плівки ПЕТФ) з алюмінієвою фольгою або без неї. 1 або 2 контурні осередкові упаковки разом з ампульним скарифікатором поміщають в пачку з картону. 5 або 10 амп. разом з ампульним скарифікатором поміщають в пачку з картону з гофрованим вкладишем. При упаковці ампул з крапкою або кільцем зламу ампульний скарифікатор не вкладають. Упаковка для стаціонарів. 4, 5 або 10 контурних осередкових упаковок поміщають у пачку з картону. 50 або 100 контурних осередкових упаковок поміщають у коробку з картону.Опис лікарської формиПрозорий безбарвний або з трохи жовтуватим відтінком розчин.Фармакотерапевтична групаХондростімулююче, репаративне.ФармакокінетикаХондроїтину сульфат натрію легко всмоктується при внутрішньом'язовому введенні. Через 30 хв після внутрішньом'язового введення виявляється в крові у значних концентраціях; через 15 хв - у синовіальній рідині. Cmax у плазмі досягається через 1 год після введення, потім концентрація препарату поступово знижується протягом 2 діб. Накопичується головним чином хрящової тканини (Cmax у суглобовому хрящі досягається через 48 год); синовіальна оболонка не є перешкодою для проникнення препарату у порожнину суглоба. Виводиться з організму, переважно, нирками протягом 24 год.ФармакодинамікаХондроїтину сульфат - основний компонент протеогліканів, що становлять разом з колагеновими волокнами хрящовий матрикс. Має хондростимулюючу, регенеруючу, протизапальну та аналгетичну дію. Хондроїтину сульфат бере участь у побудові основної речовини хрящової та кісткової тканини. Має хондропротекторні властивості; посилює обмінні процеси в гіаліновому та волокнистому хрящах та субхондральній кістці; пригнічує активність ферментів, що спричиняють деградацію (руйнування) суглобового хряща; стимулює вироблення хондроцитами протеогліканів; впливає на фосфорно-кальцієвий обмін у хрящовій тканині, стимулює її регенерацію, бере участь у побудові основної речовини кісткової та хрящової тканини. Має протизапальні та аналгетичні властивості, сприяє зниженню викиду в синовіальну рідину медіаторів запалення та больових факторів через синовіоцити та макрофаги синовіальної оболонки, пригнічує секрецію ЛТ та ПГ. Препарат перешкоджає дегенерації сполучної тканини та знижує втрату кальцію, прискорює процеси відновлення кісткової тканини. Хондроїтину сульфат уповільнює прогресування остеоартрозу та остеохондрозу. Сприяє відновленню суглобової сумки та хрящових поверхонь суглобів, перешкоджає колапсу сполучної тканини, нормалізує вироблення суглобової рідини. Клінічний ефект проявляється покращенням рухливості суглобів, зменшенням інтенсивності болю, при цьому терапевтичний ефект зберігається тривалий час після закінчення курсу терапії. При лікуванні дегенеративних змін суглобів, що супроводжуються вторинним синовітом, ефект спостерігається вже через 2-3 тижні з початку курсу. Маючи структурну схожість з гепарином, потенційно може перешкоджати утворенню фібринових тромбів у синовіальному та субхондральному мікроциркулярному руслі.Показання до застосуванняДегенеративно-дистрофічні захворювання суглобів та хребта: остеоартроз периферичних суглобів; міжхребцевий остеохондроз та остеоартроз. Для прискорення формування кісткового мозоля при переломах.Протипоказання до застосуванняпідвищена чутливість до хондроїтину сульфату; кровотечі, схильність до кровоточивості; тромбофлебіти; вагітність; період годування груддю (на час лікування годуванням груддю слід припинити); дитячий вік (дані щодо ефективності та безпеки відсутні).Вагітність та лактаціяЗастосування ін'єктрану під час вагітності протипоказане. У разі застосування препарату в період грудного вигодовування годування груддю має бути припинено.Побічна діяПри застосуванні в осіб із підвищеною чутливістю до препарату можливі реакції гіперчутливості. З боку імунної системи: алергічні реакції, ангіоневротичний набряк. З боку шкіри та підшкірної клітковини: висипання на шкірі, свербіж, еритема, кропив'янка, дерматит. З боку шлунково-кишкового тракту: диспептичні явища. У місці ін'єкцій: можливі почервоніння, свербіж, геморагії.Взаємодія з лікарськими засобамиМожливе посилення дії непрямих антикоагулянтів, антиагрегантів та фібринолітиків, що потребує більш частого контролю показників зсідання крові при сумісному застосуванні. Виявляє синергізм при одночасному застосуванні з глюкозаміном та іншими хондропротекторами.Спосіб застосування та дозиВ/м по 1 мл через день. При добрій переносимості дозу збільшують до 2 мл, починаючи з 4-ї ін'єкції. Курс лікування – 25–35 ін'єкцій. При необхідності через 6 місяців можливе проведення повторного курсу лікування. Тривалість повторних курсів лікування визначається лікарем. Для формування кісткової мозолі курс лікування становить 3-4 тижні (10-14 ін'єкцій через день).ПередозуванняВ даний час про випадки передозування препарату Ін'єктран не повідомлялося. Разом з тим можна припустити, що при перевищенні добової дози можливе посилення проявів побічної дії препарату. Лікування: симптоматичне.Запобіжні заходи та особливі вказівкиРекомендується збільшення доз під контролем лікаря для пацієнтів із надмірною масою тіла, виразковою хворобою шлунка або дванадцятипалої кишки, при одночасному прийомі діуретиків, а також на початку лікування, при необхідності прискорення клінічної відповіді. У разі розвитку алергічних реакцій або появи геморагії лікування слід припинити. Використання у педіатрії. Дані щодо ефективності та безпеки застосування хондроїтину сульфату у дітей в даний час відсутні. Вплив на здатність керувати автомобілем, механізмами. У діапазоні доз, що рекомендується, вплив на концентрацію уваги і швидкість психомоторних реакцій не встановлено. При прийомі високих доз рекомендується бути обережними при керуванні транспортними засобами, роботі з механізмами та заняттями іншими потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій. Умови відпустки з аптекЗа рецептомВідео на цю тему
5 709,00 грн
5 676,00 грн
Склад, форма випуску та упаковкаЛіофілізат для приготування розчину - 1 фл. Активні речовини: інфліксімаб – 100 мг; Допоміжні речовини: натрію гідрофосфату дигідрат – 6.1 мг, натрію дигідрофосфату дигідрат – 2.2 мг, сахароза – 500 мг, полісорбат 80 – 0.5 мг. 1 шт. - флакони скляні (1) - пачки картонні.Опис лікарської формиЛіофілізат для приготування розчину для інфузії у вигляді щільної маси білого кольору без ознак розплавлення, що не містить сторонніх включень.Фармакотерапевтична групаПрепарат із протизапальною дією. Інгібітор фактора некрозу пухлини альфа (ФНП-α)ФармакодинамікаІнгібітор ФНПα. Інфліксімаб – химерне мишано-людське моноклональне антитіло. Має високий афінітет до ФНПα, який є цитокіном з широким спектром біологічної дії, є також посередником запальної відповіді і бере участь у процесах модуляції імунної системи. Очевидно, що ФНП відіграє роль у розвитку аутоімунних та запальних захворювань. Інфліксімаб швидко зв'язується і утворює стійку сполуку з обома формами (розчинною та трансмембранною) людського ФНПα, при цьому відбувається зниження функціональної активності ФНПα. Специфічність інфліксимабу по відношенню до ФНП підтверджена його нездатністю нейтралізувати цитотоксичний ефект лімфотоксину альфа (ЛТ або ФНО) - цитокіну, що взаємодіє з тими ж рецепторами, що і ФНП. Підвищені концентрації ФНП визначалися в суглобах пацієнтів з ревматоїдним артритом і корелювали з активністю хвороби. У пацієнтів з ревматоїдним артритом терапія інфліксимабом призводила до зменшення інфільтрації клітин запалення у запалені ділянки суглобів, а також зниження експресії молекул, що опосередковують клітинну адгезію, хемоатракцію та руйнування тканин. Після терапії інфліксімабом відзначалося зниження сироваткових концентрацій інтерлейкіну-6 (ІЛ-6) та С-реактивного білка (СРБ), а також підвищення концентрації гемоглобіну у пацієнтів з ревматоїдним артритом зі зниженою порівняно з базовим рівнем концентрацією гемоглобіну. Значного зниження кількості лімфоцитів у периферичній крові або їхньої проліферативної відповіді на мітогенну стимуляцію порівняно з відповіддю клітин нелікованих пацієнтів in vitro виявлено не було. У пацієнтів з псоріазом терапія інфліксимабом призводила до зниження запалення в епідермальному шарі та нормалізації диференціювання кератиноцитів у псоріатичних бляшках. У пацієнтів з псоріатичним артритом короткочасна терапія інфліксімабом супроводжувалася зниженням кількості Т-клітин та кровоносних судин у синовіальній оболонці та ділянках шкіри, уражених псоріатичним процесом. При гістологічному дослідженні біоптатів товстої кишки, взятих до і через 4 тижні після введення інфліксімабу, було виявлено суттєве зниження концентрації ФНПα. Терапія інфліксімабом пацієнтів із хворобою Крона супроводжувалася значним зниженням концентрації неспецифічного сироваткового маркера запалення – СРБ. Загальна кількість лейкоцитів периферичної крові при терапії інфліксімабом змінювалося мінімальною мірою, хоча для лімфоцитів, моноцитів та нейтрофілів спостерігалася тенденція до нормалізації їхньої кількості. У пацієнтів, які отримували інфліксімаб, проліферативна відповідь мононуклеарних клітин периферичної крові на стимуляцію не знижувалась порівняно з такою у нелікованих пацієнтів. Не було виявлено суттєвих змін секреції цитокінів стимульованими мононуклеарними клітинами периферичної крові після терапії інфліксімабом.Вивчення мононуклеарних клітин біоптатів власної платівки слизової оболонки кишки показало, що терапія інфліксімабом викликає зниження числа клітин, що експресують ФНПα та інтерферон гама. Додаткові гістологічні дослідження підтвердили, що інфліксімаб зменшує інфільтрацію клітин запалення та вміст маркерів запалення у уражених ділянках кишки. Ендоскопічні дослідження продемонстрували загоєння слизової оболонки кишки у пацієнтів, які отримували інфліксімаб.Ендоскопічні дослідження продемонстрували загоєння слизової оболонки кишки у пацієнтів, які отримували інфліксімаб.Ендоскопічні дослідження продемонстрували загоєння слизової оболонки кишки у пацієнтів, які отримували інфліксімаб.Показання до застосуванняРевматоїдний артрит в активній формі у пацієнтів 18 років і старше (у комбінації з метотрексатом) при неефективності терапії, що проводилася раніше, включаючи лікування метотрексатом. Хвороба Крона в активній формі тяжкого ступеня (в т.ч. з утворенням нориць) у пацієнтів 18 років і старше, що не піддається стандартній терапії, включаючи кортикостероїди та/або імунодепресанти. Хвороба Крона в активній формі, середнього або тяжкого ступеня у дітей та підлітків віком від 6 до 17 років включно – при неефективності, непереносимості чи наявності протипоказань до стандартної терапії, що включає кортикостероїди та/або імунодепресанти. Виразковий коліт у дорослих при неефективності стандартної терапії.Виразковий коліт середнього або тяжкого ступеня у дітей та підлітків віком від 6 до 17 років – при недостатній ефективності стандартної терапії із застосуванням кортикостероїдів, 6-меркаптопурину або азатіоприну, або за наявності непереносимості чи протипоказань до стандартної терапії. Анкілозуючий спондиліт. Псоріатичний артрит. Псоріаз.Протипоказання до застосуванняТяжкий інфекційний процес (в т.ч. абсцес, сепсис, туберкульоз, опортуністичні інфекції), підвищена чутливість до інфліксимабу та інших мишачих білків.Вагітність та лактаціявпливати в розвитку імунної системи плода. Жінки дітородного віку в період лікування та протягом принаймні 6 місяців після його закінчення повинні використовувати надійні методи контрацепції. Невідомо, чи виділяється інфліксімаб із грудним молоком у людини. При необхідності застосування у період лактації грудне вигодовування слід припинити. Відновлення грудного вигодовування дозволяється не раніше, ніж через 6 місяців після закінчення лікування. Безпека та ефективність застосування інфліксімабу у дітей та підлітків віком до 17 років з ревматоїдним артритом або хворобою Крона не вивчені.Побічна діяЗ боку нервової системи: часто – головний біль, запаморочення, відчуття втоми; рідко – депресія, психоз, неспокій, амнезія, апатія, нервозність, сонливість. З боку травної системи: часто – нудота, діарея, біль у животі, диспепсія; рідко – запор, шлунково-стравохідний рефлюкс, хейліт, дивертикуліт, порушення функції печінки, холецистит. З боку системи кровотворення: рідко – анемія, лейкопенія, лімфаденопатія, лімфоцитоз, лімфопенія, нейтропенія, тромбоцитопенія. З боку серцево-судинної системи: часто – припливи, біль у грудях; рідко – артеріальна гіпертензія, артеріальна гіпотензія, непритомність, тромбофлебіт, брадикардія, серцебиття, спазм судин, ціаноз, порушення периферичного кровообігу, аритмія, набряки. З боку дихальної системи: часто – задишка, вірусна інфекція (грип, герпес), лихоманка, інфекції верхніх відділів дихальних шляхів, бронхіт, пневмонія; рідко – бронхоспазм, плеврит, набряк легенів. З боку органу зору: рідко – кон'юнктивіт, кератокон'юнктивіт, ендофтальміт. З боку сечовивідної системи: рідко – інфекції сечовивідних шляхів, пієлонефрит. З боку системи згортання крові: рідко – екхімоз/гематома, петехії, носова кровотеча. Дерматологічні реакції: часто - висипання, шкірні висипання, свербіж, уртикарії, пітливість, сухість шкіри; рідко – грибковий дерматит (оніхомікоз, екзема), себорея, бешиха, бородавки, фурункульоз, періорбітальний набряк, гіперкератоз, порушення пігментації шкіри, алопеція, бульозний висип. Алергічні реакції: кропив'янка, свербіж, набряк обличчя, губ, кистей, міалгія та/або артралгія з лихоманкою, утворення аутоантитіл, вовчаковий синдром. Інші: часто – лихоманка; рідко – абсцеси, целюліти, сепсис, бактеріальна та грибкова інфекції, міалгія, артралгія, вагініт, інфузійний синдром, реакція у місці ін'єкції.Взаємодія з лікарськими засобамиУ пацієнтів з ревматоїдним артритом одночасне застосування метотрексату знижує утворення антитіл до інфліксімабу та підвищує концентрацію останнього у плазмі.Спосіб застосування та дозиВводять внутрішньовенно. Разова доза – 3-10 мг/кг. Частота і тривалість застосування встановлюються індивідуально, залежно від показань та схеми терапії.Запобіжні заходи та особливі вказівкиПри застосуванні інфліксімабу можливий розвиток гострих алергічних реакцій та алергічних реакцій уповільненого типу. У деяких хворих можливе утворення антитіл до інфліксімабу, які у поодиноких випадках викликають розвиток тяжких алергічних реакцій. За відсутності толерантності до метотрексату або інших імунодепресантів нестероїдної структури (наприклад, азатіоприну, 6-меркаптопурину) і перериванні їх прийому до або протягом застосування інфліксимабу підвищується ризик утворення цих антитіл. Реакції підвищеної чутливості уповільненого типу спостерігалися з високою частотою (25%) при хворобі Крона після призначення повторного лікування через 2-4 години після первинного. Оскільки виведення інфліксімабу відбувається протягом 6 місяців, хворий протягом цього періоду повинен перебувати під наглядом лікаря для своєчасного виявлення ознак інфекційного процесу. Застосування інфліксімабу слід припинити у разі розвитку тяжкої інфекції або сепсису. При підозрі на активний туберкульозний процес лікування слід припинити, доки не буде встановлено діагноз та проведено відповідне лікування. До початку терапії інфліксімабом пацієнтів слід ретельно обстежити щодо виявлення як активного, так і латентного туберкульозного процесу. Слід враховувати, що у важких хворих та хворих з імуносупресією може бути отримана помилково-негативна туберкулінова проба. При виявленні латентного туберкульозу необхідно вжити заходів, щоб не допустити активізації процесу, а також слід оцінити співвідношення ймовірної користі та потенційного ризику застосування інфліксимаб у цієї категорії пацієнтів. При появі в період лікування симптомів, що нагадують вовчаковий синдром (стійкий висип, лихоманка, біль у суглобах, стомлюваність), і при цьому будуть визначатися антитіла до ДНК, інфліксімаб слід відмінити. Ефективність та безпека застосування інфліксімабу у хворих похилого віку, а також у пацієнтів із захворюваннями печінки та нирок не встановлена. Безпека та ефективність застосування інфліксімабу у дітей та підлітків віком до 17 років з ревматоїдним артритом або хворобою Крона не вивчені. До отримання відповідних даних слід уникати застосування цієї категорії пацієнтів.Умови зберіганняУ холодильнику +2+8 градусівУмови відпустки з аптекЗа рецептомВідео на цю тему
230,00 грн
182,00 грн
Фасовка: N5 Форма выпуска: порошок д/приготовления р-ра д/приема внутрь Упаковка: пак. Производитель: Сотекс Завод-производитель: Вилар Фармцентр(Россия). .
Склад, форма випуску та упаковкаГліцин, екстракт насіння грифонії; екстракт звіробою. допоміжні речовини: желатин; глюкози моногідрат; діоксид кремнію аморфний, магнію стеарат; діоксид титану. Вміст активних речовин у 1 капсулі: Гліцин-300 мг; 5-гідрокситриптофан-160 мг; Гіперицин, щонайменше-0,06 мг.ХарактеристикаНегативні емоції — характерна риса психологічного портрета сучасної людини, нервова система якого важко пристосовується до постійної перевтоми, стресів, надзвичайно високих ритмів повсякденного існування. Поганий настрій, дратівливість, нервові зриви в наші дні стали найпоширенішими явищами, причому боротися з ними «на власні сили» стає все важче. Що може допомогти повернути душевний спокій та втрачену радість буття? Протягом століть із цією метою використовувалися корисні рослини, здатні підвищувати емоційне тло, пробуджувати почуття впевненості у своїх силах, підтримувати позитивний настрій, не завдаючи шкоди організму. Сьогодні відомо, що більший ефект дає їхній прийом у поєднанні з природними амінокислотами, що беруть участь у регуляції вищої нервової діяльності. «Гліцин + звіробій» — комплекс речовин рослинного походження та органічних сполук, що включає екстракт звіробою, а також 5-гідрокситриптофан і гліцин, які сприяють зняттю нервової напруги та втоми, поліпшенню настрою, підвищенню розумової працездатності.Протипоказання до застосуванняІндивідуальна нестерпність компонентів.Спосіб застосування та дозиДорослим, по 1 капсулі 2 десь у день під час їжі. Тривалість прийому – 1-2 місяці. За потреби прийом можна повторити.Запобіжні заходи та особливі вказівкиПеред застосуванням проконсультуйтеся зі спеціалістом.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаГлюкозаміну сульфат, хондроїтину сульфат, МКЦ, кальцію карбонат, стеаринова кислота, гідроксипропілметилцелюлоза, діоксид кремнію, натрію карбоксиметилцелюлоза, гліцерин, карнаубський віск. Таблетки 1400 мг упаковка контурна коміркова.ХарактеристикаСприяє поліпшенню стану при: болях у суглобах та хребті, скутості у рухах та хрускіт у суглобах, запаленні суглобів.Протипоказання до застосуванняІндивідуальна нестерпність компонентів продукту.Вагітність та лактаціяУ період вагітності та грудного вигодовування прийом препарату лише за рекомендацією лікаря.Взаємодія з лікарськими засобамиГлюкозамін посилить дію препаратів тетрациклінової групи для кишківника.Спосіб застосування та дозиДорослим по 1 таблетці на день під час їжі. Тривалість прийому – 2 місяці.Запобіжні заходи та особливі вказівкиПеред застосуванням проконсультуйтеся зі спеціалістом.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаКапсули - 1 капс. Активна речовина: осельтамівір фосфат 98.5 мг, що відповідає вмісту осельтамівіру 75 мг. Допоміжні речовини: кальцію гідрофосфат – 25 мг, крохмаль кукурудзяний прежелатинізований – 46.3 мг, кроскармелоза натрію – 7.2 мг, натрію стеарилфумарат – 1.5 мг, тальк – 1.5 мг. Склад корпусу капсули: желатин – 45.2956 мг, титану діоксид – 0.9244 мг; Склад кришечки капсули: желатин – 29.1077 мг, титану діоксид – 0.3971 мг, барвник хіноліновий жовтий – 0.2739 мг, барвник сонячний захід жовтий – 0.0013 мг. 10 шт. - упаковки осередкові контурні (1) - пачки картонні.Опис лікарської формиКапсули тверді, желатинові №1; кришка жовтого кольору, корпус білого кольору; вміст капсул - суміш гранул і порошку майже білого кольору або спресована маса майже білого кольору, що розсипається при легкому натисканні.Фармакотерапевтична групаПротивірусний засіб. Є проліками, активний метаболіт (осельтамівір карбоксилат) якого селективно пригнічує нейрамінідазу вірусу грипу типів А і В. і проникненню в клітини епітелію дихальних шляхів, запобігаючи інактивації вірусу епітеліальним слизом). Осельтамівір карбоксилат діє поза клітинами і конкурентно пригнічує нейрамінідазу вірусу. Гальмує зростання вірусу грипу in vitro та пригнічує реплікацію вірусу та його патогенність in vivo. Зменшує виділення вірусів грипу А та В з організму. Не впливає на вироблення антитіл у відповідь на інактивовану вакцину проти грипу. Частота резистентності до клінічних ізолятів вірусу становить 2%.ФармакокінетикаПісля прийому внутрішньо практично повністю всмоктується із ШКТ, абсорбція не залежить від їди. Має ефект "першого проходження" через печінку. Під дією кишкових та печінкових естераз перетворюється на активний метаболіт. 75% прийнятої внутрішньо дози потрапляє у системний кровотік у вигляді активного метаболіту, менше 5% – у вигляді вихідної речовини. Плазмові концентрації як проліки, так і активного метаболіту пропорційні дозі. Середній Vd активного метаболіту – 23 л. Зв'язування з білками плазми – 3%. Виводиться у вигляді активного метаболіту переважно нирками шляхом клубочкової фільтрації та канальцевої секреції. T1/2 осельтамівіру - 1-3 год. Осельтамівіру карбоксилат далі не метаболізується і виводиться нирками, його T1/2 - 6-10 год. Нирковий кліренс - 18.8 л/ч. Виводиться через кишечник – менше 20%. У пацієнтів похилого віку (65-78 років) концентрація активного метаболіту в рівноважному стані на 25-35% вища, ніж у молодших пацієнтів. У пацієнтів з нирковою недостатністю швидкість виведення осельтамівіру карбоксилату обернено пропорційна величині КК.Клінічна фармакологіяПротивірусний засіб.Показання до застосуванняГрип типів А та В.Протипоказання до застосуванняХронічна ниркова недостатність (КК менше 10 мл/хв), печінкова недостатність, підвищена чутливість до осельтамівіру.Вагітність та лактаціяЗ обережністю застосовувати при вагітності та в період лактації. Застосування у дітей З обережністю застосовувати у дітей.Побічна діяЗ боку травної системи: нудота, блювання (зазвичай при прийомі у високих дозах або в перші дні лікування); рідко – діарея, біль у животі. З боку центральної нервової системи: безсоння, запаморочення, біль голови. З боку дихальної системи: закладеність носа, біль у горлі, кашель. Інші: почуття втоми, слабкість.Взаємодія з лікарськими засобамиЛікарські засоби, що блокують канальцеву секрецію, у 2-3 рази збільшують концентрацію активного метаболіту (внаслідок гальмування процесу активної канальцевої секреції у нирках), що не потребує корекції дози.Спосіб застосування та дозиПриймають внутрішньо, незалежно від їди. При лікуванні прийом необхідно розпочати не пізніше 2 діб від моменту розвитку симптомів захворювання у дозі 75 мг 2 рази на добу протягом 5 днів. Збільшення дози більше 150 мг на добу не призводить до посилення ефекту. Для профілактики грипу типів А та В дорослим – по 75 мг 1-2 рази на добу протягом 6 тижнів. (Під час епідемії грипу). Максимальна добова доза становить 150 мг для дорослих. У хворих з КК менше 30 мл/хв дозу зменшують до 75 мг 1 раз на добу протягом 5 днів.Запобіжні заходи та особливі вказівкиЗ обережністю застосовувати у дітей. У пацієнтів з печінковою недостатністю безпека та ефективність осельтамівіру не встановлена. Немає даних про безпеку застосування осельтамівіру при КК менше 10 мл/хв.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Активні речовини: Aconitum D3 25мг, Gelsemium D3 25мг, Ipecacuanha D3 25мг, Phosphorus D5 25мг, Bryonia D2 25мг, Eupatorium perfoliatum D1 25мг. Допоміжні речовини: лактози моногідрат, магнію стеарат, крохмаль пшеничний. 20 шт. - блістери (3) - пачки картонні.Опис лікарської формиТаблетки для розсмоктування від білого до біло-жовтого кольору, круглі, плоскі, зі скошеною кромкою.Фармакотерапевтична групаГомеопатичний препарат, який застосовується при застудних захворюваннях. Чинить протизапальну, жарознижувальну, відхаркувальну та муколітичну дію. Сприяє зміцненню імунітету.ФармакокінетикаФармакокінетика препарату Інфлюцид не вивчена.Клінічна фармакологіяГомеопатичний препарат, який застосовується при застудних захворюваннях.Показання до застосуванняПрофілактика та лікування грипу та інших ГРВІ.Протипоказання до застосуванняПідвищена чутливість до компонентів препарату. Не рекомендується призначати препарат у формі таблеток дітям до 3 років (через недостатність клінічних даних).Вагітність та лактаціяЗастосування препарату Інфлюцид при вагітності та в період лактації (грудного вигодовування) можливе лише в тому випадку, коли передбачувана користь для матері перевищує потенційний ризик для плода та дитини. Застосування у дітей Не рекомендується призначати препарат у формі таблеток дітям до 3 років (через недостатність клінічних даних). При гострому захворюванні дітям віком від 3 до 6 років призначають по 1 таб. кожні 2 год (не більше 6 разів на добу) до настання поліпшення, далі - по 1/2 таб. 3 рази на добу до повного одужання. Дітям віком від 6 до 12 років призначають по 1 таб. кожну годину (не більше 7-8 разів на добу) до настання поліпшення, далі - по 1 таб. 3 рази на добу до повного одужання. Дорослим та дітям старше 12 років призначають по 1 таб. щогодини (не більше 12 разів на добу) до настання поліпшення, далі - по 1-2 таб. 3 рази на добу до повного одужання. Для профілактики ГРВІ дітям від 3 до 6 років призначають по 1/2 таб. 2 рази на добу; дітям від 6 до 12 років – по 1 таб. 2 рази на добу; дітям віком від 12 років призначають по 1 таб. 3 рази на добу. Для профілактики ГРВІ препарат у формі розчину для прийому внутрішньо призначають дітям старше 12 років по 10-20 крапель 3 рази на добу.Побічна діяМожливі алергічні реакції.Взаємодія з лікарськими засобамиЛікарська взаємодія препарату Інфлюцид з іншими лікарськими засобами не встановлена.Спосіб застосування та дозиПри гострому захворюванні дітям віком від 3 до 6 років призначають по 1 таб. кожні 2 год (не більше 6 разів на добу) до настання поліпшення, далі - по 1/2 таб. 3 рази на добу до повного одужання. Дітям віком від 6 до 12 років призначають по 1 таб. кожну годину (не більше 7-8 разів на добу) до настання поліпшення, далі - по 1 таб. 3 рази на добу до повного одужання. Дорослим та дітям старше 12 років призначають по 1 таб. щогодини (не більше 12 разів на добу) до настання поліпшення, далі - по 1-2 таб. 3 рази на добу до повного одужання. Препарат у формі розчину для прийому внутрішньо при гострих захворюваннях призначають по 10 крапель щогодини (не більше 12 разів на добу) до настання поліпшення, далі - по 10-20 крапель 3 рази на добу до повного одужання. Для профілактики ГРВІ дітям від 3 до 6 років призначають по 1/2 таб. 2 рази на добу; дітям від 6 до 12 років – по 1 таб. 2 рази на добу; дорослим та дітям старше 12 років призначають по 1 таб. 3 рази на добу. Для профілактики ГРВІ препарат у формі розчину для прийому внутрішньо призначають дорослим та дітям старше 12 років по 10-20 крапель 3 рази на добу. Препарат слід приймати за 30 хв до або через 30 хв після їди. Таблетки слід повільно розсмоктувати у роті. Дітям від 3 до 5 років рекомендується розчиняти таблетку в невеликій кількості рідини або давати у подрібненому вигляді під язик.ПередозуванняВ даний час про випадки передозування інфлюциду не повідомлялося.Запобіжні заходи та особливі вказівкиПри застосуванні інфлюциду можливе тимчасове погіршення стану. В даному випадку пацієнт повинен припинити прийом препарату та проконсультуватися з лікарем. При застосуванні інфлюциду допускається використання інших лікарських засобів. Пацієнт повинен бути поінформований, що у разі відсутності поліпшення при гострому захворюванні через 2 дні препарат слід відмінити та проконсультуватися з лікарем. Прийом препарату Інфлюцид у формі таблеток може негативно впливати на пацієнтів з целіакією та непереносимістю лактози. Таким пацієнтам рекомендується приймати препарат у формі розчину для внутрішнього прийому.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
Фасування: N1 Форма випуску: спрей д/місцевого застосування Упакування: фл. Производитель: Алвилс Патент Завод-производитель: Флори Спрей(Россия) Действующее вещество: Мяты перечной листьев масло + Сульфаниламид + Сульфатиазол + Тимол + Эвкалипта прутовидного листьев. .
Фасування: N1 Форма випуску: аерозоль Діюча речовина: М'яти перцевої листя олія + Сульфаніламід + Сульфатіазол + Тимол + Евкаліпта прутоподібного листя. . .