Лекарства и БАД
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
Склад, форма випуску та упаковкаПігулки - 1 таб. Активні речовини: етилбромізовалеріанат - 8,20 мг, фенобарбітал - 7,50 мг, м'яти перцевого листя олія - 0,58 мг; Допоміжні речовини: бетадекс (бета-циклодекстрин) – 55,55 мг, крохмаль картопляний – 37,57 мг, лактози моногідрат – 83,70 мг, магнію алюмометасилікат – 3,50 мг, тальк – 2,00 мг, магнію стеарат 40 мг.Опис лікарської формиКруглі, плоскоциліндричні таблетки білого або майже білого кольору, з вкрапленнями, фаскою і ризиком.ХарактеристикаКорвалол – комбінований препарат, чинить седативну та спазмолітичну дію, полегшує настання природного сну. Етилбромізовалеріанат має седативну та спазмолітичну дію. Фенобарбітал сприяє зниженню збудження центральної нервової системи (ЦНС) та полегшує настання сну, посилює седативний вплив інших компонентів. Масло м'яти перцевої має рефлекторну вазодилатуючу, спазмолітичну, легку жовчогінну, антисептичну дію. Препарат застосовується як заспокійливий та судинорозширювальний засіб при функціональних розладах серцево-судинної системи, при неврозоподібних станах, при порушенні засипання, тахікардії, стані збудження з вираженими вегетативними проявами; як спазмолітичний засіб - при спазмах кишечника. Випускається у формі пігулок по 10 пігулок у контурну осередкову упаковку. Відпускається без рецепта.Фармакотерапевтична групаседативний засіб.ФармакокінетикаДані по фармакокінетиці етилбромізовалеріянату та компонентів м'яти перцевої відсутні. При внутрішньому прийомі фенобарбітал всмоктується повільно, повністю. Максимальна. концентрація в плазмі визначається через 1-2 год, зв'язок з білками плазми - 50%, у новонароджених - 30-40%. Метаболізується у печінці, індукує мікросомальні ферменти печінки ізоферментами СYР3А4, СYР3А5, СYРЗА7 (швидкість ферментативних реакцій зростає у 10-12 разів). Кумулюється в організмі. Період напіввиведення становить 2-4 дні. Виводиться нирками у вигляді глюкуроніду, близько 25% – у незміненому вигляді. Проникає у грудне молоко та через плацентарний бар'єр.ФармакодинамікаКомбінований препарат, що має седативну та спазмолітичну дію, полегшує настання природного сну. Етилбромізовалеріанат має седативну та спазмолітичну дію, обумовлену подразненням, переважно рецепторів порожнини рота та носоглотки, зниженням рефлекторної збудливості в центральних відділах нервової системи та посиленням гальмування в нейронах кори та підкіркових структурах головного мозку, а також зниженням активності. гладку мускулатуру. Фенобарбітал має седативну (у малих дозах), снодійну, міорелаксуючу та спазмолітичну дію, сприяє зниженню збудження центральної нервової системи (ЦНС) та полегшує настання сну, посилює седативний вплив інших компонентів. М'яти перцевої олії має рефлекторну вазодилатуючу, спазмолітичну, легку жовчогінну, антисептичну дію. Механізм дії пов'язаний із здатністю дратувати «холодові» рецептори слизової оболонки порожнини рота та рефлекторно розширювати переважно судини серця та головного мозку. Усуває явища метеоризму за рахунок подразнення рецепторів слизової оболонки шлунково-кишкового тракту (ШКТ), посилюючи перистальтику кишок.Показання до застосуванняЯк симптоматичний (заспокійливий і судинно-розширювальний) засіб при функціональних розладах серцево-судинної системи, при неврозоподібних станах, що супроводжуються підвищеною дратівливістю, при порушенні засипання, тахікардії, стані збудження з вираженими вегетативними проявами; як спазмолітичний засіб - при спазмах кишечника.Протипоказання до застосуванняПідвищена чутливість до компонентів препарату; тяжкі порушення функції нирок та/або печінки; вагітність; період грудного вигодовування; дитячий вік до 18 років (ефективність та безпека не встановлені); непереносимість галактози; недостатність лактази. З обережністю: Порушення функції печінки та нирок. Якщо у Вас є одне з перелічених захворювань/станів, перед прийомом препарату обов'язково проконсультуйтеся з лікарем.Вагітність та лактаціяЗастосування препарату Корвалол при вагітності протипоказане, оскільки препарат містить фенобарбітал, який проникає через плаценту і має тератогенну дію, негативно впливає на формування та подальше функціонування центральної нервової системи плода та новонародженого; проникає у грудне молоко, можливий розвиток фізичної залежності у новонародженого. За необхідності застосування в період грудного вигодовування слід вирішити питання про припинення годування грудним молоком.Побічна діяСонливість, запаморочення, уповільнення серцевого ритму. зниження здатності до концентрації уваги, алергічні реакції Можуть виникати порушення шлунково-кишкового тракту. Зазначені явища проходять при зниженні дози або припиненні прийому препарату. При тривалому застосуванні препарату можливе виникнення лікарської залежності, звикання, синдрому «скасування», а також накопичення брому в організмі та розвиток явищ бромізму (депресивний настрій, апатія, риніт, кон'юнктивіт, геморагічний діатез, порушення координації рухів). Якщо будь-які вказані в інструкції побічні ефекти посилюються, або Ви помітили будь-які інші побічні ефекти, не вказані в інструкції, повідомте про це лікаря.Взаємодія з лікарськими засобамиЛікарські засоби, що пригнічують ЦНС, посилюють дію препарату. Фенобарбітал (індуктор мікросомального окиснення) може знижувати ефективність лікарських засобів, що метаболізуються в печінці (в т.ч. похідних кумарину, гризеофульвіну, глюкокортикостероїдів, пероральних контрацептивів); посилює дію місцевоанестезуючих, аналгезуючих та снодійних лікарських засобів. Препарат посилює токсичність метотрексату. Дія препарату посилюється на фоні застосування препаратів вальпроєвої кислоти.Спосіб застосування та дозиПриймати внутрішньо, до їди, запивати водою. Дорослим зазвичай призначають по 1-2 таблетки 2 рази на добу. При тахікардії можливе збільшення разової дози до 3 таблеток. Дозування застосування препарату встановлюється індивідуально.ПередозуванняСимптоми: пригнічення центральної нервової системи (ЦНС), ністагм, атаксія, зниження артеріального тиску, збудження, запаморочення, слабкість, хронічна інтоксикація бромом (депресія, апатія, риніт, кон'юнктивіт, геморагічний діатез, порушення координації рухів). Лікування: припинення прийому препарату, промивання шлунка та проведення симптоматичної терапії, при пригніченні ЦНС – кофеїн, нікетамід.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаКраплі - 1 мл: діючі речовини: пустирника трави настойка (пустирника настойка) – 720,00 мг, етилбромізовалеріанат (етиловий ефір альфа-бромізовалеріанової кислоти) – 20,00 мг, м'яти перцевого листя масло (м'яти перцевої олія) – 1,42 мг - 1,00 мг; допоміжні речовини: вода очищена – до 1 мл. Примітка. Для отримання 1000 мл собачої кропиви настойки використовують 200 г собачої кропиви трави і достатню кількість спирту етилового 70%.Опис лікарської формиПрозора рідина зеленувато-коричневого кольору із характерним запахом. У процесі зберігання допускається помутніння та утворення осаду у вигляді частинок та/або пластівців, при струшуванні яких утворюється завись дрібних частинок.ХарактеристикаКорвалол НЕО – комбінований препарат, седативний засіб. Має седативну та спазмолітичну дію, помірну кардіотонічну дію (уповільнює ритм та збільшує силу серцевих скорочень), має помірні гіпотензивні властивості. Корвалол приймають за підвищеної нервової збудливості; як седативний засіб при порушенні сну, не пов'язаного з органічними порушеннями центральної нервової системи; неврастенія. Випускається у формі крапель (флакони по 25, 50 мл) для внутрішнього прийому. Препарат рекомендується приймати до їди, попередньо розчинивши краплі в невеликій кількості (30-40 мл) води. Відпускається без рецепта.Фармакотерапевтична групаседативний засіб.ФармакокінетикаДані по фармакокінетиці етилбромізовалеріянату, трави собачої кропиви і компонентів м'яти перцевої відсутні. Дифенгідрамін Після прийому препарату Корвалол Нео швидко всмоктується з шлунково-кишкового тракту. Зв'язок із білками плазми 98–99 %. Біодоступність дифенгідраміну – 50%. Час досягнення максимальної концентрації (ТСmax) – 1,89 годин (у найбільшій концентрації визначається у легень, селезінці, нирках, печінці, головному мозку та м'язах). Максимальна концентрація (Cmax) – 2,32 нг/мл. Площа під фармакокінетичною кривою AUC0-∞ – 11,75 нг×год/мл. Проникає крізь гематоенцефалічний бар'єр. Здається обсяг розподілу (Vd) - 179 л. Метаболізується головним чином у печінці, частково у легенях та нирках. Константа швидкості елімінації (Kel) – 0,411 год-1. Період напіввиведення (T1/2) – 1,9 години. Протягом доби повністю виводиться нирками як метаболітів, кон'югованих з глюкуроновою кислотою.Істотні кількості виводяться з грудним молоком і можуть викликати седативний ефект у дітей грудного віку (може спостерігатись парадоксальна реакція, що характеризується надмірною збудливістю).ФармакодинамікаКомбінований препарат, дія якого обумовлена властивостями речовин, що входять до нього. Має седативну та спазмолітичну дію, помірну кардіотонічну дію (уповільнює ритм та збільшує силу серцевих скорочень), має помірні гіпотензивні властивості. Етилбромізовалеріанат Етилбромізовалеріанат має седативну та спазмолітичну дію, обумовлену подразненням, переважно рецепторів порожнини рота та носоглотки, зниженням рефлекторної збудливості в центральних відділах нервової системи та посиленням гальмування в нейронах кори та підкіркових структурах головного мозку, а також зниженням активності. гладку мускулатуру. За характером дії близький до препаратів валеріани. Трава собачої кропиви Трава собачої кропивки надає виражену седативну дію (заспокійливу), помірно знижує частоту і збільшує силу серцевих скорочень, виявляє помірні гіпотензивні властивості. М'яти перцевої олії М'яти перцевої олії має рефлекторну вазодилатуючу, спазмолітичну, легку жовчогінну, антисептичну дію. Механізм дії пов'язаний із здатністю дратувати «холодові» рецептори слизової оболонки порожнини рота та рефлекторно розширювати переважно судини серця та головного мозку. Усуває явища метеоризму за рахунок подразнення рецепторів слизової оболонки шлунково-кишкового тракту (ШКТ), посилюючи перистальтику кишок. Дифенгідрамін Дифенгідрамін є блокатором Н1-гістамінових рецепторів першого покоління. Дія на центральну систему обумовлена блокадою Н1-гістамінових рецепторів м-холінорецепторів головного мозку. Зменшує або попереджає спазми гладкої мускулатури, що викликаються гістаміном, підвищення проникності капілярів, набряк тканин, свербіж і гіперемію, має протиблювотні, седативні ефекти, має снодійну дію. Антагонізм з гістаміном проявляється більшою мірою по відношенню до місцевих судинних реакцій, ніж до системних, тобто зниження артеріального тиску.Показання до застосуванняПідвищена нервова збудливість; як седативний засіб при порушенні сну, не пов'язаного з органічними порушеннями центральної нервової системи; неврастенія.Протипоказання до застосуванняПідвищена чутливість до компонентів препарату; тяжкі порушення функції нирок та/або печінки; закритокутова глаукома; гіперплазія передміхурової залози; стеноз шийки сечового міхура; бронхіальна астма; епілепсія; вагітність; період лактації (грудного вигодовування); дитячий вік до 18 років (ефективність та безпека не встановлені); порфірія; пилородуоденальний стеноз; ерозивно-виразкові ураження шлунково-кишкового тракту (у фазі загострення); стенозуюча виразкова хвороба шлунка та дванадцятипалої кишки. З обережністю Препарат слід приймати з обережністю при наступних захворюваннях/станах: захворювання печінки, порушення функції нирок, глаукома, затримка сечі, бронхіт, хронічна обструктивна хвороба легень. При тривалому застосуванні можливий розвиток резистентності. Препарат може посилювати дію алкоголю, тому приймання алкоголю під час лікування слід виключити. Слід уникати застосування у поєднанні з іншими препаратами, що мають антигістамінну дію, включаючи місцеві лікарські препарати, засоби від кашлю та застуди. Побічні дії частіше розвиваються у пацієнтів похилого віку. Слід уникати застосування літніми пацієнтами зі сплутаною свідомістю. Дифенгідрамін може посилити дзвін у вухах. Корвалол Нео містить у своєму складі етиловий спирт (див. розділ «Особливі вказівки»), тому препарат повинен застосовуватися з обережністю при алкоголізмі, а також у пацієнтів із групи високого ризику, у тому числі із захворюваннями печінки, черепно-мозковими травмами, захворюваннями головного. мозку. Якщо у Вас є одне з перелічених захворювань/станів, перед прийомом препарату обов'язково проконсультуйтеся з лікарем.Вагітність та лактаціяВагітність Дифенгідрамін здатний проникати через плаценту; описані випадки жовтяниці та екстра-пірамідних розладів у дітей, народжених жінками, які приймали під час вагітності дифенгідрамін. Прийом дифенгідраміну в третьому триместрі може призвести до несприятливих реакцій у новонародженого або передчасних пологів. Безпека Корвалолу Нео при вагітності не встановлена і його застосування в цей період протипоказане. Період грудного вигодовування Застосування дифенгідраміну в період грудного вигодовування може стати причиною підвищеного збудження та дратівливості дитини. За необхідності застосування препарату Корвалол Нео в період годування груддю слід вирішувати питання про припинення грудного вигодовування.Побічна діяПорушення з боку крові та лімфатичної системи: гемолітична анемія, тромбоцитопенія, агранулоцитоз. Порушення з боку імунної системи: алергічні реакції, включаючи висипання, кропив'янку, утруднене дихання, набряк Квінке. Порушення з боку шкіри та підшкірних тканин: фоточутливість. Психічні порушення: сплутаність свідомості, парадоксальне збудження (особливо схильні до пацієнтів похилого віку); у деяких випадках дратівливість, ейфорія. Порушення з боку нервової системи: сонливість, слабкість, зниження швидкості психомоторних реакцій, порушення координації та швидкості реакції, почуття втоми, запаморочення, зниження здатності до концентрації уваги, нестійкість, судоми, головний біль, парестезії, дискінезії; у деяких випадках безсоння, тремор. Порушення органу зору: нечітке зір. Порушення з боку органу слуху та лабіринту: дзвін у вухах. Порушення серцево-судинної системи: зниження артеріального тиску, уповільнення серцевого ритму, тахікардія, екстрасистолія. Порушення з боку дихальної системи, органів грудної клітки та середостіння: сухість слизової оболонки порожнини носа, бронхів (згущення бронхіального секрету). З боку шлунково-кишкового тракту: сухість у роті, диспепсія, нудота, блювання, дискомфорт в епігастральній ділянці, анорексія. Порушення з боку м'язової, скелетної та сполучної тканини: посмикування м'язів. Порушення з боку нирок та сечовивідних шляхів: утруднене сечовипускання, затримка сечі. Зазначені явища проходять при зниженні дози або припиненні прийому препарату. При тривалому застосуванні високих доз препарату можливий розвиток лікарської залежності, а також накопичення брому в організмі та розвиток бромізму, проявами якого бувають: депресивний настрій, апатія, риніт, кон'юнктивіт, геморагічний діатез, порушення координації рухів. Якщо будь-які з вказаних в інструкції побічних ефектів посилюються, або Ви помітили будь-які інші побічні ефекти, які не вказані в інструкції, повідомте про це лікаря.Взаємодія з лікарськими засобамиПри одночасному застосуванні лікарського препарату Корвалол Нео з етанолом і препаратами, що пригнічують діяльність центральної нервової системи (седативні, снодійні, нейролептики, транквілізатори, трициклічні антидепресанти) можливе взаємне посилення ефектів. Інгібітори моноаміноксидази (МАО) збільшують вираженість і тривалість антихолінергічних ефектів дифенгідраміну. Корвалол Нео слід приймати разом з інгібіторами МАО з обережністю або через 2 тижні після їх відміни. Дифенгідрамін може посилювати антихолінергічні ефекти інших препаратів (атропіну, трициклічних антидепресантів). Антагоністична взаємодія відзначається при спільному призначенні із психостимуляторами. Дифенгідрамін є інгібітором ізоферменту CYP2D6 цитохрому Р450. Таким чином, Корвалол Нео потенційно може взаємодіяти з лікарськими препаратами, первинний метаболізм яких здійснюється CYP2D6. Корвалол Нео посилює дію спазмолітичних, аналгетичних засобів. Алкоголь посилює ефект препарату та його токсичність. Знижує ефективність апоморфіну як блювотного засобу при лікуванні отруєння. У разі прийому одного з перерахованих препаратів перед початком застосування Корвалолу Нео необхідно проконсультуватися з лікарем.Спосіб застосування та дозиПриймати внутрішньо, до їди, 3 рази на день по 30 крапель, попередньо розчинивши в невеликій кількості (30-40 мл) води. Перед вживанням збовтати флакон. Курс лікування 10-15 днів. За рекомендацією лікаря може бути проведений повторний курс лікування, але не раніше ніж за 1 місяць.ПередозуванняПередозування можливе при частому та тривалому застосуванні препарату. При перевищенні доз, що рекомендуються, можливе посилення дозозалежних побічних ефектів. Симптоми: Пригнічення функцій центральної нервової системи, збудження або депресії, розширення зіниць, сухість у роті, парез органів шлунково-кишкового тракту, лихоманка, припливи, тремор, дистонічні реакції, галюцинації та зміни на ЕКГ. Значне передозування може спричинити рабдоміоліз, судоми, марення, токсичний психоз, аритмії, кому та серцево-судинну недостатність. Лікування при передозуванні: Спеціального антидоту немає. Промивання шлунка. При необхідності – симптоматичне лікування: препарати, що підвищують артеріальний тиск, кисень, внутрішньовенне введення рідин, що плазмозамінюють. Не можна використовувати епінефрін та аналептики. При появі симптомів передозування необхідно припинити прийом препарату Корвалол Нео та негайно звернутися до лікаря.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
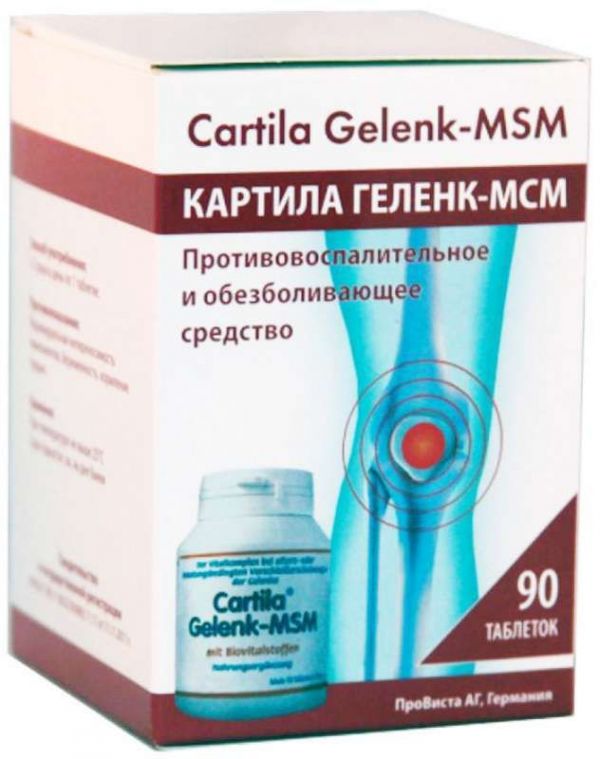
Склад, форма випуску та упаковкаМетилсульфонілметан, вітамін С, екстракт коріння лопуха великого, екстракт коріння кульбаби лікарської, екстракт трави хвоща польового, цитрусові біофлавоноїди, МКЦ (Е460), крохмаль, гліцерин (Е422), діоксид кремнію (Е551).ХарактеристикаБАД «Картила Геленк-МСМ» – це препарат на основі органічної сірки (метилсульфонілметан, ЧСЧ), яка видобувається з морських водоростей, від німецької фармацевтичної компанії ProVista AG. ЧСЧ має давно відому потужну протизапальну і знеболювальну дію. Для посилення цих цінних властивостей препарат збагачений натуральними екстрактами трав, цитрусовими біофлавоноїдами та вітаміном С. Cartila Gelenk-MSM допомагає зняти біль та зупинити запальний процес при захворюваннях суглобів, м'язів та зв'язок, хребта, а також у наступних випадках: прискорює одужання після травм (переломи, розтягування, розриви зв'язок); є активним антиоксидантом, виводить з організму токсини та шлаки (може успішно застосовуватись у програмах зниження ваги); зміцнює волосся та нігті, очищає та відновлює шкіру; допомагає у боротьбі з алергією, сприяє покращенню кровообігу; зміцнює та оздоровлює слизову оболонку тканини шлунково-кишкового тракту.Властивості компонентівКартила Геленк - ЧСЧ містить екстракти трав, що сприяють посиленню протизапальних властивостей органічного середовища, а вітамін С є додатковим антиоксидантом. Цитрусові біофлавоноїди сприяють ефективному впливу вітамінів С на організм, забезпечують повніше його засвоєння. Вони захищають організм від дії вільних радикалів, зміцнюють кровоносні судини, підвищують їхню еластичність і діють синергетично з іншими компонентами препарату (ніби допомагаючи, посилюючи їх вплив).РекомендуєтьсяЗавдяки ретельно вивіреному поєднанню компонентів, препарат рекомендується для регенерації та відновлення тканин при руйнівних запальних процесах: ЧСЧ ефективно знімає практично будь-яке запалення та зменшує біль при захворюваннях опорно-рухового апарату; ЧСЧ нейтралізує дію токсинів та прискорює їх виведення з організму; ЧСЧ підвищує фізичну витривалість та зменшує м'язові болі після занять спортом; ЧСЧ прискорює загоєння ран та опіків, ЧСЧ покращує стан шкіри, допомагає зберегти її гладкою та молодою ЧСЧ ефективно зміцнює волосся та нігті ЧСЧ є сильним антиоксдантом; ЧСЧ посилює дію вітамінів та інших поживних речовин.Протипоказання до застосуванняІндивідуальна непереносимість компонентів БАД, вагітність, годування груддю. Перед застосуванням рекомендується проконсультуватися з лікарем.Побічна діяМаючи корисні властивості, Картіла Геленк - ЧСЧ не має шкідливих побічних дій, так як до його складу входять натуральні компоненти.Спосіб застосування та дозиДорослим по 1-2 таблетки на день під час їжі. Тривалість прийому – від 1 до 3 місяців. 1-2 таблетки на день перед сніданком, протягом трьох місяців.Запобіжні заходи та особливі вказівкиБіологічно активна добавка до їжі. Чи не є лікарським засобом. Перед застосуванням рекомендується проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
6 269,00 грн
248,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептом. . .
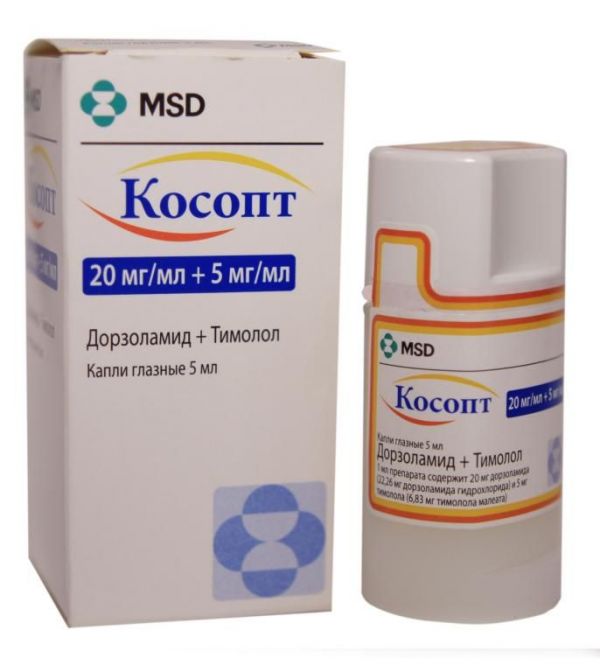
Склад, форма випуску та упаковкаКраплі очні - 1 мл: Активні речовини: дорзоламід гідрохлорид – 22.26 мг, що відповідає вмісту дорзоламіду основи – 20 мг; тимололу малеат – 6.83 мг, що відповідає вмісту тимололу основи – 5 мг; Допоміжні речовини: бензалконію хлорид (у вигляді 50% розчину бензалконію хлориду) - 0.075 мг (0.15 мг), натрію цитрат - 2.94 мг, манітол - 16 мг, гіетелоза (гідроксіетилцелюлоза) - 4. , вода д/і – qs до 1 мл. 5 мл – флакони пластикові типу "Окуметер Плюс" (1) - пачки картонні.Опис лікарської формиКраплі очні у вигляді прозорої, безбарвної або майже безбарвної, злегка в'язкої рідини.Фармакотерапевтична групаПротиглаукомний засіб для місцевого застосування (інгібітор карбоангідрази+бета-адреноблокатор).ФармакокінетикаДорзоламіду гідрохлорид Всмоктування та розподіл При місцевому застосуванні дорзоламід проникає у системний кровотік. При тривалому застосуванні дорзоламід накопичується в еритроцитах внаслідок селективного зв'язування з карбоангідразою ІІ типу, підтримуючи надзвичайно низькі концентрації вільного препарату у плазмі. Близько 33% дорзоламіду пов'язують із білками плазми крові. Метаболізм та виведення В результаті метаболізму дорзоламіду утворюється єдиний N-дезетильний метаболіт, який менш виражено блокує карбоангідразу II типу порівняно з початковою його формою, проте в той же час інгібує карбоангідразу типу I менш активний ізоензим. Метаболіт також накопичується в еритроцитах, де зв'язується головним чином з карбоангідразою І типу. Дорзоламід виводиться із сечею у незміненому вигляді та у вигляді метаболіту. Після припинення застосування препарату дорзоламід нелінійно вимивається з еритроцитів, що спочатку призводить до швидкого зниження концентрації, а потім елімінація сповільнюється. Т1/2 становить близько 4 місяців. При прийомі дорзоламіду внутрішньо, з метою моделювання максимальної системної дії під час його місцевого застосування, стабільного стану вдалося досягти через 13 тижнів. При цьому в плазмі фактично не виявили вільного препарату або його метаболітів. Інгібування карбоангідрази еритроцитів було недостатнім для того, щоб досягти фармакологічного ефекту на функцію нирок та дихання. Такі фармакокінетичні результати спостерігалися при тривалому місцевому застосуванні дорзоламіду гідрохлориду. Тим не менш, у деяких пацієнтів з нирковою недостатністю (КК 30-60 мл/хв) були виявлені більш високі концентрації метаболіту в еритроцитах, однак це не мало клінічного значення. Тимолола малеат При місцевому застосуванні тимололу малеат проникає у системний кровотік. Концентрація тимололу в плазмі вивчалася у 6 пацієнтів при місцевому застосуванні очних крапель тимололу малеату 0.5% 2 рази на добу. Середня Cmax після ранкової дози склала 0.46 нг/мл, після денної дози – 0.35 нг/мл. Гіпотензивний ефект настає через 20 хв після інстиляції, досягає максимуму через 2 години і триває щонайменше 24 год.ФармакодинамікаПротиглаукомний препарат комбінованого складу. Містить два активні компоненти: дорзоламіду гідрохлорид та тимололу малеат, кожен з яких зменшує підвищений внутрішньоочний тиск за рахунок зниження секреції внутрішньоочної рідини. Спільна дія цих речовин у складі препарату призводить до більш вираженого зниження внутрішньоочного тиску. Дорзоламід гідрохлорид є селективним інгібітором карбоангідрази II типу. Інгібування карбоангідрази циліарного тіла призводить до зниження секреції внутрішньоочного рідини, імовірно за рахунок зменшення утворення бікарбонатних іонів, що у свою чергу призводить до уповільнення транспорту натрію та рідини. Тимолола малеат є неселективним бета-адреноблокатором. Хоча точний механізм дії тимололу малеату у зниженні внутрішньоочного тиску досі не встановлено, ряд досліджень показали переважне зниження освіти, а також незначне посилення відтоку рідини.Показання до застосуванняПідвищений внутрішньоочний тиск: при відкритокутовій глаукомі; при псевдоексфоліативних глаукомі при недостатній ефективності монотерапії.Протипоказання до застосуваннягіперреактивність дихальних шляхів; бронхіальна астма (зокрема в анамнезі); важка ХОЗЛ; синусова брадикардія; СССУ; AV-блокада II та III ступеня без кардіостимулятора; виражена серцева недостатність; кардіогенний шок; ниркова недостатність тяжкого ступеня (КК гіперхлоремічний ацидоз; дистрофічні процеси у рогівці; вагітність; період лактації (грудного вигодовування); дитячий та підлітковий вік до 18 років (у зв'язку з недостатньою вивченістю ефективності та безпеки); - підвищена чутливість до компонентів препарату.Вагітність та лактаціяНе слід приймати Косопт у період вагітності та грудного вигодовування. Дорзоламід Інформації щодо застосування дорзоламіду у вагітних жінок недостатньо. Невідомо, чи проникає дорзоламід у грудне молоко жінок, що годують. У дослідженнях на щурах виявлено тератогенну дію дорзоломіду у дозах, токсичних для вагітних самок. У дитинчат лактуючих самок щурів, які отримували дорзоламід, виявлено зменшення приросту маси тіла. Тимолол Інформації щодо застосування тимололу у вагітних жінок недостатньо. Тимолол слід приймати під час вагітності, крім випадків, коли застосування тимололу є життєво необхідним. В епідеміологічних дослідженнях не виявлено впливу пероральних бета-адреноблокаторів на розвиток вроджених вад, але виявлено ризик затримки внутрішньоутробного зростання. Крім того, у новонароджених були виявлені ознаки та симптоми блокади β-адренорецепторів (брадикардія, гіпотензія, дихальна недостатність та гіпоглікемія) у разі, коли бета-адреноблокатори застосовувалися до пологів. Якщо препарат застосовувався до пологів, слід ретельно спостерігати стан новонароджених у перші дні життя. Бета-адреноблокатори проникають у грудне молоко. Лікар повинен приймати рішення про необхідність припинення грудного вигодовування або припинення прийому препарату, враховуючи потенційні серйозні побічні ефекти щодо дитини, яка перебуває на грудному вигодовуванні, та користь препарату для матері. Протипоказаний у дитячому та підлітковому віці до 18 років.Побічна діяКосопт загалом добре переноситься. У клінічних дослідженнях побічних ефектів, властивих виключно цього комбінованого препарату, не спостерігалося. Побічні реакції обмежувалися вже відомими побічними ефектами дорзоламіду гідрохлориду та/або тимололу малеату. У цілому нині системні побічні ефекти були слабко виражені і спричиняли скасування препарату. У клінічних дослідженнях Косопт призначався 1035 пацієнтам. Приблизно у 2.4% пацієнтів препарат було відмінено у зв'язку з місцевими побічними реакціями з боку ока. Приблизно 1.2% пацієнтів препарат було відмінено через місцеві побічні алергічні реакції. Найчастіше спостерігалися побічні ефекти з боку органу зору: відчуття печіння або сверблячки в оці, спотворення смаку, ерозії рогівки, ін'єкції кон'юнктиви, нечіткість зору, сльозотеча. У післяреєстраційний період спостереження відзначалися такі небажані явища: задишка, дихальна недостатність, контактний дерматит, брадикардія, AV-блокада, відшарування хсудинної оболонки ока, нудота, синдром Стівенса-Джонсона та токсичний епідермальний некроліз. Зареєстровані випадки набряку та незворотного руйнування рогівки у пацієнтів з хронічними дефектами рогівки та/або перенесли внутрішньоочну хірургічну операцію. Нижче наведено можливі побічні ефекти компонентів препарату. Дорзоламіду гідрохлорид З боку органу зору: запалення віку, подразнення та лущення віку, іридоцикліт, точковий кератит, транзиторна міопія (що проходить після відміни препарату). З боку нервової системи: біль голови, запаморочення, парестезії. Алергічні реакції: ангіоневротичний набряк, бронхоспазм, свербіж, кропив'янка. Інші: астенія/втома, носова кровотеча, подразнення глотки, сухість у роті, висипання. Тимолола малеат (місцеве застосування) Порушення з боку органу зору: кон'юнктивіт, блефарит, кератит, зниження чутливості рогівки, сухість; розлади зору, що включають зміни заломлюючої здібності ока (у ряді випадків через скасування міотиків), диплопія, птоз. Серцево-судинна система: аритмія, гіпотензія, непритомність, серцево-судинні порушення, порушення ритму, зупинка серця, набряки, парестезії, феномен Рейно. З боку дихальної системи: бронхоспазм (переважно у пацієнтів із попередньою бронхообструктивною патологією), кашель. Дерматологічні реакції: алопеція, псоріазоподібні висипання або загострення псоріазу. Алергічні реакції: анафілаксія, ангіоневротичний набряк, кропив'янка, локальні або генералізовані висипи. З боку нервової системи: біль голови, запаморочення; парестезія, депресія, безсоння, кошмарні сновидіння, зниження пам'яті, наростання симптомів міастенії. З боку травної системи: діарея, диспепсія, сухість у роті. Інші: дзвін у вухах, астенія, втома, біль у грудях, біль у животі, зниження лібідо, хвороба Пейроні, сексуальна дисфункція, системний червоний вовчак, міалгія, кульгавість, зниження температури рук та ніг, набряки. Тимолола малеат (системне застосування) Серцево-судинна система: AV-блокада II і III ступеня, синоаурикулярна блокада, погіршення артеріальної недостатності, погіршення стенокардії, вазодилатація. З боку обміну речовин: гіперглікемія, гіпоглікемія. З боку нервової системи: запаморочення, зниження концентрації уваги, підвищена сонливість. Дерматологічні реакції: свербіж шкіри, підвищений потовиділення, ексфоліативний дерматит. Інші: біль у кінцівках, зниження толерантності до фізичних навантажень, набряк легень, блювання, артралгія, слабкість, нетромбоцитопенічна пурпура, хрипи, імпотенція, порушення сечовипускання. При системному застосуванні тимололу малеату клінічно значущі зміни стандартних лабораторних показників відзначалися дуже рідко. Описано незначне підвищення залишкового азоту, калію, сечової кислоти та тригліцеридів плазми крові; незначне зниження гемоглобіну, гематокриту, холестерину ліпопротеїнів високої щільності (Хс-ЛПВЩ), проте зазначені зміни не прогресували та клінічно не виявлялися. Застосування бета-адреноблокаторів може спричинити загострення псевдопаралітичної міастенії.Взаємодія з лікарськими засобамиСпецифічних досліджень щодо взаємодії препарату Косопт з іншими лікарськими засобами не проводилося. Тим не менш, існує можливість посилення гіпотензивного ефекту та/або вираженої брадикардії при сумісному застосуванні очних крапель тимололу малеату та системних блокаторів кальцієвих каналів, катехоламін-виснажувальних засобів, бета-адреноблокаторів, антиаритмічних засобів (включаючи аміодароніком, та інгібіторів МАО. При сумісному застосуванні тимололу та інгібіторів ізоферменту CYP2D6 (наприклад, хінідин або селективні інгібітори зворотного захоплення серотоніну) повідомлялося про потенційований ефект системної блокади β-адренорецепторів (наприклад, зниження ЧСС, депресія). Внаслідок цього можливість подібної взаємодії необхідно брати до уваги у пацієнтів, які отримують Косопт. Системні бета-адреноблокатори можуть посилювати гіпоглікемічний ефект протидіабетичних препаратів та гіпертензію, що є ефектом відміни клонідину (клофеліну). Незважаючи на те, що при монотерапії препаратом Косопт ефект на зіницю мінімальний або відсутній, існують поодинокі описи розвитку мідріазу при сумісному застосуванні тимололу малеату та адреналіну. Існує ймовірність посилення відомих системних ефектів інгібування карбоангідрази при комбінованому застосуванні місцевих та системних інгібіторів карбоангідрази. Т.к. дані про застосування подібної комбінації відсутні, спільне застосування препарату Косопт та системних інгібіторів карбоангідрази не рекомендується.Спосіб застосування та дозиКосопт призначають по 1 краплі в кон'юнктивальний мішок ураженого ока (або обох очей) 2 рази на добу. Якщо Косопт призначають як заміну іншого офтальмологічного препарату для лікування глаукоми, останній слід відмінити за день до початку терапії Косоптом. У разі спільного використання з іншим місцевим офтальмологічним препаратом Косопт слід застосовувати з інтервалом не менше 10 хв. При нососльозній оклюзії (закриванні повік) на 2 хв після закапування препарату відбувається зниження його системної абсорбції, що може призвести до посилення місцевої дії. Косопт є стерильний розчин, тому пацієнти повинні бути проінструктовані, як правильно користуватися флаконом. Перед першим використанням препарату необхідно впевнитись, що захисна смужка зовні флакона не пошкоджена. У нерозкритих флаконів може бути проміжок між флаконом і ковпачком. Слід видалити захисну смужку, щоб відкрити ковпачок. Щоб відкрити флакон, необхідно відкрутити ковпачок, повертаючи його у напрямку вказівних стрілок на верхній поверхні ковпачка. Нахилити голову назад і злегка відтягнути нижню повіку вниз для появи простору між віком та оком. Перевернути флакон великим або вказівним пальцем злегка натиснути в місці спеціально позначеному на флаконі так, щоб одна крапля потрапила в око. Не можна торкатися поверхні ока або століття наконечником флакона. При неправильному використанні флакон може інфікуватися і стати причиною серйозних інфекційних ушкоджень ока та подальшої втрати зору. Після закапування препарату слід закрити очі та натиснути пальцем на внутрішній кут ока, притискаючи його до перенісся протягом 2 хв. Це сприяє утриманню препарату у вічі. Повторити пункти 4 та 5 для іншого ока, якщо це необхідно. Закрити флакон ковпачком, закрутивши його до щільного зіткнення з флаконом. При правильному закритті стрілка на ковпачку флакона повинна збігтися зі стрілкою на етикетці флакона. Не слід закручувати ковпачок занадто сильно, інакше можна пошкодити флакон або ковпачок. Не слід збільшувати отвір спеціально розробленого дозаторного наконечника.ПередозуванняДані щодо випадкового або навмисного передозування препарату Косопт відсутні. Симптоми: описані випадки ненавмисного передозування очних крапель, що містять тимололу малеат, з розвитком системних ефектів передозування бета-адреноблокаторів, які приймаються внутрішньо: запаморочення, головний біль, задишка, брадикардія, бронхоспазм, зупинка серця. Найбільш очікуваними симптомами передозування дорзоламіду є порушення електролітного балансу, розвиток ацидозу, можливі побічні ефекти ЦНС. Лікування: проведення симптоматичної та підтримуючої терапії. Слід контролювати рівень електролітів (насамперед калію) та рН плазми крові. Тимолол не видаляється при діалізі.Запобіжні заходи та особливі вказівкиЯк і інші офтальмологічні препарати, які використовуються місцево, Косопт може абсорбуватися у системний кровотік. Оскільки тимолол, що входить до складу препарату, є бета-адреноблокатором, побічні реакції, що розвиваються при системному застосуванні бета-адреноблокаторів, можуть відзначатися при місцевому застосуванні препарату. При появі перших ознак або симптомів серцевої недостатності застосування препарату Косопт слід припинити. Реакції з боку серцево-судинної та дихальної системи Пацієнти з серцево-судинними захворюваннями в анамнезі, включаючи серцеву недостатність, повинні перебувати під ретельним наглядом щодо появи ознак погіршення цих захворювань. У таких пацієнтів слід контролювати пульс. Пацієнтам із блокадою серця І ступеня слід призначати бета-адреноблокатори з обережністю внаслідок їхньої здатності уповільнювати проведення імпульсу. Зареєстровані повідомлення про випадки бронхоспазму з летальним кінцем у пацієнтів з бронхіальною астмою та випадки серцевої недостатності з летальним кінцем на фоні застосування очних крапель тимололу малеату. Пацієнтам з ХОЗЛ легкого та середнього ступеня тяжкості препарат Косопт слід призначати з обережністю і лише у випадку, якщо передбачувана користь від лікування перевищує потенційний ризик. Препарат слід обережно призначати пацієнтам з тяжкими порушеннями периферичного кровообігу (важкі форми хвороби Рейно або синдрому Рейно). Гіпоглікемія у пацієнтів із цукровим діабетом Бета-адреноблокатори повинні призначатися з обережністю пацієнтам, схильним до спонтанної гіпоглікемії або пацієнтам з цукровим діабетом (особливо лабільним перебігом цукрового діабету), на фоні прийому інсуліну або пероральних гіпоглікемічних препаратів. Бета-адреноблокатори можуть маскувати ознаки та симптоми гострої гіпоглікемії. Тиреотоксикоз Бета-адреноблокатори можуть маскувати деякі клінічні ознаки гіпертиреозу (наприклад, тахікардію). При підозрі на розвиток тиреотоксикозу пацієнти повинні перебувати під ретельним наглядом. Необхідно уникати різкого скасування бета-адреноблокаторів через ризик розвитку тиреотоксичного кризу. Анестезія у хірургії Необхідність відміни бета-адреноблокаторів у разі подальшого широкого оперативного втручання не доведена. При необхідності під час операції ефекти бета-адреноблокаторів можна усунути шляхом застосування достатніх доз адреноміметиків. Порушення функції печінки Не проводилося досліджень щодо застосування препарату Косопт у пацієнтів з печінковою недостатністю, у зв'язку з чим препарат у таких пацієнтів повинен застосовуватися з обережністю. Алергія та гіперчутливість Як і інші офтальмологічні препарати для місцевого застосування, Косопт може проникати у системний кровотік. Дороголамід, що входить до складу препарату, є сульфаніламідом. Таким чином, побічні реакції, виявлені при системному застосуванні сульфаніламідів, можуть спостерігатися при місцевому застосуванні препарату (синдром Стівенса-Джонсона та токсичний епідермальний некроліз). При появі ознак серйозних реакцій гіперчутливості препарат слід припинити. При лікуванні бета-адреноблокаторами у пацієнтів з атопією або тяжкими анафілактичними реакціями на різні алергени в анамнезі можливе посилення відповіді при повторному контакті з цими алергенами. У цій групі пацієнтів прийом епінефрину в стандартній терапевтичній дозі, що застосовується для усунення алергічних реакцій, може виявитися неефективним. Супутня терапія При використанні препарату Косопт пацієнтами, які приймають системні бета-адреноблокатори, необхідно враховувати можливе взаємне посилення фармакологічної дії препаратів як щодо відомих системних ефектів бета-адреноблокаторів, так і щодо зниження внутрішньоочного тиску. Спільне застосування препарату Косопт з іншими бета-адреноблокаторами не рекомендується. Припинення лікування При необхідності відміни місцевого застосування тимололу, як і у випадку із системними бета-адреноблокаторами, припинення терапії у пацієнтів з ІХС слід проводити поступово. Порушення з боку рогівки Бета-адреноблокатори, що застосовуються в офтальмології, можуть викликати сухість ока. Пацієнтам із порушеннями з боку рогівки препарат повинен призначатися з обережністю. Пацієнти з низькою кількістю ендотеліальних клітин мають підвищений ризик розвитку набряку рогівки. Мочекам'яна хвороба Застосування системних інгібіторів карбоангідрази може призводити до порушення кислотно-лужної рівноваги та супроводжуватися уролітіазом, особливо у пацієнтів із сечокам'яною хворобою в анамнезі. Під час застосування препарату Косопт подібних порушень не спостерігалося, повідомлення про уролітіаз були рідкісними. Т.к. до складу препарату Косопт входить інгібітор карбоангідрази, який при місцевому застосуванні може абсорбуватися та проникати у системний кровотік, при лікуванні препаратом ризик розвитку уролітіазу у пацієнтів із сечокам'яною хворобою в анамнезі може підвищуватися. Різне Пацієнтам із гострою закритокутовою глаукомою крім призначення засобів, що знижують внутрішньоочний тиск, потрібне проведення інших терапевтичних заходів. Дослідження дії препарату Косопт у пацієнтів із гострою глаукомою не проводилися. Застосування в осіб похилого віку 49% пацієнтів у клінічних дослідженнях препарату Косопт були у віці 65 років та старші, 13% пацієнтів – у віці 75 років та старші. Різниці в ефективності та безпеці препарату в цих вікових групах порівняно з молодшими пацієнтами не було. Тим не менш, не слід виключати можливості більш високої чутливості до препарату у деяких пацієнтів похилого віку. Використання контактних лінз До складу препарату Косопт входить консервант бензалконію хлорид, який може бути причиною роздратування очей. Перед застосуванням препарату лінзи необхідно вийняти і знову встановити не раніше ніж через 15 хв після закапування препарату. Бензалконію хлорид здатний знебарвлювати м'які контактні лінзи. Вплив на здатність до керування автотранспортом та управління механізмами При використанні препарату Косопт можливий розвиток побічних ефектів, які у деяких пацієнтів можуть ускладнювати керування автомобілем або працювати зі складними механізмами.Умови відпустки з аптекЗа рецептомВідео на цю тему
332,00 грн
202,00 грн
Склад, форма випуску та упаковкаПігулки - 1 таб. Активні речовини: еторикоксиб – 120 мг; Допоміжні речовини: кальцію гідрофосфат безводний – 52 мг, целюлоза мікрокристалічна – 51 мг, повідон К30 – 12 мг, магнію стеарат – 2 мг, кроскармелоза натрію – 3 мг; Склад оболонки таблетки: Опадрай II зелений 32К510003 - 3 мг: гіпромелоза 15 cPs 3.2 мг, лактози моногідрат 2.24 мг, титану діоксид 1.776 мг, тріацетин 0.64 мг, індигокармін алюмінієвий 0 0 0.0. Таблетки, покриті плівковою оболонкою, 30 мг, 60 мг, 90 мг та 120 мг. По 7 пігулок в Аl/Аl блістер. По 1 блістеру разом з інструкцією із застосування в картонну пачку. По 10 пігулок в Аl/Аl блістер. По 1, 2, 3, 5, 6, 9, 10 блістерів разом з інструкцією із застосування в картонну пачку. По 14 пігулок в Аl/Аl блістер. По 1,2, 4, 6, 7 блістерів разом із інструкцією із застосування в картонну пачку.Опис лікарської формиТаблетки, покриті плівковою оболонкою світло-зеленого кольору, круглі, двоопуклі.Фармакотерапевтична групаНестероїдні протизапальні препарати (НПЗЗ).ФармакокінетикаВсмоктування Эторикоксиб швидко всмоктується прийому внутрішньо. Абсолютна біодоступність прийому внутрішньо становить близько 100%. При застосуванні препарату у дорослих натще в дозі 120 мг один раз на день до досягнення рівноважного стану максимальна концентрація в плазмі (Сmах) становить 3,6 мкг/мл. Час досягнення Сmах (Тmах) становить приблизно 1 годину після прийому препарату. Середня геометрична площа під кривою "концентрація – час" (AUC0-24ч) склала 37,8 мкг * год / мл. Фармакокінетика эторикоксиба в діапазоні терапевтичних доз має лінійний характер. При прийомі эторикоксиба в дозі 120 мг під час їжі (їжа з високим вмістом жирів) не спостерігалося клінічно значущого впливу на ступінь абсорбції. Швидкість абсорбції при цьому змінювалася, що призводило до зниження Сmах на 36% і збільшення Тmах на 2 год. Ці дані не є клінічно значущими. У клінічних дослідженнях церикоксиб застосовувався незалежно від їди. Розподіл Еторікоксиб приблизно на 92% зв'язується з білками плазми у людини в діапазоні концентрацій від 0,05 до 5 мкг/мл. Об'єм розподілу у рівноважному стані (VdSS) становить близько 120 л. Еторикоксиб проникає через плацентарний бар'єр у щурів та кролів та гематоенцефалічний бар'єр у щурів. Метаболізм Еторикоксиб екстенсивно метаболізується, У людини виявлено п'ять метаболітів церикоксиксу. Основним метаболітом є 6'-карбоксиацетилеторикоксиб, що утворюється в результаті подальшого окислення 6'-гідроксиметилеторикоксибу. Ці основні метаболіти не мають помітної активності або слабо інгібують ЦОГ-2. Жоден із цих метаболітів не інгібує ЦОГ-1. Виведення Після одноразового внутрішньовенного введення здоровим добровольцям міченого радіоактивного церикоксибу в дозі 25 мг 70 % церикоксибу виводилося через нирки та 20 % – через кишечник, переважно у вигляді метаболітів. Менше 2% виявлялося у незміненому вигляді. Виведення еторикоксибу відбувається в основному шляхом метаболізму в печінці з подальшим виведенням нирками. Рівноважні концентрації эторикоксиба досягаються при щоденному прийомі в дозі 120 мг протягом 7 днів з коефіцієнтом кумуляції близько 2, що відповідає періоду напіввиведення близько 22 год. Плазмовий кліренс після внутрішньовенного введення 25 мг становить приблизно 50 мл/хв. Особливі групи пацієнтів Стать: фармакокінетичні параметри препарату у чоловіків та жінок не відрізняються. Літні пацієнти: фармакокінетика препарату у пацієнтів віком понад 65 років порівнянна з фармакокінетикою у пацієнтів молодшого віку. Діти: фармакокінетика еторикоксибу у дітей (60 кг, які приймали церикоксиб у дозі 90 мг 1 раз на день), була аналогічна фармакокінетиці у дорослих, які приймали церикоксиб у дозі 90 мг 1 раз на день. Безпека та ефективність застосування церикоксибу у дітей не встановлена. Печінкова недостатність: у пацієнтів з печінковою недостатністю легкого ступеня тяжкості (5-6 балів за шкалою Чайлд-П'ю) прийом еторикоксибу в дозі 60 мг 1 раз на день супроводжувався збільшенням показника AUC приблизно на 16% порівняно зі здоровими добровольцями, які приймали препарат у тій ж дозі. У пацієнтів з печінковою недостатністю середнього ступеня тяжкості (7-9 балів за шкалою Чайлд-П'ю), які отримували еторикоксиб у дозі 60 мг один раз на день через день, середнє значення AUC було таким же, як у здорових добровольців, які приймали еторикоксиб у дозі 60 мг раз на день щодня. Застосування еторикоксибу в дозі 30 мг один раз на день не вивчалося у цій групі пацієнтів. Клінічні та фармакокінетичні дані досліджень у пацієнтів з тяжкою печінковою недостатністю (>10 балів за шкалою Чайлд-П'ю) відсутні. Ниркова недостатність: фармакокінетичні показники одноразового застосування церикоксибу в дозі 120 мг у пацієнтів з нирковою недостатністю помірного та тяжкого ступеня та у пацієнтів з термінальною стадією хронічної ниркової недостатності, які перебувають на гемодіалізі, суттєво не відрізняються від показників у здорових добровольців. Гемодіаліз незначно впливає на виведення препарату (кліренс при діалізі – близько 50 мл/хв).ФармакодинамікаЕторикоксиб при пероральному прийомі в терапевтичних концентраціях є селективним інгібітором циклооксигенази типу 2 (ЦОГ-2). У дослідженнях з клінічної фармакології церикоксиб дозозалежно інгібував ЦОГ-2, не впливаючи на ЦОГ-1 при застосуванні доз до 150 мг на день. Еторикоксиб не пригнічував синтез простагландинів у слизовій оболонці шлунка і не впливав на функцію тромбоцитів. ЦОГ відповідає за синтез простагландинів. Виділено дві ізоформи цього ферменту - ЦОГ-1 та ЦОГ-2. ЦОГ-2 є ізоферментом, який індукується під дією прозапальних медіаторів і розглядається як основний фермент, який відповідає за синтез простаноїдних медіаторів болю, запалення та лихоманки. ЦОГ-2 бере участь у процесах овуляції, імплантації та закриття артеріальної протоки, регуляції функції нирок, центральної нервової системи (індукція лихоманки, відчуття болю, когнітивна функція), а також може грати певну роль у процесі загоєння виразок. ЦОГ-2 була виявлена у тканинах, що оточують виразки шлунка у людини, але її значення для загоєння виразки не встановлено. Ефективність У пацієнтів з остеоартрозом (ОА) церикоксиб при застосуванні в дозі 60 мг один раз на день викликав достовірне зменшення болю та покращення оцінки свого стану пацієнтами. Ці сприятливі ефекти спостерігалися вже другого дня лікування і зберігалися протягом 52 тижнів. Дослідження еторикоксибу в дозі 30 мг один раз на день (із застосуванням подібних методів оцінки) продемонстрували ефективність препарату порівняно з плацебо протягом усього періоду лікування (12 тижнів). У дослідженні, яке проводилося з метою визначення оптимальної дози, еторикоксиб у дозі 60 мг продемонстрував достовірно більш виражене поліпшення, ніж у дозі 30 мг для всіх 3 первинних кінцевих точок через 6 тижнів лікування. Застосування дози 30 мг на лікування ОА суглобів кистей рук не вивчалося. У пацієнтів з ревматоїдним артритом (РА) прийом еторикоксибу в дозі 60 мг або 90 мг один раз на день забезпечував достовірне зменшення болю, запалення та покращення рухливості. Ці сприятливі ефекти зберігалися протягом 12-тижневого періоду лікування. Дослідження порівняння застосування церикоксибу в дозі 60 мг і 90 мг один раз на день для лікування РА показало, що обидва режими дозування забезпечували переважну ефективність терапії порівняно з плацебо. Доза церикоксибу 90 мг один раз на день перевищувала за ефективністю дозу 60 мг один раз на день при оцінці ефекту за допомогою Глобальної Шкали. % довірчий інтервал (ДІ): -4,98 мм; -0,45 мм). У пацієнтів із гострим подагричним артритом еторикоксиб у дозі 120 мг один раз на день протягом усього періоду лікування (8 днів) зменшував помірний та сильний біль у суглобах та запалення порівняно з індометацином у дозі 50 мг 3 рази на день. Зменшення болю відзначалося вже через 4 години після початку лікування. У пацієнтів з анкілозуючим спондилітом еторикоксиб при застосуванні в дозі 90 мг один раз на день забезпечував достовірне зменшення болю в спині, запалення, скутості, а також покращення рухової функції. Клінічна ефективність эторикоксиба спостерігалася вже другого дня лікування та зберігалася протягом усього періоду лікування (52 тижні). В іншому дослідженні, в рамках якого порівнювалася ефективність застосування церикоксибу в дозі 90 мг один раз на день та 60 мг один раз на день, цей препарат продемонстрував рівну ефективність порівняно з напроксеном у дозі 1000 мг один раз на день. Серед пацієнтів, у яких не було досягнуто адекватної клінічної відповіді на терапію протягом 6 тижнів при застосуванні церикоксибу у дозі 60 мг один раз на день, збільшення добової дози до 90 мг дозволяло покращити результати лікування, оцінені за допомогою шкали інтенсивності болю у спині. -100 мм візуально-аналогова шкала), порівняно з продовженням терапії еторікоксибом у дозі 60 мг один раз на день. Середнє поліпшення склало -2,70 мм (95% ДІ: 4,88 мм; -0,52 мм). У клінічному дослідженні з вивчення болю після стоматологічних операцій эторикоксиб у дозі 90 мг призначали раз на день протягом трьох днів. У підгрупі пацієнтів з помірним болем (при вихідній оцінці) еторикоксиб у дозі 90 мг продемонстрував знеболюючий ефект, аналогічний ібупрофену в дозі 600 мг (16,11 порівняно з 16,39, Р = 0,722) та більший, ніж при застосуванні комбінації парацетамол/ кодеїн у дозі 600 мг/60 мг (11,00; Р Безпека Програма MEDAL (Багатонаціональна Програма Оцінки Довгострокового Призначення Еторікоксибу та Диклофенаку при Артріті) Програма MEDAL була проспективною програмою оцінки безпеки на підставі серцево-судинних явищ за об'єднаними даними трьох рандомізованих подвійних сліпих активно-контрольованих досліджень: MEDAL, EDGE II та EDGE. Дослідження MEDAL являло собою дослідження, тривалість якого визначалася досягненням кінцевих точок (серцево-судинних явищ), воно включало 17804 пацієнта з ОА та 5700 пацієнтів з РА, які отримували еторикоксиб у дозі 60 мг (ОА) або 90 мг (ОА та РА) або ді у дозі 150 мг на день у середньому протягом 20,3 місяців (максимум 42,3 місяці, медіана 21,3 місяці). У цьому дослідженні реєстрували лише серйозні небажані явища та випадки вибуття з дослідження внаслідок будь-якого небажаного явища. У дослідженнях EDGE та EDGE II порівнювали безпеку прийому церикоксибу та диклофенаку для шлунково-кишкового тракту (ЖКТ). До дослідження EDGE було включено 7111 пацієнтів з ОА, які отримували еторикоксиб у дозі 90 мг на день (в 1,5 рази більше за дозу, рекомендовану при ОА) або диклофенак у дозі 150 мг на день протягом у середньому 9,1 місяців (максимум 16 , 6 місяців, медіана 11,4 місяців). У дослідження EDGE II було включено 4086 пацієнтів з РА, які отримували еторикоксиб у дозі 90 мг на день або диклофенак у дозі 150 мг на день протягом середньому 19,2 місяців (максимум 33,1 місяця, медіана 24 місяці). В об'єднаній програмі MEDAL аналізували дані щодо лікування 34701 пацієнтів з ОА або РА, середня тривалість лікування склала 17,9 місяців (максимум 42,3 місяці, медіана 16,3 місяців), при цьому приблизно 12800 пацієнтів отримували лікування протягом понад 24 місяців. Пацієнти, включені до програми, при вихідній оцінці мали широкий спектр серцево-судинних та шлунково-кишкових факторів ризику. Були виключені пацієнти, які мали в анамнезі нещодавно перенесений інфаркт міокарда (ІМ), аортокоронарне шунтування або черезшкірне коронарне втручання протягом 6 місяців перед включенням до дослідження. У дослідженнях дозволялося застосовувати гастропротектори та низькі дози аспірину. Загальна безпека Достовірних відмінностей між эторикоксибом та диклофенаком щодо частоти розвитку серцево-судинних тромботичних явищ виявлено не було. Кардіоренальні небажані явища найчастіше спостерігалися при прийомі церикоксибу в порівнянні з диклофенаком, ефект був дозозалежним (див. результати нижче). Небажані явища з боку шлунково-кишкового тракту та печінки достовірно частіше спостерігалися при прийомі диклофенаку, ніж при прийомі церикоксибу. Частота небажаних явищ у дослідженнях EDGE та EDGE II та небажаних явищ, визнаних серйозними або зажадали відміни лікування, у дослідженні MEDAL була вищою при прийомі еторикоксибу порівняно з диклофенаком. Результати дослідження безпеки щодо серцево-судинної системи Частота підтверджених серйозних тромботичних серцево-судинних небажаних явищ (включаючи серцеві, цереброваскулярні та явища з боку периферичної судинної системи) була порівнянна між групами, які отримували церикоксиб або диклофенак (дані наведені в таблиці нижче). Не виявлено статистично значимих відмінностей щодо частоти тромботичних явищ між еторикоксибом та диклофенаком у всіх проаналізованих підгрупах, включаючи категорії пацієнтів з підвищеним ризиком серцево-судинних ускладнень. Відносний ризик для підтверджених серйозних серцево-судинних небажаних тромботичних явищ був подібним при прийомі еторикоксібу в дозі 60 мг або 90 мг і диклофенаку в дозі 150 мг. Частота підтверджених тромботичних серцево-судинних серйозних небажаних явищ (Об'єднана програма MEDAL) Еторікоксиб(N=16819)25 836 пацієнто-років Диклофенак(N=16483)24 766 пацієнто-років Порівняння між видами лікування Частота 1 (95% ДІ) Частота 1 (95% ДІ) Відносний ризик (95% ДІ) Підтверджені тромботичні серцево-судинні серйозні небажані явища За виконання вимог протоколу (Per protocol) 1,24 (1,11; 1,38) 1,30 (1,17; 1,45) 0,95 (0,81; 1,11) Залежно від призначеного лікування (Intent-to-treat) 1,25 (1,14; 1,36) 1,19 (1,08; 1,30) 1,05 (0,93; 1,19) Підтверджені явища з боку серця За виконання вимог протоколу (Per protocol) 0,71 (0,61; 0,82) 0,78 (0,68; 0,90) 0,90 (0,74; 1,10) Залежно від призначеного лікування (Intent-to-treat) 0,69 (0,61; 0,78) 0,70 (0,62; 0,79) 0,99 (0,84; 1,17) Підтверджені цереброваскулярні явища За виконання вимог протоколу (Per protocol) 0,34 (0,28; 0,42) 0,32 (0,25; 0,40) 1,08 (0,80; 1,46) Залежно від призначеного лікування (Intent-to-treat) 0,33 (0,28; 0,39) 0,29 (0,24; 0,35) 1,12 (0,87; 1,44) Підтверджені явища з боку периферичної судинної системи За виконання вимог протоколу (Per protocol) 0,20 (0,15; 0,27) 0,22 (0,17; 0,29) 0,92 (0,63; 1,35) Залежно від призначеного лікування (Intent-to-treat) 0,24 (0,20; 0,30) 0,23 (0,18; 0,28) 1,08 (0,81; 1,44) 1 число явищ на 100 пацієнто-років; ДІ = довірчий інтервал; N = загальна кількість пацієнтів, які виконали вимоги протоколу. При виконанні вимог протоколу: всі явища, що розвинулися на тлі досліджуваної терапії або протягом 14 днів після її припинення (виключені пацієнти, які прийняли <75% досліджуваного препарату або приймали НПЗП >10% часу, що не входять до дослідження). Залежно від призначеного лікування: всі підтверджені явища, що розвинулися до закінчення дослідження (включно з пацієнтами, які могли піддаватися не включеним до дослідження втручанням після припинення прийому досліджуваних препаратів). Загальна кількість рандомізованих пацієнтів: n = 17412 для эторикоксиба і n = 17289 для диклофенаку. Смертність від серцево-судинних явищ, а також загальна смертність у групах лікування церикоксибом та диклофенаком були порівнянними. Кардіоренальні явища Приблизно у 50% пацієнтів, включених у дослідження MEDAL, при початковій оцінці в анамнезі було зареєстровано артеріальну гіпертензію. У проведеному дослідженні частота вибування внаслідок небажаних явищ, пов'язаних з артеріальною гіпертензією, була статистично значуще вищою під час прийому эторикоксиба проти диклофенаком. Частота небажаних явищ, пов'язаних з хронічною серцевою недостатністю (випадки вибування з дослідження або серйозні небажані явища), була подібною до груп еторікоксибу в дозі 60 мг і диклофенаку в дозі 150 мг, але була вищою для еторікоксибу в дозі 90 мг порівняно з диклофеном. дозі 150 мг (і статистично значуще вище для еторикоксибу в дозі 90 мг у порівнянні з диклофенаком у дозі 150 мг у дослідженні MEDAL у пацієнтів з ОА). Частота підтверджених небажаних явищ,пов'язаних з хронічною серцевою недостатністю (серйозних, які призвели до госпіталізації або необхідності невідкладної допомоги), була незначно вищою для церикоксибу порівняно з диклофенаком у дозі 150 мг, ефект був дозозалежним. Частота випадків вибування з дослідження внаслідок небажаних явищ, пов'язаних з набряками, була вищою для еторікоксибу в дозі 150 мг, порівняно з диклофенаком у дозі 150 мг, ефект був дозозалежним (статистично значимо для еторікоксибу в дозі 90 мг, але не для етороксиксу в дозі 60 мг).була вищою для эторикоксиба порівняно з диклофенаком в дозі 150 мг, ефект був дозозалежним (статистично значуще для етіроксиксібу в дозі 90 мг, але не для етіроксиксібу в дозі 60 мг).була вищою для эторикоксиба порівняно з диклофенаком в дозі 150 мг, ефект був дозозалежним (статистично значуще для етіроксиксібу в дозі 90 мг, але не для етіроксиксібу в дозі 60 мг). Результати оцінки кардіоренальної безпеки у дослідженнях EDGE та EDGE II узгоджуються з результатами у дослідженні MEDAL В окремих дослідженнях програми MEDAL абсолютна частота вибування з дослідження в будь-якій групі лікування при прийомі еторикоксибу (60 мг або 90 мг) становила до 2,6% при артеріальній гіпертензії, до 1,9% при набряках, і до 1,1% при хронічній серцевої недостатності. У пацієнтів, які приймали церикоксиб у дозі 90 мг, частота вибуття з дослідження була вищою, ніж у пацієнтів, які приймали церикоксиб у дозі 60 мг. Результати оцінки переносимості з боку ШКТ у Програмі MEDAL У кожному з трьох досліджень, що входять до програми MEDAL, частота вибування з дослідження для будь-яких клінічних небажаних явищ з боку шлунково-кишкового тракту (наприклад, диспепсія, біль у животі, виразки) була достовірно нижчою для еторикоксибу порівняно з диклофенаком. Частота вибуття з дослідження внаслідок небажаних клінічних явищ з боку шлунково-кишкового тракту на 100 пацієнто-років за весь період дослідження становила: 3,23 для еторикоксибу та 4,96 для диклофенаку в дослідженні MEDAL; 9,12 для эторикоксиба і 12,28 для диклофенаку у дослідженні EDGE; 3,71 для еторикоксибу та 4,81 для диклофенаку в дослідженні EDGE II. Результати оцінки безпеки щодо ШКТ у Програмі MEDAL До небажаних явищ з боку верхніх відділів шлунково-кишкового тракту були віднесені перфорації, виразки та кровотечі. Ускладнені небажані явища з боку верхніх відділів шлунково-кишкового тракту включали перфорацію, непрохідність та ускладнені кровотечі; неускладнені явища включали неускладнені кровотечі та неускладнені виразки. При прийомі эторикоксиба порівняно з диклофенаком загальна частота небажаних явищ з боку верхніх відділів шлунково-кишкового тракту була достовірно нижчою. Достовірних відмінностей між етерокіксібом і диклофенаком за частотою ускладнених небажаних явищ виявлено не було. Для випадків кровотеч із верхніх відділів шлунково-кишкового тракту (ускладнених та неускладнених) не було виявлено достовірних відмінностей між еторикоксибом та диклофенаком.Перевага церикоксибу порівняно з диклофенаком щодо ускладнень з боку верхніх відділів ШКТ не була статистично значущою у пацієнтів, які одночасно приймали аспірин у низьких дозах (близько 33% пацієнтів). Частота підтверджених ускладнених та неускладнених клінічних небажаних явищ з боку верхніх відділів шлунково-кишкового тракту на 100 пацієнто-років (перфорації, виразки та кровотечі) склала 0,67 (95 % ДІ: 0,57; 0,77) для церикоксиксу та 0,97 (95 % ДІ: 0,85; 1,10) для диклофенаку, відносний ризик склав 0,69 (95% ДІ: 0,57; 0,83). При оцінці частоти підтверджених клінічних небажаних явищ з боку верхніх відділів шлунково-кишкового тракту у пацієнтів похилого віку максимальне зниження спостерігалося у пацієнтів у віці ≥75 років у групі церикоксибу в порівнянні з диклофенаком - 1,35 (95 % ДІ: 0,94; 1,87) та 2,78 (95% ДІ: 2,14; 3,56) на 100 пацієнто-років відповідно. Частота підтверджених небажаних явищ з боку нижніх відділів шлунково-кишкового тракту (перфорація тонкої або товстої кишки, непрохідність, кровотеча) достовірно не розрізнялася між групами, які приймали церикоксиб та диклофенак. Результати оцінки безпеки щодо печінки у Програмі MEDAL При прийомі эторикоксиба порівняно з диклофенаком спостерігалася статистично достовірно нижча частота вибуття з дослідження через небажані явища з боку печінки. В об'єднаній програмі MEDAL 0,3% пацієнтів, які приймали еторикоксиб, та 2,7% пацієнтів, які приймали диклофенак, вибули з дослідження через небажані явища з боку печінки. Частота небажаних явищ на 100 пацієнто-років склала 0,22 для церикоксиксу і 1,84 для диклофенаку (р Додаткові дані щодо безпеки, пов'язані з тромботичними серцево-судинними явищами У клінічних дослідженнях, за винятком Програми MEDAL, приблизно 3100 пацієнтів отримували церикоксикс у дозі ≥60 мг на день протягом 12 тижнів та довше. У цих дослідженнях не було виявлено помітних відмінностей у частоті підтверджених серйозних тромботичних серцево-судинних явищ у пацієнтів, які отримували церикоксиб у дозі ≥60 мг, плацебо або нестероїдні протизапальні засоби, що не містять напроксен. Однак у порівнянні з пацієнтами, які отримували напроксен у дозі 500 мг двічі на день, частота цих явищ була вищою у пацієнтів, які отримували еторикоксиб. Різниця в антиагрегантній активності між деякими нестероїдними протизапальними засобами, що інгібують ЦОГ-1, та селективними інгібіторами ЦОГ-2 може мати клінічне значення у пацієнтів із групи ризику тромбоемболічних подій. Селективні інгібітори ЦОГ-2 пригнічують утворення системного (і, можливо, ендотеліального) простацикліну,не впливаючи на тромбоцитарний тромбоксан. Клінічна значимість цих спостережень встановлено. Додаткові дані з безпеки щодо ШКТ У двох 12-тижневих подвійних сліпих ендоскопічних дослідженнях кумулятивна частота розвитку гастродуоденальних виразок була значно нижчою у пацієнтів, які отримували церикоксиб у дозі 120 мг один раз на день, ніж у пацієнтів, які отримували напроксен 500 мг двічі на день. або ібупрофен 800 мг тричі на день. Частота розвитку виразок при призначенні церикоксибу була вищою порівняно з плацебо. Дослідження ниркової функції у пацієнтів похилого віку У рандомізованому подвійному сліпому плацебо-контрольованому дослідженні в паралельних групах оцінювався вплив 15-денної терапії церикоксибом (90 мг), целекоксибом (200 мг двічі на день), напроксеном (500 мг двічі на день) порівняно з плацебо на виведення натрію. , артеріальний тиск (АТ) та інші параметри функції нирок у пацієнтів віком від 60 до 85 років, які отримували раціон з обмеженим споживанням натрію до 200 мекв/день. Еторикоксиб, целекоксиб і напроксен мали подібний вплив на виведення натрію нирками через 2 тижні лікування. Всі активні препарати порівняння показали збільшення систолічного АТ порівняно з плацебо, однак, еторикоксиб викликав статистично значуще збільшення систолічного АТ на 14-й день порівняно з целекоксибом і напроксеном (середня зміна систолічного АТ порівняно з вихідним: етороксіб 7,7 мм рт. ст., целекоксиб 2,4 мм рт.ст., напроксен 3,6 мм рт.ст.).Показання до застосуванняСимптоматична терапія остеоартрозу, ревматоїдного артриту, анкілозуючого спондиліту, болю та запалення, пов'язаних із гострим подагричним артритом. Короткострокова терапія помірного гострого болю після стоматологічних операцій.Протипоказання до застосуванняПідвищена чутливість до еторикоксибу або будь-якої з допоміжних речовин препарату. Виразкова хвороба шлунка та 12-палої кишки у стадії загострення, активна шлунково-кишкова кровотеча. Бронхіальна астма, бронхоспазм, гострий риніт, поліпоз носа, ангіоневротичний набряк, кропив'янка або алергічні реакції після прийому ацетилсаліцилової кислоти або нестероїдних протизапальних препаратів (НПЗЗ), у тому числі інгібіторів ЦОГ-2, в анамнезі. Вагітність та період грудного вигодовування. Тяжкі порушення функції печінки (сироватковий альбумін 10 балів за шкалою Чайлд-П'ю). Тяжка ниркова недостатність (КК Діти та підлітки до 16 років. Запальні захворювання кишок. Хронічна серцева недостатність (II-IV функціональний клас за NYHA). Неконтрольована артеріальна гіпертензія (АТ стабільно вищий за 140/90 мм рт. ст.). Підтверджена ішемічна хвороба серця, захворювання периферичних артерій та/або цереброваскулярні захворювання. Дефіцит лактази, непереносимість лактози, глюкозо-галактозна мальабсорбція. Підтверджена гіперкаліємія. З обережністю: Пацієнти з підвищеним ризиком розвитку ускладнень з боку шлунково-кишкового тракту (виразкова ураження шлунково-кишкового тракту або шлунково-кишкова кровотеча в анамнезі, наявність інфекції Helicobacter Pylori, одночасне застосування інших нестероїдних протизапальних засобів, у тому числі ацетилсаліцилової кислоти, літній вік). Пацієнти, які мають в анамнезі фактори ризику серцево-судинних ускладнень (дисліпідемія/гіперліпідемія, цукровий діабет, артеріальна гіпертензія, куріння, серцева недостатність, порушення функції лівого шлуночка, набряки та затримка рідини в організмі). Печінкова недостатність (5-9 балів за класифікацією Чайлд-П'ю). Пацієнти з дегідратацією. Пацієнти з порушеннями функції нирок (КК Пацієнти з попереднім значним зниженням функції нирок, з ослабленою функцією нирок, декомпенсованою серцевою недостатністю або цирозом печінки, що перебувають у групі ризику при тривалому застосуванні нестероїдних протизапальних засобів. Супутня терапія антикоагулянтами (наприклад, варфарин), антиагрегантами (наприклад, ацетилсаліцилова кислота, клопідогрел), препаратами, що метаболізуються сульфотрансферазами.Вагітність та лактаціяВагітність В даний час клінічних даних про застосування еторикоксибу при вагітності відсутні. У дослідженнях на тваринах спостерігалася токсична дія на репродуктивну систему. Потенційний ризик для жінок під час вагітності невідомий. Застосування еторикоксибу, як і інших лікарських препаратів, що інгібують синтез простагландинів, у III триместрі вагітності може призводити до придушення скорочень матки та передчасного закриття артеріальної протоки. Еторикоксиб протипоказаний при вагітності. Якщо під час лікування настала вагітність, церикоксиб необхідно відмінити. Грудне годування У лактуючих щурів еторикоксиб виділяється з молоком. Досліджень, що підтверджують виділення еторикоксибу з грудним молоком у жінок, не проводилося. Жінки, які приймають еторикоксиб, повинні припинити грудне вигодовування. Фертильність Застосування еторикоксибу, як і інших препаратів, що інгібують ЦОГ-2 або синтез простагландинів, не рекомендується жінкам, які планують вагітність.Побічна діяРезюме профілю безпеки Безпека застосування церикоксибу оцінювалася у клінічних дослідженнях за участю 9295 пацієнтів, у тому числі 6757 пацієнтів з ОА, РА, хронічним болем у нижній частині спини та анкілозуючим спондилітом (приблизно 600 пацієнтів з ОА або РА отримували лікування протягом одного року або більше). Профіль небажаних реакцій був подібним у пацієнтів з ОА або РА, які отримували еторикоксиб протягом одного року або довше. У клінічному дослідженні гострого подагричного артриту пацієнти отримували церикоксиб у дозі 120 мг 1 раз на день протягом 8 днів. Профіль небажаних явищ у цьому дослідженні був загалом таким самим, як і в об'єднаних дослідженнях ОА, РА та хронічного болю в нижній частині спини. Для оцінки безпеки щодо серцево-судинної системи були об'єднані дані трьох активних контрольованих досліджень, у яких брали участь 17412 пацієнтів з ОА або РА, які отримували еторикоксиб у дозі 60 мг або 90 мг, середня тривалість досліджень склала приблизно 18 місяців. У клінічних дослідженнях гострого післяопераційного болю, пов'язаного з проведенням стоматологічної операції, у яких 614 пацієнтів отримували еторикоксиб у дозі 90 мг або 120 мг, профіль небажаних ефектів загалом був подібним до профілю в об'єднаних дослідженнях ОА, РА та хронічного болю в нижній частині спини. Табличне резюме небажаних реакцій У таблиці перераховані небажані реакції, які були зареєстровані з більшою частотою при застосуванні препарату, ніж у групі плацебо, у клінічних дослідженнях, що включали пацієнтів з ОА, РА, хронічним болем у нижній частині спини або анкілозуючим спондилітом (еторикоксиб призначався у дозі 30 мг, 60 мг або 90 мг з підвищенням дози до рекомендованої протягом 12 тижнів), у програмі MEDAL, де дослідження тривали до 3,5 років, у короткострокових дослідженнях гострого болю (протягом 7 днів), а також отримані під час постмаркетингового застосування. Класифікація систем органів Небажана реакція Частота 1 Інфекційні та паразитарні захворювання альвеолярний остит часто гастроентерит, інфекції верхніх дихальних шляхів, інфекції сечовивідних шляхів не часто Порушення з боку крові та лімфатичної системи анемія (в основному в результаті шлунково-кишкової кровотечі), лейкопенія, тромбоцитопенія не часто Порушення з боку імунної системи реакції гіперчутливості 2,4 не часто ангіоневротичний набряк, анафілактичні/анафілактоїдні реакції, у тому числі шок 2 рідко Порушення з боку обміну речовин та харчування набряки/затримка рідини часто посилення або зниження апетиту, збільшення маси тіла не часто Порушення психіки тривога, депресія, зниження ясності мислення, галюцинації 2 не часто сплутаність свідомості 2 , неспокій 2 рідко Порушення з боку нервової системи запаморочення, головний біль часто порушення смаку, безсоння, парестезія/гіпестезія, сонливість не часто Порушення з боку органу зору нечіткість зору, кон'юнктивіт не часто Порушення з боку органу слуху та лабіринтні порушення дзвін у вухах, вертиго не часто Порушення з боку серця відчуття серцебиття, аритмія 2 часто фібриляція передсердь, тахікардія 2 , хронічна серцева недостатність, неспецифічні зміни на ЕКГ, стенокардія 2 , інфаркт міокарда 5 не часто Порушення з боку судин артеріальна гіпертензія часто "припливи", порушення мозкового кровообігу 5 транзиторна ішемічна атака гіпертонічний криз 2 васкуліт 2 не часто Порушення з боку дихальної системи, органів грудної клітки та середостіння. бронхоспазм 2 часто кашель, задишка, носова кровотеча не часто Порушення з боку шлунково-кишкового тракту біль в животі дуже часто метеоризм, гастрит, печія/гастроезофагеальний рефлюкс, діарея, диспепсія/дискомфорт в епігастрії, нудота, блювання, езофагіт, виразка слизової оболонки порожнини рота часто здуття живота, зміна перистальтики, сухість слизової оболонки порожнини рота, виразка гастродуоденальної, виразкова хвороба шлунка, включаючи перфорації та кровотечі, панкреатит 2 , синдром подразненого кишечника не часто Порушення з боку печінки та жовчовивідних шляхів підвищення активності АЛТ та ACT часто гепатит 2 рідко печінкова недостатність 2 , жовтяниця 2 рідко 3 Порушення з боку шкіри та підшкірних тканин екхімоз часто набряклість особи, свербіж, висип, еритема 2 , кропив'янка 2 не часто синдром Стівенса-Джонсона 2 , токсичний епідермальний некроліз 2 , фіксована лікарська еритема 2 рідко 3 Порушення з боку скелетно-м'язової та сполучної тканини м'язові судоми/спазм, скелетно-м'язовий біль/скутість не часто Порушення з боку нирок та сечовивідних шляхів протеїнурія, підвищення концентрації креатиніну в сироватці, ниркова недостатність 2,3,4 не часто Загальні розлади та порушення у місці введення астенія/слабкість, грипоподібний синдром часто біль у грудній клітці не часто Лабораторні та інструментальні дані підвищення концентрації азоту сечовини крові, підвищення активності креатинфосфокінази, гіперкаліємія, підвищення концентрації сечової кислоти не часто гіпонатріємія рідко 1 Відповідно до частоти, що враховується у клінічних дослідженнях: дуже часто (≥1/10), часто (від ≥1/100 до 2 Ця небажана реакція була зареєстрована під час постмаркетингового спостереження. Частота оцінювалася на підставі найбільшої частоти, що спостерігається у клінічних дослідженнях з урахуванням показань та затвердженої дози. 3 Частотна категорія "рідко" була визначена відповідно до керівництва (версія 2, вересень 2009 р.) для Короткої характеристики лікарського препарату на підставі розрахункової верхньої межі 95 % довірчого інтервалу для 0 явищ, враховуючи кількість пацієнтів, які отримували еторикоксиб в аналізі даних III фази , об'єднаних залежно від дози та показання (n = 15470). 4 Гіперчутливість включає терміни "алергія", "лікарська алергія", "гіперчутливість до лікарського препарату", "гіперчутливість", "гіперчутливість неуточнена", "реакція гіперчутливості" та "неспецифічна алергія". 5 За результатами даних аналізу довгострокових плацебо- та активноконтрольованих клінічних досліджень при застосуванні селективних інгібіторів ЦОГ-2 підвищується ризик розвитку серйозних артеріальних тромботичних явищ, включаючи ІМ та інсульт. З наявних даних, малоймовірно, що абсолютний ризик розвитку цих явищ перевищує 1 % на рік (нечасто). Наступні серйозні небажані явища були зареєстровані у зв'язку з прийомом НГТВП і не можуть бути виключені для еторикоксибу: нефротоксичність, включаючи інтерстиціальний нефрит та нефротичний синдром.Взаємодія з лікарськими засобамиФармакодинамічні взаємодії Пероральні антикоагулянти (варфарин). У пацієнтів, які постійно приймають варфарин, прийом еторикоксибу в дозі 120 мг на день супроводжувався збільшенням міжнародного нормалізованого відношення (МНО)/протромбінового часу приблизно на 13%. Тому у пацієнтів, які отримують пероральні антикоагулянти, слід контролювати МНО/протромбіновий час на початку лікування або при зміні дози еторикоксибу, особливо в перші кілька днів. Діуретики, інгібітори ангіотензинперетворюючого ферменту (АПФ) та антагоністи рецепторів ангіотензину II. Нестероїдні протизапальні засоби можуть послаблювати ефект діуретиків та інших антигіпертензивних лікарських препаратів. У деяких пацієнтів з порушенням функції нирок (наприклад, у пацієнтів з зневодненням або у літніх пацієнтів з порушеною функцією нирок) одночасне застосування інгібітору АПФ або антагоніста рецепторів ангіотензину II та препаратів, що інгібують ЦОГ, може призводити до додаткового погіршення функції нирок, включаючи можливий розвиток. ниркової недостатності, яка зазвичай має оборотний характер. Це слід враховувати у пацієнтів, які приймають одночасно церикоксиб з інгібіторами АПФ або антагоністами рецепторів ангіотензину ІІ. Такі комбінації слід призначати з обережністю, особливо пацієнтам похилого віку.Пацієнти повинні бути належним чином гідратовані, при цьому необхідно проводити моніторинг функції нирок на початку комбінованої терапії та періодично надалі. Ацетилсаліцилова кислота. У дослідженні у здорових добровольців церикоксиб у дозі 120 мг 1 раз на день у рівноважному стані не впливав на антитромбоцитарну активність ацетилсаліцилової кислоти (81 мг 1 раз на день). Еторикоксиб можна одночасно застосовувати з ацетилсаліциловою кислотою в низьких дозах, призначених для профілактики серцево-судинних захворювань. Тим не менш, одночасне застосування низьких доз ацетилсаліцилової кислоти та еторикоксибу може призвести до збільшення частоти виразкового ураження шлунково-кишкового тракту або інших ускладнень у порівнянні з прийомом тільки церикоксиксу. Одночасне застосування церикоксибу з ацетилсаліциловою кислотою в дозах, що перевищують рекомендовані для профілактики серцево-судинних ускладнень, а також з іншими нестероїдними протизапальними засобами не рекомендується. Циклоспорин та такролімус. Взаємодія церикоксибу з цими препаратами не вивчалася, однак, одночасне застосування циклоспорину або такролімусу з будь-яким нестероїдними протизапальними засобами може посилювати нефротоксичний ефект циклоспорину або такролімусу. При прийомі эторикоксиба у комбінації з будь-яким із цих препаратів слід контролювати функцію нирок. Фармакокінетичні взаємодії Вплив інших лікарських препаратів на фармакокінетику еторикоксибу Основний шлях метаболізму церикоксибу залежить від ферментів системи CYP. Ізофермент CYP3A4 сприяє метаболізму церикоксибу in vivo. Дослідження in vitro показують, що ізоферменти CYP2D6, CYP2C9, CYP1A2 і CYP2C19 можуть каталізувати основний шлях метаболізму, але їх кількісні характеристики in vivo не вивчені. Кетоконазол. Кетоконазол, потужний інгібітор ізоферменту CYP3A4, при прийомі здоровими добровольцями в дозі 400 мг один раз на день протягом 11 днів не надавав клінічно значущого впливу на фармакокінетику одноразової дози церикоксиксу 60 мг (збільшення AUC на 43%). Вориконазол та міконазол. Одночасне призначення сильних інгібіторів ізоферменту CYP3A4 (вориконазол для прийому всередину або міконазол місцево, у вигляді гелю для прийому всередину) та еторикоксибу викликало невелике збільшення експозиції церикоксибу, яке не визнано клінічно значущим на підставі опублікованих даних. ріфампіцин. Одночасне застосування церикоксибу та рифампіцину (потужного індуктора системи цитохромів) призводило до зниження концентрації церикоксибу в плазмі на 65 %. Така взаємодія може призвести до рецидиву симптомів при одночасному призначенні еторикоксибу з рифампіцином. Ця інформація дозволяє припустити необхідність збільшення дози, проте застосовувати еторикоксиб у дозах, що перевищують рекомендовані для кожного показання, не рекомендується, оскільки комбіноване застосування рифампіцину та еторикоксибу в таких дозах не вивчалося. Антациди. Антациди не надають клінічно значущої дії на фармакокінетику еторикоксибу. Вплив еторикоксибу на інші лікарські препарати Літій. НПЗЗ зменшують виведення літію нирками, отже, збільшують концентрацію літію у плазмі крові. При необхідності проводять частий контроль концентрації літію в крові та коригують дозу літію під час одночасного прийому з нестероїдними протизапальними засобами, а також при відміні нестероїдних протизапальних засобів. Метотрексат. У двох дослідженнях вивчалися ефекти еторикоксибу в дозах 60, 90 або 120 мг 1 раз на день протягом семи днів у пацієнтів, які отримували 1 раз на тиждень метотрексат у дозі від 7,5 до 20 мг на лікування РА. Еторикоксиб у дозах 60 та 90 мг не впливав на концентрацію метотрексату в плазмі та нирковий кліренс метотрексату. В одному дослідженні церикоксиб у дозі 120 мг не фармакокінетично впливав на метотрексат, але в іншому дослідженні концентрація метотрексату в плазмі підвищувалася на 28 %, а нирковий кліренс метотрексату знижувався на 13 %. При одночасному прийомі церикоксибу та метотрексату рекомендується вести спостереження щодо можливої появи токсичних ефектів метотрексату. Пероральні контрацептиви. Еторикоксиб у дозі 60 мг при одночасному прийомі протягом 21 дня з пероральними контрацептивами, що містять 35 мкг етинілестрадіолу (ЕЕ) та від 0,5 мг до 1 мг норетиндрону, збільшував AUC0-24 год ЕЕ на 37 % у рівноважному стані. Прийом церикоксиксу в дозі 120 мг у поєднанні з вищевказаними пероральними контрацептивами (одночасно або з інтервалом 12 годин) збільшував AUC0-24год. ЕЕ на 50-60% у рівноважному стані. Це збільшення концентрації ЕЕ слід враховувати при виборі перорального контрацептиву для одночасного застосування з церикоксибом. Подібна взаємодія може спричинити збільшення частоти розвитку небажаних явищ, пов'язаних із застосуванням пероральних контрацептивів (наприклад, венозних тромбоемболій у жінок із групи ризику). Замісна гормональна терапія (ЗГТ). Призначення еторікоксибу в дозі 120 мг одночасно з препаратами для ЗГТ, що містять кон'юговані естрогени в дозі 0,625 мг протягом 28 днів, збільшує середнє рівноважне значення AUC0-24 год некон'югованого естрону (41 %), еквіліну (76 %) та 17-2 %). Вплив доз еторикоксибу, рекомендованих для тривалого застосування (30, 60 та 90 мг), не вивчався. Еторикоксиб у дозі 120 мг змінював експозицію (AUC0-24год) даних естрогенних компонентів менш ніж удвічі порівняно з монотерапією кон'югованими естрогенами при збільшенні дози з 0,625 до 1,25 мг. Клінічне значення таких збільшення невідомо, застосування більш високих доз кон'югованих естрогенів у поєднанні з еторикоксибом не вивчалося.Підвищення концентрації естрогенів слід брати до уваги при виборі гормональної терапії в період постменопаузи при одночасному призначенні з етороксібом, оскільки збільшення експозиції естрогенів може підвищувати ризик розвитку небажаних явищ, пов'язаних із ЗГТ. Преднізон/Преднізолон. У дослідженнях лікарських взаємодій эторикоксиб не впливав на клінічно значущий вплив на фармакокінетику преднізону/преднізолону. Дігоксин. При застосуванні эторикоксибу в дозі 120 мг один раз на день протягом 10 днів у здорових добровольців не спостерігалося зміни рівноважної AUC0-24год дигоксину в плазмі або впливу на його виведення нирками. При цьому спостерігалося збільшення Стах дигоксину приблизно на 33%. Таке підвищення, як правило, не є важливим для більшості пацієнтів. Тим не менш, при одночасному застосуванні церикоксибу та дигоксину слід спостерігати за станом пацієнтів із високим ризиком прояву токсичної дії дигоксину. Вплив еторикоксибу на препарати, що метаболізуються сульфотрансферазами. Еторикоксиб є інгібітором сульфотрансферази людини (зокрема, SULT1E1) і може підвищувати концентрацію ЕЕ у сироватці крові. У зв'язку з тим, що в даний час отримано недостатньо даних про ефекти різних сульфотрансфераз, а їхня клінічна значущість для застосування багатьох лікарських препаратів ще вивчається, доцільно з обережністю призначати церикоксиб одночасно з іншими лікарськими препаратами, що метаболізуються сульфотрансферазами людини (наприклад, пероральний сальбутамол і ). Вплив етерокіксібу на препарати, що метаболізуються ізоферментами системи цитохромів. Грунтуючись на результатах досліджень in vitro, не очікується, що эторикоксиб інгібуватиме ізоферменти цитохрому Р450 (CYP) 1А2, 2С9, 2С19, 2D6, 2Е1 або 3А4. У дослідженні у здорових добровольців щоденне застосування церикоксибу в дозі 120 мг не впливало на активність ізоферменту CYP3A4 печінки при оцінці за допомогою еритроміцинового дихального тесту.Спосіб застосування та дозиВсередину, незалежно від їди, запиваючи невеликою кількістю води. Дія препарату реалізується швидше при прийомі натще. Внаслідок можливого підвищення ризику серцево-судинних ускладнень слід використовувати мінімальну ефективну дозу мінімально можливим курсом. Остеоартроз: рекомендована доза етерокіксібу становить 30 мг 1 раз на день. У разі недостатнього ефекту добова доза препарату може бути збільшена до 60 мг на добу. Добова доза при остеоартрозі не повинна перевищувати 60 мг. Ревматоїдний артрит та анкілозуючий спондиліт: рекомендована доза еторикоксібу становить 60 мг 1 раз на день. У пацієнтів із недостатнім клінічним ефектом можливе збільшення добової дози препарату до 90 мг один раз на день. Після клінічної стабілізації захворювання можливе зниження дози до 60 мг один раз на день. У разі відсутності ознак клінічного покращення слід розглянути можливість застосування інших методів лікування. Добова доза не повинна перевищувати 90 мг. Гострий подагричний артрит: рекомендована доза церикоксибу в гострому періоді становить 120 мг 1 раз на день. Тривалість застосування препарату у дозі 120 мг не перевищує 8 днів. Добова доза не повинна перевищувати 120 мг. Гострий біль після стоматологічних операцій: рекомендована доза еторикоксибу становить 90 мг 1 раз на день. Еторикоксиб слід застосовувати лише у гострий симптоматичний період тривалістю не більше 3 днів. Добова доза для усунення болю після стоматологічних операцій не повинна перевищувати 90 мг. Деяким пацієнтам можуть знадобитися додаткові засоби для забезпечення адекватного рівня знеболювання у післяопераційному періоді протягом триденного періоду терапії церикоксибом. Особливі групи пацієнтів Літні пацієнти: корекція дози не потрібна. Як і при застосуванні інших препаратів, еторикоксиб слід застосовувати з обережністю. Діти: застосування еторикоксибу у пацієнтів віком до 16 років протипоказано. Порушення функції печінки: незалежно від показання до застосування пацієнтам з порушеннями функції печінки легкого ступеня тяжкості (5-6 балів за шкалою Чайлд-П'ю) не слід перевищувати дозу 60 мг 1 раз на день, пацієнтам з порушеннями функції печінки середнього ступеня тяжкості (7 -9 балів за шкалою Чайлд-Пью) – 30 мг 1 раз на день. Рекомендується бути обережним при застосуванні препарату у пацієнтів з порушеннями функції печінки середнього ступеня тяжкості, оскільки клінічний досвід застосування препарату у даної групи пацієнтів обмежений. У зв'язку з відсутністю клінічного досвіду застосування препарату у пацієнтів з тяжкими порушеннями функції печінки (≥10 балів за шкалою Чайлд-П'ю) препарат протипоказаний для цієї групи пацієнтів. Порушення функції нирок: не потрібна корекція дози препарату при застосуванні у пацієнтів із КК ≥30 мл/хв. Застосування препарату у пацієнтів із ККПередозуванняУ клінічних дослідженнях прийом еторикоксибу в разовій дозі до 500 мг і багаторазовий прийом до 150 мг/день протягом 21 дня не викликав суттєвих токсичних ефектів. Були отримані повідомлення про гостре передозування еторикоксибом, однак, у більшості випадків про небажані реакції не повідомлялося. Найчастіші небажані реакції відповідали профілю безпеки церикоксибу (наприклад, порушення з боку шлунково-кишкового тракту, кардіоренальні явища). У разі передозування доцільно вживати звичайні підтримувальні заходи, такі як видалення невсмоктаного препарату із ШКТ, клінічне спостереження і, при необхідності, підтримуюча терапія. Еторікоксиб не виводиться при гемодіалізі; виведення еторикоксибу при перитонеальному діалізі не вивчалося.Запобіжні заходи та особливі вказівкиВплив на ШКТ У пацієнтів, які отримували еторикоксиб, спостерігалися ускладнення з боку верхніх відділів шлунково-кишкового тракту (перфорації, виразки або кровотечі), іноді з летальним кінцем. Рекомендується бути обережним при лікуванні пацієнтів з високим ризиком розвитку ускладнень з боку шлунково-кишкового тракту при застосуванні нестероїдних протизапальних засобів, зокрема, у літніх пацієнтів, що одночасно застосовують інші нестероїдні протизапальні засоби, ацетилсаліцилову кислоту або у пацієнтів із захворюваннями шлунково-кишкового тракту в анамнезі, такими як виразка та шлунково-кишкова кровотеча. Існує додатковий ризик розвитку небажаних реакцій з боку шлунково-кишкового тракту (шлунково-кишкові виразки або інші ускладнення з боку шлунково-кишкового тракту) при одночасному застосуванні церикоксибу та ацетилсаліцилової кислоти (навіть у низьких дозах). У довгострокових клінічних дослідженнях не спостерігалося достовірних відмінностей щодо безпеки для ШКТ при застосуванні селективних інгібіторів ЦОГ-2 у комбінації з ацетилсаліциловою кислотою порівняно із застосуванням нестероїдних протизапальних засобів у комбінації з ацетилсаліциловою кислотою. Вплив на серцево-судинну систему Результати клінічних досліджень свідчать про те, що застосування лікарських препаратів класу селективних інгібіторів ЦОГ-2 пов'язано з підвищеним ризиком тромбоутворення (особливо інфаркту міокарда (ІМ) та інсульту) порівняно з плацебо та деякими НПЗЗ. Ризик розвитку серцево-судинних ускладнень при застосуванні селективних інгібіторів ЦОГ-2 може зростати зі збільшенням дози та тривалості лікування, тому слід застосовувати церикоксиб протягом максимально короткого періоду часу та у найнижчій ефективній добовій дозі. Необхідно періодично оцінювати потребу пацієнта у симптоматичному лікуванні та відповідь на терапію, особливо у пацієнтів з ОА. Пацієнтам з відомими факторами ризику розвитку серцево-судинних ускладнень (наприклад, артеріальна гіпертензія, гіперліпідемія, цукровий діабет, куріння) церикоксиб необхідно призначати тільки після ретельної попередньої оцінки співвідношення користі-ризику. Селективні інгібітори ЦОГ-2 не є заміною ацетилсаліцилової кислоти при профілактиці серцево-судинних захворювань через відсутність антитромбоцитарного ефекту, тому не слід припиняти застосування антиагрегантних препаратів. Вплив на функцію нирок Ниркові простагландини можуть відігравати компенсаторну роль у підтримці ниркової перфузії. Тому за наявності умов, що негативно впливають на ниркову перфузію, призначення еторикоксибу може призвести до зменшення утворення простагландинів і, як наслідок, зниження ниркового кровотоку, і тим самим призвести до погіршення функції нирок. Найбільший ризик розвитку цієї реакції виникає у пацієнтів із значним зниженням функції нирок, некомпенсованою серцевою недостатністю або цирозом печінки в анамнезі. У таких пацієнтів необхідно проводити моніторинг функції нирок. Затримка рідини, набряки та артеріальна гіпертензія Як і у разі застосування інших препаратів, що інгібують синтез простагландинів, у пацієнтів, які приймають еторикоксиб, спостерігалися затримка рідини, набряки та артеріальна гіпертензія. Застосування будь-яких нестероїдних протизапальних засобів, включаючи церикоксикс, може бути пов'язане з виникненням або рецидивом хронічної (застійної) серцевої недостатності. Інформація про дозозалежну реакцію для церикоксибу наведена в розділі "Фармакологічні властивості". Слід виявляти обережність при призначенні церикоксибу пацієнтам із серцевою недостатністю в анамнезі, дисфункцією лівого шлуночка, артеріальною гіпертензією та пацієнтам з уже наявними набряками, що виникли з будь-якої іншої причини. При появі клінічних ознак погіршення стану у таких пацієнтів слід вжити відповідних заходів, включаючи скасування еторікоксибу. Застосування еторикоксибу, особливо у високих дозах, може бути пов'язане з розвитком більш тяжкої артеріальної гіпертензії, ніж при застосуванні деяких інших нестероїдних протизапальних засобів та селективних інгібіторів ЦОГ-2. Тому під час лікування церикоксибом слід звернути особливу увагу на моніторинг АТ, який має контролюватись протягом двох тижнів після початку лікування та періодично надалі. При значному підвищенні артеріального тиску слід розглянути альтернативне лікування. Вплив на функцію печінки Підвищення активності аланінамінотрансферази (АЛТ) та/або аспартатамінотрансферази (ACT) (приблизно в три або більше рази щодо верхньої межі норми) було зареєстровано у клінічних дослідженнях приблизно у 1% пацієнтів, які отримували еторикоксиб протягом терміну до одного року у дозах 30 мг, 60 мг та 90 мг на день. Необхідно спостерігати за станом усіх пацієнтів із симптомами та/або ознаками дисфункції печінки, а також пацієнтів із зміненими лабораторними показниками функції печінки. Якщо виникають ознаки печінкової недостатності або показники функції печінки значно відхиляються від норми (втричі вище за верхню межу норми), прийом еторикоксибу повинен бути припинений. Загальні рекомендації Якщо під час лікування у пацієнтів погіршується будь-яка з функцій органів або систем органів, описаних вище, повинні бути вжиті відповідні заходи та розглянуто питання про скасування еторикоксибу. При застосуванні эторикоксибу у пацієнтів похилого віку та у пацієнтів з порушенням функції нирок, печінки або серця необхідне відповідне медичне спостереження. З обережністю слід розпочинати лікування ерикоксибом пацієнтам із зневодненням. Перед початком терапії церикоксибом рекомендується провести регідратацію. У період постмаркетингового спостереження при застосуванні НПЗП та деяких селективних інгібіторів ЦОГ-2 дуже рідко повідомлялося про розвиток серйозних реакцій шкіри. Деякі з них, у тому числі ексфоліативний дерматит, синдром Стівенса-Джонсона та токсичний епідермальний некроліз, були з смертю. Ризик розвитку цих реакцій найбільш високий на початку курсу терапії, здебільшого протягом першого місяця лікування. Повідомлялося про розвиток серйозних реакцій гіперчутливості, таких як анафілаксія та ангіоневротичний набряк, у пацієнтів, які отримували еторикоксиб. Застосування деяких селективних інгібіторів ЦОГ-2 супроводжувалося підвищеним ризиком розвитку шкірних реакцій у пацієнтів із якоюсь лікарською алергією в анамнезі. Еторикоксиб повинен бути скасований при першій появі висипу на шкірі,уражень слизової оболонки або будь-якої іншої ознаки гіперчутливості. Застосування еторикоксибу може маскувати лихоманку та інші ознаки запалення. Застосування еторикоксибу, як і інших препаратів, що інгібують ЦОГ та синтез простагландинів, не рекомендується жінкам, які планують вагітність (див. розділ "Застосування при вагітності та в період грудного вигодовування"). Оболонка таблетки містить лактозу. Пацієнтам з такими рідкісними вродженими захворюваннями, як непереносимість лактози, дефіцит лактази або глюкозогалактозна мальабсорбція, не слід приймати цей препарат. Вплив на здатність до керування автотранспортом та управління механізмами Пацієнтам, у яких на фоні застосування церикоксибу відзначаються епізоди запаморочення, сонливості чи слабкості, слід утриматися від керування транспортними засобами та роботи з механізмами.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
353,00 грн
179,00 грн
Склад, форма випуску та упаковкаПігулки - 1 таб. Активні речовини: еторикоксиб – 60 мг; Допоміжні речовини: кальцію гідрофосфат безводний – 26 мг, целюлоза мікрокристалічна – 25.5 мг, повідон К30 – 6 мг, магнію стеарат – 1 мг, кроскармелоза натрію – 1.5 мг; Склад оболонки таблетки: Опадрай II зелений 32К510002 - 4 мг: гіпромелоза 15 cPs 1.6 мг, лактози моногідрат 1.12 мг, титану діоксид 0.628 мг, тріацетин 0.32 мг, індигокармін алюмінієвий 0.6 мг. Таблетки, покриті плівковою оболонкою, 30 мг, 60 мг, 90 мг та 120 мг. По 7 пігулок в Аl/Аl блістер. По 1 блістеру разом з інструкцією із застосування в картонну пачку. По 10 пігулок в Аl/Аl блістер. По 1, 2, 3, 5, 6, 9, 10 блістерів разом з інструкцією із застосування в картонну пачку. По 14 пігулок в Аl/Аl блістер. По 1,2, 4, 6, 7 блістерів разом із інструкцією із застосування в картонну пачку.Опис лікарської формиТаблетки, покриті плівковою оболонкою темно-зеленого кольору, круглі, двоопуклі.Фармакотерапевтична групаНестероїдні протизапальні препарати (НПЗЗ).ФармакокінетикаВсмоктування Эторикоксиб швидко всмоктується прийому внутрішньо. Абсолютна біодоступність прийому внутрішньо становить близько 100%. При застосуванні препарату у дорослих натще в дозі 120 мг один раз на день до досягнення рівноважного стану максимальна концентрація в плазмі (Сmах) становить 3,6 мкг/мл. Час досягнення Сmах (Тmах) становить приблизно 1 годину після прийому препарату. Середня геометрична площа під кривою "концентрація – час" (AUC0-24ч) склала 37,8 мкг * год / мл. Фармакокінетика церикоксибу в діапазоні терапевтичних доз має лінійний характер. При прийомі эторикоксиба в дозі 120 мг під час їжі (їжа з високим вмістом жирів) не спостерігалося клінічно значущого впливу на ступінь абсорбції. Швидкість абсорбції при цьому змінювалася, що призводило до зниження Сmах на 36% і збільшення Тmах на 2 год. Ці дані не є клінічно значущими. У клінічних дослідженнях церикоксиб застосовувався незалежно від їди. Розподіл Еторікоксиб приблизно на 92% зв'язується з білками плазми у людини в діапазоні концентрацій від 0,05 до 5 мкг/мл. Об'єм розподілу у рівноважному стані (VdSS) становить близько 120 л. Еторикоксиб проникає через плацентарний бар'єр у щурів та кролів та гематоенцефалічний бар'єр у щурів. Метаболізм Еторикоксиб екстенсивно метаболізується, У людини виявлено п'ять метаболітів церикоксиксу. Основним метаболітом є 6'-карбоксиацетилеторикоксиб, що утворюється в результаті подальшого окислення 6'-гідроксиметилеторикоксибу. Ці основні метаболіти не мають помітної активності або слабо інгібують ЦОГ-2. Жоден із цих метаболітів не інгібує ЦОГ-1. Виведення Після одноразового внутрішньовенного введення здоровим добровольцям міченого радіоактивного церикоксибу в дозі 25 мг 70 % церикоксибу виводилося через нирки та 20 % – через кишечник, переважно у вигляді метаболітів. Менше 2% виявлялося у незміненому вигляді. Виведення еторикоксибу відбувається в основному шляхом метаболізму в печінці з подальшим виведенням нирками. Рівноважні концентрації эторикоксиба досягаються при щоденному прийомі в дозі 120 мг протягом 7 днів з коефіцієнтом кумуляції близько 2, що відповідає періоду напіввиведення близько 22 год. Плазмовий кліренс після внутрішньовенного введення 25 мг становить приблизно 50 мл/хв. Особливі групи пацієнтів Стать: фармакокінетичні параметри препарату у чоловіків та жінок не відрізняються. Літні пацієнти: фармакокінетика препарату у пацієнтів віком понад 65 років порівнянна з фармакокінетикою у пацієнтів молодшого віку. Діти: фармакокінетика еторикоксибу у дітей (60 кг, які приймали церикоксиб у дозі 90 мг 1 раз на день), була аналогічна фармакокінетиці у дорослих, які приймали церикоксиб у дозі 90 мг 1 раз на день. Безпека та ефективність застосування церикоксибу у дітей не встановлена. Печінкова недостатність: у пацієнтів з печінковою недостатністю легкого ступеня тяжкості (5-6 балів за шкалою Чайлд-П'ю) прийом еторикоксибу в дозі 60 мг 1 раз на день супроводжувався збільшенням показника AUC приблизно на 16% порівняно зі здоровими добровольцями, які приймали препарат у тій ж дозі. У пацієнтів з печінковою недостатністю середнього ступеня тяжкості (7-9 балів за шкалою Чайлд-П'ю), які отримували еторикоксиб у дозі 60 мг один раз на день через день, середнє значення AUC було таким же, як у здорових добровольців, які приймали еторикоксиб у дозі 60 мг раз на день щодня. Застосування еторикоксибу в дозі 30 мг один раз на день не вивчалося у цій групі пацієнтів. Клінічні та фармакокінетичні дані досліджень у пацієнтів з тяжкою печінковою недостатністю (>10 балів за шкалою Чайлд-П'ю) відсутні. Ниркова недостатність: фармакокінетичні показники одноразового застосування церикоксибу в дозі 120 мг у пацієнтів з нирковою недостатністю помірного та тяжкого ступеня та у пацієнтів з термінальною стадією хронічної ниркової недостатності, які перебувають на гемодіалізі, суттєво не відрізняються від показників у здорових добровольців. Гемодіаліз незначно впливає на виведення препарату (кліренс при діалізі – близько 50 мл/хв).ФармакодинамікаЕторикоксиб при пероральному прийомі в терапевтичних концентраціях є селективним інгібітором циклооксигенази типу 2 (ЦОГ-2). У дослідженнях з клінічної фармакології церикоксиб дозозалежно інгібував ЦОГ-2, не впливаючи на ЦОГ-1 при застосуванні доз до 150 мг на день. Еторикоксиб не пригнічував синтез простагландинів у слизовій оболонці шлунка і не впливав на функцію тромбоцитів. ЦОГ відповідає за синтез простагландинів. Виділено дві ізоформи цього ферменту - ЦОГ-1 та ЦОГ-2. ЦОГ-2 є ізоферментом, який індукується під дією прозапальних медіаторів і розглядається як основний фермент, який відповідає за синтез простаноїдних медіаторів болю, запалення та лихоманки. ЦОГ-2 бере участь у процесах овуляції, імплантації та закриття артеріальної протоки, регуляції функції нирок, центральної нервової системи (індукція лихоманки, відчуття болю, когнітивна функція), а також може грати певну роль у процесі загоєння виразок. ЦОГ-2 була виявлена у тканинах, що оточують виразки шлунка у людини, але її значення для загоєння виразки не встановлено. Ефективність У пацієнтів з остеоартрозом (ОА) церикоксиб при застосуванні в дозі 60 мг один раз на день викликав достовірне зменшення болю та покращення оцінки свого стану пацієнтами. Ці сприятливі ефекти спостерігалися вже другого дня лікування і зберігалися протягом 52 тижнів. Дослідження еторикоксибу в дозі 30 мг один раз на день (із застосуванням подібних методів оцінки) продемонстрували ефективність препарату порівняно з плацебо протягом усього періоду лікування (12 тижнів). У дослідженні, яке проводилося з метою визначення оптимальної дози, еторикоксиб у дозі 60 мг продемонстрував достовірно більш виражене поліпшення, ніж у дозі 30 мг для всіх 3 первинних кінцевих точок через 6 тижнів лікування. Застосування дози 30 мг на лікування ОА суглобів кистей рук не вивчалося. У пацієнтів з ревматоїдним артритом (РА) прийом еторикоксибу в дозі 60 мг або 90 мг один раз на день забезпечував достовірне зменшення болю, запалення та покращення рухливості. Ці сприятливі ефекти зберігалися протягом 12-тижневого періоду лікування. Дослідження порівняння застосування церикоксибу в дозі 60 мг і 90 мг один раз на день для лікування РА показало, що обидва режими дозування забезпечували переважну ефективність терапії порівняно з плацебо. Доза церикоксибу 90 мг один раз на день перевищувала за ефективністю дозу 60 мг один раз на день при оцінці ефекту за допомогою Глобальної Шкали. % довірчий інтервал (ДІ): -4,98 мм; -0,45 мм). У пацієнтів із гострим подагричним артритом еторикоксиб у дозі 120 мг один раз на день протягом усього періоду лікування (8 днів) зменшував помірний та сильний біль у суглобах та запалення порівняно з індометацином у дозі 50 мг 3 рази на день. Зменшення болю відзначалося вже через 4 години після початку лікування. У пацієнтів з анкілозуючим спондилітом еторикоксиб при застосуванні в дозі 90 мг один раз на день забезпечував достовірне зменшення болю в спині, запалення, скутості, а також покращення рухової функції. Клінічна ефективність эторикоксиба спостерігалася вже другого дня лікування та зберігалася протягом усього періоду лікування (52 тижні). В іншому дослідженні, в рамках якого порівнювалася ефективність застосування церикоксибу в дозі 90 мг один раз на день та 60 мг один раз на день, цей препарат продемонстрував рівну ефективність порівняно з напроксеном у дозі 1000 мг один раз на день. Серед пацієнтів, у яких не було досягнуто адекватної клінічної відповіді на терапію протягом 6 тижнів при застосуванні церикоксибу у дозі 60 мг один раз на день, збільшення добової дози до 90 мг дозволяло покращити результати лікування, оцінені за допомогою шкали інтенсивності болю у спині. -100 мм візуально-аналогова шкала), порівняно з продовженням терапії еторікоксибом у дозі 60 мг один раз на день. Середнє поліпшення склало -2,70 мм (95% ДІ: 4,88 мм; -0,52 мм). У клінічному дослідженні з вивчення болю після стоматологічних операцій эторикоксиб у дозі 90 мг призначали раз на день протягом трьох днів. У підгрупі пацієнтів з помірним болем (при вихідній оцінці) еторикоксиб у дозі 90 мг продемонстрував знеболюючий ефект, аналогічний ібупрофену в дозі 600 мг (16,11 порівняно з 16,39, Р = 0,722) та більший, ніж при застосуванні комбінації парацетамол/ кодеїн у дозі 600 мг/60 мг (11,00; Р Безпека Програма MEDAL (Багатонаціональна Програма Оцінки Довгострокового Призначення Еторікоксибу та Диклофенаку при Артріті) Програма MEDAL була проспективною програмою оцінки безпеки на підставі серцево-судинних явищ за об'єднаними даними трьох рандомізованих подвійних сліпих активно-контрольованих досліджень: MEDAL, EDGE II та EDGE. Дослідження MEDAL являло собою дослідження, тривалість якого визначалася досягненням кінцевих точок (серцево-судинних явищ), воно включало 17804 пацієнта з ОА та 5700 пацієнтів з РА, які отримували еторикоксиб у дозі 60 мг (ОА) або 90 мг (ОА та РА) або ді у дозі 150 мг на день у середньому протягом 20,3 місяців (максимум 42,3 місяці, медіана 21,3 місяці). У цьому дослідженні реєстрували лише серйозні небажані явища та випадки вибуття з дослідження внаслідок будь-якого небажаного явища. У дослідженнях EDGE та EDGE II порівнювали безпеку прийому церикоксибу та диклофенаку для шлунково-кишкового тракту (ЖКТ). До дослідження EDGE було включено 7111 пацієнтів з ОА, які отримували еторикоксиб у дозі 90 мг на день (в 1,5 рази більше за дозу, рекомендовану при ОА) або диклофенак у дозі 150 мг на день протягом у середньому 9,1 місяців (максимум 16 , 6 місяців, медіана 11,4 місяців). У дослідження EDGE II було включено 4086 пацієнтів з РА, які отримували еторикоксиб у дозі 90 мг на день або диклофенак у дозі 150 мг на день протягом середньому 19,2 місяців (максимум 33,1 місяця, медіана 24 місяці). В об'єднаній програмі MEDAL аналізували дані щодо лікування 34701 пацієнтів з ОА або РА, середня тривалість лікування склала 17,9 місяців (максимум 42,3 місяці, медіана 16,3 місяців), при цьому приблизно 12800 пацієнтів отримували лікування протягом понад 24 місяців. Пацієнти, включені до програми, при вихідній оцінці мали широкий спектр серцево-судинних та шлунково-кишкових факторів ризику. Були виключені пацієнти, які мали в анамнезі нещодавно перенесений інфаркт міокарда (ІМ), аортокоронарне шунтування або черезшкірне коронарне втручання протягом 6 місяців перед включенням до дослідження. У дослідженнях дозволялося застосовувати гастропротектори та низькі дози аспірину. Загальна безпека Достовірних відмінностей між эторикоксибом та диклофенаком щодо частоти розвитку серцево-судинних тромботичних явищ виявлено не було. Кардіоренальні небажані явища найчастіше спостерігалися при прийомі церикоксибу в порівнянні з диклофенаком, ефект був дозозалежним (див. результати нижче). Небажані явища з боку шлунково-кишкового тракту та печінки достовірно частіше спостерігалися при прийомі диклофенаку, ніж при прийомі церикоксибу. Частота небажаних явищ у дослідженнях EDGE та EDGE II та небажаних явищ, визнаних серйозними або зажадали відміни лікування, у дослідженні MEDAL була вищою при прийомі еторикоксибу порівняно з диклофенаком. Результати дослідження безпеки щодо серцево-судинної системи Частота підтверджених серйозних тромботичних серцево-судинних небажаних явищ (включаючи серцеві, цереброваскулярні та явища з боку периферичної судинної системи) була порівнянна між групами, які отримували церикоксиб або диклофенак (дані наведені в таблиці нижче). Не виявлено статистично значимих відмінностей щодо частоти тромботичних явищ між еторикоксибом та диклофенаком у всіх проаналізованих підгрупах, включаючи категорії пацієнтів з підвищеним ризиком серцево-судинних ускладнень. Відносний ризик для підтверджених серйозних серцево-судинних небажаних тромботичних явищ був подібним при прийомі еторикоксібу в дозі 60 мг або 90 мг і диклофенаку в дозі 150 мг. Частота підтверджених тромботичних серцево-судинних серйозних небажаних явищ (Об'єднана програма MEDAL) Еторікоксиб(N=16819)25 836 пацієнто-років Диклофенак(N=16483)24 766 пацієнто-років Порівняння між видами лікування Частота 1 (95% ДІ) Частота 1 (95% ДІ) Відносний ризик (95% ДІ) Підтверджені тромботичні серцево-судинні серйозні небажані явища За виконання вимог протоколу (Per protocol) 1,24 (1,11; 1,38) 1,30 (1,17; 1,45) 0,95 (0,81; 1,11) Залежно від призначеного лікування (Intent-to-treat) 1,25 (1,14; 1,36) 1,19 (1,08; 1,30) 1,05 (0,93; 1,19) Підтверджені явища з боку серця За виконання вимог протоколу (Per protocol) 0,71 (0,61; 0,82) 0,78 (0,68; 0,90) 0,90 (0,74; 1,10) Залежно від призначеного лікування (Intent-to-treat) 0,69 (0,61; 0,78) 0,70 (0,62; 0,79) 0,99 (0,84; 1,17) Підтверджені цереброваскулярні явища За виконання вимог протоколу (Per protocol) 0,34 (0,28; 0,42) 0,32 (0,25; 0,40) 1,08 (0,80; 1,46) Залежно від призначеного лікування (Intent-to-treat) 0,33 (0,28; 0,39) 0,29 (0,24; 0,35) 1,12 (0,87; 1,44) Підтверджені явища з боку периферичної судинної системи За виконання вимог протоколу (Per protocol) 0,20 (0,15; 0,27) 0,22 (0,17; 0,29) 0,92 (0,63; 1,35) Залежно від призначеного лікування (Intent-to-treat) 0,24 (0,20; 0,30) 0,23 (0,18; 0,28) 1,08 (0,81; 1,44) 1 число явищ на 100 пацієнто-років; ДІ = довірчий інтервал; N = загальна кількість пацієнтів, які виконали вимоги протоколу. При виконанні вимог протоколу: всі явища, що розвинулися на тлі досліджуваної терапії або протягом 14 днів після її припинення (виключені пацієнти, які прийняли <75% досліджуваного препарату або приймали НПЗП >10% часу, що не входять до дослідження). Залежно від призначеного лікування: всі підтверджені явища, що розвинулися до закінчення дослідження (включно з пацієнтами, які могли піддаватися не включеним до дослідження втручанням після припинення прийому досліджуваних препаратів). Загальна кількість рандомізованих пацієнтів: n = 17412 для эторикоксиба і n = 17289 для диклофенаку. Смертність від серцево-судинних явищ, а також загальна смертність у групах лікування церикоксибом та диклофенаком були порівнянними. Кардіоренальні явища Приблизно у 50% пацієнтів, включених у дослідження MEDAL, при початковій оцінці в анамнезі було зареєстровано артеріальну гіпертензію. У проведеному дослідженні частота вибування внаслідок небажаних явищ, пов'язаних з артеріальною гіпертензією, була статистично значуще вищою під час прийому эторикоксиба проти диклофенаком. Частота небажаних явищ, пов'язаних з хронічною серцевою недостатністю (випадки вибування з дослідження або серйозні небажані явища), була подібною до груп еторікоксибу в дозі 60 мг і диклофенаку в дозі 150 мг, але була вищою для еторікоксибу в дозі 90 мг порівняно з диклофеном. дозі 150 мг (і статистично значуще вище для еторикоксибу в дозі 90 мг у порівнянні з диклофенаком у дозі 150 мг у дослідженні MEDAL у пацієнтів з ОА). Частота підтверджених небажаних явищ,пов'язаних з хронічною серцевою недостатністю (серйозних, які призвели до госпіталізації або необхідності невідкладної допомоги), була незначно вищою для церикоксибу порівняно з диклофенаком у дозі 150 мг, ефект був дозозалежним. Частота випадків вибування з дослідження внаслідок небажаних явищ, пов'язаних з набряками, була вищою для еторікоксибу в дозі 150 мг, порівняно з диклофенаком у дозі 150 мг, ефект був дозозалежним (статистично значимо для еторікоксибу в дозі 90 мг, але не для етороксиксу в дозі 60 мг).була вищою для эторикоксиба порівняно з диклофенаком в дозі 150 мг, ефект був дозозалежним (статистично значуще для етіроксиксібу в дозі 90 мг, але не для етіроксиксібу в дозі 60 мг).була вищою для эторикоксиба порівняно з диклофенаком в дозі 150 мг, ефект був дозозалежним (статистично значуще для етіроксиксібу в дозі 90 мг, але не для етіроксиксібу в дозі 60 мг). Результати оцінки кардіоренальної безпеки у дослідженнях EDGE та EDGE II узгоджуються з результатами у дослідженні MEDAL В окремих дослідженнях програми MEDAL абсолютна частота вибування з дослідження в будь-якій групі лікування при прийомі еторикоксибу (60 мг або 90 мг) становила до 2,6% при артеріальній гіпертензії, до 1,9% при набряках, і до 1,1% при хронічній серцевої недостатності. У пацієнтів, які приймали церикоксиб у дозі 90 мг, частота вибуття з дослідження була вищою, ніж у пацієнтів, які приймали церикоксиб у дозі 60 мг. Результати оцінки переносимості з боку ШКТ у Програмі MEDAL У кожному з трьох досліджень, що входять до програми MEDAL, частота вибування з дослідження для будь-яких клінічних небажаних явищ з боку шлунково-кишкового тракту (наприклад, диспепсія, біль у животі, виразки) була достовірно нижчою для еторикоксибу порівняно з диклофенаком. Частота вибуття з дослідження внаслідок небажаних клінічних явищ з боку шлунково-кишкового тракту на 100 пацієнто-років за весь період дослідження становила: 3,23 для еторикоксибу та 4,96 для диклофенаку в дослідженні MEDAL; 9,12 для эторикоксиба і 12,28 для диклофенаку у дослідженні EDGE; 3,71 для еторикоксибу та 4,81 для диклофенаку в дослідженні EDGE II. Результати оцінки безпеки щодо ШКТ у Програмі MEDAL До небажаних явищ з боку верхніх відділів шлунково-кишкового тракту були віднесені перфорації, виразки та кровотечі. Ускладнені небажані явища з боку верхніх відділів шлунково-кишкового тракту включали перфорацію, непрохідність та ускладнені кровотечі; неускладнені явища включали неускладнені кровотечі та неускладнені виразки. При прийомі эторикоксиба порівняно з диклофенаком загальна частота небажаних явищ з боку верхніх відділів шлунково-кишкового тракту була достовірно нижчою. Достовірних відмінностей між етерокіксібом і диклофенаком за частотою ускладнених небажаних явищ виявлено не було. Для випадків кровотеч із верхніх відділів шлунково-кишкового тракту (ускладнених та неускладнених) не було виявлено достовірних відмінностей між еторикоксибом та диклофенаком.Перевага церикоксибу порівняно з диклофенаком щодо ускладнень з боку верхніх відділів ШКТ не була статистично значущою у пацієнтів, які одночасно приймали аспірин у низьких дозах (близько 33% пацієнтів). Частота підтверджених ускладнених та неускладнених клінічних небажаних явищ з боку верхніх відділів шлунково-кишкового тракту на 100 пацієнто-років (перфорації, виразки та кровотечі) склала 0,67 (95 % ДІ: 0,57; 0,77) для церикоксиксу та 0,97 (95 % ДІ: 0,85; 1,10) для диклофенаку, відносний ризик склав 0,69 (95% ДІ: 0,57; 0,83). При оцінці частоти підтверджених клінічних небажаних явищ з боку верхніх відділів шлунково-кишкового тракту у пацієнтів похилого віку максимальне зниження спостерігалося у пацієнтів у віці ≥75 років у групі церикоксибу в порівнянні з диклофенаком - 1,35 (95 % ДІ: 0,94; 1,87) та 2,78 (95% ДІ: 2,14; 3,56) на 100 пацієнто-років відповідно. Частота підтверджених небажаних явищ з боку нижніх відділів шлунково-кишкового тракту (перфорація тонкої або товстої кишки, непрохідність, кровотеча) достовірно не розрізнялася між групами, які приймали церикоксиб та диклофенак. Результати оцінки безпеки щодо печінки у Програмі MEDAL При прийомі эторикоксиба порівняно з диклофенаком спостерігалася статистично достовірно нижча частота вибуття з дослідження через небажані явища з боку печінки. В об'єднаній програмі MEDAL 0,3% пацієнтів, які приймали еторикоксиб, та 2,7% пацієнтів, які приймали диклофенак, вибули з дослідження через небажані явища з боку печінки. Частота небажаних явищ на 100 пацієнто-років склала 0,22 для церикоксиксу і 1,84 для диклофенаку (р Додаткові дані щодо безпеки, пов'язані з тромботичними серцево-судинними явищами У клінічних дослідженнях, за винятком Програми MEDAL, приблизно 3100 пацієнтів отримували церикоксикс у дозі ≥60 мг на день протягом 12 тижнів та довше. У цих дослідженнях не було виявлено помітних відмінностей у частоті підтверджених серйозних тромботичних серцево-судинних явищ у пацієнтів, які отримували церикоксиб у дозі ≥60 мг, плацебо або нестероїдні протизапальні засоби, що не містять напроксен. Однак у порівнянні з пацієнтами, які отримували напроксен у дозі 500 мг двічі на день, частота цих явищ була вищою у пацієнтів, які отримували еторикоксиб. Різниця в антиагрегантній активності між деякими нестероїдними протизапальними засобами, що інгібують ЦОГ-1, та селективними інгібіторами ЦОГ-2 може мати клінічне значення у пацієнтів із групи ризику тромбоемболічних подій. Селективні інгібітори ЦОГ-2 пригнічують утворення системного (і, можливо, ендотеліального) простацикліну,не впливаючи на тромбоцитарний тромбоксан. Клінічна значимість цих спостережень встановлено. Додаткові дані з безпеки щодо ШКТ У двох 12-тижневих подвійних сліпих ендоскопічних дослідженнях кумулятивна частота розвитку гастродуоденальних виразок була значно нижчою у пацієнтів, які отримували церикоксиб у дозі 120 мг один раз на день, ніж у пацієнтів, які отримували напроксен 500 мг двічі на день. або ібупрофен 800 мг тричі на день. Частота розвитку виразок при призначенні церикоксибу була вищою порівняно з плацебо. Дослідження ниркової функції у пацієнтів похилого віку У рандомізованому подвійному сліпому плацебо-контрольованому дослідженні в паралельних групах оцінювався вплив 15-денної терапії церикоксибом (90 мг), целекоксибом (200 мг двічі на день), напроксеном (500 мг двічі на день) порівняно з плацебо на виведення натрію. , артеріальний тиск (АТ) та інші параметри функції нирок у пацієнтів віком від 60 до 85 років, які отримували раціон з обмеженим споживанням натрію до 200 мекв/день. Еторикоксиб, целекоксиб і напроксен мали подібний вплив на виведення натрію нирками через 2 тижні лікування. Всі активні препарати порівняння показали збільшення систолічного АТ порівняно з плацебо, однак, еторикоксиб викликав статистично значуще збільшення систолічного АТ на 14-й день порівняно з целекоксибом і напроксеном (середня зміна систолічного АТ порівняно з вихідним: етороксіб 7,7 мм рт. ст., целекоксиб 2,4 мм рт.ст., напроксен 3,6 мм рт.ст.).Показання до застосуванняСимптоматична терапія остеоартрозу, ревматоїдного артриту, анкілозуючого спондиліту, болю та запалення, пов'язаних із гострим подагричним артритом. Короткострокова терапія помірного гострого болю після стоматологічних операцій.Протипоказання до застосуванняПідвищена чутливість до еторикоксибу або будь-якої з допоміжних речовин препарату. Виразкова хвороба шлунка та 12-палої кишки у стадії загострення, активна шлунково-кишкова кровотеча. Бронхіальна астма, бронхоспазм, гострий риніт, поліпоз носа, ангіоневротичний набряк, кропив'янка або алергічні реакції після прийому ацетилсаліцилової кислоти або нестероїдних протизапальних препаратів (НПЗЗ), у тому числі інгібіторів ЦОГ-2, в анамнезі. Вагітність та період грудного вигодовування. Тяжкі порушення функції печінки (сироватковий альбумін 10 балів за шкалою Чайлд-П'ю). Тяжка ниркова недостатність (КК Діти та підлітки до 16 років. Запальні захворювання кишок. Хронічна серцева недостатність (II-IV функціональний клас за NYHA). Неконтрольована артеріальна гіпертензія (АТ стабільно вищий за 140/90 мм рт. ст.). Підтверджена ішемічна хвороба серця, захворювання периферичних артерій та/або цереброваскулярні захворювання. Дефіцит лактази, непереносимість лактози, глюкозо-галактозна мальабсорбція. Підтверджена гіперкаліємія. З обережністю: Пацієнти з підвищеним ризиком розвитку ускладнень з боку шлунково-кишкового тракту (виразкова ураження шлунково-кишкового тракту або шлунково-кишкова кровотеча в анамнезі, наявність інфекції Helicobacter Pylori, одночасне застосування інших нестероїдних протизапальних засобів, у тому числі ацетилсаліцилової кислоти, літній вік). Пацієнти, які мають в анамнезі фактори ризику серцево-судинних ускладнень (дисліпідемія/гіперліпідемія, цукровий діабет, артеріальна гіпертензія, куріння, серцева недостатність, порушення функції лівого шлуночка, набряки та затримка рідини в організмі). Печінкова недостатність (5-9 балів за класифікацією Чайлд-П'ю). Пацієнти з дегідратацією. Пацієнти з порушеннями функції нирок (КК Пацієнти з попереднім значним зниженням функції нирок, з ослабленою функцією нирок, декомпенсованою серцевою недостатністю або цирозом печінки, що перебувають у групі ризику при тривалому застосуванні нестероїдних протизапальних засобів. Супутня терапія антикоагулянтами (наприклад, варфарин), антиагрегантами (наприклад, ацетилсаліцилова кислота, клопідогрел), препаратами, що метаболізуються сульфотрансферазами.Вагітність та лактаціяВагітність В даний час клінічних даних про застосування еторикоксибу при вагітності відсутні. У дослідженнях на тваринах спостерігалася токсична дія на репродуктивну систему. Потенційний ризик для жінок під час вагітності невідомий. Застосування еторикоксибу, як і інших лікарських препаратів, що інгібують синтез простагландинів, у III триместрі вагітності може призводити до придушення скорочень матки та передчасного закриття артеріальної протоки. Еторикоксиб протипоказаний при вагітності. Якщо під час лікування настала вагітність, церикоксиб необхідно відмінити. Грудне годування У лактуючих щурів еторикоксиб виділяється з молоком. Досліджень, що підтверджують виділення еторикоксибу з грудним молоком у жінок, не проводилося. Жінки, які приймають еторикоксиб, повинні припинити грудне вигодовування. Фертильність Застосування еторикоксибу, як і інших препаратів, що інгібують ЦОГ-2 або синтез простагландинів, не рекомендується жінкам, які планують вагітність.Побічна діяРезюме профілю безпеки Безпека застосування церикоксибу оцінювалася у клінічних дослідженнях за участю 9295 пацієнтів, у тому числі 6757 пацієнтів з ОА, РА, хронічним болем у нижній частині спини та анкілозуючим спондилітом (приблизно 600 пацієнтів з ОА або РА отримували лікування протягом одного року або більше). Профіль небажаних реакцій був подібним у пацієнтів з ОА або РА, які отримували еторикоксиб протягом одного року або довше. У клінічному дослідженні гострого подагричного артриту пацієнти отримували церикоксиб у дозі 120 мг 1 раз на день протягом 8 днів. Профіль небажаних явищ у цьому дослідженні був загалом таким самим, як і в об'єднаних дослідженнях ОА, РА та хронічного болю в нижній частині спини. Для оцінки безпеки щодо серцево-судинної системи були об'єднані дані трьох активних контрольованих досліджень, у яких брали участь 17412 пацієнтів з ОА або РА, які отримували еторикоксиб у дозі 60 мг або 90 мг, середня тривалість досліджень склала приблизно 18 місяців. У клінічних дослідженнях гострого післяопераційного болю, пов'язаного з проведенням стоматологічної операції, у яких 614 пацієнтів отримували еторикоксиб у дозі 90 мг або 120 мг, профіль небажаних ефектів загалом був подібним до профілю в об'єднаних дослідженнях ОА, РА та хронічного болю в нижній частині спини. Табличне резюме небажаних реакцій У таблиці перераховані небажані реакції, які були зареєстровані з більшою частотою при застосуванні препарату, ніж у групі плацебо, у клінічних дослідженнях, що включали пацієнтів з ОА, РА, хронічним болем у нижній частині спини або анкілозуючим спондилітом (еторикоксиб призначався у дозі 30 мг, 60 мг або 90 мг з підвищенням дози до рекомендованої протягом 12 тижнів), у програмі MEDAL, де дослідження тривали до 3,5 років, у короткострокових дослідженнях гострого болю (протягом 7 днів), а також отримані під час постмаркетингового застосування. Класифікація систем органів Небажана реакція Частота 1 Інфекційні та паразитарні захворювання альвеолярний остит часто гастроентерит, інфекції верхніх дихальних шляхів, інфекції сечовивідних шляхів не часто Порушення з боку крові та лімфатичної системи анемія (в основному в результаті шлунково-кишкової кровотечі), лейкопенія, тромбоцитопенія не часто Порушення з боку імунної системи реакції гіперчутливості 2,4 не часто ангіоневротичний набряк, анафілактичні/анафілактоїдні реакції, у тому числі шок 2 рідко Порушення з боку обміну речовин та харчування набряки/затримка рідини часто посилення або зниження апетиту, збільшення маси тіла не часто Порушення психіки тривога, депресія, зниження ясності мислення, галюцинації 2 не часто сплутаність свідомості 2 , неспокій 2 рідко Порушення з боку нервової системи запаморочення, головний біль часто порушення смаку, безсоння, парестезія/гіпестезія, сонливість не часто Порушення з боку органу зору нечіткість зору, кон'юнктивіт не часто Порушення з боку органу слуху та лабіринтні порушення дзвін у вухах, вертиго не часто Порушення з боку серця відчуття серцебиття, аритмія 2 часто фібриляція передсердь, тахікардія 2 , хронічна серцева недостатність, неспецифічні зміни на ЕКГ, стенокардія 2 , інфаркт міокарда 5 не часто Порушення з боку судин артеріальна гіпертензія часто "припливи", порушення мозкового кровообігу 5 транзиторна ішемічна атака гіпертонічний криз 2 васкуліт 2 не часто Порушення з боку дихальної системи, органів грудної клітки та середостіння. бронхоспазм 2 часто кашель, задишка, носова кровотеча не часто Порушення з боку шлунково-кишкового тракту біль в животі дуже часто метеоризм, гастрит, печія/гастроезофагеальний рефлюкс, діарея, диспепсія/дискомфорт в епігастрії, нудота, блювання, езофагіт, виразка слизової оболонки порожнини рота часто здуття живота, зміна перистальтики, сухість слизової оболонки порожнини рота, виразка гастродуоденальної, виразкова хвороба шлунка, включаючи перфорації та кровотечі, панкреатит 2 , синдром подразненого кишечника не часто Порушення з боку печінки та жовчовивідних шляхів підвищення активності АЛТ та ACT часто гепатит 2 рідко печінкова недостатність 2 , жовтяниця 2 рідко 3 Порушення з боку шкіри та підшкірних тканин екхімоз часто набряклість особи, свербіж, висип, еритема 2 , кропив'янка 2 не часто синдром Стівенса-Джонсона 2 , токсичний епідермальний некроліз 2 , фіксована лікарська еритема 2 рідко 3 Порушення з боку скелетно-м'язової та сполучної тканини м'язові судоми/спазм, скелетно-м'язовий біль/скутість не часто Порушення з боку нирок та сечовивідних шляхів протеїнурія, підвищення концентрації креатиніну в сироватці, ниркова недостатність 2,3,4 не часто Загальні розлади та порушення у місці введення астенія/слабкість, грипоподібний синдром часто біль у грудній клітці не часто Лабораторні та інструментальні дані підвищення концентрації азоту сечовини крові, підвищення активності креатинфосфокінази, гіперкаліємія, підвищення концентрації сечової кислоти не часто гіпонатріємія рідко 1 Відповідно до частоти, що враховується у клінічних дослідженнях: дуже часто (≥1/10), часто (від ≥1/100 до 2 Ця небажана реакція була зареєстрована під час постмаркетингового спостереження. Частота оцінювалася на підставі найбільшої частоти, що спостерігається у клінічних дослідженнях з урахуванням показань та затвердженої дози. 3 Частотна категорія "рідко" була визначена відповідно до керівництва (версія 2, вересень 2009 р.) для Короткої характеристики лікарського препарату на підставі розрахункової верхньої межі 95 % довірчого інтервалу для 0 явищ, враховуючи кількість пацієнтів, які отримували еторикоксиб в аналізі даних III фази , об'єднаних залежно від дози та показання (n = 15470). 4 Гіперчутливість включає терміни "алергія", "лікарська алергія", "гіперчутливість до лікарського препарату", "гіперчутливість", "гіперчутливість неуточнена", "реакція гіперчутливості" та "неспецифічна алергія". 5 За результатами даних аналізу довгострокових плацебо- та активноконтрольованих клінічних досліджень при застосуванні селективних інгібіторів ЦОГ-2 підвищується ризик розвитку серйозних артеріальних тромботичних явищ, включаючи ІМ та інсульт. З наявних даних, малоймовірно, що абсолютний ризик розвитку цих явищ перевищує 1 % на рік (нечасто). Наступні серйозні небажані явища були зареєстровані у зв'язку з прийомом НГТВП і не можуть бути виключені для еторикоксибу: нефротоксичність, включаючи інтерстиціальний нефрит та нефротичний синдром.Взаємодія з лікарськими засобамиФармакодинамічні взаємодії Пероральні антикоагулянти (варфарин). У пацієнтів, які постійно приймають варфарин, прийом еторикоксибу в дозі 120 мг на день супроводжувався збільшенням міжнародного нормалізованого відношення (МНО)/протромбінового часу приблизно на 13%. Тому у пацієнтів, які отримують пероральні антикоагулянти, слід контролювати МНО/протромбіновий час на початку лікування або при зміні дози еторикоксибу, особливо в перші кілька днів. Діуретики, інгібітори ангіотензинперетворюючого ферменту (АПФ) та антагоністи рецепторів ангіотензину II. Нестероїдні протизапальні засоби можуть послаблювати ефект діуретиків та інших антигіпертензивних лікарських препаратів. У деяких пацієнтів з порушенням функції нирок (наприклад, у пацієнтів з зневодненням або у літніх пацієнтів з порушеною функцією нирок) одночасне застосування інгібітору АПФ або антагоніста рецепторів ангіотензину II та препаратів, що інгібують ЦОГ, може призводити до додаткового погіршення функції нирок, включаючи можливий розвиток. ниркової недостатності, яка зазвичай має оборотний характер. Це слід враховувати у пацієнтів, які приймають одночасно церикоксиб з інгібіторами АПФ або антагоністами рецепторів ангіотензину ІІ. Такі комбінації слід призначати з обережністю, особливо пацієнтам похилого віку.Пацієнти повинні бути належним чином гідратовані, при цьому необхідно проводити моніторинг функції нирок на початку комбінованої терапії та періодично надалі. Ацетилсаліцилова кислота. У дослідженні у здорових добровольців церикоксиб у дозі 120 мг 1 раз на день у рівноважному стані не впливав на антитромбоцитарну активність ацетилсаліцилової кислоти (81 мг 1 раз на день). Еторикоксиб можна одночасно застосовувати з ацетилсаліциловою кислотою в низьких дозах, призначених для профілактики серцево-судинних захворювань. Тим не менш, одночасне застосування низьких доз ацетилсаліцилової кислоти та еторикоксибу може призвести до збільшення частоти виразкового ураження шлунково-кишкового тракту або інших ускладнень у порівнянні з прийомом тільки церикоксиксу. Одночасне застосування церикоксибу з ацетилсаліциловою кислотою в дозах, що перевищують рекомендовані для профілактики серцево-судинних ускладнень, а також з іншими нестероїдними протизапальними засобами не рекомендується. Циклоспорин та такролімус. Взаємодія церикоксибу з цими препаратами не вивчалася, однак, одночасне застосування циклоспорину або такролімусу з будь-яким нестероїдними протизапальними засобами може посилювати нефротоксичний ефект циклоспорину або такролімусу. При прийомі эторикоксиба у комбінації з будь-яким із цих препаратів слід контролювати функцію нирок. Фармакокінетичні взаємодії Вплив інших лікарських засобів на фармакокінетику еторикоксибу Основний шлях метаболізму церикоксибу залежить від ферментів системи CYP. Ізофермент CYP3A4 сприяє метаболізму церикоксибу in vivo. Дослідження in vitro показують, що ізоферменти CYP2D6, CYP2C9, CYP1A2 і CYP2C19 можуть каталізувати основний шлях метаболізму, але їх кількісні характеристики in vivo не вивчені. Кетоконазол. Кетоконазол, потужний інгібітор ізоферменту CYP3A4, при прийомі здоровими добровольцями в дозі 400 мг один раз на день протягом 11 днів не надавав клінічно значущого впливу на фармакокінетику одноразової дози церикоксиксу 60 мг (збільшення AUC на 43%). Вориконазол та міконазол. Одночасне призначення сильних інгібіторів ізоферменту CYP3A4 (вориконазол для прийому всередину або міконазол місцево, у вигляді гелю для прийому всередину) та еторикоксибу викликало невелике збільшення експозиції церикоксибу, яке не визнано клінічно значущим на підставі опублікованих даних. ріфампіцин. Одночасне застосування церикоксибу та рифампіцину (потужного індуктора системи цитохромів) призводило до зниження концентрації церикоксибу в плазмі на 65 %. Така взаємодія може призвести до рецидиву симптомів при одночасному призначенні еторикоксибу з рифампіцином. Ця інформація дозволяє припустити необхідність збільшення дози, проте застосовувати еторикоксиб у дозах, що перевищують рекомендовані для кожного показання, не рекомендується, оскільки комбіноване застосування рифампіцину та еторикоксибу в таких дозах не вивчалося. Антациди. Антациди не надають клінічно значущої дії на фармакокінетику еторикоксибу. Вплив еторикоксибу на інші лікарські препарати Літій. НПЗЗ зменшують виведення літію нирками, отже, збільшують концентрацію літію у плазмі крові. При необхідності проводять частий контроль концентрації літію в крові та коригують дозу літію під час одночасного прийому з нестероїдними протизапальними засобами, а також при відміні нестероїдних протизапальних засобів. Метотрексат. У двох дослідженнях вивчалися ефекти еторикоксибу в дозах 60, 90 або 120 мг 1 раз на день протягом семи днів у пацієнтів, які отримували 1 раз на тиждень метотрексат у дозі від 7,5 до 20 мг на лікування РА. Еторикоксиб у дозах 60 та 90 мг не впливав на концентрацію метотрексату в плазмі та нирковий кліренс метотрексату. В одному дослідженні церикоксиб у дозі 120 мг не фармакокінетично впливав на метотрексат, але в іншому дослідженні концентрація метотрексату в плазмі підвищувалася на 28 %, а нирковий кліренс метотрексату знижувався на 13 %. При одночасному прийомі церикоксибу та метотрексату рекомендується вести спостереження щодо можливої появи токсичних ефектів метотрексату. Пероральні контрацептиви. Еторикоксиб у дозі 60 мг при одночасному прийомі протягом 21 дня з пероральними контрацептивами, що містять 35 мкг етинілестрадіолу (ЕЕ) та від 0,5 мг до 1 мг норетиндрону, збільшував AUC0-24 год ЕЕ на 37 % у рівноважному стані. Прийом церикоксиксу в дозі 120 мг у поєднанні з вищевказаними пероральними контрацептивами (одночасно або з інтервалом 12 годин) збільшував AUC0-24год. ЕЕ на 50-60% у рівноважному стані. Це збільшення концентрації ЕЕ слід враховувати при виборі перорального контрацептиву для одночасного застосування з церикоксибом. Подібна взаємодія може спричинити збільшення частоти розвитку небажаних явищ, пов'язаних із застосуванням пероральних контрацептивів (наприклад, венозних тромбоемболій у жінок із групи ризику). Замісна гормональна терапія (ЗГТ). Призначення еторікоксибу в дозі 120 мг одночасно з препаратами для ЗГТ, що містять кон'юговані естрогени в дозі 0,625 мг протягом 28 днів, збільшує середнє рівноважне значення AUC0-24 год некон'югованого естрону (41 %), еквіліну (76 %) та 17-2 %). Вплив доз еторикоксибу, рекомендованих для тривалого застосування (30, 60 та 90 мг), не вивчався. Еторикоксиб у дозі 120 мг змінював експозицію (AUC0-24год) даних естрогенних компонентів менш ніж удвічі порівняно з монотерапією кон'югованими естрогенами при збільшенні дози з 0,625 до 1,25 мг. Клінічне значення таких збільшення невідомо, застосування більш високих доз кон'югованих естрогенів у поєднанні з еторикоксибом не вивчалося.Підвищення концентрації естрогенів слід брати до уваги при виборі гормональної терапії в період постменопаузи при одночасному призначенні з етороксібом, оскільки збільшення експозиції естрогенів може підвищувати ризик розвитку небажаних явищ, пов'язаних із ЗГТ. Преднізон/Преднізолон. У дослідженнях лікарських взаємодій эторикоксиб не впливав на клінічно значущий вплив на фармакокінетику преднізону/преднізолону. Дігоксин. При застосуванні эторикоксибу в дозі 120 мг один раз на день протягом 10 днів у здорових добровольців не спостерігалося зміни рівноважної AUC0-24год дигоксину в плазмі або впливу на його виведення нирками. При цьому спостерігалося збільшення Стах дигоксину приблизно на 33%. Таке підвищення, як правило, не є важливим для більшості пацієнтів. Тим не менш, при одночасному застосуванні церикоксибу та дигоксину слід спостерігати за станом пацієнтів із високим ризиком прояву токсичної дії дигоксину. Вплив еторикоксибу на препарати, що метаболізуються сульфотрансферазами. Еторикоксиб є інгібітором сульфотрансферази людини (зокрема, SULT1E1) і може підвищувати концентрацію ЕЕ у сироватці крові. У зв'язку з тим, що в даний час отримано недостатньо даних про ефекти різних сульфотрансфераз, а їхня клінічна значущість для застосування багатьох лікарських препаратів ще вивчається, доцільно з обережністю призначати церикоксиб одночасно з іншими лікарськими препаратами, що метаболізуються сульфотрансферазами людини (наприклад, пероральний сальбутамол і ). Вплив етерокіксібу на препарати, що метаболізуються ізоферментами системи цитохромів. Грунтуючись на результатах досліджень in vitro, не очікується, що эторикоксиб інгібуватиме ізоферменти цитохрому Р450 (CYP) 1А2, 2С9, 2С19, 2D6, 2Е1 або 3А4. У дослідженні у здорових добровольців щоденне застосування церикоксибу в дозі 120 мг не впливало на активність ізоферменту CYP3A4 печінки при оцінці за допомогою еритроміцинового дихального тесту.Спосіб застосування та дозиВсередину, незалежно від їди, запиваючи невеликою кількістю води. Дія препарату реалізується швидше при прийомі натще. Внаслідок можливого підвищення ризику серцево-судинних ускладнень слід використовувати мінімальну ефективну дозу мінімально можливим курсом. Остеоартроз: рекомендована доза етерокіксібу становить 30 мг 1 раз на день. У разі недостатнього ефекту добова доза препарату може бути збільшена до 60 мг на добу. Добова доза при остеоартрозі не повинна перевищувати 60 мг. Ревматоїдний артрит та анкілозуючий спондиліт: рекомендована доза еторикоксібу становить 60 мг 1 раз на день. У пацієнтів із недостатнім клінічним ефектом можливе збільшення добової дози препарату до 90 мг один раз на день. Після клінічної стабілізації захворювання можливе зниження дози до 60 мг один раз на день. У разі відсутності ознак клінічного покращення слід розглянути можливість застосування інших методів лікування. Добова доза не повинна перевищувати 90 мг. Гострий подагричний артрит: рекомендована доза церикоксибу в гострому періоді становить 120 мг 1 раз на день. Тривалість застосування препарату у дозі 120 мг не перевищує 8 днів. Добова доза не повинна перевищувати 120 мг. Гострий біль після стоматологічних операцій: рекомендована доза еторикоксибу становить 90 мг 1 раз на день. Еторикоксиб слід застосовувати лише у гострий симптоматичний період тривалістю не більше 3 днів. Добова доза для усунення болю після стоматологічних операцій не повинна перевищувати 90 мг. Деяким пацієнтам можуть знадобитися додаткові засоби для забезпечення адекватного рівня знеболювання у післяопераційному періоді протягом триденного періоду терапії церикоксибом. Особливі групи пацієнтів Літні пацієнти: корекція дози не потрібна. Як і при застосуванні інших препаратів, еторикоксиб слід застосовувати з обережністю. Діти: застосування еторикоксибу у пацієнтів віком до 16 років протипоказано. Порушення функції печінки: незалежно від показання до застосування пацієнтам з порушеннями функції печінки легкого ступеня тяжкості (5-6 балів за шкалою Чайлд-П'ю) не слід перевищувати дозу 60 мг 1 раз на день, пацієнтам з порушеннями функції печінки середнього ступеня тяжкості (7 -9 балів за шкалою Чайлд-Пью) – 30 мг 1 раз на день. Рекомендується бути обережним при застосуванні препарату у пацієнтів з порушеннями функції печінки середнього ступеня тяжкості, оскільки клінічний досвід застосування препарату у даної групи пацієнтів обмежений. У зв'язку з відсутністю клінічного досвіду застосування препарату у пацієнтів з тяжкими порушеннями функції печінки (≥10 балів за шкалою Чайлд-П'ю) препарат протипоказаний для цієї групи пацієнтів. Порушення функції нирок: не потрібна корекція дози препарату при застосуванні у пацієнтів із КК ≥30 мл/хв. Застосування препарату у пацієнтів із ККПередозуванняУ клінічних дослідженнях прийом еторикоксибу в разовій дозі до 500 мг і багаторазовий прийом до 150 мг/день протягом 21 дня не викликав суттєвих токсичних ефектів. Були отримані повідомлення про гостре передозування еторикоксибом, однак, у більшості випадків про небажані реакції не повідомлялося. Найчастіші небажані реакції відповідали профілю безпеки церикоксибу (наприклад, порушення з боку шлунково-кишкового тракту, кардіоренальні явища). У разі передозування доцільно вживати звичайні підтримувальні заходи, такі як видалення невсмоктаного препарату із ШКТ, клінічне спостереження і, при необхідності, підтримуюча терапія. Еторікоксиб не виводиться при гемодіалізі; виведення еторикоксибу при перитонеальному діалізі не вивчалося.Запобіжні заходи та особливі вказівкиВплив на ШКТ У пацієнтів, які отримували еторикоксиб, спостерігалися ускладнення з боку верхніх відділів шлунково-кишкового тракту (перфорації, виразки або кровотечі), іноді з летальним кінцем. Рекомендується бути обережним при лікуванні пацієнтів з високим ризиком розвитку ускладнень з боку шлунково-кишкового тракту при застосуванні нестероїдних протизапальних засобів, зокрема, у літніх пацієнтів, що одночасно застосовують інші нестероїдні протизапальні засоби, ацетилсаліцилову кислоту або у пацієнтів із захворюваннями шлунково-кишкового тракту в анамнезі, такими як виразка та шлунково-кишкова кровотеча. Існує додатковий ризик розвитку небажаних реакцій з боку шлунково-кишкового тракту (шлунково-кишкові виразки або інші ускладнення з боку шлунково-кишкового тракту) при одночасному застосуванні церикоксибу та ацетилсаліцилової кислоти (навіть у низьких дозах). У довгострокових клінічних дослідженнях не спостерігалося достовірних відмінностей щодо безпеки для ШКТ при застосуванні селективних інгібіторів ЦОГ-2 у комбінації з ацетилсаліциловою кислотою порівняно із застосуванням нестероїдних протизапальних засобів у комбінації з ацетилсаліциловою кислотою. Вплив на серцево-судинну систему Результати клінічних досліджень свідчать про те, що застосування лікарських препаратів класу селективних інгібіторів ЦОГ-2 пов'язано з підвищеним ризиком тромбоутворення (особливо інфаркту міокарда (ІМ) та інсульту) порівняно з плацебо та деякими НПЗЗ. Ризик розвитку серцево-судинних ускладнень при застосуванні селективних інгібіторів ЦОГ-2 може зростати зі збільшенням дози та тривалості лікування, тому слід застосовувати церикоксиб протягом максимально короткого періоду часу та у найнижчій ефективній добовій дозі. Необхідно періодично оцінювати потребу пацієнта у симптоматичному лікуванні та відповідь на терапію, особливо у пацієнтів з ОА. Пацієнтам з відомими факторами ризику розвитку серцево-судинних ускладнень (наприклад, артеріальна гіпертензія, гіперліпідемія, цукровий діабет, куріння) церикоксиб необхідно призначати тільки після ретельної попередньої оцінки співвідношення користі-ризику. Селективні інгібітори ЦОГ-2 не є заміною ацетилсаліцилової кислоти при профілактиці серцево-судинних захворювань через відсутність антитромбоцитарного ефекту, тому не слід припиняти застосування антиагрегантних препаратів. Вплив на функцію нирок Ниркові простагландини можуть відігравати компенсаторну роль у підтримці ниркової перфузії. Тому за наявності умов, що негативно впливають на ниркову перфузію, призначення еторикоксибу може призвести до зменшення утворення простагландинів і, як наслідок, зниження ниркового кровотоку, і тим самим призвести до погіршення функції нирок. Найбільший ризик розвитку цієї реакції виникає у пацієнтів із значним зниженням функції нирок, некомпенсованою серцевою недостатністю або цирозом печінки в анамнезі. У таких пацієнтів необхідно проводити моніторинг функції нирок. Затримка рідини, набряки та артеріальна гіпертензія Як і у разі застосування інших препаратів, що інгібують синтез простагландинів, у пацієнтів, які приймають еторикоксиб, спостерігалися затримка рідини, набряки та артеріальна гіпертензія. Застосування будь-яких нестероїдних протизапальних засобів, включаючи церикоксикс, може бути пов'язане з виникненням або рецидивом хронічної (застійної) серцевої недостатності. Інформація про дозозалежну реакцію для церикоксибу наведена в розділі "Фармакологічні властивості". Слід виявляти обережність при призначенні церикоксибу пацієнтам із серцевою недостатністю в анамнезі, дисфункцією лівого шлуночка, артеріальною гіпертензією та пацієнтам з уже наявними набряками, що виникли з будь-якої іншої причини. При появі клінічних ознак погіршення стану у таких пацієнтів слід вжити відповідних заходів, включаючи скасування еторікоксибу. Застосування еторикоксибу, особливо у високих дозах, може бути пов'язане з розвитком більш тяжкої артеріальної гіпертензії, ніж при застосуванні деяких інших нестероїдних протизапальних засобів та селективних інгібіторів ЦОГ-2. Тому під час лікування церикоксибом слід звернути особливу увагу на моніторинг АТ, який має контролюватись протягом двох тижнів після початку лікування та періодично надалі. При значному підвищенні артеріального тиску слід розглянути альтернативне лікування. Вплив на функцію печінки Підвищення активності аланінамінотрансферази (АЛТ) та/або аспартатамінотрансферази (ACT) (приблизно в три або більше рази щодо верхньої межі норми) було зареєстровано у клінічних дослідженнях приблизно у 1% пацієнтів, які отримували еторикоксиб протягом терміну до одного року у дозах 30 мг, 60 мг та 90 мг на день. Необхідно спостерігати за станом усіх пацієнтів із симптомами та/або ознаками дисфункції печінки, а також пацієнтів із зміненими лабораторними показниками функції печінки. Якщо виникають ознаки печінкової недостатності або показники функції печінки значно відхиляються від норми (втричі вище за верхню межу норми), прийом еторикоксибу повинен бути припинений. Загальні рекомендації Якщо під час лікування у пацієнтів погіршується будь-яка з функцій органів або систем органів, описаних вище, повинні бути вжиті відповідні заходи та розглянуто питання про скасування еторикоксибу. При застосуванні эторикоксибу у пацієнтів похилого віку та у пацієнтів з порушенням функції нирок, печінки або серця необхідне відповідне медичне спостереження. З обережністю слід розпочинати лікування ерикоксибом пацієнтам із зневодненням. Перед початком терапії церикоксибом рекомендується провести регідратацію. У період постмаркетингового спостереження при застосуванні НПЗП та деяких селективних інгібіторів ЦОГ-2 дуже рідко повідомлялося про розвиток серйозних реакцій шкіри. Деякі з них, у тому числі ексфоліативний дерматит, синдром Стівенса-Джонсона та токсичний епідермальний некроліз, були з смертю. Ризик розвитку цих реакцій найбільш високий на початку курсу терапії, здебільшого протягом першого місяця лікування. Повідомлялося про розвиток серйозних реакцій гіперчутливості, таких як анафілаксія та ангіоневротичний набряк, у пацієнтів, які отримували еторикоксиб. Застосування деяких селективних інгібіторів ЦОГ-2 супроводжувалося підвищеним ризиком розвитку шкірних реакцій у пацієнтів із якоюсь лікарською алергією в анамнезі. Еторикоксиб повинен бути скасований при першій появі висипу на шкірі,уражень слизової оболонки або будь-якої іншої ознаки гіперчутливості. Застосування еторикоксибу може маскувати лихоманку та інші ознаки запалення. Застосування еторикоксибу, як і інших препаратів, що інгібують ЦОГ та синтез простагландинів, не рекомендується жінкам, які планують вагітність (див. розділ "Застосування при вагітності та в період грудного вигодовування"). Оболонка таблетки містить лактозу. Пацієнтам з такими рідкісними вродженими захворюваннями, як непереносимість лактози, дефіцит лактази або глюкозогалактозна мальабсорбція, не слід приймати цей препарат. Вплив на здатність до керування автотранспортом та управління механізмами Пацієнтам, у яких на фоні застосування церикоксибу відзначаються епізоди запаморочення, сонливості чи слабкості, слід утриматися від керування транспортними засобами та роботи з механізмами.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаЕліксир - 1 л: Активні речовини: насіння сосни кедрової сибірської 54 г; плоди глоду 4 г; плоди аронії чорноплідної 2 г; бруньки берези 1.5 г; кореневища з корінням елеутерококу 1 г; квітки глоду звичайного 0.5 г; Допоміжні речовини: мед натуральний – 50 г, сахароза – 22.7 г, етанол 95% – 421 г, вода очищена – до 1000 мл. 100 мл - скляні пляшки (1) - пачки картонні.Опис лікарської формиЕліксир у вигляді рідини коричневого кольору зі специфічним запахом; у процесі зберігання допускається випадання осаду.Фармакотерапевтична групаМає загальнозміцнюючу дію, збільшує фізичну працездатність, сприяє регуляції метаболічних процесів в організмі.ФармакокінетикаПрепарат являє собою водно-спиртовий екстракт із суміші рослинної лікарської сировини і містить комплекс біологічно активних речовин, у зв'язку з чим проведення фармакокінетичних досліджень не є можливим.Клінічна фармакологіяФітопрепарат із загальнозміцнюючою дією.Показання до застосуванняДля лікування астено-вегетативного синдрому різної етіології, у період відновлення після перенесених захворювань, що протікають із ураженням паренхіматозних органів.Протипоказання до застосуванняпідвищена чутливість до компонентів препарату, у тому числі до меду та продуктів бджільництва; гостра серцево-судинна та гостра ниркова недостатність; тяжкі захворювання печінки; алкоголізм; черепно-мозкова травма; захворювання головного мозку; дефіцит сахарази/ізомальтази; непереносимість фруктози; глюкозо-галактозна мальабсорбція; вік до 18 років.Вагітність та лактаціяЗастосування препарату при вагітності та в період грудного вигодовування протипоказане. Протипоказано дітям віком до 18 років.Побічна діяМожливі алергічні реакції. Якщо на фоні застосування препарату Ваш стан погіршився, і Ви помітили будь-які побічні ефекти, не зазначені в даній інструкції, зверніться до лікаря.Взаємодія з лікарськими засобамиПри одночасному застосуванні з нікотиновою кислотою, гіполіпідемічними засобами (інгібіторами абсорбції холестерину, фібратами) можливе посилення гіполіпідемічної дії. Якщо Ви приймаєте інші лікарські засоби, перед прийомом препарату обов'язково проконсультуйтеся з лікарем.Спосіб застосування та дозиВсередину по 2-3 чайні ложки (10-15 мл), розведені у 100 мл води. 2 десь у день 10-15 хвилин до їжі. Курс лікування 5-7 днів. При необхідності курс лікування може бути збільшений до 2-3 тижнів після консультації з лікарем. Перед вживанням збовтувати.ПередозуванняПри застосуванні препарату в дозах, що перевищують рекомендовані, можливі біль голови, нудота, блювання. Лікування симптоматичне.Запобіжні заходи та особливі вказівкиУ складі препарату міститься сахароза, що слід враховувати хворим на цукровий діабет. Максимальна разова доза препарату містить 0.34 г сахарози (відповідає 0.3 ХЕ (хлібних одиниць)), добова – 0,68 г (відповідає 0.68 ХЕ). Препарат містить щонайменше 37% етилового спирту. Максимальна разова доза містить 5.9 г абсолютного етилового спирту, максимальна добова доза препарату містить 11,97 г абсолютного етилового спирту. Вплив на здатність керувати транспортними засобами та працювати з механізмами Зважаючи на наявність у складі препарату спирту етилового слід утриматися від потенційно небезпечних видів діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій (управління транспортними засобами, робота з механізмами, що рухаються, робота диспетчера, оператора тощо).Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
327,00 грн
201,00 грн
Склад, форма випуску та упаковкаПігулки - 1 таб. Активні речовини: еторикоксиб – 60 мг; Допоміжні речовини: кальцію гідрофосфат безводний – 26 мг, целюлоза мікрокристалічна – 25.5 мг, повідон К30 – 6 мг, магнію стеарат – 1 мг, кроскармелоза натрію – 1.5 мг; Склад оболонки таблетки: Опадрай II зелений 32К510002 - 4 мг: гіпромелоза 15 cPs 1.6 мг, лактози моногідрат 1.12 мг, титану діоксид 0.628 мг, тріацетин 0.32 мг, індигокармін алюмінієвий 0.6 мг. Таблетки, покриті плівковою оболонкою, 30 мг, 60 мг, 90 мг та 120 мг. По 7 пігулок в Аl/Аl блістер. По 1 блістеру разом з інструкцією із застосування в картонну пачку. По 10 пігулок в Аl/Аl блістер. По 1, 2, 3, 5, 6, 9, 10 блістерів разом з інструкцією із застосування в картонну пачку. По 14 пігулок в Аl/Аl блістер. По 1,2, 4, 6, 7 блістерів разом із інструкцією із застосування в картонну пачку.Опис лікарської формиТаблетки, покриті плівковою оболонкою темно-зеленого кольору, круглі, двоопуклі.Фармакотерапевтична групаНестероїдні протизапальні препарати (НПЗЗ).ФармакокінетикаВсмоктування Эторикоксиб швидко всмоктується прийому внутрішньо. Абсолютна біодоступність прийому внутрішньо становить близько 100%. При застосуванні препарату у дорослих натще в дозі 120 мг один раз на день до досягнення рівноважного стану максимальна концентрація в плазмі (Сmах) становить 3,6 мкг/мл. Час досягнення Сmах (Тmах) становить приблизно 1 годину після прийому препарату. Середня геометрична площа під кривою "концентрація – час" (AUC0-24ч) склала 37,8 мкг * год / мл. Фармакокінетика эторикоксиба в діапазоні терапевтичних доз має лінійний характер. При прийомі эторикоксиба в дозі 120 мг під час їжі (їжа з високим вмістом жирів) не спостерігалося клінічно значущого впливу на ступінь абсорбції. Швидкість абсорбції при цьому змінювалася, що призводило до зниження Сmах на 36% і збільшення Тmах на 2 год. Ці дані не є клінічно значущими. У клінічних дослідженнях церикоксиб застосовувався незалежно від їди. Розподіл Еторікоксиб приблизно на 92% зв'язується з білками плазми у людини в діапазоні концентрацій від 0,05 до 5 мкг/мл. Об'єм розподілу у рівноважному стані (VdSS) становить близько 120 л. Еторикоксиб проникає через плацентарний бар'єр у щурів та кролів та гематоенцефалічний бар'єр у щурів. Метаболізм Еторикоксиб екстенсивно метаболізується, У людини виявлено п'ять метаболітів церикоксиксу. Основним метаболітом є 6'-карбоксиацетилеторикоксиб, що утворюється в результаті подальшого окислення 6'-гідроксиметилеторикоксибу. Ці основні метаболіти не мають помітної активності або слабо інгібують ЦОГ-2. Жоден із цих метаболітів не інгібує ЦОГ-1. Виведення Після одноразового внутрішньовенного введення здоровим добровольцям міченого радіоактивного церикоксибу в дозі 25 мг 70 % церикоксибу виводилося через нирки та 20 % – через кишечник, переважно у вигляді метаболітів. Менше 2% виявлялося у незміненому вигляді. Виведення еторикоксибу відбувається в основному шляхом метаболізму в печінці з подальшим виведенням нирками. Рівноважні концентрації эторикоксиба досягаються при щоденному прийомі в дозі 120 мг протягом 7 днів з коефіцієнтом кумуляції близько 2, що відповідає періоду напіввиведення близько 22 год. Плазмовий кліренс після внутрішньовенного введення 25 мг становить приблизно 50 мл/хв. Особливі групи пацієнтів Стать: фармакокінетичні параметри препарату у чоловіків та жінок не відрізняються. Літні пацієнти: фармакокінетика препарату у пацієнтів віком понад 65 років порівнянна з фармакокінетикою у пацієнтів молодшого віку. Діти: фармакокінетика еторикоксибу у дітей (60 кг, які приймали церикоксиб у дозі 90 мг 1 раз на день), була аналогічна фармакокінетиці у дорослих, які приймали церикоксиб у дозі 90 мг 1 раз на день. Безпека та ефективність застосування церикоксибу у дітей не встановлена. Печінкова недостатність: у пацієнтів з печінковою недостатністю легкого ступеня тяжкості (5-6 балів за шкалою Чайлд-П'ю) прийом еторикоксибу в дозі 60 мг 1 раз на день супроводжувався збільшенням показника AUC приблизно на 16% порівняно зі здоровими добровольцями, які приймали препарат у тій ж дозі. У пацієнтів з печінковою недостатністю середнього ступеня тяжкості (7-9 балів за шкалою Чайлд-П'ю), які отримували еторикоксиб у дозі 60 мг один раз на день через день, середнє значення AUC було таким же, як у здорових добровольців, які приймали еторикоксиб у дозі 60 мг раз на день щодня. Застосування еторикоксибу в дозі 30 мг один раз на день не вивчалося у цій групі пацієнтів. Клінічні та фармакокінетичні дані досліджень у пацієнтів з тяжкою печінковою недостатністю (>10 балів за шкалою Чайлд-П'ю) відсутні. Ниркова недостатність: фармакокінетичні показники одноразового застосування церикоксибу в дозі 120 мг у пацієнтів з нирковою недостатністю помірного та тяжкого ступеня та у пацієнтів з термінальною стадією хронічної ниркової недостатності, які перебувають на гемодіалізі, суттєво не відрізняються від показників у здорових добровольців. Гемодіаліз незначно впливає на виведення препарату (кліренс при діалізі – близько 50 мл/хв).ФармакодинамікаЕторикоксиб при пероральному прийомі в терапевтичних концентраціях є селективним інгібітором циклооксигенази типу 2 (ЦОГ-2). У дослідженнях з клінічної фармакології церикоксиб дозозалежно інгібував ЦОГ-2, не впливаючи на ЦОГ-1 при застосуванні доз до 150 мг на день. Еторикоксиб не пригнічував синтез простагландинів у слизовій оболонці шлунка і не впливав на функцію тромбоцитів. ЦОГ відповідає за синтез простагландинів. Виділено дві ізоформи цього ферменту - ЦОГ-1 та ЦОГ-2. ЦОГ-2 є ізоферментом, який індукується під дією прозапальних медіаторів і розглядається як основний фермент, який відповідає за синтез простаноїдних медіаторів болю, запалення та лихоманки. ЦОГ-2 бере участь у процесах овуляції, імплантації та закриття артеріальної протоки, регуляції функції нирок, центральної нервової системи (індукція лихоманки, відчуття болю, когнітивна функція), а також може грати певну роль у процесі загоєння виразок. ЦОГ-2 була виявлена у тканинах, що оточують виразки шлунка у людини, але її значення для загоєння виразки не встановлено. Ефективність У пацієнтів з остеоартрозом (ОА) церикоксиб при застосуванні в дозі 60 мг один раз на день викликав достовірне зменшення болю та покращення оцінки свого стану пацієнтами. Ці сприятливі ефекти спостерігалися вже другого дня лікування і зберігалися протягом 52 тижнів. Дослідження еторикоксибу в дозі 30 мг один раз на день (із застосуванням подібних методів оцінки) продемонстрували ефективність препарату порівняно з плацебо протягом усього періоду лікування (12 тижнів). У дослідженні, яке проводилося з метою визначення оптимальної дози, еторикоксиб у дозі 60 мг продемонстрував достовірно більш виражене поліпшення, ніж у дозі 30 мг для всіх 3 первинних кінцевих точок через 6 тижнів лікування. Застосування дози 30 мг на лікування ОА суглобів кистей рук не вивчалося. У пацієнтів з ревматоїдним артритом (РА) прийом еторикоксибу в дозі 60 мг або 90 мг один раз на день забезпечував достовірне зменшення болю, запалення та покращення рухливості. Ці сприятливі ефекти зберігалися протягом 12-тижневого періоду лікування. Дослідження порівняння застосування церикоксибу в дозі 60 мг і 90 мг один раз на день для лікування РА показало, що обидва режими дозування забезпечували переважну ефективність терапії порівняно з плацебо. Доза церикоксибу 90 мг один раз на день перевищувала за ефективністю дозу 60 мг один раз на день при оцінці ефекту за допомогою Глобальної Шкали. % довірчий інтервал (ДІ): -4,98 мм; -0,45 мм). У пацієнтів із гострим подагричним артритом еторикоксиб у дозі 120 мг один раз на день протягом усього періоду лікування (8 днів) зменшував помірний та сильний біль у суглобах та запалення порівняно з індометацином у дозі 50 мг 3 рази на день. Зменшення болю відзначалося вже через 4 години після початку лікування. У пацієнтів з анкілозуючим спондилітом еторикоксиб при застосуванні в дозі 90 мг один раз на день забезпечував достовірне зменшення болю в спині, запалення, скутості, а також покращення рухової функції. Клінічна ефективність эторикоксиба спостерігалася вже другого дня лікування та зберігалася протягом усього періоду лікування (52 тижні). В іншому дослідженні, в рамках якого порівнювалася ефективність застосування церикоксибу в дозі 90 мг один раз на день та 60 мг один раз на день, цей препарат продемонстрував рівну ефективність порівняно з напроксеном у дозі 1000 мг один раз на день. Серед пацієнтів, у яких не було досягнуто адекватної клінічної відповіді на терапію протягом 6 тижнів при застосуванні церикоксибу у дозі 60 мг один раз на день, збільшення добової дози до 90 мг дозволяло покращити результати лікування, оцінені за допомогою шкали інтенсивності болю у спині. -100 мм візуально-аналогова шкала), порівняно з продовженням терапії еторікоксибом у дозі 60 мг один раз на день. Середнє поліпшення склало -2,70 мм (95% ДІ: 4,88 мм; -0,52 мм). У клінічному дослідженні з вивчення болю після стоматологічних операцій эторикоксиб у дозі 90 мг призначали раз на день протягом трьох днів. У підгрупі пацієнтів з помірним болем (при вихідній оцінці) еторикоксиб у дозі 90 мг продемонстрував знеболюючий ефект, аналогічний ібупрофену в дозі 600 мг (16,11 порівняно з 16,39, Р = 0,722) та більший, ніж при застосуванні комбінації парацетамол/ кодеїн у дозі 600 мг/60 мг (11,00; Р Безпека Програма MEDAL (Багатонаціональна Програма Оцінки Довгострокового Призначення Еторікоксибу та Диклофенаку при Артріті) Програма MEDAL була проспективною програмою оцінки безпеки на підставі серцево-судинних явищ за об'єднаними даними трьох рандомізованих подвійних сліпих активно-контрольованих досліджень: MEDAL, EDGE II та EDGE. Дослідження MEDAL являло собою дослідження, тривалість якого визначалася досягненням кінцевих точок (серцево-судинних явищ), воно включало 17804 пацієнта з ОА та 5700 пацієнтів з РА, які отримували еторикоксиб у дозі 60 мг (ОА) або 90 мг (ОА та РА) або ді у дозі 150 мг на день у середньому протягом 20,3 місяців (максимум 42,3 місяці, медіана 21,3 місяці). У цьому дослідженні реєстрували лише серйозні небажані явища та випадки вибуття з дослідження внаслідок будь-якого небажаного явища. У дослідженнях EDGE та EDGE II порівнювали безпеку прийому церикоксибу та диклофенаку для шлунково-кишкового тракту (ЖКТ). До дослідження EDGE було включено 7111 пацієнтів з ОА, які отримували еторикоксиб у дозі 90 мг на день (в 1,5 рази більше за дозу, рекомендовану при ОА) або диклофенак у дозі 150 мг на день протягом у середньому 9,1 місяців (максимум 16 , 6 місяців, медіана 11,4 місяців). У дослідження EDGE II було включено 4086 пацієнтів з РА, які отримували еторикоксиб у дозі 90 мг на день або диклофенак у дозі 150 мг на день протягом середньому 19,2 місяців (максимум 33,1 місяця, медіана 24 місяці). В об'єднаній програмі MEDAL аналізували дані щодо лікування 34701 пацієнтів з ОА або РА, середня тривалість лікування склала 17,9 місяців (максимум 42,3 місяці, медіана 16,3 місяців), при цьому приблизно 12800 пацієнтів отримували лікування протягом понад 24 місяців. Пацієнти, включені до програми, при вихідній оцінці мали широкий спектр серцево-судинних та шлунково-кишкових факторів ризику. Були виключені пацієнти, які мали в анамнезі нещодавно перенесений інфаркт міокарда (ІМ), аортокоронарне шунтування або черезшкірне коронарне втручання протягом 6 місяців перед включенням до дослідження. У дослідженнях дозволялося застосовувати гастропротектори та низькі дози аспірину. Загальна безпека Достовірних відмінностей між эторикоксибом та диклофенаком щодо частоти розвитку серцево-судинних тромботичних явищ виявлено не було. Кардіоренальні небажані явища найчастіше спостерігалися при прийомі церикоксибу в порівнянні з диклофенаком, ефект був дозозалежним (див. результати нижче). Небажані явища з боку шлунково-кишкового тракту та печінки достовірно частіше спостерігалися при прийомі диклофенаку, ніж при прийомі церикоксибу. Частота небажаних явищ у дослідженнях EDGE та EDGE II та небажаних явищ, визнаних серйозними або зажадали відміни лікування, у дослідженні MEDAL була вищою при прийомі еторикоксибу порівняно з диклофенаком. Результати дослідження безпеки щодо серцево-судинної системи Частота підтверджених серйозних тромботичних серцево-судинних небажаних явищ (включаючи серцеві, цереброваскулярні та явища з боку периферичної судинної системи) була порівнянна між групами, які отримували церикоксиб або диклофенак (дані наведені в таблиці нижче). Не виявлено статистично значимих відмінностей щодо частоти тромботичних явищ між еторикоксибом та диклофенаком у всіх проаналізованих підгрупах, включаючи категорії пацієнтів з підвищеним ризиком серцево-судинних ускладнень. Відносний ризик для підтверджених серйозних серцево-судинних небажаних тромботичних явищ був подібним при прийомі еторикоксібу в дозі 60 мг або 90 мг і диклофенаку в дозі 150 мг. Частота підтверджених тромботичних серцево-судинних серйозних небажаних явищ (Об'єднана програма MEDAL) Еторікоксиб(N=16819)25 836 пацієнто-років Диклофенак(N=16483)24 766 пацієнто-років Порівняння між видами лікування Частота 1 (95% ДІ) Частота 1 (95% ДІ) Відносний ризик (95% ДІ) Підтверджені тромботичні серцево-судинні серйозні небажані явища За виконання вимог протоколу (Per protocol) 1,24 (1,11; 1,38) 1,30 (1,17; 1,45) 0,95 (0,81; 1,11) Залежно від призначеного лікування (Intent-to-treat) 1,25 (1,14; 1,36) 1,19 (1,08; 1,30) 1,05 (0,93; 1,19) Підтверджені явища з боку серця За виконання вимог протоколу (Per protocol) 0,71 (0,61; 0,82) 0,78 (0,68; 0,90) 0,90 (0,74; 1,10) Залежно від призначеного лікування (Intent-to-treat) 0,69 (0,61; 0,78) 0,70 (0,62; 0,79) 0,99 (0,84; 1,17) Підтверджені цереброваскулярні явища За виконання вимог протоколу (Per protocol) 0,34 (0,28; 0,42) 0,32 (0,25; 0,40) 1,08 (0,80; 1,46) Залежно від призначеного лікування (Intent-to-treat) 0,33 (0,28; 0,39) 0,29 (0,24; 0,35) 1,12 (0,87; 1,44) Підтверджені явища з боку периферичної судинної системи За виконання вимог протоколу (Per protocol) 0,20 (0,15; 0,27) 0,22 (0,17; 0,29) 0,92 (0,63; 1,35) Залежно від призначеного лікування (Intent-to-treat) 0,24 (0,20; 0,30) 0,23 (0,18; 0,28) 1,08 (0,81; 1,44) 1 число явищ на 100 пацієнто-років; ДІ = довірчий інтервал; N = загальна кількість пацієнтів, які виконали вимоги протоколу. При виконанні вимог протоколу: всі явища, що розвинулися на тлі досліджуваної терапії або протягом 14 днів після її припинення (виключені пацієнти, які прийняли <75% досліджуваного препарату або приймали НПЗП >10% часу, що не входять до дослідження). Залежно від призначеного лікування: всі підтверджені явища, що розвинулися до закінчення дослідження (включно з пацієнтами, які могли піддаватися не включеним до дослідження втручанням після припинення прийому досліджуваних препаратів). Загальна кількість рандомізованих пацієнтів: n = 17412 для эторикоксиба і n = 17289 для диклофенаку. Смертність від серцево-судинних явищ, а також загальна смертність у групах лікування церикоксибом та диклофенаком були порівнянними. Кардіоренальні явища Приблизно у 50% пацієнтів, включених у дослідження MEDAL, при початковій оцінці в анамнезі було зареєстровано артеріальну гіпертензію. У проведеному дослідженні частота вибування внаслідок небажаних явищ, пов'язаних з артеріальною гіпертензією, була статистично значуще вищою під час прийому эторикоксиба проти диклофенаком. Частота небажаних явищ, пов'язаних з хронічною серцевою недостатністю (випадки вибування з дослідження або серйозні небажані явища), була подібною до груп еторікоксибу в дозі 60 мг і диклофенаку в дозі 150 мг, але була вищою для еторікоксибу в дозі 90 мг порівняно з диклофеном. дозі 150 мг (і статистично значуще вище для еторикоксибу в дозі 90 мг у порівнянні з диклофенаком у дозі 150 мг у дослідженні MEDAL у пацієнтів з ОА). Частота підтверджених небажаних явищ,пов'язаних з хронічною серцевою недостатністю (серйозних, які призвели до госпіталізації або необхідності невідкладної допомоги), була незначно вищою для церикоксибу порівняно з диклофенаком у дозі 150 мг, ефект був дозозалежним. Частота випадків вибування з дослідження внаслідок небажаних явищ, пов'язаних з набряками, була вищою для еторікоксибу в дозі 150 мг, порівняно з диклофенаком у дозі 150 мг, ефект був дозозалежним (статистично значимо для еторікоксибу в дозі 90 мг, але не для етороксиксу в дозі 60 мг).була вищою для эторикоксиба порівняно з диклофенаком в дозі 150 мг, ефект був дозозалежним (статистично значуще для етіроксиксібу в дозі 90 мг, але не для етіроксиксібу в дозі 60 мг).була вищою для эторикоксиба порівняно з диклофенаком в дозі 150 мг, ефект був дозозалежним (статистично значуще для етіроксиксібу в дозі 90 мг, але не для етіроксиксібу в дозі 60 мг). Результати оцінки кардіоренальної безпеки у дослідженнях EDGE та EDGE II узгоджуються з результатами у дослідженні MEDAL В окремих дослідженнях програми MEDAL абсолютна частота вибування з дослідження в будь-якій групі лікування при прийомі еторикоксибу (60 мг або 90 мг) становила до 2,6% при артеріальній гіпертензії, до 1,9% при набряках, і до 1,1% при хронічній серцевої недостатності. У пацієнтів, які приймали церикоксиб у дозі 90 мг, частота вибуття з дослідження була вищою, ніж у пацієнтів, які приймали церикоксиб у дозі 60 мг. Результати оцінки переносимості з боку шлунково-кишкового тракту в Програмі MEDAL У кожному з трьох досліджень, що входять до програми MEDAL, частота вибування з дослідження для будь-яких клінічних небажаних явищ з боку шлунково-кишкового тракту (наприклад, диспепсія, біль у животі, виразки) була достовірно нижчою для еторикоксибу порівняно з диклофенаком. Частота вибуття з дослідження внаслідок небажаних клінічних явищ з боку шлунково-кишкового тракту на 100 пацієнто-років за весь період дослідження становила: 3,23 для еторикоксибу та 4,96 для диклофенаку в дослідженні MEDAL; 9,12 для эторикоксиба і 12,28 для диклофенаку у дослідженні EDGE; 3,71 для еторикоксибу та 4,81 для диклофенаку в дослідженні EDGE II. Результати оцінки безпеки щодо ШКТ у Програмі MEDAL До небажаних явищ з боку верхніх відділів шлунково-кишкового тракту були віднесені перфорації, виразки та кровотечі. Ускладнені небажані явища з боку верхніх відділів шлунково-кишкового тракту включали перфорацію, непрохідність та ускладнені кровотечі; неускладнені явища включали неускладнені кровотечі та неускладнені виразки. При прийомі эторикоксиба порівняно з диклофенаком загальна частота небажаних явищ з боку верхніх відділів шлунково-кишкового тракту була достовірно нижчою. Достовірних відмінностей між етерокіксібом і диклофенаком за частотою ускладнених небажаних явищ виявлено не було. Для випадків кровотеч із верхніх відділів шлунково-кишкового тракту (ускладнених та неускладнених) не було виявлено достовірних відмінностей між еторикоксибом та диклофенаком.Перевага церикоксибу порівняно з диклофенаком щодо ускладнень з боку верхніх відділів ШКТ не була статистично значущою у пацієнтів, які одночасно приймали аспірин у низьких дозах (близько 33% пацієнтів). Частота підтверджених ускладнених та неускладнених клінічних небажаних явищ з боку верхніх відділів шлунково-кишкового тракту на 100 пацієнто-років (перфорації, виразки та кровотечі) склала 0,67 (95 % ДІ: 0,57; 0,77) для церикоксиксу та 0,97 (95 % ДІ: 0,85; 1,10) для диклофенаку, відносний ризик склав 0,69 (95% ДІ: 0,57; 0,83). При оцінці частоти підтверджених клінічних небажаних явищ з боку верхніх відділів шлунково-кишкового тракту у пацієнтів похилого віку максимальне зниження спостерігалося у пацієнтів у віці ≥75 років у групі церикоксибу в порівнянні з диклофенаком - 1,35 (95 % ДІ: 0,94; 1,87) та 2,78 (95% ДІ: 2,14; 3,56) на 100 пацієнто-років відповідно. Частота підтверджених небажаних явищ з боку нижніх відділів шлунково-кишкового тракту (перфорація тонкої або товстої кишки, непрохідність, кровотеча) достовірно не розрізнялася між групами, які приймали церикоксиб та диклофенак. Результати оцінки безпеки щодо печінки у Програмі MEDAL При прийомі эторикоксиба порівняно з диклофенаком спостерігалася статистично достовірно нижча частота вибуття з дослідження через небажані явища з боку печінки. В об'єднаній програмі MEDAL 0,3% пацієнтів, які приймали еторикоксиб, та 2,7% пацієнтів, які приймали диклофенак, вибули з дослідження через небажані явища з боку печінки. Частота небажаних явищ на 100 пацієнто-років склала 0,22 для церикоксиксу і 1,84 для диклофенаку (р Додаткові дані щодо безпеки, пов'язані з тромботичними серцево-судинними явищами У клінічних дослідженнях, за винятком Програми MEDAL, приблизно 3100 пацієнтів отримували церикоксикс у дозі ≥60 мг на день протягом 12 тижнів та довше. У цих дослідженнях не було виявлено помітних відмінностей у частоті підтверджених серйозних тромботичних серцево-судинних явищ у пацієнтів, які отримували церикоксиб у дозі ≥60 мг, плацебо або нестероїдні протизапальні засоби, що не містять напроксен. Однак у порівнянні з пацієнтами, які отримували напроксен у дозі 500 мг двічі на день, частота цих явищ була вищою у пацієнтів, які отримували еторикоксиб. Різниця в антиагрегантній активності між деякими нестероїдними протизапальними засобами, що інгібують ЦОГ-1, та селективними інгібіторами ЦОГ-2 може мати клінічне значення у пацієнтів із групи ризику тромбоемболічних подій. Селективні інгібітори ЦОГ-2 пригнічують утворення системного (і, можливо, ендотеліального) простацикліну,не впливаючи на тромбоцитарний тромбоксан. Клінічна значимість цих спостережень встановлено. Додаткові дані з безпеки щодо ШКТ У двох 12-тижневих подвійних сліпих ендоскопічних дослідженнях кумулятивна частота розвитку гастродуоденальних виразок була значно нижчою у пацієнтів, які отримували церикоксиб у дозі 120 мг один раз на день, ніж у пацієнтів, які отримували напроксен 500 мг двічі на день. або ібупрофен 800 мг тричі на день. Частота розвитку виразок при призначенні церикоксибу була вищою порівняно з плацебо. Дослідження ниркової функції у пацієнтів похилого віку У рандомізованому подвійному сліпому плацебо-контрольованому дослідженні в паралельних групах оцінювався вплив 15-денної терапії церикоксибом (90 мг), целекоксибом (200 мг двічі на день), напроксеном (500 мг двічі на день) порівняно з плацебо на виведення натрію. , артеріальний тиск (АТ) та інші параметри функції нирок у пацієнтів віком від 60 до 85 років, які отримували раціон з обмеженим споживанням натрію до 200 мекв/день. Еторикоксиб, целекоксиб і напроксен мали подібний вплив на виведення натрію нирками через 2 тижні лікування. Всі активні препарати порівняння показали збільшення систолічного АТ порівняно з плацебо, однак, еторикоксиб викликав статистично значуще збільшення систолічного АТ на 14-й день порівняно з целекоксибом і напроксеном (середня зміна систолічного АТ порівняно з вихідним: етороксіб 7,7 мм рт. ст., целекоксиб 2,4 мм рт.ст., напроксен 3,6 мм рт.ст.).Показання до застосуванняСимптоматична терапія остеоартрозу, ревматоїдного артриту, анкілозуючого спондиліту, болю та запалення, пов'язаних із гострим подагричним артритом. Короткострокова терапія помірного гострого болю після стоматологічних операцій.Протипоказання до застосуванняПідвищена чутливість до еторикоксибу або будь-якої з допоміжних речовин препарату. Виразкова хвороба шлунка та 12-палої кишки у стадії загострення, активна шлунково-кишкова кровотеча. Бронхіальна астма, бронхоспазм, гострий риніт, поліпоз носа, ангіоневротичний набряк, кропив'янка або алергічні реакції після прийому ацетилсаліцилової кислоти або нестероїдних протизапальних препаратів (НПЗЗ), у тому числі інгібіторів ЦОГ-2, в анамнезі. Вагітність та період грудного вигодовування. Тяжкі порушення функції печінки (сироватковий альбумін 10 балів за шкалою Чайлд-П'ю). Тяжка ниркова недостатність (КК Діти та підлітки до 16 років. Запальні захворювання кишок. Хронічна серцева недостатність (II-IV функціональний клас за NYHA). Неконтрольована артеріальна гіпертензія (АТ стабільно вищий за 140/90 мм рт. ст.). Підтверджена ішемічна хвороба серця, захворювання периферичних артерій та/або цереброваскулярні захворювання. Дефіцит лактази, непереносимість лактози, глюкозо-галактозна мальабсорбція. Підтверджена гіперкаліємія. З обережністю: Пацієнти з підвищеним ризиком розвитку ускладнень з боку шлунково-кишкового тракту (виразкова ураження шлунково-кишкового тракту або шлунково-кишкова кровотеча в анамнезі, наявність інфекції Helicobacter Pylori, одночасне застосування інших нестероїдних протизапальних засобів, у тому числі ацетилсаліцилової кислоти, літній вік). Пацієнти, які мають в анамнезі фактори ризику серцево-судинних ускладнень (дисліпідемія/гіперліпідемія, цукровий діабет, артеріальна гіпертензія, куріння, серцева недостатність, порушення функції лівого шлуночка, набряки та затримка рідини в організмі). Печінкова недостатність (5-9 балів за класифікацією Чайлд-П'ю). Пацієнти з дегідратацією. Пацієнти з порушеннями функції нирок (КК Пацієнти з попереднім значним зниженням функції нирок, з ослабленою функцією нирок, декомпенсованою серцевою недостатністю або цирозом печінки, що перебувають у групі ризику при тривалому застосуванні нестероїдних протизапальних засобів. Супутня терапія антикоагулянтами (наприклад, варфарин), антиагрегантами (наприклад, ацетилсаліцилова кислота, клопідогрел), препаратами, що метаболізуються сульфотрансферазами.Вагітність та лактаціяВагітність В даний час клінічних даних про застосування еторикоксибу при вагітності відсутні. У дослідженнях на тваринах спостерігалася токсична дія на репродуктивну систему. Потенційний ризик для жінок під час вагітності невідомий. Застосування еторикоксибу, як і інших лікарських препаратів, що інгібують синтез простагландинів, у III триместрі вагітності може призводити до придушення скорочень матки та передчасного закриття артеріальної протоки. Еторикоксиб протипоказаний при вагітності. Якщо під час лікування настала вагітність, церикоксиб необхідно відмінити. Грудне годування У лактуючих щурів еторикоксиб виділяється з молоком. Досліджень, що підтверджують виділення еторикоксибу з грудним молоком у жінок, не проводилося. Жінки, які приймають еторикоксиб, повинні припинити грудне вигодовування. Фертильність Застосування еторикоксибу, як і інших препаратів, що інгібують ЦОГ-2 або синтез простагландинів, не рекомендується жінкам, які планують вагітність.Побічна діяРезюме профілю безпеки Безпека застосування церикоксибу оцінювалася у клінічних дослідженнях за участю 9295 пацієнтів, у тому числі 6757 пацієнтів з ОА, РА, хронічним болем у нижній частині спини та анкілозуючим спондилітом (приблизно 600 пацієнтів з ОА або РА отримували лікування протягом одного року або більше). Профіль небажаних реакцій був подібним у пацієнтів з ОА або РА, які отримували еторикоксиб протягом одного року або довше. У клінічному дослідженні гострого подагричного артриту пацієнти отримували церикоксиб у дозі 120 мг 1 раз на день протягом 8 днів. Профіль небажаних явищ у цьому дослідженні був загалом таким самим, як і в об'єднаних дослідженнях ОА, РА та хронічного болю в нижній частині спини. Для оцінки безпеки щодо серцево-судинної системи були об'єднані дані трьох активних контрольованих досліджень, у яких брали участь 17412 пацієнтів з ОА або РА, які отримували еторикоксиб у дозі 60 мг або 90 мг, середня тривалість досліджень склала приблизно 18 місяців. У клінічних дослідженнях гострого післяопераційного болю, пов'язаного з проведенням стоматологічної операції, у яких 614 пацієнтів отримували еторикоксиб у дозі 90 мг або 120 мг, профіль небажаних ефектів загалом був подібним до профілю в об'єднаних дослідженнях ОА, РА та хронічного болю в нижній частині спини. Табличне резюме небажаних реакцій У таблиці перераховані небажані реакції, які були зареєстровані з більшою частотою при застосуванні препарату, ніж у групі плацебо, у клінічних дослідженнях, що включали пацієнтів з ОА, РА, хронічним болем у нижній частині спини або анкілозуючим спондилітом (еторикоксиб призначався у дозі 30 мг, 60 мг або 90 мг з підвищенням дози до рекомендованої протягом 12 тижнів), у програмі MEDAL, де дослідження тривали до 3,5 років, у короткострокових дослідженнях гострого болю (протягом 7 днів), а також отримані під час постмаркетингового застосування. Класифікація систем органів Небажана реакція Частота 1 Інфекційні та паразитарні захворювання альвеолярний остит часто гастроентерит, інфекції верхніх дихальних шляхів, інфекції сечовивідних шляхів не часто Порушення з боку крові та лімфатичної системи анемія (в основному в результаті шлунково-кишкової кровотечі), лейкопенія, тромбоцитопенія не часто Порушення з боку імунної системи реакції гіперчутливості 2,4 не часто ангіоневротичний набряк, анафілактичні/анафілактоїдні реакції, у тому числі шок 2 рідко Порушення з боку обміну речовин та харчування набряки/затримка рідини часто посилення або зниження апетиту, збільшення маси тіла не часто Порушення психіки тривога, депресія, зниження ясності мислення, галюцинації 2 не часто сплутаність свідомості 2 , неспокій 2 рідко Порушення з боку нервової системи запаморочення, головний біль часто порушення смаку, безсоння, парестезія/гіпестезія, сонливість не часто Порушення з боку органу зору нечіткість зору, кон'юнктивіт не часто Порушення з боку органу слуху та лабіринтні порушення дзвін у вухах, вертиго не часто Порушення з боку серця відчуття серцебиття, аритмія 2 часто фібриляція передсердь, тахікардія 2 , хронічна серцева недостатність, неспецифічні зміни на ЕКГ, стенокардія 2 , інфаркт міокарда 5 не часто Порушення з боку судин артеріальна гіпертензія часто "припливи", порушення мозкового кровообігу 5 транзиторна ішемічна атака гіпертонічний криз 2 васкуліт 2 не часто Порушення з боку дихальної системи, органів грудної клітки та середостіння. бронхоспазм 2 часто кашель, задишка, носова кровотеча не часто Порушення з боку шлунково-кишкового тракту біль в животі дуже часто метеоризм, гастрит, печія/гастроезофагеальний рефлюкс, діарея, диспепсія/дискомфорт в епігастрії, нудота, блювання, езофагіт, виразка слизової оболонки порожнини рота часто здуття живота, зміна перистальтики, сухість слизової оболонки порожнини рота, виразка гастродуоденальної, виразкова хвороба шлунка, включаючи перфорації та кровотечі, панкреатит 2 , синдром подразненого кишечника не часто Порушення з боку печінки та жовчовивідних шляхів підвищення активності АЛТ та ACT часто гепатит 2 рідко печінкова недостатність 2 , жовтяниця 2 рідко 3 Порушення з боку шкіри та підшкірних тканин екхімоз часто набряклість особи, свербіж, висип, еритема 2 , кропив'янка 2 не часто синдром Стівенса-Джонсона 2 , токсичний епідермальний некроліз 2 , фіксована лікарська еритема 2 рідко 3 Порушення з боку скелетно-м'язової та сполучної тканини м'язові судоми/спазм, скелетно-м'язовий біль/скутість не часто Порушення з боку нирок та сечовивідних шляхів протеїнурія, підвищення концентрації креатиніну в сироватці, ниркова недостатність 2,3,4 не часто Загальні розлади та порушення у місці введення астенія/слабкість, грипоподібний синдром часто біль у грудній клітці не часто Лабораторні та інструментальні дані підвищення концентрації азоту сечовини крові, підвищення активності креатинфосфокінази, гіперкаліємія, підвищення концентрації сечової кислоти не часто гіпонатріємія рідко 1 Відповідно до частоти, що враховується у клінічних дослідженнях: дуже часто (≥1/10), часто (від ≥1/100 до 2 Ця небажана реакція була зареєстрована під час постмаркетингового спостереження. Частота оцінювалася на підставі найбільшої частоти, що спостерігається у клінічних дослідженнях з урахуванням показань та затвердженої дози. 3 Частотна категорія "рідко" була визначена відповідно до керівництва (версія 2, вересень 2009 р.) для Короткої характеристики лікарського препарату на підставі розрахункової верхньої межі 95 % довірчого інтервалу для 0 явищ, враховуючи кількість пацієнтів, які отримували еторикоксиб в аналізі даних III фази , об'єднаних залежно від дози та показання (n = 15470). 4 Гіперчутливість включає терміни "алергія", "лікарська алергія", "гіперчутливість до лікарського препарату", "гіперчутливість", "гіперчутливість неуточнена", "реакція гіперчутливості" та "неспецифічна алергія". 5 За результатами даних аналізу довгострокових плацебо- та активноконтрольованих клінічних досліджень при застосуванні селективних інгібіторів ЦОГ-2 підвищується ризик розвитку серйозних артеріальних тромботичних явищ, включаючи ІМ та інсульт. З наявних даних, малоймовірно, що абсолютний ризик розвитку цих явищ перевищує 1 % на рік (нечасто). Наступні серйозні небажані явища були зареєстровані у зв'язку з прийомом НГТВП і не можуть бути виключені для еторикоксибу: нефротоксичність, включаючи інтерстиціальний нефрит та нефротичний синдром.Взаємодія з лікарськими засобамиФармакодинамічні взаємодії Пероральні антикоагулянти (варфарин). У пацієнтів, які постійно приймають варфарин, прийом еторикоксибу в дозі 120 мг на день супроводжувався збільшенням міжнародного нормалізованого відношення (МНО)/протромбінового часу приблизно на 13%. Тому у пацієнтів, які отримують пероральні антикоагулянти, слід контролювати МНО/протромбіновий час на початку лікування або при зміні дози еторикоксибу, особливо в перші кілька днів. Діуретики, інгібітори ангіотензинперетворюючого ферменту (АПФ) та антагоністи рецепторів ангіотензину II. Нестероїдні протизапальні засоби можуть послаблювати ефект діуретиків та інших антигіпертензивних лікарських препаратів. У деяких пацієнтів з порушенням функції нирок (наприклад, у пацієнтів з зневодненням або у літніх пацієнтів з порушеною функцією нирок) одночасне застосування інгібітору АПФ або антагоніста рецепторів ангіотензину II та препаратів, що інгібують ЦОГ, може призводити до додаткового погіршення функції нирок, включаючи можливий розвиток. ниркової недостатності, яка зазвичай має оборотний характер. Це слід враховувати у пацієнтів, які приймають одночасно церикоксиб з інгібіторами АПФ або антагоністами рецепторів ангіотензину ІІ. Такі комбінації слід призначати з обережністю, особливо пацієнтам похилого віку.Пацієнти повинні бути належним чином гідратовані, при цьому необхідно проводити моніторинг функції нирок на початку комбінованої терапії та періодично надалі. Ацетилсаліцилова кислота. У дослідженні у здорових добровольців церикоксиб у дозі 120 мг 1 раз на день у рівноважному стані не впливав на антитромбоцитарну активність ацетилсаліцилової кислоти (81 мг 1 раз на день). Еторикоксиб можна одночасно застосовувати з ацетилсаліциловою кислотою в низьких дозах, призначених для профілактики серцево-судинних захворювань. Тим не менш, одночасне застосування низьких доз ацетилсаліцилової кислоти та еторикоксибу може призвести до збільшення частоти виразкового ураження шлунково-кишкового тракту або інших ускладнень у порівнянні з прийомом тільки церикоксиксу. Одночасне застосування церикоксибу з ацетилсаліциловою кислотою в дозах, що перевищують рекомендовані для профілактики серцево-судинних ускладнень, а також з іншими нестероїдними протизапальними засобами не рекомендується. Циклоспорин та такролімус. Взаємодія церикоксибу з цими препаратами не вивчалася, однак, одночасне застосування циклоспорину або такролімусу з будь-яким нестероїдними протизапальними засобами може посилювати нефротоксичний ефект циклоспорину або такролімусу. При прийомі эторикоксиба у комбінації з будь-яким із цих препаратів слід контролювати функцію нирок. Фармакокінетичні взаємодії Вплив інших лікарських препаратів на фармакокінетику еторикоксибу Основний шлях метаболізму церикоксибу залежить від ферментів системи CYP. Ізофермент CYP3A4 сприяє метаболізму церикоксибу in vivo. Дослідження in vitro показують, що ізоферменти CYP2D6, CYP2C9, CYP1A2 і CYP2C19 можуть каталізувати основний шлях метаболізму, але їх кількісні характеристики in vivo не вивчені. Кетоконазол. Кетоконазол, потужний інгібітор ізоферменту CYP3A4, при прийомі здоровими добровольцями в дозі 400 мг один раз на день протягом 11 днів не надавав клінічно значущого впливу на фармакокінетику одноразової дози церикоксиксу 60 мг (збільшення AUC на 43%). Вориконазол та міконазол. Одночасне призначення сильних інгібіторів ізоферменту CYP3A4 (вориконазол для прийому всередину або міконазол місцево, у вигляді гелю для прийому всередину) та еторикоксибу викликало невелике збільшення експозиції церикоксибу, яке не визнано клінічно значущим на підставі опублікованих даних. ріфампіцин. Одночасне застосування церикоксибу та рифампіцину (потужного індуктора системи цитохромів) призводило до зниження концентрації церикоксибу в плазмі на 65 %. Така взаємодія може призвести до рецидиву симптомів при одночасному призначенні еторикоксибу з рифампіцином. Ця інформація дозволяє припустити необхідність збільшення дози, проте застосовувати еторикоксиб у дозах, що перевищують рекомендовані для кожного показання, не рекомендується, оскільки комбіноване застосування рифампіцину та еторикоксибу в таких дозах не вивчалося. Антациди. Антациди не надають клінічно значущої дії на фармакокінетику еторикоксибу. Вплив еторикоксибу на інші лікарські препарати Літій. НПЗЗ зменшують виведення літію нирками, отже, збільшують концентрацію літію у плазмі крові. При необхідності проводять частий контроль концентрації літію в крові та коригують дозу літію під час одночасного прийому з нестероїдними протизапальними засобами, а також при відміні нестероїдних протизапальних засобів. Метотрексат. У двох дослідженнях вивчалися ефекти еторикоксибу в дозах 60, 90 або 120 мг 1 раз на день протягом семи днів у пацієнтів, які отримували 1 раз на тиждень метотрексат у дозі від 7,5 до 20 мг на лікування РА. Еторикоксиб у дозах 60 та 90 мг не впливав на концентрацію метотрексату в плазмі та нирковий кліренс метотрексату. В одному дослідженні церикоксиб у дозі 120 мг не фармакокінетично впливав на метотрексат, але в іншому дослідженні концентрація метотрексату в плазмі підвищувалася на 28 %, а нирковий кліренс метотрексату знижувався на 13 %. При одночасному прийомі церикоксибу та метотрексату рекомендується вести спостереження щодо можливої появи токсичних ефектів метотрексату. Пероральні контрацептиви. Еторикоксиб у дозі 60 мг при одночасному прийомі протягом 21 дня з пероральними контрацептивами, що містять 35 мкг етинілестрадіолу (ЕЕ) та від 0,5 мг до 1 мг норетиндрону, збільшував AUC0-24 год ЕЕ на 37 % у рівноважному стані. Прийом церикоксиксу в дозі 120 мг у поєднанні з вищевказаними пероральними контрацептивами (одночасно або з інтервалом 12 годин) збільшував AUC0-24год. ЕЕ на 50-60% у рівноважному стані. Це збільшення концентрації ЕЕ слід враховувати при виборі перорального контрацептиву для одночасного застосування з церикоксибом. Подібна взаємодія може спричинити збільшення частоти розвитку небажаних явищ, пов'язаних із застосуванням пероральних контрацептивів (наприклад, венозних тромбоемболій у жінок із групи ризику). Замісна гормональна терапія (ЗГТ). Призначення еторікоксибу в дозі 120 мг одночасно з препаратами для ЗГТ, що містять кон'юговані естрогени в дозі 0,625 мг протягом 28 днів, збільшує середнє рівноважне значення AUC0-24 год некон'югованого естрону (41 %), еквіліну (76 %) та 17-2 %). Вплив доз еторикоксибу, рекомендованих для тривалого застосування (30, 60 та 90 мг), не вивчався. Еторикоксиб у дозі 120 мг змінював експозицію (AUC0-24год) даних естрогенних компонентів менш ніж удвічі порівняно з монотерапією кон'югованими естрогенами при збільшенні дози з 0,625 до 1,25 мг. Клінічне значення таких збільшення невідомо, застосування більш високих доз кон'югованих естрогенів у поєднанні з еторикоксибом не вивчалося.Підвищення концентрації естрогенів слід брати до уваги при виборі гормональної терапії в період постменопаузи при одночасному призначенні з етороксібом, оскільки збільшення експозиції естрогенів може підвищувати ризик розвитку небажаних явищ, пов'язаних із ЗГТ. Преднізон/Преднізолон. У дослідженнях лікарських взаємодій эторикоксиб не впливав на клінічно значущий вплив на фармакокінетику преднізону/преднізолону. Дігоксин. При застосуванні эторикоксибу в дозі 120 мг один раз на день протягом 10 днів у здорових добровольців не спостерігалося зміни рівноважної AUC0-24год дигоксину в плазмі або впливу на його виведення нирками. При цьому спостерігалося збільшення Стах дигоксину приблизно на 33%. Таке підвищення, як правило, не є важливим для більшості пацієнтів. Тим не менш, при одночасному застосуванні церикоксибу та дигоксину слід спостерігати за станом пацієнтів із високим ризиком прояву токсичної дії дигоксину. Вплив еторикоксибу на препарати, що метаболізуються сульфотрансферазами. Еторикоксиб є інгібітором сульфотрансферази людини (зокрема, SULT1E1) і може підвищувати концентрацію ЕЕ у сироватці крові. У зв'язку з тим, що в даний час отримано недостатньо даних про ефекти різних сульфотрансфераз, а їхня клінічна значущість для застосування багатьох лікарських препаратів ще вивчається, доцільно з обережністю призначати церикоксиб одночасно з іншими лікарськими препаратами, що метаболізуються сульфотрансферазами людини (наприклад, пероральний сальбутамол і ). Вплив етерокіксібу на препарати, що метаболізуються ізоферментами системи цитохромів. Грунтуючись на результатах досліджень in vitro, не очікується, що эторикоксиб інгібуватиме ізоферменти цитохрому Р450 (CYP) 1А2, 2С9, 2С19, 2D6, 2Е1 або 3А4. У дослідженні у здорових добровольців щоденне застосування церикоксибу в дозі 120 мг не впливало на активність ізоферменту CYP3A4 печінки при оцінці за допомогою еритроміцинового дихального тесту.Спосіб застосування та дозиВсередину, незалежно від їди, запиваючи невеликою кількістю води. Дія препарату реалізується швидше при прийомі натще. Внаслідок можливого підвищення ризику серцево-судинних ускладнень слід використовувати мінімальну ефективну дозу мінімально можливим курсом. Остеоартроз: рекомендована доза етерокіксібу становить 30 мг 1 раз на день. У разі недостатнього ефекту добова доза препарату може бути збільшена до 60 мг на добу. Добова доза при остеоартрозі не повинна перевищувати 60 мг. Ревматоїдний артрит та анкілозуючий спондиліт: рекомендована доза еторикоксібу становить 60 мг 1 раз на день. У пацієнтів із недостатнім клінічним ефектом можливе збільшення добової дози препарату до 90 мг один раз на день. Після клінічної стабілізації захворювання можливе зниження дози до 60 мг один раз на день. У разі відсутності ознак клінічного покращення слід розглянути можливість застосування інших методів лікування. Добова доза не повинна перевищувати 90 мг. Гострий подагричний артрит: рекомендована доза церикоксибу в гострому періоді становить 120 мг 1 раз на день. Тривалість застосування препарату у дозі 120 мг не перевищує 8 днів. Добова доза не повинна перевищувати 120 мг. Гострий біль після стоматологічних операцій: рекомендована доза еторикоксибу становить 90 мг 1 раз на день. Еторикоксиб слід застосовувати лише у гострий симптоматичний період тривалістю не більше 3 днів. Добова доза для усунення болю після стоматологічних операцій не повинна перевищувати 90 мг. Деяким пацієнтам можуть знадобитися додаткові засоби для забезпечення адекватного рівня знеболювання у післяопераційному періоді протягом триденного періоду терапії церикоксибом. Особливі групи пацієнтів Літні пацієнти: корекція дози не потрібна. Як і при застосуванні інших препаратів, еторикоксиб слід застосовувати з обережністю. Діти: застосування еторикоксибу у пацієнтів віком до 16 років протипоказано. Порушення функції печінки: незалежно від показання до застосування пацієнтам з порушеннями функції печінки легкого ступеня тяжкості (5-6 балів за шкалою Чайлд-П'ю) не слід перевищувати дозу 60 мг 1 раз на день, пацієнтам з порушеннями функції печінки середнього ступеня тяжкості (7 -9 балів за шкалою Чайлд-Пью) – 30 мг 1 раз на день. Рекомендується бути обережним при застосуванні препарату у пацієнтів з порушеннями функції печінки середнього ступеня тяжкості, оскільки клінічний досвід застосування препарату у даної групи пацієнтів обмежений. У зв'язку з відсутністю клінічного досвіду застосування препарату у пацієнтів з тяжкими порушеннями функції печінки (≥10 балів за шкалою Чайлд-П'ю) препарат протипоказаний для цієї групи пацієнтів. Порушення функції нирок: не потрібна корекція дози препарату при застосуванні у пацієнтів із КК ≥30 мл/хв. Застосування препарату у пацієнтів із ККПередозуванняУ клінічних дослідженнях прийом еторикоксибу в разовій дозі до 500 мг і багаторазовий прийом до 150 мг/день протягом 21 дня не викликав суттєвих токсичних ефектів. Були отримані повідомлення про гостре передозування еторикоксибом, однак, у більшості випадків про небажані реакції не повідомлялося. Найчастіші небажані реакції відповідали профілю безпеки церикоксибу (наприклад, порушення з боку шлунково-кишкового тракту, кардіоренальні явища). У разі передозування доцільно вживати звичайні підтримувальні заходи, такі як видалення невсмоктаного препарату із ШКТ, клінічне спостереження і, при необхідності, підтримуюча терапія. Еторікоксиб не виводиться при гемодіалізі; виведення еторикоксибу при перитонеальному діалізі не вивчалося.Запобіжні заходи та особливі вказівкиВплив на ШКТ У пацієнтів, які отримували еторикоксиб, спостерігалися ускладнення з боку верхніх відділів шлунково-кишкового тракту (перфорації, виразки або кровотечі), іноді з летальним кінцем. Рекомендується бути обережним при лікуванні пацієнтів з високим ризиком розвитку ускладнень з боку шлунково-кишкового тракту при застосуванні нестероїдних протизапальних засобів, зокрема, у літніх пацієнтів, що одночасно застосовують інші нестероїдні протизапальні засоби, ацетилсаліцилову кислоту або у пацієнтів із захворюваннями шлунково-кишкового тракту в анамнезі, такими як виразка та шлунково-кишкова кровотеча. Існує додатковий ризик розвитку небажаних реакцій з боку шлунково-кишкового тракту (шлунково-кишкові виразки або інші ускладнення з боку шлунково-кишкового тракту) при одночасному застосуванні церикоксибу та ацетилсаліцилової кислоти (навіть у низьких дозах). У довгострокових клінічних дослідженнях не спостерігалося достовірних відмінностей щодо безпеки для ШКТ при застосуванні селективних інгібіторів ЦОГ-2 у комбінації з ацетилсаліциловою кислотою порівняно із застосуванням нестероїдних протизапальних засобів у комбінації з ацетилсаліциловою кислотою. Вплив на серцево-судинну систему Результати клінічних досліджень свідчать про те, що застосування лікарських препаратів класу селективних інгібіторів ЦОГ-2 пов'язано з підвищеним ризиком тромбоутворення (особливо інфаркту міокарда (ІМ) та інсульту) порівняно з плацебо та деякими НПЗЗ. Ризик розвитку серцево-судинних ускладнень при застосуванні селективних інгібіторів ЦОГ-2 може зростати зі збільшенням дози та тривалості лікування, тому слід застосовувати церикоксиб протягом максимально короткого періоду часу та у найнижчій ефективній добовій дозі. Необхідно періодично оцінювати потребу пацієнта у симптоматичному лікуванні та відповідь на терапію, особливо у пацієнтів з ОА. Пацієнтам з відомими факторами ризику розвитку серцево-судинних ускладнень (наприклад, артеріальна гіпертензія, гіперліпідемія, цукровий діабет, куріння) церикоксиб необхідно призначати тільки після ретельної попередньої оцінки співвідношення користі-ризику. Селективні інгібітори ЦОГ-2 не є заміною ацетилсаліцилової кислоти при профілактиці серцево-судинних захворювань через відсутність антитромбоцитарного ефекту, тому не слід припиняти застосування антиагрегантних препаратів. Вплив на функцію нирок Ниркові простагландини можуть відігравати компенсаторну роль у підтримці ниркової перфузії. Тому за наявності умов, що негативно впливають на ниркову перфузію, призначення еторикоксибу може призвести до зменшення утворення простагландинів і, як наслідок, зниження ниркового кровотоку, і тим самим призвести до погіршення функції нирок. Найбільший ризик розвитку цієї реакції виникає у пацієнтів із значним зниженням функції нирок, некомпенсованою серцевою недостатністю або цирозом печінки в анамнезі. У таких пацієнтів необхідно проводити моніторинг функції нирок. Затримка рідини, набряки та артеріальна гіпертензія Як і у разі застосування інших препаратів, що інгібують синтез простагландинів, у пацієнтів, які приймають еторикоксиб, спостерігалися затримка рідини, набряки та артеріальна гіпертензія. Застосування будь-яких нестероїдних протизапальних засобів, включаючи церикоксикс, може бути пов'язане з виникненням або рецидивом хронічної (застійної) серцевої недостатності. Інформація про дозозалежну реакцію для церикоксибу наведена в розділі "Фармакологічні властивості". Слід виявляти обережність при призначенні церикоксибу пацієнтам із серцевою недостатністю в анамнезі, дисфункцією лівого шлуночка, артеріальною гіпертензією та пацієнтам з уже наявними набряками, що виникли з будь-якої іншої причини. При появі клінічних ознак погіршення стану у таких пацієнтів слід вжити відповідних заходів, включаючи скасування еторікоксибу. Застосування еторикоксибу, особливо у високих дозах, може бути пов'язане з розвитком більш тяжкої артеріальної гіпертензії, ніж при застосуванні деяких інших нестероїдних протизапальних засобів та селективних інгібіторів ЦОГ-2. Тому під час лікування церикоксибом слід звернути особливу увагу на моніторинг АТ, який має контролюватись протягом двох тижнів після початку лікування та періодично надалі. При значному підвищенні артеріального тиску слід розглянути альтернативне лікування. Вплив на функцію печінки Підвищення активності аланінамінотрансферази (АЛТ) та/або аспартатамінотрансферази (ACT) (приблизно в три або більше рази щодо верхньої межі норми) було зареєстровано у клінічних дослідженнях приблизно у 1% пацієнтів, які отримували еторикоксиб протягом терміну до одного року у дозах 30 мг, 60 мг та 90 мг на день. Необхідно спостерігати за станом усіх пацієнтів із симптомами та/або ознаками дисфункції печінки, а також пацієнтів із зміненими лабораторними показниками функції печінки. Якщо виникають ознаки печінкової недостатності або показники функції печінки значно відхиляються від норми (втричі вище за верхню межу норми), прийом еторикоксибу повинен бути припинений. Загальні рекомендації Якщо під час лікування у пацієнтів погіршується будь-яка з функцій органів або систем органів, описаних вище, повинні бути вжиті відповідні заходи та розглянуто питання про скасування еторикоксибу. При застосуванні эторикоксибу у пацієнтів похилого віку та у пацієнтів з порушенням функції нирок, печінки або серця необхідне відповідне медичне спостереження. З обережністю слід розпочинати лікування ерикоксибом пацієнтам із зневодненням. Перед початком терапії церикоксибом рекомендується провести регідратацію. У період постмаркетингового спостереження при застосуванні НПЗП та деяких селективних інгібіторів ЦОГ-2 дуже рідко повідомлялося про розвиток серйозних реакцій шкіри. Деякі з них, у тому числі ексфоліативний дерматит, синдром Стівенса-Джонсона та токсичний епідермальний некроліз, були з смертю. Ризик розвитку цих реакцій найбільш високий на початку курсу терапії, здебільшого протягом першого місяця лікування. Повідомлялося про розвиток серйозних реакцій гіперчутливості, таких як анафілаксія та ангіоневротичний набряк, у пацієнтів, які отримували еторикоксиб. Застосування деяких селективних інгібіторів ЦОГ-2 супроводжувалося підвищеним ризиком розвитку шкірних реакцій у пацієнтів із якоюсь лікарською алергією в анамнезі. Еторикоксиб повинен бути скасований при першій появі висипу на шкірі,уражень слизової оболонки або будь-якої іншої ознаки гіперчутливості. Застосування еторикоксибу може маскувати лихоманку та інші ознаки запалення. Застосування еторикоксибу, як і інших препаратів, що інгібують ЦОГ та синтез простагландинів, не рекомендується жінкам, які планують вагітність (див. розділ "Застосування при вагітності та в період грудного вигодовування"). Оболонка таблетки містить лактозу. Пацієнтам з такими рідкісними вродженими захворюваннями, як непереносимість лактози, дефіцит лактази або глюкозогалактозна мальабсорбція, не слід приймати цей препарат. Вплив на здатність до керування автотранспортом та управління механізмами Пацієнтам, у яких на фоні застосування церикоксибу відзначаються епізоди запаморочення, сонливості чи слабкості, слід утриматися від керування транспортними засобами та роботи з механізмами.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
365,00 грн
222,00 грн
Склад, форма випуску та упаковкаПігулки - 1 таб. Активні речовини: еторикоксиб – 90 мг; Допоміжні речовини: кальцію безводний гідрофосфат - 39 мг, целюлоза мікрокристалічна - 38.25 мг, повідон К30 - 9 мг, магнію стеарат - 1.5 мг, кроскармеллоза натрію - 2.25 мг; Склад оболонки таблетки: Опадрай II білий 32К580000С – 6 мг: гіпромелоза 15 cPs 2.4 мг, лактози моногідрат 1.68 мг, титану діоксид 1.44 мг, тріацетин 0.48 мг. Таблетки, покриті плівковою оболонкою, 30 мг, 60 мг, 90 мг та 120 мг. По 7 пігулок в Аl/Аl блістер. По 1 блістеру разом з інструкцією із застосування в картонну пачку. По 10 пігулок в Аl/Аl блістер. По 1, 2, 3, 5, 6, 9, 10 блістерів разом з інструкцією із застосування в картонну пачку. По 14 пігулок в Аl/Аl блістер. По 1,2, 4, 6, 7 блістерів разом із інструкцією із застосування в картонну пачку.Опис лікарської формиТаблетки, покриті плівковою оболонкою білого кольору, круглі, двоопуклі.Фармакотерапевтична групаНестероїдні протизапальні препарати (НПЗЗ).ФармакокінетикаВсмоктування Эторикоксиб швидко всмоктується прийому внутрішньо. Абсолютна біодоступність прийому внутрішньо становить близько 100%. При застосуванні препарату у дорослих натще в дозі 120 мг один раз на день до досягнення рівноважного стану максимальна концентрація в плазмі (Сmах) становить 3,6 мкг/мл. Час досягнення Сmах (Тmах) становить приблизно 1 годину після прийому препарату. Середня геометрична площа під кривою "концентрація – час" (AUC0-24ч) склала 37,8 мкг * год / мл. Фармакокінетика церикоксибу в діапазоні терапевтичних доз має лінійний характер. При прийомі эторикоксиба в дозі 120 мг під час їжі (їжа з високим вмістом жирів) не спостерігалося клінічно значущого впливу на ступінь абсорбції. Швидкість абсорбції при цьому змінювалася, що призводило до зниження Сmах на 36% і збільшення Тmах на 2 год. Ці дані не є клінічно значущими. У клінічних дослідженнях церикоксиб застосовувався незалежно від їди. Розподіл Еторікоксиб приблизно на 92% зв'язується з білками плазми у людини в діапазоні концентрацій від 0,05 до 5 мкг/мл. Об'єм розподілу у рівноважному стані (VdSS) становить близько 120 л. Еторикоксиб проникає через плацентарний бар'єр у щурів та кролів та гематоенцефалічний бар'єр у щурів. Метаболізм Еторикоксиб екстенсивно метаболізується, У людини виявлено п'ять метаболітів церикоксиксу. Основним метаболітом є 6'-карбоксиацетилеторикоксиб, що утворюється в результаті подальшого окислення 6'-гідроксиметилеторикоксибу. Ці основні метаболіти не мають помітної активності або слабо інгібують ЦОГ-2. Жоден із цих метаболітів не інгібує ЦОГ-1. Виведення Після одноразового внутрішньовенного введення здоровим добровольцям міченого радіоактивного церикоксибу в дозі 25 мг 70 % церикоксибу виводилося через нирки та 20 % – через кишечник, переважно у вигляді метаболітів. Менше 2% виявлялося у незміненому вигляді. Виведення еторикоксибу відбувається в основному шляхом метаболізму в печінці з подальшим виведенням нирками. Рівноважні концентрації эторикоксиба досягаються при щоденному прийомі в дозі 120 мг протягом 7 днів з коефіцієнтом кумуляції близько 2, що відповідає періоду напіввиведення близько 22 год. Плазмовий кліренс після внутрішньовенного введення 25 мг становить приблизно 50 мл/хв. Особливі групи пацієнтів Стать: фармакокінетичні параметри препарату у чоловіків та жінок не відрізняються. Літні пацієнти: фармакокінетика препарату у пацієнтів віком понад 65 років порівнянна з фармакокінетикою у пацієнтів молодшого віку. Діти: фармакокінетика еторикоксибу у дітей (60 кг, які приймали церикоксиб у дозі 90 мг 1 раз на день), була аналогічна фармакокінетиці у дорослих, які приймали церикоксиб у дозі 90 мг 1 раз на день. Безпека та ефективність застосування церикоксибу у дітей не встановлена. Печінкова недостатність: у пацієнтів з печінковою недостатністю легкого ступеня тяжкості (5-6 балів за шкалою Чайлд-П'ю) прийом еторикоксибу в дозі 60 мг 1 раз на день супроводжувався збільшенням показника AUC приблизно на 16% порівняно зі здоровими добровольцями, які приймали препарат у тій ж дозі. У пацієнтів з печінковою недостатністю середнього ступеня тяжкості (7-9 балів за шкалою Чайлд-П'ю), які отримували еторикоксиб у дозі 60 мг один раз на день через день, середнє значення AUC було таким же, як у здорових добровольців, які приймали еторикоксиб у дозі 60 мг раз на день щодня. Застосування еторикоксибу в дозі 30 мг один раз на день не вивчалося у цій групі пацієнтів. Клінічні та фармакокінетичні дані досліджень у пацієнтів з тяжкою печінковою недостатністю (>10 балів за шкалою Чайлд-П'ю) відсутні. Ниркова недостатність: фармакокінетичні показники одноразового застосування церикоксибу в дозі 120 мг у пацієнтів з нирковою недостатністю помірного та тяжкого ступеня та у пацієнтів з термінальною стадією хронічної ниркової недостатності, які перебувають на гемодіалізі, суттєво не відрізняються від показників у здорових добровольців. Гемодіаліз незначно впливає на виведення препарату (кліренс при діалізі – близько 50 мл/хв).ФармакодинамікаЕторикоксиб при пероральному прийомі в терапевтичних концентраціях є селективним інгібітором циклооксигенази типу 2 (ЦОГ-2). У дослідженнях з клінічної фармакології церикоксиб дозозалежно інгібував ЦОГ-2, не впливаючи на ЦОГ-1 при застосуванні доз до 150 мг на день. Еторикоксиб не пригнічував синтез простагландинів у слизовій оболонці шлунка і не впливав на функцію тромбоцитів. ЦОГ відповідає за синтез простагландинів. Виділено дві ізоформи цього ферменту - ЦОГ-1 та ЦОГ-2. ЦОГ-2 є ізоферментом, який індукується під дією прозапальних медіаторів і розглядається як основний фермент, який відповідає за синтез простаноїдних медіаторів болю, запалення та лихоманки. ЦОГ-2 бере участь у процесах овуляції, імплантації та закриття артеріальної протоки, регуляції функції нирок, центральної нервової системи (індукція лихоманки, відчуття болю, когнітивна функція), а також може грати певну роль у процесі загоєння виразок. ЦОГ-2 була виявлена у тканинах, що оточують виразки шлунка у людини, але її значення для загоєння виразки не встановлено. Ефективність У пацієнтів з остеоартрозом (ОА) церикоксиб при застосуванні в дозі 60 мг один раз на день викликав достовірне зменшення болю та покращення оцінки свого стану пацієнтами. Ці сприятливі ефекти спостерігалися вже другого дня лікування і зберігалися протягом 52 тижнів. Дослідження еторикоксибу в дозі 30 мг один раз на день (із застосуванням подібних методів оцінки) продемонстрували ефективність препарату порівняно з плацебо протягом усього періоду лікування (12 тижнів). У дослідженні, яке проводилося з метою визначення оптимальної дози, еторикоксиб у дозі 60 мг продемонстрував достовірно більш виражене поліпшення, ніж у дозі 30 мг для всіх 3 первинних кінцевих точок через 6 тижнів лікування. Застосування дози 30 мг на лікування ОА суглобів кистей рук не вивчалося. У пацієнтів з ревматоїдним артритом (РА) прийом еторикоксибу в дозі 60 мг або 90 мг один раз на день забезпечував достовірне зменшення болю, запалення та покращення рухливості. Ці сприятливі ефекти зберігалися протягом 12-тижневого періоду лікування. Дослідження порівняння застосування церикоксибу в дозі 60 мг і 90 мг один раз на день для лікування РА показало, що обидва режими дозування забезпечували переважну ефективність терапії порівняно з плацебо. Доза церикоксибу 90 мг один раз на день перевищувала за ефективністю дозу 60 мг один раз на день при оцінці ефекту за допомогою Глобальної Шкали. % довірчий інтервал (ДІ): -4,98 мм; -0,45 мм). У пацієнтів із гострим подагричним артритом еторикоксиб у дозі 120 мг один раз на день протягом усього періоду лікування (8 днів) зменшував помірний та сильний біль у суглобах та запалення порівняно з індометацином у дозі 50 мг 3 рази на день. Зменшення болю відзначалося вже через 4 години після початку лікування. У пацієнтів з анкілозуючим спондилітом еторикоксиб при застосуванні в дозі 90 мг один раз на день забезпечував достовірне зменшення болю в спині, запалення, скутості, а також покращення рухової функції. Клінічна ефективність эторикоксиба спостерігалася вже другого дня лікування та зберігалася протягом усього періоду лікування (52 тижні). В іншому дослідженні, в рамках якого порівнювалася ефективність застосування церикоксибу в дозі 90 мг один раз на день та 60 мг один раз на день, цей препарат продемонстрував рівну ефективність порівняно з напроксеном у дозі 1000 мг один раз на день. Серед пацієнтів, у яких не було досягнуто адекватної клінічної відповіді на терапію протягом 6 тижнів при застосуванні церикоксибу у дозі 60 мг один раз на день, збільшення добової дози до 90 мг дозволяло покращити результати лікування, оцінені за допомогою шкали інтенсивності болю у спині. -100 мм візуально-аналогова шкала), порівняно з продовженням терапії еторікоксибом у дозі 60 мг один раз на день. Середнє поліпшення склало -2,70 мм (95% ДІ: 4,88 мм; -0,52 мм). У клінічному дослідженні з вивчення болю після стоматологічних операцій эторикоксиб у дозі 90 мг призначали раз на день протягом трьох днів. У підгрупі пацієнтів з помірним болем (при вихідній оцінці) еторикоксиб у дозі 90 мг продемонстрував знеболюючий ефект, аналогічний ібупрофену в дозі 600 мг (16,11 порівняно з 16,39, Р = 0,722) та більший, ніж при застосуванні комбінації парацетамол/ кодеїн у дозі 600 мг/60 мг (11,00; Р Безпека Програма MEDAL (Багатонаціональна Програма Оцінки Довгострокового Призначення Еторікоксибу та Диклофенаку при Артріті) Програма MEDAL була проспективною програмою оцінки безпеки на підставі серцево-судинних явищ за об'єднаними даними трьох рандомізованих подвійних сліпих активно-контрольованих досліджень: MEDAL, EDGE II та EDGE. Дослідження MEDAL являло собою дослідження, тривалість якого визначалася досягненням кінцевих точок (серцево-судинних явищ), воно включало 17804 пацієнта з ОА та 5700 пацієнтів з РА, які отримували еторикоксиб у дозі 60 мг (ОА) або 90 мг (ОА та РА) або ді у дозі 150 мг на день у середньому протягом 20,3 місяців (максимум 42,3 місяці, медіана 21,3 місяці). У цьому дослідженні реєстрували лише серйозні небажані явища та випадки вибуття з дослідження внаслідок будь-якого небажаного явища. У дослідженнях EDGE та EDGE II порівнювали безпеку прийому церикоксибу та диклофенаку для шлунково-кишкового тракту (ЖКТ). До дослідження EDGE було включено 7111 пацієнтів з ОА, які отримували еторикоксиб у дозі 90 мг на день (в 1,5 рази більше за дозу, рекомендовану при ОА) або диклофенак у дозі 150 мг на день протягом у середньому 9,1 місяців (максимум 16 , 6 місяців, медіана 11,4 місяців). У дослідження EDGE II було включено 4086 пацієнтів з РА, які отримували еторикоксиб у дозі 90 мг на день або диклофенак у дозі 150 мг на день протягом середньому 19,2 місяців (максимум 33,1 місяця, медіана 24 місяці). В об'єднаній програмі MEDAL аналізували дані щодо лікування 34701 пацієнтів з ОА або РА, середня тривалість лікування склала 17,9 місяців (максимум 42,3 місяці, медіана 16,3 місяців), при цьому приблизно 12800 пацієнтів отримували лікування протягом понад 24 місяців. Пацієнти, включені до програми, при вихідній оцінці мали широкий спектр серцево-судинних та шлунково-кишкових факторів ризику. Були виключені пацієнти, які мали в анамнезі нещодавно перенесений інфаркт міокарда (ІМ), аортокоронарне шунтування або черезшкірне коронарне втручання протягом 6 місяців перед включенням до дослідження. У дослідженнях дозволялося застосовувати гастропротектори та низькі дози аспірину. Загальна безпека Достовірних відмінностей між эторикоксибом та диклофенаком щодо частоти розвитку серцево-судинних тромботичних явищ виявлено не було. Кардіоренальні небажані явища найчастіше спостерігалися при прийомі церикоксибу в порівнянні з диклофенаком, ефект був дозозалежним (див. результати нижче). Небажані явища з боку шлунково-кишкового тракту та печінки достовірно частіше спостерігалися при прийомі диклофенаку, ніж при прийомі церикоксибу. Частота небажаних явищ у дослідженнях EDGE та EDGE II та небажаних явищ, визнаних серйозними або зажадали відміни лікування, у дослідженні MEDAL була вищою при прийомі еторикоксибу порівняно з диклофенаком. Результати дослідження безпеки щодо серцево-судинної системи Частота підтверджених серйозних тромботичних серцево-судинних небажаних явищ (включаючи серцеві, цереброваскулярні та явища з боку периферичної судинної системи) була порівнянна між групами, які отримували церикоксиб або диклофенак (дані наведені в таблиці нижче). Не виявлено статистично значимих відмінностей щодо частоти тромботичних явищ між еторикоксибом та диклофенаком у всіх проаналізованих підгрупах, включаючи категорії пацієнтів з підвищеним ризиком серцево-судинних ускладнень. Відносний ризик для підтверджених серйозних серцево-судинних небажаних тромботичних явищ був подібним при прийомі еторикоксібу в дозі 60 мг або 90 мг і диклофенаку в дозі 150 мг. Частота підтверджених тромботичних серцево-судинних серйозних небажаних явищ (Об'єднана програма MEDAL) Еторікоксиб(N=16819)25 836 пацієнто-років Диклофенак(N=16483)24 766 пацієнто-років Порівняння між видами лікування Частота 1 (95% ДІ) Частота 1 (95% ДІ) Відносний ризик (95% ДІ) Підтверджені тромботичні серцево-судинні серйозні небажані явища За виконання вимог протоколу (Per protocol) 1,24 (1,11; 1,38) 1,30 (1,17; 1,45) 0,95 (0,81; 1,11) Залежно від призначеного лікування (Intent-to-treat) 1,25 (1,14; 1,36) 1,19 (1,08; 1,30) 1,05 (0,93; 1,19) Підтверджені явища з боку серця За виконання вимог протоколу (Per protocol) 0,71 (0,61; 0,82) 0,78 (0,68; 0,90) 0,90 (0,74; 1,10) Залежно від призначеного лікування (Intent-to-treat) 0,69 (0,61; 0,78) 0,70 (0,62; 0,79) 0,99 (0,84; 1,17) Підтверджені цереброваскулярні явища За виконання вимог протоколу (Per protocol) 0,34 (0,28; 0,42) 0,32 (0,25; 0,40) 1,08 (0,80; 1,46) Залежно від призначеного лікування (Intent-to-treat) 0,33 (0,28; 0,39) 0,29 (0,24; 0,35) 1,12 (0,87; 1,44) Підтверджені явища з боку периферичної судинної системи За виконання вимог протоколу (Per protocol) 0,20 (0,15; 0,27) 0,22 (0,17; 0,29) 0,92 (0,63; 1,35) Залежно від призначеного лікування (Intent-to-treat) 0,24 (0,20; 0,30) 0,23 (0,18; 0,28) 1,08 (0,81; 1,44) 1 число явищ на 100 пацієнто-років; ДІ = довірчий інтервал; N = загальна кількість пацієнтів, які виконали вимоги протоколу. При виконанні вимог протоколу: всі явища, що розвинулися на тлі досліджуваної терапії або протягом 14 днів після її припинення (виключені пацієнти, які прийняли <75% досліджуваного препарату або приймали НПЗП >10% часу, що не входять до дослідження). Залежно від призначеного лікування: всі підтверджені явища, що розвинулися до закінчення дослідження (включно з пацієнтами, які могли піддаватися не включеним до дослідження втручанням після припинення прийому досліджуваних препаратів). Загальна кількість рандомізованих пацієнтів: n = 17412 для эторикоксиба і n = 17289 для диклофенаку. Смертність від серцево-судинних явищ, а також загальна смертність у групах лікування церикоксибом та диклофенаком були порівнянними. Кардіоренальні явища Приблизно у 50% пацієнтів, включених у дослідження MEDAL, при початковій оцінці в анамнезі було зареєстровано артеріальну гіпертензію. У проведеному дослідженні частота вибування внаслідок небажаних явищ, пов'язаних з артеріальною гіпертензією, була статистично значуще вищою під час прийому эторикоксиба проти диклофенаком. Частота небажаних явищ, пов'язаних з хронічною серцевою недостатністю (випадки вибування з дослідження або серйозні небажані явища), була подібною до груп еторікоксибу в дозі 60 мг і диклофенаку в дозі 150 мг, але була вищою для еторікоксибу в дозі 90 мг порівняно з диклофеном. дозі 150 мг (і статистично значуще вище для еторикоксибу в дозі 90 мг у порівнянні з диклофенаком у дозі 150 мг у дослідженні MEDAL у пацієнтів з ОА). Частота підтверджених небажаних явищ,пов'язаних з хронічною серцевою недостатністю (серйозних, які призвели до госпіталізації або необхідності невідкладної допомоги), була незначно вищою для церикоксибу порівняно з диклофенаком у дозі 150 мг, ефект був дозозалежним. Частота випадків вибування з дослідження внаслідок небажаних явищ, пов'язаних з набряками, була вищою для еторікоксибу в дозі 150 мг, порівняно з диклофенаком у дозі 150 мг, ефект був дозозалежним (статистично значимо для еторікоксибу в дозі 90 мг, але не для етороксиксу в дозі 60 мг).була вищою для эторикоксиба порівняно з диклофенаком в дозі 150 мг, ефект був дозозалежним (статистично значуще для етіроксиксібу в дозі 90 мг, але не для етіроксиксібу в дозі 60 мг).була вищою для эторикоксиба порівняно з диклофенаком в дозі 150 мг, ефект був дозозалежним (статистично значуще для етіроксиксібу в дозі 90 мг, але не для етіроксиксібу в дозі 60 мг). Результати оцінки кардіоренальної безпеки у дослідженнях EDGE та EDGE II узгоджуються з результатами у дослідженні MEDAL В окремих дослідженнях програми MEDAL абсолютна частота вибування з дослідження в будь-якій групі лікування при прийомі еторикоксибу (60 мг або 90 мг) становила до 2,6% при артеріальній гіпертензії, до 1,9% при набряках, і до 1,1% при хронічній серцевої недостатності. У пацієнтів, які приймали церикоксиб у дозі 90 мг, частота вибуття з дослідження була вищою, ніж у пацієнтів, які приймали церикоксиб у дозі 60 мг. Результати оцінки переносимості з боку ШКТ у Програмі MEDAL У кожному з трьох досліджень, що входять до програми MEDAL, частота вибування з дослідження для будь-яких клінічних небажаних явищ з боку шлунково-кишкового тракту (наприклад, диспепсія, біль у животі, виразки) була достовірно нижчою для еторикоксибу порівняно з диклофенаком. Частота вибуття з дослідження внаслідок небажаних клінічних явищ з боку шлунково-кишкового тракту на 100 пацієнто-років за весь період дослідження становила: 3,23 для еторикоксибу та 4,96 для диклофенаку в дослідженні MEDAL; 9,12 для эторикоксиба і 12,28 для диклофенаку у дослідженні EDGE; 3,71 для еторикоксибу та 4,81 для диклофенаку в дослідженні EDGE II. Результати оцінки безпеки щодо ШКТ у Програмі MEDAL До небажаних явищ з боку верхніх відділів шлунково-кишкового тракту були віднесені перфорації, виразки та кровотечі. Ускладнені небажані явища з боку верхніх відділів шлунково-кишкового тракту включали перфорацію, непрохідність та ускладнені кровотечі; неускладнені явища включали неускладнені кровотечі та неускладнені виразки. При прийомі эторикоксиба порівняно з диклофенаком загальна частота небажаних явищ з боку верхніх відділів шлунково-кишкового тракту була достовірно нижчою. Достовірних відмінностей між етерокіксібом і диклофенаком за частотою ускладнених небажаних явищ виявлено не було. Для випадків кровотеч із верхніх відділів шлунково-кишкового тракту (ускладнених та неускладнених) не було виявлено достовірних відмінностей між еторикоксибом та диклофенаком.Перевага церикоксибу порівняно з диклофенаком щодо ускладнень з боку верхніх відділів ШКТ не була статистично значущою у пацієнтів, які одночасно приймали аспірин у низьких дозах (близько 33% пацієнтів). Частота підтверджених ускладнених та неускладнених клінічних небажаних явищ з боку верхніх відділів шлунково-кишкового тракту на 100 пацієнто-років (перфорації, виразки та кровотечі) склала 0,67 (95 % ДІ: 0,57; 0,77) для церикоксиксу та 0,97 (95 % ДІ: 0,85; 1,10) для диклофенаку, відносний ризик склав 0,69 (95% ДІ: 0,57; 0,83). При оцінці частоти підтверджених клінічних небажаних явищ з боку верхніх відділів шлунково-кишкового тракту у пацієнтів похилого віку максимальне зниження спостерігалося у пацієнтів у віці ≥75 років у групі церикоксибу в порівнянні з диклофенаком - 1,35 (95 % ДІ: 0,94; 1,87) та 2,78 (95% ДІ: 2,14; 3,56) на 100 пацієнто-років відповідно. Частота підтверджених небажаних явищ з боку нижніх відділів шлунково-кишкового тракту (перфорація тонкої або товстої кишки, непрохідність, кровотеча) достовірно не розрізнялася між групами, які приймали церикоксиб та диклофенак. Результати оцінки безпеки щодо печінки у Програмі MEDAL При прийомі эторикоксиба порівняно з диклофенаком спостерігалася статистично достовірно нижча частота вибуття з дослідження через небажані явища з боку печінки. В об'єднаній програмі MEDAL 0,3% пацієнтів, які приймали еторикоксиб, та 2,7% пацієнтів, які приймали диклофенак, вибули з дослідження через небажані явища з боку печінки. Частота небажаних явищ на 100 пацієнто-років склала 0,22 для церикоксиксу і 1,84 для диклофенаку (р Додаткові дані щодо безпеки, пов'язані з тромботичними серцево-судинними явищами У клінічних дослідженнях, за винятком Програми MEDAL, приблизно 3100 пацієнтів отримували церикоксикс у дозі ≥60 мг на день протягом 12 тижнів та довше. У цих дослідженнях не було виявлено помітних відмінностей у частоті підтверджених серйозних тромботичних серцево-судинних явищ у пацієнтів, які отримували церикоксиб у дозі ≥60 мг, плацебо або нестероїдні протизапальні засоби, що не містять напроксен. Однак у порівнянні з пацієнтами, які отримували напроксен у дозі 500 мг двічі на день, частота цих явищ була вищою у пацієнтів, які отримували еторикоксиб. Різниця в антиагрегантній активності між деякими нестероїдними протизапальними засобами, що інгібують ЦОГ-1, та селективними інгібіторами ЦОГ-2 може мати клінічне значення у пацієнтів із групи ризику тромбоемболічних подій. Селективні інгібітори ЦОГ-2 пригнічують утворення системного (і, можливо, ендотеліального) простацикліну,не впливаючи на тромбоцитарний тромбоксан. Клінічна значимість цих спостережень встановлено. Додаткові дані з безпеки щодо ШКТ У двох 12-тижневих подвійних сліпих ендоскопічних дослідженнях кумулятивна частота розвитку гастродуоденальних виразок була значно нижчою у пацієнтів, які отримували церикоксиб у дозі 120 мг один раз на день, ніж у пацієнтів, які отримували напроксен 500 мг двічі на день. або ібупрофен 800 мг тричі на день. Частота розвитку виразок при призначенні церикоксибу була вищою порівняно з плацебо. Дослідження ниркової функції у пацієнтів похилого віку У рандомізованому подвійному сліпому плацебо-контрольованому дослідженні в паралельних групах оцінювався вплив 15-денної терапії церикоксибом (90 мг), целекоксибом (200 мг двічі на день), напроксеном (500 мг двічі на день) порівняно з плацебо на виведення натрію. , артеріальний тиск (АТ) та інші параметри функції нирок у пацієнтів віком від 60 до 85 років, які отримували раціон з обмеженим споживанням натрію до 200 мекв/день. Еторикоксиб, целекоксиб і напроксен мали подібний вплив на виведення натрію нирками через 2 тижні лікування. Всі активні препарати порівняння показали збільшення систолічного АТ порівняно з плацебо, однак, еторикоксиб викликав статистично значуще збільшення систолічного АТ на 14-й день порівняно з целекоксибом і напроксеном (середня зміна систолічного АТ порівняно з вихідним: етороксіб 7,7 мм рт. ст., целекоксиб 2,4 мм рт.ст., напроксен 3,6 мм рт.ст.).Показання до застосуванняСимптоматична терапія остеоартрозу, ревматоїдного артриту, анкілозуючого спондиліту, болю та запалення, пов'язаних із гострим подагричним артритом. Короткострокова терапія помірного гострого болю після стоматологічних операцій.Протипоказання до застосуванняПідвищена чутливість до еторикоксибу або будь-якої з допоміжних речовин препарату. Виразкова хвороба шлунка та 12-палої кишки у стадії загострення, активна шлунково-кишкова кровотеча. Бронхіальна астма, бронхоспазм, гострий риніт, поліпоз носа, ангіоневротичний набряк, кропив'янка або алергічні реакції після прийому ацетилсаліцилової кислоти або нестероїдних протизапальних препаратів (НПЗЗ), у тому числі інгібіторів ЦОГ-2, в анамнезі. Вагітність та період грудного вигодовування. Тяжкі порушення функції печінки (сироватковий альбумін 10 балів за шкалою Чайлд-П'ю). Тяжка ниркова недостатність (КК Діти та підлітки до 16 років. Запальні захворювання кишок. Хронічна серцева недостатність (II-IV функціональний клас за NYHA). Неконтрольована артеріальна гіпертензія (АТ стабільно вищий за 140/90 мм рт. ст.). Підтверджена ішемічна хвороба серця, захворювання периферичних артерій та/або цереброваскулярні захворювання. Дефіцит лактази, непереносимість лактози, глюкозо-галактозна мальабсорбція. Підтверджена гіперкаліємія. З обережністю: Пацієнти з підвищеним ризиком розвитку ускладнень з боку шлунково-кишкового тракту (виразкова ураження шлунково-кишкового тракту або шлунково-кишкова кровотеча в анамнезі, наявність інфекції Helicobacter Pylori, одночасне застосування інших нестероїдних протизапальних засобів, у тому числі ацетилсаліцилової кислоти, літній вік). Пацієнти, які мають в анамнезі фактори ризику серцево-судинних ускладнень (дисліпідемія/гіперліпідемія, цукровий діабет, артеріальна гіпертензія, куріння, серцева недостатність, порушення функції лівого шлуночка, набряки та затримка рідини в організмі). Печінкова недостатність (5-9 балів за класифікацією Чайлд-П'ю). Пацієнти з дегідратацією. Пацієнти з порушеннями функції нирок (КК Пацієнти з попереднім значним зниженням функції нирок, з ослабленою функцією нирок, декомпенсованою серцевою недостатністю або цирозом печінки, що перебувають у групі ризику при тривалому застосуванні нестероїдних протизапальних засобів. Супутня терапія антикоагулянтами (наприклад, варфарин), антиагрегантами (наприклад, ацетилсаліцилова кислота, клопідогрел), препаратами, що метаболізуються сульфотрансферазами.Вагітність та лактаціяВагітність В даний час клінічних даних про застосування еторикоксибу при вагітності відсутні. У дослідженнях на тваринах спостерігалася токсична дія на репродуктивну систему. Потенційний ризик для жінок під час вагітності невідомий. Застосування еторикоксибу, як і інших лікарських препаратів, що інгібують синтез простагландинів, у III триместрі вагітності може призводити до придушення скорочень матки та передчасного закриття артеріальної протоки. Еторикоксиб протипоказаний при вагітності. Якщо під час лікування настала вагітність, церикоксиб необхідно відмінити. Грудне годування У лактуючих щурів еторикоксиб виділяється з молоком. Досліджень, що підтверджують виділення еторикоксибу з грудним молоком у жінок, не проводилося. Жінки, які приймають еторикоксиб, повинні припинити грудне вигодовування. Фертильність Застосування еторикоксибу, як і інших препаратів, що інгібують ЦОГ-2 або синтез простагландинів, не рекомендується жінкам, які планують вагітність.Побічна діяРезюме профілю безпеки Безпека застосування церикоксибу оцінювалася у клінічних дослідженнях за участю 9295 пацієнтів, у тому числі 6757 пацієнтів з ОА, РА, хронічним болем у нижній частині спини та анкілозуючим спондилітом (приблизно 600 пацієнтів з ОА або РА отримували лікування протягом одного року або більше). Профіль небажаних реакцій був подібним у пацієнтів з ОА або РА, які отримували еторикоксиб протягом одного року або довше. У клінічному дослідженні гострого подагричного артриту пацієнти отримували церикоксиб у дозі 120 мг 1 раз на день протягом 8 днів. Профіль небажаних явищ у цьому дослідженні був загалом таким самим, як і в об'єднаних дослідженнях ОА, РА та хронічного болю в нижній частині спини. Для оцінки безпеки щодо серцево-судинної системи були об'єднані дані трьох активних контрольованих досліджень, у яких брали участь 17412 пацієнтів з ОА або РА, які отримували еторикоксиб у дозі 60 мг або 90 мг, середня тривалість досліджень склала приблизно 18 місяців. У клінічних дослідженнях гострого післяопераційного болю, пов'язаного з проведенням стоматологічної операції, у яких 614 пацієнтів отримували еторикоксиб у дозі 90 мг або 120 мг, профіль небажаних ефектів загалом був подібним до профілю в об'єднаних дослідженнях ОА, РА та хронічного болю в нижній частині спини. Табличне резюме небажаних реакцій У таблиці перераховані небажані реакції, які були зареєстровані з більшою частотою при застосуванні препарату, ніж у групі плацебо, у клінічних дослідженнях, що включали пацієнтів з ОА, РА, хронічним болем у нижній частині спини або анкілозуючим спондилітом (еторикоксиб призначався у дозі 30 мг, 60 мг або 90 мг з підвищенням дози до рекомендованої протягом 12 тижнів), у програмі MEDAL, де дослідження тривали до 3,5 років, у короткострокових дослідженнях гострого болю (протягом 7 днів), а також отримані під час постмаркетингового застосування. Класифікація систем органів Небажана реакція Частота 1 Інфекційні та паразитарні захворювання альвеолярний остит часто гастроентерит, інфекції верхніх дихальних шляхів, інфекції сечовивідних шляхів не часто Порушення з боку крові та лімфатичної системи анемія (в основному в результаті шлунково-кишкової кровотечі), лейкопенія, тромбоцитопенія не часто Порушення з боку імунної системи реакції гіперчутливості 2,4 не часто ангіоневротичний набряк, анафілактичні/анафілактоїдні реакції, у тому числі шок 2 рідко Порушення з боку обміну речовин та харчування набряки/затримка рідини часто посилення або зниження апетиту, збільшення маси тіла не часто Порушення психіки тривога, депресія, зниження ясності мислення, галюцинації 2 не часто сплутаність свідомості 2 , неспокій 2 рідко Порушення з боку нервової системи запаморочення, головний біль часто порушення смаку, безсоння, парестезія/гіпестезія, сонливість не часто Порушення з боку органу зору нечіткість зору, кон'юнктивіт не часто Порушення з боку органу слуху та лабіринтні порушення дзвін у вухах, вертиго не часто Порушення з боку серця відчуття серцебиття, аритмія 2 часто фібриляція передсердь, тахікардія 2 , хронічна серцева недостатність, неспецифічні зміни на ЕКГ, стенокардія 2 , інфаркт міокарда 5 не часто Порушення з боку судин артеріальна гіпертензія часто "припливи", порушення мозкового кровообігу 5 транзиторна ішемічна атака гіпертонічний криз 2 васкуліт 2 не часто Порушення з боку дихальної системи, органів грудної клітки та середостіння. бронхоспазм 2 часто кашель, задишка, носова кровотеча не часто Порушення з боку шлунково-кишкового тракту біль в животі дуже часто метеоризм, гастрит, печія/гастроезофагеальний рефлюкс, діарея, диспепсія/дискомфорт в епігастрії, нудота, блювання, езофагіт, виразка слизової оболонки порожнини рота часто здуття живота, зміна перистальтики, сухість слизової оболонки порожнини рота, виразка гастродуоденальної, виразкова хвороба шлунка, включаючи перфорації та кровотечі, панкреатит 2 , синдром подразненого кишечника не часто Порушення з боку печінки та жовчовивідних шляхів підвищення активності АЛТ та ACT часто гепатит 2 рідко печінкова недостатність 2 , жовтяниця 2 рідко 3 Порушення з боку шкіри та підшкірних тканин екхімоз часто набряклість особи, свербіж, висип, еритема 2 , кропив'янка 2 не часто синдром Стівенса-Джонсона 2 , токсичний епідермальний некроліз 2 , фіксована лікарська еритема 2 рідко 3 Порушення з боку скелетно-м'язової та сполучної тканини м'язові судоми/спазм, скелетно-м'язовий біль/скутість не часто Порушення з боку нирок та сечовивідних шляхів протеїнурія, підвищення концентрації креатиніну в сироватці, ниркова недостатність 2,3,4 не часто Загальні розлади та порушення у місці введення астенія/слабкість, грипоподібний синдром часто біль у грудній клітці не часто Лабораторні та інструментальні дані підвищення концентрації азоту сечовини крові, підвищення активності креатинфосфокінази, гіперкаліємія, підвищення концентрації сечової кислоти не часто гіпонатріємія рідко 1 Відповідно до частоти, що враховується у клінічних дослідженнях: дуже часто (≥1/10), часто (від ≥1/100 до 2 Ця небажана реакція була зареєстрована під час постмаркетингового спостереження. Частота оцінювалася на підставі найбільшої частоти, що спостерігається у клінічних дослідженнях з урахуванням показань та затвердженої дози. 3 Частотна категорія "рідко" була визначена відповідно до керівництва (версія 2, вересень 2009 р.) для Короткої характеристики лікарського препарату на підставі розрахункової верхньої межі 95 % довірчого інтервалу для 0 явищ, враховуючи кількість пацієнтів, які отримували еторикоксиб в аналізі даних III фази , об'єднаних залежно від дози та показання (n = 15470). 4 Гіперчутливість включає терміни "алергія", "лікарська алергія", "гіперчутливість до лікарського препарату", "гіперчутливість", "гіперчутливість неуточнена", "реакція гіперчутливості" та "неспецифічна алергія". 5 За результатами даних аналізу довгострокових плацебо- та активноконтрольованих клінічних досліджень при застосуванні селективних інгібіторів ЦОГ-2 підвищується ризик розвитку серйозних артеріальних тромботичних явищ, включаючи ІМ та інсульт. З наявних даних, малоймовірно, що абсолютний ризик розвитку цих явищ перевищує 1 % на рік (нечасто). Наступні серйозні небажані явища були зареєстровані у зв'язку з прийомом НГТВП і не можуть бути виключені для еторикоксибу: нефротоксичність, включаючи інтерстиціальний нефрит та нефротичний синдром.Взаємодія з лікарськими засобамиФармакодинамічні взаємодії Пероральні антикоагулянти (варфарин). У пацієнтів, які постійно приймають варфарин, прийом еторикоксибу в дозі 120 мг на день супроводжувався збільшенням міжнародного нормалізованого відношення (МНО)/протромбінового часу приблизно на 13%. Тому у пацієнтів, які отримують пероральні антикоагулянти, слід контролювати МНО/протромбіновий час на початку лікування або при зміні дози еторикоксибу, особливо в перші кілька днів. Діуретики, інгібітори ангіотензинперетворюючого ферменту (АПФ) та антагоністи рецепторів ангіотензину II. Нестероїдні протизапальні засоби можуть послаблювати ефект діуретиків та інших антигіпертензивних лікарських препаратів. У деяких пацієнтів з порушенням функції нирок (наприклад, у пацієнтів з зневодненням або у літніх пацієнтів з порушеною функцією нирок) одночасне застосування інгібітору АПФ або антагоніста рецепторів ангіотензину II та препаратів, що інгібують ЦОГ, може призводити до додаткового погіршення функції нирок, включаючи можливий розвиток. ниркової недостатності, яка зазвичай має оборотний характер. Це слід враховувати у пацієнтів, які приймають одночасно церикоксиб з інгібіторами АПФ або антагоністами рецепторів ангіотензину ІІ. Такі комбінації слід призначати з обережністю, особливо пацієнтам похилого віку.Пацієнти повинні бути належним чином гідратовані, при цьому необхідно проводити моніторинг функції нирок на початку комбінованої терапії та періодично надалі. Ацетилсаліцилова кислота. У дослідженні у здорових добровольців церикоксиб у дозі 120 мг 1 раз на день у рівноважному стані не впливав на антитромбоцитарну активність ацетилсаліцилової кислоти (81 мг 1 раз на день). Еторикоксиб можна одночасно застосовувати з ацетилсаліциловою кислотою в низьких дозах, призначених для профілактики серцево-судинних захворювань. Тим не менш, одночасне застосування низьких доз ацетилсаліцилової кислоти та еторикоксибу може призвести до збільшення частоти виразкового ураження шлунково-кишкового тракту або інших ускладнень у порівнянні з прийомом тільки церикоксиксу. Одночасне застосування церикоксибу з ацетилсаліциловою кислотою в дозах, що перевищують рекомендовані для профілактики серцево-судинних ускладнень, а також з іншими нестероїдними протизапальними засобами не рекомендується. Циклоспорин та такролімус. Взаємодія церикоксибу з цими препаратами не вивчалася, однак, одночасне застосування циклоспорину або такролімусу з будь-яким нестероїдними протизапальними засобами може посилювати нефротоксичний ефект циклоспорину або такролімусу. При прийомі эторикоксиба у комбінації з будь-яким із цих препаратів слід контролювати функцію нирок. Фармакокінетичні взаємодії Вплив інших лікарських препаратів на фармакокінетику еторикоксибу Основний шлях метаболізму церикоксибу залежить від ферментів системи CYP. Ізофермент CYP3A4 сприяє метаболізму церикоксибу in vivo. Дослідження in vitro показують, що ізоферменти CYP2D6, CYP2C9, CYP1A2 і CYP2C19 можуть каталізувати основний шлях метаболізму, але їх кількісні характеристики in vivo не вивчені. Кетоконазол. Кетоконазол, потужний інгібітор ізоферменту CYP3A4, при прийомі здоровими добровольцями в дозі 400 мг один раз на день протягом 11 днів не надавав клінічно значущого впливу на фармакокінетику одноразової дози церикоксиксу 60 мг (збільшення AUC на 43%). Вориконазол та міконазол. Одночасне призначення сильних інгібіторів ізоферменту CYP3A4 (вориконазол для прийому всередину або міконазол місцево, у вигляді гелю для прийому всередину) та еторикоксибу викликало невелике збільшення експозиції церикоксибу, яке не визнано клінічно значущим на підставі опублікованих даних. ріфампіцин. Одночасне застосування церикоксибу та рифампіцину (потужного індуктора системи цитохромів) призводило до зниження концентрації церикоксибу в плазмі на 65 %. Така взаємодія може призвести до рецидиву симптомів при одночасному призначенні еторикоксибу з рифампіцином. Ця інформація дозволяє припустити необхідність збільшення дози, проте застосовувати еторикоксиб у дозах, що перевищують рекомендовані для кожного показання, не рекомендується, оскільки комбіноване застосування рифампіцину та еторикоксибу в таких дозах не вивчалося. Антациди. Антациди не надають клінічно значущої дії на фармакокінетику еторикоксибу. Вплив еторикоксибу на інші лікарські препарати Літій. НПЗЗ зменшують виведення літію нирками, отже, збільшують концентрацію літію у плазмі крові. При необхідності проводять частий контроль концентрації літію в крові та коригують дозу літію під час одночасного прийому з нестероїдними протизапальними засобами, а також при відміні нестероїдних протизапальних засобів. Метотрексат. У двох дослідженнях вивчалися ефекти еторикоксибу в дозах 60, 90 або 120 мг 1 раз на день протягом семи днів у пацієнтів, які отримували 1 раз на тиждень метотрексат у дозі від 7,5 до 20 мг на лікування РА. Еторикоксиб у дозах 60 та 90 мг не впливав на концентрацію метотрексату в плазмі та нирковий кліренс метотрексату. В одному дослідженні церикоксиб у дозі 120 мг не фармакокінетично впливав на метотрексат, але в іншому дослідженні концентрація метотрексату в плазмі підвищувалася на 28 %, а нирковий кліренс метотрексату знижувався на 13 %. При одночасному прийомі церикоксибу та метотрексату рекомендується вести спостереження щодо можливої появи токсичних ефектів метотрексату. Пероральні контрацептиви. Еторикоксиб у дозі 60 мг при одночасному прийомі протягом 21 дня з пероральними контрацептивами, що містять 35 мкг етинілестрадіолу (ЕЕ) та від 0,5 мг до 1 мг норетиндрону, збільшував AUC0-24 год ЕЕ на 37 % у рівноважному стані. Прийом церикоксиксу в дозі 120 мг у поєднанні з вищевказаними пероральними контрацептивами (одночасно або з інтервалом 12 годин) збільшував AUC0-24год. ЕЕ на 50-60% у рівноважному стані. Це збільшення концентрації ЕЕ слід враховувати при виборі перорального контрацептиву для одночасного застосування з церикоксибом. Подібна взаємодія може спричинити збільшення частоти розвитку небажаних явищ, пов'язаних із застосуванням пероральних контрацептивів (наприклад, венозних тромбоемболій у жінок із групи ризику). Замісна гормональна терапія (ЗГТ). Призначення еторікоксибу в дозі 120 мг одночасно з препаратами для ЗГТ, що містять кон'юговані естрогени в дозі 0,625 мг протягом 28 днів, збільшує середнє рівноважне значення AUC0-24 год некон'югованого естрону (41 %), еквіліну (76 %) та 17-2 %). Вплив доз еторикоксибу, рекомендованих для тривалого застосування (30, 60 та 90 мг), не вивчався. Еторикоксиб у дозі 120 мг змінював експозицію (AUC0-24год) даних естрогенних компонентів менш ніж удвічі порівняно з монотерапією кон'югованими естрогенами при збільшенні дози з 0,625 до 1,25 мг. Клінічне значення таких збільшення невідомо, застосування більш високих доз кон'югованих естрогенів у поєднанні з еторикоксибом не вивчалося.Підвищення концентрації естрогенів слід брати до уваги при виборі гормональної терапії в період постменопаузи при одночасному призначенні з етороксібом, оскільки збільшення експозиції естрогенів може підвищувати ризик розвитку небажаних явищ, пов'язаних із ЗГТ. Преднізон/Преднізолон. У дослідженнях лікарських взаємодій эторикоксиб не впливав на клінічно значущий вплив на фармакокінетику преднізону/преднізолону. Дігоксин. При застосуванні эторикоксибу в дозі 120 мг один раз на день протягом 10 днів у здорових добровольців не спостерігалося зміни рівноважної AUC0-24год дигоксину в плазмі або впливу на його виведення нирками. При цьому спостерігалося збільшення Стах дигоксину приблизно на 33%. Таке підвищення, як правило, не є важливим для більшості пацієнтів. Тим не менш, при одночасному застосуванні церикоксибу та дигоксину слід спостерігати за станом пацієнтів із високим ризиком прояву токсичної дії дигоксину. Вплив еторикоксибу на препарати, що метаболізуються сульфотрансферазами. Еторикоксиб є інгібітором сульфотрансферази людини (зокрема, SULT1E1) і може підвищувати концентрацію ЕЕ у сироватці крові. У зв'язку з тим, що в даний час отримано недостатньо даних про ефекти різних сульфотрансфераз, а їхня клінічна значущість для застосування багатьох лікарських препаратів ще вивчається, доцільно з обережністю призначати церикоксиб одночасно з іншими лікарськими препаратами, що метаболізуються сульфотрансферазами людини (наприклад, пероральний сальбутамол і ). Вплив етерокіксібу на препарати, що метаболізуються ізоферментами системи цитохромів. Грунтуючись на результатах досліджень in vitro, не очікується, що эторикоксиб інгібуватиме ізоферменти цитохрому Р450 (CYP) 1А2, 2С9, 2С19, 2D6, 2Е1 або 3А4. У дослідженні у здорових добровольців щоденне застосування церикоксибу в дозі 120 мг не впливало на активність ізоферменту CYP3A4 печінки при оцінці за допомогою еритроміцинового дихального тесту.Спосіб застосування та дозиВсередину, незалежно від їди, запиваючи невеликою кількістю води. Дія препарату реалізується швидше при прийомі натще. Внаслідок можливого підвищення ризику серцево-судинних ускладнень слід використовувати мінімальну ефективну дозу мінімально можливим курсом. Остеоартроз: рекомендована доза етерокіксібу становить 30 мг 1 раз на день. У разі недостатнього ефекту добова доза препарату може бути збільшена до 60 мг на добу. Добова доза при остеоартрозі не повинна перевищувати 60 мг. Ревматоїдний артрит та анкілозуючий спондиліт: рекомендована доза еторикоксібу становить 60 мг 1 раз на день. У пацієнтів із недостатнім клінічним ефектом можливе збільшення добової дози препарату до 90 мг один раз на день. Після клінічної стабілізації захворювання можливе зниження дози до 60 мг один раз на день. У разі відсутності ознак клінічного покращення слід розглянути можливість застосування інших методів лікування. Добова доза не повинна перевищувати 90 мг. Гострий подагричний артрит: рекомендована доза церикоксибу в гострому періоді становить 120 мг 1 раз на день. Тривалість застосування препарату у дозі 120 мг не перевищує 8 днів. Добова доза не повинна перевищувати 120 мг. Гострий біль після стоматологічних операцій: рекомендована доза еторикоксибу становить 90 мг 1 раз на день. Еторикоксиб слід застосовувати лише у гострий симптоматичний період тривалістю не більше 3 днів. Добова доза для усунення болю після стоматологічних операцій не повинна перевищувати 90 мг. Деяким пацієнтам можуть знадобитися додаткові засоби для забезпечення адекватного рівня знеболювання у післяопераційному періоді протягом триденного періоду терапії церикоксибом. Особливі групи пацієнтів Літні пацієнти: корекція дози не потрібна. Як і при застосуванні інших препаратів, еторикоксиб слід застосовувати з обережністю. Діти: застосування еторикоксибу у пацієнтів віком до 16 років протипоказано. Порушення функції печінки: незалежно від показання до застосування пацієнтам з порушеннями функції печінки легкого ступеня тяжкості (5-6 балів за шкалою Чайлд-П'ю) не слід перевищувати дозу 60 мг 1 раз на день, пацієнтам з порушеннями функції печінки середнього ступеня тяжкості (7 -9 балів за шкалою Чайлд-Пью) – 30 мг 1 раз на день. Рекомендується бути обережним при застосуванні препарату у пацієнтів з порушеннями функції печінки середнього ступеня тяжкості, оскільки клінічний досвід застосування препарату у даної групи пацієнтів обмежений. У зв'язку з відсутністю клінічного досвіду застосування препарату у пацієнтів з тяжкими порушеннями функції печінки (≥10 балів за шкалою Чайлд-П'ю) препарат протипоказаний для цієї групи пацієнтів. Порушення функції нирок: не потрібна корекція дози препарату при застосуванні у пацієнтів із КК ≥30 мл/хв. Застосування препарату у пацієнтів із ККПередозуванняУ клінічних дослідженнях прийом еторикоксибу в разовій дозі до 500 мг і багаторазовий прийом до 150 мг/день протягом 21 дня не викликав суттєвих токсичних ефектів. Були отримані повідомлення про гостре передозування еторикоксибом, однак, у більшості випадків про небажані реакції не повідомлялося. Найчастіші небажані реакції відповідали профілю безпеки церикоксибу (наприклад, порушення з боку шлунково-кишкового тракту, кардіоренальні явища). У разі передозування доцільно вживати звичайні підтримувальні заходи, такі як видалення невсмоктаного препарату із ШКТ, клінічне спостереження і, при необхідності, підтримуюча терапія. Еторікоксиб не виводиться при гемодіалізі; виведення еторикоксибу при перитонеальному діалізі не вивчалося.Запобіжні заходи та особливі вказівкиВплив на ШКТ У пацієнтів, які отримували еторикоксиб, спостерігалися ускладнення з боку верхніх відділів шлунково-кишкового тракту (перфорації, виразки або кровотечі), іноді з летальним кінцем. Рекомендується бути обережним при лікуванні пацієнтів з високим ризиком розвитку ускладнень з боку шлунково-кишкового тракту при застосуванні нестероїдних протизапальних засобів, зокрема, у літніх пацієнтів, що одночасно застосовують інші нестероїдні протизапальні засоби, ацетилсаліцилову кислоту або у пацієнтів із захворюваннями шлунково-кишкового тракту в анамнезі, такими як виразка та шлунково-кишкова кровотеча. Існує додатковий ризик розвитку небажаних реакцій з боку шлунково-кишкового тракту (шлунково-кишкові виразки або інші ускладнення з боку шлунково-кишкового тракту) при одночасному застосуванні церикоксибу та ацетилсаліцилової кислоти (навіть у низьких дозах). У довгострокових клінічних дослідженнях не спостерігалося достовірних відмінностей щодо безпеки для ШКТ при застосуванні селективних інгібіторів ЦОГ-2 у комбінації з ацетилсаліциловою кислотою порівняно із застосуванням нестероїдних протизапальних засобів у комбінації з ацетилсаліциловою кислотою. Вплив на серцево-судинну систему Результати клінічних досліджень свідчать про те, що застосування лікарських препаратів класу селективних інгібіторів ЦОГ-2 пов'язано з підвищеним ризиком тромбоутворення (особливо інфаркту міокарда (ІМ) та інсульту) порівняно з плацебо та деякими НПЗЗ. Ризик розвитку серцево-судинних ускладнень при застосуванні селективних інгібіторів ЦОГ-2 може зростати зі збільшенням дози та тривалості лікування, тому слід застосовувати церикоксиб протягом максимально короткого періоду часу та у найнижчій ефективній добовій дозі. Необхідно періодично оцінювати потребу пацієнта у симптоматичному лікуванні та відповідь на терапію, особливо у пацієнтів з ОА. Пацієнтам з відомими факторами ризику розвитку серцево-судинних ускладнень (наприклад, артеріальна гіпертензія, гіперліпідемія, цукровий діабет, куріння) церикоксиб необхідно призначати тільки після ретельної попередньої оцінки співвідношення користі-ризику. Селективні інгібітори ЦОГ-2 не є заміною ацетилсаліцилової кислоти при профілактиці серцево-судинних захворювань через відсутність антитромбоцитарного ефекту, тому не слід припиняти застосування антиагрегантних препаратів. Вплив на функцію нирок Ниркові простагландини можуть відігравати компенсаторну роль у підтримці ниркової перфузії. Тому за наявності умов, що негативно впливають на ниркову перфузію, призначення еторикоксибу може призвести до зменшення утворення простагландинів і, як наслідок, зниження ниркового кровотоку, і тим самим призвести до погіршення функції нирок. Найбільший ризик розвитку цієї реакції виникає у пацієнтів із значним зниженням функції нирок, некомпенсованою серцевою недостатністю або цирозом печінки в анамнезі. У таких пацієнтів необхідно проводити моніторинг функції нирок. Затримка рідини, набряки та артеріальна гіпертензія Як і у разі застосування інших препаратів, що інгібують синтез простагландинів, у пацієнтів, які приймають еторикоксиб, спостерігалися затримка рідини, набряки та артеріальна гіпертензія. Застосування будь-яких нестероїдних протизапальних засобів, включаючи церикоксикс, може бути пов'язане з виникненням або рецидивом хронічної (застійної) серцевої недостатності. Інформація про дозозалежну реакцію для церикоксибу наведена в розділі "Фармакологічні властивості". Слід виявляти обережність при призначенні церикоксибу пацієнтам із серцевою недостатністю в анамнезі, дисфункцією лівого шлуночка, артеріальною гіпертензією та пацієнтам з уже наявними набряками, що виникли з будь-якої іншої причини. При появі клінічних ознак погіршення стану у таких пацієнтів слід вжити відповідних заходів, включаючи скасування еторікоксибу. Застосування еторикоксибу, особливо у високих дозах, може бути пов'язане з розвитком більш тяжкої артеріальної гіпертензії, ніж при застосуванні деяких інших нестероїдних протизапальних засобів та селективних інгібіторів ЦОГ-2. Тому під час лікування церикоксибом слід звернути особливу увагу на моніторинг АТ, який має контролюватись протягом двох тижнів після початку лікування та періодично надалі. При значному підвищенні артеріального тиску слід розглянути альтернативне лікування. Вплив на функцію печінки Підвищення активності аланінамінотрансферази (АЛТ) та/або аспартатамінотрансферази (ACT) (приблизно в три або більше рази щодо верхньої межі норми) було зареєстровано у клінічних дослідженнях приблизно у 1% пацієнтів, які отримували еторикоксиб протягом терміну до одного року у дозах 30 мг, 60 мг та 90 мг на день. Необхідно спостерігати за станом усіх пацієнтів із симптомами та/або ознаками дисфункції печінки, а також пацієнтів із зміненими лабораторними показниками функції печінки. Якщо виникають ознаки печінкової недостатності або показники функції печінки значно відхиляються від норми (втричі вище за верхню межу норми), прийом еторикоксибу повинен бути припинений. Загальні рекомендації Якщо під час лікування у пацієнтів погіршується будь-яка з функцій органів або систем органів, описаних вище, повинні бути вжиті відповідні заходи та розглянуто питання про скасування еторикоксибу. При застосуванні эторикоксибу у пацієнтів похилого віку та у пацієнтів з порушенням функції нирок, печінки або серця необхідне відповідне медичне спостереження. З обережністю слід розпочинати лікування ерикоксибом пацієнтам із зневодненням. Перед початком терапії церикоксибом рекомендується провести регідратацію. У період постмаркетингового спостереження при застосуванні НПЗП та деяких селективних інгібіторів ЦОГ-2 дуже рідко повідомлялося про розвиток серйозних реакцій шкіри. Деякі з них, у тому числі ексфоліативний дерматит, синдром Стівенса-Джонсона та токсичний епідермальний некроліз, були з смертю. Ризик розвитку цих реакцій найбільш високий на початку курсу терапії, здебільшого протягом першого місяця лікування. Повідомлялося про розвиток серйозних реакцій гіперчутливості, таких як анафілаксія та ангіоневротичний набряк, у пацієнтів, які отримували еторикоксиб. Застосування деяких селективних інгібіторів ЦОГ-2 супроводжувалося підвищеним ризиком розвитку шкірних реакцій у пацієнтів із якоюсь лікарською алергією в анамнезі. Еторикоксиб повинен бути скасований при першій появі висипу на шкірі,уражень слизової оболонки або будь-якої іншої ознаки гіперчутливості. Застосування еторикоксибу може маскувати лихоманку та інші ознаки запалення. Застосування еторикоксибу, як і інших препаратів, що інгібують ЦОГ та синтез простагландинів, не рекомендується жінкам, які планують вагітність (див. розділ "Застосування при вагітності та в період грудного вигодовування"). Оболонка таблетки містить лактозу. Пацієнтам з такими рідкісними вродженими захворюваннями, як непереносимість лактози, дефіцит лактази або глюкозогалактозна мальабсорбція, не слід приймати цей препарат. Вплив на здатність до керування автотранспортом та управління механізмами Пацієнтам, у яких на фоні застосування церикоксибу відзначаються епізоди запаморочення, сонливості чи слабкості, слід утриматися від керування транспортними засобами та роботи з механізмами.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаЕліксир - 1 л: Активні речовини: насіння сосни кедрової сибірської 54 г; плоди глоду 4 г; плоди аронії чорноплідної 2 г; бруньки берези 1.5 г; кореневища з корінням елеутерококу 1 г; квітки глоду звичайного 0.5 г; Допоміжні речовини: мед натуральний – 50 г, сахароза – 22.7 г, етанол 95% – 421 г, вода очищена – до 1000 мл. 250 мл - пляшки скляні (1) - пачки картонні.Опис лікарської формиЕліксир у вигляді рідини коричневого кольору зі специфічним запахом; у процесі зберігання допускається випадання осаду.Фармакотерапевтична групаМає загальнозміцнюючу дію, збільшує фізичну працездатність, сприяє регуляції метаболічних процесів в організмі.ФармакокінетикаПрепарат являє собою водно-спиртовий екстракт із суміші рослинної лікарської сировини і містить комплекс біологічно активних речовин, у зв'язку з чим проведення фармакокінетичних досліджень не є можливим.Клінічна фармакологіяФітопрепарат із загальнозміцнюючою дією.Показання до застосуванняДля лікування астено-вегетативного синдрому різної етіології, у період відновлення після перенесених захворювань, що протікають із ураженням паренхіматозних органів.Протипоказання до застосуванняпідвищена чутливість до компонентів препарату, у тому числі до меду та продуктів бджільництва; гостра серцево-судинна та гостра ниркова недостатність; тяжкі захворювання печінки; алкоголізм; черепно-мозкова травма; захворювання головного мозку; дефіцит сахарази/ізомальтази; непереносимість фруктози; глюкозо-галактозна мальабсорбція; вік до 18 років.Вагітність та лактаціяЗастосування препарату при вагітності та в період грудного вигодовування протипоказане. Протипоказано дітям віком до 18 років.Побічна діяМожливі алергічні реакції. Якщо на фоні застосування препарату Ваш стан погіршився, і Ви помітили будь-які побічні ефекти, не зазначені в даній інструкції, зверніться до лікаря.Взаємодія з лікарськими засобамиПри одночасному застосуванні з нікотиновою кислотою, гіполіпідемічними засобами (інгібіторами абсорбції холестерину, фібратами) можливе посилення гіполіпідемічної дії. Якщо Ви приймаєте інші лікарські засоби, перед прийомом препарату обов'язково проконсультуйтеся з лікарем.Спосіб застосування та дозиВсередину по 2-3 чайні ложки (10-15 мл), розведені у 100 мл води. 2 десь у день 10-15 хвилин до їжі. Курс лікування 5-7 днів. При необхідності курс лікування може бути збільшений до 2-3 тижнів після консультації з лікарем. Перед вживанням збовтувати.ПередозуванняПри застосуванні препарату в дозах, що перевищують рекомендовані, можливі біль голови, нудота, блювання. Лікування симптоматичне.Запобіжні заходи та особливі вказівкиУ складі препарату міститься сахароза, що слід враховувати хворим на цукровий діабет. Максимальна разова доза препарату містить 0.34 г сахарози (відповідає 0.3 ХЕ (хлібних одиниць)), добова – 0,68 г (відповідає 0.68 ХЕ). Препарат містить щонайменше 37% етилового спирту. Максимальна разова доза містить 5.9 г абсолютного етилового спирту, максимальна добова доза препарату містить 11,97 г абсолютного етилового спирту. Вплив на здатність керувати транспортними засобами та працювати з механізмами Зважаючи на наявність у складі препарату спирту етилового слід утриматися від потенційно небезпечних видів діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій (управління транспортними засобами, робота з механізмами, що рухаються, робота диспетчера, оператора тощо).Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Активні речовини: еторикоксиб – 90 мг; Допоміжні речовини: кальцію безводний гідрофосфат - 39 мг, целюлоза мікрокристалічна - 38.25 мг, повідон К30 - 9 мг, магнію стеарат - 1.5 мг, кроскармеллоза натрію - 2.25 мг; Склад оболонки таблетки: Опадрай II білий 32К580000С – 6 мг: гіпромелоза 15 cPs 2.4 мг, лактози моногідрат 1.68 мг, титану діоксид 1.44 мг, тріацетин 0.48 мг. Таблетки, покриті плівковою оболонкою, 30 мг, 60 мг, 90 мг та 120 мг. По 7 пігулок в Аl/Аl блістер. По 1 блістеру разом з інструкцією із застосування в картонну пачку. По 10 пігулок в Аl/Аl блістер. По 1, 2, 3, 5, 6, 9, 10 блістерів разом з інструкцією із застосування в картонну пачку. По 14 пігулок в Аl/Аl блістер. По 1,2, 4, 6, 7 блістерів разом із інструкцією із застосування в картонну пачку.Опис лікарської формиТаблетки, покриті плівковою оболонкою білого кольору, круглі, двоопуклі.Фармакотерапевтична групаНестероїдні протизапальні препарати (НПЗЗ).ФармакокінетикаВсмоктування Эторикоксиб швидко всмоктується прийому внутрішньо. Абсолютна біодоступність прийому внутрішньо становить близько 100%. При застосуванні препарату у дорослих натще в дозі 120 мг один раз на день до досягнення рівноважного стану максимальна концентрація в плазмі (Сmах) становить 3,6 мкг/мл. Час досягнення Сmах (Тmах) становить приблизно 1 годину після прийому препарату. Середня геометрична площа під кривою "концентрація – час" (AUC0-24ч) склала 37,8 мкг * год / мл. Фармакокінетика эторикоксиба в діапазоні терапевтичних доз має лінійний характер. При прийомі эторикоксиба в дозі 120 мг під час їжі (їжа з високим вмістом жирів) не спостерігалося клінічно значущого впливу на ступінь абсорбції. Швидкість абсорбції при цьому змінювалася, що призводило до зниження Сmах на 36% і збільшення Тmах на 2 год. Ці дані не є клінічно значущими. У клінічних дослідженнях церикоксиб застосовувався незалежно від їди. Розподіл Еторікоксиб приблизно на 92% зв'язується з білками плазми у людини в діапазоні концентрацій від 0,05 до 5 мкг/мл. Об'єм розподілу у рівноважному стані (VdSS) становить близько 120 л. Еторикоксиб проникає через плацентарний бар'єр у щурів та кролів та гематоенцефалічний бар'єр у щурів. Метаболізм Еторикоксиб екстенсивно метаболізується, У людини виявлено п'ять метаболітів церикоксиксу. Основним метаболітом є 6'-карбоксиацетилеторикоксиб, що утворюється в результаті подальшого окислення 6'-гідроксиметилеторикоксибу. Ці основні метаболіти не мають помітної активності або слабо інгібують ЦОГ-2. Жоден із цих метаболітів не інгібує ЦОГ-1. Виведення Після одноразового внутрішньовенного введення здоровим добровольцям міченого радіоактивного церикоксибу в дозі 25 мг 70 % церикоксибу виводилося через нирки та 20 % – через кишечник, переважно у вигляді метаболітів. Менше 2% виявлялося у незміненому вигляді. Виведення еторикоксибу відбувається в основному шляхом метаболізму в печінці з подальшим виведенням нирками. Рівноважні концентрації эторикоксиба досягаються при щоденному прийомі в дозі 120 мг протягом 7 днів з коефіцієнтом кумуляції близько 2, що відповідає періоду напіввиведення близько 22 год. Плазмовий кліренс після внутрішньовенного введення 25 мг становить приблизно 50 мл/хв. Особливі групи пацієнтів Стать: фармакокінетичні параметри препарату у чоловіків та жінок не відрізняються. Літні пацієнти: фармакокінетика препарату у пацієнтів віком понад 65 років порівнянна з фармакокінетикою у пацієнтів молодшого віку. Діти: фармакокінетика еторикоксибу у дітей (60 кг, які приймали церикоксиб у дозі 90 мг 1 раз на день), була аналогічна фармакокінетиці у дорослих, які приймали церикоксиб у дозі 90 мг 1 раз на день. Безпека та ефективність застосування церикоксибу у дітей не встановлена. Печінкова недостатність: у пацієнтів з печінковою недостатністю легкого ступеня тяжкості (5-6 балів за шкалою Чайлд-П'ю) прийом еторикоксибу в дозі 60 мг 1 раз на день супроводжувався збільшенням показника AUC приблизно на 16% порівняно зі здоровими добровольцями, які приймали препарат у тій ж дозі. У пацієнтів з печінковою недостатністю середнього ступеня тяжкості (7-9 балів за шкалою Чайлд-П'ю), які отримували еторикоксиб у дозі 60 мг один раз на день через день, середнє значення AUC було таким же, як у здорових добровольців, які приймали еторикоксиб у дозі 60 мг раз на день щодня. Застосування еторикоксибу в дозі 30 мг один раз на день не вивчалося у цій групі пацієнтів. Клінічні та фармакокінетичні дані досліджень у пацієнтів з тяжкою печінковою недостатністю (>10 балів за шкалою Чайлд-П'ю) відсутні. Ниркова недостатність: фармакокінетичні показники одноразового застосування церикоксибу в дозі 120 мг у пацієнтів з нирковою недостатністю помірного та тяжкого ступеня та у пацієнтів з термінальною стадією хронічної ниркової недостатності, які перебувають на гемодіалізі, суттєво не відрізняються від показників у здорових добровольців. Гемодіаліз незначно впливає на виведення препарату (кліренс при діалізі – близько 50 мл/хв).ФармакодинамікаЕторикоксиб при пероральному прийомі в терапевтичних концентраціях є селективним інгібітором циклооксигенази типу 2 (ЦОГ-2). У дослідженнях з клінічної фармакології церикоксиб дозозалежно інгібував ЦОГ-2, не впливаючи на ЦОГ-1 при застосуванні доз до 150 мг на день. Еторикоксиб не пригнічував синтез простагландинів у слизовій оболонці шлунка і не впливав на функцію тромбоцитів. ЦОГ відповідає за синтез простагландинів. Виділено дві ізоформи цього ферменту - ЦОГ-1 та ЦОГ-2. ЦОГ-2 є ізоферментом, який індукується під дією прозапальних медіаторів і розглядається як основний фермент, який відповідає за синтез простаноїдних медіаторів болю, запалення та лихоманки. ЦОГ-2 бере участь у процесах овуляції, імплантації та закриття артеріальної протоки, регуляції функції нирок, центральної нервової системи (індукція лихоманки, відчуття болю, когнітивна функція), а також може грати певну роль у процесі загоєння виразок. ЦОГ-2 була виявлена у тканинах, що оточують виразки шлунка у людини, але її значення для загоєння виразки не встановлено. Ефективність У пацієнтів з остеоартрозом (ОА) церикоксиб при застосуванні в дозі 60 мг один раз на день викликав достовірне зменшення болю та покращення оцінки свого стану пацієнтами. Ці сприятливі ефекти спостерігалися вже другого дня лікування і зберігалися протягом 52 тижнів. Дослідження еторикоксибу в дозі 30 мг один раз на день (із застосуванням подібних методів оцінки) продемонстрували ефективність препарату порівняно з плацебо протягом усього періоду лікування (12 тижнів). У дослідженні, яке проводилося з метою визначення оптимальної дози, еторикоксиб у дозі 60 мг продемонстрував достовірно більш виражене поліпшення, ніж у дозі 30 мг для всіх 3 первинних кінцевих точок через 6 тижнів лікування. Застосування дози 30 мг на лікування ОА суглобів кистей рук не вивчалося. У пацієнтів з ревматоїдним артритом (РА) прийом еторикоксибу в дозі 60 мг або 90 мг один раз на день забезпечував достовірне зменшення болю, запалення та покращення рухливості. Ці сприятливі ефекти зберігалися протягом 12-тижневого періоду лікування. Дослідження порівняння застосування церикоксибу в дозі 60 мг і 90 мг один раз на день для лікування РА показало, що обидва режими дозування забезпечували переважну ефективність терапії порівняно з плацебо. Доза церикоксибу 90 мг один раз на день перевищувала за ефективністю дозу 60 мг один раз на день при оцінці ефекту за допомогою Глобальної Шкали. % довірчий інтервал (ДІ): -4,98 мм; -0,45 мм). У пацієнтів із гострим подагричним артритом еторикоксиб у дозі 120 мг один раз на день протягом усього періоду лікування (8 днів) зменшував помірний та сильний біль у суглобах та запалення порівняно з індометацином у дозі 50 мг 3 рази на день. Зменшення болю відзначалося вже через 4 години після початку лікування. У пацієнтів з анкілозуючим спондилітом еторикоксиб при застосуванні в дозі 90 мг один раз на день забезпечував достовірне зменшення болю в спині, запалення, скутості, а також покращення рухової функції. Клінічна ефективність эторикоксиба спостерігалася вже другого дня лікування та зберігалася протягом усього періоду лікування (52 тижні). В іншому дослідженні, в рамках якого порівнювалася ефективність застосування церикоксибу в дозі 90 мг один раз на день та 60 мг один раз на день, цей препарат продемонстрував рівну ефективність порівняно з напроксеном у дозі 1000 мг один раз на день. Серед пацієнтів, у яких не було досягнуто адекватної клінічної відповіді на терапію протягом 6 тижнів при застосуванні церикоксибу у дозі 60 мг один раз на день, збільшення добової дози до 90 мг дозволяло покращити результати лікування, оцінені за допомогою шкали інтенсивності болю у спині. -100 мм візуально-аналогова шкала), порівняно з продовженням терапії еторікоксибом у дозі 60 мг один раз на день. Середнє поліпшення склало -2,70 мм (95% ДІ: 4,88 мм; -0,52 мм). У клінічному дослідженні з вивчення болю після стоматологічних операцій эторикоксиб у дозі 90 мг призначали раз на день протягом трьох днів. У підгрупі пацієнтів з помірним болем (при вихідній оцінці) еторикоксиб у дозі 90 мг продемонстрував знеболюючий ефект, аналогічний ібупрофену в дозі 600 мг (16,11 порівняно з 16,39, Р = 0,722) та більший, ніж при застосуванні комбінації парацетамол/ кодеїн у дозі 600 мг/60 мг (11,00; Р Безпека Програма MEDAL (Багатонаціональна Програма Оцінки Довгострокового Призначення Еторікоксибу та Диклофенаку при Артріті) Програма MEDAL була проспективною програмою оцінки безпеки на підставі серцево-судинних явищ за об'єднаними даними трьох рандомізованих подвійних сліпих активно-контрольованих досліджень: MEDAL, EDGE II та EDGE. Дослідження MEDAL являло собою дослідження, тривалість якого визначалася досягненням кінцевих точок (серцево-судинних явищ), воно включало 17804 пацієнта з ОА та 5700 пацієнтів з РА, які отримували еторикоксиб у дозі 60 мг (ОА) або 90 мг (ОА та РА) або ді у дозі 150 мг на день у середньому протягом 20,3 місяців (максимум 42,3 місяці, медіана 21,3 місяці). У цьому дослідженні реєстрували лише серйозні небажані явища та випадки вибуття з дослідження внаслідок будь-якого небажаного явища. У дослідженнях EDGE та EDGE II порівнювали безпеку прийому церикоксибу та диклофенаку для шлунково-кишкового тракту (ЖКТ). До дослідження EDGE було включено 7111 пацієнтів з ОА, які отримували еторикоксиб у дозі 90 мг на день (в 1,5 рази більше за дозу, рекомендовану при ОА) або диклофенак у дозі 150 мг на день протягом у середньому 9,1 місяців (максимум 16 , 6 місяців, медіана 11,4 місяців). У дослідження EDGE II було включено 4086 пацієнтів з РА, які отримували еторикоксиб у дозі 90 мг на день або диклофенак у дозі 150 мг на день протягом середньому 19,2 місяців (максимум 33,1 місяця, медіана 24 місяці). В об'єднаній програмі MEDAL аналізували дані щодо лікування 34701 пацієнтів з ОА або РА, середня тривалість лікування склала 17,9 місяців (максимум 42,3 місяці, медіана 16,3 місяців), при цьому приблизно 12800 пацієнтів отримували лікування протягом понад 24 місяців. Пацієнти, включені до програми, при вихідній оцінці мали широкий спектр серцево-судинних та шлунково-кишкових факторів ризику. Були виключені пацієнти, які мали в анамнезі нещодавно перенесений інфаркт міокарда (ІМ), аортокоронарне шунтування або черезшкірне коронарне втручання протягом 6 місяців перед включенням до дослідження. У дослідженнях дозволялося застосовувати гастропротектори та низькі дози аспірину. Загальна безпека Достовірних відмінностей між эторикоксибом та диклофенаком щодо частоти розвитку серцево-судинних тромботичних явищ виявлено не було. Кардіоренальні небажані явища найчастіше спостерігалися при прийомі церикоксибу в порівнянні з диклофенаком, ефект був дозозалежним (див. результати нижче). Небажані явища з боку шлунково-кишкового тракту та печінки достовірно частіше спостерігалися при прийомі диклофенаку, ніж при прийомі церикоксибу. Частота небажаних явищ у дослідженнях EDGE та EDGE II та небажаних явищ, визнаних серйозними або зажадали відміни лікування, у дослідженні MEDAL була вищою при прийомі еторикоксибу порівняно з диклофенаком. Результати дослідження безпеки щодо серцево-судинної системи Частота підтверджених серйозних тромботичних серцево-судинних небажаних явищ (включаючи серцеві, цереброваскулярні та явища з боку периферичної судинної системи) була порівнянна між групами, які отримували церикоксиб або диклофенак (дані наведені в таблиці нижче). Не виявлено статистично значимих відмінностей щодо частоти тромботичних явищ між еторикоксибом та диклофенаком у всіх проаналізованих підгрупах, включаючи категорії пацієнтів з підвищеним ризиком серцево-судинних ускладнень. Відносний ризик для підтверджених серйозних серцево-судинних небажаних тромботичних явищ був подібним при прийомі еторикоксібу в дозі 60 мг або 90 мг і диклофенаку в дозі 150 мг. Частота підтверджених тромботичних серцево-судинних серйозних небажаних явищ (Об'єднана програма MEDAL) Еторікоксиб(N=16819)25 836 пацієнто-років Диклофенак(N=16483)24 766 пацієнто-років Порівняння між видами лікування Частота 1 (95% ДІ) Частота 1 (95% ДІ) Відносний ризик (95% ДІ) Підтверджені тромботичні серцево-судинні серйозні небажані явища За виконання вимог протоколу (Per protocol) 1,24 (1,11; 1,38) 1,30 (1,17; 1,45) 0,95 (0,81; 1,11) Залежно від призначеного лікування (Intent-to-treat) 1,25 (1,14; 1,36) 1,19 (1,08; 1,30) 1,05 (0,93; 1,19) Підтверджені явища з боку серця За виконання вимог протоколу (Per protocol) 0,71 (0,61; 0,82) 0,78 (0,68; 0,90) 0,90 (0,74; 1,10) Залежно від призначеного лікування (Intent-to-treat) 0,69 (0,61; 0,78) 0,70 (0,62; 0,79) 0,99 (0,84; 1,17) Підтверджені цереброваскулярні явища За виконання вимог протоколу (Per protocol) 0,34 (0,28; 0,42) 0,32 (0,25; 0,40) 1,08 (0,80; 1,46) Залежно від призначеного лікування (Intent-to-treat) 0,33 (0,28; 0,39) 0,29 (0,24; 0,35) 1,12 (0,87; 1,44) Підтверджені явища з боку периферичної судинної системи За виконання вимог протоколу (Per protocol) 0,20 (0,15; 0,27) 0,22 (0,17; 0,29) 0,92 (0,63; 1,35) Залежно від призначеного лікування (Intent-to-treat) 0,24 (0,20; 0,30) 0,23 (0,18; 0,28) 1,08 (0,81; 1,44) 1 число явищ на 100 пацієнто-років; ДІ = довірчий інтервал; N = загальна кількість пацієнтів, які виконали вимоги протоколу. При виконанні вимог протоколу: всі явища, що розвинулися на тлі досліджуваної терапії або протягом 14 днів після її припинення (виключені пацієнти, які прийняли <75% досліджуваного препарату або приймали НПЗП >10% часу, що не входять до дослідження). Залежно від призначеного лікування: всі підтверджені явища, що розвинулися до закінчення дослідження (включно з пацієнтами, які могли піддаватися не включеним до дослідження втручанням після припинення прийому досліджуваних препаратів). Загальна кількість рандомізованих пацієнтів: n = 17412 для эторикоксиба і n = 17289 для диклофенаку. Смертність від серцево-судинних явищ, а також загальна смертність у групах лікування церикоксибом та диклофенаком були порівнянними. Кардіоренальні явища Приблизно у 50% пацієнтів, включених у дослідження MEDAL, при початковій оцінці в анамнезі було зареєстровано артеріальну гіпертензію. У проведеному дослідженні частота вибування внаслідок небажаних явищ, пов'язаних з артеріальною гіпертензією, була статистично значуще вищою під час прийому эторикоксиба проти диклофенаком. Частота небажаних явищ, пов'язаних з хронічною серцевою недостатністю (випадки вибування з дослідження або серйозні небажані явища), була подібною до груп еторікоксибу в дозі 60 мг і диклофенаку в дозі 150 мг, але була вищою для еторікоксибу в дозі 90 мг порівняно з диклофеном. дозі 150 мг (і статистично значуще вище для еторикоксибу в дозі 90 мг у порівнянні з диклофенаком у дозі 150 мг у дослідженні MEDAL у пацієнтів з ОА). Частота підтверджених небажаних явищ,пов'язаних з хронічною серцевою недостатністю (серйозних, які призвели до госпіталізації або необхідності невідкладної допомоги), була незначно вищою для церикоксибу порівняно з диклофенаком у дозі 150 мг, ефект був дозозалежним. Частота випадків вибування з дослідження внаслідок небажаних явищ, пов'язаних з набряками, була вищою для еторікоксибу в дозі 150 мг, порівняно з диклофенаком у дозі 150 мг, ефект був дозозалежним (статистично значимо для еторікоксибу в дозі 90 мг, але не для етороксиксу в дозі 60 мг).була вищою для эторикоксиба порівняно з диклофенаком в дозі 150 мг, ефект був дозозалежним (статистично значуще для етіроксиксібу в дозі 90 мг, але не для етіроксиксібу в дозі 60 мг).була вищою для эторикоксиба порівняно з диклофенаком у дозі 150 мг, ефект був дозозалежним (статистично значуще для церикоксибу в дозі 90 мг, але не для церикоксиксу в дозі 60 мг). Результати оцінки кардіоренальної безпеки у дослідженнях EDGE та EDGE II узгоджуються з результатами у дослідженні MEDAL В окремих дослідженнях програми MEDAL абсолютна частота вибування з дослідження в будь-якій групі лікування при прийомі еторикоксибу (60 мг або 90 мг) становила до 2,6% при артеріальній гіпертензії, до 1,9% при набряках, і до 1,1% при хронічній серцевої недостатності. У пацієнтів, які приймали церикоксиб у дозі 90 мг, частота вибуття з дослідження була вищою, ніж у пацієнтів, які приймали церикоксиб у дозі 60 мг. Результати оцінки переносимості з боку ШКТ у Програмі MEDAL У кожному з трьох досліджень, що входять до програми MEDAL, частота вибування з дослідження для будь-яких клінічних небажаних явищ з боку шлунково-кишкового тракту (наприклад, диспепсія, біль у животі, виразки) була достовірно нижчою для еторикоксибу порівняно з диклофенаком. Частота вибуття з дослідження внаслідок небажаних клінічних явищ з боку шлунково-кишкового тракту на 100 пацієнто-років за весь період дослідження становила: 3,23 для еторикоксибу та 4,96 для диклофенаку в дослідженні MEDAL; 9,12 для эторикоксиба і 12,28 для диклофенаку у дослідженні EDGE; 3,71 для еторикоксибу та 4,81 для диклофенаку в дослідженні EDGE II. Результати оцінки безпеки щодо ШКТ у Програмі MEDAL До небажаних явищ з боку верхніх відділів шлунково-кишкового тракту були віднесені перфорації, виразки та кровотечі. Ускладнені небажані явища з боку верхніх відділів шлунково-кишкового тракту включали перфорацію, непрохідність та ускладнені кровотечі; неускладнені явища включали неускладнені кровотечі та неускладнені виразки. При прийомі эторикоксиба порівняно з диклофенаком загальна частота небажаних явищ з боку верхніх відділів шлунково-кишкового тракту була достовірно нижчою. Достовірних відмінностей між етерокіксібом і диклофенаком за частотою ускладнених небажаних явищ виявлено не було. Для випадків кровотеч із верхніх відділів шлунково-кишкового тракту (ускладнених та неускладнених) не було виявлено достовірних відмінностей між еторикоксибом та диклофенаком.Перевага церикоксибу порівняно з диклофенаком щодо ускладнень з боку верхніх відділів ШКТ не була статистично значущою у пацієнтів, які одночасно приймали аспірин у низьких дозах (близько 33% пацієнтів). Частота підтверджених ускладнених та неускладнених клінічних небажаних явищ з боку верхніх відділів шлунково-кишкового тракту на 100 пацієнто-років (перфорації, виразки та кровотечі) склала 0,67 (95 % ДІ: 0,57; 0,77) для церикоксиксу та 0,97 (95 % ДІ: 0,85; 1,10) для диклофенаку, відносний ризик склав 0,69 (95% ДІ: 0,57; 0,83). При оцінці частоти підтверджених клінічних небажаних явищ з боку верхніх відділів шлунково-кишкового тракту у пацієнтів похилого віку максимальне зниження спостерігалося у пацієнтів у віці ≥75 років у групі церикоксибу в порівнянні з диклофенаком - 1,35 (95 % ДІ: 0,94; 1,87) та 2,78 (95% ДІ: 2,14; 3,56) на 100 пацієнто-років відповідно. Частота підтверджених небажаних явищ з боку нижніх відділів шлунково-кишкового тракту (перфорація тонкої або товстої кишки, непрохідність, кровотеча) достовірно не розрізнялася між групами, які приймали церикоксиб та диклофенак. Результати оцінки безпеки щодо печінки у Програмі MEDAL При прийомі эторикоксиба порівняно з диклофенаком спостерігалася статистично достовірно нижча частота вибуття з дослідження через небажані явища з боку печінки. В об'єднаній програмі MEDAL 0,3% пацієнтів, які приймали еторикоксиб, та 2,7% пацієнтів, які приймали диклофенак, вибули з дослідження через небажані явища з боку печінки. Частота небажаних явищ на 100 пацієнто-років склала 0,22 для церикоксиксу і 1,84 для диклофенаку (р Додаткові дані щодо безпеки, пов'язані з тромботичними серцево-судинними явищами У клінічних дослідженнях, за винятком Програми MEDAL, приблизно 3100 пацієнтів отримували церикоксикс у дозі ≥60 мг на день протягом 12 тижнів та довше. У цих дослідженнях не було виявлено помітних відмінностей у частоті підтверджених серйозних тромботичних серцево-судинних явищ у пацієнтів, які отримували церикоксиб у дозі ≥60 мг, плацебо або нестероїдні протизапальні засоби, що не містять напроксен. Однак у порівнянні з пацієнтами, які отримували напроксен у дозі 500 мг двічі на день, частота цих явищ була вищою у пацієнтів, які отримували еторикоксиб. Різниця в антиагрегантній активності між деякими нестероїдними протизапальними засобами, що інгібують ЦОГ-1, та селективними інгібіторами ЦОГ-2 може мати клінічне значення у пацієнтів із групи ризику тромбоемболічних подій. Селективні інгібітори ЦОГ-2 пригнічують утворення системного (і, можливо, ендотеліального) простацикліну,не впливаючи на тромбоцитарний тромбоксан. Клінічна значимість цих спостережень встановлено. Додаткові дані з безпеки щодо ШКТ У двох 12-тижневих подвійних сліпих ендоскопічних дослідженнях кумулятивна частота розвитку гастродуоденальних виразок була значно нижчою у пацієнтів, які отримували церикоксиб у дозі 120 мг один раз на день, ніж у пацієнтів, які отримували напроксен 500 мг двічі на день. або ібупрофен 800 мг тричі на день. Частота розвитку виразок при призначенні церикоксибу була вищою порівняно з плацебо. Дослідження ниркової функції у пацієнтів похилого віку У рандомізованому подвійному сліпому плацебо-контрольованому дослідженні в паралельних групах оцінювався вплив 15-денної терапії церикоксибом (90 мг), целекоксибом (200 мг двічі на день), напроксеном (500 мг двічі на день) порівняно з плацебо на виведення натрію. , артеріальний тиск (АТ) та інші параметри функції нирок у пацієнтів віком від 60 до 85 років, які отримували раціон з обмеженим споживанням натрію до 200 мекв/день. Еторикоксиб, целекоксиб і напроксен мали подібний вплив на виведення натрію нирками через 2 тижні лікування. Всі активні препарати порівняння показали збільшення систолічного АТ порівняно з плацебо, однак, еторикоксиб викликав статистично значуще збільшення систолічного АТ на 14-й день порівняно з целекоксибом і напроксеном (середня зміна систолічного АТ порівняно з вихідним: етороксіб 7,7 мм рт. ст., целекоксиб 2,4 мм рт.ст., напроксен 3,6 мм рт.ст.).Показання до застосуванняСимптоматична терапія остеоартрозу, ревматоїдного артриту, анкілозуючого спондиліту, болю та запалення, пов'язаних із гострим подагричним артритом. Короткострокова терапія помірного гострого болю після стоматологічних операцій.Протипоказання до застосуванняПідвищена чутливість до еторикоксибу або будь-якої з допоміжних речовин препарату. Виразкова хвороба шлунка та 12-палої кишки у стадії загострення, активна шлунково-кишкова кровотеча. Бронхіальна астма, бронхоспазм, гострий риніт, поліпоз носа, ангіоневротичний набряк, кропив'янка або алергічні реакції після прийому ацетилсаліцилової кислоти або нестероїдних протизапальних препаратів (НПЗЗ), у тому числі інгібіторів ЦОГ-2, в анамнезі. Вагітність та період грудного вигодовування. Тяжкі порушення функції печінки (сироватковий альбумін 10 балів за шкалою Чайлд-П'ю). Тяжка ниркова недостатність (КК Діти та підлітки до 16 років. Запальні захворювання кишок. Хронічна серцева недостатність (II-IV функціональний клас за NYHA). Неконтрольована артеріальна гіпертензія (АТ стабільно вищий за 140/90 мм рт. ст.). Підтверджена ішемічна хвороба серця, захворювання периферичних артерій та/або цереброваскулярні захворювання. Дефіцит лактази, непереносимість лактози, глюкозо-галактозна мальабсорбція. Підтверджена гіперкаліємія. З обережністю: Пацієнти з підвищеним ризиком розвитку ускладнень з боку шлунково-кишкового тракту (виразкова ураження шлунково-кишкового тракту або шлунково-кишкова кровотеча в анамнезі, наявність інфекції Helicobacter Pylori, одночасне застосування інших нестероїдних протизапальних засобів, у тому числі ацетилсаліцилової кислоти, літній вік). Пацієнти, які мають в анамнезі фактори ризику серцево-судинних ускладнень (дисліпідемія/гіперліпідемія, цукровий діабет, артеріальна гіпертензія, куріння, серцева недостатність, порушення функції лівого шлуночка, набряки та затримка рідини в організмі). Печінкова недостатність (5-9 балів за класифікацією Чайлд-П'ю). Пацієнти з дегідратацією. Пацієнти з порушеннями функції нирок (КК Пацієнти з попереднім значним зниженням функції нирок, з ослабленою функцією нирок, декомпенсованою серцевою недостатністю або цирозом печінки, що перебувають у групі ризику при тривалому застосуванні нестероїдних протизапальних засобів. Супутня терапія антикоагулянтами (наприклад, варфарин), антиагрегантами (наприклад, ацетилсаліцилова кислота, клопідогрел), препаратами, що метаболізуються сульфотрансферазами.Вагітність та лактаціяВагітність В даний час клінічних даних про застосування еторикоксибу при вагітності відсутні. У дослідженнях на тваринах спостерігалася токсична дія на репродуктивну систему. Потенційний ризик для жінок під час вагітності невідомий. Застосування еторикоксибу, як і інших лікарських препаратів, що інгібують синтез простагландинів, у III триместрі вагітності може призводити до придушення скорочень матки та передчасного закриття артеріальної протоки. Еторикоксиб протипоказаний при вагітності. Якщо під час лікування настала вагітність, церикоксиб необхідно відмінити. Грудне годування У лактуючих щурів еторикоксиб виділяється з молоком. Досліджень, що підтверджують виділення еторикоксибу з грудним молоком у жінок, не проводилося. Жінки, які приймають еторикоксиб, повинні припинити грудне вигодовування. Фертильність Застосування еторикоксибу, як і інших препаратів, що інгібують ЦОГ-2 або синтез простагландинів, не рекомендується жінкам, які планують вагітність.Побічна діяРезюме профілю безпеки Безпека застосування церикоксибу оцінювалася у клінічних дослідженнях за участю 9295 пацієнтів, у тому числі 6757 пацієнтів з ОА, РА, хронічним болем у нижній частині спини та анкілозуючим спондилітом (приблизно 600 пацієнтів з ОА або РА отримували лікування протягом одного року або більше). Профіль небажаних реакцій був подібним у пацієнтів з ОА або РА, які отримували еторикоксиб протягом одного року або довше. У клінічному дослідженні гострого подагричного артриту пацієнти отримували церикоксиб у дозі 120 мг 1 раз на день протягом 8 днів. Профіль небажаних явищ у цьому дослідженні був загалом таким самим, як і в об'єднаних дослідженнях ОА, РА та хронічного болю в нижній частині спини. Для оцінки безпеки щодо серцево-судинної системи були об'єднані дані трьох активних контрольованих досліджень, у яких брали участь 17412 пацієнтів з ОА або РА, які отримували еторикоксиб у дозі 60 мг або 90 мг, середня тривалість досліджень склала приблизно 18 місяців. У клінічних дослідженнях гострого післяопераційного болю, пов'язаного з проведенням стоматологічної операції, у яких 614 пацієнтів отримували еторикоксиб у дозі 90 мг або 120 мг, профіль небажаних ефектів загалом був подібним до профілю в об'єднаних дослідженнях ОА, РА та хронічного болю в нижній частині спини. Табличне резюме небажаних реакцій У таблиці перераховані небажані реакції, які були зареєстровані з більшою частотою при застосуванні препарату, ніж у групі плацебо, у клінічних дослідженнях, що включали пацієнтів з ОА, РА, хронічним болем у нижній частині спини або анкілозуючим спондилітом (еторикоксиб призначався у дозі 30 мг, 60 мг або 90 мг з підвищенням дози до рекомендованої протягом 12 тижнів), у програмі MEDAL, де дослідження тривали до 3,5 років, у короткострокових дослідженнях гострого болю (протягом 7 днів), а також отримані під час постмаркетингового застосування. Класифікація систем органів Небажана реакція Частота 1 Інфекційні та паразитарні захворювання альвеолярний остит часто гастроентерит, інфекції верхніх дихальних шляхів, інфекції сечовивідних шляхів не часто Порушення з боку крові та лімфатичної системи анемія (в основному в результаті шлунково-кишкової кровотечі), лейкопенія, тромбоцитопенія не часто Порушення з боку імунної системи реакції гіперчутливості 2,4 не часто ангіоневротичний набряк, анафілактичні/анафілактоїдні реакції, у тому числі шок 2 рідко Порушення з боку обміну речовин та харчування набряки/затримка рідини часто посилення або зниження апетиту, збільшення маси тіла не часто Порушення психіки тривога, депресія, зниження ясності мислення, галюцинації 2 не часто сплутаність свідомості 2 , неспокій 2 рідко Порушення з боку нервової системи запаморочення, головний біль часто порушення смаку, безсоння, парестезія/гіпестезія, сонливість не часто Порушення з боку органу зору нечіткість зору, кон'юнктивіт не часто Порушення з боку органу слуху та лабіринтні порушення дзвін у вухах, вертиго не часто Порушення з боку серця відчуття серцебиття, аритмія 2 часто фібриляція передсердь, тахікардія 2 , хронічна серцева недостатність, неспецифічні зміни на ЕКГ, стенокардія 2 , інфаркт міокарда 5 не часто Порушення з боку судин артеріальна гіпертензія часто "припливи", порушення мозкового кровообігу 5 транзиторна ішемічна атака гіпертонічний криз 2 васкуліт 2 не часто Порушення з боку дихальної системи, органів грудної клітки та середостіння. бронхоспазм 2 часто кашель, задишка, носова кровотеча не часто Порушення з боку шлунково-кишкового тракту біль в животі дуже часто метеоризм, гастрит, печія/гастроезофагеальний рефлюкс, діарея, диспепсія/дискомфорт в епігастрії, нудота, блювання, езофагіт, виразка слизової оболонки порожнини рота часто здуття живота, зміна перистальтики, сухість слизової оболонки порожнини рота, виразка гастродуоденальної, виразкова хвороба шлунка, включаючи перфорації та кровотечі, панкреатит 2 , синдром подразненого кишечника не часто Порушення з боку печінки та жовчовивідних шляхів підвищення активності АЛТ та ACT часто гепатит 2 рідко печінкова недостатність 2 , жовтяниця 2 рідко 3 Порушення з боку шкіри та підшкірних тканин екхімоз часто набряклість особи, свербіж, висип, еритема 2 , кропив'янка 2 не часто синдром Стівенса-Джонсона 2 , токсичний епідермальний некроліз 2 , фіксована лікарська еритема 2 рідко 3 Порушення з боку скелетно-м'язової та сполучної тканини м'язові судоми/спазм, скелетно-м'язовий біль/скутість не часто Порушення з боку нирок та сечовивідних шляхів протеїнурія, підвищення концентрації креатиніну в сироватці, ниркова недостатність 2,3,4 не часто Загальні розлади та порушення у місці введення астенія/слабкість, грипоподібний синдром часто біль у грудній клітці не часто Лабораторні та інструментальні дані підвищення концентрації азоту сечовини крові, підвищення активності креатинфосфокінази, гіперкаліємія, підвищення концентрації сечової кислоти не часто гіпонатріємія рідко 1 Відповідно до частоти, що враховується у клінічних дослідженнях: дуже часто (≥1/10), часто (від ≥1/100 до 2 Ця небажана реакція була зареєстрована під час постмаркетингового спостереження. Частота оцінювалася на підставі найбільшої частоти, що спостерігається у клінічних дослідженнях з урахуванням показань та затвердженої дози. 3 Частотна категорія "рідко" була визначена відповідно до керівництва (версія 2, вересень 2009 р.) для Короткої характеристики лікарського препарату на підставі розрахункової верхньої межі 95 % довірчого інтервалу для 0 явищ, враховуючи кількість пацієнтів, які отримували еторикоксиб в аналізі даних III фази , об'єднаних залежно від дози та показання (n = 15470). 4 Гіперчутливість включає терміни "алергія", "лікарська алергія", "гіперчутливість до лікарського препарату", "гіперчутливість", "гіперчутливість неуточнена", "реакція гіперчутливості" та "неспецифічна алергія". 5 За результатами даних аналізу довгострокових плацебо- та активноконтрольованих клінічних досліджень при застосуванні селективних інгібіторів ЦОГ-2 підвищується ризик розвитку серйозних артеріальних тромботичних явищ, включаючи ІМ та інсульт. З наявних даних, малоймовірно, що абсолютний ризик розвитку цих явищ перевищує 1 % на рік (нечасто). Наступні серйозні небажані явища були зареєстровані у зв'язку з прийомом НГТВП і не можуть бути виключені для еторикоксибу: нефротоксичність, включаючи інтерстиціальний нефрит та нефротичний синдром.Взаємодія з лікарськими засобамиФармакодинамічні взаємодії Пероральні антикоагулянти (варфарин). У пацієнтів, які постійно приймають варфарин, прийом еторикоксибу в дозі 120 мг на день супроводжувався збільшенням міжнародного нормалізованого відношення (МНО)/протромбінового часу приблизно на 13%. Тому у пацієнтів, які отримують пероральні антикоагулянти, слід контролювати МНО/протромбіновий час на початку лікування або при зміні дози еторикоксибу, особливо в перші кілька днів. Діуретики, інгібітори ангіотензинперетворюючого ферменту (АПФ) та антагоністи рецепторів ангіотензину II. Нестероїдні протизапальні засоби можуть послаблювати ефект діуретиків та інших антигіпертензивних лікарських препаратів. У деяких пацієнтів з порушенням функції нирок (наприклад, у пацієнтів з зневодненням або у літніх пацієнтів з порушеною функцією нирок) одночасне застосування інгібітору АПФ або антагоніста рецепторів ангіотензину II та препаратів, що інгібують ЦОГ, може призводити до додаткового погіршення функції нирок, включаючи можливий розвиток. ниркової недостатності, яка зазвичай має оборотний характер. Це слід враховувати у пацієнтів, які приймають одночасно церикоксиб з інгібіторами АПФ або антагоністами рецепторів ангіотензину ІІ. Такі комбінації слід призначати з обережністю, особливо пацієнтам похилого віку.Пацієнти повинні бути належним чином гідратовані, при цьому необхідно проводити моніторинг функції нирок на початку комбінованої терапії та періодично надалі. Ацетилсаліцилова кислота. У дослідженні у здорових добровольців церикоксиб у дозі 120 мг 1 раз на день у рівноважному стані не впливав на антитромбоцитарну активність ацетилсаліцилової кислоти (81 мг 1 раз на день). Еторикоксиб можна одночасно застосовувати з ацетилсаліциловою кислотою в низьких дозах, призначених для профілактики серцево-судинних захворювань. Тим не менш, одночасне застосування низьких доз ацетилсаліцилової кислоти та еторикоксибу може призвести до збільшення частоти виразкового ураження шлунково-кишкового тракту або інших ускладнень у порівнянні з прийомом тільки церикоксиксу. Одночасне застосування церикоксибу з ацетилсаліциловою кислотою в дозах, що перевищують рекомендовані для профілактики серцево-судинних ускладнень, а також з іншими нестероїдними протизапальними засобами не рекомендується. Циклоспорин та такролімус. Взаємодія церикоксибу з цими препаратами не вивчалася, однак, одночасне застосування циклоспорину або такролімусу з будь-яким нестероїдними протизапальними засобами може посилювати нефротоксичний ефект циклоспорину або такролімусу. При прийомі эторикоксиба у комбінації з будь-яким із цих препаратів слід контролювати функцію нирок. Фармакокінетичні взаємодії Вплив інших лікарських препаратів на фармакокінетику еторикоксибу Основний шлях метаболізму церикоксибу залежить від ферментів системи CYP. Ізофермент CYP3A4 сприяє метаболізму церикоксибу in vivo. Дослідження in vitro показують, що ізоферменти CYP2D6, CYP2C9, CYP1A2 і CYP2C19 можуть каталізувати основний шлях метаболізму, але їх кількісні характеристики in vivo не вивчені. Кетоконазол. Кетоконазол, потужний інгібітор ізоферменту CYP3A4, при прийомі здоровими добровольцями в дозі 400 мг один раз на день протягом 11 днів не надавав клінічно значущого впливу на фармакокінетику одноразової дози церикоксиксу 60 мг (збільшення AUC на 43%). Вориконазол та міконазол. Одночасне призначення сильних інгібіторів ізоферменту CYP3A4 (вориконазол для прийому всередину або міконазол місцево, у вигляді гелю для прийому всередину) та еторикоксибу викликало невелике збільшення експозиції церикоксибу, яке не визнано клінічно значущим на підставі опублікованих даних. ріфампіцин. Одночасне застосування церикоксибу та рифампіцину (потужного індуктора системи цитохромів) призводило до зниження концентрації церикоксибу в плазмі на 65 %. Така взаємодія може призвести до рецидиву симптомів при одночасному призначенні еторикоксибу з рифампіцином. Ця інформація дозволяє припустити необхідність збільшення дози, проте застосовувати еторикоксиб у дозах, що перевищують рекомендовані для кожного показання, не рекомендується, оскільки комбіноване застосування рифампіцину та еторикоксибу в таких дозах не вивчалося. Антациди. Антациди не надають клінічно значущої дії на фармакокінетику еторикоксибу. Вплив еторикоксибу на інші лікарські препарати Літій. НПЗЗ зменшують виведення літію нирками, отже, збільшують концентрацію літію у плазмі крові. При необхідності проводять частий контроль концентрації літію в крові та коригують дозу літію під час одночасного прийому з нестероїдними протизапальними засобами, а також при відміні нестероїдних протизапальних засобів. Метотрексат. У двох дослідженнях вивчалися ефекти еторикоксибу в дозах 60, 90 або 120 мг 1 раз на день протягом семи днів у пацієнтів, які отримували 1 раз на тиждень метотрексат у дозі від 7,5 до 20 мг на лікування РА. Еторикоксиб у дозах 60 та 90 мг не впливав на концентрацію метотрексату в плазмі та нирковий кліренс метотрексату. В одному дослідженні церикоксиб у дозі 120 мг не фармакокінетично впливав на метотрексат, але в іншому дослідженні концентрація метотрексату в плазмі підвищувалася на 28 %, а нирковий кліренс метотрексату знижувався на 13 %. При одночасному прийомі церикоксибу та метотрексату рекомендується вести спостереження щодо можливої появи токсичних ефектів метотрексату. Пероральні контрацептиви. Еторикоксиб у дозі 60 мг при одночасному прийомі протягом 21 дня з пероральними контрацептивами, що містять 35 мкг етинілестрадіолу (ЕЕ) та від 0,5 мг до 1 мг норетиндрону, збільшував AUC0-24 год ЕЕ на 37 % у рівноважному стані. Прийом церикоксиксу в дозі 120 мг у поєднанні з вищевказаними пероральними контрацептивами (одночасно або з інтервалом 12 годин) збільшував AUC0-24год. ЕЕ на 50-60% у рівноважному стані. Це збільшення концентрації ЕЕ слід враховувати при виборі перорального контрацептиву для одночасного застосування з церикоксибом. Подібна взаємодія може спричинити збільшення частоти розвитку небажаних явищ, пов'язаних із застосуванням пероральних контрацептивів (наприклад, венозних тромбоемболій у жінок із групи ризику). Замісна гормональна терапія (ЗГТ). Призначення еторікоксибу в дозі 120 мг одночасно з препаратами для ЗГТ, що містять кон'юговані естрогени в дозі 0,625 мг протягом 28 днів, збільшує середнє рівноважне значення AUC0-24 год некон'югованого естрону (41 %), еквіліну (76 %) та 17-2 %). Вплив доз еторикоксибу, рекомендованих для тривалого застосування (30, 60 та 90 мг), не вивчався. Еторикоксиб у дозі 120 мг змінював експозицію (AUC0-24год) даних естрогенних компонентів менш ніж удвічі порівняно з монотерапією кон'югованими естрогенами при збільшенні дози з 0,625 до 1,25 мг. Клінічне значення таких збільшення невідомо, застосування більш високих доз кон'югованих естрогенів у поєднанні з еторикоксибом не вивчалося.Підвищення концентрації естрогенів слід брати до уваги при виборі гормональної терапії в період постменопаузи при одночасному призначенні з етороксібом, оскільки збільшення експозиції естрогенів може підвищувати ризик розвитку небажаних явищ, пов'язаних із ЗГТ. Преднізон/Преднізолон. У дослідженнях лікарських взаємодій эторикоксиб не впливав на клінічно значущий вплив на фармакокінетику преднізону/преднізолону. Дігоксин. При застосуванні эторикоксибу в дозі 120 мг один раз на день протягом 10 днів у здорових добровольців не спостерігалося зміни рівноважної AUC0-24год дигоксину в плазмі або впливу на його виведення нирками. При цьому спостерігалося збільшення Стах дигоксину приблизно на 33%. Таке підвищення, як правило, не є важливим для більшості пацієнтів. Тим не менш, при одночасному застосуванні церикоксибу та дигоксину слід спостерігати за станом пацієнтів із високим ризиком прояву токсичної дії дигоксину. Вплив еторикоксибу на препарати, що метаболізуються сульфотрансферазами. Еторикоксиб є інгібітором сульфотрансферази людини (зокрема, SULT1E1) і може підвищувати концентрацію ЕЕ у сироватці крові. У зв'язку з тим, що в даний час отримано недостатньо даних про ефекти різних сульфотрансфераз, а їхня клінічна значущість для застосування багатьох лікарських препаратів ще вивчається, доцільно з обережністю призначати церикоксиб одночасно з іншими лікарськими препаратами, що метаболізуються сульфотрансферазами людини (наприклад, пероральний сальбутамол і ). Вплив етерокіксібу на препарати, що метаболізуються ізоферментами системи цитохромів. Грунтуючись на результатах досліджень in vitro, не очікується, що эторикоксиб інгібуватиме ізоферменти цитохрому Р450 (CYP) 1А2, 2С9, 2С19, 2D6, 2Е1 або 3А4. У дослідженні у здорових добровольців щоденне застосування церикоксибу в дозі 120 мг не впливало на активність ізоферменту CYP3A4 печінки при оцінці за допомогою еритроміцинового дихального тесту.Спосіб застосування та дозиВсередину, незалежно від їди, запиваючи невеликою кількістю води. Дія препарату реалізується швидше при прийомі натще. Внаслідок можливого підвищення ризику серцево-судинних ускладнень слід використовувати мінімальну ефективну дозу мінімально можливим курсом. Остеоартроз: рекомендована доза етерокіксібу становить 30 мг 1 раз на день. У разі недостатнього ефекту добова доза препарату може бути збільшена до 60 мг на добу. Добова доза при остеоартрозі не повинна перевищувати 60 мг. Ревматоїдний артрит та анкілозуючий спондиліт: рекомендована доза еторикоксібу становить 60 мг 1 раз на день. У пацієнтів із недостатнім клінічним ефектом можливе збільшення добової дози препарату до 90 мг один раз на день. Після клінічної стабілізації захворювання можливе зниження дози до 60 мг один раз на день. У разі відсутності ознак клінічного покращення слід розглянути можливість застосування інших методів лікування. Добова доза не повинна перевищувати 90 мг. Гострий подагричний артрит: рекомендована доза церикоксибу в гострому періоді становить 120 мг 1 раз на день. Тривалість застосування препарату у дозі 120 мг не перевищує 8 днів. Добова доза не повинна перевищувати 120 мг. Гострий біль після стоматологічних операцій: рекомендована доза еторикоксибу становить 90 мг 1 раз на день. Еторикоксиб слід застосовувати лише у гострий симптоматичний період тривалістю не більше 3 днів. Добова доза для усунення болю після стоматологічних операцій не повинна перевищувати 90 мг. Деяким пацієнтам можуть знадобитися додаткові засоби для забезпечення адекватного рівня знеболювання у післяопераційному періоді протягом триденного періоду терапії церикоксибом. Особливі групи пацієнтів Літні пацієнти: корекція дози не потрібна. Як і при застосуванні інших препаратів, еторикоксиб слід застосовувати з обережністю. Діти: застосування еторикоксибу у пацієнтів віком до 16 років протипоказано. Порушення функції печінки: незалежно від показання до застосування пацієнтам з порушеннями функції печінки легкого ступеня тяжкості (5-6 балів за шкалою Чайлд-П'ю) не слід перевищувати дозу 60 мг 1 раз на день, пацієнтам з порушеннями функції печінки середнього ступеня тяжкості (7 -9 балів за шкалою Чайлд-Пью) – 30 мг 1 раз на день. Рекомендується бути обережним при застосуванні препарату у пацієнтів з порушеннями функції печінки середнього ступеня тяжкості, оскільки клінічний досвід застосування препарату у даної групи пацієнтів обмежений. У зв'язку з відсутністю клінічного досвіду застосування препарату у пацієнтів з тяжкими порушеннями функції печінки (≥10 балів за шкалою Чайлд-П'ю) препарат протипоказаний для цієї групи пацієнтів. Порушення функції нирок: не потрібна корекція дози препарату при застосуванні у пацієнтів із КК ≥30 мл/хв. Застосування препарату у пацієнтів із ККПередозуванняУ клінічних дослідженнях прийом еторикоксибу в разовій дозі до 500 мг і багаторазовий прийом до 150 мг/день протягом 21 дня не викликав суттєвих токсичних ефектів. Були отримані повідомлення про гостре передозування еторикоксибом, однак, у більшості випадків про небажані реакції не повідомлялося. Найчастіші небажані реакції відповідали профілю безпеки церикоксибу (наприклад, порушення з боку шлунково-кишкового тракту, кардіоренальні явища). У разі передозування доцільно вживати звичайні підтримувальні заходи, такі як видалення невсмоктаного препарату із ШКТ, клінічне спостереження і, при необхідності, підтримуюча терапія. Еторікоксиб не виводиться при гемодіалізі; виведення еторикоксибу при перитонеальному діалізі не вивчалося.Запобіжні заходи та особливі вказівкиВплив на ШКТ У пацієнтів, які отримували еторикоксиб, спостерігалися ускладнення з боку верхніх відділів шлунково-кишкового тракту (перфорації, виразки або кровотечі), іноді з летальним кінцем. Рекомендується бути обережним при лікуванні пацієнтів з високим ризиком розвитку ускладнень з боку шлунково-кишкового тракту при застосуванні нестероїдних протизапальних засобів, зокрема, у літніх пацієнтів, що одночасно застосовують інші нестероїдні протизапальні засоби, ацетилсаліцилову кислоту або у пацієнтів із захворюваннями шлунково-кишкового тракту в анамнезі, такими як виразка та шлунково-кишкова кровотеча. Існує додатковий ризик розвитку небажаних реакцій з боку шлунково-кишкового тракту (шлунково-кишкові виразки або інші ускладнення з боку шлунково-кишкового тракту) при одночасному застосуванні церикоксибу та ацетилсаліцилової кислоти (навіть у низьких дозах). У довгострокових клінічних дослідженнях не спостерігалося достовірних відмінностей щодо безпеки для ШКТ при застосуванні селективних інгібіторів ЦОГ-2 у комбінації з ацетилсаліциловою кислотою порівняно із застосуванням нестероїдних протизапальних засобів у комбінації з ацетилсаліциловою кислотою. Вплив на серцево-судинну систему Результати клінічних досліджень свідчать про те, що застосування лікарських препаратів класу селективних інгібіторів ЦОГ-2 пов'язано з підвищеним ризиком тромбоутворення (особливо інфаркту міокарда (ІМ) та інсульту) порівняно з плацебо та деякими НПЗЗ. Ризик розвитку серцево-судинних ускладнень при застосуванні селективних інгібіторів ЦОГ-2 може зростати зі збільшенням дози та тривалості лікування, тому слід застосовувати церикоксиб протягом максимально короткого періоду часу та у найнижчій ефективній добовій дозі. Необхідно періодично оцінювати потребу пацієнта у симптоматичному лікуванні та відповідь на терапію, особливо у пацієнтів з ОА. Пацієнтам з відомими факторами ризику розвитку серцево-судинних ускладнень (наприклад, артеріальна гіпертензія, гіперліпідемія, цукровий діабет, куріння) церикоксиб необхідно призначати тільки після ретельної попередньої оцінки співвідношення користі-ризику. Селективні інгібітори ЦОГ-2 не є заміною ацетилсаліцилової кислоти при профілактиці серцево-судинних захворювань через відсутність антитромбоцитарного ефекту, тому не слід припиняти застосування антиагрегантних препаратів. Вплив на функцію нирок Ниркові простагландини можуть відігравати компенсаторну роль у підтримці ниркової перфузії. Тому за наявності умов, що негативно впливають на ниркову перфузію, призначення еторикоксибу може призвести до зменшення утворення простагландинів і, як наслідок, зниження ниркового кровотоку, і тим самим призвести до погіршення функції нирок. Найбільший ризик розвитку цієї реакції виникає у пацієнтів із значним зниженням функції нирок, некомпенсованою серцевою недостатністю або цирозом печінки в анамнезі. У таких пацієнтів необхідно проводити моніторинг функції нирок. Затримка рідини, набряки та артеріальна гіпертензія Як і у разі застосування інших препаратів, що інгібують синтез простагландинів, у пацієнтів, які приймають еторикоксиб, спостерігалися затримка рідини, набряки та артеріальна гіпертензія. Застосування будь-яких нестероїдних протизапальних засобів, включаючи церикоксикс, може бути пов'язане з виникненням або рецидивом хронічної (застійної) серцевої недостатності. Інформація про дозозалежну реакцію для церикоксибу наведена в розділі "Фармакологічні властивості". Слід виявляти обережність при призначенні церикоксибу пацієнтам із серцевою недостатністю в анамнезі, дисфункцією лівого шлуночка, артеріальною гіпертензією та пацієнтам з уже наявними набряками, що виникли з будь-якої іншої причини. При появі клінічних ознак погіршення стану у таких пацієнтів слід вжити відповідних заходів, включаючи скасування еторікоксибу. Застосування еторикоксибу, особливо у високих дозах, може бути пов'язане з розвитком більш тяжкої артеріальної гіпертензії, ніж при застосуванні деяких інших нестероїдних протизапальних засобів та селективних інгібіторів ЦОГ-2. Тому під час лікування церикоксибом слід звернути особливу увагу на моніторинг АТ, який має контролюватись протягом двох тижнів після початку лікування та періодично надалі. При значному підвищенні артеріального тиску слід розглянути альтернативне лікування. Вплив на функцію печінки Підвищення активності аланінамінотрансферази (АЛТ) та/або аспартатамінотрансферази (ACT) (приблизно в три або більше рази щодо верхньої межі норми) було зареєстровано у клінічних дослідженнях приблизно у 1% пацієнтів, які отримували еторикоксиб протягом терміну до одного року у дозах 30 мг, 60 мг та 90 мг на день. Необхідно спостерігати за станом усіх пацієнтів із симптомами та/або ознаками дисфункції печінки, а також пацієнтів із зміненими лабораторними показниками функції печінки. Якщо виникають ознаки печінкової недостатності або показники функції печінки значно відхиляються від норми (втричі вище за верхню межу норми), прийом еторикоксибу повинен бути припинений. Загальні рекомендації Якщо під час лікування у пацієнтів погіршується будь-яка з функцій органів або систем органів, описаних вище, повинні бути вжиті відповідні заходи та розглянуто питання про скасування еторикоксибу. При застосуванні эторикоксибу у пацієнтів похилого віку та у пацієнтів з порушенням функції нирок, печінки або серця необхідне відповідне медичне спостереження. З обережністю слід розпочинати лікування ерикоксибом пацієнтам із зневодненням. Перед початком терапії церикоксибом рекомендується провести регідратацію. У період постмаркетингового спостереження при застосуванні НПЗП та деяких селективних інгібіторів ЦОГ-2 дуже рідко повідомлялося про розвиток серйозних реакцій шкіри. Деякі з них, у тому числі ексфоліативний дерматит, синдром Стівенса-Джонсона та токсичний епідермальний некроліз, були з смертю. Ризик розвитку цих реакцій найбільш високий на початку курсу терапії, здебільшого протягом першого місяця лікування. Повідомлялося про розвиток серйозних реакцій гіперчутливості, таких як анафілаксія та ангіоневротичний набряк, у пацієнтів, які отримували еторикоксиб. Застосування деяких селективних інгібіторів ЦОГ-2 супроводжувалося підвищеним ризиком розвитку шкірних реакцій у пацієнтів із якоюсь лікарською алергією в анамнезі. Еторикоксиб повинен бути скасований при першій появі висипу на шкірі,уражень слизової оболонки або будь-якої іншої ознаки гіперчутливості. Застосування еторикоксибу може маскувати лихоманку та інші ознаки запалення. Застосування еторикоксибу, як і інших препаратів, що інгібують ЦОГ та синтез простагландинів, не рекомендується жінкам, які планують вагітність (див. розділ "Застосування при вагітності та в період грудного вигодовування"). Оболонка таблетки містить лактозу. Пацієнтам з такими рідкісними вродженими захворюваннями, як непереносимість лактози, дефіцит лактази або глюкозогалактозна мальабсорбція, не слід приймати цей препарат. Вплив на здатність до керування автотранспортом та управління механізмами Пацієнтам, у яких на фоні застосування церикоксибу відзначаються епізоди запаморочення, сонливості чи слабкості, слід утриматися від керування транспортними засобами та роботи з механізмами.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
72 714,00 грн
72 666,00 грн
Склад, форма випуску та упаковкаПігулки - 1 таб. діюча речовина: кобіметініб – 20,00 мг (у вигляді кобіметинібу геміфумарату – 22,20 мг); допоміжні речовини: целюлоза мікрокристалічна – 54,72 мг; лактози моногідрат – 36,48 мг, кроскармеллозу натрію – 4,80 мг, магнію стеарат – 1,80 мг; плівкова оболонка1: полівініловий спирт – 1,92 мг, титану діоксид (Е171) – 1,20 мг, макрогол 2 – 0,97 мг, тальк – 0,71 мг. 1 Допускається використання комерційно доступної суміші для нанесення плівкової оболонки ідентичного складу (наприклад, Opadry II White 85F18422). 2 Синонім - поліетиленгліколь, PEG 3350. Пігулки, покриті плівковою оболонкою, 20 мг. По 21 таблетці в блістер із дуплексу (ПВХ/ПВДХ) та фольги алюмінієвої. 3 блістери разом з інструкцією із застосування поміщають у картонну пачку. З метою контролю першого розкриття на упаковку наноситься голографічна захисна наклейка.Опис лікарської формиКруглі, двоопуклі таблетки, покриті плівковою оболонкою, білого кольору; на одному боці таблетки гравіювання "СОВ".Фармакотерапевтична групаПротипухлинний засіб - протеїнтирозинкінази інгібітор.ФармакокінетикаВсмоктування При прийомі кобіметинібу в дозі 60 мг у пацієнтів з онкологічними захворюваннями відзначається помірна швидкість всмоктування з медіаною часу до досягнення максимальної концентрації у плазмі (Тmах) 2.4 години. Середні показники Сmах у рівноважному стані та площі під кривою "концентрація-час" (AUC0-24) становлять 273 нг/мл і 4340 нг*ч/мл відповідно. Середнє значення коефіцієнта накопичення у рівноважному стані становить приблизно 2,4. Кобіметініб має лінійну фармакокінетику в діапазоні доз приблизно від 3,5 мг до 100 мг. Абсолютна біодоступність кобіметинібу у здорових осіб становить 45,9%. У здорових осіб було показано, що кобіметініб інтенсивно метаболізується та виводиться через кишечник. Ступінь всмоктування становить приблизно 88%, що вказує на високий рівень всмоктування та пресистемний метаболізм. Фармакокінетика кобіметинібу не змінюється при прийомі препарату з їжею (у тому числі і з високим вмістом жирів) у порівнянні з прийомом натще у здорових осіб. Оскільки їжа не впливає на фармакокінетику кобіметинібу, препарат можна приймати незалежно від їди. Розподіл Зв'язування кобіметинібу з білками плазми in vitro становить 94,8%. При цьому не спостерігається переважне зв'язування з еритроцитами людини (співвідношення кров-плазма 0,93). Об'єм розподілу у здорових осіб, які отримали дозу 2 мг внутрішньовенно, становить 1050 л. За даними популяційного фармакокінетичного аналізу обсяг розподілу в онкологічних хворих становить 806 л. Метаболізм Співвідношення кобіметінібу та його метаболітів було вивчено під час дослідження масового балансу у здорових осіб. У середньому 94% дози відновлюється протягом 17 днів. Кобіметініб інтенсивно метаболізується та виводиться через кишечник; при цьому не відзначається переважання жодного метаболіту. Основні шляхи метаболізму кобіметинібу – окислення за допомогою ізоферменту CYP3A та глюкуронування за допомогою ізоферменту UGT2B7. Кобіметініб є основною речовиною, що виявляється у плазмі крові. Частка окислених метаболітів у плазмі становить не більше 10% від загальної кількості циркулюючої радіоактивності, при цьому специфічних для людини метаболітів не виявлено. Частка незміненого препарату в калі та сечі становить 6,6% та 1,6% від введеної дози, відповідно, що вказує на те, що кобіметиніб переважно піддається метаболізму та у незначній кількості виводиться нирками. Виведення Після внутрішньовенного введення кобіметинібу в дозі 2 мг середній кліренс становить 10,7 л/год. Середній кліренс у онкологічних хворих після прийому кобіметинібу в дозі 60 мг становить 13,8 л/год. Середній період напіввиведення кобіметинібу становить 43,6 годин (діапазон від 23,1 до 69,6 годин). Фармакокінетика у спеціальних груп пацієнтів За даними популяційного фармакокінетичного аналізу стать, раса, етнічна приналежність, вихідна оцінка ECOG, а також легке та помірне порушення функції нирок не впливають на фармакокінетику кобіметинібу. Статистично значущими коваріантами для кліренсу та обсягу розподілу кобіметинібу є вік та маса тіла відповідно. Однак згідно з результатами аналізу чутливості жодна з цих коваріантів не надає клінічно значущого впливу на експозицію в рівноважному стані. Підлога За даними популяційного фармакокінетичного аналізу підлога не впливає на експозицію кобіметінібу. Особи похилого віку За даними популяційного фармакокінетичного аналізу вік не впливає на експозицію кобіметінібу. Пацієнти з порушенням функції нирок За даними доклінічних досліджень та досліджень масового балансу, кобіметініб переважно піддається метаболізму з мінімальним виведенням нирками. Спеціальні дослідження фармакокінетики кобіметинібу у пацієнтів із порушенням функції нирок не проводились. Згідно з результатами популяційного фармакокінетичного аналізу даних у пацієнтів з легким та помірним порушенням функції нирок, а також у пацієнтів з нормальною функцією нирок (кліренс креатиніну (КК) >90 мл/хв) КК не має значного впливу на експозицію кобіметинібу. За даними популяційного фармакокінетичного аналізу, порушення функції нирок легкого та середнього ступеня тяжкості не впливає на експозицію кобіметинібу. Недостатньо даних для визначення необхідності корекції дози у пацієнтів з тяжким порушенням функції нирок. Пацієнти з порушенням функції печінки Фармакокінетика кобіметинібу не була вивчена у хворих з тяжким та середнім ступенем печінкової недостатності.ФармакодинамікаМеханізм дії Шлях мітоген-активованої протеїнкінази МАРК (Mitogen-Activated Protein Kinase) / позаклітинний сигнал-регульованої кінази ERK (Extracellular signal Regulated Kinase) є основним шляхом передачі сигналу, який регулює проліферацію клітин, клітинний цикл, виживання клітин, ангіоген. Препарат Котеллік – пероральний високоселективний алостеричний інгібітор кіназ МЕК1/2 (MAPK/ERK Kinase). У біохімічних та цитологічних дослідженнях кобіметиніб продемонстрував високу інгібуючу здатність, а також активність щодо широкого спектру пухлин in vivo на моделях ксенотрансплантату пухлин, включаючи пухлини, що несуть мутації BRAF та KRAS. У біохімічних та структурних дослідженнях було показано взаємодію кобіметинібу з МЕК, з незначною чутливістю до динамічних конформаційних змін, що спостерігаються під час переходу МЕК у фосфорильовану форму. Як результат, кобіметініб зберігає зв'язувальну здатність та інгібуючу активність при фосфорилуванні МЕК. Кобіметініб показав найвищу активність щодо ліній пухлинних клітин та пухлин з високими рівнями фосфорилювання МЕК, що часто спостерігається в пухлинах з мутаціями BRAF. У доклінічних дослідженнях обробка кобіметинібом МАРК-дисрегульованих пухлинних клітин та пухлин призводить до фосфорилування кіназ ERK1/2, єдиних відомих субстратів МЕК 1/2. Передача сигналу по МАРК-шляху залежить від активності кіназ ERK1/2, які фосфорилують білкові мішені в цитоплазмі та ядрі, що в свою чергу індукують прогресування клітинного циклу, проліферацію клітин, виживання та міграцію клітин. Таким чином, кобіметініб протидіє промітогенної та онкогенної активності, що індукується через МАРК-шлях, за рахунок інгібування МЕК 1/2. Комбінація вемурафенібу та препарату Котеллік інгібує реактивацію МАРК-шляху через МЕК 1/2 за рахунок одночасного впливу на BRAF та МЕК, призводячи до більш вираженого придушення передачі сигналів, апоптозу більшої кількості пухлинних клітин та посилення пухлинних відповідей у доклінічних моделях порівняно з монотерапією. Доклінічні дані щодо безпеки Канцерогенність Дослідження канцерогенності кобіметинібу не проводилися. Мутагенність Стандартні дослідження генотоксичності дали негативні наслідки. Інше Подовження інтервалу QT В умовах in vitro кобіметініб викликає помірно виражене інгібування іонного hERG-каналу (концентрація, необхідна для інгібування hERG-каналу (IC50) = 0,5 мкМ [266 нг/мл]), що приблизно в 18 разів більше, ніж максимальна концентрація у плазмі крові (Сmах) при застосуванні в дозі 60 мг (Сmах незв'язаного препарату = 14 нг/мл [0,03 мкМ]). IC50 вемурафенібу для hERG (0,6 мкМ) у комбінації з 0,3 мкМ кобіметинібу була приблизно в 2 рази нижчою, ніж раніше визначена IC50 при монотерапії вемурафенібом. При лікуванні пацієнтів препаратом Котеллік у комбінації з вемурафенібом не спостерігалося додаткового клінічного впливу на подовження інтервалу QT. За даними доклінічних досліджень (результатів стандартних фармакологічних досліджень з безпеки, досліджень токсичності при багаторазовому застосуванні та генотоксичності) специфічних ризиків для людини не виявлено.Показання до застосуванняНеоперабельна або метастатична меланома з BRAF V600 мутацією у дорослих пацієнтів у поєднанні з вемурафенібом.Протипоказання до застосуванняПідвищена чутливість до кобіметинібу та інших компонентів препарату. Вагітність та період грудного вигодовування. Дитячий вік до 18 років (ефективність та безпека застосування не встановлені). Одночасний прийом з потужними та помірними індукторами ізоферменту CYP3A та потужними інгібіторами ізоферменту CYP3A. Тяжкий ступінь ниркової недостатності. Тяжкий і середній ступінь печінкової недостатності. З обережністю: Одночасний прийом із помірними інгібіторами ізоферменту CYP3A. Недостатність лактази, непереносимість лактози, глюкозо-галактозна мальабсорбція.Вагітність та лактаціяВагітність Відсутні дані щодо застосування препарату Котеллік у вагітних жінок. Доклінічні дослідження показали, що у тварин кобіметініб призводить до загибелі ембріонів і спричиняє вади розвитку магістральних судин та черепа у плода при клінічно значущих експозиціях (приблизно в 0,9-1,4 рази, що перевищують клінічну експозицію AUC у плазмі крові людини). Контрацепція у жінок та чоловіків Необхідно використовувати два ефективні методи контрацепції під час лікування препаратом Котеллік та протягом як мінімум трьох місяців після припинення лікування. Період грудного вигодовування Невідомо, чи виділяється кобіметініб із грудним молоком. Не можна виключити ризик для немовлят/грудних дітей. Рішення про рекомендацію грудного вигодовування або призначення препарату Котеллік повинне прийматися залежно від необхідності лікування препаратом для матері. Фертильність Вплив кобіметинібу на фертильність у людини невідомий. Спеціальні доклінічні дослідження щодо вивчення можливого негативного впливу препарату Котеллік на фертильність не проводились. У токсикологічних дослідженнях у тварин при багаторазовому застосуванні препарату спостерігалися дегенеративні зміни в репродуктивних тканинах, у тому числі підвищення рівня апоптозу/некрозу жовтих тіл та насіннєвих бульбашок, епітеліальних клітин придатка яєчка та піхви, а також епітеліальних клітин придатка яєчка.Побічна діяКлінічні дослідження У пацієнтів з пізніми стадіями меланоми з BRAF V600 мутацією при застосуванні препарату Котеллік у комбінації з вемурафенібом медіана часу до появи перших небажаних явищ ≥3 ступеня становила 0.5 місяців. Для опису частоти небажаних реакцій використовується така класифікація: дуже часто (≥10%), часто (≥1% та Нижче представлені небажані реакції (всіх ступенів), зареєстровані при застосуванні препарату Котеллік у комбінації з вемурафенібом. Порушення з боку крові та лімфатичної системи: дуже часто – анемія. Порушення з боку органу зору: дуже часто – серозна ретинопатія (включаючи явища хоріоретинопатії та відшарування сітківки, як показник серозної ретинопатії); часто – зниження гостроти зору, розлад зору. Порушення з боку шлунково-кишкового тракту: дуже часто – діарея, нудота, блювання, стоматит. Загальні розлади та порушення у місці введення: дуже часто – пірексія, часто – озноб. Порушення з боку обміну речовин та харчування: часто – зневоднення, гіпофосфатемія, гіпонатріємія, гіперглікемія. Доброякісні, злоякісні та неуточнені новоутворення (включаючи кісти та поліпи): часто – базальноклітинний рак, шкірна плоскоклітинна карцинома*, кератоакантома*. Порушення з боку шкіри та підшкірних тканин: дуже часто – фоточутливість (включає реакції фоточутливості, сонячні опіки, сонячний дерматит, актинічний еластоз), висипання, макуло-папульозний висип, акнеіформний дерматит, гіперкератоз*. Порушення з боку судин: дуже часто – підвищення артеріального тиску, кровотеча**. Порушення з боку дихальної системи, органів грудної клітки та середостіння: часто – пневмоніт. Лабораторні та інструментальні дані: дуже часто - підвищення активності креатинфосфокінази (КФК), підвищення активності аланінамінотрансферази (АЛТ), підвищення активності аспартатамінотрансферази (ACT), підвищення активності гаммаглутамілтранспептидази, підвищення активності лужної фосфатази (ЩФ), гіпоциаль концентрації креатиніну, лімфопенії, тромбоцитопенії; часто – зниження фракції викиду, підвищення концентрації білірубіну. * Див. підрозділ "Кожна плоскоклітинна карцинома, кератоакантома та гіперкератоз". **Див. підрозділ "Кровотеча". Додаткова інформація щодо окремих небажаних реакцій Кровотеча Явлення кровотечі (всіх видів та ступенів тяжкості) частіше реєстрували при застосуванні препарату Котеллік у комбінації з вемурафенібом порівняно з контрольною групою, яка отримувала монотерапію вемурафенібом (10% порівняно з 6%). При застосуванні препарату Котеллік у комбінації з вемурафенібом спостерігалася більш висока частота внутрішньомозкових крововиливів (1% порівняно з 0%), кровотеч із шлунково-кишкового тракту (ЖКТ) (3% порівняно з 1%), кровотеч із органів репродуктивної системи (2 % порівняно з 1%) та гематурії (2% порівняно з 1%). Більшість явищ відносилися до 1 або 2 ступеня та були несерйозними (9% порівняно з 5%). Явища 3-5 ступеня розвинулися у 1% та 0,4% пацієнтів відповідно. При застосуванні препарату Котеллік у комбінації з вемурафенібом медіана часу до першої появи небажаного явища становила 2,8 місяці (діапазон від 0 до 12,7 місяців). Фоточутливість Реакції фоточутливості спостерігалися з більш високою частотою при застосуванні препарату Котеллік у комбінації з вемурафенібом порівняно з контрольною групою, яка отримувала монотерапію вемурафенібом (41% порівняно з 31%). Більшість явищ були 1 або 2 ступеня, а явища ≥3 ступеня виникали у 3% пацієнтів при застосуванні препарату Котеллік у комбінації з вемурафенібом та не спостерігалися у контрольній групі (0%). Не спостерігалося жодних закономірностей за часом до появи явищ ≥3 ступеня. При виникненні явищ фоточутливості ≥3 ступеня у пацієнтів, які отримували Котеллік у комбінації з вемурафенібом, проводили переважно місцеву терапію у поєднанні з перериванням терапії обома препаратами. Під час проведення монотерапії кобіметинібом не спостерігалося ознак фототоксичності. Шкірна плоскоклітинна карцинома, кератоакантома та гіперкератоз При застосуванні препарату Котеллік у комбінації з вемурафенібом у порівнянні з контрольною групою, що отримувала монотерапію вемурафенібом, рідше реєстрували наступні небажані явища: шкірну плоскоклітинну карциному (всіх ступенів: 3% порівняно з 11%), кератоакантому (всіх 1 8%), гіперкератоз (всіх ступенів: 10% порівняно з 29%). Серозна ретинопатія У пацієнтів, які отримували препарат Котеллік, спостерігалися випадки серозної ретинопатії. Пацієнтам, у яких вперше виникли чи посилилися порушення зору, рекомендовано пройти офтальмологічний обстеження. Ведення пацієнтів із серозною ретинопатією включає переривання лікування, зниження дози або припинення терапії. Оклюзія вен сітківки відзначалася в одного пацієнта в кожній із груп терапії (у групі застосування препарату Котеллік у комбінації з вемурафенібом та в контрольній групі, яка отримувала монотерапію вемурафенібом). Дисфункція лівого шлуночка У пацієнтів, які отримували Котеллік, відзначалося зниження фракції викиду лівого шлуночка (ФВЛШ) щодо вихідного показника. ФВЛШ необхідно оцінювати перед початком лікування для визначення вихідних значень, потім через місяць лікування і щонайменше кожні 3 місяці або за клінічними показаннями до припинення лікування. Ведення пацієнтів зі зниженням ФВЛШ щодо вихідного рівня включає переривання лікування, зниження дози або припинення терапії. Відхилення лабораторних показників Відхилення лабораторних показників функції печінки У пацієнтів, які отримували Котеллік у комбінації з вемурафенібом, відзначалися відхилення лабораторних показників функції печінки, особливо АЛТ, ACT, ЛФ. Лабораторні показники функції печінки необхідно оцінювати перед початком комбінованого лікування щомісяця під час лікування або частіше (за наявності клінічних показань). Підвищення активності КФК Безсимптомне підвищення активності КФК крові частіше зустрічалося при застосуванні препарату Котеллік у комбінації з вемурафенібом у порівнянні з контрольною групою, яка отримувала монотерапію вемурафенібом (всіх ступенів: 65% порівняно з 13%; 3-4 ступеня: 11% порівняно зВзаємодія з лікарськими засобамиВплив супутніх лікарських препаратів на кобіметініб Інгібітори ізоферменту CYP3A Кобіметініб метаболізується за участю ізоферменту CYP3A. У здорових осіб у присутності потужного інгібітора ізоферменту CYP3A (ітраконозолу) AUC кобіметинібу збільшується приблизно в 7 разів. Існує ймовірність, що магнітуда взаємодії буде нижчою. Потужні інгібітори ізоферменту CYP3A Слід уникати одночасного застосування потужних інгібіторів ізоферменту CYP3A під час лікування кобіметинібом. Приклади потужних інгібіторів ізоферменту CYP3A включають, але не обмежуються ритонавіром, кобіцистатом, тіломпревіром, лопінавіром, ітраконазолом, вориконазолом, кларитроміцином, телитроміцином, позаконазолом, нефазодоном і грейпфрутовим. Якщо одночасного застосування з сильним інгібітором ізоферменту CYP3A не можна уникнути, слід ретельно стежити за безпекою пацієнтів. У разі короткочасного (≤7 днів) застосування потужних інгібіторів ізоферменту CYP3A слід розглянути можливість припинення лікування кобіметинібом під час застосування такого інгібітору. Помірні інгібітори ізоферменту CYP3A Слід бути обережними при застосуванні кобіметинібу одночасно з помірними інгібіторами ізоферменту CYP3A. Приклади помірних інгібіторів ізоферменту CYP3A включають, але не обмежуються аміодароном, еритроміцином, флуконазолом, міконазолом, дилтіаземом, верапамілом, делавірдіном, ампренавіром, фосампренавіром, іматинібом. При одночасному застосуванні кобіметинібу з помірним інгібітором ізоферменту CYP3A слід ретельно стежити за безпекою пацієнтів. Слабкі інгібітори ізоферменту CYP3A Кобіметініб можна застосовувати одночасно із слабкими інгібіторами ізоферменту CYP3A без корекції дози. Індуктори ізоферменту CYP3A Одночасне застосування кобіметинібу з потужним індуктором ізоферменту CYP3A не оцінювалося в ході клінічного дослідження, проте можливе зниження експозиції кобіметинібу. Таким чином, одночасного застосування помірних та потужних індукторів ізоферменту CYP3A (наприклад, карбамазепін, рифампіцин, фенітоїн та звіробій продірявлений) слід уникати. Необхідно розглянути можливість застосування препаратів з відсутньою або мінімальною індукцією ізоферменту CYP3A як альтернативу. Ефективність може бути знижена, оскільки існує ймовірність значного зменшення концентрації кобіметинібу при одночасному застосуванні з помірними та потужними індукторами ізоферменту CYP3A. Інгібітори Р-глікопротеїну Кобіметініб є субстратом Р-глікопротеїну. При одночасному застосуванні з інгібіторами Р-глікопротеїну, такими як циклоспорин і верапаміл, існує можливість підвищення концентрації кобіметинібу в плазмі крові. Препарати, що знижують кислотність Одночасне застосування інгібітору протонного насоса не впливає на фармакокінетику кобіметінібу. Для визначення впливу підвищення pH шлунка кобіметініб призначали здоровим особам разом із рабепразолом (інгібітором протонного насоса). При цьому підвищення pH шлунка не впливало на всмоктування кобіметінібу. Вплив кобіметинібу на супутні лікарські препарати Субстрати ізоферментів CYP3A та CYP2D6 Клінічне дослідження лікарських взаємодій у пацієнтів з онкологічним захворюванням показало, що у присутності кобіметинібу концентрації мідазоламу (чутливого субстрату CYP3A) та декстрометорфану (чутливого субстрату CYP2D6) у плазмі крові не змінювалися. Субстрати ізоферменту CYP1A2 Кобіметиніб є потенційним індуктором ізоферменту CYP1А2 in vitro, таким чином, можливе зниження експозиції субстратів даного ферменту, наприклад, теофіліну. Клінічних досліджень лікарських взаємодій з оцінки клінічної значимості даного явища не проводилося. Субстрати BCRP (breast cancer resistance protein – білок стійкості раку молочної залози) Кобіметініб є помірним інгібітором BCRP in vitro. Клінічних досліджень лікарських взаємодій для оцінки цього явища не проводилося. Клінічна значимість інгібування інтестинального BCRP може бути виключена. Інші протипухлинні препарати Вемурафеніб У пацієнтів з неоперабельною або метастатичною меланомою не відзначено клінічно значущих лікарських взаємодій між препаратом Котеллік та вемурафенібом, таким чином корекція дози не рекомендується. Вплив кобіметинібу на транспортні системи лікарських препаратів У дослідженнях in vitro показано, що кобіметініб не є субстратом транспортних білків ОАТР1В1, ОАТР1В3 та ОСТ1, будучи слабким інгібітором цих транспортних білків. Клінічна значимість цих даних встановлено.Спосіб застосування та дозиЛікування препаратом Котеллік повинен починати та контролювати лікар, який має досвід лікування пацієнтів з онкологічними захворюваннями. Перед застосуванням Котелліку в комбінації з вемурафенібом повинен бути проведений валідований тест на наявність мутації BRAF V600. При застосуванні препарату Котеллік у комбінації з вемурафенібом див. також інструкцію з медичного застосування вемурафенібу. Стандартний режим дозування Рекомендована доза Котелліку становить 60 мг (три таблетки по 20 мг) внутрішньо, один раз на добу. Препарат Котеллік слід приймати 28-денними циклами. Кожна доза препарату Котеллік складається з трьох таблеток по 20 мг (60 мг), і її слід приймати один раз на добу протягом 21 дня (період лікування з 1 по 21 день) з наступною 7-денною перервою в лікуванні препаратом Котеллік (перерва в лікування з 22 по 28 день). Кожну дозу (три таблетки по 20 мг на один прийом) можна приймати незалежно від їди. Таблетки препарату Котеллік слід ковтати повністю, запиваючи водою. Тривалість лікування Лікування препаратом Котеллік слід продовжувати доти, доки зберігається користь для пацієнта або до розвитку непереносимої токсичності. Затримка прийому або пропущені дози Якщо до прийому наступної дози залишилося 12 і більше годин, слід прийняти препарат Котеллік з метою збереження схеми лікування з прийомом один раз на добу. Якщо до прийому наступної дози залишилося менше 12 годин, лікування слід продовжити наступного дня згідно з призначеною схемою. Блювота У разі виникнення блювоти після прийому препарату Котеллік не слід приймати додаткову дозу препарату того ж дня, а слід продовжити лікування згідно з призначеною схемою наступного дня. Зміна дози Зміна дози препарату Котеллік має ґрунтуватися на оцінці лікарем безпеки та переносимості препарату у конкретного пацієнта. Якщо пропуск дози пов'язаний з появою токсичності, пропущені дози не слід відновлювати. Після зниження дози препарату не слід знову підвищувати дозу. Зміна дози Котелліку не залежить від зміни дози вемурафенібу. Рішення про зменшення дози одного або обох препаратів має ґрунтуватися на клінічній оцінці. У таблиці 1 наведено загальні рекомендації щодо зміни дози препарату Котеллік. Таблиця 1. Загальні рекомендації щодо зниження дози препарату Котеллік. Ступінь тяжкості небажаних явищ* Рекомендована доза препарату Котеллік Ступінь 1 або ступінь 2 (перенесена) Без зниження дози. Ступінь 2 (нестерпний) або ступінь 3/4 1 прояв Переривання лікування до ≤1 ступеня тяжкості небажаних явищ, відновлення терапії у дозі 40 мг один раз на добу 2 прояв Переривання лікування до ≤1 ступеня тяжкості небажаних явищ, відновлення терапії у дозі 20 мг один раз на добу 3 прояв Розглянути припинення лікування * Ступінь тяжкості небажаних явищ відповідно до Загальних критеріїв токсичності небажаних явищ Національного інституту раку США, версія 4,0 Зміна дози у разі розвитку окремих небажаних реакцій Дисфункція лівого шлуночка Слід розглянути необхідність повного припинення лікування Котелліком, якщо симптоми з боку серця пов'язані з лікуванням даним препаратом і в тому випадку, якщо не відбулося поліпшення після тимчасового переривання лікування. Таблиця 2. Зміна дози препарату Котеллік у пацієнтів із зниженням фракції викиду лівого шлуночка (ФВЛШ) порівняно з вихідним показником. Пацієнт Показник ФВЛШ Рекомендована зміна дози препарату Котеллік Показник ФВЛШ після перерви у лікуванні Рекомендована добова доза препарату Котеллік Без симптомів ≥50% (або 40-49% та зниження <10% абсолютного показника від вихідного рівня) Продовжити лікування у поточній дозі - - <40% (або 40-49% та зниження ≥ 10% абсолютного показника від вихідного рівня) Переривання лікування на 2 тижні зниження <10% абсолютного показника від вихідного рівня 1 поява: 40 мг 2 поява: 20 мг 3 поява: повне скасування <40% (або зниження ≥10% абсолютного показника від вихідного рівня) Повне скасування Із симптомами Не застосовується Переривання лікування на 4 тижні Без симптомів та зниження <10% абсолютного показника від вихідного рівня 1 поява: 40 мг 2 поява: 20 мг 3 поява: повне скасування Без симптомів та <40% (або зниження ≥10% абсолютного показника від вихідного рівня) Повне скасування Із симптомами, незалежно від ФВЛШ Повне скасування При зміні дози Котелліку лікування вемурафенібом може бути продовжено (за наявності клінічних показань). Підвищення активності креатинфосфокінази У пацієнтів з безсимптомним підвищенням активності креатинфосфокінази (КФК) немає потреби змінювати дозу препарату Котеллік або переривати його прийом. Зміна дози препарату Котеллік при застосуванні у комбінації з вемурафенібом Відхилення лабораторних показників функції печінки У разі відхилень лабораторних показників функції печінки 1 та 2 ступеня тяжкості лікування препаратом Котеллік та вемурафенібом слід продовжити у призначеній дозі. 3 ступінь тяжкості: слід продовжити лікування препаратом Котеллік у призначеній дозі. Доза вемурафенібу може бути знижена відповідно до клінічних показань (див. інструкцію з медичного застосування вемурафенібу). 4 ступінь тяжкості: лікування препаратом Котеллік та вемурафенібом слід перервати. Якщо відхилення лабораторних показників функції печінки зменшилися до ≤1 ступеня тяжкості протягом 4 тижнів, застосування препарату Котеллік слід відновити у дозі, зниженій на 20 мг, застосування вемурафенібу слід відновити відповідно до клінічних показань згідно з інструкцією з медичного застосування вемурафенібу. Лікування препаратом Котеллік та вемурафенібом слід припинити, якщо відхилення лабораторних показників функції печінки не зменшилися до ≤1 ступеня тяжкості протягом 4 тижнів або відхилення лабораторних показників функції печінки 4 ступеня тяжкості відновлюються після початкового покращення. Фоточутливість Ведення пацієнтів з фоточутливістю ≤2 ступеня тяжкості (переносимої) має включати підтримуючу терапію. У разі розвитку фоточутливості 2 ступеня (непереносимої) або ≥3 ступеня лікування препаратом Котеллік та вемурафенібом необхідно перервати до зменшення тяжкості симптомів до ≤1 ступеня. Лікування може бути відновлено без зміни дози Котелліку. Дозу вемурафенібу необхідно знизити згідно з інструкцією із застосування вемурафенібу (див. інструкцію з медичного застосування вемурафенібу). Висип Висипання може виникати як на фоні лікування препаратом Котеллік, так і вемурафенібом. При розвитку висипу лікування препаратом Котеллік та/або вемурафенібом може бути тимчасово перервано та/або можливе зниження дози одного з препаратів або обох препаратів за клінічними показаннями. Додатково, при розвитку висипки: ≤2 ступеня (переносимого) - ведення пацієнтів має включати підтримуючу терапію, лікування препаратом Котеллік може бути продовжено без зміни дози; 2 ступеня (непереносимого) або ≥3 ступеня: акнеіформний висип: необхідно дотримуватися загальних рекомендацій щодо зміни дози препарату Котеллік згідно з таблицею 1; лікування вемурафенібом може бути продовжено за зміни схеми терапії препаратом Котеллік (за наявності клінічних показань); неакнеіформний або макуло-папульозний висип: лікування препаратом Котеллік може бути продовжено без зміни дози (за клінічними показаннями); лікування вемурафенібом може бути тимчасово перервано та/або його доза знижена. Оклюзія вен сітківки У разі виникнення оклюзії вен сітківки терапія препаратом Котеллік має бути припинена. Дозування в особливих випадках Пацієнти похилого віку Корекція дози Котелліку у пацієнтів віком ≥65 років не потрібна. Пацієнти дитячого віку та підлітки Безпека та ефективність препарату Котеллік у дітей та підлітків ( Пацієнти з порушенням функції нирок За даними популяційного фармакокінетичного аналізу, у пацієнтів з порушенням функції нирок легкого або помірного ступеня корекції дози не потрібно. Безпечність та ефективність препарату Котеллік у пацієнтів з тяжким порушенням функції нирок не встановлено. Порушення функції печінки Безпечність та ефективність препарату Котеллік у пацієнтів з порушенням функції печінки не встановлені. У пацієнтів з легким ступенем печінкової недостатності корекція дози не потрібна на підставі результатів популяційного фармакокінетичного аналізу.ПередозуванняУ клінічних дослідженнях немає випадків передозування. У разі передбачуваного передозування лікування препаратом Котеллік слід призупинити та розпочати проведення підтримуючої терапії. Специфічного антидоту, який можна було б використовувати у випадках передозування Котелліком, не існує.Запобіжні заходи та особливі вказівкиПри застосуванні Котелліку в комбінації з вемурафенібом необхідно також уважно ознайомитися з інструкцією з медичного застосування вемурафенібу. Котеллік у комбінації з вемурафенібом у пацієнтів із прогресуванням захворювання при застосуванні інгібітору BRAF Дані щодо застосування препарату Котеллік у комбінації з вемурафенібом у пацієнтів з прогресуванням захворювання, які раніше застосовували інгібітор BRAF, обмежені. Згідно з цими даними, ефективність комбінації у таких пацієнтів буде нижчою. Таким чином, слід розглянути альтернативні способи лікування перед застосуванням комбінації у цій групі пацієнтів, які раніше застосовували інгібітор BRAF. Послідовність лікування після прогресування захворювання при застосуванні інгібітору BRAF не встановлено. Препарат Котеллік у комбінації з вемурафенібом у пацієнтів із метастазами головного мозку Оцінки безпеки та ефективності лікування препаратом Котеллік у комбінації з вемурафенібом у пацієнтів з метастатичною меланомою (за наявності BRAF V600 мутації) з метастазами у головний мозок не проводилося. Інтракраніальна активність кобіметинібу наразі невідома. Серозна ретинопатія У пацієнтів, які отримували інгібітори МЕК, включаючи Котеллік, спостерігалися випадки серозної ретинопатії (скупчення рідини в межах шарів сітківки). Більшість явищ включали хоріоретинопатію або відшарування сітківки. Медіана часу до появи серозної ретинопатії становить 1 місяць (діапазон 0-9 місяців). Більшість явищ, що спостерігалися в клінічних дослідженнях, вирішилися, або їхня тяжкість зменшилася до безсимптомного перебігу 1 ступеня після переривання лікування або зниження дози. Необхідно проводити оцінку нових симптомів або посилення розладу зору у пацієнтів під час кожного візиту. Пацієнтам, у яких вперше виникли або посилилися розлади зору, рекомендовано пройти офтальмологічний обстеження. У разі діагностики серозної ретинопатії слід призупинити лікування препаратом Котеллік до полегшення тяжкості зорових симптомів. Дисфункція лівого шлуночка У пацієнтів, які отримують Котеллік, відзначалося зниження фракції викиду лівого шлуночка (ФВЛШ) щодо вихідного показника. Медіана часу до виникнення явищ становить 4 місяці (1-7 місяців). ФВЛШ необхідно оцінювати перед початком лікування для визначення вихідних значень, потім через місяць лікування і щонайменше кожні 3 місяці або за клінічними показаннями до припинення лікування. Ведення пацієнтів зі зниженням ФВЛШ щодо вихідного рівня включає переривання лікування, зниження дози або припинення терапії. У всіх пацієнтів, яким було відновлено лікування препаратом Котеллік у нижчій дозі, необхідно проводити вимірювання ФВЛШ по можливості через 2 тижні, 4 тижні, 10 тижнів та 16 тижнів, а потім за клінічними показаннями. Пацієнти з вихідним значенням ФВЛШ нижче за нижню межу норми установи або нижче 50% не вивчалися. Відхилення лабораторних показників функції печінки При застосуванні препарату Котеллік у комбінації з вемурафенібом, а також при монотерапії вемурафенібом (див. інструкцію з медичного застосування вемурафенібу), можуть спостерігатися відхилення лабораторних показників функції печінки. У пацієнтів, які отримували Котеллік у комбінації з вемурафенібом, відзначалися відхилення лабораторних показників функції печінки, особливо АЛТ, ACT, ЛФ. Відхилення показників функції печінки слід оцінювати за результатами лабораторних досліджень перед початком комбінованого лікування, щомісяця під час лікування або частіше (за наявності клінічних показань). Ведення пацієнтів з відхиленнями лабораторних показників функції печінки 3-го ступеня тяжкості включає переривання лікування або зниження дози вемурафенібу. Ведення пацієнтів з відхиленнями лабораторних показників функції печінки 4 ступеня тяжкості включає переривання, зниження дози або припинення терапії як препаратом Котеллік, так і вемурафенібом. Діарея У пацієнтів, які отримували лікування препаратом Котеллік, були відмічені випадки тяжкої діареї та діареї ≥3 ступеня тяжкості. Ведення пацієнтів з діареєю включає застосування протидіарейних засобів і підтримуючу терапію. При діареї ≥3 ступеня тяжкості, що виникла, незважаючи на застосування підтримуючої терапії, слід призупинити лікування препаратом Котеллік та вемурафенібом доти, доки не буде відмічено зниження тяжкості явища до ≤1 ступеня. При відновленні діареї ≥3 ступеня тяжкості необхідно зменшити дозу препарату Котеллік та вемурафенібу. Непереносимість лактози Препарат містить лактозу. Пацієнтам з рідкісною спадковою непереносимістю галактози, вродженою недостатністю лактази або глюкозо-галактозною мальабсорбцією слід проконсультуватися з лікарем для індивідуального обговорення випадків, коли користь перевершує ризики. Взаємодія з інгібіторами ізоферменту CYP3A Слід уникати одночасного застосування препарату Котеллік із потужними інгібіторами ізоферменту CYP3A. Слід бути обережними при застосуванні кобіметинібу одночасно з помірними інгібіторами ізоферменту CYP3A. Якщо одночасного застосування з потужним або помірним інгібітором ізоферменту CYP3A не можна уникнути, слід ретельно стежити за безпекою пацієнтів, а також при необхідності знижувати дозу згідно з рекомендаціями, наведеними в таблиці 1. Знищення невикористаного препарату або препарату з терміном придатності, що минув, повинно проводитися відповідно до локальних вимог. Вплив на здатність до керування автотранспортом та управління механізмами Дослідження впливу препарату Котеллік на здатність до керування транспортними засобами та роботу з машинами та механізмами не проводилися. Під час проведення клінічних досліджень у пацієнтів, які отримували Котеллік, були зареєстровані розлади зору. Пацієнтам у разі порушень з боку зору не слід керувати транспортними засобами та працювати з машинами та механізмами без консультації лікаря.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептом
Склад, форма випуску та упаковкаСилікон.Опис лікарської формиKelo-Cote являє собою гель на основі силікону для запобігання утворенню, зменшення виразності келоїдних та гіпертрофічних рубців, отриманих в результаті хірургічних втручань, травм, ран та опіків, а також для покращення естетичного виду рубців.ХарактеристикаKelo-Cote швидко висихає, утворюючи на шкірі еластичну, водостійку та повітропроникну плівку. При нанесенні гелю Kelo-Cote на рубець, гель на місці нанесення утворює захисний бар'єр, що сприяє зменшенню хімічної, фізичної та бактеріальної дії, при цьому зберігається водний баланс шкіри. Це створює умови для нормалізації процесів синтезу колагену та не дозволяє рубцю розростатися, а також покращує зовнішній вигляд самого рубця. Після застосування засобу Kelo-Cote зменшується виразність келоїдних та гіпертрофічних рубців, свербіж та дискомфорт, відновлюється колір; рубці розгладжуються і пом'якшуються, покращується їхній естетичний вигляд. Відповідно до Міжнародних клінічних рекомендацій з терапії рубців силікон був рекомендований як перша лінія терапії для всіх видів рубців та обов'язковий елемент для запобігання утворенню та зменшення виразності келоїдних та гіпертрофічних рубців. Kelo-Cote може наноситися на шкіру в області суглобів, на місця згину, на область росту волосся, на рубцеві поверхні великих розмірів, що є наслідком опіків та великих травм. Kelo-Cote можна використовувати з пов'язками, що давлять, або іншими допоміжними засобами.ІнструкціяПереконайтеся, що шкіра на ураженій ділянці чиста та суха. Нанесіть Kelo-Cote на уражену ділянку суцільним тонким шаром і дайте йому висохнути. Наносите Kelo-Cote двічі на день. Для досягнення максимального ефекту Kelo-Cote має контактувати зі шкірою 24 години на добу. Після повного висихання гелю можна наносити сонцезахисні та косметичні засоби, а також використовувати пов'язки, що тиснуть. Якщо Kelo-Cote не висохне протягом 4-5 хвилин, можливо, гель був нанесений товстим шаром. У такому випадку акуратно видаліть надлишки і дайте гелю, що залишився, висохнути. Рекомендована тривалість застосування гелю – не менше ніж 60-90 днів. Для великих і застарілих рубців може знадобитися триваліший курс застосування. Подальше застосування гелю рекомендовано, якщо після перших 90 днів застосування покращення зовнішнього вигляду рубця продовжує спостерігатися. Час повного висихання гелю Kelo-Cote залежить від різниці температури гелю та шкіри. Щоб скоротити час висихання у жаркому кліматі, зберігайте Kelo-Cote у холодильнику. Щоб скоротити час висихання гелю за холодної погоди, можна використовувати фен для волосся (середній рівень температури).Протипоказання до застосуванняГель Kelo-Cote призначений для запобігання утворенню, зменшення виразності та поліпшення естетичного вигляду як старих, так і свіжих рубців (включаючи гіпертрофічні та келоїдні), отриманих внаслідок хірургічних втручань, травм, ран та опіків. Kelo-Cote підходить для дітей та людей з чутливою шкірою.Запобіжні заходи та особливі вказівкиУникайте попадання в очі, на слизові оболонки та відкриті рани. Не слід застосовувати Kelo-Cote при дерматологічних захворюваннях, що порушують цілісність покриву шкіри. У випадку неповного висихання Kelo-Cote на одязі можуть залишитись плями. Тільки для зовнішнього застосування. У разі виникнення подразнення на шкірі припиніть використання гелю та зверніться до лікаря.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Активна речовина: 100 мг лозартану калію. Допоміжні речовини: целюлоза мікрокристалічна – 105 мг, лактози моногідрат – 51 мг, крохмаль прежелатинізований – 41.9 мг, магнію стеарат – 2.1 мг. Склад оболонки: ;гіпролоза (з 0.3% кремнію діоксиду) - 3.6 мг, гіпромелоза - 3.6 мг, титану діоксид - 1.8 мг, віск карнауби - 0.05 мг. 14 шт. - блістери (2) - пачки картонні.Опис лікарської формиТаблетки, покриті плівковою оболонкою; білого кольору, краплевидної форми, з гравіюванням "960" на одному боці і гладкі з іншого боку.Фармакотерапевтична групаАнтигіпертензивний засіб. Є непептидним блокатором рецепторів ангіотензину ІІ. Має високу селективність і афінітет до рецепторів типу AT1 (за участю яких реалізуються основні ефекти ангіотензину II). Блокуючи зазначені рецептори, лозартан попереджає та усуває судинозвужувальну дію ангіотензину II, його стимулюючий вплив на секрецію альдостерону наднирниками та деякі інші ефекти ангіотензину II. Характеризується тривалим дією (24 год і більше), що з утворенням його активного метаболіту.ФармакокінетикаПісля прийому внутрішньо лозартан швидко абсорбується із ШКТ. Біодоступність становить близько 33%. Метаболізується при "першому проходженні" через печінку з утворенням карбоксильного метаболіту, який має більш виражену фармакологічну активність, ніж лозартан, та ряд неактивних метаболітів. C max ;в плазмі крові лозартану та активного метаболіту досягається через 1 год і 3-4 год відповідно. Зв'язування з білками плазми лозартану та активного метаболіту високе – понад 98%. T1/2 ;лозартану та активного метаболіту в кінцевій фазі становить близько 1.5-2.5 год та 3-9 год, відповідно. Лозартан виводиться із сечею та з калом (з жовчю) у незміненому вигляді та у вигляді метаболітів. Близько 35% виводиться із сечею і близько 60% – з калом.Клінічна фармакологіяАнтагоніст рецепторів ангіотензину ІІ.Показання до застосуванняАртеріальна гіпертензія. Зниження ризику асоційованої серцево-судинної захворюваності та смертності у пацієнтів з артеріальною гіпертензією та гіпертрофією лівого шлуночка, що проявляється зниженням сукупності частоти серцево-судинної смертності, частоти інсульту та інфаркту міокарда. Захист нирок у пацієнтів з цукровим діабетом 2 типу з протеїнурією - уповільнення прогресування ниркової недостатності, що виявляється зниженням частоти гіперкреатинінемії, частоти розвитку термінальної стадії ХНН, що потребує проведення гемодіалізу або трансплантації нирок, показників смертності, а також зниження протеїнурії. Хронічна серцева недостатність (у складі комбінованої терапії, при непереносимості чи неефективності терапії інгібіторами АПФ).Протипоказання до застосуванняВагітність, лактація, дитячий та підлітковий вік до 18 років, підвищена чутливість до лозартану.Вагітність та лактаціяПротипоказаний до застосування при вагітності та в період лактації. Застосування у дітей Безпека та ефективність застосування лозартану у дітей не встановлені.Побічна діяЗ боку серцево-судинної системи: запаморочення, ортостатична гіпотензія. З боку обміну речовин: гіперкаліємія. Алергічні реакції: ангіоневротичний набряк (включаючи набряки обличчя, губ, глотки та/або язика), кропив'янка. З боку травної системи: діарея, підвищення активності АЛТ. З боку ЦНС: головний біль. Дерматологічні реакції:; свербіж. Інші: порушення функції нирок, міалгії.Взаємодія з лікарськими засобамиПри одночасному застосуванні з діуретиками у високих дозах можлива гіпотензія. При одночасному застосуванні з препаратами калію, калійзберігаючими діуретиками підвищується ризик гіперкаліємії. При одночасному застосуванні з індометацином можливе зменшення ефективності лозартану. Є повідомлення розвитку інтоксикації літієм при одночасному застосуванні з літію карбонатом. При одночасному застосуванні з орлістатом зменшується антигіпертензивна дія лозартану, що може призвести до значного підвищення артеріального тиску, розвитку гіпертонічного кризу. При одночасному застосуванні з рифампіцином підвищується кліренс лозартану та зменшується його ефективність.Спосіб застосування та дозиСередня доза для внутрішнього прийому - 50 мг 1 раз на добу. При необхідності доза може бути зменшена до 25 мг на добу або збільшена до 100 мг на добу, в останньому випадку можливе застосування 2 рази на добу.Запобіжні заходи та особливі вказівкиЗ обережністю слід застосовувати при артеріальній гіпотензії, зниженні ОЦК, порушеннях водно-електролітного балансу, двосторонньому стенозі ниркових артерій або стенозі артерії єдиної нирки, при нирковій/печінковій недостатності. Пацієнтам, які мають дефіцит рідини та/або натрію, перед початком лікування необхідно провести корекцію водно-електролітних порушень або застосовувати нижчу початкову дозу. У пацієнтів з дегідратацією (наприклад, які отримують лікування діуретиками у високих дозах) на початку лікування лозартаном може виникати симптоматична гіпотензія. При порушеннях функції нирок може знадобитися зменшення дози лозартану. У пацієнтів із вказівками в анамнезі на захворювання печінки лозартан слід застосовувати у низьких дозах. При цирозі печінки концентрація лозартану у плазмі значно збільшується. У період лікування слід регулярно контролювати рівень калію в крові, особливо у пацієнтів похилого віку, у разі порушення функції нирок. Слід уникати одночасного застосування лозартану з калійзберігаючими діуретиками. Безпека та ефективність застосування лозартану у дітей не встановлені.Умови відпустки з аптекЗа рецептом
Склад, форма випуску та упаковкаПігулки - 1 таб. Активна речовина: 50 мг лозартан калію. Допоміжні речовини: целюлоза мікрокристалічна, моногідрат лактози, крохмаль прежелатинізований, магнію стеарат. Склад оболонки: ;гіпролоза (з 0.3% кремнію діоксиду), гіпромелоза, титану діоксид, віск карнауби. 14 шт. - блістери (1) - пачки картонні.Опис лікарської формиТаблетки, покриті плівковою оболонкою; білого кольору, краплевидної форми, з гравіюванням "960" на одному боці і гладкі з іншого боку.Фармакотерапевтична групаАнтигіпертензивний засіб. Є непептидним блокатором рецепторів ангіотензину ІІ. Має високу селективність і афінітет до рецепторів типу AT1 (за участю яких реалізуються основні ефекти ангіотензину II). Блокуючи зазначені рецептори, лозартан попереджає та усуває судинозвужувальну дію ангіотензину II, його стимулюючий вплив на секрецію альдостерону наднирниками та деякі інші ефекти ангіотензину II. Характеризується тривалим дією (24 год і більше), що з утворенням його активного метаболіту.ФармакокінетикаПісля прийому внутрішньо лозартан швидко абсорбується із ШКТ. Біодоступність становить близько 33%. Метаболізується при "першому проходженні" через печінку з утворенням карбоксильного метаболіту, який має більш виражену фармакологічну активність, ніж лозартан, та ряд неактивних метаболітів. C max ;в плазмі крові лозартану та активного метаболіту досягається через 1 год і 3-4 год відповідно. Зв'язування з білками плазми лозартану та активного метаболіту високе – понад 98%. T1/2 ;лозартану та активного метаболіту в кінцевій фазі становить близько 1.5-2.5 год та 3-9 год, відповідно. Лозартан виводиться із сечею та з калом (з жовчю) у незміненому вигляді та у вигляді метаболітів. Близько 35% виводиться із сечею і близько 60% – з калом.Клінічна фармакологіяАнтагоніст рецепторів ангіотензину ІІ.Показання до застосуванняАртеріальна гіпертензія. Зниження ризику асоційованої серцево-судинної захворюваності та смертності у пацієнтів з артеріальною гіпертензією та гіпертрофією лівого шлуночка, що проявляється зниженням сукупності частоти серцево-судинної смертності, частоти інсульту та інфаркту міокарда. Захист нирок у пацієнтів з цукровим діабетом 2 типу з протеїнурією - уповільнення прогресування ниркової недостатності, що виявляється зниженням частоти гіперкреатинінемії, частоти розвитку термінальної стадії ХНН, що потребує проведення гемодіалізу або трансплантації нирок, показників смертності, а також зниження протеїнурії. Хронічна серцева недостатність (у складі комбінованої терапії, при непереносимості чи неефективності терапії інгібіторами АПФ).Протипоказання до застосуванняВагітність, лактація, дитячий та підлітковий вік до 18 років, підвищена чутливість до лозартану.Вагітність та лактаціяПротипоказаний до застосування при вагітності та в період лактації. Застосування у дітей Безпека та ефективність застосування лозартану у дітей не встановлені.Побічна діяЗ боку серцево-судинної системи: запаморочення, ортостатична гіпотензія. З боку обміну речовин: гіперкаліємія. Алергічні реакції: ангіоневротичний набряк (включаючи набряки обличчя, губ, глотки та/або язика), кропив'янка. З боку травної системи: діарея, підвищення активності АЛТ. З боку ЦНС: головний біль. Дерматологічні реакції:; свербіж. Інші: порушення функції нирок, міалгії.Взаємодія з лікарськими засобамиПри одночасному застосуванні з діуретиками у високих дозах можлива гіпотензія. При одночасному застосуванні з препаратами калію, калійзберігаючими діуретиками підвищується ризик гіперкаліємії. При одночасному застосуванні з індометацином можливе зменшення ефективності лозартану. Є повідомлення розвитку інтоксикації літієм при одночасному застосуванні з літію карбонатом. При одночасному застосуванні з орлістатом зменшується антигіпертензивна дія лозартану, що може призвести до значного підвищення артеріального тиску, розвитку гіпертонічного кризу. При одночасному застосуванні з рифампіцином підвищується кліренс лозартану та зменшується його ефективність.Спосіб застосування та дозиСередня доза для внутрішнього прийому - 50 мг 1 раз на добу. При необхідності доза може бути зменшена до 25 мг на добу або збільшена до 100 мг на добу, в останньому випадку можливе застосування 2 рази на добу.Запобіжні заходи та особливі вказівкиЗ обережністю слід застосовувати при артеріальній гіпотензії, зниженні ОЦК, порушеннях водно-електролітного балансу, двосторонньому стенозі ниркових артерій або стенозі артерії єдиної нирки, при нирковій/печінковій недостатності. Пацієнтам, які мають дефіцит рідини та/або натрію, перед початком лікування необхідно провести корекцію водно-електролітних порушень або застосовувати нижчу початкову дозу. У пацієнтів з дегідратацією (наприклад, які отримують лікування діуретиками у високих дозах) на початку лікування лозартаном може виникати симптоматична гіпотензія. При порушеннях функції нирок може знадобитися зменшення дози лозартану. У пацієнтів із вказівками в анамнезі на захворювання печінки лозартан слід застосовувати у низьких дозах. При цирозі печінки концентрація лозартану у плазмі значно збільшується. У період лікування слід регулярно контролювати рівень калію в крові, особливо у пацієнтів похилого віку, у разі порушення функції нирок. Слід уникати одночасного застосування лозартану з калійзберігаючими діуретиками. Безпека та ефективність застосування лозартану у дітей не встановлені.Умови відпустки з аптекЗа рецептомВідео на цю тему
19 350,00 грн
144,00 грн
Склад, форма випуску та упаковкаЛіофілізат для приготування розчину для підшкірного введення. - 1 фл. Діюча речовина: секукінумаб - 150,00 мг; Допоміжні речовини: сахароза – 92,43 мг; гістидин/гістидину гідрохлориду моногідрат - 4,656 мг; полісорбат-80 – 0,60 мг. Ліофілізат для приготування розчину для підшкірного введення, по 150 мг у флакон з безбарвного скла класу I місткістю 6 мл, закупореному сірою гумовою пробкою, обкатаною алюмінієвим ковпачком з кришкою з поліпропілену. По 1 флакону разом із інструкцією з медичного застосування в пачку.Опис лікарської формиБілий порошок або аморфна маса.Фармакотерапевтична групаМеханізм дії Секукінумаб являє собою повністю людське антитіло (імуноглобулін G1 (IgG1), яке селективно зв'язується і нейтралізує прозапальний цитокін - інтерлейкін-17А (ІЛ-17А). Секукінумаб надає направлену дію на ІЛ-17 та інгібування його взаємодії з різними типами клітин, включаючи кератиноцити і синовіоцити.В результаті цього секукинумаб інгібує вивільнення прозапальних цитокінів, хемокінів і медіаторів пошкодження тканин, і знижує внесок ІЛ-17А в аутоімунні та запальні захворювання.У клінічно значущих концентраціях Прямим наслідком лікування секукинумабом є зниження вираженості почервоніння, ущільнення та лущення, що є результатом псоріатичного ураження. ІЛ-17A є природним цитокіном, який бере участь у нормально протікаючих реакціях запалення та імунної відповіді. ІЛ-17А відіграє ключову роль у патогенезі розвитку бляшкового псоріазу, псоріатичного артриту та анкілозуючого спондиліту. Підвищення концентрації ІЛ-17А, що продукується лімфоцитами та вродженими імунними клітинами, було виявлено в крові та уражених ділянках шкіри у пацієнтів з бляшковим псоріазом, псоріатичним артритом та анкілозуючим спондилітом. Продукція ІЛ-17А є високою у ураженій шкірі порівняно з неушкодженою шкірою у пацієнтів з бляшковим псоріазом. У синовіальній рідині у пацієнтів з псоріатичним артритом та в субхондральному кістковому мозку кісток фасеткових суглобів у пацієнтів з анкілозуючим спондилітом виявляється висока концентрація клітин, що продукують ІЛ-17А. ІЛ-17А також сприяє розвитку запалення тканин, інфільтрації нейтрофілами, деструкції кісток і тканин, а також ремоделюванню тканин, включаючи ангіогенез та фіброз.ФармакокінетикаВсмоктування Після одноразового підшкірного введення дози 150 мг або 300 мг при бляшковому псоріазі, максимальна концентрація секукінумабу в сироватці крові становила відповідно 13,7±4,8 мкг/мл або 27,3±9,5 мкг/мл в інтервалі між 5 і 6 день після введення. Після початкового щотижневого введення під час першого місяця час досягнення максимальної концентрації був між 31 і 34 днем. Максимальна концентрація у рівноважному стані (Cmax, ss ) після підшкірного введення 150 мг або 300 мг склала 27,6 мкг/мл та 55,2 мкг/мл відповідно. рівноважний стан досягається після 20 тижнів при щомісячному режимі введення. Порівняно з експозицією після одноразової дози відмічено дворазове підвищення максимальної концентрації та площі під кривою залежності концентрації від часу (AUC) після багаторазового щомісячного введення під час підтримуючої терапії. Секукінумаб абсорбується із середнім показником абсолютної біодоступності 73%. Розподіл Середній об'єм розподілу у термінальній фазі (Vz) після одноразового внутрішньовенного введення варіював між 7,10 та 8,60 л у пацієнтів з бляшковим псоріазом, ймовірно, що секукінумаб обмежено розподіляється на периферії. Концентрації секукінумабу у міжклітинній рідині шкіри у пацієнтів з бляшковим псоріазом варіювали від 28% до 39% від такої у сироватці крові на 1-2 тижні після одноразового підшкірного введення секукінумабу у дозі 300 мг. Виведення Середній системний кліренс (CL) у пацієнтів з бляшковим псоріазом становить 0,19 л/добу. Кліренс був дозо- та часзалежним, як і передбачалося для терапевтичного IgGl моноклонального антитіла, що взаємодіє з розчинною цитокінової мішенню, такою як ІЛ-17А. Середній період напіввиведення у пацієнтів із бляшковим псоріазом становив 27 днів. Період напіввиведення у окремих пацієнтів із псоріазом варіював від 17 до 41 дня. Лінійність/нелінійність Фармакокінетичні параметри при одноразовому та багаторазовому введенні секукінумабу у пацієнтів з бляшковим псоріазом були визначені в окремих дослідженнях з внутрішньовенним введенням доз, що варіювали від 1 x 0,3 мг/кг до 3х10 мг/кг та з підшкірним введенням доз, вар доза 300 мг. За всіх режимів дозування експозиція була пропорційна дозі. Фармакокінетичні параметри секукінумабу у пацієнтів з псоріатичним артритом, анкілозуючим артритом та бляшковим псоріазом однакові. Фармакокінетика в особливих клінічних випадках Пацієнти старше 65 років Грунтуючись на популяційному аналізі фармакокінетичних параметрів, кліренс у пацієнтів старше 65 років і пацієнтів молодше цієї вікової групи був подібним. Пацієнти з порушеннями функції печінки або нирок Доступні дані щодо фармакокінетики у пацієнтів з порушеннями функції печінки або нирок відсутні.ФармакодинамікаКонцентрація загального ІЛ-17А (вільного і пов'язаного з секукінумабом ІЛ-17А) підвищується внаслідок зниження кліренсу, пов'язаного з секукінумабом ІЛ-17А протягом 2-7 днів у пацієнтів, які отримують секукінумаб, вказуючи на те, що секукінумаб , що грає ключову роль у патогенезі бляшкового псоріазу У дослідженні з секукінумабом інфільтрація епідермальними нейтрофілами та різними нейтрофілзв'язаними маркерами, які підвищені у пошкодженій шкірі у пацієнтів з бляшковим псоріазом, були значно знижені після одного-двох тижнів лікування. На тлі терапії секукінумабом у пацієнтів з псоріатичним артритом та анкілозуючим спондилітом протягом 1-2 тижнів відзначалося зниження концентрації С-реактивного білка, що є маркером запалення.Показання до застосуванняЛікування псоріазу середньотяжкого та тяжкого ступеня у дорослих пацієнтів, яким показана системна терапія або фототерапія. Лікування активного псоріатичного артриту в режимі монотерапії або комбінації з метотрексатом у дорослих пацієнтів при недостатній відповіді на попередню терапію базисними препаратами. Лікування активного анкілозуючого спондиліту у дорослих пацієнтів при недостатній відповіді на стандартну терапію.Протипоказання до застосуванняТяжкі реакції гіперчутливості до секукінумабу або до інших допоміжних компонентів препарату. Клінічно значущі інфекції на стадії загострення (наприклад, активний туберкульоз). Вік до 18 років у зв'язку з відсутністю даних щодо ефективності та безпеки. Вагітність та період грудного вигодовування. З обережністю Слід бути обережними при призначенні препарату Козентикс пацієнтам з хронічними інфекціями або з анамнестичними вказівками на них через підвищений ризик розвитку інфекції, а також пацієнтам з активною стадією хвороби Крона. Оскільки знімний ковпачок попередньо заповненого шприца з пристроєм для пасивного захисту голки/попередньо заповненого шприца в автоінжекторі містить похідні натурального каучукового латексу, необхідно бути обережним при застосуванні препарату Козентикс у пацієнтів з індивідуальною непереносимістю латексу. Пацієнти, які отримують препарат Козентикс, можуть бути вакциновані інактивованими або вбитими вакцинами, введення живих вакцин не повинно проводитися. Якщо у Вас є одне з перелічених захворювань, перед прийомом препарату обов'язково проконсультуйтеся з лікарем.Вагітність та лактаціяДослідження у лабораторних тварин не показали прямого чи непрямого негативного впливу на вагітність, ембріональний/фетальний розвиток, пологи або постнатальний розвиток. Оскільки відсутні адекватні дані щодо застосування препарату Козентикс у вагітних жінок, його застосування у цій категорії пацієнтів не рекомендовано. Невідомо, чи проникає секукінумаб у грудне молоко у людини. Оскільки імуноглобуліни екскретуються із грудним молоком людини, не рекомендується застосовувати препарат Козентикс у період грудного вигодовування. Даних щодо впливу препарату Козентикс на фертильність чоловіків та жінок немає. У дослідженнях препарату Козентикс у тварин зниження фертильності не було відзначено.Побічна діяНайпоширенішими небажаними явищами (НЯ) на фоні застосування препарату Козентикс були інфекції верхніх дихальних шляхів (найчастіше назофарингіт, риніт). Більшість із них були слабо або помірно виражені. НЯ перераховані відповідно до системно-органного класу медичного словника для нормативно-правової діяльності MedDRA. У межах кожного системно-органного класу НЯ розподілено за частотою виникнення у порядку зменшення їх важливості. Для оцінки частоти використані такі критерії: дуже часто (≥1/10); часто (від ≥1/100 до Інфекційні та паразитарні захворювання: дуже часто – назофарингіт, інфекція верхніх відділів дихальних шляхів; часто – риніт, фарингіт, герпетична інфекція слизової оболонки порожнини рота; нечасто – синусит, тонзиліт, кандидозна інфекція порожнини рота, грибкове ураження шкіри, запалення зовнішнього вуха. Порушення з боку крові та лімфатичної системи: нечасто – нейтропенія. Порушення з боку органів зору: нечасто – кон'юнктивіт. Порушення з боку дихальної системи, органів грудної клітки та середостіння: часто – ринорея. Порушення з боку шлунково-кишкового тракту: часто – діарея. Порушення з боку шкіри та підшкірних тканин: часто – кропив'янка; рідко – анафілактичні реакції. Імуногенність За даними клінічних досліджень препарату Козентикс Якщо будь-які вказані в інструкції побічні ефекти посилюються, або Ви помітили будь-які інші побічні ефекти, не вказані в інструкції, повідомте про це лікаря.Взаємодія з лікарськими засобамиПрепарат Козентикс не можна призначати разом із живими вакцинами. Даних щодо взаємодії препарату Козентикс з іншими лікарськими засобами у людини немає. Немає прямих даних, що свідчать про участь ІЛ-17А в експресії ізоферментів системи цитохрому CYP450. Підвищена концентрація цитокінів за умов хронічного запального процесу пригнічує утворення деяких ізоферментів системи цитохрому. Таким чином, протизапальна терапія, в т. ч. секукінумабом, інгібітором ІЛ-17А, може призвести до нормалізації активності ізоферментів цитохрому CYP450, що супроводжується зменшенням експозиції одночасно застосовуваних препаратів, метаболізм яких здійснюється за участю зазначених ізоферментів. Т. о. не може бути виключено клінічно значущий вплив на препарати,є субстратами ізоферментів системи цитохрому з вузьким терапевтичним індексом, доза яких підбирається індивідуально (наприклад, варфарин). Слід розглянути можливість проведення терапевтичного контролю при початку терапії секукінумабом у пацієнтів, які отримують лікування препаратами вищезгаданих груп. При призначенні препарату Козентикс одночасно з метотрексатом та/або глюкокортикостероїдами у пацієнтів з псоріатичним артритом та анкілозуючим спондилітом лікарських взаємодій виявлено не було. Препарат Козентикс не повинен змішуватись з будь-якими лікарськими препаратами.Спосіб застосування та дозиПрепарат Козентикс вводиться шляхом підшкірної ін'єкції. По можливості слід уникати місця для ін'єкції ділянки шкіри, уражені псоріазом. Лікування псоріазу середньотяжкого та тяжкого ступеня у дорослих пацієнтів, яким показана системна терапія або фототерапія: рекомендована доза становить 300 мг як початкова доза на 0, 1, 2 та 3 тижні шляхом підшкірної ін'єкції, яка в подальшому вводиться щомісяця як підтримуюча доза. з 4-го тижня. Кожна доза 300 мг вводиться як двох окремих підшкірних ін'єкцій по 150 мг. Лікування активного псоріатичного артриту в режимі монотерапії або в комбінації з метотрексатом у дорослих пацієнтів при недостатній відповіді на попередню терапію базисними препаратами: рекомендована доза становить 150 мг як початкова доза на 0, 1, 2 і 3 тижні після підведення. щомісяця як підтримуюча доза, починаючи з 4-го тижня. Для пацієнтів з неадекватною відповіддю на терапію анти-ФНПα (фактор некрозу пухлини α) препаратами або для пацієнтів з псоріазом середнього та тяжкого ступеня тяжкості рекомендована доза становить 300 мг як початкова доза на 0, 1, 2 та 3 тижні шляхом підшкірної ін'єкції. в подальшому вводиться щомісяця як підтримуюча доза, починаючи з 4-го тижня. Кожна доза 300 мг вводиться як двох окремих підшкірних ін'єкцій по 150 мг. Лікування активного анкілозуючого спондиліту у дорослих пацієнтів, при недостатній відповіді на стандартну терапію: рекомендована доза становить 150 мг як початкова доза на 0, 1, 2 і 3 тижні шляхом підшкірної ін'єкції, яка в подальшому вводиться щомісяця як підтримуюча доза. -й тижня. Особливі групи пацієнтів Пацієнти з порушенням функції печінки або нирок Відсутні дані щодо застосування препарату Козентикс у цієї групи пацієнтів. Пацієнти молодші 18 років Ефективність та безпека препарату у дітей до 18 років не встановлена. Пацієнти старше 65 років Корекція дози не потрібна. Інструкції щодо приготування розчину препарату Козентикс Доведіть флакон із препаратом Козентикс, ліофілізат для приготування розчину для ін'єкцій, 150 мг, та стерильну воду для ін'єкцій до кімнатної температури. Наберіть трохи більше 1,0 мл стерильної води для ін'єкцій в одноразовий шприц з градуюванням 1 мл та вирівняйте на позначці 1,0 мл. Зніміть пластиковий ковпачок із флакона. Вставте голку шприца у флакон, що містить ліофілізат препарату Козентикс, через центр гумової пробки та відновіть ліофілізат повільним введенням 1,0 мл стерильної води для ін'єкцій у флакон. Струмінь стерильної води для ін'єкцій повинен бути спрямований на ліофілізат. Нахиліть флакон під кутом близько 45° і, утримуючи кінчиками пальців, акуратно обертайте приблизно протягом 1 хвилини. Не струшуйте та не перевертайте флакон. Залиште флакон стояти при кімнатній температурі не менше ніж на 10 хвилин для досягнення повного розчинення. Може спостерігатися спінювання розчину. Нахиліть флакон під кутом близько 45° і, утримуючи кінчиками пальців, акуратно обертайте приблизно протягом 1 хвилини. Не струшуйте та не перевертайте флакон. Залиште флакон у вертикальному положенні при кімнатній температурі приблизно на 5 хвилин. Отриманий розчин повинен бути прозорим або опалесцентним. Його колір може варіювати від безбарвного до світло-жовтого. Не використовуйте препарат, якщо ліофілізат повністю не розчиняється, або якщо рідина містить легко помітні частинки, а також якщо вона каламутна або коричневого кольору. Підготуйте необхідну кількість флаконів (1 флакон для дози 150 мг, 2 флакони для дози 300 мг). Після приготування розчин для підшкірних ін'єкцій може бути введений негайно або може зберігатися при температурі від 2°С до 8°С не більше 24 годин. Не заморожувати. Після зберігання при температурі від 2 до 8°С розчин перед введенням слід витримати при кімнатній температурі близько 20 хвилин. Розчин повинен бути використаний протягом 1 години після вилучення з умов зберігання при температурі від 2°С до 8°С. Інструкція щодо введення розчину препарату Козентикс Нахиліть флакон під кутом приблизно 45 ° і помістіть кінчик голки на дно флакона з розчином при наборі в шприц. Не перевертайте флакон. Обережно відберіть трохи більше 1,0 мл розчину для підшкірного введення з флакона в одноразовий шприц з градуюванням 1 мл і голкою відповідного розміру (наприклад, «21G х 2»). Дана голка буде використана тільки для забору препарату Козентікс в одноразовий шприц. Підготуйте потрібну кількість шприців (1 шприц для дози 150 мг, 2 шприца для дози 300 мг). Утримуючи шприц голкою вгору, злегка постукайте шприцем для переміщення бульбашок повітря догори. Замініть голку, використану для забору препарату, на іншу розміром «27 G х /г». Замініть голку, використану для забору препарату, на іншу розміром «27 G х /г». Замініть голку, використану для забору препарату, на іншу розміром «27G х ». Видаліть бульбашки повітря та просуньте поршень до позначки 1,0 мл. Продезінфікуйте місце ін'єкції спиртовим тампоном. Введіть розчин препарату Козентикс підшкірно у передньобокову поверхню стегна або нижню частину живота (за винятком п'ятисантиметрової області навколо пупка) або зовнішню поверхню плеча. Місця ін'єкції слід кожного разу міняти. Не слід вводити в область пошкодженої шкіри (стоншення, почервоніння, подразнення, ущільнення, лущення). Уникайте введення в місця з наявністю шрамів та розтяжок. Розчин, що залишився у флаконі не повинен використовуватися і повинен бути утилізований. Флакони призначені лише для одноразового використання. Утилізуйте використаний шприц у контейнер для гострих предметів (контейнер, що закривається, стійкий до проколів). З метою Вашої безпеки та здоров'я інших, голки та використані шприци в жодному разі не повинні використовуватися повторно.ПередозуванняУ ході клінічних досліджень препарату Козентикс повідомлень про випадки передозування не було. У ході клінічних досліджень дози до 30 мг/кг (тобто приблизно 2000-3000 мг) вводилися внутрішньовенно без розвитку дозолімітуючої токсичності. У разі передозування рекомендується спостереження за пацієнтами для виявлення ознак та симптомів НЯ. За необхідності слід негайно провести симптоматичне лікування.Запобіжні заходи та особливі вказівкиІнфекції Препарат Козентикс може збільшувати ризик розвитку інфекцій. У клінічних дослідженнях у пацієнтів, які отримували препарат Козентикс, спостерігалися випадки розвитку інфекції, більшість яких були легким або середнім ступенем тяжкості. Слід бути обережними при вирішенні питання про застосування препарату Козентикс у пацієнтів з хронічними інфекціями або з наявністю в анамнезі рецидивуючої інфекції. Пацієнти повинні бути проінформовані про необхідність звернення до лікаря у разі появи ознак та симптомів, що передбачають розвиток інфекції. У разі розвитку тяжкої інфекції пацієнт повинен перебувати під наглядом, препарат Козентикс не повинен вводитись до вирішення інфекції. У клінічних дослідженнях не повідомлялося про підвищену сприйнятливість до туберкульозу, проте препарат Козентикс не слід призначати пацієнтам з активною формою туберкульозу. До початку лікування препаратом Козентикс має бути прийняте рішення щодо проведення протитуберкульозної терапії у пацієнтів з латентними формами туберкульозу. Хвороба Крона Слід бути обережним при призначенні препарату Козентикс пацієнтам із загостренням хвороби Крона, оскільки в клінічних дослідженнях спостерігалося посилення перебігу хвороби Крона, в деяких випадках тяжке. Пацієнти із загостренням хвороби Крона на фоні лікування препаратом Козентікс повинні ретельно спостерігатися. Реакції гіперчутливості При виникненні анафілактичних або інших серйозних алергічних реакцій застосування препарату Козентикс слід негайно припинити, необхідно негайно розпочати відповідну симптоматичну терапію. Пацієнти з гіперчутливістю до латексу Знімний ковпачок попередньо заповненого шприца з пристроєм для пасивного захисту голки/попередньо заповненого шприца автоінжектор містить похідні натурального каучукового латексу. Хоча натуральний каучуковий латекс не виявляється в ковпачку, безпека застосування препарату Козентікс у попередньо заповненому шприці з пристроєм для пасивного захисту голки/попередньо заповненому шприці в автоінжекторі у пацієнтів з гіперчутливістю до латексу не вивчалася. Вакцинація Вакцинація живими вакцинами не повинна проводитися на фоні лікування препаратом Козентикс. Пацієнти, які отримують Козентикс, можуть бути вакциновані інактивованими або вбитими вакцинами. Після вакцинації інактивованою менінгококовою та грипозною вакциною, у пацієнтів, які отримували препарат Козентикс, відзначалася адекватна імунна відповідь у вигляді щонайменше чотириразового підвищення титру антитіл до менінгококової та грипозної вакцини. Ці дані свідчать про те, що препарат Козентикс не пригнічує розвиток імунної відповіді на введення менінгококової та грипозної вакцини. Вплив на фертильність Жінкам із збереженим дітородним потенціалом слід використовувати надійні методи контрацепції під час лікування препаратом та як мінімум протягом 20 тижнів після припинення терапії. Вплив на здатність керувати транспортними засобами та/або механізмами Відсутні дані щодо впливу препарату на здатність керувати транспортними засобами та/або механізмами.Умови зберіганняУ холодильнику +2+8 градусівУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаСилікон.Опис лікарської формиKelo-Cote являє собою гель на основі силікону для запобігання утворенню, зменшення виразності келоїдних та гіпертрофічних рубців, отриманих в результаті хірургічних втручань, травм, ран та опіків, а також для покращення естетичного виду рубців.ХарактеристикаKelo-Cote швидко висихає, утворюючи на шкірі еластичну, водостійку та повітропроникну плівку. При нанесенні гелю Kelo-Cote на рубець, гель на місці нанесення утворює захисний бар'єр, що сприяє зменшенню хімічної, фізичної та бактеріальної дії, при цьому зберігається водний баланс шкіри. Це створює умови для нормалізації процесів синтезу колагену та не дозволяє рубцю розростатися, а також покращує зовнішній вигляд самого рубця. Після застосування засобу Kelo-Cote зменшується виразність келоїдних та гіпертрофічних рубців, свербіж та дискомфорт, відновлюється колір; рубці розгладжуються і пом'якшуються, покращується їхній естетичний вигляд. Відповідно до Міжнародних клінічних рекомендацій з терапії рубців силікон був рекомендований як перша лінія терапії для всіх видів рубців та обов'язковий елемент для запобігання утворенню та зменшення виразності келоїдних та гіпертрофічних рубців. Kelo-Cote може наноситися на шкіру в області суглобів, на місця згину, на область росту волосся, на рубцеві поверхні великих розмірів, що є наслідком опіків та великих травм. Kelo-Cote можна використовувати з пов'язками, що давлять, або іншими допоміжними засобами.ІнструкціяПереконайтеся, що шкіра на ураженій ділянці чиста та суха. Нанесіть Kelo-Cote на уражену ділянку суцільним тонким шаром і дайте йому висохнути. Наносите Kelo-Cote двічі на день. Для досягнення максимального ефекту Kelo-Cote має контактувати зі шкірою 24 години на добу. Після повного висихання гелю можна наносити сонцезахисні та косметичні засоби, а також використовувати пов'язки, що тиснуть. Якщо Kelo-Cote не висохне протягом 4-5 хвилин, можливо, гель був нанесений товстим шаром. У такому випадку акуратно видаліть надлишки і дайте гелю, що залишився, висохнути. Рекомендована тривалість застосування гелю – не менше ніж 60-90 днів. Для великих і застарілих рубців може знадобитися триваліший курс застосування. Подальше застосування гелю рекомендовано, якщо після перших 90 днів застосування покращення зовнішнього вигляду рубця продовжує спостерігатися. Час повного висихання гелю Kelo-Cote залежить від різниці температури гелю та шкіри. Щоб скоротити час висихання у жаркому кліматі, зберігайте Kelo-Cote у холодильнику. Щоб скоротити час висихання гелю за холодної погоди, можна використовувати фен для волосся (середній рівень температури).Протипоказання до застосуванняГель Kelo-Cote призначений для запобігання утворенню, зменшення виразності та поліпшення естетичного вигляду як старих, так і свіжих рубців (включаючи гіпертрофічні та келоїдні), отриманих внаслідок хірургічних втручань, травм, ран та опіків. Kelo-Cote підходить для дітей та людей з чутливою шкірою.Запобіжні заходи та особливі вказівкиУникайте попадання в очі, на слизові оболонки та відкриті рани. Не слід застосовувати Kelo-Cote при дерматологічних захворюваннях, що порушують цілісність покриву шкіри. У випадку неповного висихання Kelo-Cote на одязі можуть залишитись плями. Тільки для зовнішнього застосування. У разі виникнення подразнення на шкірі припиніть використання гелю та зверніться до лікаря.Умови відпустки з аптекБез рецептаВідео на цю тему
38 053,00 грн
157,00 грн
Склад, форма випуску та упаковкаПо 1 мл у скляний шприц із закріпленою голкою із захисним ковпачком (попередньо заповнений шприц). По 1 або 2 попередньо заповнених шприца з пристроєм для пасивного захисту голки в блістер, заклеєний етикеткою, разом з інструкцією з медичного застосування в картонну пачку з контролем первинного розтину. По 1 або 2 попередньо заповнених шприца в автоінжекторах (ручках) з контролем первинного розтину, разом з інструкцією з медичного застосування в картонну пачку з контролем первинного розтину. Діюча речовина: секукинумаб 150,00 мг; допоміжні речовини: трегалози дигідрат 75,67 мг, гістидин/гістидину гідрохлориду моногідрат 3,103 мг, метіонін 0,746 мг, полісорбат-80 0,200 мг, вода для ін'єкцій 1069 мг.Опис лікарської формиВід безбарвного до світло-жовтого кольору прозорий або опалесцентний розчин.ФармакокінетикаВсмоктування Після одноразового підшкірного (п/к) введення в дозі 150 мг або 300 мг при бляшковому псоріазі максимальна концентрація секукінумабу в сироватці становила відповідно 13,7±4,8 мкг/мл або 27,3±9,5 мкг/мл в інтервалі між 5 та 6 днем після введення. Після початкового щотижневого введення протягом першого місяця максимальна концентрація досягалася між 31 та 34 днем. Максимальна концентрація в рівноважному стані (Cmax,ss) після підшкірного введення 150 мг або 300 мг склала 27,6 мкг/мл і 55,2 мкг/мл відповідно. рівноважна концентрація досягається після 20 тижнів при щомісячному режимі введення. У порівнянні з експозицією після одноразової дози відмічено дворазове підвищення максимальної концентрації та площі під фармакокінетичною кривою «концентрація-час» (AUC) після багаторазового щомісячного введення під час підтримуючої терапії. Секукінумаб всмоктується із середнім показником абсолютної біодоступності 73%. Розподіл Середній обсяг розподілу в термінальній фазі (Vz) після одноразового внутрішньовенного введення варіював між 7,10 та 8,60 л у пацієнтів з бляшковим псоріазом, що дозволяє припустити, що секукінумаб обмежено розподіляється на периферії. Концентрації секукінумабу в міжклітинній рідині шкіри у пацієнтів з бляшковим псоріазом варіювали від 28% до 39% від такої у сироватці крові на 1-2 тижні після одноразового підшкірного введення в дозі 300 мг. Середній системний кліренс (CL) у пацієнтів з бляшковим псоріазом становив 0,19л/добу. Кліренс був дозо- та час-залежним, як і передбачалося для терапевтичного IgGl моноклонального антитіла, що взаємодіє з розчинною цитокінової мішенню, такою як ІЛ-17А. Середній період напіввиведення у пацієнтів із бляшковим псоріазом становив 27 днів. Розрахунковий період напіввиведення у окремих пацієнтів із псоріазом варіював від 17 до 41 дня. Лінійність/нелінійність Фармакокінетичні параметри при одноразовому та багаторазовому введенні секукінумабу у пацієнтів з бляшковим псоріазом були визначені в кількох дослідженнях з внутрішньовенним введенням у дозах від 1×0,3 мг/кг до 3×10 мг/кг та з п/к введенням у дозах мг до багаторазової дози 300 мг. За всіх режимів дозування експозиція була пропорційна дозі. Фармакокінетичні параметри секукінумабу у пацієнтів з псоріатичним артритом, анкілозуючим спондилітом та бляшковим псоріазом однакові. Фармакокінетика в особливих клінічних випадках Пацієнти старше 65 років За даними популяційного фармакокінетичного аналізу кліренс у пацієнтів старше 65 років і пацієнтів молодше цієї вікової групи був подібним. Пацієнти з порушеннями функції печінки або нирок.ФармакодинамікаКонцентрація загального ІЛ-17А (вільного і пов'язаного з секукінумабом) у сироватці крові збільшується в межах 2-7 днів внаслідок уповільнення кліренсу, пов'язаного з секукінумабом ІЛ-17А, свідчуючи, що секукінумаб селективно зв'язується з вільним ІЛ-17А, який патогенезі бляшкового псоріазу. У дослідженні у пацієнтів з бляшковим псоріазом після одного-двох тижнів лікування секукінумабом значно знижувалися інфільтрація епідермісу нейтрофілами та кількість різних асоційованих з ними маркерів, яка часто підвищена в уражених ділянках шкіри у даних пацієнтів. На тлі терапії секукінумабом у пацієнтів з псоріатичним артритом та анкілозуючим спондилітом протягом 1-2 тижнів відзначалося зниження концентрації С-реактивного білка, що є маркером запалення.Показання до застосуванняЛікування псоріазу середньотяжкого та тяжкого ступеня у дорослих пацієнтів, яким показана системна терапія або фототерапія; Лікування активного псоріатичного артриту в монотерапії або комбінації з метотрексатом у дорослих пацієнтів при недостатній відповіді на попередню терапію базисними препаратами; Лікування активного анкілозуючого спондиліту у дорослих пацієнтів при недостатній відповіді на стандартну терапію.Протипоказання до застосуванняТяжкі реакції гіперчутливості до секукінумабу або до інших допоміжних речовин препарату. Клінічно значущі інфекції на стадії загострення (наприклад, активний туберкульоз) . Вік до 18 років у зв'язку з відсутністю даних щодо ефективності та безпеки. Вагітність та період грудного вигодовування.Вагітність та лактаціяВагітність. Резюме ризиків. Немає достатніх даних щодо застосування препарату у вагітних жінок. Дослідження у тварин не показали прямого або непрямого негативного впливу секукінумабу на вагітність, ембріональний/фетальний розвиток, пологи або постнатальний розвиток. Оскільки результати досліджень у тварин не завжди дозволяють припустити відповідь людини, препарат протипоказаний до застосування під час вагітності. Дані досліджень у тварин. У дослідженні ембріофетального розвитку при застосуванні секукінумабу у яванських макак під час органогенезу та на пізніх стадіях гестації не виявлено явищ материнської токсичності, ембріотоксичності чи тератогенних властивостей. Грудне годування . Невідомо, чи проникає секукінумаб у грудне молоко у людини. Оскільки імуноглобуліни проникають у грудне молоко людини, не рекомендується застосовувати препарат Козентикс у період грудного вигодовування. Вплив на фертильність. Дані про вплив секукінумабу на чоловічу та жіночу фертильність відсутні. У дослідженнях у тварин не відзначено прямого чи непрямого негативного впливу секукінумабу на фертильність.Побічна діяУ клінічних дослідженнях секукінумаб отримували більше 11900 пацієнтів за різними показаннями, при цьому 7100 пацієнт отримував препарат протягом мінімум 1 року. Найпоширенішими небажаними лікарськими реакціями (НЛР) на фоні застосування препарату Козентикс були інфекції верхніх дихальних шляхів (найчастіше назофарингіт, риніт). Більшість із них були легким або середнім ступенем тяжкості. У клінічних дослідженнях припинення терапії препаратом у зв'язку з розвитком НЛР знадобилося близько 1,2% пацієнтів, які отримували секукінумаб, і близько 1,2% пацієнтів, які отримували плацебо. НЛР, виявлені у клінічних дослідженнях у пацієнтів з псоріазом, перераховані нижче відповідно до системно-органного класу медичного словника для нормативно-правової діяльності MedDRA. У межах кожного системно-органного класу НРЛ розподілено за частотою виникнення у порядку зменшення їх важливості. Для оцінки частоти використані такі критерії: дуже часто (≥1/10); часто (від ≥1/100 до Інфекційні та паразитарні захворювання: дуже часто – інфекції верхніх дихальних шляхів (у тому числі: дуже часто – назофарингіт, часто – інфекція верхніх відділів дихальних шляхів, риніт, фарингіт, нечасто – синусит, тонзиліт); часто – герпетична інфекція слизової оболонки порожнини рота; нечасто – кандидозна інфекція порожнини рота, грибкове ураження шкіри стоп, зовнішній отит; частота невідома - кандидозна інфекція шкіри та слизових оболонок. Порушення з боку крові та лімфатичної системи: нечасто – нейтропенія. Порушення з боку імунної системи: рідко – анафілактичні реакції. Порушення органу зору: нечасто - кон'юнктивіт. Порушення з боку дихальної системи, органів грудної клітки та середостіння: часто – ринорея. Порушення з боку шлунково-кишкового тракту: часто – діарея. Порушення з боку шкіри та підшкірних тканин: часто – кропив'янка. Інфекції У плацебо-контрольованих клінічних дослідженнях у пацієнтів з бляшковим псоріазом відзначено розвиток інфекційних захворювань у 28,7% та 18,9% пацієнтів, які отримували секукінумаб та плацебо відповідно. Більшість випадків були легким або середнім ступенем тяжкості. Серйозні інфекційні захворювання відзначені у 0,14% пацієнтів, які отримували секукінумаб, і 0,3%, пацієнтів, які отримували плацебо. При довгостроковій терапії препаратом у клінічних дослідженнях (до 52 тижнів терапії у більшості пацієнтів) інфекції відзначено у 47,5% пацієнтів, які отримували секукінумаб, при цьому серйозні інфекції зареєстровані у 1,2% пацієнтів. Частота інфекційних захворювань була схожою у клінічних дослідженнях у пацієнтів з псоріазом, псоріатичним артритом та анкілозуючим спондилітом. Реакції гіперчутливості У клінічних дослідженнях зареєстровані випадки кропив'янки та у дуже рідкісних випадках – анафілактичних реакцій на введення препарату. Імуногенність За даними клінічних досліджень препарату Козентикс Профіль безпеки секукінумабу у пацієнтів з псоріатичним артритом та анкілозуючим спондилітом відповідав профілю безпеки у пацієнтів з псоріазом за даними клінічних досліджень. Якщо будь-які вказані в інструкції побічні ефекти посилюються, або Ви помітили будь-які інші побічні ефекти, не вказані в інструкції, повідомте про це лікаря.Взаємодія з лікарськими засобамиПрепарат Козентикс не можна застосовувати одночасно з живими вакцинами. У клінічних дослідженнях у пацієнтів з псоріазом не відмічено лікарської взаємодії між секукінумабом та мідазоламом (субстратом ізоферменту CYP ЗА4). Немає прямих даних, що свідчать про участь ІЛ-17А в експресії ізоферментів системи цитохрому CYP450. Підвищена концентрація цитокінів за умов хронічного запального процесу пригнічує утворення деяких ізоферментів системи цитохрому. Отже, протизапальна терапія, зокрема. секукінумабом, інгібітором ІЛ-17А, може призвести до нормалізації активності ізоферментів цитохрому CYP450, що супроводжується зменшенням експозиції одночасно застосовуваних препаратів, метаболізм яких здійснюється за участю зазначених ізоферментів. Таким чином,не можна виключити клінічно значущого впливу на препарати – субстрати ізоферментів системи цитохрому з вузьким терапевтичним індексом, доза яких підбирається індивідуально (наприклад, варфарин). Слід розглянути можливість терапевтичного контролю при початку терапії секукінумабом у пацієнтів, які отримують лікування препаратами вищезгаданих груп. Не виявлено лікарської взаємодії секукінумабу з метотрексатом та/або глюкокортикостероїдами при їх одночасному застосуванні у пацієнтів з псоріатичним артритом та анкілозуючим спондилітом.Спосіб застосування та дозиПрепарат Козентикс вводять шляхом підшкірної ін'єкції. По можливості слід уникати ін'єкції уражених ділянок шкіри при бляшковому псоріазі. Лікування псоріазу середньотяжкого та тяжкого ступеня у дорослих пацієнтів, яким показана системна терапія або фототерапія: рекомендована доза становить 300 мг у вигляді п/к ін'єкції як початкова доза на 0, 1, 2, 3 тижні з наступним щомісячним введенням як підтримуюча доза. починаючи з чотирьох тижнів. Кожну дозу 300 мг вводять у вигляді двох окремих підшкірних ін'єкцій по 150 мг. Лікування активного псоріатичного артриту в монотерапії або в комбінації з метотрексатом у дорослих пацієнтів при недостатній відповіді на попередню терапію базисними препаратами: рекомендована доза становить 150 мг у вигляді п/к ін'єкції як початкова доза на 0, 1, 2, 3 тижні введенням як підтримуюча доза, починаючи з 4 тижня. Залежно від клінічної відповіді дозу препарату можна збільшити до 300 мг. Для пацієнтів з неадекватною відповіддю на терапію препаратами інгібіторами ФНОа або для пацієнтів з супутнім псоріазом середнього та тяжкого ступеня тяжкості рекомендована доза становить 300 мг у вигляді п/к ін'єкції як початкова доза на 0, 1, 2, 3 тижні. якість підтримуючої дози, починаючи з 4 тижнів. Кожну дозу 300 мг вводять у вигляді двох окремих підшкірних ін'єкцій по 150 мг. Лікування активного анкілозуючого спондиліту у дорослих пацієнтів при недостатній відповіді на стандартну терапію: рекомендована доза становить 150 мг у вигляді п/к ін'єкції як початкова доза на 0, 1, 2, 3 тижні з наступним щомісячним введенням як підтримуюча доза, тижня.ПередозуванняУ ході клінічних досліджень препарату Козентикс повідомлень про випадки передозування не було. У ході клінічних досліджень внутрішньовенне введення дози до 30 мг/кг (тобто приблизно 2000-3000 мг) не супроводжувалося розвитком дозолімітуючої токсичності. У разі передозування рекомендується спостереження пацієнта для виявлення ознак та симптомів небажаних реакцій. За необхідності слід негайно провести симптоматичне лікування.Умови зберіганняУ холодильнику +2+8 градусівУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковка100% трава галеги (козлятник). Інструкція2 фільтр-пакети залити склянкою гарячої води і настояти 30 хв. Приймати по 1/3 склянки 3 десь у день 30 хв.
Склад, форма випуску та упаковка100% трава галеги (козлятник). Інструкція2 фільтр-пакети залити склянкою гарячої води і настояти 30 хв. Приймати по 1/3 склянки 3 десь у день 30 хв.
Склад, форма випуску та упаковкаНаповнювач мікрокристалічна целюлоза, натрієва сіль урідінмонофосфату, гідроксипропілметилцелюлоза (оболонка капсули), вітамін В12, магнію стеарат, гідрат оксиду кремнію, фолієва кислота, барвник заліза оксид червоний. Келтікан® комплекс реалізується через аптечну мережу в упаковках по 20 та 40 капсул.ХарактеристикаЗупинивши свій вибір на БАД Келтікан® комплекс, Ви отримаєте надійний та якісний продукт. Келтикан® комплекс містить важливі компоненти, необхідні відновлення пошкоджених нервових тканин. Завдяки цьому Келтікан® комплекс сприяє швидшому відновленню гарного самопочуття та працездатності. Що відбувається при ураженні нервів? У нашому організмі є велика кількість нервових волокон, що становлять так звану периферичну нервову систему. При ураженні цих нервів, наприклад, у разі здавлення, утиску або при тривалих перебігах протягом багатьох років порушення обміну речовин, таких як цукровий діабет, можливий розвиток неприємних і хворобливих відчуттів. Поразка периферичної нервової системи може виникати при різних станах та захворюваннях, що супроводжуються неприємними та болючими відчуттями (наприклад, захворювання хребта, невралгії). Організм людини здатний самостійно за рахунок резервних можливостей відновлювати уражені нервові волокна. Звичайно, процеси відновлення потребують достатньої кількості часу. Однак у разі надходження ззовні певних структурних елементів, необхідні відновлення нервових волокон, може надати значну допомогу. Яку допомогу може надавати БАД до їжі Келтікан® комплекс? Келтикан® комплекс містить біогенний елемент урідінмонофосфат, а також вітамін В12 та фолієву кислоту, що стимулюють власні відновлювальні процеси в організмі. Уридинмонофосфат має особливе значення для прискорення відновлення пошкоджених нервів, а фолієва кислота та вітамін В12 – для підтримки нейронного метаболізму. Клінічно доведено та документально підтверджено, що при ураженнях периферичних нервів підвищується потреба у піримідинових нуклеотидах, таких як урідінмонофосфат. Тому його надходження в організм ззовні має найважливіше значення в ході відновлення і регенерації нервів. В результаті його метаболізму забезпечується відновлення важливих компонентів клітинних мембран нейронів, а також надходження достатньої кількості ферментів до пошкоджених нейронів. Фолієва кислота та вітамін В12 мають важливе значення у підтримці нейронного метаболізму (біосинтезі білка, процесах мієлінізації), а також у профілактиці або зниженні вираженості мікроангіопатій. Що ще Вам потрібно знати про Келтікан® комплекс? Келтикан® комплекс не містить глютену або лактози, а також консервантів або речовин тваринного походження. Особи, які страждають на цукровий діабет, також можуть приймати Келтікан® комплекс. Целюлоза, яка використовується для виробництва капсул Келтікан® комплекс, не має тваринного походження, і, отже, її можуть приймати особи, які дотримуються вегетаріанського та веганського способу життя.РекомендуєтьсяЯк біологічно активна добавка до їжі - додаткового джерела вітаміну В12 і фолієвої кислоти, що містить натрієву сіль уридинмонофосфату. Келтикан® комплекс сприяє відновленню пошкоджених нервових волокон при захворюваннях хребта та периферичних нервів.Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність, годування груддю.Спосіб застосування та дозиДорослим по 1 капсулі щодня під час їжі. Тривалість прийому – 20 днів. За потреби прийом можна повторити. За наявності проблем із застосуванням (наприклад, труднощів з проковтуванням) капсула може бути відкрита, а витягнуті з неї міні-гранули можуть бути проковтнуті частинами. В одній капсулі міститься 3 мкг вітаміну В12 (300% РНП) і 400 мкг фолієвої кислоти (200% РНП). РНП - рекомендована норма споживання; *не перевищує верхній допустимий рівень.Запобіжні заходи та особливі вказівкиПеред застосуванням рекомендується проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаНаповнювач мікрокристалічна целюлоза, натрієва сіль урідінмонофосфату, гідроксипропілметилцелюлоза (оболонка капсули), вітамін В12, магнію стеарат, гідрат оксиду кремнію, фолієва кислота, барвник заліза оксид червоний. Келтікан® комплекс реалізується через аптечну мережу в упаковках по 20 та 40 капсул.ХарактеристикаЗупинивши свій вибір на БАД Келтікан® комплекс, Ви отримаєте надійний та якісний продукт. Келтикан® комплекс містить важливі компоненти, необхідні відновлення пошкоджених нервових тканин. Завдяки цьому Келтікан® комплекс сприяє швидшому відновленню гарного самопочуття та працездатності. Що відбувається при ураженні нервів? У нашому організмі є велика кількість нервових волокон, що становлять так звану периферичну нервову систему. При ураженні цих нервів, наприклад, у разі здавлення, утиску або при тривалих перебігах протягом багатьох років порушення обміну речовин, таких як цукровий діабет, можливий розвиток неприємних і хворобливих відчуттів. Поразка периферичної нервової системи може виникати при різних станах та захворюваннях, що супроводжуються неприємними та болючими відчуттями (наприклад, захворювання хребта, невралгії). Організм людини здатний самостійно за рахунок резервних можливостей відновлювати уражені нервові волокна. Звичайно, процеси відновлення потребують достатньої кількості часу. Однак у разі надходження ззовні певних структурних елементів, необхідні відновлення нервових волокон, може надати значну допомогу. Яку допомогу може надавати БАД до їжі Келтікан® комплекс? Келтикан® комплекс містить біогенний елемент урідінмонофосфат, а також вітамін В12 та фолієву кислоту, що стимулюють власні відновлювальні процеси в організмі. Уридинмонофосфат має особливе значення для прискорення відновлення пошкоджених нервів, а фолієва кислота та вітамін В12 – для підтримки нейронного метаболізму. Клінічно доведено та документально підтверджено, що при ураженнях периферичних нервів підвищується потреба у піримідинових нуклеотидах, таких як урідінмонофосфат. Тому його надходження в організм ззовні має найважливіше значення в ході відновлення і регенерації нервів. В результаті його метаболізму забезпечується відновлення важливих компонентів клітинних мембран нейронів, а також надходження достатньої кількості ферментів до пошкоджених нейронів. Фолієва кислота та вітамін В12 мають важливе значення у підтримці нейронного метаболізму (біосинтезі білка, процесах мієлінізації), а також у профілактиці або зниженні вираженості мікроангіопатій. Що ще Вам потрібно знати про Келтікан® комплекс? Келтикан® комплекс не містить глютену або лактози, а також консервантів або речовин тваринного походження. Особи, які страждають на цукровий діабет, також можуть приймати Келтікан® комплекс. Целюлоза, яка використовується для виробництва капсул Келтікан® комплекс, не має тваринного походження, і, отже, її можуть приймати особи, які дотримуються вегетаріанського та веганського способу життя.РекомендуєтьсяЯк біологічно активна добавка до їжі - додаткового джерела вітаміну В12 і фолієвої кислоти, що містить натрієву сіль уридинмонофосфату. Келтикан® комплекс сприяє відновленню пошкоджених нервових волокон при захворюваннях хребта та периферичних нервів.Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність, годування груддю.Спосіб застосування та дозиДорослим по 1 капсулі щодня під час їжі. Тривалість прийому – 20 днів. За потреби прийом можна повторити. За наявності проблем із застосуванням (наприклад, труднощів з проковтуванням) капсула може бути відкрита, а витягнуті з неї міні-гранули можуть бути проковтнуті частинами. В одній капсулі міститься 3 мкг вітаміну В12 (300% РНП) і 400 мкг фолієвої кислоти (200% РНП). РНП - рекомендована норма споживання; *не перевищує верхній допустимий рівень.Запобіжні заходи та особливі вказівкиПеред застосуванням рекомендується проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему