Противоопухолевые Со скидкой
422,00 грн
376,00 грн
Фасування: N1 Упакування: фл. Виробник: Тева Завод-виробник: Pharmachemie(Нідерланди) Діюча речовина: Етопозид. .
Дозировка: 20 мг Фасовка: N30 Форма выпуска: таб. Упаковка: упак. Производитель: Орион Корпорейшн Завод-производитель: Орион Корпорейшн(Финляндия) Действующее вещество: Торемифен.
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
18 138,00 грн
18 097,00 грн
Фасування: N2 Форма випуску: р-р для внутрішньом. Упаковка: шприц Производитель: АстраЗенека Завод-производитель: Веттер Фарма-Фертигунг ГмбХ и Ко. КГ(Германия) Действующее вещество: Фулвестрант.
Склад, форма випуску та упаковкаПігулки - 1 таб. Активна речовина: бікалутамід 150мг. Допоміжні речовини: магнію алюмінометасилікат – 30 мг, карбоксиметилкрохмаль натрію – 12 мг, магнію стеарат – 6 мг, лудіпрес – 402 мг. Склад плівкової оболонки: Опадрай II жовтий 85F32733 – 24 мг, у т. ч. полівініловий спирт – 35-49%, тальк – 9.8-25%, макрогол 3350 – 7.35-35.2%, титану діоксид та заліза оксид5 %. 7 шт. - упаковки осередкові контурні (алюміній/ПВХ) (4) - пачки картонні.Опис лікарської формиТаблетки, покриті плівковою оболонкою жовтого кольору, ромбоподібні, двоопуклі; на поперечному розрізі ядро білого кольору.Фармакотерапевтична групаАнтиандрогенний нестероїдний засіб. Зв'язуючись з рецепторами, що мають спорідненість з андрогенами, пригнічує активність андрогенів, у результаті спостерігається регресія пухлини передміхурової залози. Не має інших видів ендокринної активності.ФармакокінетикаПісля прийому внутрішньо добре всмоктується із ШКТ. Їда не впливає на біодоступність. Зв'язування із білками плазми становить 96%. Інтенсивно метаболізується у печінці шляхом окислення та утворення глюкуронідних кон'югатів. Виводиться у вигляді метаболітів із сечею та жовчю приблизно в рівних пропорціях. Можлива кумуляція бікалутаміду в організмі.Клінічна фармакологіяАнтиандрогенний нестероїдний препарат із протипухлинною активністю.Показання до застосуванняРак передміхурової залози – у складі комбінованої терапії з аналогом ГнРГ або з хірургічною кастрацією.Протипоказання до застосуванняОдночасний прийом із терфенадином, астемізолом, цизапридом; дитячий вік; підвищена чутливість до бікалутаміду. Не призначають пацієнтам жіночої статі.Вагітність та лактаціяНе призначають пацієнтам жіночої статі. Застосування у дітей Препарат не призначають дітям.Побічна діяЗ боку ендокринної системи: припливи, болючість молочних залоз та гінекомастія, зниження лібідо. З боку травної системи: біль у животі, діарея, нудота, блювання, підвищення рівня трансаміназ, жовтяниця, холестаз. З боку центральної нервової системи: можливі астенія, депресія. Дерматологічні реакції: алопеція, відновлення росту волосся, свербіж, сухість шкіри. Інші: гематурія.Взаємодія з лікарськими засобамиПри застосуванні бікалутаміду протягом 28 днів на фоні прийому мідазоламу АUC мідазоламу збільшувалася на 80%. При одночасному застосуванні бікалутаміду з циклоспорином або блокаторами кальцієвих каналів можливе потенціювання або розвиток небажаних реакцій. Теоретично можливе підвищення концентрації бікалутаміду в плазмі при його одночасному застосуванні з інгібіторами мікросомальних ферментів печінки, що може супроводжуватися збільшенням частоти виникнення небажаних реакцій. Дослідження in vitro показали, що бікалутамід може витісняти антикоагулянт кумаринового ряду варфарину з ділянок зв'язування з білками плазми.Спосіб застосування та дозиІндивідуальний, залежно від показань та схеми лікування.Запобіжні заходи та особливі вказівкиЗ обережністю застосовувати у пацієнтів з помірно вираженими та тяжкими порушеннями функції печінки, т.к. можлива кумуляція бікалутаміду в організмі. У період лікування потрібний регулярний контроль функції печінки. У разі розвитку тяжких змін необхідно припинити прийом бікалутаміду.Умови відпустки з аптекЗа рецептомВідео на цю тему
3 454,00 грн
3 411,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
1 221,00 грн
1 180,00 грн
Фасовка: N1 Форма выпуска: концентрат д/приготовления р-ра д/в/в введения Упаковка: фл. Производитель: Тева Завод-производитель: Pharmachemie(Нидерланды) Действующее вещество: Флударабин. .
Склад, форма випуску та упаковкаПігулки - 1 таб. Активна речовина: бікалутамід 50мг. Допоміжні речовини: магнію алюмінометасилікат, карбоксиметилкрохмаль натрію, магнію стеарат, лудіпрес. Склад плівкової оболонки: Опадрай II жовтий 85F32733, в т. ч. полівініловий спирт - 35-49%, тальк - 9.8-25%, макрогол 3350 - 7.35-35.2%, титану діоксид та заліза оксид жовтий - 1. 7 шт. - упаковки осередкові контурні (алюміній/ПВХ) (4) - пачки картонні.Опис лікарської формиТаблетки, покриті плівковою оболонкою жовтого кольору, ромбоподібні, двоопуклі; на поперечному розрізі ядро білого кольору.Фармакотерапевтична групаАнтиандрогенний нестероїдний засіб. Зв'язуючись з рецепторами, що мають спорідненість з андрогенами, пригнічує активність андрогенів, у результаті спостерігається регресія пухлини передміхурової залози. Не має інших видів ендокринної активності.ФармакокінетикаПісля прийому внутрішньо добре всмоктується із ШКТ. Їда не впливає на біодоступність. Зв'язування із білками плазми становить 96%. Інтенсивно метаболізується у печінці шляхом окислення та утворення глюкуронідних кон'югатів. Виводиться у вигляді метаболітів із сечею та жовчю приблизно в рівних пропорціях. Можлива кумуляція бікалутаміду в організмі.Клінічна фармакологіяАнтиандрогенний нестероїдний препарат із протипухлинною активністю.Показання до застосуванняРак передміхурової залози – у складі комбінованої терапії з аналогом ГнРГ або з хірургічною кастрацією.Протипоказання до застосуванняОдночасний прийом із терфенадином, астемізолом, цизапридом; дитячий вік; підвищена чутливість до бікалутаміду. Не призначають пацієнтам жіночої статі.Вагітність та лактаціяНе призначають пацієнтам жіночої статі. Застосування у дітей Препарат не призначають дітям.Побічна діяЗ боку ендокринної системи: припливи, болючість молочних залоз та гінекомастія, зниження лібідо. З боку травної системи: біль у животі, діарея, нудота, блювання, підвищення рівня трансаміназ, жовтяниця, холестаз. З боку центральної нервової системи: можливі астенія, депресія. Дерматологічні реакції: алопеція, відновлення росту волосся, свербіж, сухість шкіри. Інші: гематурія.Взаємодія з лікарськими засобамиПри застосуванні бікалутаміду протягом 28 днів на фоні прийому мідазоламу АUC мідазоламу збільшувалася на 80%. При одночасному застосуванні бікалутаміду з циклоспорином або блокаторами кальцієвих каналів можливе потенціювання або розвиток небажаних реакцій. Теоретично можливе підвищення концентрації бікалутаміду в плазмі при його одночасному застосуванні з інгібіторами мікросомальних ферментів печінки, що може супроводжуватися збільшенням частоти виникнення небажаних реакцій. Дослідження in vitro показали, що бікалутамід може витісняти антикоагулянт кумаринового ряду варфарину з ділянок зв'язування з білками плазми.Спосіб застосування та дозиІндивідуальний, залежно від показань та схеми лікування.Запобіжні заходи та особливі вказівкиЗ обережністю застосовувати у пацієнтів з помірно вираженими та тяжкими порушеннями функції печінки, т.к. можлива кумуляція бікалутаміду в організмі. У період лікування потрібний регулярний контроль функції печінки. У разі розвитку тяжких змін необхідно припинити прийом бікалутаміду.Умови відпустки з аптекЗа рецептомВідео на цю тему
994,00 грн
959,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
391,00 грн
360,00 грн
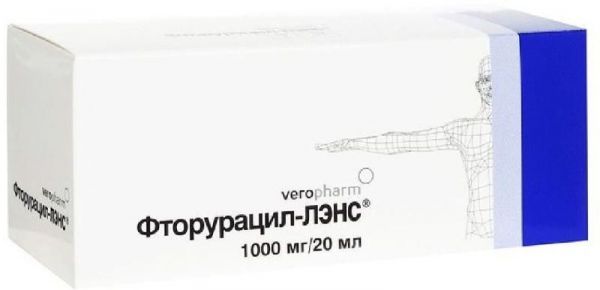
Склад, форма випуску та упаковкаРозчин для внутрішньосудинного та внутрішньопорожнинного введення прозорий - 1 мл: Активна речовина: фторурацил – 50 мг; допоміжні речовини: гідроксид натрію, вода д/і. 5 мл – ампули, пачки картонні (10).Опис лікарської формиРозчин для внутрішньосудинного та внутрішньопорожнинного введення прозорий, від безбарвного до слабо-жовтого кольору, вільний від механічних включень.Фармакотерапевтична групаФторурацил – антиметаболіт урацилу. Механізм дії обумовлений перетворенням препарату в тканинах на активний метаболіт фторуридинмонофосфат, який є конкурентним інгібітором ферменту тимідилатсинтетази, що бере участь у синтезі нуклеїнових кислот. Фторурацил порушує синтез ДНК та викликає утворення структурно недосконалої РНК, пригнічуючи поділ ракових клітин. Активні метаболіти локалізуються усередині клітини.ФармакокінетикаПісля внутрішньовенного введення препарат швидко біотрансформується до активного метаболіту фторуридину монофосфату та розподіляється у пухлинних тканинах, слизовій оболонці кишечника, кістковому мозку, печінці та інших тканинах. Легко проникає через гематоенцефалічний бар'єр, потрапляючи у спинномозкову рідину та тканини головного мозку. Метаболізується переважно в печінці з утворенням неактивних метаболітів. Період напіввиведення фторурацилу залежить від дози, що вводиться, і становить 8-22 хвилини. Близько 20% препарату виводиться нирками у незмінному вигляді протягом 6 годин (90% із цієї кількості виводиться протягом 1-го год) та 60-80% - через дихальні шляхи у формі CO2, незначна кількість виділяється з жовчю.Показання до застосуванняРак товстої та прямої кишки; рак молочної залози; рак стравоходу; рак шлунку; рак підшлункової залози; первинний рак печінки; рак яєчників; рак шийки матки; рак сечового міхура; злоякісні пухлини голови та шиї; рак передміхурової залози; рак надниркових залоз; рак вульви; рак статевого члена; карциноїд.Протипоказання до застосуванняПідвищена чутливість до фторурацилу та/або будь-якого іншого компонента препарату; вагітність та період годування груддю; виражена лейкопенія, нейтропенія, тромбоцитопенія, стоматит, виявлення слизової оболонки шлунково-кишкового тракту (ЖКТ), псевдомембранозний ентероколіт.Вагітність та лактаціяПротипоказано застосовувати препарат під час вагітності та в період лактації.Побічна діяЗ боку органів кровотворення: лейкопенія, нейтропенія, рідко – тромбоцитопенія, анемія. Найбільш значне падіння кількості лейкоцитів зазвичай спостерігається з 9 по 14 днів (аж до 25 днів), тромбоцитів – з 7 по 17 день лікування. Дуже рідко – панцитопенія, агранулоцитоз. З боку травної системи: анорексія, нудота, блювання, запалення та/або виявлення слизових оболонок шлунково-кишкового тракту (в т.ч.стоматит), діарея, кровотеча із шлунково-кишкового тракту, печія та зміна смаку, глосит, фарингіт, езофагіт, мукозит, порушення функції , холецистит. З боку серцево-судинної системи: дуже рідко – біль у серці, аритмії, ішемія міокарда, міокардит, інфаркт міокарда, стенокардія, серцева недостатність, кардіоміопатія, кардіогенний шок, зниження артеріального тиску. З боку нервової системи: рідко – мозочкова атаксія, порушення чутливості, дезорієнтація, сплутаність свідомості, ейфорія ністагм, ретробульбарний неврит, астенія, біль голови. З боку органів чуття: кон'юнктивіт, подразнення слизової оболонки очей, сльозотеча внаслідок стенозу слізних проток, світлобоязнь, катаракта, кіркова сліпота (при високих дозах), диплопія, порушення зору. З боку репродуктивної системи: оборотне пригнічення функції статевих залоз, що призводить до аменореї або азооспермії. З боку шкіри та шкірних придатків: алопеція, гіперпігментація шкіри, сухість і тріщини шкіри, телеангіектазії, синдром долонно-підошовної еритродизестезії (відчуття поколювання в кистях і стопах з подальшою появою болю, гіперемії та опухання), зміна та сх. фотосенсибілізація. Алергічні реакції: висипання на шкірі, дерматит, кропив'янка, бронхоспазм, анафілактичний шок (рідко). Інші: «приплив» крові до обличчя, лихоманка (рідко), тромбофлебіт у місці введення, носова кровотеча, кашель, задишка, гіперурикемія, слабкість, розвиток вторинних інфекцій.Взаємодія з лікарськими засобамиКальція фолінат посилює терапевтичний та токсичний ефекти фторурацилу. При застосуванні в комбінації з іншими цитостатиками та інтерфероном-альфа також може спостерігатись посилення як протипухлинного ефекту, так і токсичності фторурацилу. При тривалому сумісному застосуванні з мітоміцином С спостерігалася поява гемолітико-уремічного синдрому. Одночасне використання антикоагулянтів, похідних кумарину, таких як варфарин, може підвищувати антикоагулянтний ефект. Тіазидові діуретики можуть посилювати мієлосупресивні ефекти протипухлинних препаратів. При застосуванні в комбінації з левамізолом значно збільшується рівень гепатотоксичності (підвищення активності лужної фосфатази часто супроводжується збільшенням сироваткових трансаміназ або білірубіну). При одночасному прийомі з препаратом соривудин відзначалася виражена лейкопенія, що в деяких випадках призвела до летального результату. Фторурацил не слід застосовувати після та спільно з терапією амінофеназоном, фенілбутазоном та сульфонамідами. Хлордіазепоксид, дисульфірам, гризеофульвін та ізоніазид можуть посилювати активність фторурацилу. У зв'язку з придушенням природних захисних механізмів при лікуванні фторурацилом можлива інтенсифікація процесу реплікації вакцинного вірусу або зниження вироблення антитіл у відповідь на введення вакцини при вакцинації живими або інактивованими вакцинами, тому інтервал між закінченням застосування препарату та вакцинацією живими року.Спосіб застосування та дозиФторурацил входить до складу багатьох схем хіміотерапевтичного лікування, у зв'язку з чим при виборі шляху введення, режиму та доз у кожному індивідуальному випадку слід керуватися даними спеціальної літератури. Препарат вводять внутрішньовенно струминно або шляхом повільної інфузії, внутрішньоартеріально, внутрішньопорожнинно. Рекомендуються такі дози та режими: 500 мг/м2 або 12-13.5 мг/кг щодня протягом 3-5 днів, інтервал між курсами – 4 тижні; 600 мг/м2 або 15 мг/кг (найвища разова доза 1 г) 1 раз на тиждень, 6-10 доз; 600 мг/м2 в 1 та 8 дні внутрішньовенно у комбінаціях з іншими цитостатиками; 1 г/м2/добу внутрішньовенно краплинно у вигляді постійної інфузії протягом 96-100 год; При застосуванні у поєднанні з кальцієм фолінатом дозу фторурацилу зазвичай зменшують на 25-30%.ПередозуванняОзнаки та симптоми передозування включають нудоту, блювання, діарею, виразковий стоматит та шлункову кровотечу, пригнічення функції кісткового мозку (тромбоцитопенія, лейкопенія та агранулоцитоз). При передозуванні слід контролювати функцію кровотворення хворих протягом щонайменше 4 тижнів, у разі виникнення порушень проводять симптоматичну терапію. Специфічний антидот до фторурацилу не відомий.Запобіжні заходи та особливі вказівкиФторурацил є цитотоксичним препаратом, тому у поводженні з ним необхідно бути обережним. При появі стоматиту або діареї лікування препаратом слід припинити до зникнення цих симптомів. Початкова доза повинна бути зменшена на 1/3 або 1/2 у таких випадках: зниження маси тіла, післяопераційний період не менше ніж 30 днів після великого хірургічного втручання, недостатня функція кісткового мозку, порушення функції печінки або нирок. Слід бути обережним при призначенні хворим, які раніше піддавалися впливу високих доз радіації на область малого тазу або отримували алкілуючі препарати. У період лікування необхідно контролювати загальну кількість лейкоцитів, абсолютну кількість нейтрофілів, тромбоцитів, визначати гематокрит, гемоглобін, активність «печінкових» трансаміназ та концентрацію білірубіну, оглядати порожнину рота хворого для виявлення ознак стоматиту. Чоловікам та жінкам дітородного віку під час лікування фторурацилом та як мінімум протягом 3 місяців після цього слід застосовувати надійні методи контрацепції. У разі утворення осаду під впливом низьких температур, розчин перед використанням слід нагріти до 60°C, енергійно струшуючи, а потім охолодити до кімнатної температури. У період лікування необхідно утримуватися від керування автомобілем та занять потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови відпустки з аптекЗа рецептомВідео на цю тему
1 455,00 грн
1 411,00 грн
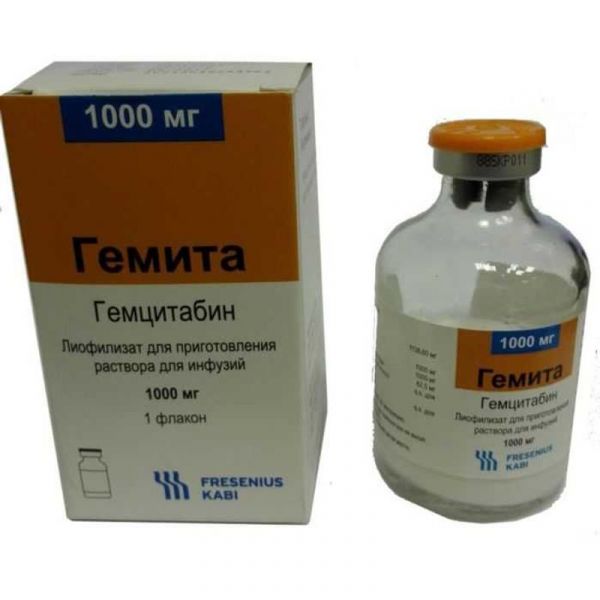
Склад, форма випуску та упаковкаЛіофілізат - 1 фл. Активна речовина: гемцитабіну гідрохлорид 227,72 мг/1138,6 мг/1594,04 мг (еквівалентно 200, 1000 та 1400 мг гемцитабіну відповідно). Допоміжні речовини: ; манітол; 200/1000/1400 мг; натрію ацетату тригідрат; - 12,5/62,5/87,5 мг; хлористоводнева кислота ;— ;qs ;для коригування ;pH; натрію гідроксид ;— ;qs ;для коригування ;pH. Ліофілізат для виготовлення розчину для інфузій 1400 мг. ;У флаконах прозорого скла, тип I ;(USP). Флакони закупорені гумовою пробкою з алюмінієвою обкаткою та запобіжним ковпачком ;(flip-off) ;з пластмаси. Кожен флакон у картонній пачці.Опис лікарської формиЛіофілізат для виготовлення розчину для інфузій.Фармакотерапевтична групаГеміт - протипухлинний препарат, антиметаболіт групи аналогів піримідину, пригнічує синтез ДНК. Виявляє циклоспецифічність, діючи на клітини у фазі S та на межі фаз G1 та S. Метаболізується у клітині під дією нуклеозидкіназ до активних дифосфатних та трифосфатних нуклеозидів. Дифосфатні нуклеозиди пригнічують дію рибонуклеотидредуктази (єдиного ферменту, що каталізує утворення дезоксинуклеозидтрифосфатів, необхідних для синтезу ДНК). Трифосфатні нуклеозиди здатні вбудовуватися в ланцюжок ДНК (меншою мірою РНК), що призводить до припинення подальшого синтезу ДНК та запрограмованого лізису клітини (апоптоз). Гемцитабін є також сильним радіосенсибілізуючим засобом навіть у концентраціях нижчих, ніж цитотоксичні.Клінічна фармакологіяАнтиметаболіт.Показання до застосуванняМісцево-поширений або метастатичний недрібноклітинний ;рак легкого ;як терапії першої лінії в комбінації з ;цисплатином ;і в монотерапії у літніх пацієнтів з функціональним статусом, рівним 2 (за шкалою ECOG-BОЗ); неоперабельний, місцево-рецидивний або метастатичний; місцево-поширений або метастатичний уротеліальний рак (рак сечового міхура, ниркової балії, сечоводів, уретри); місцево-поширений або метастатичний ;рак яєчників ;як монотерапії або в поєднанні з ;карбоплатином ;у пацієнтів з прогресуванням захворювання після проведення першої лінії терапії на основі платино-вмісних препаратів; місцево-поширений або метастатичний; рак підшлункової залози; місцево-поширений або метастатичний; рак шийки матки.Протипоказання до застосуванняВагітність; період грудного вигодовування; дитячий вік до 18 років (відсутність достатніх даних щодо ефективності та безпеки); підвищена чутливість до активної речовини або будь-якої з допоміжних речовин препарату. З обережністю слід призначати Геміту при порушенні функції печінки та/або нирок, пригніченні кістковомозкового кровотворення (у тому числі на тлі супутньої променевої або хіміотерапії), серцево-судинних захворюваннях, при метастатичному ураженні печінки, гепатиті, алкоголізмі, при одночасно проведеній променевій інфекційні захворювання вірусної, грибкової або бактеріальної природи (у тому числі вітряної віспи, що оперізує лишаї).Побічна діяПобічні реакції, що зустрічалися частіше, ніж у поодиноких випадках, перераховані відповідно до наступної градації: дуже часто (> 10%); часто (>1% до <10%); нечасто (>0.1% до <1%); рідко (>0.01% до <0.1%); дуже рідко (<0.01%). З боку органів кровотворення: дуже часто - лейкопенія, нейтропенія, тромбоцитопенія, анемія; часто – фебрильна нейтропенія; дуже рідко – тромбоцитоз. З боку травної системи: дуже часто - нудота, блювання, підвищення активності печінкових трансаміназ (АСТ, АЛТ), ЛФ; часто - ;анорексія, ;діарея, запор, ;стоматит, підвищення концентрації білірубіну; рідко – підвищення активності ГГТ. З боку сечовидільної системи: дуже часто – гематурія та протеїнурія легкого ступеня; рідко – ниркова недостатність, клінічні ознаки та симптоми, схожі з гемолітико-уремічним синдромом (зниження гемоглобіну, тромбоцитопенія, збільшення концентрації білірубіну, креатиніну, сечовини та/або активності ЛДГ у сироватці крові). З боку шкіри та підшкірних тканин: дуже часто – шкірні висипання, що супроводжуються свербінням, алопеція; часто -; шкірний свербіж, підвищена пітливість; рідко - виразки шкіри, утворення бульбашок; дуже рідко - виражені шкірні реакції, включаючи десквамацію та бульозні висипання. З боку дихальної системи: дуже часто - задишка; часто – кашель, риніт; нечасто -; бронхоспазм, інтерстиціальний пневмоніт, набряк легені; рідко – гострий респіраторний дистрес-синдром. З боку серцево-судинної системи: рідко - зниження артеріального тиску, інфаркт міокарда, серцева недостатність, аритмія. З боку нервової системи: часто - головний біль, підвищена сонливість, безсоння. Інші: дуже часто – грипоподібний синдром, периферичні набряки; часто - підвищення температури тіла, озноб, ; астенія, болі в спині,; міалгія; нечасто – набряклість особи; дуже рідко – анафілактичні реакції. Антидот для; гемцитабіна; невідомий. При введенні Геміту в дозах до 5700 мг/м2 внутрішньовенно крапельно за 30 хвилин кожні 2 тижні рівень токсичності лікування залишався прийнятним. При підозрі на передозування; гемцитабіну; слід контролювати ступінь цитопенії і при необхідності призначити підтримуючу терапію.Взаємодія з лікарськими засобамиПроменева терапія Супутня променева терапія (одночасно з введенням Геміту або з інтервалом < 7 днів до початку лікування): в даній ситуації токсичність лікування залежить від багатьох факторів, включаючи дозу ;гемцитабіна ;і частоту його введення, дозу випромінювання, метод променевої терапії, характер опромінюваної тканини та її обсяг. Було показано, що ;гемцитабін ;має радіосенсибілізуючу активність. В одному дослідженні, де пацієнти з недрібноклітинним ; раком ; легкого отримували ; гемцитабін ; оболонок, головним чином ;езофагіта ;і пневмоніту,особливо у пацієнтів з великим обсягом опромінення тканин (медіана обсягу опромінюваної тканини 4795 см3). У подальших дослідженнях було показано, що поєднання нижчих доз; гемцитабіна; і променевої терапії краще переноситься пацієнтами і характеризується передбачуваним профілем токсичності. Так, в одному з досліджень II фази пацієнтам з недрібноклітинним ;раком ;легкого проводилася променева терапія в дозі 60 Гр спільно з введенням ;гемцитабіну ;(600 мг/м2 4 рази) і ;цисплатину ;(80 мг/м2 2 рази) протягом 6 тижнів.легені проводилася променева терапія в дозі 60 Гр спільно з введенням ;гемцитабіну ;(600 мг/м2 4 рази) та ;цисплатину ;(80 мг/м2 2 рази) протягом 6 тижнів.легені проводилася променева терапія в дозі 60 Гр спільно з введенням ;гемцитабіну ;(600 мг/м2 4 рази) та ;цисплатину ;(80 мг/м2 2 рази) протягом 6 тижнів. Послідовна терапія (перерва > 7 днів): за існуючими даними, введення; гемцитабіну; більш ніж за 7 днів до початку променевої терапії або більш ніж через 7 днів після її завершення не супроводжується збільшенням токсичності, за винятком ураження шкіри, пов'язаного з введенням хіміопрепарату після опромінення. Лікування; гемцитабіном; може бути розпочато через 7 днів після опромінення або після вирішення всіх гострих променевих реакцій. Як при супутньому, так і при послідовному застосуванні ;гемцитабіна ;і променевої терапії можливе променеве ураження опромінених тканин (наприклад, ;езофагіт, коліт і пневмоніт). Інші види взаємодії При одночасному застосуванні з живими атенуйованими вакцинами можлива інтенсифікація процесу реплікації вакцинного вірусу, посилення його побічних/несприятливих ефектів та/або зниження вироблення антитіл в організмі хворого у відповідь на введення вакцини. Імунодепресанти (у тому числі ;азатіоприн, ;хлорамбуцил, глюкокортикоїд, ;циклофосфамід, ;циклоспорин, ;меркаптопурин) збільшують ризик виникнення інфекцій. Дослідження сумісності Геміт не проводилися. Змішувати препарат з іншими лікарськими засобами не рекомендується.Спосіб застосування та дозиВ/в; краплинно протягом 30 хв. Недрібноклітинний рак легені Монотерапія: рекомендована доза препарату - 1000 мг/м2; в 1-й, 8-й і 15-й дні кожного 28-денного циклу. Комбінована терапія з цисплатином: рекомендована доза препарату - 1250 мг/м2; в 1-й і 8-й день кожного 21-денного циклу або 1000 мг/м2; в 1-й, 8-й і 15-й дні кожного -денний цикл. Цисплатин вводиться в дозі 70 мг/м2; в 1-й день циклу на тлі водного навантаження після інфузії препарату Геміта. Комбінована терапія з карбоплатином: рекомендована доза препарату - 1000 або 1200 мг/м2; в 1-й і 8-й день кожного 21-денного циклу. Карбоплатин вводиться в дозі AUC 5 мг/мл/хв у 1-й день циклу після інфузії препарату Геміта. Рак молочної залози Комбінована терапія: як терапія 1-ї лінії при прогресуванні захворювання після неоад'ювантної терапії, що включає антрацикліни, рекомендована доза препарату - 1250 мг/м2; в 1-й і 8-й дні в поєднанні з паклітакселом, який вводиться після введення препарату у дозі 175 мг/м2; в 1-й день кожного 21-денного циклу внутрішньовенно краплинно приблизно протягом 3 год. Уротеліальний рак Монотерапія: рекомендована доза препарату - 1250 мг/м2; в 1-й, 8-й і 15-й дні кожного 28-денного циклу. Комбінована терапія: рекомендована доза препарату - 1000 мг/м2; в 1-й, 8-й і 15-й дні в поєднанні з цисплатином, який вводиться в дозі 70 мг/м2; відразу після інфузії препарату Геміта в 1-й або 2 день кожного 28-денного циклу. Рак яєчників Монотерапія: рекомендована доза препарату - 800-1250 мг/м2; в 1-й, 8-й і 15-й дні кожного 28-денного циклу. Рак підшлункової залози Монотерапія: рекомендована доза препарату - 1000 мг/м2; 1 раз на тиждень протягом 7 тижнів з наступною тижневою перервою. Потім препарат вводиться в 1-й, 8-й та 15-й дні кожного 28-денного циклу. Рак шийки матки (місцерозповсюджений або метастатичний) Комбінована терапія: при місцеворозповсюдженому раку (неоад'ювантно) та при метастатичному раку гемцитабін вводиться в дозі 1250 мг/м2; у 1-му та 8-му дні кожного 21-денного циклу. Цисплатин вводиться після введення препарату Геміту в дозі 70 мг/м2; в 1-й день циклу на фоні гіпергідратації. При місцеворозповсюдженому раку при одночасної променевої терапії препарат Геміта вводиться 1 раз на тиждень протягом 6 тижнів у дозі 125 мг/м2; з наступним (безпосередньо після введення препарату Геміту) введенням цисплатину в дозі 40 мг/м2; променевої терапії. Променеву терапію проводять за 28 фракцій у разовій осередковій дозі 1,8 Гр 5 днів на тиждень до сумарної осередкової дози 50,4 Гр. Зміна дози препарату у зв'язку із проявом гематологічної токсичності Початок циклу лікування. Незалежно від показань перед кожним введенням препарату необхідно оцінювати кількість тромбоцитів та гранулоцитів. Умовою початку лікування є абсолютна кількість нейтрофілів не менше 1500/мкл та кількість тромбоцитів не менше 100000/мкл. У разі розвитку гематологічної токсичності під час проведення циклу терапії доза препарату Геміт може бути зменшена або її введення відкладено відповідно до наступних рекомендацій. 1. Модифікація дози препарату Геміту, що застосовується в монотерапії або в комбінації з цисплатином при лікуванні раку сечового міхура, недрібноклітинного раку легені та раку підшлункової залози: - при абсолютній кількості нейтрофілів >1000/мкл та кількості тромбоцитів >100000/мкл доза не змінюється та становить 100% від попередньої дози; - при абсолютній кількості нейтрофілів 500-1000/мкл або кількості тромбоцитів 50000-100000/мкл доза становить 75% від попередньої дози; - при абсолютній кількості нейтрофілів <500/мкл або кількості тромбоцитів <50000/мкл введення препарату слід відкласти*. 2. Модифікація дози препарату Геміту, що застосовується у комбінації з паклітакселом при лікуванні раку молочної залози: - при абсолютній кількості нейтрофілів ≥1200/мкл та кількості тромбоцитів >75000/мкл доза не змінюється та становить 100% від стандартної дози; - при абсолютній кількості нейтрофілів 1000-1200/мкл або кількості тромбоцитів 50000-75000/мкл доза становить 75% від стандартної дози; - при абсолютній кількості нейтрофілів 700–<1000/мкл та кількості тромбоцитів ≥50000/мкл доза становить 50% від стандартної дози; - при абсолютній кількості нейтрофілів <700/мкл чи кількості тромбоцитів <50000/мкл введення препарату необхідно відкласти**. 3. Модифікація дози препарату Геміту, що застосовується в комбінації з карбоплатином при лікуванні раку яєчників: - при абсолютній кількості нейтрофілів >1500/мкл та кількості тромбоцитів ≥100000/мкл доза не змінюється та становить 100% від стандартної дози; - при абсолютній кількості нейтрофілів 1000-1500/мкл або кількості тромбоцитів 75000-100000/мкл доза становить 50% від стандартної дози; - при абсолютній кількості нейтрофілів <1000/мкл чи кількості тромбоцитів <75000/мкл введення препарату необхідно відкласти**. * ;При збільшенні кількості нейтрофілів до 500/мкл та тромбоцитів до 50000/мкл введення препарату Геміту може бути продовжено в рамках циклу. ** ;Лікування в рамках циклу не відновлюється. Чергове введення препарату Геміт проводиться в 1-й день чергового циклу, коли кількість нейтрофілів досягає значень не менше 1500/мкл і тромбоцитів; - 100000/мкл. Доза препарату Геміта на черговому циклі повинна бути зменшена на 25% при всіх показаннях у випадках, якщо за попереднього циклу спостерігалося: - зниження абсолютної кількості нейтрофілів <500/мкл, що триває понад 5 днів; - зниження абсолютної кількості нейтрофілів <100/мкл, що триває понад 3 дні; - фебрильна нейтропенія; - зниження кількості тромбоцитів <25000/мкл; цикл був відкладений більш ніж на 1 тиждень через гематологічну токсичність. Спосіб введення Інфузійне введення препарату Геміт зазвичай добре переноситься пацієнтами і може проводитися в амбулаторних умовах. У разі екстравазації інфузію припиняють та відновлюють введення препарату в іншу вену. Після введення препарату Геміт пацієнт повинен спостерігатися протягом деякого часу. Особливі групи пацієнтів Пацієнти з порушенням функції печінки та нирок. ;Застосовувати препарат Геміту у хворих з печінковою недостатністю або з порушеною функцією нирок слід з обережністю, т.к. достатніх даних щодо застосування препарату ця категорія пацієнтів не має. Ниркова недостатність помірної або середньої тяжкості (швидкість клубочкової фільтрації від 30 до 80 мл/хв) не помітно впливає на фармакокінетику гемцитабіну. Літні пацієнти (>65 років). Препарат Геміту добре переноситься пацієнтами старше 65 років. Специфічних рекомендацій щодо зміни дози препарату для цієї популяції відсутні. Діти (<18 років). ;Препарат Геміт не рекомендується призначати дітям до 18 років у зв'язку з недостатньою інформацією з безпеки та ефективності препарату в даній популяції. Рекомендації щодо приготування розчину для інфузій Як розчинник використовується лише 0,9% розчин натрію хлориду без консервантів. Для приготування розчину для інфузій вміст флакона 200 мг розчиняють не менш ніж у 5 мл, 1000 мг; - не менше ніж у 25 мл і 1400 мг; - не менш ніж у 35 мл 0,9% розчину натрію хлориду для ін'єкцій. Кожен флакон акуратно збовтують до повного розчинення ліофілізату. Отриманий розчин має бути прозорим. Максимальна концентрація гемцитабіну не повинна перевищувати 40 мг/мл. Використання розчинів з концентрацією вище 40 мг/мл може супроводжуватися неповним розчиненням. Приготовлений розчин препарату Геміту, що містить потрібну дозу препарату, перед введенням розбавляють 0,9% розчином натрію хлориду для ін'єкцій у кількості, достатній для 30-хвилинної внутрішньовенної інфузії. Перед парентеральним введенням необхідно візуально контролювати приготовлений розчин на наявність механічних домішок та зміну кольору. Приготовлений розчин препарату Геміта стабільний з фізичної та хімічної точки зору протягом 24 годин за умови, що він зберігався при контрольованій кімнатній температурі (від 20 до 25°C). З мікробіологічної точки зору, приготовлений розчин повинен бути використаний негайно. У випадку, якщо приготований розчин не був використаний відразу і його приготування проводилося в контрольованих та валідованих асептичних умовах, час зберігання зазвичай становить не більше ніж 24 години при кімнатній температурі (від 20 до 25 °C).Запобіжні заходи та особливі вказівкиЛікування Гемітою можна проводити лише під наглядом лікаря, який має досвід проведення протипухлинної хіміотерапії. Перед кожним введенням препарату необхідно визначати лейкоцитарну формулу та кількість тромбоцитів у крові. При ознаках пригнічення функції кісткового мозку, спричиненого Гемітою, необхідно припинити лікування або скоригувати дозу. Необхідно проводити регулярне обстеження хворого та оцінку функції нирок та печінки. Геміти при метастазах у печінці, при гепатиті та алкоголізмі в анамнезі, а також при цирозі печінки збільшує ризик розвитку печінкової недостатності. При появі ознак розвитку небажаних явищ з боку дихальної системи (наприклад, набряк легень, інтерстиціальний пневмоніт або респіраторний дистрес-синдром у дорослих) на фоні лікування Гемітою лікування слід припинити та призначити відповідну терапію. При появі перших ознак мікроангіопатичної гемолітичної анемії, таких як швидке зниження гемоглобіну з супутньою тромбоцитопенією, підвищення сироваткової концентрації білірубіну, креатиніну, азоту, сечовини або підвищення активності ЛДГ, препарат слід відмінити. Збільшення тривалості інфузії та частоти введень призводить до зростання токсичності. Залежно від ступеня токсичності дозу можна знижувати протягом кожного циклу або з початком нового циклу ступінчасто. Під час лікування та протягом 6 місяців після закінчення лікування препаратом слід використовувати надійні методи контрацепції. Чоловікам, які отримують Геміт, рекомендується вдатися до кріоконсервації сперми до початку лікування у зв'язку з ризиком безпліддя, зумовленим застосуванням даного препарату. Гемцитабін можна починати вводити після дозволу гострих променевих реакцій або не раніше, ніж через 7 днів після закінчення променевої терапії. Гемцитабін; в монотерапії або в комбінації з іншими протипухлинними засобами проявляє активність при прогресуючому дрібноклітинному раку легені, прогресуючому раку яєчка і раку жовчних проток. Дані про вплив терапії Гемітою на здатність керувати транспортним засобом та працювати з механізмами відсутні, однак деякі побічні дії препарату, такі як підвищена сонливість, можуть негативно впливати на здатність керувати автомобілем та виконання потенційно небезпечних видів діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій. що вимагає дотримання обережності.Умови відпустки з аптекЗа рецептомВідео на цю тему
1 628,00 грн
230,00 грн
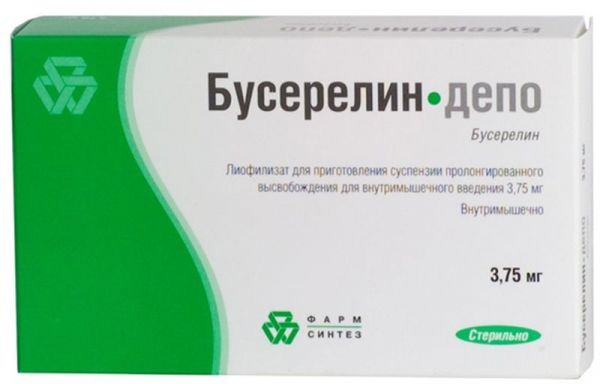
Склад, форма випуску та упаковкаЛіофілізат для приготування суспензії для внутрішньом'язового введення пролонгованої дії, що містить 3,75 мг бусереліну.Опис лікарської формиДозування 3,75 мг – 1 ін'єкція. Ліофілізат для приготування суспензії для внутрішньом'язового введення пролонгованої дії.Фармакотерапевтична групаПротипухлинний засіб, гонадотропін-рилізинг гормону (ГнРГ) аналог.Показання до застосуванняГормонозалежний рак передміхурової залози; Рак молочної залози; Ендометріоз (перед- та післяопераційний періоди); Міома матки; Гіперпластичні процеси ендометрію; Лікування безпліддя (при проведенні програми екстракорпорального запліднення (ЕКО)).Протипоказання до застосуванняВагітність; Період лактації; Підвищена чутливість до компонентів препарату.Взаємодія з лікарськими засобамиОдночасне застосування препарату "Бусерелін-лонг" з препаратами, що містять статеві гормони (наприклад, в режимі індукції овуляції), може сприяти виникненню синдрому гіперстимуляції яєчників. При одночасному застосуванні Бусерелін-лонг може знижувати ефективність гіпоглікемічних засобів.Спосіб застосування та дозиПри гормонозалежному раку передміхурової залози Бусерелін-лонг вводять у дозі 3,75 мг (1 ін'єкція) внутрішньом'язово (в/м) кожні 4 тижні. При лікуванні ендометріозу, гіперпластичних процесів ендометрію препарат вводять у дозі 3,75 мг внутрішньом'язово одноразово кожні 4 тижні. Лікування слід розпочинати у перші п'ять днів менструального циклу. Тривалість лікування – 4-6 місяців. При лікуванні міоми матки Бусерелін-лонг вводять у дозі 3,75 мг внутрішньом'язово одноразово кожні 4 тижні. Лікування слід розпочинати у перші п'ять днів менструального циклу. Тривалість лікування перед операцією 3 місяці, в інших випадках - 6 місяців; При лікуванні безпліддя методом екстракорпорального запліднення (ЕКО) Бусерелін-лонг вводять у дозі 3,75 мг (1 ін'єкція) внутрішньом'язово одноразово на початку фолікулінової (на 2-й день менструального циклу) або в середині лютеїнової фази (21 - 24 дн). менструального циклу, що передує стимуляції. Після блокади гіпофізарної функції, підтвердженої зниженням концентрації естрогенів у сироватці крові не менше, ніж на 50 % від вихідного рівня (зазвичай визначається через 12 - 15 днів після ін'єкції Бусерелін-лонг), за відсутності кіст яєчника (за даними УЗД), товщиною ендометрію більше 5 мм, починається стимуляція суперовуляції гонадотропними гормонами під ультразвуковим моніторингом та контролем рівня естрадіолу у сироватці кровіУмови відпустки з аптекЗа рецептомВідео на цю тему
879,00 грн
844,00 грн
Склад, форма випуску та упаковкаЛіофілізат – 1 фл.: гемцитабін (у формі гідрохлориду) 1000 мг. Флакони (1) - пачки картонні.Опис лікарської формиЛіофілізат для приготування розчину для інфузії білого або майже білого кольору.Фармакотерапевтична групаПротипухлинний засіб, антиметаболіт.ФармакокінетикаCmax гемцитабіну (від 3.2 до 45.5 мкг/мл) досягається через 5 хвилин після закінчення інфузій. Фармакокінетичний аналіз досліджень з одноразовим та багаторазовим введенням доз показує, що Vd значною мірою залежить від статі. Зв'язування гемцитабіну з білками плазми незначне. В організмі гемцитабін швидко метаболізується під дією цитидиндезамінази в печінці, нирках, крові та інших тканинах, в результаті чого утворюються гемцитабін моно-, ді-і трифосфати (dFdCMP, dFdCDP і dFdCTP), з яких активними вважаються dFdCDP і dFd. Гемцитабін швидко виводиться з організму з сечею переважно у вигляді неактивного метаболіту 2'-дезокси-2', 2'-дифторуридину. Менше 10% введеної внутрішньовенної дози виявляється у сечі у формі незміненого гемцитабіну. Системний кліренс, який коливається приблизно від 30 л/год/м2 до 90 л/год/м2, залежить від віку та статі: швидкість виведення у жінок приблизно на 25% нижче, ніж у чоловіків; як у чоловіків, і у жінок швидкість виведення знижується з віком. T1/2 коливається від 42 хв до 94 хв. При дотриманні рекомендованого режиму дозування повне виведення гемцитабіну відбувається протягом 5-11 годин від початку інфузії. При введенні раз на тиждень гемцитабін не накопичується в організмі. Комбінована терапія гемцитабіном та паклітакселом. При сумісному введенні гемцитабіну та паклітакселу фармакокінетика препаратів не змінюється. Комбінована терапія гемцитабіном та карбоплатином. При сумісному введенні гемцитабіну та карбоплатину фармакокінетика гемцитабіну не змінюється. Порушення функції нирок. Ниркова недостатність легкого або помірного ступеня (кліренс креатиніну 30-80 мл/хв) не істотно впливає на фармакокінетику гемцитабіну.ФармакодинамікаПротипухлинний засіб, антиметаболіт групи аналогів піримідину, пригнічує синтез ДНК. Виявляє циклоспецифічність, діючи на клітини у фазах S та Gl/S. Метаболізується у клітині під дією нуклеозидкіназ до активних дифосфатних та трифосфатних нуклеозидів. Дифосфатні нуклеозиди пригнічують дію рибонуклеотидредуктази (єдиного ферменту, що каталізує утворення дезоксинуклеозидтрифосфатів, необхідних для синтезу ДНК). Трифосфатні нуклеозиди здатні вбудовуватися в ланцюжок ДНК (меншою мірою РНК), що призводить до припинення подальшого синтезу ДНК та запрограмованої загибелі клітини (апоптоз). Гемцитабін є також сильним радіосенсибілізуючим засобом навіть у концентраціях нижчих за цитотоксичні.Клінічна фармакологіяПротипухлинний препарат. Антиметаболіт.Показання до застосуваннямісцевопоширений або метастатичний недрібноклітинний рак легені як терапії першої лінії в комбінації з цисплатином, а також у монотерапії у літніх пацієнтів з функціональним статусом, рівним 2; нерезектабельний, місцеворецидивний або метастатичний рак молочної залози у складі комбінованої терапії з паклітакселом після проведення неоад'ювантної та/або ад'ювантної терапії з включенням антрациклінів за відсутності протипоказань до їх призначення; місцевопоширений або метастатичний уротеліальний рак (рак сечового міхура, ниркової балії, сечоводів, уретри); місцевопоширений або метастатичний епітеліальний рак яєчників як монотерапія або у поєднанні з карбоплатином у пацієнтів з прогресуванням захворювання після проведення першої лінії терапії на основі платиносмістких препаратів; місцевопоширений або метастатичний рак підшлункової залози; місцеворозповсюджений або метастатичний рак шийки матки.Протипоказання до застосуванняпідвищена чутливість до активної речовини або до будь-якої з допоміжних речовин; вагітність та період годування груддю; дитячий вік до 18 років (відсутність достатніх даних щодо ефективності та безпеки). З обережністю: при порушенні функції печінки та/або нирок, пригніченні кістковомозкового кровотворення (у тому числі на тлі супутньої променевої або хіміотерапії), серцево-судинних захворюваннях в анамнезі, при метастатичному ураженні печінки, гепатиті, алкоголізмі, при одночасно проведеній променевій інфекційні захворювання вірусної, грибкової або бактеріальної природи (у тому числі вітряної віспи, що оперізує лишаї).Вагітність та лактаціяПротипоказаний: вагітність та період годування груддю. Протипоказаний дітям до 18 років (відсутність достатніх даних щодо ефективності та безпеки).Побічна діяПобічні реакції, що зустрічалися частіше, ніж у поодиноких випадках, перераховані відповідно до наступної градації: дуже часто (> 10%); часто (> 1% до 0.1% до 0.01% до З боку органів кровотворення: часто – лейкопенія, нейтропенія, тромбоцитопенія, анемія; часто – фебрильна нейтропенія; дуже рідко – тромбоцитоз. З боку системи травлення: дуже часто – нудота, блювання, підвищення активності “печінкових” трансаміназ (аспартатамінотрансферази, аланінамінотрансферази), лужної фосфатази; часто – анорексія, діарея, запор, стоматит, підвищення концентрації білірубіну; рідко – підвищення активності гамма-глутамілтрансферази; частота не може бути оцінена на підставі наявних даних - ішемічний коліт, токсичне ураження печінки, включаючи печінкову недостатність з летальним кінцем. З боку сечовидільної системи: дуже часто – гематурія та протеїнурія легкого ступеня; частота не може бути оцінена на підставі наявних дачних – гостра ниркова недостатність, клінічні ознаки та симптоми, схожі з гемолітико-уремічним синдромом (зниження гемоглобіну, тромбоцитопенія, збільшення вмісту білірубіну, креатиніну, сечовини та/або лактатдегідрогенази у сироватці). З боку шкіри та шкірних придатків: дуже часто – шкірні висипання, що супроводжуються свербінням, алопеція; часто - свербіж шкіри, підвищена пітливість; рідко - виразки, утворення бульбашок, дуже рідко - виражені шкірні реакції, включаючи десквамацію та бульозні висипання; частота може бути оцінена - синдром Лайелла, синдром Стівенса-Джонсона. З боку дихальної системи: дуже часто – задишка; часто – кашель, риніт, нечасто – бронхоспазм, інтеретиційна пневмонія; частота може бути оцінена - набряк легені, гострий респіраторний дистресс-синдром. З боку серцево-судинної системи: рідко – зниження артеріального тиску, інфаркт міокарда, частота не може бути оцінена – аритмія (переважно суправентрикулярна), серцева недостатність, клінічні ознаки периферичного васкуліту та гангрени. З боку нервової системи: часто – головний біль, підвищена сонливість, безсоння; частота може бути оцінена - інсульт. Інші: дуже часто – почуття нездужання, грипоподібний синдром, периферичні набряки; часто - підвищення температури тіла, озноб, астенія, біль у спині, міалгія; рідко – набряклість особи, реакції у місці введення; дуже рідко – анафілактичні реакції.Взаємодія з лікарськими засобамиСпецифічних досліджень взаємодій гемцитабіну не проводилося. Променева терапія Супутня променева терапія (одночасно із введенням гемцитабіну або з інтервалом Послідовна терапія (перерва > 7 днів): за існуючими даними, введення гемцитабіну більш ніж за 7 днів до початку променевої терапії або більш ніж через 7 днів після завершення не супроводжується збільшенням токсичності, за винятком ураження шкіри, пов'язаного з введенням хіміопрепарату після опромінення. Лікування гемцитабіном може бути розпочато через 7 днів після опромінення або після розв'язання всіх гострих променевих реакцій. Як при супутньому, так і при послідовному застосуванні гемцитабіну і променевої терапії можливе променеве ураження тканин, що опромінюються (напр., езофагіт, коліт і пневмоніт). Імунодепресанти (азатіоприн, хлорамбуцил, глюкокортикостероїди, циклофосфамід, циклоспорин, меркаптопурин) збільшують ризик розвитку інфекцій. Інші види взаємодії При одночасному застосуванні з живими вірусними вакцинами можлива інтенсифікація процесу реплікації вакцинного вірусу посилення його побічних/несприятливих ефектів та/або зниження вироблення антитіл в організмі хворого у відповідь на введення вакцини. Тому через ризик системних, можливо летальних ускладнень, особливо у хворих зі зниженим імунним статусом, інтервал між застосуванням гемцитабіну та таких вакцин має бути не менше ніж 3 місяці або більше (до 12 місяців) залежно від імунного статусу хворого. Дослідження сумісності гемцитабіну не проводились. Не можна змішувати гемцитабін з іншими лікарськими засобами.Спосіб застосування та дозиГемцитабін вводиться внутрішньовенно краплинно протягом 30 хвилин. Недрібноклітинний рак легені Монотерапія: доза препарату, що рекомендується, - 1000 мг/м 2 в 1, 8 і 15 дні кожного 28-денного циклу. Комбінована терапія з цисплатином: рекомендована доза препарату - 1250 мг/м 2 на 1 та 8 день кожного 21-денного циклу або 1000 мг/м 2 на 1, 8 та 15 дні кожного 28-денного циклу Цисплатин вводиться у дозі 70- /м 2 в перший день циклу на тлі водного навантаження після інфузії гемцитабіну. Комбінована терапія з карбоплатином: рекомендована доза препарату – 1000 мг/м 2 або 1200 мг/м 2 на 1 та 8 день кожного 21-денного циклу. Карбоплатин вводиться в дозі AUC 5.0 мг/мл*хв у 1 день циклу після інфузії гемцитабіну. Рак молочної залози Комбінована терапія: як терапія 1-ї лінії при прогресуванні захворювання після неоад'ювантної терапії, що включає антрацикліни; рекомендована доза препарату - 1250 мг/м 2 в 1-й та 8-й дні у поєднанні з паклітакселом у дозі 175 мг/м 2 , який вводиться в 1-й день кожного 21-денного циклу внутрішньовенно краплинно приблизно протягом 3 год, перед введенням гемцитабіну. Уротеліальний рак Монотерапія: доза препарату, що рекомендується, - 1250 мг/м 2 в 1, 8 і 15 дні кожного 28-денного циклу. Комбінована терапія: рекомендована доза препарату - 1000 мг/м 2 в 1-й, 8-й та 15-й дні у поєднанні з цисплатином, який вводиться в дозі 70 мг/м 2 відразу після інфузії гемцитабіну в 1-й або 2 -й день кожного 28-денного циклу Епітеліальний рак яєчників Монотерапія: рекомендована доза препарату - 800-1250 мг/м 2 в 1-й, 8-й та 15-й дні кожного 28-денного циклу. Комбінована терапія: рекомендована доза препарату - 1000 мг/м 2 в 1-й та 8-й дні у поєднанні з карбоплатином у дозі AUC4.0 мг/мл*хв, який вводиться одразу після інфузії гемцитабіну у 1-й день кожного 21- денного циклу. Рак підшлункової залози Монотерапія: рекомендована доза препарату - 1000 мг/м 2 1 раз на тиждень протягом 7 тижнів з наступною тижневою перервою. Потім препарат вводиться в 1-й, 8-й та 15-й дні кожного 28-денного циклу. Рак шийки матки (місцерозповсюджений або метастатичний) Комбінована терапія: При місцеворозповсюдженому раку (неоад'ювантно) та при метастатичному раку гемцитабін вводиться в дозі 1250 мг/м 2 у 1-му та 8-му дні кожного 21-денного циклу. Цисплатин вводиться в дозі 70 мг/м 2 після введення гемцитабіну в 1-й день циклу на тлі гіпергідратації. Коректор дози препарату у зв'язку із явищами гематологічної токсичності Початок циклу лікування Незалежно від показань, перед кожним введенням препарату необхідно оцінювати чисто тромбоцити та гранулоцити. Умовою початку лікування є абсолютна кількість нейтрофілів не менше 1500/мкл та кількість тромбоцитів не менше 100000/мкл. У разі розвитку гематологічної токсичності під час проведення циклу терапії доза гемцитабіну може бути зменшена або введіть її відкладено відповідно до наступних рекомендацій: Модифікація дози гемцитабіну, що застосовується в монотерапії або в комбінації з цисплатином при лікуванні раку сечового міхура, недрібноклітинного раку легені та раку підшлункової залози. Абсолютна кількість нейтрофілів (1 мкл) Кількість тромбоцитів (1 мкл) % від стандартної дози > 1000 і > 100 000 100 500 – 1000 або 50000 – 100000 75 < 500 або < 50000 Відкласти введення* * При збільшенні кількості нейтрофілів до 500/мкл та тромбоцитів до 50000/мкл введення гемцитабіну може бути продовжено в рамках циклу Модифікація дози гемцитабіну, що застосовується у комбінації з паклітакселом при лікуванні раку молочної залози. Абсолютна кількість нейтрофілів (1 мкл) Кількість тромбоцитів (1 мкл) % від стандартної дози ≥ 1200 і > 75 000 100 1000 - < 1200 або 50000 – 75000 75 700 - < 1000 і ≥ 50000 50 < 700 або < 50000 Відкласти введення* * Лікування в рамках циклу не поновлюється. Чергове введення гемцитабіну проводиться в 1 день чергового циклу при відновленні кількості нейтрофілів як мінімум до 1500/мкл і тромбоцитів до 100000/мкл Модифікація дози гемцитабіну, що застосовується в комбінації з карбоплатином при лікуванні раку яєчників Абсолютна кількість нейтрофілів (1 каст) Кількість тромбоцитів (1 мкл) % від стандартної дози > 1500 і ≥ 100000 100 1000 – 1500 або 75000 – 100000 50 < 1000 або < 75000 Скасування вступу* * Лікування в рамках циклу не поновлюється. Чергове введення гемцитабіну проводиться в 1 день чергового циклу при досягненні кількості нейтрофілів як мінімум до 1500/мкл та тромбоцитів до 100000/мкл Доза гемцитабіну на черговому циклі повинна бути зменшена на 25% при всіх показаннях у випадках, якщо за попереднього циклу спостерігалося: зниження абсолютного чиста нейтрофілів < 500/мкл, що триває понад 5 днів; зниження абсолютної кількості нейтрофілів < 100/мкл, що триває понад 3 дні; фебрильна нейтропенія; зниження чистої тромбоцитів < 25000/мкл; цикл був відкладений більш ніж на 1 тиждень через гематологічну токсичність. Корекція дози препарату у зв'язку із явищами негематологічної токсичності Для виявлення негематологічної токсичності повинні проводитись періодичний фізикальний огляд та контроль функцій печінки та нирок. Доза препарату може бути зменшена у кожному наступному циклі або протягом вже розпочатого циклу залежно від ступеня прояву токсичності препаратів, призначених пацієнтові. У разі тяжкої (3 або 4 ступінь) негематологічної токсичності, за винятком випадків нудоти/блювоти, терапію гемцитабіном слід призупинити або знизити величину дозування залежно від рішення лікаря. Рішення про відновлення лікування приймає лікар. Спосіб введення Інфузійне введення гемцитабіну зазвичай добре переноситься пацієнтами та може проводитися в амбулаторних умовах. У разі екстравазації інфузію припиняють та відновлюють введення препарату в іншу вену. Після введення гемцитабіну пацієнт повинен спостерігатися протягом певного часу. Особливі групи пацієнтів Пацієнти з порушенням функції печінки та нирок: застосовувати гемцитабін у хворих з печінковою недостатністю або з порушеною функцією нирок слід з обережністю, оскільки достатніх даних щодо застосування препарату у цієї категорії пацієнтів немає. Ниркова недостатність помірної або середньої тяжкості (швидкість клубочкової фільтрації від 30 мл/хв до 80 мл/хв) не помітно впливає на фармакокінетику гемцитабіну. Літні пацієнти (>65 років): гемцитабін добре переноситься пацієнтами старше 65 років. Специфічних рекомендацій щодо зміни дози препарату для цієї популяції відсутні. Діти (< 18 років): гемцитабін не рекомендується призначати дітям до 18 років у зв'язку з недостатньою інформацією з безпеки та ефективності препарату в даній популяції. Рекомендації щодо приготування розчину для інфузій Як розчинник використовується тільки 0.9% розчин натрію хлориду без консервантів. Для приготування розчину препарату у флакон повільно вводять необхідну кількість 0.9% розчину хлориду натрію для ін'єкцій (не менше кількості, зазначеної в таблиці нижче) і акуратно струшують флакон до повного розчинення вмісту. Дозування препарату у флаконі Необхідний об'єм 0.9% розчину хлориду натрію для ін'єкцій Об'єм відновленого розчину Концентрація гемцитабіну в розчині 200 мг 5 мл 5.26 мл 38 мг/мл 1000 мг 25 мл 26.3 мл 38 мг/мл 1500 мг 37.5 мл 39.5 мл 38 мг/мл Отриманий розчин має бути прозорим. Максимальна концентрація відновленого розчину гемцитабіну не повинна перевищувати 38 мг/мл, оскільки при більш високих концентраціях можливе неповне розчинення препарату. Приготовлений розчин гемцитабіну, що містить потрібну дозу препарату, перед введенням розбавляють 0.9% розчином натрію хлориду для ін'єкцій у кількості, достатньому для 30-хвилинної внутрішньовенної інфузії. Перед парентеральним введенням розчину препарату слід переконатися у відсутності в ньому нерозчинених частинок та зміни кольору розчину Приготовлений розчин препарату призначений лише для одноразового застосування. Весь невикористаний препарат має бути утилізовано.ПередозуванняСимптоми: мієлодепресія, парестезія, виражена шкірна висипка. При введенні гемцитабіну в дозах до 5700 мг/м2 внутрішньовенно краплинно за 30 хвилин кожні 2 тижні ознак передозування не спостерігалося. Антидот для гемцитабіну невідомий. При підозрі на передозування гемцитабіну слід контролювати рівень цитопенії та при необхідності призначити симптоматичну терапію.Запобіжні заходи та особливі вказівкиЛікування гемцитабіном можна проводити лише під наглядом лікаря, який має досвід застосування протипухлинної хіміотерапії. Перед кожним введенням гемцитабіну необхідно контролювати кількість тромбоцитів, лейкоцитів та гранулоцитів у крові. При ознаках пригнічення функції кісткового мозку, спричиненого препаратом, необхідно припинити лікування або скоригувати дозу. Зазвичай пригнічення функції кісткового мозку має короткостроковий характер, не вимагає зниження дози і рідко призводить до необхідності переривання лікування. Показники периферичної крові можуть погіршуватися після переривання терапії гемцитабіном. При застосуванні гемцитабіну у комбінації з іншими протипухлинними хіміопрепаратами необхідно враховувати ризик кумулятивного пригнічення функції кісткового мозку. Необхідно проводити регулярне обстеження хворого та оцінку функції нирок та печінки. Введення гемцитабіну при метастазах у печінці, при гепатиті та алкоголізмі в анамнезі, а також при цирозі печінки збільшує ризик розвитку печінкової недостатності. При появі ознак розвитку небажаних явищ з боку дихальної системи (наприклад, набряк легенів, інтерстиціальний пневмоніт або респіраторний дистрес-синдром у дорослих) на тлі лікування гемцитабіном лікування слід припинити та призначити відповідну терапію. При появі перших ознак мікроангіопатичної гемолітичної анемії, таких як швидке зниження гемоглобіну з супутньою тромбоцитопенією, підвищення сироваткової концентрації білірубіну, креатиніну, азоту сечовини або підвищення активності лактатдегідрогенази, гемцитабін повинен бути скасований. Збільшення тривалості інфузії та частоти введень призводить до зростання токсичності. Ризик шкірних реакцій зростає за наявності променевої терапії в анамнезі. Залежно від ступеня токсичності дозу можна знижувати протягом кожного циклу або з початком нового циклу ступінчасто. Під час лікування та протягом 6 місяців після закінчення терапії гемцитабіном слід використовувати надійні методи контрацепції. Чоловікам, які отримують гемцитабін, рекомендується вдатися до кріоконсервації сперми до початку лікування через ризик безпліддя, зумовлений застосуванням даного препарату. При лікуванні пацієнтів, які перебувають на контрольованій натрієвій дієті, слід враховувати вміст у препараті натрію в наступних кількостях: флакон 200 мг Гемцитабіну медак містить 3.5 мг ( флакон 1000 мг Гемцитабіну медак містить 17.5 мг ( флакон 1500 мг Гемцитабіну медак містить 26.3 мг ( Вплив на здатність керувати транспортним засобом та працювати з механізмами. Дані про вплив терапії гемцитабіном на здатність керувати транспортним засобом та працювати з механізмами відсутні, однак деякі побічні дії препарату, такі як підвищена сонливість, можуть негативно впливати на здатність виконувати такі дії. У період лікування гемцитабіном необхідно дотримуватися обережності при керуванні транспортними засобами та зайнятті потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
1 389,00 грн
1 346,00 грн
Склад, форма випуску та упаковкаКонцентрат для виготовлення розчину для інфузій 1 мл: гемцитабін 10 мг. 100 мл - флакони (1) - картонні пачки.Фармакотерапевтична групаПротипухлинний засіб. Чинить цитостатичну дію, яка пов'язана з інгібуванням синтезу ДНК. У клітині метаболізується до активних дифосфатних та трифосфатних нуклеозидів. Дифосфатні нуклеозиди пригнічують дію рибонуклеотидредуктази, за участю якої у клітині утворюються дезоксинуклеозидтрифосфати, необхідні для синтезу ДНК, що призводить до зниження їх концентрації у клітині. Трифосфатні нуклеозиди активно конкурують за включення до ланцюга ДНК, а також можуть включатися до РНК. Після вбудовування внутрішньоклітинних метаболітів гемцитабіну в ланцюг ДНК до ланцюгів, що ростуть, додається один додатковий нуклеотид, що призводить до повного інгібування подальшого синтезу ДНК і запрограмованої загибелі клітини.ФармакокінетикаПри внутрішньовенній інфузії гемцитабіну в дозах 500-2592 мг/м2 протягом 0.4-1.2 години Cmax у плазмі становила 3.2-45.5 мкг/мл і визначалася протягом 5 хв наприкінці інфузії. Vd у центральній частині становить 12.4 л/м2 у жінок та 17.5 л/м2 у чоловіків (індивідуальні відмінності – 91.9%). Vd у периферичній частині становить 47.4 л/м2 та не залежить від підлоги. Зв'язування із білками практично відсутнє. Системний кліренс варіює від 29.2 л/год/м2 до 92.2 л/год/м2. У жінок кліренс приблизно на 25% нижчий, ніж у чоловіків. Менше 10% виводиться із сечею у незміненому вигляді. Нирковий кліренс становить 2-7 л/год/м2. T1/2 залежить від віку та статі та становить 42-94 хв. При введенні один раз на тиждень гемцитабін не кумулює. Гемцитабін швидко метаболізується за участю цитидиндеамінази у печінці, нирках, крові та інших тканинах. При внутрішньоклітинному метаболізмі активної речовини утворюються моно-, ди- та трифосфати гемцитабіну, які мають фармакологічну активність. Ці метаболіти не визначаються ні у плазмі, ні у сечі. Основний метаболіт 2-деокси-2,2-дифлуороуридин не має фармакологічної активності і визначається в плазмі та сечі.Клінічна фармакологіяПротипухлинний препарат. Антиметаболіт.Показання до застосуванняНедрібноклітинний рак легені (IIIa-IV стадії); пізні карциноми підшлункової залози.Протипоказання до застосуванняПідвищена чутливість до гемцитабіну.Вагітність та лактаціяБезпека гемцитабіну при вагітності у людини не вивчена. В експериментальних дослідженнях показано, що гемцитабін має ембріо- та фетотоксичну дію, негативно впливає на перебіг вагітності та постнатальний розвиток. Слід уникати застосування гемцитабіну при вагітності. Жінкам дітородного віку під час лікування необхідно використовувати надійні методи контрацепції. За необхідності застосування в період лактації слід вирішити питання про припинення грудного вигодовування.Побічна діяЗ боку системи кровотворення: лейкопенія, тромбоцитопенія, анемія. З боку травної системи: нудота, блювання, діарея; рідко – запор. З боку сечовидільної системи: протеїнурія, гематурія; рідко – периферичні набряки; у поодиноких випадках – ниркова недостатність. Дерматологічні реакції: висипання на шкірі, свербіж, алопеція, стоматит; рідко - лущення, везикульозний висип, екзема. З боку лабораторних показників: транзиторне підвищення активності печінкових трансаміназ, ЛФ, збільшення концентрації білірубіну в плазмі. З боку дихальної системи: рідко – бронхоспазм, задишка. З боку ЦНС та периферичної нервової системи: рідко – сонливість, слабкість, парестезії. З боку серцево-судинної системи: рідко – артеріальна гіпотензія, набряк легенів; у поодиноких випадках – інфаркт міокарда, аритмії. Інші: грипоподібний синдром.Взаємодія з лікарськими засобамиРизик розвитку та тяжкість лейкопенії та тромбоцитопенії підвищується після попередньої терапії цитостатиками.Спосіб застосування та дозиВстановлюють індивідуально, залежно від показань та стадії захворювання, стану системи кровотворення, схеми протипухлинної терапії.Запобіжні заходи та особливі вказівкиМає деяку активність при пізніх стадіях раку молочної залози, яєчників, нирок, сечового міхура і передміхурової залози, дрібноклітинному раку легень. З обережністю застосовують у разі порушення процесів кровотворення; порушення функції печінки та/або нирок. У період лікування слід регулярно проводити контроль картини периферичної крові. При розвитку токсичного гематологічного ефекту потрібна корекція режиму дозування залежно від ступеня лейкопенії та тромбоцитопенії. Безпека та ефективність застосування гемцитабіну у дітей не вивчена. Вплив на здатність до керування автотранспортом та управління механізмами У період лікування слід утримуватися від потенційно небезпечних видів діяльності, що потребують підвищеної уваги та швидкості психомоторних реакцій.Умови відпустки з аптекЗа рецептомВідео на цю тему
402,00 грн
363,00 грн
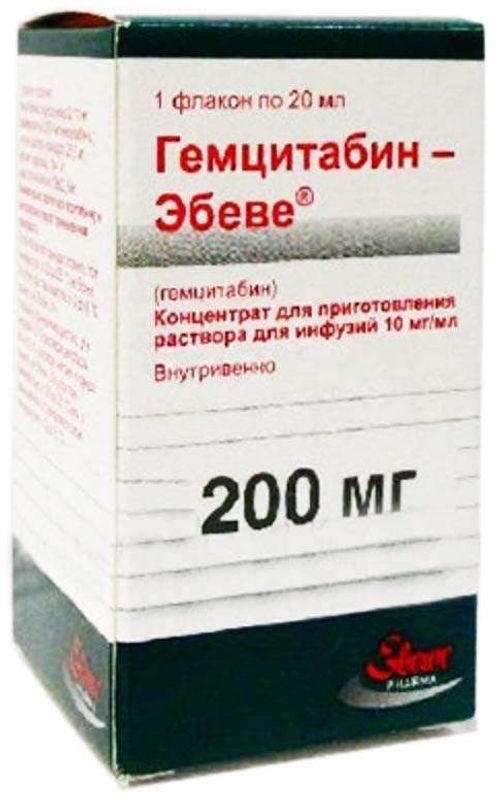
Склад, форма випуску та упаковкаКонцентрат для виготовлення розчину для інфузій 1 мл: гемцитабін 10 мг. 20 мл - флакони (1) - картонні пачки.Фармакотерапевтична групаПротипухлинний засіб. Чинить цитостатичну дію, яка пов'язана з інгібуванням синтезу ДНК. У клітині метаболізується до активних дифосфатних та трифосфатних нуклеозидів. Дифосфатні нуклеозиди пригнічують дію рибонуклеотидредуктази, за участю якої у клітині утворюються дезоксинуклеозидтрифосфати, необхідні для синтезу ДНК, що призводить до зниження їх концентрації у клітині. Трифосфатні нуклеозиди активно конкурують за включення до ланцюга ДНК, а також можуть включатися до РНК. Після вбудовування внутрішньоклітинних метаболітів гемцитабіну в ланцюг ДНК до ланцюгів, що ростуть, додається один додатковий нуклеотид, що призводить до повного інгібування подальшого синтезу ДНК і запрограмованої загибелі клітини.ФармакокінетикаПри внутрішньовенній інфузії гемцитабіну в дозах 500-2592 мг/м2 протягом 0.4-1.2 години Cmax у плазмі становила 3.2-45.5 мкг/мл і визначалася протягом 5 хв наприкінці інфузії. Vd у центральній частині становить 12.4 л/м2 у жінок та 17.5 л/м2 у чоловіків (індивідуальні відмінності – 91.9%). Vd у периферичній частині становить 47.4 л/м2 та не залежить від підлоги. Зв'язування із білками практично відсутнє. Системний кліренс варіює від 29.2 л/год/м2 до 92.2 л/год/м2. У жінок кліренс приблизно на 25% нижчий, ніж у чоловіків. Менше 10% виводиться із сечею у незміненому вигляді. Нирковий кліренс становить 2-7 л/год/м2. T1/2 залежить від віку та статі та становить 42-94 хв. При введенні один раз на тиждень гемцитабін не кумулює. Гемцитабін швидко метаболізується за участю цитидиндеамінази у печінці, нирках, крові та інших тканинах. При внутрішньоклітинному метаболізмі активної речовини утворюються моно-, ди- та трифосфати гемцитабіну, які мають фармакологічну активність. Ці метаболіти не визначаються ні у плазмі, ні у сечі. Основний метаболіт 2-деокси-2,2-дифлуороуридин не має фармакологічної активності і визначається в плазмі та сечі.Клінічна фармакологіяПротипухлинний препарат. Антиметаболіт.Показання до застосуванняНедрібноклітинний рак легені (IIIa-IV стадії); пізні карциноми підшлункової залози.Протипоказання до застосуванняПідвищена чутливість до гемцитабіну.Вагітність та лактаціяБезпека гемцитабіну при вагітності у людини не вивчена. В експериментальних дослідженнях показано, що гемцитабін має ембріо- та фетотоксичну дію, негативно впливає на перебіг вагітності та постнатальний розвиток. Слід уникати застосування гемцитабіну при вагітності. Жінкам дітородного віку під час лікування необхідно використовувати надійні методи контрацепції. За необхідності застосування в період лактації слід вирішити питання про припинення грудного вигодовування.Побічна діяЗ боку системи кровотворення: лейкопенія, тромбоцитопенія, анемія. З боку травної системи: нудота, блювання, діарея; рідко – запор. З боку сечовидільної системи: протеїнурія, гематурія; рідко – периферичні набряки; у поодиноких випадках – ниркова недостатність. Дерматологічні реакції: висипання на шкірі, свербіж, алопеція, стоматит; рідко - лущення, везикульозний висип, екзема. З боку лабораторних показників: транзиторне підвищення активності печінкових трансаміназ, ЛФ, збільшення концентрації білірубіну в плазмі. З боку дихальної системи: рідко – бронхоспазм, задишка. З боку ЦНС та периферичної нервової системи: рідко – сонливість, слабкість, парестезії. З боку серцево-судинної системи: рідко – артеріальна гіпотензія, набряк легенів; у поодиноких випадках – інфаркт міокарда, аритмії. Інші: грипоподібний синдром.Взаємодія з лікарськими засобамиРизик розвитку та тяжкість лейкопенії та тромбоцитопенії підвищується після попередньої терапії цитостатиками.Спосіб застосування та дозиВстановлюють індивідуально, залежно від показань та стадії захворювання, стану системи кровотворення, схеми протипухлинної терапії.Запобіжні заходи та особливі вказівкиМає деяку активність при пізніх стадіях раку молочної залози, яєчників, нирок, сечового міхура і передміхурової залози, дрібноклітинному раку легень. З обережністю застосовують у разі порушення процесів кровотворення; порушення функції печінки та/або нирок. У період лікування слід регулярно проводити контроль картини периферичної крові. При розвитку токсичного гематологічного ефекту потрібна корекція режиму дозування залежно від ступеня лейкопенії та тромбоцитопенії. Безпека та ефективність застосування гемцитабіну у дітей не вивчена. Вплив на здатність до керування автотранспортом та управління механізмами У період лікування слід утримуватися від потенційно небезпечних видів діяльності, що потребують підвищеної уваги та швидкості психомоторних реакцій.Умови відпустки з аптекЗа рецептомВідео на цю тему
675,00 грн
629,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
1 384,00 грн
1 354,00 грн
Склад, форма випуску та упаковкаЛіофілізат - 1 фл. Активна речовина: Гемцитабіну гідрохлорид – 1138,5 мг (відповідає гемцитабіну) – 1000 мг; Допоміжні речовини: Маннітол – 1000 мг; Натрію ацетату тригідрат 103,5 мг; Натрію гідроксид qs (для доведення pH до 2,7-3,3); Кислота хлористоводнева qs (для доведення pH до 2,7-3,3). Ліофілізат для виготовлення розчину для інфузій 1000 мг. По 200 мг, 1000 мг або 1500 мг гемцитабіну у флаконі з безбарвного скла (тип I, Е.Ф.), закупореному пробкою з хлорбутилової гуми та обжатий алюмінієвим ковпачком з полімерною захисною кришкою. На флакон наклеюється етикетка. Один флакон разом з інструкцією із застосування у картонній пачці.Опис лікарської формиБіла або майже біла ліофілізована маса чи порошок.Фармакотерапевтична групаПротипухлинний засіб - антиметаболіт.ФармакокінетикаМаксимальна концентрація гемцитабіну в плазмі (від 3,2 мкг/мл до 45,5 мкг/мл) досягається протягом 5 хвилин після закінчення інфузії. Концентрація вихідної речовини в плазмі крові, виміряна після введення дози 1000 мг/м2/30 хвилин, перевищує 5 мкг/мл протягом приблизно 30 хвилин після закінчення інфузії та 0,4 мкг/мл протягом наступної години. Розподіл Обсяг розподілу центрального компартменту становить 12,4 л/м2 у жінок та 17,5 л/м2 у чоловіків (варіабельність між суб'єктами становила 91,9%). Об'єм розподілу периферичного компартменту становив 47,4 л/м2 і залежав від статі. Зв'язування гемцитабіну з білками плазми незначне. Період напіввиведення коливається від 42 хв до 94 хв залежно від статі та віку пацієнта. За дотримання рекомендованого режиму дозування гемцитабін практично повністю виводиться протягом 5-11 годин від початку інфузії. При введенні раз на тиждень гемцитабін не накопичується в організмі. Метаболізм В організмі гемцитабін швидко метаболізується під дією цитидиндезаміназ в печінці, нирках, крові та інших тканинах, в результаті чого утворюються гемцитабін моно-, ді-і трифосфати (dFdCMP, dFdCDP і dFdCTP), з яких активними вважаються dFdCDP і dFd. Ці внутрішньоклітинні метаболіти не виявляються у плазмі крові або сечі. Основний метаболіт гемцитабіну - 2'-дезокси-2',2'-дифторуридин (dFdU), не є активним, визначається у плазмі крові та сечі. Виведення Системний кліренс варіює від 29,2 л/год/м2 до 92,2 л/год/м2, залежно від статі та віку пацієнта (варіабельність між суб'єктами 52,2%). Кліренс у жінок приблизно на 25% нижчий, ніж у чоловіків; як у чоловіків, і у жінок швидкість виведення знижується з віком. При інфузійному введенні гемцитабіну в рекомендованій дозі 1000 мг/м2 протягом 30 хвилин зниження значень кліренсу у жінок і чоловіків не обов'язково вимагає зниження дози препарату. Менше 10% введеної дози виводиться із сечею у незміненому вигляді. Нирковий кліренс становить від 2 до 7 л/год/м2. Протягом тижня після введення гемцитабіну від 92 до 98% від введеної дози виводиться з організму: 99% із сечею, переважно, у вигляді 2'-дезокси-2',2'-дифторуридину, та 1% з фекаліями. Кінетика гемцитабіну трифосфату (dFdCTP) Цей метаболіт виявляється в мононуклеарних клітинах периферичної крові, наведені нижче дані стосуються цих клітин. При введенні гемцитабіну в дозах від 35 до 350 мг/м2 поверхні тіла шляхом 30-хвилинної внутрішньовенної інфузії концентрація dFdCTP зростає пропорційно до дози гемцитабіну, досягаючи величини рівноважної концентрації 0,4-5 мкг/мл. При значеннях концентрації гемцитабіну в плазмі більше 5 мкг/мл подальшого підвищення концентрації dFdCTP не відбувається, що свідчить про насичення процесу утворення цього метаболіту. Період напіввиведення dFdCTP у термінальній фазі становить 0,7-12 год. Кінетика 2'-дезокси-2',2'-дифторурідіна Максимальні значення концентрації у плазмі (через 3-15 хвилин після закінчення 30-хвилинної інфузії препарату у дозі 1000 мг/м2): 28-52 мкг/мл. Залишкова концентрація при застосуванні препарату один раз на тиждень: 0,07-1,12 мкг/мл без явних ознак накопичення. Процес зниження концентрації dFdU в плазмі має трифазний характер, середній період напіввиведення в заключній фазі становить 65 годин (діапазон 33-84 год). Ступінь утворення dFdU із вихідної речовини: 91-98%. Середній обсяг розподілу центрального компартменту: 18 л/м2 (діапазон 11-22 л/м2). Середнє значення обсягу розподілу у стаціонарній фазі (Vss): 150 л/м2 (в діапазоні 96-228 л/м2). Препарат добре розподіляється у тканинах. Середнє значення кліренсу: 2,5 л/год/м2 (в діапазоні 1-4 л/год/м2). Виведення із сечею: повне. Комбінована терапія гемцнтабіном та паклітакселом При сумісному застосуванні гемцитабіну та паклітакселу фармакокінетика препаратів не змінюється. Комбінована терапія гемцитабіном та карбоплатином При сумісному застосуванні гемцитабіну та карбоплатину фармакокінетика гемцитабіну не змінюється. Порушення функції нирок Ниркова недостатність легкого або помірного ступеня (швидкість клубочкової фільтрації 30-80 мл/хв) не істотно впливає на фармакокінетику гемцитабіну.ФармакодинамікаПротипухлинний засіб, антиметаболіт групи аналогів піримідину, пригнічує синтез ДНК. Виявляє циклоспецифічність, діючи на клітини у фазах S та G1/S. Метаболізується у клітині під дією нуклеозидкіназ до активних дифосфатних та трифосфатних нуклеозидів. Дифосфатні нуклеозиди пригнічують дію рибонуклеотидредуктази (єдиного ферменту, що каталізує утворення дезоксинуклеозидтрифосфатів, необхідних для синтезу ДНК). Трифосфатні нуклеозиди здатні вбудовуватися в ланцюжок ДНК (меншою мірою РНК), що призводить до припинення подальшого синтезу ДНК та запрограмованої загибелі клітини (апоптозу). Гемцитабін є також сильним радіосенсибілізуючим засобом навіть у концентраціях нижчих за цитотоксичні.Показання до застосуванняМісцевий або метастатичний недрібноклітинний рак легені як терапія першої лінії в комбінації з цисплатином або карбоплатином, а також у монотерапії у літніх пацієнтів з функціональним статусом, рівним 2. Нерезектабельний, місцеворецидивний або метастатичний рак молочної залози у складі комбінованої терапії з паклітакселом після проведення неоад'ювантної та/або ад'ювантної терапії з включенням антрациклінів за відсутності протипоказань до їх призначення. Місцевий або метастатичний уротеліальний рак (рак сечового міхура, ниркової балії, сечоводів, уретри). Місцево поширений або метастатичний епітеліальний рак яєчників як монотерапія або у поєднанні з карбоплатином у пацієнтів з прогресуванням захворювання після проведення першої лінії терапії на основі платинових препаратів. Місцевий або метастатичний рак підшлункової залози. Місцевий або метастатичний рак шийки матки. Рак жовчовивідних шляхів. Показана ефективність гемцитабіну при поширеному дрібноклітинному раку легені та поширеному рефрактерному раку яєчка.Протипоказання до застосуванняПідвищена чутливість до активної речовини або до будь-якої з допоміжних речовин; вагітність; період годування груддю; дитячий вік до 18 років (відсутність достатніх даних щодо ефективності та безпеки). З обережністю: При порушенні функції печінки та/або нирок, пригніченні кістковомозкового кровотворення (у тому числі на тлі супутньої променевої або хіміотерапії), серцево-судинних захворюваннях в анамнезі, гострих інфекційних захворюваннях вірусної, грибкової або бактеріальної природи.Вагітність та лактаціяВагітність Адекватних досліджень із застосуванням гемцитабіну у жінок під час вагітності не проводилося. Проте дослідження, проведені на тваринах, виявили репродуктивну токсичність гемцитабіну, що виявляється у появі вроджених дефектів та інших впливах на розвиток ембріона або плода, перебіг вагітності та пери- та постнатальний розвиток. Застосування гемцитабіну протипоказане при вагітності. Період грудного вигодовування Невідомо, чи проникає гемцитабін у грудне молоко, тому не можна виключити можливий негативний вплив на дитину, яка перебуває на грудному вигодовуванні. Грудне вигодовування слід припинити у період застосування гемцитабіну.Побічна діяПобічні реакції, що зустрічалися частіше, ніж у поодиноких випадках, перераховані відповідно до наступної градації: дуже часто (≥ 1/10); часто (від ≥ 1/100 до Інфекційні та паразитарні захворювання: часто – інфекції; нечасто – сепсис. Порушення з боку крові та лімфатичної системи: дуже часто – анемія, лейкопенія, тромбоцитопенія; часто – фебрильна нейтропенія; нечасто – тромботична мікроангіопатія; дуже рідко – тромбоцитоз. Порушення з боку імунної системи: дуже рідко – анафілактична реакція. Порушення з боку обміну речовин та харчування: часто – анорексія. Порушення з боку системи шлунково-кишкового тракту: дуже часто - нудота, блювання, підвищення активності "печінкових" ферментів аспартатамінотрансферази (ACT), алантнамінотрансферази (АЛТ) та лужної фосфатази; часто – діарея, стоматит, виразкове ураження слизової оболонки порожнини рота, запор, підвищення концентрації білірубіну у сироватці крові; нечасто - гепатотоксичність важкого ступеня вираженості, включаючи печінкову недостатність, у деяких випадках із летальним кінцем; рідко – підвищення активності гамма-глутамілтрансферази (ГГТ); дуже рідко – ішемічний коліт. Порушення з боку нирок та сечовивідних шляхів: дуже часто – протеїнурія легкого ступеня виразності, гематурія; нечасто – ниркова недостатність; рідко – підвищення концентрації креатиніну, сечовини та лактатдегідрогенази (ЛДГ) при гемолітико-уремічному синдромі. Порушення з боку шкіри та підшкірних тканин: дуже часто – алергічні шкірні висипання легкого ступеня вираженості, що супроводжуються свербінням, алопеція (зазвичай мінімальна втрата волосся); часто - свербіж шкіри, підвищена пітливість; рідко - виразки, утворення везикул, лущення шкіри, реакції з боку шкіри важкого ступеня вираженості, включаючи десквамацію та бульозне ураження шкіри; дуже рідко – токсичний епідермальний некроліз, синдром Стівенса-Джонсона. Порушення з боку дихальної системи, органів грудної клітки та середостіння: дуже часто – задишка; часто – кашель, риніт; нечасто – бронхоспазм, інтерстиціальний пневмоніт; рідко – набряк легень, гострий респіраторний дистрес-синдром. Порушення з боку серця: нечасто – серцева недостатність, аритмія (переважно суправентрикулярна); рідко – інфаркт міокарда. Порушення з боку судин: дуже часто – набряки, периферичні набряки; рідко – зниження артеріального тиску, васкуліт периферичних судин, гангрена; дуже рідко – синдром підвищеної проникності капілярів. Порушення з боку нервової системи: часто – головний біль, безсоння, сонливість; нечасто – порушення мозкового кровообігу; дуже рідко: - синдром задньої оборотної лейкоенцефалопатії (СЗОЛ). Порушення з боку скелетно-м'язової та сполучної тканини: часто – біль у спині, міалгія. Інші: дуже часто – грипоподібний синдром. Також були зареєстровані випадки нездужання, пітливість; часто – підвищення температури тіла, астенія, озноб; рідко – реакції у місці введення, переважно легкого ступеня виразності. Гіперчутливість: анафілактоїдні реакції реєструвалися дуже рідко. Променева токсичність реєструвалася рідко. Застосування гемцитабіну в комбінації з паклітакселом при раку молочної залози Небажані явища ІІІ ступеня тяжкості Гематологічна токсичність: анемія 57%, тромбоцитопенія 53%, нейтропенія 313%. Негематологічна токсичність: фебрильна нсйтропенія 4,6%, підвищена втома 5,7%, діарея 3,1%, моторна нейропатія 2,3%, сенсорна нейропатія 5,3%. Небажані явища IV ступеня тяжкості Гематологічна токсичність: анемія 1,1%, тромбоцитопенія 0,4%, нейтропенія 17,2% (нейтропенія IV ступеня тривалістю понад 7 днів була зареєстрована у 12,6% пацієнтів). Негематологічна токсичність: фебрильна нейтропенія 0,4%, підвищена втома 0,8%, моторна нейропатія 0,4%, сенсорна нейропатія 0,4%. Застосування гемцитабіну в комбінації з цисплатином при раку сечового міхура Небажані явища ІІІ ступеня тяжкості Гематологічна токсичність: анемія 24%, тромбоцитопенія 29%. Негематологічна токсичність: нудота та блювання 22%, діарея 3%, інфекція 2%, стоматит 1%. Небажані явища IV ступеня тяжкості Гематологічна токсичність: анемія 4%, тромбоцитопенія 29%. Негематологічна токсичність: інфекція 1%. Застосування гемцитабіну в комбінації з карбоплатином при раку яєчників Небажані явища ІІІ ступеня тяжкості Гематологічна токсичність: анемія 22,3%, нейтропенія 41,7%, тромбоцитопенія 30,3%, лейкопенія 48%. Негематологічна токсичність: кровотеча 18%, фебрильна нейтропенія 11%. Небажані явища IV ступеня тяжкості Гематологічна токсичність: анемія 5,1%, нейтропенія 28,6%, тромбоцитопенія 4,6%, лейкопенія 5,1%. Негематологічна токсичність: інфекція без нейтропенії 0,6%.Взаємодія з лікарськими засобамиСпецифічних досліджень взаємодій гемцитабіну нс проводилося. Взаємодія з іншими видами терапії Променева терапія Супутня променева терапія (одночасно із введенням гемцитабіну ши з інтервалом Було показано, що гемцитабін має радіосенсибілізуючу активність. В одному дослідженні, де пацієнти з недрібноклітинним раком легені отримували гемцитабін у дозі 1000 мг/м2 протягом 6 послідовних тижнів у поєднанні з терапевтичним опроміненням на ділянку грудної клітини, була відзначена значна токсичність у вигляді важкого та потенційно загрозливого для життя запалення слизової оболонки, езофагіту і пневмоніту, особливо у пацієнтів з великим об'ємом тканин, що опромінюються (медіана обсягу опромінюваної тканини 4795 см3). У подальших дослідженнях було показано, що поєднання нижчих доз гемцитабіну та променевої терапії краще переноситься пацієнтами та дозволяє забезпечити передбачуваний профіль токсичності. Так, в одному з досліджень II фази пацієнтам з недрібноклітинним раком легені проводилася променева терапія в дозі 60 Гр спільно з введенням гемцитабіну (600 мг/м2 4 рази) та цисплатину (80 мг/м2 2 рази) протягом 6 тижнів. Послідовна променева терапія (перерва >7 днів): за існуючими даними, введення гемцитабіну більш ніж за 7 днів до початку променевої терапії або через 7 днів після її завершення не супроводжується збільшенням токсичності, за винятком ураження шкіри, пов'язаного з введенням хіміопрепарату після опромінення. . Лікування гемцитабіном може бути розпочато після вирішення всіх гострих променевих реакцій, але не раніше як через 7 днів після опромінення. Як при супутньому, так і при послідовному застосуванні гемцитабіну і променевої терапії можливе променеве ураження тканин, що опромінюються (напр., езофагіт, коліт і пневмоніт). Інші види взаємодії Через ризик системних, можливо летальних ускладнень, особливо у пацієнтів зі зниженим імунним статусом, не рекомендується застосовувати разом із гемцитабіном вакцину жовтої лихоманки та інші живі атенюйовані вакцини. Несумісність Не можна змішувати гемцитабін з іншими лікарськими засобами та розчинниками за винятком зазначених у розділі "Рекомендації з приготування розчину для інфузій".Спосіб застосування та дозиГемцитабін вводиться внутрішньовенно краплинно протягом 30 хвилин. Наведені нижче рекомендовані дози можуть бути скориговані з наступного циклу терапії або протягом циклу на підставі оцінки токсичності. Недрібноклітинний рак легені (місцерозповсюджений або метастатичний), перша лінія терапії Монотерапія: рекомендована доза препарату - 1000 мг/м2 у 1-й, 8-й та 15-й дні кожного 28-денного циклу. Комбінована терапія з цисплатином: рекомендована доза препарату - 1250 мг/м2 в 1-й та 8-й дні кожного 21-денного циклу або 1000 мг/м2 в 1-й, 8-й та 15-й дні кожного 28-денного циклу . Цисплатин вводиться у дозі 70 мг/м2 у 1-й день циклу після інфузії гемцитабіну на фоні гіпергідратації. Комбінована терапія з карбоплатином: рекомендована доза препарату - 1000 мг/м2 або 1200 мг/м2 в 1-й та 8-й дні кожного 21-денного циклу. Карбоплатин вводиться з розрахунку AUC (площа під кривою "концентрація-час") 5,0 мг/мл/хв на 1 день циклу після інфузії гемцитабіну. Рак молочної залози (нерезектабельний, містіорецидивуючий або метастатичний) Комбінована терапія з паклітакселом: як терапія першої лінії при прогресуванні захворювання після неоад'ювантної та/або ад'ювантної терапії, що включає ашращпстини, за відсутності протипоказань до них. Паклітаксел вводиться в дозі 175 мг/м2 внутрішньовенно краплинно протягом 3 годин на 1 день кожного 21-денного циклу з подальшим введенням гемцитабіну. Рекомендована доза препарату - 1250 мг/м2 у 1-й та 8-й дні кожного 21-денного циклу. Перед початком комбінованої терапії (гемцитабін + паклітаксел) абсолютна кількість гранулоцитів у крові у пацієнта має бути не менше ніж 1,5 х 109/л. Уротеліальний рак (рак сечового міхура (місцерозповсюджений, метастатичний і поверхневий), ниркової балії, сечоводу, сечівника) Монотерапія: рекомендована доза препарату – 1250 мг/м2 у 1-й, 8-й та 15-й дні кожного 28-денного циклу. Комбінована терапія з цисплатином: рекомендована доза препарату - 1000 мг/м2 в 1-й, 8-й та 15-й дні у поєднанні з цисплатином, який вводиться в дозі 70 мг/м2 відразу після інфузії гемцитабіну в 1-й або 2 -й день кожного 28-денного циклу Клінічні дослідження показали, що за дози цисплатину 100 мг/м2 спостерігається більш виражена мієлосупресія. Епітеліальний рак яєчників (місцерозповсюджений або метастатичний, резистентний до похідних платини) Монотерапія: рекомендована доза препарату - 800-1250 мг/м2 в 1-й, 8-й та 15-й дні кожного 28-денного циклу. Комбінована терапія з карбоплатином: рекомендована доза препарату - 1000 мг/м2 в 1-й та 8-й дні у поєднанні з карбоплатином, який вводиться одразу після інфузії гемцитабіну з розрахунку AUC 4,0 мг/мл/хв, на 1 день кожного 21-денного циклу. Рак підшлункової залози Рекомендована доза препарату - 1000 мг/м2 1 раз на тиждень протягом 7 тижнів з наступною тижневою перервою. Потім препарат вводиться в 1-й, 8-й та 15-й дні кожного 28-денного циклу. Рак шийки матки Комбінована терапія При місцеворозповсюдженому раку при послідовній хіміопроменевій терапії (неоад'ювантно) та при метастатичному раку гемцитабін вводиться в дозі 1250 мг/м2 у 1-му та 8-му дні кожного 21-денного циклу. Цисплатин вводиться у дозі 70 мг/м2 у 1-й день циклу на фоні гіпергідратації перед введенням гемцитабіну. При місцеворозповсюдженому раку при одночасної хіміопроменевої терапії (неоад'ювантно) гемцитабін вводиться 1 раз на тиждень за 1-2 години до початку променевої терапії в дозі 1250 мг/м2, безпосередньо після введення цисплатину в дозі 40 мг/м2. Рак жовчовивідних шляхів Комбінована терапія з цисплатином: цисплатин вводиться у дозі 70 мг/м2 у 1-й день циклу на фоні гіпергідратації з подальшим введенням гемцитабіну. Гемцитабін вводиться в дозі 1250 мг/м2 у 1-й та 8-й день кожного 21-денного циклу. Корекція дози Корекція дози препарату у зв'язку із явищами гематологічної токсичності Початок циклу терапії: незалежно від показань, перед кожним введенням препарату необхідно оцінювати кількість тромбоцитів та гранулоцитів у крові. Умовою початку лікування є абсолютна кількість гранулоцитів не менше 1,5 х 109/л та кількість тромбоцитів не менше 100 х 109/л. Під час іїкла терапії: у разі розвитку гематологічної токсичності під час проведення циклу терапії доза гемцитабіну може бути зменшена, або її введення відкладено відповідно до наступних рекомендацій: Корекція дози гемцитабіну, що застосовується в монотерапії або в комбінації з цисплатином при лікуванні раку сечового міхура, недрібноклітинного раку легені та раку підшлункової залози. Абсолютна кількість гранулоцитів (1 л) Кількість тромбоцитів (1 л) % від стандартної дози > 1 х 109 та > 100 х 109 100 0,5 х 109 - 1 х 109 або 50 х 109-100 х 109 75 < 0,5 х 109 або <50 х 109 Відкласти введення* *При збільшенні кількості нейтрофілів до 0,5 х 109/л та гранулоцитів до 50 х 109/л введення гемцитабіну може бути продовжено в рамках циклу. Корекція дози гемцитабіну, що застосовується в монотерапії або в комбінації з цисплатином при лікуванні раку сечового міхура, недрібноклітинного раку легені та раку підшлункової залози. Абсолютна кількість гранулоцитів (1 л) Кількість тромбоцитів (1 л) % від стандартної дози > 1 х 109 та > 100 х 109 100 0,5 х 109 - 1 х 109 або 50 х 109-100 х 109 75 < 0,5 х 109 або <50 х 109 Відкласти введення* *Лікування в рамках циклу не відновлюється. Чергове введення гемцитабіну проводиться в день чергового циклу при відновленні кількості гранулоцитів як мінімум до 1,5 х 109/л і тромбоцитів до 100 х 109/л. Корекція дози гемцитабіну, що застосовується в комбінації з карбоплатином при лікуванні раку яєчників Абсолютна кількість гранулоцитів (1 л) Кількість тромбоцитів (1 л) % від стандартної дози > 1,5 х 109 та ≥ 100 х 109 100 1 х 109 - 1,5 х 109 або 75 х 109 - 100 х 109 50 < 1 х 109 або < 75 х 109 Скасування вступу* *Лікування в рамках циклу не відновлюється. Чергове введення гемцитабіну проводиться в день чергового циклу при досягненні кількості гранулоцитів як мінімум до 1,5 х 109/л і тромбоцитів до 100 х 109/л. Наступні цикли терапії: доза гемцитабіну на черговому циклі повинна бути зменшена на 25% при всіх показаннях у випадках, якщо за попереднього циклу спостерігалося: зниження абсолютної кількості гранулоцитів зниження абсолютної кількості гранулоцитів фебрильна нейтропенія, зниження кількості тромбоцитів цикл був відкладений більш ніж на 1 тиждень через гематологічну токсичність. Корекція дози препарату у зв'язку із явищами негематологічної токсичності Для виявлення негематологічної токсичності повинні проводитись періодичний фізикальний огляд та контроль функцій печінки та нирок. Доза препарату може бути зменшена у кожному наступному циклі або протягом вже розпочатого циклу залежно від ступеня прояву токсичності у пацієнта. У разі тяжкої (3 або 4 ступінь) негематологічної токсичності, за винятком випадків нудоти/блювоти, терапію гемцитабіном слід призупинити або знизити величину дози в залежності від рішення лікаря. Рішення про відновлення лікування приймає лікар. Дані щодо корекції дози цисплатину, карбоплатину та паклітакселу, що застосовуються у комбінованій терапії з гемцитабіном, наведено у Резюмі характеристик цих препаратів. Спосіб введення Інфузійне введення гемцитабіну зазвичай добре переноситься пацієнтами та може проводитися в амбулаторних умовах. У разі екстравазації інфузію припиняють та відновлюють введення препарату в іншу вену. Після введення гемцитабіну необхідно проводити ретельне спостереження пацієнта протягом певного часу. Особливі групи пацієнтів Пацієнти з порушенням функції печінки та нирок: застосовувати гемцитабін у пацієнтів з печінковою недостатністю або з порушеною функцією нирок слід з обережністю, оскільки достатніх даних щодо застосування препарату у цієї категорії пацієнтів немає. Ниркова недостатність від легкого до помірного ступеня вираженості (швидкість клубочкової фільтрації від 30 мл/хв до 80 мл/хв) не надає помітного впливу на фармакокінетику гемцитабіну. Літні пацієнти (>65 років): гемцитабін добре переноситься пацієнтами старше 65 років. Специфічних рекомендацій щодо зміни дози препарату для цієї популяції відсутні. Діти ( Рекомендації щодо приготування розчину для інфузій Як розчинник слід використовувати лише 0,9% розчин натрію хлориду без консервантів. Сумісність препарату з іншими речовинами не вивчалася, тому не рекомендується змішувати приготовлений розчин гемцитабіну з іншими препаратами. Для приготування розчину препарату у флакон повільно вводять необхідну кількість 0,9% розчину хлориду натрію для ін'єкцій (не менше кількості, зазначеної в таблиці нижче) і обережно струшують флакон до повного розчинення вмісту. Дозування препарату у флаконі Необхідний об'єм 0,9% розчину хлориду натрію для ін'єкцій Об'єм відновленого розчину Концентрація гемцитабіну в розчині 200 мг 5 мл 5,26 мл 38 мг/мл 1000 мг 25 мл 26,3 мл 38 мг/мл 1500 мг 37,5 мл 39,5 мл 38 мг/мл Отриманий розчин має бути прозорим. Максимальна концентрація відновленого розчину гемцитабіну не повинна перевищувати 38 мг/мл, оскільки при більш високих концентраціях можливе неповне розчинення препарату. Приготовлений розчин гемцитабіну, що містить потрібну дозу препарату, перед введенням розбавляють 0,9% розчином натрію хлориду для ін'єкцій у кількості, достатній для 30-хвилинної внутрішньовенної інфузії. Перед парентеральним введенням розчину препарату слід переконатися у відсутності в ньому нерозчинених частинок та зміни кольору розчину. Розчин препарату не можна заморожувати (можлива кристалізація розчину). Приготовлений розчин препарату призначений лише для одноразового застосування. Необхідно дотримуватись правил безпечного приготування та поводження з цитотоксичними медичними препаратами, прийнятими в лікувальному закладі. Із препаратом не повинні працювати вагітні жінки. Приготування розчину препарату повинне проводитися досвідченим персоналом у спеціально призначеному приміщенні. Робоча поверхня повинна бути покрита одноразовим поглинаючим папером з пластиковим покриттям на звороті. Під час роботи необхідно використовувати захисні окуляри, одноразові рукавички, маску, одноразовий фартух. Необхідно використовувати запобіжні заходи, що виключають випадкове попадання препарату в очі. У разі випадкового контакту препарату з очима необхідно негайно ретельно промити їх водою. Слід акуратно збирати інфузійну систему, уникаючи протікання (рекомендується використовувати з'єднувачі типу Луєр лок). З метою зниження тиску та уникнення утворення аерозолю рекомендується використовувати голки з отворами великого діаметра. У разі прокидання препарату або протікання його розчину збирання слід проводити з використанням захисних рукавичок. При прибиранні екскрементів і блювотних мас слід бути обережними. Утилізація Весь невикористаний препарат має бути утилізовано.ПередозуванняСимптоми: мієлосупресія, парестезія, виражений шкірний висип. При введенні гемцитабіну в дозах до 5700 мг/м2 внутрішньовенно крапельно за 30 хвилин кожні 2 тижнів ознак передозування не спостерігалося. Антидот для гемцитабіну невідомий. При підозрі на передозування гемцитабіну слід контролювати показники крові та при необхідності призначити симптоматичну терапію.Запобіжні заходи та особливі вказівкиЛікування гемцитабіном можна проводити лише під наглядом лікаря, який має досвід проведення протипухлинної хіміотерапії. Збільшення тривалості інфузії та частоти введення препарату призводить до збільшення токсичності. Гематологічна токсичність Гемцитабін може пригнічувати функцію кісткового мозку, що проявляється у вигляді лейкопенії, тромбоцитопенії та анемії. Перед кожним введенням гемцитабіну необхідно контролювати кількість тромбоцитів, лейкоцитів та гранулоцитів у крові. При ознаках пригнічення функції кісткового мозку, спричиненого препаратом, необхідно припинити лікування або скоригувати дозу. Зазвичай пригнічення функції кісткового мозку носить короткочасний характер, не вимагає зниження дози і рідко призводить до необхідності переривання лікування. Показники периферичної крові можуть погіршуватися після переривання терапії гемцитабіном. У пацієнтів з порушеною функцією кровотворення лікування слід розпочинати з обережністю. При застосуванні гемцитабіну у комбінації з іншими протипухлинними хіміопрепаратами необхідно враховувати ризик кумулятивного пригнічення функції кісткового мозку. Недостатність функції печінки та нирок Необхідно проводити регулярне обстеження хворого та оцінку функції нирок та печінки (включаючи вірологічні тести). У пацієнтів з печінковою недостатністю або з порушенням функції нирок гемцитабін слід застосовувати з обережністю через відсутність чітких рекомендацій щодо дозування препарату у пацієнтів цих груп. Введення гемцитабіну при метастазах у печінці, гепатиті та алкоголізмі в анамнезі, а також при цирозі печінки збільшує ризик розвитку печінкової недостатності. У пацієнтів, які отримують гемцитабін, рідко виявляють клінічні симптоми гемолітико-уремічного синдрому (ГУС). При появі перших ознак мікроангіопатичної гемолітичної анемії, таких як швидке зниження концентрації гемоглобіну з супутньою тромбоцитопенією, підвищення сироваткової концентрації білірубіну, креатиніну, азоту сечовини або підвищення активності лактатдегідрогенази, гемцитабін повинен бути скасований. Навіть при скасуванні терапії ниркова недостатність може виявитися незворотною, що вимагатиме проведення гемодіалізу. Синдром задньої оборотної лейкоенцефалопатії Дуже рідко у пацієнтів, які отримували гемцитабін у режимі монотерапії або у складі комбінованої хіміотерапії, спостерігався синдром задньої оборотної лейкоенцефалопатії (СЗОЛ) із потенційно серйозними наслідками. Найчастіше у пацієнтів, які отримували гемцитабін з проявами СЗОЛ, зустрічаються гостре підвищення артеріального тиску та судоми, також можливі біль голови, летаргія, сплутаність свідомості, сліпота. Діагноз СЗОЛ підтверджується МРТ (магнітно-резонансною томографією). СЗОЛ зазвичай оборотний у разі проведення відповідних терапевтичних заходів. Якщо під час терапії гемцитабіном розвивається СЗОЛ, необхідно відмінити застосування препарату та проводити підтримуючі заходи, включаючи контроль артеріального тиску та протисудомну терапію. Серцево-судинні захворювання У зв'язку з ризиком розвитку серцевих та/або судинних порушень, спричинених застосуванням гемцитабіну, лікування пацієнтів із серцево-судинними захворюваннями в анамнезі повинно проводитися з особливими запобіжними засобами. Синдром підвищеної проникності капілярів Дуже рідко у пацієнтів, які отримували гемцитабін як монотерапію або у поєднанні з іншими хіміотерапевтичними препаратами, спостерігався синдром підвищеної проникності капілярів. При його виявленні на ранніх термінах та вживання адекватних заходів, стан зазвичай піддається корекції, але були зареєстровані і смертельні випадки. Цей стан характеризується системним підвищенням проникності капілярів та переходом внутрішньосудинної рідини та білків в інтерстиціальний простір. Клінічні ознаки включають генералізовані набряки, збільшення маси тіла, гіпоальбумінемію, виражене зниження артеріального тиску, гостру ниркову недостатність і набряк легенів. Якщо під час терапії гемцитабіном розвивається синдром підвищеної проникності капілярів, необхідно припинити застосування гемцитабіну та проводити підтримуючу терапію. Синдром підвищеної проникності капілярів може розвинутись у пізніх циклах хіміотерапії, у літературі описується його зв'язок із гострим респіраторним дистрес-синдромом. Захворювання легень У ході терапії гемцитабіном виявляють пов'язані з введенням препарату порушення функції легень, у деяких випадках тяжкого ступеня виразності (такі як набряк легень, інтерстиціальний пневмоніт або гострий респіраторний дистрес-синдром). При розвитку цих ефектів слід вирішити питання про відміну терапії гемцитабіном і почати відповідне лікування. Етіологія цих ефектів невідома. При ранньому проведенні підтримуючих заходів можливе покращення стану. Супутня променева терапія Ризик шкірних реакцій зростає за наявності променевої терапії в анамнезі. Залежно від ступеня токсичності, дозу препарату можна знижувати ступінчасто під час кожного циклу або з початком нового циклу лікування. Фертильність Під час лікування та протягом 6 місяців після закінчення терапії гемцитабіном слід використовувати надійні методи контрацепції. У разі настання вагітності на фоні лікування препаратом пацієнтці слід проінформувати про це свого лікаря. У дослідженнях фертильності на самцях мишей показано, що застосування гемцитабіну спричиняє гіпосперматогенез. Чоловікам, які отримують гемцитабін, рекомендується вдатися до кріоконсервації сперми до початку лікування через ризик безпліддя. Пацієнти, що знаходяться на натрієвій дієті При лікуванні пацієнтів, які перебувають на контрольованій натрієвій дієті, слід враховувати вміст препарату натрію в наступних кількостях: флакон 200 мг Гемцитабіну медак містить 3,5 мг ( флакон 1000 мг Гемцитабіну медак містить 17,5 мг ( флакон 1500 мг Гемцитабіну медак містить 26,3 мг ( Вплив на здатність до керування автотранспортом та управління механізмами Дані про вплив терапії гемцитабіном на здатність керувати транспортним засобом та працювати з механізмами відсутні, однак деякі побічні дії препарату, такі як підвищена сонливість, можуть негативно впливати на здатність виконувати такі дії. У період лікування гемцитабіном необхідно дотримуватися обережності при керуванні транспортними засобами та зайнятті потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептом
1 628,00 грн
230,00 грн
Склад, форма випуску та упаковкаЛіофілізат для приготування суспензії для внутрішньом'язового введення пролонгованої дії, що містить 3,75 мг бусереліну.Опис лікарської формиДозування 3,75 мг – 1 ін'єкція. Ліофілізат для приготування суспензії для внутрішньом'язового введення пролонгованої дії.Фармакотерапевтична групаПротипухлинний засіб, гонадотропін-рилізинг гормону (ГнРГ) аналог.Показання до застосуванняГормонозалежний рак передміхурової залози; Рак молочної залози; Ендометріоз (перед- та післяопераційний періоди); Міома матки; Гіперпластичні процеси ендометрію; Лікування безпліддя (при проведенні програми екстракорпорального запліднення (ЕКО)).Протипоказання до застосуванняВагітність; Період лактації; Підвищена чутливість до компонентів препарату.Взаємодія з лікарськими засобамиОдночасне застосування препарату "Бусерелін-лонг" з препаратами, що містять статеві гормони (наприклад, в режимі індукції овуляції), може сприяти виникненню синдрому гіперстимуляції яєчників. При одночасному застосуванні Бусерелін-лонг може знижувати ефективність гіпоглікемічних засобів.Спосіб застосування та дозиПри гормонозалежному раку передміхурової залози Бусерелін-лонг вводять у дозі 3,75 мг (1 ін'єкція) внутрішньом'язово (в/м) кожні 4 тижні. При лікуванні ендометріозу, гіперпластичних процесів ендометрію препарат вводять у дозі 3,75 мг внутрішньом'язово одноразово кожні 4 тижні. Лікування слід розпочинати у перші п'ять днів менструального циклу. Тривалість лікування – 4-6 місяців. При лікуванні міоми матки Бусерелін-лонг вводять у дозі 3,75 мг внутрішньом'язово одноразово кожні 4 тижні. Лікування слід розпочинати у перші п'ять днів менструального циклу. Тривалість лікування перед операцією 3 місяці, в інших випадках - 6 місяців; При лікуванні безпліддя методом екстракорпорального запліднення (ЕКО) Бусерелін-лонг вводять у дозі 3,75 мг (1 ін'єкція) внутрішньом'язово одноразово на початку фолікулінової (на 2-й день менструального циклу) або в середині лютеїнової фази (21 - 24 дн). менструального циклу, що передує стимуляції. Після блокади гіпофізарної функції, підтвердженої зниженням концентрації естрогенів у сироватці крові не менше, ніж на 50 % від вихідного рівня (зазвичай визначається через 12 - 15 днів після ін'єкції Бусерелін-лонг), за відсутності кіст яєчника (за даними УЗД), товщиною ендометрію більше 5 мм, починається стимуляція суперовуляції гонадотропними гормонами під ультразвуковим моніторингом та контролем рівня естрадіолу у сироватці кровіУмови відпустки з аптекЗа рецептомВідео на цю тему
2 116,00 грн
2 072,00 грн
Склад, форма випуску та упаковкаЛіофілізат - 1 фл. Активна речовина: гемцитабіну гідрохлорид 1707.8 мг, що відповідає вмісту гемцитабіну 1500 мг. Допоміжні речовини: манітол, натрію ацетату тригідрат, натрію гідроксид, хлористоводнева кислота. Флакони (1) - пачки картонні.Опис лікарської формиЛіофілізат для приготування розчину для інфузій; білого або майже білого кольору.Фармакотерапевтична групаПротипухлинний засіб, антиметаболіт групи аналогів піримідину, пригнічує синтез ДНК. Виявляє циклоспецифічність, діючи на клітини у фазах S та Gl/S. Метаболізується у клітині під дією нуклеозидкіназ до активних дифосфатних та трифосфатних нуклеозидів. Дифосфатні нуклеозиди пригнічують дію рибонуклеотидредуктази (єдиного ферменту, що каталізує утворення дезоксинуклеозидтрифосфатів, необхідних для синтезу ДНК). Трифосфатні нуклеозиди здатні вбудовуватися в ланцюжок ДНК (меншою мірою РНК), що призводить до припинення подальшого синтезу ДНК та запрограмованої загибелі клітини (апоптоз). Гемцитабін є також сильним радіосенсибілізуючим засобом навіть у концентраціях нижчих за цитотоксичні.ФармакокінетикаC max ;гемцитабіну (від 3.2 мкг/мл до 45.5 мкг/мл) досягається через 5 хвилин після закінчення інфузій. Фармакокінетичний аналіз досліджень з одноразовим і багаторазовим введенням доз показує, що Vd значною мірою залежить від статі. Зв'язування гемцитабіну з білками плазми незначне. В організмі гемцитабін швидко метаболізується під дією цитидиндезамінази в печінці, нирках, крові та інших тканинах, в результаті чого утворюються гемцитабін моно-, ді-і трифосфати (dFdCMP, dFdCDP і dFdCTP), з яких активними вважаються dFdCDP і dFd. Гемцитабін швидко виводиться з організму з сечею переважно у вигляді неактивного метаболіту 2'-дезокси-2', 2'-дифторуридину. Менше 10% введеної внутрішньовенної дози виявляється у сечі у формі незміненого гемцитабіну. Системний кліренс, який коливається приблизно від 30 л/год/м2; до 90 л/год/м2, залежить від віку та статі: швидкість виведення у жінок приблизно на 25% нижче, ніж у чоловіків; як у чоловіків, і у жінок швидкість виведення знижується з віком. T1/2; коливається від 42 хв до 94 хв. При дотриманні рекомендованого режиму дозування повне виведення гемцитабіну відбувається протягом 5-11 годин від початку інфузії. При введенні раз на тиждень гемцитабін не накопичується в організмі. Комбінована терапія гемцитабіном та паклітакселом. ;При спільному введенні гемцитабіну та паклітакселу фармакокінетика препаратів не змінюється. Комбінована терапія гемцитабіном та карбоплатином. ;При спільному введенні гемцитабіну та карбоплатину фармакокінетика гемцитабіну не змінюється. Порушення функції нирок. ;Ніркова недостатність легкого або помірного ступеня (кліренс креатиніну 30-80 мл/хв) не істотно впливає на фармакокінетику гемцитабіну.Клінічна фармакологіяПротипухлинний препарат. Антиметаболіт.Показання до застосуванняМісцево поширений або метастатичний недрібноклітинний рак легені як терапії першої лінії в комбінації з цисплатином, а також у монотерапії у літніх пацієнтів з функціональним статусом, рівним 2; нерезектабельний, місцеворецидивний або метастатичний рак молочної залози у складі комбінованої терапії з паклітакселом після проведення неоад'ювантної та/або ад'ювантної терапії з включенням антрациклінів за відсутності протипоказань до їх призначення; місцевопоширений або метастатичний уротеліальний рак (рак сечового міхура, ниркової балії, сечоводів, уретри); місцевопоширений або метастатичний епітеліальний рак яєчників як монотерапія або у поєднанні з карбоплатином у пацієнтів з прогресуванням захворювання після проведення першої лінії терапії на основі платиносмістких препаратів; місцевопоширений або метастатичний рак підшлункової залози; місцеворозповсюджений або метастатичний рак шийки матки.Протипоказання до застосуванняПідвищена чутливість до активної речовини або до будь-якої з допоміжних речовин; вагітність та період годування груддю; дитячий вік до 18 років (відсутність достатніх даних щодо ефективності та безпеки). З обережністю: ;при порушенні функції печінки та/або нирок, пригніченні кістковомозкового кровотворення (у тому числі на тлі супутньої променевої або хіміотерапії), серцево-судинних захворюваннях в анамнезі, при метастатичному ураженні печінки, гепатиті, алкоголізмі, при одночасно проведеному промені. гострі інфекційні захворювання вірусної, грибкової або бактеріальної природи (у тому числі вітряної віспи, що оперізує лишаї).Вагітність та лактаціяПротипоказаний: вагітність та період годування груддю. Застосування у дітей Протипоказаний дітям до 18 років (відсутність достатніх даних щодо ефективності та безпеки).Побічна діяПобічні реакції, що зустрічалися частіше, ніж у поодиноких випадках, перераховані відповідно до наступної градації: дуже часто (> 10%); часто (>1% до <10%); нечасто (>0.1% до <1%); рідко (>0.01% до <0.1%); дуже рідко (<0.01%). З боку органів кровотворення: часто - лейкопенія, нейтропенія, тромбоцитопенія, анемія; часто – фебрильна нейтропенія; дуже рідко – тромбоцитоз. З боку системи травлення: дуже часто - нудота, блювання, підвищення активності "печінкових" трансаміназ (аспартатамінотрансферази, аланінамінотрансферази), лужної фосфатази; часто – анорексія, діарея, запор, стоматит, підвищення концентрації білірубіну; рідко – підвищення активності гамма-глутамілтрансферази; частота не може бути оцінена на підставі наявних даних - ішемічний коліт, токсичне ураження печінки, включаючи печінкову недостатність з летальним кінцем. З боку сечовидільної системи: дуже часто - гематурія і протеїнурія легкого ступеня; частота не може бути оцінена на підставі наявних дачних – гостра ниркова недостатність, клінічні ознаки та симптоми, схожі з гемолітико-уремічним синдромом (зниження гемоглобіну, тромбоцитопенія, збільшення вмісту білірубіну, креатиніну, сечовини та/або лактатдегідрогенази у сироватці). З боку шкіри і шкірних придатків: дуже часто - шкірні висипання, що супроводжуються свербінням, алопеція; часто; шкірний свербіж, підвищена пітливість; рідко виразки, утворення бульбашок, дуже рідко виражені шкірні реакції, включаючи десквамацію та бульозні висипання; частота може бути оцінена - синдром Лайелла, синдром Стівенса-Джонсона. З боку дихальної системи: дуже часто - задишка; часто – кашель, риніт, нечасто – бронхоспазм, інтеретиційна пневмонія; частота може бути оцінена - набряк легені, гострий респіраторний дистресс-синдром. З боку серцево-судинної системи: рідко - зниження артеріального тиску, інфаркт міокарда, частота не може бути оцінена - аритмія (в основному суправентрикулярна), серцева недостатність, клінічні ознаки периферичного васкуліту та гангрени. З боку нервової системи: часто - головний біль, підвищена сонливість, безсоння; частота може бути оцінена - інсульт. Інші: дуже часто - почуття нездужання, грипоподібний синдром, периферичні набряки; часто - підвищення температури тіла, озноб, астенія, біль у спині, міалгія; рідко – набряклість особи, реакції у місці введення; дуже рідко – анафілактичні реакції.Взаємодія з лікарськими засобамиСпецифічних досліджень взаємодій гемцитабіну не проводилося. Променева терапія Супутня променева терапія (одночасно з введенням гемцитабіну або з інтервалом < 7 днів до початку лікування): ;в даній ситуації токсичність лікування залежить від багатьох факторів, включаючи дозу гемцитабіну та частоту його введення, дозу випромінювання, метод променевої терапії, характер опроміненої тканини та її Об `єм. Було показано, що гемцитабін має радіосенсибілізуючу активність. В одному дослідженні, де пацієнти з недрібноклітинним раком легені отримували гемцитабін у дозі 1000 мг/м2; протягом 6 послідовних тижнів у поєднанні з терапевтичним опроміненням на область грудної клітини, була відзначена значна токсичність, у вигляді важкого та потенційно загрозливого життя запалення слизу головним чином езофагіту та пневмоніту, особливо у пацієнтів з великим об'ємом опромінення тканин (медіана об'єму опромінюваної тканини 4795 см3).У подальших дослідженнях було показано, що поєднання нижчих доз гемцитабіну та променевої терапії краще переноситься пацієнтами та характеризується передбачуваним профілем токсичності. Так, в одному з досліджень II фази пацієнтам з недрібноклітинним раком легені проводилася променева терапія в дозі 60 Гр спільно з введенням гемцитабіну (600 мг/м2; 4 рази) та цисплатину (80 мг/м2; 2 рази) протягом 6 тижнів. Послідовна терапія (перерва > 7 днів): ;за існуючими даними, введення гемцитабіну більш ніж за 7 днів до початку променевої терапії або більш ніж через 7 днів після завершення не супроводжується збільшенням токсичності, за винятком ураження шкіри, пов'язаного з введенням хіміопрепарату після опромінення . Лікування гемцитабіном може бути розпочато через 7 днів після опромінення або після розв'язання всіх гострих променевих реакцій. Як при супутньому, так і при послідовному застосуванні гемцитабіну і променевої терапії можливе променеве ураження тканин, що опромінюються (напр., езофагіт, коліт і пневмоніт). Імунодепресанти (азатіоприн, хлорамбуцил, глюкокортикостероїди, циклофосфамід, циклоспорин, меркаптопурин) збільшують ризик розвитку інфекцій. Інші види взаємодії При одночасному застосуванні з живими вірусними вакцинами можлива інтенсифікація процесу реплікації вакцинного вірусу посилення його побічних/несприятливих ефектів та/або зниження вироблення антитіл в організмі хворого у відповідь на введення вакцини. Тому через ризик системних, можливо летальних ускладнень, особливо у хворих зі зниженим імунним статусом, інтервал між застосуванням гемцитабіну та таких вакцин має бути не менше ніж 3 місяці або більше (до 12 місяців) залежно від імунного статусу хворого. Дослідження сумісності гемцитабіну не проводились. Не можна змішувати гемцитабін з іншими лікарськими засобами.Спосіб застосування та дозиГемцитабін вводиться внутрішньовенно краплинно протягом 30 хвилин. Недрібноклітинний рак легені Монотерапія: ; рекомендована доза препарату - 1000 мг/м 2 ;в 1, 8 та 15 дні кожного 28-денного циклу. Комбінована терапія з цисплатином: ; рекомендована доза препарату - 1250 мг/м 2 ;в 1 і 8 день кожного 21-денного циклу або 1000 мг/м 2 ;в 1, 8 і 15 дні кожного 28-денного циклу Цисплатин вводиться в -100 мг/м 2 ;в 1-й день циклу на фоні водного навантаження після інфузії гемцитабіну. Комбінована терапія з карбоплатином: рекомендована доза препарату – 1000 мг/м 2 ; або 1200 мг/м 2 в 1 та 8 день кожного 21-денного циклу. Карбоплатин вводиться в дозі AUC 5.0 мг/мл*хв у 1 день циклу після інфузії гемцитабіну. Рак молочної залози Комбінована терапія: як терапія 1-ї лінії при прогресуванні захворювання після неоад'ювантної терапії, що включає антрацикліни; рекомендована доза препарату - 1250 мг/м 2 ;в 1-й та 8-й дні у поєднанні з паклітакселом у дозі 175 мг/м 2 , який вводиться в 1-й день кожного 21-денного циклу внутрішньовенно краплинно приблизно протягом 3 год, перед введенням гемцитабіну. Уротеліальний рак Монотерапія: ; рекомендована доза препарату - 1250 мг/м 2 ;в 1, 8 та 15 дні кожного 28-денного циклу. Комбінована терапія: ; рекомендована доза препарату - 1000 мг/м 2 ;в 1-й, 8-й і 15-й дні у поєднанні з цисплатином, який вводиться в дозі 70 мг/м 2 ; або на 2-й день кожного 28-денного циклу. Епітеліальний рак яєчників Монотерапія: ; рекомендована доза препарату - 800-1250 мг/м 2 ;в 1-й, 8-й та 15-й дні кожного 28-денного циклу. Комбінована терапія: ; рекомендована доза препарату - 1000 мг/м 2 ;в 1-й та 8-й дні у поєднанні з карбоплатином у дозі AUC4.0 мг/мл*хв, який вводиться відразу після інфузії гемцитабіну в 1-й день кожного 21-денний цикл. Рак підшлункової залози Монотерапія: рекомендована доза препарату – 1000 мг/м 2 ; 1 раз на тиждень протягом 7 тижнів з наступною тижневою перервою. Потім препарат вводиться в 1-й, 8-й та 15-й дні кожного 28-денного циклу. Рак шийки матки (місцерозповсюджений або метастатичний) Комбінована терапія: ;При місцеворозповсюдженому раку (неоад'ювантно) і при метастатичному раку гемцитабін вводиться в дозі 1250 мг/м 2 ;в 1-й та 8-й дні кожного 21-денного циклу. Цисплатин вводиться в дозі 70 мг/м 2 ; після введення гемцитабіну в 1-й день циклу на фоні гіпергідратації. Коректор дози препарату у зв'язку із явищами гематологічної токсичності Початок циклу лікування Незалежно від показань, перед кожним введенням препарату необхідно оцінювати чисто тромбоцити та гранулоцити. Умовою початку лікування є абсолютна кількість нейтрофілів не менше 1500/мкл та кількість тромбоцитів не менше 100000/мкл. У разі розвитку гематологічної токсичності; під час проведення циклу терапії доза гемцитабіну може бути зменшена, або її введіть відкладено відповідно до наступних рекомендацій: Модифікація дози гемцитабіну, що застосовується в монотерапії або в комбінації з цисплатином при лікуванні раку сечового міхура, недрібноклітинного раку легені та раку підшлункової залози. Абсолютна кількість нейтрофілів (1 мкл) ; Кількість тромбоцитів (1 мкл) % від стандартної дози > 1000 і > 100 000 100 500 – 1000 або 50000 – 100000 75 < 500 або < 50000 Відкласти введення* * При збільшенні кількості нейтрофілів до 500/мкл та тромбоцитів до 50000/мкл введення гемцитабіну може бути продовжено в рамках циклу Модифікація дози гемцитабіну, що застосовується у комбінації з паклітакселом при лікуванні раку молочної залози. Абсолютна кількість нейтрофілів (1 мкл) ; Кількість тромбоцитів (1 мкл) % від стандартної дози ≥ 1200 і > 75 000 100 1000 - < 1200 або 50000 – 75000 75 700 - < 1000 і ≥ 50000 50 < 700 або < 50000 Відкласти введення* * Лікування в рамках циклу не поновлюється. Чергове введення гемцитабіну проводиться в 1 день чергового циклу при відновленні кількості нейтрофілів як мінімум до 1500/мкл і тромбоцитів до 100000/мкл Модифікація дози гемцитабіну, що застосовується в комбінації з карбоплатином при лікуванні раку яєчників Абсолютна кількість нейтрофілів (1 каст) ; Кількість тромбоцитів (1 мкл) % від стандартної дози > 1500 і ≥ 100000 100 1000 – 1500 або 75000 – 100000 50 < 1000 або < 75000 Скасування вступу* * Лікування в рамках циклу не поновлюється. Чергове введення гемцитабіну проводиться в 1 день чергового циклу при досягненні кількості нейтрофілів як мінімум до 1500/мкл та тромбоцитів до 100000/мкл Доза гемцитабіну на черговому циклі повинна бути зменшена на 25% при всіх показаннях у випадках, якщо за попереднього циклу спостерігалося: зниження абсолютного чиста нейтрофілів < 500/мкл, що триває понад 5 днів; зниження абсолютної кількості нейтрофілів < 100/мкл, що триває понад 3 дні; фебрильна нейтропенія; зниження чистої тромбоцитів < 25000/мкл; цикл був відкладений більш ніж на 1 тиждень через гематологічну токсичність. Корекція дози препарату у зв'язку із явищами негематологічної токсичності Для виявлення негематологічної токсичності повинні проводитись періодичний фізикальний огляд та контроль функцій печінки та нирок. Доза препарату може бути зменшена у кожному наступному циклі або протягом вже розпочатого циклу залежно від ступеня прояву токсичності препаратів, призначених пацієнтові. У разі тяжкої (3 або 4 ступінь) негематологічної токсичності, за винятком випадків нудоти/блювоти, терапію гемцитабіном слід призупинити або знизити величину дозування залежно від рішення лікаря. Рішення про відновлення лікування приймає лікар. Спосіб введення Інфузійне введення гемцитабіну зазвичай добре переноситься пацієнтами та може проводитися в амбулаторних умовах. У разі екстравазації інфузію припиняють та відновлюють введення препарату в іншу вену. Після введення гемцитабіну пацієнт повинен спостерігатися протягом певного часу. Особливі групи пацієнтів Пацієнти з порушенням функції печінки та нирок: застосовувати гемцитабін у хворих з печінковою недостатністю або з порушеною функцією нирок слід з обережністю, оскільки достатніх даних щодо застосування препарату у цієї категорії пацієнтів немає. Ниркова недостатність помірної або середньої тяжкості (швидкість клубочкової фільтрації від 30 мл/хв до 80 мл/хв) не помітно впливає на фармакокінетику гемцитабіну. Літні пацієнти (> 65 років): гемцитабін добре переноситься пацієнтами старше 65 років. Специфічних рекомендацій щодо зміни дози препарату для цієї популяції відсутні. Діти (< 18 років): ;гемцитабін не рекомендується призначати дітям до 18 років у зв'язку з недостатньою інформацією з безпеки та ефективності препарату в даній популяції. Рекомендації щодо приготування розчину для інфузій Як розчинник використовується тільки 0.9% розчин натрію хлориду без консервантів. Для приготування розчину препарату у флакон повільно вводять необхідну кількість 0.9% розчину хлориду натрію для ін'єкцій (не менше кількості, зазначеної в таблиці нижче) і акуратно струшують флакон до повного розчинення вмісту. Дозування препарату у флаконі Необхідний об'єм 0.9% розчину хлориду натрію для ін'єкцій Об'єм відновленого розчину Концентрація гемцитабіну в розчині 200 мг 5 мл 5.26 мл 38 мг/мл 1000 мг 25 мл 26.3 мл 38 мг/мл 1500 мг 37.5 мл 39.5 мл 38 мг/мл Отриманий розчин має бути прозорим. Максимальна концентрація відновленого розчину гемцитабіну не повинна перевищувати 38 мг/мл, оскільки при більш високих концентраціях можливе неповне розчинення препарату. Приготовлений розчин гемцитабіну, що містить потрібну дозу препарату, перед введенням розбавляють 0.9% розчином натрію хлориду для ін'єкцій у кількості, достатньому для 30-хвилинної внутрішньовенної інфузії. Перед парентеральним введенням розчину препарату слід переконатися у відсутності в ньому нерозчинених частинок та зміни кольору розчину Приготовлений розчин препарату призначений лише для одноразового застосування. Весь невикористаний препарат має бути утилізовано.ПередозуванняСимптоми: мієлодепресія, парестезія, виражена шкірна висипка. При введенні гемцитабіну в дозах до 5700 мг/м2 внутрішньовенно краплинно за 30 хвилин кожні 2 тижні ознак передозування не спостерігалося. Антидот для гемцитабіну невідомий. При підозрі на передозування гемцитабіну слід контролювати рівень цитопенії та при необхідності призначити симптоматичну терапію.Запобіжні заходи та особливі вказівкиЛікування гемцитабіном можна проводити лише під наглядом лікаря, який має досвід застосування протипухлинної хіміотерапії. Перед кожним введенням гемцитабіну необхідно контролювати кількість тромбоцитів, лейкоцитів та гранулоцитів у крові. При ознаках пригнічення функції кісткового мозку, спричиненого препаратом, необхідно припинити лікування або скоригувати дозу. Зазвичай пригнічення функції кісткового мозку має короткостроковий характер, не вимагає зниження дози і рідко призводить до необхідності переривання лікування. Показники периферичної крові можуть погіршуватися після переривання терапії гемцитабіном. При застосуванні гемцитабіну у комбінації з іншими протипухлинними хіміопрепаратами необхідно враховувати ризик кумулятивного пригнічення функції кісткового мозку. Необхідно проводити регулярне обстеження хворого та оцінку функції нирок та печінки. Введення гемцитабіну при метастазах у печінці, при гепатиті та алкоголізмі в анамнезі, а також при цирозі печінки збільшує ризик розвитку печінкової недостатності. При появі ознак розвитку небажаних явищ з боку дихальної системи (наприклад, набряк легенів, інтерстиціальний пневмоніт або респіраторний дистрес-синдром у дорослих) на тлі лікування гемцитабіном лікування слід припинити та призначити відповідну терапію. При появі перших ознак мікроангіопатичної гемолітичної анемії, таких як швидке зниження гемоглобіну з супутньою тромбоцитопенією, підвищення сироваткової концентрації білірубіну, креатиніну, азоту сечовини або підвищення активності лактатдегідрогенази, гемцитабін повинен бути скасований. Збільшення тривалості інфузії та частоти введень призводить до зростання токсичності. Ризик шкірних реакцій зростає за наявності променевої терапії в анамнезі. Залежно від ступеня токсичності дозу можна знижувати протягом кожного циклу або з початком нового циклу ступінчасто. Під час лікування та протягом 6 місяців після закінчення терапії гемцитабіном слід використовувати надійні методи контрацепції. Чоловікам, які отримують гемцитабін, рекомендується вдатися до кріоконсервації сперми до початку лікування через ризик безпліддя, зумовлений застосуванням даного препарату. При лікуванні пацієнтів, які перебувають на контрольованій натрієвій дієті, слід враховувати вміст у препараті натрію в наступних кількостях: флакон 200 мг Гемцитабіну медак містить 3.5 мг (< 1 ммоль) натрію, флакон 1000 мг Гемцитабіну медак містить 17.5 мг (< 1 ммоль) натрію, флакон 1500 мг Гемцитабіну медак містить 26.3 мг (<1 ммоль) натрію. Вплив на здатність керувати транспортним засобом та працювати з механізмами. ;Дані про вплив терапії гемцитабіном на здатність керувати транспортним засобом та працювати з механізмами відсутні, однак деякі побічні дії препарату такі як підвищена сонливість, можуть негативно впливати на здатність виконувати такі дії. У період лікування гемцитабіном необхідно дотримуватися обережності при керуванні транспортними засобами та зайнятті потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови відпустки з аптекЗа рецептом
726,00 грн
690,00 грн
Склад, форма випуску та упаковкаЛіофілізат для приготування розчину - 1 фл. Активні речовини: гемцитабіну гідрохлорид – 227.7 мг, що відповідає вмісту гемцитабіну – 200 мг; Допоміжні речовини: манітол, натрію ацетату тригідрат, натрію гідроксид, хлористоводнева кислота. Флакони (1) - пачки картонні.Опис лікарської формиЛіофілізат для приготування розчину для інфузії білого або майже білого кольору.Фармакотерапевтична групаПротипухлинний засіб, антиметаболіт.ФармакокінетикаCmax гемцитабіну (від 3.2 до 45.5 мкг/мл) досягається через 5 хвилин після закінчення інфузій. Фармакокінетичний аналіз досліджень з одноразовим та багаторазовим введенням доз показує, що Vd значною мірою залежить від статі. Зв'язування гемцитабіну з білками плазми незначне. В організмі гемцитабін швидко метаболізується під дією цитидиндезамінази в печінці, нирках, крові та інших тканинах, в результаті чого утворюються гемцитабін моно-, ді-і трифосфати (dFdCMP, dFdCDP і dFdCTP), з яких активними вважаються dFdCDP і dFd. Гемцитабін швидко виводиться з організму з сечею переважно у вигляді неактивного метаболіту 2'-дезокси-2', 2'-дифторуридину. Менше 10% введеної внутрішньовенної дози виявляється у сечі у формі незміненого гемцитабіну. Системний кліренс, який коливається приблизно від 30 л/год/м2 до 90 л/год/м2, залежить від віку та статі: швидкість виведення у жінок приблизно на 25% нижче, ніж у чоловіків; як у чоловіків, і у жінок швидкість виведення знижується з віком. T1/2 коливається від 42 хв до 94 хв. При дотриманні рекомендованого режиму дозування повне виведення гемцитабіну відбувається протягом 5-11 годин від початку інфузії. При введенні раз на тиждень гемцитабін не накопичується в організмі. Комбінована терапія гемцитабіном та паклітакселом. При сумісному введенні гемцитабіну та паклітакселу фармакокінетика препаратів не змінюється. Комбінована терапія гемцитабіном та карбоплатином. При сумісному введенні гемцитабіну та карбоплатину фармакокінетика гемцитабіну не змінюється. Порушення функції нирок. Ниркова недостатність легкого або помірного ступеня (кліренс креатиніну 30-80 мл/хв) не істотно впливає на фармакокінетику гемцитабіну.ФармакодинамікаПротипухлинний засіб, антиметаболіт групи аналогів піримідину, пригнічує синтез ДНК. Виявляє циклоспецифічність, діючи на клітини у фазах S та Gl/S. Метаболізується у клітині під дією нуклеозидкіназ до активних дифосфатних та трифосфатних нуклеозидів. Дифосфатні нуклеозиди пригнічують дію рибонуклеотидредуктази (єдиного ферменту, що каталізує утворення дезоксинуклеозидтрифосфатів, необхідних для синтезу ДНК). Трифосфатні нуклеозиди здатні вбудовуватися в ланцюжок ДНК (меншою мірою РНК), що призводить до припинення подальшого синтезу ДНК та запрограмованої загибелі клітини (апоптоз). Гемцитабін є також сильним радіосенсибілізуючим засобом навіть у концентраціях нижчих за цитотоксичні.Клінічна фармакологіяПротипухлинний препарат. Антиметаболіт.Показання до застосуваннямісцевопоширений або метастатичний недрібноклітинний рак легені як терапії першої лінії в комбінації з цисплатином, а також у монотерапії у літніх пацієнтів з функціональним статусом, рівним 2; нерезектабельний, місцеворецидивний або метастатичний рак молочної залози у складі комбінованої терапії з паклітакселом після проведення неоад'ювантної та/або ад'ювантної терапії з включенням антрациклінів за відсутності протипоказань до їх призначення; місцевопоширений або метастатичний уротеліальний рак (рак сечового міхура, ниркової балії, сечоводів, уретри); місцевопоширений або метастатичний епітеліальний рак яєчників як монотерапія або у поєднанні з карбоплатином у пацієнтів з прогресуванням захворювання після проведення першої лінії терапії на основі платиносмістких препаратів; місцевопоширений або метастатичний рак підшлункової залози; місцеворозповсюджений або метастатичний рак шийки матки.Протипоказання до застосуванняпідвищена чутливість до активної речовини або до будь-якої з допоміжних речовин; вагітність та період годування груддю; дитячий вік до 18 років (відсутність достатніх даних щодо ефективності та безпеки). З обережністю: при порушенні функції печінки та/або нирок, пригніченні кістковомозкового кровотворення (у тому числі на тлі супутньої променевої або хіміотерапії), серцево-судинних захворюваннях в анамнезі, при метастатичному ураженні печінки, гепатиті, алкоголізмі, при одночасно проведеній променевій інфекційні захворювання вірусної, грибкової або бактеріальної природи (у тому числі вітряної віспи, що оперізує лишаї).Вагітність та лактаціяПротипоказаний: вагітність та період годування груддю. Протипоказаний дітям до 18 років (відсутність достатніх даних щодо ефективності та безпеки).Побічна діяПобічні реакції, що зустрічалися частіше, ніж у поодиноких випадках, перераховані відповідно до наступної градації: дуже часто (> 10%); часто (> 1% до 0.1% до 0.01% до З боку органів кровотворення: часто – лейкопенія, нейтропенія, тромбоцитопенія, анемія; часто – фебрильна нейтропенія; дуже рідко – тромбоцитоз. З боку системи травлення: дуже часто – нудота, блювання, підвищення активності “печінкових” трансаміназ (аспартатамінотрансферази, аланінамінотрансферази), лужної фосфатази; часто – анорексія, діарея, запор, стоматит, підвищення концентрації білірубіну; рідко – підвищення активності гамма-глутамілтрансферази; частота не може бути оцінена на підставі наявних даних - ішемічний коліт, токсичне ураження печінки, включаючи печінкову недостатність з летальним кінцем. З боку сечовидільної системи: дуже часто – гематурія та протеїнурія легкого ступеня; частота не може бути оцінена на підставі наявних дачних – гостра ниркова недостатність, клінічні ознаки та симптоми, схожі з гемолітико-уремічним синдромом (зниження гемоглобіну, тромбоцитопенія, збільшення вмісту білірубіну, креатиніну, сечовини та/або лактатдегідрогенази у сироватці). З боку шкіри та шкірних придатків: дуже часто – шкірні висипання, що супроводжуються свербінням, алопеція; часто - свербіж шкіри, підвищена пітливість; рідко - виразки, утворення бульбашок, дуже рідко - виражені шкірні реакції, включаючи десквамацію та бульозні висипання; частота може бути оцінена - синдром Лайелла, синдром Стівенса-Джонсона. З боку дихальної системи: дуже часто – задишка; часто – кашель, риніт, нечасто – бронхоспазм, інтеретиційна пневмонія; частота може бути оцінена - набряк легені, гострий респіраторний дистресс-синдром. З боку серцево-судинної системи: рідко – зниження артеріального тиску, інфаркт міокарда, частота не може бути оцінена – аритмія (переважно суправентрикулярна), серцева недостатність, клінічні ознаки периферичного васкуліту та гангрени. З боку нервової системи: часто – головний біль, підвищена сонливість, безсоння; частота може бути оцінена - інсульт. Інші: дуже часто – почуття нездужання, грипоподібний синдром, периферичні набряки; часто - підвищення температури тіла, озноб, астенія, біль у спині, міалгія; рідко – набряклість особи, реакції у місці введення; дуже рідко – анафілактичні реакції.Взаємодія з лікарськими засобамиСпецифічних досліджень взаємодій гемцитабіну не проводилося. Променева терапія Супутня променева терапія (одночасно із введенням гемцитабіну або з інтервалом Послідовна терапія (перерва > 7 днів): за існуючими даними, введення гемцитабіну більш ніж за 7 днів до початку променевої терапії або більш ніж через 7 днів після завершення не супроводжується збільшенням токсичності, за винятком ураження шкіри, пов'язаного з введенням хіміопрепарату після опромінення. Лікування гемцитабіном може бути розпочато через 7 днів після опромінення або після розв'язання всіх гострих променевих реакцій. Як при супутньому, так і при послідовному застосуванні гемцитабіну і променевої терапії можливе променеве ураження тканин, що опромінюються (напр., езофагіт, коліт і пневмоніт). Імунодепресанти (азатіоприн, хлорамбуцил, глюкокортикостероїди, циклофосфамід, циклоспорин, меркаптопурин) збільшують ризик розвитку інфекцій. Інші види взаємодії При одночасному застосуванні з живими вірусними вакцинами можлива інтенсифікація процесу реплікації вакцинного вірусу посилення його побічних/несприятливих ефектів та/або зниження вироблення антитіл в організмі хворого у відповідь на введення вакцини. Тому через ризик системних, можливо летальних ускладнень, особливо у хворих зі зниженим імунним статусом, інтервал між застосуванням гемцитабіну та таких вакцин має бути не менше ніж 3 місяці або більше (до 12 місяців) залежно від імунного статусу хворого. Дослідження сумісності гемцитабіну не проводились. Не можна змішувати гемцитабін з іншими лікарськими засобами.Спосіб застосування та дозиГемцитабін вводиться внутрішньовенно краплинно протягом 30 хвилин. Недрібноклітинний рак легені Монотерапія: доза препарату, що рекомендується, - 1000 мг/м 2 в 1, 8 і 15 дні кожного 28-денного циклу. Комбінована терапія з цисплатином: рекомендована доза препарату - 1250 мг/м 2 на 1 та 8 день кожного 21-денного циклу або 1000 мг/м 2 на 1, 8 та 15 дні кожного 28-денного циклу Цисплатин вводиться у дозі 70- /м 2 в перший день циклу на тлі водного навантаження після інфузії гемцитабіну. Комбінована терапія з карбоплатином: рекомендована доза препарату – 1000 мг/м 2 або 1200 мг/м 2 на 1 та 8 день кожного 21-денного циклу. Карбоплатин вводиться в дозі AUC 5.0 мг/мл*хв у 1 день циклу після інфузії гемцитабіну. Рак молочної залози Комбінована терапія: як терапія 1-ї лінії при прогресуванні захворювання після неоад'ювантної терапії, що включає антрацикліни; рекомендована доза препарату - 1250 мг/м 2 в 1-й та 8-й дні у поєднанні з паклітакселом у дозі 175 мг/м 2 , який вводиться в 1-й день кожного 21-денного циклу внутрішньовенно краплинно приблизно протягом 3 год, перед введенням гемцитабіну. Уротеліальний рак Монотерапія: доза препарату, що рекомендується, - 1250 мг/м 2 в 1, 8 і 15 дні кожного 28-денного циклу. Комбінована терапія: рекомендована доза препарату - 1000 мг/м 2 в 1-й, 8-й та 15-й дні у поєднанні з цисплатином, який вводиться в дозі 70 мг/м 2 відразу після інфузії гемцитабіну в 1-й або 2 -й день кожного 28-денного циклу Епітеліальний рак яєчників Монотерапія: рекомендована доза препарату - 800-1250 мг/м 2 в 1-й, 8-й та 15-й дні кожного 28-денного циклу. Комбінована терапія: рекомендована доза препарату - 1000 мг/м 2 в 1-й та 8-й дні у поєднанні з карбоплатином у дозі AUC4.0 мг/мл*хв, який вводиться одразу після інфузії гемцитабіну у 1-й день кожного 21- денного циклу. Рак підшлункової залози Монотерапія: рекомендована доза препарату - 1000 мг/м 2 1 раз на тиждень протягом 7 тижнів з наступною тижневою перервою. Потім препарат вводиться в 1-й, 8-й та 15-й дні кожного 28-денного циклу. Рак шийки матки (місцерозповсюджений або метастатичний) Комбінована терапія: При місцеворозповсюдженому раку (неоад'ювантно) та при метастатичному раку гемцитабін вводиться в дозі 1250 мг/м 2 у 1-му та 8-му дні кожного 21-денного циклу. Цисплатин вводиться в дозі 70 мг/м 2 після введення гемцитабіну в 1-й день циклу на тлі гіпергідратації. Коректор дози препарату у зв'язку із явищами гематологічної токсичності Початок циклу лікування Незалежно від показань, перед кожним введенням препарату необхідно оцінювати чисто тромбоцити та гранулоцити. Умовою початку лікування є абсолютна кількість нейтрофілів не менше 1500/мкл та кількість тромбоцитів не менше 100000/мкл. У разі розвитку гематологічної токсичності під час проведення циклу терапії доза гемцитабіну може бути зменшена або введіть її відкладено відповідно до наступних рекомендацій: Модифікація дози гемцитабіну, що застосовується в монотерапії або в комбінації з цисплатином при лікуванні раку сечового міхура, недрібноклітинного раку легені та раку підшлункової залози. Абсолютна кількість нейтрофілів (1 мкл) Кількість тромбоцитів (1 мкл) % від стандартної дози > 1000 і > 100 000 100 500 – 1000 або 50000 – 100000 75 < 500 або < 50000 Відкласти введення* * При збільшенні кількості нейтрофілів до 500/мкл та тромбоцитів до 50000/мкл введення гемцитабіну може бути продовжено в рамках циклу Модифікація дози гемцитабіну, що застосовується у комбінації з паклітакселом при лікуванні раку молочної залози. Абсолютна кількість нейтрофілів (1 мкл) Кількість тромбоцитів (1 мкл) % від стандартної дози ≥ 1200 і > 75 000 100 1000 - < 1200 або 50000 – 75000 75 700 - < 1000 і ≥ 50000 50 < 700 або < 50000 Відкласти введення* * Лікування в рамках циклу не поновлюється. Чергове введення гемцитабіну проводиться в 1 день чергового циклу при відновленні кількості нейтрофілів як мінімум до 1500/мкл і тромбоцитів до 100000/мкл Модифікація дози гемцитабіну, що застосовується в комбінації з карбоплатином при лікуванні раку яєчників Абсолютна кількість нейтрофілів (1 каст) Кількість тромбоцитів (1 мкл) % від стандартної дози > 1500 і ≥ 100000 100 1000 – 1500 або 75000 – 100000 50 < 1000 або < 75000 Скасування вступу* * Лікування в рамках циклу не поновлюється. Чергове введення гемцитабіну проводиться в 1 день чергового циклу при досягненні кількості нейтрофілів як мінімум до 1500/мкл та тромбоцитів до 100000/мкл Доза гемцитабіну на черговому циклі повинна бути зменшена на 25% при всіх показаннях у випадках, якщо за попереднього циклу спостерігалося: зниження абсолютного чиста нейтрофілів < 500/мкл, що триває понад 5 днів; зниження абсолютної кількості нейтрофілів < 100/мкл, що триває понад 3 дні; фебрильна нейтропенія; зниження чистої тромбоцитів < 25000/мкл; цикл був відкладений більш ніж на 1 тиждень через гематологічну токсичність. Корекція дози препарату у зв'язку із явищами негематологічної токсичності Для виявлення негематологічної токсичності повинні проводитись періодичний фізикальний огляд та контроль функцій печінки та нирок. Доза препарату може бути зменшена у кожному наступному циклі або протягом вже розпочатого циклу залежно від ступеня прояву токсичності препаратів, призначених пацієнтові. У разі тяжкої (3 або 4 ступінь) негематологічної токсичності, за винятком випадків нудоти/блювоти, терапію гемцитабіном слід призупинити або знизити величину дозування залежно від рішення лікаря. Рішення про відновлення лікування приймає лікар. Спосіб введення Інфузійне введення гемцитабіну зазвичай добре переноситься пацієнтами та може проводитися в амбулаторних умовах. У разі екстравазації інфузію припиняють та відновлюють введення препарату в іншу вену. Після введення гемцитабіну пацієнт повинен спостерігатися протягом певного часу. Особливі групи пацієнтів Пацієнти з порушенням функції печінки та нирок: застосовувати гемцитабін у хворих з печінковою недостатністю або з порушеною функцією нирок слід з обережністю, оскільки достатніх даних щодо застосування препарату у цієї категорії пацієнтів немає. Ниркова недостатність помірної або середньої тяжкості (швидкість клубочкової фільтрації від 30 мл/хв до 80 мл/хв) не помітно впливає на фармакокінетику гемцитабіну. Літні пацієнти (>65 років): гемцитабін добре переноситься пацієнтами старше 65 років. Специфічних рекомендацій щодо зміни дози препарату для цієї популяції відсутні. Діти (< 18 років): гемцитабін не рекомендується призначати дітям до 18 років у зв'язку з недостатньою інформацією з безпеки та ефективності препарату в даній популяції. Рекомендації щодо приготування розчину для інфузій Як розчинник використовується тільки 0.9% розчин натрію хлориду без консервантів. Для приготування розчину препарату у флакон повільно вводять необхідну кількість 0.9% розчину хлориду натрію для ін'єкцій (не менше кількості, зазначеної в таблиці нижче) і акуратно струшують флакон до повного розчинення вмісту. Дозування препарату у флаконі Необхідний об'єм 0.9% розчину хлориду натрію для ін'єкцій Об'єм відновленого розчину Концентрація гемцитабіну в розчині 200 мг 5 мл 5.26 мл 38 мг/мл 1000 мг 25 мл 26.3 мл 38 мг/мл 1500 мг 37.5 мл 39.5 мл 38 мг/мл Отриманий розчин має бути прозорим. Максимальна концентрація відновленого розчину гемцитабіну не повинна перевищувати 38 мг/мл, оскільки при більш високих концентраціях можливе неповне розчинення препарату. Приготовлений розчин гемцитабіну, що містить потрібну дозу препарату, перед введенням розбавляють 0.9% розчином натрію хлориду для ін'єкцій у кількості, достатньому для 30-хвилинної внутрішньовенної інфузії. Перед парентеральним введенням розчину препарату слід переконатися у відсутності в ньому нерозчинених частинок та зміни кольору розчину Приготовлений розчин препарату призначений лише для одноразового застосування. Весь невикористаний препарат має бути утилізовано.ПередозуванняСимптоми: мієлодепресія, парестезія, виражена шкірна висипка. При введенні гемцитабіну в дозах до 5700 мг/м2 внутрішньовенно краплинно за 30 хвилин кожні 2 тижні ознак передозування не спостерігалося. Антидот для гемцитабіну невідомий. При підозрі на передозування гемцитабіну слід контролювати рівень цитопенії та при необхідності призначити симптоматичну терапію.Запобіжні заходи та особливі вказівкиЛікування гемцитабіном можна проводити лише під наглядом лікаря, який має досвід застосування протипухлинної хіміотерапії. Перед кожним введенням гемцитабіну необхідно контролювати кількість тромбоцитів, лейкоцитів та гранулоцитів у крові. При ознаках пригнічення функції кісткового мозку, спричиненого препаратом, необхідно припинити лікування або скоригувати дозу. Зазвичай пригнічення функції кісткового мозку має короткостроковий характер, не вимагає зниження дози і рідко призводить до необхідності переривання лікування. Показники периферичної крові можуть погіршуватися після переривання терапії гемцитабіном. При застосуванні гемцитабіну у комбінації з іншими протипухлинними хіміопрепаратами необхідно враховувати ризик кумулятивного пригнічення функції кісткового мозку. Необхідно проводити регулярне обстеження хворого та оцінку функції нирок та печінки. Введення гемцитабіну при метастазах у печінці, при гепатиті та алкоголізмі в анамнезі, а також при цирозі печінки збільшує ризик розвитку печінкової недостатності. При появі ознак розвитку небажаних явищ з боку дихальної системи (наприклад, набряк легенів, інтерстиціальний пневмоніт або респіраторний дистрес-синдром у дорослих) на тлі лікування гемцитабіном лікування слід припинити та призначити відповідну терапію. При появі перших ознак мікроангіопатичної гемолітичної анемії, таких як швидке зниження гемоглобіну з супутньою тромбоцитопенією, підвищення сироваткової концентрації білірубіну, креатиніну, азоту сечовини або підвищення активності лактатдегідрогенази, гемцитабін повинен бути скасований. Збільшення тривалості інфузії та частоти введень призводить до зростання токсичності. Ризик шкірних реакцій зростає за наявності променевої терапії в анамнезі. Залежно від ступеня токсичності дозу можна знижувати протягом кожного циклу або з початком нового циклу ступінчасто. Під час лікування та протягом 6 місяців після закінчення терапії гемцитабіном слід використовувати надійні методи контрацепції. Чоловікам, які отримують гемцитабін, рекомендується вдатися до кріоконсервації сперми до початку лікування через ризик безпліддя, зумовлений застосуванням даного препарату. При лікуванні пацієнтів, які перебувають на контрольованій натрієвій дієті, слід враховувати вміст у препараті натрію в наступних кількостях: флакон 200 мг Гемцитабіну медак містить 3.5 мг ( флакон 1000 мг Гемцитабіну медак містить 17.5 мг ( флакон 1500 мг Гемцитабіну медак містить 26.3 мг ( Вплив на здатність керувати транспортним засобом та працювати з механізмами. Дані про вплив терапії гемцитабіном на здатність керувати транспортним засобом та працювати з механізмами відсутні, однак деякі побічні дії препарату, такі як підвищена сонливість, можуть негативно впливати на здатність виконувати такі дії. У період лікування гемцитабіном необхідно дотримуватися обережності при керуванні транспортними засобами та зайнятті потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови відпустки з аптекЗа рецептомВідео на цю тему
2 297,00 грн
2 257,00 грн
Склад, форма випуску та упаковкаЛіофілізат - 1 фл. активна речовина: гемцитабіну гідрохлорид 1140 мг, еквівалентний 1 г гемцитабіну основи; допоміжні речовини: манітол 1000 мг, ацетат натрію 62,5 мг. Поміщають у флакони зі скла типу I. По одному флаконі з інструкцією по застосуванню поміщають у картонну пачку. На пачці допускається наявність стікера "Зразок. Не для продажу." у разі безоплатного розповсюдження зразка препарату медичним установам.Опис лікарської формиЛіофілізат від білого до майже білого кольору.Фармакотерапевтична групаПротипухлинний засіб, антиметаболіт.ФармакокінетикаГемцитабін швидко виводиться з організму нирками переважно у вигляді неактивного метаболіту 2'-дезокси-2',2'-дифторуридину. Менше 10% введеної внутрішньовенної дози виявляється у сечі у формі незміненого препарату. Зв'язування гемцитабіну з білками плазми незначне. Фармакокінетичний аналіз досліджень з одноразовим та багаторазовим введенням доз показує, що обсяг розподілу значною мірою залежить від статі. Системний кліренс, який коливається приблизно від 30 л/год/м2 до 90 л/год/м2, залежить від віку та статі. Період напіввиведення коливається від 32 до 94 хвилин.ФармакодинамікаГемцитабін є антиметаболітом групи аналогів піримідину. Препарат виявляє циклоспецифічність, діючи на клітини у фазах S (фаза реплікації) та Gi/S (проміжок між фазою початкового росту та фазою реплікації). Гемцитабін метаболізується всередині клітини під дією нуклеозидкіназ з утворенням активних дифосфатних та трифосфатних нуклеозидів. Дифосфатні нуклеозиди інгібують рибонуклеотидредуктазу, яка діє як єдиний каталізатор реакцій, що призводять до утворення дезоксинуклеозидтрифосфатів, необхідних для синтезу дезоксирибонуклеїнової кислоти (ДНК). Трифосфатні нуклеозиди активно конкурують з дезоксицитидинтрифосфатом за вбудовування в молекули ДНК та рибонуклеїнової кислоти-(РНК). Після вбудовування внутрішньоклітинних метаболітів гемцитабіну в ланцюг ДНК, до ниток, що її ростуть, додається ще один додатковий нуклеотид, що призводить до повного інгібування подальшого синтезу ДНК і запрограмованої загибелі клітини, відомої як апоптоз.Показання до застосуванняМісцевий або метастатичний недрібноклітинний рак легені як терапія першої лінії в комбінації сцисплатином або карбоплатином, а також у монотерапії у літніх пацієнтів з функціональним статусом, рівним 2. Нерезектабельний, місцеворецидивний або метастатичний рак молочної залози у складі комбінованої терапії з паклітакселом після проведення неоад'ювантної та/або ад'ювантної терапії з включенням антрациклінів за відсутності протипоказань до їх призначення. Місцевий або метастатичний уротеліальний рак (рак сечового міхура, ниркової балії, сечоводів, уретри). Місцево поширений або метастатичний епітеліальний рак яєчників як монотерапія або у поєднанні з карбоплатином у пацієнтів з прогресуванням захворювання після проведення першої лінії терапії на основі платинових препаратів. Місцевий або метастатичний рак підшлункової залози. Місцевий або метастатичний рак шийки матки. Рак жовчовивідних шляхів. Показана ефективність гемцитабіну при поширеному дрібноклітинному раку легені та поширеному рефрактерному раку яєчка.Протипоказання до застосуванняПідвищена чутливість до гемцитабіну або до інших компонентів препарату. Вагітність та період годування груддю. Вік до 18 років. З обережністю: при порушенні функції печінки та/або нирок, пригніченні кістковомозкового кровотворення (у тому числі на фоні супутньої променевої або хіміотерапії), гострих інфекційних захворюваннях вірусної, грибкової або бактеріальної природи, у пацієнтів з серцево-судинними захворюваннями (в тому числіПобічна діяПобічні реакції, що зустрічалися частіше, ніж у поодиноких випадках, перераховані відповідно до наступної градації: дуже часто (≥10%); часто (≥1%, Порушення з боку системи крові та лімфатичної системи: дуже часто – анемія, лейкопенія та тромбоцитопенія; часто – фебрильна нейтропенія; дуже рідко – тромбоцитоз. Порушення з боку імунної системи: дуже рідко – анафілактична реакція. Порушення з боку обміну речовин та харчування: часто – анорексія. Порушення з боку нервової системи: часто – головний біль, безсоння, сонливість; нечасто – порушення мозкового кровообігу; дуже рідко – синдром оборотної задньої енцефалопатії. Порушення з боку серця: нечасто – серцева недостатність; аритмія, переважно суправентрикулярна; рідко – інфаркт міокарда. Порушення з боку судин: дуже часто – набряки, периферичні набряки; рідко – зниження артеріального тиску, васкуліт периферичних судин, гангрена; дуже рідко – синдром підвищеної проникності капілярів. Порушення з боку дихальної системи: дуже часто – задишка; часто – кашель, риніт; нечасто – бронхоспазм, інтерстиціальний пневмоніт; рідко – набряк легень, респіраторний дистрес-синдром дорослих. Порушення з боку системи шлунково-кишкового тракту: дуже часто - нудота, блювання, підвищення активності "печінкових" ферментів аспартатамінотрансферази (ACT), аланінамінотрансферази (АЛТ) та лужної фосфатази; часто – діарея, стоматит, виразкове ураження слизової оболонки порожнини рота, запор, підвищення концентрації білірубіну; нечасто -гепатотоксичність важкого ступеня, включаючи печінкову недостатність, у деяких випадках із летальним кінцем; рідко – підвищення концентрації гаммаглутамілтрансферази (ГГТ); дуже рідко – ішемічний коліт. Порушення з боку шкіри та підшкірних тканин: дуже часто – алергічні шкірні висипання легкого ступеня, що супроводжуються свербінням; алопеція (зазвичай мінімальна втрата волосся); часто-свербіж, пітливість; рідко - виразки, утворення везикул, лущення, шкірні реакції тяжкого ступеня, включаючи десквамацію та бульозне ураження шкіри; дуже рідко – токсичний епідермальний некроліз, синдром Стівенса-Джонсона. Порушення з боку нирок та сечовивідних шляхів: дуже часто – протеїнурія легкого ступеня та гематурія; нечасто – ниркова недостатність; рідко – підвищення концентрації креатиніну, сечовини та лактатдегідрогенази (ЛДГ) при гемолітико-уремічному синдромі. Порушення з боку скелетно-м'язової та сполучної тканини: часто – біль у спині, міалгія. Інші: дуже часто – грипоподібний синдром. Також були зареєстровані випадки нездужання, пітливість; часто-підвищення температури тіла, астенія, озноб; рідко – реакції у місці ін'єкції переважно легкого ступеня. Гіперчутливість: анафілактоїдні реакції реєструвалися дуже рідко. Променева токсичність реєструвалася рідко (див. Взаємодія з іншими видами терапії). Застосування гемцитабіну в комбінації з паклітакселом при раку молочної залози Небажані явища ІІІ ступеня тяжкості Гематологічна токсичність: анемія – 5,7%, тромбоцитопенія – 5,3%, нейтропенія – 31,3%. Негематологічна токсичність: фебрильна нейтропенія – 4,6%, підвищена стомлюваність – 5,7%, діарея – 3,1%, моторна нейропатія – 2,3%, сенсорна нейропатія – 5,3%. Небажані явища IV ступеня тяжкості Гематологічна токсичність: анемія – 1,1%, тромбоцитопенія – 0,4%, нейтропенія – 17,2% (нейтропенія IV ступеня тривалістю понад 7 днів була зареєстрована у 12,6% пацієнтів). Негематологічна токсичність: фебрильна нейтропенія – 0,4%, підвищена стомлюваність – 0,8%, моторна нейропатія – 0,4%, сенсорна нейропатія –0,4%. Застосування гемцитабіну в комбінації з цисплатином при раку сечового міхура Небажані явища ІІІ ступеня тяжкості Гематологічна токсичність: анемія – 24%, тромбоцитопенія – 29%. Негематологічна токсичність: нудота та блювання – 22%, діарея – 3%, інфекція – 2%, стоматит – 1%. Небажані явища IV ступеня тяжкості Гематологічна токсичність: анемія – 4%, тромбоцитопенія – 29%. Негематологічна токсичність: інфекція – 1%. Застосування гемцитабіну в комбінації з карбоплатином при раку яєчників Небажані явища ІІІ ступеня тяжкості Гематологічна токсичність: анемія – 22,3%, нейтропенія – 41,7%, тромбоцитопенія – 30,3%, лейкопенія –48,0%. Негематологічна токсичність: кровотеча – 1,8%, фебрильна нейтропенія – 1,1%. Небажані явища IV ступеня тяжкості Гематологічна токсичність: анемія –5,1%, нейтропенія –28,6%, тромбоцитопенія – 4,6%, лейкопенія – 5,1%. Негематологічна токсичність: інфекція без нейтропенії – 0,6%.Взаємодія з лікарськими засобамиВзаємодія з іншими видами терапії Променева терапія Одночасне застосування (спільне або з інтервалом менше 7 днів): токсичність, пов'язана з таким мультимодальним лікуванням, залежить від багатьох різних факторів: дози гемцитабіну, частоти введення гемцитабіну, дози променевої терапії, техніки планування променевої терапії, типу та обсягу опромінюваної тканини. Доклінічні та клінічні дослідження показали, що гемцитабін має радіосенсибілізуючу дію. У єдиному дослідженні, в якому гемцитабін вводився в дозі 1000 мг/м2 протягом 6 тижнів одночасно з терапевтичним опроміненням грудної клітини у пацієнтів з недрібноклітинним раком легені, була зафіксована значна токсичність у вигляді важкого та потенційно небезпечного для життя запалення слизових оболонок, ; а також пневмоніту,особливо у пацієнтів із великим обсягом опромінення тканин (медіана обсягу опромінення 4795 см3). Дослідження (дослідження II фази при недрібноклітинному раку легені), що проводилися пізніше, свідчать про доцільність введення гемцитабіну в нижчих дозах з супутньою променевою терапією з прогнозованою токсичністю. Променева терапія на ділянку грудної клітки (СОД 66 Гр) проводилася одночасно з хіміотерапією гемцитабіном у дозі 600 мг/м2 (4 введення) та цисплатином у дозі 80 мг/м2 (2 введення) протягом 6 тижнів. Декілька досліджень I та II фази показали, що при недрібноклітинному раку легені та раку підшлункової залози доцільніше проводити монотерапію гемцитабіном (у дозі до 300 мг/м2/тиждень) паралельно з променевою терапією.Оптимальний режим безпечного введення гемцитабіну з терапевтичними дозами променевої терапії ще встановлено для всіх типів новоутворень. Послідовне застосування (інтервал більше 7 днів): крім променевої реакції при введенні гемцитабіну більш ніж за 7 днів до або після променевої терапії збільшення токсичності не зареєстровано. Ці дані дозволяють припустити, що гемцитабін можна вводити через тиждень після променевої терапії або після того, як будуть дозволені гострі наслідки променевої терапії.що гемцитабін можна вводити через один тиждень після променевої терапії або після того, як буде дозволено гострі наслідки променевої терапії.що гемцитабін можна вводити через один тиждень після променевої терапії або після того, як буде дозволено гострі наслідки променевої терапії. І при одночасному, і при послідовному застосуванні гемцитабіну з променевою терапією були зареєстровані променеві пошкодження тканин, що опромінюються (наприклад, езофагіт, коліт і пневмоніт). Інші Не рекомендується спільне застосування з живими вакцинами жовтої лихоманки та іншими живими вакцинами внаслідок ризику системного захворювання з можливим летальним результатом, особливо у пацієнтів з імуносупресією.Спосіб застосування та дозиГемцитабін вводиться внутрішньовенно краплинно протягом 30 хвилин. Перед кожним введенням гемцитабіну необхідно контролювати кількість тромбоцитів, лейкоцитів та гранулоцитів у крові. При ознаках пригнічення функції кісткового мозку, спричиненого препаратом, необхідно припинити лікування або скоригувати дозу. Недрібноклітинний рак легені (місцерозповсюджений або метастатичний), перша лінія терапії. Монотерапія: Рекомендована доза препарату – 1000 мг/м2 в 1, 8 та 15 дні кожного 28-денного циклу. Комбінована терапія з цисплатином: Рекомендована доза препарату – 1250 мг/м2 на 1 та 8 день кожного 21-денного циклу або 1000 мг/м2 у 1, 8 та 15 дні кожного 28-денного циклу. Цисплатин вводиться у дозі 70 мг/м2 на 1 день циклу після інфузії гемцитабіну на фоні гіпергідратації. Комбінована терапія з карбоплатином: Рекомендована доза препарату – 1000 мг/м2 або 1200 мг/м2 на 1 та 8 день кожного 21-денного циклу. Карбоплатин вводиться з розрахунку AUC (площа під кривою «концентрація-час») 5,0 мг/мл/хв за 1 день циклу після інфузії гемцитабіну. Рак молочної залози (нерезектабельний, місцеворецидивний або метастатичний). Комбінована терапія з паклітакселом: Як терапія першої лінії при прогресуванні захворювання після неоад'ювантної та/або ад'ювантної терапії, що включає антрацикліни, за відсутності протипоказань до них. Паклітаксел вводиться в дозі 175 мг/м2 внутрішньовенно крапельно протягом 3 годин на день 21-денного циклу з подальшим введенням гемцитабіну. Рекомендована доза препарату – 1250 мг/м2 на 1 та 8 день кожного 21-денного циклу. Перед початком комбінованої терапії (гемцитабін + паклітаксел) абсолютна кількість гранулоцитів у крові у пацієнтів має бути не менше ніж 1500/мкл. Уротеліальний рак (рак сечового міхура (місцерозповсюджений, метастатичний та поверхневий), ниркової балії, сечоводу, сечовипускального каналу). Монотерапія: Рекомендована доза препарату – 1250 мг/м2 у 1, 8 та 15 дні кожного 28-денного циклу. Комбінована терапія з цисплатином: Рекомендована доза препарату — 1000 мг/м2 в 1, 8 і 15 днів у поєднанні з цисплатином, який вводиться в дозі 70 мг/м2 відразу після інфузії гемцитабіну в 1 або 2 день кожного 28-денного циклу. Клінічні дослідження показали, що за дози цисплатину 100 мг/м2 спостерігається більш виражена мієлосупресія. Епітеліальний рак яєчників (місцерозповсюджений або метастатичний, резистентний до похідних платини). Монотерапія: Рекомендована доза препарату – 800-1250 мг/м2 у 1, 8 та 15 дні кожного 28-денного циклу. Комбінована терапія з карбоплатином: Рекомендована доза препарату – 1000 мг/м2, на 1 та 8 день у поєднанні з карбоплатином з розрахунку AUC 4,0 мг/мл/хв, який вводиться відразу після інфузії гемцитабіну на 1 день кожного 21-денного циклу. Рак підшлункової залози (місцерозповсюджений або метастатичний, у т.ч. резистентний до терапії фторурацилом). Монотерапія: Рекомендована доза препарату – 1000 мг/м2 один раз на тиждень протягом 7 тижнів з наступною тижневою перервою. Потім препарат вводиться в 1, 8 та 15 дні кожного 28-денного циклу. Рак шийки матки (місцерозповсюджений або метастатичний). Комбінована терапія з цисплатином: При місцеворозповсюдженому раку при послідовній хіміопроменевій терапії (неоад'ювантно) та при метастатичному раку цисплатин вводиться в дозі 70 мг/м2 на 1 день циклу на тлі гіпергідратації з подальшим введенням гемцитабіну. Гемцитабін вводиться в дозі 1250 мг/м2 на 1 та 8 день кожного 21-денного циклу. При місцевопоширеному раку при одночасної хіміопроменевої терапії цисплатин вводиться в дозі 40 мг/м2 з наступним (безпосередньо після введення цисплатину) введенням гемцитабіну. Гемцитабін вводиться 1 раз на тиждень за 1-2 години до початку променевої терапії у дозі 125 мг/м2. Рак жовчовивідних шляхів Комбінована терапія з цисплатином: Цисплатин вводиться в дозі 70 мг/м2 на 1 день циклу на тлі гіпергідратації з подальшим введенням гемцитабіну. Гемцитабін вводиться у дозі 1250 мг/м2 на 1 та 8 день кожного 21-денного циклу. Корекція дози У разі розвитку гематологічної токсичності доза гемцитабіну може бути зменшена або його введення відкладено відповідно до наступних схем: А. Корекція дози гемцитабіну в рамках циклу при уротеліальному раку, недрібноклітинному раку легені, раку підшлункової залози як монотерапія або в комбінації з цисплатином. Корекція дози гемцитабіну в рамках циклу при уротеліальному раку, недрібноклітинному раку легені, раку підшлункової залози як монотерапія або в комбінації з цисплатином. Корекція дози гемцитабіну в рамках циклу при уротеліальному раку, недрібноклітинному раку легені, раку підшлункової залози як монотерапія або в комбінації з цисплатином. Абсолютна кількість гранулоцитів (× 109 /л) Кількість тромбоцитів (×10 9 /л) % від попередньої дози >1 і >100 100 0,5-1 або 50–100 75 <0,5 або <50 Відкласти введення Б. Корекція дози гемцитабіну в рамках циклу при раку молочної залози у комбінації з паклітакселом. Корекція дози гемцитабіну в рамках циклу при раку молочної залози у комбінації з паклітакселом Корекція дози гемцитабіну в рамках циклу при раку молочної залози у комбінації з паклітакселом Абсолютна кількість гранулоцитів (×10 9 /л) Кількість тромбоцитів (× 109 /л) % від попередньої дози ≥1,2 і >75 100 1-<1,2 або 50–75 75 0,7-<1 і ≥50 50 <0,7 або <50 Відкласти введення В. Корекція дози гемцитабіну в рамках циклу при раку яєчників у комбінації з карбоплатином. Корекція дози гемцитабіну в рамках циклу при раку яєчників у комбінації з карбоплатином Корекція дози гемцитабіну в рамках циклу при раку яєчників у комбінації з карбоплатином Абсолютна кількість гранулоцитів (×10 9 /л) Кількість тромбоцитів (×10 9 /л) % від попередньої дози >1,5 і ≥100 100 1-1,5 або 75–100 50 <1 або <75 Відкласти введення Для виявлення негематологічної токсичності необхідно проводити регулярне обстеження пацієнта та контролювати функцію печінки та нирок. Залежно від ступеня токсичності дозу можна знижувати протягом кожного циклу або з початком нового циклу ступінчасто. Введення препарату має бути відкладено доти, доки, на думку лікаря, токсичність не вирішиться. Особливі групи пацієнтів Літні пацієнти: Немає даних, що дозволяють припустити, що у пацієнтів похилого віку необхідно коригувати дозу. Пацієнти з порушенням функції печінки та нирок: Застосовувати гемцитабін у пацієнтів із печінковою недостатністю або з порушеною функцією нирок слід з обережністю, оскільки достатніх даних щодо застосування препарату у цієї категорії пацієнтів немає. Ниркова недостатність легкого або середнього ступеня тяжкості (швидкість клубочкової фільтрації від 30 мл/хв до 80 мл/хв) не має помітного впливу на фармакокінетику гемцитабіну. Діти: Гемцитабін вивчався в обмежених дослідженнях І та ІІ фази у дітей з різними типами новоутворень. Даних цих досліджень недостатньо для доказу ефективності та безпеки застосування гемцитабіну у дітей. Рекомендації щодо приготування розчину для інфузій Як розчинник використовується лише 0,9% розчин натрію хлориду без консервантів. Для приготування концентрату вміст флакону 200 мг розчиняють не менше, ніж 5 мл, і 1 г - не менше, ніж 25 мл 0,9% розчину натрію хлориду для ін'єкцій. Кожен флакон акуратно збовтують до повного розчинення ліофілізату. Отриманий розчин має бути прозорим. Максимальна концентрація гемцитабіну не повинна перевищувати 40 мг/мл. Розчини, приготовані з концентрацією вище 40 мг/мл, можуть супроводжуватися неповним розчиненням. Приготовлений концентрат гемцитабіну, що містить потрібну дозу препарату, перед введенням розбавляють 0,9% розчином хлориду натрію для ін'єкцій у кількості, достатньому для 30-хвилинної внутрішньовенної інфузії. Перед парентеральним введенням необхідно візуально контролювати приготовлений розчин на наявність механічних домішок та зміну кольору.ПередозуванняАнтидот для гемцитабіну невідомий. Клінічно допустима токсичність спостерігалася при введенні одноразових доз до 5,7 г/м2 внутрішньовенно протягом 30 хвилин кожні два тижні. У разі підозри на передозування пацієнт повинен перебувати під постійним лікарським контролем, включаючи підрахунок формули крові. За потреби пацієнту проводять симптоматичне лікування.Запобіжні заходи та особливі вказівкиЛікування гемцитабіном можна проводити лише під наглядом лікаря, який має досвід застосування протипухлинної хіміотерапії. Гематологічна токсичність Гемцитабін може пригнічувати функцію кісткового мозку, що проявляється лейкопенією, тромбоцитопенією або анемією. Перед кожним введенням гемцитабіну необхідно контролювати кількість тромбоцитів, лейкоцитів та гранулоцитів у крові. При ознаках пригнічення функції кісткового мозку, спричиненого препаратом, необхідно припинити лікування або скоригувати дозу. Функція нирок та печінки Необхідно проводити регулярне обстеження пацієнта та оцінку функції нирок та печінки. Введення гемцитабіну при метастазах у печінці, при гепатиті та алкоголізмі в анамнезі, а також при цирозі печінки збільшує ризик розвитку печінкової недостатності. У пацієнтів, які отримували гемцитабін, гемолітико-уремічний синдром реєструвався у поодиноких випадках. Терапія гемцитабіном повинна бути припинена з появою перших ознак мікроангіопатичної гемолітичної анемії, таких як швидке зниження гемоглобіну, тромбоцитопенія, підвищення концентрації сироваткового білірубіну. Ниркова недостатність може бути незворотною після припинення терапії гемцитабіном, у зв'язку з чим може знадобитися гемодіаліз. Судинні порушення Синдром підвищеної проникності капілярів, респіраторний дистрес-синдром дорослих, синдром оборотної задньої енцефалопатії з потенційно серйозними наслідками спостерігалися у пацієнтів,отримували гемцитабін у монотерапії або у комбінації з іншими хіміотерапевтичними препаратами. Ці синдроми можуть бути пов'язані з пошкодженням ендотелію судин, можливо індукованим гемцитабіном. У разі їх розвитку під час терапії слід припинити лікування гемцитабіном та вжити необхідних заходів. Функція легенів Крім респіраторного дистрес-синдрому дорослих, інші порушення функції легень, іноді тяжкого ступеня (наприклад, набряк легень, інтерстиціальний пневмоніт), були зареєстровані у пацієнтів, які отримували гемцитабін у монотерапії або у комбінації з іншими цитостатиками. Етіологія цих порушень невідома. При розвитку таких побічних ефектів необхідно припинити терапію гемцитабіном та вжити необхідних заходів. Раннє використання симптоматичної терапії може покращити ситуацію. Фертильність У дослідженнях фертильності гемцитабін викликав гіпосперматогенез у самців мишей. Тому чоловікам, які отримують терапію гемцитабіном, не рекомендується батьківство під час лікування та протягом 6 місяців після його закінчення. До початку лікування слід звернутися за додатковою консультацією щодо кріоконсервації сперми через можливу безплідність внаслідок терапії гемцитабіном. Збільшення тривалості інфузії та частоти введень призводить до зростання токсичності. Залежно від ступеня токсичності дозу можна знижувати протягом кожного циклу або з початком нового циклу ступінчасто. Вплив на здатність до керування автотранспортом та управління механізмами Досліджень впливу гемцитабіну на здатність керувати автотранспортними засобами та іншими механізмами не проводилося. Проте відомо, що гемцитабін може викликати сонливість від слабкого до помірного ступеня, особливо спільно з вживанням алкоголю. Пацієнтів слід застерігати від управління механізмами у випадках, коли вони відчувають сонливість.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
674,00 грн
629,00 грн
Склад, форма випуску та упаковкаЛіофілізат - 1 фл. активна речовина: гемцитабіну гідрохлорид 228 мг, еквівалентний 200 мг гемцитабіну основи; допоміжні речовини: манітол 200 мг, ацетат натрію 12,5 мг. Поміщають у флакони зі скла типу I. По одному флаконі з інструкцією по застосуванню поміщають у картонну пачку. На пачці допускається наявність стікера "Зразок. Не для продажу." у разі безоплатного розповсюдження зразка препарату медичним установам.Опис лікарської формиЛіофілізат від білого до майже білого кольору.Фармакотерапевтична групаПротипухлинний засіб, антиметаболіт.ФармакокінетикаГемцитабін швидко виводиться з організму нирками переважно у вигляді неактивного метаболіту 2'-дезокси-2',2'-дифторуридину. Менше 10% введеної внутрішньовенної дози виявляється у сечі у формі незміненого препарату. Зв'язування гемцитабіну з білками плазми незначне. Фармакокінетичний аналіз досліджень з одноразовим та багаторазовим введенням доз показує, що обсяг розподілу значною мірою залежить від статі. Системний кліренс, який коливається приблизно від 30 л/год/м2 до 90 л/год/м2, залежить від віку та статі. Період напіввиведення коливається від 32 до 94 хвилин.ФармакодинамікаГемцитабін є антиметаболітом групи аналогів піримідину. Препарат виявляє циклоспецифічність, діючи на клітини у фазах S (фаза реплікації) та Gi/S (проміжок між фазою початкового росту та фазою реплікації). Гемцитабін метаболізується всередині клітини під дією нуклеозидкіназ з утворенням активних дифосфатних та трифосфатних нуклеозидів. Дифосфатні нуклеозиди інгібують рибонуклеотидредуктазу, яка діє як єдиний каталізатор реакцій, що призводять до утворення дезоксинуклеозидтрифосфатів, необхідних для синтезу дезоксирибонуклеїнової кислоти (ДНК). Трифосфатні нуклеозиди активно конкурують з дезоксицитидинтрифосфатом за вбудовування в молекули ДНК та рибонуклеїнової кислоти-(РНК). Після вбудовування внутрішньоклітинних метаболітів гемцитабіну в ланцюг ДНК, до ниток, що її ростуть, додається ще один додатковий нуклеотид, що призводить до повного інгібування подальшого синтезу ДНК і запрограмованої загибелі клітини, відомої як апоптоз.Показання до застосуванняМісцевий або метастатичний недрібноклітинний рак легені як терапія першої лінії в комбінації сцисплатином або карбоплатином, а також у монотерапії у літніх пацієнтів з функціональним статусом, рівним 2. Нерезектабельний, місцеворецидивний або метастатичний рак молочної залози у складі комбінованої терапії з паклітакселом після проведення неоад'ювантної та/або ад'ювантної терапії з включенням антрациклінів за відсутності протипоказань до їх призначення. Місцевий або метастатичний уротеліальний рак (рак сечового міхура, ниркової балії, сечоводів, уретри). Місцево поширений або метастатичний епітеліальний рак яєчників як монотерапія або у поєднанні з карбоплатином у пацієнтів з прогресуванням захворювання після проведення першої лінії терапії на основі платинових препаратів. Місцевий або метастатичний рак підшлункової залози. Місцевий або метастатичний рак шийки матки. Рак жовчовивідних шляхів. Показана ефективність гемцитабіну при поширеному дрібноклітинному раку легені та поширеному рефрактерному раку яєчка.Протипоказання до застосуванняПідвищена чутливість до гемцитабіну або до інших компонентів препарату. Вагітність та період годування груддю. Вік до 18 років. З обережністю: при порушенні функції печінки та/або нирок, пригніченні кістковомозкового кровотворення (у тому числі на фоні супутньої променевої або хіміотерапії), гострих інфекційних захворюваннях вірусної, грибкової або бактеріальної природи, у пацієнтів з серцево-судинними захворюваннями (в тому числіПобічна діяПобічні реакції, що зустрічалися частіше, ніж у поодиноких випадках, перераховані відповідно до наступної градації: дуже часто (≥10%); часто (≥1%, Порушення з боку системи крові та лімфатичної системи: дуже часто – анемія, лейкопенія та тромбоцитопенія; часто – фебрильна нейтропенія; дуже рідко – тромбоцитоз. Порушення з боку імунної системи: дуже рідко – анафілактична реакція. Порушення з боку обміну речовин та харчування: часто – анорексія. Порушення з боку нервової системи: часто – головний біль, безсоння, сонливість; нечасто – порушення мозкового кровообігу; дуже рідко – синдром оборотної задньої енцефалопатії. Порушення з боку серця: нечасто – серцева недостатність; аритмія, переважно суправентрикулярна; рідко – інфаркт міокарда. Порушення з боку судин: дуже часто – набряки, периферичні набряки; рідко – зниження артеріального тиску, васкуліт периферичних судин, гангрена; дуже рідко – синдром підвищеної проникності капілярів. Порушення з боку дихальної системи: дуже часто – задишка; часто – кашель, риніт; нечасто – бронхоспазм, інтерстиціальний пневмоніт; рідко – набряк легень, респіраторний дистрес-синдром дорослих. Порушення з боку системи шлунково-кишкового тракту: дуже часто - нудота, блювання, підвищення активності "печінкових" ферментів аспартатамінотрансферази (ACT), аланінамінотрансферази (АЛТ) та лужної фосфатази; часто – діарея, стоматит, виразкове ураження слизової оболонки порожнини рота, запор, підвищення концентрації білірубіну; нечасто -гепатотоксичність важкого ступеня, включаючи печінкову недостатність, у деяких випадках із летальним кінцем; рідко – підвищення концентрації гаммаглутамілтрансферази (ГГТ); дуже рідко – ішемічний коліт. Порушення з боку шкіри та підшкірних тканин: дуже часто – алергічні шкірні висипання легкого ступеня, що супроводжуються свербінням; алопеція (зазвичай мінімальна втрата волосся); часто-свербіж, пітливість; рідко - виразки, утворення везикул, лущення, шкірні реакції тяжкого ступеня, включаючи десквамацію та бульозне ураження шкіри; дуже рідко – токсичний епідермальний некроліз, синдром Стівенса-Джонсона. Порушення з боку нирок та сечовивідних шляхів: дуже часто – протеїнурія легкого ступеня та гематурія; нечасто – ниркова недостатність; рідко – підвищення концентрації креатиніну, сечовини та лактатдегідрогенази (ЛДГ) при гемолітико-уремічному синдромі. Порушення з боку скелетно-м'язової та сполучної тканини: часто – біль у спині, міалгія. Інші: дуже часто – грипоподібний синдром. Також були зареєстровані випадки нездужання, пітливість; часто-підвищення температури тіла, астенія, озноб; рідко – реакції у місці ін'єкції переважно легкого ступеня. Гіперчутливість: анафілактоїдні реакції реєструвалися дуже рідко. Променева токсичність реєструвалася рідко (див. Взаємодія з іншими видами терапії). Застосування гемцитабіну в комбінації з паклітакселом при раку молочної залози Небажані явища ІІІ ступеня тяжкості Гематологічна токсичність: анемія – 5,7%, тромбоцитопенія – 5,3%, нейтропенія – 31,3%. Негематологічна токсичність: фебрильна нейтропенія – 4,6%, підвищена стомлюваність – 5,7%, діарея – 3,1%, моторна нейропатія – 2,3%, сенсорна нейропатія – 5,3%. Небажані явища IV ступеня тяжкості Гематологічна токсичність: анемія – 1,1%, тромбоцитопенія – 0,4%, нейтропенія – 17,2% (нейтропенія IV ступеня тривалістю понад 7 днів була зареєстрована у 12,6% пацієнтів). Негематологічна токсичність: фебрильна нейтропенія – 0,4%, підвищена стомлюваність – 0,8%, моторна нейропатія – 0,4%, сенсорна нейропатія –0,4%. Застосування гемцитабіну в комбінації з цисплатином при раку сечового міхура Небажані явища ІІІ ступеня тяжкості Гематологічна токсичність: анемія – 24%, тромбоцитопенія – 29%. Негематологічна токсичність: нудота та блювання – 22%, діарея – 3%, інфекція – 2%, стоматит – 1%. Небажані явища IV ступеня тяжкості Гематологічна токсичність: анемія – 4%, тромбоцитопенія – 29%. Негематологічна токсичність: інфекція – 1%. Застосування гемцитабіну в комбінації з карбоплатином при раку яєчників Небажані явища ІІІ ступеня тяжкості Гематологічна токсичність: анемія – 22,3%, нейтропенія – 41,7%, тромбоцитопенія – 30,3%, лейкопенія –48,0%. Негематологічна токсичність: кровотеча – 1,8%, фебрильна нейтропенія – 1,1%. Небажані явища IV ступеня тяжкості Гематологічна токсичність: анемія –5,1%, нейтропенія –28,6%, тромбоцитопенія – 4,6%, лейкопенія – 5,1%. Негематологічна токсичність: інфекція без нейтропенії – 0,6%.Взаємодія з лікарськими засобамиВзаємодія з іншими видами терапії Променева терапія Одночасне застосування (спільне або з інтервалом менше 7 днів): токсичність, пов'язана з таким мультимодальним лікуванням, залежить від багатьох різних факторів: дози гемцитабіну, частоти введення гемцитабіну, дози променевої терапії, техніки планування променевої терапії, типу та обсягу опромінюваної тканини. Доклінічні та клінічні дослідження показали, що гемцитабін має радіосенсибілізуючу дію. У єдиному дослідженні, в якому гемцитабін вводився в дозі 1000 мг/м2 протягом 6 тижнів одночасно з терапевтичним опроміненням грудної клітини у пацієнтів з недрібноклітинним раком легені, була зафіксована значна токсичність у вигляді важкого та потенційно небезпечного для життя запалення слизових оболонок, ; а також пневмоніту,особливо у пацієнтів із великим обсягом опромінення тканин (медіана обсягу опромінення 4795 см3). Дослідження (дослідження II фази при недрібноклітинному раку легені), що проводилися пізніше, свідчать про доцільність введення гемцитабіну в нижчих дозах з супутньою променевою терапією з прогнозованою токсичністю. Променева терапія на ділянку грудної клітки (СОД 66 Гр) проводилася одночасно з хіміотерапією гемцитабіном у дозі 600 мг/м2 (4 введення) та цисплатином у дозі 80 мг/м2 (2 введення) протягом 6 тижнів. Декілька досліджень I та II фази показали, що при недрібноклітинному раку легені та раку підшлункової залози доцільніше проводити монотерапію гемцитабіном (у дозі до 300 мг/м2/тиждень) паралельно з променевою терапією.Оптимальний режим безпечного введення гемцитабіну з терапевтичними дозами променевої терапії ще встановлено для всіх типів новоутворень. Послідовне застосування (інтервал більше 7 днів): крім променевої реакції при введенні гемцитабіну більш ніж за 7 днів до або після променевої терапії збільшення токсичності не зареєстровано. Ці дані дозволяють припустити, що гемцитабін можна вводити через тиждень після променевої терапії або після того, як будуть дозволені гострі наслідки променевої терапії.що гемцитабін можна вводити через один тиждень після променевої терапії або після того, як буде дозволено гострі наслідки променевої терапії.що гемцитабін можна вводити через один тиждень після променевої терапії або після того, як буде дозволено гострі наслідки променевої терапії. І при одночасному, і при послідовному застосуванні гемцитабіну з променевою терапією були зареєстровані променеві пошкодження тканин, що опромінюються (наприклад, езофагіт, коліт і пневмоніт). Інші Не рекомендується спільне застосування з живими вакцинами жовтої лихоманки та іншими живими вакцинами внаслідок ризику системного захворювання з можливим летальним результатом, особливо у пацієнтів з імуносупресією.Спосіб застосування та дозиГемцитабін вводиться внутрішньовенно краплинно протягом 30 хвилин. Перед кожним введенням гемцитабіну необхідно контролювати кількість тромбоцитів, лейкоцитів та гранулоцитів у крові. При ознаках пригнічення функції кісткового мозку, спричиненого препаратом, необхідно припинити лікування або скоригувати дозу. Недрібноклітинний рак легені (місцерозповсюджений або метастатичний), перша лінія терапії. Монотерапія: Рекомендована доза препарату – 1000 мг/м2 в 1, 8 та 15 дні кожного 28-денного циклу. Комбінована терапія з цисплатином: Рекомендована доза препарату – 1250 мг/м2 на 1 та 8 день кожного 21-денного циклу або 1000 мг/м2 у 1, 8 та 15 дні кожного 28-денного циклу. Цисплатин вводиться у дозі 70 мг/м2 на 1 день циклу після інфузії гемцитабіну на фоні гіпергідратації. Комбінована терапія з карбоплатином: Рекомендована доза препарату – 1000 мг/м2 або 1200 мг/м2 на 1 та 8 день кожного 21-денного циклу. Карбоплатин вводиться з розрахунку AUC (площа під кривою «концентрація-час») 5,0 мг/мл/хв за 1 день циклу після інфузії гемцитабіну. Рак молочної залози (нерезектабельний, місцеворецидивний або метастатичний). Комбінована терапія з паклітакселом: Як терапія першої лінії при прогресуванні захворювання після неоад'ювантної та/або ад'ювантної терапії, що включає антрацикліни, за відсутності протипоказань до них. Паклітаксел вводиться в дозі 175 мг/м2 внутрішньовенно крапельно протягом 3 годин на день 21-денного циклу з подальшим введенням гемцитабіну. Рекомендована доза препарату – 1250 мг/м2 на 1 та 8 день кожного 21-денного циклу. Перед початком комбінованої терапії (гемцитабін + паклітаксел) абсолютна кількість гранулоцитів у крові у пацієнтів має бути не менше ніж 1500/мкл. Уротеліальний рак (рак сечового міхура (місцерозповсюджений, метастатичний та поверхневий), ниркової балії, сечоводу, сечовипускального каналу). Монотерапія: Рекомендована доза препарату – 1250 мг/м2 у 1, 8 та 15 дні кожного 28-денного циклу. Комбінована терапія з цисплатином: Рекомендована доза препарату — 1000 мг/м2 в 1, 8 і 15 днів у поєднанні з цисплатином, який вводиться в дозі 70 мг/м2 відразу після інфузії гемцитабіну в 1 або 2 день кожного 28-денного циклу. Клінічні дослідження показали, що за дози цисплатину 100 мг/м2 спостерігається більш виражена мієлосупресія. Епітеліальний рак яєчників (місцерозповсюджений або метастатичний, резистентний до похідних платини). Монотерапія: Рекомендована доза препарату – 800-1250 мг/м2 у 1, 8 та 15 дні кожного 28-денного циклу. Комбінована терапія з карбоплатином: Рекомендована доза препарату – 1000 мг/м2, на 1 та 8 день у поєднанні з карбоплатином з розрахунку AUC 4,0 мг/мл/хв, який вводиться відразу після інфузії гемцитабіну на 1 день кожного 21-денного циклу. Рак підшлункової залози (місцерозповсюджений або метастатичний, у т.ч. резистентний до терапії фторурацилом). Монотерапія: Рекомендована доза препарату – 1000 мг/м2 один раз на тиждень протягом 7 тижнів з наступною тижневою перервою. Потім препарат вводиться в 1, 8 та 15 дні кожного 28-денного циклу. Рак шийки матки (місцерозповсюджений або метастатичний). Комбінована терапія з цисплатином: При місцеворозповсюдженому раку при послідовній хіміопроменевій терапії (неоад'ювантно) та при метастатичному раку цисплатин вводиться в дозі 70 мг/м2 на 1 день циклу на тлі гіпергідратації з подальшим введенням гемцитабіну. Гемцитабін вводиться в дозі 1250 мг/м2 на 1 та 8 день кожного 21-денного циклу. При місцевопоширеному раку при одночасної хіміопроменевої терапії цисплатин вводиться в дозі 40 мг/м2 з наступним (безпосередньо після введення цисплатину) введенням гемцитабіну. Гемцитабін вводиться 1 раз на тиждень за 1-2 години до початку променевої терапії у дозі 125 мг/м2. Рак жовчовивідних шляхів Комбінована терапія з цисплатином: Цисплатин вводиться в дозі 70 мг/м2 на 1 день циклу на тлі гіпергідратації з подальшим введенням гемцитабіну. Гемцитабін вводиться у дозі 1250 мг/м2 на 1 та 8 день кожного 21-денного циклу. Корекція дози У разі розвитку гематологічної токсичності доза гемцитабіну може бути зменшена або його введення відкладено відповідно до наступних схем: А. Корекція дози гемцитабіну в рамках циклу при уротеліальному раку, недрібноклітинному раку легені, раку підшлункової залози як монотерапія або в комбінації з цисплатином. Корекція дози гемцитабіну в рамках циклу при уротеліальному раку, недрібноклітинному раку легені, раку підшлункової залози як монотерапія або в комбінації з цисплатином. Корекція дози гемцитабіну в рамках циклу при уротеліальному раку, недрібноклітинному раку легені, раку підшлункової залози як монотерапія або в комбінації з цисплатином. Абсолютна кількість гранулоцитів (× 109 /л) Кількість тромбоцитів (×10 9 /л) % від попередньої дози >1 і >100 100 0,5-1 або 50–100 75 <0,5 або <50 Відкласти введення Б. Корекція дози гемцитабіну в рамках циклу при раку молочної залози у комбінації з паклітакселом. Корекція дози гемцитабіну в рамках циклу при раку молочної залози у комбінації з паклітакселом Корекція дози гемцитабіну в рамках циклу при раку молочної залози у комбінації з паклітакселом Абсолютна кількість гранулоцитів (×10 9 /л) Кількість тромбоцитів (× 109 /л) % від попередньої дози ≥1,2 і >75 100 1-<1,2 або 50–75 75 0,7-<1 і ≥50 50 <0,7 або <50 Відкласти введення В. Корекція дози гемцитабіну в рамках циклу при раку яєчників у комбінації з карбоплатином. Корекція дози гемцитабіну в рамках циклу при раку яєчників у комбінації з карбоплатином Корекція дози гемцитабіну в рамках циклу при раку яєчників у комбінації з карбоплатином Абсолютна кількість гранулоцитів (×10 9 /л) Кількість тромбоцитів (×10 9 /л) % від попередньої дози >1,5 і ≥100 100 1-1,5 або 75–100 50 <1 або <75 Відкласти введення Для виявлення негематологічної токсичності необхідно проводити регулярне обстеження пацієнта та контролювати функцію печінки та нирок. Залежно від ступеня токсичності дозу можна знижувати протягом кожного циклу або з початком нового циклу ступінчасто. Введення препарату має бути відкладено доти, доки, на думку лікаря, токсичність не вирішиться. Особливі групи пацієнтів Літні пацієнти: Немає даних, що дозволяють припустити, що у пацієнтів похилого віку необхідно коригувати дозу. Пацієнти з порушенням функції печінки та нирок: Застосовувати гемцитабін у пацієнтів із печінковою недостатністю або з порушеною функцією нирок слід з обережністю, оскільки достатніх даних щодо застосування препарату у цієї категорії пацієнтів немає. Ниркова недостатність легкого або середнього ступеня тяжкості (швидкість клубочкової фільтрації від 30 мл/хв до 80 мл/хв) не має помітного впливу на фармакокінетику гемцитабіну. Діти: Гемцитабін вивчався в обмежених дослідженнях І та ІІ фази у дітей з різними типами новоутворень. Даних цих досліджень недостатньо для доказу ефективності та безпеки застосування гемцитабіну у дітей. Рекомендації щодо приготування розчину для інфузій Як розчинник використовується лише 0,9% розчин натрію хлориду без консервантів. Для приготування концентрату вміст флакону 200 мг розчиняють не менше, ніж 5 мл, і 1 г - не менше, ніж 25 мл 0,9% розчину натрію хлориду для ін'єкцій. Кожен флакон акуратно збовтують до повного розчинення ліофілізату. Отриманий розчин має бути прозорим. Максимальна концентрація гемцитабіну не повинна перевищувати 40 мг/мл. Розчини, приготовані з концентрацією вище 40 мг/мл, можуть супроводжуватися неповним розчиненням. Приготовлений концентрат гемцитабіну, що містить потрібну дозу препарату, перед введенням розбавляють 0,9% розчином хлориду натрію для ін'єкцій у кількості, достатньому для 30-хвилинної внутрішньовенної інфузії. Перед парентеральним введенням необхідно візуально контролювати приготовлений розчин на наявність механічних домішок та зміну кольору.ПередозуванняАнтидот для гемцитабіну невідомий. Клінічно допустима токсичність спостерігалася при введенні одноразових доз до 5,7 г/м2 внутрішньовенно протягом 30 хвилин кожні два тижні. У разі підозри на передозування пацієнт повинен перебувати під постійним лікарським контролем, включаючи підрахунок формули крові. За потреби пацієнту проводять симптоматичне лікування.Запобіжні заходи та особливі вказівкиЛікування гемцитабіном можна проводити лише під наглядом лікаря, який має досвід застосування протипухлинної хіміотерапії. Гематологічна токсичність Гемцитабін може пригнічувати функцію кісткового мозку, що проявляється лейкопенією, тромбоцитопенією або анемією. Перед кожним введенням гемцитабіну необхідно контролювати кількість тромбоцитів, лейкоцитів та гранулоцитів у крові. При ознаках пригнічення функції кісткового мозку, спричиненого препаратом, необхідно припинити лікування або скоригувати дозу. Функція нирок та печінки Необхідно проводити регулярне обстеження пацієнта та оцінку функції нирок та печінки. Введення гемцитабіну при метастазах у печінці, при гепатиті та алкоголізмі в анамнезі, а також при цирозі печінки збільшує ризик розвитку печінкової недостатності. У пацієнтів, які отримували гемцитабін, гемолітико-уремічний синдром реєструвався у поодиноких випадках. Терапія гемцитабіном повинна бути припинена з появою перших ознак мікроангіопатичної гемолітичної анемії, таких як швидке зниження гемоглобіну, тромбоцитопенія, підвищення концентрації сироваткового білірубіну. Ниркова недостатність може бути незворотною після припинення терапії гемцитабіном, у зв'язку з чим може знадобитися гемодіаліз. Судинні порушення Синдром підвищеної проникності капілярів, респіраторний дистрес-синдром дорослих, синдром оборотної задньої енцефалопатії з потенційно серйозними наслідками спостерігалися у пацієнтів,отримували гемцитабін у монотерапії або у комбінації з іншими хіміотерапевтичними препаратами. Ці синдроми можуть бути пов'язані з пошкодженням ендотелію судин, можливо індукованим гемцитабіном. У разі їх розвитку під час терапії слід припинити лікування гемцитабіном та вжити необхідних заходів. Функція легенів Крім респіраторного дистрес-синдрому дорослих, інші порушення функції легень, іноді тяжкого ступеня (наприклад, набряк легень, інтерстиціальний пневмоніт), були зареєстровані у пацієнтів, які отримували гемцитабін у монотерапії або у комбінації з іншими цитостатиками. Етіологія цих порушень невідома. При розвитку таких побічних ефектів необхідно припинити терапію гемцитабіном та вжити необхідних заходів. Раннє використання симптоматичної терапії може покращити ситуацію. Фертильність У дослідженнях фертильності гемцитабін викликав гіпосперматогенез у самців мишей. Тому чоловікам, які отримують терапію гемцитабіном, не рекомендується батьківство під час лікування та протягом 6 місяців після його закінчення. До початку лікування слід звернутися за додатковою консультацією щодо кріоконсервації сперми через можливу безплідність внаслідок терапії гемцитабіном. Збільшення тривалості інфузії та частоти введень призводить до зростання токсичності. Залежно від ступеня токсичності дозу можна знижувати протягом кожного циклу або з початком нового циклу ступінчасто. Вплив на здатність до керування автотранспортом та управління механізмами Досліджень впливу гемцитабіну на здатність керувати автотранспортними засобами та іншими механізмами не проводилося. Проте відомо, що гемцитабін може викликати сонливість від слабкого до помірного ступеня, особливо спільно з вживанням алкоголю. Пацієнтів слід застерігати від управління механізмами у випадках, коли вони відчувають сонливість.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
5 202,00 грн
5 154,00 грн
Склад, форма випуску та упаковкаЛіофілізат - 1 фл. речовина, що діє: трастузумаб -150 мг; допоміжні речовини: L-гістидину гідрохлорид – 3.36 мг, L-гістидин – 2.16 мг, а, а-трегалози дигідрат – 136.2 мг, полісорбат 20 – 0.60 мг. По 150 мг трастузумабу у флакони, виготовлені з безбарвного скла гідролітичного класу I, закупорені пробками з бутилкаучуку, закриті алюмінієвими ковпачками та пластмасовими кришками. По 1 флакон разом з інструкцією по застосуванню поміщають у картонну пачку.Опис лікарської формиЛіофілізат від білого до світло-жовтого кольору. Відновлений розчин - прозора або злегка опалесцентна безбарвна або світло-жовтого кольору рідина.Фармакотерапевтична групаПротипухлинний засіб - моноклональні антитіла.ФармакокінетикаФармакокінетика трастузумабу оцінювалася на підставі популяційного фармакокінетичного аналізу з використанням двокамерної моделі з паралельним лінійним та нелінійним виведенням із центральної камери. Завдяки нелінійному виведенню, зменшення концентрації препарату супроводжувалося збільшенням загального кліренсу. Лінійний кліренс склав 0.127 л/день у пацієнтів з раком молочної залози (метастатичний рак молочної залози (мРМЗ) та ранній рак молочної залози (рРМЗ)) та 0.176 л/день у пацієнтів з поширеним раком шлунка. Значення нелінійних параметрів виведення моделі Міхаеліса-Ментен склали 8.81 мг/день для максимальної швидкості виведення (Vmax) і 8.92 мг/л для константи Міхаеліса-Ментен (Кm). Об'єм розподілу в центральній камері становив 2.62 л у пацієнтів з РМЗ та 3.63 л у пацієнтів з поширеним раком шлунка.Розраховані за допомогою популяційного аналізу значення експозиції препарату (5й - 95й перцентілі) та значення фармакокінетичних параметрів при клінічно значущих концентраціях (максимальна концентрація (Сmах) та мінімальна концентрація (Cmin)) у пацієнтів з РМЗ та поширеним раком шлунка (РРЖ) при застосуванні препарату і кожні 3 тижні представлені у таблицях 1 та 2 (у рівноважному стані). Таблиця 1. Розраховані значення популяційних фармакокінетичних показників експозиції в циклі 1 при внутрішньовенному введенні у пацієнтів з РМЗ та РРШ (5й - 95й перцентілі). Режим дозування Тип пухлини N – число пацієнтів з ''ПНІ (мкг/мл) с'-max (мкг/мл) AUC* (мкг.день/мл) 8 м г/кг + 6мг/кг 1 раз на 3 тижні мРМЖ/РРМЖ 1195 29.4 (5.8-59.5) 178 (117-291) 1373 (736-2245) РРЖ 274 23.1 (6.1 -50.3) 132 (84.2-225) 1109 (588-1938) 4 м г/кг + 2мг/кг 1 раз на тиждень мРМЖ/РРМЖ 1195 37.7 (12.3-70.9) 88.3 (58-144) 1066 (586-1754) *AUC - площа під кривою "концентрація-час" Таблиця 2. Розраховані значення популяційних фармакокінетичних показників експозиції у рівноважному стані для режимів дозування препарату Герцептин® при внутрішньовенному введенні у пацієнтів з РМЗ та РРШ (5-95й перцентілі). Режим дозування Тип пухлини N-число пацієнтів C-min,ss (мкг/мл) C-max.ss (мкг/мл) AUCSS (мкг. день/м л) Час до досягнення рівноважного стану (тижня) Діапазон значень загального кліренсу у рівноважному стані (л/день) 8мг/кг + 6мг/кг 1 раз на 3 тижні мРМЗ/рРМЗ 1195 47.4 (5-115) 179 (107-309) 1794 (673 -3618) 12 0.173 – 0.283 РРЖ 274 32.9 (6.1 -88.9) 131 (72.5 -251) 1338 (557-2875) 9 0.189 – 0.337 4м г/кг + 2мг/кг 1 раз на тиждень мРМЗ/рРМЗ 1195 66.1 (14.9-142) 109 (51.0-209) 1765 (647-3578) 12 0.201 – 0.244 Відмивальний період (washout time period) трастузумабу після внутрішньовенного введення оцінювалися за допомогою популяційного фармакокінетичного моделювання. Принаймні, у 95% пацієнтів концентрація трастузумабу у сироватці крові досягає значення Циркулюючий "злущується" позаклітинний домен рецептора HER2 (HER2-ECD) Результати пошукового аналізу коваріант на підставі інформації в підгрупах пацієнтів дозволяють припускати, що у пацієнтів з високою концентрацією "слущивающегося" рецептора HER2-ECD в плазмі крові кліренс трастузума ). Спостерігалася кореляція між антигеном, що "слущується" з клітини, і активністю сироваткової глутамат оксалоацетат трансамінази (СГОТ)/ аспартатамінотрансферази (ACT): вплив "слущивающегося" з клітини антигену на кліренс може частково пояснюватися активністю СГОТ. Вихідні концентрації "HER2-ECD, що злущується", що спостерігалися у пацієнтів з метастатичним раком шлунка, були зіставні з такими у пацієнтів з метастатичним і раннім раком молочної залози; явного впливу кліренс трастузумаба не відзначалося. Фармакокінетика у спеціальних груп пацієнтів Детальні фармакокінетичні дослідження у пацієнтів похилого віку та пацієнтів з нирковою або печінковою недостатністю не проводились. Літній вік Вік не впливає на розподіл трастузумабу. Ниркова недостатність За даними популяційного фармакокінетичного аналізу, ниркова недостатність не впливає на фармакокінетичні параметри (кліренс) трастузумабу.ФармакодинамікаТрастузумаб є рекомбінантними гуманізованими моноклональними антитілами, які вибірково взаємодіють з позаклітинним доменом рецепторів епідермального фактора росту людини 2 типу (HER2). Ці антитіла є IgG1, що складаються з людських регіонів (константні ділянки важких ланцюгів) і визначають комплементарність мишачих ділянок антитіла pl85 HER2 до HER2. Прото-онкоген HER2 або с-еrВ2 кодує трансмембранний рецептороподібний білок з молекулярною масою 185 кДа, який структурно подібний до інших членів сімейства рецепторів епідермального фактора росту. Гіперекспресія HER2 виявляється у тканині первинного раку молочної залози (РМЗ) у 15-20% пацієнтів. Загальна частота виявлення HER2-позитивного статусу в тканині поширеного раку шлунка при скринінгу пацієнтів склала 15% ІГХ (метод імуно-гістохімічної реакції) 3+ та ІГХ2+/FISH+ (метод гібридизації in situ) або 22.1% при застосуванні ширшого визначення ІГХЗ+ . Ампліфікація гена HER2 призводить до гіперекспресії білка HER2 на мембрані клітин пухлини, що, у свою чергу, викликає постійну активацію рецептора HER2. Позаклітинний домен рецептора (ECD, р105) може потрапляти ("злущуватися") у кровотік і визначатися у зразках сироватки крові. Дослідження показують, що пацієнти з раком молочної залози, у яких відзначена ампліфікація або гіперекспресія HER2 у тканині пухлини, мають меншу виживання без ознак захворювання порівняно з пацієнтами без ампліфікації або гіперекспресії HER2 у тканині пухлини. Трастузумаб блокує проліферацію пухлинних клітин людини з гіперекспресією HER2 in vivo та in vitro. In vitro антитіло-залежна клітинна цитотоксичність трастузумабу переважно спрямована на пухлинні клітини з гіперекспресією HER2. Імуногенність У дослідженні неоад'ювантно-ад'юван гної терапії раннього раку молочної залози (медіана наступного спостереження >70 місяців) у 10.1% пацієнтів, які отримували препарат Герцептин® внутрішньовенно, з'явилися антитіла до трастузумабу. Нейтралізуючі антитіла до трастузумабу були виявлені в порівнянні з вихідним рівнем у 2 з 30 пацієнтів, які отримували препарат Герцептин для внутрішньовенного введення. Клінічна значимість цих антитіл невідома. Дані антитіла не впливали на фармакокінетику, ефективність (визначена за повною патологічною відповіддю та виживання без подій) та безпеку (визначена за частотою інфузійних реакцій) препарату Герцептинк при внутрішньовенному введенні. Дані щодо імуногенності при застосуванні препарату Герцептин для лікування раку шлунка відсутні.Показання до застосуванняРак молочної залози Метастатичний рак молочної залози з пухлинною гіперекспресією HER2: у вигляді монотерапії після однієї або більше схем хіміотерапії; у комбінації з паклітакселом або доцетакселом, у разі відсутності попередньої хіміотерапії (перша лінія терапії); у комбінації з інгібіторами ароматази при позитивних гормональних рецепторах (естрогенових та/або прогестеронових) у жінок у постменопаузі. Ранні стадії раку молочної залози з пухлинною гіперекспресією HER2: у вигляді ад'ювантної терапії після проведення хірургічного втручання, завершення хіміотерапії (неоад'ювантної або ад'ювантної) та променевої терапії; у комбінації з паклітакселом або доцетакселом після ад'ювантної хіміотерапії доксорубіцином та циклофосфамідом; у комбінації з ад'ювантною хіміотерапією, що складається з доцетакселу та карбоплатину; у комбінації з неоад'ювантною хіміотерапією та наступною ад'ювантною монотерапією препаратом Герцептин®, при місцево-поширеному (включаючи запальну форму) захворюванні або у випадках, коли розмір пухлини перевищує 2 см у діаметрі. Поширений рак шлунка Поширена аденокарцинома шлунка або стравохідно-шлункового переходу з гіперекспресією пухлинної HER2: у комбінації з капецитабіном або внутрішньовенним введенням фторурацилу та препаратом платини у разі відсутності попередньої протипухлинної терапії з приводу метастатичної хвороби.Протипоказання до застосуванняПідвищена чутливість до трастузумабу, будь-якого компонента препарату чи білка миші. Вагітність та період грудного вигодовування. Дитячий вік до 18 років (ефективність та безпека застосування у дітей не встановлені). Тяжка задишка у спокої, спричинена метастазами в легені, або потребує підтримуючої терапії киснем. Хворі на ранніх стадіях РМЗ з інфарктом міокарда в анамнезі, стенокардією, що потребує лікування, застійною серцевою недостатністю (II-IV функціональний клас за NYHA), ФВЛШ З обережністю: ішемічна хвороба серця, артеріальна гіпертензія, серцева недостатність, супутні захворювання легень або метастази у легені, попередня терапія кардіотоксичними лікарськими засобами, у т.ч. антрациклінами/циклофосфамідом, фракція викиду лівого шлуночка (ФВЛШ)Вагітність та лактаціяФертильність Невідомо, чи впливає Герцептин на репродуктивну здатність. Результати досліджень у тварин не виявили ознак порушення фертильності чи негативного впливу на плід. Контрацепція Жінкам дітородного потенціалу під час лікування препаратом Герцептин® та протягом 7 місяців після закінчення лікування необхідно використовувати надійні методи контрацепції. Вагітність У разі настання вагітності під час лікування або протягом 7 місяців після останньої дози препарату необхідно попередити жінку про можливість шкідливого впливу на плід. Якщо вагітна продовжить отримувати терапію препаратом Герцептин®, вона повинна перебувати під ретельним наглядом лікарів різних спеціальностей. Період грудного вигодовування Вигодовування грудним молоком не рекомендується під час лікування та протягом 7 місяців після закінчення терапії препаратом Герцептин®.Побічна діяВ даний час найбільш серйозними та/або частими небажаними реакціями, про які повідомлялося при використанні препарату Герцептин®, є дисфункція серця, інфузійні реакції, гематотоксичність (зокрема нейтропенія), інфекції та порушення з боку легень. Для опису частоти небажаних реакцій використовується така класифікація: дуже часто (≥1/10), часто (≥1/100, але Нижче представлені небажані реакції, про які повідомлялося при застосуванні препарату Герцептин як у монотерапії, так і в комбінації з хіміотерапією у базових клінічних дослідженнях та при постмаркетинговому використанні. Частота вказана відповідно до максимально зустрічається у базових клінічних дослідженнях. Інфекційні та паразитарні захворювання: дуже часто – інфекції, назофарингіт; часто - нейтропенічний сепсис, цистит, Herpes zoster, грип, синусит, інфекції шкіри, риніт, інфекції верхніх дихальних шляхів, інфекції сечовивідних шляхів, бешиха, флегмона, фарингіт; нечасто – сепсис. Доброякісні, злоякісні та неуточнені новоутворення (включаючи кісти та поліпи): невідомо – прогресування злоякісного новоутворення, прогресування новоутворення. Порушення з боку крові та лімфатичної системи: дуже часто – фебрильна нейтропенія, анемія, нейтропенія, лейкопенія, тромбоцитопенія; невідомо – гіпопротромбінемія, імунна тромбоцитопенія. Порушення з боку імунної системи: часто – реакції гіперчутливості; невідомо – анафілактичні реакції+, анафілактичний шок+. Порушення з боку обміну речовин: дуже часто – зниження маси тіла, анорексія; невідомо – синдром лізису пухлини, гіперкаліємія. Порушення психіки: дуже часто – безсоння; часто – тривога, депресія, порушення мислення. Порушення з боку нервової системи: дуже часто – тремор1, запаморочення, головний біль, парестезії, дисгевзія (спотворення смакових сприйняттів); часто – периферична нейропатія, м'язовий гіпертонус, сонливість, атаксія; рідко – парез; невідомо – набряк мозку. Порушення з боку органу зору: дуже часто – кон'юнктивіт, підвищене сльозовиділення; часто – сухість очей; невідомо - набряк диска зорового нерва, крововилив у сітківку. Порушення з боку органу слуху та лабіринтні порушення: нечасто – глухота. Порушення з боку серцево-судинної системи: дуже часто - зниження та підвищення артеріального тиску (АТ)1, порушення серцевого ритму1, серцебиття1, тріпотіння (передсердь або шлуночків)1, зниження фракції викиду лівого шлуночка*, "припливи"; часто – серцева недостатність (застійна)+, суправентрикулярна тахіаритмія+1, кардіоміопатія, артеріальна гіпотензія+1, вазодилатація; нечасто – перикардіальний випіт; невідомо – кардіогенний шок, перикардит, брадикардія, ритм “галопу”. Порушення з боку дихальної системи, органів грудної клітки та середостіння: дуже часто - хрипи в легенях+1, задишка+, кашель, носова кровотеча, ринорея; часто – пневмонія+, бронхіальна астма, порушення функції легень, плевральний випіт+; рідко – пневмоніт; невідомо - легеневий фіброз+, дихальна недостатність+, інфільтрація легень+, гострий набряк легень+, гострий респіраторний дистрес-синдром+, бронхоспазм+, гіпоксія+, зниження насичення гемоглобіну киснем+, набряк гортані, ортопное, легкий, Порушення з боку шлунково-кишкового тракту: дуже часто – діарея, блювання, нудота, набряк губи болю в животі, диспепсія, запор, стоматит; часто – геморой, сухість у роті. Порушення з боку печінки та жовчовивідних шляхів: часто – гепатоцелюлярне пошкодження, гепатит, болючість у ділянці печінки; рідко – жовтяниця; невідомо – печінкова недостатність. Порушення з боку шкіри та підшкірних тканин: дуже часто – еритема, висипання, набряк особи1 алопеція, порушення структури нігтів, долонно-підошовний синдром; часто - акне, сухість шкіри, екхімоз, гіпергідроз, макуло-папульозний висип, свербіж, оніхоклазія, дерматит; нечасто – кропив'янка; невідомо – ангіоневротичний набряк. Порушення з боку кістково-м'язової та сполучної тканини: дуже часто – артралгія, м'язова скутість/міалгія; часто - артрит, біль у спині, оссалгія, спазми м'язів, біль у ділянці шиї, біль у кінцівках. Порушення з боку нирок та сечовивідних шляхів: часто – захворювання нирок; невідомо – мембранозний гломерулонефрит, гломерулонефропатія, ниркова недостатність. Вагітність, післяпологові та перинатальні стани: невідомо олігогідрамніон, фатальна гіпоплазія легень та гіпоплазія та/або порушення функції нирок у плода. Порушення з боку статевих органів та молочної залози: часто – запалення молочної залози/мастит. Загальні розлади та порушення в місці введення: дуже часто – астенія, біль у грудях, озноб, стомлюваність, грипоподібний синдром, інфузійні реакції, біль, гарячка, мукозит, периферичні набряки; часто - нездужання, набряки. Травми, інтоксикації та ускладнення маніпуляцій: часто – забій. + - небажані реакції, які в повідомленнях асоціювалися з летальним кінцем. 1 - небажані реакції, які переважно повідомлялися в асоціації з інфузійними реакціями. Точна відсоткова кількість не встановлена. * - небажані реакції спостерігалися при комбінованій терапії після антрациклінів та у комбінації з таксанами. Нижче представлена інформація щодо окремих небажаних реакцій. Дисфункція серця Застійна серцева недостатність II-IV функціонального класу за NYHA (класифікація Нью-Йоркської Асоціації Кардіологів) є частою небажаною реакцією при застосуванні препарату Герцептин і асоціювалася з фатальним результатом. У пацієнтів, які отримували препарат Герцептин®, спостерігалися такі ознаки та симптоми порушення функції серця: задишка, ортопное, посилення кашлю, набряк легенів, ритм “галопу” або зниження фракції викиду лівого шлуночка. У 3 базових клінічних дослідженнях застосування препарату Герцептин® у комбінації з ад'ювантною хіміотерапією частота серцевої дисфункції 3/4 ступеня (а саме симптоматична застійна серцева недостатність) не відрізнялася від такої у пацієнтів, які отримували лише хіміотерапію (тобто без препарату Герцептин®) і отримували препарат Герцептин®, послідовно після терапії таксанами (0.3-0.4%). Частота була найбільшою у пацієнтів, які отримували Герцептин® спільно з таксанами (2.0%). Досвід використання препарату Герцептин у комбінації з низькодозовими режимами антрациклінів у неоад'ювантній терапії обмежений. При застосуванні препарату Герцептин протягом одного року після завершення ад'ювантної хіміотерапії серцева недостатність III-IV функціонального класу по NYHA спостерігалася у 0.6% пацієнтів при медіані спостереження 12 місяців і у 0.8% пацієнтів при медіані спостереження 8 років. Частота легкої симптоматичної та безсимптомної дисфункції лівого шлуночка склала 4.6%. Тяжка ЗСН була оборотна в 71.4% випадків (оборотність визначалася як мінімум двома послідовними підвищеннями показника ФВЛШ ≥50% після явища). Легка симптоматична та безсимптомна дисфункція лівого шлуночка була оборотна у 79.5% випадків. Приблизно 17% явищ, пов'язаних із дисфункцією серця, виникли після завершення терапії препаратом Герцептин. У базових клінічних дослідженнях при метастатичному РМЗ частота серцевої дисфункції при внутрішньовенному введенні препарату Герцептин у поєднанні з паклітакселом варіювала від 9% до 12% порівняно з 1%-4% для монотерапії паклітакселом. Для монотерапії препаратом Герцептин частота склала 6%-9%. Найбільша частота серцевої дисфункції спостерігалася у пацієнтів, які отримують Герцептин® одночасно з антрациклінами/циклофосфамідом (27%), що значно вище, ніж для терапії антрациклінами/циклофосфамідом (7%-10%). У дослідженні з проспективним моніторингом функції серця частота симптоматичної ЗСН склала 2.2% у пацієнтів, які отримували препарат Герцептин і доцетаксел, порівняно з 0% у пацієнтів, які отримували монотерапію доцетакселом.Більшість пацієнтів (79%) із серцевою дисфункцією спостерігалося поліпшення стану після отримання стандартної терапії ЗСН. Інфузійні реакції та реакції гіперчутливості Підраховано, що близько 40% пацієнтів, які отримують Герцептин, відчувають інфузійні реакції в тій чи іншій формі. Однак більшість інфузійних реакцій є легкими та помірними за ступенем тяжкості (згідно з NCI-CTC) і мають тенденцію виникати на початку лікування, тобто. під час 1,2 та 3-ї інфузії, при наступних введеннях виникають рідше. Реакції включають наступні симптоми: озноб, лихоманка, задишка, артеріальна гіпотензія, хрипи в легенях, бронхоспазм, тахікардія, зниження насичення гемоглобіну киснем, респіраторний дистрес-синдром, висип, нудота, блювання і головний біль. Частота інфузійних реакцій всіх ступенів тяжкості варіює і залежить від показання, методології збору інформації, а також від того, чи Герцептин® вводився спільно з хіміотерапією або застосовувався в монотерапії. Тяжкі анафілактичні реакції, що вимагають негайних додаткових медичних втручань, найчастіше можуть виникати під час першої або другої інфузій препарату Герцептин, такі реакції асоціювалися з летальним результатом. В окремих випадках спостерігалися анафілактоїдні реакції. Гематологічна токсичність Дуже часто виникали фебрильна нейтропенія, лейкопенія, анемія, тромбоцитопенія та нейтропенія. Частота виникнення гіпопротромбінемії невідома. Ризик нейтропенії може бути дещо вищим при застосуванні трастузумабу в комбінації з доцетакселом після терапії препаратами антрациклінового ряду. Порушення з боку легень Із застосуванням препарату Герцептин асоціюються важкі небажані явища з боку легень (у тому числі з фатальним результатом). Дані реакції включають (але не обмежуються): інфільтрати в легенях, гострий респіраторний дистрес-синдром, пневмонію, пневмоніт, плевральний випіт, гострий набряк легень та дихальну недостатність. Перехід з лікарської форми для внутрішньовенного введення препарату Герцептин на лікарську форму для підшкірного введення та навпаки Загалом перехід з лікарської форми для внутрішньовенного введення препарату Герцептин на лікарську форму для підшкірного введення і, навпаки, у пацієнтів з ранніми стадіями HER2-позитивного РМЗ переносився добре. Частота серйозних небажаних явищ, небажаних явищ 3 ступеня тяжкості та припинення терапії через розвиток небажаних явищ до переходу на іншу лікарську форму була низькою.Взаємодія з лікарськими засобамиСпеціальні дослідження лікарських взаємодій препарату Герцептин у людини не проводилися. У клінічних дослідженнях клінічно значимих взаємодій між препаратом Герцептин і одночасно застосовуваними препаратами не відзначалося. У випадках, коли препарат Герцептин застосовувався у комбінації з доцетакселом, карбоплатином або анастрозолом, фармакокінетика вищезгаданих препаратів не змінювалася. Концентрації паклітакселу та доксорубіцину та їх основних метаболітів (6-альфа-гідроксипаклітаксел та доксорубіцинол) не змінюються у присутності трастузумабу. Тим не менш, трастузумаб може підвищити загальну експозицію одного з метаболітів доксорубіцину (7-дезокси-13-дигідродоксорубіцинон). Біологічна активність цього метаболіту та клінічне значення підвищення його експозиції невідомі. У присутності паклітакселу та доксорубіцину змін у концентрації трастузумабу не спостерігалося. Результати вивчення фармакокінетики капецитабіну та цисплатину при використанні в комбінації з трастузумабом або без нього припускають, що експозиція біологічно активних метаболітів капецитабіну (наприклад, фторурацил) не змінювалася при одночасному застосуванні цисплатину або цисплатину та трастузумабу. Однак були зареєстровані більш високі концентрації капецитабіну та триваліший період його напіввиведення при комбінації з трастузумабом. Дані також вказують, що фармакокінетика цисплатину не змінювалася при одночасному застосуванні капецитабіну або капецитабіну у комбінації з трастузумабом. Герцептин® не сумісний із 5% розчином декстрози через можливість агрегації білка. Герцептин® не можна змішувати або розчиняти разом з іншими лікарськими засобами. Ознак несумісності між розчином препарату Герцептин і інфузійними пакетами, виготовленими з полівінілхлориду, поліетилену або поліпропілену, не спостерігалося.Спосіб застосування та дозиТестування на пухлинну експресію HER2 до початку лікування препаратом Герцептин® є обов'язковим. Препарат Герцептин повинен вводитися кваліфікованим медичним персоналом. Препарат призначений для введення як у амбулаторно-поліклінічних, так і в стаціонарних умовах. Перед застосуванням препарату Герцептин® необхідно перевірити етикетку на флаконі та переконатися, що лікарська форма препарату відповідає призначеній пацієнтові ("ліофілізат для приготування концентрату для приготування розчину для інфузій", а не "розчин для підшкірного введення"). Герцептин® у лікарській формі "ліофілізат для приготування концентрату для приготування розчину для інфузій" не призначений для підшкірного введення та повинен застосовуватись лише внутрішньовенно. Перехід із лікарської форми для внутрішньовенного введення на лікарську форму для підшкірного введення та, навпаки, при введенні один раз на 3 тижні вивчався у клінічному дослідженні. Щоб не допустити помилкового введення препарату Кадсила® (трастузумаб емтанзин) замість препарату Герцептин® (трастузумаб), перед приготуванням розчину для інфузії та його введенням пацієнту необхідно перевірити етикетку на флаконі. Герцептин® у лікарській формі "ліофілізат для приготування концентрату для приготування розчину для інфузій" вводять лише внутрішньовенно краплинно! Вводити препарат внутрішньовенно струминно чи болюсно не можна! Увага! Герцептин® не сумісний із 5% розчином декстрози через можливість агрегації білка. Герцептин® не можна змішувати або розводити разом з іншими лікарськими засобами. Розчин препарату Герцептин сумісний з інфузійними пакетами, виготовленими з полівінілхлориду, поліетилену та поліпропілену. Приготування розчину Підготовка препарату до введення має проводитись в асептичних умовах. Інструкція з приготування розчину Вміст флакону з 150 мг препарату Герцептин розчиняють у 7.2 мл стерильної води для ін'єкцій. Під час розчинення слід акуратно поводитися з препаратом. При розчиненні слід уникати надлишкового піноутворення, останнє може утруднити набір потрібної дози з флакона. Стерильним шприцом повільно ввести 7.2 мл стерильної води для ін'єкцій у флакон зі 150 мг препарату Герцептин®, спрямовуючи струмінь рідини прямо на паліофілізат. Для розчинення акуратно похитати флакон обертальними рухами. Не струшувати! При розчиненні препарату часто утворюється невелика кількість піни. Щоб уникнути цього, необхідно дати розчину постояти близько 5 хвилин. Відновлений розчин - прозора або злегка опалесцентна безбарвна або світло-жовтого кольору рідина. Умови зберігання приготовленого розчину Флакон із 150 мг препарату використовується лише одноразово. Розчин препарату Герцептин® фізично та хімічно стабільний протягом 24 годин при температурі 2-8°С після розчинення стерильною водою для ін'єкцій. Чи не заморожувати! Приготування розчину для інфузії слід здійснювати безпосередньо після розчинення ліофілізату. У виняткових випадках розчин після розчинення ліофілізату може зберігатися не більше 24 годин при температурі 2-8°С, якщо розчинення ліофілізату проходило в контрольованих та валідованих асептичних умовах. При цьому за умови зберігання (правила зберігання та тривалість) відповідає спеціаліст, який розчиняє ліофілізат. Інструкція з приготування розчину для інфузії Визначити об'єм розчину: Необхідний для введення навантажувальної дози трастузумабу, що дорівнює 4 мг/кг маси тіла, або підтримуючої дози, що дорівнює 2 мг/кг, визначається за такою формулою: Об'єм (мл) = маса тіла (кг) х доза (4 мг/кг навантажувальна або 2 мг/кг підтримуюча)/21 (мг/мл, концентрація приготовленого розчину) Необхідний для введення навантажувальної дози трастузумабу, що дорівнює 8 мг/кг маси тіла, або підтримуючої дози, що дорівнює 6 мг/кг кожні 3 тижні, визначається за такою формулою: Об'єм (мл) = маса тіла (кг) х доза (8 мг/кг навантажувальна або 6 мг/кг підтримуюча)/ 21 (мг/мл, концентрація приготовленого розчину) З флакона з ліофілізатом, що розчинився, слід набрати відповідний об'єм і ввести його в інфузійний пакет з 250 мл 0.9% розчину натрію хлориду. Потім інфузійний пакет слід обережно перевернути для перемішування розчину, уникаючи піноутворення. Перед введенням розчин слід перевірити (візуально) щодо відсутності механічних домішок і зміни забарвлення. Розчин для інфузій вводять відразу після приготування. У виняткових випадках приготований розчин для інфузії може зберігатися не більше 24 годин при температурі 2-8°С, якщо розчинення ліофілізату та приготування розчину для інфузії відбувалося в контрольованих та валідованих асептичних умовах. При цьому за умови зберігання (правила зберігання та тривалість) відповідає спеціаліст, який готував розчин. Інструкції з утилізації невикористаного препарату або з терміном придатності, що минув. Попадання лікарського засобу у довкілля має бути зведено до мінімуму. Не слід утилізувати препарат за допомогою стічних вод або разом із побутовими відходами. По можливості необхідно використовувати спеціальні системи для утилізації лікарських засобів. Необхідно суворо дотримуватися наступних рекомендацій щодо використання та утилізації шприців та витратних матеріалів: Голки та шприци не можна використовувати повторно. Використані голки та шприци поміщають у захищений від проколів контейнер (ємність). Утилізацію препарату Герцептин і витратних матеріалів слід проводити відповідно до місцевих вимог. Стандартний режим дозування Під час кожного введення трастузумабу необхідно ретельно спостерігати за пацієнтом на предмет появи ознобу, лихоманки та інших інфузійних реакцій (протягом 6 годин після початку першої інфузії та протягом 2 годин після початку подальших інфузій). Слід зменшити швидкість інфузії або на якийсь час припинити введення препарату при розвитку інфузійної реакції. Відновлення інфузії можливе після зникнення симптомів інфузійних реакцій легкого та помірного ступеня тяжкості згідно з NCI-CTC (загальні критерії токсичності Національного інституту раку в США). Слід розглянути питання про припинення подальшої терапії препаратом Герцептин у разі розвитку тяжких або життєзагрозних інфузійних реакцій. Метастатичний рак молочної залози Щотижневе запровадження Доза навантаження: 4 мг/кг маси тіла у вигляді 90-хвилинної внутрішньовенної краплинної інфузії. Підтримуюча доза: 2 мг/кг маси тіла раз на тиждень. Підтримуюча доза вводиться через 1 тиждень після навантаження. Якщо попередня доза навантаження переносилася добре, препарат можна вводити у вигляді 30-хвилинної краплинної інфузії. Альтернативне введення – через 3 тижні Доза навантаження: 8 мг/кг маси тіла у вигляді 90-хвилинної внутрішньовенної краплинної інфузії. Підтримуюча доза: 6 мг/кг маси тіла кожні 3 тижні. Підтримуюча доза вводиться через 3 тижні після навантаження. Якщо попередня доза навантаження переносилася добре, препарат можна вводити у вигляді 30-хвилинної краплинної інфузії. Застосування у комбінації з паклітакселом або доцетакселом Паклітаксел або доцетаксел вводилися наступного дня після введення препарату Герцептин® (рекомендації з дозування див. у відповідних інструкціях з медичного застосування) або відразу після наступного введення препарату Герцептин®, якщо при попередньому введенні Герцептин® переносився добре. Застосування у комбінації з інгібітором ароматази Герцептин® та анастрозол вводилися на день 1. Обмежень за часом введення препарату Герцептин® та анастрозолу не було (рекомендації щодо дозування див. в інструкції з медичного застосування анастрозолу або інших інгібіторів ароматази). Ранні стадії раку молочної залози Щотижневе запровадження При щотижневому введенні Герцептин® вводиться в дозі навантаження 4 мг/кг маси тіла, далі в підтримує 2 мг/кг маси тіла один раз на тиждень. Підтримуюча доза вводиться через 1 тиждень після навантаження. Навантажувальна доза вводиться у вигляді 90-хвилинної внутрішньовенної краплинної інфузії. Якщо попередня доза навантаження переносилася добре, препарат можна вводити у вигляді 30-хвилинної краплинної інфузії. Введення через 3 тижні При введенні через 3 тижні навантаження: 8 мг/кг маси тіла (у вигляді 90-хвилинної внутрішньовенної краплинної інфузії). Підтримуюча доза: 6 мг/кг маси тіла кожні 3 тижні. Підтримуюча доза вводиться через 3 тижні після навантаження. Якщо попередня доза навантаження переносилася добре, препарат можна вводити у вигляді 30-хвилинної краплинної інфузії. Застосування препарату Герцептин при ранніх стадіях раку молочної залози вивчено в комбінації з хіміотерапією згідно зі схемами, описаними нижче. Застосування у комбінації з паклітакселом або доцетакселом після хіміотерапії доксорубіцином та циклофосфамідом Паклітаксел: 80 мг/м2 у вигляді тривалої внутрішньовенної (в/в) інфузії, щотижня, протягом 12 тижнів або 175 мг/м2 у вигляді тривалої внутрішньовенної інфузії, кожні 3 тижні протягом 4 циклів (в день 1 кожного циклу) . Доцетаксел: 100 мг/м2 у вигляді внутрішньовенної інфузії протягом 1 години, кожні 3 тижні, протягом 4 циклів (починаючи на день 2 у циклі 1, далі на день 1 у кожний наступний цикл). Герцептин®: починаючи з першої дози паклітакселу або доцетакселу, Герцептин® вводився згідно з щотижневою схемою під час хіміотерапії (навантажувальна доза 4 мг/кг, далі підтримуючою дозою 2 мг/кг щотижня). Надалі монотерапія препаратом Герцептин® тривала згідно з щотижневою схемою після застосування у комбінації з паклітакселом або згідно з введенням через 3 тижні після застосування у комбінації з доцетакселом. Загальна тривалість терапії препаратом Герцептин від першого введення склала 1 рік, незалежно від кількості отриманих або пропущених доз. Якщо паклітаксел або доцетаксел і препарат Герцептин повинні були вводитися в один день, то паклітаксел або доцетаксел вводився першим. Застосування у комбінації з доцетакселом та карбоплатином Доцетаксел/Карбоплатин (кожні 3 тижні протягом 6 циклів, починаючи з дня 2 першого циклу, далі на день 1 у кожний наступний цикл): доцетаксел у дозі 75 мг/м2 у вигляді внутрішньовенної інфузії протягом 1 год, за яким слідував карбоплатин у дозі для досягнення цільової AUC - 6 мг/мл/хв у вигляді внутрішньовенної інфузії протягом 30-60 хв. Герцептін®: Герцептин® разом з хіміотерапією вводився згідно з щотижневою схемою (навантажувальна доза 4 мг/кг, далі підтримуючою дозою 2 мг/кг щотижня). Після хіміотерапії монотерапія препаратом Герцептин ® тривала згідно з введенням через 3 тижні. Загальна тривалість терапії препаратом Герцептин від першого введення склала 1 рік, незалежно від кількості отриманих або пропущених доз. Якщо доцетаксел, карбоплатин і препарат Герцептин повинні були вводитися в один день, то першим вводився доцетаксел, за яким слідував карбоплатин, далі Герцептин. Неоад'ювантна-ад'ювантна терапія Герцептин® вводився згідно з режимом кожні 3 тижні у комбінації з неоад'ювантною хіміотерапією (10 циклів): Доксорубіцин 60 мг/м2 та паклітаксел 150 мг/м2, кожні 3 тижні, протягом 3 циклів; далі паклітаксел 175 мг/м2, кожні 3 тижні протягом 4 циклів. Далі циклофосфамід, метотрексат та фторурацил у день 1 та 8. кожні 4 тижні, протягом 3 циклів. Після проведення оперативного втручання ад'ювантна монотерапія препаратом Герцептин ® тривала згідно з режимом кожні 3 тижні. Загальна тривалість терапії препаратом Герцептин склала 1 рік. Поширений рак шлунка Введення через 3 тижні Доза навантаження: 8 мг/кг маси тіла у вигляді 90-хвилинної внутрішньовенної краплинної інфузії. Підтримуюча доза: 6 мг/кг маси тіла кожні 3 тижні. Підтримуюча доза вводиться через 3 тижні після навантаження. Якщо попередня доза навантаження переносилася добре, препарат можна вводити у вигляді 30-хвилинної краплинної інфузії. Метастатичний та ранні стадії РМЗ та поширений рак шлунка Тривалість терапії Лікування препаратом Герцептин у пацієнтів з метастатичним РМЗ або поширеним раком шлунка проводиться до прогресування захворювання або розвитку неприйнятної токсичності. Пацієнти з ранніми стадіями РМЗ повинні отримувати терапію препаратом Герцептин протягом 1 року або до рецидиву захворювання або розвитку неприйнятної токсичності (залежно від того, що відбудеться швидше). Лікування препаратом Герцептин® пацієнтів із ранніми стадіями РМЗ понад один рік не рекомендується. Пропуск у плановому введенні Якщо пропуск у плановому введенні трастузумабу становив 7 днів або менше, слід якнайшвидше ввести препарат у звичайній підтримуючій дозі (тижневий режим: 2 мг/кг маси тіла; режим кожні 3 тижні: 6 мг/кг маси тіла), не чекаючи наступного планового введення. Далі вводити препарат у підтримуючій дозі через 7 днів або 21 день відповідно до щотижневого режиму або режиму кожні 3 тижні відповідно. Якщо перерва у введенні препарату склала більше 7 днів, необхідно якнайшвидше знову ввести навантажувальну дозу трастузумабу (щотижневий режим: 4 мг/кг маси тіла; режим кожні 3 тижні: 8 мг/кг маси тіла), у вигляді 90-хвилинної внутрішньовенної краплинної інфузії. Потім продовжити введення препарату у підтримуючій дозі через 7 днів або 21 день відповідно до щотижневого режиму або режиму кожні 3 тижні відповідно. Корекція дози У період виникнення оборотної мієлосупресії, спричиненої хіміотерапією, курс терапії препаратом Герцептин® може бути продовжений після зниження дози хіміотерапії або тимчасової її відміни (згідно з відповідними рекомендаціями в інструкціях з застосування паклітакселу, доцетакселу або інгібіторного аромату). При зниженні фракції викиду лівого шлуночка (ФВЛШ. %) на ≥10 одиниць від вихідної І нижче значення 50% лікування має бути припинено. Повторна оцінка ФВЛШ має бути проведена приблизно через 3 тижні. За відсутності поліпшення показника ФВЛШ або його подальшого зниження або при появі симптомів застійної серцевої недостатності (ЗСН) необхідно розглянути питання про припинення лікування препаратом Герцептин®, якщо тільки користь для конкретного пацієнта не перевищує ризику. Усі ці пацієнти повинні бути направлені до кардіолога для проведення обстеження та перебувати під наглядом. Особливі вказівки з дозування Пацієнти похилого віку Зниження дози препарату Герцептин у пацієнтів ≥65 років не потрібне. Пацієнти з нирковою недостатністю Зміна дози препарату Герцептин у пацієнтів з легким та середнім ступенем порушення функції нирок не потрібна. У зв'язку з обмеженими даними дати рекомендації з дозування препарату у пацієнтів з тяжким ступенем порушення функції нирок неможливо. Пацієнти з печінковою недостатністю У зв'язку з відсутністю даних дати рекомендації з дозування препарату у пацієнтів з порушенням функції печінки неможливо.ПередозуванняУ клінічних дослідженнях випадків передозування не спостерігалося. Введення препарату Герцептин у разових дозах більше 10 мг/кг не вивчалося. Препарат Герцептин у дозах ≤10 мг/кг переносився добре.Запобіжні заходи та особливі вказівкиУ медичній документації хворого слід зазначати торгове найменування та номер серії препарату. Інформація, представлена в даній інструкції, стосується виключно препарату Герцептин®. Терапія препаратом Герцептин повинна призначатися тільки лікарем, який має досвід лікування онкологічних захворювань. Введення препарату проводиться за наявності доступу до набору для екстреної допомоги. Лікар, який має досвід застосування хіміотерапевтичних препаратів, повинен бути доступний у процесі терапії. HER2 тестування має бути проведено у спеціалізованій лабораторії, яка може забезпечити контроль якості процедури тестування. Герцептин® повинен використовуватися у пацієнтів з метастатичним РМЗ або ранніми стадіями РМЗ тільки за наявності пухлинної гіперекспресії HER2, визначеної методом імуно-гістохімічної реакції (ІГХ), або ампліфікації гена HER2, визначеної методом гібридизації in situ (FISH або CISH). Слід використовувати точні та валідовані методи визначення. Герцептин® повинен використовуватися у пацієнтів з метастатичним раком шлунка лише за наявності пухлинної гіперекспресії HER2, визначеної методом ІГХ як ІГХ2+ та підтвердженої результатами S1SH або FISH, або ІГХЗ+. Слід використовувати точні та валідовані методи визначення. В даний час відсутні дані з клінічних досліджень про пацієнтів, які отримували Герцептин повторно після застосування в ад'ювантній терапії. Дисфункція серця загальні вказівки Пацієнти, які отримують Герцептин як монотерапію або в комбінації з паклітакселом або доцетакселом, особливо після хіміотерапії, що включає антрацикліни (доксорубіцин або епірубіцин), мають підвищений ризик розвитку застійної серцевої недостатності (ЗСН) (II-IV функціональний клас по NYHA) або безсимптомних порушень. функції серця. Тяжкість цих явищ може варіювати від середнього до тяжкого ступеня. Ці явища можуть призвести до смерті. Крім цього, необхідно бути обережними при лікуванні пацієнтів з високим серцево-судинним ризиком, наприклад, у пацієнтів похилого віку, з артеріальною гіпертензією, документально підтвердженою ішемічною хворобою серця, застійною серцевою недостатністю, фракцією викиду лівого шлуночка (ФВЛШ) Моніторування може дозволити виявити пацієнтів з порушеннями функції серця. Вихідне кардіологічне обстеження має повторюватися кожні 3 місяці під час терапії та кожні 6 місяців після її закінчення протягом 24 місяців з моменту введення останньої дози препарату. До початку лікування препаратом Герцептин® необхідно ретельно зіставити можливу користь та ризик його застосування. За даними, отриманими в результаті популяційного фармакокінетичного моделювання, препарат Герцептин може перебувати в крові до 7 місяців після завершення терапії. У пацієнтів, які отримують антрацикліни після завершення лікування препаратом Герцептин®, можливе підвищення ризику дисфункції серця. По можливості, лікарі повинні уникати призначення хіміотерапії на основі антрациклінів протягом 7 місяців після завершення терапії препаратом Герцептин®. При застосуванні препаратів антрациклінового ряду слід проводити ретельний моніторинг функції серця. Слід оцінити необхідність проведення стандартного кардіологічного обстеження у пацієнтів із підозрою на серцево-судинні захворювання. У всіх пацієнтів слід моніторувати функцію серця під час лікування (наприклад, кожні 12 тижнів). Внаслідок моніторингу можна виявити пацієнтів, у яких розвинулися порушення функції серця. У пацієнтів з безсимптомним порушенням функції серця може бути корисним часте проведення моніторингу (наприклад, кожні 6-8 тижнів). При тривалому погіршенні функції лівого шлуночка, що не виявляється симптоматично, доцільно розглянути питання про відміну препарату, за винятком випадків, коли лікар вважає, що користь для конкретного пацієнта перевершує ризик. Безпечність продовження або відновлення терапії препаратом Герцептин у пацієнтів, у яких розвинулося порушення функції серця, не вивчалася. При зниженні фракції викиду лівого шлуночка (ФВЛШ, %) на >10 одиниць від вихідної І нижче значення 50% лікування має бути припинено. Повторна оцінка ФВЛШ має бути проведена приблизно через 3 тижні. За відсутності поліпшення показника ФВЛШ або його подальшого зниження або при появі симптомів застійної серцевої недостатності (ЗСН) необхідно розглянути питання про припинення лікування препаратом Герцептин®, якщо тільки користь для конкретного пацієнта не перевищує ризику. Усі ці пацієнти повинні бути направлені до кардіолога для проведення обстеження та перебувати під наглядом. Якщо на фоні терапії препаратом Герцептин розвивається симптоматична серцева недостатність, необхідно провести відповідну стандартну медикаментозну терапію ЗСН. У більшості пацієнтів з ЗСН або безсимптомною дисфункцією серця в базових дослідженнях спостерігалося поліпшення стану на тлі стандартної медикаментозної терапії ЗСН: інгібітори ангіотензинперетворюючого ферменту або блокатори рецепторів ангіотензину та бета-адреноблокатори. За наявності клінічної користі від застосування препарату Герцептин більшість пацієнтів з побічними реакціями з боку серця продовжили терапію без прояву додаткових клінічно значущих реакцій з боку серця. Метастатичний рак молочної залози Не рекомендується застосовувати препарат Герцептин разом у комбінації з антрациклінами для лікування метастатичного раку молочної залози. Ризик розвитку дисфункції серця у пацієнтів з метастатичним раком молочної залози підвищений при попередній терапії антрациклінами, проте він нижчий порівняно з таким при одночасному застосуванні антрациклінів та препарату Герцептин. Ранні стадії раку молочної залози Пацієнтам з ранніми стадіями раку молочної залози слід проводити кардіологічне обстеження перед початком лікування кожні 3 місяці під час терапії та кожні 6 місяців після її закінчення протягом 24 місяців з моменту введення останньої дози препарату. Рекомендується більш тривалий моніторинг після лікування препаратом Герцептин у комбінації з антрациклінами з частотою обстежень 1 раз на рік протягом 5 років з моменту введення останньої дози Герцептин або далі, якщо спостерігається постійне зниження ФВЛШ. Лікування препаратом Герцептин1* не рекомендується пацієнтам на ранніх стадіях РМЗ (ад'ювантна та неоад'ювантна терапія) з: інфарктом міокарда в анамнезі; стенокардією, яка потребує лікування: ЗСН (II-IV функціональний клас за NYHA) в анамнезі або в даний час; ФВЛШ нижче за 55%; іншими кардіоміопатіями; аритміями, що вимагають лікування: клінічно значущими вадами серця; погано контрольована артеріальна гіпертензія, за винятком артеріальної гіпертензії, що піддається стандартній медикаментозній терапії; гемодинамічно значущим перикардіальним випотом, оскільки ефективність та безпека застосування препарату у таких пацієнтів не вивчені. Ад'ювантна терапія Не рекомендується застосовувати препарат Герцептин разом у комбінації з антрациклінами у складі ад'ювантної терапії. У пацієнтів із ранніми стадіями РМЗ. отримували Герцептин після хіміотерапії на основі антрациклінів, спостерігалося підвищення частоти симптоматичних і безсимптомних небажаних явищ з боку серця в порівнянні з такими, що отримували хіміотерапію доцетакселом і карбоплатином (режими, що не містять препарати антрациклінового ряду). При цьому різниця була більша у випадках спільного застосування препарату Герцептин і таксанів. ніж за послідовного використання. Незалежно від режиму, що використовувався, більшість симптоматичних кардіальних явищ виникало в перші 18 місяців лікування. В одному з 3 проведених базових досліджень (з медіаною періоду наступного спостереження 5.5 років) спостерігалося тривале збільшення кумулятивної частоти симптоматичних кардіальних явищ або явищ, пов'язаних зі зниженням ФВЛШ: у 2.37% пацієнтів,отримували Герцептин® спільно з таксанами після терапії антрациклінами, порівняно з 1% пацієнтів у групах порівняння (у групі терапії антрациклінами та циклофосфамідом, далі таксанами, та у групі терапії таксанами, карбоплатином та препаратом Герцептин®). Ідентифікованими факторами ризику розвитку небажаних явищ з боку серця при ад'ювантній терапії препаратом Герцептин® є вік >50 років, низька вихідна ФВЛШ (25 кг/м2). Неоад'ювантна-ад'ювантна терапія Для пацієнтів із ранніми стадіями РМЗ. яким може бути призначена неоад'ювантна-ад'ювантна терапія, застосування препарату Герцептин® спільно з антрациклінами рекомендовано тільки у випадку, якщо вони раніше не отримували хіміотерапію і тільки при використанні низькодозових режимів терапії антрациклінами (максимальна сумарна доза доксорубіцину 180 мг/2 ). У пацієнтів, які отримали повний курс низькодозових антрациклінів та Герцептин у складі неоад'ювантної терапії, не рекомендується проведення додаткової цитотоксичної хіміотерапії після проведення хірургічного втручання. У всіх інших випадках рішення щодо необхідності додаткової цитотоксичної хіміотерапії приймається на підставі індивідуальних факторів. Досвід застосування трастузумабу разом із низькодозовими режимами терапії антрациклінами обмежений двома дослідженнями. При застосуванні препарату Герцептин у лікарській формі для внутрішньовенного введення спільно з неоад'ювантною хіміотерапією, що включала три цикли доксорубіцину (сумарна доза 180 мг/м2), у клінічному дослідженні частота симптоматичного порушення функції серця склала 1.7%. При застосуванні препарату Герцептин у лікарській формі для внутрішньовенного введення спільно з неоад'ювантною хіміотерапією, що включала 4 цикли епірубіцину (сумарна доза 300 мг/м2), у клінічному дослідженні частота розвитку серцевої недостатності/застійної серцевої недостатності склала 0.3% при медіані спостереження. Клінічний досвід застосування у пацієнтів віком від 65 років обмежений. Інфузійні реакції та реакції гіперчутливості При введенні препарату Герцептин виникали серйозні інфузійні реакції: задишка, артеріальна гіпотензія, хрипи в легенях, артеріальна гіпертензія, бронхоспазм, суправентрикулярна тахіаритмія, зниження насичення гемоглобіну киснем, анафілаксія, респіраторний дистрес Для зниження ризику виникнення цих явищ можна використовувати премедикація. Більшість цих реакцій виникала під час інфузії або протягом 2,5 годин від початку першого введення. При виникненні інфузійної реакції слід зменшити швидкість інфузії або на якийсь час припинити введення препарату і ретельно спостерігати за пацієнтом до усунення всіх симптомів. Для усунення цих симптомів можливе застосування анальгетиків/антипіретиків. таких як парацетамол, або антигістамінних препаратів, таких як дифенгідрамін.Більшість пацієнтів після розв'язання симптомів інфузійних реакцій змогли продовжити терапію препаратом Герцептин. Ефективна терапія серйозних реакцій полягає у застосуванні бета-адреностимуляторів, глюкокортикостероїдів, інгаляції кисню. У разі розвитку тяжких або життєзагрозних інфузійних реакцій слід розглянути питання щодо припинення подальшої терапії препаратом Герцептин. У поодиноких випадках дані реакції асоціювалися з фатальним результатом. Ризик розвитку летальних інфузійних реакцій вищий у пацієнтів із задишкою у спокої, спричиненою метастазами у легені або супутніми захворюваннями, тому таким пацієнтам не слід проводити терапію препаратом Герцептин®. Повідомлялися випадки, у яких після початкового поліпшення спостерігалося погіршення стану, і навіть випадки з відстроченим стрімким погіршенням стану. Летальний результат виникав протягом години або одного тижня після інфузії. У окремих випадках у пацієнтів з'являлися симптоми інфузійних реакцій або легеневі симптоми (через більш ніж 6 годин після початку введення препарату Герцептин®). Слід попередити пацієнтів про можливий відстрочений розвиток цих симптомів і про необхідність негайного контакту з лікарем у разі їх виникнення. Порушення з боку легень При застосуванні препарату Герцептин у реєстраційному періоді реєструвалися важкі явища з боку легень, які іноді супроводжувалися летальним результатом. Крім того, спостерігалися випадки інтерстиціальної хвороби легень (ІБЛ), включаючи легеневі інфільтрати, гострий респіраторний дистрес-синдром, пневмонію, пневмоніт, плевральний випіт, гострий набряк легень та дихальну недостатність. Фактори ризику, асоційовані з ІХЛ, включають: раніше проведену або супутню терапію іншими протипухлинними препаратами, які, як відомо, пов'язані з ІХЛ (таксани, гемцитабін, винорельбін та променева терапія). Дані явища можуть бути як прояви інфузійних реакцій, і відстрочено. Ризик тяжких реакцій з боку легень вищий у пацієнтів із метастатичним ураженням легень, супутніми захворюваннями, що супроводжуються задишкою у спокої.Тому такі пацієнти не повинні отримувати препарат Герцептін. Слід бути обережними, особливо у пацієнтів, які отримують супутню терапію таксанами, через розвиток пневмоніту. Стерильна вода для ін'єкцій, що використовується для розчинення вмісту флакону з 150 мг препарату Герцептин, не містить бензилового спирту. Вплив на здатність до керування автотранспортом та управління механізмами Дослідження щодо вивчення впливу препарату на здатність керувати автомобілем та працювати з механізмами не проводилися. У разі виникнення симптомів інфузійних реакцій пацієнтам не слід керувати автомобілем або працювати з механізмами до вирішення симптомів.Умови зберіганняУ холодильнику +2+8 градусівУмови відпустки з аптекЗа рецептомВідео на цю тему
14 918,00 грн
14 870,00 грн
Склад, форма випуску та упаковкаЛіофілізат - 1 фл. діюча речовина: трастузумаб – 440 мг; допоміжні речовини: L-гістидину гідрохлорид – 9.9 мг, L-гістидин – 6.4 мг, ос, а-трегалози дигідрат – 400.0 мг, полісорбат 20 – 1.8 мг; Розчинник (бактеріостатична вода для ін'єкцій 20 мл, що містить 1.1% бензилового спирту як антимікробний консервант): бензиловий спирт - 229.9 мг, вода для ін'єкцій - 20.9 мл. По 440 мг трастузумабу у флакон безбарвного скла (гідролітичний клас 1 ЕФ), закупорений пробкою з бутилкаучуку, обжатий алюмінієвим ковпачком і закритий пластиковою кришкою світло-зеленого кольору. По 20 мл бактеріостатичної води для ін'єкцій у флакон безбарвного скла (гідролітичний клас 1 ЕФ), закупорений пробкою з бутилкаучуку, обжатий алюмінієвим ковпачком і закритий пластиковою кришкою білого кольору. 1 флакон з препаратом (ліофілізат) та 1 флакон з розчинником разом з інструкцією із застосування поміщають у картонну пачку.Опис лікарської формиЛіофілізат від білого до світло-жовтого кольору. Відновлений розчин - прозора або злегка опалесцентна рідина від безбарвного до світло-жовтого кольору.Фармакотерапевтична групаПротипухлинний засіб - моноклональні антитіла.ФармакокінетикаФармакокінетика трастузумабу оцінювалася на підставі популяційного фармакокінетичного аналізу з використанням двокамерної моделі з паралельним лінійним та нелінійним виведенням із центральної камери. Завдяки нелінійному виведенню, зменшення концентрації препарату супроводжувалося збільшенням загального кліренсу. Лінійний кліренс склав 0.127 л/день у пацієнтів з раком молочної залози (метастатичний рак молочної залози (мРМЗ) та ранній рак молочної залози (рРМЗ)) та 0.176 л/день у пацієнтів з поширеним раком шлунка. Значення нелінійних параметрів виведення моделі Міхаеліса-Ментен склали 8.81 мг/день для максимальної швидкості виведення (Vmax) і 8.92 мг/л для константи Міхаеліса-Ментен (Кm). Об'єм розподілу в центральній камері становив 2.62 л у пацієнтів з РМЗ та 3.63 л у пацієнтів з поширеним раком шлунка.Розраховані за допомогою популяційного аналізу значення експозиції препарату (5й - 95й перцентілі) та значення фармакокінетичних параметрів при клінічно значущих концентраціях (максимальна концентрація (Сmах) та мінімальна концентрація (Cmin)) у пацієнтів з РМЗ та поширеним раком шлунка (РРЖ) при застосуванні препарату і кожні 3 тижні представлені у таблицях 1 та 2 (у рівноважному стані). Таблиця 1. Розраховані значення популяційних фармакокінетичних показників експозиції в циклі 1 при внутрішньовенному введенні у пацієнтів з РМЗ та РРШ (5й - 95й перцентілі). Режим дозування Тип пухлини N – число пацієнтів з ''ПНІ (мкг/мл) с'-max (мкг/мл) AUC* (мкг.день/мл) 8 м г/кг + 6мг/кг 1 раз на 3 тижні мРМЖ/РРМЖ 1195 29.4 (5.8-59.5) 178 (117-291) 1373 (736-2245) РРЖ 274 23.1 (6.1 -50.3) 132 (84.2-225) 1109 (588-1938) 4 м г/кг + 2мг/кг 1 раз на тиждень мРМЖ/РРМЖ 1195 37.7 (12.3-70.9) 88.3 (58-144) 1066 (586-1754) *AUC - площа під кривою "концентрація-час" Таблиця 2. Розраховані значення популяційних фармакокінетичних показників експозиції у рівноважному стані для режимів дозування препарату Герцептин® при внутрішньовенному введенні у пацієнтів з РМЗ та РРШ (5-95й перцентілі). Режим дозування Тип пухлини N-число пацієнтів C-min,ss (мкг/мл) C-max.ss (мкг/мл) AUCSS (мкг. день/м л) Час до досягнення рівноважного стану (тижня) Діапазон значень загального кліренсу у рівноважному стані (л/день) 8мг/кг + 6мг/кг 1 раз на 3 тижні мРМЗ/рРМЗ 1195 47.4 (5-115) 179 (107-309) 1794 (673 -3618) 12 0.173 – 0.283 РРЖ 274 32.9 (6.1 -88.9) 131 (72.5 -251) 1338 (557-2875) 9 0.189 – 0.337 4м г/кг + 2мг/кг 1 раз на тиждень мРМЗ/рРМЗ 1195 66.1 (14.9-142) 109 (51.0-209) 1765 (647-3578) 12 0.201 – 0.244 Відмивальний період (washout time period) трастузумабу після внутрішньовенного введення оцінювалися за допомогою популяційного фармакокінетичного моделювання. Принаймні, у 95% пацієнтів концентрація трастузумабу у сироватці крові досягає значення Циркулюючий "злущується" позаклітинний домен рецептора HER2 (HER2-ECD) Результати пошукового аналізу коваріант на підставі інформації в підгрупах пацієнтів дозволяють припускати, що у пацієнтів з високою концентрацією "слущивающегося" рецептора HER2-ECD в плазмі крові кліренс трастузума ). Спостерігалася кореляція між антигеном, що "слущується" з клітини, і активністю сироваткової глутамат оксалоацетат трансамінази (СГОТ)/ аспартатамінотрансферази (ACT): вплив "слущивающегося" з клітини антигену на кліренс може частково пояснюватися активністю СГОТ. Вихідні концентрації "HER2-ECD, що злущується", що спостерігалися у пацієнтів з метастатичним раком шлунка, були зіставні з такими у пацієнтів з метастатичним і раннім раком молочної залози; явного впливу кліренс трастузумаба не відзначалося. Фармакокінетика у спеціальних груп пацієнтів Детальні фармакокінетичні дослідження у пацієнтів похилого віку та пацієнтів з нирковою або печінковою недостатністю не проводились. Літній вік Вік не впливає на розподіл трастузумабу. Ниркова недостатність За даними популяційного фармакокінетичного аналізу, ниркова недостатність не впливає на фармакокінетичні параметри (кліренс) трастузумабу.ФармакодинамікаТрастузумаб є рекомбінантними гуманізованими моноклональними антитілами, які вибірково взаємодіють з позаклітинним доменом рецепторів епідермального фактора росту людини 2 типу (HER2). Ці антитіла є IgG1, що складаються з людських регіонів (константні ділянки важких ланцюгів) і визначають комплементарність мишачих ділянок антитіла pl85 HER2 до HER2. Прото-онкоген HER2 або с-еrВ2 кодує трансмембранний рецептороподібний білок з молекулярною масою 185 кДа, який структурно подібний до інших членів сімейства рецепторів епідермального фактора росту. Гіперекспресія HER2 виявляється у тканині первинного раку молочної залози (РМЗ) у 15-20% пацієнтів. Загальна частота виявлення HER2-позитивного статусу в тканині поширеного раку шлунка при скринінгу пацієнтів склала 15% ІГХ (метод імуно-гістохімічної реакції) 3+ та ІГХ2+/FISH+ (метод гібридизації in situ) або 22.1% при застосуванні ширшого визначення ІГХЗ+ . Ампліфікація гена HER2 призводить до гіперекспресії білка HER2 на мембрані клітин пухлини, що, у свою чергу, викликає постійну активацію рецептора HER2. Позаклітинний домен рецептора (ECD, р105) може потрапляти ("злущуватися") у кровотік і визначатися у зразках сироватки крові. Дослідження показують, що пацієнти з раком молочної залози, у яких відзначена ампліфікація або гіперекспресія HER2 у тканині пухлини, мають меншу виживання без ознак захворювання порівняно з пацієнтами без ампліфікації або гіперекспресії HER2 у тканині пухлини. Трастузумаб блокує проліферацію пухлинних клітин людини з гіперекспресією HER2 in vivo та in vitro. In vitro антитіло-залежна клітинна цитотоксичність трастузумабу переважно спрямована на пухлинні клітини з гіперекспресією HER2. Імуногенність У дослідженні неоад'ювантно-ад'юван гної терапії раннього раку молочної залози (медіана наступного спостереження >70 місяців) у 10.1% пацієнтів, які отримували препарат Герцептин® внутрішньовенно, з'явилися антитіла до трастузумабу. Нейтралізуючі антитіла до трастузумабу були виявлені в порівнянні з вихідним рівнем у 2 з 30 пацієнтів, які отримували препарат Герцептин для внутрішньовенного введення. Клінічна значимість цих антитіл невідома. Дані антитіла не впливали на фармакокінетику, ефективність (визначена за повною патологічною відповіддю та виживання без подій) та безпеку (визначена за частотою інфузійних реакцій) препарату Герцептинк при внутрішньовенному введенні. Дані щодо імуногенності при застосуванні препарату Герцептин для лікування раку шлунка відсутні.Показання до застосуванняРак молочної залози Метастатичний рак молочної залози з пухлинною гіперекспресією HER2: у вигляді монотерапії після однієї або більше схем хіміотерапії; у комбінації з паклітакселом або доцетакселом, у разі відсутності попередньої хіміотерапії (перша лінія терапії); у комбінації з інгібіторами ароматази при позитивних гормональних рецепторах (естрогенових та/або прогестеронових) у жінок у постменопаузі. Ранні стадії раку молочної залози з пухлинною гіперекспресією HER2: у вигляді ад'ювантної терапії після проведення хірургічного втручання, завершення хіміотерапії (неоад'ювантної або ад'ювантної) та променевої терапії; у комбінації з паклітакселом або доцетакселом після ад'ювантної хіміотерапії доксорубіцином та циклофосфамідом; у комбінації з ад'ювантною хіміотерапією, що складається з доцетакселу та карбоплатину; у комбінації з неоад'ювантною хіміотерапією та наступною ад'ювантною монотерапією препаратом Герцептин®, при місцево-поширеному (включаючи запальну форму) захворюванні або у випадках, коли розмір пухлини перевищує 2 см у діаметрі. Поширений рак шлунка Поширена аденокарцинома шлунка або стравохідно-шлункового переходу з гіперекспресією пухлинної HER2: у комбінації з капецитабіном або внутрішньовенним введенням фторурацилу та препаратом платини у разі відсутності попередньої протипухлинної терапії з приводу метастатичної хвороби.Протипоказання до застосуванняПідвищена чутливість до трастузумабу, будь-якого компонента препарату чи білка миші. Вагітність та період грудного вигодовування. Дитячий вік до 18 років (ефективність та безпека застосування у дітей не встановлені). Тяжка задишка у спокої, спричинена метастазами в легені, або потребує підтримуючої терапії киснем. Хворі на ранніх стадіях РМЗ з інфарктом міокарда в анамнезі, стенокардією, що потребує лікування, застійною серцевою недостатністю (II-IV функціональний клас за NYHA), ФВЛШ З обережністю: ішемічна хвороба серця, артеріальна гіпертензія, серцева недостатність, супутні захворювання легень або метастази у легені, попередня терапія кардіотоксичними лікарськими засобами, у т.ч. антрациклінами/циклофосфамідом, фракція викиду лівого шлуночка (ФВЛШ)Вагітність та лактаціяФертильність Невідомо, чи впливає Герцептин на репродуктивну здатність. Результати досліджень у тварин не виявили ознак порушення фертильності чи негативного впливу на плід. Контрацепція Жінкам дітородного потенціалу під час лікування препаратом Герцептин® та протягом 7 місяців після закінчення лікування необхідно використовувати надійні методи контрацепції. Вагітність У разі настання вагітності під час лікування або протягом 7 місяців після останньої дози препарату необхідно попередити жінку про можливість шкідливого впливу на плід. Якщо вагітна продовжить отримувати терапію препаратом Герцептин®, вона повинна перебувати під ретельним наглядом лікарів різних спеціальностей. Період грудного вигодовування Вигодовування грудним молоком не рекомендується під час лікування та протягом 7 місяців після закінчення терапії препаратом Герцептин®.Побічна діяВ даний час найбільш серйозними та/або частими небажаними реакціями, про які повідомлялося при використанні препарату Герцептин®, є дисфункція серця, інфузійні реакції, гематотоксичність (зокрема нейтропенія), інфекції та порушення з боку легень. Для опису частоти небажаних реакцій використовується така класифікація: дуже часто (≥1/10), часто (≥1/100, але Нижче представлені небажані реакції, про які повідомлялося при застосуванні препарату Герцептин як у монотерапії, так і в комбінації з хіміотерапією у базових клінічних дослідженнях та при постмаркетинговому використанні. Частота вказана відповідно до максимально зустрічається у базових клінічних дослідженнях. Інфекційні та паразитарні захворювання: дуже часто – інфекції, назофарингіт; часто - нейтропенічний сепсис, цистит, Herpes zoster, грип, синусит, інфекції шкіри, риніт, інфекції верхніх дихальних шляхів, інфекції сечовивідних шляхів, бешиха, флегмона, фарингіт; нечасто – сепсис. Доброякісні, злоякісні та неуточнені новоутворення (включаючи кісти та поліпи): невідомо – прогресування злоякісного новоутворення, прогресування новоутворення. Порушення з боку крові та лімфатичної системи: дуже часто – фебрильна нейтропенія, анемія, нейтропенія, лейкопенія, тромбоцитопенія; невідомо – гіпопротромбінемія, імунна тромбоцитопенія. Порушення з боку імунної системи: часто – реакції гіперчутливості; невідомо – анафілактичні реакції+, анафілактичний шок+. Порушення з боку обміну речовин: дуже часто – зниження маси тіла, анорексія; невідомо – синдром лізису пухлини, гіперкаліємія. Порушення психіки: дуже часто – безсоння; часто – тривога, депресія, порушення мислення. Порушення з боку нервової системи: дуже часто – тремор1, запаморочення, головний біль, парестезії, дисгевзія (спотворення смакових сприйняттів); часто – периферична нейропатія, м'язовий гіпертонус, сонливість, атаксія; рідко – парез; невідомо – набряк мозку. Порушення з боку органу зору: дуже часто – кон'юнктивіт, підвищене сльозовиділення; часто – сухість очей; невідомо - набряк диска зорового нерва, крововилив у сітківку. Порушення з боку органу слуху та лабіринтні порушення: нечасто – глухота. Порушення з боку серцево-судинної системи: дуже часто - зниження та підвищення артеріального тиску (АТ)1, порушення серцевого ритму1, серцебиття1, тріпотіння (передсердь або шлуночків)1, зниження фракції викиду лівого шлуночка*, "припливи"; часто – серцева недостатність (застійна)+, суправентрикулярна тахіаритмія+1, кардіоміопатія, артеріальна гіпотензія+1, вазодилатація; нечасто – перикардіальний випіт; невідомо – кардіогенний шок, перикардит, брадикардія, ритм “галопу”. Порушення з боку дихальної системи, органів грудної клітки та середостіння: дуже часто - хрипи в легенях+1, задишка+, кашель, носова кровотеча, ринорея; часто – пневмонія+, бронхіальна астма, порушення функції легень, плевральний випіт+; рідко – пневмоніт; невідомо - легеневий фіброз+, дихальна недостатність+, інфільтрація легень+, гострий набряк легень+, гострий респіраторний дистрес-синдром+, бронхоспазм+, гіпоксія+, зниження насичення гемоглобіну киснем+, набряк гортані, ортопное, легкий, Порушення з боку шлунково-кишкового тракту: дуже часто – діарея, блювання, нудота, набряк губи болю в животі, диспепсія, запор, стоматит; часто – геморой, сухість у роті. Порушення з боку печінки та жовчовивідних шляхів: часто – гепатоцелюлярне пошкодження, гепатит, болючість у ділянці печінки; рідко – жовтяниця; невідомо – печінкова недостатність. Порушення з боку шкіри та підшкірних тканин: дуже часто – еритема, висипання, набряк особи1 алопеція, порушення структури нігтів, долонно-підошовний синдром; часто - акне, сухість шкіри, екхімоз, гіпергідроз, макуло-папульозний висип, свербіж, оніхоклазія, дерматит; нечасто – кропив'янка; невідомо – ангіоневротичний набряк. Порушення з боку кістково-м'язової та сполучної тканини: дуже часто – артралгія, м'язова скутість/міалгія; часто - артрит, біль у спині, оссалгія, спазми м'язів, біль у ділянці шиї, біль у кінцівках. Порушення з боку нирок та сечовивідних шляхів: часто – захворювання нирок; невідомо – мембранозний гломерулонефрит, гломерулонефропатія, ниркова недостатність. Вагітність, післяпологові та перинатальні стани: невідомо олігогідрамніон, фатальна гіпоплазія легень та гіпоплазія та/або порушення функції нирок у плода. Порушення з боку статевих органів та молочної залози: часто – запалення молочної залози/мастит. Загальні розлади та порушення в місці введення: дуже часто – астенія, біль у грудях, озноб, стомлюваність, грипоподібний синдром, інфузійні реакції, біль, гарячка, мукозит, периферичні набряки; часто - нездужання, набряки. Травми, інтоксикації та ускладнення маніпуляцій: часто – забій. + - небажані реакції, які в повідомленнях асоціювалися з летальним кінцем. 1 - небажані реакції, які переважно повідомлялися в асоціації з інфузійними реакціями. Точна відсоткова кількість не встановлена. * - небажані реакції спостерігалися при комбінованій терапії після антрациклінів та у комбінації з таксанами. Нижче представлена інформація щодо окремих небажаних реакцій. Дисфункція серця Застійна серцева недостатність II-IV функціонального класу за NYHA (класифікація Нью-Йоркської Асоціації Кардіологів) є частою небажаною реакцією при застосуванні препарату Герцептин і асоціювалася з фатальним результатом. У пацієнтів, які отримували препарат Герцептин®, спостерігалися такі ознаки та симптоми порушення функції серця: задишка, ортопное, посилення кашлю, набряк легенів, ритм “галопу” або зниження фракції викиду лівого шлуночка. У 3 базових клінічних дослідженнях застосування препарату Герцептин® у комбінації з ад'ювантною хіміотерапією частота серцевої дисфункції 3/4 ступеня (а саме симптоматична застійна серцева недостатність) не відрізнялася від такої у пацієнтів, які отримували лише хіміотерапію (тобто без препарату Герцептин®) і отримували препарат Герцептин®, послідовно після терапії таксанами (0.3-0.4%). Частота була найбільшою у пацієнтів, які отримували Герцептин® спільно з таксанами (2.0%). Досвід використання препарату Герцептин у комбінації з низькодозовими режимами антрациклінів у неоад'ювантній терапії обмежений. При застосуванні препарату Герцептин протягом одного року після завершення ад'ювантної хіміотерапії серцева недостатність III-IV функціонального класу по NYHA спостерігалася у 0.6% пацієнтів при медіані спостереження 12 місяців і у 0.8% пацієнтів при медіані спостереження 8 років. Частота легкої симптоматичної та безсимптомної дисфункції лівого шлуночка склала 4.6%. Тяжка ЗСН була оборотна в 71.4% випадків (оборотність визначалася як мінімум двома послідовними підвищеннями показника ФВЛШ ≥50% після явища). Легка симптоматична та безсимптомна дисфункція лівого шлуночка була оборотна у 79.5% випадків. Приблизно 17% явищ, пов'язаних із дисфункцією серця, виникли після завершення терапії препаратом Герцептин. У базових клінічних дослідженнях при метастатичному РМЗ частота серцевої дисфункції при внутрішньовенному введенні препарату Герцептин у поєднанні з паклітакселом варіювала від 9% до 12% порівняно з 1%-4% для монотерапії паклітакселом. Для монотерапії препаратом Герцептин частота склала 6%-9%. Найбільша частота серцевої дисфункції спостерігалася у пацієнтів, які отримують Герцептин® одночасно з антрациклінами/циклофосфамідом (27%), що значно вище, ніж для терапії антрациклінами/циклофосфамідом (7%-10%). У дослідженні з проспективним моніторингом функції серця частота симптоматичної ЗСН склала 2.2% у пацієнтів, які отримували препарат Герцептин і доцетаксел, порівняно з 0% у пацієнтів, які отримували монотерапію доцетакселом.Більшість пацієнтів (79%) із серцевою дисфункцією спостерігалося поліпшення стану після отримання стандартної терапії ЗСН. Інфузійні реакції та реакції гіперчутливості Підраховано, що близько 40% пацієнтів, які отримують Герцептин, відчувають інфузійні реакції в тій чи іншій формі. Однак більшість інфузійних реакцій є легкими та помірними за ступенем тяжкості (згідно з NCI-CTC) і мають тенденцію виникати на початку лікування, тобто. під час 1,2 та 3-ї інфузії, при наступних введеннях виникають рідше. Реакції включають наступні симптоми: озноб, лихоманка, задишка, артеріальна гіпотензія, хрипи в легенях, бронхоспазм, тахікардія, зниження насичення гемоглобіну киснем, респіраторний дистрес-синдром, висип, нудота, блювання і головний біль. Частота інфузійних реакцій всіх ступенів тяжкості варіює і залежить від показання, методології збору інформації, а також від того, чи Герцептин® вводився спільно з хіміотерапією або застосовувався в монотерапії. Тяжкі анафілактичні реакції, що вимагають негайних додаткових медичних втручань, найчастіше можуть виникати під час першої або другої інфузій препарату Герцептин, такі реакції асоціювалися з летальним результатом. В окремих випадках спостерігалися анафілактоїдні реакції. Гематологічна токсичність Дуже часто виникали фебрильна нейтропенія, лейкопенія, анемія, тромбоцитопенія та нейтропенія. Частота виникнення гіпопротромбінемії невідома. Ризик нейтропенії може бути дещо вищим при застосуванні трастузумабу в комбінації з доцетакселом після терапії препаратами антрациклінового ряду. Порушення з боку легень Із застосуванням препарату Герцептин асоціюються важкі небажані явища з боку легень (у тому числі з фатальним результатом). Дані реакції включають (але не обмежуються): інфільтрати в легенях, гострий респіраторний дистрес-синдром, пневмонію, пневмоніт, плевральний випіт, гострий набряк легень та дихальну недостатність. Перехід з лікарської форми для внутрішньовенного введення препарату Герцептин на лікарську форму для підшкірного введення та навпаки Загалом перехід з лікарської форми для внутрішньовенного введення препарату Герцептин на лікарську форму для підшкірного введення і, навпаки, у пацієнтів з ранніми стадіями HER2-позитивного РМЗ переносився добре. Частота серйозних небажаних явищ, небажаних явищ 3 ступеня тяжкості та припинення терапії через розвиток небажаних явищ до переходу на іншу лікарську форму була низькою.Взаємодія з лікарськими засобамиСпеціальні дослідження лікарських взаємодій препарату Герцептин у людини не проводилися. У клінічних дослідженнях клінічно значимих взаємодій між препаратом Герцептин і одночасно застосовуваними препаратами не відзначалося. У випадках, коли препарат Герцептин застосовувався у комбінації з доцетакселом, карбоплатином або анастрозолом, фармакокінетика вищезгаданих препаратів не змінювалася. Концентрації паклітакселу та доксорубіцину та їх основних метаболітів (6-альфа-гідроксипаклітаксел та доксорубіцинол) не змінюються у присутності трастузумабу. Тим не менш, трастузумаб може підвищити загальну експозицію одного з метаболітів доксорубіцину (7-дезокси-13-дигідродоксорубіцинон). Біологічна активність цього метаболіту та клінічне значення підвищення його експозиції невідомі. У присутності паклітакселу та доксорубіцину змін у концентрації трастузумабу не спостерігалося. Результати вивчення фармакокінетики капецитабіну та цисплатину при використанні в комбінації з трастузумабом або без нього припускають, що експозиція біологічно активних метаболітів капецитабіну (наприклад, фторурацил) не змінювалася при одночасному застосуванні цисплатину або цисплатину та трастузумабу. Однак були зареєстровані більш високі концентрації капецитабіну та триваліший період його напіввиведення при комбінації з трастузумабом. Дані також вказують, що фармакокінетика цисплатину не змінювалася при одночасному застосуванні капецитабіну або капецитабіну у комбінації з трастузумабом. Герцептин® не сумісний із 5% розчином декстрози через можливість агрегації білка. Герцептин® не можна змішувати або розчиняти разом з іншими лікарськими засобами. Ознак несумісності між розчином препарату Герцептин і інфузійними пакетами, виготовленими з полівінілхлориду, поліетилену або поліпропілену, не спостерігалося.Спосіб застосування та дозиТестування на пухлинну експресію HER2 до початку лікування препаратом Герцептин® є обов'язковим. Препарат Герцептин повинен вводитися кваліфікованим медичним персоналом. Препарат призначений для введення як у амбулаторно-поліклінічних, так і в стаціонарних умовах. Перед застосуванням препарату Герцептин® необхідно перевірити етикетку на флаконі та переконатися, що лікарська форма препарату відповідає призначеній пацієнтові ("ліофілізат для приготування концентрату для приготування розчину для інфузій", а не "розчин для підшкірного введення"). Герцептин® у лікарській формі "ліофілізат для приготування концентрату для приготування розчину для інфузій" не призначений для підшкірного введення та повинен застосовуватись лише внутрішньовенно. Перехід із лікарської форми для внутрішньовенного введення на лікарську форму для підшкірного введення та, навпаки, при введенні один раз на 3 тижні вивчався у клінічному дослідженні. Щоб не допустити помилкового введення препарату Кадсила® (трастузумаб емтанзин) замість препарату Герцептин® (трастузумаб), перед приготуванням розчину для інфузії та його введенням пацієнту необхідно перевірити етикетку на флаконі. Герцептин® у лікарській формі "ліофілізат для приготування концентрату для приготування розчину для інфузій" вводять лише внутрішньовенно краплинно! Вводити препарат внутрішньовенно струминно чи болюсно не можна! Увага! Герцептин® не сумісний із 5% розчином декстрози через можливість агрегації білка. Герцептин® не можна змішувати або розводити разом з іншими лікарськими засобами. Розчин препарату Герцептин сумісний з інфузійними пакетами, виготовленими з полівінілхлориду, поліетилену та поліпропілену. Приготування розчину Підготовка препарату до введення має проводитись в асептичних умовах. Інструкція з приготування розчину Вміст флакону з 150 мг препарату Герцептин розчиняють у 7.2 мл стерильної води для ін'єкцій. Під час розчинення слід акуратно поводитися з препаратом. При розчиненні слід уникати надлишкового піноутворення, останнє може утруднити набір потрібної дози з флакона. Стерильним шприцом повільно ввести 7.2 мл стерильної води для ін'єкцій у флакон зі 150 мг препарату Герцептин®, спрямовуючи струмінь рідини прямо на паліофілізат. Для розчинення акуратно похитати флакон обертальними рухами. Не струшувати! При розчиненні препарату часто утворюється невелика кількість піни. Щоб уникнути цього, необхідно дати розчину постояти близько 5 хвилин. Відновлений розчин - прозора або злегка опалесцентна безбарвна або світло-жовтого кольору рідина. Умови зберігання приготовленого розчину Флакон із 150 мг препарату використовується лише одноразово. Розчин препарату Герцептин® фізично та хімічно стабільний протягом 24 годин при температурі 2-8°С після розчинення стерильною водою для ін'єкцій. Чи не заморожувати! Приготування розчину для інфузії слід здійснювати безпосередньо після розчинення ліофілізату. У виняткових випадках розчин після розчинення ліофілізату може зберігатися не більше 24 годин при температурі 2-8°С, якщо розчинення ліофілізату проходило в контрольованих та валідованих асептичних умовах. При цьому за умови зберігання (правила зберігання та тривалість) відповідає спеціаліст, який розчиняє ліофілізат. Інструкція з приготування розчину для інфузії Визначити об'єм розчину: Необхідний для введення навантажувальної дози трастузумабу, що дорівнює 4 мг/кг маси тіла, або підтримуючої дози, що дорівнює 2 мг/кг, визначається за такою формулою: Об'єм (мл) = маса тіла (кг) х доза (4 мг/кг навантажувальна або 2 мг/кг підтримуюча)/21 (мг/мл, концентрація приготовленого розчину) Необхідний для введення навантажувальної дози трастузумабу, що дорівнює 8 мг/кг маси тіла, або підтримуючої дози, що дорівнює 6 мг/кг кожні 3 тижні, визначається за такою формулою: Об'єм (мл) = маса тіла (кг) х доза (8 мг/кг навантажувальна або 6 мг/кг підтримуюча)/ 21 (мг/мл, концентрація приготовленого розчину) З флакона з ліофілізатом, що розчинився, слід набрати відповідний об'єм і ввести його в інфузійний пакет з 250 мл 0.9% розчину натрію хлориду. Потім інфузійний пакет слід обережно перевернути для перемішування розчину, уникаючи піноутворення. Перед введенням розчин слід перевірити (візуально) щодо відсутності механічних домішок і зміни забарвлення. Розчин для інфузій вводять відразу після приготування. У виняткових випадках приготований розчин для інфузії може зберігатися не більше 24 годин при температурі 2-8°С, якщо розчинення ліофілізату та приготування розчину для інфузії відбувалося в контрольованих та валідованих асептичних умовах. При цьому за умови зберігання (правила зберігання та тривалість) відповідає спеціаліст, який готував розчин. Інструкції з утилізації невикористаного препарату або з терміном придатності, що минув. Попадання лікарського засобу у довкілля має бути зведено до мінімуму. Не слід утилізувати препарат за допомогою стічних вод або разом із побутовими відходами. По можливості необхідно використовувати спеціальні системи для утилізації лікарських засобів. Необхідно суворо дотримуватися наступних рекомендацій щодо використання та утилізації шприців та витратних матеріалів: Голки та шприци не можна використовувати повторно. Використані голки та шприци поміщають у захищений від проколів контейнер (ємність). Утилізацію препарату Герцептин і витратних матеріалів слід проводити відповідно до місцевих вимог. Стандартний режим дозування Під час кожного введення трастузумабу необхідно ретельно спостерігати за пацієнтом на предмет появи ознобу, лихоманки та інших інфузійних реакцій (протягом 6 годин після початку першої інфузії та протягом 2 годин після початку подальших інфузій). Слід зменшити швидкість інфузії або на якийсь час припинити введення препарату при розвитку інфузійної реакції. Відновлення інфузії можливе після зникнення симптомів інфузійних реакцій легкого та помірного ступеня тяжкості згідно з NCI-CTC (загальні критерії токсичності Національного інституту раку в США). Слід розглянути питання про припинення подальшої терапії препаратом Герцептин у разі розвитку тяжких або життєзагрозних інфузійних реакцій. Метастатичний рак молочної залози Щотижневе запровадження Доза навантаження: 4 мг/кг маси тіла у вигляді 90-хвилинної внутрішньовенної краплинної інфузії. Підтримуюча доза: 2 мг/кг маси тіла раз на тиждень. Підтримуюча доза вводиться через 1 тиждень після навантаження. Якщо попередня доза навантаження переносилася добре, препарат можна вводити у вигляді 30-хвилинної краплинної інфузії. Альтернативне введення – через 3 тижні Доза навантаження: 8 мг/кг маси тіла у вигляді 90-хвилинної внутрішньовенної краплинної інфузії. Підтримуюча доза: 6 мг/кг маси тіла кожні 3 тижні. Підтримуюча доза вводиться через 3 тижні після навантаження. Якщо попередня доза навантаження переносилася добре, препарат можна вводити у вигляді 30-хвилинної краплинної інфузії. Застосування у комбінації з паклітакселом або доцетакселом Паклітаксел або доцетаксел вводилися наступного дня після введення препарату Герцептин® (рекомендації з дозування див. у відповідних інструкціях з медичного застосування) або відразу після наступного введення препарату Герцептин®, якщо при попередньому введенні Герцептин® переносився добре. Застосування у комбінації з інгібітором ароматази Герцептин® та анастрозол вводилися на день 1. Обмежень за часом введення препарату Герцептин® та анастрозолу не було (рекомендації щодо дозування див. в інструкції з медичного застосування анастрозолу або інших інгібіторів ароматази). Ранні стадії раку молочної залози Щотижневе запровадження При щотижневому введенні Герцептин® вводиться в дозі навантаження 4 мг/кг маси тіла, далі в підтримує 2 мг/кг маси тіла один раз на тиждень. Підтримуюча доза вводиться через 1 тиждень після навантаження. Навантажувальна доза вводиться у вигляді 90-хвилинної внутрішньовенної краплинної інфузії. Якщо попередня доза навантаження переносилася добре, препарат можна вводити у вигляді 30-хвилинної краплинної інфузії. Введення через 3 тижні При введенні через 3 тижні навантаження: 8 мг/кг маси тіла (у вигляді 90-хвилинної внутрішньовенної краплинної інфузії). Підтримуюча доза: 6 мг/кг маси тіла кожні 3 тижні. Підтримуюча доза вводиться через 3 тижні після навантаження. Якщо попередня доза навантаження переносилася добре, препарат можна вводити у вигляді 30-хвилинної краплинної інфузії. Застосування препарату Герцептин при ранніх стадіях раку молочної залози вивчено в комбінації з хіміотерапією згідно зі схемами, описаними нижче. Застосування у комбінації з паклітакселом або доцетакселом після хіміотерапії доксорубіцином та циклофосфамідом Паклітаксел: 80 мг/м2 у вигляді тривалої внутрішньовенної (в/в) інфузії, щотижня, протягом 12 тижнів або 175 мг/м2 у вигляді тривалої внутрішньовенної інфузії, кожні 3 тижні протягом 4 циклів (в день 1 кожного циклу) . Доцетаксел: 100 мг/м2 у вигляді внутрішньовенної інфузії протягом 1 години, кожні 3 тижні, протягом 4 циклів (починаючи на день 2 у циклі 1, далі на день 1 у кожний наступний цикл). Герцептин®: починаючи з першої дози паклітакселу або доцетакселу, Герцептин® вводився згідно з щотижневою схемою під час хіміотерапії (навантажувальна доза 4 мг/кг, далі підтримуючою дозою 2 мг/кг щотижня). Надалі монотерапія препаратом Герцептин® тривала згідно з щотижневою схемою після застосування у комбінації з паклітакселом або згідно з введенням через 3 тижні після застосування у комбінації з доцетакселом. Загальна тривалість терапії препаратом Герцептин від першого введення склала 1 рік, незалежно від кількості отриманих або пропущених доз. Якщо паклітаксел або доцетаксел і препарат Герцептин повинні були вводитися в один день, то паклітаксел або доцетаксел вводився першим. Застосування у комбінації з доцетакселом та карбоплатином Доцетаксел/Карбоплатин (кожні 3 тижні протягом 6 циклів, починаючи з дня 2 першого циклу, далі на день 1 у кожний наступний цикл): доцетаксел у дозі 75 мг/м2 у вигляді внутрішньовенної інфузії протягом 1 год, за яким слідував карбоплатин у дозі для досягнення цільової AUC - 6 мг/мл/хв у вигляді внутрішньовенної інфузії протягом 30-60 хв. Герцептін®: Герцептин® разом з хіміотерапією вводився згідно з щотижневою схемою (навантажувальна доза 4 мг/кг, далі підтримуючою дозою 2 мг/кг щотижня). Після хіміотерапії монотерапія препаратом Герцептин ® тривала згідно з введенням через 3 тижні. Загальна тривалість терапії препаратом Герцептин від першого введення склала 1 рік, незалежно від кількості отриманих або пропущених доз. Якщо доцетаксел, карбоплатин і препарат Герцептин повинні були вводитися в один день, то першим вводився доцетаксел, за яким слідував карбоплатин, далі Герцептин. Неоад'ювантна-ад'ювантна терапія Герцептин® вводився згідно з режимом кожні 3 тижні у комбінації з неоад'ювантною хіміотерапією (10 циклів): Доксорубіцин 60 мг/м2 та паклітаксел 150 мг/м2, кожні 3 тижні, протягом 3 циклів; далі паклітаксел 175 мг/м2, кожні 3 тижні протягом 4 циклів. Далі циклофосфамід, метотрексат та фторурацил у день 1 та 8. кожні 4 тижні, протягом 3 циклів. Після проведення оперативного втручання ад'ювантна монотерапія препаратом Герцептин ® тривала згідно з режимом кожні 3 тижні. Загальна тривалість терапії препаратом Герцептин склала 1 рік. Поширений рак шлунка Введення через 3 тижні Доза навантаження: 8 мг/кг маси тіла у вигляді 90-хвилинної внутрішньовенної краплинної інфузії. Підтримуюча доза: 6 мг/кг маси тіла кожні 3 тижні. Підтримуюча доза вводиться через 3 тижні після навантаження. Якщо попередня доза навантаження переносилася добре, препарат можна вводити у вигляді 30-хвилинної краплинної інфузії. Метастатичний та ранні стадії РМЗ та поширений рак шлунка Тривалість терапії Лікування препаратом Герцептин у пацієнтів з метастатичним РМЗ або поширеним раком шлунка проводиться до прогресування захворювання або розвитку неприйнятної токсичності. Пацієнти з ранніми стадіями РМЗ повинні отримувати терапію препаратом Герцептин протягом 1 року або до рецидиву захворювання або розвитку неприйнятної токсичності (залежно від того, що відбудеться швидше). Лікування препаратом Герцептин® пацієнтів із ранніми стадіями РМЗ понад один рік не рекомендується. Пропуск у плановому введенні Якщо пропуск у плановому введенні трастузумабу становив 7 днів або менше, слід якнайшвидше ввести препарат у звичайній підтримуючій дозі (тижневий режим: 2 мг/кг маси тіла; режим кожні 3 тижні: 6 мг/кг маси тіла), не чекаючи наступного планового введення. Далі вводити препарат у підтримуючій дозі через 7 днів або 21 день відповідно до щотижневого режиму або режиму кожні 3 тижні відповідно. Якщо перерва у введенні препарату склала більше 7 днів, необхідно якнайшвидше знову ввести навантажувальну дозу трастузумабу (щотижневий режим: 4 мг/кг маси тіла; режим кожні 3 тижні: 8 мг/кг маси тіла), у вигляді 90-хвилинної внутрішньовенної краплинної інфузії. Потім продовжити введення препарату у підтримуючій дозі через 7 днів або 21 день відповідно до щотижневого режиму або режиму кожні 3 тижні відповідно. Корекція дози У період виникнення оборотної мієлосупресії, спричиненої хіміотерапією, курс терапії препаратом Герцептин® може бути продовжений після зниження дози хіміотерапії або тимчасової її відміни (згідно з відповідними рекомендаціями в інструкціях з застосування паклітакселу, доцетакселу або інгібіторного аромату). При зниженні фракції викиду лівого шлуночка (ФВЛШ. %) на ≥10 одиниць від вихідної І нижче значення 50% лікування має бути припинено. Повторна оцінка ФВЛШ має бути проведена приблизно через 3 тижні. За відсутності поліпшення показника ФВЛШ або його подальшого зниження або при появі симптомів застійної серцевої недостатності (ЗСН) необхідно розглянути питання про припинення лікування препаратом Герцептин®, якщо тільки користь для конкретного пацієнта не перевищує ризику. Усі ці пацієнти повинні бути направлені до кардіолога для проведення обстеження та перебувати під наглядом. Особливі вказівки з дозування Пацієнти похилого віку Зниження дози препарату Герцептин у пацієнтів ≥65 років не потрібне. Пацієнти з нирковою недостатністю Зміна дози препарату Герцептин у пацієнтів з легким та середнім ступенем порушення функції нирок не потрібна. У зв'язку з обмеженими даними дати рекомендації з дозування препарату у пацієнтів з тяжким ступенем порушення функції нирок неможливо. Пацієнти з печінковою недостатністю У зв'язку з відсутністю даних дати рекомендації з дозування препарату у пацієнтів з порушенням функції печінки неможливо.ПередозуванняУ клінічних дослідженнях випадків передозування не спостерігалося. Введення препарату Герцептин у разових дозах більше 10 мг/кг не вивчалося. Препарат Герцептин у дозах ≤10 мг/кг переносився добре.Запобіжні заходи та особливі вказівкиУ медичній документації хворого слід зазначати торгове найменування та номер серії препарату. Інформація, представлена в даній інструкції, стосується виключно препарату Герцептин®. Терапія препаратом Герцептин повинна призначатися тільки лікарем, який має досвід лікування онкологічних захворювань. Введення препарату проводиться за наявності доступу до набору для екстреної допомоги. Лікар, який має досвід застосування хіміотерапевтичних препаратів, повинен бути доступний у процесі терапії. HER2 тестування має бути проведено у спеціалізованій лабораторії, яка може забезпечити контроль якості процедури тестування. Герцептин® повинен використовуватися у пацієнтів з метастатичним РМЗ або ранніми стадіями РМЗ тільки за наявності пухлинної гіперекспресії HER2, визначеної методом імуно-гістохімічної реакції (ІГХ), або ампліфікації гена HER2, визначеної методом гібридизації in situ (FISH або CISH). Слід використовувати точні та валідовані методи визначення. Герцептин® повинен використовуватися у пацієнтів з метастатичним раком шлунка лише за наявності пухлинної гіперекспресії HER2, визначеної методом ІГХ як ІГХ2+ та підтвердженої результатами S1SH або FISH, або ІГХЗ+. Слід використовувати точні та валідовані методи визначення. В даний час відсутні дані з клінічних досліджень про пацієнтів, які отримували Герцептин повторно після застосування в ад'ювантній терапії. Дисфункція серця загальні вказівки Пацієнти, які отримують Герцептин як монотерапію або в комбінації з паклітакселом або доцетакселом, особливо після хіміотерапії, що включає антрацикліни (доксорубіцин або епірубіцин), мають підвищений ризик розвитку застійної серцевої недостатності (ЗСН) (II-IV функціональний клас по NYHA) або безсимптомних порушень. функції серця. Тяжкість цих явищ може варіювати від середнього до тяжкого ступеня. Ці явища можуть призвести до смерті. Крім цього, необхідно бути обережними при лікуванні пацієнтів з високим серцево-судинним ризиком, наприклад, у пацієнтів похилого віку, з артеріальною гіпертензією, документально підтвердженою ішемічною хворобою серця, застійною серцевою недостатністю, фракцією викиду лівого шлуночка (ФВЛШ) Моніторування може дозволити виявити пацієнтів з порушеннями функції серця. Вихідне кардіологічне обстеження має повторюватися кожні 3 місяці під час терапії та кожні 6 місяців після її закінчення протягом 24 місяців з моменту введення останньої дози препарату. До початку лікування препаратом Герцептин® необхідно ретельно зіставити можливу користь та ризик його застосування. За даними, отриманими в результаті популяційного фармакокінетичного моделювання, препарат Герцептин може перебувати в крові до 7 місяців після завершення терапії. У пацієнтів, які отримують антрацикліни після завершення лікування препаратом Герцептин®, можливе підвищення ризику дисфункції серця. По можливості, лікарі повинні уникати призначення хіміотерапії на основі антрациклінів протягом 7 місяців після завершення терапії препаратом Герцептин®. При застосуванні препаратів антрациклінового ряду слід проводити ретельний моніторинг функції серця. Слід оцінити необхідність проведення стандартного кардіологічного обстеження у пацієнтів із підозрою на серцево-судинні захворювання. У всіх пацієнтів слід моніторувати функцію серця під час лікування (наприклад, кожні 12 тижнів). Внаслідок моніторингу можна виявити пацієнтів, у яких розвинулися порушення функції серця. У пацієнтів з безсимптомним порушенням функції серця може бути корисним часте проведення моніторингу (наприклад, кожні 6-8 тижнів). При тривалому погіршенні функції лівого шлуночка, що не виявляється симптоматично, доцільно розглянути питання про відміну препарату, за винятком випадків, коли лікар вважає, що користь для конкретного пацієнта перевершує ризик. Безпечність продовження або відновлення терапії препаратом Герцептин у пацієнтів, у яких розвинулося порушення функції серця, не вивчалася. При зниженні фракції викиду лівого шлуночка (ФВЛШ, %) на >10 одиниць від вихідної І нижче значення 50% лікування має бути припинено. Повторна оцінка ФВЛШ має бути проведена приблизно через 3 тижні. За відсутності поліпшення показника ФВЛШ або його подальшого зниження або при появі симптомів застійної серцевої недостатності (ЗСН) необхідно розглянути питання про припинення лікування препаратом Герцептин®, якщо тільки користь для конкретного пацієнта не перевищує ризику. Усі ці пацієнти повинні бути направлені до кардіолога для проведення обстеження та перебувати під наглядом. Якщо на фоні терапії препаратом Герцептин розвивається симптоматична серцева недостатність, необхідно провести відповідну стандартну медикаментозну терапію ЗСН. У більшості пацієнтів з ЗСН або безсимптомною дисфункцією серця в базових дослідженнях спостерігалося поліпшення стану на тлі стандартної медикаментозної терапії ЗСН: інгібітори ангіотензинперетворюючого ферменту або блокатори рецепторів ангіотензину та бета-адреноблокатори. За наявності клінічної користі від застосування препарату Герцептин більшість пацієнтів з побічними реакціями з боку серця продовжили терапію без прояву додаткових клінічно значущих реакцій з боку серця. Метастатичний рак молочної залози Не рекомендується застосовувати препарат Герцептин разом у комбінації з антрациклінами для лікування метастатичного раку молочної залози. Ризик розвитку дисфункції серця у пацієнтів з метастатичним раком молочної залози підвищений при попередній терапії антрациклінами, проте він нижчий порівняно з таким при одночасному застосуванні антрациклінів та препарату Герцептин. Ранні стадії раку молочної залози Пацієнтам з ранніми стадіями раку молочної залози слід проводити кардіологічне обстеження перед початком лікування кожні 3 місяці під час терапії та кожні 6 місяців після її закінчення протягом 24 місяців з моменту введення останньої дози препарату. Рекомендується більш тривалий моніторинг після лікування препаратом Герцептин у комбінації з антрациклінами з частотою обстежень 1 раз на рік протягом 5 років з моменту введення останньої дози Герцептин або далі, якщо спостерігається постійне зниження ФВЛШ. Лікування препаратом Герцептин1* не рекомендується пацієнтам на ранніх стадіях РМЗ (ад'ювантна та неоад'ювантна терапія) з: інфарктом міокарда в анамнезі; стенокардією, яка потребує лікування: ЗСН (II-IV функціональний клас за NYHA) в анамнезі або в даний час; ФВЛШ нижче за 55%; іншими кардіоміопатіями; аритміями, що вимагають лікування: клінічно значущими вадами серця; погано контрольована артеріальна гіпертензія, за винятком артеріальної гіпертензії, що піддається стандартній медикаментозній терапії; гемодинамічно значущим перикардіальним випотом, оскільки ефективність та безпека застосування препарату у таких пацієнтів не вивчені. Ад'ювантна терапія Не рекомендується застосовувати препарат Герцептин разом у комбінації з антрациклінами у складі ад'ювантної терапії. У пацієнтів із ранніми стадіями РМЗ. отримували Герцептин після хіміотерапії на основі антрациклінів, спостерігалося підвищення частоти симптоматичних і безсимптомних небажаних явищ з боку серця в порівнянні з такими, що отримували хіміотерапію доцетакселом і карбоплатином (режими, що не містять препарати антрациклінового ряду). При цьому різниця була більша у випадках спільного застосування препарату Герцептин і таксанів. ніж за послідовного використання. Незалежно від режиму, що використовувався, більшість симптоматичних кардіальних явищ виникало в перші 18 місяців лікування. В одному з 3 проведених базових досліджень (з медіаною періоду наступного спостереження 5.5 років) спостерігалося тривале збільшення кумулятивної частоти симптоматичних кардіальних явищ або явищ, пов'язаних зі зниженням ФВЛШ: у 2.37% пацієнтів,отримували Герцептин® спільно з таксанами після терапії антрациклінами, порівняно з 1% пацієнтів у групах порівняння (у групі терапії антрациклінами та циклофосфамідом, далі таксанами, та у групі терапії таксанами, карбоплатином та препаратом Герцептин®). Ідентифікованими факторами ризику розвитку небажаних явищ з боку серця при ад'ювантній терапії препаратом Герцептин® є вік >50 років, низька вихідна ФВЛШ (25 кг/м2). Неоад'ювантна-ад'ювантна терапія Для пацієнтів із ранніми стадіями РМЗ. яким може бути призначена неоад'ювантна-ад'ювантна терапія, застосування препарату Герцептин® спільно з антрациклінами рекомендовано тільки у випадку, якщо вони раніше не отримували хіміотерапію і тільки при використанні низькодозових режимів терапії антрациклінами (максимальна сумарна доза доксорубіцину 180 мг/2 ). У пацієнтів, які отримали повний курс низькодозових антрациклінів та Герцептин у складі неоад'ювантної терапії, не рекомендується проведення додаткової цитотоксичної хіміотерапії після проведення хірургічного втручання. У всіх інших випадках рішення щодо необхідності додаткової цитотоксичної хіміотерапії приймається на підставі індивідуальних факторів. Досвід застосування трастузумабу разом із низькодозовими режимами терапії антрациклінами обмежений двома дослідженнями. При застосуванні препарату Герцептин у лікарській формі для внутрішньовенного введення спільно з неоад'ювантною хіміотерапією, що включала три цикли доксорубіцину (сумарна доза 180 мг/м2), у клінічному дослідженні частота симптоматичного порушення функції серця склала 1.7%. При застосуванні препарату Герцептин у лікарській формі для внутрішньовенного введення спільно з неоад'ювантною хіміотерапією, що включала 4 цикли епірубіцину (сумарна доза 300 мг/м2), у клінічному дослідженні частота розвитку серцевої недостатності/застійної серцевої недостатності склала 0.3% при медіані спостереження. Клінічний досвід застосування у пацієнтів віком від 65 років обмежений. Інфузійні реакції та реакції гіперчутливості При введенні препарату Герцептин виникали серйозні інфузійні реакції: задишка, артеріальна гіпотензія, хрипи в легенях, артеріальна гіпертензія, бронхоспазм, суправентрикулярна тахіаритмія, зниження насичення гемоглобіну киснем, анафілаксія, респіраторний дистрес Для зниження ризику виникнення цих явищ можна використовувати премедикація. Більшість цих реакцій виникала під час інфузії або протягом 2,5 годин від початку першого введення. При виникненні інфузійної реакції слід зменшити швидкість інфузії або на якийсь час припинити введення препарату і ретельно спостерігати за пацієнтом до усунення всіх симптомів. Для усунення цих симптомів можливе застосування анальгетиків/антипіретиків. таких як парацетамол, або антигістамінних препаратів, таких як дифенгідрамін.Більшість пацієнтів після розв'язання симптомів інфузійних реакцій змогли продовжити терапію препаратом Герцептин. Ефективна терапія серйозних реакцій полягає у застосуванні бета-адреностимуляторів, глюкокортикостероїдів, інгаляції кисню. У разі розвитку тяжких або життєзагрозних інфузійних реакцій слід розглянути питання щодо припинення подальшої терапії препаратом Герцептин. У поодиноких випадках дані реакції асоціювалися з фатальним результатом. Ризик розвитку летальних інфузійних реакцій вищий у пацієнтів із задишкою у спокої, спричиненою метастазами у легені або супутніми захворюваннями, тому таким пацієнтам не слід проводити терапію препаратом Герцептин®. Повідомлялися випадки, у яких після початкового поліпшення спостерігалося погіршення стану, і навіть випадки з відстроченим стрімким погіршенням стану. Летальний результат виникав протягом години або одного тижня після інфузії. У окремих випадках у пацієнтів з'являлися симптоми інфузійних реакцій або легеневі симптоми (через більш ніж 6 годин після початку введення препарату Герцептин®). Слід попередити пацієнтів про можливий відстрочений розвиток цих симптомів і про необхідність негайного контакту з лікарем у разі їх виникнення. Порушення з боку легень При застосуванні препарату Герцептин у реєстраційному періоді реєструвалися важкі явища з боку легень, які іноді супроводжувалися летальним результатом. Крім того, спостерігалися випадки інтерстиціальної хвороби легень (ІБЛ), включаючи легеневі інфільтрати, гострий респіраторний дистрес-синдром, пневмонію, пневмоніт, плевральний випіт, гострий набряк легень та дихальну недостатність. Фактори ризику, асоційовані з ІХЛ, включають: раніше проведену або супутню терапію іншими протипухлинними препаратами, які, як відомо, пов'язані з ІХЛ (таксани, гемцитабін, винорельбін та променева терапія). Дані явища можуть бути як прояви інфузійних реакцій, і відстрочено. Ризик тяжких реакцій з боку легень вищий у пацієнтів із метастатичним ураженням легень, супутніми захворюваннями, що супроводжуються задишкою у спокої.Тому такі пацієнти не повинні отримувати препарат Герцептін. Слід бути обережними, особливо у пацієнтів, які отримують супутню терапію таксанами, через розвиток пневмоніту. Стерильна вода для ін'єкцій, що використовується для розчинення вмісту флакону з 150 мг препарату Герцептин, не містить бензилового спирту. Вплив на здатність до керування автотранспортом та управління механізмами Дослідження щодо вивчення впливу препарату на здатність керувати автомобілем та працювати з механізмами не проводилися. У разі виникнення симптомів інфузійних реакцій пацієнтам не слід керувати автомобілем або працювати з механізмами до вирішення симптомів.Умови відпустки з аптекЗа рецептомВідео на цю тему