Санофи
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
Форма випуску: крем для зовнішнього застосування Упаковка: туба Виробник: Санофі Завод-производитель: КонтрактФарма ГмбХ и Ко. КГ(Германия) Действующее вещество: Нонивамид + Никобоксил. .
Дозування: 250 мг Фасування: N20 Форма выпуска: таб. покрытые пленочной оболочкой Упаковка: уп. контурн.
Дозування: 500 мг Фасування: N10 Форма выпуска: суппозитории вагинальные Упаковка: упак. Производитель: Санофи Завод-производитель: Haupt Pharma Livron(Франция) Действующее вещество: Метронидазол. .
220,00 грн
174,00 грн
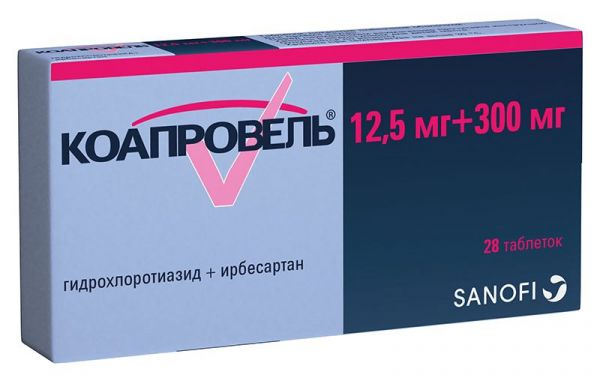
Склад, форма випуску та упаковкаТаблетки - 1 табл. активні речовини: гідрохлортіазид – 25/100 мг; допоміжні речовини: стеарат магнію; тальк; желатин; крохмаль кукурудзяний; лактози моногідрат. У блістері 20 шт.; в картонній коробці 1 блістер.Опис лікарської формиБілі або майже білі круглі плоскі пігулки з гравіюванням "Н" на одній стороні та ризиком - на іншій.Фармакотерапевтична групаДіуретичний засіб.ФармакокінетикаГідрохлортіазид неповно, проте досить швидко всмоктується із ШКТ. Ця дія зберігається протягом 6-12 годин. Після прийому внутрішньо дози в 100 мг C max у плазмі крові досягається через 1,5-2,5 год. На максимумі діуретичної активності (приблизно через 4 години після прийому) концентрація гідрохлортіазиду в плазмі становить 2 мкг/мл. Зв'язування з білками плазми становить 40%. Виводиться, в основному, через нирки (фільтрація та секреція) у незміненій формі. T 1/2 для пацієнтів з нормальною нирковою функцією становить 6,4 год, для пацієнтів з помірною нирковою недостатністю – 11,5 год, а для пацієнтів з Cl креатиніну менше 30 мл/хв – 20,7 год. Гідрохлортіазид проникає через плацентарний бар'єр та екскретується у грудне молоко.ФармакодинамікаПервинним механізмом дії тіазидних діуретиків є підвищення діурезу шляхом блокування реабсорбції іонів натрію та хлору на початку ниркових канальців. Цим вони підвищують екскрецію натрію та хлору і, отже, води. Екскреція інших електролітів, а саме калію та магнію, також збільшується. У максимальних терапевтичних дозах натрійуретичний/діуретичний ефект усіх тіазидів приблизно однаковий. Натрійурез і діурез наступають протягом 2 годин і досягають свого максимуму приблизно через 4 години. Вони також зменшують активність карбоангідрази шляхом посилення виведення іона бікарбонату, але ця дія зазвичай проявляється слабо і не впливає на рН сечі. Гідрохлортіазид має також гіпотензивні властивості. На нормальний АТ тіазидні діуретики не впливають.Показання до застосуванняартеріальна гіпертензія (як для монотерапії, так і у комбінації з іншими антигіпертензивними препаратами); набряковий синдром різного генезу (хронічна серцева недостатність, нефротичний синдром, синдром передменструальної напруги, гострий гломерулонефрит, хронічна ниркова недостатність, портальна гіпертензія, лікування кортикостероїдами); контроль поліурії, переважно при нефрогенному нецукровому діабеті; профілактика каменеутворення у сечовивідних шляхах у схильних пацієнтів (зменшення гіперкальціурії).Протипоказання до застосуванняанурія; ниркова недостатність тяжкого ступеня (КК<30 мл/хв); печінкова недостатність тяжкого ступеня; важкоконтрольований цукровий діабет; хвороба Аддісона; рефрактерна гіпокаліємія, гіпонатріємія, гіперкальціємія; дитячий вік до 3 років (для жорсткої лікарської форми); - підвищена чутливість до компонентів препарату; підвищена чутливість до похідних сульфонамідів З обережністю слід застосовувати препарат при гіпокаліємії, гіпонатріємії, гіперкальціємії, ІХС, цирозі печінки, подагрі, непереносимості лактози, серцевих глікозидах, а також у пацієнтів похилого віку.Вагітність та лактаціяПротипоказано застосування препарату у І триместрі вагітності. У ІІ та ІІІ третьому триместрах вагітності застосування препарату можливе лише в тому випадку, коли передбачувана користь для матері перевершує потенційний ризик для плода. Гідрохлортіазид проникає крізь плацентарний бар'єр. Існує небезпека жовтяниці плода або новонароджених, тромбоцитопенії та інших наслідків. Препарат виділяється із грудним молоком. За необхідності застосування препарату в період лактації слід вирішити питання про припинення грудного вигодовування. Протипоказання: дитячий вік до 3 років (для жорсткої лікарської форми).Побічна діяПорушення електролітного балансу Гіпокаліємія, гіпомагніємія, гіперкальціємія та гіпохлоремічний алкалоз: сухість у роті, спрага, нерегулярний ритм серця, зміни в настрої або психіці, судоми та біль у м'язах, нудота, блювання, незвичайна втома або слабкість. Гіпохлоремічний алкалоз може викликати печінкову енцефалопатію або печінкову кому. Гіпонатріємія: сплутаність свідомості, конвульсії, летаргія, уповільнення процесу мислення, втома, збудливість, м'язові судоми. Метаболічні явища: гіперглікемія, глюкозурія, гіперурикемія із розвитком нападу подагри. Лікування тіазидами може знижувати толерантність до глюкози, і цукровий діабет, що латентно протікає, може маніфестувати. При застосуванні високих доз можуть збільшуватися рівні ліпідів у сироватці крові. З боку шлунково-кишкового тракту: холецистит або панкреатит, холестатична жовтяниця, діарея, сіаладеніт, запор, анорексія. Серцево-судинна система: аритмії, ортостатична гіпотензія, васкуліт. З боку нервової системи та органів чуття: запаморочення, розпливчасте зір (тимчасово), головний біль, парестезії. З боку органів кровотворення: дуже рідко – лейкопенія, агранулоцитоз, тромбоцитопенія, гемолітична анемія, апластична анемія. Реакції підвищеної чутливості: кропив'янка, пурпура, некротичний васкуліт, синдром Стівенса-Джонсона, респіраторний дистрес-синдром (включаючи пневмоніт та некардіогенний набряк легені), фоточутливість, анафілактичні реакції аж до шоку. Інші явища: зниження потенції, порушення ниркової функції, інтерстиціальний нефрит.Взаємодія з лікарськими засобамиСлід уникати одночасного застосування препарату із солями літію (нирковий кліренс літію знижується, збільшується його токсичність). З обережністю застосовувати з такими препаратами: антигіпертензивними препаратами (потенціюється їх дія, може виникнути потреба у корекції дози); серцевими глікозидами (гіпокаліємія та гіпомагніємія, пов'язані з дією тіазидних діуретиків, можуть посилювати токсичність наперстянки); аміодароном (його застосування одночасно з тіазидними діуретиками може вести до підвищення ризику аритмій, пов'язаних із гіпокаліємією); гіпоглікемічними засобами для вживання (знижується їх ефективність, може розвиватися гіперглікемія); кортикостероїдними препаратами, кальцитоніном (збільшують рівень виведення калію); НПЗЗ (можуть послаблювати діуретичну та гіпотензивну дію тіазидів); недеполяризуючими міорелаксантами (їхній ефект може посилюватися); амантадином (кліренс амантадину може знижуватися гідрохлортіазидом, що призводить до збільшення концентрації амантадину в плазмі та можливої токсичності); колестираміном, який зменшує абсорбцію гідрохлортіазиду; етанолом, барбітуратами та наркотичними анальгетиками, які посилюють ефект ортостатичної гіпотензії. Вплив препарату на дані лабораторних аналізів Тіазиди можуть знижувати рівень у плазмі йоду, пов'язаного з білками. Перед проведенням аналізів функції паращитовидних залоз тіазиди слід відмінити. Концентрація білірубіну в сироватці може бути підвищена.Спосіб застосування та дозиДозу слід підбирати індивідуально. При постійному контролі встановлюється мінімально ефективна доза. Препарат слід приймати внутрішньо після їди. Дорослим При артеріальній гіпертензії початкова доза становить 25-50 мг на добу одноразово, у вигляді монотерапії або комбінації з іншими антигіпертензивними засобами. Деяким пацієнтам достатньо початкової дози 12.5 мг (як у вигляді монотерапії, так і в комбінації). Необхідно застосовувати мінімально ефективну дозу, що не перевищує 100 мг на добу. При комбінуванні Гіпотіазиду з іншими антигіпертензивними препаратами може виникнути необхідність зниження дози іншого препарату для запобігання надмірному зниженню артеріального тиску. Гіпотензивна дія проявляється протягом 3-4 днів, але для досягнення оптимального ефекту може знадобитися 3-4 тижні. Після закінчення терапії гіпотензивний ефект зберігається протягом 1 тижня. При набряковому синдромі різного генезу початкова доза становить 25-100 мг на добу одноразово або 1 раз на 2 дні. Залежно від клінічної реакції доза може бути знижена до 25-50 мг на добу одноразово або 1 раз на 2 дні. У деяких тяжких випадках на початку лікування може знадобитися збільшення дози препарату до 200 мг на добу. При синдромі передменструальної напруги препарат призначають у дозі 25 мг на добу та застосовують від початку прояву симптомів до початку менструації. При нефрогенному нецукровому діабеті рекомендується звичайна добова доза препарату 50-150 мг (у кілька прийомів). У зв'язку з посиленою втратою іонів калію та магнію в процесі лікування (рівень калію в сироватці може бути <3.0 ммоль/л) виникає потреба у заміщенні калію та магнію. Дітям Дози слід встановлювати, виходячи із маси тіла дитини. Звичайні добові педіатричні дози: 1-2 мг/кг маси тіла або 30-60 мг/м 2 поверхні тіла 1 раз/сут. Добова доза в дітей віком із 3 до 12 років становить по 37.5-100 мг.ПередозуванняНайбільш помітним проявом передозування гідрохлортіазиду є гостра втрата рідини та електролітів, що виражається в наступних ознаках та симптомах: Серцево-судинні: тахікардія, зниження артеріального тиску, шок. Нейром'язові: слабкість, сплутаність свідомості, запаморочення та спазми литкових м'язів, парестезія, порушення свідомості, втома. Шлунково-кишкові: нудота, блювання, спрага. Ниркові: поліурія, олігурія або анурія (через гемоконцентрацію). Лабораторні показники: гіпокаліємія, гіпонатріємія, гіпохлоремія, алкалоз, підвищений рівень азоту сечовини у крові (особливо у хворих на ниркову недостатність). Лікування: специфічного антидоту при передозуванні гідрохлортіазиду немає. Індукція блювання, промивання шлунка може бути способами виведення препарату. Абсорбцію препарату можна зменшити призначенням активованого вугілля. У разі зниження АТ або шоку слід відшкодувати ОЦК та електроліти (калій, натрій). Слід слідкувати за водно-електролітним балансом (особливо рівнем калію у сироватці) та функцією нирок до встановлення нормальних значень.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
211,00 грн
165,00 грн
Склад, форма випуску та упаковкаТаблетки - 1 табл. активні речовини: гідрохлортіазид – 25/100 мг; допоміжні речовини: стеарат магнію; тальк; желатин; крохмаль кукурудзяний; лактози моногідрат. У блістері 20 шт.; в картонній коробці 1 блістер.Опис лікарської формиБілі або майже білі круглі плоскі пігулки з гравіюванням "Н" на одній стороні та ризиком - на іншій.Фармакотерапевтична групаДіуретичний засіб.ФармакокінетикаГідрохлортіазид неповно, проте досить швидко всмоктується із ШКТ. Ця дія зберігається протягом 6-12 годин. Після прийому внутрішньо дози в 100 мг C max у плазмі крові досягається через 1,5-2,5 год. На максимумі діуретичної активності (приблизно через 4 години після прийому) концентрація гідрохлортіазиду в плазмі становить 2 мкг/мл. Зв'язування з білками плазми становить 40%. Виводиться, в основному, через нирки (фільтрація та секреція) у незміненій формі. T 1/2 для пацієнтів з нормальною нирковою функцією становить 6,4 год, для пацієнтів з помірною нирковою недостатністю – 11,5 год, а для пацієнтів з Cl креатиніну менше 30 мл/хв – 20,7 год. Гідрохлортіазид проникає через плацентарний бар'єр та екскретується у грудне молоко.ФармакодинамікаПервинним механізмом дії тіазидних діуретиків є підвищення діурезу шляхом блокування реабсорбції іонів натрію та хлору на початку ниркових канальців. Цим вони підвищують екскрецію натрію та хлору і, отже, води. Екскреція інших електролітів, а саме калію та магнію, також збільшується. У максимальних терапевтичних дозах натрійуретичний/діуретичний ефект усіх тіазидів приблизно однаковий. Натрійурез і діурез наступають протягом 2 годин і досягають свого максимуму приблизно через 4 години. Вони також зменшують активність карбоангідрази шляхом посилення виведення іона бікарбонату, але ця дія зазвичай проявляється слабо і не впливає на рН сечі. Гідрохлортіазид має також гіпотензивні властивості. На нормальний АТ тіазидні діуретики не впливають.Показання до застосуванняартеріальна гіпертензія (як для монотерапії, так і у комбінації з іншими антигіпертензивними препаратами); набряковий синдром різного генезу (хронічна серцева недостатність, нефротичний синдром, синдром передменструальної напруги, гострий гломерулонефрит, хронічна ниркова недостатність, портальна гіпертензія, лікування кортикостероїдами); контроль поліурії, переважно при нефрогенному нецукровому діабеті; профілактика каменеутворення у сечовивідних шляхах у схильних пацієнтів (зменшення гіперкальціурії).Протипоказання до застосуванняанурія; ниркова недостатність тяжкого ступеня (КК<30 мл/хв); печінкова недостатність тяжкого ступеня; важкоконтрольований цукровий діабет; хвороба Аддісона; рефрактерна гіпокаліємія, гіпонатріємія, гіперкальціємія; дитячий вік до 3 років (для жорсткої лікарської форми); - підвищена чутливість до компонентів препарату; підвищена чутливість до похідних сульфонамідів З обережністю слід застосовувати препарат при гіпокаліємії, гіпонатріємії, гіперкальціємії, ІХС, цирозі печінки, подагрі, непереносимості лактози, серцевих глікозидах, а також у пацієнтів похилого віку.Вагітність та лактаціяПротипоказано застосування препарату у І триместрі вагітності. У ІІ та ІІІ третьому триместрах вагітності застосування препарату можливе лише в тому випадку, коли передбачувана користь для матері перевершує потенційний ризик для плода. Гідрохлортіазид проникає крізь плацентарний бар'єр. Існує небезпека жовтяниці плода або новонароджених, тромбоцитопенії та інших наслідків. Препарат виділяється із грудним молоком. За необхідності застосування препарату в період лактації слід вирішити питання про припинення грудного вигодовування. Протипоказання: дитячий вік до 3 років (для жорсткої лікарської форми).Побічна діяПорушення електролітного балансу Гіпокаліємія, гіпомагніємія, гіперкальціємія та гіпохлоремічний алкалоз: сухість у роті, спрага, нерегулярний ритм серця, зміни в настрої або психіці, судоми та біль у м'язах, нудота, блювання, незвичайна втома або слабкість. Гіпохлоремічний алкалоз може викликати печінкову енцефалопатію або печінкову кому. Гіпонатріємія: сплутаність свідомості, конвульсії, летаргія, уповільнення процесу мислення, втома, збудливість, м'язові судоми. Метаболічні явища: гіперглікемія, глюкозурія, гіперурикемія із розвитком нападу подагри. Лікування тіазидами може знижувати толерантність до глюкози, і цукровий діабет, що латентно протікає, може маніфестувати. При застосуванні високих доз можуть збільшуватися рівні ліпідів у сироватці крові. З боку шлунково-кишкового тракту: холецистит або панкреатит, холестатична жовтяниця, діарея, сіаладеніт, запор, анорексія. Серцево-судинна система: аритмії, ортостатична гіпотензія, васкуліт. З боку нервової системи та органів чуття: запаморочення, розпливчасте зір (тимчасово), головний біль, парестезії. З боку органів кровотворення: дуже рідко – лейкопенія, агранулоцитоз, тромбоцитопенія, гемолітична анемія, апластична анемія. Реакції підвищеної чутливості: кропив'янка, пурпура, некротичний васкуліт, синдром Стівенса-Джонсона, респіраторний дистрес-синдром (включаючи пневмоніт та некардіогенний набряк легені), фоточутливість, анафілактичні реакції аж до шоку. Інші явища: зниження потенції, порушення ниркової функції, інтерстиціальний нефрит.Взаємодія з лікарськими засобамиСлід уникати одночасного застосування препарату із солями літію (нирковий кліренс літію знижується, збільшується його токсичність). З обережністю застосовувати з такими препаратами: антигіпертензивними препаратами (потенціюється їх дія, може виникнути потреба у корекції дози); серцевими глікозидами (гіпокаліємія та гіпомагніємія, пов'язані з дією тіазидних діуретиків, можуть посилювати токсичність наперстянки); аміодароном (його застосування одночасно з тіазидними діуретиками може вести до підвищення ризику аритмій, пов'язаних із гіпокаліємією); гіпоглікемічними засобами для вживання (знижується їх ефективність, може розвиватися гіперглікемія); кортикостероїдними препаратами, кальцитоніном (збільшують рівень виведення калію); НПЗЗ (можуть послаблювати діуретичну та гіпотензивну дію тіазидів); недеполяризуючими міорелаксантами (їхній ефект може посилюватися); амантадином (кліренс амантадину може знижуватися гідрохлортіазидом, що призводить до збільшення концентрації амантадину в плазмі та можливої токсичності); колестираміном, який зменшує абсорбцію гідрохлортіазиду; етанолом, барбітуратами та наркотичними анальгетиками, які посилюють ефект ортостатичної гіпотензії. Вплив препарату на дані лабораторних аналізів Тіазиди можуть знижувати рівень у плазмі йоду, пов'язаного з білками. Перед проведенням аналізів функції паращитовидних залоз тіазиди слід відмінити. Концентрація білірубіну в сироватці може бути підвищена.Спосіб застосування та дозиДозу слід підбирати індивідуально. При постійному контролі встановлюється мінімально ефективна доза. Препарат слід приймати внутрішньо після їди. Дорослим При артеріальній гіпертензії початкова доза становить 25-50 мг на добу одноразово, у вигляді монотерапії або комбінації з іншими антигіпертензивними засобами. Деяким пацієнтам достатньо початкової дози 12.5 мг (як у вигляді монотерапії, так і в комбінації). Необхідно застосовувати мінімально ефективну дозу, що не перевищує 100 мг на добу. При комбінуванні Гіпотіазиду з іншими антигіпертензивними препаратами може виникнути необхідність зниження дози іншого препарату для запобігання надмірному зниженню артеріального тиску. Гіпотензивна дія проявляється протягом 3-4 днів, але для досягнення оптимального ефекту може знадобитися 3-4 тижні. Після закінчення терапії гіпотензивний ефект зберігається протягом 1 тижня. При набряковому синдромі різного генезу початкова доза становить 25-100 мг на добу одноразово або 1 раз на 2 дні. Залежно від клінічної реакції доза може бути знижена до 25-50 мг на добу одноразово або 1 раз на 2 дні. У деяких тяжких випадках на початку лікування може знадобитися збільшення дози препарату до 200 мг на добу. При синдромі передменструального напруження препарат призначають у дозі 25 мг на добу та застосовують від початку прояву симптомів до початку менструації. При нефрогенному нецукровому діабеті рекомендується звичайна добова доза препарату 50-150 мг (у кілька прийомів). У зв'язку з посиленою втратою іонів калію та магнію в процесі лікування (рівень калію в сироватці може бути <3.0 ммоль/л) виникає потреба у заміщенні калію та магнію. Дітям Дози слід встановлювати, виходячи із маси тіла дитини. Звичайні добові педіатричні дози: 1-2 мг/кг маси тіла або 30-60 мг/м 2 поверхні тіла 1 раз/сут. Добова доза в дітей віком із 3 до 12 років становить по 37.5-100 мг.ПередозуванняНайбільш помітним проявом передозування гідрохлортіазиду є гостра втрата рідини та електролітів, що виражається в наступних ознаках та симптомах: Серцево-судинні: тахікардія, зниження артеріального тиску, шок. Нейром'язові: слабкість, сплутаність свідомості, запаморочення та спазми литкових м'язів, парестезія, порушення свідомості, втома. Шлунково-кишкові: нудота, блювання, спрага. Ниркові: поліурія, олігурія або анурія (через гемоконцентрацію). Лабораторні показники: гіпокаліємія, гіпонатріємія, гіпохлоремія, алкалоз, підвищений рівень азоту сечовини у крові (особливо у хворих на ниркову недостатність). Лікування: специфічного антидоту при передозуванні гідрохлортіазиду немає. Індукція блювання, промивання шлунка може бути способами виведення препарату. Абсорбцію препарату можна зменшити призначенням активованого вугілля. У разі зниження АТ або шоку слід відшкодувати ОЦК та електроліти (калій, натрій). Слід слідкувати за водно-електролітним балансом (особливо рівнем калію у сироватці) та функцією нирок до встановлення нормальних значень.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
25 115,00 грн
327,00 грн
Склад, форма випуску та упаковкаЛіофілізат - 1 фл. Активна речовина: лінограстим 33.6 млн. МО (263 мкг). Допоміжні речовини: манітол (D-манітол), полісорбат 20, аргінін (L-аргінін), фенілаланін (L-фенілаланін), метіонін (L-метіонін), хлористоводнева кислота. Розчинник: вода д/і – 1 мл. Флакони безбарвного скла (5) у комплекті з розчинником (амп. 5 шт.) – упаковки контурні пластикові (1) – пачки картонні.Опис лікарської формиЛіофілізат для приготування розчину для внутрішньовенного та підшкірного введення білого кольору.Фармакотерапевтична групаРекомбінантний людський глікозильований гранулоцитарний колонієстимулюючий фактор (Г-КСФ) відноситься до групи цитокінів, біологічно активних протеїнів, що регулюють диференціювання та проліферацію клітин. Г-КСФ є фактором, що стимулює клітини-попередники нейтрофілів кісткового мозку. Граноцит® 34 викликає помітне збільшення кількості нейтрофілів у периферичній крові, яка є дозозалежною в інтервалі доз 1-10 мкг/кг/добу. Повторне введення препарату в рекомендованих дозах викликає додаткове збільшення вмісту нейтрофілів у крові. Нейтрофіли, що продукуються у відповідь на введення Граноциту 34, мають нормальні хемотаксичні властивості та фагоцитарну активність. Г-КСФ здатний стимулювати проліферацію ендотеліальних клітин людини. Застосування Граноциту 34, як після хіміотерапії, так і незалежно від неї, призводить до мобілізації (виходу) у периферичну кров клітин-попередників гемопоезу, які можуть бути виділені з крові та введені внутрішньовенно хворому після високодозної хіміотерапії з метою відновлення пошкодженого кровотворення замість трансплантації. кісткового мозку або на додаток до неї. Показано, що введення хворому на аутологічні клітини-попередники гемопоезу з периферичної крові, отриманих за допомогою стимуляції Граноцитом 34, сприяє більш швидкому відновленню кровотворення порівняно з аутотрансплантацією кісткового мозку, що також суттєво зменшує тривалість тромбоцитопенії.ФармакокінетикаФармакокінетичні показники Граноциту 34 залежать від дози препарату та тривалості його введення. Існує пряма залежність між дозою та плазмовою концентрацією ленограстиму та між нейтрофільною відповіддю та концентрацією ленограстиму в плазмі. Всмоктування При повторному введенні (в/в та п/к) C max пропорційна введеній дозі; кумуляції препарату не виявлено. При використанні дози, що рекомендуються, абсолютна біодоступність препарату становить 30%. Розподіл Середній час утримання в організмі при підшкірному введенні становить 7 год. Метаболізм Лінограстим біотрансформується до пептидів. Виведення T1/2 при підшкірному введенні становить 3-4 год, при внутрішньовенному повторному - 1-1.5 год. З сечею у незміненому вигляді виводиться менше 1% від введеної дози.Клінічна фармакологіяСтимулятор лейкопоезу.Показання до застосуванняДля скорочення періоду нейтропенії та пов'язаних з нею ускладнень (у хворих з немієлопроліферативними новоутвореннями, яким проводилася мієлосупресивна терапія з подальшою трансплантацією кісткового мозку, та у тих, хто перебуває у групі підвищеного ризику розвитку тривалої вираженої нейтропенії); для зменшення тривалості вираженої нейтропенії та пов'язаних з нею ускладнень після стандартної мієлосупресивної хіміотерапії; для мобілізації периферичних клітин-попередників гемопоезу у периферичній крові.Протипоказання до застосуванняМієлоїдні новоутворення (за винятком первинно виявленого гострого мієлобластного лейкозу); вперше виявлений гострий мієлобластний лейкоз у хворих віком до 55 років за наявності сприятливих цитогенетичних прогностичних ознак; вагітність; період лактації (грудного вигодовування); підвищена чутливість до ленограстиму або до інших компонентів препарату.Вагітність та лактаціяПротипоказане застосування Граноциту 34 при вагітності. При необхідності застосування препарату у період лактації грудне вигодовування слід припинити. Застосування у дітей Встановлено безпеку та ефективність застосування препарату Граноцит® 34 при пересадці кісткового мозку у дітей віком від 2 років.Побічна діяПри застосуванні Граноциту 34 у здорових осіб найпоширенішими побічними ефектами були головний біль у 30%, біль у кістках у 23%, біль у попереку у 17.5%, астенія у 11%, біль у животі у 6% випадків. Ризик виникнення болю був вищим у осіб, що мають високі значення кількості лейкоцитів у крові, особливо, якщо кількість лейкоцитів перевищувала 50 000/мкл (відзначалося у 24% донорів), і пов'язана з аферезом тромбоцитопенії (кількість тромбоцитів менше 100 000/м 42% донорів. Минуще підвищення рівня АСТ та/або АЛТ спостерігалося у 12%, а минуще підвищення рівня ЛФ - у 16% донорів. Побічні ефекти, що спостерігаються при трансплантації кісткового мозку, такі як інфекційно-запальні ураження порожнини рота, лихоманка, діарея, біль у животі, блювання, висипання, алопеція, сепсис та інфекції, пов'язані з режимами кондиціонування, а не з прийомом Граноцита 3 на частоту появи та вираженість гострої та хронічної реакції "трансплантат-против-господаря" достовірно не визначено. Особливу увагу при трансплантації кісткового мозку слід приділяти контролю над кількістю тромбоцитів у периферичної крові, т.к. їх рівень при застосуванні препарату може бути нижчим, ніж зазвичай. При застосуванні Граноциту 34 при нейтропенії, спричиненій хіміотерапією, зазвичай спостерігаються побічні ефекти, характерні для прийому цитостатиків. Дещо частіше відзначалися біль у кістках та реакції у місці ін'єкцій (гіперемія, набряклість). Зрідка повідомлялося про появу інфільтратів у легенях, які у кількох випадках призвели до розвитку легеневої недостатності або дистрес-синдрому у дорослих. З появою на тлі застосування Граноциту 34 таких симптомів, як кашель, лихоманка, задишка, у поєднанні з рентгенологічними змінами та порушеннями дихальної функції слід призначити відповідну терапію та розглянути питання про припинення введення Граноциту 34. У дуже поодиноких випадках відзначалися різні алергічні реакції, дуже рідко з розвитком анафілактичного шоку. Вкрай рідко відзначалися випадки васкуліту, вузлуватої еритеми, піодермії, синдром Лайєлла. Загальні, але здебільшого безсимптомні випадки збільшення селезінки та дуже рідкісні випадки розриву селезінки були відмічені у здорових донорів або у пацієнтів після введення ГКСФ.Взаємодія з лікарськими засобамиМожлива взаємодія препарату Граноцит® 34 з іншими факторами, що стимулюють кровотворення, та цитокінами дотепер у клінічних дослідженнях не вивчалися.Спосіб застосування та дозиПрепарат вводять підшкірно або внутрішньовенно краплинно протягом 30 хв. При пересадці кісткового мозку, при стандартній хіміотерапії цитотоксичними засобами та для мобілізації клітин-попередників гемопоезу в периферичній крові після застосування цитостатиків препарат призначають у дозі 150 мкг (19.2 млн.МЕ)/м2 поверхні тіла/добу, що еквівалентно 5 м. МЕ)/кг маси тіла/сут. Введення препарату починають наступного дня після трансплантації кісткового мозку або закінчення хіміотерапії. Препарат вводять щодня підшкірно (при трансплантації кісткового мозку можна вводити у вигляді 30-хвилинної внутрішньовенної інфузії) доти, доки після настання очікуваного зниження рівня лейкоцитів їх кількість не відновиться до нормального показника, при досягненні якого препарат може бути відмінений. Максимальна тривалість щоденного введення препарату становить 28 днів. Для проведення мобілізації клітин-попередників гемопоезу в периферичній крові без застосування цитостатиків рекомендована доза препарату становить 10 мкг (1.28 млн.МЕ)/кг маси тіла/добу, щоденно підшкірно протягом 4-6 днів. Лейкаферез слід проводити після відновлення кількості лейкоцитів або після визначення у крові CD34+-клітин за допомогою загальноприйнятих методик. У пацієнтів, які не отримували раніше масивної хіміотерапії, часто достатньо проведення одного лейкаферезу для отримання мінімально необхідної кількості клітин (≥ 2×10 6 CD34+-клітин/кг маси тіла). У здорових донорів застосування препарату п/к протягом 5-6 днів у дозі 10 мкг (1.28 млн.МЕ)/кг маси тіла дозволяло отримати ≥3×106 CD34+-клітин/кг маси тіла в результаті одного лейкаферезу у 83% випадків та в результаті двох лейкаферезів у 97% випадків. Спеціальних досліджень в осіб похилого віку не проводилось. У зв'язку з цим рекомендацій щодо зміни режиму дозування у пацієнтів похилого віку немає. Встановлено безпеку та ефективність застосування препарату Граноцит® 34 при пересадці кісткового мозку у дітей віком від 2 років. Правила приготування розчину для ін'єкцій Для приготування розчину для підшкірного введення вміст флакона розчиняють в 1 мл розчинника, що додається, обережно перемішуючи (сильно не струшувати) близько 5 секунд. Для внутрішньовенного застосування отриманий розчин слід додатково розбавити 0.9% розчином натрію хлориду або 5% розчином декстрози до концентрації не менше ніж 0.32 млн. МО/мл (2.5 мкг/мл), але не більше ніж у 100 мл перерахованих вище розчинів. Відновлений розчин слід зберігати при температурі від 2°С до 8°С протягом 24 годин. Приготовлений розчин слід використовувати якнайшвидше.ПередозуванняЕфекти, що виникають при передозуванні препарату Граноцит 34, не вивчені.Запобіжні заходи та особливі вказівкиЛікування Граноцитом 34 повинно проводитись під наглядом лікаря, який має досвід застосування цитостатичної терапії. Г-КСФ здатний посилювати ріст мієлоїдних пухлинних клітин in vitro, подібна дія in vitro може виявлятися і на деякі пухлинні клітини немієлоїдного ряду. Не встановлена ефективність та безпека Граноциту 34 при мієлодиспластичному синдромі, вторинному гострому мієлобластному лейкозі або хронічному мієлолейкозі. Тому пацієнтам з вищезгаданою патологією Граноцит® 34 не слід призначати. Особлива увага потрібна при діагностуванні гострого мієлобластного лейкозу. Цей діагноз має бути чітко диференційований від бластного кризу хронічного мієлолейкозу. Вплив Граноциту 34 на прогресування мієлодиспластичного синдрому та трансформацію його в мієлолейкоз не було встановлено. Граноцит® 34 слід застосовувати з особливою обережністю при всіх передпухлинних ураженнях мієлоїдного паростка кісткового мозку. Т.к. деякі пухлини можуть, як виняток, мати Г-КСФ-рецептор, слід бути обережним у разі несподіваного рецидиву пухлини під час лікування людським Г-КСФ. При введенні препарату в дозі 5 мкг/кг/добу (0.64 млн. МЕ/кг/добу) при трансплантації кісткового мозку, в жодному разі кількість лейкоцитів не перевищувала 50 000/мкл. Менш ніж у 5% випадків при застосуванні препарату Граноцит® 34 у дозі 5 мкг/кг/добу (0.64 млн.МЕ/кг/добу) та цитотоксичній хіміотерапії число лейкоцитів дорівнювало або перевищувало 70 000/мкл. При цьому жодних побічних реакцій, безпосередньо пов'язаних із лейкоцитозом, не спостерігалося. У зв'язку з потенційним ризиком, пов'язаним із появою вираженого лейкоцитозу, під час лікування Граноцитом 34 слід регулярно контролювати кількість лейкоцитів у крові. Якщо кількість лейкоцитів досягає 50000/мкл, застосування Граноциту 34 має бути негайно припинено. Під час застосування Граноциту 34 для мобілізації клітин-попередників гемопоезу в периферичній крові препарат не повинен вводитись у разі підвищення кількості лейкоцитів понад 70 000/мкл. Особлива увага при трансплантації кісткового мозку має приділятись контролю кількості тромбоцитів у периферичній крові, т.к. їх рівень при застосуванні Граноциту 34 може бути нижчим, ніж зазвичай. Граноцит® 34 не слід застосовувати з метою зменшення встановлених інтервалів між курсами хіміотерапії та/або з метою збільшення доз хіміопрепаратів, т.я. Граноцит ® 34 зменшує тільки мієлотоксичність та не впливає на іншу побічну дію цитостатиків. У зв'язку з підвищеною чутливістю мієлоїдних клітин, що швидко діляться, до цитотоксичної хіміотерапії застосування Граноциту 34 не рекомендується пізніше ніж за 24 години до і раніше ніж через 24 години після закінчення хіміотерапії. Мобілізація клітин-попередників гемопоезу в периферичній крові при застосуванні Граноциту 34 після хіміотерапії порівняно із застосуванням лише одного Граноциту 34 вище. Однак вибір між обома методами мобілізації слід проводити індивідуально для кожного пацієнта з урахуванням усіх цілей лікування. У пацієнтів, яким була проведена масивна мієлосупресивна терапія та/або променева терапія, мобілізація клітин-попередників гемопоезу в периферичній крові може бути недостатньою для отримання мінімально необхідної кількості клітин і, отже, відновлення кровотворення може бути неадекватним. У пацієнтів зі значним зниженням кількості стовбурових клітин у кістковому мозку (внаслідок попередньої інтенсивної променевої або хіміотерапії) нейтрофільна відповідь іноді може бути знижена, безпека застосування препарату Граноцит® 34 у таких випадках не встановлена. Програма трансплантації клітин-попередників гемопоезу повинна плануватися на ранніх етапах курсового лікування пацієнтів, і особливу увагу слід привертати до кількості мобілізованих клітин-попередників гемопоезу в периферичній крові перед застосуванням хіміотерапії у високих дозах. Якщо кількість отриманих клітин невелика, трансплантація клітин-попередників гемопоезу має бути замінена іншими методами лікування. Т.к. результати аналізів визначення CD34+-клеток, проведених методом проточної цитометрії, у різних лабораторіях різняться, особливу увагу слід приділяти методам кількісного визначення отриманих клітин-попередників. На підставі опублікованих даних, для адекватного відновлення кровотворення рекомендовано досягнення мінімально необхідної кількості CD34+-клітин >2.0×106 кг маси тіла. Оскільки мобілізація клітин у периферичній крові не несе прямої вигоди для здорових донорів, ця процедура повинна проводитись відповідно до правил трансплантації кісткового мозку, встановлених законодавством. Ефективність та безпека препарату Граноцит® 34 у групі донорів віком від 60 років не оцінювалася. У зв'язку з цим у цієї вікової групи донорів застосовувати препарат для забору клітин-попередників гемопоезу не рекомендується. Також не варто проводити процедуру мобілізації клітин-попередників гемопоезу в осіб, молодших 18 років. Процедуру мобілізації клітин-попередників гемопоезу слід проводити лише у донорів, у яких результати клінічних та лабораторних досліджень підходять для донорства кісткового мозку. Лейкаферез не слід проводити донорам, які приймають антикоагулянти або мають порушення гемостазу. Якщо потрібно проведення більше одного лейкаферезу, то особливу увагу слід звернути на тих донорів, у яких кількість тромбоцитів перед проведенням лейкаферезу була 100 000/мкл. В цілому лейкаферез не слід проводити за показником числа тромбоцитів <75 000/мкл. По можливості слід уникати установки центрального венозного катетера. За даними довготривалого спостереження (тривалість до 6 років) за донорами був виявлено якихось серйозних ускладнень. Незважаючи на це, можливий ризик стимуляції злоякісних клонів мієлоїдних клітин. У зв'язку з цим рекомендується вести систематичне спостереження за цими особами із веденням відповідної документації у центрах з проведення лейкаферезу. Трансплантація алогенних клітин-попередників гемопоезу, мобілізованих Граноцитом 34, може супроводжуватися підвищеним ризиком розвитку хронічної реакції "трансплантат проти господаря". Дані довгострокового спостереження функціонуванням трансплантата нечисленні. До цього часу не вивчена ефективність та безпека застосування Граноциту 34 у пацієнтів з тяжкими порушеннями функції печінки та нирок. У людей застосування препарату в дозі до 40 мкг/кг/добу не супроводжувалося появою токсичних побічних ефектів, за винятком болів у кістках та м'язах. Припинення лікування Граноцитом 34 зазвичай призводить до 50% зниження кількості нейтрофілів у периферичній крові протягом 1-2 днів, потім цей показник повертається до норми протягом 1-7 днів. Збільшення кількості лейкоцитів на п'ятий день лікування до 50 000/мкл спостерігається у кожного третього хворого, який отримував Граноцит® 34 у максимальній дозі 40 мкг/кг/добу (5.12 млн. МО/кг/добу). Після введення Г-КСФ здоровим донорам або пацієнтам були відмічені випадки збільшення селезінки, в основному безсимптомні, і вкрай рідко випадки її розриву, у зв'язку з чим рекомендується ретельно контролювати розміри селезінки (фізикальний огляд, УЗД). При появі болю у верхній лівій половині черевної порожнини та під лопаткою слід виключити можливість розриву селезінки.Умови відпустки з аптекЗа рецептомВідео на цю тему
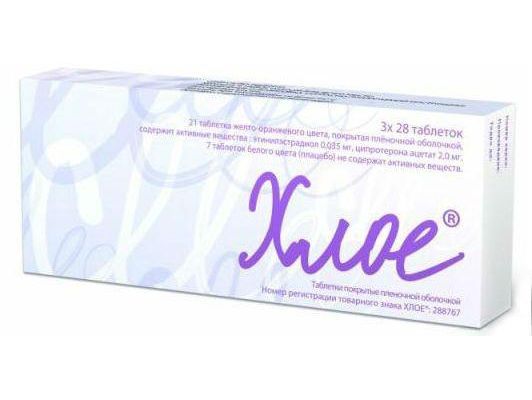
Склад, форма випуску та упаковкаТаблетки, покриті плівковою оболонкою, жовто-жовтогарячого кольору - 1 табл. Активні речовини: ціпротерону ацетат - 2 мг; етинілестрадіол - 35 мкг; допоміжні речовини: лактози моногідрат; повідон; карбоксиметилкрохмаль натрію (тип А); кремнію діоксид колоїдний безводний; алюмінію оксид колоїдний; магнію стеарат оболонка: барвник Opadry II Yellow OY-L-32901 (лактози моногідрат, гіпромелоза 2910, титану діоксид, макрогол 4000, заліза оксид жовтий, заліза оксид чорний, заліза оксид червоний, вода очищена). Таблетки-плацебо білого кольору допоміжні речовини: лактози моногідрат; повідон; карбоксиметилкрохмаль натрію (тип А); кремнію діоксид колоїдний безводний; алюмінію оксид колоїдний; магнію стеарат у блістері 28 шт. (21 шт. – жовто-оранжевого кольору та 7 шт. – білого кольору). У пачці картонної 1 або 3 блістери.Опис лікарської формиТаблетки, покриті плівковою оболонкою: жовто-оранжевого кольору, круглі, двоопуклі. Таблетки-плацебо: білого кольору, круглі, двоопуклі.Фармакотерапевтична групаКомбінований низькодозований монофазний пероральний контрацептивний препарат з антиандрогенною активністю.ФармакокінетикаЦипротерону ацетат Всмоктування. Після прийому ХЛОЕ® ципротерону ацетат повністю абсорбується із шлунково-кишкового тракту. Після прийому внутрішньо 1 табл. ХЛОЕ Cmax становить 15 нг/мл і досягається через 1,6 год. Біодоступність становить 88%. Розподіл. Ципротерону ацетат практично повністю зв'язується з альбуміном плазми, приблизно 3,5-4% знаходиться у вільному стані. Оскільки зв'язування з білками є неспецифічним, зміни рівня глобуліну, що зв'язує статеві стероїди (ГСПС), не впливають на фармакокінетику ципротерону ацетату. З грудним молоком виділяється до 0,2 % дози ципротерону ацетату. Метаболізм та виведення. Фармакокінетика ципротерону ацетату двофазна, T1/2 становить 0,8 год і 2,3 діб відповідно для першої та другої фази. Загальний плазмовий кліренс становить 3,6 мл/хв/кг. Біотрансформується шляхом гідроксилювання та кон'югування, основний метаболіт - 15b-гідроксильне похідне. Виводиться переважно у вигляді метаболітів нирками та через кишечник у співвідношенні 1:2, невелика частина – у незміненому вигляді через кишечник. T1/2 для метаболітів ципротерону ацетату становить 1,8 діб. Етинілестрадіол Всмоктування. Після прийому ХЛОЕ® етинілестрадіол швидко та повністю абсорбується із ШКТ. У процесі всмоктування та першого проходження через печінку етинілестрадіол піддається інтенсивному метаболізму, що зумовлює біодоступність, рівну приблизно 45%, та її значну індивідуальну варіабельність. Після прийому внутрішньо 1 табл., покритою плівковою оболонкою ХЛОЕ Cmax становить приблизно 80 пг/мл і досягається через 1,7 год. Розподіл. Зв'язок з білками (альбуміном) плазми крові високий (2% знаходяться у плазмі у вільному вигляді). З грудним молоком виділяється до 0,02% дози етинілестрадіолу. Етинілестрадіол збільшує печінковий синтез ГСПС та кортикостероїдзв'язуючого глобуліну (КСГ) під час безперервного прийому. На фоні лікування ХЛОЕ® концентрація ГСПС у сироватці підвищується приблизно від 100 до 300 нмоль/л, і сироваткова концентрація КСГ збільшується приблизно з 50 до 95 мкг/мл. Метаболізм та виведення. Фармакокінетика етинілестрадіолу двофазна, з T1/2 1-2 і приблизно 20 год відповідно. Плазмовий кліренс – близько 5 мл/хв/кг. Етинілестрадіол виводиться з організму у вигляді метаболітів; близько 40% – нирками, 60% – через кишечник.ФармакодинамікаМеханізм дії обумовлений антиандрогенним препаратом стероїдної будови (ципротероном ацетатом), що входять до його складу, і пероральним естрогеном (етинілестрадіолом). Ципротерону ацетат Має здатність конкурентно зв'язуватися з рецепторами природних андрогенів (в т.ч. тестостерон, дигідроепіандростерон, андростендіон), що утворюються в невеликих кількостях в організмі жінок, головним чином надниркових залоз, яєчників і шкіри. Блокуючи рецептори андрогенів в органах-мішенях, зменшує явища андрогенізації у жінок (за рахунок порушення процесів, що опосередковуються гормон-рецепторними комплексами на рівні основних внутрішньоклітинних механізмів). Таким чином, стає можливим лікування захворювань, зумовлених підвищеним утворенням андрогенів або специфічною чутливістю до цих гормонів. На тлі прийому препарату знижується посилена діяльність сальних залоз, що відіграє важливу роль у виникненні вугрів та себореї. Через 3-4 міс терапії наявний висип зазвичай зникає. Надмірна жирність волосся та шкіри зникає ще раніше. Також зменшується випадання волосся, що часто супроводжує себорею. Терапія Хлоє у жінок репродуктивного віку зменшує клінічні прояви легких форм гірсутизму; проте ефект від лікування слід очікувати лише після кількох місяців застосування. Поряд з антиандрогенними властивостями ципротерону ацетат має гестагенну активність, що імітує властивості гормону жовтого тіла. Пригнічує секрецію гіпофізом гонадотропних гормонів та гальмує овуляцію, що зумовлює контрацептивний ефект. Етинілестрадіол Підсилює центральні та периферичні впливи ципротерону ацетату на овуляцію, зберігає високу в'язкість шийкового слизу, ускладнюючи проникнення сперматозоїдів у порожнину матки та сприяючи забезпеченню надійного контрацептивного ефекту. На тлі прийому препарату цикл стає регулярнішим, рідше спостерігаються хворобливі менструації, зменшується інтенсивність кровотечі, знижується ризик залізодефіцитної анемії.Показання до застосуванняАндрогензалежні захворювання у жінок: вугри, особливо їх виражені форми, що супроводжуються себореєю, запальними явищами з утворенням вузлів (папульозно-пустульозні, вузликово-кістозні); андрогенна алопеція; легкі форми гірсутизму; контрацепція у жінок із явищами андрогенізації.Протипоказання до застосування- підвищена чутливість до компонентів препарату; одночасне застосування з іншим гормональним контрацептивом; тромбози (венозні та артеріальні) або тромбоемболії в даний час або в анамнезі (в т.ч. тромбоз глибоких вен, тромбоемболія легеневої артерії, інфаркт міокарда, цереброваскулярні порушення, наприклад, інсульт); стани, що передують тромбозу (в т.ч. стенокардія, транзиторні ішемічні атаки); множинні або виражені фактори ризику венозного або артеріального тромбозу (в т.ч. ускладнені пороки клапанного апарату серця, фібриляція передсердь, захворювання судин головного мозку або коронарних артерій; неконтрольована артеріальна гіпертензія, тяжка дисліпопротеїнемія, кінцівках, нейрохірургічні операції, великі травми, куріння старше 35 років, ожиріння з індексом маси тіла більше 30 кг/м2); виявлена спадкова або набута схильність до венозного або артеріального тромбозу, наприклад резистентність до активованого протеїну С (АПС), дефіцит антитромбіну III, дефіцит протеїну С, дефіцит протеїну S, гіпергомоцистеїнемія та наявність антифосфоліпідних антитіл (антикардилян); тяжкі захворювання печінки в даний час або в анамнезі або виражені порушення функції печінки – не раніше ніж через 6 місяців після нормалізації показників функції печінки; пухлини печінки (доброякісні та злоякісні); гормонозалежні злоякісні пухлини чи підозра на них, у т.ч. пухлини молочної залози або статевих органів (в т.ч. в анамнезі); кровотечі із піхви неясної етіології; панкреатит із вираженою гіпертригліцеридемією (в т.ч. в анамнезі); наявність в анамнезі мігрені, що супроводжувалася осередковою неврологічною симптоматикою; період грудного вигодовування; вроджені гіпербілірубінемії (синдроми Жільбера, Дубіна-Джонсона та Ротора); вік старше 40 років; гіперпролактинемія непереносимість лактози, дефіцит лактази, глюкозо-галактозна мальабсорбція; вагітність чи підозра на неї. Якщо будь-які з цих станів розвиваються вперше на фоні прийому ХЛОЕ®, препарат повинен бути негайно скасований. Препарат ХЛОЕ не призначений для застосування у чоловіків. З обережністю: епілепсія, депресія, виразковий коліт, захворювання печінки та жовчного міхура, міома матки, мастопатія, хорея, тетанія, порфірія, розсіяний склероз, варикозне розширення вен, туберкульоз, захворювання нирок, підлітковий вік (без регулярних овуляторів. серповидно-клітинна анемія, ідіопатична жовтяниця або свербіж під час попередньої вагітності, отосклероз із погіршенням слуху під час попередньої вагітності.Вагітність та лактаціяПротипоказано застосування препарату при вагітності, підозрі на вагітність та у період грудного вигодовування.Побічна діяЗ боку ендокринної системи: рідко – нагрубання, болючість, збільшення та виділення з молочних залоз, підвищення маси тіла. З боку статевої системи: рідко міжменструальні кровотечі, зміни піхвового секрету, зміна лібідо. З боку центральної нервової системи: рідко – головний біль, мігрень, зниження настрою. З боку травної системи: рідко – нудота, блювання, гастралгія. Інші: дуже рідко – погана переносимість контактних лінз, набряк повік, порушення зору, кон'юнктивіт, зниження слуху, алергічні реакції, тромбофлебіт, тромбоемболія, генералізований свербіж, жовтяниця, поява пігментних плям на обличчі (хлоазму). Перелічені побічні ефекти можуть розвиватися протягом перших кількох місяців застосування препарату і зазвичай зменшуються з часом.Взаємодія з лікарськими засобамиПри одночасному застосуванні Хлое® з індукторами мікросомальних печінкових ферментів (гідантоїнами, барбітуратами, примідоном, карбамазепіном та рифампіцином; а також, можливо, з окскарбазепіном, топіраматом, фелбаматом та гризеофульвіном); надійність контрацепції. При одночасному застосуванні з ампіциліном, рифампіцином та тетрациклінами контрацептивна надійність Хлоє® знижується.Спосіб застосування та дозиВсередину, не розжовуючи та запиваючи невеликою кількістю рідини, по 1 табл. на добу. Прийом препарату рекомендується проводити в один і той же час, переважно після сніданку або вечері. Прийом Хлоє® починають у 1-й день циклу, використовуючи таблетку відповідного дня тижня із календарної упаковки. Щоденний прийом препарату здійснюють, використовуючи таблетки з календарної упаковки послідовно, у напрямку нанесеної на фольгу стрілки, доки не будуть прийняті всі таблетки. Після закінчення прийому всіх таблеток жовто-оранжевого кольору з календарної упаковки необхідно в наступні 7 днів приймати таблетки білого кольору, що залишилися. Протягом останніх 7 днів лікувального циклу (28 днів) має виникнути менструальноподібна кровотеча (внаслідок скасування лікування). Менструація зазвичай починається через 2-3 дні після 21-го дня циклу лікування препаратом. Наступну упаковку слід розпочинати наступного дня після повністю завершеного прийому таблеток з попередньої упаковки, незалежно від факту продовження/припинення кровотечі. При переході з комбінованих пероральних контрацептивів застосування Хлое® слід починати наступного дня після прийому останньої таблетки з активними компонентами попереднього препарату, але в жодному разі не пізніше наступного дня після звичайної 7-денної перерви у прийомі (для препаратів, що містять 21 табл.) . Далі за описаною вище схемою. Якщо пацієнтка приймала попередній контрацептив щодня протягом 28 днів,застосування Хлоє® слід розпочати після прийому останньої неактивної таблетки. При переході з контрацептивів, що містять тільки гестагени (міні-пілі), Хлое® можна почати застосовувати без перерви. При використанні ін'єкційних форм контрацептивів Хлое® слід застосовувати з дня, коли має бути зроблена наступна ін'єкція. При переході з імплантату Хлоє слід застосовувати вже в день його видалення. У всіх випадках необхідно використовувати додатково бар'єрний метод контрацепції протягом перших 7 днів застосування препарату. Після аборту в І триместрі вагітності жінка може розпочати застосування Хлої негайно. В цьому випадку немає потреби у додаткових методах контрацепції. Після пологів або аборту у II триместрі вагітності застосування препарату слід розпочинати на 21-28-й день. Якщо прийом розпочато пізніше, необхідно використовувати додатково бар'єрний метод контрацепції протягом перших 7 днів застосування препарату.Якщо жінка жила статевим життям у період між пологами або абортом та початком застосування препарату, слід перш за все виключити вагітність або необхідно дочекатися першої менструації. Пропущену таблетку слід прийняти якнайшвидше, наступну таблетку — у звичайний час. При запізненні12 год надійність контрацепції може бути знижена. Якщо запізнення в прийомі таблеток склало >12 год (інтервал з моменту прийому останньої таблетки >36 год) під час 1-3-го тижня прийому препарату, жінці слід прийняти останню пропущену таблетку якнайшвидше, навіть якщо це означає прийом двох таблеток одночасно. Наступну таблетку слід прийняти у звичайний час. Додатково під час 1-2 тижнів прийому необхідно використовувати бар'єрний метод контрацепції протягом наступних 7 днів. Прийом таблетки з нової упаковки слід розпочати після закінчення поточної упаковки без перерви. Ймовірно, кровотечі відміни не буде до кінця другої упаковки,але можливі кров'янисті виділення, що мажуть, або проривна маткова кровотеча в дні прийому таблеток. Якщо у жінки було блювання в межах від 3 до 4 годин після прийому препарату, всмоктування активних речовин може бути неповним. І тут необхідно орієнтуватися на рекомендації при пропуску таблетки. Щоб відстрочити дату початку менструації, жінці слід продовжити прийом таблеток із нової упаковки препарату одразу після того, як прийнято всі таблетки з попередньої, без перерви. Таблетки з нової упаковки можуть прийматися так довго, як бажає жінка (доки упаковка не закінчиться). На тлі прийому препарату з другої упаковки у жінки можуть відзначатися мажучі виділення або проривні маткові кровотечі.І тут необхідно орієнтуватися на рекомендації при пропуску таблетки. Щоб відстрочити дату початку менструації, жінці слід продовжити прийом таблеток із нової упаковки препарату одразу після того, як прийнято всі таблетки з попередньої, без перерви. Таблетки з нової упаковки можуть прийматися так довго, як бажає жінка (доки упаковка не закінчиться). На тлі прийому препарату з другої упаковки у жінки можуть відзначатися мажучі виділення або проривні маткові кровотечі.І тут необхідно орієнтуватися на рекомендації при пропуску таблетки. Щоб відстрочити дату початку менструації, жінці слід продовжити прийом таблеток із нової упаковки препарату одразу після того, як прийнято всі таблетки з попередньої, без перерви. Таблетки з нової упаковки можуть прийматися так довго, як бажає жінка (доки упаковка не закінчиться). На тлі прийому препарату з другої упаковки у жінки можуть відзначатися мажучі виділення або проривні маткові кровотечі.поки упаковка не закінчиться. На тлі прийому препарату з другої упаковки у жінки можуть відзначатися мажучі виділення або проривні маткові кровотечі.поки упаковка не закінчиться. На тлі прийому препарату з другої упаковки у жінки можуть відзначатися мажучі виділення або проривні маткові кровотечі. Слід розпочати прийом таблеток із наступної упаковки після завершення прийому всіх 28 табл. Щоб перенести день початку менструації на другий день тижня, жінці слід укоротити найближчу перерву прийому таблеток на стільки днів, на скільки вона хоче. Чим коротший інтервал, тим вищий ризик, що вона не матиме кровотечі відміни і, надалі, мажуть кров'янисті виділення і проривні кровотечі під час прийому другої упаковки (так само як у випадку, коли вона хотіла б відстрочити початок менструації). При лікуванні гіперандрогенних станів тривалість застосування препарату визначається тяжкістю захворювання. Після зникнення симптомів рекомендується приймати препарат принаймні протягом 3-4 місяців. У разі появи рецидиву через кілька тижнів або місяців після завершення курсу можна провести повторну терапію препаратом Хлоє.ПередозуванняСимптоми: нудота, блювання, невелика піхвова кровотеча. Лікування: проводять симптоматичну терапію. Специфічного антидоту немає.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаТаблетки, покриті плівковою оболонкою, жовто-жовтогарячого кольору - 1 табл. Активні речовини: ціпротерону ацетат - 2 мг; етинілестрадіол - 35 мкг; допоміжні речовини: лактози моногідрат; повідон; карбоксиметилкрохмаль натрію (тип А); кремнію діоксид колоїдний безводний; алюмінію оксид колоїдний; магнію стеарат оболонка: барвник Opadry II Yellow OY-L-32901 (лактози моногідрат, гіпромелоза 2910, титану діоксид, макрогол 4000, заліза оксид жовтий, заліза оксид чорний, заліза оксид червоний, вода очищена). Таблетки-плацебо білого кольору допоміжні речовини: лактози моногідрат; повідон; карбоксиметилкрохмаль натрію (тип А); кремнію діоксид колоїдний безводний; алюмінію оксид колоїдний; магнію стеарат у блістері 28 шт. (21 шт. – жовто-оранжевого кольору та 7 шт. – білого кольору). У пачці картонної 1 або 3 блістери.Опис лікарської формиТаблетки, покриті плівковою оболонкою: жовто-оранжевого кольору, круглі, двоопуклі. Таблетки-плацебо: білого кольору, круглі, двоопуклі.Фармакотерапевтична групаКомбінований низькодозований монофазний пероральний контрацептивний препарат з антиандрогенною активністю.ФармакокінетикаЦипротерону ацетат Всмоктування. Після прийому ХЛОЕ® ципротерону ацетат повністю абсорбується із шлунково-кишкового тракту. Після прийому внутрішньо 1 табл. ХЛОЕ Cmax становить 15 нг/мл і досягається через 1,6 год. Біодоступність становить 88%. Розподіл. Ципротерону ацетат практично повністю зв'язується з альбуміном плазми, приблизно 3,5-4% знаходиться у вільному стані. Оскільки зв'язування з білками є неспецифічним, зміни рівня глобуліну, що зв'язує статеві стероїди (ГСПС), не впливають на фармакокінетику ципротерону ацетату. З грудним молоком виділяється до 0,2 % дози ципротерону ацетату. Метаболізм та виведення. Фармакокінетика ципротерону ацетату двофазна, T1/2 становить 0,8 год і 2,3 діб відповідно для першої та другої фази. Загальний плазмовий кліренс становить 3,6 мл/хв/кг. Біотрансформується шляхом гідроксилювання та кон'югування, основний метаболіт - 15b-гідроксильне похідне. Виводиться переважно у вигляді метаболітів нирками та через кишечник у співвідношенні 1:2, невелика частина – у незміненому вигляді через кишечник. T1/2 для метаболітів ципротерону ацетату становить 1,8 діб. Етинілестрадіол Всмоктування. Після прийому ХЛОЕ® етинілестрадіол швидко та повністю абсорбується із ШКТ. У процесі всмоктування та першого проходження через печінку етинілестрадіол піддається інтенсивному метаболізму, що зумовлює біодоступність, рівну приблизно 45%, та її значну індивідуальну варіабельність. Після прийому внутрішньо 1 табл., покритою плівковою оболонкою ХЛОЕ Cmax становить приблизно 80 пг/мл і досягається через 1,7 год. Розподіл. Зв'язок з білками (альбуміном) плазми крові високий (2% знаходяться у плазмі у вільному вигляді). З грудним молоком виділяється до 0,02% дози етинілестрадіолу. Етинілестрадіол збільшує печінковий синтез ГСПС та кортикостероїдзв'язуючого глобуліну (КСГ) під час безперервного прийому. На фоні лікування ХЛОЕ® концентрація ГСПС у сироватці підвищується приблизно від 100 до 300 нмоль/л, і сироваткова концентрація КСГ збільшується приблизно з 50 до 95 мкг/мл. Метаболізм та виведення. Фармакокінетика етинілестрадіолу двофазна, з T1/2 1-2 і приблизно 20 год відповідно. Плазмовий кліренс – близько 5 мл/хв/кг. Етинілестрадіол виводиться з організму у вигляді метаболітів; близько 40% – нирками, 60% – через кишечник.ФармакодинамікаМеханізм дії обумовлений антиандрогенним препаратом стероїдної будови (ципротероном ацетатом), що входять до його складу, і пероральним естрогеном (етинілестрадіолом). Ципротерону ацетат Має здатність конкурентно зв'язуватися з рецепторами природних андрогенів (в т.ч. тестостерон, дигідроепіандростерон, андростендіон), що утворюються в невеликих кількостях в організмі жінок, головним чином надниркових залоз, яєчників і шкіри. Блокуючи рецептори андрогенів в органах-мішенях, зменшує явища андрогенізації у жінок (за рахунок порушення процесів, що опосередковуються гормон-рецепторними комплексами на рівні основних внутрішньоклітинних механізмів). Таким чином, стає можливим лікування захворювань, зумовлених підвищеним утворенням андрогенів або специфічною чутливістю до цих гормонів. На тлі прийому препарату знижується посилена діяльність сальних залоз, що відіграє важливу роль у виникненні вугрів та себореї. Через 3-4 міс терапії наявний висип зазвичай зникає. Надмірна жирність волосся та шкіри зникає ще раніше. Також зменшується випадання волосся, що часто супроводжує себорею. Терапія Хлоє у жінок репродуктивного віку зменшує клінічні прояви легких форм гірсутизму; проте ефект від лікування слід очікувати лише після кількох місяців застосування. Поряд з антиандрогенними властивостями ципротерону ацетат має гестагенну активність, що імітує властивості гормону жовтого тіла. Пригнічує секрецію гіпофізом гонадотропних гормонів та гальмує овуляцію, що зумовлює контрацептивний ефект. Етинілестрадіол Підсилює центральні та периферичні впливи ципротерону ацетату на овуляцію, зберігає високу в'язкість шийкового слизу, ускладнюючи проникнення сперматозоїдів у порожнину матки та сприяючи забезпеченню надійного контрацептивного ефекту. На тлі прийому препарату цикл стає регулярнішим, рідше спостерігаються хворобливі менструації, зменшується інтенсивність кровотечі, знижується ризик залізодефіцитної анемії.Показання до застосуванняАндрогензалежні захворювання у жінок: вугри, особливо їх виражені форми, що супроводжуються себореєю, запальними явищами з утворенням вузлів (папульозно-пустульозні, вузликово-кістозні); андрогенна алопеція; легкі форми гірсутизму; контрацепція у жінок із явищами андрогенізації.Протипоказання до застосування- підвищена чутливість до компонентів препарату; одночасне застосування з іншим гормональним контрацептивом; тромбози (венозні та артеріальні) або тромбоемболії в даний час або в анамнезі (в т.ч. тромбоз глибоких вен, тромбоемболія легеневої артерії, інфаркт міокарда, цереброваскулярні порушення, наприклад, інсульт); стани, що передують тромбозу (в т.ч. стенокардія, транзиторні ішемічні атаки); множинні або виражені фактори ризику венозного або артеріального тромбозу (в т.ч. ускладнені пороки клапанного апарату серця, фібриляція передсердь, захворювання судин головного мозку або коронарних артерій; неконтрольована артеріальна гіпертензія, тяжка дисліпопротеїнемія, кінцівках, нейрохірургічні операції, великі травми, куріння старше 35 років, ожиріння з індексом маси тіла більше 30 кг/м2); виявлена спадкова або набута схильність до венозного або артеріального тромбозу, наприклад резистентність до активованого протеїну С (АПС), дефіцит антитромбіну III, дефіцит протеїну С, дефіцит протеїну S, гіпергомоцистеїнемія та наявність антифосфоліпідних антитіл (антикардилян); тяжкі захворювання печінки в даний час або в анамнезі або виражені порушення функції печінки – не раніше ніж через 6 місяців після нормалізації показників функції печінки; пухлини печінки (доброякісні та злоякісні); гормонозалежні злоякісні пухлини чи підозра на них, у т.ч. пухлини молочної залози або статевих органів (в т.ч. в анамнезі); кровотечі із піхви неясної етіології; панкреатит із вираженою гіпертригліцеридемією (в т.ч. в анамнезі); наявність в анамнезі мігрені, що супроводжувалася осередковою неврологічною симптоматикою; період грудного вигодовування; вроджені гіпербілірубінемії (синдроми Жільбера, Дубіна-Джонсона та Ротора); вік старше 40 років; гіперпролактинемія непереносимість лактози, дефіцит лактази, глюкозо-галактозна мальабсорбція; вагітність чи підозра на неї. Якщо будь-які з цих станів розвиваються вперше на фоні прийому ХЛОЕ®, препарат повинен бути негайно скасований. Препарат ХЛОЕ не призначений для застосування у чоловіків. З обережністю: епілепсія, депресія, виразковий коліт, захворювання печінки та жовчного міхура, міома матки, мастопатія, хорея, тетанія, порфірія, розсіяний склероз, варикозне розширення вен, туберкульоз, захворювання нирок, підлітковий вік (без регулярних овуляторів. серповидно-клітинна анемія, ідіопатична жовтяниця або свербіж під час попередньої вагітності, отосклероз із погіршенням слуху під час попередньої вагітності.Вагітність та лактаціяПротипоказано застосування препарату при вагітності, підозрі на вагітність та у період грудного вигодовування.Побічна діяЗ боку ендокринної системи: рідко – нагрубання, болючість, збільшення та виділення з молочних залоз, підвищення маси тіла. З боку статевої системи: рідко міжменструальні кровотечі, зміни піхвового секрету, зміна лібідо. З боку центральної нервової системи: рідко – головний біль, мігрень, зниження настрою. З боку травної системи: рідко – нудота, блювання, гастралгія. Інші: дуже рідко – погана переносимість контактних лінз, набряк повік, порушення зору, кон'юнктивіт, зниження слуху, алергічні реакції, тромбофлебіт, тромбоемболія, генералізований свербіж, жовтяниця, поява пігментних плям на обличчі (хлоазму). Перелічені побічні ефекти можуть розвиватися протягом перших кількох місяців застосування препарату і зазвичай зменшуються з часом.Взаємодія з лікарськими засобамиПри одночасному застосуванні Хлое® з індукторами мікросомальних печінкових ферментів (гідантоїнами, барбітуратами, примідоном, карбамазепіном та рифампіцином; а також, можливо, з окскарбазепіном, топіраматом, фелбаматом та гризеофульвіном); надійність контрацепції. При одночасному застосуванні з ампіциліном, рифампіцином та тетрациклінами контрацептивна надійність Хлоє® знижується.Спосіб застосування та дозиВсередину, не розжовуючи та запиваючи невеликою кількістю рідини, по 1 табл. на добу. Прийом препарату рекомендується проводити в один і той же час, переважно після сніданку або вечері. Прийом Хлоє® починають у 1-й день циклу, використовуючи таблетку відповідного дня тижня із календарної упаковки. Щоденний прийом препарату здійснюють, використовуючи таблетки з календарної упаковки послідовно, у напрямку нанесеної на фольгу стрілки, доки не будуть прийняті всі таблетки. Після закінчення прийому всіх таблеток жовто-оранжевого кольору з календарної упаковки необхідно в наступні 7 днів приймати таблетки білого кольору, що залишилися. Протягом останніх 7 днів лікувального циклу (28 днів) має виникнути менструальноподібна кровотеча (внаслідок скасування лікування). Менструація зазвичай починається через 2-3 дні після 21-го дня циклу лікування препаратом. Наступну упаковку слід розпочинати наступного дня після повністю завершеного прийому таблеток з попередньої упаковки, незалежно від факту продовження/припинення кровотечі. При переході з комбінованих пероральних контрацептивів застосування Хлое® слід починати наступного дня після прийому останньої таблетки з активними компонентами попереднього препарату, але в жодному разі не пізніше наступного дня після звичайної 7-денної перерви у прийомі (для препаратів, що містять 21 табл.) . Далі за описаною вище схемою. Якщо пацієнтка приймала попередній контрацептив щодня протягом 28 днів,застосування Хлоє® слід розпочати після прийому останньої неактивної таблетки. При переході з контрацептивів, що містять тільки гестагени (міні-пілі), Хлое® можна почати застосовувати без перерви. При використанні ін'єкційних форм контрацептивів Хлое® слід застосовувати з дня, коли має бути зроблена наступна ін'єкція. При переході з імплантату Хлоє слід застосовувати вже в день його видалення. У всіх випадках необхідно використовувати додатково бар'єрний метод контрацепції протягом перших 7 днів застосування препарату. Після аборту в І триместрі вагітності жінка може розпочати застосування Хлої негайно. В цьому випадку немає потреби у додаткових методах контрацепції. Після пологів або аборту у II триместрі вагітності застосування препарату слід розпочинати на 21-28-й день. Якщо прийом розпочато пізніше, необхідно використовувати додатково бар'єрний метод контрацепції протягом перших 7 днів застосування препарату.Якщо жінка жила статевим життям у період між пологами або абортом та початком застосування препарату, слід перш за все виключити вагітність або необхідно дочекатися першої менструації. Пропущену таблетку слід прийняти якнайшвидше, наступну таблетку — у звичайний час. При запізненні12 год надійність контрацепції може бути знижена. Якщо запізнення в прийомі таблеток склало >12 год (інтервал з моменту прийому останньої таблетки >36 год) під час 1-3-го тижня прийому препарату, жінці слід прийняти останню пропущену таблетку якнайшвидше, навіть якщо це означає прийом двох таблеток одночасно. Наступну таблетку слід прийняти у звичайний час. Додатково під час 1-2 тижнів прийому необхідно використовувати бар'єрний метод контрацепції протягом наступних 7 днів. Прийом таблетки з нової упаковки слід розпочати після закінчення поточної упаковки без перерви. Ймовірно, кровотечі відміни не буде до кінця другої упаковки,але можливі кров'янисті виділення, що мажуть, або проривна маткова кровотеча в дні прийому таблеток. Якщо у жінки було блювання в межах від 3 до 4 годин після прийому препарату, всмоктування активних речовин може бути неповним. І тут необхідно орієнтуватися на рекомендації при пропуску таблетки. Щоб відстрочити дату початку менструації, жінці слід продовжити прийом таблеток із нової упаковки препарату одразу після того, як прийнято всі таблетки з попередньої, без перерви. Таблетки з нової упаковки можуть прийматися так довго, як бажає жінка (доки упаковка не закінчиться). На тлі прийому препарату з другої упаковки у жінки можуть відзначатися мажучі виділення або проривні маткові кровотечі.І тут необхідно орієнтуватися на рекомендації при пропуску таблетки. Щоб відстрочити дату початку менструації, жінці слід продовжити прийом таблеток із нової упаковки препарату одразу після того, як прийнято всі таблетки з попередньої, без перерви. Таблетки з нової упаковки можуть прийматися так довго, як бажає жінка (доки упаковка не закінчиться). На тлі прийому препарату з другої упаковки у жінки можуть відзначатися мажучі виділення або проривні маткові кровотечі.І тут необхідно орієнтуватися на рекомендації при пропуску таблетки. Щоб відстрочити дату початку менструації, жінці слід продовжити прийом таблеток із нової упаковки препарату одразу після того, як прийнято всі таблетки з попередньої, без перерви. Таблетки з нової упаковки можуть прийматися так довго, як бажає жінка (доки упаковка не закінчиться). На тлі прийому препарату з другої упаковки у жінки можуть відзначатися мажучі виділення або проривні маткові кровотечі.поки упаковка не закінчиться. На тлі прийому препарату з другої упаковки у жінки можуть відзначатися мажучі виділення або проривні маткові кровотечі.поки упаковка не закінчиться. На тлі прийому препарату з другої упаковки у жінки можуть відзначатися мажучі виділення або проривні маткові кровотечі. Слід розпочати прийом таблеток із наступної упаковки після завершення прийому всіх 28 табл. Щоб перенести день початку менструації на другий день тижня, жінці слід укоротити найближчу перерву прийому таблеток на стільки днів, на скільки вона хоче. Чим коротший інтервал, тим вищий ризик, що вона не матиме кровотечі відміни і, надалі, мажуть кров'янисті виділення і проривні кровотечі під час прийому другої упаковки (так само як у випадку, коли вона хотіла б відстрочити початок менструації). При лікуванні гіперандрогенних станів тривалість застосування препарату визначається тяжкістю захворювання. Після зникнення симптомів рекомендується приймати препарат принаймні протягом 3-4 місяців. У разі появи рецидиву через кілька тижнів або місяців після завершення курсу можна провести повторну терапію препаратом Хлоє.ПередозуванняСимптоми: нудота, блювання, невелика піхвова кровотеча. Лікування: проводять симптоматичну терапію. Специфічного антидоту немає.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
941,00 грн
174,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
1 267,00 грн
195,00 грн
Склад, форма випуску та упаковкаРозчин – 1 шприц: активна речовина: еноксапарин натрію 40 мг*; розчинник: вода для ін'єкцій до 0,4 мл; * - маса розрахована на підставі вмісту еноксапарину натрію (теоретична активність 100 анти-Ха МО/мг). 1 вид упаковки По 0,2 мл або 0,4 мл, або 0,6 мл, або 0,8 мл, або 1,0 мл розчину препарату скляний шприц (тип I) відповідно. По 2 шприци в блістер. По 1 або 5 блістерів разом із інструкцією із застосування в картонну пачку. 2 вид упаковки По 0,2 мл або 0,4 мл, або 0,6 мл, або 0,8 мл, або 1,0 мл розчину препарату у скляний шприц (тип 1) із захисною системою голки відповідно. По 2 шприци в блістер. По 1 або 5 блістерів разом із інструкцією із застосування в картонну пачку.Опис лікарської формиПрозорий, від безбарвного до блідо-жовтого кольору розчин.ХарактеристикаЕноксапарин натрію - низькомолекулярний гепарин із середньою молекулярною масою близько 4500 дальтон (Так): менше 2000 Так - 68 %, більше 8000 Так -Фармакотерапевтична групаАнтикоагулянтний засіб прямої дії.ФармакокінетикаБіодоступність та абсорбція Абсолютна біодоступність еноксапарину натрію при підшкірному (п/к) введенні, що оцінюється на підставі анти-Ха активності, близька до 100%. Середня максимальна анти-Ха активність у плазмі крові відзначається через 3-5 годин після підшкірного введення і досягає приблизно 0,2, 0,4, 1,0 та 1,3 анти-Ха МО/мл після одноразового підшкірного введення препарату в дозі 20 мг, 40 мг, 1 мг/кг та 1,5 мг/кг. Внутрішньовенне болюсне введення препарату в дозі 30 мг, що супроводжується негайним підшкірним введенням препарату в дозі 1 мг/кг кожні 12 год, забезпечує початкову максимальну анти-Ха активність на рівні 1,16 МО/мл (n=16), середня експозиція препарату становить приблизно 88% від рівноважного стану, що досягається другого дня терапії. Фармакокінетика еноксапарину натрію у зазначених режимах дозування має лінійний характер. Варіабельність усередині та між групами пацієнтів низька. Після повторного підшкірного введення 40 мг еноксапарину натрію один раз на добу та підшкірного введення еноксапарину натрію в дозі 1,5 мг/кг маси тіла один раз на добу у здорових добровольців рівноважна концентрація досягається до 2 дня, причому площа під фармакокінетичною кривою в середньому на 15 % вище, ніж після одноразового введення. Після повторних підшкірних введень еноксапарину натрію в добовій дозі 1 мг/кг маси тіла двічі на добу рівноважна концентрація досягається через 3-4 дні, причому площа під фармакокінетичною кривою (AUC) в середньому на 65 % вище, ніж після одноразового введення, та середні значення максимальних концентрацій становлять відповідно 1,2 МО/мл та 0,52 МО/мл. Анти-Ха активність у плазмі крові приблизно в 10 разів нижча, ніж анти-Ха активність. Середня максимальна анти-Ха активність спостерігається приблизно через 3-4 години після підшкірного введення і досягає 0,13 МО/мл і 0,19 МО/мл після повторного введення 1 мг/кг маси тіла при дворазовому введенні та 1,5 мг/кг. маси тіла при одноразовому введенні відповідно. Розподіл Об'єм розподілу анти-Ха активності еноксапарину натрію становить приблизно 4,3 л і наближається до об'єму циркулюючої крові. Виведення Еноксапарин натрію є препаратом із низьким кліренсом. Після внутрішньовенного введення протягом 6 годин у дозі 1,5 мг/кг маси тіла середнє значення кліренсу анти-Ха у плазмі становить 0,74 л/год. Виведення препарату носить монофазний характер з періодами напіввиведення (Т1/2) близько 5 годин (після одноразового підшкірного введення) та близько 7 годин (після багаторазового введення препарату). Еноксапарин натрію в основному метаболізується в печінці шляхом десульфатування та/або деполімеризації з утворенням низькомолекулярних речовин з дуже низькою біологічною активністю. Виведення через нирки активних фрагментів препарату становить приблизно 10% від введеної дози, та загальна екскреція активних та неактивних фрагментів становить приблизно 40% від введеної дози. Особливі групи пацієнтів Пацієнти похилого віку (старше 75 років): фармакокінетичний профіль еноксапарину натрію не відрізняється у пацієнтів похилого віку та молодших пацієнтів при нормальній функції нирок. Однак унаслідок зниження функції нирок з віком може спостерігатися уповільнення виведення еноксапарину натрію у пацієнтів похилого віку. Порушення функції печінки: у дослідженні за участю пацієнтів з пізніми стадіями цирозу печінки, які отримували еноксапарин натрію в дозі 4000 ME (40 мг) один раз на добу, зниження максимальної анти-Ха активності було пов'язане зі збільшенням тяжкості порушення функції печінки (з оцінкою за шкалою Чайлд-Пью). Це зниження було зумовлено зниженням рівня AT-III, вторинним стосовно зниження синтезу АТ-III у пацієнтів з порушенням функції печінки. Порушення функції нирок: відмічено зменшення кліренсу еноксапарину натрію у пацієнтів із порушеннями функції нирок. Після повторного підшкірного введення 40 мг еноксапарину натрію один раз на добу відбувається збільшення активності анти-Ха, представленої площею під фармакокінетичною кривою (AUC) у пацієнтів з порушеннями функції нирок легкої (кліренс креатиніну (КК) ≥50 і Гемодіаліз: фармакокінетика еноксапарину натрію порівнянна з показниками в контрольній популяції після одноразових внутрішньовенних введень доз 25 ME, 50 ME або 100 МО/кг (0,25, 0.50 або 1,0 мг/кг), проте AUC була вдвічі , ніж у контрольній популяції. Маса тіла: після повторних підшкірних введень у дозуванні 1,5 мг/кг один раз на добу середня AUC анти-Ха активності в стані рівноваги незначно вища у пацієнтів із надмірною масою тіла (ІМТ 30-48 кг/м2) порівняно з пацієнтами із звичайною середньою масою тіла, тоді як максимальна анти-Ха активність плазми крові не збільшується. У пацієнтів із надмірною масою тіла при підшкірному введенні препарату кліренс дещо менший. Якщо не робити поправку дози з урахуванням маси тіла пацієнта, то після одноразового підшкірного введення 40 мг еноксапарину натрію анти-Ха активність буде на 52 % вище у жінок з масою тіла менше 45 кг і на 27 % вище у чоловіків з масою тіла менше 57 кг порівняно з пацієнтами із звичайною середньою масою тіла.ФармакодинамікаВ очищеній системі in vitro еноксапарин натрію має високу анти-Ха активність (приблизно 100 МО/мл) та низьку анти-Ха або антитромбінову активність (приблизно 28 МО/мл). Ця антикоагулянтна активність діє через антитромбін III (АТ-III), забезпечуючи антикоагулянтну активність у людей. Крім анти-Ха/IIа активності також виявлено додаткові антикоагулянтні та протизапальні властивості еноксапарину натрію як у здорових людей та пацієнтів, так і на моделях тварин. Це включає АТ-III-залежне інгібування інших факторів згортання, як фактор Vila, активацію вивільнення інгібітору шляху тканинного фактора (ПТФ), а також зниження вивільнення фактора Віллебранду з ендотелію судин у кровотік. Ці фактори забезпечують антикоагулянтний ефект еноксапарину натрію загалом. При застосуванні його у профілактичних дозах він незначно змінює активований частковий тромбопластиновий час (АЧТВ), практично не впливає на агрегацію тромбоцитів та на ступінь зв'язування фібриногену з рецепторами тромбоцитів.ІнструкціяОсобливості введення препарату Попередньо заповнений одноразовий шприц готовий до застосування. Препарат не можна вводити внутрішньом'язово! Підшкірне введення Ін'єкції бажано проводити у положенні пацієнта "лежачи". При використанні попередньо заповнених шприців на 20 мг і 40 мг, щоб уникнути втрати препарату перед ін'єкцією, не треба видаляти бульбашки повітря зі шприца. Ін'єкції слід проводити по черзі у ліву або праву передньолатеральну або задньолатеральну поверхню живота. Голку необхідно ввести на всю довжину, вертикально (не збоку), у шкірну складку, зібрану та утримувану до завершення ін'єкції між великим та вказівним пальцями. Складку шкіри відпускають лише після завершення ін'єкції. Не слід масажувати місце ін'єкції після введення препарату. Внутрішньовенне болюсне введення Внутрішньовенне болюсне введення еноксапарину натрію повинно проводитись через венозний катетер. Еноксапарин натрію не повинен змішуватись або вводитися разом з іншими лікарськими препаратами. Для того, щоб уникнути присутності в інфузійній системі слідів інших лікарських препаратів та їх взаємодії з еноксапарином натрію, венозний катетер повинен промиватися достатньою кількістю 0,9 % розчину натрію хлориду або 5 % розчину декстрози до та після внутрішньовенного болюсного введення еноксапарину. Еноксапарин натрію може безпечно вводитися з 0.9% розчином натрію хлориду та 5% розчином декстрози. Для проведення болюсного введення 30 мг еноксапарину натрію при лікуванні гострого інфаркту міокарда з підйомом сегмента ST зі скляних шприців 60 мг, 80 мг та 100 мг видаляють зайву кількість препарату для того, щоб у них залишалося лише 30 мг (0,3 мл). Доза 30 мг може безпосередньо вводитися внутрішньовенно. Для внутрішньовенного болюсного введення еноксапарину натрію через венозний катетер можуть використовуватися попередньо заповнені шприци для підшкірного введення препарату 60 мг, 80 мг і 100 мг. Рекомендується використовувати шприци 60 мг, так як це зменшує кількість препарату, що видаляється зі шприца. Шприци 20 мг не використовуються, тому що в них недостатньо препарату для болюсного введення 30 мг еноксапарину натрію. Шприци 40 мг не використовуються, тому що на них відсутні поділки і тому неможливо точно відміряти кількість 30 мг. Для підвищення точності додаткового внутрішньовенного болюсного введення малих обсягів у венозний катетер під час проведення черезшкірних коронарних втручань рекомендується розвести препарат до концентрації 3 мг/мл. Розведення розчину рекомендується проводити безпосередньо перед введенням. Для одержання розчину еноксапарину натрію з концентрацією 3 мг/мл за допомогою попередньо заповненого шприца 60 мг рекомендується використовувати ємність з інфузійним розчином 50 мл (тобто з 0,9 % розчином натрію хлориду або 5 % розчином декстрози). З ємності з інфузійним розчином за допомогою звичайного шприца вилучається та видаляється 30 мл розчину. Еноксапарин натрію (вміст шприца для підшкірного введення 60 мг) вводиться в 20 мл інфузійного розчину, що залишилися в ємності. Вміст ємності з розведеним розчином еноксапарину натрію обережно перемішується. Для введення за допомогою шприца витягується необхідний обсяг розведеного розчину еноксапарину натрію, який розраховується за формулою: Об'єм розведеного розчину = Маса тіла пацієнта (кг) х 0,1 або за допомогою наведеної нижче таблиці. Об'єми, які повинні вводитися внутрішньовенно після розведення до концентрації 3 мг/мл Маса тіла пацієнта, кг Необхідна доза (0,3 мг/кг), мг Об'єм розчину, розведеного до концентрації 3 мг/мл, необхідний для введення. 45 13,5 4,5 50 15 5 55 16,5 5,5 60 18 6 65 19,5 6,5 70 21 7 75 22,5 7,5 80 24 8 85 25,5 8,5 90 27 9 95 28,5 9,5 100 30 10 105 31,5 10,5 110 33 11 115 34,5 11,5 120 36 12 125 37,5 12,5 130 39 13 135 40,5 13,5 140 42 14 145 43,5 14,5 150 45 15 Переключення між еноксапарином натрію та пероральними антикоагулянтами: Перемикання між еноксапарином натрію та антагоністами вітаміну до (авк). Для моніторування ефекту авк необхідне спостереження лікаря та проведення лабораторних досліджень [протромбіновий час, представлений як багато]. Оскільки для розвитку максимального ефекту авк потрібен час, терапія еноксапарином натрію повинна продовжуватися в постійній дозі так довго, як необхідно для підтримання значень багато (за даними двох послідовних визначень) в бажаному терапевтичному діапазоні залежно від показань. Для пацієнтів, які отримують авк, скасування авк та введення першої дози еноксапарину натрію повинні проводитися після того, як багато знизилося нижче за межу терапевтичного діапазону. Переключення між еноксапарином натрію та пероральними антикоагулянтами прямої дії (поак). Скасування еноксапарину натрію та призначення поак повинні проводитися за 0-2 години до моменту чергового запланованого введення еноксапарину натрію відповідно до інструкції щодо застосування пероральних антикоагулянтів. Для пацієнтів, які отримують поак, введення першої дози еноксапарину натрію та відміна пероральних антикоагулянтів прямої дії повинні проводитися в момент часу, що відповідає черговому запланованому застосуванню поак. Застосування при спинальній/епідуральній анестезії або люмбальній пункції. У разі застосування антикоагулянтної терапії під час проведення епідуральної або спинальної анестезії/аналгезії або люмбальної пункції необхідне проведення неврологічного моніторування через ризик розвитку нейроаксіальних гематом. Застосування еноксапарину натрію у профілактичних дозах. Встановлення або видалення катетера повинно проводитися як мінімум 12 годин після останньої ін'єкції профілактичної дози еноксапарину натрію. При використанні безперервної техніки необхідно дотримуватися щонайменше 12 год. інтервал до видалення катетера. У пацієнтів з кк ≥15 та Застосування еноксапарину натрію у терапевтичних дозах Встановлення або видалення катетера повинно проводитися як мінімум 24 години після останньої ін'єкції терапевтичної дози еноксапарину натрію. При використанні безперервної техніки необхідно дотримуватися щонайменше 24 години інтервал до видалення катетера. У пацієнтів з кк ≥15 та Пацієнтам, які отримують еноксапарин натрію в дозах 0,75 мг/кг або 1 мг/кг маси тіла двічі на добу, не слід вводити другу дозу з метою збільшення інтервалу перед встановленням або заміною катетера. Так само слід розглянути питання про можливість відстрочення введення наступної дози препарату як мінімум на 4 години, виходячи з оцінки співвідношення користь/ризик (ризик розвитку тромбозу та кровотеч при проведенні процедури, з урахуванням наявності у пацієнтів факторів ризику). У ці часові точки все ще продовжує виявлятися анти-активність препарату, і відстрочки за часом не є гарантією того, що розвитку нейроаксіальної гематоми вдасться уникнути.Показання до застосуванняПрофілактика венозних тромбозів та емболій при хірургічних втручаннях у пацієнтів помірного та високого ризику, особливо при ортопедичних та загальнохірургічних втручаннях, включаючи онкологічні. Профілактика венозних тромбозів та емболій у пацієнтів, що знаходяться на постільному режимі, внаслідок гострих терапевтичних захворювань, включаючи гостру серцеву недостатність та декомпенсацію хронічної серцевої недостатності (III або IV клас NYHA), дихальну недостатність, а також при тяжких інфекціях та ревматичних захворюваннях при підвищеному тромбоутворення. Лікування тромбозу глибоких вен з тромбоемболією легеневої артерії або без тромбоемболії легеневої артерії, крім випадків тромбоемболії легеневої артерії, які потребують тромболітичної терапії або хірургічного втручання. Профілактика тромбоутворення у системі екстракорпорального кровообігу під час гемодіалізу. Гострий коронарний синдром: Лікування нестабільної стенокардії та інфаркту міокарда без підйому сегмента ST у поєднанні з пероральним прийомом ацетилсаліцилової кислоти. Лікування гострого інфаркту міокарда з підйомом сегмента ST у пацієнтів, які підлягають медикаментозному лікуванню або подальшому корконарному втручанню (ЧКВ).Протипоказання до застосуванняПідвищена чутливість до еноксапарину натрію, гепарину або його похідних, включаючи інші низькомолекулярні гепарини. Активна клінічно значуща кровотеча, а також стани та захворювання, при яких є високий ризик розвитку кровотечі, включаючи нещодавно перенесений геморагічний інсульт, гостру виразку шлунково-кишкового тракту (ЖКТ), наявність злоякісного новоутворення з високим ризиком кровотеч, нещодавно перенесені операції на головній та спинній мозку, офтальмологічні операції, відома чи передбачувана наявність варикозного розширених вен стравоходу, артеріовенозні мальформації, судинні аневризми, судинні аномалії спинного та головного мозку. Спінальна або епідуральна анестезія або локо-регіональна анестезія, коли еноксапарин натрію застосовувався для лікування попередніх 24 год. Імуноопосередкована гепарин-індукована громбоцитопенія (в анамнезі) протягом 100 останніх днів або наявність у крові циркулюючих антитромбоцитарних антитіл. Дитячий вік до 18 років, оскільки ефективність та безпека у даної категорії пацієнтів не встановлені. Стани, у яких є потенційний ризик розвитку кровотечі: порушення гемостазу (в т.ч. гемофілія, тромбоцитопенія, гіпокоагуляція, хвороба Віллебранда та ін), важкий васкуліт; виразкова хвороба шлунка або дванадцятипалої кишки або інші ерозивно-виразкові ураження шлунково-кишкового тракту в анамнезі; нещодавно перенесений ішемічний інсульт; неконтрольована тяжка артеріальна гіпертензія; діабетична або геморагічна ретинопатія; тяжкий цукровий діабет; нещодавно перенесена чи передбачувана неврологічна чи офтальмологічна операція; проведення спинальної або епідуральної анестезії (потенційна небезпека розвитку гематоми); спинномозкова пункція (нещодавно перенесена); недавні пологи; ендокардит бактеріальний (гострий або підгострий); перикардит або перикардіальний випіт; ниркова та/або печінкова недостатність; внутрішньоматкова контрацепція (ВМК); тяжка травма (особливо центральної нервової системи); відкриті рани на великих поверхнях; одночасний прийом препаратів, що впливають на систему гемостазу; гепарин-індукована тромбоцитопенія без циркулюючих антитіл в анамнезі (понад 100 днів). У компанії відсутні дані щодо клінічного застосування препарату Клексан при таких захворюваннях: активний туберкульоз, променева терапія (нещодавно перенесена).Вагітність та лактаціяВагітність Відомостей, що еноксапарин натрію проникає через плацентарний бар'єр під час вагітності, немає. Так як відсутні адекватні та добре контрольовані дослідження за участю вагітних жінок, а дослідження на тваринах не завжди прогнозують реакцію на введення еноксапарину натрію під час вагітності у людини, застосовувати його під час вагітності слід лише у виняткових випадках, коли є нагальна необхідність його застосування, встановлена лікарем. Рекомендується проведення контролю за станом пацієнток щодо появи ознак кровотечі або надмірної антикоагуляції, пацієнтки повинні бути попереджені про ризик виникнення кровотеч. Немає даних про підвищений ризик розвитку кровотеч, тромбоцитопенії або остеопорозу у вагітних жінок, за винятком випадків, відмічених у пацієнток із штучними клапанами серця. При плануванні епідуральної анестезії рекомендується перед її проведенням відмінити еноксапарин натрію. Період грудного вигодовування Невідомо, чи екскретується незмінений еноксапарин натрію у грудне молоко. Всмоктування еноксапарину натрію в шлунково-кишковому тракті у новонародженого малоймовірне. Препарат Клексан може застосовуватись у період грудного вигодовування.Побічна діяВивчення побічних ефектів еноксапарину натрію проводилося більш ніж у 15000 пацієнтів, які брали участь у клінічних дослідженнях, з них у 1776 пацієнтів - при профілактиці венозних тромбозів та емболій при загальнохірургічних та ортопедичних операціях: у 1169 пацієнтів постільний режим внаслідок гострих терапевтичних захворювань; у 559 пацієнтів – при лікуванні тромбозу глибоких вен з тромбоемболією легеневої артерії або без тромбоемболії легеневої артерії; у 1578 пацієнтів – при лікуванні нестабільної стенокардії та інфаркту міокарда без зубця Q; у 10176 пацієнтів – при лікуванні інфаркту міокарда з підйомом сегмента ST. Режим введення еноксапарину натрію відрізнявся залежно від показань. При профілактиці венозних тромбозів та емболій при загальнохірургічних та ортопедичних операціях або у пацієнтів, які перебувають на постільному режимі, вводилося 40 мг підшкірно один раз на добу. При лікуванні тромбозу глибоких вен з тромбоемболією легеневої артерії або без неї пацієнти отримували еноксапарин натрію з розрахунку 1 мг/кг маси тіла підшкірно кожні 12 годин або 1,5 мг/кг маси тіла підшкірно один раз на добу. При лікуванні нестабільної стенокардії та інфаркту міокарда без зубця Q доза еноксапарину натрію становила 1 мг/кг маси тіла підшкірно кожні 12 год, а у разі інфаркту міокарда з підйомом сегмента ST проводилося внутрішньовенне болюсне введення 30 мг з подальшим в кожні 12 год.Частота виникнення небажаних реакцій визначалася відповідно до класифікації Всесвітньої Організації Охорони Здоров'я: дуже часто (≥1/10); часто (≥1/100 та Порушення з боку судин: Кровотечі У клінічних дослідженнях кровотечі були найпоширенішими небажаними реакціями. До них належали великі кровотечі, що спостерігалися у 4,2% пацієнтів (кровотеча вважалася великою, якщо вона супроводжувалася зниженням вмісту гемоглобіну на 2 г/л і більше, вимагало переливання 2 або більше доз компонентів крові, а також якщо воно було заочеревинним або внутрішньочерепним. ). Деякі з цих випадків були летальними. Як і при застосуванні інших антикоагулянтів, при застосуванні еноксапарину натрію можливе виникнення кровотечі, особливо за наявності факторів ризику, що сприяють розвитку кровотечі, при проведенні інвазивних процедур або застосуванні препаратів, що порушують гемостаз. При описі кровотеч нижче знак "*" означає вказівку на такі види кровотеч: гематома, екхімози (крім ін'єкції), ранові гематоми, гематурія, носові кровотечі, шлунково-кишкові кровотечі. Дуже часто: кровотечі* при профілактиці венозних тромбозів у хірургічних пацієнтів та лікуванні тромбозу глибоких вен з тромбоемболією легеневої артерії або без неї. Часто: кровотечі* при профілактиці венозних тромбозів у пацієнтів, які перебувають на постільному режимі, та при лікуванні нестабільної стенокардії, інфаркту міокарда без зубця Q та інфаркту міокарда з підйомом сегмента ST. Нечасто: заочеревинні кровотечі та внутрішньочерепні крововиливи у пацієнтів при лікуванні тромбозу глибоких вен з тромбоемболією легеневої артерії або без неї. а також при лікуванні інфаркту міокарда із підйомом сегмента ST. Рідко: заочеревинні кровотечі при профілактиці венозних тромбозів у хірургічних пацієнтів та при лікуванні нестабільної стенокардії та інфаркту міокарда без зубця Q. Тромбоцитопенія та тромбоцитоз Часто: тромбоцитоз (кількість тромбоцитів у периферичній крові більше 400x109/л) при профілактиці венозних тромбозів у хірургічних пацієнтів та лікуванні тромбозу глибоких вен з тромбоемболією легеневої артерії або без неї. Часто: тромбоцитоз при лікуванні пацієнтів із гострим інфарктом міокарда із підйомом сегмента ST. Тромбоцитопенія при профілактиці венозних тромбозів у хірургічних пацієнтів та лікуванні тромбозу глибоких вен з тромбоемболією легеневої артерії або без неї. а також при гострому інфаркті міокарда із підйомом сегмента ST. Нечасто: тромбоцитопенія при профілактиці венозних тромбозів у пацієнтів, які перебувають на постільному режимі, та при лікуванні нестабільної стенокардії та інфаркту міокарда без зубця Q. Дуже рідко: аутоімунна тромбоцитопенія при лікуванні пацієнтів із гострим інфарктом міокарда з підйомом сегмента ST. Інші клінічно значущі небажані реакції незалежно від показань Небажані реакції, представлені нижче, згруповані за системно-органними класами, дано із зазначенням визначеної вище частоти їх виникнення та в порядку зменшення їх тяжкості. Порушення з боку крові та лімфатичної системи: - Часто: кровотеча, тромбоцитопенія, тромбоцитоз; Рідко: випадки розвитку аутоімунної тромбоцитопенії з тромбозом; у деяких випадках тромбоз ускладнювався розвитком інфаркту органів або ішемії кінцівок. Порушення з боку імунної системи: Найчастіше: алергічні реакції. Порушення з боку печінки та жовчовивідних шляхів: Дуже часто: підвищення активності "печінкових" ферментів, головним чином підвищення активності трансаміназ, що більш ніж утричі перевищує верхню межу норми. Порушення з боку шкіри та підшкірних тканин - Часто: кропив'янка, свербіж шкіри, еритема; Нечасто: бульозний дерматит. Загальні розлади та порушення у місці введення: Часто: гематома у місці ін'єкції, біль у місці ін'єкції, набряк у місці ін'єкції, кровотеча, реакції підвищеної чутливості, запалення, утворення ущільнень у місці ін'єкції. Нечасто: подразнення у місці ін'єкції, некроз шкіри у місці ін'єкції. Дані, отримані після виходу препарату ринку Наступні небажані реакції спостерігалися при постмаркетинговому застосуванні препарату Клексан. Про ці побічні реакції були спонтанні повідомлення. Порушення з боку імунної системи: Рідко: анафілактичні/анафілактоїдні реакції, включаючи шок. Порушення з боку нервової системи: Часто: біль голови. Порушення з боку судин: Рідко: при застосуванні еноксапарину натрію на тлі спінальної/епідуральної анестезії або спінальної пункції спостерігалися випадки розвитку спінальної гематоми (або нейроаксіальної гематоми). Ці реакції призводили до розвитку неврологічних порушень різного ступеня тяжкості, включаючи стійкий або необоротний параліч. Порушення з боку крові або лімфатичної системи: - Часто: геморагічна анемія; Рідко: еозинофілія. Порушення з боку шкіри та підшкірних тканин: Рідко: алопеція; у місці ін'єкції може розвинутися шкірний васкуліт, некроз шкіри, яким зазвичай передує поява пурпури або еритематозних папул (інфільтрованих та болючих). У цих випадках терапію препаратом Клексан слід припинити. Можливе утворення твердих запальних вузликів-інфільтратів у місці ін'єкцій препарату, які зникають через кілька днів і не є підставою для відміни препарату. Порушення з боку печінки та жовчовивідних шляхів: - Нечасто: гепатоцелюлярне ураження печінки; Рідко: холестатична поразка печінки. Порушення з боку скелетно-м'язової та сполучної тканини: Рідко: остеопороз при тривалій терапії (понад три місяці). Лабораторні та інструментальні дані - Рідко: гіперкаліємія.Взаємодія з лікарськими засобамиПрепарат Клексан не можна змішувати з іншими препаратами! Нерекомендовані комбінації Препарати, що впливають на гемостаз (саліцилати системної дії, ацетилсаліцилова кислота в дозах, що мають протизапальну дію, нестероїдні протизапальні препарати (НПЗП), включаючи кеторолак, інші тромболітики (алтеплаза, ретеплаза, стрептокіназа, трептокіназа, натрію. При необхідності одночасного застосування з еноксапарином натрію слід дотримуватися обережності та проводити ретельне клінічне спостереження та моніторинг відповідних лабораторних показників. Комбінації, що вимагають дотримання обережності Інші лікарські препарати, що впливають на гемостаз, такі як: інгібітори агрегації тромбоцитів, включаючи ацетилсаліцилову кислоту в дозах, що мають антиагрегантну дію (кардіопротекція), клопідогрел, тиклопідин та антагоністи глікопротеїнових ПЬ/Ша рецепторів, показані при гострому коронарному синдромі, внаслідок підвищеного ризику; декстран із молекулярною масою 40 кДа; системні глюкокортикостероїди. Лікарські препарати, що підвищують вміст калію При одночасному застосуванні з лікарськими препаратами, що підвищують вміст калію в сироватці, слід проводити клінічний та лабораторний контроль.Спосіб застосування та дозиПідшкірно, за винятком особливих випадків (див. нижче підрозділи "Лікування інфаркту міокарда з підйомом сегмента ST, медикаментозне або за допомогою черезшкірного коронарного втручання" та "Профілактика тромбоутворення в системі екстракорпорального кровообігу при проведенні гемодіалізу"). Профілактика венозних тромбозів та емболії при хірургічних втручаннях у пацієнтів помірного та високого ризику Пацієнтам з помірним ризиком розвитку тромбозів та емболій (наприклад, абдомінальні операції) рекомендована доза препарату Клексан становить 20 мг один раз на добу підшкірно. Першу ін'єкцію слід зробити за 2 години до хірургічного втручання. Пацієнтам з високим ризиком розвитку тромбозів та емболій (наприклад, при ортопедичних операціях, хірургічних операціях в онкології, пацієнтам з додатковими факторами ризику, не пов'язаними з операцією, такими як вроджена або набута тромбофілія, злоякісне новоутворення, постільний режим понад три доби, тромбоз в анамнезі, варикозне розширення вен нижніх кінцівок, вагітність) препарат рекомендується у дозі 40 мг один раз на добу підшкірно, із введенням першої дози за 12 годин до хірургічного втручання. За необхідності більш ранньої передопераційної профілактики (наприклад, у пацієнтів з високим ризиком розвитку тромбозів та тромбоемболій, що очікують відстрочену ортопедичну операцію) остання ін'єкція повинна бути зроблена за 12 годин до операції та через 12 годин після операції. Тривалість лікування препаратом Клексан у середньому становить 7-10 днів. При необхідності терапію можна продовжувати доти, доки зберігається ризик розвитку тромбозу та емболії, і доти, доки пацієнт не перейде на амбулаторний режим. При великих ортопедичних операціях може бути доцільним після початкової терапії продовження лікування шляхом введення препарату Клексан у дозі 40 мг один раз на добу протягом п'яти тижнів. Для пацієнтів з високим ризиком венозних тромбоемболій, які перенесли хірургічне втручання, абдомінальну та тазову хірургію через онкологічне захворювання, може бути доцільним збільшення тривалості введення препарату Клексан у дозі 40 мг один раз на добу протягом чотирьох тижнів. Профілактика венозних тромбозів та емболій у пацієнтів, які перебувають на постільному режимі внаслідок гострих терапевтичних захворювань Рекомендована доза препарату Клексан становить 40 мг один раз на добу, підшкірно, протягом 6-14 днів. Терапію слід продовжувати до переходу пацієнта на амбулаторний режим (максимально протягом 14 днів). Лікування тромбозу глибоких вен з тромбоемболією легеневої артерії або без тромбоемболії легеневої артерії Препарат вводиться підшкірно із розрахунку 1,5 мг/кг маси тіла один раз на добу або 1 мг/кг маси тіла двічі на добу. Режим дозування повинен вибиратися лікарем на основі оцінки ризику розвитку тромбоемболії та ризику розвитку кровотеч. У пацієнтів без тромбоемболічних ускладнень та з низьким ризиком розвитку венозної тромбоемболії препарат рекомендується вводити підшкірно із розрахунку 1.5 мг/кг маси тіла один раз на добу. У всіх інших пацієнтів, включаючи пацієнтів з ожирінням, симптоматичною тромбоемболією легеневих артерій, раком, повторною венозною тромбоемболією та проксимальним тромбозом (у здухвинній вені) препарат рекомендується застосовувати у дозі 1 мг/кг двічі на добу. Тривалість лікування загалом становить 10 днів. Слід відразу ж розпочати терапію непрямими антикоагулянтами, при цьому лікування препаратом Клексан® необхідно продовжувати до досягнення терапевтичного антикоагулянтного ефекту (значення МНО [Міжнародні Нормалізовані Відносини] повинні становити 2,0-3,0). Профілактика тромбоутворення у системі екстракорпорального кровообігу під час гемодіалізу Рекомендована доза препарату Клексан становить у середньому 1 мг/кг маси тіла. При високому ризику розвитку кровотечі дозу слід зменшити до 0,5 мг/кг маси тіла при подвійному судинному доступі або до 0,75 мг/кг при одинарному судинному доступі. При гемодіалізі препарат Клексан® слід вводити до артеріальної ділянки шунту на початку сеансу гемодіалізу. Однієї дози, як правило, достатньо для чотиригодинного сеансу, однак при виявленні фібринових кілець при тривалому гемодіалізі можна додатково ввести препарат з розрахунку 0,5-1 мг/кг маси тіла. Дані щодо пацієнтів, які застосовують еноксапарин натрію для профілактики або лікування та під час сеансів гемодіалізу, відсутні. Лікування нестабільної стенокардії та інфаркту міокарда без підйому сегмента ST Препарат Клексан® вводиться з розрахунку 1 мг/кг маси тіла кожні 12 годин підшкірно при одночасному застосуванні антитромбоцитарної терапії. Середня тривалість терапії становить щонайменше 2 дні і продовжується до стабілізації клінічного стану пацієнта. Зазвичай введення препарату продовжується від 2-х до 8-ми днів. Ацетилсаліцилова кислота рекомендується всім пацієнтам, які не мають протипоказань, з початковою дозою 150-300 мг внутрішньо з наступною підтримуючою дозою 75-325 мг один раз на добу. Лікування гострого інфаркту міокарда з підйомом сегмента ST, медикаментозне або за допомогою черезшкірного коронарного втручання Лікування починають з одноразового внутрішньовенного болюсного введення еноксапарину натрію у дозі 30 мг. Відразу після нього підшкірно вводять еноксапарин натрію в дозі 1 мг/кг маси тіла. Далі препарат застосовують підшкірно по 1 мг/кг маси тіла кожні 12 год (максимально 100 мг еноксапарину натрію для кожної з перших двох підшкірних ін'єкцій, потім - по 1 мг/кг маси тіла для підшкірних доз, що залишилися, тобто, при масі тіла більше 100 кг, разова доза не може перевищувати 100 мг). Якнайшвидше після виявлення гострого інфаркту міокарда з підйомом сегмента ST пацієнтам необхідно призначити одночасно ацетилсаліцилову кислоту і, якщо немає протипоказань, прийом ацетилсаліцилової кислоти (у дозах 75-325 мг) слід продовжувати щодня протягом не менше 30 днів. Рекомендована тривалість лікування препаратом Клексан становить 8 днів або до виписки пацієнта зі стаціонару (якщо період госпіталізації становить менше 8 днів). При комбінації з тромболітиками (фібрин-специфічними та фібрин-неспецифічними) еноксапарин натрію повинен вводитися в інтервалі від 15 хв до початку тромболітичної терапії та до 30 хв після неї. У пацієнтів віком 75 років і більше не застосовується початкове внутрішньовенне болюсне введення. Препарат вводять підшкірно в дозі 0,75 мг/кг кожні 12 год (максимально 75 мг еноксапарину натрію для кожної з перших двох підшкірних ін'єкцій, потім - по 0,75 мг/кг маси тіла для підшкірних доз, що залишилися, тобто при масі тіла більше 100 кг, разова доза не може перевищувати 75 мг. У пацієнтів, яким проводиться черезшкірне коронарне втручання, у разі якщо остання підшкірна ін'єкція еноксапарину натрію була проведена менш ніж за 8 годин до роздування введеного в місце звуження коронарної артерії балонного катетера, додаткового введення еноксапарину натрію не потрібно. Якщо ж остання підшкірна ін'єкція еноксапарину натрію проводилася більш ніж за 8 годин до роздування балонного катетера, слід додаткове внутрішньовенне болюсне введення еноксапарину натрію в дозі 0,3 мг/кг. Режим дозування у спеціальних груп пацієнтів Діти віком до 18 років Безпека та ефективність застосування еноксапарину натрію у дітей не встановлені. Пацієнти похилого віку (старше 75 років) За винятком лікування інфаркту міокарда з підйомом сегмента st для інших показань зниження доз еноксапарину натрію у пацієнтів похилого віку за відсутності порушень функції нирок не потрібно. Пацієнти з порушеннями функції нирок Тяжкі порушення функції нирок (кк ≥15 і Застосування еноксапарину натрію не рекомендується пацієнтам з термінальною стадією хронічної хвороби нирок. У пацієнтів з тяжкими порушеннями функції нирок (кк ≥15 та При застосуванні препарату у терапевтичних дозах рекомендується наступна корекція режиму дозування: Звичайний режим дозування 1 мг/кг маси тіла підшкірно двічі на добу; при тяжкій нирковій недостатності 1 мг/кг маси тіла підшкірно один раз на добу. Звичайний режим дозування 1,5 мг/кг маси тіла підшкірно раз на добу; при тяжкій нирковій недостатності 1 мг/кг маси тіла підшкірно один раз на добу. Лікування гострого інфаркту міокарда з підйомом сегмента st у пацієнтів віком до 75 років: Звичайний режим дозування - одноразово внутрішньовенне болюсне введення 30 мг плюс 1 мг/кг маси тіла підшкірно; з наступним підшкірним введенням у дозі 1 мг/кг маси тіла двічі на добу (максимально 100 мг для кожної з перших двох підшкірних ін'єкцій); при тяжкій нирковій недостатності одноразово внутрішньовенне болюсне введення 30 мг плюс 1 мг/кг маси тіла підшкірно; з наступним підшкірним введенням у дозі 1 мг/кг маси тіла один раз на добу (максимально 100 мг лише для першої підшкірної ін'єкції). Звичайний режим дозування - 0,75 мг/кг маси тіла підшкірно двічі на добу без початкового внутрішньовенного болюсного введення (максимально 75 мг для кожної з двох перших підшкірних ін'єкцій). ); при тяжкій нирковій недостатності 1 мг/кг маси тіла підшкірно один раз на добу без початкового внутрішньовенного болюсного введення (максимально 100 мг лише для першої підшкірної ін'єкції). При застосуванні препарату з профілактичною метою рекомендується корекція режиму дозування Звичайний режим дозування 40 мг підшкірно раз на добу; при тяжкій нирковій недостатності 20 мг підшкірно один раз на добу. Звичайний режим дозування 20 мг підшкірно раз на добу; при тяжкій нирковій недостатності 20 мг підшкірно один раз на добу. Рекомендована корекція режиму дозування не застосовується при гемодіалізі. Порушення функції нирок легкої (кк ≥50 та Корекція дози не потрібна, проте пацієнти повинні перебувати під ретельним наглядом лікаря. Пацієнти з порушеннями функції печінки У зв'язку з відсутністю клінічних досліджень препарат Клексан слід застосовувати з обережністю у пацієнтів з порушеннями функції печінки.Інструкція для пацієнтаІнструкція з самостійного виконання ін'єкції препарату клексан® (попередньо заповнений шприц із захисною системою голки) Вимийте руки і ділянку шкіри (місце для ін'єкції), в яку ви будете вводити препарат водою з милом. висушіть їх. Прийміть зручне положення "сидячи" або "лежачи" та розслабтеся. переконайтеся, що ви добре бачите місце, в яке маєте намір вводити препарат. оптимально використовувати крісло для відпочинку, шезлонг чи ліжко, обкладене подушками для опори. Виберіть місце для ін'єкції в правій або лівій частині живота. це місце має знаходитись на відстані як мінімум 5 сантиметрів від пупка у напрямку до боків. не виконуйте самостійну ін'єкцію на відстані 5 сантиметрів від пупка або навколо рубців або синців. чергуйте місця ін'єкцій у правій та лівій частинах живота залежно від того, куди ви вводили препарат у попередній раз. Протріть місце для ін'єкції тампоном, змоченим спиртом. Обережно зніміть ковпачок із голки шприца із препаратом клексан®. відкладіть ковпачок. шприц попередньо заповнений та готовий до використання. не натискайте на поршень для витіснення бульбашок повітря до введення голки у місце ін'єкції. це може призвести до втрати препарату. після видалення ковпачка не допускайте дотику голки до будь-яких предметів. це необхідно для збереження стерильності голки. Утримуйте шприц у руці, якою ви пишете, так, як ви тримаєте олівець, а іншою рукою обережно стисніть протерте спиртом місце для введення препарату між великим та вказівним пальцями так, щоб утворити складку шкіри. утримуйте шкірну складку весь час, доки ви вводите препарат. Утримуйте шприц таким чином, щоб голка була спрямована донизу (вертикально під кутом 90°). введіть голку на її довжину в шкірну складку. Натисніть пальцем на поршень. це забезпечить введення препарату у підшкірну жирову тканину живота. утримуйте шкірну складку весь час, доки ви вводите препарат. Витягніть голку, потягнувши її назад без відхилення від осі. захисний механізм автоматично закриє голку. тепер можна припинити утримання шкірної складки. система безпеки, що забезпечує запуск захисного механізму, активується тільки після введення всього вмісту шприца шляхом натискання поршня протягом усього його ходу. З метою запобігання утворенню синця не розтирайте місце ін'єкції після введення препарату. Помістіть використаний шприц із захисним механізмом у контейнер для гострих предметів. щільно закрийте контейнер кришкою та зберігайте його у недоступному для дітей місці. При застосуванні препарату суворо дотримуйтесь рекомендацій, наведених у даній інструкції, а також вказівок лікаря чи провізора. У разі виникнення запитань зверніться до лікаря або провізору.ПередозуванняПри підшкірному застосуванні може призвести до геморагічних ускладнень. При прийомі навіть великих доз всмоктування препарату малоймовірне. Антикоагулянтні ефекти можна переважно нейтралізувати шляхом повільного внутрішньовенного введення протаміну сульфату, доза якого залежить від дози введеного препарату. Один мг (1 мг) протаміну сульфату нейтралізує антикоагулянтний ефект одного мг (1 мг) препарату Клексан® (див. інформацію про застосування препаратів протаміну сульфату), якщо еноксапарин натрію вводився не більше ніж за 8 годин до введення протаміну. 0,5 мг протаміну нейтралізує антикоагулянтний ефект 1 мг препарату, якщо з моменту введення останнього пройшло більше 8 годин або за необхідності введення другої дози протаміну. Якщо після введення еноксапарину натрію пройшло 12 год і більше, введення протаміну не потрібно. Однак навіть при введенні великих доз протаміну сульфату, анти-Ха активність препарату Клексан повністю не нейтралізується (максимально на 60%).Запобіжні заходи та особливі вказівкиЗагальні Низькомолекулярні гепарини не є взаємозамінними, так як вони різняться по процесу виробництва, молекулярної маси, специфічної анти-Ха активності, одиницям дозування та режиму дозування, з чим пов'язані відмінності в їх фармакокінетиці та біологічній активності (антитромбінова активність та взаємодія з тромбоцитами). Тому потрібно суворо виконувати рекомендації щодо застосування кожного препарату, що належить до класу низькомолекулярних гепаринів. Кровотеча Як і при застосуванні інших антикоагулянтів, при введенні препарату Клексан можливий розвиток кровотеч будь-якої локалізації. При розвитку кровотечі необхідно знайти джерело і призначити відповідне лікування. Еноксапарин натрію, як і інші антикоагулянти, слід застосовувати з обережністю при станах з підвищеним ризиком кровотечі, таких як: порушення гемостазу; виразкова хвороба в анамнезі; нещодавно перенесений ішемічний інсульт; тяжка артеріальна гіпертензія; діабетична ретинопатія; нейрохірургічне чи офтальмологічне оперативне втручання; одночасне застосування препаратів, що впливають на гемостаз. Кровотечі у пацієнтів похилого віку При застосуванні еноксапарину натрію у профілактичних дозах у пацієнтів похилого віку не відмічено збільшення ризику кровотеч. При застосуванні препарату в терапевтичних дозах у пацієнтів похилого віку (особливо у віці 80 років та старших) існує підвищений ризик розвитку кровотеч. Рекомендується проведення ретельного нагляду за станом таких пацієнтів. Одночасне застосування інших препаратів, що впливають на гемостаз Застосування препаратів, що впливають на гемостаз (саліцилати системної дії, у тому числі ацетилсаліцилова кислота в дозах, що надають протизапальну дію, нестероїдні протизапальні засоби, включаючи кеторолак, інші тромболітики (алтеплаза, ретеплаза, стрептокіназа, тенектеплаза, доза). , крім випадків, коли їх застосування є необхідним. Якщо показано їх одночасне застосування з еноксапарином натрію, слід проводити ретельне клінічне спостереження та моніторинг відповідних лабораторних показників. Ниркова недостатність У пацієнтів з порушенням функції нирок існує підвищений ризик розвитку кровотечі через збільшення системної експозиції еноксапарину натрію. У пацієнтів з тяжкими порушеннями функції нирок (КК ≥15 та Низька маса тіла Відзначалося збільшення експозиції еноксапарину натрію при його профілактичному застосуванні у жінок з масою тіла менше 45 кг та у чоловіків з масою тіла менше 57 кг, що може призводити до підвищеного ризику розвитку кровотеч. Рекомендується проведення ретельного контролю за станом таких пацієнтів. Пацієнти з ожирінням Пацієнти з ожирінням мають підвищений ризик розвитку тромбозів та емболій. Безпека та ефективність застосування еноксапарину натрію у профілактичних дозах у пацієнтів з ожирінням (ІМТ понад 30 кг/м2) до кінця не визначена та немає загальної думки щодо корекції дози. Рекомендується проведення контролю за станом пацієнтів на предмет розвитку симптомів та ознак тромбозів та емболій. Контроль кількості тромбоцитів у периферичній крові Ризик розвитку антитіло-опосередкованої гепарин-індукованої тромбоцитопенії (ГІТ) існує і при застосуванні низькомолекулярних гепаринів, при цьому цей ризик вищий у пацієнтів, які перенесли операції на серці, та пацієнтів з онкологічними захворюваннями. Якщо розвивається тромбоцитопенія, її зазвичай виявляють між 5-м і 21-м днями після початку терапії еноксапарином натрію. У зв'язку з цим рекомендується регулярно контролювати кількість тромбоцитів у периферичній крові до початку лікування еноксапарином натрію та під час його застосування. Слід визначати кількість тромбоцитів у крові за наявності симптомів, що вказують на ГІТ (новий епізод артеріальних та/або венозних тромбоемболічних ускладнень, хворобливе ураження шкіри на місці ін'єкції, алергічна або анафілактична реакція при лікуванні).При виникненні зазначених симптомів слід поінформувати лікаря. За наявності підтвердженого значного зниження кількості тромбоцитів (на 30-50% порівняно з вихідним показником) необхідно негайно відмінити еноксапарин натрію та перевести пацієнта на іншу антикоагулянтну терапію без застосування гепаринів. Спінальна/епідуральна анестезія Описано випадки виникнення нейроаксіальних гематом при застосуванні еноксапарину натрію при одночасному проведенні спінальної/епідуральної анестезії з розвитком тривалого або необоротного паралічу. Ризик цих явищ знижується при застосуванні препарату в дозі 40 мг або нижче. Ризик підвищується при застосуванні більш високих доз еноксапарину натрію, а також при використанні постійних катетерів після операції, або при одночасному застосуванні додаткових препаратів, що впливають на гемостаз, таких як нестероїдні протизапальні засоби. Ризик також підвищується при травматично проведеній або повторній спинномозковій пункції або у пацієнтів, які мають в анамнезі вказівки на перенесені операції у ділянці хребта або деформацію хребта. Для зниження можливого ризику кровотечі, пов'язаного із застосуванням еноксапарину натрію та проведенням епідуральної або спинальної анестезії/аналгезії, необхідно враховувати фармакокінетичний профіль препарату. Встановлення або видалення катетера краще проводити при низькому антикоагулянтному ефекті еноксапарину натрію, однак точний час для досягнення достатнього зниження антикоагулянтного ефекту у різних пацієнтів невідомий. Слід додатково враховувати, що у пацієнтів із КК 15-30 мл/хв виведення еноксапарину натрію сповільнюється. Якщо за призначенням лікаря застосовується антикоагулянтна терапія під час епідуральної/спінальної анестезії або люмбальної пункції, необхідно постійне спостереження за пацієнтом для виявлення будь-яких неврологічних симптомів, таких як болі в спині, порушення сенсорних і моторних функцій (оніміння або слабкість у нижніх кінцівках), порушення функції кишечника та/або сечового міхура. Пацієнта необхідно проінструктувати про необхідність негайного інформування лікаря у разі виникнення вищеописаних симптомів. При підозрі на симптоми, характерні для гематоми спинного мозку, потрібні термінова діагностика та лікування, включаючи, за необхідності, декомпресію спинного мозку. Гепарин-індукована тромбоцитопенія Застосування еноксапарину натрію у пацієнтів, які мають в анамнезі вказівки на наявність гепарин-індукованої тромбоцитопенії протягом останніх 100 днів або за наявності циркулюючих антитіл протипоказано (див. розділ "Протипоказання"). Антитіла, що циркулюють, можуть персистувати кілька років. Еноксапарин натрію слід застосовувати з особливою обережністю у пацієнтів, які мають в анамнезі (понад 100 днів) гепарин-індуковану тромбоцитопенію без циркулюючих антитіл. Рішення про застосування еноксапарину натрію в даній ситуації має бути прийняте тільки після оцінки співвідношення користь/ризик та за відсутності безгепаринової (що не містить гепарин) альтернативної терапії. Черезшкірна коронарна ангіопластика З метою мінімізації ризику кровотечі, пов'язаного з інвазивною судинною інструментальною маніпуляцією при лікуванні нестабільної стенокардії та інфаркту міокарда без зубця Q та гострого інфаркту міокарда з підйомом сегмента ST, ці процедури слід проводити в інтервалах між введенням препарату. Це необхідно для досягнення гемостазу у місці введення катетера після проведення черезшкірного коронарного втручання. При використанні закриває пристрою інтродьюсер стегнової артерії може бути видалено негайно. При застосуванні мануальної (ручної) компресії інтродьюсер стегнової артерії слід видалити через 6 годин після останньої внутрішньовенної або підшкірної ін'єкції еноксапарину натрію. Якщо лікування еноксапарином натрію триває, наступну дозу слід вводити не раніше, ніж через 6-8 годин після видалення інтродьюсера стегнової артерії.Необхідно стежити за місцем введення інтродьюсера, щоб своєчасно виявити ознаки кровотечі та утворення гематоми. Пацієнти з механічними штучними клапанами серця Застосування еноксапарину натрію для профілактики тромбоутворення у пацієнтів з штучними механічними клапанами серця вивчено недостатньо. Є окремі повідомлення про розвиток тромбозу клапанів серця у пацієнтів із механічними штучними клапанами серця на фоні терапії еноксапарином натрію для профілактики тромбоутворення. Зважаючи на недостатність клінічних даних та наявність неоднозначних факторів, включаючи основне захворювання, оцінка таких повідомлень утруднена. Вагітні жінки з механічними штучними клапанами серця Застосування еноксапарину натрію для профілактики тромбоутворення у вагітних жінок з штучними механічними клапанами серця вивчено недостатньо. У клінічному дослідженні за участю вагітних жінок з механічними штучними клапанами серця при застосуванні еноксапарину натрію в дозі 1 мг/кг маси тіла двічі на добу для зменшення ризику тромбозів та емболій, у 2-х з 8-ми жінок утворилися тромби, які призводили до блокування клапанів серця та до смерті матері та плода. Є окремі постмаркетингові повідомлення про тромбоз клапанів серця у вагітних жінок з механічними штучними клапанами серця, які отримували лікування еноксапарином натрію для профілактики тромбоутворення. Вагітні жінки з механічними штучними клапанами серця можуть мати підвищений ризик розвитку тромбозу та емболії. Некроз шкіри/шкірний васкуліт Повідомлялося про розвиток некрозу шкіри та шкірного васкуліту при застосуванні низькомолекулярних гепаринів. У разі розвитку некрозу шкіри/шкірного васкуліту застосування препарату слід припинити. Гострий інфекційний ендокардит Застосування гепарину не рекомендується у пацієнтів із гострим інфекційним ендокардитом через ризик розвитку геморагічного інсульту. У випадку, якщо застосування препарату вважається абсолютно необхідним, рішення слід приймати тільки після ретельної індивідуальної оцінки співвідношення користі та ризику. Лабораторні випробування У дозах, що застосовуються для профілактики тромбоемболічних ускладнень, препарат Клексан істотно не впливає на час кровотечі та показники зсідання крові, а також на агрегацію тромбоцитів або на зв'язування їх з фібриногеном. При підвищенні дози може подовжуватися АЧТВ та активований час згортання крові. Збільшення АЧТВ та активованого часу згортання не знаходяться у прямій лінійній залежності від збільшення антикоагулянтної активності препарату, тому немає потреби в їх моніторингу. Гіперкаліємія Гепарини можуть пригнічувати секрецію альдостерону наднирковими залозами, що призводить до розвитку гіперкаліємії, особливо у пацієнтів з цукровим діабетом, хронічною нирковою недостатністю, попереднім метаболічним ацидозом, які приймають лікарські препарати, що підвищують вміст калію. Слід регулярно контролювати вміст калію у плазмі, особливо у пацієнтів групи ризику. Профілактика венозних тромбозів та емболій у пацієнтів з гострими терапевтичними захворюваннями, які перебувають на постільному режимі У разі розвитку гострої інфекції, гострих ревматичних станів профілактичне застосування еноксапарину натрію виправдане лише, якщо перераховані вище стани поєднуються з одним з нижчеперелічених факторів ризику венозного тромбоутворення: вік понад 75 років; злоякісні новоутворення; тромбози та емболії в анамнезі; ожиріння; гормональна терапія; серцева недостатність; хронічна дихальна недостатність. Порушення функції печінки Еноксапарин натрію слід обережно застосовувати у пацієнтів з порушеннями функції печінки внаслідок збільшення ризику кровотеч. Корекція дози на підставі моніторування анти-Ха активності у пацієнтів з цирозом печінки є ненадійною та не рекомендується. Вплив на здатність до керування автотранспортом та управління механізмами Препарат Клексан не впливає на здатність керувати транспортними засобами та механізмами.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
1 349,00 грн
207,00 грн
Склад, форма випуску та упаковкаРозчин – 1 шприц: активна речовина: еноксапарин натрію 80 мг; розчинник: вода для ін'єкцій до 0,8 мл; 1 вид упаковки По 0,2 мл або 0,4 мл, або 0,6 мл, або 0,8 мл, або 1,0 мл розчину препарату скляний шприц (тип I) відповідно. По 2 шприци в блістер. По 1 або 5 блістерів разом із інструкцією із застосування в картонну пачку. 2 вид упаковки По 0,2 мл або 0,4 мл, або 0,6 мл, або 0,8 мл, або 1,0 мл розчину препарату у скляний шприц (тип 1) із захисною системою голки відповідно. По 2 шприци в блістер. По 1 або 5 блістерів разом із інструкцією із застосування в картонну пачку.Опис лікарської формиПрозорий, від безбарвного до блідо-жовтого кольору розчин.Фармакотерапевтична групаАнтикоагулянтний засіб прямої дії.ФармакокінетикаБіодоступність та абсорбція Абсолютна біодоступність еноксапарину натрію при підшкірному (п/к) введенні, що оцінюється на підставі анти-Ха активності, близька до 100%. Середня максимальна анти-Ха активність у плазмі крові відзначається через 3-5 годин після підшкірного введення і досягає приблизно 0,2, 0,4, 1,0 та 1,3 анти-Ха МО/мл після одноразового підшкірного введення препарату в дозі 20 мг, 40 мг, 1 мг/кг та 1,5 мг/кг. Внутрішньовенне болюсне введення препарату в дозі 30 мг, що супроводжується негайним підшкірним введенням препарату в дозі 1 мг/кг кожні 12 год, забезпечує початкову максимальну анти-Ха активність на рівні 1,16 МО/мл (n=16), середня експозиція препарату становить приблизно 88% від рівноважного стану, що досягається другого дня терапії. Фармакокінетика еноксапарину натрію у зазначених режимах дозування має лінійний характер. Варіабельність усередині та між групами пацієнтів низька. Після повторного підшкірного введення 40 мг еноксапарину натрію один раз на добу та підшкірного введення еноксапарину натрію в дозі 1,5 мг/кг маси тіла один раз на добу у здорових добровольців рівноважна концентрація досягається до 2 дня, причому площа під фармакокінетичною кривою в середньому на 15 % вище, ніж після одноразового введення. Після повторних підшкірних введень еноксапарину натрію в добовій дозі 1 мг/кг маси тіла двічі на добу рівноважна концентрація досягається через 3-4 дні, причому площа під фармакокінетичною кривою (AUC) в середньому на 65 % вище, ніж після одноразового введення, та середні значення максимальних концентрацій становлять відповідно 1,2 МО/мл та 0,52 МО/мл. Анти-Ха активність у плазмі крові приблизно в 10 разів нижча, ніж анти-Ха активність. Середня максимальна анти-Ха активність спостерігається приблизно через 3-4 години після підшкірного введення і досягає 0,13 МО/мл і 0,19 МО/мл після повторного введення 1 мг/кг маси тіла при дворазовому введенні та 1,5 мг/кг. маси тіла при одноразовому введенні відповідно. Розподіл Об'єм розподілу анти-Ха активності еноксапарину натрію становить приблизно 4,3 л і наближається до об'єму циркулюючої крові. Виведення Еноксапарин натрію є препаратом із низьким кліренсом. Після внутрішньовенного введення протягом 6 годин у дозі 1,5 мг/кг маси тіла середнє значення кліренсу анти-Ха у плазмі становить 0,74 л/год. Виведення препарату носить монофазний характер з періодами напіввиведення (Т1/2) близько 5 годин (після одноразового підшкірного введення) та близько 7 годин (після багаторазового введення препарату). Еноксапарин натрію в основному метаболізується в печінці шляхом десульфатування та/або деполімеризації з утворенням низькомолекулярних речовин з дуже низькою біологічною активністю. Виведення через нирки активних фрагментів препарату становить приблизно 10% від введеної дози, та загальна екскреція активних та неактивних фрагментів становить приблизно 40% від введеної дози. Особливі групи пацієнтів Пацієнти похилого віку (старше 75 років): фармакокінетичний профіль еноксапарину натрію не відрізняється у пацієнтів похилого віку та молодших пацієнтів при нормальній функції нирок. Однак унаслідок зниження функції нирок з віком може спостерігатися уповільнення виведення еноксапарину натрію у пацієнтів похилого віку. Порушення функції печінки: у дослідженні за участю пацієнтів з пізніми стадіями цирозу печінки, які отримували еноксапарин натрію в дозі 4000 ME (40 мг) один раз на добу, зниження максимальної анти-Ха активності було пов'язане зі збільшенням тяжкості порушення функції печінки (з оцінкою за шкалою Чайлд-Пью). Це зниження було зумовлено зниженням рівня AT-III, вторинним стосовно зниження синтезу АТ-III у пацієнтів з порушенням функції печінки. Порушення функції нирок: відмічено зменшення кліренсу еноксапарину натрію у пацієнтів із порушеннями функції нирок. Після повторного підшкірного введення 40 мг еноксапарину натрію один раз на добу відбувається збільшення активності анти-Ха, представленої площею під фармакокінетичною кривою (AUC) у пацієнтів з порушеннями функції нирок легкої (кліренс креатиніну (КК) ≥50 і Гемодіаліз: фармакокінетика еноксапарину натрію порівнянна з показниками в контрольній популяції після одноразових внутрішньовенних введень доз 25 ME, 50 ME або 100 МО/кг (0,25, 0.50 або 1,0 мг/кг), проте AUC була вдвічі , ніж у контрольній популяції. Маса тіла: після повторних підшкірних введень у дозуванні 1,5 мг/кг один раз на добу середня AUC анти-Ха активності в стані рівноваги незначно вища у пацієнтів із надмірною масою тіла (ІМТ 30-48 кг/м2) порівняно з пацієнтами із звичайною середньою масою тіла, тоді як максимальна анти-Ха активність плазми крові не збільшується. У пацієнтів із надмірною масою тіла при підшкірному введенні препарату кліренс дещо менший. Якщо не робити поправку дози з урахуванням маси тіла пацієнта, то після одноразового підшкірного введення 40 мг еноксапарину натрію анти-Ха активність буде на 52 % вище у жінок з масою тіла менше 45 кг і на 27 % вище у чоловіків з масою тіла менше 57 кг порівняно з пацієнтами із звичайною середньою масою тіла.ФармакодинамікаВ очищеній системі in vitro еноксапарин натрію має високу анти-Ха активність (приблизно 100 МО/мл) та низьку анти-Ха або антитромбінову активність (приблизно 28 МО/мл). Ця антикоагулянтна активність діє через антитромбін III (АТ-III), забезпечуючи антикоагулянтну активність у людей. Крім анти-Ха/IIа активності також виявлено додаткові антикоагулянтні та протизапальні властивості еноксапарину натрію як у здорових людей та пацієнтів, так і на моделях тварин. Це включає АТ-III-залежне інгібування інших факторів згортання, як фактор Vila, активацію вивільнення інгібітору шляху тканинного фактора (ПТФ), а також зниження вивільнення фактора Віллебранду з ендотелію судин у кровотік. Ці фактори забезпечують антикоагулянтний ефект еноксапарину натрію загалом. При застосуванні його у профілактичних дозах він незначно змінює активований частковий тромбопластиновий час (АЧТВ), практично не впливає на агрегацію тромбоцитів та на ступінь зв'язування фібриногену з рецепторами тромбоцитів.Показання до застосуванняПрофілактика венозних тромбозів та емболій при хірургічних втручаннях у пацієнтів помірного та високого ризику, особливо при ортопедичних та загальнохірургічних втручаннях, включаючи онкологічні. Профілактика венозних тромбозів та емболій у пацієнтів, що знаходяться на постільному режимі, внаслідок гострих терапевтичних захворювань, включаючи гостру серцеву недостатність та декомпенсацію хронічної серцевої недостатності (III або IV клас NYHA), дихальну недостатність, а також при тяжких інфекціях та ревматичних захворюваннях при підвищеному тромбоутворення. Лікування тромбозу глибоких вен з тромбоемболією легеневої артерії або без тромбоемболії легеневої артерії, крім випадків тромбоемболії легеневої артерії, які потребують тромболітичної терапії або хірургічного втручання. Профілактика тромбоутворення у системі екстракорпорального кровообігу під час гемодіалізу. Гострий коронарний синдром: Лікування нестабільної стенокардії та інфаркту міокарда без підйому сегмента ST у поєднанні з пероральним прийомом ацетилсаліцилової кислоти. Лікування гострого інфаркту міокарда з підйомом сегмента ST у пацієнтів, які підлягають медикаментозному лікуванню або подальшому корконарному втручанню (ЧКВ).Протипоказання до застосуванняПідвищена чутливість до еноксапарину натрію, гепарину або його похідних, включаючи інші низькомолекулярні гепарини. Активна клінічно значуща кровотеча, а також стани та захворювання, при яких є високий ризик розвитку кровотечі, включаючи нещодавно перенесений геморагічний інсульт, гостру виразку шлунково-кишкового тракту (ЖКТ), наявність злоякісного новоутворення з високим ризиком кровотеч, нещодавно перенесені операції на головній та спинній мозку, офтальмологічні операції, відома чи передбачувана наявність варикозного розширених вен стравоходу, артеріовенозні мальформації, судинні аневризми, судинні аномалії спинного та головного мозку. Спінальна або епідуральна анестезія або локо-регіональна анестезія, коли еноксапарин натрію застосовувався для лікування попередніх 24 год. Імуноопосередкована гепарин-індукована громбоцитопенія (в анамнезі) протягом 100 останніх днів або наявність у крові циркулюючих антитромбоцитарних антитіл. Дитячий вік до 18 років, оскільки ефективність та безпека у даної категорії пацієнтів не встановлені. Стани, у яких є потенційний ризик розвитку кровотечі: порушення гемостазу (в т.ч. гемофілія, тромбоцитопенія, гіпокоагуляція, хвороба Віллебранда та ін), важкий васкуліт; виразкова хвороба шлунка або дванадцятипалої кишки або інші ерозивно-виразкові ураження шлунково-кишкового тракту в анамнезі; нещодавно перенесений ішемічний інсульт; неконтрольована тяжка артеріальна гіпертензія; діабетична або геморагічна ретинопатія; тяжкий цукровий діабет; нещодавно перенесена чи передбачувана неврологічна чи офтальмологічна операція; проведення спинальної або епідуральної анестезії (потенційна небезпека розвитку гематоми); спинномозкова пункція (нещодавно перенесена); недавні пологи; ендокардит бактеріальний (гострий або підгострий); перикардит або перикардіальний випіт; ниркова та/або печінкова недостатність; внутрішньоматкова контрацепція (ВМК); тяжка травма (особливо центральної нервової системи); відкриті рани на великих поверхнях; одночасний прийом препаратів, що впливають на систему гемостазу; гепарин-індукована тромбоцитопенія без циркулюючих антитіл в анамнезі (понад 100 днів). У компанії відсутні дані щодо клінічного застосування препарату Клексан при таких захворюваннях: активний туберкульоз, променева терапія (нещодавно перенесена).Вагітність та лактаціяВагітність Відомостей, що еноксапарин натрію проникає через плацентарний бар'єр під час вагітності, немає. Так як відсутні адекватні та добре контрольовані дослідження за участю вагітних жінок, а дослідження на тваринах не завжди прогнозують реакцію на введення еноксапарину натрію під час вагітності у людини, застосовувати його під час вагітності слід лише у виняткових випадках, коли є нагальна необхідність його застосування, встановлена лікарем. Рекомендується проведення контролю за станом пацієнток щодо появи ознак кровотечі або надмірної антикоагуляції, пацієнтки повинні бути попереджені про ризик виникнення кровотеч. Немає даних про підвищений ризик розвитку кровотеч, тромбоцитопенії або остеопорозу у вагітних жінок, за винятком випадків, відмічених у пацієнток із штучними клапанами серця. При плануванні епідуральної анестезії рекомендується перед її проведенням відмінити еноксапарин натрію. Період грудного вигодовування Невідомо, чи екскретується незмінений еноксапарин натрію у грудне молоко. Всмоктування еноксапарину натрію в шлунково-кишковому тракті у новонародженого малоймовірне. Препарат Клексан може застосовуватись у період грудного вигодовування.Побічна діяВивчення побічних ефектів еноксапарину натрію проводилося більш ніж у 15000 пацієнтів, які брали участь у клінічних дослідженнях, з них у 1776 пацієнтів - при профілактиці венозних тромбозів та емболій при загальнохірургічних та ортопедичних операціях: у 1169 пацієнтів постільний режим внаслідок гострих терапевтичних захворювань; у 559 пацієнтів – при лікуванні тромбозу глибоких вен з тромбоемболією легеневої артерії або без тромбоемболії легеневої артерії; у 1578 пацієнтів – при лікуванні нестабільної стенокардії та інфаркту міокарда без зубця Q; у 10176 пацієнтів – при лікуванні інфаркту міокарда з підйомом сегмента ST. Режим введення еноксапарину натрію відрізнявся залежно від показань. При профілактиці венозних тромбозів та емболій при загальнохірургічних та ортопедичних операціях або у пацієнтів, які перебувають на постільному режимі, вводилося 40 мг підшкірно один раз на добу. При лікуванні тромбозу глибоких вен з тромбоемболією легеневої артерії або без неї пацієнти отримували еноксапарин натрію з розрахунку 1 мг/кг маси тіла підшкірно кожні 12 годин або 1,5 мг/кг маси тіла підшкірно один раз на добу. При лікуванні нестабільної стенокардії та інфаркту міокарда без зубця Q доза еноксапарину натрію становила 1 мг/кг маси тіла підшкірно кожні 12 год, а у разі інфаркту міокарда з підйомом сегмента ST проводилося внутрішньовенне болюсне введення 30 мг з подальшим в кожні 12 год.Частота виникнення небажаних реакцій визначалася відповідно до класифікації Всесвітньої Організації Охорони Здоров'я: дуже часто (≥1/10); часто (≥1/100 та Порушення з боку судин: Кровотечі У клінічних дослідженнях кровотечі були найпоширенішими небажаними реакціями. До них належали великі кровотечі, що спостерігалися у 4,2% пацієнтів (кровотеча вважалася великою, якщо вона супроводжувалася зниженням вмісту гемоглобіну на 2 г/л і більше, вимагало переливання 2 або більше доз компонентів крові, а також якщо воно було заочеревинним або внутрішньочерепним. ). Деякі з цих випадків були летальними. Як і при застосуванні інших антикоагулянтів, при застосуванні еноксапарину натрію можливе виникнення кровотечі, особливо за наявності факторів ризику, що сприяють розвитку кровотечі, при проведенні інвазивних процедур або застосуванні препаратів, що порушують гемостаз. При описі кровотеч нижче знак "*" означає вказівку на такі види кровотеч: гематома, екхімози (крім ін'єкції), ранові гематоми, гематурія, носові кровотечі, шлунково-кишкові кровотечі. Дуже часто: кровотечі* при профілактиці венозних тромбозів у хірургічних пацієнтів та лікуванні тромбозу глибоких вен з тромбоемболією легеневої артерії або без неї. Часто: кровотечі* при профілактиці венозних тромбозів у пацієнтів, які перебувають на постільному режимі, та при лікуванні нестабільної стенокардії, інфаркту міокарда без зубця Q та інфаркту міокарда з підйомом сегмента ST. Нечасто: заочеревинні кровотечі та внутрішньочерепні крововиливи у пацієнтів при лікуванні тромбозу глибоких вен з тромбоемболією легеневої артерії або без неї. а також при лікуванні інфаркту міокарда із підйомом сегмента ST. Рідко: заочеревинні кровотечі при профілактиці венозних тромбозів у хірургічних пацієнтів та при лікуванні нестабільної стенокардії та інфаркту міокарда без зубця Q. Тромбоцитопенія та тромбоцитоз Часто: тромбоцитоз (кількість тромбоцитів у периферичній крові більше 400x109/л) при профілактиці венозних тромбозів у хірургічних пацієнтів та лікуванні тромбозу глибоких вен з тромбоемболією легеневої артерії або без неї. Часто: тромбоцитоз при лікуванні пацієнтів із гострим інфарктом міокарда із підйомом сегмента ST. Тромбоцитопенія при профілактиці венозних тромбозів у хірургічних пацієнтів та лікуванні тромбозу глибоких вен з тромбоемболією легеневої артерії або без неї. а також при гострому інфаркті міокарда із підйомом сегмента ST. Нечасто: тромбоцитопенія при профілактиці венозних тромбозів у пацієнтів, які перебувають на постільному режимі, та при лікуванні нестабільної стенокардії та інфаркту міокарда без зубця Q. Дуже рідко: аутоімунна тромбоцитопенія при лікуванні пацієнтів із гострим інфарктом міокарда з підйомом сегмента ST. Інші клінічно значущі небажані реакції незалежно від показань Небажані реакції, представлені нижче, згруповані за системно-органними класами, дано із зазначенням визначеної вище частоти їх виникнення та в порядку зменшення їх тяжкості. Порушення з боку крові та лімфатичної системи: - Часто: кровотеча, тромбоцитопенія, тромбоцитоз; Рідко: випадки розвитку аутоімунної тромбоцитопенії з тромбозом; у деяких випадках тромбоз ускладнювався розвитком інфаркту органів або ішемії кінцівок. Порушення з боку імунної системи: Найчастіше: алергічні реакції. Порушення з боку печінки та жовчовивідних шляхів: Дуже часто: підвищення активності "печінкових" ферментів, головним чином підвищення активності трансаміназ, що більш ніж утричі перевищує верхню межу норми. Порушення з боку шкіри та підшкірних тканин - Часто: кропив'янка, свербіж шкіри, еритема; Нечасто: бульозний дерматит. Загальні розлади та порушення у місці введення: Часто: гематома у місці ін'єкції, біль у місці ін'єкції, набряк у місці ін'єкції, кровотеча, реакції підвищеної чутливості, запалення, утворення ущільнень у місці ін'єкції. Нечасто: подразнення у місці ін'єкції, некроз шкіри у місці ін'єкції. Дані, отримані після виходу препарату ринку Наступні небажані реакції спостерігалися при постмаркетинговому застосуванні препарату Клексан. Про ці побічні реакції були спонтанні повідомлення. Порушення з боку імунної системи: Рідко: анафілактичні/анафілактоїдні реакції, включаючи шок. Порушення з боку нервової системи: Часто: біль голови. Порушення з боку судин: Рідко: при застосуванні еноксапарину натрію на тлі спінальної/епідуральної анестезії або спінальної пункції спостерігалися випадки розвитку спінальної гематоми (або нейроаксіальної гематоми). Ці реакції призводили до розвитку неврологічних порушень різного ступеня тяжкості, включаючи стійкий або необоротний параліч. Порушення з боку крові або лімфатичної системи: - Часто: геморагічна анемія; Рідко: еозинофілія. Порушення з боку шкіри та підшкірних тканин: Рідко: алопеція; у місці ін'єкції може розвинутися шкірний васкуліт, некроз шкіри, яким зазвичай передує поява пурпури або еритематозних папул (інфільтрованих та болючих). У цих випадках терапію препаратом Клексан слід припинити. Можливе утворення твердих запальних вузликів-інфільтратів у місці ін'єкцій препарату, які зникають через кілька днів і не є підставою для відміни препарату. Порушення з боку печінки та жовчовивідних шляхів: - Нечасто: гепатоцелюлярне ураження печінки; Рідко: холестатична поразка печінки. Порушення з боку скелетно-м'язової та сполучної тканини: Рідко: остеопороз при тривалій терапії (понад три місяці). Лабораторні та інструментальні дані - Рідко: гіперкаліємія.Взаємодія з лікарськими засобамиПрепарат Клексан не можна змішувати з іншими препаратами! Нерекомендовані комбінації Препарати, що впливають на гемостаз (саліцилати системної дії, ацетилсаліцилова кислота в дозах, що мають протизапальну дію, нестероїдні протизапальні препарати (НПЗП), включаючи кеторолак, інші тромболітики (алтеплаза, ретеплаза, стрептокіназа, трептокіназа, натрію. При необхідності одночасного застосування з еноксапарином натрію слід дотримуватися обережності та проводити ретельне клінічне спостереження та моніторинг відповідних лабораторних показників. Комбінації, що вимагають дотримання обережності Інші лікарські препарати, що впливають на гемостаз, такі як: інгібітори агрегації тромбоцитів, включаючи ацетилсаліцилову кислоту в дозах, що мають антиагрегантну дію (кардіопротекція), клопідогрел, тиклопідин та антагоністи глікопротеїнових ПЬ/Ша рецепторів, показані при гострому коронарному синдромі, внаслідок підвищеного ризику; декстран із молекулярною масою 40 кДа; системні глюкокортикостероїди. Лікарські препарати, що підвищують вміст калію При одночасному застосуванні з лікарськими препаратами, що підвищують вміст калію в сироватці, слід проводити клінічний та лабораторний контроль.Спосіб застосування та дозиПідшкірно, за винятком особливих випадків (див. нижче підрозділи "Лікування інфаркту міокарда з підйомом сегмента ST, медикаментозне або за допомогою черезшкірного коронарного втручання" та "Профілактика тромбоутворення в системі екстракорпорального кровообігу при проведенні гемодіалізу"). Профілактика венозних тромбозів та емболії при хірургічних втручаннях у пацієнтів помірного та високого ризику Пацієнтам з помірним ризиком розвитку тромбозів та емболій (наприклад, абдомінальні операції) рекомендована доза препарату Клексан становить 20 мг один раз на добу підшкірно. Першу ін'єкцію слід зробити за 2 години до хірургічного втручання. Пацієнтам з високим ризиком розвитку тромбозів та емболій (наприклад, при ортопедичних операціях, хірургічних операціях в онкології, пацієнтам з додатковими факторами ризику, не пов'язаними з операцією, такими як вроджена або набута тромбофілія, злоякісне новоутворення, постільний режим понад три доби, тромбоз в анамнезі, варикозне розширення вен нижніх кінцівок, вагітність) препарат рекомендується у дозі 40 мг один раз на добу підшкірно, із введенням першої дози за 12 годин до хірургічного втручання. За необхідності більш ранньої передопераційної профілактики (наприклад, у пацієнтів з високим ризиком розвитку тромбозів та тромбоемболій, що очікують відстрочену ортопедичну операцію) остання ін'єкція повинна бути зроблена за 12 годин до операції та через 12 годин після операції. Тривалість лікування препаратом Клексан у середньому становить 7-10 днів. При необхідності терапію можна продовжувати доти, доки зберігається ризик розвитку тромбозу та емболії, і доти, доки пацієнт не перейде на амбулаторний режим. При великих ортопедичних операціях може бути доцільним після початкової терапії продовження лікування шляхом введення препарату Клексан у дозі 40 мг один раз на добу протягом п'яти тижнів. Для пацієнтів з високим ризиком венозних тромбоемболій, які перенесли хірургічне втручання, абдомінальну та тазову хірургію через онкологічне захворювання, може бути доцільним збільшення тривалості введення препарату Клексан у дозі 40 мг один раз на добу протягом чотирьох тижнів. Профілактика венозних тромбозів та емболій у пацієнтів, які перебувають на постільному режимі внаслідок гострих терапевтичних захворювань Рекомендована доза препарату Клексан становить 40 мг один раз на добу, підшкірно, протягом 6-14 днів. Терапію слід продовжувати до переходу пацієнта на амбулаторний режим (максимально протягом 14 днів). Лікування тромбозу глибоких вен з тромбоемболією легеневої артерії або без тромбоемболії легеневої артерії Препарат вводиться підшкірно із розрахунку 1,5 мг/кг маси тіла один раз на добу або 1 мг/кг маси тіла двічі на добу. Режим дозування повинен вибиратися лікарем на основі оцінки ризику розвитку тромбоемболії та ризику розвитку кровотеч. У пацієнтів без тромбоемболічних ускладнень та з низьким ризиком розвитку венозної тромбоемболії препарат рекомендується вводити підшкірно із розрахунку 1.5 мг/кг маси тіла один раз на добу. У всіх інших пацієнтів, включаючи пацієнтів з ожирінням, симптоматичною тромбоемболією легеневих артерій, раком, повторною венозною тромбоемболією та проксимальним тромбозом (у здухвинній вені) препарат рекомендується застосовувати у дозі 1 мг/кг двічі на добу. Тривалість лікування загалом становить 10 днів. Слід відразу ж розпочати терапію непрямими антикоагулянтами, при цьому лікування препаратом Клексан® необхідно продовжувати до досягнення терапевтичного антикоагулянтного ефекту (значення МНО [Міжнародні Нормалізовані Відносини] повинні становити 2,0-3,0). Профілактика тромбоутворення у системі екстракорпорального кровообігу під час гемодіалізу Рекомендована доза препарату Клексан становить у середньому 1 мг/кг маси тіла. При високому ризику розвитку кровотечі дозу слід зменшити до 0,5 мг/кг маси тіла при подвійному судинному доступі або до 0,75 мг/кг при одинарному судинному доступі. При гемодіалізі препарат Клексан® слід вводити до артеріальної ділянки шунту на початку сеансу гемодіалізу. Однієї дози, як правило, достатньо для чотиригодинного сеансу, однак при виявленні фібринових кілець при тривалому гемодіалізі можна додатково ввести препарат з розрахунку 0,5-1 мг/кг маси тіла. Дані щодо пацієнтів, які застосовують еноксапарин натрію для профілактики або лікування та під час сеансів гемодіалізу, відсутні. Лікування нестабільної стенокардії та інфаркту міокарда без підйому сегмента ST Препарат Клексан® вводиться з розрахунку 1 мг/кг маси тіла кожні 12 годин підшкірно при одночасному застосуванні антитромбоцитарної терапії. Середня тривалість терапії становить щонайменше 2 дні і продовжується до стабілізації клінічного стану пацієнта. Зазвичай введення препарату продовжується від 2-х до 8-ми днів. Ацетилсаліцилова кислота рекомендується всім пацієнтам, які не мають протипоказань, з початковою дозою 150-300 мг внутрішньо з наступною підтримуючою дозою 75-325 мг один раз на добу. Лікування гострого інфаркту міокарда з підйомом сегмента ST, медикаментозне або за допомогою черезшкірного коронарного втручання Лікування починають з одноразового внутрішньовенного болюсного введення еноксапарину натрію у дозі 30 мг. Відразу після нього підшкірно вводять еноксапарин натрію в дозі 1 мг/кг маси тіла. Далі препарат застосовують підшкірно по 1 мг/кг маси тіла кожні 12 год (максимально 100 мг еноксапарину натрію для кожної з перших двох підшкірних ін'єкцій, потім - по 1 мг/кг маси тіла для підшкірних доз, що залишилися, тобто, при масі тіла більше 100 кг, разова доза не може перевищувати 100 мг). Якнайшвидше після виявлення гострого інфаркту міокарда з підйомом сегмента ST пацієнтам необхідно призначити одночасно ацетилсаліцилову кислоту і, якщо немає протипоказань, прийом ацетилсаліцилової кислоти (у дозах 75-325 мг) слід продовжувати щодня протягом не менше 30 днів. Рекомендована тривалість лікування препаратом Клексан становить 8 днів або до виписки пацієнта зі стаціонару (якщо період госпіталізації становить менше 8 днів). При комбінації з тромболітиками (фібрин-специфічними та фібрин-неспецифічними) еноксапарин натрію повинен вводитися в інтервалі від 15 хв до початку тромболітичної терапії та до 30 хв після неї. У пацієнтів віком 75 років і більше не застосовується початкове внутрішньовенне болюсне введення. Препарат вводять підшкірно в дозі 0,75 мг/кг кожні 12 год (максимально 75 мг еноксапарину натрію для кожної з перших двох підшкірних ін'єкцій, потім - по 0,75 мг/кг маси тіла для підшкірних доз, що залишилися, тобто при масі тіла більше 100 кг, разова доза не може перевищувати 75 мг. У пацієнтів, яким проводиться черезшкірне коронарне втручання, у разі якщо остання підшкірна ін'єкція еноксапарину натрію була проведена менш ніж за 8 годин до роздування введеного в місце звуження коронарної артерії балонного катетера, додаткового введення еноксапарину натрію не потрібно. Якщо ж остання підшкірна ін'єкція еноксапарину натрію проводилася більш ніж за 8 годин до роздування балонного катетера, слід додаткове внутрішньовенне болюсне введення еноксапарину натрію в дозі 0,3 мг/кг. Режим дозування у спеціальних груп пацієнтів Діти віком до 18 років Безпека та ефективність застосування еноксапарину натрію у дітей не встановлені. Пацієнти похилого віку (старше 75 років) За винятком лікування інфаркту міокарда з підйомом сегмента st для інших показань зниження доз еноксапарину натрію у пацієнтів похилого віку за відсутності порушень функції нирок не потрібно. Пацієнти з порушеннями функції нирок Тяжкі порушення функції нирок (кк ≥15 і Застосування еноксапарину натрію не рекомендується пацієнтам з термінальною стадією хронічної хвороби нирок. У пацієнтів з тяжкими порушеннями функції нирок (кк ≥15 та При застосуванні препарату у терапевтичних дозах рекомендується наступна корекція режиму дозування: Звичайний режим дозування 1 мг/кг маси тіла підшкірно двічі на добу; при тяжкій нирковій недостатності 1 мг/кг маси тіла підшкірно один раз на добу. Звичайний режим дозування 1,5 мг/кг маси тіла підшкірно раз на добу; при тяжкій нирковій недостатності 1 мг/кг маси тіла підшкірно один раз на добу. Лікування гострого інфаркту міокарда з підйомом сегмента st у пацієнтів віком до 75 років: Звичайний режим дозування - одноразово внутрішньовенне болюсне введення 30 мг плюс 1 мг/кг маси тіла підшкірно; з наступним підшкірним введенням у дозі 1 мг/кг маси тіла двічі на добу (максимально 100 мг для кожної з перших двох підшкірних ін'єкцій); при тяжкій нирковій недостатності одноразово внутрішньовенне болюсне введення 30 мг плюс 1 мг/кг маси тіла підшкірно; з наступним підшкірним введенням у дозі 1 мг/кг маси тіла один раз на добу (максимально 100 мг лише для першої підшкірної ін'єкції). Звичайний режим дозування - 0,75 мг/кг маси тіла підшкірно двічі на добу без початкового внутрішньовенного болюсного введення (максимально 75 мг для кожної з двох перших підшкірних ін'єкцій). ); при тяжкій нирковій недостатності 1 мг/кг маси тіла підшкірно один раз на добу без початкового внутрішньовенного болюсного введення (максимально 100 мг лише для першої підшкірної ін'єкції). При застосуванні препарату з профілактичною метою рекомендується корекція режиму дозування Звичайний режим дозування 40 мг підшкірно раз на добу; при тяжкій нирковій недостатності 20 мг підшкірно один раз на добу. Звичайний режим дозування 20 мг підшкірно раз на добу; при тяжкій нирковій недостатності 20 мг підшкірно один раз на добу. Рекомендована корекція режиму дозування не застосовується при гемодіалізі. Порушення функції нирок легкої (кк ≥50 та Корекція дози не потрібна, проте пацієнти повинні перебувати під ретельним наглядом лікаря. Пацієнти з порушеннями функції печінки У зв'язку з відсутністю клінічних досліджень препарат Клексан слід застосовувати з обережністю у пацієнтів з порушеннями функції печінки. Особливості введення препарату Попередньо заповнений одноразовий шприц готовий до застосування. Препарат не можна вводити внутрішньом'язово! Підшкірне введення Ін'єкції бажано проводити у положенні пацієнта "лежачи". При використанні попередньо заповнених шприців на 20 мг і 40 мг, щоб уникнути втрати препарату перед ін'єкцією, не треба видаляти бульбашки повітря зі шприца. Ін'єкції слід проводити по черзі у ліву або праву передньолатеральну або задньолатеральну поверхню живота. Голку необхідно ввести на всю довжину, вертикально (не збоку), у шкірну складку, зібрану та утримувану до завершення ін'єкції між великим та вказівним пальцями. Складку шкіри відпускають лише після завершення ін'єкції. Не слід масажувати місце ін'єкції після введення препарату. Внутрішньовенне болюсне введення Внутрішньовенне болюсне введення еноксапарину натрію повинно проводитись через венозний катетер. Еноксапарин натрію не повинен змішуватись або вводитися разом з іншими лікарськими препаратами. Для того, щоб уникнути присутності в інфузійній системі слідів інших лікарських препаратів та їх взаємодії з еноксапарином натрію, венозний катетер повинен промиватися достатньою кількістю 0,9 % розчину натрію хлориду або 5 % розчину декстрози до та після внутрішньовенного болюсного введення еноксапарину. Еноксапарин натрію може безпечно вводитися з 0.9% розчином натрію хлориду та 5% розчином декстрози. Для проведення болюсного введення 30 мг еноксапарину натрію при лікуванні гострого інфаркту міокарда з підйомом сегмента ST зі скляних шприців 60 мг, 80 мг та 100 мг видаляють зайву кількість препарату для того, щоб у них залишалося лише 30 мг (0,3 мл). Доза 30 мг може безпосередньо вводитися внутрішньовенно. Для внутрішньовенного болюсного введення еноксапарину натрію через венозний катетер можуть використовуватися попередньо заповнені шприци для підшкірного введення препарату 60 мг, 80 мг і 100 мг. Рекомендується використовувати шприци 60 мг, так як це зменшує кількість препарату, що видаляється зі шприца. Шприци 20 мг не використовуються, тому що в них недостатньо препарату для болюсного введення 30 мг еноксапарину натрію. Шприци 40 мг не використовуються, тому що на них відсутні поділки і тому неможливо точно відміряти кількість 30 мг. Для підвищення точності додаткового внутрішньовенного болюсного введення малих обсягів у венозний катетер під час проведення черезшкірних коронарних втручань рекомендується розвести препарат до концентрації 3 мг/мл. Розведення розчину рекомендується проводити безпосередньо перед введенням. Для одержання розчину еноксапарину натрію з концентрацією 3 мг/мл за допомогою попередньо заповненого шприца 60 мг рекомендується використовувати ємність з інфузійним розчином 50 мл (тобто з 0,9 % розчином натрію хлориду або 5 % розчином декстрози). З ємності з інфузійним розчином за допомогою звичайного шприца вилучається та видаляється 30 мл розчину. Еноксапарин натрію (вміст шприца для підшкірного введення 60 мг) вводиться в 20 мл інфузійного розчину, що залишилися в ємності. Вміст ємності з розведеним розчином еноксапарину натрію обережно перемішується. Для введення за допомогою шприца витягується необхідний обсяг розведеного розчину еноксапарину натрію, який розраховується за формулою: Об'єм розведеного розчину = Маса тіла пацієнта (кг) х 0,1 або за допомогою наведеної нижче таблиці. Об'єми, які повинні вводитися внутрішньовенно після розведення до концентрації 3 мг/мл Маса тіла пацієнта, кг Необхідна доза (0,3 мг/кг), мг Об'єм розчину, розведеного до концентрації 3 мг/мл, необхідний для введення. 45 13,5 4,5 50 15 5 55 16,5 5,5 60 18 6 65 19,5 6,5 70 21 7 75 22,5 7,5 80 24 8 85 25,5 8,5 90 27 9 95 28,5 9,5 100 30 10 105 31,5 10,5 110 33 11 115 34,5 11,5 120 36 12 125 37,5 12,5 130 39 13 135 40,5 13,5 140 42 14 145 43,5 14,5 150 45 15 Переключення між еноксапарином натрію та пероральними антикоагулянтами: Перемикання між еноксапарином натрію та антагоністами вітаміну до (авк). Для моніторування ефекту авк необхідне спостереження лікаря та проведення лабораторних досліджень [протромбіновий час, представлений як багато]. Оскільки для розвитку максимального ефекту авк потрібен час, терапія еноксапарином натрію повинна продовжуватися в постійній дозі так довго, як необхідно для підтримання значень багато (за даними двох послідовних визначень) в бажаному терапевтичному діапазоні залежно від показань. Для пацієнтів, які отримують авк, скасування авк та введення першої дози еноксапарину натрію повинні проводитися після того, як багато знизилося нижче за межу терапевтичного діапазону. Переключення між еноксапарином натрію та пероральними антикоагулянтами прямої дії (поак). Скасування еноксапарину натрію та призначення поак повинні проводитися за 0-2 години до моменту чергового запланованого введення еноксапарину натрію відповідно до інструкції щодо застосування пероральних антикоагулянтів. Для пацієнтів, які отримують поак, введення першої дози еноксапарину натрію та відміна пероральних антикоагулянтів прямої дії повинні проводитися в момент часу, що відповідає черговому запланованому застосуванню поак. Застосування при спинальній/епідуральній анестезії або люмбальній пункції. У разі застосування антикоагулянтної терапії під час проведення епідуральної або спинальної анестезії/аналгезії або люмбальної пункції необхідне проведення неврологічного моніторування через ризик розвитку нейроаксіальних гематом. Застосування еноксапарину натрію у профілактичних дозах. Встановлення або видалення катетера повинно проводитися як мінімум 12 годин після останньої ін'єкції профілактичної дози еноксапарину натрію. При використанні безперервної техніки необхідно дотримуватися щонайменше 12 год. інтервал до видалення катетера. У пацієнтів з кк ≥15 та Застосування еноксапарину натрію у терапевтичних дозах Встановлення або видалення катетера повинно проводитися як мінімум 24 години після останньої ін'єкції терапевтичної дози еноксапарину натрію. При використанні безперервної техніки необхідно дотримуватися щонайменше 24 години інтервал до видалення катетера. У пацієнтів з кк ≥15 та Пацієнтам, які отримують еноксапарин натрію в дозах 0,75 мг/кг або 1 мг/кг маси тіла двічі на добу, не слід вводити другу дозу з метою збільшення інтервалу перед встановленням або заміною катетера. Так само слід розглянути питання про можливість відстрочення введення наступної дози препарату як мінімум на 4 години, виходячи з оцінки співвідношення користь/ризик (ризик розвитку тромбозу та кровотеч при проведенні процедури, з урахуванням наявності у пацієнтів факторів ризику). У ці часові точки все ще продовжує виявлятися анти-активність препарату, і відстрочки за часом не є гарантією того, що розвитку нейроаксіальної гематоми вдасться уникнути.ПередозуванняПри підшкірному застосуванні може призвести до геморагічних ускладнень. При прийомі навіть великих доз всмоктування препарату малоймовірне. Антикоагулянтні ефекти можна переважно нейтралізувати шляхом повільного внутрішньовенного введення протаміну сульфату, доза якого залежить від дози введеного препарату. Один мг (1 мг) протаміну сульфату нейтралізує антикоагулянтний ефект одного мг (1 мг) препарату Клексан® (див. інформацію про застосування препаратів протаміну сульфату), якщо еноксапарин натрію вводився не більше ніж за 8 годин до введення протаміну. 0,5 мг протаміну нейтралізує антикоагулянтний ефект 1 мг препарату, якщо з моменту введення останнього пройшло більше 8 годин або за необхідності введення другої дози протаміну. Якщо після введення еноксапарину натрію пройшло 12 год і більше, введення протаміну не потрібно. Однак навіть при введенні великих доз протаміну сульфату, анти-Ха активність препарату Клексан повністю не нейтралізується (максимально на 60%).Запобіжні заходи та особливі вказівкиЗагальні Низькомолекулярні гепарини не є взаємозамінними, так як вони різняться по процесу виробництва, молекулярної маси, специфічної анти-Ха активності, одиницям дозування та режиму дозування, з чим пов'язані відмінності в їх фармакокінетиці та біологічній активності (антитромбінова активність та взаємодія з тромбоцитами). Тому потрібно суворо виконувати рекомендації щодо застосування кожного препарату, що належить до класу низькомолекулярних гепаринів. Кровотеча Як і при застосуванні інших антикоагулянтів, при введенні препарату Клексан можливий розвиток кровотеч будь-якої локалізації. При розвитку кровотечі необхідно знайти джерело і призначити відповідне лікування. Еноксапарин натрію, як і інші антикоагулянти, слід застосовувати з обережністю при станах з підвищеним ризиком кровотечі, таких як: порушення гемостазу; виразкова хвороба в анамнезі; нещодавно перенесений ішемічний інсульт; тяжка артеріальна гіпертензія; діабетична ретинопатія; нейрохірургічне чи офтальмологічне оперативне втручання; одночасне застосування препаратів, що впливають на гемостаз. Кровотечі у пацієнтів похилого віку При застосуванні еноксапарину натрію у профілактичних дозах у пацієнтів похилого віку не відмічено збільшення ризику кровотеч. При застосуванні препарату в терапевтичних дозах у пацієнтів похилого віку (особливо у віці 80 років та старших) існує підвищений ризик розвитку кровотеч. Рекомендується проведення ретельного нагляду за станом таких пацієнтів. Одночасне застосування інших препаратів, що впливають на гемостаз Застосування препаратів, що впливають на гемостаз (саліцилати системної дії, у тому числі ацетилсаліцилова кислота в дозах, що надають протизапальну дію, нестероїдні протизапальні засоби, включаючи кеторолак, інші тромболітики (алтеплаза, ретеплаза, стрептокіназа, тенектеплаза, доза). , крім випадків, коли їх застосування є необхідним. Якщо показано їх одночасне застосування з еноксапарином натрію, слід проводити ретельне клінічне спостереження та моніторинг відповідних лабораторних показників. Ниркова недостатність У пацієнтів з порушенням функції нирок існує підвищений ризик розвитку кровотечі через збільшення системної експозиції еноксапарину натрію. У пацієнтів з тяжкими порушеннями функції нирок (КК ≥15 та Низька маса тіла Відзначалося збільшення експозиції еноксапарину натрію при його профілактичному застосуванні у жінок з масою тіла менше 45 кг та у чоловіків з масою тіла менше 57 кг, що може призводити до підвищеного ризику розвитку кровотеч. Рекомендується проведення ретельного контролю за станом таких пацієнтів. Пацієнти з ожирінням Пацієнти з ожирінням мають підвищений ризик розвитку тромбозів та емболій. Безпека та ефективність застосування еноксапарину натрію у профілактичних дозах у пацієнтів з ожирінням (ІМТ понад 30 кг/м2) до кінця не визначена та немає загальної думки щодо корекції дози. Рекомендується проведення контролю за станом пацієнтів на предмет розвитку симптомів та ознак тромбозів та емболій. Контроль кількості тромбоцитів у периферичній крові Ризик розвитку антитіло-опосередкованої гепарин-індукованої тромбоцитопенії (ГІТ) існує і при застосуванні низькомолекулярних гепаринів, при цьому цей ризик вищий у пацієнтів, які перенесли операції на серці, та пацієнтів з онкологічними захворюваннями. Якщо розвивається тромбоцитопенія, її зазвичай виявляють між 5-м і 21-м днями після початку терапії еноксапарином натрію. У зв'язку з цим рекомендується регулярно контролювати кількість тромбоцитів у периферичній крові до початку лікування еноксапарином натрію та під час його застосування. Слід визначати кількість тромбоцитів у крові за наявності симптомів, що вказують на ГІТ (новий епізод артеріальних та/або венозних тромбоемболічних ускладнень, хворобливе ураження шкіри на місці ін'єкції, алергічна або анафілактична реакція при лікуванні).При виникненні зазначених симптомів слід поінформувати лікаря. За наявності підтвердженого значного зниження кількості тромбоцитів (на 30-50% порівняно з вихідним показником) необхідно негайно відмінити еноксапарин натрію та перевести пацієнта на іншу антикоагулянтну терапію без застосування гепаринів. Спінальна/епідуральна анестезія Описано випадки виникнення нейроаксіальних гематом при застосуванні еноксапарину натрію при одночасному проведенні спінальної/епідуральної анестезії з розвитком тривалого або необоротного паралічу. Ризик цих явищ знижується при застосуванні препарату в дозі 40 мг або нижче. Ризик підвищується при застосуванні більш високих доз еноксапарину натрію, а також при використанні постійних катетерів після операції, або при одночасному застосуванні додаткових препаратів, що впливають на гемостаз, таких як нестероїдні протизапальні засоби. Ризик також підвищується при травматично проведеній або повторній спинномозковій пункції або у пацієнтів, які мають в анамнезі вказівки на перенесені операції у ділянці хребта або деформацію хребта. Для зниження можливого ризику кровотечі, пов'язаного із застосуванням еноксапарину натрію та проведенням епідуральної або спинальної анестезії/аналгезії, необхідно враховувати фармакокінетичний профіль препарату. Встановлення або видалення катетера краще проводити при низькому антикоагулянтному ефекті еноксапарину натрію, однак точний час для досягнення достатнього зниження антикоагулянтного ефекту у різних пацієнтів невідомий. Слід додатково враховувати, що у пацієнтів із КК 15-30 мл/хв виведення еноксапарину натрію сповільнюється. Якщо за призначенням лікаря застосовується антикоагулянтна терапія під час епідуральної/спінальної анестезії або люмбальної пункції, необхідно постійне спостереження за пацієнтом для виявлення будь-яких неврологічних симптомів, таких як болі в спині, порушення сенсорних і моторних функцій (оніміння або слабкість у нижніх кінцівках), порушення функції кишечника та/або сечового міхура. Пацієнта необхідно проінструктувати про необхідність негайного інформування лікаря у разі виникнення вищеописаних симптомів. При підозрі на симптоми, характерні для гематоми спинного мозку, потрібні термінова діагностика та лікування, включаючи, за необхідності, декомпресію спинного мозку. Гепарин-індукована тромбоцитопенія Застосування еноксапарину натрію у пацієнтів, які мають в анамнезі вказівки на наявність гепарин-індукованої тромбоцитопенії протягом останніх 100 днів або за наявності циркулюючих антитіл протипоказано (див. розділ "Протипоказання"). Антитіла, що циркулюють, можуть персистувати кілька років. Еноксапарин натрію слід застосовувати з особливою обережністю у пацієнтів, які мають в анамнезі (понад 100 днів) гепарин-індуковану тромбоцитопенію без циркулюючих антитіл. Рішення про застосування еноксапарину натрію в даній ситуації має бути прийняте тільки після оцінки співвідношення користь/ризик та за відсутності безгепаринової (що не містить гепарин) альтернативної терапії. Черезшкірна коронарна ангіопластика З метою мінімізації ризику кровотечі, пов'язаного з інвазивною судинною інструментальною маніпуляцією при лікуванні нестабільної стенокардії та інфаркту міокарда без зубця Q та гострого інфаркту міокарда з підйомом сегмента ST, ці процедури слід проводити в інтервалах між введенням препарату. Це необхідно для досягнення гемостазу у місці введення катетера після проведення черезшкірного коронарного втручання. При використанні закриває пристрою інтродьюсер стегнової артерії може бути видалено негайно. При застосуванні мануальної (ручної) компресії інтродьюсер стегнової артерії слід видалити через 6 годин після останньої внутрішньовенної або підшкірної ін'єкції еноксапарину натрію. Якщо лікування еноксапарином натрію триває, наступну дозу слід вводити не раніше, ніж через 6-8 годин після видалення інтродьюсера стегнової артерії.Необхідно стежити за місцем введення інтродьюсера, щоб своєчасно виявити ознаки кровотечі та утворення гематоми. Пацієнти з механічними штучними клапанами серця Застосування еноксапарину натрію для профілактики тромбоутворення у пацієнтів з штучними механічними клапанами серця вивчено недостатньо. Є окремі повідомлення про розвиток тромбозу клапанів серця у пацієнтів із механічними штучними клапанами серця на фоні терапії еноксапарином натрію для профілактики тромбоутворення. Зважаючи на недостатність клінічних даних та наявність неоднозначних факторів, включаючи основне захворювання, оцінка таких повідомлень утруднена. Вагітні жінки з механічними штучними клапанами серця Застосування еноксапарину натрію для профілактики тромбоутворення у вагітних жінок з штучними механічними клапанами серця вивчено недостатньо. У клінічному дослідженні за участю вагітних жінок з механічними штучними клапанами серця при застосуванні еноксапарину натрію в дозі 1 мг/кг маси тіла двічі на добу для зменшення ризику тромбозів та емболій, у 2-х з 8-ми жінок утворилися тромби, які призводили до блокування клапанів серця та до смерті матері та плода. Є окремі постмаркетингові повідомлення про тромбоз клапанів серця у вагітних жінок з механічними штучними клапанами серця, які отримували лікування еноксапарином натрію для профілактики тромбоутворення. Вагітні жінки з механічними штучними клапанами серця можуть мати підвищений ризик розвитку тромбозу та емболії. Некроз шкіри/шкірний васкуліт Повідомлялося про розвиток некрозу шкіри та шкірного васкуліту при застосуванні низькомолекулярних гепаринів. У разі розвитку некрозу шкіри/шкірного васкуліту застосування препарату слід припинити. Гострий інфекційний ендокардит Застосування гепарину не рекомендується у пацієнтів із гострим інфекційним ендокардитом через ризик розвитку геморагічного інсульту. У випадку, якщо застосування препарату вважається абсолютно необхідним, рішення слід приймати тільки після ретельної індивідуальної оцінки співвідношення користі та ризику. Лабораторні випробування У дозах, що застосовуються для профілактики тромбоемболічних ускладнень, препарат Клексан істотно не впливає на час кровотечі та показники зсідання крові, а також на агрегацію тромбоцитів або на зв'язування їх з фібриногеном. При підвищенні дози може подовжуватися АЧТВ та активований час згортання крові. Збільшення АЧТВ та активованого часу згортання не знаходяться у прямій лінійній залежності від збільшення антикоагулянтної активності препарату, тому немає потреби в їх моніторингу. Гіперкаліємія Гепарини можуть пригнічувати секрецію альдостерону наднирковими залозами, що призводить до розвитку гіперкаліємії, особливо у пацієнтів з цукровим діабетом, хронічною нирковою недостатністю, попереднім метаболічним ацидозом, які приймають лікарські препарати, що підвищують вміст калію. Слід регулярно контролювати вміст калію у плазмі, особливо у пацієнтів групи ризику. Профілактика венозних тромбозів та емболій у пацієнтів з гострими терапевтичними захворюваннями, які перебувають на постільному режимі У разі розвитку гострої інфекції, гострих ревматичних станів профілактичне застосування еноксапарину натрію виправдане лише, якщо перераховані вище стани поєднуються з одним з нижчеперелічених факторів ризику венозного тромбоутворення: вік понад 75 років; злоякісні новоутворення; тромбози та емболії в анамнезі; ожиріння; гормональна терапія; серцева недостатність; хронічна дихальна недостатність. Порушення функції печінки Еноксапарин натрію слід обережно застосовувати у пацієнтів з порушеннями функції печінки внаслідок збільшення ризику кровотеч. Корекція дози на підставі моніторування анти-Ха активності у пацієнтів з цирозом печінки є ненадійною та не рекомендується. Вплив на здатність до керування автотранспортом та управління механізмами Препарат Клексан не впливає на здатність керувати транспортними засобами та механізмами.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаРозчин – 1 шприц: активна речовина: еноксапарин натрію 80 мг; розчинник: вода для ін'єкцій до 0,8 мл; 1 вид упаковки По 0,2 мл або 0,4 мл, або 0,6 мл, або 0,8 мл, або 1,0 мл розчину препарату скляний шприц (тип I) відповідно. По 2 шприци в блістер. По 1 або 5 блістерів разом із інструкцією із застосування в картонну пачку. 2 вид упаковки По 0,2 мл або 0,4 мл, або 0,6 мл, або 0,8 мл, або 1,0 мл розчину препарату у скляний шприц (тип 1) із захисною системою голки відповідно. По 2 шприци в блістер. По 1 або 5 блістерів разом із інструкцією із застосування в картонну пачку.Опис лікарської формиПрозорий, від безбарвного до блідо-жовтого кольору розчин.Фармакотерапевтична групаАнтикоагулянтний засіб прямої дії.ФармакокінетикаБіодоступність та абсорбція Абсолютна біодоступність еноксапарину натрію при підшкірному (п/к) введенні, що оцінюється на підставі анти-Ха активності, близька до 100%. Середня максимальна анти-Ха активність у плазмі крові відзначається через 3-5 годин після підшкірного введення і досягає приблизно 0,2, 0,4, 1,0 та 1,3 анти-Ха МО/мл після одноразового підшкірного введення препарату в дозі 20 мг, 40 мг, 1 мг/кг та 1,5 мг/кг. Внутрішньовенне болюсне введення препарату в дозі 30 мг, що супроводжується негайним підшкірним введенням препарату в дозі 1 мг/кг кожні 12 год, забезпечує початкову максимальну анти-Ха активність на рівні 1,16 МО/мл (n=16), середня експозиція препарату становить приблизно 88% від рівноважного стану, що досягається другого дня терапії. Фармакокінетика еноксапарину натрію у зазначених режимах дозування має лінійний характер. Варіабельність усередині та між групами пацієнтів низька. Після повторного підшкірного введення 40 мг еноксапарину натрію один раз на добу та підшкірного введення еноксапарину натрію в дозі 1,5 мг/кг маси тіла один раз на добу у здорових добровольців рівноважна концентрація досягається до 2 дня, причому площа під фармакокінетичною кривою в середньому на 15 % вище, ніж після одноразового введення. Після повторних підшкірних введень еноксапарину натрію в добовій дозі 1 мг/кг маси тіла двічі на добу рівноважна концентрація досягається через 3-4 дні, причому площа під фармакокінетичною кривою (AUC) в середньому на 65 % вище, ніж після одноразового введення, та середні значення максимальних концентрацій становлять відповідно 1,2 МО/мл та 0,52 МО/мл. Анти-Ха активність у плазмі крові приблизно в 10 разів нижча, ніж анти-Ха активність. Середня максимальна анти-Ха активність спостерігається приблизно через 3-4 години після підшкірного введення і досягає 0,13 МО/мл і 0,19 МО/мл після повторного введення 1 мг/кг маси тіла при дворазовому введенні та 1,5 мг/кг. маси тіла при одноразовому введенні відповідно. Розподіл Об'єм розподілу анти-Ха активності еноксапарину натрію становить приблизно 4,3 л і наближається до об'єму циркулюючої крові. Виведення Еноксапарин натрію є препаратом із низьким кліренсом. Після внутрішньовенного введення протягом 6 годин у дозі 1,5 мг/кг маси тіла середнє значення кліренсу анти-Ха у плазмі становить 0,74 л/год. Виведення препарату носить монофазний характер з періодами напіввиведення (Т1/2) близько 5 годин (після одноразового підшкірного введення) та близько 7 годин (після багаторазового введення препарату). Еноксапарин натрію в основному метаболізується в печінці шляхом десульфатування та/або деполімеризації з утворенням низькомолекулярних речовин з дуже низькою біологічною активністю. Виведення через нирки активних фрагментів препарату становить приблизно 10% від введеної дози, та загальна екскреція активних та неактивних фрагментів становить приблизно 40% від введеної дози. Особливі групи пацієнтів Пацієнти похилого віку (старше 75 років): фармакокінетичний профіль еноксапарину натрію не відрізняється у пацієнтів похилого віку та молодших пацієнтів при нормальній функції нирок. Однак унаслідок зниження функції нирок з віком може спостерігатися уповільнення виведення еноксапарину натрію у пацієнтів похилого віку. Порушення функції печінки: у дослідженні за участю пацієнтів з пізніми стадіями цирозу печінки, які отримували еноксапарин натрію в дозі 4000 ME (40 мг) один раз на добу, зниження максимальної анти-Ха активності було пов'язане зі збільшенням тяжкості порушення функції печінки (з оцінкою за шкалою Чайлд-Пью). Це зниження було зумовлено зниженням рівня AT-III, вторинним стосовно зниження синтезу АТ-III у пацієнтів з порушенням функції печінки. Порушення функції нирок: відмічено зменшення кліренсу еноксапарину натрію у пацієнтів із порушеннями функції нирок. Після повторного підшкірного введення 40 мг еноксапарину натрію один раз на добу відбувається збільшення активності анти-Ха, представленої площею під фармакокінетичною кривою (AUC) у пацієнтів з порушеннями функції нирок легкої (кліренс креатиніну (КК) ≥50 і Гемодіаліз: фармакокінетика еноксапарину натрію порівнянна з показниками в контрольній популяції після одноразових внутрішньовенних введень доз 25 ME, 50 ME або 100 МО/кг (0,25, 0.50 або 1,0 мг/кг), проте AUC була вдвічі , ніж у контрольній популяції. Маса тіла: після повторних підшкірних введень у дозуванні 1,5 мг/кг один раз на добу середня AUC анти-Ха активності в стані рівноваги незначно вища у пацієнтів із надмірною масою тіла (ІМТ 30-48 кг/м2) порівняно з пацієнтами із звичайною середньою масою тіла, тоді як максимальна анти-Ха активність плазми крові не збільшується. У пацієнтів із надмірною масою тіла при підшкірному введенні препарату кліренс дещо менший. Якщо не робити поправку дози з урахуванням маси тіла пацієнта, то після одноразового підшкірного введення 40 мг еноксапарину натрію анти-Ха активність буде на 52 % вище у жінок з масою тіла менше 45 кг і на 27 % вище у чоловіків з масою тіла менше 57 кг порівняно з пацієнтами із звичайною середньою масою тіла.ФармакодинамікаВ очищеній системі in vitro еноксапарин натрію має високу анти-Ха активність (приблизно 100 МО/мл) та низьку анти-Ха або антитромбінову активність (приблизно 28 МО/мл). Ця антикоагулянтна активність діє через антитромбін III (АТ-III), забезпечуючи антикоагулянтну активність у людей. Крім анти-Ха/IIа активності також виявлено додаткові антикоагулянтні та протизапальні властивості еноксапарину натрію як у здорових людей та пацієнтів, так і на моделях тварин. Це включає АТ-III-залежне інгібування інших факторів згортання, як фактор Vila, активацію вивільнення інгібітору шляху тканинного фактора (ПТФ), а також зниження вивільнення фактора Віллебранду з ендотелію судин у кровотік. Ці фактори забезпечують антикоагулянтний ефект еноксапарину натрію загалом. При застосуванні його у профілактичних дозах він незначно змінює активований частковий тромбопластиновий час (АЧТВ), практично не впливає на агрегацію тромбоцитів та на ступінь зв'язування фібриногену з рецепторами тромбоцитів.ІнструкціяОсобливості введення препарату Попередньо заповнений одноразовий шприц готовий до застосування. Препарат не можна вводити внутрішньом'язово! Підшкірне введення Ін'єкції бажано проводити у положенні пацієнта "лежачи". При використанні попередньо заповнених шприців на 20 мг і 40 мг, щоб уникнути втрати препарату перед ін'єкцією, не треба видаляти бульбашки повітря зі шприца. Ін'єкції слід проводити по черзі у ліву або праву передньолатеральну або задньолатеральну поверхню живота. Голку необхідно ввести на всю довжину, вертикально (не збоку), у шкірну складку, зібрану та утримувану до завершення ін'єкції між великим та вказівним пальцями. Складку шкіри відпускають лише після завершення ін'єкції. Не слід масажувати місце ін'єкції після введення препарату. Внутрішньовенне болюсне введення Внутрішньовенне болюсне введення еноксапарину натрію повинно проводитись через венозний катетер. Еноксапарин натрію не повинен змішуватись або вводитися разом з іншими лікарськими препаратами. Для того, щоб уникнути присутності в інфузійній системі слідів інших лікарських препаратів та їх взаємодії з еноксапарином натрію, венозний катетер повинен промиватися достатньою кількістю 0,9 % розчину натрію хлориду або 5 % розчину декстрози до та після внутрішньовенного болюсного введення еноксапарину. Еноксапарин натрію може безпечно вводитися з 0.9% розчином натрію хлориду та 5% розчином декстрози. Для проведення болюсного введення 30 мг еноксапарину натрію при лікуванні гострого інфаркту міокарда з підйомом сегмента ST зі скляних шприців 60 мг, 80 мг та 100 мг видаляють зайву кількість препарату для того, щоб у них залишалося лише 30 мг (0,3 мл). Доза 30 мг може безпосередньо вводитися внутрішньовенно. Для внутрішньовенного болюсного введення еноксапарину натрію через венозний катетер можуть використовуватися попередньо заповнені шприци для підшкірного введення препарату 60 мг, 80 мг і 100 мг. Рекомендується використовувати шприци 60 мг, так як це зменшує кількість препарату, що видаляється зі шприца. Шприци 20 мг не використовуються, тому що в них недостатньо препарату для болюсного введення 30 мг еноксапарину натрію. Шприци 40 мг не використовуються, тому що на них відсутні поділки і тому неможливо точно відміряти кількість 30 мг. Для підвищення точності додаткового внутрішньовенного болюсного введення малих обсягів у венозний катетер під час проведення черезшкірних коронарних втручань рекомендується розвести препарат до концентрації 3 мг/мл. Розведення розчину рекомендується проводити безпосередньо перед введенням. Для одержання розчину еноксапарину натрію з концентрацією 3 мг/мл за допомогою попередньо заповненого шприца 60 мг рекомендується використовувати ємність з інфузійним розчином 50 мл (тобто з 0,9 % розчином натрію хлориду або 5 % розчином декстрози). З ємності з інфузійним розчином за допомогою звичайного шприца вилучається та видаляється 30 мл розчину. Еноксапарин натрію (вміст шприца для підшкірного введення 60 мг) вводиться в 20 мл інфузійного розчину, що залишилися в ємності. Вміст ємності з розведеним розчином еноксапарину натрію обережно перемішується. Для введення за допомогою шприца витягується необхідний обсяг розведеного розчину еноксапарину натрію, який розраховується за формулою: Об'єм розведеного розчину = Маса тіла пацієнта (кг) х 0,1 або за допомогою наведеної нижче таблиці. Об'єми, які повинні вводитися внутрішньовенно після розведення до концентрації 3 мг/мл Маса тіла пацієнта, кг Необхідна доза (0,3 мг/кг), мг Об'єм розчину, розведеного до концентрації 3 мг/мл, необхідний для введення. 45 13,5 4,5 50 15 5 55 16,5 5,5 60 18 6 65 19,5 6,5 70 21 7 75 22,5 7,5 80 24 8 85 25,5 8,5 90 27 9 95 28,5 9,5 100 30 10 105 31,5 10,5 110 33 11 115 34,5 11,5 120 36 12 125 37,5 12,5 130 39 13 135 40,5 13,5 140 42 14 145 43,5 14,5 150 45 15 Переключення між еноксапарином натрію та пероральними антикоагулянтами: Перемикання між еноксапарином натрію та антагоністами вітаміну до (авк). Для моніторування ефекту авк необхідне спостереження лікаря та проведення лабораторних досліджень [протромбіновий час, представлений як багато]. Оскільки для розвитку максимального ефекту авк потрібен час, терапія еноксапарином натрію повинна продовжуватися в постійній дозі так довго, як необхідно для підтримання значень багато (за даними двох послідовних визначень) в бажаному терапевтичному діапазоні залежно від показань. Для пацієнтів, які отримують авк, скасування авк та введення першої дози еноксапарину натрію повинні проводитися після того, як багато знизилося нижче за межу терапевтичного діапазону. Переключення між еноксапарином натрію та пероральними антикоагулянтами прямої дії (поак). Скасування еноксапарину натрію та призначення поак повинні проводитися за 0-2 години до моменту чергового запланованого введення еноксапарину натрію відповідно до інструкції щодо застосування пероральних антикоагулянтів. Для пацієнтів, які отримують поак, введення першої дози еноксапарину натрію та відміна пероральних антикоагулянтів прямої дії повинні проводитися в момент часу, що відповідає черговому запланованому застосуванню поак. Застосування при спинальній/епідуральній анестезії або люмбальній пункції. У разі застосування антикоагулянтної терапії під час проведення епідуральної або спинальної анестезії/аналгезії або люмбальної пункції необхідне проведення неврологічного моніторування через ризик розвитку нейроаксіальних гематом. Застосування еноксапарину натрію у профілактичних дозах. Встановлення або видалення катетера повинно проводитися як мінімум 12 годин після останньої ін'єкції профілактичної дози еноксапарину натрію. При використанні безперервної техніки необхідно дотримуватися щонайменше 12 год. інтервал до видалення катетера. У пацієнтів з кк ≥15 та Застосування еноксапарину натрію у терапевтичних дозах Встановлення або видалення катетера повинно проводитися як мінімум 24 години після останньої ін'єкції терапевтичної дози еноксапарину натрію. При використанні безперервної техніки необхідно дотримуватися щонайменше 24 години інтервал до видалення катетера. У пацієнтів з кк ≥15 та Пацієнтам, які отримують еноксапарин натрію в дозах 0,75 мг/кг або 1 мг/кг маси тіла двічі на добу, не слід вводити другу дозу з метою збільшення інтервалу перед встановленням або заміною катетера. Так само слід розглянути питання про можливість відстрочення введення наступної дози препарату як мінімум на 4 години, виходячи з оцінки співвідношення користь/ризик (ризик розвитку тромбозу та кровотеч при проведенні процедури, з урахуванням наявності у пацієнтів факторів ризику). У ці часові точки все ще продовжує виявлятися анти-активність препарату, і відстрочки за часом не є гарантією того, що розвитку нейроаксіальної гематоми вдасться уникнути.Показання до застосуванняПрофілактика венозних тромбозів та емболій при хірургічних втручаннях у пацієнтів помірного та високого ризику, особливо при ортопедичних та загальнохірургічних втручаннях, включаючи онкологічні. Профілактика венозних тромбозів та емболій у пацієнтів, що знаходяться на постільному режимі, внаслідок гострих терапевтичних захворювань, включаючи гостру серцеву недостатність та декомпенсацію хронічної серцевої недостатності (III або IV клас NYHA), дихальну недостатність, а також при тяжких інфекціях та ревматичних захворюваннях при підвищеному тромбоутворення. Лікування тромбозу глибоких вен з тромбоемболією легеневої артерії або без тромбоемболії легеневої артерії, крім випадків тромбоемболії легеневої артерії, які потребують тромболітичної терапії або хірургічного втручання. Профілактика тромбоутворення у системі екстракорпорального кровообігу під час гемодіалізу. Гострий коронарний синдром: Лікування нестабільної стенокардії та інфаркту міокарда без підйому сегмента ST у поєднанні з пероральним прийомом ацетилсаліцилової кислоти. Лікування гострого інфаркту міокарда з підйомом сегмента ST у пацієнтів, які підлягають медикаментозному лікуванню або подальшому корконарному втручанню (ЧКВ).Протипоказання до застосуванняПідвищена чутливість до еноксапарину натрію, гепарину або його похідних, включаючи інші низькомолекулярні гепарини. Активна клінічно значуща кровотеча, а також стани та захворювання, при яких є високий ризик розвитку кровотечі, включаючи нещодавно перенесений геморагічний інсульт, гостру виразку шлунково-кишкового тракту (ЖКТ), наявність злоякісного новоутворення з високим ризиком кровотеч, нещодавно перенесені операції на головній та спинній мозку, офтальмологічні операції, відома чи передбачувана наявність варикозного розширених вен стравоходу, артеріовенозні мальформації, судинні аневризми, судинні аномалії спинного та головного мозку. Спінальна або епідуральна анестезія або локо-регіональна анестезія, коли еноксапарин натрію застосовувався для лікування попередніх 24 год. Імуноопосередкована гепарин-індукована громбоцитопенія (в анамнезі) протягом 100 останніх днів або наявність у крові циркулюючих антитромбоцитарних антитіл. Дитячий вік до 18 років, оскільки ефективність та безпека у даної категорії пацієнтів не встановлені. Стани, у яких є потенційний ризик розвитку кровотечі: порушення гемостазу (в т.ч. гемофілія, тромбоцитопенія, гіпокоагуляція, хвороба Віллебранда та ін), важкий васкуліт; виразкова хвороба шлунка або дванадцятипалої кишки або інші ерозивно-виразкові ураження шлунково-кишкового тракту в анамнезі; нещодавно перенесений ішемічний інсульт; неконтрольована тяжка артеріальна гіпертензія; діабетична або геморагічна ретинопатія; тяжкий цукровий діабет; нещодавно перенесена чи передбачувана неврологічна чи офтальмологічна операція; проведення спинальної або епідуральної анестезії (потенційна небезпека розвитку гематоми); спинномозкова пункція (нещодавно перенесена); недавні пологи; ендокардит бактеріальний (гострий або підгострий); перикардит або перикардіальний випіт; ниркова та/або печінкова недостатність; внутрішньоматкова контрацепція (ВМК); тяжка травма (особливо центральної нервової системи); відкриті рани на великих поверхнях; одночасний прийом препаратів, що впливають на систему гемостазу; гепарин-індукована тромбоцитопенія без циркулюючих антитіл в анамнезі (понад 100 днів). У компанії відсутні дані щодо клінічного застосування препарату Клексан при таких захворюваннях: активний туберкульоз, променева терапія (нещодавно перенесена).Вагітність та лактаціяВагітність Відомостей, що еноксапарин натрію проникає через плацентарний бар'єр під час вагітності, немає. Так як відсутні адекватні та добре контрольовані дослідження за участю вагітних жінок, а дослідження на тваринах не завжди прогнозують реакцію на введення еноксапарину натрію під час вагітності у людини, застосовувати його під час вагітності слід лише у виняткових випадках, коли є нагальна необхідність його застосування, встановлена лікарем. Рекомендується проведення контролю за станом пацієнток щодо появи ознак кровотечі або надмірної антикоагуляції, пацієнтки повинні бути попереджені про ризик виникнення кровотеч. Немає даних про підвищений ризик розвитку кровотеч, тромбоцитопенії або остеопорозу у вагітних жінок, за винятком випадків, відмічених у пацієнток із штучними клапанами серця. При плануванні епідуральної анестезії рекомендується перед її проведенням відмінити еноксапарин натрію. Період грудного вигодовування Невідомо, чи екскретується незмінений еноксапарин натрію у грудне молоко. Всмоктування еноксапарину натрію в шлунково-кишковому тракті у новонародженого малоймовірне. Препарат Клексан може застосовуватись у період грудного вигодовування.Побічна діяВивчення побічних ефектів еноксапарину натрію проводилося більш ніж у 15000 пацієнтів, які брали участь у клінічних дослідженнях, з них у 1776 пацієнтів - при профілактиці венозних тромбозів та емболій при загальнохірургічних та ортопедичних операціях: у 1169 пацієнтів постільний режим внаслідок гострих терапевтичних захворювань; у 559 пацієнтів – при лікуванні тромбозу глибоких вен з тромбоемболією легеневої артерії або без тромбоемболії легеневої артерії; у 1578 пацієнтів – при лікуванні нестабільної стенокардії та інфаркту міокарда без зубця Q; у 10176 пацієнтів – при лікуванні інфаркту міокарда з підйомом сегмента ST. Режим введення еноксапарину натрію відрізнявся залежно від показань. При профілактиці венозних тромбозів та емболій при загальнохірургічних та ортопедичних операціях або у пацієнтів, які перебувають на постільному режимі, вводилося 40 мг підшкірно один раз на добу. При лікуванні тромбозу глибоких вен з тромбоемболією легеневої артерії або без неї пацієнти отримували еноксапарин натрію з розрахунку 1 мг/кг маси тіла підшкірно кожні 12 годин або 1,5 мг/кг маси тіла підшкірно один раз на добу. При лікуванні нестабільної стенокардії та інфаркту міокарда без зубця Q доза еноксапарину натрію становила 1 мг/кг маси тіла підшкірно кожні 12 год, а у разі інфаркту міокарда з підйомом сегмента ST проводилося внутрішньовенне болюсне введення 30 мг з подальшим в кожні 12 год.Частота виникнення небажаних реакцій визначалася відповідно до класифікації Всесвітньої Організації Охорони Здоров'я: дуже часто (≥1/10); часто (≥1/100 та Порушення з боку судин: Кровотечі У клінічних дослідженнях кровотечі були найпоширенішими небажаними реакціями. До них належали великі кровотечі, що спостерігалися у 4,2% пацієнтів (кровотеча вважалася великою, якщо вона супроводжувалася зниженням вмісту гемоглобіну на 2 г/л і більше, вимагало переливання 2 або більше доз компонентів крові, а також якщо воно було заочеревинним або внутрішньочерепним. ). Деякі з цих випадків були летальними. Як і при застосуванні інших антикоагулянтів, при застосуванні еноксапарину натрію можливе виникнення кровотечі, особливо за наявності факторів ризику, що сприяють розвитку кровотечі, при проведенні інвазивних процедур або застосуванні препаратів, що порушують гемостаз. При описі кровотеч нижче знак "*" означає вказівку на такі види кровотеч: гематома, екхімози (крім ін'єкції), ранові гематоми, гематурія, носові кровотечі, шлунково-кишкові кровотечі. Дуже часто: кровотечі* при профілактиці венозних тромбозів у хірургічних пацієнтів та лікуванні тромбозу глибоких вен з тромбоемболією легеневої артерії або без неї. Часто: кровотечі* при профілактиці венозних тромбозів у пацієнтів, які перебувають на постільному режимі, та при лікуванні нестабільної стенокардії, інфаркту міокарда без зубця Q та інфаркту міокарда з підйомом сегмента ST. Нечасто: заочеревинні кровотечі та внутрішньочерепні крововиливи у пацієнтів при лікуванні тромбозу глибоких вен з тромбоемболією легеневої артерії або без неї. а також при лікуванні інфаркту міокарда із підйомом сегмента ST. Рідко: заочеревинні кровотечі при профілактиці венозних тромбозів у хірургічних пацієнтів та при лікуванні нестабільної стенокардії та інфаркту міокарда без зубця Q. Тромбоцитопенія та тромбоцитоз Часто: тромбоцитоз (кількість тромбоцитів у периферичній крові більше 400x109/л) при профілактиці венозних тромбозів у хірургічних пацієнтів та лікуванні тромбозу глибоких вен з тромбоемболією легеневої артерії або без неї. Часто: тромбоцитоз при лікуванні пацієнтів із гострим інфарктом міокарда із підйомом сегмента ST. Тромбоцитопенія при профілактиці венозних тромбозів у хірургічних пацієнтів та лікуванні тромбозу глибоких вен з тромбоемболією легеневої артерії або без неї. а також при гострому інфаркті міокарда із підйомом сегмента ST. Нечасто: тромбоцитопенія при профілактиці венозних тромбозів у пацієнтів, які перебувають на постільному режимі, та при лікуванні нестабільної стенокардії та інфаркту міокарда без зубця Q. Дуже рідко: аутоімунна тромбоцитопенія при лікуванні пацієнтів із гострим інфарктом міокарда з підйомом сегмента ST. Інші клінічно значущі небажані реакції незалежно від показань Небажані реакції, представлені нижче, згруповані за системно-органними класами, дано із зазначенням визначеної вище частоти їх виникнення та в порядку зменшення їх тяжкості. Порушення з боку крові та лімфатичної системи: - Часто: кровотеча, тромбоцитопенія, тромбоцитоз; Рідко: випадки розвитку аутоімунної тромбоцитопенії з тромбозом; у деяких випадках тромбоз ускладнювався розвитком інфаркту органів або ішемії кінцівок. Порушення з боку імунної системи: Найчастіше: алергічні реакції. Порушення з боку печінки та жовчовивідних шляхів: Дуже часто: підвищення активності "печінкових" ферментів, головним чином підвищення активності трансаміназ, що більш ніж утричі перевищує верхню межу норми. Порушення з боку шкіри та підшкірних тканин - Часто: кропив'янка, свербіж шкіри, еритема; Нечасто: бульозний дерматит. Загальні розлади та порушення у місці введення: Часто: гематома у місці ін'єкції, біль у місці ін'єкції, набряк у місці ін'єкції, кровотеча, реакції підвищеної чутливості, запалення, утворення ущільнень у місці ін'єкції. Нечасто: подразнення у місці ін'єкції, некроз шкіри у місці ін'єкції. Дані, отримані після виходу препарату ринку Наступні небажані реакції спостерігалися при постмаркетинговому застосуванні препарату Клексан. Про ці побічні реакції були спонтанні повідомлення. Порушення з боку імунної системи: Рідко: анафілактичні/анафілактоїдні реакції, включаючи шок. Порушення з боку нервової системи: Часто: біль голови. Порушення з боку судин: Рідко: при застосуванні еноксапарину натрію на тлі спінальної/епідуральної анестезії або спінальної пункції спостерігалися випадки розвитку спінальної гематоми (або нейроаксіальної гематоми). Ці реакції призводили до розвитку неврологічних порушень різного ступеня тяжкості, включаючи стійкий або необоротний параліч. Порушення з боку крові або лімфатичної системи: - Часто: геморагічна анемія; Рідко: еозинофілія. Порушення з боку шкіри та підшкірних тканин: Рідко: алопеція; у місці ін'єкції може розвинутися шкірний васкуліт, некроз шкіри, яким зазвичай передує поява пурпури або еритематозних папул (інфільтрованих та болючих). У цих випадках терапію препаратом Клексан слід припинити. Можливе утворення твердих запальних вузликів-інфільтратів у місці ін'єкцій препарату, які зникають через кілька днів і не є підставою для відміни препарату. Порушення з боку печінки та жовчовивідних шляхів: - Нечасто: гепатоцелюлярне ураження печінки; Рідко: холестатична поразка печінки. Порушення з боку скелетно-м'язової та сполучної тканини: Рідко: остеопороз при тривалій терапії (понад три місяці). Лабораторні та інструментальні дані - Рідко: гіперкаліємія.Взаємодія з лікарськими засобамиПрепарат Клексан не можна змішувати з іншими препаратами! Нерекомендовані комбінації Препарати, що впливають на гемостаз (саліцилати системної дії, ацетилсаліцилова кислота в дозах, що мають протизапальну дію, нестероїдні протизапальні препарати (НПЗП), включаючи кеторолак, інші тромболітики (алтеплаза, ретеплаза, стрептокіназа, трептокіназа, натрію. При необхідності одночасного застосування з еноксапарином натрію слід дотримуватися обережності та проводити ретельне клінічне спостереження та моніторинг відповідних лабораторних показників. Комбінації, що вимагають дотримання обережності Інші лікарські препарати, що впливають на гемостаз, такі як: інгібітори агрегації тромбоцитів, включаючи ацетилсаліцилову кислоту в дозах, що мають антиагрегантну дію (кардіопротекція), клопідогрел, тиклопідин та антагоністи глікопротеїнових ПЬ/Ша рецепторів, показані при гострому коронарному синдромі, внаслідок підвищеного ризику; декстран із молекулярною масою 40 кДа; системні глюкокортикостероїди. Лікарські препарати, що підвищують вміст калію При одночасному застосуванні з лікарськими препаратами, що підвищують вміст калію в сироватці, слід проводити клінічний та лабораторний контроль.Спосіб застосування та дозиПідшкірно, за винятком особливих випадків (див. нижче підрозділи "Лікування інфаркту міокарда з підйомом сегмента ST, медикаментозне або за допомогою черезшкірного коронарного втручання" та "Профілактика тромбоутворення в системі екстракорпорального кровообігу при проведенні гемодіалізу"). Профілактика венозних тромбозів та емболії при хірургічних втручаннях у пацієнтів помірного та високого ризику Пацієнтам з помірним ризиком розвитку тромбозів та емболій (наприклад, абдомінальні операції) рекомендована доза препарату Клексан становить 20 мг один раз на добу підшкірно. Першу ін'єкцію слід зробити за 2 години до хірургічного втручання. Пацієнтам з високим ризиком розвитку тромбозів та емболій (наприклад, при ортопедичних операціях, хірургічних операціях в онкології, пацієнтам з додатковими факторами ризику, не пов'язаними з операцією, такими як вроджена або набута тромбофілія, злоякісне новоутворення, постільний режим понад три доби, тромбоз в анамнезі, варикозне розширення вен нижніх кінцівок, вагітність) препарат рекомендується у дозі 40 мг один раз на добу підшкірно, із введенням першої дози за 12 годин до хірургічного втручання. За необхідності більш ранньої передопераційної профілактики (наприклад, у пацієнтів з високим ризиком розвитку тромбозів та тромбоемболій, що очікують відстрочену ортопедичну операцію) остання ін'єкція повинна бути зроблена за 12 годин до операції та через 12 годин після операції. Тривалість лікування препаратом Клексан у середньому становить 7-10 днів. При необхідності терапію можна продовжувати доти, доки зберігається ризик розвитку тромбозу та емболії, і доти, доки пацієнт не перейде на амбулаторний режим. При великих ортопедичних операціях може бути доцільним після початкової терапії продовження лікування шляхом введення препарату Клексан у дозі 40 мг один раз на добу протягом п'яти тижнів. Для пацієнтів з високим ризиком венозних тромбоемболій, які перенесли хірургічне втручання, абдомінальну та тазову хірургію через онкологічне захворювання, може бути доцільним збільшення тривалості введення препарату Клексан у дозі 40 мг один раз на добу протягом чотирьох тижнів. Профілактика венозних тромбозів та емболій у пацієнтів, які перебувають на постільному режимі внаслідок гострих терапевтичних захворювань Рекомендована доза препарату Клексан становить 40 мг один раз на добу, підшкірно, протягом 6-14 днів. Терапію слід продовжувати до переходу пацієнта на амбулаторний режим (максимально протягом 14 днів). Лікування тромбозу глибоких вен з тромбоемболією легеневої артерії або без тромбоемболії легеневої артерії Препарат вводиться підшкірно із розрахунку 1,5 мг/кг маси тіла один раз на добу або 1 мг/кг маси тіла двічі на добу. Режим дозування повинен вибиратися лікарем на основі оцінки ризику розвитку тромбоемболії та ризику розвитку кровотеч. У пацієнтів без тромбоемболічних ускладнень та з низьким ризиком розвитку венозної тромбоемболії препарат рекомендується вводити підшкірно із розрахунку 1.5 мг/кг маси тіла один раз на добу. У всіх інших пацієнтів, включаючи пацієнтів з ожирінням, симптоматичною тромбоемболією легеневих артерій, раком, повторною венозною тромбоемболією та проксимальним тромбозом (у здухвинній вені) препарат рекомендується застосовувати у дозі 1 мг/кг двічі на добу. Тривалість лікування загалом становить 10 днів. Слід відразу ж розпочати терапію непрямими антикоагулянтами, при цьому лікування препаратом Клексан® необхідно продовжувати до досягнення терапевтичного антикоагулянтного ефекту (значення МНО [Міжнародні Нормалізовані Відносини] повинні становити 2,0-3,0). Профілактика тромбоутворення у системі екстракорпорального кровообігу під час гемодіалізу Рекомендована доза препарату Клексан становить у середньому 1 мг/кг маси тіла. При високому ризику розвитку кровотечі дозу слід зменшити до 0,5 мг/кг маси тіла при подвійному судинному доступі або до 0,75 мг/кг при одинарному судинному доступі. При гемодіалізі препарат Клексан® слід вводити до артеріальної ділянки шунту на початку сеансу гемодіалізу. Однієї дози, як правило, достатньо для чотиригодинного сеансу, однак при виявленні фібринових кілець при тривалому гемодіалізі можна додатково ввести препарат з розрахунку 0,5-1 мг/кг маси тіла. Дані щодо пацієнтів, які застосовують еноксапарин натрію для профілактики або лікування та під час сеансів гемодіалізу, відсутні. Лікування нестабільної стенокардії та інфаркту міокарда без підйому сегмента ST Препарат Клексан® вводиться з розрахунку 1 мг/кг маси тіла кожні 12 годин підшкірно при одночасному застосуванні антитромбоцитарної терапії. Середня тривалість терапії становить щонайменше 2 дні і продовжується до стабілізації клінічного стану пацієнта. Зазвичай введення препарату продовжується від 2-х до 8-ми днів. Ацетилсаліцилова кислота рекомендується всім пацієнтам, які не мають протипоказань, з початковою дозою 150-300 мг внутрішньо з наступною підтримуючою дозою 75-325 мг один раз на добу. Лікування гострого інфаркту міокарда з підйомом сегмента ST, медикаментозне або за допомогою черезшкірного коронарного втручання Лікування починають з одноразового внутрішньовенного болюсного введення еноксапарину натрію у дозі 30 мг. Відразу після нього підшкірно вводять еноксапарин натрію в дозі 1 мг/кг маси тіла. Далі препарат застосовують підшкірно по 1 мг/кг маси тіла кожні 12 год (максимально 100 мг еноксапарину натрію для кожної з перших двох підшкірних ін'єкцій, потім - по 1 мг/кг маси тіла для підшкірних доз, що залишилися, тобто, при масі тіла більше 100 кг, разова доза не може перевищувати 100 мг). Якнайшвидше після виявлення гострого інфаркту міокарда з підйомом сегмента ST пацієнтам необхідно призначити одночасно ацетилсаліцилову кислоту і, якщо немає протипоказань, прийом ацетилсаліцилової кислоти (у дозах 75-325 мг) слід продовжувати щодня протягом не менше 30 днів. Рекомендована тривалість лікування препаратом Клексан становить 8 днів або до виписки пацієнта зі стаціонару (якщо період госпіталізації становить менше 8 днів). При комбінації з тромболітиками (фібрин-специфічними та фібрин-неспецифічними) еноксапарин натрію повинен вводитися в інтервалі від 15 хв до початку тромболітичної терапії та до 30 хв після неї. У пацієнтів віком 75 років і більше не застосовується початкове внутрішньовенне болюсне введення. Препарат вводять підшкірно в дозі 0,75 мг/кг кожні 12 год (максимально 75 мг еноксапарину натрію для кожної з перших двох підшкірних ін'єкцій, потім - по 0,75 мг/кг маси тіла для підшкірних доз, що залишилися, тобто при масі тіла більше 100 кг, разова доза не може перевищувати 75 мг. У пацієнтів, яким проводиться черезшкірне коронарне втручання, у разі якщо остання підшкірна ін'єкція еноксапарину натрію була проведена менш ніж за 8 годин до роздування введеного в місце звуження коронарної артерії балонного катетера, додаткового введення еноксапарину натрію не потрібно. Якщо ж остання підшкірна ін'єкція еноксапарину натрію проводилася більш ніж за 8 годин до роздування балонного катетера, слід додаткове внутрішньовенне болюсне введення еноксапарину натрію в дозі 0,3 мг/кг. Режим дозування у спеціальних груп пацієнтів Діти віком до 18 років Безпека та ефективність застосування еноксапарину натрію у дітей не встановлені. Пацієнти похилого віку (старше 75 років) За винятком лікування інфаркту міокарда з підйомом сегмента st для інших показань зниження доз еноксапарину натрію у пацієнтів похилого віку за відсутності порушень функції нирок не потрібно. Пацієнти з порушеннями функції нирок Тяжкі порушення функції нирок (кк ≥15 і Застосування еноксапарину натрію не рекомендується пацієнтам з термінальною стадією хронічної хвороби нирок. У пацієнтів з тяжкими порушеннями функції нирок (кк ≥15 та При застосуванні препарату у терапевтичних дозах рекомендується наступна корекція режиму дозування: Звичайний режим дозування 1 мг/кг маси тіла підшкірно двічі на добу; при тяжкій нирковій недостатності 1 мг/кг маси тіла підшкірно один раз на добу. Звичайний режим дозування 1,5 мг/кг маси тіла підшкірно раз на добу; при тяжкій нирковій недостатності 1 мг/кг маси тіла підшкірно один раз на добу. Лікування гострого інфаркту міокарда з підйомом сегмента st у пацієнтів віком до 75 років: Звичайний режим дозування - одноразово внутрішньовенне болюсне введення 30 мг плюс 1 мг/кг маси тіла підшкірно; з наступним підшкірним введенням у дозі 1 мг/кг маси тіла двічі на добу (максимально 100 мг для кожної з перших двох підшкірних ін'єкцій); при тяжкій нирковій недостатності одноразово внутрішньовенне болюсне введення 30 мг плюс 1 мг/кг маси тіла підшкірно; з наступним підшкірним введенням у дозі 1 мг/кг маси тіла один раз на добу (максимально 100 мг лише для першої підшкірної ін'єкції). Звичайний режим дозування - 0,75 мг/кг маси тіла підшкірно двічі на добу без початкового внутрішньовенного болюсного введення (максимально 75 мг для кожної з двох перших підшкірних ін'єкцій). ); при тяжкій нирковій недостатності 1 мг/кг маси тіла підшкірно один раз на добу без початкового внутрішньовенного болюсного введення (максимально 100 мг лише для першої підшкірної ін'єкції). При застосуванні препарату з профілактичною метою рекомендується корекція режиму дозування Звичайний режим дозування 40 мг підшкірно раз на добу; при тяжкій нирковій недостатності 20 мг підшкірно один раз на добу. Звичайний режим дозування 20 мг підшкірно раз на добу; при тяжкій нирковій недостатності 20 мг підшкірно один раз на добу. Рекомендована корекція режиму дозування не застосовується при гемодіалізі. Порушення функції нирок легкої (кк ≥50 та Корекція дози не потрібна, проте пацієнти повинні перебувати під ретельним наглядом лікаря. Пацієнти з порушеннями функції печінки У зв'язку з відсутністю клінічних досліджень препарат Клексан слід застосовувати з обережністю у пацієнтів з порушеннями функції печінки.ПередозуванняПри підшкірному застосуванні може призвести до геморагічних ускладнень. При прийомі навіть великих доз всмоктування препарату малоймовірне. Антикоагулянтні ефекти можна переважно нейтралізувати шляхом повільного внутрішньовенного введення протаміну сульфату, доза якого залежить від дози введеного препарату. Один мг (1 мг) протаміну сульфату нейтралізує антикоагулянтний ефект одного мг (1 мг) препарату Клексан® (див. інформацію про застосування препаратів протаміну сульфату), якщо еноксапарин натрію вводився не більше ніж за 8 годин до введення протаміну. 0,5 мг протаміну нейтралізує антикоагулянтний ефект 1 мг препарату, якщо з моменту введення останнього пройшло більше 8 годин або за необхідності введення другої дози протаміну. Якщо після введення еноксапарину натрію пройшло 12 год і більше, введення протаміну не потрібно. Однак навіть при введенні великих доз протаміну сульфату, анти-Ха активність препарату Клексан повністю не нейтралізується (максимально на 60%).Запобіжні заходи та особливі вказівкиЗагальні Низькомолекулярні гепарини не є взаємозамінними, так як вони різняться по процесу виробництва, молекулярної маси, специфічної анти-Ха активності, одиницям дозування та режиму дозування, з чим пов'язані відмінності в їх фармакокінетиці та біологічній активності (антитромбінова активність та взаємодія з тромбоцитами). Тому потрібно суворо виконувати рекомендації щодо застосування кожного препарату, що належить до класу низькомолекулярних гепаринів. Кровотеча Як і при застосуванні інших антикоагулянтів, при введенні препарату Клексан можливий розвиток кровотеч будь-якої локалізації. При розвитку кровотечі необхідно знайти джерело і призначити відповідне лікування. Еноксапарин натрію, як і інші антикоагулянти, слід застосовувати з обережністю при станах з підвищеним ризиком кровотечі, таких як: порушення гемостазу; виразкова хвороба в анамнезі; нещодавно перенесений ішемічний інсульт; тяжка артеріальна гіпертензія; діабетична ретинопатія; нейрохірургічне чи офтальмологічне оперативне втручання; одночасне застосування препаратів, що впливають на гемостаз. Кровотечі у пацієнтів похилого віку При застосуванні еноксапарину натрію у профілактичних дозах у пацієнтів похилого віку не відмічено збільшення ризику кровотеч. При застосуванні препарату в терапевтичних дозах у пацієнтів похилого віку (особливо у віці 80 років та старших) існує підвищений ризик розвитку кровотеч. Рекомендується проведення ретельного нагляду за станом таких пацієнтів. Одночасне застосування інших препаратів, що впливають на гемостаз Застосування препаратів, що впливають на гемостаз (саліцилати системної дії, у тому числі ацетилсаліцилова кислота в дозах, що надають протизапальну дію, нестероїдні протизапальні засоби, включаючи кеторолак, інші тромболітики (алтеплаза, ретеплаза, стрептокіназа, тенектеплаза, доза). , крім випадків, коли їх застосування є необхідним. Якщо показано їх одночасне застосування з еноксапарином натрію, слід проводити ретельне клінічне спостереження та моніторинг відповідних лабораторних показників. Ниркова недостатність У пацієнтів з порушенням функції нирок існує підвищений ризик розвитку кровотечі через збільшення системної експозиції еноксапарину натрію. У пацієнтів з тяжкими порушеннями функції нирок (КК ≥15 та Низька маса тіла Відзначалося збільшення експозиції еноксапарину натрію при його профілактичному застосуванні у жінок з масою тіла менше 45 кг та у чоловіків з масою тіла менше 57 кг, що може призводити до підвищеного ризику розвитку кровотеч. Рекомендується проведення ретельного контролю за станом таких пацієнтів. Пацієнти з ожирінням Пацієнти з ожирінням мають підвищений ризик розвитку тромбозів та емболій. Безпека та ефективність застосування еноксапарину натрію у профілактичних дозах у пацієнтів з ожирінням (ІМТ понад 30 кг/м2) до кінця не визначена та немає загальної думки щодо корекції дози. Рекомендується проведення контролю за станом пацієнтів на предмет розвитку симптомів та ознак тромбозів та емболій. Контроль кількості тромбоцитів у периферичній крові Ризик розвитку антитіло-опосередкованої гепарин-індукованої тромбоцитопенії (ГІТ) існує і при застосуванні низькомолекулярних гепаринів, при цьому цей ризик вищий у пацієнтів, які перенесли операції на серці, та пацієнтів з онкологічними захворюваннями. Якщо розвивається тромбоцитопенія, її зазвичай виявляють між 5-м і 21-м днями після початку терапії еноксапарином натрію. У зв'язку з цим рекомендується регулярно контролювати кількість тромбоцитів у периферичній крові до початку лікування еноксапарином натрію та під час його застосування. Слід визначати кількість тромбоцитів у крові за наявності симптомів, що вказують на ГІТ (новий епізод артеріальних та/або венозних тромбоемболічних ускладнень, хворобливе ураження шкіри на місці ін'єкції, алергічна або анафілактична реакція при лікуванні).При виникненні зазначених симптомів слід поінформувати лікаря. За наявності підтвердженого значного зниження кількості тромбоцитів (на 30-50% порівняно з вихідним показником) необхідно негайно відмінити еноксапарин натрію та перевести пацієнта на іншу антикоагулянтну терапію без застосування гепаринів. Спінальна/епідуральна анестезія Описано випадки виникнення нейроаксіальних гематом при застосуванні еноксапарину натрію при одночасному проведенні спінальної/епідуральної анестезії з розвитком тривалого або необоротного паралічу. Ризик цих явищ знижується при застосуванні препарату в дозі 40 мг або нижче. Ризик підвищується при застосуванні більш високих доз еноксапарину натрію, а також при використанні постійних катетерів після операції, або при одночасному застосуванні додаткових препаратів, що впливають на гемостаз, таких як нестероїдні протизапальні засоби. Ризик також підвищується при травматично проведеній або повторній спинномозковій пункції або у пацієнтів, які мають в анамнезі вказівки на перенесені операції у ділянці хребта або деформацію хребта. Для зниження можливого ризику кровотечі, пов'язаного із застосуванням еноксапарину натрію та проведенням епідуральної або спинальної анестезії/аналгезії, необхідно враховувати фармакокінетичний профіль препарату. Встановлення або видалення катетера краще проводити при низькому антикоагулянтному ефекті еноксапарину натрію, однак точний час для досягнення достатнього зниження антикоагулянтного ефекту у різних пацієнтів невідомий. Слід додатково враховувати, що у пацієнтів із КК 15-30 мл/хв виведення еноксапарину натрію сповільнюється. Якщо за призначенням лікаря застосовується антикоагулянтна терапія під час епідуральної/спінальної анестезії або люмбальної пункції, необхідно постійне спостереження за пацієнтом для виявлення будь-яких неврологічних симптомів, таких як болі в спині, порушення сенсорних і моторних функцій (оніміння або слабкість у нижніх кінцівках), порушення функції кишечника та/або сечового міхура. Пацієнта необхідно проінструктувати про необхідність негайного інформування лікаря у разі виникнення вищеописаних симптомів. При підозрі на симптоми, характерні для гематоми спинного мозку, потрібні термінова діагностика та лікування, включаючи, за необхідності, декомпресію спинного мозку. Гепарин-індукована тромбоцитопенія Застосування еноксапарину натрію у пацієнтів, які мають в анамнезі вказівки на наявність гепарин-індукованої тромбоцитопенії протягом останніх 100 днів або за наявності циркулюючих антитіл протипоказано (див. розділ "Протипоказання"). Антитіла, що циркулюють, можуть персистувати кілька років. Еноксапарин натрію слід застосовувати з особливою обережністю у пацієнтів, які мають в анамнезі (понад 100 днів) гепарин-індуковану тромбоцитопенію без циркулюючих антитіл. Рішення про застосування еноксапарину натрію в даній ситуації має бути прийняте тільки після оцінки співвідношення користь/ризик та за відсутності безгепаринової (що не містить гепарин) альтернативної терапії. Черезшкірна коронарна ангіопластика З метою мінімізації ризику кровотечі, пов'язаного з інвазивною судинною інструментальною маніпуляцією при лікуванні нестабільної стенокардії та інфаркту міокарда без зубця Q та гострого інфаркту міокарда з підйомом сегмента ST, ці процедури слід проводити в інтервалах між введенням препарату. Це необхідно для досягнення гемостазу у місці введення катетера після проведення черезшкірного коронарного втручання. При використанні закриває пристрою інтродьюсер стегнової артерії може бути видалено негайно. При застосуванні мануальної (ручної) компресії інтродьюсер стегнової артерії слід видалити через 6 годин після останньої внутрішньовенної або підшкірної ін'єкції еноксапарину натрію. Якщо лікування еноксапарином натрію триває, наступну дозу слід вводити не раніше, ніж через 6-8 годин після видалення інтродьюсера стегнової артерії.Необхідно стежити за місцем введення інтродьюсера, щоб своєчасно виявити ознаки кровотечі та утворення гематоми. Пацієнти з механічними штучними клапанами серця Застосування еноксапарину натрію для профілактики тромбоутворення у пацієнтів з штучними механічними клапанами серця вивчено недостатньо. Є окремі повідомлення про розвиток тромбозу клапанів серця у пацієнтів із механічними штучними клапанами серця на фоні терапії еноксапарином натрію для профілактики тромбоутворення. Зважаючи на недостатність клінічних даних та наявність неоднозначних факторів, включаючи основне захворювання, оцінка таких повідомлень утруднена. Вагітні жінки з механічними штучними клапанами серця Застосування еноксапарину натрію для профілактики тромбоутворення у вагітних жінок з штучними механічними клапанами серця вивчено недостатньо. У клінічному дослідженні за участю вагітних жінок з механічними штучними клапанами серця при застосуванні еноксапарину натрію в дозі 1 мг/кг маси тіла двічі на добу для зменшення ризику тромбозів та емболій, у 2-х з 8-ми жінок утворилися тромби, які призводили до блокування клапанів серця та до смерті матері та плода. Є окремі постмаркетингові повідомлення про тромбоз клапанів серця у вагітних жінок з механічними штучними клапанами серця, які отримували лікування еноксапарином натрію для профілактики тромбоутворення. Вагітні жінки з механічними штучними клапанами серця можуть мати підвищений ризик розвитку тромбозу та емболії. Некроз шкіри/шкірний васкуліт Повідомлялося про розвиток некрозу шкіри та шкірного васкуліту при застосуванні низькомолекулярних гепаринів. У разі розвитку некрозу шкіри/шкірного васкуліту застосування препарату слід припинити. Гострий інфекційний ендокардит Застосування гепарину не рекомендується у пацієнтів із гострим інфекційним ендокардитом через ризик розвитку геморагічного інсульту. У випадку, якщо застосування препарату вважається абсолютно необхідним, рішення слід приймати тільки після ретельної індивідуальної оцінки співвідношення користі та ризику. Лабораторні випробування У дозах, що застосовуються для профілактики тромбоемболічних ускладнень, препарат Клексан істотно не впливає на час кровотечі та показники зсідання крові, а також на агрегацію тромбоцитів або на зв'язування їх з фібриногеном. При підвищенні дози може подовжуватися АЧТВ та активований час згортання крові. Збільшення АЧТВ та активованого часу згортання не знаходяться у прямій лінійній залежності від збільшення антикоагулянтної активності препарату, тому немає потреби в їх моніторингу. Гіперкаліємія Гепарини можуть пригнічувати секрецію альдостерону наднирковими залозами, що призводить до розвитку гіперкаліємії, особливо у пацієнтів з цукровим діабетом, хронічною нирковою недостатністю, попереднім метаболічним ацидозом, які приймають лікарські препарати, що підвищують вміст калію. Слід регулярно контролювати вміст калію у плазмі, особливо у пацієнтів групи ризику. Профілактика венозних тромбозів та емболій у пацієнтів з гострими терапевтичними захворюваннями, які перебувають на постільному режимі У разі розвитку гострої інфекції, гострих ревматичних станів профілактичне застосування еноксапарину натрію виправдане лише, якщо перераховані вище стани поєднуються з одним з нижчеперелічених факторів ризику венозного тромбоутворення: вік понад 75 років; злоякісні новоутворення; тромбози та емболії в анамнезі; ожиріння; гормональна терапія; серцева недостатність; хронічна дихальна недостатність. Порушення функції печінки Еноксапарин натрію слід обережно застосовувати у пацієнтів з порушеннями функції печінки внаслідок збільшення ризику кровотеч. Корекція дози на підставі моніторування анти-Ха активності у пацієнтів з цирозом печінки є ненадійною та не рекомендується. Вплив на здатність до керування автотранспортом та управління механізмами Препарат Клексан не впливає на здатність керувати транспортними засобами та механізмами.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. діючі речовини: ірбесартан – 150 мг; гідрохлортіазид – 12,5 мг; допоміжні речовини: лактози моногідрат - 26,65 мг, целюлоза мікрокристалічна - 45,00 мг, кроскармелоза натрію - 15,00 мг, крохмаль прежелатинізований - 45,0 мг, магнію стеарат - 3,00 мг, кремнію діоксид коллоід 25 мг, барвник заліза оксид червоний (Е 172) – 0,30 мг, барвник заліза оксид жовтий (Е 172) – 0,30 мг. По 14 таблеток у ПВХ/Ал блістер. По 1, 2, 4, 7 блістерів разом із інструкцією із застосування в картонну пачку.Опис лікарської формиОвальні двоопуклі таблетки оранжево-рожевого кольору з білими вкрапленнями з гравіюванням у вигляді серця на одній стороні та номером 2775 на іншій.Фармакотерапевтична групаГіпотензивний комбінований засіб (ангіотензин II рецепторів антагоніст [АРА II] + діуретик).ФармакокінетикаНі ірбесартан, ні гідрохлортіазид не змінюють фармакокінетику один одного. Всмоктування Після прийому препарату Коапровель абсолютна біодоступність ірбесартану - 60-80%, а гідрохлортіазиду - 50-80%. Їда не впливає на біодоступність активних речовин препарату. Після внутрішнього прийому Cmax ірбесартану в плазмі крові досягається через 1.5-2 год, гідрохлортіазиду - через 1-2.5 год. Розподіл Зв'язування ірбесартану з білками плазми становить приблизно 96%, зв'язування з клітинними компонентами незначне. Vd ірбесартану становить 53-93 л (0.72-1.24 л/кг). При щоденному однократному застосуванні ірбесартану Css досягається через 3 дні, при цьому спостерігається обмежене накопичення ірбесартану в плазмі крові (менше 20%). Зв'язування з білками плазми гідрохлортіазиду становить 68%, Vd – 3.6-7.8 л/кг. Гідрохлортіазид проникає через плацентарний бар'єр та виділяється із грудним молоком. Метаболізм Після прийому внутрішньо або внутрішньовенного введення 14С-ірбесартану 80-85% радіоактивності, що циркулює в плазмі крові, припадає на незмінений ірбесартан. Ірбесартан метаболізується в печінці шляхом окислення та кон'югації з глюкуроновою кислотою. Основним метаболітом, що знаходиться в системному кровотоку, є ірбесартану глюкуронід (приблизно 6%). Окислення ірбесартану здійснюється головним чином за допомогою ізоферменту CYP2C9, участь ізоферменту CYP3A4 у метаболізмі ірбесартану є незначною. Ірбесартан не метаболізується за допомогою більшості ізоферментів, які зазвичай беруть участь у метаболізмі лікарських препаратів (CYP1A1, CYP1A2, CYP2A6, CYP2B6 CYP2D6 або CYP2E1), і не викликає їх інгібування чи індукції. Ірбесартан не індукує та не інгібує ізофермент CYP3А4. Гідрохлортіазид не метаболізується. Виведення Ірбесартан та його метаболіти виводяться з організму як через кишечник (з жовчю), так і нирками. Після прийому внутрішньо або внутрішньовенного введення 14С-ірбесартану 20% радіоактивності виявляється в сечі, а решта - у калі. Менш ніж 2% введеної дози виділяється нирками у вигляді незміненого ірбесартану. Кінцевий Т1/2 ірбесартану становить 11-15 год. Загальний кліренс внутрішньовенно введеного ірбесартану становить 157-176 мл/хв, яке нирковий кліренс становить 3-3.5 мл/хв. Гідрохлортіазид виводиться нирками. Середні значення плазмового Т1/2 гідрохлортіазиду становлять 5-15 год. Фармакокінетика у спеціальних груп пацієнтів У жінок (порівняно з чоловіками) відзначаються дещо вищі плазмові концентрації ірбесартану. Однак пов'язаних із статтю відмінностей у Т1/2 та накопиченні ірбесартану не виявляється. Корекція дози ірбесартану у жінок не потрібна. Не спостерігалося пов'язаних із статевою приналежністю відмінностей у ефектах ірбесартану. Значення AUC та Сmax ірбесартану у пацієнтів похилого віку (65-80 років) з нормальною функцією нирок та печінки були приблизно на 20-50% вищими, ніж у пацієнтів молодшого віку (18-40 років). Кінцеві Т1/2 вони були порівнянними. Не спостерігалося пов'язаних із віком відмінностей у ефектах ірбесартану. У пацієнтів з печінковою недостатністю (внаслідок цирозу печінки) легкої (функціональний клас А або 5-6 балів за шкалою Чайлд-П'ю) та середнього ступеня (функціональний клас В або 7-9 балів за шкалою Чайлд-П'ю) фармакокінетичні параметри ірбесартану істотно не змінюються. . У пацієнтів з порушенням функції нирок або пацієнтів, яким проводиться гемодіаліз, показники фармакокінетики ірбесартану істотно не змінюються. Ірбесартан не виводиться з організму за допомогою гемодіалізу. У добровольців без артеріальної гіпертензії AUC та Т1/2 ірбесартану в осіб негроїдної раси були приблизно на 20-25% вищі, ніж у осіб європеоїдної раси; Стих ірбесартану у них була практично однаковою.ФармакодинамікаКомбінований антигіпертензивний препарат, що містить антагоніст рецепторів ангіотензину II ірбесартан та тіазидний діуретик гідрохлортіазид. Комбінація інгредієнтів має адитивний гіпотензивний ефект, знижуючи АТ у вищому ступені, ніж кожен з компонентів окремо. Ірбесартан Ірбесартан є селективним антагоністом рецепторів ангіотензину II (типу AT1), який не вимагає метаболічної активації для придбання фармакологічної активності. Ангіотензин II є важливим компонентом РААС та залучений до патогенезу розвитку артеріальної гіпертензії, а також гомеостаз натрію. Ірбесартан блокує всі фізіологічно значущі ефекти ангіотензину II незалежно від джерела або шляхи його синтезу, в т.ч. виражений судинозвужувальний ефект та посилення секреції альдостерону, що реалізуються через рецептори типу АТ1, розташовані на поверхні гладком'язових клітин судин та в корі надниркових залоз. Не має агоністичної активності по відношенню до рецепторів AT1 і має набагато більшу (більш ніж у 8500 разів) спорідненість до AT1-рецепторів, ніж до АТ2-рецепторів (рецепторів, не пов'язаних із регуляцією роботи серцево-судинної системи). Ірбесартан не пригнічує ферменти РААС (такі як ренін, АПФ) і не впливає на рецептори інших гормонів або іонні канали, що беруть участь у регуляції АТ та гомеостазу натрію. Блокування ірбесартаном AT1-рецепторів перериває ланцюг зворотного зв'язку в системі ренін-ангіотензин, що призводить до збільшення концентрації реніну та ангіотензину II у плазмі крові. Після прийому ірбесартану в дозах, що рекомендуються, плазмова концентрація альдостерону знижується, не надаючи при цьому істотного впливу на вміст калію в сироватці крові (середнє значення його збільшення становить менше 0.1 мЭкв/л). Ірбесартан не надає помітного впливу на сироваткові концентрації тригліцеридів, холестерину та глюкози. Ірбесартан не впливає на концентрацію сечової кислоти у сироватці крові або на швидкість екскреції сечової кислоти нирками. Гідрохлоротіазид Гідрохлортіазид є тіазидним діуретиком, що має діуретичну, натрійуретичну та антигіпертензивну дію. Механізм антигіпертензивної дії тіазидних діуретиків, наприклад гідрохлортіазиду, до кінця невідомий. Тіазидні діуретики впливають на канальцеві механізми реабсорбції електролітів у нирках, збільшуючи екскрецію натрію та хлоридів приблизно в однакових кількостях. Натрійурез призводить до вторинної втрати калію та бікарбонату. Гідрохлортіазид збільшує активність реніну плазми крові та секрецію альдостерону, а також знижує вміст калію у сироватці крові. Одночасне застосування антагоніста рецепторів ангіотензину II сприяє зменшенню втрат калію, пов'язаних з дією тіазидних діуретиків. Ірбесартан/гідрохлортіазид Антигіпертензивний ефект ірбесартану у комбінації з гідрохлортіазидом виявляється вже після прийому його першої дози і стає значущим протягом 1-2 тижнів застосування, максимальний антигіпертензивний ефект досягається до 6-8 тижнів лікування. У довгострокових клінічних дослідженнях спостерігалося збереження антигіпертензивного ефекту комбінації ірбесартан/гідрохлортіазид протягом більше одного року. Комбінація ірбесартан/гідрохлортіазид при застосуванні в терапевтичному діапазоні доз має дозозалежну та адитивну антигіпертензивну дію. У пацієнтів, у яких на тлі монотерапії ірбесартаном у дозі 300 мг не спостерігалося достатнього зниження АТ, додавання до монотерапії ірбесартаном у дозі 300 мг 1 раз на добу гідрохлортіазиду в дозі 12.5 мг 1 раз на добу призводило до додаткового зниження діастолічного АТ до кінця між. (тобто через 24 год після прийому препаратів) на 6.1 мм рт. ст. (В порівнянні з додаванням плацебо). Спостерігалося загальне зниження систолічного АТ (САД)/діастолічного АТ (ДАД) при комбінації ірбесартану у дозі 300 мг та гідрохлортіазиду у дозі 12.5 мг (у порівнянні з прийомом плацебо) до -13.6/-11.5 мм рт. ст. Одноразовий протягом доби прийом ірбесартану у дозі 150 мг та гідрохлортіазиду у дозі 12.5 мг продемонстрував (порівняно з прийомом плацебо) середнє зниження САД/ДАД в кінці міждозового інтервалу на 12.9/6.9 мм рт. ст. відповідно. Максимальний антигіпертензивний ефект розвивався через 3 - 6 годин. ст.в порівнянні з плацебо). Виражені у відсотках показники ТУР (відносини АТ, що вимірюється в кінці міждозового інтервалу [залишкова дія] до АТ під час максимальної дії комбінації ірбесартан/гідрохлортіазид) становили щонайменше 68%.Максимальний антигіпертензивний ефект розвивався через 3 - 6 годин. ст.в порівнянні з плацебо). Виражені у відсотках показники ТУР (відносини АТ, що вимірюється в кінці міждозового інтервалу [залишкова дія] до АТ під час максимальної дії комбінації ірбесартан/гідрохлортіазид) становили щонайменше 68%.Максимальний антигіпертензивний ефект розвивався через 3 - 6 годин. ст.в порівнянні з плацебо). Виражені у відсотках показники ТУР (відносини АТ, що вимірюється в кінці міждозового інтервалу [залишкова дія] до АТ під час максимальної дії комбінації ірбесартан/гідрохлортіазид) становили щонайменше 68%.вимірюваного в кінці міждозового інтервалу [залишкова дія] до АТ під час максимальної дії комбінації ірбесартан/гідрохлортіазид) становили, як мінімум, 68%.вимірюваного в кінці міждозового інтервалу [залишкова дія] до АТ під час максимальної дії комбінації ірбесартан/гідрохлортіазид) становили, як мінімум, 68%. У клінічному дослідженні у пацієнтів з недостатнім зниженням АТ на тлі монотерапії гідрохлортіазидом у дозі 25 мг додавання ірбесартану до гідрохлортіазиду викликало додаткове середнє зниження САД/ДАД на 11.1/7.2 мм рт. ст. відповідно, порівняно з монотерапією гідрохлортіазидом. АТ знижувалося однаковою мірою у положенні стоячи й у положенні лежачи. Ортостатичні ефекти спостерігалися рідко, проте їх виникнення можливе у пацієнтів із гіпонатріємією та/або гіповолемією. Ефективність ірбесартану/гідрохлоротіазиду не залежить від віку, расової приналежності чи статі. Загальна антигіпертензивна реакція на комбінацію у пацієнтів негроїдної раси та пацієнтів інших рас була схожою. Після відміни ірбесартану АТ поступово поверталося до вихідних значень. Синдрому відміни у ірбесартану та гідрохлортіазиду не спостерігалося. При прийомі гідрохлортіазиду внутрішньо діуретичний ефект наставав протягом перших 2 год, діурез досягав максимуму приблизно через 4 год і зберігався близько 6-12 год. У двох клінічних дослідженнях оцінювалося лікування препаратом Коапровель як початкова терапія у пацієнтів з помірно вираженою (вихідне середнє значення АТ 162/98 мм рт. ст.) та тяжкою (вихідне середнє значення АТ 172/113 мм рт. ст.) артеріальною гіпертензією . В обох дослідженнях була показана достовірна перевага антигіпертензивного ефекту препарату Коапровель® (у дозах від 12.5/150 мг до 25/300 мг) як початкова терапія, у порівнянні з застосуванням як початкова терапія монотерапії ірбесартаном (у дозах від 150 мг до 3 ) та гідрохлортіазидом (у дозах від 12.5 мг до 25 мг).Показання до застосуванняАртеріальна гіпертензія помірного або тяжкого ступеня (лікування пацієнтів, яким показана комбінована терапія).Протипоказання до застосуванняниркова недостатність тяжкого ступеня (КК ≤30 мл/хв); анурія (у зв'язку з наявністю у складі препарату гідрохлортіазиду); одночасне застосування з лікарськими препаратами, що містять аліскірен, у пацієнтів з цукровим діабетом або нирковою недостатністю середнього або тяжкого ступеня (СКФ одночасне застосування з інгібіторами АПФ у пацієнтів з діабетичною нефропатією; вагітність; період лактації (грудного вигодовування); вік до 18 років (ефективність та безпека не встановлені); спадкова непереносимість галактози, недостатність лактази або синдром мальабсорбції глюкози/галактози; підвищена чутливість до активних речовин або будь-якого з допоміжних компонентів препарату; підвищена чутливість до інших похідних сульфонаміду (бо гідрохлортіазид є похідним сульфонаміду). З обережністю: стеноз аортального чи мітрального клапана; гіпертрофічна обструктивна кардіоміопатія (ГЗКМП); гіповолемія або гіпонатріємія, що виникають при інтенсивній терапії дикретиками, гемодіалізі, дотриманні дієти з обмеженням споживання кухонної солі, діареї, блювоті (небезпека надмірного зниження артеріального тиску); пацієнти з функцією нирок, яка залежить від активності РААС, зокрема. пацієнти з артеріальною гіпертензією з двостороннім або одностороннім стенозом ниркових артерій або пацієнти з хронічною серцевою недостатністю ІІІ-ІV функціонального класу (за класифікацією NYHA); ІХС та/або атеросклеротичне ураження судин головного мозку (ризик посилення ішемії міокарда або головного мозку, аж до розвитку інфаркту міокарда або інсульту при надмірному зниженні АТ); ниркова недостатність легкого та середнього ступеня (КК від 60 до 30 мл/хв) (ризик збільшення азотемії, підвищення концентрації сечової кислоти в крові, у зв'язку з наявністю у складі препарату гідрохлортіазиду, та розвитку гіперкаліємії, у зв'язку з наявністю у складі препарату ірбесартану) ; стан після трансплантації нирки (відсутність досвіду клінічного застосування); печінкова недостатність будь-якого ступеня тяжкості або прогресуючі захворювання печінки (у зв'язку з наявністю у складі препарату гідрохлортіазиду, тому що навіть незначні порушення водно-електролітного балансу у таких пацієнтів можуть спровокувати печінкову кому); цукровий діабет (у зв'язку з наявністю у складі препарату гідрохлортіазиду можливе зниження толерантності до глюкози, підвищення потреби в інсуліні та пероральних гіпоглікемічних засобах); подагра (у зв'язку з наявністю у складі препарату гідрохлортіазиду можливе підвищення концентрації солей сечової кислоти в крові); гіперкаліємія; одночасне застосування калійзберігаючих препаратів та/або замінників солі, що містять калій (ризик розвитку гіперкаліємії); системний червоний вовчак (у зв'язку з наявністю у складі препарату гідрохлортіазиду, тому є повідомлення про загострення або обтяження перебігу системного червоного вовчаку при застосуванні тіазидних діуретиків); одночасне застосування інших гіпотензивних препаратів (можливість потенціювання їхньої антигіпертензивної дії); симпатектомія (ризик посилення антигіпертензивного ефекту гідрохлортіазиду); одночасне застосування інгібіторів АПФ або аліскірену, т.я. порівняно з монотерапією, при подвійній блокаді РААС є підвищений ризик розвитку надмірного зниження артеріального тиску, гіперкаліємії та змін функції нирок; алергічна реакція на пеніциліни та сульфаніламіди в анамнезі (фактор ризику розвитку ідеосинкразичної реакції, що спостерігалася при застосуванні сульфаніламідів або похідних сульфонаміду, і виявляється у вигляді гострої закритокутової глаукоми).Вагітність та лактаціяДосвід застосування препарату Коапровель® при вагітності відсутній. З урахуванням того, що при застосуванні інгібіторів АПФ вагітними жінками у II та III триместрах вагітності спостерігалися пошкодження та загибель плоду, що розвивається, препарат Коапровель®, як і будь-який інший препарат, який впливає безпосередньо на РААС, не можна застосовувати при вагітності. Тіазидні діуретики проникають через плацентарний бар'єр і виявляються у пуповинній крові. Застосування діуретиків у вагітних рекомендується, т.к. можливий розвиток фетальної або неонатальної жовтяниці, тромбоцитопенії та, можливо, інших небажаних реакцій, що спостерігаються у дорослих. При діагностуванні вагітності під час лікування препаратом Коапровель слід якомога швидше припинити прийом препарату. Невідомо, чи виділяється ірбесартан чи його метаболіти із грудним молоком. Гідрохлортіазид виділяється із грудним молоком. Тіазидні діуретики при їх застосуванні у високих дозах, спричиняючи інтенсивний діурез, можуть пригнічувати лактацію. Препарат Коапровель протипоказаний до застосування протягом всього періоду грудного вигодовування через потенційний ризик для немовляти. Тому після оцінки співвідношення передбачуваної користі від прийому препарату для матері та потенційного ризику для дитини слід припинити або грудне вигодовування, або прийом препарату Коапровель®. Протипоказання: вік до 18 років (ефективність та безпека не встановлені). Протипоказання: вік до 18 років (ефективність та безпека не встановлені).Побічна діяНаведені нижче небажані явища представлені відповідно до наступних градацій частоти їх виникнення за класифікацією ВООЗ: дуже часто (≥1/10); часто (≥1/100, менше 1/10); нечасто (≥1/1000, менше 1/100); рідко (≥1/10000, менше 1/1000); дуже рідко (менше 1/10 000, включаючи окремі повідомлення); невідома частота (за наявними даними визначити частоту виникнення небажаного явища неможливо). Комбінація ірбесартан/гідрохлортіазид У клінічних дослідженнях безпека комбінації ірбесартану та гідрохлортіазиду була вивчена приблизно у 2750 пацієнтів, включаючи 1540 пацієнтів з артеріальною гіпертензією, які отримували це лікування протягом 6 місяців та більше 960 пацієнтів, які отримували препарат протягом одного року і більше. Побічні ефекти у пацієнтів, які отримували препарат Коапровель®, були зазвичай помірно вираженими і скороминущими, їх частота не була пов'язана з величиною дози, що приймається (у межах рекомендованого діапазону доз). Частота виникнення побічних ефектів також не залежала від віку, статі та расової приналежності. У плацебо-контрольованих дослідженнях, у яких брали участь 898 пацієнтів, які отримували комбінацію ірбесартан/гідрохлортіазид (звичайна тривалість лікування 2-3 міс), припинення лікування через яке-небудь клінічне або лабораторне небажане явище було достовірно менш частим у пацієнтів, які приймали комбінацію ірбесартану та гідрохлортіазиду (3.6%), ніж у пацієнтів, які приймали плацебо (6.8%). Небажані явища, що спостерігалися при застосуванні комбінації ірбесартан/гідрохлортіазид у плацебо-контрольованих дослідженнях у пацієнтів з артеріальною гіпертензією З боку нервової системи: часто – запаморочення, біль голови; нечасто – ортостатичне запаморочення. З боку серцево-судинної системи: нечасто – тахікардія, зміни на ЕКГ, надмірне зниження АТ, периферичні набряки (зокрема, набряки нижніх кінцівок), “припливи” крові до шкіри обличчя, синкопальні стани. З боку травної системи: часто – нудота/блювота; нечасто – діарея, сухість слизової оболонки порожнини рота, абдомінальні болі. З боку сечовивідної системи: часто – зміна частоти сечовипускання. З боку статевих органів та молочної залози: нечасто – статева дисфункція (ослаблення лібідо, еректильна дисфункція). З боку кістково-м'язової системи: нечасто – міалгія, біль у кістках, слабкість у кінцівках. Алергічні реакції: нечасто - висипання на шкірі, свербіж. Інші: часто - підвищена стомлюваність; нечасто – слабкість. Небажані явища, що спостерігалися в плацебо-контрольованих дослідженнях при застосуванні комбінації ірбесартан/гідрохлортіазид як початкове лікування у пацієнтів з артеріальною гіпертензією тяжкого та середнього ступеня тяжкості Початкове лікування комбінацією ірбесартан/гідрохлортіазид Наведені нижче небажані явища комбінації ірбесартан/гідрохлортіазид у дослідженнях, проведених у пацієнтів з артеріальною гіпертензією тяжкого та середнього ступеня тяжкості, були аналогічні описаним вище небажаним явищам, що спостерігалися у раніше проведених дослідженнях при артеріальній гіпертензії. У клінічному дослідженні, проведеному при артеріальній гіпертензії середнього ступеня тяжкості (середнє ДАТ, у положенні сидячи 90-110 мм рт. ст.), види та частота небажаних явищ, що спостерігалися у пацієнтів, які отримували препарат Коапровель як початкова терапія, були аналогічні профілю небажаних явищ у пацієнтів, які отримували початкове лікування у вигляді монотерапії ірбесартаном або гідрохлортіазидом. Не було зареєстровано випадків синкопальних станів у групі комбінованої терапії, а у групі монотерапії гідрохлортіазидом було зареєстровано 1 випадок синкопального стану. Частота вже вказаних вище небажаних явищ при терапії препаратом Коапровель®, монотерапії ірбесартаном та монотерапії гідрохлортіазидом, відповідно, склала: 0.9%, 0% та 0% для надмірного зниження АТ; 3%, 3.8% та 1% для запаморочення; 5.5%, 3.8% та 4.8% для головного болю; 1.2%, 0% та 1% для гіперкаліємії та 0.9%, 0% та 0% для гіпокаліємії. Частота відміни лікування через небажані явища при терапії препаратом Коапровель®, монотерапії ірбесартаном та монотерапії гідрохлортіазидом склала 6.7%, 3.8% та 4.8%. У клінічному дослідженні, проведеному при тяжкій артеріальній гіпертензії (ДАД у положенні сидячи ≥110 мм рт. ст.), загальна картина небажаних явищ протягом 7 тижнів спостереження була подібною у пацієнтів, які отримували як початкову терапію препарат Коапровель®, і у пацієнтів, отримували як початкову терапію ірбесартан. Частота вже вказаних вище небажаних явищ для препарату Коапровель® та ірбесартану склала, відповідно: 0% та 0% для синкопального стану; 0.6% та 0% для надмірного зниження АТ; 3.6% та 4% для запаморочення; 4.3% та 6.6% для головного болю; 0.2% та 0% для гіперкаліємії та 0.6% та 0.4% для гіпокаліємії. Частота відміни лікування через небажані явища при прийомі препарату Коапровель® та при монотерапії ірбесартаном склала 2.1% та 2.2%, відповідно. Лабораторні та інструментальні дані Клінічно значимих змін у результатах лабораторних досліджень у ході контрольованих клінічних досліджень препарату Коапровель не виявлено. Досвід постмаркетингового застосування Ірбесартан Як і у випадку з іншими антагоністами рецепторів ангіотензину II, дуже рідкісні випадки розвитку реакцій гіперчутливості (ангіоневротичний набряк, кропив'янка) спостерігалися при монотерапії ірбесартаном. Крім цього, при застосуванні ірбесартану після його виходу на ринок спостерігалися такі небажані реакції: вертиго, астенія, гіперкаліємія, жовтяниця, міалгія, підвищення показників функціональних печінкових проб, гепатит, дзвін у вухах та порушення функції нирок, включаючи випадки розвитку гострої ниркової недостатності у пацієнтів групи ризику. Гідрохлоротіазид При монотерапії гідрохлортіазидом спостерігалися такі небажані явища (незалежно від їх зв'язку з прийомом гідрохлортіазиду): анорексія, подразнення слизової оболонки шлунка, діарея, запор, жовтяниця (пов'язана з внутрішньопечінковим холестазом), панкреатит, сіалоаденез, /агранулоцитоз, тромбоцитопенія, апластична анемія, гемолітична анемія, реакції фотосенсибілізації, лихоманка, кропив'янка, некротизуючий ангіїт (васкуліт, шкірний васкуліт), респіраторний дистрес-синдром (включаючи пневмоніт та набряк легень), гіперурикемія, порушення водно-електролітного балансу (включаючи гіпонатріємію та гіпокаліємію), порушення функції нирок, інтерстиціальний нефрит, м'язові спазми, слабкість, неспокій,минуще порушення гостроти зору.Взаємодія з лікарськими засобамиВиходячи з даних досліджень in vitro, не очікується взаємодії ірбесартану з лікарськими засобами, що метаболізуються за допомогою ізоферментів CYP1A1, CYP1A2, CYP2A6, CYP2B6, CYP2E1 або CYP3A4. Ірбесартан переважно метаболізується за допомогою ізоферменту CYP2C9 і, меншою мірою, піддається глюкуронуванню. Не спостерігалося значної фармакокінетичної та фармакодинамічної взаємодії при сумісному застосуванні ірбесартану з варфарином – препаратом, що метаболізується за допомогою ізоферменту CYP2C9. Ірбесартан не змінює фармакокінетику дигоксину та симвастатину. При сумісному застосуванні ірбесартану з гідрохлортіазидом або ніфедипіном фармакокінетика ірбесартану не змінюється. Комбінація препарату Коапровель з лікарськими препаратами, що містять аліскірен, протипоказана у пацієнтів з цукровим діабетом або з нирковою недостатністю середнього та тяжкого ступеня (СКФ Застосування препарату Коапровель у поєднанні з інгібіторами АПФ протипоказане у пацієнтів з діабетичною нефропатією та не рекомендується у інших пацієнтів. На підставі досвіду, отриманого при застосуванні інших лікарських засобів, що впливають на РААС, при одночасному застосуванні препаратів калію, замінників солі, що містять калій, калійзберігаючих діуретиків або інших, здатних підвищувати вміст калію в крові лікарських засобів (гепарин), можливе підвищення вмісту калію у сироватці. крові. Одночасне застосування з ірбесартаном гідрохлортіазиду може зменшити частоту розвитку цього ефекту. У пацієнтів похилого віку, пацієнтів з гіповолемією або пацієнтів з порушеною функцією нирок застосування НПЗЗ, включаючи інгібітори ЦОГ-2, одночасно з антагоністами рецепторів ангіотензину II, включаючи ірбесартан, може призвести до погіршення функції нирок, включаючи можливий розвиток ниркової недостатності. Ці ефекти зазвичай є оборотними. Слід періодично контролювати функцію нирок у пацієнтів, які одночасно приймають ірбесартан та нестероїдні протизапальні засоби. При одночасному застосуванні антагоністів рецепторів ангіотензину II, включаючи ірбесартан, та нестероїдні протизапальні засоби, включаючи селективні інгібітори ЦОГ-2, можливе послаблення антигіпертензивного ефекту інгібіторів рецепторів ангіотензину II. При одночасному застосуванні з етанолом, барбітуратами або наркотичними засобами може спостерігатись посилення ортостатичної гіпотензії, що викликається тіазидними діуретиками. При сумісному застосуванні з пероральними гіпоглікемічними засобами та інсуліном може знадобитися збільшення дози гіпоглікемічного засобу, т.к. гідрохлортіазид може підвищувати концентрацію глюкози у крові. При одночасному застосуванні препарату Коапровель і протиподагричних засобів може знадобитися корекція доз останніх через можливість підвищення сироваткової концентрації сечової кислоти при застосуванні гідрохлортіазиду. При сумісному застосуванні з серцевими глікозидами, антиаритмічними засобами у разі виникнення гіпокаліємії та гіпомагніємії, викликаних тіазидним діуретиком, що входить до складу препарату Коапровель®, зростає небезпека розвитку аритмій. Тіазидні діуретики можуть підвищувати вміст кальцію у сироватці крові. Якщо пацієнту потрібне застосування препаратів кальцію або кальційзберігаючих препаратів (наприклад, вітаміну D), необхідно контролювати вміст кальцію у сироватці крові та проводити відповідну корекцію режиму дозування препаратів кальцію. Всмоктування гідрохлортіазиду в присутності аніонообмінних смол (колестираміну, колестиполу) знижується. Слід розділяти за часом прийом препарату Коапровель і цих препаратів не менше ніж на 4 год. Діуретики зменшують нирковий кліренс літію, у свою чергу ірбесартан збільшує сироваткові концентрації літію, що підвищує ризик розвитку токсичних ефектів літію. Слід бути обережним при одночасному застосуванні препарату Коапровель з солями літію; рекомендується контролювати вміст літію у сироватці крові. У деяких пацієнтів інгібітори синтезу ендогенних простагландинів (наприклад, нестероїдні протизапальні засоби) можуть зменшувати ефекти тіазидних діуретиків. Гідрохлортіазид, що входить до складу препарату Коапровель®, може потенціювати ефекти інших антигіпертензивних засобів, особливо гангліоблокаторів та бета-адреноблокаторів. Гідрохлоротіазид може взаємодіяти з діазоксидом; при їх поєднанні слід контролювати концентрацію глюкози в крові, сироваткову концентрацію сечової кислоти та АТ. Гідрохлортіазид може потенціювати ефекти недеполяризуючих міорелаксантів (наприклад, тубокурарину), засобів для місцевої анестезії, засобів для загальної анестезії та засобів для премедикації перед загальною анестезією, внаслідок чого може знадобитися корекція їхнього режиму дозування. При поєднанні із застосуванням гідрохлортіазиду засоби для місцевої анестезії, засоби для загальної анестезії та засоби для премедикації перед загальною анестезією слід застосовувати у зменшених дозах. Якщо можливо, прийом гідрохлортіазиду слід припинити за 1 тиждень до хірургічного втручання. Одночасне застосування карбамазепіну та гідрохлортіазиду може асоціюватися з ризиком розвитку гіпонатріємії з клінічними проявами. Слід контролювати вміст електролітів у крові під час спільного застосування цих лікарських засобів. При необхідності застосування карбамазепіну рекомендується застосовувати діуретики з іншим механізмом дії. При одночасному застосуванні з глюкокортикостероїдами, АКТГ збільшується ризик розвитку гіпокаліємії. Дія катехоламінів може бути ослаблена під впливом тіазидних діуретиків. При одночасному застосуванні з антихолінергічними лікарськими засобами (наприклад, атропіном, біпериденом) підвищується біодоступність діуретиків тіазидного ряду за рахунок уповільнення моторики ШКТ. Тіазидні діуретики можуть знижувати виділення нирками цитотоксичних засобів (циклофосфамід, метотрексат) та посилювати їх мієлосупресивні ефекти.Спосіб застосування та дозиПрепарат приймають внутрішньо, 1 раз на добу, незалежно від їди. Коапровель® призначають пацієнтам, у яких АТ недостатньо контролюється ірбесартаном або гідрохлортіазидом у монотерапії. Коапровель® 150 мг/12.5 мг (таблетки, що містять ірбесартан/гідрохлортіазид 150 мг/12.5 мг відповідно) можна призначати пацієнтам, у яких АТ недостатньо контролюється гідрохлортіазидом (12.5 мг/добу) або ірбесартаном (150 мг/добу) у монотерапії. Коапровель® 300 мг/12.5 мг (таблетки, що містять ірбесартан/гідрохлортіазид 300 мг/12.5 мг відповідно) можна призначати пацієнтам, у яких АТ недостатньо контролюється ірбесартаном (300 мг) або препаратом Коапровель® (150 мг/12.5 мг). Коапровель® 300 мг/25 мг можна застосовувати у пацієнтів, у яких не вдається досягти цільових значень артеріального тиску при застосуванні препарату Коапровель® 300 мг/12.5 мг. Як початкова терапія у пацієнтів, які потребують проведення комбінованої гіпотензивної терапії, лікування починають з препарату Коапровель® 150 мг/12.5 мг 1 раз на добу. При необхідності більшого зниження артеріального тиску доза може бути збільшена через 1-2 тижні терапії до максимальної – 300 мг/25 мг 1 раз на добу. Максимальна добова доза становить 2 таб. препарату Коапровель 150 мг/12.5 мг або 1 таб. препарату Коапровель 300 мг/25 мг. Коапровель® 300 мг/25 мг є максимальною добовою дозою, тому одночасне застосування доз, що перевищують 300 мг ірбесартану та 25 мг гідрохлортіазиду 1 раз на добу, не рекомендується. Якщо не вдається досягти цільових значень АТ при застосуванні препарату Коапровель 300 мг/25 мг, то до терапії можна додавати інші антигіпертензивні препарати (бета-адреноблокатори, блокатори повільних кальцієвих каналів пролонгованої дії). У пацієнтів з нирковою недостатністю легкого та середнього ступеня (КК більше 30 мл/хв) корекція дози не потрібна. Однак у зв'язку з наявністю у складі препарату гідрохлортіазиду застосування препарату Коапровель® не рекомендується у пацієнтів з нирковою недостатністю тяжкого ступеня (КК ≤30 мл/хв). У пацієнтів з порушенням функції печінки легкого та середнього ступеня (5-6 та 7-9 балів за шкалою Чайлд-П'ю, відповідно) корекція дози не потрібна. У зв'язку з наявністю у складі препарату гідрохлортіазиду слід дотримуватись особливої обережності при застосуванні препарату у пацієнтів з печінковою недостатністю тяжкого ступеня (більше 9 балів за шкалою Чайлд-П'ю). У пацієнтів похилого віку корекція дози не потрібна. У пацієнтів, які приймали препарат Коапровель у клінічних дослідженнях, не спостерігалося відмінностей ефективності та безпеки між пацієнтами віком 65 років та старшими та пацієнтами молодшого віку. На даний момент безпека та ефективність препарату у пацієнтів дитячого та підліткового віку не встановлена. У пацієнтів з вираженою гіповолемією та/або гіпонатріємією, наприклад, у пацієнтів, які отримують інтенсивну терапію діуретиками, порушення водно-електролітного балансу слід скоригувати до початку застосування препарату Коапровель.ПередозуванняЄ досвід застосування ірбесартану у дозах до 900 мг на добу протягом 8 тижнів без розвитку токсичних ефектів. Симптоми: найбільш поширеними симптомами, що спостерігалися у дорослих при передозуванні гідрохлортіазиду, були симптоми, спричинені порушеннями електролітного складу крові (гіпокаліємія, гіпохлоремія, гіпонатріємія) та дегідратацією, що виникають внаслідок надмірного діуретичного ефекту. У разі одночасного застосування серцевих глікозидів (наприклад, дигоксину) або антиаритмічних препаратів (наприклад, соталолу) гіпокаліємія може сприяти розвитку порушень ритму. При передозуванні препарату можливе надмірне зниження артеріального тиску, розвиток брадикардії та тахікардії. Лікування: відсутня специфічна інформація щодо лікування передозування препарату Коапровель®. Слід встановити постійне спостереження за станом пацієнта і, при необхідності, проводити симптоматичну та підтримуючу терапію, включаючи відновлення втрат рідини та електролітів. При передозуванні рекомендується викликати блювання та/або провести промивання шлунка. Ірбесартан не виводиться з організму за допомогою гемодіалізу. Ступінь виведення гідрохлортіазиду за допомогою гемодіалізу не встановлено.Запобіжні заходи та особливі вказівкиЗастосування препарату Коапровель дотепер рідко супроводжувалося надмірним зниженням артеріального тиску у пацієнтів з артеріальною гіпертензією без інших факторів ризику для розвитку надмірної артеріальної гіпотензії. Надмірне зниження артеріального тиску, що супроводжується клінічною симптоматикою, може розвинутись у пацієнтів із гіпонатріємією/гіповолемією. Гіповолемію та/або гіпонартіємію слід скоригувати до початку застосування препарату Коапровель. Тіазидні діуретики можуть потенціювати дію інших гіпотензивних засобів. Препарат Коапровель® не рекомендується призначати пацієнтам з нирковою недостатністю тяжкого ступеня (КК ≤30 мл/хв). У пацієнтів з порушеннями функції нирок можливе збільшення азотемії, пов'язане із вмістом у складі препарату гідрохлортіазиду. Немає клінічних даних щодо застосування препарату у пацієнтів, які недавно перенесли трансплантацію нирки. Коли препарат Коапровель застосовується у пацієнтів з порушеною функцією нирок, рекомендується періодичний контроль вмісту калію, концентрації креатиніну та сечової кислоти у сироватці крові. Препарат Коапровель слід застосовувати з обережністю у пацієнтів з порушеннями функції печінки або прогресуючими захворюваннями печінки, оскільки навіть невеликі зміни водно-електролітного балансу можуть спровокувати розвиток печінкової коми. Тіазиди, включаючи гідрохлортіазид, можуть викликати порушення водно-електролітного балансу (гіпокаліємію, гіпонатріємію та гіпохлоремічний алкалоз). Хоча при застосуванні тіазидних діуретиків у монотерапії, особливо у високих дозах, можливий розвиток гіпокаліємії, одночасне застосування ірбесартану може зменшувати гіпокаліємію, що викликається гідрохлортіазидом. Навпаки, через наявність у складі препарату Коапровель® ірбесартану може мати місце гіперкаліємія, особливо у пацієнтів з нирковою недостатністю, серцевою недостатністю, цукровим діабетом. Рекомендується регулярний контроль вмісту калію у сироватці крові у пацієнтів групи ризику. Калійзберігаючі діуретики, калієві добавки або замінники солі, що містять калій, слід з обережністю застосовувати разом з препаратом Коапровель®. Дефіцит хлоридів зазвичай буває незначним і,як правило, не потребує лікування. Тіазиди знижують виведення кальцію через нирки та викликають непостійне та незначне збільшення вмісту кальцію у сироватці крові. Розвиток клінічно значущої гіперкальціємії може вказувати на можливість наявності у пацієнта гіперпаратиреозу. Прийом тіазидів слід припинити перед проведенням дослідження функції паращитовидних залоз. Було продемонстровано, що тіазиди збільшують виведення іонів магнію нирками, що може призвести до розвитку гіпомагніємії.Прийом тіазидів слід припинити перед проведенням дослідження функції паращитовидних залоз. Було продемонстровано, що тіазиди збільшують виведення іонів магнію нирками, що може призвести до розвитку гіпомагніємії.Прийом тіазидів слід припинити перед проведенням дослідження функції паращитовидних залоз. Було продемонстровано, що тіазиди збільшують виведення іонів магнію нирками, що може призвести до розвитку гіпомагніємії. При лікуванні тіазидними діуретиками може розвинутись гіперглікемія та загострення подагри у деяких пацієнтів. При лікуванні тіазидними діуретиками може збільшитись потреба в інсуліні у пацієнтів з цукровим діабетом, а також можлива маніфестація латентного цукрового діабету. Лікування тіазидними діуретиками асоціювалося зі збільшенням концентрацій холестерину та тригліцеридів у крові, проте доза 12.5 мг, що міститься у препараті Коапровель®, практично не впливає на концентрацію холестерину та тригліцеридів у крові. При терапії тіазидними діуретиками у деяких пацієнтів може спостерігатися гіперурикемія або загострення перебігу подагри. Пацієнтам із ризиком розвитку порушень водно-електролітного балансу та метаболічних порушень може знадобитися моніторинг лабораторних показників. Повідомлялося про загострення або обтяження перебігу системного червоного вовчаку при застосуванні тіазидних діуретиків. Сульфаніламіди або похідні сульфонаміду можуть викликати ідіосинкразичні реакції, що призводять до розвитку минущої міопії та гострої закритокутової глаукоми. Незважаючи на те, що гідрохлортіазид є похідним сульфонаміду, дотепер повідомлялося тільки про окремі випадки розвитку гострої закритокутової глаукоми без встановлення причинно-наслідкового взаємозв'язку з його застосуванням. Симптомами гострої глаукоми є: гостре зниження гостроти зору або очний біль, які зазвичай виникають протягом періоду від декількох годин до декількох тижнів після початку застосування препарату. Гостра закритокутова глаукома, що залишилася без лікування, може призвести до стійкої втрати зору. При виникненні цих симптомів слід якнайшвидше припинити прийом препарату.Якщо при цьому не вдасться нормалізувати внутрішньоочний тиск, може знадобитися термінове терапевтичне або хірургічне лікування. Факторами ризику для розвитку гострої глаукоми є вказівки в анамнезі на алергічні реакції на сульфаніламіди і пеніциліни. Подвійна блокада РААС у разі застосування комбінації препарату Коапровель® з інгібіторами АПФ або аліскіреном не рекомендується, т.к. порівняно з монотерапією є підвищений ризик різкого зниження АТ, розвитку гіперкаліємії та порушення функції нирок. Застосування препарату Коапровель у комбінації з аліскіреном протипоказане у пацієнтів з цукровим діабетом або нирковою недостатністю. Як наслідок інгібування РААС очікується погіршення функції нирок у схильних до цього пацієнтів. У пацієнтів з функцією нирок, яка залежить від активності РААС (пацієнти з артеріальною гіпертензією та стенозом ниркової артерії однієї або обох нирок, пацієнти з хронічною серцевою недостатністю III та IV функціонального класу [за класифікацією NYHA]), лікування лікарськими препаратами, що впливають на РААС, асоціювалося з олігурією та/або прогресуючою азотемією та, рідко, з гострою нирковою недостатністю та/або смертю. Не можна унеможливити виникнення подібного ефекту при застосуванні інгібіторів рецепторів ангіотензину II, включаючи препарат Коапровель®. У пацієнтів після симпатектомії може посилюватися антигіпертензивний ефект тіазидних діуретиків. У пацієнтів зі стенозом гирла аорти та стенозом мітрального клапана, гіпертрофічною обструктивною кардіоміопатією необхідна особлива обережність при застосуванні вазодилататорів, включаючи препарат Коапровель®. Застосування препарату Коапровель при первинному гіперальдостеронізмі недоцільно, т.к. такі пацієнти зазвичай не реагують на антигіпертензивні препарати, що впливають на РААС. Гідрохлортіазид може давати позитивний результат під час проведення допінг-контролю. Розвиток алергічних реакцій на гідрохлортіазид більш ймовірний у пацієнтів з обтяженим алергологічним анамнезом або пацієнтів з бронхіальною астмою. Вплив на здатність до керування автотранспортом та управління механізмами Вплив препарату Коапровель на здатність керувати транспортними засобами або займатися іншими потенційно небезпечними видами діяльності, що вимагають підвищеної уваги та високої швидкості психомоторних реакцій, не вивчався. Виходячи з фармакодинамічних властивостей препарат Коапровель® не повинен впливати на здатність керувати транспортними засобами та займатися іншими потенційно небезпечними видами діяльності (робота на висоті, робота авіадиспетчера, робота з механізмами тощо). Однак при занятті потенційно небезпечними видами діяльності слід бути обережними.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. діючі речовини: ірбесартан – 300 мг; гідрохлортіазид – 12,5 мг; допоміжні речовини: лактози моногідрат - 65,80 мг, целюлоза мікрокристалічна 90,00 мг, кроскармелоза натрію 30,00 мг, крохмаль прежелатинізований - 90,0 мг, магнію стеарат - 6,00 мг, кремнію діоксид колоїдний , барвник заліза оксид червоний (Е 172) – 0,60 мг, барвник заліза оксид жовтий (Е 172) – 0,60 мг. По 14 таблеток у ПВХ/Ал блістер. По 1, 2, 4, 7 блістерів разом із інструкцією із застосування в картонну пачку.Опис лікарської формиОвальні двоопуклі таблетки оранжево-рожевого кольору з білими вкрапленнями з гравіюванням у вигляді серця на одній стороні та номером 2776 на іншій.Фармакотерапевтична групаГіпотензивний комбінований засіб (ангіотензин II рецепторів антагоніст [АРА II] + діуретик).ФармакокінетикаНі ірбесартан, ні гідрохлортіазид не змінюють фармакокінетику один одного. Всмоктування Після прийому препарату Коапровель абсолютна біодоступність ірбесартану - 60-80%, а гідрохлортіазиду - 50-80%. Їда не впливає на біодоступність активних речовин препарату. Після внутрішнього прийому Cmax ірбесартану в плазмі крові досягається через 1.5-2 год, гідрохлортіазиду - через 1-2.5 год. Розподіл Зв'язування ірбесартану з білками плазми становить приблизно 96%, зв'язування з клітинними компонентами незначне. Vd ірбесартану становить 53-93 л (0.72-1.24 л/кг). При щоденному однократному застосуванні ірбесартану Css досягається через 3 дні, при цьому спостерігається обмежене накопичення ірбесартану в плазмі крові (менше 20%). Зв'язування з білками плазми гідрохлортіазиду становить 68%, Vd – 3.6-7.8 л/кг. Гідрохлортіазид проникає через плацентарний бар'єр та виділяється із грудним молоком. Метаболізм Після прийому внутрішньо або внутрішньовенного введення 14С-ірбесартану 80-85% радіоактивності, що циркулює в плазмі крові, припадає на незмінений ірбесартан. Ірбесартан метаболізується в печінці шляхом окислення та кон'югації з глюкуроновою кислотою. Основним метаболітом, що знаходиться в системному кровотоку, є ірбесартану глюкуронід (приблизно 6%). Окислення ірбесартану здійснюється головним чином за допомогою ізоферменту CYP2C9, участь ізоферменту CYP3A4 у метаболізмі ірбесартану є незначною. Ірбесартан не метаболізується за допомогою більшості ізоферментів, які зазвичай беруть участь у метаболізмі лікарських препаратів (CYP1A1, CYP1A2, CYP2A6, CYP2B6 CYP2D6 або CYP2E1), і не викликає їх інгібування чи індукції. Ірбесартан не індукує та не інгібує ізофермент CYP3А4. Гідрохлортіазид не метаболізується. Виведення Ірбесартан та його метаболіти виводяться з організму як через кишечник (з жовчю), так і нирками. Після прийому внутрішньо або внутрішньовенного введення 14С-ірбесартану 20% радіоактивності виявляється в сечі, а решта - у калі. Менш ніж 2% введеної дози виділяється нирками у вигляді незміненого ірбесартану. Кінцевий Т1/2 ірбесартану становить 11-15 год. Загальний кліренс внутрішньовенно введеного ірбесартану становить 157-176 мл/хв, яке нирковий кліренс становить 3-3.5 мл/хв. Гідрохлортіазид виводиться нирками. Середні значення плазмового Т1/2 гідрохлортіазиду становлять 5-15 год. Фармакокінетика у спеціальних груп пацієнтів У жінок (порівняно з чоловіками) відзначаються дещо вищі плазмові концентрації ірбесартану. Однак пов'язаних із статтю відмінностей у Т1/2 та накопиченні ірбесартану не виявляється. Корекція дози ірбесартану у жінок не потрібна. Не спостерігалося пов'язаних із статевою приналежністю відмінностей у ефектах ірбесартану. Значення AUC та Сmax ірбесартану у пацієнтів похилого віку (65-80 років) з нормальною функцією нирок та печінки були приблизно на 20-50% вищими, ніж у пацієнтів молодшого віку (18-40 років). Кінцеві Т1/2 вони були порівнянними. Не спостерігалося пов'язаних із віком відмінностей у ефектах ірбесартану. У пацієнтів з печінковою недостатністю (внаслідок цирозу печінки) легкої (функціональний клас А або 5-6 балів за шкалою Чайлд-П'ю) та середнього ступеня (функціональний клас В або 7-9 балів за шкалою Чайлд-П'ю) фармакокінетичні параметри ірбесартану істотно не змінюються. . У пацієнтів з порушенням функції нирок або пацієнтів, яким проводиться гемодіаліз, показники фармакокінетики ірбесартану істотно не змінюються. Ірбесартан не виводиться з організму за допомогою гемодіалізу. У добровольців без артеріальної гіпертензії AUC та Т1/2 ірбесартану в осіб негроїдної раси були приблизно на 20-25% вищі, ніж у осіб європеоїдної раси; Стих ірбесартану у них була практично однаковою.ФармакодинамікаКомбінований антигіпертензивний препарат, що містить антагоніст рецепторів ангіотензину II ірбесартан та тіазидний діуретик гідрохлортіазид. Комбінація інгредієнтів має адитивний гіпотензивний ефект, знижуючи АТ у вищому ступені, ніж кожен з компонентів окремо. Ірбесартан Ірбесартан є селективним антагоністом рецепторів ангіотензину II (типу AT1), який не вимагає метаболічної активації для придбання фармакологічної активності. Ангіотензин II є важливим компонентом РААС та залучений до патогенезу розвитку артеріальної гіпертензії, а також гомеостаз натрію. Ірбесартан блокує всі фізіологічно значущі ефекти ангіотензину II незалежно від джерела або шляхи його синтезу, в т.ч. виражений судинозвужувальний ефект та посилення секреції альдостерону, що реалізуються через рецептори типу АТ1, розташовані на поверхні гладком'язових клітин судин та в корі надниркових залоз. Не має агоністичної активності по відношенню до рецепторів AT1 і має набагато більшу (більш ніж у 8500 разів) спорідненість до AT1-рецепторів, ніж до АТ2-рецепторів (рецепторів, не пов'язаних із регуляцією роботи серцево-судинної системи). Ірбесартан не пригнічує ферменти РААС (такі як ренін, АПФ) і не впливає на рецептори інших гормонів або іонні канали, що беруть участь у регуляції АТ та гомеостазу натрію. Блокування ірбесартаном AT1-рецепторів перериває ланцюг зворотного зв'язку в системі ренін-ангіотензин, що призводить до збільшення концентрації реніну та ангіотензину II у плазмі крові. Після прийому ірбесартану в дозах, що рекомендуються, плазмова концентрація альдостерону знижується, не надаючи при цьому істотного впливу на вміст калію в сироватці крові (середнє значення його збільшення становить менше 0.1 мЭкв/л). Ірбесартан не надає помітного впливу на сироваткові концентрації тригліцеридів, холестерину та глюкози. Ірбесартан не впливає на концентрацію сечової кислоти у сироватці крові або на швидкість екскреції сечової кислоти нирками. Гідрохлоротіазид Гідрохлортіазид є тіазидним діуретиком, що має діуретичну, натрійуретичну та антигіпертензивну дію. Механізм антигіпертензивної дії тіазидних діуретиків, наприклад гідрохлортіазиду, до кінця невідомий. Тіазидні діуретики впливають на канальцеві механізми реабсорбції електролітів у нирках, збільшуючи екскрецію натрію та хлоридів приблизно в однакових кількостях. Натрійурез призводить до вторинної втрати калію та бікарбонату. Гідрохлортіазид збільшує активність реніну плазми крові та секрецію альдостерону, а також знижує вміст калію у сироватці крові. Одночасне застосування антагоніста рецепторів ангіотензину II сприяє зменшенню втрат калію, пов'язаних з дією тіазидних діуретиків. Ірбесартан/гідрохлортіазид Антигіпертензивний ефект ірбесартану у комбінації з гідрохлортіазидом виявляється вже після прийому його першої дози і стає значущим протягом 1-2 тижнів застосування, максимальний антигіпертензивний ефект досягається до 6-8 тижнів лікування. У довгострокових клінічних дослідженнях спостерігалося збереження антигіпертензивного ефекту комбінації ірбесартан/гідрохлортіазид протягом більше одного року. Комбінація ірбесартан/гідрохлортіазид при застосуванні в терапевтичному діапазоні доз має дозозалежну та адитивну антигіпертензивну дію. У пацієнтів, у яких на тлі монотерапії ірбесартаном у дозі 300 мг не спостерігалося достатнього зниження АТ, додавання до монотерапії ірбесартаном у дозі 300 мг 1 раз на добу гідрохлортіазиду в дозі 12.5 мг 1 раз на добу призводило до додаткового зниження діастолічного АТ до кінця між. (тобто через 24 год після прийому препаратів) на 6.1 мм рт. ст. (В порівнянні з додаванням плацебо). Спостерігалося загальне зниження систолічного АТ (САД)/діастолічного АТ (ДАД) при комбінації ірбесартану у дозі 300 мг та гідрохлортіазиду у дозі 12.5 мг (у порівнянні з прийомом плацебо) до -13.6/-11.5 мм рт. ст. Одноразовий протягом доби прийом ірбесартану у дозі 150 мг та гідрохлортіазиду у дозі 12.5 мг продемонстрував (порівняно з прийомом плацебо) середнє зниження САД/ДАД в кінці міждозового інтервалу на 12.9/6.9 мм рт. ст. відповідно. Максимальний антигіпертензивний ефект розвивався через 3 - 6 годин. ст.в порівнянні з плацебо). Виражені у відсотках показники ТУР (відносини АТ, що вимірюється в кінці міждозового інтервалу [залишкова дія] до АТ під час максимальної дії комбінації ірбесартан/гідрохлортіазид) становили щонайменше 68%.Максимальний антигіпертензивний ефект розвивався через 3 - 6 годин. ст.в порівнянні з плацебо). Виражені у відсотках показники ТУР (відносини АТ, що вимірюється в кінці міждозового інтервалу [залишкова дія] до АТ під час максимальної дії комбінації ірбесартан/гідрохлортіазид) становили щонайменше 68%.Максимальний антигіпертензивний ефект розвивався через 3 - 6 годин. ст.в порівнянні з плацебо). Виражені у відсотках показники ТУР (відносини АТ, що вимірюється в кінці міждозового інтервалу [залишкова дія] до АТ під час максимальної дії комбінації ірбесартан/гідрохлортіазид) становили щонайменше 68%.вимірюваного в кінці міждозового інтервалу [залишкова дія] до АТ під час максимальної дії комбінації ірбесартан/гідрохлортіазид) становили, як мінімум, 68%.вимірюваного в кінці міждозового інтервалу [залишкова дія] до АТ під час максимальної дії комбінації ірбесартан/гідрохлортіазид) становили, як мінімум, 68%. У клінічному дослідженні у пацієнтів з недостатнім зниженням АТ на тлі монотерапії гідрохлортіазидом у дозі 25 мг додавання ірбесартану до гідрохлортіазиду викликало додаткове середнє зниження САД/ДАД на 11.1/7.2 мм рт. ст. відповідно, порівняно з монотерапією гідрохлортіазидом. АТ знижувалося однаковою мірою у положенні стоячи й у положенні лежачи. Ортостатичні ефекти спостерігалися рідко, проте їх виникнення можливе у пацієнтів із гіпонатріємією та/або гіповолемією. Ефективність ірбесартану/гідрохлоротіазиду не залежить від віку, расової приналежності чи статі. Загальна антигіпертензивна реакція на комбінацію у пацієнтів негроїдної раси та пацієнтів інших рас була схожою. Після відміни ірбесартану АТ поступово поверталося до вихідних значень. Синдрому відміни у ірбесартану та гідрохлортіазиду не спостерігалося. При прийомі гідрохлортіазиду внутрішньо діуретичний ефект наставав протягом перших 2 год, діурез досягав максимуму приблизно через 4 год і зберігався близько 6-12 год. У двох клінічних дослідженнях оцінювалося лікування препаратом Коапровель як початкова терапія у пацієнтів з помірно вираженою (вихідне середнє значення АТ 162/98 мм рт. ст.) та тяжкою (вихідне середнє значення АТ 172/113 мм рт. ст.) артеріальною гіпертензією . В обох дослідженнях була показана достовірна перевага антигіпертензивного ефекту препарату Коапровель® (у дозах від 12.5/150 мг до 25/300 мг) як початкова терапія, у порівнянні з застосуванням як початкова терапія монотерапії ірбесартаном (у дозах від 150 мг до 3 ) та гідрохлортіазидом (у дозах від 12.5 мг до 25 мг).Показання до застосуванняАртеріальна гіпертензія помірного або тяжкого ступеня (лікування пацієнтів, яким показана комбінована терапія).Протипоказання до застосуванняниркова недостатність тяжкого ступеня (КК ≤30 мл/хв); анурія (у зв'язку з наявністю у складі препарату гідрохлортіазиду); одночасне застосування з лікарськими препаратами, що містять аліскірен, у пацієнтів з цукровим діабетом або нирковою недостатністю середнього або тяжкого ступеня (СКФ одночасне застосування з інгібіторами АПФ у пацієнтів з діабетичною нефропатією; вагітність; період лактації (грудного вигодовування); вік до 18 років (ефективність та безпека не встановлені); спадкова непереносимість галактози, недостатність лактази або синдром мальабсорбції глюкози/галактози; підвищена чутливість до активних речовин або будь-якого з допоміжних компонентів препарату; підвищена чутливість до інших похідних сульфонаміду (бо гідрохлортіазид є похідним сульфонаміду). З обережністю: стеноз аортального чи мітрального клапана; гіпертрофічна обструктивна кардіоміопатія (ГЗКМП); гіповолемія або гіпонатріємія, що виникають при інтенсивній терапії дикретиками, гемодіалізі, дотриманні дієти з обмеженням споживання кухонної солі, діареї, блювоті (небезпека надмірного зниження артеріального тиску); пацієнти з функцією нирок, яка залежить від активності РААС, зокрема. пацієнти з артеріальною гіпертензією з двостороннім або одностороннім стенозом ниркових артерій або пацієнти з хронічною серцевою недостатністю ІІІ-ІV функціонального класу (за класифікацією NYHA); ІХС та/або атеросклеротичне ураження судин головного мозку (ризик посилення ішемії міокарда або головного мозку, аж до розвитку інфаркту міокарда або інсульту при надмірному зниженні АТ); ниркова недостатність легкого та середнього ступеня (КК від 60 до 30 мл/хв) (ризик збільшення азотемії, підвищення концентрації сечової кислоти в крові, у зв'язку з наявністю у складі препарату гідрохлортіазиду, та розвитку гіперкаліємії, у зв'язку з наявністю у складі препарату ірбесартану) ; стан після трансплантації нирки (відсутність досвіду клінічного застосування); печінкова недостатність будь-якого ступеня тяжкості або прогресуючі захворювання печінки (у зв'язку з наявністю у складі препарату гідрохлортіазиду, тому що навіть незначні порушення водно-електролітного балансу у таких пацієнтів можуть спровокувати печінкову кому); цукровий діабет (у зв'язку з наявністю у складі препарату гідрохлортіазиду можливе зниження толерантності до глюкози, підвищення потреби в інсуліні та пероральних гіпоглікемічних засобах); подагра (у зв'язку з наявністю у складі препарату гідрохлортіазиду можливе підвищення концентрації солей сечової кислоти в крові); гіперкаліємія; одночасне застосування калійзберігаючих препаратів та/або замінників солі, що містять калій (ризик розвитку гіперкаліємії); системний червоний вовчак (у зв'язку з наявністю у складі препарату гідрохлортіазиду, тому є повідомлення про загострення або обтяження перебігу системного червоного вовчаку при застосуванні тіазидних діуретиків); одночасне застосування інших гіпотензивних препаратів (можливість потенціювання їхньої антигіпертензивної дії); симпатектомія (ризик посилення антигіпертензивного ефекту гідрохлортіазиду); одночасне застосування інгібіторів АПФ або аліскірену, т.я. порівняно з монотерапією, при подвійній блокаді РААС є підвищений ризик розвитку надмірного зниження артеріального тиску, гіперкаліємії та змін функції нирок; алергічна реакція на пеніциліни та сульфаніламіди в анамнезі (фактор ризику розвитку ідеосинкразичної реакції, що спостерігалася при застосуванні сульфаніламідів або похідних сульфонаміду, і виявляється у вигляді гострої закритокутової глаукоми).Вагітність та лактаціяДосвід застосування препарату Коапровель® при вагітності відсутній. З урахуванням того, що при застосуванні інгібіторів АПФ вагітними жінками у II та III триместрах вагітності спостерігалися пошкодження та загибель плоду, що розвивається, препарат Коапровель®, як і будь-який інший препарат, який впливає безпосередньо на РААС, не можна застосовувати при вагітності. Тіазидні діуретики проникають через плацентарний бар'єр і виявляються у пуповинній крові. Застосування діуретиків у вагітних рекомендується, т.к. можливий розвиток фетальної або неонатальної жовтяниці, тромбоцитопенії та, можливо, інших небажаних реакцій, що спостерігаються у дорослих. При діагностуванні вагітності під час лікування препаратом Коапровель слід якомога швидше припинити прийом препарату. Невідомо, чи виділяється ірбесартан чи його метаболіти із грудним молоком. Гідрохлортіазид виділяється із грудним молоком. Тіазидні діуретики при їх застосуванні у високих дозах, спричиняючи інтенсивний діурез, можуть пригнічувати лактацію. Препарат Коапровель протипоказаний до застосування протягом всього періоду грудного вигодовування через потенційний ризик для немовляти. Тому після оцінки співвідношення передбачуваної користі від прийому препарату для матері та потенційного ризику для дитини слід припинити або грудне вигодовування, або прийом препарату Коапровель®. Протипоказання: вік до 18 років (ефективність та безпека не встановлені). Протипоказання: вік до 18 років (ефективність та безпека не встановлені).Побічна діяНаведені нижче небажані явища представлені відповідно до наступних градацій частоти їх виникнення за класифікацією ВООЗ: дуже часто (≥1/10); часто (≥1/100, менше 1/10); нечасто (≥1/1000, менше 1/100); рідко (≥1/10000, менше 1/1000); дуже рідко (менше 1/10 000, включаючи окремі повідомлення); невідома частота (за наявними даними визначити частоту виникнення небажаного явища неможливо). Комбінація ірбесартан/гідрохлортіазид У клінічних дослідженнях безпека комбінації ірбесартану та гідрохлортіазиду була вивчена приблизно у 2750 пацієнтів, включаючи 1540 пацієнтів з артеріальною гіпертензією, які отримували це лікування протягом 6 місяців та більше 960 пацієнтів, які отримували препарат протягом одного року і більше. Побічні ефекти у пацієнтів, які отримували препарат Коапровель®, були зазвичай помірно вираженими і скороминущими, їх частота не була пов'язана з величиною дози, що приймається (у межах рекомендованого діапазону доз). Частота виникнення побічних ефектів також не залежала від віку, статі та расової приналежності. У плацебо-контрольованих дослідженнях, у яких брали участь 898 пацієнтів, які отримували комбінацію ірбесартан/гідрохлортіазид (звичайна тривалість лікування 2-3 міс), припинення лікування через яке-небудь клінічне або лабораторне небажане явище було достовірно менш частим у пацієнтів, які приймали комбінацію ірбесартану та гідрохлортіазиду (3.6%), ніж у пацієнтів, які приймали плацебо (6.8%). Небажані явища, що спостерігалися при застосуванні комбінації ірбесартан/гідрохлортіазид у плацебо-контрольованих дослідженнях у пацієнтів з артеріальною гіпертензією З боку нервової системи: часто – запаморочення, біль голови; нечасто – ортостатичне запаморочення. З боку серцево-судинної системи: нечасто – тахікардія, зміни на ЕКГ, надмірне зниження АТ, периферичні набряки (зокрема, набряки нижніх кінцівок), “припливи” крові до шкіри обличчя, синкопальні стани. З боку травної системи: часто – нудота/блювота; нечасто – діарея, сухість слизової оболонки порожнини рота, абдомінальні болі. З боку сечовивідної системи: часто – зміна частоти сечовипускання. З боку статевих органів та молочної залози: нечасто – статева дисфункція (ослаблення лібідо, еректильна дисфункція). З боку кістково-м'язової системи: нечасто – міалгія, біль у кістках, слабкість у кінцівках. Алергічні реакції: нечасто - висипання на шкірі, свербіж. Інші: часто - підвищена стомлюваність; нечасто – слабкість. Небажані явища, що спостерігалися в плацебо-контрольованих дослідженнях при застосуванні комбінації ірбесартан/гідрохлортіазид як початкове лікування у пацієнтів з артеріальною гіпертензією тяжкого та середнього ступеня тяжкості Початкове лікування комбінацією ірбесартан/гідрохлортіазид Наведені нижче небажані явища комбінації ірбесартан/гідрохлортіазид у дослідженнях, проведених у пацієнтів з артеріальною гіпертензією тяжкого та середнього ступеня тяжкості, були аналогічні описаним вище небажаним явищам, що спостерігалися у раніше проведених дослідженнях при артеріальній гіпертензії. У клінічному дослідженні, проведеному при артеріальній гіпертензії середнього ступеня тяжкості (середнє ДАТ, у положенні сидячи 90-110 мм рт. ст.), види та частота небажаних явищ, що спостерігалися у пацієнтів, які отримували препарат Коапровель як початкова терапія, були аналогічні профілю небажаних явищ у пацієнтів, які отримували початкове лікування у вигляді монотерапії ірбесартаном або гідрохлортіазидом. Не було зареєстровано випадків синкопальних станів у групі комбінованої терапії, а у групі монотерапії гідрохлортіазидом було зареєстровано 1 випадок синкопального стану. Частота вже вказаних вище небажаних явищ при терапії препаратом Коапровель®, монотерапії ірбесартаном та монотерапії гідрохлортіазидом, відповідно, склала: 0.9%, 0% та 0% для надмірного зниження АТ; 3%, 3.8% та 1% для запаморочення; 5.5%, 3.8% та 4.8% для головного болю; 1.2%, 0% та 1% для гіперкаліємії та 0.9%, 0% та 0% для гіпокаліємії. Частота відміни лікування через небажані явища при терапії препаратом Коапровель®, монотерапії ірбесартаном та монотерапії гідрохлортіазидом склала 6.7%, 3.8% та 4.8%. У клінічному дослідженні, проведеному при тяжкій артеріальній гіпертензії (ДАД у положенні сидячи ≥110 мм рт. ст.), загальна картина небажаних явищ протягом 7 тижнів спостереження була подібною у пацієнтів, які отримували як початкову терапію препарат Коапровель®, і у пацієнтів, отримували як початкову терапію ірбесартан. Частота вже вказаних вище небажаних явищ для препарату Коапровель® та ірбесартану склала, відповідно: 0% та 0% для синкопального стану; 0.6% та 0% для надмірного зниження АТ; 3.6% та 4% для запаморочення; 4.3% та 6.6% для головного болю; 0.2% та 0% для гіперкаліємії та 0.6% та 0.4% для гіпокаліємії. Частота відміни лікування через небажані явища при прийомі препарату Коапровель® та при монотерапії ірбесартаном склала 2.1% та 2.2%, відповідно. Лабораторні та інструментальні дані Клінічно значимих змін у результатах лабораторних досліджень у ході контрольованих клінічних досліджень препарату Коапровель не виявлено. Досвід постмаркетингового застосування Ірбесартан Як і у випадку з іншими антагоністами рецепторів ангіотензину II, дуже рідкісні випадки розвитку реакцій гіперчутливості (ангіоневротичний набряк, кропив'янка) спостерігалися при монотерапії ірбесартаном. Крім цього, при застосуванні ірбесартану після його виходу на ринок спостерігалися такі небажані реакції: вертиго, астенія, гіперкаліємія, жовтяниця, міалгія, підвищення показників функціональних печінкових проб, гепатит, дзвін у вухах та порушення функції нирок, включаючи випадки розвитку гострої ниркової недостатності у пацієнтів групи ризику. Гідрохлоротіазид При монотерапії гідрохлортіазидом спостерігалися такі небажані явища (незалежно від їх зв'язку з прийомом гідрохлортіазиду): анорексія, подразнення слизової оболонки шлунка, діарея, запор, жовтяниця (пов'язана з внутрішньопечінковим холестазом), панкреатит, сіалоаденез, /агранулоцитоз, тромбоцитопенія, апластична анемія, гемолітична анемія, реакції фотосенсибілізації, лихоманка, кропив'янка, некротизуючий ангіїт (васкуліт, шкірний васкуліт), респіраторний дистрес-синдром (включаючи пневмоніт та набряк легень), гіперурикемія, порушення водно-електролітного балансу (включаючи гіпонатріємію та гіпокаліємію), порушення функції нирок, інтерстиціальний нефрит, м'язові спазми, слабкість, неспокій,минуще порушення гостроти зору.Взаємодія з лікарськими засобамиВиходячи з даних досліджень in vitro, не очікується взаємодії ірбесартану з лікарськими засобами, що метаболізуються за допомогою ізоферментів CYP1A1, CYP1A2, CYP2A6, CYP2B6, CYP2E1 або CYP3A4. Ірбесартан переважно метаболізується за допомогою ізоферменту CYP2C9 і, меншою мірою, піддається глюкуронуванню. Не спостерігалося значної фармакокінетичної та фармакодинамічної взаємодії при сумісному застосуванні ірбесартану з варфарином – препаратом, що метаболізується за допомогою ізоферменту CYP2C9. Ірбесартан не змінює фармакокінетику дигоксину та симвастатину. При сумісному застосуванні ірбесартану з гідрохлортіазидом або ніфедипіном фармакокінетика ірбесартану не змінюється. Комбінація препарату Коапровель з лікарськими препаратами, що містять аліскірен, протипоказана у пацієнтів з цукровим діабетом або з нирковою недостатністю середнього та тяжкого ступеня (СКФ Застосування препарату Коапровель у поєднанні з інгібіторами АПФ протипоказане у пацієнтів з діабетичною нефропатією та не рекомендується у інших пацієнтів. На підставі досвіду, отриманого при застосуванні інших лікарських засобів, що впливають на РААС, при одночасному застосуванні препаратів калію, замінників солі, що містять калій, калійзберігаючих діуретиків або інших, здатних підвищувати вміст калію в крові лікарських засобів (гепарин), можливе підвищення вмісту калію у сироватці. крові. Одночасне застосування з ірбесартаном гідрохлортіазиду може зменшити частоту розвитку цього ефекту. У пацієнтів похилого віку, пацієнтів з гіповолемією або пацієнтів з порушеною функцією нирок застосування НПЗЗ, включаючи інгібітори ЦОГ-2, одночасно з антагоністами рецепторів ангіотензину II, включаючи ірбесартан, може призвести до погіршення функції нирок, включаючи можливий розвиток ниркової недостатності. Ці ефекти зазвичай є оборотними. Слід періодично контролювати функцію нирок у пацієнтів, які одночасно приймають ірбесартан та нестероїдні протизапальні засоби. При одночасному застосуванні антагоністів рецепторів ангіотензину II, включаючи ірбесартан, та нестероїдні протизапальні засоби, включаючи селективні інгібітори ЦОГ-2, можливе послаблення антигіпертензивного ефекту інгібіторів рецепторів ангіотензину II. При одночасному застосуванні з етанолом, барбітуратами або наркотичними засобами може спостерігатись посилення ортостатичної гіпотензії, що викликається тіазидними діуретиками. При сумісному застосуванні з пероральними гіпоглікемічними засобами та інсуліном може знадобитися збільшення дози гіпоглікемічного засобу, т.к. гідрохлортіазид може підвищувати концентрацію глюкози у крові. При одночасному застосуванні препарату Коапровель і протиподагричних засобів може знадобитися корекція доз останніх через можливість підвищення сироваткової концентрації сечової кислоти при застосуванні гідрохлортіазиду. При сумісному застосуванні з серцевими глікозидами, антиаритмічними засобами у разі виникнення гіпокаліємії та гіпомагніємії, викликаних тіазидним діуретиком, що входить до складу препарату Коапровель®, зростає небезпека розвитку аритмій. Тіазидні діуретики можуть підвищувати вміст кальцію у сироватці крові. Якщо пацієнту потрібне застосування препаратів кальцію або кальційзберігаючих препаратів (наприклад, вітаміну D), необхідно контролювати вміст кальцію у сироватці крові та проводити відповідну корекцію режиму дозування препаратів кальцію. Всмоктування гідрохлортіазиду в присутності аніонообмінних смол (колестираміну, колестиполу) знижується. Слід розділяти за часом прийом препарату Коапровель і цих препаратів не менше ніж на 4 год. Діуретики зменшують нирковий кліренс літію, у свою чергу ірбесартан збільшує сироваткові концентрації літію, що підвищує ризик розвитку токсичних ефектів літію. Слід бути обережним при одночасному застосуванні препарату Коапровель з солями літію; рекомендується контролювати вміст літію у сироватці крові. У деяких пацієнтів інгібітори синтезу ендогенних простагландинів (наприклад, нестероїдні протизапальні засоби) можуть зменшувати ефекти тіазидних діуретиків. Гідрохлортіазид, що входить до складу препарату Коапровель®, може потенціювати ефекти інших антигіпертензивних засобів, особливо гангліоблокаторів та бета-адреноблокаторів. Гідрохлоротіазид може взаємодіяти з діазоксидом; при їх поєднанні слід контролювати концентрацію глюкози в крові, сироваткову концентрацію сечової кислоти та АТ. Гідрохлортіазид може потенціювати ефекти недеполяризуючих міорелаксантів (наприклад, тубокурарину), засобів для місцевої анестезії, засобів для загальної анестезії та засобів для премедикації перед загальною анестезією, внаслідок чого може знадобитися корекція їхнього режиму дозування. При поєднанні із застосуванням гідрохлортіазиду засоби для місцевої анестезії, засоби для загальної анестезії та засоби для премедикації перед загальною анестезією слід застосовувати у зменшених дозах. Якщо можливо, прийом гідрохлортіазиду слід припинити за 1 тиждень до хірургічного втручання. Одночасне застосування карбамазепіну та гідрохлортіазиду може асоціюватися з ризиком розвитку гіпонатріємії з клінічними проявами. Слід контролювати вміст електролітів у крові під час спільного застосування цих лікарських засобів. При необхідності застосування карбамазепіну рекомендується застосовувати діуретики з іншим механізмом дії. При одночасному застосуванні з глюкокортикостероїдами, АКТГ збільшується ризик розвитку гіпокаліємії. Дія катехоламінів може бути ослаблена під впливом тіазидних діуретиків. При одночасному застосуванні з антихолінергічними лікарськими засобами (наприклад, атропіном, біпериденом) підвищується біодоступність діуретиків тіазидного ряду за рахунок уповільнення моторики ШКТ. Тіазидні діуретики можуть знижувати виділення нирками цитотоксичних засобів (циклофосфамід, метотрексат) та посилювати їх мієлосупресивні ефекти.Спосіб застосування та дозиПрепарат приймають внутрішньо, 1 раз на добу, незалежно від їди. Коапровель® призначають пацієнтам, у яких АТ недостатньо контролюється ірбесартаном або гідрохлортіазидом у монотерапії. Коапровель® 150 мг/12.5 мг (таблетки, що містять ірбесартан/гідрохлортіазид 150 мг/12.5 мг відповідно) можна призначати пацієнтам, у яких АТ недостатньо контролюється гідрохлортіазидом (12.5 мг/добу) або ірбесартаном (150 мг/добу) у монотерапії. Коапровель® 300 мг/12.5 мг (таблетки, що містять ірбесартан/гідрохлортіазид 300 мг/12.5 мг відповідно) можна призначати пацієнтам, у яких АТ недостатньо контролюється ірбесартаном (300 мг) або препаратом Коапровель® (150 мг/12.5 мг). Коапровель® 300 мг/25 мг можна застосовувати у пацієнтів, у яких не вдається досягти цільових значень артеріального тиску при застосуванні препарату Коапровель® 300 мг/12.5 мг. Як початкова терапія у пацієнтів, які потребують проведення комбінованої гіпотензивної терапії, лікування починають з препарату Коапровель® 150 мг/12.5 мг 1 раз на добу. При необхідності більшого зниження артеріального тиску доза може бути збільшена через 1-2 тижні терапії до максимальної – 300 мг/25 мг 1 раз на добу. Максимальна добова доза становить 2 таб. препарату Коапровель 150 мг/12.5 мг або 1 таб. препарату Коапровель 300 мг/25 мг. Коапровель® 300 мг/25 мг є максимальною добовою дозою, тому одночасне застосування доз, що перевищують 300 мг ірбесартану та 25 мг гідрохлортіазиду 1 раз на добу, не рекомендується. Якщо не вдається досягти цільових значень АТ при застосуванні препарату Коапровель 300 мг/25 мг, то до терапії можна додавати інші антигіпертензивні препарати (бета-адреноблокатори, блокатори повільних кальцієвих каналів пролонгованої дії). У пацієнтів з нирковою недостатністю легкого та середнього ступеня (КК більше 30 мл/хв) корекція дози не потрібна. Однак у зв'язку з наявністю у складі препарату гідрохлортіазиду застосування препарату Коапровель® не рекомендується у пацієнтів з нирковою недостатністю тяжкого ступеня (КК ≤30 мл/хв). У пацієнтів з порушенням функції печінки легкого та середнього ступеня (5-6 та 7-9 балів за шкалою Чайлд-П'ю, відповідно) корекція дози не потрібна. У зв'язку з наявністю у складі препарату гідрохлортіазиду слід дотримуватись особливої обережності при застосуванні препарату у пацієнтів з печінковою недостатністю тяжкого ступеня (більше 9 балів за шкалою Чайлд-П'ю). У пацієнтів похилого віку корекція дози не потрібна. У пацієнтів, які приймали препарат Коапровель у клінічних дослідженнях, не спостерігалося відмінностей ефективності та безпеки між пацієнтами віком 65 років та старшими та пацієнтами молодшого віку. На даний момент безпека та ефективність препарату у пацієнтів дитячого та підліткового віку не встановлена. У пацієнтів з вираженою гіповолемією та/або гіпонатріємією, наприклад, у пацієнтів, які отримують інтенсивну терапію діуретиками, порушення водно-електролітного балансу слід скоригувати до початку застосування препарату Коапровель.ПередозуванняЄ досвід застосування ірбесартану у дозах до 900 мг на добу протягом 8 тижнів без розвитку токсичних ефектів. Симптоми: найбільш поширеними симптомами, що спостерігалися у дорослих при передозуванні гідрохлортіазиду, були симптоми, спричинені порушеннями електролітного складу крові (гіпокаліємія, гіпохлоремія, гіпонатріємія) та дегідратацією, що виникають внаслідок надмірного діуретичного ефекту. У разі одночасного застосування серцевих глікозидів (наприклад, дигоксину) або антиаритмічних препаратів (наприклад, соталолу) гіпокаліємія може сприяти розвитку порушень ритму. При передозуванні препарату можливе надмірне зниження артеріального тиску, розвиток брадикардії та тахікардії. Лікування: відсутня специфічна інформація щодо лікування передозування препарату Коапровель®. Слід встановити постійне спостереження за станом пацієнта і, при необхідності, проводити симптоматичну та підтримуючу терапію, включаючи відновлення втрат рідини та електролітів. При передозуванні рекомендується викликати блювання та/або провести промивання шлунка. Ірбесартан не виводиться з організму за допомогою гемодіалізу. Ступінь виведення гідрохлортіазиду за допомогою гемодіалізу не встановлено.Запобіжні заходи та особливі вказівкиЗастосування препарату Коапровель дотепер рідко супроводжувалося надмірним зниженням артеріального тиску у пацієнтів з артеріальною гіпертензією без інших факторів ризику для розвитку надмірної артеріальної гіпотензії. Надмірне зниження артеріального тиску, що супроводжується клінічною симптоматикою, може розвинутись у пацієнтів із гіпонатріємією/гіповолемією. Гіповолемію та/або гіпонартіємію слід скоригувати до початку застосування препарату Коапровель. Тіазидні діуретики можуть потенціювати дію інших гіпотензивних засобів. Препарат Коапровель® не рекомендується призначати пацієнтам з нирковою недостатністю тяжкого ступеня (КК ≤30 мл/хв). У пацієнтів з порушеннями функції нирок можливе збільшення азотемії, пов'язане із вмістом у складі препарату гідрохлортіазиду. Немає клінічних даних щодо застосування препарату у пацієнтів, які недавно перенесли трансплантацію нирки. Коли препарат Коапровель застосовується у пацієнтів з порушеною функцією нирок, рекомендується періодичний контроль вмісту калію, концентрації креатиніну та сечової кислоти у сироватці крові. Препарат Коапровель слід застосовувати з обережністю у пацієнтів з порушеннями функції печінки або прогресуючими захворюваннями печінки, оскільки навіть невеликі зміни водно-електролітного балансу можуть спровокувати розвиток печінкової коми. Тіазиди, включаючи гідрохлортіазид, можуть викликати порушення водно-електролітного балансу (гіпокаліємію, гіпонатріємію та гіпохлоремічний алкалоз). Хоча при застосуванні тіазидних діуретиків у монотерапії, особливо у високих дозах, можливий розвиток гіпокаліємії, одночасне застосування ірбесартану може зменшувати гіпокаліємію, що викликається гідрохлортіазидом. Навпаки, через наявність у складі препарату Коапровель® ірбесартану може мати місце гіперкаліємія, особливо у пацієнтів з нирковою недостатністю, серцевою недостатністю, цукровим діабетом. Рекомендується регулярний контроль вмісту калію у сироватці крові у пацієнтів групи ризику. Калійзберігаючі діуретики, калієві добавки або замінники солі, що містять калій, слід з обережністю застосовувати разом з препаратом Коапровель®. Дефіцит хлоридів зазвичай буває незначним і,як правило, не потребує лікування. Тіазиди знижують виведення кальцію через нирки та викликають непостійне та незначне збільшення вмісту кальцію у сироватці крові. Розвиток клінічно значущої гіперкальціємії може вказувати на можливість наявності у пацієнта гіперпаратиреозу. Прийом тіазидів слід припинити перед проведенням дослідження функції паращитовидних залоз. Було продемонстровано, що тіазиди збільшують виведення іонів магнію нирками, що може призвести до розвитку гіпомагніємії.Прийом тіазидів слід припинити перед проведенням дослідження функції паращитовидних залоз. Було продемонстровано, що тіазиди збільшують виведення іонів магнію нирками, що може призвести до розвитку гіпомагніємії.Прийом тіазидів слід припинити перед проведенням дослідження функції паращитовидних залоз. Було продемонстровано, що тіазиди збільшують виведення іонів магнію нирками, що може призвести до розвитку гіпомагніємії. При лікуванні тіазидними діуретиками може розвинутись гіперглікемія та загострення подагри у деяких пацієнтів. При лікуванні тіазидними діуретиками може збільшитись потреба в інсуліні у пацієнтів з цукровим діабетом, а також можлива маніфестація латентного цукрового діабету. Лікування тіазидними діуретиками асоціювалося зі збільшенням концентрацій холестерину та тригліцеридів у крові, проте доза 12.5 мг, що міститься у препараті Коапровель®, практично не впливає на концентрацію холестерину та тригліцеридів у крові. При терапії тіазидними діуретиками у деяких пацієнтів може спостерігатися гіперурикемія або загострення перебігу подагри. Пацієнтам із ризиком розвитку порушень водно-електролітного балансу та метаболічних порушень може знадобитися моніторинг лабораторних показників. Повідомлялося про загострення або обтяження перебігу системного червоного вовчаку при застосуванні тіазидних діуретиків. Сульфаніламіди або похідні сульфонаміду можуть викликати ідіосинкразичні реакції, що призводять до розвитку минущої міопії та гострої закритокутової глаукоми. Незважаючи на те, що гідрохлортіазид є похідним сульфонаміду, дотепер повідомлялося тільки про окремі випадки розвитку гострої закритокутової глаукоми без встановлення причинно-наслідкового взаємозв'язку з його застосуванням. Симптомами гострої глаукоми є: гостре зниження гостроти зору або очний біль, які зазвичай виникають протягом періоду від декількох годин до декількох тижнів після початку застосування препарату. Гостра закритокутова глаукома, що залишилася без лікування, може призвести до стійкої втрати зору. При виникненні цих симптомів слід якнайшвидше припинити прийом препарату.Якщо при цьому не вдасться нормалізувати внутрішньоочний тиск, може знадобитися термінове терапевтичне або хірургічне лікування. Факторами ризику для розвитку гострої глаукоми є вказівки в анамнезі на алергічні реакції на сульфаніламіди і пеніциліни. Подвійна блокада РААС у разі застосування комбінації препарату Коапровель® з інгібіторами АПФ або аліскіреном не рекомендується, т.к. порівняно з монотерапією є підвищений ризик різкого зниження АТ, розвитку гіперкаліємії та порушення функції нирок. Застосування препарату Коапровель у комбінації з аліскіреном протипоказане у пацієнтів з цукровим діабетом або нирковою недостатністю. Як наслідок інгібування РААС очікується погіршення функції нирок у схильних до цього пацієнтів. У пацієнтів з функцією нирок, яка залежить від активності РААС (пацієнти з артеріальною гіпертензією та стенозом ниркової артерії однієї або обох нирок, пацієнти з хронічною серцевою недостатністю III та IV функціонального класу [за класифікацією NYHA]), лікування лікарськими препаратами, що впливають на РААС, асоціювалося з олігурією та/або прогресуючою азотемією та, рідко, з гострою нирковою недостатністю та/або смертю. Не можна унеможливити виникнення подібного ефекту при застосуванні інгібіторів рецепторів ангіотензину II, включаючи препарат Коапровель®. У пацієнтів після симпатектомії може посилюватися антигіпертензивний ефект тіазидних діуретиків. У пацієнтів зі стенозом гирла аорти та стенозом мітрального клапана, гіпертрофічною обструктивною кардіоміопатією необхідна особлива обережність при застосуванні вазодилататорів, включаючи препарат Коапровель®. Застосування препарату Коапровель при первинному гіперальдостеронізмі недоцільно, т.к. такі пацієнти зазвичай не реагують на антигіпертензивні препарати, що впливають на РААС. Гідрохлортіазид може давати позитивний результат під час проведення допінг-контролю. Розвиток алергічних реакцій на гідрохлортіазид більш ймовірний у пацієнтів з обтяженим алергологічним анамнезом або пацієнтів з бронхіальною астмою. Вплив на здатність до керування автотранспортом та управління механізмами Вплив препарату Коапровель на здатність керувати транспортними засобами або займатися іншими потенційно небезпечними видами діяльності, що вимагають підвищеної уваги та високої швидкості психомоторних реакцій, не вивчався. Виходячи з фармакодинамічних властивостей препарат Коапровель® не повинен впливати на здатність керувати транспортними засобами та займатися іншими потенційно небезпечними видами діяльності (робота на висоті, робота авіадиспетчера, робота з механізмами тощо). Однак при занятті потенційно небезпечними видами діяльності слід бути обережними.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. діючі речовини: ірбесартан – 300 мг; гідрохлортіазид – 12,5 мг; допоміжні речовини: лактози моногідрат - 65,80 мг, целюлоза мікрокристалічна 90,00 мг, кроскармелоза натрію 30,00 мг, крохмаль прежелатинізований - 90,0 мг, магнію стеарат - 6,00 мг, кремнію діоксид колоїдний , барвник заліза оксид червоний (Е 172) – 0,60 мг, барвник заліза оксид жовтий (Е 172) – 0,60 мг. По 14 таблеток у ПВХ/Ал блістер. По 1, 2, 4, 7 блістерів разом із інструкцією із застосування в картонну пачку.Опис лікарської формиОвальні двоопуклі таблетки оранжево-рожевого кольору з білими вкрапленнями з гравіюванням у вигляді серця на одній стороні та номером 2776 на іншій.Фармакотерапевтична групаГіпотензивний комбінований засіб (ангіотензин II рецепторів антагоніст [АРА II] + діуретик).ФармакокінетикаНі ірбесартан, ні гідрохлортіазид не змінюють фармакокінетику один одного. Всмоктування Після прийому препарату Коапровель абсолютна біодоступність ірбесартану - 60-80%, а гідрохлортіазиду - 50-80%. Їда не впливає на біодоступність активних речовин препарату. Після внутрішнього прийому Cmax ірбесартану в плазмі крові досягається через 1.5-2 год, гідрохлортіазиду - через 1-2.5 год. Розподіл Зв'язування ірбесартану з білками плазми становить приблизно 96%, зв'язування з клітинними компонентами незначне. Vd ірбесартану становить 53-93 л (0.72-1.24 л/кг). При щоденному однократному застосуванні ірбесартану Css досягається через 3 дні, при цьому спостерігається обмежене накопичення ірбесартану в плазмі крові (менше 20%). Зв'язування з білками плазми гідрохлортіазиду становить 68%, Vd – 3.6-7.8 л/кг. Гідрохлортіазид проникає через плацентарний бар'єр та виділяється із грудним молоком. Метаболізм Після прийому внутрішньо або внутрішньовенного введення 14С-ірбесартану 80-85% радіоактивності, що циркулює в плазмі крові, припадає на незмінений ірбесартан. Ірбесартан метаболізується в печінці шляхом окислення та кон'югації з глюкуроновою кислотою. Основним метаболітом, що знаходиться в системному кровотоку, є ірбесартану глюкуронід (приблизно 6%). Окислення ірбесартану здійснюється головним чином за допомогою ізоферменту CYP2C9, участь ізоферменту CYP3A4 у метаболізмі ірбесартану є незначною. Ірбесартан не метаболізується за допомогою більшості ізоферментів, які зазвичай беруть участь у метаболізмі лікарських препаратів (CYP1A1, CYP1A2, CYP2A6, CYP2B6 CYP2D6 або CYP2E1), і не викликає їх інгібування чи індукції. Ірбесартан не індукує та не інгібує ізофермент CYP3А4. Гідрохлортіазид не метаболізується. Виведення Ірбесартан та його метаболіти виводяться з організму як через кишечник (з жовчю), так і нирками. Після прийому внутрішньо або внутрішньовенного введення 14С-ірбесартану 20% радіоактивності виявляється в сечі, а решта - у калі. Менш ніж 2% введеної дози виділяється нирками у вигляді незміненого ірбесартану. Кінцевий Т1/2 ірбесартану становить 11-15 год. Загальний кліренс внутрішньовенно введеного ірбесартану становить 157-176 мл/хв, яке нирковий кліренс становить 3-3.5 мл/хв. Гідрохлортіазид виводиться нирками. Середні значення плазмового Т1/2 гідрохлортіазиду становлять 5-15 год. Фармакокінетика у спеціальних груп пацієнтів У жінок (порівняно з чоловіками) відзначаються дещо вищі плазмові концентрації ірбесартану. Однак пов'язаних із статтю відмінностей у Т1/2 та накопиченні ірбесартану не виявляється. Корекція дози ірбесартану у жінок не потрібна. Не спостерігалося пов'язаних із статевою приналежністю відмінностей у ефектах ірбесартану. Значення AUC та Сmax ірбесартану у пацієнтів похилого віку (65-80 років) з нормальною функцією нирок та печінки були приблизно на 20-50% вищими, ніж у пацієнтів молодшого віку (18-40 років). Кінцеві Т1/2 вони були порівнянними. Не спостерігалося пов'язаних із віком відмінностей у ефектах ірбесартану. У пацієнтів з печінковою недостатністю (внаслідок цирозу печінки) легкої (функціональний клас А або 5-6 балів за шкалою Чайлд-П'ю) та середнього ступеня (функціональний клас В або 7-9 балів за шкалою Чайлд-П'ю) фармакокінетичні параметри ірбесартану істотно не змінюються. . У пацієнтів з порушенням функції нирок або пацієнтів, яким проводиться гемодіаліз, показники фармакокінетики ірбесартану істотно не змінюються. Ірбесартан не виводиться з організму за допомогою гемодіалізу. У добровольців без артеріальної гіпертензії AUC та Т1/2 ірбесартану в осіб негроїдної раси були приблизно на 20-25% вищі, ніж у осіб європеоїдної раси; Стих ірбесартану у них була практично однаковою.ФармакодинамікаКомбінований антигіпертензивний препарат, що містить антагоніст рецепторів ангіотензину II ірбесартан та тіазидний діуретик гідрохлортіазид. Комбінація інгредієнтів має адитивний гіпотензивний ефект, знижуючи АТ у вищому ступені, ніж кожен з компонентів окремо. Ірбесартан Ірбесартан є селективним антагоністом рецепторів ангіотензину II (типу AT1), який не вимагає метаболічної активації для придбання фармакологічної активності. Ангіотензин II є важливим компонентом РААС та залучений до патогенезу розвитку артеріальної гіпертензії, а також гомеостаз натрію. Ірбесартан блокує всі фізіологічно значущі ефекти ангіотензину II незалежно від джерела або шляхи його синтезу, в т.ч. виражений судинозвужувальний ефект та посилення секреції альдостерону, що реалізуються через рецептори типу АТ1, розташовані на поверхні гладком'язових клітин судин та в корі надниркових залоз. Не має агоністичної активності по відношенню до рецепторів AT1 і має набагато більшу (більш ніж у 8500 разів) спорідненість до AT1-рецепторів, ніж до АТ2-рецепторів (рецепторів, не пов'язаних із регуляцією роботи серцево-судинної системи). Ірбесартан не пригнічує ферменти РААС (такі як ренін, АПФ) і не впливає на рецептори інших гормонів або іонні канали, що беруть участь у регуляції АТ та гомеостазу натрію. Блокування ірбесартаном AT1-рецепторів перериває ланцюг зворотного зв'язку в системі ренін-ангіотензин, що призводить до збільшення концентрації реніну та ангіотензину II у плазмі крові. Після прийому ірбесартану в дозах, що рекомендуються, плазмова концентрація альдостерону знижується, не надаючи при цьому істотного впливу на вміст калію в сироватці крові (середнє значення його збільшення становить менше 0.1 мЭкв/л). Ірбесартан не надає помітного впливу на сироваткові концентрації тригліцеридів, холестерину та глюкози. Ірбесартан не впливає на концентрацію сечової кислоти у сироватці крові або на швидкість екскреції сечової кислоти нирками. Гідрохлоротіазид Гідрохлортіазид є тіазидним діуретиком, що має діуретичну, натрійуретичну та антигіпертензивну дію. Механізм антигіпертензивної дії тіазидних діуретиків, наприклад гідрохлортіазиду, до кінця невідомий. Тіазидні діуретики впливають на канальцеві механізми реабсорбції електролітів у нирках, збільшуючи екскрецію натрію та хлоридів приблизно в однакових кількостях. Натрійурез призводить до вторинної втрати калію та бікарбонату. Гідрохлортіазид збільшує активність реніну плазми крові та секрецію альдостерону, а також знижує вміст калію у сироватці крові. Одночасне застосування антагоніста рецепторів ангіотензину II сприяє зменшенню втрат калію, пов'язаних з дією тіазидних діуретиків. Ірбесартан/гідрохлортіазид Антигіпертензивний ефект ірбесартану у комбінації з гідрохлортіазидом виявляється вже після прийому його першої дози і стає значущим протягом 1-2 тижнів застосування, максимальний антигіпертензивний ефект досягається до 6-8 тижнів лікування. У довгострокових клінічних дослідженнях спостерігалося збереження антигіпертензивного ефекту комбінації ірбесартан/гідрохлортіазид протягом більше одного року. Комбінація ірбесартан/гідрохлортіазид при застосуванні в терапевтичному діапазоні доз має дозозалежну та адитивну антигіпертензивну дію. У пацієнтів, у яких на тлі монотерапії ірбесартаном у дозі 300 мг не спостерігалося достатнього зниження АТ, додавання до монотерапії ірбесартаном у дозі 300 мг 1 раз на добу гідрохлортіазиду в дозі 12.5 мг 1 раз на добу призводило до додаткового зниження діастолічного АТ до кінця між. (тобто через 24 год після прийому препаратів) на 6.1 мм рт. ст. (В порівнянні з додаванням плацебо). Спостерігалося загальне зниження систолічного АТ (САД)/діастолічного АТ (ДАД) при комбінації ірбесартану у дозі 300 мг та гідрохлортіазиду у дозі 12.5 мг (у порівнянні з прийомом плацебо) до -13.6/-11.5 мм рт. ст. Одноразовий протягом доби прийом ірбесартану у дозі 150 мг та гідрохлортіазиду у дозі 12.5 мг продемонстрував (порівняно з прийомом плацебо) середнє зниження САД/ДАД в кінці міждозового інтервалу на 12.9/6.9 мм рт. ст. відповідно. Максимальний антигіпертензивний ефект розвивався через 3 - 6 годин. ст.в порівнянні з плацебо). Виражені у відсотках показники ТУР (відносини АТ, що вимірюється в кінці міждозового інтервалу [залишкова дія] до АТ під час максимальної дії комбінації ірбесартан/гідрохлортіазид) становили щонайменше 68%.Максимальний антигіпертензивний ефект розвивався через 3 - 6 годин. ст.в порівнянні з плацебо). Виражені у відсотках показники ТУР (відносини АТ, що вимірюється в кінці міждозового інтервалу [залишкова дія] до АТ під час максимальної дії комбінації ірбесартан/гідрохлортіазид) становили щонайменше 68%.Максимальний антигіпертензивний ефект розвивався через 3 - 6 годин. ст.в порівнянні з плацебо). Виражені у відсотках показники ТУР (відносини АТ, що вимірюється в кінці міждозового інтервалу [залишкова дія] до АТ під час максимальної дії комбінації ірбесартан/гідрохлортіазид) становили щонайменше 68%.вимірюваного в кінці міждозового інтервалу [залишкова дія] до АТ під час максимальної дії комбінації ірбесартан/гідрохлортіазид) становили, як мінімум, 68%.вимірюваного в кінці міждозового інтервалу [залишкова дія] до АТ під час максимальної дії комбінації ірбесартан/гідрохлортіазид) становили, як мінімум, 68%. У клінічному дослідженні у пацієнтів з недостатнім зниженням АТ на тлі монотерапії гідрохлортіазидом у дозі 25 мг додавання ірбесартану до гідрохлортіазиду викликало додаткове середнє зниження САД/ДАД на 11.1/7.2 мм рт. ст. відповідно, порівняно з монотерапією гідрохлортіазидом. АТ знижувалося однаковою мірою у положенні стоячи й у положенні лежачи. Ортостатичні ефекти спостерігалися рідко, проте їх виникнення можливе у пацієнтів із гіпонатріємією та/або гіповолемією. Ефективність ірбесартану/гідрохлоротіазиду не залежить від віку, расової приналежності чи статі. Загальна антигіпертензивна реакція на комбінацію у пацієнтів негроїдної раси та пацієнтів інших рас була схожою. Після відміни ірбесартану АТ поступово поверталося до вихідних значень. Синдрому відміни у ірбесартану та гідрохлортіазиду не спостерігалося. При прийомі гідрохлортіазиду внутрішньо діуретичний ефект наставав протягом перших 2 год, діурез досягав максимуму приблизно через 4 год і зберігався близько 6-12 год. У двох клінічних дослідженнях оцінювалося лікування препаратом Коапровель як початкова терапія у пацієнтів з помірно вираженою (вихідне середнє значення АТ 162/98 мм рт. ст.) та тяжкою (вихідне середнє значення АТ 172/113 мм рт. ст.) артеріальною гіпертензією . В обох дослідженнях була показана достовірна перевага антигіпертензивного ефекту препарату Коапровель® (у дозах від 12.5/150 мг до 25/300 мг) як початкова терапія, у порівнянні з застосуванням як початкова терапія монотерапії ірбесартаном (у дозах від 150 мг до 3 ) та гідрохлортіазидом (у дозах від 12.5 мг до 25 мг).Показання до застосуванняАртеріальна гіпертензія помірного або тяжкого ступеня (лікування пацієнтів, яким показана комбінована терапія).Протипоказання до застосуванняниркова недостатність тяжкого ступеня (КК ≤30 мл/хв); анурія (у зв'язку з наявністю у складі препарату гідрохлортіазиду); одночасне застосування з лікарськими препаратами, що містять аліскірен, у пацієнтів з цукровим діабетом або нирковою недостатністю середнього або тяжкого ступеня (СКФ одночасне застосування з інгібіторами АПФ у пацієнтів з діабетичною нефропатією; вагітність; період лактації (грудного вигодовування); вік до 18 років (ефективність та безпека не встановлені); спадкова непереносимість галактози, недостатність лактази або синдром мальабсорбції глюкози/галактози; підвищена чутливість до активних речовин або будь-якого з допоміжних компонентів препарату; підвищена чутливість до інших похідних сульфонаміду (бо гідрохлортіазид є похідним сульфонаміду). З обережністю: стеноз аортального чи мітрального клапана; гіпертрофічна обструктивна кардіоміопатія (ГЗКМП); гіповолемія або гіпонатріємія, що виникають при інтенсивній терапії дикретиками, гемодіалізі, дотриманні дієти з обмеженням споживання кухонної солі, діареї, блювоті (небезпека надмірного зниження артеріального тиску); пацієнти з функцією нирок, яка залежить від активності РААС, зокрема. пацієнти з артеріальною гіпертензією з двостороннім або одностороннім стенозом ниркових артерій або пацієнти з хронічною серцевою недостатністю ІІІ-ІV функціонального класу (за класифікацією NYHA); ІХС та/або атеросклеротичне ураження судин головного мозку (ризик посилення ішемії міокарда або головного мозку, аж до розвитку інфаркту міокарда або інсульту при надмірному зниженні АТ); ниркова недостатність легкого та середнього ступеня (КК від 60 до 30 мл/хв) (ризик збільшення азотемії, підвищення концентрації сечової кислоти в крові, у зв'язку з наявністю у складі препарату гідрохлортіазиду, та розвитку гіперкаліємії, у зв'язку з наявністю у складі препарату ірбесартану) ; стан після трансплантації нирки (відсутність досвіду клінічного застосування); печінкова недостатність будь-якого ступеня тяжкості або прогресуючі захворювання печінки (у зв'язку з наявністю у складі препарату гідрохлортіазиду, тому що навіть незначні порушення водно-електролітного балансу у таких пацієнтів можуть спровокувати печінкову кому); цукровий діабет (у зв'язку з наявністю у складі препарату гідрохлортіазиду можливе зниження толерантності до глюкози, підвищення потреби в інсуліні та пероральних гіпоглікемічних засобах); подагра (у зв'язку з наявністю у складі препарату гідрохлортіазиду можливе підвищення концентрації солей сечової кислоти в крові); гіперкаліємія; одночасне застосування калійзберігаючих препаратів та/або замінників солі, що містять калій (ризик розвитку гіперкаліємії); системний червоний вовчак (у зв'язку з наявністю у складі препарату гідрохлортіазиду, тому є повідомлення про загострення або обтяження перебігу системного червоного вовчаку при застосуванні тіазидних діуретиків); одночасне застосування інших гіпотензивних препаратів (можливість потенціювання їхньої антигіпертензивної дії); симпатектомія (ризик посилення антигіпертензивного ефекту гідрохлортіазиду); одночасне застосування інгібіторів АПФ або аліскірену, т.я. порівняно з монотерапією, при подвійній блокаді РААС є підвищений ризик розвитку надмірного зниження артеріального тиску, гіперкаліємії та змін функції нирок; алергічна реакція на пеніциліни та сульфаніламіди в анамнезі (фактор ризику розвитку ідеосинкразичної реакції, що спостерігалася при застосуванні сульфаніламідів або похідних сульфонаміду, і виявляється у вигляді гострої закритокутової глаукоми).Вагітність та лактаціяДосвід застосування препарату Коапровель® при вагітності відсутній. З урахуванням того, що при застосуванні інгібіторів АПФ вагітними жінками у II та III триместрах вагітності спостерігалися пошкодження та загибель плоду, що розвивається, препарат Коапровель®, як і будь-який інший препарат, який впливає безпосередньо на РААС, не можна застосовувати при вагітності. Тіазидні діуретики проникають через плацентарний бар'єр і виявляються у пуповинній крові. Застосування діуретиків у вагітних рекомендується, т.к. можливий розвиток фетальної або неонатальної жовтяниці, тромбоцитопенії та, можливо, інших небажаних реакцій, що спостерігаються у дорослих. При діагностуванні вагітності під час лікування препаратом Коапровель слід якомога швидше припинити прийом препарату. Невідомо, чи виділяється ірбесартан чи його метаболіти із грудним молоком. Гідрохлортіазид виділяється із грудним молоком. Тіазидні діуретики при їх застосуванні у високих дозах, спричиняючи інтенсивний діурез, можуть пригнічувати лактацію. Препарат Коапровель протипоказаний до застосування протягом всього періоду грудного вигодовування через потенційний ризик для немовляти. Тому після оцінки співвідношення передбачуваної користі від прийому препарату для матері та потенційного ризику для дитини слід припинити або грудне вигодовування, або прийом препарату Коапровель®. Протипоказання: вік до 18 років (ефективність та безпека не встановлені). Протипоказання: вік до 18 років (ефективність та безпека не встановлені).Побічна діяНаведені нижче небажані явища представлені відповідно до наступних градацій частоти їх виникнення за класифікацією ВООЗ: дуже часто (≥1/10); часто (≥1/100, менше 1/10); нечасто (≥1/1000, менше 1/100); рідко (≥1/10000, менше 1/1000); дуже рідко (менше 1/10 000, включаючи окремі повідомлення); невідома частота (за наявними даними визначити частоту виникнення небажаного явища неможливо). Комбінація ірбесартан/гідрохлортіазид У клінічних дослідженнях безпека комбінації ірбесартану та гідрохлортіазиду була вивчена приблизно у 2750 пацієнтів, включаючи 1540 пацієнтів з артеріальною гіпертензією, які отримували це лікування протягом 6 місяців та більше 960 пацієнтів, які отримували препарат протягом одного року і більше. Побічні ефекти у пацієнтів, які отримували препарат Коапровель®, були зазвичай помірно вираженими і скороминущими, їх частота не була пов'язана з величиною дози, що приймається (у межах рекомендованого діапазону доз). Частота виникнення побічних ефектів також не залежала від віку, статі та расової приналежності. У плацебо-контрольованих дослідженнях, у яких брали участь 898 пацієнтів, які отримували комбінацію ірбесартан/гідрохлортіазид (звичайна тривалість лікування 2-3 міс), припинення лікування через яке-небудь клінічне або лабораторне небажане явище було достовірно менш частим у пацієнтів, які приймали комбінацію ірбесартану та гідрохлортіазиду (3.6%), ніж у пацієнтів, які приймали плацебо (6.8%). Небажані явища, що спостерігалися при застосуванні комбінації ірбесартан/гідрохлортіазид у плацебо-контрольованих дослідженнях у пацієнтів з артеріальною гіпертензією З боку нервової системи: часто – запаморочення, біль голови; нечасто – ортостатичне запаморочення. З боку серцево-судинної системи: нечасто – тахікардія, зміни на ЕКГ, надмірне зниження АТ, периферичні набряки (зокрема, набряки нижніх кінцівок), “припливи” крові до шкіри обличчя, синкопальні стани. З боку травної системи: часто – нудота/блювота; нечасто – діарея, сухість слизової оболонки порожнини рота, абдомінальні болі. З боку сечовивідної системи: часто – зміна частоти сечовипускання. З боку статевих органів та молочної залози: нечасто – статева дисфункція (ослаблення лібідо, еректильна дисфункція). З боку кістково-м'язової системи: нечасто – міалгія, біль у кістках, слабкість у кінцівках. Алергічні реакції: нечасто - висипання на шкірі, свербіж. Інші: часто - підвищена стомлюваність; нечасто – слабкість. Небажані явища, що спостерігалися в плацебо-контрольованих дослідженнях при застосуванні комбінації ірбесартан/гідрохлортіазид як початкове лікування у пацієнтів з артеріальною гіпертензією тяжкого та середнього ступеня тяжкості Початкове лікування комбінацією ірбесартан/гідрохлортіазид Наведені нижче небажані явища комбінації ірбесартан/гідрохлортіазид у дослідженнях, проведених у пацієнтів з артеріальною гіпертензією тяжкого та середнього ступеня тяжкості, були аналогічні описаним вище небажаним явищам, що спостерігалися у раніше проведених дослідженнях при артеріальній гіпертензії. У клінічному дослідженні, проведеному при артеріальній гіпертензії середнього ступеня тяжкості (середнє ДАТ, у положенні сидячи 90-110 мм рт. ст.), види та частота небажаних явищ, що спостерігалися у пацієнтів, які отримували препарат Коапровель як початкова терапія, були аналогічні профілю небажаних явищ у пацієнтів, які отримували початкове лікування у вигляді монотерапії ірбесартаном або гідрохлортіазидом. Не було зареєстровано випадків синкопальних станів у групі комбінованої терапії, а у групі монотерапії гідрохлортіазидом було зареєстровано 1 випадок синкопального стану. Частота вже вказаних вище небажаних явищ при терапії препаратом Коапровель®, монотерапії ірбесартаном та монотерапії гідрохлортіазидом, відповідно, склала: 0.9%, 0% та 0% для надмірного зниження АТ; 3%, 3.8% та 1% для запаморочення; 5.5%, 3.8% та 4.8% для головного болю; 1.2%, 0% та 1% для гіперкаліємії та 0.9%, 0% та 0% для гіпокаліємії. Частота відміни лікування через небажані явища при терапії препаратом Коапровель®, монотерапії ірбесартаном та монотерапії гідрохлортіазидом склала 6.7%, 3.8% та 4.8%. У клінічному дослідженні, проведеному при тяжкій артеріальній гіпертензії (ДАД у положенні сидячи ≥110 мм рт. ст.), загальна картина небажаних явищ протягом 7 тижнів спостереження була подібною у пацієнтів, які отримували як початкову терапію препарат Коапровель®, і у пацієнтів, отримували як початкову терапію ірбесартан. Частота вже вказаних вище небажаних явищ для препарату Коапровель® та ірбесартану склала, відповідно: 0% та 0% для синкопального стану; 0.6% та 0% для надмірного зниження АТ; 3.6% та 4% для запаморочення; 4.3% та 6.6% для головного болю; 0.2% та 0% для гіперкаліємії та 0.6% та 0.4% для гіпокаліємії. Частота відміни лікування через небажані явища при прийомі препарату Коапровель® та при монотерапії ірбесартаном склала 2.1% та 2.2%, відповідно. Лабораторні та інструментальні дані Клінічно значимих змін у результатах лабораторних досліджень у ході контрольованих клінічних досліджень препарату Коапровель не виявлено. Досвід постмаркетингового застосування Ірбесартан Як і у випадку з іншими антагоністами рецепторів ангіотензину II, дуже рідкісні випадки розвитку реакцій гіперчутливості (ангіоневротичний набряк, кропив'янка) спостерігалися при монотерапії ірбесартаном. Крім цього, при застосуванні ірбесартану після його виходу на ринок спостерігалися такі небажані реакції: вертиго, астенія, гіперкаліємія, жовтяниця, міалгія, підвищення показників функціональних печінкових проб, гепатит, дзвін у вухах та порушення функції нирок, включаючи випадки розвитку гострої ниркової недостатності у пацієнтів групи ризику. Гідрохлоротіазид При монотерапії гідрохлортіазидом спостерігалися такі небажані явища (незалежно від їх зв'язку з прийомом гідрохлортіазиду): анорексія, подразнення слизової оболонки шлунка, діарея, запор, жовтяниця (пов'язана з внутрішньопечінковим холестазом), панкреатит, сіалоаденез, /агранулоцитоз, тромбоцитопенія, апластична анемія, гемолітична анемія, реакції фотосенсибілізації, лихоманка, кропив'янка, некротизуючий ангіїт (васкуліт, шкірний васкуліт), респіраторний дистрес-синдром (включаючи пневмоніт та набряк легень), гіперурикемія, порушення водно-електролітного балансу (включаючи гіпонатріємію та гіпокаліємію), порушення функції нирок, інтерстиціальний нефрит, м'язові спазми, слабкість, неспокій,минуще порушення гостроти зору.Взаємодія з лікарськими засобамиВиходячи з даних досліджень in vitro, не очікується взаємодії ірбесартану з лікарськими засобами, що метаболізуються за допомогою ізоферментів CYP1A1, CYP1A2, CYP2A6, CYP2B6, CYP2E1 або CYP3A4. Ірбесартан переважно метаболізується за допомогою ізоферменту CYP2C9 і, меншою мірою, піддається глюкуронуванню. Не спостерігалося значної фармакокінетичної та фармакодинамічної взаємодії при сумісному застосуванні ірбесартану з варфарином – препаратом, що метаболізується за допомогою ізоферменту CYP2C9. Ірбесартан не змінює фармакокінетику дигоксину та симвастатину. При сумісному застосуванні ірбесартану з гідрохлортіазидом або ніфедипіном фармакокінетика ірбесартану не змінюється. Комбінація препарату Коапровель з лікарськими препаратами, що містять аліскірен, протипоказана у пацієнтів з цукровим діабетом або з нирковою недостатністю середнього та тяжкого ступеня (СКФ Застосування препарату Коапровель у поєднанні з інгібіторами АПФ протипоказане у пацієнтів з діабетичною нефропатією та не рекомендується у інших пацієнтів. На підставі досвіду, отриманого при застосуванні інших лікарських засобів, що впливають на РААС, при одночасному застосуванні препаратів калію, замінників солі, що містять калій, калійзберігаючих діуретиків або інших, здатних підвищувати вміст калію в крові лікарських засобів (гепарин), можливе підвищення вмісту калію у сироватці. крові. Одночасне застосування з ірбесартаном гідрохлортіазиду може зменшити частоту розвитку цього ефекту. У пацієнтів похилого віку, пацієнтів з гіповолемією або пацієнтів з порушеною функцією нирок застосування НПЗЗ, включаючи інгібітори ЦОГ-2, одночасно з антагоністами рецепторів ангіотензину II, включаючи ірбесартан, може призвести до погіршення функції нирок, включаючи можливий розвиток ниркової недостатності. Ці ефекти зазвичай є оборотними. Слід періодично контролювати функцію нирок у пацієнтів, які одночасно приймають ірбесартан та нестероїдні протизапальні засоби. При одночасному застосуванні антагоністів рецепторів ангіотензину II, включаючи ірбесартан, та нестероїдні протизапальні засоби, включаючи селективні інгібітори ЦОГ-2, можливе послаблення антигіпертензивного ефекту інгібіторів рецепторів ангіотензину II. При одночасному застосуванні з етанолом, барбітуратами або наркотичними засобами може спостерігатись посилення ортостатичної гіпотензії, що викликається тіазидними діуретиками. При сумісному застосуванні з пероральними гіпоглікемічними засобами та інсуліном може знадобитися збільшення дози гіпоглікемічного засобу, т.к. гідрохлортіазид може підвищувати концентрацію глюкози у крові. При одночасному застосуванні препарату Коапровель і протиподагричних засобів може знадобитися корекція доз останніх через можливість підвищення сироваткової концентрації сечової кислоти при застосуванні гідрохлортіазиду. При сумісному застосуванні з серцевими глікозидами, антиаритмічними засобами у разі виникнення гіпокаліємії та гіпомагніємії, викликаних тіазидним діуретиком, що входить до складу препарату Коапровель®, зростає небезпека розвитку аритмій. Тіазидні діуретики можуть підвищувати вміст кальцію у сироватці крові. Якщо пацієнту потрібне застосування препаратів кальцію або кальційзберігаючих препаратів (наприклад, вітаміну D), необхідно контролювати вміст кальцію у сироватці крові та проводити відповідну корекцію режиму дозування препаратів кальцію. Всмоктування гідрохлортіазиду в присутності аніонообмінних смол (колестираміну, колестиполу) знижується. Слід розділяти за часом прийом препарату Коапровель і цих препаратів не менше ніж на 4 год. Діуретики зменшують нирковий кліренс літію, у свою чергу ірбесартан збільшує сироваткові концентрації літію, що підвищує ризик розвитку токсичних ефектів літію. Слід бути обережним при одночасному застосуванні препарату Коапровель з солями літію; рекомендується контролювати вміст літію у сироватці крові. У деяких пацієнтів інгібітори синтезу ендогенних простагландинів (наприклад, нестероїдні протизапальні засоби) можуть зменшувати ефекти тіазидних діуретиків. Гідрохлортіазид, що входить до складу препарату Коапровель®, може потенціювати ефекти інших антигіпертензивних засобів, особливо гангліоблокаторів та бета-адреноблокаторів. Гідрохлоротіазид може взаємодіяти з діазоксидом; при їх поєднанні слід контролювати концентрацію глюкози в крові, сироваткову концентрацію сечової кислоти та АТ. Гідрохлортіазид може потенціювати ефекти недеполяризуючих міорелаксантів (наприклад, тубокурарину), засобів для місцевої анестезії, засобів для загальної анестезії та засобів для премедикації перед загальною анестезією, внаслідок чого може знадобитися корекція їхнього режиму дозування. При поєднанні із застосуванням гідрохлортіазиду засоби для місцевої анестезії, засоби для загальної анестезії та засоби для премедикації перед загальною анестезією слід застосовувати у зменшених дозах. Якщо можливо, прийом гідрохлортіазиду слід припинити за 1 тиждень до хірургічного втручання. Одночасне застосування карбамазепіну та гідрохлортіазиду може асоціюватися з ризиком розвитку гіпонатріємії з клінічними проявами. Слід контролювати вміст електролітів у крові під час спільного застосування цих лікарських засобів. При необхідності застосування карбамазепіну рекомендується застосовувати діуретики з іншим механізмом дії. При одночасному застосуванні з глюкокортикостероїдами, АКТГ збільшується ризик розвитку гіпокаліємії. Дія катехоламінів може бути ослаблена під впливом тіазидних діуретиків. При одночасному застосуванні з антихолінергічними лікарськими засобами (наприклад, атропіном, біпериденом) підвищується біодоступність діуретиків тіазидного ряду за рахунок уповільнення моторики ШКТ. Тіазидні діуретики можуть знижувати виділення нирками цитотоксичних засобів (циклофосфамід, метотрексат) та посилювати їх мієлосупресивні ефекти.Спосіб застосування та дозиПрепарат приймають внутрішньо, 1 раз на добу, незалежно від їди. Коапровель® призначають пацієнтам, у яких АТ недостатньо контролюється ірбесартаном або гідрохлортіазидом у монотерапії. Коапровель® 150 мг/12.5 мг (таблетки, що містять ірбесартан/гідрохлортіазид 150 мг/12.5 мг відповідно) можна призначати пацієнтам, у яких АТ недостатньо контролюється гідрохлортіазидом (12.5 мг/добу) або ірбесартаном (150 мг/добу) у монотерапії. Коапровель® 300 мг/12.5 мг (таблетки, що містять ірбесартан/гідрохлортіазид 300 мг/12.5 мг відповідно) можна призначати пацієнтам, у яких АТ недостатньо контролюється ірбесартаном (300 мг) або препаратом Коапровель® (150 мг/12.5 мг). Коапровель® 300 мг/25 мг можна застосовувати у пацієнтів, у яких не вдається досягти цільових значень артеріального тиску при застосуванні препарату Коапровель® 300 мг/12.5 мг. Як початкова терапія у пацієнтів, які потребують проведення комбінованої гіпотензивної терапії, лікування починають з препарату Коапровель® 150 мг/12.5 мг 1 раз на добу. При необхідності більшого зниження артеріального тиску доза може бути збільшена через 1-2 тижні терапії до максимальної – 300 мг/25 мг 1 раз на добу. Максимальна добова доза становить 2 таб. препарату Коапровель 150 мг/12.5 мг або 1 таб. препарату Коапровель 300 мг/25 мг. Коапровель® 300 мг/25 мг є максимальною добовою дозою, тому одночасне застосування доз, що перевищують 300 мг ірбесартану та 25 мг гідрохлортіазиду 1 раз на добу, не рекомендується. Якщо не вдається досягти цільових значень АТ при застосуванні препарату Коапровель 300 мг/25 мг, то до терапії можна додавати інші антигіпертензивні препарати (бета-адреноблокатори, блокатори повільних кальцієвих каналів пролонгованої дії). У пацієнтів з нирковою недостатністю легкого та середнього ступеня (КК більше 30 мл/хв) корекція дози не потрібна. Однак у зв'язку з наявністю у складі препарату гідрохлортіазиду застосування препарату Коапровель® не рекомендується у пацієнтів з нирковою недостатністю тяжкого ступеня (КК ≤30 мл/хв). У пацієнтів з порушенням функції печінки легкого та середнього ступеня (5-6 та 7-9 балів за шкалою Чайлд-П'ю, відповідно) корекція дози не потрібна. У зв'язку з наявністю у складі препарату гідрохлортіазиду слід дотримуватись особливої обережності при застосуванні препарату у пацієнтів з печінковою недостатністю тяжкого ступеня (більше 9 балів за шкалою Чайлд-П'ю). У пацієнтів похилого віку корекція дози не потрібна. У пацієнтів, які приймали препарат Коапровель у клінічних дослідженнях, не спостерігалося відмінностей ефективності та безпеки між пацієнтами віком 65 років та старшими та пацієнтами молодшого віку. На даний момент безпека та ефективність препарату у пацієнтів дитячого та підліткового віку не встановлена. У пацієнтів з вираженою гіповолемією та/або гіпонатріємією, наприклад, у пацієнтів, які отримують інтенсивну терапію діуретиками, порушення водно-електролітного балансу слід скоригувати до початку застосування препарату Коапровель.ПередозуванняЄ досвід застосування ірбесартану у дозах до 900 мг на добу протягом 8 тижнів без розвитку токсичних ефектів. Симптоми: найбільш поширеними симптомами, що спостерігалися у дорослих при передозуванні гідрохлортіазиду, були симптоми, спричинені порушеннями електролітного складу крові (гіпокаліємія, гіпохлоремія, гіпонатріємія) та дегідратацією, що виникають внаслідок надмірного діуретичного ефекту. У разі одночасного застосування серцевих глікозидів (наприклад, дигоксину) або антиаритмічних препаратів (наприклад, соталолу) гіпокаліємія може сприяти розвитку порушень ритму. При передозуванні препарату можливе надмірне зниження артеріального тиску, розвиток брадикардії та тахікардії. Лікування: відсутня специфічна інформація щодо лікування передозування препарату Коапровель®. Слід встановити постійне спостереження за станом пацієнта і, при необхідності, проводити симптоматичну та підтримуючу терапію, включаючи відновлення втрат рідини та електролітів. При передозуванні рекомендується викликати блювання та/або провести промивання шлунка. Ірбесартан не виводиться з організму за допомогою гемодіалізу. Ступінь виведення гідрохлортіазиду за допомогою гемодіалізу не встановлено.Запобіжні заходи та особливі вказівкиЗастосування препарату Коапровель дотепер рідко супроводжувалося надмірним зниженням артеріального тиску у пацієнтів з артеріальною гіпертензією без інших факторів ризику для розвитку надмірної артеріальної гіпотензії. Надмірне зниження артеріального тиску, що супроводжується клінічною симптоматикою, може розвинутись у пацієнтів із гіпонатріємією/гіповолемією. Гіповолемію та/або гіпонартіємію слід скоригувати до початку застосування препарату Коапровель. Тіазидні діуретики можуть потенціювати дію інших гіпотензивних засобів. Препарат Коапровель® не рекомендується призначати пацієнтам з нирковою недостатністю тяжкого ступеня (КК ≤30 мл/хв). У пацієнтів з порушеннями функції нирок можливе збільшення азотемії, пов'язане із вмістом у складі препарату гідрохлортіазиду. Немає клінічних даних щодо застосування препарату у пацієнтів, які недавно перенесли трансплантацію нирки. Коли препарат Коапровель застосовується у пацієнтів з порушеною функцією нирок, рекомендується періодичний контроль вмісту калію, концентрації креатиніну та сечової кислоти у сироватці крові. Препарат Коапровель слід застосовувати з обережністю у пацієнтів з порушеннями функції печінки або прогресуючими захворюваннями печінки, оскільки навіть невеликі зміни водно-електролітного балансу можуть спровокувати розвиток печінкової коми. Тіазиди, включаючи гідрохлортіазид, можуть викликати порушення водно-електролітного балансу (гіпокаліємію, гіпонатріємію та гіпохлоремічний алкалоз). Хоча при застосуванні тіазидних діуретиків у монотерапії, особливо у високих дозах, можливий розвиток гіпокаліємії, одночасне застосування ірбесартану може зменшувати гіпокаліємію, що викликається гідрохлортіазидом. Навпаки, через наявність у складі препарату Коапровель® ірбесартану може мати місце гіперкаліємія, особливо у пацієнтів з нирковою недостатністю, серцевою недостатністю, цукровим діабетом. Рекомендується регулярний контроль вмісту калію у сироватці крові у пацієнтів групи ризику. Калійзберігаючі діуретики, калієві добавки або замінники солі, що містять калій, слід з обережністю застосовувати разом з препаратом Коапровель®. Дефіцит хлоридів зазвичай буває незначним і,як правило, не потребує лікування. Тіазиди знижують виведення кальцію через нирки та викликають непостійне та незначне збільшення вмісту кальцію у сироватці крові. Розвиток клінічно значущої гіперкальціємії може вказувати на можливість наявності у пацієнта гіперпаратиреозу. Прийом тіазидів слід припинити перед проведенням дослідження функції паращитовидних залоз. Було продемонстровано, що тіазиди збільшують виведення іонів магнію нирками, що може призвести до розвитку гіпомагніємії.Прийом тіазидів слід припинити перед проведенням дослідження функції паращитовидних залоз. Було продемонстровано, що тіазиди збільшують виведення іонів магнію нирками, що може призвести до розвитку гіпомагніємії.Прийом тіазидів слід припинити перед проведенням дослідження функції паращитовидних залоз. Було продемонстровано, що тіазиди збільшують виведення іонів магнію нирками, що може призвести до розвитку гіпомагніємії. При лікуванні тіазидними діуретиками може розвинутись гіперглікемія та загострення подагри у деяких пацієнтів. При лікуванні тіазидними діуретиками може збільшитись потреба в інсуліні у пацієнтів з цукровим діабетом, а також можлива маніфестація латентного цукрового діабету. Лікування тіазидними діуретиками асоціювалося зі збільшенням концентрацій холестерину та тригліцеридів у крові, проте доза 12.5 мг, що міститься у препараті Коапровель®, практично не впливає на концентрацію холестерину та тригліцеридів у крові. При терапії тіазидними діуретиками у деяких пацієнтів може спостерігатися гіперурикемія або загострення перебігу подагри. Пацієнтам із ризиком розвитку порушень водно-електролітного балансу та метаболічних порушень може знадобитися моніторинг лабораторних показників. Повідомлялося про загострення або обтяження перебігу системного червоного вовчаку при застосуванні тіазидних діуретиків. Сульфаніламіди або похідні сульфонаміду можуть викликати ідіосинкразичні реакції, що призводять до розвитку минущої міопії та гострої закритокутової глаукоми. Незважаючи на те, що гідрохлортіазид є похідним сульфонаміду, дотепер повідомлялося тільки про окремі випадки розвитку гострої закритокутової глаукоми без встановлення причинно-наслідкового взаємозв'язку з його застосуванням. Симптомами гострої глаукоми є: гостре зниження гостроти зору або очний біль, які зазвичай виникають протягом періоду від декількох годин до декількох тижнів після початку застосування препарату. Гостра закритокутова глаукома, що залишилася без лікування, може призвести до стійкої втрати зору. При виникненні цих симптомів слід якнайшвидше припинити прийом препарату.Якщо при цьому не вдасться нормалізувати внутрішньоочний тиск, може знадобитися термінове терапевтичне або хірургічне лікування. Факторами ризику для розвитку гострої глаукоми є вказівки в анамнезі на алергічні реакції на сульфаніламіди і пеніциліни. Подвійна блокада РААС у разі застосування комбінації препарату Коапровель® з інгібіторами АПФ або аліскіреном не рекомендується, т.к. порівняно з монотерапією є підвищений ризик різкого зниження АТ, розвитку гіперкаліємії та порушення функції нирок. Застосування препарату Коапровель у комбінації з аліскіреном протипоказане у пацієнтів з цукровим діабетом або нирковою недостатністю. Як наслідок інгібування РААС очікується погіршення функції нирок у схильних до цього пацієнтів. У пацієнтів з функцією нирок, яка залежить від активності РААС (пацієнти з артеріальною гіпертензією та стенозом ниркової артерії однієї або обох нирок, пацієнти з хронічною серцевою недостатністю III та IV функціонального класу [за класифікацією NYHA]), лікування лікарськими препаратами, що впливають на РААС, асоціювалося з олігурією та/або прогресуючою азотемією та, рідко, з гострою нирковою недостатністю та/або смертю. Не можна унеможливити виникнення подібного ефекту при застосуванні інгібіторів рецепторів ангіотензину II, включаючи препарат Коапровель®. У пацієнтів після симпатектомії може посилюватися антигіпертензивний ефект тіазидних діуретиків. У пацієнтів зі стенозом гирла аорти та стенозом мітрального клапана, гіпертрофічною обструктивною кардіоміопатією необхідна особлива обережність при застосуванні вазодилататорів, включаючи препарат Коапровель®. Застосування препарату Коапровель при первинному гіперальдостеронізмі недоцільно, т.к. такі пацієнти зазвичай не реагують на антигіпертензивні препарати, що впливають на РААС. Гідрохлортіазид може давати позитивний результат під час проведення допінг-контролю. Розвиток алергічних реакцій на гідрохлортіазид більш ймовірний у пацієнтів з обтяженим алергологічним анамнезом або пацієнтів з бронхіальною астмою. Вплив на здатність до керування автотранспортом та управління механізмами Вплив препарату Коапровель на здатність керувати транспортними засобами або займатися іншими потенційно небезпечними видами діяльності, що вимагають підвищеної уваги та високої швидкості психомоторних реакцій, не вивчався. Виходячи з фармакодинамічних властивостей препарат Коапровель® не повинен впливати на здатність керувати транспортними засобами та займатися іншими потенційно небезпечними видами діяльності (робота на висоті, робота авіадиспетчера, робота з механізмами тощо). Однак при занятті потенційно небезпечними видами діяльності слід бути обережними.Умови відпустки з аптекЗа рецептомВідео на цю тему
5 224,00 грн
4 749,00 грн
Склад, форма випуску та упаковкаРозчин - 10 мл: активна речовина: калію ацетиламіносукцинат – 250 мг; допоміжні речовини: фруктоза 1000 мг, метилпарагідроксибензоат 15 мг, банановий ароматизатор 7 мг, вода очищена до 10 мл. По 10 мл препарату в ампулу темного скла (тип III), запаяну з двох сторін, з лінією розлому та нанесенням кільця на кожну зі сторін. По 10 ампул у пакувальний вкладиш із картону. По 3 пакувальні вкладки з картону разом з інструкцією із застосування в картонну пачку.Опис лікарської формиПрозорий світло-жовтий розчин із запахом банана.Фармакотерапевтична групаЗагальнотонізуючий засіб.ФармакодинамікаЧинним початком препарату є ацетиламіноянтарна кислота - біологічно активна сполука, що міститься в центральній нервовій системі ЦНС. Препарат сприяє нормалізації процесів нервової регуляції, має стимулюючий ефект.Показання до застосуванняУ складі комплексної терапії астенічного синдрому.Протипоказання до застосуванняРеакції гіперчутливості до ацетиламіноянтарної кислоти або до будь-якого з компонентів препарату. Дитячий вік до 7 років (клінічні дані відсутні). Вагітність (недостатність клінічних даних).Вагітність та лактаціяВагітність Застосування при вагітності протипоказане (у зв'язку із недостатністю даних). Жінки у період грудного вигодовування На час лікування препаратом грудне вигодовування слід припинити.Побічна діяМожливі алергічні реакції.Взаємодія з лікарськими засобамиНе було відзначено взаємодії з іншими лікарськими засобами.Спосіб застосування та дозиПрепарат призначений для вживання. Доза призначається індивідуально лікарем. Середня доза для дорослих становить 3 ампули на день: 2 – вранці та 1 – на ніч. Максимальна доза не відома. У дітей віком від 7 до 10 років рекомендований прийом внутрішньо 1 ампули вранці, у дітей віком від 10 до 18 років рекомендовано приймати внутрішньо 2 ампули вранці. Для прийому необхідно розкрити ампулу з одного боку, потім, підставивши під розкритий кінець склянку або чашку відламати протилежний кінець ампули. Після цього рідина безперешкодно виллється у підставку. Смакові якості препарату дозволяють використовувати його без попереднього розведення. У разі розведення водою можлива втрата бананового смаку. Найкращий ранковий прийом препарату. Середня тривалість лікування у дітей та дорослих становить 3 тижні. Якщо з яких-небудь причин була пропущена одна або більше доз препарату, лікування може бути продовжене без необхідності вторинної корекції дози. Лікування може бути раптово припинено без будь-яких серйозних наслідків для хворого.ПередозуванняДотепер про випадки передозування препарату Когітум не повідомлялося. Не очікується розвитку токсичних ефектів.Запобіжні заходи та особливі вказівкиВплив на здатність до керування автотранспортом та управління механізмами Малоймовірно, що препарат може вплинути на здатність керувати транспортними засобами, механізмами або заняття іншими потенційно небезпечними видами діяльності.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
1 777,00 грн
288,00 грн
Склад, форма випуску та упаковкаПігулки - 1 таб. діючі речовини: клопідогрелу гідросульфат – 97,875 мг (у перерахунку на клопідогрел – 75 мг), ацетилсаліцилова кислота – 100 мг; допоміжні речовини: ядро: манітол, макрогол-6000, целюлоза мікрокристалічна (90µm), гіпоролоза низькозаміщена, рицинова олія гідрогенізована, стеаринова кислота, кремнію діоксид колоїдний, крохмаль кукурудзяний; плівкова оболонка: барвник рожевий (лактози моногідрат, гіпромелозу, титане діоксид (Е 171), тріацетин, барвник залозі оксид червоний (Е 172). Може використовуватись Opadry® II pink 32К24375 ідентичного складу.), карнаубський віск. По 7 таблеток у ПА/Ал/ПВХ//Алюмінієвий блістер. По 1, 2 або 4 блістери разом з інструкцією із застосування в картонну пачку. По 10 таблеток у ПА/Ал/ПВX//Алюмінієвий блістер. По 10 блістерів разом із інструкцією із застосування в картонну пачку.Опис лікарської формиОвальні, двоопуклі таблетки, покриті плівковою оболонкою, світло-рожевого кольору з гравіюванням С75 на одній стороні та А100 на іншій стороні.Фармакотерапевтична групаАнтиагрегантний засіб.ФармакокінетикаВсмоктування Клопідогрів. При одноразовому та курсовому прийомі внутрішньо у дозі 75 мг на добу клопідогрел швидко всмоктується у кишечнику. Середні C max незміненого клопідогрелу в плазмі крові (приблизно 2,2–2,5 нг/мл після прийому внутрішньо разової дози 75 мг) досягаються приблизно через 45 хв після його одноразового прийому. За даними екскреції метаболітів клопідогрелу нирками, його абсорбція становить приблизно 50%. АСК. Після всмоктування АСК піддається гідролізу з утворенням саліцилової кислоти, C max якої в плазмі досягаються через 1 год після прийому АСК. Завдяки швидкому гідролізу, через 1,5-3 години після прийому внутрішньо препарату Коплавікс АСК у плазмі крові практично не визначається. Розподіл Клопідогрів. In vitro клопідогрел і його основний циркулюючий у крові неактивний метаболіт оборотно зв'язуються з білками плазми крові (на 98 і 94% відповідно), і цей зв'язок in vitro є ненасиченим аж до концентрації 100 мг/л. АСК АСК слабо зв'язується з білками плазми і має невеликий V d (10 л). Її метаболіт - саліцилова кислота - добре зв'язується з білками плазми, але її зв'язок з білками плазми залежить від її концентрації в плазмі (нелінійний зв'язок). При низьких концентраціях (<100 мкг/мл) близько 90% саліцилової кислоти зв'язується з альбуміном плазми. Саліцилова кислота добре розподіляється в тканинах та рідинах організму, включаючи ЦНС, грудне молоко та тканини плода. Метаболізм Клопідогрел інтенсивно метаболізується у печінці. In vitro та in vivo клопідогрел метаболізується за двома метаболічними шляхами. Перший шлях - метаболізм здійснюється за допомогою ферментів (естераз), що призводить до гідролізу з утворенням неактивного метаболіту - похідного карбоксильної кислоти (становить 85% від метаболітів, що циркулюють у системному кровотоку); другий шлях – метаболізм за допомогою кількох ізоферментів системи цитохрому P450. При цьому спочатку клопідогрел метаболізується до 2-оксо-клопідогрелу, що є проміжним метаболітом. Подальший метаболізм 2-оксо-клопідогрелу призводить до утворення активного метаболіту клопідогрелу - тіольного похідного клопідогрелу. Активний метаболіт утворюється переважно за допомогою CYP2С19 за участю деяких інших ізоферментів, включаючи CYP1A2, CYP2B6 та CYP3A4. Активний тіольний метаболіт клопідогрелу, який був виділений у дослідженнях in vitro, швидко та незворотно зв'язується з рецепторами тромбоцитів, інгібуючи агрегацію тромбоцитів. Після прийому навантажувальної дози клопідогрелу 300 мг C max активного метаболіту в 2 рази перевищує після прийому протягом 4 днів підтримуючої дози клопідогрелу 75 мг, при цьому його C max становить приблизно 30-60 хв після прийому клопідогрелу. АСК при прийомі у поєднанні з клопідогрелом швидко піддається гідролізу в плазмі крові до саліцилової кислоти з T 1/2 , що становить 0,3-0,4 год для доз АСК 75-100 мг. Саліцилова кислота головним чином піддається кон'югації у печінці з утворенням саліцилурової кислоти, фенольного глюкуроніду та ацильного глюкуроніду, а також великої кількості другорядних метаболітів. Виведення Клопідогрів. Протягом 120 годин після прийому внутрішньо людиною 14 С-міченого клопідогрелу близько 50% радіоактивності виділяється нирками і приблизно 46% через кишечник. Після одноразового прийому внутрішньо дози 75 мг T 1/2 клопідогрелу становить приблизно 6 год. Після одноразового та курсового прийому клопідогрелу T 1/2 основного циркулюючого в крові неактивного метаболіту становить 8 год. АСК. При прийомі препарату Коплавікс саліцилова кислота має T 1/2 з плазми крові, що становить приблизно 2 години. Після прийому токсичних доз АСК (10–20 г) плазмовий T 1/2 може збільшуватися до 20 год . /2, Що становить 6 годин або більше. Ниркова екскреція незміненої активної речовини залежить від рН сечі. При підвищенні рН більше 6,5 кліренс вільного саліцилату збільшується з <5 до >80%. Після прийому терапевтичних доз у сечі виявляється приблизно 10% прийнятої дози у вигляді саліцилової кислоти, 75% прийнятої дози у вигляді саліцилурової кислоти, 10% прийнятої дози – у вигляді фенольних глюкуронідів та 5% прийнятої дози – у вигляді ацильних глюкуронідів. Фармакогенетика За допомогою ізоферменту CYP2C19 утворюються як активний метаболіт, так і проміжний метаболіт - 2-оксо-клопідогрел. Фармакокінетика та антиагрегантна дія активного метаболіту клопідогрелу при дослідженні агрегації тромбоцитів ex vivo (in vitro дослідження агрегації тромбоцитів у крові, взятій у пацієнта, який приймав клопідогрел всередину, тобто після метаболізму клопідогрелу в організмі). Алель гена ізоферменту CYP2C19*1 відповідає повністю функціональному метаболізму, тоді як алелі генів ізоферментів CYP2C19*2 та CYP2C19*3 є нефункціональними. Алелі генів ізоферментів CYP2C19*2 та CYP2C19*3 є причиною зниження метаболізму у більшості представників європеоїдної (85%) та монголоїдної рас (99%). Інші алелі, з якими пов'язується відсутність або зниження метаболізму, зустрічаються рідше і включають, але не обмежуються алелями генів ізоферментів CYP2C19*4, *5, *6, *7 та *8. Пацієнт з низькою активністю ізоферменту CYP2C19 матиме два вказані вище алелі гена з втратою функції. Опубліковані частоти народження в загальних популяціях людей з фенотипом з низькою активністю ізоферменту CYP2C19 становлять: у європеоїдів - 2%, негроїдів - 4% і китайців - 14%.Для визначення наявного у пацієнта генотипу ізоферменту CYP2C19 існують відповідні випробування. За даними перехресного дослідження (40 здорових добровольців) та мета-аналізу шести досліджень (335 здорових добровольців, які приймали клопідогрел), до яких входили здорові добровольці з дуже високою, високою, проміжною та низькою активністю ізоферменту СYP2C19, якихось суттєвих відмінностей в експозиції активного метаболіту та в середніх значеннях інгібування агрегації тромбоцитів (ІАТ) (індукованої АДФ) у здорових добровольців з дуже високою, високою та проміжною активністю ізоферменту СYP2C19 виявлено не було. У здорових добровольців із низькою активністю ізоферменту CYP2C19 експозиція активного метаболіту знижувалася порівняно зі здоровими добровольцями з високою активністю ізоферменту CYP2C19. Коли добровольці з низькою активністю ізоферменту СYP2C19 приймали клопідогрел за схемою: 600 мг - доза навантаження/150 мг - підтримуюча доза (600/150 мг), експозиція активного метаболіту була вищою, ніж при прийомі клопідогрелу за схемою: 30. Крім цього, ІАТ було подібно до такого в групах пацієнтів, які отримують клопідогрел з більш високою інтенсивністю метаболізму за допомогою ізоферменту CYP2C19, які приймали клопідогрел за схемою: 300/75 мг. Однак у дослідженнях з урахуванням клінічних результатів режим дозування клопідогрелу для пацієнтів цієї групи (пацієнтів з низькою активністю ізоферменту CYP2C19) наразі не встановлено. Це пов'язано з тим, що проведені до цього часу клінічні дослідження не мали достатнього обсягу вибірки для виявлення відмінностей у клінічному результаті у пацієнтів із низькою активністю ізоферменту CYP2C19. Окремі групи пацієнтів Фармакокінетика активного метаболіту клопідогрелу в окремих груп пацієнтів не вивчена. Пацієнти похилого віку. У добровольців похилого віку (старше 75 років) у порівнянні з молодими добровольцями не було отримано відмінностей за показниками агрегації тромбоцитів та часу кровотечі. Не потрібна корекція дози для осіб похилого віку. Діти та підлітки. Дані відсутні. Пацієнти із порушенням функції нирок. Після повторних прийомів клопідогрелу в дозі 75 мг на добу у пацієнтів з тяжкими порушеннями функції нирок (Cl креатиніну – від 5 до 15 мл/хв) інгібування АДФ-індукованої агрегації тромбоцитів було нижчим (25%) порівняно з таким у здорових добровольців, проте подовження часу кровотечі було подібним до такого у здорових добровольців, які приймали клопідогрел у дозі 75 мг на добу. Пацієнти із порушенням функції печінки. Після щоденного протягом 10 днів прийому клопідогрелу в добовій дозі 75 мг пацієнтами з тяжкими порушеннями функції печінки (більше 9 балів за шкалою Чайлд-П'ю) інгібування АДФ-індукованої агрегації тромбоцитів було подібним до здорових добровольців. Середній час кровотечі було також можна порівняти в обох групах. Етнічна приналежність. Поширеність алелей генів ізоферменту CYP2C19, які відповідають за проміжний та знижений метаболізм, відрізняється у представників різних етнічних груп. Є обмежені літературні дані щодо їх поширеності серед представників монголоїдної раси, що не дозволяє оцінити клінічне значення впливу генотипів ізоферменту CYP2C19 на клінічні результати. На підставі фармакокінетики та особливостей метаболізму обох активних речовин препарату Коплавікс між ними не очікуються клінічно значущі фармакокінетичні взаємодії.ФармакодинамікаКлопідогрел є проліком, один з активних метаболітів якого є інгібітором агрегації тромбоцитів. Його активний метаболіт необоротно зв'язується з тромбоцитарними АДФ-рецепторами і селективно інгібує зв'язування АДФ з АДФ-рецепторами тромбоцитів та подальшу активацію комплексу GPIIb/IIIa під дією АДФ, завдяки чому пригнічується АДФ-індукована агрегація. Клопідогрел також інгібує агрегацію тромбоцитів, спричинену іншими агоністами, за рахунок того, що блокує активацію тромбоцитів АДФ, що вивільняється. У зв'язку з необоротністю зв'язку клопідогрелу з АДФ-рецепторами тромбоцитів тромбоцити залишаються несприйнятливими до стимуляції АДФ протягом всього терміну свого життя (приблизно 7–10 днів), а відновлення нормальної функції тромбоцитів відбувається зі швидкістю,відповідної швидкості поновлення тромбоцитів. У зв'язку з тим, що утворення активного метаболіту відбувається за допомогою ізоферментів системи цитохрому P450, деякі з яких можуть відрізнятися поліморфізмом або інгібуватися іншими препаратами, не у всіх пацієнтів можливе достатнє пригнічення агрегації тромбоцитів. При щоденному прийомі клопідогрелу в дозі 75 мг з першого дня прийому відзначається значне придушення АДФ-індукованої агрегації тромбоцитів, яке поступово збільшується протягом 3-7 днів і потім виходить на постійний рівень (при досягненні рівноважного стану). У рівноважному стані агрегація тромбоцитів пригнічується загалом на 40–60%. Після припинення прийому клопідогрелу агрегація тромбоцитів та час кровотечі поступово повертаються до початкового рівня в середньому протягом 5 днів. Ацетилсаліцилова кислота (АСК) Ацетилсаліцилова кислота (АСК) має відмінний від ефекту клопідогрел і доповнюючий його механізм антиагрегантної дії. АСК пригнічує агрегацію тромбоцитів за рахунок незворотного інгібування ЦОГ-1, внаслідок цього зменшення утворення тромбоксану А 2 є індуктором агрегації тромбоцитів і вазоконстрикції. Цей ефект зберігається протягом усього терміну життя тромбоцитів. АСК не змінює інгібуючого ефекту клопідогрелу на АДФ-індуковану агрегацію тромбоцитів, тоді як клопідогрел посилює вплив ацетилсаліцилової кислоти на колагеніндуковану агрегацію тромбоцитів. Обидві активні речовини в монотерапії та при одночасному застосуванні здатні запобігати розвитку атеротромбозу при будь-яких локалізаціях атеросклеротичного ураження судин, зокрема при ураженнях церебральних, коронарних або периферичних артерій. Клінічне дослідження ACTIVE-A показало, що у пацієнтів з фібриляцією передсердь, які мали як мінімум один фактор ризику розвитку судинних ускладнень, але були нездатні приймати непрямі антикоагулянти, клопідогрел у поєднанні з АСК (у порівнянні з прийомом лише однієї АСК) зменшував частоту разом узятих інсульту, інфаркту міокарда, системної тромбоемболії поза судинами ЦНС або смерті від судинних причин, переважно за рахунок зменшення ризику розвитку інсульту. Перевага прийому клопідогрелу у поєднанні з АСК у порівнянні з прийомом АСК у поєднанні з плацебо виявлялося рано і зберігалося протягом усього періоду дослідження (до 5 років). Зменшення ризику великих судинних ускладнень у групі пацієнтів, які приймали клопідогрел у поєднанні з АСК, було в основному зумовлене більшим зменшенням частоти інсультів. Ризик розвитку інсульту будь-якого ступеня тяжкості при прийомі клопідогрелу у поєднанні з АСК знижувався, а також була тенденція до зниження частоти розвитку інфаркту міокарда в групі пацієнтів, які приймали клопідогрел у поєднанні з АСК, але не спостерігалося відмінностей у частоті тромбоемболій поза судинами ЦНС або смерті причин. Крім цього, застосування клопідогрелу у поєднанні з АСК зменшувало загальну кількість днів госпіталізації з приводу серцево-судинної патології.Показання до застосуванняЦей комбінований препарат показаний для застосування у пацієнтів, які вже отримують одночасно клопідогрел та АСК. Запобігання атеротромботичним ускладненням - дорослі пацієнти з гострим коронарним синдромом: без підйому сегмента ST (нестабільна стенокардія або інфаркт міокарда без зубця Q), включаючи пацієнтів, яким було проведено стентування при черезшкірному коронарному втручанні; c підйомом сегмента ST (гострий інфаркт міокарда) при медикаментозному лікуванні та можливості проведення тромболізису. Запобігання атеротромботичних та тромбоемболічних ускладнень, включаючи інсульт, при фібриляції передсердь (миготлива аритмія): дорослі пацієнти з фібриляцією передсердь (миготлива аритмія), які мають щонайменше 1 фактор ризику розвитку судинних ускладнень, не можуть приймати непрямі антикоагулянти та мають низький ризик розвитку кровотечі.Протипоказання до застосуванняпідвищена чутливість до будь-якої з діючих або допоміжних речовин; тяжка печінкова недостатність (більше 9 балів за шкалою Чайлд-П'ю); тяжка ниркова недостатність (Cl креатиніну менше 30 мл/хв) через вміст у складі препарату АСК); гостра кровотеча, наприклад кровотеча з виразки або внутрішньочерепний крововилив; бронхіальна астма, що індукується прийомом саліцилатів та інших нестероїдних протизапальних засобів; синдром бронхіальної астми, риніту та рецидивуючого поліпозу носа та приносових пазух, гіперчутливість до НПЗП (через вміст у складі препарату АСК); мастоцитоз, при якому застосування АСК може викликати тяжкі реакції гіперчутливості, включаючи розвиток шоку, з гіперемією шкірних покривів, зниженням АТ, тахікардією та блюванням (через вміст у складі препарату АСК); рідкісні спадкові стани: непереносимість галактози; непереносимість лактози внаслідок дефіциту лактази; синдромом мальабсорбції глюкози-галактози (через вміст у складі препарату лактози); вагітність; період грудного вигодовування (див. «Застосування при вагітності та годуванні груддю»); дитячий вік до 18 років (безпека та ефективність застосування не встановлені). З обережністю: помірна печінкова недостатність (7-9 балів за шкалою Чайлд-П'ю), за якої можлива схильність до кровотеч (обмежений клінічний досвід застосування); ниркова недостатність легкого та середнього ступеня тяжкості (Cl креатиніну 60-30 мл/хв) (обмежений клінічний досвід застосування); травми, хірургічні втручання, включаючи інвазивні кардіологічні процедури або хірургічні втручання; захворювання, при яких є схильність до розвитку кровотеч, особливо внутрішньоочних або шлунково-кишкових (виразкова хвороба шлунка та дванадцятипалої кишки або шлунково-кишкова кровотеча в анамнезі, симптоми порушень з боку верхніх відділів ШКТ); недавно перенесене минуще порушення мозкового кровообігу або ішемічний інсульт; одночасне застосування НПЗП, у т.ч.,селективних інгібіторів ЦОГ-2; одночасне застосування варфарину, гепарину, інгібіторів глікопротеїну IIb/IIIа, селективних інгібіторів зворотного захоплення серотоніну (СІЗЗС) та тромболітичних препаратів; бронхіальна астма та алергія в анамнезі (підвищений ризик розвитку алергічних реакцій на АСК); подагра, гіперурикемія (АСК, у т.ч. та в низьких дозах, підвищує концентрацію сечової кислоти в крові); одночасний прийом алкоголю (етанолу) (через наявність у складі препарату АСК; пацієнти з генетично обумовленим зниженням активності ізоферменту CYP2D9; пацієнти з дефіцитом глюкозо-6-фосфатдегідрогенази (через ризик розвитку гемолізу); одночасне застосування метотрексу в0 /тиждень, наявність вказівок в анамнезі на алергічні та гематологічні реакції на інші тієнопіридини (такі як тіклопідін,празугрел) (можливість перехресних алергічних та гематологічних реакцій); одночасне застосування лікарських препаратів, що асоціюються з ризиком розвитку кровотечі та лікарських препаратів, що є субстратами ізоферменту CYP2C8 (таких як репаглінід, паклітаксел) через виявлену лікарську взаємодію.Вагітність та лактаціяЯк запобіжний засіб препарат Коплавікс не слід приймати протягом перших двох триместрів вагітності, за винятком випадків, коли клінічний стан жінки вимагає лікування клопідогрелом у комбінації з АСК. У зв'язку з наявністю у складі препарату АСК він протипоказаний у III триместрі вагітності. Дослідження на тваринах не виявили у клопідогрелу ні прямих, ні непрямих несприятливих ефектів протягом вагітності, ембріональний розвиток, пологи та постнатальний розвиток. Однак достатніх за обсягом та контрольованих досліджень у вагітних жінок не проводилося. У АСК було встановлено наявність тератогенної дії, хоча в клінічних дослідженнях було встановлено, що дози АСК до 100 мг на добу, що обмежено застосовуються в акушерстві та потребують спеціалізованого моніторингу, показали себе безпечними. Грудне вигодовування у разі лікування препаратом Коплавікс слід припинити, т.к. встановлено, що АСК виділяється в грудне молоко, а дослідження на щурах показали, що клопідогрел та/або його метаболіти також екскретуються в молоко щурів, що лакують. Виділяється чи ні клопідогрел у жіноче грудне молоко, невідомо.Побічна діяБезпека клопідогрелу в клінічних дослідженнях була вивчена більш ніж у 44000 пацієнтів, у т. ч. більш ніж у 12000 пацієнтів, які приймали його протягом року або більше, та у 30000 пацієнтів, які приймали одночасно клопідогрел та АСК; у клінічному дослідженні CURE безпека клопідогрелу у поєднанні з АСК була оцінена у понад 6200 пацієнтів, які приймали їх протягом 1 року та більше.Взаємодія з лікарськими засобамиЛікарські препарати, що асоціюються з ризиком кровотечі Є підвищений ризик розвитку кровотечі внаслідок потенційного адитивного ефекту. Одночасне застосування 23 лікарських препаратів, що асоціюються з ризиком розвитку кровотечі, слід проводити з обережністю. Тромболітики Безпека спільного застосування клопідогрелу, фібринспецифічних або нефібринспецифічних тромболітичних засобів та гепарину була проаналізована у пацієнтів із гострим інфарктом міокарда. Частота клінічно значущих кровотеч була аналогічна тій, що спостерігалася у разі спільного застосування тромболітичних препаратів та гепарину з АСК. У зв'язку з недостатністю клінічних даних щодо спільного застосування препарату Коплавікс та тромболітичних препаратів при їх спільному застосуванні слід бути обережним (див. «Особливі вказівки»). Інгібітори глікопротеїну IIb/IIIa Між інгібіторами глікопротеїну IIb/IIIa та препаратом Коплавікс можлива фармакодинамічна взаємодія, що потребує обережності при їх спільному застосуванні. Гепарин За даними клінічного дослідження, проведеного за участю здорових добровольців, при прийомі клопідогрелу не потрібно зміни дози гепарину, і не змінювалася його антикоагулянтна дія. Одночасне застосування гепарину не змінювало інгібуючої дії клопідогрелу на агрегацію тромбоцитів. Між препаратом Коплавікс та гепарином можлива фармакодинамічна взаємодія, яка може збільшувати ризик розвитку кровотеч, у зв'язку з чим спільне застосування цих препаратів потребує обережності. Непрямі антикоагулянти Одночасний прийом препарату Коплавікс та пероральних антикоагулянтів (варфарину) може збільшити інтенсивність кровотеч, у зв'язку з чим застосування цієї комбінації не рекомендується. Клопідогрел у дозі 75 мг не впливає на фармакокінетику варфарину та не змінює значення МНО у пацієнтів, які тривало приймають варфарин. Тим не менш, одночасний прийом варфарину з клопідогрелом може збільшити ризик кровотеч через незалежний вплив цих препаратів на гемостаз. НПЗП У клінічному дослідженні, проведеному за участю здорових добровольців, спільне застосування клопідогрелу та напроксену збільшувало приховані втрати крові через ШКТ. Тому застосування НПЗЗ, в т.ч. інгібіторів ЦОГ-2 у поєднанні з препаратом Коплавікс не рекомендується. Експериментальні дані свідчать на користь того, що ібупрофен (при одноразовому прийомі у дозі 400 мг у період часу між 8 год до 30 хв після безпосереднього прийому АСК у дозі 81 мг у лікарській формі негайного вивільнення) може пригнічувати ефект низьких доз АСК на агрегацію тромбоцитів . Однак при нерегулярному прийомі ібупрофену жодних клінічно значущих ефектів його на антиагрегантну дію АСК не очікується. СІОЗС Оскільки СІЗЗЗ порушують активацію тромбоцитів та збільшують ризик розвитку кровотечі, одночасне застосування СІЗЗЗ з клопідогрелом має проводитися з обережністю.Спосіб застосування та дозиВсередину, 1 раз на добу, незалежно від їди. Дорослі та пацієнти похилого віку з нормальною активністю ізоферменту CYP2C19 Гострий коронарний синдром (ГКС). Лікування починають якомога раніше після появи симптомів. Прийом препарату Коплавікс починають після прийому одноразової навантажувальної дози клопідогрелу у комбінації з АСК у вигляді окремих препаратів, а саме клопідогрел – у дозі 300 мг та АСК – у дозах 75–325 мг/добу, а при гострому інфаркті міокарда з підйомом сегменту ST поєднанні з тромболітиками або без них. Оскільки застосування більш високих доз АСК пов'язане зі збільшенням ризику кровотеч, доза АСК, що рекомендується при цьому, не повинна перевищувати 100 мг. При гострому інфаркті міокарда з підйомом сегмента ST у пацієнтів віком від 75 років лікування клопідогрелом має починатися без прийому його навантажувальної дози.У пацієнтів з ГКС без підйому сегмента ST (нестабільна стенокардія або інфаркт міокарда без зубця Q) максимальний сприятливий ефект спостерігається до 3 місяців лікування. Оптимальної тривалості лікування офіційно не визначено. Дані клінічних досліджень підтримують прийом препарату до 12 місяців. У пацієнтів з гострим інфарктом міокарда з підйомом сегмента ST лікування слід продовжувати не менше ніж 4 тижні. Фібриляція передсердь. Препарат Коплавікс слід приймати 1 раз на добу, після початку лікування клопідогрелом у дозі 75 мг та АСК у дозі 100 мг у вигляді окремих препаратів.ПередозуванняКлопідогрів Симптоми: передозування клопідогрелу може вести до збільшення часу кровотечі з подальшими ускладненнями у вигляді розвитку кровотеч. Лікування: при появі кровотечі потрібне проведення відповідного лікування. Антидот клопідогрелу не встановлено. Якщо необхідна швидка корекція часу кровотечі, що подовжився, то рекомендується переливання тромбоцитарної маси. АСК Симптоми: помірний ступінь передозування - запаморочення, дзвін у вухах, головний біль, сплутаність свідомості та симптоми з боку шлунково-кишкового тракту (нудота, блювання та біль у ділянці шлунка). При виявленні симптомів тяжкої інтоксикації виникають тяжкі порушення кислотно-основного стану. Спочатку гіпервентиляція, що виникає, призводить до розвитку дихального алкалозу. Потім розвивається дихальний ацидоз як наслідок інгібуючого впливу дихального алкалозу на дихальний центр. Також унаслідок присутності саліцилатів у крові розвивається метаболічний ацидоз. Крім цього, з'являються такі симптоми: гіпертермія та рясна потовиділення, що призводять до дегідратації, рухове занепокоєння, судоми, галюцинації та розвиток гіпоглікемії. Пригнічення нервової системи може призвести до розвитку коми, колапсу та зупинки дихання. Літальна доза АСК становить 25-30 г. Плазмова концентрація саліцилату понад 300 мг/л (1,67 ммоль/л) підтверджує наявність інтоксикації. Передозування саліцилатів, особливо у маленьких дітей, може призводити до розвитку тяжкої гіпоглікемії та потенційно фатального отруєння. При гострому та хронічному передозуванні АСК може розвинутись некардіогенний набряк легень (див. «Побічна дія»). Лікування: при виявленні симптомів тяжкого передозування потрібна госпіталізація. При помірній інтоксикації можна спробувати індукувати блювання, у разі невдачі показано промивання шлунка. Після цього слід прийняти внутрішньо (якщо пацієнт може ковтати) або ввести в шлунок через зонд активоване вугілля (адсорбент) та сольове проносне. З метою форсованого олужнення сечі для прискорення виведення саліцилатів показано внутрішньовенне краплинне введення 250 ммоль натрію бікарбонату протягом 3 годин під контролем рН сечі та кислотно-основного стану. Переважним лікуванням тяжкого передозування є гемодіаліз або перитонеальний діаліз. При необхідності застосовується симптоматичне лікування інших проявів інтоксикації.Запобіжні заходи та особливі вказівкиКровотечі та гематологічні порушення У зв'язку з ризиком розвитку кровотечі та гематологічних небажаних ефектів, у разі появи в ході лікування клінічних симптомів, підозрілих на виникнення кровотечі, слід терміново зробити клінічний аналіз крові, визначити АЧТВ (активований частковий тромбопластиновий час), кількість тромбоцитів у периферичній крові, показники функціональної тромбоцитів та провести інші необхідні дослідження. Одночасне застосування препарату Коплавікс з варфарином не рекомендується, оскільки це може збільшити інтенсивність кровотечі. У зв'язку з наявністю у складі препарату Коплавікс® двох антиагрегантних засобів його слід застосовувати з обережністю у пацієнтів, схильних до підвищеного ризику кровотечі, обумовленого травмами, хірургічними втручаннями або іншими патологічними станами, а також у пацієнтів, які приймають нестероїдні протизапальні засоби (в тому числі, інгібітори ЦОГ). 2), гепарин, інгібітори глікопротеїну IIb/IIIa, СІОЗС та тромболітичні препарати. Необхідно вести ретельне спостереження за пацієнтами щодо виключення ознак кровотечі, у тому числі і прихованого, особливо протягом перших тижнів лікування та/або після інвазивних кардіологічних процедур або хірургічного втручання. Якщо пацієнт має планове хірургічне втручання, і при цьому немає необхідності в постійній антиагрегантній терапії, то за 5-7 днів до хірургічного втручання клопідогрел слід відмінити. Препарат Коплавікс® збільшує час кровотечі і повинен застосовуватися з обережністю у пацієнтів із захворюваннями та станами, що схильні до розвитку кровотеч (особливо кровотеч із шлунково-кишкового тракту та внутрішньоочних крововиливів). Пацієнти повинні бути попереджені про те, що при прийомі препарату Коплавікс® для зупинки кровотечі їм може знадобитися більше часу, ніж зазвичай, і що у разі виникнення у них будь-яких незвичайних (по локалізації або тривалості) кровотеч їм слід повідомити про це свого лікаря. . Перед будь-яким майбутнім хірургічним втручанням і перед тим, як розпочати прийом будь-якого нового лікарського препарату, пацієнти повинні інформувати лікаря (зокрема стоматолога) про лікування препаратом Коплавікс®. Нещодавно перенесений ішемічний інсульт Було показано, що у пацієнтів з нещодавно перенесеним минущим ішемічним порушенням мозкового кровообігу або інсультом, що мають підвищений ризик розвитку повторного ішемічного ускладнення, комбінація АСК та клопідогрел збільшує можливість розвитку великих кровотеч. Тому застосування препарату Коплавікс у таких пацієнтів має проводитися з обережністю і лише у разі доведеної клінічної користі від його застосування. Тромботична тромбоцитопенічна пурпура Дуже рідко після застосування клопідогрелу (іноді навіть нетривалого) відзначалися випадки розвитку тромботичної тромбоцитопенічної пурпури (ТТП), яка характеризується тромбоцитопенією та мікроангіопатичною гемолітичною анемією, що супроводжуються неврологічними розладами, порушенням функції. ТТП є потенційно загрозливим для життя станом, що вимагає негайного лікування, включаючи плазмаферез. Набута гемофілія Повідомлялося про випадки розвитку набутої гемофілії прийому клопідогрелу. При підтвердженому ізольованому збільшенні активованого часткового тромбопластинового часу, що супроводжується або не супроводжується розвитком кровотечі, слід розглянути питання можливості розвитку набутої гемофілії. Пацієнти з підтвердженим діагнозом набутої гемофілії повинні спостерігатися та лікуватися фахівцями з цього захворювання та припинити прийом клопідогрелу. Фібриляція передсердь (миготлива аритмія) У пацієнтів з фібриляцією передсердь, що мають підвищений ризик розвитку серцево-судинних ускладнень, які могли приймати непрямі антикоагулянти, була показана перевага непрямих антикоагулянтів у порівнянні з монотерапією АСК або застосуванням комбінації клопідогрел + АСК у зменшенні ризику розвитку інсульту. Функціональна активність ізоферменту CYP2C19 У пацієнтів з низькою метаболічною активністю ізоферменту CYP2C19 при застосуванні клопідогрелу у рекомендованих дозах утворюється менше активного метаболіту клопідогрелу та зменшується його ефект на функцію тромбоцитів. Тому такі пацієнти з гострим коронарним синдромом або пацієнти, які піддаються черезшкірному коронарному втручанню та приймають клопідогрел, можуть мати більшу частоту серцево-судинних подій, ніж пацієнти з нормальною активністю ізоферменту CYP2C19. Є тести визначення генотипу CYP2C19, ці тести можна використовувати при виборі терапевтичної стратегії. Розглядається питання щодо застосування більш високих доз клопідогрелу у пацієнтів з низькою активністю ізоферменту CYP2C19, проте ефективність та безпека застосування підвищених доз клопідогрелу у пацієнтів з низькою активністю ізоферменту CYP2C19 дотепер не встановлені. Перехресні алергічні та/або гематологічні реакції між тієнопіридинами У пацієнтів слід збирати анамнез на предмет алергічних та/або гематологічних реакцій, що були раніше, на інші тієнопіридини (такі як тіклопідин, прасугрел), оскільки повідомлялося про наявність перехресних алергічних та/або гематологічних реакцій між тіенопіридинами. Тієнопіридини можуть викликати помірні та тяжкі алергічні реакції (такі як висипання на шкірі, ангіоневротичний набряк) або гематологічні реакції (такі як тромбоцитопенія і нейтропенія). Пацієнти, у яких раніше спостерігалися алергічні та/або гематологічні реакції на один із препаратів групи тієнопіридинів, можуть мати підвищений ризик розвитку подібних реакцій на інший препарат групи тієнопіридинів. Рекомендується моніторинг перехресних алергічних та/або гематологічних реакцій. Ниркова недостатність Комбінацію клопідогрел + АСК не слід застосовувати у пацієнтів з тяжкою нирковою недостатністю. Досвід застосування клопідогрелу у пацієнтів легкою та помірною нирковою недостатністю обмежений. Тому у цієї групи пацієнтів комбінація клопідогрел + АСК повинна застосовуватися з обережністю. Печінкова недостатність Комбінація клопідогрел + АСК не повинна застосовуватися у пацієнтів з тяжким ступенем печінкової недостатності. Досвід застосування клопідогрелу у пацієнтів із захворюваннями печінки середньої тяжкості, які можуть мати схильність до кровотеч, обмежений. Тому у цієї групи пацієнтів комбінація клопідогрел + АСК повинна застосовуватися з обережністю. Обережність, потрібна внаслідок наявності у складі препарату АСК У пацієнтів з бронхіальною астмою або іншими алергічними захворюваннями в анамнезі, оскільки вони мають підвищений ризик розвитку реакцій гіперчутливості. У пацієнтів з подагрою, оскільки низькі дози АСК збільшують концентрацію уратів у крові. Можлива наявність взаємозв'язку між прийомом АСК та розвитком синдрому Рея, рідкісного та небезпечного для життя захворювання, що зазвичай спостерігалося у продромальному періоді інфекцій у дітей, що протікає з розвитком енцефалопатії та гострої жирової дистрофії печінки та швидким розвитком печінкової недостатності, що може призводити до смертельного результату. Етанол може збільшувати ризик ураження шлунково-кишкового тракту при його прийомі на фоні лікування АСК. Тому слід бути обережними при вживанні алкоголю (етанолу) під час лікування АСК. Крім цього, пацієнти повинні бути попереджені про ризик розвитку кровотечі внаслідок хронічного вживання великої кількості алкоголю (етанолу) під час прийому комбінації клопідогрел + АСК. Препарат Коплавікс® повинен застосовуватися під ретельним медичним наглядом у пацієнтів з недостатністю глюкози-6-фосфатдегідрогенази (Г6ФД) через ризик розвитку гемолізу. Слід уникати одночасного прийому левотироксину та саліцилатів, особливо у дозах вище 2,0 г/добу. Вплив на шлунково-кишковий тракт Препарат Коплавікс® слід застосовувати з обережністю у пацієнтів з виразковою хворобою шлунка та дванадцятипалої кишки або шлунково-кишковими кровотечами в анамнезі або у пацієнтів з навіть незначними симптомами з боку верхніх відділів шлунково-кишкового тракту, які можуть бути проявами виразкових уражень шлунка, здатних призвести до. При лікуванні препаратом Коплавікс® у будь-який момент можуть виникнути симптоми з боку верхніх відділів шлунково-кишкового тракту, такі як гастралгія, печія, нудота, блювання та шлунково-кишкова кровотеча. Незважаючи на те, що при лікуванні препаратом Коплавікс® незначні побічні ефекти з боку шлунково-кишкового тракту, такі як диспепсичні розлади, зустрічаються часто, лікар завжди в цих випадках повинен виключати виразки слизової оболонки шлунково-кишкового тракту та кровотечі, навіть за відсутності в анамнезі патології з сторони ШКТ. Пацієнти повинні бути поінформовані про симптоми небажаних реакцій з боку шлунково-кишкового тракту та проінструктовані про те, що у разі їх появи вони повинні негайно звернутися за медичною допомогою. У пацієнтів, які одночасно приймають нікорандил та НПЗЗ, включаючи АСК та ацетилсаліцилат лізину, є підвищений ризик розвитку тяжких ускладнень, таких як утворення виразок та перфорацій у шлунково-кишковому тракті та шлунково-кишкові кровотечі. Вплив на здатність до керування автотранспортом та управління механізмами Зазвичай Коплавікс® не має істотного впливу на здатність керувати транспортними засобами та займатися іншими потенційно небезпечними видами діяльності, що потребують підвищеної концентрації уваги та швидкості психомоторних реакцій. Однак у разі виникнення у пацієнта несприятливих побічних реакцій з боку нервової системи та психіки можливе зниження концентрації уваги та швидкості психомоторних реакцій, що може перешкоджати зайняттю такими видами діяльності. У таких випадках питання про можливість заняття потенційно небезпечними видами діяльності має вирішувати лікар.Умови відпустки з аптекЗа рецептомВідео на цю тему
516,00 грн
443,00 грн
Склад, форма випуску та упаковкаПігулки - 1 таб. діючі речовини: клопідогрелу гідросульфат – 97,875 мг (у перерахунку на клопідогрел – 75 мг), ацетилсаліцилова кислота – 100 мг; допоміжні речовини: ядро: манітол, макрогол-6000, целюлоза мікрокристалічна (90µm), гіпоролоза низькозаміщена, рицинова олія гідрогенізована, стеаринова кислота, кремнію діоксид колоїдний, крохмаль кукурудзяний; плівкова оболонка: барвник рожевий (лактози моногідрат, гіпромелозу, титане діоксид (Е 171), тріацетин, барвник залозі оксид червоний (Е 172). Може використовуватись Opadry® II pink 32К24375 ідентичного складу.), карнаубський віск. По 7 таблеток у ПА/Ал/ПВХ//Алюмінієвий блістер. По 1, 2 або 4 блістери разом з інструкцією із застосування в картонну пачку. По 10 таблеток у ПА/Ал/ПВX//Алюмінієвий блістер. По 10 блістерів разом із інструкцією із застосування в картонну пачку.Опис лікарської формиОвальні, двоопуклі таблетки, покриті плівковою оболонкою, світло-рожевого кольору з гравіюванням С75 на одній стороні та А100 на іншій стороні.Фармакотерапевтична групаАнтиагрегантний засіб.ФармакокінетикаВсмоктування Клопідогрів. При одноразовому та курсовому прийомі внутрішньо у дозі 75 мг на добу клопідогрел швидко всмоктується у кишечнику. Середні C max незміненого клопідогрелу в плазмі крові (приблизно 2,2–2,5 нг/мл після прийому внутрішньо разової дози 75 мг) досягаються приблизно через 45 хв після його одноразового прийому. За даними екскреції метаболітів клопідогрелу нирками, його абсорбція становить приблизно 50%. АСК. Після всмоктування АСК піддається гідролізу з утворенням саліцилової кислоти, C max якої в плазмі досягаються через 1 год після прийому АСК. Завдяки швидкому гідролізу, через 1,5-3 години після прийому внутрішньо препарату Коплавікс АСК у плазмі крові практично не визначається. Розподіл Клопідогрів. In vitro клопідогрел і його основний циркулюючий у крові неактивний метаболіт оборотно зв'язуються з білками плазми крові (на 98 і 94% відповідно), і цей зв'язок in vitro є ненасиченим аж до концентрації 100 мг/л. АСК АСК слабо зв'язується з білками плазми і має невеликий V d (10 л). Її метаболіт - саліцилова кислота - добре зв'язується з білками плазми, але її зв'язок з білками плазми залежить від її концентрації в плазмі (нелінійний зв'язок). При низьких концентраціях (<100 мкг/мл) близько 90% саліцилової кислоти зв'язується з альбуміном плазми. Саліцилова кислота добре розподіляється в тканинах та рідинах організму, включаючи ЦНС, грудне молоко та тканини плода. Метаболізм Клопідогрел інтенсивно метаболізується у печінці. In vitro та in vivo клопідогрел метаболізується за двома метаболічними шляхами. Перший шлях - метаболізм здійснюється за допомогою ферментів (естераз), що призводить до гідролізу з утворенням неактивного метаболіту - похідного карбоксильної кислоти (становить 85% від метаболітів, що циркулюють у системному кровотоку); другий шлях – метаболізм за допомогою кількох ізоферментів системи цитохрому P450. При цьому спочатку клопідогрел метаболізується до 2-оксо-клопідогрелу, що є проміжним метаболітом. Подальший метаболізм 2-оксо-клопідогрелу призводить до утворення активного метаболіту клопідогрелу - тіольного похідного клопідогрелу. Активний метаболіт утворюється переважно за допомогою CYP2С19 за участю деяких інших ізоферментів, включаючи CYP1A2, CYP2B6 та CYP3A4. Активний тіольний метаболіт клопідогрелу, який був виділений у дослідженнях in vitro, швидко та незворотно зв'язується з рецепторами тромбоцитів, інгібуючи агрегацію тромбоцитів. Після прийому навантажувальної дози клопідогрелу 300 мг C max активного метаболіту в 2 рази перевищує після прийому протягом 4 днів підтримуючої дози клопідогрелу 75 мг, при цьому його C max становить приблизно 30-60 хв після прийому клопідогрелу. АСК при прийомі у поєднанні з клопідогрелом швидко піддається гідролізу в плазмі крові до саліцилової кислоти з T 1/2 , що становить 0,3-0,4 год для доз АСК 75-100 мг. Саліцилова кислота головним чином піддається кон'югації у печінці з утворенням саліцилурової кислоти, фенольного глюкуроніду та ацильного глюкуроніду, а також великої кількості другорядних метаболітів. Виведення Клопідогрів. Протягом 120 годин після прийому внутрішньо людиною 14 С-міченого клопідогрелу близько 50% радіоактивності виділяється нирками і приблизно 46% через кишечник. Після одноразового прийому внутрішньо дози 75 мг T 1/2 клопідогрелу становить приблизно 6 год. Після одноразового та курсового прийому клопідогрелу T 1/2 основного циркулюючого в крові неактивного метаболіту становить 8 год. АСК. При прийомі препарату Коплавікс саліцилова кислота має T 1/2 з плазми крові, що становить приблизно 2 години. Після прийому токсичних доз АСК (10–20 г) плазмовий T 1/2 може збільшуватися до 20 год . /2, Що становить 6 годин або більше. Ниркова екскреція незміненої активної речовини залежить від рН сечі. При підвищенні рН більше 6,5 кліренс вільного саліцилату збільшується з <5 до >80%. Після прийому терапевтичних доз у сечі виявляється приблизно 10% прийнятої дози у вигляді саліцилової кислоти, 75% прийнятої дози у вигляді саліцилурової кислоти, 10% прийнятої дози – у вигляді фенольних глюкуронідів та 5% прийнятої дози – у вигляді ацильних глюкуронідів. Фармакогенетика За допомогою ізоферменту CYP2C19 утворюються як активний метаболіт, так і проміжний метаболіт - 2-оксо-клопідогрел. Фармакокінетика та антиагрегантна дія активного метаболіту клопідогрелу при дослідженні агрегації тромбоцитів ex vivo (in vitro дослідження агрегації тромбоцитів у крові, взятій у пацієнта, який приймав клопідогрел всередину, тобто після метаболізму клопідогрелу в організмі). Алель гена ізоферменту CYP2C19*1 відповідає повністю функціональному метаболізму, тоді як алелі генів ізоферментів CYP2C19*2 та CYP2C19*3 є нефункціональними. Алелі генів ізоферментів CYP2C19*2 та CYP2C19*3 є причиною зниження метаболізму у більшості представників європеоїдної (85%) та монголоїдної рас (99%). Інші алелі, з якими пов'язується відсутність або зниження метаболізму, зустрічаються рідше і включають, але не обмежуються алелями генів ізоферментів CYP2C19*4, *5, *6, *7 та *8. Пацієнт з низькою активністю ізоферменту CYP2C19 матиме два вказані вище алелі гена з втратою функції. Опубліковані частоти народження в загальних популяціях людей з фенотипом з низькою активністю ізоферменту CYP2C19 становлять: у європеоїдів - 2%, негроїдів - 4% і китайців - 14%.Для визначення наявного у пацієнта генотипу ізоферменту CYP2C19 існують відповідні випробування. За даними перехресного дослідження (40 здорових добровольців) та мета-аналізу шести досліджень (335 здорових добровольців, які приймали клопідогрел), до яких входили здорові добровольці з дуже високою, високою, проміжною та низькою активністю ізоферменту СYP2C19, якихось суттєвих відмінностей в експозиції активного метаболіту та в середніх значеннях інгібування агрегації тромбоцитів (ІАТ) (індукованої АДФ) у здорових добровольців з дуже високою, високою та проміжною активністю ізоферменту СYP2C19 виявлено не було. У здорових добровольців із низькою активністю ізоферменту CYP2C19 експозиція активного метаболіту знижувалася порівняно зі здоровими добровольцями з високою активністю ізоферменту CYP2C19. Коли добровольці з низькою активністю ізоферменту СYP2C19 приймали клопідогрел за схемою: 600 мг - доза навантаження/150 мг - підтримуюча доза (600/150 мг), експозиція активного метаболіту була вищою, ніж при прийомі клопідогрелу за схемою: 30. Крім цього, ІАТ було подібно до такого в групах пацієнтів, які отримують клопідогрел з більш високою інтенсивністю метаболізму за допомогою ізоферменту CYP2C19, які приймали клопідогрел за схемою: 300/75 мг. Однак у дослідженнях з урахуванням клінічних результатів режим дозування клопідогрелу для пацієнтів цієї групи (пацієнтів з низькою активністю ізоферменту CYP2C19) наразі не встановлено. Це пов'язано з тим, що проведені до цього часу клінічні дослідження не мали достатнього обсягу вибірки для виявлення відмінностей у клінічному результаті у пацієнтів із низькою активністю ізоферменту CYP2C19. Окремі групи пацієнтів Фармакокінетика активного метаболіту клопідогрелу в окремих груп пацієнтів не вивчена. Пацієнти похилого віку. У добровольців похилого віку (старше 75 років) у порівнянні з молодими добровольцями не було отримано відмінностей за показниками агрегації тромбоцитів та часу кровотечі. Не потрібна корекція дози для осіб похилого віку. Діти та підлітки. Дані відсутні. Пацієнти із порушенням функції нирок. Після повторних прийомів клопідогрелу в дозі 75 мг на добу у пацієнтів з тяжкими порушеннями функції нирок (Cl креатиніну – від 5 до 15 мл/хв) інгібування АДФ-індукованої агрегації тромбоцитів було нижчим (25%) порівняно з таким у здорових добровольців, проте подовження часу кровотечі було подібним до такого у здорових добровольців, які приймали клопідогрел у дозі 75 мг на добу. Пацієнти із порушенням функції печінки. Після щоденного протягом 10 днів прийому клопідогрелу в добовій дозі 75 мг пацієнтами з тяжкими порушеннями функції печінки (більше 9 балів за шкалою Чайлд-П'ю) інгібування АДФ-індукованої агрегації тромбоцитів було подібним до здорових добровольців. Середній час кровотечі було також можна порівняти в обох групах. Етнічна приналежність. Поширеність алелей генів ізоферменту CYP2C19, які відповідають за проміжний та знижений метаболізм, відрізняється у представників різних етнічних груп. Є обмежені літературні дані щодо їх поширеності серед представників монголоїдної раси, що не дозволяє оцінити клінічне значення впливу генотипів ізоферменту CYP2C19 на клінічні результати. На підставі фармакокінетики та особливостей метаболізму обох активних речовин препарату Коплавікс між ними не очікуються клінічно значущі фармакокінетичні взаємодії.ФармакодинамікаКлопідогрел є проліком, один з активних метаболітів якого є інгібітором агрегації тромбоцитів. Його активний метаболіт необоротно зв'язується з тромбоцитарними АДФ-рецепторами і селективно інгібує зв'язування АДФ з АДФ-рецепторами тромбоцитів та подальшу активацію комплексу GPIIb/IIIa під дією АДФ, завдяки чому пригнічується АДФ-індукована агрегація. Клопідогрел також інгібує агрегацію тромбоцитів, спричинену іншими агоністами, за рахунок того, що блокує активацію тромбоцитів АДФ, що вивільняється. У зв'язку з необоротністю зв'язку клопідогрелу з АДФ-рецепторами тромбоцитів тромбоцити залишаються несприйнятливими до стимуляції АДФ протягом всього терміну свого життя (приблизно 7–10 днів), а відновлення нормальної функції тромбоцитів відбувається зі швидкістю,відповідної швидкості поновлення тромбоцитів. У зв'язку з тим, що утворення активного метаболіту відбувається за допомогою ізоферментів системи цитохрому P450, деякі з яких можуть відрізнятися поліморфізмом або інгібуватися іншими препаратами, не у всіх пацієнтів можливе достатнє пригнічення агрегації тромбоцитів. При щоденному прийомі клопідогрелу в дозі 75 мг з першого дня прийому відзначається значне придушення АДФ-індукованої агрегації тромбоцитів, яке поступово збільшується протягом 3-7 днів і потім виходить на постійний рівень (при досягненні рівноважного стану). У рівноважному стані агрегація тромбоцитів пригнічується загалом на 40–60%. Після припинення прийому клопідогрелу агрегація тромбоцитів та час кровотечі поступово повертаються до початкового рівня в середньому протягом 5 днів. Ацетилсаліцилова кислота (АСК) Ацетилсаліцилова кислота (АСК) має відмінний від ефекту клопідогрел і доповнюючий його механізм антиагрегантної дії. АСК пригнічує агрегацію тромбоцитів за рахунок незворотного інгібування ЦОГ-1, внаслідок цього зменшення утворення тромбоксану А 2 є індуктором агрегації тромбоцитів і вазоконстрикції. Цей ефект зберігається протягом усього терміну життя тромбоцитів. АСК не змінює інгібуючого ефекту клопідогрелу на АДФ-індуковану агрегацію тромбоцитів, тоді як клопідогрел посилює вплив ацетилсаліцилової кислоти на колагеніндуковану агрегацію тромбоцитів. Обидві активні речовини в монотерапії та при одночасному застосуванні здатні запобігати розвитку атеротромбозу при будь-яких локалізаціях атеросклеротичного ураження судин, зокрема при ураженнях церебральних, коронарних або периферичних артерій. Клінічне дослідження ACTIVE-A показало, що у пацієнтів з фібриляцією передсердь, які мали як мінімум один фактор ризику розвитку судинних ускладнень, але були нездатні приймати непрямі антикоагулянти, клопідогрел у поєднанні з АСК (у порівнянні з прийомом лише однієї АСК) зменшував частоту разом узятих інсульту, інфаркту міокарда, системної тромбоемболії поза судинами ЦНС або смерті від судинних причин, переважно за рахунок зменшення ризику розвитку інсульту. Перевага прийому клопідогрелу у поєднанні з АСК у порівнянні з прийомом АСК у поєднанні з плацебо виявлялося рано і зберігалося протягом усього періоду дослідження (до 5 років). Зменшення ризику великих судинних ускладнень у групі пацієнтів, які приймали клопідогрел у поєднанні з АСК, було в основному зумовлене більшим зменшенням частоти інсультів. Ризик розвитку інсульту будь-якого ступеня тяжкості при прийомі клопідогрелу у поєднанні з АСК знижувався, а також була тенденція до зниження частоти розвитку інфаркту міокарда в групі пацієнтів, які приймали клопідогрел у поєднанні з АСК, але не спостерігалося відмінностей у частоті тромбоемболій поза судинами ЦНС або смерті причин. Крім цього, застосування клопідогрелу у поєднанні з АСК зменшувало загальну кількість днів госпіталізації з приводу серцево-судинної патології.Показання до застосуванняЦей комбінований препарат показаний для застосування у пацієнтів, які вже отримують одночасно клопідогрел та АСК. Запобігання атеротромботичним ускладненням - дорослі пацієнти з гострим коронарним синдромом: без підйому сегмента ST (нестабільна стенокардія або інфаркт міокарда без зубця Q), включаючи пацієнтів, яким було проведено стентування при черезшкірному коронарному втручанні; c підйомом сегмента ST (гострий інфаркт міокарда) при медикаментозному лікуванні та можливості проведення тромболізису. Запобігання атеротромботичних та тромбоемболічних ускладнень, включаючи інсульт, при фібриляції передсердь (миготлива аритмія): дорослі пацієнти з фібриляцією передсердь (миготлива аритмія), які мають щонайменше 1 фактор ризику розвитку судинних ускладнень, не можуть приймати непрямі антикоагулянти та мають низький ризик розвитку кровотечі.Протипоказання до застосуванняпідвищена чутливість до будь-якої з діючих або допоміжних речовин; тяжка печінкова недостатність (більше 9 балів за шкалою Чайлд-П'ю); тяжка ниркова недостатність (Cl креатиніну менше 30 мл/хв) через вміст у складі препарату АСК); гостра кровотеча, наприклад кровотеча з виразки або внутрішньочерепний крововилив; бронхіальна астма, що індукується прийомом саліцилатів та інших нестероїдних протизапальних засобів; синдром бронхіальної астми, риніту та рецидивуючого поліпозу носа та приносових пазух, гіперчутливість до НПЗП (через вміст у складі препарату АСК); мастоцитоз, при якому застосування АСК може викликати тяжкі реакції гіперчутливості, включаючи розвиток шоку, з гіперемією шкірних покривів, зниженням АТ, тахікардією та блюванням (через вміст у складі препарату АСК); рідкісні спадкові стани: непереносимість галактози; непереносимість лактози внаслідок дефіциту лактази; синдромом мальабсорбції глюкози-галактози (через вміст у складі препарату лактози); вагітність; період грудного вигодовування (див. «Застосування при вагітності та годуванні груддю»); дитячий вік до 18 років (безпека та ефективність застосування не встановлені). З обережністю: помірна печінкова недостатність (7-9 балів за шкалою Чайлд-П'ю), за якої можлива схильність до кровотеч (обмежений клінічний досвід застосування); ниркова недостатність легкого та середнього ступеня тяжкості (Cl креатиніну 60-30 мл/хв) (обмежений клінічний досвід застосування); травми, хірургічні втручання, включаючи інвазивні кардіологічні процедури або хірургічні втручання; захворювання, при яких є схильність до розвитку кровотеч, особливо внутрішньоочних або шлунково-кишкових (виразкова хвороба шлунка та дванадцятипалої кишки або шлунково-кишкова кровотеча в анамнезі, симптоми порушень з боку верхніх відділів ШКТ); недавно перенесене минуще порушення мозкового кровообігу або ішемічний інсульт; одночасне застосування НПЗП, у т.ч.,селективних інгібіторів ЦОГ-2; одночасне застосування варфарину, гепарину, інгібіторів глікопротеїну IIb/IIIа, селективних інгібіторів зворотного захоплення серотоніну (СІЗЗС) та тромболітичних препаратів; бронхіальна астма та алергія в анамнезі (підвищений ризик розвитку алергічних реакцій на АСК); подагра, гіперурикемія (АСК, у т.ч. та в низьких дозах, підвищує концентрацію сечової кислоти в крові); одночасний прийом алкоголю (етанолу) (через наявність у складі препарату АСК; пацієнти з генетично обумовленим зниженням активності ізоферменту CYP2D9; пацієнти з дефіцитом глюкозо-6-фосфатдегідрогенази (через ризик розвитку гемолізу); одночасне застосування метотрексу в0 /тиждень, наявність вказівок в анамнезі на алергічні та гематологічні реакції на інші тієнопіридини (такі як тіклопідін,празугрел) (можливість перехресних алергічних та гематологічних реакцій); одночасне застосування лікарських препаратів, що асоціюються з ризиком розвитку кровотечі та лікарських препаратів, що є субстратами ізоферменту CYP2C8 (таких як репаглінід, паклітаксел) через виявлену лікарську взаємодію.Вагітність та лактаціяЯк запобіжний засіб препарат Коплавікс не слід приймати протягом перших двох триместрів вагітності, за винятком випадків, коли клінічний стан жінки вимагає лікування клопідогрелом у комбінації з АСК. У зв'язку з наявністю у складі препарату АСК він протипоказаний у III триместрі вагітності. Дослідження на тваринах не виявили у клопідогрелу ні прямих, ні непрямих несприятливих ефектів протягом вагітності, ембріональний розвиток, пологи та постнатальний розвиток. Однак достатніх за обсягом та контрольованих досліджень у вагітних жінок не проводилося. У АСК було встановлено наявність тератогенної дії, хоча в клінічних дослідженнях було встановлено, що дози АСК до 100 мг на добу, що обмежено застосовуються в акушерстві та потребують спеціалізованого моніторингу, показали себе безпечними. Грудне вигодовування у разі лікування препаратом Коплавікс слід припинити, т.к. встановлено, що АСК виділяється в грудне молоко, а дослідження на щурах показали, що клопідогрел та/або його метаболіти також екскретуються в молоко щурів, що лакують. Виділяється чи ні клопідогрел у жіноче грудне молоко, невідомо.Побічна діяБезпека клопідогрелу в клінічних дослідженнях була вивчена більш ніж у 44000 пацієнтів, у т. ч. більш ніж у 12000 пацієнтів, які приймали його протягом року або більше, та у 30000 пацієнтів, які приймали одночасно клопідогрел та АСК; у клінічному дослідженні CURE безпека клопідогрелу у поєднанні з АСК була оцінена у понад 6200 пацієнтів, які приймали їх протягом 1 року та більше.Взаємодія з лікарськими засобамиЛікарські препарати, що асоціюються з ризиком кровотечі Є підвищений ризик розвитку кровотечі внаслідок потенційного адитивного ефекту. Одночасне застосування 23 лікарських препаратів, що асоціюються з ризиком розвитку кровотечі, слід проводити з обережністю. Тромболітики Безпека спільного застосування клопідогрелу, фібринспецифічних або нефібринспецифічних тромболітичних засобів та гепарину була проаналізована у пацієнтів з гострим інфарктом міокарда. Частота клінічно значущих кровотеч була аналогічна тій, що спостерігалася у разі спільного застосування тромболітичних препаратів та гепарину з АСК. У зв'язку з недостатністю клінічних даних щодо спільного застосування препарату Коплавікс та тромболітичних препаратів при їх спільному застосуванні слід бути обережним (див. «Особливі вказівки»). Інгібітори глікопротеїну IIb/IIIa Між інгібіторами глікопротеїну IIb/IIIa та препаратом Коплавікс можлива фармакодинамічна взаємодія, що потребує обережності при їх спільному застосуванні. Гепарин За даними клінічного дослідження, проведеного за участю здорових добровольців, при прийомі клопідогрелу не потрібно зміни дози гепарину, і не змінювалася його антикоагулянтна дія. Одночасне застосування гепарину не змінювало інгібуючої дії клопідогрелу на агрегацію тромбоцитів. Між препаратом Коплавікс та гепарином можлива фармакодинамічна взаємодія, яка може збільшувати ризик розвитку кровотеч, у зв'язку з чим спільне застосування цих препаратів потребує обережності. Непрямі антикоагулянти Одночасний прийом препарату Коплавікс та пероральних антикоагулянтів (варфарину) може збільшити інтенсивність кровотеч, у зв'язку з чим застосування цієї комбінації не рекомендується. Клопідогрел у дозі 75 мг не впливає на фармакокінетику варфарину та не змінює значення МНО у пацієнтів, які тривало приймають варфарин. Тим не менш, одночасний прийом варфарину з клопідогрелом може збільшити ризик кровотеч через незалежний вплив цих препаратів на гемостаз. НПЗП У клінічному дослідженні, проведеному за участю здорових добровольців, спільне застосування клопідогрелу та напроксену збільшувало приховані втрати крові через ШКТ. Тому застосування НПЗЗ, в т.ч. інгібіторів ЦОГ-2 у поєднанні з препаратом Коплавікс не рекомендується. Експериментальні дані свідчать на користь того, що ібупрофен (при одноразовому прийомі у дозі 400 мг у період часу між 8 год до 30 хв після безпосереднього прийому АСК у дозі 81 мг у лікарській формі негайного вивільнення) може пригнічувати ефект низьких доз АСК на агрегацію тромбоцитів . Однак при нерегулярному прийомі ібупрофену жодних клінічно значущих ефектів його на антиагрегантну дію АСК не очікується. СІОЗС Оскільки СІЗЗЗ порушують активацію тромбоцитів та збільшують ризик розвитку кровотечі, одночасне застосування СІЗЗЗ з клопідогрелом має проводитися з обережністю.Спосіб застосування та дозиВсередину, 1 раз на добу, незалежно від їди. Дорослі та пацієнти похилого віку з нормальною активністю ізоферменту CYP2C19 Гострий коронарний синдром (ГКС). Лікування починають якомога раніше після появи симптомів. Прийом препарату Коплавікс починають після прийому одноразової навантажувальної дози клопідогрелу у комбінації з АСК у вигляді окремих препаратів, а саме клопідогрел – у дозі 300 мг та АСК – у дозах 75–325 мг/добу, а при гострому інфаркті міокарда з підйомом сегменту ST поєднанні з тромболітиками або без них. Оскільки застосування більш високих доз АСК пов'язане зі збільшенням ризику кровотеч, доза АСК, що рекомендується при цьому, не повинна перевищувати 100 мг. При гострому інфаркті міокарда з підйомом сегмента ST у пацієнтів віком від 75 років лікування клопідогрелом має починатися без прийому його навантажувальної дози.У пацієнтів з ГКС без підйому сегмента ST (нестабільна стенокардія або інфаркт міокарда без зубця Q) максимальний сприятливий ефект спостерігається до 3 місяців лікування. Оптимальної тривалості лікування офіційно не визначено. Дані клінічних досліджень підтримують прийом препарату до 12 місяців. У пацієнтів з гострим інфарктом міокарда з підйомом сегмента ST лікування слід продовжувати не менше ніж 4 тижні. Фібриляція передсердь. Препарат Коплавікс слід приймати 1 раз на добу, після початку лікування клопідогрелом у дозі 75 мг та АСК у дозі 100 мг у вигляді окремих препаратів.ПередозуванняКлопідогрів Симптоми: передозування клопідогрелу може вести до збільшення часу кровотечі з подальшими ускладненнями у вигляді розвитку кровотеч. Лікування: при появі кровотечі потрібне проведення відповідного лікування. Антидот клопідогрелу не встановлено. Якщо необхідна швидка корекція часу кровотечі, що подовжився, то рекомендується переливання тромбоцитарної маси. АСК Симптоми: помірний ступінь передозування - запаморочення, дзвін у вухах, головний біль, сплутаність свідомості та симптоми з боку шлунково-кишкового тракту (нудота, блювання та біль у ділянці шлунка). При виявленні симптомів тяжкої інтоксикації виникають тяжкі порушення кислотно-основного стану. Спочатку гіпервентиляція, що виникає, призводить до розвитку дихального алкалозу. Потім розвивається дихальний ацидоз як наслідок інгібуючого впливу дихального алкалозу на дихальний центр. Також унаслідок присутності саліцилатів у крові розвивається метаболічний ацидоз. Крім цього, з'являються такі симптоми: гіпертермія та рясна потовиділення, що призводять до дегідратації, рухове занепокоєння, судоми, галюцинації та розвиток гіпоглікемії. Пригнічення нервової системи може призвести до розвитку коми, колапсу та зупинки дихання. Літальна доза АСК становить 25-30 г. Плазмова концентрація саліцилату понад 300 мг/л (1,67 ммоль/л) підтверджує наявність інтоксикації. Передозування саліцилатів, особливо у маленьких дітей, може призводити до розвитку тяжкої гіпоглікемії та потенційно фатального отруєння. При гострому та хронічному передозуванні АСК може розвинутись некардіогенний набряк легень (див. «Побічна дія»). Лікування: при виявленні симптомів тяжкого передозування потрібна госпіталізація. При помірній інтоксикації можна спробувати індукувати блювання, у разі невдачі показано промивання шлунка. Після цього слід прийняти внутрішньо (якщо пацієнт може ковтати) або ввести в шлунок через зонд активоване вугілля (адсорбент) та сольове проносне. З метою форсованого олужнення сечі для прискорення виведення саліцилатів показано внутрішньовенне краплинне введення 250 ммоль натрію бікарбонату протягом 3 годин під контролем рН сечі та кислотно-основного стану. Переважним лікуванням тяжкого передозування є гемодіаліз або перитонеальний діаліз. При необхідності застосовується симптоматичне лікування інших проявів інтоксикації.Запобіжні заходи та особливі вказівкиКровотечі та гематологічні порушення У зв'язку з ризиком розвитку кровотечі та гематологічних небажаних ефектів, у разі появи в ході лікування клінічних симптомів, підозрілих на виникнення кровотечі, слід терміново зробити клінічний аналіз крові, визначити АЧТВ (активований частковий тромбопластиновий час), кількість тромбоцитів у периферичній крові, показники функціональної тромбоцитів та провести інші необхідні дослідження. Одночасне застосування препарату Коплавікс з варфарином не рекомендується, оскільки це може збільшити інтенсивність кровотечі. У зв'язку з наявністю у складі препарату Коплавікс® двох антиагрегантних засобів його слід застосовувати з обережністю у пацієнтів, схильних до підвищеного ризику кровотечі, обумовленого травмами, хірургічними втручаннями або іншими патологічними станами, а також у пацієнтів, які приймають нестероїдні протизапальні засоби (в тому числі, інгібітори ЦОГ). 2), гепарин, інгібітори глікопротеїну IIb/IIIa, СІОЗС та тромболітичні препарати. Необхідно вести ретельне спостереження за пацієнтами щодо виключення ознак кровотечі, у тому числі і прихованого, особливо протягом перших тижнів лікування та/або після інвазивних кардіологічних процедур або хірургічного втручання. Якщо пацієнт має планове хірургічне втручання, і при цьому немає необхідності в постійній антиагрегантній терапії, то за 5-7 днів до хірургічного втручання клопідогрел слід відмінити. Препарат Коплавікс® збільшує час кровотечі і повинен застосовуватися з обережністю у пацієнтів із захворюваннями та станами, що схильні до розвитку кровотеч (особливо кровотеч із шлунково-кишкового тракту та внутрішньоочних крововиливів). Пацієнти повинні бути попереджені про те, що при прийомі препарату Коплавікс® для зупинки кровотечі їм може знадобитися більше часу, ніж зазвичай, і що у разі виникнення у них будь-яких незвичайних (по локалізації або тривалості) кровотеч їм слід повідомити про це свого лікаря. . Перед будь-яким майбутнім хірургічним втручанням і перед тим, як розпочати прийом будь-якого нового лікарського препарату, пацієнти повинні інформувати лікаря (зокрема стоматолога) про лікування препаратом Коплавікс®. Нещодавно перенесений ішемічний інсульт Було показано, що у пацієнтів з нещодавно перенесеним минущим ішемічним порушенням мозкового кровообігу або інсультом, що мають підвищений ризик розвитку повторного ішемічного ускладнення, комбінація АСК та клопідогрел збільшує можливість розвитку великих кровотеч. Тому застосування препарату Коплавікс у таких пацієнтів має проводитися з обережністю і лише у разі доведеної клінічної користі від його застосування. Тромботична тромбоцитопенічна пурпура Дуже рідко після застосування клопідогрелу (іноді навіть нетривалого) відзначалися випадки розвитку тромботичної тромбоцитопенічної пурпури (ТТП), яка характеризується тромбоцитопенією та мікроангіопатичною гемолітичною анемією, що супроводжуються неврологічними розладами, порушенням функції. ТТП є потенційно загрозливим для життя станом, що вимагає негайного лікування, включаючи плазмаферез. Набута гемофілія Повідомлялося про випадки розвитку набутої гемофілії прийому клопідогрелу. При підтвердженому ізольованому збільшенні активованого часткового тромбопластинового часу, що супроводжується або не супроводжується розвитком кровотечі, слід розглянути питання можливості розвитку набутої гемофілії. Пацієнти з підтвердженим діагнозом набутої гемофілії повинні спостерігатися та лікуватися фахівцями з цього захворювання та припинити прийом клопідогрелу. Фібриляція передсердь (миготлива аритмія) У пацієнтів з фібриляцією передсердь, що мають підвищений ризик розвитку серцево-судинних ускладнень, які могли приймати непрямі антикоагулянти, була показана перевага непрямих антикоагулянтів у порівнянні з монотерапією АСК або застосуванням комбінації клопідогрел + АСК у зменшенні ризику розвитку інсульту. Функціональна активність ізоферменту CYP2C19 У пацієнтів з низькою метаболічною активністю ізоферменту CYP2C19 при застосуванні клопідогрелу у рекомендованих дозах утворюється менше активного метаболіту клопідогрелу та зменшується його ефект на функцію тромбоцитів. Тому такі пацієнти з гострим коронарним синдромом або пацієнти, які піддаються черезшкірному коронарному втручанню та приймають клопідогрел, можуть мати більшу частоту серцево-судинних подій, ніж пацієнти з нормальною активністю ізоферменту CYP2C19. Є тести визначення генотипу CYP2C19, ці тести можна використовувати при виборі терапевтичної стратегії. Розглядається питання щодо застосування більш високих доз клопідогрелу у пацієнтів з низькою активністю ізоферменту CYP2C19, проте ефективність та безпека застосування підвищених доз клопідогрелу у пацієнтів з низькою активністю ізоферменту CYP2C19 дотепер не встановлені. Перехресні алергічні та/або гематологічні реакції між тієнопіридинами У пацієнтів слід збирати анамнез на предмет алергічних та/або гематологічних реакцій, що були раніше, на інші тієнопіридини (такі як тіклопідин, прасугрел), оскільки повідомлялося про наявність перехресних алергічних та/або гематологічних реакцій між тіенопіридинами. Тієнопіридини можуть викликати помірні та тяжкі алергічні реакції (такі як висипання на шкірі, ангіоневротичний набряк) або гематологічні реакції (такі як тромбоцитопенія і нейтропенія). Пацієнти, у яких раніше спостерігалися алергічні та/або гематологічні реакції на один із препаратів групи тієнопіридинів, можуть мати підвищений ризик розвитку подібних реакцій на інший препарат групи тієнопіридинів. Рекомендується моніторинг перехресних алергічних та/або гематологічних реакцій. Ниркова недостатність Комбінацію клопідогрел + АСК не слід застосовувати у пацієнтів з тяжкою нирковою недостатністю. Досвід застосування клопідогрелу у пацієнтів легкою та помірною нирковою недостатністю обмежений. Тому у цієї групи пацієнтів комбінація клопідогрел + АСК повинна застосовуватися з обережністю. Печінкова недостатність Комбінація клопідогрел + АСК не повинна застосовуватися у пацієнтів з тяжким ступенем печінкової недостатності. Досвід застосування клопідогрелу у пацієнтів із захворюваннями печінки середньої тяжкості, які можуть мати схильність до кровотеч, обмежений. Тому у цієї групи пацієнтів комбінація клопідогрел + АСК повинна застосовуватися з обережністю. Обережність, потрібна внаслідок наявності у складі препарату АСК У пацієнтів з бронхіальною астмою або іншими алергічними захворюваннями в анамнезі, оскільки вони мають підвищений ризик розвитку реакцій гіперчутливості. У пацієнтів з подагрою, оскільки низькі дози АСК збільшують концентрацію уратів у крові. Можлива наявність взаємозв'язку між прийомом АСК та розвитком синдрому Рея, рідкісного та небезпечного для життя захворювання, що зазвичай спостерігалося у продромальному періоді інфекцій у дітей, що протікає з розвитком енцефалопатії та гострої жирової дистрофії печінки та швидким розвитком печінкової недостатності, що може призводити до смертельного результату. Етанол може збільшувати ризик ураження шлунково-кишкового тракту при його прийомі на фоні лікування АСК. Тому слід бути обережними при вживанні алкоголю (етанолу) під час лікування АСК. Крім цього, пацієнти повинні бути попереджені про ризик розвитку кровотечі внаслідок хронічного вживання великої кількості алкоголю (етанолу) під час прийому комбінації клопідогрел + АСК. Препарат Коплавікс® повинен застосовуватися під ретельним медичним наглядом у пацієнтів з недостатністю глюкози-6-фосфатдегідрогенази (Г6ФД) через ризик розвитку гемолізу. Слід уникати одночасного прийому левотироксину та саліцилатів, особливо у дозах вище 2,0 г/добу. Вплив на шлунково-кишковий тракт Препарат Коплавікс® слід застосовувати з обережністю у пацієнтів з виразковою хворобою шлунка та дванадцятипалої кишки або шлунково-кишковими кровотечами в анамнезі або у пацієнтів з навіть незначними симптомами з боку верхніх відділів шлунково-кишкового тракту, які можуть бути проявами виразкових уражень шлунка, здатних призвести до. При лікуванні препаратом Коплавікс® у будь-який момент можуть виникнути симптоми з боку верхніх відділів шлунково-кишкового тракту, такі як гастралгія, печія, нудота, блювання та шлунково-кишкова кровотеча. Незважаючи на те, що при лікуванні препаратом Коплавікс® незначні побічні ефекти з боку шлунково-кишкового тракту, такі як диспепсичні розлади, зустрічаються часто, лікар завжди в цих випадках повинен виключати виразки слизової оболонки шлунково-кишкового тракту та кровотечі, навіть за відсутності в анамнезі патології з сторони ШКТ. Пацієнти повинні бути поінформовані про симптоми небажаних реакцій з боку шлунково-кишкового тракту та проінструктовані про те, що у разі їх появи вони повинні негайно звернутися за медичною допомогою. У пацієнтів, які одночасно приймають нікорандил та НПЗЗ, включаючи АСК та ацетилсаліцилат лізину, є підвищений ризик розвитку тяжких ускладнень, таких як утворення виразок та перфорацій у шлунково-кишковому тракті та шлунково-кишкові кровотечі. Вплив на здатність до керування автотранспортом та управління механізмами Зазвичай Коплавікс® не має істотного впливу на здатність керувати транспортними засобами та займатися іншими потенційно небезпечними видами діяльності, що потребують підвищеної концентрації уваги та швидкості психомоторних реакцій. Однак у разі виникнення у пацієнта несприятливих побічних реакцій з боку нервової системи та психіки можливе зниження концентрації уваги та швидкості психомоторних реакцій, що може перешкоджати зайняттю такими видами діяльності. У таких випадках питання про можливість заняття потенційно небезпечними видами діяльності має вирішувати лікар.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. діюча речовина: аміодарону гідрохлорид – 200,0 мг; допоміжні речовини: лактози моногідрат, крохмаль кукурудзяний, магнію стеарат, повідон K90F, кремнію діоксид колоїдний безводний. По 10 або 15 таблеток у блістер ПВХ/Ал. По 3 блістери по 10 таблеток або 2 блістери по 15 таблеток разом з інструкцією із застосування в картонну пачку.Опис лікарської формиКруглі пігулки від білого до білого з кремуватим відтінком кольору з лінією розлому з одного боку та з фаскою з двох боків. Є гравіювання: символ у вигляді серця над лінією розлому та 200 під лінією розлому, та скіс від країв до лінії розлому.Фармакотерапевтична групаАнтиаритмічний.ФармакокінетикаБіодоступність після внутрішнього прийому у різних хворих коливається від 30 до 80% (середнє значення — близько 50%). Після одноразового прийому аміодарону Cmax у плазмі крові досягається через 3-7 годин. Проте терапевтична дія зазвичай розвивається через тиждень після початку прийому препарату (від кількох днів до 2 тижнів). Аміодарон є препаратом з повільним надходженням у тканини та високою афінністю до них. Зв'язування з білками плазми становить 95% (62% - з альбуміном, 33,5% - з бета-ліпопротеїнами). Аміодарон має великий обсяг розподілу. Протягом перших днів лікування препарат накопичується майже у всіх тканинах, особливо в жировій тканині та крім неї в печінці, легенях, селезінці та рогівці. Аміодарон метаболізується в печінці за допомогою ізоферментів CYP3A4 та CYP2C8. Його головний метаболіт – дезетиламіодарон – фармакологічно активний і може посилювати антиаритмічний ефект основної сполуки. Аміодарон та його активний метаболіт дезетиламіодарон in vitro мають здатність інгібувати ізоферменти CYP2C9, CYP2C19, CYP2D6, CYP3A4, CYP2A6, CYP2B6 та CYP2C8. Аміодарон та дезетиламіодарон також продемонстрували здатність інгібування деяких транспортерів, таких як P-глікопротеїн (P-gp) та переносник органічних катіонів (ПОК2). In vivo спостерігалася взаємодія аміодарону із субстратами ізоферментів CYP3A4, CYP2C9, CYP2D6 та P-gp. Виведення аміодарону починається через кілька днів, а досягнення рівноваги між надходженням та виведенням препарату (досягнення рівноважного стану) настає від одного до декількох місяців, залежно від індивідуальних особливостей хворого. Основним шляхом виведення аміодарону є кишківник. Аміодарон та його метаболіти не виводяться за допомогою гемодіалізу. Аміодарон має тривалий T1/2 з великою індивідуальною варіабельністю (тому при підборі дози, наприклад, її збільшенні або зменшенні, слід пам'ятати, що необхідний принаймні 1 міс для стабілізації нової плазмової концентрації аміодарону). Виведення прийому внутрішньо протікає в 2 фази: початковий T1/2 (перша фаза) - 4-21 год, T1/2 у 2-й фазі - 25-110 днів (20-100 днів). Після тривалого перорального прийому середній T1/2 – 40 днів.Після відміни препарату повне виведення аміодарону з організму може тривати кілька місяців. Кожна доза аміодарону (200 мг) містить 75 мг йоду. Частина йоду вивільняється з препарату та виявляється у сечі у вигляді йодиду (6 мг/добу при добовій дозі аміодарону 200 мг). Більшість йоду, що залишається у складі препарату, виводиться з каловими масами після проходження через печінку, проте при тривалому прийомі аміодарону концентрації йоду можуть досягати 60-80% від концентрацій аміодарону. Особливостями фармакокінетики препарату пояснюється застосування навантажувальних доз, яке спрямоване на швидке досягнення необхідного рівня насичення тканин, при якому проявляється його терапевтична дія. Фармакокінетика при нирковій недостатності: через незначність виведення препарату нирками у пацієнтів з нирковою недостатністю не потрібна корекція дози аміодарону. При внутрішньовенному введенні Кордарону його активність досягає максимуму через 15 хв і зникає приблизно через 4 години після введення. Після введення аміодарону його концентрація у крові швидко знижується у зв'язку з надходженням препарату до тканини. За відсутності повторних ін'єкцій препарат поступово виводиться. При відновленні внутрішньовенного введення або при призначенні препарату всередину аміодарон накопичується в тканинах. Аміодарон має великий обсяг розподілу і може накопичуватися майже у всіх тканинах, особливо в жировій тканині та крім неї в печінці, легенях, селезінці та рогівці. Аміодарон та його метаболіти не піддаються діалізу. В основному виводиться з жовчю та калом через кишечник. Виведення аміодарону дуже повільне. Аміодарон та його метаболіти визначаються у плазмі крові протягом 9 місяців після припинення лікування.ФармакодинамікаАміодарон відноситься до III класу антиаритмічних препаратів (клас інгібіторів реполяризації) і має унікальний механізм антиаритмічної дії, т.к. крім властивостей антиаритміків III класу (блокада калієвих каналів) він володіє ефектами антиаритміків I класу (блокада натрієвих каналів), антиаритміків IV класу (блокада кальцієвих каналів) та неконкурентною бета-адреноблокуючою дією. Крім антиаритмічної дії, у нього є антиангінальний, коронаророзширювальний, альфа- та бета-адреноблокуючий ефекти. Антиаритмічні властивості: збільшення тривалості 3-ї фази потенціалу дії кардіоміоцитів, переважно за рахунок блокування іонного струму в калієвих каналах (ефект антиаритміка III класу за класифікацією Вогана-Вільямса); зменшення автоматизму синусового вузла, що веде до зменшення частоти серцевих скорочень; неконкурентна блокада альфа- та бета-адренергічних рецепторів; уповільнення синоатріальної, передсердної та AV провідності, більш виражене при тахікардії; відсутність змін провідності шлуночків; збільшення рефрактерних періодів та зменшення збудливості міокарда передсердь та шлуночків, а також збільшення рефрактерного періоду AV вузла; уповільнення проведення та збільшення тривалості рефрактерного періоду у додаткових пучках передсердно-шлуночкового проведення. Інші ефекти: відсутність негативної інотропної дії при прийомі внутрішньо та парентеральному введенні; зниження споживання кисню міокардом за рахунок помірного зниження периферичного опору та ЧСС, а також скоротливості міокарда за рахунок бета-адреноблокуючої дії; збільшення коронарного кровотоку з допомогою прямого на гладку мускулатуру коронарних артерій; підтримання серцевого викиду за рахунок зниження тиску в аорті та зниження периферичного опору; вплив на обмін тиреоїдних гормонів: інгібування перетворення Т3 на Т4 (блокада тироксин-5-дейодинази) та блокування захоплення цих гормонів кардіоцитами та гепатоцитами, що призводить до послаблення стимулюючого впливу тиреоїдних гормонів на міокард. відновлення серцевої діяльності при зупинці серця, спричиненої фібриляцією шлуночків, резистентною до кардіоверсії. Терапевтичні ефекти спостерігаються загалом через тиждень після початку прийому препарату (від кількох днів до двох тижнів). Після припинення його прийому аміодарон визначається у плазмі протягом 9 міс. Слід брати до уваги можливість збереження фармакодинамічної дії аміодарону протягом 10-30 днів після його відміни.Показання до застосуванняПрофілактика рецидивів Загрозливих для життя шлуночкових аритмій, включаючи шлуночкову тахікардію та фібриляцію шлуночків (лікування має бути розпочато в стаціонарі при ретельному кардіомоніторному контролі). Надшлуночкових пароксизмальних тахікардій: документованих нападів рецидивуючої стійкої надшлуночкової пароксизмальної тахікардії у пацієнтів із органічними захворюваннями серця; документованих нападів стійкої рецидивуючої надшлуночкової пароксизмальної тахікардії у пацієнтів без органічних захворювань серця, коли антиаритмічні препарати інших класів не ефективні або є протипоказання до їх застосування; документованих нападів рецидивуючої стійкої надшлуночкової пароксизмальної тахікардії у пацієнтів із синдромом Вольфа-Паркінсона-Уайта. Фібриляції передсердь (миготливої аритмії) та тріпотіння передсердь. Профілактика раптової аритмічної смерті у пацієнтів групи високого ризику Пацієнти після нещодавно перенесеного інфаркту міокарда, що мають більше 10 шлуночкових екстрасистол за 1 годину, клінічні прояви хронічної серцевої недостатності та знижену фракцію викиду лівого шлуночка (менше 40 %). Препарат Кордарон може застосовуватись при лікуванні порушень ритму у пацієнтів з ішемічною хворобою серця та/або порушеннями функції лівого шлуночка.Протипоказання до застосуванняПідвищена чутливість до йоду, аміодарону чи допоміжних речовин препарату. Непереносимість галактози, дефіцит лактази, синдром глюкозо-галактозної мальабсорбції (препарат містить лактозу). Синдром слабкості синусового вузла, синусова брадикардія, синоатріальна блокада за відсутності у пацієнта встановленого електрокардіостимулятора (ризик "зупинки" синусового вузла). Атріовентрикулярна блокада ІІ-ІІІ ступеня, за відсутності у пацієнта встановленого електрокардіостимулятора. Гіпокаліємія, гіпомагніємія. Поєднання з препаратами здатними подовжувати інтервал QT та викликати розвиток пароксизмальних тахікардій, включаючи поліморфну шлуночкову тахікардію типу "пірует": антиаритмічні препарати IA класу (хінідин, гідрохінідин, дизопірамід, прокаїнамід); антиаритмічні препарати ІІІ класу (дофетилід, ібутилід, бретилія тозилат), дронендарон, соталол; інші (не антиаритмічні) препарати, такі як нейролептики: фенотіазини (хлорпромазин, ціамемазин, левомепромазин, тіоридазин, трифлуоперазин, флуфеназин), бензаміди (амісульприд, сультоприд, сульприд, тіаприд), бутирофени; сертиндол, пімозід; антидепресанти: трициклічні антидепресанти, селективні інгібітори зворотного захоплення серотоніну (циталопрам, есциталопрам); антибактеріальні засоби: фторхінолони (левофлоксацин, моксифлоксацин, спарфлоксацин, ципрофлоксацин); макроліди (еритроміцин при внутрішньовенному введенні, азитроміцин, кларитроміцин, рокситроміцин, спіраміцин), ко-тримоксазол; протигрибкові засоби: азоли (воріконазол, ітраконазол, кетоконазол, флуконазол); протималярійні засоби (хінін, хлорохін, мефлохін, галофантрин, лумефантрін);протипротозойні засоби (пентамідин при парентеральному введенні); протипухлинні засоби (вандетаніб, миш'яку триоксид, оксаліплатин); протиблювотні засоби (домперидон, ондансетрон); засоби, що впливають на моторику шлунково-кишкового тракту (цизапрід); антигістамінні засоби (мізоластин, астемізол, терфенадін); інші лікарські засоби (дифеманілу метилсульфат, беприділ). Вроджене або набуте подовження інтервалу QT. Дисфункція щитовидної залози (гіпотиреоз, гіпертиреоз). Інтерстиціальна хвороба легень. Вагітність. Період грудного вигодовування. Вік до 18 років (ефективність та безпека не встановлені). З обережністю: При декомпенсованій або тяжкій хронічній серцевій недостатності (III-IV функціональний клас за класифікацією NYHA). При атріовентрикулярній блокаді І ступеня. У пацієнтів похилого віку. У пацієнтів з електрокардіостимулятором/імплантованим кардіовертером-дефібрилятором. При одночасному застосуванні із препаратами, здатними подовжувати інтервал QT. При одночасному застосуванні з софосбувіром у монотерапії або у комбінації з іншими противірусними препаратами прямої дії проти вірусного гепатиту С (такими як даклатасвір, симепревір, ледіпасвір). При порушеннях функції щитовидної залози в анамнезі. При порушеннях функції печінки. При бронхіальній астмі. При тяжкій дихальній недостатності.Вагітність та лактаціяВагітність Доступна в даний час клінічна інформація недостатня для визначення можливості або неможливості виникнення вад розвитку у ембріона при застосуванні аміодарону в першому триместрі вагітності. Оскільки щитовидна залоза плода починає зв'язувати йод тільки з 14-го тижня вагітності, то не очікується впливу на неї аміодарону у разі його раннього застосування. Надлишок йоду при застосуванні препарату після цього періоду може призвести до появи лабораторних симптомів гіпотиреозу у новонародженого або навіть формування у нього клінічно значущого зоба. Зважаючи на вплив препарату на щитовидну залозу плода, аміодарон протипоказаний у період вагітності, за винятком особливих випадків, коли очікувана користь перевищує ризик (при життєзагрозливих шлуночкових порушеннях ритму серця). Період лактації Аміодарон виділяється у грудне молоко у значних кількостях, тому він протипоказаний у період годування груддю (тому у цей період препарат слід відмінити або припинити грудне вигодовування).Побічна діяЧастота побічних ефектів була визначена таким чином: дуже часто – ≥10%, часто – ≥1%, Пігулки. Серцево-судинна система: часто — помірна брадикардія, вираженість якої залежить від дози препарату. Нечасто – порушення провідності (синоатріальна блокада, AV блокада різних ступенів); аритмогенна дія (є повідомлення про виникнення нових аритмій або посилення існуючих, у деяких випадках з подальшою зупинкою серця). У світлі наявних даних неможливо визначити, чи це наслідком застосування препарату, чи пов'язані з тяжкістю ураження серця, чи є наслідком неефективності лікування. Ці ефекти спостерігаються переважно у випадках застосування Кордарону спільно з ЛЗ, що подовжують період реполяризації шлуночків серця (інтервал QTc) або при порушеннях електролітного балансу. Дуже рідко – виражена брадикардія або, у виняткових випадках, зупинка синусового вузла,які відзначалися у деяких хворих (пацієнти з дисфункцією синусового вузла та пацієнти похилого віку). Частота не відома – прогресування хронічної серцевої недостатності (при тривалому застосуванні). З боку травної системи: дуже часто – нудота, блювання, зниження апетиту, притуплення або втрата смакових відчуттів, відчуття тяжкості в епігастрії, особливо на початку лікування; проходять після зменшення дози; ізольоване підвищення активності трансаміназ у сироватці крові, зазвичай помірне (1,5-3-кратне перевищення нормальних значень) і знижується при зменшенні дози або навіть спонтанно. Часто – гостре ураження печінки з підвищенням трансаміназ та/або жовтяницею, включаючи розвиток печінкової недостатності, іноді фатальної. Дуже рідко – хронічні захворювання печінки (псевдоалкогольний гепатит, цироз) іноді фатальні. Навіть при помірному підвищенні активності трансаміназ у крові, що спостерігається після лікування, що тривало понад 6 місяців, слід підозрювати хронічне ураження печінки. З боку дихальної системи: часто повідомлялося про випадки розвитку інтерстиціального або альвеолярного пневмоніту та облітеруючого бронхіоліту з пневмонією, що іноді закінчуються летальним результатом. Відмічено кілька випадків плевриту. Ці зміни можуть призвести до розвитку легеневого фіброзу, однак вони, в основному, оборотні при ранній відміні аміодарону з призначенням кортикостероїдів або без призначення. Клінічні прояви зазвичай зникають протягом 3-4 тижнів. Відновлення рентгенологічної картини та функції легень відбувається повільніше (кілька місяців). Поява у пацієнта, що отримує аміодарон, вираженої задишки або сухого кашлю, як супроводжуються, так і не супроводжуються погіршенням загального стану (підвищеною стомлюваністю, зниженням маси тіла,підвищенням температури тіла) вимагає проведення рентгенографії грудної клітки та, при необхідності, відміни препарату. Дуже рідко – бронхоспазм у пацієнтів із тяжкою дихальною недостатністю, особливо у пацієнтів із бронхіальною астмою; гострий респіраторний дистрес-синдром, іноді з летальним кінцем і іноді безпосередньо після хірургічних втручань (передбачається можливість взаємодії з високими дозами кисню). Частота не відома - легенева кровотеча.Частота не відома - легенева кровотеча.Частота не відома - легенева кровотеча. З боку органів чуття: дуже часто – мікровідкладення в епітелії рогівки, що складаються зі складних ліпідів, включаючи ліпофусцин, вони зазвичай обмежені областю зіниці та не вимагають припинення лікування та зникають після відміни препарату. Іноді можуть викликати порушення зору як появи кольорового ореолу чи нечіткості контурів при яскравому освітленні. Дуже рідко були описані кілька випадків невриту зорового нерва/зорової нейропатії. Їхній зв'язок з аміодароном досі не встановлений. Однак, оскільки неврит зорового нерва може призводити до сліпоти, при появі нечіткості зору або зниження гостроти зору на фоні прийому Кордарону, рекомендується провести повне офтальмологічне обстеження, включаючи фундоскопію, та у разі виявлення невриту зорового нерва припинити прийом аміодарону. Ендокринні порушення: часто - гіпотиреоз з його класичними проявами: збільшенням маси тіла, мерзлякуватістю, апатією, зниженою активністю, сонливістю, надмірною порівняно з очікуваною дією аміодарону брадикардією. Діагноз підтверджується виявленням підвищеного рівня ТТГ сироватки. Нормалізація функції щитовидної залози зазвичай спостерігається протягом 1-3 місяців після припинення лікування. У ситуаціях, пов'язаних із небезпекою для життя, лікування аміодароном може бути продовжено, з одночасним додатковим призначенням L-тироксину під контролем рівня ТТГ у сироватці крові. Гіпертиреоз, поява якого можлива під час лікування та після нього (були описані випадки гіпертиреозу, що розвинувся через кілька місяців після відміни аміодарону). Гіпертиреоз протікає більш потай з невеликою кількістю симптомів:незначна незрозуміла втрата маси тіла, зменшення антиаритмічної та/або антиангінальної ефективності; психічні розлади у пацієнтів похилого віку чи навіть явища тиреотоксикозу. Діагноз підтверджується виявленням зниженого рівня ТТГ сироватки крові (надчутливий критерій). При виявленні гіпертиреозу аміодарон має бути скасовано. Нормалізація функції щитовидної залози зазвичай відбувається протягом декількох місяців після відміни препарату. При цьому клінічна симптоматика нормалізується раніше (через 3-4 тижні), ніж відбувається нормалізація рівня гормонів щитовидної залози. Тяжкі випадки можуть призводити до смерті, тому в таких випадках потрібне невідкладне лікарське втручання. Лікування у кожному окремому випадку підбирається індивідуально. Якщо стан хворого погіршується, як через самий тиреотоксикоз,так і у зв'язку з небезпечним дисбалансом між потребою міокарда в кисні та його доставкою, рекомендується негайно розпочати лікування кортикостероїдами (1 мг/кг), продовжуючи його досить довго (3 міс), замість застосування синтетичних антитиреоїдних препаратів, які не завжди можуть бути ефективними у цьому випадку. Дуже рідко – синдром порушення секреції антидіуретичного гормону. З боку шкірних покривів: дуже часто – фотосенсибілізація. Часто - у разі тривалого застосування препарату у високих добових дозах може спостерігатися сірувата або блакитна пігментація шкіри; після припинення лікування ця пігментація повільно зникає. Дуже рідко - в ході променевої терапії можуть зустрічатися випадки еритеми, є повідомлення про шкірний висип, зазвичай малоспецифічний, окремі випадки ексфоліативного дерматиту (зв'язок з препаратом не встановлена); алопеція. З боку центральної нервової системи: часто – тремор або інші екстрапірамідні симптоми; порушення сну, зокрема. кошмарні сновидіння. Рідко – сенсомоторні, моторні та змішані периферичні нейропатії та/або міопатія, зазвичай оборотні після відміни препарату. Дуже рідко – мозочкова атаксія, доброякісна внутрішньочерепна гіпертензія (псевдопухлина головного мозку), головний біль. Інші: дуже рідко – васкуліт, епідидиміт, кілька випадків імпотенції (зв'язок із препаратом не встановлено), тромбоцитопенія, гемолітична анемія, апластична анемія. Розчин для ін'єкцій З боку серцево-судинної системи: часто - брадикардія (зазвичай помірне ушкодження ЧСС); зниження АТ, зазвичай помірне і минуще. Випадки артеріальної гіпотензії або колапсу спостерігалися при передозуванні або надто швидкому введенні препарату. Дуже рідко - проаритмогенна дія (є повідомлення про виникнення нових аритмій і в т.ч. поліморфної шлуночкової тахікардії типу «пірует», або посилення існуючих - у деяких випадках з подальшою зупинкою серця). Ці ефекти спостерігаються переважно у випадках застосування Кордарону спільно з ЛЗ, що подовжують період реполяризації шлуночків серця (інтервал QTс) або при порушеннях електролітного балансу (див. «Взаємодія»). У світлі наявних даних неможливо визначити, чи викликано виникнення цих порушень ритму Кордароном, чи пов'язане з тяжкістю кардіальної патології,або є наслідком неефективності лікування. Виражена брадикардія або у виняткових випадках, зупинка синусового вузла, які відзначалися у деяких хворих (пацієнти з дисфункцією синусового вузла та пацієнти похилого віку), припливи крові до шкіри обличчя, прогресування серцевої недостатності (можливе при внутрішньовенному струменевому введенні). З боку дихальної системи: дуже рідко – кашель, задишка, інтерстиціальний пневмоніт; бронхоспазм та/або апное у хворих з тяжкою дихальною недостатністю, особливо у пацієнтів з бронхіальною астмою; гострий респіраторний дистрес-синдром, іноді з летальним кінцем і іноді безпосередньо після хірургічних втручань (передбачається можливість взаємодії з високими концентраціями кисню). З боку травної системи: дуже часто – нудота. Дуже рідко - ізольоване підвищення активності печінкових трансаміназ у сироватці крові, зазвичай помірне (1,5-3-кратне перевищення нормальних значень) і знижується при зменшенні дози або навіть спонтанно. Гостре ураження печінки (протягом 24 годин після введення аміодарону) з підвищенням трансаміназ та/або жовтяницею, включаючи розвиток печінкової недостатності, іноді фатальної. З боку шкірних покривів: дуже рідко – почуття жару, підвищене потовиділення. З боку центральної нервової системи: дуже рідко – доброякісна внутрішньочерепна гіпертензія (псевдопухлина головного мозку), головний біль. Порушення з боку імунної системи: дуже рідко – анафілактичний шок. Невідома частота – ангіоневротичний набряк. Реакції у місці введення: часто запальні реакції, такі як поверхневий флебіт, при введенні безпосередньо в периферичну вену. Реакції в місці введення, такі як біль, еритема, набряк, некроз, транссудація, інфільтрація, запалення, ущільнення, тромбофлебіт, флебіт, целюліт, інфекція, пігментація.Взаємодія з лікарськими засобамиПрепарати, здатні викликати двонаправлену шлуночкову «піруетну» тахікардію або збільшувати тривалість інтервалу QT Препарати, здатні викликати шлуночкову «піруетну» тахікардію. Комбінована терапія препаратами, які можуть викликати шлуночкову «піруетну» тахікардію протипоказана, оскільки збільшується ризик розвитку потенційно летальної шлуночкової «піруетної» тахікардії. Антиаритмічні препарати: ІА класу (хінідин, гідрохінідин, дизопірамід, прокаїнамід), соталол, беприділ. Інші (не антиаритмічні) препарати: вінкамін; деякі нейролептики - фенотіазини (хлорпромазин, ціамемазин, левомепромазин, тіоридазин, трифлуоперазин, флуфеназин), бензаміди (амісульприд, сультоприд, сульприд, тіаприд, вераліприд), бутірофенони (дроперидол, галдолі); трициклічні антидепресанти; цизаприд; макролідні антибіотики (еритроміцин при внутрішньовенному введенні, спіраміцин); азоли; протим'ялярійні препарати (хінін, хлорохін, мефлохін, галофантрин, лумефантрін); пентамідин при парентеральному введенні; дифеманілу метилсульфат; мізоластин; астемізол; терфенадін. Препарати, що здатні збільшувати тривалість інтервалу QT. Спільний прийом аміодарону з препаратами, здатними збільшувати тривалість інтервалу QT, повинен ґрунтуватися на ретельній оцінці для кожного пацієнта співвідношення очікуваної користі та потенційного ризику (можливість зростання ризику шлуночкової «піруетної» тахікардії). При застосуванні таких комбінацій необхідний постійний контроль ЕКГ (для виявлення подовження інтервалу QT), вміст калію та магнію в крові. У пацієнтів, які приймають аміодарон, слід уникати застосування фторхінолонів, включаючи моксифлоксацин. Препарати, що зменшують частоту серцевих скорочень або викликають порушення автоматизму або провідності Комбінована терапія із цими препаратами не рекомендується. Бета-адреноблокатори, БКК, що зменшують ЧСС (верапаміл, дилтіазем), можуть викликати порушення автоматизму (розвиток надмірної брадикардії) та провідності. Препарати, здатні викликати гіпокаліємію Нерекомендовані комбінації. З проносними, стимулюючими перистальтику кишечника, здатні викликати гіпокаліємію, яка збільшує ризик розвитку шлуночкової «піруетної» тахікардії. При поєднанні з аміодароном слід застосовувати проносні інші групи. Комбінації, що потребують обережності при застосуванні. з діуретиками, що спричиняють гіпокаліємію (у монотерапії або комбінаціях з іншими препаратами); системними кортикостероїдами (ГКС, мінералокортикостероїдами), тетракозактидом; амфотерицином (в/в введення). Необхідно запобігати розвитку гіпоглікемії, а у разі її виникнення відновлювати до нормального рівня вміст калію в крові, контролювати концентрацію електролітів у крові та ЕКГ (на предмет можливого подовження інтервалу QT), у разі виникнення шлуночкової «піруетної» тахікардії не слід застосовувати антиаритмічні препарати ( бути розпочато шлуночкову кардіостимуляцію, можливе внутрішньовенне введення солей магнію). Препарати для інгаляційного наркозу Повідомлялося про можливість розвитку таких важких ускладнень у пацієнтів, які отримують аміодарон, при отриманні ними загального наркозу: брадикардії (резистентної до введення атропіну), артеріальної гіпотензії, порушення провідності, зниження серцевого викиду. Спостерігалися дуже рідкісні випадки тяжких ускладнень з боку дихальної системи, іноді фатальних – гострий дихальний дистрес синдром дорослих, який розвивався безпосередньо після хірургічного втручання, виникнення якого пов'язують із високими концентраціями кисню. Препарати, що уріжають серцевий ритм Клонідин, гуанфацин, інгібітори холінестерази (донепезил, галантамін, рівастигмін, такрин, амбенонію хлорид, піридостигміну бромід, неостигміну бромід), пілокарпін – ризик розвитку надмірної брадикардії (кумулятивні ефекти).Спосіб застосування та дозиПрепарат слід приймати лише за призначенням лікаря. Таблетки приймають внутрішньо до їди і запивають достатньою кількістю води. Навантажувальна ("насичувальна") доза: можуть бути застосовані різні схеми насичення. У стаціонарі: початкова доза, розділена на кілька прийомів, становить від 600 - 800 мг (до максимальної 1200 мг) на добу до сумарної дози 10 г (зазвичай протягом 5-8 днів). Амбулаторно: початкова доза, розділена на кілька прийомів, становить від 600 до 800 мг на добу до сумарної дози 10 г (зазвичай протягом 10-14 днів). Підтримуюча доза: може варіювати у різних пацієнтів від 100 мг до 400 мг/добу. Слід застосовувати мінімальну ефективну дозу відповідно до індивідуального терапевтичного ефекту. Оскільки Кордарон має дуже великий період напіввиведення, його можна приймати через день або робити перерви у його прийомі 2 дні на тиждень. Середня терапевтична разова доза – 200 мг. Середня терапевтична добова доза – 400 мг. Максимальна разова доза – 400 мг. Максимальна добова доза – 1200 мг. Зниження дози/Скасування препарату Побічні ефекти препарату повільно зникають зі зниженням концентрації аміодарону в тканинах. Після відміни препарату залишковий, пов'язаний із тканиною аміодарон, може чинити захисну антиаритмічну дію протягом одного місяця. Проте слід враховувати ймовірність розвитку аритмії у період. Особливі групи пацієнтів Аміодарон сильно зв'язується з білками плазми та має тривалий період напіввиведення. У пацієнтів з життєзагрозливими аритміями через тривалий період напіввиведення пропуск дози не має істотного впливу на загальний терапевтичний ефект. Слід застосовувати мінімальні ефективні дози, а пацієнта регулярно контролювати виявлення клінічної симптоматики надлишкової дози амиодарона. За необхідності терапія може бути скоригована. Діти Безпека та ефективність аміодарону у дітей не встановлені. Літні пацієнти У пацієнтів похилого віку слід застосовувати мінімальну ефективну дозу через ризик розвитку вираженої брадикардії та порушень провідності. Особливу увагу слід приділити моніторингу функції щитовидної залози.ПередозуванняСимптоми: при пероральному прийомі великих доз описано кілька випадків синусової брадикардії, зупинки серця, нападів шлуночкової тахікардії, пароксизмальної тахікардії типу «пірует» і ураження печінки. Можливе уповільнення атріовентрикулярної провідності, посилення серцевої недостатності, що вже була. Лікування: симптоматичне (промивання шлунка, призначення активованого вугілля (якщо препарат прийнято нещодавно), в інших випадках проводять симптоматичну терапію: при брадикардії – бета-адреностимулятори або встановлення кардіостимулятора, при тахікардії типу «пірует» – внутрішньовенне введення солей магнію або кардіостимуляція. Ні аміодарон, ні його метаболіти не видаляються при гемодіалізі, специфічного антидоту немає. Інформації щодо передозування аміодарону для внутрішньовенного введення немає.Запобіжні заходи та особливі вказівкиАміодарон може викликати тяжкі небажані реакції з боку серця, щитовидної залози, очей, легень, печінки, шкіри та периферичної нервової системи. Оскільки ці небажані реакції можуть бути відстроченими, пацієнти, які тривалий час приймають препарат Кордарон®, повинні перебувати під ретельним наглядом протягом усього періоду лікування, а також протягом декількох місяців після його припинення. Побічні ефекти препарату Кордарон зазвичай є дозозалежними, тому для мінімізації можливості їх виникнення слід застосовувати мінімальні ефективні дози. Порушення з боку серця Перед початком прийому препарату Кордарон® рекомендується провести електрокардіографічне дослідження (ЕКГ) та визначити вміст калію у сироватці крові. Гіпокаліємія повинна бути скоригована до початку застосування препарату Кордарон. Фармакологічна дія препарату Кордарон® викликає зміни ЕКГ: подовження інтервалу QT, QTC (коригованого), пов'язане з подовженням періоду реполяризації шлуночків серця, з можливою появою хвиль U. Проте ці зміни не є проявом токсичної дії препарату Кордарон®. Допустимо збільшення інтервалу QTC не більше 450 мс або не більше ніж на 25% початкової величини. Застосування аміодарону у високих дозах може призвести до розвитку вираженої брадикардії та порушень провідності серця з появою ідіовентрикулярного серцевого ритму, особливо у пацієнтів похилого віку та при одночасному застосуванні серцевих глікозидів. У таких випадках застосування препарату має бути припинено. При необхідності можуть бути призначені бета-адреноміметики або глюкагон. З урахуванням тривалого періоду напіввиведення аміодарону слід розглянути можливість встановлення тимчасового штучного водія ритму серця. Аміодарон може застосовуватися у пацієнтів з латентною або маніфестною хронічною серцевою недостатністю. При цьому слід з обережністю застосовувати препарат при декомпенсованій або тяжкій хронічній серцевій недостатності (III-IV функціональний клас за NYHA), т.к. аміодарон в окремих випадках може призводити до її обтяження. У пацієнтів похилого віку підвищений ризик розвитку вираженої брадикардії під час застосування аміодарону. У разі виникнення атріовентрикулярної блокади І ступеня слід посилити спостереження за станом пацієнта. У разі розвитку атріовентрикулярної блокади ІІ та ІІІ ступеня, синоатріальної блокади або двоіучкової/трипучкової внутрішньошлуночкової блокади, лікування препаратом Кордарон® повинно бути припинено. Повідомлялося про виникнення нових порушень ритму або обтяження вже наявних порушень ритму, іноді зі смертю. Дуже важливо, хоч і складно, проводити диференціальний діагноз між недостатньою антиаритмічною ефективністю препарату та його аритмогенною дією (незалежно від того, поєднується воно чи ні з погіршенням тяжкості захворювання серця). При застосуванні препарату Кордарон про аритмогенну дію повідомлялося значно рідше, ніж при застосуванні інших протиаритмічних препаратів. Як правило, воно спостерігалося за наявності факторів, що збільшують тривалість інтервалу QT, таких як взаємодія з іншими лікарськими засобами та/або порушення вмісту електролітів у крові. Незважаючи на здатність збільшувати тривалість інтервалу QT, аміодарон має низький потенціал щодо провокування поліморфної шлуночкової тахікардії типу "пірует". Пацієнти з електрокардіостимулятором/імплантованим кардіовертером-дефібрилятором У пацієнтів, які тривалий час отримують антиаритмічні лікарські засоби, повідомлялося про випадки збільшення частоти дефібриляції шлуночків та/або збільшення порога спрацьовування електрокардіостимулятора або імплантованого кардіовертера-дефібрилятора (ІКД). Аміодарон може підвищувати поріг кардіостимуляції у пацієнтів з електрокардіостимулятором, а також поріг дефібриляції у пацієнтів з ІКД. У зв'язку з цим для забезпечення адекватного функціонування зазначених пристроїв, що імплантуються, у пацієнтів, які отримують терапію препаратом Кордарон®, рекомендується регулярно контролювати параметри кардіостимуляції/дефібриляції. Виражена брадикардія при одночасному застосуванні аміодарону з противірусними препаратами При застосуванні препарату Кордарон у комбінації з софосбувіром у монотерапії або у комбінації з іншими противірусними препаратами прямої дії проти вірусного гепатиту С, такими як даклатасвір, симепревір, ледіпасвір, спостерігалися випадки розвитку вираженої, потенційно загрозливої для життя брадикардії, а також блоку. Тому одночасне застосування цих препаратів з препаратом Кордарон не рекомендується. Якщо не можна уникнути одночасного застосування цих препаратів з препаратом Кордарон, рекомендується ретельне спостереження за пацієнтами після початку прийому софозбувіру в комбінації з іншими противірусними препаратами прямої дії. Після початку одночасного застосування софозбувіру пацієнти, які належать до групи високого ризику розвитку брадіаритмії, повинні безперервно спостерігатися в умовах стаціонару протягом не менше 48 годин. Внаслідок тривалого періоду напіввиведення аміодарону також слід проводити відповідний моніторинг у пацієнтів, які припинили прийом препарату Кордарон протягом останніх декількох місяців до початку лікування софосбувіром у монотерапії або у комбінації з іншими противірусними препаратами прямої дії. Пацієнти, які приймають вищезазначені лікарські препарати проти вірусного гепатиту С у поєднанні з препаратом Кордарон®, як у поєднанні з іншими лікарськими препаратами, що уповільнюють серцевий ритм, так і без поєднання з такими лікарськими препаратами, повинні бути поінформовані про симптоми, що вказують на розвиток брадикардії та блокади. серця. У разі появи вони повинні негайно звернутися за медичною допомогою. Порушення з боку щитовидної залози Аміодарон може викликати розвиток як гіпотиреозу (зниження функції щитовидної залози), так і гіпертиреозу (підвищення функції щитовидної залози), особливо у пацієнтів із наявністю захворювань щитовидної залози в анамнезі. Оскільки аміодарон містить йод, його прийом може порушувати поглинання радіоактивного йоду та спотворювати результати радіоізотопного дослідження щитовидної залози. Однак прийом препарату не впливає на достовірність визначення концентрації вільного трийодтироніну (Т3), тироксину (Т4) та тиреотропного гормону (ТТГ) (за допомогою ультрачутливого аналізу) у сироватці крові. Перед застосуванням аміодарону у всіх пацієнтів слід провести клінічне та лабораторне обстеження (визначення концентрації ТТГ у сироватці крові, за допомогою ультрачутливого аналізу) для виявлення порушень функції щитовидної залози. Слід регулярно (з інтервалом у 6 місяців) обстежувати пацієнта під час лікування аміодароном та протягом декількох місяців після його припинення з метою виявлення клінічних або лабораторних ознак зміни функції щитовидної залози. Особливо ретельне спостереження необхідне при застосуванні препарату у пацієнтів похилого віку та пацієнтів з наявністю в анамнезі захворювань щитовидної залози. При підозрі на порушення функції щитовидної залози необхідно здійснити визначення концентрації ТТГ у сироватці крові (за допомогою ультрачутливого аналізу). Аміодарон інгібує периферичне перетворення тироксину (Т4) на трийодтиронін (Т3) і може викликати ізольовані біохімічні зміни (збільшення концентрації вільного Т4 у сироватці крові, при незначно зниженій або навіть нормальній концентрації вільного Т3 у сироватці крові) у клінічних причин для відміни препарату Кордарон. Гіпотиреоз Розвиток гіпотиреозу можна запідозрити з появою наступних клінічних ознак: збільшення маси тіла, непереносимість холоду, зниження активності, виражена брадикардія. Діагноз підтверджується підвищенням концентрації ТТГ у сироватці крові, визначеного за допомогою ультрачутливого аналізу. Нормалізація функції щитовидної залози зазвичай спостерігається протягом 1-3 місяців після припинення лікування. У ситуаціях, пов'язаних з небезпекою для життя (наприклад, при застосуванні препарату для профілактики загрозливих для життя шлуночкових аритмій), лікування препаратом Кордарон може бути продовжене з одночасним додатковим застосуванням препаратів левотироксину під контролем концентрації ТТГ у сироватці крові. Гіпертиреоз Під час прийому препарату Кордарон або протягом декількох місяців після його припинення можливий розвиток гіпертиреозу. Слід звертати особливу увагу на такі симптоми, як зниження маси тіла, астенія, занепокоєння, емоційна лабільність, прискорене серцебиття, виникнення або прискорення порушень ритму та/або нападів стенокардії, виникнення або обтяження хронічної серцевої недостатності. Діагноз підтверджується виявленням зниження концентрації ТТГ у сироватці крові, що визначається за допомогою ультрачутливого аналізу. У цьому випадку прийом препарату Кордарон повинен бути припинений. Відновлення зазвичай відбувається протягом кількох місяців після відміни лікування; спочатку спостерігається зникнення клінічних проявів, та був відбувається нормалізація лабораторних показників функції щитовидної залози.Тяжкі випадки аміодарон-індукованого тиреотоксикозу, які іноді можуть призводити до смерті (як через самий тиреотоксикоз, так і у зв'язку з небезпечним дисбалансом між потребою міокарда в кисні і його доставкою), вимагають невідкладного лікування. Лікування має підбиратися в кожному конкретному випадку індивідуально: антитиреоїдні препарати (які можуть бути не завжди ефективні), глюкокортикостероїди, бета-адреноблокатори.бета-адреноблокатори.бета-адреноблокатори. Порушення з боку органу зору Аміодарон може спричинити розвиток нейропатії/невриту зорового нерва. З появою нечіткості зору або зниження гостроти зору необхідно терміново провести повне офтальмологічне обстеження, включаючи огляд очного дна (фундоскопію). У разі виявлення нейропатії та/або невриту зорового нерва препарат Кордарон® необхідно відмінити через небезпеку їх прогресування аж до розвитку сліпоти. Незалежно від наявності або відсутності порушень органу зору, при тривалому застосуванні препарату Кордарон® рекомендується щорічне офтальмологічне обстеження. Порушення з боку легень При застосуванні аміодарону відзначалися ураження легень (інтерстиціальний/альвеолярний пневмоніт або фіброз, плеврит, облітеруючий бронхіоліт з пневмонітом, що організується), іноді з летальним результатом. Проявами легеневої токсичності є задишка (яка може бути вираженою та не відповідати тяжкості ураження серцево-судинної системи), непродуктивний сухий кашель та погіршенням загального стану (підвищена стомлюваність, зниження маси тіла, гарячка). Симптоми, як правило, спочатку виражені трохи, проте швидко прогресують. У більшості випадків ураження легень розвиваються при тривалому застосуванні аміодарону, але в окремих випадках вони можуть виникати через короткий час (від кількох днів до кількох тижнів) після початку лікування. Перед застосуванням аміодарону у всіх пацієнтів рекомендується провести ретельне клінічне обстеження; у ряді випадків доцільно виконання рентгенографії органів грудної клітки. При підозрі на розвиток інтерстиціального пневмоніту слід провести рентгенологічне дослідження легень та дослідження функції зовнішнього дихання. Рентгенологічні прояви в початковій стадії інтерстиціального пневмоніту буває складно відрізнити від застійних явищ, спричинених лівошлуночковою серцевою недостатністю. При необхідності слід провести додаткове обстеження (наприклад, визначення тиску "заклинювання" легеневої за допомогою катетера Свана-Ганца), а також виключити інші можливі причини появи задишки та інших симптомів (інфекційні захворювання нижніх дихальних шляхів, тромбоемболія легеневої артерії, злоякісні). ). Інтерстиціальний пневмоніт зазвичай є оборотним при ранній відміні аміодарону з поєднанням з терапією глюкокортикостероїдами або без неї. Клінічні симптоми зазвичай дозволяються протягом 3-4 тижнів. Поліпшення рентгенологічної картини та функції легень відбувається повільніше (протягом кількох місяців). У деяких випадках, незважаючи на відміну аміодарону, ураження легенів залишається незворотнім. У окремих пацієнтів після дозволу інтерстиціального пневмоніту відновлення терапії аміодароном у нижчих дозах не призводило до повторного розвитку легеневої токсичності. Незалежно від наявності або відсутності під час лікування препаратом Кордарон® симптоматики ураження легень, рекомендується кожні 6 місяців проводити рентгенологічне дослідження легень та функціональні легеневі проби. У пацієнтів, які приймали препарат Кордарон®, у дуже поодиноких випадках, зазвичай безпосередньо після хірургічного втручання, спостерігалося серйозне дихальне ускладнення (гострий респіраторний дистрес-синдром дорослих), іноді з летальним кінцем; передбачається можливість зв'язку його розвитку із взаємодією з високими концентраціями кисню. Порушення з боку печінки При застосуванні аміодарону спостерігалися різні захворювання печінки (в т.ч. жовтяниця, гепатит, цироз печінки та печінкова недостатність). Тяжкі ураження печінки з летальним результатом спостерігалися в основному при тривалому застосуванні аміодарону, але в окремих випадках вони можуть розвиватися через короткий час після початку лікування (особливо при внутрішньовенному введенні препарату). Рекомендується оцінити активність "печінкових" трансаміназ (ACT та АЛТ) та інші показники функції печінки перед початком прийому аміодарону, а також регулярний моніторинг функціональних "печінкових" тестів (контроль активності "печінкових" трансаміназ) під час лікування та протягом 6 місяців після його припинення . Якщо активність "печінкових" трансаміназ у 3 рази і більше перевищує верхню межу норми (ВГН), слід зменшити дозу аміодарону або припинити прийом препарату. На початку терапії може відзначатися ізольоване підвищення активності "печінкових" трансаміназ від 1,5 до 3 паз вище за ВГН. У таких випадках показники функціональних "печінкових" тестів можуть повернутись до нормальних значень після зменшення дози аміодарону. У разі розвитку гострого ураження печінки (підвищення активності, "печінкових" трансаміназ та/або жовтяниця) застосування препарату має бути припинено. При застосуванні аміодарону протягом більш ніж 6 місяців описано розвиток хронічного ураження печінки, яке може проявлятися мінімально вираженими клінічними ознаками (гепатомегалія) та змінами лабораторних показників (підвищення активності "печінкових" трансаміназ від 1,5 у ≤ 5 разів вище від ВГН). При гістологічному дослідженні біоптатів печінки виявляються зміни, подібні до алкогольного гепатиту, або ознаки цирозу. У разі необхідний регулярний моніторинг функціональних " печінкових " тестів. Зазвичай зазначені клінічні та лабораторні зміни є оборотними та регресують після відміни аміодарону, проте повідомлялося про випадки прогресування-ураження печінки з летальним результатом. У зв'язку з потенційним ризиком гепатотоксичності препарат Кордарон® слід з особливою обережністю застосовувати у пацієнтів з порушеннями функції печінки. Під час лікування рекомендується виключити (або щонайменше обмежити) прийом алкоголю. Порушення з боку шкіри та підшкірних тканин При застосуванні аміодарону відзначалися такі загрозливі для життя або навіть смертельні шкірні реакції, як синдром Стівенса-Джонсона та токсичний епідермальний некроліз. Слід негайно припинити лікування препаратом Кордарон® при появі прогресуючого висипу на шкірі, часто з утворенням бульбашок, або пошкоджень слизових оболонок. Аміодарон досить часто спричиняє фотосенсибілізацію. Пацієнтів слід попередити про те, щоб вони під час лікування уникали впливу прямих сонячних променів або вживали захисних заходів (наприклад, застосування сонцезахисного крему, носіння відповідного одягу). Нейпом'язові порушення Препарат Кордарон може викликати периферичну сенсорно-моторну нейропатію та/або міопатію. Відновлення зазвичай відбувається протягом декількох місяців після відміни препарату Кордарон, але може бути іноді неповним. Лікарська взаємодія Не рекомендується одночасне застосування препарату Кордарон з наступними лікарськими засобами: бета-адреноблокаторами, блокаторами "повільних" кальцієвих каналів, що уріжають серцевий ритм (верапаміл, дилтіазем); проносними засобами, що стимулюють перистальтику кишечника (можуть спричинити гіпокаліємію). Первинна дисфункція трансплантату (ПДТ) протягом 24 годин після трансплантації серця Застосування аміодарону перед трансплантацією серця пов'язане з підвищеним ризиком розвитку ПДТ (дані ретроспективних досліджень). ПДТ є життєзагрозним ускладненням при трансплантації серця, що виявляється як дисфункція лівого, правого або обох шлуночків, і що розвивається протягом 24 годин після трансплантації серця, для якої не встановлено іншої причини. У випадку пацієнтів, внесених у чергу на трансплантацію серця, слід якомога раніше оцінити можливість застосування альтернативного антиаритмічного препарату. Загальна та місцева анестезія Перед хірургічним втручанням слід повідомити лікаря-анестезіолога про те, що пацієнт приймає препарат Кордарон. На фоні прийому препарату Кордарон® можливе збільшення гемодинамічних ризиків, властивих місцевій або загальній анестезії (особливо це відноситься до ушкодження серцевого ритму, уповільнення провідності та зниження скоротливості серця). Вплив на здатність до керування автотранспортом та управління механізмами Виходячи з даних безпеки немає доказів того, що аміодарон порушує здатність керувати транспортними засобами або займатися іншими потенційно небезпечними видами діяльності. Однак як запобіжний засіб пацієнтам з пароксизмами тяжких порушень ритму в період лікування препаратом Кордарон® бажано утримуватися від керування транспортними засобами та занять потенційно небезпечними видами діяльності, що потребують підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
1 671,00 грн
158,00 грн
Склад, форма випуску та упаковкаРозчин для підшкірного введення - 1 мл: Активні речовини: інсулін гларгін 3.6378 мг, що відповідає вмісту людського інсуліну 100 ОД; Допоміжні речовини: метакрезол (м-крезол), цинку хлорид, гліцерол (85%), гідроксид натрію, хлористоводнева кислота, вода д/і. 3 мл - картриджі безбарвного скла (5) - упаковки коміркові контурні (1) - пачки картонні.Опис лікарської формиПрозорий безбарвний розчин.Фармакотерапевтична групаІнсулін гларгін є аналогом людського інсуліну. Отримано методом рекомбінації ДНК бактерій виду Escherichia coli (штами К12). Відрізняється низькою розчинністю у нейтральному середовищі. У складі препарату Лантус він повністю розчинний, що забезпечується кислим середовищем розчину для ін'єкцій (рН = 4). Після введення в підшкірно-жирову клітковину розчин унаслідок своєї кислотності вступає в реакцію нейтралізації з утворенням мікропреципітатів, з яких постійно вивільняються невеликі кількості інсуліну гларгіну, забезпечуючи плавний (без піків) профіль кривої "концентрація-час", а також більшу тривалість дії препарату. Параметри зв'язування з інсуліновими рецепторами інсуліну гларгіну та людського інсуліну дуже близькі. Інсулін гларгін має біологічну дію аналогічну ендогенному інсуліну. Найбільш важливою дією інсуліну є регулювання метаболізму глюкози. Інсулін та його аналоги знижують вміст глюкози в крові, стимулюючи споживання глюкози периферичними тканинами (особливо скелетною мускулатурою та жировою тканиною), а також інгібуючи утворення глюкози у печінці (глюконеогенез). Інсулін пригнічує ліполіз в адипоцитах та протеоліз, одночасно посилюючи синтез білка. Збільшена тривалість дії інсуліну гларгіну безпосередньо зумовлена низькою швидкістю його абсорбції, що дозволяє застосовувати препарат 1 раз на добу. Початок дії в середньому – через 1 год після підшкірного введення. Середня тривалість дії - 24 год, максимальна - 29 год. Характер дії інсуліну та його аналогів (наприклад, інсуліну гларгіну) у часі може суттєво змінюватися як у різних пацієнтів, так і в одного й того самого пацієнта. Тривалість дії препарату Лантус обумовлена його введенням у підшкірно-жирову клітковину.Показання до застосуванняЦукровий діабет, що вимагає лікування інсуліном, у дорослих, підлітків та дітей старше 6 років.Протипоказання до застосуванняпідвищена чутливість до інсуліну гларгіну або будь-якої з допоміжних речовин; дитячий вік до 6 років (клінічних даних щодо застосування нині немає). З обережністю слід застосовувати у вагітних.Побічна діяГіпоглікемія — небажаний наслідок інсулінотерапії, що найчастіше зустрічається, може виникати, якщо доза інсуліну виявляється занадто високою в порівнянні з потребою в ньому. Приступи важкої гіпоглікемії, що особливо повторюються, можуть призводити до ураження нервової системи. Епізоди тривалої та вираженої гіпоглікемії можуть загрожувати життю пацієнтів. Психоневрологічним порушенням на тлі гіпоглікемії («сутінкова» свідомість або його втрата, судомний синдром) зазвичай передують симптоми адренергічної контррегуляції (активація симпатоадреналової системи у відповідь на гіпоглікемію): почуття голоду, дратівливість, «холодний» піт, тахікардія (чим швидше розвивається) вона значніша, тим сильніше виражені симптоми адренергічної контррегуляції). Небажані явища з боку очей.Значні зміни регуляції вмісту глюкози в крові можуть спричинити тимчасові порушення зору внаслідок зміни тургору тканин та показника заломлення кришталика ока. Довгострокова нормалізація вмісту глюкози у крові знижує ризик прогресування діабетичної ретинопатії. Інсулінотерапія, що супроводжується різкими коливаннями вмісту глюкози в крові, може призводити до тимчасових погіршень перебігу діабетичної ретинопатії. У пацієнтів з проліферативною ретинопатією, що особливо не отримують лікування фотокоагуляцією, епізоди важкої гіпоглікемії можуть призводити до розвитку скороминущої втрати зору. Ліподистрофія. Як і при лікуванні будь-якими іншими препаратами інсуліну, у місці ін'єкцій може розвиватися ліподистрофія та локальна затримка абсорбції/всмоктування інсуліну.У ході клінічних досліджень при проведенні інсулінотерапії із застосуванням Лантуса ліподистрофія спостерігалася у 1-2% хворих, тоді як ліпоатрофія була взагалі нехарактерною. Постійна зміна місць ін'єкцій у межах областей тіла, рекомендованих для підшкірного введення інсуліну, може сприяти зменшенню вираженості цієї реакції або запобігти її розвитку. Місцеві реакції в галузі введення та алергічні реакції. У ході клінічних досліджень при проведенні інсулінотерапії із застосуванням Лантуса реакції у місці введення спостерігалися у 3-4% пацієнтів. До таких реакцій належали почервоніння, біль, свербіж, кропив'янка, набряк чи запалення. Більшість незначних реакцій у місці введення інсулінів зазвичай дозволяються в період часу від кількох днів до кількох тижнів.Алергічні реакції гіперчутливості негайного типу інсулін розвиваються рідко. Подібні реакції на інсулін (включаючи інсулін гларгін) або допоміжні речовини можуть проявлятися розвитком генералізованих реакцій шкіри, ангіоневротичного набряку, бронхоспазму, артеріальної гіпотензії або шоку і можуть, таким чином, становити загрозу життю хворого. Інші реакції. Застосування інсуліну може спричинити утворення антитіл до нього. У ході клінічних досліджень у груп пацієнтів, які отримували лікування інсуліном-ізофаном та інсуліном гларгіном, утворення антитіл, що перехресно реагували з людським інсуліном, спостерігалося з однаковою частотою. У поодиноких випадках наявність таких антитіл до інсуліну може викликати необхідність корекції дозування з метою усунення тенденції до розвитку гіпо- або гіперглікемії.Рідко інсулін може викликати затримку виведення натрію та утворення набряків, особливо якщо інтенсифікована інсулінотерапія призводить до поліпшення недостатньої регуляції метаболічних процесів.Взаємодія з лікарськими засобамиРяд ЛЗ впливає на метаболізм глюкози, що може вимагати корекції дози інсуліну гларгіну. До препаратів, які можуть посилювати гіпоглікемічну дію інсуліну та підвищувати схильність до розвитку гіпоглікемії, відносяться пероральні гіпоглікемічні засоби, інгібітори АПФ, дизопірамід, фібрати, флуоксетин, інгібітори МАО, пентоксифілін, пропоксифен і саліцами. До препаратів, які можуть послаблювати гіпоглікемічну дію інсуліну, належать глюкокортикостероїди, даназол, діазоксид, діуретики, глюкагон, ізоніазид, естрогени, гестагени, похідні фенотіазину, соматотропін, такі симпатоміметики, як епінефрин (адреналін), сальбуталін. протеаз, деякі нейролептики (наприклад, оланзапін або клозапін). Бета-адреноблокатори, клонідин,солі літію чи алкоголь можуть як посилювати, і послаблювати гипогликемическое дію інсуліну. Пентамідин може спричиняти гіпоглікемію, яка іноді змінюється гіперглікемією. Крім того, під впливом таких препаратів симпатолітичної дії, як бета-адреноблокатори, клонідин, гуанфацин та резерпін ознаки адренергічної контррегуляції можуть зменшуватись або бути відсутніми.Спосіб застосування та дозиП/к, підшкірно-жирову клітковину живота, плеча або стегна, завжди в один і той же час 1 раз на добу. Місця ін'єкцій повинні чергуватись при кожній новій ін'єкції в межах рекомендованих областей для підшкірного введення препарату. В/в введення звичайної дози, призначеної для підшкірного введення, може спричинити розвиток тяжкої гіпоглікемії. Доза Лантуса та час доби для його введення підбирається індивідуально. У пацієнтів з цукровим діабетом типу 2 Лантус може застосовуватися як у вигляді монотерапії, так і у комбінації з іншими гіпоглікемічними ЛЗ. Перехід із лікування іншими гіпоглікемічними препаратами на Лантус. При заміні схеми лікування інсулінами середньої тривалості дії або тривалого на схему лікування Лантусом може знадобитися корекція добової дози базального інсуліну,а також виникнути необхідність у зміні супутньої протидіабетичної терапії (доз і режиму введення інсулінів короткої дії, що додатково застосовуються, або їх аналогів або доз пероральних гіпоглікемічних препаратів). При переведенні пацієнтів із дворазового протягом доби введення інсуліну-ізофану на одноразове введення Лантуса з метою зниження ризику розвитку гіпоглікемії у нічний та ранній ранковий час слід зменшити початкову дозу базального інсуліну на 20-30% у перші тижні лікування. Протягом періоду зниження дози можна збільшити дози короткого інсуліну, а далі режим дозування має бути індивідуально скоригований. Лантус не слід змішувати з іншими інсуліновими препаратами або розводити. При змішуванні або розведенні може змінитися профіль його дії в часі, крім того,змішування з іншими інсулінами може спричинити випадання осаду. Як і при застосуванні інших аналогів людського інсуліну, у пацієнтів, які отримують високі дози препаратів внаслідок наявності антитіл до людського інсуліну, при переході на Лантус може спостерігатися поліпшення реакції на введення інсуліну. У процесі переходу на Лантус та в перші тижні після нього потрібен ретельний контроль вмісту глюкози у крові. У разі покращення регуляції метаболізму та обумовленого цим підвищення чутливості до інсуліну може стати необхідною подальша корекція режиму дозування. Корекція дози також може бути потрібна, наприклад, при зміні маси тіла пацієнта, його способу життя, часу доби для введення препарату або при появі інших обставин,сприяють підвищенню схильності до розвитку гіпо-або гіперглікемії. Препарат не слід вводити внутрішньовенно. Тривалість дії Лантуса обумовлена його введенням у підшкірно-жирову тканину.ПередозуванняСимптоми: важка та іноді тривала гіпоглікемія, що загрожує життю хворого. Лікування: епізоди помірної гіпоглікемії зазвичай купуються шляхом прийому внутрішньо легкозасвоюваних вуглеводів. Може виникнути потреба зміни схеми дозування препарату, режиму харчування або фізичної активності. Епізоди тяжчої гіпоглікемії, що супроводжуються комою, судомами або неврологічними розладами, вимагають внутрішньом'язового або підшкірного введення глюкагону, а також внутрішньовенного введення концентрованого розчину декстрози. Може знадобитися тривалий прийом вуглеводів та нагляд фахівця, т.к. гіпоглікемія здатна рецидивувати після видимого клінічного покращення.Запобіжні заходи та особливі вказівкиВказівки щодо сумісності. Лантус не можна змішувати з будь-якими іншими ЛЗ. Необхідно переконатися, щоб у шприцах не було залишків інших ЛЗ.Умови відпустки з аптекЗа рецептомВідео на цю тему
1 586,00 грн
175,00 грн
Склад, форма випуску та упаковкаРозчин - 1 мл: активна речовина: інсулін гларгін 100 ОД (3,6378 мг); допоміжні речовини: метакрезол (м-крезол) 2,7 мг, цинку хлорид 0,0626 мг (відповідає 30 мкг цинку), гліцерол (85%) 20 мг, натрію гідроксид до pH 4,0, хлористоводнева кислота до pH 4,0 , вода для ін'єкцій до 1 мл. По 3 мл препарату в картридж із прозорого, безбарвного скла (тип I). Картридж закупорений з одного боку бромбутилової пробкою і обтиснутий алюмінієвим ковпачком, з іншого боку – бромбутиловим плунжером. Картридж вмонтовано в одноразову шприц-ручку СолоСтар®. По 5 шприц-ручок СолоСтар® разом з інструкцією із застосування в картонну пачку, забезпечену картонним фіксатором.Опис лікарської формиПрозора, безбарвна чи майже безбарвна рідина.Фармакотерапевтична групаГіпоглікемічний засіб – інсуліну тривалої дії аналог.ФармакокінетикаПорівняльне вивчення концентрацій інсуліну гларгіну та інсуліну-ізофану в сироватці крові у здорових людей та пацієнтів з цукровим діабетом, після підшкірного введення препаратів виявило більш повільну та значно більшу абсорбцію, а також відсутність піку концентрації в інсуліну гларгіну порівняно з інсуліном-ізофаном. При одноразовому протягом доби підшкірному введенні препарату Лантус СолоСтар рівноважна концентрація інсуліну гларгіну в крові досягається через 2-4 доби при щоденному введенні. При внутрішньовенному введенні періоди напіввиведення інсуліну гларгіну та людського інсуліну були порівнянними. При введенні інсуліну пларгіну в ділянку живота, плеча чи стегна не виявлено достовірних відмінностей у концентраціях інсуліну у сироватці крові. Порівняно з людським інсуліном середньої тривалості дії інсулін гларгін характеризується меншою варіабельністю фармакокінетичного профілю, як в одного і того ж, так і в різних пацієнтів. У людини в підшкірно-жировій клітковині інсулін гларгін частково розщеплюється з боку карбоксильного кінця (С-кінця) (3-ланцюга (бета-ланцюга) з утворенням двох активних метаболітів M1 (21A-Gly-інсуліну) та М2 (21A-Gly-des -30B-Thr-інсуліну) Переважно в плазмі крові циркулює метаболіт M1 Системна експозиція метаболіту M1 збільшується при збільшенні дози препарату. інсулін гларгін і метаболіт М2 не вдавалося в системному кровотоку У випадках, коли все-таки вдавалося виявити в крові інсулін гларгін і метаболіт М2, їх концентрації не залежали від введеної дози препарату Лантус® СолоСтар®. Фармакокінетика у спеціальних груп пацієнтів Вік та стать: інформація про вплив віку та статі на фармакокінетику інсуліну гларгіну відсутня. Однак ці фактори не викликали відмінностей у безпеці та ефективності препарату. Куріння: в рамках клінічних досліджень аналіз підгруп не виявив відмінностей у безпеці та ефективності інсуліну гларгіну для даної групи пацієнтів порівняно із загальною популяцією. Ожиріння: у пацієнтів з ожирінням не було показано жодних відмінностей у безпеці та ефективності інсуліну гларгіну та інсуліну-ізофану порівняно з пацієнтами з нормальною масою тіла. Показники фармакокінетики у дітей: у дітей з цукровим діабетом 1 типу у віці від 2 до 6 років концентрації інсуліну гларгіну та його основних метаболітів М1 та М2 у плазмі крові перед введенням чергової дози, були подібні до таких у дорослих, що свідчить про відсутність накопичення гларгіну та його метаболітів при постійному застосуванні інсуліну гларгіну у дітей.ФармакодинамікаІнсулін гларгін є аналогом людського інсуліну, отриманим методом рекомбінації ДНК бактерій виду Escherichia соli (штами К12), і відрізняється низькою розчинністю в нейтральному середовищі. У складі препарату Лантус СолоСтар інсулін гларгін повністю розчинний, що забезпечується кислою реакцією розчину для ін'єкцій (pH 4). Після введення в підшкірно-жирову клітковину кисла реакція розчину нейтралізується, що призводить до утворення мікропреципітатів, з яких постійно вивільняються невеликі кількості інсуліну гларгіну, забезпечуючи передбачуваний, плавний (без піків) профіль кривої "концентрація-час", а також пролонгована. Інсулін гларгін метаболізується до двох активних метаболітів M1 та М2. Зв'язок з інсуліновими рецепторами: кінетика зв'язування зі специфічними рецепторами інсуліну у інсуліну гларгіну та його метаболітів M1 та М2 дуже близька такій у людського інсуліну, у зв'язку з чим інсулін гларгін здатний здійснювати біологічну дію, аналогічну такому у ендогенного ин. Найбільш важливою дією інсуліну та його аналогів, у тому числі інсуліну гларгіну, є регуляція метаболізму глюкози. Інсулін та його аналоги знижують концентрацію глюкози в крові, стимулюючи поглинання глюкози периферичними тканинами (особливо скелетною мускулатурою та жировою тканиною) та інгібуючи утворення глюкози в печінці. Інсулін пригнічує ліполіз в адипоцитах та інгібує протеоліз, збільшуючи одночасно синтез білка. Пролонгована дія інсуліну гларгіну безпосередньо пов'язана зі зниженою швидкістю його абсорбції, що дозволяє застосовувати препарат один раз на добу. Після підшкірного введення початок його дії настає в середньому через 1 год. Середня тривалість дії становить 24 год, максимальна - 29 год. Тривалість дії інсуліну та його аналогів, таких як інсулін гларгін,може суттєво різнитися у різних пацієнтів або в одного й того самого пацієнта. Була показана ефективність застосування препарату Лантус СолоСтар у дітей віком старше 2 років з цукровим діабетом 1 типу. У дітей вікової групи 2-6 років частота виникнення гіпоглікемії з клінічними проявами при застосуванні інсуліну гларгіну була чисельно нижчою, як протягом доби, так і в нічний час порівняно із застосуванням інсуліну-ізофану (відповідно, в середньому 25,5 епізодів проти 33,0 епізодів у одного пацієнта протягом одного року). При п'ятирічному спостереженні за пацієнтами з цукровим діабетом 2 типу не спостерігалося достовірних відмінностей у прогресуванні діабетичної ретинопатії під час лікування інсуліном гларгіном порівняно з інсуліном-ізофаном. Зв'язок з рецепторами інсуліноподібного фактора росту 1 (ІФР-1): афінність інсуліну гларгіну до рецептора ІФР-1 приблизно в 5-8 разів вища, ніж у людського інсуліну (але приблизно в 70-80 разів нижче, ніж у ІФР-1), у той же час, у порівнянні з людським інсуліном, у метаболітів інсуліну гларгіну M1 та М2 афінність до рецептора ІФР-1 дещо менша. Загальна терапевтична концентрація інсуліну (інсуліну гларгіну та його метаболітів), що визначається у пацієнтів з цукровим діабетом 1 типу, була помітно нижчою за концентрацію, необхідну для напівмаксимального зв'язування з рецепторами ІФР-1 та подальшої активації мітогенно-проліферативного шляху, що запускається через рецептори ІФ. Фізіологічні концентрації ендогенного ІФР-1 можуть активувати мітогенно-проліферативний шлях, проте терапевтичні концентрації інсуліну, що визначаються при інсулінотерапії, включаючи лікування препаратом Лантус® СолоСтар®, значно нижчі від фармакологічних концентрацій, необхідних для активації мітогенно-проліферативного шляху. Дослідження ORIGIN (Outcome Reduction with Initial Glargine INtervention) було міжнародним, багатоцентровим, рандомізованим дослідженням, проведеним у 12537 пацієнтів з високим ризиком розвитку серцево-судинних захворювань та з порушеною глікемією натще (НГН), порушеною толерантністю до глюкози. діабету 2 типи. Учасники дослідження були рандомізовані на групи (1:1): група пацієнтів, які отримують інсулін гларгін (n=6264), який титрувався до досягнення концентрації глюкози крові натще (ГКН) ≤5,3 ммоль, та група пацієнтів, які отримують стандартне лікування (n =6273). Перша кінцева точка дослідження являла собою час до розвитку серцево-судинної смерті, першого розвитку нефатального інфаркту міокарда або нефатального інсульту, а друга кінцева точка являла собою час до першого виникнення будь-якого ускладнення з перерахованих вище або до проведення процедури реваскуляризації (коронарних, сонних або сонних) , або до госпіталізації щодо розвитку серцевої недостатності. Другими кінцевими точками були смертність з будь-якої причини і комбінований показник мікросудинних результатів. Дослідження ORIGIN показало, що лікування інсуліном гларгіном у порівнянні зі стандартною гіпоглікемічною терапією не змінювало ризик розвитку серцево-судинних ускладнень або серцево-судинної смертності; не було виявлено відмінностей у показниках будь-якого компонента, що становить кінцеві точки, смертності від усіх причин, комбінованому показнику мікросудинних наслідків. На початку дослідження медіана значень HbAlc становила 6,4%. Медіана значень показника HbAlc під час лікування знаходилась у діапазоні 5,9-6,4% у групі інсуліну гларгіну та 6,2-6,6% у групі стандартного лікування протягом усього періоду спостереження. У групі пацієнтів, які отримували інсулін гларгін, частота розвитку тяжкої гіпоглікемії становила 1,05 епізод на 100 пацієнто-років терапії, а в групі пацієнтів, які отримували стандартну гіпоглікемічну терапію - 0,30 епізоду на 100 пацієнто-років терапії. Частота розвитку легкої гіпоглікемії становила в групі пацієнтів, які отримували інсулін гларгін, 7,71 епізодів на 100 пацієнто-років терапії, а в групі пацієнтів, які отримували стандартну гіпоглікемічну терапію - 2,44 епізоди на 100 пацієнто-років терапії. У дослідженні тривалістю 6 років у 42% пацієнтів у групі, які отримували інсулін гларгін, не було відзначено жодних випадків гіпоглікемії. Медіана змін маси тіла в порівнянні з результатом на останньому візиті лікування була на 2,2 кг вище у групі інсуліну гларгіну, ніж у групі стандартного лікування.Показання до застосуванняЦукровий діабет, що вимагає лікування інсуліном, у дорослих, підлітків та дітей старше 2 років.Протипоказання до застосуванняПідвищена чутливість до інсуліну гларгіну або будь-якого з допоміжних компонентів препарату. Дитячий вік до 2 років (відсутність клінічних даних щодо застосування). З обережністю: вагітні жінки (можливість зміни потреби в інсуліні протягом вагітності та після пологів).Вагітність та лактаціяПацієнтки повинні інформувати лікаря про справжню або заплановану вагітність. Не проводилося рандомізованих контрольованих клінічних досліджень із застосування інсуліну гларгіну у вагітних жінок. Велика кількість спостережень (більше 1000 результатів вагітностей при ретроспективному та проспективному спостереженні) при постмаркетинговому застосуванні інсуліну гларгіну показали відсутність у нього будь-яких специфічних ефектів протягом та результат вагітності або на стан плодів або здоров'я новонароджених. Крім того, з метою оцінки безпеки застосування інсуліну гларгіну та інсуліну-ізофану у вагітних жінок з раніше наявним або гестаційним цукровим діабетом був проведений мета-аналіз восьми спостережних клінічних досліджень, що включав жінок, у яких під час вагітності застосовувався інсулін гларгін (n=331) та інсулін ізофан (n=371). Цей мета-аналіз не виявив істотних відмінностей щодо безпеки щодо здоров'я матерів або новонароджених при застосуванні інсуліну гларгіну та інсуліну-ізофану під час вагітності. У дослідженнях на тваринах не було отримано прямих або непрямих даних про ембріотоксичну або фетотоксичну дію інсуліну гларгіну. Для пацієнток з раніше наявним або гестаційним цукровим діабетом важливо протягом всієї вагітності підтримувати адекватну регуляцію метаболічних процесів, щоб запобігти появі небажаних наслідків, пов'язаних з гіперглікемією. Препарат Лантус® СолоСтар® може застосовуватись при вагітності за клінічними показаннями. Потреба в інсуліні може знижуватися в перший триместр вагітності та, в цілому, збільшуватися протягом другого та третього триместрів. Безпосередньо після пологів потреба в інсуліні швидко зменшується (зростає ризик розвитку гіпоглікемії). У умовах істотне значення має ретельний контроль концентрації глюкози у крові. Пацієнткам у період годування груддю може знадобитися корекція режиму дозування інсуліну та дієти.Побічна діяНаведені нижче небажані реакції (HP) представлені за системами органів (відповідно до класифікації Медичного словника з нормативно-правової діяльності (MedDRA)) відповідно до наступних градацій частоти їх виникнення: дуже часто (≥ 10%); часто (≥ 1%); Порушення з боку обміну речовин та харчування - Дуже часто: гіпоглікемія. Гіпоглікемія, що найчастіше зустрічається небажана реакція при інсулінотерапії, може виникнути, якщо доза інсуліну виявляється надто високою порівняно з потребою в ньому. Симптоми розвитку гіпоглікемії зазвичай виникають раптово. Однак часто психоневрологічним порушенням на тлі нейроглікопенії (почуття втоми, незвичайна стомлюваність або слабкість, зниження здатності до концентрації уваги, сонливість, зорові розлади, головний біль, нудота, сплутаність свідомості або його втрата, судомний синдром) зазвичай передують симптоми адренергічної контррегуляції (активації адреналової системи у відповідь на гіпоглікемію): почуття голоду, дратівливість, нервове збудження або тремор, занепокоєння, блідість шкірних покривів, "холодний" піт, тахікардія,виражене серцебиття (чим швидше розвивається гіпоглікемія і що вона важча, тим сильніше виражені симптоми адренергічної контррегуляції). Приступи важкої гіпоглікемії, що особливо повторюються, можуть призводити до ураження нервової системи. Епізоди тривалої та вираженої гіпоглікемії можуть загрожувати життю пацієнтів, тому що при наростанні гіпоглікемії можливий навіть смертельний результат. Порушення з боку імунної системи: - Рідко: алергічні реакції. Алергічні реакції негайного типу інсулін розвиваються рідко. Подібні реакції на інсулін (включаючи інсулін гларгін) або допоміжні речовини можуть проявлятися розвитком генералізованих шкірних реакцій, ангіоневротичного набряку, бронхоспазму, зниження артеріального тиску або шоку і можуть, таким чином, загрожувати життю пацієнта. Застосування інсуліну може спричинити утворення антитіл до нього. Утворення антитіл, що перехресно реагують з людським інсуліном та інсуліном гларгіном, спостерігається з однаковою частотою при застосуванні інсуліну-ізофану та інсуліну гларгіну. У поодиноких випадках наявність таких антитіл до інсуліну може викликати необхідність корекції режиму дозування з метою усунення тенденції до розвитку гіпо- або гіперглікемії. Порушення з боку нервової системи - Дуже рідко: дисгевзія (порушення або спотворення смакових відчуттів). Порушення з боку органу зору: - Рідко: порушення зору (значні зміни регуляції вмісту глюкози в крові можуть викликати тимчасові порушення зору внаслідок зміни тургору тканин та показника заломлення кришталика ока); ретинопатія (довгострокова нормалізація вмісту глюкози у крові знижує ризик прогресування діабетичної ретинопатії, проте інсулінотерапія, що супроводжується різкими коливаннями концентрацій глюкози у крові, може супроводжуватися тимчасовим погіршенням перебігу діабетичної ретинопатії). У пацієнтів з проліферативною ретинопатією, що особливо не отримують лікування фотокоагуляцією, епізоди важкої гіпоглікемії можуть призводити до розвитку скороминущої втрати зору. Порушення з боку шкіри та підшкірних тканин - Часто: ліподистрофія (у 1-2% пацієнтів). Як і при лікуванні будь-якими іншими препаратами інсуліну, на місці ін'єкцій може розвиватися ліподистрофія, здатна уповільнити місцеву абсорбцію інсуліну. Нечасто: ліпоатрофія Постійна зміна місць ін'єкцій у межах областей тіла, рекомендованих для підшкірного введення інсуліну, може сприяти зменшенню вираженості цієї реакції або запобігти її розвитку. Порушення з боку скелетно-м'язової та сполучної тканини - Дуже рідко: міалгія. Загальні розлади та порушення у місці введення - Часто: реакції у місці введення (3-4%) (почервоніння, біль, свербіж, кропив'янка, набряк або запалення). Більшість незначних реакцій у місці введення інсулінів зазвичай дозволяються в період часу від кількох днів до кількох тижнів; Рідко: затримка натрію, набряки (особливо якщо інтенсифікована інсулінотерапія призводить до поліпшення раніше недостатнього метаболічного контролю). Профіль безпеки для пацієнтів молодше 18 років, загалом, подібний до профілю безпеки для пацієнтів старше 18 років. У пацієнтів молодше 18 років відносно частіше виникають реакції у місці введення та шкірні реакції (висип, кропив'янка). Дані з безпеки у пацієнтів, молодших 2 років, відсутні.Взаємодія з лікарськими засобамиФармакодинамічна взаємодія Пероральні гіпоглікемічні засоби, інгібітори ангіотензинперетворюючого ферменту, дизопірамід фібрати, флуоксетин, інгібітори моноаміноксидази, пентоксифілін, пропоксифен, саліцилати та сульфаніламідні протимікробні засоби - можуть посилити гіпоглікемічну дію. Одночасний прийом з інсуліном гларгіном може вимагати корекції дози інсуліну. Глюкокортикостероїди, даназол, діазоксид, діуретики, глюкагон, ізоніазид, естрогени та гестагени (наприклад, у гормональних контрацептивах), похідні фенотіазину, соматотропін, симпатоміметики (наприклад, епінефрин [адреналін], сальбутазино, альбутамол, нейролептики (наприклад, оланзапін або клозапін) можуть послабити гіпоглікемічну дію інсуліну. Одночасний прийом з інсуліном гларгіном може вимагати корекції дози інсуліну гларгіну. Бета-адреноблокатори, клонідин, солі літію або алкоголь – можливе як посилення, так і ослаблення гіпоглікемічної дії інсуліну. Пентамідин – при поєднанні з інсуліном може спричиняти гіпоглікемію, яка іноді змінюється гіперглікемією. Препарати симпатолітичної дії, такі як бета-адреноблокатори, клонідин, гуанетидин і резерпін - можуть зменшуватися або відсутні ознаки адренергічної контррегуляції (активації симпатичної нервової системи) при розвитку гіпоглікемії. Фармацевтична взаємодія При змішуванні препарату Лантус® СолоСтар© з іншими лікарськими речовинами, у тому числі з іншими інсулінами, а також розведенні препарату можливе утворення осаду або зміна профілю дії препарату в часі.Спосіб застосування та дозиЗагальні рекомендації Лантус® СолоСтар® слід вводити підшкірно 1 раз на добу будь-якої пори дня, але щодня в один і той самий час. У пацієнтів з цукровим діабетом 2 типу Лантус® СолоСтар® може застосовуватися як у вигляді монотерапії, так і в комбінації з іншими гіпоглікемічними препаратами. Цільові значення концентрації глюкози в крові, а також дози та час введення або прийому гіпоглікемічних препаратів повинні визначатися та коригуватися індивідуально. Корекція дози також може бути потрібна, наприклад, при зміні маси тіла пацієнта, його способу життя, зміні часу введення дози інсуліну або при інших станах, які можуть збільшити схильність до розвитку гіпо-або гіперглікемії. Будь-які зміни дози інсуліну повинні проводитися з обережністю та під медичним наглядом. Препарат Лантус СолоСтар не є інсуліном вибору для лікування діабетичного кетоацидозу. У цьому випадку перевагу слід надавати внутрішньовенному введенню інсуліну короткої дії. При схемах лікування, які включають ін'єкції базального і прандиального інсуліну, задоволення потреб у базальному інсуліну зазвичай вводиться 40-60% від добової дози інсуліну як інсуліну гларгіну. У пацієнтів з цукровим діабетом 2 типу, що приймають гіпоглікемічні препарати для внутрішнього прийому, комбінована терапія починається з дози інсуліну гларгіну 10 ОД один раз на добу і в подальшому схема лікування коригується індивідуально. У всіх пацієнтів із цукровим діабетом рекомендується моніторинг концентрації глюкози у крові. Перехід із лікування іншими гіпоглікемічними препаратами на Лантус® СолоСтар® При переведенні пацієнта зі схеми лікування із застосуванням інсуліну середньої тривалості дії або тривалої дії на схему лікування із застосуванням препарату Лантус® СолоСтар® може знадобитися корекція кількості (доз) та часу введення інсуліну короткої дії або його аналога протягом доби або зміна доз пероральних гіпоглікемічних препаратів . При переведенні пацієнтів з одноразового протягом доби введення інсуліну-ізофану на одноразове протягом доби введення препарату Лантус® СолоСтар® початкові дози інсуліну зазвичай не змінюються (тобто застосовується кількість ОД препарату Лантус® СолоСтар® на добу, що дорівнює кількості ME інсуліну-ізофану на добу). ). При переведенні пацієнтів з дворазового протягом доби введення інсуліну-ізофану на одноразове введення препарату Лантус® СолоСтар® перед сном з метою зниження ризику розвитку гіпоглікемії у нічний та ранній ранковий час початкова добова доза інсуліну гларгіну зазвичай зменшується на 20% (порівняно з добовою дозою інсуліну-ізофану), а потім вона коригується залежно від реакції пацієнта. Лантус СолоСтар не слід змішувати з іншими препаратами інсуліну або розводити. Необхідно переконатися, щоб у шприцах не було залишків інших лікарських засобів. При змішуванні або розведенні може змінитися профіль інсуліну гларгіну в часі. При переході з людського інсуліну на препарат Лантус СолоСтар і протягом перших тижнів після нього рекомендується ретельний метаболічний моніторинг (контроль концентрації глюкози в крові) під медичним наглядом, з корекцією при необхідності режиму дозування інсуліну. Як і при застосуванні інших аналогів людського інсуліну, це особливо стосується пацієнтів, які внаслідок наявності у них антитіл до людського інсуліну потребують застосування високих доз людського інсуліну. У таких пацієнтів при застосуванні інсуліну гларгіну може спостерігатись значне поліпшення реакції на введення інсуліну. При поліпшенні метаболічного контролю та обумовленого цим підвищення чутливості тканин до інсуліну може виникнути потреба у корекції режиму дозування інсуліну. Змішування та розведення Препарат Лантус СолоСтар не можна змішувати з іншими інсулінами. Змішування може змінити співвідношення час/дія препарату Лантус СолоСтар, а також призвести до випадання осаду. Особливі групи пацієнтів Діти Препарат Лантус® СолоСтар® може застосовуватися у дітей старше 2-річного віку. Застосування у дітей віком до 2 років не вивчалося. Пацієнти похилого віку У пацієнтів похилого віку з цукровим діабетом, рекомендується застосування помірних початкових доз, повільне їх збільшення та застосування помірних підтримуючих доз. Спосіб застосування Препарат Лантус СолоСтар вводиться у вигляді підшкірних ін'єкцій. Препарат Лантус СолоСтар не призначений для внутрішньовенного введення. Тривала тривалість дії інсуліну гларгіну спостерігається лише при його введенні у підшкірно-жирову клітковину. Внутрішньовенне введення звичайної підшкірної дози може спричинити важку гіпоглікемію. Лантус® СолоСтар® повинен вводитися у підшкірно-жирову клітковину живота, плечей чи стегон. Місця ін'єкцій повинні чергуватись при кожній новій ін'єкції в межах рекомендованих областей для підшкірного введення препарату. Як і у разі інших типів інсуліну, ступінь абсорбції, а, отже, початок та тривалість його дії, можуть змінюватися під впливом фізичного навантаження та інших змін стану пацієнта. Лантус СолоСтар - це прозорий розчин, а не суспензія. Тому ресуспендування перед застосуванням не потрібне. При несправності шприц-ручки Лантус® СолоСтар® інсулін гларгін можна витягти з картриджа в шприц (придатний для інсуліну 100 МО/мл) та зробити необхідну ін'єкцію.ПередозуванняПередозування інсуліну може призводити до тяжкої та іноді тривалої гіпоглікемії, що загрожує життю хворого. Лікування Епізоди помірної гіпоглікемії зазвичай усуваються шляхом прийому внутрішньо швидко засвоюваних вуглеводів. Може виникнути потреба зміни схеми дозування препарату, режиму харчування або фізичної активності. Епізоди тяжчої гіпоглікемії, що виявляються комою, судомами або неврологічними розладами, вимагають внутрішньом'язового або підшкірного введення глюкагону, а також внутрішньовенного введення концентрованого розчину декстрози (глюкози). Може знадобитися тривалий прийом вуглеводів та спостереження спеціаліста, оскільки після видимого клінічного покращення можливий рецидив гіпоглікемії.Запобіжні заходи та особливі вказівкиЛантус СолоСтар не є препаратом вибору для лікування діабетичного кетоацидозу. У таких випадках рекомендується внутрішньовенне введення інсуліну короткої дії. У зв'язку з обмеженим досвідом застосування препарату Лантус СолоСтар не було можливості оцінити його ефективність та безпеку при лікуванні пацієнтів з порушенням функції печінки або пацієнтів із середньо-тяжкою або тяжкою нирковою недостатністю. У пацієнтів з порушенням функції нирок потреба в інсуліні може зменшитися через уповільнення його елімінації. У пацієнтів похилого віку прогресуюче погіршення функції нирок може призвести до стійкого зниження потреби в інсуліні. У пацієнтів з тяжкою печінковою недостатністю потреба в інсуліні може бути знижена через зниження здатності до глюконеогенезу та уповільнення біотрансформації інсуліну. У разі неефективного контролю за рівнем вмісту глюкози в крові, а також за наявності тенденції до розвитку гіпо- або гіперглікемії, перш ніж приступати до корекції режиму дозування, слід перевірити точність виконання запропонованої схеми лікування, дотримання вказівок щодо місць введення препарату та правильність техніки проведення підшкірних ін'єкцій з урахуванням всіх факторів, що впливають на це. Гіпоглікемія Час розвитку гіпоглікемії залежить від профілю дії інсулінів і може, таким чином, змінюватися при зміні схеми лікування. Внаслідок збільшення часу надходження до організму інсуліну тривалої дії при використанні препарату Лантус® СолоСтар®, слід очікувати меншої ймовірності розвитку нічної гіпоглікемії, тоді як у ранні ранкові години ця ймовірність розвитку гіпоглікемії вища. При виникненні гіпоглікемії у пацієнтів, які отримують Лантус СолоСтар, слід враховувати можливість уповільнення виходу зі стану гіпоглікемії у зв'язку з пролонгованою дією інсуліну гларгіну. Пацієнтам, у яких епізоди гіпоглікемії можуть мати особливе клінічне значення, таким як пацієнти з вираженим стенозом коронарних артерій або судин головного мозку (ризик розвитку кардіальних та церебральних ускладнень гіпоглікемії), а також пацієнтам з проліферативною ретинопатією, особливо якщо вони не отримують лікування фотокоагуля минущої втрати зору слідом за гіпоглікемією) слід дотримуватися особливої обережності та інтенсифікувати моніторинг рівня глюкози в крові. Пацієнти повинні бути попереджені про стани, за яких симптоми-провісники гіпоглікемії можуть зменшитися. У пацієнтів окремих груп ризику симптоми гіпоглікемії можуть змінюватися, бути менш вираженими або відсутніми. До них відносяться: пацієнти, у яких помітно покращала регуляція вмісту глюкози в крові; пацієнти, у яких гіпоглікемія розвивається поступово; пацієнти похилого віку; пацієнти, які переведені з інсуліну тваринного походження на людський інсулін; пацієнти із нейропатією; пацієнти із тривалим анамнезом цукрового діабету; пацієнти, які страждають на психічні розлади; пацієнти, які отримують супутнє лікування іншими лікарськими засобами. Такі ситуації можуть призводити до розвитку тяжкої гіпоглікемії (з можливою втратою свідомості) до того, як пацієнт усвідомлює, що розвивається гіпоглікемія. У разі якщо відзначаються нормальні або знижені показники глікозильованого гемоглобіну, необхідно враховувати можливість розвитку нерозпізнаних епізодів гіпоглікемії, що повторюються (особливо в нічний час). Дотримання пацієнтами схеми дозування та режиму харчування, правильне введення інсуліну та знання симптомів-провісників гіпоглікемії сприяють суттєвому зниженню ризику розвитку гіпоглікемії. Фактори, що підвищують схильність до гіпоглікемії, за наявності яких потрібне особливо ретельне спостереження і може бути потрібна корекція дози інсуліну: зміна місця запровадження інсуліну; підвищення чутливості до інсуліну (наприклад, усунення стресових факторів); незвична, підвищена чи тривала фізична активність; інтеркурентні захворювання, що супроводжуються блюванням, діареєю; порушення дієти та режиму харчування; пропущений прийом їжі; споживання алкоголю; деякі некомпенсовані ендокринні порушення (наприклад, гіпотиреоз, недостатність аденогіпофіза або кори надниркових залоз); супутнє лікування деякими іншими лікарськими засобами. Інтеркурентні захворювання При інтеркурентних захворюваннях потрібний інтенсивніший контроль рівня глюкози в крові. У багатьох випадках показано проведення аналізу на наявність кетонових тіл у сечі, також часто потрібна корекція режиму дозування інсуліну. Потреба інсуліні нерідко зростає. Хворі на цукровий діабет 1 типу повинні продовжувати регулярне споживання, принаймні, невеликої кількості вуглеводів, навіть якщо вони здатні споживати їжу лише в малих обсягах або взагалі не можуть їсти або якщо у них є блювота тощо, і вони ніколи не повинні Дуже припиняти введення інсуліну. Інструкція з використання та звернення попередньо заповненої шприц-ручки СолоСтар® Перед першим використанням шприц-ручку Лантус® СолоСтар® необхідно витримати за кімнатної температури 1-2 години. Перед використанням слід оглянути картридж усередині шприц-ручки. Його слід використовувати тільки у випадку, якщо розчин прозорий, безбарвний, не містить видимих твердих частинок і консистенції нагадує воду. Порожні шприц-ручки СолоСтар® не повинні використовуватися повторно та підлягають знищенню. Для запобігання інфікуванню попередньо заповнена шприц-ручка повинна використовуватися тільки одним пацієнтом і не передаватися іншій особі. Поводження зі шприц-ручкою СолоСтар Перед використанням шприц-ручки СолоСтар® уважно прочитайте інформацію щодо використання. Важлива інформація щодо використання шприц-ручки СолоСтар® Перед кожним використанням необхідно з обережністю приєднати нову голку до шприц-ручки та провести тест на безпеку. Необхідно використовувати лише голки, сумісні із СолоСтар®. Необхідно вживати спеціальні запобіжні заходи, щоб уникнути нещасних випадків, пов'язаних із застосуванням голки, і можливістю перенесення інфекції. У жодному разі не використовуйте шприц-ручку СолоСтар® при її пошкодженні або в тому випадку, якщо Ви не впевнені, що вона працюватиме належним чином. Завжди майте запасну шприц-ручку СолоСтар® на випадок втрати або пошкодження Вашого екземпляра шприц-ручки СолоСтар®. Інструкція зі зберігання Будь ласка, вивчіть розділ "Умови зберігання" щодо правил зберігання шприц-ручки СолоСтар®. Якщо шприц-ручка СолоСтар® зберігається в холодильнику, витягніть її звідти за 1-2 години перед передбачуваною ін'єкцією, щоб розчин прийняв кімнатну температуру. Введення охолодженого інсуліну є болючим. Використана шприц-ручка СолоСтар® повинна бути знищена. Експлуатація Шприц-ручку СолоСтар® необхідно оберігати від пилу та бруду. Зовнішню сторону шприц-ручки СолоСтар можна очищати, протираючи її вологою тканиною. Не занурюйте в рідину, не промивайте та не змащуйте шприц-ручку СолоСтар®, оскільки цим Ви можете її пошкодити. Шприц-ручка СолоСтар® точно дозує інсулін та безпечна у роботі. Вона також потребує дбайливого поводження. Уникайте ситуацій, у яких може статися пошкодження шприц-ручки СолоСтар®. Якщо Ви підозрюєте, що Ваш екземпляр шприц-ручки СолоСтар® був пошкоджений, використовуйте нову шприц-ручку. Стадія 1. Контроль інсуліну Необхідно перевірити етикетку на шприц-ручці СолоСтар®, щоб переконатися, що він містить відповідний інсулін. Для Лантуса® шприц-ручка СолоСтар® сірого кольору з пурпурною кнопкою для введення ін'єкції. Після зняття ковпачка шприца-ручки контролюють зовнішній вигляд інсуліну, що міститься в ній: розчин інсуліну повинен бути прозорий, безбарвний, не містити видимих твердих частинок і за консистенцією нагадувати воду. Стадія 2. Приєднання голки Необхідно використовувати лише голки, сумісні зі шприц-ручкою СолоСтар®. Для кожної наступної ін'єкції завжди застосовують нову стерильну голку. Після видалення ковпачка голку необхідно обережно встановити на шприц-ручці. Стадія 3. Виконання випробувань на безпеку Перед введенням кожної ін'єкції необхідно провести тест на безпеку та переконатися, що шприц-ручка та голка добре працюють та бульбашки повітря видалені. Відміряють дозу, що дорівнює 2 одиницям. Зовнішній та внутрішній ковпачки голки мають бути зняті. Розташовуючи шприц-ручку голкою вгору, обережно постукують по картриджу з інсуліном пальцем таким чином, щоб усі бульбашки повітря попрямували до голки. Повністю натискають кнопку введення ін'єкції. Якщо інсулін з'являється на кінчику голки, це означає, що шприц-ручка та голка працюють правильно. Якщо появи інсуліну на кінчику голки не спостерігається, стадія 3 може бути повторена доти, поки інсулін не з'явиться на кінчику голки. Стадія 4. Вибір дози Дозу можна встановити з точністю до 1 одиниці від мінімальної дози 1 одиниця до максимальної дози 80 одиниць. Якщо необхідно ввести дозу, що перевищує 80 одиниць, слід провести 2 або більше ін'єкцій. Дозувальне вікно має показувати “0” після завершення випробування на безпеку. Після цього може бути встановлена потрібна доза. Стадія 5. Введення дози Пацієнт має бути поінформований про техніку проведення ін'єкції медичним працівником. Голку необхідно ввести під шкіру. Кнопка введення ін'єкції має бути повністю натиснута. Вона утримується в цьому положенні ще 10 секунд до моменту вилучення голки. Таким чином, забезпечується запровадження вибраної дози інсуліну повністю. Стадія 6. Вилучення та викидання голки У всіх випадках голка після кожної ін'єкції має бути видалена та викинута. Цим забезпечується профілактика забруднення та/або внесення інфекції, потрапляння повітря в ємність для інсуліну та витоку інсуліну. При видаленні та викиданні голки повинні бути здійснені спеціальні запобіжні заходи. Дотримуйтесь рекомендованих заходів безпеки для видалення та викидання голок (наприклад, техніка надягання ковпачка однією рукою) для того, щоб зменшити ризик нещасних випадків, пов'язаних із застосуванням голки, а також запобігання інфікуванню. Після видалення голки слід закрити шприц-ручку СолоСтар® ковпачком.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаКапсули - 1 капс. активна речовина: альфа-токоферолу ацетат – 100/200/400 мг; допоміжні речовини: олія соняшникова - 7,5/15/30 мг; оболонка капсули: желатин – 49,38/71,824/112,225 мг; гліцерол 85% - 27,46/39,934/62,397 мг; метил-парагідроксибензоат - 0,049/0,072/0,112 мг; барвник червоний Понсо 4R (E124) - 0,22/0,319/0,499 мг; вода очищена - 32,898/47,851/74,768 мг. Капсули, 100, 200, 400 мг. Капсули 100 мг, 200 мг: по 30 капсул у флаконах темного скла. Капсули 400 мг: по 20 або 30 капсул у флаконах темного скла. Кожен флакон поміщений у картонну пачку.Опис лікарської формиЧервоні овальні капсули заповнені прозорою світло-жовтою олією.Фармакотерапевтична групаВідновлює дефіцит вітаміну E.ФармакокінетикаАбсорбція з дванадцятипалої кишки (необхідна присутність солей жовчних кислот, жирів, нормальне функціонування підшлункової залози) – 20–40%. При підвищенні дози рівень абсорбції знижується. Tmax — 4 год. Депонується у всіх органах та тканинах, особливо у жировій тканині. Проникає через плаценту в недостатній кількості: у кров плода проникає 20-30% від концентрації в крові матері. Проникає у грудне молоко. Екскреція в основному через шлунково-кишковий тракт, з жовчю - понад 90%, менш ніж 6% виділяється нирками у вигляді глюкуронідів та інших метаболітів.ФармакодинамікаБіологічно активні токофероли захищають проміжні сполуки клітинного дихання від окиснення функціональних груп молекул. Активні токофероли здатні окислюватися в семіхінони, які знову відновлюються в організмі до токоферолів. Якщо токофероли є в організмі людини у достатній кількості, вони захищають нестійкі медіатори та метаболіти клітинного дихання від окиснення. У окислювально-відновних процесах лише на рівні клітинного метаболізму у патологічних умовах вони грають буферну роль. Вітамін Е (α-токоферол), найефективніший із токоферолів, в організмі людини діє як клітинний антиоксидант та речовина, що зв'язує вільні радикали кисню. Вітамін Е має антиоксидантну дію, бере участь у біосинтезі гему та білків, проліферації клітин, інших найважливіших процесах тканинного метаболізму, попереджає гемоліз еритроцитів. Необхідний для розвитку та функціонування сполучної тканини, а також для зміцнення стінок кровоносних судин. Є природним антиоксидантом, гальмує перекисне окиснення ліпідів вільними радикалами. Активує фагоцитоз та використовується для підтримки нормальної резистентності до еритроцитів. У великих дозах запобігає агрегації тромбоцитів.РекомендуєтьсяПрофілактика та лікування гіповітамінозу вітаміну Е, в т.ч.: дегенеративні та проліферативні зміни скелетно-м'язової системи, зокрема м'язова дистрофія, аміотрофічний бічний склероз (у складі комплексної терапії); хронічний гепатит (у складі комплексної терапії); стани реконвалесценції після тяжких захворювань, травм, операцій; тяжкі фізичні навантаження; порушення менструального циклу (у складі комплексної терапії при гормональному лікуванні порушень менструального циклу).Протипоказання до застосування- підвищена чутливість до компонентів препарату; гострий інфаркт міокарда; дитячий вік. З обережністю: У хворих на важкий кардіосклероз, перенесений інфарктом міокарда, при підвищеному ризику розвитку тромбоемболій; гіпотромбінемія, спричинена недостатністю вітаміну К, може погіршитися при застосуванні вітаміну Е в дозі понад 400 ME (1 мг – 1,21 ME).Вагітність та лактаціяУ період вагітності та грудного вигодовування прийом препарату лише за рекомендацією лікаря.Побічна діяЗазвичай при застосуванні рекомендованих доз побічні ефекти не спостерігаються. З боку імунної системи: Алергічні реакції. З боку шлунково-кишкового тракту: діарея, нудота, гастралгія. З боку обміну речовин та харчування: гіперкреатинінурія, підвищення активності КФК, підвищення концентрації холестерину у сироватці крові. З боку судин: тромбофлебіти, тромбоемболія легеневої артерії.Взаємодія з лікарськими засобамиПосилює ефект кортикостероїдів, НПЗЗ, серцевих глікозидів. Підвищує ефективність протиепілептичних засобів у хворих на епілепсію (у яких підвищено вміст у крові продуктів перекисного окиснення ліпідів). Високі дози заліза посилюють окисні процеси в організмі, що підвищує потребу у вітаміні Е. Одночасне застосування вітаміну Е в дозі більше 400 ME/сут з антикоагулянтами (похідними кумарину та індандіону) підвищує ризик розвитку гіпопротромбінемії та кровотеч. Вітамін Е посилює дію антикоагулянтів, якщо дози перевищують 400 МО/добу. Не рекомендується одночасний прийом інших вітамінних комплексів, що містять вітамін Е, щоб уникнути передозування. Призначення вітаміну Е у високих дозах може спричинити дефіцит вітаміну А в організмі. Колестирамін, колестипол, мінеральні олії знижують всмоктування вітаміну Е.Спосіб застосування та дозиВсередину. Препарат призначений лише для прийому дорослими пацієнтами. Лікування гіповітамінозу вітаміну Е - капс. по 100 мг 1 раз на добу до усунення симптомів гіповітамінозу. Гіповітаміноз Е, що супроводжується дегенеративними та проліферативними змінами скелетно-м'язової системи, зокрема м'язовою дистрофією, аміотрофічним боковим склерозом (у складі комплексної терапії) – капс. по 100 мг 1 раз на день протягом 1-2 місяців. Гіповітаміноз Е, що супроводжується хронічним гепатитом (у складі комплексної терапії) – капс. по 100 мг 1 раз на день. Гіповітаміноз Е при станах реконвалесценції після тяжких захворювань, травм, операцій – капс. по 100 мг 1 раз на добу протягом 1-2 тижнів. Гіповітаміноз Е при підвищених фізичних навантаженнях – капс. по 100 мг 1 раз на день під час підвищених фізичних навантажень. Гіповітаміноз Е, що супроводжується порушеннями менструального циклу (у складі комплексної терапії при гормональному лікуванні порушень менструального циклу) – капс. по 300-400 мг через день послідовно, починаючи з 17-го дня циклу до останнього дня циклу (день перед першим днем менструації).ПередозуванняСимптоми: високі дози вітаміну Е (400-800 мг на добу протягом тривалого часу) можуть викликати порушення зору, діарею, запаморочення, головний біль, нудоту, сильну стомлюваність, непритомність, зростання білого волосся на ділянках алопеції при бульозному епідермолізі. Дуже високі дози (що перевищують 800 мг протягом тривалого часу) можуть викликати кровотечу у пацієнтів із недостатністю вітаміну К; вони можуть порушити метаболізм гормонів щитовидної залози та збільшити ризик тромбофлебітів та тромбоемболій у чутливих пацієнтів. Лікування: симптоматичне, відміна препарату, призначення кортикостероїдів.Запобіжні заходи та особливі вказівкиПри вродженому бульозному епідермолізі в місцях, уражених алопецією, може почати рости біле волосся. Нестача вітаміну К в організмі, що викликає гіпопротромбінемію, може збільшуватися при застосуванні високих доз вітаміну Е (більше 400 МО/сут). Вітамін Е посилює дію антикоагулянтів, якщо дози перевищують 400 МО/добу. Щоб уникнути його передозування, не рекомендується одночасний прийом інших вітамінних комплексів, що містять вітамін Е. Вплив на здатність керувати транспортними засобами чи механізмами. Прийом препарату Вітамін Е Зентіва, капсули не впливає на здатність людини керувати транспортними засобами чи механізмами.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему