Все товары
Склад, форма випуску та упаковкаТаблетки - 1 таб.: ментол 4 мг, олія евкаліптова 500 мкг. 10 шт. - Упаковки коміркові контурні.Фармакотерапевтична групаКомбінований препарат. Ментол - місцевоподразнюючий засіб, ефект якого в основному обумовлений рефлекторними реакціями, пов'язаними з подразненням чутливих слизових оболонок рецепторів. Має легку місцевоанестезуючу ("відволікаючу") дію, має слабкі антисептичні властивості. Евкаліптова олія має стимулюючу дію на рецептори слизових оболонок і чинить протизапальну та протимікробну дію.Клінічна фармакологіяФітопрепарат з протимікробною та протизапальною дією для місцевого застосування у ЛОР-практиці та стоматології.Показання до застосуванняЗапальні захворювання верхніх відділів дихальних шляхів (тонзиліт, ларингіт, фарингіт, трахеїт); кашель; риніт (гострий та хронічний).Протипоказання до застосуванняПідвищена чутливість до компонентів препарату.Побічна діяМожливі алергічні реакції.Спосіб застосування та дозиТаблетку слід тримати у роті до повного розсмоктування.Умови зберіганняУ прохолодному місці +8+15 градусУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаВода очищена, гліцерин, екстракт кори дуба, екстракт звіробою, екстракт волоського горіха, калію йодид.ХарактеристикаСпрей з характерним смаком та запахом м'яти та евкаліпту. Невеликий розмір часток, що утворюються при розпиленні спрею, обумовлює високий рівень їх проникнення в складки, кишені, порожнини та інші важкодоступні місця на слизових оболонках рота. Флакон герметично закритий. Засіб не забруднюється ззовні, не висихає та захищено від вологи. Компактність упаковки дозволяє носити спрей із собою постійно. Дозатор-розпилювач забезпечує точне нанесення та дозування.Властивості компонентівЕвкаліптова олія пригнічує канцерогенні оральні бактерії на кшталт Streptococcus mutans та Streptococcus sobrinus. Евкаліптова олія має яскраво виражений хвойний, терпкий і холодний аромат. Основними компонентами складу евкаліптової олії є: Цинеол – це головний активний компонент, він має яскраво виражену антисептичну та протизапальну дію. Дубильні речовини - характеризуються особливим терпким смаком. Дубильні речовини при взаємодії з білками, викликають їх часткове згортання, і створюють водонепроникну захисну альбумінатну плівку (дублення), на чому заснована їхня бактерицидна та протизапальна дія на слизових оболонках. Масло м'яти перцевої надзвичайно ефективний засіб проти анаеробних бактерій, що існують у середовищі з низьким вмістом кисню (наприклад, у ротовій порожнині), та здатних викликати захворювання ясен. За рахунок високого вмісту ментолу олія м'яти ефективно бореться з неприємним запахом із рота. Лівоментол. Ментол має слабкі місцевоанестезуючі властивості, стимулює холодові рецептори шкіри та слизових, є слабким антисептиком. Охолодна дія ментолу на шкірні рецептори дозволяє знизити подразнення та свербіння.ІнструкціяУ вигляді зрошення 2-3 і більше разів на добу, після їди або в проміжках між їдою. Перед використанням зніміть з флакона захисний ковпачок. Натиснути 2-3 рази для того, щоб розчин надійшов у розпилювач і виділився у вигляді стабільного струменя, спрямовуючи розпилювач у різні боки. Після нанесення спрею на слизову оболонку бажано не ковтати слину якомога довше. При обробці слизових оболонок порожнини рота необхідно утримувати препарат у роті не менше 3-х хвилин.Протипоказання до застосуванняІндивідуальна нестерпність компонентів, гіперчутливість.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаВода очищена (water), камфора (camphor), олія рослинна (vegetable oil).ХарактеристикаКамфорне розтирання PELLESANA, м'яко розігріваючи та покращуючи кровообіг, допоможе впоратися з больовим синдромом, зменшити запалення та прискорити регенерацію.ІнструкціяНаносити на проблемні ділянки тіла. Збагачення косметичних засобів – 3-6 крапель на флакон.Протипоказання до застосуванняІндивідуальна нестерпність компонентів продукту.Умови відпустки з аптекБез рецептаВідео на цю тему
19 523,00 грн
19 490,00 грн
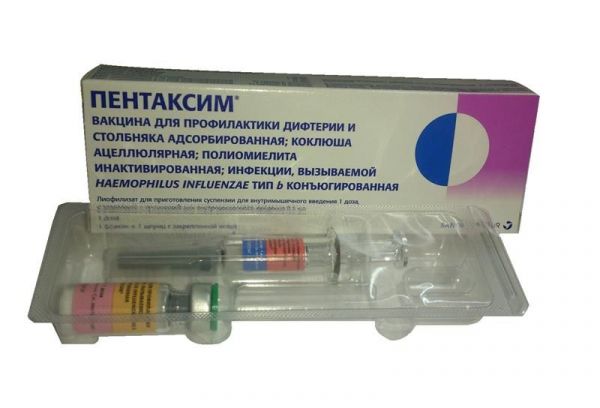
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
4 090,00 грн
4 059,00 грн
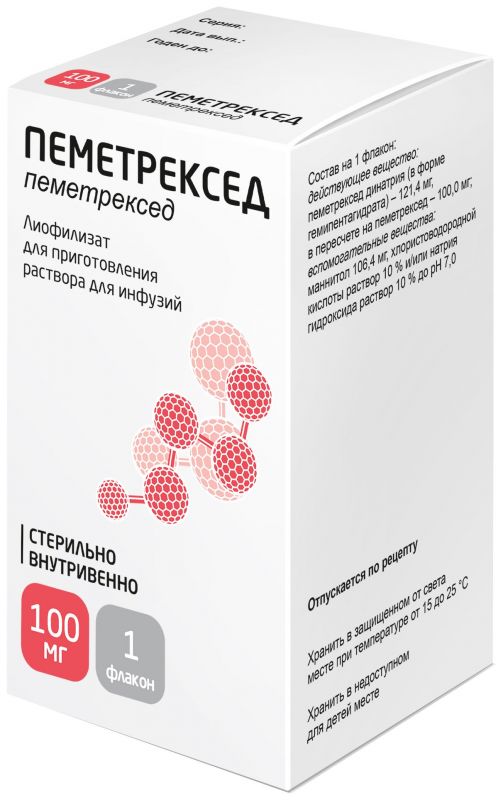
Склад, форма випуску та упаковкаЛіофілізат - 1 фл. Активна речовина: пеметрекседу динатрію геміпентагідрат 121.4 мг, що відповідає вмісту пеметрекседу 100 мг. Допоміжні речовини: манітол - 106.4 мг, хлористоводнева кислота або натрію гідроксид (10% розчин, для підтримки рівня pH) - до pH 7.0. 100 мг – Флакони безбарвного скла (тип I) (1) – пачки картонні.Опис лікарської формиЛіофілізат для приготування розчину для інфузії у вигляді пористої маси від білого до білого з жовтуватим відтінком кольору.Фармакотерапевтична групаПротипухлинний засіб, антиметаболіт. Є антифолатом, інгібує тимідилат-синтетазу (TC), дигідрофолат-редуктазу (ДГФР), гліцинамід-рибонуклеотид-формілтрансферазу (ГАРФТ) – ключові фолат-залежні ферменти при біосинтезі тимідинових та пуринових нуклеотів. Пеметрексед надходить у клітини за допомогою переносника відновлених фолатів та білкових фолат-зв'язувальних транспортних систем. Вступаючи в клітину, пеметрексед швидко і ефективно перетворюється на поліглутаматні форми за допомогою ферменту фоліл-поліглутамат-синтетази. Поліглутаматні форми затримуються в клітинах і є потужнішими інгібіторами ТС, ГАРФТ. Поліглутамація - це процес, залежний від часу та концентрації, який зустрічається в пухлинних клітинах і, меншою мірою, у нормальних тканинах. У поліглутамованих метаболітів збільшений T1/2,внаслідок цього збільшується тривалість дії препарату на пухлинні клітини. При комбінованому застосуванні пеметрекседу та цисплатину у дослідженнях in vitro спостерігався синергізм протипухлинної дії.ФармакокінетикаУ рівноважному стані Vd пеметрекседу складає 16.1 л. Зв'язування із білками плазми – близько 81%. Пеметрексед обмежено піддається метаболізму печінки. У перші 24 години після введення 70-90% виводиться нирками в незміненому вигляді. Загальний плазмовий кліренс пеметрекседу становить 92 мл/хв, T1/2 із плазми становить 3.5 год у пацієнтів з нормальною функцією нирок. При нирковій недостатності тяжкого ступеня зв'язування з білками плазми не змінюється.Клінічна фармакологіяПротипухлинний препарат. Антиметаболіт.Показання до застосуванняМісцево-поширений або метастатичний неклітинний (несквамозний), недрібноклітинний рак легені - у комбінації з цисплатином як перша лінія терапії. Місцево-поширений або метастатичний неклітинний (несквамозний), недрібноклітинний рак легені без прогресування захворювання після чотирьох циклів першої лінії хіміотерапії на основі препаратів платини - для підтримуючої терапії. Місцево-поширений або метастатичний, неплоскоклітинний, недрібноклітинний рак легені - як монотерапія для терапії другої лінії. Лікування злоякісної мезотеліоми плеври у пацієнтів, які раніше не отримували хіміотерапію, з неоперабельною пухлиною або за наявності протипоказань до хірургічної операції.Протипоказання до застосуванняВагітність, лактація, підвищена чутливість до пеметрекседу. Пеметрексед не призначений для терапії пацієнтів з плоскоклітинним недрібноклітинним раком легені.Вагітність та лактаціяЗастосування при вагітності та в період лактації (грудного вигодовування) протипоказане. Застосування у дітей Пеметрексед не рекомендується використовувати у педіатрії, т.к. безпека та ефективність застосування у дітей не встановлена.Побічна діяЗ боку системи кровотворення: дуже часто – лейкопенія, нейтропенія, анемія; часто – тромбоцитопенія. З боку травної системи: дуже часто – нудота, блювання, анорексія, стоматит/фарингіт, діарея, підвищення рівня АЛТ та АСТ; часто – запори, біль у животі. Дерматологічні реакції: дуже часто - висипання/лущення; часто - свербіж шкіри, алопеція; рідко – багатоформна еритема. З боку периферичної нервової системи: часто – сенсорна чи моторна невропатія. З боку сечовидільної системи: часто – підвищення рівня креатиніну. З боку серцево-судинної системи: рідко – суправентрикулярна тахікардія. Інші: дуже часто – підвищена стомлюваність; часто - гарячка, фебрильна нейтропенія, алергічні реакції та приєднання вторинних інфекцій без нейтропенії.Взаємодія з лікарськими засобамиСпільне застосування з нефротоксичними препаратами та/або нирковими речовинами може знизити кліренс пеметрекседу. Результати досліджень in vitro свідчать, що пеметрексед мінімально взаємодіє з препаратами, які метаболізуються CYP3A, CYP2D6, CYP2C9, CYP1A2. Фармакокінетика пеметрекседу не змінюється при застосуванні фолієвої кислоти внутрішньо, вітаміну В12 в/м та при комбінованому застосуванні з цисплатином. Загальний кліренс платини не порушується під час застосування пеметрекседу. Пеметрексед можна застосовувати разом з ібупрофеном (по 400 мг 4 рази на добу) у хворих з нормальною функцією нирок (КК 80 мл/хв). При призначенні ібупрофену разом з пеметрекседом у хворих з нирковою недостатністю легкого або середнього ступеня тяжкості (КК 45-79 мл/хв) необхідно бути обережним. У пацієнтів з нирковою недостатністю легкого та середнього ступеня тяжкості не рекомендується застосування НПЗЗ з коротким T1/2 протягом 2 днів перед застосуванням пеметрекседу, в день застосування та протягом 2 днів після застосування. Зважаючи на відсутність даних про можливу взаємодію між пеметрекседом і НПЗЗ з великим T1/2, усі пацієнти, які отримують НПЗЗ, повинні перервати їх застосування мінімум за 5 днів до прийому пеметрекседу, в день прийому та протягом 2 днів після прийому. Якщо потрібне спільне призначення НПЗЗ, пацієнтам потрібен суворий моніторинг токсичності, особливо мієлосупресії та токсичності з боку шлунково-кишкового тракту. Пеметрексед несумісний із розчином Рінгера лактату та розчином Рінгера. Спільне застосування пеметрекседу з іншими препаратами та розчинами не досліджено і тому не рекомендується.Спосіб застосування та дозиВводять внутрішньовенно у вигляді інфузії. Режим дозування індивідуальний, залежно від показань, схеми лікування, функції печінки.Запобіжні заходи та особливі вказівкиПеред кожним введенням пеметрекседу необхідно проводити загальний аналіз крові з підрахунком лейкоцитарної формули та кількості тромбоцитів. Для оцінки функції нирок та печінки необхідно періодично проводити біохімічний аналіз крові. Перед початком застосування абсолютна кількість нейтрофілів становитиме ≥1500/мкл, тромбоцитів ≥100 000/мкл. Призначення фолієвої кислоти та вітаміну В12 знижує токсичність пеметрекседу та необхідність зменшення дози при гематологічній та негематологічній токсичності 3-4 ступеня, в т.ч. нейтропенії, фебрильної нейтропенії та інфекції з нейтропенією 3-4 ступеня. Хворим з клінічними проявами асциту та плевриту необхідно дренування випоту перед початком застосування пеметрекседу, тому що вплив цих станів на дію пеметрекседу не відомий. Пеметрексед не рекомендується використовувати у педіатрії, т.к. безпека та ефективність застосування у дітей не встановлена.Умови відпустки з аптекЗа рецептомВідео на цю тему
15 422,00 грн
15 378,00 грн
Склад, форма випуску та упаковкаЛіофілізат - 1 фл. Активна речовина: пеметрекседу динатрію геміпентагідрат 121.4 мг, що відповідає вмісту пеметрекседу 100 мг. Допоміжні речовини: манітол - 106.4 мг, хлористоводнева кислота або натрію гідроксид (10% розчин, для підтримки рівня pH) - до pH 7.0. 500 мг - Флакони безбарвного скла (тип I) (1) - пачки картонні.Опис лікарської формиЛіофілізат для приготування розчину для інфузії у вигляді пористої маси від білого до білого з жовтуватим відтінком кольору.Фармакотерапевтична групаПротипухлинний засіб, антиметаболіт. Є антифолатом, інгібує тимідилат-синтетазу (TC), дигідрофолат-редуктазу (ДГФР), гліцинамід-рибонуклеотид-формілтрансферазу (ГАРФТ) – ключові фолат-залежні ферменти при біосинтезі тимідинових та пуринових нуклеотів. Пеметрексед надходить у клітини за допомогою переносника відновлених фолатів та білкових фолат-зв'язувальних транспортних систем. Вступаючи в клітину, пеметрексед швидко і ефективно перетворюється на поліглутаматні форми за допомогою ферменту фоліл-поліглутамат-синтетази. Поліглутаматні форми затримуються в клітинах і є потужнішими інгібіторами ТС, ГАРФТ. Поліглутамація - це процес, залежний від часу та концентрації, який зустрічається в пухлинних клітинах і, меншою мірою, у нормальних тканинах. У поліглутамованих метаболітів збільшений T1/2,внаслідок цього збільшується тривалість дії препарату на пухлинні клітини. При комбінованому застосуванні пеметрекседу та цисплатину у дослідженнях in vitro спостерігався синергізм протипухлинної дії.ФармакокінетикаУ рівноважному стані Vd пеметрекседу складає 16.1 л. Зв'язування із білками плазми – близько 81%. Пеметрексед обмежено піддається метаболізму печінки. У перші 24 години після введення 70-90% виводиться нирками в незміненому вигляді. Загальний плазмовий кліренс пеметрекседу становить 92 мл/хв, T1/2 із плазми становить 3.5 год у пацієнтів з нормальною функцією нирок. При нирковій недостатності тяжкого ступеня зв'язування з білками плазми не змінюється.Клінічна фармакологіяПротипухлинний препарат. Антиметаболіт.Показання до застосуванняМісцево-поширений або метастатичний неклітинний (несквамозний), недрібноклітинний рак легені - у комбінації з цисплатином як перша лінія терапії. Місцево-поширений або метастатичний неклітинний (несквамозний), недрібноклітинний рак легені без прогресування захворювання після чотирьох циклів першої лінії хіміотерапії на основі препаратів платини - для підтримуючої терапії. Місцево-поширений або метастатичний, неплоскоклітинний, недрібноклітинний рак легені - як монотерапія для терапії другої лінії. Лікування злоякісної мезотеліоми плеври у пацієнтів, які раніше не отримували хіміотерапію, з неоперабельною пухлиною або за наявності протипоказань до хірургічної операції.Протипоказання до застосуванняВагітність, лактація, підвищена чутливість до пеметрекседу. Пеметрексед не призначений для терапії пацієнтів з плоскоклітинним недрібноклітинним раком легені.Вагітність та лактаціяЗастосування при вагітності та в період лактації (грудного вигодовування) протипоказане. Застосування у дітей Пеметрексед не рекомендується використовувати у педіатрії, т.к. безпека та ефективність застосування у дітей не встановлена.Побічна діяЗ боку системи кровотворення: дуже часто – лейкопенія, нейтропенія, анемія; часто – тромбоцитопенія. З боку травної системи: дуже часто – нудота, блювання, анорексія, стоматит/фарингіт, діарея, підвищення рівня АЛТ та АСТ; часто – запори, біль у животі. Дерматологічні реакції: дуже часто - висипання/лущення; часто - свербіж шкіри, алопеція; рідко – багатоформна еритема. З боку периферичної нервової системи: часто – сенсорна чи моторна невропатія. З боку сечовидільної системи: часто – підвищення рівня креатиніну. З боку серцево-судинної системи: рідко – суправентрикулярна тахікардія. Інші: дуже часто – підвищена стомлюваність; часто - гарячка, фебрильна нейтропенія, алергічні реакції та приєднання вторинних інфекцій без нейтропенії.Взаємодія з лікарськими засобамиСпільне застосування з нефротоксичними препаратами та/або нирковими речовинами може знизити кліренс пеметрекседу. Результати досліджень in vitro свідчать, що пеметрексед мінімально взаємодіє з препаратами, які метаболізуються CYP3A, CYP2D6, CYP2C9, CYP1A2. Фармакокінетика пеметрекседу не змінюється при застосуванні фолієвої кислоти внутрішньо, вітаміну В12 в/м та при комбінованому застосуванні з цисплатином. Загальний кліренс платини не порушується під час застосування пеметрекседу. Пеметрексед можна застосовувати разом з ібупрофеном (по 400 мг 4 рази на добу) у хворих з нормальною функцією нирок (КК 80 мл/хв). При призначенні ібупрофену разом з пеметрекседом у хворих з нирковою недостатністю легкого або середнього ступеня тяжкості (КК 45-79 мл/хв) необхідно бути обережним. У пацієнтів з нирковою недостатністю легкого та середнього ступеня тяжкості не рекомендується застосування НПЗЗ з коротким T1/2 протягом 2 днів перед застосуванням пеметрекседу, в день застосування та протягом 2 днів після застосування. Зважаючи на відсутність даних про можливу взаємодію між пеметрекседом і НПЗЗ з великим T1/2, усі пацієнти, які отримують НПЗЗ, повинні перервати їх застосування мінімум за 5 днів до прийому пеметрекседу, в день прийому та протягом 2 днів після прийому. Якщо потрібне спільне призначення НПЗЗ, пацієнтам потрібен суворий моніторинг токсичності, особливо мієлосупресії та токсичності з боку шлунково-кишкового тракту. Пеметрексед несумісний із розчином Рінгера лактату та розчином Рінгера. Спільне застосування пеметрекседу з іншими препаратами та розчинами не досліджено і тому не рекомендується.Спосіб застосування та дозиВводять внутрішньовенно у вигляді інфузії. Режим дозування індивідуальний, залежно від показань, схеми лікування, функції печінки.Запобіжні заходи та особливі вказівкиПеред кожним введенням пеметрекседу необхідно проводити загальний аналіз крові з підрахунком лейкоцитарної формули та кількості тромбоцитів. Для оцінки функції нирок та печінки необхідно періодично проводити біохімічний аналіз крові. Перед початком застосування абсолютна кількість нейтрофілів становитиме ≥1500/мкл, тромбоцитів ≥100 000/мкл. Призначення фолієвої кислоти та вітаміну В12 знижує токсичність пеметрекседу та необхідність зменшення дози при гематологічній та негематологічній токсичності 3-4 ступеня, в т.ч. нейтропенії, фебрильної нейтропенії та інфекції з нейтропенією 3-4 ступеня. Хворим з клінічними проявами асциту та плевриту необхідно дренування випоту перед початком застосування пеметрекседу, тому що вплив цих станів на дію пеметрекседу не відомий. Пеметрексед не рекомендується використовувати у педіатрії, т.к. безпека та ефективність застосування у дітей не встановлена.Умови відпустки з аптекЗа рецептомВідео на цю тему
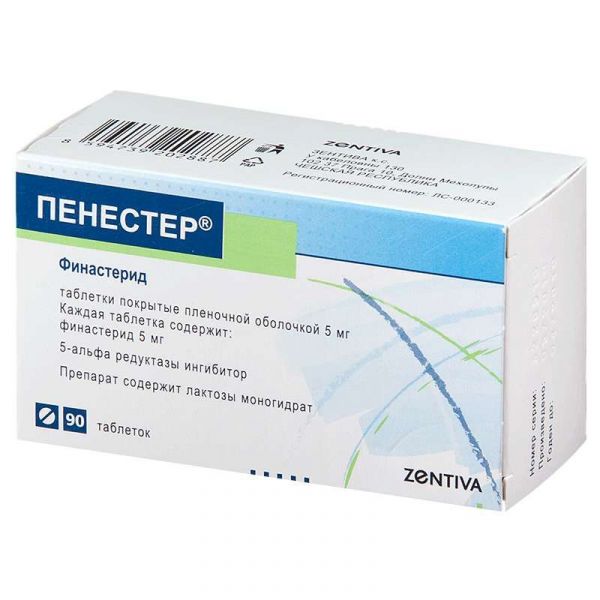
Склад, форма випуску та упаковкаПігулки - 1 таб. Активні речовини: фінастерид – 5 мг; Допоміжні речовини: лактози моногідрат, крохмаль кукурудзяний, повідон K30, карбоксиметилкрохмаль натрію (тип А), докузат натрію, магнію стеарат. Склад плівкової оболонки: гіпромелоза 2910/5, макрогол 6000, тальк, титану діоксид, емульсія симетикону SE4, барвник заліза оксид жовтий. По 10 або 15 таблеток у блістері з ПВХ/ПВДХ/Аl. По 3 або 6 блістерів (10 таблеток) або по 2, 4 або 6 блістерів (по 15 таблеток) у картонній пачці разом з інструкцією із застосування.Опис лікарської формиКруглі, двоопуклі таблетки світло-жовтого кольору, покриті плівковою оболонкою.Фармакотерапевтична групаПрепарат для лікування доброякісної гіперплазії передміхурової залози. Інгібітор 5α-редуктази.ФармакокінетикаВсмоктування Cmax фінастериду в плазмі досягається приблизно через 2 години після прийому внутрішньо. Абсорбція фінастериду із шлунково-кишкового тракту завершується через 6-8 годин після прийому внутрішньо. Біодоступність фінастериду при вживанні становить приблизно 80% від внутрішньовенної референсної дози і не залежить від їди. Розподіл Зв'язування з білками плазми становить приблизно 93%. Плазмовий кліренс становить близько 165 мл/хв, що здається Vd - 76 л. При тривалій терапії спостерігається повільне накопичення фінастериду у невеликих кількостях. При щоденному прийомі фінастериду внутрішньо в дозі 5 мг його мінімальна Css у плазмі досягає 8-10 нг/мл і з часом залишається стабільною. У пацієнтів, які отримували препарат протягом 7-10 днів, фінастерид виявлявся у спинномозковій рідині. При прийомі препарату в дозі 5 мг/добу фінастерид у незначних кількостях виявляється у насінній рідині. Метаболізм та виведення T1/2 фінастериду в середньому дорівнює 6 годин. У чоловіків після одноразового прийому внутрішньо дози фінастериду, міченого 14С, 39% прийнятої дози виводиться нирками у вигляді метаболітів (незмінений фінастерид практично не виводиться нирками); 57% – через кишечник. У цьому дослідженні були ідентифіковані 2 метаболіти фінастериду, які мають незначну інгібуючу дію щодо 5α-редуктази порівняно з фінастеридом. Фармакокінетика в особливих клінічних випадках У літньому віці швидкість виведення фінастериду дещо знижується. З віком T1/2 збільшується: у чоловіків 18-60 років середній T1/2 становить 6 год, а у чоловіків старше 70 років - 8 год. потрібно. У пацієнтів з хронічною нирковою недостатністю (КК від 9 до 55 мл/хв) розподіл міченого 14С фінастериду при прийомі одноразової дози не відрізнявся від такого у здорових добровольців. Зв'язування фінастериду з білками плазми також не відрізнялося у пацієнтів з порушенням функції нирок. При нирковій недостатності частина метаболітів фінастериду, яка нормується екскретується нирками, виводиться через кишечник. Це проявляється збільшенням кількості метаболітів фінастериду в калі при відповідному зниженні їхньої концентрації в сечі. У пацієнтів з нирковою недостатністю, які не потребують гемодіалізу, корекція дози фінастериду не потрібна.ФармакодинамікаФінастерид - синтетична 4-азастероїдна сполука. Є специфічним конкурентним інгібітором 5α-редуктази II типу – внутрішньоклітинного ферменту, який перетворює тестостерон на активний андроген – дигідротестостерон (ДГТ). При доброякісній гіперплазії передміхурової залози (ДГПЗ) її збільшення залежить від перетворення тестостерону на ДГТ у простаті. Фінастерид високоефективно знижує концентрацію ДГТ як у плазмі, так і в тканині передміхурової залози. Пригнічення утворення ДГТ супроводжується зменшенням розмірів передміхурової залози, збільшенням максимальної швидкості сечовипускання та зниженням вираженості симптомів, пов'язаних із гіперплазією передміхурової залози. Фінастерид не має спорідненості з рецепторами андрогенів. Згідно з результатами клінічного дослідження (PLESS), в якому брали участь пацієнти з помірно або значно вираженими симптомами ДГПЗ та збільшенням передміхурової залози, финастерид знижував частоту виникнення гострої затримки сечі з 7/100 до 3/100 за 4-річний період, а частоту потреби у хірургічному. втручання (трансуретральної резекції простати (ТУРП) або простатектомії) - з 10/100 до 5/100. Ці зміни також асоціювалися з покращенням симптоматики ДГПЗ (зниження на 2 пункти за шкалою симптомів quasi-AUA), стійким зменшенням об'єму передміхурової залози приблизно на 20% та стабільним збільшенням швидкості струму сечі. Дослідження MTOPS (Medical Therapy Of Prostate Symptoms) тривалістю від 4 до 6 років, в рамках якого 3047 чоловіків із симптомами ДГПЗ були рандомізовані на групи, які отримують: фінастерид у дозі 5 мг на добу; доксазозин у дозі 4 мг на добу або 8 мг на добу; комбінацію фінастериду в дозі 5 мг на добу та доксазозину в дозі 4 мг на добу або 8 мг на добу; чи плацебо. Лікування призводило до значного зниження ризику клінічного прогресування ДГПЗ, яке на фоні застосування фінастериду становило 34% (р=0.002), доксазозину – 39% (рПоказання до застосуванняЛікування ДГПЗ та профілактика урологічних ускладнень з метою: зниження ризику гострої затримки сечі; зниження ризику необхідності проведення хірургічних втручань, зокрема. трансуретральної резекції (ТУР) передміхурової залози та простатектомії; Лікування з метою зменшення розмірів збільшеної передміхурової залози, поліпшення сечовипускання та зменшення вираженості симптомів, пов'язаних із ДГПЗ; У поєднанні з доксазозином зниження ризику прогресування симптомів, що з ДГПЖ.Протипоказання до застосуванняспадкова непереносимість лактози, дефіцит лактази або порушення всмоктування глюкози/галактози; вагітність та застосування препарату у жінок із збереженим репродуктивним потенціалом; вік до 18 років; підвищена чутливість до фінастериду та/або інших компонентів препарату. З обережністю слід призначати препарат пацієнтам з великим обсягом залишкової сечі та/або суттєво зниженою швидкістю сечовипускання (пацієнти повинні регулярно спостерігатися лікарем щодо виявлення обструктивної уропатії), пацієнтам з печінковою недостатністю, а також пацієнтам похилого віку.Вагітність та лактаціяЗастосування препарату Пенестер протипоказане при вагітності та жінкам із збереженим репродуктивним потенціалом. У зв'язку зі здатністю інгібіторів 5α-редуктази II типу пригнічувати перетворення тестостерону на дигідротестостерон, дані засоби, в т.ч. Фінастерид, при застосуванні у вагітних можуть викликати аномалії розвитку зовнішніх статевих органів у плода чоловічої статі. Фінастерид не показаний для застосування у жінок. Даних про екскрецію фінастериду із грудним молоком немає. Невеликі кількості фінастериду були виявлені у спермі пацієнтів, які отримували фінастерид у дозі 5 мг на добу. Хоча клінічні дані щодо впливу фінастериду на плід чоловічої статі відсутні, жінкам із збереженим репродуктивним потенціалом слід уникати контакту з насіннєвою рідиною чоловіків, які приймають фінастерид. Жінкам із збереженим репродуктивним потенціалом та вагітним слід уникати контакту з пошкодженими пігулками фінастериду, т.к. здатність препарату пригнічувати перетворення тестостерону на ДГТ може спричинити порушення розвитку статевих органів у плода чоловічої статі. Протипоказаний у віці до 18 років.Побічна діяНебажані реакції, виявлені під час клінічних досліджень (дослідження PLESS) Побічні реакції розділені за системно-органними класами відповідно до класифікації MedDRA. Частота побічних реакцій визначалася відповідно до наступної градації (класифікація ВООЗ): дуже часто (більше 1/10); часто (від понад 1/100 до менше 1/10); нечасто (від понад 1/1000 до 1/100); рідко (від понад 1/10000 до менше 1/1000); дуже рідко (від 1/10 000, включаючи окремі повідомлення). Порушення психіки: часто – зниження лібідо. З боку шкіри та підшкірних тканин: нечасто – шкірний висип. З боку статевих органів та молочної залози: часто – порушення сексуальної функції; нечасто – порушення еякуляції, зменшення обсягу еякуляту, збільшення грудних залоз, болючість у ділянці грудних залоз. В рамках дослідження MTOPS порівнювалося застосування фінастериду в дозі 5 мг/добу (n=768), доксазозину в дозі 4 мг/добу або 8 мг/добу (n=756), комбінованої терапії фінастеридом у дозі 5 мг/добу та доксазозином у дозі. 4 або 8 мг/добу (n=786), та плацебо (n=737). Відповідно до результатів даного дослідження профіль безпеки та переносимості комбінованої терапії загалом збігався з профілем її окремих компонентів. Частота порушень еякуляції у пацієнтів, які отримують комбіновану терапію, була сумісною із сумою частоти виникнення даного небажаного явища на тлі двох видів монотерапії. Було проведено 7-річне плацебо-контрольоване дослідження РСРТ, у якому брали участь 18 882 здорові чоловіки. Доступні для аналізу дані пункційної біопсії передміхурової залози були отримані щодо 9060 суб'єктів, при цьому рак передміхурової залози був виявлений у 803 (18.4%) чоловіків, які отримували фінастерид у добовій дозі 5 мг, і у 1147 (24.4%) чоловіків, що отримували плац. Згідно з результатами пункційної біопсії рак передміхурової залози з баловим показником 710 за шкалою Глісона був діагностований у 280 (6.4%) чоловіків з групи, які отримували фінастерид у добовій дозі 5 мг, у той час як у групі плацебо рак з таким ступенем диференціювання 5.1%) пацієнтів. Результати додаткового аналізу свідчили, що збільшення поширеності низькодиференційованого раку передміхурової залози,те, що спостерігалося в групі пацієнтів, які отримували фінастерид у добовій дозі 5 мг, може бути пояснено системною помилкою при оцінці результатів, пов'язаних із впливом терапії фінастеридом у дозі 5 мг 1 раз на добу на об'єм передміхурової залози. Із загальної кількості випадків раку передміхурової залози, діагностованих у цьому дослідженні, на момент постановки діагнозу приблизно 98% випадків було віднесено до локалізованого раку (клінічна стадія T1 або T2). Клінічна значимість даних про пухлинний процес зі ступенем диференціювання 7-10 балів за шкалою Глісон невідома.діагностованих у цьому дослідженні, на момент постановки діагнозу приблизно 98% випадків було віднесено до локалізованого раку (клінічна стадія T1 або T2). Клінічна значимість даних про пухлинний процес зі ступенем диференціювання 7-10 балів за шкалою Глісон невідома.діагностованих у цьому дослідженні, на момент постановки діагнозу приблизно 98% випадків було віднесено до локалізованого раку (клінічна стадія T1 або T2). Клінічна значимість даних про пухлинний процес зі ступенем диференціювання 7-10 балів за шкалою Глісон невідома. Відомості, отримані на підставі післяреєстраційного досвіду застосування препарату Частота небажаних реакцій невідома, т.к. на підставі отриманих даних встановити частоту та причинно-наслідковий зв'язок з дією фінастериду не завжди можливо, оскільки повідомлення про дані реакції надходили добровільно по популяції невідомого розміру. З боку імунної системи: частота невідома – реакції гіперчутливості, в т.ч. шкірний свербіж, кропив'янка, ангіоневротичний набряк (включаючи набряк губ, обличчя та гортані). З боку печінки та жовчовивідних шляхів: частота невідома – підвищення активності печінкових трансаміназ. З боку серцево-судинної системи: частота невідома – відчуття серцебиття. Порушення психіки: частота невідома – депресія, зниження лібідо, яке зберігається після припинення терапії. З боку статевих органів та молочної залози: частота невідома – сексуальна дисфункція (еректильна дисфункція та порушення еякуляції), яка зберігається після припинення лікування, болючість яєчок, чоловіче безпліддя та/або зниження якості насіннєвої рідини. Після відміни фінастериду якість насіннєвої рідини приходила до норми або покращувалася. Лабораторні показники При оцінці результатів лабораторних досліджень необхідно враховувати, що у пацієнтів, які отримують лікування фінастеридом, вміст ПСА у плазмі знижується. Більшість пацієнтів протягом перших місяців терапії відзначається швидке зниження показника ПСА з його наступною стабілізацією. Вихідне значення ПСА, що встановлюється після проведення терапії финастеридом, становить приблизно половину відповідного показника, що відзначалося на початок лікування. Таким чином, у пацієнтів, які отримують лікування фінастеридом протягом 6 місяців або більше, значення ПСА слід подвоювати порівняно з нормальними значеннями чоловіків, які не отримували лікування. Інших відмінностей у значеннях стандартних лабораторних показників між групами пацієнтів, які отримували фінастерид та плацебо, не спостерігалося.Взаємодія з лікарськими засобамиКлінічно значущої взаємодії коїться з іншими препаратами виявлено був. Фінастерид метаболізується переважно за участю ізоферменту CYP3A4 системи цитохрому Р450, не суттєво впливаючи на функцію цієї системи. Хоча ризик впливу фінастериду на фармакокінетику інших препаратів оцінюється як невисокий, існує ймовірність того, що інгібітори або індуктори ізоферменту CYP3A4 системи цитохрому Р450 впливатимуть на плазмову концентрацію фінастериду. Тим не менш, враховуючи наявні дані з безпеки, малоймовірним, що підвищення концентрації финастерида, пов'язане з супутнім застосуванням таких інгібіторів, матиме клінічне значення. Не було виявлено клінічно значущої взаємодії при комбінованому застосуванні фінастериду з пропранололом, дигоксином, глібенкламідом, варфарином, теофіліном та феназоном.Спосіб застосування та дозиПрепарат приймають внутрішньо по 5 мг 1 раз на добу, незалежно від їди. Тривалість терапії до оцінки її ефективності повинна становити не менше 6 місяців, тому курс лікування має бути досить тривалим. Фінастерид можна застосовувати у вигляді монотерапії, а також у комбінації з доксазозином. Немає достатніх клінічних даних щодо застосування препарату у пацієнтів із печінковою недостатністю. У пацієнтів з різними стадіями ниркової недостатності (при зниженні КК до 9 мл/хв) корекція дози не потрібна, оскільки спеціальні дослідження не продемонстрували жодних змін. фармакокінетичного профілю фінастериду Пацієнтам похилого віку корекція дози не потрібна, хоча фармакокінетичні дослідження вказують на те, що виведення фінастериду у пацієнтів віком від 70 років дещо знижується.ПередозуванняПацієнти отримували фінастерид одноразово в дозах до 400 мг, при багаторазовому введенні препарату в дозах до 80 мг на добу протягом 3 місяців небажаних реакцій не спостерігалося. Передозування фінастериду не потребує спеціального лікування.Запобіжні заходи та особливі вказівкиВказівки загального характеру Щоб уникнути обструктивних ускладнень, необхідно здійснювати ретельне спостереження пацієнтів з великим обсягом залишкової сечі та/або значно утрудненим сечовипусканням. Слід враховувати можливість виникнення потреби у хірургічному втручанні. Вплив на вміст ПСА та діагностику раку передміхурової залози До цього часу не доведено клінічних переваг застосування фінастериду у пацієнтів з раком передміхурової залози. У контрольованих клінічних дослідженнях у пацієнтів із ДГПЗ та підвищеною концентрацією ПСА у плазмі крові проводився моніторинг вмісту ПСА та результатів досліджень біопсії передміхурової залози. Було встановлено, що застосування фінастериду, мабуть, не змінює частоти виявлення раку передміхурової залози і не впливає на частоту його виникнення у пацієнтів, які приймали фінастерид або плацебо. Перед початком лікування та періодично в процесі терапії фінастеридом рекомендується проводити ректальне дослідження та застосовувати інші методи діагностики раку передміхурової залози. Визначення ПСА в плазмі також використовується для виявлення раку передміхурової залози. В цілому, вихідна концентрація ПСА вище 10 нг/мл говорить про необхідність подальшого обстеження пацієнта та проведення біопсії простати. При визначенні концентрації ПСА в межах 4-10 нг/мл потрібне подальше обстеження пацієнта. У чоловіків із ДГПЗ нормальні значення ПСА не дозволяють виключити рак передміхурової залози, незалежно від лікування фінастеридом. Вихідна концентрація ПСА нижче 4 нг/мл також не виключає рак передміхурової залози. Фінастерид викликає зменшення концентрації сироваткового ПСА приблизно на 50% у пацієнтів з ДГПЗ, навіть за наявності раку передміхурової залози. Даний факт необхідно брати до уваги при оцінці вмісту ПСА у пацієнтів із ДГПЗ, які отримують лікування фінастеридом, т.я. зниження концентрації ПСА не виключає наявності супутнього раку передміхурової залози. Це зниження очікується за будь-якого діапазону значень концентрації ПСА, хоча воно може відрізнятися у конкретних пацієнтів. Аналіз значень ПСА більш ніж у 3000 пацієнтів у 4-річному подвійному сліпому плацебо-контрольованому дослідженні PLESS підтвердив, що у пацієнтів, які приймали фінастерид протягом 6 місяців або більше, значення ПСА повинні бути подвоєні для їх порівняння з нормальними значеннями даного показника у пацієнтів, не одержують лікування препаратом.Ця корекція зберігає чутливість та специфічність аналізу ПСА та можливість виявлення раку передміхурової залози. Будь-яке збільшення концентрації ПСА, що зберігається, у пацієнтів, які отримують лікування фінастеридом, вимагає ретельного обстеження для з'ясування причини, яка може полягати в недотриманні режиму прийому препарату. Фінастерид суттєво не знижує відсоток вільного ПСА (ставлення вільного ПСА до загального). Цей показник залишається незмінним навіть під впливом прийому препарату. Якщо для діагностики раку передміхурової залози використовується відсоток вільного ПСА, корекція значень цього показника не є обов'язковою.вимагає ретельного обстеження для з'ясування причини, що може полягати у недотриманні режиму прийому препарату. Фінастерид суттєво не знижує відсоток вільного ПСА (ставлення вільного ПСА до загального). Цей показник залишається незмінним навіть під впливом прийому препарату. Якщо для діагностики раку передміхурової залози використовується відсоток вільного ПСА, корекція значень цього показника не є обов'язковою.вимагає ретельного обстеження для з'ясування причини, що може полягати у недотриманні режиму прийому препарату. Фінастерид суттєво не знижує відсоток вільного ПСА (ставлення вільного ПСА до загального). Цей показник залишається незмінним навіть під впливом прийому препарату. Якщо для діагностики раку передміхурової залози використовується відсоток вільного ПСА, корекція значень цього показника не є обов'язковою. Рак молочної залози у чоловіків У ході клінічних досліджень, а також протягом постреєстраційного періоду у чоловіків, які приймають финастерид, було виявлено випадки раку молочної залози. Лікарі повинні інструктувати своїх пацієнтів про необхідність негайно повідомляти про будь-які зміни тканини молочної залози, такі як поява ущільнень, біль, гінекомастія або виділення із сосків. Вплив на здатність до керування автотранспортом та управління механізмами Про несприятливий вплив препарату на здатність керувати транспортними засобами та працювати з механізмами не повідомлялося.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Активні речовини: фінастерид – 5 мг; Допоміжні речовини: лактози моногідрат, крохмаль кукурудзяний, повідон K30, карбоксиметилкрохмаль натрію (тип А), докузат натрію, магнію стеарат. Склад плівкової оболонки: гіпромелоза 2910/5, макрогол 6000, тальк, титану діоксид, емульсія симетикону SE4, барвник заліза оксид жовтий. По 10 або 15 таблеток у блістері з ПВХ/ПВДХ/Аl. По 3 або 6 блістерів (10 таблеток) або по 2, 4 або 6 блістерів (по 15 таблеток) у картонній пачці разом з інструкцією із застосування.Опис лікарської формиКруглі, двоопуклі таблетки світло-жовтого кольору, покриті плівковою оболонкою.Фармакотерапевтична групаПрепарат для лікування доброякісної гіперплазії передміхурової залози. Інгібітор 5α-редуктази.ФармакокінетикаВсмоктування Cmax фінастериду в плазмі досягається приблизно через 2 години після прийому внутрішньо. Абсорбція фінастериду із шлунково-кишкового тракту завершується через 6-8 годин після прийому внутрішньо. Біодоступність фінастериду при вживанні становить приблизно 80% від внутрішньовенної референсної дози і не залежить від їди. Розподіл Зв'язування з білками плазми становить приблизно 93%. Плазмовий кліренс становить близько 165 мл/хв, що здається Vd - 76 л. При тривалій терапії спостерігається повільне накопичення фінастериду у невеликих кількостях. При щоденному прийомі фінастериду внутрішньо в дозі 5 мг його мінімальна Css у плазмі досягає 8-10 нг/мл і з часом залишається стабільною. У пацієнтів, які отримували препарат протягом 7-10 днів, фінастерид виявлявся у спинномозковій рідині. При прийомі препарату в дозі 5 мг/добу фінастерид у незначних кількостях виявляється у насінній рідині. Метаболізм та виведення T1/2 фінастериду в середньому дорівнює 6 годин. У чоловіків після одноразового прийому внутрішньо дози фінастериду, міченого 14С, 39% прийнятої дози виводиться нирками у вигляді метаболітів (незмінений фінастерид практично не виводиться нирками); 57% – через кишечник. У цьому дослідженні були ідентифіковані 2 метаболіти фінастериду, які мають незначну інгібуючу дію щодо 5α-редуктази порівняно з фінастеридом. Фармакокінетика в особливих клінічних випадках У літньому віці швидкість виведення фінастериду дещо знижується. З віком T1/2 збільшується: у чоловіків 18-60 років середній T1/2 становить 6 год, а у чоловіків старше 70 років - 8 год. потрібно. У пацієнтів з хронічною нирковою недостатністю (КК від 9 до 55 мл/хв) розподіл міченого 14С фінастериду при прийомі одноразової дози не відрізнявся від такого у здорових добровольців. Зв'язування фінастериду з білками плазми також не відрізнялося у пацієнтів з порушенням функції нирок. При нирковій недостатності частина метаболітів фінастериду, яка нормується екскретується нирками, виводиться через кишечник. Це проявляється збільшенням кількості метаболітів фінастериду в калі при відповідному зниженні їхньої концентрації в сечі. У пацієнтів з нирковою недостатністю, які не потребують гемодіалізу, корекція дози фінастериду не потрібна.ФармакодинамікаФінастерид - синтетична 4-азастероїдна сполука. Є специфічним конкурентним інгібітором 5α-редуктази II типу – внутрішньоклітинного ферменту, який перетворює тестостерон на активний андроген – дигідротестостерон (ДГТ). При доброякісній гіперплазії передміхурової залози (ДГПЗ) її збільшення залежить від перетворення тестостерону на ДГТ у простаті. Фінастерид високоефективно знижує концентрацію ДГТ як у плазмі, так і в тканині передміхурової залози. Пригнічення утворення ДГТ супроводжується зменшенням розмірів передміхурової залози, збільшенням максимальної швидкості сечовипускання та зниженням вираженості симптомів, пов'язаних із гіперплазією передміхурової залози. Фінастерид не має спорідненості з рецепторами андрогенів. Згідно з результатами клінічного дослідження (PLESS), в якому брали участь пацієнти з помірно або значно вираженими симптомами ДГПЗ та збільшенням передміхурової залози, финастерид знижував частоту виникнення гострої затримки сечі з 7/100 до 3/100 за 4-річний період, а частоту потреби у хірургічному. втручання (трансуретральної резекції простати (ТУРП) або простатектомії) - з 10/100 до 5/100. Ці зміни також асоціювалися з покращенням симптоматики ДГПЗ (зниження на 2 пункти за шкалою симптомів quasi-AUA), стійким зменшенням об'єму передміхурової залози приблизно на 20% та стабільним збільшенням швидкості струму сечі. Дослідження MTOPS (Medical Therapy Of Prostate Symptoms) тривалістю від 4 до 6 років, в рамках якого 3047 чоловіків із симптомами ДГПЗ були рандомізовані на групи, які отримують: фінастерид у дозі 5 мг на добу; доксазозин у дозі 4 мг на добу або 8 мг на добу; комбінацію фінастериду в дозі 5 мг на добу та доксазозину в дозі 4 мг на добу або 8 мг на добу; чи плацебо. Лікування призводило до значного зниження ризику клінічного прогресування ДГПЗ, яке на фоні застосування фінастериду становило 34% (р=0.002), доксазозину – 39% (рПоказання до застосуванняЛікування ДГПЗ та профілактика урологічних ускладнень з метою: зниження ризику гострої затримки сечі; зниження ризику необхідності проведення хірургічних втручань, зокрема. трансуретральної резекції (ТУР) передміхурової залози та простатектомії; Лікування з метою зменшення розмірів збільшеної передміхурової залози, поліпшення сечовипускання та зменшення вираженості симптомів, пов'язаних із ДГПЗ; У поєднанні з доксазозином зниження ризику прогресування симптомів, що з ДГПЖ.Протипоказання до застосуванняспадкова непереносимість лактози, дефіцит лактази або порушення всмоктування глюкози/галактози; вагітність та застосування препарату у жінок із збереженим репродуктивним потенціалом; вік до 18 років; підвищена чутливість до фінастериду та/або інших компонентів препарату. З обережністю слід призначати препарат пацієнтам з великим обсягом залишкової сечі та/або суттєво зниженою швидкістю сечовипускання (пацієнти повинні регулярно спостерігатися лікарем щодо виявлення обструктивної уропатії), пацієнтам з печінковою недостатністю, а також пацієнтам похилого віку.Вагітність та лактаціяЗастосування препарату Пенестер протипоказане при вагітності та жінкам із збереженим репродуктивним потенціалом. У зв'язку зі здатністю інгібіторів 5α-редуктази II типу пригнічувати перетворення тестостерону на дигідротестостерон, дані засоби, в т.ч. Фінастерид, при застосуванні у вагітних можуть викликати аномалії розвитку зовнішніх статевих органів у плода чоловічої статі. Фінастерид не показаний для застосування у жінок. Даних про екскрецію фінастериду із грудним молоком немає. Невеликі кількості фінастериду були виявлені у спермі пацієнтів, які отримували фінастерид у дозі 5 мг на добу. Хоча клінічні дані щодо впливу фінастериду на плід чоловічої статі відсутні, жінкам із збереженим репродуктивним потенціалом слід уникати контакту з насіннєвою рідиною чоловіків, які приймають фінастерид. Жінкам із збереженим репродуктивним потенціалом та вагітним слід уникати контакту з пошкодженими пігулками фінастериду, т.к. здатність препарату пригнічувати перетворення тестостерону на ДГТ може спричинити порушення розвитку статевих органів у плода чоловічої статі. Протипоказаний у віці до 18 років.Побічна діяНебажані реакції, виявлені під час клінічних досліджень (дослідження PLESS) Побічні реакції розділені за системно-органними класами відповідно до класифікації MedDRA. Частота побічних реакцій визначалася відповідно до наступної градації (класифікація ВООЗ): дуже часто (більше 1/10); часто (від понад 1/100 до менше 1/10); нечасто (від понад 1/1000 до 1/100); рідко (від понад 1/10000 до менше 1/1000); дуже рідко (від 1/10 000, включаючи окремі повідомлення). Порушення психіки: часто – зниження лібідо. З боку шкіри та підшкірних тканин: нечасто – шкірний висип. З боку статевих органів та молочної залози: часто – порушення сексуальної функції; нечасто – порушення еякуляції, зменшення обсягу еякуляту, збільшення грудних залоз, болючість у ділянці грудних залоз. В рамках дослідження MTOPS порівнювалося застосування фінастериду в дозі 5 мг/добу (n=768), доксазозину в дозі 4 мг/добу або 8 мг/добу (n=756), комбінованої терапії фінастеридом у дозі 5 мг/добу та доксазозином у дозі. 4 або 8 мг/добу (n=786), та плацебо (n=737). Відповідно до результатів даного дослідження профіль безпеки та переносимості комбінованої терапії загалом збігався з профілем її окремих компонентів. Частота порушень еякуляції у пацієнтів, які отримують комбіновану терапію, була сумісною із сумою частоти виникнення даного небажаного явища на тлі двох видів монотерапії. Було проведено 7-річне плацебо-контрольоване дослідження РСРТ, у якому брали участь 18 882 здорові чоловіки. Доступні для аналізу дані пункційної біопсії передміхурової залози були отримані щодо 9060 суб'єктів, при цьому рак передміхурової залози був виявлений у 803 (18.4%) чоловіків, які отримували фінастерид у добовій дозі 5 мг, і у 1147 (24.4%) чоловіків, що отримували плац. Згідно з результатами пункційної біопсії рак передміхурової залози з баловим показником 710 за шкалою Глісона був діагностований у 280 (6.4%) чоловіків з групи, які отримували фінастерид у добовій дозі 5 мг, у той час як у групі плацебо рак з таким ступенем диференціювання 5.1%) пацієнтів. Результати додаткового аналізу свідчили, що збільшення поширеності низькодиференційованого раку передміхурової залози,те, що спостерігалося в групі пацієнтів, які отримували фінастерид у добовій дозі 5 мг, може бути пояснено системною помилкою при оцінці результатів, пов'язаних із впливом терапії фінастеридом у дозі 5 мг 1 раз на добу на об'єм передміхурової залози. Із загальної кількості випадків раку передміхурової залози, діагностованих у цьому дослідженні, на момент постановки діагнозу приблизно 98% випадків було віднесено до локалізованого раку (клінічна стадія T1 або T2). Клінічна значимість даних про пухлинний процес зі ступенем диференціювання 7-10 балів за шкалою Глісон невідома.діагностованих у цьому дослідженні, на момент постановки діагнозу приблизно 98% випадків було віднесено до локалізованого раку (клінічна стадія T1 або T2). Клінічна значимість даних про пухлинний процес зі ступенем диференціювання 7-10 балів за шкалою Глісон невідома.діагностованих у цьому дослідженні, на момент постановки діагнозу приблизно 98% випадків було віднесено до локалізованого раку (клінічна стадія T1 або T2). Клінічна значимість даних про пухлинний процес зі ступенем диференціювання 7-10 балів за шкалою Глісон невідома. Відомості, отримані на підставі післяреєстраційного досвіду застосування препарату Частота небажаних реакцій невідома, т.к. на підставі отриманих даних встановити частоту та причинно-наслідковий зв'язок з дією фінастериду не завжди можливо, оскільки повідомлення про дані реакції надходили добровільно по популяції невідомого розміру. З боку імунної системи: частота невідома – реакції гіперчутливості, в т.ч. шкірний свербіж, кропив'янка, ангіоневротичний набряк (включаючи набряк губ, обличчя та гортані). З боку печінки та жовчовивідних шляхів: частота невідома – підвищення активності печінкових трансаміназ. З боку серцево-судинної системи: частота невідома – відчуття серцебиття. Порушення психіки: частота невідома – депресія, зниження лібідо, яке зберігається після припинення терапії. З боку статевих органів та молочної залози: частота невідома – сексуальна дисфункція (еректильна дисфункція та порушення еякуляції), яка зберігається після припинення лікування, болючість яєчок, чоловіче безпліддя та/або зниження якості насіннєвої рідини. Після відміни фінастериду якість насіннєвої рідини приходила до норми або покращувалася. Лабораторні показники При оцінці результатів лабораторних досліджень необхідно враховувати, що у пацієнтів, які отримують лікування фінастеридом, вміст ПСА у плазмі знижується. Більшість пацієнтів протягом перших місяців терапії відзначається швидке зниження показника ПСА з його наступною стабілізацією. Вихідне значення ПСА, що встановлюється після проведення терапії финастеридом, становить приблизно половину відповідного показника, що відзначалося на початок лікування. Таким чином, у пацієнтів, які отримують лікування фінастеридом протягом 6 місяців або більше, значення ПСА слід подвоювати порівняно з нормальними значеннями чоловіків, які не отримували лікування. Інших відмінностей у значеннях стандартних лабораторних показників між групами пацієнтів, які отримували фінастерид та плацебо, не спостерігалося.Взаємодія з лікарськими засобамиКлінічно значущої взаємодії коїться з іншими препаратами виявлено був. Фінастерид метаболізується переважно за участю ізоферменту CYP3A4 системи цитохрому Р450, не суттєво впливаючи на функцію цієї системи. Хоча ризик впливу фінастериду на фармакокінетику інших препаратів оцінюється як невисокий, існує ймовірність того, що інгібітори або індуктори ізоферменту CYP3A4 системи цитохрому Р450 впливатимуть на плазмову концентрацію фінастериду. Тим не менш, враховуючи наявні дані з безпеки, малоймовірним, що підвищення концентрації финастерида, пов'язане з супутнім застосуванням таких інгібіторів, матиме клінічне значення. Не було виявлено клінічно значущої взаємодії при комбінованому застосуванні фінастериду з пропранололом, дигоксином, глібенкламідом, варфарином, теофіліном та феназоном.Спосіб застосування та дозиПрепарат приймають внутрішньо по 5 мг 1 раз на добу, незалежно від їди. Тривалість терапії до оцінки її ефективності повинна становити не менше 6 місяців, тому курс лікування має бути досить тривалим. Фінастерид можна застосовувати у вигляді монотерапії, а також у комбінації з доксазозином. Немає достатніх клінічних даних щодо застосування препарату у пацієнтів із печінковою недостатністю. У пацієнтів з різними стадіями ниркової недостатності (при зниженні КК до 9 мл/хв) корекція дози не потрібна, оскільки спеціальні дослідження не продемонстрували жодних змін. фармакокінетичного профілю фінастериду Пацієнтам похилого віку корекція дози не потрібна, хоча фармакокінетичні дослідження вказують на те, що виведення фінастериду у пацієнтів віком від 70 років дещо знижується.ПередозуванняПацієнти отримували фінастерид одноразово в дозах до 400 мг, при багаторазовому введенні препарату в дозах до 80 мг на добу протягом 3 місяців небажаних реакцій не спостерігалося. Передозування фінастериду не потребує спеціального лікування.Запобіжні заходи та особливі вказівкиВказівки загального характеру Щоб уникнути обструктивних ускладнень, необхідно здійснювати ретельне спостереження пацієнтів з великим обсягом залишкової сечі та/або значно утрудненим сечовипусканням. Слід враховувати можливість виникнення потреби у хірургічному втручанні. Вплив на вміст ПСА та діагностику раку передміхурової залози До цього часу не доведено клінічних переваг застосування фінастериду у пацієнтів з раком передміхурової залози. У контрольованих клінічних дослідженнях у пацієнтів із ДГПЗ та підвищеною концентрацією ПСА у плазмі крові проводився моніторинг вмісту ПСА та результатів досліджень біопсії передміхурової залози. Було встановлено, що застосування фінастериду, мабуть, не змінює частоти виявлення раку передміхурової залози і не впливає на частоту його виникнення у пацієнтів, які приймали фінастерид або плацебо. Перед початком лікування та періодично в процесі терапії фінастеридом рекомендується проводити ректальне дослідження та застосовувати інші методи діагностики раку передміхурової залози. Визначення ПСА в плазмі також використовується для виявлення раку передміхурової залози. В цілому, вихідна концентрація ПСА вище 10 нг/мл говорить про необхідність подальшого обстеження пацієнта та проведення біопсії простати. При визначенні концентрації ПСА в межах 4-10 нг/мл потрібне подальше обстеження пацієнта. У чоловіків із ДГПЗ нормальні значення ПСА не дозволяють виключити рак передміхурової залози, незалежно від лікування фінастеридом. Вихідна концентрація ПСА нижче 4 нг/мл також не виключає рак передміхурової залози. Фінастерид викликає зменшення концентрації сироваткового ПСА приблизно на 50% у пацієнтів з ДГПЗ, навіть за наявності раку передміхурової залози. Даний факт необхідно брати до уваги при оцінці вмісту ПСА у пацієнтів із ДГПЗ, які отримують лікування фінастеридом, т.я. зниження концентрації ПСА не виключає наявності супутнього раку передміхурової залози. Це зниження очікується за будь-якого діапазону значень концентрації ПСА, хоча воно може відрізнятися у конкретних пацієнтів. Аналіз значень ПСА більш ніж у 3000 пацієнтів у 4-річному подвійному сліпому плацебо-контрольованому дослідженні PLESS підтвердив, що у пацієнтів, які приймали фінастерид протягом 6 місяців або більше, значення ПСА повинні бути подвоєні для їх порівняння з нормальними значеннями даного показника у пацієнтів, не одержують лікування препаратом.Ця корекція зберігає чутливість та специфічність аналізу ПСА та можливість виявлення раку передміхурової залози. Будь-яке збільшення концентрації ПСА, що зберігається, у пацієнтів, які отримують лікування фінастеридом, вимагає ретельного обстеження для з'ясування причини, яка може полягати в недотриманні режиму прийому препарату. Фінастерид суттєво не знижує відсоток вільного ПСА (ставлення вільного ПСА до загального). Цей показник залишається незмінним навіть під впливом прийому препарату. Якщо для діагностики раку передміхурової залози використовується відсоток вільного ПСА, корекція значень цього показника не є обов'язковою.вимагає ретельного обстеження для з'ясування причини, що може полягати у недотриманні режиму прийому препарату. Фінастерид суттєво не знижує відсоток вільного ПСА (ставлення вільного ПСА до загального). Цей показник залишається незмінним навіть під впливом прийому препарату. Якщо для діагностики раку передміхурової залози використовується відсоток вільного ПСА, корекція значень цього показника не є обов'язковою.вимагає ретельного обстеження для з'ясування причини, що може полягати у недотриманні режиму прийому препарату. Фінастерид суттєво не знижує відсоток вільного ПСА (ставлення вільного ПСА до загального). Цей показник залишається незмінним навіть під впливом прийому препарату. Якщо для діагностики раку передміхурової залози використовується відсоток вільного ПСА, корекція значень цього показника не є обов'язковою. Рак молочної залози у чоловіків У ході клінічних досліджень, а також протягом постреєстраційного періоду у чоловіків, які приймають финастерид, було виявлено випадки раку молочної залози. Лікарі повинні інструктувати своїх пацієнтів про необхідність негайно повідомляти про будь-які зміни тканини молочної залози, такі як поява ущільнень, біль, гінекомастія або виділення із сосків. Вплив на здатність до керування автотранспортом та управління механізмами Про несприятливий вплив препарату на здатність керувати транспортними засобами та працювати з механізмами не повідомлялося.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
220,00 грн
175,00 грн
Склад, форма випуску та упаковкаГранули – 1 пак. (5 г): Аскорбінова кислота - 0,2 г; бромгексину гідрохлорид – 0,008 г; кальцію глюконату моногідрат – 0,2 г; парацетамол – 0,5 г; рутозиду тригідрат - 0,02 г; Допоміжні речовини: лимонна кислота-0,05 г, сахароза (цукор) - 3,977 г, натрію сахаринат - 0,025 г, повідон (повідон До 17) - 0,02 г. Гранули для приготування розчину для вживання. По 5 г гранул у пакетик із паперу з полімерним покриттям або буфленом. По 5, 10 пакетиків разом з інструкцією з медичного застосування поміщають у картонну пачку.Опис лікарської формиСуміш гранул круглої, циліндричної або неправильної форми, білого, білого з жовтуватим відтінком і жовтувато-зеленого кольору.Фармакотерапевтична групаПротивірусний засіб.ФармакодинамікаПентафлуцин Бронхо є комбінованим лікарським препаратом. Фармакологічні ефекти обумовлені комплексним впливом компонентів, що входять до складу препарату. Аскорбінова кислота - відіграє важливу роль у регуляції окисно-відновних процесів, вуглеводного обміну, згортання крові, регенерації тканин, підвищує опірність організму. Бромгексин - муколітичний (секретолітичний) засіб, що надає відхаркувальну та слабку протикашльову дію. Знижує в'язкість мокротиння (деполімеризує мукопротеїнові та мукополісахаридні волокна, збільшує серозний компонент бронхіального секрету); активує миготливий епітелій, збільшує об'єм та покращує відходження мокротиння. Стимулює вироблення ендогенного сурфактанту, що забезпечує стабільність альвеолярних клітин у процесі дихання. Кальція глюконат - є джерелом кальцію в організмі, виявляє антиалергічну дію (механізм неясний), запобігає розвитку підвищеної проникності та ламкості судин, що зумовлюють геморагічні процеси при грипі та гострій респіраторній вірусній інфекції, а також відновлює капілярний кровообіг. Для лікування алергічних захворювань чи ускладнень рекомендується його спільне застосування з антигістамінними препаратами. Парацетамол – ненаркотичний аналгетик, блокує фермент циклооксигеназу 1-го типу (ЦОГ-1) та фермент циклооксигеназу 2-го типу (ЦОГ-2) переважно у центральній нервовій системі, впливаючи не центри болю та терморегуляції. У запалених тканинах клітинні пероксидази нейтралізують вплив парацетамолу на циклооксигеназу, що пояснює практично повну відсутність протизапального ефекту. Рутозид - зменшує проникність і ламкість капілярів, має антиоксидантні властивості.Показання до застосуванняПентафлуцин-Бронхо застосовується у дорослих для симптоматичного лікування гострих респіраторних захворювань (ГРЗ) та гострих респіраторних вірусних інфекцій (ГРВІ), що супроводжуються високою температурою, ознобом, ломотою в тілі, головним та м'язовим болем; запаленням трахеї та утрудненням відходження в'язкого мокротиння; підвищення неспецифічної опірності організму до інфекційних захворювань.Протипоказання до застосуванняПідвищена чутливість до компонентів препарату; печінкова та/або ниркова недостатність тяжкого ступеня; захворювання крові зі схильністю до крововиливів; виразкова хвороба (на стадії загострення); декомпенсований цукровий діабет; дефіцит глюкозо-6-фосфатдегідрогенази; вагітність та період грудного вигодовування; артеріальна гіпертензія; гіпероксалурія; гіперкальціурія; гіперкальціємія; нефроуролітіаз; одночасне застосування з іншими лікарськими засобами, що містять парацетамол; алкоголізм; дитячий вік (до 18 років); вроджена непереносимість фруктози, глюкозогалактозна мальабсорбція, дефіцит сахарази/ізомальтази. З обережністю: Вроджені гіпербілірубінемії (синдром Жільбера, Дубіна-Джонсона та Ротора). Літній вік; печінкова або ниркова недостатність легкої та середньої тяжкості; захворювання серцево-судинної системи; гіперкоагуляція; дегідратація; бронхіальна астма, у тому числі і в анамнезі; виразкова хвороба шлунка та дванадцятипалої кишки. До складу препарату входить цукор (1 пакетик містить 0,33 ХЕ цукру), що слід враховувати хворим на цукровий діабет.Вагітність та лактаціяЗастосування препарату під час вагітності та у період лактації протипоказане. При необхідності застосування препарату в період грудного вигодовування слід припинити грудне вигодовування.Побічна діяАскорбінова кислота: Порушення з боку нирок та сечовивідних шляхів: помірна поллакіурія (при прийомі дози більше 600 мг на добу), при тривалому застосуванні великих доз – гіпероксалурія, нефролітіаз (з кальцію оксалату), ушкодження гломерулярного апарату нирок. Порушення з боку шлунково-кишкового тракту: подразнення слизової оболонки шлунково-кишкового тракту. Порушення з боку шкіри та підшкірних тканин: шкірний висип, гіперемія шкіри. Вплив на результати лабораторних та інструментальних досліджень: тромбоцитоз, гіперпротромбінемія, еритропенія, нейтрофільний лейкоцитоз, гіпокаліємія. Порушення ендокринної системи: пригнічення функції інсулярного апарату підшлункової залози (гіперглікемія, глюкозурія). Бромгексин: Порушення з боку шлунково-кишкового тракту: диспепсія, зокрема нудота, блювання; загострення виразкової хвороби шлунка та 12-палої кишки. Порушення з боку шкіри та підшкірних тканин: висипання на шкірі. Порушення з боку дихальної системи, органів грудної клітки та середостіння: риніт. Порушення з боку нервової системи: запаморочення, біль голови. Вплив на результати лабораторних та інструментальних досліджень: підвищення активності "печінкових" трансаміназ у сироватці крові. Кальцію глюконат: Порушення з боку шлунково-кишкового тракту: запор, подразнення слизової оболонки шлунково-кишкового тракту, нудота, блювання. Парацетамол: Порушення з боку шлунково-кишкового тракту: нудота, біль у епігастрії. Порушення з боку крові та лімфатичної системи: анемія, тромбоцитопенія, метгемоглобінемія, агранулоцитоз, гемолітична анемія. Порушення з боку шкіри та підшкірних тканин: висипання на шкірі, свербіж, кропив'янка. Порушення з боку імунної системи: ангіоневротичний набряк, багатоформна ексудативна еритема (у тому числі синдром Стівена-Джонсона, токсичний епідермальний некроліз (синдром Лайєлла)) та гострий генералізований екзантематозний пустульоз. Порушення з боку дихальної системи, органів грудної клітки та середостіння: бронхоспазм у пацієнтів, чутливих до ацетилсаліцилової кислоти та інших нестероїдних протизапальних засобів. При тривалому застосуванні у високих дозах можлива гепатотоксична та нефротоксична дія. Рутозид: Алергічні реакції: шкірний висип Порушення з боку шлунково-кишкового тракту: нудота, діарея, печія. Порушення з боку нервової системи: біль голови. З боку серцево-судинної системи: "припливи" крові до обличчя. Якщо будь-які вказані в інструкції побічні ефекти посилюються, або Ви помітили будь-які інші побічні ефекти, не вказані в інструкції, повідомте про це лікаря.Взаємодія з лікарськими засобамиСлід уникати комбінації препарату з барбітуратами, протисудомними засобами, фенітоїном, карбамазепіном, рифампіцином, зидовудином та іншими індукторами мікросомальних ферментів печінки. Аскорбінова кислота: підвищує концентрацію в крові бензилпеніциліну та тетрациклінів; у дозі 1 г/добу підвищує біодоступність етинілестрадіолу (у тому числі пероральних контрацептивів, що входить до складу). Знижує ефективність гепарину та непрямих антикоагулянтів. Покращує всмоктування у кишечнику препаратів заліза (переводить тривалентне залізо у двовалентне); може підвищувати виведення заліза при одночасному застосуванні з дефероксаміном. Ацетилсаліцилова кислота (АСК), пероральні контрацептиви, свіжі соки та лужне питво знижують всмоктування та засвоєння. При одночасному застосуванні з АСК підвищується виведення із сечею аскорбінової кислоти та знижується виведення АСК. АСК знижує абсорбцію аскорбінової кислоти приблизно 30%. Збільшує ризик розвитку кристалурії при лікуванні саліцилатами та сульфаніламідами короткої дії, уповільнює виведення нирками кислот, збільшує виведення лікарських засобів, що мають лужну реакцію (зокрема алкалоїдів), знижує концентрацію у крові пероральних контрацептивів. При одночасному застосуванні зменшує хронотропну дію ізопреналіну. Бромгексин - не призначають одночасно з лікарськими засобами, що пригнічують кашльовий центр (у тому числі кодеїн), оскільки це ускладнює відходження розрідженого мокротиння (накопичення бронхіального секрету в дихальних шляхах). Несумісний із лужними розчинами. Бромгексин сприяє проникненню антибіотиків (амоксицилін, еритроміцин, цефалексин, окситетрациклін), сульфаніламідних лікарських засобів у бронхіальний секрет у перші 4-5 днів протимікробної терапії. Кальція глюконат: при одночасному застосуванні з хінідином можливе уповільнення внутрішньошлуночкової провідності та підвищення токсичності хінідину. Утворює нерозчинні комплекси з антибіотиками ряду тетрацикліну (знижує антибактеріальний ефект). Уповільнює абсорбцію тетрациклінів, дигоксину, пероральних препаратів заліза (інтервал між їхніми прийомами має бути не менше 2 годин). При поєднанні з тіазидовими діуретиками може посилювати гіперкальціємію, знижувати ефект кальцитоніну при гіперкальціємії. Знижує біодоступність фенітоїну. Фармацевтично несумісний з карбонатами, саліцилатами, сульфатами (утворює нерозчинні або важкорозчинні солі кальцію). Зменшує ефект блокаторів повільних кальцієвих каналів. Парацетамол: знижує ефективність урикозуричних лікарських засобів. Супутнє застосування парацетамолу у високих дозах збільшує ефект антикоагулянтних лікарських засобів (зниження синтезу прокоагулянтних факторів у печінці). При сумісному застосуванні з етанолом можливий розвиток гострого панкреатиту. Тривале сумісне використання парацетамолу та інших нестероїдних протизапальних препаратів підвищує ризик розвитку нефропатії та ниркового папілярного некрозу, настання термінальної стадії ниркової недостатності. Дифлунісал підвищує плазмову концентрацію парацетамолу на 50% – ризик розвитку гепатотоксичності. Мієлотоксичні лікарські засоби посилюють прояв гематотоксичності препарату. Рутозид: фармакологічний ефект посилюється аскорбіновою кислотою.Спосіб застосування та дозиВміст одного пакетика розчину розчинити в 1/2 склянки (125 мл) гарячої води (t=70°C) та випити. Допускається незначний осад у склянці. Застосовувати свіжоприготовлений розчин. Перед застосуванням збовтувати. Пентафлуцин-Бронхо застосовують внутрішньо після їди по 1 пакетику 3-4 рази на день протягом 3-5 діб. Інтервал між прийомами препарату не менше ніж 4 години. Пацієнтам з порушенням функції печінки або синдромом Жильбера необхідно зменшити добову дозу або збільшити інтервал між прийомами препарату до 8 годин. Пацієнтам з порушенням функції нирок часовий інтервал між прийомами препарату повинен становити не менше 8 годин при кліренсі креатиніну менше 10 мл/хв, не менше 6 годин – при кліренсі креатиніну 10-50 мл/хв.ПередозуванняСимптоми (обумовлені парацетамолом): протягом перших 24 годин після прийому – блідість шкірних покривів, нудота, блювання, анорексія, абдомінальний біль; порушення метаболізму глюкози, метаболічний ацидоз, гіпокаліємія. Симптоми порушення функції печінки можуть виникнути через 12-48 годин після передозування. Після 3-5 днів хронічного передозування - жовтяниця, лихоманка, печінковий запах з рота, геморагічний діатез, гіпоглікемію. При тяжкому передозуванні – печінкова недостатність з прогресуючою енцефалопатією, кома, смерть; гостра ниркова недостатність із тубулярним некрозом (у т.ч. за відсутності тяжкого ураження печінки); аритмія, панкреатит. Гепатотоксичний ефект у дорослих проявляється прийому 10 г і більше. У особливих клінічних групах пацієнтів знижено поріг передозування - у літніх пацієнтів; у тих, хто приймає певні лікарські препарати (наприклад, індуктори мікросомальних ферментів печінки), алкоголь; у пацієнтів, які страждають на виснаження. Лікування: потерпілому слід зробити промивання шлунка, призначити адсорбенти (активоване вугілля) та звернутися до лікаря. Симптоматична терапія: введення донаторів SH-груп і попередників синтезу глутатіону - метіоніну протягом 8-9 годин після передозування та ацетилцистеїну - протягом 8 год. Необхідність у проведенні додаткових терапевтичних заходів (далі введення метіоніну, внутрішньовенне введення парацетамолу в крові, а також від часу, який минув після його прийому. Симптоми передозування аскорбіновою кислотою: діарея, нудота, метеоризм, абдомінальний біль спастичного характеру, прискорене сечовипускання, нефролітіаз, безсоння, дратівливість, гіпоглікемія. При застосуванні більше 1000 мг – головний біль, підвищена збудливість центральної нервової системи, безсоння, нудота, блювота, діарея, гіперацидний гастрит, пошкодження слизової оболонки шлунково-кишкового тракту, пригнічення функції інсулярного апарату підшлункової залози, гіперокукліза, пошкодження гломерулярного апарату нирок, зниження проникності капілярів (можливе погіршення трофіки тканин, підвищення артеріального тиску, гіперкоагуляція, розвиток мікроангіопатії).Високі дози аскорбінової кислоти (більше 3000 мг) можуть спричинити тимчасову осмотичну діарею та порушення роботи шлунково-кишкового тракту, такі як нудота, дискомфорт у ділянці шлунка. Лікування: симптоматичне, форсований діурез. Симптоми передозування кальцію глюконатом: гіперкальціємія, при хронічному передозуванні можуть розвинутись загальна та м'язова слабкість, депресія, психічні порушення, порушення апетиту, нудота, блювання, запор, зниження артеріального тиску, порушення серцевого ритму. Лікування: парентеральне введення кальцитоніну в дозі 5-10 МО/кг/добу на 500 мл 0,9% розчину натрію хлориду протягом 6 годин. Симптоми передозування бромгексином гідрохлоридом: диспепсичні розлади, у тому числі нудота, блювання, діарея. Лікування: штучне блювання, промивання шлунка (у перші 1-2 години після прийому). Рутозид. Відомості про передозування відсутні.Запобіжні заходи та особливі вказівкиЩоб уникнути токсичного ураження печінки, не слід поєднувати прийом препарату з вживанням алкогольних напоїв. Вплив на здатність до керування автотранспортом та управління механізмами У період лікування необхідно дотримуватись обережності при керуванні транспортними засобами, механізмами та при зайнятті потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
267,00 грн
221,00 грн
Склад, форма випуску та упаковкаГранули – 1 пак. (3 г): Активні речовини: аскорбінова кислота 0,05 г, дифенгідраміну гідрохлорид 0,01 г, кальцію глюконату моногідрат 0,1 г, парацетамол 0,25 г, рутозиду тригідрат 0,01 г; Допоміжні речовини: лимонна кислота 0,03 г, сахароза (цукор) 2,523 г, сахаринат натрію дигідрат (сахарін розчинний) 0,015 г, повідон (полівінілпіролідон К17) 0,012 г. По 3 г гранул у пакетик.
233,00 грн
157,00 грн
Склад, форма випуску та упаковкаГранули – 1 пак. (3 г): Активні речовини: аскорбінова кислота 0,05 г, дифенгідраміну гідрохлорид 0,01 г, кальцію глюконату моногідрат 0,1 г, парацетамол 0,25 г, рутозиду тригідрат 0,01 г; Допоміжні речовини: лимонна кислота 0,03 г, сахароза (цукор) 2,523 г, сахаринат натрію дигідрат (сахарін розчинний) 0,015 г, повідон (полівінілпіролідон К17) 0,012 г. По 3 г гранул у пакетик.
215,00 грн
178,00 грн
Склад, форма випуску та упаковкаГранули – 1 пак. (5 г): Активні речовини: парацетамол – 500 мг, аскорбінова кислота (вітамін C) – 200 мг, глюконат кальцію – 200 мг, димедрол (дифенгідраміну гідрохлорид) – 20 мг, рутин (рутозид) – 20 мг. Допоміжні компоненти: полівінілпіролідон (повідон), цукор (цукроза), сахарин розчинний (натрію сахаринат), лимонна кислота.
204,00 грн
173,00 грн
Склад, форма випуску та упаковкаГранули – 1 пак. (5 г): Активні речовини: парацетамол – 500 мг, аскорбінова кислота (вітамін C) – 200 мг, глюконат кальцію – 200 мг, димедрол (дифенгідраміну гідрохлорид) – 20 мг, рутин (рутозид) – 20 мг. Допоміжні компоненти: полівінілпіролідон (повідон), цукор (цукроза), сахарин розчинний (натрію сахаринат), лимонна кислота.
233,00 грн
184,00 грн
Склад, форма випуску та упаковкаГранули – 1 пак. (5 г): Активні речовини: аскорбінова кислота 200 мг, кальцію глюконату моногідрат 200 мг, кофеїну моногідрат 20 мг, парацетамол 500 мг, рутозид (у формі тригідрату) 20 мг; Допоміжні речовини: повідон 17. 4 мг, цукор 3.
765,00 грн
Склад, форма випуску та упаковкаГранули – 1 пак. (5 г): Активні речовини: аскорбінова кислота 200 мг, кальцію глюконату моногідрат 200 мг, кофеїну моногідрат 20 мг, парацетамол 500 мг, рутозид (у формі тригідрату) 20 мг; Допоміжні речовини: повідон 17. 4 мг, цукор 3.
783,00 грн
Склад, форма випуску та упаковкаЛіофілізат - 1 доза: Активна речовина: полісахарид Haemophilus influenzae тип b, кон'югований зі правцевим анатоксином 10 мкг. Допоміжні речовини: сахароза – 42.5 мг, трометамол – 0.6 мг. 1 доза ліофілізату - флакон скляний у комплекті з 0.5 мл (1 доза) суспензії в шприці скляному місткістю 1 мл із закріпленою голкою - упаковка коміркова - пачка картонна. * не містить феноловий червоний.Опис лікарської формиЛіофілізат для приготування суспензії для внутрішньом'язового введення.Фармакотерапевтична групаІмуногенність після первинної імунізації У дослідженнях імуногенності у дітей, вакцинованих трьома дозами лікарського препарату Пентаксим® , починаючи з тримісячного віку, у 100% дітей було досягнуто серопротективного рівня антитіл до антигенів дифтерії та правця (≥0.01 МО/мл). Більш ніж у 88% дітей спостерігалося чотириразове збільшення титрів антитіл до кашлюкового анатоксину та філаментозного аглютиніну через 1 міс після завершення первинної імунізації. За відсутності серологічного корелята протекції чотириразове збільшення титрів після імунізації можна вважати сероконверсією. Як мінімум у 99% дітей після курсу первинної імунізації були досягнуті поствакцинальні титри проти вірусів поліомієліту типу 1, 2 і 3, що перевищують граничне значення рівне 5 (величина, зворотна до розведення, при якій спостерігається серонейтралізація), що вважається захисним. Через 1 міс після закінчення курсу первинної імунізації, що складається з трьох доз, як мінімум у 92% щеплених дітей 1-го року життя титр антитіл до капсульного полісахариду Haemophilus influenzae тип b був вище захисного рівня 0.15 мкг/мл, необхідного для короткочасного захисту від гемофільної інфекції. Через 1 місяць після третього щеплення концентрація антитіл до капсульного полісахариду Haemophilus influenzae тип b вище 1 мкг/мл, необхідна для забезпечення тривалого захисту від інвазивної гемофільної інфекції, спостерігалася у більш ніж 67% щеплених. Імуногенність після ревакцинації Дослідження імуногенності у дітей другого року життя, щеплених трьома дозами вакцини Пентаксим ® у межах первинної імунізації, показали високий рівень антитіл до всіх активних речовин лікарського препарату після ревакцинації цієї ж вакциною. У всіх дітей рівень антитіл перевищував 0.1 МО/мл для основного компонента, і спостерігалося в середньому п'ятикратне збільшення титрів антитіл до кашлюкового анатоксину та філаментозного аглютиніну. У всіх дітей спостерігався достатній рівень антитіл до вірусів поліомієліту типів 1, 2 та 3. Більш ніж у 97% дітей рівень антитіл до збудника дифтерії перевищував 0.1 МО/мл. Титр антитіл до капсульного полісахариду Haemophilus influenzae тип b перевищував 1 мкг/мл після ревакцинації у більш ніж 99% дітей. Ці дані підтверджують індукцію імунологічної пам'яті після первинної вакцинації.Клінічна фармакологіяВакцина для профілактики дифтерії, правця, кашлюку, поліомієліту та захворювань, спричинених Haemophilus influenzae типу b.Показання до застосуванняПервинна вакцинація та ревакцинація дітей проти дифтерії, правця, кашлюку, поліомієліту та інфекції, що викликається Haemophilus influenzae тип b (менінгіт, септицемія, артрит, епіглоттит, пневмонія, остеомієліт та інші).Протипоказання до застосуванняПрогресуюча енцефалопатія, що супроводжується судомами або без них; енцефалопатія неясної етіології, що розвинулася протягом 7 днів після введення будь-якої вакцини, що містить антигени Bordetella pertussis; сильна реакція, що розвинулася протягом 48 годин після попередньої вакцинації вакциною, що містить кашлюковий компонент: підвищення температури тіла до 40°С і вище, синдром тривалого незвичайного плачу (довше 3 год), фебрильні або афебрильні судоми, гіпотонічний-гіпореактивний синдром; гіперчутливість на попереднє введення дифтерійної, правцевої, коклюшної вакцин, вакцин проти поліомієліту або інфекції, що викликається Haemophilus influenzae тип b; захворювання, що супроводжуються підвищенням температури тіла, гостре інфекційне чи хронічне захворювання на стадії загострення. Вакцинацію проводять через 2-4 тижні після одужання або у період реконвалесценції чи ремісії. При легких ГРВІ, гострих кишкових захворюваннях та інших щеплення проводять відразу після нормалізації температури; встановлена гіперчутливість до будь-якого компонента вакцини, а також глютаральдегіду, неоміцину, стрептоміцину та поліміксину В. З обережністю: за наявності в анамнезі у дитини фебрильних судом, не пов'язаних з попередньою вакцинацією, слід стежити за температурою тіла щепленого протягом 48 годин після вакцинації та при її підвищенні, за призначенням лікаря, застосовувати антипіретичні (жарознижувальні) препарати; при тромбоцитопенії та інших порушеннях згортання крові введення вакцини має проводитися з обережністю через ризик розвитку кровотечі при внутрішньом'язовій ін'єкції.Вагітність та лактаціяОскільки вакцина Пентаксим® застосовується для вакцинації дітей, то дані про вплив препарату протягом вагітності та годування груддю відсутні.Побічна діяНебажані явища, представлені нижче, перераховані відповідно до системно-органних класів і частоти народження. Частоту народження визначали на підставі наступних критеріїв: дуже часто (≥1/10), часто (≥1/100 до <1/10), нечасто (≥1/1000 до <1/100), рідко (≥1/10 000) до <1/1000), дуже рідко (<1/10 000), частота невідома (не можна оцінити за наявними даними). Дані клінічних досліджень У ході проведення трьох досліджень серед дітей першого року життя, які отримали перші три дози вакцини Пентаксим®, найчастіші реакції включали дратівливість (15.2%) та реакції в місці ін'єкції, такі як почервоніння (11.2%) та ущільнення >2 см (15.1%) . У ході дослідження, проведеного у Швеції, після трьох доз вакцини Пентаксим®, введеної у віці 3, 5 та 12 місяців, найбільш часті реакції включали дратівливість (24.1%) та реакції в місці ін'єкції, такі як почервоніння (13.4%) та ущільнення ( 12,5%). Зазначені ознаки та симптоми зазвичай розвиваються протягом 48 годин після вакцинації та проходять мимовільно, не вимагаючи специфічного лікування. При ревакцинації відзначається тенденція до зростання частоти виникнення загальних розладів та порушень у місці ін'єкції. З боку обміну речовин та харчування: дуже часто – анорексія. З боку психіки: дуже часто – нервозність (дратівливість), незвичайний плач; часто – порушення сну; нечасто – тривалий плач. З боку нервової системи: дуже часто – безсоння. З боку травної системи: дуже часто – блювання; часто – діарея. Загальні розлади та порушення в місці введення: дуже часто – почервоніння у місці ін'єкції, гарячка (≥38°С), болючість та набряк у місці ін'єкції; часто - ущільнення у місці ін'єкції; нечасто – почервоніння та набряк (≥5 см) у місці ін'єкції, гарячка (≥39°С); рідко - гарячка (≥40°С), дифузний набряк однієї або обох кінцівок може спостерігатися після введення вакцин, що містять капсульний полісахарид Haemophilus influenzae тип b. Якщо така реакція розвивається, виникає вона в основному після первинної вакцинації і спостерігається протягом перших декількох годин після вакцинації. Ця реакція може супроводжуватися ціанозом, почервонінням, минущою пурпурою та сильним плачем. Перелічені симптоми проходять мимовільно без наслідків протягом 24 год. Дані післяреєстраційного спостереження Т.к. спонтанні повідомлення про небажані явища при комерційному застосуванні препарату були отримані дуже рідко і з популяції з невизначеною кількістю пацієнтів, їх частоту класифікували як "частота невідома". З боку імунної системи: анафілактичні реакції, такі як набряк обличчя, набряк Квінке, шок. З боку дихальної системи: у глибоко недоношених дітей (народжених терміном 28 тижнів або раніше) протягом 2-3 днів після вакцинації можуть спостерігатися випадки подовження інтервалів часу між дихальними рухами. З боку нервової системи: судоми, що супроводжуються або не супроводжуються лихоманкою, гіпотонічні реакції або епізоди гіпотонії-гіпореспонсивності. З боку шкіри та шкірних тканин: висипання, кропив'янка. Загальні розлади та порушення у місці введення: виражений набряк (≥5 см) у місці ін'єкції, у т.ч. набряк, що розповсюджується за один або обидва суглоби. Ці реакції з'являлися через 24-72 години після введення вакцини і могли супроводжуватися почервонінням, підвищенням температури шкіри в місці ін'єкції, чутливістю або болючістю в місці ін'єкції. Дані симптоми зникали самостійно протягом 3-5 днів без додаткового лікування. Припускають, що ймовірність розвитку подібних реакцій збільшується в залежності від кількості введень ацелюлярного коклюшного компонента, ця ймовірність вища після 4-ї та 5-ї дози такої вакцини. Потенційні побічні реакції Компанія має дані, що після введення інших вакцин, що містять правцевий анатоксин, спостерігалися неврит плечового нерва і синдром Гійєна-Барре.Взаємодія з лікарськими засобамиЗа винятком імуносупресивної терапії немає достовірних даних про можливий взаємний вплив при використанні інших лікарських препаратів, в т.ч. з іншими вакцинами. Суспензію, що містить вакцину для профілактики дифтерії та правця адсорбовану, коклюшу ацелюлярну, поліомієліту інактивовану, не можна змішувати з будь-якими іншими лікарськими препаратами, за винятком додається ліофілізату вакцини для профілактики інфекції, що викликається Haem. Відновлену вакцину не можна змішувати з іншими лікарськими засобами та вакцинами. Лікар повинен бути поінформований про нещодавно проведене або збігається за часом з вакцинацією введення дитині будь-якого іншого лікарського препарату (в т.ч. безрецептурного).Спосіб застосування та дозиРазова доза вакцини становить 0,5 мл. Первинна вакцинація Відповідно до Національного календаря профілактичних щеплень Російської Федерації курс первинної вакцинації складається з 3 доз вакцини, що вводяться з інтервалом у 1.5 міс: у віці 3, 4.5 та 6 міс. Тим не менш, за рекомендацією лікаря можуть застосовуватися й інші схеми тридозової імунізації (наприклад, 2-3-4 міс, 2-4-6 міс або 3-4-5 міс). Ревакцинація Ревакцинацію проводять одноразово у віці 18 місяців. При порушенні графіка вакцинації, наступні інтервали між введенням чергової дози вакцини не змінюються, в т.ч. інтервал перед 4-ю (ревакцинуючою) дозою - 12 міс. Під час проведення вакцинації/ревакцинації керуються наступним графіком: 1-е щеплення, вік дитини (вводять повний препарат Пентаксим® [ суспензію+ліофілізат]) 2-е щеплення (через 1.5 міс), вводять: 3-те щеплення (через 1.5 міс), вводять: Ревакцинація (через 12 міс), вводять: До 6 міс суспензію+ ліофілізат суспензію+ ліофілізат суспензію+ ліофілізат 6-12 міс суспензію+ ліофілізат суспензію суспензію+ ліофілізат 13 міс і старше суспензію суспензію суспензію У всіх випадках порушення графіка вакцинації лікар повинен керуватися інструкцією із застосування лікарського препарату та рекомендаціями Національного календаря профілактичних щеплень Російської Федерації. Спосіб введення Вакцину вводять внутрішньом'язово. Рекомендоване місце введення: дітям віком до 24 місяців - середня третина передньолатеральної поверхні стегна; дітям старше 24 місяців - дельтовидний м'яз плеча. Не вводити внутрішньовенно або внутрішньовенно. Перед введенням необхідно переконатися, що голка не потрапила до кровоносної судини. Для варіанта упаковки з двома окремими голками (16 мм 25G, 25 мм 23G) перед приготуванням вакцини одну з двох голок слід щільно закріпити, обертаючи її на чверть обороту щодо шприца. Вибір голки залежить від товщини підшкірно-жирового шару у дитини на місці ін'єкції. Для приготування вакцини, попередньо видаливши пластикову кольорову кришечку з флакона, повністю ввести попередньо збовтану суспензію для внутрішньом'язового введення (вакцина для профілактики дифтерії, правця, кашлюку і поліомієліту) через голку з шприца у флакон з ліофілізом. influenzae тип b). Збовтати флакон, не виймаючи з нього шприца, і дочекатися повного розчинення ліофілізату (не більше 3 хв). Отримана суспензія повинна бути каламутною та мати білуватий відтінок. Вакцина не повинна використовуватись у разі зміни забарвлення чи наявності сторонніх частинок. Приготовлену вакцину слід повністю набрати в той же шприц. Готову вакцину слід запровадити негайно.ПередозуванняДані відсутні.Запобіжні заходи та особливі вказівкиВакцина Пентаксим® не формує імунітет проти інфекції, викликаної іншими серотипами Haemophilus influenzae, а також проти менінгітів іншої етіології. Лікар повинен бути поінформований про всі випадки побічних реакцій, у т.ч. не перерахованих у цій інструкції. Перед кожним щепленням, для запобігання можливим алергійним та іншим реакціям, лікар повинен уточнити стан здоров'я, історію імунізації, анамнез пацієнта та найближчих родичів (зокрема, алергологічний), випадки побічних ефектів на попередні введення вакцин. Лікар повинен мати у своєму розпорядженні лікарські засоби та інструменти, необхідні при розвитку реакції гіперчутливості. Імуносупресивна терапія або стан імунодефіциту можуть бути причиною слабкої імунної відповіді на введення вакцини. У цих випадках рекомендується відкласти вакцинацію до закінчення такої терапії чи ремісії захворювання. Тим не менш, особам з хронічним імунодефіцитом (наприклад, ВІЛ-інфекція) вакцинація рекомендована, навіть якщо імунна відповідь може бути ослабленою. При розвитку в анамнезі синдрому Гійєна-Барре або невриту плечового нерва у відповідь на будь-яку вакцину, що містить правцевий анатоксин, рішення про вакцинацію препаратом Пентаксим® має бути засноване на ретельній оцінці потенційної користі та можливого ризику. Як правило, у таких випадках виправданим є завершення первинної імунізації у дітей першого року життя (якщо запроваджено менше 3 доз). Потенційний ризик розвитку апное та необхідність моніторингу дихання протягом 48-72 годин слід враховувати при проведенні первинного курсу імунізації у глибоко недоношених дітей, які народилися на терміні 28 тижнів або раніше, особливо у анамнезі, що мають ознаки незрілості дихальної системи. Оскільки користь імунізації цієї групи дітей є високою, вакцинацію не слід відкладати або вважати протипоказаною. Оскільки антиген капсулярного полісахариду Haemophilus influenzae тип b виводиться через нирки, протягом 1-2 тижнів після вакцинації при аналізі сечі може реєструватися позитивний тест на інфекцію, що викликається Haemophilus influenzae тип b. У цей період необхідно проведення інших тестів для підтвердження діагнозу інфекції, що викликається Haemophilus influenzae тип b. Вплив на здатність до керування автотранспортом та управління механізмами Оскільки вакцина Пентаксим® застосовується для вакцинації дітей, вплив препарату на здатність керувати транспортними засобами та займатися іншими потенційно небезпечними видами діяльності не вивчався.Умови відпустки з аптекЗа рецептомВідео на цю тему
370,00 грн
167,00 грн
Склад, форма випуску та упаковкаГель для зовнішнього застосування - 1 г: Активні компоненти: кетопрофен – 50 мг; Допоміжні речовини: настоянка червоного стручкового перцю - 40 мг, диметилсульфоксид (димексид) - 30 мг, камфора - 30 мг, олія м'яти перцевої листя - 9 мг, гіпромелоза - 20 мг, натрію гідроксид - 7.5 мг, етанол 96% - 3 вода очищена – до 1000 мг. Гель по 30 г, 50 г або 100 г у тубах алюмінієвих з бушонами полімерними, за ТУ 9467-004-32807885-2008. Тубу разом з інструкцією із застосування поміщають у пачку з картону.Опис лікарської формиГель для зовнішнього застосування: прозорий або напівпрозорий, однорідний, від жовтуватого до червонувато-коричневого кольору, з характерним запахом; допускається наявність опалесценції та бульбашок повітря.Фармакотерапевтична групаНестероїдні протизапальні засоби для зовнішнього застосування.ФармакокінетикаПри прийомі внутрішньо та ректальному введенні кетопрофен добре абсорбується із ШКТ. Cmax у плазмі прийому внутрішньо досягається через 1-5 год (залежно від лікарської форми), при ректальному введенні - через 45-60 хв, внутрішньом'язовому введенні - через 20-30 хв, внутрішньовенному введенні - через 5 хв. Зв'язування із білками плазми становить 99%. Внаслідок вираженої ліпофільності швидко проникає через гематоенцефалічний бар'єр. Css у плазмі крові та спинномозковій рідині зберігається від 2 до 18 год. Кетопрофен добре проникає в синовіальну рідину, де його концентрація через 4 години після прийому перевищує таку в плазмі. Метаболізується шляхом зв'язування з глюкуроновою кислотою та меншою мірою за рахунок гідроксилювання. Виводиться головним чином нирками та значно меншою мірою через кишечник. T1/2 кетопрофену з плазми після прийому внутрішньо становить 1.5-2 год, після ректального введення - близько 2 год, після внутрішньом'язового введення - 1.27 год, після внутрішньовенного введення - 2 год.ФармакодинамікаНПЗЗ, похідне пропіонової кислоти. Чинить аналгетичну, протизапальну та жарознижувальну дію. Механізм дії пов'язаний з пригніченням активності ЦОГ – основного ферменту метаболізму арахідонової кислоти, що є попередником простагландинів, які відіграють головну роль у патогенезі запалення, болю та лихоманки. Виражена аналгетичну дію кетопрофену обумовлена двома механізмами: периферичним (опосередковано, через придушення синтезу простагландинів) і центральним (обумовленим інгібуванням синтезу простагландинів у центральній і периферичній нервовій системі, а також дією на біологічну активність інших нейротропних субстанцій, що грають ключову роль мозку). Крім того, кетопрофен має антибрадикінінову активність, стабілізує лізосомальні мембрани, викликає значне гальмування активності нейтрофілів у хворих з ревматоїдним артритом. Пригнічує агрегацію тромбоцитів.Показання до застосуванняСуглобовий синдром (ревматоїдний артрит, остеоартрит, анкілозуючий спондиліт, подагра); симптоматичне лікування запально-дегенеративних захворювань опорно-рухового апарату (періартрит, артросиновіт, тендиніт, тендосиновіт, бурсит, люмбаго), болі в хребті, невралгії, міалгії. Неускладнені травми, зокрема спортивні, вивихи, розтягнення або розрив зв'язок та сухожилля, забиття, посттравматичні болі. У складі комбінованої терапії запальних захворювань вен, лімфатичних судин, лімфовузлів (флебіт, перифлебіт, лімфангіїт, поверхневий лімфаденіт).Протипоказання до застосуванняДля прийому внутрішньо: ерозивно-виразкові ураження шлунково-кишкового тракту у фазі загострення, "аспіринова тріада", виражені порушення функції печінки та/або нирок; ІІІ триместр вагітності; вік до 15 років (для пігулок ретард); підвищена чутливість до кетопрофену та саліцилатів. Для ректального застосування: проктит та кровотечі з прямої кишки в анамнезі. Для зовнішнього застосування: мокнучі дерматози, екзема, інфіковані садна, рани.Вагітність та лактаціяПротипоказаний до застосування у III триместрі вагітності. У І та ІІ триместрах вагітності застосування кетопрофену можливе у випадках, коли потенційна користь для матері перевищує потенційний ризик для плода. При необхідності застосування кетопрофену у період лактації грудне вигодовування рекомендується припинити.Побічна діяЗ боку травної системи: біль в епігастральній ділянці, нудота, блювання, запор або діарея, анорексія, гастралгії, порушення функції печінки; рідко – ерозивно-виразкові ураження ШКТ, кровотечі та перфорації ШКТ. З боку центральної нервової системи: головний біль, запаморочення, шум у вухах, сонливість. З боку сечовидільної системи: порушення функції нирок. Алергічні реакції: шкірний висип; рідко – бронхоспазм. Місцеві реакції: при застосуванні у формі свічок можливе подразнення слизової оболонки прямої кишки, хвороблива дефекація; при застосуванні у формі гелю - свербіж, шкірний висип у місці нанесення.Взаємодія з лікарськими засобамиПри одночасному застосуванні кетопрофену з іншими НПЗЗ підвищується ризик розвитку ерозивно-виразкових уражень ШКТ та кровотеч; з антигіпертензивними засобами (в т.ч. з бета-адреноблокаторами, інгібіторами АПФ, діуретиками) – можливе зменшення їхньої дії; з тромболітиками – підвищення ризику розвитку кровотеч. При одночасному застосуванні з ацетилсаліциловою кислотою можливе зменшення зв'язування кетопрофену з білками плазми та збільшення його плазмового кліренсу; з гепарином, тиклопідином – підвищення ризику розвитку кровотеч; з препаратами літію – можливе підвищення концентрації літію у плазмі крові до токсичної за рахунок зниження його ниркової екскреції. При одночасному застосуванні з діуретиками підвищується ризик розвитку ниркової недостатності внаслідок зменшення ниркового кровотоку, зумовленого пригніченням синтезу простагландинів, і на тлі гіповолемії. При одночасному застосуванні з пробенецидом можливе зменшення кліренсу кетопрофену та його зв'язування з білками плазми; з метотрексатом – можливе посилення побічної дії метотрексату. При одночасному застосуванні варфарину можливий розвиток тяжких, іноді фатальних кровотеч.Спосіб застосування та дозиПрепарат призначений для зовнішнього застосування. Гель слід наносити на чисту суху шкіру. Невелику кількість гелю (3-5 см) наносять тонким шаром, з подальшим обережним втиранням у запалені або болючі ділянки тіла. Препарат слід наносити 2-3 десь у день. Тривалість курсу лікування не повинна перевищувати 14 днів.ПередозуванняПри випадковому застосуванні препарату в дозі, що перевищує рекомендовану, ризик розвитку симптомів передозування мінімальний у зв'язку із вкрай низькою системною абсорбцією кетопрофену при зовнішньому застосуванні. При появі місцевих побічних ефектів слід відмінити препарат та промити місце нанесення. При випадковому проковтуванні великих кількостей гелю можлива поява системних небажаних реакцій, притаманних НПЗП. Необхідне промивання шлунка, прийом активованого вугілля.Запобіжні заходи та особливі вказівкиЗ особливою обережністю застосовують у пацієнтів із захворюваннями печінки та нирок, захворюваннями ШКТ в анамнезі, диспептичними симптомами, одразу після серйозних хірургічних втручань. У процесі лікування необхідний систематичний контроль функції печінки та нирок.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаГель для зовнішнього застосування - 1 г: Активні компоненти: кетопрофен – 50 мг; Допоміжні речовини: настоянка червоного стручкового перцю - 40 мг, диметилсульфоксид (димексид) - 30 мг, камфора - 30 мг, олія м'яти перцевої листя - 9 мг, гіпромелоза - 20 мг, натрію гідроксид - 7.5 мг, етанол 96% - 3 вода очищена – до 1000 мг. Гель по 30 г, 50 г або 100 г у тубах алюмінієвих з бушонами полімерними, за ТУ 9467-004-32807885-2008. Тубу разом з інструкцією із застосування поміщають у пачку з картону.Опис лікарської формиГель для зовнішнього застосування: прозорий або напівпрозорий, однорідний, від жовтуватого до червонувато-коричневого кольору, з характерним запахом; допускається наявність опалесценції та бульбашок повітря.Фармакотерапевтична групаНестероїдні протизапальні засоби для зовнішнього застосування.ФармакокінетикаПри прийомі внутрішньо та ректальному введенні кетопрофен добре абсорбується із ШКТ. Cmax у плазмі прийому внутрішньо досягається через 1-5 год (залежно від лікарської форми), при ректальному введенні - через 45-60 хв, внутрішньом'язовому введенні - через 20-30 хв, внутрішньовенному введенні - через 5 хв. Зв'язування із білками плазми становить 99%. Внаслідок вираженої ліпофільності швидко проникає через гематоенцефалічний бар'єр. Css у плазмі крові та спинномозковій рідині зберігається від 2 до 18 год. Кетопрофен добре проникає в синовіальну рідину, де його концентрація через 4 години після прийому перевищує таку в плазмі. Метаболізується шляхом зв'язування з глюкуроновою кислотою та меншою мірою за рахунок гідроксилювання. Виводиться головним чином нирками та значно меншою мірою через кишечник. T1/2 кетопрофену з плазми після прийому внутрішньо становить 1.5-2 год, після ректального введення - близько 2 год, після внутрішньом'язового введення - 1.27 год, після внутрішньовенного введення - 2 год.ФармакодинамікаНПЗЗ, похідне пропіонової кислоти. Чинить аналгетичну, протизапальну та жарознижувальну дію. Механізм дії пов'язаний з пригніченням активності ЦОГ – основного ферменту метаболізму арахідонової кислоти, що є попередником простагландинів, які відіграють головну роль у патогенезі запалення, болю та лихоманки. Виражена аналгетичну дію кетопрофену обумовлена двома механізмами: периферичним (опосередковано, через придушення синтезу простагландинів) і центральним (обумовленим інгібуванням синтезу простагландинів у центральній і периферичній нервовій системі, а також дією на біологічну активність інших нейротропних субстанцій, що грають ключову роль мозку). Крім того, кетопрофен має антибрадикінінову активність, стабілізує лізосомальні мембрани, викликає значне гальмування активності нейтрофілів у хворих з ревматоїдним артритом. Пригнічує агрегацію тромбоцитів.Показання до застосуванняСуглобовий синдром (ревматоїдний артрит, остеоартрит, анкілозуючий спондиліт, подагра); симптоматичне лікування запально-дегенеративних захворювань опорно-рухового апарату (періартрит, артросиновіт, тендиніт, тендосиновіт, бурсит, люмбаго), болі в хребті, невралгії, міалгії. Неускладнені травми, зокрема спортивні, вивихи, розтягнення або розрив зв'язок та сухожилля, забиття, посттравматичні болі. У складі комбінованої терапії запальних захворювань вен, лімфатичних судин, лімфовузлів (флебіт, перифлебіт, лімфангіїт, поверхневий лімфаденіт).Протипоказання до застосуванняДля прийому внутрішньо: ерозивно-виразкові ураження шлунково-кишкового тракту у фазі загострення, "аспіринова тріада", виражені порушення функції печінки та/або нирок; ІІІ триместр вагітності; вік до 15 років (для пігулок ретард); підвищена чутливість до кетопрофену та саліцилатів. Для ректального застосування: проктит та кровотечі з прямої кишки в анамнезі. Для зовнішнього застосування: мокнучі дерматози, екзема, інфіковані садна, рани.Вагітність та лактаціяПротипоказаний до застосування у III триместрі вагітності. У І та ІІ триместрах вагітності застосування кетопрофену можливе у випадках, коли потенційна користь для матері перевищує потенційний ризик для плода. При необхідності застосування кетопрофену у період лактації грудне вигодовування рекомендується припинити.Побічна діяЗ боку травної системи: біль в епігастральній ділянці, нудота, блювання, запор або діарея, анорексія, гастралгії, порушення функції печінки; рідко – ерозивно-виразкові ураження ШКТ, кровотечі та перфорації ШКТ. З боку центральної нервової системи: головний біль, запаморочення, шум у вухах, сонливість. З боку сечовидільної системи: порушення функції нирок. Алергічні реакції: шкірний висип; рідко – бронхоспазм. Місцеві реакції: при застосуванні у формі свічок можливе подразнення слизової оболонки прямої кишки, хвороблива дефекація; при застосуванні у формі гелю - свербіж, шкірний висип у місці нанесення.Взаємодія з лікарськими засобамиПри одночасному застосуванні кетопрофену з іншими НПЗЗ підвищується ризик розвитку ерозивно-виразкових уражень ШКТ та кровотеч; з антигіпертензивними засобами (в т.ч. з бета-адреноблокаторами, інгібіторами АПФ, діуретиками) – можливе зменшення їхньої дії; з тромболітиками – підвищення ризику розвитку кровотеч. При одночасному застосуванні з ацетилсаліциловою кислотою можливе зменшення зв'язування кетопрофену з білками плазми та збільшення його плазмового кліренсу; з гепарином, тиклопідином – підвищення ризику розвитку кровотеч; з препаратами літію – можливе підвищення концентрації літію у плазмі крові до токсичної за рахунок зниження його ниркової екскреції. При одночасному застосуванні з діуретиками підвищується ризик розвитку ниркової недостатності внаслідок зменшення ниркового кровотоку, зумовленого пригніченням синтезу простагландинів, і на тлі гіповолемії. При одночасному застосуванні з пробенецидом можливе зменшення кліренсу кетопрофену та його зв'язування з білками плазми; з метотрексатом – можливе посилення побічної дії метотрексату. При одночасному застосуванні варфарину можливий розвиток тяжких, іноді фатальних кровотеч.Спосіб застосування та дозиПрепарат призначений для зовнішнього застосування. Гель слід наносити на чисту суху шкіру. Невелику кількість гелю (3-5 см) наносять тонким шаром, з подальшим обережним втиранням у запалені або болючі ділянки тіла. Препарат слід наносити 2-3 десь у день. Тривалість курсу лікування не повинна перевищувати 14 днів.ПередозуванняПри випадковому застосуванні препарату в дозі, що перевищує рекомендовану, ризик розвитку симптомів передозування мінімальний у зв'язку із вкрай низькою системною абсорбцією кетопрофену при зовнішньому застосуванні. При появі місцевих побічних ефектів слід відмінити препарат та промити місце нанесення. При випадковому проковтуванні великих кількостей гелю можлива поява системних небажаних реакцій, притаманних НПЗП. Необхідне промивання шлунка, прийом активованого вугілля.Запобіжні заходи та особливі вказівкиЗ особливою обережністю застосовують у пацієнтів із захворюваннями печінки та нирок, захворюваннями ШКТ в анамнезі, диспептичними симптомами, одразу після серйозних хірургічних втручань. У процесі лікування необхідний систематичний контроль функції печінки та нирок.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаГель для зовнішнього застосування - 1 г: Активні компоненти: кетопрофен – 50 мг; Допоміжні речовини: настоянка червоного стручкового перцю - 40 мг, диметилсульфоксид (димексид) - 30 мг, камфора - 30 мг, олія м'яти перцевої листя - 9 мг, гіпромелоза - 20 мг, натрію гідроксид - 7.5 мг, етанол 96% - 3 вода очищена – до 1000 мг. Гель по 30 г, 50 г або 100 г у тубах алюмінієвих з бушонами полімерними, за ТУ 9467-004-32807885-2008. Тубу разом з інструкцією із застосування поміщають у пачку з картону.Опис лікарської формиГель для зовнішнього застосування: прозорий або напівпрозорий, однорідний, від жовтуватого до червонувато-коричневого кольору, з характерним запахом; допускається наявність опалесценції та бульбашок повітря.Фармакотерапевтична групаНестероїдні протизапальні засоби для зовнішнього застосування.ФармакокінетикаПри прийомі внутрішньо та ректальному введенні кетопрофен добре абсорбується із ШКТ. Cmax у плазмі прийому внутрішньо досягається через 1-5 год (залежно від лікарської форми), при ректальному введенні - через 45-60 хв, внутрішньом'язовому введенні - через 20-30 хв, внутрішньовенному введенні - через 5 хв. Зв'язування із білками плазми становить 99%. Внаслідок вираженої ліпофільності швидко проникає через гематоенцефалічний бар'єр. Css у плазмі крові та спинномозковій рідині зберігається від 2 до 18 год. Кетопрофен добре проникає в синовіальну рідину, де його концентрація через 4 години після прийому перевищує таку в плазмі. Метаболізується шляхом зв'язування з глюкуроновою кислотою та меншою мірою за рахунок гідроксилювання. Виводиться головним чином нирками та значно меншою мірою через кишечник. T1/2 кетопрофену з плазми після прийому внутрішньо становить 1.5-2 год, після ректального введення - близько 2 год, після внутрішньом'язового введення - 1.27 год, після внутрішньовенного введення - 2 год.ФармакодинамікаНПЗЗ, похідне пропіонової кислоти. Чинить аналгетичну, протизапальну та жарознижувальну дію. Механізм дії пов'язаний з пригніченням активності ЦОГ – основного ферменту метаболізму арахідонової кислоти, що є попередником простагландинів, які відіграють головну роль у патогенезі запалення, болю та лихоманки. Виражена аналгетичну дію кетопрофену обумовлена двома механізмами: периферичним (опосередковано, через придушення синтезу простагландинів) і центральним (обумовленим інгібуванням синтезу простагландинів у центральній і периферичній нервовій системі, а також дією на біологічну активність інших нейротропних субстанцій, що грають ключову роль мозку). Крім того, кетопрофен має антибрадикінінову активність, стабілізує лізосомальні мембрани, викликає значне гальмування активності нейтрофілів у хворих з ревматоїдним артритом. Пригнічує агрегацію тромбоцитів.Показання до застосуванняСуглобовий синдром (ревматоїдний артрит, остеоартрит, анкілозуючий спондиліт, подагра); симптоматичне лікування запально-дегенеративних захворювань опорно-рухового апарату (періартрит, артросиновіт, тендиніт, тендосиновіт, бурсит, люмбаго), болі в хребті, невралгії, міалгії. Неускладнені травми, зокрема спортивні, вивихи, розтягнення або розрив зв'язок та сухожилля, забиття, посттравматичні болі. У складі комбінованої терапії запальних захворювань вен, лімфатичних судин, лімфовузлів (флебіт, перифлебіт, лімфангіїт, поверхневий лімфаденіт).Протипоказання до застосуванняДля прийому внутрішньо: ерозивно-виразкові ураження шлунково-кишкового тракту у фазі загострення, "аспіринова тріада", виражені порушення функції печінки та/або нирок; ІІІ триместр вагітності; вік до 15 років (для пігулок ретард); підвищена чутливість до кетопрофену та саліцилатів. Для ректального застосування: проктит та кровотечі з прямої кишки в анамнезі. Для зовнішнього застосування: мокнучі дерматози, екзема, інфіковані садна, рани.Вагітність та лактаціяПротипоказаний до застосування у III триместрі вагітності. У І та ІІ триместрах вагітності застосування кетопрофену можливе у випадках, коли потенційна користь для матері перевищує потенційний ризик для плода. При необхідності застосування кетопрофену у період лактації грудне вигодовування рекомендується припинити.Побічна діяЗ боку травної системи: біль в епігастральній ділянці, нудота, блювання, запор або діарея, анорексія, гастралгії, порушення функції печінки; рідко – ерозивно-виразкові ураження ШКТ, кровотечі та перфорації ШКТ. З боку центральної нервової системи: головний біль, запаморочення, шум у вухах, сонливість. З боку сечовидільної системи: порушення функції нирок. Алергічні реакції: шкірний висип; рідко – бронхоспазм. Місцеві реакції: при застосуванні у формі свічок можливе подразнення слизової оболонки прямої кишки, хвороблива дефекація; при застосуванні у формі гелю - свербіж, шкірний висип у місці нанесення.Взаємодія з лікарськими засобамиПри одночасному застосуванні кетопрофену з іншими НПЗЗ підвищується ризик розвитку ерозивно-виразкових уражень ШКТ та кровотеч; з антигіпертензивними засобами (в т.ч. з бета-адреноблокаторами, інгібіторами АПФ, діуретиками) – можливе зменшення їхньої дії; з тромболітиками – підвищення ризику розвитку кровотеч. При одночасному застосуванні з ацетилсаліциловою кислотою можливе зменшення зв'язування кетопрофену з білками плазми та збільшення його плазмового кліренсу; з гепарином, тиклопідином – підвищення ризику розвитку кровотеч; з препаратами літію – можливе підвищення концентрації літію у плазмі крові до токсичної за рахунок зниження його ниркової екскреції. При одночасному застосуванні з діуретиками підвищується ризик розвитку ниркової недостатності внаслідок зменшення ниркового кровотоку, зумовленого пригніченням синтезу простагландинів, і на тлі гіповолемії. При одночасному застосуванні з пробенецидом можливе зменшення кліренсу кетопрофену та його зв'язування з білками плазми; з метотрексатом – можливе посилення побічної дії метотрексату. При одночасному застосуванні варфарину можливий розвиток тяжких, іноді фатальних кровотеч.Спосіб застосування та дозиПрепарат призначений для зовнішнього застосування. Гель слід наносити на чисту суху шкіру. Невелику кількість гелю (3-5 см) наносять тонким шаром, з подальшим обережним втиранням у запалені або болючі ділянки тіла. Препарат слід наносити 2-3 десь у день. Тривалість курсу лікування не повинна перевищувати 14 днів.ПередозуванняПри випадковому застосуванні препарату в дозі, що перевищує рекомендовану, ризик розвитку симптомів передозування мінімальний у зв'язку із вкрай низькою системною абсорбцією кетопрофену при зовнішньому застосуванні. При появі місцевих побічних ефектів слід відмінити препарат та промити місце нанесення. При випадковому проковтуванні великих кількостей гелю можлива поява системних небажаних реакцій, притаманних НПЗП. Необхідне промивання шлунка, прийом активованого вугілля.Запобіжні заходи та особливі вказівкиЗ особливою обережністю застосовують у пацієнтів із захворюваннями печінки та нирок, захворюваннями ШКТ в анамнезі, диспептичними симптомами, одразу після серйозних хірургічних втручань. У процесі лікування необхідний систематичний контроль функції печінки та нирок.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. діючі речовини: парацетамол – 325,0 мг, напроксен – 100,0 мг, кофеїн безводний – 50,0 мг, дротаверину гідрохлорид – 40,0 мг, феніраміну малеат – 10.0 мг; Допоміжні речовини: целюлоза мікрокристалічна - 128,0000 мг, крохмаль картопляний - 55,3800 мг, кроскармелоза натрію - 32,0000 мг, гіпролоза (гідроксипропілцелюлоза) - 32,5200 мг, 000000 ) – 0,3000 мг, магнію стеарат – 7,2000 мг, тальк – 16,1200 мг, барвник хіноліновий жовтий (Е 104) – 0,4608 мг, індигокармін (Е 132) – 0,0192 мг; Оболонка: гіпромелоза (гідроксипропілметилцелюлоза) - 12,1700 мг, повідон (полівінілпіролідон середньомолекулярний медичний, повідон-К25) -3,8700 мг, полісорбат-80 (твін-80) - 1,1000 мг, титану діоксид тальк - 4,2180 мг, барвник хіноліновий жовтий (Е 104) - 0,2000 мг, індигокармін (Е 132) -0,0127 мг або Оболонка ОПАДРАЙ 13А210001 Зелений (OPADRY 13А210002 1700 мг, повідон -3,8700 мг, полісорбат-80 - 1,1000 мг, титану діоксид - 3,4300 мг, тальк - 4,2180 мг, хіноліновий жовтий - 0,2000 мг, FD&C блакитний #2/ індіго кармін 0,0127 мг]. По 2, 4, 6, 10 або 12 таблеток у контурне осередкове пакування з плівки полівінілхлоридної та фольги алюмінієвої друкованої лакованої. 1 або 2 контурні коміркові упаковки разом з інструкцією із застосування в пачку з картону.Опис лікарської формиТаблетки, покриті плівковою оболонкою від світло-зеленого до зеленого кольору, двоопуклі у формі капсули зі скошеними краями, з ризиком на одному боці та тисненням PENTALGIN на інший. На поперечному розрізі ядро світло-зеленого кольору із білими вкрапленнями.Фармакотерапевтична групаАналгезуючий засіб (аналгезуючий ненаркотичний засіб+НПЗП+психостимулюючий засіб+спазмолітичний засіб+H1-гістамінових рецепторів блокатор).ФармакодинамікаКомбінований препарат, що має аналгетичну, протизапальну, спазмолітичну, жарознижувальну дію. Парацетамол - ненаркотичний аналгетик, має жарознижувальну та знеболювальну дію, обумовлену блокадою циклооксигенази в центральній нервовій системі та впливом на центри болю та терморегуляції. Напроксен - нестероїдний протизапальний препарат, що має протизапальну, аналгетичну та жарознижувальну дію, пов'язану з неселективним придушенням активності циклооксигенази, що регулює синтез простагландинів. Кофеїн – викликає розширення кровоносних судин скелетних м'язів, серця, нирок; підвищує розумову та фізичну працездатність, сприяє усуненню втоми та сонливості; збільшує проникність гістогематичних бар'єрів та підвищує біодоступність ненаркотичних аналгетиків, сприяючи цим посиленню терапевтичного ефекту. Чинить тонізуючу дію на судини головного мозку. Дротаверин - має міотропну спазмолітичну дію, обумовлену інгібуванням фосфодіестерази IV, діє на гладкі м'язи в шлунково-кишковому тракті, жовчовивідних шляхах, сечостатевих та судинних системах. Фенірамін – блокатор Н1-гістамінових рецепторів. Має спазмолітичну та легку седативну дію, зменшує явища ексудації, а також посилює аналгетичну дію парацетамолу та напроксену.Показання до застосуванняБольовий синдром різного генезу, у тому числі при болях у суглобах, м'язах, радикуліті, менструальних болях, невралгіях, зубному та головному болях (у тому числі при головному болі, обумовленому спазмом судин головного мозку). Больовий синдром, пов'язаний зі спазмом гладкої мускулатури, у тому числі при хронічному холециститі, жовчнокам'яній хворобі, постхолецистектомічному синдромі, нирковій коліці. Посттравматичний та післяопераційний больовий синдром, у тому числі супроводжується запаленням. Простудні захворювання, що супроводжуються гарячковим синдромом (як симптоматична терапія).Протипоказання до застосуванняПідвищена чутливість до компонентів препарату, ерозивно-виразкові ураження шлунково-кишкового тракту (у фазі загострення), шлунково-кишкова кровотеча, повне або неповне поєднання бронхіальної астми, рецидивуючого поліпозу носа та приносових кислот і непереносимості числа в анамнезі, тяжка печінкова та/або ниркова недостатність, пригнічення кістковомозкового кровотворення, стан після проведення аорто-коронарного шунтування; тяжкі органічні захворювання серцево-судинної системи (у тому числі гострий інфаркт міокарда), пароксизмальна тахікардія, часта шлуночкова екстрасистолія, тяжка артеріальна гіпертензія, гіперкаліємія, дитячий вік до 18 років, вагітність та період лактації. З обережністю: Цереброваскулярні захворювання, цукровий діабет, захворювання периферичних артерій, виразкові ураження шлунково-кишкового тракту в анамнезі, ниркова та печінкова недостатність легкого або середнього ступеня тяжкості, вірусний гепатит, алкогольне ураження печінки, доброякісні гіпербілірубінемії (синдром) та схильність до судомних нападів, дефіцит глюкозо-6-фосфатдегідрогенази, літній вік. Якщо у Вас є одне з перелічених захворювань/станів, перед прийомом препарату обов'язково проконсультуйтеся з лікарем.Вагітність та лактаціяПрепарат протипоказаний для застосування при вагітності. При необхідності застосування препарату в період лактації слід припинити вигодовування груддю.Побічна діяАлергічні реакції: висипання на шкірі, свербіж, кропив'янка, ангіоневротичний набряк. З боку органів кровотворення: тромбоцитопенія, лейкопенія, агранулоцитоз, анемія, метгемоглобінемія. З боку нервової системи: збудження, тривожність, посилення рефлексів, тремор, біль голови, порушення сну, запаморочення, зниження концентрації уваги. З боку серцево-судинної системи: серцебиття, аритмії, підвищення артеріального тиску. З боку травної системи: ерозивно-виразкові ураження шлунково-кишкового тракту, нудота, блювання, дискомфорт в епігастрії, біль у животі, запор, порушення функції печінки. З боку сечовидільної системи: Порушення функції нирок. З боку органів чуття: зниження слуху, шум у вухах, підвищення внутрішньоочного тиску у пацієнтів із закритокутовою глаукомою. Інші: дерматит, тахіпное (почастішання дихання). Якщо будь-які вказані в інструкції побічні ефекти посилюються, або Ви помітили будь-які інші побічні ефекти, не вказані в інструкції, повідомте про це лікаря.Взаємодія з лікарськими засобамиСлід уникати одночасного прийому препарату з барбітуратами, трициклічними антидепресантами, рифампіцином та алкогольними напоями (збільшується ризик гепатотоксичної дії). Парацетамол посилює дію антикоагулянтів непрямої дії та знижує ефективність урикозуричних препаратів. Тривале використання барбітуратів знижує ефективність парацетамолу. Одночасне застосування парацетамолу з етанолом підвищує ризик виникнення гострого панкреатиту. Інгібітори мікросомального окиснення (в т.ч. циметидину) знижують ризик гепатотоксичної дії парацетамолу. Дифлунісал підвищує плазмову концентрацію парацетамолу на 50%, що підвищує ризик розвитку гепатотоксичності. Напроксен може викликати зменшення діуретичного ефекту фуросеміду, посилення ефекту непрямих антикоагулянтів, підвищує токсичність сульфаніламідів та метотрексату, знижує виведення літію та підвищує його концентрацію у плазмі крові. При сумісному застосуванні кофеїну та барбітуратів, примідону, протисудомних засобів (похідні гідантоїну, особливо фенітоїн) можливе посилення метаболізму та збільшення кліренсу кофеїну; при одночасному прийомі кофеїну та циметидину, пероральних контрацептивних засобів, дисульфіраму, ципрофлоксацину, норфлоксацину – зниження метаболізму кофеїну в печінці (уповільнення його виведення та збільшення концентрації в крові). Одночасне вживання кофеїновмісних напоїв та інших засобів, що стимулюють центральну нервову систему, може призводити до надмірної стимуляції центральної нервової системи. При одночасному застосуванні дротаверин може послабити протипаркінсонічний ефект леводопи. При одночасному застосуванні феніраміну з транквілізаторами, снодійними засобами, інгібіторами моноаміноксидази, алкоголем можливе посилення гнітючого впливу на центральну нервову систему.Спосіб застосування та дозиВсередину. Препарат приймають по 1 таблетці 1-3 десь у день. Максимальна добова доза – 4 таблетки. Тривалість лікування не більше 3 днів як жарознижувальний засіб і не більше 5 днів - як знеболюючий. Продовження лікування препаратом можливе лише після консультації з лікарем. Не перевищувати вказану дозу!ПередозуванняСимптоми: блідість шкірних покровів, анорексія (відсутність апетиту), біль у животі, нудота, блювання, шлунково-кишкова кровотеча, збудження, руховий занепокоєння, сплутаність свідомості, тахікардія, аритмія, гіпертермія (підвищення температури тіла), тремор або м'язові посмикування; епілептичні напади, підвищення активності "печінкових" трансаміназ, гепатонекроз, збільшення протромбінового часу. Симптоми порушення функції печінки можуть виникнути через 12-48 годин після передозування. При тяжкому передозуванні розвивається печінкова недостатність з прогресуючою енцефалопатією, кома, смерть; гостра ниркова недостатність із тубулярним некрозом; аритмія, панкреатит. При підозрі передозування необхідно негайно звернутися за лікарською допомогою. Лікування: промивання шлунка із наступним прийомом активованого вугілля. Специфічним антидотом при отруєнні парацетамолом є ацетилцистеїн. Введення ацетилцистеїну актуальне протягом 8 год. При шлунково-кишковій кровотечі необхідно введення антацидних засобів та промивання шлунка крижаним 0,9% розчином хлориду натрію; підтримання вентиляції легень та оксигенації; при епілептичних нападах – внутрішньовенне введення діазепаму; підтримання балансу рідини та солей.Запобіжні заходи та особливі вказівкиСлід уникати одночасного застосування препарату з іншими засобами, що містять парацетамол та/або інші нестероїдні протизапальні препарати, а також із засобами для полегшення симптомів застуди, грипу та закладеності носа. При застосуванні препарату понад 5-7 днів слід контролювати показники периферичної крові та функціональний стан печінки. Парацетамол спотворює результати лабораторних досліджень вмісту глюкози та сечової кислоти у плазмі крові. При необхідності визначення 17-кетостероїдів препарат слід відмінити за 48 годин до дослідження. Слід враховувати, що напроксен збільшує час кровотечі. Вплив кофеїну на центральну нервову систему залежить від типу нервової системи і може проявлятися як збудженням, і гальмуванням вищої нервової діяльності. У період лікування не слід вживати спиртовмісні напої. Вплив на здатність до керування автотранспортом та управління механізмами У період лікування необхідно дотримуватися обережності при керуванні автотранспортом та зайнятті іншими потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. діючі речовини: парацетамол – 325,0 мг, напроксен – 100,0 мг, кофеїн безводний – 50,0 мг, дротаверину гідрохлорид – 40,0 мг, феніраміну малеат – 10.0 мг; Допоміжні речовини: целюлоза мікрокристалічна - 128,0000 мг, крохмаль картопляний - 55,3800 мг, кроскармелоза натрію - 32,0000 мг, гіпролоза (гідроксипропілцелюлоза) - 32,5200 мг, 000000 ) – 0,3000 мг, магнію стеарат – 7,2000 мг, тальк – 16,1200 мг, барвник хіноліновий жовтий (Е 104) – 0,4608 мг, індигокармін (Е 132) – 0,0192 мг; Оболонка: гіпромелоза (гідроксипропілметилцелюлоза) - 12,1700 мг, повідон (полівінілпіролідон середньомолекулярний медичний, повідон-К25) -3,8700 мг, полісорбат-80 (твін-80) - 1,1000 мг, титану діоксид тальк - 4,2180 мг, барвник хіноліновий жовтий (Е 104) - 0,2000 мг, індигокармін (Е 132) -0,0127 мг або Оболонка ОПАДРАЙ 13А210001 Зелений (OPADRY 13А210002 1700 мг, повідон -3,8700 мг, полісорбат-80 - 1,1000 мг, титану діоксид - 3,4300 мг, тальк - 4,2180 мг, хіноліновий жовтий - 0,2000 мг, FD&C блакитний #2/ індіго кармін 0,0127 мг]. По 2, 4, 6, 10 або 12 таблеток у контурне осередкове пакування з плівки полівінілхлоридної та фольги алюмінієвої друкованої лакованої. 1 або 2 контурні коміркові упаковки разом з інструкцією із застосування в пачку з картону.Опис лікарської формиТаблетки, покриті плівковою оболонкою від світло-зеленого до зеленого кольору, двоопуклі у формі капсули зі скошеними краями, з ризиком на одному боці та тисненням PENTALGIN на інший. На поперечному розрізі ядро світло-зеленого кольору із білими вкрапленнями.Фармакотерапевтична групаАналгезуючий засіб (аналгезуючий ненаркотичний засіб+НПЗП+психостимулюючий засіб+спазмолітичний засіб+H1-гістамінових рецепторів блокатор).ФармакодинамікаКомбінований препарат, що має аналгетичну, протизапальну, спазмолітичну, жарознижувальну дію. Парацетамол - ненаркотичний аналгетик, має жарознижувальну та знеболювальну дію, обумовлену блокадою циклооксигенази в центральній нервовій системі та впливом на центри болю та терморегуляції. Напроксен - нестероїдний протизапальний препарат, що має протизапальну, аналгетичну та жарознижувальну дію, пов'язану з неселективним придушенням активності циклооксигенази, що регулює синтез простагландинів. Кофеїн – викликає розширення кровоносних судин скелетних м'язів, серця, нирок; підвищує розумову та фізичну працездатність, сприяє усуненню втоми та сонливості; збільшує проникність гістогематичних бар'єрів та підвищує біодоступність ненаркотичних аналгетиків, сприяючи цим посиленню терапевтичного ефекту. Чинить тонізуючу дію на судини головного мозку. Дротаверин - має міотропну спазмолітичну дію, обумовлену інгібуванням фосфодіестерази IV, діє на гладкі м'язи в шлунково-кишковому тракті, жовчовивідних шляхах, сечостатевих та судинних системах. Фенірамін – блокатор Н1-гістамінових рецепторів. Має спазмолітичну та легку седативну дію, зменшує явища ексудації, а також посилює аналгетичну дію парацетамолу та напроксену.Показання до застосуванняБольовий синдром різного генезу, у тому числі при болях у суглобах, м'язах, радикуліті, менструальних болях, невралгіях, зубному та головному болях (у тому числі при головному болі, обумовленому спазмом судин головного мозку). Больовий синдром, пов'язаний зі спазмом гладкої мускулатури, у тому числі при хронічному холециститі, жовчнокам'яній хворобі, постхолецистектомічному синдромі, нирковій коліці. Посттравматичний та післяопераційний больовий синдром, у тому числі супроводжується запаленням. Простудні захворювання, що супроводжуються гарячковим синдромом (як симптоматична терапія).Протипоказання до застосуванняПідвищена чутливість до компонентів препарату, ерозивно-виразкові ураження шлунково-кишкового тракту (у фазі загострення), шлунково-кишкова кровотеча, повне або неповне поєднання бронхіальної астми, рецидивуючого поліпозу носа та приносових кислот і непереносимості числа в анамнезі, тяжка печінкова та/або ниркова недостатність, пригнічення кістковомозкового кровотворення, стан після проведення аорто-коронарного шунтування; тяжкі органічні захворювання серцево-судинної системи (у тому числі гострий інфаркт міокарда), пароксизмальна тахікардія, часта шлуночкова екстрасистолія, тяжка артеріальна гіпертензія, гіперкаліємія, дитячий вік до 18 років, вагітність та період лактації. З обережністю: Цереброваскулярні захворювання, цукровий діабет, захворювання периферичних артерій, виразкові ураження шлунково-кишкового тракту в анамнезі, ниркова та печінкова недостатність легкого або середнього ступеня тяжкості, вірусний гепатит, алкогольне ураження печінки, доброякісні гіпербілірубінемії (синдром) та схильність до судомних нападів, дефіцит глюкозо-6-фосфатдегідрогенази, літній вік. Якщо у Вас є одне з перелічених захворювань/станів, перед прийомом препарату обов'язково проконсультуйтеся з лікарем.Вагітність та лактаціяПрепарат протипоказаний для застосування при вагітності. При необхідності застосування препарату в період лактації слід припинити вигодовування груддю.Побічна діяАлергічні реакції: висипання на шкірі, свербіж, кропив'янка, ангіоневротичний набряк. З боку органів кровотворення: тромбоцитопенія, лейкопенія, агранулоцитоз, анемія, метгемоглобінемія. З боку нервової системи: збудження, тривожність, посилення рефлексів, тремор, біль голови, порушення сну, запаморочення, зниження концентрації уваги. З боку серцево-судинної системи: серцебиття, аритмії, підвищення артеріального тиску. З боку травної системи: ерозивно-виразкові ураження шлунково-кишкового тракту, нудота, блювання, дискомфорт в епігастрії, біль у животі, запор, порушення функції печінки. З боку сечовидільної системи: Порушення функції нирок. З боку органів чуття: зниження слуху, шум у вухах, підвищення внутрішньоочного тиску у пацієнтів із закритокутовою глаукомою. Інші: дерматит, тахіпное (почастішання дихання). Якщо будь-які вказані в інструкції побічні ефекти посилюються, або Ви помітили будь-які інші побічні ефекти, не вказані в інструкції, повідомте про це лікаря.Взаємодія з лікарськими засобамиСлід уникати одночасного прийому препарату з барбітуратами, трициклічними антидепресантами, рифампіцином та алкогольними напоями (збільшується ризик гепатотоксичної дії). Парацетамол посилює дію антикоагулянтів непрямої дії та знижує ефективність урикозуричних препаратів. Тривале використання барбітуратів знижує ефективність парацетамолу. Одночасне застосування парацетамолу з етанолом підвищує ризик виникнення гострого панкреатиту. Інгібітори мікросомального окиснення (в т.ч. циметидину) знижують ризик гепатотоксичної дії парацетамолу. Дифлунісал підвищує плазмову концентрацію парацетамолу на 50%, що підвищує ризик розвитку гепатотоксичності. Напроксен може викликати зменшення діуретичного ефекту фуросеміду, посилення ефекту непрямих антикоагулянтів, підвищує токсичність сульфаніламідів та метотрексату, знижує виведення літію та підвищує його концентрацію у плазмі крові. При сумісному застосуванні кофеїну та барбітуратів, примідону, протисудомних засобів (похідні гідантоїну, особливо фенітоїн) можливе посилення метаболізму та збільшення кліренсу кофеїну; при одночасному прийомі кофеїну та циметидину, пероральних контрацептивних засобів, дисульфіраму, ципрофлоксацину, норфлоксацину – зниження метаболізму кофеїну в печінці (уповільнення його виведення та збільшення концентрації в крові). Одночасне вживання кофеїновмісних напоїв та інших засобів, що стимулюють центральну нервову систему, може призводити до надмірної стимуляції центральної нервової системи. При одночасному застосуванні дротаверин може послабити протипаркінсонічний ефект леводопи. При одночасному застосуванні феніраміну з транквілізаторами, снодійними засобами, інгібіторами моноаміноксидази, алкоголем можливе посилення гнітючого впливу на центральну нервову систему.Спосіб застосування та дозиВсередину. Препарат приймають по 1 таблетці 1-3 десь у день. Максимальна добова доза – 4 таблетки. Тривалість лікування не більше 3 днів як жарознижувальний засіб і не більше 5 днів - як знеболюючий. Продовження лікування препаратом можливе лише після консультації з лікарем. Не перевищувати вказану дозу!ПередозуванняСимптоми: блідість шкірних покровів, анорексія (відсутність апетиту), біль у животі, нудота, блювання, шлунково-кишкова кровотеча, збудження, руховий занепокоєння, сплутаність свідомості, тахікардія, аритмія, гіпертермія (підвищення температури тіла), тремор або м'язові посмикування; епілептичні напади, підвищення активності "печінкових" трансаміназ, гепатонекроз, збільшення протромбінового часу. Симптоми порушення функції печінки можуть виникнути через 12-48 годин після передозування. При тяжкому передозуванні розвивається печінкова недостатність з прогресуючою енцефалопатією, кома, смерть; гостра ниркова недостатність із тубулярним некрозом; аритмія, панкреатит. При підозрі передозування необхідно негайно звернутися за лікарською допомогою. Лікування: промивання шлунка із наступним прийомом активованого вугілля. Специфічним антидотом при отруєнні парацетамолом є ацетилцистеїн. Введення ацетилцистеїну актуальне протягом 8 год. При шлунково-кишковій кровотечі необхідно введення антацидних засобів та промивання шлунка крижаним 0,9% розчином хлориду натрію; підтримання вентиляції легень та оксигенації; при епілептичних нападах – внутрішньовенне введення діазепаму; підтримання балансу рідини та солей.Запобіжні заходи та особливі вказівкиСлід уникати одночасного застосування препарату з іншими засобами, що містять парацетамол та/або інші нестероїдні протизапальні препарати, а також із засобами для полегшення симптомів застуди, грипу та закладеності носа. При застосуванні препарату понад 5-7 днів слід контролювати показники периферичної крові та функціональний стан печінки. Парацетамол спотворює результати лабораторних досліджень вмісту глюкози та сечової кислоти у плазмі крові. При необхідності визначення 17-кетостероїдів препарат слід відмінити за 48 годин до дослідження. Слід враховувати, що напроксен збільшує час кровотечі. Вплив кофеїну на центральну нервову систему залежить від типу нервової системи і може проявлятися як збудженням, і гальмуванням вищої нервової діяльності. У період лікування не слід вживати спиртовмісні напої. Вплив на здатність до керування автотранспортом та управління механізмами У період лікування необхідно дотримуватися обережності при керуванні автотранспортом та зайнятті іншими потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. діючі речовини: парацетамол – 325,0 мг, напроксен – 100,0 мг, кофеїн безводний – 50,0 мг, дротаверину гідрохлорид – 40,0 мг, феніраміну малеат – 10.0 мг; Допоміжні речовини: целюлоза мікрокристалічна - 128,0000 мг, крохмаль картопляний - 55,3800 мг, кроскармелоза натрію - 32,0000 мг, гіпролоза (гідроксипропілцелюлоза) - 32,5200 мг, 000000 ) – 0,3000 мг, магнію стеарат – 7,2000 мг, тальк – 16,1200 мг, барвник хіноліновий жовтий (Е 104) – 0,4608 мг, індигокармін (Е 132) – 0,0192 мг; Оболонка: гіпромелоза (гідроксипропілметилцелюлоза) - 12,1700 мг, повідон (полівінілпіролідон середньомолекулярний медичний, повідон-К25) -3,8700 мг, полісорбат-80 (твін-80) - 1,1000 мг, титану діоксид тальк - 4,2180 мг, барвник хіноліновий жовтий (Е 104) - 0,2000 мг, індигокармін (Е 132) -0,0127 мг або Оболонка ОПАДРАЙ 13А210001 Зелений (OPADRY 13А210002 1700 мг, повідон -3,8700 мг, полісорбат-80 - 1,1000 мг, титану діоксид - 3,4300 мг, тальк - 4,2180 мг, хіноліновий жовтий - 0,2000 мг, FD&C блакитний #2/ індіго кармін 0,0127 мг]. По 2, 4, 6, 10 або 12 таблеток у контурне осередкове пакування з плівки полівінілхлоридної та фольги алюмінієвої друкованої лакованої. 1 або 2 контурні коміркові упаковки разом з інструкцією із застосування в пачку з картону.Опис лікарської формиТаблетки, покриті плівковою оболонкою від світло-зеленого до зеленого кольору, двоопуклі у формі капсули зі скошеними краями, з ризиком на одному боці та тисненням PENTALGIN на інший. На поперечному розрізі ядро світло-зеленого кольору із білими вкрапленнями.Фармакотерапевтична групаАналгезуючий засіб (аналгезуючий ненаркотичний засіб+НПЗП+психостимулюючий засіб+спазмолітичний засіб+H1-гістамінових рецепторів блокатор).ФармакодинамікаКомбінований препарат, що має аналгетичну, протизапальну, спазмолітичну, жарознижувальну дію. Парацетамол - ненаркотичний аналгетик, має жарознижувальну та знеболювальну дію, обумовлену блокадою циклооксигенази в центральній нервовій системі та впливом на центри болю та терморегуляції. Напроксен - нестероїдний протизапальний препарат, що має протизапальну, аналгетичну та жарознижувальну дію, пов'язану з неселективним придушенням активності циклооксигенази, що регулює синтез простагландинів. Кофеїн – викликає розширення кровоносних судин скелетних м'язів, серця, нирок; підвищує розумову та фізичну працездатність, сприяє усуненню втоми та сонливості; збільшує проникність гістогематичних бар'єрів та підвищує біодоступність ненаркотичних аналгетиків, сприяючи цим посиленню терапевтичного ефекту. Чинить тонізуючу дію на судини головного мозку. Дротаверин - має міотропну спазмолітичну дію, обумовлену інгібуванням фосфодіестерази IV, діє на гладкі м'язи в шлунково-кишковому тракті, жовчовивідних шляхах, сечостатевих та судинних системах. Фенірамін – блокатор Н1-гістамінових рецепторів. Має спазмолітичну та легку седативну дію, зменшує явища ексудації, а також посилює аналгетичну дію парацетамолу та напроксену.Показання до застосуванняБольовий синдром різного генезу, у тому числі при болях у суглобах, м'язах, радикуліті, менструальних болях, невралгіях, зубному та головному болях (у тому числі при головному болі, обумовленому спазмом судин головного мозку). Больовий синдром, пов'язаний зі спазмом гладкої мускулатури, у тому числі при хронічному холециститі, жовчнокам'яній хворобі, постхолецистектомічному синдромі, нирковій коліці. Посттравматичний та післяопераційний больовий синдром, у тому числі супроводжується запаленням. Простудні захворювання, що супроводжуються гарячковим синдромом (як симптоматична терапія).Протипоказання до застосуванняПідвищена чутливість до компонентів препарату, ерозивно-виразкові ураження шлунково-кишкового тракту (у фазі загострення), шлунково-кишкова кровотеча, повне або неповне поєднання бронхіальної астми, рецидивуючого поліпозу носа та приносових кислот і непереносимості числа в анамнезі, тяжка печінкова та/або ниркова недостатність, пригнічення кістковомозкового кровотворення, стан після проведення аорто-коронарного шунтування; тяжкі органічні захворювання серцево-судинної системи (у тому числі гострий інфаркт міокарда), пароксизмальна тахікардія, часта шлуночкова екстрасистолія, тяжка артеріальна гіпертензія, гіперкаліємія, дитячий вік до 18 років, вагітність та період лактації. З обережністю: Цереброваскулярні захворювання, цукровий діабет, захворювання периферичних артерій, виразкові ураження шлунково-кишкового тракту в анамнезі, ниркова та печінкова недостатність легкого або середнього ступеня тяжкості, вірусний гепатит, алкогольне ураження печінки, доброякісні гіпербілірубінемії (синдром) та схильність до судомних нападів, дефіцит глюкозо-6-фосфатдегідрогенази, літній вік. Якщо у Вас є одне з перелічених захворювань/станів, перед прийомом препарату обов'язково проконсультуйтеся з лікарем.Вагітність та лактаціяПрепарат протипоказаний для застосування при вагітності. При необхідності застосування препарату в період лактації слід припинити вигодовування груддю.Побічна діяАлергічні реакції: висипання на шкірі, свербіж, кропив'янка, ангіоневротичний набряк. З боку органів кровотворення: тромбоцитопенія, лейкопенія, агранулоцитоз, анемія, метгемоглобінемія. З боку нервової системи: збудження, тривожність, посилення рефлексів, тремор, біль голови, порушення сну, запаморочення, зниження концентрації уваги. З боку серцево-судинної системи: серцебиття, аритмії, підвищення артеріального тиску. З боку травної системи: ерозивно-виразкові ураження шлунково-кишкового тракту, нудота, блювання, дискомфорт в епігастрії, біль у животі, запор, порушення функції печінки. З боку сечовидільної системи: Порушення функції нирок. З боку органів чуття: зниження слуху, шум у вухах, підвищення внутрішньоочного тиску у пацієнтів із закритокутовою глаукомою. Інші: дерматит, тахіпное (почастішання дихання). Якщо будь-які вказані в інструкції побічні ефекти посилюються, або Ви помітили будь-які інші побічні ефекти, не вказані в інструкції, повідомте про це лікаря.Взаємодія з лікарськими засобамиСлід уникати одночасного прийому препарату з барбітуратами, трициклічними антидепресантами, рифампіцином та алкогольними напоями (збільшується ризик гепатотоксичної дії). Парацетамол посилює дію антикоагулянтів непрямої дії та знижує ефективність урикозуричних препаратів. Тривале використання барбітуратів знижує ефективність парацетамолу. Одночасне застосування парацетамолу з етанолом підвищує ризик виникнення гострого панкреатиту. Інгібітори мікросомального окиснення (в т.ч. циметидину) знижують ризик гепатотоксичної дії парацетамолу. Дифлунісал підвищує плазмову концентрацію парацетамолу на 50%, що підвищує ризик розвитку гепатотоксичності. Напроксен може викликати зменшення діуретичного ефекту фуросеміду, посилення ефекту непрямих антикоагулянтів, підвищує токсичність сульфаніламідів та метотрексату, знижує виведення літію та підвищує його концентрацію у плазмі крові. При сумісному застосуванні кофеїну та барбітуратів, примідону, протисудомних засобів (похідні гідантоїну, особливо фенітоїн) можливе посилення метаболізму та збільшення кліренсу кофеїну; при одночасному прийомі кофеїну та циметидину, пероральних контрацептивних засобів, дисульфіраму, ципрофлоксацину, норфлоксацину – зниження метаболізму кофеїну в печінці (уповільнення його виведення та збільшення концентрації в крові). Одночасне вживання кофеїновмісних напоїв та інших засобів, що стимулюють центральну нервову систему, може призводити до надмірної стимуляції центральної нервової системи. При одночасному застосуванні дротаверин може послабити протипаркінсонічний ефект леводопи. При одночасному застосуванні феніраміну з транквілізаторами, снодійними засобами, інгібіторами моноаміноксидази, алкоголем можливе посилення гнітючого впливу на центральну нервову систему.Спосіб застосування та дозиВсередину. Препарат приймають по 1 таблетці 1-3 десь у день. Максимальна добова доза – 4 таблетки. Тривалість лікування не більше 3 днів як жарознижувальний засіб і не більше 5 днів - як знеболюючий. Продовження лікування препаратом можливе лише після консультації з лікарем. Не перевищувати вказану дозу!ПередозуванняСимптоми: блідість шкірних покровів, анорексія (відсутність апетиту), біль у животі, нудота, блювання, шлунково-кишкова кровотеча, збудження, руховий занепокоєння, сплутаність свідомості, тахікардія, аритмія, гіпертермія (підвищення температури тіла), тремор або м'язові посмикування; епілептичні напади, підвищення активності "печінкових" трансаміназ, гепатонекроз, збільшення протромбінового часу. Симптоми порушення функції печінки можуть виникнути через 12-48 годин після передозування. При тяжкому передозуванні розвивається печінкова недостатність з прогресуючою енцефалопатією, кома, смерть; гостра ниркова недостатність із тубулярним некрозом; аритмія, панкреатит. При підозрі передозування необхідно негайно звернутися за лікарською допомогою. Лікування: промивання шлунка із наступним прийомом активованого вугілля. Специфічним антидотом при отруєнні парацетамолом є ацетилцистеїн. Введення ацетилцистеїну актуальне протягом 8 год. При шлунково-кишковій кровотечі необхідно введення антацидних засобів та промивання шлунка крижаним 0,9% розчином хлориду натрію; підтримання вентиляції легень та оксигенації; при епілептичних нападах – внутрішньовенне введення діазепаму; підтримання балансу рідини та солей.Запобіжні заходи та особливі вказівкиСлід уникати одночасного застосування препарату з іншими засобами, що містять парацетамол та/або інші нестероїдні протизапальні препарати, а також із засобами для полегшення симптомів застуди, грипу та закладеності носа. При застосуванні препарату понад 5-7 днів слід контролювати показники периферичної крові та функціональний стан печінки. Парацетамол спотворює результати лабораторних досліджень вмісту глюкози та сечової кислоти у плазмі крові. При необхідності визначення 17-кетостероїдів препарат слід відмінити за 48 годин до дослідження. Слід враховувати, що напроксен збільшує час кровотечі. Вплив кофеїну на центральну нервову систему залежить від типу нервової системи і може проявлятися як збудженням, і гальмуванням вищої нервової діяльності. У період лікування не слід вживати спиртовмісні напої. Вплив на здатність до керування автотранспортом та управління механізмами У період лікування необхідно дотримуватися обережності при керуванні автотранспортом та зайнятті іншими потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. речовини: парацетамол - 325,0 мг, напроксен натрію - 220,0 мг, кофеїн безводний - 50,0 мг; допоміжні речовини: целюлоза мікрокристалічна (целюлоза мікрокристалічна 101) - 175,50 мг, повідон (полівінілпіролідон середньомолекулярний, повідон К-30) - 36,00 мг, кроскармелоза (кроскармеллоза натрію) - 0,0 , тальк – 18,00 мг, магнію стеарат – 7,00 мг, кремнію діоксид колоїдний – 4,50 мг; Оболонка: Опадрай 13А200004 Фіолетовий - 30,000 мг %) – 1,167 мг, індигокармін алюмінієвий лак (блакитний 2) – 0,279 мг]. Пігулки, покриті плівковою оболонкою, 50 мг + 220 мг + 325 мг. По 10 таблеток в контурне осередкове впакування з полівінілхлоридної плівки або плівки ПВХ/ПВДХ і фольги алюмінієвої друкованої лакованої. 1 або 2 контурні коміркові упаковки разом з інструкцією з медичного застосування поміщають у пачку з картону.Опис лікарської формиТаблетки овальної форми, двоопуклі, покриті плівковою оболонкою від світло-фіолетового до фіолетового кольору. На поперечному розрізі ядро білого чи майже білого кольору.Фармакотерапевтична групаАналгезуючий засіб комбінований (нестероїдний протизапальний засіб + аналгетичний ненаркотичний засіб + психостимулюючий засіб).ФармакокінетикаНапроксен: швидко і повністю всмоктується із шлунково-кишкового тракту (ШКТ). Біодоступність – 95% (прийом їжі практично не впливає ні на повноту, ні на швидкість всмоктування). Час досягнення максимальної концентрації в крові (Тmах) – 1-2 години. Зв'язок із білками плазми крові > 99 %. Період напіввиведення (Т1/2) – 12-15 годин. Метаболізм відбувається у печінці до диметилнапроксена за участю ізоферменту CYP2C9. Кліренс – 0,13 мл/хв/кг. Виводиться на 98% нирками, 10% виводиться у незміненому вигляді, з жовчю – 0,5-2,5%. Рівноважна концентрація в плазмі визначається після прийому 4-5 доз препарату (2-3 дні). Парацетамол: легко всмоктується з шлунково-кишкового тракту, Сmах досягається через 0,5-2 год і становить 5-20 мкг/мл, зв'язок з білками плазми - 15%. Проникає крізь гематоенцефалічний бар'єр. Парацетамол метаболізується у печінці та виводиться нирками, головним чином, у вигляді глюкуронідів та сульфатних кон'югатів. Менше 5% парацетамолу виводиться у незміненому вигляді. Т1/2 варіюється від 1 до 4 год. Кофеїн: повністю і швидко всмоктується з шлунково-кишкового тракту, Сmах досягається через 50-75 хв і становить 1,58-1,76 мг/л. Швидко розподіляється у всіх органах та тканинах організму, легко проникає через гематоенцефалічний бар'єр та плаценту. Зв'язок із білками крові – 25-36 %. Метаболізм у печінці піддається більше 90%. Т1/2 у дорослих становить 3,9-5,3 год (іноді – до 10 год) Виведення кофеїну та його метаболітів здійснюється нирками (у незмінному вигляді у дорослих виводиться 1-2 %).ФармакодинамікаНапроксен: нестероїдний протизапальний засіб, має знеболювальну, жарознижувальну та протизапальну дію. Механізм дії обумовлений неселективним пригніченням активності циклооксигенази -1 і -2 (ЦОГ-1, ЦОГ-2), що регулює синтез простагландинів. Застосування напроксену у вигляді солі напроксену натрію забезпечує більш швидке всмоктування та швидке настання знеболювального ефекту. Парацетамол: ненаркотичний аналгетик, виявляє жарознижувальну та знеболювальну дію, обумовлену блокадою циклооксигенази в центральній нервовій системі та впливом на центри болю та терморегуляції. Кофеїн: зменшує сонливість, відчуття втоми, підвищує розумову та фізичну працездатність; розширює кровоносні судини скелетних м'язів, серця, нирок, знижує агрегацію тромбоцитів. У даній комбінації кофеїн у малій дозі практично не чинить симулюючої дії на центральну нервову систему, підвищує тонус судин головного мозку та сприяє прискоренню кровотоку. Кофеїн підвищує проникність гістогематичних бар'єрів і збільшує біодоступність ненаркотичних анальгетиків, також знижує активність ЦОГ, т.к. є антагоністом аденозинових А(2А) та А(2В) рецепторів, що сприяє посиленню знеболювальної дії анальгетиків. У реєстраційному клінічному дослідженні препарату Пенталгін НЕО підтверджено перевагу щодо впливу на загальне полегшення болю (показник TOTPAR) над монопрепаратом напроксену та над комбінованим препаратом парацетамолу та кофеїну.Показання до застосуванняБольовий синдром різного генезу: при захворюваннях опорно-рухового апарату (остеоартроз периферичних суглобів та хребта, у тому числі з радикулярним синдромом, артрит, міалгія); невралгія; зубний біль; біль голови, мігрень; альгодисменорея; посттравматичний (розтяжки та забиття) та післяопераційний больовий синдром, що супроводжується запаленням. Препарат Пенталгін® НЕО застосовується для симптоматичної терапії (для зменшення болю та запалення) та на прогресування основного захворювання не впливає.Протипоказання до застосуванняГіперчутливість до напроксену, напроксену натрію, інших нестероїдних протизапальних препаратів (НПЗП) або ксантинів; - підвищена чутливість до інших компонентів препарату; повне або неповне поєднання бронхіальної астми, рецидивуючого поліпозу носа або приносових пазух та непереносимості ацетилсаліцилової кислоти та інших нестероїдних протизапальних засобів (у тому числі в анамнезі); період після проведення аортокоронарного шунтування; ерозивно-виразкові ураження ШКТ (у фазі загострення), активна шлунково-кишкова кровотеча; гемофілія та інші порушення згортання крові та порушення гемостазу; цереброваскулярна кровотеча або інші кровотечі; декомпенсована серцева недостатність; органічні захворювання серцево-судинної системи (гострий інфаркт міокарда, тяжкий перебіг ішемічної хвороби серця, тяжка артеріальна гіпертензія), пароксизмальна тахікардія, часта шлуночкова екстрасистолія; виражена печінкова недостатність або активне захворювання печінки; виражена ниркова недостатність (кліренс креатиніну (КК) менше 30 мл/хв), прогресуючі захворювання нирок, підтверджена гіперкаліємія; підвищена збудливість, порушення сну, тривожні розлади (агорофобія, панічні розлади); вагітність, період грудного вигодовування; дитячий вік до 18 років. З обережністю: Ішемічна хвороба серця, цереброваскулярні захворювання, застійна серцева недостатність, дисліпідемія/гіперліпідемія, цукровий діабет, печінкова недостатність легкого та середнього ступеня тяжкості з підвищенням рівня трансаміназ, доброякісні гіпербілірубінемії (в т.ч. синдром Жильбера, алкогольне ураження) куріння, глаукома, порушення функції нирок (КК 30-60 мл/хв), виразкове ураження шлунково-кишкового тракту в анамнезі, наявність інфекції Helicobacter pylori, дефіцит глюкозо-6-фосфатдегідрогенази; епілепсія та схильність до судомних нападів, літній вік, системний червоний вовчак або змішані захворювання сполучної тканини (синдром Шарпа), тривале застосування нестероїдних протизапальних засобів, часте вживання алкоголю, тяжкі соматичні захворювання, супутня терапія наступними препаратами: антикоагулянти,антиагреганти, пероральні глюкокортикоїди, селективні інгібітори зворотного захоплення серотоніну. Якщо у Вас є одне з перелічених захворювань/станів, перед прийомом препарату обов'язково проконсультуйтеся з лікарем.Вагітність та лактаціяЗастосування препарату Пенталгін НЕО протипоказане при вагітності та в період грудного вигодовування.Побічна діяНебажані ефекти, які можуть розвиватися під час лікування препаратом Пенталгін® НЕО, класифіковані відповідно до наступної частоти народження: дуже часто (≥ 1/10), часто (від ≥ 1/100 до < 1/10), нечасто (від ≥1 /1 000 до < 1/100), рідко (від ≥ 1/10 000 до < 1/1 000), дуже рідко (< 1/10 000), частота невідома (не може бути визначена на підставі наявних даних). Порушення з боку крові та лімфатичної системи: нечасто: еозинофілія, гранулоцитопенія, лейкопенія, тромбоцитопенія; дуже рідко – метгемоглобінемія, гемолітична анемія. Порушення з боку нервової системи: часто: біль голови, вертиго, запаморочення, сонливість; нечасто: тремор, парестезії, біль голови, депресія, порушення сну, розлад уваги, безсоння, нездужання. Психічні розлади: часто: нервозність; нечасто: безсоння; рідко: тривога, ейфоричний настрій, внутрішня напруга. Порушення органу зору: часто: порушення зору. Порушення з боку органу слуху та лабіринтні порушення: часто: шум у вухах, порушення слуху; нечасто: зниження слуху. Порушення з боку серця: часто: набряклість, відчуття серцебиття; нечасто: застійна серцева недостатність, тахікардія, аритмія; частота невідома – підвищення артеріального тиску. Порушення з боку дихальної системи, органів грудної клітки та середостіння: часто: задишка; нечасто: еозинофільні пневмонії; дуже рідко: бронхоспазм (у пацієнтів з гіперчутливістю до ацетилсаліцилової кислоти та інших нестероїдних протизапальних засобів). Порушення шлунково-кишкового тракту: часто: запор, біль у животі, диспепсія, нудота, діарея, стоматит, метеоризм; нечасто: шлунково-кишкова кровотеча та/або перфорація шлунка, кривава блювота, мелена, блювання; сухість в роті; дуже рідко: рецидив чи загострення виразкового коліту чи хвороби Крона; Частота невідома: гастрит. Порушення з боку печінки та жовчовивідних шляхів: нечасто: підвищення активності "печінкових" ферментів, жовтяниця; дуже рідко: порушення функції печінки. Порушення з боку шкіри та підшкірних тканин: часто: свербіж шкіри, висипання на шкірі, екхімози, пурпура; нечасто: алопеція, фотодерматози; дуже рідко: бульозні реакції, включаючи синдром Стівенса-Джонсона та токсичний епідермальний некроліз. Порушення з боку скелетно-м'язової та сполучної тканини: нечасто: міалгія та м'язова слабкість. Порушення з боку нирок та сечовивідних шляхів: нечасто: гломерулонефрит, гематурія, інтерстиціальний нефрит, нефротичний синдром, ниркова недостатність, нирковий папілярний некроз. Загальні розлади та порушення у місці введення: часто: спрага, підвищене потовиділення; нечасто: реакції підвищеної чутливості, порушення менструального циклу, гіпертермія (озноб та лихоманка). Дані щодо посилення або розширення спектра небажаних явищ окремих компонентів при застосуванні їх у складі комбінації відповідно до інструкції з медичного застосування відсутні. У разі виникнення побічних ефектів слід звернутися до лікаря.Взаємодія з лікарськими засобамиІнші ННЗН, включаючи селективні інгібітори циклооксигенази-2, кортикостероїди: зростання ризику побічних ефектів напроксену з боку шлунково-кишкового тракту. Пропранолол та інші бета-адреноблокатори: напроксен може знижувати антигіпертензивну дію препаратів. Кофеїн може пригнічувати терапевтичні ефекти бета-адреноблокаторів. Серцеві глікозиди: кофеїн прискорює всмоктування та посилює дію серцевих глікозидів, підвищує їхню токсичність. Діуретики: напроксен може зменшувати сечогінну дію діуретиків, інгібувати натрійуретичну дію фуросеміду. Діуретики можуть підвищувати ризик нефротоксичності нестероїдних протизапальних засобів. Літії: напроксен знижує виведення літію, що призводить до збільшення концентрації літію у плазмі крові. Мієлотоксичні препарати: посилення гематоксичності напроксену. Циклоспорин: збільшення ризику ниркової недостатності. Пробенецид: збільшує концентрацію напроксену у плазмі крові. Метотрексат, фенітоїн, сульфаніламід: напроксен уповільнює їхню екскрецію, що збільшує ризик розвитку їх токсичної дії. Антацидні препарати, що містять магній та алюміній: зменшення абсорбції напроксену. Антикоагулянти: напроксен може посилювати дію антикоагулянтів, парацетамол при тривалому застосуванні посилює дію непрямих антикоагулянтів. Антитромбоцитарні препарати, селективні інгібітори зворотного захоплення серотоніну: підвищення ризику шлунково-кишкової кровотечі. Міфепристон: не рекомендується одночасний прийом нестероїдних протизапальних засобів протягом 8-12 днів після застосування міфепристону. Такролімус: одночасне застосування нестероїдних протизапальних засобів підвищує ризик нефротоксичності. Дифлунісал: підвищення концентрації парацетамолу в плазмі, що підвищує ризик розвитку гепатотоксичності. Індуктори мікросомальних ферментів печінки: можливе підвищення гепатотоксичної дії парацетамолу. Інгібітори мікросомальних ферментів печінки: зниження ризику гепатотоксичної дії парацетамолу. Хлорамфенікол: парацетамол збільшує час виведення хлорамфеніколу. Метоклопрамід, домперидон: збільшення швидкості всмоктування парацетамолу. Колестирамін: зниження швидкості всмоктування парацетамолу. Теофіліну: кофеїн знижує екскрецію теофіліну. Барбітурати, примідон, протисудомні засоби: можливе посилення метаболізму та збільшення кліренсу кофеїну. Циметидин, пероральні контрацептиви, дисульфірам, ципрофлоксацин, норфлоксацин: можливе зниження метаболізму кофеїну в печінці (уповільнення його виведення та збільшення концентрації у крові). Препарати кальцію: кофеїн знижує їх всмоктування у ШКТ. Наркотичні та снодійні лікарські засоби: кофеїн знижує їх ефективність. Алкоголь: збільшення ризику ураження печінки та гострого панкреатиту.Спосіб застосування та дозиВсередину. Таблетки слід приймати з достатньою кількістю води. Разова доза – 1 таблетка. Частота прийому - 1-3 десь у день, з інтервалом щонайменше 4 годин. Максимальна добова доза – 3 таблетки. Тривалість застосування препарату – не більше 5 днів.ПередозуванняСимптоми: сонливість, диспептичні розлади (печія, нудота, блювання, біль у животі), головний біль, шум у вухах, слабкість, пітливість, блідість шкірних покровів, тривога, збудження, руховий неспокій, анорексія, сплутаність свідомості, та , тремор або м'язові посмикування; у тяжких випадках - кривава блювота, мелена, порушення свідомості, судоми, ниркова та/або печінкова недостатність. При підозрі передозування препарату необхідно негайно звернутися за лікарською допомогою. Лікування. Потерпілому слід зробити промивання шлунка та призначити ентеросорбенти (активоване вугілля). Необхідність у проведенні додаткових терапевтичних заходів визначається залежно від тяжкості стану та виразності симптомів інтоксикації.Запобіжні заходи та особливі вказівкиЗагальні Не перевищуйте доз, наведених в інструкції. Для зниження ризику розвитку небажаних явищ слід використовувати ефективну мінімальну дозу мінімально можливим коротким курсом. При збереженні чи посиленні больового синдрому і натомість терапії слід звернутися до лікаря. При тривалому застосуванні препарату потрібний контроль периферичної крові та функціонального стану печінки. Препарат не слід приймати разом з іншими протизапальними та болезаспокійливими препаратами, за винятком призначень лікаря. Слід уникати застосування препарату протягом 48 годин до хірургічного втручання. При необхідності визначення 17-кортикостероїдів слід відмінити за 48 годин до дослідження. Аналогічно напроксен може впливати на визначення 5-гідроксиіндолоцтової кислоти в сечі. Застосування напроксену, як і інших препаратів, що блокують синтез простагландинів, може впливати на фертильність, тому не рекомендується жінкам, які планують вагітність. Під час лікування слід відмовитися від вживання алкогольних напоїв (див. Розділ "Лікарські взаємодії"). При застосуванні препарату слід обмежити споживання продуктів, що містять кофеїн, оскільки надмірне надходження кофеїну може призвести до нервозності, дратівливості, безсоння та, у деяких випадках, почастішання серцебиття. Вплив на лабораторні показники Застосування парацетамолу може вплинути на результати визначення сечової кислоти за методом фосфорновольфрамової кислоти та глікемії глюкозооксидазним/пероксидазним методом. Кофеїн може спотворювати результати проби з дипіридамолом; під час проведення дослідження необхідно протягом 8-12 год утриматися від прийому кофеїну. Кожна таблетка містить приблизно 20 мг натрію. При обмеженні споживання солі це необхідно враховувати. Вплив на здатність до керування автотранспортом та управління механізмами Напроксен і кофеїн, що входять до складу препарату, можуть впливати на швидкість психомоторної реакції, тому на період прийому слід бути обережним при керуванні автомобілем і виконанні завдань, що вимагають підвищеної уваги.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. речовини: парацетамол - 325,0 мг, напроксен натрію - 220,0 мг, кофеїн безводний - 50,0 мг; допоміжні речовини: целюлоза мікрокристалічна (целюлоза мікрокристалічна 101) - 175,50 мг, повідон (полівінілпіролідон середньомолекулярний, повідон К-30) - 36,00 мг, кроскармелоза (кроскармеллоза натрію) - 0,0 , тальк – 18,00 мг, магнію стеарат – 7,00 мг, кремнію діоксид колоїдний – 4,50 мг; Оболонка: Опадрай 13А200004 Фіолетовий - 30,000 мг %) – 1,167 мг, індигокармін алюмінієвий лак (блакитний 2) – 0,279 мг]. Пігулки, покриті плівковою оболонкою, 50 мг + 220 мг + 325 мг. По 10 таблеток в контурне осередкове впакування з полівінілхлоридної плівки або плівки ПВХ/ПВДХ і фольги алюмінієвої друкованої лакованої. 1 або 2 контурні коміркові упаковки разом з інструкцією з медичного застосування поміщають у пачку з картону.Опис лікарської формиТаблетки овальної форми, двоопуклі, покриті плівковою оболонкою від світло-фіолетового до фіолетового кольору. На поперечному розрізі ядро білого чи майже білого кольору.Фармакотерапевтична групаАналгезуючий засіб комбінований (нестероїдний протизапальний засіб + аналгетичний ненаркотичний засіб + психостимулюючий засіб).ФармакокінетикаНапроксен: швидко і повністю всмоктується із шлунково-кишкового тракту (ШКТ). Біодоступність – 95% (прийом їжі практично не впливає ні на повноту, ні на швидкість всмоктування). Час досягнення максимальної концентрації в крові (Тmах) – 1-2 години. Зв'язок із білками плазми крові > 99 %. Період напіввиведення (Т1/2) – 12-15 годин. Метаболізм відбувається у печінці до диметилнапроксена за участю ізоферменту CYP2C9. Кліренс – 0,13 мл/хв/кг. Виводиться на 98% нирками, 10% виводиться у незміненому вигляді, з жовчю – 0,5-2,5%. Рівноважна концентрація в плазмі визначається після прийому 4-5 доз препарату (2-3 дні). Парацетамол: легко всмоктується з шлунково-кишкового тракту, Сmах досягається через 0,5-2 год і становить 5-20 мкг/мл, зв'язок з білками плазми - 15%. Проникає крізь гематоенцефалічний бар'єр. Парацетамол метаболізується у печінці та виводиться нирками, головним чином, у вигляді глюкуронідів та сульфатних кон'югатів. Менше 5% парацетамолу виводиться у незміненому вигляді. Т1/2 варіюється від 1 до 4 год. Кофеїн: повністю і швидко всмоктується з шлунково-кишкового тракту, Сmах досягається через 50-75 хв і становить 1,58-1,76 мг/л. Швидко розподіляється у всіх органах та тканинах організму, легко проникає через гематоенцефалічний бар'єр та плаценту. Зв'язок із білками крові – 25-36 %. Метаболізм у печінці піддається більше 90%. Т1/2 у дорослих становить 3,9-5,3 год (іноді – до 10 год) Виведення кофеїну та його метаболітів здійснюється нирками (у незмінному вигляді у дорослих виводиться 1-2 %).ФармакодинамікаНапроксен: нестероїдний протизапальний засіб, має знеболювальну, жарознижувальну та протизапальну дію. Механізм дії обумовлений неселективним пригніченням активності циклооксигенази -1 і -2 (ЦОГ-1, ЦОГ-2), що регулює синтез простагландинів. Застосування напроксену у вигляді солі напроксену натрію забезпечує більш швидке всмоктування та швидке настання знеболювального ефекту. Парацетамол: ненаркотичний аналгетик, виявляє жарознижувальну та знеболювальну дію, обумовлену блокадою циклооксигенази в центральній нервовій системі та впливом на центри болю та терморегуляції. Кофеїн: зменшує сонливість, відчуття втоми, підвищує розумову та фізичну працездатність; розширює кровоносні судини скелетних м'язів, серця, нирок, знижує агрегацію тромбоцитів. У даній комбінації кофеїн у малій дозі практично не чинить симулюючої дії на центральну нервову систему, підвищує тонус судин головного мозку та сприяє прискоренню кровотоку. Кофеїн підвищує проникність гістогематичних бар'єрів і збільшує біодоступність ненаркотичних анальгетиків, також знижує активність ЦОГ, т.к. є антагоністом аденозинових А(2А) та А(2В) рецепторів, що сприяє посиленню знеболювальної дії анальгетиків. У реєстраційному клінічному дослідженні препарату Пенталгін НЕО підтверджено перевагу щодо впливу на загальне полегшення болю (показник TOTPAR) над монопрепаратом напроксену та над комбінованим препаратом парацетамолу та кофеїну.Показання до застосуванняБольовий синдром різного генезу: при захворюваннях опорно-рухового апарату (остеоартроз периферичних суглобів та хребта, у тому числі з радикулярним синдромом, артрит, міалгія); невралгія; зубний біль; біль голови, мігрень; альгодисменорея; посттравматичний (розтяжки та забиття) та післяопераційний больовий синдром, що супроводжується запаленням. Препарат Пенталгін® НЕО застосовується для симптоматичної терапії (для зменшення болю та запалення) та на прогресування основного захворювання не впливає.Протипоказання до застосуванняГіперчутливість до напроксену, напроксену натрію, інших нестероїдних протизапальних препаратів (НПЗП) або ксантинів; - підвищена чутливість до інших компонентів препарату; повне або неповне поєднання бронхіальної астми, рецидивуючого поліпозу носа або приносових пазух та непереносимості ацетилсаліцилової кислоти та інших нестероїдних протизапальних засобів (у тому числі в анамнезі); період після проведення аортокоронарного шунтування; ерозивно-виразкові ураження ШКТ (у фазі загострення), активна шлунково-кишкова кровотеча; гемофілія та інші порушення згортання крові та порушення гемостазу; цереброваскулярна кровотеча або інші кровотечі; декомпенсована серцева недостатність; органічні захворювання серцево-судинної системи (гострий інфаркт міокарда, тяжкий перебіг ішемічної хвороби серця, тяжка артеріальна гіпертензія), пароксизмальна тахікардія, часта шлуночкова екстрасистолія; виражена печінкова недостатність або активне захворювання печінки; виражена ниркова недостатність (кліренс креатиніну (КК) менше 30 мл/хв), прогресуючі захворювання нирок, підтверджена гіперкаліємія; підвищена збудливість, порушення сну, тривожні розлади (агорофобія, панічні розлади); вагітність, період грудного вигодовування; дитячий вік до 18 років. З обережністю: Ішемічна хвороба серця, цереброваскулярні захворювання, застійна серцева недостатність, дисліпідемія/гіперліпідемія, цукровий діабет, печінкова недостатність легкого та середнього ступеня тяжкості з підвищенням рівня трансаміназ, доброякісні гіпербілірубінемії (в т.ч. синдром Жильбера, алкогольне ураження) куріння, глаукома, порушення функції нирок (КК 30-60 мл/хв), виразкове ураження шлунково-кишкового тракту в анамнезі, наявність інфекції Helicobacter pylori, дефіцит глюкозо-6-фосфатдегідрогенази; епілепсія та схильність до судомних нападів, літній вік, системний червоний вовчак або змішані захворювання сполучної тканини (синдром Шарпа), тривале застосування нестероїдних протизапальних засобів, часте вживання алкоголю, тяжкі соматичні захворювання, супутня терапія наступними препаратами: антикоагулянти,антиагреганти, пероральні глюкокортикоїди, селективні інгібітори зворотного захоплення серотоніну. Якщо у Вас є одне з перелічених захворювань/станів, перед прийомом препарату обов'язково проконсультуйтеся з лікарем.Вагітність та лактаціяЗастосування препарату Пенталгін НЕО протипоказане при вагітності та в період грудного вигодовування.Побічна діяНебажані ефекти, які можуть розвиватися під час лікування препаратом Пенталгін® НЕО, класифіковані відповідно до наступної частоти народження: дуже часто (≥ 1/10), часто (від ≥ 1/100 до < 1/10), нечасто (від ≥1 /1 000 до < 1/100), рідко (від ≥ 1/10 000 до < 1/1 000), дуже рідко (< 1/10 000), частота невідома (не може бути визначена на підставі наявних даних). Порушення з боку крові та лімфатичної системи: нечасто: еозинофілія, гранулоцитопенія, лейкопенія, тромбоцитопенія; дуже рідко – метгемоглобінемія, гемолітична анемія. Порушення з боку нервової системи: часто: біль голови, вертиго, запаморочення, сонливість; нечасто: тремор, парестезії, біль голови, депресія, порушення сну, розлад уваги, безсоння, нездужання. Психічні розлади: часто: нервозність; нечасто: безсоння; рідко: тривога, ейфоричний настрій, внутрішня напруга. Порушення органу зору: часто: порушення зору. Порушення з боку органу слуху та лабіринтні порушення: часто: шум у вухах, порушення слуху; нечасто: зниження слуху. Порушення з боку серця: часто: набряклість, відчуття серцебиття; нечасто: застійна серцева недостатність, тахікардія, аритмія; частота невідома – підвищення артеріального тиску. Порушення з боку дихальної системи, органів грудної клітки та середостіння: часто: задишка; нечасто: еозинофільні пневмонії; дуже рідко: бронхоспазм (у пацієнтів з гіперчутливістю до ацетилсаліцилової кислоти та інших нестероїдних протизапальних засобів). Порушення шлунково-кишкового тракту: часто: запор, біль у животі, диспепсія, нудота, діарея, стоматит, метеоризм; нечасто: шлунково-кишкова кровотеча та/або перфорація шлунка, кривава блювота, мелена, блювання; сухість в роті; дуже рідко: рецидив чи загострення виразкового коліту чи хвороби Крона; Частота невідома: гастрит. Порушення з боку печінки та жовчовивідних шляхів: нечасто: підвищення активності "печінкових" ферментів, жовтяниця; дуже рідко: порушення функції печінки. Порушення з боку шкіри та підшкірних тканин: часто: свербіж шкіри, висипання на шкірі, екхімози, пурпура; нечасто: алопеція, фотодерматози; дуже рідко: бульозні реакції, включаючи синдром Стівенса-Джонсона та токсичний епідермальний некроліз. Порушення з боку скелетно-м'язової та сполучної тканини: нечасто: міалгія та м'язова слабкість. Порушення з боку нирок та сечовивідних шляхів: нечасто: гломерулонефрит, гематурія, інтерстиціальний нефрит, нефротичний синдром, ниркова недостатність, нирковий папілярний некроз. Загальні розлади та порушення у місці введення: часто: спрага, підвищене потовиділення; нечасто: реакції підвищеної чутливості, порушення менструального циклу, гіпертермія (озноб та лихоманка). Дані щодо посилення або розширення спектра небажаних явищ окремих компонентів при застосуванні їх у складі комбінації відповідно до інструкції з медичного застосування відсутні. У разі виникнення побічних ефектів слід звернутися до лікаря.Взаємодія з лікарськими засобамиІнші ННЗН, включаючи селективні інгібітори циклооксигенази-2, кортикостероїди: зростання ризику побічних ефектів напроксену з боку шлунково-кишкового тракту. Пропранолол та інші бета-адреноблокатори: напроксен може знижувати антигіпертензивну дію препаратів. Кофеїн може пригнічувати терапевтичні ефекти бета-адреноблокаторів. Серцеві глікозиди: кофеїн прискорює всмоктування та посилює дію серцевих глікозидів, підвищує їхню токсичність. Діуретики: напроксен може зменшувати сечогінну дію діуретиків, інгібувати натрійуретичну дію фуросеміду. Діуретики можуть підвищувати ризик нефротоксичності нестероїдних протизапальних засобів. Літії: напроксен знижує виведення літію, що призводить до збільшення концентрації літію у плазмі крові. Мієлотоксичні препарати: посилення гематоксичності напроксену. Циклоспорин: збільшення ризику ниркової недостатності. Пробенецид: збільшує концентрацію напроксену у плазмі крові. Метотрексат, фенітоїн, сульфаніламід: напроксен уповільнює їхню екскрецію, що збільшує ризик розвитку їх токсичної дії. Антацидні препарати, що містять магній та алюміній: зменшення абсорбції напроксену. Антикоагулянти: напроксен може посилювати дію антикоагулянтів, парацетамол при тривалому застосуванні посилює дію непрямих антикоагулянтів. Антитромбоцитарні препарати, селективні інгібітори зворотного захоплення серотоніну: підвищення ризику шлунково-кишкової кровотечі. Міфепристон: не рекомендується одночасний прийом нестероїдних протизапальних засобів протягом 8-12 днів після застосування міфепристону. Такролімус: одночасне застосування нестероїдних протизапальних засобів підвищує ризик нефротоксичності. Дифлунісал: підвищення концентрації парацетамолу в плазмі, що підвищує ризик розвитку гепатотоксичності. Індуктори мікросомальних ферментів печінки: можливе підвищення гепатотоксичної дії парацетамолу. Інгібітори мікросомальних ферментів печінки: зниження ризику гепатотоксичної дії парацетамолу. Хлорамфенікол: парацетамол збільшує час виведення хлорамфеніколу. Метоклопрамід, домперидон: збільшення швидкості всмоктування парацетамолу. Колестирамін: зниження швидкості всмоктування парацетамолу. Теофіліну: кофеїн знижує екскрецію теофіліну. Барбітурати, примідон, протисудомні засоби: можливе посилення метаболізму та збільшення кліренсу кофеїну. Циметидин, пероральні контрацептиви, дисульфірам, ципрофлоксацин, норфлоксацин: можливе зниження метаболізму кофеїну в печінці (уповільнення його виведення та збільшення концентрації у крові). Препарати кальцію: кофеїн знижує їх всмоктування у ШКТ. Наркотичні та снодійні лікарські засоби: кофеїн знижує їх ефективність. Алкоголь: збільшення ризику ураження печінки та гострого панкреатиту.Спосіб застосування та дозиВсередину. Таблетки слід приймати з достатньою кількістю води. Разова доза – 1 таблетка. Частота прийому - 1-3 десь у день, з інтервалом щонайменше 4 годин. Максимальна добова доза – 3 таблетки. Тривалість застосування препарату – не більше 5 днів.ПередозуванняСимптоми: сонливість, диспептичні розлади (печія, нудота, блювання, біль у животі), головний біль, шум у вухах, слабкість, пітливість, блідість шкірних покровів, тривога, збудження, руховий неспокій, анорексія, сплутаність свідомості, та , тремор або м'язові посмикування; у тяжких випадках - кривава блювота, мелена, порушення свідомості, судоми, ниркова та/або печінкова недостатність. При підозрі передозування препарату необхідно негайно звернутися за лікарською допомогою. Лікування. Потерпілому слід зробити промивання шлунка та призначити ентеросорбенти (активоване вугілля). Необхідність у проведенні додаткових терапевтичних заходів визначається залежно від тяжкості стану та виразності симптомів інтоксикації.Запобіжні заходи та особливі вказівкиЗагальні Не перевищуйте доз, наведених в інструкції. Для зниження ризику розвитку небажаних явищ слід використовувати ефективну мінімальну дозу мінімально можливим коротким курсом. При збереженні чи посиленні больового синдрому і натомість терапії слід звернутися до лікаря. При тривалому застосуванні препарату потрібний контроль периферичної крові та функціонального стану печінки. Препарат не слід приймати разом з іншими протизапальними та болезаспокійливими препаратами, за винятком призначень лікаря. Слід уникати застосування препарату протягом 48 годин до хірургічного втручання. При необхідності визначення 17-кортикостероїдів слід відмінити за 48 годин до дослідження. Аналогічно напроксен може впливати на визначення 5-гідроксиіндолоцтової кислоти в сечі. Застосування напроксену, як і інших препаратів, що блокують синтез простагландинів, може впливати на фертильність, тому не рекомендується жінкам, які планують вагітність. Під час лікування слід відмовитися від вживання алкогольних напоїв (див. Розділ "Лікарські взаємодії"). При застосуванні препарату слід обмежити споживання продуктів, що містять кофеїн, оскільки надмірне надходження кофеїну може призвести до нервозності, дратівливості, безсоння та, у деяких випадках, почастішання серцебиття. Вплив на лабораторні показники Застосування парацетамолу може вплинути на результати визначення сечової кислоти за методом фосфорновольфрамової кислоти та глікемії глюкозооксидазним/пероксидазним методом. Кофеїн може спотворювати результати проби з дипіридамолом; під час проведення дослідження необхідно протягом 8-12 год утриматися від прийому кофеїну. Кожна таблетка містить приблизно 20 мг натрію. При обмеженні споживання солі це необхідно враховувати. Вплив на здатність до керування автотранспортом та управління механізмами Напроксен і кофеїн, що входять до складу препарату, можуть впливати на швидкість психомоторної реакції, тому на період прийому слід бути обережним при керуванні автомобілем і виконанні завдань, що вимагають підвищеної уваги.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему