Все товары
1 737,00 грн
163,00 грн
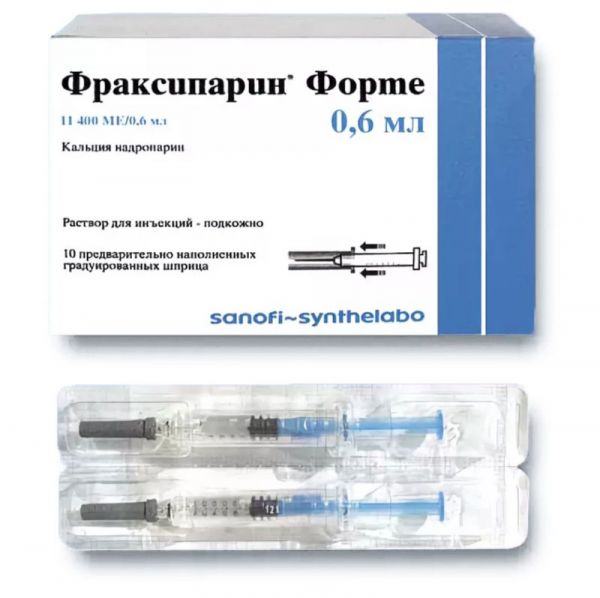
Склад, форма випуску та упаковкаРозчин - 1 мл: Активна речовина: надропарин кальцію - 9500 ME анти Ха-факторної активності в 1 мл; Допоміжні речовини: розчин гідроксиду кальцію (або розбавлена хлористоводнева кислота) - достатня кількість для доведення pH до 5,0 - 7,0; вода для ін'єкцій – до 1,0 мл. По 0,3 мл, 0,4 мл, 0,6 мл, 0,8 мл або 1,0 мл препарату в однодозовий скляний шприц із захисним корпусом, наконечником з голкою з нержавіючої сталі, закритою ковпачком. По 2 шприца упаковують у прозорий блістер із ПBX/ПЕ плівки. По 1 або 5 блістерів (по 2 або 10 шприців) разом з інструкцією із застосування поміщають у картонну пачку.Опис лікарської формиПрозорий або слабо-опалесцентний, безбарвний або світло-жовтий розчин.Фармакотерапевтична групаАнтикоагулянтний засіб прямої дії.ФармакокінетикаФармакокінетичні властивості надропарину визначаються з урахуванням біологічної активності, тобто. вимірювання анти-Ха-факторної активності. Абсорбція Після підшкірного введення максимальна анти-Ха активність (Сmах) досягається приблизно через 3 - 5 год (Тmах) - Біодоступність практично повна (близько 98%). Після внутрішньовенного введення максимальна анти-Ха активність досягається через 10 хвилин, і період напіввиведення становить близько 2 год. Виведення Період напіввиведення після підшкірного введення становить близько 3,5 год. Проте анти-Ха активність зберігається протягом щонайменше 18 годин після введення надропарину в дозі 1900 анти-Ха ME. Особливі групи пацієнтів Пацієнти похилого віку Як правило, ниркова функція знижується з віком, тому елімінація надропарину може уповільнюватися. Можлива ниркова недостатність у цій групі пацієнтів потребує оцінки та відповідної корекції дози. Пацієнти з нирковою недостатністю У клінічному дослідженні, присвяченому вивченню фармакокінетики надропарину при внутрішньовенному введенні, у пацієнтів з різним ступенем ниркової недостатності було встановлено кореляцію між кліренсом надропарину та кліренсом креатиніну. У пацієнтів з помірною нирковою недостатністю (кліренс креатиніну 36 - 43 мл/хв) AUC та період напіввиведення були збільшені на 52% та 39% відповідно у порівнянні зі здоровими добровольцями. У цих пацієнтів плазмовий кліренс надропарину був знижений до 63% нормальних значень. У дослідженні спостерігався широкий діапазон міжіндивідуальної варіабельності. У пацієнтів з тяжкою нирковою недостатністю (кліренс креатиніну 10-20 мл/хв) AUC та період напіввиведення були підвищені до 95% та 112% відповідно порівняно зі здоровими добровольцями.Плазмовий кліренс надропарину у пацієнтів з тяжкою нирковою недостатністю був знижений до 50% від пацієнта з нормальною функцією нирок. У пацієнтів з тяжкою нирковою недостатністю (кліренс креатиніну 3 - 6 мл/хв), що перебувають на гемодіалізі, AUC та період напіввиведення були збільшені на 62% та 65% відповідно у порівнянні зі здоровими добровольцями. Плазмовий кліренс надропарину у пацієнтів з тяжкою нирковою недостатністю, що перебувають на гемодіалізі, був знижений до 67% від нормальних значень.Плазмовий кліренс надропарину у пацієнтів з тяжкою нирковою недостатністю, що перебувають на гемодіалізі, був знижений до 67% від нормальних значень.Плазмовий кліренс надропарину у пацієнтів з тяжкою нирковою недостатністю, що перебувають на гемодіалізі, був знижений до 67% від нормальних значень.ФармакодинамікаМеханізм дії Надропарин – це низькомолекулярний гепарин (НМГ), отриманий шляхом деполімеризації зі стандартного гепарину. Він являє собою глікозаміноглікан із середньою молекулярною масою приблизно 4300 дальтон. Надропарин виявляє високу здатність до зв'язування з білком плазми антитромбіном III (AT III). Це зв'язування призводить до прискореного пригнічення фактора Ха, чим і обумовлений високий антитромботичний потенціал надропарину. Інші механізми, що забезпечують антитромботічну дію надропарину, включають активацію інгібітору перетворення тканинного фактора (TFPI), активацію фібринолізу за допомогою прямого вивільнення активатора тканинного плазміногену з ендотеліальних клітин та модифікацію реологічних властивостей крові (зниження в'язкості крові) і збільшення пров. Фармакодинаміка Надропарин характеризується вищою активністю щодо фактора Ха порівняно з активністю щодо фактора На. Він має як негайну, так і продовжену антитромботичну активність. У порівнянні з нефракціонованим гепарином (НФГ) надропарин має менший вплив на функції тромбоцитів та їх здатність до агрегації та мало виражений вплив на первинний гемостаз.ІнструкціяВлаштування шприца Запобіжник голки Поршень Тримач Захисний корпус Підготовка до ін'єкції та техніка підшкірного введення 1. Ретельно вимийте руки з водою та милом і висушіть рушником. 2. Вийміть попередньо заповнений шприц із пачки та повірте, що: термін придатності препарату не минув; шприц не був розкритий та не пошкоджений. 3. Прийміть положення сидячи або лежачи. Виберіть місце в нижній частині живота, крім області приблизно 5 см навколо пупка. Переважно вводити препарат у праву та ліву сторони передньої черевної стінки почергово. Це допоможе зменшити дискомфорт у місці ін'єкції. Якщо введення в нижню частину живота неможливе, зверніться за порадою до лікаря або медичної сестри. 4. Обробіть місце ін'єкції тампоном, змоченим спиртом. 5. Зніміть захисний ковпачок, прокрутивши спочатку, а потім потягніть його по прямій лінії від захисного корпусу. Викиньте захисний ковпачок. Якщо об'єм розчину в шприці більший, ніж необхідно для ін'єкції, Ви повинні видалити надлишок розчину перед ін'єкцією. Тримайте шприц голкою вниз. Обережно натискайте на поршень доти, доки нижня частина поршня не опиниться на лінії об'єму, призначеного лікарем. Надлишки розчину необхідно викинути. Тепер шприц готовий до використання. Не торкайтеся голки після зняття ковпачка і не допускайте контакту голки з будь-якими поверхнями. Ви можете помітити бульбашки повітря у шприці. Не намагайтеся видаляти бульбашки повітря перед ін'єкцією – це може призвести до втрати частини препарату. 6. Обережно затисніть шкіру для формування складки. Шкірну складку необхідно утримувати великим та вказівним пальцями до закінчення введення препарату. 7. Тримайте шприц міцно. Голку слід вводити перпендикулярно, а не під кутом, на всю довжину затиснутої складки шкіри. 8. Введіть вміст шприца, натиснувши на поршень. Потім акуратно видаліть голку та притисніть місце ін'єкції тампоном, змоченим спиртом. Не слід розтирати місце застосування препарату після ін'єкції. 9. Після ін'єкції на використаний шприц встановлюється система захисту: утримуючи використаний шприц в одній руці за захисний корпус, іншою рукою потягніть за тримач для вивільнення клямки та зсуву корпусу для захисту голки до чутного клацання, що позначає фіксацію захисного корпусу. Утилізуйте використаний шприц відповідно до звичайної процедури утилізації медичних відходів. При застосуванні препарату суворо дотримуйтесь рекомендацій, наведених у даній інструкції, а також вказівок лікаря. У разі виникнення запитань, зверніться до лікаря.Показання до застосуванняПрофілактика тромбоемболічних ускладнень: при загальнохірургічних та ортопедичних втручаннях; у пацієнтів з високим ризиком тромбоутворення (при гострій дихальній недостатності та/або респіраторній інфекції та/або серцевій недостатності), які перебувають на постільному режимі у зв'язку з гострою терапевтичною патологією або госпіталізованими до відділень реанімації або інтенсивної терапії. Лікування тромбоемболії легеневої артерії середнього/важкого ступеня тяжкості або проксимального тромбозу глибоких вен нижніх кінцівок. Профілактика зсідання крові під час гемодіалізу. Лікування нестабільної стенокардії та інфаркту міокарда без зубця Q.Протипоказання до застосуванняПідвищена чутливість до надропарину або до будь-якого іншого компонента препарату. Наявність в анамнезі тяжкої гепарин-індукованої тромбоцитопенії (ГІТ) II типу, спричиненої застосуванням нефракціонованого або низькомолекулярного гепарину, або будь-якої тромбоцитопенії, спричиненої застосуванням надропарину. Тромбоцитопенія у поєднанні з позитивним тестом на антитромбоцитарні антитіла in vitro у присутності надропарину кальцію (див. розділ "Особливі вказівки"). Ознаки кровотечі або підвищений ризик кровотечі, пов'язаний із порушенням гемостазу, за винятком ДВЗ-синдрому, не викликаного гепарином. Органічні ураження органів зі схильністю до кровоточивості (наприклад, гостра виразка шлунка або дванадцятипалої кишки). Внутрішньочерепний крововилив. Гострий інфекційний ендокардит. Тяжка ниркова недостатність (кліренс креатиніну менше 30 мл/хв) у пацієнтів, які отримують Фраксипарин з метою лікування тромбоемболій та венозних тромбозів, нестабільної стенокардії та інфаркту міокарда без зубця Q. Травми або оперативні втручання на головному та спинному мозку або на очах. Місцева та регіонарна анестезія при плановій хірургії у пацієнтів, які отримують Фраксипарин з метою лікування тромбоемболії легеневої артерії, тромбозу глибоких вен, нестабільної стенокардії та інфаркту міокарда без зубця Q. З обережністю: Печінкова недостатність. Ниркова недостатність. Тяжка артеріальна гіпертензія. Виразки в анамнезі або інші захворювання з підвищеним ризиком кровотечі. Хоріоретинальні судинні захворювання. Післяопераційний період після операцій на головному та спинному мозку або на очах. При перевищенні рекомендованої тривалості лікування (10 днів). Недотримання рекомендованих умов лікування (особливо тривалості та встановлення дози на основі маси тіла для курсового застосування). У комбінації з препаратами, що посилюють ризик кровотечі, такими як ацетилсаліцилова кислота та інші саліцилати, нестероїдні протизапальні препарати (НПЗП), антиагрегантні засоби. Літній вік. Пацієнти із масою тіла менше 40 кг. Проведення спінальної або епідуральної анестезії (ризик розвитку гематоми), спинномозкова пункція (у т. ч. нещодавно перенесена). При тривалому застосуванні високих доз низькомолекулярних гепаринів не можна виключати ризик розвитку остеопорозу, особливо у пацієнтів із підвищеним ризиком розвитку остеопорозу.Вагітність та лактаціяВагітність Досліди на тваринах не показали тератогенного чи фетотоксичного ефектів надропарину. Застосування для профілактики та І триместрі вагітності Наявних клінічних даних недостатньо для оцінки можливого тератогенного та фетотоксичного ефектів надропарину у людини при застосуванні у профілактичних дозах у І триместрі вагітності та у терапевтичних дозах протягом усієї вагітності. Тому слід уникати застосування Фраксипарину у профілактичних дозах у І триместрі вагітності та у терапевтичних дозах протягом усієї вагітності. Застосування для профілактики у ІІ та ІІІ триместрах вагітності При застосуванні надропарину протягом II та III триместру вагітності у обмеженої кількості пацієнток не було виявлено ознак тератогенної або фетотоксичної дії препарату. Однак для оцінки впливу надропарину необхідні подальші дослідження. Тому застосовувати Фраксипарин у профілактичних дозах у II та III триместрах вагітності слід лише у разі потреби. При необхідності застосування епідуральної анестезії рекомендується зупинення профілактичного лікування гепарином не менше ніж за 12 годин до анестезії. Грудне годування В даний час є лише обмежені дані щодо виділення надропарину в грудне молоко, хоча всмоктування надропарину у новонароджених малоймовірне. У зв'язку з цим застосування надропарину у період грудного вигодовування не протипоказане. Фертильність Дані клінічних досліджень щодо впливу надропарину на фертильність відсутні.Побічна діяВикористана наступна класифікація небажаних реакцій залежно від частоти народження: дуже часто (>1/10), часто (>1/100, 1/1000, 1/10,000, З боку крові та лімфатичної системи: Дуже часто – Кровотеча1; Рідко - тромбоцитопенію, включаючи гепарин-індуковану тромбоцитопенію, тромбоцитоз; Дуже рідко – еозинофілія, оборотна після припинення лікування. З боку імунної системи: Дуже рідко – реакції гіперчутливості (включаючи ангіоневротичний набряк та шкірні реакції, бронхоспазм), анафілактоїдні реакції. З боку обміну речовин: Дуже рідко: оборотна гіперкаліємія, пов'язана з гіпоальдостеронізмом, індукована гепарином або його похідними у пацієнтів з групи ризику. З боку статевих органів: Дуже рідко – пріапізм. З боку шкіри та підшкірних тканин: Рідко - Шкірний висип, кропив'янка, еритема, свербіж шкіри. Лабораторні та інструментальні дані: Часто - підвищення активності "печінкових" трансаміназ, як правило, транзиторне. Загальні розлади та порушення у місці введення: Дуже часто – Гематоми у місці ін'єкції2; Часто – реакції в місці ін'єкції; Рідко – Кальциноз у місці ін'єкції3; Дуже рідко – некроз у місці ін'єкції. 1 Геморагічні прояви найчастіше виявлялися у пацієнтів з іншими факторами ризику. 2 У деяких випадках відбувається утворення твердих вузликів, які не пов'язані з інкапсулюванням гепарину. Ці вузлики зазвичай зникають за кілька днів після появи. 3 Кальциноз частіше зустрічається у пацієнтів із порушенням фосфорно-кальцієвого обміну, наприклад, у пацієнтів із хронічною нирковою недостатністю.Взаємодія з лікарськими засобамиЗастосування деяких препаратів та класів препаратів збільшує ризик розвитку гіперкаліємії. До таких препаратів відносяться: солі калію, калійзберігаючі діуретики, інгібітори АПФ, блокатори рецепторів ангіотензину II, нестероїдні протизапальні засоби, гепарини (низкомолекулярні або нефракціоновані), циклоспорин і такролімус, триметоприм. Розвиток гіперкаліємії може залежати від поєднання кількох факторів ризику. При комбінації перерахованих вище препаратів з надропарином підвищується ризик гіперкаліємії. Нерекомендовані комбінації Застосування надропарину не рекомендується пацієнтам, які використовують інші препарати, які можуть збільшити ризик кровотечі: ацетилсаліцилова кислота у дозах, що застосовуються для знеболювання та інші саліцилати; нестероїдні протизапальні препарати та глюкокортикостероїди для системного застосування; антиагреганти (абциксимаб, ацетилсаліцилова кислота в дозах, що застосовуються для запобігання згортанню за кардіологічними та неврологічними показаннями, берапрост, клопідогрел, ептифібатид, ілопрост, тіклопідін, тирофібан). Спільне застосування надропарину з даними препаратами підвищує ризик розвитку кровотеч, оскільки саліцилати та НПЗП пригнічують активність тромбоцитів та негативно впливають на слизову оболонку шлунка та дванадцятипалої кишки. Для знеболювання та зниження температури слід застосовувати препарати, які не містять саліцилатів (наприклад, парацетамол). У ході клінічних досліджень при лікуванні нестабільної стенокардії та інфаркту міокарда без зубця Q надропарин застосовували у комбінації з аспірином у дозах, що не перевищують 325 мг на добу. За необхідності спільного застосування надропарину з нестероїдними протизапальними засобами слід забезпечити ретельний клінічний моніторинг. Спільне застосування надропарину з декстраном 40 (для парентерального застосування) підвищує ризик розвитку кровотеч, оскільки декстран 40 пригнічує активність тромбоцитів. Комбінації, які слід застосовувати з обережністю Слід обережно призначати надропарин пацієнтам, які приймають пероральні антикоагулянти, оскільки таке поєднання призводить до взаємного посилення ефекту. При заміні надропарину пероральним антикоагулянтом слід забезпечити посилене клінічне спостереження та продовжувати застосування надропарину до стабілізації міжнародного нормалізованого відношення (МНО) до необхідного значення. Комбінації, які слід брати до уваги Спільне застосування надропарину з препаратами, що впливають на гемостаз на різних рівнях, збільшує ризик кровотеч. Таким чином, у пацієнтів різного віку спільне застосування НМГ у терапевтичних дозах з антикоагулянтами для перорального застосування, антиагрегантами (абциксимаб, нестероїдні протизапальні засоби, ацетилсаліцилова кислота, клопідогрел, ептифібатид, ілопрост, тиклопідин, тирофібан) та тромотілоСпосіб застосування та дозиНадропарин слід вводити підшкірно або внутрішньовенно болюсно. Лікування нестабільної стенокардії та інфаркту міокарда без зубця Q: перше введення – внутрішньовенно. Гемодіаліз: введення до артеріальної лінії екстракорпорального контуру гемодіалізу. Не вводити внутрішньом'язово. Дози Профілактика тромбоемболічних ускладнень При загальнохірургічних втручаннях Рекомендована доза Фраксипарину становить 0,3 мл (2850 анти-Ха ME) підшкірно за 2-4 години до операції. Потім Фраксипарин вводять 1 раз на день протягом періоду ризику тромбоутворення (але не менше 7 днів) і до переведення пацієнта на амбулаторний режим. При ортопедичних втручаннях Фраксипарин призначають підшкірно з розрахунку 38 анти-Ха МО/кг ваги, дозування залежить від маси тіла пацієнта (вказана в Таблиці 1 нижче) і може бути збільшена до 50% на 4-й післяопераційний день. Початкова доза призначається за 12 годин до операції, друга доза - через 12 годин після завершення операції. Далі Фраксипарин продовжують застосовувати 1 раз на добу протягом періоду ризику тромбоутворення до переведення пацієнта на амбулаторний режим. Мінімальний термін терапії становить 10 днів. Таблиця 1. Дозування Фраксипарину при профілактиці тромбоемболічних ускладнень при ортопедичних втручаннях Маса тіла пацієнта (кг) Доза Фраксипарину, що вводиться за 12 годин до та через 12 годин після операції, далі 1 раз на добу до 3-го дня після операції Доза Фраксипарину, що вводиться один раз на добу, починаючи з 4-го дня після операції Об'єм, мл Анті-Ха ME Об'єм, мл Анті-Ха ME <50 0,2 1900 0,3 2850 50-69 0,3 2850 0,4 3800 ≥70 0,4 3800 0,6 5700 У пацієнтів з високим ризиком тромбоутворення (при гострій дихальній недостатності та/або респіраторній інфекції та/або серцевій недостатності), які перебувають на постільному режимі у зв'язку з гострою терапевтичною патологією або госпіталізованими до відділень реанімації або інтенсивної терапії Фраксіпарин призначають підшкірно 1 раз на добу. Доза залежить від маси тіла пацієнта та вказана в Таблиці 2 нижче. Фраксипарин застосовують протягом усього періоду ризику тромбоутворення. Таблиця 2. Дозування Фраксипарину при профілактиці тромбоемболічних ускладнень у пацієнтів із високим ризиком тромбоутворення Маса тіла пацієнта (кг) Доза Фраксипарину, що вводиться 1 раз на день Об'єм Фраксипарину, мл Аїті-Ха ME ≤70 0,4 3800 >70 0,6 5700 Для пацієнтів похилого віку доцільно зниження дози до 0,3 мл (2 850 анти-Ха ME). Лікування тромбоемболії легеневої артерії середнього/важкого ступеня тяжкості або проксимального тромбозу глибоких вен нижніх кінцівок За відсутності протипоказань необхідно якомога раніше розпочати терапію пероральними антикоагулянтами. При лікуванні тромбоемболії терапія Фраксипарином повинна продовжуватися доти, доки не буде досягнуто цільових показників Міжнародного Нормалізованого Відносини. Фраксипарин призначають підшкірно 2 десь у день (кожні 12 годин) протягом 10 днів. Доза залежить від маси тіла пацієнта та вказана в Таблиці 3 нижче (з розрахунку 86 анти-Ха МО/кг маси тіла). Таблиця 3. Дозування Фраксипарину при лікуванні тромбоемболії легеневої артерії середнього/важкого ступеня тяжкості або проксимального тромбозу глибоких вен нижніх кінцівок Маса тіла пацієнта (кг) Двічі на день, тривалість 10 днів Об'єм (мл) Анті-Ха ME <50 0,4 3800 50-59 0,5 4750 60-69 0,6 5700 70-79 0,7 6650 80-89 0,8 7600 ≥90 0,9 8550 Профілактика зсідання крові в системі екстракорпорального кровообігу при гемодіалізі Доза Фраксипарину повинна бути встановлена для кожного пацієнта індивідуально з урахуванням технічних умов проведення діалізу. Фраксипарин вводиться одноразово до артеріальної лінії петлі діалізу на початку кожного сеансу. Для пацієнтів, які не мають підвищеного ризику кровотечі, рекомендовані початкові дози, достатні для проведення 4-х годинного сеансу діалізу в залежності від маси тіла (див. Таблицю 4). Таблиця 4. Початкові дози Фраксипарину при профілактиці зсідання крові в системі екстракорпорального кровообігу при гемодіалізі Маса тіла пацієнта (кг) Ін'єкція в артеріальну лінію петлі діалізу на початку сеансу діалізу Об'єм (мл) Анті-Ха ME <50 0,3 2850 50-69 0,4 3800 ≥70 0,6 5700 У пацієнтів з підвищеним ризиком кровотечі рекомендовано застосовувати половинну дозу для проведення діалізу. Якщо сеанс діалізу триває довше 4 годин, Фраксипарин може бути введений додатково у менших дозах. При проведенні наступних сеансів діалізу доза повинна підбиратися індивідуально залежно від ефектів, що спостерігаються. Слід спостерігати за пацієнтом протягом процедури діалізу у зв'язку з можливим виникненням кровотеч або ознак тромбоутворення у системі діалізу. Лікування нестабільної стенокардії та інфаркту міокарда без зубця Q Фраксипарин призначають підшкірно 2 десь у день (кожні 12 годин). Тривалість лікування зазвичай становить 6 днів. У клінічних дослідженнях пацієнтам з нестабільною стенокардією/інфарктом міокарда без зубця Q Фраксипарин призначався у комбінації з ацетилсаліциловою кислотою у дозі 325 мг на добу. Початкова доза застосовується як одноразова внутрішньовенна болюсна ін'єкція, наступні дози вводяться підшкірно. Дози залежить від маси тіла пацієнта та вказані в Таблиці 5 нижче з розрахунку 86 анти-Ха МО/кг маси тіла. Таблиця 5. Дозування Фраксипарину при лікуванні нестабільної стенокардії та інфаркту міокарда без зубця Q Маса тіла пацієнта (кг) Початкова доза для внутрішньовенного введення (болюсно) Підшкірна ін'єкція (кожні 12 годин) Анті-Ха ME <50 0,4 мл 0,4 мл 3800 50-59 0,5 мл 0,5 мл 4750 60-69 0,6 мл 0,6 мл 5700 70-79 0,7 мл 0,7 мл 6650 80-89 0,8 мл 0,8 мл 7600 90-99 0,9 мл 0,9 мл 8550 ≥100 1,0 мл 1,0 мл 9500 Особливі групи пацієнтів Пацієнти похилого віку Профілактика тромбоемболічних ускладнень при загальнохірургічних втручаннях, профілактика зсідання крові під час гемодіалізу та лікування нестабільної стенокардії та інфаркту міокарда без зубця Q У пацієнтів похилого віку коригування доз не потрібне, за винятком пацієнтів із нирковою недостатністю. До початку лікування Фраксіпарином рекомендується провести оцінку функції нирок. Профілактика тромбоемболічних ускладнень у пацієнтів з високим ризиком тромбоутворення (при гострій дихальній недостатності та/або респіраторній інфекції та/або серцевій недостатності), які перебувають на постільному режимі або госпіталізовані до відділень реанімації або інтенсивної терапії У пацієнтів похилого віку може знадобитися зниження дози до 0,3 мл (2850 анти-Ха ME). Ниркова недостатність Профілактика тромбоемболії У пацієнтів з легким нирковою недостатністю (кліренс креатиніну ≥ 50 мл/хв) зниження дози не потрібне. У пацієнтів з помірною та тяжкою нирковою недостатністю спостерігається зниження екскреції надропарину, що призводить до підвищеного ризику виникнення тромбоемболії та кровотеч. Якщо, враховуючи індивідуальні фактори ризику кровотеч і тромбоемболії у пацієнтів з помірною нирковою недостатністю (кліренс креатиніну ≥ 30 мл/хв і менше 50 мл/хв), лікар приймає рішення про зниження дози, доза повинна бути знижена на 25% - 33% . Доза Фраксипарину повинна бути знижена на 25-33% у пацієнтів з тяжкою нирковою недостатністю (кліренс креатиніну менше 30 мл/хв). Лікування тромбоемболій, нестабільної стенокардії та інфаркту міокарда без зубця Q У пацієнтів з нирковою недостатністю (кліренс креатиніну > 50 мл/хв) зниження дози не потрібне. У пацієнтів з помірною та тяжкою нирковою недостатністю спостерігається зниження екскреції надропарину, що призводить до підвищеного ризику розвитку тромбоемболії та кровотеч. Якщо, враховуючи індивідуальні фактори ризику кровотеч та тромбоемболії у пацієнтів з помірною нирковою недостатністю (кліренс креатиніну ≥ 30 мл/хв і менше 50 мл/хв), лікар приймає рішення про зниження дози, доза повинна бути знижена на 25% - 33%. Фраксипарин протипоказаний пацієнтам із тяжкою нирковою недостатністю. Пацієнти з печінковою недостатністю Не проводилося спеціальних досліджень цієї групи пацієнтів. загальні вказівки Особливу увагу слід приділяти конкретним інструкціям із застосування кожного лікарського препарату, що належить до класу низькомолекулярних гепаринів, т.к. їм можуть бути використані різні одиниці дозування (ME чи мг). Саме тому при тривалому лікуванні неприпустиме чергування надропарину з іншими НМГ. Необхідно звертати увагу, який саме препарат використовується - Фраксипарин чи Фраксипарин Форте, т.к. це також впливає на режим дозування. Градовані шприци призначені для добору дози залежно від маси тіла пацієнта. Фраксипарин не призначений для внутрішньом'язового введення. При лікуванні Фраксипарином слід проводити клінічний моніторинг вимірювання кількості тромбоцитів. Необхідно дотримуватись рекомендацій щодо часу дозування Фраксипарину, якщо пацієнту проводиться спінальна/епідуральна анестезія або люмбальна пункція.ПередозуванняСимптоми Основною клінічною ознакою передозування при підшкірному чи внутрішньовенному введенні є кровотеча. Необхідно стежити за кількістю тромбоцитів та іншими параметрами системи згортання крові. Незначні кровотечі не вимагають спеціальної терапії: зазвичай досить буває знизити або ввести пізніше дозу Фраксипарину. Лікування Розглядати призначення протаміну сульфату необхідно лише у тяжких випадках передозування. Протаміну сульфат має виражену нейтралізуючу дію по відношенню до антикоагулянтних ефектів гепарину, проте деяка анти-Ха активність надропарину зберігається. 0,6 мл сульфату протаміну нейтралізує близько 950 анти-Ха ME надропарину. Доза протаміну сульфату розраховується з урахуванням часу, що минув після гепарину, з можливим зниженням дози антидоту.Запобіжні заходи та особливі вказівкиГепарин-індукована тромбоцитопенія Оскільки при застосуванні гепаринів існує можливість розвитку гепариніндукованої тромбоцитопенії, протягом усього курсу лікування Фраксипарином необхідно контролювати рівень тромбоцитів. Повідомлялося про поодинокі випадки ГІТ, у тому числі тяжкі, які могли бути пов'язані з артеріальним або венозним тромбозами. Можливість розвитку ГІТ важливо враховувати у таких випадках: при тромбоцитопенії; при значному зменшенні рівня тромбоцитів (на 30% – 50% порівняно з нормальними показниками); при негативній динаміці клінічних проявів тромбозу, щодо якого пацієнт отримує лікування; у разі виникнення тромбозу на фоні лікування флебіту, легеневої емболії, тромбозу артерій нижніх кінцівок, інфаркту міокарда або інсульту; при ДВЗ-синдромі. У таких випадках необхідно негайно організувати постійний моніторинг рівня тромбоцитів. Застосування надропарину слід припинити. Зазначені ефекти мають імуноалергічну природу і зазвичай відзначаються між 5-м та 21-м днем лікування, але можуть виникати і раніше, якщо у пацієнта була гепарин-індукована тромбоцитопенія в анамнезі. Також повідомлялося про окремі випадки розвитку ГІТ після 21 дня лікування. За наявності гепарин-індукованої тромбоцитопенії в анамнезі (на фоні звичайних або низькомолекулярних гепаринів) лікування Фраксипарином може бути призначене за необхідності. Однак у цій ситуації показано суворий клінічний моніторинг і щонайменше щоденний вимір числа тромбоцитів. У разі виникнення тромбоцитопенії застосування Фраксипарину слід негайно припинити. Якщо тромбоцитопенія розвивається на фоні лікування гепаринами (звичайними або низькомолекулярними), слід розглянути можливість призначення антикоагулянтів інших груп. Якщо інші препарати недоступні, а лікування антикоагулянтами необхідно продовжити, можливе застосування іншого низькомолекулярного гепарину. У цьому випадку слід щодня спостерігати за кількістю тромбоцитів у крові та лікування має бути припинено якомога раніше, оскільки ознаки вихідної тромбоцитопенії продовжують спостерігатися після заміни препарату. Контроль агрегації тромбоцитів, заснований на тестах in vitro, має обмежене значення при діагностиці гепарин-індукованої тромбоцитопенії. Слід виявляти обережність при призначенні Фраксипарину в таких ситуаціях, оскільки вони можуть бути пов'язані з підвищеним ризиком кровотечі: печінкова недостатність; тяжка артеріальна гіпертензія; історія виразкової хвороби або інших органічних уражень, що можуть кровоточити; хоріоретинальні судинні захворювання; післяопераційний період після операції на головному мозку, спинному мозку чи очах; літній вік; пацієнти із масою тіла менше 40 кг. Лабораторний моніторинг Контроль рівня тромбоцитів у пацієнтів, які отримують НМГ та мають фактори ризику гепарин-індукованої тромбоцитопенії Для своєчасного виявлення ГІТ під час лікування оптимально проводити моніторинг стану пацієнтів так: Після хірургічного втручання або травми (за останні 3 місяці): при застосуванні надропарину з метою лікування або профілактики необхідний регулярний біологічний моніторинг, оскільки захворюваність на ГІТ у таких пацієнтів становить 0,1% і навіть >1%. Визначення концентрації тромбоцитів слід проводити: до початку лікування НМГ або в перші 24 години після початку лікування; 2 рази на тиждень протягом першого місяця лікування (період максимального ризику); 1 раз на тиждень до закінчення лікування у разі тривалої терапії. За відсутності хірургічного втручання або травми за останні 3 місяці: при застосуванні надропарину з метою лікування або профілактики регулярний біологічний моніторинг необхідний у таких випадках: за наявності в анамнезі терапії НФГ або НМГ за останні 6 місяців - через захворюваність на ГІТ > 0,1% і навіть >1%; за наявності супутніх захворювань - через потенційну небезпеку ГІТ у таких пацієнтів. В інших випадках, через низьку захворюваність на ГІТ ( до початку лікування НМГ або перші 24 год після початку терапії; при появі специфічних клінічних ознак ГІТ (артеріальна або венозна тромбоемболія, хворобливе ураження шкіри у місці ін'єкції, ознаки алергії та гіперчутливості під час терапії). Слід повідомляти пацієнтам про можливість появи подібних клінічних ознак та необхідність звернутися до свого лікаря у разі їх появи. Можливість розвитку ГІТ слід розглянути у разі зниження вмісту тромбоцитів до рівня При легкій нирковій недостатності (кліренс креатиніну ≥ 50 мл/хв) не потрібно знижувати дозу надропарину. Будь-яке значне зниження рівня тромбоцитів (на 30%-50% від вихідного значення) вимагає термінової уваги ще до того, як рівень досягне критичного граничного значення. У разі зниження рівня тромбоцитів необхідно: негайно оцінити динаміку тромбоцитопенії; припинити застосування гепарину, якщо підтверджено зниження рівня тромбоцитів, що продовжується, за відсутності інших очевидних причин тромбоцитопенії; провести профілактику чи лікування тромботичного ускладнення ГІТ. Якщо потрібне подальше лікування антикоагулянтами, слід замінити гепарин антикоагулянтом іншого класу у профілактичній або терапевтичній дозі залежно від ситуації. У разі заміни гепарину на антагоністи вітаміну К (АВК) останні слід призначати лише після нормалізації рівня тромбоцитів, тому що в іншому випадку існує ризик посилення тромботичного ефекту. Заміна гепарину антагоністами вітаміну К Необхідно забезпечити ретельний клінічний та лабораторний моніторинг (протромбіновий час за Квіком та міжнародне нормалізоване відношення) для контролю за дією АВК. Оскільки повна дія антагоністів вітаміну К проявляється через деякий період часу, слід продовжувати введення гепарину в еквівалентній дозі, поки це необхідно для досягнення рівня МНО, допустимого при даному показанні, при двох послідовних вимірах. Особливі групи пацієнтів Пацієнти з нирковою недостатністю Оскільки надропарин в основному виводиться нирками, це призводить до зменшення екскреції надропарину у пацієнтів з нирковою недостатністю. Тому у такої групи пацієнтів є більший ризик кровотечі і потрібна велика обережність при лікуванні. Рішення про зменшення або збереження дози для пацієнта з кліренсом креатиніну від 30 до 50 мл/хв приймається лікарем, який має оцінити індивідуальний ризик кровотечі для пацієнта порівняно з ризиком розвитку тромбоемболії. Пацієнти похилого віку Перед початком лікування Фраксипарин необхідно оцінити функцію нирок. Гіперкаліємія Гепарини можуть пригнічувати секрецію альдостерону, що може призвести до гіперкаліємії, особливо у пацієнтів з підвищеним калієм у крові або у пацієнтів з ризиком підвищення вмісту калію в крові, наприклад, у пацієнтів з цукровим діабетом, хронічною нирковою недостатністю, метаболічним ацидозом або у пацієнтів, які приймають. препарати, які можуть викликати гіперкаліємію (наприклад, інгібітори ангіотензин-перетворюючої дії, нестероїдні протизапальні засоби (НПЗЗ)). Ризик гіперкаліємії підвищується при тривалій терапії, але зазвичай оборотний при відміні. У пацієнтів, які перебувають у групі ризику, слід контролювати рівень калію у крові. Спінальна/епідуральна анестезія/спинномозкова пункція та супутні лікарські препарати Ризик виникнення спинальних/епідуральних гематом після використання надропарину, що призводять до неврологічним розладам, у тому числі тривалим або постійним паралічам, підвищується у пацієнтів із встановленими епідуральними катетерами або супутнім застосуванням інших ліків, які можуть вплинути на гемостаз, такі як НПЗЗ, антиагрегантні антикоагулянти. Ризик також збільшується при проведенні травматичних або повторних епідуральних або спинномозкових пункцій. Тому питання про комбіноване застосування нейроаксіальної блокади та антикоагулянтів має вирішуватися індивідуально після оцінки співвідношення користь/ризик у наступних ситуаціях: у пацієнтів, які вже отримують антикоагулянти, має бути обґрунтовано необхідність спінальної або епідуральної анестезії; у пацієнтів, яким планується елективне хірургічне втручання із застосуванням спинальної або епідуральної анестезії, має бути обґрунтовано необхідність введення антикоагулянтів. Якщо пацієнту проводиться люмбальна пункція або спинальна або епідуральна анестезія, слід дотримуватись інтервалу мінімум 12 годин між введенням Фраксипарину у профілактичних дозах або 24 години у терапевтичних дозах та введенням або видаленням спинального/епідурального катетера або голки. Для пацієнтів з нирковою недостатністю можуть розглядатися тривалі інтервали. Необхідно ретельне спостереження за пацієнтом з метою виявлення ознак та симптомів неврологічних порушень, таких як біль у спині, сенсорні або рухові порушення (оніміння або слабкість нижніх кінцівок), проблеми із сечовим міхуром та/або кишечником. Пацієнтів слід проінструктувати про необхідність інформування лікаря у разі неврологічних симптомів. При виявленні порушень у неврологічному статусі пацієнта потрібна термінова відповідна терапія, включаючи декомпресію спинного мозку. Саліцилати, нестероїдні протизапальні препарати та антиагрегантні засоби При профілактиці або лікуванні венозних тромбоемболій, а також при профілактиці зсідання крові в системі екстракорпорального кровообігу при гемодіалізі не рекомендується спільне призначення Фраксипарину з такими препаратами, як ацетилсаліцилова кислота, інші саліцилати, НПЗЗ та антирегант. це може збільшити ризик розвитку кровотеч. Якщо таких комбінацій не можна уникнути, необхідно проводити ретельне клінічне та біологічне спостереження. У клінічних дослідженнях у пацієнтів з нестабільною стенокардією та інфарктом міокарда без підвищення зубця Q надропарин застосовувався у комбінації з ацетилсаліциловою кислотою у дозах, що не перевищують 325 мг на добу. Некроз шкіри Про шкірні некрози повідомлялося дуже рідко. Цьому передували пурпури або інфільтровані або болючі еритематозні плями з присутністю або відсутністю загальних ознак. У таких випадках лікування має бути негайно припинено. Алергія на латекс Ковпачок голки попередньо заповненого шприца складається з натуральної зневодненої гуми - похідного латексу, що може стати причиною алергічної реакції. Пацієнти з механічними клапанними протезами (включаючи вагітні жінки) Застосування надропарину кальцію для профілактики тромбоутворення у пацієнтів з штучними механічними клапанами серця вивчено недостатньо. У зв'язку з неможливістю оцінити ефективність та безпеку застосування препарату Фраксипарин для зниження ризику тромбозів та емболій у пацієнтів з механічними штучними клапанами серця не рекомендується. Вагітні жінки з механічними штучними клапанами серця мають високий ризик розвитку тромбозів та емболій. Наявний обмежений досвід застосування надропарину кальцію не дозволяє рекомендувати застосування препарату Фраксипарин для зниження ризику тромбозів та емболій у вагітних жінок із механічними штучними клапанами серця. Низька маса тіла Перед початком лікування Фраксипарин необхідно оцінити функцію нирок. Пацієнти з ожирінням У пацієнтів з ожирінням є підвищений ризик виникнення тромбоемболічних ускладнень. Безпека та ефективність профілактичних доз Фраксипарину не повністю оцінені у пацієнтів з ожирінням (індекс маси тіла > 30 кг/м2) та рекомендації щодо добору дози відсутні. Тому рекомендується спостереження даних пацієнтів щодо появи ознак і симптомів тромбоемболічних ускладнень. Діти В даний час недостатньо клінічних даних щодо ефективності та безпеки застосування Фраксипарину у пацієнтів до 18 років, у зв'язку з чим призначення Фраксипарину дітям та підліткам не рекомендується. Вплив на здатність до керування автотранспортом та управління механізмами Немає даних про вплив Фраксипарину на здатність керувати транспортними засобами та механізмами.Умови відпустки з аптекЗа рецептомВідео на цю тему
2 668,00 грн
175,00 грн
Склад, форма випуску та упаковкаРозчин - 1 мл: Активна речовина: надропарин кальцію - 9500 ME анти Ха-факторної активності в 1 мл; Допоміжні речовини: розчин гідроксиду кальцію (або розбавлена хлористоводнева кислота) - достатня кількість для доведення pH до 5,0 - 7,0; вода для ін'єкцій – до 1,0 мл. По 0,3 мл, 0,4 мл, 0,6 мл, 0,8 мл або 1,0 мл препарату в однодозовий скляний шприц із захисним корпусом, наконечником з голкою з нержавіючої сталі, закритою ковпачком. По 2 шприца упаковують у прозорий блістер із ПBX/ПЕ плівки. По 1 або 5 блістерів (по 2 або 10 шприців) разом з інструкцією із застосування поміщають у картонну пачку.Опис лікарської формиПрозорий або слабо-опалесцентний, безбарвний або світло-жовтий розчин.Фармакотерапевтична групаАнтикоагулянтний засіб прямої дії.ФармакокінетикаФармакокінетичні властивості надропарину визначаються з урахуванням біологічної активності, тобто. вимірювання анти-Ха-факторної активності. Абсорбція Після підшкірного введення максимальна анти-Ха активність (Сmах) досягається приблизно через 3 - 5 год (Тmах) - Біодоступність практично повна (близько 98%). Після внутрішньовенного введення максимальна анти-Ха активність досягається через 10 хвилин, і період напіввиведення становить близько 2 год. Виведення Період напіввиведення після підшкірного введення становить близько 3,5 год. Проте анти-Ха активність зберігається протягом щонайменше 18 годин після введення надропарину в дозі 1900 анти-Ха ME. Особливі групи пацієнтів Пацієнти похилого віку Як правило, ниркова функція знижується з віком, тому елімінація надропарину може уповільнюватися. Можлива ниркова недостатність у цій групі пацієнтів потребує оцінки та відповідної корекції дози. Пацієнти з нирковою недостатністю У клінічному дослідженні, присвяченому вивченню фармакокінетики надропарину при внутрішньовенному введенні, у пацієнтів з різним ступенем ниркової недостатності було встановлено кореляцію між кліренсом надропарину та кліренсом креатиніну. У пацієнтів з помірною нирковою недостатністю (кліренс креатиніну 36 - 43 мл/хв) AUC та період напіввиведення були збільшені на 52% та 39% відповідно у порівнянні зі здоровими добровольцями. У цих пацієнтів плазмовий кліренс надропарину був знижений до 63% нормальних значень. У дослідженні спостерігався широкий діапазон міжіндивідуальної варіабельності. У пацієнтів з тяжкою нирковою недостатністю (кліренс креатиніну 10-20 мл/хв) AUC та період напіввиведення були підвищені до 95% та 112% відповідно порівняно зі здоровими добровольцями.Плазмовий кліренс надропарину у пацієнтів з тяжкою нирковою недостатністю був знижений до 50% від пацієнта з нормальною функцією нирок. У пацієнтів з тяжкою нирковою недостатністю (кліренс креатиніну 3 - 6 мл/хв), що перебувають на гемодіалізі, AUC та період напіввиведення були збільшені на 62% та 65% відповідно у порівнянні зі здоровими добровольцями. Плазмовий кліренс надропарину у пацієнтів з тяжкою нирковою недостатністю, що перебувають на гемодіалізі, був знижений до 67% від нормальних значень.Плазмовий кліренс надропарину у пацієнтів з тяжкою нирковою недостатністю, що перебувають на гемодіалізі, був знижений до 67% від нормальних значень.Плазмовий кліренс надропарину у пацієнтів з тяжкою нирковою недостатністю, що перебувають на гемодіалізі, був знижений до 67% від нормальних значень.ФармакодинамікаМеханізм дії Надропарин – це низькомолекулярний гепарин (НМГ), отриманий шляхом деполімеризації зі стандартного гепарину. Він являє собою глікозаміноглікан із середньою молекулярною масою приблизно 4300 дальтон. Надропарин виявляє високу здатність до зв'язування з білком плазми антитромбіном III (AT III). Це зв'язування призводить до прискореного пригнічення фактора Ха, чим і обумовлений високий антитромботичний потенціал надропарину. Інші механізми, що забезпечують антитромботічну дію надропарину, включають активацію інгібітору перетворення тканинного фактора (TFPI), активацію фібринолізу за допомогою прямого вивільнення активатора тканинного плазміногену з ендотеліальних клітин та модифікацію реологічних властивостей крові (зниження в'язкості крові) і збільшення пров. Фармакодинаміка Надропарин характеризується вищою активністю щодо фактора Ха порівняно з активністю щодо фактора На. Він має як негайну, так і продовжену антитромботичну активність. У порівнянні з нефракціонованим гепарином (НФГ) надропарин має менший вплив на функції тромбоцитів та їх здатність до агрегації та мало виражений вплив на первинний гемостаз.ІнструкціяВлаштування шприца Запобіжник голки Поршень Тримач Захисний корпус Підготовка до ін'єкції та техніка підшкірного введення 1. Ретельно вимийте руки з водою та милом і висушіть рушником. 2. Вийміть попередньо заповнений шприц із пачки та повірте, що: термін придатності препарату не минув; шприц не був розкритий та не пошкоджений. 3. Прийміть положення сидячи або лежачи. Виберіть місце в нижній частині живота, крім області приблизно 5 см навколо пупка. Переважно вводити препарат у праву та ліву сторони передньої черевної стінки почергово. Це допоможе зменшити дискомфорт у місці ін'єкції. Якщо введення в нижню частину живота неможливе, зверніться за порадою до лікаря або медичної сестри. 4. Обробіть місце ін'єкції тампоном, змоченим спиртом. 5. Зніміть захисний ковпачок, прокрутивши спочатку, а потім потягніть його по прямій лінії від захисного корпусу. Викиньте захисний ковпачок. Якщо об'єм розчину в шприці більший, ніж необхідно для ін'єкції, Ви повинні видалити надлишок розчину перед ін'єкцією. Тримайте шприц голкою вниз. Обережно натискайте на поршень доти, доки нижня частина поршня не опиниться на лінії об'єму, призначеного лікарем. Надлишки розчину необхідно викинути. Тепер шприц готовий до використання. Не торкайтеся голки після зняття ковпачка і не допускайте контакту голки з будь-якими поверхнями. Ви можете помітити бульбашки повітря у шприці. Не намагайтеся видаляти бульбашки повітря перед ін'єкцією – це може призвести до втрати частини препарату. 6. Обережно затисніть шкіру для формування складки. Шкірну складку необхідно утримувати великим та вказівним пальцями до закінчення введення препарату. 7. Тримайте шприц міцно. Голку слід вводити перпендикулярно, а не під кутом, на всю довжину затиснутої складки шкіри. 8. Введіть вміст шприца, натиснувши на поршень. Потім акуратно видаліть голку та притисніть місце ін'єкції тампоном, змоченим спиртом. Не слід розтирати місце застосування препарату після ін'єкції. 9. Після ін'єкції на використаний шприц встановлюється система захисту: утримуючи використаний шприц в одній руці за захисний корпус, іншою рукою потягніть за тримач для вивільнення клямки та зсуву корпусу для захисту голки до чутного клацання, що позначає фіксацію захисного корпусу. Утилізуйте використаний шприц відповідно до звичайної процедури утилізації медичних відходів. При застосуванні препарату суворо дотримуйтесь рекомендацій, наведених у даній інструкції, а також вказівок лікаря. У разі виникнення запитань, зверніться до лікаря.Показання до застосуванняПрофілактика тромбоемболічних ускладнень: при загальнохірургічних та ортопедичних втручаннях; у пацієнтів з високим ризиком тромбоутворення (при гострій дихальній недостатності та/або респіраторній інфекції та/або серцевій недостатності), які перебувають на постільному режимі у зв'язку з гострою терапевтичною патологією або госпіталізованими до відділень реанімації або інтенсивної терапії. Лікування тромбоемболії легеневої артерії середнього/важкого ступеня тяжкості або проксимального тромбозу глибоких вен нижніх кінцівок. Профілактика зсідання крові під час гемодіалізу. Лікування нестабільної стенокардії та інфаркту міокарда без зубця Q.Протипоказання до застосуванняПідвищена чутливість до надропарину або до будь-якого іншого компонента препарату. Наявність в анамнезі тяжкої гепарин-індукованої тромбоцитопенії (ГІТ) II типу, спричиненої застосуванням нефракціонованого або низькомолекулярного гепарину, або будь-якої тромбоцитопенії, спричиненої застосуванням надропарину. Тромбоцитопенія у поєднанні з позитивним тестом на антитромбоцитарні антитіла in vitro у присутності надропарину кальцію (див. розділ "Особливі вказівки"). Ознаки кровотечі або підвищений ризик кровотечі, пов'язаний із порушенням гемостазу, за винятком ДВЗ-синдрому, не викликаного гепарином. Органічні ураження органів зі схильністю до кровоточивості (наприклад, гостра виразка шлунка або дванадцятипалої кишки). Внутрішньочерепний крововилив. Гострий інфекційний ендокардит. Тяжка ниркова недостатність (кліренс креатиніну менше 30 мл/хв) у пацієнтів, які отримують Фраксипарин з метою лікування тромбоемболій та венозних тромбозів, нестабільної стенокардії та інфаркту міокарда без зубця Q. Травми або оперативні втручання на головному та спинному мозку або на очах. Місцева та регіонарна анестезія при плановій хірургії у пацієнтів, які отримують Фраксипарин з метою лікування тромбоемболії легеневої артерії, тромбозу глибоких вен, нестабільної стенокардії та інфаркту міокарда без зубця Q. З обережністю: Печінкова недостатність. Ниркова недостатність. Тяжка артеріальна гіпертензія. Виразки в анамнезі або інші захворювання з підвищеним ризиком кровотечі. Хоріоретинальні судинні захворювання. Післяопераційний період після операцій на головному та спинному мозку або на очах. При перевищенні рекомендованої тривалості лікування (10 днів). Недотримання рекомендованих умов лікування (особливо тривалості та встановлення дози на основі маси тіла для курсового застосування). У комбінації з препаратами, що посилюють ризик кровотечі, такими як ацетилсаліцилова кислота та інші саліцилати, нестероїдні протизапальні препарати (НПЗП), антиагрегантні засоби. Літній вік. Пацієнти із масою тіла менше 40 кг. Проведення спінальної або епідуральної анестезії (ризик розвитку гематоми), спинномозкова пункція (у т. ч. нещодавно перенесена). При тривалому застосуванні високих доз низькомолекулярних гепаринів не можна виключати ризик розвитку остеопорозу, особливо у пацієнтів із підвищеним ризиком розвитку остеопорозу.Вагітність та лактаціяВагітність Досліди на тваринах не показали тератогенного чи фетотоксичного ефектів надропарину. Застосування для профілактики та І триместрі вагітності Наявних клінічних даних недостатньо для оцінки можливого тератогенного та фетотоксичного ефектів надропарину у людини при застосуванні у профілактичних дозах у І триместрі вагітності та у терапевтичних дозах протягом усієї вагітності. Тому слід уникати застосування Фраксипарину у профілактичних дозах у І триместрі вагітності та у терапевтичних дозах протягом усієї вагітності. Застосування для профілактики у ІІ та ІІІ триместрах вагітності При застосуванні надропарину протягом II та III триместру вагітності у обмеженої кількості пацієнток не було виявлено ознак тератогенної або фетотоксичної дії препарату. Однак для оцінки впливу надропарину необхідні подальші дослідження. Тому застосовувати Фраксипарин у профілактичних дозах у II та III триместрах вагітності слід лише у разі потреби. При необхідності застосування епідуральної анестезії рекомендується зупинення профілактичного лікування гепарином не менше ніж за 12 годин до анестезії. Грудне годування В даний час є лише обмежені дані щодо виділення надропарину в грудне молоко, хоча всмоктування надропарину у новонароджених малоймовірне. У зв'язку з цим застосування надропарину у період грудного вигодовування не протипоказане. Фертильність Дані клінічних досліджень щодо впливу надропарину на фертильність відсутні.Побічна діяВикористана наступна класифікація небажаних реакцій залежно від частоти народження: дуже часто (>1/10), часто (>1/100, 1/1000, 1/10,000, З боку крові та лімфатичної системи: Дуже часто – Кровотеча1; Рідко - тромбоцитопенію, включаючи гепарин-індуковану тромбоцитопенію, тромбоцитоз; Дуже рідко – еозинофілія, оборотна після припинення лікування. З боку імунної системи: Дуже рідко – реакції гіперчутливості (включаючи ангіоневротичний набряк та шкірні реакції, бронхоспазм), анафілактоїдні реакції. З боку обміну речовин: Дуже рідко: оборотна гіперкаліємія, пов'язана з гіпоальдостеронізмом, індукована гепарином або його похідними у пацієнтів з групи ризику. З боку статевих органів: Дуже рідко – пріапізм. З боку шкіри та підшкірних тканин: Рідко - Шкірний висип, кропив'янка, еритема, свербіж шкіри. Лабораторні та інструментальні дані: Часто - підвищення активності "печінкових" трансаміназ, як правило, транзиторне. Загальні розлади та порушення у місці введення: Дуже часто – Гематоми у місці ін'єкції2; Часто – реакції в місці ін'єкції; Рідко – Кальциноз у місці ін'єкції3; Дуже рідко – некроз у місці ін'єкції. 1 Геморагічні прояви найчастіше виявлялися у пацієнтів з іншими факторами ризику. 2 У деяких випадках відбувається утворення твердих вузликів, які не пов'язані з інкапсулюванням гепарину. Ці вузлики зазвичай зникають за кілька днів після появи. 3 Кальциноз частіше зустрічається у пацієнтів із порушенням фосфорно-кальцієвого обміну, наприклад, у пацієнтів із хронічною нирковою недостатністю.Взаємодія з лікарськими засобамиЗастосування деяких препаратів та класів препаратів збільшує ризик розвитку гіперкаліємії. До таких препаратів відносяться: солі калію, калійзберігаючі діуретики, інгібітори АПФ, блокатори рецепторів ангіотензину II, нестероїдні протизапальні засоби, гепарини (низкомолекулярні або нефракціоновані), циклоспорин і такролімус, триметоприм. Розвиток гіперкаліємії може залежати від поєднання кількох факторів ризику. При комбінації перерахованих вище препаратів з надропарином підвищується ризик гіперкаліємії. Нерекомендовані комбінації Застосування надропарину не рекомендується пацієнтам, які використовують інші препарати, які можуть збільшити ризик кровотечі: ацетилсаліцилова кислота у дозах, що застосовуються для знеболювання та інші саліцилати; нестероїдні протизапальні препарати та глюкокортикостероїди для системного застосування; антиагреганти (абциксимаб, ацетилсаліцилова кислота в дозах, що застосовуються для запобігання згортанню за кардіологічними та неврологічними показаннями, берапрост, клопідогрел, ептифібатид, ілопрост, тіклопідін, тирофібан). Спільне застосування надропарину з даними препаратами підвищує ризик розвитку кровотеч, оскільки саліцилати та НПЗП пригнічують активність тромбоцитів та негативно впливають на слизову оболонку шлунка та дванадцятипалої кишки. Для знеболювання та зниження температури слід застосовувати препарати, які не містять саліцилатів (наприклад, парацетамол). У ході клінічних досліджень при лікуванні нестабільної стенокардії та інфаркту міокарда без зубця Q надропарин застосовували у комбінації з аспірином у дозах, що не перевищують 325 мг на добу. За необхідності спільного застосування надропарину з нестероїдними протизапальними засобами слід забезпечити ретельний клінічний моніторинг. Спільне застосування надропарину з декстраном 40 (для парентерального застосування) підвищує ризик розвитку кровотеч, оскільки декстран 40 пригнічує активність тромбоцитів. Комбінації, які слід застосовувати з обережністю Слід обережно призначати надропарин пацієнтам, які приймають пероральні антикоагулянти, оскільки таке поєднання призводить до взаємного посилення ефекту. При заміні надропарину пероральним антикоагулянтом слід забезпечити посилене клінічне спостереження та продовжувати застосування надропарину до стабілізації міжнародного нормалізованого відношення (МНО) до необхідного значення. Комбінації, які слід брати до уваги Спільне застосування надропарину з препаратами, що впливають на гемостаз на різних рівнях, збільшує ризик кровотеч. Таким чином, у пацієнтів різного віку спільне застосування НМГ у терапевтичних дозах з антикоагулянтами для перорального застосування, антиагрегантами (абциксимаб, нестероїдні протизапальні засоби, ацетилсаліцилова кислота, клопідогрел, ептифібатид, ілопрост, тиклопідин, тирофібан) та тромотілоСпосіб застосування та дозиНадропарин слід вводити підшкірно або внутрішньовенно болюсно. Лікування нестабільної стенокардії та інфаркту міокарда без зубця Q: перше введення – внутрішньовенно. Гемодіаліз: введення до артеріальної лінії екстракорпорального контуру гемодіалізу. Не вводити внутрішньом'язово. Дози Профілактика тромбоемболічних ускладнень При загальнохірургічних втручаннях Рекомендована доза Фраксипарину становить 0,3 мл (2850 анти-Ха ME) підшкірно за 2-4 години до операції. Потім Фраксипарин вводять 1 раз на день протягом періоду ризику тромбоутворення (але не менше 7 днів) і до переведення пацієнта на амбулаторний режим. При ортопедичних втручаннях Фраксипарин призначають підшкірно з розрахунку 38 анти-Ха МО/кг ваги, дозування залежить від маси тіла пацієнта (вказана в Таблиці 1 нижче) і може бути збільшена до 50% на 4-й післяопераційний день. Початкова доза призначається за 12 годин до операції, друга доза - через 12 годин після завершення операції. Далі Фраксипарин продовжують застосовувати 1 раз на добу протягом періоду ризику тромбоутворення до переведення пацієнта на амбулаторний режим. Мінімальний термін терапії становить 10 днів. Таблиця 1. Дозування Фраксипарину при профілактиці тромбоемболічних ускладнень при ортопедичних втручаннях Маса тіла пацієнта (кг) Доза Фраксипарину, що вводиться за 12 годин до та через 12 годин після операції, далі 1 раз на добу до 3-го дня після операції Доза Фраксипарину, що вводиться один раз на добу, починаючи з 4-го дня після операції Об'єм, мл Анті-Ха ME Об'єм, мл Анті-Ха ME <50 0,2 1900 0,3 2850 50-69 0,3 2850 0,4 3800 ≥70 0,4 3800 0,6 5700 У пацієнтів з високим ризиком тромбоутворення (при гострій дихальній недостатності та/або респіраторній інфекції та/або серцевій недостатності), які перебувають на постільному режимі у зв'язку з гострою терапевтичною патологією або госпіталізованими до відділень реанімації або інтенсивної терапії Фраксіпарин призначають підшкірно 1 раз на добу. Доза залежить від маси тіла пацієнта та вказана в Таблиці 2 нижче. Фраксипарин застосовують протягом усього періоду ризику тромбоутворення. Таблиця 2. Дозування Фраксипарину при профілактиці тромбоемболічних ускладнень у пацієнтів із високим ризиком тромбоутворення Маса тіла пацієнта (кг) Доза Фраксипарину, що вводиться 1 раз на день Об'єм Фраксипарину, мл Аїті-Ха ME ≤70 0,4 3800 >70 0,6 5700 Для пацієнтів похилого віку доцільно зниження дози до 0,3 мл (2 850 анти-Ха ME). Лікування тромбоемболії легеневої артерії середнього/важкого ступеня тяжкості або проксимального тромбозу глибоких вен нижніх кінцівок За відсутності протипоказань необхідно якомога раніше розпочати терапію пероральними антикоагулянтами. При лікуванні тромбоемболії терапія Фраксипарином повинна продовжуватися доти, доки не буде досягнуто цільових показників Міжнародного Нормалізованого Відносини. Фраксипарин призначають підшкірно 2 десь у день (кожні 12 годин) протягом 10 днів. Доза залежить від маси тіла пацієнта та вказана в Таблиці 3 нижче (з розрахунку 86 анти-Ха МО/кг маси тіла). Таблиця 3. Дозування Фраксипарину при лікуванні тромбоемболії легеневої артерії середнього/важкого ступеня тяжкості або проксимального тромбозу глибоких вен нижніх кінцівок Маса тіла пацієнта (кг) Двічі на день, тривалість 10 днів Об'єм (мл) Анті-Ха ME <50 0,4 3800 50-59 0,5 4750 60-69 0,6 5700 70-79 0,7 6650 80-89 0,8 7600 ≥90 0,9 8550 Профілактика зсідання крові в системі екстракорпорального кровообігу при гемодіалізі Доза Фраксипарину повинна бути встановлена для кожного пацієнта індивідуально з урахуванням технічних умов проведення діалізу. Фраксипарин вводиться одноразово до артеріальної лінії петлі діалізу на початку кожного сеансу. Для пацієнтів, які не мають підвищеного ризику кровотечі, рекомендовані початкові дози, достатні для проведення 4-х годинного сеансу діалізу в залежності від маси тіла (див. Таблицю 4). Таблиця 4. Початкові дози Фраксипарину при профілактиці зсідання крові в системі екстракорпорального кровообігу при гемодіалізі Маса тіла пацієнта (кг) Ін'єкція в артеріальну лінію петлі діалізу на початку сеансу діалізу Об'єм (мл) Анті-Ха ME <50 0,3 2850 50-69 0,4 3800 ≥70 0,6 5700 У пацієнтів з підвищеним ризиком кровотечі рекомендовано застосовувати половинну дозу для проведення діалізу. Якщо сеанс діалізу триває довше 4 годин, Фраксипарин може бути введений додатково у менших дозах. При проведенні наступних сеансів діалізу доза повинна підбиратися індивідуально залежно від ефектів, що спостерігаються. Слід спостерігати за пацієнтом протягом процедури діалізу у зв'язку з можливим виникненням кровотеч або ознак тромбоутворення у системі діалізу. Лікування нестабільної стенокардії та інфаркту міокарда без зубця Q Фраксипарин призначають підшкірно 2 десь у день (кожні 12 годин). Тривалість лікування зазвичай становить 6 днів. У клінічних дослідженнях пацієнтам з нестабільною стенокардією/інфарктом міокарда без зубця Q Фраксипарин призначався у комбінації з ацетилсаліциловою кислотою у дозі 325 мг на добу. Початкова доза застосовується як одноразова внутрішньовенна болюсна ін'єкція, наступні дози вводяться підшкірно. Дози залежить від маси тіла пацієнта та вказані в Таблиці 5 нижче з розрахунку 86 анти-Ха МО/кг маси тіла. Таблиця 5. Дозування Фраксипарину при лікуванні нестабільної стенокардії та інфаркту міокарда без зубця Q Маса тіла пацієнта (кг) Початкова доза для внутрішньовенного введення (болюсно) Підшкірна ін'єкція (кожні 12 годин) Анті-Ха ME <50 0,4 мл 0,4 мл 3800 50-59 0,5 мл 0,5 мл 4750 60-69 0,6 мл 0,6 мл 5700 70-79 0,7 мл 0,7 мл 6650 80-89 0,8 мл 0,8 мл 7600 90-99 0,9 мл 0,9 мл 8550 ≥100 1,0 мл 1,0 мл 9500 Особливі групи пацієнтів Пацієнти похилого віку Профілактика тромбоемболічних ускладнень при загальнохірургічних втручаннях, профілактика зсідання крові під час гемодіалізу та лікування нестабільної стенокардії та інфаркту міокарда без зубця Q У пацієнтів похилого віку коригування доз не потрібне, за винятком пацієнтів із нирковою недостатністю. До початку лікування Фраксіпарином рекомендується провести оцінку функції нирок. Профілактика тромбоемболічних ускладнень у пацієнтів з високим ризиком тромбоутворення (при гострій дихальній недостатності та/або респіраторній інфекції та/або серцевій недостатності), які перебувають на постільному режимі або госпіталізовані до відділень реанімації або інтенсивної терапії У пацієнтів похилого віку може знадобитися зниження дози до 0,3 мл (2850 анти-Ха ME). Ниркова недостатність Профілактика тромбоемболії У пацієнтів з легким нирковою недостатністю (кліренс креатиніну ≥ 50 мл/хв) зниження дози не потрібне. У пацієнтів з помірною та тяжкою нирковою недостатністю спостерігається зниження екскреції надропарину, що призводить до підвищеного ризику виникнення тромбоемболії та кровотеч. Якщо, враховуючи індивідуальні фактори ризику кровотеч і тромбоемболії у пацієнтів з помірною нирковою недостатністю (кліренс креатиніну ≥ 30 мл/хв і менше 50 мл/хв), лікар приймає рішення про зниження дози, доза повинна бути знижена на 25% - 33% . Доза Фраксипарину повинна бути знижена на 25-33% у пацієнтів з тяжкою нирковою недостатністю (кліренс креатиніну менше 30 мл/хв). Лікування тромбоемболій, нестабільної стенокардії та інфаркту міокарда без зубця Q У пацієнтів з нирковою недостатністю (кліренс креатиніну > 50 мл/хв) зниження дози не потрібне. У пацієнтів з помірною та тяжкою нирковою недостатністю спостерігається зниження екскреції надропарину, що призводить до підвищеного ризику розвитку тромбоемболії та кровотеч. Якщо, враховуючи індивідуальні фактори ризику кровотеч та тромбоемболії у пацієнтів з помірною нирковою недостатністю (кліренс креатиніну ≥ 30 мл/хв і менше 50 мл/хв), лікар приймає рішення про зниження дози, доза повинна бути знижена на 25% - 33%. Фраксипарин протипоказаний пацієнтам із тяжкою нирковою недостатністю. Пацієнти з печінковою недостатністю Не проводилося спеціальних досліджень цієї групи пацієнтів. загальні вказівки Особливу увагу слід приділяти конкретним інструкціям із застосування кожного лікарського препарату, що належить до класу низькомолекулярних гепаринів, т.к. їм можуть бути використані різні одиниці дозування (ME чи мг). Саме тому при тривалому лікуванні неприпустиме чергування надропарину з іншими НМГ. Необхідно звертати увагу, який саме препарат використовується - Фраксипарин чи Фраксипарин Форте, т.к. це також впливає на режим дозування. Градовані шприци призначені для добору дози залежно від маси тіла пацієнта. Фраксипарин не призначений для внутрішньом'язового введення. При лікуванні Фраксипарином слід проводити клінічний моніторинг вимірювання кількості тромбоцитів. Необхідно дотримуватись рекомендацій щодо часу дозування Фраксипарину, якщо пацієнту проводиться спінальна/епідуральна анестезія або люмбальна пункція.ПередозуванняСимптоми Основною клінічною ознакою передозування при підшкірному чи внутрішньовенному введенні є кровотеча. Необхідно стежити за кількістю тромбоцитів та іншими параметрами системи згортання крові. Незначні кровотечі не вимагають спеціальної терапії: зазвичай досить буває знизити або ввести пізніше дозу Фраксипарину. Лікування Розглядати призначення протаміну сульфату необхідно лише у тяжких випадках передозування. Протаміну сульфат має виражену нейтралізуючу дію по відношенню до антикоагулянтних ефектів гепарину, проте деяка анти-Ха активність надропарину зберігається. 0,6 мл сульфату протаміну нейтралізує близько 950 анти-Ха ME надропарину. Доза протаміну сульфату розраховується з урахуванням часу, що минув після гепарину, з можливим зниженням дози антидоту.Запобіжні заходи та особливі вказівкиГепарин-індукована тромбоцитопенія Оскільки при застосуванні гепаринів існує можливість розвитку гепариніндукованої тромбоцитопенії, протягом усього курсу лікування Фраксипарином необхідно контролювати рівень тромбоцитів. Повідомлялося про поодинокі випадки ГІТ, у тому числі тяжкі, які могли бути пов'язані з артеріальним або венозним тромбозами. Можливість розвитку ГІТ важливо враховувати у таких випадках: при тромбоцитопенії; при значному зменшенні рівня тромбоцитів (на 30% – 50% порівняно з нормальними показниками); при негативній динаміці клінічних проявів тромбозу, щодо якого пацієнт отримує лікування; у разі виникнення тромбозу на фоні лікування флебіту, легеневої емболії, тромбозу артерій нижніх кінцівок, інфаркту міокарда або інсульту; при ДВЗ-синдромі. У таких випадках необхідно негайно організувати постійний моніторинг рівня тромбоцитів. Застосування надропарину слід припинити. Зазначені ефекти мають імуноалергічну природу і зазвичай відзначаються між 5-м та 21-м днем лікування, але можуть виникати і раніше, якщо у пацієнта була гепарин-індукована тромбоцитопенія в анамнезі. Також повідомлялося про окремі випадки розвитку ГІТ після 21 дня лікування. За наявності гепарин-індукованої тромбоцитопенії в анамнезі (на фоні звичайних або низькомолекулярних гепаринів) лікування Фраксипарином може бути призначене за необхідності. Однак у цій ситуації показано суворий клінічний моніторинг і щонайменше щоденний вимір числа тромбоцитів. У разі виникнення тромбоцитопенії застосування Фраксипарину слід негайно припинити. Якщо тромбоцитопенія розвивається на фоні лікування гепаринами (звичайними або низькомолекулярними), слід розглянути можливість призначення антикоагулянтів інших груп. Якщо інші препарати недоступні, а лікування антикоагулянтами необхідно продовжити, можливе застосування іншого низькомолекулярного гепарину. У цьому випадку слід щодня спостерігати за кількістю тромбоцитів у крові та лікування має бути припинено якомога раніше, оскільки ознаки вихідної тромбоцитопенії продовжують спостерігатися після заміни препарату. Контроль агрегації тромбоцитів, заснований на тестах in vitro, має обмежене значення при діагностиці гепарин-індукованої тромбоцитопенії. Слід виявляти обережність при призначенні Фраксипарину в таких ситуаціях, оскільки вони можуть бути пов'язані з підвищеним ризиком кровотечі: печінкова недостатність; тяжка артеріальна гіпертензія; історія виразкової хвороби або інших органічних уражень, що можуть кровоточити; хоріоретинальні судинні захворювання; післяопераційний період після операції на головному мозку, спинному мозку чи очах; літній вік; пацієнти із масою тіла менше 40 кг. Лабораторний моніторинг Контроль рівня тромбоцитів у пацієнтів, які отримують НМГ та мають фактори ризику гепарин-індукованої тромбоцитопенії Для своєчасного виявлення ГІТ під час лікування оптимально проводити моніторинг стану пацієнтів так: Після хірургічного втручання або травми (за останні 3 місяці): при застосуванні надропарину з метою лікування або профілактики необхідний регулярний біологічний моніторинг, оскільки захворюваність на ГІТ у таких пацієнтів становить 0,1% і навіть >1%. Визначення концентрації тромбоцитів слід проводити: до початку лікування НМГ або в перші 24 години після початку лікування; 2 рази на тиждень протягом першого місяця лікування (період максимального ризику); 1 раз на тиждень до закінчення лікування у разі тривалої терапії. За відсутності хірургічного втручання або травми за останні 3 місяці: при застосуванні надропарину з метою лікування або профілактики регулярний біологічний моніторинг необхідний у таких випадках: за наявності в анамнезі терапії НФГ або НМГ за останні 6 місяців - через захворюваність на ГІТ > 0,1% і навіть >1%; за наявності супутніх захворювань - через потенційну небезпеку ГІТ у таких пацієнтів. В інших випадках, через низьку захворюваність на ГІТ ( до початку лікування НМГ або перші 24 год після початку терапії; при появі специфічних клінічних ознак ГІТ (артеріальна або венозна тромбоемболія, хворобливе ураження шкіри у місці ін'єкції, ознаки алергії та гіперчутливості під час терапії). Слід повідомляти пацієнтам про можливість появи подібних клінічних ознак та необхідність звернутися до свого лікаря у разі їх появи. Можливість розвитку ГІТ слід розглянути у разі зниження вмісту тромбоцитів до рівня При легкій нирковій недостатності (кліренс креатиніну ≥ 50 мл/хв) не потрібно знижувати дозу надропарину. Будь-яке значне зниження рівня тромбоцитів (на 30%-50% від вихідного значення) вимагає термінової уваги ще до того, як рівень досягне критичного граничного значення. У разі зниження рівня тромбоцитів необхідно: негайно оцінити динаміку тромбоцитопенії; припинити застосування гепарину, якщо підтверджено зниження рівня тромбоцитів, що продовжується, за відсутності інших очевидних причин тромбоцитопенії; провести профілактику чи лікування тромботичного ускладнення ГІТ. Якщо потрібне подальше лікування антикоагулянтами, слід замінити гепарин антикоагулянтом іншого класу у профілактичній або терапевтичній дозі залежно від ситуації. У разі заміни гепарину на антагоністи вітаміну К (АВК) останні слід призначати лише після нормалізації рівня тромбоцитів, тому що в іншому випадку існує ризик посилення тромботичного ефекту. Заміна гепарину антагоністами вітаміну К Необхідно забезпечити ретельний клінічний та лабораторний моніторинг (протромбіновий час за Квіком та міжнародне нормалізоване відношення) для контролю за дією АВК. Оскільки повна дія антагоністів вітаміну К проявляється через деякий період часу, слід продовжувати введення гепарину в еквівалентній дозі, поки це необхідно для досягнення рівня МНО, допустимого при даному показанні, при двох послідовних вимірах. Особливі групи пацієнтів Пацієнти з нирковою недостатністю Оскільки надропарин в основному виводиться нирками, це призводить до зменшення екскреції надропарину у пацієнтів з нирковою недостатністю. Тому у такої групи пацієнтів є більший ризик кровотечі і потрібна велика обережність при лікуванні. Рішення про зменшення або збереження дози для пацієнта з кліренсом креатиніну від 30 до 50 мл/хв приймається лікарем, який має оцінити індивідуальний ризик кровотечі для пацієнта порівняно з ризиком розвитку тромбоемболії. Пацієнти похилого віку Перед початком лікування Фраксипарин необхідно оцінити функцію нирок. Гіперкаліємія Гепарини можуть пригнічувати секрецію альдостерону, що може призвести до гіперкаліємії, особливо у пацієнтів з підвищеним калієм у крові або у пацієнтів з ризиком підвищення вмісту калію в крові, наприклад, у пацієнтів з цукровим діабетом, хронічною нирковою недостатністю, метаболічним ацидозом або у пацієнтів, які приймають. препарати, які можуть викликати гіперкаліємію (наприклад, інгібітори ангіотензин-перетворюючої дії, нестероїдні протизапальні засоби (НПЗЗ)). Ризик гіперкаліємії підвищується при тривалій терапії, але зазвичай оборотний при відміні. У пацієнтів, які перебувають у групі ризику, слід контролювати рівень калію у крові. Спінальна/епідуральна анестезія/спинномозкова пункція та супутні лікарські препарати Ризик виникнення спинальних/епідуральних гематом після використання надропарину, що призводять до неврологічним розладам, у тому числі тривалим або постійним паралічам, підвищується у пацієнтів із встановленими епідуральними катетерами або супутнім застосуванням інших ліків, які можуть вплинути на гемостаз, такі як НПЗЗ, антиагрегантні антикоагулянти. Ризик також збільшується при проведенні травматичних або повторних епідуральних або спинномозкових пункцій. Тому питання про комбіноване застосування нейроаксіальної блокади та антикоагулянтів має вирішуватися індивідуально після оцінки співвідношення користь/ризик у наступних ситуаціях: у пацієнтів, які вже отримують антикоагулянти, має бути обґрунтовано необхідність спінальної або епідуральної анестезії; у пацієнтів, яким планується елективне хірургічне втручання із застосуванням спинальної або епідуральної анестезії, має бути обґрунтовано необхідність введення антикоагулянтів. Якщо пацієнту проводиться люмбальна пункція або спинальна або епідуральна анестезія, слід дотримуватись інтервалу мінімум 12 годин між введенням Фраксипарину у профілактичних дозах або 24 години у терапевтичних дозах та введенням або видаленням спинального/епідурального катетера або голки. Для пацієнтів з нирковою недостатністю можуть розглядатися тривалі інтервали. Необхідно ретельне спостереження за пацієнтом з метою виявлення ознак та симптомів неврологічних порушень, таких як біль у спині, сенсорні або рухові порушення (оніміння або слабкість нижніх кінцівок), проблеми із сечовим міхуром та/або кишечником. Пацієнтів слід проінструктувати про необхідність інформування лікаря у разі неврологічних симптомів. При виявленні порушень у неврологічному статусі пацієнта потрібна термінова відповідна терапія, включаючи декомпресію спинного мозку. Саліцилати, нестероїдні протизапальні препарати та антиагрегантні засоби При профілактиці або лікуванні венозних тромбоемболій, а також при профілактиці зсідання крові в системі екстракорпорального кровообігу при гемодіалізі не рекомендується спільне призначення Фраксипарину з такими препаратами, як ацетилсаліцилова кислота, інші саліцилати, НПЗЗ та антирегант. це може збільшити ризик розвитку кровотеч. Якщо таких комбінацій не можна уникнути, необхідно проводити ретельне клінічне та біологічне спостереження. У клінічних дослідженнях у пацієнтів з нестабільною стенокардією та інфарктом міокарда без підвищення зубця Q надропарин застосовувався у комбінації з ацетилсаліциловою кислотою у дозах, що не перевищують 325 мг на добу. Некроз шкіри Про шкірні некрози повідомлялося дуже рідко. Цьому передували пурпури або інфільтровані або болючі еритематозні плями з присутністю або відсутністю загальних ознак. У таких випадках лікування має бути негайно припинено. Алергія на латекс Ковпачок голки попередньо заповненого шприца складається з натуральної зневодненої гуми - похідного латексу, що може стати причиною алергічної реакції. Пацієнти з механічними клапанними протезами (включаючи вагітні жінки) Застосування надропарину кальцію для профілактики тромбоутворення у пацієнтів з штучними механічними клапанами серця вивчено недостатньо. У зв'язку з неможливістю оцінити ефективність та безпеку застосування препарату Фраксипарин для зниження ризику тромбозів та емболій у пацієнтів з механічними штучними клапанами серця не рекомендується. Вагітні жінки з механічними штучними клапанами серця мають високий ризик розвитку тромбозів та емболій. Наявний обмежений досвід застосування надропарину кальцію не дозволяє рекомендувати застосування препарату Фраксипарин для зниження ризику тромбозів та емболій у вагітних жінок із механічними штучними клапанами серця. Низька маса тіла Перед початком лікування Фраксипарин необхідно оцінити функцію нирок. Пацієнти з ожирінням У пацієнтів з ожирінням є підвищений ризик виникнення тромбоемболічних ускладнень. Безпека та ефективність профілактичних доз Фраксипарину не повністю оцінені у пацієнтів з ожирінням (індекс маси тіла > 30 кг/м2) та рекомендації щодо добору дози відсутні. Тому рекомендується спостереження даних пацієнтів щодо появи ознак і симптомів тромбоемболічних ускладнень. Діти В даний час недостатньо клінічних даних щодо ефективності та безпеки застосування Фраксипарину у пацієнтів до 18 років, у зв'язку з чим призначення Фраксипарину дітям та підліткам не рекомендується. Вплив на здатність до керування автотранспортом та управління механізмами Немає даних про вплив Фраксипарину на здатність керувати транспортними засобами та механізмами.Умови відпустки з аптекЗа рецептомВідео на цю тему
4 781,00 грн
196,00 грн
Дозування: 11400 ме Фасування: N10 Форма випуску: р-р д/ін'єкцій Упаковка: шприц Виробник: Аспен Фарма Трейдінг Лімітед Завод-виробник: Glaxo Wellcome Production(Велика Британія) Действующее вещество: Надропарин кальция. . .
2 740,00 грн
155,00 грн
Склад, форма випуску та упаковкаПігулки - 1 таб. Діюча речовина: тадалафіл – 20,000 мг; Допоміжні речовини: лактози моногідрат (цукор молочний) – 273,300 мг; целюлоза мікрокристалічна – 57,000 мг; кроскармелоза натрію – 24,000 мг; гіпоролоза – 2,660 мг; натрію лаурилсульфат – 1,140 мг; магнію стеарат – 1,900 мг; Склад оболонки: гіпромелоза – 5,800 мг; макрогол-4000 – 1,700 мг; титану діоксид – 2,300 мг; барвник заліза оксид жовтий – 0,200 мг. Пігулки, покриті плівковою оболонкою 20 мг. По 1, 2, 10, 14 або 28 таблеток у контурне осередкове пакування з плівки полівінілхлоридної та фольги алюмінієвої друкованої лакованої. По 8, 10, 14, 20, 28, 30, 40, 50 або 100 таблеток у банки з поліетилентерефталату для лікарських засобів або поліпропіленові для лікарських засобів, закупорені кришками з поліетилену високого тиску з контролем першого розкриття, або кришками поліпропілен -повернути" або кришками з поліетилену низького тиску з контролем першого розтину. Одну банку або 1, 2, 3, 4, 5 або 10 контурних осередкових упаковок разом з інструкцією із застосування поміщають у картонну упаковку (пачку). Допускається комплектація по 2 або 3 картонні упаковки (пачки) до групового упаковки (транспортної тари) з картону для споживчої тари.Опис лікарської формиКруглі, двоопуклі таблетки з ризиком, покриті плівковою оболонкою від світло-жовтого до коричнево-жовтого кольору. На поперечному розрізі видно два шари: ядро білого або майже білого кольору та плівкова оболонка.Фармакотерапевтична групаЕректильна дисфункція Засіб лікування - ФДЕ5-інгібітор.ФармакокінетикаВсмоктування Після прийому внутрішньо тадалафіл швидко всмоктується. Середня максимальна концентрація (Сmах) у плазмі крові досягається в середньому через 2 години після прийому внутрішньо. Швидкість і ступінь всмоктування тадалафілу не залежать від їди, тому препарат можна застосовувати незалежно від їди. Час прийому (вранці або ввечері) не має клінічно значущого ефекту на швидкість та ступінь всмоктування. Фармакокінетика тадалафілу у здорових добровольців лінійна щодо часу та дози. У діапазоні доз від 2,5 до 20 мг площа під кривою "концентрація-час" (AUC) збільшується пропорційно дозі. Рівноважні концентрації в плазмі досягаються протягом 5 днів при прийомі препарату 1 раз на добу. Фармакокінетика тадалафілу у пацієнтів з порушенням ерекції аналогічна фармакокінетиці препарату у пацієнтів без порушення ерекції. Розподіл Середній обсяг розподілу становить близько 63 л, що свідчить про те, що тадалафіл розподіляється у тканинах організму. У терапевтичних концентраціях 94% тадалафілу пов'язують із білками плазми крові. Зв'язування з білками плазми не змінюється при порушеній функції нирок. У здорових добровольців менше 0,0005% введеної дози виявлено у спермі. Метаболізм Тадалафіл переважно метаболізується за участю ізоферменту CYP3A4 цитохрому Р450. Основним циркулюючим метаболітом є метилкатехолглюкуронід. Цей метаболіт принаймні у 13000 разів менш активний щодо ФДЕ-5, ніж тадалафіл. Отже, концентрація цього метаболіту не є клінічно значущою. Виведення У здорових добровольців середній кліренс тадалафілу при прийомі внутрішньо становить 2,5 л/год, а середній період напіввиведення (Т1/2) – 17,5 год. Тадалафіл виводиться переважно у вигляді неактивних метаболітів, переважно кишечником (близько 61 % дози). і, меншою мірою, нирками (близько 36% дози). Літні пацієнти Здорові літні добровольці (65 років і старше) мали нижчий кліренс тадалафілу при прийомі внутрішньо, що виражалося у збільшенні AUC на 25% зі здоровими добровольцями у віці від 19 до 45 років. Ця відмінність не є клінічно значущою і не потребує добору дози. Пацієнти з нирковою недостатністю У клінічних дослідженнях показано, що при прийомі одиничної дози тадалафілу (5-20 мг) AUC збільшується приблизно у 2 рази у пацієнтів з легкою (кліренс креатиніну (КК) 51-80 мл/хв), середньою (КК 31-50 мл/хв.) ) та термінальною нирковою недостатністю (проведення діалізу). У пацієнтів на гемодіалізі Сmах тадалафілу на 41% вище, ніж у здорових добровольців. Тадалафіл практично не виводиться при гемодіалізі. Пацієнти з печінковою недостатністю Фармакокінетика тадалафілу у пацієнтів з легкою та середньотяжкою печінковою недостатністю (класи А та В за класифікацією Чайлд-П'ю) можна порівняти з такою у здорових добровольців. Щодо пацієнтів з тяжкою печінковою недостатністю (клас С за класифікацією Чайлд-П'ю) дані обмежені, тому перед застосуванням препарату необхідно проводити оцінку співвідношення користь/ризик. Пацієнти з цукровим діабетом У пацієнтів із цукровим діабетом на фоні застосування тадалафілу AUC менше приблизно на 19%, ніж у здорових добровольців. Ця відмінність не потребує підбору дози.ФармакодинамікаТадалафіл є оборотним селективним інгібітором специфічної фосфодіестерази 5 типу (ФДЕ-5) циклічного гуанозинмонофосфату (цГМФ). Коли сексуальне збудження викликає місцеве вивільнення оксиду азоту, пригнічення ФДЕ-5 тадалафілом веде до підвищення концентрації цГМФ в печеристому тілі статевого члена. Наслідком цього є розслаблення гладких м'язів артерій та приплив крові до тканин статевого члена, що викликає ерекцію. Дослідження in vitro показали, що тадалафіл є селективним інгібітором ФДЕ-5. ФДЕ-5 є ферментом, представленим у гладкій мускулатурі печеристого тіла, судин та внутрішніх органів, у скелетних м'язах, тромбоцитах, нирках, легенях та мозочку. Дія тадалафілу на ФДЕ-5 є більш активною, ніж на інші фосфодіестерази. Тадалафіл є в 10 000 разів більш потужним щодо ФДЕ-5, ніж щодо інших типів фосфодіестерази (ФДЕ-1, ФДЕ-2, ФДЕ-4 та ФДЕ-7), які локалізуються в серці, головному мозку, кровоносних судинах, печінці. , лейкоцитах та інших органах. Тадалафіл у 10 000 разів активніше блокує ФДЕ-5, ніж ФДЕ-3 – фермент, який виявляється у серці та кровоносних судинах. Ця селективність щодо ФДЕ-5 у порівнянні з ФДЕ-3 має важливе значення, оскільки ФДЕ-3 є ферментом,беруть участь у скороченні серцевого м'яза. Крім того, тадалафіл приблизно в 700 разів активніше щодо ФДЕ-5, ніж ФДЕ-6, виявленої в сітківці і відповідає за фотопередачу. Дія тадалафілу щодо ФДЕ-5 у 9000 разів більш виражена, ніж його вплив на ФДЕ-8, ФДЕ-9 та ФДЕ-10, та у 14 разів більш виражене, ніж на ФДЕ-11. Розподіл у тканинах та фізіологічні ефекти інгібування ФДЕ-8 – ФДЕ-11 дотепер не з'ясовані.Розподіл у тканинах та фізіологічні ефекти інгібування ФДЕ-8 – ФДЕ-11 дотепер не з'ясовані.Розподіл у тканинах та фізіологічні ефекти інгібування ФДЕ-8 – ФДЕ-11 дотепер не з'ясовані. Тадалафіл у здорових добровольців не викликає достовірної зміни систолічного та діастолічного артеріального тиску в порівнянні з плацебо у положенні лежачи (середнє максимальне зниження становить 1,6 та 0,8 мм рт. ст. відповідно) та у положенні стоячи (середнє максимальне зниження становить 0, 2 і 4,6 мм рт.ст., відповідно). Тадалафіл не викликає достовірної зміни частоти серцевих скорочень. Тадалафіл не викликає змін розпізнавання кольорів (блакитний/зелений), що пояснюється його низькою спорідненістю з ФДЕ-6. Крім того, не спостерігається вплив тадалафілу на гостроту зору, електроретинограму, внутрішньоочний тиск та розмір зіниці. З метою оцінки впливу щоденного прийому тадалафілу на сперматогенез було проведено декілька досліджень. У жодному з досліджень не спостерігалося небажаного впливу на морфологію сперматозоїдів та їхню рухливість. В одному з досліджень було виявлено зниження середньої концентрації сперматозоїдів у порівнянні із плацебо. Зниження концентрації сперматозоїдів пов'язано з вищою частотою еякуляції. Крім того, при порівнянні тадалафілу з плацебо не спостерігалося небажаного впливу на середню концентрацію статевих гормонів (тестостерону, лютеїнізуючого гормону та фолікулостимулюючого гормону). Еректильна дисфункція (ЕД) У проведених дослідженнях тадалафіл показав статистично значуще покращення еректильної функції та можливості проведення повноцінного статевого акту. Тадалафіл не має ефекту у відсутності сексуального збудження. Ефективність та безпека тадалафілу вивчалась у ході клінічних досліджень. Було відмічено покращення ерекції у пацієнтів з ЕД усіх ступенів тяжкості при прийомі 5 мг тадалафілу 1 раз на добу протягом 36 годин після прийому, а також підтримання ерекції протягом 16 хв після прийому порівняно з плацебо. У дослідженнях первинної ефективності застосування 5 мг тадалафілу 57% та 67% спроб статевого акту були успішними порівняно з 31% та 37% при прийомі плацебо. У дослідженнях пацієнтів із вторинною ЕД на тлі цукрового діабету 41% спроб статевого акту були успішними порівняно з 28% при прийомі плацебо. Доброякісна гіперплазія передміхурової залози (ДГПЗ) У пацієнтів з ДГПЗ тадалафіл, інгібуючи ФДЕ-5, призводить до підвищення концентрації цГМФ не тільки в печеристому тілі статевого члена, а й у гладкій мускулатурі передміхурової залози, сечового міхура та судинах, що їх кровопостачають. Це своє чергу збільшує перфузію крові у цих органах як наслідок, зменшує вираженість симптомів ДГПЖ. Розслаблення гладкої мускулатури передміхурової залози та сечового міхура та інгібування аферентної іннервації сечового міхура можуть додатково посилювати судинні ефекти. У ході клінічних досліджень було показано зменшення симптомів ДГПЗ протягом 1 тижня після прийому 5 мг тадалафілу проти плацебо. У дослідженнях, що включають пацієнтів з ЕД та симптомами ДГПЗ, при застосуванні 5 мг тадалафілу 71,9% спроб статевого акту були успішними порівняно з 48,3% при прийомі плацебо, та спостерігалося значне покращення еректильної функції та зменшення симптомів з боку передміхурової залози.Показання до застосуванняЕректильна дисфункція; симптоми з боку нижніх сечовивідних шляхів у пацієнтів із ДГПЗ (для дозування 5 мг); еректильна дисфункція у пацієнтів із симптомами з боку сечовивідних шляхів у пацієнтів із ДГПЗ (для дозування 5 мг).Протипоказання до застосуванняПідвищена чутливість до тадалафілу або будь-якої речовини, що входить до складу препарату; прийом препаратів, що містять будь-які органічні нітрати; дитячий вік до 18 років; наявність протипоказань до сексуальної активності у пацієнтів із захворюваннями серцево-судинної системи: інфаркт міокарда протягом останніх 90 днів, нестабільна стенокардія, виникнення нападу стенокардії під час статевого акту, хронічна серцева недостатність II-IV класів за класифікацією NYHA, неконтрольована аритмія АТ втрата зору внаслідок неартеріальної передньої ішемічної нейропатії зорового нерва (незалежно від зв'язку з прийомом інгібіторів ФДЕ-5); одночасний прийом доксазозину, інших лікарських засобів для лікування еректильної дисфункції, стимуляторів гуанілатциклази (ріоцигуат); застосування у пацієнтів з тяжкою нирковою недостатністю (КК дефіцит лактази, непереносимість лактози, глюкозо-галактозна мальабсорбція. З обережністю: Тяжка печінкова недостатність (клас С за класифікацією Чайлд-П'ю) через недостатню кількість даних щодо ефективності/безпеки препарату; одночасне застосування селективних альфа-адреноблокаторів, сильних інгібіторів ізоферменту CYP3A4 (ритонавір, саквінавір, кетоконазол, ітраконазол, еритроміцин), інгібіторів 5-альфа-редуктази; схильність до приапізму (при серповидно-клітинній анемії, множинні мієломи або лейкозі), анатомічна деформація статевого члена (кутове викривлення, кавернозний фіброз або хвороба Пейроні).Вагітність та лактаціяПрепарат не призначений для застосування у жінок.Побічна діяЗа даними Всесвітньої Організації Охорони Здоров'я (ВООЗ), небажані реакції класифіковані відповідно до їх частоти розвитку наступним чином: дуже часто (≥1/10), часто (≥1/100, Порушення з боку імунної системи: нечасто – реакції гіперчутливості; рідко – ангіоневротичний отек3. Порушення з боку нервової системи: часто – головний біль; нечасто – запаморочення; рідко – інсульт1 (в т.ч. геморагічний), транзиторні ішемічні атаки1, непритомність, мігрень3, епілептичний напад, транзиторна амнезія. Порушення з боку органу зору: нечасто – нечіткість зорового сприйняття, больові відчуття у очному яблуку; рідко - порушення полів зору, припухлість повік, ін'єкція судин склери, неартеріальна передня ішемічна оптична нейропатія3, оклюзія судин сітківки3. Порушення з боку органу слуху та лабіринтні порушення: нечасто - шум/дзвін у вухах; рідко – раптова втрата слуха2. Порушення з боку серця1: нечасто – відчуття серцебиття, тахікардія; рідко – інфаркт міокарда, шлуночкові порушення ритму3, нестабільна стенокардія3. Порушення з боку судин: часто – "припливи" крові; нечасто – зниження артеріального тиску (АТ) (у пацієнтів, які приймають гіпотензивні засоби), підвищення АТ. Порушення з боку дихальної системи, органів грудної клітки та середостіння: часто – закладеність носа; нечасто – задишка, носова кровотеча. Порушення з боку шлунково-кишкового тракту: часто – диспепсія, гастроезофагеальний рефлюкс; нечасто – біль у животі. Порушення з боку шкіри та підшкірної клітковини: нечасто – висип, гіпергідроз (підвищена пітливість); рідко – кропив'янка, синдром Стівенса-Джонсона3, ексфоліативний дерматит3. Порушення з боку скелетно-м'язової та сполучної тканини: часто – біль у спині, біль у кінцівках, міалгія. Порушення з боку нирок та сечовивідних шляхів: часто – гематурія. Порушення з боку статевих органів та молочної залози: нечасто – кровотеча зі статевого члена, гемоспермія; рідко - тривала ерекція, пріапізм3. Загальні розлади та порушення у місці введення: нечасто – біль у грудній клітці1; рідко – набряк особи3, раптова серцева смерть1,3. 1 Спостерігалися у пацієнтів, які раніше мали серцево-судинні фактори ризику. Однак неможливо точно визначити, пов'язані ці явища безпосередньо з цими факторами ризику, з тадалафілом, із сексуальним збудженням або з комбінацією цих чи інших факторів. 2 Про раптову втрату слуху повідомлялося в невеликій кількості випадків під час постмаркетингових та клінічних досліджень при застосуванні всіх ФДЕ-5 інгібіторів, включаючи тадалафіл. 3 Побічні реакції, виявлені в ході постмаркетингових досліджень, які не спостерігалися в ході клінічних плацебо-контрольованих досліджень.Взаємодія з лікарськими засобамиБезпека та ефективність комбінації тадалафілу з іншими видами лікування порушень ерекції не вивчалися, тому застосування таких комбінацій не рекомендується. Вплив інших препаратів на тадалафіл Тадалафіл здебільшого метаболізується за участю ізоферменту CYP3A4. Селективний інгібітор ізоферменту CYP3A4 кетоконазол у дозі 400 мг/добу збільшує AUC тадалафілу (20 мг) у 4 рази та Сmах на 22%, а кетоконазол у дозі 200 мг/добу збільшує AUC тадалафілу (10 мг) у 2 рази щодо AUC та Сmах тільки для тадалафілу. Ритонавір (200 мг 2 рази на добу), інгібітор ізоферментів CYP3A4, CYP2C9, CYP2C19 та CYP2D6, збільшує AUC тадалафілу (20 мг) в 2 рази без зміни Сmах. Незважаючи на те, що специфічні взаємодії не вивчалися, можна припустити, що інші інгібітори ВІЛ-протеази, наприклад, саквінавір, та інгібітори ізоферменту CYP3A4, такі як еритроміцин, кларитроміцин та ітраконазол, а також грейпфрутовий сік, обережністю (через підвищення ризику розвитку небажаних реакцій). Селективний індуктор ізоферменту CYP3A4 рифампіцин (600 мг на добу) знижує AUC тадалафілу (10 мг) на 88% та Сmах на 46% щодо цих величин для тадалафілу окремо. Можна припускати, що одночасне застосування інших індукторів ізоферменту CYP3A4 (таких як фенобарбітал, фенітої та карбамазепін) також знижує плазмові концентрації тадалафілу. Одночасний прийом антациду (магнію гідроксид/алюмінію гідроксид) та тадалафілу знижує швидкість всмоктування тадалафілу без зміни його AUC. Вплив тадалафілу на інші препарати Відомо, що тадалафіл посилює гіпотензивну дію нітратів. Це відбувається в результаті адитивної дії нітратів та тадалафілу на метаболізм оксиду азоту II (NО) та цГМФ. Тому застосування тадалафілу на фоні нітратів протипоказано. Одночасне застосування тадалафілу із доксазозином протипоказане. При одночасному застосуванні тадалафілу (5 мг на добу) здоровими добрбвейбцями та альфа-адреноблокаторами доксазозину (4-8 мг на добу) спостерігалося посилення гіпотензивної дії доксазозину. Деякі пацієнти відчували симптоми, пов'язані зі зниженням АТ, включаючи непритомність, протягом 12 год. В обмеженій кількості досліджень не спостерігалося значного зниження артеріального тиску при застосуванні тадалафілу здоровими добровольцями, які приймали селективні альфа-адреноблокатори (тамсулозин. алфузозин). Незважаючи на це такі комбінації слід застосовувати з обережністю, починати з мінімальної дози альфа-адреноблокатора з поступовим її підвищенням. У доклінічних та клінічних дослідженнях було показано значне посилення гіпотензивного ефекту при одночасному застосуванні інгібіторів ФДЕ-5 та ріоцигуату (стимулятор гуанілатциклази), тому прийом такої комбінації препаратів протипоказаний. Тадалафіл має системні судинорозширюючі властивості і може посилювати дію гіпотензивних засобів, спрямоване на зниження артеріального тиску. Вивчалися препарати наступних груп гіпотензивних препаратів: блокатори "повільних" кальцієвих каналів (амлодипін), інгібітори ангіотензинперетворюючого ферменту (еналаприл), бета-адреноблокатори (метопролол), тіазидні діуретики (бендофлуазид), блокатори рецепторів. Додатково у пацієнтів з погано контрольованою артеріальною гіпертензією, які приймали кілька гіпотензивних засобів, спостерігалося дещо більше зниження артеріального тиску. Переважна більшість пацієнтів це зниження був пов'язані з розвитком гипотензивных симптомів. Пацієнтам, які отримують лікування гіпотензивними препаратами та приймають тадалафіл, повинні бути надані відповідні клінічні рекомендації. При одночасному застосуванні тадалафілу та фінастериду (інгібітор 5-альфа-редуктази) не спостерігалося зміни профілю небажаних реакцій порівняно із застосуванням комбінації плацебо + фінастерид, проте при прийомі цих препаратів слід бути обережним через недостатню кількість клінічних даних. Дослідження підтвердили, що тадалафіл не інгібує та не індукує ізоферменти системи цитохрому Р450 CYP1A2, CYP3A4, CYP2C9, CYP2C19, CYP2D6, CYP2E1. Тадалафіл не має клінічно значущого ефекту на фармакокінетику або фармакодинаміку теофіліну (субстрат CYP1A2), не впливає на AUC S-варфарину або R-варфарину (субстрати CYP2C9) і не змінює протромбіновий час при одночасному прийомі з варфарином. Тадалафіл (10 мг, 20 мг) не збільшує тривалість кровотечі, що викликається ацетилсаліцилової кислотою (АСК). Біодоступність етинілестрадіолу та тербуталіну при прийомі внутрішньо разом з тадалафілом підвищується, проте клінічне значення такої взаємодії не визначено. Тадалафіл не впливає на концентрацію алкоголю, так само як і алкоголь не впливає на концентрацію тадалафілу. При високих дозах алкоголю (0,7 г/кг) прийом тадалафілу не викликав статистично значущого зниження середньої АТ. У деяких пацієнтів спостерігалися постуральне запаморочення та ортостатична гіпотензія. При прийомі тадалафілу у поєднанні з нижчими дозами алкоголю (0,6 г/кг) зниження АТ не спостерігалося, а запаморочення виникало з такою самою частотою, що при прийомі алкоголю окремо. Вивчення взаємодій між тадалафілом та препаратами для лікування цукрового діабету не проводилося.Спосіб застосування та дозиДля прийому всередину. Застосування препарату при ЕД Для пацієнтів з частою сексуальною активністю (більше двох разів на тиждень) рекомендована частота прийому: щодня, 5 мг (1 таблетка) 1 раз на добу, одночасно, незалежно від їди. Доза повинна періодично контролюватись і переглядатися, за необхідності. Добова доза може бути знижена до 2,5 мг, залежно від індивідуальної чутливості. Для пацієнтів з нечастою сексуальною активністю (рідше двох разів на тиждень) рекомендована частота прийому: 20 мг (1 таблетка або 4 таблетки у дозі 5 мг) безпосередньо перед сексуальною активністю згідно з інструкцією з медичного застосування. Максимальна добова доза становить 20 мг. Застосування препарату при ДГПЗ або ЕД + ДГПЗ Рекомендована доза препарату становить 5 мг (1 таблетка) 1 раз на добу. Препарат слід приймати приблизно в один і той же час дня, незалежно від їди та часу сексуальної активності. Тривалість лікування встановлюється лікарем індивідуально. У пацієнтів з нирковою недостатністю тяжкого ступеня (КК У пацієнтів з нирковою недостатністю легкої (КК 51 -80 мл/хв) та середнього ступеня тяжкості (КК 31-50 мл/хв) або печінковою недостатністю легкого та середнього ступеня тяжкості (класи А та В за класифікацією Чайлд-П'ю), а також у літніх пацієнтів корекція дози не потрібна.ПередозуванняПри призначенні тадалафілу одноразово в дозі до 500 мг здоровим особам і багаторазово в дозі до 100 мг на добу пацієнтам з ЕД небажані реакції були зіставні, як і застосування нижчих доз. У разі передозування слід проводити симптоматичне лікування. При гемодіалізі тадалафілу практично не виводиться.Запобіжні заходи та особливі вказівкиДіагностика ЕД та ДГПЗ повинна включати виявлення основної причини захворювання, відповідне медичне обстеження, визначення тактики лікування та індивідуальну оцінку співвідношення користь/ризик. Сексуальна активність має потенційний ризик для пацієнтів із серцево-судинними захворюваннями, тому лікування ЕД не слід проводити у чоловіків із такими захворюваннями серця, при яких сексуальна активність не рекомендована. Як і інші ФДЕ-5 інгібітори, тадалафіл може чинити системну судиннорозширювальну дію, що може призводити до транзиторного зниження АТ та посилення гіпотензивної дії нітратів, альфа-адреноблокаторів (див. розділ "Взаємодія з іншими лікарськими засобами"). Перед призначенням препарату необхідно ретельно оцінити ймовірність виникнення подібних небажаних реакцій у пацієнтів із серцево-судинними захворюваннями. Пацієнти з передбачуваним діагнозом ДГПЗ повинні пройти обстеження для виключення раку передміхурової залози. Неартеріальна передня ішемічна оптична нейропатія (НАПІОН) є причиною порушення зору, включаючи повну втрату зору. Є рідкісні постмаркетингові повідомлення про випадки розвитку НАПІОН, за часом пов'язані з прийомом інгібіторів ФДЕ-5. В даний час неможливо визначити, чи існує прямий зв'язок між розвитком НАПІОН та прийомом інгібіторів ФДЕ-5 або іншими факторами. Необхідно попередити пацієнтів, що у разі раптової втрати зору слід припинити прийом тадалафілу та звернутися за медичною допомогою. Пацієнти також повинні бути проінформовані, що у людей, які перенесли НАПІОН, підвищений ризик повторного розвитку НАПІОН. Є повідомлення про виникнення приапізму при застосуванні інгібіторів ФДЕ-5, включаючи тадалафіл. Пацієнти повинні бути проінформовані про необхідність негайного звернення за медичною допомогою у разі виникнення ерекції, що триває 4 години та більше. Несвоєчасне лікування приапізму веде до пошкодження тканин статевого члена, внаслідок чого може настати необоротна імпотенція. Ефективність препарату у пацієнтів, які перенесли хірургічну операцію на органах малого тазу або радикальну нервозберігаючу простатектомію, невідома. Вплив на здатність до керування автотранспортом та управління механізмами Незважаючи на те, що частота виникнення запаморочення на тлі плацебо і тадалафілу однакова, в період лікування необхідно дотримуватися обережності при керуванні автотранспортом та заняттями іншими потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій. Пацієнти повинні бути обізнані про можливий розвиток сонливості при прийомі препарату, особливо на початку терапії або у поєднанні з алкоголем.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Діюча речовина: тадалафіл – 20,000 мг; Допоміжні речовини: лактози моногідрат (цукор молочний) – 273,300 мг; целюлоза мікрокристалічна – 57,000 мг; кроскармелоза натрію – 24,000 мг; гіпоролоза – 2,660 мг; натрію лаурилсульфат – 1,140 мг; магнію стеарат – 1,900 мг; Склад оболонки: гіпромелоза – 5,800 мг; макрогол-4000 – 1,700 мг; титану діоксид – 2,300 мг; барвник заліза оксид жовтий – 0,200 мг. Пігулки, покриті плівковою оболонкою 20 мг. По 1, 2, 10, 14 або 28 таблеток у контурне осередкове пакування з плівки полівінілхлоридної та фольги алюмінієвої друкованої лакованої. По 8, 10, 14, 20, 28, 30, 40, 50 або 100 таблеток у банки з поліетилентерефталату для лікарських засобів або поліпропіленові для лікарських засобів, закупорені кришками з поліетилену високого тиску з контролем першого розкриття, або кришками поліпропілен -повернути" або кришками з поліетилену низького тиску з контролем першого розтину. Одну банку або 1, 2, 3, 4, 5 або 10 контурних осередкових упаковок разом з інструкцією із застосування поміщають у картонну упаковку (пачку). Допускається комплектація по 2 або 3 картонні упаковки (пачки) до групового упаковки (транспортної тари) з картону для споживчої тари.Опис лікарської формиКруглі, двоопуклі таблетки з ризиком, покриті плівковою оболонкою від світло-жовтого до коричнево-жовтого кольору. На поперечному розрізі видно два шари: ядро білого або майже білого кольору та плівкова оболонка.Фармакотерапевтична групаЕректильна дисфункція Засіб лікування - ФДЕ5-інгібітор.ФармакокінетикаВсмоктування Після прийому внутрішньо тадалафіл швидко всмоктується. Середня максимальна концентрація (Сmах) у плазмі крові досягається в середньому через 2 години після прийому внутрішньо. Швидкість і ступінь всмоктування тадалафілу не залежать від їди, тому препарат можна застосовувати незалежно від їди. Час прийому (вранці або ввечері) не має клінічно значущого ефекту на швидкість та ступінь всмоктування. Фармакокінетика тадалафілу у здорових добровольців лінійна щодо часу та дози. У діапазоні доз від 2,5 до 20 мг площа під кривою "концентрація-час" (AUC) збільшується пропорційно дозі. Рівноважні концентрації в плазмі досягаються протягом 5 днів при прийомі препарату 1 раз на добу. Фармакокінетика тадалафілу у пацієнтів з порушенням ерекції аналогічна фармакокінетиці препарату у пацієнтів без порушення ерекції. Розподіл Середній обсяг розподілу становить близько 63 л, що свідчить про те, що тадалафіл розподіляється у тканинах організму. У терапевтичних концентраціях 94% тадалафілу пов'язують із білками плазми крові. Зв'язування з білками плазми не змінюється при порушеній функції нирок. У здорових добровольців менше 0,0005% введеної дози виявлено у спермі. Метаболізм Тадалафіл переважно метаболізується за участю ізоферменту CYP3A4 цитохрому Р450. Основним циркулюючим метаболітом є метилкатехолглюкуронід. Цей метаболіт принаймні у 13000 разів менш активний щодо ФДЕ-5, ніж тадалафіл. Отже, концентрація цього метаболіту не є клінічно значущою. Виведення У здорових добровольців середній кліренс тадалафілу при прийомі внутрішньо становить 2,5 л/год, а середній період напіввиведення (Т1/2) – 17,5 год. Тадалафіл виводиться переважно у вигляді неактивних метаболітів, переважно кишечником (близько 61 % дози). і, меншою мірою, нирками (близько 36% дози). Літні пацієнти Здорові літні добровольці (65 років і старше) мали нижчий кліренс тадалафілу при прийомі внутрішньо, що виражалося у збільшенні AUC на 25% зі здоровими добровольцями у віці від 19 до 45 років. Ця відмінність не є клінічно значущою і не потребує добору дози. Пацієнти з нирковою недостатністю У клінічних дослідженнях показано, що при прийомі одиничної дози тадалафілу (5-20 мг) AUC збільшується приблизно у 2 рази у пацієнтів з легкою (кліренс креатиніну (КК) 51-80 мл/хв), середньою (КК 31-50 мл/хв.) ) та термінальною нирковою недостатністю (проведення діалізу). У пацієнтів на гемодіалізі Сmах тадалафілу на 41% вище, ніж у здорових добровольців. Тадалафіл практично не виводиться при гемодіалізі. Пацієнти з печінковою недостатністю Фармакокінетика тадалафілу у пацієнтів з легкою та середньотяжкою печінковою недостатністю (класи А та В за класифікацією Чайлд-П'ю) можна порівняти з такою у здорових добровольців. Щодо пацієнтів з тяжкою печінковою недостатністю (клас С за класифікацією Чайлд-П'ю) дані обмежені, тому перед застосуванням препарату необхідно проводити оцінку співвідношення користь/ризик. Пацієнти з цукровим діабетом У пацієнтів із цукровим діабетом на фоні застосування тадалафілу AUC менше приблизно на 19%, ніж у здорових добровольців. Ця відмінність не потребує підбору дози.ФармакодинамікаТадалафіл є оборотним селективним інгібітором специфічної фосфодіестерази 5 типу (ФДЕ-5) циклічного гуанозинмонофосфату (цГМФ). Коли сексуальне збудження викликає місцеве вивільнення оксиду азоту, пригнічення ФДЕ-5 тадалафілом веде до підвищення концентрації цГМФ в печеристому тілі статевого члена. Наслідком цього є розслаблення гладких м'язів артерій та приплив крові до тканин статевого члена, що викликає ерекцію. Дослідження in vitro показали, що тадалафіл є селективним інгібітором ФДЕ-5. ФДЕ-5 є ферментом, представленим у гладкій мускулатурі печеристого тіла, судин та внутрішніх органів, у скелетних м'язах, тромбоцитах, нирках, легенях та мозочку. Дія тадалафілу на ФДЕ-5 є більш активною, ніж на інші фосфодіестерази. Тадалафіл є в 10 000 разів більш потужним щодо ФДЕ-5, ніж щодо інших типів фосфодіестерази (ФДЕ-1, ФДЕ-2, ФДЕ-4 та ФДЕ-7), які локалізуються в серці, головному мозку, кровоносних судинах, печінці. , лейкоцитах та інших органах. Тадалафіл у 10 000 разів активніше блокує ФДЕ-5, ніж ФДЕ-3 – фермент, який виявляється у серці та кровоносних судинах. Ця селективність щодо ФДЕ-5 у порівнянні з ФДЕ-3 має важливе значення, оскільки ФДЕ-3 є ферментом,беруть участь у скороченні серцевого м'яза. Крім того, тадалафіл приблизно в 700 разів активніше щодо ФДЕ-5, ніж ФДЕ-6, виявленої в сітківці і відповідає за фотопередачу. Дія тадалафілу щодо ФДЕ-5 у 9000 разів більш виражена, ніж його вплив на ФДЕ-8, ФДЕ-9 та ФДЕ-10, та у 14 разів більш виражене, ніж на ФДЕ-11. Розподіл у тканинах та фізіологічні ефекти інгібування ФДЕ-8 – ФДЕ-11 дотепер не з'ясовані.Розподіл у тканинах та фізіологічні ефекти інгібування ФДЕ-8 – ФДЕ-11 дотепер не з'ясовані.Розподіл у тканинах та фізіологічні ефекти інгібування ФДЕ-8 – ФДЕ-11 дотепер не з'ясовані. Тадалафіл у здорових добровольців не викликає достовірної зміни систолічного та діастолічного артеріального тиску в порівнянні з плацебо у положенні лежачи (середнє максимальне зниження становить 1,6 та 0,8 мм рт. ст. відповідно) та у положенні стоячи (середнє максимальне зниження становить 0, 2 і 4,6 мм рт.ст., відповідно). Тадалафіл не викликає достовірної зміни частоти серцевих скорочень. Тадалафіл не викликає змін розпізнавання кольорів (блакитний/зелений), що пояснюється його низькою спорідненістю з ФДЕ-6. Крім того, не спостерігається вплив тадалафілу на гостроту зору, електроретинограму, внутрішньоочний тиск та розмір зіниці. З метою оцінки впливу щоденного прийому тадалафілу на сперматогенез було проведено декілька досліджень. У жодному з досліджень не спостерігалося небажаного впливу на морфологію сперматозоїдів та їхню рухливість. В одному з досліджень було виявлено зниження середньої концентрації сперматозоїдів у порівнянні із плацебо. Зниження концентрації сперматозоїдів пов'язано з вищою частотою еякуляції. Крім того, при порівнянні тадалафілу з плацебо не спостерігалося небажаного впливу на середню концентрацію статевих гормонів (тестостерону, лютеїнізуючого гормону та фолікулостимулюючого гормону). Еректильна дисфункція (ЕД) У проведених дослідженнях тадалафіл показав статистично значуще покращення еректильної функції та можливості проведення повноцінного статевого акту. Тадалафіл не має ефекту у відсутності сексуального збудження. Ефективність та безпека тадалафілу вивчалась у ході клінічних досліджень. Було відмічено покращення ерекції у пацієнтів з ЕД усіх ступенів тяжкості при прийомі 5 мг тадалафілу 1 раз на добу протягом 36 годин після прийому, а також підтримання ерекції протягом 16 хв після прийому порівняно з плацебо. У дослідженнях первинної ефективності застосування 5 мг тадалафілу 57% та 67% спроб статевого акту були успішними порівняно з 31% та 37% при прийомі плацебо. У дослідженнях пацієнтів із вторинною ЕД на тлі цукрового діабету 41% спроб статевого акту були успішними порівняно з 28% при прийомі плацебо. Доброякісна гіперплазія передміхурової залози (ДГПЗ) У пацієнтів з ДГПЗ тадалафіл, інгібуючи ФДЕ-5, призводить до підвищення концентрації цГМФ не тільки в печеристому тілі статевого члена, а й у гладкій мускулатурі передміхурової залози, сечового міхура та судинах, що їх кровопостачають. Це своє чергу збільшує перфузію крові у цих органах як наслідок, зменшує вираженість симптомів ДГПЖ. Розслаблення гладкої мускулатури передміхурової залози та сечового міхура та інгібування аферентної іннервації сечового міхура можуть додатково посилювати судинні ефекти. У ході клінічних досліджень було показано зменшення симптомів ДГПЗ протягом 1 тижня після прийому 5 мг тадалафілу проти плацебо. У дослідженнях, що включають пацієнтів з ЕД та симптомами ДГПЗ, при застосуванні 5 мг тадалафілу 71,9% спроб статевого акту були успішними порівняно з 48,3% при прийомі плацебо, та спостерігалося значне покращення еректильної функції та зменшення симптомів з боку передміхурової залози.Показання до застосуванняЕректильна дисфункція; симптоми з боку нижніх сечовивідних шляхів у пацієнтів із ДГПЗ (для дозування 5 мг); еректильна дисфункція у пацієнтів із симптомами з боку сечовивідних шляхів у пацієнтів із ДГПЗ (для дозування 5 мг).Протипоказання до застосуванняПідвищена чутливість до тадалафілу або будь-якої речовини, що входить до складу препарату; прийом препаратів, що містять будь-які органічні нітрати; дитячий вік до 18 років; наявність протипоказань до сексуальної активності у пацієнтів із захворюваннями серцево-судинної системи: інфаркт міокарда протягом останніх 90 днів, нестабільна стенокардія, виникнення нападу стенокардії під час статевого акту, хронічна серцева недостатність II-IV класів за класифікацією NYHA, неконтрольована аритмія АТ втрата зору внаслідок неартеріальної передньої ішемічної нейропатії зорового нерва (незалежно від зв'язку з прийомом інгібіторів ФДЕ-5); одночасний прийом доксазозину, інших лікарських засобів для лікування еректильної дисфункції, стимуляторів гуанілатциклази (ріоцигуат); застосування у пацієнтів з тяжкою нирковою недостатністю (КК дефіцит лактази, непереносимість лактози, глюкозо-галактозна мальабсорбція. З обережністю: Тяжка печінкова недостатність (клас С за класифікацією Чайлд-П'ю) через недостатню кількість даних щодо ефективності/безпеки препарату; одночасне застосування селективних альфа-адреноблокаторів, сильних інгібіторів ізоферменту CYP3A4 (ритонавір, саквінавір, кетоконазол, ітраконазол, еритроміцин), інгібіторів 5-альфа-редуктази; схильність до приапізму (при серповидно-клітинній анемії, множинні мієломи або лейкозі), анатомічна деформація статевого члена (кутове викривлення, кавернозний фіброз або хвороба Пейроні).Вагітність та лактаціяПрепарат не призначений для застосування у жінок.Побічна діяЗа даними Всесвітньої Організації Охорони Здоров'я (ВООЗ), небажані реакції класифіковані відповідно до їх частоти розвитку наступним чином: дуже часто (≥1/10), часто (≥1/100, Порушення з боку імунної системи: нечасто – реакції гіперчутливості; рідко – ангіоневротичний отек3. Порушення з боку нервової системи: часто – головний біль; нечасто – запаморочення; рідко – інсульт1 (в т.ч. геморагічний), транзиторні ішемічні атаки1, непритомність, мігрень3, епілептичний напад, транзиторна амнезія. Порушення з боку органу зору: нечасто – нечіткість зорового сприйняття, больові відчуття у очному яблуку; рідко - порушення полів зору, припухлість повік, ін'єкція судин склери, неартеріальна передня ішемічна оптична нейропатія3, оклюзія судин сітківки3. Порушення з боку органу слуху та лабіринтні порушення: нечасто - шум/дзвін у вухах; рідко – раптова втрата слуха2. Порушення з боку серця1: нечасто – відчуття серцебиття, тахікардія; рідко – інфаркт міокарда, шлуночкові порушення ритму3, нестабільна стенокардія3. Порушення з боку судин: часто – "припливи" крові; нечасто – зниження артеріального тиску (АТ) (у пацієнтів, які приймають гіпотензивні засоби), підвищення АТ. Порушення з боку дихальної системи, органів грудної клітки та середостіння: часто – закладеність носа; нечасто – задишка, носова кровотеча. Порушення з боку шлунково-кишкового тракту: часто – диспепсія, гастроезофагеальний рефлюкс; нечасто – біль у животі. Порушення з боку шкіри та підшкірної клітковини: нечасто – висип, гіпергідроз (підвищена пітливість); рідко – кропив'янка, синдром Стівенса-Джонсона3, ексфоліативний дерматит3. Порушення з боку скелетно-м'язової та сполучної тканини: часто – біль у спині, біль у кінцівках, міалгія. Порушення з боку нирок та сечовивідних шляхів: часто – гематурія. Порушення з боку статевих органів та молочної залози: нечасто – кровотеча зі статевого члена, гемоспермія; рідко - тривала ерекція, пріапізм3. Загальні розлади та порушення у місці введення: нечасто – біль у грудній клітці1; рідко – набряк особи3, раптова серцева смерть1,3. 1 Спостерігалися у пацієнтів, які раніше мали серцево-судинні фактори ризику. Однак неможливо точно визначити, пов'язані ці явища безпосередньо з цими факторами ризику, з тадалафілом, із сексуальним збудженням або з комбінацією цих чи інших факторів. 2 Про раптову втрату слуху повідомлялося в невеликій кількості випадків під час постмаркетингових та клінічних досліджень при застосуванні всіх ФДЕ-5 інгібіторів, включаючи тадалафіл. 3 Побічні реакції, виявлені в ході постмаркетингових досліджень, які не спостерігалися в ході клінічних плацебо-контрольованих досліджень.Взаємодія з лікарськими засобамиБезпека та ефективність комбінації тадалафілу з іншими видами лікування порушень ерекції не вивчалися, тому застосування таких комбінацій не рекомендується. Вплив інших препаратів на тадалафіл Тадалафіл здебільшого метаболізується за участю ізоферменту CYP3A4. Селективний інгібітор ізоферменту CYP3A4 кетоконазол у дозі 400 мг/добу збільшує AUC тадалафілу (20 мг) у 4 рази та Сmах на 22%, а кетоконазол у дозі 200 мг/добу збільшує AUC тадалафілу (10 мг) у 2 рази щодо AUC та Сmах тільки для тадалафілу. Ритонавір (200 мг 2 рази на добу), інгібітор ізоферментів CYP3A4, CYP2C9, CYP2C19 та CYP2D6, збільшує AUC тадалафілу (20 мг) в 2 рази без зміни Сmах. Незважаючи на те, що специфічні взаємодії не вивчалися, можна припустити, що інші інгібітори ВІЛ-протеази, наприклад, саквінавір, та інгібітори ізоферменту CYP3A4, такі як еритроміцин, кларитроміцин та ітраконазол, а також грейпфрутовий сік, обережністю (через підвищення ризику розвитку небажаних реакцій). Селективний індуктор ізоферменту CYP3A4 рифампіцин (600 мг на добу) знижує AUC тадалафілу (10 мг) на 88% та Сmах на 46% щодо цих величин для тадалафілу окремо. Можна припускати, що одночасне застосування інших індукторів ізоферменту CYP3A4 (таких як фенобарбітал, фенітої та карбамазепін) також знижує плазмові концентрації тадалафілу. Одночасний прийом антациду (магнію гідроксид/алюмінію гідроксид) та тадалафілу знижує швидкість всмоктування тадалафілу без зміни його AUC. Вплив тадалафілу на інші препарати Відомо, що тадалафіл посилює гіпотензивну дію нітратів. Це відбувається в результаті адитивної дії нітратів та тадалафілу на метаболізм оксиду азоту II (NО) та цГМФ. Тому застосування тадалафілу на фоні нітратів протипоказано. Одночасне застосування тадалафілу із доксазозином протипоказане. При одночасному застосуванні тадалафілу (5 мг на добу) здоровими добрбвейбцями та альфа-адреноблокаторами доксазозину (4-8 мг на добу) спостерігалося посилення гіпотензивної дії доксазозину. Деякі пацієнти відчували симптоми, пов'язані зі зниженням АТ, включаючи непритомність, протягом 12 год. В обмеженій кількості досліджень не спостерігалося значного зниження артеріального тиску при застосуванні тадалафілу здоровими добровольцями, які приймали селективні альфа-адреноблокатори (тамсулозин. алфузозин). Незважаючи на це такі комбінації слід застосовувати з обережністю, починати з мінімальної дози альфа-адреноблокатора з поступовим її підвищенням. У доклінічних та клінічних дослідженнях було показано значне посилення гіпотензивного ефекту при одночасному застосуванні інгібіторів ФДЕ-5 та ріоцигуату (стимулятор гуанілатциклази), тому прийом такої комбінації препаратів протипоказаний. Тадалафіл має системні судинорозширюючі властивості і може посилювати дію гіпотензивних засобів, спрямоване на зниження артеріального тиску. Вивчалися препарати наступних груп гіпотензивних препаратів: блокатори "повільних" кальцієвих каналів (амлодипін), інгібітори ангіотензинперетворюючого ферменту (еналаприл), бета-адреноблокатори (метопролол), тіазидні діуретики (бендофлуазид), блокатори рецепторів. Додатково у пацієнтів з погано контрольованою артеріальною гіпертензією, які приймали кілька гіпотензивних засобів, спостерігалося дещо більше зниження артеріального тиску. Переважна більшість пацієнтів це зниження був пов'язані з розвитком гипотензивных симптомів. Пацієнтам, які отримують лікування гіпотензивними препаратами та приймають тадалафіл, повинні бути надані відповідні клінічні рекомендації. При одночасному застосуванні тадалафілу та фінастериду (інгібітор 5-альфа-редуктази) не спостерігалося зміни профілю небажаних реакцій порівняно із застосуванням комбінації плацебо + фінастерид, проте при прийомі цих препаратів слід бути обережним через недостатню кількість клінічних даних. Дослідження підтвердили, що тадалафіл не інгібує та не індукує ізоферменти системи цитохрому Р450 CYP1A2, CYP3A4, CYP2C9, CYP2C19, CYP2D6, CYP2E1. Тадалафіл не має клінічно значущого ефекту на фармакокінетику або фармакодинаміку теофіліну (субстрат CYP1A2), не впливає на AUC S-варфарину або R-варфарину (субстрати CYP2C9) і не змінює протромбіновий час при одночасному прийомі з варфарином. Тадалафіл (10 мг, 20 мг) не збільшує тривалість кровотечі, що викликається ацетилсаліцилової кислотою (АСК). Біодоступність етинілестрадіолу та тербуталіну при прийомі внутрішньо разом з тадалафілом підвищується, проте клінічне значення такої взаємодії не визначено. Тадалафіл не впливає на концентрацію алкоголю, так само як і алкоголь не впливає на концентрацію тадалафілу. При високих дозах алкоголю (0,7 г/кг) прийом тадалафілу не викликав статистично значущого зниження середньої АТ. У деяких пацієнтів спостерігалися постуральне запаморочення та ортостатична гіпотензія. При прийомі тадалафілу у поєднанні з нижчими дозами алкоголю (0,6 г/кг) зниження АТ не спостерігалося, а запаморочення виникало з такою самою частотою, що при прийомі алкоголю окремо. Вивчення взаємодій між тадалафілом та препаратами для лікування цукрового діабету не проводилося.Спосіб застосування та дозиДля прийому всередину. Застосування препарату при ЕД Для пацієнтів з частою сексуальною активністю (більше двох разів на тиждень) рекомендована частота прийому: щодня, 5 мг (1 таблетка) 1 раз на добу, одночасно, незалежно від їди. Доза повинна періодично контролюватись і переглядатися, за необхідності. Добова доза може бути знижена до 2,5 мг, залежно від індивідуальної чутливості. Для пацієнтів з нечастою сексуальною активністю (рідше двох разів на тиждень) рекомендована частота прийому: 20 мг (1 таблетка або 4 таблетки у дозі 5 мг) безпосередньо перед сексуальною активністю згідно з інструкцією з медичного застосування. Максимальна добова доза становить 20 мг. Застосування препарату при ДГПЗ або ЕД + ДГПЗ Рекомендована доза препарату становить 5 мг (1 таблетка) 1 раз на добу. Препарат слід приймати приблизно в один і той же час дня, незалежно від їди та часу сексуальної активності. Тривалість лікування встановлюється лікарем індивідуально. У пацієнтів з нирковою недостатністю тяжкого ступеня (КК У пацієнтів з нирковою недостатністю легкої (КК 51 -80 мл/хв) та середнього ступеня тяжкості (КК 31-50 мл/хв) або печінковою недостатністю легкого та середнього ступеня тяжкості (класи А та В за класифікацією Чайлд-П'ю), а також у літніх пацієнтів корекція дози не потрібна.ПередозуванняПри призначенні тадалафілу одноразово в дозі до 500 мг здоровим особам і багаторазово в дозі до 100 мг на добу пацієнтам з ЕД небажані реакції були зіставні, як і застосування нижчих доз. У разі передозування слід проводити симптоматичне лікування. При гемодіалізі тадалафілу практично не виводиться.Запобіжні заходи та особливі вказівкиДіагностика ЕД та ДГПЗ повинна включати виявлення основної причини захворювання, відповідне медичне обстеження, визначення тактики лікування та індивідуальну оцінку співвідношення користь/ризик. Сексуальна активність має потенційний ризик для пацієнтів із серцево-судинними захворюваннями, тому лікування ЕД не слід проводити у чоловіків із такими захворюваннями серця, при яких сексуальна активність не рекомендована. Як і інші ФДЕ-5 інгібітори, тадалафіл може чинити системну судиннорозширювальну дію, що може призводити до транзиторного зниження АТ та посилення гіпотензивної дії нітратів, альфа-адреноблокаторів (див. розділ "Взаємодія з іншими лікарськими засобами"). Перед призначенням препарату необхідно ретельно оцінити ймовірність виникнення подібних небажаних реакцій у пацієнтів із серцево-судинними захворюваннями. Пацієнти з передбачуваним діагнозом ДГПЗ повинні пройти обстеження для виключення раку передміхурової залози. Неартеріальна передня ішемічна оптична нейропатія (НАПІОН) є причиною порушення зору, включаючи повну втрату зору. Є рідкісні постмаркетингові повідомлення про випадки розвитку НАПІОН, за часом пов'язані з прийомом інгібіторів ФДЕ-5. В даний час неможливо визначити, чи існує прямий зв'язок між розвитком НАПІОН та прийомом інгібіторів ФДЕ-5 або іншими факторами. Необхідно попередити пацієнтів, що у разі раптової втрати зору слід припинити прийом тадалафілу та звернутися за медичною допомогою. Пацієнти також повинні бути проінформовані, що у людей, які перенесли НАПІОН, підвищений ризик повторного розвитку НАПІОН. Є повідомлення про виникнення приапізму при застосуванні інгібіторів ФДЕ-5, включаючи тадалафіл. Пацієнти повинні бути проінформовані про необхідність негайного звернення за медичною допомогою у разі виникнення ерекції, що триває 4 години та більше. Несвоєчасне лікування приапізму веде до пошкодження тканин статевого члена, внаслідок чого може настати необоротна імпотенція. Ефективність препарату у пацієнтів, які перенесли хірургічну операцію на органах малого тазу або радикальну нервозберігаючу простатектомію, невідома. Вплив на здатність до керування автотранспортом та управління механізмами Незважаючи на те, що частота виникнення запаморочення на тлі плацебо і тадалафілу однакова, в період лікування необхідно дотримуватися обережності при керуванні автотранспортом та заняттями іншими потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій. Пацієнти повинні бути обізнані про можливий розвиток сонливості при прийомі препарату, особливо на початку терапії або у поєднанні з алкоголем.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Діюча речовина: тадалафіл – 20,000 мг; Допоміжні речовини: лактози моногідрат (цукор молочний) – 273,300 мг; целюлоза мікрокристалічна – 57,000 мг; кроскармелоза натрію – 24,000 мг; гіпоролоза – 2,660 мг; натрію лаурилсульфат – 1,140 мг; магнію стеарат – 1,900 мг; Склад оболонки: гіпромелоза – 5,800 мг; макрогол-4000 – 1,700 мг; титану діоксид – 2,300 мг; барвник заліза оксид жовтий – 0,200 мг. Пігулки, покриті плівковою оболонкою 20 мг. По 1, 2, 10, 14 або 28 таблеток у контурне осередкове пакування з плівки полівінілхлоридної та фольги алюмінієвої друкованої лакованої. По 8, 10, 14, 20, 28, 30, 40, 50 або 100 таблеток у банки з поліетилентерефталату для лікарських засобів або поліпропіленові для лікарських засобів, закупорені кришками з поліетилену високого тиску з контролем першого розкриття, або кришками поліпропілен -повернути" або кришками з поліетилену низького тиску з контролем першого розтину. Одну банку або 1, 2, 3, 4, 5 або 10 контурних осередкових упаковок разом з інструкцією із застосування поміщають у картонну упаковку (пачку). Допускається комплектація по 2 або 3 картонні упаковки (пачки) до групового упаковки (транспортної тари) з картону для споживчої тари.Опис лікарської формиКруглі, двоопуклі таблетки з ризиком, покриті плівковою оболонкою від світло-жовтого до коричнево-жовтого кольору. На поперечному розрізі видно два шари: ядро білого або майже білого кольору та плівкова оболонка.Фармакотерапевтична групаЕректильна дисфункція Засіб лікування - ФДЕ5-інгібітор.ФармакокінетикаВсмоктування Після прийому внутрішньо тадалафіл швидко всмоктується. Середня максимальна концентрація (Сmах) у плазмі крові досягається в середньому через 2 години після прийому внутрішньо. Швидкість і ступінь всмоктування тадалафілу не залежать від їди, тому препарат можна застосовувати незалежно від їди. Час прийому (вранці або ввечері) не має клінічно значущого ефекту на швидкість та ступінь всмоктування. Фармакокінетика тадалафілу у здорових добровольців лінійна щодо часу та дози. У діапазоні доз від 2,5 до 20 мг площа під кривою "концентрація-час" (AUC) збільшується пропорційно дозі. Рівноважні концентрації в плазмі досягаються протягом 5 днів при прийомі препарату 1 раз на добу. Фармакокінетика тадалафілу у пацієнтів з порушенням ерекції аналогічна фармакокінетиці препарату у пацієнтів без порушення ерекції. Розподіл Середній обсяг розподілу становить близько 63 л, що свідчить про те, що тадалафіл розподіляється у тканинах організму. У терапевтичних концентраціях 94% тадалафілу пов'язують із білками плазми крові. Зв'язування з білками плазми не змінюється при порушеній функції нирок. У здорових добровольців менше 0,0005% введеної дози виявлено у спермі. Метаболізм Тадалафіл переважно метаболізується за участю ізоферменту CYP3A4 цитохрому Р450. Основним циркулюючим метаболітом є метилкатехолглюкуронід. Цей метаболіт принаймні у 13000 разів менш активний щодо ФДЕ-5, ніж тадалафіл. Отже, концентрація цього метаболіту не є клінічно значущою. Виведення У здорових добровольців середній кліренс тадалафілу при прийомі внутрішньо становить 2,5 л/год, а середній період напіввиведення (Т1/2) – 17,5 год. Тадалафіл виводиться переважно у вигляді неактивних метаболітів, переважно кишечником (близько 61 % дози). і, меншою мірою, нирками (близько 36% дози). Літні пацієнти Здорові літні добровольці (65 років і старше) мали нижчий кліренс тадалафілу при прийомі внутрішньо, що виражалося у збільшенні AUC на 25% зі здоровими добровольцями у віці від 19 до 45 років. Ця відмінність не є клінічно значущою і не потребує добору дози. Пацієнти з нирковою недостатністю У клінічних дослідженнях показано, що при прийомі одиничної дози тадалафілу (5-20 мг) AUC збільшується приблизно у 2 рази у пацієнтів з легкою (кліренс креатиніну (КК) 51-80 мл/хв), середньою (КК 31-50 мл/хв.) ) та термінальною нирковою недостатністю (проведення діалізу). У пацієнтів на гемодіалізі Сmах тадалафілу на 41% вище, ніж у здорових добровольців. Тадалафіл практично не виводиться при гемодіалізі. Пацієнти з печінковою недостатністю Фармакокінетика тадалафілу у пацієнтів з легкою та середньотяжкою печінковою недостатністю (класи А та В за класифікацією Чайлд-П'ю) можна порівняти з такою у здорових добровольців. Щодо пацієнтів з тяжкою печінковою недостатністю (клас С за класифікацією Чайлд-П'ю) дані обмежені, тому перед застосуванням препарату необхідно проводити оцінку співвідношення користь/ризик. Пацієнти з цукровим діабетом У пацієнтів із цукровим діабетом на фоні застосування тадалафілу AUC менше приблизно на 19%, ніж у здорових добровольців. Ця відмінність не потребує підбору дози.ФармакодинамікаТадалафіл є оборотним селективним інгібітором специфічної фосфодіестерази 5 типу (ФДЕ-5) циклічного гуанозинмонофосфату (цГМФ). Коли сексуальне збудження викликає місцеве вивільнення оксиду азоту, пригнічення ФДЕ-5 тадалафілом веде до підвищення концентрації цГМФ в печеристому тілі статевого члена. Наслідком цього є розслаблення гладких м'язів артерій та приплив крові до тканин статевого члена, що викликає ерекцію. Дослідження in vitro показали, що тадалафіл є селективним інгібітором ФДЕ-5. ФДЕ-5 є ферментом, представленим у гладкій мускулатурі печеристого тіла, судин та внутрішніх органів, у скелетних м'язах, тромбоцитах, нирках, легенях та мозочку. Дія тадалафілу на ФДЕ-5 є більш активною, ніж на інші фосфодіестерази. Тадалафіл є в 10 000 разів більш потужним щодо ФДЕ-5, ніж щодо інших типів фосфодіестерази (ФДЕ-1, ФДЕ-2, ФДЕ-4 та ФДЕ-7), які локалізуються в серці, головному мозку, кровоносних судинах, печінці. , лейкоцитах та інших органах. Тадалафіл у 10 000 разів активніше блокує ФДЕ-5, ніж ФДЕ-3 – фермент, який виявляється у серці та кровоносних судинах. Ця селективність щодо ФДЕ-5 у порівнянні з ФДЕ-3 має важливе значення, оскільки ФДЕ-3 є ферментом,беруть участь у скороченні серцевого м'яза. Крім того, тадалафіл приблизно в 700 разів активніше щодо ФДЕ-5, ніж ФДЕ-6, виявленої в сітківці і відповідає за фотопередачу. Дія тадалафілу щодо ФДЕ-5 у 9000 разів більш виражена, ніж його вплив на ФДЕ-8, ФДЕ-9 та ФДЕ-10, та у 14 разів більш виражене, ніж на ФДЕ-11. Розподіл у тканинах та фізіологічні ефекти інгібування ФДЕ-8 – ФДЕ-11 дотепер не з'ясовані.Розподіл у тканинах та фізіологічні ефекти інгібування ФДЕ-8 – ФДЕ-11 дотепер не з'ясовані.Розподіл у тканинах та фізіологічні ефекти інгібування ФДЕ-8 – ФДЕ-11 дотепер не з'ясовані. Тадалафіл у здорових добровольців не викликає достовірної зміни систолічного та діастолічного артеріального тиску в порівнянні з плацебо у положенні лежачи (середнє максимальне зниження становить 1,6 та 0,8 мм рт. ст. відповідно) та у положенні стоячи (середнє максимальне зниження становить 0, 2 і 4,6 мм рт.ст., відповідно). Тадалафіл не викликає достовірної зміни частоти серцевих скорочень. Тадалафіл не викликає змін розпізнавання кольорів (блакитний/зелений), що пояснюється його низькою спорідненістю з ФДЕ-6. Крім того, не спостерігається вплив тадалафілу на гостроту зору, електроретинограму, внутрішньоочний тиск та розмір зіниці. З метою оцінки впливу щоденного прийому тадалафілу на сперматогенез було проведено декілька досліджень. У жодному з досліджень не спостерігалося небажаного впливу на морфологію сперматозоїдів та їхню рухливість. В одному з досліджень було виявлено зниження середньої концентрації сперматозоїдів у порівнянні із плацебо. Зниження концентрації сперматозоїдів пов'язано з вищою частотою еякуляції. Крім того, при порівнянні тадалафілу з плацебо не спостерігалося небажаного впливу на середню концентрацію статевих гормонів (тестостерону, лютеїнізуючого гормону та фолікулостимулюючого гормону). Еректильна дисфункція (ЕД) У проведених дослідженнях тадалафіл показав статистично значуще покращення еректильної функції та можливості проведення повноцінного статевого акту. Тадалафіл не має ефекту у відсутності сексуального збудження. Ефективність та безпека тадалафілу вивчалась у ході клінічних досліджень. Було відмічено покращення ерекції у пацієнтів з ЕД усіх ступенів тяжкості при прийомі 5 мг тадалафілу 1 раз на добу протягом 36 годин після прийому, а також підтримання ерекції протягом 16 хв після прийому порівняно з плацебо. У дослідженнях первинної ефективності застосування 5 мг тадалафілу 57% та 67% спроб статевого акту були успішними порівняно з 31% та 37% при прийомі плацебо. У дослідженнях пацієнтів із вторинною ЕД на тлі цукрового діабету 41% спроб статевого акту були успішними порівняно з 28% при прийомі плацебо. Доброякісна гіперплазія передміхурової залози (ДГПЗ) У пацієнтів з ДГПЗ тадалафіл, інгібуючи ФДЕ-5, призводить до підвищення концентрації цГМФ не тільки в печеристому тілі статевого члена, а й у гладкій мускулатурі передміхурової залози, сечового міхура та судинах, що їх кровопостачають. Це своє чергу збільшує перфузію крові у цих органах як наслідок, зменшує вираженість симптомів ДГПЖ. Розслаблення гладкої мускулатури передміхурової залози та сечового міхура та інгібування аферентної іннервації сечового міхура можуть додатково посилювати судинні ефекти. У ході клінічних досліджень було показано зменшення симптомів ДГПЗ протягом 1 тижня після прийому 5 мг тадалафілу проти плацебо. У дослідженнях, що включають пацієнтів з ЕД та симптомами ДГПЗ, при застосуванні 5 мг тадалафілу 71,9% спроб статевого акту були успішними порівняно з 48,3% при прийомі плацебо, та спостерігалося значне покращення еректильної функції та зменшення симптомів з боку передміхурової залози.Показання до застосуванняЕректильна дисфункція; симптоми з боку нижніх сечовивідних шляхів у пацієнтів із ДГПЗ (для дозування 5 мг); еректильна дисфункція у пацієнтів із симптомами з боку сечовивідних шляхів у пацієнтів із ДГПЗ (для дозування 5 мг).Протипоказання до застосуванняПідвищена чутливість до тадалафілу або будь-якої речовини, що входить до складу препарату; прийом препаратів, що містять будь-які органічні нітрати; дитячий вік до 18 років; наявність протипоказань до сексуальної активності у пацієнтів із захворюваннями серцево-судинної системи: інфаркт міокарда протягом останніх 90 днів, нестабільна стенокардія, виникнення нападу стенокардії під час статевого акту, хронічна серцева недостатність II-IV класів за класифікацією NYHA, неконтрольована аритмія АТ втрата зору внаслідок неартеріальної передньої ішемічної нейропатії зорового нерва (незалежно від зв'язку з прийомом інгібіторів ФДЕ-5); одночасний прийом доксазозину, інших лікарських засобів для лікування еректильної дисфункції, стимуляторів гуанілатциклази (ріоцигуат); застосування у пацієнтів з тяжкою нирковою недостатністю (КК дефіцит лактази, непереносимість лактози, глюкозо-галактозна мальабсорбція. З обережністю: Тяжка печінкова недостатність (клас С за класифікацією Чайлд-П'ю) через недостатню кількість даних щодо ефективності/безпеки препарату; одночасне застосування селективних альфа-адреноблокаторів, сильних інгібіторів ізоферменту CYP3A4 (ритонавір, саквінавір, кетоконазол, ітраконазол, еритроміцин), інгібіторів 5-альфа-редуктази; схильність до приапізму (при серповидно-клітинній анемії, множинні мієломи або лейкозі), анатомічна деформація статевого члена (кутове викривлення, кавернозний фіброз або хвороба Пейроні).Вагітність та лактаціяПрепарат не призначений для застосування у жінок.Побічна діяЗа даними Всесвітньої Організації Охорони Здоров'я (ВООЗ), небажані реакції класифіковані відповідно до їх частоти розвитку наступним чином: дуже часто (≥1/10), часто (≥1/100, Порушення з боку імунної системи: нечасто – реакції гіперчутливості; рідко – ангіоневротичний отек3. Порушення з боку нервової системи: часто – головний біль; нечасто – запаморочення; рідко – інсульт1 (в т.ч. геморагічний), транзиторні ішемічні атаки1, непритомність, мігрень3, епілептичний напад, транзиторна амнезія. Порушення з боку органу зору: нечасто – нечіткість зорового сприйняття, больові відчуття у очному яблуку; рідко - порушення полів зору, припухлість повік, ін'єкція судин склери, неартеріальна передня ішемічна оптична нейропатія3, оклюзія судин сітківки3. Порушення з боку органу слуху та лабіринтні порушення: нечасто - шум/дзвін у вухах; рідко – раптова втрата слуха2. Порушення з боку серця1: нечасто – відчуття серцебиття, тахікардія; рідко – інфаркт міокарда, шлуночкові порушення ритму3, нестабільна стенокардія3. Порушення з боку судин: часто – "припливи" крові; нечасто – зниження артеріального тиску (АТ) (у пацієнтів, які приймають гіпотензивні засоби), підвищення АТ. Порушення з боку дихальної системи, органів грудної клітки та середостіння: часто – закладеність носа; нечасто – задишка, носова кровотеча. Порушення з боку шлунково-кишкового тракту: часто – диспепсія, гастроезофагеальний рефлюкс; нечасто – біль у животі. Порушення з боку шкіри та підшкірної клітковини: нечасто – висип, гіпергідроз (підвищена пітливість); рідко – кропив'янка, синдром Стівенса-Джонсона3, ексфоліативний дерматит3. Порушення з боку скелетно-м'язової та сполучної тканини: часто – біль у спині, біль у кінцівках, міалгія. Порушення з боку нирок та сечовивідних шляхів: часто – гематурія. Порушення з боку статевих органів та молочної залози: нечасто – кровотеча зі статевого члена, гемоспермія; рідко - тривала ерекція, пріапізм3. Загальні розлади та порушення у місці введення: нечасто – біль у грудній клітці1; рідко – набряк особи3, раптова серцева смерть1,3. 1 Спостерігалися у пацієнтів, які раніше мали серцево-судинні фактори ризику. Однак неможливо точно визначити, пов'язані ці явища безпосередньо з цими факторами ризику, з тадалафілом, із сексуальним збудженням або з комбінацією цих чи інших факторів. 2 Про раптову втрату слуху повідомлялося в невеликій кількості випадків під час постмаркетингових та клінічних досліджень при застосуванні всіх ФДЕ-5 інгібіторів, включаючи тадалафіл. 3 Побічні реакції, виявлені в ході постмаркетингових досліджень, які не спостерігалися в ході клінічних плацебо-контрольованих досліджень.Взаємодія з лікарськими засобамиБезпека та ефективність комбінації тадалафілу з іншими видами лікування порушень ерекції не вивчалися, тому застосування таких комбінацій не рекомендується. Вплив інших препаратів на тадалафіл Тадалафіл здебільшого метаболізується за участю ізоферменту CYP3A4. Селективний інгібітор ізоферменту CYP3A4 кетоконазол у дозі 400 мг/добу збільшує AUC тадалафілу (20 мг) у 4 рази та Сmах на 22%, а кетоконазол у дозі 200 мг/добу збільшує AUC тадалафілу (10 мг) у 2 рази щодо AUC та Сmах тільки для тадалафілу. Ритонавір (200 мг 2 рази на добу), інгібітор ізоферментів CYP3A4, CYP2C9, CYP2C19 та CYP2D6, збільшує AUC тадалафілу (20 мг) в 2 рази без зміни Сmах. Незважаючи на те, що специфічні взаємодії не вивчалися, можна припустити, що інші інгібітори ВІЛ-протеази, наприклад, саквінавір, та інгібітори ізоферменту CYP3A4, такі як еритроміцин, кларитроміцин та ітраконазол, а також грейпфрутовий сік, обережністю (через підвищення ризику розвитку небажаних реакцій). Селективний індуктор ізоферменту CYP3A4 рифампіцин (600 мг на добу) знижує AUC тадалафілу (10 мг) на 88% та Сmах на 46% щодо цих величин для тадалафілу окремо. Можна припускати, що одночасне застосування інших індукторів ізоферменту CYP3A4 (таких як фенобарбітал, фенітої та карбамазепін) також знижує плазмові концентрації тадалафілу. Одночасний прийом антациду (магнію гідроксид/алюмінію гідроксид) та тадалафілу знижує швидкість всмоктування тадалафілу без зміни його AUC. Вплив тадалафілу на інші препарати Відомо, що тадалафіл посилює гіпотензивну дію нітратів. Це відбувається в результаті адитивної дії нітратів та тадалафілу на метаболізм оксиду азоту II (NО) та цГМФ. Тому застосування тадалафілу на фоні нітратів протипоказано. Одночасне застосування тадалафілу із доксазозином протипоказане. При одночасному застосуванні тадалафілу (5 мг на добу) здоровими добрбвейбцями та альфа-адреноблокаторами доксазозину (4-8 мг на добу) спостерігалося посилення гіпотензивної дії доксазозину. Деякі пацієнти відчували симптоми, пов'язані зі зниженням АТ, включаючи непритомність, протягом 12 год. В обмеженій кількості досліджень не спостерігалося значного зниження артеріального тиску при застосуванні тадалафілу здоровими добровольцями, які приймали селективні альфа-адреноблокатори (тамсулозин. алфузозин). Незважаючи на це такі комбінації слід застосовувати з обережністю, починати з мінімальної дози альфа-адреноблокатора з поступовим її підвищенням. У доклінічних та клінічних дослідженнях було показано значне посилення гіпотензивного ефекту при одночасному застосуванні інгібіторів ФДЕ-5 та ріоцигуату (стимулятор гуанілатциклази), тому прийом такої комбінації препаратів протипоказаний. Тадалафіл має системні судинорозширюючі властивості і може посилювати дію гіпотензивних засобів, спрямоване на зниження артеріального тиску. Вивчалися препарати наступних груп гіпотензивних препаратів: блокатори "повільних" кальцієвих каналів (амлодипін), інгібітори ангіотензинперетворюючого ферменту (еналаприл), бета-адреноблокатори (метопролол), тіазидні діуретики (бендофлуазид), блокатори рецепторів. Додатково у пацієнтів з погано контрольованою артеріальною гіпертензією, які приймали кілька гіпотензивних засобів, спостерігалося дещо більше зниження артеріального тиску. Переважна більшість пацієнтів це зниження був пов'язані з розвитком гипотензивных симптомів. Пацієнтам, які отримують лікування гіпотензивними препаратами та приймають тадалафіл, повинні бути надані відповідні клінічні рекомендації. При одночасному застосуванні тадалафілу та фінастериду (інгібітор 5-альфа-редуктази) не спостерігалося зміни профілю небажаних реакцій порівняно із застосуванням комбінації плацебо + фінастерид, проте при прийомі цих препаратів слід бути обережним через недостатню кількість клінічних даних. Дослідження підтвердили, що тадалафіл не інгібує та не індукує ізоферменти системи цитохрому Р450 CYP1A2, CYP3A4, CYP2C9, CYP2C19, CYP2D6, CYP2E1. Тадалафіл не має клінічно значущого ефекту на фармакокінетику або фармакодинаміку теофіліну (субстрат CYP1A2), не впливає на AUC S-варфарину або R-варфарину (субстрати CYP2C9) і не змінює протромбіновий час при одночасному прийомі з варфарином. Тадалафіл (10 мг, 20 мг) не збільшує тривалість кровотечі, що викликається ацетилсаліцилової кислотою (АСК). Біодоступність етинілестрадіолу та тербуталіну при прийомі внутрішньо разом з тадалафілом підвищується, проте клінічне значення такої взаємодії не визначено. Тадалафіл не впливає на концентрацію алкоголю, так само як і алкоголь не впливає на концентрацію тадалафілу. При високих дозах алкоголю (0,7 г/кг) прийом тадалафілу не викликав статистично значущого зниження середньої АТ. У деяких пацієнтів спостерігалися постуральне запаморочення та ортостатична гіпотензія. При прийомі тадалафілу у поєднанні з нижчими дозами алкоголю (0,6 г/кг) зниження АТ не спостерігалося, а запаморочення виникало з такою самою частотою, що при прийомі алкоголю окремо. Вивчення взаємодій між тадалафілом та препаратами для лікування цукрового діабету не проводилося.Спосіб застосування та дозиДля прийому всередину. Застосування препарату при ЕД Для пацієнтів з частою сексуальною активністю (більше двох разів на тиждень) рекомендована частота прийому: щодня, 5 мг (1 таблетка) 1 раз на добу, одночасно, незалежно від їди. Доза повинна періодично контролюватись і переглядатися, за необхідності. Добова доза може бути знижена до 2,5 мг, залежно від індивідуальної чутливості. Для пацієнтів з нечастою сексуальною активністю (рідше двох разів на тиждень) рекомендована частота прийому: 20 мг (1 таблетка або 4 таблетки у дозі 5 мг) безпосередньо перед сексуальною активністю згідно з інструкцією з медичного застосування. Максимальна добова доза становить 20 мг. Застосування препарату при ДГПЗ або ЕД + ДГПЗ Рекомендована доза препарату становить 5 мг (1 таблетка) 1 раз на добу. Препарат слід приймати приблизно в один і той же час дня, незалежно від їди та часу сексуальної активності. Тривалість лікування встановлюється лікарем індивідуально. У пацієнтів з нирковою недостатністю тяжкого ступеня (КК У пацієнтів з нирковою недостатністю легкої (КК 51 -80 мл/хв) та середнього ступеня тяжкості (КК 31-50 мл/хв) або печінковою недостатністю легкого та середнього ступеня тяжкості (класи А та В за класифікацією Чайлд-П'ю), а також у літніх пацієнтів корекція дози не потрібна.ПередозуванняПри призначенні тадалафілу одноразово в дозі до 500 мг здоровим особам і багаторазово в дозі до 100 мг на добу пацієнтам з ЕД небажані реакції були зіставні, як і застосування нижчих доз. У разі передозування слід проводити симптоматичне лікування. При гемодіалізі тадалафілу практично не виводиться.Запобіжні заходи та особливі вказівкиДіагностика ЕД та ДГПЗ повинна включати виявлення основної причини захворювання, відповідне медичне обстеження, визначення тактики лікування та індивідуальну оцінку співвідношення користь/ризик. Сексуальна активність має потенційний ризик для пацієнтів із серцево-судинними захворюваннями, тому лікування ЕД не слід проводити у чоловіків із такими захворюваннями серця, при яких сексуальна активність не рекомендована. Як і інші ФДЕ-5 інгібітори, тадалафіл може чинити системну судиннорозширювальну дію, що може призводити до транзиторного зниження АТ та посилення гіпотензивної дії нітратів, альфа-адреноблокаторів (див. розділ "Взаємодія з іншими лікарськими засобами"). Перед призначенням препарату необхідно ретельно оцінити ймовірність виникнення подібних небажаних реакцій у пацієнтів із серцево-судинними захворюваннями. Пацієнти з передбачуваним діагнозом ДГПЗ повинні пройти обстеження для виключення раку передміхурової залози. Неартеріальна передня ішемічна оптична нейропатія (НАПІОН) є причиною порушення зору, включаючи повну втрату зору. Є рідкісні постмаркетингові повідомлення про випадки розвитку НАПІОН, за часом пов'язані з прийомом інгібіторів ФДЕ-5. В даний час неможливо визначити, чи існує прямий зв'язок між розвитком НАПІОН та прийомом інгібіторів ФДЕ-5 або іншими факторами. Необхідно попередити пацієнтів, що у разі раптової втрати зору слід припинити прийом тадалафілу та звернутися за медичною допомогою. Пацієнти також повинні бути проінформовані, що у людей, які перенесли НАПІОН, підвищений ризик повторного розвитку НАПІОН. Є повідомлення про виникнення приапізму при застосуванні інгібіторів ФДЕ-5, включаючи тадалафіл. Пацієнти повинні бути проінформовані про необхідність негайного звернення за медичною допомогою у разі виникнення ерекції, що триває 4 години та більше. Несвоєчасне лікування приапізму веде до пошкодження тканин статевого члена, внаслідок чого може настати необоротна імпотенція. Ефективність препарату у пацієнтів, які перенесли хірургічну операцію на органах малого тазу або радикальну нервозберігаючу простатектомію, невідома. Вплив на здатність до керування автотранспортом та управління механізмами Незважаючи на те, що частота виникнення запаморочення на тлі плацебо і тадалафілу однакова, в період лікування необхідно дотримуватися обережності при керуванні автотранспортом та заняттями іншими потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій. Пацієнти повинні бути обізнані про можливий розвиток сонливості при прийомі препарату, особливо на початку терапії або у поєднанні з алкоголем.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Діюча речовина: тадалафіл – 20,000 мг; Допоміжні речовини: лактози моногідрат (цукор молочний) – 273,300 мг; целюлоза мікрокристалічна – 57,000 мг; кроскармелоза натрію – 24,000 мг; гіпоролоза – 2,660 мг; натрію лаурилсульфат – 1,140 мг; магнію стеарат – 1,900 мг; Склад оболонки: гіпромелоза – 5,800 мг; макрогол-4000 – 1,700 мг; титану діоксид – 2,300 мг; барвник заліза оксид жовтий – 0,200 мг. Пігулки, покриті плівковою оболонкою 20 мг. По 1, 2, 10, 14 або 28 таблеток у контурне осередкове пакування з плівки полівінілхлоридної та фольги алюмінієвої друкованої лакованої. По 8, 10, 14, 20, 28, 30, 40, 50 або 100 таблеток у банки з поліетилентерефталату для лікарських засобів або поліпропіленові для лікарських засобів, закупорені кришками з поліетилену високого тиску з контролем першого розкриття, або кришками поліпропілен -повернути" або кришками з поліетилену низького тиску з контролем першого розтину. Одну банку або 1, 2, 3, 4, 5 або 10 контурних осередкових упаковок разом з інструкцією із застосування поміщають у картонну упаковку (пачку). Допускається комплектація по 2 або 3 картонні упаковки (пачки) до групового упаковки (транспортної тари) з картону для споживчої тари.Опис лікарської формиКруглі, двоопуклі таблетки з ризиком, покриті плівковою оболонкою від світло-жовтого до коричнево-жовтого кольору. На поперечному розрізі видно два шари: ядро білого або майже білого кольору та плівкова оболонка.Фармакотерапевтична групаЕректильна дисфункція Засіб лікування - ФДЕ5-інгібітор.ФармакокінетикаВсмоктування Після прийому внутрішньо тадалафіл швидко всмоктується. Середня максимальна концентрація (Сmах) у плазмі крові досягається в середньому через 2 години після прийому внутрішньо. Швидкість і ступінь всмоктування тадалафілу не залежать від їди, тому препарат можна застосовувати незалежно від їди. Час прийому (вранці або ввечері) не має клінічно значущого ефекту на швидкість та ступінь всмоктування. Фармакокінетика тадалафілу у здорових добровольців лінійна щодо часу та дози. У діапазоні доз від 2,5 до 20 мг площа під кривою "концентрація-час" (AUC) збільшується пропорційно дозі. Рівноважні концентрації в плазмі досягаються протягом 5 днів при прийомі препарату 1 раз на добу. Фармакокінетика тадалафілу у пацієнтів з порушенням ерекції аналогічна фармакокінетиці препарату у пацієнтів без порушення ерекції. Розподіл Середній обсяг розподілу становить близько 63 л, що свідчить про те, що тадалафіл розподіляється у тканинах організму. У терапевтичних концентраціях 94% тадалафілу пов'язують із білками плазми крові. Зв'язування з білками плазми не змінюється при порушеній функції нирок. У здорових добровольців менше 0,0005% введеної дози виявлено у спермі. Метаболізм Тадалафіл переважно метаболізується за участю ізоферменту CYP3A4 цитохрому Р450. Основним циркулюючим метаболітом є метилкатехолглюкуронід. Цей метаболіт принаймні у 13000 разів менш активний щодо ФДЕ-5, ніж тадалафіл. Отже, концентрація цього метаболіту не є клінічно значущою. Виведення У здорових добровольців середній кліренс тадалафілу при прийомі внутрішньо становить 2,5 л/год, а середній період напіввиведення (Т1/2) – 17,5 год. Тадалафіл виводиться переважно у вигляді неактивних метаболітів, переважно кишечником (близько 61 % дози). і, меншою мірою, нирками (близько 36% дози). Літні пацієнти Здорові літні добровольці (65 років і старше) мали нижчий кліренс тадалафілу при прийомі внутрішньо, що виражалося у збільшенні AUC на 25% зі здоровими добровольцями у віці від 19 до 45 років. Ця відмінність не є клінічно значущою і не потребує добору дози. Пацієнти з нирковою недостатністю У клінічних дослідженнях показано, що при прийомі одиничної дози тадалафілу (5-20 мг) AUC збільшується приблизно у 2 рази у пацієнтів з легкою (кліренс креатиніну (КК) 51-80 мл/хв), середньою (КК 31-50 мл/хв.) ) та термінальною нирковою недостатністю (проведення діалізу). У пацієнтів на гемодіалізі Сmах тадалафілу на 41% вище, ніж у здорових добровольців. Тадалафіл практично не виводиться при гемодіалізі. Пацієнти з печінковою недостатністю Фармакокінетика тадалафілу у пацієнтів з легкою та середньотяжкою печінковою недостатністю (класи А та В за класифікацією Чайлд-П'ю) можна порівняти з такою у здорових добровольців. Щодо пацієнтів з тяжкою печінковою недостатністю (клас С за класифікацією Чайлд-П'ю) дані обмежені, тому перед застосуванням препарату необхідно проводити оцінку співвідношення користь/ризик. Пацієнти з цукровим діабетом У пацієнтів із цукровим діабетом на фоні застосування тадалафілу AUC менше приблизно на 19%, ніж у здорових добровольців. Ця відмінність не потребує підбору дози.ФармакодинамікаТадалафіл є оборотним селективним інгібітором специфічної фосфодіестерази 5 типу (ФДЕ-5) циклічного гуанозинмонофосфату (цГМФ). Коли сексуальне збудження викликає місцеве вивільнення оксиду азоту, пригнічення ФДЕ-5 тадалафілом веде до підвищення концентрації цГМФ в печеристому тілі статевого члена. Наслідком цього є розслаблення гладких м'язів артерій та приплив крові до тканин статевого члена, що викликає ерекцію. Дослідження in vitro показали, що тадалафіл є селективним інгібітором ФДЕ-5. ФДЕ-5 є ферментом, представленим у гладкій мускулатурі печеристого тіла, судин та внутрішніх органів, у скелетних м'язах, тромбоцитах, нирках, легенях та мозочку. Дія тадалафілу на ФДЕ-5 є більш активною, ніж на інші фосфодіестерази. Тадалафіл є в 10 000 разів більш потужним щодо ФДЕ-5, ніж щодо інших типів фосфодіестерази (ФДЕ-1, ФДЕ-2, ФДЕ-4 та ФДЕ-7), які локалізуються в серці, головному мозку, кровоносних судинах, печінці. , лейкоцитах та інших органах. Тадалафіл у 10 000 разів активніше блокує ФДЕ-5, ніж ФДЕ-3 – фермент, який виявляється у серці та кровоносних судинах. Ця селективність щодо ФДЕ-5 у порівнянні з ФДЕ-3 має важливе значення, оскільки ФДЕ-3 є ферментом,беруть участь у скороченні серцевого м'яза. Крім того, тадалафіл приблизно в 700 разів активніше щодо ФДЕ-5, ніж ФДЕ-6, виявленої в сітківці і відповідає за фотопередачу. Дія тадалафілу щодо ФДЕ-5 у 9000 разів більш виражена, ніж його вплив на ФДЕ-8, ФДЕ-9 та ФДЕ-10, та у 14 разів більш виражене, ніж на ФДЕ-11. Розподіл у тканинах та фізіологічні ефекти інгібування ФДЕ-8 – ФДЕ-11 дотепер не з'ясовані.Розподіл у тканинах та фізіологічні ефекти інгібування ФДЕ-8 – ФДЕ-11 дотепер не з'ясовані.Розподіл у тканинах та фізіологічні ефекти інгібування ФДЕ-8 – ФДЕ-11 дотепер не з'ясовані. Тадалафіл у здорових добровольців не викликає достовірної зміни систолічного та діастолічного артеріального тиску в порівнянні з плацебо у положенні лежачи (середнє максимальне зниження становить 1,6 та 0,8 мм рт. ст. відповідно) та у положенні стоячи (середнє максимальне зниження становить 0, 2 і 4,6 мм рт.ст., відповідно). Тадалафіл не викликає достовірної зміни частоти серцевих скорочень. Тадалафіл не викликає змін розпізнавання кольорів (блакитний/зелений), що пояснюється його низькою спорідненістю з ФДЕ-6. Крім того, не спостерігається вплив тадалафілу на гостроту зору, електроретинограму, внутрішньоочний тиск та розмір зіниці. З метою оцінки впливу щоденного прийому тадалафілу на сперматогенез було проведено декілька досліджень. У жодному з досліджень не спостерігалося небажаного впливу на морфологію сперматозоїдів та їхню рухливість. В одному з досліджень було виявлено зниження середньої концентрації сперматозоїдів у порівнянні із плацебо. Зниження концентрації сперматозоїдів пов'язано з вищою частотою еякуляції. Крім того, при порівнянні тадалафілу з плацебо не спостерігалося небажаного впливу на середню концентрацію статевих гормонів (тестостерону, лютеїнізуючого гормону та фолікулостимулюючого гормону). Еректильна дисфункція (ЕД) У проведених дослідженнях тадалафіл показав статистично значуще покращення еректильної функції та можливості проведення повноцінного статевого акту. Тадалафіл не має ефекту у відсутності сексуального збудження. Ефективність та безпека тадалафілу вивчалась у ході клінічних досліджень. Було відмічено покращення ерекції у пацієнтів з ЕД усіх ступенів тяжкості при прийомі 5 мг тадалафілу 1 раз на добу протягом 36 годин після прийому, а також підтримання ерекції протягом 16 хв після прийому порівняно з плацебо. У дослідженнях первинної ефективності застосування 5 мг тадалафілу 57% та 67% спроб статевого акту були успішними порівняно з 31% та 37% при прийомі плацебо. У дослідженнях пацієнтів із вторинною ЕД на тлі цукрового діабету 41% спроб статевого акту були успішними порівняно з 28% при прийомі плацебо. Доброякісна гіперплазія передміхурової залози (ДГПЗ) У пацієнтів з ДГПЗ тадалафіл, інгібуючи ФДЕ-5, призводить до підвищення концентрації цГМФ не тільки в печеристому тілі статевого члена, а й у гладкій мускулатурі передміхурової залози, сечового міхура та судинах, що їх кровопостачають. Це своє чергу збільшує перфузію крові у цих органах як наслідок, зменшує вираженість симптомів ДГПЖ. Розслаблення гладкої мускулатури передміхурової залози та сечового міхура та інгібування аферентної іннервації сечового міхура можуть додатково посилювати судинні ефекти. У ході клінічних досліджень було показано зменшення симптомів ДГПЗ протягом 1 тижня після прийому 5 мг тадалафілу проти плацебо. У дослідженнях, що включають пацієнтів з ЕД та симптомами ДГПЗ, при застосуванні 5 мг тадалафілу 71,9% спроб статевого акту були успішними порівняно з 48,3% при прийомі плацебо, та спостерігалося значне покращення еректильної функції та зменшення симптомів з боку передміхурової залози.Показання до застосуванняЕректильна дисфункція; симптоми з боку нижніх сечовивідних шляхів у пацієнтів із ДГПЗ (для дозування 5 мг); еректильна дисфункція у пацієнтів із симптомами з боку сечовивідних шляхів у пацієнтів із ДГПЗ (для дозування 5 мг).Протипоказання до застосуванняПідвищена чутливість до тадалафілу або будь-якої речовини, що входить до складу препарату; прийом препаратів, що містять будь-які органічні нітрати; дитячий вік до 18 років; наявність протипоказань до сексуальної активності у пацієнтів із захворюваннями серцево-судинної системи: інфаркт міокарда протягом останніх 90 днів, нестабільна стенокардія, виникнення нападу стенокардії під час статевого акту, хронічна серцева недостатність II-IV класів за класифікацією NYHA, неконтрольована аритмія АТ втрата зору внаслідок неартеріальної передньої ішемічної нейропатії зорового нерва (незалежно від зв'язку з прийомом інгібіторів ФДЕ-5); одночасний прийом доксазозину, інших лікарських засобів для лікування еректильної дисфункції, стимуляторів гуанілатциклази (ріоцигуат); застосування у пацієнтів з тяжкою нирковою недостатністю (КК дефіцит лактази, непереносимість лактози, глюкозо-галактозна мальабсорбція. З обережністю: Тяжка печінкова недостатність (клас С за класифікацією Чайлд-П'ю) через недостатню кількість даних щодо ефективності/безпеки препарату; одночасне застосування селективних альфа-адреноблокаторів, сильних інгібіторів ізоферменту CYP3A4 (ритонавір, саквінавір, кетоконазол, ітраконазол, еритроміцин), інгібіторів 5-альфа-редуктази; схильність до приапізму (при серповидно-клітинній анемії, множинні мієломи або лейкозі), анатомічна деформація статевого члена (кутове викривлення, кавернозний фіброз або хвороба Пейроні).Вагітність та лактаціяПрепарат не призначений для застосування у жінок.Побічна діяЗа даними Всесвітньої Організації Охорони Здоров'я (ВООЗ), небажані реакції класифіковані відповідно до їх частоти розвитку наступним чином: дуже часто (≥1/10), часто (≥1/100, Порушення з боку імунної системи: нечасто – реакції гіперчутливості; рідко – ангіоневротичний отек3. Порушення з боку нервової системи: часто – головний біль; нечасто – запаморочення; рідко – інсульт1 (в т.ч. геморагічний), транзиторні ішемічні атаки1, непритомність, мігрень3, епілептичний напад, транзиторна амнезія. Порушення з боку органу зору: нечасто – нечіткість зорового сприйняття, больові відчуття у очному яблуку; рідко - порушення полів зору, припухлість повік, ін'єкція судин склери, неартеріальна передня ішемічна оптична нейропатія3, оклюзія судин сітківки3. Порушення з боку органу слуху та лабіринтні порушення: нечасто - шум/дзвін у вухах; рідко – раптова втрата слуха2. Порушення з боку серця1: нечасто – відчуття серцебиття, тахікардія; рідко – інфаркт міокарда, шлуночкові порушення ритму3, нестабільна стенокардія3. Порушення з боку судин: часто – "припливи" крові; нечасто – зниження артеріального тиску (АТ) (у пацієнтів, які приймають гіпотензивні засоби), підвищення АТ. Порушення з боку дихальної системи, органів грудної клітки та середостіння: часто – закладеність носа; нечасто – задишка, носова кровотеча. Порушення з боку шлунково-кишкового тракту: часто – диспепсія, гастроезофагеальний рефлюкс; нечасто – біль у животі. Порушення з боку шкіри та підшкірної клітковини: нечасто – висип, гіпергідроз (підвищена пітливість); рідко – кропив'янка, синдром Стівенса-Джонсона3, ексфоліативний дерматит3. Порушення з боку скелетно-м'язової та сполучної тканини: часто – біль у спині, біль у кінцівках, міалгія. Порушення з боку нирок та сечовивідних шляхів: часто – гематурія. Порушення з боку статевих органів та молочної залози: нечасто – кровотеча зі статевого члена, гемоспермія; рідко - тривала ерекція, пріапізм3. Загальні розлади та порушення у місці введення: нечасто – біль у грудній клітці1; рідко – набряк особи3, раптова серцева смерть1,3. 1 Спостерігалися у пацієнтів, які раніше мали серцево-судинні фактори ризику. Однак неможливо точно визначити, пов'язані ці явища безпосередньо з цими факторами ризику, з тадалафілом, із сексуальним збудженням або з комбінацією цих чи інших факторів. 2 Про раптову втрату слуху повідомлялося в невеликій кількості випадків під час постмаркетингових та клінічних досліджень при застосуванні всіх ФДЕ-5 інгібіторів, включаючи тадалафіл. 3 Побічні реакції, виявлені в ході постмаркетингових досліджень, які не спостерігалися в ході клінічних плацебо-контрольованих досліджень.Взаємодія з лікарськими засобамиБезпека та ефективність комбінації тадалафілу з іншими видами лікування порушень ерекції не вивчалися, тому застосування таких комбінацій не рекомендується. Вплив інших препаратів на тадалафіл Тадалафіл здебільшого метаболізується за участю ізоферменту CYP3A4. Селективний інгібітор ізоферменту CYP3A4 кетоконазол у дозі 400 мг/добу збільшує AUC тадалафілу (20 мг) у 4 рази та Сmах на 22%, а кетоконазол у дозі 200 мг/добу збільшує AUC тадалафілу (10 мг) у 2 рази щодо AUC та Сmах тільки для тадалафілу. Ритонавір (200 мг 2 рази на добу), інгібітор ізоферментів CYP3A4, CYP2C9, CYP2C19 та CYP2D6, збільшує AUC тадалафілу (20 мг) в 2 рази без зміни Сmах. Незважаючи на те, що специфічні взаємодії не вивчалися, можна припустити, що інші інгібітори ВІЛ-протеази, наприклад, саквінавір, та інгібітори ізоферменту CYP3A4, такі як еритроміцин, кларитроміцин та ітраконазол, а також грейпфрутовий сік, обережністю (через підвищення ризику розвитку небажаних реакцій). Селективний індуктор ізоферменту CYP3A4 рифампіцин (600 мг на добу) знижує AUC тадалафілу (10 мг) на 88% та Сmах на 46% щодо цих величин для тадалафілу окремо. Можна припускати, що одночасне застосування інших індукторів ізоферменту CYP3A4 (таких як фенобарбітал, фенітої та карбамазепін) також знижує плазмові концентрації тадалафілу. Одночасний прийом антациду (магнію гідроксид/алюмінію гідроксид) та тадалафілу знижує швидкість всмоктування тадалафілу без зміни його AUC. Вплив тадалафілу на інші препарати Відомо, що тадалафіл посилює гіпотензивну дію нітратів. Це відбувається в результаті адитивної дії нітратів та тадалафілу на метаболізм оксиду азоту II (NО) та цГМФ. Тому застосування тадалафілу на фоні нітратів протипоказано. Одночасне застосування тадалафілу із доксазозином протипоказане. При одночасному застосуванні тадалафілу (5 мг на добу) здоровими добрбвейбцями та альфа-адреноблокаторами доксазозину (4-8 мг на добу) спостерігалося посилення гіпотензивної дії доксазозину. Деякі пацієнти відчували симптоми, пов'язані зі зниженням АТ, включаючи непритомність, протягом 12 год. В обмеженій кількості досліджень не спостерігалося значного зниження артеріального тиску при застосуванні тадалафілу здоровими добровольцями, які приймали селективні альфа-адреноблокатори (тамсулозин. алфузозин). Незважаючи на це такі комбінації слід застосовувати з обережністю, починати з мінімальної дози альфа-адреноблокатора з поступовим її підвищенням. У доклінічних та клінічних дослідженнях було показано значне посилення гіпотензивного ефекту при одночасному застосуванні інгібіторів ФДЕ-5 та ріоцигуату (стимулятор гуанілатциклази), тому прийом такої комбінації препаратів протипоказаний. Тадалафіл має системні судинорозширюючі властивості і може посилювати дію гіпотензивних засобів, спрямоване на зниження артеріального тиску. Вивчалися препарати наступних груп гіпотензивних препаратів: блокатори "повільних" кальцієвих каналів (амлодипін), інгібітори ангіотензинперетворюючого ферменту (еналаприл), бета-адреноблокатори (метопролол), тіазидні діуретики (бендофлуазид), блокатори рецепторів. Додатково у пацієнтів з погано контрольованою артеріальною гіпертензією, які приймали кілька гіпотензивних засобів, спостерігалося дещо більше зниження артеріального тиску. Переважна більшість пацієнтів це зниження був пов'язані з розвитком гипотензивных симптомів. Пацієнтам, які отримують лікування гіпотензивними препаратами та приймають тадалафіл, повинні бути надані відповідні клінічні рекомендації. При одночасному застосуванні тадалафілу та фінастериду (інгібітор 5-альфа-редуктази) не спостерігалося зміни профілю небажаних реакцій порівняно із застосуванням комбінації плацебо + фінастерид, проте при прийомі цих препаратів слід бути обережним через недостатню кількість клінічних даних. Дослідження підтвердили, що тадалафіл не інгібує та не індукує ізоферменти системи цитохрому Р450 CYP1A2, CYP3A4, CYP2C9, CYP2C19, CYP2D6, CYP2E1. Тадалафіл не має клінічно значущого ефекту на фармакокінетику або фармакодинаміку теофіліну (субстрат CYP1A2), не впливає на AUC S-варфарину або R-варфарину (субстрати CYP2C9) і не змінює протромбіновий час при одночасному прийомі з варфарином. Тадалафіл (10 мг, 20 мг) не збільшує тривалість кровотечі, що викликається ацетилсаліцилової кислотою (АСК). Біодоступність етинілестрадіолу та тербуталіну при прийомі внутрішньо разом з тадалафілом підвищується, проте клінічне значення такої взаємодії не визначено. Тадалафіл не впливає на концентрацію алкоголю, так само як і алкоголь не впливає на концентрацію тадалафілу. При високих дозах алкоголю (0,7 г/кг) прийом тадалафілу не викликав статистично значущого зниження середньої АТ. У деяких пацієнтів спостерігалися постуральне запаморочення та ортостатична гіпотензія. При прийомі тадалафілу у поєднанні з нижчими дозами алкоголю (0,6 г/кг) зниження АТ не спостерігалося, а запаморочення виникало з такою самою частотою, що при прийомі алкоголю окремо. Вивчення взаємодій між тадалафілом та препаратами для лікування цукрового діабету не проводилося.Спосіб застосування та дозиДля прийому всередину. Застосування препарату при ЕД Для пацієнтів з частою сексуальною активністю (більше двох разів на тиждень) рекомендована частота прийому: щодня, 5 мг (1 таблетка) 1 раз на добу, одночасно, незалежно від їди. Доза повинна періодично контролюватись і переглядатися, за необхідності. Добова доза може бути знижена до 2,5 мг, залежно від індивідуальної чутливості. Для пацієнтів з нечастою сексуальною активністю (рідше двох разів на тиждень) рекомендована частота прийому: 20 мг (1 таблетка або 4 таблетки у дозі 5 мг) безпосередньо перед сексуальною активністю згідно з інструкцією з медичного застосування. Максимальна добова доза становить 20 мг. Застосування препарату при ДГПЗ або ЕД + ДГПЗ Рекомендована доза препарату становить 5 мг (1 таблетка) 1 раз на добу. Препарат слід приймати приблизно в один і той же час дня, незалежно від їди та часу сексуальної активності. Тривалість лікування встановлюється лікарем індивідуально. У пацієнтів з нирковою недостатністю тяжкого ступеня (КК У пацієнтів з нирковою недостатністю легкої (КК 51 -80 мл/хв) та середнього ступеня тяжкості (КК 31-50 мл/хв) або печінковою недостатністю легкого та середнього ступеня тяжкості (класи А та В за класифікацією Чайлд-П'ю), а також у літніх пацієнтів корекція дози не потрібна.ПередозуванняПри призначенні тадалафілу одноразово в дозі до 500 мг здоровим особам і багаторазово в дозі до 100 мг на добу пацієнтам з ЕД небажані реакції були зіставні, як і застосування нижчих доз. У разі передозування слід проводити симптоматичне лікування. При гемодіалізі тадалафілу практично не виводиться.Запобіжні заходи та особливі вказівкиДіагностика ЕД та ДГПЗ повинна включати виявлення основної причини захворювання, відповідне медичне обстеження, визначення тактики лікування та індивідуальну оцінку співвідношення користь/ризик. Сексуальна активність має потенційний ризик для пацієнтів із серцево-судинними захворюваннями, тому лікування ЕД не слід проводити у чоловіків із такими захворюваннями серця, при яких сексуальна активність не рекомендована. Як і інші ФДЕ-5 інгібітори, тадалафіл може чинити системну судиннорозширювальну дію, що може призводити до транзиторного зниження АТ та посилення гіпотензивної дії нітратів, альфа-адреноблокаторів (див. розділ "Взаємодія з іншими лікарськими засобами"). Перед призначенням препарату необхідно ретельно оцінити ймовірність виникнення подібних небажаних реакцій у пацієнтів із серцево-судинними захворюваннями. Пацієнти з передбачуваним діагнозом ДГПЗ повинні пройти обстеження для виключення раку передміхурової залози. Неартеріальна передня ішемічна оптична нейропатія (НАПІОН) є причиною порушення зору, включаючи повну втрату зору. Є рідкісні постмаркетингові повідомлення про випадки розвитку НАПІОН, за часом пов'язані з прийомом інгібіторів ФДЕ-5. В даний час неможливо визначити, чи існує прямий зв'язок між розвитком НАПІОН та прийомом інгібіторів ФДЕ-5 або іншими факторами. Необхідно попередити пацієнтів, що у разі раптової втрати зору слід припинити прийом тадалафілу та звернутися за медичною допомогою. Пацієнти також повинні бути проінформовані, що у людей, які перенесли НАПІОН, підвищений ризик повторного розвитку НАПІОН. Є повідомлення про виникнення приапізму при застосуванні інгібіторів ФДЕ-5, включаючи тадалафіл. Пацієнти повинні бути проінформовані про необхідність негайного звернення за медичною допомогою у разі виникнення ерекції, що триває 4 години та більше. Несвоєчасне лікування приапізму веде до пошкодження тканин статевого члена, внаслідок чого може настати необоротна імпотенція. Ефективність препарату у пацієнтів, які перенесли хірургічну операцію на органах малого тазу або радикальну нервозберігаючу простатектомію, невідома. Вплив на здатність до керування автотранспортом та управління механізмами Незважаючи на те, що частота виникнення запаморочення на тлі плацебо і тадалафілу однакова, в період лікування необхідно дотримуватися обережності при керуванні автотранспортом та заняттями іншими потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій. Пацієнти повинні бути обізнані про можливий розвиток сонливості при прийомі препарату, особливо на початку терапії або у поєднанні з алкоголем.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Діюча речовина: тадалафіл – 5,000 мг; Допоміжні речовини: лактози моногідрат (цукор молочний) – 68,325 мг; целюлоза мікрокристалічна – 14,250 мг; кроскармелоза натрію – 6,000 мг; гіпоролоза – 0,665 мг; натрію лаурилсульфат – 0,285 мг; магнію стеарат – 0,475 мг; Склад оболонки: гіпромелоза – 1,450 мг; макрогол-4000 – 0,425 мг; титану діоксид – 0,575 мг; барвник заліза оксид жовтий – 0,050 мг. Пігулки, покриті плівковою оболонкою 5 мг. По 1, 2, 10, 14 або 28 таблеток у контурне осередкове пакування з плівки полівінілхлоридної та фольги алюмінієвої друкованої лакованої. По 8, 10, 14, 20, 28, 30, 40, 50 або 100 таблеток у банки з поліетилентерефталату для лікарських засобів або поліпропіленові для лікарських засобів, закупорені кришками з поліетилену високого тиску з контролем першого розкриття, або кришками поліпропілен -повернути" або кришками з поліетилену низького тиску з контролем першого розтину. Одну банку або 1, 2, 3, 4, 5 або 10 контурних осередкових упаковок разом з інструкцією із застосування поміщають у картонну упаковку (пачку). Допускається комплектація по 2 або 3 картонні упаковки (пачки) до групового упаковки (транспортної тари) з картону для споживчої тари.Опис лікарської формиКруглі, двоопуклі таблетки з ризиком, покриті плівковою оболонкою від світло-жовтого до коричнево-жовтого кольору. На поперечному розрізі видно два шари: ядро білого або майже білого кольору та плівкова оболонка.Фармакотерапевтична групаЕректильна дисфункція Засіб лікування - ФДЕ5-інгібітор.ФармакокінетикаВсмоктування Після прийому внутрішньо тадалафіл швидко всмоктується. Середня максимальна концентрація (Сmах) у плазмі крові досягається в середньому через 2 години після прийому внутрішньо. Швидкість і ступінь всмоктування тадалафілу не залежать від їди, тому препарат можна застосовувати незалежно від їди. Час прийому (вранці або ввечері) не має клінічно значущого ефекту на швидкість та ступінь всмоктування. Фармакокінетика тадалафілу у здорових добровольців лінійна щодо часу та дози. У діапазоні доз від 2,5 до 20 мг площа під кривою "концентрація-час" (AUC) збільшується пропорційно дозі. Рівноважні концентрації в плазмі досягаються протягом 5 днів при прийомі препарату 1 раз на добу. Фармакокінетика тадалафілу у пацієнтів з порушенням ерекції аналогічна фармакокінетиці препарату у пацієнтів без порушення ерекції. Розподіл Середній обсяг розподілу становить близько 63 л, що свідчить про те, що тадалафіл розподіляється у тканинах організму. У терапевтичних концентраціях 94% тадалафілу пов'язують із білками плазми крові. Зв'язування з білками плазми не змінюється при порушеній функції нирок. У здорових добровольців менше 0,0005% введеної дози виявлено у спермі. Метаболізм Тадалафіл переважно метаболізується за участю ізоферменту CYP3A4 цитохрому Р450. Основним циркулюючим метаболітом є метилкатехолглюкуронід. Цей метаболіт принаймні у 13000 разів менш активний щодо ФДЕ-5, ніж тадалафіл. Отже, концентрація цього метаболіту не є клінічно значущою. Виведення У здорових добровольців середній кліренс тадалафілу при прийомі внутрішньо становить 2,5 л/год, а середній період напіввиведення (Т1/2) – 17,5 год. Тадалафіл виводиться переважно у вигляді неактивних метаболітів, переважно кишечником (близько 61 % дози). і, меншою мірою, нирками (близько 36% дози). Літні пацієнти Здорові літні добровольці (65 років і старше) мали нижчий кліренс тадалафілу при прийомі внутрішньо, що виражалося у збільшенні AUC на 25% зі здоровими добровольцями у віці від 19 до 45 років. Ця відмінність не є клінічно значущою і не потребує добору дози. Пацієнти з нирковою недостатністю У клінічних дослідженнях показано, що при прийомі одиничної дози тадалафілу (5-20 мг) AUC збільшується приблизно у 2 рази у пацієнтів з легкою (кліренс креатиніну (КК) 51-80 мл/хв), середньою (КК 31-50 мл/хв.) ) та термінальною нирковою недостатністю (проведення діалізу). У пацієнтів на гемодіалізі Сmах тадалафілу на 41% вище, ніж у здорових добровольців. Тадалафіл практично не виводиться при гемодіалізі. Пацієнти з печінковою недостатністю Фармакокінетика тадалафілу у пацієнтів з легкою та середньотяжкою печінковою недостатністю (класи А та В за класифікацією Чайлд-П'ю) можна порівняти з такою у здорових добровольців. Щодо пацієнтів з тяжкою печінковою недостатністю (клас С за класифікацією Чайлд-П'ю) дані обмежені, тому перед застосуванням препарату необхідно проводити оцінку співвідношення користь/ризик. Пацієнти з цукровим діабетом У пацієнтів із цукровим діабетом на фоні застосування тадалафілу AUC менше приблизно на 19%, ніж у здорових добровольців. Ця відмінність не потребує підбору дози.ФармакодинамікаТадалафіл є оборотним селективним інгібітором специфічної фосфодіестерази 5 типу (ФДЕ-5) циклічного гуанозинмонофосфату (цГМФ). Коли сексуальне збудження викликає місцеве вивільнення оксиду азоту, пригнічення ФДЕ-5 тадалафілом веде до підвищення концентрації цГМФ в печеристому тілі статевого члена. Наслідком цього є розслаблення гладких м'язів артерій та приплив крові до тканин статевого члена, що викликає ерекцію. Дослідження in vitro показали, що тадалафіл є селективним інгібітором ФДЕ-5. ФДЕ-5 є ферментом, представленим у гладкій мускулатурі печеристого тіла, судин та внутрішніх органів, у скелетних м'язах, тромбоцитах, нирках, легенях та мозочку. Дія тадалафілу на ФДЕ-5 є більш активною, ніж на інші фосфодіестерази. Тадалафіл є в 10 000 разів більш потужним щодо ФДЕ-5, ніж щодо інших типів фосфодіестерази (ФДЕ-1, ФДЕ-2, ФДЕ-4 та ФДЕ-7), які локалізуються в серці, головному мозку, кровоносних судинах, печінці. , лейкоцитах та інших органах. Тадалафіл у 10 000 разів активніше блокує ФДЕ-5, ніж ФДЕ-3 – фермент, який виявляється у серці та кровоносних судинах. Ця селективність щодо ФДЕ-5 у порівнянні з ФДЕ-3 має важливе значення, оскільки ФДЕ-3 є ферментом,беруть участь у скороченні серцевого м'яза. Крім того, тадалафіл приблизно в 700 разів активніше щодо ФДЕ-5, ніж ФДЕ-6, виявленої в сітківці і відповідає за фотопередачу. Дія тадалафілу щодо ФДЕ-5 у 9000 разів більш виражена, ніж його вплив на ФДЕ-8, ФДЕ-9 та ФДЕ-10, та у 14 разів більш виражене, ніж на ФДЕ-11. Розподіл у тканинах та фізіологічні ефекти інгібування ФДЕ-8 – ФДЕ-11 дотепер не з'ясовані.Розподіл у тканинах та фізіологічні ефекти інгібування ФДЕ-8 – ФДЕ-11 дотепер не з'ясовані.Розподіл у тканинах та фізіологічні ефекти інгібування ФДЕ-8 – ФДЕ-11 дотепер не з'ясовані. Тадалафіл у здорових добровольців не викликає достовірної зміни систолічного та діастолічного артеріального тиску в порівнянні з плацебо у положенні лежачи (середнє максимальне зниження становить 1,6 та 0,8 мм рт. ст. відповідно) та у положенні стоячи (середнє максимальне зниження становить 0, 2 і 4,6 мм рт.ст., відповідно). Тадалафіл не викликає достовірної зміни частоти серцевих скорочень. Тадалафіл не викликає змін розпізнавання кольорів (блакитний/зелений), що пояснюється його низькою спорідненістю з ФДЕ-6. Крім того, не спостерігається вплив тадалафілу на гостроту зору, електроретинограму, внутрішньоочний тиск та розмір зіниці. З метою оцінки впливу щоденного прийому тадалафілу на сперматогенез було проведено декілька досліджень. У жодному з досліджень не спостерігалося небажаного впливу на морфологію сперматозоїдів та їхню рухливість. В одному з досліджень було виявлено зниження середньої концентрації сперматозоїдів у порівнянні із плацебо. Зниження концентрації сперматозоїдів пов'язано з вищою частотою еякуляції. Крім того, при порівнянні тадалафілу з плацебо не спостерігалося небажаного впливу на середню концентрацію статевих гормонів (тестостерону, лютеїнізуючого гормону та фолікулостимулюючого гормону). Еректильна дисфункція (ЕД) У проведених дослідженнях тадалафіл показав статистично значуще покращення еректильної функції та можливості проведення повноцінного статевого акту. Тадалафіл не має ефекту у відсутності сексуального збудження. Ефективність та безпека тадалафілу вивчалась у ході клінічних досліджень. Було відмічено покращення ерекції у пацієнтів з ЕД усіх ступенів тяжкості при прийомі 5 мг тадалафілу 1 раз на добу протягом 36 годин після прийому, а також підтримання ерекції протягом 16 хв після прийому порівняно з плацебо. У дослідженнях первинної ефективності застосування 5 мг тадалафілу 57% та 67% спроб статевого акту були успішними порівняно з 31% та 37% при прийомі плацебо. У дослідженнях пацієнтів із вторинною ЕД на тлі цукрового діабету 41% спроб статевого акту були успішними порівняно з 28% при прийомі плацебо. Доброякісна гіперплазія передміхурової залози (ДГПЗ) У пацієнтів з ДГПЗ тадалафіл, інгібуючи ФДЕ-5, призводить до підвищення концентрації цГМФ не тільки в печеристому тілі статевого члена, а й у гладкій мускулатурі передміхурової залози, сечового міхура та судинах, що їх кровопостачають. Це своє чергу збільшує перфузію крові у цих органах як наслідок, зменшує вираженість симптомів ДГПЖ. Розслаблення гладкої мускулатури передміхурової залози та сечового міхура та інгібування аферентної іннервації сечового міхура можуть додатково посилювати судинні ефекти. У ході клінічних досліджень було показано зменшення симптомів ДГПЗ протягом 1 тижня після прийому 5 мг тадалафілу проти плацебо. У дослідженнях, що включають пацієнтів з ЕД та симптомами ДГПЗ, при застосуванні 5 мг тадалафілу 71,9% спроб статевого акту були успішними порівняно з 48,3% при прийомі плацебо, та спостерігалося значне покращення еректильної функції та зменшення симптомів з боку передміхурової залози.Показання до застосуванняЕректильна дисфункція; симптоми з боку нижніх сечовивідних шляхів у пацієнтів із ДГПЗ (для дозування 5 мг); еректильна дисфункція у пацієнтів із симптомами з боку сечовивідних шляхів у пацієнтів із ДГПЗ (для дозування 5 мг).Протипоказання до застосуванняПідвищена чутливість до тадалафілу або будь-якої речовини, що входить до складу препарату; прийом препаратів, що містять будь-які органічні нітрати; дитячий вік до 18 років; наявність протипоказань до сексуальної активності у пацієнтів із захворюваннями серцево-судинної системи: інфаркт міокарда протягом останніх 90 днів, нестабільна стенокардія, виникнення нападу стенокардії під час статевого акту, хронічна серцева недостатність II-IV класів за класифікацією NYHA, неконтрольована аритмія АТ втрата зору внаслідок неартеріальної передньої ішемічної нейропатії зорового нерва (незалежно від зв'язку з прийомом інгібіторів ФДЕ-5); одночасний прийом доксазозину, інших лікарських засобів для лікування еректильної дисфункції, стимуляторів гуанілатциклази (ріоцигуат); застосування у пацієнтів з тяжкою нирковою недостатністю (КК дефіцит лактази, непереносимість лактози, глюкозо-галактозна мальабсорбція. З обережністю: Тяжка печінкова недостатність (клас С за класифікацією Чайлд-П'ю) через недостатню кількість даних щодо ефективності/безпеки препарату; одночасне застосування селективних альфа-адреноблокаторів, сильних інгібіторів ізоферменту CYP3A4 (ритонавір, саквінавір, кетоконазол, ітраконазол, еритроміцин), інгібіторів 5-альфа-редуктази; схильність до приапізму (при серповидно-клітинній анемії, множинні мієломи або лейкозі), анатомічна деформація статевого члена (кутове викривлення, кавернозний фіброз або хвороба Пейроні).Вагітність та лактаціяПрепарат не призначений для застосування у жінок.Побічна діяЗа даними Всесвітньої Організації Охорони Здоров'я (ВООЗ), небажані реакції класифіковані відповідно до їх частоти розвитку наступним чином: дуже часто (≥1/10), часто (≥1/100, Порушення з боку імунної системи: нечасто – реакції гіперчутливості; рідко – ангіоневротичний отек3. Порушення з боку нервової системи: часто – головний біль; нечасто – запаморочення; рідко – інсульт1 (в т.ч. геморагічний), транзиторні ішемічні атаки1, непритомність, мігрень3, епілептичний напад, транзиторна амнезія. Порушення з боку органу зору: нечасто – нечіткість зорового сприйняття, больові відчуття у очному яблуку; рідко - порушення полів зору, припухлість повік, ін'єкція судин склери, неартеріальна передня ішемічна оптична нейропатія3, оклюзія судин сітківки3. Порушення з боку органу слуху та лабіринтні порушення: нечасто - шум/дзвін у вухах; рідко – раптова втрата слуха2. Порушення з боку серця1: нечасто – відчуття серцебиття, тахікардія; рідко – інфаркт міокарда, шлуночкові порушення ритму3, нестабільна стенокардія3. Порушення з боку судин: часто – "припливи" крові; нечасто – зниження артеріального тиску (АТ) (у пацієнтів, які приймають гіпотензивні засоби), підвищення АТ. Порушення з боку дихальної системи, органів грудної клітки та середостіння: часто – закладеність носа; нечасто – задишка, носова кровотеча. Порушення з боку шлунково-кишкового тракту: часто – диспепсія, гастроезофагеальний рефлюкс; нечасто – біль у животі. Порушення з боку шкіри та підшкірної клітковини: нечасто – висип, гіпергідроз (підвищена пітливість); рідко – кропив'янка, синдром Стівенса-Джонсона3, ексфоліативний дерматит3. Порушення з боку скелетно-м'язової та сполучної тканини: часто – біль у спині, біль у кінцівках, міалгія. Порушення з боку нирок та сечовивідних шляхів: часто – гематурія. Порушення з боку статевих органів та молочної залози: нечасто – кровотеча зі статевого члена, гемоспермія; рідко - тривала ерекція, пріапізм3. Загальні розлади та порушення у місці введення: нечасто – біль у грудній клітці1; рідко – набряк особи3, раптова серцева смерть1,3. 1 Спостерігалися у пацієнтів, які раніше мали серцево-судинні фактори ризику. Однак неможливо точно визначити, пов'язані ці явища безпосередньо з цими факторами ризику, з тадалафілом, із сексуальним збудженням або з комбінацією цих чи інших факторів. 2 Про раптову втрату слуху повідомлялося в невеликій кількості випадків під час постмаркетингових та клінічних досліджень при застосуванні всіх ФДЕ-5 інгібіторів, включаючи тадалафіл. 3 Побічні реакції, виявлені в ході постмаркетингових досліджень, які не спостерігалися в ході клінічних плацебо-контрольованих досліджень.Взаємодія з лікарськими засобамиБезпека та ефективність комбінації тадалафілу з іншими видами лікування порушень ерекції не вивчалися, тому застосування таких комбінацій не рекомендується. Вплив інших препаратів на тадалафіл Тадалафіл здебільшого метаболізується за участю ізоферменту CYP3A4. Селективний інгібітор ізоферменту CYP3A4 кетоконазол у дозі 400 мг/добу збільшує AUC тадалафілу (20 мг) у 4 рази та Сmах на 22%, а кетоконазол у дозі 200 мг/добу збільшує AUC тадалафілу (10 мг) у 2 рази щодо AUC та Сmах тільки для тадалафілу. Ритонавір (200 мг 2 рази на добу), інгібітор ізоферментів CYP3A4, CYP2C9, CYP2C19 та CYP2D6, збільшує AUC тадалафілу (20 мг) в 2 рази без зміни Сmах. Незважаючи на те, що специфічні взаємодії не вивчалися, можна припустити, що інші інгібітори ВІЛ-протеази, наприклад, саквінавір, та інгібітори ізоферменту CYP3A4, такі як еритроміцин, кларитроміцин та ітраконазол, а також грейпфрутовий сік, обережністю (через підвищення ризику розвитку небажаних реакцій). Селективний індуктор ізоферменту CYP3A4 рифампіцин (600 мг на добу) знижує AUC тадалафілу (10 мг) на 88% та Сmах на 46% щодо цих величин для тадалафілу окремо. Можна припускати, що одночасне застосування інших індукторів ізоферменту CYP3A4 (таких як фенобарбітал, фенітої та карбамазепін) також знижує плазмові концентрації тадалафілу. Одночасний прийом антациду (магнію гідроксид/алюмінію гідроксид) та тадалафілу знижує швидкість всмоктування тадалафілу без зміни його AUC. Вплив тадалафілу на інші препарати Відомо, що тадалафіл посилює гіпотензивну дію нітратів. Це відбувається в результаті адитивної дії нітратів та тадалафілу на метаболізм оксиду азоту II (NО) та цГМФ. Тому застосування тадалафілу на фоні нітратів протипоказано. Одночасне застосування тадалафілу із доксазозином протипоказане. При одночасному застосуванні тадалафілу (5 мг на добу) здоровими добрбвейбцями та альфа-адреноблокаторами доксазозину (4-8 мг на добу) спостерігалося посилення гіпотензивної дії доксазозину. Деякі пацієнти відчували симптоми, пов'язані зі зниженням АТ, включаючи непритомність, протягом 12 год. В обмеженій кількості досліджень не спостерігалося значного зниження артеріального тиску при застосуванні тадалафілу здоровими добровольцями, які приймали селективні альфа-адреноблокатори (тамсулозин. алфузозин). Незважаючи на це такі комбінації слід застосовувати з обережністю, починати з мінімальної дози альфа-адреноблокатора з поступовим її підвищенням. У доклінічних та клінічних дослідженнях було показано значне посилення гіпотензивного ефекту при одночасному застосуванні інгібіторів ФДЕ-5 та ріоцигуату (стимулятор гуанілатциклази), тому прийом такої комбінації препаратів протипоказаний. Тадалафіл має системні судинорозширюючі властивості і може посилювати дію гіпотензивних засобів, спрямоване на зниження артеріального тиску. Вивчалися препарати наступних груп гіпотензивних препаратів: блокатори "повільних" кальцієвих каналів (амлодипін), інгібітори ангіотензинперетворюючого ферменту (еналаприл), бета-адреноблокатори (метопролол), тіазидні діуретики (бендофлуазид), блокатори рецепторів. Додатково у пацієнтів з погано контрольованою артеріальною гіпертензією, які приймали кілька гіпотензивних засобів, спостерігалося дещо більше зниження артеріального тиску. Переважна більшість пацієнтів це зниження був пов'язані з розвитком гипотензивных симптомів. Пацієнтам, які отримують лікування гіпотензивними препаратами та приймають тадалафіл, повинні бути надані відповідні клінічні рекомендації. При одночасному застосуванні тадалафілу та фінастериду (інгібітор 5-альфа-редуктази) не спостерігалося зміни профілю небажаних реакцій порівняно із застосуванням комбінації плацебо + фінастерид, проте при прийомі цих препаратів слід бути обережним через недостатню кількість клінічних даних. Дослідження підтвердили, що тадалафіл не інгібує та не індукує ізоферменти системи цитохрому Р450 CYP1A2, CYP3A4, CYP2C9, CYP2C19, CYP2D6, CYP2E1. Тадалафіл не має клінічно значущого ефекту на фармакокінетику або фармакодинаміку теофіліну (субстрат CYP1A2), не впливає на AUC S-варфарину або R-варфарину (субстрати CYP2C9) і не змінює протромбіновий час при одночасному прийомі з варфарином. Тадалафіл (10 мг, 20 мг) не збільшує тривалість кровотечі, що викликається ацетилсаліцилової кислотою (АСК). Біодоступність етинілестрадіолу та тербуталіну при прийомі внутрішньо разом з тадалафілом підвищується, проте клінічне значення такої взаємодії не визначено. Тадалафіл не впливає на концентрацію алкоголю, так само як і алкоголь не впливає на концентрацію тадалафілу. При високих дозах алкоголю (0,7 г/кг) прийом тадалафілу не викликав статистично значущого зниження середньої АТ. У деяких пацієнтів спостерігалися постуральне запаморочення та ортостатична гіпотензія. При прийомі тадалафілу у поєднанні з нижчими дозами алкоголю (0,6 г/кг) зниження АТ не спостерігалося, а запаморочення виникало з такою самою частотою, що при прийомі алкоголю окремо. Вивчення взаємодій між тадалафілом та препаратами для лікування цукрового діабету не проводилося.Спосіб застосування та дозиДля прийому всередину. Застосування препарату при ЕД Для пацієнтів з частою сексуальною активністю (більше двох разів на тиждень) рекомендована частота прийому: щодня, 5 мг (1 таблетка) 1 раз на добу, одночасно, незалежно від їди. Доза повинна періодично контролюватись і переглядатися, за необхідності. Добова доза може бути знижена до 2,5 мг, залежно від індивідуальної чутливості. Для пацієнтів з нечастою сексуальною активністю (рідше двох разів на тиждень) рекомендована частота прийому: 20 мг (1 таблетка або 4 таблетки у дозі 5 мг) безпосередньо перед сексуальною активністю згідно з інструкцією з медичного застосування. Максимальна добова доза становить 20 мг. Застосування препарату при ДГПЗ або ЕД + ДГПЗ Рекомендована доза препарату становить 5 мг (1 таблетка) 1 раз на добу. Препарат слід приймати приблизно в один і той же час дня, незалежно від їди та часу сексуальної активності. Тривалість лікування встановлюється лікарем індивідуально. У пацієнтів з нирковою недостатністю тяжкого ступеня (КК У пацієнтів з нирковою недостатністю легкої (КК 51 -80 мл/хв) та середнього ступеня тяжкості (КК 31-50 мл/хв) або печінковою недостатністю легкого та середнього ступеня тяжкості (класи А та В за класифікацією Чайлд-П'ю), а також у літніх пацієнтів корекція дози не потрібна.ПередозуванняПри призначенні тадалафілу одноразово в дозі до 500 мг здоровим особам і багаторазово в дозі до 100 мг на добу пацієнтам з ЕД небажані реакції були зіставні, як і застосування нижчих доз. У разі передозування слід проводити симптоматичне лікування. При гемодіалізі тадалафілу практично не виводиться.Запобіжні заходи та особливі вказівкиДіагностика ЕД та ДГПЗ повинна включати виявлення основної причини захворювання, відповідне медичне обстеження, визначення тактики лікування та індивідуальну оцінку співвідношення користь/ризик. Сексуальна активність має потенційний ризик для пацієнтів із серцево-судинними захворюваннями, тому лікування ЕД не слід проводити у чоловіків із такими захворюваннями серця, при яких сексуальна активність не рекомендована. Як і інші ФДЕ-5 інгібітори, тадалафіл може чинити системну судиннорозширювальну дію, що може призводити до транзиторного зниження АТ та посилення гіпотензивної дії нітратів, альфа-адреноблокаторів (див. розділ "Взаємодія з іншими лікарськими засобами"). Перед призначенням препарату необхідно ретельно оцінити ймовірність виникнення подібних небажаних реакцій у пацієнтів із серцево-судинними захворюваннями. Пацієнти з передбачуваним діагнозом ДГПЗ повинні пройти обстеження для виключення раку передміхурової залози. Неартеріальна передня ішемічна оптична нейропатія (НАПІОН) є причиною порушення зору, включаючи повну втрату зору. Є рідкісні постмаркетингові повідомлення про випадки розвитку НАПІОН, за часом пов'язані з прийомом інгібіторів ФДЕ-5. В даний час неможливо визначити, чи існує прямий зв'язок між розвитком НАПІОН та прийомом інгібіторів ФДЕ-5 або іншими факторами. Необхідно попередити пацієнтів, що у разі раптової втрати зору слід припинити прийом тадалафілу та звернутися за медичною допомогою. Пацієнти також повинні бути проінформовані, що у людей, які перенесли НАПІОН, підвищений ризик повторного розвитку НАПІОН. Є повідомлення про виникнення приапізму при застосуванні інгібіторів ФДЕ-5, включаючи тадалафіл. Пацієнти повинні бути проінформовані про необхідність негайного звернення за медичною допомогою у разі виникнення ерекції, що триває 4 години та більше. Несвоєчасне лікування приапізму веде до пошкодження тканин статевого члена, внаслідок чого може настати необоротна імпотенція. Ефективність препарату у пацієнтів, які перенесли хірургічну операцію на органах малого тазу або радикальну нервозберігаючу простатектомію, невідома. Вплив на здатність до керування автотранспортом та управління механізмами Незважаючи на те, що частота виникнення запаморочення на тлі плацебо і тадалафілу однакова, в період лікування необхідно дотримуватися обережності при керуванні автотранспортом та заняттями іншими потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій. Пацієнти повинні бути обізнані про можливий розвиток сонливості при прийомі препарату, особливо на початку терапії або у поєднанні з алкоголем.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Діюча речовина: тадалафіл – 5,000 мг; Допоміжні речовини: лактози моногідрат (цукор молочний) – 68,325 мг; целюлоза мікрокристалічна – 14,250 мг; кроскармелоза натрію – 6,000 мг; гіпоролоза – 0,665 мг; натрію лаурилсульфат – 0,285 мг; магнію стеарат – 0,475 мг; Склад оболонки: гіпромелоза – 1,450 мг; макрогол-4000 – 0,425 мг; титану діоксид – 0,575 мг; барвник заліза оксид жовтий – 0,050 мг. Пігулки, покриті плівковою оболонкою 5 мг. По 1, 2, 10, 14 або 28 таблеток у контурне осередкове пакування з плівки полівінілхлоридної та фольги алюмінієвої друкованої лакованої. По 8, 10, 14, 20, 28, 30, 40, 50 або 100 таблеток у банки з поліетилентерефталату для лікарських засобів або поліпропіленові для лікарських засобів, закупорені кришками з поліетилену високого тиску з контролем першого розкриття, або кришками поліпропілен -повернути" або кришками з поліетилену низького тиску з контролем першого розтину. Одну банку або 1, 2, 3, 4, 5 або 10 контурних осередкових упаковок разом з інструкцією із застосування поміщають у картонну упаковку (пачку). Допускається комплектація по 2 або 3 картонні упаковки (пачки) до групового упаковки (транспортної тари) з картону для споживчої тари.Опис лікарської формиКруглі, двоопуклі таблетки з ризиком, покриті плівковою оболонкою від світло-жовтого до коричнево-жовтого кольору. На поперечному розрізі видно два шари: ядро білого або майже білого кольору та плівкова оболонка.Фармакотерапевтична групаЕректильна дисфункція Засіб лікування - ФДЕ5-інгібітор.ФармакокінетикаВсмоктування Після прийому внутрішньо тадалафіл швидко всмоктується. Середня максимальна концентрація (Сmах) у плазмі крові досягається в середньому через 2 години після прийому внутрішньо. Швидкість і ступінь всмоктування тадалафілу не залежать від їди, тому препарат можна застосовувати незалежно від їди. Час прийому (вранці або ввечері) не має клінічно значущого ефекту на швидкість та ступінь всмоктування. Фармакокінетика тадалафілу у здорових добровольців лінійна щодо часу та дози. У діапазоні доз від 2,5 до 20 мг площа під кривою "концентрація-час" (AUC) збільшується пропорційно дозі. Рівноважні концентрації в плазмі досягаються протягом 5 днів при прийомі препарату 1 раз на добу. Фармакокінетика тадалафілу у пацієнтів з порушенням ерекції аналогічна фармакокінетиці препарату у пацієнтів без порушення ерекції. Розподіл Середній обсяг розподілу становить близько 63 л, що свідчить про те, що тадалафіл розподіляється у тканинах організму. У терапевтичних концентраціях 94% тадалафілу пов'язують із білками плазми крові. Зв'язування з білками плазми не змінюється при порушеній функції нирок. У здорових добровольців менше 0,0005% введеної дози виявлено у спермі. Метаболізм Тадалафіл переважно метаболізується за участю ізоферменту CYP3A4 цитохрому Р450. Основним циркулюючим метаболітом є метилкатехолглюкуронід. Цей метаболіт принаймні у 13000 разів менш активний щодо ФДЕ-5, ніж тадалафіл. Отже, концентрація цього метаболіту не є клінічно значущою. Виведення У здорових добровольців середній кліренс тадалафілу при прийомі внутрішньо становить 2,5 л/год, а середній період напіввиведення (Т1/2) – 17,5 год. Тадалафіл виводиться переважно у вигляді неактивних метаболітів, переважно кишечником (близько 61 % дози). і, меншою мірою, нирками (близько 36% дози). Літні пацієнти Здорові літні добровольці (65 років і старше) мали нижчий кліренс тадалафілу при прийомі внутрішньо, що виражалося у збільшенні AUC на 25% зі здоровими добровольцями у віці від 19 до 45 років. Ця відмінність не є клінічно значущою і не потребує добору дози. Пацієнти з нирковою недостатністю У клінічних дослідженнях показано, що при прийомі одиничної дози тадалафілу (5-20 мг) AUC збільшується приблизно у 2 рази у пацієнтів з легкою (кліренс креатиніну (КК) 51-80 мл/хв), середньою (КК 31-50 мл/хв.) ) та термінальною нирковою недостатністю (проведення діалізу). У пацієнтів на гемодіалізі Сmах тадалафілу на 41% вище, ніж у здорових добровольців. Тадалафіл практично не виводиться при гемодіалізі. Пацієнти з печінковою недостатністю Фармакокінетика тадалафілу у пацієнтів з легкою та середньотяжкою печінковою недостатністю (класи А та В за класифікацією Чайлд-П'ю) можна порівняти з такою у здорових добровольців. Щодо пацієнтів з тяжкою печінковою недостатністю (клас С за класифікацією Чайлд-П'ю) дані обмежені, тому перед застосуванням препарату необхідно проводити оцінку співвідношення користь/ризик. Пацієнти з цукровим діабетом У пацієнтів із цукровим діабетом на фоні застосування тадалафілу AUC менше приблизно на 19%, ніж у здорових добровольців. Ця відмінність не потребує підбору дози.ФармакодинамікаТадалафіл є оборотним селективним інгібітором специфічної фосфодіестерази 5 типу (ФДЕ-5) циклічного гуанозинмонофосфату (цГМФ). Коли сексуальне збудження викликає місцеве вивільнення оксиду азоту, пригнічення ФДЕ-5 тадалафілом веде до підвищення концентрації цГМФ в печеристому тілі статевого члена. Наслідком цього є розслаблення гладких м'язів артерій та приплив крові до тканин статевого члена, що викликає ерекцію. Дослідження in vitro показали, що тадалафіл є селективним інгібітором ФДЕ-5. ФДЕ-5 є ферментом, представленим у гладкій мускулатурі печеристого тіла, судин та внутрішніх органів, у скелетних м'язах, тромбоцитах, нирках, легенях та мозочку. Дія тадалафілу на ФДЕ-5 є більш активною, ніж на інші фосфодіестерази. Тадалафіл є в 10 000 разів більш потужним щодо ФДЕ-5, ніж щодо інших типів фосфодіестерази (ФДЕ-1, ФДЕ-2, ФДЕ-4 та ФДЕ-7), які локалізуються в серці, головному мозку, кровоносних судинах, печінці. , лейкоцитах та інших органах. Тадалафіл у 10 000 разів активніше блокує ФДЕ-5, ніж ФДЕ-3 – фермент, який виявляється у серці та кровоносних судинах. Ця селективність щодо ФДЕ-5 у порівнянні з ФДЕ-3 має важливе значення, оскільки ФДЕ-3 є ферментом,беруть участь у скороченні серцевого м'яза. Крім того, тадалафіл приблизно в 700 разів активніше щодо ФДЕ-5, ніж ФДЕ-6, виявленої в сітківці і відповідає за фотопередачу. Дія тадалафілу щодо ФДЕ-5 у 9000 разів більш виражена, ніж його вплив на ФДЕ-8, ФДЕ-9 та ФДЕ-10, та у 14 разів більш виражене, ніж на ФДЕ-11. Розподіл у тканинах та фізіологічні ефекти інгібування ФДЕ-8 – ФДЕ-11 дотепер не з'ясовані.Розподіл у тканинах та фізіологічні ефекти інгібування ФДЕ-8 – ФДЕ-11 дотепер не з'ясовані.Розподіл у тканинах та фізіологічні ефекти інгібування ФДЕ-8 – ФДЕ-11 дотепер не з'ясовані. Тадалафіл у здорових добровольців не викликає достовірної зміни систолічного та діастолічного артеріального тиску в порівнянні з плацебо у положенні лежачи (середнє максимальне зниження становить 1,6 та 0,8 мм рт. ст. відповідно) та у положенні стоячи (середнє максимальне зниження становить 0, 2 і 4,6 мм рт.ст., відповідно). Тадалафіл не викликає достовірної зміни частоти серцевих скорочень. Тадалафіл не викликає змін розпізнавання кольорів (блакитний/зелений), що пояснюється його низькою спорідненістю з ФДЕ-6. Крім того, не спостерігається вплив тадалафілу на гостроту зору, електроретинограму, внутрішньоочний тиск та розмір зіниці. З метою оцінки впливу щоденного прийому тадалафілу на сперматогенез було проведено декілька досліджень. У жодному з досліджень не спостерігалося небажаного впливу на морфологію сперматозоїдів та їхню рухливість. В одному з досліджень було виявлено зниження середньої концентрації сперматозоїдів у порівнянні із плацебо. Зниження концентрації сперматозоїдів пов'язано з вищою частотою еякуляції. Крім того, при порівнянні тадалафілу з плацебо не спостерігалося небажаного впливу на середню концентрацію статевих гормонів (тестостерону, лютеїнізуючого гормону та фолікулостимулюючого гормону). Еректильна дисфункція (ЕД) У проведених дослідженнях тадалафіл показав статистично значуще покращення еректильної функції та можливості проведення повноцінного статевого акту. Тадалафіл не має ефекту у відсутності сексуального збудження. Ефективність та безпека тадалафілу вивчалась у ході клінічних досліджень. Було відмічено покращення ерекції у пацієнтів з ЕД усіх ступенів тяжкості при прийомі 5 мг тадалафілу 1 раз на добу протягом 36 годин після прийому, а також підтримання ерекції протягом 16 хв після прийому порівняно з плацебо. У дослідженнях первинної ефективності застосування 5 мг тадалафілу 57% та 67% спроб статевого акту були успішними порівняно з 31% та 37% при прийомі плацебо. У дослідженнях пацієнтів із вторинною ЕД на тлі цукрового діабету 41% спроб статевого акту були успішними порівняно з 28% при прийомі плацебо. Доброякісна гіперплазія передміхурової залози (ДГПЗ) У пацієнтів з ДГПЗ тадалафіл, інгібуючи ФДЕ-5, призводить до підвищення концентрації цГМФ не тільки в печеристому тілі статевого члена, а й у гладкій мускулатурі передміхурової залози, сечового міхура та судинах, що їх кровопостачають. Це своє чергу збільшує перфузію крові у цих органах як наслідок, зменшує вираженість симптомів ДГПЖ. Розслаблення гладкої мускулатури передміхурової залози та сечового міхура та інгібування аферентної іннервації сечового міхура можуть додатково посилювати судинні ефекти. У ході клінічних досліджень було показано зменшення симптомів ДГПЗ протягом 1 тижня після прийому 5 мг тадалафілу проти плацебо. У дослідженнях, що включають пацієнтів з ЕД та симптомами ДГПЗ, при застосуванні 5 мг тадалафілу 71,9% спроб статевого акту були успішними порівняно з 48,3% при прийомі плацебо, та спостерігалося значне покращення еректильної функції та зменшення симптомів з боку передміхурової залози.Показання до застосуванняЕректильна дисфункція; симптоми з боку нижніх сечовивідних шляхів у пацієнтів із ДГПЗ (для дозування 5 мг); еректильна дисфункція у пацієнтів із симптомами з боку сечовивідних шляхів у пацієнтів із ДГПЗ (для дозування 5 мг).Протипоказання до застосуванняПідвищена чутливість до тадалафілу або будь-якої речовини, що входить до складу препарату; прийом препаратів, що містять будь-які органічні нітрати; дитячий вік до 18 років; наявність протипоказань до сексуальної активності у пацієнтів із захворюваннями серцево-судинної системи: інфаркт міокарда протягом останніх 90 днів, нестабільна стенокардія, виникнення нападу стенокардії під час статевого акту, хронічна серцева недостатність II-IV класів за класифікацією NYHA, неконтрольована аритмія АТ втрата зору внаслідок неартеріальної передньої ішемічної нейропатії зорового нерва (незалежно від зв'язку з прийомом інгібіторів ФДЕ-5); одночасний прийом доксазозину, інших лікарських засобів для лікування еректильної дисфункції, стимуляторів гуанілатциклази (ріоцигуат); застосування у пацієнтів з тяжкою нирковою недостатністю (КК дефіцит лактази, непереносимість лактози, глюкозо-галактозна мальабсорбція. З обережністю: Тяжка печінкова недостатність (клас С за класифікацією Чайлд-П'ю) через недостатню кількість даних щодо ефективності/безпеки препарату; одночасне застосування селективних альфа-адреноблокаторів, сильних інгібіторів ізоферменту CYP3A4 (ритонавір, саквінавір, кетоконазол, ітраконазол, еритроміцин), інгібіторів 5-альфа-редуктази; схильність до приапізму (при серповидно-клітинній анемії, множинні мієломи або лейкозі), анатомічна деформація статевого члена (кутове викривлення, кавернозний фіброз або хвороба Пейроні).Вагітність та лактаціяПрепарат не призначений для застосування у жінок.Побічна діяЗа даними Всесвітньої Організації Охорони Здоров'я (ВООЗ), небажані реакції класифіковані відповідно до їх частоти розвитку наступним чином: дуже часто (≥1/10), часто (≥1/100, Порушення з боку імунної системи: нечасто – реакції гіперчутливості; рідко – ангіоневротичний отек3. Порушення з боку нервової системи: часто – головний біль; нечасто – запаморочення; рідко – інсульт1 (в т.ч. геморагічний), транзиторні ішемічні атаки1, непритомність, мігрень3, епілептичний напад, транзиторна амнезія. Порушення з боку органу зору: нечасто – нечіткість зорового сприйняття, больові відчуття у очному яблуку; рідко - порушення полів зору, припухлість повік, ін'єкція судин склери, неартеріальна передня ішемічна оптична нейропатія3, оклюзія судин сітківки3. Порушення з боку органу слуху та лабіринтні порушення: нечасто - шум/дзвін у вухах; рідко – раптова втрата слуха2. Порушення з боку серця1: нечасто – відчуття серцебиття, тахікардія; рідко – інфаркт міокарда, шлуночкові порушення ритму3, нестабільна стенокардія3. Порушення з боку судин: часто – "припливи" крові; нечасто – зниження артеріального тиску (АТ) (у пацієнтів, які приймають гіпотензивні засоби), підвищення АТ. Порушення з боку дихальної системи, органів грудної клітки та середостіння: часто – закладеність носа; нечасто – задишка, носова кровотеча. Порушення з боку шлунково-кишкового тракту: часто – диспепсія, гастроезофагеальний рефлюкс; нечасто – біль у животі. Порушення з боку шкіри та підшкірної клітковини: нечасто – висип, гіпергідроз (підвищена пітливість); рідко – кропив'янка, синдром Стівенса-Джонсона3, ексфоліативний дерматит3. Порушення з боку скелетно-м'язової та сполучної тканини: часто – біль у спині, біль у кінцівках, міалгія. Порушення з боку нирок та сечовивідних шляхів: часто – гематурія. Порушення з боку статевих органів та молочної залози: нечасто – кровотеча зі статевого члена, гемоспермія; рідко - тривала ерекція, пріапізм3. Загальні розлади та порушення у місці введення: нечасто – біль у грудній клітці1; рідко – набряк особи3, раптова серцева смерть1,3. 1 Спостерігалися у пацієнтів, які раніше мали серцево-судинні фактори ризику. Однак неможливо точно визначити, пов'язані ці явища безпосередньо з цими факторами ризику, з тадалафілом, із сексуальним збудженням або з комбінацією цих чи інших факторів. 2 Про раптову втрату слуху повідомлялося в невеликій кількості випадків під час постмаркетингових та клінічних досліджень при застосуванні всіх ФДЕ-5 інгібіторів, включаючи тадалафіл. 3 Побічні реакції, виявлені в ході постмаркетингових досліджень, які не спостерігалися в ході клінічних плацебо-контрольованих досліджень.Взаємодія з лікарськими засобамиБезпека та ефективність комбінації тадалафілу з іншими видами лікування порушень ерекції не вивчалися, тому застосування таких комбінацій не рекомендується. Вплив інших препаратів на тадалафіл Тадалафіл здебільшого метаболізується за участю ізоферменту CYP3A4. Селективний інгібітор ізоферменту CYP3A4 кетоконазол у дозі 400 мг/добу збільшує AUC тадалафілу (20 мг) у 4 рази та Сmах на 22%, а кетоконазол у дозі 200 мг/добу збільшує AUC тадалафілу (10 мг) у 2 рази щодо AUC та Сmах тільки для тадалафілу. Ритонавір (200 мг 2 рази на добу), інгібітор ізоферментів CYP3A4, CYP2C9, CYP2C19 та CYP2D6, збільшує AUC тадалафілу (20 мг) в 2 рази без зміни Сmах. Незважаючи на те, що специфічні взаємодії не вивчалися, можна припустити, що інші інгібітори ВІЛ-протеази, наприклад, саквінавір, та інгібітори ізоферменту CYP3A4, такі як еритроміцин, кларитроміцин та ітраконазол, а також грейпфрутовий сік, обережністю (через підвищення ризику розвитку небажаних реакцій). Селективний індуктор ізоферменту CYP3A4 рифампіцин (600 мг на добу) знижує AUC тадалафілу (10 мг) на 88% та Сmах на 46% щодо цих величин для тадалафілу окремо. Можна припускати, що одночасне застосування інших індукторів ізоферменту CYP3A4 (таких як фенобарбітал, фенітої та карбамазепін) також знижує плазмові концентрації тадалафілу. Одночасний прийом антациду (магнію гідроксид/алюмінію гідроксид) та тадалафілу знижує швидкість всмоктування тадалафілу без зміни його AUC. Вплив тадалафілу на інші препарати Відомо, що тадалафіл посилює гіпотензивну дію нітратів. Це відбувається в результаті адитивної дії нітратів та тадалафілу на метаболізм оксиду азоту II (NО) та цГМФ. Тому застосування тадалафілу на фоні нітратів протипоказано. Одночасне застосування тадалафілу із доксазозином протипоказане. При одночасному застосуванні тадалафілу (5 мг на добу) здоровими добрбвейбцями та альфа-адреноблокаторами доксазозину (4-8 мг на добу) спостерігалося посилення гіпотензивної дії доксазозину. Деякі пацієнти відчували симптоми, пов'язані зі зниженням АТ, включаючи непритомність, протягом 12 год. В обмеженій кількості досліджень не спостерігалося значного зниження артеріального тиску при застосуванні тадалафілу здоровими добровольцями, які приймали селективні альфа-адреноблокатори (тамсулозин. алфузозин). Незважаючи на це такі комбінації слід застосовувати з обережністю, починати з мінімальної дози альфа-адреноблокатора з поступовим її підвищенням. У доклінічних та клінічних дослідженнях було показано значне посилення гіпотензивного ефекту при одночасному застосуванні інгібіторів ФДЕ-5 та ріоцигуату (стимулятор гуанілатциклази), тому прийом такої комбінації препаратів протипоказаний. Тадалафіл має системні судинорозширюючі властивості і може посилювати дію гіпотензивних засобів, спрямоване на зниження артеріального тиску. Вивчалися препарати наступних груп гіпотензивних препаратів: блокатори "повільних" кальцієвих каналів (амлодипін), інгібітори ангіотензинперетворюючого ферменту (еналаприл), бета-адреноблокатори (метопролол), тіазидні діуретики (бендофлуазид), блокатори рецепторів. Додатково у пацієнтів з погано контрольованою артеріальною гіпертензією, які приймали кілька гіпотензивних засобів, спостерігалося дещо більше зниження артеріального тиску. Переважна більшість пацієнтів це зниження був пов'язані з розвитком гипотензивных симптомів. Пацієнтам, які отримують лікування гіпотензивними препаратами та приймають тадалафіл, повинні бути надані відповідні клінічні рекомендації. При одночасному застосуванні тадалафілу та фінастериду (інгібітор 5-альфа-редуктази) не спостерігалося зміни профілю небажаних реакцій порівняно із застосуванням комбінації плацебо + фінастерид, проте при прийомі цих препаратів слід бути обережним через недостатню кількість клінічних даних. Дослідження підтвердили, що тадалафіл не інгібує та не індукує ізоферменти системи цитохрому Р450 CYP1A2, CYP3A4, CYP2C9, CYP2C19, CYP2D6, CYP2E1. Тадалафіл не має клінічно значущого ефекту на фармакокінетику або фармакодинаміку теофіліну (субстрат CYP1A2), не впливає на AUC S-варфарину або R-варфарину (субстрати CYP2C9) і не змінює протромбіновий час при одночасному прийомі з варфарином. Тадалафіл (10 мг, 20 мг) не збільшує тривалість кровотечі, що викликається ацетилсаліцилової кислотою (АСК). Біодоступність етинілестрадіолу та тербуталіну при прийомі внутрішньо разом з тадалафілом підвищується, проте клінічне значення такої взаємодії не визначено. Тадалафіл не впливає на концентрацію алкоголю, так само як і алкоголь не впливає на концентрацію тадалафілу. При високих дозах алкоголю (0,7 г/кг) прийом тадалафілу не викликав статистично значущого зниження середньої АТ. У деяких пацієнтів спостерігалися постуральне запаморочення та ортостатична гіпотензія. При прийомі тадалафілу у поєднанні з нижчими дозами алкоголю (0,6 г/кг) зниження АТ не спостерігалося, а запаморочення виникало з такою самою частотою, що при прийомі алкоголю окремо. Вивчення взаємодій між тадалафілом та препаратами для лікування цукрового діабету не проводилося.Спосіб застосування та дозиДля прийому всередину. Застосування препарату при ЕД Для пацієнтів з частою сексуальною активністю (більше двох разів на тиждень) рекомендована частота прийому: щодня, 5 мг (1 таблетка) 1 раз на добу, одночасно, незалежно від їди. Доза повинна періодично контролюватись і переглядатися, за необхідності. Добова доза може бути знижена до 2,5 мг, залежно від індивідуальної чутливості. Для пацієнтів з нечастою сексуальною активністю (рідше двох разів на тиждень) рекомендована частота прийому: 20 мг (1 таблетка або 4 таблетки у дозі 5 мг) безпосередньо перед сексуальною активністю згідно з інструкцією з медичного застосування. Максимальна добова доза становить 20 мг. Застосування препарату при ДГПЗ або ЕД + ДГПЗ Рекомендована доза препарату становить 5 мг (1 таблетка) 1 раз на добу. Препарат слід приймати приблизно в один і той же час дня, незалежно від їди та часу сексуальної активності. Тривалість лікування встановлюється лікарем індивідуально. У пацієнтів з нирковою недостатністю тяжкого ступеня (КК У пацієнтів з нирковою недостатністю легкої (КК 51 -80 мл/хв) та середнього ступеня тяжкості (КК 31-50 мл/хв) або печінковою недостатністю легкого та середнього ступеня тяжкості (класи А та В за класифікацією Чайлд-П'ю), а також у літніх пацієнтів корекція дози не потрібна.ПередозуванняПри призначенні тадалафілу одноразово в дозі до 500 мг здоровим особам і багаторазово в дозі до 100 мг на добу пацієнтам з ЕД небажані реакції були зіставні, як і застосування нижчих доз. У разі передозування слід проводити симптоматичне лікування. При гемодіалізі тадалафілу практично не виводиться.Запобіжні заходи та особливі вказівкиДіагностика ЕД та ДГПЗ повинна включати виявлення основної причини захворювання, відповідне медичне обстеження, визначення тактики лікування та індивідуальну оцінку співвідношення користь/ризик. Сексуальна активність має потенційний ризик для пацієнтів із серцево-судинними захворюваннями, тому лікування ЕД не слід проводити у чоловіків із такими захворюваннями серця, при яких сексуальна активність не рекомендована. Як і інші ФДЕ-5 інгібітори, тадалафіл може чинити системну судиннорозширювальну дію, що може призводити до транзиторного зниження АТ та посилення гіпотензивної дії нітратів, альфа-адреноблокаторів (див. розділ "Взаємодія з іншими лікарськими засобами"). Перед призначенням препарату необхідно ретельно оцінити ймовірність виникнення подібних небажаних реакцій у пацієнтів із серцево-судинними захворюваннями. Пацієнти з передбачуваним діагнозом ДГПЗ повинні пройти обстеження для виключення раку передміхурової залози. Неартеріальна передня ішемічна оптична нейропатія (НАПІОН) є причиною порушення зору, включаючи повну втрату зору. Є рідкісні постмаркетингові повідомлення про випадки розвитку НАПІОН, за часом пов'язані з прийомом інгібіторів ФДЕ-5. В даний час неможливо визначити, чи існує прямий зв'язок між розвитком НАПІОН та прийомом інгібіторів ФДЕ-5 або іншими факторами. Необхідно попередити пацієнтів, що у разі раптової втрати зору слід припинити прийом тадалафілу та звернутися за медичною допомогою. Пацієнти також повинні бути проінформовані, що у людей, які перенесли НАПІОН, підвищений ризик повторного розвитку НАПІОН. Є повідомлення про виникнення приапізму при застосуванні інгібіторів ФДЕ-5, включаючи тадалафіл. Пацієнти повинні бути проінформовані про необхідність негайного звернення за медичною допомогою у разі виникнення ерекції, що триває 4 години та більше. Несвоєчасне лікування приапізму веде до пошкодження тканин статевого члена, внаслідок чого може настати необоротна імпотенція. Ефективність препарату у пацієнтів, які перенесли хірургічну операцію на органах малого тазу або радикальну нервозберігаючу простатектомію, невідома. Вплив на здатність до керування автотранспортом та управління механізмами Незважаючи на те, що частота виникнення запаморочення на тлі плацебо і тадалафілу однакова, в період лікування необхідно дотримуватися обережності при керуванні автотранспортом та заняттями іншими потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій. Пацієнти повинні бути обізнані про можливий розвиток сонливості при прийомі препарату, особливо на початку терапії або у поєднанні з алкоголем.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Активна речовина: левоцетиризину дигідрохлорид – 5,0 мг. Допоміжні речовини: целюлоза мікрокристалічна – 53,2 мг, кроскармеллозу натрію – 3,8 мг, крохмаль прежелатинізований – 32,04 мг, кремнію діоксид колоїдний – 0,48 мг, магнію стеарат – 0,48 мг. Оболонка таблетки: опадрай II білий – 3,8 мг (лактози моногідрат – 1,37 мг, гіпромелоза – 1,06 мг, титану діоксид – 0.99 мг, макрогол 3000 – 0,38 мг). 10 шт. в упаковці.Опис лікарської формиКруглі, двоопуклі таблетки, вкриті плівковою оболонкою білого кольору. На поперечному розрізі – внутрішній шар білого або майже білого кольору.Фармакотерапевтична групаЛевоцетиризин – це R-енантіомер цетиризину; конкуретний антагоніст гістаміну; блокує Н1-гістамінові рецептори, спорідненість до яких у 2 рази вища, ніж у цетиризину. Левоцетиризин впливає на гістамінозалежну стадію алергічних реакцій; зменшує міграцію еозинофілів, зменшує судинну проникність, обмежує вивільнення медіаторів запалення. Попереджає розвиток та полегшує перебіг алергічних реакцій, надає протиексудативну, протисвербіжну дію; практично не чинить антихолінергічної та антисеротонінової дії. У терапевтичних дозах практично не має седативної дії.ФармакокінетикаФармакокінетичні параметри левоцетиризину змінюються лінійно залежно від дози та практично не відрізняються від фармакокінетики цетиризину. Абсорбція: Швидко та повністю всмоктується при прийомі внутрішньо. Прийом їжі не впливає на повноту всмоктування, але знижує його швидкість. Максимальна концентрація (Сmах) у плазмі досягається через 0,9 годину і становить 270 нг/мл. Постійний рівень концентрації препарату досягається через дві доби прийому. Розподіл: Зв'язування з білками плазми – 90%. Об'єм розподілу (Vd) становить 0,4 л/кг. Біодоступність сягає 100%. Проникає у грудне молоко. Метаболізм: Менше 14% препарату метаболізується у печінці шляхом N- та О-деалкілування з утворенням фармакологічно неактивного метаболіту. Через низький рівень метаболізму та відсутність метаболічного потенціалу (у його метаболізмі система цитохрому задіяна мінімально) взаємодія левоцетиризину з іншими лікарськими препаратами є малоймовірною. Виведення: У дорослих Т1/2 (період напіввиведення) становить 7,9 ± 1,9 години, а загальний кліренс становить 0,63 мл/хв/кг, у маленьких дітей Т1/2 укорочений. Близько 85,4% прийнятої дози препарату виводиться нирками, близько 12,9% через кишечник. Спеціальні групи: Пацієнти з нирковою недостатністю При нирковій недостатності (кліренс креатиніну (КК) < 40 мл/хв) кліренс знижується (у пацієнтів, які перебувають на гемодіалізі – на 80%), Т1/2 подовжується. Менше 10% левоцетиризину видаляється під час стандартної 4-годинної процедури гемодіалізу. Діти Дані з дослідження фармакокінетики препарату у 14 дітей віком від 6 до 11 років з масою тіла від 20 до 40 кг при пероральному прийомі одноразово 5 мг левоцетиризину показали, що показники Сmах і площа під кривою (AUC) приблизно вдвічі перевищують аналогічні показники у дорослих здорових людей під час перехресного контролю. Дані, отримані в ході аналізу, показали, що прийом препарату в дозі 1,25 мг у дітей віком від 6 місяців до 5 років призводить до концентрації у плазмі, що відповідає такій у дорослих при прийомі 5 мг один раз на добу. Літні пацієнти Дані з фармакокінетики у пацієнтів похилого віку обмежені. При повторному прийомі 30 мг левоцетиризину один раз на добу протягом 6 днів у 9 літніх пацієнтів (вік від 65 до 74 років) загальний кліренс був приблизно на 33% нижче, ніж у дорослих молодшого віку. Було показано, що розподіл рацемату цетиризину більше залежить від функції нирок, ніж віку. Це твердження також може бути застосовано і до левоцетиризину, так як обидва препарати і левоцетиризин, і цетиризин виводяться переважно із сечею. Тому у пацієнтів похилого віку доза левоцетиризину повинна бути скоригована залежно від функції нирок.Клінічна фармакологіяПротиалергічний засіб - блокатор H1-гістамінових рецепторів.Показання до застосуванняЛікування симптомів цілорічного (персистуючого) та сезонного (інтермітуючого) алергічних ринітів та алергічного кон'юнктивіту, таких як свербіж, чхання, закладеність носа, ринорея, сльозотеча, гіперемія кон'юнктиви; поліноз (сінна лихоманка); кропив'янка; інші алергічні дерматози, що супроводжуються свербінням та висипаннями. У разі потреби, будь ласка, проконсультуйтеся з лікарем перед застосуванням лікарського засобу.Протипоказання до застосуванняПідвищена чутливість до діючої речовини, цетиризину, гідроксизину, будь-якого похідного піперазину або будь-якої іншої допоміжної речовини препарату; дефіцит лактази, непереносимість лактози, глюкозо-галактозна мальабсорбція; термінальна стадія ниркової недостатності (кліренс креатиніну менше 10 мл/хв); дитячий вік до 6 років (для таблеток, через обмеженість даних щодо ефективності та безпеки).Вагітність та лактаціяВагітність Дані щодо застосування левоцетиризину під час вагітності практично відсутні або обмежені (менше 300 результатів вагітності). Однак застосування цетиризину, рацемату левоцетиризину, при вагітності (більше 1000 результатів вагітностей) не супроводжувалося вадами розвитку та внутрішньоутробним та неонатальним токсичним впливом. У дослідженнях на тваринах не виявлено прямого або непрямого несприятливого впливу на перебіг вагітності, ембріональний та фетальний розвиток, пологи та постнатальний розвиток. При призначенні левоцетиризину вагітним слід бути обережними. Період грудного вигодовування Цетиризин, рацемат левоцетиризину, екскретується із грудним молоком. Тому також можливо і виділення левоцетиризину з грудним молоком. У дітей, які перебувають на грудному вигодовуванні, можлива поява побічних реакцій на левоцетиризин. Тому необхідно бути обережними при призначенні левоцетиризину в період грудного вигодовування. Фертильність Клінічні дані щодо левоцетиризину відсутні.Побічна діяКлінічні дослідження Під час проведення клінічних досліджень у чоловіків та жінок 12-71 років з частотою 1% і більше (часто ≥ 1/100, <1/10), зустрічалися такі побічні ефекти: головний біль, сонливість, сухість у роті, стомлюваність, нечасто ≥ 1/1000, <1/100) зустрічалися астенія та біль у животі. Під час проведення клінічних досліджень у дітей віком від 6 до 12 років із частотою 1% і більше (часто ≥1/100, <1/10) зустрічалися головний біль та сонливість. Післяреєстраційні дослідження Частота побічних ефектів невідома (не може бути оцінена за наявними даними). З боку імунної системи: реакції гіперчутливості, включаючи анафілаксію. З боку метаболізму та розладів харчування: підвищення апетиту. З боку психіки: тривога, агресія, порушення, депресія, галюцинації, безсоння, суїцидальні думки. З боку нервової системи: судоми, тромбоз синусів твердої мозкової оболонки, парестезія, запаморочення, непритомність, тремор, дисгевзія. З боку слуху: вертиго З боку органу зору: порушення зору, нечіткість зорового сприйняття, запальні прояви. Серцево-судинна система: стенокардія, тахікардія, відчуття серцебиття, тромбоз яремної вени. З боку дихальної системи: задишка, посилення симптомів риніту. З боку травної системи: нудота, блювання, діарея. Гепатобіліарні розлади: гепатит, зміна функціональних спроб печінки. З боку нирок та сечовидільної системи: дизурія, затримка сечі. З боку шкіри та м'яких тканин: ангіоневротичний набряк, стійка лікарська еритема, свербіж, висипання, кропив'янка, гіпотрихоз, тріщини, фотосенсибілізація. З боку кістково-м'язової системи: біль у м'язах, артралгія. Загальні розлади: периферичні набряки, збільшення маси тіла. Інше: перехресна реактивність. Якщо будь-які вказані в інструкції побічні ефекти посилюються, або Ви помітили будь-які інші побічні ефекти, не вказані в інструкції, повідомте про це лікаря.Взаємодія з лікарськими засобамиВивчення взаємодії левоцетиризину з іншими препаратами не проводилося. При вивченні лікарської взаємодії рацемату цетиризину з антипірином, псевдоефедрином, циметидином, кетоконазолом, еритроміцином, азитроміцином, гліпізидом та діазепамом клінічно значимих небажаних взаємодій не виявлено. При одночасному застосуванні з теофіліном (400 мг на добу) загальний кліренс цетиризину знижується на 16% (кінетика теофіліну не змінюється). При одночасному застосуванні рітановіру (600 мг 2 рази на день) та цетиризину (10 мг на день) показано у дослідженні, що експозиція цетиризину збільшувалася на 40%, а експозиція рітановіру незначно змінювалася (-11%). У ряді випадків при одночасному застосуванні левоцетиризину з алкоголем або лікарськими засобами, що мають переважний вплив на центральну нервову систему (ЦНС), може спричинити загальмованість та погіршення працездатності.Спосіб застосування та дозиПрепарат приймають внутрішньо під час їди або натще, не розжовуючи, запиваючи невеликою кількістю води. Добову дозу рекомендується приймати за один прийом. Дорослі та діти старше 6 років: добова доза становить 5 мг. Максимальна добова доза – 5 мг. Дітям віком до 6 років таблетки не призначають: для них використовують іншу, рідку лікарську форму. Оскільки левоцетиризин виводиться з організму нирками, при призначенні препарату пацієнтам із нирковою недостатністю та пацієнтам похилого віку дозу слід коригувати залежно від величини кліренсу креатиніну.ПередозуванняСимптоми передозування: сонливість (у дорослих), збудження та занепокоєння, що змінюються сонливістю (у дітей). Лікування передозування: відразу після прийому препарату необхідно промити шлунок або викликати блювоту. Рекомендується проведення симптоматичної та підтримуючої терапії. Специфічного антидоту немає. Гемодіаліз неефективний.Запобіжні заходи та особливі вказівкиІнтервали між дозами повинні бути підібрані індивідуально, залежно від ниркової функції. У період лікування рекомендується утримуватись від вживання етанолу (алкоголю). Таблетки Левоцетиризин містять моногідрат лактози, тому їх не слід призначати пацієнтам з непереносимістю лактози, спадковим дефіцитом лактази або синдромом мальабсорбції глюкози-галактози. За наявності у пацієнтів сприятливих факторів до затримки сечі (наприклад, пошкодження спинного мозку, гіперплазія передміхурової залози) слід бути обережним, оскільки левоцетиризин може збільшувати ризик затримки сечі.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Активна речовина: левоцетиризину дигідрохлорид – 5,0 мг. Допоміжні речовини: целюлоза мікрокристалічна – 53,2 мг, кроскармеллозу натрію – 3,8 мг, крохмаль прежелатинізований – 32,04 мг, кремнію діоксид колоїдний – 0,48 мг, магнію стеарат – 0,48 мг. Оболонка таблетки: опадрай II білий – 3,8 мг (лактози моногідрат – 1,37 мг, гіпромелоза – 1,06 мг, титану діоксид – 0.99 мг, макрогол 3000 – 0,38 мг). 30 шт. в упаковці.Опис лікарської формиКруглі, двоопуклі таблетки, вкриті плівковою оболонкою білого кольору. На поперечному розрізі – внутрішній шар білого або майже білого кольору.Фармакотерапевтична групаЛевоцетиризин – це R-енантіомер цетиризину; конкуретний антагоніст гістаміну; блокує Н1-гістамінові рецептори, спорідненість до яких у 2 рази вища, ніж у цетиризину. Левоцетиризин впливає на гістамінозалежну стадію алергічних реакцій; зменшує міграцію еозинофілів, зменшує судинну проникність, обмежує вивільнення медіаторів запалення. Попереджає розвиток та полегшує перебіг алергічних реакцій, надає протиексудативну, протисвербіжну дію; практично не чинить антихолінергічної та антисеротонінової дії. У терапевтичних дозах практично не має седативної дії.ФармакокінетикаФармакокінетичні параметри левоцетиризину змінюються лінійно залежно від дози та практично не відрізняються від фармакокінетики цетиризину. Абсорбція: Швидко та повністю всмоктується при прийомі внутрішньо. Прийом їжі не впливає на повноту всмоктування, але знижує його швидкість. Максимальна концентрація (Сmах) у плазмі досягається через 0,9 годину і становить 270 нг/мл. Постійний рівень концентрації препарату досягається через дві доби прийому. Розподіл: Зв'язування з білками плазми – 90%. Об'єм розподілу (Vd) становить 0,4 л/кг. Біодоступність сягає 100%. Проникає у грудне молоко. Метаболізм: Менше 14% препарату метаболізується у печінці шляхом N- та О-деалкілування з утворенням фармакологічно неактивного метаболіту. Через низький рівень метаболізму та відсутність метаболічного потенціалу (у його метаболізмі система цитохрому задіяна мінімально) взаємодія левоцетиризину з іншими лікарськими препаратами є малоймовірною. Виведення: У дорослих Т1/2 (період напіввиведення) становить 7,9 ± 1,9 години, а загальний кліренс становить 0,63 мл/хв/кг, у маленьких дітей Т1/2 укорочений. Близько 85,4% прийнятої дози препарату виводиться нирками, близько 12,9% через кишечник. Спеціальні групи: Пацієнти з нирковою недостатністю При нирковій недостатності (кліренс креатиніну (КК) < 40 мл/хв) кліренс знижується (у пацієнтів, які перебувають на гемодіалізі – на 80%), Т1/2 подовжується. Менше 10% левоцетиризину видаляється під час стандартної 4-годинної процедури гемодіалізу. Діти Дані з дослідження фармакокінетики препарату у 14 дітей віком від 6 до 11 років з масою тіла від 20 до 40 кг при пероральному прийомі одноразово 5 мг левоцетиризину показали, що показники Сmах і площа під кривою (AUC) приблизно вдвічі перевищують аналогічні показники у дорослих здорових людей під час перехресного контролю. Дані, отримані в ході аналізу, показали, що прийом препарату в дозі 1,25 мг у дітей віком від 6 місяців до 5 років призводить до концентрації у плазмі, що відповідає такій у дорослих при прийомі 5 мг один раз на добу. Літні пацієнти Дані з фармакокінетики у пацієнтів похилого віку обмежені. При повторному прийомі 30 мг левоцетиризину один раз на добу протягом 6 днів у 9 літніх пацієнтів (вік від 65 до 74 років) загальний кліренс був приблизно на 33% нижче, ніж у дорослих молодшого віку. Було показано, що розподіл рацемату цетиризину більше залежить від функції нирок, ніж віку. Це твердження також може бути застосовано і до левоцетиризину, так як обидва препарати і левоцетиризин, і цетиризин виводяться переважно із сечею. Тому у пацієнтів похилого віку доза левоцетиризину повинна бути скоригована залежно від функції нирок.Клінічна фармакологіяПротиалергічний засіб - блокатор H1-гістамінових рецепторів.Показання до застосуванняЛікування симптомів цілорічного (персистуючого) та сезонного (інтермітуючого) алергічних ринітів та алергічного кон'юнктивіту, таких як свербіж, чхання, закладеність носа, ринорея, сльозотеча, гіперемія кон'юнктиви; поліноз (сінна лихоманка); кропив'янка; інші алергічні дерматози, що супроводжуються свербінням та висипаннями. У разі потреби, будь ласка, проконсультуйтеся з лікарем перед застосуванням лікарського засобу.Протипоказання до застосуванняПідвищена чутливість до діючої речовини, цетиризину, гідроксизину, будь-якого похідного піперазину або будь-якої іншої допоміжної речовини препарату; дефіцит лактази, непереносимість лактози, глюкозо-галактозна мальабсорбція; термінальна стадія ниркової недостатності (кліренс креатиніну менше 10 мл/хв); дитячий вік до 6 років (для таблеток, через обмеженість даних щодо ефективності та безпеки).Вагітність та лактаціяВагітність Дані щодо застосування левоцетиризину під час вагітності практично відсутні або обмежені (менше 300 результатів вагітності). Однак застосування цетиризину, рацемату левоцетиризину, при вагітності (більше 1000 результатів вагітностей) не супроводжувалося вадами розвитку та внутрішньоутробним та неонатальним токсичним впливом. У дослідженнях на тваринах не виявлено прямого або непрямого несприятливого впливу на перебіг вагітності, ембріональний та фетальний розвиток, пологи та постнатальний розвиток. При призначенні левоцетиризину вагітним слід бути обережними. Період грудного вигодовування Цетиризин, рацемат левоцетиризину, екскретується із грудним молоком. Тому також можливо і виділення левоцетиризину з грудним молоком. У дітей, які перебувають на грудному вигодовуванні, можлива поява побічних реакцій на левоцетиризин. Тому необхідно бути обережними при призначенні левоцетиризину в період грудного вигодовування. Фертильність Клінічні дані щодо левоцетиризину відсутні.Побічна діяКлінічні дослідження Під час проведення клінічних досліджень у чоловіків та жінок 12-71 років з частотою 1% і більше (часто ≥ 1/100, <1/10), зустрічалися такі побічні ефекти: головний біль, сонливість, сухість у роті, стомлюваність, нечасто ≥ 1/1000, <1/100) зустрічалися астенія та біль у животі. Під час проведення клінічних досліджень у дітей віком від 6 до 12 років із частотою 1% і більше (часто ≥1/100, <1/10) зустрічалися головний біль та сонливість. Післяреєстраційні дослідження Частота побічних ефектів невідома (не може бути оцінена за наявними даними). З боку імунної системи: реакції гіперчутливості, включаючи анафілаксію. З боку метаболізму та розладів харчування: підвищення апетиту. З боку психіки: тривога, агресія, порушення, депресія, галюцинації, безсоння, суїцидальні думки. З боку нервової системи: судоми, тромбоз синусів твердої мозкової оболонки, парестезія, запаморочення, непритомність, тремор, дисгевзія. З боку слуху: вертиго З боку органу зору: порушення зору, нечіткість зорового сприйняття, запальні прояви. Серцево-судинна система: стенокардія, тахікардія, відчуття серцебиття, тромбоз яремної вени. З боку дихальної системи: задишка, посилення симптомів риніту. З боку травної системи: нудота, блювання, діарея. Гепатобіліарні розлади: гепатит, зміна функціональних спроб печінки. З боку нирок та сечовидільної системи: дизурія, затримка сечі. З боку шкіри та м'яких тканин: ангіоневротичний набряк, стійка лікарська еритема, свербіж, висипання, кропив'янка, гіпотрихоз, тріщини, фотосенсибілізація. З боку кістково-м'язової системи: біль у м'язах, артралгія. Загальні розлади: периферичні набряки, збільшення маси тіла. Інше: перехресна реактивність. Якщо будь-які вказані в інструкції побічні ефекти посилюються, або Ви помітили будь-які інші побічні ефекти, не вказані в інструкції, повідомте про це лікаря.Взаємодія з лікарськими засобамиВивчення взаємодії левоцетиризину з іншими препаратами не проводилося. При вивченні лікарської взаємодії рацемату цетиризину з антипірином, псевдоефедрином, циметидином, кетоконазолом, еритроміцином, азитроміцином, гліпізидом та діазепамом клінічно значимих небажаних взаємодій не виявлено. При одночасному застосуванні з теофіліном (400 мг на добу) загальний кліренс цетиризину знижується на 16% (кінетика теофіліну не змінюється). При одночасному застосуванні рітановіру (600 мг 2 рази на день) та цетиризину (10 мг на день) показано у дослідженні, що експозиція цетиризину збільшувалася на 40%, а експозиція рітановіру незначно змінювалася (-11%). У ряді випадків при одночасному застосуванні левоцетиризину з алкоголем або лікарськими засобами, що мають переважний вплив на центральну нервову систему (ЦНС), може спричинити загальмованість та погіршення працездатності.Спосіб застосування та дозиПрепарат приймають внутрішньо під час їди або натще, не розжовуючи, запиваючи невеликою кількістю води. Добову дозу рекомендується приймати за один прийом. Дорослі та діти старше 6 років: добова доза становить 5 мг. Максимальна добова доза – 5 мг. Дітям віком до 6 років таблетки не призначають: для них використовують іншу, рідку лікарську форму. Оскільки левоцетиризин виводиться з організму нирками, при призначенні препарату пацієнтам із нирковою недостатністю та пацієнтам похилого віку дозу слід коригувати залежно від величини кліренсу креатиніну.ПередозуванняСимптоми передозування: сонливість (у дорослих), збудження та занепокоєння, що змінюються сонливістю (у дітей). Лікування передозування: відразу після прийому препарату необхідно промити шлунок або викликати блювоту. Рекомендується проведення симптоматичної та підтримуючої терапії. Специфічного антидоту немає. Гемодіаліз неефективний.Запобіжні заходи та особливі вказівкиІнтервали між дозами повинні бути підібрані індивідуально, залежно від ниркової функції. У період лікування рекомендується утримуватись від вживання етанолу (алкоголю). Таблетки Левоцетиризин містять моногідрат лактози, тому їх не слід призначати пацієнтам з непереносимістю лактози, спадковим дефіцитом лактази або синдромом мальабсорбції глюкози-галактози. За наявності у пацієнтів сприятливих факторів до затримки сечі (наприклад, пошкодження спинного мозку, гіперплазія передміхурової залози) слід бути обережним, оскільки левоцетиризин може збільшувати ризик затримки сечі.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаСпрей назальний - 1 мл: Активні компоненти: фенілефрину гідрохлорид - 2.5 мг; цетиризину дигідрохлорид – 2.5 мг; Допоміжні речовини: гліцерол – 40 мг, натрію гідрофосфат (безводний) – 2.5 мг, калію дигідрофосфат – 1.5 мг, динатрію едетат – 0.2 мг, бензалконію хлориду розчин 50% – 0.1 мг у перерахунку на 10 мл . 15 мл - флакони пластмасові (1) з розпилювачем для назального застосування - картонні пачки.Опис лікарської формиСпрей назальний у вигляді прозорого, безбарвного або світло-жовтого розчину.Фармакотерапевтична групаПротиалергічний засіб комбінований (H1-гістамінових рецепторів блокатор + альфа-адреноміметик).ФармакокінетикаПрепарат призначений для місцевого інтраназального застосування, його активність не залежить від концентрації активних речовин у плазмі.ФармакодинамікаКомбінований препарат для інтраназального застосування для патогенетичного та симптоматичного лікування, що має судинозвужувальну та протиалергічну дію. Фенілефрин - агоніст α1-адренорецепторів (симпатоміметик), викликає звуження кровоносних судин слизової оболонки порожнини носа, зменшує набряк слизових оболонок та гіперемію тканин, застійні явища у слизовій оболонці порожнини носа. Відновлення повітряної прохідності носоглотки покращує самопочуття пацієнта та знижує небезпеку можливих ускладнень, спричинених застоєм слизового секрету. Цетиризин - блокатор гістамінових H1-рецепторів, має протиалергічну дію, зменшує проникність капілярів, попереджає розвиток набряку слизової оболонки порожнини носа та придаткових пазух. До складу препарату входить допоміжна зволожуюча речовина гліцерол, що сприяє утриманню вологи, що допомагає забезпечити зволоження при сухості та подразненні слизової оболонки порожнини носа.Показання до застосуваннягострий риніт (у т.ч. при застудних захворюваннях); алергічний риніт (у т.ч. при сінній лихоманці); вазомоторний риніт; хронічний риніт; гострий та хронічний синусит; гострий середній отит (як допоміжний метод лікування); підготовка до хірургічних втручань в області носа та усунення набряку слизової оболонки порожнини носа та придаткових пазух після хірургічних втручань у цій галузі.Протипоказання до застосуванняатрофічний риніт; закритокутова глаукома; прийом інгібіторів МАО (одночасний або попередні 14 днів); вагітність; період лактації (грудного вигодовування); вік до 18 років (дані щодо ефективності та безпеки у дітей відсутні); підвищена чутливість до фенілефрину, цетиризину або інших компонентів препарату. З обережністю: серцево-судинні захворювання, у т.ч. артеріальна гіпертензія, аритмії, генералізований атеросклероз; стенокардія; гіпертиреоз; аденома передміхурової залози; обструкція шийки сечового міхура (наприклад, внаслідок гіпертрофії передміхурової залози); хронічна ниркова недостатність; підвищена судомна активність; цукровий діабет; епілепсія; пацієнтам з вираженими реакціями на симпатоміметики, що виявляються у вигляді безсоння, запаморочення, тремору, серцевої аритмії або підвищення артеріального тиску (як і у разі застосування будь-яких місцевих судинозвужувальних засобів); пацієнтам похилого віку.Вагітність та лактаціяУ зв'язку з відсутністю даних застосування препарату протипоказане при вагітності та в період грудного вигодовування. Протипоказано застосування препарату віком до 18 років (дані щодо ефективності та безпеки у дітей відсутні).Побічна діяЦетиризин у комбінації з фенілефрином у вигляді спрею в терапевтичних дозах переноситься добре, проте можуть спостерігатися побічні дії, описані нижче. Класифікація частоти розвитку побічних ефектів згідно з рекомендаціями ВООЗ: дуже часто (≥1/10); часто (від ≥1/100 до З боку системи кровотворення: дуже рідко – тромбоцитопенія. Психічні порушення: нечасто – збудження; рідко – агресія, сплутаність свідомості, депресія, галюцинації, порушення сну; дуже рідко – тик; частота невідома – суїцидальні ідеї, порушення сну (включаючи кошмарні сновидіння). З боку нервової системи: нечасто – парестезії; рідко – судоми; дуже рідко - збочення смаку, дискінезія, дистонія, непритомність, тремор; частота невідома – головний біль, запаморочення, порушення пам'яті, у т.ч. амнезія. З боку органу зору: дуже рідко – порушення акомодації, нечіткість зору, ністагм. З боку органу слуху та лабіринту: частота невідома – вертиго, глухота. З боку серцево-судинної системи: рідко – тахікардія; частота невідома – аритмія, підвищення артеріального тиску, васкуліт. З боку дихальної системи: рідко – дискомфорт у ділянці носа, сухість чи печіння у носі, поколювання, чхання; кровотеча з носа; бензалконію хлорид, що входить до складу препарату, може спричинити подразнення слизової оболонки порожнини носа; частота невідома - набряк та гіперемія слизової оболонки порожнини носа, слизові та водянисті виділення з носа, утруднення носового дихання. З боку травної системи: нечасто – діарея; рідко – печінкова недостатність із зміною функціональних печінкових проб (підвищення активності трансаміназ, ЛФ, ГГТ та білірубіну); Частота невідома – підвищення апетиту. З боку сечовидільної системи: дуже рідко – дизурія; частота невідома – затримка сечі. З боку кістково-м'язової системи: частота невідома – артралгія. З боку шкіри та підшкірної клітковини: нечасто – висип, свербіж. Алергічні реакції: рідко – реакції гіперчутливості, кропив'янка; дуже рідко – ангіоневротичний набряк, анафілактичний шок, стійка лікарська еритема. Інші: нечасто – астенія, нездужання.Взаємодія з лікарськими засобамиНе слід застосовувати препарат одночасно з три- та тетрациклічними антидепресантами, бета-адреноблокаторами, інгібіторами МАО (прокарбазин, селегілін), мапротиліном, гуанедрелом, гуанетидином. Тиреоїдні гормони при системній абсорбції фенілефрину збільшують (взаємно) пов'язаний з ними ризик виникнення коронарної недостатності (особливо при коронарному атеросклерозі).Спосіб застосування та дозиПрепарат застосовують інтраназально. Рекомендована доза для дорослих - 1-2 впорскування в кожну ніздрю 2-3 рази на добу. Препарат не слід застосовувати безперервно понад 7 днів. Перед введенням препарату слід ретельно очистити носові ходи. Флакон слід тримати вертикально розпилювачем догори. Нахилити голову, вставити наконечник флакона в носовий хід, 1 раз коротким різким рухом натиснути на розпилювач. Під час упорскування рекомендується зробити легкий вдих через ніс.ПередозуванняВкрай низька системна абсорбція препарату при місцевому застосуванні робить передозування практично неможливим. Симптоми При випадковому одноразовому прийомі внутрішньо цетиризину в дозі 50 мг можуть спостерігатися сплутаність свідомості, діарея, запаморочення, підвищена стомлюваність, біль голови, нездужання, мідріаз, свербіж, занепокоєння, слабкість, седативний ефект, сонливість, ступор, тахікардія, . Передозування фенілефрину може виявлятися порушеннями серцевого ритму, підвищенням артеріального тиску, збудженням. Лікування: промивання шлунка або стимуляція блювання, призначення активованого вугілля, прийом великої кількості рідини; підтримуюча та симптоматична терапія. Специфічного антидоту немає. Гемодіаліз неефективний. При передозуванні пацієнта необхідно звернутися до лікаря.Запобіжні заходи та особливі вказівкиПрепарат призначений лише для місцевого інтраназального застосування. Препарат не слід застосовувати безперервно протягом 7 днів. Тривале або надмірне застосування препарату може спричинити тахіфілаксію та ефект "рикошету", пов'язаний з повторним розвитком закладеності носа (медикаментозний риніт), призвести до розвитку системної судинозвужувальної дії. Як і при застосуванні інших судинозвужувальних засобів, не слід перевищувати рекомендовані дози препарату. В іншому випадку можливий розвиток проявів системної дії препарату, особливо у пацієнтів похилого віку. Не слід застосовувати фенілефрин пацієнтам протягом 2 тижнів після відміни інгібіторів МАО, оскільки вони можуть посилювати вираженість адренергічних ефектів симпатоміметичних засобів та збільшити ризик виникнення побічних ефектів з боку серцево-судинної системи. Вплив на здатність до керування автотранспортом та управління механізмами Слід бути обережними при керуванні транспортними засобами та механізмами, а також виконанні інших видів діяльності, що вимагають концентрації уваги та швидкості психомоторних реакцій, т.к. при застосуванні препарату існує можливість виникнення запаморочення.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
235,00 грн
164,00 грн
Склад, форма випуску та упаковкакларитроміцин таблетки, вкриті плівковою оболонкою 1 таблетка, покрита плівковою оболонкою, 250 мг/500 мг містить: Ядро: Діюча речовина: Кларитроміцин 250,00 мг/500,00 мг Допоміжні речовини: Крохмаль кукурудзяний, целюлоза мікрокристалічна (тип 101), целюлоза мікрокристалічна (тип 102), кремнію діоксид колоїдний, крохмаль прежелатинізований, полакрилін калію, тальк, магнію стеарат Оболонка плівкова: Гіпромелоза 6 cps, тальк, барвник заліза оксид жовтий (Е172), пропіленгліколь, титану діоксид (Е171)Опис лікарської формиТаблетки 250 мг: Овальні, двоопуклі таблетки, покриті плівковою оболонкою світло-коричнево-жовтого кольору. Вид на зламі: шорстка маса білого кольору із шаром оболонки світло-коричнево-жовтого кольору. Таблетки 500 мг: Овальні, двоопуклі таблетки, покриті плівковою оболонкою світло-коричнево-жовтого кольору. Вид на зламі: шорстка маса білого кольору із шаром оболонки світло-коричнево-жовтого кольору.Фармакотерапевтична групаантибіотик – макролідФармакокінетикаВсмоктування Препарат швидко всмоктується з шлунково-кишкового тракту. Абсолютна біодоступність становить близько 50%. При багаторазовому прийомі дози препарату кумуляції практично не виявлено, характер метаболізму в організмі людини не змінювався. Їда безпосередньо перед прийомом препарату збільшувала біодоступність препарату в середньому на 25 %. Кларитроміцин може застосовуватися незалежно від часу їди. Розподіл, метаболізм та виведення In vitro Кларитроміцин зв'язується з білками плазми на 70% у концентрації від 0,45 до 4,5 мкг/мл. При концентрації 45 мкг/мл зв'язування знижується до 41%, ймовірно, через насичення місць зв'язування. Це спостерігається лише при концентраціях, що багаторазово перевищують терапевтичну концентрацію. Invivo Дослідження в умовах in vivo на тваринах показали, що кларитроміцин присутній у всіх тканинах, за винятком центральної нервової системи (ЦНС), у концентраціях, що у кілька разів перевищують плазмові. Найбільш високі концентрації (в 10-20 разів вище плазмових) виявлялися в печінці та легенях. Здорові добровольці При застосуванні кларитроміцину в дозі 250 мг 2 рази на день максимальна рівноважна концентрація (С mах ) кларитроміцину та 14-ОН-кларитроміцину в плазмі крові досягалася через 2-3 дні і становила 1 мкг/мл та 0,6 мкг/мл відповідно. Період напіввиведення (Т 1/2 ) кларитроміцину та його основного метаболіту склав 3-4 години та 5-6 годин, відповідно. При застосуванні кларитроміцину в дозі 500 мг 2 рази на день . 83 мкг/мл відповідно. Т 1/2 кларитроміцину та його основного метаболіту становив 4,5-4,8 години та 6,9-8,7 години, відповідно. З mах 14-ОН-кларитроміцину в плазмі крові не збільшувалася пропорційно прийнятій внутрішньо дозі кларитроміцину, у той час як Т 1/2 як кларитроміцину, так і 14-ОН-кларитроміцин мав тенденцію до подовження з підвищенням дози. Така нелінійна фармакокінетика кларитроміцину у поєднанні зі зменшенням утворення 14-гідроксильованих та N-деметилованих продуктів при високих дозах вказує на нелінійний метаболізм кларитроміцину, який стає більш вираженим при високих дозах. Нирками виводиться близько 37,9% після прийому внутрішньо кларитроміцину в дозі 250 мг і 46% після прийому кларитроміцину в дозі 1200 мг, через кишечник виводиться близько 40,2% та 29,1% відповідно. Пацієнти Кларитроміцин та 14-ОН-кларитроміцин швидко проникають у тканини та рідини організму. Є обмежені дані, що свідчать про те, що концентрація кларитроміцину в цереброспінальній рідині при внутрішньому прийомі незначна (т. Е. Тільки 1-2% від концентрації в сироватці крові при нормальній проникності гематоенцефалічного бар'єру). Концентрація в тканинах зазвичай у кілька разів вища, ніж у сироватці крові. У таблиці наведено приклади тканинних та сироваткових концентрацій: Концентрації (250 мг кожні 12 годин) Вид тканини Тканинні (мкг/г) Сироваткові (мкг/мл) Мигдалики 1,6 0,8 Легкі 8,8 1,7 Порушення функції печінки У пацієнтів із середнім та тяжким ступенем порушення функції печінки, але із збереженою функцією нирок, корекція дози кларитроміцину не потрібна. Рівноважна концентрація у плазмі крові та системний кліренс кларитроміцину не відрізняються у пацієнтів цієї групи та здорових пацієнтів. Рівноважна концентрація 14-ОН-кларитроміцину у пацієнтів з порушеннями функції печінки нижча, ніж у здорових добровольців. Порушення функції нирок При порушенні функції нирок збільшуються З mах та мінімальна концентрація (З min ) кларитроміцину в плазмі крові, Т 1/2 , площа під кривою «концентрація-час» (AUC) кларитроміцину та його метаболіту (14-ОН-кларитроміцину). Константа елімінації та виведення нирками зменшуються. Ступінь змін цих параметрів залежить від рівня порушення функції нирок. Пацієнти похилого віку У пацієнтів похилого віку концентрація кларитроміцину та його метаболіту 14-ОН-кларитроміцину в плазмі була вищою, а виведення повільніше, ніж у групи молодих людей. Однак після корекції з урахуванням ниркового кліренсу креатиніну (КК) не було відмінностей у обох групах. Таким чином, основний вплив на фармакокінетичні параметри кларитроміцину має функція нирок, а не вік. Пацієнти з мікобактеріальними інфекціями Рівноважні концентрації кларитроміцину і 14-ОН-кларитроміцину у пацієнтів з ВІЛ-інфекцією, які отримували кларитроміцин у нормальних дозах (500 мг 2 рази на день), були подібними до таких показників у здорових людей. Однак при застосуванні кларитроміцину у більш високих дозах, які можуть бути потрібні для лікування мікобактеріальних інфекцій, концентрації антибіотика можуть значно перевищувати звичайні. У пацієнтів з ВІЛ-інфекцією, які приймали кларитроміцин у дозі 1000 мг/добу або 2000 мг/добу на 2 прийоми, рівноважні значення С mах зазвичай становили 2-4 мкг/мл та 5-10 мкг/мл відповідно. При застосуванні кларитроміцину у вищих дозах відзначалося подовження Т 1/2У порівнянні з таким показником у здорових добровольців, які отримували кларитроміцин у нормальних дозах. Підвищення концентрації у плазмі крові та подовження Т 1/2 при застосуванні кларитроміцину у більш високих дозах пов'язане з нелінійною фармакокінетикою препарату. Комбіноване лікування з омепразолом Кларитроміцин по 500 мг 3 рази на добу в комбінації з омепразолом у дозі 40 мг на добу сприяє подовженню Т 1/2 та збільшенню AUC 0-24 омепразолу. У всіх пацієнтів, які отримували комбіновану терапію, у порівнянні з пацієнтами, які отримували один омепразол, спостерігалося підвищення на 89% AUC 0-24 та на 34% Т 1/2 омепразолу. У кларитроміцину С mах , C min та AUC 0 - 8збільшувалися, відповідно, на 10%, 27% та 15% порівняно з аналогічними показниками при застосуванні кларитроміцину без омепразолу. У рівноважному стані концентрації кларитроміцину в слизовій оболонці шлунка через 6 годин після прийому кларитроміцину в групі, що отримувала комбінацію, у 25 разів перевищували такі показники порівняно з пацієнтами, які отримували один кларитроміцин. Концентрації кларитроміцину в тканинах шлунка через 6 годин після прийому кларитроміцину та омепразолу в 2 рази перевищували дані, отримані у групі пацієнтів, які отримували один кларитроміцин.ФармакодинамікаКларитроміцин є напівсинтетичним антибіотиком групи макролідів і чинить антибактеріальну дію, взаємодіючи з 50S рибосомальною субодиницею та пригнічуючи синтез білка, чутливих до нього бактерій. Кларитроміцин продемонстрував високу активність в умовах in vitro щодо як стандартних лабораторних штамів бактерій, так і виділених у пацієнтів у ході клінічної практики. Виявляє високу активність щодо багатьох аеробних та анаеробних грампозитивних та грамнегативних мікроорганізмів. Мінімальні переважні концентрації (МПК) кларитроміцину для більшості збудників менше, ніж МПК еритроміцину в середньому на одне log 2 розведення. Кларитроміцин в умовах in vitro є високоактивним щодо Legionella pneumophila, Mycoplasma pneumoniae. Чинить бактерицидну дію щодо Helicobacter pylori, дана активність кларитроміцину вище при нейтральному pH, ніж при кислому. Крім того, дані в умовах in vitro та in vivo вказують на те, що кларитроміцин діє на клінічно значущі види мікобактерій. Enterobacteriaceae та Pseudomonas spp. так само як і інші грамнегативні бактерії, що не ферментують лактозу, не чутливі до кларитроміцину. Активність кларитроміцину щодо більшості штамів наведених нижче мікроорганізмів доведена як в умовах in vitro, так і в клінічній практиці при захворюваннях, перелічених у розділі «Показання до застосування». Аеробні грампозитивні мікроорганізми: - Staphylococcus aureus, - Streptococcus pneumoniae, - Streptococcus pyogenes, -Listeria monocytogenes Аеробні грамнегативні мікроорганізми: -Haemophilusinfluenzae, -Haemophilus parainfluenzae, -Moraxella catarrhalis, -Neisseria gonorrhoeae, -Legionella pneumophila Інші мікроорганізми: - Mycoplasma pneumoniae, - Chlamydia pneumoniae (TWAR) Мікобактерії: - Mycobacterium leprae, - Mycobacterium kansasii, - Mycobacterium chelonae, -Mycobacterium fortuitum, – Mycobacterium avium complex (MAC) – комплекс, що включає: Mycobacterium avium, Mycobacterium intracellulare. Продукція бета-лактамази не впливає на активність кларитроміцину. Більшість штамів стафілококів, резистентних до метициліну та оксациліну, мають стійкість і до кларитроміцину. Helicobacter pylori Чутливість Helicobacter pylori до кларитроміцину вивчалася на ізолятах Helicobacter pylori, виділених від 104 пацієнтів на початок терапії препаратом. У 4 пацієнтів були виділені резистентні до кларитроміцину штами Helicobacter pylori, у 2 пацієнтів – штами з помірною резистентністю, у решти 98 пацієнтів ізоляти Helicobacter pylori були чутливі до кларитроміцину. Кларитроміцин діє в умовах in vitro і щодо більшості штамів наступних мікроорганізмів (проте безпека та ефективність застосування кларитроміцину в клінічній практиці не підтверджена клінічними дослідженнями, і практичне значення залишається незрозумілим): Аеробні грампозитивні мікроорганізми: - Streptococcus agalactiae, - Streptococci (групи С, F, G), - Viridansgroupstreptococci Аеробні грамнегативні мікроорганізми: - Bordetella pertussis, – Pasteurella multocida Анаеробні грампозитивні мікроорганізми: - Clostridiumperfringens, - Peptococcusniger, - Propionibacteriumacnes Анаеробні грамнегативні мікроорганізми: – Bacteroidesmelaninogenicus Спірохети: – Borreliaburgdorferi, - Treponema pallidum Кампілобактерії: – Campilobacter jejuni Основним метаболітом кларитроміцину в організмі людини є мікробіологічно активний метаболіт 14-гідроксикларитроміцин (14-ОН-кларитроміцин). Мікробіологічна активність метаболіту така ж, як у вихідної речовини, або вдвічі слабша щодо більшості мікроорганізмів. Виняток становить Haemophilus influenzae, щодо якої ефективність метаболіту вдвічі вища. Вихідне з'єднання та його основний метаболіт мають або адитивний, або синергічний ефект щодо Haemophilus influenzae в умовах in vitro та in vivo залежно від штаму бактерій. Тест на чутливість Кількісні методи, що вимагають вимірювання діаметра зони придушення росту, дають найбільш точні оцінки чутливості бактерій до антимікробних препаратів. Одна з рекомендованих методик визначення чутливості використовує диски, імпрегновані 15 мкг кларитроміцину (диско-дифузійний метод Кірбі-Бауера), при інтерпретації тесту діаметри зон придушення росту корелюють зі значеннями МПК кларитроміцину. Значення МПК визначаються методом розведення у бульйоні чи агарі. З використанням цих методик звіт з лабораторії у тому, що штам є «чутливим», свідчить про те, що збудник інфекції, ймовірно, відповість на лікування. Відповідь «резистентна» вказує на те, що збудник, можливо, не відповість на лікування. Відповідь «проміжна чутливість» передбачає, що терапевтичний ефект препарату може бути неоднозначним або мікроорганізм може виявитися чутливим при використанні більш високих доз препарату. Проміжна чутливість також називається "помірною чутливістю".Показання до застосуванняІнфекційно-запальні захворювання, спричинені чутливими до кларитроміцину мікроорганізмами: інфекції нижніх дихальних шляхів (такі як бронхіт, пневмонія); інфекції верхніх дихальних шляхів (такі як фарингіт, синусит); інфекції шкіри та м'яких тканин (такі як фолікуліт, запалення підшкірної клітковини, пика); дисеміновані або локалізовані мікобактеріальні інфекції, спричинені Mycobacterium avium та Mycobacterium intracellulare; локалізовані інфекції, спричинені Mycobacterium chelonae, Mycobacterium fortuitum та Mycobacterium kansasii; профілактика поширення інфекції, зумовленої комплексом Mycobacterium avium (MAC) у ВІЛ-інфікованих пацієнтів із вмістом лімфоцитів CD4 (Т-хелперних лімфоцитів) не більше 100 за 1 мм3; ерадикація Helicobacter pylori та зниження частоти рецидивів виразки дванадцятипалої кишки; одонтогенні інфекції.Протипоказання до застосуванняПідвищена чутливість до кларитроміцину, інших компонентів препарату та інших макролідів. Одночасний прийом кларитроміцину з наступними препаратами: астемізол, цизаприд, пімозід, терфенадин (див. розділ «Взаємодія з іншими лікарськими засобами»). Одночасний прийом кларитроміцину з алкалоїдами ріжків, наприклад, ерготамін, дигідроерготамін (див. розділ «Взаємодія з іншими лікарськими засобами»). Одночасний прийом кларитроміцину з мідазоламом для внутрішнього застосування (див. розділ «Взаємодія з іншими лікарськими засобами»). Одночасний прийом кларитроміцину з інгібіторами ГМГ-КоА-редуктази (статинами), які значною мірою метаболізуються ізоферментом CYP3A4 (ловастатин, симвастатин), у зв'язку з підвищенням ризику міопатії, включаючи рабдоміоліз (див. розділ "Взаємодія з іншими"). Одночасний прийом кларитроміцину з колхіцином. Одночасний прийом кларитроміцину з тикагрелором або ранолазином. Подовження інтервалу QT (вроджене або документально підтверджене придбане подовження інтервалу QT) на електрокардіограмі (ЕКГ) в анамнезі, шлуночкова аритмія, включаючи шлуночкову тахікардію типу «пірует». Гіпокаліємія (ризик подовження інтервалу QT на ЕКГ). Тяжка печінкова недостатність, що протікає одночасно з нирковою недостатністю. Холестатична жовтяниця/гепатит в анамнезі, що розвинулися при застосуванні кларитроміцину (див. розділ «Особливі вказівки»). Порфирія. Період грудного вигодовування. Вік до 12 років (ефективність та безпека не встановлені). Ниркова недостатність середнього та тяжкого ступеня. Печінкова недостатність середнього та тяжкого ступеня. Одночасний прийом кларитроміцину з бензодіазепінами, такими як алпразол, триазол, мідазол для внутрішньовенного застосування (див. розділ «Взаємодія з іншими лікарськими засобами»). Одночасний прийом з препаратами, які метаболізуються ізоферментом CYP3A, наприклад, карбамазепін, цилостазол, циклоспорин, дизопірамід, метилпреднізолон, омепразол, непрямі антикоагулянти (наприклад, варфарин), хінідин, рифабутин, силденафіл, такролі. засобами»). Одночасний прийом з препаратами, що індукують ізофермент CYP3A4, наприклад, рифампіцин, фенітоїн, карбамазепін, фенобарбітал, препарати Звіробою продірявленого (див. розділ «Взаємодія з іншими лікарськими засобами»). Одночасний прийом кларитроміцину зі статинами, які не залежать від метаболізму ізоферменту CYP3A (наприклад, флувастатин) (див. розділ «Взаємодія з іншими лікарськими засобами»). Одночасний прийом із блокаторами «повільних» кальцієвих каналів, які метаболізуються ізоферментом CYP3A4 (наприклад, верапаміл, амлодипін, дилтіазем). Пацієнти з ішемічною хворобою серця (ІХС), тяжкою серцевою недостатністю, гіпомагніємією, порушеннями провідності або клінічно значущою брадикардією, а також пацієнти, які одночасно приймають антиаритмічні препарати ІА класу (хінідин, прокаїнамід) та ІІІ класу (дофетилід, аміодарон, соталол). Вагітність.Вагітність та лактаціяБезпека застосування кларитроміцину при вагітності та в період грудного вигодовування не встановлена. Застосування кларитроміцину при вагітності (особливо в І триместрі) можливе лише у випадку, коли відсутня альтернативна терапія, а потенційна користь для матері перевищує потенційний ризик для плода. Кларитроміцин виводиться із грудним молоком. При необхідності прийому в період грудного вигодовування годування груддю слід припинити. Протипоказаний особам віком до 12 років (ефективність та безпека не встановлені). Звичайна рекомендована доза кларитроміцину у дітей віком від 12 років – 250 мг 2 рази на день.Побічна діяКласифікація частоти розвитку побічних ефектів (кількість зареєстрованих випадків/кількість пацієнтів), рекомендована Всесвітньою організацією охорони здоров'я (ВООЗ): дуже часто ≥ 1/10 часто від ≥ 1/100 до < 1/10 нечасто від ≥ 1/1000 до < 1/100 рідко від ≥ 1/10000 до < 1/1000 дуже рідко <1/10000 частота невідома може бути оцінена з урахуванням наявних даних. Інфекційні та паразитарні захворювання: нечасто: целюліт(1), кандидоз, гастроентерит(2), вторинні інфекції(3) (у тому числі вагінальні); частота невідома: псевдомембранозний коліт, пика. Порушення з боку імунної системи: часто: шкірний висип; нечасто: анафілактоїдна реакція (1), гіперчутливість, дерматит бульозний (1), свербіж шкіри, кропив'янка, макулопапульозний висип (3); частота невідома: анафілактична реакція, ангіоневротичний набряк, синдром Стівенса-Джонсона, токсичний епідермальний некроліз, лікарський висип з еозинофілією та системною симптоматикою (DRESS-синдром). Порушення з боку обміну речовин та харчування: Нечасто: анорексія, зниження апетиту. Порушення психіки: часто: безсоння; нечасто: занепокоєння, підвищена збудливість (3); частота невідома: психотичні розлади, сплутаність свідомості, деперсоналізація, депресія, дезорієнтація, галюцинації, порушення сновидінь («жахливі» сновидіння), манія. Порушення з боку нервової системи: часто: головний біль, дисгезія (перекручення смаку); нечасто: непритомність(1), дискінезія(1), запаморочення, сонливість, тремор; частота невідома: судоми, парестезія, агевзія (втрата смакових відчуттів), паросмія, аносмія. Порушення з боку органу слуху та лабіринтні порушення: нечасто: вертиго, порушення слуху, дзвін у вухах; Частота невідома: глухота. Порушення з боку серця: нечасто: раптова зупинка серця (1), фібриляція передсердь (1), подовження інтервалу QT на ЕКГ, екстрасистолія (1), серцебиття; частота невідома: шлуночкова тахікардія, зокрема типу «пірует», фібриляція шлуночків. Порушення з боку судин: часто: вазодилатація; Частота невідома: кровотеча. Порушення з боку дихальної системи, органів грудної клітки та середостіння: нечасто: бронхіальна астма (1), носова кровотеча (2), тромбоемболія легеневої артерії (1). Порушення з боку травної системи: часто: діарея, блювання, диспепсія, нудота, біль у ділянці живота; нечасто: езофагіт(1), гастроезофагеальна рефлюксна хвороба(2), гастрит, прокталгія(2), стоматит, глосит, здуття живота(4), запор, сухість слизової оболонки порожнини рота, відрижка, метеоризм; частота невідома: гострий панкреатит, зміна кольору язика та зубів. Порушення з боку печінки та жовчовивідних шляхів: нечасто: холестаз(4), гепатит, у тому числі холестатичний або гепатоцелюлярний(4); частота невідома: печінкова недостатність, холестатична жовтяниця. Порушення з боку шкіри та підшкірних тканин: часто: інтенсивне потовиділення; частота невідома: акне, гострий генералізований екзантематозний пустульоз (ОГЕП). Порушення з боку скелетно-м'язової та сполучної тканини: нечасто: м'язовий спазм (3), кістково-м'язова скутість (1), міалгія (2); частота невідома: рабдоміоліз (2, *), міопатія. Порушення з боку нирок та сечовивідних шляхів: частота невідома: ниркова недостатність, інтерстиціальний нефрит. Загальні розлади та порушення у місці введення: нечасто: нездужання(4), гіпертермія(3), астенія, біль у грудній клітці(4), озноб(4), підвищена стомлюваність(4). Лабораторні та інструментальні дані: часто: - відхилення лабораторних показників функції печінки; нечасто: підвищення концентрації креатиніну(1), сечовини(1) у плазмі крові, зміна відношення альбумін/глобулін(1), лейкопенія, нейтропенія(4), еозинофілія(4), тромбоцитемія(3), підвищення активності аланінамінотрансферази (AJIT), аспартатамінотрансферази (ACT), гамма-глутамілтрансферази (ГГТ)(4), лужної фосфатази(4) (ЩФ), лактатдегідрогенази (ЛДГ)(4) у плазмі крові; частота невідома: агранулоцитоз, тромбоцитопенія, збільшення значення міжнародного нормалізованого відношення (МНО), подовження протромбінового часу, зміна кольору сечі, підвищення концентрації білірубіну у плазмі крові. Пацієнти зі зниженим імунітетом У пацієнтів зі СНІДом та іншими імунодефіцитними станами, які отримують кларитроміцин у більш високих дозах протягом тривалого часу для лікування мікобактеріальних інфекцій, часто важко відрізнити небажані ефекти препарату від симптомів ВІЛ-інфекції або супутнього захворювання. Найчастішими небажаними явищами у пацієнтів, які приймали добову дозу кларитроміцину, що дорівнює 1000 мг, були: нудота, блювання, дисгевзія, біль у ділянці живота, діарея, шкірний висип, метеоризм, головний біль, запор, порушення слуху, підвищення активності ACT та АЛ плазмі крові. Також відзначалися випадки небажаних явищ із низькою частотою виникнення, такі як задишка, безсоння та сухість слизової оболонки порожнини рота. У пацієнтів із зниженим імунітетом проводили оцінку лабораторних показників, аналізуючи їх значні відхилення від норми (різке підвищення чи зниження). На підставі даного критерію у 2-3% пацієнтів, які отримували кларитроміцин у дозі 1000 мг щоденно, було зареєстровано значне підвищення активності ACT та АЛТ у плазмі, а також зниження кількості лейкоцитів та тромбоцитів. У невеликої кількості пацієнтів також було зареєстровано підвищення концентрації залишкового азоту сечовини у плазмі. *У деяких повідомленнях про рабдоміоліз кларитроміцин приймався одночасно з іншими лікарськими засобами (ЛЗ), з прийомом яких, як відомо, пов'язаний розвиток рабдоміолізу (статини, фібрати, колхіцин або алопуринол). (1) Повідомлення про дані побічних реакцій були отримані лише при застосуванні кларитроміцину у лікарській формі ліофілізат для приготування розчину для інфузій. (2) Повідомлення про дані побічних реакцій були отримані лише при застосуванні кларитроміцину у лікарській формі таблетки з пролонгованим вивільненням, покриті плівковою оболонкою. (3) Повідомлення про дані побічних реакцій були отримані лише при застосуванні кларитроміцину у лікарській формі порошок для приготування суспензії для прийому внутрішньо. (4) Повідомлення про дані побічних реакцій були отримані лише при застосуванні кларитроміцину у лікарській формі таблетки, покриті плівковою оболонкою.Взаємодія з лікарськими засобамиЗастосування наступних лікарських засобів одночасно з кларитроміцином протипоказане у зв'язку з можливістю розвитку серйозних побічних ефектів. Цизаприд, пімозід, терфенадин та астемізол При одночасному прийомі кларитроміцину з цизапридом, пимозидом, терфенадином або астемізолом повідомлялося про підвищення концентрації останніх у плазмі крові, що може призвести до подовження інтервалу QT на ЕКГ та появі серцевих аритмій, включаючи шлуночкову тахікардію (в тому числі шлуночкову та фібриляцію шлуночків (див. розділ "Протипоказання"). Алкалоїди ріжків Постмаркетингові дослідження показують, що при одночасному застосуванні кларитроміцину з ерготаміном або дигідроерготаміном можливі наступні ефекти, пов'язані з гострим отруєнням препаратами групи ерготамінів: судинний спазм, ішемія кінцівок та інших тканин, включаючи центральну нервову систему (ЦНС). Одночасне застосування кларитроміцину та алкалоїдів ріжків протипоказане (див. розділ «Протипоказання»). Інгібітори ГМГ-КоА-редуктази (статини) Одночасний прийом кларитроміцину з ловастатином або симвастатином протипоказаний (див. розділ «Протипоказання») у зв'язку з тим, що дані статини значною мірою метаболізуються ізоферментом CYP3A4, і одночасне застосування з кларитроміцином підвищує їх сироваткові концентрації, що призводить до підвищення рабдоміоліз. Повідомлялося про випадки рабдоміолізу у пацієнтів, які приймали кларитроміцин одночасно з цими препаратами. У разі необхідності застосування кларитроміцину слід припинити прийом ловастатину або симвастатину на час терапії. Кларитроміцин слід застосовувати з обережністю у разі комбінованої терапії з іншими статинами. Рекомендується застосовувати статини, метаболізм яких не залежить від ізоферменту CYP3A (наприклад, флувастатин). У разі потреби одночасного прийому рекомендується приймати найменшу дозу статину. Слід контролювати розвиток ознак та симптомів міопатії. Мідазолам для прийому внутрішньо При одночасному застосуванні внутрішньо мідазоламу та кларитроміцину у формі таблеток (500 мг 2 рази на день) відзначалося збільшення AUC мідазоламу у 7 разів. Одночасний прийом кларитроміцину та мідазоламу для прийому внутрішньо протипоказаний (див. розділ «Протипоказання»). Вплив інших лікарських засобів на кларитроміцин Лікарські препарати, що є індукторами ізоферменту CYP3A (наприклад, рифампіцин, фенітоїн, карбамазепін, фенобарбітал, препарати Звіробою продірявленого) можуть індукувати метаболізм кларитроміцину. Це може призвести до субтерапевтичної концентрації кларитроміцину та, відповідно, до зниження його ефективності. Крім того, необхідно спостерігати за концентрацією індуктора ізоферменту CYP3A у плазмі крові, яка може підвищитися через інгібування ізоферменту CYP3A кларитроміцином. При одночасному застосуванні рифабутину та кларитроміцину спостерігалося підвищення концентрації рифабутину та зниження концентрації кларитроміцину в плазмі крові з підвищеним ризиком розвитку увеїту. Наступні препарати мають доведений або передбачуваний вплив на концентрацію кларитроміцину в плазмі крові, у разі їх одночасного застосування з кларитроміцином може знадобитися корекція доз або перехід на альтернативне лікування Ефавіренз, невірапін, рифампіцин, рифабутин та рифапентин Потужні індуктори системи цитохрому Р450, такі як ефавіренз, невірапін, рифампіцин, рифабутин і рифапентин можуть прискорювати метаболізм кларитроміцину і, таким чином, знижувати концентрацію кларитроміцину в плазмі крові та послаблювати терапевтичний ефект, і разом з тим кларитроміцину – метаболіту, який також є мікробіологічно активним. Оскільки мікробіологічна активність кларитроміцину та 14-ОН-кларитроміцину відрізняється щодо різних бактерій, терапевтичний ефект може знижуватися при одночасному застосуванні кларитроміцину та індукторів системи цитохрому Р450. Етравірін Концентрація кларитроміцину в плазмі знижується при одночасному застосуванні з етравірином, але підвищується концентрація в плазмі активного метаболіту 14-ОН-кларитроміцину. Оскільки 14-ОН-кларитроміцин має низьку активність по відношенню до інфекцій MAC, може змінюватися загальна активність щодо цих збудників, тому для лікування MAC слід розглядати альтернативне лікування. Флуконазол Одночасний прийом флуконазолу в дозі 200 мг щоденно та кларитроміцину в дозі 500 мг 2 рази на день у 21 здорового добровольця призвело до збільшення середнього значення мінімальної рівноважної концентрації кларитроміцину та AUC на 33 % та 18 % відповідно. При цьому одночасний прийом значно не впливав на середню рівноважну концентрацію активного метаболіту 14-ОН-кларитроміцину. Корекція дози кларитроміцину у разі одночасного прийому флуконазолу не потрібна. Рітонавір Фармакокінетичне дослідження показало, що одночасний прийом ритонавіру в дозі 200 мг кожні 8 годин та кларитроміцину в дозі 500 мг кожні 12 годин призвів до помітного пригнічення метаболізму кларитроміцину. При одночасному прийомі ритонавіру С(mах) кларитроміцину в плазмі збільшилася на 31%, C(min) збільшилася на 182% і AUC збільшилася на 77%. Було відзначено практично повне придушення утворення 14-ОН-кларитроміцину. Завдяки широкому терапевтичному діапазону кларитроміцину зменшення його дози у пацієнтів із нормальною нирковою функцією не потрібне. У пацієнтів з нирковою недостатністю доцільно розглянути наступні варіанти корекції дози: при КК 30-60 мл/хв доза кларитроміцину повинна бути зменшена на 50 %, при КК менше 30 мл/хв доза кларитроміцину повинна бути зменшена на 75 %.Ритонавір не слід одночасно приймати з кларитроміцином у дозах, що перевищують 1 г на добу. Подібні корекції доз повинні розглядатися у пацієнтів зі зниженою функцією нирок, якщо ритонавір використовується як фармакокінетичний «підсилювач» при застосуванні інших інгібіторів протеази ВІЛ, включаючи атазанавір та саквінавір (див. підрозділ «Двонаправлена взаємодія лікарських засобів»). Дія кларитроміцину на інші лікарські препарати Антиаритмічні засоби (хінідин та дизопірамід) Можливе виникнення шлуночкової тахікардії типу «пірует» при одночасному застосуванні кларитроміцину та хінідину або дизопіраміду. При одночасному прийомі кларитроміцину з цими препаратами слід регулярно проводити контроль ЕКГ щодо подовження інтервалу QT, а також слід контролювати сироваткові концентрації цих препаратів. У постмаркетинговому періоді застосування повідомлялося про випадки розвитку гіпоглікемії при одночасному прийомі кларитроміцину та дизопіраміду. Необхідно контролювати концентрацію глюкози крові при одночасному застосуванні кларитроміцину та дизопіраміду. Гіпоглікемічні засоби для внутрішнього застосування/інсулін При одночасному застосуванні кларитроміцину та гіпоглікемічних засобів для прийому внутрішньо (наприклад, похідні сульфонілсечовини) та/або інсуліну може спостерігатися виражена гіпоглікемія. Одночасне застосування кларитроміцину з деякими гіпоглікемічними препаратами (наприклад, натеглінід, піоглітазон, репаглінід та росиглітазон) може призвести до інгібування ізоферменту CYP3A кларитроміцином, внаслідок чого може розвинутись гіпоглікемія. Рекомендується ретельний контроль за концентрацією глюкози крові. Взаємодія зумовлена ізоферментом CYP3A Одночасний прийом кларитроміцину, який, як відомо, інгібує ізофермент CYP3A, та препаратів, що первинно метаболізуються ізоферментом CYP3A, може асоціюватися із взаємним підвищенням їх концентрацій, що може посилити або продовжити як терапевтичні, так і побічні ефекти. Кларитроміцин слід обережно застосовувати пацієнтам, які отримують препарати, які є субстратами ізоферменту CYP3A, особливо якщо ці препарати мають вузький терапевтичний діапазон (наприклад, карбамазепін) та/або препарати, які інтенсивно метаболізуються цим ізоферментом. У разі необхідності повинна проводитися корекція дози препарату, який приймається одночасно з кларитроміцином. Також, по можливості, повинен проводитися моніторинг сироваткових концентрацій препаратів, що первинно метаболізуються ізоферментом CYP3A. Метаболізм наступних препаратів/класів здійснюється тим самим ізоферментом CYP3A, що і метаболізм кларитроміцину: алпразолам, карбамазепін, цилостазол, циклоспорин, дизопірамід, метилпреднізолон, мідазолам, омепразол, непрямі антикоагулянти (наприклад, варфаніни рифабутин, силденафіл, такролімус, тріазолам та вінбластин. Також до агоністів ізоферменту CYP3A належать такі препарати, що протипоказані до одночасного застосування з кларитроміцином: астемізол, цизаприд, пімозід, терфенадин, ловастатин, симвастатин та алкалоїди ріжків (див. розділ «Протипоказання»). До препаратів, що взаємодіють подібним чином через інші ізоферменти в рамках системи цитохрому Р450, відносяться: фенітоїн, теофілін та вальпроєва кислота. Непрямі антикоагулянти При одночасному прийомі варфарину та кларитроміцину можлива кровотеча, виражене збільшення МНО та подовження протромбінового часу. У разі одночасного застосування з варфарином або іншими непрямими антикоагулянтами необхідно контролювати МНО та протромбіновий час. Омепразол Кларитроміцин (по 500 мг кожні 8 годин) досліджувався у здорових дорослих добровольців у поєднанні з омепразолом (по 40 мг щодня). При одночасному застосуванні кларитроміцину та омепразолу рівноважні плазмові концентрації омепразолу були збільшені (C(max), AUC(0-24) та Т(1/2) збільшилися на 30%, 89% та 34%, відповідно). Середнє значення pH шлунка протягом 24 годин склало 5,2 (при прийомі омепразолу окремо) і 5,7 (при прийомі омепразолу одночасно з кларитроміцином). Силденафіл, тадалафіл та варденафіл Кожен із цих інгібіторів фосфодіестерази метаболізується принаймні частково за участю ізоферменту CYP3A. У той же час, ізофермент CYP3A може інгібуватися в присутності кларитроміцину. Одночасне застосування кларитроміцину з силденафілом, тадалафілом або варденафілом може призвести до збільшення інгібуючої дії на фосфодіестеразу. При застосуванні цих препаратів одночасно з кларитроміцином слід розглянути можливість зменшення дози силденафілу, тадалафілу та варденафілу. Теофілін, карбамазепін При одночасному застосуванні кларитроміцину та теофіліну або карбамазепіну можливе підвищення концентрації даних препаратів у системному кровотоку. Толтеродін Первинний метаболізм толтеродину здійснюється через ізофермент CYP2D6. Однак у частині популяції, позбавленої CYP2D6, метаболізм відбувається через ізофермент CYP3A. У цій групі населення пригнічення ізоферменту CYP3A призводить до значно більших концентрацій толтеродину в сироватці крові. У популяції з низьким рівнем метаболізму через ізофермент CYP2D6 може знадобитися зниження дози толтеродину при одночасному застосуванні інгібіторів ізоферменту CYP3A, таких як кларитроміцин. Бензодіазепіни (наприклад, алпразолам, мідазолам, тріазолам) При одночасному застосуванні мідазоламу та таблеток кларитроміцину (500 мг 2 рази на день) відзначалося збільшення AUC мідазоламу у 2,7 раза після внутрішньовенного введення мідазоламу. Якщо одночасно з кларитроміцином застосовується внутрішньовенна форма мідазоламу, слід ретельно контролювати стан пацієнта для можливої корекції дози. Введення лікарського препарату через слизову оболонку порожнини рота, що дає можливість обійти пресистемну елімінацію лікарського препарату, швидше за все, призведе до взаємодії аналогічного до того, що спостерігається при внутрішньовенному введенні мідазоламу, а не при прийомі внутрішньо. Такі ж запобіжні заходи слід застосовувати і до інших бензодіазепінів, які метаболізуються ізоферментом CYP3A, включаючи триазолів та алпразолів. Для бензодіазепінів,виведення яких не залежить від ізоферменту CYP3A (темазепам, нітразепам, лоразепам), малоймовірно клінічно значуща взаємодія з кларитроміцином. При одночасному застосуванні кларитроміцину та триазоламу можлива дія на ЦНС, наприклад, сонливість та сплутаність свідомості. У зв'язку з цим у разі одночасного застосування рекомендується стежити за симптомами порушення ЦНС. Взаємодія з іншими препаратами Колхіцін Колхіцин є субстратом як для ізоферменту CYP3A, так і для білка-переносника P-глікопротеїну (Pgp). Відомо, що кларитроміцин та інші макроліди є інгібіторами ізоферменту CYP3A та Pgp. При одночасному застосуванні кларитроміцину та колхіцину інгібування Pgp та/або ізоферменту CYP3A може призвести до посилення дії колхіцину. Слід контролювати розвиток клінічних симптомів отруєння колхіцином. Зареєстровані постмаркетингові повідомлення про випадки отруєння колхіцином при одночасному прийомі з кларитроміцином, частіше у пацієнтів похилого віку. Деякі з описаних випадків відбувалися у пацієнтів із нирковою недостатністю. Як повідомлялося, деякі випадки закінчувалися летальним кінцем. Одночасне застосування кларитроміцину та колхіцину протипоказане (див. розділ «Протипоказання»). Дігоксин Передбачається, що дигоксин є субстратом PGP. Відомо, що кларитроміцин пригнічує Pgp. При одночасному застосуванні кларитроміцину та дигоксину інгібування Pgp кларитроміцином може призвести до посилення дії дигоксину. Одночасний прийом дигоксину та кларитроміцину також може призвести до підвищення сироваткової концентрації дигоксину. У деяких пацієнтів спостерігалися клінічні симптоми отруєння дигоксином, включаючи потенційно летальні аритмії. При одночасному прийомі кларитроміцину та дигоксину слід ретельно контролювати концентрацію дигоксину у сироватці крові. Зідовудін Одночасний прийом таблеток кларитроміцину та зидовудину внутрішньо дорослими ВІЛ-інфікованими пацієнтами може призвести до зниження рівноважної концентрації зидовудину в плазмі крові. Оскільки кларитроміцин впливає на всмоктування зидовудину при прийомі внутрішньо, взаємодії можна значно уникнути, приймаючи кларитроміцин і зидовудін з інтервалом в 4 години. Подібної взаємодії не спостерігали у ВІЛ-інфікованих дітей, які приймали дитячу суспензію кларитроміцину з зидовудином або дидезоксіїнозином. Оскільки кларитроміцин може перешкоджати всмоктуванню зидовудину при їх одночасному прийомі внутрішньо у дорослих пацієнтів, така взаємодія навряд чи можлива при застосуванні кларитроміцину внутрішньовенно. Фенітоїн та вальпроєва кислота Є дані про взаємодію інгібіторів ізоферменту CYP3A (включаючи кларитроміцин) з препаратами, які не метаболізуються за допомогою ізоферменту CYP3A (фенітоїн та вальпроєва кислота). Для цих препаратів при одночасному застосуванні з кларитроміцином рекомендується визначення їх сироваткових концентрацій, оскільки є повідомлення про їх підвищення. Двоспрямована взаємодія лікарських засобів Атазанавір Кларитроміцин та атазанавір є як субстратами, так і інгібіторами ізоферменту CYP3A. Існує свідчення двонаправленої взаємодії цих препаратів. Одночасне застосування кларитроміцину (500 мг 2 рази на день) та атазанавіру (400 мг 1 раз на день) може призвести до дворазового збільшення впливу кларитроміцину та зменшення впливу 14-ОН-кларитроміцину на 70 % зі збільшенням AUC атазанавіру на 28 %. Завдяки широкому терапевтичному діапазону кларитроміцину зменшення його дози у пацієнтів із нормальною нирковою функцією не потрібне. У пацієнтів з нирковою недостатністю середнього ступеня тяжкості (КК 30-60 мл/хв) доза кларитроміцину повинна бути зменшена на 50%. У пацієнтів з КК менше 30 мл/хв дозу кларитроміцину слід зменшити на 75%, застосовуючи для цього відповідну лікарську форму кларитроміцину.Кларитроміцин у дозах, що перевищують 1000 мг на добу, не можна застосовувати одночасно з інгібіторами протеаз. Блокатори «повільних» кальцієвих каналів При одночасному застосуванні кларитроміцину та блокаторів «повільних» кальцієвих каналів, які метаболізуються ізоферментом CYP3A4 (наприклад, верапаміл, амлодипін, дилтіазем), слід бути обережним, оскільки існує ризик виникнення артеріальної гіпотензії. При одночасному застосуванні можуть підвищуватися плазмові концентрації кларитроміцину та блокаторів «повільних» кальцієвих каналів. Артеріальна гіпотензія, брадіаритмія та лактоацидоз можливі при одночасному прийомі кларитроміцину та верапамілу. Ітраконазол Кларитроміцин та ітраконазол є субстратами та інгібіторами ізоферменту CYP3A, що визначає двонаправлену взаємодію препаратів. Кларитроміцин може підвищити концентрацію ітраконазолу в плазмі, тоді як ітраконазол може підвищити плазмову концентрацію кларитроміцину. Пацієнтів, які одночасно приймають ітраконазол та кларитроміцин, слід ретельно обстежити на наявність симптомів посилення або збільшення тривалості фармакологічних ефектів цих препаратів. Саквінавір Кларитроміцин та саквінавір є субстратами та інгібіторами ізоферменту CYP3A, що визначає двоспрямовану взаємодію препаратів. Одночасне застосування кларитроміцину (500 мг 2 рази на день) та саквінавіру (у м'яких желатинових капсулах, 1200 мг 3 рази на день) у 12 здорових добровольців викликало збільшення AUC та С(mах )саквінавіру в плазмі крові на 177 % та 187 %, , У порівнянні з прийомом саквінавіру окремо. Значення AUC та С(mах) кларитроміцину були приблизно на 40 % вищими, ніж при терапії одним кларитроміцином. При одночасному застосуванні цих двох препаратів протягом обмеженого часу у дозах/складах, зазначених вище, корекція дози не потрібна. Результати дослідження лікарських взаємодій із застосуванням саквінавіру в м'яких желатинових капсулах можуть не відповідати ефектам,спостерігається при застосуванні саквінавіру в твердих желатинових капсулах. Результати дослідження лікарських взаємодій при терапії саквінавіром окремо можуть не відповідати ефектам, що спостерігаються при терапії комбінацією саквінавір/ритонавір. При прийомі саквінавіру одночасно з ритонавіром слід враховувати потенційний вплив ритонавіру на кларитроміцин.Спосіб застосування та дозиВсередину, незалежно від часу їди. Звичайна рекомендована доза кларитроміцину у дорослих та дітей старше 12 років – 250 мг 2 рази на день. Препарат Фромілід 500 мг 2 рази на день застосовують у разі більш тяжких інфекцій. Звичайна тривалість лікування становить від 5 до 14 днів. Виняток становлять позалікарняна пневмонія та синусит, які вимагають лікування від 6 до 14 днів. Дози для лікування мікобактеріальних інфекцій, крім туберкульозу При мікобактеріальних інфекціях рекомендована доза препарату Фромілід 500 мг 2 рази на день. Лікування дисемінованих MAC інфекцій у пацієнтів зі СНІД слід продовжувати доти, доки є клінічна та мікробіологічна ефективність. Кларитроміцин слід призначати у комбінації з іншими антимікробними препаратами, активними щодо цих збудників. Тривалість лікування інших нетуберкульозних мікобактеріальних інфекцій встановлює лікар. Для профілактики інфекцій, спричинених MAC Рекомендована доза препарату Фромілід для дорослих – 500 мг 2 рази на день. При одонтогенних інфекціях доза препарату Фромілід становить 250 мг 2 рази на день протягом 5 днів. Для ерадикації Helicobacter pylori У пацієнтів з виразковою хворобою, викликаною інфекцією Helicobacter pylori, препарату Фромілід® можна застосовувати по 500 мг 2 рази на день у комбінації з іншими антимікробними препаратами та інгібіторами протонного насоса протягом 7-14 днів, відповідно до національних та міжнародних рекомендацій. Helicobacter pylori. Пацієнти з нирковою недостатністю Пацієнтам з КК менше 30 мл/хв призначають половину звичайної дози кларитроміцину, тобто 250 мг 1 раз на день або при більш тяжких інфекціях по 250 мг 2 рази на день. Лікування таких пацієнтів продовжують трохи більше 14 днів.ПередозуванняСимптоми: прийом внутрішньо великої дози кларитроміцину може викликати симптоми порушень з боку шлунково-кишкового тракту. У одного пацієнта з біполярним розладом в анамнезі після прийому 8 г кларитроміцину описані зміни психічного стану, параноїдальна поведінка, гіпокаліємія та гіпоксемія. Лікування: при передозуванні слід видалити неабсорбований препарат із шлунково-кишкового тракту (промивання шлунка, прийом активованого вугілля та ін.) та провести симптоматичну терапію. Гемодіаліз та перитонеальний діаліз не мають істотного впливу на концентрацію кларитроміцину в сироватці крові, що характерно і для інших лікарських препаратів групи макролідів.Запобіжні заходи та особливі вказівкиТривалий прийом антибіотиків може призводити до утворення колоній зі збільшенням кількості нечутливих бактерій та грибів. При суперінфекції слід призначити відповідну терапію. При застосуванні кларитроміцину повідомлялося про печінкову дисфункцію (підвищення активності «печінкових» ферментів у плазмі крові, гепатоцелюлярний та/або холестатичний гепатит із жовтяницею або без). Печінкова дисфункція може бути важкою, але є оборотною. Є випадки печінкової недостатності з летальним результатом, головним чином пов'язані з наявністю серйозних супутніх захворювань та/або одночасним застосуванням інших лікарських засобів. При появі ознак і симптомів гепатиту, таких як анорексія, жовтяниця, потемніння сечі, свербіж шкіри, болючість живота при пальпації, необхідно негайно припинити терапію кларитроміцином. За наявності хронічних захворювань печінки необхідно проводити регулярний контроль активності печінкових ферментів сироватки крові. При лікуванні практично всіма антибактеріальними засобами, у тому числі макролідами, описані випадки псевдомембранозного коліту, тяжкість якого може змінюватись від легкого до загрозливого життя. При лікуванні практично всіма антибактеріальними препаратами, у тому числі кларитроміцином, описані випадки Clostridium difficile-асоційованої діареї, тяжкість якої може змінюватись від легкої діареї до загрозливого життя коліту. Антибактеріальні препарати можуть змінити нормальну мікрофлору кишечника, що може спричинити зростання Clostridium difficile. Псевдомембранозний коліт, викликаний Clostridium difficile, необхідно підозрювати у всіх пацієнтів з появою діареї після застосування антибактеріальних засобів. Після проведення курсу антибіотикотерапії потрібне ретельне медичне спостереження за пацієнтом.Описувалися випадки розвитку псевдомембранозного коліту через 2 місяці після застосування антибіотиків. З боку серцево-судинної системи При лікуванні макролідами, включаючи кларитроміцин, спостерігалося збільшення часу реполяризації шлуночків серця та подовження інтервалу QT, що сприяло ризику розвитку серцевої аритмії та шлуночкової тахікардії типу «пірует» (див. розділ «Побічна дія»). У зв'язку з тим, що такі ситуації можуть призвести до збільшення ризику розвитку шлуночкових аритмій (у тому числі шлуночкової тахікардії типу «пірует»), кларитроміцин слід застосовувати з обережністю у таких пацієнтів: пацієнти з ІХС, серцевою недостатністю тяжкого ступеня, порушеннями провідності або клінічно значущою брадикардією; пацієнти з порушеннями водно-електролітного обміну, такими як гіпомагніємія. Кларитроміцин не слід застосовувати у пацієнтів з гіпокаліємією (див. розділ "Протипоказання"); пацієнти, які одночасно застосовують інші лікарські препарати, що призводять до подовження інтервалу QT (див. розділ «Взаємодія з іншими лікарськими засобами»). Протипоказано одночасне застосування кларитроміцину з астемізолом, цизапридом, пимозидом та терфенадином (див. розділ «Протипоказання»). Кларитроміцин не слід застосовувати у пацієнтів із вродженим або документально підтвердженим подовженням інтервалу QT, а також із вказівками в анамнезі на епізоди шлуночкової аритмії (див. розділ «Протипоказання»). У ході епідеміологічних досліджень з вивчення ризику несприятливих серцево-судинних наслідків при застосуванні макролідів було отримано неоднозначні результати. У деяких короткострокових наглядових дослідженнях було встановлено ризик розвитку аритмії, інфаркту міокарда та смерті від серцево-судинних захворювань, пов'язаний із застосуванням макролідів, включаючи кларитроміцин. При призначенні кларитроміцину слід співвідносити передбачувану користь від прийому препарату з цими ризиками. Можливий розвиток перехресної резистентності до кларитроміцину та інших антибіотиків групи макролідів, а також лінкоміцину та кліндаміцину. Враховуючи зростаючу резистентність Streptococcus pneumoniae до макролідів, важливо проводити тестування чутливості при призначенні кларитроміцину пацієнтам із позалікарняною пневмонією. При шпитальній пневмонії кларитроміцин слід застосовувати у комбінації з відповідними антибіотиками. Інфекції шкіри та м'яких тканин легкої та середньої тяжкості найчастіше викликані Staphylococcus aureus та Streptococcus pyogenes. При цьому обидва збудники можуть бути стійкими до макролідів. Тому важливо проводити тест визначення чутливості до антибіотиків. Макроліди можна застосовувати при інфекціях, викликаних Corynebacterium minutissimum, захворюваннях acne vulgaris і бешихі, а також у тих ситуаціях, коли не можна застосовувати пеніцилін. У разі появи гострих реакцій гіперчутливості, таких як анафілактична реакція, тяжкі шкірні небажані реакції (ТКНР) (наприклад, ОГЭП), синдром Стівенса-Джонсона, токсичний епідермальний некроліз та лікарський висип з еозинофілією та системною симптоматикою (DRESS- припинити прийом кларитроміцину та почати відповідну терапію. У разі одночасного застосування з варфарином або іншими непрямими антикоагулянтами необхідно контролювати МНО та протромбіновий час (див. розділ «Взаємодія з іншими лікарськими засобами»). Застосування при хронічних захворюваннях: Протипоказаний пацієнтам з тяжкою печінковою недостатністю, що протікає одночасно з нирковою недостатністю. Застосовувати з обережністю пацієнтам з нирковою та печінковою недостатністю середнього та тяжкого ступеня. Пацієнти з нирковою недостатністю Пацієнтам з КК менше 30 мл/хв призначають половину звичайної дози кларитроміцину, тобто 250 мг 1 раз на день або при більш тяжких інфекціях по 250 мг 2 рази на день. Лікування таких пацієнтів продовжують трохи більше 14 днів. Вплив на керування транспортними засобами: Дані щодо впливу кларитроміцину на здатність до керування автомобілем та механізмами відсутні. Слід бути обережними при керуванні транспортними засобами та механізмами, враховуючи потенційну можливість запаморочення, вертиго, сплутаності свідомості та дезорієнтації, які можуть виникнути при застосуванні даного препарату.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
378,00 грн
164,00 грн
Склад, форма випуску та упаковкакларитроміцин таблетки, вкриті плівковою оболонкою 1 таблетка, покрита плівковою оболонкою, 250 мг/500 мг містить: Ядро: Діюча речовина: Кларитроміцин 250,00 мг/500,00 мг Допоміжні речовини: Крохмаль кукурудзяний, целюлоза мікрокристалічна (тип 101), целюлоза мікрокристалічна (тип 102), кремнію діоксид колоїдний, крохмаль прежелатинізований, полакрилін калію, тальк, магнію стеарат Оболонка плівкова: Гіпромелоза 6 cps, тальк, барвник заліза оксид жовтий (Е172), пропіленгліколь, титану діоксид (Е171)Опис лікарської формиТаблетки 250 мг: Овальні, двоопуклі таблетки, покриті плівковою оболонкою світло-коричнево-жовтого кольору. Вид на зламі: шорстка маса білого кольору із шаром оболонки світло-коричнево-жовтого кольору. Таблетки 500 мг: Овальні, двоопуклі таблетки, покриті плівковою оболонкою світло-коричнево-жовтого кольору. Вид на зламі: шорстка маса білого кольору із шаром оболонки світло-коричнево-жовтого кольору.Фармакотерапевтична групаантибіотик – макролідФармакокінетикаВсмоктування Препарат швидко всмоктується з шлунково-кишкового тракту. Абсолютна біодоступність становить близько 50%. При багаторазовому прийомі дози препарату кумуляції практично не виявлено, характер метаболізму в організмі людини не змінювався. Їда безпосередньо перед прийомом препарату збільшувала біодоступність препарату в середньому на 25 %. Кларитроміцин може застосовуватися незалежно від часу їди. Розподіл, метаболізм та виведення In vitro Кларитроміцин зв'язується з білками плазми на 70% у концентрації від 0,45 до 4,5 мкг/мл. При концентрації 45 мкг/мл зв'язування знижується до 41%, ймовірно, через насичення місць зв'язування. Це спостерігається лише при концентраціях, що багаторазово перевищують терапевтичну концентрацію. Invivo Дослідження в умовах in vivo на тваринах показали, що кларитроміцин присутній у всіх тканинах, за винятком центральної нервової системи (ЦНС), у концентраціях, що у кілька разів перевищують плазмові. Найбільш високі концентрації (в 10-20 разів вище плазмових) виявлялися в печінці та легенях. Здорові добровольці При застосуванні кларитроміцину в дозі 250 мг 2 рази на день максимальна рівноважна концентрація (С mах ) кларитроміцину та 14-ОН-кларитроміцину в плазмі крові досягалася через 2-3 дні і становила 1 мкг/мл та 0,6 мкг/мл відповідно. Період напіввиведення (Т 1/2 ) кларитроміцину та його основного метаболіту склав 3-4 години та 5-6 годин, відповідно. При застосуванні кларитроміцину в дозі 500 мг 2 рази на день . 83 мкг/мл відповідно. Т 1/2 кларитроміцину та його основного метаболіту становив 4,5-4,8 години та 6,9-8,7 години, відповідно. З mах 14-ОН-кларитроміцину в плазмі крові не збільшувалася пропорційно прийнятій внутрішньо дозі кларитроміцину, у той час як Т 1/2 як кларитроміцину, так і 14-ОН-кларитроміцин мав тенденцію до подовження з підвищенням дози. Така нелінійна фармакокінетика кларитроміцину у поєднанні зі зменшенням утворення 14-гідроксильованих та N-деметилованих продуктів при високих дозах вказує на нелінійний метаболізм кларитроміцину, який стає більш вираженим при високих дозах. Нирками виводиться близько 37,9% після прийому внутрішньо кларитроміцину в дозі 250 мг і 46% після прийому кларитроміцину в дозі 1200 мг, через кишечник виводиться близько 40,2% та 29,1% відповідно. Пацієнти Кларитроміцин та 14-ОН-кларитроміцин швидко проникають у тканини та рідини організму. Є обмежені дані, що свідчать про те, що концентрація кларитроміцину в цереброспінальній рідині при внутрішньому прийомі незначна (т. Е. Тільки 1-2% від концентрації в сироватці крові при нормальній проникності гематоенцефалічного бар'єру). Концентрація в тканинах зазвичай у кілька разів вища, ніж у сироватці крові. У таблиці наведено приклади тканинних та сироваткових концентрацій: Концентрації (250 мг кожні 12 годин) Вид тканини Тканинні (мкг/г) Сироваткові (мкг/мл) Мигдалики 1,6 0,8 Легкі 8,8 1,7 Порушення функції печінки У пацієнтів із середнім та тяжким ступенем порушення функції печінки, але із збереженою функцією нирок, корекція дози кларитроміцину не потрібна. Рівноважна концентрація у плазмі крові та системний кліренс кларитроміцину не відрізняються у пацієнтів цієї групи та здорових пацієнтів. Рівноважна концентрація 14-ОН-кларитроміцину у пацієнтів з порушеннями функції печінки нижча, ніж у здорових добровольців. Порушення функції нирок При порушенні функції нирок збільшуються З mах та мінімальна концентрація (З min ) кларитроміцину в плазмі крові, Т 1/2 , площа під кривою «концентрація-час» (AUC) кларитроміцину та його метаболіту (14-ОН-кларитроміцину). Константа елімінації та виведення нирками зменшуються. Ступінь змін цих параметрів залежить від рівня порушення функції нирок. Пацієнти похилого віку У пацієнтів похилого віку концентрація кларитроміцину та його метаболіту 14-ОН-кларитроміцину в плазмі була вищою, а виведення повільніше, ніж у групи молодих людей. Однак після корекції з урахуванням ниркового кліренсу креатиніну (КК) не було відмінностей у обох групах. Таким чином, основний вплив на фармакокінетичні параметри кларитроміцину має функція нирок, а не вік. Пацієнти з мікобактеріальними інфекціями Рівноважні концентрації кларитроміцину і 14-ОН-кларитроміцину у пацієнтів з ВІЛ-інфекцією, які отримували кларитроміцин у нормальних дозах (500 мг 2 рази на день), були подібними до таких показників у здорових людей. Однак при застосуванні кларитроміцину у більш високих дозах, які можуть бути потрібні для лікування мікобактеріальних інфекцій, концентрації антибіотика можуть значно перевищувати звичайні. У пацієнтів з ВІЛ-інфекцією, які приймали кларитроміцин у дозі 1000 мг/добу або 2000 мг/добу на 2 прийоми, рівноважні значення С mах зазвичай становили 2-4 мкг/мл та 5-10 мкг/мл відповідно. При застосуванні кларитроміцину у вищих дозах відзначалося подовження Т 1/2У порівнянні з таким показником у здорових добровольців, які отримували кларитроміцин у нормальних дозах. Підвищення концентрації у плазмі крові та подовження Т 1/2 при застосуванні кларитроміцину у більш високих дозах пов'язане з нелінійною фармакокінетикою препарату. Комбіноване лікування з омепразолом Кларитроміцин по 500 мг 3 рази на добу в комбінації з омепразолом у дозі 40 мг на добу сприяє подовженню Т 1/2 та збільшенню AUC 0-24 омепразолу. У всіх пацієнтів, які отримували комбіновану терапію, у порівнянні з пацієнтами, які отримували один омепразол, спостерігалося підвищення на 89% AUC 0-24 та на 34% Т 1/2 омепразолу. У кларитроміцину С mах , C min та AUC 0 - 8збільшувалися, відповідно, на 10%, 27% та 15% порівняно з аналогічними показниками при застосуванні кларитроміцину без омепразолу. У рівноважному стані концентрації кларитроміцину в слизовій оболонці шлунка через 6 годин після прийому кларитроміцину в групі, що отримувала комбінацію, у 25 разів перевищували такі показники порівняно з пацієнтами, які отримували один кларитроміцин. Концентрації кларитроміцину в тканинах шлунка через 6 годин після прийому кларитроміцину та омепразолу в 2 рази перевищували дані, отримані у групі пацієнтів, які отримували один кларитроміцин.ФармакодинамікаКларитроміцин є напівсинтетичним антибіотиком групи макролідів і чинить антибактеріальну дію, взаємодіючи з 50S рибосомальною субодиницею та пригнічуючи синтез білка, чутливих до нього бактерій. Кларитроміцин продемонстрував високу активність в умовах in vitro щодо як стандартних лабораторних штамів бактерій, так і виділених у пацієнтів у ході клінічної практики. Виявляє високу активність щодо багатьох аеробних та анаеробних грампозитивних та грамнегативних мікроорганізмів. Мінімальні переважні концентрації (МПК) кларитроміцину для більшості збудників менше, ніж МПК еритроміцину в середньому на одне log 2 розведення. Кларитроміцин в умовах in vitro є високоактивним щодо Legionella pneumophila, Mycoplasma pneumoniae. Чинить бактерицидну дію щодо Helicobacter pylori, дана активність кларитроміцину вище при нейтральному pH, ніж при кислому. Крім того, дані в умовах in vitro та in vivo вказують на те, що кларитроміцин діє на клінічно значущі види мікобактерій. Enterobacteriaceae та Pseudomonas spp. так само як і інші грамнегативні бактерії, що не ферментують лактозу, не чутливі до кларитроміцину. Активність кларитроміцину щодо більшості штамів наведених нижче мікроорганізмів доведена як в умовах in vitro, так і в клінічній практиці при захворюваннях, перелічених у розділі «Показання до застосування». Аеробні грампозитивні мікроорганізми: - Staphylococcus aureus, - Streptococcus pneumoniae, - Streptococcus pyogenes, -Listeria monocytogenes Аеробні грамнегативні мікроорганізми: -Haemophilusinfluenzae, -Haemophilus parainfluenzae, -Moraxella catarrhalis, -Neisseria gonorrhoeae, -Legionella pneumophila Інші мікроорганізми: - Mycoplasma pneumoniae, - Chlamydia pneumoniae (TWAR) Мікобактерії: - Mycobacterium leprae, - Mycobacterium kansasii, - Mycobacterium chelonae, -Mycobacterium fortuitum, – Mycobacterium avium complex (MAC) – комплекс, що включає: Mycobacterium avium, Mycobacterium intracellulare. Продукція бета-лактамази не впливає на активність кларитроміцину. Більшість штамів стафілококів, резистентних до метициліну та оксациліну, мають стійкість і до кларитроміцину. Helicobacter pylori Чутливість Helicobacter pylori до кларитроміцину вивчалася на ізолятах Helicobacter pylori, виділених від 104 пацієнтів на початок терапії препаратом. У 4 пацієнтів були виділені резистентні до кларитроміцину штами Helicobacter pylori, у 2 пацієнтів – штами з помірною резистентністю, у решти 98 пацієнтів ізоляти Helicobacter pylori були чутливі до кларитроміцину. Кларитроміцин діє в умовах in vitro і щодо більшості штамів наступних мікроорганізмів (проте безпека та ефективність застосування кларитроміцину в клінічній практиці не підтверджена клінічними дослідженнями, і практичне значення залишається незрозумілим): Аеробні грампозитивні мікроорганізми: - Streptococcus agalactiae, - Streptococci (групи С, F, G), - Viridansgroupstreptococci Аеробні грамнегативні мікроорганізми: - Bordetella pertussis, – Pasteurella multocida Анаеробні грампозитивні мікроорганізми: - Clostridiumperfringens, - Peptococcusniger, - Propionibacteriumacnes Анаеробні грамнегативні мікроорганізми: – Bacteroidesmelaninogenicus Спірохети: – Borreliaburgdorferi, - Treponema pallidum Кампілобактерії: – Campilobacter jejuni Основним метаболітом кларитроміцину в організмі людини є мікробіологічно активний метаболіт 14-гідроксикларитроміцин (14-ОН-кларитроміцин). Мікробіологічна активність метаболіту така ж, як у вихідної речовини, або вдвічі слабша щодо більшості мікроорганізмів. Виняток становить Haemophilus influenzae, щодо якої ефективність метаболіту вдвічі вища. Вихідне з'єднання та його основний метаболіт мають або адитивний, або синергічний ефект щодо Haemophilus influenzae в умовах in vitro та in vivo залежно від штаму бактерій. Тест на чутливість Кількісні методи, що вимагають вимірювання діаметра зони придушення росту, дають найбільш точні оцінки чутливості бактерій до антимікробних препаратів. Одна з рекомендованих методик визначення чутливості використовує диски, імпрегновані 15 мкг кларитроміцину (диско-дифузійний метод Кірбі-Бауера), при інтерпретації тесту діаметри зон придушення росту корелюють зі значеннями МПК кларитроміцину. Значення МПК визначаються методом розведення у бульйоні чи агарі. З використанням цих методик звіт з лабораторії у тому, що штам є «чутливим», свідчить про те, що збудник інфекції, ймовірно, відповість на лікування. Відповідь «резистентна» вказує на те, що збудник, можливо, не відповість на лікування. Відповідь «проміжна чутливість» передбачає, що терапевтичний ефект препарату може бути неоднозначним або мікроорганізм може виявитися чутливим при використанні більш високих доз препарату. Проміжна чутливість також називається "помірною чутливістю".Показання до застосуванняІнфекційно-запальні захворювання, спричинені чутливими до кларитроміцину мікроорганізмами: інфекції нижніх дихальних шляхів (такі як бронхіт, пневмонія); інфекції верхніх дихальних шляхів (такі як фарингіт, синусит); інфекції шкіри та м'яких тканин (такі як фолікуліт, запалення підшкірної клітковини, пика); дисеміновані або локалізовані мікобактеріальні інфекції, спричинені Mycobacterium avium та Mycobacterium intracellulare; локалізовані інфекції, спричинені Mycobacterium chelonae, Mycobacterium fortuitum та Mycobacterium kansasii; профілактика поширення інфекції, зумовленої комплексом Mycobacterium avium (MAC) у ВІЛ-інфікованих пацієнтів із вмістом лімфоцитів CD4 (Т-хелперних лімфоцитів) не більше 100 за 1 мм3; ерадикація Helicobacter pylori та зниження частоти рецидивів виразки дванадцятипалої кишки; одонтогенні інфекції.Протипоказання до застосуванняПідвищена чутливість до кларитроміцину, інших компонентів препарату та інших макролідів. Одночасний прийом кларитроміцину з наступними препаратами: астемізол, цизаприд, пімозід, терфенадин (див. розділ «Взаємодія з іншими лікарськими засобами»). Одночасний прийом кларитроміцину з алкалоїдами ріжків, наприклад, ерготамін, дигідроерготамін (див. розділ «Взаємодія з іншими лікарськими засобами»). Одночасний прийом кларитроміцину з мідазоламом для внутрішнього застосування (див. розділ «Взаємодія з іншими лікарськими засобами»). Одночасний прийом кларитроміцину з інгібіторами ГМГ-КоА-редуктази (статинами), які значною мірою метаболізуються ізоферментом CYP3A4 (ловастатин, симвастатин), у зв'язку з підвищенням ризику міопатії, включаючи рабдоміоліз (див. розділ "Взаємодія з іншими"). Одночасний прийом кларитроміцину з колхіцином. Одночасний прийом кларитроміцину з тикагрелором або ранолазином. Подовження інтервалу QT (вроджене або документально підтверджене придбане подовження інтервалу QT) на електрокардіограмі (ЕКГ) в анамнезі, шлуночкова аритмія, включаючи шлуночкову тахікардію типу «пірует». Гіпокаліємія (ризик подовження інтервалу QT на ЕКГ). Тяжка печінкова недостатність, що протікає одночасно з нирковою недостатністю. Холестатична жовтяниця/гепатит в анамнезі, що розвинулися при застосуванні кларитроміцину (див. розділ «Особливі вказівки»). Порфирія. Період грудного вигодовування. Вік до 12 років (ефективність та безпека не встановлені). Ниркова недостатність середнього та тяжкого ступеня. Печінкова недостатність середнього та тяжкого ступеня. Одночасний прийом кларитроміцину з бензодіазепінами, такими як алпразол, триазол, мідазол для внутрішньовенного застосування (див. розділ «Взаємодія з іншими лікарськими засобами»). Одночасний прийом з препаратами, які метаболізуються ізоферментом CYP3A, наприклад, карбамазепін, цилостазол, циклоспорин, дизопірамід, метилпреднізолон, омепразол, непрямі антикоагулянти (наприклад, варфарин), хінідин, рифабутин, силденафіл, такролі. засобами»). Одночасний прийом з препаратами, що індукують ізофермент CYP3A4, наприклад, рифампіцин, фенітоїн, карбамазепін, фенобарбітал, препарати Звіробою продірявленого (див. розділ «Взаємодія з іншими лікарськими засобами»). Одночасний прийом кларитроміцину зі статинами, які не залежать від метаболізму ізоферменту CYP3A (наприклад, флувастатин) (див. розділ «Взаємодія з іншими лікарськими засобами»). Одночасний прийом із блокаторами «повільних» кальцієвих каналів, які метаболізуються ізоферментом CYP3A4 (наприклад, верапаміл, амлодипін, дилтіазем). Пацієнти з ішемічною хворобою серця (ІХС), тяжкою серцевою недостатністю, гіпомагніємією, порушеннями провідності або клінічно значущою брадикардією, а також пацієнти, які одночасно приймають антиаритмічні препарати ІА класу (хінідин, прокаїнамід) та ІІІ класу (дофетилід, аміодарон, соталол). Вагітність.Вагітність та лактаціяБезпека застосування кларитроміцину при вагітності та в період грудного вигодовування не встановлена. Застосування кларитроміцину при вагітності (особливо в І триместрі) можливе лише у випадку, коли відсутня альтернативна терапія, а потенційна користь для матері перевищує потенційний ризик для плода. Кларитроміцин виводиться із грудним молоком. При необхідності прийому в період грудного вигодовування годування груддю слід припинити. Протипоказаний особам віком до 12 років (ефективність та безпека не встановлені). Звичайна рекомендована доза кларитроміцину у дітей віком від 12 років – 250 мг 2 рази на день.Побічна діяКласифікація частоти розвитку побічних ефектів (кількість зареєстрованих випадків/кількість пацієнтів), рекомендована Всесвітньою організацією охорони здоров'я (ВООЗ): дуже часто ≥ 1/10 часто від ≥ 1/100 до < 1/10 нечасто від ≥ 1/1000 до < 1/100 рідко від ≥ 1/10000 до < 1/1000 дуже рідко <1/10000 частота невідома може бути оцінена з урахуванням наявних даних. Інфекційні та паразитарні захворювання: нечасто: целюліт(1), кандидоз, гастроентерит(2), вторинні інфекції(3) (у тому числі вагінальні); частота невідома: псевдомембранозний коліт, пика. Порушення з боку імунної системи: часто: шкірний висип; нечасто: анафілактоїдна реакція (1), гіперчутливість, дерматит бульозний (1), свербіж шкіри, кропив'янка, макулопапульозний висип (3); частота невідома: анафілактична реакція, ангіоневротичний набряк, синдром Стівенса-Джонсона, токсичний епідермальний некроліз, лікарський висип з еозинофілією та системною симптоматикою (DRESS-синдром). Порушення з боку обміну речовин та харчування: Нечасто: анорексія, зниження апетиту. Порушення психіки: часто: безсоння; нечасто: занепокоєння, підвищена збудливість (3); частота невідома: психотичні розлади, сплутаність свідомості, деперсоналізація, депресія, дезорієнтація, галюцинації, порушення сновидінь («жахливі» сновидіння), манія. Порушення з боку нервової системи: часто: головний біль, дисгезія (перекручення смаку); нечасто: непритомність(1), дискінезія(1), запаморочення, сонливість, тремор; частота невідома: судоми, парестезія, агевзія (втрата смакових відчуттів), паросмія, аносмія. Порушення з боку органу слуху та лабіринтні порушення: нечасто: вертиго, порушення слуху, дзвін у вухах; Частота невідома: глухота. Порушення з боку серця: нечасто: раптова зупинка серця (1), фібриляція передсердь (1), подовження інтервалу QT на ЕКГ, екстрасистолія (1), серцебиття; частота невідома: шлуночкова тахікардія, зокрема типу «пірует», фібриляція шлуночків. Порушення з боку судин: часто: вазодилатація; Частота невідома: кровотеча. Порушення з боку дихальної системи, органів грудної клітки та середостіння: нечасто: бронхіальна астма (1), носова кровотеча (2), тромбоемболія легеневої артерії (1). Порушення з боку травної системи: часто: діарея, блювання, диспепсія, нудота, біль у ділянці живота; нечасто: езофагіт(1), гастроезофагеальна рефлюксна хвороба(2), гастрит, прокталгія(2), стоматит, глосит, здуття живота(4), запор, сухість слизової оболонки порожнини рота, відрижка, метеоризм; частота невідома: гострий панкреатит, зміна кольору язика та зубів. Порушення з боку печінки та жовчовивідних шляхів: нечасто: холестаз(4), гепатит, у тому числі холестатичний або гепатоцелюлярний(4); частота невідома: печінкова недостатність, холестатична жовтяниця. Порушення з боку шкіри та підшкірних тканин: часто: інтенсивне потовиділення; частота невідома: акне, гострий генералізований екзантематозний пустульоз (ОГЕП). Порушення з боку скелетно-м'язової та сполучної тканини: нечасто: м'язовий спазм (3), кістково-м'язова скутість (1), міалгія (2); частота невідома: рабдоміоліз (2, *), міопатія. Порушення з боку нирок та сечовивідних шляхів: частота невідома: ниркова недостатність, інтерстиціальний нефрит. Загальні розлади та порушення у місці введення: нечасто: нездужання(4), гіпертермія(3), астенія, біль у грудній клітці(4), озноб(4), підвищена стомлюваність(4). Лабораторні та інструментальні дані: часто: - відхилення лабораторних показників функції печінки; нечасто: підвищення концентрації креатиніну(1), сечовини(1) у плазмі крові, зміна відношення альбумін/глобулін(1), лейкопенія, нейтропенія(4), еозинофілія(4), тромбоцитемія(3), підвищення активності аланінамінотрансферази (AJIT), аспартатамінотрансферази (ACT), гамма-глутамілтрансферази (ГГТ)(4), лужної фосфатази(4) (ЩФ), лактатдегідрогенази (ЛДГ)(4) у плазмі крові; частота невідома: агранулоцитоз, тромбоцитопенія, збільшення значення міжнародного нормалізованого відношення (МНО), подовження протромбінового часу, зміна кольору сечі, підвищення концентрації білірубіну у плазмі крові. Пацієнти зі зниженим імунітетом У пацієнтів зі СНІДом та іншими імунодефіцитними станами, які отримують кларитроміцин у більш високих дозах протягом тривалого часу для лікування мікобактеріальних інфекцій, часто важко відрізнити небажані ефекти препарату від симптомів ВІЛ-інфекції або супутнього захворювання. Найчастішими небажаними явищами у пацієнтів, які приймали добову дозу кларитроміцину, що дорівнює 1000 мг, були: нудота, блювання, дисгевзія, біль у ділянці живота, діарея, шкірний висип, метеоризм, головний біль, запор, порушення слуху, підвищення активності ACT та АЛ плазмі крові. Також відзначалися випадки небажаних явищ із низькою частотою виникнення, такі як задишка, безсоння та сухість слизової оболонки порожнини рота. У пацієнтів із зниженим імунітетом проводили оцінку лабораторних показників, аналізуючи їх значні відхилення від норми (різке підвищення чи зниження). На підставі даного критерію у 2-3% пацієнтів, які отримували кларитроміцин у дозі 1000 мг щоденно, було зареєстровано значне підвищення активності ACT та АЛТ у плазмі, а також зниження кількості лейкоцитів та тромбоцитів. У невеликої кількості пацієнтів також було зареєстровано підвищення концентрації залишкового азоту сечовини у плазмі. *У деяких повідомленнях про рабдоміоліз кларитроміцин приймався одночасно з іншими лікарськими засобами (ЛЗ), з прийомом яких, як відомо, пов'язаний розвиток рабдоміолізу (статини, фібрати, колхіцин або алопуринол). (1) Повідомлення про дані побічних реакцій були отримані лише при застосуванні кларитроміцину у лікарській формі ліофілізат для приготування розчину для інфузій. (2) Повідомлення про дані побічних реакцій були отримані лише при застосуванні кларитроміцину у лікарській формі таблетки з пролонгованим вивільненням, покриті плівковою оболонкою. (3) Повідомлення про дані побічних реакцій були отримані лише при застосуванні кларитроміцину у лікарській формі порошок для приготування суспензії для прийому внутрішньо. (4) Повідомлення про дані побічних реакцій були отримані лише при застосуванні кларитроміцину у лікарській формі таблетки, покриті плівковою оболонкою.Взаємодія з лікарськими засобамиЗастосування наступних лікарських засобів одночасно з кларитроміцином протипоказане у зв'язку з можливістю розвитку серйозних побічних ефектів. Цизаприд, пімозід, терфенадин та астемізол При одночасному прийомі кларитроміцину з цизапридом, пимозидом, терфенадином або астемізолом повідомлялося про підвищення концентрації останніх у плазмі крові, що може призвести до подовження інтервалу QT на ЕКГ та появі серцевих аритмій, включаючи шлуночкову тахікардію (в тому числі шлуночкову та фібриляцію шлуночків (див. розділ "Протипоказання"). Алкалоїди ріжків Постмаркетингові дослідження показують, що при одночасному застосуванні кларитроміцину з ерготаміном або дигідроерготаміном можливі наступні ефекти, пов'язані з гострим отруєнням препаратами групи ерготамінів: судинний спазм, ішемія кінцівок та інших тканин, включаючи центральну нервову систему (ЦНС). Одночасне застосування кларитроміцину та алкалоїдів ріжків протипоказане (див. розділ «Протипоказання»). Інгібітори ГМГ-КоА-редуктази (статини) Одночасний прийом кларитроміцину з ловастатином або симвастатином протипоказаний (див. розділ «Протипоказання») у зв'язку з тим, що дані статини значною мірою метаболізуються ізоферментом CYP3A4, і одночасне застосування з кларитроміцином підвищує їх сироваткові концентрації, що призводить до підвищення рабдоміоліз. Повідомлялося про випадки рабдоміолізу у пацієнтів, які приймали кларитроміцин одночасно з цими препаратами. У разі необхідності застосування кларитроміцину слід припинити прийом ловастатину або симвастатину на час терапії. Кларитроміцин слід застосовувати з обережністю у разі комбінованої терапії з іншими статинами. Рекомендується застосовувати статини, метаболізм яких не залежить від ізоферменту CYP3A (наприклад, флувастатин). У разі потреби одночасного прийому рекомендується приймати найменшу дозу статину. Слід контролювати розвиток ознак та симптомів міопатії. Мідазолам для прийому внутрішньо При одночасному застосуванні внутрішньо мідазоламу та кларитроміцину у формі таблеток (500 мг 2 рази на день) відзначалося збільшення AUC мідазоламу у 7 разів. Одночасний прийом кларитроміцину та мідазоламу для прийому внутрішньо протипоказаний (див. розділ «Протипоказання»). Вплив інших лікарських засобів на кларитроміцин Лікарські препарати, що є індукторами ізоферменту CYP3A (наприклад, рифампіцин, фенітоїн, карбамазепін, фенобарбітал, препарати Звіробою продірявленого) можуть індукувати метаболізм кларитроміцину. Це може призвести до субтерапевтичної концентрації кларитроміцину та, відповідно, до зниження його ефективності. Крім того, необхідно спостерігати за концентрацією індуктора ізоферменту CYP3A у плазмі крові, яка може підвищитися через інгібування ізоферменту CYP3A кларитроміцином. При одночасному застосуванні рифабутину та кларитроміцину спостерігалося підвищення концентрації рифабутину та зниження концентрації кларитроміцину в плазмі крові з підвищеним ризиком розвитку увеїту. Наступні препарати мають доведений або передбачуваний вплив на концентрацію кларитроміцину в плазмі крові, у разі їх одночасного застосування з кларитроміцином може знадобитися корекція доз або перехід на альтернативне лікування Ефавіренз, невірапін, рифампіцин, рифабутин та рифапентин Потужні індуктори системи цитохрому Р450, такі як ефавіренз, невірапін, рифампіцин, рифабутин і рифапентин можуть прискорювати метаболізм кларитроміцину і, таким чином, знижувати концентрацію кларитроміцину в плазмі крові та послаблювати терапевтичний ефект, і разом з тим кларитроміцину – метаболіту, який також є мікробіологічно активним. Оскільки мікробіологічна активність кларитроміцину та 14-ОН-кларитроміцину відрізняється щодо різних бактерій, терапевтичний ефект може знижуватися при одночасному застосуванні кларитроміцину та індукторів системи цитохрому Р450. Етравірін Концентрація кларитроміцину в плазмі знижується при одночасному застосуванні з етравірином, але підвищується концентрація в плазмі активного метаболіту 14-ОН-кларитроміцину. Оскільки 14-ОН-кларитроміцин має низьку активність по відношенню до інфекцій MAC, може змінюватися загальна активність щодо цих збудників, тому для лікування MAC слід розглядати альтернативне лікування. Флуконазол Одночасний прийом флуконазолу в дозі 200 мг щоденно та кларитроміцину в дозі 500 мг 2 рази на день у 21 здорового добровольця призвело до збільшення середнього значення мінімальної рівноважної концентрації кларитроміцину та AUC на 33 % та 18 % відповідно. При цьому одночасний прийом значно не впливав на середню рівноважну концентрацію активного метаболіту 14-ОН-кларитроміцину. Корекція дози кларитроміцину у разі одночасного прийому флуконазолу не потрібна. Рітонавір Фармакокінетичне дослідження показало, що одночасний прийом ритонавіру в дозі 200 мг кожні 8 годин та кларитроміцину в дозі 500 мг кожні 12 годин призвів до помітного пригнічення метаболізму кларитроміцину. При одночасному прийомі ритонавіру С(mах) кларитроміцину в плазмі збільшилася на 31%, C(min) збільшилася на 182% і AUC збільшилася на 77%. Було відзначено практично повне придушення утворення 14-ОН-кларитроміцину. Завдяки широкому терапевтичному діапазону кларитроміцину зменшення його дози у пацієнтів із нормальною нирковою функцією не потрібне. У пацієнтів з нирковою недостатністю доцільно розглянути наступні варіанти корекції дози: при КК 30-60 мл/хв доза кларитроміцину повинна бути зменшена на 50 %, при КК менше 30 мл/хв доза кларитроміцину повинна бути зменшена на 75 %.Ритонавір не слід одночасно приймати з кларитроміцином у дозах, що перевищують 1 г на добу. Подібні корекції доз повинні розглядатися у пацієнтів зі зниженою функцією нирок, якщо ритонавір використовується як фармакокінетичний «підсилювач» при застосуванні інших інгібіторів протеази ВІЛ, включаючи атазанавір та саквінавір (див. підрозділ «Двонаправлена взаємодія лікарських засобів»). Дія кларитроміцину на інші лікарські препарати Антиаритмічні засоби (хінідин та дизопірамід) Можливе виникнення шлуночкової тахікардії типу «пірует» при одночасному застосуванні кларитроміцину та хінідину або дизопіраміду. При одночасному прийомі кларитроміцину з цими препаратами слід регулярно проводити контроль ЕКГ щодо подовження інтервалу QT, а також слід контролювати сироваткові концентрації цих препаратів. У постмаркетинговому періоді застосування повідомлялося про випадки розвитку гіпоглікемії при одночасному прийомі кларитроміцину та дизопіраміду. Необхідно контролювати концентрацію глюкози крові при одночасному застосуванні кларитроміцину та дизопіраміду. Гіпоглікемічні засоби для внутрішнього застосування/інсулін При одночасному застосуванні кларитроміцину та гіпоглікемічних засобів для прийому внутрішньо (наприклад, похідні сульфонілсечовини) та/або інсуліну може спостерігатися виражена гіпоглікемія. Одночасне застосування кларитроміцину з деякими гіпоглікемічними препаратами (наприклад, натеглінід, піоглітазон, репаглінід та росиглітазон) може призвести до інгібування ізоферменту CYP3A кларитроміцином, внаслідок чого може розвинутись гіпоглікемія. Рекомендується ретельний контроль за концентрацією глюкози крові. Взаємодія зумовлена ізоферментом CYP3A Одночасний прийом кларитроміцину, який, як відомо, інгібує ізофермент CYP3A, та препаратів, що первинно метаболізуються ізоферментом CYP3A, може асоціюватися із взаємним підвищенням їх концентрацій, що може посилити або продовжити як терапевтичні, так і побічні ефекти. Кларитроміцин слід обережно застосовувати пацієнтам, які отримують препарати, які є субстратами ізоферменту CYP3A, особливо якщо ці препарати мають вузький терапевтичний діапазон (наприклад, карбамазепін) та/або препарати, які інтенсивно метаболізуються цим ізоферментом. У разі необхідності повинна проводитися корекція дози препарату, який приймається одночасно з кларитроміцином. Також, по можливості, повинен проводитися моніторинг сироваткових концентрацій препаратів, що первинно метаболізуються ізоферментом CYP3A. Метаболізм наступних препаратів/класів здійснюється тим самим ізоферментом CYP3A, що і метаболізм кларитроміцину: алпразолам, карбамазепін, цилостазол, циклоспорин, дизопірамід, метилпреднізолон, мідазолам, омепразол, непрямі антикоагулянти (наприклад, варфаніни рифабутин, силденафіл, такролімус, тріазолам та вінбластин. Також до агоністів ізоферменту CYP3A належать такі препарати, що протипоказані до одночасного застосування з кларитроміцином: астемізол, цизаприд, пімозід, терфенадин, ловастатин, симвастатин та алкалоїди ріжків (див. розділ «Протипоказання»). До препаратів, що взаємодіють подібним чином через інші ізоферменти в рамках системи цитохрому Р450, відносяться: фенітоїн, теофілін та вальпроєва кислота. Непрямі антикоагулянти При одночасному прийомі варфарину та кларитроміцину можлива кровотеча, виражене збільшення МНО та подовження протромбінового часу. У разі одночасного застосування з варфарином або іншими непрямими антикоагулянтами необхідно контролювати МНО та протромбіновий час. Омепразол Кларитроміцин (по 500 мг кожні 8 годин) досліджувався у здорових дорослих добровольців у поєднанні з омепразолом (по 40 мг щодня). При одночасному застосуванні кларитроміцину та омепразолу рівноважні плазмові концентрації омепразолу були збільшені (C(max), AUC(0-24) та Т(1/2) збільшилися на 30%, 89% та 34%, відповідно). Середнє значення pH шлунка протягом 24 годин склало 5,2 (при прийомі омепразолу окремо) і 5,7 (при прийомі омепразолу одночасно з кларитроміцином). Силденафіл, тадалафіл та варденафіл Кожен із цих інгібіторів фосфодіестерази метаболізується принаймні частково за участю ізоферменту CYP3A. У той же час, ізофермент CYP3A може інгібуватися в присутності кларитроміцину. Одночасне застосування кларитроміцину з силденафілом, тадалафілом або варденафілом може призвести до збільшення інгібуючої дії на фосфодіестеразу. При застосуванні цих препаратів одночасно з кларитроміцином слід розглянути можливість зменшення дози силденафілу, тадалафілу та варденафілу. Теофілін, карбамазепін При одночасному застосуванні кларитроміцину та теофіліну або карбамазепіну можливе підвищення концентрації даних препаратів у системному кровотоку. Толтеродін Первинний метаболізм толтеродину здійснюється через ізофермент CYP2D6. Однак у частині популяції, позбавленої CYP2D6, метаболізм відбувається через ізофермент CYP3A. У цій групі населення пригнічення ізоферменту CYP3A призводить до значно більших концентрацій толтеродину в сироватці крові. У популяції з низьким рівнем метаболізму через ізофермент CYP2D6 може знадобитися зниження дози толтеродину при одночасному застосуванні інгібіторів ізоферменту CYP3A, таких як кларитроміцин. Бензодіазепіни (наприклад, алпразолам, мідазолам, тріазолам) При одночасному застосуванні мідазоламу та таблеток кларитроміцину (500 мг 2 рази на день) відзначалося збільшення AUC мідазоламу у 2,7 раза після внутрішньовенного введення мідазоламу. Якщо одночасно з кларитроміцином застосовується внутрішньовенна форма мідазоламу, слід ретельно контролювати стан пацієнта для можливої корекції дози. Введення лікарського препарату через слизову оболонку порожнини рота, що дає можливість обійти пресистемну елімінацію лікарського препарату, швидше за все, призведе до взаємодії аналогічного до того, що спостерігається при внутрішньовенному введенні мідазоламу, а не при прийомі внутрішньо. Такі ж запобіжні заходи слід застосовувати і до інших бензодіазепінів, які метаболізуються ізоферментом CYP3A, включаючи триазолів та алпразолів. Для бензодіазепінів,виведення яких не залежить від ізоферменту CYP3A (темазепам, нітразепам, лоразепам), малоймовірно клінічно значуща взаємодія з кларитроміцином. При одночасному застосуванні кларитроміцину та триазоламу можлива дія на ЦНС, наприклад, сонливість та сплутаність свідомості. У зв'язку з цим у разі одночасного застосування рекомендується стежити за симптомами порушення ЦНС. Взаємодія з іншими препаратами Колхіцін Колхіцин є субстратом як для ізоферменту CYP3A, так і для білка-переносника P-глікопротеїну (Pgp). Відомо, що кларитроміцин та інші макроліди є інгібіторами ізоферменту CYP3A та Pgp. При одночасному застосуванні кларитроміцину та колхіцину інгібування Pgp та/або ізоферменту CYP3A може призвести до посилення дії колхіцину. Слід контролювати розвиток клінічних симптомів отруєння колхіцином. Зареєстровані постмаркетингові повідомлення про випадки отруєння колхіцином при одночасному прийомі з кларитроміцином, частіше у пацієнтів похилого віку. Деякі з описаних випадків відбувалися у пацієнтів із нирковою недостатністю. Як повідомлялося, деякі випадки закінчувалися летальним кінцем. Одночасне застосування кларитроміцину та колхіцину протипоказане (див. розділ «Протипоказання»). Дігоксин Передбачається, що дигоксин є субстратом PGP. Відомо, що кларитроміцин пригнічує Pgp. При одночасному застосуванні кларитроміцину та дигоксину інгібування Pgp кларитроміцином може призвести до посилення дії дигоксину. Одночасний прийом дигоксину та кларитроміцину також може призвести до підвищення сироваткової концентрації дигоксину. У деяких пацієнтів спостерігалися клінічні симптоми отруєння дигоксином, включаючи потенційно летальні аритмії. При одночасному прийомі кларитроміцину та дигоксину слід ретельно контролювати концентрацію дигоксину у сироватці крові. Зідовудін Одночасний прийом таблеток кларитроміцину та зидовудину внутрішньо дорослими ВІЛ-інфікованими пацієнтами може призвести до зниження рівноважної концентрації зидовудину в плазмі крові. Оскільки кларитроміцин впливає на всмоктування зидовудину при прийомі внутрішньо, взаємодії можна значно уникнути, приймаючи кларитроміцин і зидовудін з інтервалом в 4 години. Подібної взаємодії не спостерігали у ВІЛ-інфікованих дітей, які приймали дитячу суспензію кларитроміцину з зидовудином або дидезоксіїнозином. Оскільки кларитроміцин може перешкоджати всмоктуванню зидовудину при їх одночасному прийомі внутрішньо у дорослих пацієнтів, така взаємодія навряд чи можлива при застосуванні кларитроміцину внутрішньовенно. Фенітоїн та вальпроєва кислота Є дані про взаємодію інгібіторів ізоферменту CYP3A (включаючи кларитроміцин) з препаратами, які не метаболізуються за допомогою ізоферменту CYP3A (фенітоїн та вальпроєва кислота). Для цих препаратів при одночасному застосуванні з кларитроміцином рекомендується визначення їх сироваткових концентрацій, оскільки є повідомлення про їх підвищення. Двоспрямована взаємодія лікарських засобів Атазанавір Кларитроміцин та атазанавір є як субстратами, так і інгібіторами ізоферменту CYP3A. Існує свідчення двонаправленої взаємодії цих препаратів. Одночасне застосування кларитроміцину (500 мг 2 рази на день) та атазанавіру (400 мг 1 раз на день) може призвести до дворазового збільшення впливу кларитроміцину та зменшення впливу 14-ОН-кларитроміцину на 70 % зі збільшенням AUC атазанавіру на 28 %. Завдяки широкому терапевтичному діапазону кларитроміцину зменшення його дози у пацієнтів із нормальною нирковою функцією не потрібне. У пацієнтів з нирковою недостатністю середнього ступеня тяжкості (КК 30-60 мл/хв) доза кларитроміцину повинна бути зменшена на 50%. У пацієнтів з КК менше 30 мл/хв дозу кларитроміцину слід зменшити на 75%, застосовуючи для цього відповідну лікарську форму кларитроміцину.Кларитроміцин у дозах, що перевищують 1000 мг на добу, не можна застосовувати одночасно з інгібіторами протеаз. Блокатори «повільних» кальцієвих каналів При одночасному застосуванні кларитроміцину та блокаторів «повільних» кальцієвих каналів, які метаболізуються ізоферментом CYP3A4 (наприклад, верапаміл, амлодипін, дилтіазем), слід бути обережним, оскільки існує ризик виникнення артеріальної гіпотензії. При одночасному застосуванні можуть підвищуватися плазмові концентрації кларитроміцину та блокаторів «повільних» кальцієвих каналів. Артеріальна гіпотензія, брадіаритмія та лактоацидоз можливі при одночасному прийомі кларитроміцину та верапамілу. Ітраконазол Кларитроміцин та ітраконазол є субстратами та інгібіторами ізоферменту CYP3A, що визначає двонаправлену взаємодію препаратів. Кларитроміцин може підвищити концентрацію ітраконазолу в плазмі, тоді як ітраконазол може підвищити плазмову концентрацію кларитроміцину. Пацієнтів, які одночасно приймають ітраконазол та кларитроміцин, слід ретельно обстежити на наявність симптомів посилення або збільшення тривалості фармакологічних ефектів цих препаратів. Саквінавір Кларитроміцин та саквінавір є субстратами та інгібіторами ізоферменту CYP3A, що визначає двоспрямовану взаємодію препаратів. Одночасне застосування кларитроміцину (500 мг 2 рази на день) та саквінавіру (у м'яких желатинових капсулах, 1200 мг 3 рази на день) у 12 здорових добровольців викликало збільшення AUC та С(mах )саквінавіру в плазмі крові на 177 % та 187 %, , У порівнянні з прийомом саквінавіру окремо. Значення AUC та С(mах) кларитроміцину були приблизно на 40 % вищими, ніж при терапії одним кларитроміцином. При одночасному застосуванні цих двох препаратів протягом обмеженого часу у дозах/складах, зазначених вище, корекція дози не потрібна. Результати дослідження лікарських взаємодій із застосуванням саквінавіру в м'яких желатинових капсулах можуть не відповідати ефектам,спостерігається при застосуванні саквінавіру в твердих желатинових капсулах. Результати дослідження лікарських взаємодій при терапії саквінавіром окремо можуть не відповідати ефектам, що спостерігаються при терапії комбінацією саквінавір/ритонавір. При прийомі саквінавіру одночасно з ритонавіром слід враховувати потенційний вплив ритонавіру на кларитроміцин.Спосіб застосування та дозиВсередину, незалежно від часу їди. Звичайна рекомендована доза кларитроміцину у дорослих та дітей старше 12 років – 250 мг 2 рази на день. Препарат Фромілід 500 мг 2 рази на день застосовують у разі більш тяжких інфекцій. Звичайна тривалість лікування становить від 5 до 14 днів. Виняток становлять позалікарняна пневмонія та синусит, які вимагають лікування від 6 до 14 днів. Дози для лікування мікобактеріальних інфекцій, крім туберкульозу При мікобактеріальних інфекціях рекомендована доза препарату Фромілід 500 мг 2 рази на день. Лікування дисемінованих MAC інфекцій у пацієнтів зі СНІД слід продовжувати доти, доки є клінічна та мікробіологічна ефективність. Кларитроміцин слід призначати у комбінації з іншими антимікробними препаратами, активними щодо цих збудників. Тривалість лікування інших нетуберкульозних мікобактеріальних інфекцій встановлює лікар. Для профілактики інфекцій, спричинених MAC Рекомендована доза препарату Фромілід для дорослих – 500 мг 2 рази на день. При одонтогенних інфекціях доза препарату Фромілід становить 250 мг 2 рази на день протягом 5 днів. Для ерадикації Helicobacter pylori У пацієнтів з виразковою хворобою, викликаною інфекцією Helicobacter pylori, препарату Фромілід® можна застосовувати по 500 мг 2 рази на день у комбінації з іншими антимікробними препаратами та інгібіторами протонного насоса протягом 7-14 днів, відповідно до національних та міжнародних рекомендацій. Helicobacter pylori. Пацієнти з нирковою недостатністю Пацієнтам з КК менше 30 мл/хв призначають половину звичайної дози кларитроміцину, тобто 250 мг 1 раз на день або при більш тяжких інфекціях по 250 мг 2 рази на день. Лікування таких пацієнтів продовжують трохи більше 14 днів.ПередозуванняСимптоми: прийом внутрішньо великої дози кларитроміцину може викликати симптоми порушень з боку шлунково-кишкового тракту. У одного пацієнта з біполярним розладом в анамнезі після прийому 8 г кларитроміцину описані зміни психічного стану, параноїдальна поведінка, гіпокаліємія та гіпоксемія. Лікування: при передозуванні слід видалити неабсорбований препарат із шлунково-кишкового тракту (промивання шлунка, прийом активованого вугілля та ін.) та провести симптоматичну терапію. Гемодіаліз та перитонеальний діаліз не мають істотного впливу на концентрацію кларитроміцину в сироватці крові, що характерно і для інших лікарських препаратів групи макролідів.Запобіжні заходи та особливі вказівкиТривалий прийом антибіотиків може призводити до утворення колоній зі збільшенням кількості нечутливих бактерій та грибів. При суперінфекції слід призначити відповідну терапію. При застосуванні кларитроміцину повідомлялося про печінкову дисфункцію (підвищення активності «печінкових» ферментів у плазмі крові, гепатоцелюлярний та/або холестатичний гепатит із жовтяницею або без). Печінкова дисфункція може бути важкою, але є оборотною. Є випадки печінкової недостатності з летальним результатом, головним чином пов'язані з наявністю серйозних супутніх захворювань та/або одночасним застосуванням інших лікарських засобів. При появі ознак і симптомів гепатиту, таких як анорексія, жовтяниця, потемніння сечі, свербіж шкіри, болючість живота при пальпації, необхідно негайно припинити терапію кларитроміцином. За наявності хронічних захворювань печінки необхідно проводити регулярний контроль активності печінкових ферментів сироватки крові. При лікуванні практично всіма антибактеріальними засобами, у тому числі макролідами, описані випадки псевдомембранозного коліту, тяжкість якого може змінюватись від легкого до загрозливого життя. При лікуванні практично всіма антибактеріальними препаратами, у тому числі кларитроміцином, описані випадки Clostridium difficile-асоційованої діареї, тяжкість якої може змінюватись від легкої діареї до загрозливого життя коліту. Антибактеріальні препарати можуть змінити нормальну мікрофлору кишечника, що може спричинити зростання Clostridium difficile. Псевдомембранозний коліт, викликаний Clostridium difficile, необхідно підозрювати у всіх пацієнтів з появою діареї після застосування антибактеріальних засобів. Після проведення курсу антибіотикотерапії потрібне ретельне медичне спостереження за пацієнтом.Описувалися випадки розвитку псевдомембранозного коліту через 2 місяці після застосування антибіотиків. З боку серцево-судинної системи При лікуванні макролідами, включаючи кларитроміцин, спостерігалося збільшення часу реполяризації шлуночків серця та подовження інтервалу QT, що сприяло ризику розвитку серцевої аритмії та шлуночкової тахікардії типу «пірует» (див. розділ «Побічна дія»). У зв'язку з тим, що такі ситуації можуть призвести до збільшення ризику розвитку шлуночкових аритмій (у тому числі шлуночкової тахікардії типу «пірует»), кларитроміцин слід застосовувати з обережністю у таких пацієнтів: пацієнти з ІХС, серцевою недостатністю тяжкого ступеня, порушеннями провідності або клінічно значущою брадикардією; пацієнти з порушеннями водно-електролітного обміну, такими як гіпомагніємія. Кларитроміцин не слід застосовувати у пацієнтів з гіпокаліємією (див. розділ "Протипоказання"); пацієнти, які одночасно застосовують інші лікарські препарати, що призводять до подовження інтервалу QT (див. розділ «Взаємодія з іншими лікарськими засобами»). Протипоказане одночасне застосування кларитроміцину з астемізолом, цизапридом, пимозидом та терфенадином (див. розділ «Протипоказання»). Кларитроміцин не слід застосовувати у пацієнтів з вродженим або документально підтвердженим подовженням інтервалу QT, а також із вказівками в анамнезі на епізоди шлуночкової аритмії (див. розділ «Протипоказання»). У ході епідеміологічних досліджень з вивчення ризику несприятливих серцево-судинних наслідків при застосуванні макролідів було отримано неоднозначні результати. У деяких короткострокових наглядових дослідженнях було встановлено ризик розвитку аритмії, інфаркту міокарда та смерті від серцево-судинних захворювань, пов'язаний із застосуванням макролідів, включаючи кларитроміцин. При призначенні кларитроміцину слід співвідносити передбачувану користь від прийому препарату з цими ризиками. Можливий розвиток перехресної резистентності до кларитроміцину та інших антибіотиків групи макролідів, а також лінкоміцину та кліндаміцину. Враховуючи зростаючу резистентність Streptococcus pneumoniae до макролідів, важливо проводити тестування чутливості при призначенні кларитроміцину пацієнтам із позалікарняною пневмонією. При шпитальній пневмонії кларитроміцин слід застосовувати у комбінації з відповідними антибіотиками. Інфекції шкіри та м'яких тканин легкої та середньої тяжкості найчастіше викликані Staphylococcus aureus та Streptococcus pyogenes. При цьому обидва збудники можуть бути стійкими до макролідів. Тому важливо проводити тест визначення чутливості до антибіотиків. Макроліди можна застосовувати при інфекціях, викликаних Corynebacterium minutissimum, захворюваннях acne vulgaris і бешихі, а також у тих ситуаціях, коли не можна застосовувати пеніцилін. У разі появи гострих реакцій гіперчутливості, таких як анафілактична реакція, тяжкі шкірні небажані реакції (ТКНР) (наприклад, ОГЭП), синдром Стівенса-Джонсона, токсичний епідермальний некроліз та лікарський висип з еозинофілією та системною симптоматикою (DRESS- припинити прийом кларитроміцину та почати відповідну терапію. У разі одночасного застосування з варфарином або іншими непрямими антикоагулянтами необхідно контролювати МНО та протромбіновий час (див. розділ «Взаємодія з іншими лікарськими засобами»). Застосування при хронічних захворюваннях: Протипоказаний пацієнтам з тяжкою печінковою недостатністю, що протікає одночасно з нирковою недостатністю. Застосовувати з обережністю пацієнтам з нирковою та печінковою недостатністю середнього та тяжкого ступеня. Пацієнти з нирковою недостатністю Пацієнтам з КК менше 30 мл/хв призначають половину звичайної дози кларитроміцину, тобто 250 мг 1 раз на день або при більш тяжких інфекціях по 250 мг 2 рази на день. Лікування таких пацієнтів продовжують трохи більше 14 днів. Вплив на керування транспортними засобами: Дані щодо впливу кларитроміцину на здатність до керування автомобілем та механізмами відсутні. Слід бути обережними при керуванні транспортними засобами та механізмами, враховуючи потенційну можливість запаморочення, вертиго, сплутаності свідомості та дезорієнтації, які можуть виникнути при застосуванні даного препарату.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
452,00 грн
153,00 грн
Склад, форма випуску та упаковкаПігулки - 1 таб. Діюча речовина: кларитроміцин 500 мг; допоміжні речовини: натрію алгінат, натрію кальцію алгінат, лактози моногідрат, повідон К25, полісорбат-80, кремнію діоксид колоїдний, магнію стеарат, тальк; Оболонка плівкова: гіпромелоза, тальк, барвник заліза оксид жовтий (Е172), титану діоксид (Е171), пропіленгліколь По 5 або 7 таблеток поміщають у блістер із ПВХ/ПВДХ - алюмінієвої фольги (PVC/PVDC-Al). По 1 блістеру (блістер по 5 таблеток) або по 1 або 2 блістери (блістер по 7 таблеток) поміщають у картонну пачку разом з інструкцією по застосуванню.Опис лікарської формиОвальні, двоопуклі таблетки, покриті плівковою оболонкою коричнево-жовтого кольору, з маркуванням U на одній стороні. Вид на зламі: шорстка маса білого або майже білого кольору з плівковою оболонкою коричнево-жовтого кольору.Фармакотерапевтична групаАнтибіотик-макролід.ФармакокінетикаВсмоктування Препарат швидко всмоктується з шлунково-кишкового тракту. Абсолютна біодоступність становить близько 50%. При прийомі повторних доз кумуляції практично не виявлено, і характер метаболізму в організмі людини не змінювався. Розподіл, метаболізм та виведення In vitro Кларитроміцин зв'язується з білками плазми на 70% у концентрації від 0,45 до 4,5 мкг/мл. При концентрації 45 мкг/мл зв'язування знижується до 41%, ймовірно, через насичення місць зв'язування. Це спостерігається лише при концентраціях, що багаторазово перевищують терапевтичну концентрацію. Здорові добровольці У пацієнтів, які приймають 500 мг кларитроміцину 1 раз на добу після прийому їжі, максимальна концентрація (Сmах) кларитроміцину та 14-ОН-кларитроміцину в плазмі крові становила 1,3 мкг/мл та 0,48 мкг/мл відповідно. Період напіввиведення (Т1/2) кларитроміцину та Т1/2 його основного метаболіту склали 5,3 години та 7,7 годин відповідно. При прийомі разової дози кларитроміцину в лікарській формі таблетки з пролонгованим вивільненням, покриті плівковою оболонкою, 1000 мг (500 мг 2 рази на добу), Смах кларитроміцину та його гідроксильованого метаболіту в плазмі крові становила 2,4 мкг/мл/мл мл відповідно. Т1/2 кларитроміцину при прийомі в дозі 1000 мг становив 5,8 години, тоді як аналогічний показник для 14-ОН-кларитроміцину становив 8,9 години. Час досягнення максимальної концентрації (ТСmах) при прийомі внутрішньо як 500 мг, так і 1000 мг кларитроміцину становить приблизно 6 годин. Стах 14-ОН-кларитроміцину в плазмі крові не збільшувалася пропорційно прийнятій всередину дозі кларитроміцину, у той час як Т1/2 як кларитроміцину, так і його гідроксильованого метаболіту мав тенденцію до подовження з підвищенням дози. Така нелінійна фармакокінетика кларитроміцину у поєднанні зі зменшенням утворення 14-гідроксильованих та N-деметилованих продуктів при високих дозах вказує на нелінійний метаболізм кларитроміцину, який стає більш вираженим при високих дозах. Нирками виводиться приблизно 40% прийнятої дози кларитроміцину. Через кишечник виводиться приблизно 30%. Пацієнти Кларитроміцин та його метаболіт (14-ОН-кларитроміцин) швидко проникають у тканини та рідини організму. Є обмежені дані, що свідчать про те, що концентрація кларитроміцину в цереброспінальній рідині при внутрішньому прийомі незначна (т. Е. Тільки 1-2% від концентрації в сироватці крові при нормальній проникності гематоенцефалічного бар'єру). Концентрація в тканинах зазвичай у кілька разів вища, ніж у сироватці крові. Порушення функції печінки У пацієнтів із середнім та тяжким ступенем порушення функції печінки, але із збереженою функцією нирок корекція дози кларитроміцину не потрібна. Рівноважна концентрація у плазмі крові та системний кліренс кларитроміцину не відрізняються у пацієнтів цієї групи та здорових пацієнтів. Рівноважна концентрація 14-ОН-кларитроміцину у пацієнтів з порушенням функції печінки нижча, ніж у здорових добровольців. Порушення функції нирок При порушенні функції нирок збільшуються Сmах та мінімальна концентрація (Cmin) кларитроміцину в плазмі крові, Т1/2, площа під кривою "концентрація-час" (AUC) кларитроміцину та його метаболіту (14-ОН-кларитроміцину). Константа елімінації та виведення нирками зменшуються. Ступінь змін цих параметрів залежить від рівня порушення функції нирок. Пацієнти похилого віку У пацієнтів похилого віку концентрація кларитроміцину та його метаболіту (14-ОН-кларитроміцину) у плазмі крові була вищою, а виведення повільніше, ніж у групи молодих людей. Однак після корекції з урахуванням ниркового кліренсу креатиніну (КК) не було відмінностей у обох групах. Таким чином, основний вплив на фармакокінетичні параметри кларитроміцину має функція нирок, а не вік.ФармакодинамікаКларитроміцин є напівсинтетичним антибіотиком групи макролідів і має антибактеріальну дію, взаємодіючи з 50S рибосомальною субодиницею і пригнічуючи синтез білка бактерій, чутливих до нього. Кларитроміцин продемонстрував високу активність в умовах in vitro щодо стандартних лабораторних штамів бактерій, так і виділених у пацієнтів під час клінічної практики. Виявляє високу активність щодо багатьох аеробних та анаеробних грампозитивних та грамнегативних мікроорганізмів. Мінімальні переважні концентрації (МПК) кларитроміцину для більшості збудників менше, ніж МПК еритроміцину в середньому на одне log2 розведення. Кларитроміцин в умовах in vitro є високоактивним щодо Legionella pneumophila, Mycoplasma pneumoniae. Чинить бактерицидну дію щодо Helicobacter pylori, дана активність кларитроміцину вище при нейтральному значенні pH, ніж при кислому. Крім того, дані, отримані в умовах in vitro та in vivo, вказують на те, що кларитроміцин діє на клінічно значущі види мікобактерій. Enterobacteriaceae і Pseudomonas spp., так само як і інші грамнегативні бактерії, що не ферментують лактозу, не чутливі до кларитроміцину. Активність кларитроміцину щодо більшості штамів, наведених нижче мікроорганізмів, доведена як в умовах in vitro, так і в клінічній практиці при захворюваннях, перелічених у розділі "Показання до застосування". Аеробні грампозитивні мікроорганізми: Staphylococcus aureus, Streptococcus pneumoniae, Streptococcus pyogenes, Listeria monocytogenes. Аеробні грамнегативні мікроорганізми: Haemophilus influenzae, Haemophilus parainfluenzae, Moraxella catarrhalis, Neisseria gonorrhoeae, Legionella pneumophila. Інші мікроорганізми: Mycoplasma pneumoniae, Chlamydia pneumoniae (TWAR). Мікобактерії: Mycobacterium leprae, Mycobacterium kansasii, Mycobacterium chelonae, Mycobacterium fortuitum, Mycobacterium avium complex (MAC) – комплекс, що включає: Mycobacterium avium, Mycobacterium intracellulare. Продукція бета-лактамази не впливає на активність кларитроміцину. Більшість штамів стафілококів, резистентних до метициліну та оксациліну, мають стійкість і до кларитроміцину. Helicobacter pylori Чутливість Helicobacter pylori до кларитроміцину вивчалася на ізолятах Helicobacter pylori, виділених від 104 пацієнтів на початок терапії кларитромицином. У 4 пацієнтів були виділені резистентні до кларитроміцину штами Helicobacter pylori, у 2 пацієнтів – штами з помірною резистентністю, у решти – 98 пацієнтів ізоляти Helicobacter pylori були чутливі до кларитроміцину. Кларитроміцин діє в умовах in vitro і щодо більшості штамів наступних мікроорганізмів (проте безпека та ефективність застосування кларитроміцину в клінічній практиці не підтверджена клінічними дослідженнями, і практичне значення залишається незрозумілим): Аеробні грампозитивні мікроорганізми: Streptococcus agalactiae, Streptococci (групи С, F, G), Viridans group streptococci. Аеробні грамнегативні мікроорганізми: Bordetella pertussis, Pasteurella multocida. Анаеробні грампозитивні мікроорганізми: Clostridium perfringens, Peptococcus niger, Propionibacterium acnes. Анаеробні грамнегативні мікроорганізми: Bacteroides melaninogenicus. Спірохети: Borrelia burgdorferi, Treponema pallidum. Кампілобактерії: Campilobacter jejuni. Основним метаболітом кларитроміцину в організмі людини є мікробіологічно активний метаболіт 14-гідроксикларитроміцин (14-ОН-кларитроміцин). Мікробіологічна активність метаболіту така ж, як у вихідної речовини, або вдвічі слабша щодо більшості мікроорганізмів. Виняток становить Haemophilus influenzae, щодо якої ефективність метаболіту вдвічі вища. Вихідне з'єднання та його основний метаболіт мають або адитивний, або синергічний ефект щодо Haemophilus influenzae в умовах in vitro та in vivo залежно від штаму бактерій. Тест визначення чутливості Кількісні методи, що вимагають вимірювання діаметра зони придушення росту, дають найбільш точні оцінки чутливості бактерій до антимікробних препаратів. Одна з рекомендованих методик визначення чутливості використовує диски, імпрегновані 15 мкг кларитроміцину (диско-дифузійний метод Кірбі-Бауера); при інтерпретації тесту діаметри зон пригнічення зростання корелюють зі значеннями МПК кларитроміцину. Значення МПК визначаються методом розведення у бульйоні чи агарі. При використанні цих методик звіт з лабораторії про те, що штам є "чутливим", свідчить про те, що збудник інфекції, ймовірно, відповість на лікування. Відповідь "резистентна" вказує на те, що збудник, можливо, не відповість на лікування. Відповідь "проміжна чутливість" передбачає, що терапевтичний ефект препарату може бути неоднозначним або мікроорганізм може виявитися чутливим при застосуванні більш високих доз препарату (проміжна чутливість також називається "помірною чутливістю").Показання до застосуванняІнфекційно-запальні захворювання, спричинені чутливими до кларитроміцину мікроорганізмами: інфекції нижніх дихальних шляхів (такі як бронхіт, пневмонія); інфекції верхніх дихальних шляхів та ЛОР-органів (тонзиліт, фарингіт, синусит, гострий середній отит); інфекції шкіри та м'яких тканин (такі як фолікуліт, запалення підшкірної клітковини, пика).Протипоказання до застосуванняГіперчутливість до кларитроміцину, макролідів та інших компонентів препарату. Одночасний прийом кларитроміцину з наступними препаратами: астемізол, цизаприд, домперидон, пімозід, терфенадин. Одночасний прийом кларитроміцину з алкалоїдами ріжків, наприклад, ерготамін, дигідроерготамін. Одночасний прийом кларитроміцину з мідазоламом для внутрішнього прийому. Одночасний прийом кларитроміцину з інгібіторами ГМГ-КоА-редуктази (статинами), які значною мірою метаболізуються ізоферментом CYP3A4 (ловастатин, симвастатин) у зв'язку з підвищенням ризику міопатії, включаючи рабдоміоліз. Одночасний прийом кларитроміцину з колхіцином. Одночасний прийом кларитроміцину з тикагрелором або ранолазином. Подовження інтервалу QT на електрокардіограмі (ЕКГ) (вроджене або набуте документально підтверджене подовження інтервалу QT) в анамнезі, шлуночкова аритмія, включаючи шлуночкову тахікардію або шлуночкову тахікардію типу "пірует" в анамнезі. Гіпокаліємія (ризик подовження інтервалу QT на ЕКГ). Печінкова недостатність тяжкого ступеня, що протікає одночасно з нирковою недостатністю. Холестатична жовтяниця/гепатит в анамнезі, що розвинулися при застосуванні кларитроміцину. Порфирія. Період грудного вигодовування. Вік до 18 років (за показаннями: тонзиліт, гострий середній отит), до 12 років (за іншими показаннями). Непереносимість лактози, дефіцит лактази, синдром глюкозо-галактозної мальабсорбції. З обережністю: Ниркова недостатність середнього та тяжкого ступеня тяжкості. Печінкова недостатність середнього та тяжкого ступеня тяжкості. Одночасний прийом кларитроміцину з бензодіазепінами, такими як алпразол, триазол, мідазол для внутрішньовенного застосування або для нанесення на слизову оболонку порожнини рота. Одночасний прийом з препаратами, що метаболізуються ізоферментом CYP3A, наприклад, карбамазепін, цилостазол, циклоспорин, дизопірамід, ібрутиніб, метилпреднізолон, омепразол, непрямі антикоагулянти (наприклад, варфарин), хінідин, ріфабутін, силден. Одночасний прийом з препаратами, що індукують ізофермент CYP3A4, наприклад, рифампіцин, фенітоїн, карбамазепін, фенобарбітал, препарати Звіробою продірявленого. Одночасний прийом із блокаторами "повільних" кальцієвих каналів (БМКК), які метаболізуються ізоферментом CYP3A4 (наприклад, верапаміл, амлодипін, дилтіазем). Одночасний прийом зі статинами, які не залежать від метаболізму ізоферменту CYP3A (наприклад, флувастатин). Пацієнти з ішемічною хворобою серця (ІБО), тяжкою серцевою недостатністю, гіпомагніємією, порушенням провідності або клінічно значущою брадикардією, а також пацієнти, які одночасно приймають антиаритмічні препарати IA класу (хінідин, прокаїнамід) та III класу (дофетилід, аміодарон, соталол). Вагітність.Вагітність та лактаціяБезпека застосування кларитроміцину при вагітності та в період грудного вигодовування не встановлена. Застосування кларитроміцину при вагітності (особливо в І триместрі) можливе лише у випадку, коли відсутня альтернативна терапія, а потенційна користь для матері перевищує потенційний ризик для плода. Кларитроміцин виводиться із грудним молоком. При необхідності прийому в період грудного вигодовування годування груддю слід припинити.Побічна діяКласифікація частоти розвитку побічних ефектів (кількість зареєстрованих випадків/кількість пацієнтів), рекомендована Всесвітньою організацією охорони здоров'я (ВООЗ): дуже часто ≥1/10; часто від ≥ 1/100 до Алергічні реакції: часто - шкірний висип; нечасто - анафілактоїдна реакція1, гіперчутливість, бульозний дерматит1, свербіж шкіри. кропив'янка, макулопапульозний висип3; частота невідома - анафілактична реакція, ангіоневротичний набряк, серйозні шкірні небажані реакції (наприклад, гострий генералізований екзантематозний пустульоз), синдром Стівенса-Джонсона, токсичний епідермальний некроліз, лікарський висип з еозинофілією та системною симптоматикою. З боку нервової системи: часто – головний біль, безсоння; нечасто - непритомність1, дискінезія1, запаморочення, сонливість, тремор, занепокоєння, підвищена збудливість3; частота невідома - судоми, психотичні розлади, сплутаність свідомості, деперсоналізація, депресія, дезорієнтація, галюцинації, порушення сновидінь ("жахливі" сновидіння), парестезія, манія. З боку шкірних покривів: часто – підвищене потовиділення; частота невідома – акне. З боку сечостатевої системи: частота невідома – ниркова недостатність, інтерстиціальний нефрит. З боку обміну речовин: нечасто – анорексія, зниження апетиту. З боку опорно-рухового апарату: нечасто – м'язовий спазм3, кістково-м'язова скутість1, міалгія2; частота невідома – рабдоміоліз2*, міопатія. З боку травної системи: часто – діарея, блювання, диспепсія, нудота, біль у ділянці живота; нечасто - езофагіт1, гастроезофагеальна рефлюксна хвороба2, гастрит, прокталгія2, стоматит, глосит, здуття живота4, запор, сухість слизової оболонки порожнини рота, відрижка, метеоризм, холестаз4, гепатит, цел; частота невідома – гострий панкреатит, зміна кольору язика та зубів, печінкова недостатність, холестатична жовтяниця. З боку дихальної системи: нечасто – бронхіальна астма1, носова кровотеча2, тромбоемболія легеневої артерії1. З боку органів чуття: часто – дисгевзія; нечасто - вертиго, порушення слуху, дзвін у вухах; частота невідома – глухота, агевзія (втрата смакових відчуттів), паросмія, аносмія. З боку серцево-судинної системи: часто – вазодилатація1; нечасто – зупинка серця1, фібриляція передсердь1, подовження інтервалу QT на ЕКГ, екстрасистолія1, відчуття серцебиття; частота невідома – шлуночкова тахікардія, у тому числі типу “пірует”, фібриляція шлуночків, кровотеча. Лабораторні показники: часто – відхилення лабораторних показників функції печінки; нечасто - підвищення сироваткової концентрації креатиніну1, підвищення сироваткової концентрації сечовини1, зміна співвідношення альбумін/глобулін1, лейкопенія, нейтропенія4, еозинофілія4, тромбоцитемія3, підвищення активності аланінамінотрансферази (АЛТ), аспартатаміфтранс )4, лактатдегідрогенази (ЛДГ)4 у плазмі крові; частота невідома – агранулоцитоз, тромбоцитопенія, збільшення значення міжнародного нормалізованого відношення (МНО), подовження протромбінового часу, зміна кольору сечі, підвищення концентрації білірубіну у плазмі крові. Інші: дуже часто – флебіт у місці ін'єкції1; часто - біль у місці ін'єкції1, запалення у місці ін'єкції1; нечасто - нездужання4, гіпертермія3, астенія, біль у грудній клітці4, озноб4, підвищена стомлюваність4. Інфекційні та паразитарні захворювання: нечасто – целюліт1, кандидоз, гастроентерит2, вторинні інфекції3 (у тому числі вагінальні); частота невідома - псевдомембранозний коліт, пика. Діти Передбачається, що частота, тип та тяжкість небажаних реакцій у дітей така сама, як у дорослих. Пацієнти зі зниженим імунітетом У пацієнтів із синдромом набутого імунодефіциту (СНІД) та іншими імунодефіцитами, які отримують кларитроміцин у більш високих дозах протягом тривалого часу для лікування мікобактеріальних інфекцій, часто важко відрізнити небажані ефекти препарату від симптомів ВІЛ-інфекції або супутнього захворювання. Найчастішими небажаними явищами у пацієнтів, які приймали добову дозу кларитроміцину, що дорівнює 1000 мг, були: нудота, блювання, дисгевзія, біль у ділянці живота, діарея, шкірний висип, метеоризм, головний біль, запор, порушення слуху, підвищення активності ACT та АЛ плазмі крові. Також відзначалися випадки небажаних явищ із низькою частотою виникнення, такі як задишка, безсоння та сухість слизової оболонки порожнини рота. У пацієнтів із зниженим імунітетом проводили оцінку лабораторних показників, аналізуючи їх значні відхилення від норми (різке підвищення чи зниження). На підставі даного критерію у 2-3% пацієнтів, які отримували кларитроміцин у дозі 1000 мг щодня, було зареєстровано значне підвищення активності ACT та АЛТ у плазмі, а також зниження кількості лейкоцитів та тромбоцитів. У невеликої кількості пацієнтів було зареєстровано підвищення сироваткової концентрації залишкового азоту сечовини. * У деяких повідомленнях про рабдоміоліз кларитроміцин приймався одночасно з іншими лікарськими засобами, з прийомом яких, як відомо, пов'язаний розвиток рабдоміолізу (статини, фібрати, колхіцин або алопуринол). 1 Повідомлення про дані побічних реакцій були отримані під час клінічних досліджень, а також післяреєстраційного застосування кларитроміцину у лікарській формі ліофілізат для приготування розчину для інфузій. 2 Повідомлення про дані побічних реакцій були отримані під час клінічних досліджень, а також післяреєстраційного застосування кларитроміцину у лікарській формі таблетки з пролонгованим вивільненням, покриті плівковою оболонкою. 3 Повідомлення про дані побічних реакцій були отримані під час клінічних досліджень, а також післяреєстраційного застосування кларитроміцину у лікарській формі порошок для приготування суспензії для прийому внутрішньо. 4 Повідомлення про дані побічних реакцій були отримані під час клінічних досліджень, а також післяреєстраційного застосування кларитроміцину у лікарській формі таблетки, покриті плівковою оболонкою.Взаємодія з лікарськими засобамиЗастосування наступних лікарських засобів одночасно з кларитроміцином протипоказане у зв'язку з можливістю розвитку серйозних побічних ефектів. Цизаприд, домперидон, пімозід, терфенадип та астемізол При одночасному прийомі кларитроміцину з цизапридом, пимозидом, домперидоном, терфенадином або астемізолом повідомлялося про підвищення концентрації останніх у плазмі крові, що може призвести до подовження інтервалу QT на ЕКГ та появі серцевих аритмій, включаючи шлуночкову тахікардію (в тому числі шлуночкову тахікардію). ) та фібриляцію шлуночків. Алкалоїди ріжків Післяреєстраційні дослідження показують, що при одночасному застосуванні кларитроміцину з ерготаміном або дигідроерготаміном можливі наступні ефекти, пов'язані з гострим отруєнням препаратами групи ерготамінів: судинний спазм, ішемія кінцівок та інших тканин, включаючи центральну нервову систему (ЦНС). Одночасне застосування кларитроміцину та алкалоїдів ріжків протипоказане. Інгібітори ГМГ-КоА-редуктази (статини) Одночасний прийом кларитроміцину з ловастатином або симвастатином протипоказаний у зв'язку з тим, що дані статини значною мірою метаболізуються ізоферментом CYP3A4, і одночасне застосування з кларитроміцином підвищує їх сироваткові концентрації, що призводить до підвищення ризику розвитку міопатії, включаючи рабдомі. Повідомлялося про випадки рабдоміолізу у пацієнтів, які приймали кларитроміцин одночасно з цими препаратами. У разі необхідності застосування кларитроміцину слід припинити прийом ловастатину або симвастатину на час терапії. Кларитроміцин слід застосовувати з обережністю у разі комбінованої терапії з іншими статинами. Рекомендується застосовувати статини, метаболізм яких не залежить від ізоферменту CYP3A (наприклад, флувастатин). У разі потреби одночасного прийому рекомендується приймати найменшу дозу статину. Слід контролювати розвиток ознак та симптомів міопатії. Мідазолам для прийому внутрішньо При одночасному застосуванні внутрішньо мідазоламу та кларитроміцину у лікарській формі таблетки (500 мг 2 рази на добу) відзначалося збільшення AUC мідазоламу у 7 разів. Одночасне застосування кларитроміцину та мідазоламу для прийому внутрішньо протипоказане. Вплив інших лікарських засобів на кларитроміцин Лікарські препарати, що є індукторами ізоферменту CYP3A (наприклад, рифампіцин, фенітоїн, карбамазепін, фенобарбітал, препарати Звіробою продірявленого) можуть індукувати метаболізм кларитроміцину. Це може призвести до субтерапевтичної концентрації кларитроміцину та відповідно до зниження його ефективності. Крім того, необхідно спостерігати за концентрацією індуктора ізоферменту CYP3A у плазмі крові, яка може підвищитися через інгібування ізоферменту CYP3A кларитроміцином. При одночасному застосуванні рифабутину та кларитроміцину спостерігалося підвищення концентрації рифабутину та зниження концентрації кларитроміцину в плазмі крові з підвищеним ризиком розвитку увеїту. Наступні препарати мають доведений або передбачуваний вплив на концентрацію кларитроміцину в плазмі крові, у разі їх одночасного застосування з кларитроміцином може знадобитися корекція дози або перехід на альтернативне лікування Ефавіренз, невірапін, рифампіцин, рифабутин та рифапентин Потужні індуктори системи цитохрому Р450, такі як ефавіренз, невірапін, рифампіцин, рифабутин і рифапентин можуть прискорювати метаболізм кларитроміцину і, таким чином, знижувати концентрацію кларитроміцину в плазмі крові, а також послаблювати терапевтичний ефект. ВІН-кларитроміцину - метаболіту, що також є мікробіологічно активним. Оскільки мікробіологічна активність кларитроміцину та 14-ОН-кларитроміцину відрізняється щодо різних бактерій, терапевтичний ефект може знижуватися при одночасному застосуванні кларитроміцину та індукторів системи цитохрому Р450. Етравірін Концентрація кларитроміцину в плазмі знижується при одночасному застосуванні з етравірином, а концентрація активного метаболіту 14-ОН-кларитроміцину в плазмі крові підвищується. Оскільки 14-ОН-кларитроміцин має низьку активність по відношенню до інфекцій MAC, може змінюватися загальна активність щодо цих збудників, тому для лікування MAC слід розглядати альтернативне лікування. Флуконазол Одночасний прийом флуконазолу в дозі 200 мг щоденно та кларитроміцину в дозі 500 мг 2 рази на добу у 21 здорового добровольця призвело до збільшення середнього значення мінімальної рівноважної концентрації кларитроміцину та AUC на 33% та 18% відповідно. При цьому одночасний прийом значно не впливав на середню рівноважну концентрацію активного метаболіту 14-ОН-кларитроміцину. Корекція дози кларитроміцину у разі одночасного прийому флуконазолу не потрібна. Рітонавір Фармакокінетичне дослідження показало, що одночасний прийом ритонавіру в дозі 200 мг кожні 8 годин та кларитроміцину в дозі 500 мг кожні 12 годин призвів до помітного пригнічення метаболізму кларитроміцину. При одночасному прийомі ритонавіру Сmах кларитроміцину в плазмі збільшилася на 31%, Cmin збільшилася на 182% і AUC збільшилася на 77%. Було відзначено практично повне придушення утворення 14-ОН-кларитроміцину. Завдяки широкому терапевтичному діапазону кларитроміцину зменшення його дози у пацієнтів із нормальною нирковою функцією не потрібне. У пацієнтів з нирковою недостатністю доцільно розглянути такі варіанти корекції дози: при КК 30-60 мл/хв. доза кларитроміцину повинна бути зменшена на 50%. У пацієнтів з нирковою недостатністю доцільно розглянути наступні варіанти корекції дози: при КК 30-60 мл/хв доза кларитроміцину повинна бути зменшена на 50%, при КК менше 30 мл/хв доза кларитроміцину повинна бути зменшена на 75%. Ритонавір не слід одночасно приймати з кларитроміцином у дозах, що перевищують 1 г на добу. Подібні корекції доз повинні розглядатися у пацієнтів зі зниженою функцією нирок, якщо ритонавір застосовується як фармакокінетичний "підсилювач" при застосуванні інших інгібіторів протеази ВІЛ, включаючи атазанавір та саквінавір. Дія кларитроміцину на інші лікарські препарати Антиаритмічні засоби (хінідин та дизопірамід) Можливе виникнення шлуночкової тахікардії типу "пірует" при одночасному застосуванні кларитроміцину та хінідину або дизопіраміду. При одночасному прийомі кларитроміцину з цими препаратами слід регулярно проводити контроль ЕКГ щодо подовження інтервалу QT, а також слід контролювати сироваткові концентрації цих препаратів. У післяреєстраційному періоді повідомлялося про випадки розвитку гіпоглікемії при одночасному прийомі кларитроміцину та дизопіраміду. Необхідно контролювати концентрацію глюкози в крові при одночасному застосуванні кларитроміцину та дизопіраміду. Гіпоглікемічні засоби для внутрішнього застосування/інсулін При одночасному застосуванні кларитроміцину та гіпоглікемічних засобів для прийому внутрішньо (наприклад, похідні сульфонілсечовини) та/або інсуліну може спостерігатися виражена гіпоглікемія. Одночасне застосування кларитроміцину з деякими гіпоглікемічними препаратами (наприклад, натеглінід, піоглітазон, репаглінід та росиглітазон) може призвести до інгібування ізоферменту CYP3A кларитроміцином, внаслідок чого може розвинутись гіпоглікемія. Рекомендується ретельний контроль концентрації глюкози у крові. Взаємодія зумовлена ізоферментом CYP3A Одночасний прийом кларитроміцину, який, як відомо, інгібує ізофермент CYP3A, та препаратів, що первинно метаболізуються ізоферментом CYP3A, може асоціюватися із взаємним підвищенням їх концентрацій, що може посилити або продовжити як терапевтичні, так і побічні ефекти. Кларитроміцин слід обережно застосовувати пацієнтам, які отримують препарати, які є субстратами ізоферменту CYP3A, особливо якщо ці препарати мають вузький терапевтичний діапазон (наприклад, карбамазепін) та/або препарати, які інтенсивно метаболізуються цим ізоферментом. У разі потреби повинна проводитися корекція дози препарату, який приймається одночасно з кларитроміцином; також по можливості повинен проводитися моніторинг сироваткових концентрацій препаратів, що первинно метаболізуються ізоферментом CYP3A. Метаболізм наступних препаратів/класів здійснюється тим же ізоферментом CYP3A, що і метаболізм кларитроміцину (але цей список не є вичерпним): алпразолам, карбамазепін, цилостазол, циклоспорин, дизопірамід, ібрутиніб, метилпреднізолон, мідазолам наприклад, варфарин), атипові антипсихотичні засоби (наприклад, кветіапін), хінідин, рифабутин, силденафіл, сиролімус, такролімус, тріазолам та вінбластин. До препаратів, що взаємодіють подібним чином через інші ізоферменти в рамках системи цитохрому Р450, відносяться: фенітоїн, теофілін та вальпроєва кислота. Непрямі антикоагулянти При одночасному прийомі варфарину та кларитроміцину можлива кровотеча, виражене збільшення МНО та подовження протромбінового часу. У разі одночасного застосування з варфарином або іншими непрямими антикоагулянтами необхідно контролювати МНО та протромбіновий час. Омепразол Кларитроміцин (по 500 мг кожні 8 годин) досліджувався у здорових дорослих добровольців у поєднанні з омепразолом (по 40 мг щодня). При одночасному застосуванні кларитроміцину та омепразолу рівноважні плазмові концентрації омепразолу були збільшені (Сmах, AUC0-24 та Т1/2 збільшилися на 30%, 89% та 34% відповідно). Середнє значення pH шлунка протягом 24 годин склало 5,2 (при прийомі омепразолу окремо) та 5,7 (при прийомі омепразолу одночасно з кларитроміцином). Силденафіл, тадалафіл та варденафіл Кожен із цих інгібіторів фосфодіестерази метаболізується принаймні частково за участю ізоферменту CYP3A. У той же час, ізофермент CYP3A може інгібуватися в присутності кларитроміцину. Одночасне застосування кларитроміцину з силденафілом, тадалафілом або варденафілом може призвести до збільшення інгібуючої дії на фосфодіестеразу. При застосуванні цих препаратів одночасно з кларитроміцином слід розглянути можливість зменшення дози силденафілу, тадалафілу та варденафілу. Теофілін, карбамазепін При одночасному застосуванні кларитроміцину та теофіліну або карбамазепіну можливе підвищення концентрації даних препаратів у системному кровотоку. Толтеродін Первинний метаболізм толтеродину здійснюється через ізофермент CYP2D6. Однак у частині популяції, позбавленої CYP2D6, метаболізм відбувається через ізофермент CYP3A. У цій групі населення пригнічення ізоферменту CYP3A призводить до значно більших концентрацій толтеродину в сироватці крові. У популяції з низьким рівнем метаболізму через ізофермент CYP2D6 може знадобитися зниження дози толтеродину при одночасному застосуванні інгібіторів ізоферменту CYP3A, таких як кларитроміцин. Бензодіазепіни (наприклад, алпразолам, мідазолам, тріазолам) При одночасному застосуванні мідазоламу та таблеток кларитроміцину (500 мг 2 рази на добу) відзначалося збільшення AUC мідазоламу у 2,7 раза після внутрішньовенного введення мідазоламу. Якщо одночасно з кларитроміцином застосовується мідазолам у лікарській формі розчин для внутрішньовенного введення, слід ретельно контролювати стан пацієнта для можливої корекції дози мідазоламу. Введення лікарського препарату через слизову оболонку порожнини рота, що дає можливість обійти пресистемну елімінацію лікарського препарату, швидше за все, призведе до взаємодії, аналогічної тому, що спостерігається при внутрішньовенному введенні мідазоламу, а не прийому внутрішньо. Такі ж запобіжні заходи слід застосовувати і до інших бензодіазепінів, які метаболізуються ізоферментом CYP3A, включаючи триазолів та алпразолів. Для бензодіазепінів, виведення яких не залежить від ізоферменту CYP3A (темазепам, нітразепам, лоразепам), малоймовірно клінічно значуща взаємодія з кларитроміцином. При одночасному застосуванні кларитроміцину та триазоламу можлива дія на ЦНС, наприклад, сонливість та сплутаність свідомості. У зв'язку з цим, у разі одночасного застосування рекомендується стежити за симптомами порушення ЦНС. Взаємодії з іншими лікарськими засобами Колхіцін Колхіцин є субстратом як ізоферменту CYP3A, так і білка-переносника Р-глікопротеїну (Pgp). Відомо, що кларитроміцин та інші макроліди є інгібіторами ізоферменту CYP3A та Pgp. При одночасному застосуванні кларитроміцину та колхіцину інгібування Pgp та/або ізоферменту CYP3A може призвести до посилення дії колхіцину. Слід контролювати розвиток клінічних симптомів отруєння колхіцином. Зареєстровані постреєстраційні повідомлення про випадки отруєння колхіцином при його одночасному прийомі з кларитроміцином, частіше у пацієнтів похилого віку. Деякі з описаних випадків відбувалися у пацієнтів із нирковою недостатністю. Як повідомлялося, деякі випадки закінчувалися летальним кінцем. Одночасне застосування кларитроміцину та колхіцину протипоказане. Дігоксин Передбачається, що дигоксин є субстратом PGP. Відомо, що кларитроміцин пригнічує Pgp. При одночасному застосуванні кларитроміцину та дигоксину інгібування Pgp кларитроміцином може призвести до посилення дії дигоксину. Одночасний прийом дигоксину та кларитроміцину також може призвести до підвищення сироваткової концентрації дигоксину. У деяких пацієнтів спостерігалися клінічні симптоми отруєння дигоксином, включаючи потенційно летальні аритмії. При одночасному прийомі кларитроміцину та дигоксину слід ретельно контролювати концентрацію дигоксину у сироватці крові. Зідовудін Одночасний прийом таблеток кларитроміцину та зидовудину внутрішньо дорослими ВІЛ-інфікованими пацієнтами може призвести до зниження рівноважної концентрації зидовудину в плазмі крові. Оскільки кларитроміцин може перешкоджати всмоктуванню зидовудину при прийомі внутрішньо, взаємодії можна значно уникнути, приймаючи кларитроміцин і зидовудін з інтервалом в 4 години. Подібної взаємодії не спостерігали у ВІЛ-інфікованих дітей, які отримують дитячу суспензію кларитроміцину з зидовудином або дидезоксіїнозином. Оскільки кларитроміцин може перешкоджати всмоктуванню зидовудину при їх одночасному прийомі внутрішньо у дорослих пацієнтів, така взаємодія навряд чи можлива при застосуванні кларитроміцину внутрішньовенно. Фенітоїн та вальпроєва кислота Є дані про взаємодію інгібіторів ізоферменту CYP3A (включаючи кларитроміцин) з препаратами, які не метаболізуються за допомогою ізоферменту CYP3A (фенітоїн та вальпроєва кислота). Для цих препаратів при одночасному застосуванні з кларитроміцином рекомендується визначення їх сироваткових концентрацій, оскільки є повідомлення про їх підвищення. Двоспрямована взаємодія лікарських засобів Атазанавір Кларитроміцин та атазанавір є як субстратами, так і інгібіторами ізоферменту CYP3A. Існує свідчення двонаправленої взаємодії цих препаратів. Одночасне застосування кларитроміцину (500 мг 2 рази на добу) та атазанавіру (400 мг 1 раз на добу) може призвести до дворазового збільшення дії кларитроміцину та зменшення дії 14-ОН-кларитроміцину на 70% зі збільшенням AUC атазанавіру на 28%. Завдяки широкому терапевтичному діапазону кларитроміцину зменшення його дози у пацієнтів з нормальною нирковою функцією не потрібне. У пацієнтів з нирковою недостатністю середнього ступеня тяжкості (КК 30-60 мл/хв) доза кларитроміцину повинна бути зменшена на 50%. У пацієнтів з КК менше 30 мл/хв дозу кларитроміцину слід зменшити на 75%, застосовуючи для цього відповідну лікарську форму кларитроміцину. Кларитроміцин у дозах, що перевищують 1000 мг на добу, не можна застосовувати одночасно з інгібіторами протеаз. БМКК При одночасному застосуванні кларитроміцину та БМКК, які метаболізуються ізоферментом CYP3A4 (наприклад, верапаміл, амлодипін, дилтіазем), слід бути обережним, оскільки існує ризик виникнення артеріальної гіпотензії. При одночасному застосуванні можуть підвищуватися плазмові концентрації кларитроміцину та БМКК. Артеріальна гіпотензія, брадіаритмія та лактоацидоз можливі при одночасному прийомі кларитроміцину та верапамілу. Ітраконазол Кларитроміцин та ітраконазол є субстратами та інгібіторами ізоферменту CYP3A, що визначає двонаправлену взаємодію препаратів. Кларитроміцин може підвищити концентрацію ітраконазолу в плазмі, тоді як ітраконазол може підвищити плазмову концентрацію кларитроміцину. Пацієнтів, які одночасно приймають ітраконазол та кларитроміцин, слід ретельно обстежити на наявність симптомів посилення або збільшення тривалості фармакологічних ефектів цих препаратів. Саквінавір Кларитроміцин та саквінавір є субстратами та інгібіторами ізоферменту CYP3A, що визначає двоспрямовану взаємодію препаратів. Одночасне застосування кларитроміцину (500 мг 2 рази на добу) і саквінавіру (в м'яких желатинових капсулах, 1200мг 3 рази на добу) у 12 здорових добровольців викликало збільшення AUC і Смах саквінавіру в плазмі крові на 177% і 187% відповідно. окремо. Значення AUC та Сmах кларитроміцину були приблизно на 40% вищі, ніж при терапії одним кларитроміцином. При одночасному застосуванні цих двох препаратів протягом обмеженого часу у дозах/складах, зазначених вище, корекція дози не потрібна. Результати дослідження лікарських взаємодій із застосуванням саквінавіру у м'яких желатинових капсулах можуть не відповідати ефектам, що спостерігаються при застосуванні саквінавіру у твердих желатинових капсулах. Результати дослідження лікарських взаємодій при терапії саквінавіром окремо можуть не відповідати ефектам, що спостерігаються при терапії комбінацією саквінавір/ритонавір. При прийомі саквінавіру одночасно з ритонавіром слід враховувати потенційний вплив ритонавіру на кларитроміцин.Спосіб застосування та дозиВсередину. Таблетку слід ковтати повністю, не розламувати і не розжовувати. Дорослим та дітям старше 12 років – по 1 таблетці (500 мг) 1 раз на добу під час їжі. При тонзиліті та гострому середньому отиті: дорослим та дітям старше 18 років – по 1 таблетці (500 мг) 1 раз на добу під час їжі. При тяжких інфекціях дозу збільшують до 2 таблеток (1000 мг) 1 раз на добу під час їжі. Звичайна тривалість лікування від 5 до 14 днів. Виняток становлять позалікарняна пневмонія та синусит, які вимагають лікування від 6 до 14 днів. Порушення функції нирок Для пацієнтів з нирковою недостатністю важкого ступеня (КК менше 30 мл/хв) звичайна рекомендована доза становить 250 мг 1 раз на добу, у цьому випадку можливе застосування препарату Фромілід®, таблетки, вкриті плівковою оболонкою, 250 мг. При більш тяжких інфекціях рекомендована доза становить 1 таблетка 500 мг із пролонгованим вивільненням кларитроміцину. У пацієнтів з нирковою недостатністю середнього ступеня тяжкості (КК від 30 до 60 мл/хв) корекція дози не потрібна.ПередозуванняСимптоми: прийом внутрішньо великої дози кларитроміцину може викликати симптоми порушень з боку шлунково-кишкового тракту. У одного пацієнта з біполярним розладом в анамнезі після прийому 8 г кларитроміцину описані зміни психічного стану, параноїдальна поведінка, гіпокаліємія та гіпоксемія. Лікування: при передозуванні слід видалити неабсорбований препарат із шлунково-кишкового тракту (промивання шлунка, прийом активованого вугілля та ін.) та провести симптоматичну терапію. Гемодіаліз та перитонеальний діаліз не мають істотного впливу на концентрацію кларитроміцину в сироватці крові, що характерно і для інших лікарських препаратів групи макролідів.Запобіжні заходи та особливі вказівкиТривалий прийом антибіотиків може призводити до утворення колоній зі збільшенням кількості нечутливих бактерій та грибів. При суперінфекції слід призначити відповідну терапію. Призначення кларитроміцину вагітним жінкам має проводитися при ретельній оцінці співвідношення ризику та користі, особливо протягом перших трьох місяців вагітності. При застосуванні кларитроміцину повідомлялося про порушення функції печінки (підвищення активності "печінкових" ферментів у плазмі крові, гепатоцелюлярний та/або холестатичний гепатит з жовтяницею або без). Порушення функції печінки може бути важким, але є оборотним. Є випадки печінкової недостатності з летальним результатом головним чином пов'язані з наявністю серйозних супутніх захворювань та/або одночасним застосуванням інших лікарських засобів. При появі ознак та симптомів гепатиту, таких як анорексія, жовтяниця, потемніння сечі, свербіж, болючість живота при пальпації, необхідно негайно припинити терапію кларитроміцином. За наявності хронічних захворювань печінки необхідно проводити регулярний контроль активності печінкових ферментів сироватки крові. При лікуванні практично всіма антибактеріальними засобами, у тому числі кларитроміцином, описані випадки псевдомембранозного коліту, тяжкість якого може змінюватись від легкого до загрозливого життя. При лікуванні практично всіма антибактеріальними препаратами, у тому числі кларитроміцином, описані випадки Clostridium difficile-асоційованої діареї, тяжкість якої може змінюватись від легкої діареї до загрозливого життя коліту. Антибактеріальні препарати можуть змінити нормальну мікрофлору кишечника, що може спричинити зростання Clostridium difficile. Псевдомембранозний коліт, викликаний Clostridium difficile, необхідно підозрювати у всіх пацієнтів, у яких після застосування антибактеріальних засобів розвинулася діарея. Після проведення курсу антибіотикотерапії потрібне ретельне медичне спостереження за пацієнтом.Описувалися випадки розвитку псевдомембранозного коліту через 2 місяці після прийому антибіотиків. При лікуванні макролідами, включаючи кларитроміцин, спостерігалося подовження серцевої реполяризації та інтервалу QT, збільшуючи ризик розвитку серцевої аритмії та шлуночкової тахікардії типу “пірует”. Оскільки такі ситуації можуть призвести до збільшення ризику розвитку шлуночкових аритмій (у тому числі шлуночкової тахікардії типу "пірует"), то: Кларитроміцин не повинен застосовуватися у таких категорій пацієнтів: у пацієнтів із гіпокаліємією; одночасне застосування кларитроміцину з астемізолом, цизапридом, домперидоном, пімозидом та терфенадином протипоказано; у пацієнтів із вродженим або набутим зареєстрованим подовженням інтервалу QT або наявністю шлуночкової аритмії в анамнезі. Кларитроміцин повинен застосовуватися з обережністю у таких категорій пацієнтів: у пацієнтів з ІХС, тяжкою серцевою недостатністю, порушеннями провідності або клінічно значущою брадикардією; у пацієнтів з електролітними порушеннями, такими як гіпомагніємія; у пацієнтів, які одночасно приймають інші лікарські препарати, пов'язані з подовженням інтервалу QT. У ході епідеміологічних досліджень з вивчення ризику несприятливих серцево-судинних наслідків при застосуванні макролідів було отримано неоднозначні результати. У деяких спостережних дослідженнях було встановлено рідкісний короткочасний ризик розвитку аритмії, інфаркту міокарда та смерті від серцево-судинних захворювань, пов'язаних із застосуванням макролідів, включаючи кларитроміцин. При призначенні кларитроміцину слід співвідносити передбачувану користь від прийому препарату з цими ризиками. Можливий розвиток перехресної резистентності до кларитроміцину та інших антибіотиків групи макролідів, а також лінкоміцину та кліндаміцину. Враховуючи зростаючу резистентність Streptococcus pneumoniae до макролідів, важливо проводити тестування чутливості при призначенні кларитроміцину пацієнтам із позалікарняною пневмонією. При шпитальній пневмонії кларитроміцин слід застосовувати у комбінації з відповідними антибіотиками. Інфекції шкіри та м'яких тканин легкого та середнього ступеня тяжкості найчастіше викликані Staphylococcus aureus та Streptococcus pyogenes. При цьому обидва збудники можуть бути стійкими до макролідів. Тому важливо проводити тест на чутливість. Макроліди можна застосовувати при інфекціях, викликаних Corynebacterium minutissimum, захворюваннях вугри вульгарні та пика, а також у тих ситуаціях, коли не можна застосовувати пеніцилін. У разі появи гострих реакцій гіперчутливості, таких як анафілактична реакція, серйозні шкірні небажані реакції (наприклад, гострий генералізований екзантематозний пустульоз), синдром Стівенса-Джонсона, токсичний епідермальний некроліз та лікарський висип з еозинофілією та Систем симптом прийом кларитроміцину та почати відповідну терапію. У разі одночасного застосування з варфарином або іншими непрямими антикоагулянтами необхідно контролювати МНО та протромбіновий час. Спеціальна інформація про допоміжні речовини Препарат Фромілід уно містить лактозу, тому протипоказаний при таких станах: непереносимість лактози, дефіцит лактази, синдром глюкозо-галактозної мальабсорбції. Вплив на здатність до керування автотранспортом та управління механізмами Дані щодо впливу кларитроміцину на здатність керувати транспортними засобами, механізмами відсутні. Слід бути обережними при керуванні транспортними засобами, механізмами, враховуючи потенційну можливість запаморочення, вертиго, сплутаності свідомості та дезорієнтації, які можуть виникнути при застосуванні даного препарату.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
273,00 грн
153,00 грн
Склад, форма випуску та упаковкаПігулки - 1 таб. Діюча речовина: кларитроміцин 500 мг; допоміжні речовини: натрію алгінат, натрію кальцію алгінат, лактози моногідрат, повідон К25, полісорбат-80, кремнію діоксид колоїдний, магнію стеарат, тальк; Оболонка плівкова: гіпромелоза, тальк, барвник заліза оксид жовтий (Е172), титану діоксид (Е171), пропіленгліколь По 5 або 7 таблеток поміщають у блістер із ПВХ/ПВДХ - алюмінієвої фольги (PVC/PVDC-Al). По 1 блістеру (блістер по 5 таблеток) або по 1 або 2 блістери (блістер по 7 таблеток) поміщають у картонну пачку разом з інструкцією по застосуванню.Опис лікарської формиОвальні, двоопуклі таблетки, покриті плівковою оболонкою коричнево-жовтого кольору, з маркуванням U на одній стороні. Вид на зламі: шорстка маса білого або майже білого кольору з плівковою оболонкою коричнево-жовтого кольору.Фармакотерапевтична групаАнтибіотик-макролід.ФармакокінетикаВсмоктування Препарат швидко всмоктується з шлунково-кишкового тракту. Абсолютна біодоступність становить близько 50%. При прийомі повторних доз кумуляції практично не виявлено, і характер метаболізму в організмі людини не змінювався. Розподіл, метаболізм та виведення In vitro Кларитроміцин зв'язується з білками плазми на 70% у концентрації від 0,45 до 4,5 мкг/мл. При концентрації 45 мкг/мл зв'язування знижується до 41%, ймовірно, через насичення місць зв'язування. Це спостерігається лише при концентраціях, що багаторазово перевищують терапевтичну концентрацію. Здорові добровольці У пацієнтів, які приймають 500 мг кларитроміцину 1 раз на добу після прийому їжі, максимальна концентрація (Сmах) кларитроміцину та 14-ОН-кларитроміцину в плазмі крові становила 1,3 мкг/мл та 0,48 мкг/мл відповідно. Період напіввиведення (Т1/2) кларитроміцину та Т1/2 його основного метаболіту склали 5,3 години та 7,7 годин відповідно. При прийомі разової дози кларитроміцину в лікарській формі таблетки з пролонгованим вивільненням, покриті плівковою оболонкою, 1000 мг (500 мг 2 рази на добу), Смах кларитроміцину та його гідроксильованого метаболіту в плазмі крові становила 2,4 мкг/мл/мл мл відповідно. Т1/2 кларитроміцину при прийомі в дозі 1000 мг становив 5,8 години, тоді як аналогічний показник для 14-ОН-кларитроміцину становив 8,9 години. Час досягнення максимальної концентрації (ТСmах) при прийомі внутрішньо як 500 мг, так і 1000 мг кларитроміцину становить приблизно 6 годин. Стах 14-ОН-кларитроміцину в плазмі крові не збільшувалася пропорційно прийнятій всередину дозі кларитроміцину, у той час як Т1/2 як кларитроміцину, так і його гідроксильованого метаболіту мав тенденцію до подовження з підвищенням дози. Така нелінійна фармакокінетика кларитроміцину у поєднанні зі зменшенням утворення 14-гідроксильованих та N-деметилованих продуктів при високих дозах вказує на нелінійний метаболізм кларитроміцину, який стає більш вираженим при високих дозах. Нирками виводиться приблизно 40% прийнятої дози кларитроміцину. Через кишечник виводиться приблизно 30%. Пацієнти Кларитроміцин та його метаболіт (14-ОН-кларитроміцин) швидко проникають у тканини та рідини організму. Є обмежені дані, що свідчать про те, що концентрація кларитроміцину в цереброспінальній рідині при внутрішньому прийомі незначна (тобто тільки 1-2% від концентрації в сироватці крові при нормальній проникності гематоенцефалічного бар'єру). Концентрація в тканинах зазвичай у кілька разів вища, ніж у сироватці крові. Порушення функції печінки У пацієнтів із середнім та тяжким ступенем порушення функції печінки, але із збереженою функцією нирок корекція дози кларитроміцину не потрібна. Рівноважна концентрація у плазмі крові та системний кліренс кларитроміцину не відрізняються у пацієнтів цієї групи та здорових пацієнтів. Рівноважна концентрація 14-ОН-кларитроміцину у пацієнтів з порушенням функції печінки нижча, ніж у здорових добровольців. Порушення функції нирок При порушенні функції нирок збільшуються Сmах та мінімальна концентрація (Cmin) кларитроміцину в плазмі крові, Т1/2, площа під кривою "концентрація-час" (AUC) кларитроміцину та його метаболіту (14-ОН-кларитроміцину). Константа елімінації та виведення нирками зменшуються. Ступінь змін цих параметрів залежить від рівня порушення функції нирок. Пацієнти похилого віку У пацієнтів похилого віку концентрація кларитроміцину та його метаболіту (14-ОН-кларитроміцину) у плазмі крові була вищою, а виведення повільніше, ніж у групи молодих людей. Однак після корекції з урахуванням ниркового кліренсу креатиніну (КК) не було відмінностей у обох групах. Таким чином, основний вплив на фармакокінетичні параметри кларитроміцину має функція нирок, а не вік.ФармакодинамікаКларитроміцин є напівсинтетичним антибіотиком групи макролідів і має антибактеріальну дію, взаємодіючи з 50S рибосомальною субодиницею і пригнічуючи синтез білка бактерій, чутливих до нього. Кларитроміцин продемонстрував високу активність в умовах in vitro щодо стандартних лабораторних штамів бактерій, так і виділених у пацієнтів під час клінічної практики. Виявляє високу активність щодо багатьох аеробних та анаеробних грампозитивних та грамнегативних мікроорганізмів. Мінімальні переважні концентрації (МПК) кларитроміцину для більшості збудників менше, ніж МПК еритроміцину в середньому на одне log2 розведення. Кларитроміцин в умовах in vitro є високоактивним щодо Legionella pneumophila, Mycoplasma pneumoniae. Чинить бактерицидну дію щодо Helicobacter pylori, дана активність кларитроміцину вище при нейтральному значенні pH, ніж при кислому. Крім того, дані, отримані в умовах in vitro та in vivo, вказують на те, що кларитроміцин діє на клінічно значущі види мікобактерій. Enterobacteriaceae і Pseudomonas spp., так само як і інші грамнегативні бактерії, що не ферментують лактозу, не чутливі до кларитроміцину. Активність кларитроміцину щодо більшості штамів, наведених нижче мікроорганізмів, доведена як в умовах in vitro, так і в клінічній практиці при захворюваннях, перелічених у розділі "Показання до застосування". Аеробні грампозитивні мікроорганізми: Staphylococcus aureus, Streptococcus pneumoniae, Streptococcus pyogenes, Listeria monocytogenes. Аеробні грамнегативні мікроорганізми: Haemophilus influenzae, Haemophilus parainfluenzae, Moraxella catarrhalis, Neisseria gonorrhoeae, Legionella pneumophila. Інші мікроорганізми: Mycoplasma pneumoniae, Chlamydia pneumoniae (TWAR). Мікобактерії: Mycobacterium leprae, Mycobacterium kansasii, Mycobacterium chelonae, Mycobacterium fortuitum, Mycobacterium avium complex (MAC) – комплекс, що включає: Mycobacterium avium, Mycobacterium intracellulare. Продукція бета-лактамази не впливає на активність кларитроміцину. Більшість штамів стафілококів, резистентних до метициліну та оксациліну, мають стійкість і до кларитроміцину. Helicobacter pylori Чутливість Helicobacter pylori до кларитроміцину вивчалася на ізолятах Helicobacter pylori, виділених від 104 пацієнтів на початок терапії кларитромицином. У 4 пацієнтів були виділені резистентні до кларитроміцину штами Helicobacter pylori, у 2 пацієнтів – штами з помірною резистентністю, у решти – 98 пацієнтів ізоляти Helicobacter pylori були чутливі до кларитроміцину. Кларитроміцин діє в умовах in vitro і щодо більшості штамів наступних мікроорганізмів (проте безпека та ефективність застосування кларитроміцину в клінічній практиці не підтверджена клінічними дослідженнями, і практичне значення залишається незрозумілим): Аеробні грампозитивні мікроорганізми: Streptococcus agalactiae, Streptococci (групи С, F, G), Viridans group streptococci. Аеробні грамнегативні мікроорганізми: Bordetella pertussis, Pasteurella multocida. Анаеробні грампозитивні мікроорганізми: Clostridium perfringens, Peptococcus niger, Propionibacterium acnes. Анаеробні грамнегативні мікроорганізми: Bacteroides melaninogenicus. Спірохети: Borrelia burgdorferi, Treponema pallidum. Кампілобактерії: Campilobacter jejuni. Основним метаболітом кларитроміцину в організмі людини є мікробіологічно активний метаболіт 14-гідроксикларитроміцин (14-ОН-кларитроміцин). Мікробіологічна активність метаболіту така ж, як у вихідної речовини, або вдвічі слабша щодо більшості мікроорганізмів. Виняток становить Haemophilus influenzae, щодо якої ефективність метаболіту вдвічі вища. Вихідне з'єднання та його основний метаболіт мають або адитивний, або синергічний ефект щодо Haemophilus influenzae в умовах in vitro та in vivo залежно від штаму бактерій. Тест визначення чутливості Кількісні методи, що вимагають вимірювання діаметра зони придушення росту, дають найбільш точні оцінки чутливості бактерій до антимікробних препаратів. Одна з рекомендованих методик визначення чутливості використовує диски, імпрегновані 15 мкг кларитроміцину (диско-дифузійний метод Кірбі-Бауера); при інтерпретації тесту діаметри зон пригнічення зростання корелюють зі значеннями МПК кларитроміцину. Значення МПК визначаються методом розведення у бульйоні чи агарі. При використанні цих методик звіт з лабораторії про те, що штам є "чутливим", свідчить про те, що збудник інфекції, ймовірно, відповість на лікування. Відповідь "резистентна" вказує на те, що збудник, можливо, не відповість на лікування. Відповідь "проміжна чутливість" передбачає, що терапевтичний ефект препарату може бути неоднозначним або мікроорганізм може виявитися чутливим при застосуванні більш високих доз препарату (проміжна чутливість також називається "помірною чутливістю").Показання до застосуванняІнфекційно-запальні захворювання, спричинені чутливими до кларитроміцину мікроорганізмами: інфекції нижніх дихальних шляхів (такі як бронхіт, пневмонія); інфекції верхніх дихальних шляхів та ЛОР-органів (тонзиліт, фарингіт, синусит, гострий середній отит); інфекції шкіри та м'яких тканин (такі як фолікуліт, запалення підшкірної клітковини, пика).Протипоказання до застосуванняГіперчутливість до кларитроміцину, макролідів та інших компонентів препарату. Одночасний прийом кларитроміцину з наступними препаратами: астемізол, цизаприд, домперидон, пімозід, терфенадин. Одночасний прийом кларитроміцину з алкалоїдами ріжків, наприклад, ерготамін, дигідроерготамін. Одночасний прийом кларитроміцину з мідазоламом для внутрішнього прийому. Одночасний прийом кларитроміцину з інгібіторами ГМГ-КоА-редуктази (статинами), які значною мірою метаболізуються ізоферментом CYP3A4 (ловастатин, симвастатин) у зв'язку з підвищенням ризику міопатії, включаючи рабдоміоліз. Одночасний прийом кларитроміцину з колхіцином. Одночасний прийом кларитроміцину з тикагрелором або ранолазином. Подовження інтервалу QT на електрокардіограмі (ЕКГ) (вроджене або набуте документально підтверджене подовження інтервалу QT) в анамнезі, шлуночкова аритмія, включаючи шлуночкову тахікардію або шлуночкову тахікардію типу "пірует" в анамнезі. Гіпокаліємія (ризик подовження інтервалу QT на ЕКГ). Печінкова недостатність тяжкого ступеня, що протікає одночасно з нирковою недостатністю. Холестатична жовтяниця/гепатит в анамнезі, що розвинулися при застосуванні кларитроміцину. Порфирія. Період грудного вигодовування. Вік до 18 років (за показаннями: тонзиліт, гострий середній отит), до 12 років (за іншими показаннями). Непереносимість лактози, дефіцит лактази, синдром глюкозо-галактозної мальабсорбції. З обережністю: Ниркова недостатність середнього та тяжкого ступеня тяжкості. Печінкова недостатність середнього та тяжкого ступеня тяжкості. Одночасний прийом кларитроміцину з бензодіазепінами, такими як алпразол, триазол, мідазол для внутрішньовенного застосування або для нанесення на слизову оболонку порожнини рота. Одночасний прийом з препаратами, що метаболізуються ізоферментом CYP3A, наприклад, карбамазепін, цилостазол, циклоспорин, дизопірамід, ібрутиніб, метилпреднізолон, омепразол, непрямі антикоагулянти (наприклад, варфарин), хінідин, ріфабутін, силден. Одночасний прийом з препаратами, що індукують ізофермент CYP3A4, наприклад, рифампіцин, фенітоїн, карбамазепін, фенобарбітал, препарати Звіробою продірявленого. Одночасний прийом із блокаторами "повільних" кальцієвих каналів (БМКК), які метаболізуються ізоферментом CYP3A4 (наприклад, верапаміл, амлодипін, дилтіазем). Одночасний прийом зі статинами, які не залежать від метаболізму ізоферменту CYP3A (наприклад, флувастатин). Пацієнти з ішемічною хворобою серця (ІБО), тяжкою серцевою недостатністю, гіпомагніємією, порушенням провідності або клінічно значущою брадикардією, а також пацієнти, які одночасно приймають антиаритмічні препарати IA класу (хінідин, прокаїнамід) та III класу (дофетилід, аміодарон, соталол). Вагітність.Вагітність та лактаціяБезпека застосування кларитроміцину при вагітності та в період грудного вигодовування не встановлена. Застосування кларитроміцину при вагітності (особливо в І триместрі) можливе лише у випадку, коли відсутня альтернативна терапія, а потенційна користь для матері перевищує потенційний ризик для плода. Кларитроміцин виводиться із грудним молоком. При необхідності прийому в період грудного вигодовування годування груддю слід припинити.Побічна діяКласифікація частоти розвитку побічних ефектів (кількість зареєстрованих випадків/кількість пацієнтів), рекомендована Всесвітньою організацією охорони здоров'я (ВООЗ): дуже часто ≥1/10; часто від ≥ 1/100 до Алергічні реакції: часто - шкірний висип; нечасто - анафілактоїдна реакція1, гіперчутливість, бульозний дерматит1, свербіж шкіри. кропив'янка, макулопапульозний висип3; частота невідома - анафілактична реакція, ангіоневротичний набряк, серйозні шкірні небажані реакції (наприклад, гострий генералізований екзантематозний пустульоз), синдром Стівенса-Джонсона, токсичний епідермальний некроліз, лікарський висип з еозинофілією та системною симптоматикою. З боку нервової системи: часто – головний біль, безсоння; нечасто - непритомність1, дискінезія1, запаморочення, сонливість, тремор, занепокоєння, підвищена збудливість3; частота невідома - судоми, психотичні розлади, сплутаність свідомості, деперсоналізація, депресія, дезорієнтація, галюцинації, порушення сновидінь ("жахливі" сновидіння), парестезія, манія. З боку шкірних покривів: часто – підвищене потовиділення; частота невідома – акне. З боку сечостатевої системи: частота невідома – ниркова недостатність, інтерстиціальний нефрит. З боку обміну речовин: нечасто – анорексія, зниження апетиту. З боку опорно-рухового апарату: нечасто – м'язовий спазм3, кістково-м'язова скутість1, міалгія2; частота невідома – рабдоміоліз2*, міопатія. З боку травної системи: часто – діарея, блювання, диспепсія, нудота, біль у ділянці живота; нечасто - езофагіт1, гастроезофагеальна рефлюксна хвороба2, гастрит, прокталгія2, стоматит, глосит, здуття живота4, запор, сухість слизової оболонки порожнини рота, відрижка, метеоризм, холестаз4, гепатит, цел; частота невідома – гострий панкреатит, зміна кольору язика та зубів, печінкова недостатність, холестатична жовтяниця. З боку дихальної системи: нечасто – бронхіальна астма1, носова кровотеча2, тромбоемболія легеневої артерії1. З боку органів чуття: часто – дисгевзія; нечасто - вертиго, порушення слуху, дзвін у вухах; частота невідома – глухота, агевзія (втрата смакових відчуттів), паросмія, аносмія. З боку серцево-судинної системи: часто – вазодилатація1; нечасто – зупинка серця1, фібриляція передсердь1, подовження інтервалу QT на ЕКГ, екстрасистолія1, відчуття серцебиття; частота невідома – шлуночкова тахікардія, у тому числі типу “пірует”, фібриляція шлуночків, кровотеча. Лабораторні показники: часто – відхилення лабораторних показників функції печінки; нечасто - підвищення сироваткової концентрації креатиніну1, підвищення сироваткової концентрації сечовини1, зміна співвідношення альбумін/глобулін1, лейкопенія, нейтропенія4, еозинофілія4, тромбоцитемія3, підвищення активності аланінамінотрансферази (АЛТ), аспартатаміфтранс )4, лактатдегідрогенази (ЛДГ)4 у плазмі крові; частота невідома – агранулоцитоз, тромбоцитопенія, збільшення значення міжнародного нормалізованого відношення (МНО), подовження протромбінового часу, зміна кольору сечі, підвищення концентрації білірубіну у плазмі крові. Інші: дуже часто – флебіт у місці ін'єкції1; часто - біль у місці ін'єкції1, запалення у місці ін'єкції1; нечасто - нездужання4, гіпертермія3, астенія, біль у грудній клітці4, озноб4, підвищена стомлюваність4. Інфекційні та паразитарні захворювання: нечасто – целюліт1, кандидоз, гастроентерит2, вторинні інфекції3 (у тому числі вагінальні); частота невідома - псевдомембранозний коліт, пика. Діти Передбачається, що частота, тип та тяжкість небажаних реакцій у дітей така сама, як у дорослих. Пацієнти зі зниженим імунітетом У пацієнтів із синдромом набутого імунодефіциту (СНІД) та іншими імунодефіцитами, які отримують кларитроміцин у більш високих дозах протягом тривалого часу для лікування мікобактеріальних інфекцій, часто важко відрізнити небажані ефекти препарату від симптомів ВІЛ-інфекції або супутнього захворювання. Найчастішими небажаними явищами у пацієнтів, які приймали добову дозу кларитроміцину, що дорівнює 1000 мг, були: нудота, блювання, дисгевзія, біль у ділянці живота, діарея, шкірний висип, метеоризм, головний біль, запор, порушення слуху, підвищення активності ACT та АЛ плазмі крові. Також відзначалися випадки небажаних явищ із низькою частотою виникнення, такі як задишка, безсоння та сухість слизової оболонки порожнини рота. У пацієнтів із зниженим імунітетом проводили оцінку лабораторних показників, аналізуючи їх значні відхилення від норми (різке підвищення чи зниження). На підставі даного критерію у 2-3% пацієнтів, які отримували кларитроміцин у дозі 1000 мг щодня, було зареєстровано значне підвищення активності ACT та АЛТ у плазмі, а також зниження кількості лейкоцитів та тромбоцитів. У невеликої кількості пацієнтів було зареєстровано підвищення сироваткової концентрації залишкового азоту сечовини. * У деяких повідомленнях про рабдоміоліз кларитроміцин приймався одночасно з іншими лікарськими засобами, з прийомом яких, як відомо, пов'язаний розвиток рабдоміолізу (статини, фібрати, колхіцин або алопуринол). 1 Повідомлення про дані побічних реакцій були отримані під час клінічних досліджень, а також післяреєстраційного застосування кларитроміцину у лікарській формі ліофілізат для приготування розчину для інфузій. 2 Повідомлення про дані побічних реакцій були отримані під час клінічних досліджень, а також післяреєстраційного застосування кларитроміцину у лікарській формі таблетки з пролонгованим вивільненням, покриті плівковою оболонкою. 3 Повідомлення про дані побічних реакцій були отримані під час клінічних досліджень, а також післяреєстраційного застосування кларитроміцину у лікарській формі порошок для приготування суспензії для прийому внутрішньо. 4 Повідомлення про дані побічних реакцій були отримані під час клінічних досліджень, а також післяреєстраційного застосування кларитроміцину у лікарській формі таблетки, покриті плівковою оболонкою.Взаємодія з лікарськими засобамиЗастосування наступних лікарських засобів одночасно з кларитроміцином протипоказане у зв'язку з можливістю розвитку серйозних побічних ефектів. Цизаприд, домперидон, пімозід, терфенадип та астемізол При одночасному прийомі кларитроміцину з цизапридом, пимозидом, домперидоном, терфенадином або астемізолом повідомлялося про підвищення концентрації останніх у плазмі крові, що може призвести до подовження інтервалу QT на ЕКГ та появі серцевих аритмій, включаючи шлуночкову тахікардію (в тому числі шлуночкову тахікардію). ) та фібриляцію шлуночків. Алкалоїди ріжків Післяреєстраційні дослідження показують, що при одночасному застосуванні кларитроміцину з ерготаміном або дигідроерготаміном можливі наступні ефекти, пов'язані з гострим отруєнням препаратами групи ерготамінів: судинний спазм, ішемія кінцівок та інших тканин, включаючи центральну нервову систему (ЦНС). Одночасне застосування кларитроміцину та алкалоїдів ріжків протипоказане. Інгібітори ГМГ-КоА-редуктази (статини) Одночасний прийом кларитроміцину з ловастатином або симвастатином протипоказаний у зв'язку з тим, що дані статини значною мірою метаболізуються ізоферментом CYP3A4, і одночасне застосування з кларитроміцином підвищує їх сироваткові концентрації, що призводить до підвищення ризику розвитку міопатії, включаючи рабдомі. Повідомлялося про випадки рабдоміолізу у пацієнтів, які приймали кларитроміцин одночасно з цими препаратами. У разі необхідності застосування кларитроміцину слід припинити прийом ловастатину або симвастатину на час терапії. Кларитроміцин слід застосовувати з обережністю у разі комбінованої терапії з іншими статинами. Рекомендується застосовувати статини, метаболізм яких не залежить від ізоферменту CYP3A (наприклад, флувастатин). У разі потреби одночасного прийому рекомендується приймати найменшу дозу статину. Слід контролювати розвиток ознак та симптомів міопатії. Мідазолам для прийому внутрішньо При одночасному застосуванні внутрішньо мідазоламу та кларитроміцину у лікарській формі таблетки (500 мг 2 рази на добу) відзначалося збільшення AUC мідазоламу у 7 разів. Одночасне застосування кларитроміцину та мідазоламу для прийому внутрішньо протипоказане. Вплив інших лікарських засобів на кларитроміцин Лікарські препарати, що є індукторами ізоферменту CYP3A (наприклад, рифампіцин, фенітоїн, карбамазепін, фенобарбітал, препарати Звіробою продірявленого) можуть індукувати метаболізм кларитроміцину. Це може призвести до субтерапевтичної концентрації кларитроміцину та відповідно до зниження його ефективності. Крім того, необхідно спостерігати за концентрацією індуктора ізоферменту CYP3A у плазмі крові, яка може підвищитися через інгібування ізоферменту CYP3A кларитроміцином. При одночасному застосуванні рифабутину та кларитроміцину спостерігалося підвищення концентрації рифабутину та зниження концентрації кларитроміцину в плазмі крові з підвищеним ризиком розвитку увеїту. Наступні препарати мають доведений або передбачуваний вплив на концентрацію кларитроміцину в плазмі крові, у разі їх одночасного застосування з кларитроміцином може знадобитися корекція дози або перехід на альтернативне лікування Ефавіренз, невірапін, рифампіцин, рифабутин та рифапентин Потужні індуктори системи цитохрому Р450, такі як ефавіренз, невірапін, рифампіцин, рифабутин і рифапентин можуть прискорювати метаболізм кларитроміцину і, таким чином, знижувати концентрацію кларитроміцину в плазмі крові, а також послаблювати терапевтичний ефект. ВІН-кларитроміцину - метаболіту, що також є мікробіологічно активним. Оскільки мікробіологічна активність кларитроміцину та 14-ОН-кларитроміцину відрізняється щодо різних бактерій, терапевтичний ефект може знижуватися при одночасному застосуванні кларитроміцину та індукторів системи цитохрому Р450. Етравірін Концентрація кларитроміцину в плазмі знижується при одночасному застосуванні з етравірином, а концентрація активного метаболіту 14-ОН-кларитроміцину в плазмі крові підвищується. Оскільки 14-ОН-кларитроміцин має низьку активність по відношенню до інфекцій MAC, може змінюватися загальна активність щодо цих збудників, тому для лікування MAC слід розглядати альтернативне лікування. Флуконазол Одночасний прийом флуконазолу в дозі 200 мг щоденно та кларитроміцину в дозі 500 мг 2 рази на добу у 21 здорового добровольця призвело до збільшення середнього значення мінімальної рівноважної концентрації кларитроміцину та AUC на 33% та 18% відповідно. При цьому одночасний прийом значно не впливав на середню рівноважну концентрацію активного метаболіту 14-ОН-кларитроміцину. Корекція дози кларитроміцину у разі одночасного прийому флуконазолу не потрібна. Рітонавір Фармакокінетичне дослідження показало, що одночасний прийом ритонавіру в дозі 200 мг кожні 8 годин та кларитроміцину в дозі 500 мг кожні 12 годин призвів до помітного пригнічення метаболізму кларитроміцину. При одночасному прийомі ритонавіру Сmах кларитроміцину в плазмі збільшилася на 31%, Cmin збільшилася на 182% і AUC збільшилася на 77%. Було відзначено практично повне придушення утворення 14-ОН-кларитроміцину. Завдяки широкому терапевтичному діапазону кларитроміцину зменшення його дози у пацієнтів із нормальною нирковою функцією не потрібне. У пацієнтів з нирковою недостатністю доцільно розглянути такі варіанти корекції дози: при КК 30-60 мл/хв. доза кларитроміцину повинна бути зменшена на 50%. У пацієнтів з нирковою недостатністю доцільно розглянути наступні варіанти корекції дози: при КК 30-60 мл/хв доза кларитроміцину повинна бути зменшена на 50%, при КК менше 30 мл/хв доза кларитроміцину повинна бути зменшена на 75%. Ритонавір не слід одночасно приймати з кларитроміцином у дозах, що перевищують 1 г на добу. Подібні корекції доз повинні розглядатися у пацієнтів зі зниженою функцією нирок, якщо ритонавір застосовується як фармакокінетичний "підсилювач" при застосуванні інших інгібіторів протеази ВІЛ, включаючи атазанавір та саквінавір. Дія кларитроміцину на інші лікарські препарати Антиаритмічні засоби (хінідин та дизопірамід) Можливе виникнення шлуночкової тахікардії типу "пірует" при одночасному застосуванні кларитроміцину та хінідину або дизопіраміду. При одночасному прийомі кларитроміцину з цими препаратами слід регулярно проводити контроль ЕКГ щодо подовження інтервалу QT, а також слід контролювати сироваткові концентрації цих препаратів. У післяреєстраційному періоді повідомлялося про випадки розвитку гіпоглікемії при одночасному прийомі кларитроміцину та дизопіраміду. Необхідно контролювати концентрацію глюкози в крові при одночасному застосуванні кларитроміцину та дизопіраміду. Гіпоглікемічні засоби для внутрішнього застосування/інсулін При одночасному застосуванні кларитроміцину та гіпоглікемічних засобів для прийому внутрішньо (наприклад, похідні сульфонілсечовини) та/або інсуліну може спостерігатися виражена гіпоглікемія. Одночасне застосування кларитроміцину з деякими гіпоглікемічними препаратами (наприклад, натеглінід, піоглітазон, репаглінід та росиглітазон) може призвести до інгібування ізоферменту CYP3A кларитроміцином, внаслідок чого може розвинутись гіпоглікемія. Рекомендується ретельний контроль концентрації глюкози у крові. Взаємодія зумовлена ізоферментом CYP3A Одночасний прийом кларитроміцину, який, як відомо, інгібує ізофермент CYP3A, та препаратів, що первинно метаболізуються ізоферментом CYP3A, може асоціюватися із взаємним підвищенням їх концентрацій, що може посилити або продовжити як терапевтичні, так і побічні ефекти. Кларитроміцин слід обережно застосовувати пацієнтам, які отримують препарати, які є субстратами ізоферменту CYP3A, особливо якщо ці препарати мають вузький терапевтичний діапазон (наприклад, карбамазепін) та/або препарати, які інтенсивно метаболізуються цим ізоферментом. У разі потреби повинна проводитися корекція дози препарату, який приймається одночасно з кларитроміцином; також по можливості повинен проводитися моніторинг сироваткових концентрацій препаратів, що первинно метаболізуються ізоферментом CYP3A. Метаболізм наступних препаратів/класів здійснюється тим же ізоферментом CYP3A, що і метаболізм кларитроміцину (але цей список не є вичерпним): алпразолам, карбамазепін, цилостазол, циклоспорин, дизопірамід, ібрутиніб, метилпреднізолон, мідазолам наприклад, варфарин), атипові антипсихотичні засоби (наприклад, кветіапін), хінідин, рифабутин, силденафіл, сиролімус, такролімус, тріазолам та вінбластин. До препаратів, що взаємодіють подібним чином через інші ізоферменти в рамках системи цитохрому Р450, відносяться: фенітоїн, теофілін та вальпроєва кислота. Непрямі антикоагулянти При одночасному прийомі варфарину та кларитроміцину можлива кровотеча, виражене збільшення МНО та подовження протромбінового часу. У разі одночасного застосування з варфарином або іншими непрямими антикоагулянтами необхідно контролювати МНО та протромбіновий час. Омепразол Кларитроміцин (по 500 мг кожні 8 годин) досліджувався у здорових дорослих добровольців у поєднанні з омепразолом (по 40 мг щодня). При одночасному застосуванні кларитроміцину та омепразолу рівноважні плазмові концентрації омепразолу були збільшені (Сmах, AUC0-24 та Т1/2 збільшилися на 30%, 89% та 34% відповідно). Середнє значення pH шлунка протягом 24 годин склало 5,2 (при прийомі омепразолу окремо) та 5,7 (при прийомі омепразолу одночасно з кларитроміцином). Силденафіл, тадалафіл та варденафіл Кожен із цих інгібіторів фосфодіестерази метаболізується принаймні частково за участю ізоферменту CYP3A. У той же час, ізофермент CYP3A може інгібуватися в присутності кларитроміцину. Одночасне застосування кларитроміцину з силденафілом, тадалафілом або варденафілом може призвести до збільшення інгібуючої дії на фосфодіестеразу. При застосуванні цих препаратів одночасно з кларитроміцином слід розглянути можливість зменшення дози силденафілу, тадалафілу та варденафілу. Теофілін, карбамазепін При одночасному застосуванні кларитроміцину та теофіліну або карбамазепіну можливе підвищення концентрації даних препаратів у системному кровотоку. Толтеродін Первинний метаболізм толтеродину здійснюється через ізофермент CYP2D6. Однак у частині популяції, позбавленої CYP2D6, метаболізм відбувається через ізофермент CYP3A. У цій групі населення пригнічення ізоферменту CYP3A призводить до значно більших концентрацій толтеродину в сироватці крові. У популяції з низьким рівнем метаболізму через ізофермент CYP2D6 може знадобитися зниження дози толтеродину при одночасному застосуванні інгібіторів ізоферменту CYP3A, таких як кларитроміцин. Бензодіазепіни (наприклад, алпразолам, мідазолам, тріазолам) При одночасному застосуванні мідазоламу та таблеток кларитроміцину (500 мг 2 рази на добу) відзначалося збільшення AUC мідазоламу у 2,7 раза після внутрішньовенного введення мідазоламу. Якщо одночасно з кларитроміцином застосовується мідазолам у лікарській формі розчин для внутрішньовенного введення, слід ретельно контролювати стан пацієнта для можливої корекції дози мідазоламу. Введення лікарського препарату через слизову оболонку порожнини рота, що дає можливість обійти пресистемну елімінацію лікарського препарату, швидше за все, призведе до взаємодії, аналогічної тому, що спостерігається при внутрішньовенному введенні мідазоламу, а не прийому внутрішньо. Такі ж запобіжні заходи слід застосовувати і до інших бензодіазепінів, які метаболізуються ізоферментом CYP3A, включаючи триазолів та алпразолів. Для бензодіазепінів, виведення яких не залежить від ізоферменту CYP3A (темазепам, нітразепам, лоразепам), малоймовірно клінічно значуща взаємодія з кларитроміцином. При одночасному застосуванні кларитроміцину та триазоламу можлива дія на ЦНС, наприклад, сонливість та сплутаність свідомості. У зв'язку з цим, у разі одночасного застосування рекомендується стежити за симптомами порушення ЦНС. Взаємодії з іншими лікарськими засобами Колхіцін Колхіцин є субстратом як ізоферменту CYP3A, так і білка-переносника Р-глікопротеїну (Pgp). Відомо, що кларитроміцин та інші макроліди є інгібіторами ізоферменту CYP3A та Pgp. При одночасному застосуванні кларитроміцину та колхіцину інгібування Pgp та/або ізоферменту CYP3A може призвести до посилення дії колхіцину. Слід контролювати розвиток клінічних симптомів отруєння колхіцином. Зареєстровані постреєстраційні повідомлення про випадки отруєння колхіцином при його одночасному прийомі з кларитроміцином, частіше у пацієнтів похилого віку. Деякі з описаних випадків відбувалися у пацієнтів із нирковою недостатністю. Як повідомлялося, деякі випадки закінчувалися летальним кінцем. Одночасне застосування кларитроміцину та колхіцину протипоказане. Дігоксин Передбачається, що дигоксин є субстратом PGP. Відомо, що кларитроміцин пригнічує Pgp. При одночасному застосуванні кларитроміцину та дигоксину інгібування Pgp кларитроміцином може призвести до посилення дії дигоксину. Одночасний прийом дигоксину та кларитроміцину також може призвести до підвищення сироваткової концентрації дигоксину. У деяких пацієнтів спостерігалися клінічні симптоми отруєння дигоксином, включаючи потенційно летальні аритмії. При одночасному прийомі кларитроміцину та дигоксину слід ретельно контролювати концентрацію дигоксину у сироватці крові. Зідовудін Одночасний прийом таблеток кларитроміцину та зидовудину внутрішньо дорослими ВІЛ-інфікованими пацієнтами може призвести до зниження рівноважної концентрації зидовудину в плазмі крові. Оскільки кларитроміцин може перешкоджати всмоктуванню зидовудину при прийомі внутрішньо, взаємодії можна значно уникнути, приймаючи кларитроміцин і зидовудін з інтервалом в 4 години. Подібної взаємодії не спостерігали у ВІЛ-інфікованих дітей, які отримують дитячу суспензію кларитроміцину з зидовудином або дидезоксіїнозином. Оскільки кларитроміцин може перешкоджати всмоктуванню зидовудину при їх одночасному прийомі внутрішньо у дорослих пацієнтів, така взаємодія навряд чи можлива при застосуванні кларитроміцину внутрішньовенно. Фенітоїн та вальпроєва кислота Є дані про взаємодію інгібіторів ізоферменту CYP3A (включаючи кларитроміцин) з препаратами, які не метаболізуються за допомогою ізоферменту CYP3A (фенітоїн та вальпроєва кислота). Для цих препаратів при одночасному застосуванні з кларитроміцином рекомендується визначення їх сироваткових концентрацій, оскільки є повідомлення про їх підвищення. Двоспрямована взаємодія лікарських засобів Атазанавір Кларитроміцин та атазанавір є як субстратами, так і інгібіторами ізоферменту CYP3A. Існує свідчення двонаправленої взаємодії цих препаратів. Одночасне застосування кларитроміцину (500 мг 2 рази на добу) та атазанавіру (400 мг 1 раз на добу) може призвести до дворазового збільшення дії кларитроміцину та зменшення дії 14-ОН-кларитроміцину на 70% зі збільшенням AUC атазанавіру на 28%. Завдяки широкому терапевтичному діапазону кларитроміцину зменшення його дози у пацієнтів з нормальною нирковою функцією не потрібне. У пацієнтів з нирковою недостатністю середнього ступеня тяжкості (КК 30-60 мл/хв) доза кларитроміцину повинна бути зменшена на 50%. У пацієнтів з КК менше 30 мл/хв дозу кларитроміцину слід зменшити на 75%, застосовуючи для цього відповідну лікарську форму кларитроміцину. Кларитроміцин у дозах, що перевищують 1000 мг на добу, не можна застосовувати одночасно з інгібіторами протеаз. БМКК При одночасному застосуванні кларитроміцину та БМКК, які метаболізуються ізоферментом CYP3A4 (наприклад, верапаміл, амлодипін, дилтіазем), слід бути обережним, оскільки існує ризик виникнення артеріальної гіпотензії. При одночасному застосуванні можуть підвищуватися плазмові концентрації кларитроміцину та БМКК. Артеріальна гіпотензія, брадіаритмія та лактоацидоз можливі при одночасному прийомі кларитроміцину та верапамілу. Ітраконазол Кларитроміцин та ітраконазол є субстратами та інгібіторами ізоферменту CYP3A, що визначає двонаправлену взаємодію препаратів. Кларитроміцин може підвищити концентрацію ітраконазолу в плазмі, тоді як ітраконазол може підвищити плазмову концентрацію кларитроміцину. Пацієнтів, які одночасно приймають ітраконазол та кларитроміцин, слід ретельно обстежити на наявність симптомів посилення або збільшення тривалості фармакологічних ефектів цих препаратів. Саквінавір Кларитроміцин та саквінавір є субстратами та інгібіторами ізоферменту CYP3A, що визначає двоспрямовану взаємодію препаратів. Одночасне застосування кларитроміцину (500 мг 2 рази на добу) і саквінавіру (в м'яких желатинових капсулах, 1200мг 3 рази на добу) у 12 здорових добровольців викликало збільшення AUC і Смах саквінавіру в плазмі крові на 177% і 187% відповідно. окремо. Значення AUC та Сmах кларитроміцину були приблизно на 40% вищі, ніж при терапії одним кларитроміцином. При одночасному застосуванні цих двох препаратів протягом обмеженого часу у дозах/складах, зазначених вище, корекція дози не потрібна. Результати дослідження лікарських взаємодій із застосуванням саквінавіру у м'яких желатинових капсулах можуть не відповідати ефектам, що спостерігаються при застосуванні саквінавіру у твердих желатинових капсулах. Результати дослідження лікарських взаємодій при терапії саквінавіром окремо можуть не відповідати ефектам, що спостерігаються при терапії комбінацією саквінавір/ритонавір. При прийомі саквінавіру одночасно з ритонавіром слід враховувати потенційний вплив ритонавіру на кларитроміцин.Спосіб застосування та дозиВсередину. Таблетку слід ковтати повністю, не розламувати і не розжовувати. Дорослим та дітям старше 12 років – по 1 таблетці (500 мг) 1 раз на добу під час їжі. При тонзиліті та гострому середньому отиті: дорослим та дітям старше 18 років – по 1 таблетці (500 мг) 1 раз на добу під час їжі. При тяжких інфекціях дозу збільшують до 2 таблеток (1000 мг) 1 раз на добу під час їжі. Звичайна тривалість лікування від 5 до 14 днів. Виняток становлять позалікарняна пневмонія та синусит, які вимагають лікування від 6 до 14 днів. Порушення функції нирок Для пацієнтів з нирковою недостатністю важкого ступеня (КК менше 30 мл/хв) звичайна рекомендована доза становить 250 мг 1 раз на добу, у цьому випадку можливе застосування препарату Фромілід®, таблетки, вкриті плівковою оболонкою, 250 мг. При більш тяжких інфекціях рекомендована доза становить 1 таблетка 500 мг із пролонгованим вивільненням кларитроміцину. У пацієнтів з нирковою недостатністю середнього ступеня тяжкості (КК від 30 до 60 мл/хв) корекція дози не потрібна.ПередозуванняСимптоми: прийом внутрішньо великої дози кларитроміцину може викликати симптоми порушень з боку шлунково-кишкового тракту. У одного пацієнта з біполярним розладом в анамнезі після прийому 8 г кларитроміцину описані зміни психічного стану, параноїдальна поведінка, гіпокаліємія та гіпоксемія. Лікування: при передозуванні слід видалити неабсорбований препарат із шлунково-кишкового тракту (промивання шлунка, прийом активованого вугілля та ін.) та провести симптоматичну терапію. Гемодіаліз та перитонеальний діаліз не мають істотного впливу на концентрацію кларитроміцину в сироватці крові, що характерно і для інших лікарських препаратів групи макролідів.Запобіжні заходи та особливі вказівкиТривалий прийом антибіотиків може призводити до утворення колоній зі збільшенням кількості нечутливих бактерій та грибів. При суперінфекції слід призначити відповідну терапію. Призначення кларитроміцину вагітним жінкам має проводитися при ретельній оцінці співвідношення ризику та користі, особливо протягом перших трьох місяців вагітності. При застосуванні кларитроміцину повідомлялося про порушення функції печінки (підвищення активності "печінкових" ферментів у плазмі крові, гепатоцелюлярний та/або холестатичний гепатит з жовтяницею або без). Порушення функції печінки може бути важким, але є оборотним. Є випадки печінкової недостатності з летальним результатом головним чином пов'язані з наявністю серйозних супутніх захворювань та/або одночасним застосуванням інших лікарських засобів. При появі ознак та симптомів гепатиту, таких як анорексія, жовтяниця, потемніння сечі, свербіж, болючість живота при пальпації, необхідно негайно припинити терапію кларитроміцином. За наявності хронічних захворювань печінки необхідно проводити регулярний контроль активності печінкових ферментів сироватки крові. При лікуванні практично всіма антибактеріальними засобами, у тому числі кларитроміцином, описані випадки псевдомембранозного коліту, тяжкість якого може змінюватись від легкого до загрозливого життя. При лікуванні практично всіма антибактеріальними препаратами, у тому числі кларитроміцином, описані випадки Clostridium difficile-асоційованої діареї, тяжкість якої може змінюватись від легкої діареї до загрозливого життя коліту. Антибактеріальні препарати можуть змінити нормальну мікрофлору кишечника, що може спричинити зростання Clostridium difficile. Псевдомембранозний коліт, викликаний Clostridium difficile, необхідно підозрювати у всіх пацієнтів, у яких після застосування антибактеріальних засобів розвинулася діарея. Після проведення курсу антибіотикотерапії потрібне ретельне медичне спостереження за пацієнтом.Описувалися випадки розвитку псевдомембранозного коліту через 2 місяці після прийому антибіотиків. При лікуванні макролідами, включаючи кларитроміцин, спостерігалося подовження серцевої реполяризації та інтервалу QT, збільшуючи ризик розвитку серцевої аритмії та шлуночкової тахікардії типу “пірует”. Оскільки такі ситуації можуть призвести до збільшення ризику розвитку шлуночкових аритмій (у тому числі шлуночкової тахікардії типу "пірует"), то: Кларитроміцин не повинен застосовуватися у таких категорій пацієнтів: у пацієнтів із гіпокаліємією; одночасне застосування кларитроміцину з астемізолом, цизапридом, домперидоном, пімозидом та терфенадином протипоказано; у пацієнтів із вродженим або набутим зареєстрованим подовженням інтервалу QT або наявністю шлуночкової аритмії в анамнезі. Кларитроміцин повинен застосовуватися з обережністю у таких категорій пацієнтів: у пацієнтів з ІХС, тяжкою серцевою недостатністю, порушеннями провідності або клінічно значущою брадикардією; у пацієнтів з електролітними порушеннями, такими як гіпомагніємія; у пацієнтів, які одночасно приймають інші лікарські препарати, пов'язані з подовженням інтервалу QT. У ході епідеміологічних досліджень з вивчення ризику несприятливих серцево-судинних наслідків при застосуванні макролідів було отримано неоднозначні результати. У деяких спостережних дослідженнях було встановлено рідкісний короткочасний ризик розвитку аритмії, інфаркту міокарда та смерті від серцево-судинних захворювань, пов'язаних із застосуванням макролідів, включаючи кларитроміцин. При призначенні кларитроміцину слід співвідносити передбачувану користь від прийому препарату з цими ризиками. Можливий розвиток перехресної резистентності до кларитроміцину та інших антибіотиків групи макролідів, а також лінкоміцину та кліндаміцину. Враховуючи зростаючу резистентність Streptococcus pneumoniae до макролідів, важливо проводити тестування чутливості при призначенні кларитроміцину пацієнтам із позалікарняною пневмонією. При шпитальній пневмонії кларитроміцин слід застосовувати у комбінації з відповідними антибіотиками. Інфекції шкіри та м'яких тканин легкого та середнього ступеня тяжкості найчастіше викликані Staphylococcus aureus та Streptococcus pyogenes. При цьому обидва збудники можуть бути стійкими до макролідів. Тому важливо проводити тест на чутливість. Макроліди можна застосовувати при інфекціях, викликаних Corynebacterium minutissimum, захворюваннях вугри вульгарні та пика, а також у тих ситуаціях, коли не можна застосовувати пеніцилін. У разі появи гострих реакцій гіперчутливості, таких як анафілактична реакція, серйозні шкірні небажані реакції (наприклад, гострий генералізований екзантематозний пустульоз), синдром Стівенса-Джонсона, токсичний епідермальний некроліз та лікарський висип з еозинофілією та Систем симптом прийом кларитроміцину та почати відповідну терапію. У разі одночасного застосування з варфарином або іншими непрямими антикоагулянтами необхідно контролювати МНО та протромбіновий час. Спеціальна інформація про допоміжні речовини Препарат Фромілід уно містить лактозу, тому протипоказаний при таких станах: непереносимість лактози, дефіцит лактази, синдром глюкозо-галактозної мальабсорбції. Вплив на здатність до керування автотранспортом та управління механізмами Дані щодо впливу кларитроміцину на здатність керувати транспортними засобами, механізмами відсутні. Слід бути обережними при керуванні транспортними засобами, механізмами, враховуючи потенційну можливість запаморочення, вертиго, сплутаності свідомості та дезорієнтації, які можуть виникнути при застосуванні даного препарату.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
303,00 грн
149,00 грн
Склад, форма випуску та упаковкаПігулки - 1 таб. Діюча речовина: кларитроміцин 500 мг; допоміжні речовини: натрію алгінат, натрію кальцію алгінат, лактози моногідрат, повідон К25, полісорбат-80, кремнію діоксид колоїдний, магнію стеарат, тальк; Оболонка плівкова: гіпромелоза, тальк, барвник заліза оксид жовтий (Е172), титану діоксид (Е171), пропіленгліколь По 5 або 7 таблеток поміщають у блістер із ПВХ/ПВДХ - алюмінієвої фольги (PVC/PVDC-Al). По 1 блістеру (блістер по 5 таблеток) або по 1 або 2 блістери (блістер по 7 таблеток) поміщають у картонну пачку разом з інструкцією по застосуванню.Опис лікарської формиОвальні, двоопуклі таблетки, покриті плівковою оболонкою коричнево-жовтого кольору, з маркуванням U на одній стороні. Вид на зламі: шорстка маса білого або майже білого кольору з плівковою оболонкою коричнево-жовтого кольору.Фармакотерапевтична групаАнтибіотик-макролід.ФармакокінетикаВсмоктування Препарат швидко всмоктується з шлунково-кишкового тракту. Абсолютна біодоступність становить близько 50%. При прийомі повторних доз кумуляції практично не виявлено, і характер метаболізму в організмі людини не змінювався. Розподіл, метаболізм та виведення In vitro Кларитроміцин зв'язується з білками плазми на 70% у концентрації від 0,45 до 4,5 мкг/мл. При концентрації 45 мкг/мл зв'язування знижується до 41%, ймовірно, через насичення місць зв'язування. Це спостерігається лише при концентраціях, що багаторазово перевищують терапевтичну концентрацію. Здорові добровольці У пацієнтів, які приймають 500 мг кларитроміцину 1 раз на добу після прийому їжі, максимальна концентрація (Сmах) кларитроміцину та 14-ОН-кларитроміцину в плазмі крові становила 1,3 мкг/мл та 0,48 мкг/мл відповідно. Період напіввиведення (Т1/2) кларитроміцину та Т1/2 його основного метаболіту склали 5,3 години та 7,7 годин відповідно. При прийомі разової дози кларитроміцину в лікарській формі таблетки з пролонгованим вивільненням, покриті плівковою оболонкою, 1000 мг (500 мг 2 рази на добу), Смах кларитроміцину та його гідроксильованого метаболіту в плазмі крові становила 2,4 мкг/мл/мл мл відповідно. Т1/2 кларитроміцину при прийомі в дозі 1000 мг становив 5,8 години, тоді як аналогічний показник для 14-ОН-кларитроміцину становив 8,9 години. Час досягнення максимальної концентрації (ТСmах) при прийомі внутрішньо як 500 мг, так і 1000 мг кларитроміцину становить приблизно 6 годин. Стах 14-ОН-кларитроміцину в плазмі крові не збільшувалася пропорційно прийнятій всередину дозі кларитроміцину, у той час як Т1/2 як кларитроміцину, так і його гідроксильованого метаболіту мав тенденцію до подовження з підвищенням дози. Така нелінійна фармакокінетика кларитроміцину у поєднанні зі зменшенням утворення 14-гідроксильованих та N-деметилованих продуктів при високих дозах вказує на нелінійний метаболізм кларитроміцину, який стає більш вираженим при високих дозах. Нирками виводиться приблизно 40% прийнятої дози кларитроміцину. Через кишечник виводиться приблизно 30%. Пацієнти Кларитроміцин та його метаболіт (14-ОН-кларитроміцин) швидко проникають у тканини та рідини організму. Є обмежені дані, що свідчать про те, що концентрація кларитроміцину в цереброспінальній рідині при внутрішньому прийомі незначна (т. Е. Тільки 1-2% від концентрації в сироватці крові при нормальній проникності гематоенцефалічного бар'єру). Концентрація в тканинах зазвичай у кілька разів вища, ніж у сироватці крові. Порушення функції печінки У пацієнтів із середнім та тяжким ступенем порушення функції печінки, але із збереженою функцією нирок корекція дози кларитроміцину не потрібна. Рівноважна концентрація у плазмі крові та системний кліренс кларитроміцину не відрізняються у пацієнтів цієї групи та здорових пацієнтів. Рівноважна концентрація 14-ОН-кларитроміцину у пацієнтів з порушенням функції печінки нижча, ніж у здорових добровольців. Порушення функції нирок При порушенні функції нирок збільшуються Сmах та мінімальна концентрація (Cmin) кларитроміцину в плазмі крові, Т1/2, площа під кривою "концентрація-час" (AUC) кларитроміцину та його метаболіту (14-ОН-кларитроміцину). Константа елімінації та виведення нирками зменшуються. Ступінь змін цих параметрів залежить від рівня порушення функції нирок. Пацієнти похилого віку У пацієнтів похилого віку концентрація кларитроміцину та його метаболіту (14-ОН-кларитроміцину) у плазмі крові була вищою, а виведення повільніше, ніж у групи молодих людей. Однак після корекції з урахуванням ниркового кліренсу креатиніну (КК) не було відмінностей у обох групах. Таким чином, основний вплив на фармакокінетичні параметри кларитроміцину має функція нирок, а не вік.ФармакодинамікаКларитроміцин є напівсинтетичним антибіотиком групи макролідів і має антибактеріальну дію, взаємодіючи з 50S рибосомальною субодиницею і пригнічуючи синтез білка бактерій, чутливих до нього. Кларитроміцин продемонстрував високу активність в умовах in vitro щодо стандартних лабораторних штамів бактерій, так і виділених у пацієнтів під час клінічної практики. Виявляє високу активність щодо багатьох аеробних та анаеробних грампозитивних та грамнегативних мікроорганізмів. Мінімальні переважні концентрації (МПК) кларитроміцину для більшості збудників менше, ніж МПК еритроміцину в середньому на одне log2 розведення. Кларитроміцин в умовах in vitro є високоактивним щодо Legionella pneumophila, Mycoplasma pneumoniae. Чинить бактерицидну дію щодо Helicobacter pylori, дана активність кларитроміцину вище при нейтральному значенні pH, ніж при кислому. Крім того, дані, отримані в умовах in vitro та in vivo, вказують на те, що кларитроміцин діє на клінічно значущі види мікобактерій. Enterobacteriaceae і Pseudomonas spp., так само як і інші грамнегативні бактерії, що не ферментують лактозу, не чутливі до кларитроміцину. Активність кларитроміцину щодо більшості штамів, наведених нижче мікроорганізмів, доведена як в умовах in vitro, так і в клінічній практиці при захворюваннях, перелічених у розділі "Показання до застосування". Аеробні грампозитивні мікроорганізми: Staphylococcus aureus, Streptococcus pneumoniae, Streptococcus pyogenes, Listeria monocytogenes. Аеробні грамнегативні мікроорганізми: Haemophilus influenzae, Haemophilus parainfluenzae, Moraxella catarrhalis, Neisseria gonorrhoeae, Legionella pneumophila. Інші мікроорганізми: Mycoplasma pneumoniae, Chlamydia pneumoniae (TWAR). Мікобактерії: Mycobacterium leprae, Mycobacterium kansasii, Mycobacterium chelonae, Mycobacterium fortuitum, Mycobacterium avium complex (MAC) – комплекс, що включає: Mycobacterium avium, Mycobacterium intracellulare. Продукція бета-лактамази не впливає на активність кларитроміцину. Більшість штамів стафілококів, резистентних до метициліну та оксациліну, мають стійкість і до кларитроміцину. Helicobacter pylori Чутливість Helicobacter pylori до кларитроміцину вивчалася на ізолятах Helicobacter pylori, виділених від 104 пацієнтів на початок терапії кларитромицином. У 4 пацієнтів були виділені резистентні до кларитроміцину штами Helicobacter pylori, у 2 пацієнтів – штами з помірною резистентністю, у решти – 98 пацієнтів ізоляти Helicobacter pylori були чутливі до кларитроміцину. Кларитроміцин діє в умовах in vitro і щодо більшості штамів наступних мікроорганізмів (проте безпека та ефективність застосування кларитроміцину в клінічній практиці не підтверджена клінічними дослідженнями, і практичне значення залишається незрозумілим): Аеробні грампозитивні мікроорганізми: Streptococcus agalactiae, Streptococci (групи С, F, G), Viridans group streptococci. Аеробні грамнегативні мікроорганізми: Bordetella pertussis, Pasteurella multocida. Анаеробні грампозитивні мікроорганізми: Clostridium perfringens, Peptococcus niger, Propionibacterium acnes. Анаеробні грамнегативні мікроорганізми: Bacteroides melaninogenicus. Спірохети: Borrelia burgdorferi, Treponema pallidum. Кампілобактерії: Campilobacter jejuni. Основним метаболітом кларитроміцину в організмі людини є мікробіологічно активний метаболіт 14-гідроксикларитроміцин (14-ОН-кларитроміцин). Мікробіологічна активність метаболіту така ж, як у вихідної речовини, або вдвічі слабша щодо більшості мікроорганізмів. Виняток становить Haemophilus influenzae, щодо якої ефективність метаболіту вдвічі вища. Вихідне з'єднання та його основний метаболіт мають або адитивний, або синергічний ефект щодо Haemophilus influenzae в умовах in vitro та in vivo залежно від штаму бактерій. Тест визначення чутливості Кількісні методи, що вимагають вимірювання діаметра зони придушення росту, дають найбільш точні оцінки чутливості бактерій до антимікробних препаратів. Одна з рекомендованих методик визначення чутливості використовує диски, імпрегновані 15 мкг кларитроміцину (диско-дифузійний метод Кірбі-Бауера); при інтерпретації тесту діаметри зон пригнічення зростання корелюють зі значеннями МПК кларитроміцину. Значення МПК визначаються методом розведення у бульйоні чи агарі. При використанні цих методик звіт з лабораторії про те, що штам є "чутливим", свідчить про те, що збудник інфекції, ймовірно, відповість на лікування. Відповідь "резистентна" вказує на те, що збудник, можливо, не відповість на лікування. Відповідь "проміжна чутливість" передбачає, що терапевтичний ефект препарату може бути неоднозначним або мікроорганізм може виявитися чутливим при застосуванні більш високих доз препарату (проміжна чутливість також називається "помірною чутливістю").Показання до застосуванняІнфекційно-запальні захворювання, спричинені чутливими до кларитроміцину мікроорганізмами: інфекції нижніх дихальних шляхів (такі як бронхіт, пневмонія); інфекції верхніх дихальних шляхів та ЛОР-органів (тонзиліт, фарингіт, синусит, гострий середній отит); інфекції шкіри та м'яких тканин (такі як фолікуліт, запалення підшкірної клітковини, пика).Протипоказання до застосуванняГіперчутливість до кларитроміцину, макролідів та інших компонентів препарату. Одночасний прийом кларитроміцину з наступними препаратами: астемізол, цизаприд, домперидон, пімозід, терфенадин. Одночасний прийом кларитроміцину з алкалоїдами ріжків, наприклад, ерготамін, дигідроерготамін. Одночасний прийом кларитроміцину з мідазоламом для внутрішнього прийому. Одночасний прийом кларитроміцину з інгібіторами ГМГ-КоА-редуктази (статинами), які значною мірою метаболізуються ізоферментом CYP3A4 (ловастатин, симвастатин) у зв'язку з підвищенням ризику міопатії, включаючи рабдоміоліз. Одночасний прийом кларитроміцину з колхіцином. Одночасний прийом кларитроміцину з тикагрелором або ранолазином. Подовження інтервалу QT на електрокардіограмі (ЕКГ) (вроджене або набуте документально підтверджене подовження інтервалу QT) в анамнезі, шлуночкова аритмія, включаючи шлуночкову тахікардію або шлуночкову тахікардію типу "пірует" в анамнезі. Гіпокаліємія (ризик подовження інтервалу QT на ЕКГ). Печінкова недостатність тяжкого ступеня, що протікає одночасно з нирковою недостатністю. Холестатична жовтяниця/гепатит в анамнезі, що розвинулися при застосуванні кларитроміцину. Порфирія. Період грудного вигодовування. Вік до 18 років (за показаннями: тонзиліт, гострий середній отит), до 12 років (за іншими показаннями). Непереносимість лактози, дефіцит лактази, синдром глюкозо-галактозної мальабсорбції. З обережністю: Ниркова недостатність середнього та тяжкого ступеня тяжкості. Печінкова недостатність середнього та тяжкого ступеня тяжкості. Одночасний прийом кларитроміцину з бензодіазепінами, такими як алпразол, триазол, мідазол для внутрішньовенного застосування або для нанесення на слизову оболонку порожнини рота. Одночасний прийом з препаратами, що метаболізуються ізоферментом CYP3A, наприклад, карбамазепін, цилостазол, циклоспорин, дизопірамід, ібрутиніб, метилпреднізолон, омепразол, непрямі антикоагулянти (наприклад, варфарин), хінідин, ріфабутін, силден. Одночасний прийом з препаратами, що індукують ізофермент CYP3A4, наприклад, рифампіцин, фенітоїн, карбамазепін, фенобарбітал, препарати Звіробою продірявленого. Одночасний прийом із блокаторами "повільних" кальцієвих каналів (БМКК), які метаболізуються ізоферментом CYP3A4 (наприклад, верапаміл, амлодипін, дилтіазем). Одночасний прийом зі статинами, які не залежать від метаболізму ізоферменту CYP3A (наприклад, флувастатин). Пацієнти з ішемічною хворобою серця (ІБО), тяжкою серцевою недостатністю, гіпомагніємією, порушенням провідності або клінічно значущою брадикардією, а також пацієнти, які одночасно приймають антиаритмічні препарати IA класу (хінідин, прокаїнамід) та III класу (дофетилід, аміодарон, соталол). Вагітність.Вагітність та лактаціяБезпека застосування кларитроміцину при вагітності та в період грудного вигодовування не встановлена. Застосування кларитроміцину при вагітності (особливо в І триместрі) можливе лише у випадку, коли відсутня альтернативна терапія, а потенційна користь для матері перевищує потенційний ризик для плода. Кларитроміцин виводиться із грудним молоком. При необхідності прийому в період грудного вигодовування годування груддю слід припинити.Побічна діяКласифікація частоти розвитку побічних ефектів (кількість зареєстрованих випадків/кількість пацієнтів), рекомендована Всесвітньою організацією охорони здоров'я (ВООЗ): дуже часто ≥1/10; часто від ≥ 1/100 до Алергічні реакції: часто - шкірний висип; нечасто - анафілактоїдна реакція1, гіперчутливість, бульозний дерматит1, свербіж шкіри. кропив'янка, макулопапульозний висип3; частота невідома - анафілактична реакція, ангіоневротичний набряк, серйозні шкірні небажані реакції (наприклад, гострий генералізований екзантематозний пустульоз), синдром Стівенса-Джонсона, токсичний епідермальний некроліз, лікарський висип з еозинофілією та системною симптоматикою. З боку нервової системи: часто – головний біль, безсоння; нечасто - непритомність1, дискінезія1, запаморочення, сонливість, тремор, занепокоєння, підвищена збудливість3; частота невідома - судоми, психотичні розлади, сплутаність свідомості, деперсоналізація, депресія, дезорієнтація, галюцинації, порушення сновидінь ("жахливі" сновидіння), парестезія, манія. З боку шкірних покривів: часто – підвищене потовиділення; частота невідома – акне. З боку сечостатевої системи: частота невідома – ниркова недостатність, інтерстиціальний нефрит. З боку обміну речовин: нечасто – анорексія, зниження апетиту. З боку опорно-рухового апарату: нечасто – м'язовий спазм3, кістково-м'язова скутість1, міалгія2; частота невідома – рабдоміоліз2*, міопатія. З боку травної системи: часто – діарея, блювання, диспепсія, нудота, біль у ділянці живота; нечасто - езофагіт1, гастроезофагеальна рефлюксна хвороба2, гастрит, прокталгія2, стоматит, глосит, здуття живота4, запор, сухість слизової оболонки порожнини рота, відрижка, метеоризм, холестаз4, гепатит, цел; частота невідома – гострий панкреатит, зміна кольору язика та зубів, печінкова недостатність, холестатична жовтяниця. З боку дихальної системи: нечасто – бронхіальна астма1, носова кровотеча2, тромбоемболія легеневої артерії1. З боку органів чуття: часто – дисгевзія; нечасто - вертиго, порушення слуху, дзвін у вухах; частота невідома – глухота, агевзія (втрата смакових відчуттів), паросмія, аносмія. З боку серцево-судинної системи: часто – вазодилатація1; нечасто – зупинка серця1, фібриляція передсердь1, подовження інтервалу QT на ЕКГ, екстрасистолія1, відчуття серцебиття; частота невідома – шлуночкова тахікардія, у тому числі типу “пірует”, фібриляція шлуночків, кровотеча. Лабораторні показники: часто – відхилення лабораторних показників функції печінки; нечасто - підвищення сироваткової концентрації креатиніну1, підвищення сироваткової концентрації сечовини1, зміна співвідношення альбумін/глобулін1, лейкопенія, нейтропенія4, еозинофілія4, тромбоцитемія3, підвищення активності аланінамінотрансферази (АЛТ), аспартатаміфтранс )4, лактатдегідрогенази (ЛДГ)4 у плазмі крові; частота невідома – агранулоцитоз, тромбоцитопенія, збільшення значення міжнародного нормалізованого відношення (МНО), подовження протромбінового часу, зміна кольору сечі, підвищення концентрації білірубіну у плазмі крові. Інші: дуже часто – флебіт у місці ін'єкції1; часто - біль у місці ін'єкції1, запалення у місці ін'єкції1; нечасто - нездужання4, гіпертермія3, астенія, біль у грудній клітці4, озноб4, підвищена стомлюваність4. Інфекційні та паразитарні захворювання: нечасто – целюліт1, кандидоз, гастроентерит2, вторинні інфекції3 (у тому числі вагінальні); частота невідома - псевдомембранозний коліт, пика. Діти Передбачається, що частота, тип та тяжкість небажаних реакцій у дітей така сама, як у дорослих. Пацієнти зі зниженим імунітетом У пацієнтів із синдромом набутого імунодефіциту (СНІД) та іншими імунодефіцитами, які отримують кларитроміцин у більш високих дозах протягом тривалого часу для лікування мікобактеріальних інфекцій, часто важко відрізнити небажані ефекти препарату від симптомів ВІЛ-інфекції або супутнього захворювання. Найчастішими небажаними явищами у пацієнтів, які приймали добову дозу кларитроміцину, що дорівнює 1000 мг, були: нудота, блювання, дисгевзія, біль у ділянці живота, діарея, шкірний висип, метеоризм, головний біль, запор, порушення слуху, підвищення активності ACT та АЛ плазмі крові. Також відзначалися випадки небажаних явищ із низькою частотою виникнення, такі як задишка, безсоння та сухість слизової оболонки порожнини рота. У пацієнтів із зниженим імунітетом проводили оцінку лабораторних показників, аналізуючи їх значні відхилення від норми (різке підвищення чи зниження). На підставі даного критерію у 2-3% пацієнтів, які отримували кларитроміцин у дозі 1000 мг щодня, було зареєстровано значне підвищення активності ACT та АЛТ у плазмі, а також зниження кількості лейкоцитів та тромбоцитів. У невеликої кількості пацієнтів було зареєстровано підвищення сироваткової концентрації залишкового азоту сечовини. * У деяких повідомленнях про рабдоміоліз кларитроміцин приймався одночасно з іншими лікарськими засобами, з прийомом яких, як відомо, пов'язаний розвиток рабдоміолізу (статини, фібрати, колхіцин або алопуринол). 1 Повідомлення про дані побічних реакцій були отримані під час клінічних досліджень, а також післяреєстраційного застосування кларитроміцину у лікарській формі ліофілізат для приготування розчину для інфузій. 2 Повідомлення про дані побічних реакцій були отримані під час клінічних досліджень, а також післяреєстраційного застосування кларитроміцину у лікарській формі таблетки з пролонгованим вивільненням, покриті плівковою оболонкою. 3 Повідомлення про дані побічних реакцій були отримані під час клінічних досліджень, а також післяреєстраційного застосування кларитроміцину у лікарській формі порошок для приготування суспензії для прийому внутрішньо. 4 Повідомлення про дані побічних реакцій були отримані під час клінічних досліджень, а також післяреєстраційного застосування кларитроміцину у лікарській формі таблетки, покриті плівковою оболонкою.Взаємодія з лікарськими засобамиЗастосування наступних лікарських засобів одночасно з кларитроміцином протипоказане у зв'язку з можливістю розвитку серйозних побічних ефектів. Цизаприд, домперидон, пімозід, терфенадип та астемізол При одночасному прийомі кларитроміцину з цизапридом, пимозидом, домперидоном, терфенадином або астемізолом повідомлялося про підвищення концентрації останніх у плазмі крові, що може призвести до подовження інтервалу QT на ЕКГ та появі серцевих аритмій, включаючи шлуночкову тахікардію (в тому числі шлуночкову тахікардію). ) та фібриляцію шлуночків. Алкалоїди ріжків Післяреєстраційні дослідження показують, що при одночасному застосуванні кларитроміцину з ерготаміном або дигідроерготаміном можливі наступні ефекти, пов'язані з гострим отруєнням препаратами групи ерготамінів: судинний спазм, ішемія кінцівок та інших тканин, включаючи центральну нервову систему (ЦНС). Одночасне застосування кларитроміцину та алкалоїдів ріжків протипоказане. Інгібітори ГМГ-КоА-редуктази (статини) Одночасний прийом кларитроміцину з ловастатином або симвастатином протипоказаний у зв'язку з тим, що дані статини значною мірою метаболізуються ізоферментом CYP3A4, і одночасне застосування з кларитроміцином підвищує їх сироваткові концентрації, що призводить до підвищення ризику розвитку міопатії, включаючи рабдомі. Повідомлялося про випадки рабдоміолізу у пацієнтів, які приймали кларитроміцин одночасно з цими препаратами. У разі необхідності застосування кларитроміцину слід припинити прийом ловастатину або симвастатину на час терапії. Кларитроміцин слід застосовувати з обережністю у разі комбінованої терапії з іншими статинами. Рекомендується застосовувати статини, метаболізм яких не залежить від ізоферменту CYP3A (наприклад, флувастатин). У разі потреби одночасного прийому рекомендується приймати найменшу дозу статину. Слід контролювати розвиток ознак та симптомів міопатії. Мідазолам для прийому внутрішньо При одночасному застосуванні внутрішньо мідазоламу та кларитроміцину у лікарській формі таблетки (500 мг 2 рази на добу) відзначалося збільшення AUC мідазоламу у 7 разів. Одночасне застосування кларитроміцину та мідазоламу для прийому внутрішньо протипоказане. Вплив інших лікарських засобів на кларитроміцин Лікарські препарати, що є індукторами ізоферменту CYP3A (наприклад, рифампіцин, фенітоїн, карбамазепін, фенобарбітал, препарати Звіробою продірявленого) можуть індукувати метаболізм кларитроміцину. Це може призвести до субтерапевтичної концентрації кларитроміцину та відповідно до зниження його ефективності. Крім того, необхідно спостерігати за концентрацією індуктора ізоферменту CYP3A у плазмі крові, яка може підвищитися через інгібування ізоферменту CYP3A кларитроміцином. При одночасному застосуванні рифабутину та кларитроміцину спостерігалося підвищення концентрації рифабутину та зниження концентрації кларитроміцину в плазмі крові з підвищеним ризиком розвитку увеїту. Наступні препарати мають доведений або передбачуваний вплив на концентрацію кларитроміцину в плазмі крові, у разі їх одночасного застосування з кларитроміцином може знадобитися корекція дози або перехід на альтернативне лікування Ефавіренз, невірапін, рифампіцин, рифабутин та рифапентин Потужні індуктори системи цитохрому Р450, такі як ефавіренз, невірапін, рифампіцин, рифабутин і рифапентин можуть прискорювати метаболізм кларитроміцину і, таким чином, знижувати концентрацію кларитроміцину в плазмі крові, а також послаблювати терапевтичний ефект. ВІН-кларитроміцину - метаболіту, що також є мікробіологічно активним. Оскільки мікробіологічна активність кларитроміцину та 14-ОН-кларитроміцину відрізняється щодо різних бактерій, терапевтичний ефект може знижуватися при одночасному застосуванні кларитроміцину та індукторів системи цитохрому Р450. Етравірін Концентрація кларитроміцину в плазмі знижується при одночасному застосуванні з етравірином, а концентрація активного метаболіту 14-ОН-кларитроміцину в плазмі крові підвищується. Оскільки 14-ОН-кларитроміцин має низьку активність по відношенню до інфекцій MAC, може змінюватися загальна активність щодо цих збудників, тому для лікування MAC слід розглядати альтернативне лікування. Флуконазол Одночасний прийом флуконазолу в дозі 200 мг щоденно та кларитроміцину в дозі 500 мг 2 рази на добу у 21 здорового добровольця призвело до збільшення середнього значення мінімальної рівноважної концентрації кларитроміцину та AUC на 33% та 18% відповідно. При цьому одночасний прийом значно не впливав на середню рівноважну концентрацію активного метаболіту 14-ОН-кларитроміцину. Корекція дози кларитроміцину у разі одночасного прийому флуконазолу не потрібна. Рітонавір Фармакокінетичне дослідження показало, що одночасний прийом ритонавіру в дозі 200 мг кожні 8 годин та кларитроміцину в дозі 500 мг кожні 12 годин призвів до помітного пригнічення метаболізму кларитроміцину. При одночасному прийомі ритонавіру Сmах кларитроміцину в плазмі збільшилася на 31%, Cmin збільшилася на 182% і AUC збільшилася на 77%. Було відзначено практично повне придушення утворення 14-ОН-кларитроміцину. Завдяки широкому терапевтичному діапазону кларитроміцину зменшення його дози у пацієнтів із нормальною нирковою функцією не потрібне. У пацієнтів з нирковою недостатністю доцільно розглянути такі варіанти корекції дози: при КК 30-60 мл/хв. доза кларитроміцину повинна бути зменшена на 50%. У пацієнтів з нирковою недостатністю доцільно розглянути наступні варіанти корекції дози: при КК 30-60 мл/хв доза кларитроміцину повинна бути зменшена на 50%, при КК менше 30 мл/хв доза кларитроміцину повинна бути зменшена на 75%. Ритонавір не слід одночасно приймати з кларитроміцином у дозах, що перевищують 1 г на добу. Подібні корекції доз повинні розглядатися у пацієнтів зі зниженою функцією нирок, якщо ритонавір застосовується як фармакокінетичний "підсилювач" при застосуванні інших інгібіторів протеази ВІЛ, включаючи атазанавір та саквінавір. Дія кларитроміцину на інші лікарські препарати Антиаритмічні засоби (хінідин та дизопірамід) Можливе виникнення шлуночкової тахікардії типу "пірует" при одночасному застосуванні кларитроміцину та хінідину або дизопіраміду. При одночасному прийомі кларитроміцину з цими препаратами слід регулярно проводити контроль ЕКГ щодо подовження інтервалу QT, а також слід контролювати сироваткові концентрації цих препаратів. У післяреєстраційному періоді повідомлялося про випадки розвитку гіпоглікемії при одночасному прийомі кларитроміцину та дизопіраміду. Необхідно контролювати концентрацію глюкози в крові при одночасному застосуванні кларитроміцину та дизопіраміду. Гіпоглікемічні засоби для внутрішнього застосування/інсулін При одночасному застосуванні кларитроміцину та гіпоглікемічних засобів для прийому внутрішньо (наприклад, похідні сульфонілсечовини) та/або інсуліну може спостерігатися виражена гіпоглікемія. Одночасне застосування кларитроміцину з деякими гіпоглікемічними препаратами (наприклад, натеглінід, піоглітазон, репаглінід та росиглітазон) може призвести до інгібування ізоферменту CYP3A кларитроміцином, внаслідок чого може розвинутись гіпоглікемія. Рекомендується ретельний контроль концентрації глюкози у крові. Взаємодія зумовлена ізоферментом CYP3A Одночасний прийом кларитроміцину, який, як відомо, інгібує ізофермент CYP3A, та препаратів, що первинно метаболізуються ізоферментом CYP3A, може асоціюватися із взаємним підвищенням їх концентрацій, що може посилити або продовжити як терапевтичні, так і побічні ефекти. Кларитроміцин слід обережно застосовувати пацієнтам, які отримують препарати, які є субстратами ізоферменту CYP3A, особливо якщо ці препарати мають вузький терапевтичний діапазон (наприклад, карбамазепін) та/або препарати, які інтенсивно метаболізуються цим ізоферментом. У разі потреби повинна проводитися корекція дози препарату, який приймається одночасно з кларитроміцином; також по можливості повинен проводитися моніторинг сироваткових концентрацій препаратів, що первинно метаболізуються ізоферментом CYP3A. Метаболізм наступних препаратів/класів здійснюється тим же ізоферментом CYP3A, що і метаболізм кларитроміцину (але цей список не є вичерпним): алпразолам, карбамазепін, цилостазол, циклоспорин, дизопірамід, ібрутиніб, метилпреднізолон, мідазолам наприклад, варфарин), атипові антипсихотичні засоби (наприклад, кветіапін), хінідин, рифабутин, силденафіл, сиролімус, такролімус, тріазолам та вінбластин. До препаратів, що взаємодіють подібним чином через інші ізоферменти в рамках системи цитохрому Р450, відносяться: фенітоїн, теофілін та вальпроєва кислота. Непрямі антикоагулянти При одночасному прийомі варфарину та кларитроміцину можлива кровотеча, виражене збільшення МНО та подовження протромбінового часу. У разі одночасного застосування з варфарином або іншими непрямими антикоагулянтами необхідно контролювати МНО та протромбіновий час. Омепразол Кларитроміцин (по 500 мг кожні 8 годин) досліджувався у здорових дорослих добровольців у поєднанні з омепразолом (по 40 мг щодня). При одночасному застосуванні кларитроміцину та омепразолу рівноважні плазмові концентрації омепразолу були збільшені (Сmах, AUC0-24 та Т1/2 збільшилися на 30%, 89% та 34% відповідно). Середнє значення pH шлунка протягом 24 годин склало 5,2 (при прийомі омепразолу окремо) та 5,7 (при прийомі омепразолу одночасно з кларитроміцином). Силденафіл, тадалафіл та варденафіл Кожен із цих інгібіторів фосфодіестерази метаболізується принаймні частково за участю ізоферменту CYP3A. У той же час, ізофермент CYP3A може інгібуватися в присутності кларитроміцину. Одночасне застосування кларитроміцину з силденафілом, тадалафілом або варденафілом може призвести до збільшення інгібуючої дії на фосфодіестеразу. При застосуванні цих препаратів одночасно з кларитроміцином слід розглянути можливість зменшення дози силденафілу, тадалафілу та варденафілу. Теофілін, карбамазепін При одночасному застосуванні кларитроміцину та теофіліну або карбамазепіну можливе підвищення концентрації даних препаратів у системному кровотоку. Толтеродін Первинний метаболізм толтеродину здійснюється через ізофермент CYP2D6. Однак у частині популяції, позбавленої CYP2D6, метаболізм відбувається через ізофермент CYP3A. У цій групі населення пригнічення ізоферменту CYP3A призводить до значно більших концентрацій толтеродину в сироватці крові. У популяції з низьким рівнем метаболізму через ізофермент CYP2D6 може знадобитися зниження дози толтеродину при одночасному застосуванні інгібіторів ізоферменту CYP3A, таких як кларитроміцин. Бензодіазепіни (наприклад, алпразолам, мідазолам, тріазолам) При одночасному застосуванні мідазоламу та таблеток кларитроміцину (500 мг 2 рази на добу) відзначалося збільшення AUC мідазоламу у 2,7 раза після внутрішньовенного введення мідазоламу. Якщо одночасно з кларитроміцином застосовується мідазолам у лікарській формі розчин для внутрішньовенного введення, слід ретельно контролювати стан пацієнта для можливої корекції дози мідазоламу. Введення лікарського препарату через слизову оболонку порожнини рота, що дає можливість обійти пресистемну елімінацію лікарського препарату, швидше за все, призведе до взаємодії, аналогічної тому, що спостерігається при внутрішньовенному введенні мідазоламу, а не прийому внутрішньо. Такі ж запобіжні заходи слід застосовувати і до інших бензодіазепінів, які метаболізуються ізоферментом CYP3A, включаючи триазолів та алпразолів. Для бензодіазепінів, виведення яких не залежить від ізоферменту CYP3A (темазепам, нітразепам, лоразепам), малоймовірно клінічно значуща взаємодія з кларитроміцином. При одночасному застосуванні кларитроміцину та триазоламу можлива дія на ЦНС, наприклад, сонливість та сплутаність свідомості. У зв'язку з цим, у разі одночасного застосування рекомендується стежити за симптомами порушення ЦНС. Взаємодії з іншими лікарськими засобами Колхіцін Колхіцин є субстратом як ізоферменту CYP3A, так і білка-переносника Р-глікопротеїну (Pgp). Відомо, що кларитроміцин та інші макроліди є інгібіторами ізоферменту CYP3A та Pgp. При одночасному застосуванні кларитроміцину та колхіцину інгібування Pgp та/або ізоферменту CYP3A може призвести до посилення дії колхіцину. Слід контролювати розвиток клінічних симптомів отруєння колхіцином. Зареєстровані постреєстраційні повідомлення про випадки отруєння колхіцином при його одночасному прийомі з кларитроміцином, частіше у пацієнтів похилого віку. Деякі з описаних випадків відбувалися у пацієнтів із нирковою недостатністю. Як повідомлялося, деякі випадки закінчувалися летальним кінцем. Одночасне застосування кларитроміцину та колхіцину протипоказане. Дігоксин Передбачається, що дигоксин є субстратом PGP. Відомо, що кларитроміцин пригнічує Pgp. При одночасному застосуванні кларитроміцину та дигоксину інгібування Pgp кларитроміцином може призвести до посилення дії дигоксину. Одночасний прийом дигоксину та кларитроміцину також може призвести до підвищення сироваткової концентрації дигоксину. У деяких пацієнтів спостерігалися клінічні симптоми отруєння дигоксином, включаючи потенційно летальні аритмії. При одночасному прийомі кларитроміцину та дигоксину слід ретельно контролювати концентрацію дигоксину у сироватці крові. Зідовудін Одночасний прийом таблеток кларитроміцину та зидовудину внутрішньо дорослими ВІЛ-інфікованими пацієнтами може призвести до зниження рівноважної концентрації зидовудину в плазмі крові. Оскільки кларитроміцин може перешкоджати всмоктуванню зидовудину при прийомі внутрішньо, взаємодії можна значно уникнути, приймаючи кларитроміцин і зидовудін з інтервалом в 4 години. Подібної взаємодії не спостерігали у ВІЛ-інфікованих дітей, які отримують дитячу суспензію кларитроміцину з зидовудином або дидезоксіїнозином. Оскільки кларитроміцин може перешкоджати всмоктуванню зидовудину при їх одночасному прийомі внутрішньо у дорослих пацієнтів, така взаємодія навряд чи можлива при застосуванні кларитроміцину внутрішньовенно. Фенітоїн та вальпроєва кислота Є дані про взаємодію інгібіторів ізоферменту CYP3A (включаючи кларитроміцин) з препаратами, які не метаболізуються за допомогою ізоферменту CYP3A (фенітоїн та вальпроєва кислота). Для цих препаратів при одночасному застосуванні з кларитроміцином рекомендується визначення їх сироваткових концентрацій, оскільки є повідомлення про їх підвищення. Двоспрямована взаємодія лікарських засобів Атазанавір Кларитроміцин та атазанавір є як субстратами, так і інгібіторами ізоферменту CYP3A. Існує свідчення двонаправленої взаємодії цих препаратів. Одночасне застосування кларитроміцину (500 мг 2 рази на добу) та атазанавіру (400 мг 1 раз на добу) може призвести до дворазового збільшення дії кларитроміцину та зменшення дії 14-ОН-кларитроміцину на 70% зі збільшенням AUC атазанавіру на 28%. Завдяки широкому терапевтичному діапазону кларитроміцину зменшення його дози у пацієнтів з нормальною нирковою функцією не потрібне. У пацієнтів з нирковою недостатністю середнього ступеня тяжкості (КК 30-60 мл/хв) доза кларитроміцину повинна бути зменшена на 50%. У пацієнтів з КК менше 30 мл/хв дозу кларитроміцину слід зменшити на 75%, застосовуючи для цього відповідну лікарську форму кларитроміцину. Кларитроміцин у дозах, що перевищують 1000 мг на добу, не можна застосовувати одночасно з інгібіторами протеаз. БМКК При одночасному застосуванні кларитроміцину та БМКК, які метаболізуються ізоферментом CYP3A4 (наприклад, верапаміл, амлодипін, дилтіазем), слід бути обережним, оскільки існує ризик виникнення артеріальної гіпотензії. При одночасному застосуванні можуть підвищуватися плазмові концентрації кларитроміцину та БМКК. Артеріальна гіпотензія, брадіаритмія та лактоацидоз можливі при одночасному прийомі кларитроміцину та верапамілу. Ітраконазол Кларитроміцин та ітраконазол є субстратами та інгібіторами ізоферменту CYP3A, що визначає двонаправлену взаємодію препаратів. Кларитроміцин може підвищити концентрацію ітраконазолу в плазмі, тоді як ітраконазол може підвищити плазмову концентрацію кларитроміцину. Пацієнтів, які одночасно приймають ітраконазол та кларитроміцин, слід ретельно обстежити на наявність симптомів посилення або збільшення тривалості фармакологічних ефектів цих препаратів. Саквінавір Кларитроміцин та саквінавір є субстратами та інгібіторами ізоферменту CYP3A, що визначає двоспрямовану взаємодію препаратів. Одночасне застосування кларитроміцину (500 мг 2 рази на добу) і саквінавіру (в м'яких желатинових капсулах, 1200мг 3 рази на добу) у 12 здорових добровольців викликало збільшення AUC і Смах саквінавіру в плазмі крові на 177% і 187% відповідно. окремо. Значення AUC та Сmах кларитроміцину були приблизно на 40% вищі, ніж при терапії одним кларитроміцином. При одночасному застосуванні цих двох препаратів протягом обмеженого часу у дозах/складах, зазначених вище, корекція дози не потрібна. Результати дослідження лікарських взаємодій із застосуванням саквінавіру у м'яких желатинових капсулах можуть не відповідати ефектам, що спостерігаються при застосуванні саквінавіру у твердих желатинових капсулах. Результати дослідження лікарських взаємодій при терапії саквінавіром окремо можуть не відповідати ефектам, що спостерігаються при терапії комбінацією саквінавір/ритонавір. При прийомі саквінавіру одночасно з ритонавіром слід враховувати потенційний вплив ритонавіру на кларитроміцин.Спосіб застосування та дозиВсередину. Таблетку слід ковтати повністю, не розламувати і не розжовувати. Дорослим та дітям старше 12 років – по 1 таблетці (500 мг) 1 раз на добу під час їжі. При тонзиліті та гострому середньому отиті: дорослим та дітям старше 18 років – по 1 таблетці (500 мг) 1 раз на добу під час їжі. При тяжких інфекціях дозу збільшують до 2 таблеток (1000 мг) 1 раз на добу під час їжі. Звичайна тривалість лікування від 5 до 14 днів. Виняток становлять позалікарняна пневмонія та синусит, які вимагають лікування від 6 до 14 днів. Порушення функції нирок Для пацієнтів з нирковою недостатністю важкого ступеня (КК менше 30 мл/хв) звичайна рекомендована доза становить 250 мг 1 раз на добу, у цьому випадку можливе застосування препарату Фромілід®, таблетки, вкриті плівковою оболонкою, 250 мг. При більш тяжких інфекціях рекомендована доза становить 1 таблетка 500 мг із пролонгованим вивільненням кларитроміцину. У пацієнтів з нирковою недостатністю середнього ступеня тяжкості (КК від 30 до 60 мл/хв) корекція дози не потрібна.ПередозуванняСимптоми: прийом внутрішньо великої дози кларитроміцину може викликати симптоми порушень з боку шлунково-кишкового тракту. У одного пацієнта з біполярним розладом в анамнезі після прийому 8 г кларитроміцину описані зміни психічного стану, параноїдальна поведінка, гіпокаліємія та гіпоксемія. Лікування: при передозуванні слід видалити неабсорбований препарат із шлунково-кишкового тракту (промивання шлунка, прийом активованого вугілля та ін.) та провести симптоматичну терапію. Гемодіаліз та перитонеальний діаліз не мають істотного впливу на концентрацію кларитроміцину в сироватці крові, що характерно і для інших лікарських препаратів групи макролідів.Запобіжні заходи та особливі вказівкиТривалий прийом антибіотиків може призводити до утворення колоній зі збільшенням кількості нечутливих бактерій та грибів. При суперінфекції слід призначити відповідну терапію. Призначення кларитроміцину вагітним жінкам має проводитися при ретельній оцінці співвідношення ризику та користі, особливо протягом перших трьох місяців вагітності. При застосуванні кларитроміцину повідомлялося про порушення функції печінки (підвищення активності "печінкових" ферментів у плазмі крові, гепатоцелюлярний та/або холестатичний гепатит з жовтяницею або без). Порушення функції печінки може бути важким, але є оборотним. Є випадки печінкової недостатності з летальним результатом головним чином пов'язані з наявністю серйозних супутніх захворювань та/або одночасним застосуванням інших лікарських засобів. При появі ознак та симптомів гепатиту, таких як анорексія, жовтяниця, потемніння сечі, свербіж, болючість живота при пальпації, необхідно негайно припинити терапію кларитроміцином. За наявності хронічних захворювань печінки необхідно проводити регулярний контроль активності печінкових ферментів сироватки крові. При лікуванні практично всіма антибактеріальними засобами, у тому числі кларитроміцином, описані випадки псевдомембранозного коліту, тяжкість якого може змінюватись від легкого до загрозливого життя. При лікуванні практично всіма антибактеріальними препаратами, у тому числі кларитроміцином, описані випадки Clostridium difficile-асоційованої діареї, тяжкість якої може змінюватись від легкої діареї до загрозливого життя коліту. Антибактеріальні препарати можуть змінити нормальну мікрофлору кишечника, що може спричинити зростання Clostridium difficile. Псевдомембранозний коліт, викликаний Clostridium difficile, необхідно підозрювати у всіх пацієнтів, у яких після застосування антибактеріальних засобів розвинулася діарея. Після проведення курсу антибіотикотерапії потрібне ретельне медичне спостереження за пацієнтом.Описувалися випадки розвитку псевдомембранозного коліту через 2 місяці після прийому антибіотиків. При лікуванні макролідами, включаючи кларитроміцин, спостерігалося подовження серцевої реполяризації та інтервалу QT, збільшуючи ризик розвитку серцевої аритмії та шлуночкової тахікардії типу “пірует”. Оскільки такі ситуації можуть призвести до збільшення ризику розвитку шлуночкових аритмій (у тому числі шлуночкової тахікардії типу "пірует"), то: Кларитроміцин не повинен застосовуватися у таких категорій пацієнтів: у пацієнтів із гіпокаліємією; одночасне застосування кларитроміцину з астемізолом, цизапридом, домперидоном, пімозидом та терфенадином протипоказано; у пацієнтів із вродженим або набутим зареєстрованим подовженням інтервалу QT або наявністю шлуночкової аритмії в анамнезі. Кларитроміцин повинен застосовуватися з обережністю у таких категорій пацієнтів: у пацієнтів з ІХС, тяжкою серцевою недостатністю, порушеннями провідності або клінічно значущою брадикардією; у пацієнтів з електролітними порушеннями, такими як гіпомагніємія; у пацієнтів, які одночасно приймають інші лікарські препарати, пов'язані з подовженням інтервалу QT. У ході епідеміологічних досліджень з вивчення ризику несприятливих серцево-судинних наслідків при застосуванні макролідів було отримано неоднозначні результати. У деяких спостережних дослідженнях було встановлено рідкісний короткочасний ризик розвитку аритмії, інфаркту міокарда та смерті від серцево-судинних захворювань, пов'язаних із застосуванням макролідів, включаючи кларитроміцин. При призначенні кларитроміцину слід співвідносити передбачувану користь від прийому препарату з цими ризиками. Можливий розвиток перехресної резистентності до кларитроміцину та інших антибіотиків групи макролідів, а також лінкоміцину та кліндаміцину. Враховуючи зростаючу резистентність Streptococcus pneumoniae до макролідів, важливо проводити тестування чутливості при призначенні кларитроміцину пацієнтам із позалікарняною пневмонією. При шпитальній пневмонії кларитроміцин слід застосовувати у комбінації з відповідними антибіотиками. Інфекції шкіри та м'яких тканин легкого та середнього ступеня тяжкості найчастіше викликані Staphylococcus aureus та Streptococcus pyogenes. При цьому обидва збудники можуть бути стійкими до макролідів. Тому важливо проводити тест на чутливість. Макроліди можна застосовувати при інфекціях, викликаних Corynebacterium minutissimum, захворюваннях вугри вульгарні та пика, а також у тих ситуаціях, коли не можна застосовувати пеніцилін. У разі появи гострих реакцій гіперчутливості, таких як анафілактична реакція, серйозні шкірні небажані реакції (наприклад, гострий генералізований екзантематозний пустульоз), синдром Стівенса-Джонсона, токсичний епідермальний некроліз та лікарський висип з еозинофілією та Систем симптом прийом кларитроміцину та почати відповідну терапію. У разі одночасного застосування з варфарином або іншими непрямими антикоагулянтами необхідно контролювати МНО та протромбіновий час. Спеціальна інформація про допоміжні речовини Препарат Фромілід уно містить лактозу, тому протипоказаний при таких станах: непереносимість лактози, дефіцит лактази, синдром глюкозо-галактозної мальабсорбції. Вплив на здатність до керування автотранспортом та управління механізмами Дані щодо впливу кларитроміцину на здатність керувати транспортними засобами, механізмами відсутні. Слід бути обережними при керуванні транспортними засобами, механізмами, враховуючи потенційну можливість запаморочення, вертиго, сплутаності свідомості та дезорієнтації, які можуть виникнути при застосуванні даного препарату.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаСпрей - 1 мл: Butane, propane, izobutane, methylal, menthol. Флакон 400мл.ХарактеристикаСпортивне заморожування Frostforce Coolant Spray – миттєво знеболює, зменшує набряк, перешкоджає утворенню гематоми, значно знижує рівень запального процесу. Діє протягом тривалого часу. Застосовується для надання першої допомоги/знеболювання при травмах, забитих місцях, розтягненнях/розривах зв'язок, для полегшення гострого та хронічного болю опорно-рухового апарату. Не обпалює шкіру, не викликає побічних ефектів, не викликає больових/неприємних відчуттів після закінчення своєї дії. Спортивне заморожування є одним із найдоступніших і універсальних засобів першої допомоги при травмах. Холодотерапія повсюдно використовується спортсменами та лікарями у сфері спортивної медицини, а також у побуті при різних травмах. Зокрема, спортивне заморожування може розглядатися як частина популярного в усьому світі методу надання екстреної медичної допомоги при травмах (забитих місцях, розтягненнях) RICE (rest/спокій, ice/лід, compression/тиск, elevation/піднятий стан). Охолодний спрей з холодоагентом (холодоагент спрей) Frostforce, миттєво та ефективно охолоджує травмовану ділянку. Холод забезпечує зниження болю та зменшення запалення шляхом різкого скорочення кров'яного потоку у місці пошкодження. Завдяки вмісту ментолу Frostforce Coolant Spray має приємний, освіжаючий аромат. Гіпоалергенно. Спортивне заморожування застосовується у спорті (заморожування для спортсменів) для зменшення набряклості при різних травмах (забитих місцях, розтягненнях зв'язок і м'язів, вивихах), викликаних падінням або ударом; у побуті – зі зняттям набряку, запалення, болю; при проведенні епіляції, при укусах комах та інших випадках. Спорт, і професійний, і аматорський, тісно пов'язаний із травмами та забоями. При цьому дуже важливим є своєчасне швидке надання першої допомоги. У таких випадках не обійтися без аерозолю Frostforce Coolant Spray. Своєчасне застосування охолодного спрею Pharmacels допоможе сконцентруватися на результаті, а не на больових відчуттях. Спортивне заморожування швидко наноситься, ефективно знижує біль, набряки та ідеально підходить для швидкого знеболювання та надання першої допомоги до прибуття лікаря, у польових умовах. Спортивне заморожування також знаходить своє застосування в побуті. З Frostforce Coolant Spray навіть така малоприємна процедура, як епіляція, може стати менш хворобливою. Достатньо лише нанести невелику кількість спортивної заморозки на шкіру перед початком процедури. Спортивне заморожування також ефективне при укусах комах. Спрей знімає роздратування, свербіння та заспокоює шкіру після укусу. Frostforce Coolant Spray полегшує неприємні відчуття, зменшує запалення та забезпечує тривалу дію, приємно охолоджуючи шкіру.РекомендуєтьсяНадання першої допомоги/знеболення при травмах, забоях, розтягуваннях/розривах зв'язок, для полегшення гострого та хронічного болю опорно-рухового апарату.Протипоказання до застосуванняОхолодний спрей "Фрост" не можна використовувати при індивідуальній непереносимості компонентів.Вагітність та лактаціяПротипоказаний вагітним жінкам, які годують жінкам та дітям у неповнолітньому віці.Запобіжні заходи та особливі вказівкиТільки для зовнішнього застосування. Уникайте попадання в очі. У разі попадання в очі, негайно промийте їх водою.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаХарчові волокна цукрових буряків, лактулоза, желатин (капсула), сухий сік цукрових буряків, сенни екстракт сухий, сенний лист, порошок плодів чорносливу, порошок плодів інжиру, порошок плодів абрикосу, плоди фенхелю звичайного.Характеристика«Фрутолакс» капсули для осіб, які потребують покращення моторно-евакуаторної функції кишечника. Рекомендовані як біологічно активна добавка до їжі – джерела лактулози, сіннозидів.РекомендуєтьсяДля осіб, які потребують поліпшення моторно-евакуаторної функції кишечника.Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність, годування груддю, гострі кишкові захворювання.Спосіб застосування та дозиДорослим по 2-4 капсули, дітям старше 14 років по 2 капсули у другій половині дня під час їжі. Тривалість прийому – 2 тижні. За потреби прийом можна повторити.Запобіжні заходи та особливі вказівкиПеред застосуванням слід проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаІнулін, лактит, екстракт сенни, порошок сливи, порошок персика, магнію стеарат (агент антистежуючий), піридоксину гідрохлорид (Вітамін В6), тіаміну гідрохлорид (Вітамін В1). Містить підсолоджувач лактит. При надмірному вживанні може мати проносну дію.ХарактеристикаПричини виникнення такої делікатної проблеми, як затримка випорожнень або запор, не завжди можуть бути пов'язані з гострими або хронічними захворюваннями шлунково-кишкового тракту. Неправильне харчування, недостатнє споживання рідини, гіподинамія, стрес – все це може порушити перистальтику кишечника та призвести до погіршення якості життя. «Фрутослабін®» – комплексний засіб, який допомагає організму боротися із запорами, тому що до його складу входять рослинні компоненти сенни, сливи та персика, а також лактит та вітаміни. Вони сприяють полегшенню акта дефекації, і навіть нормалізації мікрофлори кишечника.Властивості компонентівІнулін. Рослинний компонент, який сприятливо впливає на зростання корисної мікрофлори кишечника та зміцнення місцевого імунітету. Органічні кислоти. Порошок персика та сливи містять органічні кислоти та харчові волокна, які сприяють спорожненню кишечника. Вітаміни групи B. Вітаміни В1 та В6 беруть участь у багатьох обмінних процесах в організмі. Доброчинно впливають на правильний обмін речовин. Екстракт сенни. Має делікатні проносні властивості за рахунок позитивного впливу на моторну функцію кишечника. лактит. Під дією кишкової флори розщеплюється в товстому кишечнику на низькомолекулярні органічні кислоти, що підвищують осмотичний тиск, що сприяє збільшенню калових мас, їх розм'якшенню та полегшенню акта дефекації.РекомендуєтьсяЯк біологічно активну добавку до їжі - додаткового джерела вітамінів В1 і В6, джерела антраценпохідних (сеннозидів A і B), лактиту та інуліну.Протипоказання до застосуванняІндивідуальна непереносимість компонентів, схильність до діареї, хронічні захворювання шлунково-кишкового тракту на стадії загострення, вагітність, годування груддю.Спосіб застосування та дозиДорослим по 2 таблетки увечері під час їжі. Тривалість прийому 2 тижні.Запобіжні заходи та особливі вказівкиПеред застосуванням рекомендується проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
Фасування: N30 Форма випуску: мармеладні пастилки Упаковка: банку Виробник: Евалар ЗАТ Завод-виробник: Евалар ЗАТ(Росія). . .
403,00 грн
360,00 грн
Склад, форма випуску та упаковкаЦукор, патока крохмальна, желатин, лимонна кислота (регулятор кислотності), аскорбінова кислота, цитрусовий пектин (агент желюючий), концентрований сік чорної моркви (барвник), цинку цитрат, сік концентрований яблучний, ароматизатор натуральний «Полуниця», а- смако-ароматична добавка натуральний йогуртовий порошок, калію йодид, інозитол, глазурувальник (рослинна олія, віск карнаубський), марганцю глюконат, холекапьциферол, піридоксину гідрохлорид, ціанокобаламін, ретинолу пальмітаєт, оф,ХарактеристикаЩоденне насичення організму вітамінами і мікроелементами входить до факторів, що забезпечує хороше самопочуття та міцне здоров'я. Вітаміни – це речовини, які грають найважливішу роль здоров'я людини і необхідні нормально функціонувати всіх систем організму. Більшість їх міститься у продуктах харчування. Вітаміни беруть активну участь у процесі обміну речовин, тому їх недолік несприятливо впливає на самопочуття людини, а в деяких випадках навіть призводить до захворювань – авітамінозів. Для нормальної життєдіяльності дорослої людини потрібні вітаміни A, B1, B2, C та інші. Всі вітаміни в процесі впливу на організм людини знаходяться в близькій залежності один від одного, а це означає, що нестача одних може порушити правильну дію інших. Ось чому не можна недооцінювати роль вітамінів у житті. Щоб не допустити дефіциту вітамінів або заповнити їх недолік, зверніть увагу на Фруттілар Мультивітаміни. Це збалансований склад вітамінів та мінералів для щоденної підтримки здоров'я, енергії та доброго самопочуття. Збагачує раціон харчування та заповнює потребу організму у вітамінах, мінералах.Властивості компонентівВітамін С – найсильніший антиоксидант. Сприяє зміцненню імунної системи, має протизапальні, антисептичні властивості; сприятливо впливає на енергетичні процеси, підвищуючи витривалість; зміцнює судини, нормалізує проникність стінок, знижує ризик розвитку атеросклерозу; впливає на стан нервової системи, підвищує стресостійкість. Вітамін Е є основним представником групи антиоксидантів. Він має омолоджуючу дію, уповільнюючи старіння клітин. Діючи разом із вітаміном А захищає легені від впливу забрудненого повітря, прискорює загоєння опіків. Необхідний для нормальної роботи м'язів і нервової системи, покращує роботу серця, стимулює кровообіг і утворення червоних кров'яних тілець, перешкоджає утворенню кров'яних тромбів, сприяє природній терморегуляції тіла, підвищує імунітет у похилому віці і перешкоджають розвитку катаракти та атрофії м'язів, захищає клітини від агресивного впливу. променів, ультрафіолетового випромінювання (сонячного та штучного), хімічних речовин (в їжі та воді). Вітаміна В необхідний для нормальної роботи центральної нервової системи, допомагає позбутися нічних спазмів м'язів, судом литкових м'язів, оніміння рук. Також він потрібний для нормального синтезу нуклеїнових кислот, які перешкоджають старінню організму та для підтримки імунітету. Також Пиридоксин бере участь у побудові ферментів, які забезпечують нормальну роботу понад 60 різних ферментативних систем, покращує засвоєння ненасичених жирних кислот. Вітамін В1 (тіамін) необхідний нормальної роботи кожної клітини організму, особливо нервових клітин. Він стимулює роботу мозку, необхідний для серцево-судинної та ендокринної систем, для обміну речовини ацетилхоліну, що є хімічним передавачем нервового збудження. Тіамін нормалізує кислотність шлункового соку, рухову функцію шлунка та кишечника, підвищує опірність організму до інфекцій. Він покращує травлення, нормалізує роботу м'язів та серця, сприяє зростанню організму та бере участь у жировому, білковому та водному обміні. Тіамін бере участь у процесі перетворення глюкози на енергію. Вітамін В2 (рибофлавін) бере активну участь в утворенні деяких гормонів та еритроцитів, синтезі АТФ (аденозинтрифосфорна кислота - "паливо життя"), захищає сітківку від надмірного впливу УФ-променів, забезпечує адаптацію до темряви, підвищує гостроту зору та сприйняття кольору та світла. Рибофлавін потрібен для зростання та оновлення тканин, позитивно впливає на стан нервової системи, печінки, шкіри, слизових оболонок. Він необхідний для нормального розвитку плода при вагітності та для зростання дітей. Зберігає шкіру, нігті та волосся здоровим. Вітамін А необхідний зміцнення імунітету, хорошого зору. Є важливим вітаміном та потужним антиоксидантом. Тому отримання достатньої кількості вітаміну А абсолютно необхідне підтримки загального стану здоров'я. Користь вітаміну А полягає у підтримці шкіри здорової та чистої. Також він є ключовим фактором профілактики захворювань, підтримці імунітету та здоров'я кісток. Фолієва кислота – водорозчинний вітамін групи B – бере участь у синтезі імунних клітин крові, активізації метаболізму, сприяє нормалізації функції травного тракту. Біотин отримав свою назву від грец. bios – життя через його здатність стимулювати зростання дріжджів та бактерій. Він допомагає нам підтримувати молодий та привабливий зовнішній вигляд, оскільки відіграє важливу роль у підтримці здоров'я волосся, нігтів та шкіри. Вітамін D3 впливає на обмін кальцію та фосфору, підвищуючи проникність епітелію кишечника для кальцію та фосфору. При цьому забезпечуються необхідні концентрації їх у крові. Регулює мінералізацію кісткової тканини. Основна функція вітаміну D - забезпечення нормального зростання та розвитку кісток, попередження рахіту та остеопорозу. Він регулює мінеральний обмін та сприяє відкладенню кальцію в кістковій тканині та дентині, таким чином, перешкоджаючи остеомаляції (розм'якшенню) кісток. Вітамін В12 Основна функція вітаміну В12 – забезпечення нормального кровотворення – необхідний для утворення червоних кров'яних тілець. Він сприятливо впливає на жировий обмін у печінці, стан центральної та периферичної нервової системи, на обмін речовин (особливо білковий), стимулює ріст, знижує вміст холестерину в крові. Інозит є у всіх тканинах організму людини. Найвища концентрація холіну знаходиться в головному мозку, серці та кришталику ока. Інозит працює в тісній взаємодії з холіном як один з основних компонентів клітинних мембран. Він важливий для зростання клітин у головному мозку, оболонки очей та кишечника. Цинк бере участь у формуванні імунітету та підтримці функції чоловічих статевих залоз (він є складовою чоловічого статевого гормону дигідрокситестостерону). Ймовірно, тому у найбільшій кількості він міститься у тканинах тестикул та шишкоподібної залози, яка має пряме відношення до реалізації сексуальної функції чоловіків та жінок. Цинк відноситься до мінеральних антиоксидантів, ліпотропних факторів, що беруть участь разом із вітаміном В6 в утворенні ненасичених жирних кислот. Марганець - мікроелемент, який називають захисником клітин. Важливе значення марганець має у підтримці функцій статевих залоз, нервової та імунної систем, опорно-рухового апарату, необхідний для зростання максимально ефективної роботи мозку, правильного метаболізму цукру, інсуліну і холестерину, підтримує процес відновлення шкіри при ранах. У поєднанні з кальцієм марганець пом'якшує передменструальний синдром. Організму марганець потрібен для нормального метаболізму жиру, для побудови кісток і сполучних тканин, для вироблення енергії, для синтезу холестерину і нуклеотидів (ДНК), необхідних кожній клітині, що живе для поділу. Йод важливий у розвиток інтелекту. Він є обов'язковим компонентом гормонів, які регулюють обмін речовин та беруть участь у регуляції функції серцево-судинної системи, вони важливі для розвитку центральної нервової системи, для стійкості організму до несприятливих факторів зовнішнього середовища. Селен сприяє зміцненню імунітету і стимулює утворення білкових молекул, що мають захисні властивості. На особливу увагу заслуговують антиоксидантні властивості селену. Вченими встановлено, що основу багатьох захворювань лежать порушення біохімічних процесів, зумовлені дією шкідливих частинок – вільних радикалів. Селен захищає клітини людського тіла від згубного впливу таких частинок, тобто виявляє антиоксидантні властивості. Завдяки цьому мікроелементу значно продовжується термін активної життєдіяльності клітин та нейтралізуються небезпечні для організму речовини. Саме тому селен можна розглядати як мікроелемент, що забезпечує довголіття.Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність, годування груддю.Спосіб застосування та дозиДорослим – по 1 пастилці на день, допускається прийом до 3 пастилок на день. Тривалість прийому – не менше 1 місяця. За потреби курс прийому можна повторювати.Запобіжні заходи та особливі вказівкиПеред застосуванням рекомендується проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
389,00 грн
359,00 грн
Склад, форма випуску та упаковкаПатока крохмальна, цукор, желатин, Лимонна кислота (регулятор кислотності), пектин цитрусовий (агент желюючий), аскорбінова кислота, цинку цитрат, ароматизатор натуральний "Апельсин", молочна кислота (регулятор кислотності), сік концентрований яблучний, барвник натуральний , глазурувальник (олія, віск карнаубський), вітамін D у формі холекальциферолу.ХарактеристикаНа сьогоднішній день більшість фахівців найважливішим вітаміном – вітамін D, який бере участь у багатьох процесах в організмі. Його основне завдання – допомагати організму засвоювати магній та кальцій, щоб наші кістки та зуби були здоровими. Міцність нашого скелета і правильна структура кісток і зубів залежать від вмісту вітаміну D. Нестача вітаміну D в організмі призводить до зниження засвоєння кальцію з їжі, організм при цьому використовує ("вимиває") запаси кальцію з кісток, що призводить до їх крихкості. Це особливо важливо для жінок, тому що вони втрачають більше кальцію, ніж чоловіки, коли виношують та годують грудьми дітей. Якщо жінка відчуває нестачу вітаміну D, то з віком у неї може розвинутися не тільки остеопороз – дуже небезпечне захворювання, при якому кістки стоншуються і стають крихкими – але й можуть виникнути проблеми із серцево-судинною системою, послабшати імунітет тощо. І, що найголовніше, саме від рівня вітаміну D в організмі залежить те, наскільки сильним буде імунітет. Дослідження Гарвардської медичної школи, засноване більш ніж 50 наукових працях, підтвердило, що вітамін D – одне із головних чинників підтримки природного імунітету, оскільки він бере участь у освіті імунних клітин, включаючи всі види лімфоцитів. Виходить, що дефіцит вітаміну D – це серйозний удар імунітету. І варто докласти всіх зусиль, щоб його виключити.Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність, годування груддю.Спосіб застосування та дозиДорослим – по 1 пастилці на день після їди. Тривалість прийому – 2-3 місяці.Запобіжні заходи та особливі вказівкиПеред застосуванням рекомендується проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
400,00 грн
354,00 грн
Фасовка: N30 Форма выпуска: пастилки жевательные Упаковка: блистер Производитель: Эвалар ЗАО Завод-производитель: Эвалар ЗАО(Россия). . .