Все товары
Склад, форма випуску та упаковкаОлігофруктоза, лактат кальцію, інулін, дикрахмалфосфат ацетильований, полівініловий спирт (Е1203), поліетиленгліколь (Е1521), тальк, діоксид кремнію, стеарат кальцію Таблетки покриті плівковою оболонкою масою 710,5 мг (± 5%) 60 шт. в упаковціХарактеристикаБіологічно активна добавка СТІМ є метапребіотиком, так як у складі є пребіотики інулін та олігофруктоза, що стимулюють зростання власної мікробіоти, та метабіотик лактат кальцію, що додатково її захищає.РекомендуєтьсяЯк біологічно активна добавка до їжі - джерела пребіотиків-поліфруктозанів (інуліну, олігофруктози)Протипоказання до застосуванняІндивідуальна непереносимість компонентів препарату, вагітність, годування груддю. Перед застосуванням рекомендується проконсультуватися з лікарем.Спосіб застосування та дозиДітям з 7 до 14 років – по 1 таблетці 3 рази на день, дітям старше 14 років – по 1-2 таблетці 3 рази на день, дорослим – по 1-2 таблетці 3 рази на день. Тривалість прийому – 14 днів. За потреби прийом можна повторити.Запобіжні заходи та особливі вказівкиПеред застосуванням проконсультуйтеся зі спеціалістом.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаТаблетки – 1 таб.:. Олігофруктоза P95 (фруктоолігосахариди) - 270 мг; Інулін GR (фруктополісахариди) – 116 мг; Лактат кальцію – 104 мг; Допоміжні речовини для формування таблетки – діоксид кремнію та стеарат кальцію в сумі – 10 мг.ХарактеристикаМікробіота кишечника здорової людини на 90% складається з біфідобактерій – мікроорганізмів, необхідних для нормальної життєдіяльності людини. Неправильне харчування, шкідливі звички, несприятливий вплив довкілля, використання антибіотиків знижують кількість біфідобактерій в кишечнику, які місце негайно займають патогенні, шкідливі в людини мікроби. Це порушення біологічної рівноваги між умовно-патогенною та корисною мікробіотою називається дисбактеріозом, що призводить до суттєвого зниження колонізаційної резистентності слизової оболонки шлунково-кишкового тракту. На жаль, в даний час близько 95% населення Росії страждає на дисбактеріоз кишечника. При цьому клініко-лабораторному синдромі порушується нормальне травлення, з'являються діарея або запори, спастичні болі в ділянці живота, підвищена газоутворення, алергічні реакції. Надалі цей стан веде до погіршення роботи печінки, підшлункової залози, зниження імунітету, трамбоутворення, захворювань опорно-рухового апарату та інших патологій. Стімбіфід випускається у вигляді пігулок плоско-овальної форми білого кольору масою 500 мг. Метапребіотик СТИМБІФІД ПЛЮС є інноваційною розробкою російських учених Наукового товариства «Мікробіота» на основі глибоких фундаментальних досліджень кишкової мікробіоти, а також безпечних та ефективних методів її корекції. Дослідження лягли в основу «Наукового відкриття» та захищені двома патентами Російської Федерації. Метапребіотик СТИМБІФІД ПЛЮС відновлює індивідуальну мікробіоту кишечника, створюючи пріоритетні умови для розмноження біфідобактерій, лактобацил та кишкової палички, які, пригнічуючи ріст патогенної мікробіоти, витісняють її з організму. Істотне зростання нормобіоти призводить до підвищення колонізаційної резистентності слизової оболонки ШКТ. Метапребіотик СТИМБІФІД ПЛЮС є подальшим розвитком та глибокою оптимізацією пребіотика Стімбіфід і складається з двох компонентів – пребіотичного та метабіотичного. Вузконаправлений пребіотичний компонент - природні фруктоолігосахариди (ФОС) і фруктополісахариди (ФПС) з оптимізованим співвідношенням коротких (GFn, n=2-8) і довгих (GFn, п=2-60) ланцюжків, що забезпечує зниження біфідобактерій ексклюзив кишки. Метабіотичний компонент – лактат кальцію. Є потужним стимулятором зростання та розмноження нормобіоти (патенти РФ).РекомендуєтьсяПоєднання в СТИМБІФІД ПЛЮС одночасно метабіотика і пребіотика з різними механізмами дії сприяє:. безпечного та ефективного відновлення власної (індивідуальної) мікробіоти кишечника, у тому числі при одночасному прийомі антибіотиків; підвищенню колонізаційної резистентності слизової оболонки шлунково-кишкового тракту при інфекційній патології; ерадикації Helicobacter pylori; усунення запорів (ефект дієтичного/харчового волокна).Протипоказання до застосуванняІндивідуальна нестерпність компонентів продукту.Вагітність та лактаціяПрепарат протипоказаний при вагітності, годуванні груддю.Спосіб застосування та дозиДорослим та дітям з 14 років по 2 табл. 3 десь у день під час їжі. Тривалість прийому 1 місяць. Кількість курсів не обмежена. Дітям віком до 3-х років по 1 табл. 3 десь у день під час їжі. З метою адаптації шлунково-кишкового тракту до фруктосахаридів можливе плавне збільшення добової дози до рекомендованої протягом 2-3 діб. Так, наприклад, для дорослих та дітей (з 14 років) у перший та другий день – по 1 табл. 3 десь у день, третій - по 2 табл. З на день (повна добове дозування). Аналогічно інших вікових груп.Запобіжні заходи та особливі вказівкиПеред застосуванням рекомендується проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
Фасування: N40 Форма випуску таб. Упаковка: блістер Виробник: Медстар Завод-виробник: В-Мін ТОВ(Росія). .
Дозування: 550 мг Фасування: N80 Форма випуску таб. Виробник: В-МІН+ Завод-виробник: В-МІН + (Росія). .
Склад, форма випуску та упаковкаТаблетка – 1 табл.: екстракт ехінацеї пурпурової – 100 мг. аскорбінова кислота – 4 мг. целюлоза мікрокристалічна МКЦ. Пігулки, 60 шт.Опис лікарської формиТаблетки, вкриті оболонкою, або таблетки масою 0.53 г.Фармакотерапевтична групаВідновлює імунітет. Виводить із організму токсини. Протиалергетік. Перешкоджає запальним процесам. Має антиоксидантні властивості. Благотворно діє мембрани клітин.ІнструкціяПриймати під час їжі. Тривалість прийому – 20 днів. За потреби тривалість прийому можна збільшити до 3 місяців.Показання до застосуванняЦей препарат застосовується для загального зміцнення імунної системи та підвищення імунітету.РекомендуєтьсяРекомендовано використовувати як профілактичний засіб з метою зниження ризику різних простудних захворювань.Спосіб застосування та дозиДорослим по 1 таблетці 1-2 десь у день. За потреби допускається прийом до 4 таблеток на день.Умови відпустки з аптекБез рецепта
Склад, форма випуску та упаковка1 мл розчину для прийому внутрішньо містить 200 мг цитруліну малату; у пакетиках або ампулах по 10 мл, у картонній коробці 18 шт.Фармакотерапевтична групаНормалізує обмінні процеси. Ліквідує надлишок іонів амонію та лактату за рахунок активізації циклу сечовини та відновлення нормального функціонування циклу Кребса та, як наслідок, глюконеогенез.Показання до застосуванняКорекція ацидозу та гіперамоніємії, в т.ч. в осіб похилого віку, післяопераційному періоді, у спортсменів; перевтома, втома, реконвалесценція, астенія вагітних, діабетична астенія, сексуальна астенія.РекомендуєтьсяВідсутність цукру дозволяє призначати пацієнтам із цукровим діабетом.Протипоказання до застосуванняІндивідуальна нестерпність.Побічна діяМожливі неприємні відчуття у ділянці шлунка (на початку лікування).Спосіб застосування та дозиВсередину, під час їжі, запиваючи 1/2 склянки звичайної або підсолодженої води. Дорослим та пацієнтам похилого віку призначають по 10 мл 3 рази на добу; дітям віком до 5 років – 10 мл 1 раз на добу; від 5 до 15 років – по 10 мл 2 рази на добу при курсовому лікуванні не більше 12 днів.Запобіжні заходи та особливі вказівкиЗ обережністю призначають хворим, які перебувають на дієті без солі (1 пакетик або ампула містять 30 мг натрію).Умови відпустки з аптекБез рецептаВідео на цю тему
Дозування: 480 мг Фасування: N30 Форма выпуска: капс. Упаковка: блистер Производитель: Квадрат-С ООО Завод-производитель: Квадрат-С(Россия). .
82 521,00 грн
171,00 грн
Склад, форма випуску та упаковкаТаблетки, покриті плівковою оболонкою - 1 табл. активна речовина: регорафеніб – 40 мг; допоміжні речовини: МКЦ – 100 мг; кроскармелоза натрію – 154 мг; магнію стеарат – 3,6 мг; повідон 25 - 160 мг; кремнію діоксид колоїдний – 2,4 мг; оболонка плівкова: Opadry II™ 85G35294 рожевий (заліза оксид червоний Е172 - 0,0648 мг, заліза оксид жовтий Е172 - 0,0732 мг, лецитин - 2,28 мг, полівініловий спирт, частково гідролізований -5,28 мг, ,4 мг, титану діоксид Е171 - - 2,28 мг) - 12 мг. Пігулки, покриті плівковою оболонкою, 40 мг. За 28 табл. з вологопоглиначем у непрозорому флаконі білого кольору з ПЕВП з кришкою, що загвинчується, з герметизуючою вставкою і пристроєм проти розкриття флакона дітьми. 1 або 3 фл. поміщені у картонну пачку.Опис лікарської формиОвальні пігулки, покриті плівковою оболонкою, світло-рожевого кольору, на одному боці методом видавлювання нанесено «40», з іншого боку — «BAYER».Фармакотерапевтична групаПротипухлинний.ФармакокінетикаВсмоктування. Після прийому таблеток регорафенібу його середня відносна біодоступність у порівнянні з розчином для внутрішнього прийому становить 69-83%. Середнє значення Cmax регорафенібу в плазмі становить близько 2,5 мг/л приблизно через 3-4 години після одноразової пероральної дози регорафенібу 160 мг (4 табл. по 40 мг). Найбільша концентрація регорафенібу та його основних фармакологічно активних метаболітів М-2 (N-оксид) та М-5 (N-оксид та N-дезметил) досягається після прийому сніданку з низьким вмістом жирів у порівнянні з прийомом після сніданку з високим вмістом жирів або прийомом натще. У порівнянні з прийомом натще експозиція регорафенібу збільшується на 48% - при прийомі після сніданку з високим вмістом жирів і на 36% - при прийомі після сніданку з низьким вмістом жирів. У порівнянні з прийомом натще експозиція метаболітів М-2 і М-5 вище при прийомі регорафенібу після сніданку з низьким вмістом жирів і нижче при прийомі після сніданку з високим вмістом жирів. Розподіл. AUC демонструє кілька піків як для регорафенібу, так і для його основних циркулюючих метаболітів протягом 24 годин після прийому дози, що пов'язано з печінково-кишковою рециркуляцією препарату. Зв'язок регорафенібу з білками плазми in vitro високий і становить 99,5%. Метаболізм. Метаболізм регорафенібу здійснюється головним чином у печінці шляхом окислення, опосередкованого ізоферментом CYP3A4, а також шляхом глюкуронування, опосередкованого UGT1A9. У плазмі виявляються два основних та шість другорядних метаболітів регорафенібу. Основні циркулюючі в плазмі крові метаболіти регорафенібу М-2 (N-оксид) і М-5 (N-оксид і N-дезметил) мають фармакологічну активність і їх Css, подібні до Css регорафенібу. In vitro зв'язок М-2 та М-5 з білками крові вищий, ніж у регорафенібу і становить 99,8 та 99,95% відповідно. Метаболіти можуть бути відновлені та гідролізовані мікрофлорою ШКТ, при цьому можливе повторне всмоктування некон'югованого препарату та його метаболітів (печінково-кишкова рециркуляція). Виведення. T1/2 регорафенібу та його метаболіту М-2 з плазми становить від 20 до 30 годин після прийому внутрішньо. Середній T1/2 метаболіту М-5 становить близько 60 годин (40-100 годин). Приблизно 90% дози радіоактивного препарату виводяться протягом 12 днів після його прийому, при цьому 71% виводиться через кишечник (47% у вигляді вихідної сполуки і 24% у вигляді метаболітів) і близько 19% нирками у вигляді глюкуронідів. У рівноважному стані виведення глюкуронідів нирками зменшується та становить менше 10%. Вихідна сполука, виявлена в калових масах, може бути продуктом шлунково-кишкового розщеплення глюкуронідів або продуктом відновлення метаболіту М-2 (N-оксиду), або залишком неабсорбованого препарату. Лінійність/нелінійність. Системна дія регорафенібу при Css зростає пропорційно дозі при дозі до 60 мг і менш пропорційно при дозах понад 60 мг. Накопичення препарату при Css приблизно в 2 рази перевищує концентрацію у плазмі, яка відповідає T1/2 та частоті прийому ЛЗ. Після перорального прийому регорафенібу у дозі 160 мг його середня Css у плазмі досягає 3,9 мг/л (8,1 мкмоль). Співвідношення Cmax і Cmin регорафенібу у плазмі становить менше 2. Для обох метаболітів М-2 та М-5 властиве нелінійне накопичення у плазмі крові. Після одноразового прийому регорафенібу концентрації метаболітів М-2 та М-5 набагато нижчі, ніж у вихідної сполуки. Css М-2 і М-5 можна порівняти з Css регорафенібу. Фармакокінетика у різних груп пацієнтів Порушення функції печінки. У пацієнтів з легким (клас А за класифікацією Чайлд-Пью) або помірним (клас В за класифікацією Чайлд-Пью) ступенем печінкової недостатності, фармакокінетичні параметри регорафенібу були такими ж, як у пацієнтів з нормальною функцією печінки. У пацієнтів з тяжким ступенем печінкової недостатності (клас З класифікації Чайлд-П'ю) фармакокінетика регорафенібу не вивчена. Оскільки печінка має велике значення у виведенні регорафенібу, у пацієнтів із тяжким порушенням функції печінки можливе посилення дії препарату. Порушення функції нирок. У пацієнтів з легким та середнім ступенем ниркової недостатності експозиція регорафенібу та його метаболітів М-2 та М-5 у рівноважному стані є такою самою, як у пацієнтів з нормальною функцією нирок. У пацієнтів з тяжким ступенем ниркової недостатності або термінальною стадією ниркової недостатності фармакокінетика регорафенібу не вивчена. Літній вік. Вплив віку на фармакокінетику регорафенібу у пацієнтів віком від 29 до 85 років не виявлено. Підлога. Не виявлено відмінностей у фармакокінетиці регорафенібу залежно від статі. Етнічна приналежність. Не виявлено відмінностей у фармакокінетичних параметрах регорафенібу залежно від приналежності до етнічної групи. Електрофізіологія серця/подовження QT. У пацієнтів з онкологічними захворюваннями не було виявлено подовження інтервалу QT у рівноважному стані при прийомі регорафенібу у дозі 160 мг.ФармакодинамікаМеханізм дії. Регорафеніб є інгібітором численних протеїнкіназ, включаючи кінази, що беруть участь в ангіогенезі пухлини (VEGFR -1,-2,-3, TIE2), онкогенезі (KIT, RET, RAF-1, BRAF, BRAFF600E), а також входять до складу мікро PDGFR, FGFR). Зокрема, регорафеніб інгібує мутантну кіназу KIT, ключовий онкогенний фактор у розвитку стромальних пухлин ШКТ. Завдяки цьому регорафеніб блокує проліферацію пухлинних клітин. У доклінічних дослідженнях було показано, що регорафеніб має виражену протипухлинну дію на широкому спектрі пухлинних моделей, включаючи колоректальний рак та гастроінтестинальні стромальні пухлини. Ефект препарату пов'язаний з його антиангіогенним та антипроліферативним впливом. Крім того, регорафеніб показує антиметастатичну дію in vivo. Основні метаболіти препарату в організмі людини (М-2 та М-5) за своєю ефективністю на моделях in vitro та in vivo можна порівняти з регорафенібом.Показання до застосуванняметастатичний колоректальний рак у пацієнтів, яким уже проводилася або не показана хіміотерапія фторпіримідиновими препаратами, терапія, спрямована проти судинного ендотеліального фактора росту (VEGF) та терапія, спрямована проти рецепторів епідермального фактора росту (EGFR) при дикому типі KRAS; неоперабельні або метастатичні гастроінтестинальні стромальні пухлини у пацієнтів при прогресуванні на терапії іматинібом та сунітінібом або непереносимості даного виду лікування.Протипоказання до застосуванняпідвищена чутливість до регорафенібу або будь-якого іншого компонента, що входить до складу препарату; тяжкий ступінь печінкової недостатності (клас З класифікації Чайлд-П'ю); тяжкий ступінь ниркової недостатності (досвід клінічного застосування відсутній); вагітність; період грудного вигодовування; дитячий вік до 18 років. З ОБЕРЕЖНІСТЮ Необхідно дотримуватись додаткової обережності при призначенні препарату в наступних ситуаціях: при порушеннях функції печінки легкого та середнього ступеня тяжкості; за наявності мутації KRAS у пухлини; за наявності факторів ризику кровотечі, а також при сумісному застосуванні з антикоагулянтами та іншими препаратами, що підвищують ризик кровотеч; при ішемічній хворобі серця.Вагітність та лактаціяЖінок репродуктивного віку необхідно поінформувати про небезпеку препарату Стіварга для плода. Під час лікування та протягом 8 тижнів після терапії препаратом Стіварга® жінки та чоловіки репродуктивного віку повинні застосовувати надійні методи контрацепції. Дані щодо застосування препарату Стіварга® у вагітних жінок відсутні. Враховуючи механізм дії регорафенібу, можливий негативний вплив препарату Стіварга на плід. Дослідження на тваринах продемонстрували репродуктивну токсичність регорафенібу. Не встановлено, чи виділяються регорафеніб та його метаболіти з жіночим молоком. Дослідження на тваринах показали, що регорафеніб та його метаболіти виділяються з грудним молоком. Оскільки не можна виключити можливість негативного впливу регорафенібу на ріст та розвиток дітей раннього віку, слід припинити грудне вигодовування у період лікування препаратом Стіварга®. Фертильність. Не проводилося спеціальних досліджень застосування регорафенібу з метою оцінки його впливу на фертильність людини. У дослідженнях на тваринах спостерігалося зниження чоловічої та жіночої фертильності.Побічна діяЗагальний профіль безпеки препарату Стіварга® оцінюється на даних клінічних досліджень за участю понад 1200 пацієнтів, які отримували терапію у плацебо-контрольованих клінічних дослідженнях ІІІ фази. Ця група включала 500 пацієнтів з метастатичним колоректальним раком та 132 пацієнти з гастроінтестинальними стромальними пухлинами. У клінічних дослідженнях найчастішими небажаними реакціями (≥30% пацієнтів) були астенія/втома, долонно-підошовна еритродизестезія, діарея, зниження апетиту та споживання їжі, підвищення артеріального тиску, дисфонія, інфекції. Найбільш серйозними небажаними реакціями при прийомі препарату Стіварга були ураження печінки, кровотечі, проходження ШКТ. Наведені нижче небажані явища, зазначені при застосуванні препарату Стіварга® під час клінічних досліджень, розподілені за частотою виникнення відповідно до наступної градації: дуже часто (≥1/10), часто (від ≥1/100 до Для класифікації та опису конкретної реакції, її синонімів та пов'язаних з нею станів, використовується найбільш відповідний термін із MedDRA. У кожній частотній групі небажані явища представлені порядку зменшення їх значимості. З боку крові та лімфатичної системи: дуже часто – тромбоцитопенія, анемія; часто – лейкопенія. З боку серця та судин: дуже часто – кровотечі1, підвищення артеріального тиску; нечасто інфаркт міокарда, ішемія міокарда, гіпертонічний криз. З боку дихальної системи, органів грудної клітки та середостіння: дуже часто – дисфонія. З боку шкіри та підшкірних тканин: дуже часто – долонно-підошовна еритродизестезія, висипання на шкірі, алопеція; часто – сухість шкіри, ексфоліативний дерматит; нечасто – ураження нігтів, мультиформна еритема; рідко – синдром Стівенса-Джонсона, токсичний епідермальний некроліз. З боку шлунково-кишкового тракту: дуже часто – діарея, стоматит, блювання, нудота; часто - порушення смаку, сухість слизової оболонки порожнини рота, гастроезофагеальний рефлюкс, гастроентерит; нечасто - прорив ШКТ1, нориць ШКТ. З боку печінки та жовчовивідних шляхів: дуже часто – гіпербілірубіємія; часто – підвищення активності трансаміназ; нечасто - тяжке порушення функції печінки ^ 1,2. З боку нервової системи: дуже часто – головний біль; часто - тремор; рідко – синдром задньої оборотної енцефалопатії. З боку скелетно-м'язової та сполучної тканини: часто – м'язово-скелетна ригідність. З боку нирок та сечовивідних шляхів: часто – протеїнурія. З боку ендокринної системи: часто – гіпотиреоз. З боку обміну речовин та харчування: дуже часто – зниження апетиту та споживання їжі; часто - гіпокаліємія, гіпофосфатемія, гіпокальціємія, гіпонатріємія, гіпомагніємія, гіперурикемія. Лабораторні та інструментальні дані: дуже часто – зниження маси тіла; часто – збільшення активності амілази та ліпази, відхилення від нормального значення MHO. Доброякісні, злоякісні та неуточнені новоутворення (включаючи кісти та поліпи): рідко – кератоакантома/плоскоклітинний рак шкіри. Інфекційні та паразитарні захворювання: дуже часто – інфекції. Загальні розлади та порушення у місці введення: дуже часто – астенія/загальна слабкість, біль різної локалізації, підвищення температури тіла, запалення слизових оболонок. 1 Повідомлялося про смерть в результаті несприятливої реакції. 2 Відповідно до критеріїв Міжнародної робочої групи експертів з лікарського ураження печінки. Ураження печінки. Тяжке лікарське ураження печінки зі смертельним наслідком спостерігалося у трьох пацієнтів з більш ніж 1200 пацієнтів, які брали участь у всіх клінічних дослідженнях та отримували терапію препаратом Стіварга (0,25%). У двох із цих пацієнтів відзначалися метастази у печінці. Дисфункція печінки у цих пацієнтів почалася протягом перших двох місяців терапії та характеризувалася пошкодженням гепатоцитів з підвищенням активності трансаміназ >20×ВГН, що супроводжується збільшенням концентрації білірубіну. В результаті біопсії печінки у двох пацієнтів було виявлено некроз клітин печінки із запальним інфільтратом. Кровотечі. У двох плацебо-контрольованих дослідженнях III фази загальна частота кровотеч у пацієнтів, які отримували препарат Стіварга, склала 19,3%. Більшість випадків кровотечі мали легкий або помірний ступінь тяжкості (1-ий та 2-й ступінь: 16,9%). Найчастіше відзначалася носова кровотеча (7,6%). Літальні наслідки у пацієнтів, які отримували препарат Стіварга, відзначалися рідко (0,6%) і частіше були пов'язані з ураженням дихальної, травної та сечостатевої систем. інфекції. У двох плацебо-контрольованих дослідженнях ІІІ фази інфекційні захворювання найчастіше відзначалися у пацієнтів, які отримували лікування препаратом Стіварга®, порівняно з пацієнтами, які отримували плацебо (все ступеня: 31% порівняно з 14,4%). Найчастіше інфекції у пацієнтів, які отримували препарат Стіварга®, мали легкий або помірний ступінь виразності (1-й та 2-й ступінь: 22,9%) та включали інфекції сечовивідних шляхів (6,8%), назофарингіт (4,2%). , а також кандидоз шкіри та слизових та системний мікоз (2,4%). Не спостерігалися відмінності щодо частоти летальних випадків у зв'язку з розвитком інфекції у пацієнтів, які отримували препарат Стіварга® (0,6%) та у пацієнтів, які отримували плацебо (0,6%). Долонно-підошовна еритродизестезія. У плацебо-контрольованому дослідженні III фази загальна частота виникнення долонно-підошовної еритродизестезії у пацієнтів з метастатичним колоректальним раком, які приймали препарат Стіварга, склала 45,2% і у пацієнтів, які отримують плацебо – 7,1%. У плацебо-контрольованому дослідженні III фази у пацієнтів з гастроінтестинальними стромальними пухлинами загальна частота виникнення долонно-підошовної еритродизестезії склала 66,7% – у пацієнтів, які отримували терапію препаратом Стіварга®, та 15,2% – у пацієнтів, які одержували. В обох дослідженнях більшість випадків долонно-підошовної еритродизестезії у пацієнтів, які отримували препарат Стіварга® відзначалося під час першого циклу лікування та мало легкий або середній ступінь тяжкості (1-ий та 2-й ступеня: 28,6% у пацієнтів – з метастатичним колоректальним раком та 44,7% – у пацієнтів з гастроінтестинальними стромальними пухлинами). Частота виникнення долонно-підошовної еритродизестезії 3-го ступеня склала 16,6% у пацієнтів з метастатичним колоректальним раком та 22% у пацієнтів з гастроінтестинальними стромальними пухлинами. Підвищення артеріального тиску. У плацебо-контрольованому дослідженні III фази у пацієнтів з метастатичним колоректальним раком загальна частота випадків підвищення АТ становила 30,4% у пацієнтів, які приймали препарат Стіварга®, та 7,9% у пацієнтів, які приймали плацебо. У плацебо-контрольованому дослідженні Ш фази у пацієнтів з гастроінтестинальними стромальними пухлинами загальна частота випадків підвищення АТ становила 59,1% – у пацієнтів, які отримували препарат Стіварга®, та 27,3% – у пацієнтів, які отримували плацебо. В обох дослідженнях більшість випадків підвищення артеріального тиску у пацієнтів, які отримували препарат Стіварга®, були зареєстровані протягом першого циклу лікування. При цьому випадки підвищення АТ мали легкий та помірний ступінь тяжкості (1-й та 2-й ступінь: 22,8% - у пацієнтів з метастатичним колоректальним раком та 31,1% – у пацієнтів із гастроінтестинальними стромальними пухлинами). Частота випадків підвищення АТ 2-го ступеня склала 7,6% (у пацієнтів з колоректальним раком) та 27,3% (у пацієнтів з гастроінтестинальними стромальними пухлинами). Було зареєстровано один випадок підвищення АТ 4-го ступеня у пацієнта з гастроінтестинальною стромальною пухлиною. Протеїнурія. У плацебо-контрольованому дослідженні III фази серед пацієнтів з метастатичним колоректальним раком частота випадків протеїнурії, пов'язаної з лікуванням, склала 7,4% у пацієнтів, які отримували терапію препаратом Стіварга®, порівняно з 2,4% у пацієнтів, які приймали плацебо. Після розвитку протеїнурії у 40,5% пацієнтів із групи препарату Стіварга® та 66,7% пацієнтів із групи плацебо стан не повернувся до вихідного значення. У плацебо-контрольованому дослідженні III фази серед пацієнтів з гастроінтестинальними стромальними пухлинами загальна частота випадків протеїнурії склала 6,8% у пацієнтів, які отримують терапію препаратом Стіварга®, порівняно з 1,5% у пацієнтів, які приймали плацебо. З боку серця та судин. У всіх клінічних дослідженнях, що проводилися, небажані явища у вигляді порушень з боку серця (все ступеня) частіше реєструвалися (20,5 щодо 10,4%) у пацієнтів, які отримували терапію препаратом Стіварга®, у віці 75 років або старше (N=78), ніж у пацієнтів, які отримували терапію препаратом Стіварга®, віком до 75 років (N=995). Лабораторні та інструментальні дані. У двох плацебо-контрольованих дослідженнях III фази у 26,1% пацієнтів, які отримували терапію препаратом Стіварга®, і у 15,1% пацієнтів, які отримували плацебо, концентрація ТТГ була вищою за ВГН. Значення ТТГ, що в 4 рази перевищують ВГН, були зареєстровані у 6,9% пацієнтів, які отримували терапію препаратом Стіварга®, та у 0,7% пацієнтів, які приймали плацебо. Концентрація вільного трийодтироніну (Т3 вільний) менша від нижньої межі норми відзначалася у 25,6% пацієнтів, які отримують терапію Стіварга®, та у 20,9% пацієнтів, які отримують плацебо. Концентрація вільного тироксину (Т4 вільний) менша від нижньої межі норми відзначалася у 8% пацієнтів у групі терапії препаратом Стіварга® та у 6,6% пацієнтів із групи плацебо. Загалом, приблизно у 7% пацієнтів, які отримують терапію препаратом Стіварга®, розвинувся гіпотиреоз,що вимагає застосування замісної гормонотерапії.Взаємодія з лікарськими засобамиФармакокінетичні взаємодії Індуктори СУР3А4/інгібітори CYP3A4 та UGT1А9. In vitro було показано, що регорафеніб метаболізується цитохромом CYP3A4 та УДФ-ГТ (UGT1A9). Застосування кетоконазолу (400 мг протягом 18 днів) — сильного інгібітору ізоферменту CYP3A4 — у поєднанні з однократним прийомом регорафенібу (160 мг на 5-й день) призводило до збільшення середньої дії (AUC) регорафенібу приблизно на 33% і зниження метаболітів, М-2 (N-оксид) та М-5 (N-оксид та N-дезметил) приблизно на 90%. Не рекомендується застосовувати препарат Стиварга® разом з сильними інгібіторами CYP3A4 (наприклад кларитроміцин, грейпфрутовий сік, ітраконазол, кетоконазол, позаконазол, телитроміцин та вориконазол), оскільки їх вплив на вплив регорафенібу в стабільному стані. не вивчалося. Не рекомендується застосовувати сильні інгібітори UGT1A9 (наприклад, мефенамінова кислота, дифлунізал та ніфлумова кислота) під час терапії регорафенібом, оскільки їх вплив на експозицію регорафенібу та його метаболітів у рівноважному стані не вивчався. Застосування рифампіну (600 мг протягом 9 днів) – сильного індуктора CYP3A4 – у поєднанні з одноразовим прийомом регорафенібу (160 мг на 7-й день) призводило до зниження середньої дії (AUC) регорафенібу приблизно на 50%, збільшення середнього впливу активного мета. -5 у 3-4 рази, при цьому не відзначалося зміни експозиції активного метаболіту М-2. Інші сильні індуктори CYP3A4 (наприклад, фенітоїн, карбамазепін, фенобарбітал) можуть збільшувати метаболізм регорафенібу. Не рекомендується застосовувати препарат Стіварга разом з сильними індукторами CYP3A4 або підбирати ЛЗ, які не впливають на CYP3A4 або індукують його мінімальною мірою. Субстрати UGT1A1 та UGT1A9. In vitro було показано, що регорафеніб, як і його активний метаболіт М-2, пригнічує глюкуронізацію під дією UGT1А1 і UGT1A9, тоді як метаболіт М-5 пригнічує UGT1A1 тільки в концентраціях, які досягаються в рівноважному стані in vivo. Застосування регорафенібу з подальшою 5-денною перервою перед призначенням іринотекану призводило до збільшення середньої дії (AUC) SN-38-субстрату UGT1A1 та активного метаболіту іринотекану приблизно на 44%. Також відзначалося збільшення AUC іринотекану приблизно на 28%. Ці дані показують, що комбіноване застосування регорафенібу може збільшувати системну експозицію субстратів UGT1A1 та UGT1A9. Субстрати білка резистентності раку молочної залози (BCRP) та Р-глікопротеїну. In vitro було показано, що регорафеніб (IC50 близько 40-70 нмоль) та його метаболіти М-2 (IC50 390 нмоль) та М-5 (IC50 150 нмоль) є інгібіторами білка резистентності раку молочної залози BCRP (breast cancer). Регорафеніб (IC50 близько 2 мкмоль) та його метаболіт М-2 (IC50 1,5 мкмоль) пригнічують Р-глікопротеїн. Комбіноване застосування з регорафенібом може підвищувати концентрацію у плазмі супутніх субстратів BCRP (наприклад, метотрексат) або субстратів Р-глікопротеїну (наприклад, дигоксин). Інгібітори Р-глікопротеїну та BCRP/стимулятори Р-глікопротеїну та BCRP. Дослідження in vitro показують, що метаболіти регорафенібу М-2 та М-5 є субстратами Р-глікопротеїну та BCRP. Інгібітори та стимулятори BCRP та Р-глікопротеїну можуть перешкоджати експозиції М-2 та М-5. Клінічна значимість даних результатів досліджень невідома. Селективні субстрати ізоформи CYP. In vitro було показано, що регорафеніб є конкурентоспроможним інгібітором цитохромів CYP2C8, CYP2C9, CYP2B6 у концентраціях, які досягаються in vivo у стабільному стані (Cmax у плазмі 8,1 мкмоль). In vitro інгібуюча дія щодо CYP3A4 та CYP2C19 менш виражена. Було проведено дослідження з метою оцінки впливу прийому регорафенібу у дозі 160 мг протягом 14 днів на фармакокінетику маркерних субстратів CYP2C8 (розиглітазон), CYP2C9 (варфарин), CYP2C19 (омепразол) та CYP3A4 (мідазолам). Фармакокінетичні дані показують, що регорафеніб можна застосовувати спільно з субстратами CYP2C8, CYP2C9, CYP3A4 та CYP2C19. При цьому не наголошується на клінічно значущій взаємодії між лікарськими препаратами. Антибіотики. Профіль концентрація-час показує, що регорафеніб та його метаболіти можуть піддаватися печінково-кишковій циркуляції. Комбіноване застосування антибіотиків, що впливають на флору ШКТ, може порушити печінково-кишкову циркуляцію регорафенібу та призвести до зменшення його експозиції. Клінічна значимість цієї взаємодії невідома, але може бути причиною зниження ефективності регорафенібу. Комплексоутворюючі сполуки солей жовчних кислот. Існує ймовірність, що регорафеніб та його метаболіти М-2 та М-5 можуть піддаватися печінково-кишковій циркуляції (див. «Фармакокінетика). Комплексоутворюючі сполуки солей жовчних кислот, такі як холестирамін та холестагель можуть взаємодіяти з регорафенібом, утворюючи нерозчинні комплекси, що впливають на абсорбцію (або реабсорбцію), що потенційно може призвести до зниження експозиції. Клінічне значення даних потенційних взаємодій невідоме, але може призвести до зниження ефективності регорафенібу.Спосіб застосування та дозиВсередину таблетки слід ковтати повністю, запиваючи водою. Препарат Стіварга повинен призначатися тільки лікарем, який має досвід протипухлинної терапії. Рекомендована добова доза препарату Стіварга становить 160 мг (4 табл. по 40 мг). Препарат призначається 1 раз на день протягом 3 тижнів. Наступного тижня (4-й тиждень від початку лікування) слідує перерва в прийомі препарату. Період, тривалістю 4 тижні від початку прийому, є одним курсом лікування препаратом Стіварга®. Таблетки приймають щодня (1 раз на добу) в один і той же час після їди, що містить низьке ( Якщо черговий прийом препарату пропущений, пацієнт повинен прийняти таблетку того ж дня, щойно про це згадає. Не слід приймати подвійну дозу препарату протягом одного дня, щоб компенсувати пропущений прийом. У разі блювання після прийому препарату Стіварга додаткову таблетку приймати не слід. Лікування продовжують доти, доки зберігається клінічна ефективність препарату або до появи його неприйнятної токсичної дії. Корекція дози Індивідуальна переносимість та безпека лікування може вимагати тимчасового припинення терапії та/або зменшення дози препарату Стіварга®. Коригування дози на кожному етапі зниження дози становить 40 мг (1 табл.). Найменша рекомендована доза препарату Стіварга становить 80 мг на добу. Максимальна добова доза становить 160 мг. Рекомендації щодо корекції дози препарату Стіварга® при розвитку долонно-підошовної еритродизестезії Ступінь шкірної токсичності Епізоди шкірної токсичності Рекомендації щодо корекції дози препарату Стіварга ® 1-й ступінь Будь-хто Лікування препаратом Стіварга ® продовжити в тій же дозі та негайно розпочати підтримуючу симптоматичну терапію 2-й ступінь 1-й епізод Зменшити дозу препарату Стіварга на 40 мг (1 табл.) і негайно розпочати підтримуючу терапію У разі відсутності покращення протягом 7 днів, призупинити терапію препаратом Стіварга® доти , доки шкірна токсичність не знизиться до ступеня 0–1 Повторне підвищення дози препарату проводять за рекомендацією лікаря Відсутність зменшення інтенсивності шкірної симптоматики протягом 7 днів або 2-й епізод Зупинити терапію препаратом Стіварга ® доти, доки шкірна токсичність не знизиться до ступеня 0-1 При відновленні терапії знизити дозу препарату Стіварга на 40 мг (1 табл.) Повторне підвищення дози препарату проводять за рекомендацією лікаря 3-й епізод Зупинити терапію препаратом Стіварга ® доти, доки шкірна токсичність не знизиться до ступеня 0-1 При відновленні терапії знизити дозу препарату Стіварга на 40 мг (1 табл.) Повторне підвищення дози препарату проводять за рекомендацією лікаря 4-й епізод Терапію препаратом Стіварга слід припинити 3-й ступінь 1-й епізод Негайно розпочати підтримуючу терапію. Зупинити терапію препаратом Стіварга® мінімум на 7 днів і доти, доки шкірна токсичність не знизиться до ступеня 0–1 При відновленні терапії знизити дозу препарату Стіварга на 40 мг (1 табл.) Повторне підвищення дози препарату проводять за рекомендацією лікаря 2-й епізод Негайно розпочати підтримуючу терапію. Зупинити терапію препаратом Стіварга® мінімум на 7 днів і доти, доки шкірна токсичність не знизиться до ступеня 0–1 При відновленні терапії знизити дозу препарату Стіварга на 40 мг (1 табл.) 3-й епізод Терапію препаратом Стіварга слід припинити Рекомендації щодо корекції дози препарату Стіварга® при погіршенні біохімічних показників функції печінки Ступінь підвищення активності АЛТ та/або АСТ Епізоди Рекомендації щодо корекції дози препарату Стіварга ® ≤5 перевищень ВГН (максимально 2-й ступінь) Будь-хто Лікування препаратом Стіварга ® продовжують Проводити щотижневий моніторинг функції печінки доти, доки ступінь підвищення активності трансаміназ не повернеться до вихідного рівня або не становитиме <3 перевищення ВГН (1-ий ступінь). від >5 до ≤20 перевищень ВГН (третій ступінь) 1-й епізод Зупинити терапію препаратом Стіварга® . Проводити щотижневий моніторинг функції печінки доти, доки ступінь підвищення активності трансаміназ не повернеться до вихідного рівня або не становитиме <3 перевищення ВГН. Терапію відновити, якщо очікувана користь пацієнта перевищує ризик розвитку гепатотоксичності. Зменшити дозу препарату Стіварга на 40 мг (1 табл.) Проводити щотижневий моніторинг функції печінки протягом мінімум 4 тижнів. Повторний епізод Терапію препаратом Стіварга слід припинити >20 перевищень ВГН (4-й ступінь) Будь-хто Терапію препаратом Стіварга слід припинити >3 перевищень ВГН (2-й ступінь або вище) з перевищенням рівня білірубіну >2 Будь-хто Терапію препаратом Стіварга слід припинити Проводити щотижневий моніторинг функції печінки до стану дозволу або доти, доки показники функції печінки не повернуться до початкового рівня Виняток: пацієнти з синдромом Жільбера, у яких відмічено підвищення активності трансаміназ, повинні отримувати терапію відповідно до рекомендацій, наведених вище та що стосуються підвищення активності АЛТ та/або ACT Особливі групи пацієнтів Пацієнти із порушенням функції печінки. Печінка має велике значення у виведенні регорафенібу. Не було виявлено клінічно значимих відмінностей у впливі препарату Стіварга® у пацієнтів із середнім (клас А за класифікацією Чайлд-П'ю) та помірним (клас В за класифікацією Чайлд-Пью) порушенням функції печінки порівняно з пацієнтами з нормальною функцією печінки. Пацієнтам із середнім та помірним порушенням функції печінки корекція дози не потрібна. Рекомендується проводити моніторинг функції печінки на фоні терапії препаратом Стіварга у даної категорії пацієнтів. Не рекомендується лікування препаратом Стіварга® пацієнтів з тяжким порушенням функції печінки (клас С класифікації Чайлд-П'ю), оскільки застосування препарату у даної категорії пацієнтів не вивчене. Пацієнти із порушенням функції нирок. У клінічних дослідженнях не було значних відмінностей безпеки та ефективності препарату Стіварга® у пацієнтів з легким ступенем ниркової недостатності показник швидкості клубочкової фільтрації (рСКФ) — 60–89 мл/хв/1,73 м2 у порівнянні з пацієнтами з нормальною функцією нирок. Обмежені дані з фармакокінетики не виявили відмінностей в експозиції у пацієнтів із середнім ступенем ниркової недостатності (РСКФ 30-59 мл/хв/1,73 м2). Пацієнтам з легким та середнім ступенем ниркової недостатності зниження дози препарату не потрібне. Застосування препарату Стіварга® у пацієнтів з тяжким ступенем ниркової недостатності (РСКФ Діти. Безпека та ефективність призначення препарату Стіварга® у дітей та підлітків до 18 років не встановлена. Пацієнти похилого віку. У клінічних дослідженнях не було значних відмінностей безпеки та ефективності препарату Стіварга® у літніх (65 років і старше) пацієнтів у порівнянні з молодшими пацієнтами. Пацієнтам похилого віку корекція дози не потрібна. Підлога. У клінічних дослідженнях не відзначалося значних відмінностей безпеки та ефективності препарату Стіварга між пацієнтами чоловічої та жіночої статі. Корекція дози препарату в залежності від статі пацієнта не потрібна. Етнічна приналежність. У клінічних дослідженнях не було значних відмінностей безпеки та ефективності препарату Стіварга® у пацієнтів різних етнічних груп. Коригування дози препарату в залежності від етнічної приналежності пацієнта не потрібне.ПередозуванняСимптоми: у клінічних дослідженнях максимальна добова доза препарату Стіварга складала 220 мг. Найчастішими небажаними реакціями при даній дозі були небажані реакції з боку шкіри, дисфонія, діарея, запалення слизових оболонок, сухість слизової оболонки порожнини рота, зниження апетиту, підвищення АТ, загальна слабкість. Лікування: специфічний антидот не відомий. У разі передозування прийом препарату Стіварга слід припинити та застосовувати стандартну симптоматичну терапію. Пацієнт повинен бути під наглядом лікаря до стабілізації стану.Запобіжні заходи та особливі вказівкиДія на печінку У пацієнтів, які отримували лікування препаратом Стіварга, часто реєструвалися відхилення значень біохімічних показників функції печінки (АЛТ, ACT та білірубін). У невеликій частині пацієнтів відзначалися тяжкі порушення показників функції печінки (3-4-го ступеня тяжкості) та клінічно виражені порушення функції печінки (в т.ч. з летальним результатом). До початку лікування препаратом Стіварга рекомендується визначити показники функції печінки (ACT, АЛТ, білірубін). Протягом перших двох місяців терапії слід проводити контроль функції печінки щонайменше кожні 2 тижні, потім не рідше 1 разу на місяць, а також згідно з клінічними показниками. Оскільки регорафеніб є інгібітором УДФ-ГТ (UGTEA1), у пацієнтів із синдромом Жильбера можлива поява слабкої непрямої (некон'югованої) гіпербілірубінемії. Якщо у хворих, які отримують лікування препаратом Стіварга®, відзначається погіршення показників функції печінки, пов'язане з терапією (без явної альтернативної причини, наприклад механічної жовтяниці або прогресування основного захворювання), лікарю слід змінити дозу препарату та спостерігати за станом пацієнта. Печінка має велике значення у виведенні регорафенібу. При застосуванні препарату Стіварга® у пацієнтів з легким та помірним порушенням функції печінки слід проводити ретельний контроль за станом пацієнта. Не рекомендується застосування препарату Стіварга у пацієнтів з тяжким порушенням функції печінки (клас С за класифікацією Чайлд-П'ю), оскільки він не вивчений у даної категорії пацієнтів (можливе збільшення експозиції препарату). Пацієнти з пухлинами та мутаціями в гені KRAS У пацієнтів з мутаціями в гені KRAS спостерігалося значне поліпшення показників виживання без прогресування (ВБП) і було зареєстровано чисельно слабший вплив на загальне виживання (ВВ). Зважаючи на значну токсичність, пов'язану з терапією, лікарям рекомендують уважно оцінювати користь та ризик при призначенні регорафенібу пацієнтам з пухлинами, що мають мутації у гені KRAS. Кровотечі У хворих, які отримували препарат Стіварга, було зареєстровано підвищення частоти епізодів кровотеч, у деяких випадках з летальним результатом. За наявності факторів ризику кровотечі, а також при сумісному призначенні з антикоагулянтами (наприклад, варфарин, фенпрокумон) або іншими лікарськими засобами, що підвищують ризик кровотечі, слід контролювати показники коагулограми та загального аналізу крові. При появі тяжкої кровотечі, яка потребує екстреного медичного втручання, слід розглянути питання про припинення лікування препаратом Стіварга®. Ішемія міокарда та інфаркт міокарда При прийомі препарату Стіварга відзначалося збільшення частоти випадків ішемії міокарда та інфаркту міокарда. Пацієнти з нестабільною стенокардією або появою стенокардії (протягом 3 місяців до початку терапії препаратом Стіварга®), недавнім інфарктом міокарда (у період 6 місяців до початку терапії препаратом Стіварга®) та пацієнти з серцевою недостатністю 2 класу та вище за класифікацією Нью-Йоркської кардіологічної асоціації були виключені з клінічних досліджень. У пацієнтів з ІХС необхідно відстежувати клінічні ознаки та симптоми ішемії міокарда. При виникненні ішемії та/або інфаркту міокарда слід припинити терапію препаратом Стіварга до нормалізації стану. При прийнятті рішення щодо відновлення терапії лікар повинен оцінювати співвідношення користі від прийому препарату з потенційним ризиком у кожного окремого пацієнта. Якщо клінічні прояви ішемії зберігаються, відновлювати терапію годі було. Синдром оборотної задньої енцефалопатії У пацієнтів, які отримували препарат Стіварга, були зареєстровані випадки розвитку оборотної задньої енцефалопатії. Зворотна задня енцефалопатія виявлялася у вигляді судом, головного болю, зміни свідомості, порушення зору або кіркової сліпоти, іноді у поєднанні з артеріальною гіпертензією. Для підтвердження діагнозу пацієнтам слід провести томографію мозку. У разі розвитку оборотної задньої енцефалопатії слід припинити лікування препаратом Стіварга, проводити контроль АТ та підтримуючу терапію. Проведення і свищ ШКТ У пацієнтів, які отримували препарат Стіварга®, були зареєстровані випадки прокидання ШКТ та утворення свища ШКТ. Ці події були пов'язані з пухлинами у черевній порожнині. У разі прободіння ШКТ або утворення нориці терапію препаратом Стіварга слід припинити. Підвищення АТ На фоні терапії препаратом Стіварга було зареєстровано збільшення частоти підвищення АТ. Перед початком та під час лікування препаратом Стіварга® слід регулярно контролювати АТ та коригувати його підвищення відповідно до прийнятих стандартів лікування. У разі розвитку тяжкої або стійкої артеріальної гіпертензії, стійкої до адекватної антигіпертензивної терапії, лікар повинен тимчасово перервати терапію та/або знизити дозу препарату. У разі розвитку гіпертонічного кризу лікування препаратом Стіварга слід відмінити. Порушення загоєння ран У разі проведення великих хірургічних втручань рекомендується тимчасове припинення терапії препаратом Стіварга®, оскільки лікарські препарати, що мають антиангіогенні властивості, можуть пригнічувати або погіршувати загоєння ран. Рішення про відновлення терапії після хірургічних втручань має ґрунтуватися на клінічній оцінці адекватності загоєння рани. Шкірна токсичність Найчастішими небажаними реакціями при прийомі препарату Стіварга® були долонно-підошовна еритродизестезія та висипання. З метою профілактики розвитку долонно-підошовної еритродизестезії слід контролювати утворення мозолів та використовувати спеціальні вкладиші для взуття та рукавички для запобігання тиску на підошви та долоні. Для лікування долонно-підошовної еритродизестезії можна використовувати кератолітичні креми (наприклад, креми на основі сечовини, саліцилової кислоти або альфа-гідроксильної кислоти, які слід наносити тільки на уражені ділянки шкіри) та зволожуючі креми у великій кількості для полегшення симптомів. При необхідності тимчасово припиняють лікування та/або знижують дозу препарату Стіварга® або у тяжких або повторюваних випадках шкірних реакцій, терапію препаратом Стіварга® припиняють. Відхилення значень лабораторних показників При застосуванні препарату Стіварга було зареєстровано підвищення частоти електролітних порушень (включаючи гіпофосфатемію, гіпокальціємію, гіпонатріємію та гіпокаліємію) та порушень метаболізму (включаючи збільшення концентрації ТТГ, збільшення активності амілази). Відхилення від норми зазвичай мали легкий або помірний характер і не супроводжувалися клінічними проявами. У разі виникнення електролітних порушень або порушень метаболізму корекція дози або припинення терапії не потрібна. Під час терапії препаратом Стіварга® рекомендується контролювати біохімічні та метаболічні показники. При необхідності призначають замісну терапію відповідно до прийнятих стандартів лікування. У випадках стійких або рецидивуючих порушень слід розглянути можливість тимчасового припинення лікування або зниження дози.або повного припинення терапії препаратом Стіварга®. Інформація про деякі інгредієнти Добова доза регорафенібу 160 г містить 2427 ммоль (або 558 мг) натрію. На це слід звернути увагу пацієнтів, які дотримуються дієти, що контролює споживання натрію. Добова доза регорафенібу 160 г містить 1,68 мг лецитину (отриманий із сої). Системна токсичність Після повторного введення дози у мишей, щурів та собак спостерігалися небажані реакції з боку низки органів, насамперед нирок, печінки, травного тракту, щитовидної залози, лімфатичної/кровотворної системи, ендокринної системи, репродуктивної системи та шкіри. У 26-тижневому дослідженні токсичності при введенні повторних доз щурів спостерігалося невелике збільшення частоти випадків потовщення AV клапанів серця. Причиною цього явища може бути прискорення вікового фізіологічного процесу. Дані реакції спостерігалися при системних експозиціях, що знаходяться в діапазоні або нижче діапазону передбачуваної експозиції у людини (основано на порівнянні AUC). Зміни зубів і кісток, а також небажані явища в репродуктивній системі були найбільш виражені у молодих тварин, а також у молодих щурів, що вказує на потенційний ризик для дітей і підлітків. Тератогенність та ембріотоксичність Спеціальних досліджень впливу регорафенібу на фертильність не проводилися. Слід враховувати здатність регорафенібу надавати несприятливий вплив на репродуктивну систему чоловіків та жінок. У дослідженні на щурах і собаках після багаторазового застосування регорафенібу при експозиціях нижче за передбачувану експозицію у людини (при порівнянні AUC) спостерігалися морфологічні зміни в яєчках, яєчниках та матці. Спостережені зміни були оборотні лише частково. У дослідженні на кроликах при експозиції нижче за передбачувану експозицію у людини спостерігалася ембріотоксичність (при порівнянні AUC). В основному були виявлені порушення формування сечовидільної системи, серця та великих судин, кісток. Вплив на здатність керувати автомобілем, механізмами. Спеціальні дослідження не проводилися, проте при виникненні небажаних явищ, які можуть впливати на зазначені здібності, рекомендується уникати керування транспортними засобами та занять іншими потенційно небезпечними видами діяльності, що потребують підвищеної концентрації уваги та швидкості психомоторних реакцій (до зникнення цих симптомів).Умови відпустки з аптекЗа рецептомВідео на цю тему
Умови зберіганняУ холодильнику +2+8 градусівУмови відпустки з аптекБез рецептаВідео на цю тему.
Дозировка: 3 % Форма выпуска: мазь Упаковка: туба Производитель: Ретиноиды Завод-производитель: Ретиноиды(Россия) Действующее вещество: Диоксометилтетрагидропиримидин. . .
Склад, форма випуску та упаковкаAqua, PEG-12, Propylene Glycol, Glycerin, Cyclopentasiloxane, Niacinamide, Aesculus Hippocastanum (Horse Chestnut) Bark Extract (екстракт кінського каштану), Inonotus Obliquus (Mushroom) Extract (екстракт чаги), Gink Mentha Piperita (Peppermint) Oil (м'ятна олія), Acrylates/C10-30 Alkyl Acrylate Crosspolymer, Allantoin, Camphor, Caprylyl Glycol, Citric Acid, Disodium EDTA, Ethylparaben, Glucose, Lactic Acid, Menthol, Menthen ,Parfum, PEG-40 Hydrogenated Castor Oil, Phenoxyethanol, Potassium Sorbate, Sodium Benzoate, Triethanolamine, Citral, Citronellol, Geraniol, Limonene, LinaloolХарактеристикаГель для ніг Венотон від бренду Сто Рецептів Краси активної дії на основі кінських каштанів, чаги та м'ятної олії зменшує тяжкість та напругу в ногах, тонізує, створює ефект ніг, що відпочили. Сприяє підвищенню тонусу судин та вен, усуває симптоми проблем з ногами – почуття втоми, тяжкості, напруження та набряклості. Активні компоненти складу славляться своїми корисними властивостями у косметології: М'ята сприяє відновленню харчування шкіри, нормалізує роботу сальних залоз, стимулює кровообіг, сприяє розгладжуванню зморшок; ментол чудово охолоджує та освіжає шкіру, стимулює кровообіг та зміцнює судини, виводить токсини, заспокоює та знеболює подразнену шкіру, нормалізує роботу сальних залоз та підсушує шкіру, відбілює пігментні плями; ефірна олія м'яти має виражену антисептичну та ранозагоювальну дію, що ефективно при лікуванні вугрової висипки, грибку, інших різних шкірних захворювань. М'ята – відмінний компонент для засобів від втоми в м'язах, чудовий природний протимікробний та освіжаючий компонент. Кінський каштан посилює мікроциркуляцію в шкірному покриві, сприяє усуненню запалень шкіри, розсмоктування підшкірних крововиливів, поліпшення кольору шкіри; знімає та перешкоджає утворенню набряків у тканинах. Тепер тобі не страшні підбори та довгі продукти! Зроби гель для ніг Венотон від бренду Сто Рецептів Краси своїм вірним супутником у довгих прогулянках! Всі продукти бренду Сто рецептів краси готуються на 100% натуральній основі, компоненти якої зазначені у складі, за технологією холодного приготування (особлива холодна стадія додавання активних компонентів), яка дозволяє зберегти всю користь корисних компонентів рецепту. Вибери свій корисний рецепт від бренду Сто Рецептів Краси!ІнструкціяНанесіть гель на стопи і гомілку (знизу вгору), що масажують рухами до повного вбирання.Запобіжні заходи та особливі вказівкиВикористання в харчових цілях неприпустимоУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаСироп гомеопатичний - 100 р.: Активні компоненти: Pulsatilla (пульсатилла) C6 – 0,95г, Rumex crispus (румекс кріспус) C6 – 0,95г, Bryonia (бріонія) C3 – 0,95г, Ipeca (іпека) C3 – 0,95г, Spongia tosta (спонгія тоста) ) C3 - 0,95 г, Sticta pulmonaria (стикту пульмонарію) C3 - 0,95 г, Antimonium tartaricum (антимоніум тартарикум) C6 - 0,95 г, Myocarde (міокарде) C6 - 0,95 г, Coccus cacti (коккус , 95г, Drosera (дрозера) MT - 0,95г. Допоміжні компоненти: сироп Толу; сироп Полігала; карамель; бензойна кислота; етанол 96%; сироп сахарози – до 100 г. у флаконі темного скла 200 мл; у пачці картонної 1 флакон.ХарактеристикаГомеопатичний засіб.Показання до застосуванняСимптоматичне лікування кашлю різної етіології.Протипоказання до застосуванняПідвищена індивідуальна чутливість до окремих компонентів препарату.Вагітність та лактаціяПотрібна консультація лікаря. При застосуванні слід враховувати, що кожні 15 мл сиропу містять 0,206 г етанолу, кожні 5 мл сиропу містять 0,069 г етанолу.Побічна діяНа даний момент інформація про побічні дії препарату відсутня. У разі виникнення побічних ефектів слід звернутися до лікаря.Спосіб застосування та дозиДорослим: по 15 мл за допомогою мірного ковпачка 3-5 разів на день. Дітям: по 5 мл за допомогою мірного ковпачка 3-5 разів на день. Тривалість застосування погоджувати із лікарем.ПередозуванняВипадки передозування досі не були зареєстровані.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
ХарактеристикаГель для ясен СТОМАДЕНТ ZD рекомендований для догляду за проблемними яснами та слизовою оболонкою порожнини рота. Комплексна дія натуральних екстрактів прополісу, шавлії, липи, кори дуба і вівса, відомих своїми бактерицидним, в'язким, заспокійливим і пом'якшувальним властивостями, а також антисептичного компонента хлоргексидину біглюконату, допомагає прискорити процеси регенерації слизу. Гель також зменшує дискомфорт ясен від носіння брекетів та протезів, при прорізуванні зубів мудрості.ІнструкціяВранці та ввечері після чищення зубів нанести гель на ясна за допомогою ватної палички або чистим сухим пальцем, розподіливши його по всій поверхні ясен або локально. Для досягнення максимального ефекту після нанесення гелю не обполіскувати порожнину рота, не приймати їжу та рідину протягом 30 хвилин. З профілактичною метою наносити гель вранці та ввечері протягом 7-14 днів.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаРозчин - 1 мл: Діюча речовина: гесектидин – 1,00 мг; Допоміжні речовини: пропіленгліколь - 100,00 мг, полісорбат-20 - 10,00 мг, лимонної кислоти моногідрат - 0,40 мг, натрію сахаринат - 0,30 мг, рацементол - 0,15 мг, метилсаліцилат - 0,10 мг, барвник азорубін – 0,10 мг, етанол 96 % – 0,10 мл, вода – до 1,00 мл. По 200 мл у флакон темного скла, закупорений алюмінієвою кришкою з контролем першого розкриття, або пластиковою кришкою, що нагвинчується, з механізмом захисту від дітей, ущільнювачем і контролем першого розтину. По 1 флакон з інструкцією по застосуванню поміщають у картонну пачку.Опис лікарської формиПрозора рідина червоного кольору.Фармакотерапевтична групаАнтисептичний засіб.ФармакокінетикаГесектидин добре адгезується на слизовій оболонці і практично не всмоктується. Після одноразового застосування гесектидин виявляється на слизовій оболонці ротової порожнини протягом 65 годин. У зубних бляшках активні концентрації зберігаються протягом 10-14 годин після застосування.ФармакодинамікаАнтисептичний препарат для місцевого застосування в оториноларингології та стоматології. Протимікробна дія гесектидину пов'язана з придушенням окисних реакцій метаболізму мікробних клітин (антагоніст, тіаміну). Препарат має антибактеріальну дію щодо грамнегативних та грампозитивних бактерій, Pseudomonas aeruginosa та Proteus spp. та протигрибкову дію (у тому числі щодо грибів роду Candida). При концентрації 100 мг/мл досягається пригнічення збільшення більшості штамів бактерій. Розвитку стійкості немає. Гесектидин надає слабку аналгетичну дію на слизову оболонку.Показання до застосуванняЗапальні та інфекційні захворювання порожнини рота та глотки: ангіни (в т.ч. ангіни з ураженням бічних валиків, ангіна Плаута-Венсана), фарингіт, гінгівіт та кровоточивість ясен, періодонтопатії, стоматит, глосит, афтозні виразки з метою, профіл альвеол після видалення зубів, грибкові інфекції порожнини рота та глотки, особливо кандидозний стоматит, до та після операцій у порожнині рота та глотки, додаткова гігієна порожнини рота при загальних захворюваннях, усунення неприємного запаху з рота, особливо у разі пухлин порожнини рота, що руйнуються.Протипоказання до застосуванняДитячий вік віком до 5 років. Підвищена чутливість до будь-якого компонента препарату. Гіперчутливість, атрофічний фарингіт, вагітність (I триместр).Вагітність та лактаціяВідсутні достатні дані щодо проникнення гесектидину через плаценту та грудне молоко. Можливе використання препарату під час вагітності, якщо потенційна користь матері перевищує ризик для плода. За необхідності застосування препарату в період лактації необхідно вирішити питання про припинення грудного вигодовування.Побічна діяПечіння, подразнення та помірна сухість слизової оболонки порожнини рота, алергічні реакції. При тривалому застосуванні можлива зміна смакових відчуттів. Після припинення застосування препарату побічні ефекти зникають.Взаємодія з лікарськими засобамиЧи не описано.Спосіб застосування та дозиМісцево. Для полоскання необхідно користуватися нерозведеним препаратом. Розчин не можна ковтати. Потрібно виплюнути розчин після полоскання. При захворюваннях порожнини рота у дорослих та дітей віком від 5 років полоскати порожнину рота 10-15 мл (одна столова ложка) нерозведеного розчину препарату протягом 30 секунд. При захворюваннях горла у дорослих та дітей віком від 5 років застосовують полоскання такою ж кількістю нерозведеного розчину препарату протягом 30 секунд. При лікуванні захворювань ротової порожнини препарат можна наносити за допомогою тампона. Застосовують 2 рази на добу (переважно вранці та ввечері), після їди. Тривалість застосування препарату визначається індивідуально. Якщо симптоми захворювання не зникають після 5 днів застосування препарату та/або супроводжуються підвищеною температурою, слід звернутися до лікаря.ПередозуванняПри випадковому проковтуванні великих кількостей препарату можлива поява нудоти та блювоти! При передозуванні необхідно промити шлунок та призначити симптоматичну терапію.Запобіжні заходи та особливі вказівкиНе використовувати препарат у категорії пацієнтів, які самостійно не можуть проводити цю процедуру (полоскання). Вплив на здатність до керування автотранспортом та управління механізмами Препарат не впливає на здатність керувати транспортними засобами або працювати з механізмами. Препарат містить 10% етанолу (спирту етилового 96%). Препарат слід приймати не пізніше ніж за 30 хв до початку керування транспортним засобом.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаДля отримання 100 г препарату необхідно: ромашки квіток (Matricaria chamomilla L.) – 13,0 г, дуба кори (Quercus robur L.) – 13,0 г, шавлії листя (Salvia officinalis L.) – 13,0 г, арніки трави (Arnica montana L.) – 6,5 г, лепехи кореневищ (Acorns calamus L.) – 6,5 г, м'яти перцевої трави (Menta piperita L.) – 6,5 г, чебрецю звичайної трави (Thymus vulgaris L.). ) -6,5 р. По 50 мл і 100 мл у флакони оранжевого гідролітичного скла III типу з поліетиленовим обмежувачем витікання, закупорені поліетиленовими кришками, що загвинчуються, з контролем першого розтину. Кожен флакон разом з інструкцією із застосування та поліпропіленовим мірним стаканчиком поміщений у картонну пачку.Опис лікарської формиРідина коричневого кольору із характерним запахом. У процесі зберігання можливе утворення невеликого помутніння та осаду.Фармакотерапевтична групаПротизапальний засіб рослинного походження.ФармакодинамікаПрепарат має протизапальну, в'яжучу та антисептичну дію.Показання до застосуванняЗастосовують для полоскань при запальних захворюваннях ротової порожнини: стоматит, гінгівіт, пародонтит та ін.Протипоказання до застосуванняПідвищена чутливість до компонентів препарату; дитячий вік (до 12 років).Вагітність та лактаціяЗастосування препарату під час вагітності та лактації можливе лише за призначенням лікаря.Побічна діяМожливі алергічні реакції.Взаємодія з лікарськими засобамиЧи не описано.Спосіб застосування та дози7,5 мл препарату розвести у 50 мл (1/4 склянки) теплої кип'яченої води. Отриманий розчин використовуватиме полоскань порожнини рота. Процедуру повторювати 3-4 десь у день. Курс лікування 10 – 15 днів. Проведення повторного курсу лікування можливе після консультації з лікарем. Для дозування використовувати мірну склянку, вкладену в упаковку. Перед вживанням збовтувати.ПередозуванняДо цього часу випадки передозування не описані.Запобіжні заходи та особливі вказівкиПрепарат містить 60 – 70% (об'ємних) етанолу.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаДля отримання 100 г препарату необхідно: ромашки квіток (Matricaria chamomilla L.) – 13,0 г, дуба кори (Quercus robur L.) – 13,0 г, шавлії листя (Salvia officinalis L.) – 13,0 г, арніки трави (Arnica montana L.) – 6,5 г, лепехи кореневищ (Acorns calamus L.) – 6,5 г, м'яти перцевої трави (Menta piperita L.) – 6,5 г, чебрецю звичайної трави (Thymus vulgaris L.). ) -6,5 р. По 50 мл і 100 мл у флакони оранжевого гідролітичного скла III типу з поліетиленовим обмежувачем витікання, закупорені поліетиленовими кришками, що загвинчуються, з контролем першого розтину. Кожен флакон разом з інструкцією із застосування та поліпропіленовим мірним стаканчиком поміщений у картонну пачку.Опис лікарської формиРідина коричневого кольору із характерним запахом. У процесі зберігання можливе утворення невеликого помутніння та осаду.Фармакотерапевтична групаПротизапальний засіб рослинного походження.ФармакодинамікаПрепарат має протизапальну, в'яжучу та антисептичну дію.Показання до застосуванняЗастосовують для полоскань при запальних захворюваннях ротової порожнини: стоматит, гінгівіт, пародонтит та ін.Протипоказання до застосуванняПідвищена чутливість до компонентів препарату; дитячий вік (до 12 років).Вагітність та лактаціяЗастосування препарату під час вагітності та лактації можливе лише за призначенням лікаря.Побічна діяМожливі алергічні реакції.Взаємодія з лікарськими засобамиЧи не описано.Спосіб застосування та дози7,5 мл препарату розвести у 50 мл (1/4 склянки) теплої кип'яченої води. Отриманий розчин використовуватиме полоскань порожнини рота. Процедуру повторювати 3-4 десь у день. Курс лікування 10 – 15 днів. Проведення повторного курсу лікування можливе після консультації з лікарем. Для дозування використовувати мірну склянку, вкладену в упаковку. Перед вживанням збовтувати.ПередозуванняДо цього часу випадки передозування не описані.Запобіжні заходи та особливі вказівкиПрепарат містить 60 – 70% (об'ємних) етанолу.Умови відпустки з аптекБез рецептаВідео на цю тему
Фасування: N1 Форма випуску: рідкий екстракт Упакування: фл. Виробник: Фітофарм Кленка АТ Завод-виробник: Фітофарм Кленка АТ(Польща). .
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
Склад, форма випуску та упаковкаРозчин – 100 гр. : Дуба черешкового кори 11,0 г; Шавлія лікарського листя 11,0 г; Ромашки аптечної квітки 10,0 г; Звіробою продірявленої трави 6,5 г; чебрецю звичайної трави 5,5 г; М'яти перцевого листя 5,5 г; Календули лікарської квітки 5,0 г; Горіхи чорного плодів 4,6 г; Ялиця сибірської хвої з пагонами 4,0 г; Горіхи чорного навколоплідників 1,08 г; Горіхи чорного листя 0,82 г; Сорбат калію (консервант) 0,455 г; Вода очищена qs Екстракт рідкий для місцевого застосування. По 100 мл у флакони оранжевого гідролітичного скла III типу поліетиленовим обмежувачем витікання, закупорені поліетиленовими кришками, що загвинчуються, з контролем першого розтину.
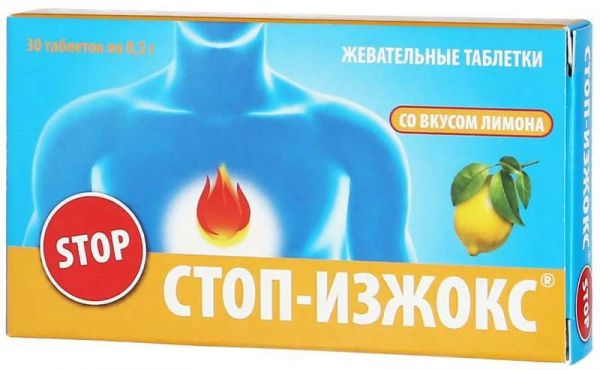
Склад, форма випуску та упаковкаКальцій карбонат, магній карбонат, цукроза, ізомальтит Е953, стеоринова кислота Е570, діоксид кремнію Е551, кальцію стеарат Е470, ароматизатор харчовий «Лимон» Упаковка: 15 таблеток по 0,55 г в індивідуальній упаковці.Характеристика"Стоп-Ізжокс-жувальні таблетки зі смаком лимона" (Біологічно активна добавка (БАД) до їжі) забезпечують швидку і тривалу нейтралізацію надлишкової соляної кислоти шлункового соку, тим самим чинить захисну дію на слизову оболонку шлунка.РекомендуєтьсяДодаткове джерело кальцію; Печії, відрижки, періодичні болі в області шлунка; Почуття переповнення і тяжкості в епігастральній області;Протипоказання до застосуванняІндивідуальна непереносимість компонентівСпосіб застосування та дозиДорослим по 1 жувальній пігулці 2 рази на день під час їжі.Запобіжні заходи та особливі вказівкиПеред застосуванням проконсультуйтеся зі спеціалістом.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаКальцій карбонат, магній карбонат, цукроза, ізомальтит Е953, стеоринова кислота Е570, діоксид кремнію Е551, кальцію стеарат Е470, ароматизатор харчовий. Упаковка: 30 пігулок по 0,55 г в індивідуальній упаковці.Характеристика"Стоп-Ізжокс-жувальні таблетки (біологічно активна добавка-БАД) до їжі забезпечують швидку і тривалу нейтралізацію надлишкової соляної кислоти шлункового соку, тим самим надає захисну дію на слизову оболонку шлунка.РекомендуєтьсяДодаткове джерело кальцію; Печії, відрижки, періодичні болі в області шлунка; Почуття переповнення і тяжкості в епігастральній області;Протипоказання до застосуванняІндивідуальна непереносимість компонентівСпосіб застосування та дозиДорослим по 1 жувальній пігулці 2 рази на день під час їжі.Запобіжні заходи та особливі вказівкиПеред застосуванням проконсультуйтеся зі спеціалістом.Умови відпустки з аптекБез рецептаВідео на цю тему
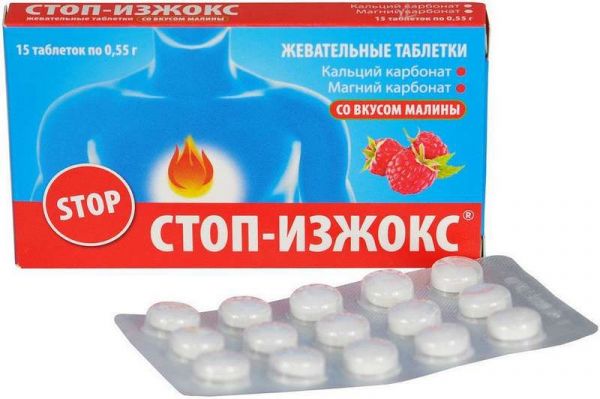
Склад, форма випуску та упаковкаКальцій карбонат, магній карбонат, цукроза, ізомальтит Е953, стеоринова кислота Е570, діоксид кремнію Е551, кальцію стеарат Е470, ароматизатор харчовий. Упаковка: 15 таблеток по 0,55 г в індивідуальній упаковці.Характеристика"Стоп-Ізжокс-жувальні таблетки (біологічно активна добавка-БАД) до їжі забезпечують швидку і тривалу нейтралізацію надлишкової соляної кислоти шлункового соку, тим самим надає захисну дію на слизову оболонку шлунка.РекомендуєтьсяДодаткове джерело кальцію; Печії, відрижки, періодичні болі в області шлунка; Почуття переповнення і тяжкості в епігастральній області;Протипоказання до застосуванняІндивідуальна непереносимість компонентівСпосіб застосування та дозиДорослим по 1 жувальній пігулці 2 рази на день під час їжі.Запобіжні заходи та особливі вказівкиПеред застосуванням проконсультуйтеся зі спеціалістом.Умови відпустки з аптекБез рецептаВідео на цю тему
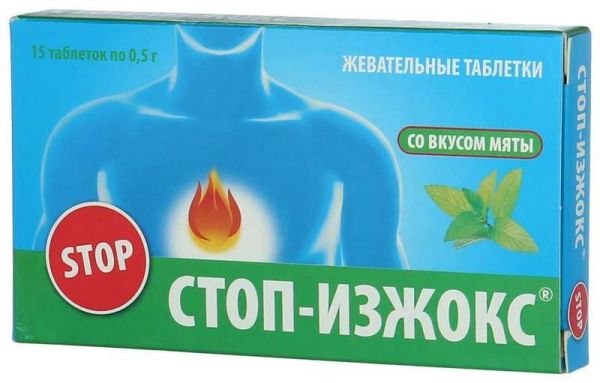
Склад, форма випуску та упаковкаКальцій карбонат, магній карбонат, цукроза, ізомальтит Е953, стеоринова кислота Е570, діоксид кремнію Е551, кальцію стеарат Е470, ароматизатор харчовий. Упаковка: 15 таблеток по 0,55 г в індивідуальній упаковці.Характеристика"Стоп-Ізжокс-жувальні таблетки (біологічно активна добавка-БАД) до їжі забезпечують швидку і тривалу нейтралізацію надлишкової соляної кислоти шлункового соку, тим самим надає захисну дію на слизову оболонку шлунка.РекомендуєтьсяДодаткове джерело кальцію; Печії, відрижки, періодичні болі в області шлунка; Почуття переповнення і тяжкості в епігастральній області;Протипоказання до застосуванняІндивідуальна непереносимість компонентівСпосіб застосування та дозиДорослим по 1 жувальній пігулці 2 рази на день під час їжі.Запобіжні заходи та особливі вказівкиПеред застосуванням проконсультуйтеся зі спеціалістом.Умови відпустки з аптекБез рецептаВідео на цю тему
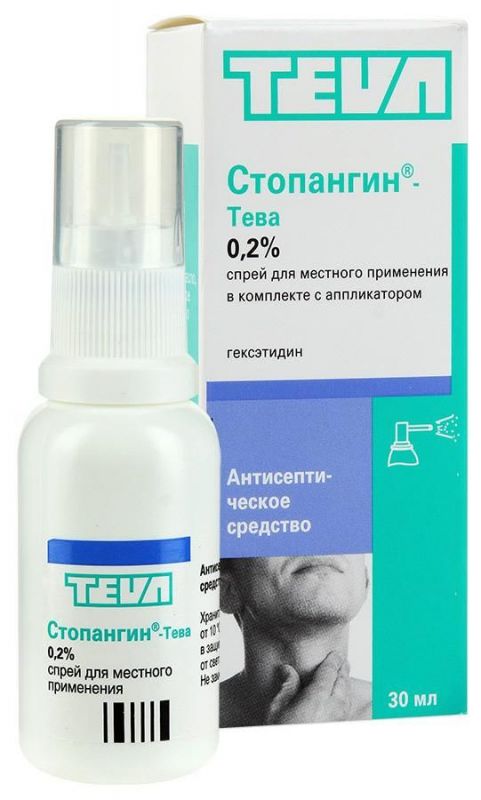
Склад, форма випуску та упаковка1 флакон містить: Активна речовина: гесектидин – 0,0577 г; допоміжні речовини: метилсаліцилат; анісове ефірне масло; евкаліптова ефірна олія; ефірна олія квіток апельсина; сассафрасне ефірне масло; ефірна олія м'яти перцевої; лівоментол; натрію сахаринату моногідрат; гліцерол 85%; етанол 96%.Фармакотерапевтична групаСтопангін – антисептичний засіб для місцевого застосування. Має також протигрибкову активність і аналгетичні властивості при нанесенні на слизову оболонку. Стопангін має обволікаючу дію. Ефект триває 10 – 12 годин.Показання до застосуваннязапальні захворювання порожнини рота та гортані (ангіна, тонзиліт, фарингіт, стоматит, афти, глосит, пародонтоз та пародонтопатії, інфікування альвеол); грибкові захворювання порожнини рота та гортані (молочниця); до та після оперативних втручань, а також травми порожнини рота та гортані; як допоміжний засіб при комплексному лікуванні ангін.Протипоказання до застосуванняПри сухому фарингіті атрофічного типу, дітям до 8 років, а також під час вагітності (1 триместр).Вагітність та лактаціяСтопангін протипоказаний при вагітності, лактації та дітям до 8 років.Побічна діяМісцеві реакції: можливе відчуття печіння слизової оболонки ротової порожнини (швидко мимовільно проходить). Інші: у виняткових випадках у пацієнтів із підвищеною чутливістю можливі алергічні реакції; при випадковому проковтуванні препарату при полосканні можлива нудота (проходить мимоволі). У разі появи незвичайних реакцій пацієнт повинен порадитися з лікарем щодо доцільності подальшого застосування препарату.Спосіб застосування та дозиМісцево. Препарат слід застосовувати після їди або в проміжках між їдою протягом 5-7 днів. Зняти захисний ковпачок та приєднати аплікатор. Натиснути 2-3 рази, щоб розчин надійшов у розпилювач. Потім затримати подих і пирснути на уражену ділянку. Процедуру слід проводити 2 рази на день, якщо лікар не призначив інакше. Після застосування аплікатор слід ополоснути теплою водою.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему