Акционные товары
61 338,00 грн
996,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
Склад, форма випуску та упаковкаПластик, зуби металеві.ХарактеристикаЗастосовується після обробки лосьйоном Педикулен Ультра для позбавлення від загиблих вошей та гнид.Умови відпустки з аптекБез рецептаВідео на цю тему
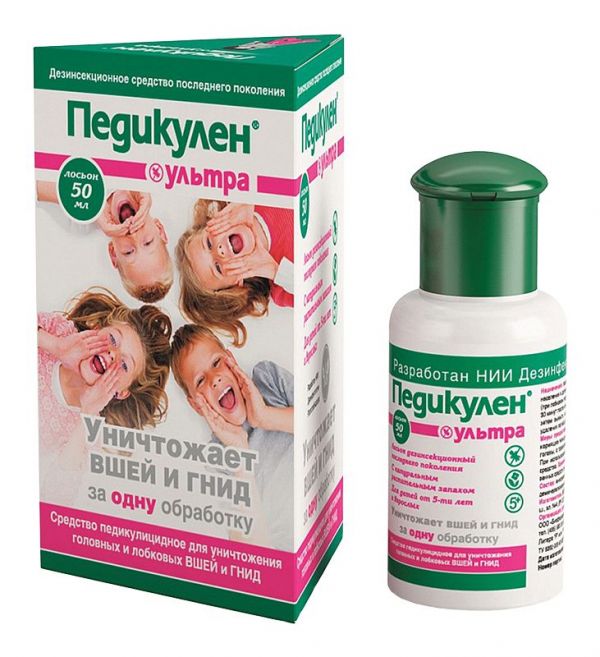
Склад, форма випуску та упаковкаЛосьйон - 1 мл.: Анісова олія 6%. Допоміжні речовини: спирт ізопропіловий (або етиловий) 78%, функціональні добавки – до 100%. Лосьйон у флаконі 50 мл.ХарактеристикаЗнищення ВШ і ГНІД за одне застосування.Фармакотерапевтична групаПедикулен ультра - педикуліцидний лосьйон для знищення головних та лобкових вошей та гнид за одне застосування. Прозора рідина від безбарвного до світло-жовтого кольору із запахом анісу.ІнструкціяНорма витрати засобу становить від 10 до 60 мл або від 3 до 9 застосувань (розпорошень) залежно від зараженості комахами, довжини та густини волосся. Волосся голови або волосисті частини тіла (при лобковому педикульозі), рясно зволожують засобом, злегка втираючи його в шкіру. Через 30 хвилин після нанесення засобу змити його проточною водою з оброблених частин тіла, потім вимити звичайним способом. Волосся голови прочісувати частим гребенем для видалення загиблих комах.Протипоказання до застосуванняПідвищена чутливість до компонентів засобу, дитячий вік до 5 років, вагітність та годування груддю, захворювання та пошкодження волосистих частин тіла та голови.Вагітність та лактаціяПротипоказано при вагітності та дітям до 5 років.Запобіжні заходи та особливі вказівкиТільки для зовнішнього застосування. Уникайте попадання в очі. У разі попадання в очі, негайно промийте їх водою.Умови відпустки з аптекБез рецептаВідео на цю тему
518,00 грн
334,00 грн
Склад, форма випуску та упаковкаЛосьйон - 1 мл. : Анісова олія 6%. Допоміжні речовини: спирт ізопропіловий (або етиловий) 78%, функціональні добавки – до 100%.
1 062,00 грн
302,00 грн
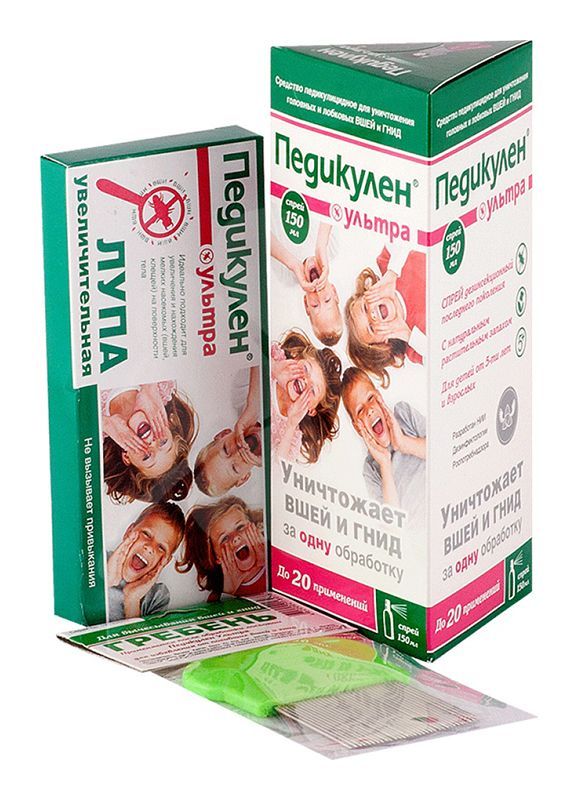
Склад, форма випуску та упаковкаШампунь: вазелінове масло, лаурет сульфат та пропіленгліколь, лаурет-3, сорбітан олеат, масло жасмину ефірне, консервант, антиоксидант; Кондиціонер-спрей: двофазний диметикон, каприлік/каприк тригліцериди, олія жожоба, парфумерна композиція; Гребінець з ручкою із пластику та зубцями зі сталі; Екранна лупа: скло, пластик чорного кольору 1 флакон 50 мл. + 1 флакон 150мл. + лупа + гребіньХарактеристикаПедикулен Ультра є серією засобів, які були розроблені вітчизняними фармацевтами спеціально для боротьби з вошами та гнидами на волосяній частині голови. Засіб ефективний і для лобкових площадок. Головною діючою речовиною всієї серії є анісове масло, яке не переносять більшість комах. Допоміжними речовинами лосьйону та шампуню є вазелінове масло, завдяки якому кожен паразит виявляється, як би в окремій капсулі. Основна речовина паралізує відразу рухи, а потім і дихання, після чого настає смерть. Спрей-кондиціонер допоможе після обробки, його формула полегшить розчісування та нейтралізує згубний вплив діючих речовин на структуру волосся. Густий гребінець допоможе позбутися мертвих комах та гнид. Виріб виконаний із натуральних міцних, гіпоалергенних матеріалів, тому його застосування дозволено навіть новонародженим. Гребінь має густу структуру зубців, крізь які не проникне жоден паразит. Лупа не має жодних особливостей у будові, але з її допомогою огляд волосяних покривів пацієнта буде ретельнішим. Найчастіше застосовується лосьйон Педикулен ультра, його ставлять в одну лінійку із шампунем. Ефективність обох препаратів приблизно однакова, а застосування лосьйону трохи простіше. Препарат є прозорою жовтуватою рідиною, яка при розтині і нанесенні буде сильно пахнути анісовим маслом. Обумовлено це складом препарату: на 6% він складається з олії анісу; 78% займає етиловий спирт; решта відводиться для функціональних добавок.Фармакотерапевтична групаЗнищення вошей та гнид за одну обробку. Розроблено інститутом Дезінфектології Росспоживнагляду. Для дітей від 5-ти років та дорослих. З натуральним рослинним запахом.ІнструкціяНайчастіше для виведення паразитів з волосяної частини голови та інших частин тіла застосовують лосьйон та спрей Педикулен Ультра у тандемі. Ці препарати відмінно доповнюють один одного, але можуть позбавити паразитів і сольно. Лосьйон Педикулен Ультра застосовується для позбавлення як від головних вошей, так і від лобкових площадок, спосіб застосування буде приблизно однаковим з невеликою різницею. Виведення лобкових паразитів виглядає приблизно так: засіб рясно наносять на ватний тампон; щедро змащують всю область ураження, враховуючи шкірні покриви та волосся; очікують 20-30 хвилин; змивають теплою водою із господарським милом. Слідкуйте за тим, щоб засіб не потрапив на слизові. Педикульоз на голові лікують за допомогою лосьйону так: перед початком процедури важливо добре розчісувати волосся; ватний тампон або диск рясно змочити засобом; нанести лосьйон на голову, починаючи з шкірних покривів і далі по всій довжині волосся; одягнути пакет із поліетилену або косинку такої ж якості, щільно зав'язати її; залишити на півгодини; змити нанесений засіб теплою водою; обов'язково провести процедуру вичісування. Засіб прямо впливає на вошей та площиць, їх личинки при цьому залишаються живими. За рахунок впливу на них анісової олії клейкість капсули до волоска значно знижується. Процес вичісування значно полегшується, гниди не так міцно тримаються за волосинки. Спрей-кондиціонер зазвичай наносять після застосування лосьйону або шампуню, для дітей віком до п'яти років його можна застосовувати перед кожним вичісуванням. Засіб значно полегшує процес розчісування волосся після змивання протипедикульозного препарату, масло жожоба відновлює шкірні покриви та структуру волосся після засобів такого типу. Застосовують спрей так: балончик із засобом добре збовтують; розпилення проводять з відривом щонайменше 25 див; обробляють переважно волосся; проводять процедуру вичісування; Після цього рекомендовано змити засіб теплою водою зі звичайним шампунем.Показання до застосуванняШампунь - для знищення головних вошей та їх личинок у дорослих людей та дітей з 3 років. Лосьйон та спрей для знищення головних та лобкових вошей та їх яєць (гнід) у дорослого населення та дітей з 5 років.Протипоказання до застосуванняПідвищена чутливість, вагітність, годування груддю, дитячий вік до 3 років.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаАнісова олія 6%; спирт ізопропіловий (або етиловий) 78%, функціональні добавки – до 100%. Спрей, гребінь та лупа.Фармакотерапевтична групаПедикулен ультра - дезінсекційний засіб, що знищує вошей та гнид за одне застосування.Властивості компонентівДія анісу відома дуже давно. Численні джерела вказують, що від анісу гинуть комахи: воші, клопи, моль, таргани, членистоногі кліщі. Анісове масло повністю паралізує членистоногих і їх вбиває.ІнструкціяРясно зволожте волосся засобом "Педикулен ультра", злегка втираючи у волосся. Через 30 хвилин після нанесення ретельно змийте засіб водою. Використовуйте кондиціонер для волосся для легшого розчісування. Ретельно вичешіть вологе волосся гребенем, починаючи від коріння до кінчиків. Після кожного вичісування очищайте гребінь рушником. Проводіть процедуру поки волосся і шкіра голови не стануть чистими. Перевірте результат за допомогою лупи "Педикулен Ультра" з 3-кратним збільшенням.РекомендуєтьсяДля застосування населенням у побуті з метою знищення головних та лобкових вошей та яєць (гнід) у дорослого населення та дітей з п'яти років та у практиці медичної дезінсекції фахівцями організацій, які мають право займатися дезінфекційною діяльністю.Протипоказання до застосуванняПідвищена чутливість до компонентів засобу; Дитячий вік віком до 5 років; Захворювання та пошкодження волосистих частин тіла та голови;Вагітність та лактаціяПротипоказаний під час лактації, при вагітності. Не застосовувати дітям віком до 3-х років.Запобіжні заходи та особливі вказівкиЗасіб не становить небезпеки для здоров'я пацієнтів, що обробляються, і медичного персоналу при дотриманні рекомендованих режимів використання. Не приймати внутрішньо. При роботі із засобом необхідно використовувати гумові рукавички та дотримуватися правил особистої гігієни. Щоб уникнути попадання кошти на слизові оболонки очей і носоглотки перед обробкою волосся слід пов'язати навколо голови (нижче за волосся) бавовняну косинку, згорнуту джгутом. При використанні пацієнтом контактних лінз слід зняти їх перед застосуванням засобу. Для запобігання слизових оболонок статевих органів та анального отвору слід використовувати марлеві або ватяні тампони. При появі сверблячки, ознак подразнення або висипки на шкірі засіб слід змити негайно. При необхідності звернутися по лікарську допомогу. При випадковому попаданні кошти на слизові оболонки очей, носа та інших органів слід ретельно промити великою кількістю води. З появою подразнення слизових оболонок очей закапати 20% чи 30% розчин сульфацилу натрію. Приміщення, де проводиться масова обробка уражених педикульозом людей, необхідно періодично провітрювати. При отруєнні через дихальні шляхи слід негайно вивести потерпілого на свіже повітря, прополоскати рота водою або 2% розчином харчової соди. Звернутися до лікаря. При випадковому проковтуванні промити шлунок водою або 2% розчином харчової соди, викликати блювоту, потім дати випити 1-2 склянки води з додаванням адсорбенту.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаШампунь - 1 мл: вазелінове масло, лаурет сульфат та пропіленгліколь, лаурет-3, сорбітанолеат, масло жасмину ефірне, консервант, антиоксидант. Флакон 200мл. ХарактеристикаПедикулен ультра – дезінсекційний засіб. 100% знищення вошей та їх личинок! Вазелінове масло у складі шампуню обволікає вошей та гнид, не пропускаючи до них кисень, внаслідок чого комахи та личинки гинуть.ІнструкціяНанести необхідну кількість засобу на сухе волосся, ретельно втираючи до коріння до повного змочування волосся. Довге та густе волосся слід обробляти по пасмах. Через 3 години прочісати волосся частим гребенем для вичісування загиблих вошей та гнид, після цього вимити волосся теплою водою. За необхідності повторити обробку через 7-8 днів. Переваги: Викликає 100% загибель вошей та їх личинок Знищує, а не присипляє комах. Рекомендований дорослим та дітям з 3-х років Клінічно доведена ефективність Ретельно вичешіть волосся гребенем, починаючи від коріння до кінчиків. Якщо волосся довге, то перед вичісуванням розподіліть волосся на пасмо. Після кожного вичісування очищайте гребінець рушником або ватними дисками. Проводіть процедуру поки волосся і шкіра голови не стануть чистими.РекомендуєтьсяДля застосування населенням у побуті з метою знищення головних вошей та їх личинок у дорослого населення та дітей з трьох років та у практиці медичної дезінсекції фахівцями організацій, які мають право займатися дезінфекційною діяльністю.Протипоказання до застосуванняПідвищена чутливість до компонентів засобу дитячий вік до 3 років, захворювання та пошкодження волосистих частин тіла та голови.Вагітність та лактаціяПротипоказаний під час лактації, при вагітності.Запобіжні заходи та особливі вказівкиЗасіб не становить небезпеки для здоров'я пацієнтів, що обробляються, і медичного персоналу при дотриманні рекомендованих режимів використання. Не приймати внутрішньо. При роботі із засобом необхідно використовувати гумові рукавички та дотримуватися правил особистої гігієни. При використанні пацієнтом контактних лінз слід зняти їх перед застосуванням засобу. При появі сверблячки, ознак подразнення або висипки на шкірі засіб слід змити негайно. При необхідності звернутися по лікарську допомогу. При випадковому попаданні кошти на слизові оболонки очей, носа та інших органів слід ретельно промити великою кількістю води. З появою подразнення слизових оболонок очей закапати 20% чи 30% розчин сульфацилу натрію. Приміщення, де проводиться масова обробка уражених педикульозом людей, необхідно періодично провітрювати. При випадковому проковтуванні промити шлунок водою або 2% розчином харчової соди, викликати блювоту, потім дати випити 1-2 склянки води з додаванням адсорбенту.Умови відпустки з аптекБез рецептаВідео на цю тему
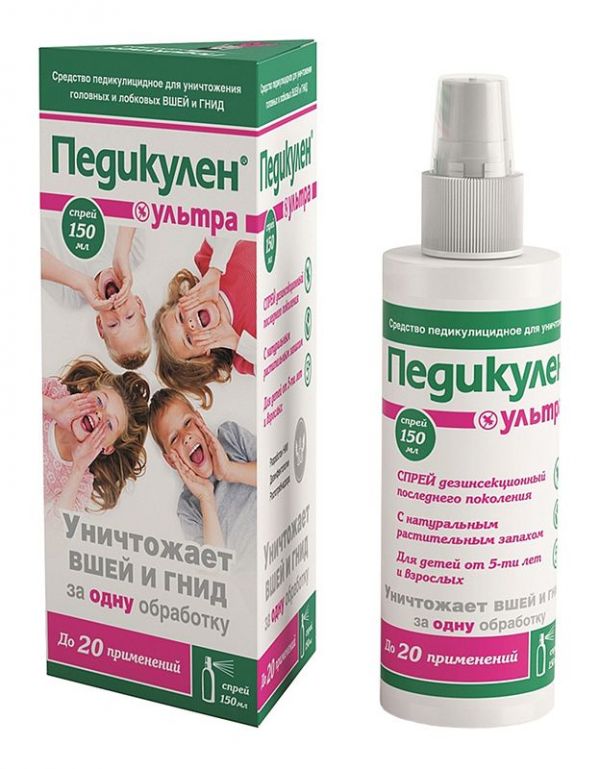
Склад, форма випуску та упаковкаАнісова олія 6%; спирт ізопропіловий (або етиловий) 78%, функціональні добавки – до 100%. Спрей 150мл.Фармакотерапевтична групаПедикулен ультра - дезінсекційний засіб, що знищує вошей та гнид за одне застосування.Властивості компонентівДія анісу відома дуже давно. Численні джерела вказують, що від анісу гинуть комахи: воші, клопи, моль, таргани, членистоногі кліщі. Анісове масло повністю паралізує членистоногих і їх вбиває.ІнструкціяВолосся голови або волосисті частини тіла (при лобковому педикульозі), рясно зволожують засобом, злегка втираючи його в шкіру. Через 30 хвилин після нанесення засобу змити його проточною водою з оброблених частин тіла, потім вимити звичайним способом. Норма витрати засобу становить від 10 до 60 мл залежно від зараженості комахами, довжини та густини волосся.РекомендуєтьсяДля застосування населенням у побуті з метою знищення головних та лобкових вошей та яєць (гнід) у дорослого населення та дітей з п'яти років та у практиці медичної дезінсекції фахівцями організацій, які мають право займатися дезінфекційною діяльністю.Протипоказання до застосуванняПідвищена чутливість до компонентів засобу; Дитячий вік віком до 5 років; Захворювання та пошкодження волосистих частин тіла та голови;Вагітність та лактаціяПротипоказаний під час лактації, при вагітності. Не застосовувати дітям віком до 3-х років.Запобіжні заходи та особливі вказівкиЗасіб не становить небезпеки для здоров'я пацієнтів, що обробляються, і медичного персоналу при дотриманні рекомендованих режимів використання. Не приймати внутрішньо. При роботі із засобом необхідно використовувати гумові рукавички та дотримуватися правил особистої гігієни. Щоб уникнути попадання кошти на слизові оболонки очей і носоглотки перед обробкою волосся слід пов'язати навколо голови (нижче за волосся) бавовняну косинку, згорнуту джгутом. При використанні пацієнтом контактних лінз слід зняти їх перед застосуванням засобу. Для запобігання слизових оболонок статевих органів та анального отвору слід використовувати марлеві або ватяні тампони. При появі сверблячки, ознак подразнення або висипки на шкірі засіб слід змити негайно. При необхідності звернутися по лікарську допомогу. При випадковому попаданні кошти на слизові оболонки очей, носа та інших органів слід ретельно промити великою кількістю води. З появою подразнення слизових оболонок очей закапати 20% чи 30% розчин сульфацилу натрію. Приміщення, де проводиться масова обробка уражених педикульозом людей, необхідно періодично провітрювати. При отруєнні через дихальні шляхи слід негайно вивести потерпілого на свіже повітря, прополоскати рота водою або 2% розчином харчової соди. Звернутися до лікаря. При випадковому проковтуванні промити шлунок водою або 2% розчином харчової соди, викликати блювоту, потім дати випити 1-2 склянки води з додаванням адсорбенту.Умови відпустки з аптекБез рецептаВідео на цю тему
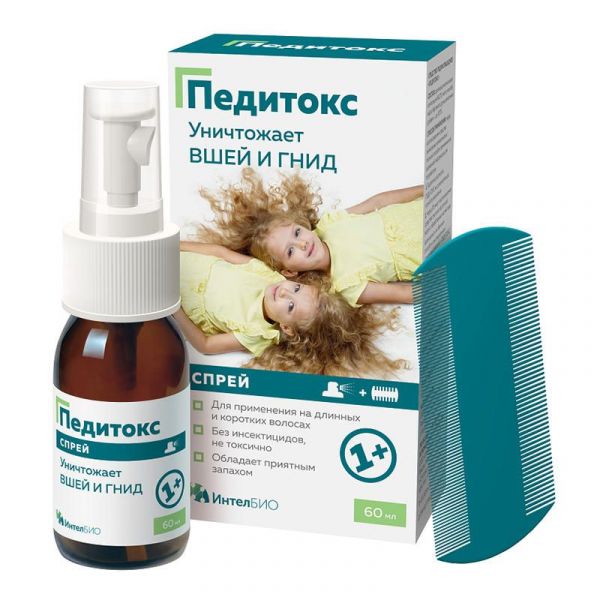
Склад, форма випуску та упаковкаПодвійна диметиконовая композиція 90,2%, олія жожоба, олія бергамота, функціональні добавки - до 100%.ХарактеристикаПодвійна диметиконовая композиція та натуральні олії у засобі ПЕДІТОКС працюють фізичним способом: обволікають комаху, проникають у дихальну систему та закупорюють її. В результаті воші, їх личинки та гніди гинуть від ядухи та дегідратації. Олія бергамота згубно діє на дихальну систему паразитів за рахунок терпеноїду гераніолу, що входить до складу терпеноїду. Вважається, що механізм його дії обумовлений конкурентним інгібуванням ферменту ацетилхолінестерази, що призводить до смерті комахи. Масло жожоба знімає роздратування, спричинене укусами комах, свербінням та розчісами та сприяє загоєнню.ІнструкціяПеред використанням спрею ПЕДІТОКС перевірте наявність вошей та гнид у всіх членів сім'ї. Всіх заражених вошами обробіть засобом ПЕДІТОКС в один день, щоб уникнути повторного зараження. На скляний флакон закріпити насадку-розпилювач. У разі використання спрею флакон необхідно тримати вертикально. Ретельно розпиліть ПЕДІТОКС на сухе, попередньо розчесане волосся, починаючи з коріння. Під час використання тримайте флакон на відстані 10 см від ділянки, що обробляється. Розподіліть склад по всій довжині волосся, починаючи з коріння, до повного зволоження. Волосисті частини тіла (при лобковому педикульозі) рясно зволожують засобом, злегка втираючи його в шкіру. Через 30 хвилин після нанесення засобу змити його проточною водою з оброблених частин тіла, потім вимити їх звичайним способом або спеціальним шампунем для волосся «ПЕДІТОКС. Догляд після обробки». Волосся голови ретельно прочешіть спеціальним гребенем у комплекті, починаючи з коріння, для видалення загиблих комах, личинок та гнид. Довге та густе волосся прочісуйте по пасмах. Очищайте гребінь після кожного прочісування за допомогою серветки або ватяних дисків. Через 7-10 днів повторити обробку. Норма витрати засобу становить від 30 до 60 мл залежно від зараженості комахами, довжини та густини волосся.РекомендуєтьсяДля знищення головних та лобкових вошей, їх личинок та гнид у дорослих та дітей з 1 року.Протипоказання до застосуванняІндивідуальна нестерпність компонентів продукту.Запобіжні заходи та особливі вказівкиТільки для зовнішнього застосування. Уникайте попадання в очі. У разі попадання в очі, негайно промийте їх водою.Умови відпустки з аптекБез рецептаВідео на цю тему
5 758,00 грн
464,00 грн
Склад, форма випуску та упаковкаРозчин – 1 шприц-тюбик: діюча речовина: пегінтерферон альфа-2а (40 кДа) – 135 мкг або 180 мкг; допоміжні речовини: натрію хлорид - 4,0 мг, бензиловий спирт - 5,0 мг, натрію ацетату тригідрат - 1,3085 мг, оцтова кислота крижана - 0,0231 мг, полісорбат 80 - 0,025 мг, натрію ацетакс кислота 10% pH 6,0, вода для ін'єкцій до 0,5 мл. 1. Упаковка у шприц-тюбики По 135 мкг/0,5 мл або 180 мкг/0,5 мл препарату в шприц-тюбик, корпус якого виготовлений з нейтрального скла типу 1 (ЕФ), що закривається з одного боку поршнем, виготовленим із пластмаси, на кінці якого є диск з бутил каучуку, ламінованого фторполімером. З іншого боку шприц-тюбик закупорений наконечником з бутилкаучуку, ламінованого фторполімером. 1 шприц-тюбик разом з 1 стерильною голкою для ін'єкцій (голка для ін'єкцій вкладена в пластмасовий контейнер) та інструкцією із застосування поміщають у картонну пачку. 2. Упаковка в автоінжектор Проклік ™ По 135 мкг/0.5 мл або 180 мкг/0.5 мл препарату в шприц-тюбик з вбудованою захищеною голкою, корпус якого виготовлений з нейтрального скла типу 1 (ЕФ), що закривається з одного боку диском з бутилкаучуку, ламінованого фторполімером, з іншого боку - з не містить латекс ноліізопренового каучуку. Шприц-тюбик із препаратом вбудований у пластиковий автоінжектор ПроКліктм, що складається з корпусу з контрольним віконцем, захисного ковпачка та кнопки активації. Внутрішній пристрій автоінжектора передбачає також циліндр, що захищає голку, і поршень, який через систему механічного пуску з'єднаний з кнопкою активації. 1 автоінжектор ПроКлік™ поміщають у картонну пачку з інструкцією із застосування.Опис лікарської формиПрозорий розчин від безбарвного до жовтого кольору.Фармакотерапевтична групаІмуностимулятор-інтерферони.ФармакокінетикаВсмоктування Після одноразового підшкірного введення 180 мкг пэгінтерферону альфа-2а здоровим добровольцям препарат визначається у сироватці крові через 3-6 годин. Протягом 24 годин концентрація у сироватці крові досягає близько 80% від максимальної. Всмоктування пегінтерферону альфа-2а тривале, максимальні концентрації у сироватці спостерігаються через 72-96 годин після введення препарату. Абсолютна біодоступність пэгінтерферону альфа-2а становить 84% і аналогічна до інтерферону альфа-2а. Розподіл Пегінтерферон альфа-2а виявляється переважно в крові та позаклітинній рідині. Об'єм розподілу у рівноважному стані (Vss) після внутрішньовенного введення становить 6-14 л. За даними мас-спектрометрії, розподіли по тканинах та ауторадіолюмінографії, отриманих у дослідженнях на щурах, пегінтерферон альфа-2а виявляється у високих концентраціях у крові і також у печінці, нирках та кістковому мозку. Метаболізм Особливості метаболізму пэгінтерферону альфа-2а не повністю вивчені; проте дослідження на щурах свідчать, що радіомаркований препарат виводиться переважно нирками. Виведення Системний кліренс пэгінтерферону альфа-2а у людини у 100 разів нижчий, ніж аналогічний показник для інтерферону альфа-2а. Після внутрішньовенного введення термінальний період напіввиведення у здорових добровольців становить 60-80 годин порівняно з 3-4 годинами для звичайного інтерферону. Після підшкірного введення термінальний період напіввиведення становить близько 160 годин (від 84 до 353 годин). Термінальний період напіввиведення після підшкірного введення може показувати не лише виведення, а й тривалість всмоктування пегінтерферону альфа-2а. При введенні пегінтерферону альфа-2а 1 раз на тиждень спостерігається дозозалежне збільшення системного впливу у здорових добровольців та у пацієнтів з хронічним гепатитом (ХГВ) або С. У пацієнтів з хронічним гепатитом В і С через 6-8 тижнів терапії пегінтерфероном альфа-2а один раз на тиждень досягається рівноважна концентрація, яка у 2-3 рази вища, ніж після одноразового введення. Після 8 тижня лікування при введенні препарату один раз на тиждень подальшої кумуляції не відбувається. Через 48 тижнів терапії співвідношення максимальної та мінімальної концентрації становить 1.5-2.0. Концентрації пэгінтерферону альфа-2а у сироватці підтримуються протягом усього тижня (168 год) після введення (див. рис.1). Рисунок 1. Середні рівноважні концентрації пегінтерферону альфа-2а у пацієнтів з хронічним гепатитом С, які отримували монотерапію препаратом Пегасіс 180 мкг/тиждень або комбінацію Пегасіс®/рибавірин: монотерапія, 48 тижнів; комбінація з рибавірином, 48 тижнів. Вісь X: Час (дні) після введення препарату Пегасіс® 1 раз на тиждень Вісь Y: Середня рівноважна концентрація (нг/мл) Фармакокінетика в особливих популяціях пацієнтів Пацієнти з порушенням функції нирок Застосування препарату Пегасіс® вивчали у пацієнтів з ХГС та помірним (кліренс креатиніну 30-50 мл/хв) або тяжким (кліренс креатиніну менше 30 мл/хв) ступенем ниркової недостатності, а також у пацієнтів з термінальною стадією ниркової недостатності, що потребує хронічного глюкози. У пацієнтів з помірним ступенем ниркової недостатності, які отримували препарат Пегасіс у дозі 180 мкг один раз на тиждень, відзначалися подібні експозиції пэгінтерферону альфа-2а у плазмі порівняно з пацієнтами з нормальною функцією нирок. У пацієнтів з тяжким ступенем ниркової недостатності, які отримували препарат Пегасіс у дозі 180 мкг один раз на тиждень, відзначалася на 60% вища експозиція пегінтерферону альфа-2а, ніж у пацієнтів з нормальною функцією нирок. Таким чином, у пацієнтів з тяжким ступенем ниркової недостатності рекомендується зниження дози препарату Пегасіс до 135 мкг один раз на тиждень. У пацієнтів з термінальною стадією ниркової недостатності, що потребує проведення хронічного гемодіалізу, застосування препарату Пегасіс у дозі 135 мкг один раз на тиждень призводило до зниження експозиції пэгінтерферону альфа-2а на 34% порівняно з пацієнтами з нормальною функцією нирок. Незважаючи на нижчу експозицію пэгінтерферону альфа-2а в плазмі, у пацієнтів з термінальною стадією ниркової недостатності відзначалася максимально висока частота серйозних небажаних явищ порівняно з іншими групами пацієнтів, ймовірно, обумовлена тяжкістю та складністю супутніх захворювань у пацієнтів з термінальною нирковою стадією. Підлога Фармакокінетичні показники препарату Пегасіс у жінок та чоловіків після одноразової підшкірної ін'єкції можна порівняти. Літній вік У пацієнтів старше 62 років всмоктування препарату Пегасіс після одноразової підшкірної ін'єкції 180 мкг було уповільненим (проте стійким) порівняно з молодими здоровими добровольцями (tmax 115 годин проти 82 годин). Площа під кривою "концентрація - час" (AUC) злегка збільшується у пацієнтів старше 62 років (1663 проти 1295 нг х год/мл), але максимальні концентрації у пацієнтів молодше і старше 62 років однакові (9.1 та 10.3 нг/мл, відповідно) . На підставі даних експозиції, фармакодинамічної відповіді та перенесення зниження початкової дози препарату у таких пацієнтів не потрібно. Пацієнти з цирозом та без цирозу Фармакокінетика препарату Пегасіс у здорових добровольців та пацієнтів з гепатитом В або С однакова. У пацієнтів із компенсованим цирозом фармакокінетичні характеристики такі самі, як у пацієнтів без цирозу (клас А за шкалою Чайлд-П'ю). Місце ін'єкції Підшкірне введення препарату Пегасіс® повинно бути обмежене областю передньої черевної стінки та стегон, оскільки ступінь всмоктування, на підставі AUC, був на 20-30% вищим за ін'єкції саме в ці області. Концентрація препарату була нижчою в дослідженнях, у яких Пегасіс® вводили підшкірно в плече.ФармакодинамікаХарактеристика препарату Пегільований інтерферон альфа-2а являє собою кон'югат ПЕГ (біс-монометоксиполіетиленгліколю) з інтерфероном альфа-2а. Інтерферон альфа-2а виробляється біосинтетичним методом за технологією рекомбінантної ДНК і є похідним продуктом клонованого гена людського лейкоцитарного інтерферону, введеного та експресованого у клітинах Е. coli. Фармакодинаміка Структура ПЕГ (біс-монометоксиполіетиленгліколю) безпосередньо впливає на клініко-фармакологічні характеристики препарату Пегасіс®. Зокрема, розмір та ступінь розгалуженості ПЕГ з молекулярною масою 40 кДа визначає показники всмоктування, розподілу та виведення пегінтерферону альфа-2а. Активність препарату Пегасіс не слід порівнювати з іншими пегільованими або непегільованими білками того ж терапевтичного класу. Так само як інтерферон альфа-2а, Пегасіс® має противірусну та антипроліферативну активність in vitro. У пацієнтів з хронічним гепатитом (ХГС) зниження рівня РНК вірусу гепатиту С (ВГС) при відповіді на терапію препаратом Пегасіс у дозі 180 мкг відбувається у 2 фази. Перша фаза відзначається через 24-36 годин після першої ін'єкції препарату, друга фаза настає протягом наступних 4-16 тижнів у пацієнтів із стійкою вірусологічною відповіддю. Рибавірин не має значного впливу на кінетику вірусу протягом перших 4-6 тижнів у тих пацієнтів, які отримують комбіновану терапію рибавірином та пегільованим інтерфероном альфа-2а або інтерфероном альфа.Показання до застосуванняХронічний гепатит С Хронічний гепатит С у дорослих пацієнтів із компенсованим захворюванням печінки (у тому числі з або без цирозу печінки, з клінічно стабільною коінфекцією ВІЛ) у комбінації з іншими лікарськими препаратами для лікування хронічного гепатиту С. Хронічний гепатит В Хронічний гепатит У HBeAg-позитивний або HBeAg-негативний у дорослих пацієнтів з компенсованим ураженням печінки та ознаками вірусної реплікації, підвищеною активністю АЛТ та гістологічно підтвердженим запаленням печінки та/або фіброзом.Протипоказання до застосуванняПідвищена чутливість до інтерферонів альфа, генно-інженерних препаратів, отриманих за допомогою E.coli, до поліетиленгліколю або будь-якого іншого компонента препарату. Аутоімуний гепатит. Тяжка печінкова недостатність або декомпенсований цироз печінки. Цироз із сумою балів ≥ 6 за шкалою Чайлд-П'ю у пацієнтів з ко-інфекцією ВІЛ-ХГС за умови, якщо підвищення цього показника не пов'язане з непрямою гіпербілірубінемією внаслідок прийому таких препаратів як атазанавір та індинавір. Тяжкі серцево-судинні захворювання у фазі декомпенсації, у тому числі з нестабільним погано контрольованим перебігом у попередні 6 місяців. Одночасний прийом із телбівудином. Дитячий вік до 18 років (для цієї лікарської форми у зазначених дозуваннях). Вагітність. Період годування груддю.Вагітність та лактаціяВплив препарату Пегасіс на фертильність не вивчався. При застосуванні пегінтерферону альфа-2а, як і інших інтерферонів альфа, відмічено подовження менструального циклу зі зниженням та пізнішим настанням максимальних концентрацій 17β-естрадіолу та прогестерону у тварин. Після відміни препарату спостерігалася нормалізація менструального циклу. Вплив пегінтерферону альфа-2а на фертильність чоловіків не вивчався. Однак запровадження інтерферону альфа-2а протягом 5 місяців не впливало на фертильність у тварин. Тератогенні ефекти препарату Пегасіс не вивчалися. Застосування інтерферону альфа-2а призводило до достовірного збільшення спонтанних абортів у макак-резус. У потомства, народженого вчасно, жодних тератогенних ефектів не відзначалося. Однак при лікуванні препаратом Пегасіс, як і іншими інтерферонами альфа, жінкам дітородного віку слід застосовувати ефективні методи контрацепції. Пегасис не слід призначати при вагітності. Невідомо, чи виводиться Пегасіс або компоненти препарату з грудним молоком. Для виключення небажаного впливу препарату Пегасіс або рибавірину на дитину під час годування груддю слід припинити або грудне вигодовування, або терапію з урахуванням потенційних переваг для матері. У рибавірину в дослідженнях на тваринах виявлено виражені тератогенні ефекти та здатність викликати смерть плода. Рибавірин протипоказаний вагітним та чоловікам, партнерки яких вагітні. Терапію рибавірином слід призначати до отримання негативного тесту на вагітність, проведеного безпосередньо перед передбачуваним початком терапії. Жінки, здатні до дітонародження, або чоловіки, партнерки яких здатні до дітонародження, повинні бути поінформовані про тератогенні ефекти рибавірину та необхідність проведення ефективної контрацепції (не менше 2 способів) під час лікування та протягом 6 місяців після закінчення терапії (див. інструкцію з медичного). застосування рибавірину).Побічна діяХронічний гепатит С Частота та ступінь тяжкості найпоширеніших побічних реакцій при лікуванні препаратом Пегасіс® та інтерфероном альфа-2а однакові. Найпоширеніші побічні реакції при лікуванні препаратом Пегасіс у дозі 180 мкг виражені, як правило, легко або помірно і не вимагають корекції дози або відміни препарату. Хронічний гепатит В Протягом курсу терапії (48 тижнів) та під час спостереження без лікування (24 тижні) профіль безпеки препарату Пегасіс® був подібним до такого при ХГС, хоча частота побічних ефектів при ХГВ була значно меншою, за винятком частоти виникнення лихоманки. У 88% пацієнтів, які отримували Пегасіс®, були відмічені небажані явища порівняно з 53% пацієнтів, які отримували ламівудін. Серйозні небажані явища були зареєстровані у 6% та 4% пацієнтів відповідно. У 5% пацієнтів, які отримували Пегасіс®, і менш ніж у 1% пацієнтів, які отримували ламівудін, терапія була скасована через небажані явища. Частота відміни препарату не відрізняється у пацієнтів із цирозом та без цирозу печінки. Хронічний гепатит С – пацієнти, які раніше не відповіли на лікування Загалом профіль безпеки препарату Пегасіс® у комбінації з рибавірином у пацієнтів, які раніше не відповіли на лікування, був подібним до таких у пацієнтів, які раніше не отримували лікування. У клінічному дослідженні, що включало 72 і 48-тижневе лікування пацієнтів, які не відповіли на раніше проведену терапію пегільованим інтерфероном альфа-2b/рибавірином, лабораторні відхилення або небажані явища призводили до відміни препарату Пегасіс у 12% пацієнтів, отримували лікування протягом 72 тижнів. У групі пацієнтів, які отримували лікування протягом 48 тижнів, лабораторні відхилення або небажані явища призводили до відміни препарату Пегасіс® у 6%, а відміни рибавірину – у 7%. Аналогічно у пацієнтів з цирозом частота відміни терапії препаратом Пегасіс® та рибавірином була вищою у групі пацієнтів, які отримували лікування протягом 72 тижнів (13% та 15%), ніж у групі пацієнтів, які отримували лікування протягом 48 тижнів (6% та 6%) ).До дослідження не включалися пацієнти зі скасуванням раніше проведеної терапії (пегільованим інтерфероном альфа-2b/рибавірином) через гематологічну токсичність. В інше 48-тижневе клінічне дослідження були включені пацієнти з вираженим фіброзом або цирозом (від 3 до 6 балів за шкалою Ishak), які раніше не відповіли на терапію та мали початкове число тромбоцитів 50000 клітин/мкл. У перші 20 тижнів дослідження спостерігалися такі лабораторні відхилення з боку гематологічних показників: анемія (Нb менше ніж 10 г/дл у 26 % пацієнтів); нейтропенія (АГН менше 750 клітин/мкл у 30% пацієнтів); тромбоцитопенію (число тромбоцитів менше 50000 клітин/мкл у 13% пацієнтів). Ко-інфекція ВІЛ-ХГС Профіль безпеки препарату Пегасіс® (монотерапія або комбінація з рибавірином) у пацієнтів з ко-інфекцією ВІЛ-ХГС подібний до пацієнтів з ХГС. До інших небажаних явищ, що зустрічалися у ≥1% - ≤2% пацієнтів з ко-інфекцією ВІЛ-ХГС при лікуванні препаратом Пегасіс® /рибавірином, відносяться: гіперлактацидемія/лактатацидоз, грип, пневмонія, емоційна лабільність, апатія, дзвін у горлі та гортані, хейліт, набута ліподистрофія та хроматурія. Терапія препаратом Пегасіс® асоціювалася зі зниженням абсолютної кількості CD4+ лімфоцитів у перші 4 тижні лікування без зміни їхнього відсоткового вмісту. Кількість CD4+ лімфоцитів поверталася до вихідного при зниженні дози або після відміни терапії. Призначення препарату Пегасіс не впливало негативно на показник вірусного навантаження ВІЛ під час терапії та в період спостереження після закінчення терапії. Дані щодо застосування у пацієнтів із кількістю CD4+ лімфоцитів менше 200 клітин/мкл обмежені. Побічні реакції при монотерапії препаратом Пегасіс® хронічного гепатиту В та хронічного гепатиту С, а також при терапії препаратом Пегасіс® у комбінації з рибавірином хронічного гепатиту С у клінічних дослідженнях та при постреєстраційному використанні Для опису частоти побічних реакцій у клінічних дослідженнях використовуються такі категорії: дуже часто (≥1/10), часто (≥1/100); Інфекційні та паразитарні захворювання: часто – інфекції верхніх дихальних шляхів, бронхіт, кандидоз порожнини рота, простий герпес, грибкові, вірусні та бактеріальні інфекції; нечасто – пневмонія, інфекції шкіри; рідко – ендокардит, зовнішній отит; невідомо – сепсис. Доброякісні та злоякісні новоутворення: нечасто – новоутворення печінки. Порушення з боку крові та лімфатичної системи: часто – тромбоцитопенія, анемія, лімфоаденопатія; рідко – панцитопенія; дуже рідко – апластична анемія; невідомо – парціальна червоноклітинна аплазія кісткового мозку. Порушення з боку імунної системи: нечасто – саркоїдоз, тиреоїдит; рідко – анафілаксія, системний червоний вовчак, ревматоїдний артрит; дуже рідко – ідіопатична або тромботична тромбоцитопенічна пурпура, ангіоневротичний набряк; невідомо - відторгнення печінкових та ниркових трансплантатів, хвороба Фогта-Коянагі-Харада. Порушення з боку ендокринної системи: часто – гіпотиреоз, гіпертиреоз; нечасто – цукровий діабет; рідко – діабетичний кетоацидоз. Порушення з боку обміну речовин та харчування: дуже часто – анорексія; нечасто – дегідратація. Порушення психіки: дуже часто - депресія, занепокоєння, безсоння; часто – емоційні розлади, зміни настрою, агресивність, нервозність, зниження лібідо; нечасто – суїцидальні думки, галюцинації; рідко – суїцид, психічні розлади; невідомо – манія, біполярні розлади, гоміцидальні ідеї. Порушення з боку нервової системи: дуже часто – головний біль, запаморочення, порушення концентрації уваги; часто – порушення пам'яті, непритомність, слабкість, мігрень, гіпестезія, гіперестезія, парестезія, тремор, порушення смакових відчуттів, нічні кошмари, сонливість; нечасто – периферична нейропатія; рідко – кома, судоми, неврит лицевого нерва; невідомо – ішемічний інсульт. Порушення з боку органу зору: часто – затуманений зір, біль у очному яблуці, запальні захворювання очей, ксерофтальмія; нечасто – крововилив у сітківку; рідко – неврит зорового нерва, набряк диска зорового нерва, ураження судин сітківки, ретинопатія, виразка рогівки; дуже рідко – втрата зору; невідомо – відшарування сітківки (серйозні випадки). Порушення з боку органу слуху та лабіринтні порушення: часто – вертиго, біль у вусі; нечасто – втрата слуху. Порушення з боку серцево-судинної системи: часто – тахікардія, відчуття серцебиття, периферичні набряки, почервоніння; нечасто – артеріальна гіпертензія; рідко – інфаркт міокарда, хронічна серцева недостатність, стенокардія, суправентрикулярна тахікардія, аритмія, фібриляція передсердь, перикардит, кардіоміопатія, крововилив у головний мозок, васкуліт; невідомо – ішемія периферичних судин. Порушення з боку дихальної системи, органів грудної клітки та середостіння: дуже часто – задишка, кашель; часто - задишка при фізичному навантаженні, носова кровотеча, назофарингіт, набряк пазух, закладеність носа, риніт, біль у горлі; нечасто - свистяче дихання; рідко - інтерстиціальний пневмоніт (включаючи випадки з летальним кінцем), емболія легеневої артерії; невідомо - легенева артеріальна гіпертензія. Порушення з боку шлунково-кишкового тракту: дуже часто – діарея, нудота, біль у животі; часто - блювання, диспепсія, дисфагія, виразка слизової оболонки порожнини рота, кровоточивість ясен, глосит, стоматит, метеоризм, сухість слизової оболонки порожнини рота; нечасто – шлунково-кишкова кровотеча; рідко – пептична виразка, панкреатит; невідомо – ішемічний коліт, пігментація мови. Порушення з боку печінки та жовчовивідних шляхів: нечасто – порушення функції печінки; рідко – печінкова недостатність, холангіт, жирова дистрофія печінки. Порушення з боку шкіри та підшкірних тканин: дуже часто – алопеція, дерматит, свербіж, сухість шкіри; часто - висипання, підвищене потовиділення, псоріаз, кропив'янка, екзема, ураження шкіри, реакції фотосенсибілізації, нічні поти; дуже рідко – токсичний епідермальний некроліз, синдром Стівенса-Джонсона, мультиформна еритема. Порушення з боку скелетно-м'язової та сполучної тканини: дуже часто – міалгії, артралгії; часто – біль у спині, шиї, кістках, артрит, м'язова слабкість, кістково-м'язовий біль, м'язові спазми; рідко – міозит; невідомо – рабдоміоліз. Порушення з боку нирок та сечовивідних шляхів: рідко – ниркова недостатність. Порушення з боку статевих органів та молочної залози: часто – імпотенція. Загальні розлади та порушення в місці введення: дуже часто - гарячка, озноб, біль, астенія, стомлюваність, дратівливість, реакції в місці ін'єкції; часто - біль у грудній клітці, грипоподібний синдром, нездужання, загальмованість, "припливи", спрага, зниження маси тіла. Травми, інтоксикації та ускладнення маніпуляцій: рідко – передозування. *Ці побічні реакції зустрічалися часто (≥1/100; § Характерно для препаратів інтерферонів. нижче підрозділ "Легенева артеріальна гіпертензія". Опис окремих небажаних реакцій Легенева артеріальна гіпертензія При лікуванні препаратами інтерферону альфа були зареєстровані випадки легеневої артеріальної гіпертензії (ЛАГ), особливо у пацієнтів з факторами ризику ЛАГ (такими як портальна гіпертензія, ВІЛ-інфекція, цироз). Повідомлення про ЛАГ були отримані у різні моменти часу, як правило, через кілька місяців після початку терапії інтерферонами альфа. Лабораторні показники Терапія препаратом Пегасіс® супроводжувалася наступними змінами лабораторних показників: підвищенням активності АЛТ, гіпербілірубінемією, електролітними порушеннями (гіпокаліємія, гіпокальціємія, гіпофосфатемія), гіпо- та гіперглікемією, гіпертригліцеридемією. При монотерапії препаратом Пегасіс і при комбінованій терапії з рибавірином у 2% пацієнтів спостерігалося підвищення активності АЛТ, що призводило до зменшення дози або припинення лікування. Терапія препаратом Пегасіс® асоціювалася зі зниженням гематологічних показників (лейкопенією, нейтропенією, лімфопенією, тромбоцитопенією та зниженням Нb), які покращувалися при зміні дози та поверталися до вихідного рівня через 4-8 тижнів після припинення терапії. У 24% пацієнтів, які отримували препарат Пегасіс® у дозі 180 мкг та рибавірин у дозі 1000-1200 мг протягом 48 тижнів, спостерігалася нейтропенія середнього ступеня тяжкості (АГН: 0,749-0,5 х 109/л), а у 5% пацієнтів - важка нейтропенія (АГН: Антитіла до інтерферону: у 1-5% пацієнтів, які отримували Пегасіс, відзначалося утворення нейтралізуючих антитіл до інтерферону. Як і при терапії іншими інтерферонами, антитіла, що нейтралізують, до інтерферону частіше спостерігалися при хронічному гепатиті В. Однак кореляція між появою антитіл і ефективністю лікування не виявлена. Функція щитовидної залози: терапія препаратом Пегасіс® асоціювалася з клінічно значущими змінами лабораторних показників функції щитовидної залози, які вимагали медичного втручання. Частота виникнення (4.9%) цих змін при терапії препаратом Пегасіс та іншими інтерферонами однакова. Лабораторні показники при коінфекції ВІЛ-ХГС Незважаючи на те, що явища гематологічної токсичності (нейтропенія, тромбоцитопенія, анемія) у пацієнтів з коінфекцією ВІЛ-ХГС зустрічаються частіше, більшість з них коригуються зміною дози та використанням факторів росту, і передчасне скасування терапії потрібне рідко. Зниження абсолютної кількості нейтрофілів нижче 500 клітин/мкл спостерігалося у 13% та 11% пацієнтів, які отримували монотерапію препаратом Пегасіс® та терапію препаратом Пегасіс®/рибавірином, відповідно. Зниження тромбоцитів нижче 50000 клітин/мкл спостерігалося при монотерапії препаратом Пегасіс у 10% пацієнтів, а при комбінованій терапії – у 8%. У 7% пацієнтів, які отримували монотерапію препаратом Пегасіс®, та у 14% пацієнтів, які отримували Пегасіс/рибавірин, була зареєстрована анемія (НbВзаємодія з лікарськими засобамиДослідження вивчення взаємодії проводилися лише в дорослих. Терапія препаратом Пегасіс® 180 мкг/тиждень протягом 4-х тижнів не впливала на фармакокінетичний профіль толбутаміду, мефенітоїну, дебризохіну та дапсону у здорових чоловіків-добровольців, що свідчить про те, що Пегасіс® in vivo не впливає на метабол Р450 2С9, 2С19, 2D6 та 3А4. Пегасис є помірним інгібітором активності ізоферменту 1А2 цитохрому Р450, виявлено збільшення площі під кривою "концентрація-час" (AUC) теофіліну приблизно на 25%. У пацієнтів, які одночасно отримують теофілін та Пегасіс®, необхідно контролювати концентрацію теофіліну в сироватці та проводити відповідну корекцію дози теофіліну. Взаємодія між теофіліном та препаратом Пегасіс®, мабуть, досягає максимуму більш ніж через 4 тижні терапії препаратом Пегасіс®. Моноінфекція вірусом гепатиту С та вірусом гепатиту В У фармакокінетичному дослідженні у 24 пацієнтів з ХГС терапія препаратом Пегасіс® 180 мкг/тиждень протягом 4 тижнів супроводжувалася збільшенням середніх рівнів метаболітів метадону (одночасна терапія метадоном у дозі від 30 мг до 150 мг; медіана дози 95 мг). Клінічне значення цієї взаємодії не визначено, рекомендується ретельно контролювати симптоми інтоксикації метадоном. Зокрема, пацієнти, які приймають високі дози метадону, мають ризик подовження інтервалу QTc. Азатіоприн: при застосуванні рибавірину в комбінації з азатіоприном можливе посилення мієлотоксичної дії азатіоприну. Рибавірин інгібує інозинмонофосфат дегідрогеназу - фермент, що бере участь у метаболізмі азатіоприну. У свою чергу пригнічення активності даного ферменту призводить до підвищення рівня 6-метилтіоінозинмонофосфату, що асоційовано з ризиком мієлотоксичності у пацієнтів, які отримують азатіоприн. Можливе призначення рибавірину в комбінації з азатіоприном, якщо очікувана користь терапії перевищує потенційний ризик. У разі необхідно проводити ретельний моніторинг складу крові щодо розвитку мієлотоксичності. У разі виникнення мієлотоксичності комбіновану терапію слід відмінити (див. також "Особливі вказівки"). Не виявлено фармакокінетичної взаємодії між препаратом Пегасіс® та рибавірином у пацієнтів із ХГС та препаратом Пегасіс® та ламівудином у пацієнтів із ХГВ. Комбінація телбівудину в дозі 600 мг/добу та пегільованого інтерферону альфа-2а у дозі 180 мкг 1 раз на тиждень підшкірно для лікування ХГВ асоціюється з підвищеним ризиком розвитку периферичної нейропатії, механізм розвитку якої невідомий. Не можна виключити підвищений ризик розвитку периферичної нейропатії та інших інтерферонів (як стандартних, і пегільованих). Крім того, в даний час не встановлено користь комбінації телбівудину та інтерферонів альфа (пегільованих або стандартних). Таким чином, комбінація препарату Пегасіс та телбівудину протипоказана. Ко-інфекція ВІЛ-ХГС У додатковому 12-тижневому фармакокінетичному дослідженні у 47 пацієнтів з ко-інфекцією ВІЛ-ХГС, метою якого було визначити вплив рибавірину на внутрішньоклітинне фосфорилювання деяких нуклеозидних інгібіторів зворотної транскриптази (НІОТ) (ламівудін і зидовудин або ставудін), очевидних. Однак через істотні коливання значень, довірчі інтервали були досить широкі. Одночасний прийом НДПТ, очевидно, не впливав на експозицію рибавірину у плазмі. Не рекомендується комбінація диданозину та рибавірину. Рибавірин збільшує експозицію диданозину та його активного метаболіту (дидеоксіаденозин 5-трифосфат) in vitro, що може призводити до розвитку фатальної печінкової недостатності, периферичної нейропатії, панкреатиту, симптоматичної гіперлактатемії/лактації дозу. При використанні зидовудину в комплексній терапії ВІЛ повідомлялося про погіршення анемії, пов'язаної з рибавірином. Проте точний механізм цього явища підлягає визначенню. Через підвищений ризик виникнення анемії одночасне застосування рибавірину та зидовудину не рекомендується. Якщо комбінована антиретровірусна терапія вже проводиться, слід розглянути можливість заміни зидовудину, особливо у пацієнтів, які мали в анамнезі анемію, спричинену зидовудіном. Фармацевтична несумісність Забороняється змішувати Пегасіс з іншими лікарськими засобами, оскільки дослідження за сумісністю відсутні.Спосіб застосування та дози(Для пацієнтів старше 18 років) Лікування препаратом Пегасіс® повинно проводитись під наглядом кваліфікованого лікаря, який має досвід проведення терапії у пацієнтів із хронічним гепатитом В та С. У разі використання препарату Пегасіс у комбінації з іншими лікарськими препаратами слід ознайомитися з інструкцією з медичного застосування цих препаратів. Монотерапія препаратом Пегасіс показана лише у разі наявності протипоказань до інших лікарських препаратів для лікування хронічного гепатиту С. Стандартний режим дозування Препарат вводять підшкірно (п/к) в ділянку передньої черевної стінки або стегна 1 раз на тиждень. Перед введенням препарат необхідно оглядати на предмет відсутності сторонніх домішок та зміни кольору. Пацієнтів слід ретельно інструктувати про важливість правильного зберігання та знищення використаних матеріалів та застерігати від повторного використання будь-яких голок та шприців. Хронічний гепатит В При HBeAg-позитивному та HBeAg-негативному хронічному гепатиті В – 1 раз на тиждень протягом 48 тижнів у разовій дозі 180 мкг. Хронічний гепатит С Пацієнти, які раніше не отримували лікування Рекомендована доза препарату Пегасіс становить 180 мкг 1 раз на тиждень у комбінації з рибавірином (перорально) або у вигляді монотерапії. Режим дозування рибавірину, який слід використовувати у комбінації з препаратом Пегасіс®, наведено у таблиці 1. Рибавірин слід приймати під час їди. Тривалість терапії - подвійна терапія (Пегасіс® та рибавірин) При комбінованій з рибавірином терапії тривалість терапії та доза рибавірину залежать від генотипу вірусу (див. таблицю 1). Таблиця 1. Режим дозування препарату Пегасіс і рибавірину у пацієнтів з ХГС. Генотип Доза препарату Пегасіс® Доза рибавірину Тривалість Генотип 1 з низьким вірусним навантаженням та швидкою вірусологічною відповіддю * 180 мкг Вага <75 кг = 1,000 мг Вага ≥75 кг = 1,200 мг 24 або 48 тижнів Генотип 1 з високим вірусним навантаженням та швидкою вірусологічною відповіддю* 180 мкг Вага <75 кг = 1,000 мг Вага ≥75 кг = 1,200 мг 48 тижнів Генотип 4 із швидкою вірусологічною відповіддю* 180 мкг Вага <75 кг = 1,000 мг Вага ≥75 кг = 1,200 мг 24 або 48 тижнів Генотип 1 або 4 без швидкої вірусологічної відповіді 180 мкг Вага <75 кг = 1,000 мг Вага ≥75 кг = 1,200 мг 48 тижнів Генотип 2 або 3 без швидкої вірусологічної відповіді** 180 мкг 800 мг 24 тижні Генотип 2 або 3 з низьким вірусним навантаженням та швидкою вірусологічною відповіддю** 180 мкг 800 мг 16 або 24 тижні Генотип 2 або 3 з високим вірусним навантаженням та швидкою вірусологічною відповіддю** 180 мкг 800 мг 24 тижні *Швидка вірусологічна відповідь (РНК ВГС не визначається) на 4 та 24 тижні лікування ** Швидка вірусологічна відповідь (результат визначення РНК ВГС негативний) до 4 тижня лікування Низьке вірусне навантаження = ≤800,000 МО/мл Високе вірусне навантаження = >800,000 МО/мл Тривалість терапії у пацієнтів з генотипом 1, у яких на 4-му тижні лікування визначається РНК ВГС, повинна становити 48 тижнів, незалежно від вихідного вірусного навантаження. Тривалість терапії протягом 24 тижнів можна розглядати у пацієнтів: з генотипом 1 та вихідно низьким вірусним навантаженням (≤800,000 МО/мл); з генотипом 4, у яких на 4-му тижні результат визначення РНК ВГС негативний і залишається негативним на 24-му тижні. Однак загальна тривалість терапії протягом 24 тижнів може бути асоційована з більшим ризиком рецидиву, ніж 48-тижнева тривалість лікування. При вирішенні питання про тривалість терапії у таких пацієнтів слід враховувати перенесення комбінованої терапії та додаткові прогностичні фактори, такі як ступінь фіброзу. З ще більшою обережністю слід підходити до питання про скорочення тривалості терапії у пацієнтів з генотипом 1 та вихідно високим вірусним навантаженням (>800,000 МО/мл), у яких на 4 тижні результат визначення РНК ВГС негативний і залишається негативним на 24 тижні, оскільки обмежені доступні дані припускають, що скорочення тривалості терапії може дуже негативно вплинути на стійку вірусологічну відповідь. У пацієнтів з генотипом 2 або 3 і РНК ВГС, що визначається, на 4 тижні лікування, незалежно від вихідного вірусного навантаження, тривалість терапії повинна становити 24 тижні. Можливе скорочення терапії до 16 тижнів в окремих групах пацієнтів з генотипом 2 або 3, низьким вірусним навантаженням (вихідно ≤800,000 МО/мл), що не визначається РНК ВГС до 4 тижня і залишається негативним до 16 тижнів. При 16-тижневій тривалості терапії можливе збільшення ризику рецидиву порівняно з 24-тижневою терапією. При вирішенні питання про тривалість терапії у таких пацієнтів слід враховувати переносимість комбінованої терапії та додаткові клінічні та прогностичні фактори, такі як ступінь фіброзу. З ще більшою обережністю слід підходити до питання про скорочення тривалості терапії у пацієнтів з генотипом 2 або 3 та вихідно високим вірусним навантаженням (> 800,000 МО/мл), у яких до 4 тижня результат визначення РНК ВГС негативний, оскільки обмежені дані припускають, що скорочення тривалість терапії може вкрай негативно вплинути на стійкість вірусологічної відповіді. Клінічні дані щодо пацієнтів з генотипом 5 та 6 обмежені, рекомендується комбінована терапія препаратом Пегасіс® та рибавірином (1000/1200 мг) протягом 48 тижнів. Рекомендована тривалість монотерапії препаратом Пегасіс становить 48 тижнів. Пацієнти, які раніше отримували лікування Рекомендована доза препарату Пегасіс у комбінації з рибавірином становить 180 мкг 1 раз на тиждень. Доза рибавірину становить 1000 мг на добу (вага При виявленні вірусу на 12-му тижні лікування терапію слід припинити. Рекомендована загальна тривалість терапії становить 48 тижнів. При вирішенні питання про лікування пацієнтів з генотипом 1, які не відповіли на попереднє лікування пегільованим інтерфероном та рибавірином, загальна тривалість терапії, що рекомендується, повинна становити 72 тижні. Ко-інфекція ВІЛ-ХГС 180 мкг 1 раз на тиждень як монотерапія або в комбінації з рибавірином (800 мг) протягом 48 тижнів, незалежно від генотипу. Безпека та ефективність комбінованої терапії з рибавірином у дозі понад 800 мг та тривалістю менше 48 тижнів вивчена недостатньо. Тривалість терапії при використанні препарату Пегасіс у комбінації з іншими лікарськими препаратами Слід також ознайомитись з інструкціями щодо медичного застосування препаратів, що використовуються у комбінації з препаратом Пегасіс®. Прогнозування ефективності лікування - подвійна терапія (Пегасис та рибавірин) Пацієнти, які раніше не отримували лікування Визначення ранньої вірусологічної відповіді (зниження вірусного навантаження нижче за поріг визначення або не менше ніж на 2 log10) на 12 тижні терапії може прогнозувати досягнення стійкої вірусологічної відповіді (див. таблицю 2). Прогностична цінність відсутності стійкої вірусологічної відповіді (УВО) на 12-му тижні монотерапії препаратом Пегасіс становить 98%. Подібна прогностична цінність відсутності УВО виявлена у пацієнтів з ко-інфекцією ВІЛ-ХГС, які отримували монотерапію препаратом Пегасіс® або комбіновану терапію препаратом Пегасіс® та рибавірином (100% та 98%, відповідно). При ко-інфекції ВІЛ-ХГС прогностична цінність УВО 45% та 70% виявлена відповідно у пацієнтів з генотипами 1 та 2/3, які отримували комбіновану терапію. Таблиця 2. Прогностична цінність вірусологічної відповіді на 12 тижні комбінованої терапії у рекомендованому режимі Генотип Негативний результат Позитивний результат Відсутність відповіді на 12 тижні Відсутність стійкої відповіді Прогностична цінність Відповідь на 12 тижні Стійка відповідь Прогностична цінність Генотип 1 (n=569) 102 97 95% 467 271 58% Генотип 2 та 3 (n=96) 3 3 100% 93 81 87% Пацієнти, які раніше отримували лікування У пацієнтів, які раніше не відповіли на лікування, при повторному лікуванні протягом 48 тижнів (генотип 2 і 3) або 72 тижнів (генотип 1 і 4) було показано, що супресія вірусу на 12 тижні (РНК ВГС нижче 50 МО/мл) є прогностичним критерієм УВО. Імовірність відсутності УВО після 48 або 72 тижнів лікування у разі, якщо придушення вірусу не було відзначено на 12 тижні, склала 96% та 96% відповідно. Імовірність досягнення УВО після 48 або 72 тижнів лікування у випадку, якщо супресія вірусу була відзначена на 12 тижні, склала 35% та 57% відповідно. Припинення лікування Рекомендовано припинення лікування за відсутності зниження рівня РНК ВГС не менше ніж на 2 log10 від вихідного рівня або невизначеного рівня РНК ВГС до 12-го тижня терапії. Крім того, лікування слід припинити, якщо пацієнти не досягли невизначеного рівня РНК ВГС до 24-го тижня. Вказівки щодо корекції дози у зв'язку з побічною дією Загальні Якщо корекція дози потрібна через клінічні або лабораторні реакції середнього та тяжкого ступеня тяжкості, зазвичай достатньо знизити дозу препарату до 135 мкг. Однак у деяких випадках необхідно зменшити дозу до 90 мкг або 45 мкг. Після вирішення побічних реакцій можна розглянути питання збільшення дози препарату, аж до початкової. Гематологічні Зменшення дози рекомендується при зниженні нейтрофілів менше 750 клітин/мкл. У пацієнтів з абсолютним числом нейтрофілів (АЧН) менше 500 клітин/мкл лікування слід перервати доти, доки цей показник не перевищить 1000 клітин/мкл. Застосування препарату Пегасіс® слід відновити у дозі 90 мкг під періодичним контролем кількості нейтрофілів (періодичність контролю визначається лікарем у кожному конкретному випадку індивідуально). Зменшення дози до 90 мкг рекомендується при зниженні тромбоцитів менше 50000 клітин/мкл. У пацієнтів із числом тромбоцитів менше 25000 клітин/мкл препарат слід відмінити. Рекомендації щодо лікування анемії, що виникла під час терапії: 1) Доза рибавірину знижується до 600 мг на добу (200 мг вранці та 400 мг увечері) в одній із наступних ситуацій: Нb знижується менше 10 г/дл, але залишається більше 8,5 г/дл у пацієнтів без супутньої серцево-судинної патології; Нb знижується на 2 г/дл або більше протягом будь-яких 4 тижнів терапії у пацієнтів із стабільним серцево-судинним захворюванням. Не рекомендується збільшувати дозу рибавірину до початкової. 2) Прийом рибавірину повинен бути припинений в одній із таких ситуацій: Нb знижується менше 8,5 г/дл у пацієнтів без супутньої серцево-судинної патології; Hb залишається менше 12 г/дл через 4 тижні, незважаючи на зниження дози, у пацієнтів із стабільним серцево-судинним захворюванням. Після припинення прийому рибавірину та дозволу побічної дії можна відновити його прийом у дозі 600 мг/добу з подальшим підвищенням до 800 мг/добу на розсуд лікаря. Не рекомендується збільшувати дозу рибавірину до початкової (1000 мг або 1200 мг). При непереносимості рибавірину слід продовжити монотерапію препаратом Пегасіс. Таблиця 3. Корекція дози при побічній дії (додаткову інформацію див. вище в тексті Зниження дози рибавірину до 600 мг Призупинення прийому рибавірину Зменшення дози препарату Пегасіс до 135/90/45 мкг. Призупинення прийому препарату Пегасіс® Скасування комбінованого лікування Абсолютна кількість нейтрофілів <750 клітин/мкл <500 клітин/мкл Число тромбоцитів <50 000 клітин/мкл >25 000 клітин/мкл <25 000 клітин/мкл Нb Відсутність серцево-судинного захворювання <10 г/дл та ≥8,5 г/дл <8,5 г/дл Нb Стабільне серцево-судинне захворювання зниження на ≥2 г/дл протягом будь-яких 4 тижнів терапії <12 г/дл, навіть через 4 тижні терапії у зниженій дозі Пов'язані з порушенням функції печінки У пацієнтів із хронічним гепатитом С характерні коливання у відхиленнях від норми результатів печінкових проб. Як і при терапії іншими препаратами інтерферону альфа, при терапії препаратом Пегасіс® спостерігається підвищення активності АЛТ вище за показник до лікування, у тому числі й у пацієнтів з вірусологічною відповіддю. У клінічних дослідженнях у 8 із 451 пацієнта з хронічним гепатитом С, які отримували комбіновану терапію, спостерігалося ізольоване підвищення активності АЛТ (що перевищує верхню межу норми у ≥10 разів; або перевищує вихідний рівень у ≥2 рази для пацієнтів з вихідним рівнем активності АЛТ у 10 разів вище верхньої межі норми), що зникло без зміни дози. При прогресуючому підвищенні активності АЛТ порівняно з показниками до лікування дозу препарату Пегасіс® потрібно спочатку зменшити до 135 мкг. Якщо активність АЛТ, незважаючи на зниження дози, продовжує збільшуватись або супроводжується підвищенням концентрації білірубіну або ознаками декомпенсації печінкового процесу, препарат слід відмінити. У пацієнтів з хронічним гепатитом В можливе скороминуще збільшення активності АЛТ, що іноді перевищує верхню межу норми в 10 разів, що може свідчити про імунний кліренс. Лікування зазвичай не слід розпочинати, якщо активність АЛТ перевищує верхню межу норми більш ніж у 10 разів. Продовження терапії потребує частішого контролю активності АЛТ. При зниженні дози або тимчасовому відміні препарату Пегасіс® терапія може бути відновлена після нормалізації активності АЛТ. Особливі групи пацієнтів Ниркова недостатність Пацієнтам з легким або помірним ступенем ниркової недостатності корекції дози не потрібно. Пацієнтам з тяжким ступенем ниркової недостатності рекомендується зниження дози препарату Пегасіс до 135 мкг один раз на тиждень. Пацієнтам з термінальною стадією ниркової недостатності слід застосовувати препарат Пегасіс у початковій дозі 135 мкг один раз на тиждень. Незалежно від початкової дози та ступеня тяжкості ниркової недостатності таких пацієнтів необхідно ретельно спостерігати та знижувати дозу у разі виникнення побічних реакцій. Дані щодо застосування у дітей із порушенням функції нирок відсутні. Печінкова недостатність У пацієнтів із компенсованим цирозом печінки (клас А по Чайлд-П'ю) Пегасіс® ефективний та безпечний. У пацієнтів з декомпенсованим цирозом (клас В/С з Чайлд-П'ю або кровотеча з варикозно-розширених вен стравоходу) застосування препарату Пегасіс не вивчалося. Літній вік У пацієнтів похилого віку корекція дози (180 мкг, один раз на тиждень) не потрібна. Діти та підлітки Препарат Пегасіс® не зареєстрований для застосування у пацієнтів віком до 18 років. Розчин препарату Пегасіс протипоказаний новонародженим та дітям до 3 років, оскільки містить бензиловий спирт, здатний викликати у пацієнтів даної вікової категорії неврологічні та інші ускладнення, іноді фатальні.ПередозуванняОписано випадки передозування препарату Пегасіс® при введенні препарату протягом двох днів поспіль (без дотримання тижневого інтервалу) та при щоденному введенні протягом одного тижня (сумарна доза 1260 мкг на тиждень). Будь-яких незвичайних, серйозних і впливових на лікування небажаних явищ не відмічено. У клінічних дослідженнях при раку нирки та хронічному мієлолейкозі препарат вводили у дозах до 540 та 630 мкг на тиждень. Ознаками токсичності, що обмежують подальше застосування в цих дозах, були стомлюваність, підвищення активності печінкових ферментів, нейтропенія та тромбоцитопенія, які можуть виникнути при лікуванні звичайними інтерферонами. Специфічний антидот відсутній. Гемодіаліз та перитонеальний діаліз неефективні.Запобіжні заходи та особливі вказівкиУ медичній документації хворого слід зазначати торгове найменування та номер серії препарату (Пегасіс®). Заміна препарату на будь-який інший біологічний лікарський препарат вимагає погодження з лікарем. Інформація, представлена в даній інструкції, стосується лише препарату Пегасіс®. Нейропсихічні розлади У деяких пацієнтів, як під час лікування препаратом Пегасіс®, так і протягом 6 місяців після припинення лікування, спостерігалися тяжкі побічні реакції з боку центральної нервової системи (ЦНС), зокрема депресія, суїцидальна налаштованість та суїцидальні спроби. При терапії інтерферонами альфа спостерігалися інші побічні реакції з боку ЦНС, у тому числі агресивна поведінка, іноді спрямована проти інших людей (наприклад, гоміцидальні ідеї), сплутаність свідомості, порушення психічного статусу. Слід уважно спостерігати за станом пацієнтів (незалежно від віку) виявлення ознак або симптомів психічних розладів. Якщо такі симптоми виникають, то лікар повинен пам'ятати про потенційну серйозність цих небажаних явищ та необхідність відповідного лікування. У випадку, якщо симптоми психічних розладів зберігаються або погіршуються або виявляється суїцидальна налаштованість, рекомендується відмінити терапію препаратом Пегасіс і надати необхідне відповідне лікування. Пацієнти з тяжкими психічними захворюваннями (у тому числі в анамнезі) Якщо прийнято рішення про необхідність лікування препаратом Пегасіс® пацієнтів з тяжкими психічними захворюваннями (у тому числі в анамнезі), терапію слід розпочинати лише після проведення відповідного обстеження та лікування психічного розладу. Пацієнти, що вживають/зловживають психоактивними речовинами: пацієнти, інфіковані ВГС і які мають порушення, пов'язані з вживанням психоактивних речовин (алкоголь, каннабіоїди тощо), знаходяться в групі підвищеного ризику розвитку психічних розладів або загострення вже існуючих при лікуванні інтерферонами. Якщо лікування інтерферонами альфа є необхідним у цих пацієнтів, слід ретельно оцінити наявність супутніх психічних захворювань та потенціал використання інших речовин, а також адекватно контролювати їх до початку терапії. Слід ретельно спостерігати за пацієнтами як під час терапії, і після її припинення. Для оцінки ризиків перед початком лікуванняпід час терапії та при спостереженні після завершення терапії слід використовувати міждисциплінарний підхід із залученням за необхідності психіатра та нарколога. У разі повторного виникнення чи розвитку психічних порушень та вживання психоактивних речовин рекомендується раннє втручання. Лабораторні показники до та під час лікування До початку лікування препаратом Пегасіс® усім пацієнтам рекомендується пройти стандартні загальні клінічні та біохімічні аналізи крові. Ініціація терапії можлива за наступних вихідних показників: число тромбоцитів ≥90000 клітин/мкл, абсолютна кількість нейтрофілів ≥1500 клітин/мкл, компенсована функція щитовидної залози (ТТГ та Т4 у межах нормальних показників), кількість CD4+ лімфоцитів ≥200 клітин/мкл або CD4+ ≥100 - Після початку терапії загальний клінічний аналіз крові необхідно повторити через 2 та 4 тижні, а біохімічний – через 4 тижні; додаткові лабораторні аналізи слід проводити періодично під час терапії (зокрема моніторинг концентрації глюкози у крові). У клінічних дослідженнях при лікуванні препаратом Пегасіс знижувалося як загальна кількість лейкоцитів, так і абсолютна кількість нейтрофілів (АЧН) зазвичай з другого тижня терапії. Прогресуюче зниження АЧН через 8 тижнів терапії траплялося нечасто. Зниження АЧН було оборотним після зменшення дози або відміни препарату, у більшості пацієнтів показник АЧН досягав нормального значення через 8 тижнів і повертався до вихідного значення у всіх пацієнтів приблизно через 16 тижнів. Терапія препаратом Пегасіс пов'язана зі зниженням кількості тромбоцитів, які поверталися до початкового рівня протягом періоду спостереження після лікування. У деяких випадках може бути потрібна зміна дози. У клінічних дослідженнях при комбінованому лікуванні препаратом Пегасіс® та рибавірином виникнення анемії (Нb Потрібно бути обережними при призначенні препарату Пегасіс® у комбінації з іншими мієлотоксичними препаратами. У літературі описані випадки виникнення панцитопенії та супресії кісткового мозку через 3-7 тижнів після початку застосування рибавірину у комбінації з азатіоприном. Мієлотоксичність мала оборотний характер і зникала протягом 4-6 тижнів після відміни противірусної терапії ХГС та азатіоприну. Після відновлення одного з видів лікування (противірусна терапія або азатіоприн) подібний ефект надалі не розвивався (див. також "Взаємодія з іншими лікарськими засобами"). Необхідно зважити потенційний ризик та користь перед початком терапії у пацієнтів з ХГС з невдачею раніше проведеної терапії та перервали терапію у зв'язку з гематологічними небажаними явищами, оскільки використання препарату Пегасіс у таких пацієнтів недостатньо вивчене. Ендокринна система При використанні інтерферонів альфа, у тому числі препарату Пегасіс®, спостерігалися порушення функції щитовидної залози або погіршення захворювань щитовидної залози, що існували раніше. Перед початком терапії препаратом Пегасіс слід досліджувати рівні ТТГ та Т4. Лікування препаратом Пегасис може бути розпочато або продовжено, якщо рівень ТТГ може підтримуватись у межах нормальних значень медикаментозно. У разі виникнення клінічних симптомів можливої дисфункції щитовидної залози необхідно досліджувати ТТГ під час терапії. Як і при терапії іншими інтерферонами, при застосуванні препарату Пегасіс® спостерігалися гіпоглікемія, гіперглікемія та цукровий діабет. Пацієнти з переліченими вище станами, які не піддаються адекватній корекції, не повинні починати монотерапію препаратом Пегасіс® або комбіновану терапію препаратом Пегасіс®/ рибавірином, а у разі розвитку подібних станів під час лікування терапію слід припинити. Серцево-судинна система Артеріальна гіпертензія, суправентрикулярні аритмії, хронічна серцева недостатність, біль у грудній клітці та інфаркт міокарда асоціювалися з терапією інтерферонами альфа, включаючи Пегасіс®. Пацієнтам із серцево-судинною патологією перед початком терапії рекомендується робити електрокардіограму. У разі погіршення серцево-судинного статусу терапію слід перервати або скасувати. У пацієнтів із серцево-судинними захворюваннями анемія може призвести до необхідності знизити дозу або припинити прийом рибавірину. Порушення функції печінки При розвитку печінкової недостатності Пегасіс слід відмінити. Як і при терапії іншими інтерферонами альфа, збільшення активності АЛТ порівняно з вихідним значенням спостерігалося під час терапії препаратом Пегасіс®, включаючи пацієнтів з вірусологічною відповіддю. При прогресуючому або клінічно значущому збільшенні активності АЛТ, незважаючи на зниження дози, або якщо це збільшення супроводжується підвищенням концентрації прямого білірубіну, терапію слід відмінити. На відміну від ХГС, при ХГВ загострення захворювання печінки нерідко зустрічається і супроводжується минущим і потенційно значущим підвищенням активності АЛТ. У клінічних дослідженнях раптове виражене підвищення активності АЛТ при терапії препаратом Пегасіс у пацієнтів з ХГВ супроводжувалося легкими змінами інших лабораторних показників без ознак декомпенсації функції печінки. У половині випадків раптового підвищення активності АЛТ, що у 10 разів перевищує верхню межу норми, доза препарату Пегасіс® була знижена або терапія була тимчасово відмінена до нормалізації показника, тоді як у другої половини пацієнтів терапію продовжували без змін. Рекомендується частіше контролювати функцію печінки у всіх випадках. Реакції гіперчутливості При терапії інтерфероном альфа рідко спостерігаються серйозні реакції гіперчутливості негайного типу (наприклад, кропив'янка, ангіоневротичний набряк, бронхоспазм, анафілаксія). У разі розвитку подібних реакцій терапію скасовують та негайно призначають відповідну медикаментозну терапію. Минущий висип не вимагає відміни терапії. Аутоімунні захворювання При лікуванні інтерферонами альфа описано виникнення аутоантитіл та аутоімунних захворювань. У групі підвищеного ризику перебувають пацієнти зі схильністю до розвитку аутоімунних захворювань. Пацієнти з ознаками або симптомами, подібними до ознак аутоімунних захворювань, повинні проходити ретельне обстеження та повторну оцінку співвідношення користі та ризику від продовження терапії інтерфероном. Є повідомлення про випадки розвитку синдрому Фогта-Коянагі-Харада (Vogt-Koyanagi-Harada (VKH) syndrome) у пацієнтів з ХГС, які отримували лікування інтерфероном. Цей синдром є гранулематозним запальним захворюванням, що вражає очі, слуховий апарат, мозкові оболонки і шкіру. При підозрі на синдром Фогта-Коянагі-Харада необхідно припинити противірусне лікування та розглянути можливість призначення глюкокортикостероїдної терапії. Гарячка та інфекції Незважаючи на те, що лихоманка може бути пов'язана з грипоподібним синдромом, який часто виникає при терапії інтерфероном, необхідно виключити інші причини персистуючої лихоманки (зокрема, серйозні бактеріальні, вірусні та грибкові інфекції), особливо у пацієнтів з нейтропенією. При прийомі інтерферонів альфа, включаючи Пегасіс®, повідомлялося про серйозні інфекції (бактеріальні, вірусні, грибкові). Слід негайно призначити відповідну специфічну терапію та скасувати Пегасіс®. Офтальмологічні зміни Як і при терапії іншими інтерферонами, при лікуванні препаратом Пегасіс® у поодиноких випадках відзначалася ретинопатія, включаючи крововилив у сітківку, "ватні" ексудати, набряк диска зорового нерва, неврит зорового нерва і тромбоз артерій або вен сітківки. Усім пацієнтам перед призначенням терапії необхідно провести офтальмологічне обстеження виявлення патології очного дна. З появою скарг на погіршення гостроти зору чи звуження полів зору слід негайно провести повне офтальмологічне обстеження. Пацієнтам із супутніми захворюваннями органу зору (наприклад, діабетична або гіпертонічна ретинопатія) необхідно проводити додаткові огляди під час терапії препаратом Пегасіс®. У разі виникнення або погіршення офтальмологічного захворювання терапію слід відмінити. Зміни органів дихання Як і при терапії інтерферонами альфа, при лікуванні препаратом Пегасіс® спостерігалися побічні реакції з боку органів дихання, включаючи задишку, легеневі інфільтрати, пневмонію та пневмоніт. При появі персистуючих (стійких) інфільтратів або інфільтратів неясного генезу або порушення функції дихання терапію слід відмінити. Зміни з боку шкіри Застосування інтерферонів альфа асоціювалося із загостренням або індукуванням псоріазу та саркоїдозу. Пацієнтам з псоріазом Пегасіс слід призначати з обережністю, а при появі або загостренні захворювання розглянути питання про відміну терапії. Пацієнти після трансплантації Безпека та ефективність монотерапії препаратом Пегасіс® або його комбінації з рибавірином у пацієнтів після трансплантації печінки та інших органів та тканин не встановлені. Як при призначенні інших інтерферонів альфа, при застосуванні препарату Пегасіс® як монотерапія або у комбінації з рибавірином виявлено випадки відторгнення печінкових та ниркових трансплантатів. Ко-інфекція ВІЛ-ХГС Перед початком лікування слід уважно ознайомитися з можливими побічними ефектами антиретровірусних препаратів, які пацієнт прийматиме разом із препаратами для терапії ХГС. У пацієнтів, які одночасно отримували ставудин та інтерферон з або без рибавірину, частота виникнення панкреатиту та/або лактацидозу склала 3%. Пацієнти з коінфекцією ВІЛ-ХГС, які отримують високоактивну антиретровірусну терапію (ВААРТ), можуть перебувати в групі ризику щодо розвитку лактацидозу. Тому слід дотримуватися обережності при додаванні препарату Пегасіс® та рибавірину до ВААРТ (див. інструкцію з медичного застосування рибавірину). У пацієнтів з ко-інфекцією та вираженим цирозом, які отримують ВААРТ, при лікуванні інтерферонами альфа, включаючи Пегасіс®, у комбінації з рибавірином або монотерапією, підвищений ризик розвитку фатальної печінкової недостатності. Вихідні показники, які можуть бути пов'язані з печінковою декомпенсацією у пацієнтів з коінфекцією та цирозом, включають: підвищений сироватковий білірубін, знижений Нb, підвищену лужну фосфатазу або знижений рівень тромбоцитів та лікування диданозином (ddl). Одночасне застосування рибавірину та зидовудину не рекомендується через підвищений ризик виникнення анемії. Необхідний ретельний моніторинг щодо виявлення ознак і симптомів печінкової декомпенсації (включаючи асцит, енцефалопатію, кровотечу з варикознорозширених вен, порушення синтетичної функції печінки; показник >7 балів за шкалою Чайлд-П'ю) у пацієнтів з ко-інфекцією. Показник за шкалою Чайлд-П'ю не завжди достовірно відображає наявність печінкової декомпенсації та може змінюватись під впливом таких факторів, як непряма гіпербілірубінемія, гіпоальбумінемія внаслідок медикаментозної терапії. При розвитку печінкової декомпенсації терапію препаратом Пегасіс слід негайно відмінити. Слід виявляти обережність при призначенні препарату Пегасіс® пацієнтам з низьким рівнем CD4+ лімфоцитів через недостатність даних щодо ефективності та безпеки застосування препарату Пегасіс® у пацієнтів з коінфекцією ВІЛ-ХГС із кількістю CD4+ лімфоцитів менше 200 клітин/мкл. Стоматологічні зміни У пацієнтів, які отримують комбіновану терапію препаратом Пегасіс® та рибавірином, спостерігалася патологія зубів та пародонту, яка може призвести до втрати зубів. Крім того, тривалий курс лікування препаратом Пегасіс® та рибавірином може викликати сухість порожнини рота, що руйнує вплив на зуби та слизову оболонку ротової порожнини. Пацієнти повинні ретельно чистити зуби двічі на день та регулярно проходити обстеження у стоматолога. У деяких пацієнтів може виникати блювання, після якого рекомендується ретельно полоскати рот. Використання пегінтерферону як тривалої підтримуючої терапії (використання поза зареєстрованими показаннями) У рандомізованому контрольованому дослідженні (HALT-C) у пацієнтів з ХГС та фіброзом різної стадії, які не відповіли на попередню терапію, при монотерапії препаратом Пегасіс® у дозі 90 мкг на тиждень протягом 3,5 років не відзначалося значного скорочення швидкості прогресування фіброзу або пов'язаних із ним клінічних явищ. Зростання та розвиток (діти) У дітей та підлітків віком від 5 до 17 років, які отримували комбіновану терапію препаратом Пегасіс® та рибавірином протягом 48 тижнів, часто спостерігалася затримка росту та уповільнення приросту маси тіла під час терапії. Через 2 роки після завершення лікування зниження відсотка для маси тіла на 15 і більше відсотків порівняно з вихідними значеннями спостерігалося у 16% дітей, а зниження відсотка для зростання на 15 і більше відсотків - у 11% дітей. Дані тривалого періоду спостереження припускають малоймовірність асоціації терапії препаратом Пегасіс з стійким гальмуванням зростання у дітей. Через 5-6 років після завершення лікування у дітей, що спостерігалося зниженням процентилю для зростання на 15 і більше відсотків порівняно з вихідними значеннями через 2 роки після завершення лікування, показники зростання поверталися до показників, порівнянним з вихідними значеннями, або були виявлені причини затримки зростання, не пов'язані з проведеним лікуванням. Вплив на здатність до керування автотранспортом та управління механізмами Пегасіс® надає слабкий або невеликий вплив на здатність до керування транспортними засобами та роботу з машинами та механізмами. У разі виникнення запаморочення, сонливості, сплутаності свідомості та стомлюваності, слід відмовитися від водіння транспортного засобу або роботи з машинами та механізмами.Умови відпустки з аптекЗа рецептомВідео на цю тему
Умови зберіганняУ прохолодному місці +8+15 градусУмови відпустки з аптекБез рецептаВідео на цю тему.
Склад, форма випуску та упаковкаТаблетки - 1 таб.: ментол 4 мг, олія евкаліптова 500 мкг. 10 шт. - Упаковки коміркові контурні.Фармакотерапевтична групаКомбінований препарат. Ментол - місцевоподразнюючий засіб, ефект якого в основному обумовлений рефлекторними реакціями, пов'язаними з подразненням чутливих слизових оболонок рецепторів. Має легку місцевоанестезуючу ("відволікаючу") дію, має слабкі антисептичні властивості. Евкаліптова олія має стимулюючу дію на рецептори слизових оболонок і чинить протизапальну та протимікробну дію.Клінічна фармакологіяФітопрепарат з протимікробною та протизапальною дією для місцевого застосування у ЛОР-практиці та стоматології.Показання до застосуванняЗапальні захворювання верхніх відділів дихальних шляхів (тонзиліт, ларингіт, фарингіт, трахеїт); кашель; риніт (гострий та хронічний).Протипоказання до застосуванняПідвищена чутливість до компонентів препарату.Побічна діяМожливі алергічні реакції.Спосіб застосування та дозиТаблетку слід тримати у роті до повного розсмоктування.Умови зберіганняУ прохолодному місці +8+15 градусУмови відпустки з аптекБез рецептаВідео на цю тему
8 180,00 грн
8 118,00 грн
Склад, форма випуску та упаковкаЛіофілізат - 1 фл. Активна речовина: пеметрекседу динатрію геміпентагідрат 121.4 мг, що відповідає вмісту пеметрекседу 100 мг. Допоміжні речовини: манітол - 106.4 мг, хлористоводнева кислота або натрію гідроксид (10% розчин, для підтримки рівня pH) - до pH 7.0. 100 мг – Флакони безбарвного скла (тип I) (1) – пачки картонні.Опис лікарської формиЛіофілізат для приготування розчину для інфузії у вигляді пористої маси від білого до білого з жовтуватим відтінком кольору.Фармакотерапевтична групаПротипухлинний засіб, антиметаболіт. Є антифолатом, інгібує тимідилат-синтетазу (TC), дигідрофолат-редуктазу (ДГФР), гліцинамід-рибонуклеотид-формілтрансферазу (ГАРФТ) – ключові фолат-залежні ферменти при біосинтезі тимідинових та пуринових нуклеотів. Пеметрексед надходить у клітини за допомогою переносника відновлених фолатів та білкових фолат-зв'язувальних транспортних систем. Вступаючи в клітину, пеметрексед швидко і ефективно перетворюється на поліглутаматні форми за допомогою ферменту фоліл-поліглутамат-синтетази. Поліглутаматні форми затримуються в клітинах і є потужнішими інгібіторами ТС, ГАРФТ. Поліглутамація - це процес, залежний від часу та концентрації, який зустрічається в пухлинних клітинах і, меншою мірою, у нормальних тканинах. У поліглутамованих метаболітів збільшений T1/2,внаслідок цього збільшується тривалість дії препарату на пухлинні клітини. При комбінованому застосуванні пеметрекседу та цисплатину у дослідженнях in vitro спостерігався синергізм протипухлинної дії.ФармакокінетикаУ рівноважному стані Vd пеметрекседу складає 16.1 л. Зв'язування із білками плазми – близько 81%. Пеметрексед обмежено піддається метаболізму печінки. У перші 24 години після введення 70-90% виводиться нирками в незміненому вигляді. Загальний плазмовий кліренс пеметрекседу становить 92 мл/хв, T1/2 із плазми становить 3.5 год у пацієнтів з нормальною функцією нирок. При нирковій недостатності тяжкого ступеня зв'язування з білками плазми не змінюється.Клінічна фармакологіяПротипухлинний препарат. Антиметаболіт.Показання до застосуванняМісцево-поширений або метастатичний неклітинний (несквамозний), недрібноклітинний рак легені - у комбінації з цисплатином як перша лінія терапії. Місцево-поширений або метастатичний неклітинний (несквамозний), недрібноклітинний рак легені без прогресування захворювання після чотирьох циклів першої лінії хіміотерапії на основі препаратів платини - для підтримуючої терапії. Місцево-поширений або метастатичний, неплоскоклітинний, недрібноклітинний рак легені - як монотерапія для терапії другої лінії. Лікування злоякісної мезотеліоми плеври у пацієнтів, які раніше не отримували хіміотерапію, з неоперабельною пухлиною або за наявності протипоказань до хірургічної операції.Протипоказання до застосуванняВагітність, лактація, підвищена чутливість до пеметрекседу. Пеметрексед не призначений для терапії пацієнтів з плоскоклітинним недрібноклітинним раком легені.Вагітність та лактаціяЗастосування при вагітності та в період лактації (грудного вигодовування) протипоказане. Застосування у дітей Пеметрексед не рекомендується використовувати у педіатрії, т.к. безпека та ефективність застосування у дітей не встановлена.Побічна діяЗ боку системи кровотворення: дуже часто – лейкопенія, нейтропенія, анемія; часто – тромбоцитопенія. З боку травної системи: дуже часто – нудота, блювання, анорексія, стоматит/фарингіт, діарея, підвищення рівня АЛТ та АСТ; часто – запори, біль у животі. Дерматологічні реакції: дуже часто - висипання/лущення; часто - свербіж шкіри, алопеція; рідко – багатоформна еритема. З боку периферичної нервової системи: часто – сенсорна чи моторна невропатія. З боку сечовидільної системи: часто – підвищення рівня креатиніну. З боку серцево-судинної системи: рідко – суправентрикулярна тахікардія. Інші: дуже часто – підвищена стомлюваність; часто - гарячка, фебрильна нейтропенія, алергічні реакції та приєднання вторинних інфекцій без нейтропенії.Взаємодія з лікарськими засобамиСпільне застосування з нефротоксичними препаратами та/або нирковими речовинами може знизити кліренс пеметрекседу. Результати досліджень in vitro свідчать, що пеметрексед мінімально взаємодіє з препаратами, які метаболізуються CYP3A, CYP2D6, CYP2C9, CYP1A2. Фармакокінетика пеметрекседу не змінюється при застосуванні фолієвої кислоти внутрішньо, вітаміну В12 в/м та при комбінованому застосуванні з цисплатином. Загальний кліренс платини не порушується під час застосування пеметрекседу. Пеметрексед можна застосовувати разом з ібупрофеном (по 400 мг 4 рази на добу) у хворих з нормальною функцією нирок (КК 80 мл/хв). При призначенні ібупрофену разом з пеметрекседом у хворих з нирковою недостатністю легкого або середнього ступеня тяжкості (КК 45-79 мл/хв) необхідно бути обережним. У пацієнтів з нирковою недостатністю легкого та середнього ступеня тяжкості не рекомендується застосування НПЗЗ з коротким T1/2 протягом 2 днів перед застосуванням пеметрекседу, в день застосування та протягом 2 днів після застосування. Зважаючи на відсутність даних про можливу взаємодію між пеметрекседом і НПЗЗ з великим T1/2, усі пацієнти, які отримують НПЗЗ, повинні перервати їх застосування мінімум за 5 днів до прийому пеметрекседу, в день прийому та протягом 2 днів після прийому. Якщо потрібне спільне призначення НПЗЗ, пацієнтам потрібен суворий моніторинг токсичності, особливо мієлосупресії та токсичності з боку шлунково-кишкового тракту. Пеметрексед несумісний із розчином Рінгера лактату та розчином Рінгера. Спільне застосування пеметрекседу з іншими препаратами та розчинами не досліджено і тому не рекомендується.Спосіб застосування та дозиВводять внутрішньовенно у вигляді інфузії. Режим дозування індивідуальний, залежно від показань, схеми лікування, функції печінки.Запобіжні заходи та особливі вказівкиПеред кожним введенням пеметрекседу необхідно проводити загальний аналіз крові з підрахунком лейкоцитарної формули та кількості тромбоцитів. Для оцінки функції нирок та печінки необхідно періодично проводити біохімічний аналіз крові. Перед початком застосування абсолютна кількість нейтрофілів становитиме ≥1500/мкл, тромбоцитів ≥100 000/мкл. Призначення фолієвої кислоти та вітаміну В12 знижує токсичність пеметрекседу та необхідність зменшення дози при гематологічній та негематологічній токсичності 3-4 ступеня, в т.ч. нейтропенії, фебрильної нейтропенії та інфекції з нейтропенією 3-4 ступеня. Хворим з клінічними проявами асциту та плевриту необхідно дренування випоту перед початком застосування пеметрекседу, тому що вплив цих станів на дію пеметрекседу не відомий. Пеметрексед не рекомендується використовувати у педіатрії, т.к. безпека та ефективність застосування у дітей не встановлена.Умови відпустки з аптекЗа рецептомВідео на цю тему
30 844,00 грн
30 756,00 грн
Склад, форма випуску та упаковкаЛіофілізат - 1 фл. Активна речовина: пеметрекседу динатрію геміпентагідрат 121.4 мг, що відповідає вмісту пеметрекседу 100 мг. Допоміжні речовини: манітол - 106.4 мг, хлористоводнева кислота або натрію гідроксид (10% розчин, для підтримки рівня pH) - до pH 7.0. 500 мг - Флакони безбарвного скла (тип I) (1) - пачки картонні.Опис лікарської формиЛіофілізат для приготування розчину для інфузії у вигляді пористої маси від білого до білого з жовтуватим відтінком кольору.Фармакотерапевтична групаПротипухлинний засіб, антиметаболіт. Є антифолатом, інгібує тимідилат-синтетазу (TC), дигідрофолат-редуктазу (ДГФР), гліцинамід-рибонуклеотид-формілтрансферазу (ГАРФТ) – ключові фолат-залежні ферменти при біосинтезі тимідинових та пуринових нуклеотів. Пеметрексед надходить у клітини за допомогою переносника відновлених фолатів та білкових фолат-зв'язувальних транспортних систем. Вступаючи в клітину, пеметрексед швидко і ефективно перетворюється на поліглутаматні форми за допомогою ферменту фоліл-поліглутамат-синтетази. Поліглутаматні форми затримуються в клітинах і є потужнішими інгібіторами ТС, ГАРФТ. Поліглутамація - це процес, залежний від часу та концентрації, який зустрічається в пухлинних клітинах і, меншою мірою, у нормальних тканинах. У поліглутамованих метаболітів збільшений T1/2,внаслідок цього збільшується тривалість дії препарату на пухлинні клітини. При комбінованому застосуванні пеметрекседу та цисплатину у дослідженнях in vitro спостерігався синергізм протипухлинної дії.ФармакокінетикаУ рівноважному стані Vd пеметрекседу складає 16.1 л. Зв'язування із білками плазми – близько 81%. Пеметрексед обмежено піддається метаболізму печінки. У перші 24 години після введення 70-90% виводиться нирками в незміненому вигляді. Загальний плазмовий кліренс пеметрекседу становить 92 мл/хв, T1/2 із плазми становить 3.5 год у пацієнтів з нормальною функцією нирок. При нирковій недостатності тяжкого ступеня зв'язування з білками плазми не змінюється.Клінічна фармакологіяПротипухлинний препарат. Антиметаболіт.Показання до застосуванняМісцево-поширений або метастатичний неклітинний (несквамозний), недрібноклітинний рак легені - у комбінації з цисплатином як перша лінія терапії. Місцево-поширений або метастатичний неклітинний (несквамозний), недрібноклітинний рак легені без прогресування захворювання після чотирьох циклів першої лінії хіміотерапії на основі препаратів платини - для підтримуючої терапії. Місцево-поширений або метастатичний, неплоскоклітинний, недрібноклітинний рак легені - як монотерапія для терапії другої лінії. Лікування злоякісної мезотеліоми плеври у пацієнтів, які раніше не отримували хіміотерапію, з неоперабельною пухлиною або за наявності протипоказань до хірургічної операції.Протипоказання до застосуванняВагітність, лактація, підвищена чутливість до пеметрекседу. Пеметрексед не призначений для терапії пацієнтів з плоскоклітинним недрібноклітинним раком легені.Вагітність та лактаціяЗастосування при вагітності та в період лактації (грудного вигодовування) протипоказане. Застосування у дітей Пеметрексед не рекомендується використовувати у педіатрії, т.к. безпека та ефективність застосування у дітей не встановлена.Побічна діяЗ боку системи кровотворення: дуже часто – лейкопенія, нейтропенія, анемія; часто – тромбоцитопенія. З боку травної системи: дуже часто – нудота, блювання, анорексія, стоматит/фарингіт, діарея, підвищення рівня АЛТ та АСТ; часто – запори, біль у животі. Дерматологічні реакції: дуже часто - висипання/лущення; часто - свербіж шкіри, алопеція; рідко – багатоформна еритема. З боку периферичної нервової системи: часто – сенсорна чи моторна невропатія. З боку сечовидільної системи: часто – підвищення рівня креатиніну. З боку серцево-судинної системи: рідко – суправентрикулярна тахікардія. Інші: дуже часто – підвищена стомлюваність; часто - гарячка, фебрильна нейтропенія, алергічні реакції та приєднання вторинних інфекцій без нейтропенії.Взаємодія з лікарськими засобамиСпільне застосування з нефротоксичними препаратами та/або нирковими речовинами може знизити кліренс пеметрекседу. Результати досліджень in vitro свідчать, що пеметрексед мінімально взаємодіє з препаратами, які метаболізуються CYP3A, CYP2D6, CYP2C9, CYP1A2. Фармакокінетика пеметрекседу не змінюється при застосуванні фолієвої кислоти внутрішньо, вітаміну В12 в/м та при комбінованому застосуванні з цисплатином. Загальний кліренс платини не порушується під час застосування пеметрекседу. Пеметрексед можна застосовувати разом з ібупрофеном (по 400 мг 4 рази на добу) у хворих з нормальною функцією нирок (КК 80 мл/хв). При призначенні ібупрофену разом з пеметрекседом у хворих з нирковою недостатністю легкого або середнього ступеня тяжкості (КК 45-79 мл/хв) необхідно бути обережним. У пацієнтів з нирковою недостатністю легкого та середнього ступеня тяжкості не рекомендується застосування НПЗЗ з коротким T1/2 протягом 2 днів перед застосуванням пеметрекседу, в день застосування та протягом 2 днів після застосування. Зважаючи на відсутність даних про можливу взаємодію між пеметрекседом і НПЗЗ з великим T1/2, усі пацієнти, які отримують НПЗЗ, повинні перервати їх застосування мінімум за 5 днів до прийому пеметрекседу, в день прийому та протягом 2 днів після прийому. Якщо потрібне спільне призначення НПЗЗ, пацієнтам потрібен суворий моніторинг токсичності, особливо мієлосупресії та токсичності з боку шлунково-кишкового тракту. Пеметрексед несумісний із розчином Рінгера лактату та розчином Рінгера. Спільне застосування пеметрекседу з іншими препаратами та розчинами не досліджено і тому не рекомендується.Спосіб застосування та дозиВводять внутрішньовенно у вигляді інфузії. Режим дозування індивідуальний, залежно від показань, схеми лікування, функції печінки.Запобіжні заходи та особливі вказівкиПеред кожним введенням пеметрекседу необхідно проводити загальний аналіз крові з підрахунком лейкоцитарної формули та кількості тромбоцитів. Для оцінки функції нирок та печінки необхідно періодично проводити біохімічний аналіз крові. Перед початком застосування абсолютна кількість нейтрофілів становитиме ≥1500/мкл, тромбоцитів ≥100 000/мкл. Призначення фолієвої кислоти та вітаміну В12 знижує токсичність пеметрекседу та необхідність зменшення дози при гематологічній та негематологічній токсичності 3-4 ступеня, в т.ч. нейтропенії, фебрильної нейтропенії та інфекції з нейтропенією 3-4 ступеня. Хворим з клінічними проявами асциту та плевриту необхідно дренування випоту перед початком застосування пеметрекседу, тому що вплив цих станів на дію пеметрекседу не відомий. Пеметрексед не рекомендується використовувати у педіатрії, т.к. безпека та ефективність застосування у дітей не встановлена.Умови відпустки з аптекЗа рецептомВідео на цю тему
1 434,00 грн
1 342,00 грн
Склад, форма випуску та упаковкаПігулки - 1 таб. Активні речовини: фінастерид – 5 мг; Допоміжні речовини: лактози моногідрат, крохмаль кукурудзяний, повідон K30, карбоксиметилкрохмаль натрію (тип А), докузат натрію, магнію стеарат. Склад плівкової оболонки: гіпромелоза 2910/5, макрогол 6000, тальк, титану діоксид, емульсія симетикону SE4, барвник заліза оксид жовтий. По 10 або 15 таблеток у блістері з ПВХ/ПВДХ/Аl. По 3 або 6 блістерів (10 таблеток) або по 2, 4 або 6 блістерів (по 15 таблеток) у картонній пачці разом з інструкцією із застосування.Опис лікарської формиКруглі, двоопуклі таблетки світло-жовтого кольору, покриті плівковою оболонкою.Фармакотерапевтична групаПрепарат для лікування доброякісної гіперплазії передміхурової залози. Інгібітор 5α-редуктази.ФармакокінетикаВсмоктування Cmax фінастериду в плазмі досягається приблизно через 2 години після прийому внутрішньо. Абсорбція фінастериду із шлунково-кишкового тракту завершується через 6-8 годин після прийому внутрішньо. Біодоступність фінастериду при вживанні становить приблизно 80% від внутрішньовенної референсної дози і не залежить від їди. Розподіл Зв'язування з білками плазми становить приблизно 93%. Плазмовий кліренс становить близько 165 мл/хв, що здається Vd - 76 л. При тривалій терапії спостерігається повільне накопичення фінастериду у невеликих кількостях. При щоденному прийомі фінастериду внутрішньо в дозі 5 мг його мінімальна Css у плазмі досягає 8-10 нг/мл і з часом залишається стабільною. У пацієнтів, які отримували препарат протягом 7-10 днів, фінастерид виявлявся у спинномозковій рідині. При прийомі препарату в дозі 5 мг/добу фінастерид у незначних кількостях виявляється у насінній рідині. Метаболізм та виведення T1/2 фінастериду в середньому дорівнює 6 годин. У чоловіків після одноразового прийому внутрішньо дози фінастериду, міченого 14С, 39% прийнятої дози виводиться нирками у вигляді метаболітів (незмінений фінастерид практично не виводиться нирками); 57% – через кишечник. У цьому дослідженні були ідентифіковані 2 метаболіти фінастериду, які мають незначну інгібуючу дію щодо 5α-редуктази порівняно з фінастеридом. Фармакокінетика в особливих клінічних випадках У літньому віці швидкість виведення фінастериду дещо знижується. З віком T1/2 збільшується: у чоловіків 18-60 років середній T1/2 становить 6 год, а у чоловіків старше 70 років - 8 год. потрібно. У пацієнтів з хронічною нирковою недостатністю (КК від 9 до 55 мл/хв) розподіл міченого 14С фінастериду при прийомі одноразової дози не відрізнявся від такого у здорових добровольців. Зв'язування фінастериду з білками плазми також не відрізнялося у пацієнтів з порушенням функції нирок. При нирковій недостатності частина метаболітів фінастериду, яка нормується екскретується нирками, виводиться через кишечник. Це проявляється збільшенням кількості метаболітів фінастериду в калі при відповідному зниженні їхньої концентрації в сечі. У пацієнтів з нирковою недостатністю, які не потребують гемодіалізу, корекція дози фінастериду не потрібна.ФармакодинамікаФінастерид - синтетична 4-азастероїдна сполука. Є специфічним конкурентним інгібітором 5α-редуктази II типу – внутрішньоклітинного ферменту, який перетворює тестостерон на активний андроген – дигідротестостерон (ДГТ). При доброякісній гіперплазії передміхурової залози (ДГПЗ) її збільшення залежить від перетворення тестостерону на ДГТ у простаті. Фінастерид високоефективно знижує концентрацію ДГТ як у плазмі, так і в тканині передміхурової залози. Пригнічення утворення ДГТ супроводжується зменшенням розмірів передміхурової залози, збільшенням максимальної швидкості сечовипускання та зниженням вираженості симптомів, пов'язаних із гіперплазією передміхурової залози. Фінастерид не має спорідненості з рецепторами андрогенів. Згідно з результатами клінічного дослідження (PLESS), в якому брали участь пацієнти з помірно або значно вираженими симптомами ДГПЗ та збільшенням передміхурової залози, финастерид знижував частоту виникнення гострої затримки сечі з 7/100 до 3/100 за 4-річний період, а частоту потреби у хірургічному. втручання (трансуретральної резекції простати (ТУРП) або простатектомії) - з 10/100 до 5/100. Ці зміни також асоціювалися з покращенням симптоматики ДГПЗ (зниження на 2 пункти за шкалою симптомів quasi-AUA), стійким зменшенням об'єму передміхурової залози приблизно на 20% та стабільним збільшенням швидкості струму сечі. Дослідження MTOPS (Medical Therapy Of Prostate Symptoms) тривалістю від 4 до 6 років, в рамках якого 3047 чоловіків із симптомами ДГПЗ були рандомізовані на групи, які отримують: фінастерид у дозі 5 мг на добу; доксазозин у дозі 4 мг на добу або 8 мг на добу; комбінацію фінастериду в дозі 5 мг на добу та доксазозину в дозі 4 мг на добу або 8 мг на добу; чи плацебо. Лікування призводило до значного зниження ризику клінічного прогресування ДГПЗ, яке на фоні застосування фінастериду становило 34% (р=0.002), доксазозину – 39% (рПоказання до застосуванняЛікування ДГПЗ та профілактика урологічних ускладнень з метою: зниження ризику гострої затримки сечі; зниження ризику необхідності проведення хірургічних втручань, зокрема. трансуретральної резекції (ТУР) передміхурової залози та простатектомії; Лікування з метою зменшення розмірів збільшеної передміхурової залози, поліпшення сечовипускання та зменшення вираженості симптомів, пов'язаних із ДГПЗ; У поєднанні з доксазозином зниження ризику прогресування симптомів, що з ДГПЖ.Протипоказання до застосуванняспадкова непереносимість лактози, дефіцит лактази або порушення всмоктування глюкози/галактози; вагітність та застосування препарату у жінок із збереженим репродуктивним потенціалом; вік до 18 років; підвищена чутливість до фінастериду та/або інших компонентів препарату. З обережністю слід призначати препарат пацієнтам з великим обсягом залишкової сечі та/або суттєво зниженою швидкістю сечовипускання (пацієнти повинні регулярно спостерігатися лікарем щодо виявлення обструктивної уропатії), пацієнтам з печінковою недостатністю, а також пацієнтам похилого віку.Вагітність та лактаціяЗастосування препарату Пенестер протипоказане при вагітності та жінкам із збереженим репродуктивним потенціалом. У зв'язку зі здатністю інгібіторів 5α-редуктази II типу пригнічувати перетворення тестостерону на дигідротестостерон, дані засоби, в т.ч. Фінастерид, при застосуванні у вагітних можуть викликати аномалії розвитку зовнішніх статевих органів у плода чоловічої статі. Фінастерид не показаний для застосування у жінок. Даних про екскрецію фінастериду із грудним молоком немає. Невеликі кількості фінастериду були виявлені у спермі пацієнтів, які отримували фінастерид у дозі 5 мг на добу. Хоча клінічні дані щодо впливу фінастериду на плід чоловічої статі відсутні, жінкам із збереженим репродуктивним потенціалом слід уникати контакту з насіннєвою рідиною чоловіків, які приймають фінастерид. Жінкам із збереженим репродуктивним потенціалом та вагітним слід уникати контакту з пошкодженими пігулками фінастериду, т.к. здатність препарату пригнічувати перетворення тестостерону на ДГТ може спричинити порушення розвитку статевих органів у плода чоловічої статі. Протипоказаний у віці до 18 років.Побічна діяНебажані реакції, виявлені під час клінічних досліджень (дослідження PLESS) Побічні реакції розділені за системно-органними класами відповідно до класифікації MedDRA. Частота побічних реакцій визначалася відповідно до наступної градації (класифікація ВООЗ): дуже часто (більше 1/10); часто (від понад 1/100 до менше 1/10); нечасто (від понад 1/1000 до 1/100); рідко (від понад 1/10000 до менше 1/1000); дуже рідко (від 1/10 000, включаючи окремі повідомлення). Порушення психіки: часто – зниження лібідо. З боку шкіри та підшкірних тканин: нечасто – шкірний висип. З боку статевих органів та молочної залози: часто – порушення сексуальної функції; нечасто – порушення еякуляції, зменшення обсягу еякуляту, збільшення грудних залоз, болючість у ділянці грудних залоз. В рамках дослідження MTOPS порівнювалося застосування фінастериду в дозі 5 мг/добу (n=768), доксазозину в дозі 4 мг/добу або 8 мг/добу (n=756), комбінованої терапії фінастеридом у дозі 5 мг/добу та доксазозином у дозі. 4 або 8 мг/добу (n=786), та плацебо (n=737). Відповідно до результатів даного дослідження профіль безпеки та переносимості комбінованої терапії загалом збігався з профілем її окремих компонентів. Частота порушень еякуляції у пацієнтів, які отримують комбіновану терапію, була сумісною із сумою частоти виникнення даного небажаного явища на тлі двох видів монотерапії. Було проведено 7-річне плацебо-контрольоване дослідження РСРТ, у якому брали участь 18 882 здорові чоловіки. Доступні для аналізу дані пункційної біопсії передміхурової залози були отримані щодо 9060 суб'єктів, при цьому рак передміхурової залози був виявлений у 803 (18.4%) чоловіків, які отримували фінастерид у добовій дозі 5 мг, і у 1147 (24.4%) чоловіків, що отримували плац. Згідно з результатами пункційної біопсії рак передміхурової залози з баловим показником 710 за шкалою Глісона був діагностований у 280 (6.4%) чоловіків з групи, які отримували фінастерид у добовій дозі 5 мг, у той час як у групі плацебо рак з таким ступенем диференціювання 5.1%) пацієнтів. Результати додаткового аналізу свідчили, що збільшення поширеності низькодиференційованого раку передміхурової залози,те, що спостерігалося в групі пацієнтів, які отримували фінастерид у добовій дозі 5 мг, може бути пояснено системною помилкою при оцінці результатів, пов'язаних із впливом терапії фінастеридом у дозі 5 мг 1 раз на добу на об'єм передміхурової залози. Із загальної кількості випадків раку передміхурової залози, діагностованих у цьому дослідженні, на момент постановки діагнозу приблизно 98% випадків було віднесено до локалізованого раку (клінічна стадія T1 або T2). Клінічна значимість даних про пухлинний процес зі ступенем диференціювання 7-10 балів за шкалою Глісон невідома.діагностованих у цьому дослідженні, на момент постановки діагнозу приблизно 98% випадків було віднесено до локалізованого раку (клінічна стадія T1 або T2). Клінічна значимість даних про пухлинний процес зі ступенем диференціювання 7-10 балів за шкалою Глісон невідома.діагностованих у цьому дослідженні, на момент постановки діагнозу приблизно 98% випадків було віднесено до локалізованого раку (клінічна стадія T1 або T2). Клінічна значимість даних про пухлинний процес зі ступенем диференціювання 7-10 балів за шкалою Глісон невідома. Відомості, отримані на підставі післяреєстраційного досвіду застосування препарату Частота небажаних реакцій невідома, т.к. на підставі отриманих даних встановити частоту та причинно-наслідковий зв'язок з дією фінастериду не завжди можливо, оскільки повідомлення про дані реакції надходили добровільно по популяції невідомого розміру. З боку імунної системи: частота невідома – реакції гіперчутливості, в т.ч. шкірний свербіж, кропив'янка, ангіоневротичний набряк (включаючи набряк губ, обличчя та гортані). З боку печінки та жовчовивідних шляхів: частота невідома – підвищення активності печінкових трансаміназ. З боку серцево-судинної системи: частота невідома – відчуття серцебиття. Порушення психіки: частота невідома – депресія, зниження лібідо, яке зберігається після припинення терапії. З боку статевих органів та молочної залози: частота невідома – сексуальна дисфункція (еректильна дисфункція та порушення еякуляції), яка зберігається після припинення лікування, болючість яєчок, чоловіче безпліддя та/або зниження якості насіннєвої рідини. Після відміни фінастериду якість насіннєвої рідини приходила до норми або покращувалася. Лабораторні показники При оцінці результатів лабораторних досліджень необхідно враховувати, що у пацієнтів, які отримують лікування фінастеридом, вміст ПСА у плазмі знижується. Більшість пацієнтів протягом перших місяців терапії відзначається швидке зниження показника ПСА з його наступною стабілізацією. Вихідне значення ПСА, що встановлюється після проведення терапії финастеридом, становить приблизно половину відповідного показника, що відзначалося на початок лікування. Таким чином, у пацієнтів, які отримують лікування фінастеридом протягом 6 місяців або більше, значення ПСА слід подвоювати порівняно з нормальними значеннями чоловіків, які не отримували лікування. Інших відмінностей у значеннях стандартних лабораторних показників між групами пацієнтів, які отримували фінастерид та плацебо, не спостерігалося.Взаємодія з лікарськими засобамиКлінічно значущої взаємодії коїться з іншими препаратами виявлено був. Фінастерид метаболізується переважно за участю ізоферменту CYP3A4 системи цитохрому Р450, не суттєво впливаючи на функцію цієї системи. Хоча ризик впливу фінастериду на фармакокінетику інших препаратів оцінюється як невисокий, існує ймовірність того, що інгібітори або індуктори ізоферменту CYP3A4 системи цитохрому Р450 впливатимуть на плазмову концентрацію фінастериду. Тим не менш, враховуючи наявні дані з безпеки, малоймовірним, що підвищення концентрації финастерида, пов'язане з супутнім застосуванням таких інгібіторів, матиме клінічне значення. Не було виявлено клінічно значущої взаємодії при комбінованому застосуванні фінастериду з пропранололом, дигоксином, глібенкламідом, варфарином, теофіліном та феназоном.Спосіб застосування та дозиПрепарат приймають внутрішньо по 5 мг 1 раз на добу, незалежно від їди. Тривалість терапії до оцінки її ефективності повинна становити не менше 6 місяців, тому курс лікування має бути досить тривалим. Фінастерид можна застосовувати у вигляді монотерапії, а також у комбінації з доксазозином. Немає достатніх клінічних даних щодо застосування препарату у пацієнтів із печінковою недостатністю. У пацієнтів з різними стадіями ниркової недостатності (при зниженні КК до 9 мл/хв) корекція дози не потрібна, оскільки спеціальні дослідження не продемонстрували жодних змін. фармакокінетичного профілю фінастериду Пацієнтам похилого віку корекція дози не потрібна, хоча фармакокінетичні дослідження вказують на те, що виведення фінастериду у пацієнтів віком від 70 років дещо знижується.ПередозуванняПацієнти отримували фінастерид одноразово в дозах до 400 мг, при багаторазовому введенні препарату в дозах до 80 мг на добу протягом 3 місяців небажаних реакцій не спостерігалося. Передозування фінастериду не потребує спеціального лікування.Запобіжні заходи та особливі вказівкиВказівки загального характеру Щоб уникнути обструктивних ускладнень, необхідно здійснювати ретельне спостереження пацієнтів з великим обсягом залишкової сечі та/або значно утрудненим сечовипусканням. Слід враховувати можливість виникнення потреби у хірургічному втручанні. Вплив на вміст ПСА та діагностику раку передміхурової залози До цього часу не доведено клінічних переваг застосування фінастериду у пацієнтів з раком передміхурової залози. У контрольованих клінічних дослідженнях у пацієнтів із ДГПЗ та підвищеною концентрацією ПСА у плазмі крові проводився моніторинг вмісту ПСА та результатів досліджень біопсії передміхурової залози. Було встановлено, що застосування фінастериду, мабуть, не змінює частоти виявлення раку передміхурової залози і не впливає на частоту його виникнення у пацієнтів, які приймали фінастерид або плацебо. Перед початком лікування та періодично в процесі терапії фінастеридом рекомендується проводити ректальне дослідження та застосовувати інші методи діагностики раку передміхурової залози. Визначення ПСА в плазмі також використовується для виявлення раку передміхурової залози. В цілому, вихідна концентрація ПСА вище 10 нг/мл говорить про необхідність подальшого обстеження пацієнта та проведення біопсії простати. При визначенні концентрації ПСА в межах 4-10 нг/мл потрібне подальше обстеження пацієнта. У чоловіків із ДГПЗ нормальні значення ПСА не дозволяють виключити рак передміхурової залози, незалежно від лікування фінастеридом. Вихідна концентрація ПСА нижче 4 нг/мл також не виключає рак передміхурової залози. Фінастерид викликає зменшення концентрації сироваткового ПСА приблизно на 50% у пацієнтів з ДГПЗ, навіть за наявності раку передміхурової залози. Даний факт необхідно брати до уваги при оцінці вмісту ПСА у пацієнтів із ДГПЗ, які отримують лікування фінастеридом, т.я. зниження концентрації ПСА не виключає наявності супутнього раку передміхурової залози. Це зниження очікується за будь-якого діапазону значень концентрації ПСА, хоча воно може відрізнятися у конкретних пацієнтів. Аналіз значень ПСА більш ніж у 3000 пацієнтів у 4-річному подвійному сліпому плацебо-контрольованому дослідженні PLESS підтвердив, що у пацієнтів, які приймали фінастерид протягом 6 місяців або більше, значення ПСА повинні бути подвоєні для їх порівняння з нормальними значеннями даного показника у пацієнтів, не одержують лікування препаратом.Ця корекція зберігає чутливість та специфічність аналізу ПСА та можливість виявлення раку передміхурової залози. Будь-яке збільшення концентрації ПСА, що зберігається, у пацієнтів, які отримують лікування фінастеридом, вимагає ретельного обстеження для з'ясування причини, яка може полягати в недотриманні режиму прийому препарату. Фінастерид суттєво не знижує відсоток вільного ПСА (ставлення вільного ПСА до загального). Цей показник залишається незмінним навіть під впливом прийому препарату. Якщо для діагностики раку передміхурової залози використовується відсоток вільного ПСА, корекція значень цього показника не є обов'язковою.вимагає ретельного обстеження для з'ясування причини, що може полягати у недотриманні режиму прийому препарату. Фінастерид суттєво не знижує відсоток вільного ПСА (ставлення вільного ПСА до загального). Цей показник залишається незмінним навіть під впливом прийому препарату. Якщо для діагностики раку передміхурової залози використовується відсоток вільного ПСА, корекція значень цього показника не є обов'язковою.вимагає ретельного обстеження для з'ясування причини, що може полягати у недотриманні режиму прийому препарату. Фінастерид суттєво не знижує відсоток вільного ПСА (ставлення вільного ПСА до загального). Цей показник залишається незмінним навіть під впливом прийому препарату. Якщо для діагностики раку передміхурової залози використовується відсоток вільного ПСА, корекція значень цього показника не є обов'язковою. Рак молочної залози у чоловіків У ході клінічних досліджень, а також протягом постреєстраційного періоду у чоловіків, які приймають финастерид, було виявлено випадки раку молочної залози. Лікарі повинні інструктувати своїх пацієнтів про необхідність негайно повідомляти про будь-які зміни тканини молочної залози, такі як поява ущільнень, біль, гінекомастія або виділення із сосків. Вплив на здатність до керування автотранспортом та управління механізмами Про несприятливий вплив препарату на здатність керувати транспортними засобами та працювати з механізмами не повідомлялося.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
466,00 грн
368,00 грн
Склад, форма випуску та упаковкаГранули – 1 пак. (5 г): Активні речовини: аскорбінова кислота 200 мг, кальцію глюконату моногідрат 200 мг, кофеїну моногідрат 20 мг, парацетамол 500 мг, рутозид (у формі тригідрату) 20 мг; Допоміжні речовини: повідон 17. 4 мг, цукор 3.
740,00 грн
334,00 грн
Склад, форма випуску та упаковкаГель для зовнішнього застосування - 1 г: Активні компоненти: кетопрофен – 50 мг; Допоміжні речовини: настоянка червоного стручкового перцю - 40 мг, диметилсульфоксид (димексид) - 30 мг, камфора - 30 мг, олія м'яти перцевої листя - 9 мг, гіпромелоза - 20 мг, натрію гідроксид - 7.5 мг, етанол 96% - 3 вода очищена – до 1000 мг. Гель по 30 г, 50 г або 100 г у тубах алюмінієвих з бушонами полімерними, за ТУ 9467-004-32807885-2008. Тубу разом з інструкцією із застосування поміщають у пачку з картону.Опис лікарської формиГель для зовнішнього застосування: прозорий або напівпрозорий, однорідний, від жовтуватого до червонувато-коричневого кольору, з характерним запахом; допускається наявність опалесценції та бульбашок повітря.Фармакотерапевтична групаНестероїдні протизапальні засоби для зовнішнього застосування.ФармакокінетикаПри прийомі внутрішньо та ректальному введенні кетопрофен добре абсорбується із ШКТ. Cmax у плазмі прийому внутрішньо досягається через 1-5 год (залежно від лікарської форми), при ректальному введенні - через 45-60 хв, внутрішньом'язовому введенні - через 20-30 хв, внутрішньовенному введенні - через 5 хв. Зв'язування із білками плазми становить 99%. Внаслідок вираженої ліпофільності швидко проникає через гематоенцефалічний бар'єр. Css у плазмі крові та спинномозковій рідині зберігається від 2 до 18 год. Кетопрофен добре проникає в синовіальну рідину, де його концентрація через 4 години після прийому перевищує таку в плазмі. Метаболізується шляхом зв'язування з глюкуроновою кислотою та меншою мірою за рахунок гідроксилювання. Виводиться головним чином нирками та значно меншою мірою через кишечник. T1/2 кетопрофену з плазми після прийому внутрішньо становить 1.5-2 год, після ректального введення - близько 2 год, після внутрішньом'язового введення - 1.27 год, після внутрішньовенного введення - 2 год.ФармакодинамікаНПЗЗ, похідне пропіонової кислоти. Чинить аналгетичну, протизапальну та жарознижувальну дію. Механізм дії пов'язаний з пригніченням активності ЦОГ – основного ферменту метаболізму арахідонової кислоти, що є попередником простагландинів, які відіграють головну роль у патогенезі запалення, болю та лихоманки. Виражена аналгетичну дію кетопрофену обумовлена двома механізмами: периферичним (опосередковано, через придушення синтезу простагландинів) і центральним (обумовленим інгібуванням синтезу простагландинів у центральній і периферичній нервовій системі, а також дією на біологічну активність інших нейротропних субстанцій, що грають ключову роль мозку). Крім того, кетопрофен має антибрадикінінову активність, стабілізує лізосомальні мембрани, викликає значне гальмування активності нейтрофілів у хворих з ревматоїдним артритом. Пригнічує агрегацію тромбоцитів.Показання до застосуванняСуглобовий синдром (ревматоїдний артрит, остеоартрит, анкілозуючий спондиліт, подагра); симптоматичне лікування запально-дегенеративних захворювань опорно-рухового апарату (періартрит, артросиновіт, тендиніт, тендосиновіт, бурсит, люмбаго), болі в хребті, невралгії, міалгії. Неускладнені травми, зокрема спортивні, вивихи, розтягнення або розрив зв'язок та сухожилля, забиття, посттравматичні болі. У складі комбінованої терапії запальних захворювань вен, лімфатичних судин, лімфовузлів (флебіт, перифлебіт, лімфангіїт, поверхневий лімфаденіт).Протипоказання до застосуванняДля прийому внутрішньо: ерозивно-виразкові ураження шлунково-кишкового тракту у фазі загострення, "аспіринова тріада", виражені порушення функції печінки та/або нирок; ІІІ триместр вагітності; вік до 15 років (для пігулок ретард); підвищена чутливість до кетопрофену та саліцилатів. Для ректального застосування: проктит та кровотечі з прямої кишки в анамнезі. Для зовнішнього застосування: мокнучі дерматози, екзема, інфіковані садна, рани.Вагітність та лактаціяПротипоказаний до застосування у III триместрі вагітності. У І та ІІ триместрах вагітності застосування кетопрофену можливе у випадках, коли потенційна користь для матері перевищує потенційний ризик для плода. При необхідності застосування кетопрофену у період лактації грудне вигодовування рекомендується припинити.Побічна діяЗ боку травної системи: біль в епігастральній ділянці, нудота, блювання, запор або діарея, анорексія, гастралгії, порушення функції печінки; рідко – ерозивно-виразкові ураження ШКТ, кровотечі та перфорації ШКТ. З боку центральної нервової системи: головний біль, запаморочення, шум у вухах, сонливість. З боку сечовидільної системи: порушення функції нирок. Алергічні реакції: шкірний висип; рідко – бронхоспазм. Місцеві реакції: при застосуванні у формі свічок можливе подразнення слизової оболонки прямої кишки, хвороблива дефекація; при застосуванні у формі гелю - свербіж, шкірний висип у місці нанесення.Взаємодія з лікарськими засобамиПри одночасному застосуванні кетопрофену з іншими НПЗЗ підвищується ризик розвитку ерозивно-виразкових уражень ШКТ та кровотеч; з антигіпертензивними засобами (в т.ч. з бета-адреноблокаторами, інгібіторами АПФ, діуретиками) – можливе зменшення їхньої дії; з тромболітиками – підвищення ризику розвитку кровотеч. При одночасному застосуванні з ацетилсаліциловою кислотою можливе зменшення зв'язування кетопрофену з білками плазми та збільшення його плазмового кліренсу; з гепарином, тиклопідином – підвищення ризику розвитку кровотеч; з препаратами літію – можливе підвищення концентрації літію у плазмі крові до токсичної за рахунок зниження його ниркової екскреції. При одночасному застосуванні з діуретиками підвищується ризик розвитку ниркової недостатності внаслідок зменшення ниркового кровотоку, зумовленого пригніченням синтезу простагландинів, і на тлі гіповолемії. При одночасному застосуванні з пробенецидом можливе зменшення кліренсу кетопрофену та його зв'язування з білками плазми; з метотрексатом – можливе посилення побічної дії метотрексату. При одночасному застосуванні варфарину можливий розвиток тяжких, іноді фатальних кровотеч.Спосіб застосування та дозиПрепарат призначений для зовнішнього застосування. Гель слід наносити на чисту суху шкіру. Невелику кількість гелю (3-5 см) наносять тонким шаром, з подальшим обережним втиранням у запалені або болючі ділянки тіла. Препарат слід наносити 2-3 десь у день. Тривалість курсу лікування не повинна перевищувати 14 днів.ПередозуванняПри випадковому застосуванні препарату в дозі, що перевищує рекомендовану, ризик розвитку симптомів передозування мінімальний у зв'язку із вкрай низькою системною абсорбцією кетопрофену при зовнішньому застосуванні. При появі місцевих побічних ефектів слід відмінити препарат та промити місце нанесення. При випадковому проковтуванні великих кількостей гелю можлива поява системних небажаних реакцій, притаманних НПЗП. Необхідне промивання шлунка, прийом активованого вугілля.Запобіжні заходи та особливі вказівкиЗ особливою обережністю застосовують у пацієнтів із захворюваннями печінки та нирок, захворюваннями ШКТ в анамнезі, диспептичними симптомами, одразу після серйозних хірургічних втручань. У процесі лікування необхідний систематичний контроль функції печінки та нирок.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаРозчин для ін'єкцій – 5%. Активна речовина: Пентаміну – 50 г; допоміжні речовини: води для ін'єкцій – до 1 л. в ампулах по 1 мл; в упакуванні 10 ампул.Опис лікарської формиПрозора безбарвна рідина.Фармакотерапевтична групаПрепарат має гангліоблокуючу активність. Блокує н-холінорецептори вегетативних гангліїв, гальмує передачу нервового збудження з прегангліонарних на постгангліонарні волокна вегетативних нервів. У великих дозах може блокувати н-холінорецептори нейром'язових синапсів та ЦНС. Перериваючи проведення нервових імпульсів через вегетативні ганглії, змінює функції органів, які мають вегетативну іннервацію.Показання до застосуванняГіпертонічний криз, спазми периферичних судин, кишечника та жовчовивідних шляхів, ниркова колька, бронхіальна астма (купування гострих нападів), еклампсія, каузалгія, набряк мозку, набряк легень; в анестезіології – для контрольованої гіпотонії; в урологічній практиці – при цистоскопії у чоловіків (для полегшення проходження цистоскопа через уретру).Протипоказання до застосуванняАртеріальна гіпотензія, інфаркт міокарда, закритокутова форма глаукоми, печінкова недостатність, ниркова недостатність, дегенеративні зміни ЦНС, тромбофлебіт.Вагітність та лактаціяДані щодо безпеки застосування азаметонію броміду при вагітності та в період лактації (грудного вигодовування) відсутні.Побічна діяСухість у роті, слабкість, запаморочення, тахікардія, мідріаз, ортостатична гіпотензія.Взаємодія з лікарськими засобамиГіпотензивний ефект препарату знижується при сумісному застосуванні з трициклічними антидепресантами, мезатоном, ефедрином; посилюється – з недеполяризуючими міорелаксантами, іншими антигіпертензивними засобами.Спосіб застосування та дозиПри спазмах судин та інших неекстренних станах препарат вводять внутрішньом'язово, початковій дозі 1 мл 5% розчину, при необхідності збільшують дозу до 1,5-2 мл 2-3 рази на день. Найвища разова доза дорослих -0,15 г (3 мл 5% розчину), добова - 0,45 г. При гіпертонічних кризах, набряку легень, набряку мозку, вводять внутрішньовенно повільно (під контролем АТ) 0,2 - 0,5 мл 5% розчину, розведених у 20 мл ізотонічного розчину хлориду натрію або 5% розчину глюкози або внутрішньом'язово 2 мл 5% розчину. Для керованої артеріальної гіпотензії внутрішньовенно краплинно перед операцією вводять 40-60 мг (0,8 - 1,2 мл 5% розчину), при необхідності - 120-180 мг (2,4 - 3,6 мл 5% розчину) . Препарат вводять внутрішньом'язово та внутрішньовенно.Запобіжні заходи та особливі вказівкиДля запобігання розвитку ортостатичної гіпотензії після введення препарату хворі повинні перебувати у положенні лежачи протягом 1-2 годин.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаГранули пролонгованої дії - 1 пак. Активні речовини: месалазин – 1000/2000 мг; Допоміжні речовини: етилцелюлоза – 4/8 мг – 15/30 мг, повідон – 50/100 мг. По 1 г або 2 г гранул у пакетик із поліефіру/алюмінієвої фольги/поліетилену низької щільності. По 50, 60, 100, 120 або 150 пакетиків у картонній пачці з інструкцією із застосування. По 30, 50, 60 або 120 пакетиків у картонній пачці з інструкцією із застосування.Опис лікарської формиЦиліндричні гранули від світло-сірого до світло-коричневого кольору.Фармакотерапевтична групаПротизапальний кишковий засіб.ФармакокінетикаПісля прийому внутрішньо месалазин повільно вивільняється з лікарської форми в дистальному відділі тонкої кишки та у товстій кишці. Зв'язування із білками плазми становить 43%. Метаболізується в слизовій оболонці кишечника та в печінці з утворенням N-ацетил-5-АСК. T1/2 становить 0.5-2 год. Месалазин виводиться із сечею, переважно в ацетильованій формі.ФармакодинамікаПротизапальний засіб із переважною локалізацією дії в кишечнику. Месалазин (5-аміносаліцилова кислота) інгібує активність нейтрофільної ліпооксигенази та синтез метаболітів арахідонової кислоти (простагландинів та лейкотрієнів), які є медіаторами запалення. Гальмує міграцію, дегрануляцію, фагоцитоз нейтрофілів, а також секрецію імуноглобулінів лімфоцитами. Месалазин має антиоксидантні властивості, зв'язуючись з вільними кисневими радикалами.Показання до застосуванняНеспецифічний виразковий коліт та хвороба Крона (профілактика та лікування загострень).Протипоказання до застосуваннязахворювання крові; виражені порушення функції печінки та/або нирок; Підвищена чутливість до препарату.Вагітність та лактаціяУ І триместрі вагітності застосування можливе лише за суворими показаннями. Якщо дозволяє індивідуальне перебіг захворювання, то останні 2-4 тижні вагітності прийом месалазину слід припинити. При необхідності застосування в період лактації слід вирішити питання про припинення грудного вигодовування через відсутність достатнього клінічного досвіду застосування месалазину у цієї категорії пацієнтів. Протипоказаний у дитячому віці до 2 років. Застосування у дітей віком до 2 років можливе лише у випадку, якщо передбачувана користь терапії перевищує потенційний ризик для дитини.Побічна діядіарея, нудота, печія, біль у животі; біль голови, порушення сну; шкірний висип, свербіж; порушення картини крові.Взаємодія з лікарськими засобамиПри одночасному застосуванні месалазину з азатіоприном, меркаптопурином підвищується токсичність азатіоприну та меркаптопурину; з варфарином – описаний випадок зменшення ефективності варфарину.Спосіб застосування та дозиГранули рекомендується приймати після їди, не розжовуючи. Вміст одного пакетика висипати на язик і запитати водою чи соком. Діти старше 6 років та підлітки: дозування підбирається індивідуально. Рекомендована доза в період загострення становить 20 - 30 мг месалазину на кілограм маси тіла на добу в кілька прийомів, максимальна разова доза не більше 75 мг/кг, максимальна добова доза не більше 4 г. Рекомендована доза становить 20 - 30 мг/кг/ добу, максимальна добова доза не більше 2 г. Дітям із масою тіла понад 40 кг рекомендується призначати дози для дорослих. Дорослі: дозування підбирається індивідуально. Рекомендована доза в період загострення до 4 г на добу, розділених на кілька прийомів, що підтримує терапія 2 - 4 г на добу, розділених на кілька прийомів. Тривалість терапії визначається лікарем.ПередозуванняВипадки передозування препаратом Пентаса рідкі. При передозуванні відсутні ознаки нефротоксичності або гепатотоксичності, але можуть виявитися симптоми отруєння саліцилатами, нудота, блювання, слабкість, сонливість, гіпервентиляція та набряк легень. Є повідомлення про пацієнтів, які приймали месалазин у дозі 8 г протягом місяця без побічних явищ. Специфічний антидот відсутній. Рекомендується проводити симптоматичну та підтримуючу терапію. При лікуванні стаціонарі необхідний ретельний контроль за функцією нирок.Запобіжні заходи та особливі вказівкиНа початку та протягом усього курсу лікування слід регулярно контролювати склад периферичної крові, рівень сечовини, креатиніну. У разі виражених патологічних змін складу крові (підвищена кровоточивість, підшкірні крововиливи, біль у горлі, лихоманка), розвитку перикардиту, міокардиту та синдрому гострої непереносимості препарат необхідно відмінити. Не рекомендується призначати дітям віком до 2 років.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаТаблетки пролонгованої дії – 1 табл.: активна речовина – месалазин 500 мг; допоміжні речовини: повідон; етилцелюлоза; магнію стеарат; тальк; МКЦ – до 750 мг. По 10 таблеток у блістер із алюмінієвої фольги. По 2, 3, 5, 6, 9 або 10 блістерів з інструкцією із застосування в картонну пачку. По 50 таблеток у пластиковому флаконі з кришкою, що загвинчується, запаяною термоплівкою, в картонній пачці з інструкцією та застосування. На картонну пачку можливе нанесення стікера для контролю першого розкриття.Опис лікарської формиТаблетки круглої форми, білого з сіруватим відтінком кольору з численними вкрапленнями світло-коричневого кольору з фаскою, ризиком та гравіюванням "500 mg" на одній стороні та "PENTASA" на іншій.Фармакотерапевтична групаПротизапальний кишковий засіб.ФармакокінетикаПісля прийому внутрішньо месалазин повільно вивільняється з лікарської форми в дистальному відділі тонкої кишки та у товстій кишці. Зв'язування із білками плазми становить 43%. Метаболізується в слизовій оболонці кишечника та в печінці з утворенням N-ацетил-5-АСК. T1/2 становить 0.5-2 год. Месалазин виводиться із сечею, переважно в ацетильованій формі.ФармакодинамікаПротизапальний засіб із переважною локалізацією дії в кишечнику. Месалазин (5-аміносаліцилова кислота) інгібує активність нейтрофільної ліпооксигенази та синтез метаболітів арахідонової кислоти (простагландинів та лейкотрієнів), які є медіаторами запалення. Гальмує міграцію, дегрануляцію, фагоцитоз нейтрофілів, а також секрецію імуноглобулінів лімфоцитами. Месалазин має антиоксидантні властивості, зв'язуючись з вільними кисневими радикалами.Показання до застосуванняНеспецифічний виразковий коліт та хвороба Крона (профілактика та лікування загострень).Протипоказання до застосуваннязахворювання крові; виражені порушення функції печінки та/або нирок; Підвищена чутливість до препарату.Вагітність та лактаціяУ І триместрі вагітності застосування можливе лише за суворими показаннями. Якщо дозволяє індивідуальне перебіг захворювання, то останні 2-4 тижні вагітності прийом месалазину слід припинити. При необхідності застосування в період лактації слід вирішити питання про припинення грудного вигодовування через відсутність достатнього клінічного досвіду застосування месалазину у цієї категорії пацієнтів. Протипоказаний у дитячому віці до 2 років. Застосування у дітей віком до 2 років можливе лише у випадку, якщо передбачувана користь терапії перевищує потенційний ризик для дитини.Побічна діядіарея, нудота, печія, біль у животі; біль голови, порушення сну; шкірний висип, свербіж; порушення картини крові.Взаємодія з лікарськими засобамиПри одночасному застосуванні месалазину з азатіоприном, меркаптопурином підвищується токсичність азатіоприну та меркаптопурину; з варфарином – описаний випадок зменшення ефективності варфарину.Спосіб застосування та дозиТаблетки рекомендується приймати після їжі не розжовуючи. Для полегшення проковтування таблетку можна розділити на кілька частин або розчинити у воді чи соці безпосередньо перед прийомом. Язвений коліт Гострий період: по 2 таблетки 2-4 десь у день. Підтримуюча терапія: по 1 таблетці 2-3 десь у день. Хвороба Крона Гострий період: по 2 – 4 таблетки 4 рази на день. Підтримуюча терапія: по 2-4 таблетки 2 рази на день або 2-3 таблетки 3 рази на день. Діти Доза підбирається індивідуально, зазвичай 20-30 мг месалазину на 1 кг маси тіла на добу в кілька прийомів.ПередозуванняВипадки передозування препаратом Пентаса рідкі. При передозуванні відсутні ознаки нефротоксичності або гепатотоксичності, але можуть виявитися симптоми отруєння саліцилатами, нудота, блювання, слабкість, сонливість, гіпервентиляція та набряк легень. Є повідомлення про пацієнтів, які приймали месалазин у дозі 8 г протягом місяця без побічних явищ. Специфічний антидот відсутній. Рекомендується проводити симптоматичну та підтримуючу терапію. При лікуванні стаціонарі необхідний ретельний контроль за функцією нирок.Запобіжні заходи та особливі вказівкиНа початку та протягом усього курсу лікування слід регулярно контролювати склад периферичної крові, рівень сечовини, креатиніну. У разі виражених патологічних змін складу крові (підвищена кровоточивість, підшкірні крововиливи, біль у горлі, лихоманка), розвитку перикардиту, міокардиту та синдрому гострої непереносимості препарат необхідно відмінити. Не рекомендується призначати дітям віком до 2 років.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаТаблетки пролонгованої дії – 1 табл.: активна речовина – месалазин 500 мг; допоміжні речовини: повідон; етилцелюлоза; магнію стеарат; тальк; МКЦ – до 750 мг. По 10 таблеток у блістер із алюмінієвої фольги. По 2, 3, 5, 6, 9 або 10 блістерів з інструкцією із застосування в картонну пачку. По 50 таблеток у пластиковому флаконі з кришкою, що загвинчується, запаяною термоплівкою, в картонній пачці з інструкцією та застосування. На картонну пачку можливе нанесення стікера для контролю першого розкриття.Опис лікарської формиТаблетки круглої форми, білого з сіруватим відтінком кольору з численними вкрапленнями світло-коричневого кольору з фаскою, ризиком та гравіюванням "500 mg" на одній стороні та "PENTASA" на іншій.Фармакотерапевтична групаПротизапальний кишковий засіб.ФармакокінетикаПісля прийому внутрішньо месалазин повільно вивільняється з лікарської форми в дистальному відділі тонкої кишки та у товстій кишці. Зв'язування із білками плазми становить 43%. Метаболізується в слизовій оболонці кишечника та в печінці з утворенням N-ацетил-5-АСК. T1/2 становить 0.5-2 год. Месалазин виводиться із сечею, переважно в ацетильованій формі.ФармакодинамікаПротизапальний засіб із переважною локалізацією дії в кишечнику. Месалазин (5-аміносаліцилова кислота) інгібує активність нейтрофільної ліпооксигенази та синтез метаболітів арахідонової кислоти (простагландинів та лейкотрієнів), які є медіаторами запалення. Гальмує міграцію, дегрануляцію, фагоцитоз нейтрофілів, а також секрецію імуноглобулінів лімфоцитами. Месалазин має антиоксидантні властивості, зв'язуючись з вільними кисневими радикалами.Показання до застосуванняНеспецифічний виразковий коліт та хвороба Крона (профілактика та лікування загострень).Протипоказання до застосуваннязахворювання крові; виражені порушення функції печінки та/або нирок; Підвищена чутливість до препарату.Вагітність та лактаціяУ І триместрі вагітності застосування можливе лише за суворими показаннями. Якщо дозволяє індивідуальне перебіг захворювання, то останні 2-4 тижні вагітності прийом месалазину слід припинити. При необхідності застосування в період лактації слід вирішити питання про припинення грудного вигодовування через відсутність достатнього клінічного досвіду застосування месалазину у цієї категорії пацієнтів. Протипоказаний у дитячому віці до 2 років. Застосування у дітей віком до 2 років можливе лише у випадку, якщо передбачувана користь терапії перевищує потенційний ризик для дитини.Побічна діядіарея, нудота, печія, біль у животі; біль голови, порушення сну; шкірний висип, свербіж; порушення картини крові.Взаємодія з лікарськими засобамиПри одночасному застосуванні месалазину з азатіоприном, меркаптопурином підвищується токсичність азатіоприну та меркаптопурину; з варфарином – описаний випадок зменшення ефективності варфарину.Спосіб застосування та дозиТаблетки рекомендується приймати після їжі не розжовуючи. Для полегшення проковтування таблетку можна розділити на кілька частин або розчинити у воді чи соці безпосередньо перед прийомом. Язвений коліт Гострий період: по 2 таблетки 2-4 десь у день. Підтримуюча терапія: по 1 таблетці 2-3 десь у день. Хвороба Крона Гострий період: по 2 – 4 таблетки 4 рази на день. Підтримуюча терапія: по 2-4 таблетки 2 рази на день або 2-3 таблетки 3 рази на день. Діти Доза підбирається індивідуально, зазвичай 20-30 мг месалазину на 1 кг маси тіла на добу в кілька прийомів.ПередозуванняВипадки передозування препаратом Пентаса рідкі. При передозуванні відсутні ознаки нефротоксичності або гепатотоксичності, але можуть виявитися симптоми отруєння саліцилатами, нудота, блювання, слабкість, сонливість, гіпервентиляція та набряк легень. Є повідомлення про пацієнтів, які приймали месалазин у дозі 8 г протягом місяця без побічних явищ. Специфічний антидот відсутній. Рекомендується проводити симптоматичну та підтримуючу терапію. При лікуванні стаціонарі необхідний ретельний контроль за функцією нирок.Запобіжні заходи та особливі вказівкиНа початку та протягом усього курсу лікування слід регулярно контролювати склад периферичної крові, рівень сечовини, креатиніну. У разі виражених патологічних змін складу крові (підвищена кровоточивість, підшкірні крововиливи, біль у горлі, лихоманка), розвитку перикардиту, міокардиту та синдрому гострої непереносимості препарат необхідно відмінити. Не рекомендується призначати дітям віком до 2 років.Умови відпустки з аптекЗа рецептомВідео на цю тему
576,00 грн
322,00 грн
Склад, форма випуску та упаковкаПігулки - 1 таб. Активна речовина: пентоксифілін 400 мг. Допоміжні речовини: кальцію стеарат, крохмаль картопляний, гіпромелоза (гідроксипропілметилцелюлоза), лактози моногідрат (цукор молочний), повідон (полівінілпіролідон низькомолекулярний). Склад оболонки: гіпромелоза (гідроксипропілметилцелюлоза), полісорбат 80 (твін 80), акрил-із (сополімер метакрилової кислоти з етилакрилатом 1:1 (40%), титану діоксид (15%), тальк (37.25%), триетилцитрат (4. , кремнію діоксид колоїдний безводний (1.25%), гідрокарбонат натрію (1.2%), натрію лаурилсульфат (0.5%)), кислотний червоний 2C або барвник азорубін (кармуазин). 10 шт. - упаковки контурні осередкові (2) - пачки картонні.Опис лікарської формиТаблетки з пролонгованим вивільненням, покриті плівковою оболонкою; рожевого кольору, круглі, двоопуклі; на поперечному розрізі ядро таблетки білого чи майже білого кольору.Фармакотерапевтична групаПрепарат Пентоксифілін-СЗ зменшує в'язкість крові та покращує реологічні властивості крові (плинність) за рахунок: покращення порушеної деформованості еритроцитів; зменшення агрегації тромбоцитів та еритроцитів; зниження концентрації фібриногену; зниження активності лейкоцитів та зменшення адгезії лейкоцитів до ендотелію судин. Як діюча речовина препарат Пентоксифілін-СЗ містить похідне ксантину – пентоксифілін. Механізм його дії пов'язаний з інгібуванням фосфодіестерази та накопиченням циклічного аденозинмонофосфату (цАМФ) у клітинах гладкої мускулатури судин та формених елементів крові. Виявляючи слабку міотропну судинну дію, пентоксифілін дещо зменшує ОПСС і незначно розширює коронарні судини. Пентоксифілін має слабкий позитивний інотропний ефект на серці. Покращує мікроциркуляцію у зонах порушеного кровообігу. Лікування препаратом Пентоксифілін-СЗ призводить до покращення симптоматики порушень мозкового кровообігу. При оклюзійних захворюваннях периферичних артерій застосування препарату Пентоксифілін-СЗ призводить до подовження дистанції ходьби, усунення нічних судом у литкових м'язах та зникнення болю у спокої.ФармакокінетикаВсмоктування Після прийому внутрішньо пентоксифілін майже повністю всмоктується. Пентоксифілін піддається ефекту "первинного проходження" через печінку. Абсолютна біодоступність вихідної субстанції становить 19±13%. Пролонговане вивільнення пентоксифіліну дозволяє підтримувати його постійну (безпікову) концентрацію в крові, що забезпечує кращу переносимість препарату у лікарській формі з пролонгованим вивільненням. Метаболізм та виведення Концентрація основного активного метаболіту 1-(5-гідроксигексил)-3,7-диметилксантину (метаболіт I) у плазмі крові в 2 рази перевищує концентрацію вихідного пентоксифіліну. Метаболіт I знаходиться з пентоксифіліном у оборотному біохімічному редокс-рівновазі. Тому пентоксифілін та метаболіт I розглядаються разом як активна одиниця. Внаслідок цього доступність активної субстанції значно більша. T1/2; пентоксифіліну після перорального введення становить 1.6 год. Пентоксифілін повністю метаболізується і більш ніж 90% виводиться нирками у формі некон'югованих водорозчинних метаболітів. Фармакокінетика у спеціальних груп пацієнтів У; пацієнтів з порушеннями функції нирок; виведення метаболітів уповільнюється. У; пацієнтів з порушеннями функції печінки; T1/2; пентоксифіліну подовжується і абсолютна біодоступність збільшується.Клінічна фармакологіяПрепарат, що покращує мікроциркуляцію. Ангіопротектор.Показання до застосуванняОклюзійна хвороба периферичних артерій атеросклеротичного або діабетичного генезу (наприклад, "переміжна" кульгавість, діабетична ангіопатія); трофічні порушення (наприклад, трофічні виразки гомілок, гангрена); порушення мозкового кровообігу (наслідки церебрального атеросклерозу, як, наприклад, зниження концентрації уваги, запаморочення, погіршення пам'яті), ішемічні та постінсультні стани; порушення кровообігу в сітківці та судинній оболонці ока; отосклероз, дегенеративні зміни на тлі патології судин внутрішнього вуха та зниження слуху.Протипоказання до застосуванняПідвищена чутливість до пентоксифіліну, інших метилксантинів або до будь-якої допоміжної речовини препарату; масивні кровотечі (ризик посилення кровотечі); великі крововиливу в сітчасту оболонку ока (ризик посилення кровотечі); крововилив у мозок; гострий інфаркт міокарда; вік до 18 років; вагітність (недостатньо даних); період грудного вигодовування (недостатньо даних); непереносимість галактози, дефіцит лактази та синдром глюкозо-галактозної мальабсорбції. З обережністю тяжкі порушення ритму серця (ризик погіршення аритмії); артеріальна гіпотензія (ризик подальшого зниження АТ); хронічна серцева недостатність; виразкова хвороба шлунка та дванадцятипалої кишки; порушення функції нирок (КК нижче 30 мл/хв) (ризик кумуляції та підвищений ризик розвитку побічних ефектів); тяжкі порушення функції печінки (ризик кумуляції та підвищений ризик побічних ефектів); нещодавно перенесені оперативні втручання; підвищений ризик розвитку кровотеч (наприклад, при порушеннях у системі згортання крові (ризик розвитку більш тяжких кровотеч)); одночасне застосування з антикоагулянтами (в т.ч. непрямими антикоагулянтами [антагоністами вітаміну К]); одночасне застосування з інгібіторами агрегації тромбоцитів (клопідогрел, ептифібатид, тирофібан, епопростенол, ілопрост, абциксимаб, анагрелід, НПЗП [крім селективних інгібіторів ЦОГ-2], ацетилсалідину кислота, тик) одночасне застосування з гіпоглікемічними засобами (інсуліном та гіпоглікемічними засобами для прийому внутрішньо); одночасне застосування з ципрофлоксацином; одночасне застосування з теофіліном.Вагітність та лактаціяПрепарат Пентоксифілін-СЗ протипоказаний до застосування при вагітності (бо недостатньо даних). Пентоксифілін проникає у грудне молоко у незначних кількостях. За необхідності застосування препарату слід припинити грудне вигодовування (з огляду на відсутність досвіду застосування).Побічна діяНижче представлені побічні реакції, що відзначалися у клінічних дослідженнях та при постмаркетинговому застосуванні препарату (частота невідома). З боку нервової системи: головний біль, запаморочення, асептичний менінгіт, судоми. Порушення психіки: ; ажитація, порушення сну, тривога. З боку серця: тахікардія, аритмія, зниження артеріального тиску, стенокардія. З боку судин: "припливи" крові до шкірних покривів, кровотечі (в т.ч. кровотечі з судин шкіри, слизових оболонок, шлунка, кишечника). З боку травної системи: ;ксеростомія (сухість порожнини рота), анорексія, атонія кишечника, відчуття тиску та переповнення в області шлунка, нудота, блювання, діарея, запор, гіперсалівація (підвищене слиновиділення). З боку печінки та жовчовивідних шляхів: внутрішньопечінковий холестаз, підвищення активності "печінкових" трансаміназ, підвищення активності ЛФ. З боку системи кровотворення та лімфатичної системи: ; лейкопенія/нейтропенія, тромбоцитопенія, панцитопенія, гіпофібриногенемія. З боку органу зору: порушення зору, худоби. З боку шкіри та підшкірних тканин: ; шкірний свербіж, шкірний висип, еритема (почервоніння шкіри), кропив'янка, ламкість нігтів, набряки. З боку імунної системи: анафілактичні/анафілактоїдні реакції, ангіоневротичний набряк, анафілактичний шок, бронхоспазм.Взаємодія з лікарськими засобамиЗ гіпотензивними засобами Пентоксифілін підвищує ризик розвитку артеріальної гіпотензії при одночасному застосуванні з гіпотензивними засобами (наприклад, інгібітори АПФ) або іншими лікарськими засобами, що мають потенційний антигіпертензивний ефект (наприклад, нітрати). З лікарськими засобами, що впливають на систему згортання крові Пентоксифілін може посилювати дію лікарських засобів, що впливають на систему згортання крові (прямі та непрямі антикоагулянти, тромболітики, антибіотики, такі як цефалоспорини). При сумісному застосуванні пентоксифіліну та непрямих антикоагулянтів (антагоністів вітаміну К) у постмаркетингових дослідженнях відзначалися випадки посилення антикоагулянтної дії (ризик розвитку кровотеч). Тому на початку прийому пентоксифіліну або зміні його дози рекомендується контролювати ступінь вираженості антикоагулянтної дії у пацієнтів, які приймають цю комбінацію препаратів, наприклад, проводити регулярний контроль МНО. З циметидином Циметидин підвищує концентрацію пентоксифіліну та активного метаболіту I у плазмі крові (ризик виникнення побічних ефектів). З іншими ксантинами Спільне призначення з іншими ксантинами може призводити до надмірного нервового збудження. З гіпоглікемічними засобами (інсуліном та гіпоглікемічними засобами для прийому внутрішньо) Гіпоглікемічна дія інсуліну або гіпоглікемічних засобів для внутрішнього застосування може посилюватися при одночасному застосуванні пентоксифіліну (підвищений ризик розвитку гіпоглікемії). Необхідний суворий контроль за станом таких пацієнтів, включаючи регулярний глікемічний контроль. З теофіліном У деяких пацієнтів при одночасному застосуванні пентоксифіліну та теофіліну відзначається збільшення концентрації теофіліну. Надалі це може призводити до збільшення або посилення побічних дій, пов'язаних із теофіліном. З ципрофлоксацином У деяких пацієнтів при одночасному застосуванні пентоксифіліну та ципрофлоксацину відзначається збільшення концентрації пентоксифіліну у плазмі крові. Надалі це може призводити до збільшення або посилення побічних дій, пов'язаних із застосуванням цієї комбінації. З інгібіторами агрегації тромбоцитів При одночасному застосуванні пентоксифіліну з інгібіторами агрегації тромбоцитів (клопідогрел, ептифібатид, тирофібан, епопростенол, ілопрост, абциксимаб, анагрелід, НПЗП [крім селективних інгібіторів ЦОГ-2], ацетилсаліц . Тому через ризик розвитку кровотечі слід з обережністю застосовувати пентоксифілін одночасно з переліченими вище інгібіторами агрегації тромбоцитів.Спосіб застосування та дозиТаблетки, покриті кишковорозчинною оболонкою (100 мг) Препарат приймають внутрішньо після їди. Таблетки покриті спеціальною оболонкою, розчинною в кишечнику, тому їх ковтають повністю, запиваючи невеликою кількістю води. Приймають по 200 мг (2 таблетки) 3 рази на добу. При необхідності дозу поступово збільшують до 1200 мг на добу, розділені на 2-3 прийоми. Максимальна добова доза – 1200 мг. Курс лікування 1-3 місяці. У пацієнтів з хронічною нирковою недостатністю (КК<10 мл/хв) дозу зменшують у 2 рази. Тривалість лікування та режим дозування препаратом Пентоксифілін-СЗ встановлюються лікарем індивідуально, залежно від клінічної картини захворювання та одержуваного терапевтичного ефекту. Таблетки з пролонгованим вивільненням (400 мг) Дозу встановлює лікар відповідно до індивідуальних особливостей хворого. Препарат слід ковтати повністю під час або відразу після їди, запиваючи достатньою кількістю води. Звичайна доза становить 1 таб. 400 мг 2 або 3 рази на добу. Максимальна добова доза – 1200 мг. У пацієнтів з порушенням функції нирок (КК<30 мл/хв) доза може бути знижена до 1-2 таблеток на добу. Зменшення дози, з урахуванням індивідуальної переносимості, необхідне у пацієнтів з тяжким порушенням функції печінки. Лікування може бути розпочато малими дозами у пацієнтів з низьким артеріальним тиском, а також у осіб, які перебувають у групі ризику через можливе зниження артеріального тиску (пацієнти з тяжкою формою ІХС або з гемодинамічно значущими стенозами судин головного мозку). У цих випадках доза може бути збільшена лише поступово.ПередозуванняСимптоми: запаморочення, нудота, блювання типу "кавової гущі", падіння АТ, тахікардія, аритмія, почервоніння шкірних покривів, втрата свідомості, озноб, арефлексія, тоніко-клонічні судоми. Лікування: ;у разі виникнення описаних вище порушень необхідно терміново звернутися до лікаря. Лікування симптоматичне. При появі перших ознак передозування (потівливість, нудота, ціаноз) негайно припиняють прийом препарату. Якщо препарат прийнято нещодавно, слід забезпечити заходи, спрямовані на запобігання подальшому всмоктування препарату шляхом його виведення (промивання шлунка) або уповільнення всмоктування (наприклад, прийом активованого вугілля). Особлива увага має бути спрямована на підтримання АТ та функції дихання. При судомних нападах вводять діазепам. Специфічний антидот невідомий.Запобіжні заходи та особливі вказівкиЛікування слід проводити під контролем артеріального тиску. У пацієнтів з цукровим діабетом, які приймають гіпоглікемічні засоби, призначення великих доз пентоксифіліну може спричинити виражену гіпоглікемію (може знадобитися корекція доз гіпоглікемічних засобів та проведення глікемічного контролю). При призначенні препарату Пентоксифілін-СЗ одночасно з антикоагулянтами необхідний контроль показників системи згортання крові. У пацієнтів, які недавно перенесли оперативне втручання, необхідний регулярний контроль гемоглобіну та гематокриту. Пацієнтам з низьким та нестабільним АТ необхідно зменшити дозу пентоксифіліну. У пацієнтів похилого віку може знадобитися зменшення дози пентоксифіліну (підвищення біодоступності та зниження швидкості виведення). Безпека та ефективність пентоксифіліну у дітей вивчені недостатньо. Куріння може знижувати терапевтичну ефективність препарату. Вплив на здатність до керування транспортними засобами та механізмами Враховуючи можливі побічні ефекти (наприклад, запаморочення), слід дотримуватися обережності при керуванні автотранспортом та заняттях потенційно небезпечними видами діяльності.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
420,00 грн
288,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
616,00 грн
292,00 грн
Склад, форма випуску та упаковкаТаблетки - 1; таб.: пентоксифілін 400 мг. 10 шт. - упаковки осередкові контурні (2) - пачки картонні.Опис лікарської формиТаблетки, вкриті кишковорозчинною оболонкою.Фармакотерапевтична групаЗасіб, що покращує мікроциркуляцію, ангіопротектор, похідне диметилксантину. Пентоксифілін зменшує в'язкість крові, викликає дезагрегацію тромбоцитів, підвищує еластичність еритроцитів (за рахунок впливу на патологічно змінену деформованість еритроцитів), покращує мікроциркуляцію та збільшує концентрацію кисню у тканинах. Підвищує концентрацію цАМФ у тромбоцитах та АТФ в еритроцитах з одночасним насиченням енергетичного потенціалу, що у свою чергу призводить до вазодилатації, зниження ОПСС, зростання ударного об'єму крові та хвилинного об'єму крові без значної зміни ЧСС. Розширюючи коронарні артерії, збільшує доставку кисню до міокарда, розширюючи судини легень, покращує оксигенацію крові. Підвищує тонус дихальної мускулатури (міжреберних м'язів та діафрагми). В/в введення, поряд із зазначеною вище дією, призводить до посилення колатерального кровообігу, збільшення об'єму крові через одиницю перерізу. Підвищує концентрацію АТФ у мозку, сприятливо впливає біоелектричну діяльність ЦНС. Покращує мікроциркуляцію у зонах порушеного кровопостачання. При оклюзійному ураженні периферичних артерій (переміжній хромоті) призводить до подовження дистанції ходьби, усунення нічних судом литкових м'язів і болів у спокої.ФармакокінетикаПісля прийому внутрішньо добре всмоктується із ШКТ. Зазначається незначний метаболізм при "першому проходженні" через печінку. Зв'язується із мембранами еритроцитів. Піддається біотрансформації спочатку в еритроцитах, потім у печінці. Деякі метаболіти є активними. T1/2 ;з плазми незміненої речовини становить 0.4-0.8 год, метаболітів - 1-1.6 год. Через 24 год більша частина дози виводиться із сечею у вигляді метаболітів, менша частина (близько 4%) - через кишечник. Виведення пентоксифіліну зменшується у пацієнтів похилого віку та при захворюваннях печінки.Клінічна фармакологіяПрепарат, що покращує мікроциркуляцію. Ангіопротектор.Показання до застосуванняПорушення периферичного кровообігу (в т.ч. при хромоті, що перемежується), пов'язані з хронічними оклюзійними розладами кровообігу в артеріальних судинах нижніх кінцівок. Ішемічне порушення мозкового кровообігу, ішемічний інсульт та постінсультні стани; церебральний атеросклероз (запаморочення, біль голови, порушення пам'яті, порушення сну), дисциркуляторна енцефалопатія, вірусна нейроінфекція (профілактика можливого порушення мікроциркуляції). ІХС, стан після перенесеного інфаркту міокарда. Діабетична ангіопатія. Гострі порушення кровообігу в сітківці та судинній оболонці ока, гостра ішемічна невропатія зорового нерва. Отосклероз, дегенеративні зміни на тлі патології судин внутрішнього вуха із поступовим зниженням слуху. ХОЗЛ, бронхіальна астма. Імпотенція судинного генезу.Протипоказання до застосуванняГострий інфаркт міокарда, порфірія, масивна кровотеча, геморагічний інсульт, крововилив у сітківку ока, вагітність, період лактації. Для внутрішньовенного введення (додатково) - аритмії, виражений атеросклероз коронарних або мозкових артерій, неконтрольована гіпотензія. Підвищена чутливість до пентоксифіліну та інших похідних ксантину.Вагітність та лактаціяАдекватних та добре контрольованих клінічних досліджень безпеки застосування пентоксифіліну при вагітності не проведено. Пентоксифілін та його метаболіти виділяються з грудним молоком. При необхідності застосування у період лактації слід припинити грудне вигодовування. Застосування у дітей З обережністю застосовувати у дітей та підлітків віком до 18 років (ефективність та безпека не вивчені).Побічна діяЗ боку ЦНС: головний біль, запаморочення; тривожність, порушення сну, судоми. Дерматологічні реакції: гіперемія шкіри обличчя, "припливи" крові до шкіри обличчя і верхньої частини грудної клітини, набряки, підвищена ламкість нігтів. З боку травної системи: ;сухість у роті, зниження апетиту, атонія кишечника, загострення холециститу, холестатичний гепатит, підвищення активності печінкових трансаміназ та ЛФ. З боку органу зору: порушення зору, худоби. З боку серцево-судинної системи: тахікардія, аритмія, кардіалгія, прогресування стенокардії, зниження артеріального тиску. З боку системи кровотворення: ;тромбоцитопенія, лейкопенія, панцитопенія. З боку системи згортання крові: гіпофібриногенемія, кровотечі з судин шкіри, слизових оболонок, шлунка, кишечника. Алергічні реакції: свербіж, гіперемія шкіри, кропив'янка, ангіоневротичний набряк, анафілактичний шок.Взаємодія з лікарськими засобамиПентоксифілін може потенціювати дію антигіпертензивних препаратів. На тлі парентерального застосування пентоксифіліну у високих дозах можливе посилення гіпоглікемічної дії інсуліну у пацієнтів із цукровим діабетом. При одночасному застосуванні з кеторолаком можливе підвищення ризику кровотеч та/або збільшення протромбінового часу; з мелоксикамом – підвищення ризику розвитку кровотеч; з симпатолітиками, гангліоблокаторами та вазодилататорами - можливе зниження АТ; з гепарином, фібринолітичними препаратами – посилення протизгортаючої дії. Циметидин значно збільшує концентрацію пентоксифіліну в плазмі, у зв'язку з цим при одночасному застосуванні може підвищуватися ймовірність розвитку побічних ефектів.Спосіб застосування та дозиЗастосовують внутрішньовенно (струменево або краплинно), внутрішньовенно (струменево або краплинно), внутрішньом'язово, внутрішньо. Доза та схема лікування встановлюються індивідуально.Запобіжні заходи та особливі вказівкиЗ обережністю застосовувати при лабільності АТ (схильність до артеріальної гіпотензії), хронічної серцевої недостатності, виразковій хворобі шлунка та дванадцятипалої кишки (для прийому внутрішньо), після нещодавно перенесених оперативних втручань, при печінковій та/або нирковій недостатності, у дітей та підлітків 18 років (ефективність та безпека не вивчені). При порушеннях функції нирок або тяжких порушеннях функції печінки потрібна корекція режиму дозування пентоксифіліну. У період лікування слід контролювати рівень артеріального тиску. При одночасному застосуванні з антигіпертензивними засобами, інсуліном, пероральними гіпоглікемічними препаратами може знадобитися зменшення дози пентоксифіліну. При одночасному застосуванні з антикоагулянтами слід ретельно контролювати показники зсідання крові.Умови відпустки з аптекЗа рецептомВідео на цю тему