Лекарства и БАД Хиты продаж
4 019,00 грн
326,00 грн
Склад, форма випуску та упаковкаРозчин – 1 амп.: Аллоферон [Гістидил-гліцил-валіл-серил-гліцил-гістидил-гліцил-глутамініл-гістидил-гліцил-валіл-гістидил-гліцин] 1,0 мг. Ліофілізат для виготовлення розчину для підшкірного введення 1,0 мг. 1,0 мг в ампулу із безбарвного скла. 1, 2, 3, 5 або 10 ампул поміщають у контурну коміркову упаковку. 1 або 2 контурні коміркові упаковки разом з інструкцією із застосування поміщають у пачку з картонуОпис лікарської формиЛіофілізований порошок або пориста біла маса. Гігроскопічний.Фармакотерапевтична групаПротивірусний, імуномодулюючий засіб.ФармакокінетикаШвидко проникає в кров, де взаємодіє з імунокомпетентними клітинами, після чого визначення концентрації Аллоферону утруднене через близьку структурну схожість його метаболітів із білками сироватки крові. Підвищення концентрації інтерферону відзначалося через 2 години після введення препарату та зберігалося на високому рівні (2-2,5 рази вище звичайного фонового) протягом 6-8 годин з досягненням вихідних значень до кінця доби. Підвищена функціональна активність природних кілерів спостерігалася протягом 7 днів після введення препарату.ФармакодинамікаАллоферон є олігопептид. За характером фармакологічної дії найбільш подібний до інтерферону альфа. Аллоферон є ефективним індуктором синтезу ендогенних інтерферонів та активатором системи природних кілерів, здатний стимулювати розпізнавання та лізис дефектних клітин цитотоксичними лімфоцитами. В експериментах продемонстрована висока ефективність щодо інфекцій, що викликаються вірусами грипу А та В, гепатиту В та С, герпесу 1 та 2 типів та папіломи людини (онкогенні типи). Аллоферон не має загальної токсичності, алергенних властивостей, мутагенної та канцерогенної дії, не має ембріотоксичної дії і не впливає на репродуктивну функцію.Показання до застосуванняХронічна папіломавірусна інфекція, спричинена онкогенними вірусами папіломи людини, хронічний рецидивуючий герпес 1 та 2 типів, у складі комплексної терапії середньотяжкої (жовтяничної) форми гострого гепатиту В.Протипоказання до застосуванняГіперчутливість, вагітність та грудне вигодовування (на час лікування припиняють), виражені аутоімунні захворювання. Дитячий вік.Побічна діяВ окремих випадках можливі слабкість, запаморочення, утворення нових елементів висипу (при герпетичній інфекції).Взаємодія з лікарськими засобамиПри лікуванні хронічного рецидивуючого генітального герпесу може призначатися в комбінації з ацикловіром і його похідними (препарати мають різний механізм дії і доповнюють один одного в лікуванні вірусної інфекції). При гострому гепатиті препарат призначається на тлі загальноприйнятої базисної терапії. Взаємодія з іншими лікарськими засобами не виявлено.Спосіб застосування та дозиПрепарат вводять підшкірно. Стандартний курс лікування інфекцій, спричинених онкогенними типами вірусу папіломи людини, включає ін'єкції препарату у дозі 1 мг через день, всього на курс 6 ін'єкцій. Стандартний курс лікування рецидиву герпесу включає ін'єкції препарату в дозі 1 мг через день, всього курс 3 ін'єкції. При середньотяжких формах гострого гепатиту препарат вводять після верифікації діагнозу в дозі 1 мг 3 рази на тиждень протягом 3-х тижнів (всього 9 ін'єкцій). Для приготування розчину для ін'єкцій як розчинник використовувати 1 мл 0,9 % розчину хлориду натрію.ПередозуванняДо цього часу випадків передозування препарату не було встановлено.Запобіжні заходи та особливі вказівкиУ монотерапії Алокін-альфа рекомендується використовувати для лікування папіломавірусної інфекції, спричиненої онкогенними типами вірусу, за відсутності клінічних та субклінічних уражень шийки матки та аногенітальної ділянки. У складі комплексної терапії - для лікування клінічних та субклінічних форм уражень шийки матки та аногенітальної області папіломавірусної інфекції, спричиненої онкогенними типами вірусу. Лікування хронічного рецидивуючого герпесу 1 і 2 типів рекомендується починати з появою найперших ознак захворювання. При гепатиті В - пізніше 7-го дня від початку появи жовтяниці. Вплив на здатність до керування автотранспортом та управління механізмами У разі запаморочення необхідно утриматися від керування автомобілем та роботи з технікою.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаГель: Активні інгредієнти: входять пептид Алостатин 1; допоміжні інгредієнти: вода, карбопол, алантоїн, феноксиетанол, етилгексілгліцерин, гідроксид натрію. Алломедін випускається по 4г і по 10г у тубі.ХарактеристикаАлломедин® - прозорий гідрогель, призначений для догляду за шкірою, а також захисту від порушення нормального функціонування. Алломедін® оптимально доглядає шкіру та слизові оболонки при проявах папіломавірусної інфекції. Він здатний призвести до усунення зовнішніх проявів папіломавірусної інфекції та перешкоджати виникненню повторних проявів. Алломедін®, завдяки властивостям пептиду Аллостатин 1, що входить до його складу, оптимально доглядає за чутливою шкірою губ, обличчя і тіла, сприяє відновленню та підтримці її еластичності, природного зовнішнього вигляду. Алломедін® — гідрогель без кольору та запаху, має легку текстуру, швидко вбирається, не залишаючи слідів на поверхні шкіри, що дозволяє застосовувати його одночасно з основним доглядом та наносити декоративну косметику. Алломедін® не має подразнюючої та сенсибілізуючої дії на шкіру. Фармакотерапевтична група: Противірусні засоби. Фармакологічна дія Алломедін® - інноваційний дерматологічний засіб, що містить унікальний синтетичний пептид Аллостатин®* 1, який призначений для захисту шкіри та слизових оболонок від проявів вірусних інфекцій, що викликають запальні процеси та новоутворення епітеліальних тканин. Алостатини – інноваційні синтетичні пептиди, створені з урахуванням природних алоферонов. Природні алоферони – речовини, виділені з імунної системи комах, що надають противірусну дію за рахунок активації цитотоксичних клітин (Т-кілерів та НК-клітин), що призводить до смерті інфікованих клітин шляхом апоптозу. Аллостатин® 1 зберігає всі властивості природних алоферонів і в той же час має ряд переваг, які роблять його застосування особливо перспективним у дерматології та косметології. Проникаючи в тканину епітелію, Аллостатин® 1 активує розпізнавання клітин імунної системи організму патологічно змінених клітин шкіри та слизових та запускає каскад фізіологічних реакцій, спрямованих на захист шкіри та слизових від проявів вірусних інфекцій. При цьому Аллостатин® 1 не надає шкідливої дії на навколишні нормальні клітини. Усуваючи прояви вірусних інфекцій та стимулюючи подальшу регенерацію епітелію, Аллостатин® 1 забезпечує швидке відновлення нормального стану шкіри. Алломедін® оптимально доглядає шкіру при появі перших симптомів герпесу та відновлює її природний вигляд. У цьому випадку неприємні суб'єктивні відчуття (печіння, свербіж, набряк, почервоніння) зникають вже за кілька годин і розвиток герпетичних висипів може припинитися. Якщо період перших симптомів загострення пропущено, для повного відновлення може знадобитися 3-6 днів. Досвід застосування Алломедіна показує, що частим результатом його використання є тривале збереження природного фізіологічного стану шкіри. Алломедін® оптимально доглядає шкіру та слизові оболонки при проявах папіломавірусної інфекції. Він здатний призвести до усунення зовнішніх проявів папіломавірусної інфекції та перешкоджати виникненню повторних проявів.Протипоказання до застосуванняАлломедін® відповідає високим стандартам безпеки дермато-косметологічних засобів. До цього часу будь-які небажані побічні ефекти застосування Алломедіну® не описані. Не виключає можливості індивідуальної непереносимості компонентів гелю окремими людьми. У разі його використання протипоказано. У ряді випадків застосування Алломедіна може викликати появу додаткових герпетичних висипань. Цей ефект пов'язаний із посиленням імунологічної активності організму. Така реакція може сприйматися як погіршення стану, проте вона сприяє виявленню та знищенню вогнищ розмноження вірусу та досягненню за рахунок цього стійкого позитивного ефекту. Існування прихованої вірусної інфекції може свідчити про можливий дефект у системі противірусного імунітету. З цього приводу слід проконсультуватися з лікарем-фахівцем (бажано імунологом).Побічна діяАлломедін® відповідає високим стандартам безпеки дермато-косметологічних засобів. До цього часу будь-які небажані побічні ефекти застосування Алломедіну® не описані. Не виключає можливості індивідуальної непереносимості компонентів гелю окремими людьми. У разі його використання протипоказано. У ряді випадків застосування Алломедіна може викликати появу додаткових герпетичних висипань. Цей ефект пов'язаний із посиленням імунологічної активності організму. Така реакція може сприйматися як погіршення стану, проте вона сприяє виявленню та знищенню вогнищ розмноження вірусу та досягненню за рахунок цього стійкого позитивного ефекту. Існування прихованої вірусної інфекції може свідчити про можливий дефект у системі противірусного імунітету. З цього приводу слід проконсультуватися з лікарем-фахівцем (бажано імунологом).Спосіб застосування та дозиАлломедин® рекомендується наносити тонким шаром на ділянки шкіри губ, обличчя та тіла особливо чутливі до зовнішніх впливів (сонячного опромінення, переохолодження, дегідратації, подразнення). Гель достатньо наносити 2-3 рази на день або при необхідності для відновлення та підтримання функціонального стану шкіри.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаГель: Активні інгредієнти: входять пептид Алостатин 1; допоміжні інгредієнти: вода, карбопол, алантоїн, феноксиетанол, етилгексілгліцерин, гідроксид натрію. Алломедін випускається по 4г і по 10г у тубі.ХарактеристикаАлломедин® - прозорий гідрогель, призначений для догляду за шкірою, а також захисту від порушення нормального функціонування. Алломедін® оптимально доглядає шкіру та слизові оболонки при проявах папіломавірусної інфекції. Він здатний призвести до усунення зовнішніх проявів папіломавірусної інфекції та перешкоджати виникненню повторних проявів. Алломедін®, завдяки властивостям пептиду Аллостатин 1, що входить до його складу, оптимально доглядає за чутливою шкірою губ, обличчя і тіла, сприяє відновленню та підтримці її еластичності, природного зовнішнього вигляду. Алломедін® — гідрогель без кольору та запаху, має легку текстуру, швидко вбирається, не залишаючи слідів на поверхні шкіри, що дозволяє застосовувати його одночасно з основним доглядом та наносити декоративну косметику. Алломедін® не має подразнюючої та сенсибілізуючої дії на шкіру. Фармакотерапевтична група: Противірусні засоби. Фармакологічна дія Алломедін® - інноваційний дерматологічний засіб, що містить унікальний синтетичний пептид Аллостатин®* 1, який призначений для захисту шкіри та слизових оболонок від проявів вірусних інфекцій, що викликають запальні процеси та новоутворення епітеліальних тканин. Алостатини – інноваційні синтетичні пептиди, створені з урахуванням природних алоферонов. Природні алоферони – речовини, виділені з імунної системи комах, що надають противірусну дію за рахунок активації цитотоксичних клітин (Т-кілерів та НК-клітин), що призводить до смерті інфікованих клітин шляхом апоптозу. Аллостатин® 1 зберігає всі властивості природних алоферонів і в той же час має ряд переваг, які роблять його застосування особливо перспективним у дерматології та косметології. Проникаючи в тканину епітелію, Аллостатин® 1 активує розпізнавання клітин імунної системи організму патологічно змінених клітин шкіри та слизових та запускає каскад фізіологічних реакцій, спрямованих на захист шкіри та слизових від проявів вірусних інфекцій. При цьому Аллостатин® 1 не надає шкідливої дії на навколишні нормальні клітини. Усуваючи прояви вірусних інфекцій та стимулюючи подальшу регенерацію епітелію, Аллостатин® 1 забезпечує швидке відновлення нормального стану шкіри. Алломедін® оптимально доглядає шкіру при появі перших симптомів герпесу та відновлює її природний вигляд. У цьому випадку неприємні суб'єктивні відчуття (печіння, свербіж, набряк, почервоніння) зникають вже за кілька годин і розвиток герпетичних висипів може припинитися. Якщо період перших симптомів загострення пропущено, для повного відновлення може знадобитися 3-6 днів. Досвід застосування Алломедіна показує, що частим результатом його використання є тривале збереження природного фізіологічного стану шкіри. Алломедін® оптимально доглядає шкіру та слизові оболонки при проявах папіломавірусної інфекції. Він здатний призвести до усунення зовнішніх проявів папіломавірусної інфекції та перешкоджати виникненню повторних проявів.Протипоказання до застосуванняАлломедін® відповідає високим стандартам безпеки дермато-косметологічних засобів. До цього часу будь-які небажані побічні ефекти застосування Алломедіну® не описані. Не виключає можливості індивідуальної непереносимості компонентів гелю окремими людьми. У разі його використання протипоказано. У ряді випадків застосування Алломедіна може викликати появу додаткових герпетичних висипань. Цей ефект пов'язаний із посиленням імунологічної активності організму. Така реакція може сприйматися як погіршення стану, проте вона сприяє виявленню та знищенню вогнищ розмноження вірусу та досягненню за рахунок цього стійкого позитивного ефекту. Існування прихованої вірусної інфекції може свідчити про можливий дефект у системі противірусного імунітету. З цього приводу слід проконсультуватися з лікарем-фахівцем (бажано імунологом).Побічна діяАлломедін® відповідає високим стандартам безпеки дермато-косметологічних засобів. До цього часу будь-які небажані побічні ефекти застосування Алломедіну® не описані. Не виключає можливості індивідуальної непереносимості компонентів гелю окремими людьми. У разі його використання протипоказано. У ряді випадків застосування Алломедіна може викликати появу додаткових герпетичних висипань. Цей ефект пов'язаний із посиленням імунологічної активності організму. Така реакція може сприйматися як погіршення стану, проте вона сприяє виявленню та знищенню вогнищ розмноження вірусу та досягненню за рахунок цього стійкого позитивного ефекту. Існування прихованої вірусної інфекції може свідчити про можливий дефект у системі противірусного імунітету. З цього приводу слід проконсультуватися з лікарем-фахівцем (бажано імунологом).Спосіб застосування та дозиАлломедин® рекомендується наносити тонким шаром на ділянки шкіри губ, обличчя та тіла особливо чутливі до зовнішніх впливів (сонячного опромінення, переохолодження, дегідратації, подразнення). Гель достатньо наносити 2-3 рази на день або при необхідності для відновлення та підтримання функціонального стану шкіри.Умови відпустки з аптекБез рецептаВідео на цю тему
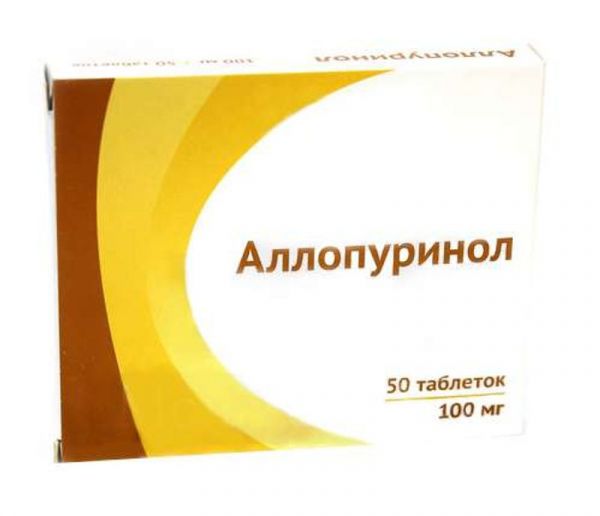
Склад, форма випуску та упаковкаПігулки - 1 таб. активні речовини: алопуринол – 100 мг; допоміжні речовини: сахароза (цукор-пісок рафінований) – 20 мг, крохмаль картопляний – 77.68 мг, магнію стеарат (магній стеариновокислий) – 1 мг, желатин харчовий – 1.32 мг. 10 шт. - упаковки осередкові контурні (5) - пачки картонні. 50 шт. - банки темного скла (1); - пачки картонні.Опис лікарської формиПігулки білого або білого з кремуватим відтінком кольору, плоскоциліндричної форми з фаскою.Фармакотерапевтична групаПротиподагричний засіб, ксантиноксидази, інгібітор.ФармакокінетикаПісля прийому внутрішньо майже повністю (на 90%) абсорбується із ШКТ. Метаболізується з утворенням аллоксантину, який зберігає здатність досить довго пригнічувати ксантиноксидазу. Cmax алопуринолу у плазмі крові досягається в середньому через 1.5 год, аллоксантину – через 4.5 год після одноразового прийому. T1/2 алопуринолу становить 1-2 год, аллоксантина - близько 15 год. Близько 20% прийнятої дози виводиться через кишечник, решта - нирками.ФармакодинамікаЗасіб, що порушує синтез сечової кислоти. Є структурним аналогом гіпоксантину. Інгібує фермент ксантиноксидазу, який бере участь у перетворенні гіпоксантину на ксантин та ксантину на сечову кислоту. Цим обумовлено зменшення концентрації сечової кислоти та її солей у рідких середовищах організму та сечі, що сприяє розчиненню наявних уратних відкладень та запобігає їх утворенню у тканинах та нирках. При прийомі алопуринолу підвищується виділення із сечею гіпоксантину та ксантину.Показання до застосуванняЛікування та профілактика подагри та гіперурикемії різного генезу (в т.ч. у поєднанні з нефролітіазом, нирковою недостатністю, уратною нефропатією). Рецидивні змішані оксалатно-кальцієві ниркові камені за наявності гіперурікозурії. Підвищена освіта уратів внаслідок ферментних порушень. Профілактика гострої нефропатії при цитостатичній та променевій терапії пухлин та лейкозів, а також при повному лікувальному голодуванні.Протипоказання до застосуванняВиражені порушення функції печінки та/або нирок, вагітність, лактація, підвищена чутливість до алопуринолу.Вагітність та лактаціяПротипоказаний до застосування при вагітності та в період лактації (грудного вигодовування). У дітей застосовують лише при злоякісних новоутвореннях (особливо лейкозах), а також при деяких ферментних порушеннях (синдром Льоша-Ніхена). Режим дозування встановлюється індивідуально, під контролем концентрації уратів та сечової кислоти в крові та сечі: дітям віком до 15 років – 10-20 мг/кг/добу або 100-400 мг/добу.Побічна діяЗ боку серцево-судинної системи: у поодиноких випадках – артеріальна гіпертензія, брадикардія. З боку травної системи: можливі диспептичні явища (в т.ч. нудота, блювання), діарея, підвищення транзиторної активності трансаміназ у сироватці крові; рідко – гепатит; у поодиноких випадках - стоматит, порушення функції печінки (минуще підвищення активності трансаміназ і ЛФ), стеаторея. З боку ЦНС та периферичної нервової системи: у поодиноких випадках – слабкість, підвищена стомлюваність, головний біль, запаморочення, атаксія, сонливість, депресія, кома, парези, парестезії, судоми, невропатії, порушення зору, катаракта, зміни сосочка зорового нерва, порушення смакових відчуттів. З боку системи кровотворення: в окремих випадках – тромбоцитопенія, агранулоцитоз та апластична анемія, лейкопенія (найбільш ймовірні у хворих з порушеннями функції нирок). З боку сечовидільної системи: рідко – інтерстиціальний нефрит; у поодиноких випадках – набряки, уремія, гематурія. З боку ендокринної системи: у поодиноких випадках – безпліддя, імпотенція, гінекомастія, цукровий діабет. З боку обміну речовин: у поодиноких випадках – гіперліпідемія. Алергічні реакції: шкірний висип, гіперемія, свербіж; в окремих випадках – ангіоімунобластна лімфаденопатія, артралгія, підвищення температури, еозинофілія, лихоманка, синдром Стівенса-Джонсона, синдром Лайєлла. Дерматологічні реакції: у поодиноких випадках – фурункульоз, алопеція, знебарвлення волосся.Взаємодія з лікарськими засобамиПри одночасному застосуванні алопуринол посилює дію кумаринових антикоагулянтів, аденіну арабінозиду, а також гіпоглікемічних препаратів (особливо у разі порушення функції нирок). Урикозуричні засоби та саліцилати у високих дозах знижують активність алопуринолу. При одночасному застосуванні алопуринолу та цитостатиків частіше проявляється мієлотоксична дія, ніж при роздільному застосуванні. При одночасному застосуванні алопуринолу та азатіоприну або меркаптопурину спостерігається кумуляція останніх в організмі, т.к. у зв'язку з інгібуванням алопуринолом активності ксантиноксидази, необхідної для біотрансформації лікарських засобів, уповільнюється їхній метаболізм та елімінація.Спосіб застосування та дозиВстановлюють індивідуально, під контролем концентрації уратів та сечової кислоти в крові та сечі. Дорослим прийому внутрішньо - 100-900 мг/сут, залежно від тяжкості перебігу захворювання. Частота прийому 2-4 рази на добу після їди. Дітям до 15 років - 10-20 мг/кг/сут або 100-400 мг/сут. Максимальні дози: при порушеннях функції нирок (в т.ч. обумовлених уратовою нефропатією) – 100 мг на добу. Збільшення дози можливе в тих випадках, коли на тлі терапії, що проводиться, зберігається підвищена концентрація уратів в крові і сечі.Запобіжні заходи та особливі вказівкиЗ обережністю слід застосовувати алопуринол при порушеннях функції печінки та нирок (в обох випадках необхідне зниження дози), гіпофункції щитовидної залози. У початковий період курсу терапії алопуринолом необхідне систематичне проведення оцінки показників функції печінки. У період лікування алопуринолом добова кількість рідини, що споживається, повинна бути не менше 2 л (під контролем діурезу). На початку курсу лікування подагри може виникнути загострення захворювання. Для профілактики можна застосовувати НПЗЗ або колхіцин (по 0.5 мг 3 рази на добу). Слід враховувати, що при адекватній терапії алопуринолом можливе розчинення великого уратного каміння в нирковій балії і подальше їх потрапляння в сечоводу. Асимптоматична гіперурикемія не є показанням до застосування алопуринолу. У дітей застосовують лише при злоякісних новоутвореннях (особливо лейкозах), а також при деяких ферментних порушеннях (синдром Льоша-Ніхена). Для корекції гіперурикемії у пацієнтів з пухлинними захворюваннями алопуринол рекомендується застосовувати перед початком лікування цитостатиками. У таких випадках слід застосовувати ефективну мінімальну дозу. Крім того, з метою зменшення ризику відкладення ксантинів у сечовивідних шляхах необхідно вжити заходів для підтримки оптимального діурезу та олужнення сечі. При одночасному застосуванні алопуринолу та цитостатиків необхідний більш частий контроль картини периферичної крові. У період прийому алопуринолу не допускається вживання алкоголю. Вплив на здатність до керування автотранспортом та управління механізмами З обережністю застосовувати у пацієнтів, діяльність яких потребує високої концентрації уваги та швидких психомоторних реакцій.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
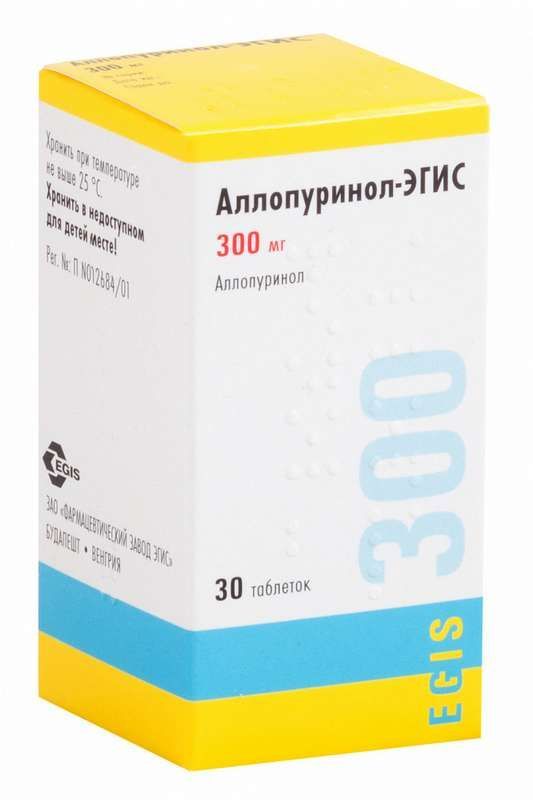
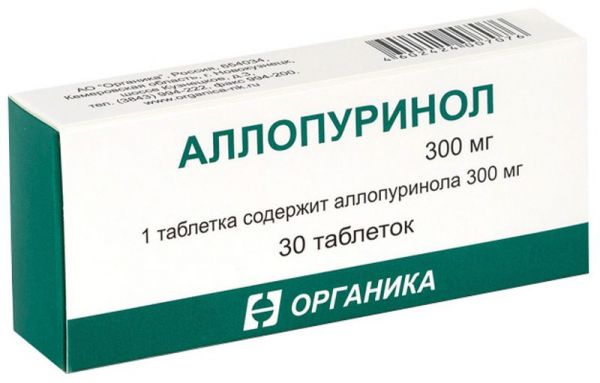
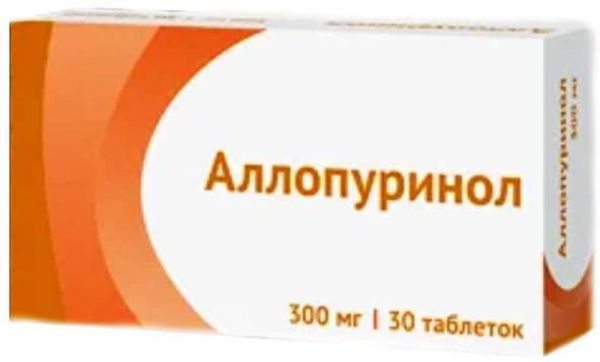
Склад, форма випуску та упаковкаПігулки - 1 таб. Алопурінол - 100,0 мг. допоміжні речовини: целюлоза мікрокристалічна – 54,0 мг; крохмаль кукурудзяний – 25,0 мг; карбоксиметилкрохмаль натрію – 10,0 мг; повідон-К25 – 8,0 мг; кремнію діоксид колоїдний – 1,0 мг; магнію стеарат – 2,0 мг. По 10, 14, 25 або 30 таблеток у контурне осередкове пакування з плівки полівінілхлоридної та фольги алюмінієвої друкованої лакованої. По 10, 20, 30, 40, 50 або 100 таблеток у банки з поліетилентерефталату для лікарських засобів або поліпропіленові для лікарських засобів, закупорені кришками з поліетилену високого тиску з контролем першого розтину, або кришками поліпропіленовими з системою "натиснути- з поліетилену низького тиску з контролем першого розтину. Одну банку або 1, 2, 3, 4, 5, 6, 7, 8, 9 або 10 контурних осередкових упаковок разом з інструкцією по застосуванню поміщають у картонну упаковку (пачку).Опис лікарської формиКруглі плоскоциліндричні пігулки білого або білого з жовтуватим відтінком кольору з ризиком з одного боку та фасками з двох боків.Фармакотерапевтична групаПротиподагричний засіб – ксантиноксидази інгібітор.ФармакокінетикаВсмоктування Алопуринол активний при пероральному застосуванні. Він швидко всмоктується із верхніх відділів шлунково-кишкового тракту. За даними фармакокінетичних досліджень, алопуринол визначається в крові вже через 30-60 хвилин після прийому. Біодоступність алопуринолу варіює від 67% до 90%. Максимальна концентрація препарату в плазмі зазвичай реєструється приблизно через 1,5 години після перорального прийому. Потім концентрація алопуринолу швидко знижується. Через 6 годин після прийому в плазмі визначається лише слідова концентрація препарату. Максимальна концентрація активного метаболіту - оксипуринола зазвичай реєструється через 3-5 годин після перорального прийому алопуринолу. Рівень оксипуринолу в плазмі знижується значно повільніше. Розподіл Алопуринол майже не зв'язується з білками плазми, тому зміни рівня зв'язування з білками не повинні значно впливати на кліренс препарату. Об'єм розподілу алопуринолу, що здається, становить приблизно 1,6 літра/кг, що говорить про досить виражене поглинання препарату тканинами. Вміст алопуринолу в різних тканинах людини не вивчений, проте дуже ймовірно, що алопуринол і оксипуринол у максимальній концентрації накопичуються в печінці та слизовій оболонці кишечника, де реєструється висока активність ксантиноксидази. Біотрансформація Під дією ксантиноксидази та альдегідоксидази алопуринол метаболізується з утворенням оксипуринолу. Оксипуринол пригнічує активність ксантиноксидази. Проте, оксипуринол - менш потужний інгібітор ксантиноксидази, проти аллопуринолом, проте його період напіввиведення значно більше. Завдяки цим властивостям після прийому разової добової дози алопуринолу ефективне пригнічення активності ксантиноксидази підтримується протягом 24 годин. У пацієнтів з нормальною функцією нирок вміст оксипуринолу в плазмі повільно збільшується аж до досягнення рівноважної концентрації. Після прийому алопуринолу в дозі 300 мг на добу, концентрація алопуринолу в плазмі крові, як правило, становить 5-10 мг/л. До інших метаболітів алопуринолу відносяться алопуринол-рибозид і оксипуринол-7-рибозид. Виведення Приблизно 20% прийнятого per os алопуринолу виводиться через кишечник у незміненому вигляді. Близько 10% добової дози екскретуються клубочковим апаратом нирки як незміненого аллопуринола. Ще 70% добової дози алопуринолу виводиться із сечею у формі оксипуринолу. Оксипуринол виводиться нирками у незміненому вигляді, однак у зв'язку з канальцевою реабсорбцією він має тривалий період напіввиведення. Період напіввиведення алопуринолу становить 1-2 години, тоді як період напіввиведення оксипуринолу варіює від 13 до 30 годин. Такі значні відмінності, ймовірно, пов'язані з відмінностями у структурі досліджень та/або кліренсі креатиніну у пацієнтів. Пацієнти з порушеною функцією нирок У пацієнтів з порушеною функцією нирок виведення алопуринолу та оксипуринолу може значно сповільнюватися, що при тривалій терапії призводить до зростання концентрації цих сполук у плазмі крові. У пацієнтів з порушеною функцією нирок та кліренсом креатиніну 10-20 мл/хв після тривалої терапії алопуринолом у дозі 300 мг на добу концентрація оксипуринолу в плазмі досягала орієнтовно 30 мг/л. Така концентрація оксипуринолу може визначатися у пацієнтів з нормальною функцією нирок на фоні терапії алопуринолом у дозі 600 мг на добу. Отже, при лікуванні пацієнтів із порушенням функції нирок дозу алопуринолу необхідно знижувати. Літні пацієнти У пацієнтів похилого віку значні зміни фармакокінетичних властивостей алопуринолу малоймовірні. Виняток становлять пацієнти із супутньою патологією нирок.ФармакодинамікаАлопуринол є структурним аналогом гіпоксантину. Алопуринол, а також його основний активний метаболіт – оксипуринол, пригнічують ксантиноксидазу – фермент, що забезпечує перетворення гіпоксантину на ксантин, та ксантину на сечову кислоту. Алопуринол зменшує концентрацію сечової кислоти у сироватці крові та сечі; таким чином він запобігає відкладенню кристалів сечової кислоти в тканинах та/або сприяє їх розчиненню. Крім придушення катаболізму пуринів у деяких (але не у всіх) пацієнтів з гіперурикемією, велика кількість ксантину та гіпоксантину стає доступною для повторного утворення пуринових основ, що призводить до пригнічення біосинтезу пуринів de novo за механізмом зворотного зв'язку, що опосередковано пригніченням ферменту гіпоксантин-гуанін. -трансферази. Інші метаболіти алопуринолу - алопуринол-рибозид та оксипуринол-7 рибозид.Показання до застосуванняПригнічення утворення сечової кислоти та її солей при підтвердженому накопиченні цих сполук (наприклад, подагра, шкірні тофуси, нефролітіаз) або передбачуваному клінічному ризику їх накопичення (наприклад, лікування злоякісних новоутворень може ускладнюватися розвитком гострої сечокислої нефропатії). До основних клінічних станів, які можуть супроводжуватися накопиченням сечової кислоти та її солей, відносяться: ідіопатична подагра; сечокам'яна хвороба (утворення конкрементів із сечової кислоти); гостра сечокисла нефропатія; пухлинні захворювання та мієлопроліферативний синдром з високою швидкістю оновлення клітинної популяції, коли гіперурикемія виникає спонтанно або після проведення цитотоксичної терапії; певні ферментативні порушення, що супроводжуються гіперпродукцією солей сечової кислоти, наприклад, знижена активність гіпоксантин-гуанін-фосфорибозилтрансферази (включаючи синдром Льоша-Найхана), знижена активність глюкозо-6-фосфатази (включаючи глікогенози -амідо-трансферази, знижена активність аденін-фосфорибозилтрансферази Лікування сечокам'яної хвороби, що супроводжується утворенням 2,8-дигідроксиаденінових (2,8-ДГА) конкрементів у зв'язку зі зниженою активністю аденін-фосфорибозилтрансферази. Профілактика та лікування сечокам'яної хвороби, що супроводжується утворенням змішаних кальцієво-оксалатних конкрементів на тлі гіперурікозурії, коли дієта та підвищене споживання рідини були безуспішними.Протипоказання до застосуванняГіперчутливість до алопуринолу або будь-якої з допоміжних речовин, що входять до складу препарату. Печінкова недостатність, хронічна ниркова недостатність (стадія азотемії), первинний гемохроматоз, безсимптомна гіперурикемія, гострий напад подагри, дитячий вік до 3-х років (з урахуванням твердої лікарської форми) Вагітність, період грудного вигодовування. З обережністю: Порушення функції печінки, гіпотиреоз, цукровий діабет, артеріальна гіпертензія, одночасний прийом інгібіторів ангіотензинперетворюючого ферменту (АПФ) або діуретиків, дитячий вік (до 15 років призначають тільки під час цитостатичної терапії лейкозів та ін. злоякісних захворювань; літній вік.Вагітність та лактаціяВ даний час даних щодо безпеки терапії алопуринолом у період вагітності недостатньо, хоча цей препарат широко застосовувався протягом довгих років без явних несприятливих наслідків. Вагітним жінкам не слід приймати таблетки Алопуринол, за винятком тих випадків, коли не існує менш небезпечного альтернативного лікування та захворювання становить більший ризик для матері та плода, ніж прийом препарату. Згідно з наявними повідомленнями, алопуринол та оксипуринол виділяються з грудним молоком. У жінок, які приймають алопуринол у дозі 300 мг/добу, концентрація алопуринолу та оксипуринолу у грудному молоці досягала, відповідно, 1,4 мг/л та 53,7 мг/л. Проте, відомостей про вплив алопуринолу та його метаболітів на немовлят, які перебувають на грудному вигодовуванні, відсутні. Таким чином, препарат Алопуринол таблетки не рекомендується в період грудного вигодовування.Побічна діяВідсутні сучасні клінічні дані визначення частоти розвитку побічних ефектів. Їх частота може варіювати в залежності від дози та від того, чи призначався препарат як монотерапія або у комбінації з іншими препаратами. Класифікація частоти розвитку побічних ефектів заснована на приблизній оцінці, більшість побічних ефектів відсутні дані визначення частоти їх розвитку. Класифікація небажаних реакцій залежно від частоти народження виглядає наступним чином: дуже часті (≥1/10), часті (від ≥1/100 до Небажані реакції, пов'язані з терапією алопуринолом, що спостерігаються в постреєстраційному періоді, зустрічаються рідко або дуже рідко. У загальній популяції пацієнтів, здебільшого, мають легкий характер. Частота розвитку небажаних явищ збільшується при порушеннях функції нирок та (або) печінки. Інфекції та паразитарні захворювання: дуже рідкісні – фурункульоз. Порушення з боку системи крові та лімфатичної системи: дуже рідкісні – агранулоцитоз, апластична анемія, тромбоцитопенія, гранулоцитоз, лейкопенія, лейкоцитоз, еозинофілія та аплазія, що стосується лише еритроцитів. Дуже рідко надходили повідомлення про тромбоцитопенію, агранулоцитоз і апластичні анемії, особливо у осіб з порушеннями функції нирок та/або печінки, що наголошує на необхідності прояву особливої обережності у цих груп пацієнтів. Порушення з боку імунної системи: нечасті – реакції гіперчутливості; рідкісні - тяжкі реакції гіперчутливості, включаючи шкірні реакції з відшаруванням епідермісу, лихоманкою, лімфаденопатією, артралгією та (або) еозинофілією (у тому числі синдром Стівенса-Джонсона та токсичний епідермальний некроліз). Супутній васкуліт або реакції з боку тканини можуть мати різні прояви, включаючи гепатит, ураження нирок, гострий холангіт, ксантинові конкременти і, в окремих випадках, судоми. Крім того, дуже рідко спостерігався розвиток анафілактичного шоку. При розвитку тяжких небажаних реакцій терапію алопуринолом необхідно негайно припинити та не відновлювати.При відстроченій мультиорганній гіперчутливості (відомій як синдром лікарської гіперчутливості /DRESS/) можуть розвиватися такі симптоми в різних комбінаціях: лихоманка, шкірний висип, васкуліт, лімфаденопатія, псевдолімфома, артралгія, лейкопенія, еозинофілія, гепатоспленом проток (руйнування або зникнення внутрішньопечінкових жовчних проток). При розвитку таких реакцій у будь-який період лікування Алопуринол слід негайно скасувати і ніколи не відновлювати. Генералізовані реакції гіперчутливості розвивалися у пацієнтів з порушеною функцією нирок та печінки. Такі випадки іноді мали летальний кінець; дуже рідкісні – ангіоімунобластна лімфаденопатія.псевдолімфома, артралгія, лейкопенія, еозинофілія, гепатоспленомегалія, зміна результатів печінкових функціональних тестів, синдром жовчних проток, що зникають (руйнування або зникнення внутрішньопечінкових жовчних проток). При розвитку таких реакцій у будь-який період лікування Алопуринол слід негайно скасувати і ніколи не відновлювати. Генералізовані реакції гіперчутливості розвивалися у пацієнтів з порушеною функцією нирок та печінки. Такі випадки іноді мали летальний кінець; дуже рідкісні – ангіоімунобластна лімфаденопатія.псевдолімфома, артралгія, лейкопенія, еозинофілія, гепатоспленомегалія, зміна результатів печінкових функціональних тестів, синдром жовчних проток, що зникають (руйнування або зникнення внутрішньопечінкових жовчних проток). При розвитку таких реакцій у будь-який період лікування Алопуринол слід негайно скасувати і ніколи не відновлювати. Генералізовані реакції гіперчутливості розвивалися у пацієнтів з порушеною функцією нирок та печінки. Такі випадки іноді мали летальний кінець; дуже рідкісні – ангіоімунобластна лімфаденопатія.Алопуринол слід негайно відмінити і ніколи не відновлювати. Генералізовані реакції гіперчутливості розвивалися у пацієнтів з порушеною функцією нирок та печінки. Такі випадки іноді мали летальний кінець; дуже рідкісні – ангіоімунобластна лімфаденопатія.Алопуринол слід негайно відмінити і ніколи не відновлювати. Генералізовані реакції гіперчутливості розвивалися у пацієнтів з порушеною функцією нирок та печінки. Такі випадки іноді мали летальний кінець; дуже рідкісні – ангіоімунобластна лімфаденопатія. Ангіоімунобластну лімфаденопатію дуже рідко діагностували після біопсії лімфовузлів з приводу генералізованої лімфаденопатії. Ангіоімунобластна лімфаденопатія носить оборотний характер і регресує після припинення терапії алопуринолом. Порушення з боку обміну речовин та харчування: дуже рідкісні – цукровий діабет, гіперліпідемія. Порушення психіки: дуже рідкісні – депресія. Порушення з боку нервової системи: дуже рідкісні – кома, параліч, атаксія, нейропатія, парестезія, сонливість, головний біль, збочення смакових відчуттів. Порушення органу зору: дуже рідкісні - катаракта, порушення зору, макулярні зміни. Порушення з боку органу слуху та лабіринтні розлади: дуже рідкісні – запаморочення (вертиго). Порушення з боку серця: дуже рідкісні – стенокардія, брадикардія. Порушення з боку судин: дуже рідкісні – підвищення артеріального тиску. Порушення з боку шлунково-кишкового тракту: нечасті – блювання, нудота, діарея. У раніше проведених клінічних дослідженнях спостерігали нудоту та блювоту, проте пізніші спостереження підтвердили, що ці реакції не є клінічно значущою проблемою і їх можна уникнути, призначаючи алопуринол після їди; дуже рідкісні - рецидивні кривава блювота, стеаторея, стоматит, зміни частоти дефекації; частота невідома – біль у животі. Порушення з боку печінки та жовчовивідних шляхів: нечасті – безсимптомне збільшення концентрації печінкових ферментів (підвищений рівень лужної фосфатази та трансаміназ у сироватці крові); рідкісні - гепатит (включаючи некротичну та гранулематозну форми). Порушення функції печінки можуть розвиватися без явних ознак генералізованої гіперчутливості Порушення з боку шкіри та підшкірних тканин: часті – висип; рідкісні – тяжкі реакції з боку шкіри: синдром Стівенса-Джонсона (ССД) та токсичний епідермальний некроліз (ТЕН); дуже рідкісні - ангіоневротичний набряк, локальна медикаментозна висипка, алопеція, знебарвлення волосся. У пацієнтів, які приймають алопуринол, найбільш поширені небажані реакції з боку шкіри. З огляду на терапії препаратом ці реакції можуть розвиватися у час. Шкірні реакції можуть проявлятися свербінням, макулопапульозними та лускатими висипаннями. В інших випадках може розвинутись пурпура. У поодиноких випадках спостерігається ексфоліативне ураження шкіри (ССД/ТЕН). При розвитку подібних реакцій терапію алопуринолом необхідно негайно припинити. Якщо реакція з боку шкіри має легкий характер, то після зникнення цих змін можна відновити прийом алопуринолу в меншій дозі (наприклад, 50 мг на добу). Згодом дозу можна поступово збільшити. При рецидивуванні шкірних реакцій терапію алопуринолом потрібно припинити і більше не відновлювати,оскільки подальший прийом препарату може призвести до розвитку тяжких реакцій гіперчутливості. Згідно з наявними відомостями, на фоні терапії алопуринолом ангіоневротичний набряк розвивався ізольовано, а також у поєднанні із симптомами генералізованої реакції гіперчутливості. Порушення з боку скелетно-м'язової та сполучної тканини: дуже рідкісні – міалгія. Порушення з боку нирок та сечовивідних шляхів: дуже рідкісні – гематурія, ниркова недостатність, уремія; частота невідома – сечокам'яна хвороба. Порушення з боку репродуктивної системи та молочної залози: дуже рідкісні – чоловіче безпліддя, еректильна дисфункція, гінекомастія. Загальні розлади та порушення у місці введення препарату: дуже рідкісні – набряк, загальне нездужання, загальна слабкість, лихоманка. Згідно з наявними відомостями, на тлі терапії алопуринолом лихоманка розвивалася як ізольовано, так і у поєднанні із симптомами генералізованої реакції гіперчутливості. Повідомлення про можливі побічні реакції У разі виникнення побічних реакцій, у тому числі не зазначених у цій інструкції, слід припинити застосування лікарського засобу. У післяреєстраційному періоді важлива будь-яка інформація про можливі побічні реакції, оскільки ці повідомлення допомагають постійно відстежувати безпеку препарату. Співробітники сфери охорони здоров'я зобов'язані повідомляти про будь-які підозри на побічні реакції до органів місцевого фармаконагляду.Взаємодія з лікарськими засобами6-меркаптопуріп та азатіоприн Азатіоприн метаболізується з утворенням 6-меркаптопурину, який інактивується ферментом ксантиноксидазою. У випадках, коли терапія 6-меркаптопурином або азатіоприном поєднується з алопуринолом, пацієнтам слід призначати лише одну чверть від звичайної дози 6-меркаптопурину або азатіоприну, оскільки пригнічення активності ксантиноксидази збільшує тривалість дії цих сполук. Відарабін (аденіна арабінозід) У присутності алопуринолу період напіввиведення відарабіну збільшується. При одночасному застосуванні цих препаратів необхідно дотримуватись особливої настороженості щодо посилених токсичних ефектів терапії. Саліцилати та урикозуричні засоби Основним активним метаболітом алопуринолу є оксипуринол, який виводиться нирками аналогічно до солей сечової кислоти. Отже, лікарські препарати з урикозуричною активністю, такі як пробенецид або високі дози саліцилатів, можуть посилювати виведення оксипуринолу. У свою чергу посилене виведення оксипуринолу супроводжується зменшенням терапевтичної активності аллопуринолу, проте значущість цього виду взаємодії необхідно оцінювати індивідуально в кожному випадку. Хлорпропамід При одночасному застосуванні алопуринолу та хлорпропаміду у пацієнтів з порушеною функцією нирок збільшується ризик розвитку тривалої гіпоглікемії, оскільки на етапі канальцевої екскреції алопуринол та хлорпропамід конкурують між собою. Антикоагулянти похідні кумарину При одночасному застосуванні з алопуринолом спостерігалося посилення ефектів варфарину та інших антикоагулянтів похідних кумарину. У зв'язку з цим необхідно ретельно контролювати стан пацієнтів, які отримують супутню терапію цими препаратами. Фенітоїн Алопуринол здатний пригнічувати окиснення фенітоїну в печінці, проте клінічна значимість цієї взаємодії не встановлена. Теофілін Відомо, що алопуринол пригнічує метаболізм теофіліну. Подібну взаємодію можна пояснити участю ксантиноксидази у процесі біотрансформації теофіліну в організмі людини. Концентрацію теофіліну в сироватці крові необхідно контролювати на початку супутньої терапії алопуринолом, а також зі збільшенням дози останнього. Ампіцилін та амоксицилін У пацієнтів, які одночасно отримували ампіцилін або амоксицилін та алопуринол, реєструвалася підвищена частота розвитку реакцій з боку шкіри, порівняно з пацієнтами, які не отримували подібну супутню терапію. Причину цього виду лікарської взаємодії не встановлено. Тим не менш, пацієнтам, які отримують алопуринол, замість ампіциліну та амоксициліну рекомендується призначати інші антибактеріальні препарати. Цитотоксичні лікарські засоби (циклофосфамід, доксорубіцин, блеоміцин, прокарбазин, мехлоретамін) У пацієнтів, які страждають на пухлинні захворювання (крім лейкозів) і отримують алопуринол, спостерігалося посилене пригнічення діяльності кісткового мозку циклофосфамідом та іншими цитотоксичними препаратами. Проте, згідно з результатами контрольованих досліджень, у яких взяли участь пацієнти, які отримують циклофосфамід, доксорубіцин, блеоміцин, прокарбазин та (або) мехлоретамін (хлорметину гідрохлорид), супутня терапія алопуринолом не посилювала токсичний вплив цих цитотоксичних препаратів. Циклоспорин Згідно з деякими повідомленнями, концентрація циклоспорину в плазмі може збільшуватися на тлі супутньої терапії алопуринолом. При одночасному застосуванні цих препаратів необхідно враховувати можливість посилення токсичності циклоспорину. Діданозин У здорових добровольців та ВІЛ-інфікованих пацієнтів, які отримують диданозин, на фоні супутньої терапії алопуринолом (300 мг на добу) спостерігалося збільшення СMAХ (максимальна концентрація препарату в плазмі крові) та AUC (площа під кривою концентрація-час) диданозину приблизно вдвічі. Період напіввиведення диданозину у своїй не змінювався. Як правило, одночасне застосування цих лікарських засобів не рекомендується. Якщо супутня терапія неминуча, може знадобитися зниження дози диданозину та ретельне спостереження за станом пацієнта. Інгібітори АПФ Одночасне застосування іАПФ з алопуринолом супроводжується підвищеним ризиком розвитку лейкопенії, таким чином ці препарати слід комбінувати з обережністю. Тіазидні діуретики Одночасне застосування тіазидних діуретиків, у тому числі гідрохлортіазиду, може підвищити ризик розвитку побічних ефектів гіперчутливості, пов'язаних з алопуринолом, особливо у пацієнтів з порушеннями функції нирок.Спосіб застосування та дозиВсередину. Препарат слід приймати один раз на день після їди, запиваючи великою кількістю води. Якщо добова доза перевищує 300 мг або спостерігаються симптоми непереносимості з боку шлунково-кишкового тракту, дозу необхідно ділити на кілька прийомів. Дорослі пацієнти Щоб зменшити ризик розвитку побічних ефектів, рекомендується використовувати алопуринол у початковій дозі 100 мг один раз на день. Якщо цієї дози недостатньо для того, щоб належним чином знизити концентрацію сечової кислоти в сироватці крові, то добову дозу можна поступово збільшувати до досягнення бажаного ефекту. Слід виявляти особливу обережність у разі порушення функції нирок. При підвищенні дози алопуринолу кожні 1-3 тижні необхідно визначати концентрацію сечової кислоти у сироватці крові. При доборі дози препарату рекомендується використовувати такі режими дозування (залежно від вибраного режиму дозування рекомендуються таблетки 100 мг або 300 мг). Рекомендована доза препарату становить: 100-200 мг на добу при легкому перебігу захворювання; 300-600 мг на добу при середньотяжкому перебігу; 700-900 мг на добу при тяжкому перебігу. Якщо при розрахунку дози виходити з маси тіла пацієнта, то доза алопуринолу повинна становити від 2 до 10 мг/кг/добу. Діти та підлітки віком до 15 років Рекомендована доза для дітей від 3 до 10 років: 5-10 мг/кг/добу. Для низьких доз використовують таблетки 100 мг, які за допомогою ризику можна розділити на дві однакові дози по 50 мг. Рекомендована доза для дітей віком від 10 до 15 років 10-20 мг/кг/добу. Добова доза не повинна перевищувати 400 мг. Алопуринол рідко застосовується для дитячої терапії. Виняток становлять злоякісні онкологічні захворювання (особливо лейкози) та деякі ферментативні порушення (наприклад, синдром Льоша-Найхана). Літні пацієнти Оскільки спеціальні дані щодо застосування алопуринолу у популяції людей похилого віку відсутні, для лікування таких пацієнтів слід використовувати препарат у мінімальній дозі, що забезпечує достатнє зниження концентрації сечової кислоти у сироватці крові. Особливу увагу необхідно приділити рекомендаціям щодо добору дози препарату для пацієнтів з порушеною функцією нирок. Порушення функції нирок Оскільки алопуринол та його метаболіти виводяться з організму нирками, порушення функції нирок може призводити до затримки препарату та його метаболітів в організмі з подальшим подовженням періоду напіввиведення цих сполук із плазми крові. При тяжкій нирковій недостатності рекомендується застосовувати алопуринол у дозі нижче 100 мг на добу або використовувати разові дози по 100 мг з інтервалом більше одного дня. Якщо умови дозволяють контролювати концентрацію оксипуринолу в плазмі крові, то дозу алопуринолу слід підібрати таким чином, щоб рівень оксипуринолу в плазмі був нижчий за 100 мкмоль/л (15,2 мг/л). Алопуринол та його похідні видаляються з організму за допомогою гемодіалізу. Якщо сеанси гемодіалізу проводяться 2-3 рази на тиждень, то доцільно визначити необхідність переходу на альтернативний режим терапії – прийом 300-400 мг алопуринолу відразу після завершення сеансу гемодіалізу (між сеансами гемодіалізу препарат не приймається). У пацієнтів з порушеннями функції нирок комбінування алопуринолу з тіазидними діуретиками слід проводити з винятковою обережністю. Алопуринол слід призначати у найнижчих ефективних дозах при ретельному моніторуванні функції нирок. Порушення функції печінки При порушеній функції печінки дозу препарату слід зменшити. На ранньому етапі лікування рекомендується здійснювати моніторинг лабораторних показників функції печінки. Стани, що супроводжуються посиленням обміну солеї сечової кислоти (наприклад, пухлинні захворювання, синдром Льоша-Найхана) Перед початком терапії цитотоксичними препаратами рекомендується корекцію існуючої гіперурикемії та (або) гіперурикозурії за допомогою алопуринолу. Велике значення має адекватна гідратація, що сприяє підтримці оптимального діурезу, а також олужнення сечі, завдяки якому збільшується розчинність сечової кислоти та її солей. Доза алопуринолу повинна бути близькою до нижньої межі рекомендованого діапазону доз. Якщо порушення функції нирок обумовлено розвитком гострої сечокислої нефропатії або іншої ниркової патології, лікування слід продовжувати відповідно до рекомендацій, представлених у розділі "Порушення функції нирок". Описані заходи можуть зменшити ризик накопичення ксантину та сечової кислоти, що ускладнює перебіг хвороби. Рекомендації щодо моніторингу Для корекції дози препарату необхідно з оптимальними інтервалами оцінювати концентрацію солей сечової кислоти у сироватці крові, а також рівень сечової кислоти та уратів сечі.ПередозуванняСимптоми Нудота, блювання, діарея та запаморочення. Тяжке передозування алопуринолу може призвести до значного пригнічення активності ксантиноксидази. Сам собою цей ефект не повинен супроводжуватися небажаними реакціями. Виняток становить вплив на супутню терапію, особливо на лікування 6-меркаптопурином та (або) азатіоприном. Лікування Специфічний антидот алопуринолу невідомий. Адекватна гідратація, що підтримує оптимальний діурез, сприяє виведенню алопуринолу та його похідних із сечею. За наявності клінічних показань виконується гемодіаліз.Запобіжні заходи та особливі вказівкиСиндром лікарської гіперчутливості, ССД та ТЕН На фоні застосування алопуринолу надходили повідомлення про розвиток загрозливих для життя реакцій з боку шкіри, такі як синдром Стівенса-Джонсона і токсичний епідермальний некроліз (ССД/ТЕН). Пацієнтів слід інформувати про симптоми цих реакцій (прогресуючий шкірний висип, часто з бульбашками та ураженням слизових) і ретельно моніторувати їх розвиток. Найчастіше ССД/ТЕН розвиваються на перших тижнях прийому препарату. За наявності ознак та симптомів ССД/ТЕН препарат Алопуринол слід негайно відмінити та більше не призначати. Маніфестація реакцій гіперчутливості до алопуринолу може бути різною, включаючи макулопапульозну екзантему, синдром лікарської гіперчутливості (DRESS) та ССД/ТЕН. Ці реакції є клінічним діагнозом і їх клінічні прояви є основою для прийняття відповідних рішень.Терапію препаратом Алопуринол слід негайно припинити при появі висипу на шкірі або інших проявів реакції гіперчутливості. Не можна відновлювати терапію у пацієнтів із синдромом гіперчутливості та ССД/ТЕН. Кортикостероїди можуть застосовуватись для лікування шкірних реакцій при гіперчутливості. Хронічне порушення функції нирок Пацієнти з хронічним порушенням функції нирок мають більший ризик розвитку реакцій гіперчутливості, пов'язаних з алопуринолом, у тому числі ССД/ТЕН. Алель HLA-B*5801 Було встановлено, що присутність алелю HLA-B*5801 пов'язана з розвитком синдрому гіперчутливості до алопуринолу та ССД/ТЕН. Частота присутності алеля HLA- В * 5801 різна в різних етнічних групах і може досягати 20% у популяції китайців Хань, близько 12% у корейців та 1-2% у японців та європейців. Застосування генотипування прийняття рішень про терапії аллопуринолом не досліджувалося. Якщо відомо, що пацієнт є носієм алелю HLA-B*5801, то алопуринол слід призначати лише, якщо користь лікування перевершує ризик. Слід дуже уважно стежити за розвитком синдрому гіперчутливості та ССД/ТЕН. Пацієнт повинен бути проінформований про необхідність негайного скасування лікування при першій появі таких симптомів. Порушення функції печінки та нирок При лікуванні пацієнтів з порушеною функцією нирок або печінки дозу алопуринолу необхідно знизити. У пацієнтів, які отримують лікування артеріальною гіпертензією або серцевою недостатністю (наприклад, пацієнти, які приймають діуретики або інгібітори АПФ), може спостерігатися супутнє порушення функції нирок, тому алопуринол у цій групі пацієнтів слід використовувати з обережністю. Безсимптомна гіперурикемія сама по собі не є показанням до застосування алопуринолу. У таких випадках поліпшення стану пацієнтів може бути досягнуто завдяки змінам дієти та споживанню рідини поряд з усуненням основної причини гіперурикемії. Гострий напад подагри Алопуринол не слід застосовувати до повного усунення гострого нападу подагри, оскільки цим можна спровокувати додаткове загострення захворювання. Аналогічно терапії урикозуричними засобами, початок лікування алопуринолом може спровокувати гострий напад подагри. Щоб уникнути цього ускладнення, рекомендується проводити профілактичну терапію нестероїдними протизапальними препаратами або колхіцином протягом щонайменше одного місяця до призначення алопуринолу. Детальні відомості про рекомендовані дози, застереження та запобіжні заходи можна знайти у відповідній літературі. Якщо гострий напад подагри розвивається на тлі терапії алопуринолом, то прийом препарату слід продовжити в тій же дозі, а для лікування нападу необхідно призначити нестероїдний протизапальний засіб. Відкладення ксантину У випадках, коли утворення сечової кислоти значно посилено (наприклад, злоякісна пухлинна патологія та відповідна протипухлинна терапія, синдром Льоша-Найхана), абсолютна концентрація ксантину в сечі в поодиноких випадках може істотно збільшитися, що сприяє відкладенню ксантину в тканинах сечових. Імовірність відкладення ксантину в тканинах можна звести до мінімуму завдяки адекватній гідратації, що забезпечує оптимальне розведення сечі. Вклинення конкрементів із сечової кислоти Адекватна терапія алопуринолом може призводити до розчинення великих конкрементів з сечової кислоти, що знаходяться в ниркових баліях, однак, ймовірність вклинення цих конкрементів в сечоводи невелика. Гемохроматоз Основний ефект алопуринолу при лікуванні подагри полягає у придушенні активності ферменту ксантиноксидази. Ксантиноксидаза може брати участь у зменшенні вмісту та виведенні заліза, що депонується у печінці. Дослідження, що демонструють безпеку терапії алопуринолом у популяції пацієнтів із гемохроматозом, відсутні. Пацієнтам з гемохроматозом, а також їхнім кровним родичам алопуринол слід призначати з обережністю. Вплив на здатність до керування автотранспортом та управління механізмами На тлі терапії алопуринолом спостерігався розвиток таких небажаних реакцій, як сонливість, запаморочення (вертиго) та атаксія. Ці небажані явища можуть вплинути на здатність до керування автотранспортом та управління механізмами. Пацієнти, які приймають препарат Алопуринол таблетки, не повинні керувати транспортними засобами та механізмами доти, доки вони не будуть впевнені в тому, що алопуринол не надає несприятливого впливу на відповідні здібності.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Діюча речовина: 300 мг алопуринолу в кожній таблетці; допоміжні речовини: магнію стеарат 3 мг, кремнію діоксид колоїдний безводний 3 мг, желатин 12 мг, карбоксиметилкрохмаль натрію (тип А) 20 мг, целюлоза мікрокристалічна 52 мг. По 30 таблеток у флаконі з коричневого скла з ПЕ кришкою з контролем першого розтину та амортизатором гармошкою. 1 флакон у картонній пачці разом із інструкцією з медичного застосування.Опис лікарської формиКруглі плоскі пігулки білого або сірувато-білого кольору, з фаскою, з ризиком на одній та з гравіюванням Е 352 з іншого боку, без або майже без запаху. За допомогою ризику таблетки можна розділити на дві однакові дози.Фармакотерапевтична групаПротиподагричний засіб – ксантиноксидази інгібітор.ФармакокінетикаВсмоктування Алопуринол активний при пероральному застосуванні. Він швидко всмоктується із верхніх відділів шлунково-кишкового тракту. За даними фармакокінетичних досліджень, алопуринол визначається в крові вже через 30-60 хвилин після прийому. Біодоступність алопуринолу варіює від 67% до 90%. Максимальна концентрація препарату в плазмі зазвичай реєструється приблизно через 1,5 години після перорального прийому. Потім концентрація алопуринолу швидко знижується. Через 6 годин після прийому в плазмі визначається лише слідова концентрація препарату. Максимальна концентрація активного метаболіту - оксипуринола зазвичай реєструється через 3-5 годин після перорального прийому алопуринолу. Рівень оксипуринолу в плазмі знижується значно повільніше. Розподіл Алопуринол майже не зв'язується з білками плазми, тому зміни рівня зв'язування з білками не повинні значно впливати на кліренс препарату. Об'єм розподілу алопуринолу, що здається, становить приблизно 1,6 літра/кг, що говорить про досить виражене поглинання препарату тканинами. Вміст алопуринолу в різних тканинах людини не вивчений, проте дуже ймовірно, що алопуринол і оксипуринол у максимальній концентрації накопичуються в печінці та слизовій оболонці кишечника, де реєструється висока активність ксантиноксидази. Біотрансформація Під дією ксантиноксидази та альдегідоксидази алопуринол метаболізується з утворенням оксипуринолу. Оксипуринол пригнічує активність ксантиноксидази. Проте, оксипуринол - менш потужний інгібітор ксантиноксидази, проти аллопуринолом, проте його період напіввиведення значно більше. Завдяки цим властивостям після прийому разової добової дози алопуринолу ефективне пригнічення активності ксантиноксидази підтримується протягом 24 годин. У хворих із нормальною функцією нирок вміст оксипуринолу у плазмі крові повільно збільшується аж до досягнення рівноважної концентрації. Після прийому алопуринолу в дозі 300 мг на добу, концентрація алопуринолу в плазмі крові, як правило, становить 5-10 мг/л. До інших метаболітів алопуринолу відносяться алопуринол-рибозид і оксипуринол-7-рибозид. Виведення Приблизно 20% прийнятого per os алопуринолу виводиться з калом у незміненому вигляді. Близько 10% добової дози екскретуються клубочковим апаратом нирки як незміненого аллопуринола. Ще 70% добової дози алопуринолу виводиться із сечею у формі оксипуринолу. Оксипуринол виводиться нирками у незміненому вигляді, однак у зв'язку з канальцевою реабсорбцією він має тривалий період напіввиведення. Період напіввиведення алопуринолу становить 1-2 години, тоді як період напіввиведення оксипуринолу варіює від 13 до 30 годин. Такі значні відмінності, ймовірно, пов'язані з відмінностями у структурі досліджень та/або кліренсі креатиніну у пацієнтів. Пацієнти з порушеною функцією нирок У хворих з порушеною функцією нирок виведення алопуринолу та оксипуринолу може значно сповільнюватися, що при тривалій терапії призводить до зростання концентрації цих сполук у плазмі крові. У пацієнтів з порушеною функцією нирок та кліренсом креатиніну 10-20 мл/хв після тривалої терапії алопуринолом у дозі 300 мг на добу концентрація оксипуринолу в плазмі досягала орієнтовно 30 мг/л. Така концентрація оксипуринолу може визначатися у пацієнтів з нормальною функцією нирок на фоні терапії алопуринолом у дозі 600 мг на добу. Отже, при лікуванні пацієнтів із порушенням функції нирок дозу алопуринолу необхідно знижувати. Літні пацієнти У пацієнтів похилого віку значні зміни фармакокінетичних властивостей алопуринолу малоймовірні. Виняток становлять пацієнти із супутньою патологією нирок.ФармакодинамікаАлопуринол є структурним аналогом гіпоксантину. Алопуринол, а також його основний активний метаболіт - оксипуринол, що інгібують ксантиноксидазу - фермент, що забезпечує перетворення гіпоксантину на ксантин, та ксантину на сечову кислоту. Алопуринол зменшує концентрацію сечової кислоти як у сироватці, так і в сечі. Тим самим він запобігає відкладенню кристалів сечової кислоти в тканинах та (або) сприяє їх розчиненню. Крім придушення катаболізму пуринів у деяких (але не у всіх) пацієнтів з гіперурикемією, велика кількість ксантину та гіпоксантину стає доступною для повторного утворення пуринових основ, що призводить до пригнічення біосинтезу пуринів de novo за механізмом зворотного зв'язку, що опосередковано пригніченням ферменту гіпоксантин-гуанін. -трансферази.Інші метаболіти алопуринолу - алопуринол-рибозид та оксипуринол-7 рибозид.Показання до застосуванняПригнічення утворення сечової кислоти та її солей при підтвердженому накопиченні цих сполук (наприклад, подагра, шкірні тофуси, нефролітіаз) або передбачуваному клінічному ризику їх накопичення (наприклад, лікування злоякісних новоутворень може ускладнюватися розвитком гострої сечокислої нефропатії). До основних клінічних станів, які можуть супроводжуватися накопиченням сечової кислоти та її солей, відносяться: ідіопатична подагра; сечокам'яна хвороба (утворення конкрементів із сечової кислоти); гостра сечокисла нефропатія; пухлинні захворювання та мієлопроліферативний синдром з високою швидкістю оновлення клітинної популяції, коли гіперурикемія виникає спонтанно або після проведення цитотоксичної терапії; певні ферментативні порушення, що супроводжуються гіперпродукцією солей сечової кислоти, наприклад, знижена активність гіпоксантин-гуанін- фосфорибозилтрансферази (включаючи синдром Льоша-Найхана), знижена активність глюкозо-6-фосфатази (включаючи глікогенози -амідо-трансферази, знижена активність аденін-фосфорибозилтрансферази Лікування сечокам'яної хвороби, що супроводжується утворенням 2,8-дигідроксиаденінових (2,8-ДГА) конкрементів у зв'язку зі зниженою активністю аденін-фосфорибозилтрансферази. Профілактика та лікування сечокам'яної хвороби, що супроводжується утворенням змішаних кальцієво-оксалатних конкрементів на тлі гіперурікозурії, коли дієта та підвищене споживання рідини були безуспішними.Протипоказання до застосуванняГіперчутливість до алопуринолу або будь-якої з допоміжних речовин, що входять до складу препарату. Печінкова недостатність, хронічна ниркова недостатність (стадія азотемії), первинний гемохроматоз, безсимптомна гіперурикемія, гострий напад подагри, дитячий вік до 3-х років (з урахуванням твердої лікарської форми) Вагітність, період грудного вигодовування. Пацієнти з рідкісними спадковими захворюваннями, такими як непереносимість галактози, дефіцит лактази або глюкозо-галактозною мальабсорбцією, не повинні приймати препарат (до складу препарату входить лактози моногідрат). З обережністю: Порушення функції печінки, гіпотиреоз, цукровий діабет, артеріальна гіпертензія, одночасний прийом інгібіторів ангіотензинперетворюючого ферменту (АПФ) або діуретиків, дитячий вік (до 15 років призначають тільки під час цитостатичної терапії лейкозів та ін. злоякісних захворювань; літній вік.Вагітність та лактаціяВагітність В даний час даних з безпеки терапії алопуринолом у період вагітності недостатньо, хоча цей препарат широко застосовувався протягом довгих ліг без явних несприятливих наслідків. Вагітним жінкам не слід приймати таблетки Алопуринол-ЕГІС, за винятком тих випадків, коли не існує менш небезпечного альтернативного лікування та захворювання становить більший ризик для матері та плода, ніж прийом препарату. Період грудного вигодовування Згідно з наявними повідомленнями, алопуринол та оксипуринол виділяються з грудним молоком. У жінок, які приймають алопуринол у дозі 300 мг/добу, концентрація алопуринолу та оксипуринолу у грудному молоці досягала, відповідно, 1,4 мг/л та 53,7 мг/л. Проте, відомостей про вплив алопуринолу та його метаболітів на немовлят, які перебувають на грудному вигодовуванні, відсутні. Таким чином, препарат Алопуринол-ЕГІС таблетки не рекомендується в період грудного вигодовування.Побічна діяВідсутні сучасні клінічні дані визначення частоти розвитку побічних ефектів. Їх частота може варіювати в залежності від дози та від того, чи призначався препарат як монотерапія або у комбінації з іншими препаратами. Класифікація частоти розвитку побічних ефектів заснована на приблизній оцінці, більшість побічних ефектів відсутні дані визначення частоти їх розвитку. Класифікація небажаних реакцій залежно від частоти народження виглядає наступним чином: дуже часті (≥1/10), часті (від ≥1/100 до Небажані реакції, пов'язані з терапією алопуринолом, що спостерігаються в постреєстраційному періоді, зустрічаються рідко або дуже рідко. У загальній популяції пацієнтів здебільшого мають легкий характер. Частота розвитку небажаних явищ збільшується при порушеннях функції нирок та (або) печінки. Інфекції та паразитарні захворювання: дуже рідкісні: фурункульоз. Порушення з боку системи крові та лімфатичної системи: дуже рідкісні: агранулоцитоз, апластична анемія, тромбоцитопенія, гранулоцитоз, лейкопенія, лейкоцитоз, еозинофілія та аплазія, що стосується лише еритроцитів; Дуже рідко надходили повідомлення про тромбоцитопенію, агранулоцитоз і апластичні анемії, особливо у осіб з порушеннями функції нирок та/або печінки, що наголошує на необхідності прояву особливої обережності у цих груп пацієнтів. Порушення з боку імунної системи: нечасті: реакції гіперчутливості; рідкісні: важкі реакції гіперчутливості, включаючи шкірні реакції з відшаруванням епідермісу, лихоманкою, лімфаденопатією, артралгією та (або) еозинофілією (у тому числі синдром Стівенса-Джонсона та токсичний епідермальний некроліз) (див. розділ "Порушення з боку шкіри та підшкірних) . Супутній васкуліт або реакції з боку тканини можуть мати різні прояви, включаючи гепатит, ураження нирок, гострий холангіт, ксантинові конкременти і, в окремих випадках, судоми. Крім того, дуже рідко спостерігався розвиток анафілактичного шоку. При розвитку тяжких небажаних реакцій терапію алопуринолом необхідно негайно припинити та не відновлювати.При відстроченій мультиорганній гіперчутливості (відомій як синдром лікарської гіперчутливості /DRESS/) можуть розвиватися наступні симптоми в різних комбінаціях: лихоманка, шкірний висип, васкуліт, лімфаденопатія, псевдолімфома, артралгія, лейкопенія, еозинофілія, гепато-спіно зникають жовчних проток (руйнування або зникнення внутрішньопечінкових жовчних проток). При розвитку таких реакцій у будь-який період лікування Алопуринол-ЕГИС слід негайно скасувати і ніколи не відновлювати. Генералізовані реакції гіперчутливості розвивалися у хворих з порушеною функцією нирок та (або) печінки. Такі випадки іноді мали летальний кінець; дуже рідкісні: ангіоімунобластна лімфаденопатія.Ангіоімунобластну лімфаденопатію дуже рідко діагностували після біопсії лімфовузлів з приводу генералізованої лімфаденопатії. Ангіоімунобластна лімфаденопатія носить оборотний характер і регресує після припинення терапії алопуринолом. Порушення з боку обміну речовин та харчування: дуже рідкісні: цукровий діабет, гіперліпідемія. Порушення психіки: дуже рідкісні: депресія. Порушення з боку нервової системи: дуже рідкісні: кома, параліч, атаксія, нейропатія, парестезія, сонливість, головний біль, спотворення смакових відчуттів. Порушення органу зору: дуже рідкісні: катаракта, порушення зору, макулярні зміни. Порушення з боку органу слуху та лабіринтні розлади: дуже рідкісні: запаморочення (вертиго). Порушення серця: дуже рідкісні: стенокардія, брадикардія. Порушення з боку судин: дуже рідкісні: підвищення артеріального тиску. Порушення з боку шлунково-кишкового тракту: нечасті: блювання, нудота, діарея. ; дуже рідкісні: рецидивні кривава блювота, стеаторея, стоматит, зміни частоти дефекації; Частота невідома: біль у животі. Порушення з боку печінки та жовчовивідних шляхів: нечасті: безсимптомне збільшення концентрації печінкових ферментів (підвищений рівень лужної фосфатази та трансаміназ у сироватці крові); рідкісні: гепатит (включаючи некротичну та гранулематозну форми). Порушення функції печінки можуть розвиватися без явних ознак генералізованої гіперчутливості Порушення з боку шкіри та підшкірних тканин: часті: висипання; рідкісні: тяжкі реакції з боку шкіри: синдром Стівенса-Джонсона (ССД) та токсичний епідермальний некроліз (ТЕН), дуже рідкісні: ангіоневротичний набряк, локальний медикаментозний висип, алопеція, знебарвлення волосся. У пацієнтів, які приймають алопуринол, найбільш поширені небажані реакції з боку шкіри. З огляду на терапії препаратом ці реакції можуть розвиватися у час. Шкірні реакції можуть проявлятися свербінням, макулопапульозними та лускатими висипаннями. В інших випадках може розвинутись пурпура. У поодиноких випадках спостерігається ексфоліативне ураження шкіри (ССД/ТЕН). При розвитку подібних реакцій терапію алопуринолом необхідно негайно припинити. Якщо реакція з боку шкіри має легкий характер, то після зникнення цих змін можна відновити прийом алопуринолу в меншій дозі (наприклад, 50 мг на добу). Згодом дозу можна поступово збільшити. При рецидивуванні шкірних реакцій терапію алопуринолом потрібно припинити і більше не відновлювати,оскільки подальший прийом препарату може призвести до розвитку тяжких реакцій гіперчутливості. Згідно з наявними відомостями, на фоні терапії алопуринолом ангіоневротичний набряк розвивався ізольовано, а також у поєднанні із симптомами генералізованої реакції гіперчутливості. Порушення з боку скелетно-м'язової та сполучної тканини: дуже рідкісні: міалгія. Порушення з боку нічок та сечовивідних шляхів: дуже рідкісні: гематурія, ниркова недостатність, уремія, частота невідома: сечокам'яна хвороба. Порушення з боку репродуктивної системи та молочної залози: дуже рідкісні: чоловіче безпліддя, еректильна дисфункція, гінекомастія. Загальні розлади та порушення у місці введення препарату: дуже рідкісні: набряк, загальне нездужання, загальна слабкість, лихоманка. Згідно з наявними відомостями, на тлі терапії алопуринолом лихоманка розвивалася як ізольовано, так і у поєднанні із симптомами генералізованої реакції гіперчутливості. Повідомлення про можливі побічні реакції У разі виникнення побічних реакцій, у тому числі не зазначених у цій інструкції, слід припинити застосування лікарського засобу. У післяреєстраційному періоді важлива будь-яка інформація про можливі побічні реакції, оскільки ці повідомлення допомагають постійно відстежувати безпеку препарату. Співробітники сфери охорони здоров'я зобов'язані повідомляти про будь-які підозри на побічні реакції до органів місцевого фармаконагляду.Взаємодія з лікарськими засобами6-меркаптопурин та азатіоприн Азатіоприн метаболізується з утворенням 6-меркаптопурину, який інактивується ферментом ксантиноксидазою. У випадках, коли терапія 6-меркаптопурином або азатіоприном поєднується з алопуринолом, пацієнтам слід призначати лише одну чверть від звичайної дози 6-меркаптопурину або азатіоприну, оскільки пригнічення активності ксантиноксидази збільшує тривалість дії цих сполук. Відарабін (аденіна арабінозід) У присутності алопуринолу період напіввиведення відарабіну збільшується. При одночасному застосуванні цих препаратів необхідно дотримуватись особливої настороженості щодо посилених токсичних ефектів терапії. Саліцилати та урикозуричні засоби Основним активним метаболітом алопуринолу є оксипуринол, який виводиться нирками аналогічно до солей сечової кислоти. Отже, лікарські препарати з урикозуричною активністю, такі як пробенецид або високі дози саліцилатів, можуть посилювати виведення оксипуринолу. У свою чергу посилене виведення оксипуринолу супроводжується зменшенням терапевтичної активності аллопуринолу, проте значущість цього виду взаємодії необхідно оцінювати індивідуально в кожному випадку. Хлорпропамід При одночасному застосуванні алопуринолу та хлорпропаміду у пацієнтів з порушеною функцією нирок збільшується ризик розвитку тривалої гіпоглікемії, оскільки на етапі канальцевої екскреції алопуринол та хлорпропамід конкурують між собою. Антикоагулянти похідні кумарину При одночасному застосуванні з алопуринолом спостерігалося посилення ефектів варфарину та інших антикоагулянтів похідних кумарину. У зв'язку з цим необхідно ретельно контролювати стан пацієнтів, які отримують супутню терапію цими препаратами. Фенітоїн Алопуринол здатний пригнічувати окиснення фенітоїну в печінці, проте клінічна значимість цієї взаємодії не встановлена. Теофілін Відомо, що алопуринол пригнічує метаболізм теофіліну. Подібну взаємодію можна пояснити участю ксантиноксидази у процесі біотрансформації теофіліну в організмі людини. Концентрацію теофіліну в сироватці крові необхідно контролювати на початку супутньої терапії алопуринолом, а також зі збільшенням дози останнього. Ампіцилін та амоксицилін У пацієнтів, які одночасно отримували ампіцилін або амоксицилін та алопуринол, реєструвалася підвищена частота розвитку реакцій з боку шкіри, порівняно з пацієнтами, які не отримували подібну супутню терапію. Причину цього виду лікарської взаємодії не встановлено. Тим не менш, пацієнтам, які отримують алопуринол, замість ампіциліну та амоксициліну рекомендується призначати інші антибактеріальні препарати. Цитотоксичні лікарські засоби (циклофосфамід, доксорубіцин, блеоміцин, прокарбазин, мехлоретамін) У пацієнтів, які страждають на пухлинні захворювання (крім лейкозів) і отримують алопуринол, спостерігалося посилене пригнічення діяльності кісткового мозку циклофосфамідом та іншими цитотоксичними препаратами. Проте, згідно з результатами контрольованих досліджень, у яких взяли участь пацієнти, які отримують циклофосфамід, доксорубіцин, блеоміцин, прокарбазин та (або) мехлоретамін (хлорметину гідрохлорид), супутня терапія алопуринолом не посилювала токсичний вплив цих цитотоксичних препаратів. Циклоспорин Згідно з деякими повідомленнями, концентрація циклоспорину в плазмі може збільшуватися на тлі супутньої терапії алопуринолом. При одночасному застосуванні цих препаратів необхідно враховувати можливість посилення токсичності циклоспорину. Діданозин У здорових добровольців та ВІЛ-інфікованих пацієнтів, які отримують диданозин, на фоні супутньої терапії алопуринолом (300 мг на добу) спостерігалося збільшення Сmах (максимальна концентрація препарату в плазмі крові) та AUC (площа під кривою концентрація-час) диданозину приблизно вдвічі. Період напіввиведення диданозину у своїй не змінювався. Як правило, одночасне застосування цих лікарських засобів не рекомендується. Якщо супутня терапія неминуча, може знадобитися зниження дози диданозину та ретельне спостереження за станом пацієнта. Інгібітори АПФ Одночасне застосування іАПФ з алопуринолом супроводжується підвищеним ризиком розвитку лейкопенії, таким чином ці препарати слід комбінувати з обережністю. Тіазидні діуретики Одночасне застосування тіазидних діуретиків, у тому числі гідрохлортіазид, може підвищити ризик розвитку побічних ефектів гіперчутливості, пов'язаних з алопуринолом, особливо у пацієнтів з порушеннями функції нирок.Спосіб застосування та дозиВсередину. Препарат слід приймати один раз на день після їди, запиваючи великою кількістю води. Якщо добова доза перевищує 300 мг або спостерігаються симптоми непереносимості з боку шлунково-кишкового тракту, дозу необхідно ділити на кілька прийомів. Дорослі пацієнти Для того, щоб зменшити ризик розвитку побічних ефектів, рекомендується використовувати алопуринол у початковій дозі 100 мг один раз на день. Якщо цієї дози недостатньо для того, щоб належним чином знизити концентрацію сечової кислоти в сироватці крові, то добову дозу можна поступово збільшувати до досягнення бажаного ефекту. Слід виявляти особливу обережність у разі порушення функції нирок. При підвищенні дози алопуринолу кожні 1-3 тижні необхідно визначати концентрацію сечової кислоти у сироватці крові. При доборі дози препарату рекомендується використовувати такі режими дозування (залежно від вибраного режиму дозування рекомендуються таблетки 100 мг або 300 мг). Рекомендована доза препарату становить: 100-200 мг на добу при легкому перебігу захворювання; 300-600 мг на добу при середньотяжкому перебігу; 700-900 мг на добу при тяжкому перебігу. Якщо при розрахунку дози виходити з маси тіла пацієнта, то доза алопуринолу повинна становити від 2 до 10 мг/кг/добу. Діти та підлітки віком до 15 років Рекомендована доза для дітей від 3 до 10 років: 5-10 мг/кг/добу. Для низьких доз використовують таблетки 100 мг, які за допомогою ризику можна розділити на дві однакові дози по 50 мг. Рекомендована доза для дітей віком від 10 до 15 років 10-20 мг/кг/добу. Добова доза не повинна перевищувати 400 мг. Алопуринол рідко застосовується для дитячої терапії. Виняток становлять злоякісні онкологічні захворювання (особливо лейкози) та деякі ферментативні порушення (наприклад, синдром Льоша-Найхана). Літні пацієнти Оскільки спеціальні дані щодо застосування алопуринолу у популяції людей похилого віку відсутні, для лікування таких пацієнтів слід використовувати препарат у мінімальній дозі, що забезпечує достатнє зниження концентрації сечової кислоти у сироватці крові. Особливу увагу необхідно приділити рекомендаціям щодо добору дози препарату для пацієнтів з порушеною функцією нирок. Порушення функції нирок Оскільки алопуринол та його метаболіти виводяться з організму нирками, порушення функції нирок може призводити до затримки препарату та його метаболітів в організмі з подальшим подовженням періоду напіввиведення цих сполук із плазми крові. При тяжкій нирковій недостатності рекомендується застосовувати алопуринол у дозі нижче 100 мг на добу або використовувати разові дози по 100 мг з інтервалом більше одного дня. Якщо умови дозволяють контролювати концентрацію оксипуринолу в плазмі крові, то дозу алопуринолу слід підібрати таким чином, щоб рівень оксипуринолу в плазмі був нижчий за 100 мкмоль/л (15,2 мг/л). Алопуринол та його похідні видаляються з організму за допомогою гемодіалізу. Якщо сеанси гемодіалізу проводяться 2-3 рази на тиждень, то доцільно визначити необхідність переходу на альтернативний режим терапії – прийом 300-400 мг алопуринолу відразу після завершення сеансу гемодіалізу (між сеансами гемодіалізу препарат не приймається). У пацієнтів з порушеннями функції нирок комбінування алопуринолу з тіазидними діуретиками слід проводити з винятковою обережністю. Алопуринол слід призначати у найнижчих ефективних дозах при ретельному моніторуванні функції нирок. Порушення функції печінки При порушеній функції печінки дозу препарату слід зменшити. На ранньому етапі лікування рекомендується здійснювати моніторинг лабораторних показників функції печінки. Стани, що супроводжуються посиленням обміну солей сечової кислоти (наприклад, пухлинні захворювання, синдром Льоша-Найхана) Перед початком терапії цитотоксичними препаратами рекомендується корекцію існуючої гіперурикемії та (або) гіперурикозурії за допомогою алопуринолу. Велике значення має адекватна гідратація, що сприяє підтримці оптимального діурезу, а також олужнення сечі, завдяки якому збільшується розчинність сечової кислоти та її солей. Доза алопуринолу повинна бути близькою до нижньої межі рекомендованого діапазону доз. Якщо порушення функції нирок обумовлено розвитком гострої сечокислої нефропатії або іншої ниркової патології, лікування слід продовжувати відповідно до рекомендацій, представлених у розділі "Порушення функції нирок". Описані заходи можуть зменшити ризик накопичення ксантину та сечової кислоти, що ускладнює перебіг хвороби. Рекомендації щодо моніторингу Для корекції дози препарату необхідно з оптимальними інтервалами оцінювати концентрацію солей сечової кислоти у сироватці крові, а також рівень сечової кислоти та уратів сечі.ПередозуванняСимптоми: нудота, блювання, діарея та запаморочення. Тяжке передозування алопуринолу може призвести до значного пригнічення активності ксантиноксидази. Сам собою цей ефект не повинен супроводжуватися небажаними реакціями. Виняток становить вплив на супутню терапію, особливо на лікування 6-меркаптопурином та (або) азатіоприном. Лікування: Специфічний антидот алопуринолу невідомий. Адекватна гідратація, що підтримує оптимальний діурез, сприяє виведенню алопуринолу та його похідних із сечею. За наявності клінічних показань виконується гемодіаліз.Запобіжні заходи та особливі вказівкиСиндром лікарської гіперчутливості, ССД та ТЕН На фоні застосування алопуринолу надходили повідомлення про розвиток загрозливих для життя реакцій з боку шкіри, такі як синдром Стівенса-Джонсона і токсичний епідермальний некроліз (ССД/ТЕН). Пацієнтів слід інформувати про симптоми цих реакцій (прогресуючий шкірний висип, часто з бульбашками та ураженням слизових) і ретельно моніторувати їх розвиток. Найчастіше ССД/ТЕН розвиваються на перших тижнях прийому препарату. За наявності ознак та симптомів ССД/ТЕН препарат Алопуринол-ЕГІС слід негайно відмінити та більше не призначати! Маніфестація реакцій гіперчутливості до алопуринолу може бути різною, включаючи макулопапульозну екзантему, синдром лікарської гіперчутливості (DRESS) та ССД/ТЕН. Ці реакції є клінічним діагнозом і їх клінічні прояви є основою для прийняття відповідних рішень. Терапію препаратом Алопуринол-ЕГІС слід негайно припинити при появі висипу на шкірі або інших проявів реакції гіперчутливості. Не можна відновлювати терапію у пацієнтів із синдромом гіперчутливості та ССД/ТЕН. Кортикостероїди можуть застосовуватись для лікування шкірних реакцій при гіперчутливості. Хронічне порушення функції нирок Пацієнти з хронічним порушенням функції нирок мають більший ризик розвитку реакцій гіперчутливості, пов'язаних з алопуринолом, у тому числі ССД/ТЕН. Алель HLA-B*5801 Було встановлено, що присутність алелю HLA-B*5801 пов'язана з розвитком синдрому гіперчутливості до алопуринолу та ССД/ТЕН. Частота присутності алеля HLA- В * 5801 різна в різних етнічних групах і може досягати 20% у популяції китайців Хань, близько 12% у корейців та 1-2% у японців та європейців. Застосування генотипування прийняття рішень про терапії аллопуринолом не досліджувалося. Якщо відомо, що пацієнт є носієм алелю HLA-B*5801, то алопуринол слід призначати лише, якщо користь лікування перевершує ризик. Слід дуже уважно стежити за розвитком синдрому гіперчутливості та ССД/ТЕН. Пацієнт повинен бути проінфоримований про необхідність негайного скасування лікування при першій появі таких симптомів. Порушення функції печінки та нирок При лікуванні пацієнтів з порушеною функцією нирок або печінки дозу алопуринолу необхідно знизити. У пацієнтів, які отримують лікування артеріальною гіпертензією або серцевою недостатністю (наприклад, пацієнти, які приймають діуретики або інгібітори АПФ), може спостерігатися супутнє порушення функції нирок, тому алопуринол у цій групі пацієнтів слід використовувати з обережністю. Безсимптомна гіперурикемія сама по собі не є показанням до застосування алопуринолу. У таких випадках поліпшення стану пацієнтів може бути досягнуто завдяки змінам дієти та споживанню рідини поряд з усуненням основної причини гіперурикемії. Гострий напад подагри. Алопуринол не слід застосовувати до повного усунення гострого нападу подагри, оскільки цим можна спровокувати додаткове загострення захворювання. Аналогічно терапії урикозуричними засобами, початок лікування алопуринолом може спровокувати гострий напад подагри. Щоб уникнути цього ускладнення, рекомендується проводити профілактичну терапію нестероїдними протизапальними препаратами або колхіцином протягом щонайменше одного місяця до призначення алопуринолу. Детальні відомості про рекомендовані дози, застереження та запобіжні заходи можна знайти у відповідній літературі. Якщо гострий напад подагри розвивається на тлі терапії алопуринолом, то прийом препарату слід продовжити в тій же дозі, а для лікування нападу необхідно призначити нестероїдний протизапальний засіб. Відкладення ксантину У випадках, коли утворення сечової кислоти значно посилено (наприклад, злоякісна пухлинна патологія та відповідна протипухлинна терапія, синдром Льоша-Найхана), абсолютна концентрація ксантину в сечі в поодиноких випадках може істотно збільшитися, що сприяє відкладенню ксантину в тканинах сечових пут. Імовірність відкладення ксантину в тканинах можна звести до мінімуму завдяки адекватній гідратації, що забезпечує оптимальне розведення сечі. Вклинення конкрементів із сечової кислоти Адекватна терапія алопуринолом може призводити до розчинення великих конкрементів з сечової кислоти, що знаходяться в ниркових баліях, однак, ймовірність вклинення цих конкрементів в сечоводи невелика. Гемохроматоз Основний ефект алопуринолу при лікуванні подагри полягає у придушенні активності ферменту ксантиноксидази. Ксантиноксидаза може брати участь у зменшенні вмісту та виведенні заліза, що депонується у печінці. Дослідження, що демонструють безпеку терапії алопуринолом у популяції хворих на гемохроматоз, відсутні. Пацієнтам з гемохроматозом, а також їхнім кровним родичам алопуринол слід призначати з обережністю. Лактоза Кожна 100 мг таблетка Алопуринол-ЕГИС містить 50 мг лактози. Отже, цей препарат не повинні приймати пацієнти з рідкісною спадковою непереносимістю галактози, недостатністю лактази та синдромом мальабсорбції глюкози та галактози. Вплив на здатність до керування автотранспортом та управління механізмами На тлі терапії алопуринолом спостерігався розвиток таких небажаних реакцій, як сонливість, запаморочення (вертиго) та атаксія. Ці небажані явища можуть вплинути на здатність до керування автотранспортом та управління механізмами. Пацієнти, які приймають препарат Алопуринол-ЕГИС таблетки, не повинні керувати транспортними засобами та механізмами доти, доки вони не будуть впевнені в тому, що алопуринол не надає несприятливого впливу на відповідні здібності.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. активні речовини: алопуринол – 300 мг; допоміжні речовини: лактози моногідрат (цукор молочний) – 49 мг, целюлоза мікрокристалічна – 20 мг, карбоксиметилкрохмаль натрію (примогель) – 20 мг, желатин харчовий – 5 мг, магнію стеарат – 4 мг, кремнію діоксид колоїдний (аеро). 10 шт. - упаковки осередкові контурні (3, 5) - пачки картонні. 30 шт. - банки темного скла (1); - пачки картонні. 50 шт. - банки темного скла (1); - пачки картонні.Опис лікарської формиТаблетки білого або майже білого, круглі, плоскоциліндричні, з фаскою та ризиком.Фармакотерапевтична групаПротиподагричний засіб, ксантиноксидази, інгібітор.ФармакокінетикаПісля прийому внутрішньо майже повністю (на 90%) абсорбується із ШКТ. Метаболізується з утворенням аллоксантину, який зберігає здатність досить довго пригнічувати ксантиноксидазу. Cmax алопуринолу у плазмі крові досягається в середньому через 1.5 год, аллоксантину – через 4.5 год після одноразового прийому. T1/2 алопуринолу становить 1-2 год, аллоксантина - близько 15 год. Близько 20% прийнятої дози виводиться через кишечник, решта - нирками.ФармакодинамікаЗасіб, що порушує синтез сечової кислоти. Є структурним аналогом гіпоксантину. Інгібує фермент ксантиноксидазу, який бере участь у перетворенні гіпоксантину на ксантин та ксантину на сечову кислоту. Цим обумовлено зменшення концентрації сечової кислоти та її солей у рідких середовищах організму та сечі, що сприяє розчиненню наявних уратних відкладень та запобігає їх утворенню у тканинах та нирках. При прийомі алопуринолу підвищується виділення із сечею гіпоксантину та ксантину.Показання до застосуванняЛікування та профілактика подагри та гіперурикемії різного генезу (в т.ч. у поєднанні з нефролітіазом, нирковою недостатністю, уратною нефропатією). Рецидивні змішані оксалатно-кальцієві ниркові камені за наявності гіперурікозурії. Підвищена освіта уратів внаслідок ферментних порушень. Профілактика гострої нефропатії при цитостатичній та променевій терапії пухлин та лейкозів, а також при повному лікувальному голодуванні.Протипоказання до застосуванняВиражені порушення функції печінки та/або нирок, вагітність, лактація, підвищена чутливість до алопуринолу.Вагітність та лактаціяПротипоказаний до застосування при вагітності та в період лактації (грудного вигодовування). У дітей застосовують лише при злоякісних новоутвореннях (особливо лейкозах), а також при деяких ферментних порушеннях (синдром Льоша-Ніхена). Режим дозування встановлюється індивідуально, під контролем концентрації уратів та сечової кислоти в крові та сечі: дітям віком до 15 років – 10-20 мг/кг/добу або 100-400 мг/добу.Побічна діяЗ боку серцево-судинної системи: у поодиноких випадках – артеріальна гіпертензія, брадикардія. З боку травної системи: можливі диспептичні явища (в т.ч. нудота, блювання), діарея, підвищення транзиторної активності трансаміназ у сироватці крові; рідко – гепатит; у поодиноких випадках - стоматит, порушення функції печінки (минуще підвищення активності трансаміназ і ЛФ), стеаторея. З боку ЦНС та периферичної нервової системи: у поодиноких випадках – слабкість, підвищена стомлюваність, головний біль, запаморочення, атаксія, сонливість, депресія, кома, парези, парестезії, судоми, невропатії, порушення зору, катаракта, зміни сосочка зорового нерва, порушення смакових відчуттів. З боку системи кровотворення: в окремих випадках – тромбоцитопенія, агранулоцитоз та апластична анемія, лейкопенія (найбільш ймовірні у хворих з порушеннями функції нирок). З боку сечовидільної системи: рідко – інтерстиціальний нефрит; у поодиноких випадках – набряки, уремія, гематурія. З боку ендокринної системи: у поодиноких випадках – безпліддя, імпотенція, гінекомастія, цукровий діабет. З боку обміну речовин: у поодиноких випадках – гіперліпідемія. Алергічні реакції: шкірний висип, гіперемія, свербіж; в окремих випадках – ангіоімунобластна лімфаденопатія, артралгія, підвищення температури, еозинофілія, лихоманка, синдром Стівенса-Джонсона, синдром Лайєлла. Дерматологічні реакції: у поодиноких випадках – фурункульоз, алопеція, знебарвлення волосся.Взаємодія з лікарськими засобамиПри одночасному застосуванні алопуринол посилює дію кумаринових антикоагулянтів, аденіну арабінозиду, а також гіпоглікемічних препаратів (особливо у разі порушення функції нирок). Урикозуричні засоби та саліцилати у високих дозах знижують активність алопуринолу. При одночасному застосуванні алопуринолу та цитостатиків частіше проявляється мієлотоксична дія, ніж при роздільному застосуванні. При одночасному застосуванні алопуринолу та азатіоприну або меркаптопурину спостерігається кумуляція останніх в організмі, т.к. у зв'язку з інгібуванням алопуринолом активності ксантиноксидази, необхідної для біотрансформації лікарських засобів, уповільнюється їхній метаболізм та елімінація.Спосіб застосування та дозиВстановлюють індивідуально, під контролем концентрації уратів та сечової кислоти в крові та сечі. Дорослим прийому внутрішньо - 100-900 мг/сут, залежно від тяжкості перебігу захворювання. Частота прийому 2-4 рази на добу після їди. Дітям до 15 років - 10-20 мг/кг/сут або 100-400 мг/сут. Максимальні дози: при порушеннях функції нирок (в т.ч. обумовлених уратовою нефропатією) – 100 мг на добу. Збільшення дози можливе в тих випадках, коли на тлі терапії, що проводиться, зберігається підвищена концентрація уратів в крові і сечі.Запобіжні заходи та особливі вказівкиЗ обережністю слід застосовувати алопуринол при порушеннях функції печінки та нирок (в обох випадках необхідне зниження дози), гіпофункції щитовидної залози. У початковий період курсу терапії алопуринолом необхідне систематичне проведення оцінки показників функції печінки. У період лікування алопуринолом добова кількість рідини, що споживається, повинна бути не менше 2 л (під контролем діурезу). На початку курсу лікування подагри може виникнути загострення захворювання. Для профілактики можна застосовувати НПЗЗ або колхіцин (по 0.5 мг 3 рази на добу). Слід враховувати, що при адекватній терапії алопуринолом можливе розчинення великого уратного каміння в нирковій балії і подальше їх потрапляння в сечоводу. Асимптоматична гіперурикемія не є показанням до застосування алопуринолу. У дітей застосовують лише при злоякісних новоутвореннях (особливо лейкозах), а також при деяких ферментних порушеннях (синдром Льоша-Ніхена). Для корекції гіперурикемії у пацієнтів з пухлинними захворюваннями алопуринол рекомендується застосовувати перед початком лікування цитостатиками. У таких випадках слід застосовувати ефективну мінімальну дозу. Крім того, з метою зменшення ризику відкладення ксантинів у сечовивідних шляхах необхідно вжити заходів для підтримки оптимального діурезу та олужнення сечі. При одночасному застосуванні алопуринолу та цитостатиків необхідний більш частий контроль картини периферичної крові. У період прийому алопуринолу не допускається вживання алкоголю. Вплив на здатність до керування автотранспортом та управління механізмами З обережністю застосовувати у пацієнтів, діяльність яких потребує високої концентрації уваги та швидких психомоторних реакцій.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Алопурінол - 300,0 мг. допоміжні речовини: целюлоза мікрокристалічна - 162,0 мг, крохмаль кукурудзяний - 75,0 мг, карбоксиметилкрохмаль натрію - 30,0 мг, повідон-К25 - 24,0 мг, кремнію діоксид колоїдний - 3,0 мг, магнію стеарат 0мг. По 10, 14, 25 або 30 таблеток у контурне осередкове пакування з плівки полівінілхлоридної та фольги алюмінієвої друкованої лакованої. По 10, 20, 30, 40, 50 або 100 таблеток у банки з поліетилентерефталату для лікарських засобів або поліпропіленові для лікарських засобів, закупорені кришками з поліетилену високого тиску з контролем першого розтину, або кришками поліпропіленовими з системою "натиснути- з поліетилену низького тиску з контролем першого розтину. Одну банку або 1, 2, 3, 4, 5, 6, 7, 8, 9 або 10 контурних осередкових упаковок разом з інструкцією по застосуванню поміщають у картонну упаковку (пачку).Опис лікарської формиКруглі плоскоциліндричні пігулки білого або білого з жовтуватим відтінком кольору з ризиком з одного боку та фасками з двох боків.Фармакотерапевтична групаПротиподагричний засіб – ксантиноксидази інгібітор.ФармакокінетикаВсмоктування Алопуринол активний при пероральному застосуванні. Він швидко всмоктується із верхніх відділів шлунково-кишкового тракту. За даними фармакокінетичних досліджень, алопуринол визначається в крові вже через 30-60 хвилин після прийому. Біодоступність алопуринолу варіює від 67% до 90%. Максимальна концентрація препарату в плазмі зазвичай реєструється приблизно через 1,5 години після перорального прийому. Потім концентрація алопуринолу швидко знижується. Через 6 годин після прийому в плазмі визначається лише слідова концентрація препарату. Максимальна концентрація активного метаболіту - оксипуринола зазвичай реєструється через 3-5 годин після перорального прийому алопуринолу. Рівень оксипуринолу в плазмі знижується значно повільніше. Розподіл Алопуринол майже не зв'язується з білками плазми, тому зміни рівня зв'язування з білками не повинні значно впливати на кліренс препарату. Об'єм розподілу алопуринолу, що здається, становить приблизно 1,6 літра/кг, що говорить про досить виражене поглинання препарату тканинами. Вміст алопуринолу в різних тканинах людини не вивчений, проте дуже ймовірно, що алопуринол і оксипуринол у максимальній концентрації накопичуються в печінці та слизовій оболонці кишечника, де реєструється висока активність ксантиноксидази. Біотрансформація Під дією ксантиноксидази та альдегідоксидази алопуринол метаболізується з утворенням оксипуринолу. Оксипуринол пригнічує активність ксантиноксидази. Проте, оксипуринол - менш потужний інгібітор ксантиноксидази, проти аллопуринолом, проте його період напіввиведення значно більше. Завдяки цим властивостям після прийому разової добової дози алопуринолу ефективне пригнічення активності ксантиноксидази підтримується протягом 24 годин. У пацієнтів з нормальною функцією нирок вміст оксипуринолу в плазмі повільно збільшується аж до досягнення рівноважної концентрації. Після прийому алопуринолу в дозі 300 мг на добу, концентрація алопуринолу в плазмі крові, як правило, становить 5-10 мг/л. До інших метаболітів алопуринолу відносяться алопуринол-рибозид і оксипуринол-7-рибозид. Виведення Приблизно 20% прийнятого per os алопуринолу виводиться через кишечник у незміненому вигляді. Близько 10% добової дози екскретуються клубочковим апаратом нирки як незміненого аллопуринола. Ще 70% добової дози алопуринолу виводиться із сечею у формі оксипуринолу. Оксипуринол виводиться нирками у незміненому вигляді, однак у зв'язку з канальцевою реабсорбцією він має тривалий період напіввиведення. Період напіввиведення алопуринолу становить 1-2 години, тоді як період напіввиведення оксипуринолу варіює від 13 до 30 годин. Такі значні відмінності, ймовірно, пов'язані з відмінностями у структурі досліджень та/або кліренсі креатиніну у пацієнтів. Пацієнти з порушеною функцією нирок У пацієнтів з порушеною функцією нирок виведення алопуринолу та оксипуринолу може значно сповільнюватися, що при тривалій терапії призводить до зростання концентрації цих сполук у плазмі крові. У пацієнтів з порушеною функцією нирок та кліренсом креатиніну 10-20 мл/хв після тривалої терапії алопуринолом у дозі 300 мг на добу концентрація оксипуринолу в плазмі досягала орієнтовно 30 мг/л. Така концентрація оксипуринолу може визначатися у пацієнтів з нормальною функцією нирок на фоні терапії алопуринолом у дозі 600 мг на добу. Отже, при лікуванні пацієнтів із порушенням функції нирок дозу алопуринолу необхідно знижувати. Літні пацієнти У пацієнтів похилого віку значні зміни фармакокінетичних властивостей алопуринолу малоймовірні. Виняток становлять пацієнти із супутньою патологією нирок.ФармакодинамікаАлопуринол є структурним аналогом гіпоксантину. Алопуринол, а також його основний активний метаболіт – оксипуринол, пригнічують ксантиноксидазу – фермент, що забезпечує перетворення гіпоксантину на ксантин, та ксантину на сечову кислоту. Алопуринол зменшує концентрацію сечової кислоти у сироватці крові та сечі; таким чином він запобігає відкладенню кристалів сечової кислоти в тканинах та/або сприяє їх розчиненню. Крім придушення катаболізму пуринів у деяких (але не у всіх) пацієнтів з гіперурикемією, велика кількість ксантину та гіпоксантину стає доступною для повторного утворення пуринових основ, що призводить до пригнічення біосинтезу пуринів de novo за механізмом зворотного зв'язку, що опосередковано пригніченням ферменту гіпоксантин-гуанін. -трансферази. Інші метаболіти алопуринолу - алопуринол-рибозид та оксипуринол-7 рибозид.Показання до застосуванняПригнічення утворення сечової кислоти та її солей при підтвердженому накопиченні цих сполук (наприклад, подагра, шкірні тофуси, нефролітіаз) або передбачуваному клінічному ризику їх накопичення (наприклад, лікування злоякісних новоутворень може ускладнюватися розвитком гострої сечокислої нефропатії). До основних клінічних станів, які можуть супроводжуватися накопиченням сечової кислоти та її солей, відносяться: ідіопатична подагра; сечокам'яна хвороба (утворення конкрементів із сечової кислоти); гостра сечокисла нефропатія; пухлинні захворювання та мієлопроліферативний синдром з високою швидкістю оновлення клітинної популяції, коли гіперурикемія виникає спонтанно або після проведення цитотоксичної терапії; певні ферментативні порушення, що супроводжуються гіперпродукцією солей сечової кислоти, наприклад, знижена активність гіпоксантин-гуанін-фосфорибозилтрансферази (включаючи синдром Льоша-Найхана), знижена активність глюкозо-6-фосфатази (включаючи глікогенози -амідо-трансферази, знижена активність аденін-фосфорибозилтрансферази Лікування сечокам'яної хвороби, що супроводжується утворенням 2,8-дигідроксиаденінових (2,8-ДГА) конкрементів у зв'язку зі зниженою активністю аденін-фосфорибозилтрансферази. Профілактика та лікування сечокам'яної хвороби, що супроводжується утворенням змішаних кальцієво-оксалатних конкрементів на тлі гіперурікозурії, коли дієта та підвищене споживання рідини були безуспішними.Протипоказання до застосуванняГіперчутливість до алопуринолу або будь-якої з допоміжних речовин, що входять до складу препарату. Печінкова недостатність, хронічна ниркова недостатність (стадія азотемії), первинний гемохроматоз, безсимптомна гіперурикемія, гострий напад подагри, дитячий вік до 3-х років (з урахуванням твердої лікарської форми) Вагітність, період грудного вигодовування. З обережністю: Порушення функції печінки, гіпотиреоз, цукровий діабет, артеріальна гіпертензія, одночасний прийом інгібіторів ангіотензинперетворюючого ферменту (АПФ) або діуретиків, дитячий вік (до 15 років призначають тільки під час цитостатичної терапії лейкозів та ін. злоякісних захворювань; літній вік.Вагітність та лактаціяВ даний час даних щодо безпеки терапії алопуринолом у період вагітності недостатньо, хоча цей препарат широко застосовувався протягом довгих років без явних несприятливих наслідків. Вагітним жінкам не слід приймати таблетки Алопуринол, за винятком тих випадків, коли не існує менш небезпечного альтернативного лікування та захворювання становить більший ризик для матері та плода, ніж прийом препарату. Згідно з наявними повідомленнями, алопуринол та оксипуринол виділяються з грудним молоком. У жінок, які приймають алопуринол у дозі 300 мг/добу, концентрація алопуринолу та оксипуринолу у грудному молоці досягала, відповідно, 1,4 мг/л та 53,7 мг/л. Проте, відомостей про вплив алопуринолу та його метаболітів на немовлят, які перебувають на грудному вигодовуванні, відсутні. Таким чином, препарат Алопуринол таблетки не рекомендується в період грудного вигодовування.Побічна діяВідсутні сучасні клінічні дані визначення частоти розвитку побічних ефектів. Їх частота може варіювати в залежності від дози та від того, чи призначався препарат як монотерапія або у комбінації з іншими препаратами. Класифікація частоти розвитку побічних ефектів заснована на приблизній оцінці, більшість побічних ефектів відсутні дані визначення частоти їх розвитку. Класифікація небажаних реакцій залежно від частоти народження виглядає наступним чином: дуже часті (≥1/10), часті (від ≥1/100 до Небажані реакції, пов'язані з терапією алопуринолом, що спостерігаються в постреєстраційному періоді, зустрічаються рідко або дуже рідко. У загальній популяції пацієнтів, здебільшого, мають легкий характер. Частота розвитку небажаних явищ збільшується при порушеннях функції нирок та (або) печінки. Інфекції та паразитарні захворювання: дуже рідкісні – фурункульоз. Порушення з боку системи крові та лімфатичної системи: дуже рідкісні – агранулоцитоз, апластична анемія, тромбоцитопенія, гранулоцитоз, лейкопенія, лейкоцитоз, еозинофілія та аплазія, що стосується лише еритроцитів. Дуже рідко надходили повідомлення про тромбоцитопенію, агранулоцитоз і апластичні анемії, особливо у осіб з порушеннями функції нирок та/або печінки, що наголошує на необхідності прояву особливої обережності у цих груп пацієнтів. Порушення з боку імунної системи: нечасті – реакції гіперчутливості; рідкісні - тяжкі реакції гіперчутливості, включаючи шкірні реакції з відшаруванням епідермісу, лихоманкою, лімфаденопатією, артралгією та (або) еозинофілією (у тому числі синдром Стівенса-Джонсона та токсичний епідермальний некроліз). Супутній васкуліт або реакції з боку тканини можуть мати різні прояви, включаючи гепатит, ураження нирок, гострий холангіт, ксантинові конкременти і, в окремих випадках, судоми. Крім того, дуже рідко спостерігався розвиток анафілактичного шоку. При розвитку тяжких небажаних реакцій терапію алопуринолом необхідно негайно припинити та не відновлювати.При відстроченій мультиорганній гіперчутливості (відомій як синдром лікарської гіперчутливості /DRESS/) можуть розвиватися такі симптоми в різних комбінаціях: лихоманка, шкірний висип, васкуліт, лімфаденопатія, псевдолімфома, артралгія, лейкопенія, еозинофілія, гепатоспленом проток (руйнування або зникнення внутрішньопечінкових жовчних проток). При розвитку таких реакцій у будь-який період лікування Алопуринол слід негайно скасувати і ніколи не відновлювати. Генералізовані реакції гіперчутливості розвивалися у пацієнтів з порушеною функцією нирок та печінки. Такі випадки іноді мали летальний кінець; дуже рідкісні – ангіоімунобластна лімфаденопатія.псевдолімфома, артралгія, лейкопенія, еозинофілія, гепатоспленомегалія, зміна результатів печінкових функціональних тестів, синдром жовчних проток, що зникають (руйнування або зникнення внутрішньопечінкових жовчних проток). При розвитку таких реакцій у будь-який період лікування Алопуринол слід негайно скасувати і ніколи не відновлювати. Генералізовані реакції гіперчутливості розвивалися у пацієнтів з порушеною функцією нирок та печінки. Такі випадки іноді мали летальний кінець; дуже рідкісні – ангіоімунобластна лімфаденопатія.псевдолімфома, артралгія, лейкопенія, еозинофілія, гепатоспленомегалія, зміна результатів печінкових функціональних тестів, синдром жовчних проток, що зникають (руйнування або зникнення внутрішньопечінкових жовчних проток). При розвитку таких реакцій у будь-який період лікування Алопуринол слід негайно скасувати і ніколи не відновлювати. Генералізовані реакції гіперчутливості розвивалися у пацієнтів з порушеною функцією нирок та печінки. Такі випадки іноді мали летальний кінець; дуже рідкісні – ангіоімунобластна лімфаденопатія.Алопуринол слід негайно відмінити і ніколи не відновлювати. Генералізовані реакції гіперчутливості розвивалися у пацієнтів з порушеною функцією нирок та печінки. Такі випадки іноді мали летальний кінець; дуже рідкісні – ангіоімунобластна лімфаденопатія.Алопуринол слід негайно відмінити і ніколи не відновлювати. Генералізовані реакції гіперчутливості розвивалися у пацієнтів з порушеною функцією нирок та печінки. Такі випадки іноді мали летальний кінець; дуже рідкісні – ангіоімунобластна лімфаденопатія. Ангіоімунобластну лімфаденопатію дуже рідко діагностували після біопсії лімфовузлів з приводу генералізованої лімфаденопатії. Ангіоімунобластна лімфаденопатія носить оборотний характер і регресує після припинення терапії алопуринолом. Порушення з боку обміну речовин та харчування: дуже рідкісні – цукровий діабет, гіперліпідемія. Порушення психіки: дуже рідкісні – депресія. Порушення з боку нервової системи: дуже рідкісні – кома, параліч, атаксія, нейропатія, парестезія, сонливість, головний біль, збочення смакових відчуттів. Порушення органу зору: дуже рідкісні - катаракта, порушення зору, макулярні зміни. Порушення з боку органу слуху та лабіринтні розлади: дуже рідкісні – запаморочення (вертиго). Порушення з боку серця: дуже рідкісні – стенокардія, брадикардія. Порушення з боку судин: дуже рідкісні – підвищення артеріального тиску. Порушення з боку шлунково-кишкового тракту: нечасті – блювання, нудота, діарея. У раніше проведених клінічних дослідженнях спостерігали нудоту та блювоту, проте пізніші спостереження підтвердили, що ці реакції не є клінічно значущою проблемою і їх можна уникнути, призначаючи алопуринол після їди; дуже рідкісні - рецидивні кривава блювота, стеаторея, стоматит, зміни частоти дефекації; частота невідома – біль у животі. Порушення з боку печінки та жовчовивідних шляхів: нечасті – безсимптомне збільшення концентрації печінкових ферментів (підвищений рівень лужної фосфатази та трансаміназ у сироватці крові); рідкісні - гепатит (включаючи некротичну та гранулематозну форми). Порушення функції печінки можуть розвиватися без явних ознак генералізованої гіперчутливості Порушення з боку шкіри та підшкірних тканин: часті – висип; рідкісні – тяжкі реакції з боку шкіри: синдром Стівенса-Джонсона (ССД) та токсичний епідермальний некроліз (ТЕН); дуже рідкісні - ангіоневротичний набряк, локальна медикаментозна висипка, алопеція, знебарвлення волосся. У пацієнтів, які приймають алопуринол, найбільш поширені небажані реакції з боку шкіри. З огляду на терапії препаратом ці реакції можуть розвиватися у час. Шкірні реакції можуть проявлятися свербінням, макулопапульозними та лускатими висипаннями. В інших випадках може розвинутись пурпура. У поодиноких випадках спостерігається ексфоліативне ураження шкіри (ССД/ТЕН). При розвитку подібних реакцій терапію алопуринолом необхідно негайно припинити. Якщо реакція з боку шкіри має легкий характер, то після зникнення цих змін можна відновити прийом алопуринолу в меншій дозі (наприклад, 50 мг на добу). Згодом дозу можна поступово збільшити. При рецидивуванні шкірних реакцій терапію алопуринолом потрібно припинити і більше не відновлювати,оскільки подальший прийом препарату може призвести до розвитку тяжких реакцій гіперчутливості. Згідно з наявними відомостями, на фоні терапії алопуринолом ангіоневротичний набряк розвивався ізольовано, а також у поєднанні із симптомами генералізованої реакції гіперчутливості. Порушення з боку скелетно-м'язової та сполучної тканини: дуже рідкісні – міалгія. Порушення з боку нирок та сечовивідних шляхів: дуже рідкісні – гематурія, ниркова недостатність, уремія; частота невідома – сечокам'яна хвороба. Порушення з боку репродуктивної системи та молочної залози: дуже рідкісні – чоловіче безпліддя, еректильна дисфункція, гінекомастія. Загальні розлади та порушення у місці введення препарату: дуже рідкісні – набряк, загальне нездужання, загальна слабкість, лихоманка. Згідно з наявними відомостями, на тлі терапії алопуринолом лихоманка розвивалася як ізольовано, так і у поєднанні із симптомами генералізованої реакції гіперчутливості. Повідомлення про можливі побічні реакції У разі виникнення побічних реакцій, у тому числі не зазначених у цій інструкції, слід припинити застосування лікарського засобу. У післяреєстраційному періоді важлива будь-яка інформація про можливі побічні реакції, оскільки ці повідомлення допомагають постійно відстежувати безпеку препарату. Співробітники сфери охорони здоров'я зобов'язані повідомляти про будь-які підозри на побічні реакції до органів місцевого фармаконагляду.Взаємодія з лікарськими засобами6-меркаптопуріп та азатіоприн Азатіоприн метаболізується з утворенням 6-меркаптопурину, який інактивується ферментом ксантиноксидазою. У випадках, коли терапія 6-меркаптопурином або азатіоприном поєднується з алопуринолом, пацієнтам слід призначати лише одну чверть від звичайної дози 6-меркаптопурину або азатіоприну, оскільки пригнічення активності ксантиноксидази збільшує тривалість дії цих сполук. Відарабін (аденіна арабінозід) У присутності алопуринолу період напіввиведення відарабіну збільшується. При одночасному застосуванні цих препаратів необхідно дотримуватись особливої настороженості щодо посилених токсичних ефектів терапії. Саліцилати та урикозуричні засоби Основним активним метаболітом алопуринолу є оксипуринол, який виводиться нирками аналогічно до солей сечової кислоти. Отже, лікарські препарати з урикозуричною активністю, такі як пробенецид або високі дози саліцилатів, можуть посилювати виведення оксипуринолу. У свою чергу посилене виведення оксипуринолу супроводжується зменшенням терапевтичної активності аллопуринолу, проте значущість цього виду взаємодії необхідно оцінювати індивідуально в кожному випадку. Хлорпропамід При одночасному застосуванні алопуринолу та хлорпропаміду у пацієнтів з порушеною функцією нирок збільшується ризик розвитку тривалої гіпоглікемії, оскільки на етапі канальцевої екскреції алопуринол та хлорпропамід конкурують між собою. Антикоагулянти похідні кумарину При одночасному застосуванні з алопуринолом спостерігалося посилення ефектів варфарину та інших антикоагулянтів похідних кумарину. У зв'язку з цим необхідно ретельно контролювати стан пацієнтів, які отримують супутню терапію цими препаратами. Фенітоїн Алопуринол здатний пригнічувати окиснення фенітоїну в печінці, проте клінічна значимість цієї взаємодії не встановлена. Теофілін Відомо, що алопуринол пригнічує метаболізм теофіліну. Подібну взаємодію можна пояснити участю ксантиноксидази у процесі біотрансформації теофіліну в організмі людини. Концентрацію теофіліну в сироватці крові необхідно контролювати на початку супутньої терапії алопуринолом, а також зі збільшенням дози останнього. Ампіцилін та амоксицилін У пацієнтів, які одночасно отримували ампіцилін або амоксицилін та алопуринол, реєструвалася підвищена частота розвитку реакцій з боку шкіри, порівняно з пацієнтами, які не отримували подібну супутню терапію. Причину цього виду лікарської взаємодії не встановлено. Тим не менш, пацієнтам, які отримують алопуринол, замість ампіциліну та амоксициліну рекомендується призначати інші антибактеріальні препарати. Цитотоксичні лікарські засоби (циклофосфамід, доксорубіцин, блеоміцин, прокарбазин, мехлоретамін) У пацієнтів, які страждають на пухлинні захворювання (крім лейкозів) і отримують алопуринол, спостерігалося посилене пригнічення діяльності кісткового мозку циклофосфамідом та іншими цитотоксичними препаратами. Проте, згідно з результатами контрольованих досліджень, у яких взяли участь пацієнти, які отримують циклофосфамід, доксорубіцин, блеоміцин, прокарбазин та (або) мехлоретамін (хлорметину гідрохлорид), супутня терапія алопуринолом не посилювала токсичний вплив цих цитотоксичних препаратів. Циклоспорин Згідно з деякими повідомленнями, концентрація циклоспорину в плазмі може збільшуватися на тлі супутньої терапії алопуринолом. При одночасному застосуванні цих препаратів необхідно враховувати можливість посилення токсичності циклоспорину. Діданозин У здорових добровольців та ВІЛ-інфікованих пацієнтів, які отримують диданозин, на фоні супутньої терапії алопуринолом (300 мг на добу) спостерігалося збільшення СMAХ (максимальна концентрація препарату в плазмі крові) та AUC (площа під кривою концентрація-час) диданозину приблизно вдвічі. Період напіввиведення диданозину у своїй не змінювався. Як правило, одночасне застосування цих лікарських засобів не рекомендується. Якщо супутня терапія неминуча, може знадобитися зниження дози диданозину та ретельне спостереження за станом пацієнта. Інгібітори АПФ Одночасне застосування іАПФ з алопуринолом супроводжується підвищеним ризиком розвитку лейкопенії, таким чином ці препарати слід комбінувати з обережністю. Тіазидні діуретики Одночасне застосування тіазидних діуретиків, у тому числі гідрохлортіазиду, може підвищити ризик розвитку побічних ефектів гіперчутливості, пов'язаних з алопуринолом, особливо у пацієнтів з порушеннями функції нирок.Спосіб застосування та дозиВсередину. Препарат слід приймати один раз на день після їди, запиваючи великою кількістю води. Якщо добова доза перевищує 300 мг або спостерігаються симптоми непереносимості з боку шлунково-кишкового тракту, дозу необхідно ділити на кілька прийомів. Дорослі пацієнти Щоб зменшити ризик розвитку побічних ефектів, рекомендується використовувати алопуринол у початковій дозі 100 мг один раз на день. Якщо цієї дози недостатньо для того, щоб належним чином знизити концентрацію сечової кислоти в сироватці крові, то добову дозу можна поступово збільшувати до досягнення бажаного ефекту. Слід виявляти особливу обережність у разі порушення функції нирок. При підвищенні дози алопуринолу кожні 1-3 тижні необхідно визначати концентрацію сечової кислоти у сироватці крові. При доборі дози препарату рекомендується використовувати такі режими дозування (залежно від вибраного режиму дозування рекомендуються таблетки 100 мг або 300 мг). Рекомендована доза препарату становить: 100-200 мг на добу при легкому перебігу захворювання; 300-600 мг на добу при середньотяжкому перебігу; 700-900 мг на добу при тяжкому перебігу. Якщо при розрахунку дози виходити з маси тіла пацієнта, то доза алопуринолу повинна становити від 2 до 10 мг/кг/добу. Діти та підлітки віком до 15 років Рекомендована доза для дітей від 3 до 10 років: 5-10 мг/кг/добу. Для низьких доз використовують таблетки 100 мг, які за допомогою ризику можна розділити на дві однакові дози по 50 мг. Рекомендована доза для дітей віком від 10 до 15 років 10-20 мг/кг/добу. Добова доза не повинна перевищувати 400 мг. Алопуринол рідко застосовується для дитячої терапії. Виняток становлять злоякісні онкологічні захворювання (особливо лейкози) та деякі ферментативні порушення (наприклад, синдром Льоша-Найхана). Літні пацієнти Оскільки спеціальні дані щодо застосування алопуринолу у популяції людей похилого віку відсутні, для лікування таких пацієнтів слід використовувати препарат у мінімальній дозі, що забезпечує достатнє зниження концентрації сечової кислоти у сироватці крові. Особливу увагу необхідно приділити рекомендаціям щодо добору дози препарату для пацієнтів з порушеною функцією нирок. Порушення функції нирок Оскільки алопуринол та його метаболіти виводяться з організму нирками, порушення функції нирок може призводити до затримки препарату та його метаболітів в організмі з подальшим подовженням періоду напіввиведення цих сполук із плазми крові. При тяжкій нирковій недостатності рекомендується застосовувати алопуринол у дозі нижче 100 мг на добу або використовувати разові дози по 100 мг з інтервалом більше одного дня. Якщо умови дозволяють контролювати концентрацію оксипуринолу в плазмі крові, то дозу алопуринолу слід підібрати таким чином, щоб рівень оксипуринолу в плазмі був нижчий за 100 мкмоль/л (15,2 мг/л). Алопуринол та його похідні видаляються з організму за допомогою гемодіалізу. Якщо сеанси гемодіалізу проводяться 2-3 рази на тиждень, то доцільно визначити необхідність переходу на альтернативний режим терапії – прийом 300-400 мг алопуринолу відразу після завершення сеансу гемодіалізу (між сеансами гемодіалізу препарат не приймається). У пацієнтів з порушеннями функції нирок комбінування алопуринолу з тіазидними діуретиками слід проводити з винятковою обережністю. Алопуринол слід призначати у найнижчих ефективних дозах при ретельному моніторуванні функції нирок. Порушення функції печінки При порушеній функції печінки дозу препарату слід зменшити. На ранньому етапі лікування рекомендується здійснювати моніторинг лабораторних показників функції печінки. Стани, що супроводжуються посиленням обміну солеї сечової кислоти (наприклад, пухлинні захворювання, синдром Льоша-Найхана) Перед початком терапії цитотоксичними препаратами рекомендується корекцію існуючої гіперурикемії та (або) гіперурикозурії за допомогою алопуринолу. Велике значення має адекватна гідратація, що сприяє підтримці оптимального діурезу, а також олужнення сечі, завдяки якому збільшується розчинність сечової кислоти та її солей. Доза алопуринолу повинна бути близькою до нижньої межі рекомендованого діапазону доз. Якщо порушення функції нирок обумовлено розвитком гострої сечокислої нефропатії або іншої ниркової патології, лікування слід продовжувати відповідно до рекомендацій, представлених у розділі "Порушення функції нирок". Описані заходи можуть зменшити ризик накопичення ксантину та сечової кислоти, що ускладнює перебіг хвороби. Рекомендації щодо моніторингу Для корекції дози препарату необхідно з оптимальними інтервалами оцінювати концентрацію солей сечової кислоти у сироватці крові, а також рівень сечової кислоти та уратів сечі.ПередозуванняСимптоми Нудота, блювання, діарея та запаморочення. Тяжке передозування алопуринолу може призвести до значного пригнічення активності ксантиноксидази. Сам собою цей ефект не повинен супроводжуватися небажаними реакціями. Виняток становить вплив на супутню терапію, особливо на лікування 6-меркаптопурином та (або) азатіоприном. Лікування Специфічний антидот алопуринолу невідомий. Адекватна гідратація, що підтримує оптимальний діурез, сприяє виведенню алопуринолу та його похідних із сечею. За наявності клінічних показань виконується гемодіаліз.Запобіжні заходи та особливі вказівкиСиндром лікарської гіперчутливості, ССД та ТЕН На фоні застосування алопуринолу надходили повідомлення про розвиток загрозливих для життя реакцій з боку шкіри, такі як синдром Стівенса-Джонсона і токсичний епідермальний некроліз (ССД/ТЕН). Пацієнтів слід інформувати про симптоми цих реакцій (прогресуючий шкірний висип, часто з бульбашками та ураженням слизових) і ретельно моніторувати їх розвиток. Найчастіше ССД/ТЕН розвиваються на перших тижнях прийому препарату. За наявності ознак та симптомів ССД/ТЕН препарат Алопуринол слід негайно відмінити та більше не призначати. Маніфестація реакцій гіперчутливості до алопуринолу може бути різною, включаючи макулопапульозну екзантему, синдром лікарської гіперчутливості (DRESS) та ССД/ТЕН. Ці реакції є клінічним діагнозом і їх клінічні прояви є основою для прийняття відповідних рішень.Терапію препаратом Алопуринол слід негайно припинити при появі висипу на шкірі або інших проявів реакції гіперчутливості. Не можна відновлювати терапію у пацієнтів із синдромом гіперчутливості та ССД/ТЕН. Кортикостероїди можуть застосовуватись для лікування шкірних реакцій при гіперчутливості. Хронічне порушення функції нирок Пацієнти з хронічним порушенням функції нирок мають більший ризик розвитку реакцій гіперчутливості, пов'язаних з алопуринолом, у тому числі ССД/ТЕН. Алель HLA-B*5801 Було встановлено, що присутність алелю HLA-B*5801 пов'язана з розвитком синдрому гіперчутливості до алопуринолу та ССД/ТЕН. Частота присутності алеля HLA- В * 5801 різна в різних етнічних групах і може досягати 20% у популяції китайців Хань, близько 12% у корейців та 1-2% у японців та європейців. Застосування генотипування прийняття рішень про терапії аллопуринолом не досліджувалося. Якщо відомо, що пацієнт є носієм алелю HLA-B*5801, то алопуринол слід призначати лише, якщо користь лікування перевершує ризик. Слід дуже уважно стежити за розвитком синдрому гіперчутливості та ССД/ТЕН. Пацієнт повинен бути проінформований про необхідність негайного скасування лікування при першій появі таких симптомів. Порушення функції печінки та нирок При лікуванні пацієнтів з порушеною функцією нирок або печінки дозу алопуринолу необхідно знизити. У пацієнтів, які отримують лікування артеріальною гіпертензією або серцевою недостатністю (наприклад, пацієнти, які приймають діуретики або інгібітори АПФ), може спостерігатися супутнє порушення функції нирок, тому алопуринол у цій групі пацієнтів слід використовувати з обережністю. Безсимптомна гіперурикемія сама по собі не є показанням до застосування алопуринолу. У таких випадках поліпшення стану пацієнтів може бути досягнуто завдяки змінам дієти та споживанню рідини поряд з усуненням основної причини гіперурикемії. Гострий напад подагри Алопуринол не слід застосовувати до повного усунення гострого нападу подагри, оскільки цим можна спровокувати додаткове загострення захворювання. Аналогічно терапії урикозуричними засобами, початок лікування алопуринолом може спровокувати гострий напад подагри. Щоб уникнути цього ускладнення, рекомендується проводити профілактичну терапію нестероїдними протизапальними препаратами або колхіцином протягом щонайменше одного місяця до призначення алопуринолу. Детальні відомості про рекомендовані дози, застереження та запобіжні заходи можна знайти у відповідній літературі. Якщо гострий напад подагри розвивається на тлі терапії алопуринолом, то прийом препарату слід продовжити в тій же дозі, а для лікування нападу необхідно призначити нестероїдний протизапальний засіб. Відкладення ксантину У випадках, коли утворення сечової кислоти значно посилено (наприклад, злоякісна пухлинна патологія та відповідна протипухлинна терапія, синдром Льоша-Найхана), абсолютна концентрація ксантину в сечі в поодиноких випадках може істотно збільшитися, що сприяє відкладенню ксантину в тканинах сечових. Імовірність відкладення ксантину в тканинах можна звести до мінімуму завдяки адекватній гідратації, що забезпечує оптимальне розведення сечі. Вклинення конкрементів із сечової кислоти Адекватна терапія алопуринолом може призводити до розчинення великих конкрементів з сечової кислоти, що знаходяться в ниркових баліях, однак, ймовірність вклинення цих конкрементів в сечоводи невелика. Гемохроматоз Основний ефект алопуринолу при лікуванні подагри полягає у придушенні активності ферменту ксантиноксидази. Ксантиноксидаза може брати участь у зменшенні вмісту та виведенні заліза, що депонується у печінці. Дослідження, що демонструють безпеку терапії алопуринолом у популяції пацієнтів із гемохроматозом, відсутні. Пацієнтам з гемохроматозом, а також їхнім кровним родичам алопуринол слід призначати з обережністю. Вплив на здатність до керування автотранспортом та управління механізмами На тлі терапії алопуринолом спостерігався розвиток таких небажаних реакцій, як сонливість, запаморочення (вертиго) та атаксія. Ці небажані явища можуть вплинути на здатність до керування автотранспортом та управління механізмами. Пацієнти, які приймають препарат Алопуринол таблетки, не повинні керувати транспортними засобами та механізмами доти, доки вони не будуть впевнені в тому, що алопуринол не надає несприятливого впливу на відповідні здібності.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаСуспензія - 1 пак. Алюмінію гідроксид гель - 4,36 г (у перерахунку на Al2О3 - 436 мг); Магнію гідроксид наступу - 700 мг (у перерахунку на MgO - 150 мг); Допоміжні речовини: Водню пероксиду розчин 30% - 0,82 мг, сорбітол - 1602,300 мг, гіетелоза - 21,80 мг, метилпарагідроксибензоат - 21,80 мг, пропілпарагідроксибензоат - 2,726 мг, бутілпарагідрок, 6 мг, пропіленгліколь – 654,00 мг, макрогол 4000 – 436,00 мг, лимона олія – 3,27 мг, етанол 96 % – 196,20 мг, вода очищена до 10 мл. Суспензія для вживання. 10 або 20 пакетиків разом із інструкцією із застосування у картонній пачці.Опис лікарської формиСуспензія білого або майже білого кольору із характерним запахом лимона. При зберіганні на поверхні може виділятись шар прозорої рідини. При енергійному збовтуванні гомогенність суспензії відновлюється.Фармакотерапевтична групаАнтацидний засіб.ФармакокінетикаАлгелдрат Всмоктування – резорбуються невеликі кількості препарату, які практично не змінюють концентрацію солей алюмінію у крові. Розподіл – ні. Метаболізм – ні. Виведення – виводиться через кишечник. Магнію гідроксид Всмоктування - іони магнію резорбуються близько 10% прийнятої дози і не змінюють концентрації іонів магнію в крові. Розподіл – зазвичай локально. Метаболізм – ні. Виведення – виводиться через кишечник.ФармакодинамікаАлмагель - лікарський засіб, що є збалансованою комбінацією алгелдрату (алюмінію гідроксиду) і магнію гідроксиду. Він нейтралізує вільну соляну кислоту в шлунку, знижує активність пепсину, що призводить до зменшення активності шлункового соку, що перетравлює. Чинить обволікаючу, адсорбуючу дію. Захищає слизову оболонку шлунка за рахунок стимулювання синтезу простагландинів (цитопротективна дія). Це захищає слизову оболонку від запальних та ерозивно-геморрагічних уражень внаслідок застосування подразнюючих та ульцерогенних агентів, таких як етиловий спирт та нестероїдні протизапальні препарати (наприклад, індометацин, диклофенак, аспірин, ацетилсаліцилова кислота, кортикостероїдні препарати). Терапевтичний ефект після прийому препарату настає через 3-5 хвилин.Тривалість дії залежить від швидкості випорожнення шлунка. При прийомі натще дію триває до 60 хвилин. При прийомі через годину після їди антацидна дія може тривати до 3 годин. Не викликає вторинної гіперсекреції шлункового соку.Показання до застосуванняЛікування Гострий гастрит; хронічний гастрит із підвищеною та нормальною секреторною функцією шлунка (у фазі загострення); гострий дуоденіт, ентерит, коліт; виразкова хвороба шлунка та дванадцятипалої кишки (у фазі загострення); грижа стравохідного отвору діафрагми, гастроезофагеальний рефлюкс, рефлюкс-езофагіт, дуоденогастральний рефлюкс; симптоматичні виразки шлунково-кишкового тракту різного генезу; ерозії слизової оболонки верхніх відділів шлунково-кишкового тракту; гострий панкреатит; загострення хронічного панкреатиту; печія та болі в епігастрії після похибок у харчуванні, надмірного вживання етанолу, нікотину, кави, прийому лікарських засобів, що подразнюють слизову оболонку шлунка. Профілактика шлункових та дуоденальних порушень – зменшення подразнюючої та ульцерогенної дії, пов'язаної з прийомом лікарських препаратів, що подразнюють слизову оболонку шлунка.Протипоказання до застосуванняГіперчутливість до діючої або до будь-якої допоміжної речовини, що входить до складу препарату. Тяжка форма ниркової недостатності (через небезпеку розвитку гіпермагніємії та алюмінієвої інтоксикації). Вагітність. Хвороба Альцгеймера. Гіпофосфатемія. Дитячий вік віком до 10 років. Вроджена непереносимість фруктози (містить сорбітол).Вагітність та лактаціяДослідження на тваринах показали, що немає даних про наявність тератогенного потенціалу чи інших небажаних ефектів на ембріон та/або плід. Немає клінічних даних щодо застосування Алмагелю вагітними жінками. Препарат не рекомендується під час вагітності, але якщо передбачувана користь від його застосування перевищує потенційний ризик для плода, слід приймати під наглядом лікаря не більше 5-6 днів. Немає даних про виділення активних речовин препарату із грудним молоком. Алмагель можна застосовувати в період годування груддю лише після ретельної оцінки співвідношення користі для матері та потенційного ризику для новонародженого. У період годування груддю рекомендується застосовувати трохи більше 5-6 днів під наглядом лікаря.Побічна діяАлмагель може спричинити запор, який проходить після зменшення дози. У поодиноких випадках спостерігаються нудота, блювання, спазм шлунка, зміна смакових відчуттів, алергічні реакції та гіпермагніємія (підвищення рівня магнію, крові). При тривалому прийомі препарату хворими з нирковою недостатністю та на діалізі можливі зміни настрою та розумової активності; При тривалому прийомі високих доз препарату поряд з дефіцитом фосфору в їжі, можливо виникнення остеомаляції.Взаємодія з лікарськими засобамиМоже абсорбувати деякі лікарські засоби, зменшуючи таким чином їх всмоктування, тому при одночасному прийомі інших лікарських засобів їх необхідно приймати за 1-2 години до або після прийому Алмагелю. Алмагель зменшує кислотність шлункового соку і це може вплинути на дію великої кількості лікарських засобів при одночасному прийомі. Алмагель знижує ефект блокаторів гістамінових Н2-рецепторів (циметидин, ранітидин, фамотидин), серцевих глікозидів, солей заліза, препаратів літію, хінідину, мексилетину, фенотіазинових препаратів, антибіотиків тетрациклінового ряду, ципрофлоксацину, ізоніу. При одночасному прийомі кишковорозчинних препаратів підвищений pH шлункового соку може призвести до прискореного порушення юс оболонки та спричинити подразнення шлунка та дванадцятипалої кишки. Алмагель може вплинути на результати деяких лабораторних та функціональних досліджень та тестів: він знижує рівень шлункової секреції щодо її кислотності; змінює результати тестів з використанням технеції (ТС99), наприклад сцинтиграфія кісток та деякі тести для дослідження стравоходу, підвищує сироватковий рівень фосфору, значення pH сироватки та сечі.Спосіб застосування та дозиЛікування Дорослим та дітям старше 15 років По 5-10 мл (1-2 мірні ложки) або 1 пакетик 3-4 рази на день. При необхідності разову дозу можна збільшити до 15 мл (3 мірні ложки). Дітям від 10 до 15 років Застосовують у дозі, що дорівнює половині дози для дорослих - по 1 мірній ложці 2-4 рази на день або по 2 мірні ложки 1-2 рази на день або по 1 пакетику 1-2 рази на день. Препарат приймають через 45-60 хвилин після їди і ввечері перед сном. Після досягнення терапевтичного ефекту добову дозу зменшують до 5 мл (1 мірна ложка) 3-4 рази на добу або по 1 пакетику 1-2 рази на добу протягом 15-20 днів. Не рекомендується приймати рідини протягом 15 хвилин після прийому препарату Алмагель. Перед застосуванням суспензію необхідно ретельно гомогенізувати, струшуючи флакон або розминаючи та струшуючи пакетик. Для профілактики По 5-15 мл (1-3 мірні ложки) або 1 пакетик за 15 хвилин до прийому препаратів з подразливою дією.ПередозуванняПри одноразовому перевищенні дози не спостерігаються інші ознаки передозування, крім запору, метеоризму, відчуття металевого смаку в роті. При тривалому прийомі високих доз можливі утворення каменів у нирках, поява важких запорів, легка сонливість, гіпермагніємія. Можуть спостерігатися також ознаки метаболічного алкалозу: зміна настрою чи розумової активності, оніміння чи біль у м'язах, дратівливість та швидка стомлюваність, уповільнення дихання, неприємні смакові відчуття. У цих випадках необхідно відразу вжити заходів щодо швидкого виведення препарату з організму – промивання шлунка, стимуляція блювання, прийом активованого вугілля.Запобіжні заходи та особливі вказівкиНе рекомендується застосування препарату у хворих із тяжким запором; при болю в шлунку неясного походження та при підозрі на гострий апендицит; за наявності виразкового коліту, дивертикульозу, колостомії або ілеостомії; при хронічній діареї; гострий геморой; при зміні кислотно-лужної рівноваги в організмі, а також за наявності метаболічного алкалозу; при цирозі печінки; тяжкої серцевої недостатності; при токсикозі вагітних; при порушеннях функції нирок (кліренс креатиніну При тривалому прийомі препарату (більше 20 днів) необхідний регулярний лікарський контроль сироваткового рівня магнію при лікуванні хворих з нирковою недостатністю. Препарат не містить цукру, що дозволяє приймати його хворим на цукровий діабет. Препарат містить сорбітол, який протипоказаний при вродженій непереносимості фруктози. Вплив на здатність до керування автотранспортом та управління механізмами Алмагель не впливає на здатність керувати автомобілем та працювати з механізмами. При прийомі в рекомендованій добовій дозі етиловий спирт, що міститься в препараті, не впливає на здатність керувати автомобілем і роботу з механізмами.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаСуспензія - 5 мл: Алюмінію гідроксид гель -2,18 г (у перерахунку на Al2О3 - 218 мг); Магнію гідроксид наступу - 350 мг (у перерахунку на MgO - 75 мг); Допоміжні речовини: Водню пероксиду розчин 30% - 0,41 мг, сорбітол - 801,15 мг, гієтеллоза - 10,90 мг, метилпарагідроксибензоат - 10,90 мг, пропілпарагідроксибснзоат - 1,363 мг, бутілпарагідрокібензо3 мг, пропіленгліколь – 327,00 мг, макрогол 4000 – 218,00 мг, лимона олія – 1,635 мг, етанол 96 % – 98,10 мг, вода очищена до 5 мл. Суспензія для вживання. По 170 мл препарату у флаконі з темного скла або з поліетилентерефталату з пластмасовим ковпачком, що нагвинчується. Кожен флакон разом з інструкцією із застосування та мірною ложкою па 5 мл у картонній пачці. По 10 мл препарату в пакетику із багатошарової фольги.Опис лікарської формиСуспензія білого або майже білого кольору із характерним запахом лимона. При зберіганні на поверхні може виділятись шар прозорої рідини. При енергійному збовтуванні гомогенність суспензії відновлюється.Фармакотерапевтична групаАнтацидний засіб.ФармакокінетикаАлгелдрат Всмоктування – резорбуються невеликі кількості препарату, які практично не змінюють концентрацію солей алюмінію у крові. Розподіл – ні. Метаболізм – ні. Виведення – виводиться через кишечник. Магнію гідроксид Всмоктування - іони магнію резорбуються близько 10% прийнятої дози і не змінюють концентрації іонів магнію в крові. Розподіл – зазвичай локально. Метаболізм – ні. Виведення – виводиться через кишечник.ФармакодинамікаАлмагель - лікарський засіб, що є збалансованою комбінацією алгелдрату (алюмінію гідроксиду) і магнію гідроксиду. Він нейтралізує вільну соляну кислоту в шлунку, знижує активність пепсину, що призводить до зменшення активності шлункового соку, що перетравлює. Чинить обволікаючу, адсорбуючу дію. Захищає слизову оболонку шлунка за рахунок стимулювання синтезу простагландинів (цитопротективна дія). Це захищає слизову оболонку від запальних та ерозивно-геморрагічних уражень внаслідок застосування подразнюючих та ульцерогенних агентів, таких як етиловий спирт та нестероїдні протизапальні препарати (наприклад, індометацин, диклофенак, аспірин, ацетилсаліцилова кислота, кортикостероїдні препарати). Терапевтичний ефект після прийому препарату настає через 3-5 хвилин.Тривалість дії залежить від швидкості випорожнення шлунка. При прийомі натще дію триває до 60 хвилин. При прийомі через годину після їди антацидна дія може тривати до 3 годин. Не викликає вторинної гіперсекреції шлункового соку.Показання до застосуванняЛікування Гострий гастрит; хронічний гастрит із підвищеною та нормальною секреторною функцією шлунка (у фазі загострення); гострий дуоденіт, ентерит, коліт; виразкова хвороба шлунка та дванадцятипалої кишки (у фазі загострення); грижа стравохідного отвору діафрагми, гастроезофагеальний рефлюкс, рефлюкс-езофагіт, дуоденогастральний рефлюкс; симптоматичні виразки шлунково-кишкового тракту різного генезу; ерозії слизової оболонки верхніх відділів шлунково-кишкового тракту; гострий панкреатит; загострення хронічного панкреатиту; печія та болі в епігастрії після похибок у харчуванні, надмірного вживання етанолу, нікотину, кави, прийому лікарських засобів, що подразнюють слизову оболонку шлунка. Профілактика шлункових та дуоденальних порушень – зменшення подразнюючої та ульцерогенної дії, пов'язаної з прийомом лікарських препаратів, що подразнюють слизову оболонку шлунка.Протипоказання до застосуванняГіперчутливість до діючої або до будь-якої допоміжної речовини, що входить до складу препарату. Тяжка форма ниркової недостатності (через небезпеку розвитку гіпермагніємії та алюмінієвої інтоксикації). Вагітність. Хвороба Альцгеймера. Гіпофосфатемія. Дитячий вік віком до 10 років. Вроджена непереносимість фруктози (містить сорбітол).Вагітність та лактаціяДослідження на тваринах показали, що немає даних про наявність тератогенного потенціалу чи інших небажаних ефектів на ембріон та/або плід. Немає клінічних даних щодо застосування Алмагелю вагітними жінками. Препарат не рекомендується під час вагітності, але якщо передбачувана користь від його застосування перевищує потенційний ризик для плода, слід приймати під наглядом лікаря не більше 5-6 днів. Немає даних про виділення активних речовин препарату із грудним молоком. Алмагель можна застосовувати в період годування груддю лише після ретельної оцінки співвідношення користі для матері та потенційного ризику для новонародженого. У період годування груддю рекомендується застосовувати трохи більше 5-6 днів під наглядом лікаря.Побічна діяАлмагель може спричинити запор, який проходить після зменшення дози. У поодиноких випадках спостерігаються нудота, блювання, спазм шлунка, зміна смакових відчуттів, алергічні реакції та гіпермагніємія (підвищення рівня магнію, крові). При тривалому прийомі препарату хворими з нирковою недостатністю та на діалізі можливі зміни настрою та розумової активності; При тривалому прийомі високих доз препарату поряд з дефіцитом фосфору в їжі, можливо виникнення остеомаляції.Взаємодія з лікарськими засобамиМоже абсорбувати деякі лікарські засоби, зменшуючи таким чином їх всмоктування, тому при одночасному прийомі інших лікарських засобів їх необхідно приймати за 1-2 години до або після прийому Алмагелю. Алмагель зменшує кислотність шлункового соку і це може вплинути на дію великої кількості лікарських засобів при одночасному прийомі. Алмагель знижує ефект блокаторів гістамінових Н2-рецепторів (циметидин, ранітидин, фамотидин), серцевих глікозидів, солей заліза, препаратів літію, хінідину, мексилетину, фенотіазинових препаратів, антибіотиків тетрациклінового ряду, ципрофлоксацину, ізоніу. При одночасному прийомі кишковорозчинних препаратів підвищений pH шлункового соку може призвести до прискореного порушення юс оболонки та спричинити подразнення шлунка та дванадцятипалої кишки. Алмагель може вплинути на результати деяких лабораторних та функціональних досліджень та тестів: він знижує рівень шлункової секреції щодо її кислотності; змінює результати тестів з використанням технеції (ТС99), наприклад сцинтиграфія кісток та деякі тести для дослідження стравоходу, підвищує сироватковий рівень фосфору, значення pH сироватки та сечі.Спосіб застосування та дозиЛікування Дорослим та дітям старше 15 років По 5-10 мл (1-2 мірні ложки) або 1 пакетик 3-4 рази на день. При необхідності разову дозу можна збільшити до 15 мл (3 мірні ложки). Дітям від 10 до 15 років Застосовують у дозі, що дорівнює половині дози для дорослих - по 1 мірній ложці 2-4 рази на день або по 2 мірні ложки 1-2 рази на день або по 1 пакетику 1-2 рази на день. Препарат приймають через 45-60 хвилин після їди і ввечері перед сном. Після досягнення терапевтичного ефекту добову дозу зменшують до 5 мл (1 мірна ложка) 3-4 рази на добу або по 1 пакетику 1-2 рази на добу протягом 15-20 днів. Не рекомендується приймати рідини протягом 15 хвилин після прийому препарату Алмагель. Перед застосуванням суспензію необхідно ретельно гомогенізувати, струшуючи флакон або розминаючи та струшуючи пакетик. Для профілактики По 5-15 мл (1-3 мірні ложки) або 1 пакетик за 15 хвилин до прийому препаратів з подразливою дією.ПередозуванняПри одноразовому перевищенні дози не спостерігаються інші ознаки передозування, крім запору, метеоризму, відчуття металевого смаку в роті. При тривалому прийомі високих доз можливі утворення каменів у нирках, поява важких запорів, легка сонливість, гіпермагніємія. Можуть спостерігатися також ознаки метаболічного алкалозу: зміна настрою чи розумової активності, оніміння чи біль у м'язах, дратівливість та швидка стомлюваність, уповільнення дихання, неприємні смакові відчуття. У цих випадках необхідно відразу вжити заходів щодо швидкого виведення препарату з організму – промивання шлунка, стимуляція блювання, прийом активованого вугілля.Запобіжні заходи та особливі вказівкиНе рекомендується застосування препарату у хворих із тяжким запором; при болю в шлунку неясного походження та при підозрі на гострий апендицит; за наявності виразкового коліту, дивертикульозу, колостомії або ілеостомії; при хронічній діареї; гострий геморой; при зміні кислотно-лужної рівноваги в організмі, а також за наявності метаболічного алкалозу; при цирозі печінки; тяжкої серцевої недостатності; при токсикозі вагітних; при порушеннях функції нирок (кліренс креатиніну При тривалому прийомі препарату (більше 20 днів) необхідний регулярний лікарський контроль сироваткового рівня магнію при лікуванні хворих з нирковою недостатністю. Препарат не містить цукру, що дозволяє приймати його хворим на цукровий діабет. Препарат містить сорбітол, який протипоказаний при вродженій непереносимості фруктози. Вплив на здатність до керування автотранспортом та управління механізмами Алмагель не впливає на здатність керувати автомобілем та працювати з механізмами. При прийомі в рекомендованій добовій дозі етиловий спирт, що міститься в препараті, не впливає на здатність керувати автомобілем і роботу з механізмами.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаСуспензія - 1 фл. Алюмінію гідроксид гель - 4,36 г (у перерахунку на Al2О3 - 436 мг); Магнію гідроксид пасту – 700 мг (у перерахунку на MgO – 150 мг); Бензокаїн – 218 мг; Допоміжні речовини: Водню пероксиду розчин 30% - 0,82 мг, сорбітол - 1602,30 мг, гієтеллоза - 30,52 мг, метилпарагідроксибензоат - 21,80 мг, пропілпарагідроксибензоат - 2,726 мг, бутілпарагідротіно6 мг, пропіленгліколь – 654,00 мг, макрогол 4000 – 436,00 мг, лимона олія – 3,27 мг, етанол 96% – 196,20 мг, вода очищена до 10 мл. По 10 мл препарату в пакетику із багатошарової фольги. 10 або 20 пакетиків разом із інструкцією із застосування у картонній пачці.Опис лікарської формиСуспензія білого або майже білого кольору із характерним запахом лимона. При зберіганні на поверхні може виділятись шар прозорої рідини. При енергійному збовтуванні гомогенність суспензії відновлюється.Фармакотерапевтична групаАнтацидний засіб + місцевоанестезуючий засіб.ФармакокінетикаАлгелдрат Всмоктування – резорбуються невеликі кількості препарату, які практично не змінюють концентрацію солей алюмінію у крові. Розподіл – ні. Метаболізм – ні. Виведення – виводиться через кишечник. Магнію гідроксид Всмоктування - іони магнію резорбуються близько 10% прийнятої дози і не змінюють концентрації іонів магнію в крові. Розподіл – зазвичай локально. Метаболізм – ні. Виведення – виводиться через кишечник. Бензокаїн Бензокаїн всмоктується у мінімальних кількостях і практично не чинить системних ефектів на організм. Його місцевий знеболюючий ефект настає через 1-2 хвилини після прийому суспензії.ФармакодинамікаАлмагель А лікарський засіб, що є збалансованою комбінацією алгелдрату (алюмінію гідроксиду), магнію гідроксиду і бензокаїну. Він нейтралізує вільну соляну кислоту в шлунку, знижує активність пепсину, що призводить до зменшення активності шлункового соку, що перетравлює. Чинить обволікаючу, адсорбуючу дію. Захищає слизову оболонку шлунка за рахунок стимулювання синтезу простагландинів (цитопротективна дія). Це оберігає слизову оболонку - від запальних та ерозивно-геморагічних уражень в результаті застосування подразнюючих та ульцерогенних агентів, таких як етиловий спирт та нестероїдні протизапальні препарати (наприклад, індометацин, диклофенак, аспірин, ацетилсаліцилова кислота, кортикостероїд).Терапевтичний ефект після прийому препарату настає через 3-5 хвилин. Тривалість дії залежить від швидкості випорожнення шлунка. При прийомі натще дію триває до 60 хвилин. При прийомі через годину після їди антацидна дія може тривати до 3 годин. Не викликає вторинної гіперсекреції шлункового соку. Бензокаїн має місцеву знеболювальну дію за наявності вираженого больового синдрому.Показання до застосуванняГострий гастрит; хронічний гастрит із підвищеною та нормальною секреторною функцією шлунка (у фазі загострення); гострий дуоденіт, ентерит, коліт; виразкова хвороба шлунка та дванадцятипалої кишки (у фазі загострення); грижа стравохідного отвору діафрагми, гастроезофагеальний рефлюкс, рефлюкс-езофагіт, дуоденогастральний рефлюкс; симптоматичні виразки шлунково-кишкового тракту різного генезу; ерозії слизової оболонки верхніх відділів шлунково-кишкового тракту; гострий панкреатит; загострення хронічного панкреатиту; печія та болі в епігастрії після похибок у харчуванні, надмірного вживання етанолу, нікотину, кави, прийому лікарських засобів, що подразнюють слизову оболонку шлунка.Протипоказання до застосуванняГіперчутливість до будь-якого компонента, що входить до складу препарату. Тяжка форма ниркової недостатності (через небезпеку розвитку гіпермагніємії та алюмінієвої інтоксикації). Не призначають дітям, оскільки є небезпека розвитку метгемоглобінемії. Вагітність та період лактації.Вагітність та лактаціяАлмагель А не призначають під час вагітності та годування груддю, тому що він містить бензокаїн.Побічна діяАлмагель А може спричинити запор, який проходить після зменшення дози. У поодиноких випадках спостерігаються нудота, блювання, спазм шлунка, зміна смакових відчуттів, алергічні реакції та гіпермагніємія. При тривалому прийомі препарату у пацієнтів з нирковою недостатністю та перебувають на діалізі можливі зміни настрою та розумової активності. При тривалому прийомі високих доз препарату поряд з дефіцитом фосфору в їжі можливе виникнення остеомаляції.Взаємодія з лікарськими засобамиМоже абсорбувати деякі лікарські засоби, зменшуючи таким чином їх всмоктування, тому при одночасному прийомі інших лікарських засобів їх необхідно приймати за 1-2 години до або після прийому Алмагелю А. Алмагель А зменшує кислотність шлункового соку і це може вплинути на дію великої кількості лікарських засобів при одночасному прийомі. Алмагель А зменшує всмоктування резерпіну, блокаторів гістамінових Н2-рецепторів, серцевих глікозидів, солей заліза, препаратів літію, хінідину, мексилетину, фенотіазинових препаратів, антибіотиків тетрациклінового ряду, ципрофлоксацину, ізоніазиду та кет. При одночасному прийомі кишковорозчинних таблеток підвищений pH шлункового соку може призвести до прискореного порушення їх оболонки та спричинити подразнення шлунка та дванадцятипалої кишки. Алмагель А не слід приймати одночасно з сульфаніламідами, зважаючи на наявність бензокаїну у його складі! Алмагель А може вплинути на результати деяких лабораторних та функціональних досліджень та тестів: він знижує рівень шлункової секреції щодо її кислотності; порушує тест візуалізації дивертикулів та сцинтиграфії кісток за допомогою технеції (ТС99); помірно та на короткий час підвищує сироватковий рівень гастрину, підвищує сироватковий рівень фосфору, pH сироватки та сечі.Спосіб застосування та дозиДорослим По 5-10 мл (1-2 мірні ложки або 1 пакетик) 3-4 рази на день за 10-15 хвилин до їди. Максимальна тривалість лікування становить 7 днів, потім переходять на лікування препаратом Алмагель. Не рекомендується приймати рідини протягом 15 хвилин після прийому препарату. Перед застосуванням суспензію необхідно ретельно гомогенізувати, струшуючи флакон або розминаючи та струшуючи пакетик.ПередозуванняПри одноразовому перевищенні дози немає інших ознак передозування крім запору, метеоризму, відчуття металевого смаку. При тривалому прийомі високих доз можливі нефрокальциноз, поява важких запорів, легка сонливість, гіпермагніємія. Можуть спостерігатися також ознаки метаболічного алкалозу: зміна настрою чи розумової активності, оніміння чи біль у м'язах, дратівливість та швидка стомлюваність, уповільнення дихання, неприємні смакові відчуття. Необхідно відразу вжити заходів щодо швидкого виведення медикаменту з організму за допомогою промивання шлунка (індукція блювання, прийом активованого вугілля).Запобіжні заходи та особливі вказівкиНе рекомендується застосування препарату у хворих із тяжким звичним запором; при симптомах гострого апендициту; за наявності метаболічного алкалозу, цирозу печінки, тяжкої серцевої недостатності; за наявності виразкового коліту, дивертикульозу, колостомії або ілеостомії (підвищений ризик розвитку порушень водно-електролітного балансу); хронічної діареї; гострий геморой; порушення функції нирок (кліренс креатиніну Під час лікування Алмагелем А необхідно уникати вживання алкоголю та кислот (лимонного соку, оцту тощо) через можливість ослаблення місцевої знеболювальної дії бензокаїну. При прийомі препарату виникає оніміння та анестезія слизової оболонки ротової порожнини та язика. Це явище минуще і вимагає терапевтичних заходів. Препарат не містить цукру, що дозволяє приймати його хворим на діабет. Препарат містить сорбітол, який протипоказаний при вродженій непереносимості фруктози. Вплив на здатність до керування автотранспортом та управління механізмами Алмагель А не впливає на здатність керувати автотранспортом та роботу з механізмами. При прийомі в рекомендованій добовій дозі етиловий спирт, що міститься в препараті, не впливає на здатність керувати автомобілем і роботу з механізмами.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаСуспензія - 5 мл: Алюмінію гідроксид гель - 2,18 г (у перерахунку на Al2О3 - 218 мг); Магнію гідроксид паста – 350 мг (у перерахунку на MgO – 75 мг); Бензокаїн – 109 мг; Допоміжні речовини: Водню пероксиду розчин 30% - 0,41 мг, сорбітол - 801,15 мг, гієтеллоза - 15,26 мг, метилпарагідроксибензоат - 10,90 мг, пронілпарагідроксибензоат - 1,363 мг, бутілпарагідротіна3 мг, пропілегліколь – 327,00 мг, макрогол 4000 – 218,00 мг, лимона олія – 1,635 мг, етанол –96% 98,10 мг, вода очищена до 5 мл. По 170 мл препарату у флаконі з темного скла або з поліетилентерефталату з пластмасовим ковпачком, що нагвинчується. Кожен флакон разом з інструкцією із застосування та мірною ложкою на 5 мл у картонній пачці.Опис лікарської формиСуспензія білого або майже білого кольору із характерним запахом лимона. При зберіганні на поверхні може виділятись шар прозорої рідини. При енергійному збовтуванні гомогенність суспензії відновлюється.Фармакотерапевтична групаАнтацидний засіб + місцевоанестезуючий засіб.ФармакокінетикаАлгелдрат Всмоктування – резорбуються невеликі кількості препарату, які практично не змінюють концентрацію солей алюмінію у крові. Розподіл – ні. Метаболізм – ні. Виведення – виводиться через кишечник. Магнію гідроксид Всмоктування - іони магнію резорбуються близько 10% прийнятої дози і не змінюють концентрації іонів магнію в крові. Розподіл – зазвичай локально. Метаболізм – ні. Виведення – виводиться через кишечник. Бензокаїн Бензокаїн всмоктується у мінімальних кількостях і практично не чинить системних ефектів на організм. Його місцевий знеболюючий ефект настає через 1-2 хвилини після прийому суспензії.ФармакодинамікаАлмагель А лікарський засіб, що є збалансованою комбінацією алгелдрату (алюмінію гідроксиду), магнію гідроксиду і бензокаїну. Він нейтралізує вільну соляну кислоту в шлунку, знижує активність пепсину, що призводить до зменшення активності шлункового соку, що перетравлює. Чинить обволікаючу, адсорбуючу дію. Захищає слизову оболонку шлунка за рахунок стимулювання синтезу простагландинів (цитопротективна дія). Це оберігає слизову оболонку - від запальних та ерозивно-геморагічних уражень в результаті застосування подразнюючих та ульцерогенних агентів, таких як етиловий спирт та нестероїдні протизапальні препарати (наприклад, індометацин, диклофенак, аспірин, ацетилсаліцилова кислота, кортикостероїд).Терапевтичний ефект після прийому препарату настає через 3-5 хвилин. Тривалість дії залежить від швидкості випорожнення шлунка. При прийомі натще дію триває до 60 хвилин. При прийомі через годину після їди антацидна дія може тривати до 3 годин. Не викликає вторинної гіперсекреції шлункового соку. Бензокаїн має місцеву знеболювальну дію за наявності вираженого больового синдрому.Показання до застосуванняГострий гастрит; хронічний гастрит із підвищеною та нормальною секреторною функцією шлунка (у фазі загострення); гострий дуоденіт, ентерит, коліт; виразкова хвороба шлунка та дванадцятипалої кишки (у фазі загострення); грижа стравохідного отвору діафрагми, гастроезофагеальний рефлюкс, рефлюкс-езофагіт, дуоденогастральний рефлюкс; симптоматичні виразки шлунково-кишкового тракту різного генезу; ерозії слизової оболонки верхніх відділів шлунково-кишкового тракту; гострий панкреатит; загострення хронічного панкреатиту; печія та болі в епігастрії після похибок у харчуванні, надмірного вживання етанолу, нікотину, кави, прийому лікарських засобів, що подразнюють слизову оболонку шлунка.Протипоказання до застосуванняГіперчутливість до будь-якого компонента, що входить до складу препарату. Тяжка форма ниркової недостатності (через небезпеку розвитку гіпермагніємії та алюмінієвої інтоксикації). Не призначають дітям, оскільки є небезпека розвитку метгемоглобінемії. Вагітність та період лактації.Вагітність та лактаціяАлмагель А не призначають під час вагітності та годування груддю, тому що він містить бензокаїн.Побічна діяАлмагель А може спричинити запор, який проходить після зменшення дози. У поодиноких випадках спостерігаються нудота, блювання, спазм шлунка, зміна смакових відчуттів, алергічні реакції та гіпермагніємія. При тривалому прийомі препарату у пацієнтів з нирковою недостатністю та перебувають на діалізі можливі зміни настрою та розумової активності. При тривалому прийомі високих доз препарату поряд з дефіцитом фосфору в їжі можливе виникнення остеомаляції.Взаємодія з лікарськими засобамиМоже абсорбувати деякі лікарські засоби, зменшуючи таким чином їх всмоктування, тому при одночасному прийомі інших лікарських засобів їх необхідно приймати за 1-2 години до або після прийому Алмагелю А. Алмагель А зменшує кислотність шлункового соку і це може вплинути на дію великої кількості лікарських засобів при одночасному прийомі. Алмагель А зменшує всмоктування резерпіну, блокаторів гістамінових Н2-рецепторів, серцевих глікозидів, солей заліза, препаратів літію, хінідину, мексилетину, фенотіазинових препаратів, антибіотиків тетрациклінового ряду, ципрофлоксацину, ізоніазиду та кет. При одночасному прийомі кишковорозчинних таблеток підвищений pH шлункового соку може призвести до прискореного порушення їх оболонки та спричинити подразнення шлунка та дванадцятипалої кишки. Алмагель А не слід приймати одночасно з сульфаніламідами, зважаючи на наявність бензокаїну у його складі! Алмагель А може вплинути на результати деяких лабораторних та функціональних досліджень та тестів: він знижує рівень шлункової секреції щодо її кислотності; порушує тест візуалізації дивертикулів та сцинтиграфії кісток за допомогою технеції (ТС99); помірно та на короткий час підвищує сироватковий рівень гастрину, підвищує сироватковий рівень фосфору, pH сироватки та сечі.Спосіб застосування та дозиДорослим По 5-10 мл (1-2 мірні ложки або 1 пакетик) 3-4 рази на день за 10-15 хвилин до їди. Максимальна тривалість лікування становить 7 днів, потім переходять на лікування препаратом Алмагель. Не рекомендується приймати рідини протягом 15 хвилин після прийому препарату. Перед застосуванням суспензію необхідно ретельно гомогенізувати, струшуючи флакон або розминаючи та струшуючи пакетик.ПередозуванняПри одноразовому перевищенні дози немає інших ознак передозування крім запору, метеоризму, відчуття металевого смаку. При тривалому прийомі високих доз можливі нефрокальциноз, поява важких запорів, легка сонливість, гіпермагніємія. Можуть спостерігатися також ознаки метаболічного алкалозу: зміна настрою чи розумової активності, оніміння чи біль у м'язах, дратівливість та швидка стомлюваність, уповільнення дихання, неприємні смакові відчуття. Необхідно відразу вжити заходів щодо швидкого виведення медикаменту з організму за допомогою промивання шлунка (індукція блювання, прийом активованого вугілля).Запобіжні заходи та особливі вказівкиНе рекомендується застосування препарату у хворих із тяжким звичним запором; при симптомах гострого апендициту; за наявності метаболічного алкалозу, цирозу печінки, тяжкої серцевої недостатності; за наявності виразкового коліту, дивертикульозу, колостомії або ілеостомії (підвищений ризик розвитку порушень водно-електролітного балансу); хронічної діареї; гострий геморой; порушення функції нирок (кліренс креатиніну Під час лікування Алмагелем А необхідно уникати вживання алкоголю та кислот (лимонного соку, оцту тощо) через можливість ослаблення місцевої знеболювальної дії бензокаїну. При прийомі препарату виникає оніміння та анестезія слизової оболонки ротової порожнини та язика. Це явище минуще і вимагає терапевтичних заходів. Препарат не містить цукру, що дозволяє приймати його хворим на діабет. Препарат містить сорбітол, який протипоказаний при вродженій непереносимості фруктози. Вплив на здатність до керування автотранспортом та управління механізмами Алмагель А не впливає на здатність керувати автотранспортом та роботу з механізмами. При прийомі в рекомендованій добовій дозі етиловий спирт, що міститься в препараті, не впливає на здатність керувати автомобілем і роботу з механізмами.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаСуспензія - 1 пак. Активні речовини: Алгелдрат (Алюмінію гідроксид гель – у перерахунку на алюмінію гідроксид) – 340 мг; Магнію гідроксид (Магнію гідроксид паста - у перерахунку на магнію гідроксид) - 395 мг; Симетикон (емульсія симетикону – у перерахунку на диметикон) – 36 мг; Вміст допоміжних речовин у 5 мл суспензії: водню пероксиду розчин 30% 0,495 мг, сорбітол 474,60 мг, натрію сахаринат 1,13 мг, гієтеллоза 5,65 мг, лимонної кислоти моногідрат 5,65 мг, етілзопара 3,40 мг, пропіленгліколь 113,00 мг, макрогол 4000 452,00 мг, апельсиновий ароматизатор 2,26 мг, етанол 96 % 113,00 мг, вода очищена до 5 мл. По 10 мл препарату в пакетику із багатошарової фольги. 10 або 20 пакетиків разом із інструкцією із застосування у картонній пачці.Опис лікарської формиБіла або майже біла суспензія, із запахом апельсина.Фармакотерапевтична групаАнтацидний засіб + вторгнень засіб.ФармакокінетикаСиметикон внаслідок фізіологічної та хімічної інертності не всмоктується до органів та тканин і після проходження через шлунково-кишковий тракт (ЖКТ) виводиться у незмінному вигляді. Абсорбція іонів алюмінію та магнію в кишечнику – низька. При нормальній функції нирок концентрація алюмінію та магнію в крові не змінюється. У хворих з хронічною нирковою недостатністю рівень алюмінію та магнію в крові може підвищитися до токсичних значень внаслідок порушення їх виведення.ФармакодинамікаКомбінований засіб, дія якого обумовлена компонентами, що входять до його складу. Має антацидну, адсорбуючу, обволікаючу, вітрогонну дію. Алгелдрат (алюмінію гідроксид) та магнію гідроксид нейтралізують вільну соляну кислоту в шлунку, знижують кислотність шлункового соку, пов'язують жовчні кислоти. Послаблююча дія магнію гідроксиду врівноважує здатність алгелдрату уповільнювати моторику кишок. Симетикон ускладнює утворення газових бульбашок та сприяє їхньому руйнуванню. Гази, що вивільняються при цьому, поглинаються стінками кишечника і виводяться з організму завдяки перистальтиці.Показання до застосуванняГострий гастрит; хронічний гастрит із підвищеною та нормальною секреторною функцією шлунка (у фазі загострення); гострий дуоденіт, дуоденогастральний рефлюкс; виразкова хвороба шлунка та дванадцятипалої кишки (у фазі загострення); симптоматичні виразки шлунково-кишкового тракту різного генезу; ерозії слизової оболонки верхніх відділів шлунково-кишкового тракту; гастроезофагеальний рефлюкс, рефлюкс-езофагіт; гострий панкреатит; загострення хронічного панкреатиту; гастралгія, печія (після надмірного вживання етанолу, нікотину, кави, прийому лікарських засобів; некоректної дієти, що негативно позначається на функціонуванні ШКТ); метеоризм; бродильна або гнильна диспепсія.Протипоказання до застосуванняГіперчутливість, хронічна ниркова недостатність, вагітність, хвороба Альцгеймера, гіпофосфатемія, дитячий вік до 10 років, уроджена непереносимість фруктози. З обережністю: Період лактації, захворювання печінки, алкоголізм, черепно-мозкова травма, захворювання головного мозку, епілепсія, дитячий та підлітковий вік з 10 до 18 років.Вагітність та лактаціяЧерез відсутність даних контрольованих клінічних випробувань жінкам, що годують груддю, Алмагель® Нео слід приймати тільки після консультації з лікарем.Побічна діяАлергічні реакції, нудота, блювання, зміна смакових відчуттів, запор, діарея. При тривалому прийомі у високих дозах – гіпофосфатемія, гіпокальціємія, гіперкальціурія, остеомаляція, остеопороз, гіпермагніємія, гіпералюмініємія, енцефалопатія, нефрокальциноз, порушення функції нирок. У хворих із супутньою нирковою недостатністю – спрага, зниження артеріального тиску, гіпорефлексія.Взаємодія з лікарськими засобамиАлмагель® Нео знижує та уповільнює абсорбцію дигоксину, індометацину, саліцилатів, хлорпромазину, фенітоїну, блокаторів Н2-гістамінових рецепторів, бета-адреноблокаторів, дифлунісала, кетоконазолу та ітраконазоліну, антикоагулянтів, барбітуратів, фексофенадину, дипіридамолу, залцитабіну, хенодезоксихолевої та ефсодезоксихолевої кислот, пеніциламіну та лансопразолу. М-холіноблокатори, уповільнюючи спорожнення шлунка, посилюють та подовжують дію препарату.Спосіб застосування та дозиДорослі Всередину, але 2 мірні ложки або по 1 пакетику суспензії з апельсиновим смаком 4 рази на добу через I годину після їди і ввечері перед сном. При необхідності разову дозу можна збільшити до 3 мірних ложок 4 десь у день. Максимальна добова доза не повинна перевищувати 12 мірних ложок. Діти старше 10 років Дозування визначає лікар-зазвичай 1/2 дози для дорослих. Курс лікування – не більше 4 тижнів. Перед застосуванням суспензію необхідно ретельно гомогенізувати, струшуючи флакон або розминаючи та струшуючи пакетик. Бажано приймати Алмагель Нео не розбавляючи водою і не запиваючи. Рекомендується прийом рідини протягом півгодини після прийому препарату.ПередозуванняСимптоми. Тривале застосування високих доз може призвести до розвитку гіпермагніємії, що характеризується швидкою стомлюваністю, почервонінням обличчя, виснаженням, м'язовою слабкістю та неадекватністю поведінки. Можуть спостерігатися також ознаки метаболічного алкалозу: зміна настрою, порушення розумової діяльності, оніміння або біль у м'язах, нервозність та швидка стомлюваність, уповільнення дихання, неприємні смакові відчуття. Невідкладні заходи. Необхідно відразу вжити заходів щодо швидкого виведення препарату – промивання шлунка, стимуляція блювання, прийом активованого вугілля.Запобіжні заходи та особливі вказівкиІнтервал між прийомом Алмагелю Нео та інших лікарських засобів повинен становити 1-2 години. При тривалому прийомі слід забезпечити достатнє надходження фосфору з їжею. Через відсутність даних контрольованих клінічних випробувань жінкам, що годують груддю, Алмагель® Нео слід приймати тільки після консультації з лікарем. Одна мірна ложка (5 мл) препарату містить 0,113 г етилового спирту. Один пакетик (10 мл) препарату містить 0226 г етилового спирту. Внаслідок цього можливе виникнення ускладнень у пацієнтів із захворюваннями печінки та мозку, у хворих на алкоголізм та епілепсію, у вагітних та дітей до 18 років. Добова доза препарату (8 мірних ложок або 4 пакетики) містить 0,904 г етилового спирту, максимальна добова доза суспензії (12 мірних ложок або 6 пакетиків) містить 1,356 г етилового спирту. Одна мірна ложка (5 мл) препарату Алмагель® Нео містить 0,475 г сорбітолу. Один пакетик (10 мл) суспензії містить 0,950 г сорбітолу. Сорбітол протипоказаний при вродженій непереносимості фруктози і може спричинити подразнення шлунка та діарею. Вплив на здатність до керування автотранспортом та управління механізмами Алмагель® Нео не впливає на здатність керувати автотранспортом та роботи з механізмами, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови відпустки з аптекБез рецептаВідео на цю тему
Фасування: N20 Форма выпуска: суспензия д/приема внутрь Упаковка: пак. Производитель: Тева Завод-производитель: Балканфарма-Троян АД(Болгария) Действующее вещество: Алгелдрат + Магния гидроксид + Симетикон. .
Склад, форма випуску та упаковкаСуспензія - 5 мл: Активні речовини: Алгелдрат (Алюмінію гідроксид гель – у перерахунку на алюмінію гідроксид) – 340 мг; Магнію гідроксид (Магнію гідроксид паста - у перерахунку на магнію гідроксид) - 395 мг; Симетикон (емульсія симетикону – у перерахунку на диметикон) – 36 мг; Вміст допоміжних речовин у 5 мл суспензії: водню пероксиду розчин 30% 0,495 мг, сорбітол 474,60 мг, натрію сахаринат 1,13 мг, гієтеллоза 5,65 мг, лимонної кислоти моногідрат 5,65 мг, етілзопара 3,40 мг, пропіленгліколь 113,00 мг, макрогол 4000 452,00 мг, апельсиновий ароматизатор 2,26 мг, етанол 96 % 113,00 мг, вода очищена до 5 мл. По 170 мл або по 200 мл препарату у флаконі з темного скла або з поліетилентерефгалату з пластмасовим ковпачком, що нагвинчується. Кожен флакон разом з інструкцією із застосування та мірною ложкою на 5 мл у картонній пачці.Опис лікарської формиБіла або майже біла суспензія, із запахом апельсина.Фармакотерапевтична групаАнтацидний засіб + вторгнень засіб.ФармакокінетикаСиметикон внаслідок фізіологічної та хімічної інертності не всмоктується до органів та тканин і після проходження через шлунково-кишковий тракт (ЖКТ) виводиться у незмінному вигляді. Абсорбція іонів алюмінію та магнію в кишечнику – низька. При нормальній функції нирок концентрація алюмінію та магнію в крові не змінюється. У хворих з хронічною нирковою недостатністю рівень алюмінію та магнію в крові може підвищитися до токсичних значень внаслідок порушення їх виведення.ФармакодинамікаКомбінований засіб, дія якого обумовлена компонентами, що входять до його складу. Має антацидну, адсорбуючу, обволікаючу, вітрогонну дію. Алгелдрат (алюмінію гідроксид) та магнію гідроксид нейтралізують вільну соляну кислоту в шлунку, знижують кислотність шлункового соку, пов'язують жовчні кислоти. Послаблююча дія магнію гідроксиду врівноважує здатність алгелдрату уповільнювати моторику кишок. Симетикон ускладнює утворення газових бульбашок та сприяє їхньому руйнуванню. Гази, що вивільняються при цьому, поглинаються стінками кишечника і виводяться з організму завдяки перистальтиці.Показання до застосуванняГострий гастрит; хронічний гастрит із підвищеною та нормальною секреторною функцією шлунка (у фазі загострення); гострий дуоденіт, дуоденогастральний рефлюкс; виразкова хвороба шлунка та дванадцятипалої кишки (у фазі загострення); симптоматичні виразки шлунково-кишкового тракту різного генезу; ерозії слизової оболонки верхніх відділів шлунково-кишкового тракту; гастроезофагеальний рефлюкс, рефлюкс-езофагіт; гострий панкреатит; загострення хронічного панкреатиту; гастралгія, печія (після надмірного вживання етанолу, нікотину, кави, прийому лікарських засобів; некоректної дієти, що негативно позначається на функціонуванні ШКТ); метеоризм; бродильна або гнильна диспепсія.Протипоказання до застосуванняГіперчутливість, хронічна ниркова недостатність, вагітність, хвороба Альцгеймера, гіпофосфатемія, дитячий вік до 10 років, уроджена непереносимість фруктози. З обережністю: Період лактації, захворювання печінки, алкоголізм, черепно-мозкова травма, захворювання головного мозку, епілепсія, дитячий та підлітковий вік з 10 до 18 років.Вагітність та лактаціяЧерез відсутність даних контрольованих клінічних випробувань жінкам, що годують груддю, Алмагель® Нео слід приймати тільки після консультації з лікарем.Побічна діяАлергічні реакції, нудота, блювання, зміна смакових відчуттів, запор, діарея. При тривалому прийомі у високих дозах – гіпофосфатемія, гіпокальціємія, гіперкальціурія, остеомаляція, остеопороз, гіпермагніємія, гіпералюмініємія, енцефалопатія, нефрокальциноз, порушення функції нирок. У хворих із супутньою нирковою недостатністю – спрага, зниження артеріального тиску, гіпорефлексія.Взаємодія з лікарськими засобамиАлмагель® Нео знижує та уповільнює абсорбцію дигоксину, індометацину, саліцилатів, хлорпромазину, фенітоїну, блокаторів Н2-гістамінових рецепторів, бета-адреноблокаторів, дифлунісала, кетоконазолу та ітраконазоліну, антикоагулянтів, барбітуратів, фексофенадину, дипіридамолу, залцитабіну, хенодезоксихолевої та ефсодезоксихолевої кислот, пеніциламіну та лансопразолу. М-холіноблокатори, уповільнюючи спорожнення шлунка, посилюють та подовжують дію препарату.Спосіб застосування та дозиДорослі Всередину, але 2 мірні ложки або по 1 пакетику суспензії з апельсиновим смаком 4 рази на добу через I годину після їди і ввечері перед сном. При необхідності разову дозу можна збільшити до 3 мірних ложок 4 десь у день. Максимальна добова доза не повинна перевищувати 12 мірних ложок. Діти старше 10 років Дозування визначає лікар-зазвичай 1/2 дози для дорослих. Курс лікування – не більше 4 тижнів. Перед застосуванням суспензію необхідно ретельно гомогенізувати, струшуючи флакон або розминаючи та струшуючи пакетик. Бажано приймати Алмагель Нео не розбавляючи водою і не запиваючи. Рекомендується прийом рідини протягом півгодини після прийому препарату.ПередозуванняСимптоми. Тривале застосування високих доз може призвести до розвитку гіпермагніємії, що характеризується швидкою стомлюваністю, почервонінням обличчя, виснаженням, м'язовою слабкістю та неадекватністю поведінки. Можуть спостерігатися також ознаки метаболічного алкалозу: зміна настрою, порушення розумової діяльності, оніміння або біль у м'язах, нервозність та швидка стомлюваність, уповільнення дихання, неприємні смакові відчуття. Невідкладні заходи. Необхідно відразу вжити заходів щодо швидкого виведення препарату – промивання шлунка, стимуляція блювання, прийом активованого вугілля.Запобіжні заходи та особливі вказівкиІнтервал між прийомом Алмагелю Нео та інших лікарських засобів повинен становити 1-2 години. При тривалому прийомі слід забезпечити достатнє надходження фосфору з їжею. Через відсутність даних контрольованих клінічних випробувань жінкам, що годують груддю, Алмагель® Нео слід приймати тільки після консультації з лікарем. Одна мірна ложка (5 мл) препарату містить 0,113 г етилового спирту. Один пакетик (10 мл) препарату містить 0226 г етилового спирту. Внаслідок цього можливе виникнення ускладнень у пацієнтів із захворюваннями печінки та мозку, у хворих на алкоголізм та епілепсію, у вагітних та дітей до 18 років. Добова доза препарату (8 мірних ложок або 4 пакетики) містить 0,904 г етилового спирту, максимальна добова доза суспензії (12 мірних ложок або 6 пакетиків) містить 1,356 г етилового спирту. Одна мірна ложка (5 мл) препарату Алмагель® Нео містить 0,475 г сорбітолу. Один пакетик (10 мл) суспензії містить 0,950 г сорбітолу. Сорбітол протипоказаний при вродженій непереносимості фруктози і може спричинити подразнення шлунка та діарею. Вплив на здатність до керування автотранспортом та управління механізмами Алмагель® Нео не впливає на здатність керувати автотранспортом та роботи з механізмами, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови відпустки з аптекБез рецептаВідео на цю тему
266,00 грн
239,00 грн
Склад, форма випуску та упаковкаКальція карбонат, носій МКЦ, магнію карбонат, агенти антиспостереження аеросил (діоксид кремнію) та магнію стеарат, желатин, ароматизатор м'ята, підсолоджувач аспартам. Містить джерело фенілаланіну.Опис лікарської формиГелеподібна суспензія із м'ятним смаком.Характеристика"Алмаксон" забезпечує швидку та тривалу нейтралізацію надлишкової соляної кислоти шлункового соку. Чинить захисну дію на слизову оболонку шлунка. Швидко та ефективно позбавляє печії (3-5 хвилин).Властивості компонентівАльгінат натрію-високомолекулярний полісахарид, відноситься до класу розчинних харчових волокон (поряд з пектином та агар-агаром). Альгінат натрію виробляють із бурих та червоних водоростей. Солі альгінової кислоти є хорошими ентеросорбентами, які пов'язують та виводять із організму важкі метали. Реагує з соляною кислотою, що міститься в шлунку, утворює гелевий бар'єр, що перешкоджає закидання кислоти в стравохід і зменшує подразнення слизової оболонки. Є додатковим джерелом харчових волокон. Карбонат кальцію-сіль вугільної кислоти. Має здатність нейтралізувати соляну кислоту, послаблюючи її ушкоджуючу дію, тим самим зменшуючи неприємні відчуття у шлунку. Натрію гідрокарбонат-натрієва сіль вугільної кислоти. Має швидкий протикислотний ефект, сприяє захисту органів травлення. Кальцій-мікроелемент, що входить до складу кісткової тканини.РекомендуєтьсяРекомендується як біологічно активна добавка до їжі - додаткового джерела кальцію, що містить магній.Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність та корилення груддю, сечокам'яна хвороба, фенілкетонурія.Спосіб застосування та дозиПеред вживанням суспензію в саші-пакеті рекомендується розім'яти в руках. Дорослим по 10 мл (1 пакетик) 3 десь у день їжі. Тривалість прийому 4-6 тижнів. За потреби прийом можна повторити. Можливі повторні прийоми протягом року.Запобіжні заходи та особливі вказівкиПеред застосуванням рекомендується проконсультуватися з лікарем. Не є ліками.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаКальція карбонат, носій МКЦ, магнію карбонат, агенти антиспостереження аеросил (діоксид кремнію) та магнію стеарат, желатин, ароматизатор м'ята, підсолоджувач аспартам. Містить джерело фенілаланіну.Опис лікарської формиГелеподібна суспензія із м'ятним смаком.Характеристика"Алмаксон" забезпечує швидку та тривалу нейтралізацію надлишкової соляної кислоти шлункового соку. Чинить захисну дію на слизову оболонку шлунка. Швидко та ефективно позбавляє печії (3-5 хвилин).Властивості компонентівАльгінат натрію-високомолекулярний полісахарид, відноситься до класу розчинних харчових волокон (поряд з пектином та агар-агаром). Альгінат натрію виробляють із бурих та червоних водоростей. Солі альгінової кислоти є хорошими ентеросорбентами, які пов'язують та виводять із організму важкі метали. Реагує з соляною кислотою, що міститься в шлунку, утворює гелевий бар'єр, що перешкоджає закидання кислоти в стравохід і зменшує подразнення слизової оболонки. Є додатковим джерелом харчових волокон. Карбонат кальцію-сіль вугільної кислоти. Має здатність нейтралізувати соляну кислоту, послаблюючи її ушкоджуючу дію, тим самим зменшуючи неприємні відчуття у шлунку. Натрію гідрокарбонат-натрієва сіль вугільної кислоти. Має швидкий протикислотний ефект, сприяє захисту органів травлення. Кальцій-мікроелемент, що входить до складу кісткової тканини.РекомендуєтьсяРекомендується як біологічно активна добавка до їжі - додаткового джерела кальцію, що містить магній.Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність та корилення груддю, сечокам'яна хвороба, фенілкетонурія.Спосіб застосування та дозиПеред вживанням суспензію в саші-пакеті рекомендується розім'яти в руках. Дорослим по 10 мл (1 пакетик) 3 десь у день їжі. Тривалість прийому 4-6 тижнів. За потреби прийом можна повторити. Можливі повторні прийоми протягом року.Запобіжні заходи та особливі вказівкиПеред застосуванням рекомендується проконсультуватися з лікарем. Не є ліками.Умови відпустки з аптекБез рецептаВідео на цю тему
244,00 грн
231,00 грн
Склад, форма випуску та упаковкаКальцію карбонат, магнію карбонат, мікрокристалічна целюлоза, аеросил (діоксид кремнію), магнію стеарат, желатин, ароматизатор (апельсин), аспартам.ХарактеристикаТаблетка Алмаксон містить кальцію карбонат та магнію карбонат нейтралізують соляну кислоту і тим самим зменшують неприємні відчуття у шлунку.РекомендуєтьсяРекомендується як біологічно активна добавка до їжі - додаткового джерела кальцію, що містить магній, що надає захисну дію на слизову оболонку шлунка.Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність та корилення груддю, сечокам'яна хвороба, фенілкетонурія.Спосіб застосування та дозиДорослим з появою симптомів 1-2 таб. слід розжувати (або тримати в роті до повного розчинення) по 1 таблетці 2 рази на день або по 2 таблетці 1 раз на день. Тривалість прийому: 1 місяць.Запобіжні заходи та особливі вказівкиПеред застосуванням рекомендується проконсультуватися з лікарем. Не є ліками.Умови відпустки з аптекБез рецептаВідео на цю тему
245,00 грн
232,00 грн
Склад, форма випуску та упаковкаКальція карбонат, носій МКЦ, магнію карбонат, агенти антистежують аеросил (діоксид кремнію) та магнію стеарат, желатин, ароматизатор апельсин, підсолоджувач аспартам. Містить джерело фенілаланіну. Жувальні таблетки 1,0 г з м'ятним чи апельсиновим смаком.Характеристика"Алмаксон" забезпечує швидку та тривалу нейтралізацію надлишкової соляної кислоти шлункового соку. Чинить захисну дію на слизову оболонку шлунка. Швидко та ефективно позбавляє печії (3-5 хвилин).РекомендуєтьсяРекомендується як біологічно активна добавка до їжі - додаткового джерела кальцію, що містить магній.Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність та корилення груддю, сечокам'яна хвороба, фенілкетонурія.Спосіб застосування та дозиДорослим з появою симптомів 1-2 таб. слід розжувати (або тримати в роті до повного розчинення) по 1 таблетці 2 рази на день або по 2 таблетці 1 раз на день. Тривалість прийому: 1 місяць.Запобіжні заходи та особливі вказівкиПеред застосуванням рекомендується проконсультуватися з лікарем. Не є ліками.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаТаблетки покриті плівковою оболонкою з маркуванням "M" на одній із сторін - 1 таб. Активні речовини: монтелукаст натрію – 10.4 мг (відповідає вмісту монтелукасту – 10 мг); Допоміжні речовини: ядро - мікрокристалічна целюлоза - 89.3 мг, гіпоролоза - 4 мг, кроскармелоза натрію - 6 мг, лактози моногідрат - 89.3 мг, магнію стеарат - 1 мг; плівкова оболонка - опадрай II бежевий 31F27012 (лактози моногідрат - 1.44 мг, гіпромелоза 15cP - 1.12 мг, титану діоксид - 1.011 мг, макрогол 4000 - 0.4 мг, барвник заліза оксид жовтий 0 0 0 0 0 0 0 0 0 - 0 0 0 0 0 0 0 0 0 мг. По 10 або 14 таблеток в Ал/Ал блістері. По 3 блістери (по 10 таблеток), по 2 або 7 блістерів (по 14 таблеток) у картонній пачці разом з інструкцією з медичного застосування.Опис лікарської формиТаблетки, покриті плівковою оболонкою бежевого кольору, квадратні, із закругленими кутами, двоопуклі, з маркуванням "M" на одній із сторін.Фармакотерапевтична групаАнтагоніст лейкотрієнових рецепторів. Препарат для лікування бронхіальної астми та алергічного риніту.ФармакокінетикаВсмоктування Після вживання монтелукаст швидко і майже повністю всмоктується. У дорослих пацієнтів після прийому таблеток жувальних у дозі 5 мг натще Сmах у плазмі крові досягається через 2 год. Середнє значення біодоступності - 73%, ця величина знижується до 63% при прийомі монтелукасту з їжею. Після прийому таблеток жувальних у дозі 4 мг натщесерце у пацієнтів віком від 2 до 5 років Сmах досягається через 2 год. плівковою оболонкою, у дозі 10 мг. У дорослих пацієнтів після прийому натще таблеток, покритих плівковою оболонкою, у дозі 10 мг середнє значення Cmax у плазмі крові досягається через 3 год. Середнє значення біодоступності – 64%; при вживанні одночасно з їжею значення біодоступності та Cmax не порушуються. Розподіл Зв'язування монтелукасту з білками плазми становить понад 99%. Vd у рівноважному стані у середньому становить 8-11 л. Доклінічні дослідження виявили мінімальне проникнення монтелукасту через гематоенцефалічний бар'єр. Через 24 години після прийому концентрація монтелукасту мінімальна і в інших тканинах. Метаболізм Монтелукаст активно метаболізується у печінці. При застосуванні в терапевтичних дозах Css метаболітів монтелукасту в плазмі у дорослих та дітей не визначається. Дослідження in vitro показали, що в процесі метаболізму монтелукасту беруть участь ізоферменти цитохрому Р450 (3А4, 2А6 і 2С9), при цьому в терапевтичних концентраціях монтелукаст не пригнічує ізоферменти цитохрому Р450: 3А4,1С, 2С, 2С. Метаболіти мають незначний терапевтичний ефект монтелукасту. Виведення T1/2 монтелукасту у молодих здорових дорослих добровольців становить від 2.7 до 5.5 год. Плазмовий кліренс монтелукасту у здорових дорослих добровольців становить у середньому 45 мл/хв. Після перорального прийому монтелукасту 86% загальної кількості виводиться через кишечник протягом 5 днів та менше 0.2% - нирками, що поряд з даними про його біодоступність підтверджує виведення монтелукасту та його метаболітів переважно з жовчю. Фармакокінетика в особливих клінічних випадках Фармакокінетика монтелукасту у жінок та чоловіків однакова. У пацієнтів похилого віку або пацієнтів з печінковою недостатністю легкого та середнього ступеня тяжкості не потрібна корекція режиму дозування монтелукасту. Фармакокінетика монтелукасту у пацієнтів із нирковою недостатністю не оцінювалася. Оскільки монтелукаст та його метаболіти не виводяться нирками, корекції дози цієї категорії пацієнтів не потрібно. Даних про характер фармакокінетики монтелукасту у пацієнтів з тяжкими порушеннями функції печінки (більше 9 балів за шкалою Чайлд-П'ю) немає. При прийомі монтелукасту у високих дозах (у 20 і 60 разів, що перевищують рекомендовані дози для дорослих), спостерігається зниження концентрації теофіліну в плазмі крові. При прийомі монтелукасту в дозах (10 мг 1 раз на добу) даного ефекту не спостерігається. ФармакодинамікаАнтагоніст лейкотрієнових рецепторів. Цистеїніл-лейкотрієни (LTC4, LTD4, LTE4) - сильні прозапальні ейкозаноїди, які вивільняються з різних клітин, включаючи огрядні клітини та еозинофіли. Ці важливі проастматичні медіатори зв'язуються з цистеїніл-лейкотрієновими рецепторами (CysLT), присутніми в дихальних шляхах людини та відповідають за реакцію бронхоспазму, виділення мокротиння, проникність судин та збільшення кількості еозинофілів. Монтелукаст - активна при пероральному прийомі з'єднання, яке має велику спорідненість і селективність до CysLT1-рецепторів. Монтелукаст у дозі менше 5 мг усуває бронхоспазм, індукований інгаляцією LTD4. Бронходилатируючий ефект спостерігається протягом 2 годин після перорального застосування. Бронходилатируючий ефект бета2-адреноміметиків посилюється при прийомі монтелукасту. Монтелукаст пригнічує як ранню, і пізню стадії бронхоспазму, викликаного впливом антигенів. Монтелукаст знижує кількість еозинофілів у периферичній крові у дорослих та дітей, а також значно знижує кількість еозинофілів у дихальних шляхах. У пацієнтів з підвищеною чутливістю до ацетилсаліцилової кислоти, які отримують інгаляційні та/або пероральні кортикостероїди, додавання до терапії монтелукасту забезпечує кращий контроль захворювання.Показання до застосуванняПрофілактика та тривале лікування бронхіальної астми, включаючи: попередження денних та нічних симптомів захворювання у дітей віком від 2 років і старше (для таблеток жувальних 4 мг та 5 мг) та у дорослих та підлітків з 15 років (для таблеток, покритих плівковою оболонкою, 10 мг); лікування бронхіальної астми у дітей віком від 6 років і старше (для таблеток жувальних 4 мг та 5 мг) та у дорослих та підлітків з 15 років (для таблеток, покритих плівковою оболонкою, 10 мг) з підвищеною чутливістю до ацетилсаліцилової кислоти; попередження бронхоспазму, викликаного фізичним навантаженням, у дітей віком від 2 років і старше (для таблеток жувальних 4 мг та 5 мг) та у дорослих та підлітків з 15 років (для таблеток, покритих плівковою оболонкою, 10 мг). Полегшення симптомів сезонного та цілорічного алергічного риніту у дітей віком від 2 років (для таблеток жувальних 4 мг та 5 мг) та у дорослих та підлітків з 15 років (для таблеток, покритих плівковою оболонкою, 10 мг).Протипоказання до застосуваннягіперчутливість до активної речовини або будь-якого допоміжного компонента препарату; дитячий вік до 2 років (для таблеток жувальних 4 мг); дитячий вік до 6 років (для пігулок жувальних 5 мг); дитячий вік до 15 років (для пігулок 10 мг); рідкі спадкові захворювання, такі як непереносимість галактози, недостатність лактази або глюкозо-галактозна мальабсорбція; фенілкетонурія (для пігулок жувальних), т.к. таблетки містять аспартам.Вагітність та лактаціяЗастосування препарату Алмонт при вагітності можливе, якщо передбачувана користь для матері перевищує потенційний ризик для плода. Рішення про скасування грудного вигодовування на період застосування препарату Алмонт приймається на підставі оцінки про ймовірну користь для матері та потенційного ризику для дитини. Протипоказано застосування препарату у дитячому віці до 2 років (для дозування 4 мг), дитячому віці до 6 років (для дозування 5 мг), дитячому та підлітковому віці до 15 років (для таблеток 10 мг).Побічна діяІнфекційні та паразитарні захворювання: інфекції верхніх дихальних шляхів. З боку системи крові та лімфатичної системи: підвищення схильності до кровотеч, тромбоцитопенії. З боку імунної системи: реакції гіперчутливості, у т.ч. анафілаксія, еозинофільна інфільтрація печінки З боку психіки: патологічні сновидіння (включаючи нічні кошмари), галюцинації, безсоння, сомнамбулізм, дратівливість, тривога, неспокій, ажитація (включаючи агресивну поведінку або ворожість), тремор, депресія, дезорієнтація, суїцидальні думки. З боку нервової системи: біль голови, запаморочення, сонливість, парестезія/гіпестезії, судоми. Серцево-судинна система: відчуття серцебиття. З боку дихальної системи: носова кровотеча. З боку шлунково-кишкового тракту: діарея, сухість у роті, диспепсія, нудота, блювання, біль у животі, панкреатит. З боку печінки та жовчовивідних шляхів: збільшення активності АЛТ та АСТ, гепатит (включаючи холестатичні, гепатоцелюлярні та змішані ураження печінки). З боку шкіри та підшкірних тканин: ангіоневротичний набряк, схильність до появи гематом, кропив'янка, свербіж шкіри, висипання, вузлувата еритема, багатоформна еритема. З боку кістково-м'язової системи: артралгія, міалгія, включаючи м'язові судоми. Інші: астенія/втома, нездужання, набряки, пірексія, спрага; у дуже поодиноких випадках під час лікування монтелукастом повідомлялося про розвиток синдрому Черджа-Стросса.Взаємодія з лікарськими засобамиУ пацієнтів, які одночасно отримували фенобарбітал, AUC монтелукасту зменшувалась приблизно на 40%, проте корекція режиму дозування у таких пацієнтів не потрібна. Оскільки монтелукаст метаболізується ізоферментом CYP3A4, слід бути обережним, особливо у дітей, якщо монтелукаст одночасно застосовується з індукторами ізоферменту CYP3A4, такими як фенітоїн, фенобарбітал і рифампіцин. Монтелукаст можна призначати разом з іншими лікарськими засобами, які традиційно застосовуються для профілактики та тривалого лікування бронхіальної астми та/або алергічного риніту. Монтелукаст у рекомендованій терапевтичній дозі не справляв клінічно значущого ефекту на фармакокінетику наступних препаратів: теофілін, преднізон, преднізолон, пероральні контрацептиви (етинілестрадіол/норетинодрел 35/1), терфенадин, дигоксин та варфарин. У дослідженнях in vitro встановлено, що монтелукаст є сильним інгібітором ізоферменту CYP2C8. Однак при дослідженні лікарської взаємодії in vivo монтелукасту та росиглітазону (маркерний субстрат, представник препаратів, що первинно метаболізуються ізоферментом CYP2C8) не отримано підтвердження інгібування монтелукастом ізоферменту CYP2C8. Таким чином, у клінічній практиці не передбачається впливу монтелукасту на CYP2С8-опосередкований метаболізм низки лікарських препаратів, у т.ч. паклітакселу, росиглітазону, репаглініду. Дослідження in vitro показали, що монтелукаст є субстратом ізоферменту CYP2C8 і меншою мірою ізоферментів CYP2C9 і CYP3А4. Дані клінічного дослідження лікарської взаємодії щодо монтелукасту та гемфіброзилу (інгібітора як CYP2C8, так і CYP2С9) демонструють, що гемфіброзил підвищує ефект системного впливу монтелукасту у 4.4 рази. Спільний прийом ітраконазолу, сильного інгібітора ізоферменту CYP3A4, разом з гемфіброзилом та монтелукастом не призводив до додаткового підвищення ефекту системного впливу монтелукасту. Вплив гемфіброзилу на системний вплив монтелукасту не може вважатися клінічно значущим на підставі даних безпеки при застосуванні в дозах, що перевищують схвалену дозу 10 мг для дорослих пацієнтів (наприклад,200 мг на добу для дорослих пацієнтів протягом 22 тижнів і до 900 мг на добу для пацієнтів, які приймають препарат протягом приблизно 1 тижня, не спостерігалося клінічно значущих негативних ефектів. Таким чином, при сумісному прийомі разом з гемфіброзилом корекції дози монтелукасту не потрібно. За результатами досліджень in vitro не передбачається клінічно значущої взаємодії з іншими відомими інгібіторами ізоферменту CYP2C8 (наприклад, з триметопримом). Крім того, спільний прийом монтелукасту з одним лише ітраконазолом не призводив до суттєвого підвищення ефекту системного впливу монтелукасту.при сумісному прийомі разом із гемфіброзилом корекції дози монтелукасту не потрібно. За результатами досліджень in vitro не передбачається клінічно значущої взаємодії з іншими відомими інгібіторами ізоферменту CYP2C8 (наприклад, з триметопримом). Крім того, спільний прийом монтелукасту з одним лише ітраконазолом не призводив до суттєвого підвищення ефекту системного впливу монтелукасту.при сумісному прийомі разом із гемфіброзилом корекції дози монтелукасту не потрібно. За результатами досліджень in vitro не передбачається клінічно значущої взаємодії з іншими відомими інгібіторами ізоферменту CYP2C8 (наприклад, з триметопримом). Крім того, спільний прийом монтелукасту з одним лише ітраконазолом не призводив до суттєвого підвищення ефекту системного впливу монтелукасту. Комбіноване лікування з бронходилататорами Препарат Алмонт є обґрунтованим доповненням монотерапії бронходилататорами, якщо останні не забезпечують адекватного контролю бронхіальної астми. Після досягнення терапевтичного ефекту від лікування препаратом Алмонт можна розпочати поступове зниження дози бронходилататорів. Комбіноване лікування з інгаляційними кортикостероїдами Лікування препаратом Алмонт забезпечує додатковий терапевтичний ефект пацієнтам, які застосовують інгаляційні кортикостероїди. Після досягнення стабілізації стану можна розпочати поступове зниження дози кортикостероїдів під наглядом лікаря. У деяких випадках допустима повна відміна інгаляційних кортикостероїдів, проте різка заміна інгаляційних кортикостероїдів на препарат Алмонт не рекомендується.Спосіб застосування та дозиПрепарат приймають внутрішньо. Жувальні таблетки приймають за 1 годину до або через 2 години після їди; таблетку слід розжувати. Таблетки, покриті плівковою оболонкою, приймають внутрішньо, незалежно від їди, не розжовуючи, запиваючи достатньою кількістю рідини. Дорослим та підліткам з 15 років призначають 10 мг (1 таблетка, покрита плівковою оболонкою) 1 раз на добу. При бронхіальній астмі або бронхіальній астмі та алергічному риніті дітям віком від 2 до 6 років призначають по 1 жувальній таблетці 4 мг 1 раз на добу ввечері; дітям віком від 6 до 14 років - по 1 жувальній таблетці 5 мг 1 раз на добу ввечері. При алергічному риніті дітям віком від 2 до 6 років призначають по 1 жувальній таблетці 4 мг 1 раз на добу, дітям віком від 6 до 14 років - по 1 жувальній таблетці 5 мг 1 раз на добу в індивідуальному режимі в залежності від часу найбільшого. Загострення симптомів. Не потрібна корекція дози всередині цих вікових груп. Прийом препарату дітьми здійснюється під наглядом дорослих. Терапевтичний ефект препарату Алмонт, що дозволяє контролювати симптоми астми, досягається протягом доби після прийому. Пацієнту рекомендується продовжувати прийом препарату як у періоди контрольованого перебігу бронхіальної астми, так і в період загострення бронхіальної астми. Пацієнтам з нирковою недостатністю та пацієнтам з печінковою недостатністю легкого та середнього ступеня тяжкості спеціального підбору дози не потрібно. Немає даних про застосування монтелукасту у пацієнтів із тяжкими порушеннями функції печінки. Пацієнтам похилого віку корекція дози не потрібна. Не потрібна корекція дози залежно від статі пацієнта.ПередозуванняСимптоми передозування препарату у пацієнтів з хронічною бронхіальною астмою при застосуванні в дозі, що перевищує 200 мг на добу, протягом 22 тижнів та дозі 900 мг на добу протягом 1 тижня, не виявлені. Є повідомлення про гостре передозування монтелукасту (при прийомі не менше 1 г на добу) у постмаркетинговому періоді та у клінічних дослідженнях у дорослих та дітей. Клінічні та лабораторні дані при цьому свідчать про відповідність профілю безпеки препарату у дітей, дорослих та пацієнтів похилого віку. Найчастішими симптомами були почуття спраги, сонливість, блювання, психомоторне збудження, біль голови і біль у животі. Лікування: проведення симптоматичної терапії. Дані щодо можливості виведення монтелукасту шляхом перитонеального діалізу або гемодіалізу відсутні.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаТаблетки покриті плівковою оболонкою з маркуванням "M" на одній із сторін - 1 таб. Активні речовини: монтелукаст натрію – 10.4 мг (відповідає вмісту монтелукасту – 10 мг); Допоміжні речовини: ядро - мікрокристалічна целюлоза - 89.3 мг, гіпоролоза - 4 мг, кроскармелоза натрію - 6 мг, лактози моногідрат - 89.3 мг, магнію стеарат - 1 мг; плівкова оболонка - опадрай II бежевий 31F27012 (лактози моногідрат - 1.44 мг, гіпромелоза 15cP - 1.12 мг, титану діоксид - 1.011 мг, макрогол 4000 - 0.4 мг, барвник заліза оксид жовтий 0 0 0 0 0 0 0 0 0 - 0 0 0 0 0 0 0 0 0 мг. По 10 або 14 таблеток в Ал/Ал блістері. По 3 блістери (по 10 таблеток), по 2 або 7 блістерів (по 14 таблеток) у картонній пачці разом з інструкцією з медичного застосування.Опис лікарської формиТаблетки, покриті плівковою оболонкою бежевого кольору, квадратні, із закругленими кутами, двоопуклі, з маркуванням "M" на одній із сторін.Фармакотерапевтична групаАнтагоніст лейкотрієнових рецепторів. Препарат для лікування бронхіальної астми та алергічного риніту.ФармакокінетикаВсмоктування Після вживання монтелукаст швидко і майже повністю всмоктується. У дорослих пацієнтів після прийому таблеток жувальних у дозі 5 мг натще Сmах у плазмі крові досягається через 2 год. Середнє значення біодоступності - 73%, ця величина знижується до 63% при прийомі монтелукасту з їжею. Після прийому таблеток жувальних у дозі 4 мг натщесерце у пацієнтів віком від 2 до 5 років Сmах досягається через 2 год. плівковою оболонкою, у дозі 10 мг. У дорослих пацієнтів після прийому натще таблеток, покритих плівковою оболонкою, у дозі 10 мг середнє значення Cmax у плазмі крові досягається через 3 год. Середнє значення біодоступності – 64%; при вживанні одночасно з їжею значення біодоступності та Cmax не порушуються. Розподіл Зв'язування монтелукасту з білками плазми становить понад 99%. Vd у рівноважному стані у середньому становить 8-11 л. Доклінічні дослідження виявили мінімальне проникнення монтелукасту через гематоенцефалічний бар'єр. Через 24 години після прийому концентрація монтелукасту мінімальна і в інших тканинах. Метаболізм Монтелукаст активно метаболізується у печінці. При застосуванні в терапевтичних дозах Css метаболітів монтелукасту в плазмі у дорослих та дітей не визначається. Дослідження in vitro показали, що в процесі метаболізму монтелукасту беруть участь ізоферменти цитохрому Р450 (3А4, 2А6 і 2С9), при цьому в терапевтичних концентраціях монтелукаст не пригнічує ізоферменти цитохрому Р450: 3А4,1С, 2С, 2С. Метаболіти мають незначний терапевтичний ефект монтелукасту. Виведення T1/2 монтелукасту у молодих здорових дорослих добровольців становить від 2.7 до 5.5 год. Плазмовий кліренс монтелукасту у здорових дорослих добровольців становить у середньому 45 мл/хв. Після перорального прийому монтелукасту 86% загальної кількості виводиться через кишечник протягом 5 днів та менше 0.2% - нирками, що поряд з даними про його біодоступність підтверджує виведення монтелукасту та його метаболітів переважно з жовчю. Фармакокінетика в особливих клінічних випадках Фармакокінетика монтелукасту у жінок та чоловіків однакова. У пацієнтів похилого віку або пацієнтів з печінковою недостатністю легкого та середнього ступеня тяжкості не потрібна корекція режиму дозування монтелукасту. Фармакокінетика монтелукасту у пацієнтів із нирковою недостатністю не оцінювалася. Оскільки монтелукаст та його метаболіти не виводяться нирками, корекції дози цієї категорії пацієнтів не потрібно. Даних про характер фармакокінетики монтелукасту у пацієнтів з тяжкими порушеннями функції печінки (більше 9 балів за шкалою Чайлд-П'ю) немає. При прийомі монтелукасту у високих дозах (у 20 і 60 разів, що перевищують рекомендовані дози для дорослих), спостерігається зниження концентрації теофіліну в плазмі крові. При прийомі монтелукасту в дозах (10 мг 1 раз на добу) даного ефекту не спостерігається. ФармакодинамікаАнтагоніст лейкотрієнових рецепторів. Цистеїніл-лейкотрієни (LTC4, LTD4, LTE4) - сильні прозапальні ейкозаноїди, які вивільняються з різних клітин, включаючи огрядні клітини та еозинофіли. Ці важливі проастматичні медіатори зв'язуються з цистеїніл-лейкотрієновими рецепторами (CysLT), присутніми в дихальних шляхах людини та відповідають за реакцію бронхоспазму, виділення мокротиння, проникність судин та збільшення кількості еозинофілів. Монтелукаст - активна при пероральному прийомі з'єднання, яке має велику спорідненість і селективність до CysLT1-рецепторів. Монтелукаст у дозі менше 5 мг усуває бронхоспазм, індукований інгаляцією LTD4. Бронходилатируючий ефект спостерігається протягом 2 годин після перорального застосування. Бронходилатируючий ефект бета2-адреноміметиків посилюється при прийомі монтелукасту. Монтелукаст пригнічує як ранню, і пізню стадії бронхоспазму, викликаного впливом антигенів. Монтелукаст знижує кількість еозинофілів у периферичній крові у дорослих та дітей, а також значно знижує кількість еозинофілів у дихальних шляхах. У пацієнтів з підвищеною чутливістю до ацетилсаліцилової кислоти, які отримують інгаляційні та/або пероральні кортикостероїди, додавання до терапії монтелукасту забезпечує кращий контроль захворювання.Показання до застосуванняПрофілактика та тривале лікування бронхіальної астми, включаючи: попередження денних та нічних симптомів захворювання у дітей віком від 2 років і старше (для таблеток жувальних 4 мг та 5 мг) та у дорослих та підлітків з 15 років (для таблеток, покритих плівковою оболонкою, 10 мг); лікування бронхіальної астми у дітей віком від 6 років і старше (для таблеток жувальних 4 мг та 5 мг) та у дорослих та підлітків з 15 років (для таблеток, покритих плівковою оболонкою, 10 мг) з підвищеною чутливістю до ацетилсаліцилової кислоти; попередження бронхоспазму, викликаного фізичним навантаженням, у дітей віком від 2 років і старше (для таблеток жувальних 4 мг та 5 мг) та у дорослих та підлітків з 15 років (для таблеток, покритих плівковою оболонкою, 10 мг). Полегшення симптомів сезонного та цілорічного алергічного риніту у дітей віком від 2 років (для таблеток жувальних 4 мг та 5 мг) та у дорослих та підлітків з 15 років (для таблеток, покритих плівковою оболонкою, 10 мг).Протипоказання до застосуваннягіперчутливість до активної речовини або будь-якого допоміжного компонента препарату; дитячий вік до 2 років (для таблеток жувальних 4 мг); дитячий вік до 6 років (для пігулок жувальних 5 мг); дитячий вік до 15 років (для пігулок 10 мг); рідкі спадкові захворювання, такі як непереносимість галактози, недостатність лактази або глюкозо-галактозна мальабсорбція; фенілкетонурія (для пігулок жувальних), т.к. таблетки містять аспартам.Вагітність та лактаціяЗастосування препарату Алмонт при вагітності можливе, якщо передбачувана користь для матері перевищує потенційний ризик для плода. Рішення про скасування грудного вигодовування на період застосування препарату Алмонт приймається на підставі оцінки про ймовірну користь для матері та потенційного ризику для дитини. Протипоказано застосування препарату у дитячому віці до 2 років (для дозування 4 мг), дитячому віці до 6 років (для дозування 5 мг), дитячому та підлітковому віці до 15 років (для таблеток 10 мг).Побічна діяІнфекційні та паразитарні захворювання: інфекції верхніх дихальних шляхів. З боку системи крові та лімфатичної системи: підвищення схильності до кровотеч, тромбоцитопенії. З боку імунної системи: реакції гіперчутливості, у т.ч. анафілаксія, еозинофільна інфільтрація печінки З боку психіки: патологічні сновидіння (включаючи нічні кошмари), галюцинації, безсоння, сомнамбулізм, дратівливість, тривога, неспокій, ажитація (включаючи агресивну поведінку або ворожість), тремор, депресія, дезорієнтація, суїцидальні думки. З боку нервової системи: біль голови, запаморочення, сонливість, парестезія/гіпестезії, судоми. Серцево-судинна система: відчуття серцебиття. З боку дихальної системи: носова кровотеча. З боку шлунково-кишкового тракту: діарея, сухість у роті, диспепсія, нудота, блювання, біль у животі, панкреатит. З боку печінки та жовчовивідних шляхів: збільшення активності АЛТ та АСТ, гепатит (включаючи холестатичні, гепатоцелюлярні та змішані ураження печінки). З боку шкіри та підшкірних тканин: ангіоневротичний набряк, схильність до появи гематом, кропив'янка, свербіж шкіри, висипання, вузлувата еритема, багатоформна еритема. З боку кістково-м'язової системи: артралгія, міалгія, включаючи м'язові судоми. Інші: астенія/втома, нездужання, набряки, пірексія, спрага; у дуже поодиноких випадках під час лікування монтелукастом повідомлялося про розвиток синдрому Черджа-Стросса.Взаємодія з лікарськими засобамиУ пацієнтів, які одночасно отримували фенобарбітал, AUC монтелукасту зменшувалась приблизно на 40%, проте корекція режиму дозування у таких пацієнтів не потрібна. Оскільки монтелукаст метаболізується ізоферментом CYP3A4, слід бути обережним, особливо у дітей, якщо монтелукаст одночасно застосовується з індукторами ізоферменту CYP3A4, такими як фенітоїн, фенобарбітал і рифампіцин. Монтелукаст можна призначати разом з іншими лікарськими засобами, які традиційно застосовуються для профілактики та тривалого лікування бронхіальної астми та/або алергічного риніту. Монтелукаст у рекомендованій терапевтичній дозі не справляв клінічно значущого ефекту на фармакокінетику наступних препаратів: теофілін, преднізон, преднізолон, пероральні контрацептиви (етинілестрадіол/норетинодрел 35/1), терфенадин, дигоксин та варфарин. У дослідженнях in vitro встановлено, що монтелукаст є сильним інгібітором ізоферменту CYP2C8. Однак при дослідженні лікарської взаємодії in vivo монтелукасту та росиглітазону (маркерний субстрат, представник препаратів, що первинно метаболізуються ізоферментом CYP2C8) не отримано підтвердження інгібування монтелукастом ізоферменту CYP2C8. Таким чином, у клінічній практиці не передбачається впливу монтелукасту на CYP2С8-опосередкований метаболізм низки лікарських препаратів, у т.ч. паклітакселу, росиглітазону, репаглініду. Дослідження in vitro показали, що монтелукаст є субстратом ізоферменту CYP2C8 і меншою мірою ізоферментів CYP2C9 і CYP3А4. Дані клінічного дослідження лікарської взаємодії щодо монтелукасту та гемфіброзилу (інгібітора як CYP2C8, так і CYP2С9) демонструють, що гемфіброзил підвищує ефект системного впливу монтелукасту у 4.4 рази. Спільний прийом ітраконазолу, сильного інгібітора ізоферменту CYP3A4, разом з гемфіброзилом та монтелукастом не призводив до додаткового підвищення ефекту системного впливу монтелукасту. Вплив гемфіброзилу на системний вплив монтелукасту не може вважатися клінічно значущим на підставі даних безпеки при застосуванні в дозах, що перевищують схвалену дозу 10 мг для дорослих пацієнтів (наприклад,200 мг на добу для дорослих пацієнтів протягом 22 тижнів і до 900 мг на добу для пацієнтів, які приймають препарат протягом приблизно 1 тижня, не спостерігалося клінічно значущих негативних ефектів. Таким чином, при сумісному прийомі разом з гемфіброзилом корекції дози монтелукасту не потрібно. За результатами досліджень in vitro не передбачається клінічно значущої взаємодії з іншими відомими інгібіторами ізоферменту CYP2C8 (наприклад, з триметопримом). Крім того, спільний прийом монтелукасту з одним лише ітраконазолом не призводив до суттєвого підвищення ефекту системного впливу монтелукасту.при сумісному прийомі разом із гемфіброзилом корекції дози монтелукасту не потрібно. За результатами досліджень in vitro не передбачається клінічно значущої взаємодії з іншими відомими інгібіторами ізоферменту CYP2C8 (наприклад, з триметопримом). Крім того, спільний прийом монтелукасту з одним лише ітраконазолом не призводив до суттєвого підвищення ефекту системного впливу монтелукасту.при сумісному прийомі разом із гемфіброзилом корекції дози монтелукасту не потрібно. За результатами досліджень in vitro не передбачається клінічно значущої взаємодії з іншими відомими інгібіторами ізоферменту CYP2C8 (наприклад, з триметопримом). Крім того, спільний прийом монтелукасту з одним лише ітраконазолом не призводив до суттєвого підвищення ефекту системного впливу монтелукасту. Комбіноване лікування з бронходилататорами Препарат Алмонт є обґрунтованим доповненням монотерапії бронходилататорами, якщо останні не забезпечують адекватного контролю бронхіальної астми. Після досягнення терапевтичного ефекту від лікування препаратом Алмонт можна розпочати поступове зниження дози бронходилататорів. Комбіноване лікування з інгаляційними кортикостероїдами Лікування препаратом Алмонт забезпечує додатковий терапевтичний ефект пацієнтам, які застосовують інгаляційні кортикостероїди. Після досягнення стабілізації стану можна розпочати поступове зниження дози кортикостероїдів під наглядом лікаря. У деяких випадках допустима повна відміна інгаляційних кортикостероїдів, проте різка заміна інгаляційних кортикостероїдів на препарат Алмонт не рекомендується.Спосіб застосування та дозиПрепарат приймають внутрішньо. Жувальні таблетки приймають за 1 годину до або через 2 години після їди; таблетку слід розжувати. Таблетки, покриті плівковою оболонкою, приймають внутрішньо, незалежно від їди, не розжовуючи, запиваючи достатньою кількістю рідини. Дорослим та підліткам з 15 років призначають 10 мг (1 таблетка, покрита плівковою оболонкою) 1 раз на добу. При бронхіальній астмі або бронхіальній астмі та алергічному риніті дітям віком від 2 до 6 років призначають по 1 жувальній таблетці 4 мг 1 раз на добу ввечері; дітям віком від 6 до 14 років - по 1 жувальній таблетці 5 мг 1 раз на добу ввечері. При алергічному риніті дітям віком від 2 до 6 років призначають по 1 жувальній таблетці 4 мг 1 раз на добу, дітям віком від 6 до 14 років - по 1 жувальній таблетці 5 мг 1 раз на добу в індивідуальному режимі в залежності від часу найбільшого. Загострення симптомів. Не потрібна корекція дози всередині цих вікових груп. Прийом препарату дітьми здійснюється під наглядом дорослих. Терапевтичний ефект препарату Алмонт, що дозволяє контролювати симптоми астми, досягається протягом доби після прийому. Пацієнту рекомендується продовжувати прийом препарату як у періоди контрольованого перебігу бронхіальної астми, так і в період загострення бронхіальної астми. Пацієнтам з нирковою недостатністю та пацієнтам з печінковою недостатністю легкого та середнього ступеня тяжкості спеціального підбору дози не потрібно. Немає даних про застосування монтелукасту у пацієнтів із тяжкими порушеннями функції печінки. Пацієнтам похилого віку корекція дози не потрібна. Не потрібна корекція дози залежно від статі пацієнта.ПередозуванняСимптоми передозування препарату у пацієнтів з хронічною бронхіальною астмою при застосуванні в дозі, що перевищує 200 мг на добу, протягом 22 тижнів та дозі 900 мг на добу протягом 1 тижня, не виявлені. Є повідомлення про гостре передозування монтелукасту (при прийомі не менше 1 г на добу) у постмаркетинговому періоді та у клінічних дослідженнях у дорослих та дітей. Клінічні та лабораторні дані при цьому свідчать про відповідність профілю безпеки препарату у дітей, дорослих та пацієнтів похилого віку. Найчастішими симптомами були почуття спраги, сонливість, блювання, психомоторне збудження, біль голови і біль у животі. Лікування: проведення симптоматичної терапії. Дані щодо можливості виведення монтелукасту шляхом перитонеального діалізу або гемодіалізу відсутні.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаТаблетки жувальні з гравіюванням "М4" - 1 таб. Активні речовини: монтелукаст натрію – 4.16 мг (відповідає вмісту монтелукасту – 4 мг); Допоміжні речовини: манітол - 160.96 мг, целюлоза мікрокристалічна - 52.8 мг, гіпоролоза - 7.2 мг, кроскармелоза натрію - 7.2 мг, барвник Pigment Blend PB-24880 (лактози моногідрат - 3.6 мг, фарб. магнію стеарат – 2.4 мг, аспартам – 1.2 мг, ароматизатор вишневий (Silarom Cherry Flavour 1219813182) – 0.08 мг. По 10 або 14 таблеток в Ал/Ал блістері. По 3 блістери (по 10 таблеток), по 2 або 7 блістерів (по 14 таблеток) у картонній пачці разом з інструкцією з медичного застосування.Опис лікарської формиПігулки жувальні овальні, двоопуклі, рожевого кольору з вкрапленнями та з гравіюванням "М4" на одній стороні.Фармакотерапевтична групаАнтагоніст лейкотрієнових рецепторів. Препарат для лікування бронхіальної астми та алергічного риніту.ФармакокінетикаВсмоктування Після вживання монтелукаст швидко і майже повністю всмоктується. У дорослих пацієнтів після прийому таблеток жувальних у дозі 5 мг натще Сmах у плазмі крові досягається через 2 год. Середнє значення біодоступності - 73%, ця величина знижується до 63% при прийомі монтелукасту з їжею. Після прийому таблеток жувальних у дозі 4 мг натщесерце у пацієнтів віком від 2 до 5 років Сmах досягається через 2 год. плівковою оболонкою, у дозі 10 мг. У дорослих пацієнтів після прийому натще таблеток, покритих плівковою оболонкою, у дозі 10 мг середнє значення Cmax у плазмі крові досягається через 3 год. Середнє значення біодоступності – 64%; при вживанні одночасно з їжею значення біодоступності та Cmax не порушуються. Розподіл Зв'язування монтелукасту з білками плазми становить понад 99%. Vd у рівноважному стані у середньому становить 8-11 л. Доклінічні дослідження виявили мінімальне проникнення монтелукасту через гематоенцефалічний бар'єр. Через 24 години після прийому концентрація монтелукасту мінімальна і в інших тканинах. Метаболізм Монтелукаст активно метаболізується у печінці. При застосуванні в терапевтичних дозах Css метаболітів монтелукасту в плазмі у дорослих та дітей не визначається. Дослідження in vitro показали, що в процесі метаболізму монтелукасту беруть участь ізоферменти цитохрому Р450 (3А4, 2А6 і 2С9), при цьому в терапевтичних концентраціях монтелукаст не пригнічує ізоферменти цитохрому Р450: 3А4,1С, 2С, 2С. Метаболіти мають незначний терапевтичний ефект монтелукасту. Виведення T1/2 монтелукасту у молодих здорових дорослих добровольців становить від 2.7 до 5.5 год. Плазмовий кліренс монтелукасту у здорових дорослих добровольців становить у середньому 45 мл/хв. Після перорального прийому монтелукасту 86% загальної кількості виводиться через кишечник протягом 5 днів та менше 0.2% - нирками, що поряд з даними про його біодоступність підтверджує виведення монтелукасту та його метаболітів переважно з жовчю. Фармакокінетика в особливих клінічних випадках Фармакокінетика монтелукасту у жінок та чоловіків однакова. У пацієнтів похилого віку або пацієнтів з печінковою недостатністю легкого та середнього ступеня тяжкості не потрібна корекція режиму дозування монтелукасту. Фармакокінетика монтелукасту у пацієнтів із нирковою недостатністю не оцінювалася. Оскільки монтелукаст та його метаболіти не виводяться нирками, корекції дози цієї категорії пацієнтів не потрібно. Даних про характер фармакокінетики монтелукасту у пацієнтів з тяжкими порушеннями функції печінки (більше 9 балів за шкалою Чайлд-П'ю) немає. При прийомі монтелукасту у високих дозах (у 20 і 60 разів, що перевищують рекомендовані дози для дорослих), спостерігається зниження концентрації теофіліну в плазмі крові. При прийомі монтелукасту в дозах (10 мг 1 раз на добу) даного ефекту не спостерігається. ФармакодинамікаАнтагоніст лейкотрієнових рецепторів. Цистеїніл-лейкотрієни (LTC4, LTD4, LTE4) - сильні прозапальні ейкозаноїди, які вивільняються з різних клітин, включаючи огрядні клітини та еозинофіли. Ці важливі проастматичні медіатори зв'язуються з цистеїніл-лейкотрієновими рецепторами (CysLT), присутніми в дихальних шляхах людини та відповідають за реакцію бронхоспазму, виділення мокротиння, проникність судин та збільшення кількості еозинофілів. Монтелукаст - активна при пероральному прийомі з'єднання, яке має велику спорідненість і селективність до CysLT1-рецепторів. Монтелукаст у дозі менше 5 мг усуває бронхоспазм, індукований інгаляцією LTD4. Бронходилатируючий ефект спостерігається протягом 2 годин після перорального застосування. Бронходилатируючий ефект бета2-адреноміметиків посилюється при прийомі монтелукасту. Монтелукаст пригнічує як ранню, і пізню стадії бронхоспазму, викликаного впливом антигенів. Монтелукаст знижує кількість еозинофілів у периферичній крові у дорослих та дітей, а також значно знижує кількість еозинофілів у дихальних шляхах. У пацієнтів з підвищеною чутливістю до ацетилсаліцилової кислоти, які отримують інгаляційні та/або пероральні кортикостероїди, додавання до терапії монтелукасту забезпечує кращий контроль захворювання.Показання до застосуванняПрофілактика та тривале лікування бронхіальної астми, включаючи: попередження денних та нічних симптомів захворювання у дітей віком від 2 років і старше (для таблеток жувальних 4 мг та 5 мг) та у дорослих та підлітків з 15 років (для таблеток, покритих плівковою оболонкою, 10 мг); лікування бронхіальної астми у дітей віком від 6 років і старше (для таблеток жувальних 4 мг та 5 мг) та у дорослих та підлітків з 15 років (для таблеток, покритих плівковою оболонкою, 10 мг) з підвищеною чутливістю до ацетилсаліцилової кислоти; попередження бронхоспазму, викликаного фізичним навантаженням, у дітей віком від 2 років і старше (для таблеток жувальних 4 мг та 5 мг) та у дорослих та підлітків з 15 років (для таблеток, покритих плівковою оболонкою, 10 мг). Полегшення симптомів сезонного та цілорічного алергічного риніту у дітей віком від 2 років (для таблеток жувальних 4 мг та 5 мг) та у дорослих та підлітків з 15 років (для таблеток, покритих плівковою оболонкою, 10 мг).Протипоказання до застосуваннягіперчутливість до активної речовини або будь-якого допоміжного компонента препарату; дитячий вік до 2 років (для таблеток жувальних 4 мг); дитячий вік до 6 років (для пігулок жувальних 5 мг); дитячий вік до 15 років (для пігулок 10 мг); рідкі спадкові захворювання, такі як непереносимість галактози, недостатність лактази або глюкозо-галактозна мальабсорбція; фенілкетонурія (для пігулок жувальних), т.к. таблетки містять аспартам.Вагітність та лактаціяЗастосування препарату Алмонт при вагітності можливе, якщо передбачувана користь для матері перевищує потенційний ризик для плода. Рішення про скасування грудного вигодовування на період застосування препарату Алмонт приймається на підставі оцінки про ймовірну користь для матері та потенційного ризику для дитини. Протипоказано застосування препарату у дитячому віці до 2 років (для дозування 4 мг), дитячому віці до 6 років (для дозування 5 мг), дитячому та підлітковому віці до 15 років (для таблеток 10 мг).Побічна діяІнфекційні та паразитарні захворювання: інфекції верхніх дихальних шляхів. З боку системи крові та лімфатичної системи: підвищення схильності до кровотеч, тромбоцитопенії. З боку імунної системи: реакції гіперчутливості, у т.ч. анафілаксія, еозинофільна інфільтрація печінки З боку психіки: патологічні сновидіння (включаючи нічні кошмари), галюцинації, безсоння, сомнамбулізм, дратівливість, тривога, неспокій, ажитація (включаючи агресивну поведінку або ворожість), тремор, депресія, дезорієнтація, суїцидальні думки. З боку нервової системи: біль голови, запаморочення, сонливість, парестезія/гіпестезії, судоми. Серцево-судинна система: відчуття серцебиття. З боку дихальної системи: носова кровотеча. З боку шлунково-кишкового тракту: діарея, сухість у роті, диспепсія, нудота, блювання, біль у животі, панкреатит. З боку печінки та жовчовивідних шляхів: збільшення активності АЛТ та АСТ, гепатит (включаючи холестатичні, гепатоцелюлярні та змішані ураження печінки). З боку шкіри та підшкірних тканин: ангіоневротичний набряк, схильність до появи гематом, кропив'янка, свербіж шкіри, висипання, вузлувата еритема, багатоформна еритема. З боку кістково-м'язової системи: артралгія, міалгія, включаючи м'язові судоми. Інші: астенія/втома, нездужання, набряки, пірексія, спрага; у дуже поодиноких випадках під час лікування монтелукастом повідомлялося про розвиток синдрому Черджа-Стросса.Взаємодія з лікарськими засобамиУ пацієнтів, які одночасно отримували фенобарбітал, AUC монтелукасту зменшувалась приблизно на 40%, проте корекція режиму дозування у таких пацієнтів не потрібна. Оскільки монтелукаст метаболізується ізоферментом CYP3A4, слід бути обережним, особливо у дітей, якщо монтелукаст одночасно застосовується з індукторами ізоферменту CYP3A4, такими як фенітоїн, фенобарбітал і рифампіцин. Монтелукаст можна призначати разом з іншими лікарськими засобами, які традиційно застосовуються для профілактики та тривалого лікування бронхіальної астми та/або алергічного риніту. Монтелукаст у рекомендованій терапевтичній дозі не справляв клінічно значущого ефекту на фармакокінетику наступних препаратів: теофілін, преднізон, преднізолон, пероральні контрацептиви (етинілестрадіол/норетинодрел 35/1), терфенадин, дигоксин та варфарин. У дослідженнях in vitro встановлено, що монтелукаст є сильним інгібітором ізоферменту CYP2C8. Однак при дослідженні лікарської взаємодії in vivo монтелукасту та росиглітазону (маркерний субстрат, представник препаратів, що первинно метаболізуються ізоферментом CYP2C8) не отримано підтвердження інгібування монтелукастом ізоферменту CYP2C8. Таким чином, у клінічній практиці не передбачається впливу монтелукасту на CYP2С8-опосередкований метаболізм низки лікарських препаратів, у т.ч. паклітакселу, росиглітазону, репаглініду. Дослідження in vitro показали, що монтелукаст є субстратом ізоферменту CYP2C8 і меншою мірою ізоферментів CYP2C9 і CYP3А4. Дані клінічного дослідження лікарської взаємодії щодо монтелукасту та гемфіброзилу (інгібітора як CYP2C8, так і CYP2С9) демонструють, що гемфіброзил підвищує ефект системного впливу монтелукасту у 4.4 рази. Спільний прийом ітраконазолу, сильного інгібітора ізоферменту CYP3A4, разом з гемфіброзилом та монтелукастом не призводив до додаткового підвищення ефекту системного впливу монтелукасту. Вплив гемфіброзилу на системний вплив монтелукасту не може вважатися клінічно значущим на підставі даних безпеки при застосуванні в дозах, що перевищують схвалену дозу 10 мг для дорослих пацієнтів (наприклад,200 мг на добу для дорослих пацієнтів протягом 22 тижнів і до 900 мг на добу для пацієнтів, які приймають препарат протягом приблизно 1 тижня, не спостерігалося клінічно значущих негативних ефектів. Таким чином, при сумісному прийомі разом з гемфіброзилом корекції дози монтелукасту не потрібно. За результатами досліджень in vitro не передбачається клінічно значущої взаємодії з іншими відомими інгібіторами ізоферменту CYP2C8 (наприклад, з триметопримом). Крім того, спільний прийом монтелукасту з одним лише ітраконазолом не призводив до суттєвого підвищення ефекту системного впливу монтелукасту.при сумісному прийомі разом із гемфіброзилом корекції дози монтелукасту не потрібно. За результатами досліджень in vitro не передбачається клінічно значущої взаємодії з іншими відомими інгібіторами ізоферменту CYP2C8 (наприклад, з триметопримом). Крім того, спільний прийом монтелукасту з одним лише ітраконазолом не призводив до суттєвого підвищення ефекту системного впливу монтелукасту.при сумісному прийомі разом із гемфіброзилом корекції дози монтелукасту не потрібно. За результатами досліджень in vitro не передбачається клінічно значущої взаємодії з іншими відомими інгібіторами ізоферменту CYP2C8 (наприклад, з триметопримом). Крім того, спільний прийом монтелукасту з одним лише ітраконазолом не призводив до суттєвого підвищення ефекту системного впливу монтелукасту. Комбіноване лікування з бронходилататорами Препарат Алмонт є обґрунтованим доповненням монотерапії бронходилататорами, якщо останні не забезпечують адекватного контролю бронхіальної астми. Після досягнення терапевтичного ефекту від лікування препаратом Алмонт можна розпочати поступове зниження дози бронходилататорів. Комбіноване лікування з інгаляційними кортикостероїдами Лікування препаратом Алмонт забезпечує додатковий терапевтичний ефект пацієнтам, які застосовують інгаляційні кортикостероїди. Після досягнення стабілізації стану можна розпочати поступове зниження дози кортикостероїдів під наглядом лікаря. У деяких випадках допустима повна відміна інгаляційних кортикостероїдів, проте різка заміна інгаляційних кортикостероїдів на препарат Алмонт не рекомендується.Спосіб застосування та дозиПрепарат приймають внутрішньо. Жувальні таблетки приймають за 1 годину до або через 2 години після їди; таблетку слід розжувати. Таблетки, покриті плівковою оболонкою, приймають внутрішньо, незалежно від їди, не розжовуючи, запиваючи достатньою кількістю рідини. Дорослим та підліткам з 15 років призначають 10 мг (1 таблетка, покрита плівковою оболонкою) 1 раз на добу. При бронхіальній астмі або бронхіальній астмі та алергічному риніті дітям віком від 2 до 6 років призначають по 1 жувальній таблетці 4 мг 1 раз на добу ввечері; дітям віком від 6 до 14 років - по 1 жувальній таблетці 5 мг 1 раз на добу ввечері. При алергічному риніті дітям віком від 2 до 6 років призначають по 1 жувальній таблетці 4 мг 1 раз на добу, дітям віком від 6 до 14 років - по 1 жувальній таблетці 5 мг 1 раз на добу в індивідуальному режимі в залежності від часу найбільшого. Загострення симптомів. Не потрібна корекція дози всередині цих вікових груп. Прийом препарату дітьми здійснюється під наглядом дорослих. Терапевтичний ефект препарату Алмонт, що дозволяє контролювати симптоми астми, досягається протягом доби після прийому. Пацієнту рекомендується продовжувати прийом препарату як у періоди контрольованого перебігу бронхіальної астми, так і в період загострення бронхіальної астми. Пацієнтам з нирковою недостатністю та пацієнтам з печінковою недостатністю легкого та середнього ступеня тяжкості спеціального підбору дози не потрібно. Немає даних про застосування монтелукасту у пацієнтів із тяжкими порушеннями функції печінки. Пацієнтам похилого віку корекція дози не потрібна. Не потрібна корекція дози залежно від статі пацієнта.ПередозуванняСимптоми передозування препарату у пацієнтів з хронічною бронхіальною астмою при застосуванні в дозі, що перевищує 200 мг на добу, протягом 22 тижнів та дозі 900 мг на добу протягом 1 тижня, не виявлені. Є повідомлення про гостре передозування монтелукасту (при прийомі не менше 1 г на добу) у постмаркетинговому періоді та у клінічних дослідженнях у дорослих та дітей. Клінічні та лабораторні дані при цьому свідчать про відповідність профілю безпеки препарату у дітей, дорослих та пацієнтів похилого віку. Найчастішими симптомами були почуття спраги, сонливість, блювання, психомоторне збудження, біль голови і біль у животі. Лікування: проведення симптоматичної терапії. Дані щодо можливості виведення монтелукасту шляхом перитонеального діалізу або гемодіалізу відсутні.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаТаблетки жувальні з гравіюванням "М4" - 1 таб. Активні речовини: монтелукаст натрію – 4.16 мг (відповідає вмісту монтелукасту – 4 мг); Допоміжні речовини: манітол - 160.96 мг, целюлоза мікрокристалічна - 52.8 мг, гіпоролоза - 7.2 мг, кроскармелоза натрію - 7.2 мг, барвник Pigment Blend PB-24880 (лактози моногідрат - 3.6 мг, фарб. магнію стеарат – 2.4 мг, аспартам – 1.2 мг, ароматизатор вишневий (Silarom Cherry Flavour 1219813182) – 0.08 мг. По 10 або 14 таблеток в Ал/Ал блістері. По 3 блістери (по 10 таблеток), по 2 або 7 блістерів (по 14 таблеток) у картонній пачці разом з інструкцією з медичного застосування.Опис лікарської формиПігулки жувальні овальні, двоопуклі, рожевого кольору з вкрапленнями та з гравіюванням "М4" на одній стороні.Фармакотерапевтична групаАнтагоніст лейкотрієнових рецепторів. Препарат для лікування бронхіальної астми та алергічного риніту.ФармакокінетикаВсмоктування Після вживання монтелукаст швидко і майже повністю всмоктується. У дорослих пацієнтів після прийому таблеток жувальних у дозі 5 мг натще Сmах у плазмі крові досягається через 2 год. Середнє значення біодоступності - 73%, ця величина знижується до 63% при прийомі монтелукасту з їжею. Після прийому таблеток жувальних у дозі 4 мг натщесерце у пацієнтів віком від 2 до 5 років Сmах досягається через 2 год. плівковою оболонкою, у дозі 10 мг. У дорослих пацієнтів після прийому натще таблеток, покритих плівковою оболонкою, у дозі 10 мг середнє значення Cmax у плазмі крові досягається через 3 год. Середнє значення біодоступності – 64%; при вживанні одночасно з їжею значення біодоступності та Cmax не порушуються. Розподіл Зв'язування монтелукасту з білками плазми становить понад 99%. Vd у рівноважному стані у середньому становить 8-11 л. Доклінічні дослідження виявили мінімальне проникнення монтелукасту через гематоенцефалічний бар'єр. Через 24 години після прийому концентрація монтелукасту мінімальна і в інших тканинах. Метаболізм Монтелукаст активно метаболізується у печінці. При застосуванні в терапевтичних дозах Css метаболітів монтелукасту в плазмі у дорослих та дітей не визначається. Дослідження in vitro показали, що в процесі метаболізму монтелукасту беруть участь ізоферменти цитохрому Р450 (3А4, 2А6 і 2С9), при цьому в терапевтичних концентраціях монтелукаст не пригнічує ізоферменти цитохрому Р450: 3А4,1С, 2С, 2С. Метаболіти мають незначний терапевтичний ефект монтелукасту. Виведення T1/2 монтелукасту у молодих здорових дорослих добровольців становить від 2.7 до 5.5 год. Плазмовий кліренс монтелукасту у здорових дорослих добровольців становить у середньому 45 мл/хв. Після перорального прийому монтелукасту 86% загальної кількості виводиться через кишечник протягом 5 днів та менше 0.2% - нирками, що поряд з даними про його біодоступність підтверджує виведення монтелукасту та його метаболітів переважно з жовчю. Фармакокінетика в особливих клінічних випадках Фармакокінетика монтелукасту у жінок та чоловіків однакова. У пацієнтів похилого віку або пацієнтів з печінковою недостатністю легкого та середнього ступеня тяжкості не потрібна корекція режиму дозування монтелукасту. Фармакокінетика монтелукасту у пацієнтів із нирковою недостатністю не оцінювалася. Оскільки монтелукаст та його метаболіти не виводяться нирками, корекції дози цієї категорії пацієнтів не потрібно. Даних про характер фармакокінетики монтелукасту у пацієнтів з тяжкими порушеннями функції печінки (більше 9 балів за шкалою Чайлд-П'ю) немає. При прийомі монтелукасту у високих дозах (у 20 і 60 разів, що перевищують рекомендовані дози для дорослих), спостерігається зниження концентрації теофіліну в плазмі крові. При прийомі монтелукасту в дозах (10 мг 1 раз на добу) даного ефекту не спостерігається. ФармакодинамікаАнтагоніст лейкотрієнових рецепторів. Цистеїніл-лейкотрієни (LTC4, LTD4, LTE4) - сильні прозапальні ейкозаноїди, які вивільняються з різних клітин, включаючи огрядні клітини та еозинофіли. Ці важливі проастматичні медіатори зв'язуються з цистеїніл-лейкотрієновими рецепторами (CysLT), присутніми в дихальних шляхах людини та відповідають за реакцію бронхоспазму, виділення мокротиння, проникність судин та збільшення кількості еозинофілів. Монтелукаст - активна при пероральному прийомі з'єднання, яке має велику спорідненість і селективність до CysLT1-рецепторів. Монтелукаст у дозі менше 5 мг усуває бронхоспазм, індукований інгаляцією LTD4. Бронходилатируючий ефект спостерігається протягом 2 годин після перорального застосування. Бронходилатируючий ефект бета2-адреноміметиків посилюється при прийомі монтелукасту. Монтелукаст пригнічує як ранню, і пізню стадії бронхоспазму, викликаного впливом антигенів. Монтелукаст знижує кількість еозинофілів у периферичній крові у дорослих та дітей, а також значно знижує кількість еозинофілів у дихальних шляхах. У пацієнтів з підвищеною чутливістю до ацетилсаліцилової кислоти, які отримують інгаляційні та/або пероральні кортикостероїди, додавання до терапії монтелукасту забезпечує кращий контроль захворювання.Показання до застосуванняПрофілактика та тривале лікування бронхіальної астми, включаючи: попередження денних та нічних симптомів захворювання у дітей віком від 2 років і старше (для таблеток жувальних 4 мг та 5 мг) та у дорослих та підлітків з 15 років (для таблеток, покритих плівковою оболонкою, 10 мг); лікування бронхіальної астми у дітей віком від 6 років і старше (для таблеток жувальних 4 мг та 5 мг) та у дорослих та підлітків з 15 років (для таблеток, покритих плівковою оболонкою, 10 мг) з підвищеною чутливістю до ацетилсаліцилової кислоти; попередження бронхоспазму, викликаного фізичним навантаженням, у дітей віком від 2 років і старше (для таблеток жувальних 4 мг та 5 мг) та у дорослих та підлітків з 15 років (для таблеток, покритих плівковою оболонкою, 10 мг). Полегшення симптомів сезонного та цілорічного алергічного риніту у дітей віком від 2 років (для таблеток жувальних 4 мг та 5 мг) та у дорослих та підлітків з 15 років (для таблеток, покритих плівковою оболонкою, 10 мг).Протипоказання до застосуваннягіперчутливість до активної речовини або будь-якого допоміжного компонента препарату; дитячий вік до 2 років (для таблеток жувальних 4 мг); дитячий вік до 6 років (для пігулок жувальних 5 мг); дитячий вік до 15 років (для пігулок 10 мг); рідкі спадкові захворювання, такі як непереносимість галактози, недостатність лактази або глюкозо-галактозна мальабсорбція; фенілкетонурія (для пігулок жувальних), т.к. таблетки містять аспартам.Вагітність та лактаціяЗастосування препарату Алмонт при вагітності можливе, якщо передбачувана користь для матері перевищує потенційний ризик для плода. Рішення про скасування грудного вигодовування на період застосування препарату Алмонт приймається на підставі оцінки про ймовірну користь для матері та потенційного ризику для дитини. Протипоказано застосування препарату у дитячому віці до 2 років (для дозування 4 мг), дитячому віці до 6 років (для дозування 5 мг), дитячому та підлітковому віці до 15 років (для таблеток 10 мг).Побічна діяІнфекційні та паразитарні захворювання: інфекції верхніх дихальних шляхів. З боку системи крові та лімфатичної системи: підвищення схильності до кровотеч, тромбоцитопенії. З боку імунної системи: реакції гіперчутливості, у т.ч. анафілаксія, еозинофільна інфільтрація печінки З боку психіки: патологічні сновидіння (включаючи нічні кошмари), галюцинації, безсоння, сомнамбулізм, дратівливість, тривога, неспокій, ажитація (включаючи агресивну поведінку або ворожість), тремор, депресія, дезорієнтація, суїцидальні думки. З боку нервової системи: біль голови, запаморочення, сонливість, парестезія/гіпестезії, судоми. Серцево-судинна система: відчуття серцебиття. З боку дихальної системи: носова кровотеча. З боку шлунково-кишкового тракту: діарея, сухість у роті, диспепсія, нудота, блювання, біль у животі, панкреатит. З боку печінки та жовчовивідних шляхів: збільшення активності АЛТ та АСТ, гепатит (включаючи холестатичні, гепатоцелюлярні та змішані ураження печінки). З боку шкіри та підшкірних тканин: ангіоневротичний набряк, схильність до появи гематом, кропив'янка, свербіж шкіри, висипання, вузлувата еритема, багатоформна еритема. З боку кістково-м'язової системи: артралгія, міалгія, включаючи м'язові судоми. Інші: астенія/втома, нездужання, набряки, пірексія, спрага; у дуже поодиноких випадках під час лікування монтелукастом повідомлялося про розвиток синдрому Черджа-Стросса.Взаємодія з лікарськими засобамиУ пацієнтів, які одночасно отримували фенобарбітал, AUC монтелукасту зменшувалась приблизно на 40%, проте корекція режиму дозування у таких пацієнтів не потрібна. Оскільки монтелукаст метаболізується ізоферментом CYP3A4, слід бути обережним, особливо у дітей, якщо монтелукаст одночасно застосовується з індукторами ізоферменту CYP3A4, такими як фенітоїн, фенобарбітал і рифампіцин. Монтелукаст можна призначати разом з іншими лікарськими засобами, які традиційно застосовуються для профілактики та тривалого лікування бронхіальної астми та/або алергічного риніту. Монтелукаст у рекомендованій терапевтичній дозі не справляв клінічно значущого ефекту на фармакокінетику наступних препаратів: теофілін, преднізон, преднізолон, пероральні контрацептиви (етинілестрадіол/норетинодрел 35/1), терфенадин, дигоксин та варфарин. У дослідженнях in vitro встановлено, що монтелукаст є сильним інгібітором ізоферменту CYP2C8. Однак при дослідженні лікарської взаємодії in vivo монтелукасту та росиглітазону (маркерний субстрат, представник препаратів, що первинно метаболізуються ізоферментом CYP2C8) не отримано підтвердження інгібування монтелукастом ізоферменту CYP2C8. Таким чином, у клінічній практиці не передбачається впливу монтелукасту на CYP2С8-опосередкований метаболізм низки лікарських препаратів, у т.ч. паклітакселу, росиглітазону, репаглініду. Дослідження in vitro показали, що монтелукаст є субстратом ізоферменту CYP2C8 і меншою мірою ізоферментів CYP2C9 і CYP3А4. Дані клінічного дослідження лікарської взаємодії щодо монтелукасту та гемфіброзилу (інгібітора як CYP2C8, так і CYP2С9) демонструють, що гемфіброзил підвищує ефект системного впливу монтелукасту у 4.4 рази. Спільний прийом ітраконазолу, сильного інгібітора ізоферменту CYP3A4, разом з гемфіброзилом та монтелукастом не призводив до додаткового підвищення ефекту системного впливу монтелукасту. Вплив гемфіброзилу на системний вплив монтелукасту не може вважатися клінічно значущим на підставі даних безпеки при застосуванні в дозах, що перевищують схвалену дозу 10 мг для дорослих пацієнтів (наприклад,200 мг на добу для дорослих пацієнтів протягом 22 тижнів і до 900 мг на добу для пацієнтів, які приймають препарат протягом приблизно 1 тижня, не спостерігалося клінічно значущих негативних ефектів. Таким чином, при сумісному прийомі разом з гемфіброзилом корекції дози монтелукасту не потрібно. За результатами досліджень in vitro не передбачається клінічно значущої взаємодії з іншими відомими інгібіторами ізоферменту CYP2C8 (наприклад, з триметопримом). Крім того, спільний прийом монтелукасту з одним лише ітраконазолом не призводив до суттєвого підвищення ефекту системного впливу монтелукасту.при сумісному прийомі разом із гемфіброзилом корекції дози монтелукасту не потрібно. За результатами досліджень in vitro не передбачається клінічно значущої взаємодії з іншими відомими інгібіторами ізоферменту CYP2C8 (наприклад, з триметопримом). Крім того, спільний прийом монтелукасту з одним лише ітраконазолом не призводив до суттєвого підвищення ефекту системного впливу монтелукасту.при сумісному прийомі разом із гемфіброзилом корекції дози монтелукасту не потрібно. За результатами досліджень in vitro не передбачається клінічно значущої взаємодії з іншими відомими інгібіторами ізоферменту CYP2C8 (наприклад, з триметопримом). Крім того, спільний прийом монтелукасту з одним лише ітраконазолом не призводив до суттєвого підвищення ефекту системного впливу монтелукасту. Комбіноване лікування з бронходилататорами Препарат Алмонт є обґрунтованим доповненням монотерапії бронходилататорами, якщо останні не забезпечують адекватного контролю бронхіальної астми. Після досягнення терапевтичного ефекту від лікування препаратом Алмонт можна розпочати поступове зниження дози бронходилататорів. Комбіноване лікування з інгаляційними кортикостероїдами Лікування препаратом Алмонт забезпечує додатковий терапевтичний ефект пацієнтам, які застосовують інгаляційні кортикостероїди. Після досягнення стабілізації стану можна розпочати поступове зниження дози кортикостероїдів під наглядом лікаря. У деяких випадках допустима повна відміна інгаляційних кортикостероїдів, проте різка заміна інгаляційних кортикостероїдів на препарат Алмонт не рекомендується.Спосіб застосування та дозиПрепарат приймають внутрішньо. Жувальні таблетки приймають за 1 годину до або через 2 години після їди; таблетку слід розжувати. Таблетки, покриті плівковою оболонкою, приймають внутрішньо, незалежно від їди, не розжовуючи, запиваючи достатньою кількістю рідини. Дорослим та підліткам з 15 років призначають 10 мг (1 таблетка, покрита плівковою оболонкою) 1 раз на добу. При бронхіальній астмі або бронхіальній астмі та алергічному риніті дітям віком від 2 до 6 років призначають по 1 жувальній таблетці 4 мг 1 раз на добу ввечері; дітям віком від 6 до 14 років - по 1 жувальній таблетці 5 мг 1 раз на добу ввечері. При алергічному риніті дітям віком від 2 до 6 років призначають по 1 жувальній таблетці 4 мг 1 раз на добу, дітям віком від 6 до 14 років - по 1 жувальній таблетці 5 мг 1 раз на добу в індивідуальному режимі в залежності від часу найбільшого. Загострення симптомів. Не потрібна корекція дози всередині цих вікових груп. Прийом препарату дітьми здійснюється під наглядом дорослих. Терапевтичний ефект препарату Алмонт, що дозволяє контролювати симптоми астми, досягається протягом доби після прийому. Пацієнту рекомендується продовжувати прийом препарату як у періоди контрольованого перебігу бронхіальної астми, так і в період загострення бронхіальної астми. Пацієнтам з нирковою недостатністю та пацієнтам з печінковою недостатністю легкого та середнього ступеня тяжкості спеціального підбору дози не потрібно. Немає даних про застосування монтелукасту у пацієнтів із тяжкими порушеннями функції печінки. Пацієнтам похилого віку корекція дози не потрібна. Не потрібна корекція дози залежно від статі пацієнта.ПередозуванняСимптоми передозування препарату у пацієнтів з хронічною бронхіальною астмою при застосуванні в дозі, що перевищує 200 мг на добу, протягом 22 тижнів та дозі 900 мг на добу протягом 1 тижня, не виявлені. Є повідомлення про гостре передозування монтелукасту (при прийомі не менше 1 г на добу) у постмаркетинговому періоді та у клінічних дослідженнях у дорослих та дітей. Клінічні та лабораторні дані при цьому свідчать про відповідність профілю безпеки препарату у дітей, дорослих та пацієнтів похилого віку. Найчастішими симптомами були почуття спраги, сонливість, блювання, психомоторне збудження, біль голови і біль у животі. Лікування: проведення симптоматичної терапії. Дані щодо можливості виведення монтелукасту шляхом перитонеального діалізу або гемодіалізу відсутні.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаТаблетки жувальні з гравіюванням "М5" - 1 таб. Активні речовини: монтелукаст натрію – 5.2 мг (відповідає вмісту монтелукасту – 5 мг); Допоміжні речовини: манітол - 201.2 мг, целюлоза мікрокристалічна - 66 мг, гіпоролоза - 9 мг, кроскармелоза натрію - 9 мг, барвник Pigment Blend PB-24880 (лактози моногідрат - 4.5 мг, барвник заліза оксид мг червоний) магнію стеарат – 3 мг, аспартам – 1.5 мг, ароматизатор вишневий (Silarom Cherry Flavour 1219813182) – 0.1 мг. По 10 або 7 таблеток у Ал/Ал блістері. По 3 блістери (по 10 таблеток), по 4 або 14 блістерів (по 7 таблеток) у картонній пачці разом з інструкцією з медичного застосування.Опис лікарської формиПігулки жувальні круглі, двоопуклі, рожевого кольору з вкрапленнями і з гравіюванням "М5" на одній стороні.Фармакотерапевтична групаАнтагоніст лейкотрієнових рецепторів. Препарат для лікування бронхіальної астми та алергічного риніту.ФармакокінетикаВсмоктування Після вживання монтелукаст швидко і майже повністю всмоктується. У дорослих пацієнтів після прийому таблеток жувальних у дозі 5 мг натще Сmах у плазмі крові досягається через 2 год. Середнє значення біодоступності - 73%, ця величина знижується до 63% при прийомі монтелукасту з їжею. Після прийому таблеток жувальних у дозі 4 мг натщесерце у пацієнтів віком від 2 до 5 років Сmах досягається через 2 год. плівковою оболонкою, у дозі 10 мг. У дорослих пацієнтів після прийому натще таблеток, покритих плівковою оболонкою, у дозі 10 мг середнє значення Cmax у плазмі крові досягається через 3 год. Середнє значення біодоступності – 64%; при вживанні одночасно з їжею значення біодоступності та Cmax не порушуються. Розподіл Зв'язування монтелукасту з білками плазми становить понад 99%. Vd у рівноважному стані у середньому становить 8-11 л. Доклінічні дослідження виявили мінімальне проникнення монтелукасту через гематоенцефалічний бар'єр. Через 24 години після прийому концентрація монтелукасту мінімальна і в інших тканинах. Метаболізм Монтелукаст активно метаболізується у печінці. При застосуванні в терапевтичних дозах Css метаболітів монтелукасту в плазмі у дорослих та дітей не визначається. Дослідження in vitro показали, що в процесі метаболізму монтелукасту беруть участь ізоферменти цитохрому Р450 (3А4, 2А6 і 2С9), при цьому в терапевтичних концентраціях монтелукаст не пригнічує ізоферменти цитохрому Р450: 3А4,1С, 2С, 2С. Метаболіти мають незначний терапевтичний ефект монтелукасту. Виведення T1/2 монтелукасту у молодих здорових дорослих добровольців становить від 2.7 до 5.5 год. Плазмовий кліренс монтелукасту у здорових дорослих добровольців становить у середньому 45 мл/хв. Після перорального прийому монтелукасту 86% загальної кількості виводиться через кишечник протягом 5 днів та менше 0.2% - нирками, що поряд з даними про його біодоступність підтверджує виведення монтелукасту та його метаболітів переважно з жовчю. Фармакокінетика в особливих клінічних випадках Фармакокінетика монтелукасту у жінок та чоловіків однакова. У пацієнтів похилого віку або пацієнтів з печінковою недостатністю легкого та середнього ступеня тяжкості не потрібна корекція режиму дозування монтелукасту. Фармакокінетика монтелукасту у пацієнтів із нирковою недостатністю не оцінювалася. Оскільки монтелукаст та його метаболіти не виводяться нирками, корекції дози цієї категорії пацієнтів не потрібно. Даних про характер фармакокінетики монтелукасту у пацієнтів з тяжкими порушеннями функції печінки (більше 9 балів за шкалою Чайлд-П'ю) немає. При прийомі монтелукасту у високих дозах (у 20 і 60 разів, що перевищують рекомендовані дози для дорослих), спостерігається зниження концентрації теофіліну в плазмі крові. При прийомі монтелукасту в дозах (10 мг 1 раз на добу) даного ефекту не спостерігається. ФармакодинамікаАнтагоніст лейкотрієнових рецепторів. Цистеїніл-лейкотрієни (LTC4, LTD4, LTE4) - сильні прозапальні ейкозаноїди, які вивільняються з різних клітин, включаючи огрядні клітини та еозинофіли. Ці важливі проастматичні медіатори зв'язуються з цистеїніл-лейкотрієновими рецепторами (CysLT), присутніми в дихальних шляхах людини та відповідають за реакцію бронхоспазму, виділення мокротиння, проникність судин та збільшення кількості еозинофілів. Монтелукаст - активна при пероральному прийомі з'єднання, яке має велику спорідненість і селективність до CysLT1-рецепторів. Монтелукаст у дозі менше 5 мг усуває бронхоспазм, індукований інгаляцією LTD4. Бронходилатируючий ефект спостерігається протягом 2 годин після перорального застосування. Бронходилатируючий ефект бета2-адреноміметиків посилюється при прийомі монтелукасту. Монтелукаст пригнічує як ранню, і пізню стадії бронхоспазму, викликаного впливом антигенів. Монтелукаст знижує кількість еозинофілів у периферичній крові у дорослих та дітей, а також значно знижує кількість еозинофілів у дихальних шляхах. У пацієнтів з підвищеною чутливістю до ацетилсаліцилової кислоти, які отримують інгаляційні та/або пероральні кортикостероїди, додавання до терапії монтелукасту забезпечує кращий контроль захворювання.Показання до застосуванняПрофілактика та тривале лікування бронхіальної астми, включаючи: попередження денних та нічних симптомів захворювання у дітей віком від 2 років і старше (для таблеток жувальних 4 мг та 5 мг) та у дорослих та підлітків з 15 років (для таблеток, покритих плівковою оболонкою, 10 мг); лікування бронхіальної астми у дітей віком від 6 років і старше (для таблеток жувальних 4 мг та 5 мг) та у дорослих та підлітків з 15 років (для таблеток, покритих плівковою оболонкою, 10 мг) з підвищеною чутливістю до ацетилсаліцилової кислоти; попередження бронхоспазму, викликаного фізичним навантаженням, у дітей віком від 2 років і старше (для таблеток жувальних 4 мг та 5 мг) та у дорослих та підлітків з 15 років (для таблеток, покритих плівковою оболонкою, 10 мг). Полегшення симптомів сезонного та цілорічного алергічного риніту у дітей віком від 2 років (для таблеток жувальних 4 мг та 5 мг) та у дорослих та підлітків з 15 років (для таблеток, покритих плівковою оболонкою, 10 мг).Протипоказання до застосуваннягіперчутливість до активної речовини або будь-якого допоміжного компонента препарату; дитячий вік до 2 років (для таблеток жувальних 4 мг); дитячий вік до 6 років (для пігулок жувальних 5 мг); дитячий вік до 15 років (для пігулок 10 мг); рідкі спадкові захворювання, такі як непереносимість галактози, недостатність лактази або глюкозо-галактозна мальабсорбція; фенілкетонурія (для пігулок жувальних), т.к. таблетки містять аспартам.Вагітність та лактаціяЗастосування препарату Алмонт при вагітності можливе, якщо передбачувана користь для матері перевищує потенційний ризик для плода. Рішення про скасування грудного вигодовування на період застосування препарату Алмонт приймається на підставі оцінки про ймовірну користь для матері та потенційного ризику для дитини. Протипоказано застосування препарату у дитячому віці до 2 років (для дозування 4 мг), дитячому віці до 6 років (для дозування 5 мг), дитячому та підлітковому віці до 15 років (для таблеток 10 мг).Побічна діяІнфекційні та паразитарні захворювання: інфекції верхніх дихальних шляхів. З боку системи крові та лімфатичної системи: підвищення схильності до кровотеч, тромбоцитопенії. З боку імунної системи: реакції гіперчутливості, у т.ч. анафілаксія, еозинофільна інфільтрація печінки З боку психіки: патологічні сновидіння (включаючи нічні кошмари), галюцинації, безсоння, сомнамбулізм, дратівливість, тривога, неспокій, ажитація (включаючи агресивну поведінку або ворожість), тремор, депресія, дезорієнтація, суїцидальні думки. З боку нервової системи: біль голови, запаморочення, сонливість, парестезія/гіпестезії, судоми. Серцево-судинна система: відчуття серцебиття. З боку дихальної системи: носова кровотеча. З боку шлунково-кишкового тракту: діарея, сухість у роті, диспепсія, нудота, блювання, біль у животі, панкреатит. З боку печінки та жовчовивідних шляхів: збільшення активності АЛТ та АСТ, гепатит (включаючи холестатичні, гепатоцелюлярні та змішані ураження печінки). З боку шкіри та підшкірних тканин: ангіоневротичний набряк, схильність до появи гематом, кропив'янка, свербіж шкіри, висипання, вузлувата еритема, багатоформна еритема. З боку кістково-м'язової системи: артралгія, міалгія, включаючи м'язові судоми. Інші: астенія/втома, нездужання, набряки, пірексія, спрага; у дуже поодиноких випадках під час лікування монтелукастом повідомлялося про розвиток синдрому Черджа-Стросса.Взаємодія з лікарськими засобамиУ пацієнтів, які одночасно отримували фенобарбітал, AUC монтелукасту зменшувалась приблизно на 40%, проте корекція режиму дозування у таких пацієнтів не потрібна. Оскільки монтелукаст метаболізується ізоферментом CYP3A4, слід бути обережним, особливо у дітей, якщо монтелукаст одночасно застосовується з індукторами ізоферменту CYP3A4, такими як фенітоїн, фенобарбітал і рифампіцин. Монтелукаст можна призначати разом з іншими лікарськими засобами, які традиційно застосовуються для профілактики та тривалого лікування бронхіальної астми та/або алергічного риніту. Монтелукаст у рекомендованій терапевтичній дозі не справляв клінічно значущого ефекту на фармакокінетику наступних препаратів: теофілін, преднізон, преднізолон, пероральні контрацептиви (етинілестрадіол/норетинодрел 35/1), терфенадин, дигоксин та варфарин. У дослідженнях in vitro встановлено, що монтелукаст є сильним інгібітором ізоферменту CYP2C8. Однак при дослідженні лікарської взаємодії in vivo монтелукасту та росиглітазону (маркерний субстрат, представник препаратів, що первинно метаболізуються ізоферментом CYP2C8) не отримано підтвердження інгібування монтелукастом ізоферменту CYP2C8. Таким чином, у клінічній практиці не передбачається впливу монтелукасту на CYP2С8-опосередкований метаболізм низки лікарських препаратів, у т.ч. паклітакселу, росиглітазону, репаглініду. Дослідження in vitro показали, що монтелукаст є субстратом ізоферменту CYP2C8 і меншою мірою ізоферментів CYP2C9 і CYP3А4. Дані клінічного дослідження лікарської взаємодії щодо монтелукасту та гемфіброзилу (інгібітора як CYP2C8, так і CYP2С9) демонструють, що гемфіброзил підвищує ефект системного впливу монтелукасту у 4.4 рази. Спільний прийом ітраконазолу, сильного інгібітора ізоферменту CYP3A4, разом з гемфіброзилом та монтелукастом не призводив до додаткового підвищення ефекту системного впливу монтелукасту. Вплив гемфіброзилу на системний вплив монтелукасту не може вважатися клінічно значущим на підставі даних безпеки при застосуванні в дозах, що перевищують схвалену дозу 10 мг для дорослих пацієнтів (наприклад,200 мг на добу для дорослих пацієнтів протягом 22 тижнів і до 900 мг на добу для пацієнтів, які приймають препарат протягом приблизно 1 тижня, не спостерігалося клінічно значущих негативних ефектів. Таким чином, при сумісному прийомі разом з гемфіброзилом корекції дози монтелукасту не потрібно. За результатами досліджень in vitro не передбачається клінічно значущої взаємодії з іншими відомими інгібіторами ізоферменту CYP2C8 (наприклад, з триметопримом). Крім того, спільний прийом монтелукасту з одним лише ітраконазолом не призводив до суттєвого підвищення ефекту системного впливу монтелукасту.при сумісному прийомі разом із гемфіброзилом корекції дози монтелукасту не потрібно. За результатами досліджень in vitro не передбачається клінічно значущої взаємодії з іншими відомими інгібіторами ізоферменту CYP2C8 (наприклад, з триметопримом). Крім того, спільний прийом монтелукасту з одним лише ітраконазолом не призводив до суттєвого підвищення ефекту системного впливу монтелукасту.при сумісному прийомі разом із гемфіброзилом корекції дози монтелукасту не потрібно. За результатами досліджень in vitro не передбачається клінічно значущої взаємодії з іншими відомими інгібіторами ізоферменту CYP2C8 (наприклад, з триметопримом). Крім того, спільний прийом монтелукасту з одним лише ітраконазолом не призводив до суттєвого підвищення ефекту системного впливу монтелукасту. Комбіноване лікування з бронходилататорами Препарат Алмонт є обґрунтованим доповненням монотерапії бронходилататорами, якщо останні не забезпечують адекватного контролю бронхіальної астми. Після досягнення терапевтичного ефекту від лікування препаратом Алмонт можна розпочати поступове зниження дози бронходилататорів. Комбіноване лікування з інгаляційними кортикостероїдами Лікування препаратом Алмонт забезпечує додатковий терапевтичний ефект пацієнтам, які застосовують інгаляційні кортикостероїди. Після досягнення стабілізації стану можна розпочати поступове зниження дози кортикостероїдів під наглядом лікаря. У деяких випадках допустима повна відміна інгаляційних кортикостероїдів, проте різка заміна інгаляційних кортикостероїдів на препарат Алмонт не рекомендується.Спосіб застосування та дозиПрепарат приймають внутрішньо. Жувальні таблетки приймають за 1 годину до або через 2 години після їди; таблетку слід розжувати. Таблетки, покриті плівковою оболонкою, приймають внутрішньо, незалежно від їди, не розжовуючи, запиваючи достатньою кількістю рідини. Дорослим та підліткам з 15 років призначають 10 мг (1 таблетка, покрита плівковою оболонкою) 1 раз на добу. При бронхіальній астмі або бронхіальній астмі та алергічному риніті дітям віком від 2 до 6 років призначають по 1 жувальній таблетці 4 мг 1 раз на добу ввечері; дітям віком від 6 до 14 років - по 1 жувальній таблетці 5 мг 1 раз на добу ввечері. При алергічному риніті дітям віком від 2 до 6 років призначають по 1 жувальній таблетці 4 мг 1 раз на добу, дітям віком від 6 до 14 років - по 1 жувальній таблетці 5 мг 1 раз на добу в індивідуальному режимі в залежності від часу найбільшого. Загострення симптомів. Не потрібна корекція дози всередині цих вікових груп. Прийом препарату дітьми здійснюється під наглядом дорослих. Терапевтичний ефект препарату Алмонт, що дозволяє контролювати симптоми астми, досягається протягом доби після прийому. Пацієнту рекомендується продовжувати прийом препарату як у періоди контрольованого перебігу бронхіальної астми, так і в період загострення бронхіальної астми. Пацієнтам з нирковою недостатністю та пацієнтам з печінковою недостатністю легкого та середнього ступеня тяжкості спеціального підбору дози не потрібно. Немає даних про застосування монтелукасту у пацієнтів із тяжкими порушеннями функції печінки. Пацієнтам похилого віку корекція дози не потрібна. Не потрібна корекція дози залежно від статі пацієнта.ПередозуванняСимптоми передозування препарату у пацієнтів з хронічною бронхіальною астмою при застосуванні в дозі, що перевищує 200 мг на добу, протягом 22 тижнів та дозі 900 мг на добу протягом 1 тижня, не виявлені. Є повідомлення про гостре передозування монтелукасту (при прийомі не менше 1 г на добу) у постмаркетинговому періоді та у клінічних дослідженнях у дорослих та дітей. Клінічні та лабораторні дані при цьому свідчать про відповідність профілю безпеки препарату у дітей, дорослих та пацієнтів похилого віку. Найчастішими симптомами були почуття спраги, сонливість, блювання, психомоторне збудження, біль голови і біль у животі. Лікування: проведення симптоматичної терапії. Дані щодо можливості виведення монтелукасту шляхом перитонеального діалізу або гемодіалізу відсутні.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему