Иммунитет
1 179,00 грн
617,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
1 650,00 грн
1 605,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
956,00 грн
917,00 грн
Дозування: 40 мг/мл Фасування: N28 Форма випуску: р-р д/інфузій Упакування: фл. Производитель: Дальхимфарм ОАО Завод-производитель: Дальхимфарм ОАО(Россия) Действующее вещество: Натрия гидрокарбонат. .
189,00 грн
149,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
179,00 грн
151,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
Дозування: 0. 9% Фасування: N1 Форма випуску: р-р д/інфузій Упакування: упак. Діюча речовина: Натрію хлорид.
869,00 грн
820,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
199,00 грн
155,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
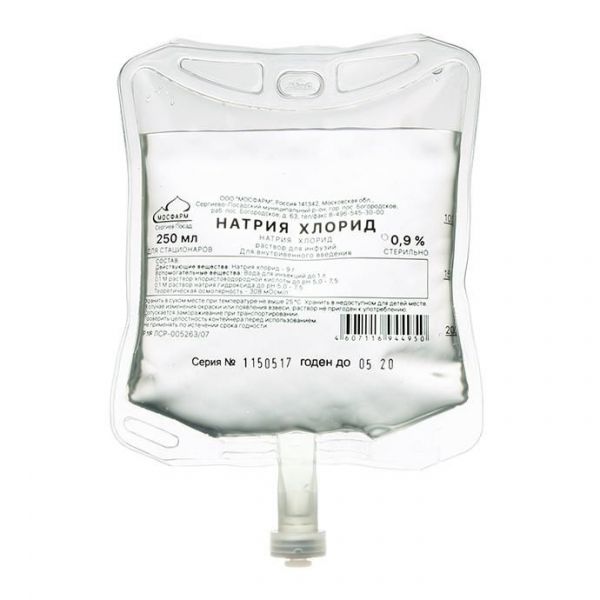
Дозування: 0. 9% Фасування: N28 Форма випуску: р-р д/інфузій Упаковка: фл. Производитель: Мосфарм ООО Завод-производитель: Мосфарм ООО(Россия) Действующее вещество: Натрия хлорид.
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
Дозування: 0. 9% Фасування: N1 Форма випуску: р-р д/інфузій Упакування: фл. Виробник: Мосфарм ТОВ Завод-виробник: Мосфарм ТОВ(Росія) Діюча речовина: Натрію хлорид.
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
Фасування: N28 Форма выпуска: р-р д/инфузий Упаковка: контейнер полимерный Производитель: Мосфарм ООО Завод-производитель: Мосфарм ООО(Россия) Действующее вещество: Натрия хлорид. . .