Все товары
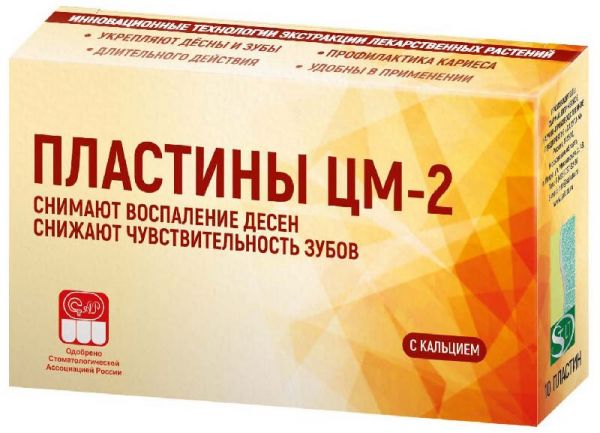
Склад, форма випуску та упаковкаСкладаються з водорозчинних екстрактів лікарських трав (звіробою, шавлії, деревію), вітамінів (С, групи В), мінеральних речовин (калію, натрію, кальцію, магнію, заліза, цинку та ін). Основу пластин складає желатин.ХарактеристикаВбивають анаеробні мікроорганізми (замість антибіотиків). Відновлює мікроорганізми умовної нормофлори у ротоносоглотці (замість пробіотиків). Швидко та високоефективно (протягом 5-7 днів регулярного застосування) знімає ознаки запалення – кровоточивість, набряклість, почервоніння, біль та ін. (замість протизапальних засобів). Виражено підвищує місцевий імунітет (секреторний імуноглобулін А, лізоцим, систему комплементу) замість імуностимуляторів. Зміцнює судини (замість судинозміцнюючих засобів). Відновлює кровообіг у яснах, особливо у перші 20 хвилин застосування; усувають застійні явища та знижують тромбоутворення; (замість засобів, що покращують мікроциркуляцію). Відновлюють обмін речовин та ферментів у ротовій порожнині (замість засобів, що відновлюють обмінні ферментативні процеси). Мають виражені антиоксидантні властивості (замість антиоксидантів). Відновлюють сполучнотканинні структури ясен і зміцнюють зуби (замість препаратів, що відновлюють сполучнотканину структуру ясен).ІнструкціяПластину накладають на зовнішню поверхню ясен, через губу фіксують руками до повного прилипання (5-10 секунд). Мовою відокремлюють пластину від губи. Перед застосуванням видалити слину! Краще прополоскати Тонзиналом чи водою! Пластина розсмоктується 2-3 години, залишки можна видалити.Показання до застосуванняПри гінгівіті, пародонтиті, пародонтозі та при всіх запальних захворюваннях та проявах у яснах, після зняття зубного каміння та відвідування стоматолога для усунення неминучих мікротравм ясен.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаСкладаються з водорозчинних екстрактів лікарських трав (звіробою, шавлії, деревію), вітамінів (С, групи В), мінеральних речовин (калію, натрію, кальцію, магнію, заліза, цинку та ін). Основу пластин складає желатин.ХарактеристикаВбивають анаеробні мікроорганізми (замість антибіотиків). Відновлює мікроорганізми умовної нормофлори у ротоносоглотці (замість пробіотиків). Швидко та високоефективно (протягом 5-7 днів регулярного застосування) знімає ознаки запалення – кровоточивість, набряклість, почервоніння, біль та ін. (замість протизапальних засобів). Виражено підвищує місцевий імунітет (секреторний імуноглобулін А, лізоцим, систему комплементу) замість імуностимуляторів. Зміцнює судини (замість судинозміцнюючих засобів). Відновлює кровообіг у яснах, особливо у перші 20 хвилин застосування; усувають застійні явища та знижують тромбоутворення; (замість засобів, що покращують мікроциркуляцію). Відновлюють обмін речовин та ферментів у ротовій порожнині (замість засобів, що відновлюють обмінні ферментативні процеси). Мають виражені антиоксидантні властивості (замість антиоксидантів). Відновлюють сполучнотканинні структури ясен і зміцнюють зуби (замість препаратів, що відновлюють сполучнотканину структуру ясен).ІнструкціяПластини ЦМ-2 з кальцієм рекомендується накладати на ясна і частково (2-5 мм) на зуби, т.к. Кальцій всмоктується через емаль зуба. Одна пластина довго надає активне лікування безпосередньо в осередку запалення понад 6 годин!Показання до застосуванняЗастосовують при карієсі (особливо на початку захворювання, коли емаль ціла, але порушений мінеральний обмін), гіперестезії (гіперчутливості зубів), при порушенні емалі та кісткових тканин.Умови відпустки з аптекБез рецептаВідео на цю тему
ХарактеристикаЗастосовується для фіксації захисних пов'язок, тампонів, зондів, катетерів; добре пропускає повітря; гіпоалергенний поліакрилатний клей – безболісне видалення; рекомендується для дітей та людей з особливо чутливою шкірою; можливість розриву пластиру без використання ножиць.Умови відпустки з аптекБез рецептаВідео на цю тему
205,00 грн
182,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
205,00 грн
158,00 грн
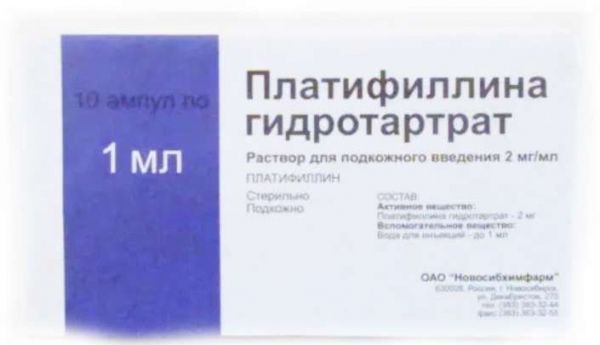
Склад, форма випуску та упаковкаРозчин - 1 мл: Активна речовина: платифіліну гідротартрат – 2 мг; допоміжна речовина: вода для ін'єкцій до 1 мл. Розчин для підшкірного введення 2 мг/мл. По 1 мл у ампули нейтрального скла. По 10 ампул з інструкцією із застосування і ножем для розтину ампул або ампульним скарифікатором поміщають в коробку з картону. По 5 або 10 ампул поміщають в контурну осередкову упаковку з полівінілхлоридної плівки або стрічки поліетилентерефталатної і фольги алюмінієвої або паперу з поліетиленовим покриттям або без фольги, або без паперу. По 1 або 2 контурні коміркові упаковки з інструкцією по застосуванню і ножем, для розтину ампул або ампульним скарифікатором поміщають в пачку з картону. При упаковці ампул з кільцем зламу або точкою надлому ніж для розтину ампул або ампульний скарифікатор не вкладають.Опис лікарської формиПрозора безбарвна рідина.Фармакотерапевтична групаСпазмолітик з міотропною та м-холіноблокуючою дією.ФармакокінетикаЛегко проходить через гістогематичні бар'єри (включаючи гематоенцефалічний бар'єр), клітинні та синаптичні мембрани. При введенні високих доз накопичується в центральній нервовій системі у значних концентраціях. Метаболізується у печінці. Піддається гідролізу з утворенням платинецьину та платінецинової кислоти. Виводиться нирками та кишечником. Чи не кумулює.ФармакодинамікаМ-холіноблокатор, порівняно з атропіном, має менший вплив на периферичні м-холінорецептори (по дії на гладком'язові клітини органів шлунково-кишкового тракту (ШКТ) та циркулярного м'яза райдужної оболонки в 5-10 разів слабші за атропін). Блокуючи м-холінорецептори, порушує передачу нервових імпульсів з постгангліонарних холінергічних нервів на іннервовані ними ефекторні органи та тканини (серце, гладком'язові органи, залози зовнішньої секреції); пригнічує також н-холінорецептори (значно слабші). Холіноблокуюча дія більшою мірою проявляється на тлі підвищеного тонусу парасимпатичної частини вегетативної нервової системи або дії м-холіностимуляторів. У меншій мірі, ніж атропін, викликає тахікардію, особливо при застосуванні у великих дозах. Зменшуючи вплив n.vagus, покращує провідність серця, збільшує збудливість міокарда, збільшує хвилинний об'єм крові. Має пряму міотропну спазмолітичну дію, викликає розширення дрібних судин шкіри. У високих дозах пригнічує судинно-руховий центр і блокує симпатичні ганглії, внаслідок чого розширюються судини і знижується артеріальний тиск (головним чином при внутрішньовенному введенні). Слабше атропіну пригнічує секрецію залоз внутрішньої секреції. Викликає виражене зниження тонусу гладких м'язів; амплітуди та частоти перистальтичних скорочень шлунка, дванадцятипалої кишки, тонкої та товстої кишки, помірне зниження тонусу жовчного міхура (у осіб з гіперкінезією жовчовивідних шляхів); при гіпокінезії – тонус жовчного міхура підвищується до нормального вмісту. Викликає розслаблення гладкої мускулатури матки, сечового міхура та сечовивідних шляхів, виявляючи спазмолітичну дію, усуває больовий синдром. Розслаблює гладку мускулатуру бронхів, спричинену підвищенням тонусу n.vagus або холіностимуляторами, збільшує хвилинний об'єм дихання, пригнічує секрецію бронхіальних залоз; знижує тонус сфінктерів. При закапуванні в кон'юнктивальний мішок ока і парентеральному введенні викликає розширення зіниці (внаслідок розслаблення кругового м'яза райдужної оболонки. Одночасно підвищується внутрішньоочний тиск і настає параліч акомодації (розслаблення війного м'яза циліарного тіла). Порушує головний мозок та дихальний центр, переважно – спинний мозок (у високих дозах можливі судоми, пригнічення центральної нервової системи (ЦНС), судиннорухового та дихального центрів). Проникає крізь гематоенцефалічний бар'єр.Показання до застосуванняВиразкова хвороба шлунка та дванадцятипалої кишки (у складі комбінованої терапії), пілороспазм, холецистит, холелітіаз, кишкова, ниркова та жовчна кольки.Протипоказання до застосуванняПідвищена індивідуальна чутливість, вагітність, лактація. З обережністю Захворювання серцево-судинної системи, при яких збільшення частоти серцевих скорочень (ЧСС) може бути небажаним: миготлива аритмія, тахікардія, хронічна серцева недостатність, ішемічна хвороба серця, мітральний стеноз, артеріальна гіпертензія, гостра кровотеча. Гіпертиреоз (можливе посилення тахікардії). Підвищена температура тіла (може ще підвищуватись внаслідок придушення активності сальних залоз). Рефлюкс-езофагіт, грижа стравохідного отвору діафрагми, що поєднується з рефлюкс-езофагітом (зниження моторики, стравоходу та шлунка та розслаблення нижнього стравохідного сфінктера можуть сприяти уповільненню у випорожнення шлунка та посиленню гастроезофагеального рефлюксу). Захворювання шлунково-кишкового тракту, що супроводжуються непрохідністю: ахалазія і стеноз воротаря (можливе зниження моторики і тонусу, що призводить до непрохідності та затримки вмісту шлунка). Атонія кишечника у хворих похилого віку або ослаблених хворих (можливий розвиток непрохідності), паралітична кишкова непрохідність. Захворювання з підвищеним внутрішньоочним тиском: закритокутова глаукома (мідріатичний ефект, що призводить до підвищення внутрішньоочного тиску, може викликати гострий напад), відкритокутова глаукома (мідріатичний ефект може викликати деяке підвищення внутрішньоочного тиску, може знадобитися корекція терапії), вік старше 4 недіагностованої глаукоми). Неспецифічний виразковий коліт (високі дози можуть пригнічувати перистальтику кишечника, підвищуючи ймовірність паралітичної непрохідності кишечника, крім того, можливий прояв або загострення такого ускладнення, як токсичний мегаколон). Сухість слизової оболонки порожнини рота (тривале застосування може викликати подальше посилення виразності ксеростомії). Печінкова недостатність (зниження метаболізму) та ниркова недостатність (ризик розвитку побічних ефектів-внаслідок зниження виведення). Хронічні захворювання легень, особливо у дітей молодшого віку та ослаблених хворих (зменшення бронхіальної секреції може призводити до згущення секрету та утворення пробок у бронхах). Міастенія (стан, може, погіршується через інгібування ацетилхоліну). Вегетативна (автономна) невропатія (затримка сечі і параліч акомодації можуть посилюватися), гіперплазія передміхурової залози без обструкції сечовивідних шляхів, затримка сечі або схильність до неї, або захворювання, що супроводжуються обструкцією сечовивідних шляхів (в т.ч. ). Гестоз (можливе посилення артеріальної гіпертензії). Пошкодження мозку в дітей віком (ефекти з боку центральної нервової системи можуть посилюватися). Хвороба Дауна (можливо незвичайне: розширення зіниць та підвищення частоти серцевих скорочень). Центральний параліч у дітей (реакція на холіноблокатори може бути найбільш виражена).Вагітність та лактаціяЗастосування під час вагітності протипоказане. При необхідності застосування препарату в період лактації на час лікування слід припинити вигодовування груддю.Побічна діяСухість слизової оболонки ротової порожнини, спрага, зниження артеріального тиску, тахікардія, мідріаз, параліч акомодації, атонія кишечника, запаморочення, головний біль, фотофобія, судома, затримка сечі; гострий психоз (у високих дозах), ателектаз легені.Взаємодія з лікарськими засобамиПідсилює седативну та снодійну дію фенобарбіталу, пентобарбіталу, магнію сульфату. Інші м-холіноблокатори, амантадин, галоперидол, фенотіазин, інгібітори моноаміноксидази, трициклічні антидепресанти, деякі антигістамінні препарати підвищують ризик розвитку побічних ефектів. Антагонізм з інгібіторами холінестерази. Морфін посилює пригнічуючу дію на серцево-судинну систему, інгібітори моноаміноксидази - позитивний хроно- та батмотропний ефекти; серцеві глікозиди – позитивна батмотропна дія; хінідин, прокаїнамід - м-холіноблокуюча дія. При болях, пов'язаних із спазмами гладкої мускулатури, дію посилюють анальгетики, седативні засоби, транквілізатори; при судинних спазмах - гіпотензивні та седативні засоби.Спосіб застосування та дозиПідшкірно дорослим і дітям старше, 14 років. купірування спастичних болів - 1-2 мл 0,2% розчину 1-2 рази на добу. Діти: новонароджені та грудні - 0,035 мг/кг (0,0175 мл/кг), 1-5 років - 0,03 мг/кг (0,015 мл/кг), 6-10 років - 6,025 мг/кг (0,0125) мл/кг), 11-14 років – 0,02 мг/кг (0,01 мл/кг).ПередозуванняСимптоми: паралітична кишкова непрохідність, гостра затримка сечі (у хворих на аденому передміхурової залози), параліч акомодації, підвищення внутрішньоочного тиску; сухість слизової оболонки порожнини рота, носа, горла, утруднення ковтання, мови, мідріаз (до повного зникнення райдужної оболонки), тремор, судоми, гіпертермія, збудження, пригнічення центральної нервової системи, придушення активності дихального та судинно-рухового центрів. Лікування: форсований діурез; парентеральне введення м-холіноміметиків та інгібіторів холінестерази. При гіпертермії – вологі обтирання, жарознижувальні засоби, при збудженні – внутрішньовенне введення тіопенталу натрію; при мідріазі – місцево, у вигляді очних крапель пілокарпін. У разі розвитку нападу глаукоми негайно в кон'юнктивальний мішок закопують 1% розчин пілокарпіну через кожну годину по 2 краплі та підшкірно – 1 мл 0,05 % розчину Прозерину (неостигміну метил сульфату) 3-4 рази на добу.Запобіжні заходи та особливі вказівкиПід час лікування необхідно здійснювати регулярний контроль артеріального тиску та пульсу. У період лікування слід уникати вживання алкогольних напоїв. Вплив на здатність до керування автотранспортом та управління механізмами Необхідно утримуватися від керування транспортними засобами та занять іншими потенційно небезпечними видами діяльності, що потребують підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Дозировка: 5 мг Фасовка: N10 Форма выпуска: таб. Действующее вещество: Платифиллин. .
7 843,00 грн
163,00 грн
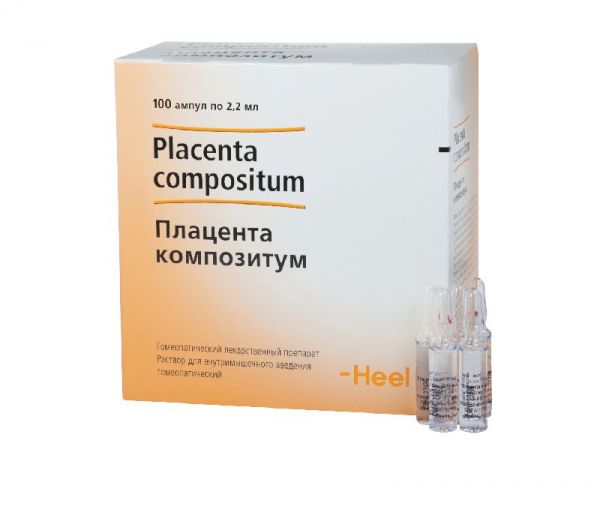
Склад, форма випуску та упаковка(на одну ампулу 2,2 мл (=2,2 г)): Активні компоненти: Placenta suis (плацента суїс) D6 22 мкл, Embryo suis (ембріо суїс) D8 22 мкл, Vena suis (вена суїс) D8 22 мкл, Arteria suis (артерія суіс) D10 22 мкл, Funiculus umbilicalis suis (фунікулюс умбілікаліс суіс) D10 22 мкл, Hypophysis suis (гіпофізис суіс) D10 22 мкл, Secale cornutum (секалі корнутум) D4 22 мкл мкл, Nicotiana tabacum (нікотиана табакум) D10 22 мкл, Strophanthus gratus (строфантус гратус) D6 22 мкл, Aesculus hippocastanum (ескулюс гіппокаштанум) D4 22 мкл, Melilotus officinalis (мелілотус офricum2 мкл, Natrium pyruvicum (натріум пірувікум) D8 22 мкл, Barium carbonicum (баріум карбонікум) D13 22 мкл, Plumbum jodatum (плюмбум йодатум) D18 22 мкл,Vipera berus (віпера берус) D10 22 мкл; Solanum nigrum (солянум нігрум) D6 22 мкл; Допоміжні речовини: вода для ін'єкцій 1804 мг, хлорид натрію для встановлення ізотонії.Опис лікарської формиБезбарвна прозора рідина без запаху.Фармакотерапевтична групаБагатокомпонентний гомеопатичний препарат, дія якого зумовлена компонентами, що входять до його складу.Показання до застосуванняУ комплексній терапії атеросклерозу судин головного мозку, дисциркуляторної енцефалопатії.Протипоказання до застосуванняПідвищена чутливість до компонентів препарату, захворювання щитовидної залози. Вік до 18 років у зв'язку з недостатністю клінічних даних.Вагітність та лактаціяЗастосування препарату можливе, якщо очікувана користь для матері перевищує потенційний ризик для плода та дитини. Потрібна консультація лікаря.Побічна діяМожливі алергічні реакції.Взаємодія з лікарськими засобамиПризначення комплексних гомеопатичних препаратів не виключає використання інших лікарських засобів, які застосовуються при цьому захворюванні.Спосіб застосування та дозиКратність та тривалість введення препарату встановлюється лікарем індивідуально або по 2,2 мл (вміст 1 ампули) внутрішньом'язово через день. Середній курс лікування становить 3 тижні. Проведення повторного курсу можливе після консультації з лікарем.ПередозуванняВипадки передозування досі не були зареєстровані.Запобіжні заходи та особливі вказівкиПри прийомі гомеопатичних лікарських засобів можуть тимчасово загострюватись наявні симптоми (первинне погіршення). У цьому випадку слід припинити прийом препарату та проконсультуватися з лікарем. З появою побічних ефектів слід звернутися до лікаря.Умови відпустки з аптекЗа рецептомВідео на цю тему
492,00 грн
164,00 грн
Склад, форма випуску та упаковка(на одну ампулу 2,2 мл (=2,2 г)): Активні компоненти: Placenta suis (плацента суїс) D6 22 мкл, Embryo suis (ембріо суїс) D8 22 мкл, Vena suis (вена суїс) D8 22 мкл, Arteria suis (артерія суіс) D10 22 мкл, Funiculus umbilicalis suis (фунікулюс умбілікаліс суіс) D10 22 мкл, Hypophysis suis (гіпофізис суіс) D10 22 мкл, Secale cornutum (секалі корнутум) D4 22 мкл мкл, Nicotiana tabacum (нікотиана табакум) D10 22 мкл, Strophanthus gratus (строфантус гратус) D6 22 мкл, Aesculus hippocastanum (ескулюс гіппокаштанум) D4 22 мкл, Melilotus officinalis (мелілотус офricum2 мкл, Natrium pyruvicum (натріум пірувікум) D8 22 мкл, Barium carbonicum (баріум карбонікум) D13 22 мкл, Plumbum jodatum (плюмбум йодатум) D18 22 мкл,Vipera berus (віпера берус) D10 22 мкл; Solanum nigrum (солянум нігрум) D6 22 мкл; Допоміжні речовини: вода для ін'єкцій 1804 мг, хлорид натрію для встановлення ізотонії.Опис лікарської формиБезбарвна прозора рідина без запаху.Фармакотерапевтична групаБагатокомпонентний гомеопатичний препарат, дія якого зумовлена компонентами, що входять до його складу.Показання до застосуванняУ комплексній терапії атеросклерозу судин головного мозку, дисциркуляторної енцефалопатії.Протипоказання до застосуванняПідвищена чутливість до компонентів препарату, захворювання щитовидної залози. Вік до 18 років у зв'язку з недостатністю клінічних даних.Вагітність та лактаціяЗастосування препарату можливе, якщо очікувана користь для матері перевищує потенційний ризик для плода та дитини. Потрібна консультація лікаря.Побічна діяМожливі алергічні реакції.Взаємодія з лікарськими засобамиПризначення комплексних гомеопатичних препаратів не виключає використання інших лікарських засобів, які застосовуються при цьому захворюванні.Спосіб застосування та дозиКратність та тривалість введення препарату встановлюється лікарем індивідуально або по 2,2 мл (вміст 1 ампули) внутрішньом'язово через день. Середній курс лікування становить 3 тижні. Проведення повторного курсу можливе після консультації з лікарем.ПередозуванняВипадки передозування досі не були зареєстровані.Запобіжні заходи та особливі вказівкиПри прийомі гомеопатичних лікарських засобів можуть тимчасово загострюватись наявні симптоми (первинне погіршення). У цьому випадку слід припинити прийом препарату та проконсультуватися з лікарем. З появою побічних ефектів слід звернутися до лікаря.Умови відпустки з аптекЗа рецептомВідео на цю тему
1 150,00 грн
164,00 грн
Склад, форма випуску та упаковкаПігулки - 1 таб. діюча речовина: клопідогрел гідросульфат у формі II - 391,5 мг (у перерахунку на клопідогрел - 300,0 мг); допоміжні речовини: ядро таблетки: манітол; макрогол-6000; целюлоза мікрокристалічна (з низьким вмістом води, 90 мкм); гіпозолоза низькозаміщена; рицинова олія гідрогенізована; плівкова оболонка: опадрай рожевий (лактози моногідрат, гіпромелозу, титану діоксид (Е 171), тріацетин, барвник заліза оксид червоний (Е 172)), карнаубський віск. По 10 таблеток у блістер із фольги алюмінієвої/ фольги алюмінієвої. По 1 або 3 блістери разом з інструкцією із застосування в картонну пачку.Опис лікарської формиДовгасті пігулки, покриті плівковою оболонкою рожевого кольору, з гравіюванням "300" на одній стороні та "1332" на іншій стороні.Фармакотерапевтична групаАнтиагрегантний засіб.ФармакокінетикаВсмоктування При одноразовому та повторному прийомі внутрішньо у дозі 75 мг на добу клопідогрел швидко всмоктується. Середнє значення максимальної концентрації (Сmax) незміненого клопідогрелу в плазмі крові (приблизно 2,2-2,5 нг/мл після прийому внутрішньо разової дози 75 мг) досягається приблизно через 45 хв після прийому препарату. За даними екскреції метаболітів клопідогрелу через нирки його абсорбція становить приблизно 50%. Розподіл In vitro клопідогрел і його основний циркулюючий у крові неактивний метаболіт оборотно зв'язуються з білками плазми крові (на 98% і 94%, відповідно), і цей зв'язок є ненасиченим до концентрації 100 мг/мл. Метаболізм Клопідогрел інтенсивно метаболізується у печінці. In vitro та in vivo клопідогрел метаболізується двома шляхами: перший здійснюється за допомогою естераз і призводить до гідролізу клопідогрелу з утворенням неактивного похідного карбоксильної кислоти (85 % від циркулюючих метаболітів); другий шлях здійснюється за допомогою ізоферментів цитохром Р450. Спочатку клопідогрел метаболізується до 2-оксо-клопідогрелу, що є проміжним метаболітом. Подальший метаболізм 2-оксо-клопідогрелу призводить до утворення активного метаболіту клопідогрелу - тіольного похідного клопідогрелу. In vitro цей активний метаболіт утворюється головним чином за допомогою ізоферменту CYP2C19. але в його освіті також беруть участь деякі інші ізоферменти, включаючи CYP1A2, CYP2B6 та CYP3A4. Активний тіольний метаболіт клопідогрелу, виділений у in vitro дослідженнях, швидко та незворотно зв'язується з рецепторами тромбоцитів, блокуючи таким чином агрегацію тромбоцитів. Смах активного метаболіту клопідогрелу після одноразового прийому його навантажувальної дози 300 мг у 2 рази перевищує таку після 4-х днів прийому підтримуючої дози клопідогрелу 75 мг. Сmax досягається приблизно 30-60 хв. Виведення Протягом 120 годин після прийому внутрішньо людиною 14С-міченого клопідогрелу близько 50% радіоактивності виводиться через нирки та приблизно 46% радіоактивності виводиться через кишечник. Після одноразового прийому внутрішньо дозування в 75 мг період напіввиведення (Т1/2) клопідогрелу становить приблизно 6 годин. Фармакогенетика За допомогою ізоферменту CYP2C19 утворюються як активний метаболіт, так і проміжний метаболіт - 2-оксо-клопідогрел. Фармакокінетика та антиагрегантна дія активного метаболіту клопідогрелу, при дослідженні агрегації тромбоцитів ex vivo, варіюють залежно від генотипу ізоферменту CYP2C19. Алель гена CYP2CI9*1 відповідає повністю функціональному метаболізму, тоді як алелі генів CYP2C19*2 та CYP2C19*3 є нефункціональними. Алелі генів CYP2C19*2 та CYP2C 19*3 є причиною зниження метаболізму у більшості представників європеоїдної (85%) та монголоїдної раси (99%). Інші алелі, з якими пов'язана відсутність або зниження метаболізму, зустрічаються рідше і включають, але не обмежуються алелями генів CYP2C19*4, *5, *6, *7 і *8.Пацієнти з низькою активністю ізоферменту CYP2CI9 повинні мати дві зазначені вище алелі гена з втратою функції. Опубліковані частоти фенотипів пацієнтів з низькою активністю ізоферменту CYP2C19 у пацієнтів європеоїдної раси становлять 2%, у пацієнтів негроїдної раси - 4% і у монголоїдної раси - 14%. Існують спеціальні тести для визначення наявного у пацієнта генотипу ізоферменту CYP2C19. За даними перехресного дослідження (40 добровольців) за участю добровольців з дуже високою, високою, проміжною та низькою активністю ізоферменту CYP2C19, будь-яких суттєвих відмінностей в експозиції активного метаболіту та у середніх значеннях інгібування агрегації тромбоцитів (ІАТ), індукованої АД дуже високою, високою та проміжною активністю ізоферменту CYP2C19 виявлено не було. У добровольців із низькою активністю ізоферменту CYP2C19 експозиція активного метаболіту знижувалась на 63-71 % порівняно з добровольцями з високою активністю ізоферменту CYP2C19. При використанні схеми лікування 300 мг навантажувальна доза/75 мг підтримуюча доза (300 мг/75 мг) у добровольців з низькою активністю ізоферменту CYP2C19 антитромбоцитарна дія знижувалась із середніми значеннями ІАТ,складовими 24% (через 24 год) та 37% (на 5 день дослідження) порівняно з ІАТ, складовими 39% (через 24 год) та 58% (на 5 день дослідження), у добровольців з високою активністю ізоферменту CYP2C19 та 37% (через 24 год) та 60% (на 5 день дослідження) у добровольців із проміжною активністю ізоферменту CYP2C19. Коли добровольці з низькою активністю ізоферменту CYP2C19 отримували препарат за схемою лікування 600 мг навантажувальна доза/150 мг підтримуюча доза (600 мг/150 мг), експозиція активного метаболіту була вищою, ніж при прийомі за схемою лікування 300 мг/75 мг. Крім цього, ІАТ становило 32% (через 24 год) і 61% (на 5 день дослідження), що було більше такого у добровольців з низькою активністю ізоферменту CYP2C19, які отримували лікування за схемою 300 мг/75 мг, і було подібно до такого в групах пацієнтів з більш високою інтенсивністю CYP2C 19 метаболізму. одержували лікування за схемою 300 мг/75 мг. Однак у дослідженнях з урахуванням клінічних результатів режим дозування клопідогрелу для пацієнтів цієї групи (пацієнтів з низькою активністю ізоферменту CYP2C19) наразі не встановлено. Аналогічно результатам даного дослідження мета-аналіз шести досліджень, до якого увійшли дані 335 добровольців, які отримували клопідогрел і перебували в стані досягнення рівноважної концентрації, показав, що в порівнянні з добровольцями з високою активністю ізоферменту CYP2C19, у добровольців з проміжною активністю ізоферменту CYP2C знижувалася на 28%, а у добровольців з низькою активністю ізоферменту CYP2C19 - на 72%, тоді як ІАТ було знижено з відмінностями в ІАТ на 5,9% та 21,4% відповідно. Не проводилося оцінки впливу генотипу CYP2CI9 на клінічні результати у пацієнтів, які отримували клопідогрел, у проспективних рандомізованих контрольованих дослідженнях. Проте зараз є кілька ретроспективних аналізів. Результати генотипування отримані в ході наступних клінічних досліджень: CURE, CHARISMA, CLARITY-TIM1 28, TRITON-TIMI 38 та ACT1VE-A, а також у кількох опублікованих когортних дослідженнях. У дослідженні TRITON-TIMI 38 та 3-х когортних дослідженнях (Collet, Sibbing, Giusti) пацієнти комбінованої групи з проміжною або низькою активністю ізоферменту CYP2C19 мали більш високу частоту серцево-судинних ускладнень (смерть, інфаркт міокарда та інсульт). з такими у пацієнтів із високою активністю ізоферменту CYP2C19. У дослідженні CHARISMA та одному когортному дослідженні (Simon) збільшення частоти серцево-судинних ускладнень спостерігалося тільки у пацієнтів з низькою активністю ізоферменту CYP2C19 (при їх порівнянні з пацієнтами з високою активністю ізоферменту CYP2C19). Дослідження CURE, CLARITY. ACTIVE- і одному з когортних досліджень (Trenk), не спостерігалося збільшення частоти серцево-судинних ускладнень в залежності від інтенсивності CYP2C 19- метаболізму. Особливі групи пацієнтів Фармакокінетика активного метаболіту клопідогрелу в спеціальних групах пацієнтів не вивчалася. Пацієнти старші 75 років: у добровольців старше 75 років при порівнянні з молодими добровольцями не було отримано відмінностей за показниками агрегації тромбоцитів та часу кровотечі. Корекція дози не потрібна. Дитячий вік до 18 років: клінічні дані відсутні. Пацієнти з порушенням функції нирок Після повторних прийомів клопідогрелу в дозі 75 мг/добу у пацієнтів з тяжкими порушеннями функції нирок (кліренс креатиніну (КК) від 5 мл/хв до 15 мл/хв) інгібування АДФ-індукованої агрегації тромбоцитів було нижчим (на 25 %) порівняно з таким у здорових добровольців, проте подовження часу кровотечі було подібним до такого у здорових добровольців, які отримували клопідогрел у дозуванні 75 мг на добу. Пацієнти з порушенням функції печінки Не було значних відмінностей у ступені інгібування АДФ-індукованої агрегації тромбоцитів після щоденного прийому клопідогрелу у добовій дозі 75 мг протягом 10 днів у пацієнтів з тяжкими порушеннями функції печінки порівняно зі здоровими добровольцями. Середній час кровотечі також можна порівняти в обох групах. Расова приналежність Поширеність алелей генів ізоферменту CYP2C19, що зумовлюють проміжну та низьку активність цього ізоферменту, відрізняється у представників різних расових груп. Є обмежені літературні дані про їх поширеність у представників монголоїдної раси, що не дозволяє оцінити значення генотипування ізоферменту CYP2C19 для розвитку ішемічних ускладнень.ФармакодинамікаКлопідогрел є проліком, один з активних метаболітів якого є інгібітором агрегації тромбоцитів. Для утворення активного метаболіту, який пригнічує агрегацію тромбоцитів, клопідогрел повинен метаболізуватися за допомогою ізоферментів системи цитохрому Р450 (CYP450). Активний метаболіт клопідогрелу селективно інгібує зв'язування аденозиндифосфату (АДФ) з P2Yi2 рецептором тромбоцитів та подальшу АДФ-опосередковану активацію комплексу GPIIb/IIIa, що призводить до придушення агрегації тромбоцитів. Завдяки необоротному зв'язуванню, тромбоцити залишаються несприйнятливими до стимуляції АДФ протягом всього терміну свого життя (приблизно 7-10 днів), а відновлення нормальної функції тромбоцитів відбувається зі швидкістю, що відповідає швидкості оновлення тромбоцитів. Агрегація тромбоцитів, спричинена агоністами, відмінними від АДФ. також інгібується за рахунок блокади посиленої активації тромбоцитів АДФ, що вивільняється. Оскільки утворення активного метаболіту відбувається за допомогою ізоферментів системи цитохрому Р450, деякі з яких можуть відрізнятися поліморфізмом або інгібуватися іншими препаратами, не у всіх пацієнтів можливе адекватне пригнічення агрегації тромбоцитів. При щоденному прийомі клопідогрелу в дозі 75 мг з першого ж дня прийому відзначається значне пригнічення АДФ-індукованої агрегації тромбоцитів, яке поступово збільшується протягом 3-7 днів і потім виходить на постійний рівень (при досягненні рівноважного стану). У рівноважному стані агрегація тромбоцитів пригнічується загалом на 40-60 %. Після припинення прийому клопідогрелу агрегація тромбоцитів та час кровотечі поступово повертаються до початкового рівня, в середньому, протягом 5 днів. У ході клінічного дослідження ACTIVE-А показано, що у пацієнтів з фібриляцією передсердь, які мали щонайменше. один фактор ризику розвитку судинних ускладнень, але були нездатні приймати непрямі антикоагулянти, клопідогрел у поєднанні з ацетилсаліциловою кислотою (АСК) (у порівнянні з прийомом тільки однієї АСК) зменшував частоту разом узятих інсульту, інфаркту міокарда, системної тромбоемболії поза центральною або судинної смерті, переважно за рахунок зменшення ризику розвитку інсульту. Ефективність прийому клопідогрелу у поєднанні з АСК виявлялася рано і зберігалася до 5 років. Зменшення ризику великих судинних ускладнень у групі пацієнтів, які приймали клопідогрел у поєднанні з АСК, спостерігалося переважно за рахунок більшого зменшення частоти інсультів. Ризик розвитку інсульту будь-якої тяжкості при прийомі клопідогрелу у поєднанні з АСК знижувався, а також спостерігалася тенденція до зниження частоти розвитку інфаркту міокарда в групі, яка отримувала лікування клопідогрелом у поєднанні з АСК, але не спостерігалося відмінностей у частоті тромбоемболій поза ЦНС або судинної смерті. Крім цього, прийом клопідогрелу у поєднанні з АСК зменшував загальну кількість днів госпіталізації з серцево-судинних причин. Перехід з терапії потужним інгібітором рецепторів P2Y12 на лікування клопідогрелом у поєднанні з АСК після завершення гострої фази гострого інфаркту міокарда (ГІМ) вивчався у двох рандомізованих ініційованих дослідником клінічних дослідженнях (TOPIC та TROPICAL-ACS). У рандомізованому відкритому клінічному дослідженні TOPIC брали участь пацієнти, які перенесли ГІМ, яким виконувалось черезшкірне коронарне втручання (ЧКВ). Пацієнти, які отримували АСК та один з найбільш потужних інгібіторів рецепторів P2Y12, у яких не розвинулися несприятливі події протягом одного місяця, або були переведені на терапію фіксованою комбінацією АСК та клопідогрелу (деескалація подвійної антитромбоцитарної терапії (ДАТ)) або продовжили приймати Постійна ДАТ). Події, включені в комбіновану первинну кінцеву точку (смерть від ускладнень серцево-судинних захворювань (ССЗ), інсульт, екстрена реваскуляризація та кровотечі типу 2 або тяжкі кровотечі за шкалою BARC (Дослідницького академічного консорціуму за кровотечами)), через один були зареєстровані у 43 з 322 пацієнтів (13,4%) у групі деескалації ДАТ та 85 пацієнтів з 323 (26,3 %) у групі незмінної ДАТ (р Статистично значуща відмінність в основному зумовлена скороченням кількості випадків кровотечі, у тому числі кровотеч, які за шкалою BARC більш або рівні 2 (4% у групі деескалації та 14,9% у групі, що отримувала незмінену ДАТ), при цьому не спостерігалося істотних відмінностей у частоті ішемічних ускладнень (р = 0,36). До рандомізованого відкритого клінічного дослідження TROPICAL-ACS було включено 2610 пацієнтів з ГІМ. підтвердженим аналізом на біомаркери після проведення ЧКВ. Пацієнти були рандомізовані до груп для отримання прасугрелу (дні 0-14) або прасугрелу (дні 0-7), а потім клопідогрелу (дні 8-14) у комбінації з АСК. На 14-й день було проведено оцінку функції тромбоцитів. Пацієнти з першої групи терапії лише прасугрелом продовжували приймати прасугрел протягом 11,5 місяці. У пацієнтів із групи заміни терапії було виконано аналіз на високу реактивність тромбоцитів (ДРТ). Пацієнти з ДРТ ≥ 46 одиниць були переведені на терапію прасугрелом, яку отримували протягом 11,5 місяця. Пацієнти з ДРТПоказання до застосуванняВторинна профілактика атеротромботичних ускладнень: У дорослих пацієнтів після нещодавно перенесеного інфаркту міокарда (з давністю від декількох днів до 35 днів), нещодавно перенесеного ішемічного інсульту (з давністю від 7 днів до 6 місяців) або при діагностованій оклюзійній хворобі периферичних артерій прийом клопідогрелу знижував частоту комбінованої ішемічний інсульт (з летальними наслідками або без нього), повторний інфаркт міокарда (з летальними наслідками або без нього) та іншу серцево-судинну смерть. У дорослих пацієнтів із гострим коронарним синдромом: гострий коронарний синдром без підйому сегмента ST (нестабільна стенокардія/інфаркт міокарда без зубця Q), включаючи пацієнтів, які повинні отримувати медикаментозне лікування, та пацієнтів, яким показано черезшкірне коронарне втручання (зі стенуванням або без стентування) або аортокоронарне шунтування (АКШ). Прийом клопідогрелу знижував частоту комбінованої кінцевої точки, що включала серцево-судинну смерть, інфаркт міокарда або інсульт, а також частоту комбінованої кінцевої точки, що включала серцево-судинну смерть, інфаркт міокарда, інсульт, рефрактерну ішемію. гострий інфаркт міокарда із підйомом сегмента ST. Прийом клопідогрелу знижував смертність від будь-яких причин, а також частоту комбінованої кінцевої точки, що включала смерть, повторний інфаркт міокарда або інсульт. Профілактика атеротромботичних та тромбоемболічних ускладнень у дорослих пацієнтів з фібриляцією передсердь (миготливою аритмією) Показано, що у пацієнтів з фібриляцією передсердь з підвищеним ризиком судинних ускладнень терапія непрямими антикоагулянтами, які є антагоністами вітаміну К (АВК), пов'язана з більшою клінічною користю порівняно із застосуванням тільки АСК або комбінації клопідогрелу з АСК щодо зниження. Пацієнтам з фібриляцією передсердь (миготливою аритмією), що мають, як мінімум, один фактор ризику розвитку судинних ускладнень, які не можуть приймати АВК (наприклад, за наявного особливого ризику кровотечі, нездатності пацієнта, на думку лікаря, адекватно контролювати МНО (міжнародне нормалізоване) ставлення) або у разі неприйняття пацієнтом лікування АВК), для запобігання атеротромботичних та тромбоемболічних ускладнень. включаючи інсульт, показаний прийом клопідогрелу в комбінації з АСК. Показано, що клопідогрел у комбінації з АСК знижував частоту комбінованої кінцевої точки, що включала інсульт, інфаркт міокарда, системну тромбоемболію поза ЦНС або серцево-судинну смерть, переважно за рахунок зниження частоти розвитку інсульту.Протипоказання до застосуванняПідвищена чутливість до клопідогрелу або будь-якої з допоміжних речовин препарату. Тяжка печінкова недостатність. Гостра кровотеча, наприклад, кровотеча з виразки або внутрішньочерепний крововилив. Рідкісна спадкова непереносимість галактози, дефіцит лактази та глюкозо-галактозна мальабсорбція. Вагітність та період грудного вигодовування. Дитячий вік до 18 років (безпека та ефективність застосування не встановлені). З обережністю: При помірній печінковій недостатності, при якій можлива схильність до кровотечі (обмежений клінічний досвід застосування). При нирковій недостатності (обмежений клінічний досвід застосування). При захворюваннях, при яких є схильність до розвитку кровотеч (зокрема шлунково-кишкових або внутрішньоочних), і, особливо, при одночасному застосуванні лікарських засобів, які можуть спричинити ушкодження слизової оболонки шлунково-кишкового тракту (таких як АСК та нестероїдні протизапальні препарати ( НПЗП)). У пацієнтів, у яких є підвищений ризик розвитку кровотечі: через травму, хірургічне втручання або інші патологічні стани, а також у пацієнтів, які отримують лікування АСК, гепарином, варфарином, інгібіторами глікопротеїну IIb/IIIa, НПЗЗ, у тому числі селективними інгібіторами. -2 (ЦОГ-2), а також іншими лікарськими засобами, застосування яких пов'язане з ризиком кровотеч, селективними інгібіторами зворотного захоплення серотоніну (СІОЗС). При одночасному застосуванні з лікарськими засобами, що є субстратами ізоферменту CYP2C8 (репаглінід, паклітаксел). У пацієнтів із низькою активністю ізоферменту CYP2C19. При вказівках в анамнезені алергічні та гематологічні реакції на інші тієнопіридини (такі як тіклопідін, прасугрел). При нещодавно перенесеному минущому порушенні мозкового кровообігу або ішемічному інсульті.Вагітність та лактаціяВагітність Дослідження на тваринах не виявили ні прямих, ні непрямих несприятливих ефектів протягом вагітності, ембріональний розвиток, пологи та постнатальний розвиток. Так як не завжди за результатами досліджень на тваринах можна передбачити реакцію у людини, і внаслідок відсутності даних контрольованих клінічних досліджень щодо прийому клопідогрелу вагітними жінками, як запобіжний засіб не рекомендується прийом клопідогрелу під час вагітності, за винятком тих випадків, коли, на думку лікаря , Його застосування настійно необхідне. Період грудного вигодовування У дослідженнях на щурах показано, що клопідогрел та/або його метаболіти виділяються з грудним молоком. Невідомо, чи виділяється клопідогрел із грудним молоком людини. Так як багато лікарських засобів виділяються з грудним молоком і існує ризик розвитку потенційних несприятливих явищ у дитини, яка перебуває на грудному вигодовуванні, слід прийняти рішення про припинення грудного вигодовування або про відміну препарату з урахуванням необхідності його застосування для матері.Побічна діяДані, отримані під час клінічних досліджень Безпека клопідогрелу вивчена більш ніж у 44 000 пацієнтів, у тому числі більш ніж у 12 000 пацієнтів, які отримували лікування протягом року або більше. Загалом переносимість клопідогрелу в дозі 75 мг/добу у дослідженні CAPRIE відповідала переносимості АСК у дозі 325 мг/добу, незалежно від віку, статі та расової належності пацієнтів. Нижче наведено клінічно значущі небажані явища, що спостерігалися у п'яти великих клінічних дослідженнях: CAPRIE, CURE, CLARITY, COMMIT та ACTIVE-A. Кровотечі та крововиливу Порівняння монотерапії клопідогрелом та АСК У клінічному дослідженні CAPRIE загальна частота всіх кровотеч у пацієнтів, які приймали клопідогрел, та у пацієнтів, які приймали АСК, склала 9,3%. Частота важких кровотеч при застосуванні клопідогрелу та АСК була порівнянною: 1,4 % та 1,6 % відповідно. Загалом частота розвитку шлунково-кишкових кровотеч у пацієнтів, які приймали клопідогрел, та у пацієнтів, які приймали АСК, становила 2.0 % та 2,7 %, відповідно, у тому числі частота шлунково-кишкових кровотеч, які потребували госпіталізації, становила 0,7 % та 1,1% відповідно. Загальна частота кровотеч іншої локалізації при прийомі клопідогрелу порівняно з прийомом АСК була вищою (7,3% проти 6,5%, відповідно). Однак частота важких кровотеч при застосуванні клопідогрелу та АСК була порівнянною (0,6% або 0,4% відповідно). Найчастіше повідомлялося про розвиток наступних кровотеч: пурпура / синці, носова кровотеча. Рідше повідомлялося про розвиток гематом, гематурії та очних крововиливів (головним чином, кон'юнктивальних). Частота внутрішньочерепних крововиливів при застосуванні клопідогрелу та АСК була порівнянною (0,4 % або 0,5 % відповідно). Порівняння комбінованої терапії клопідогрел+АСК та плацебо+АСК У клінічному дослідженні CURE у пацієнтів, які приймали клопідогрел+АСК, у порівнянні з пацієнтами, які приймали плацебо+АСК, спостерігалося збільшення частоти розвитку великих кровотеч (3,7 % порівняно 2,7 %), та малих кровотеч (5,1 % за порівняно 2.4%). В основному, джерелами великих кровотеч були шлунково-кишковий тракт (ШКТ) та місця пункції артерій. Частота розвитку загрозливих для життя кровотеч у пацієнтів, які приймали клопідогрел+АСК у порівнянні з пацієнтами, які приймали плацебо+АСК, достовірно не відрізнялася (2,2 % та 1,8 %, відповідно), частота розвитку фатальних кровотеч була однаковою (0.2 % при обох види терапії). Частота виникнення не загрожують життю великих кровотеч була достовірно вищою у пацієнтів, які приймали клопідогрел+АСК, порівняно з пацієнтами, які приймали плацебо+АСК (1,6 % та 1 %, відповідно), але частота розвитку внутрішньочерепних крововиливів була однаковою (0,1 % за обох видів терапії). Частота розвитку великих кровотеч у групі клопідогрел+АСК залежала від дози АСК (< 100 мг: 2,6%; 100-200 мг: 3,5 %; > 200 мг: 4,9 %), а також частота розвитку великих кровотеч у групі плацебо+АСК (< 100 мг: 2,0%; 100-200 мг: 2,3%; > 200 мг: 4,0%). У пацієнтів, які припинили антитромбоцитарну терапію більш ніж за 5 днів до аортокоронарного шунтування, не відзначалося почастішання випадків розвитку великих кровотеч протягом 7 днів після втручання (4,4% у групі клопідогрел+АСК та 5,3% у групі плацебо+АСК). У пацієнтів, які продовжували антитромбоцитарну терапію протягом останніх п'яти днів перед аортокоронарним шунтуванням, частота цих подій після втручання становила 9,6% (у групі клопідогрел+АСК) та 6,3% (у групі плацебо+АСК). У клінічному дослідженні CLARITY частота великих кровотеч (визначуваних як внутрішньочерепні кровотечі або кровотечі зі зниженням гемоглобіну > 5 г/дл) в обох групах (клопідогрел+АСК і плацебо+АСК) була порівнянною в обох групах лікування (1,3 % проти 1, 1% у групі клопідогрел+АСК та групі плацебо+АСК, відповідно). Вона була однаковою у підгрупах пацієнтів, розділених за вихідними характеристиками та за видами фібринолітичної терапії або гепаринотерапії. Частота виникнення фатальних кровотеч (0.8% проти 0,6%) та внутрішньочерепних крововиливів (0,5% проти 0,7%) при лікуванні клопідогрел+АСК та плацебо+АСК, відповідно, була низькою та порівнянною в обох групах лікування. У клінічному дослідженні COMMIT загальна частота нецеребральних великих кровотеч або церебральних кровотеч була низькою та однаковою (0,6% у групі клопідогрел+АСК та 0,5% у групі плацебо+АСК). У клінічному дослідженні ACTIVE-A частота розвитку великих кровотеч у групі клопідогрел+АСК була вищою, ніж у групі плацебо+АСК (6,7 % проти 4,3 % відповідно). Великі кровотечі переважно були позачерепними в обох групах (5,3% проти 3,5%), головним чином, із шлунково-кишкового тракту (3,5% проти 1,8%). У групі клопідогрел+АСК внутрішньочерепних крововиливів було більше порівняно з групою плацебо+АСК (1,4% проти 0.8%, відповідно). Відсутні статистично значущі відмінності між цими групами лікування у частоті виникнення фатальних кровотеч (1,1% проти 0,7%) та геморагічного інсульту (0,8% проти 0.6%). Порушення з боку крові У дослідженні CAPRIE, тяжка нейтропенія ( У двох із 9599 пацієнтів, які приймали клопідогрел, спостерігалася повна відсутність нейтрофілів у периферичній крові, якого не спостерігалося в жодного з 9586 пацієнтів, які приймали АСК. Незважаючи на те, що ризик розвитку мієлотоксичної дії при прийомі клопідогрелу є досить низьким, якщо у пацієнта, який приймає клопідогрел, спостерігається підвищення температури або з'являються інші ознаки інфекції. слід обстежити пацієнта щодо можливої нейтропенії. При лікуванні клопідогрелом в одному випадку спостерігався розвиток апластичної анемії. Частота виникнення тяжкої тромбоцитопенії ( У дослідженнях CURE та CLARITY спостерігалася порівнянна кількість пацієнтів із тромбоцитопенією або нейтропенією в обох групах лікування. Інші клінічно значущі небажані реакції, що спостерігалися під час проведення клінічних досліджень CAPRIE, CURE, CLARITY COMMIT та ACTIVE-A Частота виникнення небажаних реакцій визначалася відповідно до класифікації Всесвітньої Організації Охорони Здоров'я: дуже часто (≥ 1/10); часто (≥ 1/100 та < 1/10); нечасто (≥ 1/1000 та < 1/100); рідко (≥ 1/10000 та < 1/1000); дуже рідко (< 1/10000), частота невідома (не може бути підрахована на підставі наявних даних). Порушення з боку нервової системи: нечасто – головний біль, запаморочення, парестезія; рідко – вертиго. Порушення з боку шлунково-кишкового тракту: часто – диспепсія, абдомінальні болі, діарея; нечасто - нудота, гастрит, здуття живота, запор, блювання, виразка шлунка, виразка дванадцятипалої кишки. Порушення з боку шкіри та підшкірних тканин: нечасто – шкірний висип, свербіж шкіри. Порушення з боку крові та лімфатичної системи: нечасто – збільшення часу кровотечі, зниження кількості тромбоцитів у периферичній крові; лейкопенія, зниження кількості нейтрофілів у периферичній крові, еозинофілія. Постмаркетинговий досвід застосування препарату Порушення з боку крові та лімфатичної системи: частота невідома - випадки серйозних кровотеч, переважно підшкірних, скелетно-м'язових, очних крововиливів (кон'юнктивальних, в тканині та сітківку ока), кровотеч з дихальних шляхів (кровохаркання, легеневі кровотечі) кровотеч із післяопераційних ран та випадки кровотеч із летальним результатом (особливо внутрішньочерепних крововиливів, шлунково-кишкових кровотеч та заочеревинних крововиливів); агранулоцитозу, гранулоцитопенії, апластичної анемії/панцитопенії, тромботичної тромбоцитопенічної пурпури (ТТП), придбаної гемофілії А. Порушення з боку серця: частота невідома – синдром Коунісу (вазоспастична алергічна стенокардія/алергічний інфаркт міокарда), зумовлений реакцією гіперчутливості на клопідогрел. Порушення з боку імунної системи: частота невідома – анафілактоїдні реакції, сироваткова хвороба; перехресні алергічні та гематологічні реакції з іншими тієнопіридинами (такими як тіклопідин, прасугрел), аутоімунний інсуліновий синдром (може призводити до серйозної гіпоглікемії, особливо у пацієнтів з MLA DRA4 серотипом). Порушення психіки: частота невідома – сплутаність свідомості, галюцинації. Порушення з боку нервової системи: частота невідома – порушення смакового сприйняття, агевзія. Порушення з боку судин: частота невідома – васкуліт, зниження артеріального тиску. Порушення з боку дихальної системи, органів грудної клітки та середостіння: частота невідома – бронхоспазм, інтерстиційна пневмонія, еозинофільна пневмонія. Порушення з боку шлунково-кишкового тракту: частота невідома – коліт (зокрема виразковий коліт або лімфоцитарний коліт), панкреатит, стоматит. Порушення з боку печінки та жовчовивідних шляхів: частота невідома – гепатит (неінфекційний), гостра печінкова недостатність. Порушення з боку шкіри та підшкірних тканин: частота невідома - макульозно-папульозний еритематозний або ексфоліативний висип, кропив'янка, свербіж шкіри, ангіоневротичний набряк, бульозний дерматит (багатоформна еритема, синдром Стівенса-Джонсона, токсичний ендоз гіперчутливості, лікарський висип з еозинофілією та системними проявами (DRESS-синдром), екзема, плоский лишай. Порушення з боку скелетно-м'язової та сполучної тканини: частота невідома – артралгія (біль у суглобах), артрит, міалгія. Порушення з боку нирок та сечовивідних шляхів: частота невідома – гломерулонефрит. Порушення з боку статевих органів та молочної залози: частота невідома – гінекомастія. Загальні розлади та порушення у місці введення: частота невідома – лихоманка. Лабораторні та інструментальні дані: частота невідома – відхилення від норми лабораторних показників функціонального стану печінки, підвищення концентрації креатиніну в крові.Взаємодія з лікарськими засобамиЛікарські засоби, застосування яких пов'язане із ризиком розвитку кровотечі Є підвищений ризик розвитку кровотечі внаслідок їхнього потенційного адитивного ефекту з клопідогрелом. Лікування слід проводити з обережністю. Тромболітики Безпека одночасного застосування клопідогрелу, фібрин-специфічних або фібрин-неспецифічних тромболітичних засобів та гепарину була вивчена у пацієнтів з гострим інфарктом міокарда. Частота клінічно значущих кровотеч була аналогічна тій, що спостерігалася у разі спільного застосування тромболітичних засобів та гепарину з АСК. Блокатори глікопротеїну IIb/III У зв'язку з можливістю фармакодинамічної взаємодії між клопідогрелом та блокаторами глікопротеїну IIb/IIIа, їх одночасне застосування потребує обережності, особливо у пацієнтів, які мають підвищений ризик розвитку кровотечі (при травмах та хірургічних втручаннях або інших патологічних станах). Ін'єкційні антикоагулянти (наприклад, гепарин) За даними клінічного дослідження, проведеного за участю здорових добровольців, при прийомі клопідогрелу не потрібно зміни дози гепарину і не змінювалася його антикоагулянтна дія. Одночасне застосування гепарину не змінювало антиагрегантної дії клопідогрелу. Між клопідогрелом та гепарином можлива фармакодинамічна взаємодія, яка може збільшувати ризик розвитку кровотеч. При одночасному застосуванні слід бути обережними. Пероральні антикоагулянти (наприклад, варфарин) Хоча прийом клопідогрелу 75 мг/добу не змінював фармакокінетику варфарину (субстрату ізоферменту CYP2C9) або МНО у пацієнтів, які тривало одержують лікування варфарином, одночасний прийом клопідогрелу збільшує ризик кровотечі у зв'язку з його незалежним додатковим впливом на згортання. Тому слід дотримуватися обережності при одночасному прийомі варфарину та клопідогрелу. Ацетилсаліцилова кислота (АСК) АСК не змінює інгібуючого АДФ-індуковану агрегацію тромбоцитів ефекту клопідогрелу, але клопідогрел потенціює вплив АСК на колаген-індуковану агрегацію тромбоцитів. Тим не менш, одночасний з клопідогрелом прийом АСК по 500 мг 2 рази на день протягом однієї доби не викликав суттєвого збільшення часу кровотечі, що викликається прийомом клопідогрелу. Оскільки між клопідогрелом і АСК можлива фармакодинамічна взаємодія, що призводить до підвищення ризику кровотечі, тому при їх одночасному застосуванні слід бути обережним. Тим не менш, у клінічних дослідженнях пацієнти отримували комбіновану терапію клопідогрелом та АСК (75-325 мг один раз на добу) до одного року. Нестероїдні протизапальні препарати (НПЗЗ) У клінічному дослідженні, проведеному за участю здорових добровольців, спільне застосування клопідогрелу та напроксену збільшувало приховані втрати крові через ШКТ. Однак, у зв'язку з відсутністю досліджень щодо взаємодії клопідогрелу з іншими НПЗП, наразі не відомо. є підвищений ризик шлунково-кишкових кровотеч при прийомі клопідогрелу разом з іншими нестероїдними протизапальними засобами. Тому при одночасному застосуванні нестероїдних протизапальних засобів, у тому числі інгібіторів ЦОГ-2 з клопідогрелом. слід дотримуватися обережності. Селективні інгібітори зворотного захоплення серотоніну (СІЗЗС) Оскільки СІЗЗЗ порушують активацію тромбоцитів та збільшують ризик розвитку кровотечі. При одночасному застосуванні слід бути обережними. Індуктори ізоферменту CYP2C19 Оскільки клопідогрел метаболізується до свого активного метаболіту частково за допомогою ізоферменту CYP2C19, очікується, що застосування лікарських засобів, які індукують активність цього ізоферменту, може призвести до збільшення концентрації активного метаболіту клопідогрелу. Рифампіцин, як потужний індуктор ізоферменту CYP2C19, при одночасному застосуванні з клопідогрелом, призводить як до збільшення концентрації активного метаболіту клопідогрелу, так і до інгібування тромбоцитів, що може підвищувати ризик виникнення кровотечі. В якості запобіжного заходу не рекомендується застосовувати одночасно потужні індуктори ізоферменту CYP2C19 і клопідогрел. Інгібітори ізоферменту CYP2C19 Оскільки клопідогрел метаболізується до утворення свого активного метаболіту частково за допомогою ізоферменту CYP2C19, застосування лікарських засобів, що інгібують цей ізофермент, може призвести до зменшення утворення активного метаболіту клопідогрелу. Клінічне значення цієї взаємодії встановлено. Як запобіжний засіб слід уникати одночасного застосування клопідогрелу та потужних або помірних інгібіторів ізоферменту CYP2C19. Потужними та помірними інгібіторами ізоферменту CYP2C19 є омепразол, езомепразол, флувоксамін, флуоксетин, моклобемід, вориконазол, флуконазол, тіклопідін, ципрофлоксацин, циметидин, карбамазепін, окскарбазепін. Слід уникати одночасного застосування з клопідогрелом інгібіторів протонної помпи, які є потужними або помірними інгібіторами ізоферменту CYP2C19 (наприклад, омепразолу, езомепразолу) (див. розділ "Фармакокінетика, підрозділ, Фармакогенетика", розділ "Особливі. Якщо інгібітори протонної помпи повинні прийматися одночасно з клопідогрелом, слід приймати інгібітор протонної помпи з найменшим інгібуванням ізоферменту CYP2C19, такий як пантопразол та лансопразол. Було проведено низку клінічних досліджень з клопідогрелом та іншими, одночасно застосовуваними лікарськими засобами, з метою вивчення можливих фармакодинамічних та фармакокінетичних взаємодій, які показали, що: при одночасному застосуванні клопідогрелу з атенололом та/або ніфедипіном клінічно значущої фармакодинамічної взаємодії не спостерігалося; одночасне застосування фенобарбіталу та естрогенів не мало істотного впливу на фармакодинаміку клопідогрелу; фармакокінетичні показники дигоксину та теофшліну не змінювалися при їх одночасному застосуванні з клопідогрелом; антацидні засоби не зменшували абсорбції клопідогрелу; фенітоїн та толбутамід можна з безпекою застосовувати одночасно з клопідогрелом (дослідження CAPR1E). Малоймовірно, що клопідогрел може впливати на метаболізм інших лікарських засобів, таких як фенітоїн та толбутамід, а також нестероїдні протизапальні засоби, які метаболізуються за допомогою ізоферменту CYP2C9 цитохрому Р450; інгібітори АПФ, діуретики, бета-адреноблокатори, блокатори "повільних" кальцієвих каналів, гіполіпідемічні засоби, коронарні вазодилататори, гіпоглікемічні засоби (в т.ч. інсулін), протиепшептичні засоби, гормонозамісна терапія та блокатори глікопротеїн небажаних взаємодій не виявлено. Лікарські засоби, що є субстратами ізоферменту CYP2C8 Показано, що клопідогрел збільшував системну експозицію репаглініду у здорових добровольців. Дослідження in vitro показали, що збільшення системної експозиції репаглініду є наслідком пригнічення ізоферменту CYP2C8 глюкуронідним метаболітом клопідогрелу. Слід бути обережними при одночасному застосуванні клопідогрелу та лікарських засобів, що метаболізуються за допомогою ізоферменту CYP2C8 (наприклад, репаглініду, паклітакселу) у зв'язку з ризиком збільшення їх плазмових концентрацій. Опіоїдні агоністи Як і у випадку інших пероральних інгібіторів P2Y12, одночасне застосування опіоїдних агоністів може затримувати та зменшувати абсорбцію клопідогрелу, ймовірно, через сповільнене випорожнення шлунка. Клінічне значення цієї взаємодії невідоме. Слід розглянути можливість призначення парентерального антиагрегантного препарату у пацієнтів із гострим коронарним синдромом, які потребують одночасного застосування морфіну або інших опіоїдних агоністів.Спосіб застосування та дозиВсередину, незалежно від їди. Дозування 300 мг клопідогрелу, призначене для застосування як навантажувальна доза пацієнтам з гострим коронарним синдромом (див. "Показання до застосування"). Гострий коронарний синдром без піднесення сегмента ST (нестабільна стенокардія, інфаркт міокарда без зубця Q) Лікування клопідогрелом слід починати з одноразового прийому дози навантаження 300 мг, а потім продовжувати його прийом у дозуванні 75 мг один раз на добу. Одночасно з клопідогрелом необхідно приймати АСК у дозі від 75 до 325 мг 1 раз на добу. У клінічному дослідженні CURE більшість пацієнтів із гострим коронарним синдромом додатково отримували лікування гепарином. Гострий інфаркт міокарда з підйомом сегмента ST Рекомендована добова доза клопідогрелу становить 75 мг одноразово і приймається разом з АСК із застосуванням або без застосування тромболітиків. Прийом клопідогрелу можна починати як з дози навантаження, так і без неї (у дослідженні CLARITY приймалася навантажувальна доза 300 мг). У пацієнтів старше 75 років лікування клопідогрелом має починатися без прийому його дози навантаження. Фармакогенетика (пацієнти з генетично обумовленою зниженою активністю ізоферменту CYP2C19) Низька активність ізоферменту CYP2C19 пов'язана із зменшенням антиагрегантної дії клопідогрелу. Режим застосування більш високих доз (600 мг навантажувальна доза, потім 150 мг один раз на добу щодня) у пацієнтів з низькою активністю ізоферменту CYP2C19 збільшує антиагрегантну дію клопідогрелу (див. розділ "Фармакокінетика" підрозділ "Фармакогенетика"). У пацієнтів з низькою активністю ізоферменту CYP2C19 можна розглянути питання про застосування більш високих доз клопідогрелу. Точний режим дозування для цієї популяції пацієнтів у клінічних дослідженнях, що враховують клінічні результати, не встановлено. Особливі групи пацієнтів Дитячий вік до 18 років: безпека та ефективність застосування препарату у педіатричних популяціях не встановлені. Пацієнти старше 75 років: корекція дози не потрібна. У добровольців старше 75 років у порівнянні з молодими добровольцями не було отримано відмінностей за показниками агрегації тромбоцитів та часу кровотечі. Пацієнти з порушенням функції нирок Після повторних прийомів клопідогрелу в дозі 75 мг/добу у пацієнтів з тяжким ураженням нирок (кліренс креатиніну (КК) від 5 до 15 мл/хв) інгібування АДФ-індукованої агрегації тромбоцитів (25 %) було нижчим порівняно з таким у здорових добровольців однак, подовження часу кровотечі порівняно з даними у здорових добровольців, які отримували клопідогрел у дозі 75 мг на добу. Пацієнти з порушенням функції печінки Після щоденного прийому клопідогрелу протягом 10 днів у добовій дозі 75 мг у пацієнтів з тяжким ураженням печінки інгібування АДФ-індукованої агрегації тромбоцитів можна порівняти з даними у здорових добровольців. Середній час кровотечі також можна порівняти в обох групах. Пацієнти різної етнічної приналежності Поширеність алелей генів ізоферменту CYP2C19, відповідальних за проміжний і знижений метаболізм клопідогрелу до його активного метаболіту, відрізняється у представників різних етнічних груп (див. розділ Фармакокінетика, підрозділ "Фармакогенетика"). CYP2C19 на клінічні результати. Підлога У невеликому дослідженні, що порівнює фармакодинамічні властивості клопідогрелу у чоловіків та жінок, у жінок спостерігалося менше інгібування АДФ-індукованої агрегації тромбоцитів, але відмінностей у подовженні часу кровотечі не було. У великому контрольованому дослідженні CAPRIE (клопідогрел у порівнянні з АСК у пацієнтів з ризиком розвитку ішемічних ускладнень), частота клінічних результатів, інших побічних дій та відхилень від норми клініко-лабораторних показників була однаковою як у чоловіків, так і у жінок.ПередозуванняСимптоми передозування Передозування клопідогрелу може призвести до збільшення часу кровотечі з подальшими ускладненнями у вигляді розвитку кровотеч. Заходи щодо надання допомоги при передозуванні З появою кровотечі потрібне проведення відповідних лікувальних заходів. Антидот клопідогрелу не встановлено. Якщо необхідна швидка корекція часу кровотечі, що подовжився, то рекомендується проведення переливання тромбоцитарної маси.Запобіжні заходи та особливі вказівкиПри лікуванні клопідогрелом, особливо протягом перших тижнів лікування та/або після інвазивних кардіологічних процедур/хірургічного втручання, необхідно вести ретельне спостереження за пацієнтами щодо виключення ознак кровотечі, у тому числі і прихованого. Кровотечі та гематологічні порушення У зв'язку з ризиком розвитку кровотечі та небажаних явищ з боку крові у разі появи в ході лікування клінічних симптомів, підозрілих на виникнення кровотечі, слід терміново зробити загальний клінічний аналіз крові, визначити активований частковий тромбопластиновий час (АЧТВ), кількість тромбоцитів, показники функціональної активності тром та провести інші необхідні дослідження. Одночасне застосування клопідогрелу з варфарином може посилити ризик кровотечі (див. розділ "Взаємодія з іншими лікарськими засобами"), тому слід бути обережним при одночасному застосуванні клопідогрелу та варфарину. Клопідогрел, як і інші антитромбоцитарні засоби, слід застосовувати з обережністю у пацієнтів, які мають підвищений ризик розвитку кровотечі, пов'язаний з травмами, хірургічними втручаннями або іншими патологічними станами, а також у пацієнтів, які приймають АСК, НПЗП (у тому числі інгібітори ЦОГ-2). , гепарин, блокатори глікопротеїну IIb/IIIа, СІОЗС та потужні індуктори ізоферменту CYP2C19 Якщо пацієнт має планову хірургічну операцію, і при цьому немає необхідності в антитромбоцитарному ефекті, то за 5-7 днів до операції прийом клопідогрелу слід припинити. Клопідогрел подовжує час кровотечі і повинен застосовуватися з обережністю у пацієнтів із захворюваннями, що схильні до розвитку кровотеч (особливо, шлунково-кишкових та внутрішньоочних). Препарати, які можуть спричинити пошкодження слизової оболонки шлунково-кишкового тракту (такі як АСК, нестероїдні протизапальні засоби) у пацієнтів, які приймають клопідогрел, слід застосовувати з обережністю. Пацієнти повинні бути попереджені про те, що при прийомі клопідогрелу (одного або в комбінації з АСК) для зупинки кровотечі може знадобитися більше часу, а також про те, що у разі виникнення у них незвичайної (по локалізації або тривалості) кровотечі їм слід повідомити про це свого лікаря. Перед будь-якою майбутньою операцією та перед початком прийому будь-якого нового лікарського препарату пацієнти повинні повідомляти лікаря (включаючи стоматолога) про прийом клопідогрелу. Нещодавно перенесений ішемічний інсульт Показано, що у пацієнтів з нещодавно перенесеним минущим порушенням мозкового кровообігу або інсультом, що мають високий ризик розвитку повторних ішемічних ускладнень, комбінація АСК та клопідогрелу підвищує частоту розвитку великих кровотеч. Тому така комбінована терапія повинна проводитися з обережністю і лише у разі доведеної клінічної користі від її застосування. Прийом клопідогрелу не рекомендується при гострому інсульті з давністю менше 7 днів (оскільки відсутні дані щодо його застосування при цьому стані). Тромботична тромбоцитопенічна пурпура (ТТП) Дуже рідко після застосування клопідогрелу (іноді навіть нетривалого) відзначалися випадки розвитку тромботичної тромбоцитопенічної пурпури (ТТП), яка характеризується тромбоцитопенією та мікроангіопатичною гемолітичною анемією, що супроводжуються неврологічними розладами, порушенням функції. ТТП є потенційно загрозливим для життя станом, що вимагає негайного лікування, включаючи плазмаферез. Набута гемофілія Повідомлялося про випадки розвитку набутої гемофілії прийому клопідогрелу. При підтвердженому ізольованому збільшенні АЧТВ, що супроводжується або не супроводжується розвитком кровотечі, слід розглянути питання можливості розвитку набутої гемофілії. Пацієнти з підтвердженим діагнозом набутої гемофілії повинні спостерігатися та лікуватися фахівцями з цього захворювання та припинити прийом клопідогрелу. Функціональна активність ізоферменту CYP2C19 У пацієнтів з низькою активністю ізоферменту CYP2C19 при застосуванні клопідогрелу в рекомендованих дозах утворюється менше активного метаболіту клопідогрелу і слабше виражена його антиагрегантна дія, у зв'язку з чим при прийомі звичайно рекомендованих доз клопідогрелу при гострому коронарному синдромі. судинних ускладнень, ніж у пацієнтів із нормальною активністю ізоферменту CYP2C19. Очікується, що застосування лікарських засобів, які індукують активність ізоферменту CYP2C19, може спричинити збільшення концентрації активного метаболіту клопідогрелу та підвищувати ризик виникнення кровотечі. В якості запобіжного заходу не рекомендується застосовувати одночасно потужні індуктори ізоферменту CYP2C19 і клопідогрел. Є тести визначення генотипу CYP2C19, які можуть бути використані для допомоги у виборі терапевтичної стратегії. Слід розглянути питання застосування більш високих доз клопідогрелу у пацієнтів з низькою активністю CYP2C19. Перехресні алергічні та/або гематологічні реакції між тієнопіридинами У пацієнтів слід збирати анамнез на предмет алергічних та/або гематологічних реакцій, що були раніше, на інші тієнопіридини (такі як тіклопідин, прасугрел), оскільки повідомлялося про наявність перехресних алергічних та/або гематологічних реакцій між тіенопіридинами (див. розділ "Побічна дія"). Тієнопіридини можуть викликати помірні та тяжкі алергічні реакції (такі як висипання на шкірі, ангіоневротичний набряк) або гематологічні реакції (такі як тромбоцитопенія і нейтропенія). Пацієнти, у яких раніше спостерігалися алергічні та/або гематологічні реакції на один із препаратів групи тієнопіридинів, можуть мати підвищений ризик розвитку подібних реакцій на інший препарат групи тієнопіридинів. Рекомендується моніторинг перехресних алергічних та/або гематологічних реакцій. Ниркова недостатність Досвід застосування клопідогрелу у пацієнтів з тяжкою нирковою недостатністю обмежений. Тому слід з обережністю застосовувати клопідогрел у цієї групи пацієнтів. Печінкова недостатність Є обмежений досвід застосування клопідогрелу у пацієнтів з тяжкими захворюваннями печінки, які можуть бути схильними до розвитку геморагічного діатезу. Тому слід з обережністю застосовувати клопідогрел у цієї групи пацієнтів. Вплив на здатність до керування автотранспортом та управління механізмами Препарат Плавікс® не істотно впливає на здібності, необхідні для керування автомобілем або заняття іншими потенційно небезпечними видами діяльності.Умови відпустки з аптекЗа рецептомВідео на цю тему
1 205,00 грн
185,00 грн
Склад, форма випуску та упаковкаПігулки - 1 таб. діюча речовина: клопідогрел гідросульфат у формі II - 97,875 мг (у перерахунку на клопідогрел - 75,0 мг); допоміжні речовини: манітол, макрогол-6000, целюлоза мікрокристалічна (з низьким вмістом води, 90 мкм), гіпоролоза низькозаміщена, рицинова олія гідрогенізована; плівкова оболонка: опадрай рожевий (лактози моногідрат, гіпромелозу, титану діоксид (Е 171), тріацетин, барвник заліза оксид червоний (Е 172)), карнаубський віск. По 7, 10 або 14 таблеток у блістер з ПВХ/ПВДХ та фольги алюмінієвої або ПА/Ал/ПВХ та фольги алюмінієвої. По 1, 2 або 3 блістери по 7 або 14 таблеток; по 1, 2, 3 або 10 блістерів по 10 таблеток разом з інструкцією із застосування в картонну пачку.Опис лікарської формиКруглі, злегка двоопуклі таблетки, покриті плівковою оболонкою рожевого кольору, з гравіюванням "75" з одного боку і "1171" з іншого боку.Фармакотерапевтична групаАнтиагрегантний засіб.ФармакокінетикаВсмоктування При одноразовому та повторному прийомі внутрішньо у дозі 75 мг на добу клопідогрел швидко всмоктується. Середнє значення максимальної концентрації (Сmax) незміненого клопідогрелу в плазмі крові (приблизно 2,2-2,5 нг/мл після прийому внутрішньо разової дози 75 мг) досягається приблизно через 45 хв після прийому препарату. За даними екскреції метаболітів клопідогрелу через нирки його абсорбція становить приблизно 50%. Розподіл In vitro клопідогрел і його основний циркулюючий у крові неактивний метаболіт оборотно зв'язуються з білками плазми крові (на 98% і 94%, відповідно), і цей зв'язок є ненасиченим до концентрації 100 мг/мл. Метаболізм Клопідогрел інтенсивно метаболізується у печінці. In vitro та in vivo клопідогрел метаболізується двома шляхами: перший здійснюється за допомогою естераз і призводить до гідролізу клопідогрелу з утворенням неактивного похідного карбоксильної кислоти (85 % від циркулюючих метаболітів); другий шлях здійснюється за допомогою ізоферментів цитохром Р450. Спочатку клопідогрел метаболізується до 2-оксо-клопідогрелу, що є проміжним метаболітом. Подальший метаболізм 2-оксо-клопідогрелу призводить до утворення активного метаболіту клопідогрелу - тіольного похідного клопідогрелу. In vitro цей активний метаболіт утворюється головним чином за допомогою ізоферменту CYP2C19. але в його освіті також беруть участь деякі інші ізоферменти, включаючи CYP1A2, CYP2B6 та CYP3A4. Активний тіольний метаболіт клопідогрелу, виділений у in vitro дослідженнях, швидко та незворотно зв'язується з рецепторами тромбоцитів, блокуючи таким чином агрегацію тромбоцитів. Смах активного метаболіту клопідогрелу після одноразового прийому його навантажувальної дози 300 мг у 2 рази перевищує таку після 4-х днів прийому підтримуючої дози клопідогрелу 75 мг. Сmax досягається приблизно 30-60 хв. Виведення Протягом 120 годин після прийому внутрішньо людиною 14С-міченого клопідогрелу близько 50% радіоактивності виводиться через нирки та приблизно 46% радіоактивності виводиться через кишечник. Після одноразового прийому внутрішньо дозування в 75 мг період напіввиведення (Т1/2) клопідогрелу становить приблизно 6 годин. Фармакогенетика За допомогою ізоферменту CYP2C19 утворюються як активний метаболіт, так і проміжний метаболіт - 2-оксо-клопідогрел. Фармакокінетика та антиагрегантна дія активного метаболіту клопідогрелу, при дослідженні агрегації тромбоцитів ex vivo, варіюють залежно від генотипу ізоферменту CYP2C19. Алель гена CYP2CI9*1 відповідає повністю функціональному метаболізму, тоді як алелі генів CYP2C19*2 та CYP2C19*3 є нефункціональними. Алелі генів CYP2C19*2 та CYP2C 19*3 є причиною зниження метаболізму у більшості представників європеоїдної (85%) та монголоїдної раси (99%). Інші алелі, з якими пов'язана відсутність або зниження метаболізму, зустрічаються рідше і включають, але не обмежуються алелями генів CYP2C19*4, *5, *6, *7 і *8.Пацієнти з низькою активністю ізоферменту CYP2CI9 повинні мати дві зазначені вище алелі гена з втратою функції. Опубліковані частоти фенотипів пацієнтів з низькою активністю ізоферменту CYP2C19 у пацієнтів європеоїдної раси становлять 2%, у пацієнтів негроїдної раси - 4% і у монголоїдної раси - 14%. Існують спеціальні тести для визначення наявного у пацієнта генотипу ізоферменту CYP2C19. За даними перехресного дослідження (40 добровольців) за участю добровольців з дуже високою, високою, проміжною та низькою активністю ізоферменту CYP2C19, будь-яких суттєвих відмінностей в експозиції активного метаболіту та у середніх значеннях інгібування агрегації тромбоцитів (ІАТ), індукованої АД дуже високою, високою та проміжною активністю ізоферменту CYP2C19 виявлено не було. У добровольців із низькою активністю ізоферменту CYP2C19 експозиція активного метаболіту знижувалась на 63-71 % порівняно з добровольцями з високою активністю ізоферменту CYP2C19. При використанні схеми лікування 300 мг навантажувальна доза/75 мг підтримуюча доза (300 мг/75 мг) у добровольців з низькою активністю ізоферменту CYP2C19 антитромбоцитарна дія знижувалась із середніми значеннями ІАТ,складовими 24% (через 24 год) та 37% (на 5 день дослідження) порівняно з ІАТ, складовими 39% (через 24 год) та 58% (на 5 день дослідження), у добровольців з високою активністю ізоферменту CYP2C19 та 37% (через 24 год) та 60% (на 5 день дослідження) у добровольців із проміжною активністю ізоферменту CYP2C19. Коли добровольці з низькою активністю ізоферменту CYP2C19 отримували препарат за схемою лікування 600 мг навантажувальна доза/150 мг підтримуюча доза (600 мг/150 мг), експозиція активного метаболіту була вищою, ніж при прийомі за схемою лікування 300 мг/75 мг. Крім цього, ІАТ становило 32% (через 24 год) і 61% (на 5 день дослідження), що було більше такого у добровольців з низькою активністю ізоферменту CYP2C19, які отримували лікування за схемою 300 мг/75 мг, і було подібно до такого в групах пацієнтів з більш високою інтенсивністю CYP2C 19 метаболізму. одержували лікування за схемою 300 мг/75 мг. Однак у дослідженнях з урахуванням клінічних результатів режим дозування клопідогрелу для пацієнтів цієї групи (пацієнтів з низькою активністю ізоферменту CYP2C19) наразі не встановлено. Аналогічно результатам даного дослідження мета-аналіз шести досліджень, до якого увійшли дані 335 добровольців, які отримували клопідогрел і перебували в стані досягнення рівноважної концентрації, показав, що в порівнянні з добровольцями з високою активністю ізоферменту CYP2C19, у добровольців з проміжною активністю ізоферменту CYP2C знижувалася на 28%, а у добровольців з низькою активністю ізоферменту CYP2C19 - на 72%, тоді як ІАТ було знижено з відмінностями в ІАТ на 5,9% та 21,4% відповідно. Не проводилося оцінки впливу генотипу CYP2CI9 на клінічні результати у пацієнтів, які отримували клопідогрел, у проспективних рандомізованих контрольованих дослідженнях. Проте зараз є кілька ретроспективних аналізів. Результати генотипування отримані в ході наступних клінічних досліджень: CURE, CHARISMA, CLARITY-TIM1 28, TRITON-TIMI 38 та ACT1VE-A, а також у кількох опублікованих когортних дослідженнях. У дослідженні TRITON-TIMI 38 та 3-х когортних дослідженнях (Collet, Sibbing, Giusti) пацієнти комбінованої групи з проміжною або низькою активністю ізоферменту CYP2C19 мали більш високу частоту серцево-судинних ускладнень (смерть, інфаркт міокарда та інсульт). з такими у пацієнтів із високою активністю ізоферменту CYP2C19. У дослідженні CHARISMA та одному когортному дослідженні (Simon) збільшення частоти серцево-судинних ускладнень спостерігалося тільки у пацієнтів з низькою активністю ізоферменту CYP2C19 (при їх порівнянні з пацієнтами з високою активністю ізоферменту CYP2C19). Дослідження CURE, CLARITY. ACTIVE- і одному з когортних досліджень (Trenk), не спостерігалося збільшення частоти серцево-судинних ускладнень в залежності від інтенсивності CYP2C 19- метаболізму. Особливі групи пацієнтів Фармакокінетика активного метаболіту клопідогрелу в спеціальних групах пацієнтів не вивчалася. Пацієнти старші 75 років: у добровольців старше 75 років при порівнянні з молодими добровольцями не було отримано відмінностей за показниками агрегації тромбоцитів та часу кровотечі. Корекція дози не потрібна. Дитячий вік до 18 років: клінічні дані відсутні. Пацієнти з порушенням функції нирок Після повторних прийомів клопідогрелу в дозі 75 мг/добу у пацієнтів з тяжкими порушеннями функції нирок (кліренс креатиніну (КК) від 5 мл/хв до 15 мл/хв) інгібування АДФ-індукованої агрегації тромбоцитів було нижчим (на 25 %) порівняно з таким у здорових добровольців, проте подовження часу кровотечі було подібним до такого у здорових добровольців, які отримували клопідогрел у дозуванні 75 мг на добу. Пацієнти з порушенням функції печінки Не було значних відмінностей у ступені інгібування АДФ-індукованої агрегації тромбоцитів після щоденного прийому клопідогрелу у добовій дозі 75 мг протягом 10 днів у пацієнтів з тяжкими порушеннями функції печінки порівняно зі здоровими добровольцями. Середній час кровотечі також можна порівняти в обох групах. Расова приналежність Поширеність алелей генів ізоферменту CYP2C19, що зумовлюють проміжну та низьку активність цього ізоферменту, відрізняється у представників різних расових груп. Є обмежені літературні дані про їх поширеність у представників монголоїдної раси, що не дозволяє оцінити значення генотипування ізоферменту CYP2C19 для розвитку ішемічних ускладнень.ФармакодинамікаКлопідогрел є проліком, один з активних метаболітів якого є інгібітором агрегації тромбоцитів. Для утворення активного метаболіту, який пригнічує агрегацію тромбоцитів, клопідогрел повинен метаболізуватися за допомогою ізоферментів системи цитохрому Р450 (CYP450). Активний метаболіт клопідогрелу селективно інгібує зв'язування аденозиндифосфату (АДФ) з P2Yi2 рецептором тромбоцитів та подальшу АДФ-опосередковану активацію комплексу GPIIb/IIIa, що призводить до придушення агрегації тромбоцитів. Завдяки необоротному зв'язуванню, тромбоцити залишаються несприйнятливими до стимуляції АДФ протягом всього терміну свого життя (приблизно 7-10 днів), а відновлення нормальної функції тромбоцитів відбувається зі швидкістю, що відповідає швидкості оновлення тромбоцитів. Агрегація тромбоцитів, спричинена агоністами, відмінними від АДФ. також інгібується за рахунок блокади посиленої активації тромбоцитів АДФ, що вивільняється. Оскільки утворення активного метаболіту відбувається за допомогою ізоферментів системи цитохрому Р450, деякі з яких можуть відрізнятися поліморфізмом або інгібуватися іншими препаратами, не у всіх пацієнтів можливе адекватне пригнічення агрегації тромбоцитів. При щоденному прийомі клопідогрелу в дозі 75 мг з першого ж дня прийому відзначається значне пригнічення АДФ-індукованої агрегації тромбоцитів, яке поступово збільшується протягом 3-7 днів і потім виходить на постійний рівень (при досягненні рівноважного стану). У рівноважному стані агрегація тромбоцитів пригнічується загалом на 40-60 %. Після припинення прийому клопідогрелу агрегація тромбоцитів та час кровотечі поступово повертаються до початкового рівня, в середньому, протягом 5 днів. У ході клінічного дослідження ACTIVE-А показано, що у пацієнтів з фібриляцією передсердь, які мали щонайменше. один фактор ризику розвитку судинних ускладнень, але були нездатні приймати непрямі антикоагулянти, клопідогрел у поєднанні з ацетилсаліциловою кислотою (АСК) (у порівнянні з прийомом тільки однієї АСК) зменшував частоту разом узятих інсульту, інфаркту міокарда, системної тромбоемболії поза центральною або судинної смерті, переважно за рахунок зменшення ризику розвитку інсульту. Ефективність прийому клопідогрелу у поєднанні з АСК виявлялася рано і зберігалася до 5 років. Зменшення ризику великих судинних ускладнень у групі пацієнтів, які приймали клопідогрел у поєднанні з АСК, спостерігалося переважно за рахунок більшого зменшення частоти інсультів. Ризик розвитку інсульту будь-якої тяжкості при прийомі клопідогрелу у поєднанні з АСК знижувався, а також спостерігалася тенденція до зниження частоти розвитку інфаркту міокарда в групі, яка отримувала лікування клопідогрелом у поєднанні з АСК, але не спостерігалося відмінностей у частоті тромбоемболій поза ЦНС або судинної смерті. Крім цього, прийом клопідогрелу у поєднанні з АСК зменшував загальну кількість днів госпіталізації з серцево-судинних причин. Перехід з терапії потужним інгібітором рецепторів P2Y12 на лікування клопідогрелом у поєднанні з АСК після завершення гострої фази гострого інфаркту міокарда (ГІМ) вивчався у двох рандомізованих ініційованих дослідником клінічних дослідженнях (TOPIC та TROPICAL-ACS). У рандомізованому відкритому клінічному дослідженні TOPIC брали участь пацієнти, які перенесли ГІМ, яким виконувалось черезшкірне коронарне втручання (ЧКВ). Пацієнти, які отримували АСК та один з найбільш потужних інгібіторів рецепторів P2Y12, у яких не розвинулися несприятливі події протягом одного місяця, або були переведені на терапію фіксованою комбінацією АСК та клопідогрелу (деескалація подвійної антитромбоцитарної терапії (ДАТ)) або продовжили приймати Постійна ДАТ). Події, включені в комбіновану первинну кінцеву точку (смерть від ускладнень серцево-судинних захворювань (ССЗ), інсульт, екстрена реваскуляризація та кровотечі типу 2 або тяжкі кровотечі за шкалою BARC (Дослідницького академічного консорціуму за кровотечами)), через один були зареєстровані у 43 з 322 пацієнтів (13,4%) у групі деескалації ДАТ та 85 пацієнтів з 323 (26,3 %) у групі незмінної ДАТ (р Статистично значуща відмінність в основному зумовлена скороченням кількості випадків кровотечі, у тому числі кровотеч, які за шкалою BARC більш або рівні 2 (4% у групі деескалації та 14,9% у групі, що отримувала незмінену ДАТ), при цьому не спостерігалося істотних відмінностей у частоті ішемічних ускладнень (р = 0,36). До рандомізованого відкритого клінічного дослідження TROPICAL-ACS було включено 2610 пацієнтів з ГІМ. підтвердженим аналізом на біомаркери після проведення ЧКВ. Пацієнти були рандомізовані до груп для отримання прасугрелу (дні 0-14) або прасугрелу (дні 0-7), а потім клопідогрелу (дні 8-14) у комбінації з АСК. На 14-й день було проведено оцінку функції тромбоцитів. Пацієнти з першої групи терапії лише прасугрелом продовжували приймати прасугрел протягом 11,5 місяці. У пацієнтів із групи заміни терапії було виконано аналіз на високу реактивність тромбоцитів (ДРТ). Пацієнти з ДРТ ≥ 46 одиниць були переведені на терапію прасугрелом, яку отримували протягом 11,5 місяця. Пацієнти з ДРТПоказання до застосуванняВторинна профілактика атеротромботичних ускладнень: У дорослих пацієнтів після нещодавно перенесеного інфаркту міокарда (з давністю від декількох днів до 35 днів), нещодавно перенесеного ішемічного інсульту (з давністю від 7 днів до 6 місяців) або при діагностованій оклюзійній хворобі периферичних артерій прийом клопідогрелу знижував частоту комбінованої ішемічний інсульт (з летальними наслідками або без нього), повторний інфаркт міокарда (з летальними наслідками або без нього) та іншу серцево-судинну смерть. У дорослих пацієнтів із гострим коронарним синдромом: гострий коронарний синдром без підйому сегмента ST (нестабільна стенокардія/інфаркт міокарда без зубця Q), включаючи пацієнтів, які повинні отримувати медикаментозне лікування, та пацієнтів, яким показано черезшкірне коронарне втручання (зі стенуванням або без стентування) або аортокоронарне шунтування (АКШ). Прийом клопідогрелу знижував частоту комбінованої кінцевої точки, що включала серцево-судинну смерть, інфаркт міокарда або інсульт, а також частоту комбінованої кінцевої точки, що включала серцево-судинну смерть, інфаркт міокарда, інсульт, рефрактерну ішемію. гострий інфаркт міокарда із підйомом сегмента ST. Прийом клопідогрелу знижував смертність від будь-яких причин, а також частоту комбінованої кінцевої точки, що включала смерть, повторний інфаркт міокарда або інсульт. Профілактика атеротромботичних та тромбоемболічних ускладнень у дорослих пацієнтів з фібриляцією передсердь (миготливою аритмією) Показано, що у пацієнтів з фібриляцією передсердь з підвищеним ризиком судинних ускладнень терапія непрямими антикоагулянтами, які є антагоністами вітаміну К (АВК), пов'язана з більшою клінічною користю порівняно із застосуванням тільки АСК або комбінації клопідогрелу з АСК щодо зниження. Пацієнтам з фібриляцією передсердь (миготливою аритмією), що мають, як мінімум, один фактор ризику розвитку судинних ускладнень, які не можуть приймати АВК (наприклад, за наявного особливого ризику кровотечі, нездатності пацієнта, на думку лікаря, адекватно контролювати МНО (міжнародне нормалізоване) ставлення) або у разі неприйняття пацієнтом лікування АВК), для запобігання атеротромботичних та тромбоемболічних ускладнень. включаючи інсульт, показаний прийом клопідогрелу в комбінації з АСК. Показано, що клопідогрел у комбінації з АСК знижував частоту комбінованої кінцевої точки, що включала інсульт, інфаркт міокарда, системну тромбоемболію поза ЦНС або серцево-судинну смерть, переважно за рахунок зниження частоти розвитку інсульту.Протипоказання до застосуванняПідвищена чутливість до клопідогрелу або будь-якої з допоміжних речовин препарату. Тяжка печінкова недостатність. Гостра кровотеча, наприклад, кровотеча з виразки або внутрішньочерепний крововилив. Рідкісна спадкова непереносимість галактози, дефіцит лактази та глюкозо-галактозна мальабсорбція. Вагітність та період грудного вигодовування. Дитячий вік до 18 років (безпека та ефективність застосування не встановлені). З обережністю: При помірній печінковій недостатності, при якій можлива схильність до кровотечі (обмежений клінічний досвід застосування). При нирковій недостатності (обмежений клінічний досвід застосування). При захворюваннях, при яких є схильність до розвитку кровотеч (зокрема шлунково-кишкових або внутрішньоочних), і, особливо, при одночасному застосуванні лікарських засобів, які можуть спричинити ушкодження слизової оболонки шлунково-кишкового тракту (таких як АСК та нестероїдні протизапальні препарати ( НПЗП)). У пацієнтів, у яких є підвищений ризик розвитку кровотечі: через травму, хірургічне втручання або інші патологічні стани, а також у пацієнтів, які отримують лікування АСК, гепарином, варфарином, інгібіторами глікопротеїну IIb/IIIa, НПЗЗ, у тому числі селективними інгібіторами. -2 (ЦОГ-2), а також іншими лікарськими засобами, застосування яких пов'язане з ризиком кровотеч, селективними інгібіторами зворотного захоплення серотоніну (СІОЗС). При одночасному застосуванні з лікарськими засобами, що є субстратами ізоферменту CYP2C8 (репаглінід, паклітаксел). У пацієнтів із низькою активністю ізоферменту CYP2C19. При вказівках в анамнезені алергічні та гематологічні реакції на інші тієнопіридини (такі як тіклопідін, прасугрел). При нещодавно перенесеному минущому порушенні мозкового кровообігу або ішемічному інсульті.Вагітність та лактаціяВагітність Дослідження на тваринах не виявили ні прямих, ні непрямих несприятливих ефектів протягом вагітності, ембріональний розвиток, пологи та постнатальний розвиток. Так як не завжди за результатами досліджень на тваринах можна передбачити реакцію у людини, і внаслідок відсутності даних контрольованих клінічних досліджень щодо прийому клопідогрелу вагітними жінками, як запобіжний засіб не рекомендується прийом клопідогрелу під час вагітності, за винятком тих випадків, коли, на думку лікаря , Його застосування настійно необхідне. Період грудного вигодовування У дослідженнях на щурах показано, що клопідогрел та/або його метаболіти виділяються з грудним молоком. Невідомо, чи виділяється клопідогрел із грудним молоком людини. Так як багато лікарських засобів виділяються з грудним молоком і існує ризик розвитку потенційних несприятливих явищ у дитини, яка перебуває на грудному вигодовуванні, слід прийняти рішення про припинення грудного вигодовування або про відміну препарату з урахуванням необхідності його застосування для матері.Побічна діяДані, отримані під час клінічних досліджень Безпека клопідогрелу вивчена більш ніж у 44 000 пацієнтів, у тому числі більш ніж у 12 000 пацієнтів, які отримували лікування протягом року або більше. Загалом переносимість клопідогрелу в дозі 75 мг/добу у дослідженні CAPRIE відповідала переносимості АСК у дозі 325 мг/добу, незалежно від віку, статі та расової належності пацієнтів. Нижче наведено клінічно значущі небажані явища, що спостерігалися у п'яти великих клінічних дослідженнях: CAPRIE, CURE, CLARITY, COMMIT та ACTIVE-A. Кровотечі та крововиливу Порівняння монотерапії клопідогрелом та АСК У клінічному дослідженні CAPRIE загальна частота всіх кровотеч у пацієнтів, які приймали клопідогрел, та у пацієнтів, які приймали АСК, склала 9,3%. Частота важких кровотеч при застосуванні клопідогрелу та АСК була порівнянною: 1,4 % та 1,6 % відповідно. Загалом частота розвитку шлунково-кишкових кровотеч у пацієнтів, які приймали клопідогрел, та у пацієнтів, які приймали АСК, становила 2.0 % та 2,7 %, відповідно, у тому числі частота шлунково-кишкових кровотеч, які потребували госпіталізації, становила 0,7 % та 1,1% відповідно. Загальна частота кровотеч іншої локалізації при прийомі клопідогрелу порівняно з прийомом АСК була вищою (7,3% проти 6,5%, відповідно). Однак частота важких кровотеч при застосуванні клопідогрелу та АСК була порівнянною (0,6% або 0,4% відповідно). Найчастіше повідомлялося про розвиток наступних кровотеч: пурпура / синці, носова кровотеча. Рідше повідомлялося про розвиток гематом, гематурії та очних крововиливів (головним чином, кон'юнктивальних). Частота внутрішньочерепних крововиливів при застосуванні клопідогрелу та АСК була порівнянною (0,4 % або 0,5 % відповідно). Порівняння комбінованої терапії клопідогрел+АСК та плацебо+АСК У клінічному дослідженні CURE у пацієнтів, які приймали клопідогрел+АСК, у порівнянні з пацієнтами, які приймали плацебо+АСК, спостерігалося збільшення частоти розвитку великих кровотеч (3,7 % порівняно 2,7 %), та малих кровотеч (5,1 % за порівняно 2.4%). В основному, джерелами великих кровотеч були шлунково-кишковий тракт (ШКТ) та місця пункції артерій. Частота розвитку загрозливих для життя кровотеч у пацієнтів, які приймали клопідогрел+АСК у порівнянні з пацієнтами, які приймали плацебо+АСК, достовірно не відрізнялася (2,2 % та 1,8 %, відповідно), частота розвитку фатальних кровотеч була однаковою (0.2 % при обох види терапії). Частота виникнення не загрожують життю великих кровотеч була достовірно вищою у пацієнтів, які приймали клопідогрел+АСК, порівняно з пацієнтами, які приймали плацебо+АСК (1,6 % та 1 %, відповідно), але частота розвитку внутрішньочерепних крововиливів була однаковою (0,1 % за обох видів терапії). Частота розвитку великих кровотеч у групі клопідогрел+АСК залежала від дози АСК (< 100 мг: 2,6%; 100-200 мг: 3,5 %; > 200 мг: 4,9 %), а також частота розвитку великих кровотеч у групі плацебо+АСК (< 100 мг: 2,0%; 100-200 мг: 2,3%; > 200 мг: 4,0%). У пацієнтів, які припинили антитромбоцитарну терапію більш ніж за 5 днів до аортокоронарного шунтування, не відзначалося почастішання випадків розвитку великих кровотеч протягом 7 днів після втручання (4,4% у групі клопідогрел+АСК та 5,3% у групі плацебо+АСК). У пацієнтів, які продовжували антитромбоцитарну терапію протягом останніх п'яти днів перед аортокоронарним шунтуванням, частота цих подій після втручання становила 9,6% (у групі клопідогрел+АСК) та 6,3% (у групі плацебо+АСК). У клінічному дослідженні CLARITY частота великих кровотеч (визначуваних як внутрішньочерепні кровотечі або кровотечі зі зниженням гемоглобіну > 5 г/дл) в обох групах (клопідогрел+АСК і плацебо+АСК) була порівнянною в обох групах лікування (1,3 % проти 1, 1% у групі клопідогрел+АСК та групі плацебо+АСК, відповідно). Вона була однаковою у підгрупах пацієнтів, розділених за вихідними характеристиками та за видами фібринолітичної терапії або гепаринотерапії. Частота виникнення фатальних кровотеч (0.8% проти 0,6%) та внутрішньочерепних крововиливів (0,5% проти 0,7%) при лікуванні клопідогрел+АСК та плацебо+АСК, відповідно, була низькою та порівнянною в обох групах лікування. У клінічному дослідженні COMMIT загальна частота нецеребральних великих кровотеч або церебральних кровотеч була низькою та однаковою (0,6% у групі клопідогрел+АСК та 0,5% у групі плацебо+АСК). У клінічному дослідженні ACTIVE-A частота розвитку великих кровотеч у групі клопідогрел+АСК була вищою, ніж у групі плацебо+АСК (6,7 % проти 4,3 % відповідно). Великі кровотечі переважно були позачерепними в обох групах (5,3% проти 3,5%), головним чином, із шлунково-кишкового тракту (3,5% проти 1,8%). У групі клопідогрел+АСК внутрішньочерепних крововиливів було більше порівняно з групою плацебо+АСК (1,4% проти 0.8%, відповідно). Відсутні статистично значущі відмінності між цими групами лікування у частоті виникнення фатальних кровотеч (1,1% проти 0,7%) та геморагічного інсульту (0,8% проти 0.6%). Порушення з боку крові У дослідженні CAPRIE, тяжка нейтропенія ( У двох із 9599 пацієнтів, які приймали клопідогрел, спостерігалася повна відсутність нейтрофілів у периферичній крові, якого не спостерігалося в жодного з 9586 пацієнтів, які приймали АСК. Незважаючи на те, що ризик розвитку мієлотоксичної дії при прийомі клопідогрелу є досить низьким, якщо у пацієнта, який приймає клопідогрел, спостерігається підвищення температури або з'являються інші ознаки інфекції. слід обстежити пацієнта щодо можливої нейтропенії. При лікуванні клопідогрелом в одному випадку спостерігався розвиток апластичної анемії. Частота виникнення тяжкої тромбоцитопенії ( У дослідженнях CURE та CLARITY спостерігалася порівнянна кількість пацієнтів із тромбоцитопенією або нейтропенією в обох групах лікування. Інші клінічно значущі небажані реакції, що спостерігалися під час проведення клінічних досліджень CAPRIE, CURE, CLARITY COMMIT та ACTIVE-A Частота виникнення небажаних реакцій визначалася відповідно до класифікації Всесвітньої Організації Охорони Здоров'я: дуже часто (≥ 1/10); часто (≥ 1/100 та < 1/10); нечасто (≥ 1/1000 та < 1/100); рідко (≥ 1/10000 та < 1/1000); дуже рідко (< 1/10000), частота невідома (не може бути підрахована на підставі наявних даних). Порушення з боку нервової системи: нечасто – головний біль, запаморочення, парестезія; рідко – вертиго. Порушення з боку шлунково-кишкового тракту: часто – диспепсія, абдомінальні болі, діарея; нечасто - нудота, гастрит, здуття живота, запор, блювання, виразка шлунка, виразка дванадцятипалої кишки. Порушення з боку шкіри та підшкірних тканин: нечасто – шкірний висип, свербіж шкіри. Порушення з боку крові та лімфатичної системи: нечасто – збільшення часу кровотечі, зниження кількості тромбоцитів у периферичній крові; лейкопенія, зниження кількості нейтрофілів у периферичній крові, еозинофілія. Постмаркетинговий досвід застосування препарату Порушення з боку крові та лімфатичної системи: частота невідома - випадки серйозних кровотеч, переважно підшкірних, скелетно-м'язових, очних крововиливів (кон'юнктивальних, в тканині та сітківку ока), кровотеч з дихальних шляхів (кровохаркання, легеневі кровотечі) кровотеч із післяопераційних ран та випадки кровотеч із летальним результатом (особливо внутрішньочерепних крововиливів, шлунково-кишкових кровотеч та заочеревинних крововиливів); агранулоцитозу, гранулоцитопенії, апластичної анемії/панцитопенії, тромботичної тромбоцитопенічної пурпури (ТТП), придбаної гемофілії А. Порушення з боку серця: частота невідома – синдром Коунісу (вазоспастична алергічна стенокардія/алергічний інфаркт міокарда), зумовлений реакцією гіперчутливості на клопідогрел. Порушення з боку імунної системи: частота невідома – анафілактоїдні реакції, сироваткова хвороба; перехресні алергічні та гематологічні реакції з іншими тієнопіридинами (такими як тіклопідин, прасугрел), аутоімунний інсуліновий синдром (може призводити до серйозної гіпоглікемії, особливо у пацієнтів з MLA DRA4 серотипом). Порушення психіки: частота невідома – сплутаність свідомості, галюцинації. Порушення з боку нервової системи: частота невідома – порушення смакового сприйняття, агевзія. Порушення з боку судин: частота невідома – васкуліт, зниження артеріального тиску. Порушення з боку дихальної системи, органів грудної клітки та середостіння: частота невідома – бронхоспазм, інтерстиційна пневмонія, еозинофільна пневмонія. Порушення з боку шлунково-кишкового тракту: частота невідома – коліт (зокрема виразковий коліт або лімфоцитарний коліт), панкреатит, стоматит. Порушення з боку печінки та жовчовивідних шляхів: частота невідома – гепатит (неінфекційний), гостра печінкова недостатність. Порушення з боку шкіри та підшкірних тканин: частота невідома - макульозно-папульозний еритематозний або ексфоліативний висип, кропив'янка, свербіж шкіри, ангіоневротичний набряк, бульозний дерматит (багатоформна еритема, синдром Стівенса-Джонсона, токсичний ендоз гіперчутливості, лікарський висип з еозинофілією та системними проявами (DRESS-синдром), екзема, плоский лишай. Порушення з боку скелетно-м'язової та сполучної тканини: частота невідома – артралгія (біль у суглобах), артрит, міалгія. Порушення з боку нирок та сечовивідних шляхів: частота невідома – гломерулонефрит. Порушення з боку статевих органів та молочної залози: частота невідома – гінекомастія. Загальні розлади та порушення у місці введення: частота невідома – лихоманка. Лабораторні та інструментальні дані: частота невідома – відхилення від норми лабораторних показників функціонального стану печінки, підвищення концентрації креатиніну в крові.Взаємодія з лікарськими засобамиЛікарські засоби, застосування яких пов'язане із ризиком розвитку кровотечі Є підвищений ризик розвитку кровотечі внаслідок їхнього потенційного адитивного ефекту з клопідогрелом. Лікування слід проводити з обережністю. Тромболітики Безпека одночасного застосування клопідогрелу, фібрин-специфічних або фібрин-неспецифічних тромболітичних засобів та гепарину була вивчена у пацієнтів з гострим інфарктом міокарда. Частота клінічно значущих кровотеч була аналогічна тій, що спостерігалася у разі спільного застосування тромболітичних засобів та гепарину з АСК. Блокатори глікопротеїну IIb/III У зв'язку з можливістю фармакодинамічної взаємодії між клопідогрелом та блокаторами глікопротеїну IIb/IIIа, їх одночасне застосування потребує обережності, особливо у пацієнтів, які мають підвищений ризик розвитку кровотечі (при травмах та хірургічних втручаннях або інших патологічних станах). Ін'єкційні антикоагулянти (наприклад, гепарин) За даними клінічного дослідження, проведеного за участю здорових добровольців, при прийомі клопідогрелу не потрібно зміни дози гепарину і не змінювалася його антикоагулянтна дія. Одночасне застосування гепарину не змінювало антиагрегантної дії клопідогрелу. Між клопідогрелом та гепарином можлива фармакодинамічна взаємодія, яка може збільшувати ризик розвитку кровотеч. При одночасному застосуванні слід бути обережними. Пероральні антикоагулянти (наприклад, варфарин) Хоча прийом клопідогрелу 75 мг/добу не змінював фармакокінетику варфарину (субстрату ізоферменту CYP2C9) або МНО у пацієнтів, які тривало одержують лікування варфарином, одночасний прийом клопідогрелу збільшує ризик кровотечі у зв'язку з його незалежним додатковим впливом на згортання. Тому слід дотримуватися обережності при одночасному прийомі варфарину та клопідогрелу. Ацетилсаліцилова кислота (АСК) АСК не змінює інгібуючого АДФ-індуковану агрегацію тромбоцитів ефекту клопідогрелу, але клопідогрел потенціює вплив АСК на колаген-індуковану агрегацію тромбоцитів. Тим не менш, одночасний з клопідогрелом прийом АСК по 500 мг 2 рази на день протягом однієї доби не викликав суттєвого збільшення часу кровотечі, що викликається прийомом клопідогрелу. Оскільки між клопідогрелом і АСК можлива фармакодинамічна взаємодія, що призводить до підвищення ризику кровотечі, тому при їх одночасному застосуванні слід бути обережним. Тим не менш, у клінічних дослідженнях пацієнти отримували комбіновану терапію клопідогрелом та АСК (75-325 мг один раз на добу) до одного року. Нестероїдні протизапальні препарати (НПЗЗ) У клінічному дослідженні, проведеному за участю здорових добровольців, спільне застосування клопідогрелу та напроксену збільшувало приховані втрати крові через ШКТ. Однак, у зв'язку з відсутністю досліджень щодо взаємодії клопідогрелу з іншими НПЗП, наразі не відомо. є підвищений ризик шлунково-кишкових кровотеч при прийомі клопідогрелу разом з іншими нестероїдними протизапальними засобами. Тому при одночасному застосуванні нестероїдних протизапальних засобів, у тому числі інгібіторів ЦОГ-2 з клопідогрелом. слід дотримуватися обережності. Селективні інгібітори зворотного захоплення серотоніну (СІЗЗС) Оскільки СІЗЗЗ порушують активацію тромбоцитів та збільшують ризик розвитку кровотечі. При одночасному застосуванні слід бути обережними. Індуктори ізоферменту CYP2C19 Оскільки клопідогрел метаболізується до свого активного метаболіту частково за допомогою ізоферменту CYP2C19, очікується, що застосування лікарських засобів, які індукують активність цього ізоферменту, може призвести до збільшення концентрації активного метаболіту клопідогрелу. Рифампіцин, як потужний індуктор ізоферменту CYP2C19, при одночасному застосуванні з клопідогрелом, призводить як до збільшення концентрації активного метаболіту клопідогрелу, так і до інгібування тромбоцитів, що може підвищувати ризик виникнення кровотечі. В якості запобіжного заходу не рекомендується застосовувати одночасно потужні індуктори ізоферменту CYP2C19 і клопідогрел. Інгібітори ізоферменту CYP2C19 Оскільки клопідогрел метаболізується до утворення свого активного метаболіту частково за допомогою ізоферменту CYP2C19, застосування лікарських засобів, що інгібують цей ізофермент, може призвести до зменшення утворення активного метаболіту клопідогрелу. Клінічне значення цієї взаємодії встановлено. Як запобіжний засіб слід уникати одночасного застосування клопідогрелу та потужних або помірних інгібіторів ізоферменту CYP2C19. Потужними та помірними інгібіторами ізоферменту CYP2C19 є омепразол, езомепразол, флувоксамін, флуоксетин, моклобемід, вориконазол, флуконазол, тіклопідін, ципрофлоксацин, циметидин, карбамазепін, окскарбазепін. Слід уникати одночасного застосування з клопідогрелом інгібіторів протонної помпи, які є потужними або помірними інгібіторами ізоферменту CYP2C19 (наприклад, омепразолу, езомепразолу) (див. розділ "Фармакокінетика, підрозділ, Фармакогенетика", розділ "Особливі. Якщо інгібітори протонної помпи повинні прийматися одночасно з клопідогрелом, слід приймати інгібітор протонної помпи з найменшим інгібуванням ізоферменту CYP2C19, такий як пантопразол та лансопразол. Було проведено низку клінічних досліджень з клопідогрелом та іншими, одночасно застосовуваними лікарськими засобами, з метою вивчення можливих фармакодинамічних та фармакокінетичних взаємодій, які показали, що: при одночасному застосуванні клопідогрелу з атенололом та/або ніфедипіном клінічно значущої фармакодинамічної взаємодії не спостерігалося; одночасне застосування фенобарбіталу та естрогенів не мало істотного впливу на фармакодинаміку клопідогрелу; фармакокінетичні показники дигоксину та теофшліну не змінювалися при їх одночасному застосуванні з клопідогрелом; антацидні засоби не зменшували абсорбції клопідогрелу; фенітоїн та толбутамід можна з безпекою застосовувати одночасно з клопідогрелом (дослідження CAPR1E). Малоймовірно, що клопідогрел може впливати на метаболізм інших лікарських засобів, таких як фенітоїн та толбутамід, а також нестероїдні протизапальні засоби, які метаболізуються за допомогою ізоферменту CYP2C9 цитохрому Р450; інгібітори АПФ, діуретики, бета-адреноблокатори, блокатори "повільних" кальцієвих каналів, гіполіпідемічні засоби, коронарні вазодилататори, гіпоглікемічні засоби (в т.ч. інсулін), протиепшептичні засоби, гормонозамісна терапія та блокатори глікопротеїн небажаних взаємодій не виявлено. Лікарські засоби, що є субстратами ізоферменту CYP2C8 Показано, що клопідогрел збільшував системну експозицію репаглініду у здорових добровольців. Дослідження in vitro показали, що збільшення системної експозиції репаглініду є наслідком пригнічення ізоферменту CYP2C8 глюкуронідним метаболітом клопідогрелу. Слід бути обережними при одночасному застосуванні клопідогрелу та лікарських засобів, що метаболізуються за допомогою ізоферменту CYP2C8 (наприклад, репаглініду, паклітакселу) у зв'язку з ризиком збільшення їх плазмових концентрацій. Опіоїдні агоністи Як і у випадку інших пероральних інгібіторів P2Y12, одночасне застосування опіоїдних агоністів може затримувати та зменшувати абсорбцію клопідогрелу, ймовірно, через сповільнене випорожнення шлунка. Клінічне значення цієї взаємодії невідоме. Слід розглянути можливість призначення парентерального антиагрегантного препарату у пацієнтів із гострим коронарним синдромом, які потребують одночасного застосування морфіну або інших опіоїдних агоністів.Спосіб застосування та дозиВсередину, незалежно від їди. Нещодавно перенесений інфаркт міокарда, нещодавно перенесений інсульт та діагностована оклюзійна хвороба периферичних артерій Рекомендована доза – 75 мг один раз на добу. Гострий коронарний синдром без піднесення сегмента ST (нестабільна стенокардія, інфаркт міокарда без зубця Q) Лікування клопідогрелом слід починати з одноразового прийому дози навантаження 300 мг, а потім продовжувати його прийом у дозуванні 75 мг один раз на добу. Одночасно з клопідогрелом необхідно приймати АСК у дозі від 75 до 325 мг 1 раз на добу. У клінічному дослідженні CURE більшість пацієнтів із гострим коронарним синдромом додатково отримували лікування гепарином. Гострий інфаркт міокарда з підйомом сегмента ST Рекомендована добова доза клопідогрелу становить 75 мг одноразово і приймається разом з АСК із застосуванням або без застосування тромболітиків. Прийом клопідогрелу можна починати як з дози навантаження, так і без неї (у дослідженні CLARITY приймалася навантажувальна доза 300 мг). У пацієнтів старше 75 років лікування клопідогрелом має починатися без прийому його дози навантаження. Фібриляція передсердь Клопідогрел слід приймати у добовій дозі 75 мг. У комбінації з клопідогрелом необхідно приймати АСК у дозі 75-100 мг щодня. Фармакогенетика (пацієнти з генетично обумовленою зниженою активністю ізоферменту CYP2C19) Низька активність ізоферменту CYP2C19 пов'язана із зменшенням антиагрегантної дії клопідогрелу. Режим застосування більш високих доз (600 мг навантажувальна доза, потім 150 мг один раз на добу щодня) у пацієнтів з низькою активністю ізоферменту CYP2C19 збільшує антиагрегантну дію клопідогрелу. У пацієнтів з низькою активністю ізоферменту CYP2C19 можна розглянути питання про застосування більш високих доз клопідогрелу. Точний режим дозування для цієї популяції пацієнтів у клінічних дослідженнях, що враховують клінічні результати, не встановлено. Спеціальні групи патентів Дитячий вік до 18 років: безпека та ефективність застосування препарату у педіатричних популяціях не встановлені. Пацієнти старше 75 років: корекція дози не потрібна. У добровольців старше 75 років у порівнянні з молодими добровольцями не було отримано відмінностей за показниками агрегації тромбоцитів та часу кровотечі. Пацієнти з порушенням функції нирок Після повторних прийомів клопідогрелу у дозуванні 75 мг/добу у пацієнтів з тяжким ураженням нирок (КК від 5 до 15 мл/хв) інгібування АДФ-індукованої агрегації тромбоцитів (25 %) було нижчим порівняно з таким у здорових добровольців, проте подовження часу кровотечі порівняно з даними у здорових добровольців, які отримували клопідогрел у дозуванні 75 мг на добу. Пацієнти з порушенням функції печінки Після щоденного прийому клопідогрелу протягом 10 днів у добовій дозі 75 мг у пацієнтів з тяжким ураженням печінки інгібування АДФ-індукованої агрегації тромбоцитів можна порівняти з даними у здорових добровольців. Середній час кровотечі також можна порівняти в обох групах. Пацієнти різної етнічної приналежності Поширеність алелей генів ізоферменту CYP2C19, які відповідають за проміжний та знижений метаболізм клопідогрелу до його активного метаболіту, відрізняється у представників різних етнічних груп. Є лише обмежені дані для представників монголоїдної раси щодо оцінки впливу генотипу ізоферменту CYP2C19 на клінічні результуючі події. Підлога У невеликому дослідженні, що порівнює фармакодинамічні властивості клопідогрелу у чоловіків та жінок, у жінок спостерігалося менше інгібування АДФ-індукованої агрегації тромбоцитів, але відмінностей у подовженні часу кровотечі не було. У великому контрольованому дослідженні CAPRIE (клопідогрел у порівнянні з АСК у пацієнтів з ризиком розвитку ішемічних ускладнень), частота клінічних результатів, інших побічних дій та відхилень від норми клініко-лабораторних показників була однаковою як у чоловіків, так і у жінок.ПередозуванняСимптоми передозування Передозування клопідогрелу може призвести до збільшення часу кровотечі з подальшими ускладненнями у вигляді розвитку кровотеч. Заходи щодо надання допомоги при передозуванні З появою кровотечі потрібне проведення відповідних лікувальних заходів. Антидот клопідогрелу не встановлено. Якщо необхідна швидка корекція часу кровотечі, що подовжився, то рекомендується проведення переливання тромбоцитарної маси.Запобіжні заходи та особливі вказівкиПри лікуванні клопідогрелом, особливо протягом перших тижнів лікування та/або після інвазивних кардіологічних процедур/хірургічного втручання, необхідно вести ретельне спостереження за пацієнтами щодо виключення ознак кровотечі, у тому числі і прихованого. Кровотечі та гематологічні порушення У зв'язку з ризиком розвитку кровотечі та небажаних явищ з боку крові у разі появи в ході лікування клінічних симптомів, підозрілих на виникнення кровотечі, слід терміново зробити загальний клінічний аналіз крові, визначити активований частковий тромбопластиновий час (АЧТВ), кількість тромбоцитів, показники функціональної активності тром та провести інші необхідні дослідження. Одночасне застосування клопідогрелу з варфарином може посилити ризик кровотечі (див. розділ "Взаємодія з іншими лікарськими засобами"), тому слід бути обережним при одночасному застосуванні клопідогрелу та варфарину. Клопідогрел, як і інші антитромбоцитарні засоби, слід застосовувати з обережністю у пацієнтів, які мають підвищений ризик розвитку кровотечі, пов'язаний з травмами, хірургічними втручаннями або іншими патологічними станами, а також у пацієнтів, які приймають АСК, НПЗП (у тому числі інгібітори ЦОГ-2). , гепарин, блокатори глікопротеїну IIb/IIIа, СІОЗС та потужні індуктори ізоферменту CYP2C19 Якщо пацієнт має планову хірургічну операцію, і при цьому немає необхідності в антитромбоцитарному ефекті, то за 5-7 днів до операції прийом клопідогрелу слід припинити. Клопідогрел подовжує час кровотечі і повинен застосовуватися з обережністю у пацієнтів із захворюваннями, що схильні до розвитку кровотеч (особливо, шлунково-кишкових та внутрішньоочних). Препарати, які можуть спричинити пошкодження слизової оболонки шлунково-кишкового тракту (такі як АСК, нестероїдні протизапальні засоби) у пацієнтів, які приймають клопідогрел, слід застосовувати з обережністю. Пацієнти повинні бути попереджені про те, що при прийомі клопідогрелу (одного або в комбінації з АСК) для зупинки кровотечі може знадобитися більше часу, а також про те, що у разі виникнення у них незвичайної (по локалізації або тривалості) кровотечі їм слід повідомити про це свого лікаря. Перед будь-якою майбутньою операцією та перед початком прийому будь-якого нового лікарського препарату пацієнти повинні повідомляти лікаря (включаючи стоматолога) про прийом клопідогрелу. Нещодавно перенесений ішемічний інсульт Показано, що у пацієнтів з нещодавно перенесеним минущим порушенням мозкового кровообігу або інсультом, що мають високий ризик розвитку повторних ішемічних ускладнень, комбінація АСК та клопідогрелу підвищує частоту розвитку великих кровотеч. Тому така комбінована терапія повинна проводитися з обережністю і лише у разі доведеної клінічної користі від її застосування. Прийом клопідогрелу не рекомендується при гострому інсульті з давністю менше 7 днів (оскільки відсутні дані щодо його застосування при цьому стані). Тромботична тромбоцитопенічна пурпура (ТТП) Дуже рідко після застосування клопідогрелу (іноді навіть нетривалого) відзначалися випадки розвитку тромботичної тромбоцитопенічної пурпури (ТТП), яка характеризується тромбоцитопенією та мікроангіопатичною гемолітичною анемією, що супроводжуються неврологічними розладами, порушенням функції. ТТП є потенційно загрозливим для життя станом, що вимагає негайного лікування, включаючи плазмаферез. Набута гемофілія Повідомлялося про випадки розвитку набутої гемофілії прийому клопідогрелу. При підтвердженому ізольованому збільшенні АЧТВ, що супроводжується або не супроводжується розвитком кровотечі, слід розглянути питання можливості розвитку набутої гемофілії. Пацієнти з підтвердженим діагнозом набутої гемофілії повинні спостерігатися та лікуватися фахівцями з цього захворювання та припинити прийом клопідогрелу. Функціональна активність ізоферменту CYP2C19 У пацієнтів з низькою активністю ізоферменту CYP2C19 при застосуванні клопідогрелу в рекомендованих дозах утворюється менше активного метаболіту клопідогрелу і слабше виражена його антиагрегантна дія, у зв'язку з чим при прийомі звичайно рекомендованих доз клопідогрелу при гострому коронарному синдромі. судинних ускладнень, ніж у пацієнтів із нормальною активністю ізоферменту CYP2C19. Очікується, що застосування лікарських засобів, які індукують активність ізоферменту CYP2C19, може спричинити збільшення концентрації активного метаболіту клопідогрелу та підвищувати ризик виникнення кровотечі. В якості запобіжного заходу не рекомендується застосовувати одночасно потужні індуктори ізоферменту CYP2C19 і клопідогрел. Є тести визначення генотипу CYP2C19, які можуть бути використані для допомоги у виборі терапевтичної стратегії. Слід розглянути питання застосування більш високих доз клопідогрелу у пацієнтів з низькою активністю CYP2C19. Перехресні алергічні та/або гематологічні реакції між тієнопіридинами У пацієнтів слід збирати анамнез на предмет алергічних та/або гематологічних реакцій, що були раніше, на інші тієнопіридини (такі як тіклопідин, прасугрел), оскільки повідомлялося про наявність перехресних алергічних та/або гематологічних реакцій між тіенопіридинами (див. розділ "Побічна дія"). Тієнопіридини можуть викликати помірні та тяжкі алергічні реакції (такі як висипання на шкірі, ангіоневротичний набряк) або гематологічні реакції (такі як тромбоцитопенія і нейтропенія). Пацієнти, у яких раніше спостерігалися алергічні та/або гематологічні реакції на один із препаратів групи тієнопіридинів, можуть мати підвищений ризик розвитку подібних реакцій на інший препарат групи тієнопіридинів. Рекомендується моніторинг перехресних алергічних та/або гематологічних реакцій. Ниркова недостатність Досвід застосування клопідогрелу у пацієнтів з тяжкою нирковою недостатністю обмежений. Тому слід з обережністю застосовувати клопідогрел у цієї групи пацієнтів. Печінкова недостатність Є обмежений досвід застосування клопідогрелу у пацієнтів з тяжкими захворюваннями печінки, які можуть бути схильними до розвитку геморагічного діатезу. Тому слід з обережністю застосовувати клопідогрел у цієї групи пацієнтів. Вплив на здатність до керування автотранспортом та управління механізмами Препарат Плавікс® не істотно впливає на здібності, необхідні для керування автомобілем або заняття іншими потенційно небезпечними видами діяльності.Умови відпустки з аптекЗа рецептомВідео на цю тему
1 745,00 грн
187,00 грн
Склад, форма випуску та упаковкаПігулки - 1 таб. діюча речовина: клопідогрел гідросульфат у формі II - 97,875 мг (у перерахунку на клопідогрел - 75,0 мг); допоміжні речовини: манітол, макрогол-6000, целюлоза мікрокристалічна (з низьким вмістом води, 90 мкм), гіпоролоза низькозаміщена, рицинова олія гідрогенізована; плівкова оболонка: опадрай рожевий (лактози моногідрат, гіпромелозу, титану діоксид (Е 171), тріацетин, барвник заліза оксид червоний (Е 172)), карнаубський віск. По 7, 10 або 14 таблеток у блістер з ПВХ/ПВДХ та фольги алюмінієвої або ПА/Ал/ПВХ та фольги алюмінієвої. По 1, 2 або 3 блістери по 7 або 14 таблеток; по 1, 2, 3 або 10 блістерів по 10 таблеток разом з інструкцією із застосування в картонну пачку.Опис лікарської формиКруглі, злегка двоопуклі таблетки, покриті плівковою оболонкою рожевого кольору, з гравіюванням "75" з одного боку і "1171" з іншого боку.Фармакотерапевтична групаАнтиагрегантний засіб.ФармакокінетикаВсмоктування При одноразовому та повторному прийомі внутрішньо у дозі 75 мг на добу клопідогрел швидко всмоктується. Середнє значення максимальної концентрації (Сmax) незміненого клопідогрелу в плазмі крові (приблизно 2,2-2,5 нг/мл після прийому внутрішньо разової дози 75 мг) досягається приблизно через 45 хв після прийому препарату. За даними екскреції метаболітів клопідогрелу через нирки його абсорбція становить приблизно 50%. Розподіл In vitro клопідогрел і його основний циркулюючий у крові неактивний метаболіт оборотно зв'язуються з білками плазми крові (на 98% і 94%, відповідно), і цей зв'язок є ненасиченим до концентрації 100 мг/мл. Метаболізм Клопідогрел інтенсивно метаболізується у печінці. In vitro та in vivo клопідогрел метаболізується двома шляхами: перший здійснюється за допомогою естераз і призводить до гідролізу клопідогрелу з утворенням неактивного похідного карбоксильної кислоти (85 % від циркулюючих метаболітів); другий шлях здійснюється за допомогою ізоферментів цитохром Р450. Спочатку клопідогрел метаболізується до 2-оксо-клопідогрелу, що є проміжним метаболітом. Подальший метаболізм 2-оксо-клопідогрелу призводить до утворення активного метаболіту клопідогрелу - тіольного похідного клопідогрелу. In vitro цей активний метаболіт утворюється головним чином за допомогою ізоферменту CYP2C19. але в його освіті також беруть участь деякі інші ізоферменти, включаючи CYP1A2, CYP2B6 та CYP3A4. Активний тіольний метаболіт клопідогрелу, виділений у in vitro дослідженнях, швидко та незворотно зв'язується з рецепторами тромбоцитів, блокуючи таким чином агрегацію тромбоцитів. Смах активного метаболіту клопідогрелу після одноразового прийому його навантажувальної дози 300 мг у 2 рази перевищує таку після 4-х днів прийому підтримуючої дози клопідогрелу 75 мг. Сmax досягається приблизно 30-60 хв. Виведення Протягом 120 годин після прийому внутрішньо людиною 14С-міченого клопідогрелу близько 50% радіоактивності виводиться через нирки та приблизно 46% радіоактивності виводиться через кишечник. Після одноразового прийому внутрішньо дозування в 75 мг період напіввиведення (Т1/2) клопідогрелу становить приблизно 6 годин. Фармакогенетика За допомогою ізоферменту CYP2C19 утворюються як активний метаболіт, так і проміжний метаболіт - 2-оксо-клопідогрел. Фармакокінетика та антиагрегантна дія активного метаболіту клопідогрелу, при дослідженні агрегації тромбоцитів ex vivo, варіюють залежно від генотипу ізоферменту CYP2C19. Алель гена CYP2CI9*1 відповідає повністю функціональному метаболізму, тоді як алелі генів CYP2C19*2 та CYP2C19*3 є нефункціональними. Алелі генів CYP2C19*2 та CYP2C 19*3 є причиною зниження метаболізму у більшості представників європеоїдної (85%) та монголоїдної раси (99%). Інші алелі, з якими пов'язана відсутність або зниження метаболізму, зустрічаються рідше і включають, але не обмежуються алелями генів CYP2C19*4, *5, *6, *7 і *8.Пацієнти з низькою активністю ізоферменту CYP2CI9 повинні мати дві зазначені вище алелі гена з втратою функції. Опубліковані частоти фенотипів пацієнтів з низькою активністю ізоферменту CYP2C19 у пацієнтів європеоїдної раси становлять 2%, у пацієнтів негроїдної раси - 4% і у монголоїдної раси - 14%. Існують спеціальні тести для визначення наявного у пацієнта генотипу ізоферменту CYP2C19. За даними перехресного дослідження (40 добровольців) за участю добровольців з дуже високою, високою, проміжною та низькою активністю ізоферменту CYP2C19, будь-яких суттєвих відмінностей в експозиції активного метаболіту та у середніх значеннях інгібування агрегації тромбоцитів (ІАТ), індукованої АД дуже високою, високою та проміжною активністю ізоферменту CYP2C19 виявлено не було. У добровольців із низькою активністю ізоферменту CYP2C19 експозиція активного метаболіту знижувалась на 63-71 % порівняно з добровольцями з високою активністю ізоферменту CYP2C19. При використанні схеми лікування 300 мг навантажувальна доза/75 мг підтримуюча доза (300 мг/75 мг) у добровольців з низькою активністю ізоферменту CYP2C19 антитромбоцитарна дія знижувалась із середніми значеннями ІАТ,складовими 24% (через 24 год) та 37% (на 5 день дослідження) порівняно з ІАТ, складовими 39% (через 24 год) та 58% (на 5 день дослідження), у добровольців з високою активністю ізоферменту CYP2C19 та 37% (через 24 год) та 60% (на 5 день дослідження) у добровольців із проміжною активністю ізоферменту CYP2C19. Коли добровольці з низькою активністю ізоферменту CYP2C19 отримували препарат за схемою лікування 600 мг навантажувальна доза/150 мг підтримуюча доза (600 мг/150 мг), експозиція активного метаболіту була вищою, ніж при прийомі за схемою лікування 300 мг/75 мг. Крім цього, ІАТ становило 32% (через 24 год) і 61% (на 5 день дослідження), що було більше такого у добровольців з низькою активністю ізоферменту CYP2C19, які отримували лікування за схемою 300 мг/75 мг, і було подібно до такого в групах пацієнтів з більш високою інтенсивністю CYP2C 19 метаболізму. одержували лікування за схемою 300 мг/75 мг. Однак у дослідженнях з урахуванням клінічних результатів режим дозування клопідогрелу для пацієнтів цієї групи (пацієнтів з низькою активністю ізоферменту CYP2C19) наразі не встановлено. Аналогічно результатам даного дослідження мета-аналіз шести досліджень, до якого увійшли дані 335 добровольців, які отримували клопідогрел і перебували в стані досягнення рівноважної концентрації, показав, що в порівнянні з добровольцями з високою активністю ізоферменту CYP2C19, у добровольців з проміжною активністю ізоферменту CYP2C знижувалася на 28%, а у добровольців з низькою активністю ізоферменту CYP2C19 - на 72%, тоді як ІАТ було знижено з відмінностями в ІАТ на 5,9% та 21,4% відповідно. Не проводилося оцінки впливу генотипу CYP2CI9 на клінічні результати у пацієнтів, які отримували клопідогрел, у проспективних рандомізованих контрольованих дослідженнях. Проте зараз є кілька ретроспективних аналізів. Результати генотипування отримані в ході наступних клінічних досліджень: CURE, CHARISMA, CLARITY-TIM1 28, TRITON-TIMI 38 та ACT1VE-A, а також у кількох опублікованих когортних дослідженнях. У дослідженні TRITON-TIMI 38 та 3-х когортних дослідженнях (Collet, Sibbing, Giusti) пацієнти комбінованої групи з проміжною або низькою активністю ізоферменту CYP2C19 мали більш високу частоту серцево-судинних ускладнень (смерть, інфаркт міокарда та інсульт). з такими у пацієнтів із високою активністю ізоферменту CYP2C19. У дослідженні CHARISMA та одному когортному дослідженні (Simon) збільшення частоти серцево-судинних ускладнень спостерігалося тільки у пацієнтів з низькою активністю ізоферменту CYP2C19 (при їх порівнянні з пацієнтами з високою активністю ізоферменту CYP2C19). Дослідження CURE, CLARITY. ACTIVE- і одному з когортних досліджень (Trenk), не спостерігалося збільшення частоти серцево-судинних ускладнень в залежності від інтенсивності CYP2C 19- метаболізму. Особливі групи пацієнтів Фармакокінетика активного метаболіту клопідогрелу в спеціальних групах пацієнтів не вивчалася. Пацієнти старші 75 років: у добровольців старше 75 років при порівнянні з молодими добровольцями не було отримано відмінностей за показниками агрегації тромбоцитів та часу кровотечі. Корекція дози не потрібна. Дитячий вік до 18 років: клінічні дані відсутні. Пацієнти з порушенням функції нирок Після повторних прийомів клопідогрелу в дозі 75 мг/добу у пацієнтів з тяжкими порушеннями функції нирок (кліренс креатиніну (КК) від 5 мл/хв до 15 мл/хв) інгібування АДФ-індукованої агрегації тромбоцитів було нижчим (на 25 %) порівняно з таким у здорових добровольців, проте подовження часу кровотечі було подібним до такого у здорових добровольців, які отримували клопідогрел у дозуванні 75 мг на добу. Пацієнти з порушенням функції печінки Не було значних відмінностей у ступені інгібування АДФ-індукованої агрегації тромбоцитів після щоденного прийому клопідогрелу у добовій дозі 75 мг протягом 10 днів у пацієнтів з тяжкими порушеннями функції печінки порівняно зі здоровими добровольцями. Середній час кровотечі також можна порівняти в обох групах. Расова приналежність Поширеність алелей генів ізоферменту CYP2C19, що зумовлюють проміжну та низьку активність цього ізоферменту, відрізняється у представників різних расових груп. Є обмежені літературні дані про їх поширеність у представників монголоїдної раси, що не дозволяє оцінити значення генотипування ізоферменту CYP2C19 для розвитку ішемічних ускладнень.ФармакодинамікаКлопідогрел є проліком, один з активних метаболітів якого є інгібітором агрегації тромбоцитів. Для утворення активного метаболіту, який пригнічує агрегацію тромбоцитів, клопідогрел повинен метаболізуватися за допомогою ізоферментів системи цитохрому Р450 (CYP450). Активний метаболіт клопідогрелу селективно інгібує зв'язування аденозиндифосфату (АДФ) з P2Yi2 рецептором тромбоцитів та подальшу АДФ-опосередковану активацію комплексу GPIIb/IIIa, що призводить до придушення агрегації тромбоцитів. Завдяки необоротному зв'язуванню, тромбоцити залишаються несприйнятливими до стимуляції АДФ протягом всього терміну свого життя (приблизно 7-10 днів), а відновлення нормальної функції тромбоцитів відбувається зі швидкістю, що відповідає швидкості оновлення тромбоцитів. Агрегація тромбоцитів, спричинена агоністами, відмінними від АДФ. також інгібується за рахунок блокади посиленої активації тромбоцитів АДФ, що вивільняється. Оскільки утворення активного метаболіту відбувається за допомогою ізоферментів системи цитохрому Р450, деякі з яких можуть відрізнятися поліморфізмом або інгібуватися іншими препаратами, не у всіх пацієнтів можливе адекватне пригнічення агрегації тромбоцитів. При щоденному прийомі клопідогрелу в дозі 75 мг з першого ж дня прийому відзначається значне пригнічення АДФ-індукованої агрегації тромбоцитів, яке поступово збільшується протягом 3-7 днів і потім виходить на постійний рівень (при досягненні рівноважного стану). У рівноважному стані агрегація тромбоцитів пригнічується загалом на 40-60 %. Після припинення прийому клопідогрелу агрегація тромбоцитів та час кровотечі поступово повертаються до початкового рівня, в середньому, протягом 5 днів. У ході клінічного дослідження ACTIVE-А показано, що у пацієнтів з фібриляцією передсердь, які мали щонайменше. один фактор ризику розвитку судинних ускладнень, але були нездатні приймати непрямі антикоагулянти, клопідогрел у поєднанні з ацетилсаліциловою кислотою (АСК) (у порівнянні з прийомом тільки однієї АСК) зменшував частоту разом узятих інсульту, інфаркту міокарда, системної тромбоемболії поза центральною або судинної смерті, переважно за рахунок зменшення ризику розвитку інсульту. Ефективність прийому клопідогрелу у поєднанні з АСК виявлялася рано і зберігалася до 5 років. Зменшення ризику великих судинних ускладнень у групі пацієнтів, які приймали клопідогрел у поєднанні з АСК, спостерігалося переважно за рахунок більшого зменшення частоти інсультів. Ризик розвитку інсульту будь-якої тяжкості при прийомі клопідогрелу у поєднанні з АСК знижувався, а також спостерігалася тенденція до зниження частоти розвитку інфаркту міокарда в групі, яка отримувала лікування клопідогрелом у поєднанні з АСК, але не спостерігалося відмінностей у частоті тромбоемболій поза ЦНС або судинної смерті. Крім цього, прийом клопідогрелу у поєднанні з АСК зменшував загальну кількість днів госпіталізації з серцево-судинних причин. Перехід з терапії потужним інгібітором рецепторів P2Y12 на лікування клопідогрелом у поєднанні з АСК після завершення гострої фази гострого інфаркту міокарда (ГІМ) вивчався у двох рандомізованих ініційованих дослідником клінічних дослідженнях (TOPIC та TROPICAL-ACS). У рандомізованому відкритому клінічному дослідженні TOPIC брали участь пацієнти, які перенесли ГІМ, яким виконувалось черезшкірне коронарне втручання (ЧКВ). Пацієнти, які отримували АСК та один з найбільш потужних інгібіторів рецепторів P2Y12, у яких не розвинулися несприятливі події протягом одного місяця, або були переведені на терапію фіксованою комбінацією АСК та клопідогрелу (деескалація подвійної антитромбоцитарної терапії (ДАТ)) або продовжили приймати Постійна ДАТ). Події, включені в комбіновану первинну кінцеву точку (смерть від ускладнень серцево-судинних захворювань (ССЗ), інсульт, екстрена реваскуляризація та кровотечі типу 2 або тяжкі кровотечі за шкалою BARC (Дослідницького академічного консорціуму за кровотечами)), через один були зареєстровані у 43 з 322 пацієнтів (13,4%) у групі деескалації ДАТ та 85 пацієнтів з 323 (26,3 %) у групі незмінної ДАТ (р Статистично значуща відмінність в основному зумовлена скороченням кількості випадків кровотечі, у тому числі кровотеч, які за шкалою BARC більш або рівні 2 (4% у групі деескалації та 14,9% у групі, що отримувала незмінену ДАТ), при цьому не спостерігалося істотних відмінностей у частоті ішемічних ускладнень (р = 0,36). До рандомізованого відкритого клінічного дослідження TROPICAL-ACS було включено 2610 пацієнтів з ГІМ. підтвердженим аналізом на біомаркери після проведення ЧКВ. Пацієнти були рандомізовані до груп для отримання прасугрелу (дні 0-14) або прасугрелу (дні 0-7), а потім клопідогрелу (дні 8-14) у комбінації з АСК. На 14-й день було проведено оцінку функції тромбоцитів. Пацієнти з першої групи терапії лише прасугрелом продовжували приймати прасугрел протягом 11,5 місяці. У пацієнтів із групи заміни терапії було виконано аналіз на високу реактивність тромбоцитів (ДРТ). Пацієнти з ДРТ ≥ 46 одиниць були переведені на терапію прасугрелом, яку отримували протягом 11,5 місяця. Пацієнти з ДРТПоказання до застосуванняВторинна профілактика атеротромботичних ускладнень: У дорослих пацієнтів після нещодавно перенесеного інфаркту міокарда (з давністю від декількох днів до 35 днів), нещодавно перенесеного ішемічного інсульту (з давністю від 7 днів до 6 місяців) або при діагностованій оклюзійній хворобі периферичних артерій прийом клопідогрелу знижував частоту комбінованої ішемічний інсульт (з летальними наслідками або без нього), повторний інфаркт міокарда (з летальними наслідками або без нього) та іншу серцево-судинну смерть. У дорослих пацієнтів із гострим коронарним синдромом: гострий коронарний синдром без підйому сегмента ST (нестабільна стенокардія/інфаркт міокарда без зубця Q), включаючи пацієнтів, які повинні отримувати медикаментозне лікування, та пацієнтів, яким показано черезшкірне коронарне втручання (зі стенуванням або без стентування) або аортокоронарне шунтування (АКШ). Прийом клопідогрелу знижував частоту комбінованої кінцевої точки, що включала серцево-судинну смерть, інфаркт міокарда або інсульт, а також частоту комбінованої кінцевої точки, що включала серцево-судинну смерть, інфаркт міокарда, інсульт, рефрактерну ішемію. гострий інфаркт міокарда із підйомом сегмента ST. Прийом клопідогрелу знижував смертність від будь-яких причин, а також частоту комбінованої кінцевої точки, що включала смерть, повторний інфаркт міокарда або інсульт. Профілактика атеротромботичних та тромбоемболічних ускладнень у дорослих пацієнтів з фібриляцією передсердь (миготливою аритмією) Показано, що у пацієнтів з фібриляцією передсердь з підвищеним ризиком судинних ускладнень терапія непрямими антикоагулянтами, які є антагоністами вітаміну К (АВК), пов'язана з більшою клінічною користю порівняно із застосуванням тільки АСК або комбінації клопідогрелу з АСК щодо зниження. Пацієнтам з фібриляцією передсердь (миготливою аритмією), що мають, як мінімум, один фактор ризику розвитку судинних ускладнень, які не можуть приймати АВК (наприклад, за наявного особливого ризику кровотечі, нездатності пацієнта, на думку лікаря, адекватно контролювати МНО (міжнародне нормалізоване) ставлення) або у разі неприйняття пацієнтом лікування АВК), для запобігання атеротромботичних та тромбоемболічних ускладнень. включаючи інсульт, показаний прийом клопідогрелу в комбінації з АСК. Показано, що клопідогрел у комбінації з АСК знижував частоту комбінованої кінцевої точки, що включала інсульт, інфаркт міокарда, системну тромбоемболію поза ЦНС або серцево-судинну смерть, переважно за рахунок зниження частоти розвитку інсульту.Протипоказання до застосуванняПідвищена чутливість до клопідогрелу або будь-якої з допоміжних речовин препарату. Тяжка печінкова недостатність. Гостра кровотеча, наприклад, кровотеча з виразки або внутрішньочерепний крововилив. Рідкісна спадкова непереносимість галактози, дефіцит лактази та глюкозо-галактозна мальабсорбція. Вагітність та період грудного вигодовування. Дитячий вік до 18 років (безпека та ефективність застосування не встановлені). З обережністю: При помірній печінковій недостатності, при якій можлива схильність до кровотечі (обмежений клінічний досвід застосування). При нирковій недостатності (обмежений клінічний досвід застосування). При захворюваннях, при яких є схильність до розвитку кровотеч (зокрема шлунково-кишкових або внутрішньоочних), і, особливо, при одночасному застосуванні лікарських засобів, які можуть спричинити ушкодження слизової оболонки шлунково-кишкового тракту (таких як АСК та нестероїдні протизапальні препарати ( НПЗП)). У пацієнтів, у яких є підвищений ризик розвитку кровотечі: через травму, хірургічне втручання або інші патологічні стани, а також у пацієнтів, які отримують лікування АСК, гепарином, варфарином, інгібіторами глікопротеїну IIb/IIIa, НПЗЗ, у тому числі селективними інгібіторами. -2 (ЦОГ-2), а також іншими лікарськими засобами, застосування яких пов'язане з ризиком кровотеч, селективними інгібіторами зворотного захоплення серотоніну (СІОЗС). При одночасному застосуванні з лікарськими засобами, що є субстратами ізоферменту CYP2C8 (репаглінід, паклітаксел). У пацієнтів із низькою активністю ізоферменту CYP2C19. При вказівках в анамнезені алергічні та гематологічні реакції на інші тієнопіридини (такі як тіклопідін, прасугрел). При нещодавно перенесеному минущому порушенні мозкового кровообігу або ішемічному інсульті.Вагітність та лактаціяВагітність Дослідження на тваринах не виявили ні прямих, ні непрямих несприятливих ефектів протягом вагітності, ембріональний розвиток, пологи та постнатальний розвиток. Так як не завжди за результатами досліджень на тваринах можна передбачити реакцію у людини, і внаслідок відсутності даних контрольованих клінічних досліджень щодо прийому клопідогрелу вагітними жінками, як запобіжний засіб не рекомендується прийом клопідогрелу під час вагітності, за винятком тих випадків, коли, на думку лікаря , Його застосування настійно необхідне. Період грудного вигодовування У дослідженнях на щурах показано, що клопідогрел та/або його метаболіти виділяються з грудним молоком. Невідомо, чи виділяється клопідогрел із грудним молоком людини. Так як багато лікарських засобів виділяються з грудним молоком і існує ризик розвитку потенційних несприятливих явищ у дитини, яка перебуває на грудному вигодовуванні, слід прийняти рішення про припинення грудного вигодовування або про відміну препарату з урахуванням необхідності його застосування для матері.Побічна діяДані, отримані під час клінічних досліджень Безпека клопідогрелу вивчена більш ніж у 44 000 пацієнтів, у тому числі більш ніж у 12 000 пацієнтів, які отримували лікування протягом року або більше. Загалом переносимість клопідогрелу в дозі 75 мг/добу у дослідженні CAPRIE відповідала переносимості АСК у дозі 325 мг/добу, незалежно від віку, статі та расової належності пацієнтів. Нижче наведено клінічно значущі небажані явища, що спостерігалися у п'яти великих клінічних дослідженнях: CAPRIE, CURE, CLARITY, COMMIT та ACTIVE-A. Кровотечі та крововиливу Порівняння монотерапії клопідогрелом та АСК У клінічному дослідженні CAPRIE загальна частота всіх кровотеч у пацієнтів, які приймали клопідогрел, та у пацієнтів, які приймали АСК, склала 9,3%. Частота важких кровотеч при застосуванні клопідогрелу та АСК була порівнянною: 1,4 % та 1,6 % відповідно. Загалом частота розвитку шлунково-кишкових кровотеч у пацієнтів, які приймали клопідогрел, та у пацієнтів, які приймали АСК, становила 2.0 % та 2,7 %, відповідно, у тому числі частота шлунково-кишкових кровотеч, які потребували госпіталізації, становила 0,7 % та 1,1% відповідно. Загальна частота кровотеч іншої локалізації при прийомі клопідогрелу порівняно з прийомом АСК була вищою (7,3% проти 6,5%, відповідно). Однак частота важких кровотеч при застосуванні клопідогрелу та АСК була порівнянною (0,6% або 0,4% відповідно). Найчастіше повідомлялося про розвиток наступних кровотеч: пурпура / синці, носова кровотеча. Рідше повідомлялося про розвиток гематом, гематурії та очних крововиливів (головним чином, кон'юнктивальних). Частота внутрішньочерепних крововиливів при застосуванні клопідогрелу та АСК була порівнянною (0,4 % або 0,5 % відповідно). Порівняння комбінованої терапії клопідогрел+АСК та плацебо+АСК У клінічному дослідженні CURE у пацієнтів, які приймали клопідогрел+АСК, у порівнянні з пацієнтами, які приймали плацебо+АСК, спостерігалося збільшення частоти розвитку великих кровотеч (3,7 % порівняно 2,7 %), та малих кровотеч (5,1 % за порівняно 2.4%). В основному, джерелами великих кровотеч були шлунково-кишковий тракт (ШКТ) та місця пункції артерій. Частота розвитку загрозливих для життя кровотеч у пацієнтів, які приймали клопідогрел+АСК у порівнянні з пацієнтами, які приймали плацебо+АСК, достовірно не відрізнялася (2,2 % та 1,8 %, відповідно), частота розвитку фатальних кровотеч була однаковою (0.2 % при обох види терапії). Частота виникнення не загрожують життю великих кровотеч була достовірно вищою у пацієнтів, які приймали клопідогрел+АСК, порівняно з пацієнтами, які приймали плацебо+АСК (1,6 % та 1 %, відповідно), але частота розвитку внутрішньочерепних крововиливів була однаковою (0,1 % за обох видів терапії). Частота розвитку великих кровотеч у групі клопідогрел+АСК залежала від дози АСК (< 100 мг: 2,6%; 100-200 мг: 3,5 %; > 200 мг: 4,9 %), а також частота розвитку великих кровотеч у групі плацебо+АСК (< 100 мг: 2,0%; 100-200 мг: 2,3%; > 200 мг: 4,0%). У пацієнтів, які припинили антитромбоцитарну терапію більш ніж за 5 днів до аортокоронарного шунтування, не відзначалося почастішання випадків розвитку великих кровотеч протягом 7 днів після втручання (4,4% у групі клопідогрел+АСК та 5,3% у групі плацебо+АСК). У пацієнтів, які продовжували антитромбоцитарну терапію протягом останніх п'яти днів перед аортокоронарним шунтуванням, частота цих подій після втручання становила 9,6% (у групі клопідогрел+АСК) та 6,3% (у групі плацебо+АСК). У клінічному дослідженні CLARITY частота великих кровотеч (визначуваних як внутрішньочерепні кровотечі або кровотечі зі зниженням гемоглобіну > 5 г/дл) в обох групах (клопідогрел+АСК і плацебо+АСК) була порівнянною в обох групах лікування (1,3 % проти 1, 1% у групі клопідогрел+АСК та групі плацебо+АСК, відповідно). Вона була однаковою у підгрупах пацієнтів, розділених за вихідними характеристиками та за видами фібринолітичної терапії або гепаринотерапії. Частота виникнення фатальних кровотеч (0.8% проти 0,6%) та внутрішньочерепних крововиливів (0,5% проти 0,7%) при лікуванні клопідогрел+АСК та плацебо+АСК, відповідно, була низькою та порівнянною в обох групах лікування. У клінічному дослідженні COMMIT загальна частота нецеребральних великих кровотеч або церебральних кровотеч була низькою та однаковою (0,6% у групі клопідогрел+АСК та 0,5% у групі плацебо+АСК). У клінічному дослідженні ACTIVE-A частота розвитку великих кровотеч у групі клопідогрел+АСК була вищою, ніж у групі плацебо+АСК (6,7 % проти 4,3 % відповідно). Великі кровотечі переважно були позачерепними в обох групах (5,3% проти 3,5%), головним чином, із шлунково-кишкового тракту (3,5% проти 1,8%). У групі клопідогрел+АСК внутрішньочерепних крововиливів було більше порівняно з групою плацебо+АСК (1,4% проти 0.8%, відповідно). Відсутні статистично значущі відмінності між цими групами лікування у частоті виникнення фатальних кровотеч (1,1% проти 0,7%) та геморагічного інсульту (0,8% проти 0.6%). Порушення з боку крові У дослідженні CAPRIE, тяжка нейтропенія ( У двох із 9599 пацієнтів, які приймали клопідогрел, спостерігалася повна відсутність нейтрофілів у периферичній крові, якого не спостерігалося в жодного з 9586 пацієнтів, які приймали АСК. Незважаючи на те, що ризик розвитку мієлотоксичної дії при прийомі клопідогрелу є досить низьким, якщо у пацієнта, який приймає клопідогрел, спостерігається підвищення температури або з'являються інші ознаки інфекції. слід обстежити пацієнта щодо можливої нейтропенії. При лікуванні клопідогрелом в одному випадку спостерігався розвиток апластичної анемії. Частота виникнення тяжкої тромбоцитопенії ( У дослідженнях CURE та CLARITY спостерігалася порівнянна кількість пацієнтів із тромбоцитопенією або нейтропенією в обох групах лікування. Інші клінічно значущі небажані реакції, що спостерігалися під час проведення клінічних досліджень CAPRIE, CURE, CLARITY COMMIT та ACTIVE-A Частота виникнення небажаних реакцій визначалася відповідно до класифікації Всесвітньої Організації Охорони Здоров'я: дуже часто (≥ 1/10); часто (≥ 1/100 та < 1/10); нечасто (≥ 1/1000 та < 1/100); рідко (≥ 1/10000 та < 1/1000); дуже рідко (< 1/10000), частота невідома (не може бути підрахована на підставі наявних даних). Порушення з боку нервової системи: нечасто – головний біль, запаморочення, парестезія; рідко – вертиго. Порушення з боку шлунково-кишкового тракту: часто – диспепсія, абдомінальні болі, діарея; нечасто - нудота, гастрит, здуття живота, запор, блювання, виразка шлунка, виразка дванадцятипалої кишки. Порушення з боку шкіри та підшкірних тканин: нечасто – шкірний висип, свербіж шкіри. Порушення з боку крові та лімфатичної системи: нечасто – збільшення часу кровотечі, зниження кількості тромбоцитів у периферичній крові; лейкопенія, зниження кількості нейтрофілів у периферичній крові, еозинофілія. Постмаркетинговий досвід застосування препарату Порушення з боку крові та лімфатичної системи: частота невідома - випадки серйозних кровотеч, переважно підшкірних, скелетно-м'язових, очних крововиливів (кон'юнктивальних, в тканині та сітківку ока), кровотеч з дихальних шляхів (кровохаркання, легеневі кровотечі) кровотеч із післяопераційних ран та випадки кровотеч із летальним результатом (особливо внутрішньочерепних крововиливів, шлунково-кишкових кровотеч та заочеревинних крововиливів); агранулоцитозу, гранулоцитопенії, апластичної анемії/панцитопенії, тромботичної тромбоцитопенічної пурпури (ТТП), придбаної гемофілії А. Порушення з боку серця: частота невідома – синдром Коунісу (вазоспастична алергічна стенокардія/алергічний інфаркт міокарда), зумовлений реакцією гіперчутливості на клопідогрел. Порушення з боку імунної системи: частота невідома – анафілактоїдні реакції, сироваткова хвороба; перехресні алергічні та гематологічні реакції з іншими тієнопіридинами (такими як тіклопідин, прасугрел), аутоімунний інсуліновий синдром (може призводити до серйозної гіпоглікемії, особливо у пацієнтів з MLA DRA4 серотипом). Порушення психіки: частота невідома – сплутаність свідомості, галюцинації. Порушення з боку нервової системи: частота невідома – порушення смакового сприйняття, агевзія. Порушення з боку судин: частота невідома – васкуліт, зниження артеріального тиску. Порушення з боку дихальної системи, органів грудної клітки та середостіння: частота невідома – бронхоспазм, інтерстиційна пневмонія, еозинофільна пневмонія. Порушення з боку шлунково-кишкового тракту: частота невідома – коліт (зокрема виразковий коліт або лімфоцитарний коліт), панкреатит, стоматит. Порушення з боку печінки та жовчовивідних шляхів: частота невідома – гепатит (неінфекційний), гостра печінкова недостатність. Порушення з боку шкіри та підшкірних тканин: частота невідома - макульозно-папульозний еритематозний або ексфоліативний висип, кропив'янка, свербіж шкіри, ангіоневротичний набряк, бульозний дерматит (багатоформна еритема, синдром Стівенса-Джонсона, токсичний ендоз гіперчутливості, лікарський висип з еозинофілією та системними проявами (DRESS-синдром), екзема, плоский лишай. Порушення з боку скелетно-м'язової та сполучної тканини: частота невідома – артралгія (біль у суглобах), артрит, міалгія. Порушення з боку нирок та сечовивідних шляхів: частота невідома – гломерулонефрит. Порушення з боку статевих органів та молочної залози: частота невідома – гінекомастія. Загальні розлади та порушення у місці введення: частота невідома – лихоманка. Лабораторні та інструментальні дані: частота невідома – відхилення від норми лабораторних показників функціонального стану печінки, підвищення концентрації креатиніну в крові.Взаємодія з лікарськими засобамиЛікарські засоби, застосування яких пов'язане із ризиком розвитку кровотечі Є підвищений ризик розвитку кровотечі внаслідок їхнього потенційного адитивного ефекту з клопідогрелом. Лікування слід проводити з обережністю. Тромболітики Безпека одночасного застосування клопідогрелу, фібрин-специфічних або фібрин-неспецифічних тромболітичних засобів та гепарину була вивчена у пацієнтів з гострим інфарктом міокарда. Частота клінічно значущих кровотеч була аналогічна тій, що спостерігалася у разі спільного застосування тромболітичних засобів та гепарину з АСК. Блокатори глікопротеїну IIb/III У зв'язку з можливістю фармакодинамічної взаємодії між клопідогрелом та блокаторами глікопротеїну IIb/IIIа, їх одночасне застосування потребує обережності, особливо у пацієнтів, які мають підвищений ризик розвитку кровотечі (при травмах та хірургічних втручаннях або інших патологічних станах). Ін'єкційні антикоагулянти (наприклад, гепарин) За даними клінічного дослідження, проведеного за участю здорових добровольців, при прийомі клопідогрелу не потрібно зміни дози гепарину і не змінювалася його антикоагулянтна дія. Одночасне застосування гепарину не змінювало антиагрегантної дії клопідогрелу. Між клопідогрелом та гепарином можлива фармакодинамічна взаємодія, яка може збільшувати ризик розвитку кровотеч. При одночасному застосуванні слід бути обережними. Пероральні антикоагулянти (наприклад, варфарин) Хоча прийом клопідогрелу 75 мг/добу не змінював фармакокінетику варфарину (субстрату ізоферменту CYP2C9) або МНО у пацієнтів, які тривало одержують лікування варфарином, одночасний прийом клопідогрелу збільшує ризик кровотечі у зв'язку з його незалежним додатковим впливом на згортання. Тому слід дотримуватися обережності при одночасному прийомі варфарину та клопідогрелу. Ацетилсаліцилова кислота (АСК) АСК не змінює інгібуючого АДФ-індуковану агрегацію тромбоцитів ефекту клопідогрелу, але клопідогрел потенціює вплив АСК на колаген-індуковану агрегацію тромбоцитів. Тим не менш, одночасний з клопідогрелом прийом АСК по 500 мг 2 рази на день протягом однієї доби не викликав суттєвого збільшення часу кровотечі, що викликається прийомом клопідогрелу. Оскільки між клопідогрелом і АСК можлива фармакодинамічна взаємодія, що призводить до підвищення ризику кровотечі, тому при їх одночасному застосуванні слід бути обережним. Тим не менш, у клінічних дослідженнях пацієнти отримували комбіновану терапію клопідогрелом та АСК (75-325 мг один раз на добу) до одного року. Нестероїдні протизапальні препарати (НПЗЗ) У клінічному дослідженні, проведеному за участю здорових добровольців, спільне застосування клопідогрелу та напроксену збільшувало приховані втрати крові через ШКТ. Однак, у зв'язку з відсутністю досліджень щодо взаємодії клопідогрелу з іншими НПЗП, наразі не відомо. є підвищений ризик шлунково-кишкових кровотеч при прийомі клопідогрелу разом з іншими нестероїдними протизапальними засобами. Тому при одночасному застосуванні нестероїдних протизапальних засобів, у тому числі інгібіторів ЦОГ-2 з клопідогрелом. слід дотримуватися обережності. Селективні інгібітори зворотного захоплення серотоніну (СІЗЗС) Оскільки СІЗЗЗ порушують активацію тромбоцитів та збільшують ризик розвитку кровотечі. При одночасному застосуванні слід бути обережними. Індуктори ізоферменту CYP2C19 Оскільки клопідогрел метаболізується до свого активного метаболіту частково за допомогою ізоферменту CYP2C19, очікується, що застосування лікарських засобів, які індукують активність цього ізоферменту, може призвести до збільшення концентрації активного метаболіту клопідогрелу. Рифампіцин, як потужний індуктор ізоферменту CYP2C19, при одночасному застосуванні з клопідогрелом, призводить як до збільшення концентрації активного метаболіту клопідогрелу, так і до інгібування тромбоцитів, що може підвищувати ризик виникнення кровотечі. В якості запобіжного заходу не рекомендується застосовувати одночасно потужні індуктори ізоферменту CYP2C19 і клопідогрел. Інгібітори ізоферменту CYP2C19 Оскільки клопідогрел метаболізується до утворення свого активного метаболіту частково за допомогою ізоферменту CYP2C19, застосування лікарських засобів, що інгібують цей ізофермент, може призвести до зменшення утворення активного метаболіту клопідогрелу. Клінічне значення цієї взаємодії встановлено. Як запобіжний засіб слід уникати одночасного застосування клопідогрелу та потужних або помірних інгібіторів ізоферменту CYP2C19. Потужними та помірними інгібіторами ізоферменту CYP2C19 є омепразол, езомепразол, флувоксамін, флуоксетин, моклобемід, вориконазол, флуконазол, тіклопідін, ципрофлоксацин, циметидин, карбамазепін, окскарбазепін. Слід уникати одночасного застосування з клопідогрелом інгібіторів протонної помпи, які є потужними або помірними інгібіторами ізоферменту CYP2C19 (наприклад, омепразолу, езомепразолу) (див. розділ "Фармакокінетика, підрозділ, Фармакогенетика", розділ "Особливі. Якщо інгібітори протонної помпи повинні прийматися одночасно з клопідогрелом, слід приймати інгібітор протонної помпи з найменшим інгібуванням ізоферменту CYP2C19, такий як пантопразол та лансопразол. Було проведено низку клінічних досліджень з клопідогрелом та іншими, одночасно застосовуваними лікарськими засобами, з метою вивчення можливих фармакодинамічних та фармакокінетичних взаємодій, які показали, що: при одночасному застосуванні клопідогрелу з атенололом та/або ніфедипіном клінічно значущої фармакодинамічної взаємодії не спостерігалося; одночасне застосування фенобарбіталу та естрогенів не мало істотного впливу на фармакодинаміку клопідогрелу; фармакокінетичні показники дигоксину та теофшліну не змінювалися при їх одночасному застосуванні з клопідогрелом; антацидні засоби не зменшували абсорбції клопідогрелу; фенітоїн та толбутамід можна з безпекою застосовувати одночасно з клопідогрелом (дослідження CAPR1E). Малоймовірно, що клопідогрел може впливати на метаболізм інших лікарських засобів, таких як фенітоїн та толбутамід, а також нестероїдні протизапальні засоби, які метаболізуються за допомогою ізоферменту CYP2C9 цитохрому Р450; інгібітори АПФ, діуретики, бета-адреноблокатори, блокатори "повільних" кальцієвих каналів, гіполіпідемічні засоби, коронарні вазодилататори, гіпоглікемічні засоби (в т.ч. інсулін), протиепшептичні засоби, гормонозамісна терапія та блокатори глікопротеїн небажаних взаємодій не виявлено. Лікарські засоби, що є субстратами ізоферменту CYP2C8 Показано, що клопідогрел збільшував системну експозицію репаглініду у здорових добровольців. Дослідження in vitro показали, що збільшення системної експозиції репаглініду є наслідком пригнічення ізоферменту CYP2C8 глюкуронідним метаболітом клопідогрелу. Слід бути обережними при одночасному застосуванні клопідогрелу та лікарських засобів, що метаболізуються за допомогою ізоферменту CYP2C8 (наприклад, репаглініду, паклітакселу) у зв'язку з ризиком збільшення їх плазмових концентрацій. Опіоїдні агоністи Як і у випадку інших пероральних інгібіторів P2Y12, одночасне застосування опіоїдних агоністів може затримувати та зменшувати абсорбцію клопідогрелу, ймовірно, через сповільнене випорожнення шлунка. Клінічне значення цієї взаємодії невідоме. Слід розглянути можливість призначення парентерального антиагрегантного препарату у пацієнтів із гострим коронарним синдромом, які потребують одночасного застосування морфіну або інших опіоїдних агоністів.Спосіб застосування та дозиВсередину, незалежно від їди. Нещодавно перенесений інфаркт міокарда, нещодавно перенесений інсульт та діагностована оклюзійна хвороба периферичних артерій Рекомендована доза – 75 мг один раз на добу. Гострий коронарний синдром без піднесення сегмента ST (нестабільна стенокардія, інфаркт міокарда без зубця Q) Лікування клопідогрелом слід починати з одноразового прийому дози навантаження 300 мг, а потім продовжувати його прийом у дозуванні 75 мг один раз на добу. Одночасно з клопідогрелом необхідно приймати АСК у дозі від 75 до 325 мг 1 раз на добу. У клінічному дослідженні CURE більшість пацієнтів із гострим коронарним синдромом додатково отримували лікування гепарином. Гострий інфаркт міокарда з підйомом сегмента ST Рекомендована добова доза клопідогрелу становить 75 мг одноразово і приймається разом з АСК із застосуванням або без застосування тромболітиків. Прийом клопідогрелу можна починати як з дози навантаження, так і без неї (у дослідженні CLARITY приймалася навантажувальна доза 300 мг). У пацієнтів старше 75 років лікування клопідогрелом має починатися без прийому його дози навантаження. Фібриляція передсердь Клопідогрел слід приймати у добовій дозі 75 мг. У комбінації з клопідогрелом необхідно приймати АСК у дозі 75-100 мг щодня. Фармакогенетика (пацієнти з генетично обумовленою зниженою активністю ізоферменту CYP2C19) Низька активність ізоферменту CYP2C19 пов'язана із зменшенням антиагрегантної дії клопідогрелу. Режим застосування більш високих доз (600 мг навантажувальна доза, потім 150 мг один раз на добу щодня) у пацієнтів з низькою активністю ізоферменту CYP2C19 збільшує антиагрегантну дію клопідогрелу. У пацієнтів з низькою активністю ізоферменту CYP2C19 можна розглянути питання про застосування більш високих доз клопідогрелу. Точний режим дозування для цієї популяції пацієнтів у клінічних дослідженнях, що враховують клінічні результати, не встановлено. Спеціальні групи патентів Дитячий вік до 18 років: безпека та ефективність застосування препарату у педіатричних популяціях не встановлені. Пацієнти старше 75 років: корекція дози не потрібна. У добровольців старше 75 років у порівнянні з молодими добровольцями не було отримано відмінностей за показниками агрегації тромбоцитів та часу кровотечі. Пацієнти з порушенням функції нирок Після повторних прийомів клопідогрелу у дозуванні 75 мг/добу у пацієнтів з тяжким ураженням нирок (КК від 5 до 15 мл/хв) інгібування АДФ-індукованої агрегації тромбоцитів (25 %) було нижчим порівняно з таким у здорових добровольців, проте подовження часу кровотечі порівняно з даними у здорових добровольців, які отримували клопідогрел у дозуванні 75 мг на добу. Пацієнти з порушенням функції печінки Після щоденного прийому клопідогрелу протягом 10 днів у добовій дозі 75 мг у пацієнтів з тяжким ураженням печінки інгібування АДФ-індукованої агрегації тромбоцитів можна порівняти з даними у здорових добровольців. Середній час кровотечі також можна порівняти в обох групах. Пацієнти різної етнічної приналежності Поширеність алелей генів ізоферменту CYP2C19, які відповідають за проміжний та знижений метаболізм клопідогрелу до його активного метаболіту, відрізняється у представників різних етнічних груп. Є лише обмежені дані для представників монголоїдної раси щодо оцінки впливу генотипу ізоферменту CYP2C19 на клінічні результуючі події. Підлога У невеликому дослідженні, що порівнює фармакодинамічні властивості клопідогрелу у чоловіків та жінок, у жінок спостерігалося менше інгібування АДФ-індукованої агрегації тромбоцитів, але відмінностей у подовженні часу кровотечі не було. У великому контрольованому дослідженні CAPRIE (клопідогрел у порівнянні з АСК у пацієнтів з ризиком розвитку ішемічних ускладнень), частота клінічних результатів, інших побічних дій та відхилень від норми клініко-лабораторних показників була однаковою як у чоловіків, так і у жінок.ПередозуванняСимптоми передозування Передозування клопідогрелу може призвести до збільшення часу кровотечі з подальшими ускладненнями у вигляді розвитку кровотеч. Заходи щодо надання допомоги при передозуванні З появою кровотечі потрібне проведення відповідних лікувальних заходів. Антидот клопідогрелу не встановлено. Якщо необхідна швидка корекція часу кровотечі, що подовжився, то рекомендується проведення переливання тромбоцитарної маси.Запобіжні заходи та особливі вказівкиПри лікуванні клопідогрелом, особливо протягом перших тижнів лікування та/або після інвазивних кардіологічних процедур/хірургічного втручання, необхідно вести ретельне спостереження за пацієнтами щодо виключення ознак кровотечі, у тому числі і прихованого. Кровотечі та гематологічні порушення У зв'язку з ризиком розвитку кровотечі та небажаних явищ з боку крові у разі появи в ході лікування клінічних симптомів, підозрілих на виникнення кровотечі, слід терміново зробити загальний клінічний аналіз крові, визначити активований частковий тромбопластиновий час (АЧТВ), кількість тромбоцитів, показники функціональної активності тром та провести інші необхідні дослідження. Одночасне застосування клопідогрелу з варфарином може посилити ризик кровотечі (див. розділ "Взаємодія з іншими лікарськими засобами"), тому слід бути обережним при одночасному застосуванні клопідогрелу та варфарину. Клопідогрел, як і інші антитромбоцитарні засоби, слід застосовувати з обережністю у пацієнтів, які мають підвищений ризик розвитку кровотечі, пов'язаний з травмами, хірургічними втручаннями або іншими патологічними станами, а також у пацієнтів, які приймають АСК, НПЗП (у тому числі інгібітори ЦОГ-2). , гепарин, блокатори глікопротеїну IIb/IIIа, СІОЗС та потужні індуктори ізоферменту CYP2C19 Якщо пацієнт має планову хірургічну операцію, і при цьому немає необхідності в антитромбоцитарному ефекті, то за 5-7 днів до операції прийом клопідогрелу слід припинити. Клопідогрел подовжує час кровотечі і повинен застосовуватися з обережністю у пацієнтів із захворюваннями, що схильні до розвитку кровотеч (особливо, шлунково-кишкових та внутрішньоочних). Препарати, які можуть спричинити пошкодження слизової оболонки шлунково-кишкового тракту (такі як АСК, нестероїдні протизапальні засоби) у пацієнтів, які приймають клопідогрел, слід застосовувати з обережністю. Пацієнти повинні бути попереджені про те, що при прийомі клопідогрелу (одного або в комбінації з АСК) для зупинки кровотечі може знадобитися більше часу, а також про те, що у разі виникнення у них незвичайної (по локалізації або тривалості) кровотечі їм слід повідомити про це свого лікаря. Перед будь-якою майбутньою операцією та перед початком прийому будь-якого нового лікарського препарату пацієнти повинні повідомляти лікаря (включаючи стоматолога) про прийом клопідогрелу. Нещодавно перенесений ішемічний інсульт Показано, що у пацієнтів з нещодавно перенесеним минущим порушенням мозкового кровообігу або інсультом, що мають високий ризик розвитку повторних ішемічних ускладнень, комбінація АСК та клопідогрелу підвищує частоту розвитку великих кровотеч. Тому така комбінована терапія повинна проводитися з обережністю і лише у разі доведеної клінічної користі від її застосування. Прийом клопідогрелу не рекомендується при гострому інсульті з давністю менше 7 днів (оскільки відсутні дані щодо його застосування при цьому стані). Тромботична тромбоцитопенічна пурпура (ТТП) Дуже рідко після застосування клопідогрелу (іноді навіть нетривалого) відзначалися випадки розвитку тромботичної тромбоцитопенічної пурпури (ТТП), яка характеризується тромбоцитопенією та мікроангіопатичною гемолітичною анемією, що супроводжуються неврологічними розладами, порушенням функції. ТТП є потенційно загрозливим для життя станом, що вимагає негайного лікування, включаючи плазмаферез. Набута гемофілія Повідомлялося про випадки розвитку набутої гемофілії прийому клопідогрелу. При підтвердженому ізольованому збільшенні АЧТВ, що супроводжується або не супроводжується розвитком кровотечі, слід розглянути питання можливості розвитку набутої гемофілії. Пацієнти з підтвердженим діагнозом набутої гемофілії повинні спостерігатися та лікуватися фахівцями з цього захворювання та припинити прийом клопідогрелу. Функціональна активність ізоферменту CYP2C19 У пацієнтів з низькою активністю ізоферменту CYP2C19 при застосуванні клопідогрелу в рекомендованих дозах утворюється менше активного метаболіту клопідогрелу і слабше виражена його антиагрегантна дія, у зв'язку з чим при прийомі звичайно рекомендованих доз клопідогрелу при гострому коронарному синдромі. судинних ускладнень, ніж у пацієнтів із нормальною активністю ізоферменту CYP2C19. Очікується, що застосування лікарських засобів, які індукують активність ізоферменту CYP2C19, може спричинити збільшення концентрації активного метаболіту клопідогрелу та підвищувати ризик виникнення кровотечі. В якості запобіжного заходу не рекомендується застосовувати одночасно потужні індуктори ізоферменту CYP2C19 і клопідогрел. Є тести визначення генотипу CYP2C19, які можуть бути використані для допомоги у виборі терапевтичної стратегії. Слід розглянути питання застосування більш високих доз клопідогрелу у пацієнтів з низькою активністю CYP2C19. Перехресні алергічні та/або гематологічні реакції між тієнопіридинами У пацієнтів слід збирати анамнез на предмет алергічних та/або гематологічних реакцій, що були раніше, на інші тієнопіридини (такі як тіклопідин, прасугрел), оскільки повідомлялося про наявність перехресних алергічних та/або гематологічних реакцій між тіенопіридинами (див. розділ "Побічна дія"). Тієнопіридини можуть викликати помірні та тяжкі алергічні реакції (такі як висипання на шкірі, ангіоневротичний набряк) або гематологічні реакції (такі як тромбоцитопенія і нейтропенія). Пацієнти, у яких раніше спостерігалися алергічні та/або гематологічні реакції на один із препаратів групи тієнопіридинів, можуть мати підвищений ризик розвитку подібних реакцій на інший препарат групи тієнопіридинів. Рекомендується моніторинг перехресних алергічних та/або гематологічних реакцій. Ниркова недостатність Досвід застосування клопідогрелу у пацієнтів з тяжкою нирковою недостатністю обмежений. Тому слід з обережністю застосовувати клопідогрел у цієї групи пацієнтів. Печінкова недостатність Є обмежений досвід застосування клопідогрелу у пацієнтів з тяжкими захворюваннями печінки, які можуть бути схильними до розвитку геморагічного діатезу. Тому слід з обережністю застосовувати клопідогрел у цієї групи пацієнтів. Вплив на здатність до керування автотранспортом та управління механізмами Препарат Плавікс® не істотно впливає на здібності, необхідні для керування автомобілем або заняття іншими потенційно небезпечними видами діяльності.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. діюча речовина: клопідогрел гідросульфат у формі II - 97,875 мг (у перерахунку на клопідогрел - 75,0 мг); допоміжні речовини: манітол, макрогол-6000, целюлоза мікрокристалічна (з низьким вмістом води, 90 мкм), гіпоролоза низькозаміщена, рицинова олія гідрогенізована; плівкова оболонка: опадрай рожевий (лактози моногідрат, гіпромелозу, титану діоксид (Е 171), тріацетин, барвник заліза оксид червоний (Е 172)), карнаубський віск. По 7, 10 або 14 таблеток у блістер з ПВХ/ПВДХ та фольги алюмінієвої або ПА/Ал/ПВХ та фольги алюмінієвої. По 1, 2 або 3 блістери по 7 або 14 таблеток; по 1, 2, 3 або 10 блістерів по 10 таблеток разом з інструкцією із застосування в картонну пачку.Опис лікарської формиКруглі, злегка двоопуклі таблетки, покриті плівковою оболонкою рожевого кольору, з гравіюванням "75" з одного боку і "1171" з іншого боку.Фармакотерапевтична групаАнтиагрегантний засіб.ФармакокінетикаВсмоктування При одноразовому та повторному прийомі внутрішньо у дозі 75 мг на добу клопідогрел швидко всмоктується. Середнє значення максимальної концентрації (Сmax) незміненого клопідогрелу в плазмі крові (приблизно 2,2-2,5 нг/мл після прийому внутрішньо разової дози 75 мг) досягається приблизно через 45 хв після прийому препарату. За даними екскреції метаболітів клопідогрелу через нирки його абсорбція становить приблизно 50%. Розподіл In vitro клопідогрел і його основний циркулюючий у крові неактивний метаболіт оборотно зв'язуються з білками плазми крові (на 98% і 94%, відповідно), і цей зв'язок є ненасиченим до концентрації 100 мг/мл. Метаболізм Клопідогрел інтенсивно метаболізується у печінці. In vitro та in vivo клопідогрел метаболізується двома шляхами: перший здійснюється за допомогою естераз і призводить до гідролізу клопідогрелу з утворенням неактивного похідного карбоксильної кислоти (85 % від циркулюючих метаболітів); другий шлях здійснюється за допомогою ізоферментів цитохром Р450. Спочатку клопідогрел метаболізується до 2-оксо-клопідогрелу, що є проміжним метаболітом. Подальший метаболізм 2-оксо-клопідогрелу призводить до утворення активного метаболіту клопідогрелу - тіольного похідного клопідогрелу. In vitro цей активний метаболіт утворюється головним чином за допомогою ізоферменту CYP2C19. але в його освіті також беруть участь деякі інші ізоферменти, включаючи CYP1A2, CYP2B6 та CYP3A4. Активний тіольний метаболіт клопідогрелу, виділений у in vitro дослідженнях, швидко та незворотно зв'язується з рецепторами тромбоцитів, блокуючи таким чином агрегацію тромбоцитів. Смах активного метаболіту клопідогрелу після одноразового прийому його навантажувальної дози 300 мг у 2 рази перевищує таку після 4-х днів прийому підтримуючої дози клопідогрелу 75 мг. Сmax досягається приблизно 30-60 хв. Виведення Протягом 120 годин після прийому внутрішньо людиною 14С-міченого клопідогрелу близько 50% радіоактивності виводиться через нирки та приблизно 46% радіоактивності виводиться через кишечник. Після одноразового прийому внутрішньо дозування в 75 мг період напіввиведення (Т1/2) клопідогрелу становить приблизно 6 годин. Фармакогенетика За допомогою ізоферменту CYP2C19 утворюються як активний метаболіт, так і проміжний метаболіт - 2-оксо-клопідогрел. Фармакокінетика та антиагрегантна дія активного метаболіту клопідогрелу, при дослідженні агрегації тромбоцитів ex vivo, варіюють залежно від генотипу ізоферменту CYP2C19. Алель гена CYP2CI9*1 відповідає повністю функціональному метаболізму, тоді як алелі генів CYP2C19*2 та CYP2C19*3 є нефункціональними. Алелі генів CYP2C19*2 та CYP2C 19*3 є причиною зниження метаболізму у більшості представників європеоїдної (85%) та монголоїдної раси (99%). Інші алелі, з якими пов'язана відсутність або зниження метаболізму, зустрічаються рідше і включають, але не обмежуються алелями генів CYP2C19*4, *5, *6, *7 і *8.Пацієнти з низькою активністю ізоферменту CYP2CI9 повинні мати дві зазначені вище алелі гена з втратою функції. Опубліковані частоти фенотипів пацієнтів з низькою активністю ізоферменту CYP2C19 у пацієнтів європеоїдної раси становлять 2%, у пацієнтів негроїдної раси - 4% і у монголоїдної раси - 14%. Існують спеціальні тести для визначення наявного у пацієнта генотипу ізоферменту CYP2C19. За даними перехресного дослідження (40 добровольців) за участю добровольців з дуже високою, високою, проміжною та низькою активністю ізоферменту CYP2C19, будь-яких суттєвих відмінностей в експозиції активного метаболіту та у середніх значеннях інгібування агрегації тромбоцитів (ІАТ), індукованої АД дуже високою, високою та проміжною активністю ізоферменту CYP2C19 виявлено не було. У добровольців із низькою активністю ізоферменту CYP2C19 експозиція активного метаболіту знижувалась на 63-71 % порівняно з добровольцями з високою активністю ізоферменту CYP2C19. При використанні схеми лікування 300 мг навантажувальна доза/75 мг підтримуюча доза (300 мг/75 мг) у добровольців з низькою активністю ізоферменту CYP2C19 антитромбоцитарна дія знижувалась із середніми значеннями ІАТ,складовими 24% (через 24 год) та 37% (на 5 день дослідження) порівняно з ІАТ, складовими 39% (через 24 год) та 58% (на 5 день дослідження), у добровольців з високою активністю ізоферменту CYP2C19 та 37% (через 24 год) та 60% (на 5 день дослідження) у добровольців із проміжною активністю ізоферменту CYP2C19. Коли добровольці з низькою активністю ізоферменту CYP2C19 отримували препарат за схемою лікування 600 мг навантажувальна доза/150 мг підтримуюча доза (600 мг/150 мг), експозиція активного метаболіту була вищою, ніж при прийомі за схемою лікування 300 мг/75 мг. Крім цього, ІАТ становило 32% (через 24 год) і 61% (на 5 день дослідження), що було більше такого у добровольців з низькою активністю ізоферменту CYP2C19, які отримували лікування за схемою 300 мг/75 мг, і було подібно до такого в групах пацієнтів з більш високою інтенсивністю CYP2C 19 метаболізму. одержували лікування за схемою 300 мг/75 мг. Однак у дослідженнях з урахуванням клінічних результатів режим дозування клопідогрелу для пацієнтів цієї групи (пацієнтів з низькою активністю ізоферменту CYP2C19) наразі не встановлено. Аналогічно результатам даного дослідження мета-аналіз шести досліджень, до якого увійшли дані 335 добровольців, які отримували клопідогрел і перебували в стані досягнення рівноважної концентрації, показав, що в порівнянні з добровольцями з високою активністю ізоферменту CYP2C19, у добровольців з проміжною активністю ізоферменту CYP2C знижувалася на 28%, а у добровольців з низькою активністю ізоферменту CYP2C19 - на 72%, тоді як ІАТ було знижено з відмінностями в ІАТ на 5,9% та 21,4% відповідно. Не проводилося оцінки впливу генотипу CYP2CI9 на клінічні результати у пацієнтів, які отримували клопідогрел, у проспективних рандомізованих контрольованих дослідженнях. Проте зараз є кілька ретроспективних аналізів. Результати генотипування отримані в ході наступних клінічних досліджень: CURE, CHARISMA, CLARITY-TIM1 28, TRITON-TIMI 38 та ACT1VE-A, а також у кількох опублікованих когортних дослідженнях. У дослідженні TRITON-TIMI 38 та 3-х когортних дослідженнях (Collet, Sibbing, Giusti) пацієнти комбінованої групи з проміжною або низькою активністю ізоферменту CYP2C19 мали більш високу частоту серцево-судинних ускладнень (смерть, інфаркт міокарда та інсульт). з такими у пацієнтів із високою активністю ізоферменту CYP2C19. У дослідженні CHARISMA та одному когортному дослідженні (Simon) збільшення частоти серцево-судинних ускладнень спостерігалося тільки у пацієнтів з низькою активністю ізоферменту CYP2C19 (при їх порівнянні з пацієнтами з високою активністю ізоферменту CYP2C19). Дослідження CURE, CLARITY. ACTIVE- і одному з когортних досліджень (Trenk), не спостерігалося збільшення частоти серцево-судинних ускладнень в залежності від інтенсивності CYP2C 19- метаболізму. Особливі групи пацієнтів Фармакокінетика активного метаболіту клопідогрелу в спеціальних групах пацієнтів не вивчалася. Пацієнти старші 75 років: у добровольців старше 75 років при порівнянні з молодими добровольцями не було отримано відмінностей за показниками агрегації тромбоцитів та часу кровотечі. Корекція дози не потрібна. Дитячий вік до 18 років: клінічні дані відсутні. Пацієнти з порушенням функції нирок Після повторних прийомів клопідогрелу в дозі 75 мг/добу у пацієнтів з тяжкими порушеннями функції нирок (кліренс креатиніну (КК) від 5 мл/хв до 15 мл/хв) інгібування АДФ-індукованої агрегації тромбоцитів було нижчим (на 25 %) порівняно з таким у здорових добровольців, проте подовження часу кровотечі було подібним до такого у здорових добровольців, які отримували клопідогрел у дозуванні 75 мг на добу. Пацієнти з порушенням функції печінки Не було значних відмінностей у ступені інгібування АДФ-індукованої агрегації тромбоцитів після щоденного прийому клопідогрелу у добовій дозі 75 мг протягом 10 днів у пацієнтів з тяжкими порушеннями функції печінки порівняно зі здоровими добровольцями. Середній час кровотечі також можна порівняти в обох групах. Расова приналежність Поширеність алелей генів ізоферменту CYP2C19, що зумовлюють проміжну та низьку активність цього ізоферменту, відрізняється у представників різних расових груп. Є обмежені літературні дані про їх поширеність у представників монголоїдної раси, що не дозволяє оцінити значення генотипування ізоферменту CYP2C19 для розвитку ішемічних ускладнень.ФармакодинамікаКлопідогрел є проліком, один з активних метаболітів якого є інгібітором агрегації тромбоцитів. Для утворення активного метаболіту, який пригнічує агрегацію тромбоцитів, клопідогрел повинен метаболізуватися за допомогою ізоферментів системи цитохрому Р450 (CYP450). Активний метаболіт клопідогрелу селективно інгібує зв'язування аденозиндифосфату (АДФ) з P2Yi2 рецептором тромбоцитів та подальшу АДФ-опосередковану активацію комплексу GPIIb/IIIa, що призводить до придушення агрегації тромбоцитів. Завдяки необоротному зв'язуванню, тромбоцити залишаються несприйнятливими до стимуляції АДФ протягом всього терміну свого життя (приблизно 7-10 днів), а відновлення нормальної функції тромбоцитів відбувається зі швидкістю, що відповідає швидкості оновлення тромбоцитів. Агрегація тромбоцитів, спричинена агоністами, відмінними від АДФ. також інгібується за рахунок блокади посиленої активації тромбоцитів АДФ, що вивільняється. Оскільки утворення активного метаболіту відбувається за допомогою ізоферментів системи цитохрому Р450, деякі з яких можуть відрізнятися поліморфізмом або інгібуватися іншими препаратами, не у всіх пацієнтів можливе адекватне пригнічення агрегації тромбоцитів. При щоденному прийомі клопідогрелу в дозі 75 мг з першого ж дня прийому відзначається значне пригнічення АДФ-індукованої агрегації тромбоцитів, яке поступово збільшується протягом 3-7 днів і потім виходить на постійний рівень (при досягненні рівноважного стану). У рівноважному стані агрегація тромбоцитів пригнічується загалом на 40-60 %. Після припинення прийому клопідогрелу агрегація тромбоцитів та час кровотечі поступово повертаються до початкового рівня, в середньому, протягом 5 днів. У ході клінічного дослідження ACTIVE-А показано, що у пацієнтів з фібриляцією передсердь, які мали щонайменше. один фактор ризику розвитку судинних ускладнень, але були нездатні приймати непрямі антикоагулянти, клопідогрел у поєднанні з ацетилсаліциловою кислотою (АСК) (у порівнянні з прийомом тільки однієї АСК) зменшував частоту разом узятих інсульту, інфаркту міокарда, системної тромбоемболії поза центральною або судинної смерті, переважно за рахунок зменшення ризику розвитку інсульту. Ефективність прийому клопідогрелу у поєднанні з АСК виявлялася рано і зберігалася до 5 років. Зменшення ризику великих судинних ускладнень у групі пацієнтів, які приймали клопідогрел у поєднанні з АСК, спостерігалося переважно за рахунок більшого зменшення частоти інсультів. Ризик розвитку інсульту будь-якої тяжкості при прийомі клопідогрелу у поєднанні з АСК знижувався, а також спостерігалася тенденція до зниження частоти розвитку інфаркту міокарда в групі, яка отримувала лікування клопідогрелом у поєднанні з АСК, але не спостерігалося відмінностей у частоті тромбоемболій поза ЦНС або судинної смерті. Крім цього, прийом клопідогрелу у поєднанні з АСК зменшував загальну кількість днів госпіталізації з серцево-судинних причин. Перехід з терапії потужним інгібітором рецепторів P2Y12 на лікування клопідогрелом у поєднанні з АСК після завершення гострої фази гострого інфаркту міокарда (ГІМ) вивчався у двох рандомізованих ініційованих дослідником клінічних дослідженнях (TOPIC та TROPICAL-ACS). У рандомізованому відкритому клінічному дослідженні TOPIC брали участь пацієнти, які перенесли ГІМ, яким виконувалось черезшкірне коронарне втручання (ЧКВ). Пацієнти, які отримували АСК та один з найбільш потужних інгібіторів рецепторів P2Y12, у яких не розвинулися несприятливі події протягом одного місяця, або були переведені на терапію фіксованою комбінацією АСК та клопідогрелу (деескалація подвійної антитромбоцитарної терапії (ДАТ)) або продовжили приймати Постійна ДАТ). Події, включені в комбіновану первинну кінцеву точку (смерть від ускладнень серцево-судинних захворювань (ССЗ), інсульт, екстрена реваскуляризація та кровотечі типу 2 або тяжкі кровотечі за шкалою BARC (Дослідницького академічного консорціуму за кровотечами)), через один були зареєстровані у 43 з 322 пацієнтів (13,4%) у групі деескалації ДАТ та 85 пацієнтів з 323 (26,3 %) у групі незмінної ДАТ (р Статистично значуща відмінність в основному зумовлена скороченням кількості випадків кровотечі, у тому числі кровотеч, які за шкалою BARC більш або рівні 2 (4% у групі деескалації та 14,9% у групі, що отримувала незмінену ДАТ), при цьому не спостерігалося істотних відмінностей у частоті ішемічних ускладнень (р = 0,36). До рандомізованого відкритого клінічного дослідження TROPICAL-ACS було включено 2610 пацієнтів з ГІМ. підтвердженим аналізом на біомаркери після проведення ЧКВ. Пацієнти були рандомізовані до груп для отримання прасугрелу (дні 0-14) або прасугрелу (дні 0-7), а потім клопідогрелу (дні 8-14) у комбінації з АСК. На 14-й день було проведено оцінку функції тромбоцитів. Пацієнти з першої групи терапії лише прасугрелом продовжували приймати прасугрел протягом 11,5 місяці. У пацієнтів із групи заміни терапії було виконано аналіз на високу реактивність тромбоцитів (ДРТ). Пацієнти з ДРТ ≥ 46 одиниць були переведені на терапію прасугрелом, яку отримували протягом 11,5 місяця. Пацієнти з ДРТПоказання до застосуванняВторинна профілактика атеротромботичних ускладнень: У дорослих пацієнтів після нещодавно перенесеного інфаркту міокарда (з давністю від декількох днів до 35 днів), нещодавно перенесеного ішемічного інсульту (з давністю від 7 днів до 6 місяців) або при діагностованій оклюзійній хворобі периферичних артерій прийом клопідогрелу знижував частоту комбінованої ішемічний інсульт (з летальними наслідками або без нього), повторний інфаркт міокарда (з летальними наслідками або без нього) та іншу серцево-судинну смерть. У дорослих пацієнтів із гострим коронарним синдромом: гострий коронарний синдром без підйому сегмента ST (нестабільна стенокардія/інфаркт міокарда без зубця Q), включаючи пацієнтів, які повинні отримувати медикаментозне лікування, та пацієнтів, яким показано черезшкірне коронарне втручання (зі стенуванням або без стентування) або аортокоронарне шунтування (АКШ). Прийом клопідогрелу знижував частоту комбінованої кінцевої точки, що включала серцево-судинну смерть, інфаркт міокарда або інсульт, а також частоту комбінованої кінцевої точки, що включала серцево-судинну смерть, інфаркт міокарда, інсульт, рефрактерну ішемію. гострий інфаркт міокарда із підйомом сегмента ST. Прийом клопідогрелу знижував смертність від будь-яких причин, а також частоту комбінованої кінцевої точки, що включала смерть, повторний інфаркт міокарда або інсульт. Профілактика атеротромботичних та тромбоемболічних ускладнень у дорослих пацієнтів з фібриляцією передсердь (миготливою аритмією) Показано, що у пацієнтів з фібриляцією передсердь з підвищеним ризиком судинних ускладнень терапія непрямими антикоагулянтами, які є антагоністами вітаміну К (АВК), пов'язана з більшою клінічною користю порівняно із застосуванням тільки АСК або комбінації клопідогрелу з АСК щодо зниження. Пацієнтам з фібриляцією передсердь (миготливою аритмією), що мають, як мінімум, один фактор ризику розвитку судинних ускладнень, які не можуть приймати АВК (наприклад, за наявного особливого ризику кровотечі, нездатності пацієнта, на думку лікаря, адекватно контролювати МНО (міжнародне нормалізоване) ставлення) або у разі неприйняття пацієнтом лікування АВК), для запобігання атеротромботичних та тромбоемболічних ускладнень. включаючи інсульт, показаний прийом клопідогрелу в комбінації з АСК. Показано, що клопідогрел у комбінації з АСК знижував частоту комбінованої кінцевої точки, що включала інсульт, інфаркт міокарда, системну тромбоемболію поза ЦНС або серцево-судинну смерть, переважно за рахунок зниження частоти розвитку інсульту.Протипоказання до застосуванняПідвищена чутливість до клопідогрелу або будь-якої з допоміжних речовин препарату. Тяжка печінкова недостатність. Гостра кровотеча, наприклад, кровотеча з виразки або внутрішньочерепний крововилив. Рідкісна спадкова непереносимість галактози, дефіцит лактази та глюкозо-галактозна мальабсорбція. Вагітність та період грудного вигодовування. Дитячий вік до 18 років (безпека та ефективність застосування не встановлені). З обережністю: При помірній печінковій недостатності, при якій можлива схильність до кровотечі (обмежений клінічний досвід застосування). При нирковій недостатності (обмежений клінічний досвід застосування). При захворюваннях, при яких є схильність до розвитку кровотеч (зокрема шлунково-кишкових або внутрішньоочних), і, особливо, при одночасному застосуванні лікарських засобів, які можуть спричинити ушкодження слизової оболонки шлунково-кишкового тракту (таких як АСК та нестероїдні протизапальні препарати ( НПЗП)). У пацієнтів, у яких є підвищений ризик розвитку кровотечі: через травму, хірургічне втручання або інші патологічні стани, а також у пацієнтів, які отримують лікування АСК, гепарином, варфарином, інгібіторами глікопротеїну IIb/IIIa, НПЗЗ, у тому числі селективними інгібіторами. -2 (ЦОГ-2), а також іншими лікарськими засобами, застосування яких пов'язане з ризиком кровотеч, селективними інгібіторами зворотного захоплення серотоніну (СІОЗС). При одночасному застосуванні з лікарськими засобами, що є субстратами ізоферменту CYP2C8 (репаглінід, паклітаксел). У пацієнтів із низькою активністю ізоферменту CYP2C19. При вказівках в анамнезені алергічні та гематологічні реакції на інші тієнопіридини (такі як тіклопідін, прасугрел). При нещодавно перенесеному минущому порушенні мозкового кровообігу або ішемічному інсульті.Вагітність та лактаціяВагітність Дослідження на тваринах не виявили ні прямих, ні непрямих несприятливих ефектів протягом вагітності, ембріональний розвиток, пологи та постнатальний розвиток. Так як не завжди за результатами досліджень на тваринах можна передбачити реакцію у людини, і внаслідок відсутності даних контрольованих клінічних досліджень щодо прийому клопідогрелу вагітними жінками, як запобіжний засіб не рекомендується прийом клопідогрелу під час вагітності, за винятком тих випадків, коли, на думку лікаря , Його застосування настійно необхідне. Період грудного вигодовування У дослідженнях на щурах показано, що клопідогрел та/або його метаболіти виділяються з грудним молоком. Невідомо, чи виділяється клопідогрел із грудним молоком людини. Так як багато лікарських засобів виділяються з грудним молоком і існує ризик розвитку потенційних несприятливих явищ у дитини, яка перебуває на грудному вигодовуванні, слід прийняти рішення про припинення грудного вигодовування або про відміну препарату з урахуванням необхідності його застосування для матері.Побічна діяДані, отримані під час клінічних досліджень Безпека клопідогрелу вивчена більш ніж у 44 000 пацієнтів, у тому числі більш ніж у 12 000 пацієнтів, які отримували лікування протягом року або більше. Загалом переносимість клопідогрелу в дозі 75 мг/добу у дослідженні CAPRIE відповідала переносимості АСК у дозі 325 мг/добу, незалежно від віку, статі та расової належності пацієнтів. Нижче наведено клінічно значущі небажані явища, що спостерігалися у п'яти великих клінічних дослідженнях: CAPRIE, CURE, CLARITY, COMMIT та ACTIVE-A. Кровотечі та крововиливу Порівняння монотерапії клопідогрелом та АСК У клінічному дослідженні CAPRIE загальна частота всіх кровотеч у пацієнтів, які приймали клопідогрел, та у пацієнтів, які приймали АСК, склала 9,3%. Частота важких кровотеч при застосуванні клопідогрелу та АСК була порівнянною: 1,4 % та 1,6 % відповідно. Загалом частота розвитку шлунково-кишкових кровотеч у пацієнтів, які приймали клопідогрел, та у пацієнтів, які приймали АСК, становила 2.0 % та 2,7 %, відповідно, у тому числі частота шлунково-кишкових кровотеч, які потребували госпіталізації, становила 0,7 % та 1,1% відповідно. Загальна частота кровотеч іншої локалізації при прийомі клопідогрелу порівняно з прийомом АСК була вищою (7,3% проти 6,5%, відповідно). Однак частота важких кровотеч при застосуванні клопідогрелу та АСК була порівнянною (0,6% або 0,4% відповідно). Найчастіше повідомлялося про розвиток наступних кровотеч: пурпура / синці, носова кровотеча. Рідше повідомлялося про розвиток гематом, гематурії та очних крововиливів (головним чином, кон'юнктивальних). Частота внутрішньочерепних крововиливів при застосуванні клопідогрелу та АСК була порівнянною (0,4 % або 0,5 % відповідно). Порівняння комбінованої терапії клопідогрел+АСК та плацебо+АСК У клінічному дослідженні CURE у пацієнтів, які приймали клопідогрел+АСК, у порівнянні з пацієнтами, які приймали плацебо+АСК, спостерігалося збільшення частоти розвитку великих кровотеч (3,7 % порівняно 2,7 %), та малих кровотеч (5,1 % за порівняно 2.4%). В основному, джерелами великих кровотеч були шлунково-кишковий тракт (ШКТ) та місця пункції артерій. Частота розвитку загрозливих для життя кровотеч у пацієнтів, які приймали клопідогрел+АСК у порівнянні з пацієнтами, які приймали плацебо+АСК, достовірно не відрізнялася (2,2 % та 1,8 %, відповідно), частота розвитку фатальних кровотеч була однаковою (0.2 % при обох види терапії). Частота виникнення не загрожують життю великих кровотеч була достовірно вищою у пацієнтів, які приймали клопідогрел+АСК, порівняно з пацієнтами, які приймали плацебо+АСК (1,6 % та 1 %, відповідно), але частота розвитку внутрішньочерепних крововиливів була однаковою (0,1 % за обох видів терапії). Частота розвитку великих кровотеч у групі клопідогрел+АСК залежала від дози АСК (< 100 мг: 2,6%; 100-200 мг: 3,5 %; > 200 мг: 4,9 %), а також частота розвитку великих кровотеч у групі плацебо+АСК (< 100 мг: 2,0%; 100-200 мг: 2,3%; > 200 мг: 4,0%). У пацієнтів, які припинили антитромбоцитарну терапію більш ніж за 5 днів до аортокоронарного шунтування, не відзначалося почастішання випадків розвитку великих кровотеч протягом 7 днів після втручання (4,4% у групі клопідогрел+АСК та 5,3% у групі плацебо+АСК). У пацієнтів, які продовжували антитромбоцитарну терапію протягом останніх п'яти днів перед аортокоронарним шунтуванням, частота цих подій після втручання становила 9,6% (у групі клопідогрел+АСК) та 6,3% (у групі плацебо+АСК). У клінічному дослідженні CLARITY частота великих кровотеч (визначуваних як внутрішньочерепні кровотечі або кровотечі зі зниженням гемоглобіну > 5 г/дл) в обох групах (клопідогрел+АСК і плацебо+АСК) була порівнянною в обох групах лікування (1,3 % проти 1, 1% у групі клопідогрел+АСК та групі плацебо+АСК, відповідно). Вона була однаковою у підгрупах пацієнтів, розділених за вихідними характеристиками та за видами фібринолітичної терапії або гепаринотерапії. Частота виникнення фатальних кровотеч (0.8% проти 0,6%) та внутрішньочерепних крововиливів (0,5% проти 0,7%) при лікуванні клопідогрел+АСК та плацебо+АСК, відповідно, була низькою та порівнянною в обох групах лікування. У клінічному дослідженні COMMIT загальна частота нецеребральних великих кровотеч або церебральних кровотеч була низькою та однаковою (0,6% у групі клопідогрел+АСК та 0,5% у групі плацебо+АСК). У клінічному дослідженні ACTIVE-A частота розвитку великих кровотеч у групі клопідогрел+АСК була вищою, ніж у групі плацебо+АСК (6,7 % проти 4,3 % відповідно). Великі кровотечі переважно були позачерепними в обох групах (5,3% проти 3,5%), головним чином, із шлунково-кишкового тракту (3,5% проти 1,8%). У групі клопідогрел+АСК внутрішньочерепних крововиливів було більше порівняно з групою плацебо+АСК (1,4% проти 0.8%, відповідно). Відсутні статистично значущі відмінності між цими групами лікування у частоті виникнення фатальних кровотеч (1,1% проти 0,7%) та геморагічного інсульту (0,8% проти 0.6%). Порушення з боку крові У дослідженні CAPRIE, тяжка нейтропенія ( У двох із 9599 пацієнтів, які приймали клопідогрел, спостерігалася повна відсутність нейтрофілів у периферичній крові, якого не спостерігалося в жодного з 9586 пацієнтів, які приймали АСК. Незважаючи на те, що ризик розвитку мієлотоксичної дії при прийомі клопідогрелу є досить низьким, якщо у пацієнта, який приймає клопідогрел, спостерігається підвищення температури або з'являються інші ознаки інфекції. слід обстежити пацієнта щодо можливої нейтропенії. При лікуванні клопідогрелом в одному випадку спостерігався розвиток апластичної анемії. Частота виникнення тяжкої тромбоцитопенії ( У дослідженнях CURE та CLARITY спостерігалася порівнянна кількість пацієнтів із тромбоцитопенією або нейтропенією в обох групах лікування. Інші клінічно значущі небажані реакції, що спостерігалися під час проведення клінічних досліджень CAPRIE, CURE, CLARITY COMMIT та ACTIVE-A Частота виникнення небажаних реакцій визначалася відповідно до класифікації Всесвітньої Організації Охорони Здоров'я: дуже часто (≥ 1/10); часто (≥ 1/100 та < 1/10); нечасто (≥ 1/1000 та < 1/100); рідко (≥ 1/10000 та < 1/1000); дуже рідко (< 1/10000), частота невідома (не може бути підрахована на підставі наявних даних). Порушення з боку нервової системи: нечасто – головний біль, запаморочення, парестезія; рідко – вертиго. Порушення з боку шлунково-кишкового тракту: часто – диспепсія, абдомінальні болі, діарея; нечасто - нудота, гастрит, здуття живота, запор, блювання, виразка шлунка, виразка дванадцятипалої кишки. Порушення з боку шкіри та підшкірних тканин: нечасто – шкірний висип, свербіж шкіри. Порушення з боку крові та лімфатичної системи: нечасто – збільшення часу кровотечі, зниження кількості тромбоцитів у периферичній крові; лейкопенія, зниження кількості нейтрофілів у периферичній крові, еозинофілія. Постмаркетинговий досвід застосування препарату Порушення з боку крові та лімфатичної системи: частота невідома - випадки серйозних кровотеч, переважно підшкірних, скелетно-м'язових, очних крововиливів (кон'юнктивальних, в тканині та сітківку ока), кровотеч з дихальних шляхів (кровохаркання, легеневі кровотечі) кровотеч із післяопераційних ран та випадки кровотеч із летальним результатом (особливо внутрішньочерепних крововиливів, шлунково-кишкових кровотеч та заочеревинних крововиливів); агранулоцитозу, гранулоцитопенії, апластичної анемії/панцитопенії, тромботичної тромбоцитопенічної пурпури (ТТП), придбаної гемофілії А. Порушення з боку серця: частота невідома – синдром Коунісу (вазоспастична алергічна стенокардія/алергічний інфаркт міокарда), зумовлений реакцією гіперчутливості на клопідогрел. Порушення з боку імунної системи: частота невідома – анафілактоїдні реакції, сироваткова хвороба; перехресні алергічні та гематологічні реакції з іншими тієнопіридинами (такими як тіклопідин, прасугрел), аутоімунний інсуліновий синдром (може призводити до серйозної гіпоглікемії, особливо у пацієнтів з MLA DRA4 серотипом). Порушення психіки: частота невідома – сплутаність свідомості, галюцинації. Порушення з боку нервової системи: частота невідома – порушення смакового сприйняття, агевзія. Порушення з боку судин: частота невідома – васкуліт, зниження артеріального тиску. Порушення з боку дихальної системи, органів грудної клітки та середостіння: частота невідома – бронхоспазм, інтерстиційна пневмонія, еозинофільна пневмонія. Порушення з боку шлунково-кишкового тракту: частота невідома – коліт (зокрема виразковий коліт або лімфоцитарний коліт), панкреатит, стоматит. Порушення з боку печінки та жовчовивідних шляхів: частота невідома – гепатит (неінфекційний), гостра печінкова недостатність. Порушення з боку шкіри та підшкірних тканин: частота невідома - макульозно-папульозний еритематозний або ексфоліативний висип, кропив'янка, свербіж шкіри, ангіоневротичний набряк, бульозний дерматит (багатоформна еритема, синдром Стівенса-Джонсона, токсичний ендоз гіперчутливості, лікарський висип з еозинофілією та системними проявами (DRESS-синдром), екзема, плоский лишай. Порушення з боку скелетно-м'язової та сполучної тканини: частота невідома – артралгія (біль у суглобах), артрит, міалгія. Порушення з боку нирок та сечовивідних шляхів: частота невідома – гломерулонефрит. Порушення з боку статевих органів та молочної залози: частота невідома – гінекомастія. Загальні розлади та порушення у місці введення: частота невідома – лихоманка. Лабораторні та інструментальні дані: частота невідома – відхилення від норми лабораторних показників функціонального стану печінки, підвищення концентрації креатиніну в крові.Взаємодія з лікарськими засобамиЛікарські засоби, застосування яких пов'язане із ризиком розвитку кровотечі Є підвищений ризик розвитку кровотечі внаслідок їхнього потенційного адитивного ефекту з клопідогрелом. Лікування слід проводити з обережністю. Тромболітики Безпека одночасного застосування клопідогрелу, фібрин-специфічних або фібрин-неспецифічних тромболітичних засобів та гепарину була вивчена у пацієнтів з гострим інфарктом міокарда. Частота клінічно значущих кровотеч була аналогічна тій, що спостерігалася у разі спільного застосування тромболітичних засобів та гепарину з АСК. Блокатори глікопротеїну IIb/III У зв'язку з можливістю фармакодинамічної взаємодії між клопідогрелом та блокаторами глікопротеїну IIb/IIIа, їх одночасне застосування потребує обережності, особливо у пацієнтів, які мають підвищений ризик розвитку кровотечі (при травмах та хірургічних втручаннях або інших патологічних станах). Ін'єкційні антикоагулянти (наприклад, гепарин) За даними клінічного дослідження, проведеного за участю здорових добровольців, при прийомі клопідогрелу не потрібно зміни дози гепарину і не змінювалася його антикоагулянтна дія. Одночасне застосування гепарину не змінювало антиагрегантної дії клопідогрелу. Між клопідогрелом та гепарином можлива фармакодинамічна взаємодія, яка може збільшувати ризик розвитку кровотеч. При одночасному застосуванні слід бути обережними. Пероральні антикоагулянти (наприклад, варфарин) Хоча прийом клопідогрелу 75 мг/добу не змінював фармакокінетику варфарину (субстрату ізоферменту CYP2C9) або МНО у пацієнтів, які тривало одержують лікування варфарином, одночасний прийом клопідогрелу збільшує ризик кровотечі у зв'язку з його незалежним додатковим впливом на згортання. Тому слід дотримуватися обережності при одночасному прийомі варфарину та клопідогрелу. Ацетилсаліцилова кислота (АСК) АСК не змінює інгібуючого АДФ-індуковану агрегацію тромбоцитів ефекту клопідогрелу, але клопідогрел потенціює вплив АСК на колаген-індуковану агрегацію тромбоцитів. Тим не менш, одночасний з клопідогрелом прийом АСК по 500 мг 2 рази на день протягом однієї доби не викликав суттєвого збільшення часу кровотечі, що викликається прийомом клопідогрелу. Оскільки між клопідогрелом і АСК можлива фармакодинамічна взаємодія, що призводить до підвищення ризику кровотечі, тому при їх одночасному застосуванні слід бути обережним. Тим не менш, у клінічних дослідженнях пацієнти отримували комбіновану терапію клопідогрелом та АСК (75-325 мг один раз на добу) до одного року. Нестероїдні протизапальні препарати (НПЗЗ) У клінічному дослідженні, проведеному за участю здорових добровольців, спільне застосування клопідогрелу та напроксену збільшувало приховані втрати крові через ШКТ. Однак, у зв'язку з відсутністю досліджень щодо взаємодії клопідогрелу з іншими НПЗП, наразі не відомо. є підвищений ризик шлунково-кишкових кровотеч при прийомі клопідогрелу разом з іншими нестероїдними протизапальними засобами. Тому при одночасному застосуванні нестероїдних протизапальних засобів, у тому числі інгібіторів ЦОГ-2 з клопідогрелом. слід дотримуватися обережності. Селективні інгібітори зворотного захоплення серотоніну (СІЗЗС) Оскільки СІЗЗЗ порушують активацію тромбоцитів та збільшують ризик розвитку кровотечі. При одночасному застосуванні слід бути обережними. Індуктори ізоферменту CYP2C19 Оскільки клопідогрел метаболізується до свого активного метаболіту частково за допомогою ізоферменту CYP2C19, очікується, що застосування лікарських засобів, які індукують активність цього ізоферменту, може призвести до збільшення концентрації активного метаболіту клопідогрелу. Рифампіцин, як потужний індуктор ізоферменту CYP2C19, при одночасному застосуванні з клопідогрелом, призводить як до збільшення концентрації активного метаболіту клопідогрелу, так і до інгібування тромбоцитів, що може підвищувати ризик виникнення кровотечі. В якості запобіжного заходу не рекомендується застосовувати одночасно потужні індуктори ізоферменту CYP2C19 і клопідогрел. Інгібітори ізоферменту CYP2C19 Оскільки клопідогрел метаболізується до утворення свого активного метаболіту частково за допомогою ізоферменту CYP2C19, застосування лікарських засобів, що інгібують цей ізофермент, може призвести до зменшення утворення активного метаболіту клопідогрелу. Клінічне значення цієї взаємодії встановлено. Як запобіжний засіб слід уникати одночасного застосування клопідогрелу та потужних або помірних інгібіторів ізоферменту CYP2C19. Потужними та помірними інгібіторами ізоферменту CYP2C19 є омепразол, езомепразол, флувоксамін, флуоксетин, моклобемід, вориконазол, флуконазол, тіклопідін, ципрофлоксацин, циметидин, карбамазепін, окскарбазепін. Слід уникати одночасного застосування з клопідогрелом інгібіторів протонної помпи, які є потужними або помірними інгібіторами ізоферменту CYP2C19 (наприклад, омепразолу, езомепразолу) (див. розділ "Фармакокінетика, підрозділ, Фармакогенетика", розділ "Особливі. Якщо інгібітори протонної помпи повинні прийматися одночасно з клопідогрелом, слід приймати інгібітор протонної помпи з найменшим інгібуванням ізоферменту CYP2C19, такий як пантопразол та лансопразол. Було проведено низку клінічних досліджень з клопідогрелом та іншими, одночасно застосовуваними лікарськими засобами, з метою вивчення можливих фармакодинамічних та фармакокінетичних взаємодій, які показали, що: при одночасному застосуванні клопідогрелу з атенололом та/або ніфедипіном клінічно значущої фармакодинамічної взаємодії не спостерігалося; одночасне застосування фенобарбіталу та естрогенів не мало істотного впливу на фармакодинаміку клопідогрелу; фармакокінетичні показники дигоксину та теофшліну не змінювалися при їх одночасному застосуванні з клопідогрелом; антацидні засоби не зменшували абсорбції клопідогрелу; фенітоїн та толбутамід можна з безпекою застосовувати одночасно з клопідогрелом (дослідження CAPR1E). Малоймовірно, що клопідогрел може впливати на метаболізм інших лікарських засобів, таких як фенітоїн та толбутамід, а також нестероїдні протизапальні засоби, які метаболізуються за допомогою ізоферменту CYP2C9 цитохрому Р450; інгібітори АПФ, діуретики, бета-адреноблокатори, блокатори "повільних" кальцієвих каналів, гіполіпідемічні засоби, коронарні вазодилататори, гіпоглікемічні засоби (в т.ч. інсулін), протиепшептичні засоби, гормонозамісна терапія та блокатори глікопротеїн небажаних взаємодій не виявлено. Лікарські засоби, що є субстратами ізоферменту CYP2C8 Показано, що клопідогрел збільшував системну експозицію репаглініду у здорових добровольців. Дослідження in vitro показали, що збільшення системної експозиції репаглініду є наслідком пригнічення ізоферменту CYP2C8 глюкуронідним метаболітом клопідогрелу. Слід бути обережними при одночасному застосуванні клопідогрелу та лікарських засобів, що метаболізуються за допомогою ізоферменту CYP2C8 (наприклад, репаглініду, паклітакселу) у зв'язку з ризиком збільшення їх плазмових концентрацій. Опіоїдні агоністи Як і у випадку інших пероральних інгібіторів P2Y12, одночасне застосування опіоїдних агоністів може затримувати та зменшувати абсорбцію клопідогрелу, ймовірно, через сповільнене випорожнення шлунка. Клінічне значення цієї взаємодії невідоме. Слід розглянути можливість призначення парентерального антиагрегантного препарату у пацієнтів із гострим коронарним синдромом, які потребують одночасного застосування морфіну або інших опіоїдних агоністів.Спосіб застосування та дозиВсередину, незалежно від їди. Нещодавно перенесений інфаркт міокарда, нещодавно перенесений інсульт та діагностована оклюзійна хвороба периферичних артерій Рекомендована доза – 75 мг один раз на добу. Гострий коронарний синдром без піднесення сегмента ST (нестабільна стенокардія, інфаркт міокарда без зубця Q) Лікування клопідогрелом слід починати з одноразового прийому дози навантаження 300 мг, а потім продовжувати його прийом у дозуванні 75 мг один раз на добу. Одночасно з клопідогрелом необхідно приймати АСК у дозі від 75 до 325 мг 1 раз на добу. У клінічному дослідженні CURE більшість пацієнтів із гострим коронарним синдромом додатково отримували лікування гепарином. Гострий інфаркт міокарда з підйомом сегмента ST Рекомендована добова доза клопідогрелу становить 75 мг одноразово і приймається разом з АСК із застосуванням або без застосування тромболітиків. Прийом клопідогрелу можна починати як з дози навантаження, так і без неї (у дослідженні CLARITY приймалася навантажувальна доза 300 мг). У пацієнтів старше 75 років лікування клопідогрелом має починатися без прийому його дози навантаження. Фібриляція передсердь Клопідогрел слід приймати у добовій дозі 75 мг. У комбінації з клопідогрелом необхідно приймати АСК у дозі 75-100 мг щодня. Фармакогенетика (пацієнти з генетично обумовленою зниженою активністю ізоферменту CYP2C19) Низька активність ізоферменту CYP2C19 пов'язана із зменшенням антиагрегантної дії клопідогрелу. Режим застосування більш високих доз (600 мг навантажувальна доза, потім 150 мг один раз на добу щодня) у пацієнтів з низькою активністю ізоферменту CYP2C19 збільшує антиагрегантну дію клопідогрелу. У пацієнтів з низькою активністю ізоферменту CYP2C19 можна розглянути питання про застосування більш високих доз клопідогрелу. Точний режим дозування для цієї популяції пацієнтів у клінічних дослідженнях, що враховують клінічні результати, не встановлено. Спеціальні групи патентів Дитячий вік до 18 років: безпека та ефективність застосування препарату у педіатричних популяціях не встановлені. Пацієнти старше 75 років: корекція дози не потрібна. У добровольців старше 75 років у порівнянні з молодими добровольцями не було отримано відмінностей за показниками агрегації тромбоцитів та часу кровотечі. Пацієнти з порушенням функції нирок Після повторних прийомів клопідогрелу у дозуванні 75 мг/добу у пацієнтів з тяжким ураженням нирок (КК від 5 до 15 мл/хв) інгібування АДФ-індукованої агрегації тромбоцитів (25 %) було нижчим порівняно з таким у здорових добровольців, проте подовження часу кровотечі порівняно з даними у здорових добровольців, які отримували клопідогрел у дозуванні 75 мг на добу. Пацієнти з порушенням функції печінки Після щоденного прийому клопідогрелу протягом 10 днів у добовій дозі 75 мг у пацієнтів з тяжким ураженням печінки інгібування АДФ-індукованої агрегації тромбоцитів можна порівняти з даними у здорових добровольців. Середній час кровотечі також можна порівняти в обох групах. Пацієнти різної етнічної приналежності Поширеність алелей генів ізоферменту CYP2C19, які відповідають за проміжний та знижений метаболізм клопідогрелу до його активного метаболіту, відрізняється у представників різних етнічних груп. Є лише обмежені дані для представників монголоїдної раси щодо оцінки впливу генотипу ізоферменту CYP2C19 на клінічні результуючі події. Підлога У невеликому дослідженні, що порівнює фармакодинамічні властивості клопідогрелу у чоловіків та жінок, у жінок спостерігалося менше інгібування АДФ-індукованої агрегації тромбоцитів, але відмінностей у подовженні часу кровотечі не було. У великому контрольованому дослідженні CAPRIE (клопідогрел у порівнянні з АСК у пацієнтів з ризиком розвитку ішемічних ускладнень), частота клінічних результатів, інших побічних дій та відхилень від норми клініко-лабораторних показників була однаковою як у чоловіків, так і у жінок.ПередозуванняСимптоми передозування Передозування клопідогрелу може призвести до збільшення часу кровотечі з подальшими ускладненнями у вигляді розвитку кровотеч. Заходи щодо надання допомоги при передозуванні З появою кровотечі потрібне проведення відповідних лікувальних заходів. Антидот клопідогрелу не встановлено. Якщо необхідна швидка корекція часу кровотечі, що подовжився, то рекомендується проведення переливання тромбоцитарної маси.Запобіжні заходи та особливі вказівкиПри лікуванні клопідогрелом, особливо протягом перших тижнів лікування та/або після інвазивних кардіологічних процедур/хірургічного втручання, необхідно вести ретельне спостереження за пацієнтами щодо виключення ознак кровотечі, у тому числі і прихованого. Кровотечі та гематологічні порушення У зв'язку з ризиком розвитку кровотечі та небажаних явищ з боку крові у разі появи в ході лікування клінічних симптомів, підозрілих на виникнення кровотечі, слід терміново зробити загальний клінічний аналіз крові, визначити активований частковий тромбопластиновий час (АЧТВ), кількість тромбоцитів, показники функціональної активності тром та провести інші необхідні дослідження. Одночасне застосування клопідогрелу з варфарином може посилити ризик кровотечі (див. розділ "Взаємодія з іншими лікарськими засобами"), тому слід бути обережним при одночасному застосуванні клопідогрелу та варфарину. Клопідогрел, як і інші антитромбоцитарні засоби, слід застосовувати з обережністю у пацієнтів, які мають підвищений ризик розвитку кровотечі, пов'язаний з травмами, хірургічними втручаннями або іншими патологічними станами, а також у пацієнтів, які приймають АСК, НПЗП (у тому числі інгібітори ЦОГ-2). , гепарин, блокатори глікопротеїну IIb/IIIа, СІОЗС та потужні індуктори ізоферменту CYP2C19 Якщо пацієнт має планову хірургічну операцію, і при цьому немає необхідності в антитромбоцитарному ефекті, то за 5-7 днів до операції прийом клопідогрелу слід припинити. Клопідогрел подовжує час кровотечі і повинен застосовуватися з обережністю у пацієнтів із захворюваннями, що схильні до розвитку кровотеч (особливо, шлунково-кишкових та внутрішньоочних). Препарати, які можуть спричинити пошкодження слизової оболонки шлунково-кишкового тракту (такі як АСК, нестероїдні протизапальні засоби) у пацієнтів, які приймають клопідогрел, слід застосовувати з обережністю. Пацієнти повинні бути попереджені про те, що при прийомі клопідогрелу (одного або в комбінації з АСК) для зупинки кровотечі може знадобитися більше часу, а також про те, що у разі виникнення у них незвичайної (по локалізації або тривалості) кровотечі їм слід повідомити про це свого лікаря. Перед будь-якою майбутньою операцією та перед початком прийому будь-якого нового лікарського препарату пацієнти повинні повідомляти лікаря (включаючи стоматолога) про прийом клопідогрелу. Нещодавно перенесений ішемічний інсульт Показано, що у пацієнтів з нещодавно перенесеним минущим порушенням мозкового кровообігу або інсультом, що мають високий ризик розвитку повторних ішемічних ускладнень, комбінація АСК та клопідогрелу підвищує частоту розвитку великих кровотеч. Тому така комбінована терапія повинна проводитися з обережністю і лише у разі доведеної клінічної користі від її застосування. Прийом клопідогрелу не рекомендується при гострому інсульті з давністю менше 7 днів (оскільки відсутні дані щодо його застосування при цьому стані). Тромботична тромбоцитопенічна пурпура (ТТП) Дуже рідко після застосування клопідогрелу (іноді навіть нетривалого) відзначалися випадки розвитку тромботичної тромбоцитопенічної пурпури (ТТП), яка характеризується тромбоцитопенією та мікроангіопатичною гемолітичною анемією, що супроводжуються неврологічними розладами, порушенням функції. ТТП є потенційно загрозливим для життя станом, що вимагає негайного лікування, включаючи плазмаферез. Набута гемофілія Повідомлялося про випадки розвитку набутої гемофілії прийому клопідогрелу. При підтвердженому ізольованому збільшенні АЧТВ, що супроводжується або не супроводжується розвитком кровотечі, слід розглянути питання можливості розвитку набутої гемофілії. Пацієнти з підтвердженим діагнозом набутої гемофілії повинні спостерігатися та лікуватися фахівцями з цього захворювання та припинити прийом клопідогрелу. Функціональна активність ізоферменту CYP2C19 У пацієнтів з низькою активністю ізоферменту CYP2C19 при застосуванні клопідогрелу в рекомендованих дозах утворюється менше активного метаболіту клопідогрелу і слабше виражена його антиагрегантна дія, у зв'язку з чим при прийомі звичайно рекомендованих доз клопідогрелу при гострому коронарному синдромі. судинних ускладнень, ніж у пацієнтів із нормальною активністю ізоферменту CYP2C19. Очікується, що застосування лікарських засобів, які індукують активність ізоферменту CYP2C19, може спричинити збільшення концентрації активного метаболіту клопідогрелу та підвищувати ризик виникнення кровотечі. В якості запобіжного заходу не рекомендується застосовувати одночасно потужні індуктори ізоферменту CYP2C19 і клопідогрел. Є тести визначення генотипу CYP2C19, які можуть бути використані для допомоги у виборі терапевтичної стратегії. Слід розглянути питання застосування більш високих доз клопідогрелу у пацієнтів з низькою активністю CYP2C19. Перехресні алергічні та/або гематологічні реакції між тієнопіридинами У пацієнтів слід збирати анамнез на предмет алергічних та/або гематологічних реакцій, що були раніше, на інші тієнопіридини (такі як тіклопідин, прасугрел), оскільки повідомлялося про наявність перехресних алергічних та/або гематологічних реакцій між тіенопіридинами (див. розділ "Побічна дія"). Тієнопіридини можуть викликати помірні та тяжкі алергічні реакції (такі як висипання на шкірі, ангіоневротичний набряк) або гематологічні реакції (такі як тромбоцитопенія і нейтропенія). Пацієнти, у яких раніше спостерігалися алергічні та/або гематологічні реакції на один із препаратів групи тієнопіридинів, можуть мати підвищений ризик розвитку подібних реакцій на інший препарат групи тієнопіридинів. Рекомендується моніторинг перехресних алергічних та/або гематологічних реакцій. Ниркова недостатність Досвід застосування клопідогрелу у пацієнтів з тяжкою нирковою недостатністю обмежений. Тому слід з обережністю застосовувати клопідогрел у цієї групи пацієнтів. Печінкова недостатність Є обмежений досвід застосування клопідогрелу у пацієнтів з тяжкими захворюваннями печінки, які можуть бути схильними до розвитку геморагічного діатезу. Тому слід з обережністю застосовувати клопідогрел у цієї групи пацієнтів. Вплив на здатність до керування автотранспортом та управління механізмами Препарат Плавікс® не істотно впливає на здібності, необхідні для керування автомобілем або заняття іншими потенційно небезпечними видами діяльності.Умови відпустки з аптекЗа рецептомВідео на цю тему
1 760,00 грн
163,00 грн
Склад, форма випуску та упаковка1 флакон містить: колаген: 100 мкг; фосфат кальцію [Ca3(PO4)2]: 1 мкг; хлорид натрію [NaCl]: 18 мг; вода для ін'єкцій [H2O]: до 2 мл. Щільність імплантату: 1003-1009 г/мл. В'язкість імплантату: 1,50 - 2,30 мПа?с; pH імплантату: 5,2-7,0. Осмоляльність імплантату: 285-315 мОсм/кг. Механічні домішки імплантату: > 10 мкм: 25 мкм: Вага імпланту у флаконі: 2,06 - 2,18 р. Об'єм, що видобувається: 10 мл (x 5 флаконів) Бактеріальні ендотоксини:ХарактеристикаПЛЕКСАТРОН являє собою імплантат колаген-містить для внутрішньосуглобового і періартикулярного введення, який сприяє збільшенню обсягу рухів завдяки уповільненню процесів деградації хрящової тканини суглобових поверхонь і відновленню пошкоджень, що виникли в результаті: старіння, порушення постави, супутніх хронічних захворювань, тканини. ПЛЕКСАТРОН – це медичний виріб, який особливо ефективний при лікуванні кульшового суглоба. Має наступні терапевтичні функції: бар'єрний ефект; Змащувальний ефект; Механічна підтримка під час проведення іншого медикаментозного лікування. Медичний виріб ПЛЕКСАТРОН призначений для використання кваліфікованим персоналом у приватних чи державних медичних установах з метою: Збільшення обсягу рухів у кульшовому суглобі; Підвищення еластичності м'язової тканини в попереково-крижової області; Зміцнення навколосуглобової м'язової тканини; Місцевого полегшення болю, болю під час руху, і навіть болю, викликаної порушенням постави.ІнструкціяТехніка періартикулярного введення (місце введення необхідно обробити антисептиком; голка вводиться на глибину 6-8 мм). Рекомендується використовувати такі матеріали та обладнання: Матеріали для антисептичної обробки шкіри: рукавички одноразового застосування, розчин йоду, спиртовий розчин, стерильні марлеві серветки, хлоретиловий спрей для обробки шкіри; Голки: стерильні типорозміри 27G; Шприци: об'ємом 5 або 10 см3 відповідно до об'єму розчину. Техніка внутрішньосуглобової ін'єкції Рекомендується використовувати такі матеріали та обладнання: Матеріали для антисептичної обробки шкіри: рукавички одноразового застосування, розчин йоду, спиртовий розчин, стерильні марлеві серветки, хлоретиловий спрей для обробки шкіри; У місці ін'єкції рекомендується застосування місцевого анестетика; Голки: стерильні типорозміри 22 G; Шприци: об'ємом 2 см3 відповідно до об'єму розчину.РекомендуєтьсяПЛЕКСАТРОН може застосовуватися як самостійне лікування або комбіновану терапію (спільно з виробами того ж спектра), що дозволяє підібрати персональне лікування та досягти позитивних клінічних результатів.Протипоказання до застосуванняПід час лікування необхідно ретельне спостереження пацієнтів, які приймають антикоагулянти, або з діагностованою ламкістю судин. Випадків підвищеної чутливості до складу плексатрона не спостерігалося. Однак пацієнтам з підвищеною чутливістю до компонентів необхідно виконати шкірно-алергічну пробу у формі підшкірної ін'єкції в руку з оцінкою результату через 1 годину.Спосіб застосування та дозиПротокол лікування: 1 ін'єкція на тиждень протягом 10 тижнів поспіль. Схема лікування підбирається індивідуально.Запобіжні заходи та особливі вказівкиПри болі в тазостегновому суглобі необхідно проведення диференціальної діагностики для виявлення болю, викликаного первинною та метастатичною онкологією, відбитого болю, викликаного невралгією поперекового відділу хребта, пахвинної грижі. Легке почервоніння у місці ін'єкції може бути наслідком механічної дії голки або шкірною реакцією. При введенні можуть виникнути ознаки печіння/болі в місці введення, які проходять мимовільно протягом 5-10 хвилин після процедури. До та після введення шкіру необхідно обробити антисептиком. Піогенні бактерії можуть призвести до утворення абсцесу у місці ін'єкції.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. активні речовини: фелодипін – 2,5/5/10 мг; допоміжні речовини: парафін; етанол; гідроксипропіл целюлоза; гідроксипропілметил целюлоза; заліза оксид Е 172; лактоза безводна; МКЦ; поліетилен гліколь 6000; поліоксил 40 гідрогенізована рицинова олія; пропив галлат; натрію алюмінію силікат; натрію стеарил фумарат; титану діоксид Е 171; вода очищена. у пластикових флаконах по 30 шт.; у пачці картонної 1 флакон.Опис лікарської формиТаблетки, вкриті оболонкою, пролонгованої дії, яка обумовлена наявністю матриксу з гідрофільного гелю, що забезпечує поступове вивільнення активної речовини. Плендил 2,5 мг: жовті двоопуклі круглі таблетки діаметром 8,5 мм, з одного боку яких вигравірувано A/FL, з іншого – 2,5. Плендил 5 мг: рожеві двоопуклі круглі таблетки діаметром 9 мм, на одній стороні яких вигравірувано A/Fm, на іншій – 5. Плендил 10 мг: червоно-коричневі двоопуклі круглі таблетки діаметром 9 мм, з одного боку яких вигравіровано A/FE, з іншого – 10.Фармакотерапевтична групаГіпотензивний, антиангінальний.ФармакокінетикаСистемна біодоступність фелодипії становить приблизно 15% і не залежить від прийому їжі. Однак швидкість абсорбції, але не її ступінь, може змінюватися в залежності від їди, і Cmax в плазмі, таким чином, підвищується приблизно на 65%. Cmax у плазмі досягається через 3-5 год. Препарат зв'язується з білками плазми на 99%. Vd у рівноважному стані становить 10 л/кг. T1/2 становить приблизно 25 год, фаза плато досягається приблизно 5 днів. Не кумулює навіть за тривалого прийому. Загальний плазмовий кліренс становить 1200 мл/хв. Зменшений кліренс у хворих похилого віку та у пацієнтів зі зниженою функцією печінки призводить до збільшення концентрації фелодипіну у плазмі крові. Водночас вікова ознака лише частково пояснює індивідуальні зміни плазмової концентрації фелодипіну. Фелодипін метаболізується в печінці, всі ідентифіковані метаболіти не мають вазодиляторного ефекту (гемодинамічної активності). Близько 70% від прийнятої дози виділяється у вигляді метаболітів із сечею, решта – з фекаліями. Менш 0.5% виділяється із сечею у незміненому вигляді. За порушення функції нирок плазмова концентрація фелодипіну не змінюється, але спостерігається кумуляція неактивних метаболітів. Фелодипін не виводиться при гемодіалізі.ФармакодинамікаБлокатор повільних кальцієвих каналів, що застосовується для лікування артеріальної гіпертензії та стабільної стенокардії. Фелодипін - похідне дигідропіридину, являє собою рацемічну суміш. Фелодипін знижує артеріальний тиск за рахунок зниження загального периферичного судинного опору, особливо в артеріолах. Провідність і скоротлива здатність гладкої мускулатури судин пригнічується шляхом на кальцієві канали клітинних мембран. Завдяки високій селективності щодо гладкої мускулатури артеріол, фелодипін у терапевтичних дозах не має негативного інотропного ефекту на скоротливість або провідність серця. Фелодипін розслаблює гладку мускулатуру дихальних шляхів. Показано, що фелодипін незначно впливає на моторику ШКТ. При тривалому застосуванні фелодипін не має клінічно значущого ефекту на вміст ліпідів у крові.У пацієнтів із цукровим діабетом 2 типу при застосуванні фелодипіну протягом 6 місяців не відзначено клінічно значущого впливу на метаболічні процеси (HbA1c). Фелодипін можна також призначати пацієнтам зі зниженою функцією лівого шлуночка, які отримують стандартну терапію, та пацієнтам з бронхіальною астмою, цукровим діабетом, подагрою або гіперліпідемією. Антигіпертензивний ефект: зниження артеріального тиску при прийомі фелодипіну обумовлене зменшенням периферичного судинного опору. Фелодипін ефективно знижує АТ у пацієнтів з артеріальною гіпертензією як у положенні лежачи, так і в положенні сидячи та стоячи, у стані спокою та при фізичному навантаженні. Оскільки фелодипін не впливає на гладку мускулатуру вен або адренергічний вазомоторний контроль, то розвиток ортостатичної гіпотензії не відбувається. На початку лікування, внаслідок зниження артеріального тиску на фоні прийому фелодипіну, може спостерігатися тимчасове рефлекторне збільшення ЧСС та серцевого викиду. Збільшенню ЧСС перешкоджає одночасне з фелодипіном застосування β-адреноблокаторів. Дія фелодипіну на артеріальний тиск і периферичний судинний опір корелює з плазмовою концентрацією фелодипіну. При рівноважному стані клінічний ефект зберігається між прийомом доз та зниження артеріального тиску зберігається протягом 24 год. Лікування фелодипіном призводить до регресії гіпертрофії лівого шлуночка. Фелодипін має натрійуретичним і діуретичним ефектом і не має калійуретичним ефектом. При прийомі фелодипіну знижується канальцева реабсорбія натрію та води, що пояснює відсутність затримки солей та рідини в організмі. Фелодипін знижує судинний опір у нирках та посилює перфузію нирок. Фелодипін не впливає на клубочкову фільтрацію та екскрецію альбуміну. У дослідженні НОП (Hypertension Optimal Treatment Study - Дослідження з Оптимальної Терапії Гіпертензії), за участю 18.790 пацієнтів з артеріальною гіпертензією легкого - середнього ступеня тяжкості, застосування Пленділа в комбінації з інгібіторами АПФ, бета-адреноблокаторами діа менше 90 мм. у 93% пацієнтів. У цьому ж дослідженні, частота серцево-судинних ускладнень у пацієнтів з цукровим діабетом 2 типу (п=1.501) виявилася значно нижчою (50%) у групі пацієнтів, у яких вдалося досягти зниження діастолічного АТ до рівня Для лікування артеріальної гіпертензії Пленділ може застосовуватися як монотерапія або комбінація з іншими антигілертензивними препаратами, такими як бета-адреноблокатори, діуретики або інгібітори АПФ. Антиішемічний ефект: Застосування фелодипіну призводить до покращення кровопостачання міокарда за рахунок дилятації коронарних судин. Зменшення навантаження на серце забезпечується за рахунок зниження периферичного судинного опору (зниження навантаження, що долається серцевим м'язом), що призводить до зниження потреби міокарда в кисні. Фелодипін знімає спазм коронарних судин. Фелодипін покращує скорочувальну здатність та зменшує частоту нападів стенокардії у пацієнтів із стабільною стенокардією напруги. На початку терапії може спостерігатися тимчасове збільшення ЧСС, що купується призначенням бета-адреноблокаторів. Ефект настає через 2 години і триває протягом 24 годин. Для лікування стабільної стенокардії фелодипін може застосовуватися у комбінації з бета-адреноблокаторами або у вигляді монотерапії.Показання до застосуванняАртеріальна гіпертензія, стенокардія.Протипоказання до застосуваннясерцева недостатність у стадії декомпенсації; гострий інфаркт міокарда; нестабільна стенокардія; вік до 18 років (ефективність та безпека не встановлені); підвищена чутливість до фелодипіну або до інших компонентів, що входять до складу препарату. З обережністю: аортальний стеноз, лабільність артеріального тиску, порушення функції печінки, виражена ниркова недостатність.Вагітність та лактаціяВагітність В даний час немає достатніх даних щодо застосування фелодипіну у вагітних. На основі отриманих у тварин даних про порушення розвитку плода, фелодипін не повинен призначатися під час вагітності. Блокатори "повільних" кальцієвих каналів можуть пригнічувати скорочення матки при передчасних пологах, водночас недостатньо даних, що підтверджують збільшення тривалості фізіологічних пологів. Можливий ризик розвитку гіпоксії плода за наявності у матері артеріальної гіпотензії та зменшення перфузії в матці за рахунок перерозподілу кровотоку та периферичної вазодилатації. Лактація Фелодипін проникає у грудне молоко. При прийомі матір'ю фелодипіну в терапевтичних дозах лише незначна кількість препарату потрапляє з грудним молоком дитині. Недостатній досвід застосування фелодипіну жінками у період лактації не виключає ризик впливу препарату на дітей, які перебувають на грудному вигодовуванні, тому не рекомендується призначати фелодипін жінкам у період лактації. При необхідності продовження терапії для досягнення клінічного ефекту слід розглянути питання щодо припинення грудного вигодовування. Протипоказання: вік до 18 років (ефективність та безпека не встановлені).Побічна діяЧасто (більше 1%): біль голови, припливи, периферичні набряки. Іноді (0,1-1%): тахікардія, серцебиття, відчуття втоми, запаморочення, парестезія, нудота, висипання, свербіж. Рідко (0,01-0,1%): непритомність, блювання, артралгія, міалгія, сексуальні порушення, імпотенція, кропив'янка. Дуже рідко (менше 0,01%): гіперплазія ясен, підвищення рівня печінкових ферментів, фотосенсибілізація, лакіурія, алергічні реакції (лихоманка, ангіоневротичний набряк).Взаємодія з лікарськими засобамиФелодипін є субстратом CYP 3A4. Препарати, що індукують або інгібують CYP 3A4, значно впливають на концентрацію фелодипіну в плазмі крові. Препарати, що індукують систему цитохрому Р450: фенітоїн, карбамазепін фелодипіну на 82%. Слід уникати спільного призначення з індукторами CYP 3A4. Препарати, що інгібують систему цитохрому Р450: протигрибкові препарати азолового ряду (ітраконазол, кетоконазол), макролідні антибіотики (наприклад, еритроміцин) та інгібітори ВІЛ-протеаз є інгібіторами ферментної системи CYP 3A4. При сумісному призначенні ітраконазолу Cmax фелодипіну збільшується у 8 разів, AUC у 6 разів. При сумісному призначенні еритроміцину Cmax та AUC фелодипіну збільшується приблизно у 2.5 рази. Слід уникати спільного призначення фелідипіну та інгібіторів CYP 3A4. Сік грейпфрута пригнічує ферментну систему CYP 3A4. Застосування фелодипіну з грейпфрутовим соком збільшує Cmax та AUC фелодипіну приблизно у 2 рази. Слід уникати сумісного застосування. Такролімус: фелодипін може спричинити збільшення концентрації такролімусу у плазмі крові. При сумісному застосуванні рекомендується контролювати концентрацію такролімусу в сироватці крові, може знадобитися коригування дози такролімусу. Циклоспорин: при сумісному призначенні циклоспорину та фелодипіну Cmax фелодипіну збільшується на 150%, AUC збільшується на 60%. Проте, вплив фелодипіну на фармакокінетичні показники циклоспорину є мінімальним. Циметидин: спільне застосування циметидину та фелодипіну призводить до збільшення Cmax та AUC фелодипіну на 55%.Спосіб застосування та дозиВсередину таблетки рекомендується приймати вранці, запиваючи водою. Таблетки не можна розламувати, кришити чи розжовувати. Препарат можна приймати натще або після легкого сніданку, що не містить великої кількості жирів або вуглеводів. Даних щодо застосування фелодипіну у дітей немає. Артеріальна гіпертензія. Доза повинна підбиратися індивідуально. Початкова доза – 5 мг 1 раз на добу. При необхідності дозу можна збільшити або додати інший антигіпертензивний препарат. Звичайна підтримуюча доза Пленділу становить від 5 до 10 мг 1 раз на добу. У пацієнтів похилого віку слід розглянути можливість початку лікування з добової дози 2,5 мг. Стенокардія. Доза повинна підбиратися індивідуально. Початкова доза – 5 мг 1 раз на добу, за необхідності збільшують дозу до 10 мг 1 раз на добу.ПередозуванняТоксичність: 10 мг фелодипіну у 2-річної дитини викликало незначну інтоксикацію. 150-200 мг фелодипії у 17-річного пацієнта та 250 мг у дорослого викликало інтоксикацію від незначного ступеня до помірної. Ймовірно, фелодіїн надає більш значний ефект на периферичний кровообіг, ніж на серце порівняно з іншими препаратами даної терапевтичної групи. Симптоми: при передозуванні симптоми інтоксикації виявляються через 12-16 годин після прийому препарату, тяжкі симптоми можуть виникати через кілька днів після прийому. Можуть відзначатися такі симптоми: брадикардія (іноді тахікардія), виражене зниження артеріального тиску, AV блокада І-ІІІ ступенів, шлуночкова екстрасистолія, передсердно-шлуночкова дисоціація, асистолія, фібриляція шлуночків; біль голови, запаморочення, порушення свідомості (або кома), судоми; задишка, набряк легень (не серцевий) та апное; у дорослих можливий розвиток респіраторного дистрес-синдрому; ацидоз, гіпокаліємія, гіперглікемія, можливо гіпокальціємія; почервоніння особи, що супроводжується "припливами", гіпотермія; нудота та блювання. Найбільший ризик має вплив передозування на циркуляцію. Лікування: Призначення активованого вугілля, у разі потреби промивання шлунка, у ряді випадків ефективне навіть на пізній стадії інтоксикації. Специфічний антидот – препарати кальцію. Важливо! Атропін (0.25-0.5 мг внутрішньовенно для дорослих, 10-20 мкг/кг для дітей) повинен бути призначений до промивання шлунка (через ризик стимулювання блукаючого нерва). Контроль ЕКГ. За необхідності забезпечити прохідність дихальних шляхів та адекватну вентиляцію легень. Показано корекцію кислотно-основного стану та електролітів сироватки крові. У разі брадикардії та AV-блокади призначають атропін 0.5-1 мг внутрішньовенно дорослим (20-50 мкг/кг дітям), при необхідності повторюють введення, або спочатку вводять ізопреналін 0.05-0.1 мкг/кг/хв. При гострій інтоксикації на ранній стадії може знадобитися встановлення штучного водія ритму. Зниження АТ коригують внутрішньовенно введенням рідини, дорослим внутрішньовенно вводять розчин кальцію глюконату (9 мг Са/мл) 20-30 мл протягом 5 хв або у вигляді інфузії (3-5 мг Са/кг дітям),при необхідності повторюють введення у тій же дозі. При необхідності інфузійно вводять норепінефрін (адреналін) або допамін. При гострій інтоксикації може бути призначений глюкагон. При зупинці серця через передозування можуть знадобитися реанімаційні заходи протягом декількох годин. При судомах призначають діазепам. Проводиться інше симптоматичне лікування.Запобіжні заходи та особливі вказівкиПотрібно дотримуватись особливої обережності при наступних станах: аортальний стеноз, порушення функції печінки, виражена ниркова недостатність (КК) Спільне застосування препаратів, що інгібують ферментну систему CYP 3A4, призводить до значного збільшення концентрації фелодипіну в плазмі крові, у зв'язку з чим слід уникати таких комбінацій. Слід уникати прийому препарату з грейпфрутовим соком через значне збільшення концентрації фелодипіну в плазмі. Вплив на здатність керувати автомобілем та іншими механізмами. При керуванні автомобілем або іншими механізмами, що потребують підвищеної уваги, слід враховувати можливість розвитку запаморочення та слабкості на фоні прийому препарату. На початку терапії або в період збільшення дози пацієнтам слід утримуватися від занять небезпечною діяльністю, що потребує концентрації уваги та швидкості психомоторних реакцій.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Активна речовина: цилостазол 100 мг. Допоміжні речовини: Крохмаль картопляний прежелатинізований 84,0 мг, целюлоза мікрокристалічна 35,0 мг; кармелозу кальцію 2,2 мг; магнію стеарат 2,3 мг; гіпромелоза 26,5 мг. Таблетки 100 мг – 60 шт в уп.Фармакотерапевтична групаПлетакс – це антиагрегантний засіб. Основним механізмом фармакологічної дії цилостазолу є інгібування фосфодіестерази 3 типу і, отже, підвищення внутрішньоклітинного вмісту циклічного аденозинмонофосфату (цАМФ) у різних органах та тканинах. В експериментальних та невеликих клінічних дослідженнях встановлено, що цилостазол має вазодилатуючу дію. Цилостазол розширює переважно стегнові артерії, меншою мірою - хребетну, сонну та верхню брижову артерії. Ниркові артерії не чутливі до дії цилостазолу. Цилостазол інгібує проліферацію гладком'язових, клітин людини та щурів в умовах in vitro.Клінічна фармакологіяАнтиагреганти.Показання до застосуванняСимптоматичне лікування хромоти, що перемежується. Цилостазол ;застосовується для збільшення максимальної відстані та відстані, що проходить без болю, у пацієнтів з переміжною кульгавістю, у яких немає болів у спокої і відсутні ознаки ;некрозу ;периферичних тканин (хронічна ішемія нижніх кінцівок II ступеня за класифікацією Фонтейну). Цилостазол ;призначений для застосування в якості терапії другого ряду у пацієнтів з переміжною кульгавістю, у яких зміна способу життя (що включають припинення куріння і програми фізичної реабілітації, що проводяться під наглядом спеціаліста) та інші належні втручання виявилися недостатніми для зменшення симптомів перемежування.Протипоказання до застосуванняПідвищена чутливість до цилостазолу або до будь-якого іншого компонента препарату; Тяжка ниркова недостатність (кліренс креатиніну <25 мл/хв); Помірна або важка; печінкова недостатність; Хронічна серцева недостатність; Схильність до кровотеч ;(наприклад, виразкова хвороба шлунка або дванадцятипалої кишки в стадії загострення, недавно [протягом останніх 6 місяців] перенесений ;геморагічний інсульт, проліферативна діабетична ;ретинопатія, погано контрольована ;артеріальна гіпертензія); Шлуночкова тахікардія, фібриляція шлуночків або політопна шлуночкова екстрасистолія в анамнезі (незалежно від наявності або відсутності адекватної антиаритмічної терапії); Подовжений інтервал QT на ЕКГ; Тяжка тахіаритмія в анамнезі; Нестабільна ;стенокардія ;або ;інфаркт міокарда ;протягом останніх б місяців; Інвазивне втручання на коронарних артеріях протягом останніх місяців; Одночасне застосування двох і більше антиагрегантних або антикоагулянтних лікарських засобів (наприклад, ацетилсаліцилової кислоти,; клопідогрелу,; гепарину,; Варфарину,; Одночасне застосування потужних інгібіторів CYP3A4 або CYP2C19 (наприклад, циметидину, ділтіазему, еритроміцину, кетоконазолу, лансопразолу, омепразолу та інгібіторів протеази ВІЛ-1); Вагітність; Період грудного вигодовування; Вік молодший 18 років (безпека та ефективність не вивчені). З обережністю Печінкова недостатність; легкого ступеня тяжкості; Хронічна ішемічна хвороба серця (зокрема, стабільна; стенокардія; напруги); Передсердна або шлуночкова екстрасистолія, фібриляція або тріпотіння передсердь; Цукровий діабет; Одновременное применение лекарственных препаратов, снижающих артериальное давление; Одновременное применение лекарственных препаратов, снижающих свертываемость крови; Одновременное применение субстратов CYP3A4 или CYP2C19 (например, ;цизаприда, ;мидазолама, ;нифедипина, ;верапамила); Пожилой возраст.Побочные действияНаиболее часто сообщаемыми побочными эффектами в клинических исследованиях были ;головная боль ;(> 30%), ;диарея ;и нарушения стула (>15% каждый). Эти побочные эффекты были легкой и умеренной степени интенсивности. Нарушения со стороны крови и лимфатической системы Часто: экхимоз. Нечасто: анемия. Редко: увеличения времени ;кровотечения, тромбоцитоз. Частота неизвестна: склонность к ;кровотечениям, тромбоцитопения, гранулоцитопия, ;агранулоцитоз, ;лейкопения, панцитопения, ;апластическая анемия. Нарушения со стороны иммунной системы Нечасто: алергічні реакції. Порушення з боку обміну речовин та харчування Часто: набряки (периферичні набряки, набряк особи), анорексія. Нечасто: гіперглікемія, цукровий діабет. Порушення психіки Нечасто: ;занепокоєння. Порушення з боку нервової системи Дуже часто: головний біль Часто: запаморочення. Нечасто: безсоння, порушення сну (незвичайні сновидіння), внутрішньочерепний крововилив. Частота невідома: парез, гіпостезія. Порушення з боку органу зору Часто: внутрішньоочний крововилив. Частота невідома: ;кон'юнктивіт. Порушення з боку органу слуху та лабіринтні порушення Частота невідома: дзвін у вухах. Порушення з боку серця Часто: серцебиття, тахікардія, ;стенокардія, ;аритмія, шлуночкові ;екстрасистоли. Нечасто: інфаркт міокарда, фібриляція передсердь, хронічна серцева недостатність, надшлуночкова тахікардія, шлуночкова тахікардія, синкопальний стан. Порушення з боку судин Часто: ортостатична гіпотензія. Нечасто: припливи спека, артеріальна гіпертензія, артеріальна гіпотензія. Порушення з боку дихальної системи, органів грудної клітки та середостіння. Часто: риніт, фарингіт. Нечасто: задишка; (диспное), пневмонія, кашель, легенева кровотеча, кровотеча з дихальних шляхів. Частота невідома: інтерстиційна пневмонія. Порушення з боку шлунково-кишкового тракту Дуже часто: діарея, порушення стільця. Часто: нудота, блювання, диспепсія, метеоризм, біль у животі, шлунково-кишкові кровотечі. Нечасто: гастрит. Порушення з боку печінки та жовчовивідних шляхів Частота невідома: гепатит, відхилення показників функції печінки від нормальних значень, жовтяниця. Порушення з боку шкіри та підшкірних тканин Часто: шкірний висип, ;шкірний свербіж. Нечасто: ;екзема, шкірні висипання, синдром Стівенса-Джонсона, токсичний епідермальний некроліз, ;кропивниця, підшкірний крововилив. Порушення з боку скелетно-м'язової та сполучної тканини Нечасто: ; міалгія, внутрішньом'язові гематоми. Порушення з боку нирок та сечовивідних шляхів Рідко: ниркова недостатність, порушення ниркової функції. Частота невідома: гематурія, півлакурія. Загальні розлади та порушення разом Часто: біль у грудях, ; астенія. Нечасто: озноб, нездужання. Частота невідома: пірексія, біль. Лабораторні та інструментальні дані Частота невідома: підвищення вмісту сечової кислоти в крові, підвищення вмісту сечовини в крові, підвищення вмісту креатиніну в крові. Збільшення частоти виникнення серцебиття і периферичних набряків відмчали при застосуванні ;цілостазолу ;у поєднанні з іншими вазодилататорами, що викликають рефлекторну тахікардію (наприклад, з дигідропіридиновими блокаторами 'повільних' кальцієвих каналів). Цилостазол; сам по собі підвищує ризик; кровотечі, і цей ризик може бути додатково збільшений при одночасному застосуванні; цилостазолу; з будь-яким іншим лікарським препаратом, що володіє таким же; Ризик внутрішньоочного крововиливу може бути підвищений у пацієнтів із цукровим діабетом. Встановлено більш високу частоту виникнення діареї та прискореного серцебиття у пацієнтів старше 70 років. Передозування Симптоми Інформація про гостре передозування; цилостазолу; у людини обмежена. Очікувані симптоми передозування: виражений головний біль, діарея, тахікардія, артеріальна гіпотензія, порушення серцевого ритму. Лікування Симптоматичне. У разі передозування необхідне ретельне спостереження та обстеження пацієнта. Необхідно очистити шлунок, викликавши блювання, або виконати промивання шлунка відповідно до загальноприйнятих рекомендацій. Внаслідок високого ступеня зв'язку з білками плазми гемодіаліз та перитонеальний діаліз практично неефективні.Взаємодія з лікарськими засобамиАцетилсаліцилова кислота Короткострокове (протягом ≤ 4 днів) одночасне застосування ;цилостазолу ;і ацетилсаліцилової кислоти призводить до збільшення на 23-25% АДФ-індукованої агрегації тромбоцитів в умовах ex vivo порівняно з монотерапією ацетилсаліцилової кислоти. У зв'язку зі збільшенням ризику виникнення ;кровотеч ;при одночасному застосуванні з ;цілостазолом ;необхідне ретельне спостереження. Клопідогрел; та інші антиагрегантні лікарські засоби У дослідженні у здорових добровольців одночасне застосування; цілостазолу; з; клопідогрелом; При застосуванні ;клопідогрелу ;як у вигляді монотерапії так і в поєднанні з ;цілостазолом, у здорових добровольців збільшувався час ;кровотечі. Прийом ;цілостазолу ;не приводив до додаткового значного подовження часу ;кровотечі. Тим не менш, рекомендується дотримуватися обережності при одночасному застосуванні; цилостазолу; з будь-яким препаратом, що інгібує агрегацію тромбоцитів. Рекомендується регулярно контролювати час кровотечі. Застосування ;цілостазолу ;протипоказане пацієнтам, які отримують одночасно два або більше антиагрегантних та/або антикоагулянтних лікарських засобів. Пероральні антикоагулянти У клінічному дослідженні одноразовий прийом ;цилостазолу ;не інгібував метаболізм ;варфарину ;і не впливав на показники згортання крові (ПВ, АЧТВ, час ;кровотечі). Тим не менш, рекомендується дотримуватися обережності при одночасному застосуванні; цилостазолу; з будь-яким антикоагулянтним препаратом. Цилостазола протипоказано пацієнтам, які отримують одночасно два або більше антиагрегантних та/або антикоагулянтних лікарських засобів. Інгібітори коферментів цитохрому Р450 У печінці ;цилостазол ;в основному метаболізується під впливом ферментів цитохрому Р450, переважно CYP3A4 і CYP2C19 і, меншою мірою, CYP1A2. Вважається, що дегидроцилостазол, в 4-7 разів перевищує ;цилостазол ;по можливості інгібувати агрегацію тромбоцитів, утворюється переважно з участю CYP3A4. 4'-транс-гідроксицилостазол, що має у п'ять разів менш виражену здатність інгібувати агрегацію тромбоцитів, утворюється в основному під дією CYP2C19. Відповідно, препарати, що інгібують CYP3A4 (наприклад, деякі макроліди [еритроміцин, ;кларитроміцин], азольні протигрибкові препарати [кетоконазол, ;ітраконазол], інгібітори протеаз ВІЛ) і CYP2C19 (наприклад, інгібітори протон активність; цилостазолу;та можуть сприяти посиленню його небажаних ефектів. Відповідно, пацієнтам, які отримують потужні інгібітори CYP3A4 або CYP2C19, рекомендується призначати цілостазол у дозі 50 мг 2 рази на добу. Еритроміцин При одночасному прийомі; цилостазолу; з; На підставі змін показників AUC встановлено, що загальна фармакологічна активність ;цилостазолу ;при одночасному застосуванні з ;еритроміцином ;збільшується на 34%. Рекомендується зменшення дози ;цилостазолу ;до 50 мг 2 рази на добу при одночасному застосуванні з ;еритроміцином ;та іншими препаратами даної групи (наприклад, з ;кларитроміцином). При одночасному прийомі ;цилостазолу ;з ;кетоконазолом ;(потужний інгібітор CYP3A4) показник AUC ;цилостазолу ;збільшується на 117%, показник AUC дегідроцилостазолу зменшується на 15%, показник AUC 4'-транс-гидроксициста. На підставі змін показників AUC встановлено, що загальна фармакологічна активність ;цилостазолу ;при одночасному застосуванні з ;кетоконазолом ;збільшується на 34%. Рекомендується зменшення дози ;цилостазолу ;до 50 мг 2 рази на добу при одночасному застосуванні з ;кетоконазолом ;та іншими препаратами даної групи (наприклад, з ;ітраконазолом). Ділтіазем При одночасному прийомі ;цилостазолу ;з ;дилтіаземом ;(слабкий інгібітор CYP3A4) показники AUC ;цилостазолу, дегідроцилостазолу і 4'-транс-гідроксицилостазолу збільшуються відповідно на 44%, на 4% і на 43%. На підставі змін показників AUC встановлено, що загальна фармакологічна активність ;цилостазолу ;при одночасному застосуванні з ;ділтіаземом ;збільшується на 19%. Корекція дози ;цілостазолу ;при одночасному застосуванні з ;дилтіаземом ;не потрібно. Грейпфрутовий сік При одноразовому прийомі 100 мг ;цілостазолу ;одночасно з 240 мл грейпфрутового соку (інгібітор кишкового CYP3A4) суттєвої зміни фармакокінетичних показників ;цилостазолу ;не відзначалося. Корекція дози; цілостазолу; не потрібна. Тим не менш, прийом грейпрутового соку в більшій кількості може впливати на фармакокінетику; цилостазолу. Омепразол При одночасному прийомі ;цилостазолу ;з ;омепразолом ;(потужний інгібітор CYP2C19) показники AUC ;цилостазолу ;і дегідроцилостазолу збільшуються відповідно на 22% і на 68%, при цьому показник AUC 4'-транс-гідроксицилостазолу. На підставі змін показників AUC встановлено, що загальна фармакологічна активність ;цилостазолу ;при одночасному застосуванні з ;омепразолом ;збільшується на 47%. Рекомендується зменшення дози ;цилостазолу ;до 50 мг 2 рази на добу при одночасному застосуванні з ;омепразолом. Субстрати ізоферментів цитохрому Р450 Цилостазол ;збільшує показники AUC ;ловастатину ;(субстрат CYP3A4) та його бета-гідроксиліюго метаболіту на 70%. Рекомендується бути обережним при одночасному застосуванні ;цилостазолу ;з субстратами CYP3A4, що мають вузький терапевтичний діапазон (такими, як ;цизаприд, галофантрин, німозид, алкалоїди ріжків). Також рекомендується бути обережним при одночасному застосуванні ;цилостазолу ;з інгібіторами ГМГ-КоА-редуктази (статинами), метаболізуючими за участю CYP3A4 (симвастатин, ;аторвастатин ;і ;ловастатин). Індуктори іюферментів цитохрому Р450 Вплив препаратів, що збільшують активність CYP3A4 і CYP2C19 (таких, як ;карбамазепін, ;фенітоїн, ;рифампіцин, препарати Звіробою продірявленого), на фармакокінетику ;цилостазолу ;не вивчалося. При одночасному прийомі теоретично можливе зниження антиагрегантного ефекту; цилостазолу, тому необхідно регулярно контролювати час кровотечі. У клінічних дослідженнях встановлено, що куріння (фактор, що посилює активність CYP1A2) зменшує концентрацію цилостазолу в плазмі крові на 18%. Інші препарати Необхідно бути обережними при одночасному застосуванні ;цилостазолу ;з будь-якими препаратами, що знижують артеріальний тиск (в т.ч. з нітратами та інгібіторами фосфодіестерази-5), оскільки можливий адитивний ефект з розвитком артеріальної гіпотензії та рефлекторної тахікардії.Спосіб застосування та дозиПрепарат застосовують внутрішньо. Рекомендоване дозування; цилостазолу; становить 100 мг двічі на добу. Слід приймати ;цилостазол ;за 30 хвилин до їди. При прийомі ;цилостазолу ;під час їжі відзначається збільшення максимальної концентрації (Сmax) у плазмі крові, що може асоціюватися зі збільшенням частоти небажаних явищ. У разі пропуску прийому препарату необхідно прийняти наступну таблетку у звичайний час. Не слід приймати подвійну дозу цілостазолу. Терапію ;цілостазолом ;слід починати під наглядом лікаря, що має досвід лікування переміжної кульгавості. Лікар повинен повторно оцінити стан пацієнта через 3 місяці лікування, якщо терапія; цілостазолом; Пацієнти, які отримують лікування ;цилостазолом, повинні продовжувати виконувати рекомендації щодо зміни способу життя (відмова від куріння, фізичні вправи) та медикаментозну терапію (прийом гіполіпідемічних та антиагрегантних лікарських засобів), спрямовані на зменшення ризику серцево-судинних ускладнень. ;Цилостазол ;не є заміною зазначеного лікування. Застосування в спеціальних групах пацієнтів Літній вік Відсутні спеціальні вимоги до зміни дозування; цилостазолу; у літніх пацієнтів. Ниркова недостатність У пацієнтів з кліренсом креатиніну >25 мл/хв зміна дозування не потрібна. ;Цилостазол ;протипоказаний до застосування у пацієнтів з кліренсом креатиніну <25 мл/хв. Печінкова недостатність У пацієнтів з легкою печінковою недостатністю зміна дозування не потрібна. Відсутній досвід застосування ;цилостазолу ;у пацієнтів з помірною та тяжкою печінковою недостатністю. Оскільки ;цилостазол ;значною мірою метаболізується ферментами мікросомального окиснення печінки, застосування препарату протипоказане у пацієнтів з помірною та тяжкою печінковою недостатністю. Одночасний прийом потужних інгібіторів CYP3A4 або CYP2C19 У пацієнтів, які отримують препарати, які мають потужну інгібуючу дію на CYP3A4 (наприклад, деякі макроліди), або препарати, які мають потужну інгібуючу дію на CYP2C19 (наприклад, омепразол) слід зменшити дозу цилостазолу до 50 мг двічі на добу.Запобіжні заходи та особливі вказівкиПеред початком терапії; цілостазолом; слід оцінити можливість призначення інших способів лікування, таких як хірургічна реваскуляризація або консервативна терапія. За рахунок механізму фармакологічної дії; цилостазол; може викликати тахікардію, серцебиття, тахіаритмію та/або артеріальну гіпотензію. При прийомі ;цилостазолу ;частота серцевих скорочень може збільшуватися на 5-7 ударів на хвилину, що може спровокувати напад ;стенокардії ;у пацієнтів із групи ризику (наприклад, у пацієнтів зі стабільною ;стенокардією). Пацієнти, що мають підвищений ризик розвитку тяжких серцево-судинних ускладнень внаслідок збільшення частоти серцевого ритму (наприклад, пацієнти зі стабільною ІХС), потребують ретельного спостереження під час лікування цилостазолом. Застосування ;цілостазолу ;протипоказане у пацієнтів з нестабільною ;стенокардією ;або інфарктом міокарда/інвазивним втручанням на коронарних артеріях протягом останніх 6 місяців, а також у пацієнтів з тяжкою тахіаритмією в анамнезі. Необхідно бути обережними при призначенні ;цилостазолу ;пацієнтам з передсердною або шлуночковою екстрасистолією, а також пацієнтам з фібриляцією передсердь або тремтінням передсердь. Слід попередити пацієнта про необхідність повідомляти про будь-який випадок; кровотечі; або появи 'синяка' (підшкірної гематоми) при невеликому забитому місці. У разі розвитку крововиливу в сітківку ока прийом цилостазолу необхідно припинити. Оскільки ;цилостазол ;є інгібітором агрегації тромбоцитів, підвищується ризик ;кровотечі ;при хірургічних втручаннях (включаючи малі інвазивні процедури, такі як видалення зуба). При планованих хірургічних втручаннях (якщо антиагрегантна дія небажана); цилостазол; слід відмінити за 5 днів до операції. Повідомлялося про рідкісні або дуже рідкісні випадки гематологічних порушень, включаючи тромбоцитопенію, лейкопенію, агранулоцитоз, панцитопенію або аплатичну анемію. У більшості випадків ці порушення проходили після припинення прийому цілостазолу. Однак у кількох випадках панцитопенія і ;апластична анемія ;привели до летального результату. Пацієнта слід попередити про необхідність негайно повідомляти лікаря про будь-які симптоми, які можуть бути ранніми проявами гематологічних ускладнень, таких як висока лихоманка (пірексія) і ангіна. Слід виконати розгорнутий аналіз крові при підозрі на інфекцію або з появою клінічних симптомів гематологічних ускладнень. Необхідно негайно припинити прийом цилостазолу; у разі появи клінічних симптомів або лабораторних ознак гематологічних ускладнень. Слід бути обережним при одночасному застосуванні ;цилостазолу ;з лікарськими препаратами, що знижують артеріальний тиск (можливість адитивної дії з розвитком артеріальної гіпотензії та рефлекторної тахікардії) а також знижують згортання крові або інгібують агрегацію тромбоцитів. Вплив на здатність керувати транспортними засобами, механізмами Цилостазол; може викликати; запаморочення. Рекомендується бути обережним при керуванні транспортними засобами або роботі з механізмами в період лікування.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Активна речовина: цилостазол 50 мг. Крохмаль картопляний прежелатинізований, целюлоза мікрокристалічна; кармелозу кальцію; магнію стеарат; гіпромелоза. Таблетки 50 мг – 30 шт в уп.Фармакотерапевтична групаПлетакс – це антиагрегантний засіб. Основним механізмом фармакологічної дії цилостазолу є інгібування фосфодіестерази 3 типу і, отже, підвищення внутрішньоклітинного вмісту циклічного аденозинмонофосфату (цАМФ) у різних органах та тканинах. В експериментальних та невеликих клінічних дослідженнях встановлено, що цилостазол має вазодилатуючу дію. Цилостазол розширює переважно стегнові артерії, меншою мірою - хребетну, сонну та верхню брижову артерії. Ниркові артерії не чутливі до дії цилостазолу. Цилостазол інгібує проліферацію гладком'язових, клітин людини та щурів в умовах in vitro.Клінічна фармакологіяАнтиагреганти.Показання до застосуванняСимптоматичне лікування хромоти, що перемежується. Цилостазол ;застосовується для збільшення максимальної відстані та відстані, що проходить без болю, у пацієнтів з переміжною кульгавістю, у яких немає болів у спокої і відсутні ознаки ;некрозу ;периферичних тканин (хронічна ішемія нижніх кінцівок II ступеня за класифікацією Фонтейну). Цилостазол ;призначений для застосування в якості терапії другого ряду у пацієнтів з переміжною кульгавістю, у яких зміна способу життя (що включають припинення куріння і програми фізичної реабілітації, що проводяться під наглядом спеціаліста) та інші належні втручання виявилися недостатніми для зменшення симптомів перемежування.Протипоказання до застосуванняПідвищена чутливість до цилостазолу або до будь-якого іншого компонента препарату; Тяжка ниркова недостатність (кліренс креатиніну <25 мл/хв); Помірна або важка; печінкова недостатність; Хронічна серцева недостатність; Схильність до кровотеч ;(наприклад, виразкова хвороба шлунка або дванадцятипалої кишки в стадії загострення, недавно [протягом останніх 6 місяців] перенесений ;геморагічний інсульт, проліферативна діабетична ;ретинопатія, погано контрольована ;артеріальна гіпертензія); Шлуночкова тахікардія, фібриляція шлуночків або політопна шлуночкова екстрасистолія в анамнезі (незалежно від наявності або відсутності адекватної антиаритмічної терапії); Подовжений інтервал QT на ЕКГ; Тяжка тахіаритмія в анамнезі; Нестабільна ;стенокардія ;або ;інфаркт міокарда ;протягом останніх б місяців; Інвазивне втручання на коронарних артеріях протягом останніх місяців; Одночасне застосування двох і більше антиагрегантних або антикоагулянтних лікарських засобів (наприклад, ацетилсаліцилової кислоти,; клопідогрелу,; гепарину,; Варфарину,; Одночасне застосування потужних інгібіторів CYP3A4 або CYP2C19 (наприклад, циметидину, ділтіазему, еритроміцину, кетоконазолу, лансопразолу, омепразолу та інгібіторів протеази ВІЛ-1); Вагітність; Період грудного вигодовування; Вік молодший 18 років (безпека та ефективність не вивчені). З обережністю Печінкова недостатність; легкого ступеня тяжкості; Хронічна ішемічна хвороба серця (зокрема, стабільна; стенокардія; напруги); Передсердна або шлуночкова екстрасистолія, фібриляція або тріпотіння передсердь; Цукровий діабет; Одночасне застосування лікарських засобів, що знижують артеріальний тиск; Одночасне застосування лікарських препаратів, що знижують згортання крові; Одночасне застосування субстратів CYP3A4 або CYP2C19 (наприклад, цизаприду, мідазоламу, ніфедипіну, верапамілу); Літній вік.Побічна діяНайбільш часто сполученими побічними ефектами в клінічних дослідженнях були ; головний біль ; (> 30%), ; діарея ; і порушення стільця (> 15% кожен). Ці побічні ефекти були легким і помірним ступенем інтенсивності. Порушення з боку крові та лімфатичної системи Часто: екхімоз. Нечасто анемія. Рідко: збільшення часу; кровотечі, тромбоцитоз. Частота невідома: схильність до; кровотеч, тромбоцитопенія, гранулоцитопія,; агранулоцитоз,; лейкопенія, панцитопенія,; апластична анемія. Порушення з боку імунної системи Нечасто: алергічні реакції. Порушення з боку обміну речовин та харчування Часто: набряки (периферичні набряки, набряк особи), анорексія. Нечасто: гіперглікемія, цукровий діабет. Порушення психіки Нечасто: ;занепокоєння. Порушення з боку нервової системи Дуже часто: головний біль Часто: запаморочення. Нечасто: безсоння, порушення сну (незвичайні сновидіння), внутрішньочерепний крововилив. Частота невідома: парез, гіпостезія. Порушення з боку органу зору Часто: внутрішньоочний крововилив. Частота невідома: ;кон'юнктивіт. Порушення з боку органу слуху та лабіринтні порушення Частота невідома: дзвін у вухах. Порушення з боку серця Часто: серцебиття, тахікардія, ;стенокардія, ;аритмія, шлуночкові ;екстрасистоли. Нечасто: інфаркт міокарда, фібриляція передсердь, хронічна серцева недостатність, надшлуночкова тахікардія, шлуночкова тахікардія, синкопальний стан. Порушення з боку судин Часто: ортостатична гіпотензія. Нечасто: припливи спека, артеріальна гіпертензія, артеріальна гіпотензія. Порушення з боку дихальної системи, органів грудної клітки та середостіння. Часто: риніт, фарингіт. Нечасто: задишка; (диспное), пневмонія, кашель, легенева кровотеча, кровотеча з дихальних шляхів. Частота невідома: інтерстиційна пневмонія. Порушення з боку шлунково-кишкового тракту Дуже часто: діарея, порушення стільця. Часто: нудота, блювання, диспепсія, метеоризм, біль у животі, шлунково-кишкові кровотечі. Нечасто: гастрит. Порушення з боку печінки та жовчовивідних шляхів Частота невідома: гепатит, відхилення показників функції печінки від нормальних значень, жовтяниця. Порушення з боку шкіри та підшкірних тканин Часто: шкірний висип, ;шкірний свербіж. Нечасто: ;екзема, шкірні висипання, синдром Стівенса-Джонсона, токсичний епідермальний некроліз, ;кропивниця, підшкірний крововилив. Порушення з боку скелетно-м'язової та сполучної тканини Нечасто: ; міалгія, внутрішньом'язові гематоми. Порушення з боку нирок та сечовивідних шляхів Рідко: ниркова недостатність, порушення ниркової функції. Частота невідома: гематурія, півлакурія. Загальні розлади та порушення разом Часто: біль у грудях, ; астенія. Нечасто: озноб, нездужання. Частота невідома: пірексія, біль. Лабораторні та інструментальні дані Частота невідома: підвищення вмісту сечової кислоти в крові, підвищення вмісту сечовини в крові, підвищення вмісту креатиніну в крові. Збільшення частоти виникнення серцебиття і периферичних набряків відмчали при застосуванні ;цілостазолу ;у поєднанні з іншими вазодилататорами, що викликають рефлекторну тахікардію (наприклад, з дигідропіридиновими блокаторами 'повільних' кальцієвих каналів). Цилостазол; сам по собі підвищує ризик; кровотечі, і цей ризик може бути додатково збільшений при одночасному застосуванні; цилостазолу; з будь-яким іншим лікарським препаратом, що володіє таким же; Ризик внутрішньоочного крововиливу може бути підвищений у пацієнтів із цукровим діабетом. Встановлено більш високу частоту виникнення діареї та прискореного серцебиття у пацієнтів старше 70 років. Передозування Симптоми Інформація про гостре передозування; цилостазолу; у людини обмежена. Очікувані симптоми передозування: виражений головний біль, діарея, тахікардія, артеріальна гіпотензія, порушення серцевого ритму. Лікування Симптоматичне. У разі передозування необхідне ретельне спостереження та обстеження пацієнта. Необхідно очистити шлунок, викликавши блювання, або виконати промивання шлунка відповідно до загальноприйнятих рекомендацій. Внаслідок високого ступеня зв'язку з білками плазми гемодіаліз та перитонеальний діаліз практично неефективні.Взаємодія з лікарськими засобамиАцетилсаліцилова кислота Короткострокове (протягом ≤ 4 днів) одночасне застосування ;цилостазолу ;і ацетилсаліцилової кислоти призводить до збільшення на 23-25% АДФ-індукованої агрегації тромбоцитів в умовах ex vivo порівняно з монотерапією ацетилсаліцилової кислоти. У зв'язку зі збільшенням ризику виникнення ;кровотеч ;при одночасному застосуванні з ;цілостазолом ;необхідне ретельне спостереження. Клопідогрел; та інші антиагрегантні лікарські засоби У дослідженні у здорових добровольців одночасне застосування; цілостазолу; з; клопідогрелом; При застосуванні ;клопідогрелу ;як у вигляді монотерапії так і в поєднанні з ;цілостазолом, у здорових добровольців збільшувався час ;кровотечі. Прийом ;цілостазолу ;не приводив до додаткового значного подовження часу ;кровотечі. Тим не менш, рекомендується дотримуватися обережності при одночасному застосуванні; цилостазолу; з будь-яким препаратом, що інгібує агрегацію тромбоцитів. Рекомендується регулярно контролювати час кровотечі. Застосування ;цілостазолу ;протипоказане пацієнтам, які отримують одночасно два або більше антиагрегантних та/або антикоагулянтних лікарських засобів. Пероральні антикоагулянти У клінічному дослідженні одноразовий прийом ;цилостазолу ;не інгібував метаболізм ;варфарину ;і не впливав на показники згортання крові (ПВ, АЧТВ, час ;кровотечі). Тим не менш, рекомендується дотримуватися обережності при одночасному застосуванні; цилостазолу; з будь-яким антикоагулянтним препаратом. Цилостазола протипоказано пацієнтам, які отримують одночасно два або більше антиагрегантних та/або антикоагулянтних лікарських засобів. Інгібітори коферментів цитохрому Р450 У печінці ;цилостазол ;в основному метаболізується під впливом ферментів цитохрому Р450, переважно CYP3A4 і CYP2C19 і, меншою мірою, CYP1A2. Вважається, що дегидроцилостазол, в 4-7 разів перевищує ;цилостазол ;по можливості інгібувати агрегацію тромбоцитів, утворюється переважно з участю CYP3A4. 4'-транс-гідроксицилостазол, що має у п'ять разів менш виражену здатність інгібувати агрегацію тромбоцитів, утворюється в основному під дією CYP2C19. Відповідно, препарати, що інгібують CYP3A4 (наприклад, деякі макроліди [еритроміцин, ;кларитроміцин], азольні протигрибкові препарати [кетоконазол, ;ітраконазол], інгібітори протеаз ВІЛ) і CYP2C19 (наприклад, інгібітори протон активність; цилостазолу;та можуть сприяти посиленню його небажаних ефектів. Відповідно, пацієнтам, які отримують потужні інгібітори CYP3A4 або CYP2C19, рекомендується призначати цілостазол у дозі 50 мг 2 рази на добу. Еритроміцин При одночасному прийомі; цилостазолу; з; На підставі змін показників AUC встановлено, що загальна фармакологічна активність ;цилостазолу ;при одночасному застосуванні з ;еритроміцином ;збільшується на 34%. Рекомендується зменшення дози ;цилостазолу ;до 50 мг 2 рази на добу при одночасному застосуванні з ;еритроміцином ;та іншими препаратами даної групи (наприклад, з ;кларитроміцином). При одночасному прийомі ;цилостазолу ;з ;кетоконазолом ;(потужний інгібітор CYP3A4) показник AUC ;цилостазолу ;збільшується на 117%, показник AUC дегідроцилостазолу зменшується на 15%, показник AUC 4'-транс-гидроксициста. На підставі змін показників AUC встановлено, що загальна фармакологічна активність ;цилостазолу ;при одночасному застосуванні з ;кетоконазолом ;збільшується на 34%. Рекомендується зменшення дози ;цилостазолу ;до 50 мг 2 рази на добу при одночасному застосуванні з ;кетоконазолом ;та іншими препаратами даної групи (наприклад, з ;ітраконазолом). Ділтіазем При одночасному прийомі ;цилостазолу ;з ;дилтіаземом ;(слабкий інгібітор CYP3A4) показники AUC ;цилостазолу, дегідроцилостазолу і 4'-транс-гідроксицилостазолу збільшуються відповідно на 44%, на 4% і на 43%. На підставі змін показників AUC встановлено, що загальна фармакологічна активність ;цилостазолу ;при одночасному застосуванні з ;ділтіаземом ;збільшується на 19%. Корекція дози ;цілостазолу ;при одночасному застосуванні з ;дилтіаземом ;не потрібно. Грейпфрутовий сік При одноразовому прийомі 100 мг ;цілостазолу ;одночасно з 240 мл грейпфрутового соку (інгібітор кишкового CYP3A4) суттєвої зміни фармакокінетичних показників ;цилостазолу ;не відзначалося. Корекція дози; цілостазолу; не потрібна. Тим не менш, прийом грейпрутового соку в більшій кількості може впливати на фармакокінетику; цилостазолу. Омепразол При одночасному прийомі ;цилостазолу ;з ;омепразолом ;(потужний інгібітор CYP2C19) показники AUC ;цилостазолу ;і дегідроцилостазолу збільшуються відповідно на 22% і на 68%, при цьому показник AUC 4'-транс-гідроксицилостазолу. На підставі змін показників AUC встановлено, що загальна фармакологічна активність ;цилостазолу ;при одночасному застосуванні з ;омепразолом ;збільшується на 47%. Рекомендується зменшення дози ;цилостазолу ;до 50 мг 2 рази на добу при одночасному застосуванні з ;омепразолом. Субстрати ізоферментів цитохрому Р450 Цилостазол ;збільшує показники AUC ;ловастатину ;(субстрат CYP3A4) та його бета-гідроксиліюго метаболіту на 70%. Рекомендується бути обережним при одночасному застосуванні ;цилостазолу ;з субстратами CYP3A4, що мають вузький терапевтичний діапазон (такими, як ;цизаприд, галофантрин, німозид, алкалоїди ріжків). Також рекомендується бути обережним при одночасному застосуванні ;цилостазолу ;з інгібіторами ГМГ-КоА-редуктази (статинами), метаболізуючими за участю CYP3A4 (симвастатин, ;аторвастатин ;і ;ловастатин). Індуктори іюферментів цитохрому Р450 Вплив препаратів, що збільшують активність CYP3A4 і CYP2C19 (таких, як ;карбамазепін, ;фенітоїн, ;рифампіцин, препарати Звіробою продірявленого), на фармакокінетику ;цилостазолу ;не вивчалося. При одночасному прийомі теоретично можливе зниження антиагрегантного ефекту; цилостазолу, тому необхідно регулярно контролювати час кровотечі. У клінічних дослідженнях встановлено, що куріння (фактор, що посилює активність CYP1A2) зменшує концентрацію цилостазолу в плазмі крові на 18%. Інші препарати Необхідно бути обережними при одночасному застосуванні ;цилостазолу ;з будь-якими препаратами, що знижують артеріальний тиск (в т.ч. з нітратами та інгібіторами фосфодіестерази-5), оскільки можливий адитивний ефект з розвитком артеріальної гіпотензії та рефлекторної тахікардії.Спосіб застосування та дозиПрепарат застосовують внутрішньо. Рекомендоване дозування; цилостазолу; становить 100 мг двічі на добу. Слід приймати ;цилостазол ;за 30 хвилин до їди. При прийомі ;цилостазолу ;під час їжі відзначається збільшення максимальної концентрації (Сmax) у плазмі крові, що може асоціюватися зі збільшенням частоти небажаних явищ. У разі пропуску прийому препарату необхідно прийняти наступну таблетку у звичайний час. Не слід приймати подвійну дозу цілостазолу. Терапію ;цілостазолом ;слід починати під наглядом лікаря, що має досвід лікування переміжної кульгавості. Лікар повинен повторно оцінити стан пацієнта через 3 місяці лікування, якщо терапія; цілостазолом; Пацієнти, які отримують лікування ;цилостазолом, повинні продовжувати виконувати рекомендації щодо зміни способу життя (відмова від куріння, фізичні вправи) та медикаментозну терапію (прийом гіполіпідемічних та антиагрегантних лікарських засобів), спрямовані на зменшення ризику серцево-судинних ускладнень. ;Цилостазол ;не є заміною зазначеного лікування. Застосування в спеціальних групах пацієнтів Літній вік Відсутні спеціальні вимоги до зміни дозування; цилостазолу; у літніх пацієнтів. Ниркова недостатність У пацієнтів з кліренсом креатиніну >25 мл/хв зміна дозування не потрібна. ;Цилостазол ;протипоказаний до застосування у пацієнтів з кліренсом креатиніну <25 мл/хв. Печінкова недостатність У пацієнтів з легкою печінковою недостатністю зміна дозування не потрібна. Відсутній досвід застосування ;цилостазолу ;у пацієнтів з помірною та тяжкою печінковою недостатністю. Оскільки ;цилостазол ;значною мірою метаболізується ферментами мікросомального окиснення печінки, застосування препарату протипоказане у пацієнтів з помірною та тяжкою печінковою недостатністю. Одночасний прийом потужних інгібіторів CYP3A4 або CYP2C19 У пацієнтів, які отримують препарати, які мають потужну інгібуючу дію на CYP3A4 (наприклад, деякі макроліди), або препарати, які мають потужну інгібуючу дію на CYP2C19 (наприклад, омепразол) слід зменшити дозу цилостазолу до 50 мг двічі на добу.Запобіжні заходи та особливі вказівкиПеред початком терапії; цілостазолом; слід оцінити можливість призначення інших способів лікування, таких як хірургічна реваскуляризація або консервативна терапія. За рахунок механізму фармакологічної дії; цилостазол; може викликати тахікардію, серцебиття, тахіаритмію та/або артеріальну гіпотензію. При прийомі ;цилостазолу ;частота серцевих скорочень може збільшуватися на 5-7 ударів на хвилину, що може спровокувати напад ;стенокардії ;у пацієнтів із групи ризику (наприклад, у пацієнтів зі стабільною ;стенокардією). Пацієнти, що мають підвищений ризик розвитку тяжких серцево-судинних ускладнень внаслідок збільшення частоти серцевого ритму (наприклад, пацієнти зі стабільною ІХС), потребують ретельного спостереження під час лікування цилостазолом. Застосування ;цілостазолу ;протипоказане у пацієнтів з нестабільною ;стенокардією ;або інфарктом міокарда/інвазивним втручанням на коронарних артеріях протягом останніх 6 місяців, а також у пацієнтів з тяжкою тахіаритмією в анамнезі. Необхідно бути обережними при призначенні ;цилостазолу ;пацієнтам з передсердною або шлуночковою екстрасистолією, а також пацієнтам з фібриляцією передсердь або тремтінням передсердь. Слід попередити пацієнта про необхідність повідомляти про будь-який випадок; кровотечі; або появи 'синяка' (підшкірної гематоми) при невеликому забитому місці. У разі розвитку крововиливу в сітківку ока прийом цилостазолу необхідно припинити. Оскільки ;цилостазол ;є інгібітором агрегації тромбоцитів, підвищується ризик ;кровотечі ;при хірургічних втручаннях (включаючи малі інвазивні процедури, такі як видалення зуба). При планованих хірургічних втручаннях (якщо антиагрегантна дія небажана); цилостазол; слід відмінити за 5 днів до операції. Повідомлялося про рідкісні або дуже рідкісні випадки гематологічних порушень, включаючи тромбоцитопенію, лейкопенію, агранулоцитоз, панцитопенію або аплатичну анемію. У більшості випадків ці порушення проходили після припинення прийому цілостазолу. Однак у кількох випадках панцитопенія і ;апластична анемія ;привели до летального результату. Пацієнта слід попередити про необхідність негайно повідомляти лікаря про будь-які симптоми, які можуть бути ранніми проявами гематологічних ускладнень, таких як висока лихоманка (пірексія) і ангіна. Слід виконати розгорнутий аналіз крові при підозрі на інфекцію або з появою клінічних симптомів гематологічних ускладнень. Необхідно негайно припинити прийом цилостазолу; у разі появи клінічних симптомів або лабораторних ознак гематологічних ускладнень. Слід бути обережним при одночасному застосуванні ;цилостазолу ;з лікарськими препаратами, що знижують артеріальний тиск (можливість адитивної дії з розвитком артеріальної гіпотензії та рефлекторної тахікардії) а також знижують згортання крові або інгібують агрегацію тромбоцитів. Вплив на здатність керувати транспортними засобами, механізмами Цилостазол; може викликати; запаморочення. Рекомендується бути обережним при керуванні транспортними засобами або роботі з механізмами в період лікування.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. чинна речовина пароксетину мезилат 25,83 мг, у перерахунку на пароксетин 20,00 мг; допоміжні речовини: кальцію безводний гідрофосфат 317,75 мг, карбоксиметилкрохмаль натрію 5,95 мг, магнію стеарат 7,00 мг; плівкова оболонка: лактози моногідрат 3,81 мг, гіпромелоза 2,97 мг, титану діоксид (Е171) 2,60 мг, макрогол 4000 1,06 мг, заліза оксид жовтий (Е172) 0,16 мг, заліза оксид червоний (Е17 0,002 мг. По 10 таблеток у блістер із ПВХ/ПЕ/ПВДХ/ алюмінієвої фольги. По 3 блістери разом з інструкцією із застосування в картонну пачку.Опис лікарської формиКруглі пігулки, покриті плівковою оболонкою, від жовтого до оранжевого кольору, з гравіюванням "РОТ 20" на одному боці та ризиком на обох сторонах.Фармакотерапевтична групаАнтидепресант.ФармакокінетикаПароксетин добре всмоктується після прийому внутрішньо та піддається метаболізму першого проходження через печінку. Оскільки метаболізм пароксетину включає стадію першого проходження через печінку, його кількість, що визначається в системній циркуляції менше, ніж абсорбується зі шлунково-кишкового тракту. При збільшенні дози пароксетину або при багаторазовому дозуванні, коли зростає навантаження на організм, відбувається часткове поглинання ефекту першого проходження через печінку та зниження плазмового кліренсу пароксетину. В результаті цього можливе підвищення концентрації пароксетину в плазмі та коливання фармакокінетичних параметрів, що може спостерігатися лише у тих. пацієнтів, які при прийомі низьких доз досягають низької концентрації препарату у плазмі. Пароксетин екстенсивно розподіляється у тканинах, і фармакокінетичні розрахунки показують, що лише 1% його присутній у плазмі, причому у терапевтичних концентраціях 95% пов'язано з білками плазми. Рівноважна концентрація досягається до 7-14 днів після початку лікування, і фармакокінетика під час тривалого лікування не змінюється. Клінічні ефекти пароксетину (побічна дія та ефективність) не корелюють з його концентрацією у плазмі. Основні метаболіти пароксетину являють собою полярні та кон'юговані, продукти окислення та метилювання, які швидко виводяться з організму, мають слабку фармакологічну активність і не впливають на його терапевтичну дію. При метаболізмі пароксетину не порушується обумовлене його дією селективне захоплення серотоніну. Виділення незміненого пароксетину з сечею зазвичай становить менше 2% дози, причому метаболіти становлять близько 64% від дози. Кишечник екскретує близько 36% дози, ймовірно з жовчю, а незмінений пароксетин становить менше 1% від дози. Таким чином, пароксетин виводиться переважно як метаболітів. Виведення з організму метаболітів пароксетину є біфазним, спочатку в результаті метаболізму першого проходження через печінку, а потім воно контролюється системною елімінацією. Період напіввиведення зазвичай становить близько 16-24 годин. Фармакокінетика в особливих клінічних випадках У пацієнтів з тяжкими порушеннями функції нирок (КК менше 30 мл/хв) та у пацієнтів з порушеннями функції печінки концентрація пароксетину у плазмі підвищена. У пацієнтів похилого віку при застосуванні пароксетину у дозі 20, 30,40 мг на добу, мінімальна концентрація у плазмі підвищувалася на 70-80%, що слід враховувати при доборі початкової дози.ФармакодинамікаПароксетин є потужним та селективним інгібітором захоплення 5-гідрокситриптаміну (5-НТ, серотоніну) нейронами головного мозку, що визначає його антидепресивну дію та ефективність при лікуванні обсесивно-компульсивного (ОКР) та панічного розладу. Пароксетин має низький афінітет до мускаринових холінергічних рецепторів, має лише слабкі антихолінергічні властивості. Маючи селективну дію, на відміну від трициклічних антидепресантів, пароксетин показав низький афінітет до α-1, α-2, β-адренорецепторів, а також до дофамінових (Д2), 5-HT1-, 5-НТ2-серотонінових та Hi-гістамінових рецепторів . Пароксетин не пригнічує ЦНС, не порушує психомоторні функції і не потенціює пригнічуючу дію на них етанолу. Як і інші селективні інгібітори зворотного захоплення серотоніну, пароксетин спричиняє симптоми надмірної стимуляції 5-НТ-рецепторів при введенні тваринам, які раніше отримували інгібітори моноаміноксидази (МАО) або триптофан. За даними дослідження поведінки та змін ЕЕГ, у пароксетину виявляються слабкі активуючі властивості при застосуванні доз, що перевищують ті, що потрібні для інгібування зворотного захоплення серотоніну. За своєю природою його активуючі властивості не є "амфетаміноподібними". У здорових добровольців він не викликає значної зміни артеріального тиску, частоти серцевих скорочень та ЕКГ. На відміну від антидепресантів, які пригнічують захоплення норадреналіну, пароксетин набагато слабше пригнічує антигіпертензивні ефекти гуанетидину.Показання до застосуванняДепресивний розлад; обсесивно-компульсивний розлад (ДКР); панічне розлад, у тому числі з агорафобією; соціальний тривожний розлад/соціальна фобія; генералізоване тривожне розлад; посттравматичний стресовий розлад.Протипоказання до застосуванняГіперчутливість до пароксетину та інших компонентів препарату; одночасне застосування з необоротними інгібіторами МАО (ІМАО) та протягом 14 днів після їх відміни, оборотними інгібіторами МАО та протягом 24 годин після їх відміни, тіоридазином, пімозидом; вагітність; період грудного вигодовування; дитячий вік до 18 років (ефективність та безпека не встановлена); непереносимість лактози; дефіцит лактази; глюкозо-галактозна мальабсорбція. З обережністю: Печінкова недостатність; ниркова недостатність; закритокутова глаукома; гіперплазія передміхурової залози; манія; патологія серця; епілепсія; при нестабільній епілепсії слід уникати прийому препарату; судомні стани; застосування електроімпульсної терапії; прийом препаратів та наявність захворювань, що підвищують ризик кровотечі; наявність факторів ризику підвищеної кровоточивості; літній вік.Вагітність та лактаціяФертильність. Пароксетин, як і інші селективні інгібітори зворотного захоплення серотоніну. можуть впливати на якість насіннєвої рідини. Цей ефект оборотний після відміни препарату. Вагітність. Не виявлено тератогенної чи виборчої ембріотоксичної активності. При прийомі препарату у першому триместрі вагітності збільшується ризик уроджених аномалій, зокрема серцево-судинної системи. При застосуванні на пізніх термінах вагітності збільшується ризик розвитку легеневої персистуючої гіпертензії новонароджених. Пароксетин протипоказаний до застосування при вагітності та в період грудного вигодовування.Побічна діяЧастота розвитку побічних ефектів класифікована згідно з рекомендаціями Всесвітньої організації охорони здоров'я: дуже часто – не менше 10%; часто – не менше 1%, але менше 10%; нечасто – не менше 0,1%, але менше 1%; рідко – не менше 0,01%, але менше 0,1%; дуже рідко (включаючи поодинокі випадки) – менше 0,01%. З боку крові та лімфатичної системи: нечасто – аномальна кровотеча, переважно, крововилив у шкіру та слизові оболонки (найчастіше синці); дуже рідко-тромбоцитопенія. З боку нервової системи: часто – сонливість, тремор, парестезії, безсоння, запаморочення, ненормальні сновидіння (у тому числі кошмари); нечасто – сплутаність свідомості, галюцинації, екстрапірамідні симптоми; рідко – манії, тривога, деперсоналізація, панічні атаки, синдром неспокійних ніг, судоми, акатизія; дуже рідко – серотоніновий синдром (ажитація, сплутаність свідомості, діафорез, галюцинації, гіперрефлексія, міоклонус, тахікардія, тремор, підвищене потовиділення, озноб); частота невідома - суїцидальні думки, суїцидальна поведінка (під час терапії пароксетином або ранні терміни після припинення лікування). У пацієнтів з руховими порушеннями або які приймають нейролептики – екстрапірамідні розлади з оромандибулярною дистонією. Деякі симптоми (сонливість, безсоння, ажитація, сплутаність свідомості, галюцинації, манії) можуть бути зумовлені основним захворюванням. З боку органу зору: часто – нечіткість зору; нечасто – мідріаз; дуже рідко - закрггвугільна глаукома. З боку органу слуху: частота невідома – шум у вухах. З боку серцево-судинної системи: нечасто – транзиторне підвищення або зниження АТ (зазвичай у пацієнтів з артеріальною гіпертензією та тривогою), синусова тахікардія, ортостатична гіпотензія; дуже рідко – периферичні набряки. З боку травної системи: дуже часто – нудота, зниження апетиту; часто – сухість у роті, блювання, запор, діарея; рідко – підвищення активності "печінкових" трансаміназ; дуже рідко – шлунково-кишкова кровотеча, гепатит (іноді, з жовтяницею), печінкова недостатність (при розвитку побічних ефектів з боку печінки питання доцільності припинення терапії слід вирішувати у випадках, коли відзначається тривале підвищення показників функціональних проб). З боку сечовивідної системи: рідко – затримка сечовипускання, нетримання сечі. З боку сечостатевої системи: дуже часто – сексуальна дисфункція; рідко – пріапізм. З боку ендокринної системи: рідко – гіпопролактинемія/галакторея та гіпонатріємія (в основному у літніх пацієнтів), яка іноді обумовлена синдромом недостатньої секреції антидіуретичного гормону. З боку опорно-рухового апарату: рідко – артралгія, міалгія. Алергічні реакції: дуже рідко – ангіоневротичний набряк, кропив'янка; рідко - шкірний висип; реакції фоточутливості Інші: дуже часто – астенія, холестеринемія, зниження апетиту, посилення потовиділення, позіхання, збільшення маси тіла; дуже рідко – периферичні набряки. Синдром "скасування" пароксетину; часто - запаморочення, сенсорні порушення, порушення сну, тривога, біль голови; нечасто – ажитація, нудота, тремор, сплутаність свідомості, пітливість, діарея.Взаємодія з лікарськими засобамиЗастосування пароксетину з ІМАО, у тому числі з лінезолідом – антибіотиком, що трансформується у неселективний оборотний ІМАО, протипоказане у зв'язку з високим ризиком розвитку серотонінового синдрому. Необхідний ретельний клінічний контроль стану пацієнтів при одночасному застосуванні пароксетину з серотонінергічними препаратами, у тому числі з L-триптофаном, триптанами, трамадолом, іншими препаратами групи селективних інгібіторів зворотного захоплення серотоніну (СІОЗС), літієм та рослинними препаратами, що містять. . може розвинутись серотоніновий синдром. Потрібен контроль стану пацієнта при одночасному застосуванні пароксетину з фентанілом, що застосовується для загального наркозу або для лікування хронічного болю. При одночасному застосуванні пароксетину з пімозидом у низькій дозі (2 мг одноразово) було зареєстровано підвищення концентрації пімозиду, що пояснюється властивістю пароксетину інгібувати ізофермент CYP2D6. Внаслідок вузького терапевтичного індексу пімозиду та його відомої здатності подовжувати інтервал QT, спільне застосування пімозиду та пароксетину протипоказано. Метаболізм та фармакокінетика пароксетину можуть змінюватися під впливом індукції або інгібування мікросомальних ферментів печінки, що беруть участь у його метаболізмі. При застосуванні пароксетину одночасно з інгібіторами ферментів, що беруть участь у метаболізмі лікарських препаратів, слід оцінити доцільність застосування дози пароксетину, що знаходиться у нижній частині діапазону терапевтичних доз. Початкову дозу пароксетину не потрібно коригувати, якщо його застосовують одночасно з препаратом, який є відомим індуктором ферментів, що беруть участь у метаболізмі лікарських препаратів (наприклад, карбамазепін, рифампіцин, фенобарбітал, фенітоїн). Будь-яке подальше коригування дози пароксетину має визначатися його клінічними ефектами (переносимість та ефективність). Одночасне застосування фосампренавіру/ритонавіру з пароксетином призводило до значного зниження концентрації пароксетину в плазмі. Будь-яка подальша корекція дози пароксетину повинна визначатися його клінічними ефектами (переносимість та ефективність). Щоденний прийом пароксетину значно підвищує концентрації в плазмі проциклідину. При виникненні антихолінергічних ефектів дозу проциклідину слід зменшити. Одночасне застосування пароксетину з протисудомними препаратами, у тому числі з карбамазепіном, фенітоїном, вальпроатом натрію, не впливає на їхню фармакокінетику та фармакодинаміку у пацієнтів з епілепсією. Клінічні дослідження показали, що абсорбція та фармакокінетика пароксетину не залежать або практично не залежать (тобто існуюча залежність не потребує зміни дози) від їди, антацидів, дигоксину, пропранололу, алкоголю. Як і інші антидепресанти, включаючи інші препарати групи СІОЗС, пароксетин пригнічує ізофермент CYP2D6, що відноситься до системи цитохрому Р450. Інгібування ізоферменту CYP2D6 може призводити до підвищення концентрацій у плазмі одночасно застосовуваних препаратів, які метаболізуються цим ізоферментом. До таких препаратів відносяться трициклічні антидепресанти (у тому числі амітриптилін, нортриптилін, іміпрамін та дезіпрамін), нейролептики фенотіазинового ряду (у тому числі перфеназин та тіоридазин), рисперидон, атомоксетин, деякі антиаритмічні препарати типу Iс (у тому числі пропафенон) . Одночасне застосування пароксетину з тамоксифеном може призвести до зниження концентрації активного метаболіту тамоксифену ,в плазмі крові" за рахунок пригнічення ізоферменту CYP2D6, і як наслідок, зменшити ефективність тамоксифену. Дослідження взаємодії in vivo при одночасному застосуванні, в умовах рівноважного стану, пароксетину і тер є субстратом ферменту CYP3А4, що показало, що пароксетин не впливає на фармакокінетику терфенадину, небажаних реакцій. Рекомендується бути обережним у пацієнтів, які приймають СІОЗС одночасно з антикоагулянтними препаратами (у тому числі варфарином), лікарськими препаратами, про які відомо, що вони можуть вплинути на функціональний стан тромбоцитів та підвищити ризик розвитку кровотечі (у тому числі з клозапіном), фенотіазинами, трицикліками. антидепресантами, нестероїдними протизапальними препаратами (у тому числі ацетилсаліцилової кислоти, іншими інгібіторами циклооксигенази-2).Спосіб застосування та дозиВнутрішньо, 1 раз на добу, вранці, під час їжі. Таблетку ковтають повністю, запиваючи водою. Доза підбирається індивідуально протягом перших двох-трьох тижнів після початку терапії та згодом за необхідності коригується. Депресивний розлад – 20 мг 1 раз на добу. У разі необхідності дозу поступово збільшують на 10 мг/добу, максимально до 50 мг/добу залежно від реакції пацієнта, максимальна добова доза не повинна перевищувати 50 мг. Через 2 -3 тижні після початку лікування слід оцінити ефективність та необхідність корекції дози пароксетину. Для усунення депресивних синдромів і запобігання рецидивам необхідно дотримуватися адекватної тривалості купуючої та підтримуючої терапії, яка може тривати кілька місяців і більше. При обсесивно-компульсивних розладах початкова терапевтична доза – 20 мг на добу з наступним щотижневим збільшенням на 10 мг. Середня терапевтична доза, що рекомендується, - 40 мг на добу, при необхідності доза може бути збільшена до 60 мг на добу. Тривалість підтримуючої терапії – від 6 місяців і більше. При панічних розладах початкова доза – 10 мг на добу (для зниження можливого ризику загострення панічної симптоматики), з наступним щотижневим збільшенням на 10 мг. Середня терапевтична доза – 40 мг на добу. Максимальна доза – 50 мг на добу. Низька початкова доза рекомендується для мінімізації можливого посилення симптоматики панічного розладу, що може виникати на початку лікування будь-якими антидепресантами. Рекомендується дотримуватися адекватних термінів терапії (від 3 місяців і більше). Соціально-тривожні розлади/соціофобія: початкова доза становить 20 мг на добу; при відсутності ефекту протягом як мінімум двох тижнів можливе збільшення дози максимально до 50 мг на добу. Дозу слід збільшувати на 10 мг з інтервалами не менше тижня відповідно до клінічного ефекту. Тривалість підтримуючої терапії від 3 місяців та більше. Генералізовані тривожні розлади: початкова та рекомендована дози – 20 мг на добу. За відсутності ефекту протягом щонайменше 2 тижнів можливе збільшення дози максимально до 50 мг на добу. Дозу слід збільшувати на 10 мг на добу з інтервалами не менше тижня відповідно до клінічного ефекту. Тривалість підтримуючої терапії від 2 місяців та більше. Посттравматичний стресовий розлад: для більшості пацієнтів початкова та терапевтична дози становлять 20 мг на добу. У деяких випадках рекомендується збільшення дози пароксетину до 50 мг на добу. Дозу слід збільшувати на 10 мг щотижня відповідно до клінічного ефекту. Тривалість під тримає терапії від 3 місяців і більше. При нирковій та/або печінковій недостатності рекомендована доза становить 20 мг на добу. Для пацієнтів похилого віку початкова доза - 10 мг, добова доза не повинна перевищувати 40 мг. Відміна препарату Плізіл. З метою попередження розвитку синдрому "скасування" припинення прийому препарату Плізил проводиться поступово і може бути рекомендована наступна схема відміни: зниження добової дози на 10 мг на тиждень; після досягнення дози 20 мг на добу пацієнти продовжують приймати цю дозу протягом 1 тижня і лише після цього препарат скасовують повністю. Якщо симптоми, відміни розвиваються під час, зниження дози або після відміни препарату, доцільно відновити прийом раніше призначеної дози. Надалі лікар може продовжити зниження дози, але повільніше. Застосування пароксетину в дітей віком протипоказано, т.к. безпека та ефективність пароксетину для даної вікової групи не встановлені.ПередозуванняСимптоми: нудота, блювання, тремор, сухість у роті, мідріаз, нечіткість зору, ністагм, лихоманка, зміни артеріального тиску, головний біль, мимовільні м'язові скорочення, ажитація, тривожність, синусова тахікардія, пітливість, сонливість. У дуже рідкісних випадках при одночасному прийомі з іншими психотропними засобами та/або алкоголем відзначалися зміни на електрокардіограмі, кома, а також смерть. Лікування: промивання шлунка, активоване вугілля. При необхідності – симптоматична терапія. Специфічного антидоту немає.Запобіжні заходи та особливі вказівкиПід час лікування препаратом Плізил необхідно приділяти особливу увагу пацієнтам, які мають в анамнезі суїцидальну поведінку або суїцидальні думки, пацієнтам віком до 25 років, а також пацієнтам, які мають суїцидальні думки до початку лікування. Пацієнтів та обслуговуючий персонал слід попередити про необхідність стежити за погіршенням їх стану та/або появою суїцидальних думок/суїцидальної поведінки або думок про заподіяння собі шкоди під час всього курсу лікування, особливо на початку лікування та під час зміни дози препарату Плізил (збільшення та зниження) . У разі виникнення цих симптомів необхідно негайно звернутися за медичною допомогою. Необхідно пам'ятати, що такі симптоми як ажитація, акатизія або манія можуть бути пов'язані з основним захворюванням або бути наслідком терапії, що застосовується. Ймовірність виникнення акатизії найвища у перші кілька тижнів лікування. При виникненні симптомів клінічного погіршення (включаючи нові симптоми) та/або суїцидальних думок/поведінки, особливо при раптовій їх появі, наростанні тяжкості проявів, або в тому випадку, якщо вони не були частиною попереднього симптомокомплексу у даного пацієнта, необхідно переглянути режим терапії відміни препарату Плізил. У поодиноких випадках на фоні лікування пароксетином може виникнути серотоніновий синдром або симптоматика, подібна до злоякісного нейролептичного синдрому, особливо якщо пароксетин застосовують одночасно з іншими серотонінергічними препаратами та/або нейролептиками. Ці синдроми представляють потенційну загрозу життю і тому лікування пароксетином необхідно припинити у разі їх виникнення (вони характеризуються такими симптомами: гіпертермія, м'язова ригідність, міоклонус, вегетативні розлади з можливими швидкими змінами показників життєво важливих функцій, зміни психічного статусу, вкрай виражену ажитацію, що прогресує до делірію і коми) і почати підтримуючу симптоматичну терапію.Пароксетин не слід застосовувати одночасно з попередниками серотоніну (як-от L-триптофан, окситриптан) у зв'язку з ризиком розвитку серотонінергічного синдрому. Великий депресивний епізод може бути початковим проявом біполярного розладу. Лікування такого епізоду одним тільки антидепресантом може збільшити ймовірність прискореного розвитку змішаного/маніакального епізоду у пацієнтів, які схильні до ризику виникнення біполярного розладу. Перед початком лікування антидепресантом необхідно провести ретельний скринінг для оцінки ризику виникнення у даного пацієнта біполярного розладу; такий скринінг повинен включати збір детального психіатричного анамнезу, включаючи дані про наявність у сім'ї випадків суїциду, біполярного розладу та депресії. Препарат Плізил слід застосовувати з обережністю у пацієнтів, які мають в анамнезі манію. Лікування препаратом Плізил слід починати обережно, не раніше як через 2 тижні після припинення терапії інгібіторами МАО; дозу препарату Плізил слід підвищувати поступово до досягнення оптимального терапевтичного ефекту. Рекомендується бути обережним при лікуванні препаратом Плізил пацієнтів з порушенням функції нирок і пацієнтів з порушеннями функції печінки. Як і інші антидепресанти, препарат Плізил слід застосовувати з обережністю у пацієнтів з епілепсією. Частота судомних нападів у пацієнтів, які приймають пароксетин, не перевищує 0,1%. У разі виникнення судомного нападу лікування препаратом Плізил слід припинити. Є обмежений досвід одночасного застосування пароксетину та електросудомної терапії. Препарат Плізил (як інші селективні інгібітори зворотного захоплення серотоніну) може викликати мідріаз. Препарат Плізил необхідно застосовувати з обережністю у пацієнтів із закритокутовою глаукомою. При лікуванні препаратом Плізил гіпонатріємія виникає рідко і переважно у пацієнтів похилого віку і нівелюється після його відміни. Повідомлялося про крововиливи у шкіру та слизові оболонки (включаючи шлунково-кишкові кровотечі) у пацієнтів, які приймають пароксетин, тому препарат Плізил слід застосовувати з обережністю у пацієнтів, які одночасно отримують препарати, що підвищують ризик кровотеч, у пацієнтів із відомою схильністю до кровотеч та у пацієнтів. із захворюваннями, що привертають до кровотеч. При лікуванні пацієнтів із захворюваннями серця слід дотримуватися запобіжних заходів, контролюючи функціональний стан серцево-судинної системи. Як і при відміні багатьох психотропних лікарських препаратів, припинення лікування пароксетином (особливо різке) може викликати такі симптоми, як запаморочення, сенсорні порушення (включаючи парестезію та відчуття розряду електричного струму), порушення сну (включаючи яскраві сни), ажитація або тривога, нудота , головний біль, тремор, сплутаність, свідомість, діарея та пітливість. У більшості пацієнтів ці симптоми є легкими або помірно вираженими і проходять мимовільно. Зазвичай симптоми відміни виникають у перші кілька днів після відміни препарату, однак у поодиноких випадках відмічені після випадкового пропускання однієї дози. Як правило, ці симптоми проходять самостійно протягом двох тижнів, але деякі пацієнти зберігаються до 2-3 міс. и більше.Рекомендується поступово знижувати дозу пароксетину (протягом кількох тижнів або місяців перед його повним скасуванням залежно від стану пацієнта). Виникнення симптомів відміни означає, що препарат Плизил викликає залежність. Виявлено зв'язок переломів кісток з прийомом антидепресантів, включаючи СІЗЗС. Можливість переломів кісток слід враховувати під час застосування препарату Плізил. При лікуванні або профілактиці раку грудей препаратом тамоксифен слід враховувати, що ефективність тамоксифену зменшується при одночасному застосуванні з пароксетином, більшою мірою ризик зростає при одночасному застосуванні протягом тривалого часу. Вплив на здатність до керування автотранспортом та управління механізмами Терапія препаратом Ппізил не викликає когнітивних порушень та психомоторної загальмованості. Проте, як і при лікуванні будь-якими психотропними препаратами, при застосуванні препарату Плізил пацієнтам слід бути обережними при виконанні дій, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаТаблетки – 1 таб. Активна речовина: пароксетину мезилат 25.83 мг, що відповідає вмісту пароксетину 20 мг; Допоміжні речовини: кальцію безводний гідрофосфат, карбоксиметилкрохмаль натрію, магнію стеарат; оболонка: лактози моногідрат, гіпромелоза, титану діоксид (Е171), макрогол 4000, заліза оксид жовтий (Е172), заліза оксид червоний (Е172). 10 шт. - блістери (3) - пачки картонні.Опис лікарської формиПігулки, покриті плівковою оболонкою від жовтого до оранжевого кольору, круглі, з гравіюванням "РОТ 20" на одному боці та ризиком на обох сторонах.Фармакотерапевтична групаАнтидепресант, селективний інгібітор зворотного захоплення серотоніну. Має біциклічну структуру, відмінну від структури інших відомих антидепресантів. Чинить антидепресивну та анксіолітичну дію при досить вираженому стимулюючому (активізуючому) ефекті. Антидепресивна (тимоаналептична) дія пов'язана зі здатністю пароксетину вибірково блокувати зворотне захоплення серотоніну пресинаптичною мембраною, чим зумовлено підвищення вільного вмісту цього нейромедіатора в синаптичній щілині та посилення його активності в ЦНС. Вплив на м-холінорецептори, α- та β-адренорецептори незначний, що визначає вкрай слабку вираженість відповідних побічних ефектів.ФармакокінетикаПісля прийому внутрішньо пароксетин добре абсорбується із ШКТ. Їда не впливає на абсорбцію. Css встановлюється до 7-14 дня з початку терапії. Основними метаболітами пароксетину є полярні та кон'юговані продукти окиснення та метилювання. З огляду на низьку фармакологічну активність метаболітів їх вплив на терапевтичну ефективність малоймовірний. T1/2 у середньому становить 16-24 год. Менш, ніж 2% виводиться із сечею у незміненому вигляді, решта - як метаболітів або з сечею (64%), або жовчю. Виведення пароксетину має двофазний характер. При тривалому безперервному прийомі фармакокінетичні параметри не змінюються.ІнструкціяПриймати внутрішньо.Показання до застосуванняЕндогенні, невротичні та реактивні депресії.Протипоказання до застосуванняОдночасний прийом інгібіторів МАО та період до 14 днів після їх відміни, підвищена чутливість до пароксетину.Побічна діяЗ боку ЦНС: рідко (при застосуванні в дозах понад 20 мг на добу) – сонливість, тремор, астенія, безсоння. З боку травної системи: рідко (при застосуванні в дозах понад 20 мг на добу) – нудота, сухість у роті; в окремих випадках – запори. Інші: рідко (при застосуванні в дозах понад 20 мг на добу) – посилення потовиділення, порушення еякуляції.Взаємодія з лікарськими засобамиПри одночасному застосуванні з пароксетином можливе підвищення концентрацій у плазмі крові засобів, що метаболізуються за участю ізоферменту CYP2D6 системи цитохрому Р450 (антидепресантів, антипсихотичних засобів похідних фенотіазину, антиаритмічних препаратів ІС класу). При одночасному застосуванні засобів, що індукують або інгібують білковий метаболізм, можливі зміни метаболізму та фармакокінетичних параметрів пароксетину. При одночасному застосуванні посилюється дія алпразоламу внаслідок зменшення його метаболізму через інгібування ізоферментів CYP3A системи цитохрому P450 під впливом пароксетину. При одночасному застосуванні з варфарином пероральними антикоагулянтами можливе збільшення часу кровотечі при незміненому протромбіновому часі. При одночасному застосуванні з декстрометорфаном, дигідроерготаміном описані випадки серотонінового синдрому. При одночасному застосуванні з інтерфероном можлива зміна антидепресивної дії пароксетину. Одночасне застосування триптофану може спричинити розвиток серотонінового синдрому, що виявляється ажитацією, занепокоєнням, розладами з боку шлунково-кишкового тракту, включаючи діарею. При одночасному застосуванні з перфеназином посилює побічні ефекти з боку ЦНС через інгібування метаболізму перфеназину під впливом пароксетину. При одночасному застосуванні підвищується концентрація в плазмі трициклічних антидепресантів, виникає ризик розвитку серотонінового синдрому. Одночасний прийом циметидину підвищує концентрацію пароксетину у плазмі крові.Спосіб застосування та дозиПочаткова доза становить 10-20 мг на добу. При необхідності, залежно від показань, дозу збільшують до 40-60 мг на добу. Збільшення дози проводять поступово – на 10 мг з інтервалом на 1 тиждень. Частота прийому – 1 раз на добу. Лікування тривале. Ефективність терапії оцінюється через 6-8 тижнів. Для літніх та ослаблених хворих, а також при порушеннях функції нирок та печінки початкова доза – 10 мг на добу; максимальна доза – 40 мг на добу.Запобіжні заходи та особливі вказівкиПрипинення застосування пароксетину слід проводити, поступово зменшуючи дозу, щоб уникнути синдрому відміни, який проявляється запамороченням, нудотою, блюванням, безсонням, сплутаністю свідомості, підвищеним потовиділенням. У період лікування пароксетином протипоказано вживання алкоголю. З обережністю застосовувати через 14 днів після відміни інгібіторів МАО, поступово збільшуючи дозу. Інгібітори МАО не слід призначати протягом 2 тижнів після повного скасування пароксетину. Вплив на здатність до керування автотранспортом та управління механізмами. З обережністю застосовувати у пацієнтів, діяльність яких пов'язана з необхідністю високої концентрації уваги та швидкості психомоторних реакцій.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Активна речовина: клопідогрелу гідросульфатеквівалентно клопідогрелу 75 мг; допоміжні речовини: повідон K 30, кроскармелоза натрію, лактози моногідрат, целюлоза мікрокристалічна, олія касторова гідрогенізована; оболонка плівкова: опадрай білий (титану діоксид, гіпромелоза, тальк, макрогол), титану діоксид. У упаковці 28 штук.Опис лікарської формиКруглі двоопуклі таблетки, покриті плівковою оболонкою, білого або майже білого з жовтуватим відтінком кольору, з ризиком, без запаху або майже без запаху; на поперечному розрізі видно ядро білого чи майже білого кольору.ФармакокінетикаПісля одноразового прийому та при курсовому прийомі внутрішньо у дозі 75 мг на добу клопідогрел швидко всмоктується. Абсорбція та біодоступність – висока. Однак концентрація вихідної речовини в плазмі низька і через 2 години після прийому не досягає межі виміру (0,025 мкг/л). Зв'язок із білками плазми – 98-94%. Є проліками. Клопідогрел швидко метаболізується у печінці. Активний метаболіт у крові не виявляється. Основний метаболіт, що визначається, - неактивне похідне карбоксилової кислоти, час досягнення максимальної концентрації (TCmax) якого після повторних пероральних доз 75 мг досягається через 1 год, максимальна концентрація (Cmax) - близько 3 мг/л. Близько 50% препарату виводиться нирками та приблизно 46% кишечником протягом 120 годин після введення. Період напіввиведення (T1/2) основного метаболіту після одноразового та повторного прийому становить 8 годин. Концентрації виділених нирками метаболітів – 50%. Концентрація основного метаболіту в плазмі після прийому 75 мг на добу нижче у пацієнтів з тяжкою хронічною нирковою недостатністю (кліренс креатиніну (КК) 5-15 мл/хв) порівняно з хворими з хронічною нирковою недостатністю середньої тяжкості (КК від 30 до 60 мл/ хв) та здоровими особами.ФармакодинамікаКлопідогрел – антиагрегантний засіб. Вибірково зменшує зв'язування аденозиндифосфату (АДФ) з рецепторами на тромбоцитах та активацію рецепторів глікопротеїну IIb/IIIa під дією АДФ, послаблюючи агрегацію тромбоцитів. Зменшує агрегацію тромбоцитів, спричинену іншими агоністами, запобігаючи їх активації звільненим АДФ, не впливає на активність фосфодіестерази (ФДЕ). Необоротно зв'язується з АДФ-рецепторами тромбоцитів, які залишаються несприйнятливими до стимуляції АДФ протягом життєвого циклу (близько 7 днів). Гальмування агрегації тромбоцитів спостерігається через 2 години після прийому (40% інгібування) початкової дози 400 мг. Максимальний ефект (60% пригнічення агрегації) розвивається через 4-7 днів постійного прийому в дозі 50-100 мг на добу. Антиагрегантний ефект зберігається на весь період життя тромбоцитів (7-10 днів).Показання до застосуванняПрофілактика тромботичних ускладнень у пацієнтів з інфарктом міокарда, ішемічним інсультом або оклюзією периферичних артерій. У комбінації з ацетилсаліциловою кислотою (АСК) для профілактики тромботичних ускладнень при гострому коронарному синдромі: з підйомом сегмента ST за можливості проведення тромболітичної терапії; без підйому сегмента ST (нестабільна стенокардія чи інфаркт міокарда без зубця Q), зокрема. у хворих, що піддаються стентуванню.Протипоказання до застосуванняПідвищена чутливість до активного або будь-якого допоміжного компонента препарату. Непереносимість лактози, дефіцит лактази та синдром глюкозо-галактозної мальабсорбції. Тяжка печінкова недостатність. Гостра кровотеча (в т.ч. виразка або внутрішньочерепний крововилив).Вагітність та лактаціяПротипоказано дітям до 18 років, при вагітності та лактації.Побічна діяКровотеча – найчастіша реакція, яка зустрічається протягом першого місяця прийому препарату. Випадки сильної кровотечі зареєстровані у пацієнтів, які приймають клопідогрел одночасно з АСК або клопідогрел з АСК та гепарином. Частота побічних ефектів визначена згідно з такими визначеннями: дуже часто - більше 1/10, часто - більше 1/100 і менше 1/10, нечасто - більше 1/1000 і менше 1/100, рідко - більше 1/10000 і менше 1/ 1000, дуже рідко - менше 1/10000, включаючи поодинокі випадки. У межах кожного класу частот небажані ефекти представлені порядку зменшення ступеня тяжкості. З боку органів кровотворення: нечасто – тромбоцитопенія, лейкопенія, еозинофілія; рідко – нейтропепія, в т.ч. виражена; дуже рідко – тромботична тромбоцитопенічна пурпура, анемія у т.ч. апластична, панцитопенія, агранулоцитоз, тяжка тромбоцитопенія, гранулоцитопенія. З боку нервової системи: нечасто – головний біль, запаморочення, парестезії, внутрішньочерепна кровотеча, у т.ч. з летальним кінцем; дуже рідко – сплутаність свідомості, галюцинації, порушення смаку. З боку органів чуття: нечасто – крововилив у кон'юнктиву, очі, сітківку; рідко – вертиго. З боку серцево-судинної системи: часто – гематома; дуже рідко – тяжкі кровотечі, кровотеча з операційної рани, васкуліт, зниження артеріального тиску. З боку дихальної системи: дуже часто – носова кровотеча; дуже рідко – бронхоспазм, інтерстиціальний пневмоніт, легенева кровотеча, кровохаркання. З боку травної системи: часто – діарея, біль у животі, диспепсія, кровотеча із ШКТ; нечасто – виразка шлунка та 12-палої кишки, гастрит, блювання, нудота, запор, метеоризм; рідко – заочеревинна кровотеча; дуже рідко – панкреатит, коліт, у т.ч. виразковий або лімфоцитарний, стоматит, гостра печінкова недостатність, гепатит, порушення функціональних проб печінки, кровотеча із ШКТ із летальним результатом. З боку шкірних покровів: часто – підшкірні крововиливи; нечасто - шкірний висип, свербіж, пурпура; дуже рідко – ангіоневротичний набряк, кропив'янка, еритематозний висип, багатоформна еритема, синдром Стівенса-Джонсона, токсичний епідермальний некроліз, екзема, червоний плоский лишай. З боку опорно-рухового апарату: дуже рідко – гемартроз, артрит, артралгія, міалгія. З боку сечостатевої системи: нечасто – гематурія; дуже рідко – гломерулонефрит, гіперкреатинінемія. Алергічні реакції: дуже рідко – анафілактичні реакції, сироваткова хвороба. Лабораторні показники: нечасто – подовження часу кровотечі, порушення функціональних проб печінки, підвищення концентрації креатиніну крові. Інше – дуже рідко: підвищення температури тіла.Взаємодія з лікарськими засобамиОдночасний прийом варфарину з клопідогрелом може збільшити інтенсивність кровотеч, тому застосування цієї комбінації не рекомендується. Призначення інгібіторів глікопротеїну IIb/IIIa, АСК, гепарину разом із клопідогрелом підвищує ризик розвитку кровотеч. При одночасному застосуванні з нестероїдними протизапальними засобами може підвищуватися ризик кровотеч. Одночасне застосування з інгібіторами CYP2C19 (наприклад, омепразол) не рекомендується. Активний метаболіт клопідоргела пригнічує активність ізоферменту CYP2C9, внаслідок чого можуть підвищуватися концентрації фенітоїну, толбутаміду та нестероїдних протизапальних засобів у плазмі.Спосіб застосування та дозиДля профілактики тромботичних ускладнень у пацієнтів з інфарктом міокарда, ішемічним інсультом або оклюзією периферичних артерій – по 75 мг 1 раз на добу. У хворих з інфарктом міокарда лікування можна починати з перших днів по 35-й день інфаркту міокарда, а у хворих з ішемічним інсультом – у термін від 7 днів до 6 місяців після ішемічного інсульту. Для профілактики тромботичних ускладнень при гострому коронарному синдромі без підйому сегмента ST (нестабільна стенокардія, інфаркт міокарда без зубця Q) – починають з одноразового прийому навантажувальної дози – 300 мг, а потім приймають по 75 мг на добу (у поєднанні з АСК у дозах 7 325 мг на добу, рекомендована доза – 100 мг на добу). Максимальний сприятливий ефект настає через 3 місяці. Курс лікування – до 1 року. Для профілактики тромботичних ускладнень при гострому коронарному синдромі з підйомом сегмента ST (гострий інфаркт міокарда з підйомом сегмента ST) - по 75 мг на добу з первісним одноразовим прийомом дози навантаження в комбінації з АСК і тромболітиками (або без тромболітиків). Комбіновану терапію починають якомога раніше після появи симптомів і продовжують протягом принаймні 4 тижнів. У пацієнтів старше 75 років лікування клопідогрелом має починатися без прийому його дози навантаження. У пацієнтів із генетично обумовленим зниженням функції ізоферменту CYP2C19 можливе зменшення ефекту клопідогрелу. Оптимальний режим дозування таких пацієнтів не встановлений. Досвід застосування у пацієнтів з хронічною нирковою недостатністю або помірним ступенем печінкової недостатності обмежений. Приймати внутрішньо, незалежно від їди.ПередозуванняПередозування клопідогрелом може призвести до подовження часу кровотечі та подальших геморагічних ускладнень. При виявленні кровотечі має бути застосоване відповідне лікування. Не виявлено антидотів фармацевтичної активності клопідогрелу. Якщо необхідна швидка корекція часу кровотечі, що подовжився, рекомендується переливання тромбоцитарної маси.Запобіжні заходи та особливі вказівкиУ період лікування необхідно контролювати показники системи гемостазу (активований частковий тромбопластиновий час (АЧТВ), кількість тромбоцитів, тести функціональної активності тромбоцитів); регулярно досліджувати функціональну активність печінки. Клопідогрел слід застосовувати з обережністю у пацієнтів, з ризиком вираженої кровотечі при травмі, хірургічному втручанні, у пацієнтів, які мають ушкодження, схильні до кровотечі (особливо шлунково-кишкові та внутрішньоочні), а також у пацієнтів, які отримують АСК, нестероїдні протизапальні препарати. числа інгібітори ЦОГ-2), гепарин або інгібітори глікопротеїну IIb/IIIa. За пацієнтами необхідно ретельно спостерігати для виявлення будь-яких ознак кровотечі, зокрема прихованої, особливо протягом перших тижнів застосування препарату та/або після інвазивних процедур на серці або хірургічних операцій. Одночасне застосування клопідогрелу та варфарину не рекомендується, оскільки воно може посилити кровотечу. У разі хірургічних втручань, якщо антиагрегантна дія небажана, курс лікування слід припинити за 7 днів до операції. Хворих слід попередити про те, що оскільки зупинка кровотечі, що виникає на тлі застосування клопідогрелу (у поєднанні з АСК або без неї), вимагає більшого часу, вони повинні повідомляти лікаря про кожен випадок кровотечі. Хворі повинні також інформувати лікаря про прийом препарату, якщо їх чекають оперативні втручання. Після прийому клопідогрелу тромботична тромбоцитопенічна пурпура (ТТП) виявлялася дуже рідко, іноді після короткочасного застосування. Цей стан характеризується тромбоцитопенією та мікроангіопатичною гемолітичною анемією у поєднанні з неврологічними ознаками, порушенням функції нирок або лихоманкою. ТТП - потенційно смертельний стан, що потребує негайного лікування, у тому числі із застосуванням плазмаферезу. Через відсутність даних клопідогрел не можна рекомендувати при гострих (менше 7 днів) ішемічних інсультах. Досвід застосування клопідогрелу у пацієнтів з порушенням функції нирок обмежений, тому цим хворим клопідогрел слід призначати з обережністю. При тяжких порушеннях функції печінки слід пам'ятати про ризик розвитку геморагічного діатезу, досвід застосування препарату у пацієнтів з помірним порушенням функції печінки обмежений, тому цим пацієнтам клопідогрел слід призначати з обережністю.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаЕкстракти листя маніоку їстівного (Manihot esculenta Crantz M. Utilissima Pohl.), листя гуацуми в'язлистої (Guazuma ulmifolia), кореневищ куркуми Гейне (Curcuma heyneana Val.), кореневищ імбиру пурпурного (Za Juss.) Moldenke). Пігулки, 50 шт.ХарактеристикаСприяє пропорційній корекції фігури, нормалізації ліпідного та вуглеводного обміну.Фармакотерапевтична групаТаблетки плоский живіт виготовляються із суміші рослинних екстрактів, приготованих за сучасними технологіями, корисні чоловікам і жінкам для контролю жирових відкладень, особливо в області живота, та підтримки стрункої фігури. У класичній східній фітотерапії цей рецепт застосовується для зменшення жирових відкладень в області живота та інших частинах тіла активного виведення жирів і холестерину з організму зміцнення м'язів живота і підтримки стрункої фігури. .РекомендуєтьсяПоказано для людей з порушенням ліпідного та вуглеводного обміну.Протипоказання до застосуванняІндивідуальна непереносимість компонентів продукту, вагітним і жінкам, що годують, дітям.Вагітність та лактаціяНе застосовувати дітям та вагітним.Спосіб застосування та дозиДорослим по 1 таблетці 1-2 десь у день. Тривалість прийому – 30-60 днів. Приймати під час їжі.Запобіжні заходи та особливі вказівкиПеред застосуванням проконсультуйтеся зі спеціалістом.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаЕкстракт плюща. Носії целюлоза мікрокристалічна та крохмаль кукурудзяний. компоненти плівкового покриття: гідроксипропілметилцелюлоза, твін 80 (емульгатор): діоксид титану, міднохлорофіліновий, натуральний екстракт картамусу (барвники), поліетиленгліколь (глазувач); кроскарамеллоза (носій), стеарат кальцію та діоксид кремнію аморфний (агенти антистежують) Упаковка: таблетки 50 шт. покритих оболонкою по 250 мгХарактеристикаПлющ при кашлі Евалар рекомендується як при сухому, так і при вологому кашлі дорослим та дітям старше 14 років. Рослинний засіб випускається у зручній для прийому формі – у таблетках. Тепер не потрібно виміряти дозування сиропу або чекати на розчинення порошку в склянці води. Досить просто запитати таблетку водою будь-якої миті!Фармакотерапевтична групаПри сухому і вологому кашлі, має м'яку відхаркувальну дію, сприяє розрідженню та виведенню мокротиння (у тому числі важковідокремлюваного мокротиння), пом'якшенню кашлю та полегшенню дихання, зменшенню частоти нападів кашлю, прискоренню одужання при захворюваннях верхніх дихальних шляхів. Джерело:https://apteka.ru/catalog/plyushch-pri-kashle-evalar-n50-tabl-po-po-250mg-_5ab4e57a3e14a/ © Apteka.RUІнструкціяДорослим та дітям старше 14 років по 1 тану 3 рази на день перед їдою. Тривалість прийому не менше 10 днів до повного зникнення кашлю. За потреби курс прийому можна повторити.Показання до застосуванняРекомендується як біологічно активна добавка до їжі - додаткового джерела, що містить гедеракозід СПротипоказання до застосуванняІндивідуальна нестерпність компонентів.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкааскорбінова кислота, екстракт листя плюща, глюкози моногідрат; полівінілпіролідон; тальк, діоксид кремнію аморфний, стеарат магнію; ароматизатор натуральний «Ефірна олія евкаліпту». Вміст активних речовин у 1 таблетці: Вітамін С-90 мг; Гедеракозід С, не менше -4,15 мг. Харчова цінність 1 таблетки: вуглеводи – 0,9 г. Енергетична цінність 1 таблетки – 15,3 кДж/3,6 ккал.ХарактеристикаПроцес дихання в людини багато в чому залежить стану бронхів. Нерідко вже при невеликому звуженні, що може бути викликано скороченням м'язів у відповідь на дію цілого ряду факторів, з'являється дискомфорт при видиху, а іноді і при вдиху. Іншою проблемою, що свідчить про труднощі в роботі дихальної системи, є кашель спочатку сухий, потім з мокротою. Її відходження сприяє очищенню бронхів, проте часто буває недостатнім та непродуктивним. Тим часом існують природні для організму рослинні засоби, які, з одного боку, допомагають розслабляти бронхіальну мускулатуру, а з іншого — сприяють розрідженню мокротиння та його виведенню з легенів. Серед них — плющ, що виявляє помітні відхаркувальні та спазмолітичні властивості. Плющ у таблетках містить екстракт листя цієї рослини та аскорбінову кислоту – компоненти, що допомагають боротися з кашлем, полегшувати дихання, а також запобігати розвитку застуди та зміцнювати імунний захист. Таблетки відрізняються приємним ароматом евкаліптової олії.РекомендуєтьсяРекомендується як біологічно активна добавка до їжі - додаткового джерела вітаміну С, що містить гедеракозід С.Протипоказання до застосуванняІндивідуальна непереносимість компонентів препарату, вагітність, годування груддю.Спосіб застосування та дозиДорослим, по 1 таблетці 3 десь у день. Таблетки слід розсмоктати у роті. Тривалість прийому – 7–10 днів. За потреби курс прийому можна повторити.Запобіжні заходи та особливі вказівкиПеред застосуванням рекомендується проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
Фасування: N20 Форма випуску таб. Упаковка: блістер Виробник: Грін Сайд Завод-производитель: Грин Сайд ООО(Россия). .
Склад, форма випуску та упаковкаЕкстракт розторопші; мікрокристалічна целюлоза та крохмаль картопляний (носії), фруктоза, діоксид кремнію та стеарат кальцію (агенти антистежуючі).ХарактеристикаАктивні компоненти "Нірочний збір" сприяють: - покращення функціонального стану нирок та сечового міхура; - Надають сечогінну; - спазмолітична та антисептична дії; - перешкоджають утворенню піску та каміння в нирках та сечовому міхурі.РекомендуєтьсяСприяє поліпшенню функціонального стану нирок та сечового міхура, надає сечогінну, спазмолітичну та антисептичну дії, що перешкоджає утворенню піску та каміння у нирках та сечовому міхурі.Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність, годування груддю.Спосіб застосування та дозиДорослим приймати по 1 таблетці 2 десь у день їжі. Тривалість прийому: щонайменше 3 місяців. При необхідності прийом БАД можна повторити за місяць.Запобіжні заходи та особливі вказівкиБіологічно активна добавка (БАД) до їжі. Чи не є лікарським засобом. Перед застосуванням рекомендується проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему