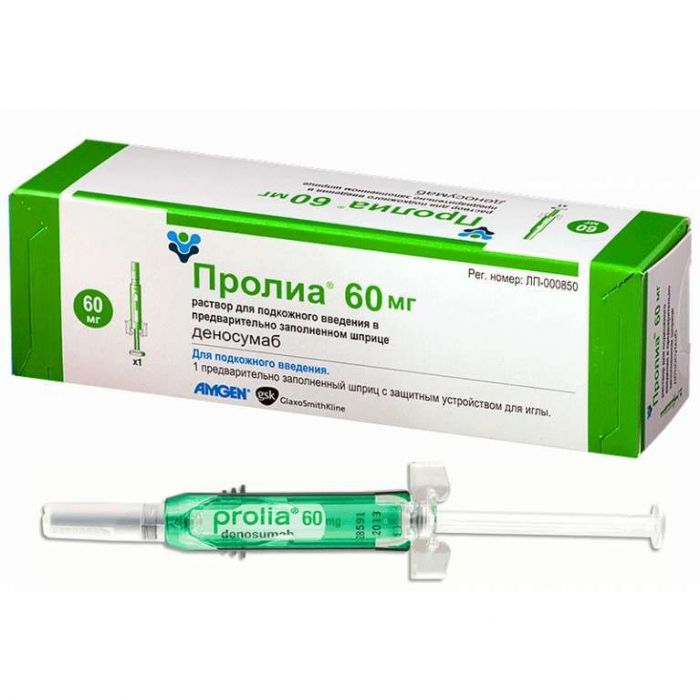
Пролиа 60мг 1мл раствор для подкожного введения шприц Цены
-
Страна:Нидерланды
-
Форма выпуска:р-р д/подкожного введения
-
Дозировка:60 мг
-
Фасовка:N1
Ингибирующее костную резорбцию.
Пролиа 60мг 1мл раствор для подкожного введения шприц инструкция на украинскомСклад, форма випуску та упаковка
Розчин для підшкірного введення – 1 мл. Кожен попередньо заповнений шприц містить:
активна речовина: деносумаб – 60 мг; допоміжні речовини: сорбітол (Е420) – 47 мг; оцтова кислота крижана - 1 мг; полісорбат 20 - 0,1 мг; натрію гідроксид - до рН 5,0-5,5; вода для ін'єкцій – до 1 мл.Розчин для підшкірного введення 60 мг/мл. В одноразовому попередньо заповненому шприці (ПЗШ) 1 мл зі скла I гідролітичного класу з голкою 27G з нержавіючої сталі, еластомерним ковпачком та еластомірним плунжером, ламінованим фторполімером (із захисним пристроєм для голки або без нього). Маркований шприц поміщають у пачку картонну.
ПЗШ може бути додатково поміщений у контурне осередкове впакування з термоетикеткою. Кожну контурну осередкову упаковку поміщають у картонну пачку.
Пачка картонна забезпечена відривною карткою-нагадуванням з двома наклейками, що нагадують.
Проліа™ є стерильний продукт і не містить консервантів.
Опис лікарської форми
Прозора рідина від безбарвного до світло-жовтого кольору практично вільна від видимих включень.
Фармакотерапевтична група
Інгібуючу кісткову резорбцію.
Фармакокінетика
При підшкірному введенні деносумаб характеризується нелінійною фармакокінетикою, дозозалежною в широкому діапазоні доз, та дозозалежним збільшенням експозиції для дози 60 мг (або 1 мг/кг) і вище.
Всмоктування
Після підшкірного введення деносумабу в дозі 60 мг біодоступність склала 61% і Cmax - 6 мкг/мл (діапазон 1-17 мкг/мл), дані параметри спостерігалися через 10 днів (діапазон 2-28 днів). Після досягнення Cmax вміст препарату в сироватці крові знижувався з T1/2 26 днів (діапазон 6-52 дні) і далі протягом 3 місяців (діапазон 1,5-4,5 міс). У 53% пацієнтів деносумаб не виявлявся у сироватці крові після 6 місяців від останнього введення препарату.
Розподіл
Не спостерігалися зміни фармакокінетичних параметрів деносумабу, а також кумуляції за весь час прийому багаторазових доз препарату по 60 мг кожні 6 місяців.
Метаболізм
Деносумаб складається з амінокислот та вуглеводів, як звичайний імуноглобулін. На підставі даних доклінічних досліджень, очікується, що метаболізм деносумабу відбуватиметься шляхом кліренсу імуноглобулінів, результатом якого буде розпад на невеликі пептидні ланцюги та окремі амінокислоти.
Виведення
На підставі доклінічних даних, виведення деносумабу відбуватиметься шляхом виведення всіх імуноглобулінів, результатом якого буде розпад на невеликі пептидні ланцюги та окремі амінокислоти.
Окремі групи пацієнтів
Пацієнти похилого віку (65 років або старше). Вік не має значного впливу на фармакокінетику деносумабу, за даними фармакокінетичного аналізу у популяції пацієнтів від 28 до 87 років.
Діти та підлітки (до 18 років). Фармакокінетика у дітей не вивчалась.
Расова приналежність. Фармакокінетика деносумабу не залежить від расової приналежності.
Пацієнти з нирковою недостатністю. У дослідженні даних 55 пацієнтів з різним ступенем ниркової недостатності, включаючи пацієнтів, що перебувають на діалізі, ступінь ниркової недостатності не впливав на фармакокінетику та фармакодинаміку деносумабу, тому не потрібна корекція режиму дозування деносумабу при хронічній нирковій недостатності.
Хронічна печінкова недостатність. Досліджень впливу недостатності функції печінки на фармакокінетику деносумабу не проводилось.
Фармакодинаміка
Механізм дії
Деносумаб є повністю людським моноклональним антитілом (IgG2), що має високу афінність і специфічність до ліганду рецептора активатора ядерного фактора κВ (RANKL), і тим самим перешкоджає активації єдиного рецептора RANKL — активатора ядерного фактора κВ (RANK), розташованого на поверхні. попередників. Таким чином, запобігання взаємодії RANKL/RANK пригнічує утворення, активацію та тривалість існування остеокластів. В результаті деносумаб зменшує кісткову резорбцію та збільшує масу та міцність кортикального та трабекулярного шарів кістки.
Фармакодинамічні ефекти
Призначення деносумабу в дозі 60 мг призводило до швидкого зменшення сироваткових концентрацій маркера резорбції кісткової тканини – 1С-телопептиду (СТХ) – приблизно на 70% протягом 6 годин після підшкірного введення та приблизно на 85% протягом наступних 3 днів. Зменшення концентрації СТХ залишалося стабільним у 6-місячному інтервалі між дозуванням. Швидкість зниження концентрації СТХ у сироватці крові частково зменшувалася при зниженні концентрації деносумабу у сироватці крові, що відображає оборотність впливу деносумабу на ремоделювання кістки. Ці ефекти спостерігалися протягом усього курсу лікування. Відповідно до фізіологічного взаємозв'язку процесів утворення та резорбції при ремоделюванні кісткової тканини,спостерігалося зменшення вмісту маркерів утворення кістки (наприклад, кістковоспецифічної ЛФ та сироваткового N-кінцевого пропептиду колагену I типу) з першого місяця після введення першої дози деносумабу. Маркери ремоделювання кістки (маркери утворення кістки та резорбції кістки), як правило, досягали концентрацій періоду до початку лікування не пізніше ніж через 9 місяців після прийому останньої дози препарату. Після відновлення лікування деносумабом ступінь зниження концентрацій СТХ була подібна до ступеня зниження концентрації СТХ на початку курсу лікування деносумабом.Після відновлення лікування деносумабом ступінь зниження концентрацій СТХ була подібна до ступеня зниження концентрації СТХ на початку курсу лікування деносумабом.Після відновлення лікування деносумабом ступінь зниження концентрацій СТХ була подібна до ступеня зниження концентрації СТХ на початку курсу лікування деносумабом.
Було показано, що переведення з лікування алендроновою кислотою (середня тривалість застосування – 3 роки) на деносумаб призводить до додаткового зниження концентрації СТХ у сироватці порівняно з групою жінок у постменопаузі з низькою кістковою масою, які продовжували лікування алендроновою кислотою. Водночас зміни вмісту кальцію у сироватці були однаковими в обох групах.
В експериментальних дослідженнях інгібування RANK/RANKL одночасно із зв'язуванням остеопротегерину з Fc-фрагментом (OPG-Fc) призводило до уповільнення зростання кістки та порушення прорізування зубів. Тому лікування деносумабом може гальмувати ріст кісток із відкритими зонами зростання у дітей та призводити до порушень прорізування зубів.
Імуногенність
Деносумаб — людське моноклональне антитіло, тому, як і інших ЛЗ білкової природи, існує теоретичний ризик імуногенності. Більш ніж 13000 пацієнтів було обстежено на предмет утворення зв'язувальних антитіл з використанням методу чутливої електрохемілюмінесценції у поєднанні з імунологічним аналізом. Менш ніж у 1% пацієнтів, які приймали деносумаб протягом 5 років, визначалися антитіла (включаючи існуючі раніше, транзиторні та зростаючі). Серопозитивні пацієнти були далі обстежені щодо утворення нейтралізуючих антитіл, використовуючи хемілюмінісцентний аналіз у культурі клітин in vitro, нейтралізуючих антитіл не виявлено. Не було виявлено змін фармакокінетичного профілю, токсичного профілю або клінічної відповіді, зумовлених утворенням антитіл.
Клінічна ефективність
Лікування остеопорозу у постменопаузі
У жінок із постменопаузальним остеопорозом Проліа™ збільшує мінеральну щільність кістки, зменшує частоту переломів шийки стегна, вертебральних та невертебральних переломів. Ефективність та безпека деносумабу у лікуванні постменопаузального остеопорозу була доведена у дослідженні тривалістю 3 роки. Результати дослідження показують, що деносумаб суттєво, порівняно з плацебо, знижує ризик виникнення вертебральних та невертебральних переломів, переломів шийки стегна у жінок із остеопорозом у постменопаузі. У дослідження було включено 7808 жінок, з яких у 23,6% відзначалися переломи хребців, що часто зустрічаються. Усі три кінцеві точки ефективності щодо переломів досягали статистично значимих значень, що оцінюються за попередньо заданою послідовною схемою тестування.
Зниження ризику виникнення нових вертебральних переломів при застосуванні деносумабу протягом більш як 3 років залишалося стабільним та значущим. Ризик знижувався незалежно від 10-річної ймовірності виникнення великих остеопоротичних переломів. На зниження ризику також не впливали наявність переломів хребців, що часто зустрічаються, в анамнезі, невертебральні переломи, вік пацієнтів, мінеральна щільність кістки, рівень ремоделювання кістки і попередня терапія з приводу остеопорозу.
У жінок старше 75 років у постменопаузі деносумаб зменшував частоту виникнення нових вертебральних переломів, та, за даними post hoc аналізу, зменшував частоту переломів шийки стегна.
Зменшення частоти виникнення невертебральних переломів спостерігалося незалежно від 10-річної ймовірності виникнення великих остеопоротичних переломів. Деносумаб суттєво, в порівнянні з плацебо, збільшував мінеральну щільність кістки у всіх анатомічних областях. Мінеральну щільність кістки визначали через 1, 2 та 3 роки після початку терапії. Подібний вплив на мінеральну щільність кістки зазначено в поперековому відділі хребта незалежно від віку, расової приналежності, індексу маси тіла (ІМТ), мінеральної щільності кістки та ремоделювання кістки. Гістологічні дослідження підтвердили нормальну архітектоніку кістки та, як і очікувалося, зниження кісткового ремоделювання порівняно з плацебо. Не відмічено патологічних змін, включаючи фіброз, остеомаляцію та порушення архітектоніки кісткової тканини.
Клінічна ефективність при лікуванні втрати кісткової маси, спричиненої гормондеприваційною терапією або терапією інгібіторами ароматази.
Лікування втрати кісткової маси, спричиненої депривацією андрогенів.
Ефективність та безпека деносумабу при лікуванні втрати кісткової маси, асоційованої зі зниженням концентрації андрогенів, були доведені у 3-річному дослідженні, що включало 1468 пацієнтів з неметастатичним раком передміхурової залози. Істотне збільшення мінеральної щільності кістки визначали в поперековому відділі хребта, всієї стегнової кістки, шийці стегнової кістки, рожні стегнової кістки через 1 міс після прийому першої дози. Збільшення мінеральної густини кістки в поперековому відділі хребта не залежало від віку, расової приналежності, географічного регіону, ІМТ, початкових значень мінеральної густини кістки, ремоделювання кістки; тривалості проведення гормондеприваційної терапії та наявності вертебрального перелому в анамнезі.
Деносумаб значно зменшував ризик виникнення нових вертебральних переломів протягом трьох років застосування. Зменшення ризику спостерігалося через 1 рік та через 2 роки після початку терапії. Деносумаб також знижував ризик виникнення більш ніж одного остеопоротичного перелому будь-якої локалізації.
Лікування втрати кісткової маси у жінок, які отримують терапію інгібіторами ароматази щодо раку молочної залози.
Ефективність та безпека деносумабу в лікуванні втрати кісткової маси, спричиненої ад'ювантною терапією інгібітором ароматази, оцінювалася у 2-річному дослідженні, що включало 252 пацієнтки з неметастатичним раком молочної залози. Деносумаб значно збільшував мінеральну щільність кістки у всіх анатомічних областях порівняно з плацебо протягом 2 років. Збільшення мінеральної щільності кістки спостерігалося в поперековому відділі хребта через місяць після прийому першої дози. Позитивний вплив на мінеральну щільність кістки у люмбальному відділі хребта відзначали незалежно від віку, тривалості терапії інгібітором ароматази, ІМТ, попередньої хіміотерапії, попереднього використання селективного модулятора рецепторів естрогену (СМРЕ) та часу, що пройшов від.
Показання до застосуваннялікування постменопаузального остеопорозу; лікування втрати кісткової маси у жінок, які отримують терапію інгібіторами ароматази з приводу раку молочної залози та у чоловіків, з раком передміхурової залози, які отримують гормондеприваційну терапію.
Протипоказання до застосуванняпідвищена чутливість до будь-якого компонента препарату; гіпокальціємія.
Вагітність та лактація
Немає жодних даних щодо застосування препарату під час вагітності. Проліа не рекомендується для застосування у вагітних жінок.
У токсикологічних дослідженнях на нижчих приматах було показано, що в дозах, що 100-кратно перевищують рекомендовані для клінічного застосування, деносумаб не впливав на фертильність або розвиток плода.
Експерименти на мишах з вимкненим геном показали, що відсутність RANKL може призводити до порушення розвитку лімфатичних вузлів у плода, а в постнатальному періоді може бути причиною порушення прорізування зубів та зростання кісток; також можливий вплив на дозрівання молочної залози, що може спричинити ослаблення лактації.
Пацієнткам, у яких вагітність настала під час лікування препаратом Проліа™, слід зареєструватись у Програмі спостереження вагітності компанії Амджен. Пацієнти або лікарі, у яких вони перебувають під наглядом, можуть зателефонувати за телефоном, зазначеним у кінці цієї інструкції для реєстрації у Програмі спостереження.
Невідомо, чи деносумаб виводиться в грудне молоко. Оскільки відомо, що потенційно деносумаб може викликати небажані реакції у дітей грудного віку, необхідно або припинити грудне вигодовування або скасувати препарат.
Побічна дія
Дані, отримані при контрольованому застосуванні у клінічних дослідженнях.
Небажані реакції наводяться за класами систем органів термінах Медичного словника регуляторної діяльності (MedDRA). Частота виникнення визначена таким чином: дуже часто -1 з 10; часто ->1 з 100 і <1 з 10; нечасто -> 1 з 1000 і <1 з 100; рідко -> 1 з 10000 і <1 з 1000; дуже рідко <1 із 10000.
У кожній групі систем органів та частоти повідомлень небажані реакції наводяться за зменшенням ступеня серйозності.
Інфекції та інвазії: нечасто – запалення підшкірної клітковини.
З боку метаболізму та електролітного обміну: дуже рідко – гіпокальціємія.
З боку органів зору: часто – катаракта.
З боку шкіри та підшкірно-жирової клітковини: нечасто – екзема.
З боку кістково-м'язової системи та сполучної тканини: часто – біль у кінцівках, рідко – остеонекроз щелепи.
Взаємодія з лікарськими засобами
Рекомендується приймати препарати кальцію та вітаміну D під час застосування препарату Проліа™.
Гіпокальціємія може бути скоригована прийомом препаратів кальцію та вітаміну D у адекватних дозах перед початком терапії деносумабом. Рекомендується контроль концентрації кальцію у пацієнтів, схильних до гіпокальціємії.
Спосіб застосування та дози
Вступ
Проведення ін'єкції препарату вимагає попереднього навчання – див. рекомендації щодо введення препарату, наведені наприкінці цього розділу.
Доза
Рекомендована доза препарату Проліа - одна підшкірна ін'єкція 60 мг кожні 6 міс. Протягом курсу лікування рекомендується додатково приймати препарати кальцію та вітамін D.
Застосування в окремих груп пацієнтів
Діти. Препарат Проліа не рекомендований до застосування в педіатрії, тому ефективність та безпека даного препарату не вивчалися у цій віковій групі.
Пацієнти похилого віку. На основі наявних даних про ефективність та безпеку препарату в даній віковій групі не потрібна корекція режиму дозування препарату.
Ниркова недостатність
На основі наявних даних про ефективність та безпеку препарату в даній групі пацієнтів не потрібна корекція режиму дозування препарату.
У пацієнтів з тяжкою нирковою недостатністю (Cl креатиніну <30 мл/хв) або на діалізі існує великий ризик розвитку гіпокальціємії. Таким пацієнтам необхідно додатково приймати препарати кальцію та вітамін D.
Печінкова недостатність. Ефективність та безпека не вивчалися.
Слід оцінити розчин перед введенням щодо наявності включень або зміни кольору. Розчин не можна використовувати при помутнінні або зміні кольору. Чи не струшувати.
Щоб уникнути дискомфорту в місці введення, слід зігріти розчин до кімнатної температури (до 25 ° C) перед ін'єкцією, а потім повільно ввести весь вміст попередньо заповненого шприца. Шприц із залишками препарату викинути. Детальні рекомендації щодо самостійного підшкірного введення препарату включені в дану інструкцію з медичного застосування.
Будь-які кількості невикористаного препарату або невикористані матеріали повинні бути знищені відповідно до місцевих вимог.
Інструкції з застосування препарату Проліа™, попередньо заповнені шприци із захисним пристроєм для голки.
У цьому розділі наводиться інформація щодо правильного проведення ін'єкції попередньо заповненим шприцом (ПЗШ) із захисним пристроєм для голки. Дуже важливо, щоб перед тим, як ви приступите до самостійних ін'єкцій, лікар, медична сестра докладно проінструктували вас з техніки виконання ін'єкції. Якщо у вас виникнуть питання щодо техніки виконання ін'єкції, зверніться до лікаря або медичної сестри.
Перед початком ін'єкції
Перед використанням ПЗШ уважно прочитайте всі інструкції.
Для зменшення ризику випадкового уколу кожен ПЗШ оснащений запобіжником – захисним пристроєм для голки, що автоматично активується для закривання голки після завершення ін'єкції.
Не намагайтеся розбирати ПЗШ або активувати запобіжник перед ін'єкцією. Не використовуйте ПЗШ, якщо ковпачок був видалений або запобіжник голки активовано.
Як використовувати попередньо заповнений шприц?
Ваш лікар призначив вам препарат Проліа ПЗШ для підшкірних ін'єкцій. Ви повинні ввести весь вміст шприца одноразово і повторити ін'єкцію через 6 міс, як призначено лікарем.
Обладнання
Для самостійної ін'єкції вам знадобиться:
Нова ПЗШ препарату Проліа™; Змочені спиртом тампони чи подібні матеріали.Що ви повинні зробити до введення Проліа™ підшкірно?
Дістати шприц із холодильника. Не брати ПЗШ за поршень або захисний ковпачок, це може призвести до пошкодження пристрою. Залишити ПЗШ за кімнатної температури для більш комфортної ін'єкції. Не підігрівати ПЗШ будь-яким іншим способом (наприклад, у мікрохвильовій печі або в гарячій воді). Не залишати шприц під прямим сонячним промінням. Не струшувати ПЗШ. Не видаляти ковпачок ПЗШ, доки ви не готові до ін'єції. Перевірити термін придатності ПЗШ. Термін придатності вказаний на упаковці як «РОК ДО: ММ.РРРР». Не використовувати ПЗШ після останнього дня вказаного місяця зберігання. Перевірити зовнішній вигляд препарату Проліа. Розчин має бути прозорим, безбарвним чи світло-жовтим. Якщо розчин помутніли або пофарбовані інакше, препарат використовувати не можна. Вибрати комфортне, добре освітлене місце та чисту поверхню, де можна зручно розмістити всі необхідні матеріали. Ретельно вимити руки.Як правильно вибрати місце для ін'єкції?
Найкраще робити ін'єкції у верхню частину стегон та живота. Якщо ін'єкції робить хтось інший, можна використовувати тильну поверхню рук.
Якщо область, куди ви зібралися робити ін'єкцію, почервоніла або набрякла, слід вибрати інше місце ін'єкції.
Як робити ін'єкцію?
Продезінфікувати місце ін'єкції за допомогою змоченого спирту тампона. Щоб уникнути вигину голки, акуратно потягнути ковпачок з голки відразу без скручування, як показано на малюнку. Не торкатися голки і не натискати на поршень. Якщо всередині ПЗШ помітні маленькі бульбашки повітря, немає необхідності видаляти їх перед ін'єкцією. Введення розчину з бульбашками повітря є безпечним. Затиснути шкіру (не стискаючи) між великим і вказівним пальцями. Ввести голку, як показував вам лікар чи медична сестра. Повільно і плавно натиснути на поршень, одночасно притримуючи складку. Натискати на поршень слід доти, поки шприц не спорожніє. Запобіжник голки не спрацює, доки шприц не спустіє. Поки натиснутий поршень, видаліть голку зі шкіри і відпустіть шкірну складку.Потім відпустіть поршень і дозвольте шприцу піднятися вгору, поки вся голка не покриється запобіжником голки. Якщо запобіжник не активувався, можливо, ви не виконали ін'єкцію повністю. Зателефонуйте лікарю, якщо вважаєте, що ви не отримали повну дозу.
Чи не надягати ковпачок на голку. Якщо виступить кров у місці ін'єкційного проколу, акуратно стерти її ватним тампоном чи тканиною. Чи не розтирати місце ін'єкції. При необхідності можна заклеїти місце ін'єкції пластиром. Використовувати один ПЗШ лише для однієї ін'єкції. Не використовувати препарат, що залишився в шприці.
Пам'ятайте: у разі виникнення проблем зверніться за допомогою або порадою до лікаря або медичної сестри.
Знищення використаних шприців
Не надягати назад ковпачок на використаний шприц.
Зберігати використаний шприц у недоступному для дітей місці.
Використаний шприц повинен бути утилізований відповідно до місцевих правил. Запитайте у лікаря чи провізора, як знищити препарат, якщо він більше не потрібний. Ці заходи допоможуть захисту довкілля.
Передозування
У клінічних дослідженнях не виявлено випадків передозування препарату.
У клінічних дослідженнях вводили дози деносумабу до 180 мг кожні 4 тижні (кумулятивна доза до 1080 мг на 6 міс).
Запобіжні заходи та особливі вказівки
У пацієнтів, які отримують препарат Проліа™, можуть розвинутись інфекції шкіри та її придатків (переважно запалення підшкірної клітковини), що в окремих випадках потребують госпіталізації. Про такі реакції частіше повідомлялося для групи деносумабу (0,4%), ніж групи плацебо (0,1%) (див. «Побічні дії»). У цьому загальна частота виникнення шкірних інфекцій можна порівняти у групах деносумабу і плацебо. Пацієнтів слід проінструктувати про необхідність негайно звернутися за лікарською допомогою у разі розвитку симптомів та ознак запалення підшкірної клітковини.
У пацієнтів з поширеним раком, які отримували 120 мг деносумабу кожні 4 тижні, повідомлялося про розвиток випадків остеонекрозу щелепи. Є окремі повідомлення розвитку остеонекроза щелепи при дозі 60 мг кожні 6 міс.
Особи з алергією на латекс не повинні стосуватися гумового ковпачка голки (похідне латексу).
Вплив на здатність до керування автотранспортом та поводження з технікою. Досліджень впливу на здатність до керування автотранспортними засобами та управління механізмами не проводилося.
Умови відпустки з аптек
За рецептом
Відео на цю темуИнформация, касающаяся данного товара
Производит Пролиа 60мг 1мл раствор для подкожного введения шприц компания Амджен Европа Б.В.. Само производство расположено в стране Нидерланды.
Тут Вы всегда можете купить Пролиа 60мг 1мл раствор для подкожного введения шприц онлайн в Украине и оформить доставку на дом (работаем со всеми городами). Если Вы ищете Пролиа 60мг 1мл раствор для подкожного введения шприц в Украине, то Вам однозначно к нам! Мы продаем нашу продукцию в таких городах как Киев, Винница, Кропивницкий (Кировоград), Полтава, Харьков, Днепр, Луганск, Ровно, Херсон, Донецк, Луцк, Хмельницкий, Житомир, Львов, Сумы, Черкассы, Запорожье, Николаев, Тернополь, Чернигов, Ивано-Франковск, Одесса, Ужгород, Черновцы и в любом другом городе. Есть еще похожий товар в рекомендуемом блоке, присмотритесь. Необходима быстрая доставка Пролиа 60мг 1мл раствор для подкожного введения шприц? Мы отправляем продукцию в день заказа или на следующий рабочий день. Не болейте!
Если Вас заинтересовал этот товар, обратите внимание на его аналоги: Эксджива 120мг (70мг/мл) 1,7мл 1 шт. раствор для подкожного введения, Альфа д3-тева 1мкг 30 шт. капсулы, Остеогенон 830мг 40 шт. таблетки, Рокальтрол 0,25мкг 30 шт. капсулы, Цель т 2,2мл 5 шт. раствор для инъекций biologische heilmittel heel gmbh.