Вредные привычки
Склад, форма випуску та упаковкаУ 1 таблетці міститься: Ацетилсаліцилова кислота – 324 мг, натрію гідрокарбонат висушений (87,5 % натрію гідрокарбонату, 12,5 % натрію карбонату) – 1625 мг, лимонна кислота – 965 мг; Допоміжні речовини: повідон 25 2 мг, диметикон/силікат* 1 мг, досс-натрію бензоат** 0,1 мг, сахарінат натрію 2 мг, ароматизатор лимонний 1,95 мг, ароматизатор лаймовий 1,95 мг. * суміш диметикону та кальцію силікату у співвідношенні 70:30. ** суміш докузату натрію та натрію бензоату у співвідношенні 85:15.Опис лікарської формиКруглі, плоскі таблетки білого кольору, на одній стороні гравіювання «ALKA SELTZER» у опуклому колі, що виступає по периметру. Зворотний бік має фаску.ФармакокінетикаПісля прийому внутрішньо АСК швидко повністю абсорбується із шлунково-кишкового тракту. У період абсорбції і відразу після неї АСК перетворюється на основний активний метаболіт – саліцилову кислоту. АСК досягає максимальної концентрації у плазмі крові через 10-20 хвилин, а саліцилова кислота – через 0,3-2 години. Близько 80% АСК та саліцилової кислоти зв'язується з білками плазми та швидко розподіляється у тканинах. Саліцилова кислота метаболізується в печінці з утворенням метаболітів - саліцилурату, саліциловофенольного глюкуроніду, саліцилацилового глюкуроніду, гентизинової та гентізурової кислот. Виділяється у грудне молоко та проникає через плаценту. Елімінація саліцилової кислоти дозозалежна. Період напіввиведення варіює від 2-3 годин при прийомі препарату в низьких дозах приблизно до 15 годин при використанні високих доз.Саліцилова кислота та її метаболіти екскретуються, головним чином, нирками.Показання до застосуванняCімптоматичне лікування больового синдрому слабкої та помірної виразності: головного болю (в т.ч. після споживання алкоголю), зубного болю, болю в горлі, болю в спині та м'язах, болю в суглобах, болю при менструації. Підвищена температура тіла при застудних та інших інфекційно-запальних захворюваннях (у дорослих та дітей старше 15 років).Протипоказання до застосуванняПідвищена чутливість до ацетилсаліцилової кислоти та інших нестероїдних протизапальних засобів або інших компонентів препарату. Ерозивно-виразкові ураження шлунково-кишкового тракту (у фазі загострення). Геморагічні діатези. Сполучене застосування метотрексату в дозі 15 мг на тиждень і більше. Повне та неповне поєднання бронхіальної астми, рецидивуючого поліпозу носа та приносових пазух та непереносимості ацетилсаліцилової кислоти або ін. нестероїдних протизапальних препаратів (в т.ч. в анамнезі). Вагітність (I та III триместр), період грудного вигодовування. Препарат не призначають дітям до 15 років з гострими респіраторними захворюваннями, спричиненими вірусними інфекціями, через ризик розвитку синдрому Рейє (енцефалопатія та гостра жирова дистрофія печінки з гострим розвитком печінкової недостатності). З обережністю При супутній терапії антикоагулянтами, подагрі, виразкової хвороби шлунка та/або дванадцятипалої кишки (в анамнезі), включаючи хронічний або рецидивуючий перебіг виразкової хвороби, або епізоди шлунково-кишкових кровотеч; ниркова та/або печінкова недостатність, дефіцит глюкозо-6-фосфатдегідрогенази, серцева недостатність, вагітність ІІ триместр.Побічна діяЗ боку шлунково-кишкового тракту: біль у животі, печія, нудота, блювання, явні (блювота з кров'ю, дьогтеподібний стілець) або приховані ознаки шлунково-кишкової кровотечі, які можуть призводити до залізодефіцитної анемії, ерозивно-виразкові ураження (у тому числі з перфорацією) шлунково-кишкового тракту, поодинокі випадки – порушення функції печінки (підвищення активності «печінкових» трансаміназ). З боку центральної нервової системи: запаморочення, шум у вухах (зазвичай ознаки передозування). Порушення ризику кровотечі, що є наслідком впливу ацетилсаліцилової кислоти на агрегацію тромбоцитів. Алергічні реакції: висипання на шкірі, анафілактичні реакції, бронхоспазм, набряк Квінке. При появі подібних симптомів рекомендується припинити прийом препарату і негайно звернутися до лікаря.Взаємодія з лікарськими засобамиСпільне застосування: з метотрексатом у дозі 15 мг на тиждень або більше: підвищується гемолітична цитотоксичність метотрексату (знижується нирковий кліренс метотрексату та метотрексат заміщується саліцилатами у зв'язку з білками плазми); з антикоагулянтами, наприклад, гепарином: підвищується ризик кровотечі внаслідок інгібування функції тромбоцитів, пошкодження слизової оболонки шлунково-кишкового тракту, витіснення антикоагулянтів (пероральних) із зв'язку з білками плазми крові; з іншими нестероїдними протизапальними препаратами, а також з великими дозами саліцилатів (3 г на день або більше): внаслідок синергічної взаємодії, підвищується ризик виникнення виразки шлунка та дванадцятипалої кишки та кровотечі із шлунково-кишкового тракту; з урикозуричними засобами, наприклад бензбромарон: знижує урикозуричний ефект; з дигоксином: концентрація дигоксину підвищується внаслідок зниження ниркової екскреції; з гіпоглікемічними препаратами, наприклад, інсуліном: підвищується гіпоглікемічна дія гіпоглікімічних препаратів внаслідок гіпоглікемічної дії ацетилсаліцилової кислоти; з препаратами групи тромболітиків: ризик виникнення кровотечі збільшується; з діуретиками: знижується гломерулярна фільтрація внаслідок зниження синтезу простагландинів; з системними глюкокортикостероїдами, крім гідрокортизону, що використовується як замісна терапія при хворобі Аддісона: при застосуванні глюкокортикостероїдів знижується концентрація саліцилатів у крові за рахунок підвищення виведення останніх; з інгібіторами ангіотензинперетворюючого ферменту: у дозі 3 г на добу та більше знижується гломерулярна фільтрація за рахунок інгібування дії простагландинів та, як наслідок, знижується антигіпертензивний ефект; з вальпроєвою кислотою: підвищується токсичність вальпроєвої кислоти; з етанолом: зростає ризик ушкоджуючого впливу на слизову оболонку шлунково-кишкового тракту та збільшується час кровотечі.Спосіб застосування та дозиПрепарат призначений для дорослих та дітей віком від 15 років. Всередину приймати в разовій дозі по 1-3 таблетки (інтервал між прийомами повинен становити 4-8 годин). Максимальна добова доза не повинна перевищувати 9 таблеток (3 г). Спосіб застосування: Розчинити попередньо 1-3 таблетки в 1 склянці (200 мл) води. Тривалість лікування (без консультації з лікарем) не повинна перевищувати 5 днів при призначенні як знеболювальний засіб і більше 3 днів - як жарознижувальний засіб.ПередозуванняСимптоми. Передозування середнього ступеня тяжкості: нудота, блювання, шум у вухах, порушення слуху, головний біль, запаморочення та сплутаність свідомості. Ці симптоми відбуваються при зниженні дози препарату. Тяжке передозування: лихоманка, гіпервентиляція, кетоз, респіраторний алкалоз, метаболічний ацидоз, кома, кардіогенний шок, дихальна недостатність, виражена гіпоглікемія. Лікування: госпіталізація, лаваж, прийом активованого вугілля, моніторинг кислотно-лужного балансу, лужний діурез для того, щоб отримати рН сечі між 7,5-8 (форсований лужний діурез вважається досягнутим, якщо концентрація саліцилатів у плазмі становить понад 500 мг/л ( 3,6 ммоль/л) у дорослих або 300 мг/л (2,2 ммоль/л) у дітей), гемодіаліз, відшкодування втрати рідини, симптоматична терапія.Запобіжні заходи та особливі вказівкиАцетилсаліцилова кислота може спричинити бронхоспазм, напад бронхіальної астми або інші реакції підвищеної чутливості. Факторами ризику є наявність бронхіальної астми, поліпів носа, лихоманки, хронічних бронхолегеневих захворювань, випадків алергії в анамнезі (алергічні риніти, висипання на шкірі). Ацетилсаліцилова кислота може підвищувати схильність до кровоточивості, що пов'язано з її інгібуючим впливом на агрегацію тромбоцитів. Це слід враховувати в разі потреби хірургічних втручань, включаючи такі невеликі втручання, як видалення зуба. Перед хірургічним втручанням, для зменшення кровоточивості в ході операції і в післяопераційному періоді, слід відмінити прийом препарату за 5-7 днів і повідомити лікаря. Дітям не можна призначати препарати, що містять ацетилсаліцилову кислоту, оскільки у разі вірусної інфекції підвищується ризик виникнення синдрому Рейє. Симптомами синдрому Рейє є тривале блювання, гостра енцефалопатія, збільшення печінки. При необхідності застосування препарату у період лактації грудне вигодовування слід припинити. Ацетилсаліцилова кислота зменшує виведення сечової кислоти з організму, що може спричинити гострий напад подагри у схильних пацієнтів. В одній таблетці шипучої Алка-Зельтцера міститься 477 мг натрію, що слід враховувати при дієті з контрольованим споживанням натрію. Не виявлено впливу прийому препарату на керування автотранспортним засобом та іншими механізмами.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
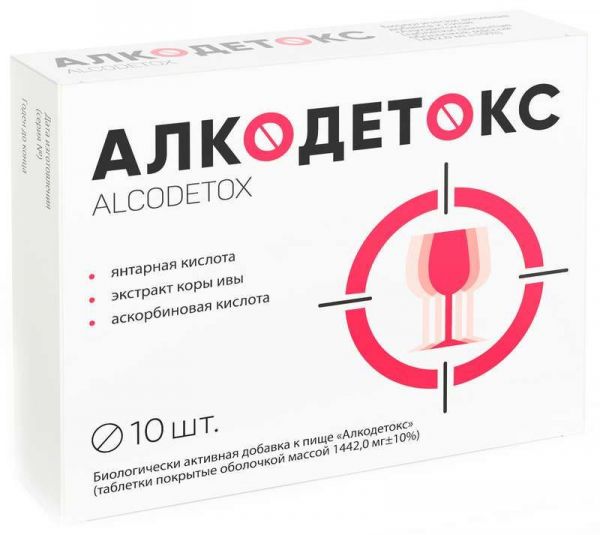
Склад, форма випуску та упаковкаЕкстракт кори верби, Е460, янтарна кислота, аскорбінова кислота, екстракт грифонії, Е1202, Е1201, Е570, кальцію пантотенат, оболонка таблетки (Е464, Е1521, Е171, оксид заліза жовтий, оксид заліза червоний).ХарактеристикаДілові зустрічі, посиденьки з друзями, клубні вечірки часто супроводжуються розпиванням спиртних напоїв. А зранку треба добре почуватися і не шкодувати про вчорашній день. Компоненти, що входять до складу комплексної біологічно активної добавки до їжі "Алкодетокс", сприяють полегшенню симптомів похмілля.Властивості компонентівВітамін С покращує детоксикаційну функцію печінки, а таніни захищають її клітини та посилюють дію Вітаміну С. Саліцин, діючи, аналогічно аспірину, розріджує кров і допомагає запобігти набрякам на ранок. Таніни та Вітамін С активно сприяють виведенню токсинів з організму. Бурштинова кислота прискорює перетворення шкідливого ацетальдегіду на нешкідливу оцтову кислоту та захищає клітини від дії токсинів. Допомагає окислювати низку елементів, які додатково отруюють організм. Бурштинова кислота нормалізує обмінні процеси в організмі, тим самим допомагає швидше вивести залишки всіх токсинів. Пантотенова кислота полегшує реабілітацію організму, благотворно впливає на слизові. Саліцин має потогінну та сечогінну дію, завдяки якій токсини виходять швидше, а також надає знеболювальну дію. 5-гідрокситриптофан, або 5-НТР, відновлює здоровий сон, порушений інтоксикацією, та покращує емоційне тло.РекомендуєтьсяЯк біологічно активна добавка до їжі - джерела бурштинової кислоти і танінів, додаткового джерела вітаміну С і пантотенової кислоти, що містить 5-гідрокситриптофан.Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність, годування груддю. Перед застосуванням рекомендується проконсультуватися з лікарем.Спосіб застосування та дозиДорослим приймати по 2 таблетки щодня під час їжі. Тривалість прийому – 2 тижні. За потреби прийом можна повторити.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаСкладається з екстрактів лікарських рослин (пророщені плоди розторопші, квітки безсмертника, трави звіробою, горця пташиного (спориш), листя брусниці, мучниці, кропиви, капусти білокачанної, коріння солодки, і оману, незамінних амінокислот (метіон). , лимонна), вітамінів (С, В), фруктози, полівінілпіролідону, солей калію, натрію бікорбонату, природних ароматизаторів та коректорів смаку.Опис лікарської формиПорошок для приготування розчину для вживання.Фармакотерапевтична групаЗагальнозміцнюючий фітозасіб має протиалкогольну, дезінтоксикаційну, седативну, гепатопротекторну, вегетостабілізуючу, антидепресантну дію, додаткове джерело вітамінів, амінокислот, органічних кислот і флавоноїдів. Перешкоджає сп'яненню, швидше знижує рівень алкоголю в організмі та допомагає вийти зі стану сп'яніння, знімає головний біль, нудоту, відновлює координацію руху та інші порушення при сп'яненні. Прискорює роботу печінки, виводить з організму токсини, знижує патологічний потяг до алкоголю. Усуває головний біль, не пов'язані з прийомом алкоголю, наприклад, при мігрені.Показання до застосуванняЗняття похмільного синдрому.Протипоказання до застосуванняІндивідуальна нестерпність компонентів препарату.Побічна діяАлергічні реакції.Спосіб застосування та дозиДорослим по 1 пакетику порошку (2,5 г) 2-3 десь у день під час їжі, попередньо розчинивши 100 мл кип'яченої води. Тривалість прийому – 3-5 днів, при необхідності прийом можна повторити.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаАскорбінова кислота, холіну бітартрат, лецитин, бурштинова кислота, таурин, екстракт плодів розторопші плямистої, екстракт листя артишока, цистеїн, метіонін, ресвератрол, L-карнітин, піридоксину гідрохлорид, тіаміну гідрохлорид, оболонка капсули (ХарактеристикаБіологічно активна добавка до їжі, джерело силімарину, ресвератролу, бурштинової кислоти, таурину, додаткове джерело вітамінів С, В1, В6, що містить холін. Не є ліками.Протипоказання до застосуванняІндивідуальна нестерпність компонентів.Спосіб застосування та дозиДорослим по 2 капсулі 1 раз на день за 20-30 хвилин до їди або через 40-60 хвилин після їди. Тривалість прийому: 4-6 тижнів. За потреби прийом можна повторити. Можливі повторні прийоми протягом року.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковка1 капс. містить: екстракти імбиру, елеутерококу, солодки, гуарани, женьшеню, мате, лимонну кислоту, бурштинову кислоту. У упаковці 5 шт.ХарактеристикаКапсули Антидринк – на основі натуральних компонентів допоможуть швидко вивести алкоголь з організму, а заодно впоратися з синдромом похмілля та небажаними наслідками надмірного вживання алкоголю: головним болем, серцево-судинними порушеннями, спрагою, нудотою, тремтінням, запамороченням, втомою та координацією. Антидринк прискорює обмін речовин та виведення алкоголю з організму, знижує прояви алкогольної інтоксикації, полегшує вихід із похмілля, дозволяє скоротити час між прийняттям алкоголю та керуванням автомобіля.РекомендуєтьсяАбстинентний синдром.Протипоказання до застосуванняІндивідуальна непереносимість компонентів Антидринк, вагітність, годування груддю. Перед застосуванням проконсультуватися з лікарем.Побічна діяАлергічні реакції.Спосіб застосування та дозиАнтидринк приймають внутрішньо по 3 – 5 капсул на день під час їжі, одночасно.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаФруктове пюре, янтарна, фумарова, аскорбінова кислоти, глутамат натрію, цукрозамінник Е951, ароматизатор натуральний або ідентичний натуральному.ХарактеристикаЖувальні фруктові пастилки "Антипохмелін" допоможуть уникнути отруєння алкоголем, мінімізувати похмільний синдром та відчувати себе бадьорим та здоровим. Оптимізують обмінні процеси на тканинному рівні, сприяє прискореній та ефективній переробці алкоголю та продуктів його перетворення, також відновлюють процеси обміну вуглеводів, порушені в результаті алкогольного ексцесу, перешкоджає розвитку алкогольного токсикозу. Дія активних компонентів антипохмеліну клінічно доведена!ІнструкціяДорослим по 2 пастилки до, під час та після вживання алкоголю, всього 6-8 пастилок залежно від кількості прийнятого спиртного.Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність, годування груддю.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаКраплі - 100 гр. Активні речовини: Acidum sulfuricum (ацидум сульфурикум) D4, Acidum arsenicosum (Arsenicum album) (ацидум арсенікозум (арсенікум альбум)) D8, Lycopodium clavatum (Lycopodium) (лікоподиум (Стрихнос нукс-вімка) D6, Sulfur (сульфур) D12; Допоміжні речовини: спирту етилового (етанолу) близько 20% (за обсягом). По 25 мл у флакон-крапельницю темного скла з пробками (крапельницею або глухою) і кришкою з поліетилену, що нагвинчується.
Фасування: N6 Форма випуску таб. розчинні Упаковка: банку Виробник: ОФМ ТОВ Завод-виробник: Малкут ЗАТ(Білорусь). .
262,00 грн
155,00 грн
Склад, форма випуску та упаковкаПігулки - 1 таб. Активна речовина: Янтарна кислота 200 мг; Селен 70 мкг; Дигідрокверцетин – 3 мг; Допоміжні речовини: декстроза, лимонна кислота, карбонат натрію, мальтодекстрин, поліетиленгліколь, ароматизатор, сукралоза. Пігулки шипучі масою 4 г з ароматом апельсин/лимон 10 шт.ХарактеристикаЗавдяки антиоксидантам-бурштинової кислоти та органічного селену-Далімаг, що входять до складу, надає комплексну дію на організм людини, зменшує токсичну дію алкоголю, прискорює процес окислення етанолу та виведення з організму токсичних речовин, захищає клітини печінки, крові, серця, головного мозку від ураження токсичними речовинами. та їх отруйної дії. Зменшує спиртовий "вихлоп" при диханні. Далімаг може бути використаний з метою тонізуючого енергетичного напою для поліпшення самопочуття, підвищення бадьорості, зняття втоми та поганого самопочуття за несприятливих метеоумов, а також у разі високого рівня задимлення та утримання в повітрі СО2, важких металів та інших забруднювачів повітря.РекомендуєтьсяРекомендується як біологічно активна добавка до їжі - додаткового джерела селену, джерела бурштинової кислоти, що містить дигідрокверцетин.Протипоказання до застосуванняІндивідуальна непереносимість компонентів препарату, вагітність, годування груддю, порушення вуглеводного обміну.Спосіб застосування та дози1 таблетку розчинити у 200 мл води кімнатної температури. Приймати дорослим 1 раз на день під час їжі. Тривалість прийому – 1 місяць.Запобіжні заходи та особливі вказівкиПеред застосуванням рекомендується проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Активна речовина: Янтарна кислота 200 мг; Селен 70 мкг; Дигідрокверцетин – 3 мг; Допоміжні речовини: декстроза, лимонна кислота, карбонат натрію, мальтодекстрин, поліетиленгліколь, ароматизатор, сукралоза. Пігулки шипучі масою 4 г з ароматом лайма 10 шт.ХарактеристикаЗавдяки антиоксидантам-бурштинової кислоти та органічного селену-Далімаг, що входять до складу, надає комплексну дію на організм людини, зменшує токсичну дію алкоголю, прискорює процес окислення етанолу та виведення з організму токсичних речовин, захищає клітини печінки, крові, серця, головного мозку від ураження токсичними речовинами. та їх отруйної дії. Зменшує спиртовий "вихлоп" при диханні. Далімаг може бути використаний з метою тонізуючого енергетичного напою для поліпшення самопочуття, підвищення бадьорості, зняття втоми та поганого самопочуття за несприятливих метеоумов, а також у разі високого рівня задимлення та утримання в повітрі СО2, важких металів та інших забруднювачів повітря.РекомендуєтьсяРекомендується як біологічно активна добавка до їжі - додаткового джерела селену, джерела бурштинової кислоти, що містить дигідрокверцетин.Протипоказання до застосуванняІндивідуальна непереносимість компонентів препарату, вагітність, годування груддю, порушення вуглеводного обміну.Спосіб застосування та дози1 таблетку розчинити у 200 мл води кімнатної температури. Приймати дорослим 1 раз на день під час їжі. Тривалість прийому – 1 місяць.Запобіжні заходи та особливі вказівкиПеред застосуванням рекомендується проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
Фасування: N10 Форма випуску таб. шипучі Упаковка: туба Производитель: Пез Продакшн Юроп Кфт Завод-производитель: Pez Production Europe Kft(Венгрия). .
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
375,00 грн
343,00 грн
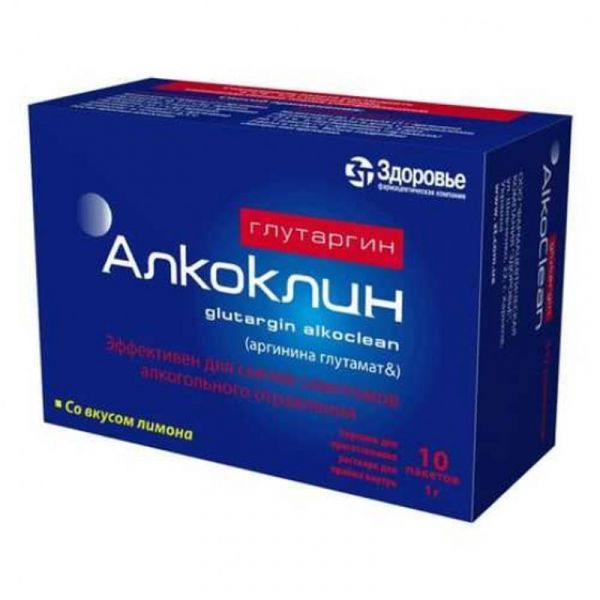
Склад, форма випуску та упаковкаПорошок - 1 пак. активний інгредієнт: аргініну глутамату (у перерахунку на 100% речовину) 1,0 г; допоміжні речовини: гліцин 0,50 г, манітол (Е 421) 0,79 г, лимонна кислота (безводна) 0,60 г, аспартам (Е 951) 0,06 г, ароматизатор "Лимон" 0,05 г. По 3 г порошку (1 г аргініну глутамату) у пакет (№ 1) або в спарені пакети (№ 2); по два, п'ять чи десять пакетів (№ 1) або по п'ять спарених пакетів (№ 2) у пачці з картону.Опис лікарської формиПорошок від білого до білого із жовтуватим відтінком кольору з фруктовим запахом.Фармакотерапевтична групаГепатопротекторний засіб.ФармакокінетикаЧи не вивчалася.ФармакодинамікаГлутаргін алкоклін є сполукою аргініну та глутамінової кислоти, які відіграють важливу роль у забезпеченні біохімічних процесів нейтралізації та виведення з організму високотоксичного метаболіту обміну азотистих речовин – аміаку. Має гепатопротекторну дію, володіючи антиоксидантною, антитоксичною та мембраностабілізуючою активністю, позитивно впливає на процеси енергозабезпечення в гепатоцитах. При алкогольній інтоксикації Глутаргін алкоклін стимулює утилізацію алкоголю в монооксигеназній системі печінки, попереджає пригнічення ключового ферменту утилізації етанолу – алкогольдегідрогенази; прискорює інактивацію та виведення токсичних продуктів метаболізму етанолу внаслідок збільшення утворення та окислення бурштинової кислоти; знижує пригнічуючий вплив алкоголю на ЦНС за рахунок нейромедіаторних властивостей збуджуючої глутамінової кислоти. Глутаргін алкоклін не виявляє ембріотоксичних, гонадотоксичних та мутагенних ефектів, не викликає алергічних та імунотоксичних реакцій.Показання до застосуванняПрофілактика сп'яніння та гепатотоксичної дії алкоголю. Лікування гострої алкогольної інтоксикації легкого та середнього ступеня тяжкості, а також у складі комплексної терапії постинтоксикаційних розладів після гострого алкогольного отруєння тяжкого ступеня.Протипоказання до застосуванняПідвищена чутливість до компонентів препарату; дитячий вік до 18 років; період вагітності та годування груддю; фенілкетонурія, оскільки препарат містить аспартам. З обережністю: гарячковий стан; підвищена збудливість; тяжкі порушення фільтраційної (азотовиділюючої) функції нирок (кліренс креатиніну менше 30 мл/хв).Побічна діяРідко можуть спостерігатися почуття легкого дискомфорту в епігастральній ділянці та нудота безпосередньо після застосування препарату, що проходять самостійно.Взаємодія з лікарськими засобамиСлід бути обережним при поєднанні препарату Глутаргін з наступними лікарськими засобами: амінофілін підвищує концентрацію ендогенного інсуліну в крові під впливом Глутаргіну алкокліну. Глутаргін алкоклін може посилювати ефект антиагрегантних засобів (дипіридамол та ін), попереджає та послаблює нейротоксичні явища, які можуть виникати при терапії ізоніазидом, послаблює ефект вінбластину.Спосіб застосування та дозиПрепарат призначають дорослим внутрішньо, незалежно від їди, попередньо розчинивши пакет в 1/4-1/2 склянки води. Для профілактики сп'яніння та гепатотоксичної дії алкоголю призначають 2 пакети (2 г аргініну глутамату) за 1-2 год до прийому алкоголю або 1 пакет (1 г аргініну глутамату) за 1 год до прийому алкоголю та 1 пакет (1 г аргініну глутамату) протягом 0,5 години після прийому алкоголю. Для лікування гострої алкогольної інтоксикації легкої та середньої тяжкості призначають по 1 пакету (1 г аргініну глутамату) 4 рази на день з інтервалами 1-2,5 год, у наступні 2-3 дні – по 1 пакету (1 г аргініну глутамату) 2 рази на добу. При алкогольному отруєнні тяжкого ступеня після курсу внутрішньовенного застосування препарату Глутаргін призначають по 1 пакету (1 г аргініну глутамату) Глутаргіну алкокліну 2 рази на добу протягом 20 днів у складі комплексної терапії.ПередозуванняСимптоми: нудота, блювання, біль у ділянці грудної клітки, відчуття дискомфорту в епігастральній ділянці, безсоння, минуще короткочасне зниження артеріального тиску, атріовентрикулярна блокада, алергічні реакції. Лікування: симптоматичне, при необхідності прийом антигістамінних засобів, у тяжких випадках – внутрішньовенне введення глюкокортикостероїдів.Запобіжні заходи та особливі вказівкиПри призначенні пацієнтам з порушеннями функцій ендокринних залоз слід враховувати, що препарат може незначно збільшувати секрецію інсуліну та гормону росту, що не потребує корекції медикаментозної терапії у пацієнтів із цукровим діабетом та/або акромегалією. Вплив на здатність до керування автотранспортом та управління механізмами Препарат не впливає на здатність керувати транспортними засобами.Умови відпустки з аптекБез рецептаВідео на цю тему
242,00 грн
207,00 грн
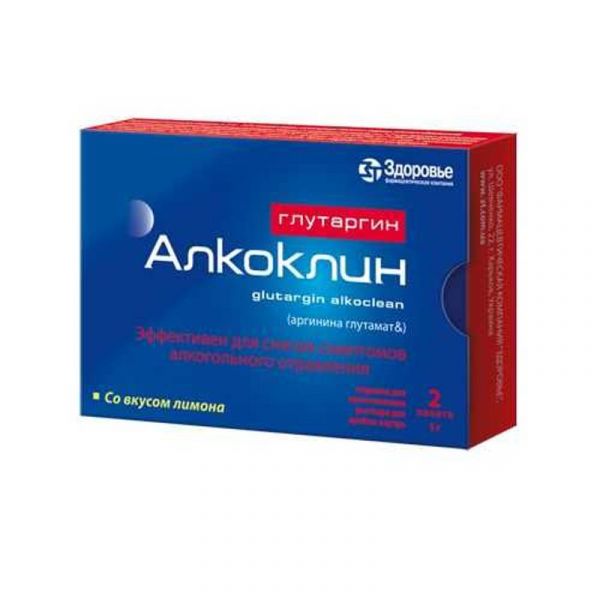
Склад, форма випуску та упаковкаПорошок - 1 пак. активний інгредієнт: аргініну глутамату (у перерахунку на 100% речовину) 1,0 г; допоміжні речовини: гліцин 0,50 г, манітол (Е 421) 0,79 г, лимонна кислота (безводна) 0,60 г, аспартам (Е 951) 0,06 г, ароматизатор "Лимон" 0,05 г. По 3 г порошку (1 г аргініну глутамату) у пакет (№ 1) або в спарені пакети (№ 2); по два, п'ять чи десять пакетів (№ 1) або по п'ять спарених пакетів (№ 2) у пачці з картону.Опис лікарської формиПорошок від білого до білого із жовтуватим відтінком кольору з фруктовим запахом.Фармакотерапевтична групаГепатопротекторний засіб.ФармакокінетикаЧи не вивчалася.ФармакодинамікаГлутаргін алкоклін є сполукою аргініну та глутамінової кислоти, які відіграють важливу роль у забезпеченні біохімічних процесів нейтралізації та виведення з організму високотоксичного метаболіту обміну азотистих речовин – аміаку. Має гепатопротекторну дію, володіючи антиоксидантною, антитоксичною та мембраностабілізуючою активністю, позитивно впливає на процеси енергозабезпечення в гепатоцитах. При алкогольній інтоксикації Глутаргін алкоклін стимулює утилізацію алкоголю в монооксигеназній системі печінки, попереджає пригнічення ключового ферменту утилізації етанолу – алкогольдегідрогенази; прискорює інактивацію та виведення токсичних продуктів метаболізму етанолу внаслідок збільшення утворення та окислення бурштинової кислоти; знижує пригнічуючий вплив алкоголю на ЦНС за рахунок нейромедіаторних властивостей збуджуючої глутамінової кислоти. Глутаргін алкоклін не виявляє ембріотоксичних, гонадотоксичних та мутагенних ефектів, не викликає алергічних та імунотоксичних реакцій.Показання до застосуванняПрофілактика сп'яніння та гепатотоксичної дії алкоголю. Лікування гострої алкогольної інтоксикації легкого та середнього ступеня тяжкості, а також у складі комплексної терапії постинтоксикаційних розладів після гострого алкогольного отруєння тяжкого ступеня.Протипоказання до застосуванняПідвищена чутливість до компонентів препарату; дитячий вік до 18 років; період вагітності та годування груддю; фенілкетонурія, оскільки препарат містить аспартам. З обережністю: гарячковий стан; підвищена збудливість; тяжкі порушення фільтраційної (азотовиділюючої) функції нирок (кліренс креатиніну менше 30 мл/хв).Побічна діяРідко можуть спостерігатися почуття легкого дискомфорту в епігастральній ділянці та нудота безпосередньо після застосування препарату, що проходять самостійно.Взаємодія з лікарськими засобамиСлід бути обережним при поєднанні препарату Глутаргін з наступними лікарськими засобами: амінофілін підвищує концентрацію ендогенного інсуліну в крові під впливом Глутаргіну алкокліну. Глутаргін алкоклін може посилювати ефект антиагрегантних засобів (дипіридамол та ін), попереджає та послаблює нейротоксичні явища, які можуть виникати при терапії ізоніазидом, послаблює ефект вінбластину.Спосіб застосування та дозиПрепарат призначають дорослим внутрішньо, незалежно від їди, попередньо розчинивши пакет в 1/4-1/2 склянки води. Для профілактики сп'яніння та гепатотоксичної дії алкоголю призначають 2 пакети (2 г аргініну глутамату) за 1-2 год до прийому алкоголю або 1 пакет (1 г аргініну глутамату) за 1 год до прийому алкоголю та 1 пакет (1 г аргініну глутамату) протягом 0,5 години після прийому алкоголю. Для лікування гострої алкогольної інтоксикації легкої та середньої тяжкості призначають по 1 пакету (1 г аргініну глутамату) 4 рази на день з інтервалами 1-2,5 год, у наступні 2-3 дні – по 1 пакету (1 г аргініну глутамату) 2 рази на добу. При алкогольному отруєнні тяжкого ступеня після курсу внутрішньовенного застосування препарату Глутаргін призначають по 1 пакету (1 г аргініну глутамату) Глутаргіну алкокліну 2 рази на добу протягом 20 днів у складі комплексної терапії.ПередозуванняСимптоми: нудота, блювання, біль у ділянці грудної клітки, відчуття дискомфорту в епігастральній ділянці, безсоння, минуще короткочасне зниження артеріального тиску, атріовентрикулярна блокада, алергічні реакції. Лікування: симптоматичне, при необхідності прийом антигістамінних засобів, у тяжких випадках – внутрішньовенне введення глюкокортикостероїдів.Запобіжні заходи та особливі вказівкиПри призначенні пацієнтам з порушеннями функцій ендокринних залоз слід враховувати, що препарат може незначно збільшувати секрецію інсуліну та гормону росту, що не потребує корекції медикаментозної терапії у пацієнтів із цукровим діабетом та/або акромегалією. Вплив на здатність до керування автотранспортом та управління механізмами Препарат не впливає на здатність керувати транспортними засобами.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаПігулки У 1 таблетці: активний інгредієнт: аргініну глутамату (у перерахунку на 100% речовину) 1,0 г. допоміжні речовини: целюлоза мікрокристалічна (МКЦ 101), кросповідон, стеарат кальцію.Опис лікарської формиТаблетки білого кольору, двоопуклі, довгастої форми з ризиком.ХарактеристикаУсуває причину алкогольної інтоксикації та захищає печінку та ЦНС від токсичної дії алкоголю. Може застосовуватися як для профілактики сп'яніння, так лікування алкогольної інтоксикації. Як сіллю двох амінокислот, АЛКОКЛІН Глутаргін добре переноситься і практично не викликає розвитку побічних ефектів.Фармакотерапевтична групаГепатопротекторний засіб.ФармакокінетикаЧи не вивчалася.ФармакодинамікаГлутаргін алкоклін є сполукою аргініну та глутамінової кислоти, які відіграють важливу роль у забезпеченні біохімічних процесів нейтралізації та виведення з організму високотоксичного метаболіту обміну азотистих речовин – аміаку. Має гепатопротекторну дію, володіючи антиоксидантною, антигіпоксичною та мембраностабілізуючою активністю, позитивно впливає на процеси енергозабезпечення в гепатоцитах. При алкогольній інтоксикації Глутаргін алкоклін стимулює утилізацію алкоголю у монооксигеназній системі печінки, попереджає пригнічення ключового ферменту утилізації етанолу – алкогольдегідрогенази; прискорює інактивацію та виведення токсичних продуктів метаболізму етанолу внаслідок збільшення утворення та окислення бурштинової кислоти; знижує пригнічуючий вплив алкоголю на ЦНС за рахунок нейромедіаторних властивостей збуджуючої глутамінової кислоти. Глутаргін алкоклін не виявляє ембріотоксичних, гонадотоксичних та мутагенних ефектів, не викликає алергічних та імунотоксичних реакцій.Показання до застосуванняПрофілактика сп'яніння та гепатотоксичної дії алкоголю. Лікування гострої алкогольної інтоксикації легкого та середнього ступеня тяжкості, а також у складі комплексної терапії постинтоксикаційних розладів після гострого алкогольного отруєння тяжкого ступеня.Протипоказання до застосуванняпідвищена чутливість до компонентів препарату дитячий вік до 18 років період вагітності та годування груддю фенілкетонурія, оскільки препарат містить аспартамПобічна діяРідко можуть спостерігатися почуття легкого дискомфорту в епігастральній ділянці та нудота безпосередньо після застосування препарату, що проходять самостійно.Взаємодія з лікарськими засобамиСлід бути обережним при поєднанні препарату Глутаргін з наступними лікарськими засобами: амінофілін підвищує концентрацію ендогенного інсуліну в крові під впливом Глутаргіну алкокліну. Глутаргін алкоклін може посилювати ефект антиагрегантних засобів (дипіридамол та ін), попереджає та послаблює нейротоксичні явища, які можуть виникати при терапії ізоніазидом, послаблює ефект вінбластину.Спосіб застосування та дозиПрепарат призначають дорослим внутрішньо незалежно від їди. Для профілактики сп'яніння та гепатотоксичної дії алкоголю призначають по 2 таблетки (2 г) за 1-2 год до прийому алкоголю або 1 таблетку (1 г) за 1 год до прийому алкоголю та 1 таблетку (1 г) протягом 0,5 год після прийому алкоголю. Для лікування гострої алкогольної інтоксикації легкої та середньої тяжкості призначають по 1 таблетці (1 г) 4 рази на день з інтервалами 1–2,5 години, у наступні 2–3 дні – по 1 таблетці 2 рази на добу. При алкогольному отруєнні тяжкого ступеня після курсу внутрішньовенного застосування препарату Глутаргіна призначають по 1 таблетці (1 г) Глутаргіну алкокліну 2 рази на добу протягом 20 днів у складі комплексної терапії.ПередозуванняСимптоми: нудота, блювання, біль у ділянці грудної клітки, відчуття дискомфорту в епігастральній ділянці, безсоння, минуще короткочасне зниження артеріального тиску, атріовентрикулярна блокада, алергічні реакції. Лікування: симптоматичне, при необхідності прийом антигістамінних засобів, у тяжких випадках – внутрішньовенне введення глюкокортикостероїдів.Запобіжні заходи та особливі вказівкиЗ обережністю: гарячковий стан підвищена збудливість тяжкі порушення фільтраційної (азотовидільної) функції нирок (кліренс креатиніну менше 30 мл/хв)Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. активний інгредієнт: аргініну глутамату (у перерахунку на 100% речовину) 1,0 г; допоміжні речовини: целюлоза мікрокристалічна (МКЦ 101) 0,110 г, кросповідон 0,020 г, кальцію стеарат 0,010 г. По 1 або 10 таблеток у контурній комірковій упаковці. По 2 контурні коміркові упаковки по 1 таблетці або 1 контурна коміркова упаковка по 10 таблеток разом з інструкцією з медичного застосування в пачці з картону.Опис лікарської формиТаблетки білого кольору, двоопуклі, довгастої форми з ризиком.Фармакотерапевтична групаГепатопротекторний засіб.ФармакокінетикаЧи не вивчалася.ФармакодинамікаГлутаргін алкоклін є сполукою аргініну та глутамінової кислоти, які відіграють важливу роль у забезпеченні біохімічних процесів нейтралізації та виведення з організму високотоксичного метаболіту обміну азотистих речовин – аміаку. Має гепатопротекторну дію, володіючи антиоксидантною, антигіпоксичною та мембраностабілізуючою активністю, позитивно впливає на процеси енергозабезпечення в гепатоцитах. При алкогольній інтоксикації Глутаргін алкоклін стимулює утилізацію алкоголю в монооксигеназній системі печінки, попереджає пригнічення ключового ферменту утилізації етанолу – алкогольдегідрогенази; прискорює інактивацію та виведення токсичних продуктів метаболізму етанолу внаслідок збільшення утворення та окислення бурштинової кислоти; знижує пригнічуючий вплив алкоголю на ЦНС за рахунок нейромедіаторних властивостей збуджуючої глутамінової кислоти. Глутаргін алкоклін не виявляє ембріотоксичних, гонадотоксичних та мутагенних ефектів, не викликає алергічних та імунотоксичних реакцій.Показання до застосуванняЗменшення симптомів алкогольного сп'яніння та абстинентного стану, у тому числі у профілактичних цілях. Профілактика гепатотоксичної дії алкоголю.Протипоказання до застосуванняПідвищена чутливість до компонентів препарату; дитячий вік до 18 років; період вагітності та годування груддю. З обережністю: гарячковий стан; підвищена збудливість; тяжкі порушення фільтраційної (азотовидільної) функції нирок (кліренс креатиніну менше 30 мл/хв)Побічна діяРідко можуть спостерігатися почуття легкого дискомфорту в епігастральній ділянці та нудота безпосередньо після застосування препарату, що проходять самостійно.Взаємодія з лікарськими засобамиСлід бути обережним при поєднанні препарату Глутаргін з наступними лікарськими засобами: амінофілін підвищує концентрацію ендогенного інсуліну в крові під впливом Глутаргіну алкокліну. Глутаргін алкоклін може посилювати ефект антиагрегантних засобів (дипіридамол та ін), попереджає та послаблює нейротоксичні явища, які можуть виникати при терапії ізоніазидом, послаблює ефект вінбластину.Спосіб застосування та дозиПрепарат призначають дорослим внутрішньо незалежно від їди. Для профілактики сп'яніння та гепатотоксичної дії алкоголю призначають по 2 таблетки (2 г) за 1-2 год до прийому алкоголю або 1 таблетку (1 г) за 1 год до прийому алкоголю та 1 таблетку (1 г) протягом 0,5 год після прийому алкоголю.ПередозуванняСимптоми: нудота, блювання, біль у ділянці грудної клітки, відчуття дискомфорту в епігастральній ділянці, безсоння, минуще короткочасне зниження артеріального тиску, атріовентрикулярна блокада, алергічні реакції. Лікування: симптоматичне, при необхідності прийом антигістамінних засобів, у тяжких випадках – внутрішньовенне введення глюкокортикостероїдів.Запобіжні заходи та особливі вказівкиПри призначенні пацієнтам з порушеннями функцій ендокринних залоз слід враховувати, що препарат може незначно збільшувати секрецію інсуліну та гормону росту, що не потребує корекції медикаментозної терапії у пацієнтів із цукровим діабетом та/або акромегалією. Вплив на здатність до керування автотранспортом та управління механізмами Препарат не впливає на здатність керувати транспортними засобами.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаСорбіт (носій), екстракт трави зеленого вівса, гліцин, діоксид кремнію аморфний та стеарат кальцію (агенти антистежують), альгінат натрію (носій), екстракт пуерарії (кудзу), стеаринова кислота рослинного походження (агент антистеджуючий), м'ятна олія, ). Містить підсолоджувач сорбіт, який при надмірному вживанні може мати проносну дію. Вміст у 30 таблетках (добовому прийомі) та % від рекомендованого рівня добового споживання (адекватного рівня) Екстракт трави зеленого вівса в тому числі ізовітексин, не менше 1 1800 мг 10,8 мг 108 %2 М'ятна олія 21 мг - Екстракт пуерарії (кудзу) 150 мг - Гліцин не менше 1 1050 мг 30% В упаковці 100 пігулок по 0,53 г. ХарактеристикаБудь-якій людині, яка бажає кинути палити, дуже важко зробити це самостійно. Причина в тому, що в організмі курця формуються складні фізіологічні процеси, що викликають потяг до куріння. Корида допоможе тим, хто вирішив кинути палити.Властивості компонентівЕкстракт вівса з трави, зібраної в період цвітіння, містить найбільшу кількість біологічно активних речовин, що сприятливо впливають на нервову систему і сприяють виробленню у курця сталого зниження потягу до тютюнопаління. Оновлений склад Корида містить екстракт вівса як основний біологічно активний компонент, що сприяє відвиканню від куріння і підтримує організм у момент, коли важко розлучитися зі шкідливою звичкою. Зниження потягу до куріння при застосуванні Кориди відбувається за рахунок природних для організму умовно-рефлекторних реакцій. Крім того, в період відвикання від куріння екстракт вівса сприяє покращенню функціонального стану шлунково-кишкового тракту та печінки. Масло м'яти перцевої надає м'яку заспокійливу дію та сприяє притоку кисню до клітин та тканин. Ментол, що міститься в м'ятній олії, стимулює дихальний центр та периферичні нейрорецептори слизових оболонок, що посилює капілярний кровообіг, покращує харчування бронхолегеневої тканини. Гліцин – одна з перших амінокислот, виділених із природних джерел. Вона була відкрита як продукт гідролізу тваринного клею (білка желатину). Гліцин відноситься до групи замінних амінокислот. Ця речовина міститься у всіх тканинах організму, особливо багато його в головному та спинному мозку. Він бере участь у ряді важливих для організму процесів, будучи попередником креатиніну, пуринів, цукрів, глутатіону та деяких гормонів. Гліцин має стресопротекторну, антистресорну, ноотропну, седативну та детоксикувальну дію. Бере участь у процесах обміну речовин. І саме на цьому ґрунтується його лікувальний вплив на організм. Пуерарія дольчаста - Pueraria lobata (Willd.). Інші назви – пуерарія волосиста, кудзу. Дерев'яниста листопадна ліана сімейства бобових - Fabaceae. З лікувальною метою використовують коріння, листя, квіти та рідше боби. Ізофлавоноїди коренів рослини – дайдзін, дайдзеїн, пуерарин, біоханін А та геністеїн діють як пастки вільних радикалів, інгібують перекисне окиснення лінолевої кислоти та активність ліпоксигенази. Пуерарія активує обмінні процеси у головному мозку, покращує пам'ять. У східній медицині коріння пуерарії пайчастої використовують у лікуванні алкогольної та нікотинової залежності, для зниження артеріального тиску, при захворюваннях, пов'язаних з порушенням кровообігу в головному мозку, серці та скелетних м'язах, для лікування діареї, мігрені, кору, алергічних захворювань,як жарознижувальний і відхаркувальний засіб. Експериментально доведено протизапальну, аналгетичну та міорелаксантну активність ізофлавоноїдів кудзу та їх метаболітів.РекомендуєтьсяРекомендації щодо застосування Кориди як засіб для зниження потягу до тютюнопаління та відвикання від тютюну в осіб з нікотиновою залежністю засновані на результатах клінічних досліджень. Тривалість періоду «кидання» — до зняття нікотинової залежності — залежить від індивідуальних можливостей організму і зажадав від психологічного настрою. Таблетки бажано завжди мати при собі протягом усього періоду «кидання», щоб своєчасно перервати бажання закурити. Дотримуйтесь рекомендацій щодо застосування. Курс прийому має бути не менше 4 тижнів. Для успішного вирішення поставленого завдання, крім ефективності препарату, потрібна і ваша організованість – не зупиняйтесь на половині шляху, доведіть розпочате до кінця.Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність, годування груддю. Перед застосуванням слід проконсультуватися з лікарем.Спосіб застосування та дозиДорослим по 1 таблетці до 30 разів на день, розсмоктуючи у роті до повного розчинення. Тривалість прийому – 1 місяць. При необхідності курс прийому можна повторити.Умови відпустки з аптекБез рецептаВідео на цю тему
Дозування: 500 мг Фасування: N30 Форма випуску таб. Упаковка: блістер Виробник: СіЕсСі ЛТД Завод-виробник: Baldacci Laboratoire spa(Італія) Діюча речовина: Метадоксин. .
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
Склад, форма випуску та упаковкаЕкстракт розторопші плямистої, екстракт кореня куркуми, екстракт гуарани, екстракт кореня кудзу, екстракт листя шовковиці, екстракт, цибульний екстракт, ФО (Ферментована ламінарія), мед (цукрозамінник).ХарактеристикаСприяє лікуванню похмілля; Полегшує головний біль та мігрень; Зменшує неприємний запах з рота та спрагу після прийняття спиртного; Захищає та покращує функцію печінки; Сприяє покращенню розкладання алкоголю; Покращує загальну концентрацію; Знімає стрес;Фармакотерапевтична групаЗасіб від похмілля, має протверезний ефект.Властивості компонентівЕкстракт розторопші плямистої (діючий інгредієнт, є антиоксидантом у 10 разів сильнішим, ніж вітамін E. запобігає ранньому розвитку алкогольної хвороби печінки. захищає мембрани клітин печінки та відновлює клітини печінки); Екстракт кореня куркуми (захищає клітини печінки і сприяє жовчоутворенню. захищає травний тракт і має загоювальну дію. покращує стан жирів (наприклад, контроль рівня холестерину) і запобігає ураженню травної системи, що викликається вживанням алкоголю); Екстракт гуарани (зміцнює нерви. знімає втому. полегшує: втому, головний біль, мігрень. запобігає ураженню травної системи, що викликається вживанням алкоголю); Екстракт кореня кудзу (знімає: жар, головний біль, підвищений кров'яний тиск. полегшує: головний біль, м'язовий біль, спричинений потовиділенням. сприяють лікуванню похмільного синдрому); Екстракт листя шовковиці (містить вітаміни A, B1, B2 та D. покращує функцію кишечника. сприяє зняттю спраги, полегшенню болю в животі, діареї); Екстракт вільхи (багатий танінами, тритерпеноїдами та флавоноїдами. виводить токсини та захищає печінку. сприяє лікуванню таких форм алкогольної хвороби печінки, як гепатит, цироз, стеатоз); Цибулевий екстракт (знижує рівень холестерину та жирів у крові. виводить токсини з печінки та кишечника (містить глутатіон). знижує рівень жирів у печінці та кишечнику та знімає втому. сприяє засвоєнню вітаміну B); ФЛ (Ферментована ламінарія) (підсилює загальний протипохмільний ефект. активізує клітини мозку. знімає стрес. покращує концентрацію);Протипоказання до застосуванняІндивідуальна нестерпність компонентів.Спосіб застосування та дозиЗастосування по 100мл. Приймати до та (або) після вживання спиртних напоїв сприяє зниженню похмільного синдрому вранці.Запобіжні заходи та особливі вказівкиПеред застосуванням рекомендується проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
Фасування: N7 Форма випуску: пластир трансдермальний Упакування: упак. Виробник: Джонсон & Джонсон Завод-виробник: McNeil AB(Швеція) Действующее вещество: Никотин. .
Фасовка: N7 Форма выпуска: пластырь трансдермальный Упаковка: упак. Производитель: Джонсон & Джонсон Завод-производитель: McNeil AB(Швеция) Действующее вещество: Никотин. .
959,00 грн
926,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
733,00 грн
686,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
590,00 грн
543,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
595,00 грн
552,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
413,00 грн
363,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
429,00 грн
395,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
429,00 грн
388,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
296,00 грн
248,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
294,00 грн
248,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
426,00 грн
395,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
433,00 грн
224,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
341,00 грн
163,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
392,00 грн
363,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
414,00 грн
381,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
651,00 грн
404,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
Склад, форма випуску та упаковкаКраплі - 100 р.: Активні речовини: Антитіла до мозковоспецифічного білка S-100 афінно очищені – 1,0 г*; Допоміжні речовини: спирт етиловий 95% 21,8г, вода очищена 77,2г. * Вводяться у вигляді водно-спиртової суміші з вмістом не більше 10-1991 нг/г активної форми діючої речовини. По 25 мл у флакони зі скла марки ОС, або у флакони з пофарбованого скла, закупорені полімерними пробками з дозуючим пристроєм (крапельницею) і кришками полімерними гвинтовими з контролем першого розтину. Кожен флакон разом з інструкцією з медичного застосування поміщають у пачку з картону.Опис лікарської формиБезбарвна прозора рідина із характерним спиртовим запахом.Фармакотерапевтична групаАлкоголізму засобу лікування.ФармакодинамікаПрепарат модифікує функціональну активність білка S-100, що здійснює в мозку поєднання інформаційних та метаболічних процесів. Сенситизує нейрональну мембрану, модулює синаптичну пластичність нейронів. Має модифікуючу дію на функціональний стан структур мозку, що беруть участь у формуванні алкогольної залежності: гіпоталамуса, гіпокампа та ін. При алкогольній залежності надає нормалізуючий вплив на систему позитивного емоційного підкріплення, що призводить до зниження частоти самостимуляції латерального гіпоталамуса. Знижує ниркову активність нейронів гіпокампу; зменшує кількість циркулюючих імунокомплексів у периферичній крові, що корелює зі зниженням споживання етанолу. Сприяє посиленню гальмівних впливів ГАМК у ЦНС. Експериментально встановлено,що препарат відновлює нейромедіаторний баланс та умовнорефлекторну діяльність. Підвищує стійкість мозку до гіпоксії та до токсичних впливів.Показання до застосуванняВиявляє протиалкогольну дію, зменшуючи потяг до алкоголю та знижуючи ймовірність рецидивів. Монотерапія алкогольного абстинентного синдрому легкого та середнього ступеня тяжкості. Препарат полегшує як психопатологічні порушення (занепокоєння, психічна напруга, безсоння, дратівливість, тривога, зниження настрою, інтенсивний потяг до спиртного), так і соматовегетативні розлади (слабкість, пітливість, головний біль, тремор, тахікардія, порушення травлення) алкогольного .Протипоказання до застосуванняПідвищена індивідуальна чутливість до компонентів препарату, вагітність та період лактації.Побічна діяМожливі реакції індивідуальної підвищеної чутливості до компонентів препарату.Взаємодія з лікарськими засобамиВипадків несумісності з іншими лікарськими засобами досі не виявлено.Спосіб застосування та дозиНа один прийом - 10 крапель у їдальні ложці води (не під час їди). У стані похмілля у перші 2 години препарат приймають по 10 крапель кожні 30 хвилин; у наступні 8 -10 годин – по 10 крапель на годину. У разі настання сну прийом поновлюють після пробудження. Надалі при поліпшенні стану препарат приймають по 10 крапель кожні 2-3 години (4-6 прийомів на добу) протягом 2-3 днів. При обтяженні симптомів алкогольної абстиненції необхідно приєднати лікарські засоби, які традиційно використовуються в детоксикації. Для профілактики рецидивів препарат приймають по 10 крапель 1-2 десь у добу протягом 2-3 місяців; після випадкового вживання алкоголю прийняти додатково 10 крапель препарату 2 рази – вдень та на ніч.ПередозуванняДо цього часу випадків передозування не спостерігалося.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Активні речовини: Антитіла до мозковоспецифічного білка S-100 афінно очищені – 0,003 г*; Допоміжні речовини: лактози моногідрат 0,267 г, целюлоза мікрокристалічна 0,03 г, стеарат магнію 0,003 г. * Наносяться на лактозу у вигляді водно-спиртової суміші з вмістом не більше КГ1991 нг/г активної форми діючої речовини. По 20 таблеток у контурній комірковій упаковці з плівки полівінілхлоридної та алюмінієвої фольги. По 1, 2 або 5 контурних осередкових упаковок разом з інструкцією з медичного застосування поміщають у пачку з картону.Опис лікарської формиПігулки плоскоциліндричної форми, з ризиком та фаскою, від білого до майже білого кольору. На плоскій стороні з ризиком нанесено напис MATERIA MEDICA, на іншій плоскій стороні нанесено напис PROPROTEN 100.Фармакотерапевтична групаАлкоголізму засобу лікування.ФармакодинамікаПрепарат модифікує функціональну активність білка S-100, що здійснює в мозку поєднання інформаційних та метаболічних процесів. Сенситизує нейрональну мембрану, модулює синаптичну пластичність нейронів. Має модифікуючу дію на функціональний стан структур мозку, що беруть участь у формуванні алкогольної залежності: гіпоталамуса, гіпокампа та ін. При алкогольній залежності надає нормалізуючий вплив на систему позитивного емоційного підкріплення, що призводить до зниження частоти самостимуляції латерального гіпоталамуса. Знижує ниркову активність нейронів гіпокампу; зменшує кількість циркулюючих імунокомплексів у периферичній крові, що корелює зі зниженням споживання етанолу. Сприяє посиленню гальмівних впливів ГАМК у ЦНС. Експериментально встановлено,що препарат відновлює нейромедіаторний баланс та умовнорефлекторну діяльність. Підвищує стійкість мозку до гіпоксії та до токсичних впливів.Показання до застосуванняВиявляє протиалкогольну дію, зменшуючи потяг до алкоголю та знижуючи ймовірність рецидивів. Монотерапія алкогольного абстинентного синдрому легкого та середнього ступеня тяжкості. Препарат полегшує як психопатологічні порушення (занепокоєння, психічна напруга, безсоння, дратівливість, тривога, зниження настрою, інтенсивний потяг до спиртного), так і соматовегетативні розлади (слабкість, пітливість, головний біль, тремор, тахікардія, порушення травлення) алкогольного .Протипоказання до застосуванняПідвищена індивідуальна чутливість до компонентів препарату, вагітність та період лактації.Побічна діяМожливі реакції підвищеної індивідуальної чутливості до компонентів препарату.Взаємодія з лікарськими засобамиВипадків несумісності з іншими лікарськими засобами досі не виявлено.Спосіб застосування та дозиНа один прийом - 1 таблетку тримати в роті до повного розчинення - (не під час їди). У стані похмілля перші 2 години препарат приймають по 1 таблетці кожні 30 хвилин; наступні 8 -10 годин – по 1 таблетці на годину. У разі настання сну прийом поновлюють після пробудження. Надалі при поліпшенні стану препарат приймають по 1 таблетці кожні 2-3 години (4-6 таблеток на добу) протягом 2-3 днів. При обтяженні симптомів алкогольної абстиненції необхідно приєднати лікарські засоби, які традиційно використовуються в детоксикації. Для профілактики рецидивів препарат приймають по 1-2 таблетки на добу протягом 2-3 місяців; після випадкового вживання алкоголю прийняти додатково 2 таблетки препарату 2 рази – вдень та на ніч.ПередозуванняПри випадковому передозуванні можливі диспепсичні явища, зумовлені наповнювачами, що входять до складу препарату.Запобіжні заходи та особливі вказівкиДо складу препарату входить лактози моногідрат, у зв'язку з чим його не рекомендується призначати пацієнтам з вродженою галактоземією, синдромом мальабсорбції глюкози або при вродженій лактазній недостатності.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Активні речовини: Антитіла до мозковоспецифічного білка S-100 афінно очищені – 0,003 г*; Допоміжні речовини: лактози моногідрат 0,267 г, целюлоза мікрокристалічна 0,03 г, стеарат магнію 0,003 г. * Наносяться на лактозу у вигляді водно-спиртової суміші з вмістом не більше КГ1991 нг/г активної форми діючої речовини. По 20 таблеток у контурній комірковій упаковці з плівки полівінілхлоридної та алюмінієвої фольги. По 1, 2 або 5 контурних осередкових упаковок разом з інструкцією з медичного застосування поміщають у пачку з картону.Опис лікарської формиПігулки плоскоциліндричної форми, з ризиком та фаскою, від білого до майже білого кольору. На плоскій стороні з ризиком нанесено напис MATERIA MEDICA, на іншій плоскій стороні нанесено напис PROPROTEN 100.Фармакотерапевтична групаАлкоголізму засобу лікування.ФармакодинамікаПрепарат модифікує функціональну активність білка S-100, що здійснює в мозку поєднання інформаційних та метаболічних процесів. Сенситизує нейрональну мембрану, модулює синаптичну пластичність нейронів. Має модифікуючу дію на функціональний стан структур мозку, що беруть участь у формуванні алкогольної залежності: гіпоталамуса, гіпокампа та ін. При алкогольній залежності надає нормалізуючий вплив на систему позитивного емоційного підкріплення, що призводить до зниження частоти самостимуляції латерального гіпоталамуса. Знижує ниркову активність нейронів гіпокампу; зменшує кількість циркулюючих імунокомплексів у периферичній крові, що корелює зі зниженням споживання етанолу. Сприяє посиленню гальмівних впливів ГАМК у ЦНС. Експериментально встановлено,що препарат відновлює нейромедіаторний баланс та умовнорефлекторну діяльність. Підвищує стійкість мозку до гіпоксії та до токсичних впливів.Показання до застосуванняВиявляє протиалкогольну дію, зменшуючи потяг до алкоголю та знижуючи ймовірність рецидивів. Монотерапія алкогольного абстинентного синдрому легкого та середнього ступеня тяжкості. Препарат полегшує як психопатологічні порушення (занепокоєння, психічна напруга, безсоння, дратівливість, тривога, зниження настрою, інтенсивний потяг до спиртного), так і соматовегетативні розлади (слабкість, пітливість, головний біль, тремор, тахікардія, порушення травлення) алкогольного .Протипоказання до застосуванняПідвищена індивідуальна чутливість до компонентів препарату, вагітність та період лактації.Побічна діяМожливі реакції підвищеної індивідуальної чутливості до компонентів препарату.Взаємодія з лікарськими засобамиВипадків несумісності з іншими лікарськими засобами досі не виявлено.Спосіб застосування та дозиНа один прийом - 1 таблетку тримати в роті до повного розчинення - (не під час їди). У стані похмілля перші 2 години препарат приймають по 1 таблетці кожні 30 хвилин; наступні 8 -10 годин – по 1 таблетці на годину. У разі настання сну прийом поновлюють після пробудження. Надалі при поліпшенні стану препарат приймають по 1 таблетці кожні 2-3 години (4-6 таблеток на добу) протягом 2-3 днів. При обтяженні симптомів алкогольної абстиненції необхідно приєднати лікарські засоби, які традиційно використовуються в детоксикації. Для профілактики рецидивів препарат приймають по 1-2 таблетки на добу протягом 2-3 місяців; після випадкового вживання алкоголю прийняти додатково 2 таблетки препарату 2 рази – вдень та на ніч.ПередозуванняПри випадковому передозуванні можливі диспепсичні явища, зумовлені наповнювачами, що входять до складу препарату.Запобіжні заходи та особливі вказівкиДо складу препарату входить лактози моногідрат, у зв'язку з чим його не рекомендується призначати пацієнтам з вродженою галактоземією, синдромом мальабсорбції глюкози або при вродженій лактазній недостатності.Умови відпустки з аптекБез рецептаВідео на цю тему
ХарактеристикаНабір. Пластирі призначені для боротьби із тютюновою залежністю. Не містять нікотину. Основна активна речовина – сонікотинель. Діє у 2-х напрямках: знижує потяг до нікотину - надходячи в клітини, сонікотинель зв'язується з нікотиновими рецепторами, конкурентно замінюючи нікотин, тим самим знижує потребу організму в ньому; очищає організм від токсинів, що накопичилися - впливаючи на дихальні центри, сонікотинель забезпечує активний виведення токсинів з легенів, тим самим очищаючи організм. Розмір: 5 см х 7,5 смУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаКапсули - 1 капс. Активні речовини: pinus (сосна, екстракт кори), Acinus semen extract, Lepidium meyenii (мака перуанська), Thymus serpyllum L. (тим'ян повзучий, екстракт), Vitamin C (вітамін С), Vitamin Е (вітамін Е), Zinc sulfate ( цинку, Vitamin В6 (вітамін В6), Vitamin В2 (вітамін В2), Vitamin В1 (вітамін В1), Selenium (селен); Допоміжні речовини: магнію оксид, цинку оксид, крохмаль картопляний; 36 штук в інд/упаковці.Фармакотерапевтична групаЗахисне.Дія на організмКомпоненти комплексу ефективно блокують негативні наслідки куріння на організм людини, сприяють його зміцненню та відновленню.Властивості компонентівЕкстракт кори сосни - містить пікногенол, найпотужніший антиоксидант, який захищає від негативного впливу вільних радикалів, покращує циркуляцію крові, запобігає набрякам, тромбозам вен, зменшує головний біль, втому, запаморочення та безсоння, уповільнює старіння шкіри. ефективний проти підвищеної тривожності. Екстракт виноградних кісточок - містить проантоціанідини, що знижують ушкодження клітин вільними радикалами, що дозволяє зміцнити імунну систему, запобігти серцево-судинним захворюванням, знизити ризик розвитку захворювань від дії токсинів та несприятливих екологічних наслідків. Мака перуанська – підвищує життєву енергію та витривалість, нормалізує гормональний дисбаланс, збільшує потенцію у чоловіків та бажання у жінок, перешкоджає процесам старіння організму. Чебрець повзучий - очищає верхні дихальні шляхи та легені, сприяє відходженню мокротиння та заспокоює болі, полегшує дихання, нормалізує травлення. Вітаміни С, Е – зміцнюють імунітет, нейтралізують вільні радикали, регулюють згортання крові, запобігають утворенню тромбів, стимулюють синтез колагену, зберігають молодість шкіри. Цинк - нормалізує обмін речовин, регулює діяльність репродуктивної системи та залоз внутрішньої секреції. Вітаміни В1, В2, В6 – підвищують стійкість організму до несприятливих факторів зовнішнього середовища. важливі для нормального функціонування нервової та кровоносної систем. Селен - знешкоджує найнебезпечніші та агресивніші вільні радикали, оберігає від отруєнь тютюновим димом, запобігає руйнуванню та некрозу печінки, виводячи з організму важкі метали.ІнструкціяПриймати препарат під час їди.РекомендуєтьсяЯк захист організму від шкоди активного та пасивного тютюнопаління.Протипоказання до застосуванняІндивідуальна непереносимість, вагітність та годування груддю.Вагітність та лактаціяПротипоказано.Спосіб застосування та дозиДорослим по 1 капсулі 1-2 десь у день.Умови відпустки з аптекБез рецептаВідео на цю тему
609,00 грн
187,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
2 001,00 грн
404,00 грн
Склад, форма випуску та упаковкаТаблетки, покриті плівковою оболонкою - 1 табл. активна речовина: налмефен гідрохлориду дигідрат - 21,917 мг. (у перерахунку на налмефен гідрохлорид - 20 мг; на налмефен - 18,06 мг); допоміжні речовини: МКЦ – 61,4 мг; лактоза безводна – 60,683 мг; кросповідон (тип А) - 4,5 мг; магнію стеарат – 1,5 мг; оболонка плівкова: Opadry OY-S-28849 білий (гіпромелоза (5мПа·с), макрогол 400, титану діоксид (Е171)) - 4,5 мг. Пігулки, покриті плівковою оболонкою, 18 мг. По 7 чи 14 табл. у контурній комірковій упаковці (блістері) з ПВХ/ПВДХ та фольги алюмінієвої. 1 бл. по 7 табл.; 1 чи 2 бл. по 14 табл. поміщають у картонну пачку.Опис лікарської формиОвальні, двоопуклі, білі пігулки, покриті плівковою оболонкою, з тисненням «S» на одній стороні.Фармакотерапевтична групаАнтиалкогольне.ФармакокінетикаВсмоктування. Після однократної пероральної дози 18,06 мг налмефен швидко всмоктується. Cmax у плазмі крові – 16,5 нг/мл – досягається приблизно через 1,5 год. Експозиція (AUC) становить 131 нг·ч/мл. Абсолютна біодоступність налмефен після прийому внутрішньо становить 41%. Одночасний прийом з їжею з високим вмістом жирів збільшує загальну експозицію (AUC) на 30% і Cmax на 50%, при цьому Tmax у плазмі збільшується на 30 хв, що не вважається клінічно значущим. Розподіл. Зв'язування із білками плазми становить близько 30%. Здається Vd - близько 3200 л. За даними, отриманими в ході дослідження позитронно-емісійною томографією (ПЕТ), після одноразового та повторного прийому налмефену у добовій дозі 18,06 мг зв'язування 94-100% рецепторів досягається вже через 3 години, що передбачає, що налмефен легко проникає через гематоенцефалічний бар'єр. Біотрансформація. При прийомі внутрішньо налмефен піддається екстенсивному метаболізму до основного метаболіту налмефен-3-О-глюкуроніду, головним чином під дією ізоферменту UGT2B7 та меншою мірою за рахунок ізоферментів UGT1A3 та UGT1A8. Відносно невелика кількість налмефен метаболізується до норналмефен під дією ізоферменту CYP3A4/5 і налмефен-3-О-сульфату сульфуванням. Норналмефен у свою чергу перетворюється на норналмефен-3-О-глюкуронід і норналмефен-3-О-сульфат. Метаболіти не вносять значних внесків у фармакодинамічні ефекти, пов'язані з впливом на опіоїдні рецептори у людей, за винятком налмефен-3-О-сульфату, який має порівнянну з налмефеном активність. Однак концентрація налмефен-3-Осульфату становить менше 10% від концентрації налмефену. Тому малоймовірно,що цей метаболіт робить значний внесок у розвиток фармакологічних ефектів налмефену. Виведення. Зв'язування з глюкуронідами є основним механізмом, що визначає кліренс налмефену. Ниркова екскреція є основним шляхом виведення налмефену та його метаболітів. 54% виводиться із сечею у вигляді налмефен-3-О-глюкуроніду, сам же налмефен та інші його метаболіти визначаються у сечі у кількості, що не перевищує 3% кожен. Кліренс налмефену при внутрішньому прийомі становить 169 л/год. Кінцевий T1/2 дорівнює 12,5 год. Наведені дані про розподіл, метаболізм і виведення налмефену свідчать про його високий печінковий кліренс. Лінійність/нелінійність. Фармакокінетика налмефену має дозоннезалежний лінійний характер у діапазоні доз від 18,06 до 72,24 мг. У рівноважному стані порівняно з одноразовим прийомом налмефену спостерігається збільшення Cmax у 4,4 рази та загальної експозиції препарату (AUC0–τ) у 4,3 рази. Не виявлено значних відмінностей у фармакокінетиці налмефену залежно від статі, віку чи етнічної приналежності. Виявлено, що розмір тіла мінімально впливає на фармакокінетичні параметри налмефену (зі збільшенням розміру тіла кліренс зростає), але, ймовірно, ця відмінність не є клінічно значущою. Порушення функції нирок. В даний час немає даних щодо фармакокінетики налмефену при пероральному прийомі у пацієнтів з нирковою недостатністю. Введення 1 мг налмефену внутрішньовенно пацієнтам з тяжкою нирковою недостатністю призводило до збільшення експозиції налмефену (скоригована з урахуванням дози AUCinf) у 1,6 раза порівняно зі здоровими суб'єктами. T1/2 збільшувався до 26 год проти здоровими суб'єктами. Порушення функції печінки. При прийомі одноразової дози налмефену 18,06 мг у пацієнтів з легкою та помірною печінковою недостатністю спостерігалося збільшення експозиції налмефену порівняно зі здоровими суб'єктами. У пацієнтів з легкою печінковою недостатністю спостерігалося збільшення експозиції препарату в 1,5 рази та зниження кліренсу приблизно на 35%. У пацієнтів з помірною печінковою недостатністю експозиція зростала у 2,9 раза, Cmax у 1,7 раза, а кліренс знижувався приблизно на 60%. Зміни Tmax та T1/2 не мали клінічного значення в жодній групі пацієнтів. В даний час немає даних щодо фармакокінетики налмефену після перорального прийому у пацієнтів з тяжкою печінковою недостатністю. Літні пацієнти. Спеціальних досліджень фармакокінетики налмефену після перорального прийому у пацієнтів віком 65 років і більше не проводилося. У дослідженні з внутрішньовенним введенням налмефену не виявлено значних відмінностей фармакокінетики між віковими групами.ФармакодинамікаМеханізм дії Налмефен є модулятором опіоїдної системи з вираженою спорідненістю до μ-, δ- і κ-рецепторів. Дослідження in vitro показали, що налмефен є селективним лігандом опіоїдних рецепторів, виявляючи властивості антагоніста щодо μ- та δ-рецепторів та часткового агоніста щодо κ-рецепторів. Дослідження in vivo показали, що налмефен знижує споживання алкоголю, очевидно, модулюючи кортико-мезолімбічні функції. Дані, отримані з доклінічних досліджень, клінічних досліджень та літератури, не передбачають наявності у налмефена здатності викликати залежність або зловживання. Клінічна ефективність та безпека Ефективність налмефену у зниженні споживання алкоголю у пацієнтів із алкогольною залежністю оцінювалася у двох дослідженнях. З досліджень виключалися пацієнти з алкогольним делірієм в анамнезі, галюцинаціями, судомними нападами, серйозними психічними розладами, пацієнти із значним порушенням функцій печінки. Також виключалися пацієнти, у яких на момент скринінгу або рандомізації було виявлено виражені фізичні симптоми відміни алкоголю. Більшість пацієнтів (80%), включених у дослідження, на момент скринінгу мали високий або дуже високий рівень ризику розвитку шкідливих наслідків вживання алкоголю (згідно з визначенням ВООЗ, прийом >60 г/сут чистого алкоголю для чоловіків та >40 г/сут чистого алкоголю для жінок), з них 65% зберегли високий або дуже високий рівень ризику до моменту рандомізації. Обидва дослідження були рандомізованими подвійними сліпими плацебо-контрольованими дослідженнями в паралельних групах, і через 6 місяців лікування пацієнти, які отримували налмефен, були повторно рандомізовані, щоб отримувати або налмефен, або плацебо протягом 1 міс т.зв. run-out періоду. Ефективність налмефену також вивчалася в 1-річному рандомізованому подвійному сліпому плацебо-контрольованому дослідженні у паралельних групах. Загалом у цих дослідженнях було проліковано 1941 пацієнт, у тому числі 1144 пацієнта отримували налмефен у дозі 18 мг (за потреби). Під час першого візиту оцінювався клінічний статус пацієнта, соціальна ситуація та характер споживання алкоголю (за словами пацієнта). При рандомізації, яка проводилася через 1-2 тижні, повторно оцінювався рівень ризику розвитку шкідливих наслідків вживання алкоголю та призначалася терапія налмефеном у комплексі з психосоціальною інтервенцією (BRENDA), спрямованою на підтримку прихильності до лікування та зниження споживання алкоголю. Налмефен приймався за необхідності, що становить у середньому половину днів перебування у дослідженні. Ефективність налмефену оцінювалася за двома основними критеріями: зміна кількості днів важкого пияцтва (ДТП) на місяць за період між вихідним обстеженням та 6-м міс та зміна добової дози алкоголю (СДА) за період між вихідним обстеженням та 6-м міс. ДТП визначався як день, коли споживалося ≥60 г чистого алкоголю чоловіками та ≥40 г жінками. У період між вихідним візитом (скринінгом) та рандомізацією у деяких пацієнтів було відзначено значне зменшення ДТП та СДА, зумовлене нефармакологічними ефектами. У дослідженнях 1 (n=579) та 2 (n=655) 18 та 33% від загальної кількості пацієнтів, які брали участь у дослідженні, відповідно значно знизили споживання алкоголю в період між скринінгом і рандомізацією. Що стосується пацієнтів із спочатку високим і дуже високим ризиком розвитку шкідливих наслідків вживання алкоголю, то з них у 35% показники покращилися через нефармакологічні причини в період між скринінгом і рандомізацією. У цих пацієнтів на момент рандомізації кількість споживаного алкоголю була настільки невеликою, що можливості подальшого поліпшення були дуже обмеженими (вихідний рівень майже відповідав мінімальному). Пацієнти, що зберегли високий і дуже високий рівень ризику розвитку шкідливих наслідків вживання алкоголю між скринінгом та рандомізацією, ретроспективно склали цільову популяцію. У цій групі ефект лікування був значнішим, ніж у популяції загалом. Клінічна ефективність налмефену та достовірність даних аналізувалися у пацієнтів з високим та дуже високим ризиком розвитку шкідливих наслідків вживання алкоголю при скринінгу та рандомізації. Спочатку у таких пацієнтів спостерігалося в середньому 23 ДТП/міс (у 11% пацієнтів менше 14 ДТП/міс) при добовому споживанні 106 г чистого алкоголю. У більшості пацієнтів рівень алкогольної залежності, виміряний за шкалою алкогольної залежності, був низьким (0-13 балів у 55% пацієнтів) або проміжним (14-21 бал у 36% пацієнтів). Ретроспективний аналіз ефективності у пацієнтів з високим та дуже високим рівнем ризику розвитку шкідливих наслідків вживання алкоголю на момент рандомізації У Дослідженні 1 частка пацієнтів, що вибули з дослідження, була вищою у групі налмефену, ніж у групі плацебо (50 і 32% відповідно). Кількість ДТП при вихідному обстеженні становило 23 дні на місяць як у групі налмефену (n=171), так і у групі плацебо (n=167). Серед пацієнтів, які продовжили участь у дослідженні та у яких були отримані дані щодо ефективності через 6 міс, кількість ДТП склала 9 днів на місяць у групі налмефену (n=85) та 14 днів на місяць у групі плацебо (n=114). При вихідному обстеженні СДА склала 102 г у групі налмефену та 99 г у групі плацебо. Серед пацієнтів, які продовжили участь у дослідженні, та у яких були отримані дані щодо ефективності через 6 міс, СДА склала 40 г у групі налмефену та 57 г у групі плацебо. У Дослідженні 2 частка пацієнтів, що вибули з дослідження, була вищою у групі налмефену, ніж у групі плацебо (30 і 28% відповідно). При вихідному обстеженні кількість ДТП склала 23 дні на місяць у групі налмефену (n=148) та 22 дні на місяць у групі плацебо (n=155). Серед пацієнтів, які продовжили участь у дослідженні та у яких були отримані дані щодо ефективності через 6 міс, кількість ДТП склала 10 днів на місяць у групі налмефену (n=103) та 12 днів на місяць у групі плацебо (n=111). При вихідному обстеженні СДА склала 113 г у групі налмефену та 108 г у групі плацебо. Серед пацієнтів, які продовжили участь у дослідженні та у яких були отримані дані щодо ефективності через 6 міс, СДА склала 44 г у групі налмефену та 52 г у групі плацебо. Річне дослідження До дослідження було включено 665 пацієнтів, 52% з них мали високий або дуже високий ризик розвитку шкідливих наслідків вживання алкоголю на момент скринінгу, у свою чергу, 52% цих пацієнтів (27% від загальної популяції) зберегли високий або дуже високий рівень ризику до моменту рандомізації. У даній цільовій популяції серед пацієнтів, що достроково припинили лікування, більше пацієнтів було в групі налмефену (45%) порівняно з пацієнтами, що припинили лікування, у групі плацебо (31%). При вихідному обстеженні кількість ДТП склала 19 днів на місяць як у групі налмефену (n = 141), так і у групі плацебо (n = 42). Серед пацієнтів, які продовжили участь у дослідженні та у яких були отримані дані щодо ефективності через 1 рік, кількість ДТП склала 5 днів на місяць у групі налмефену (n=78) та 10 днів на місяць у групі плацебо (n=29).При вихідному обстеженні СДА становила 100 г у групі налмефену та 101 г у групі плацебо. Серед пацієнтів, які продовжили участь у дослідженні та у яких були отримані дані щодо ефективності через 1 рік, СДА склала 24 г у групі налмефену та 47 г у групі плацебо.Показання до застосуванняЗниження споживання алкоголю у дорослих пацієнтів з алкогольною залежністю, які мають високий ризик зловживання алкоголем, за відсутності фізичних проявів синдрому відміни або необхідності проведення негайної детоксикації. Селінкро рекомендовано застосовувати у поєднанні з тривалою психосоціальною підтримкою, спрямованою на збереження прихильності до лікування та зниження споживання алкоголю. Селінкро призначається після 2 тижнів спостереження за пацієнтом з високим ризиком зловживання алкоголем.Протипоказання до застосуваннягіперчутливість до налмефену чи будь-якого з компонентів препарату; спадкова непереносимість галактози, дефіцит лактази або глюкозо-галактозна мальабсорбція; застосування у пацієнтів, які нині приймають опіоїдні анальгетики; поточна чи недавня опіоїдна залежність; гострі симптоми відміни опіоїдів; підозра на недавній прийом опіоїдів; тяжка печінкова недостатність (класифікація по Чайлд-П'ю); тяжка ниркова недостатність (розрахована швидкість клубочкової фільтрації (рСКФ)) стан скасування алкоголю (включаючи галюцинації, судоми та алкогольний делірій) у недавньому минулому; вагітність; період грудного вигодовування; дитячий та підлітковий вік (до 18 років) (ефективність та безпека застосування не підтверджені). З обережністю: супутні психічні розлади у фазі декомпенсації (у зв'язку з відсутністю клінічних даних); судомні розлади в анамнезі, включаючи судоми, що розвиваються при скасуванні алкоголю; легка або помірна ниркова або печінкова недостатність, підвищений рівень АЛТ та АСТ (більш ніж у 3 рази перевищує ВГН); одночасне застосування потужних інгібіторів ізоферменту UGT2B7 протягом тривалого часу; літні пацієнти (≥65 років).Вагітність та лактаціяДані щодо застосування налмефену у вагітних жінок обмежені (менше 300 випадків наслідків вагітності). Дослідження у тварин виявили репродуктивну токсичність налмефену. Дослідження у тварин не виявили прямий шкідливий вплив налмефену щодо фертильності, вагітності, ембріо-фетального розвитку, пологів та постнатального розвитку. У дослідженні ембріо-фетальної токсичності у кроликів спостерігалося зниження маси плода та затримка осифікації (процесу формування кісткової тканини), будь-які інші серйозні порушення не були виявлені. Експозиція (AUC) при прийомі вищої нетоксичної дози (NOAEL/ВНТД) при цих небажаних ефектах була нижчою за експозицію при прийомі терапевтичної дози, рекомендованої для людини. Збільшення частоти появи мертвонароджених дитинчат і зменшення їх постнатальної виживання спостерігалося в дослідженнях пре-і постнатальної токсичності у щурів. Цей ефект вважався непрямим і пов'язаним із токсичністю у самок. Доклінічні дані не виявили особливої небезпеки налмефену для людини на підставі стандартних досліджень фармакологічної безпеки, токсичності при багаторазовому застосуванні, генотоксичності та канцерогенного потенціалу. Селінкро не рекомендується застосовувати під час вагітності. Доступні фармакодинамічні та токсикологічні дані у тварин показали здатність налмефену та метаболітів проникати у грудне молоко. Невідомо, чи налмефен проникає в грудне молоко людини. В даний час не можна виключити потенційний ризик для новонароджених/немовлят, тому Селінкро не рекомендується застосовувати під час грудного вигодовування. Фертильність. Дослідження на щурах не виявили впливу налмефену на фертильність, процес спарювання, вагітність або процес сперматогенезу.Побічна діяУ клінічних дослідженнях понад 3000 пацієнтів одержали лікування налмефеном. Загалом профіль безпеки виглядав подібним чином у всіх проведених дослідженнях. Найбільш поширеними небажаними реакціями були нудота, запаморочення, безсоння та біль голови. Більшість цих реакцій мала легкий і середній ступінь тяжкості і відзначалася лише на початку лікування. Сплутаність свідомості та, рідше, галюцинації та дисоціативні розлади також спостерігалися в ході клінічних досліджень. Більшість цих реакцій мала легкий і середній ступінь тяжкості і відзначалася лише на початку лікування (перший годинник або дні). Більшість подібних небажаних реакцій дозволяли при продовженні терапії та не відновлювалися при повторному застосуванні препарату. Ці розлади, що загалом мають короткочасний характер, можуть бути симптомами алкогольних психозів, алкогольного похмільного синдрому або коморбідних психічних розладів. Розрахунок частоти небажаних побічних реакцій проводився на підставі результатів трьох рандомізованих подвійних сліпих плацебо-контрольованих досліджень у пацієнтів з алкогольною залежністю (1144 пацієнти отримували Селінкро в режимі «за потребою» та 797 отримували плацебо в режимі «за потребою»). Частота визначається так: дуже часто (≥1/10), часто (від ≥1/100 до Органи та системи органів Частота Небажана реакція З боку обміну речовин та харчування Часто Зниження апетиту Порушення психіки Дуже часто Безсоння Часто Розлади сну Сплутаність свідомості Занепокоєння Зниження лібідо ( в т.ч. відсутність) Частота невідома Галюцинації ( в т.ч. слухові, тактильні, зорові та соматичні) Дисоціативні розлади З боку нервової системи Дуже часто Запаморочення Головний біль Часто Сонливість Тремор Розлади уваги Парестезія Гіпестезія З боку серця Часто Тахікардія Відчуття серцебиття З боку шлунково-кишкового тракту Дуже часто Нудота Часто Блювота Сухість в роті З боку шкіри та підшкірних тканин Часто Підвищене потовиділення З боку скелетно-м'язової та сполучної тканини Часто М'язові спазми Загальні розлади та порушення у місці введення Часто Стомлюваність Астенія нездужання Відчуття зміненості стану ( в т.ч. відчуття туману в голові, заціпеніння) Лабораторні та інструментальні дані Часто Зниження маси тіла Взаємодія з лікарськими засобамиДослідження взаємодії з іншими лікарськими засобами in vivo не проводились. Відповідно до даних досліджень in vitro, немає підстав припускати наявність клінічно значущої взаємодії між налмефеном або його метаболітами та лікарськими препаратами, що піддаються метаболізму за участю більшості ізоферментів CYP450 та UGT або мембранними переносниками. Одночасне застосування з препаратами, які є потужними інгібіторами ізоферменту UGT2B7 (наприклад, диклофенак, флуконазол, медроксипрогестерону ацетат, меклофенамова кислота), може значно підвищити експозицію налмефену. Рідкісне застосування цих лікарських препаратів одночасно з налмефеном навряд чи може призвести до клінічно значущих наслідків. У той же час, у разі тривалого одночасного застосування потужних інгібіторів ізоферменту UGT2B7 не можна виключати потенційно можливе підвищення експозиції налмефену.Відповідно одночасне застосування з індукторами UGT (наприклад, дексаметазон, фенобарбітал, рифампіцин, омепразол) може потенційно призвести до зниження концентрації налмефену в плазмі нижче терапевтичного рівня. У разі застосування налмефену одночасно з опіоїдними агоністами (наприклад, деякі протикашльові, протизастудні, протидіарейні засоби та опіоїдні анальгетики) може спостерігатися зниження їх терапевтичного ефекту. Не існує клінічно значущої фармакокінетичної взаємодії між налмефеном та алкоголем. Після застосування налмефену може спостерігатися незначне погіршення когнітивних та психомоторних функцій. Однак результат одночасного прийому налмефену та алкоголю не перевищував суму ефектів кожної речовини, що застосовувалася окремо. Одночасне застосування алкоголю та Селінкро не запобігає розвитку алкогольної інтоксикації.Спосіб застосування та дозиПід час первинного візиту до призначення Селінкро лікарю необхідно оцінити клінічний стан пацієнта та рівень споживання алкоголю (за його словами). У випадках, де потрібна додаткова інформація, пацієнту пропонується зареєструвати рівень споживання алкоголю приблизно протягом наступних 2 тижнів. Тим пацієнтам, у яких протягом цих двох тижнів зберігся порівняний з початковим рівень споживання алкоголю, Селінкро може бути призначений при повторному візиті. Селінкро рекомендовано застосовувати у поєднанні з психосоціальною підтримкою, спрямованою на збереження прихильності до лікування та зниження рівня споживання алкоголю. Селінкро не призначений для досягнення негайної помірності від алкоголю. Зниження споживання алкоголю є проміжною метою на шляху до повної помірності. Селінкро застосовується за потребою. Рішення про прийом препарату приймає сам пацієнт: у ті дні, коли, на його думку, висока ймовірність вживання алкоголю, за 1-2 години до передбачуваного моменту приймається 1 табл. Селінкро у дозі 18 мг. Якщо пацієнт почав вживати алкоголь, не прийнявши попередньо таблетку Селінкро, йому потрібно це зробити якнайшвидше. Максимальна добова доза Селінкро становить 1 табл. У ході клінічних досліджень максимальне покращення спостерігалося протягом перших 4 тижнів терапії. Відповідь пацієнта на лікування та доцільність продовження фармакотерапії необхідно оцінювати регулярно (наприклад, щомісяця). Лікар повинен постійно визначати прогрес пацієнта у зниженні споживання алкоголю, його загальний стан, відданість терапії та виникнення побічних ефектів. Тривалість клінічних досліджень Селінкро не перевищувала 12 місяців, тому його призначення на термін більше одного року має здійснюватися з обережністю. Спосіб застосування Всередину, незалежно від їди. Пігулки, покриті плівковою оболонкою, слід приймати повністю. Таблетки не слід ділити або іншим способом порушувати їхню цілісність, т.к. налмефен може спричинити подразнення у разі прямого контакту зі шкірою. Особливі групи пацієнтів Літні пацієнти (≥65 років). У даної групи пацієнтів корекція дози не потрібна. Порушення функції нирок. У пацієнтів з легкою та помірною нирковою недостатністю корекція дози не потрібна. Порушення функції печінки. У пацієнтів з легкою та помірною печінковою недостатністю корекція дози не потрібна. Діти та підлітки (до 18 років). Безпека та ефективність Селінкро у пацієнтів віком до 18 років не встановлена. Дані щодо цієї вікової групи відсутні.ПередозуванняУ дослідженні у пацієнтів з діагнозом патологічної пристрасті до азартних ігор налмефен застосовувався у дозах до 90 мг на добу протягом 16 тижнів. У дослідженні у пацієнтів з інтерстиціальним циститом 20 пацієнтів приймали налмефен у дозі 108 мг на добу протягом 2 років. Повідомлялося про випадок одноразового прийому налмефену в дозі 450 мг, який не супроводжувався зміною АТ, ЧСС, частотою дихальних рухів або температурою тіла. У цих випадках профіль безпеки налмефену відповідав описаному вище розділу «Побічні дії», однак досвід спостереження обмежений. Лікування: при передозуванні рекомендується симптоматична терапія та спостереження за станом пацієнта.Запобіжні заходи та особливі вказівкиСелінкро не призначений для досягнення негайної помірності від алкоголю. Зниження споживання алкоголю є проміжною метою на шляху до повної помірності. Застосування опіоїдів. В екстреній ситуації, коли пацієнту, який приймає Селінкро, необхідно введення опіоїдів, дози останніх, необхідні для досягнення бажаного ефекту, можуть перевищувати стандартні. При цьому слід уважно відстежувати симптоми пригнічення дихання, що є результатом введення опіоїдів та інші небажані реакції. Якщо для надання допомоги пацієнту в екстреній ситуації необхідне введення опіоїдів, їх дози слід підбирати індивідуально. У разі, коли потрібне застосування надто високих доз опіоїдів, слід ретельно спостерігати за станом пацієнта. Селінкро необхідно тимчасово відмінити за 1 тиждень до передбачуваного застосування опіоїдів, наприклад, у ході планового хірургічного втручання. Лікар, який призначає Селінкро, повинен рекомендувати пацієнтові повідомити медичних працівників про час останнього прийому препарату у випадках, коли стає необхідним застосування опіоїдів. Необхідно бути обережним у випадку, коли лікарські препарати, що містять опіоїди (наприклад протикашльові препарати та опіоїдні анальгетики), застосовуються у пацієнтів, які вже отримують терапію Селінкро. Налмефен протипоказаний у пацієнтів, які нині приймають опіоїдні аналгетики. Хвороби, що супруводжують Психічні розлади. У ході проведення клінічних досліджень повідомлялося про побічні реакції з боку психіки. Якщо у пацієнта виникають розлади психіки, не пов'язані з початком застосування Селінкро та/або вони не є тимчасовими, лікар повинен врахувати альтернативні причини виникнення цих симптомів та оцінити необхідність продовження терапії препаратом Селінкро. Селінкро не досліджувався у пацієнтів із нестабільним перебігом психічних захворювань. Слід призначати Селінкро з обережністю пацієнтам із супутніми психічними захворюваннями у фазі декомпенсації, у т.ч. пацієнтам із діагнозом «великий депресивний розлад». Судорожні розлади. Досвід застосування препарату у пацієнтів із судомними розладами в анамнезі, включаючи судоми, що розвиваються при відміні алкоголю, обмежений. Рекомендується бути обережним, якщо Селінкро застосовується з метою зменшення споживання алкоголю в цій групі пацієнтів. Порушення функції нирок чи печінки. Селінкро активно метаболізується в печінці та виводиться переважно із сечею. З цієї причини слід бути обережним при призначенні Селінкро пацієнтам з легкою або помірною нирковою або печінковою недостатністю. Слід бути обережними при призначенні Селінкро пацієнтам з підвищеним рівнем АЛТ і АСТ (більш ніж у 3 рази перевищують ВГН), т.к. дана категорія пацієнтів виключалася під час клінічних досліджень. Літні пацієнти (≥65 років). Клінічні дані щодо застосування Селінкро у пацієнтів з алкогольною залежністю у віці 65 років та старші обмежені. Слід бути обережними при призначенні Селінкро пацієнтам віком 65 років і старше. Інші. Слід бути обережними при одночасному застосуванні Селінкро з потужними інгібіторами ізоферменту UGT2B7. лактоза. Пацієнти з такими рідкісними спадковими проблемами, як непереносимість галактози, дефіцит лактази або глюкозо-галактозна мальабсорбція не повинні застосовувати цей препарат. Вплив на здатність керувати транспортними засобами та працювати з механізмами. Вплив налмефену на здатність керувати транспортними засобами та працювати з механізмами не вивчався. Селінкро може викликати небажані реакції, такі як нудота, запаморочення, безсоння та біль голови. Більшість цих реакцій мала легкий і середній ступінь тяжкості і відзначалася лише на початку лікування. Пацієнтам, які приймають Селінкро, не рекомендується керувати транспортними засобами та працювати з механізмами доти, доки не буде з'ясовано індивідуальну реакцію на препарат.Умови відпустки з аптекЗа рецептомВідео на цю тему
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
Состав, форма выпуска и упаковкаТаблетки, покрытые пленочной оболочкой - 1 табл.: активное вещество: цитизин - 1,5 мг; вспомогательные вещества: лактозы моногидрат — 28 мг; МКЦ — 67,5 мг; тальк — 2 мг; магния стеарат — 1 мг; оболонка плівкова: Опадрай II коричневий 8 F 26948 – 3 мг: полівініловий спирт частково гідролізований – 1,2 мг; титану діоксид (Е171) - 0,654 мг; макрогол 3350 - 0,606 мг; тальк – 0,444 мг; заліза оксид жовтий (Е172) – 0,062 мг, заліза оксид червоний (Е172) – 0,018 мг, заліза оксид чорний (Е172) – 0,016 мг. Пігулки, покриті плівковою оболонкою, 1,5 мг. У бл. із ПВХ-плівки/фольги алюмінієвої, 50 шт. 2 бл. у картонному вкладиші з календарем прийому в картонній пачці.Опис лікарської формиТаблетки: круглі, двоопуклі, покриті плівковою оболонкою світло-коричневого кольору. Вид на зламі – від білого до бежевого кольору.Фармакотерапевтична групаН-холіноміметичне.ФармакокінетикаФармакокінетичні дослідження на людях не проводились.ФармакодинамікаАлкалоїд цитизин, що є активною речовиною препарату, має н-холіноміметичну дію; збуджує ганглії вегетативної нервової системи, рефлекторно стимулює дихальний центр, викликає виділення адреналіну з мозкової речовини надниркових залоз, підвищує артеріальний тиск. При близькій схожості з механізмом дії нікотину, цитизин має набагато нижчу токсичність і більший терапевтичний індекс. Цитизин конкурентно пригнічує взаємодію нікотину з відповідними рецепторами, що веде до поступового зменшення та зникнення нікотинової залежності.Показання до застосуванняНікотинова залежність (для полегшення відмови від куріння). Фізична та психологічна залежність від нікотину вважається певним типом захворювання, що призводить до нездатності помірності від куріння, навіть при розумінні його негативних ефектів.Протипоказання до застосуваннягіперчутливість до активної або будь-якої з допоміжних речовин препарату; гострий інфаркт міокарда; нестабільна стенокардія; аритмія серця; нещодавно перенесене порушення мозкового кровообігу; атеросклероз; тяжка артеріальна гіпертензія; недостатність лактази, галактоземія, синдром мальабсорбції глюкози-галактози (до складу препарату входить лактоза); вагітність; період грудного вигодовування; вік до 18 та після 65 років. З обережністю: інші форми ішемічної хвороби серця (стабільна стенокардія, безсимптомна (тиха) ішемія міокарда, вазоспастична стенокардія, синдром "X" (мікросудинна стенокардія); серцева недостатність, підвищений АТ; захворювання судин головного мозку; облітеруючі артеріальні захворювання, гіпер шлунка, цукровий діабет, ниркова або печінкова недостатність, деякі форми шизофренії, наявність хромафінних пухлин надниркових залоз, гастроезофагеальна рефлюксна хвороба, особи з тривалим стажем куріння та особи старше 40-45 років.Вагітність та лактаціяТабекс не слід застосовувати жінкам під час вагітності та в період грудного вигодовування.Побічна діяПрепарат зазвичай добре переноситься, побічні явища, що спостерігаються, виражені слабо або помірно. Більшість із них з'являються на початку лікування та проходять самостійно. Найчастіше вони пов'язані з відмовою від тютюнопаління і виявляються запамороченням, головним болем та безсонням. У рекомендованих дозах препарат Табекс не викликає серйозних несприятливих ефектів. Можливі такі побічні дії З боку ССС: тахікардія, незначне підвищення артеріального тиску, відчуття серцебиття. З боку центральної нервової системи: головний біль, запаморочення, безсоння або сонливість, підвищена дратівливість. З боку дихальної системи: задишка. З боку шлунково-кишкового тракту: сухість у роті, нудота, біль у животі, запори, діарея, зміни смаку та апетиту. З боку скелетно-м'язової та сполучної тканини: біль у м'язах. З боку обміну речовин та харчування: зниження маси тіла, підвищене потовиділення. Інші: біль у грудній клітці.Взаємодія з лікарськими засобамиПісля припинення тютюнопаління можуть посилюватися побічні дії теофіліну, ропініролу, клозапіну та оланзапіну. При одночасному застосуванні препарату Табекс® з ацетилхоліном, карбахолом, галантаміном, піридостигміном, ривастигміном, дистигміном можливе посилення холіноміметичних побічних дій (слинотеча, сльозотеча, бронхіальна секреція з кашлем, терапія. підвищений тонус м'язів чи раптові скорочення м'язів). Застосування препарату Табекс одночасно з ловастатином, симвастатином, флувастатином, правастатином та ін. підвищує ризик появи болю в м'язах. Одночасне застосування препарату Табекс з гіпотензивними засобами (пропранолол та ін.) може послабити їхній ефект.Спосіб застосування та дозиВсередину повністю запиваючи достатньою кількістю рідини. Не слід перевищувати рекомендовані дози. Прийом препарату бажано розпочинати після встановлення пацієнта на повну відмову від куріння. Препарат слід застосовувати за наступною схемою: з 1 по 3 день - по 1 табл. 6 разів на день (кожні 2 години), поступово зменшуючи кількість викурених сигарет. Таблетку слід приймати між епізодами куріння для подовження інтервалів між викурюванням сигарет, щоб максимально знизити їхнє споживання. Інтервал прийому кожні 2 години повинен дотримуватися. Якщо результат незадовільний, лікування слід припинити і через 2-3 місяці можна почати його знову. При хорошому ефекті лікування продовжують за наступною схемою: з 4 по 12-й день - по 1 табл. кожні 2,5 год; з 13-го по 16-й день - по 1 табл. кожні 3 год; з 17-го по 20-й день – по 1 табл. кожні 5 год; з 21-го по 25-й день - по 1-2 табл. в день. Настійно рекомендується відмовитися від куріння не пізніше 5-го дня від початку лікування. Поєднання медикаментозної терапії із консультаціями, в т.ч. з заходами психологічної підтримки пацієнта, що достовірно підвищує ефективність лікування.ПередозуванняСимптоми: нудота, блювання, розширення зіниць, загальна слабкість, тахікардія, клонічні судоми, параліч дихання. Настають у разі, коли пацієнт не дотримується режиму дозування і приймає препарат у дозах, що у кілька разів перевищують терапевтичні. Лікування: промивання шлунка, призначення активованого вугілля, інфузійне введення водно-сольових розчинів, а також 5 або 10% розчину глюкози, призначення протисудомних засобів, кардіотоніків, дихальних аналептиків та інших симптоматичних засобів. Слід відстежувати роботу органів дихання, АТ та ЧСС.Запобіжні заходи та особливі вказівкиПрийом препарату слід розпочати лише тоді, коли пацієнт має серйозний намір відмовитись від куріння. Особам із тривалим стажем куріння та особам старше 40–45 років препарат Табекс слід застосовувати лише після консультації з лікарем. При застосуванні препарату не слід перевищувати рекомендованих доз. Лікування препаратом та продовження куріння може призвести до посилення побічних дій нікотину (нікотинова інтоксикація). Лікарський препарат містить допоміжну речовину лактозу. Пацієнтам з рідкісними спадковими проблемами непереносимості галактози, з лактазним дефіцитом (тип Лапп) або глюкозо-галактозною мальабсорбцією не слід застосовувати лікарський препарат. Вплив на здатність керувати транспортними засобами та працювати з механізмами. Хоча на тлі застосування препарату будь-якого негативного впливу на здатність керувати автотранспортом та роботу з механізмами не спостерігалося, проте внаслідок можливого виникнення сонливості та інших побічних реакцій слід бути обережним у перелічених ситуаціях.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Активна речовина: дисульфірам – 150 мг; Допоміжні речовини: крохмаль картопляний – 2,70 мг, целюлоза мікрокристалічна – 23,80 мг, кремнію діоксид колоїдний – 0,85 мг, кроскармелоза натрію – 0,85 мг, стеаринова кислота – 0,36 мг, магнію стеарат мг. По 10 таблеток у контурне осередкове пакування з плівки полівінілхлоридної та фольги алюмінієвої друкованої лакованої. По 3 або 5 контурних осередкових упаковок разом з інструкцією із застосування поміщають у пачку з картону.Опис лікарської формиКруглі, плоскоциліндричні пігулки білого або білого зі злегка жовтувато-зеленим відтінком кольору, з фаскою.Фармакотерапевтична групаЗасіб для лікування алкоголізму.ФармакокінетикаАбсорбція після перорального прийому – 70-90 %. Швидко метаболізується в печінці шляхом відновлення діетилдітіокарбамат, що виділяється у вигляді глюкуроніду нирками, або трансформується в діетиламін і сірковуглець, пропорція якого варіює від 4 до 53%. Останній виділяється через легені. Мінімальний вміст дисульфіраму в крові – близько 20 нг/мл.ФармакодинамікаДисульфірам інгібує фермент ацетальдегіддегідрогеназу, що бере участь у метаболізмі етанолу, що призводить до збільшення концентрації ацетальдегіду, що є метаболітом етанолу, в 5-10 разів. Ацетальдегід викликає ряд неприємних відчуттів: "припливи" крові до шкіри обличчя, нудоту, блювання, почуття нездужання, тахікардію, зниження артеріального тиску. В результаті відбувається вироблення умовно-рефлекторної реакції огиди до смаку та запаху спиртних напоїв. Сила реакцій, викликаних препаратом, пропорційна прийнятій дозі. Максимальний терапевтичний ефект досягається через 12 годин після перорального прийому та може тривати протягом 10-14 днів після припинення лікування. Чим триваліший курс терапії, тим більше виражені ефекти препарату.Показання до застосуванняДисульфірам використовується як допоміжна терапія хронічного алкоголізму у пацієнтів, які проходять лікування з приводу алкогольної залежності, які мають намір перебувати у стані утримання від алкоголю з метою досягнення найкращого ефекту підтримуючої та психотерапії. Дисульфірам не виліковує алкоголізм. При використанні як монотерапія, без відповідної мотивації та підтримуючого лікування не надає значного впливу на алкогольну поведінку в осіб з хронічним алкоголізмом.Протипоказання до застосуванняГіперчутливість, тиреотоксикоз, захворювання серцево-судинної системи (в т.ч., різко виражений кардіосклероз, атеросклероз мозкових судин, тяжке ураження міокарда, перед- та постінфарктні стани, аневризму аорти, оклюзія коронарних судин, артеріальна гіпертензія серцево-судинної системи в стадії декомпенсації), хронічна обструктивна хвороба легень, туберкульоз легень з кровохарканням, бронхіальна астма, виражена емфізема легень, ерозивні ураження слизової оболонки шлунково-кишкового тракту, виразкова хвороба шлунка та дванадцятипалої кишки ( кишкового тракту, хвороби нирок, печінкова недостатність, цукровий діабет, епілепсія, інфекційні захворювання центральної нервової системи, полінейропатія, неврит слухового та очного нервів,глаукоми, злоякісні пухлини, вагітність, період лактації. В окремих випадках при тривалому прийомі тетураму можуть спостерігатися гострі психози, що нагадують гострий алкогольний параноїд, гострий алкогольний галюциноз або алкогольний делірій. Можливий перехід галюцинаторного синдрому в параноїдний, параноїдний - в шизофреноподібний і т.д. Одночасний (або в недавньому минулому) прийом метронідазолу, паральдегіду, етанолу або етанолвмісних лікарських засобів та продуктів. Дитячий вік віком до 18 років. З обережністю: пацієнти старше 60 років, виразкова хвороба шлунка та дванадцятипалої кишки (в стадії ремісії), ендартеріїт, залишкові явища порушення мозкового кровообігу, психози на фоні прийому дисульфіраму в анамнезі.Вагітність та лактаціяПротипоказано застосовувати препарат при вагітності та в період годування груддю.Побічна дія"Металевий" присмак у роті, неприємний запах (обумовлений сірковуглецем) у хворих з колостомою, гепатит, неврит зорового нерва, периферичний неврит, поліневропатія нижніх кінцівок, нервово-психічні розлади, зниження пам'яті, дезорієнтація в часі та просторі, , шкірні алергічні реакції Побічні ефекти, зумовлені асоціацією дисульфіраметанол: колапс, аритмія, стенокардія, інфаркт міокарда, набряк мозку, крововилив у мозок.Взаємодія з лікарськими засобамиДисульфірам слід призначати з обережністю пацієнтам, які приймають фенітоїн та його похідні, оскільки одночасний прийом препаратів може призвести до інтоксикації фенітоїном. Перед призначенням дисульфіраму, хворим, які приймають фенітоїн, слід визначати базовий рівень фенітоїну в сироватці крові та надалі здійснювати контроль вмісту фенітоїну в крові з метою корекції дози препарату. Дисульфірам посилює ефект непрямих антикоагулянтів та збільшує ризик кровотеч. У разі одночасного призначення з пероральними антикоагулянтами необхідно здійснювати більш частий контроль вмісту протромбіну та корекцію доз антикоагулянтів. Необхідно також коригувати дозу дисульфіраму на початку та після закінчення курсу терапії, оскільки дисульфірам може подовжувати протромбіновий час. Ефекти дисульфіраму, зокрема. нейротоксичні,посилюють трициклічні антидепресанти (амітріптілін), метронідазол, ізоніазид. Метронідазол підвищує ризик розвитку порушень психіки, виникнення марення. При одночасному призначенні з ізоніазидом підвищується ризик виникнення порушень поведінки та координації рухів. При виявленні цих ознак прийом дисульфірів повинен бути припинений. Дисульфірам підвищує концентрацію в плазмі препаратів, що метаболізуються в печінці, внаслідок інгібування мікросомальних ферментів печінки. Посилює токсичні ефекти феназону, хлордіазепоксиду та діазепаму шляхом інгібування їх метаболізму. Аскорбінова кислота знижує реакцію на етанол.Спосіб застосування та дозиПеред початком лікування тривалість утримання від алкоголю повинна становити не менше 12 годин. Режим дозування на початку терапії Протягом 1 -2 перших тижнів лікування разова доза дисульфіраму повинна становити не більше 500 мг на добу. Препарат приймають вранці натще, перед сніданком. Зазвичай дисульфірам приймають у ранковий час, однак у разі появи седативного ефекту препарат може призначатися на ніч. Щоб мінімізувати або усунути седативний ефект, дозу можна скоригувати у бік зниження. Підтримуюча терапія Середня доза, що підтримує, становить 250 мг/с (діапазон від 125 до 500 мг), максимальна добова доза 500 мг. Тривалість терапії Щоденний регулярний прийом дисульфіраму повинен продовжуватися до повного одужання пацієнта, коли він може здійснювати самоконтроль над вживанням алкоголю. Прийом препарату має продовжуватись до досягнення стійкої ремісії.ПередозуванняСимптоми: сплутаність свідомості, колапс, коматозний стан, неврологічні ускладнення. Специфічного лікування передозування дисульфіраму немає. При тяжкій дисульфірам-алкогольній реакції тривалістю 1,5 год застосовують оксигенотерапію, вдихання карбогену (суміш 95 % кисню та 5 % вуглекислого газу), внутрішньовенно вводять високі дози аскорбінової кислоти (до 1 г), ефедрину сульфат та антигістамінний препарат. Необхідно моніторувати концентрацію калію в сироватці крові, особливо у випадках, якщо пацієнт приймає препарати наперстянки.Запобіжні заходи та особливі вказівкиПрепарат у жодному разі не можна приймати у стані алкогольної інтоксикації. Неприпустиме призначення препарату без попередження пацієнта. Родичі пацієнта повинні бути проінструктовані лікарем про особливості застосування препарату. Дисульфірам з особливою обережністю слід застосовувати при наступних супутніх захворюваннях: цукровий діабет, гіпотиреоз, епілепсія, хронічний та гострий нефрит, а також у пацієнтів віком від 65 років. Зареєстровані дані про гепатотоксичність препарату, включаючи печінкову недостатність, що потребує трансплантації печінки або смертельним наслідком. Тяжкі, а іноді летальні гепатити, спричинені терапією дисульфірамом, можуть розвинутись через багато місяців після завершення лікування препаратом. Пацієнта необхідно попередити про необхідність повідомляти лікаря про всі ранні симптоми прояву гепатиту, таких як швидка стомлюваність, слабкість, нездужання, зниження апетиту, нудота, блювання, жовтяниця, поява сечі темного кольору.Кожні 10-14 днів з початку терапії дисульфірамом пацієнту слід проводити контрольне дослідження параметрів функції печінки, включаючи загальний та біохімічний аналіз крові. Пацієнти, що приймають дисульфірам не повинні піддаватися впливу етилендіброміду та його пари. Результати досліджень на щурах продемонстрували, що інгаляційне введення етилендиброміду при застосуванні дисульфіраму підвищує розвиток пухлин та смертність у щурів. Аналогічних даних про дію пари діетилброміду на пацієнтів немає. Реакція взаємодії алкоголю та дисульфіраму: Пацієнт повинен бути поінформований про всі наслідки вживання алкоголю під час лікування дисульфірамом. Пацієнт повинен бути попереджений про неприпустимість таємного вживання алкоголю, а також алкоголю у складі харчових продуктів (соуси), лікарських препаратів (спиртсодержащіе лікарські засоби), парфумерії. Вживання алкоголю одночасно з дисульфірамом, навіть у невеликих кількостях викликає почервоніння обличчя, пульсацію в області голови та шиї, пульсуючий головний біль, утруднення дихання, нудоту, рвоту, пітливість, спрагу, біль за грудиною, почастішання серцебиття, задишку, слабкість, сплутаність і непритомність, виражене занепокоєння, запаморочення, порушення зору. У тяжких випадках може розвинутися пригнічення дихання, серцево-судинна недостатність, судоми та смерть. Інтенсивність реакції індивідуальна, але, як правило, пропорційна прийнятій внутрішньо кількості алкоголю і дисульфіраму. Початкові прояви реакції можуть спостерігатися у осіб з підвищеною чутливістю зі збільшенням концентрації алкоголю всього до 5-10 мг на 100 мл крові. Повний розвиток симптомів розвивається при концентрації алкоголю 50 мг на 100 мл. крові. При рівні алкоголю у крові від 125 мг до 150 мг на 100 мл відзначається непритомність. Тривалість реакції варіює від 30 - 60 хв до кількох годин; у тяжких випадках - до того часу, поки алкоголь визначається у крові. Вплив на здатність до керування автотранспортом та управління механізмами Препарат впливає здатність керувати транспортними засобами чи роботу з іншими механізмами.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Діюча речовина: дисульфірам – 150,0 мг; Допоміжні речовини: крохмаль картопляний – 18,7 мг, кремнію діоксид колоїдний (аеросил) – 1,8 мг, повідон (повідон К17) – 2,5 мг, стеаринова кислота – 1,5 мг, кроскармелоза натрію – 5,5 мг.Опис лікарської формиКруглі, плоскоциліндричні пігулки білого або білого зі злегка жовтувато-зеленим відтінком кольору, з фаскою.ХарактеристикаТетур містить дисульфірам, який бере безпосередню участь у медикаментозному лікуванні алкогольної залежності. Після прийому етанолу на фоні лікування дисульфірамом збільшується концентрація ацетальдегіду та розвиваються певні неприємні відчуття («припливи» крові до шкіри обличчя, нудота, блювання, тахікардія, зниження артеріального тиску). В результаті відбувається вироблення умовно-рефлекторної реакції до смаку та запаху етанолу. Випускається у формі таблеток (150 мг) по 10 або 15 таблеток у контурній комірковій упаковці. Відпускається за рецептом.Фармакотерапевтична групаПрепарати, що застосовуються при алкогольній залежностіФармакокінетикаАбсорбція після перорального прийому – 70-90%. Швидко метаболізується в печінці шляхом відновлення діетилдітіокарбамат, що виділяється у вигляді глюкуроніду нирками, або трансформується в діетиламін і сірковуглець, пропорція якого варіює від 4 до 53%. Останній виділяється через легені. Інші метаболіти виводяться із сечею. Інгібітор ізоферменту CYP2E1.ФармакодинамікаУ процесі метаболізму етанол метаболізується у печінці за допомогою ферменту ацетальдегіддегідрогенази. Дисульфірам необоротно інгібує ацетальдегіддегідрогеназу, що призводить до підвищення концентрації метаболіту етанолу – ацетальдегіду. Після прийому етанолу на фоні лікування дисульфірамом збільшується концентрація ацетальдегіду та розвиваються певні неприємні відчуття («припливи» крові до шкіри обличчя, нудота, блювання, тахікардія, зниження артеріального тиску). В результаті відбувається вироблення умовно-рефлекторної реакції до смаку та запаху етанолу. Максимальний терапевтичний ефект досягається через 12 годин після прийому внутрішньо і може тривати протягом 10-14 днів після припинення лікування.Показання до застосуванняЛікування та профілактика рецидивів хронічного алкоголізму.Протипоказання до застосуванняПідвищена чутливість до дисульфіраму або допоміжних речовин препарату; печінкова недостатність тяжкого ступеня; дихальна недостатність тяжкого ступеня; ниркова недостатність тяжкого ступеня; діабет; інсульт в анамнезі або тяжкі органічні ураження головного мозку; нервово-психічні розлади; епілепсія та судомний синдром будь-якого генезу; захворювання серцево-судинної системи, включаючи ішемічну хворобу серця; прийом спиртних напоїв або лікарських засобів, що містять етанол, протягом попередніх 24 годин; вагітність та дітородний вік (за відсутності застосування контрацепції); період грудного вигодовування; дитячий вік до 18 років (у зв'язку з відсутністю даних щодо ефективності та безпеки); одночасний прийом ізоніазиду, метронідазолу, орнідазолу, секнідазолу, тинідазолу, фенітоїну (див.розділ "Взаємодія з іншими лікарськими засобами"). З обережністю: ниркова недостатність (ризик розвитку тяжчої дисульфірам-етанолової реакції); гіпотиреоз (ризик розвитку тяжчої дисульфірам-етанолової реакції); нікелевий дерматит (підвищений ризик гепатиту); виразкова хвороба шлунка та дванадцятипалої кишки (див. розділ «Побічна дія»). - Неврит зорового нерва (див. розділ «Побічна дія»); у пацієнтів, які приймають кокаїн (ризик подовження інтервалу QT, див. розділ «Взаємодія з іншими лікарськими засобами»); пацієнти віком від 60 років.Вагітність та лактаціяВагітність Препарат Тетурам протипоказаний для застосування у вагітних жінок (у зв'язку з відсутністю клінічних даних). Період грудного вигодовування Безпека застосування препарату Тетурам у період грудного вигодовування не встановлена. Тому препарат протипоказаний жінкам у період грудного вигодовування.Побічна діяНебажані реакції представлені відповідно до наступних градацій частоти їх розвитку: дуже часто (≥ 10 %); часто (≥1%, <10%); нечасто (≥0,1%, <1%); рідко (≥0,01%, <0,1%); дуже рідко, включаючи окремі повідомлення ( Небажані реакції, пов'язані з дисульфірамом Порушення з боку шлунково-кишкового тракту Часто: дисгевзія (порушення смаку). Нечасто: аномальний запах випорожнення. Порушення з боку печінки та жовчовивідних шляхів Частота невідома: печінкова недостатність, фульмінантний гепатит, гепатит (переважно цитолітичний). Порушення з боку нервової системи Дуже часто: головний біль. Часто: сонливість. Нечасто: полінейропатія. Частота невідома: неврит зорового нерва, судоми, амнезія, енцефалопатія. Порушення з боку психіки Частота невідома: нервово-психічні розлади, сплутаність свідомості. Порушення з боку судин Частота невідома: артеріальна гіпертензія. Порушення з боку шкіри та підшкірних тканин Частота невідома: алергічний дерматит. Загальні розлади Дуже часто: астенія Небажані реакції, пов'язані з комбінацією дисульфірам-етанол Порушення з боку нервової системи Частота невідома: судоми, набряк мозку, субдуральний крововилив. Порушення з боку серця Частота невідома: тахікардія, аритмія, стенокардія, інфаркт міокарда (іноді з летальним кінцем). Порушення з боку судин Частота невідома: "припливи" крові до шкіри обличчя, зниження артеріального тиску, серцево-судинний колапс. Порушення з боку дихальної системи, органів грудної клітини та середостіння Частота невідома: пригнічення дихання Порушення з боку шлунково-кишкового тракту Частота невідома: нудота, блювання. Порушення з боку шкіри та підшкірних тканин Частота невідома: еритема (гіперемія покривів шкіри). Загальні розлади Частота невідома: нездужання. При тривалому прийомі дисульфіраму: Психози, що нагадують алкогольні, гепатит, гастрит. У пацієнтів із серцево-судинними захворюваннями можливий тромбоз судин головного мозку, тому при скаргах на парестезію в кінцівках та обличчі слід негайно відмінити препарат. Загострення поліневриту. При прийомі етанолу в дозах понад 50–80 мл (у перерахунку на 40 % етанол) на фоні прийому препарату розвиваються тяжкі порушення функції серцево-судинної та дихальної систем, набряки, судоми. У цьому випадку терміново проводять дезінтоксикаційну та симптоматичну терапію.Взаємодія з лікарськими засобамиДисульфірам може підвищувати концентрацію деяких лікарських засобів, що зазнають мікросомального окиснення в печінці за допомогою ізоферменту CYP2E1 (див. розділ «Фармакокінетика»). Протипоказані комбінації З етанолом Дисульфірам-етанолові реакції: «припливи» крові до шкіри обличчя, почервоніння шкіри, нудота, блювання, зниження артеріального тиску, тахікардія, слабкість або тяжкі реакції (див. розділ «Побічна дія»). Слід уникати прийому спиртних напоїв та етанолвмісних лікарських засобів. Діазепам може послаблювати дисульфірам-етанолову реакцію, також її незначно послаблюють аскорбінова кислота та антигістамінні препарати. Небажані комбінації З ізоніазидом Дисульфірам підвищує ризик виникнення поведінкових та координаційних порушень. З похідними нітроімідазолу (метронідазол, орнідазол, секнідазол, тинідазол) Гострий делірій, сплутаність свідомості. З фенітоїном Значне та швидке підвищення плазмових концентрацій фенітоїну, що призводить до підвищення ризику розвитку токсичних ефектів (оскільки дисульфірам інгібує метаболізм фенітоїну). Якщо застосування цієї комбінації не вдається уникнути, слід контролювати стан пацієнта та концетрацію фенітоїну в плазмі під час та після закінчення лікування дисульфірамом. З гепатотоксичними лікарськими засобами Слід уникати сумісного прийому дисульфіраму та гепатотоксичних лікарських засобів. засобів через можливе ураження печінки. Комбінації, які потребують обережності з варфарином та іншими непрямими антикоагулянтами Посилення антикоагулянтної дії та збільшення ризику кровотечі (зниження метаболізму варфарину у печінці). Рекомендується більш частий контроль міжнародного нормалізованого відношення (МНО) та корекція дози антикоагулянтів на початку прийому дисульфіраму та протягом 8 днів після його відміни. З теофіліном Дисульфірам знижує метаболізм теофіліну. Тому доза теофіліну має бути скоригована (зниження доз) залежно від клінічних симптомів та концентрації теофіліну у плазмі. З бензодіазепінами Дисульфірам може посилювати седативний ефект бензодіазепінів за рахунок інгібування їх мікросомального окиснення (особливо хлордіазепоксиду та діазепаму). Дозування бензодіазепіну має бути скориговано відповідно до клінічних проявів. З трициклічними антидепресантами (амітріптілін) Посилення дисульфірам-етанолової реакції (реакції непереносимості етанолу) у разі прийому етанолу на фоні лікування дисульфірамом при одночасному прийомі трициклічних антидепресантів. З рифампіцином Дисульфірам уповільнює окислення та виведення рифампіцину нирками. З пімозидом При одночасному застосуванні з пимозидом у дуже поодиноких випадках може виникати посилення органічного мозкового синдрому. З кокаїном Дисульфірам інгібує метаболізм кокаїну, що може призводити до значного збільшення концентрації кокаїну та підвищеного ризику подовження QT.Спосіб застосування та дозиЛікування призначається після ретельного обстеження пацієнта та попередження про наслідки та ускладнення. Пацієнт не повинен приймати алкоголь (етанол) за 5-7 днів до початку лікування, тест на наявність етанолу в крові має бути негативним. Препарат приймають внутрішньо не більше 500 мг 1 раз на добу вранці під час їжі за індивідуальною схемою: доза поступово знижується до 150 мг на добу. Дозу можна змінювати у бік збільшення або зменшення залежно від реакції пацієнта. Дисульфірам-етанолова проба Через 7-10 днів проводять дисульфірам-етанолову пробу (після прийому 500 мг препарату пацієнт приймає 20-30 мл 40 % етанолу), при слабкій дисульфірам-етаноловій реакції (можливі «припливи» крові до шкіри обличчя, гіперемія шкірних покровів, нудота, блювання. , слабкість, тахікардія, зниження артеріального тиску) дозу етанолу збільшують на 10-20 мл (максимальна доза 120 мл у перерахунку на 40% етанол). Пробу повторюють через 1–2 дні у стаціонарі та через 3–5 днів амбулаторно, з корекцією доз етанолу та/або препарату за потребою. Надалі препарат можна застосовувати у підтримуючій дозі 150 мг на добу протягом 1-3 років. Не рекомендується проводити дисульфірам-етанолову пробу у пацієнтів віком від 50 років.ПередозуванняПередозування лише дисульфіраму може спровокувати розвиток порушень з боку нервової системи: порушення свідомості (у тому числі сплутаність свідомості, кому, енцефалопатію), екстрапірамідні симптоми, судоми, колапс. Передозування при прийомі комбінації дисульфірам-етанол (переважно при суїцидальних спробах) викликає пригнічення свідомості аж до коми, серцево-судинний колапс, неврологічні ускладнення. Лікування: симптоматичне, спрямоване на відновлення та підтримання функціонального стану серцево-судинної та дихальної систем.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Активна речовина: дисульфірам – 150 мг; Допоміжні речовини: крохмаль картопляний – 2,70 мг, целюлоза мікрокристалічна – 23,80 мг, кремнію діоксид колоїдний – 0,85 мг, кроскармелоза натрію – 0,85 мг, стеаринова кислота – 0,36 мг, магнію стеарат мг. По 10 таблеток у контурне осередкове пакування з плівки полівінілхлоридної та фольги алюмінієвої друкованої лакованої. По 3 або 5 контурних осередкових упаковок разом з інструкцією із застосування поміщають у пачку з картону.Опис лікарської формиКруглі, плоскоциліндричні пігулки білого або білого зі злегка жовтувато-зеленим відтінком кольору, з фаскою.Фармакотерапевтична групаЗасіб для лікування алкоголізму.ФармакокінетикаАбсорбція після перорального прийому – 70-90 %. Швидко метаболізується в печінці шляхом відновлення діетилдітіокарбамат, що виділяється у вигляді глюкуроніду нирками, або трансформується в діетиламін і сірковуглець, пропорція якого варіює від 4 до 53%. Останній виділяється через легені. Мінімальний вміст дисульфіраму в крові – близько 20 нг/мл.ФармакодинамікаДисульфірам інгібує фермент ацетальдегіддегідрогеназу, що бере участь у метаболізмі етанолу, що призводить до збільшення концентрації ацетальдегіду, що є метаболітом етанолу, в 5-10 разів. Ацетальдегід викликає ряд неприємних відчуттів: "припливи" крові до шкіри обличчя, нудоту, блювання, почуття нездужання, тахікардію, зниження артеріального тиску. В результаті відбувається вироблення умовно-рефлекторної реакції огиди до смаку та запаху спиртних напоїв. Сила реакцій, викликаних препаратом, пропорційна прийнятій дозі. Максимальний терапевтичний ефект досягається через 12 годин після перорального прийому та може тривати протягом 10-14 днів після припинення лікування. Чим триваліший курс терапії, тим більше виражені ефекти препарату.Показання до застосуванняДисульфірам використовується як допоміжна терапія хронічного алкоголізму у пацієнтів, які проходять лікування з приводу алкогольної залежності, які мають намір перебувати у стані утримання від алкоголю з метою досягнення найкращого ефекту підтримуючої та психотерапії. Дисульфірам не виліковує алкоголізм. При використанні як монотерапія, без відповідної мотивації та підтримуючого лікування не надає значного впливу на алкогольну поведінку в осіб з хронічним алкоголізмом.Протипоказання до застосуванняГіперчутливість, тиреотоксикоз, захворювання серцево-судинної системи (в т.ч., різко виражений кардіосклероз, атеросклероз мозкових судин, тяжке ураження міокарда, перед- та постінфарктні стани, аневризму аорти, оклюзія коронарних судин, артеріальна гіпертензія серцево-судинної системи в стадії декомпенсації), хронічна обструктивна хвороба легень, туберкульоз легень з кровохарканням, бронхіальна астма, виражена емфізема легень, ерозивні ураження слизової оболонки шлунково-кишкового тракту, виразкова хвороба шлунка та дванадцятипалої кишки ( кишкового тракту, хвороби нирок, печінкова недостатність, цукровий діабет, епілепсія, інфекційні захворювання центральної нервової системи, полінейропатія, неврит слухового та очного нервів,глаукоми, злоякісні пухлини, вагітність, період лактації. В окремих випадках при тривалому прийомі тетураму можуть спостерігатися гострі психози, що нагадують гострий алкогольний параноїд, гострий алкогольний галюциноз або алкогольний делірій. Можливий перехід галюцинаторного синдрому в параноїдний, параноїдний - в шизофреноподібний і т.д. Одночасний (або в недавньому минулому) прийом метронідазолу, паральдегіду, етанолу або етанолвмісних лікарських засобів та продуктів. Дитячий вік віком до 18 років. З обережністю: пацієнти старше 60 років, виразкова хвороба шлунка та дванадцятипалої кишки (в стадії ремісії), ендартеріїт, залишкові явища порушення мозкового кровообігу, психози на фоні прийому дисульфіраму в анамнезі.Вагітність та лактаціяПротипоказано застосовувати препарат при вагітності та в період годування груддю.Побічна дія"Металевий" присмак у роті, неприємний запах (обумовлений сірковуглецем) у хворих з колостомою, гепатит, неврит зорового нерва, периферичний неврит, поліневропатія нижніх кінцівок, нервово-психічні розлади, зниження пам'яті, дезорієнтація в часі та просторі, , шкірні алергічні реакції Побічні ефекти, зумовлені асоціацією дисульфіраметанол: колапс, аритмія, стенокардія, інфаркт міокарда, набряк мозку, крововилив у мозок.Взаємодія з лікарськими засобамиДисульфірам слід призначати з обережністю пацієнтам, які приймають фенітоїн та його похідні, оскільки одночасний прийом препаратів може призвести до інтоксикації фенітоїном. Перед призначенням дисульфіраму, хворим, які приймають фенітоїн, слід визначати базовий рівень фенітоїну в сироватці крові та надалі здійснювати контроль вмісту фенітоїну в крові з метою корекції дози препарату. Дисульфірам посилює ефект непрямих антикоагулянтів та збільшує ризик кровотеч. У разі одночасного призначення з пероральними антикоагулянтами необхідно здійснювати більш частий контроль вмісту протромбіну та корекцію доз антикоагулянтів. Необхідно також коригувати дозу дисульфіраму на початку та після закінчення курсу терапії, оскільки дисульфірам може подовжувати протромбіновий час. Ефекти дисульфіраму, зокрема. нейротоксичні,посилюють трициклічні антидепресанти (амітріптілін), метронідазол, ізоніазид. Метронідазол підвищує ризик розвитку порушень психіки, виникнення марення. При одночасному призначенні з ізоніазидом підвищується ризик виникнення порушень поведінки та координації рухів. При виявленні цих ознак прийом дисульфірів повинен бути припинений. Дисульфірам підвищує концентрацію в плазмі препаратів, що метаболізуються в печінці, внаслідок інгібування мікросомальних ферментів печінки. Посилює токсичні ефекти феназону, хлордіазепоксиду та діазепаму шляхом інгібування їх метаболізму. Аскорбінова кислота знижує реакцію на етанол.Спосіб застосування та дозиПеред початком лікування тривалість утримання від алкоголю повинна становити не менше 12 годин. Режим дозування на початку терапії Протягом 1 -2 перших тижнів лікування разова доза дисульфіраму повинна становити не більше 500 мг на добу. Препарат приймають вранці натще, перед сніданком. Зазвичай дисульфірам приймають у ранковий час, однак у разі появи седативного ефекту препарат може призначатися на ніч. Щоб мінімізувати або усунути седативний ефект, дозу можна скоригувати у бік зниження. Підтримуюча терапія Середня доза, що підтримує, становить 250 мг/с (діапазон від 125 до 500 мг), максимальна добова доза 500 мг. Тривалість терапії Щоденний регулярний прийом дисульфіраму повинен продовжуватися до повного одужання пацієнта, коли він може здійснювати самоконтроль над вживанням алкоголю. Прийом препарату має продовжуватись до досягнення стійкої ремісії.ПередозуванняСимптоми: сплутаність свідомості, колапс, коматозний стан, неврологічні ускладнення. Специфічного лікування передозування дисульфіраму немає. При тяжкій дисульфірам-алкогольній реакції тривалістю 1,5 год застосовують оксигенотерапію, вдихання карбогену (суміш 95 % кисню та 5 % вуглекислого газу), внутрішньовенно вводять високі дози аскорбінової кислоти (до 1 г), ефедрину сульфат та антигістамінний препарат. Необхідно моніторувати концентрацію калію в сироватці крові, особливо у випадках, якщо пацієнт приймає препарати наперстянки.Запобіжні заходи та особливі вказівкиПрепарат у жодному разі не можна приймати у стані алкогольної інтоксикації. Неприпустиме призначення препарату без попередження пацієнта. Родичі пацієнта повинні бути проінструктовані лікарем про особливості застосування препарату. Дисульфірам з особливою обережністю слід застосовувати при наступних супутніх захворюваннях: цукровий діабет, гіпотиреоз, епілепсія, хронічний та гострий нефрит, а також у пацієнтів віком від 65 років. Зареєстровані дані про гепатотоксичність препарату, включаючи печінкову недостатність, що потребує трансплантації печінки або смертельним наслідком. Тяжкі, а іноді летальні гепатити, спричинені терапією дисульфірамом, можуть розвинутись через багато місяців після завершення лікування препаратом. Пацієнта необхідно попередити про необхідність повідомляти лікаря про всі ранні симптоми прояву гепатиту, таких як швидка стомлюваність, слабкість, нездужання, зниження апетиту, нудота, блювання, жовтяниця, поява сечі темного кольору.Кожні 10-14 днів з початку терапії дисульфірамом пацієнту слід проводити контрольне дослідження параметрів функції печінки, включаючи загальний та біохімічний аналіз крові. Пацієнти, що приймають дисульфірам не повинні піддаватися впливу етилендіброміду та його пари. Результати досліджень на щурах продемонстрували, що інгаляційне введення етилендиброміду при застосуванні дисульфіраму підвищує розвиток пухлин та смертність у щурів. Аналогічних даних про дію пари діетилброміду на пацієнтів немає. Реакція взаємодії алкоголю та дисульфіраму: Пацієнт повинен бути поінформований про всі наслідки вживання алкоголю під час лікування дисульфірамом. Пацієнт повинен бути попереджений про неприпустимість таємного вживання алкоголю, а також алкоголю у складі харчових продуктів (соуси), лікарських препаратів (спиртсодержащіе лікарські засоби), парфумерії. Вживання алкоголю одночасно з дисульфірамом, навіть у невеликих кількостях викликає почервоніння обличчя, пульсацію в області голови та шиї, пульсуючий головний біль, утруднення дихання, нудоту, рвоту, пітливість, спрагу, біль за грудиною, почастішання серцебиття, задишку, слабкість, сплутаність і непритомність, виражене занепокоєння, запаморочення, порушення зору. У тяжких випадках може розвинутися пригнічення дихання, серцево-судинна недостатність, судоми та смерть. Інтенсивність реакції індивідуальна, але, як правило, пропорційна прийнятій внутрішньо кількості алкоголю і дисульфіраму. Початкові прояви реакції можуть спостерігатися у осіб з підвищеною чутливістю зі збільшенням концентрації алкоголю всього до 5-10 мг на 100 мл крові. Повний розвиток симптомів розвивається при концентрації алкоголю 50 мг на 100 мл. крові. При рівні алкоголю у крові від 125 мг до 150 мг на 100 мл відзначається непритомність. Тривалість реакції варіює від 30 - 60 хв до кількох годин; у тяжких випадках - до того часу, поки алкоголь визначається у крові. Вплив на здатність до керування автотранспортом та управління механізмами Препарат впливає здатність керувати транспортними засобами чи роботу з іншими механізмами.Умови відпустки з аптекЗа рецептомВідео на цю тему
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
Склад, форма випуску та упаковкаПігулки - 1 таб. Активної речовини: Дисульфірама (тетурама) – 150 мг; Допоміжні речовини: крохмаль картопляний – 19,97 мг, кальцію стеарат – 0,601 мг, кремнію діоксид колоїдний (аеросил) – 9,429 мг. По 10 таблеток у контурне осередкове впакування. 3 або 5 контурних упаковок разом з інструкцією по застосуванню поміщають у картонну пачку.Опис лікарської формиТаблетки білого або білого зі злегка жовтувато-зеленим відтінком кольору, круглі, плоскоциліндричної форми з фаскою.Фармакотерапевтична групаЗасіб для лікування алкоголізму.ФармакокінетикаАбсорбція після перорального прийому – 70-90 %. Швидко метаболізується в печінці шляхом відновлення діетилдітіокарбамат, екскретований у вигляді глюкуроніду нирками, або трансформується в діетиламін і сірковуглець (пропорція якого варіює від 4% до 53%). Сірковуглець виділяється через легені.ФармакодинамікаДисульфірам інгібує ацетальдегіддегідрогеназу, що бере участь у метаболізмі етанолу; збільшує концентрацію ацетальдегіду, що є метаболітом етанолу і викликає ряд неприємних відчуттів після його вживання ("припливи" крові до шкіри обличчя, нудоту, блювання, відчуття нездужання, тахікардію, зниження артеріального тиску). В результаті відбувається вироблення умовно-рефлекторної реакції огиди до смаку та запаху етанолу. Тривалість дії препарату – 48 годин.Показання до застосуванняУ складі комплексної терапії алкоголізму (поведінкова терапія, психотерапія тощо). Препарат призначається лише у разі, якщо пацієнт хоче відмовитися від вживання алкоголю з власної волі.Протипоказання до застосуванняГіперчутливість до компонентів препарату, тиреотоксикоз, захворювання серцево-судинної системи в стадії компенсації (у тому числі різко виражений кардіосклероз, атеросклероз мозкових судин, перед- та постінфарктні стани, аневризму аорти; ішемічна хвороба серця, артеріальна гіпертензія II-III ступеня, хронічна серцева туберкульоз легень з кровохарканням, бронхіальна астма, хронічна обструктивна хвороба легень, ерозивні ураження слизової оболонки шлунково-кишкового тракту, виразкова хвороба шлунка та 12-палої кишки (в стадії загострення), кровотеча із шлунково-кишкового тракту, діабет, епілепсія, нервово-психічні захворювання, інфекційні захворювання центральної нервової системи, поліневропатія, неврит слухового та зорового нервів, глаукома,злоякісні пухлини, алкогольна інтоксикація, вагітність, період лактації, дитячий вік до 18 років. З обережністю: вік старше 60 років, виразкова хвороба шлунка та 12-палої кишки (в стадії ремісії), ендартеріїт, залишкові явища порушення мозкового кровообігу, психози на фоні прийому дисульфіраму в анамнезі.Вагітність та лактаціяПротипоказаний.Побічна дія"Металевий" присмак у роті, неприємний запах (обумовлений сірковуглецем) у хворих з колостомою, гепатит, поліневропатія нижніх кінцівок, нервово-психічні розлади, зниження пам'яті, дезорієнтація у часі та просторі, астенія, головний біль, шкірні алергічні реакції. Побічні ефекти, зумовлені одночасним застосуванням дисульфіраму та вживання етанолу: серцево-судинний колапс, аритмія, стенокардія, інфаркт міокарда, набряк мозку, геморагічний інсульт, описані випадки дихальної недостатності (дихальні депресії, менінгеальні кровотечі). При прийомі доз алкоголю понад 50-80 мл (у перерахунку на 40% етанол) на фоні прийому препарату розвиваються тяжкі порушення серцево-судинної та дихальної систем, набряки, судоми. І тут терміново проводять дезинтоксикационную терапію, вводять аналептики.Взаємодія з лікарськими засобамиПротипоказані комбінації: Алкоголь. Реакція непереносимості ("припливи" крові, еритема, блювання, тахікардія). Уникати прийому спиртних напоїв та лікарських засобів, що містять спирт. Небажані комбінації: Ізоніазид. Порушення поведінки та координації. Похідні нітроімідазолу (метронідазол, ординазол, секнідазол, тинідазол). Деліріозні розлади, сплутаність свідомості. Фенітоїн. Істотний та швидкий підйом концентрації фенітоїну в плазмі з токсичними симптомами (пригнічення його метаболізму). Якщо комбінації не можна уникнути, слід проводити клінічне спостереження та контроль концентрації дисульфіраму в плазмі під час та після лікування Тетурамом. Комбінації, що потребують обережності: Варфарин (та інші непрямі антикоагулянти). Підвищений ефект непрямих антикоагулянтів та небезпека кровотечі (уповільнення метаболізму варфарину в печінці). Рекомендується частіший контроль концентрації варфарину та корекція дози антикоагулянтів протягом 8 днів після відміни Тетураму. Теофілін. Дисульфірам пригнічує метаболізм теофіліну. Як результат цього, доза теофіліну має бути знижена, залежно від клінічних симптомів та концентрації препарату у плазмі. Бензодіазепіни. Тетурам може потенціювати седативний ефект бензодіазепінів шляхом інгібування їх окисного метаболізму (особливо хлордіазепоксиду та діазепаму). Доза похідних бензодіазепіну повинна бути скоригована відповідно до клінічних проявів. Трициклічні антидепресанти. Посилення реакції непереносимості алкоголю, якщо хворі на лікування Тетурамом, приймають спиртні напої.Спосіб застосування та дозиЛікування призначається після ретельного обстеження хворого та попередження про наслідки та ускладнення. Зазвичай лікування Тетурам проводять у кілька етапів за наступною схемою. Препарат приймається внутрішньо по 150-500 мг двічі на добу. Через 7-10 днів від початку лікування проводять першу дисульфірам-алкогольну пробу (20-30 мл 40% етанол після прийому 500 мг препарату), при слабкій реакції дозу алкоголю збільшують на 10-20 мл (максимальна доза горілки 100-120 мл ). Пробу повторюють через 1-2 дні в стаціонарі та через 3-5 днів амбулаторно з корекцією доз алкоголю та/або препарату за потребою. Надалі можна використовувати підтримуючу дозу 150-200 мг на добу протягом 1-3 років.ПередозуванняСимптоми: грудка, колапс, неврологічні ускладнення. Проводять симптоматичне лікування, спрямоване на відновлення та підтримання функціонального стану серцево-судинної системи, дихальної системи.Запобіжні заходи та особливі вказівкиХворих слід попередити про небезпеку реакції непереносимості спиртних напоїв. Тетурам слід обережно приймати у хворих з нирковою недостатністю або гіпотиреозом, особливо при ризику можливого поєднання з алкоголем. Поліневропатія, що виникає при застосуванні препарату, зникає у разі призначення вітамінів групи В. У разі одночасного застосування з непрямими антикоагулянтами необхідно здійснювати частіший контроль міжнародного нормалізованого відношення та корекцію доз антикоагулянтів, що пов'язано з підвищеним ризиком розвитку кровотечі. Перед застосуванням препарату повністю ліквідувати абстинентні явища. За 1-3 дні слід повністю скасувати прийом снодійних засобів, транквілізаторів, антидепресантів та нейролептиків. Вплив на здатність до керування автотранспортом та управління механізмами Тетурам протипоказаний під час роботи водіям транспорту та іншим особам, які виконують роботу, що потребує швидких реакцій, точних рухів та концентрації уваги.Умови відпустки з аптекЗа рецептомВідео на цю тему
8 380,00 грн
169,00 грн
Склад, форма випуску та упаковкаПорошок для приготування суспензії для внутрішньом'язового введення пролонгованої дії: Порошок: налтрексон, інкапсульований у сополімер молочної та гліколевої кислоти (полімер: 75:25 DL JN1). У флаконі міститься 430 мг налтрексону (надлишок 12,9%); Розчинник: кармелоза натрію (карбоксиметилцелюлоза натрію), полісорбат 20, натрію хлорид, вода для ін'єкцій. У флаконі міститься 4,0 мл розчинника. Порошок: Кількість порошку, що містить 430 мг налтрексону (надлишок 12,9%) поміщають у скляний флакон місткістю 5 мл, закупорений гумовою пробкою та обкатаний алюмінієвим ковпачком з пластмасовою кришкою, що полегшує розтин. Розчинник: 4 мл розчинника поміщають у скляний флакон місткістю 5 мл, закупорений гумовою пробкою та обкатаний алюмінієвим ковпачком з пластмасовою кришкою, що полегшує розтин. Один флакон з порошком, один флакон з 4 мл розчинника, один 5 мл шприц, одна коротка голка для приготування суспензії, дві голки для ін'єкції із захисним ковпачком, в пачку картонну разом з інструкцією з медичного застосування.Опис лікарської формиСтерильний порошок та стерильний розчинник для приготування суспензії для внутрішньом'язового введення пролонгованої дії. Порошок від білого або майже білого до світло-жовто-коричневого кольору без видимих сторонніх включень; легко суспендується у розчиннику без утворення агломератів. Розчинник: прозора безбарвна рідина. Відновлена суспензія від білого до білого з жовтувато-коричневим відтінком кольору; повинна проходити через голку (яка входить до комплекту) з невеликим опором або без опору. Не повинно бути виходу розчинника без суспензії.Фармакотерапевтична групаЛікарські засоби для лікування алкогольної залежності.ФармакокінетикаВсмоктування Вівітрол є препаратом пролонгованої дії, призначений для внутрішньом'язових ін'єкцій кожні 4 тижні або 1 раз на місяць. Після внутрішньом'язового введення зміна концентрації налтрексону в плазмі крові характеризується початковим піком з максимумом приблизно через 2 години після введення та другим піком через 2-3 дні. Починаючи приблизно з 14-го дня після введення препарату, його концентрація в плазмі поступово знижується, але концентрація, що вимірюється, зберігається більше 1 місяця. Максимальна концентрація (Сmах) і площа під кривою "концентрація-час" налтрексону та його основного метаболіту - 6-бета-налтрексолу - у плазмі крові пропорційні введеній дозі Вівітролу. Загальна експозиція налтрексону після одноразового введення 380 мг Вівітролу в 3-4 рази вище порівняно з його вживанням у кількості 50 мг протягом 28 днів. Після першої ін'єкції рівноважна концентрація досягається до кінця міждозового інтервалу. Після повторного введення Вівітролу спостерігається мінімальна кумуляція (менше 15%) налтрексону або 6-бета налтрексолу. Розподіл Налтрексон слабо зв'язується з білками плазми in vitro (21%). Метаболізм Налтрексон піддається активному метаболізму в організмі. Основний метаболіт – 6-бета-налтрексол – утворюється цитозольним ферментом дигідродіолдегідрогеназою. Ферменти системи цитохрому Р450 беруть участь у метаболізмі налтрексона. Іншими метаболітами є 2-гідрокси-3-метокси-6-бета-налтрексол і 2-гідрокси-3-метокси-налтрексон. Налтрексон та його метаболіти утворюють кон'югати з глюкуроновою кислотою. При внутрішньом'язовому введенні Вівітролу у порівнянні з пероральним утворюється значно менше 6-бета-налтрексолу, що спричинено зниженим пресистемним метаболізмом у печінці. Виведення з організму Налтрексон та його метаболіти виводяться в основному із сечею, причому у незміненому вигляді виводиться мінімальна кількість препарату. Період напіввиведення налтрексону становить 5-10 днів і залежить від рівня деградації полімеру. Період напіввиведення 6-бета-налтрексолу становить 5-10 днів. Фармакокінетика у пацієнтів з нирковою та печінковою недостатністю Печінкова недостатність Фармакокінетика Вівітролу не змінюється у пацієнтів з легким або помірно вираженим порушенням функції печінки (класи А та В по Чайлд-П'ю). Таким хворим на корекцію дози не потрібно. У хворих із тяжким порушенням функції печінки фармакокінетика Вівітролу не вивчалась. Ниркова недостатність Результати фармакокінетичних аналізів вказують, що легка ниркова недостатність (кліренс креатиніну 50-80 мл/хв) майже не впливає на фармакокінетику Вівітролу і необхідність корекції дози препарату відсутня, У хворих з помірно вираженою та важкою нирковою недостатністю фармакокінетика Вплив статі Дослідження, проведене за участю здорових пацієнтів обох статей (18 жінок та 18 чоловіків), показало, що стать пацієнтів не впливає на фармакокінетику Вівітролу. Вплив віку та раси Фармакокінетика Вівітрола не вивчалася у літніх пацієнтів, дітей та представників різних рас.ФармакодинамікаФармакодинамічні властивості Налтрексон є антагоністом опіоїдних рецепторів з найбільшою спорідненістю до опіоїдних мю-рецепторів. Крім блокади опіоїдних рецепторів, препарат не має іншої фармакологічної активності. Застосування препарату з невідомих причин може спричинити звуження зіниці. Застосування Вівітролу не викликає звикання чи лікарської залежності. У пацієнтів з фізичною опіоїдною залежністю введення препарату спричиняє симптоми "скасування". Нейробіологічні механізми, відповідальні зниження споживання алкоголю, які спостерігаються в пацієнтів з алкогольною залежністю, які лікуються налтрексоном, зрозумілі не повною мірою, але передбачається, що механізм дії зачіпає ендогенну опіоїдну систему. Налтрексон блокує дію опіоїдів, конкурентно зв'язуючись із опіоїдними рецепторами. Блокада дії налтрексону може бути усунена запровадженням високих доз опіоїдів, що може призвести до підвищення вивільнення гістаміну з характерною клінічною картиною. Зв'язування з опіоїдними рецепторами може блокувати ефекти опіоїдних ендогенних пептидів. Вівітрол не є засобом аверсивної терапії і не викликає дисульфірамоподібної реакції при прийомі опіатів або алкоголю.Показання до застосуванняПрепарат показаний для лікування алкогольної залежності у пацієнтів, здатних утриматися від алкоголю перед початком лікування. Пацієнти не повинні активно вживати алкоголь на початку лікування Вівітролом. Препарат показаний для запобігання рецидиву опіоїдної залежності після опіоїдної детоксикації. Опіоїдзалежні пацієнти, включаючи пацієнтів, які отримують лікування проти алкогольної залежності, не повинні приймати опіоїди на початку лікування препаратом. Лікування препаратом має бути частиною відповідної програми усунення залежності, що включає психосоціальну підтримку. Діти та літні хворі Дані щодо безпеки та ефективності застосування препарату у дітей відсутні. У клінічні випробування Вівітролу було включено недостатню кількість пацієнтів старше 65 років, щоб порівняти ефект від лікування у літніх пацієнтів та у молодших хворих.Протипоказання до застосуванняВівітрол протипоказаний: хворим, які приймають наркотичні анальгетики; при прийомі опіоїдів на фоні лікування; хворим у стані гострого скасування опіоїдів (опіоїдний абстинентний синдром); хворим, які не пройшли провокаційну пробу налоксоном або мають позитивний результат аналізу на наявність опіоїдів у сечі; хворим з гіперчутливістю до діючої речовини препарату, або до будь-якого з його наповнювачів та компонентів розчинника; при тяжких порушеннях функції печінки (включаючи гострий гепатит та печінкову недостатність); ппри вагітності та лактації; дитячий вік до 18 років. З обережністю: Застосування при печінковій недостатності Пацієнтам з легким або помірно вираженим порушенням функції печінки (класи А та В по Чайлд-П'ю) корекції дози не потрібні. У хворих із тяжким порушенням функції печінки фармакокінетика Вівітролу не вивчалась. Таким пацієнтам Вівітрол, як і всі інші внутрішньом'язові ін'єкції, слід призначати з обережністю через ризик, пов'язаний із внутрішньом'язовою ін'єкцією (наприклад, за наявності тромбоцитопенії та порушення коагуляції). Застосування при нирковій недостатності Пацієнтам з легкою нирковою недостатністю (кліренс креатиніну 50-80 мл/хв) корекція дози не потрібна. У хворих з помірно вираженою та тяжкою нирковою недостатністю фармакокінетика Вівітролу не вивчалася. З огляду на те, що налтрексон та його первинний метаболіт виводяться з організму головним чином із сечею, рекомендується з обережністю призначати Вівітрол пацієнтам з помірною або тяжкою нирковою недостатністю.Вагітність та лактаціяВагітність Дія Вівітролу на вагітних жінок не вивчена. Призначати Вівітрол під час вагітності слід лише в тому випадку, якщо потенційна користь для матері від його застосування перевищує потенційний ризик для плода. Лактація При пероральному прийомі налтрексону було відзначено виділення налтрексону та 6-бета-налтрексолу з грудним молоком. Через потенційну канцерогенність та ймовірність виникнення у грудних дітей серйозних побічних явищ, слід припинити лікування препаратом Вівітрол під час годування груддю або припинити грудне вигодовування під час лікування препаратом, залежно від ступеня важливості терапії для матері.Побічна діяУ клінічних дослідженнях тривалістю до 6 місяців 9% пацієнтів з алкогольною залежністю, яких лікували Вівітролом, припинили лікування через побічні ефекти. У групі пацієнтів, яким вводили плацебо, лікування через побічні явища припинили 7% пацієнтів. Найбільш часті причини відмови від лікування Вівітролом були реакції у місці введення (3%), нудота (2%), вагітність (1%), головний біль (1%) та суїцидальна поведінка (0,3%). У групі хворих, які отримують ін'єкції плацебо, лікування припинило лише 1% пацієнтів через виникнення реакцій у місці введення. У клінічних дослідженнях тривалістю до 6 місяців 2% пацієнтів з опіоїдною залежністю, яких лікували Вівітролом, припинили лікування через побічні ефекти. У групі пацієнтів, яким вводили плацебо, лікування через побічні явища припинили 2% пацієнтів. Нижче перераховані побічні явища, у пацієнтів з алкогольною залежністю, що зустрічаються в ході клінічних досліджень у більш ніж 5% випадків (часті), ступінь виразності цих побічних явищ характеризувалася як легка та помірна. З боку шлунково-кишкового тракту: Нудота, блювання, діарея, часті позиви до дефекації, шлунково-кишковий розлад, частий рідкий випорожнення, біль у животі, дискомфорт у шлунку, сухість у роті, анорексія, зниження апетиту, порушення апетиту. З боку дихальної системи: Інфекції верхніх дихальних шляхів, ларингіт, синусит, фарингіт (у тому числі стрептококовий), назофарингіт. Загальні розлади та реакції у місці введення: Біль, болючість, ущільнення, припухлість, свербіж, крововилив, астенія, летаргія, млявість. З боку опорно-рухової системи: Артрит, біль у суглобах, скутість суглобів, біль у спині, біль у кінцівках, спазм м'язів, посмикування м'язів, скутість м'язів. З боку шкіри та підшкірних тканин: Висипання, папульозні висипання, пітниця. З боку нервової системи: головний біль, мігрень, запаморочення, непритомність, сонливість, тривога, седативний стан. Побічні явища у пацієнтів з опіоїдною залежністю були переважно такими ж, як і у пацієнтів з алкогольною залежністю. Нижче перераховані побічні явища у пацієнтів з опіоїдною залежністю, що зустрічаються в ході клінічних досліджень у понад 2% випадків (часті), ступінь виразності цих побічних явищ характеризувалася як легка та помірна. Лабораторні показники: Збільшення активності аланінамінотрансферази, аспартатамінотрансферази та гамма-глутамілтрансферази. З боку дихальної системи: Назофарингіт, грип. З боку нервової системи: Безсоння, біль голови. Серцево-судинна система: Підвищення артеріального тиску. Загальні розлади та реакції у місці введення: Біль. З боку шлунково-кишкового тракту Зубний біль. Побічні явища, виявлені під час передреєстраційних досліджень препарату: З боку шлунково-кишкового тракту: Перекручення смаку, збільшення апетиту, рефлюкс-езофагіт, запор, метеоризм, геморой, коліт, шлунково-кишкова кровотеча, паралітична непрохідність кишечника, параректальний абсцес, гастроентерит, абсцес зуба, диском. Загальні розлади та реакції у місці введення: Підвищення температури, летаргія, біль у грудях, стисненість у грудях, збільшення або зменшення маси тіла, тремтіння, озноб, набряк обличчя. Психічні розлади: Подразливість, порушення сну, синдром "скасування" алкоголю, ажитація, ейфорія, делірій. Порушення уваги, мігрень, зниження розумової діяльності, судоми, ішемічний інсульт, аневризми мозкових артерій, парестезія. З боку органів чуття: нечіткий зір, кон'юнктивіт. З боку опорно-рухової системи: Біль у кінцівках, спазм м'язів, скутість у суглобах, міалгія. З боку шкіри та підшкірних тканин: Посилене потовиділення, у тому числі вночі, свербіж. З боку дихальної системи: Біль у горлі, задишка, закладеність носа, обструктивний бронхіт, бронхіт, пневмонія, ларингіт, синусит, інфекції верхніх дихальних шляхів. З боку обміну речовин: Тепловий удар, зневоднення, гіперхолестеринемія. Серцево-судинна система: "Припливи", тромбоз глибоких вен, легеневий тромбоз, прискорене серцебиття, фібриляція передсердь, інфаркт міокарда, стенокардія, нестабільна стенокардія, хронічна серцева недостатність, атеросклероз коронарних артерій. З боку крові та лімфатичної системи: Лімфаденопатія, у тому числі запалення шийних лімфатичних вузлів, підвищення вмісту лейкоцитів у крові. З боку імунної системи: Сезонна алергія, реакції гіперчутливості, у тому числі ангіоневротичний набряк та кропив'янка, погресування ВІЛ-інфекції у ВІЛ-інфікованих пацієнтів. З боку сечостатевої системи: Мимовільний аборт, зниження лібідо, інфекції сечовивідних шляхів. З боку гепатобіліарної системи: Холелітіаз, збільшення активності аланінамінотрансферази та аспартатамінотрансферази, гострий холецистит.Взаємодія з лікарськими засобамиВзаємодія Вівітролу з іншими препаратами не вивчена. Налтрексон є антагоністом опіод-вмісних лікарських засобів (наприклад, препаратів від кашлю, застуди, антидіарейних препаратів та опіодних анальгетиків). Оскільки налтрексон є субстратом ферментів системи цитохрому, індуктори чи інгібітори цих ферментів навряд чи вплинуть на кліренс Вівітролу. Досліджень для оцінки клінічної значущості впливу інших препаратів на метаболізм Вівітролу проведено не було, тому слід бути обережним і оцінювати можливий ризик і потенційну користь при призначенні Вівітролу спільно з іншими препаратами. Показники безпеки застосування Вівітролу спільно з антидепресантами і без них однакові.Спосіб застосування та дозиВівітрол повинні вводити кваліфіковані медичні працівники тільки з використанням компонентів, що є в упаковці. Не можна замінювати компоненти упаковки. Рекомендована доза Вівітролу становить 380 мг/м один раз на 4 тижні або один раз на місяць. Препарат слід вводити в сідничний м'яз, чергуючи сідниці. Вівітрол не можна вводити внутрішньовенно та підшкірно! Якщо хворий пропустить введення чергової дози, наступна ін'єкція має бути зроблена якнайшвидше. Перед застосуванням Вівітролу не потрібний пероральний прийом налтрексону. Відновлення лікування після перерви Дані щодо відновлення лікування після перерви відсутні. Переведення хворих з алкогольною залежністю з перорального налтрексону на Вівітрол Немає систематичних даних про переведення хворих з перорального налтрексону на Вівітрол. Для приготування суспензії слід використовувати тільки розчинник, що поставляється в комплекті. Вводити препарат слід тільки голкою, що перебуває в комплекті. Усі компоненти упаковки - флакон із порошком, флакон із розчинником, голка для приготування суспензії та голка для ін'єкції із захисним ковпачком - необхідні для введення препарату. У комплекті також є запасна голка для ін'єкції із захисним ковпачком. Не замінюйте компоненти, що знаходяться в комплекті. Щоб забезпечити точне дозування, необхідно чітко дотримуватися вказівок щодо приготування та введення препарату. Дотримуйтесь правил асептики. У набір входять: 1 флакон із порошком; 1 флакон із розчинником; 1 одноразовий шприц; 1 коротка голка для приготування суспензії; 2 голки для ін'єкції із захисним ковпачком. Інструкція із застосування препарату; Перед використанням дістаньте упаковку з препаратом із холодильника та дайте їй нагрітися до кімнатної температури (приблизно 45 хвилин). Для полегшення перемішування постукайте денцем флакона з порошком по твердій поверхні, щоб розпушити порошок. Зніміть алюмінієві кришки з обох флаконів. Не використовуйте препарат, якщо кришка флаконів пошкоджена або відсутня. Протріть шийки флаконів спиртовою серветкою. Надягніть коротку голку для приготування суспензії на шприц і відберіть 3,4 мл розчинника з флакона з розчинником. У флаконі залишиться кілька розчинників. Введіть 3,4 мл розчинника у флакон із порошком. Перемішайте розчинник та порошок, інтенсивно струшуючи флакон протягом приблизно 1 хвилини. Перед тим, як продовжити, переконайтеся, що суспензія однорідна. Правильно перемішана суспензія має бути молочно-білого кольору, без грудок і вільно стікати по стінках флакона. Відразу після приготування відберіть у шприц 4,2 мл суспензії, використовуючи голку для приготування суспензії. Зніміть цю голку та надягніть на шприц голку для ін'єкції. Перед ін'єкцією постукайте по шприцю для вивільнення бульбашок повітря, потім обережно натисніть на поршень, поки в шприці не залишиться 4 мл суспензії. Суспензія готова до негайного введення. Голку шприца вводять глибоко в сідничний м'яз. Після цього підсмоктуючим рухом поршня перевіряють, чи голка не потрапила в судину (якщо потрапила, в шприц закидається кров). З появою крові необхідно повторити процедуру, попередньо замінивши голку на запасну. Препарат вводять плавним рухом глибоко в сідничний м'яз. Суспензію вводять поперемінно у різні сідниці. Вівітрол не можна вводити внутрішньовенно та підшкірно. Після введення препарату закрийте голку захисним ковпачком, притиснувши однією рукою до твердої поверхні і тримаючи в напрямку від себе. Використання ковпачка, що захищає, попереджає розбризкування рідини, яка може залишатися на голці після ін'єкції. Викиньте використані та невикористані компоненти упаковки.Запобіжні заходи та особливі вказівкиГепатотоксичність Прийом надмірних доз налтрексону може призвести до гепатоцелюлярних порушень. Налтрексон протипоказаний при гострих гепатитах та печінковій недостатності. Призначення Вівітролу пацієнтам із гострими захворюваннями печінки має бути ретельно продумане та обґрунтоване, беручи до уваги ризик виникнення порушень функції печінки. Співвідношення між безпечною дозою налтрексону та дозою, що викликає порушення печінки ≤ 5 разів. При застосуванні у рекомендованих дозах Вівітрол не є гепатотоксичним. Пацієнтів слід попередити про ризик виникнення порушень печінки та радити звертатися за медичною допомогою у разі виникнення симптомів гепатиту. У разі виникнення таких симптомів лікування Вівітролом має бути припинено. Еозинофільна пневмонія У ході клінічних досліджень було діагностовано один випадок виникнення та один випадок підозри на еозинофільну пневмонію. В обох випадках хворим була потрібна госпіталізація, лікування проводилося за допомогою антибіотиків та глюкокортикостероїдів. Слід враховувати можливість розвитку еозинофільної пневмонії у хворого, який отримує Вівітрол, та радити пацієнтам при появі таких симптомів, як прогресуюча задишка та гіпоксія, негайно звертатися за медичною допомогою. Лікарям слід зважати на можливість розвитку еозинофільної пневмонії у пацієнтів, резистентних до антибіотиків. Реакції гіперчутливості При прийомі препарату Вівітрол можуть розвиватися такі побічні явища, як кропив'янка, ангіоневротичний набряк, анафілаксія. Пацієнтів слід попередити, що у разі розвитку реакцій гіперчутливості слід негайно звернутися до лікаря та припинити подальше лікування препаратом. Передозування опіоїдів після спроби подолати їхню блокаду Після опіоїдної детоксикації у пацієнтів зазвичай знижено толерантність до опіоїдів. Вівітрол блокує ефекти екзогенних опіоїдів протягом 28 днів, проте відомі випадки смертельного передозування опіоїдами у пацієнтів, які приймали опіоїди перед введенням нової дози Вівітролу або у разі пропуску наступної ін'єкції Вівітролу. Пацієнти, які пройшли лікування Вівітролом, можуть бути чутливі до менших доз опіоїдів, ніж до лікування. Це може спричинити потенційно небезпечну для життя опіоїдну інтоксикацію (дихальну недостатність або зупинку дихання, колапс тощо). Слід попередити пацієнтів про те, що після припинення лікування Вівітролом вони можуть виявитися чутливими до нижчих доз опіоїдів. Важливо пам'ятати про зниження толерантності до опіоїдів наприкінці інтервалу дозування, тобто приблизно через місяць після ін'єкції препарату та у разі пропуску наступної ін'єкції. Пацієнтів та членів їх сімей слід попередити про підвищену чутливість до опіоїдів та ризик передозування опіоїдами. Незважаючи на те, що Вівітрол є сильним антагоністом опіоїдних рецепторів із тривалим фармакологічним ефектом, викликану ним блокаду можна подолати. Пацієнти, які намагаються подолати цю блокаду введенням великих доз екзогенних опіоїдів, ризикують отримати смертельну дозу опіоїдів і надати своє життя небезпеці. Концентрація опіоїдів у плазмі відразу після їх прийому може бути достатньою для подолання конкурентної блокади опіоїдних рецепторів, і як наслідок у пацієнта може миттєво розвинутись опіоїдна інтоксикація, що загрожує життю, що виявляється пригніченням дихання, колапсом. Пацієнти повинні усвідомлювати всю серйозність наслідків спроб подолати блокаду опіоїдних рецепторів. Вплив препарату на тривалість сутичок та пологи Вплив препарату на тривалість переймів та пологи невідомий. Вплив препарату на лабораторні показники крові У пацієнтів, які отримують лікування Вівітролом, було відзначено підвищення вмісту еозинофілів у крові, проте після кількох місяців лікування вміст еозинофілів нормалізувався. У пацієнтів, які отримують високі дози, спостерігалося зниження вмісту тромбоцитів у середньому на 17, 8 х 103 мкл. Однак під час рандомізованих контрольованих досліджень вплив Вівітролу на збільшення кровотеч не доведено. У пацієнтів з опіоїдною залежністю, які отримували лікування препаратом протягом 24 тижнів, спостерігалося зниження вмісту тромбоцитів у середньому на 62,8 х 103 мкл. У пацієнтів у групі плацебо вміст тромбоцитів знижувався в середньому на 39,9 х 103 мкл. Однак під час рандомізованих контрольованих досліджень вплив Вівітролу на збільшення кровотеч не доведено. Підвищення активності аспартатамінотрансферази в крові на фоні лікування Вівітролом було таким самим, як при лікуванні пероральним налтрексоном і становило 1,5% порівняно з 0,9% у групі пацієнтів, які отримують плацебо. У клінічних дослідженнях тривалістю до 6 місяців за участю пацієнтів з опіоїдною залежністю 89% пацієнтів було поставлено діагноз гепатиту С, 41% пацієнтів – ВІЛ-інфекція. У дослідженні часто спостерігалося збільшення активності "печінкових" ферментів (аланінамінотрансферази, аспартатамінотрансферази та гамма-глутамілтрансферази). Ці побічні явища частіше спостерігалися у групі пацієнтів, які отримують лікування Вівітролом 380 мг, ніж у групі пацієнтів, які отримують плацебо. Пацієнтів з активністю аланінамінотрансферази або аспартатамінотрансферази, що перевищує верхню межу норми більш ніж утричі, не включали до дослідження. У пацієнтів, які отримували лікування Вівітролом, підвищення активності трансаміназ більш ніж у 3 рази порівняно з верхньою межею норми та потребу негайного лікування спостерігалося частіше, ніж у пацієнтів, які отримують плацебо. Таке збільшення активності ферментів спостерігалося у 20% пацієнтів, які отримували лікування Вівітролом, порівняно з 13% пацієнтів у групі плацебо. Підвищення активності аспартатамінотрансферази більш ніж утричі порівняно з верхньою межею норми також частіше спостерігалося у групі пацієнтів, які отримували лікування Вівітролом (14%), порівняно з пацієнтами у групі плацебо (11%). У пацієнтів з опіоїдною залежністю, які отримували лікування Вівітролом, активність аланінамінотрансферази підвищувалася в середньому на 61 МО/л, у пацієнтів у групі плацебо – в середньому на 48 МО/л. У пацієнтів з опіоїдною залежністю, які отримували лікування Вівітролом, активність аспартатамінотрансферази підвищувалася в середньому на 40 МО/л, у пацієнтів у групі плацебо – в середньому на 31 МО/л. У ході клінічних досліджень у пацієнтів, які отримують Вівітрол, спостерігалося підвищення активності креатинфосфокінази, як правило, у 1-2 рази порівняно з верхньою межею норми. Подібне підвищення активності креатинфосфокінази спостерігається також під час лікування пероральним налтрексоном. Однак відомі випадки 4-кратного і навіть 35-кратного підвищення активності цього ферменту в групі пацієнтів, які отримують пероральний налтрексон та Вівітрол відповідно. У 39% пацієнтів з опіоїдною залежністю, які отримували лікування Вівітролом, спостерігалося підвищення активності креатинфосфокінази вище нормальних значень, у групі пацієнтів, які отримували плацебо, підвищення активності креатинфосфокінази спостерігалося у 32% пацієнтів. У деяких випадках у пацієнтів, які отримували плацебо, активність креатинфосфокінази підвищувалась у 41,8 разів у порівнянні з верхньою межею норми; у групі пацієнтів, які отримували лікування Вівітролом, відомі випадки підвищення активності креатинфосфокінази у 22,1 рази порівняно з верхньою межею норми. При проведенні деяких імуноферментних аналізів сечі можлива поява хибнопозитивних результатів на низку препаратів, особливо на опіоїди. Додаткова інформація наводиться в інструкціях щодо проведення конкретних аналізів. Попередження та запобіжні заходи Усунення блокади Вівітролу В екстреній ситуації у випадку з пацієнтами, які отримують лікування Вівітролом, передбачуваним способом зняття болю є регіонарна аналгезія, седація бензодіазепіном та застосування ненаркотичних аналгетиків або загальної анестезії. У ситуаціях, що вимагають застосування наркотичної аналгезії, необхідна доза опіоїдів може виявитися вищою за звичайну, внаслідок чого пригнічення дихання може бути більш глибоким і тривалим. Переважно застосування швидкодіючого наркотичного аналгетика, що знижує тривалість пригнічення дихання. Кількість анальгетика, що вводиться, слід визначати відповідно до потреб пацієнта. Можуть виникнути неопосередковані рецепторами явища (наприклад, набряк обличчя, свербіж, генералізована еритема або бронхоспазм), ймовірно, через секрецію гістаміну. Незалежно від засобу, вибраного для усунення блокади Вівітролу, пацієнт повинен піддаватися ретельному моніторингу відповідним кваліфікованим медперсоналом у спеціально обладнаному відділенні реанімації. Депресія та суїцидальна поведінка Під час контрольованих клінічних досліджень Вівітролу несприятливі явища суїцидального характеру (суїцидальні думки, спроби самогубства, вчинені самогубства) були нечастими, проте зустрічалися у групі пацієнтів, які отримують лікування Вівітролом частіше, ніж у групі пацієнтів, які отримують плацебо (1% проти 0). У деяких випадках суїцидальні думки та поведінка з'являлися у пацієнта після завершення дослідження, але були наслідком депресії, що розвинулася під час лікування препаратом. Мали місце два скоєні самогубства, в обох випадках пацієнти лікувалися Вівітролом. Припинення прийому препарату, пов'язане з проявом депресії, частіше відбувалося у групі пацієнтів, які приймають Вівітрол (1%), ніж у групі плацебо (0). У 24-тижневому плацебо-контрольованому дослідженні несприятливі явища, пов'язані з депресивними настроями, спостерігалися у 10% пацієнтів, які отримують лікування Вівітролом у дозі 380 мг, а у групі пацієнтів, які отримують ін'єкції плацебо – у 5%. Слід уважно стежити за появою ознак депресії або суїцидальних думок у пацієнтів із алкогольною залежністю, у тому числі пацієнтів, які отримують лікування Вівітролом. Членів сімей та доглядачів за пацієнтами людей слід попередити про необхідність уважно стежити за виникненням симптомів депресії або суїцидальної поведінки та негайно повідомляти про виникнення таких симптомів лікарю. Реакції у місці ін'єкції Ін'єкції Вівітролу можуть супроводжуватися болем, хворобливістю, ущільненням, припухлістю, еритемою та свербінням. Під час клінічних досліджень у одного пацієнта утворилося ущільнення, яке через 4 тижні після ін'єкції продовжувало збільшуватись з подальшим розвитком некрозу, для видалення якого знадобилося хірургічне втручання. У ході постреєстраційних спостережень були відмічені інші випадки реакцій у місці ін'єкції, що включають абсцес, стерильний абсцес, ущільнення та некроз, для усунення деяких з них знадобилося хірургічне втручання. Пацієнтів слід попереджати про необхідність інформувати лікаря про виникнення будь-якої реакції в місці ін'єкції препарату. Скасування алкоголю Застосування Вівітролу не тільки не виключає, а й не знижує прояву симптомів, пов'язаних зі скасуванням прийому алкоголю. Оклюзія сітківки Оклюзія ретинальної артерії після ін'єкції іншого лікарського засобу, що містить кополімер молочної та гліколевої кислоти, у постреєстраційних дослідженнях зустрічалася дуже рідко, і мала місце за наявності аномального артеріовенозного анастомозу. Під час клінічних та післяреєстраційних досліджень Вівітролу не було відзначено жодного випадку непрохідності ретинальної артерії. Вівітрол слід застосовувати у вигляді ін'єкції в сідничний м'яз і уникати випадкового попадання в кровоносну судину. Вплив на здатність до керування автотранспортом та управління механізмами У ході лікування препаратом Вівітрол може виникати запаморочення. У разі виникнення запаморочення слід утриматися від керування транспортом, а також від роботи з технікою.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаСуміш "Зінал Компаунд" (Zinal Compound) - амінокислотний хелат цинку, янтарна кислота, хлорела, глютамінова кислота, корінь елеутеракокка колючого, кореневища імбиру аптечного, екстракт гінкго білоба, спіруліну, 5 В.ХарактеристикаІталійський продукт ЗіналПро від бренду Mediana Group, єдиний препарат, що ефективно запобігає симптомам похмілля, що нейтралізує алкоголь у крові протягом короткого часу. Усуває запах алкоголю (перегар) і потяг до вживання алкоголю наступного дня. Має виражений протверезний ефект. Активні компоненти ЗіналПро сприяють очищенню та захисту печінки від токсичних речовин, що утворюються в результаті розпаду етанолу.РекомендуєтьсяЯк біологічно активну добавку до їжі - додаткового джерела вітаміну В1, цинку, джерела елеутеразидів, флавоноїдів (флавонолів та їх глікозидів) та янтарної кислоти.Протипоказання до застосуванняПідвищена нервова збудливість, безсоння, підвищений артеріальний тиск, порушення ритму серцевої діяльності, індивідуальна непереносимість компонентів, вагітність, годування груддю. Перед застосуванням рекомендується проконсультуватися з лікарем.Спосіб застосування та дозиПри вживанні протягом вечора помірних доз алкоголю, відповідних 200 грн. міцного алкоголю (40 градусів та вище) або 0,75 л. (сухого вина) – по 3 капсули після закінчення прийому алкоголю або перед сном. При вживанні високих доз міцного алкоголю до 300 - 500 гр. або 1,5л. сухого вина – по 4 капсули після закінчення прийому алкоголю або перед сном. Для досягнення гарного самопочуття (протверезний ефект) - по 2-3 капсули разово. Для досягнення ефекту тверезості, збереження ясності розуму, відсутності характерних ознак сп'яніння, при прийомі великих доз алкоголю під час проведення переговорів, заходів, вечірок тощо – по 4 капсули до та 4 капсули під час прийому алкоголю. Для зниження тяги до вживання алкоголю та корекції рівня цинку в організмі (при легкому або помірному дефіциті) – по 1 капсулі вранці та ввечері протягом 3-х місяців. Для повного усунення дефіциту цинку - по 1 капсулі вранці і ввечері протягом 6 місяців.Запобіжні заходи та особливі вказівкиПеред застосуванням проконсультуйтеся зі спеціалістом.Умови відпустки з аптекБез рецептаВідео на цю тему
Фасування: N10 Форма випуску: порошок Упаковка: стіки Виробник: Біотики Завод-виробник: Біотики(Росія). . .
Склад, форма випуску та упаковкаМіститься 60 мг кореневища Аїра, 16 мг листя м'яти перцевої, а також допоміжний неактивний компонент – сорбіт, цукор та мікрокристалічна целюлоза. Випускається у таблетках для розсмоктування 0,5 г, запечатаних у флакони по 100 табл. Опис лікарської формиТаблетки для розсмоктування.