Лекарства и БАД Со скидкой
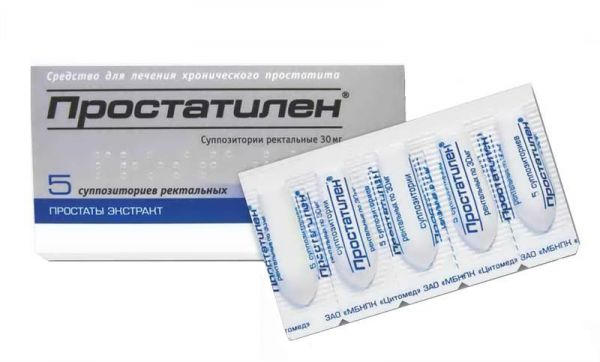
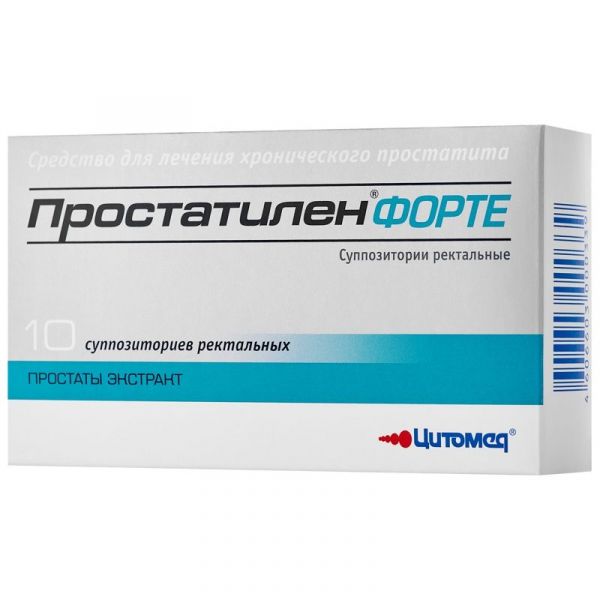
Склад, форма випуску та упаковкаСупозиторії ректальні – 1 супп.: екстракт простати (субстанція Простатилен є екстрактом простати з додаванням гліцину) - 50 мг; Допоміжні речовини: диметилсульфоксид – 90 мг, макрогол 1500 – достатня кількість для отримання супозиторію масою 2.8 г. 5 штук. - упаковки осередкові контурні (1) - пачки картонні. 5 штук. - упаковки осередкові контурні (2) - пачки картонні.Опис лікарської формиСупозиторії ректальні торпедоподібної форми, від білого до жовтого кольору, допускається мармуровість; на зрізі допускається мармуровість, наявність повітряного стрижня або торпедоподібного заглиблення.Фармакотерапевтична групаПрепарат тваринного походження, що застосовується при захворюваннях передміхурової залози.ФармакокінетикаДані про фармакокінетику препарату не надано.ФармакодинамікаПрепарат тваринного походження. Має органотропну дію на передміхурову залозу. Зменшує рівень набряку, лейкоцитарної інфільтрації передміхурової залози, нормалізує секреторну функцію епітеліальних клітин, збільшує число лецитинових зерен у секреті ацинусів, стимулює м'язовий тонус сечового міхура. Зменшує тромбоутворення, має антиагрегантну активність, перешкоджає розвитку тромбозу венул у передміхуровій залозі.Показання до застосуванняхронічний абактеріальний простатит; стани до та після оперативних втручань на передміхуровій залозі; доброякісна гіперплазія передміхурової залози.Протипоказання до застосуваннядитячий та підлітковий вік до 18 років; - підвищена чутливість до компонентів препарату.Вагітність та лактаціяЖінкам препарат не призначається. Протипоказане призначення дітям віком до 18 років.Побічна діяАлергічні реакції: кропив'янка. У разі алергічних реакцій слід припинити лікування, призначити антигістамінні препарати.Взаємодія з лікарськими засобамиСумісний із антибактеріальними препаратами, що застосовуються для лікування простатиту.Спосіб застосування та дозиСупозиторії ректально вводять по 1 шт. (50 мг) 1 раз на добу (вранці або ввечері). Супозиторій глибоко вводять у задній прохід після дефекації або очисної клізми. Перед застосуванням супозиторій слід змочити водою. Після введення бажано перебування хворого на ліжку протягом 30-40 хвилин. Курс лікування – не менше 10 днів при хронічному простатиті, не менше 15 днів – при доброякісній гіперплазії передміхурової залози.ПередозуванняПрепарат Простатилен не токсичний, передозування не спостерігалося.Запобіжні заходи та особливі вказівкиОсобливостей дії при першому введенні та при його відміні препарат не має. Застосування препарату при хронічних захворюваннях особливостей немає.Умови зберіганняУ холодильнику +2+8 градусівУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаТаблети - 1 таб. Активні речовини: кофеїн – 50,0 мг, парацетамол – 250,0 мг, пропіфеназон – 150,0 мг; допоміжні речовини: целюлоза мікрокристалічна - 100,0 мг, кроскармелозу натрію - 8,0 мг, карбоксиметилкрохмаль натрію - 44,8 мг, повідон (полівінілпіролідон) - 18,0 мг, кремнію діоксид колоїдний - 3,2 мг, маг 0 мг. Пігулки. По 10 таблеток у контурне осередкове пакування з плівки полівінілхлоридної та фольги алюмінієвої друкованої лакованої. По 10, 20, 30, 40, 50, 60 або 100 таблеток у банки полімерні для лікарських засобів. Одну банку або 1, 2, 3, 4, 5, 6 або 10 контурних осередкових упаковок разом з інструкцією із застосування поміщають у пачку з картону.Опис лікарської формиКруглі пігулки від білого до білого з бежевим відтінком кольору, з незначною мармуровістю, плоскоциліндричною формою, з фаскою з двох боків та ризиком з одного боку.Фармакотерапевтична групаАналгезуючий засіб комбінований (НПЗП+аналгезуючий ненаркотичний засіб+психостимулюючий засіб).ФармакокінетикаПарацетамол Абсорбція – висока, зв'язок з білками плазми – 15%, час досягнення максимальної концентрації у плазмі крові (ТСтах) – 20-30 хв. Проникає через гематоенцефалічний бар'єр (ГЕБ). Менше 1% від прийнятої матір'ю, що годує, дози проникає в грудне молоко. Терапевтична ефективна концентрація парацетамолу у плазмі досягається при його призначенні у дозі 10-15 мг/кг. Метаболізується в печінці: 80% вступає в реакцію кон'югації з глюкуроновою та сірчаною кислотами з утворенням неактивних метаболітів; 17% піддається гідроксилювання з утворенням неактивних метаболітів, які кон'югують з глутатіоном та утворюють неактивні метаболіти. При нестачі глутадіону ці метаболіти можуть блокувати ферментні системи гепатоцитів та викликати їхній некроз. Період напіввиведення – 2-3 год. У літніх пацієнтів знижується кліренс парацетамолу та збільшується період напіввиведення. Виводиться нирками у незміненому вигляді 3%. Пропіфеназон Максимальна концентрація пропіфеназону у плазмі досягається через 30 хв. Метаболізується у печінці. Період напіввиведення становить 1-1,5 год. Поєднання з парацетамолом збільшує час його виведення на 40%, що відіграє значну роль, тому що дозволяє скоротити кількість прийомів препарату протягом доби. Виводиться нирками. Кофеїн Час досягнення максимальної концентрації – 1 год; період напіввиведення – 3,5 год; 65-80% кофеїну виводиться нирками головним чином у вигляді 1-метилксатину, 1-метилмочової кислоти та ацетильованих похідних урацилу, невелика кількість перетворюється на теофілін та теобромін.ФармакодинамікаСафістон є комбінованим препаратом, дія якого визначається компонентами, що входять до його складу. Поєднання трьох компонентів препарату призводить до взаємного посилення їхньої фармакологічної дії. Парацетамол і пропіфеназон мають знеболювальну і жарознижувальну дію. Парацетамол – ненаркотичний аналгетик. Блокує циклооксигеназу (ЦОГ) лише у центральній нервовій системі (ЦНС), впливаючи на центри болю та терморегуляції (у запалених тканинах клітинні пероксидази нейтралізують вплив парацетамолу на ЦОГ), що пояснює практично повну відсутність протизапального ефекту. Відсутність впливу на синтез простогландинів (ПГ) у периферичних тканинах обумовлює відсутність у нього негативного впливу на водно-сольовий обмін (затримка натрію та води) та слизову оболонку шлунково-кишкового тракту. Пропіфеназон є похідним піразолону. Механізм дії здійснюється шляхом інгібування ЦОГ, що бере участь у освіті простагландинів з арахідонової кислоти. Кофеїн підвищує рефлекторну збудливість спинного мозку, збуджує дихальний та судинно-руховий центри, розширює кровоносні судини скелетних м'язів, головного мозку, серця, нирок, знижує агрегацію тромбоцитів; зменшує сонливість, відчуття втоми. У даній комбінації кофеїн у малій дозі практично не чинить стимулюючої дії на центральну нервову систему, проте сприяє регуляції тонусу судин мозку, зменшує сонливість, посилює болезаспокійливу дію інших компонентів препарату.Показання до застосуванняЗастосовують для усунення больового синдрому слабкої та середньої інтенсивності різного генезу: головний біль, мігрень, зубний біль, артралгії, міалгії, альгодисменорея, а також як жарознижувальний засіб при гарячкових станах на тлі інфекційно-запальних захворювань (ГРВІ, у тому числі грип і т .П.).Протипоказання до застосуванняПідвищена чутливість до компонентів препарату, тяжка ниркова та/або печінкова недостатність, дефіцит ферменту глюкозо-6-фосфатдегідрогенази, пригнічення кістковомозкового кровотворення (лейкопенія, анемія, в т.ч. гемолітична), гостра гематопорфірія, повне або небронхіальне носа і приносових пазух і непереносимості ієстероїдних протизапальних препаратів (у тому числі в анамнезі), стани, що супроводжуються пригніченням дихання, внутрішньочерепна гіпертензія, гострий інфаркт міокарда, ішемічна хвороба серця, аритмії, артеріальна гіпертензія, виразкова хвороба, , період лактації у жінок, дитячий вік до 12 років З обережністю доброякісні гіпербілірубінемії (в т.ч. синдром Жільбера, Дубіна-Джонсона, Ротора), літній вік, алкоголізм, епілепсія та схильність до судомних нападів.Вагітність та лактаціяЗастосування препарату при вагітності та в період грудного вигодовування протипоказане.Побічна діяЗ боку центральної нервової системи: запаморочення, безсоння. З боку шлунково-кишкового тракту: нудота, блювання, тяжкість та неприємні відчуття в ділянці шлунка. Порушення з боку кровотворної системи: тромбоцитопенія, агранулоцитоз, гемолітична анемія. Алергічні реакції: висипання на шкірі, свербіж, кропив'янка, набряк Квінке, мультиформна ексудативна еритема (в т.ч. синдром Стівенса-Джонсона), токсичний епідермальний некроліз (синдром Лайєла).Взаємодія з лікарськими засобамиЕфективність препарату може знизитись при одночасному застосуванні з холістираміном, холінолітиками, антидепресантами, лужними речовинами. При одночасному застосуванні Сафістону з барбітуратами, протисудомними препаратами, етанолом значно підвищується гепатотоксична дія. Метоклопрамід прискорює всмоктування парацетамолу. Під впливом парацетамолу період напіввиведення хлорафеніколу збільшується у 5 разів. Одночасне застосування парацетамолу у високих дозах збільшує ефект антикоагулянтів. Мієлотоксичні засоби посилюють прояви гематотоксичності парацетамолу. Кофеїн прискорює всмоктування ерготаміну; знижує всмоктування препаратів кальцію; знижує ефект наркотичних та снодійних засобів, збільшує виведення препаратів літію; прискорює всмоктування та посилює дію серцевих глікозидів, підвищує їх токсичність. Одночасне застосування кофеїну з бета-адреноблокаторами може призводити до взаємного придушення терапевтичних ефектів, з бета-адреноміметиками до додаткової стимуляції центральної нервової системи та інших токсичних ефектів. Кофеїн може знижувати кліренс теофіліну, і можливо інших ксантинів, збільшуючи можливість адитивних фармакодинамічних та інших токсичних ефектів. Інгібітори моноамінооксидази, фуразолідон, прокарбазин, селегілін та великі дози кофеїну можуть викликати розвиток небезпечних аритмій серця або виражене підвищення артеріального тиску.Нікотин підвищує швидкість виведення кофеїну. Кофеїн є антагоністом аденозину. Пропіфеназол може посилювати дію пероральних гіполіпідемічних засобів, сульфаніламідних препаратів, антикоагулянтів, ульцерогенний ефект глюкокортикостероїдів, знижує ефективність калійзберігаючих діуретиків.Спосіб застосування та дозиПризначають дорослим по 1 – 2 таблетки, дітям 12-18 років – 1 таблетку 1-3 рази на добу, бажано через 1-2 години після їжі, запиваючи великою кількістю рідини. Максимальна разова доза – 2 таблетки. Добова доза не повинна перевищувати 6 таблеток. Препарат не слід приймати більше 5 днів як знеболюючий засіб і не більше 3 днів як жарознижувальний засіб без призначення та спостереження лікаря. Збільшення добової дози або тривалості лікування можливе лише під наглядом лікаря. Не перевищуйте рекомендовану дозу.ПередозуванняСимптоми: (обумовлені парацетамолом, виявляються після прийому 10-15 г) блідість шкірних покривів, зниження апетиту, нудота, блювання, біль в епігастральній ділянці, гепатотоксична та нефротоксична дія, у тяжких випадках - печінкова недостатність, гепатонекроз, підвищення активності , збільшення протромбінового часу, енцефалопатія та коматозний стан Лікування: промивання шлунка, призначення активованого вугілля, симптоматична терапія, введення донаторів SH-груп та попередників синтезу глутатіону – метіоніну через 8-9 годин після передозування та N-ацетилцистеїну через 12 годин. Високі дози кофеїну викликають наступні симптоми: головний біль, тремор, дратівливість, гастралгія, ажитація, руховий неспокій, сплутаність свідомості, тахікардія, аритмія, гіпертермія, прискорене сечовипускання, головний біль, нудота, блювота, дзвін тоніко-клонічні). Лікування: промивання шлунка, прийом активованого вугілля, проносних засобів, підтримка вентиляції легень та оксигенації, при судомах внутрішньовенно діазепам, фенобарбітал, підтримка водно-електролітного балансу.Запобіжні заходи та особливі вказівкиПри тривалому застосуванні препарату (більше 5 днів) потрібний контроль картини периферичної крові та функціонального стану печінки. Під час лікування слід відмовитися від вживання алкогольних напоїв (підвищення ризику шлунково-кишкової кровотечі). Надмірне вживання кофеїновмісних продуктів (кава, чай) на фоні лікування може викликати симптоми передозування. Прийом препарату може ускладнити встановлення діагнозу при гострому абдомінальному больовому синдромі. Вплив на здатність до керування автотранспортом та управління механізмами У період прийому препарату слід дотримуватися обережності при керуванні транспортними засобами та зайнятті іншими видами діяльності, що потребує підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
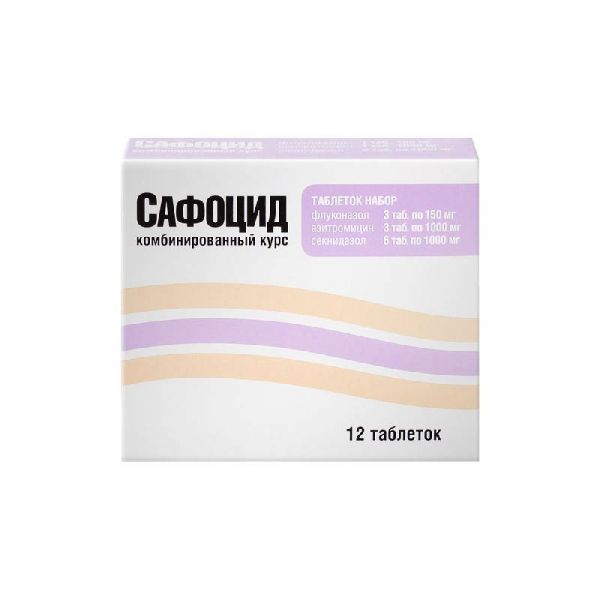
Склад, форма випуску та упаковкаФлуконазол 1 таблетка містить: активна речовина: флуконазол – 150 мг; допоміжні речовини: целюлоза мікрокристалічна, кальцію гідрофосфат, кроскармелоза натрію, магнію стеарат, діоксид колоїдний кремнію, барвник червоний [Понсо 4R] [Е 124]. Азітроміцин 1 таблетка, покрита плівковою оболонкою, містить: активна речовина: азитроміцин дигідрат – 1048 мг (у перерахунку на азитроміцин – 1000 мг); допоміжні речовини: натрію лаурилсульфат, кроскармелоза натрію, повідон-К30, магнію стеарат, кремнію діоксид колоїдний; склад оболонки: гіпромелоза (гідроксипропілметилцелюлоза), діетилфталат, тальк, титану діоксид, макрогол-4000, барвник червоний [Понсо 4R] [Е 124]. Секнідазол 1 таблетка, покрита плівковою оболонкою, містить: активна речовина: секнідазол – 1000 мг; допоміжні речовини: крохмаль кукурудзяний, целюлоза мікрокристалічна, кремнію діоксид колоїдний, карбоксиметилкрохмаль натрію, повідон (PVPK - 30), тальк, магнію стеарат; склад оболонки: гіпромелоза (гідроксипропілметилцелюлоза), діетилфталат, тальк, титану діоксид, макрогол-4000. Таблеток набір. По 4 таблетки (одна таблетка – флуконазол, одна таблетка – азитроміцин, дві таблетки – секнідазол) у контурне осередкове пакування (блістер) з плівки полівінілхлоридної та фольги алюмінієвої. 1 або 3 блістери разом з інструкцією із застосування в картонну пачку.Опис лікарської формиТаблеток набірХарактеристикаФлуконазол Плоскоциліндричні таблетки рожевого кольору з фаскою та ризиком. На зламі пігулки рожевого кольору. Азітроміцин Капсулоподібні двоопуклі таблетки, покриті плівковою оболонкою рожевого кольору, з ризиком. На зламі ядро таблетки білого або майже білого кольору. Секнідазол Капсулоподібні двоопуклі таблетки, покриті плівковою оболонкою білого або майже білого кольору, з ризиком. На зламі пігулки білого або майже білого кольору.ФармакокінетикаФлуконазол Абсорбція – висока, біодоступність – 90%. Одночасний прийом їжі не впливає на абсорбцію препарату. Після прийому внутрішньо натще 150 мг час досягнення максимальної концентрації - 0,5-1,5 год, максимальна концентрація флуконазолу в плазмі (Cmax) становить 90% від концентрації в плазмі при внутрішньовенному введенні в дозі 2,5-3,5 мг/л . Зв'язок із білками плазми – 11-12%. Концентрація в плазмі залежить від дози. Флуконазол добре проникає у всі біологічні рідини організму. Концентрація активної речовини в грудному молоці, суглобовій рідині, слині, мокротинні та перитонеальній рідині аналогічна такій у плазмі. Постійні значення у вагінальному секреті досягаються через 8 годин після прийому внутрішньо і утримуються на цьому рівні не менше 24 годин. Добре проникає в спинномозкову рідину (СМР),при грибковому менінгіті концентрація у СМР становить близько 85% від такої у плазмі. У потовій рідині, епідермісі та роговому шарі (селективне накопичення) досягаються концентрації, що перевищують сироваткові. Обсяг розподілу наближається до загального вмісту води у організмі; період напіввиведення (T1/2) флуконазолу становить близько 30 год. Виводиться переважно нирками (80% – у незміненому вигляді, 11% – у вигляді метаболітів). Кліренс флуконазолу пропорційний кліренсу креатиніну (КК). Фармакокінетика флуконазолу суттєво залежить від функціонального стану нирок, при цьому існує зворотна залежність між T1/2 та КК. Після гемодіалізу протягом 3 годин концентрація флуконазолу у плазмі знижується на 50%. Тривалий період напіввиведення з плазми дозволяє приймати флуконазол при вагінальному кандидозі одноразово. Азітроміцин Азитроміцин швидко всмоктується із шлунково-кишкового тракту (ЖКТ), що зумовлено його стійкістю у кислому середовищі та ліпофільністю. Після прийому внутрішньо 500 мг максимальна концентрація азитроміцину в плазмі досягається через 2,5 - 2,96 год і становить 0,4 мг/л. Біодоступність становить 37%. Азитроміцин добре проникає у дихальні шляхи, органи та тканини урогенітального тракту (зокрема у передміхурову залозу), у шкіру та м'які тканини. Висока концентрація в тканинах (у 10-50 разів вища, ніж у плазмі крові) та тривалий період напіввиведення зумовлені низьким зв'язуванням азитроміцину з білками плазми крові, а також його здатністю проникати в еукаріотичні клітини та концентруватися у середовищі з низьким рН, що оточує лізосоми. Це, у свою чергу, визначає великий обсяг розподілу (31,1 л/кг) і високий плазмовий кліренс.Здатність азитроміцину накопичуватись переважно у лізосомах особливо важлива для елімінації внутрішньоклітинних збудників. Доведено, що фагоцити доставляють азитроміцин у місця локалізації інфекції, де він вивільняється у процесі фагоцитозу. Концентрація азитроміцину в осередках інфекції достовірно вища, ніж у здорових тканинах (в середньому на 24-34%) та корелює зі ступенем запального набряку. Незважаючи на високу концентрацію у фагоцитах, азитроміцин не істотно впливає на їх функцію. Азитроміцин зберігається у бактерицидних концентраціях протягом 5-7 днів після прийому останньої дози. У печінці деметилюється, метаболіти, що утворюються, не активні. У азитроміцину дуже довгий період напіввиведення – 35-50 год. Період напіввиведення із тканин значно більший. Азитроміцин виводиться, в основному, у незміненому вигляді – 50% кишечником,6% нирками. Секнідазол Після прийому внутрішньо швидко всмоктується із ШКТ; біодоступність – близько 80%. Після одноразового прийому внутрішньо 2 г максимальна концентрація в плазмі досягається через 3-4 години. Метаболізується в печінці. Період напіввиведення секнідазолу з плазми становить близько 25 год. Препарат повільно виводиться з організму, в основному нирками; близько 50% прийнятої дози екскретується за 120 год. Проходить через гематоенцефалічний та плацентарний бар'єри, екскретується у грудне молоко.ФармакодинамікаФлуконазол Триазольний протигрибковий засіб є потужним селективним інгібітором синтезу стеролів у клітині грибів. Має високоспецифічну дію, інгібуючи активність ферментів грибів, залежних від цитохрому P450. Блокує перетворення ланостеролу клітин грибів на мембранний ліпід - ергостерол; збільшує проникність клітинної мембрани, порушує її зростання та реплікацію. Флуконазол продемонстрував активність in vitro та у клінічних дослідженнях щодо наступних мікроорганізмів: Candida albicans, Candida glabrata (багато штами помірно чутливі), Candida parapsilosis, Candida tropicalis, Cryptococcus neoformans. Активний при опортуністичних мікозах, у т.ч. викликаних Candida spp. (включаючи генералізовані форми кандидозу на фоні імунодепресії), Cryptococcus neoformans та Coccidioides immitis (включаючи внутрішньочерепні інфекції),Microsporum spp. та Trichophyton spp; при ендемічних мікозах, спричинених Blastomyces dermatidis, Histoplasma capsulatum (в т.ч. при імунодепресії). Не має антиандрогенної активності. Азітроміцин Антибактеріальний засіб широкого спектра дії, азалід, діє бактеріостатично. Зв'язуючись із 50S субодиницею рибосом, пригнічує пептидтранслоказу на стадії трансляції, пригнічує синтез білка, уповільнює ріст та розмноження бактерій, у високих концентраціях має бактерицидний ефект. Має активність щодо низки грампозитивних, грамнегативних, анаеробних, внутрішньоклітинних та інших мікроорганізмів. У більшості випадків до азитроміцину чутливі: аеробні грампозитивні мікроорганізми: Staphylococcus aureus (метицилін-чутливий), Streptococcus pneumoniae (пеніцилін-чутливий), Streptococcus pyogenes, Streptococcus agalactiae, стрептококи груп аеробні грамнегативні мікроорганізми: Haemophilus influenzae, Haemophilus parainfluenzae, Legionella pneumophila, Moraxella catarrhalis, Pasteurella multocida, Neisseria gonorrhoeae; анаеробні мікроорганізми: Clostridium perfringens, Fusobacterium spp., Prevotella spp., Porphyriomonas spp., Peptostreptococcus spp.; інші мікроорганізми: Chlamydia trachomatis, Chlamydia pneumoniae, Chlamydia psittaci, Mycoplasma pneumoniae, Mycoplasma hominis, Borrelia burgdorferi. Мікроорганізми з резистентністю до азитроміцину: Streptococcus pneumoniae (пеніцилін-стійкий). Мікроорганізми, спочатку стійкі: аеробні грампозитивні мікроорганізми: Enterococcus faecalis, Staphylococcus spp. (метицилін-стійкі стафілококи з дуже високою частотою мають набуту стійкість до макролідів); грампозитивні бактерії, стійкі до еритроміцину; анаероби: Bacteroides fragilis. Секнідазол Протимікробний та протипротозойний засіб; похідне нітроімідазолу. Має бактерицидну (проти грампозитивних та грамнегативних анаеробних бактерій) та амебіцидну (внутрішньо- та позакишкову) дію. Секнідазол особливо активний щодо Trichomonas vaginalis, Giardia lamblia, Entamoeba histolytica. Взаємодіє з ДНК мікробної клітини, викликає порушення спіральної структури, розрив ниток, придушення синтезу нуклеїнових кислот та загибель клітини.Клінічна фармакологіяПротимікробний засіб комбінованийПоказання до застосуванняПоєднані інфекції сечостатевого тракту, що передаються статевим шляхом, такі як гонорея, трихомоніаз, хламідіоз, бактеріальний вагіноз, грибкові інфекції, а також специфічні та неспецифічні цистити, уретрити, вульвовагініти та цервіцити.Протипоказання до застосуванняПідвищена чутливість до флуконазолу, інших компонентів препарату або азольних сполук з подібною структурою флуконазолу; підвищена чутливість до азитроміцину або до інших компонентів препарату; підвищена чутливість до еритроміцину, інших макролідів, кетолідів; підвищена чутливість до секнідазолу, інших похідних імідазолу або до інших компонентів препарату. Одночасне застосування з препаратами, що збільшують інтервал QT та метаболізуються за допомогою ізоферменту CYP3A4, такими як цизаприд, астемізол, еритроміцин, пімозід, хінідин та аміодарон (див. розділ «Взаємодія з іншими лікарськими засобами»); одночасний прийом з ерготаміном, дигідроерготаміном. Порушення функції печінки тяжкого ступеня, органічні захворювання центральної нервової системи, захворювання крові (зокрема в анамнезі); вагітність, період грудного вигодовування; дитячий вік до 18 років.Вагітність та лактаціяЗастосування при вагітності та в період грудного вигодовування протипоказане.Побічна діяФлуконазол Переносимість препарату зазвичай дуже хороша. З боку нервової системи: біль голови, запаморочення, судоми, зміна смаку, парестезія, безсоння, сонливість, тремор. З боку травної системи: біль у животі, блювання, нудота, діарея, метеоризм, диспепсія, сухість слизової оболонки ротової порожнини, запор; підвищення сироваткової активності амінотрансфераз (аланінамінотрансферази (АЛТ), аспартатамінотрансферази (АСТ)), лужної фосфатази, гепатит, гепатоцелюлярний некроз, жовтяниця, холестаз, гепатоцелюлярне пошкодження, порушення функції печінки, підвищення концентрації печінки; Алергічні реакції: шкірні висипання, свербіж шкіри, кропив'янка, алопеція, ексфоліативні ураження шкіри, включаючи синдром Стівенса-Джонсона і токсичний епідермальний некроліз, гострий генералізований екзантематозний пустульоз, лікарський висип, анафілаксія (включаючи ангіо). З боку крові та лімфатичної системи: лейкопенія, включаючи нейтропенію та агранулоцитоз, тромбоцитопенію, анемію. Серцево-судинна система: збільшення інтервалу QT на ЕКГ, аритмія шлуночкова тахісистолічна типу «пірует». З боку обміну речовин: підвищення концентрації холестерину та тригліцеридів у плазмі крові, гіпокаліємія. Інші: слабкість, астенія, підвищена стомлюваність, лихоманка, підвищена пітливість, міалгія, вертиго. Азітроміцин З боку травної системи: діарея, нудота, блювання, біль у животі, метеоризм, диспепсія, запор, гастрит, дисфагія, здуття живота, сухість слизової оболонки порожнини рота, відрижка, виразки слизової оболонки порожнини рота, підвищення секреції слин , панкреатит; гепатит, порушення функції печінки, холестатична жовтяниця, печінкова недостатність (у поодиноких випадках з летальним результатом в основному на тлі тяжкого порушення функції печінки), некроз печінки, фульмінантний гепатит. Алергічні реакції: шкірний висип, свербіж шкіри, кропив'янка, дерматит, сухість шкіри, пітливість, реакція фотосенсибілізації, синдром Стівенса-Джонсона, токсичний епідермальний некроліз, мультиформна еритема, ангіоневротичний набряк, реакція гіперчутливості, анафілактична. Інфекційні захворювання: кандидоз, у тому числі слизової оболонки порожнини рота та геніталій, пневмонія, фарингіт, гастроентерит, респіраторні захворювання, риніт, псевдомембранозний коліт. З боку нирок та сечовивідних шляхів: дизурія, біль у ділянці нирок, інтерстиціальний нефрит, гостра ниркова недостатність. З боку серцево-судинної системи: відчуття серцебиття, «припливи» крові до обличчя, зниження артеріального тиску, збільшення інтервалу QT на електрокардіограмі, аритмія шлуночкова тахісистолічна типу «пірует», шлуночкова тахікардія. З боку нервової системи: головний біль, запаморочення, порушення смакових відчуттів, парестезії, сонливість, безсоння, нервозність, ажитація, гіпестезія, тривога, агресія, непритомність, судоми, психомоторна гіперактивність, втрата нюху, збочення нюху, втрата смакових відчуттів , галюцинації. З боку крові та лімфатичної системи: лейкопенія, нейтропенія, еозинофілія, тромбоцитопенія, гемолітична анемія. З боку органу слуху та лабіринтні порушення: розлад слуху, вертиго, порушення слуху, у тому числі глухота та/або шум у вухах. З боку опорно-рухового апарату: остеоартрит, міалгія, біль у спині, біль у шиї, артралгія. Інші: астенія, анорексія, нездужання, відчуття втоми, набряк обличчя, біль у грудях, лихоманка, периферичні набряки; метрорагії, порушення функції яєчок, порушення зору, задишка, носова кровотеча. Лабораторні дані: зниження кількості лімфоцитів, підвищення кількості еозинофілів, підвищення кількості базофілів, підвищення кількості моноцитів, підвищення кількості нейтрофілів, зниження концентрації бікарбонатів у плазмі крові, підвищення активності АСТ, АЛТ, підвищення концентрації білірубіну у плазмі крові, підвищення концентрації сечовини у плазмі крові, підвищення концентрації креатиніну в плазмі крові; вмісту натрію в плазмі крові. Секнідазол З боку травної системи: нудота, блювання, біль у животі, «металевий» присмак у роті, глосит, стоматит. З боку крові та лімфатичної системи: лейкопенія (помірна та оборотна). З боку нервової системи: запаморочення, порушення координації рухів, атаксія, парестезія, полінейропатія. Алергічні реакції: кропив'янка, висипання, ангіоневротичний набряк, анафілактична реакція. Інші: гарячка.Взаємодія з лікарськими засобамиФлуконазол Одночасне застосування з такими препаратами протипоказано: Астемізол: одночасне застосування з астемізолом або іншими препаратами, метаболізм яких здійснюється ізоферментами системи цитохрому Р450 може супроводжуватися підвищенням плазмових концентрацій цих засобів. Підвищені концентрації астемізолу в плазмі можуть призводити до подовження інтервалу QT і в деяких випадках до розвитку аритмії шлуночкової тахісистолічної типу «пірует». Аміодарон: можливе інгібування метаболізму аміодарону; одночасне застосування може призводити до подовження інтервалу QT. Пімозід: можливе підвищення концентрації пімозиду в плазмі, що може призводити до подовження інтервалу QT та розвитку аритмії типу «пірует». Терфенадин: можливе виникнення серйозних аритмій внаслідок збільшення інтервалу QT. Одночасний прийом флуконазолу в дозах 400 мг на добу та більше з терфенадином протипоказаний. Лікування флуконазолом у дозах менше 400 мг на добу у поєднанні з терфенадином слід проводити під ретельним контролем. Хінідин: можливе інгібування метаболізму хінідину; застосування хінідину асоціюється з подовженням інтервалу QT та рідкісними випадками розвитку аритмії шлуночкової тахісистолічної типу «пірует». Цизаприд: при одночасному застосуванні можливе виражене збільшення плазмової концентрації цизаприду та розвиток небажаних реакцій з боку серця (збільшення інтервалу QT на ЕКГ, аритмія типу «пірует»). Еритроміцин: одночасне застосування потенційно призводить до підвищеного ризику розвитку кардіотоксичності (подовження інтервалу QT, аритмія шлуночкова типу «пірует») та, внаслідок цього, раптової серцевої смерті. Слід бути обережним і, можливо, коригувати дози при одночасному застосуванні наступних препаратів і флуконазолу: Препарати, що впливають на флуконазол: Гідрохлортіазид збільшує концентрацію флуконазолу у плазмі на 40% (клінічна значущість малоймовірна). Рифампіцин підвищує метаболізм флуконазолу, внаслідок чого зменшується його концентрація у плазмі. Може знадобитися підвищення дози флуконазолу. Препарати, на які впливає флуконазол: Флуконазол є потужним інгібітором ізоферментів CYP2C9 та CYP2C19 цитохрому P450 та помірним інгібітором ізоферменту CYP3A4. Крім того, крім перерахованих далі ефектів, існує ризик підвищення в плазмі концентрації та інших лікарських засобів, що метаболізуються ізоферментами CYP2C9, CYP2C19 і CYP3A4 при одночасному застосуванні з флуконазолом. У зв'язку з цим слід бути обережним при одночасному застосуванні перелічених препаратів, а при необхідності подібних комбінацій пацієнти повинні перебувати під ретельним медичним наглядом. Слід враховувати, що інгібуючий ефект флуконазолу зберігається протягом 4-5 днів після відміни препарату через тривалий період напіввиведення. Алфентаніл: відзначається зменшення кліренсу та збільшення періоду напіввиведення алфентанілу; може знадобитися корекція дози алфентанілу. Азитроміцин: при одночасному застосуванні вираженої фармакокінетичної взаємодії між обома препаратами не встановлено. Амітриптілін, нортриптілін: відзначається збільшення ефекту; при необхідності слід коригувати дозу амітриптиліну/нортриптиліну. Антикоагулянти: у пацієнтів, які отримують антикоагулянти кумаринового типу або похідні індандіону, необхідно постійно контролювати протромбіновий час у період терапії та протягом 8 днів після одночасного застосування (можливе збільшення протромбінового часу). Алкалоїди барвінку: можливе збільшення концентрації алкалоїдів барвінку (наприклад, вінкрістину та вінбластину) у плазмі крові (ризик нейротоксичності). Бензодіазепіни (короткої дії): флуконазол підвищує плазмові концентрації мідазоламу та тріазоламу; може знадобитися зниження дози бензодіазепінів та ретельний контроль стану пацієнтів. Блокатори кальцієвих каналів: деякі антагоністи кальцію (ніфедипін, ісрадипін, амлодипін, верапаміл та фелодипін) метаболізуються ізоферментом CYP3A4. Флуконазол може підвищувати системну експозицію антагоністів кальцію. Рекомендовано контроль розвитку побічних ефектів. Вітамін А. Є повідомлення про один випадок розвитку небажаних реакцій з боку центральної нервової системи (ЦНС) у вигляді псевдопухлини мозку при одночасному застосуванні повністю трансретиноєвої кислоти та флуконазолу, які зникли після відміни флуконазолу. При застосуванні цієї комбінації слід пам'ятати про можливість виникнення небажаних реакцій із боку ЦНС. Вориконазол (інгібітор ізоферментів CYP2C9, CYP2C19 та CYP3A4): одночасне застосування вориконазолу та флуконазолу призводить до збільшення концентрації та AUC вориконазолу. Одночасне застосування цих препаратів не рекомендується. Галофантрин: флуконазол може збільшувати концентрацію галофантрину у плазмі крові; можливий розвиток аритмії шлуночкової тахісистолічної типу «пірует», тому спільне застосування їх не рекомендується. Зідовудін: флуконазол підвищує Cmax та AUC зидовудину відповідно на 84% та 74%, внаслідок зниження його кліренсу приблизно на 45%. Тому можливе підвищення ризику побічних ефектів зидовудину. Пацієнти повинні ретельно спостерігатися щодо розвитку пов'язаних із зидовудином побічних реакцій. Івакафтор: при одночасному застосуванні з ивакафтором, стимулятором муковісцидозного регулятора трансмембранної провідності (CFTR), спостерігалося збільшення експозиції ивакафтора в 3 рази та експозиції гідроксиметил-івакафтора (М1) у 1,9 рази. Пацієнтам, які одночасно приймають помірні інгібітори CYP3А, такі як флуконазол та еритроміцин, рекомендується зниження дози івакафтору до 150 мг один раз на добу. Карбамазепін: флуконазол підвищує плазмову концентрацію карбамазепіну на 30%. Необхідно враховувати ризик розвитку токсичності карбамазепіну. Лозартан: флуконазол пригнічує метаболізм лозартану до активного метаболіту (Е-31 74); потрібен регулярний контроль артеріального тиску. Метадон: флуконазол може збільшувати концентрацію плазми метадону; може знадобитися корекція дози метадону. Нестероїдні протизапальні препарати (НПЗЗ): флуконазол може збільшувати системну експозицію нестероїдних протизапальних засобів. Невірапін: спільний прийом з флуконазолом збільшує приблизно на 100% експозицію невірапіну. Необхідне ретельне спостереження за пацієнтами. Можливе збільшення періоду напіввиведення пероральних гіпоглікемічних засобів – похідних сульфонілсечовини (хлорпропамід, глібенкламід, гліпізид, толбутамід) при одночасному прийомі з флуконазолом. Пероральні контрацептиви: при застосуванні 200 мг флуконазолу спостерігалося збільшення AUC етинілестрадіолу на 40% та левоноргестрелу – на 24%. Не очікується впливу флуконазолу на ефективність комбінованих пероральних контрацептивів. Рифабутин: можливе збільшення концентрації рифабутину у плазмі; при одночасному застосуванні описані випадки увеїту. Саквінавір: при одночасному застосуванні з флуконазолом AUC саквінавіру підвищується приблизно на 50%, Cmax – на 55%, кліренс саквінавіру зменшується приблизно на 50%; може знадобитися корекція дози саквінавіру. Флуконазол підвищує концентрацію сиролімусу у плазмі крові; потрібна корекція дози сиролімусу залежно від ефекту/концентрації. Флуконазол підвищує концентрацію у плазмі такролімусу; пацієнтів слід ретельно спостерігати (ризик нефротоксичної дії) та коригувати у дозу такролімусу залежно від ступеня підвищення його концентрації у плазмі крові. Флуконазол підвищує концентрацію теофіліну у плазмі крові; хворі, які мають ймовірність розвитку теофілінової інтоксикації, повинні перебувати під наглядом з метою раннього виявлення симптомів передозування теофіліну. Тофацитініб: експозиція тофацитинібу збільшується при його сумісному застосуванні з препаратами, які є одночасно помірними інгібіторами ізоферменту CYP3A4 та потужними інгібіторами ізоферменту CYP2С19 (наприклад, флуконазол). Можливо, може бути потрібна корекція дози тофацитинібу. Флуконазол підвищує концентрацію фенітоїну у плазмі крові; необхідні контроль концентрації фенітоїну в плазмі крові та, при необхідності, корекція дози. Фентаніл: флуконазол значно подовжує час виведення фентанілу; підвищення концентрації фентанілу може призвести до пригнічення дихальної функції. При одночасному застосуванні флуконазолу з інгібіторами ГМГ-КоА-редуктази, що метаболізуються ізоферментом CYP3A4 (такими як аторвастатин та симвастатин) або ізоферментом CYP2D6 (такими як флувастатин), ризик розвитку міопатії та рабдоміолізу збільшується. У разі необхідності одночасної терапії зазначеними препаратами слід спостерігати пацієнтів з метою виявлення симптомів міопатії та рабдоміолізу. Циклоспорин: можливе підвищення концентрації циклоспорину при одночасному застосуванні з флуконазолом у дозі 200 мг на добу. Циклофосфамід: при одночасному застосуванні з флуконазолом відзначається збільшення сироваткових концентрацій білірубіну та креатиніну. Ця комбінація допустима з урахуванням ризику збільшення концентрацій білірубіну та креатиніну. Азітроміцин Азитроміцин слабо взаємодіє із ізоферментами цитохрому P450. Не виявлено, що азитроміцин бере участь у фармакокінетичних взаємодіях аналогічних еритроміцину та інших макролідів, азитроміцин не є індуктором та інгібітором ізоферментів цитохрому P450. Антациди (алюміній і магній містять) уповільнюють і знижують абсорбцію. Антикоагулянти: при сумісному застосуванні з антикоагулянтами непрямої дії кумаринового ряду (варфарин) можливе посилення антикоагуляційного ефекту; Пацієнтам необхідний ретельний контроль протромбінового часу. Дигоксин: можливе підвищення концентрації дигоксину у плазмі крові; при сумісному прийомі необхідно контролювати концентрацію дигоксину в крові. Зідовудін: азитроміцин незначно впливає на фармакокінетику, у тому числі виведення нирками, зидовудину та його глюкуронідного метаболіту, проте збільшується концентрація активного метаболіту – фосфорильованого зидовудину в моноядерних клітинах периферичної крові (клінічне значення даного факту не визначено). Нелфінавір: при одночасному застосуванні спостерігалося підвищення рівноважної концентрації азитроміцину у плазмі; клінічно значущих побічних ефектів немає і корекції дози азитроміцину не потрібно. Рифабутин: при одночасному застосуванні спостерігалася нейтропенія. Незважаючи на те, що нейтропенія асоціювалася із застосуванням рифабутину, зв'язок між застосуванням комбінації азитроміцину та рифабутину та нейтропенією не встановлений. Інгібітори ГМГ-КоА-редуктази: були отримані окремі повідомлення про випадки рабдоміолізу у пацієнтів, які одночасно приймають азитроміцин та інгібітори ГМГ-КоА-редуктази. Терфенадин: необхідно враховувати, що при одночасному застосуванні з антибіотиками класу макролідів можливі аритмія та подовження інтервалу QT. Циклоспорин: при одночасному застосуванні необхідно контролювати концентрацію циклоспорину в плазмі та відповідно коригувати дозу. Циметидин не впливає на фармакокінетику азитроміцину за умови застосування циметидину за 2 години до азитроміцину. Ерготамін та дигідроерготамін: посилення токсичної дії (вазоспазм, дизестезія); спільне застосування не рекомендується. Секнідазол Підсилює дію непрямих антикоагулянтів (похідних кумарину або індандіону) та підвищує ризик виникнення кровотеч за рахунок зниження печінкового метаболізму антикоагулянтів. Одночасний прийом з дисульфірамом призводить до розвитку гострого делірію, сплутаності свідомості; спільне застосування не рекомендується. Аналогічно дисульфірам викликає непереносимість етанолу (див. розділ «Особливі вказівки»).Спосіб застосування та дозиВсередину. Приймають одночасно всі 4 таблетки, що входять до складу блістера, з урахуванням прийому їжі (бо всмоктування азитроміцину змінюється при одночасному прийомі їжі, його краще прийняти за годину до їжі або через 2 години після їжі), одноразово.ПередозуванняВипадки передозування набору таблеток Сафоциду не описані. У разі передозування слід негайно звернутися до лікаря. Флуконазол. Симптоми: галюцинації, параноїдальна поведінка. Лікування: симптоматичне; промивання шлунка (за потреби), форсований діурез. Гемодіаліз протягом 3 годин знижує концентрацію флуконазолу у плазмі крові приблизно на 50%. Азітроміцин. Симптоми: нудота, тимчасова втрата слуху, блювання, діарея. Лікування: симптоматичне; прийом активованого вугілля; контроль життєво важливих функцій. Секнідазол. Симптоми: посилення дозозалежних побічних ефектів. Лікування: симптоматичне; промивання шлунка; прийом активованого вугілля.Запобіжні заходи та особливі вказівкиПорушення функції печінки легкого та середнього ступеня тяжкості; термінальна ниркова недостатність із ШКФ (швидкість клубочкової фільтрації) менше 10 мл/хв; у пацієнтів з наявністю проаритмогенних факторів (особливо у літніх пацієнтів): з вродженим або набутим подовженням інтервалу QT, у пацієнтів, які отримують терапію антиаритмічними препаратами класів IA (прокаїнамід) та III (дофетилід, соталол), антидепресантами (циталопрамцин) левофлоксацин), з порушеннями водно-електролітного балансу, особливо у разі гіпокаліємії або гіпомагніємії, з клінічно значущою брадикардією, аритмією серця або тяжкою серцевою недостатністю, з органічними захворюваннями серця; одночасне застосування дигоксину, варфарину, циклоспорину; одночасний прийом терфенадину; міастенія.Умови відпустки з аптекЗа рецептомВідео на цю тему
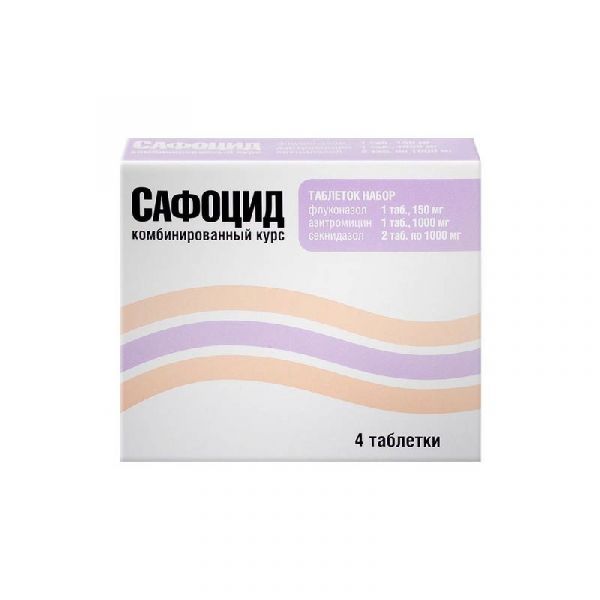
Склад, форма випуску та упаковкаФлуконазол 1 таблетка містить: активна речовина: флуконазол – 150 мг; допоміжні речовини: целюлоза мікрокристалічна, кальцію гідрофосфат, кроскармелоза натрію, магнію стеарат, діоксид колоїдний кремнію, барвник червоний [Понсо 4R] [Е 124]. Азітроміцин 1 таблетка, покрита плівковою оболонкою, містить: активна речовина: азитроміцин дигідрат – 1048 мг (у перерахунку на азитроміцин – 1000 мг); допоміжні речовини: натрію лаурилсульфат, кроскармелоза натрію, повідон-К30, магнію стеарат, кремнію діоксид колоїдний; склад оболонки: гіпромелоза (гідроксипропілметилцелюлоза), діетилфталат, тальк, титану діоксид, макрогол-4000, барвник червоний [Понсо 4R] [Е 124]. Секнідазол 1 таблетка, покрита плівковою оболонкою, містить: активна речовина: секнідазол – 1000 мг; допоміжні речовини: крохмаль кукурудзяний, целюлоза мікрокристалічна, кремнію діоксид колоїдний, карбоксиметилкрохмаль натрію, повідон (PVPK - 30), тальк, магнію стеарат; склад оболонки: гіпромелоза (гідроксипропілметилцелюлоза), діетилфталат, тальк, титану діоксид, макрогол-4000. Таблеток набір. По 4 таблетки (одна таблетка – флуконазол, одна таблетка – азитроміцин, дві таблетки – секнідазол) у контурне осередкове пакування (блістер) з плівки полівінілхлоридної та фольги алюмінієвої. 1 або 3 блістери разом з інструкцією із застосування в картонну пачку.Опис лікарської формиТаблеток набірХарактеристикаФлуконазол Плоскоциліндричні таблетки рожевого кольору з фаскою та ризиком. На зламі пігулки рожевого кольору. Азітроміцин Капсулоподібні двоопуклі таблетки, покриті плівковою оболонкою рожевого кольору, з ризиком. На зламі ядро таблетки білого або майже білого кольору. Секнідазол Капсулоподібні двоопуклі таблетки, покриті плівковою оболонкою білого або майже білого кольору, з ризиком. На зламі пігулки білого або майже білого кольору.ФармакокінетикаФлуконазол Абсорбція – висока, біодоступність – 90%. Одночасний прийом їжі не впливає на абсорбцію препарату. Після прийому внутрішньо натще 150 мг час досягнення максимальної концентрації - 0,5-1,5 год, максимальна концентрація флуконазолу в плазмі (Cmax) становить 90% від концентрації в плазмі при внутрішньовенному введенні в дозі 2,5-3,5 мг/л . Зв'язок із білками плазми – 11-12%. Концентрація в плазмі залежить від дози. Флуконазол добре проникає у всі біологічні рідини організму. Концентрація активної речовини в грудному молоці, суглобовій рідині, слині, мокротинні та перитонеальній рідині аналогічна такій у плазмі. Постійні значення у вагінальному секреті досягаються через 8 годин після прийому внутрішньо і утримуються на цьому рівні не менше 24 годин. Добре проникає в спинномозкову рідину (СМР),при грибковому менінгіті концентрація у СМР становить близько 85% від такої у плазмі. У потовій рідині, епідермісі та роговому шарі (селективне накопичення) досягаються концентрації, що перевищують сироваткові. Обсяг розподілу наближається до загального вмісту води у організмі; період напіввиведення (T1/2) флуконазолу становить близько 30 год. Виводиться переважно нирками (80% – у незміненому вигляді, 11% – у вигляді метаболітів). Кліренс флуконазолу пропорційний кліренсу креатиніну (КК). Фармакокінетика флуконазолу суттєво залежить від функціонального стану нирок, при цьому існує зворотна залежність між T1/2 та КК. Після гемодіалізу протягом 3 годин концентрація флуконазолу у плазмі знижується на 50%. Тривалий період напіввиведення з плазми дозволяє приймати флуконазол при вагінальному кандидозі одноразово. Азітроміцин Азитроміцин швидко всмоктується із шлунково-кишкового тракту (ЖКТ), що зумовлено його стійкістю у кислому середовищі та ліпофільністю. Після прийому внутрішньо 500 мг максимальна концентрація азитроміцину в плазмі досягається через 2,5 - 2,96 год і становить 0,4 мг/л. Біодоступність становить 37%. Азитроміцин добре проникає у дихальні шляхи, органи та тканини урогенітального тракту (зокрема у передміхурову залозу), у шкіру та м'які тканини. Висока концентрація в тканинах (у 10-50 разів вища, ніж у плазмі крові) та тривалий період напіввиведення зумовлені низьким зв'язуванням азитроміцину з білками плазми крові, а також його здатністю проникати в еукаріотичні клітини та концентруватися у середовищі з низьким рН, що оточує лізосоми. Це, у свою чергу, визначає великий обсяг розподілу (31,1 л/кг) і високий плазмовий кліренс.Здатність азитроміцину накопичуватись переважно у лізосомах особливо важлива для елімінації внутрішньоклітинних збудників. Доведено, що фагоцити доставляють азитроміцин у місця локалізації інфекції, де він вивільняється у процесі фагоцитозу. Концентрація азитроміцину в осередках інфекції достовірно вища, ніж у здорових тканинах (в середньому на 24-34%) та корелює зі ступенем запального набряку. Незважаючи на високу концентрацію у фагоцитах, азитроміцин не істотно впливає на їх функцію. Азитроміцин зберігається у бактерицидних концентраціях протягом 5-7 днів після прийому останньої дози. У печінці деметилюється, метаболіти, що утворюються, не активні. У азитроміцину дуже довгий період напіввиведення – 35-50 год. Період напіввиведення із тканин значно більший. Азитроміцин виводиться, в основному, у незміненому вигляді – 50% кишечником,6% нирками. Секнідазол Після прийому внутрішньо швидко всмоктується із ШКТ; біодоступність – близько 80%. Після одноразового прийому внутрішньо 2 г максимальна концентрація в плазмі досягається через 3-4 години. Метаболізується в печінці. Період напіввиведення секнідазолу з плазми становить близько 25 год. Препарат повільно виводиться з організму, в основному нирками; близько 50% прийнятої дози екскретується за 120 год. Проходить через гематоенцефалічний та плацентарний бар'єри, екскретується у грудне молоко.ФармакодинамікаФлуконазол Триазольний протигрибковий засіб є потужним селективним інгібітором синтезу стеролів у клітині грибів. Має високоспецифічну дію, інгібуючи активність ферментів грибів, залежних від цитохрому P450. Блокує перетворення ланостеролу клітин грибів на мембранний ліпід - ергостерол; збільшує проникність клітинної мембрани, порушує її зростання та реплікацію. Флуконазол продемонстрував активність in vitro та у клінічних дослідженнях щодо наступних мікроорганізмів: Candida albicans, Candida glabrata (багато штами помірно чутливі), Candida parapsilosis, Candida tropicalis, Cryptococcus neoformans. Активний при опортуністичних мікозах, у т.ч. викликаних Candida spp. (включаючи генералізовані форми кандидозу на фоні імунодепресії), Cryptococcus neoformans та Coccidioides immitis (включаючи внутрішньочерепні інфекції),Microsporum spp. та Trichophyton spp; при ендемічних мікозах, спричинених Blastomyces dermatidis, Histoplasma capsulatum (в т.ч. при імунодепресії). Не має антиандрогенної активності. Азітроміцин Антибактеріальний засіб широкого спектра дії, азалід, діє бактеріостатично. Зв'язуючись із 50S субодиницею рибосом, пригнічує пептидтранслоказу на стадії трансляції, пригнічує синтез білка, уповільнює ріст та розмноження бактерій, у високих концентраціях має бактерицидний ефект. Має активність щодо низки грампозитивних, грамнегативних, анаеробних, внутрішньоклітинних та інших мікроорганізмів. У більшості випадків до азитроміцину чутливі: аеробні грампозитивні мікроорганізми: Staphylococcus aureus (метицилін-чутливий), Streptococcus pneumoniae (пеніцилін-чутливий), Streptococcus pyogenes, Streptococcus agalactiae, стрептококи груп аеробні грамнегативні мікроорганізми: Haemophilus influenzae, Haemophilus parainfluenzae, Legionella pneumophila, Moraxella catarrhalis, Pasteurella multocida, Neisseria gonorrhoeae; анаеробні мікроорганізми: Clostridium perfringens, Fusobacterium spp., Prevotella spp., Porphyriomonas spp., Peptostreptococcus spp.; інші мікроорганізми: Chlamydia trachomatis, Chlamydia pneumoniae, Chlamydia psittaci, Mycoplasma pneumoniae, Mycoplasma hominis, Borrelia burgdorferi. Мікроорганізми з резистентністю до азитроміцину: Streptococcus pneumoniae (пеніцилін-стійкий). Мікроорганізми, спочатку стійкі: аеробні грампозитивні мікроорганізми: Enterococcus faecalis, Staphylococcus spp. (метицилін-стійкі стафілококи з дуже високою частотою мають набуту стійкість до макролідів); грампозитивні бактерії, стійкі до еритроміцину; анаероби: Bacteroides fragilis. Секнідазол Протимікробний та протипротозойний засіб; похідне нітроімідазолу. Має бактерицидну (проти грампозитивних та грамнегативних анаеробних бактерій) та амебіцидну (внутрішньо- та позакишкову) дію. Секнідазол особливо активний щодо Trichomonas vaginalis, Giardia lamblia, Entamoeba histolytica. Взаємодіє з ДНК мікробної клітини, викликає порушення спіральної структури, розрив ниток, придушення синтезу нуклеїнових кислот та загибель клітини.Клінічна фармакологіяПротимікробний засіб комбінованийПоказання до застосуванняПоєднані інфекції сечостатевого тракту, що передаються статевим шляхом, такі як гонорея, трихомоніаз, хламідіоз, бактеріальний вагіноз, грибкові інфекції, а також специфічні та неспецифічні цистити, уретрити, вульвовагініти та цервіцити.Протипоказання до застосуванняПідвищена чутливість до флуконазолу, інших компонентів препарату або азольних сполук з подібною структурою флуконазолу; підвищена чутливість до азитроміцину або до інших компонентів препарату; підвищена чутливість до еритроміцину, інших макролідів, кетолідів; підвищена чутливість до секнідазолу, інших похідних імідазолу або до інших компонентів препарату. Одночасне застосування з препаратами, що збільшують інтервал QT та метаболізуються за допомогою ізоферменту CYP3A4, такими як цизаприд, астемізол, еритроміцин, пімозід, хінідин та аміодарон (див. розділ «Взаємодія з іншими лікарськими засобами»); одночасний прийом з ерготаміном, дигідроерготаміном. Порушення функції печінки тяжкого ступеня, органічні захворювання центральної нервової системи, захворювання крові (зокрема в анамнезі); вагітність, період грудного вигодовування; дитячий вік до 18 років.Вагітність та лактаціяЗастосування при вагітності та в період грудного вигодовування протипоказане.Побічна діяФлуконазол Переносимість препарату зазвичай дуже хороша. З боку нервової системи: біль голови, запаморочення, судоми, зміна смаку, парестезія, безсоння, сонливість, тремор. З боку травної системи: біль у животі, блювання, нудота, діарея, метеоризм, диспепсія, сухість слизової оболонки ротової порожнини, запор; підвищення сироваткової активності амінотрансфераз (аланінамінотрансферази (АЛТ), аспартатамінотрансферази (АСТ)), лужної фосфатази, гепатит, гепатоцелюлярний некроз, жовтяниця, холестаз, гепатоцелюлярне пошкодження, порушення функції печінки, підвищення концентрації печінки; Алергічні реакції: шкірні висипання, свербіж шкіри, кропив'янка, алопеція, ексфоліативні ураження шкіри, включаючи синдром Стівенса-Джонсона і токсичний епідермальний некроліз, гострий генералізований екзантематозний пустульоз, лікарський висип, анафілаксія (включаючи ангіо). З боку крові та лімфатичної системи: лейкопенія, включаючи нейтропенію та агранулоцитоз, тромбоцитопенію, анемію. Серцево-судинна система: збільшення інтервалу QT на ЕКГ, аритмія шлуночкова тахісистолічна типу «пірует». З боку обміну речовин: підвищення концентрації холестерину та тригліцеридів у плазмі крові, гіпокаліємія. Інші: слабкість, астенія, підвищена стомлюваність, лихоманка, підвищена пітливість, міалгія, вертиго. Азітроміцин З боку травної системи: діарея, нудота, блювання, біль у животі, метеоризм, диспепсія, запор, гастрит, дисфагія, здуття живота, сухість слизової оболонки порожнини рота, відрижка, виразки слизової оболонки порожнини рота, підвищення секреції слин , панкреатит; гепатит, порушення функції печінки, холестатична жовтяниця, печінкова недостатність (у поодиноких випадках з летальним результатом в основному на тлі тяжкого порушення функції печінки), некроз печінки, фульмінантний гепатит. Алергічні реакції: шкірний висип, свербіж шкіри, кропив'янка, дерматит, сухість шкіри, пітливість, реакція фотосенсибілізації, синдром Стівенса-Джонсона, токсичний епідермальний некроліз, мультиформна еритема, ангіоневротичний набряк, реакція гіперчутливості, анафілактична. Інфекційні захворювання: кандидоз, у тому числі слизової оболонки порожнини рота та геніталій, пневмонія, фарингіт, гастроентерит, респіраторні захворювання, риніт, псевдомембранозний коліт. З боку нирок та сечовивідних шляхів: дизурія, біль у ділянці нирок, інтерстиціальний нефрит, гостра ниркова недостатність. З боку серцево-судинної системи: відчуття серцебиття, «припливи» крові до обличчя, зниження артеріального тиску, збільшення інтервалу QT на електрокардіограмі, аритмія шлуночкова тахісистолічна типу «пірует», шлуночкова тахікардія. З боку нервової системи: головний біль, запаморочення, порушення смакових відчуттів, парестезії, сонливість, безсоння, нервозність, ажитація, гіпестезія, тривога, агресія, непритомність, судоми, психомоторна гіперактивність, втрата нюху, збочення нюху, втрата смакових відчуттів , галюцинації. З боку крові та лімфатичної системи: лейкопенія, нейтропенія, еозинофілія, тромбоцитопенія, гемолітична анемія. З боку органу слуху та лабіринтні порушення: розлад слуху, вертиго, порушення слуху, у тому числі глухота та/або шум у вухах. З боку опорно-рухового апарату: остеоартрит, міалгія, біль у спині, біль у шиї, артралгія. Інші: астенія, анорексія, нездужання, відчуття втоми, набряк обличчя, біль у грудях, лихоманка, периферичні набряки; метрорагії, порушення функції яєчок, порушення зору, задишка, носова кровотеча. Лабораторні дані: зниження кількості лімфоцитів, підвищення кількості еозинофілів, підвищення кількості базофілів, підвищення кількості моноцитів, підвищення кількості нейтрофілів, зниження концентрації бікарбонатів у плазмі крові, підвищення активності АСТ, АЛТ, підвищення концентрації білірубіну у плазмі крові, підвищення концентрації сечовини у плазмі крові, підвищення концентрації креатиніну в плазмі крові; вмісту натрію в плазмі крові. Секнідазол З боку травної системи: нудота, блювання, біль у животі, «металевий» присмак у роті, глосит, стоматит. З боку крові та лімфатичної системи: лейкопенія (помірна та оборотна). З боку нервової системи: запаморочення, порушення координації рухів, атаксія, парестезія, полінейропатія. Алергічні реакції: кропив'янка, висипання, ангіоневротичний набряк, анафілактична реакція. Інші: гарячка.Взаємодія з лікарськими засобамиФлуконазол Одночасне застосування з такими препаратами протипоказано: Астемізол: одночасне застосування з астемізолом або іншими препаратами, метаболізм яких здійснюється ізоферментами системи цитохрому Р450 може супроводжуватися підвищенням плазмових концентрацій цих засобів. Підвищені концентрації астемізолу в плазмі можуть призводити до подовження інтервалу QT і в деяких випадках до розвитку аритмії шлуночкової тахісистолічної типу «пірует». Аміодарон: можливе інгібування метаболізму аміодарону; одночасне застосування може призводити до подовження інтервалу QT. Пімозід: можливе підвищення концентрації пімозиду в плазмі, що може призводити до подовження інтервалу QT та розвитку аритмії типу «пірует». Терфенадин: можливе виникнення серйозних аритмій внаслідок збільшення інтервалу QT. Одночасний прийом флуконазолу в дозах 400 мг на добу та більше з терфенадином протипоказаний. Лікування флуконазолом у дозах менше 400 мг на добу у поєднанні з терфенадином слід проводити під ретельним контролем. Хінідин: можливе інгібування метаболізму хінідину; застосування хінідину асоціюється з подовженням інтервалу QT та рідкісними випадками розвитку аритмії шлуночкової тахісистолічної типу «пірует». Цизаприд: при одночасному застосуванні можливе виражене збільшення плазмової концентрації цизаприду та розвиток небажаних реакцій з боку серця (збільшення інтервалу QT на ЕКГ, аритмія типу «пірует»). Еритроміцин: одночасне застосування потенційно призводить до підвищеного ризику розвитку кардіотоксичності (подовження інтервалу QT, аритмія шлуночкова типу «пірует») та, внаслідок цього, раптової серцевої смерті. Слід бути обережним і, можливо, коригувати дози при одночасному застосуванні наступних препаратів і флуконазолу: Препарати, що впливають на флуконазол: Гідрохлортіазид збільшує концентрацію флуконазолу у плазмі на 40% (клінічна значущість малоймовірна). Рифампіцин підвищує метаболізм флуконазолу, внаслідок чого зменшується його концентрація у плазмі. Може знадобитися підвищення дози флуконазолу. Препарати, на які впливає флуконазол: Флуконазол є потужним інгібітором ізоферментів CYP2C9 та CYP2C19 цитохрому P450 та помірним інгібітором ізоферменту CYP3A4. Крім того, крім перерахованих далі ефектів, існує ризик підвищення в плазмі концентрації та інших лікарських засобів, що метаболізуються ізоферментами CYP2C9, CYP2C19 і CYP3A4 при одночасному застосуванні з флуконазолом. У зв'язку з цим слід бути обережним при одночасному застосуванні перелічених препаратів, а при необхідності подібних комбінацій пацієнти повинні перебувати під ретельним медичним наглядом. Слід враховувати, що інгібуючий ефект флуконазолу зберігається протягом 4-5 днів після відміни препарату через тривалий період напіввиведення. Алфентаніл: відзначається зменшення кліренсу та збільшення періоду напіввиведення алфентанілу; може знадобитися корекція дози алфентанілу. Азитроміцин: при одночасному застосуванні вираженої фармакокінетичної взаємодії між обома препаратами не встановлено. Амітриптілін, нортриптілін: відзначається збільшення ефекту; при необхідності слід коригувати дозу амітриптиліну/нортриптиліну. Антикоагулянти: у пацієнтів, які отримують антикоагулянти кумаринового типу або похідні індандіону, необхідно постійно контролювати протромбіновий час у період терапії та протягом 8 днів після одночасного застосування (можливе збільшення протромбінового часу). Алкалоїди барвінку: можливе збільшення концентрації алкалоїдів барвінку (наприклад, вінкрістину та вінбластину) у плазмі крові (ризик нейротоксичності). Бензодіазепіни (короткої дії): флуконазол підвищує плазмові концентрації мідазоламу та тріазоламу; може знадобитися зниження дози бензодіазепінів та ретельний контроль стану пацієнтів. Блокатори кальцієвих каналів: деякі антагоністи кальцію (ніфедипін, ісрадипін, амлодипін, верапаміл та фелодипін) метаболізуються ізоферментом CYP3A4. Флуконазол може підвищувати системну експозицію антагоністів кальцію. Рекомендовано контроль розвитку побічних ефектів. Вітамін А. Є повідомлення про один випадок розвитку небажаних реакцій з боку центральної нервової системи (ЦНС) у вигляді псевдопухлини мозку при одночасному застосуванні повністю трансретиноєвої кислоти та флуконазолу, які зникли після відміни флуконазолу. При застосуванні цієї комбінації слід пам'ятати про можливість виникнення небажаних реакцій із боку ЦНС. Вориконазол (інгібітор ізоферментів CYP2C9, CYP2C19 та CYP3A4): одночасне застосування вориконазолу та флуконазолу призводить до збільшення концентрації та AUC вориконазолу. Одночасне застосування цих препаратів не рекомендується. Галофантрин: флуконазол може збільшувати концентрацію галофантрину у плазмі крові; можливий розвиток аритмії шлуночкової тахісистолічної типу «пірует», тому спільне застосування їх не рекомендується. Зідовудін: флуконазол підвищує Cmax та AUC зидовудину відповідно на 84% та 74%, внаслідок зниження його кліренсу приблизно на 45%. Тому можливе підвищення ризику побічних ефектів зидовудину. Пацієнти повинні ретельно спостерігатися щодо розвитку пов'язаних із зидовудином побічних реакцій. Івакафтор: при одночасному застосуванні з ивакафтором, стимулятором муковісцидозного регулятора трансмембранної провідності (CFTR), спостерігалося збільшення експозиції ивакафтора в 3 рази та експозиції гідроксиметил-івакафтора (М1) у 1,9 рази. Пацієнтам, які одночасно приймають помірні інгібітори CYP3А, такі як флуконазол та еритроміцин, рекомендується зниження дози івакафтору до 150 мг один раз на добу. Карбамазепін: флуконазол підвищує плазмову концентрацію карбамазепіну на 30%. Необхідно враховувати ризик розвитку токсичності карбамазепіну. Лозартан: флуконазол пригнічує метаболізм лозартану до активного метаболіту (Е-31 74); потрібен регулярний контроль артеріального тиску. Метадон: флуконазол може збільшувати концентрацію плазми метадону; може знадобитися корекція дози метадону. Нестероїдні протизапальні препарати (НПЗЗ): флуконазол може збільшувати системну експозицію нестероїдних протизапальних засобів. Невірапін: спільний прийом з флуконазолом збільшує приблизно на 100% експозицію невірапіну. Необхідне ретельне спостереження за пацієнтами. Можливе збільшення періоду напіввиведення пероральних гіпоглікемічних засобів – похідних сульфонілсечовини (хлорпропамід, глібенкламід, гліпізид, толбутамід) при одночасному прийомі з флуконазолом. Пероральні контрацептиви: при застосуванні 200 мг флуконазолу спостерігалося збільшення AUC етинілестрадіолу на 40% та левоноргестрелу – на 24%. Не очікується впливу флуконазолу на ефективність комбінованих пероральних контрацептивів. Рифабутин: можливе збільшення концентрації рифабутину у плазмі; при одночасному застосуванні описані випадки увеїту. Саквінавір: при одночасному застосуванні з флуконазолом AUC саквінавіру підвищується приблизно на 50%, Cmax – на 55%, кліренс саквінавіру зменшується приблизно на 50%; може знадобитися корекція дози саквінавіру. Флуконазол підвищує концентрацію сиролімусу у плазмі крові; потрібна корекція дози сиролімусу залежно від ефекту/концентрації. Флуконазол підвищує концентрацію у плазмі такролімусу; пацієнтів слід ретельно спостерігати (ризик нефротоксичної дії) та коригувати у дозу такролімусу залежно від ступеня підвищення його концентрації у плазмі крові. Флуконазол підвищує концентрацію теофіліну у плазмі крові; хворі, які мають ймовірність розвитку теофілінової інтоксикації, повинні перебувати під наглядом з метою раннього виявлення симптомів передозування теофіліну. Тофацитініб: експозиція тофацитинібу збільшується при його сумісному застосуванні з препаратами, які є одночасно помірними інгібіторами ізоферменту CYP3A4 та потужними інгібіторами ізоферменту CYP2С19 (наприклад, флуконазол). Можливо, може бути потрібна корекція дози тофацитинібу. Флуконазол підвищує концентрацію фенітоїну у плазмі крові; необхідні контроль концентрації фенітоїну в плазмі крові та, при необхідності, корекція дози. Фентаніл: флуконазол значно подовжує час виведення фентанілу; підвищення концентрації фентанілу може призвести до пригнічення дихальної функції. При одночасному застосуванні флуконазолу з інгібіторами ГМГ-КоА-редуктази, що метаболізуються ізоферментом CYP3A4 (такими як аторвастатин та симвастатин) або ізоферментом CYP2D6 (такими як флувастатин), ризик розвитку міопатії та рабдоміолізу збільшується. У разі необхідності одночасної терапії зазначеними препаратами слід спостерігати пацієнтів з метою виявлення симптомів міопатії та рабдоміолізу. Циклоспорин: можливе підвищення концентрації циклоспорину при одночасному застосуванні з флуконазолом у дозі 200 мг на добу. Циклофосфамід: при одночасному застосуванні з флуконазолом відзначається збільшення сироваткових концентрацій білірубіну та креатиніну. Ця комбінація допустима з урахуванням ризику збільшення концентрацій білірубіну та креатиніну. Азітроміцин Азитроміцин слабо взаємодіє із ізоферментами цитохрому P450. Не виявлено, що азитроміцин бере участь у фармакокінетичних взаємодіях аналогічних еритроміцину та інших макролідів, азитроміцин не є індуктором та інгібітором ізоферментів цитохрому P450. Антациди (алюміній і магній містять) уповільнюють і знижують абсорбцію. Антикоагулянти: при сумісному застосуванні з антикоагулянтами непрямої дії кумаринового ряду (варфарин) можливе посилення антикоагуляційного ефекту; Пацієнтам необхідний ретельний контроль протромбінового часу. Дигоксин: можливе підвищення концентрації дигоксину у плазмі крові; при сумісному прийомі необхідно контролювати концентрацію дигоксину в крові. Зідовудін: азитроміцин незначно впливає на фармакокінетику, у тому числі виведення нирками, зидовудину та його глюкуронідного метаболіту, проте збільшується концентрація активного метаболіту – фосфорильованого зидовудину в моноядерних клітинах периферичної крові (клінічне значення даного факту не визначено). Нелфінавір: при одночасному застосуванні спостерігалося підвищення рівноважної концентрації азитроміцину у плазмі; клінічно значущих побічних ефектів немає і корекції дози азитроміцину не потрібно. Рифабутин: при одночасному застосуванні спостерігалася нейтропенія. Незважаючи на те, що нейтропенія асоціювалася із застосуванням рифабутину, зв'язок між застосуванням комбінації азитроміцину та рифабутину та нейтропенією не встановлений. Інгібітори ГМГ-КоА-редуктази: були отримані окремі повідомлення про випадки рабдоміолізу у пацієнтів, які одночасно приймають азитроміцин та інгібітори ГМГ-КоА-редуктази. Терфенадин: необхідно враховувати, що при одночасному застосуванні з антибіотиками класу макролідів можливі аритмія та подовження інтервалу QT. Циклоспорин: при одночасному застосуванні необхідно контролювати концентрацію циклоспорину в плазмі та відповідно коригувати дозу. Циметидин не впливає на фармакокінетику азитроміцину за умови застосування циметидину за 2 години до азитроміцину. Ерготамін та дигідроерготамін: посилення токсичної дії (вазоспазм, дизестезія); спільне застосування не рекомендується. Секнідазол Підсилює дію непрямих антикоагулянтів (похідних кумарину або індандіону) та підвищує ризик виникнення кровотеч за рахунок зниження печінкового метаболізму антикоагулянтів. Одночасний прийом з дисульфірамом призводить до розвитку гострого делірію, сплутаності свідомості; спільне застосування не рекомендується. Аналогічно дисульфірам викликає непереносимість етанолу (див. розділ «Особливі вказівки»).Спосіб застосування та дозиВсередину. Приймають одночасно всі 4 таблетки, що входять до складу блістера, з урахуванням прийому їжі (бо всмоктування азитроміцину змінюється при одночасному прийомі їжі, його краще прийняти за годину до їжі або через 2 години після їжі), одноразово.ПередозуванняВипадки передозування набору таблеток Сафоциду не описані. У разі передозування слід негайно звернутися до лікаря. Флуконазол. Симптоми: галюцинації, параноїдальна поведінка. Лікування: симптоматичне; промивання шлунка (за потреби), форсований діурез. Гемодіаліз протягом 3 годин знижує концентрацію флуконазолу у плазмі крові приблизно на 50%. Азітроміцин. Симптоми: нудота, тимчасова втрата слуху, блювання, діарея. Лікування: симптоматичне; прийом активованого вугілля; контроль життєво важливих функцій. Секнідазол. Симптоми: посилення дозозалежних побічних ефектів. Лікування: симптоматичне; промивання шлунка; прийом активованого вугілля.Запобіжні заходи та особливі вказівкиПорушення функції печінки легкого та середнього ступеня тяжкості; термінальна ниркова недостатність із ШКФ (швидкість клубочкової фільтрації) менше 10 мл/хв; у пацієнтів з наявністю проаритмогенних факторів (особливо у літніх пацієнтів): з вродженим або набутим подовженням інтервалу QT, у пацієнтів, які отримують терапію антиаритмічними препаратами класів IA (прокаїнамід) та III (дофетилід, соталол), антидепресантами (циталопрамцин) левофлоксацин), з порушеннями водно-електролітного балансу, особливо у разі гіпокаліємії або гіпомагніємії, з клінічно значущою брадикардією, аритмією серця або тяжкою серцевою недостатністю, з органічними захворюваннями серця; одночасне застосування дигоксину, варфарину, циклоспорину; одночасний прийом терфенадину; міастенія.Умови відпустки з аптекЗа рецептомВідео на цю тему
6 695,00 грн
363,00 грн
Умови зберіганняУ холодильнику +2+8 градусівУмови відпустки з аптекЗа рецептомВідео на цю тему.
10 336,00 грн
133,00 грн
Склад, форма випуску та упаковкаРозчин для підшкірного введення – 1 мл: активна речовина: ліраглутид – 6 мг (в одній попередньо заповненій шприц-ручці міститься 3 мл розчину, що відповідає 18 мг ліраглутиду); допоміжні речовини: натрію гідрофосфату дигідрат – 1,42 мг; фенол - 5,5 мг; пропіленгліколь - 14 мг; кислота хлористоводнева/натрію гідроксид (для корекції рН); вода для ін'єкцій – до 1 мл. Розчин для підшкірного введення 6 мг/мл. По 3 мл у картриджі зі скла I гідролітичного класу, закупорені дисками з бромбутилової гуми/поліізопрену з одного боку та поршнями з бромбутилової гуми з іншого. Картридж запаяний у пластикову мультидозову одноразову шприц-ручку для багаторазових ін'єкцій. По 5 мультидозових одноразових шприц-ручок у картонну пачку.Опис лікарської формиПрозорий, безбарвний чи майже безбарвний розчин.Фармакотерапевтична групаЗнижувальне масу тіла.ФармакокінетикаВсмоктування. Всмоктування ліраглутиду після підшкірного введення відбувається повільно, час досягнення Tmax – близько 11 години після введення. У пацієнтів з ожирінням (ІМТ 30-40 кг/м2) після введення ліраглутиду в дозі 3 мг середня рівноважна концентрація ліраглутиду (AUCτ/24) досягає приблизно 31 нмоль/л. У діапазоні доз від 0,6 до 3 мг експозиція ліраглутиду збільшується пропорційно дозі. Абсолютна біодоступність ліраглутиду після підшкірного введення становить приблизно 55%. Розподіл. Середній здається Vd після підшкірного введення ліраглутиду в дозі 3 мг становить 20-25 л (у осіб з масою тіла близько 100 кг). Ліраглутид значною мірою пов'язується з білками плазми (>98%). Метаболізм. Протягом 24 годин після введення здоровим добровольцям одноразової дози [3Н]-ліраглутиду головним компонентом у плазмі залишався незмінений ліраглутид. Було виявлено 2 метаболіти (≤9 і ≤5% від рівня загальної радіоактивності у плазмі крові). Виведення. Ліраглутид метаболізується ендогенно подібно до великих білків без участі будь-якого специфічного органу як основного шляху виведення. Після введення дози [3Н]-ліраглутиду незмінений ліраглутид не визначався у сечі або калі. Лише незначна частина введеної радіоактивності у вигляді метаболітів ліраглутиду виводилася нирками або через кишечник (6 та 5% відповідно). Радіоактивні речовини виділяються нирками або через кишечник, в основному, протягом перших 6-8 днів і є 3 метаболітами. Середній кліренс після підшкірного введення ліраглутиду становить приблизно 0,9-1,4 л/год, T1/2 становить приблизно 13 год. Особливі групи пацієнтів Літній вік. Корекція дози з урахуванням віку не потрібна. Згідно з результатами популяційного фармакокінетичного аналізу у пацієнтів з ожирінням або надмірною масою тіла у віці 18-82 років, вік не надавав клінічно значущого впливу на фармакокінетику ліраглутиду при підшкірному введенні в дозі 3 мг. Підлога. На основі даних популяційного фармакокінетичного аналізу, у жінок скоригований за масою тіла кліренс ліраглутиду після підшкірного введення в дозі 3 мг на 24% менше, ніж у чоловіків. На підставі даних відповідної реакції на вплив препарату, корекція дози з урахуванням статі не потрібна. Етнічна приналежність. Згідно з результатами популяційного фармакокінетичного аналізу, в який були включені дані досліджень у пацієнтів з ожирінням або надмірною масою тіла європеоїдної, негроїдної, азіатської та латиноамериканської расових груп, етнічна приналежність не впливала на фармакокінетику ліраглутиду. Маса тіла. Експозиція ліраглутиду зменшується зі збільшенням вихідної маси тіла. Застосування ліраглутиду в дозі 3 мг щодня забезпечує адекватну експозицію в діапазоні маси тіла 60-234 кг, згідно з оцінкою реакції у відповідь на системну експозицію препарату в клінічних дослідженнях. Експозицію ліраглутиду у пацієнтів із масою тіла більше 234 кг не вивчали. Порушення функції печінки. Фармакокінетику ліраглутиду оцінювали у пацієнтів з різним ступенем порушення функції печінки у дослідженні одноразової дози (0,75 мг). Експозиція ліраглутиду була на 23 і 13% менша у пацієнтів з порушенням функції печінки легкого або середнього ступеня тяжкості відповідно порівняно зі здоровими добровольцями. Експозиція була значно меншою (на 44%) у пацієнтів з порушенням функції печінки тяжкого ступеня (>9 балів за класифікацією Child Pugh). Ниркова недостатність. У дослідженні одноразової дози (0,75 мг) експозиція ліраглутиду була меншою у пацієнтів із нирковою недостатністю порівняно з особами з нормальною функцією нирок. Експозиція ліраглутиду була меншою на 33, 14, 27 та 26%, відповідно, у пацієнтів з нирковою недостатністю легкої (Cl креатиніну 50–80 мл/хв), середнього (30–50 мл/хв), тяжкого ступеня (<30 мл/ хв) і у пацієнтів з термінальною стадією ниркової недостатності, які потребують гемодіалізу. Діти. Клінічні дослідження ефективності та безпеки препарату Саксенда® у дітей не проводились.ФармакодинамікаМеханізм дії Діюча речовина препарату Саксенда® — ліраглутид — є аналогом людського глюкагоноподібного пептиду-1 (ГПП-1), вироблений методом біотехнології рекомбінантної ДНК з використанням штаму Saccharomyces cerevisiae, що має 97% гомологічності амінокислотної 1 Ліраглутид зв'язується та активує рецептор ГПП-1 (ГПП-1Р). Ліраглутид стійкий до метаболічного розпаду, його T1/2 з плазми після підшкірного введення становить 13 год. Фармакокінетичний профіль ліраглутиду, що дозволяє вводити його пацієнтам 1 раз на добу, є результатом самоасоціації, внаслідок якої відбувається уповільнене всмоктування препарату; зв'язування із білками плазми; а також стійкості до дипептидилпептидази-4 (ДПП-4) та нейтральної ендопептидази (НЕП). ГПП-1 є фізіологічним регулятором апетиту та споживання їжі. ГПП-1Р виявлено у кількох областях головного мозку, задіяних у регулюванні апетиту. У дослідженнях на тваринах введення ліраглутиду призводило до його захоплення в специфічних галузях головного мозку, включаючи гіпоталамус, де ліраглутид за допомогою специфічної активації ГПП-1Р посилював сигнали про насичення та послаблював сигнали про голод, тим самим призводячи до зменшення маси тіла. Ліраглутид зменшує масу тіла у людини переважно через зменшення маси жирової тканини. Зменшення маси тіла відбувається за рахунок зменшення споживання їжі. Ліраглутид не збільшує 24-годинну витрату енергії. Ліраглутид регулює апетит за допомогою посилення почуття наповнення шлунка та насичення, одночасно послаблюючи почуття голоду та зменшуючи передбачуване споживання їжі. Ліраглутид стимулює секрецію інсуліну і зменшує невиправдано високу секрецію глюкагону глюкозозалежним чином, а також покращує функцію бета-клітин підшлункової залози, що призводить до зниження концентрації глюкози натще і після їди. Механізм зниження концентрації глюкози також включає невелику затримку випорожнення шлунка. У довгострокових клінічних дослідженнях за участю пацієнтів із надмірною масою тіла або ожирінням застосування препарату Саксенда® у поєднанні з низькокалорійною дієтою та посиленою фізичною активністю призводило до значного зниження маси тіла. Вплив на апетит, споживання калорій, витрата енергії, спорожнення шлунка та концентрацію глюкози натще і після їди Фармакодинамічні ефекти ліраглутиду вивчали у 5-тижневому дослідженні за участю 49 пацієнтів з ожирінням (ІМТ — 30–40 кг/м2) без цукрового діабету. Апетит, споживання калорій та витрата енергії Вважається, що зниження маси тіла при застосуванні препарату Саксенда пов'язане з регулюванням апетиту та кількості споживаних калорій. Апетит оцінювали перед та протягом 5 год після стандартного сніданку; необмежене споживання їжі оцінювали під час наступного обіду. Препарат Саксенда® збільшував почуття насичення та наповнення шлунка після їди та зменшував почуття голоду та оцінну кількість передбачуваного споживання їжі, а також зменшував необмежене споживання їжі порівняно з плацебо. При оцінці за допомогою респіраторної камери не відзначалося пов'язаного з терапією збільшення 24-годинної витрати енергії. Випорожнення шлунка Застосування препарату Саксенда® призводило до невеликої затримки спорожнення шлунка протягом першої години після їди, внаслідок чого зменшувалася швидкість підвищення концентрації, а також загальна концентрація глюкози крові після їди. Концентрація глюкози, інсуліну та глюкагону натще та після їди Концентрацію глюкози, інсуліну і глюкагону натще і після їди оцінювали перед і протягом 5 годин після стандартизованого їди. Порівняно з плацебо препарат Саксенда® зменшував концентрацію глюкози крові натще і після їди (AUC0–60 хв) протягом першої години після їди, а також зменшував 5-годинну AUC глюкози та наростаючу концентрацію глюкози (AUC0–300 хв). Крім того, препарат Саксенда® зменшував постпрандіальну концентрацію глюкагону (AUC0–300 хв) та інсуліну (AUC0–60 хв) та наростаючу концентрацію інсуліну (iAUC0–60 хв) після їди порівняно з плацебо. Концентрацію натще і наростаючу концентрацію глюкози та інсуліну також оцінювали під час перорального тесту толерантності до глюкози або без порушення толерантності до глюкози. Порівняно з плацебо препарат Саксенда® зменшував концентрацію натще і наростаючу концентрацію глюкози. Ефект був більш вираженим у пацієнтів із порушенням толерантності до глюкози. Крім того, препарат Саксенда зменшував концентрацію натще і збільшував наростаючу концентрацію інсуліну порівняно з плацебо. Вплив на концентрацію натще і наростаючу концентрацію глюкози у пацієнтів з цукровим діабетом типу 2 з надмірною масою тіла або ожирінням Препарат Саксенда® знижував концентрацію глюкози натще і середню наростаючу постпрандіальну концентрацію глюкози (через 90 хв після їди, середнє значення для 3-х прийомів їжі на добу) порівняно з плацебо. Функція бета-клітин підшлункової залози У клінічних дослідженнях тривалістю до одного року із застосуванням препарату Саксенда® у пацієнтів з надмірною масою тіла або ожирінням та з цукровим діабетом або без такого було продемонстровано покращення та збереження функції бета-клітин підшлункової залози при використанні таких методів вимірювання, як гомеостатична модель оцінки функції бета -клітин (НОМА-В) та співвідношення концентрацій проінсуліну та інсуліну. Клінічна ефективність та безпека Ефективність та безпека застосування препарату Саксенда® для тривалої корекції маси тіла у поєднанні з низькокалорійною дієтою та посиленням фізичної активності була вивчена у 4 рандомізованих подвійних сліпих плацебо-контрольованих дослідженнях (3 дослідження тривалістю 56 тижнів та 1 дослідження тривалістю 32 тижнів). Дослідження включали загалом 5358 пацієнтів 4 різних популяцій: 1) пацієнти з ожирінням або надмірною масою тіла, а також з одним із наступних станів/захворювань: порушення толерантності до глюкози, артеріальна гіпертензія, дисліпідемія; 2) пацієнти з ожирінням або надмірною масою тіла з недостатньо контрольованим цукровим діабетом типу 2 (значення HbА1c у діапазоні 7-10%), до початку дослідження для корекції HbА1c у цих пацієнтів застосовували: дієту та фізичні вправи, метформін,препарати сульфонілсечовини, глітазону окремо або у будь-яких комбінаціях; 3) пацієнти з ожирінням з обструктивним апное середнього або тяжкого ступеня; 4) пацієнти з ожирінням або надмірною масою тіла та супутньою артеріальною гіпертензією або дисліпідемією, які досягли зниження маси тіла не менше ніж на 5% за допомогою низькокалорійної дієти. Маса тіла Більше виражене зниження маси тіла було досягнуто у пацієнтів з ожирінням/надлишковою масою тіла, які отримували препарат Саксенда®, у порівнянні з пацієнтами, які отримували плацебо, у всіх досліджених групах, у т.ч. з наявністю або відсутністю порушення толерантності до глюкози, цукровим діабетом типу 2 та обструктивним апное середнього або тяжкого ступеня. У дослідженні 1 (пацієнти з ожирінням та надмірною масою тіла, з наявністю або відсутністю порушення толерантності до глюкози) зниження маси тіла становило 8% у пацієнтів, які отримували препарат Саксенда у порівнянні з 2,6% у групі плацебо. У дослідженні 2 (пацієнти з ожирінням та надмірною масою тіла з цукровим діабетом типу 2) зниження маси тіла склало 5,9% у пацієнтів, які отримували препарат Саксенда®, порівняно з 2% у групі плацебо. У дослідженні 3 (пацієнти з ожирінням та надмірною масою тіла з обструктивним апное середнього або тяжкого ступеня) зниження маси тіла склало 5,7% у пацієнтів, які отримували препарат Саксенда®, порівняно з 1,6% у групі плацебо. У дослідженні 4 (пацієнти з ожирінням та надмірною масою тіла після попередньої втрати маси тіла не менше ніж 5%) подальше зниження маси тіла становило 6,3% у пацієнтів, які отримували препарат Саксенда®, порівняно з 0,2% у групі плацебо. У дослідженні 4 більша кількість пацієнтів зберегла втрату маси тіла, яка була досягнута до початку лікування препаратом Саксенда® у порівнянні з плацебо (81,4 та 48,9% відповідно). Крім того, у всіх досліджених популяціях більша частина пацієнтів, які отримували препарат Саксенда®, досягли зниження маси тіла не менше ніж на 5% і більш ніж на 10% порівняно з пацієнтами, які отримували плацебо. У дослідженні 1 (пацієнти з ожирінням та надмірною масою тіла з наявністю або відсутністю порушення толерантності до глюкози) зниження маси тіла не менше ніж 5% на 56-й нед терапії відмічено у 63,5% пацієнтів, які отримували препарат Саксенда®, порівняно з 26,6% у групі плацебо. Співвідношення пацієнтів, у яких зниження маси тіла на 56 тижнів терапії досягло більш ніж 10%, становить 32,8% у групі пацієнтів, які отримували препарат Саксенда®, порівняно з 10,1% у групі плацебо. Загалом зниження маси тіла відбулося у приблизно 92% пацієнтів, які отримували препарат Саксенда®, порівняно з приблизно 65% у групі плацебо. Зниження маси тіла після 12 тижнів терапії препаратом Саксенда® Пацієнти з ранньою відповіддю на терапію були визначені як пацієнти, у яких було досягнуто зниження маси тіла не менше ніж на 5% після 12 тижнів терапії (4 тижні збільшення дози та 12 тижнів терапії в дозі 3 мг). У двох дослідженнях (пацієнти з ожирінням або надмірною масою тіла без та з цукровим діабетом типу 2) у 67,5 та 50,4% пацієнтів було досягнуто зниження маси тіла не менше ніж на 5% після 12 тижнів терапії. При продовженні терапії препаратом Саксенда® (до 1 року) 86,2% з цих пацієнтів досягли зниження маси тіла не менше ніж на 5% та 51% – не менше ніж на 10%. Середнє зниження маси тіла цих пацієнтів, які завершили дослідження, становило 11,2% проти вихідним значенням. У пацієнтів, які досягли зниження маси тіла менш ніж на 5% після 12 тижнів терапії в дозі 3 мг і завершили дослідження (1 рік), середнє зниження маси тіла становило 3,8%. Контроль глікемії Терапія препаратом Саксенда® суттєво покращувала глікемічні показники в субпопуляціях з нормоглікемією, порушенням толерантності до глюкози (середнє зниження HbА1с – 0,3%) та цукровим діабетом типу 2 (середнє зниження HbA1c – 1,3%) порівняно з плацебо - 0,1 та 0,4% відповідно). У дослідженні за участю пацієнтів з порушенням толерантності до глюкози цукровий діабет типу 2 розвинувся у меншої кількості пацієнтів, які отримували препарат Саксенда®, порівняно з групою плацебо (0,2 та 1,1% відповідно). У більшої кількості пацієнтів із порушенням толерантності до глюкози спостерігався зворотний розвиток цього стану порівняно з групою плацебо (69,2 та 32,7% відповідно). У дослідженні за участю пацієнтів із цукровим діабетом типу 2 69,2 та 56,5% пацієнтів, які отримували препарат Саксенда®, досягли цільового значення HbА1с Кардіометаболічні параметри У дослідженні за участю пацієнтів з ожирінням або надмірною масою тіла з або без порушення толерантності до глюкози при застосуванні препарату Саксенда® спостерігалося суттєве зниження сАД (на 4,3 проти 1,5 пункту), дАД (на 2,7 проти 1,8 пункту) ), кола талії (на 8,2 проти 4 см) та значна зміна концентрації ліпідів натще (зниження загального Хс на 3,2 проти 0,9%; зниження ЛПНГ на 3,1 проти 0,7%; збільшення ЛПВП на 2, 3 проти 0,5%, зниження тригліцеридів на 13,6 проти 4,8% порівняно з плацебо. Індекс апное-гіпное При застосуванні препарату Саксенда® спостерігалося суттєве зниження порівняно з плацебо тяжкості обструктивного апное, що оцінювалось зі зменшення індексу апное-гіпное (ІАГ) на 12,2 та 6,1 випадків на годину відповідно. Імуногенність З урахуванням потенційних імуногенних властивостей білкових та пептидних лікарських препаратів у пацієнтів можуть з'явитися антитіла до ліраглутиду після терапії препаратом Саксенда®. У клінічних дослідженнях у 2,5% пацієнтів, які отримували препарат Саксенда, з'явилися антитіла до ліраглутиду. Утворення антитіл не спричинило зниження ефективності препарату Саксенда®. Оцінка серцево-судинних явищ Значні небажані серцево-судинні явища (МАСЕ) були оцінені групою зовнішніх незалежних експертів та визначені як несмертельний інфаркт міокарда, несмертельний інсульт та смерть через серцево-судинну патологію. У всіх довгострокових клінічних дослідженнях із застосуванням препарату Саксенда® було відмічено 6 МАСЕ у пацієнтів, які отримували препарат Саксенда®, та 10 МАСЕ – у отримували плацебо. Відношення ризиків та 95% ДІ при порівнянні препарату Саксенда® та плацебо склало 0,31 [0,1; 0,92]. У клінічних дослідженнях 3-ї фази спостерігалося збільшення ЧСС у середньому на 2,5 уд/хв (від 1,6 до 3,6 уд/хв в окремих дослідженнях) у пацієнтів, які отримували препарат Саксенда®. Найбільше збільшення ЧСС спостерігалося після 6 тижнів терапії. Це збільшення було оборотним і зникало після припинення терапії ліраглутидом. Результати оцінки пацієнтів Препарат Саксенда® у порівнянні з плацебо покращував оцінки, що визначаються пацієнтами, за окремими показниками. Було відзначено значне поліпшення загальної оцінки спрощеного опитувальника впливу маси тіла на якість життя (IWQoL-Lite) і всіх шкал опитувальника для оцінки якості життя SF-36, що вказує на позитивний вплив на фізичний та психологічний компонент якості життя. Доклінічні дані щодо безпеки Доклінічні дані, засновані на дослідженнях фармакологічної безпеки, токсичності повторних доз та генотоксичності, не виявили жодної небезпеки для людини. У 2-річних дослідженнях канцерогенності у щурів та мишей були виявлені пухлини С-клітин щитовидної залози, які не призводили до летального результату. Нетоксична доза (NOAEL) у щурів не встановлена. У мавп, які отримували терапію протягом 20 місяців, розвиток цих пухлин не спостерігалося. Результати, отримані в ході досліджень на гризунах, обумовлені тим, що гризуни виявляють особливу чутливість щодо опосередкованого рецептором ГПП-1 не специфічного генотоксичного механізму. Значимість даних для людини є низькою, проте не може бути повністю виключена. Поява інших новоутворень, пов'язаних із терапією, відзначено не було. У дослідженнях на тваринах не виявлено прямого несприятливого ефекту препарату на фертильність, але було відзначено незначне збільшення частоти ранньої ембріональної смерті при застосуванні найвищих доз препарату. Введення ліраглутиду в середині гестаційного періоду викликало зменшення маси тіла матері та зростання плода з невивченим до кінця впливом на ребра у щурів, а у кролів – відхилення у будові скелета. Зростання новонароджених у щурів було знижено під час терапії ліраглутидом, і це зниження зберігалося після закінчення грудного вигодовування у групі, яка отримувала високі дози препарату. Невідомо, чим зумовлено таке зниження зростання новонароджених особин щурів - зниженням споживання калорій материнськими особинами або прямим впливом ГПП-1 на плід/новонароджених.Показання до застосуванняЯк доповнення до низькокалорійної дієти та посиленого фізичного навантаження для тривалого застосування з метою корекції маси тіла у дорослих пацієнтів з ІМТ: ≥30 кг/м2 (ожиріння) або ≥27 кг/м2 таПротипоказання до застосуванняпідвищена чутливість до ліраглутиду або до будь-якого з допоміжних компонентів препарату; медулярний рак щитовидної залози в анамнезі, зокрема. у сімейному; множинна ендокринна неоплазія ІІ типу; тяжка депресія, суїцидальні думки або поведінка, у т.ч. в анамнезі; порушення функції нирок тяжкого ступеня; порушення функції печінки тяжкого ступеня; серцева недостатність III–IV функціонального класу (відповідно до класифікації NYHA); одночасне застосування інших препаратів для корекції маси тіла; одночасне застосування з інсуліном; вторинне ожиріння на фоні ендокринологічних захворювань або розладів харчової поведінки, або на фоні застосування лікарських засобів, які можуть призвести до збільшення маси тіла; запальні захворювання кишечника та діабетичний парез шлунка (досвід застосування препарату Саксенда® у пацієнтів обмежений). Застосування ліраглутиду у таких пацієнтів не рекомендується, оскільки воно пов'язане з транзиторними небажаними реакціями з боку шлунково-кишкового тракту, включаючи нудоту, блювання та діарею; період вагітності; період грудного вигодовування; дитячий вік до 18 років. З обережністю: у пацієнтів з хронічною серцевою недостатністю класу I–II відповідно до класифікації NYHA, порушення функції печінки легкого або середнього ступеня тяжкості, панкреатиту в анамнезі, захворювань щитовидної залози; у пацієнтів віком ≥75 років.Вагітність та лактаціяДані щодо застосування препарату Саксенда у вагітних жінок обмежені. У дослідженнях на тваринах була продемонстрована репродуктивна токсичність (див. Доклінічні дані з безпеки). Потенційний ризик для людини невідомий. Застосування препарату Саксенда у період вагітності протипоказане. При плануванні або настанні вагітності терапію препаратом Саксенда необхідно припинити. Невідомо, чи ліраглутид проникає в грудне молоко людини. У дослідженнях на тваринах було продемонстровано, що проникнення ліраглутиду та структурно близьких метаболітів у грудне молоко є низьким. У доклінічних дослідженнях було продемонстровано пов'язане з терапією уповільнення зростання новонароджених щурів, які перебувають на грудному вигодовуванні. У зв'язку з відсутністю досвіду застосування препарат Саксенда протипоказаний під час грудного вигодовування.Побічна діяПрограма клінічних досліджень препарату Саксенда® складається з 5 завершених клінічних досліджень, у яких взяли участь 5813 пацієнтів з ожирінням або надмірною масою тіла і, як мінімум, з одним пов'язаним з надлишковою масою тіла супутнім захворюванням. В цілому, порушення з боку шлунково-кишкового тракту були найпоширенішими побічними ефектами під час терапії препаратом Саксенда®. Нижче наведено перелік небажаних реакцій, зареєстрованих у ході клінічних досліджень. Небажані реакції розподілені по групам відповідно до систем органів MedDRA та частоти. Частота визначена так: дуже часто (≥1/10); часто (≥1/100 до З боку шлунково-кишкового тракту: дуже часто – нудота, блювання, діарея, запор; часто - сухість у роті, диспепсія, гастрит, гастроезофагеальний рефлюкс, біль у верхніх відділах живота, метеоризм, відрижка, здуття живота; нечасто – панкреатит. З боку імунної системи: рідко – анафілактичні реакції. З боку обміну речовин та харчування: часто – гіпоглікемія; нечасто – дегідратація. Порушення психіки: часто безсоння. З боку нервової системи: часто запаморочення, дисгевзія. Серце: нечасто – тахікардія. З боку печінки та жовчовивідних шляхів: часто – холелітіаз; нечасто – холецистит. З боку шкіри та підшкірних тканин: нечасто – кропив'янка. З боку нирок та сечовивідних шляхів: рідко – гостра ниркова недостатність, порушення функції нирок. Загальні розлади та порушення у місці введення: часто - реакції у місці введення, астенія, стомлюваність; нечасто – нездужання. Опис окремих небажаних реакцій Гіпоглікемія у пацієнтів без цукрового діабету типу 2. У клінічних дослідженнях за участю пацієнтів з надмірною масою тіла або ожирінням без цукрового діабету типу 2, які отримували терапію препаратом Саксенда® у поєднанні з дієтою та фізичними навантаженнями, тяжких гіпоглікемій (вимагають надання допомоги третьою особою) не було. Про симптоми гіпоглікемії повідомляли 1,6% пацієнтів, які отримували препарат Саксенда®, та 1,1% пацієнтів, які отримували плацебо; однак ці випадки не були підтверджені вимірюванням концентрації глюкози крові. Найчастіше відзначалася легка гіпоглікемія. Гіпоглікемія у пацієнтів з цукровим діабетом типу 2. У клінічному дослідженні за участю пацієнтів з надмірною масою тіла або ожирінням та цукровим діабетом типу 2, які отримували терапію препаратом Саксенда® у поєднанні з дієтою та фізичними навантаженнями, випадки тяжкої гіпоглікемії (вимагають надання допомоги) були відзначені у 0,7% пацієнтів, які отримували препарат Саксенда®, і лише у пацієнтів, які одночасно отримували терапію похідними сульфонілсечовини. Також у цій групі пацієнтів підтверджена гіпоглікемія (концентрація глюкози ≤3,9 ммоль/л у поєднанні з симптомами) була відзначена у 43,6% пацієнтів, які отримували препарат Саксенда®, та 27,3% пацієнтів, які отримували плацебо. Серед пацієнтів, які не отримували одночасно сульфонілсечовини, підтверджена гіпоглікемія була відзначена у 15,7% пацієнтів, які отримували препарат Саксенда®,та у 7,6% пацієнтів, які отримували плацебо. Небажані реакції з боку шлунково-кишкового тракту. Більшість реакцій з боку шлунково-кишкового тракту були легким або середнім ступенем тяжкості, минущими і, в більшості випадків, не призводили до припинення терапії. Реакції зазвичай виникали у перші тижні терапії, та їх прояви поступово зменшувалися протягом кількох днів чи тижнів під час продовження терапії. У пацієнтів віком ≥65 років можуть спостерігатися більш виражені прояви небажаних реакцій з боку шлунково-кишкового тракту під час терапії препаратом Саксенда®. У пацієнтів з порушенням функції нирок легкого або середнього ступеня тяжкості (Cl креатиніну ≥30 мл/хв) можуть спостерігатися більш виражені прояви небажаних реакцій з боку шлунково-кишкового тракту під час терапії препаратом Саксенда®. Алергічні реакції. Було відмічено кілька випадків анафілактичних реакцій з такими симптомами, як артеріальна гіпотензія, серцебиття, задишка або периферичні набряки. Анафілактичні реакції потенційно можуть бути загрозливими для життя. Реакції у місці введення. У пацієнтів, які отримували препарат Саксенда, були описані реакції в місці введення. Ці реакції, як правило, були легким, носили транзиторний характер і в більшості випадків зникали при продовженні терапії. Тахікардія. У клінічних дослідженнях тахікардія була відзначена у 0,6% пацієнтів, які отримували препарат Саксенда®, та у 0,1% пацієнтів, які отримували плацебо. Більшість явищ були легким або середнім ступенем тяжкості. Явлення були поодинокими і здебільшого проходили при продовженні терапії препаратом Саксенда®.Взаємодія з лікарськими засобамиОцінка лікарської взаємодії in vitro. Була продемонстрована дуже низька здатність ліраглутиду до фармакокінетичних взаємодій з іншими діючими речовинами, зумовленим метаболізмом у системі цитохрому Р450 (CYP) та зв'язуванням із білками плазми крові. Оцінка лікарської взаємодії in vivo. Невелика затримка спорожнення шлунка при застосуванні ліраглутиду може впливати на всмоктування препаратів, що одночасно застосовуються для прийому внутрішньо. У дослідженнях взаємодії не було продемонстровано якесь клінічно значуще уповільнення всмоктування, тому корекція дози препаратів не потрібна. Дослідження взаємодії проводили із застосуванням ліраглутиду у дозі 1,8 мг. Вплив на швидкість спорожнення шлунка був однаковим при застосуванні ліраглутиду у дозі 1,8 мг та 3 мг (AUC0–300 хв парацетамолу). У кількох пацієнтів, які отримували ліраглутид, було відмічено щонайменше один епізод важкої діареї. Діарея може впливати на всмоктування одночасно застосовуваних лікарських препаратів для внутрішнього застосування. Варфарин та інші похідні кумарину. Досліджень взаємодії не проводили. Клінічно значуща взаємодія з діючими речовинами з низькою розчинністю або з вузьким терапевтичним індексом, таким як варфарин, не може бути виключена. Після початку лікування препаратом Саксенда® у пацієнтів, які отримують варфарин або інші похідні кумарину, рекомендується більш частий контроль MHO. Парацетамол (ацетамінофен). Ліраглутид не змінював загальну експозицію парацетамолу після одноразової дози 1000 мг. Cmax парацетамолу було знижено на 31%, а медіана Tmax збільшено на 15 хв. Корекція дози при супутньому застосуванні парацетамолу не потрібна. Аторвастатин. Ліраглутид не змінював загальну експозицію аторвастатину після застосування одноразової дози аторвастатину 40 мг. Тому корекція дози аторвастатину при застосуванні у поєднанні з ліраглутидом не потрібна. Cmax аторвастатину була знижена на 38%, а медіана Tmax збільшена з 1 до 3 годин при застосуванні ліраглутиду. Гризеофульвін. Ліраглутид не змінював загальну експозицію гризеофульвіну після застосування одноразової дози гризеофульвіну 500 мг. Cmax гризеофульвіну було збільшено на 37%, а медіана Tmax не змінилася. Корекція дози гризеофульвіну та інших сполук з низькою розчинністю та високою проникною здатністю не потрібна. Дігоксин. Застосування одноразової дози дигоксину 1 мг у поєднанні з ліраглутидом призвело до зменшення AUC дигоксину на 16%, зменшення Cmax на 31%. Медіана Tmax збільшилася з 1 до 1,5 год. З урахуванням даних результатів корекція дози дигоксину не потрібна. Лізіноприл. Застосування одноразової дози лізиноприлу 20 мг у поєднанні з ліраглутидом призвело до зменшення AUC лізиноприлу на 15%, зменшення Cmax на 27%. Медіана Tmax лізиноприлу збільшилася з 6 до 8 год. З урахуванням даних результатів корекція дози лізиноприлу не потрібна. Пероральні гормональні контрацептивні засоби. Ліраглутид призводив до зменшення Cmax етинілестрадіолу та левоноргестрелу на 12 і 13% відповідно після застосування одноразової дози перорального гормонального контрацептивного препарату. Tmax обох лікарських речовин на фоні застосування ліраглутиду збільшувався на 1,5 год. Таким чином, не очікується вплив на контрацептивний ефект при сумісному застосуванні з ліраглутидом. Несумісність. Лікарські речовини, додані до препарату Саксенда можуть викликати руйнування ліраглутиду. У зв'язку з відсутністю досліджень сумісності цей лікарський препарат не можна змішувати з іншими лікарськими засобами.Спосіб застосування та дозиП/к. Препарат не можна вводити внутрішньовенно або внутрішньом'язово. Препарат Саксенда® вводять один раз на добу будь-коли, незалежно від їди. Його слід вводити в ділянку живота, стегна чи плеча. Місце та час ін'єкції може бути змінено без корекції дози. Тим не менш, бажано робити ін'єкції приблизно в той самий час доби після вибору найбільш зручного часу. Дози. Початкова доза становить 0,6 мг на добу. Дозу збільшують до 3 мг на добу, додаючи по 0,6 мг з інтервалами не менше 1 тиж для поліпшення шлунково-кишкової переносимості (див. таблицю). Якщо зі збільшенням дози нова погано переноситься пацієнтом протягом 2 тижнів поспіль, слід розглянути питання припинення терапії. Застосування препарату у добовій дозі більше 3 мг не рекомендується. Показники Доза, мг Тижня Збільшення дози протягом 4 тижнів 0,6 1-а 1,2 2-а 1,8 3-тя 2,4 4-та Терапевтична доза 3 Терапію препаратом Саксенда слід припинити, якщо після 12 тижнів застосування препарату в дозі 3 мг на добу втрата в масі тіла склала менше 5% від вихідного значення. Необхідність продовження терапії слід щорічно переглядати. Пропущена доза. Якщо після звичайного часу введення дози пройшло менше 12 годин, пацієнт повинен ввести нову якнайшвидше. Якщо до звичайного часу введення наступної дози залишилося менше 12 годин, пацієнт не повинен вводити пропущену, а відновити введення препарату з наступної запланованої дози. Не слід вводити додаткову або підвищену дозу для компенсації пропущеної. Пацієнти з цукровим діабетом типу 2. Препарат Саксенда не слід застосовувати в комбінації з іншими агоністами рецепторів ГПП-1. На початку терапії препаратом Саксенда® рекомендується зменшити дози одночасно застосовуваних секретагогів інсуліну (таких як препарати сульфонілсечовини) для зменшення ризику розвитку гіпоглікемії. Особливі групи пацієнтів Пацієнти похилого віку (≥65 років). Корекція дози з урахуванням віку не потрібна. Досвід застосування препарату у пацієнтів віком ≥75 років обмежений, застосовувати препарат у таких пацієнтів потрібно з обережністю. Ниркова недостатність. У пацієнтів з порушенням функції нирок легкого або середнього ступеня (Cl креатиніну ≥30 мл/хв) корекція дози не потрібна. Є обмежений досвід застосування препарату Саксенда у пацієнтів з порушенням функції нирок тяжкого ступеня (Cl креатиніну Порушення функції печінки. У пацієнтів з порушенням функції печінки легкого або середнього ступеня тяжкості дози не потрібно. У пацієнтів з порушенням функції печінки легкого або середнього ступеня тяжкості препарат слід застосовувати з обережністю. Застосування препарату Саксенда у пацієнтів з порушенням функції печінки тяжкого ступеня протипоказано. Діти. Застосування препарату Саксенда® у дітей та підлітків віком до 18 років протипоказане через відсутність даних щодо безпеки та ефективності. Перед використанням попередньо заповненої шприц-ручки з препаратом Саксенда слід уважно прочитати цю інструкцію. Використовувати шприц-ручку лише після того, як пацієнт навчився нею користуватися під керівництвом лікаря чи медсестри. Перевірити маркування на етикетці шприц-ручки, щоб переконатися, що вона містить препарат Саксенда® 6 мг/мл, а потім уважно вивчити наведені нижче ілюстрації, на яких показано деталі шприц-ручки та голки. Якщо пацієнт слабкозорий або має серйозні проблеми із зором, і він не може розрізнити цифри на лічильнику дози, не використовувати шприц-ручку без сторонньої допомоги. Допомогти може людина без порушень зору, навчена правильному використанню попередньо заповненої шприц-ручки із препаратом Саксенда®. Попередньо заповнена шприц-ручка містить 18 мг ліраглутиду та дозволяє вибрати дозу 0,6 мг, 1,2 мг, 1,8 мг, 2,4 мг та 3,0 мг. Шприц-ручка Саксенда® розроблена для використання з одноразовими голками НовоФайн® або НовоТвіст® довжиною до 8 мм. Голки не входять до упаковки. Важлива інформація. Звернути увагу на інформацію, зазначену як важливу, це необхідно для безпечного використання шприц-ручки. Попередньо заповнена шприц-ручка із препаратом Саксенда® та голка. I. Підготовка шприц-ручки з голкою для використання Перевірити назву та колірний код на етикетці шприц-ручки, щоб переконатися, що міститься препарат Саксенда®. Це особливо важливо, якщо пацієнт застосовує різні ін'єкційні препарати. Застосування неправильного препарату може бути шкідливим для здоров'я. Зняти ковпачок із шприц-ручки. Переконатись, що розчин у шприц-ручці прозорий та безбарвний. Подивитися у вікно шкали залишку. Якщо препарат каламутний, шприц-ручку не можна використовувати. Взяти нову одноразову голку та видалити захисну наклейку. Одягти голку на шприц-ручку і повернути її, щоб голка щільно трималася на шприц-ручці. Зняти зовнішній ковпачок голки, але не викидати його. Він знадобиться після завершення ін'єкції, щоб безпечно зняти голку. Зняти та викинути внутрішній ковпачок голки. Якщо пацієнт спробує надягти внутрішній ковпачок назад на голку, він може вколотися. На кінці голки може виникнути крапля розчину. Це нормальне явище, проте пацієнт все одно повинен перевірити надходження препарату, якщо використовується нова шприц-ручка вперше. Не слід приєднувати нову голку до того часу, поки пацієнт нічого очікувати готовий зробити ін'єкцію. Важлива інформація. Завжди використовувати нову голку для кожної ін'єкції, щоб уникнути закупорки голки, зараження, інфікування та введення неправильної дози препарату. Ніколи не використовувати голку, якщо вона погнута чи пошкоджена. ІІ. Перевірка надходження препарату Перед першою ін'єкцією за допомогою нової шприц-ручки перевірити надходження препарату. Якщо шприц-ручка вже є у використанні, то перейти до операції III «Встановлення дози». Повертати селектор дози доти, доки в індикаторному вікні символ перевірки надходження препарату (vvw) не порівняється з вказівником дози. Тримати шприц-ручку голкою вгору. Натиснути пускову кнопку та утримувати її в цьому положенні, доки лічильник дози не повернеться до нуля. "0" повинен стояти навпроти вказівника дози. На кінці голки має з'явитися крапля розчину. На кінці голки може залишатися невелика крапля, але вона не буде введена при ін'єкції. Якщо крапля розчину на кінці голки не з'явилася, необхідно повторити операцію ІІ "Перевірка надходження препарату", але не більше 6 разів. Якщо крапля розчину не з'явилася, слід поміняти голку та повторити цю операцію. Якщо крапля розчину препарату Саксенда так і не з'явилася, слід утилізувати шприц-ручку та використовувати нову. Важлива інформація. Перед використанням нової шприц-ручки вперше необхідно переконатися, що на кінці голки з'явилася крапля розчину. Це гарантує надходження препарату. Якщо крапля розчину не з'явилася, препарат не буде введений, навіть якщо лічильник дозування рухатиметься. Це може вказувати на те, що голка закупорена або пошкоджена. Якщо пацієнт не перевірить надходження препарату перед першою ін'єкцією за допомогою нової шприц-ручки, він може не ввести необхідну дозу і очікуваний ефект препарату Саксенда не буде досягнутий. ІІІ. Встановлення дози Повертати селектор дози, щоб набрати необхідну пацієнтові дозу (0,6 мг, 1,2 мг, 1,8 мг, 2,4 мг або 3 мг). Якщо дозу було встановлено неправильно, повертайте селектор дози вперед або назад, доки не буде встановлено правильну дозу. Максимальна доза, яку можна встановити становить 3 мг. Селектор дози дає змогу змінити дозу. Тільки лічильник дози та покажчик дози покажуть кількість мг препарату у вибраній пацієнтом дозі. Пацієнт може набрати до 3 мг на дозу. Якщо у шприц-ручці, що використовується, міститься менше 3 мг, лічильник дози зупиниться перш, ніж у віконці з'явиться 3. При кожному повороті селектора дози лунають клацання, звук клацань залежить від того, в яку сторону обертається селектор дози (вперед, назад або якщо набрана доза перевищує кількість мг препарату, що залишилася в шприц-ручці). Не слід рахувати ці клацання. Важлива інформація. Перед кожною ін'єкцією перевіряти, скільки препарату пацієнт набрав за лічильником і вказівником дози. Не слід рахувати клацання шприц-ручки. Шкала залишку показує приблизну кількість розчину, що залишився в шприц-ручці, тому її не можна використовувати для відмірювання дози препарату. Не намагатись вибрати інші дози, крім доз 0,6; 1,2; 1,8; 2,4 або 3 мг. Цифри в індикаторному вікні повинні знаходитись навпроти вказівника дозування - таке положення гарантує, що пацієнт отримає правильну дозу препарату. Скільки препарату лишилося? Шкала залишку показує приблизну кількість препарату, що залишився в шприц-ручці Щоб точно визначити скільки препарату залишилося, використовувати лічильник дози. Повертати селектор дози до зупинки лічильника. Якщо він показує «3», у шприц-ручці залишилося щонайменше 3 мг препарату. Якщо лічильник дози показує менше "3", це означає, що в шприц-ручці залишилася недостатня кількість препарату, щоб ввести повну дозу 3 мг. Якщо необхідно ввести більше препарату, ніж залишилося в шприц-ручці Тільки якщо пацієнта навчили лікаря або медсестру, він може розділити дозу препарату між двома шприц-ручками. Використовувати калькулятор, щоб спланувати дози, як рекомендовано лікарем або медсестрою. Важлива інформація. Необхідно бути дуже уважним, щоб розрахувати дозу. Якщо немає впевненості, як правильно розділити дозу при використанні двох шприц-ручок, слід встановити та ввести повну дозу за допомогою нової шприц-ручки. IV. Введення препарату Ввести голку під шкіру, використовуючи техніку ін'єкцій, рекомендовану лікарем або медсестрою. Переконайтеся, що лічильник дози знаходиться в полі зору пацієнта. Не торкатися лічильника дози пальцями - це може перервати ін'єкцію. Натиснути пускову кнопку до упору та утримувати її в цьому положенні, доки лічильник дози не покаже «0». "0" повинен знаходитися точно напроти вказівника дози. При цьому пацієнт може почути чи відчути клацання. Утримувати голку під шкірою після того, як лічильник дози повернувся до нульової позначки, і повільно рахувати до 6. Якщо пацієнт витягне голку з-під шкіри раніше, він побачить, як препарат випливає з голки. У цьому випадку буде введено неповну дозу препарату. Витягти голку з-під шкіри. Якщо в місці ін'єкції з'явилася кров, притиснути до місця уколу ватний тампон. Не масажувати місце уколу. Після завершення ін'єкції можна побачити краплю розчину на кінці голки. Це нормально та не впливає на дозу препарату, яка була введена. Важлива інформація. Завжди звірятися з показаннями лічильника дози, щоб знати, скільки препарату Саксенда® введено. Утримувати пускову кнопку, доки лічильник дози не покаже «0». Як виявити закупорку чи пошкодження голки? Якщо після довгого натискання на пускову кнопку на лічильнику дози не з'являється "0", це може означати закупорку або пошкодження голки. Це означає, що пацієнт не отримав препарат, навіть якщо лічильник доз змінив положення вихідної дози, яку пацієнт встановив. Що робити із закупореною голкою? Зняти голку як описано в операції V «Після завершення ін'єкції» та повторити всі кроки, починаючи з операції I «Підготовка шприц-ручки та нової голки». Слід переконатися, що встановлено необхідну пацієнтові дозу. Ніколи не торкатися лічильника дози під час введення препарату. Це може перервати ін'єкцію. V. Після завершення ін'єкції Поклавши зовнішній ковпачок голки на плоску поверхню, ввести кінець голки всередину ковпачка, не торкаючись його голки. Коли голка увійде в ковпачок, обережно вдягнути ковпачок на голку. Відгвинтити голку і викинути її, дотримуючись запобіжних заходів, згідно з інструкцією лікаря або медсестри. Після кожної ін'єкції надягати на шприц-ручку ковпачок, щоб захистити розчин, що міститься в ній, від впливу світла. Завжди необхідно викидати голку після кожної ін'єкції, щоб забезпечити комфортну ін'єкцію та уникнути закупорки голок. Якщо голка буде закупорена, пацієнт не зможе запровадити препарат. Викидати порожню шприц-ручку з від'єднаною голкою, відповідно до рекомендацій, даних лікарем, медсестрою, фармацевтом або відповідно до місцевих вимог. Важлива інформація. Щоб уникнути випадкових уколів голкою, ніколи не намагайтеся надягти внутрішній ковпачок назад на голку. Завжди видаляти голку зі шприц-ручки після кожної ін'єкції. Це дозволить уникнути закупорки голки, зараження, інфікування, витікання розчину та запровадження неправильної дози препарату. Зберігати шприц-ручку та голки в недоступному для всіх, особливо для дітей місці. Ніколи не передавати свою шприц-ручку з препаратом та голки до неї іншим особам. Особи, які здійснюють догляд за хворим, повинні звертатися з використаними голками з особливою обережністю, щоб уникнути випадкових уколів та перехресного інфікування. Догляд за шприц-ручкою Не залишати шприц-ручку в автомобілі або будь-якому іншому місці, де вона може піддаватися впливу надто високих або надто низьких температур. Не застосовувати препарат Саксенда, якщо він був заморожений. У цьому випадку очікуваного ефекту від застосування препарату не буде досягнуто. Захищати шприц-ручку від попадання на неї пилу, забруднень та всіх видів рідин. Не мити шприц-ручку, не занурювати її в рідину і не змащувати. При необхідності шприц-ручку можна очищати вологою тканиною, змоченою м'яким миючим засобом. Не можна кидати або вдаряти шприц-ручку об тверду поверхню. Якщо пацієнт упустив шприц-ручку або сумнівається у її справності, слід приєднати нову голку та перевірити надходження препарату перед тим, як зробити ін'єкцію. Не допускається повторне наповнення шприц-ручки. Порожню шприц-ручку слід одразу викинути. Не намагатися самостійно полагодити шприц-ручку або розібрати її на частини.ПередозуванняЗа даними клінічних досліджень та післяреєстраційного застосування ліраглутиду, були зареєстровані випадки передозування (вводилася доза 72 мг, що у 24 рази більше за рекомендовану для корекції маси тіла). Також зареєстровано один випадок, коли вводилася шестиразова доза (18 мг на добу) протягом 7 місяців. Симптоми: ці випадки передозування супроводжувалися сильною нудотою, блюванням та діареєю, але у всіх випадках стан пацієнтів відновився без ускладнень. У жодному разі був відзначено важкої гіпоглікемії. Лікування: проведення відповідної симптоматичної терапії.Запобіжні заходи та особливі вказівкиУ пацієнтів з цукровим діабетом не можна застосовувати препарат Саксенда як заміну інсуліну. Серцево-судинна недостатність. Досвід застосування у пацієнтів із ХСН класу I–II відповідно до класифікації NYHA обмежений, тому препарат Саксенда® слід застосовувати з обережністю. панкреатит. Застосування агоністів рецепторів ГПП-1 асоціювалося із ризиком розвитку гострого панкреатиту. Повідомлялося про декілька випадків розвитку гострого панкреатиту при застосуванні ліраглутиду. Пацієнти повинні бути поінформовані про характерні симптоми гострого панкреатиту. У разі підозри на розвиток панкреатиту застосування препарату Саксенда слід припинити; у разі підтвердження гострого панкреатиту терапію відновлювати не слід. Слід бути обережними при застосуванні препарату у пацієнтів з панкреатитом в анамнезі. Холелітіаз та холецистит. У клінічних дослідженнях була відзначена більш висока частота розвитку холелітіазу та холециститу у пацієнтів, які отримували препарат Саксенда®, порівняно з пацієнтами, які отримували плацебо. Це може бути частково пояснено тим, що зниження маси тіла може збільшити ризик розвитку холелітіазу та, отже, холециститу. Холелітіаз та холецистит можуть призвести до госпіталізації та холецистектомії. Пацієнти повинні бути поінформовані про характерні симптоми холелітіазу та холециститу. Захворювання щитовидної залози. У ході клінічних досліджень за участю пацієнтів з цукровим діабетом типу 2 були відмічені небажані явища з боку щитовидної залози, включаючи збільшення концентрації кальцитоніну в сироватці крові, зоб та новоутворення щитовидної залози, особливо у пацієнтів, які вже мають захворювання щитовидної залози. У пацієнтів із захворюваннями щитовидної залози препарат Саксенда слід застосовувати з обережністю. У постмаркетинговому періоді у пацієнтів, які отримували ліраглутид, було виявлено випадки медулярного раку щитовидної залози. Наявних даних недостатньо для встановлення або виключення причинно-наслідкового зв'язку виникнення медулярного раку щитовидної залози із застосуванням ліраглутиду у людини. Препарат Саксенда протипоказаний до застосування у пацієнтів з медулярним раком щитовидної залози в анамнезі, в т.ч. сімейному, та множинній ендокринній неоплазії II типу. Необхідно проінформувати пацієнта про ризик медулярного раку щитовидної залози та про симптоми пухлини щитовидної залози (ущільнення в ділянці шиї, дисфагія, задишка, непрохідна захриплість голосу). Поточний контроль концентрації кальцитоніну в сироватці крові або УЗД щитовидної залози не має суттєвого значення для раннього виявлення медулярного раку щитовидної залози у пацієнтів, які застосовують препарат Саксенда®. Значне підвищення концентрації кальцитоніну в сироватці може свідчити про наявність медулярного раку щитовидної залози, пацієнти з медулярним раком щитовидної залози зазвичай мають концентрацію кальцитоніну більше 50 нг/л. При виявленні підвищення концентрації кальцитоніну в сироватці необхідно провести подальше обстеження пацієнта. Пацієнти з вузлами щитовидної залози, які були виявлені при медогляді або УЗД щитовидної залози, також повинні бути додатково обстежені. ЧСС. У клінічних дослідженнях відзначалося збільшення ЧСС. Клінічна значущість збільшення ЧСС при застосуванні препарату Саксенда®, особливо у пацієнтів із серцевими та цереброваскулярними захворюваннями, залишається неясною через обмежений досвід застосування препарату у цих пацієнтів. Слід проводити контроль ЧСС з інтервалами, що відповідають звичайній клінічній практиці. Пацієнтів слід проінформувати про симптоми тахікардії (відчуття серцебиття або відчуття прискореного серцебиття у спокої). У пацієнтів із клінічно значущою постійною тахікардією у стані спокою слід припинити терапію препаратом Саксенда®. Зневоднення. Ознаки та симптоми зневоднення, включаючи порушення функції нирок та гостру ниркову недостатність, були відзначені у пацієнтів, які отримували агоністи рецепторів ГПП-1. Пацієнти, які отримують препарат Саксенда®, повинні бути поінформовані про потенційний ризик зневоднення, пов'язаного з побічними ефектами з боку шлунково-кишкового тракту, та про необхідність профілактики гіповолемії. Гіпоглікемія у пацієнтів з надмірною масою тіла або ожирінням та цукровим діабетом типу 2. Ризик розвитку гіпоглікемії може бути вищим у пацієнтів з цукровим діабетом типу 2, які отримують препарат Саксенда® у комбінації з похідними сульфонілсечовини. Цей ризик може бути зменшений шляхом зниження дози похідної сульфонілсечовини. Додавання препарату Саксенда до терапії у пацієнтів, які отримують інсулін, не оцінювали. Суїцидальні думки та поведінка. У ході клінічних досліджень 6 (0,2%) з 3384 пацієнтів, які отримували препарат Саксенда®, повідомили про появу суїцидальних думок, один із пацієнтів зробив спробу суїциду. У пацієнтів (1941 особа), які отримували плацебо, це не було відзначено. Пацієнтів необхідно контролювати щодо появи або погіршення депресії, суїцидальних думок або поведінки та/або будь-яких несподіваних змін у настрої або поведінці. У пацієнтів із суїцидальними думками або поведінкою застосування препарату Саксенда слід припинити. Протипоказано застосовувати препарат Саксенда у пацієнтів із суїцидальними спробами або активними суїцидальними думками в анамнезі. Рак грудей. У ході клінічних досліджень повідомлялося про підтверджений рак грудей у 14 (0,6%) з 2379 жінок, які отримували препарат Саксенда®, порівняно з 3 (0,2%) з 1300 жінок, які отримували плацебо, включаючи інвазивний рак (11 випадків у жінок, які отримували препарат Саксенда®, та 3 випадки у жінок, які отримували плацебо) та внутрішньопротокова карцинома in situ (3 випадки у жінок, які отримували препарат Саксенда®, та 1 випадок у жінки, яка отримувала плацебо). Більшість випадків раку були естроген-і прогестеронзалежними. Неможливо визначити, чи були ці випадки пов'язані із застосуванням препарату Саксенда через їхню невелику кількість. Крім того, немає достатніх даних, щоб визначити, чи Саксенда® впливає на вже існуючі новоутворення молочної залози. Папілярний рак щитовидної залози. У ході клінічних досліджень повідомлялося про підтверджену папілярну карциному щитовидної залози у 7 (0,2%) з 3291 пацієнтів, які отримували препарат Саксенда®, порівняно з відсутністю її у групі пацієнтів, які отримували плацебо (1843 пацієнти). З усіх випадків 4 карциноми були менше 1 см у найбільшому діаметрі та 4 були діагностовані за результатами гістології після проведеної за медичними показаннями тиреоїдектомії. Неоплазії ободової та прямої кишки. У ході клінічних досліджень повідомлялося про підтверджені доброякісні неоплазії ободової та прямої кишки (переважно аденомах ободової кишки) у 17 (0,5%) з 3291 пацієнтів, які отримували препарат Саксенда®, порівняно з 4 (0,2%) з 1843 пацієнтів, отримували плацебо. Було зареєстровано два підтверджені випадки злоякісної карциноми ободової та прямої кишки (0,1%) у пацієнтів, які отримували препарат Саксенда®, та жодного у пацієнтів, які отримували плацебо. Порушення серцевої провідності. У ході клінічних досліджень у 11 (0,3%) з 3384 пацієнтів, які отримували препарат Саксенда®, повідомлялося про розвиток порушень серцевої провідності, таких як AV блокада 1-го ступеня, блокада правої ніжки пучка Гіса або блокада лівої ніжки пучка Гіса. У пацієнтів (1941 особа), які отримували плацебо, про розвиток порушень серцевої провідності не повідомлялося. Фертильність. За винятком незначного зменшення кількості живих зародків, результати досліджень тварин не вказують на наявність несприятливого впливу на фертильність. Посібник із застосування. Препарат Саксенда® не можна застосовувати, якщо він виглядає інакше, ніж прозора та безбарвна або майже безбарвна рідина. Препарат Саксенда не можна застосовувати, якщо він був заморожений. Препарат Саксенда можна вводити за допомогою голок довжиною до 8 мм. Шприц-ручка призначена для використання з одноразовими голками НовоФайн або НовоТвіст. Ін'єкційні голки не включені в упаковку. Пацієнт повинен бути проінформований про те, що використану голку слід викидати після кожної ін'єкції, а також про те, що не можна зберігати шприц-ручку із приєднаною голкою. Такий захід дозволить запобігти блокуванню голок, забруднення, інфікування та витікання препарату зі шприц-ручки та гарантує точність дозування. Вплив на здатність керувати транспортними засобами та механізмами. Препарат Саксенда не впливає або незначно впливає на здатність керувати транспортними засобами та механізмами. У зв'язку з ризиком розвитку гіпоглікемії при застосуванні препарату, особливо при комбінованому застосуванні з препаратами сульфонілсечовини у пацієнтів з цукровим діабетом типу 2, слід бути обережними при керуванні транспортними засобами та механізмами.Умови відпустки з аптекЗа рецептомВідео на цю тему
216,00 грн
150,00 грн
Склад, форма випуску та упаковкаАерозоль - 1 мл: Активна речовина: Сальбутамолу сульфат – 0,120 мг (у перерахунку на сальбутамол) – (0,100 мг); Допоміжні речовини: Етанол (спирт етиловий абсолютований)-5,905 мг; Олеїнова кислота – 0,009 мг; Пропелент R 134а (1,1,1,2-тетрафторетан) - 67,966 мг.Опис лікарської формиСуспензія білого або майже білого кольору, що знаходиться під тиском у балоні з нержавіючої сталі з клапаном дозованої дії та розпилювальною насадкою; препарат при виході з балона розпорошується у вигляді аерозольного струменя.ХарактеристикаСальбутамол-Фармстандарт - бронходилатируючий засіб. Чинить бронходилатируючий ефект, попереджаючи або купуючи спазм бронхів, знижує опір у дихальних шляхах. У рекомендованих терапевтичних дозах не має негативного впливу на серцево-судинну систему. Має ряд метаболічних ефектів: знижує концентрацію калію в плазмі крові, впливає на глікогеноліз та виділення інсуліну. Препарат застосовується при бронхіальній астмі (для купірування та запобігання нападам) та при хронічній обструктивній хворобі легень, хронічному бронхіті. Випускається у формі аерозолю для інгаляцій дозованого, 100 мкг/доза, по 200 доз препарату в алюмінієвому балоні з клапаном дозуючої дії, оснащеного насадкою розпилювання. Відпускають за рецептом.Фармакотерапевтична групабронходилатируючий засіб – β2-адреноміметик селективний.ФармакокінетикаВсмоктування Після інгаляції 10-20% дози сальбутамолу досягають нижніх дихальних шляхів. Інша частина дози залишається в інгаляторі або відкладається в ротоглотці і потім проковтується. Фракція, що потрапила в дихальні шляхи, абсорбується в легеневі тканини та кров, але не метаболізується у легенях. Розподіл Ступінь зв'язування сальбутамолу з білками плазми становить 10 %. Метаболізм При попаданні в системний кровообіг сальбутамол піддається печінковому метаболізму. Проковтнута частина інгаляційної дози абсорбується зі шлунково-кишкового тракту і піддається активному метаболізму при «першому проходженні» через печінку, перетворюючись на фенольний сульфат. Виведення Введений внутрішньовенно сальбутамол має період напіввиведення 4-6 годин. Сальбутамол виводиться переважно нирками у вигляді кон'югату – неактивного 4'-О-сульфату (фенольний сульфат) та частково у незміненому вигляді, а незначна частина сальбутамолу екскретується через кишечник. Більшість дози сальбутамолу екскретується протягом 72 годин.ФармакодинамікаСальбутамол є селективним агоністом β2-адренорецепторів (β2-адреноміметиком). У терапевтичних дозах він діє на β2-адренорецептори гладкої мускулатури бронхів, незначно впливаючи або взагалі не впливаючи на β1-адренорецептори міокарда. Чинить бронходилатируючий ефект, попереджаючи або купуючи спазм бронхів, знижує опір у дихальних шляхах. Збільшує життєву ємність легень. Збільшує мукоциліарний кліренс (при хронічному бронхіті до 36%), стимулює секрецію слизу, активує миготливий епітелій. У рекомендованих терапевтичних дозах не негативно впливає на серцево-судинну систему, не викликає підвищення артеріального тиску. У меншій мірі порівняно з лікарськими засобами цієї групи має позитивну хроно- та інотропну дію. Викликає розширення коронарних артерій. Має ряд метаболічних ефектів: знижує концентрацію калію в плазмі крові, впливає на глікогеноліз та виділення інсуліну, надає гіперглікемічний (особливо у пацієнтів з бронхіальною астмою) та ліполітичний ефекти, збільшує ризик розвитку ацидозу. Після застосування інгаляційної дози сальбутамолу дія розвивається швидко, початок ефекту – через 5 хвилин, максимум – через 30-90 хвилин (75% максимального ефекту досягається протягом 5 хвилин), тривалість – 4-6 годин.Показання до застосуванняБронхіальна астма: усунення нападів бронхіальної астми, у тому числі при загостренні бронхіальної астми тяжкого перебігу; запобігання нападам бронхоспазму, пов'язаних з впливом алергену або спричиненим фізичним навантаженням; застосування як одного з компонентів при тривалій підтримувальній терапії бронхіальної астми. Хронічна обструктивна хвороба легень (ХОЗЛ), що супроводжується оборотною обструкцією дихальних шляхів, хронічний бронхіт.Протипоказання до застосуванняГіперчутливість до діючої речовини або будь-якого іншого компонента, що входить до складу препарату; ведення передчасних пологів; загрозливий аборт; дитячий вік до 2 років. З обережністю: Сальбутамол-Фармстандарт слід застосовувати з обережністю у пацієнтів з тиреотоксикозом, тахіаритмією, міокардитом, вадами серця, аортальним стенозом, ішемічною хворобою серця, тяжкою хронічною серцевою недостатністю, артеріальною гіпертензією, феохромоцитом, декоматом у період грудного вигодовуванняВагітність та лактаціяДаних про вплив сальбутамолу на фертильність людини немає. Вагітним жінкам сальбутамол призначається тільки в тому випадку, коли очікувана користь пацієнтки перевищує потенційний ризик для плода. Є дані про рідкісні випадки різних вад розвитку у дітей, включаючи формування «вовчої пащі» та вад розвитку кінцівок, на фоні прийому матерями сальбутамолу під час вагітності. У деяких із цих випадків матері приймали кілька супутніх лікарських засобів протягом вагітності. З огляду на відсутність постійного характеру дефектів та фонової частоти виникнення вроджених аномалій, що становить від 2 до 3 %, причинно-наслідковий зв'язок із прийомом сальбутамолу не встановлено. Період грудного вигодовування: Сальбутамол, ймовірно, проникає в грудне молоко, і тому не рекомендується призначати його жінкам, що годують, за винятком тих випадків, коли очікувана користь для самої матері перевищує потенційний ризик для дитини. Немає даних про те, чи має присутній у грудному молоці сальбутамол шкідливу дію на новонародженого.Побічна діяНебажані реакції, подані нижче, перераховані відповідно до ураження органів та систем органів. Частота народження оцінюється таким чином: дуже часто (> 1/10), часто (> 1/100 і < 1/10), нечасто (> 1/1000 і < 1/100), рідко (> 1/10000 і < 1 /1000), дуже рідко (<1/10000). Порушення з боку імунної системи: дуже рідко – реакції гіперчутливості, включаючи ангіоневротичний набряк, кропив'янку, бронхоспазм, зниження артеріального тиску та колапс. Порушення з боку обміну речовин та харчування: рідко – гіперглікемія, гіпокаліємія. Терапія агоністами β2-адренорецепторів може призводити до клінічно значущої гіпокаліємії. Порушення з боку нервової системи: часто – тремор, біль голови; дуже рідко – гіперактивність. Порушення серця: часто – тахікардія; нечасто – ішемія міокарда, сильне серцебиття (пальпітація); дуже рідко – аритмії, включаючи миготливу аритмію; суправентрикулярна тахікардія та екстрасистолія. Порушення з боку судин: рідко – периферична вазодилатація. Порушення з боку дихальної системи, органів грудної клітки та середостіння: дуже рідко – парадоксальний бронхоспазм. Порушення з боку шлунково-кишкового тракту: нечасто – подразнення слизової оболонки ротової порожнини та глотки. Порушення з боку скелетно-м'язової та сполучної тканини: нечасто – м'язові судоми. Якщо будь-які з вказаних в інструкції небажаних реакцій посилюються або Ви помітили будь-які інші небажані реакції, які не вказані в інструкції, повідомте про це лікаря.Взаємодія з лікарськими засобамиНе рекомендується одночасно застосовувати сальбутамол та неселективні блокатори β-адренорецепторів, такі як пропранолол. Сальбутамол не протипоказаний пацієнтам, які отримують інгібітори моноаміноксидази (ІМАО). У пацієнтів з тиреотоксикозом сальбутамол посилює дію стимуляторів центральної нервової системи та тахікардію. Теофілін та інші ксантини при одночасному застосуванні підвищують ймовірність розвитку тахіаритмій. Одночасне застосування з антихолінергічними засобами (в т. ч. інгаляційними) може сприяти підвищенню внутрішньоочного тиску. Діуретики та глюкокортикостероїди посилюють гіпокаліємічну дію сальбутамолу. Взаємодія Сальбутамолу з Леводопою, засобами для інгаляційної анестезії, інгібіторами МАО та трициклічними антидепресантами, серцевими глікозидами може призвести до ризику різкого зниження артеріального тиску.Спосіб застосування та дозиСальбутамол-фармстандарт призначений тільки для інгаляційного застосування. Підвищена потреба застосування агоністів β2-адренорецепторів може бути ознакою посилення бронхіальної астми. У подібній ситуації може бути потрібна переоцінка схеми лікування пацієнта з розглядом доцільності призначення одночасної терапії глюкокортикостероїдами (ГКС). Доза або кратність застосування сальбутамолу може бути збільшена лише за рекомендацією лікаря, оскільки передозування може супроводжуватися розвитком небажаних реакцій. Тривалість дії сальбутамолу у більшості пацієнтів становить від 4 до 6 годин. У пацієнтів, які зазнають труднощів у синхронізації вдиху із застосуванням дозуючого аерозольного інгалятора під тиском, може бути використаний спейсер. У дітей та немовлят, які отримують сальбутамол, доцільно використання педіатричного спейсерного пристрою з лицьовою маскою. При виникненні неприємних відчуттів у роті та першіння у горлі після інгаляції слід прополоскати рот водою. Купірування нападу бронхоспазму Дорослі: Рекомендована доза становить 100 або 200 мкг (1 або 2 інгаляції). Діти: Рекомендована доза становить 100 мкг (1 інгаляція), при необхідності доза може бути збільшена до 200 мкг (2 інгаляції). Не рекомендується застосовувати препарат Сальбутамол-Фармстандарт частіше 4-х разів на добу. Потреба частого застосування максимальних доз препарату Сальбутамол-Фармстандарт або в раптовому збільшенні дози свідчить про погіршення перебігу бронхіальної астми (див. розділ «Особливі вказівки»). Запобігання нападам бронхоспазму, пов'язаним з впливом алергену або спричиненим фізичним навантаженням Дорослі: Рекомендована доза становить 200 мкг (2 інгаляції) за 10-15 хвилин до дії провокуючого фактора або навантаження. Діти: Рекомендована доза становить 100 мкг (1 інгаляція) за 10-15 хвилин до дії провокуючого фактора або навантаження, при необхідності доза може бути збільшена до 200 мкг (2 інгаляції). Тривала підтримуюча терапія Дорослі Діти Рекомендована доза становить до 200 мкг (2 інгаляції) 4 рази на добу.ПередозуванняСимптоми Ознаками та симптомами передозування сальбутамолу є тимчасові явища, фармакологічно зумовлені стимуляцією β-адренергічних рецепторів, такі як зниження артеріального тиску, тахікардія, м'язовий тремор, нудота, блювання, гіперглікемія, лактоацидоз. При застосуванні високих доз, а також при передозуванні бета-агоністів короткої дії спостерігався розвиток лактоацидозу, тому при передозуванні може бути показаний контроль за підвищенням лактату сироваткового та можливістю розвитку метаболічного ацидозу (особливо при збереженні або погіршенні тахіпное, незважаючи на усунення інших ознак бронхоспазу; як свистяче дихання) (див. розділи «Особливі вказівки» та «Побічна дія»). Застосування високих доз сальбутамолу може спричинити гіпокаліємію, тому необхідно контролювати концентрацію калію в плазмі. Лікування Слід скасувати сальбутамол і призначити відповідну симптоматичну терапію. Кардіоселективні β-адреноблокатори у пацієнтів з наявністю кардіальної симптоматики (наприклад, тахікардія, відчуття серцебиття) повинні застосовуватися з обережністю через ризик виникнення бронхоспазму.Умови відпустки з аптекЗа рецептомВідео на цю тему
229,00 грн
154,00 грн
Склад, форма випуску та упаковкаАерозоль - 1 доза: Діюча речовина: сальбутамолу сульфат – 0,1205 мг (у перерахунку на сальбутамол – 0,100 мг); Допоміжні речовини: етанол (етанол абсолютований) – 1,9000 мг; норфлуран (1,1,1,2-тетрафторетан, хладон 134а) – 27,1600 мг. Аерозол для інгаляцій дозований, 100 мкг/доза. По 200 доз препарату в балон алюмінієвий із клапаном дозуючої дії та насадкою-інгалятором із захисним ковпачком. Кожен балон разом з інструкцією із застосування поміщають у картонну пачку.Опис лікарської формиСуспензія білого або майже білого кольору, що знаходиться під тиском у балоні алюмінієвому з дозуючим клапаном та насадкою-інгалятором із захисним ковпачком; препарат при виході з балона розпорошується у вигляді аерозольного струменя, що залишає на склі білу пляму.Фармакотерапевтична групаБронходилатируючий засіб - бета2-адреноміметик селективний.ФармакокінетикаВсмоктування Після інгаляції 10-20% дози сальбутамолу досягає нижніх дихальних шляхів. Інша частина дози залишається в інгаляторі або відкладається в ротоглотці і потім проковтується. Фракція, що відклала у дихальних шляхах, абсорбується у легеневі тканини та кров, але не метаболізується у легенях. Розподіл Ступінь зв'язування сальбутамолу із білками плазми становить 10%. Метаболізм При попаданні в системний кровотік сальбутамол піддається печінковому метаболізму та екскретується переважно нирками у незміненому вигляді або у вигляді фенольного сульфату. Проковтнута частина інгаляційної дози абсорбується зі шлунково-кишкового тракту і піддається значному метаболізму при "першому проходженні" через печінку, перетворюючись на фенольний сульфат. Незмінений сальбутамол та кон'югат екскретуються переважно нирками. Виведення Введений внутрішньовенно сальбутамол має період напіввиведення 4-6 годин. Виводиться частково нирками та частково внаслідок метаболізму до 4'-О-сульфату (фенольний сульфат), який також виводиться переважно нирками. Через кишечник екскретується лише незначна частина введеної дози сальбутамолу. Більшість дози сальбутамолу, введеної в організм внутрішньовенним, пероральним або інгаляційним шляхом, екскретується протягом 72 годин.ФармакодинамікаСальбутамол є селективним агоністом бета2-адренорецепторів. У терапевтичних дозах він діє на бета2-адренорецептори гладкої мускулатури бронхів і надає нетривалу (від 4 до 6 годин) бронхорозширювальну дію на бета2-адренорецептори зі швидким настанням дії (протягом 5 хвилин) при оборотній обструкції дихальних шляхів. Чинить бронходилатируючий ефект, попереджаючи або купуючи спазм бронхів, знижує опір у дихальних шляхах. Збільшує життєву ємність легень. Збільшує мукоциліарний кліренс (при хронічному бронхіті до 36%), стимулює секрецію слизу, активує миготливий епітелій. У рекомендованих терапевтичних дозах не негативно впливає на серцево-судинну систему, не викликає підвищення артеріального тиску. У меншій мірі, у порівнянні з лікарськими препаратами цієї групи, має позитивну хроно- та інотропну дію. Викликає розширення коронарних артерій. Має ряд метаболічних ефектів: знижує концентрацію калію в плазмі, впливає на глікогеноліз та виділення інсуліну, надає гіперглікемічний (особливо у пацієнтів з бронхіальною астмою) та ліполітичний ефект, збільшує ризик розвитку ацидозу.ІнструкціяПідготовка інгалятора: Перед першим застосуванням препарату слід зняти захисний ковпачок із мундштука насадки-інгалятора, що встановлена на балоні та штоку клапана. Потім струшити балон кілька разів вертикальними рухами вгору-вниз, перевернути балон насадкою-інгалятором вниз і, натиснувши вказівним пальцем на денце балона, зробити два розпилення в повітря, щоб перевірити справність препарату. Після перерви у застосуванні препарату протягом кількох днів або більш тривалого часу слід зробити так само одне розпилення в повітря. Використання інгалятора: Зніміть з насадки-інгалятора захисний ковпачок та переконайтеся, що вихідна трубка (мундштук) насадки-інгалятора є чистою. Тримайте балон із встановленою на ньому насадкою-інгалятором між вказівним та великим пальцями у вертикальному положенні, при цьому великий палець повинен розташовуватися під основою насадки-інгалятора, а вказівний палець - над денцем балона. Інтенсивно струсіть алюмінієвий балон із встановленою на ньому насадкою-інгалятором вертикальними рухами вгору-вниз. Зробіть глибокий видих через рот. Не видихайте в інгалятор! Щільно затисніть губами вихідну трубку (мундштук) насадки інгалятора. Балон повинен бути спрямований дном нагору! Зробіть повільний та глибокий вдих. У момент вдиху натисніть вказівним пальцем на денце балона, випускаючи дозу препарату Сальбутамол-фармстандарт ВЧ, і продовжуйте повільно вдихати. Видаліть мундштук насадки-інгалятора з рота і затримайте дихання на 10 секунд або на той час, який не викликає дискомфорту. Повільно видихніть. Після інгаляції прополощіть рот водою, щоб змити ліки, які потрапили під час інгаляції на слизову оболонку ротової порожнини. Не слід ковтати разом зі слиною ліки, що потрапили при інгаляції на слизову оболонку ротової порожнини, і воду, якою Ви змиєте ці ліки. Якщо потрібно ввести ще одну дозу препарату, зачекайте 1 хвилину і повторіть всі дії, починаючи з дій, описаних у пункті 2, і закінчуючи діями, описаними в пункті 6. Закрийте мундштук насадки-інгалятора захисним ковпачком. Під час виконання дій відповідно до пунктів 3 та 4 не поспішайте. У момент випуску дози ліки важливо робити вдих якомога повільніше. Перед використанням потренуйтеся перед дзеркалом. Якщо Ви помітили "пар", що виходить з куточків рота, то почніть дії знову з кроку 2. Якщо Ви помітили "пар", що виходить з верхівки насадки-інгалятора, необхідно або ретельно встановити шток клапана, яким герметизований балон, в посадкове місце всередині насадки-інгалятора або провести чищення насадки-інгалятора. Чищення насадки-інгалятора Насадку-інгалятор слід чистити принаймні раз на тиждень. Вийміть алюмінієвий балон із насадки-інгалятора. Акуратно прополощіть насадку-інгалятор та захисний ковпачок теплою водою. Не можна використовувати гарячу воду! Струсіть насадку-інгалятор та захисний ковпачок, щоб видалити залишки води та висушити їх без використання нагрівальних пристроїв. Не допускайте контакту алюмінієвого балона з водою! Балон розрахований на 200 інгаляцій, після чого балон слід замінити. ПОПЕРЕДЖЕННЯ: пластиковий мундштук для рота розроблений спеціально для препарату Сальбутамол-фармстандарт ВЧ і служить для точного дозування препарату. Мундштук не повинен використовуватися з іншими дозованими аерозолями. Також не можна використовувати препарат Сальбутамол-фармстандарт ВЧ з будь-якими іншими адаптерами, крім мундштука, що поставляється разом з препаратом. Вміст балона перебуває під тиском. Балон не можна відкривати і нагрівати вище 50 °С! Якщо у Вас виникнуть труднощі з інгалятором, зв'яжіться з лікарем. Дітям молодшого віку необхідно використовувати інгалятор під контролем або за допомогою дорослих.Показання до застосуванняБронхіальна астма усунення симптомів бронхіальної астми при їх виникненні; запобігання нападам бронхоспазму, пов'язаних з впливом алергену або спричиненим фізичним навантаженням; застосування як одного з компонентів при тривалій підтримувальній терапії бронхіальної астми. Інші хронічні захворювання легень, що супроводжуються оборотною обструкцією дихальних шляхів, включаючи хронічну обструктивну хворобу (ХОЗЛ), хронічний бронхіт, емфізему легень. Бронходилататори не повинні бути єдиним або основним компонентом терапії бронхіальної астми нестабільного або тяжкого перебігу. За відсутності реакції на сальбутамол у пацієнтів з тяжкою бронхіальною астмою рекомендується проводити терапію глюкокортикостероїдами (ГКС) з метою досягнення та підтримання контролю захворювання. Відсутність реакції на терапію сальбутамолом може вказувати на необхідність термінової консультації лікаря або лікування.Протипоказання до застосуванняГіперчутливість до сальбутамолу або будь-якого іншого компонента, що входить до складу препарату; дитячий вік до 2 років; ведення передчасних пологів; загрозливий аборт. З обережністю: Сальбутамол-фармстандарт ВЧ слід застосовувати з обережністю у пацієнтів з тахіаритмією; ішемічну хворобу серця; міокардитом; пороками серця; аортальний стеноз; тяжкою хронічною серцевою недостатністю; артеріальною гіпертензією; тиреотоксикоз; феохромоцитомою; декомпенсований цукровий діабет; глаукомою; а також при вагітності та в період грудного вигодовування.Вагітність та лактаціяФертильність Немає даних про вплив сальбутамолу на фертильність людини. У доклінічних дослідженнях небажаного впливу фертильність тварин виявлено був. Вагітність Вагітним жінкам препарат слід призначати лише в тому випадку, якщо очікувана користь для матері перевищує потенційний ризик для плода. У ході постреєстраційного спостереження були виявлені рідкісні випадки різних вад розвитку у дітей, включаючи формування "вовчої пащі" та вад розвитку кінцівок, на фоні прийому сальбутамолу матерями під час вагітності. У деяких випадках матері приймали кілька супутніх лікарських препаратів протягом вагітності. З огляду на відсутність постійного характеру дефектів та фонової частоти виникнення вроджених аномалій, що становить від 2 до 3%, причинно-наслідковий зв'язок із прийомом препарату не встановлено. Період грудного вигодовування Сальбутамол, ймовірно, проникає в грудне молоко, і тому його не рекомендується призначати жінкам, що годують, за винятком тих випадків, коли очікувана користь для самої матері переважує потенційний ризик для дитини. Немає даних про те, чи має присутній у грудному молоці сальбутамол шкідливу дію на новонародженого.Побічна діяНебажані реакції, представлені нижче, перераховані відповідно до ураження органів і систем органів і частотою народження. Частота народження оцінюється таким чином: дуже часто (≥ 1/10), часто (≥ 1/100 і < 1/10), нечасто (≥ 1/1000 і < 1/100), рідко (≥ 1/10000 і < 1 /1000), дуже рідко (< 1/10000, включаючи окремі випадки). Категорії частоти були сформовані на підставі клінічних досліджень препарату та післяреєстраційного спостереження. Частота народження небажаних реакцій Порушення з боку імунної системи: дуже рідко – реакції гіперчутливості, включаючи ангіоневротичний набряк, кропив'янку, бронхоспазм, зниження артеріального тиску та колапс. Порушення з боку обміну речовин та харчування: Рідко – гіпокаліємія. Терапія бета2-агоністами може призводити до клінічно значущої гіпокаліємії. Порушення з боку нервової системи: Часто – тремор, головний біль; Дуже рідко: гіперактивність. Порушення з боку серця: Часто – тахікардія; Нечасто – відчуття серцебиття; Дуже рідко – аритмії, включаючи миготливу аритмію; суправентрикулярна тахікардія та екстрасистолія. Порушення з боку судин: Рідко – периферична вазодилятація. Порушення з боку дихальної системи, органів грудної клітки та середостіння: Дуже рідко – парадоксальний бронхоспазм. Порушення з боку шлунково-кишкового тракту: Нечасто – подразнення слизової оболонки порожнини рота та глотки. Порушення з боку скелетно-м'язової та сполучної тканини: Нечасто – м'язові судоми.Взаємодія з лікарськими засобамиНе рекомендується одночасно застосовувати сальбутамол та неселективні блокатори β-адренорецепторів, такі як пропранолол. Сальбутамол не протипоказаний пацієнтам, які отримують інгібітори моноаміноксидази (ІМАО). У пацієнтів з тиреотоксикозом сальбутамол посилює дію стимуляторів центральної нервової системи та тахікардію. Теофілін та інші ксантини при одночасному застосуванні підвищують ймовірність розвитку тахіаритмій. Одночасне застосування з антихолінергічними засобами (в т.ч. інгаляційними) може сприяти підвищенню внутрішньоочного тиску. Діуретики та глюкокортикостероїди посилюють гіпокаліємічну дію сальбутамолу. Взаємодія сальбутамолу з леводопою, засобами для інгаляційної анестезії, інгібіторами МАО та трициклічними антидепресантами, серцевими глікозидами може призвести до ризику різкого зниження артеріального тиску.Спосіб застосування та дозиПрепарат Сальбутамол-фармстандарт ВЧ призначений тільки для інгаляційного введення шляхом вдихання через рот. Підвищена потреба застосування агоністів бета2-адренорецепторів може бути ознакою посилення бронхіальної астми. У подібній ситуації може знадобитися переоцінка схеми лікування пацієнта з розглядом доцільності призначення одночасної терапії кортикостероїдами. Оскільки передозування може супроводжуватися розвитком небажаних реакцій, доза або кратність застосування препарату може бути збільшена лише за рекомендацією лікаря. Тривалість дії сальбутамолу у більшості пацієнтів становить від 4 до 6 годин. У пацієнтів, які зазнають труднощів у синхронізації вдиху із застосуванням дозуючого аерозольного інгалятора під тиском, може бути використаний спейсер. У дітей та немовлят, які одержують препарат Сальбутамол-Фармстандарт ВЧ, доцільно використання педіатричного спейсерного пристрою з лицьовою маскою. Купірування нападу бронхоспазму Дорослі Доза, що рекомендується, становить 100 або 200 мкг. Діти 100 мкг, при необхідності, доза може бути збільшена до 200 мкг. Не рекомендується застосовувати інгалятор Сальбутамол-фармстандарт ВЧ частіше чотирьох разів на добу. Потреба в такому частому застосуванні додаткових доз препарату Сальбутамол-Фармстандарт ВЧ або різке збільшення дози свідчить про погіршення перебігу астми. Запобігання нападам бронхоспазму, пов'язаним з впливом алергену або спричиненим фізичним навантаженням Дорослі 200 мкг за 10-15 хв до дії провокуючого фактора чи навантаження. Діти 100 мкг за 10 15 хв до дії провокуючого фактора або навантаження, при необхідності доза може бути збільшена до 200 мкг. Тривала підтримуюча терапія Дорослі До 200 мкг 4 десь у добу. Діти До 200 мкг 4 десь у добу.ПередозуванняОзнаками та симптомами передозування сальбутамолу є тимчасові явища, фармакологічно опосередковані стимуляцією бета-адренергічних рецепторів, такі як зниження артеріального тиску, тахікардія, м'язовий тремор, нудота, блювання. Застосування великих доз сальбутамолу може спричинити метаболічні зміни, включаючи гіпокаліємію, необхідно контролювати концентрацію калію у сироватці крові. При застосуванні високих доз, а також при передозуванні бета-агоністів короткої дії спостерігався розвиток лактатацидозу, тому при передозуванні може бути показаний контроль над підвищенням лактату сироваткового та можливість розвитку метаболічного ацидозу (особливо при збереженні або погіршенні тахіпное, незважаючи на усунення інших ознак бронхоспазму. як свистяче дихання).Запобіжні заходи та особливі вказівкиЛікування бронхіальної астми рекомендується проводити поетапно, контролюючи клінічну відповідь пацієнта на лікування та функцію легень. Бронходилататори не повинні бути єдиним або основним компонентом терапії бронхіальної астми нестабільного або тяжкого перебігу. Підвищення потреби застосування бронходилататорів короткої дії, зокрема агоністів бета2-адренорецепторів, для полегшення симптомів бронхіальної астми свідчить про погіршення перебігу захворювання. У разі слід переглянути план лікування пацієнта. Раптове та прогресуюче погіршення бронхіальної астми може становити потенційну загрозу для життя пацієнта, тому у подібних ситуаціях слід розглянути доцільність призначення або збільшення дози кортикостероїдів. У пацієнтів групи ризику рекомендується проводити щоденний моніторинг пікової швидкості видиху. Терапія агоністами бета2-адренорецепторів, особливо при введенні парентерально або за допомогою небулайзера, може призводити до гіпокаліємії. Особливу обережність рекомендується виявляти при лікуванні тяжких нападів бронхіальної астми, оскільки в цих випадках гіпокаліємія може посилюватися внаслідок одночасного застосування похідних ксантину, глюкокортикостероїдів, діуретиків, а також внаслідок гіпоксії. У таких ситуаціях рекомендується контролювати концентрацію калію у сироватці крові. Як і при використанні інших засобів для інгаляційної терапії, прийом сальбутамолу може розвиватися парадоксальний бронхоспазм з посиленням хрипів відразу після застосування препарату. Цей стан вимагає негайного лікування з використанням альтернативної форми випуску сальбутамолу або іншого інгаляційного бронходилятатора короткої дії. Препарат Сальбутамол-Фармстандарт ВЧ слід негайно відмінити, оцінити стан пацієнта та, при необхідності, призначити інший швидкодіючий бронходилататор для продовження лікування. У разі відсутності ефекту від застосування раніше ефективної дози інгаляційного сальбутамолу протягом принаймні трьох годин пацієнт повинен звернутися до лікаря щодо необхідності вживання будь-яких додаткових заходів. Слід проінструктувати пацієнтів щодо правильного використання інгалятора Сальбутамол-Фармстандарт ВЧ. Вплив на здатність до керування автотранспортом та управління механізмами Дані щодо впливу препарату сальбутамол на здатність керувати транспортними засобами та механізмами відсутні. У разі розвитку таких небажаних реакцій, як м'язові судоми або бронхоспазм, утриматися від керування транспортними засобами та механізмами, а також від занять іншими потенційно небезпечними видами діяльності, що потребують підвищеної концентрації уваги та швидкості психомоторних реакцій. Вміст однієї дози препарату 1,90 мг етанолу безводного настільки мало, що не може вплинути на здатність керувати автомобілем та/або іншими механізмами.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаСупозиторії – 1 суп.: Діюча речовина: Простати екстракт (Простатилен®)* (у перерахунку на водорозчинні пептиди 5 мг) – 50 мг; Допоміжні речовини: Диметилсульфоксид – 90 мг; Макрогол-400 – 112 мг; Макрогол-1500 – достатня кількість для отримання супозиторію масою 2800 мг. * - субстанція Простатилен® є простати екстракт з додаванням гліцину. Ректальні супозиторії 5 мг. По 5 супозиторіїв у контурну осередкову упаковку з полімерної плівки (полівінілхлорид/поліетилен (ПВХ/ПЕ) або полівінілхлорид/полівініліденхлорид/поліетилен (ПВХ/ПВДХ/ПЕ)). Одна або дві контурні коміркові упаковки разом з інструкцією із застосування в пачку з картону.Опис лікарської формиСупозиторії торпедоподібної форми, від білого до жовтого кольору, допускається мармуровість. На зрізі допускається мармуровість, наявність повітряного стрижня або лійкоподібного заглиблення.Фармакотерапевтична групаПростатит хронічного засобу лікування.ФармакодинамікаМає органотропну дію на передміхурову залозу. Зменшує рівень набряку, лейкоцитарної інфільтрації передміхурової залози, нормалізує секреторну функцію епітеліальних клітин, збільшує число лецитинових зерен у секреті ацинусів, стимулює м'язовий тонус сечового міхура. Зменшує тромбоутворення, має антиагрегантну активність, перешкоджає розвитку тромбозу венул у передміхуровій залозі.Показання до застосуванняХронічний абактеріальний простатит, стани до та після операцій на передміхуровій залозі, доброякісна гіперплазія передміхурової залози.Протипоказання до застосуванняГіперчутливість до компонентів препарату; дитячий вік до 18 років.Побічна діяМожливі алергічні реакції (кропив'янка). У цьому випадку застосування препарату припиняють та призначають антигістамінні засоби.Взаємодія з лікарськими засобамиСумісний із антибактеріальними препаратами, що застосовуються для лікування простатиту.Спосіб застосування та дозиРектально. По одному супозиторію 50 мг 1 раз на добу (вранці або ввечері). Супозиторій глибоко вводять у задній прохід після дефекації або очисної клізми. Перед застосуванням супозиторій слід змочити водою. Після введення бажано перебування хворого на ліжку протягом 30-40 хвилин. Курс лікування – не менше 10 днів при хронічному простатиті, не менше 15 днів – при доброякісній гіперплазії передміхурової залози.ПередозуванняПрепарат не токсичний, випадків передозування немає.Запобіжні заходи та особливі вказівкиНе впливає на здатність займатися потенційно небезпечними видами діяльності, що потребують особливої уваги та швидких реакцій, наприклад, керування транспортними засобами.Умови зберіганняУ холодильнику +2+8 градусівУмови відпустки з аптекБез рецептаВідео на цю тему
212,00 грн
151,00 грн
Склад, форма випуску та упаковкаАерозоль - 1 доза: сальбутамол 100 мкг. 200 доз - балони аерозольні алюмінієві з клапаном дозуючої дії (1) - картонні пачки.Фармакотерапевтична групаБета-адреноміметик з переважним впливом на β2-адренорецептори (що локалізуються, зокрема, у бронхах, міометрії, кровоносних судинах). Попереджає та купує бронхоспазм; знижує опір у дихальних шляхах, збільшує життєву ємність легень. Запобігає виділенню гістаміну, що повільно реагує субстанції з опасистих клітин та факторів хемотаксису нейтрофілів. Порівняно з іншими препаратами цієї групи має менш виражений позитивний хроно- та інотропний вплив на міокард. Викликає розширення коронарних артерій, що практично не знижує АТ. Чинить токолітичну дію, знижуючи тонус і скорочувальну активність міометрію.ФармакокінетикаПри застосуванні аерозолю спостерігається швидке всмоктування сальбутамолу у кров; однак його концентрації у плазмі крові при застосуванні в рекомендованих дозах дуже низькі або не досягають межі виявлення. Після прийому внутрішньо сальбутамол добре всмоктується із ШКТ. Зв'язування із білками плазми становить 10%. Метаболізується при "першому проходженні" через печінку та, можливо, у стінці кишечника; основний метаболіт – неактивний сульфатний кон'югат. Сальбутамол не метаболізується в легенях, таким чином його кінцевий метаболізм та виведення після інгаляції залежить від способу застосування, який визначає співвідношення між вдихуваним та ненавмисно проковтнутим сальбутамолом. T1/2; із плазми крові становить 2-7 год. Сальбутамол швидко виводиться із сечею у вигляді метаболітів та незміненої речовини; у невеликих кількостях виводиться із калом.Клінічна фармакологіяБронхолітичний препарат – бета2-адреноміметик.Показання до застосуванняПопередження та усунення бронхоспазму при всіх формах бронхіальної астми. Оборотна обструкція дихальних шляхів при хронічному бронхіті та емфіземі легень, бронхообструктивний синдром у дітей. Погрозливі передчасні пологи із скорочувальною діяльністю матки; пологи до 37-38 тижнів вагітності; істміко-цервікальна недостатність, зменшення ЧСС плода залежно від скорочень матки у періоди розкриття шийки матки та вигнання. У профілактичних цілях при операціях на вагітній матці (накладання циркулярного шва за недостатності внутрішнього зіва матки).Протипоказання до застосуванняЗагроза викидня в I та II триместрах вагітності, передчасне відшарування плаценти, кровотеча або токсикоз у III триместрі вагітності; дитячий вік до 2 років; підвищена чутливість до сальбутамолу.Вагітність та лактаціяСальбутамол протипоказаний при загрозі викидня в I та II триместрах вагітності, передчасному відшаруванні плаценти, кровотечі або токсикозі у III триместрі вагітності. У разі необхідності застосування сальбутамолу при вагітності слід співвіднести очікувану користь лікування для матері та потенційний ризик для плода. В даний час недостатньо даних щодо безпеки застосування сальбутамолу на ранніх термінах вагітності. Сальбутамол виділяється з грудним молоком, тому за необхідності застосування в період лактації слід також оцінити очікувану користь лікування для матері та можливий ризик для дитини. Застосування у дітей Протипоказаний у дитячому віці до 2 років.Побічна діяЗ боку серцево-судинної системи: ; минуще розширення периферичних судин, помірна тахікардія. З боку ЦНС: головний біль, запаморочення, нудота, блювання. З боку обміну речовин:; гіпокаліємія. Алергічні реакції: в поодиноких випадках - ангіоневротичний набряк, алергічні реакції у вигляді шкірного висипу, кропив'янка, артеріальна гіпотензія, колапс. Інші: ;тремор кистей рук, внутрішнє тремтіння, напруженість; рідко – парадоксальний бронхоспазм, м'язові судоми.Взаємодія з лікарськими засобамиПри одночасному застосуванні сальбутамолу з некардіоселективними бета-адреноблокаторами можливе взаємне пригнічення терапевтичних ефектів; з теофіліном – підвищується ризик розвитку тахікардії та аритмії, зокрема надшлуночкової екстрасистолії. При одночасному застосуванні сальбутамолу та похідних ксантину, кортикостероїдів або діуретиків зростає ризик розвитку гіпокаліємії.Спосіб застосування та дозиВсередину як бронхорозширювальний засіб дорослим і дітям старше 12 років - по 2-4 мг 3-4 рази на добу, при необхідності доза може бути підвищена до 8 мг 4 рази на добу. Дітям віком 6-12 років – по 2 мг 3-4 рази на добу; дітям 2-6 років – 1-2 мг 3 рази на добу. При інгаляційному введенні доза залежить від лікарської форми, що застосовується, частота застосування залежить від показань та клінічної ситуації. Як токолітичний засіб вводять внутрішньовенно краплинно в дозі 1-2 мг.Запобіжні заходи та особливі вказівкиЗ обережністю застосовують при тахіаритміях та інших порушеннях серцевого ритму, артеріальної гіпертензії, міокардиті, пороках серця, аортальному стенозі, цукровому діабеті, тиреотоксикозі, глаукомі, гострій серцевій недостатності (за умови ретельного контролю лікаря). Збільшення дози або частоти прийому сальбутамолу слід проводити під контролем лікаря. Скорочення інтервалу можливе лише у виняткових випадках і має бути суворо обґрунтованим. При застосуванні сальбутамолу є ризик розвитку гіпокаліємії, тому в період лікування у пацієнтів з бронхіальною астмою тяжкого перебігу слід контролювати рівень калію в крові. Ризик гіпокаліємії зростає при гіпоксії.Умови відпустки з аптекЗа рецептомВідео на цю тему
208,00 грн
174,00 грн
Склад, форма випуску та упаковкаАерозоль - 1 доза: Активна речовина: сальбутамолу сульфат 124 мкг, що відповідає вмісту сальбутамолу 100 мкг. Допоміжні речовини: гідрофторалкан (HFA-134a) – 26.46 мг, етанол – 3.42 мг. 200 доз - балони алюмінієві (1) з дозуючим пристроєм - картонні пачки.Опис лікарської формиАерозоль для інгаляцій дозований при розпиленні на скло утворює пляму білого кольору.Фармакотерапевтична групаСальбутамол є стимулятором β2-адренорецепторів. У терапевтичних дозах він діє на β2-адренорецептори гладкої мускулатури бронхів, виявляючи виражений бронхолітичний ефект, попереджає та купує бронхоспазм, збільшує життєву ємність легень. Запобігає виділенню гістаміну, що повільно реагує субстанції з опасистих клітин та факторів хемотаксису нейтрофілів. Викликає незначний позитивний хроно- та інотропний ефект, розширює коронарні артерії практично не знижує АТ. Чинить токолітичну дію: знижує тонус і скорочувальну активність міометрію. Має ряд метаболічних ефектів: знижує вміст К+ у плазмі, впливає на глікогеноліз та виділення інсуліну, надає гіперглікемічний (особливо у пацієнтів з бронхіальною астмою) та ліполітичний ефект, збільшує ризик розвитку ацидозу. Дія препарату починається через 5 хв після інгаляційного введення та триває протягом 4-6 год.ФармакокінетикаПісля інгаляційного введення від 10 до 20% дози потрапляє у дихальні шляхи. Решта затримується в приладі або осідає в ротоглотці і потім проковтується. Частина дози, що залишається в дихальних шляхах, абсорбується тканинами легень, не піддаючись метаболізму в легенях, і потрапляє у кровотік. При попаданні в системний кровотік вона може метаболізуватися в печінці і виводиться з сечею в незмінному вигляді або у вигляді фенольного сульфату. Ступінь зв'язування сальбутамолу із білками плазми становить 10%. C maxплазмі крові – 30 нг/мл. Частина дози, що надійшла в шлунково-кишковому тракті, всмоктується і піддається інтенсивному метаболізму під час "першого проходження" через печінку, перетворюючись на фенольний сульфат. Незмінений препарат та кон'югат виводяться переважно із сечею. Більшість дози сальбутамолу, введеної внутрішньовенно, внутрішньо або інгаляційно, виводиться протягом 72 год. T1/2 - 3.7-5 год.Клінічна фармакологіяБронхолітичний препарат – бета2-адреноміметик.Показання до застосуванняПопередження та усунення бронхоспазму при бронхіальній астмі, хронічній обструктивній хворобі легень (ХОЗЛ), хронічному бронхіті, емфіземі легень.Протипоказання до застосуванняПорушення ритму (пароксизмальна тахікардія, політопна шлуночкова екстрасистолія); міокардит; вади серця; аортальний стеноз; ішемічна хвороба серця; тахіаритмія; тиреотоксикоз; декомпенсований цукровий діабет; глаукому; епілептичні напади; пилородуоденальне звуження; ниркова або печінкова недостатність; одночасний прийом неселективних бета-адреноблокаторів; вагітність; дитячий вік до 2-х років; підвищена чутливість до будь-якого компонента препарату. З обережністю – хронічна серцева недостатність, гіпертиреоз, артеріальна гіпертензія, феохромоцитома.Вагітність та лактаціяПротипоказаний при вагітності. У період лактації призначається лише тоді, коли очікувана користь для матері перевищує будь-який можливий ризик для дитини. Застосування у дітей Дітям від 2 до 12 років: при розвитку нападу бронхіальної астми, а також для запобігання нападам бронхіальної астми, пов'язаних з впливом алергену або спричиненим фізичним навантаженням, рекомендована доза становить 100-200 мкг (1 або 2 інгаляції).Побічна діяСаламол Еко може викликати тремор пальців, який є типовим побічним ефектом для всіх β2-адренорецепторів агоністів. Може відзначатися головний біль, запаморочення, підвищена збудливість, тривожність, порушення сну, безсоння, розширення периферичних судин (гіперемія шкіри обличчя), незначне компенсаторне збільшення ЧСС, підвищення артеріального тиску, поява болю в грудній клітці, артралгія. Можуть розвиватися реакції підвищеної чутливості (що включають ангіоневротичний набряк, кропив'янку, еритему, закладеність носа, бронхоспазм, артеріальну гіпотензію та колапс); м'язові судоми, нудота, блювання, диспепсія. Інгаляційні препарати можуть спричинити парадоксальний бронхоспазм. Інгаляційні препарати можуть викликати подразнення слизової оболонки ротової порожнини та глотки (фарингіт), кашель. Терапія сальбутамолом може викликати гіпокаліємію, яка може становити серйозну небезпеку для пацієнта, а також оборотні метаболічні порушення, наприклад збільшення концентрації глюкози в крові. Препарат може викликати збудження та підвищення рухової активності у дітей. Можлива поява аритмій (включаючи фібриляцію передсердь, надшлуночкову тахікардію та екстрасистолію).Взаємодія з лікарськими засобамиТеофілін та інші ксантини при одночасному застосуванні із сальбутамолом підвищують ймовірність розвитку тахіаритмій; засоби для інгаляційної анестезії, леводопа – важких шлуночкових аритмій. Не рекомендується застосовувати Саламол Еко та неселективні блокатори бета-адренорецепторів, такі як пропранолол. Інгібітори МАО та трициклічні антидепресанти посилюють дію сальбутамолу та можуть призвести до різкого зниження АТ. Сальбутамол посилює дію стимуляторів ЦНС, побічну дію гормонів щитовидної залози, серцевих глікозидів. Знижує ефективність гіпотензивних препаратів, нітратів. Гіпокаліємія може посилюватися внаслідок одночасного застосування похідних ксантину, кортикостероїдів, діуретиків. Одночасне призначення з антихолінергічними засобами (в т.ч. інгаляційними) може сприяти підвищенню внутрішньоочного тиску.Спосіб застосування та дозиДорослим та дітям старше 12 років: по 100-200 мкг (1-2 інгаляційні дози) для усунення нападів ядухи. Для контролю за перебігом астми легкого ступеня тяжкості - по 1-2 дози 1-4 рази на добу та середнього ступеня тяжкості захворювання - у тій же дозі в комбінації з іншими протиастматичними препаратами. Для профілактики астми фізичного зусилля – за 20-30 хв до навантаження 1-2 дози на прийом. Дітям від 2 до 12 років: при розвитку нападу бронхіальної астми, а також для запобігання нападам бронхіальної астми, пов'язаних з впливом алергену або спричиненим фізичним навантаженням, рекомендована доза становить 100-200 мкг (1 або 2 інгаляції). Добова доза повинна перевищувати 800 мкг (8 інгаляцій). Інструкція з використання інгалятора Перевірте роботу інгалятора перед першим використанням, а також якщо Ви не користувалися ним якийсь час. 1. Зніміть ковпачок з інгалятора. Переконайтеся, що у вихідній трубці немає пилу та бруду. 2. Тримайте балон у вертикальному положенні, поклавши великий палець на денце, а вказівний палець – на верхівку балона. 3. Інтенсивно струсіть балон вгору-вниз. 4. Зробіть якомога глибший видих (без напруги). Щільно затисніть губами вихідну трубку балончика. 5. Робіть повільний глибокий вдих. Під час вдиху натисніть вказівним пальцем на клапан балончика, випускаючи дозу ліків. Продовжуйте повільно вдихати. 6. Вийміть із рота трубку інгалятора і затримайте дихання на 10 с або стільки, на скільки зможете без напруги. Повільно видихніть. Якщо потрібно більше однієї дози ліки, зачекайте приблизно хвилину і потім повторіть дії, починаючи з кроку 2. Надягніть ковпачок на інгалятор. При виконанні кроків 3 та 4 не поспішайте. У момент випуску дози ліки важливо робити вдих якомога повільніше. Спочатку потреніруйтесь біля дзеркала. Якщо Ви помітите пару, що виходить з верхівки балончика або з кутів рота, почніть знову з кроку 2. Чищення інгалятора Інгалятор слід чистити принаймні 1 раз на тиждень. Вийміть металевий балон із пластикового футляра та сполосніть футляр та ковпачок теплою водою. Не користуйтеся гарячою водою. Ретельно висушіть, але не користуйтеся при цьому нагрівальними пристроями. Помістіть балон назад у футляр і надягніть ковпачок. Не занурюйте металевий балон у воду.ПередозуванняСимптоми: нудота, блювання, підвищена збудливість, галюцинації, тахікардія, тріпотіння шлуночків, розширення периферичних судин, зниження артеріального тиску, гіпоксія, ацидоз, гіпокаліємія, гіперглікемія, м'язовий тремор, головний біль. Лікування: відміна препарату, кардіоселективні бета-адреноблокатори; симптоматична терапія. При підозрі передозування слід контролювати рівень калію в сироватці крові.Запобіжні заходи та особливі вказівкиУ пацієнтів з тяжким або нестабільним перебігом бронхіальної астми застосування бронходилататорів не повинно бути основним або єдиним методом терапії. Якщо дія звичайної дози Саламол Еко стає менш ефективною або менш тривалою (дія препарату повинна зберігатися не менше 3 годин), пацієнту слід звернутися до лікаря. Часте застосування сальбутамолу може призвести до посилення бронхоспазму, раптової смерті, у зв'язку з чим між прийомами чергових доз препарату необхідно робити перерви на кілька годин. Підвищення потреби застосування інгаляційних агоністів β2-адренорецепторів з короткою тривалістю дії для контролю симптомів бронхіальної астми свідчить про загострення захворювання. У таких випадках слід переглянути план лікування пацієнта та вирішити питання про призначення або збільшення дози інгаляційних або системних кортикостероїдів. Терапія агоністами β2-адренорецепторів може призводити до гіпокаліємії. Особливу обережність рекомендується виявляти при лікуванні тяжких нападів бронхіальної астми, оскільки в цих випадках гіпокаліємія може посилюватися внаслідок одночасного застосування похідних ксантину, глюкокортикостероїдів, діуретиків, а також внаслідок гіпоксії. У таких ситуаціях необхідно контролювати рівень калію у сироватці крові. Балон із Саламолом Еко не можна проколювати, розбирати чи кидати у вогонь, навіть якщо він порожній. Як і більшість інших засобів для інгаляцій в аерозольних упаковках, Саламол Еко може бути менш ефективним за низьких температур. При охолодженні балона рекомендується дістати його із пластмасового корпусу та зігріти руками протягом декількох хвилин.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
220,00 грн
183,00 грн
Склад, форма випуску та упаковкаАерозоль - 1 доза: сальбутамол 100 мкг. 200 доз 12 мл – балони аерозольні алюмінієві з клапаном дозуючої дії (1) – пачки картонні.Фармакотерапевтична групаБета-адреноміметик з переважним впливом на β2-адренорецептори (що локалізуються, зокрема, у бронхах, міометрії, кровоносних судинах). Попереджає та купує бронхоспазм; знижує опір у дихальних шляхах, збільшує життєву ємність легень. Запобігає виділенню гістаміну, що повільно реагує субстанції з опасистих клітин та факторів хемотаксису нейтрофілів. Порівняно з іншими препаратами цієї групи має менш виражений позитивний хроно- та інотропний вплив на міокард. Викликає розширення коронарних артерій, що практично не знижує АТ. Чинить токолітичну дію, знижуючи тонус і скорочувальну активність міометрію.ФармакокінетикаПри застосуванні аерозолю спостерігається швидке всмоктування сальбутамолу у кров; однак його концентрації у плазмі крові при застосуванні в рекомендованих дозах дуже низькі або не досягають межі виявлення. Після прийому внутрішньо сальбутамол добре всмоктується із ШКТ. Зв'язування із білками плазми становить 10%. Метаболізується при "першому проходженні" через печінку та, можливо, у стінці кишечника; основний метаболіт – неактивний сульфатний кон'югат. Сальбутамол не метаболізується в легенях, таким чином його кінцевий метаболізм та виведення після інгаляції залежить від способу застосування, який визначає співвідношення між вдихуваним та ненавмисно проковтнутим сальбутамолом. T1/2; із плазми крові становить 2-7 год. Сальбутамол швидко виводиться із сечею у вигляді метаболітів та незміненої речовини; у невеликих кількостях виводиться із калом.Клінічна фармакологіяБронхолітичний препарат – бета2-адреноміметик.Показання до застосуванняПопередження та усунення бронхоспазму при всіх формах бронхіальної астми. Оборотна обструкція дихальних шляхів при хронічному бронхіті та емфіземі легень, бронхообструктивний синдром у дітей. Погрозливі передчасні пологи із скорочувальною діяльністю матки; пологи до 37-38 тижнів вагітності; істміко-цервікальна недостатність, зменшення ЧСС плода залежно від скорочень матки у періоди розкриття шийки матки та вигнання. У профілактичних цілях при операціях на вагітній матці (накладання циркулярного шва за недостатності внутрішнього зіва матки).Протипоказання до застосуванняЗагроза викидня в I та II триместрах вагітності, передчасне відшарування плаценти, кровотеча або токсикоз у III триместрі вагітності; дитячий вік до 2 років; підвищена чутливість до сальбутамолу.Вагітність та лактаціяСальбутамол протипоказаний при загрозі викидня в I та II триместрах вагітності, передчасному відшаруванні плаценти, кровотечі або токсикозі у III триместрі вагітності. У разі необхідності застосування сальбутамолу при вагітності слід співвіднести очікувану користь лікування для матері та потенційний ризик для плода. В даний час недостатньо даних щодо безпеки застосування сальбутамолу на ранніх термінах вагітності. Сальбутамол виділяється з грудним молоком, тому за необхідності застосування в період лактації слід також оцінити очікувану користь лікування для матері та можливий ризик для дитини. Застосування у дітей Протипоказаний у дитячому віці до 2 років.Побічна діяЗ боку серцево-судинної системи: ; минуще розширення периферичних судин, помірна тахікардія. З боку ЦНС: головний біль, запаморочення, нудота, блювання. З боку обміну речовин:; гіпокаліємія. Алергічні реакції: в поодиноких випадках - ангіоневротичний набряк, алергічні реакції у вигляді шкірного висипу, кропив'янка, артеріальна гіпотензія, колапс. Інші: ;тремор кистей рук, внутрішнє тремтіння, напруженість; рідко – парадоксальний бронхоспазм, м'язові судоми.Взаємодія з лікарськими засобамиПри одночасному застосуванні сальбутамолу з некардіоселективними бета-адреноблокаторами можливе взаємне пригнічення терапевтичних ефектів; з теофіліном – підвищується ризик розвитку тахікардії та аритмії, зокрема надшлуночкової екстрасистолії. При одночасному застосуванні сальбутамолу та похідних ксантину, кортикостероїдів або діуретиків зростає ризик розвитку гіпокаліємії.Спосіб застосування та дозиВсередину як бронхорозширювальний засіб дорослим і дітям старше 12 років - по 2-4 мг 3-4 рази на добу, при необхідності доза може бути підвищена до 8 мг 4 рази на добу. Дітям віком 6-12 років – по 2 мг 3-4 рази на добу; дітям 2-6 років – 1-2 мг 3 рази на добу. При інгаляційному введенні доза залежить від лікарської форми, що застосовується, частота застосування залежить від показань та клінічної ситуації. Як токолітичний засіб вводять внутрішньовенно краплинно в дозі 1-2 мг.Запобіжні заходи та особливі вказівкиЗ обережністю застосовують при тахіаритміях та інших порушеннях серцевого ритму, артеріальної гіпертензії, міокардиті, пороках серця, аортальному стенозі, цукровому діабеті, тиреотоксикозі, глаукомі, гострій серцевій недостатності (за умови ретельного контролю лікаря). Збільшення дози або частоти прийому сальбутамолу слід проводити під контролем лікаря. Скорочення інтервалу можливе лише у виняткових випадках і має бути суворо обґрунтованим. При застосуванні сальбутамолу є ризик розвитку гіпокаліємії, тому в період лікування у пацієнтів з бронхіальною астмою тяжкого перебігу слід контролювати рівень калію в крові. Ризик гіпокаліємії зростає при гіпоксії.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
222,00 грн
185,00 грн
Склад, форма випуску та упаковкаАерозоль - 1 доза: сальбутамол 100 мкг. 200 доз - балони аерозольні алюмінієві з клапаном дозуючої дії (1) - картонні пачки.Фармакотерапевтична групаБета-адреноміметик з переважним впливом на β2-адренорецептори (що локалізуються, зокрема, у бронхах, міометрії, кровоносних судинах). Попереджає та купує бронхоспазм; знижує опір у дихальних шляхах, збільшує життєву ємність легень. Запобігає виділенню гістаміну, що повільно реагує субстанції з опасистих клітин та факторів хемотаксису нейтрофілів. Порівняно з іншими препаратами цієї групи має менш виражений позитивний хроно- та інотропний вплив на міокард. Викликає розширення коронарних артерій, що практично не знижує АТ. Чинить токолітичну дію, знижуючи тонус і скорочувальну активність міометрію.ФармакокінетикаПри застосуванні аерозолю спостерігається швидке всмоктування сальбутамолу у кров; однак його концентрації у плазмі крові при застосуванні в рекомендованих дозах дуже низькі або не досягають межі виявлення. Після прийому внутрішньо сальбутамол добре всмоктується із ШКТ. Зв'язування із білками плазми становить 10%. Метаболізується при "першому проходженні" через печінку та, можливо, у стінці кишечника; основний метаболіт – неактивний сульфатний кон'югат. Сальбутамол не метаболізується в легенях, таким чином його кінцевий метаболізм та виведення після інгаляції залежить від способу застосування, який визначає співвідношення між вдихуваним та ненавмисно проковтнутим сальбутамолом. T1/2; із плазми крові становить 2-7 год. Сальбутамол швидко виводиться із сечею у вигляді метаболітів та незміненої речовини; у невеликих кількостях виводиться із калом.Клінічна фармакологіяБронхолітичний препарат – бета2-адреноміметик.Показання до застосуванняПопередження та усунення бронхоспазму при всіх формах бронхіальної астми. Оборотна обструкція дихальних шляхів при хронічному бронхіті та емфіземі легень, бронхообструктивний синдром у дітей. Погрозливі передчасні пологи із скорочувальною діяльністю матки; пологи до 37-38 тижнів вагітності; істміко-цервікальна недостатність, зменшення ЧСС плода залежно від скорочень матки у періоди розкриття шийки матки та вигнання. У профілактичних цілях при операціях на вагітній матці (накладання циркулярного шва за недостатності внутрішнього зіва матки).Протипоказання до застосуванняЗагроза викидня в I та II триместрах вагітності, передчасне відшарування плаценти, кровотеча або токсикоз у III триместрі вагітності; дитячий вік до 2 років; підвищена чутливість до сальбутамолу.Вагітність та лактаціяСальбутамол протипоказаний при загрозі викидня в I та II триместрах вагітності, передчасному відшаруванні плаценти, кровотечі або токсикозі у III триместрі вагітності. У разі необхідності застосування сальбутамолу при вагітності слід співвіднести очікувану користь лікування для матері та потенційний ризик для плода. В даний час недостатньо даних щодо безпеки застосування сальбутамолу на ранніх термінах вагітності. Сальбутамол виділяється з грудним молоком, тому за необхідності застосування в період лактації слід також оцінити очікувану користь лікування для матері та можливий ризик для дитини. Застосування у дітей Протипоказаний у дитячому віці до 2 років.Побічна діяЗ боку серцево-судинної системи: ; минуще розширення периферичних судин, помірна тахікардія. З боку ЦНС: головний біль, запаморочення, нудота, блювання. З боку обміну речовин:; гіпокаліємія. Алергічні реакції: в поодиноких випадках - ангіоневротичний набряк, алергічні реакції у вигляді шкірного висипу, кропив'янка, артеріальна гіпотензія, колапс. Інші: ;тремор кистей рук, внутрішнє тремтіння, напруженість; рідко – парадоксальний бронхоспазм, м'язові судоми.Взаємодія з лікарськими засобамиПри одночасному застосуванні сальбутамолу з некардіоселективними бета-адреноблокаторами можливе взаємне пригнічення терапевтичних ефектів; з теофіліном – підвищується ризик розвитку тахікардії та аритмії, зокрема надшлуночкової екстрасистолії. При одночасному застосуванні сальбутамолу та похідних ксантину, кортикостероїдів або діуретиків зростає ризик розвитку гіпокаліємії.Спосіб застосування та дозиВсередину як бронхорозширювальний засіб дорослим і дітям старше 12 років - по 2-4 мг 3-4 рази на добу, при необхідності доза може бути підвищена до 8 мг 4 рази на добу. Дітям віком 6-12 років – по 2 мг 3-4 рази на добу; дітям 2-6 років – 1-2 мг 3 рази на добу. При інгаляційному введенні доза залежить від лікарської форми, що застосовується, частота застосування залежить від показань та клінічної ситуації. Як токолітичний засіб вводять внутрішньовенно краплинно в дозі 1-2 мг.Запобіжні заходи та особливі вказівкиЗ обережністю застосовують при тахіаритміях та інших порушеннях серцевого ритму, артеріальної гіпертензії, міокардиті, пороках серця, аортальному стенозі, цукровому діабеті, тиреотоксикозі, глаукомі, гострій серцевій недостатності (за умови ретельного контролю лікаря). Збільшення дози або частоти прийому сальбутамолу слід проводити під контролем лікаря. Скорочення інтервалу можливе лише у виняткових випадках і має бути суворо обґрунтованим. При застосуванні сальбутамолу є ризик розвитку гіпокаліємії, тому в період лікування у пацієнтів з бронхіальною астмою тяжкого перебігу слід контролювати рівень калію в крові. Ризик гіпокаліємії зростає при гіпоксії.Умови відпустки з аптекЗа рецептомВідео на цю тему
Фасування: N1 Форма випуску: крем-скраб Упаковка: банку Виробник: Фарм-МІК Завод-виробник: Фарм-МІК(Росія). . .
Форма випуску: крем-скраб Упаковка: банку Виробник: Фарм-МІК Завод-виробник: Фарм-МІК(Росія). . .
477,00 грн
213,00 грн
Склад, форма випуску та упаковкаАерозоль - 1 доза: Активні речовини: салметеролу ксинафоат 36.3 мкг, що відповідає вмісту салметеролу 25 мкг, флутиказону пропіонат 125 мкг. Допоміжні речовини: 1,1,1,2-тетрафторетан (HFA-134a) – 73.024 мг, поліетиленгліколь 1000 – 0.01464 мг. 120 доз - балончики аерозольні алюмінієві (1) з клапаном дозуючої дії та мундштуком - пачки картонні.Опис лікарської формиАерозоль для інгаляцій дозований у вигляді суспензії білого або майже білого кольору.Фармакотерапевтична групаСальмекорт - комбінований бронходилатируючий засіб (містить салмотерол та флутиказону пропіонат). Салметерол; - селективний агоніст β2-адренорецепторів тривалої дії (не менше 12 год). Молекула салметерола має довгий бічний ланцюг, який зв'язується із зовнішнім доменом рецептора. Завдяки цим фармакологічним властивостям салметерол ефективніший для попередження гістамін-індукованого бронхоспазму і викликає більш тривалу бронходилатацію порівняно зі звичайними агоністами β2-рецепторів короткої дії. Ефективно та довго інгібує вивільнення в тканинах легких медіаторів опасистих клітин, таких як гістамін, лейкотрієни та PgD2. Пригнічує ранню та пізню стадію алергічної реакції; після введення одноразової дози зменшується гіперреактивність бронхів, інгібування пізньої стадії зберігається протягом більше 30 годин після прийому одноразової дози, коли бронходилатируючий ефект вже відсутній. Флутиказона пропіонат; - глюкокортикостероїд місцевого дії. При інгаляційному введенні в рекомендованих дозах має виражену протизапальну та протиалергічну дію, що призводить до зменшення вираженості симптомів та зниження частоти загострень захворювань, що супроводжуються обструкцією дихальних шляхів. При тривалому застосуванні інгаляційного флутиказону пропіонату в максимальних дозах добова та резервна секреція гормонів кори надниркових залоз залишається в межах норми у дорослих та дітей. Залишкове зниження резервної функції надниркових залоз може зберігатися протягом тривалого часу після терапії.ФармакокінетикаНемає даних, що свідчать, що спільне інгаляційне введення салметеролу та флутиказону пропіонату впливає на фармакокінетику кожної з цих речовин. Салметерол Після інгаляційного введення в терапевтичних дозах утворюються дуже низькі концентрації препарату в плазмі (200 пг/мл і менше). При регулярному застосуванні інгаляційного салметеролу у системному кровотоку визначається гідроксинафтоєва кислота в концентраціях до 100 нг/мл. Флутиказону пропіонат Після інгаляційного введення відносна біодоступність становить від 10 до 30% залежно від системи доставки препарату. Системна абсорбція відбувається переважно у легенях. Частина дози, що вдихається, може проковтуватися, але її системна дія мінімальна внаслідок слабкої розчинності препарату у воді та інтенсивного метаболізму при "першому проходженні" через печінку. Біодоступність флутиказону при ковтанні становить менше 1%. Існує пряма залежність між величиною вдихається дози і системним ефектом флутиказону, Vd становить близько 300 л. Метаболізується у печінці до неактивного метаболіту за участю CYP3A4 системи цитохрому Р450. Менш 5% метаболіту виводиться із сечею. Плазмовий кліренс дорівнює 1.15 л/хв. T1/2; близько 8 год.Клінічна фармакологіяПрепарат із протизапальною та бронхолітичною дією.Показання до застосуванняПрепарат Сальмекорт призначений для регулярного лікування бронхіальної астми у пацієнтів, яким показана комбінована терапія бета 2 -адреноміметиком тривалої дії та глюкокортикостероїдами для інгаляційного застосування: у пацієнтів з недостатнім контролем захворювання на фоні постійної монотерапії кортикостероїдів для інгаляційного застосування при періодичному використанні бета 2 -адреноміметика короткої дії; у пацієнтів з адекватним контролем захворювання на фоні терапії кортикостероїдами для інгаляційного застосування та бета 2 -адреноміметиком тривалої дії; як стартова підтримуюча терапія у пацієнтів з персистуючою бронхіальною астмою (щоденне виникнення симптомів, щоденне використання засобів для швидкого усунення симптомів) за наявності показань до призначення кортикостероїдів для досягнення контролю над захворюванням; підтримуюча терапія у пацієнтів з ХОЗЛ, у яких значення обсягу форсованого видиху (ОФВ1) <60% від належних величин (до інгаляції бронходилататора) з повторними загостреннями в анамнезі, і у яких виражені симптоми захворювання зберігаються, незважаючи на регулярну терапію бронходилататорами.Протипоказання до застосуванняГіперчутливість до одного або кількох компонентів препарату; дитячий вік (до 4 років). З обережністю Як і всі інші інгаляційні препарати, що містять кортикостероїди, препарат Сальмекорт слід застосовувати з обережністю у пацієнтів з гострим або латентним туберкульозом легень, грибковими, вірусними або бактеріальними інфекціями органів дихання, при тиреотоксикозі. При прийомі будь-яких препаратів групи симпатоміметиків, особливо при перевищенні терапевтичних доз, можливий розвиток серцево-судинних явищ, як збільшення систолічного АТ і ЧСС. З цієї причини Сальмекорт слід з обережністю призначати пацієнтам, які страждають на серцево-судинні захворювання, в т.ч. з аритміями, такими як суправентикулярна тахікардія та екстрасистолія, шлуночкова екстрасистолія, фібриляція передсердь. Усі симпатоміметичні препарати у дозах, що перевищують терапевтичні, можуть спричинити транзиторне зниження рівня калію у сироватці крові, тому препарат Сальмекорт слід з обережністю призначати пацієнтам із гіпокаліємією. Будь-який інгаляційний кортикостероїд може викликати системні ефекти, особливо при тривалому використанні у високих дозах, тому препарат слід застосовувати з обережністю при глаукомі, катаракті, остеопорозі (див. розділ "Особливі вказівки та запобіжні заходи при застосуванні"). Є дуже рідкісні повідомлення про підвищення рівня глюкози в крові, тому пацієнтам із цукровим діабетом слід застосовувати препарат Сальмекорт з обережністю (див. розділ "Побічна дія").Вагітність та лактаціяВагітним жінкам та жінкам у період лактації слід призначати препарат лише в тому випадку, якщо очікувана користь для матері перевищує будь-який можливий ризик для плода чи дитини. Недостатньо даних про застосування салметеролу та флутиказону пропіонату при вагітності та в період лактації. Вагітність Надмірна системна концентрація активного бета2-адреноміметика та кортикостероїдів впливає на плід. Великий клінічний досвід застосування препаратів даного класу свідчить, що при використанні терапевтичних доз ці ефекти не є клінічно значущими. Салметерол і флутиказону пропіонат не мають генотоксичності. Період лактації Концентрація салметеролу та флутиказону пропіонату в плазмі крові після вдихання препарату в терапевтичних дозах вкрай низька, тому їх концентрація у грудному молоці має бути такою ж низькою. Немає даних про концентрацію салметеролу та флутиказону пропіонату у грудному молоці жінок у період лактації. Застосування у дітей Застосування препарату дітям до 4 років протипоказане.Побічна діяУсі небажані реакції, представлені нижче, характерні для діючих речовин - салметеролу та флутиказону пропіонату окремо. Профіль безпеки препарату Сальмекорт не відрізняється від профілю небажаних реакцій діючих речовин. Небажані реакції, представлені нижче, перераховані відповідно до ураження органів і систем органів і частотою народження. Частота народження визначається таким чином: дуже часто (≥1/10), часто (≥1/100 та <1/10), нечасто (≥1/1000 та <1/100), рідко (≥1/10 000 та < 1/1000), дуже рідко (<1/10000, включаючи окремі випадки). Інфекції та інвазії: часто - кандидоз ротової порожнини та глотки, пневмонія (у пацієнтів з ХОЗЛ). З боку імунної системи: ; нечасто - шкірні реакції гіперчутливості; рідко – анафілактичні реакції, ангіоневротичний набряк (головним чином, набряк обличчя та ротоглотки), бронхоспазм. З боку ендокринної системи: ; можливі системні ефекти включають (див. розділи "З обережністю" та "Особливі вказівки"); рідко – синдром Кушинга, кушінгоїдні симптоми, пригнічення функції надниркових залоз, затримка росту у дітей та підлітків, зниження мінеральної щільності кісткової тканини. З боку органів зору: нечасто - катаракта; рідко – глаукома. З боку обміну речовин та харчування: ; нечасто - гіперглікемія; дуже рідко – гіпокаліємія. Порушення психіки: ; нечасто - тривожність, порушення сну; рідко – зміни у поведінці, в т.ч. підвищена активність та дратівливість (особливо у дітей). З боку нервової системи: дуже часто - головний біль (див. розділ "Особливі вказівки"); нечасто – тремор (див. розділ "Особливі вказівки"). З боку серцево-судинної системи: ;нечасто - прискорене серцебиття (див. розділ "З обережністю" та "Особливі вказівки"), тахікардія, фібриляція передсердь; рідко – аритмія, включаючи шлуночкову екстрасистолію, надшлуночкову тахікардію, екстрасистолію. З боку дихальної системи: ; часто - захриплість голосу та/або дисфонія; нечасто – подразнення глотки; рідко – парадоксальний бронхоспазм (див. розділ "Особливі вказівки"). З боку шкіри та підшкірних тканин: ;нечасто - синці. З боку кістково-м'язової системи: часто - м'язові спазми, артралгія. З боку травної системи: дуже рідко - диспепсія, нудота. Діти та підлітки Теоретично можливий розвиток системних реакцій, що включають синдром Кушинга, кушінгоїдні симптоми, пригнічення функції надниркових залоз, затримку росту у дітей та підлітків. Дуже рідко можуть виникати тривога, порушення сну та поведінкові розлади, включаючи гіперактивність та дратівливість.Взаємодія з лікарськими засобамиЧерез небезпеку розвитку бронхоспазму слід уникати застосування селективних та неселективних бета-адреноблокаторів за винятком тих випадків, коли вони вкрай необхідні пацієнтові. Салметерол Поєднане застосування з кетоконазолом слід уникати, якщо користь від застосування не перевищує потенційного ризику виникнення системних побічних реакцій при лікуванні салметеролом. Існує схожий ризик взаємодії з іншими сильними інгібіторами CYP3A4 (ітраконазол, телітроміцин, ритонавір). Флутиказону пропіонат У звичайних ситуаціях інгаляції флутиказону пропіонату супроводжуються низькими концентраціями його в плазмі внаслідок інтенсивного метаболізму при "першому проходженні" та високого системного кліренсу під впливом ізоферменту CYP3A4 системи цитохрому Р450 у кишечнику та печінці. Завдяки цьому клінічно значущі взаємодії за участю флутиказону пропіонату малоймовірні. Ритонавір, як високоактивний інгібітор ферменту CYP3A4, може викликати різке підвищення концентрації флутиказону пропіонату в плазмі, внаслідок чого суттєво знижуються концентрації сироваткового кортизолу. Спільне застосування з рітановіром викликає такі побічні ефекти, як синдром Кушинга та пригнічення функції надниркових залоз. Враховуючи сказане, слід уникати одночасного застосування флутиказону пропіонату та рітановіру, крім тих випадків, коли потенційна користь для пацієнта перевищує ризик системних побічних ефектів кортикостероїдів. Інші інгібітори ізоферменту CYP3A4 викликають мізерне (еритроміцин) та незначне (кетоконазол) підвищення вмісту флутиказону пропіонату в плазмі, при якому практично не знижуються концентрації сироваткового кортизолу. Незважаючи на це, рекомендується бути обережним при одночасному застосуванні сильних інгібіторів CYP3A4 (наприклад, кетоконазолу), оскільки при таких комбінаціях не виключається підвищення концентрації флутиказону пропіонату в плазмі. Похідні ксантину, кортикостероїдів та діуретики підвищують ризик розвитку гіпокаліємії (особливо у пацієнтів із загостренням бронхіальної астми, при гіпоксії). Інгібітори МАО та трициклічні антидепресанти збільшують ризик розвитку побічних ефектів із боку серцево-судинної системи. Сумісний з кромогліцієвою кислотою.Спосіб застосування та дозиІнгаляційно. Тільки для інгаляційного застосування. Пацієнт повинен бути поінформований про те, що для отримання оптимального ефекту препарат слід застосовувати регулярно, навіть за відсутності клінічних симптомів бронхіальної астми та ХОЗЛ. Лікар повинен регулярно оцінювати ефективність лікування пацієнта. Визначення тривалості курсу терапії та зміна дози препарату можливе лише за рекомендацією лікаря. Початкову дозу препарату визначають на підставі дози флутиказону, яка рекомендується для лікування цього ступеня тяжкості. Потім початкову дозу слід поступово знижувати до найменшої ефективної дози. Під час лікування пацієнту слід регулярно спостерігатися у лікаря з метою вибору оптимальної дози. Пацієнту не слід самостійно змінювати дози, призначені лікарем. Бронхіальна астма Якщо прийом препарату Сальмекорт 2 рази на добу забезпечує контроль симптомів, в рамках зниження дози до мінімально ефективної можливе зниження частоти прийому препарату до 1 разу на добу. Пацієнту слід призначати таку форму препарату Сальмекорт, яка містить дозу флутиказону пропіонату, що відповідає тяжкості захворювання. Якщо терапія інгаляційними глюкокортикостероїдами не забезпечує адекватний контроль захворювання, то їх заміна на препарат Сальмекорт у дозі, терапевтично еквівалентній дозі ГКС, що вводяться, може поліпшити контроль течії астми. У пацієнтів, у яких можна контролювати перебіг астми виключно за допомогою інгаляційних кортикостероїдів, їх заміна на препарат Сальмекорт може дозволити знизити дозу кортикостероїдів, необхідну для контролю перебігу астми. Рекомендовані дози Дорослі та діти віком від 12 років та старші: 2 інгаляції (25 мкг салметеролу та 50 мкг флутиказону пропіонату) 2 рази/добу, або 2 інгаляції (25 мкг салметеролу та 125 мкг флутиказону пропіонату) 2 рази/добу, або 2 інгаляції (25 мкг салметеролу та 250 мкг флутиказону проніонату) 2 рази на добу. Діти у віці 4 років та старші: 2 інгаляції (25 мкг салметеролу та 50 мкг флутиказону пропіонату) 2 рази на добу. Усі пацієнти, які приймають препарат як підтримуючу терапію, повинні пройти консультацію лікаря через 6-12 тижнів після первісного прийому. Хронічна обструктивна хвороба легень Для дорослих пацієнтів максимальна рекомендована доза становить 2 інгаляції (25 мкг салметеролу та 250 мкг флутиказону пропіонату) 2 рази на добу. Особливі групи пацієнтів Немає необхідності знижувати дозу препарату Сальмекорт у пацієнтів похилого віку, а також у пацієнтів з порушенням функції нирок або печінки. Інструкція з використання інгалятора Перед кожним застосуванням інгалятор слід струшувати. Перевірка інгалятора 1. Перед першим застосуванням або якщо інгалятор не використовувався 2 дні або більше, необхідно провести перевірку інгалятора. Для цього проводять 4 натискання (інгаляції) у повітря. Використання інгалятора 2. Зняти кришку з мундштука. При цьому мундштук повинен залишатись щільно прикріпленим до флакона (інгалятора); якщо інгалятор зберігався без кришки, необхідно перевірити мундштук на предмет забруднення. 3. Взяти інгалятор у руки мундштуком вниз так, щоб один палець знаходився на дні інгалятора, а інший палець або два на верхньому кінці інгалятора. Зробити видих і помістити мундштук між зубами. 4. Щільно обхопити мундштук губами і трохи нахилити голову назад. Повільно розпочати вдих і одночасно натиснути на дно балончика. Продовжити вдих до кінця. 5. Витягти інгалятор із ротової порожнини та затримати дихання на 10 сек або настільки, наскільки це комфортно. Повільно видихнути. Примітка: Після кожної інгаляції необхідно прополоскати рот та/або горло водою. Це допоможе знизити сухість, пов'язану із прийомом препарату. Перерва між інгаляціями повинна становити не менше 1 хв. При повторній інгаляції повторити кроки 2-5. Після використання необхідно закрити мундштук захисною кришкою. Перші кілька інгаляцій рекомендується проводити, контролюючи себе перед дзеркалом. Якщо Ви бачите, що відбувається "відплив" препарату через рот або з отвору між мундштуком та тілом інгалятора, це свідчить про неправильну техніку інгаляції. Інгаляції маленьким дітям мають проводитись під наглядом дорослого. Діти старшого віку та дорослі зі слабкими руками повинні тримати інгалятор двома руками. При цьому обидва вказівні пальці повинні розташовуватися на верхній частині інгалятора, а обидва великі пальці - на підставі нижче за мундштук. Очищення інгалятора Очищення інгалятора має проводитися мінімум 1 раз на добу. 1. Вийміть металевий балончик із препаратом із тіла інгалятора. Зніміть наконечник, що розпиляє. 2. Промийте мундштук та інгалятор під теплою проточною водою. 3. Ретельно протріть сухою тканиною або ватним тампоном. Слід уникати перегріву. 4. Зберіть інгалятор. Після використання всіх доз на упаковці металевий балончик слід викинути.ПередозуванняНе рекомендується призначення препарату у дозах, що перевищують зазначені у розділі "Спосіб застосування та дози". Дуже важливо регулярно переглядати режим дозування пацієнта та знижувати дозу до найнижчої з рекомендованих доз, що забезпечує ефективний контроль захворювання ("Спосіб застосування та дози"). Симптоми Очікувані симптоми та ознаки передозування салметеролу типові для надмірної бета2-адренергічної стимуляції, і включають тремор, головний біль, тахікардію, підвищення систолічного артеріального тиску та гіпокаліємію. Гостре передозування флутиказону пропіонату при інгаляційному введенні може спровокувати тимчасове пригнічення гіпоталамо-гіпофізарно-надниркової системи. Зазвичай це вимагає прийняття якихось екстрених заходів, оскільки нормальна функція надниркових залоз відновлюється протягом кількох днів. При прийомі препарату в дозах вище рекомендованих протягом тривалого періоду часу можливе значне пригнічення функції кори надниркових залоз. Описані рідкісні випадки гострого адреналового кризу, які виникали переважно у дітей, які отримували дози вище рекомендованих протягом тривалого часу (кілька місяців або років). Гострий адреналіновий криз проявляється гіпоглікемією, що супроводжується сплутаністю свідомості та/або судомами. До ситуацій, які можуть бути пусковими факторами гострого адреналового кризу, відносяться травма, хірургічне втручання, інфекція або будь-яке швидке зниження дози флутиказону пропіонату, що вдихається, до складу препарату Сальмекорт. Лікування Відсутнє специфічне лікування передозування салметеролу та флутиказону пропіонату. У разі передозування слід проводити підтримуючу терапію та спостерігати за станом пацієнта. При застосуванні препарату в дозах, що перевищують вказані в інструкції протягом тривалого часу, може спостерігатись пригнічення функції кори надниркових залоз.Запобіжні заходи та особливі вказівкиПрепарат Сальмекорт не призначений для полегшення гострих симптомів, оскільки в таких випадках слід застосовувати швидко та короткодіючий інгаляційний бронходилататор (наприклад, сальбутамол). Пацієнтів необхідно поінформувати про те, щоб вони завжди мали під рукою препарат для усунення гострих симптомів. Комбінація салметеролу і флутиказону пропіонату може використовуватися для початкової підтримуючої терапії у пацієнтів з персистуючою бронхіальною астмою (щоденне виникнення симптомів або щоденне використання засобів для усунення нападів) за наявності показань до призначення кортикостероїдів та приблизної їх дози. Частіше застосування бронходилататорів короткої дії для полегшення симптомів свідчить про погіршення контролю над захворюванням, у таких ситуаціях пацієнт повинен звертатися до лікаря. Раптове погіршення контролю бронхіальної астми, що посилюється, становить потенційну загрозу життю, у таких ситуаціях пацієнт також повинен звертатися до лікаря. Лікар повинен розглянути можливість більш високої дози кортикостероїдів. Якщо доза препарату Сальмекорт не забезпечує адекватний контроль над захворюванням, пацієнт також повинен звернутися до лікаря. Пацієнтам з астмою не можна різко припиняти лікування препаратом Сальмекорт через небезпеку розвитку загострення, дозу препарату слід поступово знижувати під контролем лікаря. У пацієнтів з ХОЗЛ відміна препарату може супроводжуватися симптомами декомпенсації та потребує спостереження лікаря. У пацієнтів з ХОЗЛ, які отримують препарат Сальмекорт, можливе збільшення частоти пневмонії (див. розділ "Побічна дія"). Лікарям слід пам'ятати про можливість розвитку пневмонії у пацієнтів з ХОЗЛ, оскільки клінічна картина загострення ХОЗЛ та пневмонії часто схожі. Будь-який інгаляційний кортикостероїд може викликати системні реакції, особливо при тривалому використанні у високих дозах; однак ймовірність виникнення таких симптомів набагато нижча, ніж при лікуванні пероральними глюкокортикостероїдами (див. розділ "Передозування"). та глаукому. Тому при лікуванні астми важливо знижувати дозу до найнижчої, що забезпечує ефективний контроль над захворюванням. В екстрених та планових ситуаціях, здатних викликати стрес, завжди необхідно пам'ятати про можливість пригнічення функції надниркових залоз і бути готовим до застосування кортикостероїдів (див. розділ "Передозування"). При проведенні реанімаційних заходів чи хірургічних втручань потрібно визначення ступеня надниркової недостатності. Рекомендується регулярно вимірювати зростання дітей, які отримують тривалу терапію інгаляційними глюкокортикостероїдами. Зважаючи на можливість пригнічення функції надниркових залоз, пацієнтів, переведених з пероральних кортикостероїдів на інгаляційну терапію флутиказону пропіонатом, слід лікувати з особливою обережністю та регулярно контролювати функцію кори надниркових залоз. При переведенні пацієнтів з прийому системних кортикостероїдів на інгаляційну терапію можуть виявлятися алергічні реакції (наприклад, алергічний риніт, екзема), які раніше пригнічувалися системними кортикостероїдами. У таких ситуаціях рекомендується проводити симптоматичне лікування антигістамінними препаратами та/або препаратами місцевої дії, в т.ч. ГКС для місцевого застосування. Після початку лікування інгаляційним флутиказоном пропіонатом системні глюкокортикоїди слід скасовувати поступово, такі пацієнти повинні мати при собі спеціальну картку пацієнта, що містить вказівку про можливу потребу в додатковому введенні глюкокортикостероїдів у стресових ситуаціях. У пацієнтів із загостренням бронхіальної астми, гіпоксією необхідно контролювати концентрацію іонів калію у плазмі. Є дуже рідкісні повідомлення підвищення концентрації глюкози у крові. Про це слід пам'ятати при призначенні комбінації салметеролу з флутиказону пропіонатом пацієнтам із цукровим діабетом (див. розділ "Побічна дія"). Через можливість виникнення системних ефектів кортикостероїдів, включаючи синдром Кушинга та пригнічення функції надниркових залоз, слід уникати спільного застосування флутиказону пропіонату та ритонавіру, за винятком випадків, коли потенційна користь для пацієнта перевищує ризик, пов'язаний із системними ефектами кортикостероїдів (див. розділ "Взаємодія з іншими лікарськими засобами"). При прийомі салметеролу ризик серйозних небажаних реакцій з боку дихальної системи або летального результату у пацієнтів афроамериканського походження, ймовірно, є вищим, ніж у інших пацієнтів. Значення фармакогенетичних факторів чи інших причин невідоме. Вплив супутнього застосування інгаляційних кортикостероїдів на ризик виникнення летальних наслідків у пацієнтів з астмою не вивчався. Як і інші інгаляційні препарати, Сальмекорт може викликати парадоксальний бронхоспазм, що проявляється наростанням задишки безпосередньо після застосування. У цьому випадку слід негайно застосувати швидко- та короткодіючий інгаляційний бронходилататор, скасувати Сальмекорт та розпочати, при необхідності, альтернативну терапію (див. розділ "Побічна дія"). Можливе виникнення побічних реакцій, пов'язаних із фармакологічною дією бета2-антагоністів, таких як тремор, відчуття серцебиття та головний біль. Однак дані реакції носять короткочасний характер, і їхня вираженість зменшується при регулярній терапії (див. розділ "Побічна дія"). Вплив на здатність до керування автотранспортом та управління механізмами У клінічних дослідженнях не отримано даних щодо впливу препарату на здатність керувати транспортними засобами та іншими механізмами, проте слід враховувати побічні дії, які може спричинити препарат.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаСупозиторії – 1 супп.: Активна речовина: екстракт простати 50 мг. допоміжні речовини: диметилсульфоксид, макрогол. * субстанція Простатилен®; являє собою екстракт простати з додаванням гліцину. 5 штук. - упаковки осередкові контурні (2) - пачки картонні.Опис лікарської формиСупозиторії ректальні торпедоподібної форми, від білого до жовтого кольору, допускається мармуровість; на зрізі допускається мармуровість, наявність повітряного стрижня або торпедоподібного заглиблення.Фармакотерапевтична групаПрепарат тваринного походження, що застосовується при захворюваннях передміхурової залози.ФармакокінетикаДані про фармакокінетику препарату не надано.ФармакодинамікаПрепарат тваринного походження. Має органотропну дію на передміхурову залозу. Зменшує рівень набряку, лейкоцитарної інфільтрації передміхурової залози, нормалізує секреторну функцію епітеліальних клітин, збільшує число лецитинових зерен у секреті ацинусів, стимулює м'язовий тонус сечового міхура. Зменшує тромбоутворення, має антиагрегантну активність, перешкоджає розвитку тромбозу венул у передміхуровій залозі.Показання до застосуванняхронічний абактеріальний простатит; стани до та після оперативних втручань на передміхуровій залозі; доброякісна гіперплазія передміхурової залози.Протипоказання до застосуваннядитячий та підлітковий вік до 18 років; - підвищена чутливість до компонентів препарату.Вагітність та лактаціяЖінкам препарат не призначається. Протипоказане призначення дітям віком до 18 років.Побічна діяАлергічні реакції: кропив'янка. У разі алергічних реакцій слід припинити лікування, призначити антигістамінні препарати.Взаємодія з лікарськими засобамиСумісний із антибактеріальними препаратами, що застосовуються для лікування простатиту.Спосіб застосування та дозиСупозиторії ректально вводять по 1 шт. (50 мг) 1 раз на добу (вранці або ввечері). Супозиторій глибоко вводять у задній прохід після дефекації або очисної клізми. Перед застосуванням супозиторій слід змочити водою. Після введення бажано перебування хворого на ліжку протягом 30-40 хвилин. Курс лікування – не менше 10 днів при хронічному простатиті, не менше 15 днів – при доброякісній гіперплазії передміхурової залози.ПередозуванняПрепарат Простатилен не токсичний, передозування не спостерігалося.Запобіжні заходи та особливі вказівкиОсобливостей дії при першому введенні та при його відміні препарат не має. Застосування препарату при хронічних захворюваннях особливостей немає.Умови відпустки з аптекБез рецептаВідео на цю тему
670,00 грн
268,00 грн
Склад, форма випуску та упаковкаАерозоль - 1 доза: Активні речовини: салметеролу ксинафоат 36.3 мкг, що відповідає вмісту салметеролу 25 мкг, флутиказону пропіонат 250 мкг; Допоміжні речовини: 1,1,1,2-тетрафторетан (HFA-134a) – 73.024 мг, поліетиленгліколь 1000 – 0.01464 мг. 120 доз - балончики аерозольні алюмінієві (1) з клапаном дозуючої дії та мундштуком - пачки картонні.Опис лікарської формиАерозоль для інгаляцій дозований у вигляді суспензії білого або майже білого кольору.Фармакотерапевтична групаСальмекорт - комбінований бронходилатируючий засіб (містить салмотерол та флутиказону пропіонат). Салметерол; - селективний агоніст β2-адренорецепторів тривалої дії (не менше 12 год). Молекула салметерола має довгий бічний ланцюг, який зв'язується із зовнішнім доменом рецептора. Завдяки цим фармакологічним властивостям салметерол ефективніший для попередження гістамін-індукованого бронхоспазму і викликає більш тривалу бронходилатацію порівняно зі звичайними агоністами β2-рецепторів короткої дії. Ефективно та довго інгібує вивільнення в тканинах легких медіаторів опасистих клітин, таких як гістамін, лейкотрієни та PgD2. Пригнічує ранню та пізню стадію алергічної реакції; після введення одноразової дози зменшується гіперреактивність бронхів, інгібування пізньої стадії зберігається протягом більше 30 годин після прийому одноразової дози, коли бронходилатируючий ефект вже відсутній. Флутиказона пропіонат; - глюкокортикостероїд місцевого дії. При інгаляційному введенні в рекомендованих дозах має виражену протизапальну та протиалергічну дію, що призводить до зменшення вираженості симптомів та зниження частоти загострень захворювань, що супроводжуються обструкцією дихальних шляхів. При тривалому застосуванні інгаляційного флутиказону пропіонату в максимальних дозах добова та резервна секреція гормонів кори надниркових залоз залишається в межах норми у дорослих та дітей. Залишкове зниження резервної функції надниркових залоз може зберігатися протягом тривалого часу після терапії.ФармакокінетикаНемає даних, що свідчать, що спільне інгаляційне введення салметеролу та флутиказону пропіонату впливає на фармакокінетику кожної з цих речовин. Салметерол Після інгаляційного введення в терапевтичних дозах утворюються дуже низькі концентрації препарату в плазмі (200 пг/мл і менше). При регулярному застосуванні інгаляційного салметеролу у системному кровотоку визначається гідроксинафтоєва кислота в концентраціях до 100 нг/мл. Флутиказону пропіонат Після інгаляційного введення відносна біодоступність становить від 10 до 30% залежно від системи доставки препарату. Системна абсорбція відбувається переважно у легенях. Частина дози, що вдихається, може проковтуватися, але її системна дія мінімальна внаслідок слабкої розчинності препарату у воді та інтенсивного метаболізму при "першому проходженні" через печінку. Біодоступність флутиказону при ковтанні становить менше 1%. Існує пряма залежність між величиною вдихається дози і системним ефектом флутиказону, Vd становить близько 300 л. Метаболізується у печінці до неактивного метаболіту за участю CYP3A4 системи цитохрому Р450. Менш 5% метаболіту виводиться із сечею. Плазмовий кліренс дорівнює 1.15 л/хв. T1/2; близько 8 год.Клінічна фармакологіяПрепарат із протизапальною та бронхолітичною дією.Показання до застосуванняПрепарат Сальмекорт призначений для регулярного лікування бронхіальної астми у пацієнтів, яким показана комбінована терапія бета 2 -адреноміметиком тривалої дії та глюкокортикостероїдами для інгаляційного застосування: у пацієнтів з недостатнім контролем захворювання на фоні постійної монотерапії кортикостероїдів для інгаляційного застосування при періодичному використанні бета 2 -адреноміметика короткої дії; у пацієнтів з адекватним контролем захворювання на фоні терапії кортикостероїдами для інгаляційного застосування та бета 2 -адреноміметиком тривалої дії; як стартова підтримуюча терапія у пацієнтів з персистуючою бронхіальною астмою (щоденне виникнення симптомів, щоденне використання засобів для швидкого усунення симптомів) за наявності показань до призначення кортикостероїдів для досягнення контролю над захворюванням; підтримуюча терапія у пацієнтів з ХОЗЛ, у яких значення обсягу форсованого видиху (ОФВ1) <60% від належних величин (до інгаляції бронходилататора) з повторними загостреннями в анамнезі, і у яких виражені симптоми захворювання зберігаються, незважаючи на регулярну терапію бронходилататорами.Протипоказання до застосуванняГіперчутливість до одного або кількох компонентів препарату; дитячий вік (до 4 років). З обережністю Як і всі інші інгаляційні препарати, що містять кортикостероїди, препарат Сальмекорт слід застосовувати з обережністю у пацієнтів з гострим або латентним туберкульозом легень, грибковими, вірусними або бактеріальними інфекціями органів дихання, при тиреотоксикозі. При прийомі будь-яких препаратів групи симпатоміметиків, особливо при перевищенні терапевтичних доз, можливий розвиток серцево-судинних явищ, як збільшення систолічного АТ і ЧСС. З цієї причини Сальмекорт слід з обережністю призначати пацієнтам, які страждають на серцево-судинні захворювання, в т.ч. з аритміями, такими як суправентикулярна тахікардія та екстрасистолія, шлуночкова екстрасистолія, фібриляція передсердь. Усі симпатоміметичні препарати у дозах, що перевищують терапевтичні, можуть спричинити транзиторне зниження рівня калію у сироватці крові, тому препарат Сальмекорт слід з обережністю призначати пацієнтам із гіпокаліємією. Будь-який інгаляційний кортикостероїд може викликати системні ефекти, особливо при тривалому використанні у високих дозах, тому препарат слід застосовувати з обережністю при глаукомі, катаракті, остеопорозі (див. розділ "Особливі вказівки та запобіжні заходи при застосуванні"). Є дуже рідкісні повідомлення про підвищення рівня глюкози в крові, тому пацієнтам із цукровим діабетом слід застосовувати препарат Сальмекорт з обережністю (див. розділ "Побічна дія").Вагітність та лактаціяВагітним жінкам та жінкам у період лактації слід призначати препарат лише в тому випадку, якщо очікувана користь для матері перевищує будь-який можливий ризик для плода чи дитини. Недостатньо даних про застосування салметеролу та флутиказону пропіонату при вагітності та в період лактації. Вагітність Надмірна системна концентрація активного бета2-адреноміметика та кортикостероїдів впливає на плід. Великий клінічний досвід застосування препаратів даного класу свідчить, що при використанні терапевтичних доз ці ефекти не є клінічно значущими. Салметерол і флутиказону пропіонат не мають генотоксичності. Період лактації Концентрація салметеролу та флутиказону пропіонату в плазмі крові після вдихання препарату в терапевтичних дозах вкрай низька, тому їх концентрація у грудному молоці має бути такою ж низькою. Немає даних про концентрацію салметеролу та флутиказону пропіонату у грудному молоці жінок у період лактації. Застосування у дітей Застосування препарату дітям до 4 років протипоказане.Побічна діяУсі небажані реакції, представлені нижче, характерні для діючих речовин - салметеролу та флутиказону пропіонату окремо. Профіль безпеки препарату Сальмекорт не відрізняється від профілю небажаних реакцій діючих речовин. Небажані реакції, представлені нижче, перераховані відповідно до ураження органів і систем органів і частотою народження. Частота народження визначається таким чином: дуже часто (≥1/10), часто (≥1/100 та <1/10), нечасто (≥1/1000 та <1/100), рідко (≥1/10 000 та < 1/1000), дуже рідко (<1/10000, включаючи окремі випадки). Інфекції та інвазії: часто - кандидоз ротової порожнини та глотки, пневмонія (у пацієнтів з ХОЗЛ). З боку імунної системи: ; нечасто - шкірні реакції гіперчутливості; рідко – анафілактичні реакції, ангіоневротичний набряк (головним чином, набряк обличчя та ротоглотки), бронхоспазм. З боку ендокринної системи: ; можливі системні ефекти включають (див. розділи "З обережністю" та "Особливі вказівки"); рідко – синдром Кушинга, кушінгоїдні симптоми, пригнічення функції надниркових залоз, затримка росту у дітей та підлітків, зниження мінеральної щільності кісткової тканини. З боку органів зору: нечасто - катаракта; рідко – глаукома. З боку обміну речовин та харчування: ; нечасто - гіперглікемія; дуже рідко – гіпокаліємія. Порушення психіки: ; нечасто - тривожність, порушення сну; рідко – зміни у поведінці, в т.ч. підвищена активність та дратівливість (особливо у дітей). З боку нервової системи: дуже часто - головний біль (див. розділ "Особливі вказівки"); нечасто – тремор (див. розділ "Особливі вказівки"). З боку серцево-судинної системи: ;нечасто - прискорене серцебиття (див. розділ "З обережністю" та "Особливі вказівки"), тахікардія, фібриляція передсердь; рідко – аритмія, включаючи шлуночкову екстрасистолію, надшлуночкову тахікардію, екстрасистолію. З боку дихальної системи: ; часто - захриплість голосу та/або дисфонія; нечасто – подразнення глотки; рідко – парадоксальний бронхоспазм (див. розділ "Особливі вказівки"). З боку шкіри та підшкірних тканин: ;нечасто - синці. З боку кістково-м'язової системи: часто - м'язові спазми, артралгія. З боку травної системи: дуже рідко - диспепсія, нудота. Діти та підлітки Теоретично можливий розвиток системних реакцій, що включають синдром Кушинга, кушінгоїдні симптоми, пригнічення функції надниркових залоз, затримку росту у дітей та підлітків. Дуже рідко можуть виникати тривога, порушення сну та поведінкові розлади, включаючи гіперактивність та дратівливість.Взаємодія з лікарськими засобамиЧерез небезпеку розвитку бронхоспазму слід уникати застосування селективних та неселективних бета-адреноблокаторів за винятком тих випадків, коли вони вкрай необхідні пацієнтові. Салметерол Поєднане застосування з кетоконазолом слід уникати, якщо користь від застосування не перевищує потенційного ризику виникнення системних побічних реакцій при лікуванні салметеролом. Існує схожий ризик взаємодії з іншими сильними інгібіторами CYP3A4 (ітраконазол, телітроміцин, ритонавір). Флутиказону пропіонат У звичайних ситуаціях інгаляції флутиказону пропіонату супроводжуються низькими концентраціями його в плазмі внаслідок інтенсивного метаболізму при "першому проходженні" та високого системного кліренсу під впливом ізоферменту CYP3A4 системи цитохрому Р450 у кишечнику та печінці. Завдяки цьому клінічно значущі взаємодії за участю флутиказону пропіонату малоймовірні. Ритонавір, як високоактивний інгібітор ферменту CYP3A4, може викликати різке підвищення концентрації флутиказону пропіонату в плазмі, внаслідок чого суттєво знижуються концентрації сироваткового кортизолу. Спільне застосування з рітановіром викликає такі побічні ефекти, як синдром Кушинга та пригнічення функції надниркових залоз. Враховуючи сказане, слід уникати одночасного застосування флутиказону пропіонату та рітановіру, крім тих випадків, коли потенційна користь для пацієнта перевищує ризик системних побічних ефектів кортикостероїдів. Інші інгібітори ізоферменту CYP3A4 викликають мізерне (еритроміцин) та незначне (кетоконазол) підвищення вмісту флутиказону пропіонату в плазмі, при якому практично не знижуються концентрації сироваткового кортизолу. Незважаючи на це, рекомендується бути обережним при одночасному застосуванні сильних інгібіторів CYP3A4 (наприклад, кетоконазолу), оскільки при таких комбінаціях не виключається підвищення концентрації флутиказону пропіонату в плазмі. Похідні ксантину, кортикостероїдів та діуретики підвищують ризик розвитку гіпокаліємії (особливо у пацієнтів із загостренням бронхіальної астми, при гіпоксії). Інгібітори МАО та трициклічні антидепресанти збільшують ризик розвитку побічних ефектів із боку серцево-судинної системи. Сумісний з кромогліцієвою кислотою.Спосіб застосування та дозиІнгаляційно. Тільки для інгаляційного застосування. Пацієнт повинен бути поінформований про те, що для отримання оптимального ефекту препарат слід застосовувати регулярно, навіть за відсутності клінічних симптомів бронхіальної астми та ХОЗЛ. Лікар повинен регулярно оцінювати ефективність лікування пацієнта. Визначення тривалості курсу терапії та зміна дози препарату можливе лише за рекомендацією лікаря. Початкову дозу препарату визначають на підставі дози флутиказону, яка рекомендується для лікування цього ступеня тяжкості. Потім початкову дозу слід поступово знижувати до найменшої ефективної дози. Під час лікування пацієнту слід регулярно спостерігатися у лікаря з метою вибору оптимальної дози. Пацієнту не слід самостійно змінювати дози, призначені лікарем. Бронхіальна астма Якщо прийом препарату Сальмекорт 2 рази на добу забезпечує контроль симптомів, в рамках зниження дози до мінімально ефективної можливе зниження частоти прийому препарату до 1 разу на добу. Пацієнту слід призначати таку форму препарату Сальмекорт, яка містить дозу флутиказону пропіонату, що відповідає тяжкості захворювання. Якщо терапія інгаляційними глюкокортикостероїдами не забезпечує адекватний контроль захворювання, то їх заміна на препарат Сальмекорт у дозі, терапевтично еквівалентній дозі ГКС, що вводяться, може поліпшити контроль течії астми. У пацієнтів, у яких можна контролювати перебіг астми виключно за допомогою інгаляційних кортикостероїдів, їх заміна на препарат Сальмекорт може дозволити знизити дозу кортикостероїдів, необхідну для контролю перебігу астми. Рекомендовані дози Дорослі та діти віком від 12 років та старші: 2 інгаляції (25 мкг салметеролу та 50 мкг флутиказону пропіонату) 2 рази/добу, або 2 інгаляції (25 мкг салметеролу та 125 мкг флутиказону пропіонату) 2 рази/добу, або 2 інгаляції (25 мкг салметеролу та 250 мкг флутиказону проніонату) 2 рази на добу. Діти у віці 4 років та старші: 2 інгаляції (25 мкг салметеролу та 50 мкг флутиказону пропіонату) 2 рази на добу. Усі пацієнти, які приймають препарат як підтримуючу терапію, повинні пройти консультацію лікаря через 6-12 тижнів після первісного прийому. Хронічна обструктивна хвороба легень Для дорослих пацієнтів максимальна рекомендована доза становить 2 інгаляції (25 мкг салметеролу та 250 мкг флутиказону пропіонату) 2 рази на добу. Особливі групи пацієнтів Немає необхідності знижувати дозу препарату Сальмекорт у пацієнтів похилого віку, а також у пацієнтів з порушенням функції нирок або печінки. Інструкція з використання інгалятора Перед кожним застосуванням інгалятор слід струшувати. Перевірка інгалятора 1. Перед першим застосуванням або якщо інгалятор не використовувався 2 дні або більше, необхідно провести перевірку інгалятора. Для цього проводять 4 натискання (інгаляції) у повітря. Використання інгалятора 2. Зняти кришку з мундштука. При цьому мундштук повинен залишатись щільно прикріпленим до флакона (інгалятора); якщо інгалятор зберігався без кришки, необхідно перевірити мундштук на предмет забруднення. 3. Взяти інгалятор у руки мундштуком вниз так, щоб один палець знаходився на дні інгалятора, а інший палець або два на верхньому кінці інгалятора. Зробити видих і помістити мундштук між зубами. 4. Щільно обхопити мундштук губами і трохи нахилити голову назад. Повільно розпочати вдих і одночасно натиснути на дно балончика. Продовжити вдих до кінця. 5. Витягти інгалятор із ротової порожнини та затримати дихання на 10 сек або настільки, наскільки це комфортно. Повільно видихнути. Примітка: Після кожної інгаляції необхідно прополоскати рот та/або горло водою. Це допоможе знизити сухість, пов'язану із прийомом препарату. Перерва між інгаляціями повинна становити не менше 1 хв. При повторній інгаляції повторити кроки 2-5. Після використання необхідно закрити мундштук захисною кришкою. Перші кілька інгаляцій рекомендується проводити, контролюючи себе перед дзеркалом. Якщо Ви бачите, що відбувається "відплив" препарату через рот або з отвору між мундштуком та тілом інгалятора, це свідчить про неправильну техніку інгаляції. Інгаляції маленьким дітям мають проводитись під наглядом дорослого. Діти старшого віку та дорослі зі слабкими руками повинні тримати інгалятор двома руками. При цьому обидва вказівні пальці повинні розташовуватися на верхній частині інгалятора, а обидва великі пальці - на підставі нижче за мундштук. Очищення інгалятора Очищення інгалятора має проводитися мінімум 1 раз на добу. 1. Вийміть металевий балончик із препаратом із тіла інгалятора. Зніміть наконечник, що розпиляє. 2. Промийте мундштук та інгалятор під теплою проточною водою. 3. Ретельно протріть сухою тканиною або ватним тампоном. Слід уникати перегріву. 4. Зберіть інгалятор. Після використання всіх доз на упаковці металевий балончик слід викинути.ПередозуванняНе рекомендується призначення препарату у дозах, що перевищують зазначені у розділі "Спосіб застосування та дози". Дуже важливо регулярно переглядати режим дозування пацієнта та знижувати дозу до найнижчої з рекомендованих доз, що забезпечує ефективний контроль захворювання ("Спосіб застосування та дози"). Симптоми Очікувані симптоми та ознаки передозування салметеролу типові для надмірної бета2-адренергічної стимуляції, і включають тремор, головний біль, тахікардію, підвищення систолічного артеріального тиску та гіпокаліємію. Гостре передозування флутиказону пропіонату при інгаляційному введенні може спровокувати тимчасове пригнічення гіпоталамо-гіпофізарно-надниркової системи. Зазвичай це вимагає прийняття якихось екстрених заходів, оскільки нормальна функція надниркових залоз відновлюється протягом кількох днів. При прийомі препарату в дозах вище рекомендованих протягом тривалого періоду часу можливе значне пригнічення функції кори надниркових залоз. Описані рідкісні випадки гострого адреналового кризу, які виникали переважно у дітей, які отримували дози вище рекомендованих протягом тривалого часу (кілька місяців або років). Гострий адреналіновий криз проявляється гіпоглікемією, що супроводжується сплутаністю свідомості та/або судомами. До ситуацій, які можуть бути пусковими факторами гострого адреналового кризу, відносяться травма, хірургічне втручання, інфекція або будь-яке швидке зниження дози флутиказону пропіонату, що вдихається, до складу препарату Сальмекорт. Лікування Відсутнє специфічне лікування передозування салметеролу та флутиказону пропіонату. У разі передозування слід проводити підтримуючу терапію та спостерігати за станом пацієнта. При застосуванні препарату в дозах, що перевищують вказані в інструкції протягом тривалого часу, може спостерігатись пригнічення функції кори надниркових залоз.Запобіжні заходи та особливі вказівкиПрепарат Сальмекорт не призначений для полегшення гострих симптомів, оскільки в таких випадках слід застосовувати швидко та короткодіючий інгаляційний бронходилататор (наприклад, сальбутамол). Пацієнтів необхідно поінформувати про те, щоб вони завжди мали під рукою препарат для усунення гострих симптомів. Комбінація салметеролу і флутиказону пропіонату може використовуватися для початкової підтримуючої терапії у пацієнтів з персистуючою бронхіальною астмою (щоденне виникнення симптомів або щоденне використання засобів для усунення нападів) за наявності показань до призначення кортикостероїдів та приблизної їх дози. Частіше застосування бронходилататорів короткої дії для полегшення симптомів свідчить про погіршення контролю над захворюванням, у таких ситуаціях пацієнт повинен звертатися до лікаря. Раптове погіршення контролю бронхіальної астми, що посилюється, становить потенційну загрозу життю, у таких ситуаціях пацієнт також повинен звертатися до лікаря. Лікар повинен розглянути можливість більш високої дози кортикостероїдів. Якщо доза препарату Сальмекорт не забезпечує адекватний контроль над захворюванням, пацієнт також повинен звернутися до лікаря. Пацієнтам з астмою не можна різко припиняти лікування препаратом Сальмекорт через небезпеку розвитку загострення, дозу препарату слід поступово знижувати під контролем лікаря. У пацієнтів з ХОЗЛ відміна препарату може супроводжуватися симптомами декомпенсації та потребує спостереження лікаря. У пацієнтів з ХОЗЛ, які отримують препарат Сальмекорт, можливе збільшення частоти пневмонії (див. розділ "Побічна дія"). Лікарям слід пам'ятати про можливість розвитку пневмонії у пацієнтів з ХОЗЛ, оскільки клінічна картина загострення ХОЗЛ та пневмонії часто схожі. Будь-який інгаляційний кортикостероїд може викликати системні реакції, особливо при тривалому використанні у високих дозах; однак ймовірність виникнення таких симптомів набагато нижча, ніж при лікуванні пероральними глюкокортикостероїдами (див. розділ "Передозування"). та глаукому. Тому при лікуванні астми важливо знижувати дозу до найнижчої, що забезпечує ефективний контроль над захворюванням. В екстрених та планових ситуаціях, здатних викликати стрес, завжди необхідно пам'ятати про можливість пригнічення функції надниркових залоз і бути готовим до застосування кортикостероїдів (див. розділ "Передозування"). При проведенні реанімаційних заходів чи хірургічних втручань потрібно визначення ступеня надниркової недостатності. Рекомендується регулярно вимірювати зростання дітей, які отримують тривалу терапію інгаляційними глюкокортикостероїдами. Зважаючи на можливість пригнічення функції надниркових залоз, пацієнтів, переведених з пероральних кортикостероїдів на інгаляційну терапію флутиказону пропіонатом, слід лікувати з особливою обережністю та регулярно контролювати функцію кори надниркових залоз. При переведенні пацієнтів з прийому системних кортикостероїдів на інгаляційну терапію можуть виявлятися алергічні реакції (наприклад, алергічний риніт, екзема), які раніше пригнічувалися системними кортикостероїдами. У таких ситуаціях рекомендується проводити симптоматичне лікування антигістамінними препаратами та/або препаратами місцевої дії, в т.ч. ГКС для місцевого застосування. Після початку лікування інгаляційним флутиказоном пропіонатом системні глюкокортикоїди слід скасовувати поступово, такі пацієнти повинні мати при собі спеціальну картку пацієнта, що містить вказівку про можливу потребу в додатковому введенні глюкокортикостероїдів у стресових ситуаціях. У пацієнтів із загостренням бронхіальної астми, гіпоксією необхідно контролювати концентрацію іонів калію у плазмі. Є дуже рідкісні повідомлення підвищення концентрації глюкози у крові. Про це слід пам'ятати при призначенні комбінації салметеролу з флутиказону пропіонатом пацієнтам із цукровим діабетом (див. розділ "Побічна дія"). Через можливість виникнення системних ефектів кортикостероїдів, включаючи синдром Кушинга та пригнічення функції надниркових залоз, слід уникати спільного застосування флутиказону пропіонату та ритонавіру, за винятком випадків, коли потенційна користь для пацієнта перевищує ризик, пов'язаний із системними ефектами кортикостероїдів (див. розділ "Взаємодія з іншими лікарськими засобами"). При прийомі салметеролу ризик серйозних небажаних реакцій з боку дихальної системи або летального результату у пацієнтів афроамериканського походження, ймовірно, є вищим, ніж у інших пацієнтів. Значення фармакогенетичних факторів чи інших причин невідоме. Вплив супутнього застосування інгаляційних кортикостероїдів на ризик виникнення летальних наслідків у пацієнтів з астмою не вивчався. Як і інші інгаляційні препарати, Сальмекорт може викликати парадоксальний бронхоспазм, що проявляється наростанням задишки безпосередньо після застосування. У цьому випадку слід негайно застосувати швидко- та короткодіючий інгаляційний бронходилататор, скасувати Сальмекорт та розпочати, при необхідності, альтернативну терапію (див. розділ "Побічна дія"). Можливе виникнення побічних реакцій, пов'язаних із фармакологічною дією бета2-антагоністів, таких як тремор, відчуття серцебиття та головний біль. Однак дані реакції носять короткочасний характер, і їхня вираженість зменшується при регулярній терапії (див. розділ "Побічна дія"). Вплив на здатність до керування автотранспортом та управління механізмами У клінічних дослідженнях не отримано даних щодо впливу препарату на здатність керувати транспортними засобами та іншими механізмами, проте слід враховувати побічні дії, які може спричинити препарат.Умови відпустки з аптекЗа рецептомВідео на цю тему
377,00 грн
204,00 грн
Склад, форма випуску та упаковкаАерозоль - 1 доза: Активні речовини: салметеролу ксинафоат 36.3 мкг, що відповідає вмісту салметеролу 25 мкг, флутиказону пропіонат 50 мкг; Допоміжні речовини: 1,1,1,2-тетрафторетан (HFA-134a) – 73.099 мг, поліетиленгліколь 1000 – 0.01464 мг. 120 доз - балончики аерозольні алюмінієві (1) з клапаном дозуючої дії та мундштуком - пачки картонні.Опис лікарської формиАерозоль для інгаляцій дозований у вигляді суспензії білого або майже білого кольору.Фармакотерапевтична групаСальмекорт - комбінований бронходилатируючий засіб (містить салмотерол та флутиказону пропіонат). Салметерол; - селективний агоніст β2-адренорецепторів тривалої дії (не менше 12 год). Молекула салметерола має довгий бічний ланцюг, який зв'язується із зовнішнім доменом рецептора. Завдяки цим фармакологічним властивостям салметерол ефективніший для попередження гістамін-індукованого бронхоспазму і викликає більш тривалу бронходилатацію порівняно зі звичайними агоністами β2-рецепторів короткої дії. Ефективно та довго інгібує вивільнення в тканинах легких медіаторів опасистих клітин, таких як гістамін, лейкотрієни та PgD2. Пригнічує ранню та пізню стадію алергічної реакції; після введення одноразової дози зменшується гіперреактивність бронхів, інгібування пізньої стадії зберігається протягом більше 30 годин після прийому одноразової дози, коли бронходилатируючий ефект вже відсутній. Флутиказона пропіонат; - глюкокортикостероїд місцевого дії. При інгаляційному введенні в рекомендованих дозах має виражену протизапальну та протиалергічну дію, що призводить до зменшення вираженості симптомів та зниження частоти загострень захворювань, що супроводжуються обструкцією дихальних шляхів. При тривалому застосуванні інгаляційного флутиказону пропіонату в максимальних дозах добова та резервна секреція гормонів кори надниркових залоз залишається в межах норми у дорослих та дітей. Залишкове зниження резервної функції надниркових залоз може зберігатися протягом тривалого часу після терапії.ФармакокінетикаНемає даних, що свідчать, що спільне інгаляційне введення салметеролу та флутиказону пропіонату впливає на фармакокінетику кожної з цих речовин. Салметерол Після інгаляційного введення в терапевтичних дозах утворюються дуже низькі концентрації препарату в плазмі (200 пг/мл і менше). При регулярному застосуванні інгаляційного салметеролу у системному кровотоку визначається гідроксинафтоєва кислота в концентраціях до 100 нг/мл. Флутиказону пропіонат Після інгаляційного введення відносна біодоступність становить від 10 до 30% залежно від системи доставки препарату. Системна абсорбція відбувається переважно у легенях. Частина дози, що вдихається, може проковтуватися, але її системна дія мінімальна внаслідок слабкої розчинності препарату у воді та інтенсивного метаболізму при "першому проходженні" через печінку. Біодоступність флутиказону при ковтанні становить менше 1%. Існує пряма залежність між величиною вдихається дози і системним ефектом флутиказону, Vd становить близько 300 л. Метаболізується у печінці до неактивного метаболіту за участю CYP3A4 системи цитохрому Р450. Менш 5% метаболіту виводиться із сечею. Плазмовий кліренс дорівнює 1.15 л/хв. T1/2; близько 8 год.Клінічна фармакологіяПрепарат із протизапальною та бронхолітичною дією.Показання до застосуванняПрепарат Сальмекорт призначений для регулярного лікування бронхіальної астми у пацієнтів, яким показана комбінована терапія бета 2 -адреноміметиком тривалої дії та глюкокортикостероїдами для інгаляційного застосування: у пацієнтів з недостатнім контролем захворювання на фоні постійної монотерапії кортикостероїдів для інгаляційного застосування при періодичному використанні бета 2 -адреноміметика короткої дії; у пацієнтів з адекватним контролем захворювання на фоні терапії кортикостероїдами для інгаляційного застосування та бета 2 -адреноміметиком тривалої дії; як стартова підтримуюча терапія у пацієнтів з персистуючою бронхіальною астмою (щоденне виникнення симптомів, щоденне використання засобів для швидкого усунення симптомів) за наявності показань до призначення кортикостероїдів для досягнення контролю над захворюванням; підтримуюча терапія у пацієнтів з ХОЗЛ, у яких значення обсягу форсованого видиху (ОФВ1) <60% від належних величин (до інгаляції бронходилататора) з повторними загостреннями в анамнезі, і у яких виражені симптоми захворювання зберігаються, незважаючи на регулярну терапію бронходилататорами.Протипоказання до застосуванняГіперчутливість до одного або кількох компонентів препарату; дитячий вік (до 4 років). З обережністю Як і всі інші інгаляційні препарати, що містять кортикостероїди, препарат Сальмекорт слід застосовувати з обережністю у пацієнтів з гострим або латентним туберкульозом легень, грибковими, вірусними або бактеріальними інфекціями органів дихання, при тиреотоксикозі. При прийомі будь-яких препаратів групи симпатоміметиків, особливо при перевищенні терапевтичних доз, можливий розвиток серцево-судинних явищ, як збільшення систолічного АТ і ЧСС. З цієї причини Сальмекорт слід з обережністю призначати пацієнтам, які страждають на серцево-судинні захворювання, в т.ч. з аритміями, такими як суправентикулярна тахікардія та екстрасистолія, шлуночкова екстрасистолія, фібриляція передсердь. Усі симпатоміметичні препарати у дозах, що перевищують терапевтичні, можуть спричинити транзиторне зниження рівня калію у сироватці крові, тому препарат Сальмекорт слід з обережністю призначати пацієнтам із гіпокаліємією. Будь-який інгаляційний кортикостероїд може викликати системні ефекти, особливо при тривалому використанні у високих дозах, тому препарат слід застосовувати з обережністю при глаукомі, катаракті, остеопорозі (див. розділ "Особливі вказівки та запобіжні заходи при застосуванні"). Є дуже рідкісні повідомлення про підвищення рівня глюкози в крові, тому пацієнтам із цукровим діабетом слід застосовувати препарат Сальмекорт з обережністю (див. розділ "Побічна дія").Вагітність та лактаціяВагітним жінкам та жінкам у період лактації слід призначати препарат лише в тому випадку, якщо очікувана користь для матері перевищує будь-який можливий ризик для плода чи дитини. Недостатньо даних про застосування салметеролу та флутиказону пропіонату при вагітності та в період лактації. Вагітність Надмірна системна концентрація активного бета2-адреноміметика та кортикостероїдів впливає на плід. Великий клінічний досвід застосування препаратів даного класу свідчить, що при використанні терапевтичних доз ці ефекти не є клінічно значущими. Салметерол і флутиказону пропіонат не мають генотоксичності. Період лактації Концентрація салметеролу та флутиказону пропіонату в плазмі крові після вдихання препарату в терапевтичних дозах вкрай низька, тому їх концентрація у грудному молоці має бути такою ж низькою. Немає даних про концентрацію салметеролу та флутиказону пропіонату у грудному молоці жінок у період лактації. Застосування у дітей Застосування препарату дітям до 4 років протипоказане.Побічна діяУсі небажані реакції, представлені нижче, характерні для діючих речовин - салметеролу та флутиказону пропіонату окремо. Профіль безпеки препарату Сальмекорт не відрізняється від профілю небажаних реакцій діючих речовин. Небажані реакції, представлені нижче, перераховані відповідно до ураження органів і систем органів і частотою народження. Частота народження визначається таким чином: дуже часто (≥1/10), часто (≥1/100 та <1/10), нечасто (≥1/1000 та <1/100), рідко (≥1/10 000 та < 1/1000), дуже рідко (<1/10000, включаючи окремі випадки). Інфекції та інвазії: часто - кандидоз ротової порожнини та глотки, пневмонія (у пацієнтів з ХОЗЛ). З боку імунної системи: ; нечасто - шкірні реакції гіперчутливості; рідко – анафілактичні реакції, ангіоневротичний набряк (головним чином, набряк обличчя та ротоглотки), бронхоспазм. З боку ендокринної системи: ; можливі системні ефекти включають (див. розділи "З обережністю" та "Особливі вказівки"); рідко – синдром Кушинга, кушінгоїдні симптоми, пригнічення функції надниркових залоз, затримка росту у дітей та підлітків, зниження мінеральної щільності кісткової тканини. З боку органів зору: нечасто - катаракта; рідко – глаукома. З боку обміну речовин та харчування: ; нечасто - гіперглікемія; дуже рідко – гіпокаліємія. Порушення психіки: ; нечасто - тривожність, порушення сну; рідко – зміни у поведінці, в т.ч. підвищена активність та дратівливість (особливо у дітей). З боку нервової системи: дуже часто - головний біль (див. розділ "Особливі вказівки"); нечасто – тремор (див. розділ "Особливі вказівки"). З боку серцево-судинної системи: ;нечасто - прискорене серцебиття (див. розділ "З обережністю" та "Особливі вказівки"), тахікардія, фібриляція передсердь; рідко – аритмія, включаючи шлуночкову екстрасистолію, надшлуночкову тахікардію, екстрасистолію. З боку дихальної системи: ; часто - захриплість голосу та/або дисфонія; нечасто – подразнення глотки; рідко – парадоксальний бронхоспазм (див. розділ "Особливі вказівки"). З боку шкіри та підшкірних тканин: ;нечасто - синці. З боку кістково-м'язової системи: часто - м'язові спазми, артралгія. З боку травної системи: дуже рідко - диспепсія, нудота. Діти та підлітки Теоретично можливий розвиток системних реакцій, що включають синдром Кушинга, кушінгоїдні симптоми, пригнічення функції надниркових залоз, затримку росту у дітей та підлітків. Дуже рідко можуть виникати тривога, порушення сну та поведінкові розлади, включаючи гіперактивність та дратівливість.Взаємодія з лікарськими засобамиЧерез небезпеку розвитку бронхоспазму слід уникати застосування селективних та неселективних бета-адреноблокаторів за винятком тих випадків, коли вони вкрай необхідні пацієнтові. Салметерол Поєднане застосування з кетоконазолом слід уникати, якщо користь від застосування не перевищує потенційного ризику виникнення системних побічних реакцій при лікуванні салметеролом. Існує схожий ризик взаємодії з іншими сильними інгібіторами CYP3A4 (ітраконазол, телітроміцин, ритонавір). Флутиказону пропіонат У звичайних ситуаціях інгаляції флутиказону пропіонату супроводжуються низькими концентраціями його в плазмі внаслідок інтенсивного метаболізму при "першому проходженні" та високого системного кліренсу під впливом ізоферменту CYP3A4 системи цитохрому Р450 у кишечнику та печінці. Завдяки цьому клінічно значущі взаємодії за участю флутиказону пропіонату малоймовірні. Ритонавір, як високоактивний інгібітор ферменту CYP3A4, може викликати різке підвищення концентрації флутиказону пропіонату в плазмі, внаслідок чого суттєво знижуються концентрації сироваткового кортизолу. Спільне застосування з рітановіром викликає такі побічні ефекти, як синдром Кушинга та пригнічення функції надниркових залоз. Враховуючи сказане, слід уникати одночасного застосування флутиказону пропіонату та рітановіру, крім тих випадків, коли потенційна користь для пацієнта перевищує ризик системних побічних ефектів кортикостероїдів. Інші інгібітори ізоферменту CYP3A4 викликають мізерне (еритроміцин) та незначне (кетоконазол) підвищення вмісту флутиказону пропіонату в плазмі, при якому практично не знижуються концентрації сироваткового кортизолу. Незважаючи на це, рекомендується бути обережним при одночасному застосуванні сильних інгібіторів CYP3A4 (наприклад, кетоконазолу), оскільки при таких комбінаціях не виключається підвищення концентрації флутиказону пропіонату в плазмі. Похідні ксантину, кортикостероїдів та діуретики підвищують ризик розвитку гіпокаліємії (особливо у пацієнтів із загостренням бронхіальної астми, при гіпоксії). Інгібітори МАО та трициклічні антидепресанти збільшують ризик розвитку побічних ефектів із боку серцево-судинної системи. Сумісний з кромогліцієвою кислотою.Спосіб застосування та дозиІнгаляційно. Тільки для інгаляційного застосування. Пацієнт повинен бути поінформований про те, що для отримання оптимального ефекту препарат слід застосовувати регулярно, навіть за відсутності клінічних симптомів бронхіальної астми та ХОЗЛ. Лікар повинен регулярно оцінювати ефективність лікування пацієнта. Визначення тривалості курсу терапії та зміна дози препарату можливе лише за рекомендацією лікаря. Початкову дозу препарату визначають на підставі дози флутиказону, яка рекомендується для лікування цього ступеня тяжкості. Потім початкову дозу слід поступово знижувати до найменшої ефективної дози. Під час лікування пацієнту слід регулярно спостерігатися у лікаря з метою вибору оптимальної дози. Пацієнту не слід самостійно змінювати дози, призначені лікарем. Бронхіальна астма Якщо прийом препарату Сальмекорт 2 рази на добу забезпечує контроль симптомів, в рамках зниження дози до мінімально ефективної можливе зниження частоти прийому препарату до 1 разу на добу. Пацієнту слід призначати таку форму препарату Сальмекорт, яка містить дозу флутиказону пропіонату, що відповідає тяжкості захворювання. Якщо терапія інгаляційними глюкокортикостероїдами не забезпечує адекватний контроль захворювання, то їх заміна на препарат Сальмекорт у дозі, терапевтично еквівалентній дозі ГКС, що вводяться, може поліпшити контроль течії астми. У пацієнтів, у яких можна контролювати перебіг астми виключно за допомогою інгаляційних кортикостероїдів, їх заміна на препарат Сальмекорт може дозволити знизити дозу кортикостероїдів, необхідну для контролю перебігу астми. Рекомендовані дози Дорослі та діти віком від 12 років та старші: 2 інгаляції (25 мкг салметеролу та 50 мкг флутиказону пропіонату) 2 рази/добу, або 2 інгаляції (25 мкг салметеролу та 125 мкг флутиказону пропіонату) 2 рази/добу, або 2 інгаляції (25 мкг салметеролу та 250 мкг флутиказону проніонату) 2 рази на добу. Діти у віці 4 років та старші: 2 інгаляції (25 мкг салметеролу та 50 мкг флутиказону пропіонату) 2 рази на добу. Усі пацієнти, які приймають препарат як підтримуючу терапію, повинні пройти консультацію лікаря через 6-12 тижнів після первісного прийому. Хронічна обструктивна хвороба легень Для дорослих пацієнтів максимальна рекомендована доза становить 2 інгаляції (25 мкг салметеролу та 250 мкг флутиказону пропіонату) 2 рази на добу. Особливі групи пацієнтів Немає необхідності знижувати дозу препарату Сальмекорт у пацієнтів похилого віку, а також у пацієнтів з порушенням функції нирок або печінки. Інструкція з використання інгалятора Перед кожним застосуванням інгалятор слід струшувати. Перевірка інгалятора 1. Перед першим застосуванням або якщо інгалятор не використовувався 2 дні або більше, необхідно провести перевірку інгалятора. Для цього проводять 4 натискання (інгаляції) у повітря. Використання інгалятора 2. Зняти кришку з мундштука. При цьому мундштук повинен залишатись щільно прикріпленим до флакона (інгалятора); якщо інгалятор зберігався без кришки, необхідно перевірити мундштук на предмет забруднення. 3. Взяти інгалятор у руки мундштуком вниз так, щоб один палець знаходився на дні інгалятора, а інший палець або два на верхньому кінці інгалятора. Зробити видих і помістити мундштук між зубами. 4. Щільно обхопити мундштук губами і трохи нахилити голову назад. Повільно розпочати вдих і одночасно натиснути на дно балончика. Продовжити вдих до кінця. 5. Витягти інгалятор із ротової порожнини та затримати дихання на 10 сек або настільки, наскільки це комфортно. Повільно видихнути. Примітка: Після кожної інгаляції необхідно прополоскати рот та/або горло водою. Це допоможе знизити сухість, пов'язану із прийомом препарату. Перерва між інгаляціями повинна становити не менше 1 хв. При повторній інгаляції повторити кроки 2-5. Після використання необхідно закрити мундштук захисною кришкою. Перші кілька інгаляцій рекомендується проводити, контролюючи себе перед дзеркалом. Якщо Ви бачите, що відбувається "відплив" препарату через рот або з отвору між мундштуком та тілом інгалятора, це свідчить про неправильну техніку інгаляції. Інгаляції маленьким дітям мають проводитись під наглядом дорослого. Діти старшого віку та дорослі зі слабкими руками повинні тримати інгалятор двома руками. При цьому обидва вказівні пальці повинні розташовуватися на верхній частині інгалятора, а обидва великі пальці - на підставі нижче за мундштук. Очищення інгалятора Очищення інгалятора має проводитися мінімум 1 раз на добу. 1. Вийміть металевий балончик із препаратом із тіла інгалятора. Зніміть наконечник, що розпиляє. 2. Промийте мундштук та інгалятор під теплою проточною водою. 3. Ретельно протріть сухою тканиною або ватним тампоном. Слід уникати перегріву. 4. Зберіть інгалятор. Після використання всіх доз на упаковці металевий балончик слід викинути.ПередозуванняНе рекомендується призначення препарату у дозах, що перевищують зазначені у розділі "Спосіб застосування та дози". Дуже важливо регулярно переглядати режим дозування пацієнта та знижувати дозу до найнижчої з рекомендованих доз, що забезпечує ефективний контроль захворювання ("Спосіб застосування та дози"). Симптоми Очікувані симптоми та ознаки передозування салметеролу типові для надмірної бета2-адренергічної стимуляції, і включають тремор, головний біль, тахікардію, підвищення систолічного артеріального тиску та гіпокаліємію. Гостре передозування флутиказону пропіонату при інгаляційному введенні може спровокувати тимчасове пригнічення гіпоталамо-гіпофізарно-надниркової системи. Зазвичай це вимагає прийняття якихось екстрених заходів, оскільки нормальна функція надниркових залоз відновлюється протягом кількох днів. При прийомі препарату в дозах вище рекомендованих протягом тривалого періоду часу можливе значне пригнічення функції кори надниркових залоз. Описані рідкісні випадки гострого адреналового кризу, які виникали переважно у дітей, які отримували дози вище рекомендованих протягом тривалого часу (кілька місяців або років). Гострий адреналіновий криз проявляється гіпоглікемією, що супроводжується сплутаністю свідомості та/або судомами. До ситуацій, які можуть бути пусковими факторами гострого адреналового кризу, відносяться травма, хірургічне втручання, інфекція або будь-яке швидке зниження дози флутиказону пропіонату, що вдихається, до складу препарату Сальмекорт. Лікування Відсутнє специфічне лікування передозування салметеролу та флутиказону пропіонату. У разі передозування слід проводити підтримуючу терапію та спостерігати за станом пацієнта. При застосуванні препарату в дозах, що перевищують вказані в інструкції протягом тривалого часу, може спостерігатись пригнічення функції кори надниркових залоз.Запобіжні заходи та особливі вказівкиПрепарат Сальмекорт не призначений для полегшення гострих симптомів, оскільки в таких випадках слід застосовувати швидко та короткодіючий інгаляційний бронходилататор (наприклад, сальбутамол). Пацієнтів необхідно поінформувати про те, щоб вони завжди мали під рукою препарат для усунення гострих симптомів. Комбінація салметеролу і флутиказону пропіонату може використовуватися для початкової підтримуючої терапії у пацієнтів з персистуючою бронхіальною астмою (щоденне виникнення симптомів або щоденне використання засобів для усунення нападів) за наявності показань до призначення кортикостероїдів та приблизної їх дози. Частіше застосування бронходилататорів короткої дії для полегшення симптомів свідчить про погіршення контролю над захворюванням, у таких ситуаціях пацієнт повинен звертатися до лікаря. Раптове погіршення контролю бронхіальної астми, що посилюється, становить потенційну загрозу життю, у таких ситуаціях пацієнт також повинен звертатися до лікаря. Лікар повинен розглянути можливість більш високої дози кортикостероїдів. Якщо доза препарату Сальмекорт не забезпечує адекватний контроль над захворюванням, пацієнт також повинен звернутися до лікаря. Пацієнтам з астмою не можна різко припиняти лікування препаратом Сальмекорт через небезпеку розвитку загострення, дозу препарату слід поступово знижувати під контролем лікаря. У пацієнтів з ХОЗЛ відміна препарату може супроводжуватися симптомами декомпенсації та потребує спостереження лікаря. У пацієнтів з ХОЗЛ, які отримують препарат Сальмекорт, можливе збільшення частоти пневмонії (див. розділ "Побічна дія"). Лікарям слід пам'ятати про можливість розвитку пневмонії у пацієнтів з ХОЗЛ, оскільки клінічна картина загострення ХОЗЛ та пневмонії часто схожі. Будь-який інгаляційний кортикостероїд може викликати системні реакції, особливо при тривалому використанні у високих дозах; однак ймовірність виникнення таких симптомів набагато нижча, ніж при лікуванні пероральними глюкокортикостероїдами (див. розділ "Передозування"). та глаукому. Тому при лікуванні астми важливо знижувати дозу до найнижчої, що забезпечує ефективний контроль над захворюванням. В екстрених та планових ситуаціях, здатних викликати стрес, завжди необхідно пам'ятати про можливість пригнічення функції надниркових залоз і бути готовим до застосування кортикостероїдів (див. розділ "Передозування"). При проведенні реанімаційних заходів чи хірургічних втручань потрібно визначення ступеня надниркової недостатності. Рекомендується регулярно вимірювати зростання дітей, які отримують тривалу терапію інгаляційними глюкокортикостероїдами. Зважаючи на можливість пригнічення функції надниркових залоз, пацієнтів, переведених з пероральних кортикостероїдів на інгаляційну терапію флутиказону пропіонатом, слід лікувати з особливою обережністю та регулярно контролювати функцію кори надниркових залоз. При переведенні пацієнтів з прийому системних кортикостероїдів на інгаляційну терапію можуть виявлятися алергічні реакції (наприклад, алергічний риніт, екзема), які раніше пригнічувалися системними кортикостероїдами. У таких ситуаціях рекомендується проводити симптоматичне лікування антигістамінними препаратами та/або препаратами місцевої дії, в т.ч. ГКС для місцевого застосування. Після початку лікування інгаляційним флутиказоном пропіонатом системні глюкокортикоїди слід скасовувати поступово, такі пацієнти повинні мати при собі спеціальну картку пацієнта, що містить вказівку про можливу потребу в додатковому введенні глюкокортикостероїдів у стресових ситуаціях. У пацієнтів із загостренням бронхіальної астми, гіпоксією необхідно контролювати концентрацію іонів калію у плазмі. Є дуже рідкісні повідомлення підвищення концентрації глюкози у крові. Про це слід пам'ятати при призначенні комбінації салметеролу з флутиказону пропіонатом пацієнтам із цукровим діабетом (див. розділ "Побічна дія"). Через можливість виникнення системних ефектів кортикостероїдів, включаючи синдром Кушинга та пригнічення функції надниркових залоз, слід уникати спільного застосування флутиказону пропіонату та ритонавіру, за винятком випадків, коли потенційна користь для пацієнта перевищує ризик, пов'язаний із системними ефектами кортикостероїдів (див. розділ "Взаємодія з іншими лікарськими засобами"). При прийомі салметеролу ризик серйозних небажаних реакцій з боку дихальної системи або летального результату у пацієнтів афроамериканського походження, ймовірно, є вищим, ніж у інших пацієнтів. Значення фармакогенетичних факторів чи інших причин невідоме. Вплив супутнього застосування інгаляційних кортикостероїдів на ризик виникнення летальних наслідків у пацієнтів з астмою не вивчався. Як і інші інгаляційні препарати, Сальмекорт може викликати парадоксальний бронхоспазм, що проявляється наростанням задишки безпосередньо після застосування. У цьому випадку слід негайно застосувати швидко- та короткодіючий інгаляційний бронходилататор, скасувати Сальмекорт та розпочати, при необхідності, альтернативну терапію (див. розділ "Побічна дія"). Можливе виникнення побічних реакцій, пов'язаних із фармакологічною дією бета2-антагоністів, таких як тремор, відчуття серцебиття та головний біль. Однак дані реакції носять короткочасний характер, і їхня вираженість зменшується при регулярній терапії (див. розділ "Побічна дія"). Вплив на здатність до керування автотранспортом та управління механізмами У клінічних дослідженнях не отримано даних щодо впливу препарату на здатність керувати транспортними засобами та іншими механізмами, проте слід враховувати побічні дії, які може спричинити препарат.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПіна ректальна дозована - 1 аплікація активні речовини: месалазин (5-АСК) – 1000 мг; Допоміжні речовини: пропіленгліколь - 3. 4364 г, натрію дисульфіт - 0. 05 г, полісорбат 60 - 0.
Склад, форма випуску та упаковкасклад Супозиторії ректальні 250мг - 1 супп. активні речовини: месалазин (5-АСК) – 2500 мг; допоміжні речовини: жир твердий. 5 штук.
Склад, форма випуску та упаковкасклад Супозиторії ректальні 250мг - 1 супп. активні речовини: месалазин (5-АСК) – 2500 мг; допоміжні речовини: жир твердий. 5 штук.
309,00 грн
282,00 грн
Склад, форма випуску та упаковкаЛіофілізат для приготування розчину - 1 амп. екстракт простати (у перерахунку на водорозчинні пептиди) – 5 мг; Допоміжні речовини: гліцин – 25 мг. 5 мг - ампули безбарвного скла (5) - упаковки коміркові контурні (1) - пачки картонні. 5 мг - ампули безбарвного скла (5) - упаковки коміркові контурні (2) - пачки картонні. 5 мг – ампули безбарвного скла (5) – пачки картонні.Опис лікарської формиЛіофілізат для приготування розчину для внутрішньом'язового введення у вигляді порошку або пористої маси білого або білого з жовтуватим відтінком кольору.Фармакотерапевтична групаПрепарат тваринного походження, що застосовується при захворюваннях передміхурової залози.ФармакокінетикаДані про фармакокінетику препарату не надано.ФармакодинамікаПрепарат тваринного походження. Має органотропну дію на передміхурову залозу. Зменшує рівень набряку, лейкоцитарної інфільтрації передміхурової залози, нормалізує секреторну функцію епітеліальних клітин, збільшує число лецитинових зерен у секреті ацинусів, стимулює м'язовий тонус сечового міхура. Зменшує тромбоутворення, має антиагрегантну активність, перешкоджає розвитку тромбозу венул у передміхуровій залозі.Показання до застосуванняхронічний абактеріальний простатит; стани до та після оперативних втручань на передміхуровій залозі; доброякісна гіперплазія передміхурової залози.Протипоказання до застосуваннядитячий та підлітковий вік до 18 років; - підвищена чутливість до компонентів препарату.Вагітність та лактаціяЖінкам препарат не призначається. Протипоказане призначення дітям віком до 18 років.Побічна діяАлергічні реакції: кропив'янка. У разі алергічних реакцій слід припинити лікування, призначити антигістамінні препарати.Взаємодія з лікарськими засобамиСумісний із антибактеріальними препаратами, що застосовуються для лікування простатиту.Спосіб застосування та дозиПрепарат вводять внутрішньом'язово по 5-10 мг 1 раз на добу. Перед введенням ліофілізат розчиняють в 1-2 мл 0.9% розчину хлориду натрію, або 0.25-0.5% розчину новокаїну, або води для ін'єкцій. Тривалість лікування становить 5-10 днів. При необхідності курс може бути повторений через 1-6 місяців. При пропущенні одного або кількох введень препарату лікування не припиняють, рекомендовано подовження курсу лікування на кількість пропущених днів застосування.ПередозуванняПрепарат Простатилен не токсичний, передозування не спостерігалося.Запобіжні заходи та особливі вказівкиОсобливостей дії при першому введенні та при його відміні препарат не має. Застосування препарату при хронічних захворюваннях особливостей немає.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкасклад Супозиторії ректальні 250мг - 1 супп. активні речовини: месалазин (5-АСК) – 2500 мг; допоміжні речовини: жир твердий. 5 штук.