Лекарства и БАД Со скидкой
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
1 628,00 грн
230,00 грн
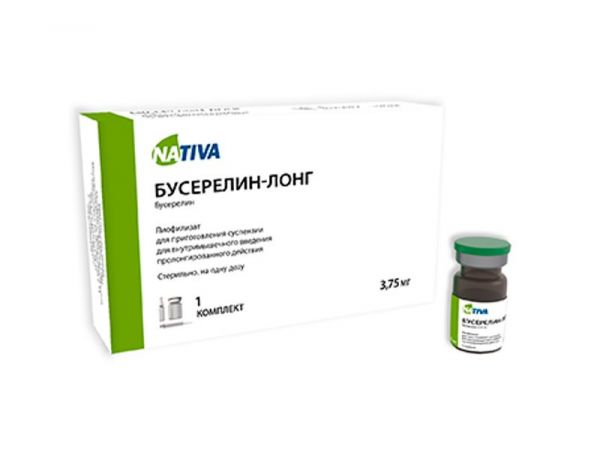
Склад, форма випуску та упаковкаЛіофілізат для приготування суспензії для внутрішньом'язового введення пролонгованої дії, що містить 3,75 мг бусереліну.Опис лікарської формиДозування 3,75 мг – 1 ін'єкція. Ліофілізат для приготування суспензії для внутрішньом'язового введення пролонгованої дії.Фармакотерапевтична групаПротипухлинний засіб, гонадотропін-рилізинг гормону (ГнРГ) аналог.Показання до застосуванняГормонозалежний рак передміхурової залози; Рак молочної залози; Ендометріоз (перед- та післяопераційний періоди); Міома матки; Гіперпластичні процеси ендометрію; Лікування безпліддя (при проведенні програми екстракорпорального запліднення (ЕКО)).Протипоказання до застосуванняВагітність; Період лактації; Підвищена чутливість до компонентів препарату.Взаємодія з лікарськими засобамиОдночасне застосування препарату "Бусерелін-лонг" з препаратами, що містять статеві гормони (наприклад, в режимі індукції овуляції), може сприяти виникненню синдрому гіперстимуляції яєчників. При одночасному застосуванні Бусерелін-лонг може знижувати ефективність гіпоглікемічних засобів.Спосіб застосування та дозиПри гормонозалежному раку передміхурової залози Бусерелін-лонг вводять у дозі 3,75 мг (1 ін'єкція) внутрішньом'язово (в/м) кожні 4 тижні. При лікуванні ендометріозу, гіперпластичних процесів ендометрію препарат вводять у дозі 3,75 мг внутрішньом'язово одноразово кожні 4 тижні. Лікування слід розпочинати у перші п'ять днів менструального циклу. Тривалість лікування – 4-6 місяців. При лікуванні міоми матки Бусерелін-лонг вводять у дозі 3,75 мг внутрішньом'язово одноразово кожні 4 тижні. Лікування слід розпочинати у перші п'ять днів менструального циклу. Тривалість лікування перед операцією 3 місяці, в інших випадках - 6 місяців; При лікуванні безпліддя методом екстракорпорального запліднення (ЕКО) Бусерелін-лонг вводять у дозі 3,75 мг (1 ін'єкція) внутрішньом'язово одноразово на початку фолікулінової (на 2-й день менструального циклу) або в середині лютеїнової фази (21 - 24 дн). менструального циклу, що передує стимуляції. Після блокади гіпофізарної функції, підтвердженої зниженням концентрації естрогенів у сироватці крові не менше, ніж на 50 % від вихідного рівня (зазвичай визначається через 12 - 15 днів після ін'єкції Бусерелін-лонг), за відсутності кіст яєчника (за даними УЗД), товщиною ендометрію більше 5 мм, починається стимуляція суперовуляції гонадотропними гормонами під ультразвуковим моніторингом та контролем рівня естрадіолу у сироватці кровіУмови відпустки з аптекЗа рецептомВідео на цю тему
538,00 грн
489,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
254,00 грн
222,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
296,00 грн
254,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
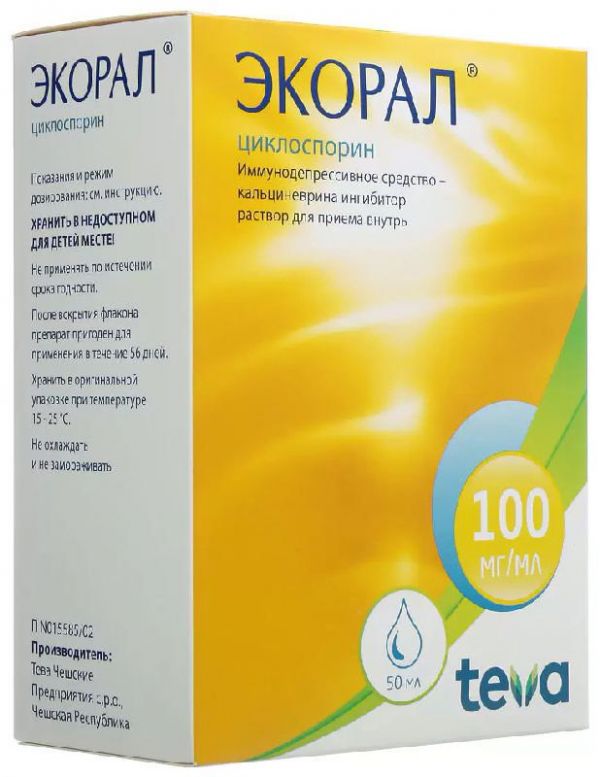
Дозировка: 100 мг Фасовка: N50 Форма выпуска: капс. мягкие Упаковка: блистер Производитель: Тева Завод-производитель: Тева Чешские Предприятия с. р.
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
Склад, форма випуску та упаковкаЛимонна кислота та гідрокарбонат натрію (регулятори кислотності), сорбіт (носій), мальтодекстрин (загусник), сік бузини чорної порошкоподібний, аскорбінова кислота (вітамін С), буряки екстракт (барвник натуральний), ароматизатор натуральний «Ягідний мікс», декстроза, поліет носій), цинку сульфат, сукралоза (підсолоджувач), полідиметилсилоксан (піногасник).ХарактеристикаЗміцнення імунітету – актуальне завдання завжди та для всіх! Саме міцний імунітет і стає першою лінією оборони при зустрічі з вірусами, і при належній фортеці здатний захистити нас не тільки від грипу та застуд – подбавши про його зміцнення, ви загалом будете набагато стійкішими до інфекцій та хронічних захворювань. Для підтримки та зміцнення імунітету зверніть увагу на шипучі таблетки БУЗИНА ІМУНІТЕТ У складі: сік бузини чорної, багатий біологічно активними компонентами для зміцнення імунної системи. У ягодах бузини містяться антоціанідини - речовини, відомі своєю імуностимулюючою дією. Дослідження показали, що екстракт бузини є чудовим засобом для полегшення симптомів ГРВІ. Крім бузини, до складу входять такі необхідні для зміцнення імунної системи вітаміни С і цинк.РекомендуєтьсяРекомендується як біологічно активна добавка до їжі - додаткового джерела вітаміну С і цинку.Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність, годування груддю.Спосіб застосування та дозиДорослим по 1 таблетці 2 рази на день під час їжі, попередньо розчинивши 200 мл води кімнатної температури. Тривалість прийому – не менше 20 днів.Запобіжні заходи та особливі вказівкиПеред застосуванням рекомендується проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаЕкстракт коренів кропиви, желатин (оболонка капсули), екстракт плодів пальми сабаль, екстракт насіння гарбуза, лактоза, цинку лактат, антистежуючий агент діоксид кремнію (аеросил), барвники харчові-діоксид титану, кармуазин, оксид заліза чорний (оболонка капсули). РекомендуєтьсяЯк біологічно активну добавку до їжі - додаткове джерело цинку. Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність, годування груддю.
Склад, форма випуску та упаковкаСировина рослинна подрібнена (порошок) чистотілу трави. Упаковка: 20 фільтр-пакетиків х 1,5 г.ХарактеристикаПротизапальний засіб рослинного походженняФармакотерапевтична групаНастій трави чистотілу має місцеву протизапальну дію.Інструкція8 фільтр-пакетів (12 г) поміщають у скляний або емальований посуд, заливають 200 мл (1 склянка) окропу, накривають і настоюють 15 хвилин, періодично натискаючи на пакетики ложкою, потім їх віджимають. Об'єм отриманого настою доводять кип'яченою водою до 200 мл. Застосовують зовнішньо для ванн (1-2 склянки на ванну) або як примочок (без розведення).Показання до застосуванняЯк місцевий протизапальний засіб у дерматології при шкірних захворюваннях, що супроводжуються свербінням (дерматит, псоріаз, екзема та ін.) – у складі комплексної терапії.Протипоказання до застосуванняПідвищена чутливість до препарату.Побічна діяМожливі алергічні реакції.Умови відпустки з аптекБез рецептаВідео на цю тему
Дозування: 25 мг Фасування: N50 Форма выпуска: капс. мягкие Упаковка: блистер Производитель: Тева Завод-производитель: Тева Чешские Предприятия с. р.
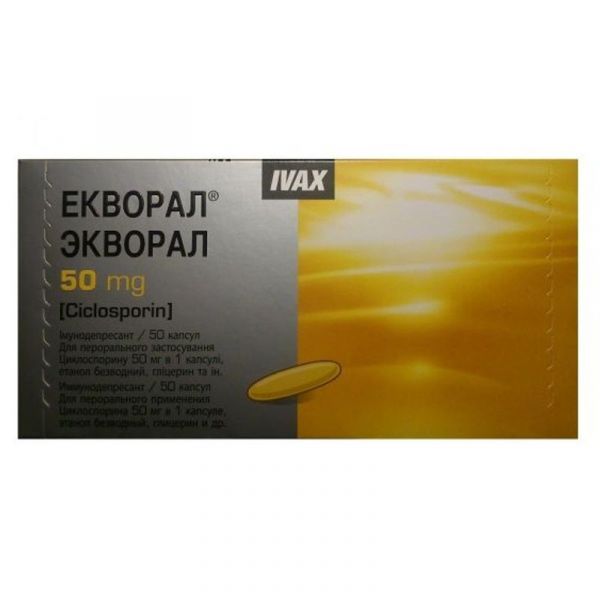
Дозировка: 50 мг Фасовка: N50 Форма выпуска: капс. мягкие Упаковка: блистер Производитель: Тева Завод-производитель: IVAX Pharmaceuticals Действующее вещество: Циклоспорин. .
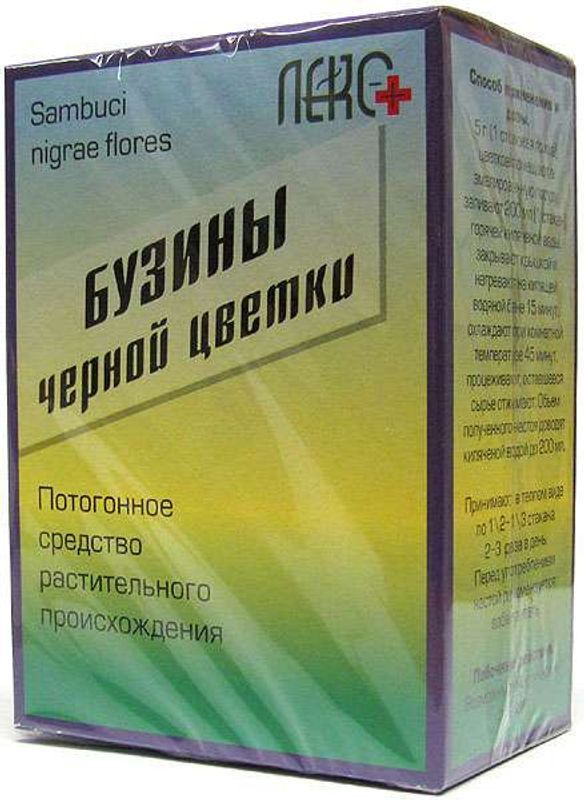
Склад, форма випуску та упаковкаБузини чорні квіти. Квітки цілісні по 50 г, 100 г у картонній пачці з внутрішнім пакетом з паперу або поліпропілену. Текст інструкції із застосування повністю нанесено на пачку.Опис лікарської формиОкремі квіти та бутони на коротких голих квітконіжках або без них. Квітки зі слабо помітною пятизубчатой спайнолистою чашечкою і віночком з 4-5 пелюсток, зрощених біля основи, діаметром до 5 мм. Тичинок 5, що приросли до трубки віночка, зав'язь напівнижня, тригніздна. Колір зеленувато-жовтий, жовтуватий, жовтий, темно-жовтий зі світло-коричневими та коричневими вкрапленнями. Запах ароматний. Смак водного вилучення пряний.ХарактеристикаКвітки бузини містять флавоноїди, ефірну олію, глікозид самбунігрін та інші.Фармакотерапевтична групаПотогінний засіб рослинного походження.ФармакодинамікаНастій із квіток бузини чорної має потогінну дію.Інструкція5 г (1 столова ложка) квіток поміщають в емальований посуд, заливають 200 мл (1 склянка) гарячої кип'яченої води, накривають кришкою і настоюють на киплячій водяній бані 15 хв, охолоджують при кімнатній температурі 45 хв, проціджують, що залишилося від сировини. Об'єм отриманого настою доводять кип'яченою водою до 200 мл. Приймають внутрішньо по 1/3 склянки теплого настою 2-3 десь у день. Перед застосуванням настій рекомендується збовтувати.Показання до застосуванняГострі респіраторні вірусні інфекції, зокрема грип (симптоматична терапія).Протипоказання до застосуванняПідвищена чутливість до препарату, вагітність, період грудного вигодовування. Дитячий вік віком до 12 років.Побічна діяМожливі алергічні реакції.Взаємодія з лікарськими засобамиЧи не описано.ПередозуванняВипадки передозування досі не були зареєстровані.Запобіжні заходи та особливі вказівкиПотогінної дії лікарського препарату сприяє тепле питво. За відсутності ефекту (зниження температури тіла) на фоні застосування препарату протягом 24 годин необхідно звернутися до лікаря. Застосування препарату не впливає на керування транспортними засобами та заняття іншими потенційно небезпечними видами діяльності, що потребують підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаСировина рослинна подрібнена (порошок) чистотілу трави. Упаковка: 20 фільтр-пакетиків х 1,5 г.ХарактеристикаПротизапальний засіб рослинного походженняФармакотерапевтична групаНастій трави чистотілу має місцеву протизапальну дію.Інструкція8 фільтр-пакетів (12 г) поміщають у скляний або емальований посуд, заливають 200 мл (1 склянка) окропу, накривають і настоюють 15 хвилин, періодично натискаючи на пакетики ложкою, потім їх віджимають. Об'єм отриманого настою доводять кип'яченою водою до 200 мл. Застосовують зовнішньо для ванн (1-2 склянки на ванну) або як примочок (без розведення).Показання до застосуванняЯк місцевий протизапальний засіб у дерматології при шкірних захворюваннях, що супроводжуються свербінням (дерматит, псоріаз, екзема та ін.) – у складі комплексної терапії.Протипоказання до застосуванняПідвищена чутливість до препарату.Побічна діяМожливі алергічні реакції.Умови відпустки з аптекБез рецептаВідео на цю тему
Дозування: 800 мг Фасування: N30 Форма випуску таб. Упаковка: блістер Виробник: Ейсай Юроп Лімітед Завод-производитель: Бьял-Портела энд Ка С. А.
10 091,00 грн
10 058,00 грн
Умови зберіганняУ холодильнику +2+8 градусівУмови відпустки з аптекЗа рецептомВідео на цю тему.
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
Склад, форма випуску та упаковкаЦукор, вода, сік плодів бузини чорної, аскорбінова кислота (вітамін С), лимонна кислота (регулятор кислотності), сульфат цинку, екстракт плодів бузини чорної, натуральний ароматизатор «Ягідний мікс», холекальциферол (вітамін D), піридоксину гідрохлорид (вітамін В6) , фолієва кислота.ХарактеристикаСьогодні бузина користується великою популярністю у всьому світі, оскільки є природним активатором імунітету. Вся справа в її пігментах антоціанах, які стимулюють функції імунної системи і мають противірусні властивості. Корисні властивості супер-ягоди бузини підтверджені багатьма дослідженнями. Вчені відкрили її потужний антиоксидантний, противірусний та протизапальний потенціал. Сучасній науковій медицині відома також жарознижувальна, протимікробна та відхаркувальна дія бузини. Американські фахівці встановили, що екстракти та настої бузини зменшують тяжкість та тривалість перебігу грипу. Їхні ізраїльські колеги стверджують, що тривалість захворювання скорочується в середньому на 4 дні.Властивості компонентівЕвалар Сироп бузини виготовляється з плодів чорної бузини, рівень антиоксидантної активності якої вдвічі вищий, ніж у чорниці та журавлини. Адже журавлина і чорниця тривалий час вважалися лідерами за вмістом антиоксидантів. Склад посилений вітамінами С, D, B6, фолієвою кислотою та цинком. Ці мікроелементи також позитивно впливають на імунітет людини. Вітамін С (аскорбінова кислота) – визнаний імуностимулятор. Він посилює вироблення білків інтерферонів. Має протизапальні властивості, сприяє нейтралізації вільних радикалів та захисту клітин легень від їх агресивного впливу. Вітамін D дуже важливий для здоров'я, тому що підвищує імунітет, знижує рівень запалення та вірусної активності, а також бере участь ще у двохстах функціях організму. Прийом вітаміну D сприяє зниженню захворюваності на ГРВІ, у тому числі нової коронавірусної інфекції COVID-195. Вітамін В6 потрібен для нормального синтезу нуклеїнових кислот, які перешкоджають старінню організму, та для підтримки імунітету. Фолієва кислота (фолат) бере участь у синтезі імунних клітин крові, активізації метаболізму, сприяє нормалізації функції травного тракту. Цинк, за останніми даними, перешкоджає розмноженню коронавірусу за рахунок здатності блокувати активність ферменту РНК-полімерази та ферменту АПФ2, які допомагають вірусу проникнути в клітину.Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність, годування груддю.Спосіб застосування та дозиДорослим та дітям з 3 років по 1 чайній ложці (5 мл) 2 рази на день під час їжі. Тривалість прийому – 1 місяць.Запобіжні заходи та особливі вказівкиПеред застосуванням рекомендується проконсультуватися з лікарем. Перед застосуванням БАД дітьми проконсультуватись із лікарем-педіатром.Умови відпустки з аптекБез рецептаВідео на цю тему
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
1 717,00 грн
1 670,00 грн
Фасування: N30 Форма випуску: трансдермальна терапевтична система Упаковка: пакет Виробник: Новартіс Консьюмер Хелс Завод-виробник: Новартіс Консьюмер Хелс (Швейцарія) Діюча речовина: Ривастигмін. . .
Дозування: 1. 5 мг Фасування: N28 Форма випуску: капс. Упаковка: уп.
Фасування: N1 Форма випуску: р-р д/прийому всередину Упакування: фл. Производитель: Новартис Консьюмер Хелс Завод-производитель: Новартис Фарма С. а.
Склад, форма випуску та упаковкаГель - 100 гр. активна речовина: кетопрофен у перерахунку на 100% речовину 2,5 г; допоміжні речовини: етанол (спирт етиловий ректифікований), карбомер 940 або 980, трометамол, метилпарагідроксибензоат (ніпагін), лаванди олія, апельсина квіток олія (неролієва олія), вода очищена. По 30, 50 або 100 г у тубі алюмінієвої. Кожна туба разом із інструкцією із застосування у пачці з картону.Опис лікарської формиБезбарвний, майже прозорий гель із специфічним запахом. Допускається наявність опалесценції.Фармакотерапевтична групаНестероїдний протизапальний препарат.ФармакокінетикаПри місцевому застосуванні у вигляді гелю всмоктується надзвичайно повільно та практично не кумулює в організмі. Біодоступність гелю – близько 5%. Після застосування у дозі 50-150 мг концентрація у плазмі через 5-8 годин – 0,08-0,15 мкг/мл.ФармакодинамікаКетопрофен – нестероїдний протизапальний препарат (НПЗЗ). Чинить місцеву протизапальну, антиексудативну та аналгетичну дію. Забезпечує місцеве лікування уражень суглобів, сухожилля, зв'язок, м'язів. При суглобовому синдромі викликає ослаблення болів у суглобах у спокої та під час руху, зменшення ранкової скутості та припухлості суглобів. Кетопрофен не має катаболічного впливу на суглобовий хрящ.Показання до застосуванняГострі та хронічні запальні захворювання опорно-рухового апарату (суглобовий синдром при загостренні подагри, ревматоїдний артрит, псоріатичний артрит, анкілозуючий спондилоартрит, остеоартроз, остеохондроз з корінковим синдромом, радикуліт, запальне ураження зв'язувань, суц, буржуаз, суц, буржуаз) М'язові болі ревматичного та неревматичного походження. Посттравматичне запалення м'яких тканин та опорно-рухового апарату (пошкодження та розриви зв'язок, забиття).Протипоказання до застосуванняПідвищена чутливість до кетопрофену або інших нестероїдних протизапальних препаратів, ушкодження шкірних покривів (мокнучі дерматози, екзема, інфіковані садна, рани), вагітність ІІІ триместр та період лактації, дитячий вік (до 6 років). З обережністю: ерозивно-виразкове ураження шлунково-кишкового тракту, виражені порушення функції нирок та печінки, хронічна серцева недостатність, бронхіальна астма, вагітність І-ІІ триместр, печінкова порфірія.Побічна діяМісцеві реакції: алергічний дерматит, екзема, гіперемія шкіри, фотодерматит, бульозний дерматит, висип, пурпура. Системні реакції: кропив'янка, генералізований шкірний висип, набряки, фотосенсибілізація, стоматит.Взаємодія з лікарськими засобамиПри зовнішньому застосуванні кетопрофену взаємодія з іншими лікарськими засобами не встановлена.Спосіб застосування та дозиЗовнішньо. Дорослим та дітям з 12 років наносять невелику кількість гелю (3-5 см) 2-3 рази на день тонким шаром, з подальшим тривалим та обережним втиранням у запалені або болючі ділянки тіла. Дітям з 6 до 12 років наносять не більше 1 -2 см препарату не частіше ніж 2 рази на день. Тривалість курсу лікування має перевищувати 14 днів без консультації лікаря. Можна використовувати при фонофорезі.ПередозуванняВкрай низька системна абсорбція активних компонентів препарату при зовнішньому застосуванні робить передозування практично неможливим.Запобіжні заходи та особливі вказівкиПрепарат слід наносити тільки на непошкоджені ділянки шкіри, уникаючи попадання на відкриті рани, очі та слизові оболонки. Після аплікації необхідно вимити руки. Не застосовувати з оклюзійними пов'язками. Перед застосуванням гелю пацієнтам з порушенням функції печінки та нирок, шлунково-кишковими захворюваннями в анамнезі, бронхіальною астмою, серцевою недостатністю необхідно проконсультуватися з лікарем. Гель має величину pH, близьку до величини pH шкіри.Умови відпустки з аптекБез рецептаВідео на цю тему
Дозування: 3 мг Фасування: N28 Форма випуску: капс. Упаковка: уп. контурні.