Акционные товары
Склад, форма випуску та упаковкаСупозиторії – 1 суп.: діючі речовини: кофеїн – 50 мг, напроксен – 75 мг, саліциламід – 600 мг; допоміжні речовини: жир твердий (Вітепсол, марки H 15, W 35, Супосир, марки NA 15, NAS 50) - до одержання супозиторію масою 2,20 г. Супозиторії ректальні. По 5 супозиторіїв у контурній комірковій упаковці. Дві контурні коміркові упаковки разом з інструкцією з медичного застосування препарату поміщають у картонну пачку.Опис лікарської формиСупозиторії білого або білого з жовтуватим або кремуватим відтінком кольору, торпедоподібної форми. На поздовжньому зрізі супозиторію повинні бути відсутні вкраплення, допускається наявність повітряного стрижня або лійкоподібного заглиблення.Фармакотерапевтична групаАналгезуючий засіб комбінований (НПЗП+психостимулюючий засіб).ФармакодинамікаЦефекон Н - комбінований препарат, що має аналгетичну, жарознижувальну та протизапальну дію. Напроксен та саліциламід є нестероїдними протизапальними препаратами (НПЗП), механізм дії яких пов'язаний з інгібуванням синтезу простагландинів та впливом на центр терморегуляції у гіпоталамусі. Кофеїн має психостимулюючу, аналептичну та спазмолітичну дію на гладку мускулатуру.Показання до застосуванняяк знеболюючий засіб при больовому синдромі легкої та середньої тяжкості: невралгія, міалгія, ішіас, люмбаго; дегенеративно-дистрофічні захворювання опорно-рухового апарату (остеохондроз, остеоартроз, анкілозуючий спондиліт); головний та зубний біль, мігрень; дисменорея (болючі менструації); як жарознижувальний засіб: гарячковий синдром при застудних, інфекційних, запальних захворюваннях.Протипоказання до застосуванняГіперчутливість до компонентів препарату, виразкова хвороба шлунка та дванадцятипалої кишки (фаза загострення), повне або неповне поєднання бронхіальної астми, рецидивуючого поліпозу носа та приносових пазух та непереносимості ацетилсаліцилової кислоти або ін. НПВП ниркова та/або печінкова недостатність, артеріальна гіпертензія, органічні захворювання серцево-судинної системи, серцева недостатність, захворювання крові, набряки, патологія вестибулярного апарату, підвищена збудливість, безсоння, закритокутова глаукома, дитячий вік (до 16 років), вагітність, період лактації.Побічна діяАлергічні реакції, запаморочення, збудження, сонливість, уповільнення швидкості психомоторних реакцій, шум у вухах, тахікардія, підвищення артеріального тиску, тромбоцитопенія, агранулоцитоз, апластична анемія, порушення функції печінки та/або нирок; свербіж і біль у прямій кишці.Взаємодія з лікарськими засобамиНапроксен зменшує гіпотензивну дію бета-адреноблокаторів. При одночасному застосуванні напроксен може спричинити зменшення діуретичного ефекту фуросеміду. Напроксен підвищує токсичність фенітоїну, сульфаніламідів, метотрексату. Саліциламід посилює дію непрямих антикоагулянтів, антиагрегантів, фібринолітиків. Саліциламід збільшує ризик розвитку побічних ефектів глюкокортикостероїдів, мінералокортикостероїдів, естрогенів при сумісному застосуванні. При одночасному застосуванні саліциламіду з мієлотоксичними лікарськими засобами збільшується ризик пригнічення мозкового кровообігу (гемопоезу). Кофеїн прискорює всмоктування та посилює дію серцевих глікозидів, підвищує їхню токсичність. Спільне застосування кофеїну з бета-адреноблокаторами може призводити до взаємного придушення терапевтичних ефектів; з адренергічними бронхорозширювальними лікарськими засобами – до додаткової стимуляції центральної нервової системи та ін. адитивним токсичним ефектам.Спосіб застосування та дозиРектально. Супозиторій звільняють від контурної клітинної упаковки і після мимовільного спорожнення кишечника або очисної клізми вводять глибоко в пряму кишку по 1 супозиторію 1-3 рази на добу. Після введення супозиторію необхідно перебування у горизонтальному положенні протягом 30-40 хвилин. Тривалість прийому без консультації з лікарем не більше 5 днів при призначенні як знеболювальний засіб і 3-х днів як жарознижувальний засіб.ПередозуванняПро випадки передозування препарату Цефекон Н не повідомлялося.Умови відпустки з аптекБез рецептаВідео на цю тему
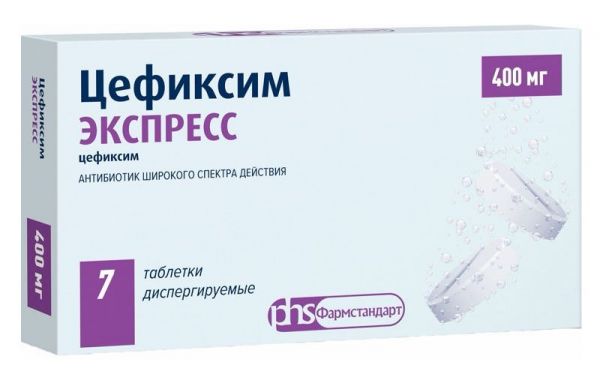
Склад, форма випуску та упаковкаПігулки - 1 таб. Діюча речовина: цефіксіма тригідрат – 447,7 мг у перерахунку на цефіксім – 400,0 мг; допоміжні речовини: целюлоза мікрокристалічна 102, гіпоролоза низькозаміщена (гідроксипропілцелюлоза низькозаміщена), кремнію діоксид колоїдний (аеросил), повідон К30, магнію стеарат, сахарин, ароматизатор полуничний*, барвник сонячний захід жовтий0 * Склад ароматизатора: натуральні смакоароматичні речовини, мальтодекстрин, гуміарабік (Е414), тріацетин (Е1518), 1,2-пропіленгліколь (Е1520), оцтова кислота (Е260) або натуральні ароматичні речовини, пропіленгліколь (Е5) Пігулки дисперговані, 400 мг. 7 таблеток у контурній комірковій упаковці з плівки ПВХ/ПВДХ та фольги алюмінієвої друкованої лакованої. 7 таблеток у контурній комірковій упаковці з плівки ПВХ та фольги алюмінієвої друкованої лакованої. 1 контурне осередкове впакування разом з інструкцією з медичного застосування поміщають у пачку з картону. 21 таблетка у поліпропіленовому флаконі, закупореному кришкою з поліетилену високого тиску з силікагелем і контролем першого розтину. 1 флакон разом з інструкцією із застосування поміщають у пачку з картону.Опис лікарської формиТаблетки рожево-жовтого кольору з вкрапленнями білого та червоного кольору, овальні, двоопуклі з ризиком з одного боку, з характерним запахом полуниці.Фармакотерапевтична групаАнтибіотик-цефалоспорин.ФармакокінетикаАбсорбція При прийомі внутрішньо біодоступність становить 40-50% і не залежить від їди. Максимальна концентрація в плазмі (Сmax) у дорослих після перорального прийому в дозі 400 мг досягається через 3-4 години і становить 2,5-4,9 мкг/мл, після прийому в дозі 200 мг – 1,49-3,25. мкг/мл. Прийом їжі на абсорбцію препарату із шлунково-кишкового тракту (ЖКТ) істотного впливу не має. Розподіл Об'єм розподілу при введенні 200 мг цефіксіма склав 6,7 л, при досягненні рівноважної концентрації – 16,8 л. З білками плазми зв'язується близько 65% цефіксиму. Найбільш високі концентрації цефіксім створює в сечі та жовчі. Цефіксім проникає через плаценту. Концентрація цефіксиму в крові пупкового канатику досягала 1/6-1/2 концентрації препарату в плазмі крові матері; у грудному молоці препарат не визначається. Метаболізм та виведення Період напіввиведення у дорослих та дітей становить 3-4 год. Цефіксім не метаболізується в печінці; 50-55% від прийнятої дози виводиться із сечею у незміненому вигляді протягом 24 год. Близько 10% цефіксиму виводиться із жовчю. Фармакокінетика в особливих клінічних ситуаціях За наявності у пацієнта ниркової недостатності очікується збільшення періоду напіввиведення і, відповідно, вищої концентрації препарату у плазмі та уповільнення його елімінації нирками. У пацієнтів з кліренсом креатиніну 30 мл/хв при прийомі 400 мг цефіксіма період напіввиведення збільшується до 7-8 годин, максимальна концентрація в плазмі становить в середньому 7,53 мкг/мл, а виведення із сечею за 24 год – 5,5%. У пацієнтів із цирозом печінки період напіввиведення зростає до 6,4 год, час досягнення максимальної концентрації (ТСmax) – 5,2 год; одночасно збільшується частка препарату, що елімінується нирками. Сmax та площа під фармакокінетичною кривою не змінюється.ФармакодинамікаЦефіксім – напівсинтетичний антибіотик широкого спектру дії, з групи цефалоспоринів III покоління для вживання. Чинить бактерицидну дію. Механізм дії пов'язаний із пригніченням синтезу клітинної стінки бактерій. Цефіксим стійкий до дії β-лактамаз, що продукуються багатьма грампозитивними та грамнегативними бактеріями. Спектр протимікробної активності В умовах клінічної практики та in vitro ефективність цефіксиму підтверджена при інфекціях, викликаних Streptococcus pneumoniae, Streptococcus pyogenes, Haemophilus influenzae, Moraxella catarrhalis, Escherichia coli, Proteus mirabilis, Neisseria gonorrhoeae. Цефіксім також має активність in vitro проти грампозитивних – Streptococcus agalactiae та грамнегативних бактерій – Haemophilus parainfluenzae, Proteus vulgaris, Klebsiella pneumoniae, Klebsiella oxytoca, Pasteurella multocida, Providencia spp. Salmonella spp. До препарату стійкі Pseudomonas spp., Enterococcus spp., Listeria monocytogenes, більшість штамів Enterobacter spp., Staphylococcus spp. (в т.ч. метицилінорезистентні штами), Bacteroides fragilis, Clostridium spp.Показання до застосуванняІнфекційно-запальні захворювання, спричинені чутливими до препарату мікроорганізмами: стрептококовий тонзиліт та фарингіт; синусити; гострий бронхіт; загострення хронічного бронхіту; гострий середній отит; неускладнені інфекції сечовивідних шляхів; неускладнена гонорея; шигельоз.Протипоказання до застосуванняГіперчутливість до цефіксіму або до компонентів препарату; гіперчутливість до цефалоспоринів або пеніцилінів; не рекомендується для застосування у дітей з хронічною нирковою недостатністю та у дітей з масою тіла менше 25 кг у даній лікарській формі. З обережністю: похилого віку, ниркова недостатність, коліт (в анамнезі), вагітність.Вагітність та лактаціяЗ обережністю при вагітності.Побічна діяПобічні ефекти класифікуються за частотою зареєстрованих випадків: дуже часто: (>10%); часто (1-10%); нечасто (0,1-1%); рідко (0,01-0,1%); дуже рідко (≤0,01%). З боку системи крові та органів кровотворення: Дуже рідко: транзиторна лейкопенія, агранулоцитоз, панцитопенія, тромбоцитопенія або еозинофілія. Відзначалися окремі випадки порушень зсідання крові; Частота невідома: гемолітична анемія. Алергічні реакції: Рідко: алергічні реакції (наприклад: кропив'янка, висипання, мультиформна еритема, свербіж шкіри); Дуже рідко: синдром Лайєлла (токсичний епідермальний некроліз); інші алергічні реакції, пов'язані із сенсибілізацією – лікарська лихоманка, синдром, подібний до сироваткової хвороби, гемолітична анемія та інтерстиціальний нефрит, синдром Стівенса-Джонсона, анафілактичний шок. У деяких пацієнтів відзначалися випадки виникнення синдрому лікарського висипу з еозинофілією та системними проявами. З боку нервової системи: Нечасто: головний біль, запаморочення, дисфорія, неспокій. З боку дихальної системи: Частота невідома: диспное. Реакції з боку травної системи: Часто: біль у животі, порушення травлення, нудота, блювання та діарея; Дуже рідко: псевдомембранозний коліт. З боку гепатобіліарної системи: Рідко: підвищення активності лужної фосфатази та "печінкових" трансаміназ, підвищення концентрації білірубіну в крові; Дуже рідко: окремі випадки гепатиту та холестатичної жовтяниці. З боку сечостатевої системи: Дуже рідко: невелике підвищення концентрації креатиніну та сечовини в крові, гематурія, можливий розвиток гострої ниркової недостатності, що супроводжується тубулоінтерстиціальним нефритом.Взаємодія з лікарськими засобамиБлокатори канальцевої секреції (пробенецид та ін) уповільнюють виведення цефіксиму через нирки, що може призвести до симптомів передозування. Цефіксім знижує протромбіновий індекс, посилює дію непрямих антикоагулянтів. При одночасному застосуванні цефіксиму з карбамазепіном спостерігалося збільшення концентрації останнього у плазмі; у разі доцільно проведення терапевтичного лікарського моніторингу.Спосіб застосування та дозиДля дорослих та дітей з масою тіла понад 50 кг добова доза становить 400 мг на один або два прийоми. Дітям з масою тіла 25-50 кг препарат призначається у дозі 200 мг на добу за один прийом. Таблетку можна проковтнути, запиваючи достатньою кількістю води, або розвести у воді та випити отриману суспензію відразу після приготування. Препарат можна приймати незалежно від їди. Тривалість лікування залежить від характеру перебігу захворювання та виду інфекції. Після зникнення симптомів інфекції та/або лихоманки доцільно продовжувати прийом препарату протягом щонайменше 48-72 годин. Курс лікування при інфекціях дихальних шляхів та ЛОР-органів становить 7-14 днів. При тонзилофарингіті, спричиненому Streptococcus pyogenes, тривалість лікування повинна бути не менше 10 днів. При неускладненій гонореї препарат призначають у дозі 400 мг одноразово. При неускладнених інфекціях нижніх сечових шляхів у жінок препарат може призначатися протягом 3-7 днів, при неускладнених інфекціях верхніх сечових шляхів у жінок – 14 днів. При неускладнених інфекціях верхніх та нижніх сечових шляхів у чоловіків тривалість лікування становить 7-14 днів. При порушенні функції нирок дозу встановлюють залежно від показника кліренсу креатиніну у сироватці. При кліренсі креатиніну 21-60 мл/хв або у пацієнтів, які перебувають на гемодіалізі, рекомендується використовувати інші лікарські форми препарату через необхідність зменшення добової дози на 25%. При кліренсі креатиніну 20 мл/хв і менше або у пацієнтів, які перебувають на перитонеальному діалізі, добову дозу слід зменшити у 2 рази.ПередозуванняПри прийомі дози, що перевищує максимальну добову, можливе збільшення частоти описаних вище дозозалежних побічних ефектів. Лікування: промивання шлунка; проводять симптоматичну та підтримуючу терапію. Гемодіаліз та перитонеальний діаліз не ефективні.Запобіжні заходи та особливі вказівкиБлокатори канальцевої секреції (пробенецид та ін) уповільнюють виведення цефіксиму через нирки, що може призвести до симптомів передозування. Цефіксім знижує протромбіновий індекс, посилює дію непрямих антикоагулянтів. При одночасному застосуванні цефіксиму з карбамазепіном спостерігалося збільшення концентрації останнього у плазмі; у разі доцільно проведення терапевтичного лікарського моніторингу. Вплив на здатність до керування автотранспортом та управління механізмами Досліджень впливу препарату Цефіксім ЕКСПРЕС на здатність керувати транспортними засобами та механізмами не проводилося. У зв'язку з можливими несприятливими ефектами (наприклад, запаморочення), слід бути обережними.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
486,00 грн
0,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
492,00 грн
0,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему.
109,00 грн
99,00 грн
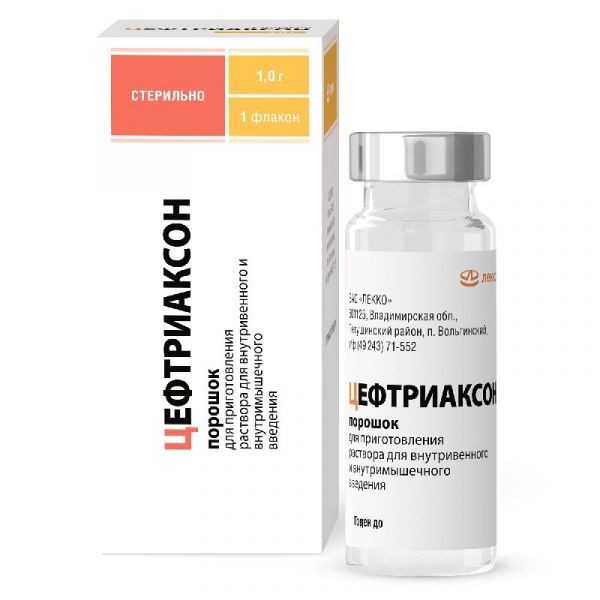
Склад, форма випуску та упаковкаПорошок – 1 гр: Діюча речовина: Цефтріаксон натрію трисесквігідрат у перерахунку на цефтріаксон - 1,0 г.Опис лікарської формиПорошок білого або білого із жовтуватим відтінком кольору.ХарактеристикаЦефтріаксон – арентеральний цефалоспориновий антибіотик III покоління. Бактерицидна активність цефтріаксону обумовлена придушенням синтезу клітинної стінки. Препарат застосовують при інфекціях, спричинених чутливими до цефтріаксону збудниками: сепсис; менінгіті; дисемінованої хвороби Лайма (II та III стадії захворювання); інфекціях органів черевної порожнини (перитоніті, інфекціях жовчних шляхів та шлунково-кишкового тракту); інфекції кісток, суглобів, м'яких тканин, шкіри, а також ранові інфекції; інфекції у хворих з ослабленим імунітетом; інфекціях нирок та сечовивідних шляхів; інфекції дихальних шляхів, особливо пневмонія, та інфекції ЛОР-органів; інфекціях статевих органів, включаючи гонорею, як приопераційну профілактику інфекцій. Випускається у формі порошку для приготування розчину для внутрішньовенного та внутрішньом'язового введення, 1,0 г. Відпускається за рецептом.Фармакотерапевтична групаАнтибіотик-цефалоспоринФармакокінетикаФармакокінетика цефтріаксону має нелінійний характер. Усі основні фармакокінетичні параметри, засновані на загальних концентраціях препарату, за винятком періоду напіввиведення, залежать від дози та зростають менш ніж пропорційно до її збільшення. Нелінійність характерна для фармакокінетичних параметрів, що залежать від загальної концентрації цефтріаксону в плазмі (не тільки вільного цефтріаксону), і пояснюється насиченням зв'язування препарату з білками плазми. Всмоктування. Максимальна концентрація у плазмі після одноразового внутрішньом'язового введення 1 г препарату становить близько 81 мг/л та досягається в межах 2-3 годин після введення. Площі під кривою «концентрація в плазмі – час» після внутрішньовенного та внутрішньом'язового введення однакові. Це означає, що біодоступність цефтріаксону після внутрішньом'язового введення становить 100%. Після внутрішньовенного болюсного введення 500 мг та 1000 мг цефтріаксону середня максимальна концентрація у плазмі крові склала 120 мг/л та 200 мг/л, відповідно. Після внутрішньовенної інфузії 500 мг, 1000 мг, 2000 мг цефтріаксону концентрація препарату в плазмі становить приблизно 80, 150 і 250 мг/л, відповідно. Після внутрішньом'язової ін'єкції значення середньої максимальної концентрації цефтріаксону в плазмі крові приблизно вдвічі нижче,ніж після внутрішньовенного введення еквівалентної дози. Розподіл. Об'єм розподілу цефтріаксону дорівнює 7-12 л. Після введення в дозі 1-2 г, цефтріаксон добре проникає у тканини та рідини організму. Протягом більше 24 годин його концентрації набагато перевищують мінімальні переважні концентрації для більшості збудників інфекцій більш ніж у 60 тканинах та рідинах (у тому числі в легенях, серці, жовчних шляхах, печінці, мигдаликах, середньому вусі та слизовій оболонці носа, кістках, а також спинномозковій). , плевральній та синовіальній рідинах та секреті передміхурової залози). Після внутрішньовенного застосування цефтріаксон швидко проникає у спинномозкову рідину, де бактерицидні концентрації щодо чутливих мікроорганізмів зберігаються протягом 24 годин. Зв'язування із білками. Цефтріаксон оборотно зв'язується з альбуміном. Ступінь зв'язування становить приблизно 95% при значеннях концентрації цефтріаксону у плазмі крові менше 100 мг/л. Частка пов'язаного з білком плазми цефтріаксону зменшується зі зростанням його концентрації, оскільки зв'язування насичуване і становить близько 85 % при значеннях концентрації 300 мг/л. Проникнення до окремих тканин. Цефтріаксон проникає через мозкові оболонки, найбільше при їх запаленні. Середня максимальна концентрація цефтріаксону в спинномозковій рідині досягає 25% від концентрації цефтріаксону в плазмі крові у пацієнтів з бактеріальним менінгітом, і лише 2% у пацієнтів із незапаленими мозковими оболонками. Максимальна концентрація цефтріаксону у спинномозковій рідині досягається через 4-6 годин після внутрішньовенного введення. Цефтріаксон проходить через плацентарний бар'єр та у малих концентраціях потрапляє у грудне молоко. Метаболізм. Цефтріаксон не піддається системному метаболізму, а перетворюється на неактивні метаболіти під дією кишкової мікрофлори. Виведення. Загальний плазмовий кліренс цефтріаксону становить 10-22 мл/хв. Нирковий кліренс дорівнює 5-12 мл/хв. 50-60% цефтріаксону виводиться у незмінному вигляді нирками, а 40-50% – у незміненому вигляді кишечником. Період напіввиведення цефтріаксону становить близько 8 годин. Фармакокінетика в особливих клінічних випадках Новонароджені, грудні діти та діти віком до 12 років. У новонароджених дітей період напіввиведення цефтріаксону збільшено порівняно з іншими віковими групами. У перші 14 днів життя концентрація вільного цефтріаксону в плазмі може бути додатково підвищена через низьку клубочкову фільтрацію та особливості зв'язування препарату з білками плазми. У пацієнтів дитячого віку період напіввиведення менший, ніж у новонароджених та дорослих. Значення плазмового кліренсу та обсягу розподілу загального цефтріаксону вище у новонароджених, немовлят та дітей молодше 12 років порівняно з таким у дорослих. Порушення функції нирок чи печінки. У хворих з порушенням функції нирок або печінки фармакокінетика цефтріаксону змінюється незначною мірою, відзначається лише невелике збільшення періоду напіввиведення (менш ніж у 2 рази) навіть у пацієнтів з тяжкою нирковою недостатністю. Цей процес може пояснюватися компенсаторним підвищенням клеренсу нирок внаслідок зниження ступеня зв'язування з білками плазми крові та відповідного збільшення кліренсу загального цефтріаксону. У пацієнтів із печінковою недостатністю період напіввиведення не збільшується. Таких пацієнтів відбувається компенсаторне підвищення ниркового кліренсу. Причиною також є збільшення концентрації вільного цефтріаксону в плазмі, що сприяє парадоксальному підвищенню загального кліренсу препарату на тлі збільшення обсягу розподілу. Пацієнти похилого віку. У пацієнтів старше 75 років період напіввиведення, в середньому, у два або три рази більший, ніж у дорослих пацієнтів.ФармакодинамікаЦефтріаксон – парентеральний цефалоспориновий антибіотик III покоління. Бактерицидна активність цефтріаксону обумовлена придушенням синтезу клітинної стінки. In vitro цефтріаксон має широкий спектр дії щодо грамнегативних та грампозитивних мікроорганізмів. Він високостійкий до більшості β-лактамаз (як пеніциліназ, так і цефалоспориназ), що виробляються грампозитивними та грамнегативними бактеріями. Цефтріаксон зазвичай активний щодо наступних мікроорганізмів: Грампозитивні аероби: Staphylococcus aureus (метициліночутливий), коагулазо-негативні стафілококи, Streptococcus pyogenes (β-гемолітичний, групи А), Streptococcus agalactiae (β-гемолітичний, групи В), β-гемолітичні стрептококи viridans, Streptococcus pneumoniae. Примітка. Метициліностійкі Staphylococcus spp. резистентні до цефалоспоринів, у тому числі до цефтріаксону. Як правило, Enterococcus faecalis, Enterococcus faecium та Listeria monocytogenes також є стійкими. Грамнегативні аероби: Acinetobacter lwoffii, Acinetobacter anitratus (головним чином, А. baumannii)*, Aeromonas hydrophila, Alcaligenes faecalis, Alcaligenes odorans, алкалігеноподібні бактерії, Borrelia burgdorferi, C. c., Cr. *, Escherichia coli, Enterobacter aerogenes*, Enterobacter cloacae*, Enterobacter spp. (Інші)*, Haemophilus ducreyi, Haemophilus influenzae, Haemophilus parainfluenzae, Hafnia alvei, Klebsiella oxytoca, Klebsiella pneumoniae**, Moraxella catarrhalis (раніше називалася Branhamella catarrhalis), Morapp. (інші), Morganella morganii, Neisseria gonorrhoeae, Neisseria meningitidis, Pasteurella multocida, Plesiomonas shigelloides, Proteus mirabilis, Proteus penneri*, Proteus vulgaris*, Pseudomonas fluorescens*,Pseudomonas spp. (інші) Providencia rettgeri*, Providencia spp. (інші) Salmonella typhi, Salmonella spp. (Нетифоїдні); Serratia marcescens, Serratia spp. (Інші)*, Shigella spp., Vibrio spp., Yersinia enterocolitica, Yersinia spp. (Інші). * Деякі ізоляти цих видів стійкі до цефтріаксону, головним чином, внаслідок утворення β-лактамаз, що кодуються хромосомами. ** Деякі ізоляти цих видів стійкі внаслідок утворення цілого ряду плазмідо-опосередкованих β-лактамаз. Примітка. Багато штами вищевказаних мікроорганізмів, полірезистентні до інших антибіотиків, таких як амінопеніциліни та уреїдопеніциліни, цефалоспорини першого та другого покоління та аміноглікозиди, чутливі до цефтріаксону. Treponema pallidum чутлива до цефтріаксону in vitro та в експериментах на тваринах. Клінічні випробування показують, що цефтріаксон має хорошу ефективність щодо первинного і вторинного сифілісу. За дуже невеликими винятками клінічні ізоляти P. aeruginosa стійкі до цефтріаксону. Анаероби: Bacteroides spp. (жовчочутливі) *, Clostridium spp. (крім С. difficile), Fusobacterium nuсleatum, Fusobacterium spp. (Інші), Gaffkya anaerobica (раніше називалася Peptococcus), Peptostreptococcus spp. *Деякі ізоляти цих видів стійкі до цефтріаксону через утворення β-лактамаз. Примітка. Багато штами β-лактамазоутворюючих Bacteroides spp. (зокрема, B. fFragilis) стійкі. Стійкий і Clostridium difficile. Чутливість до цефтріаксону можна визначати диско-дифузійним методом або методом серійних розведень на агарі або бульйоні, використовуючи стандартну методику, подібну до тієї, яку рекомендує Інститут клінічних та лабораторних стандартів (ІКЛЗ). Для визначення слід брати диски з цефтріаксоном, так як у дослідженнях in vitro показано, що цефтріаксон активний щодо окремих штамів, які виявляють стійкість під час використання дисків, призначених для всієї групи цефалоспоринів. Замість стандартів ІКЛС для визначення чутливості мікроорганізмів можна використовувати інші добре стандартизовані нормативи, наприклад, Німецького інституту стандартизації DIN (Deutsches Institut fur Normung) та міжнародні рекомендації ICS (International Collaborative Study), що дозволяють адекватно інтерпретувати стан чутливості.Показання до застосуванняІнфекції, спричинені чутливими до цефтріаксону збудниками: сепсис; менінгіт; дисемінована хвороба Лайма (II та III стадії захворювання); інфекції органів черевної порожнини (перитоніт, інфекції жовчних шляхів та шлунково-кишкового тракту); інфекції кісток, суглобів, м'яких тканин, шкіри, а також ранові інфекції; інфекції у хворих із ослабленим імунітетом; інфекції нирок та сечовивідних шляхів; інфекції дихальних шляхів, особливо пневмонія, та інфекції ЛОР-органів; інфекції статевих органів, включаючи гонорею. Періопераційна профілактика інфекцій.Протипоказання до застосуванняГіперчутливість. Підвищена чутливість до цефтріаксону та будь-якого іншого компонента препарату. Підвищена чутливість до цефалоспоринів. Тяжкі реакції гіперчутливості (наприклад, анафілактичні реакції) до інших β-лактамних антибіотиків (пеніциліни, монобактами та карбапенеми) в анамнезі. Недоношеним дітям віком до 41 тижня включно (сумарно гестаційний та хронологічний вік) застосування цефтріаксону протипоказане. Доношені новонароджені (≤28-денного віку). Гіпербілірубінемія, жовтяниця або ацидоз, гіпоальбумінемія у новонароджених (дослідження in vitro показали, що цефтріаксон може витісняти білірубін у зв'язку із сироватковим альбуміном, підвищуючи ризик розвитку білірубінової енцефалопатії у таких пацієнтів). Новонароджені (≤ 28 днів), яким вже призначено або передбачається внутрішньовенне лікування кальцієвмісними розчинами, включаючи тривалі кальційвмісні інфузії, наприклад, при парентеральному харчуванні, через ризик утворення преципітатів кальцієвих солей цефтріаксону (див. розділи «Спосіб застосування та дози» та «Взаємодія» з іншими лікарськими засобами»). Описані окремі фатальні випадки утворення преципітатів у легенях та нирках у новонароджених, які отримували цефтріаксон та кальційвмісні розчини.При цьому в окремих випадках був використаний один венозний доступ, і утворення преципітатів спостерігалося безпосередньо в системі внутрішньовенного введення; також описаний, як мінімум, один випадок зі смертельним наслідком при різних венозних доступах і в різний час введення препарату Цефтріаксон і розчинів кальцію. Подібні випадки спостерігалися лише у новонароджених (див. підрозділ «Постреєстраційне спостереження»). Лідокаїн. Перед проведенням внутрішньом'язової ін'єкції цефтріаксону з використанням лідокаїну необхідно виключити наявність протипоказань до лідокаїну. Протипоказання до застосування лідокаїну наведено в інструкції з медичного застосування лідокаїну. Розчини цефтріаксону, що містять лідокаїн, не можна вводити внутрішньовенно. З обережністю: Період грудного вигодовування. Нетяжкі раки гіперчутливості до інших β-лактамних антибіотиків (пеніциліни, монобактами та карбапенеми) в анамнезіВагітність та лактаціяВагітність. Цефтріаксон проникає крізь плацентарний бар'єр. Безпека застосування при вагітності у жінок не встановлена. Доклінічні дослідження репродуктивності не виявили ембріотоксичної, фетотоксичної, тератогенної дії або інших несприятливих ефектів препарату на плодючість самців та самок, процес пологів, перинатальний та постнатальний розвиток плода. При вагітності, особливо у перший триместр, слід призначати лише за суворими показаннями, за умови, що передбачувана користь для матері перевищує потенційний ризик для плода. Період грудного вигодовування. У малих концентраціях цефтріаксон потрапляє до грудного молока. Малоймовірний вплив цефтріаксону на дитину, що перебуває на грудному вигодовуванні, при його застосуванні матір'ю в терапевтичних дозах, проте не можна виключити ризик розвитку діареї, грибкових інфекцій слизових оболонок та реакції гіперчутливості у дитини. Необхідно припинити грудне вигодовування або припинити/утриматися від терапії цефтріаксоном, беручи до уваги переваги грудного вигодовування для дитини та користь терапії для матері.Побічна діяНайчастішими небажаними реакціями, зареєстрованими на тлі терапії цефтріаксоном у клінічних дослідженнях, є еозинофілія, лейкопенія, тромбоцитопенія, діарея, висип та підвищення активності печінкових ферментів. Для опису частоти небажаних реакцій використовується така класифікація: дуже часті (≥ 1/10), часті (≥ 1/100 та < 1/10), нечасті (≥ 1/1000 та < 1/100), рідкісні (≥ 1/10000) та < 1/1000) та дуже рідкісні (< 1/10000), включаючи поодинокі випадки. Небажані реакції згруповані відповідно до класів систем органів медичного словника для нормативно-правової діяльності MedDRA. Інфекційні та паразитарні захворювання: нечасто – мікози статевих органів; рідко – псевдомембранозний коліт. Порушення з боку системи крові та лімфатичної системи: часто – еозинофілія, лейкопенія, тромбоцитопенія; нечасто – гранулоцитопенія, анемія, коагулопатія. Порушення з боку нервової системи: нечасто – головний біль та запаморочення. Порушення з боку дихальної системи, органів грудної клітки та середостіння: рідко – бронхоспазм. Порушення з боку шлунково-кишкового тракту: часто – діарея, неоформлений стілець; нечасто – нудота, блювання. Порушення з боку печінки та жовчовивідних шляхів: часто – підвищення активності печінкових ферментів (аспартатамінотрансферази (АСТ), аланінамінотрансферази (АЛТ), лужної фосфатази (ЩФ)). Порушення з боку шкіри та підшкірних тканин: часто – висип; нечасто - свербіж; рідко – кропив'янка. Порушення з боку нирок та сечовивідних шляхів: рідко – гематурія, глюкозурія. Загальні розлади та порушення у місці введення: нечасто – флебіт, біль у місці введення, підвищення температури тіла; рідко – набряки, озноб. Вплив на результати лабораторних та інструментальних досліджень: нечасто – збільшення концентрації креатиніну в крові. Післяреєстраційне спостереження Нижче описано побічні явища, що спостерігалися при застосуванні цефтріаксону у післяреєстраційному періоді. Визначення частот побічних явищ, що спостерігалися, а також їх зв'язку із застосуванням цефтріаксону, не завжди можливе, тому що неможливо встановити точний розмір популяції пацієнтів. Порушення шлунково-кишкового тракту: панкреатит, стоматит, глосит, порушення смаку. Порушення з боку крові та лімфатичної системи: тромбоцитоз, збільшення тромбопластинового та протромбінового часу, гемолітична анемія. Описано окремі випадки агранулоцитозу Порушення імунної системи: анафілактичний шок, гіперчутливість. Порушення з боку шкіри та підшкірних тканин: гострий генералізований екзантематозний пустульоз, окремі випадки тяжких побічних реакцій (ексудативна мультиформна еритема, синдром Стівенса-Джонсона, токсичний епідермальний некроліз (синдром Лайєла)). Порушення з боку нервової системи: судоми. Порушення з боку органів слуху та лабіринтні порушення: вертиго. Інфекції та паразитарні захворювання: суперінфекції. Відомі також наступні небажані реакції: освіта преципітатів кальцієвих солей цефтріаксону в жовчному міхурі з відповідною симптоматикою, білірубінова енцефалопатія, гіпербілірубінемія, олігурія, вагініт, підвищене потовиділення, «припливи», алергічний пневмонії, анафілактичні або анафілактоїдні реакції. Описано окремі фатальні випадки утворення преципітатів у легенях та нирках за результатами дослідження аутопсії у новонароджених, які отримували цефтріаксон та кальціймісткі розчини. При цьому в окремих випадках був використаний один венозний доступ, і утворення преципітатів спостерігалося безпосередньо в системі внутрішньовенного введення. Також описаний, як мінімум, один випадок зі смертельним наслідком при різних венозних доступах і в різний час введення цефтріаксону та розчинів кальцію. При цьому за результатами дослідження аутопсії у новонародженого преципітати не були виявлені. Подібні випадки спостерігалися лише у новонароджених (див. розділ «Особливі вказівки»). Зареєстровані випадки утворення преципітатів цефтріаксону в сечовивідних шляхах, головним чином, у дітей, які отримували великі добові дози препарату ≥80 мг/кг на добу, або кумулятивні дози більше 10 г, а також мали додаткові фактори ризику (зневоднення, постільний режим). Утворення преципітатів у нирках може протікати безсимптомно або виявлятися клінічно, може проводити до обструкції сечоводів та постренальної гострої ниркової недостатності. Це небажане явище має оборотний характер і зникає після припинення терапії цефтріаксоном. Загальні розлади та порушення у місці введення: флебіт після внутрішньовенного введення. Його можна уникнути, вводячи препарат повільно протягом 5 хвилин, переважно у велику вену. Внутрішньом'язова ін'єкція без застосування лідокаїну болісна. Вплив на результати лабораторних аналізів При лікуванні цефтріаксоном у хворих можуть відзначати хибнопозитивні результати проби Кумбуса, проби на галактоземію, при визначенні глюкози в сечі неферментними методами (у ході терапії цефтріаксоном глюкозурію при необхідності потрібно визначати лише ферментним методом). Цефтріаксон може спричинити недостовірне зниження показників глікемії, отриманих за допомогою деяких пристроїв моніторингу вмісту глюкози в крові. За необхідності слід використовувати альтернативні способи визначення глюкози у крові.Взаємодія з лікарськими засобамиПри одночасному застосуванні великих доз цефтріаксону та петлевих діуретиків (наприклад, фуросеміду) порушень функції нирок не спостерігалося. Є суперечливі дані щодо ймовірності підвищення нефротоксичності аміноглікозидів при їх застосуванні з цефалоспоринами, тому необхідно проводити моніторинг ниркової функції та концентрації аміноглікозидів у крові. Вживання алкоголю після введення цефтріаксону не супроводжувалося дисульфірамоподібною реакцією. Цефтріаксон не містить N-метилтіотетразольної групи, яка могла б викликати непереносимість етанолу та кровоточивість, що властиво деяким іншим цефалоспоринам. Пробенецид не впливає на виведення цефтріаксону. Бактеріостатичні антибіотики знижують бактеріальний ефект цефтріаксону. In vitro було виявлено антагонізм між хлорамфеніколом та цефтріаксоном. Не можна використовувати розчинники,містять кальцій, такі як розчин Рінгера або розчин Хартмана, при приготуванні розчинів цефтріаксону для внутрішньовенного введення та їх подальшого розведення через можливе утворення преципітатів. Утворення преципітатів кальцієвих солей цефтріаксону може відбуватися і при змішуванні цефтріаксону і кальційвмісних розчинів при використанні одного венозного доступу. Не можна використовувати цефтріаксон одночасно з кальційвмісними розчинами для внутрішньовенного введення, у тому числі з тривалими інфузіями кальційвмісних розчинів, наприклад, при парентеральному живленні з використанням Y-конектора. Для всіх груп пацієнтів, крім новонароджених, можливе послідовне введення цефтріаксону та кальційвмісних розчинів при ретельному промиванні інфузійних систем між вливаннями сумісною рідиною.Для оцінки взаємодії цефтріаксону та кальцію проведено два дослідження in vitro: одне з використанням плазми крові дорослої людини, інше – плазми пуповинної крові новонародженого. Були проаналізовані різні комбінації цефтріаксону з вихідною концентрацією до 1 мМ (максимальна концентрація, яку досягає цефтріаксон in vitro при інфузійному введенні 2 г препарату протягом не менше 30 хвилин) та кальцію з вихідною концентрацією до 12 мМ (48 мг/дл). Зниження концентрації цефтріаксону в плазмі спостерігалося при використанні кальцію в концентрації 6 мМ (24 мг/дл) і вище для плазми дорослої людини та в концентрації 4 мМ (16 мг/дл) і вище для плазми новонародженого, що свідчить про підвищений ризик утворення кальцієвих солей. цефтріаксону у новонароджених (див. розділи «Спосіб застосування та дози», «Протипоказання»).Цефтріаксон фармацевтично несумісний з амсакрином, ванкоміцином, флуконазолом та аміноглікозидами. При застосуванні антагоністів вітаміну К на фоні терапії цефтріаксон підвищується ризик кровотечі. Слід постійно контролювати параметри зсідання крові та за необхідності коригувати дозу антикоагулянту як у ході, так і після закінчення терапії цефтріаксоном. Показаний синергізм між цефтріаксоном та аміноглікозидами щодо багатьох грамнегативних бактерій. Незважаючи на те, що підвищена ефективність таких комбінацій не завжди передбачувана, її слід мати на увазі при важких інфекціях, що загрожують життю, таких як обумовлені Pseudomonas aeruginosa.При застосуванні антагоністів вітаміну К на фоні терапії цефтріаксон підвищується ризик кровотечі. Слід постійно контролювати параметри зсідання крові та за необхідності коригувати дозу антикоагулянту як у ході, так і після закінчення терапії цефтріаксоном. Показаний синергізм між цефтріаксоном та аміноглікозидами щодо багатьох грамнегативних бактерій. Незважаючи на те, що підвищена ефективність таких комбінацій не завжди передбачувана, її слід мати на увазі при важких інфекціях, що загрожують життю, таких як обумовлені Pseudomonas aeruginosa.При застосуванні антагоністів вітаміну К на фоні терапії цефтріаксон підвищується ризик кровотечі. Слід постійно контролювати параметри зсідання крові та за необхідності коригувати дозу антикоагулянту як у ході, так і після закінчення терапії цефтріаксоном. Показаний синергізм між цефтріаксоном та аміноглікозидами щодо багатьох грамнегативних бактерій. Незважаючи на те, що підвищена ефективність таких комбінацій не завжди передбачувана, її слід мати на увазі при важких інфекціях, що загрожують життю, таких як обумовлені Pseudomonas aeruginosa.Незважаючи на те, що підвищена ефективність таких комбінацій не завжди передбачувана, її слід мати на увазі при важких інфекціях, що загрожують життю, таких як обумовлені Pseudomonas aeruginosa.Незважаючи на те, що підвищена ефективність таких комбінацій не завжди передбачувана, її слід мати на увазі при важких інфекціях, що загрожують життю, таких як обумовлені Pseudomonas aeruginosa.Спосіб застосування та дозиВнутрішньовенно, внутрішньом'язово. Стандартний режим дозування Дорослі та діти старше 12 років ≥ 50 кг: по 1-2 г один раз на добу (кожні 24 години). У важких випадках або при інфекціях, збудники яких мають лише помірну чутливість до цефтріаксону, добову дозу можна збільшити до 4 г. Тривалість лікування залежить від перебігу захворювання. Як і завжди при антибіотикотерапії, введення препарату Цефтріаксон слід продовжувати хворим ще протягом 48-72 годин після нормалізації температури та підтвердження ерадикації збудника. Зазвичай курс лікування становить 4-14 днів; при ускладнених інфекціях може знадобитися більш тривале введення. Курс лікування при інфекціях, спричинених Streptococcus pyogenes, повинен становити щонайменше 10 днів. Вступ Загальним правилом має бути використання розчинів одразу після приготування. Для внутрішньом'язової ін'єкції 1 г препарату Цефтріаксон розчиняють у 3,5 мл 1 % розчину лідокаїну та вводять глибоко у досить великий м'яз (ягідка). Рекомендується вводити не більше 1 г в один і той же м'яз. Розчин, що містить лідокаїн, не можна вводити внутрішньовенно. Для внутрішньовенної ін'єкції 1 г препарату Цефтріаксон розчиняють у 10 мл стерильної води для ін'єкції; вводять внутрішньовенно повільно протягом 5 хвилин, переважно у велику вену. внутрішньовенна інфузія повинна тривати не менше 30 хвилин. Для приготування розчину розводять 2 г препарату Цефтріаксон у 40 мл одного з наступних інфузійних розчинів, що не містять іонів кальцію: 0,9 % розчин натрію хлориду, 0,45 % розчин натрію хлориду + 2,5 % розчин декстрози, 5 % розчин декстрози, 10% розчин декстрози, 6% розчин декстрану в 5% розчині декстрози, 6-10% розчин гідроксиетилкрохмалю, вода для ін'єкцій. Розчини препарату Цефтріаксон не можна змішувати або додавати до розчинів, що містять інші протимікробні препарати або інші розчинники, за винятком перерахованих вище, через можливу несумісність. Не можна використовувати для приготування розчинів Цефтріаксону для внутрішньовенного введення та їх подальшого розведення розчинники, що містять кальцій, такі як розчин Рінгера або розчин Хартмана, через можливе утворення преципітатів. Утворення преципітатів кальцієвих солей цефтріаксону може відбуватися і при змішуванні препарату та кальційвмісних розчинів при використанні одного венозного доступу. Не можна використовувати цефтріаксон одночасно з кальційвмісними розчинами для внутрішньовенного введення, у тому числі з тривалими інфузіями кальційвмісних розчинів, наприклад, при парентеральному живленні з використанням Y-конектора. Для всіх груп пацієнтів, крім новонароджених,можливе послідовне введення препарату Цефтріаксон та кальційвмісних розчинів при ретельному промиванні інфузійних систем між вливаннями сумісної рідини (див. розділ «Взаємодія з іншими лікарськими засобами»). Не надходило повідомлень про взаємодію цефтріаксону та пероральних кальційвмісних препаратів або взаємодію цефтріаксону для внутрішньом'язового введення та кальційвмісних препаратів (для внутрішньовенного або перорального застосування). Дозування в особливих випадках У хворих із порушенням функції печінки немає необхідності зменшувати дозу за умови відсутності порушень функції нирок. У хворих із порушенням функції нирок немає необхідності зменшувати дозу за умови відсутності порушення функції печінки. Добова доза Цефтріаксону не повинна перевищувати 2 г лише у випадках ниркової недостатності з кліренсом креатиніну менше 10 мл/хв. Цефтріаксон не виводиться при гемодіалізі або перитонеальному діалізі, тому введення пацієнту додаткової дози Цефтріаксону після закінчення діалізу не потрібно. При поєднанні тяжкої ниркової та печінкової недостатності слід ретельно спостерігати за ефективністю та безпекою застосування препарату. Хворі літнього та старечого віку. Зазвичай дози для дорослих без поправок на вік за умови відсутності тяжкої ниркової та печінкової недостатності. Діти Новонароджені, грудні діти та діти молодші 12 років При призначенні препарату Цефтріаксон один раз на добу рекомендується дотримуватись наступних режимів дозування: – новонароджені (до 14 днів): 20-50 мг/кг маси тіла один раз на добу; добова доза повинна перевищувати 50 мг/кг маси тіла; - новонароджені, грудні діти та діти молодшого віку (з 15 днів до 12 років): 20-80 мг/кг маси тіла один раз на добу; - дітям із масою тіла понад 50 кг призначають дози дорослих. Недоношеним дітям віком до 41 тижня включно (сумарно гестаційний та хронологічний вік) застосування цефтріаксону протипоказане. Цефтріаксон протипоказаний новонародженим (≤ 28 днів), яким вже призначено або передбачається внутрішньовенне лікування кальцієвмісними розчинами, включаючи тривалі кальційвмісні інфузії, наприклад, при парентеральному харчуванні через ризик утворення преципітатів кальцієвих солей цефтріаксону (див. розділ «Протипоказання»). Грудним дітям та дітям віком до 12 років внутрішньовенні дози 50 мг/кг або вище слід вводити краплинно протягом не менше 30 хвилин. Новонародженим внутрішньовенне введення слід проводити протягом 60 хвилин, щоб знизити потенційний ризик розвитку білірубінової енцефалопатії. Менінгіт. При бактеріальному менінгіті у немовлят та дітей молодшого віку лікування починають з дози 100 мг/кг (але не більше 4 г) 1 раз на добу. Після ідентифікації збудника та визначення його чутливості дозу можна відповідно зменшити. Найкращі результати при менінгококовому менінгіті досягалися при тривалості лікування в 4 дні, при менінгіті, викликаному Haemophilus influenza – 6 днів, Streptococcus pneumoniae – 7 днів. Хвороба Лайма. 50 мг/кг (вища добова доза – 2 г) дорослим та дітям один раз на добу протягом 14 днів. Гонорея (викликана пеніцилінзоутворюючими та пеніцилінозоутворюючими штамами). Одноразове внутрішньом'язове введення 250 мг препарату Цефтріаксон дорослим пацієнтам та дітям віком від 12 років ≥ 50 кг. Гострий середній отит. При лікуванні гострого середнього отиту у дітей рекомендується одноразове внутрішньом'язове введення дози 50 мг/кг (але не більше 1 г). Дорослим рекомендується одноразове внутрішньом'язове введення в дозі 1-2 г. Згідно з обмеженими даними, у тяжких випадках або при неефективності попередньої терапії препарат Цефтріаксон може бути ефективним при внутрішньом'язовому введенні в дозі 1-2 г на добу протягом 3 днів. Профілактика післяопераційних інфекцій. Залежно від рівня інфекційного ризику вводиться 1-2 г препарату Цефтріаксон одноразово за 30-90 хв до початку операції. При операціях на товстій та прямій кишці добре зарекомендувало себе одночасне (але роздільне, див. підрозділ «Введення») введення препарату Цефтріаксон та одного з 5-нітроімідазолів, наприклад, орнідазолу.ПередозуванняСимптоми: нудота, блювання, діарея. Лікування: симптоматична терапія (специфічного антидоту немає). Гемодіаліз та перитонеальний діаліз неефективні.Умови відпустки з аптекЗа рецептомВідео на цю тему
416,00 грн
356,00 грн
Склад, форма випуску та упаковкаПорошок - 1 мг: Активна речовина: цефуроксим – 750 г. Порошок у скляному флаконі по 750 мг у картонній упаковці.Опис лікарської формиПорошок для приготування розчину для внутрішньовенного і внутрішньом'язового введення: гігроскопічний, від білого до жовтого кольору.Фармакотерапевтична групаБактерицидний, антибактеріальний.ФармакокінетикаПісля внутрішньом'язового введення 750 мг цефуроксиму Сmах (максимальна концентрація) досягається через 15-60 хвилин, вона становить 0,027 мг/мл. Після внутрішньовенного введення 750 і 1500 мг Сmах цефуроксиму досягається через 15 хвилин і становить 0,05 і 0,1 мг/мл відповідно. Час збереження терапевтичної концентрації – 5,3 та 8 годин відповідно. Т1/2 (період напіввиведення) при внутрішньовенному та внутрішньом'язовому введенні знаходиться в діапазоні від 1,3 до 1,5 годин, у новонароджених дітей цей показник більше - 2-2,5 години. Зв'язок із білками плазми становить 33-50%. У печінці не метаболізується. Виводиться нирками 85-90% речовини у незміненому вигляді (канальцевою секрецією та клубочковою фільтрацією) протягом 8 годин (більша частина розчину – за перші 6 годин, при цьому створюються високі концентрації у сечі); через 24 години виводиться у повному обсязі (у співвідношенні 1:1 шляхом канальцевої секреції та клубочкової фільтрації). Цефуроксим у терапевтичній концентрації реєструється у плевральній рідині, мокротинні, жовчі, міокарді, м'яких тканинах та шкірі. Концентрації речовини, які вищі за мінімальну переважну концентрацію для більшості мікроорганізмів, можуть бути досягнуті у внутрішньоочній та синовіальній рідинах, а також у кістковій тканині. Цефуроксим проникає через гематоенцефалічний бар'єр при менінгіті. Проходить через плаценту та проникає у грудне молоко.Цефуроксим проникає через гематоенцефалічний бар'єр при менінгіті. Проходить через плаценту та проникає у грудне молоко.Цефуроксим проникає через гематоенцефалічний бар'єр при менінгіті. Проходить через плаценту та проникає у грудне молоко.ФармакодинамікаПригнічує транспептидазу, порушує біосинтез мукопептиду клітинної стінки мікроорганізмів. Має широкий спектр дії, стабільний у присутності більшості бета-лактамаз, діє на штами, стійкі до ампіциліну та амоксициліну. Активен в отношении аэробных грамположительных микроорганизмов: Staphylococcus aureus (включая пенициллиназы продуцирующие штаммы), Streptococcus pneumoniae, Streptococcus pyogenes и других стрептококков, и аэробных грамотрицательных микроорганизмов: Enterobacter spp., Escherichia coli, Haemophilus influenzae (включая штаммы, вырабатывающие пенициллиназу), Haemophilus parainfluenzae, Klebsiella pneumoniae, Moraxella catarrhalis, Morganella morganii, Neisseria meningitidis, Neisseria gonorrhoeae (в т.ч. пеніциліназ продукуючі штами), Proteus mirabilis, Proteus rettgeri, деякі штами Citrobacter spp., Sal. мікроорганізмів, анаеробів: Clostridium spp.,Peptococcus та Peptostreptococcus spp., Bacteroides, Fusobacterium spp. До цефуроксиму резистентні деякі штами ентерококів, наприклад Enterococcus faecalis, метицилінрезистентні стафілококи. До цефуроксиму не чутливі Pseudomonas spp., Campylobacter spp., Acinetobacter calcoaceticus та більшість штамів Serratia spp. та Proteus vulgaris, деякі штами Morganella morganii, Enterobacter cloacae, Citrobacter spp.Показання до застосуванняІнфекції дихальних шляхів (включаючи пневмонію, бронхіт, абсцес легень, емпієма плеври та ін.), ЛОР-органів (включаючи отит, тонзиліт, синусит, фарингіт та ін.), шкіри та м'яких тканин (включаючи піодермію, рожу, імпет фурункульоз, ранові інфекції, еризипелоїд та ін., сечовивідних шляхів (включаючи цистит, пієлонефрит, бактеріурію, безсимптомну гонорею та ін.), органів малого тазу (включаючи аднексит, ендометрит, цервіцит), суглобів і кісток ( ін.), менінгіт, сепсис, лайм-бореліоз; Операції на органах черевної порожнини, грудної клітки, тазу, суглобів, включаючи операції на стравоході, серці, легенях, судинній хірургії, ортопедичні операції (з профілактичною метою при високому ступені ризику розвитку інфекційних ускладнень);Протипоказання до застосуванняОслаблений/виснажений стан; Хронічна ниркова недостатність; Хвороби шлунково-кишкового тракту, включаючи обтяжений анамнез за неспецифічним виразковим колітом; Кровотечі; період новонародженості, недоношеність; Вагітність та період грудного годування.Вагітність та лактаціяПротипоказано при вагітності та дітям у період новонародженості.Побічна діяЗ боку нервової системи та органів чуття: головний біль, сонливість, зниження слуху. З боку серцево-судинної системи та крові (кровотворення, гемостаз): зниження гемоглобіну та гематокриту, транзиторна еозинофілія, транзиторна нейтропенія та лейкопенія, апластична та гемолітична анемії, тромбоцитопенія, агранулоцитоз, гіпопротромбінем. З боку органів шлунково-кишкового тракту: діарея, нудота, блювання, запор, метеоризм, спазми та біль у животі, диспепсія, виразки в порожнині рота, анорексія, спрага, глосит, псевдомембранозний коліт, транзиторне підвищення активності трансаміназ, ЛФ та ЛГГ , холестаз. З боку сечостатевої системи: порушення функції нирок, підвищення креатиніну та/або азоту сечовини у сироватці крові, зниження кліренсу креатиніну, дизурія, свербіж у промежині, вагініт. Алергічні реакції: висипання, свербіж, кропив'янка, лікарська лихоманка або озноб, сироваткова хвороба, бронхоспазм, багатоформна еритема, інтерстиціальний нефрит, синдром Стівенса-Джонсона, анафілактичний шок. Інші: біль у грудях, укорочення дихання, дисбактеріоз, суперінфекція, кандидоз, у т.ч. кандидоз ротової порожнини, судоми (при нирковій недостатності), позитивний тест Кумбса; місцеві реакції - біль або інфільтрат у місці ін'єкції, тромбофлебіт після внутрішньовенного введення.Взаємодія з лікарськими засобамиКанальцева секреція сповільнюється при одночасному прийомі пероральних форм "петлевих" діуретиків, також відзначається підвищення концентрації антибіотика в крові та зниження ниркового кліренсу. Ризик розвитку невротичних ефектів підвищується при одночасному застосуванні з аміноглікозидами. Цефуроксим несумісний із розчином декстрози, хлориду натрію, Лідокаїну, розчином Рінгера, гепарином, розчином Хартмана.Спосіб застосування та дозиІн'єкції антибактеріального препарату: тричі на день по 750 мг, у тяжких випадках дозу препарату підвищують до 1500, приймають триразово. Оптимальне дозування при більшості інфекцій: 60 мг/кг/добу. Лікування гонореї: внутрішньом'язово 1500 мг одноразово або дозу поділяють на дві ін'єкції. Бактеріальний менінгіт: кожні 8 годин вводять внутрішньовенно по 3 г антибіотика. При оперативних втручаннях внутрішньовенно 1500 мг, потім внутрішньом'язово тричі на добу по 750 мг два дні. При пневмонії внутрішньовенно або внутрішньом'язово 2-3 рази на день по 1500 мг курс лікування 2-3 дні, потім переходять на пероральні форми: двічі на день по 500 мг курс лікування 7-10 днів. Лікування загострення хронічного бронхіту: внутрішньовенно, внутрішньом'язово по 750 мг двічі на день, 2-3 дні. Препарат вводять внутрішньом'язово, внутрішньовенно.ПередозуванняСудоми, збудження нервової системи.Запобіжні заходи та особливі вказівкиУ пацієнтів з алергією на пеніциліни можливий розвиток алергічної відповіді на введення цефалоспоринових антибіотиків. Антибактеріальна терапія потребує контролю за функціонуванням ниркової системи. У період застосування лікарського засобу можлива реєстрація неправдивої реакції Кумбса. Приготовлений розчин зберігають не більше 7 годин при кімнатній температурі, при зберіганні в холодильнику – дві доби. Злегка пожовклий розчин антибіотика вважається придатним для застосування.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
16 528,00 грн
570,00 грн
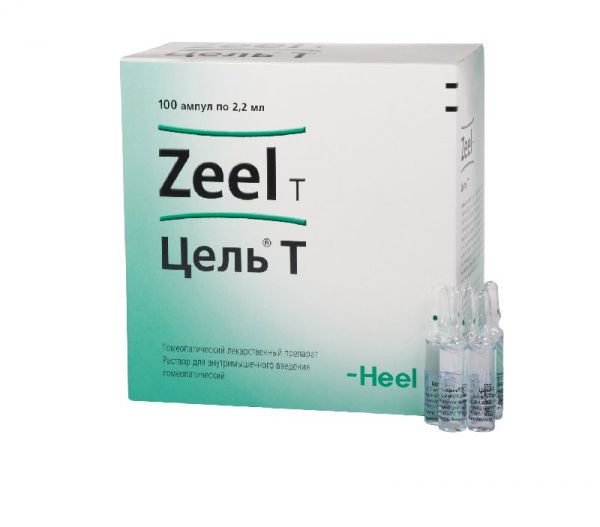
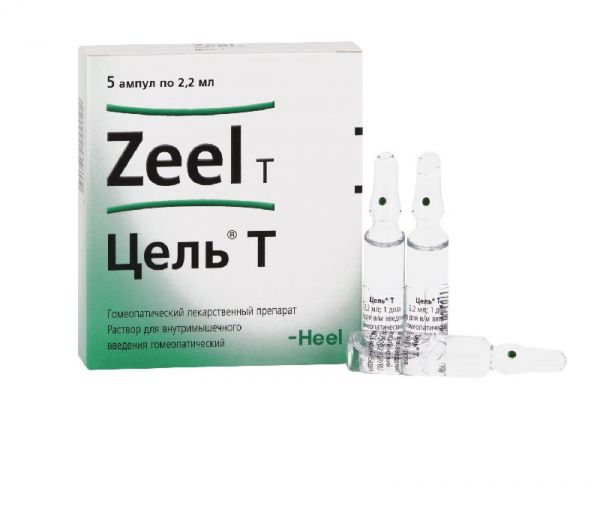
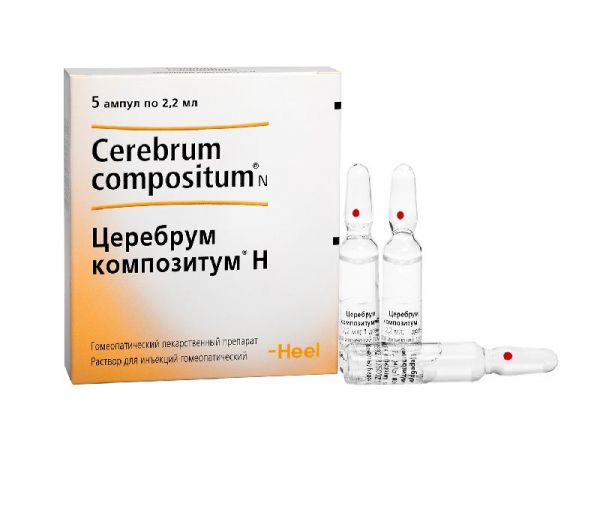
Склад, форма випуску та упаковка(на 1 ампулу 2,2 мл (= 2,2 г)): Активні компоненти: Cartilago suis (Картиляго суіс) D6 2,2 мг, Funiculus umbilicalis suis (Фунікулюс умбілікаліс суіс) D6 2,2 мг, Embryo totalis suis ( Ембріо тоталіс суіс) D6 2,2 мг, Placenta totalis suis (Плацента тоталіс суіс) D6 2,2 мг, Solanum dulcamara (Dulcamara) (Соланум дулькамара (Дулькамара)) D3 11,0 мг, Symphytum officinale (Symphytum officinale (Симфітум)) D6 11,0 мг, Nadidum (Надидум) D8 2,2 мг, Coenzym А (Коензим A) D8 2,2 мг, Sanguinaria canadensis (Sanguinaria) (Сангвінарія канаденсіс (Сангвінаріа)) D4 3,3 мг, Natrium diethyloxalaceticum (Natriumdiethyloxalacetat) (Натріум діетилоксалацетикум (Натріумдіетилоксалацетат)) D8 2,2 мг, Acidum DL-α-liponicum (Acidum α-liponicum) (Ацидум DL-α-ліпонікумToxicodendron quercifolium (Rhus toxicodendron) (Токсикодендрон кверцифоліум (Рус токсикодендрон)) D2 11,0 мг, Arnica montana (Arnica) (Арніка Монтана (Арніка)) D4 220,0 мг, Sulfur (Сульфур) D6 3,96 Допоміжні речовини: хлорид натрію для встановлення ізотонії близько 9 мг/мл, вода для ін'єкцій до 2,2 мл.Опис лікарської формиБезбарвна прозора рідина без запаху.Фармакотерапевтична групаБагатокомпонентний гомеопатичний препарат, дія якого зумовлена компонентами, що входять до його складу.Показання до застосуванняУ комплексній терапії артрозів різної етіології, спондилоартрозів та плечолопаткових періартритів.Протипоказання до застосуванняПідвищена індивідуальна чутливість до компонентів препарату, особливо до токсикодендрону дуболистого та рослин родини айстрових. Вік до 18 років у зв'язку з недостатністю клінічних даних. З обережністю: захворювання печінки, при одноразовому прийомі гепатотоксичних речовин.Вагітність та лактаціяЗастосування препарату можливе, якщо очікувана користь для матері перевищує потенційний ризик для плода та дитини. Потрібна консультація лікаря.Побічна діяМожливі алергічні реакції.У випадках непереносимості токсикодендрону дуболистого (Rhus toxicodendron) та рослини сімейства айстрових (наприклад, арніка) вкрай рідко може розвинутись реакція, що супроводжується підвищенням температури, почервонінням, болем у місці введення ін'єкції. Для лікарських засобів та рецептур, що містять сангвінарію, у літературі описані поодинокі випадки підвищення в крові активності «печінкових» ферментів (трансаміназ) та значень білірубіну. У дуже поодиноких випадках шлунково-кишкові розлади. При виявленні побічних ефектів необхідно припинити прийом препарату та проконсультуватися з лікарем.Взаємодія з лікарськими засобамиПризначення комплексних гомеопатичних препаратів не виключає використання інших лікарських засобів, які застосовуються при цьому захворюванні.Спосіб застосування та дозиЯкщо не призначено інакше, внутрішньом'язово вводити по 2,2 мл (вміст 1 ампули) 2 рази на тиждень. Доза, кратність прийому та тривалість курсу лікування призначається лікарем. Середній курс лікування становить 4-5 тижнів. Проведення повторного курсу можливе після консультації з лікарем.ПередозуванняВипадки передозування досі не були зареєстровані.Запобіжні заходи та особливі вказівкиПри прийомі гомеопатичних лікарських засобів можуть тимчасово загострюватись наявні симптоми (первинне погіршення). У цьому випадку слід припинити прийом препарату та проконсультуватися з лікарем. При появі побічних ефектів, які не описані в інструкції з медичного застосування, слід припинити прийом препарату та повідомити про це лікаря.Умови відпустки з аптекЗа рецептомВідео на цю тему
1 058,00 грн
818,00 грн
Склад, форма випуску та упаковка(на 1 ампулу 2,2 мл (= 2,2 г)): Активні компоненти: Cartilago suis (Картиляго суіс) D6 2,2 мг, Funiculus umbilicalis suis (Фунікулюс умбілікаліс суіс) D6 2,2 мг, Embryo totalis suis ( Ембріо тоталіс суіс) D6 2,2 мг, Placenta totalis suis (Плацента тоталіс суіс) D6 2,2 мг, Solanum dulcamara (Dulcamara) (Соланум дулькамара (Дулькамара)) D3 11,0 мг, Symphytum officinale (Symphytum officinale (Симфітум)) D6 11,0 мг, Nadidum (Надидум) D8 2,2 мг, Coenzym А (Коензим A) D8 2,2 мг, Sanguinaria canadensis (Sanguinaria) (Сангвінарія канаденсіс (Сангвінаріа)) D4 3,3 мг, Natrium diethyloxalaceticum (Natriumdiethyloxalacetat) (Натріум діетилоксалацетикум (Натріумдіетилоксалацетат)) D8 2,2 мг, Acidum DL-α-liponicum (Acidum α-liponicum) (Ацидум DL-α-ліпонікумToxicodendron quercifolium (Rhus toxicodendron) (Токсикодендрон кверцифоліум (Рус токсикодендрон)) D2 11,0 мг, Arnica montana (Arnica) (Арніка Монтана (Арніка)) D4 220,0 мг, Sulfur (Сульфур) D6 3,96 Допоміжні речовини: хлорид натрію для встановлення ізотонії близько 9 мг/мл, вода для ін'єкцій до 2,2 мл.Опис лікарської формиБезбарвна прозора рідина без запаху.Фармакотерапевтична групаБагатокомпонентний гомеопатичний препарат, дія якого зумовлена компонентами, що входять до його складу.Показання до застосуванняУ комплексній терапії артрозів різної етіології, спондилоартрозів та плечолопаткових періартритів.Протипоказання до застосуванняПідвищена індивідуальна чутливість до компонентів препарату, особливо до токсикодендрону дуболистого та рослин родини айстрових. Вік до 18 років у зв'язку з недостатністю клінічних даних. З обережністю: захворювання печінки, при одноразовому прийомі гепатотоксичних речовин.Вагітність та лактаціяЗастосування препарату можливе, якщо очікувана користь для матері перевищує потенційний ризик для плода та дитини. Потрібна консультація лікаря.Побічна діяМожливі алергічні реакції.У випадках непереносимості токсикодендрону дуболистого (Rhus toxicodendron) та рослини сімейства айстрових (наприклад, арніка) вкрай рідко може розвинутись реакція, що супроводжується підвищенням температури, почервонінням, болем у місці введення ін'єкції. Для лікарських засобів та рецептур, що містять сангвінарію, у літературі описані поодинокі випадки підвищення в крові активності «печінкових» ферментів (трансаміназ) та значень білірубіну. У дуже поодиноких випадках шлунково-кишкові розлади. При виявленні побічних ефектів необхідно припинити прийом препарату та проконсультуватися з лікарем.Взаємодія з лікарськими засобамиПризначення комплексних гомеопатичних препаратів не виключає використання інших лікарських засобів, які застосовуються при цьому захворюванні.Спосіб застосування та дозиЯкщо не призначено інакше, внутрішньом'язово вводити по 2,2 мл (вміст 1 ампули) 2 рази на тиждень. Доза, кратність прийому та тривалість курсу лікування призначається лікарем. Середній курс лікування становить 4-5 тижнів. Проведення повторного курсу можливе після консультації з лікарем.ПередозуванняВипадки передозування досі не були зареєстровані.Запобіжні заходи та особливі вказівкиПри прийомі гомеопатичних лікарських засобів можуть тимчасово загострюватись наявні симптоми (первинне погіршення). У цьому випадку слід припинити прийом препарату та проконсультуватися з лікарем. При появі побічних ефектів, які не описані в інструкції з медичного застосування, слід припинити прийом препарату та повідомити про це лікаря.Умови відпустки з аптекЗа рецептомВідео на цю тему
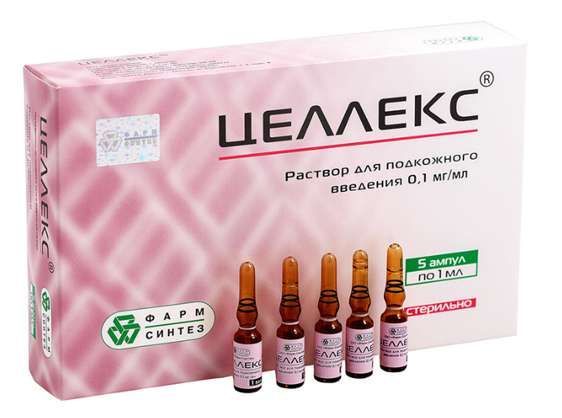
Склад, форма випуску та упаковкаРозчин для підшкірного введення – 1 мл: активна речовина: Целлекс® субстанція-розчин (заморожений у перерахунку на білок) – 0,1 мг; допоміжні речовини: гліцин – 3,75 мг; натрію гідрофосфату дигідрат - 2,99 мг; натрію дигідрофосфату моногідрат - 0,47 мг; натрію хлорид – 5,85 мг; вода для ін'єкцій – до 1 мл; склад активної речовини на 1 мл: активна речовина – поліпептиди з головного мозку ембріонів свиней, у перерахунку на загальний білок – 0,9–2,4 мг (номінальний вміст загального білка – 1,65 мг на 1 мл субстанції); допоміжні речовини – гліцин – 3,75 мг, 0,1М розчин динатрію гідрофосфату – до рН 7,8 (близько 0,8 мг сухої речовини), натрію хлорид – 5,85 мг, полісорбат 80 – 0,005 мг, вода очищена – до 1мл. Розчин для підшкірного введення 0,1 мг/мл. В ампулах темного скла місткістю 1 або 2 мл імпортних, що мають кільце натягу для розтину, або ампулах, що мають точку розлому, 1 або 2 мл. Допускається колірне маркування ампул у вигляді двох зелених смужок. 1, 2, 5 амп. по 1 або 2 мл у контурній комірковій упаковці з плівки ПВХ. 1 або 2 контурні осередкові упаковки в картонній пачці. У кожній пачці стерильні шприцеві фільтри з діаметром пор 0,22 мкм у кількості, що дорівнює кількості ампул.Опис лікарської формиРозчин: прозора безбарвна або світло-жовта рідина без запаху або зі специфічним запахом. Допускається опалесценція. Допускається наявність окремих ниток коагуляту.Фармакотерапевтична групаНейропротективний.ФармакокінетикаСкладний склад препарату Целлекс®, активна фракція якого складається із збалансованої та стабільної суміші біологічно активних білків та поліпептидів, що мають сумарну поліфункціональну дію, не дозволяє провести звичайний фармакокінетичний аналіз окремих компонентів.ФармакодинамікаНаявність тканеспецифічних сигнальних білків і поліпептидів - факторів росту, диференціювання нервових клітин у препараті - обумовлює його пряму нейрорепаративну дію за рахунок регуляції концентрацій пулу нейротрансмітерів з гальмуванням спіловою збудливих амінокислот. Препарат активує вторинну нейропротекцію за рахунок стимуляції процесів синаптогенезу, відновлення сигналів аутофагії, покращення тканинної імунорегуляції з гальмуванням імуногенної цитотоксичності макрофагів. При цьому відзначається тканеспецифічна та системна репаративна дія препарату з відновленням регенеративного та репаративного потенціалу клітин мозку, зменшенням кількості пошкоджених клітин та вираженості перифокального набряку в зоні пенумбри (дозволяє досягти значного обмеження вогнища некрозу мозкової тканини) з відновленням мікроциркуляції та загальної перфузії. Відновлення та регуляторна стимуляція різних компартментів ЦНС із системним впливом факторів зростання, диференціювання та сигнальних молекул забезпечує зниження термінів відновлення та реабілітації пацієнтів з пошкодженнями ЦНС та периферичної нервової системи судинного генезу та відновлення рухової, чутливої та когнітивної функцій. Терапевтичний ефект зазвичай розвивається через 3-5 днів від початку введення препарату.Показання до застосуванняЦереброваскулярні хвороби - гострі порушення мозкового кровообігу в гострому та ранньому реабілітаційному періоді перебігу захворювання, у складі комплексної терапії.Протипоказання до застосуванняепілепсія; маніакальний психоз; продуктивне марення; делірій; вік до 18 років (у зв'язку із недостатністю клінічних даних). З обережністю: алергічні реакції на препарати білково-пептидної природи в анамнезі.Вагітність та лактаціяВідсутність відповідних досліджень не дозволяє застосовувати препарат даного контингенту хворих.Побічна діяМожуть відзначатися алергічні реакції у вигляді невираженої гіперемії у місці введення, реакції гіперчутливості (шкірний висип, свербіж, ангіоневротичний набряк), субфебрилітет, порушення сну, головний біль.Взаємодія з лікарськими засобамиПри сумісному застосуванні з психостимулюючими препаратами та алкоголем можливе психомоторне збудження, порушення сну. Можливе зменшення активності засобів для наркозу, транквілізаторів, нейролептиків.Спосіб застосування та дозиП/к. Дорослі: 0,1-0,2 мг 1 раз на добу підшкірно протягом 10 днів, залежно від тяжкості стану хворого. За потреби проводять повторний курс через 10 днів. Дослідження щодо застосування препарату у дитячій практиці не проводились. Правила введення розчину Препарат вводиться підшкірно через стерильний шприцевий фільтр, що входить до комплекту. Для введення набирають необхідну кількість препарату Целлекс у шприц, знімають голку, потім надягають на шприц стерильний шприцевий фільтр з діаметром пор 0,22 мкм. Беруть нову голку та надягають її на стерильний шприцевий фільтр. Препарат готовий до застосування.ПередозуванняВ даний час випадки передозування препарату Целлекс не відмічені.Запобіжні заходи та особливі вказівкиЗ особливою обережністю призначається при артеріальній гіпертензії злоякісного перебігу на стадії декомпенсації, симпатоадреналових кризах на кшталт панічних атак, виражених тривожно-депресивних розладах. При вагітності дія препарату не вивчена. Препарат не містить пріонові інфекції та віруси. Вплив на здатність керувати транспортними засобами та працювати з механізмами. В даний час немає даних про вплив препарату Целлекс на здатність керувати автомобілем і роботу з механізмами, що вимагають підвищеної уваги і швидкості психічних і рухових реакцій.Умови відпустки з аптекЗа рецептомВідео на цю тему
698,00 грн
0,00 грн
Склад, форма випуску та упаковкаРозчин для внутрішньовенного та внутрішньом'язового введення - 4 мл: активні речовини: цитиколін натрію – 1045 мг (еквівалентно 1000 мг цитиколіну); допоміжні речовини: 1М хлористоводнева кислота або 1М натрію гідроксид - до рН 6,7-7,1; вода для ін'єкцій – до 4 мл. В ампулах нейтрального скла (гідролітичний тип I) із захисною пластиковою трубкою та білою смугою для розлому ампул по 4 мл, у контурній комірковій упаковці 3 ампули; у картонній пачці 1 упаковка або в контурній комірковій упаковці 5 ампул; у картонній пачці 1 або 2 упаковки.Опис лікарської формиПрозора безбарвна рідина.ФармакокінетикаОскільки цитиколін є природною сполукою, яка міститься в організмі, класичне фармакокінетичне дослідження виконати неможливо у зв'язку зі складністю кількісного визначення екзогенного та ендогенного цитиколіну. У фармакокінетичному дослідженні на здорових добровольцях із призначенням внутрішньо міченого С14-цитиколіну спостерігалося практично повне його всмоктування. Протягом 5 днів після призначення дози з фекаліями екскретувалося <1% призначеної дози.ФармакодинамікаЦитиколін, будучи попередником ключових ультраструктурних компонентів клітинної мембрани (переважно фосфоліпідів), володіє широким спектром дії - сприяє відновленню пошкоджених мембран клітин, інгібує дію фосфоліпаз, перешкоджаючи надмірному утворенню вільних радикалів, а також запобігає загибелі клітин, дії на механізм. У гострому періоді інсульту зменшує обсяг пошкодженої тканини, покращує холінергічну передачу. При черепно-мозковій травмі (ЧМТ) зменшує тривалість посттравматичної коми та вираженість неврологічних симптомів. Цитиколін зменшує виразність симптомів, що спостерігаються при гіпоксії, таких як погіршення пам'яті, емоційна лабільність, безініціативність, труднощі при виконанні повсякденних дій та самообслуговуванні. Ефективний у лікуванні когнітивних, чутливих та рухових неврологічних порушень дегенеративної та судинної етіології.Показання до застосуванняЦераксон – ноотропний засіб, ефективний у лікуванні когнітивних, чутливих та рухових неврологічних порушень дегенеративної та судинної етіології. Цераксон застосовується в гострому та відновному періоді ішемічного інсульту, у відновному періоді геморагічного інсульту, у гострому та відновлювальному періоді черепно-мозкової травми, у випадках когнітивних порушень при дегенеративних та судинних захворюваннях головного мозку.Протипоказання до застосуванняЦераксон протипоказаний хворим з ваготонією (переважання тонусу парасимпатичної частини вегетативної нервової системи) та при гіперчутливості до будь-якого з компонентів препарату. Цераксон не застосовується у дітей віком до 18 років.Вагітність та лактаціяУ період вагітності Цераксон призначається, тільки якщо очікувана користь перевершує потенційний ризик. При призначенні Цераксон в період лактації жінкам слід припинити грудне вигодовування. Цераксон не застосовується у дітей віком до 18 років.Побічна діяПри застосуванні Цераксону можливе виникнення алергічних реакцій (висипання, свербіж шкіри, анафілактичний шок), безсоння, головного болю, запаморочення, збудження, тремору, відчуття оніміння в паралізованих кінцівках, нудоти, зниження апетиту, зміна активності печінкових ферментів, жар. У деяких випадках Цераксон може стимулювати парасимпатичну систему, а також надавати короткочасну гіпотензивну дію.Взаємодія з лікарськими засобамиЦитиколін посилює ефекти L-дигідроксифенілаланіну. Не слід призначати одночасно з ЛЗ, що містять меклофеноксат.Спосіб застосування та дозиПрепарат призначають внутрішньовенно або внутрішньом'язово. Внутрішньовенно препарат призначають у формі повільної внутрішньовенної ін'єкції (протягом 3-5 хвилин, залежно від призначеної дози) або краплинного внутрішньовенного вливання (40-60 крапель на хвилину). Внутрішньовенний шлях введення краще, ніж внутрішньом'язовий. При внутрішньом'язовому введенні слід уникати повторного введення препарату в те саме місце. Рекомендований режим дозування Гострий період ішемічного інсульту та черепно-мозкової травми (ЧМТ): 1000 мг кожні 12 годин з першої доби після встановлення діагнозу, тривалість лікування не менше 6 тижнів. Через 3-5 днів від початку лікування (якщо не порушена функція ковтання) можливий перехід на пероральні форми препарату Цераксон. Відновлювальний період ішемічного та геморагічного інсультів, відновлювальний період ЧМТ, когнітивні та поведінкові порушення при дегенеративних та судинних захворюваннях головного мозку: 500-2000 мг на день. Дозування та тривалість лікування залежно від тяжкості симптомів захворювання. Можливе застосування пероральних форм препарату Цераксон. Літні пацієнти При призначенні Цераксону літнім пацієнтам корекції дози не потрібні. Розчин в ампулі призначений для одноразового застосування. Він має бути негайно використаний після розтину ампули. Препарат сумісний з усіма видами внутрішньовенних ізотонічних розчинів та розчинів декстрози.ПередозуванняЗ огляду на низьку токсичність препарату випадки передозування не описані навіть при перевищенні терапевтичних доз.Запобіжні заходи та особливі вказівкиЦитиколін не впливає на здатність до керування транспортними засобами та використання механізмів.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
550,00 грн
0,00 грн
Склад, форма випуску та упаковкаРозчин для внутрішньовенного та внутрішньом'язового введення - 4 мл:Опис лікарської формиПрозора безбарвна рідина.ФармакокінетикаОскільки цитиколін є природною сполукою, яка міститься в організмі, класичне фармакокінетичне дослідження виконати неможливо у зв'язку зі складністю кількісного визначення екзогенного та ендогенного цитиколіну. У фармакокінетичному дослідженні на здорових добровольцях із призначенням внутрішньо міченого С14-цитиколіну спостерігалося практично повне його всмоктування. Протягом 5 днів після призначення дози з фекаліями екскретувалося <1% призначеної дози.Фармакодинамікадопоміжні речовини: 1М хлористоводнева кислота або 1М натрію гідроксид - до рН 6,7-7,1; вода для ін'єкцій – до 4 мл.Показання до застосуванняЦераксон – ноотропний засіб, ефективний у лікуванні когнітивних, чутливих та рухових неврологічних порушень дегенеративної та судинної етіології. Цераксон застосовується в гострому та відновному періоді ішемічного інсульту, у відновному періоді геморагічного інсульту, у гострому та відновлювальному періоді черепно-мозкової травми, у випадках когнітивних порушень при дегенеративних та судинних захворюваннях головного мозку.Протипоказання до застосуванняЦераксон протипоказаний хворим з ваготонією (переважання тонусу парасимпатичної частини вегетативної нервової системи) та при гіперчутливості до будь-якого з компонентів препарату. Цераксон не застосовується у дітей віком до 18 років.Вагітність та лактаціяактивні речовини: цитиколін натрію – 522,5 мг (еквівалентно 500 мг цитиколіну);Побічна діяПри застосуванні Цераксону можливе виникнення алергічних реакцій (висипання, свербіж шкіри, анафілактичний шок), безсоння, головного болю, запаморочення, збудження, тремору, відчуття оніміння в паралізованих кінцівках, нудоти, зниження апетиту, зміна активності печінкових ферментів, жар. У деяких випадках Цераксон може стимулювати парасимпатичну систему, а також надавати короткочасну гіпотензивну дію.Взаємодія з лікарськими засобамиЦитиколін посилює ефекти L-дигідроксифенілаланіну. Не слід призначати одночасно з ЛЗ, що містять меклофеноксат.Спосіб застосування та дозиПрепарат призначають внутрішньовенно або внутрішньом'язово. Внутрішньовенно препарат призначають у формі повільної внутрішньовенної ін'єкції (протягом 3-5 хвилин, залежно від призначеної дози) або краплинного внутрішньовенного вливання (40-60 крапель на хвилину). Внутрішньовенний шлях введення краще, ніж внутрішньом'язовий. При внутрішньом'язовому введенні слід уникати повторного введення препарату в те саме місце. Рекомендований режим дозування Гострий період ішемічного інсульту та черепно-мозкової травми (ЧМТ): 1000 мг кожні 12 годин з першої доби після встановлення діагнозу, тривалість лікування не менше 6 тижнів. Через 3-5 днів від початку лікування (якщо не порушена функція ковтання) можливий перехід на пероральні форми препарату Цераксон. Відновлювальний період ішемічного та геморагічного інсультів, відновлювальний період ЧМТ, когнітивні та поведінкові порушення при дегенеративних та судинних захворюваннях головного мозку: 500-2000 мг на день. Дозування та тривалість лікування залежно від тяжкості симптомів захворювання. Можливе застосування пероральних форм препарату Цераксон. Літні пацієнти При призначенні Цераксону літнім пацієнтам корекції дози не потрібні. Розчин в ампулі призначений для одноразового застосування. Він має бути негайно використаний після розтину ампули. Препарат сумісний з усіма видами внутрішньовенних ізотонічних розчинів та розчинів декстрози.ПередозуванняЗ огляду на низьку токсичність препарату випадки передозування не описані навіть при перевищенні терапевтичних доз.Запобіжні заходи та особливі вказівкиЦитиколін не впливає на здатність до керування транспортними засобами та використання механізмів.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
647,00 грн
589,00 грн
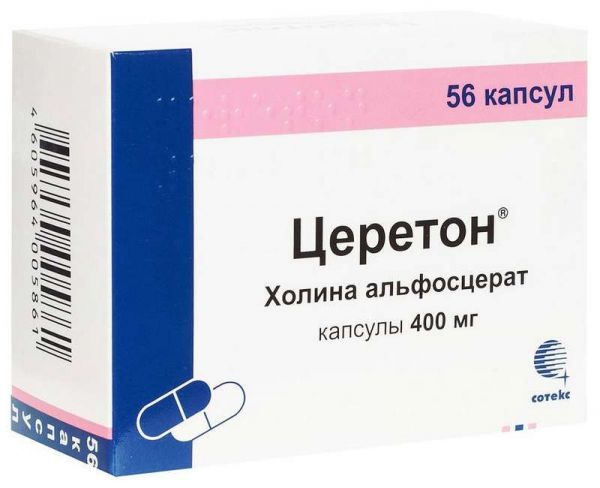
Фасування: N40 Форма випуску таб. Виробник: Клініка Інституту Біорегу Завод-виробник: Клініка Інституту біорег. та геронтології(Росія).
Склад, форма випуску та упаковкаРозчин - 1 мл: Активна речовина: 1 мл водного розчину містить 215,2 мг концентрату церебролізину (комплекс пептидів, отриманих з головного мозку свині). Активна фракція Церебролізину представлена пептидами, молекулярна вага яких не перевищує 10000 дальтон; Допоміжні речовини гідроксид натрію і вода для ін'єкцій. Ампули 1мл, 2мл. По 1 мл, 2 мл у скляні ампули коричневого кольору (відповідно до стандарту DIN-ISO 9187-1-B-1-br; та DIN-ISO 9187-1 -В-2-br відповідно; номінальна місткість 1 мл, 2 мл;тип 1, Євр.Ф.). По 10 ампул поміщають у контурну осередкову упаковку з ПВХ, покриту вощеним папером. Одну контурну осередкову упаковку з інструкцією із застосування поміщають у картонну пачку. Ампули 5мл, 10мл, 20мл. По 5 мл, 10 мл, 20 мл у скляні ампули коричневого кольору (відповідно до стандарту DIN-ISO 9187-1-В-5br, DIN-ISO 9187-1-В-10- br та, DIN-ISO 9187-1 -B-20-br відповідно, поминальна місткість (5 мл, 10 мл, 20 мл; тип 1, Євр.Ф.). По 5 ампул поміщають у контурну осередкову упаковку з ПВХ, покриту вощеним папером. Одну контурну осередкову упаковку з інструкцією із застосування поміщають у картонну пачку. Флакони 30 мл. По 30 мл у флакон із коричневого скла, закупорений гумовою пробкою під алюмінієвою запобіжною обкаткою з отвором для голки в центрі та закритий захисною пластмасовою кришкою (відповідно до стандарту DIN-ISO 8362-4 50Н br-1; номінальна місткість 30; , Євр.Ф.) По 1 або 5 флаконів з інструкцією із застосування поміщають у картонну пачку. Упаковка "in bulk" (для стаціонарів та для розфасовки на ЗАТ "Біоком", Росія): По 10 ампул (1 мл, 2 мл) поміщають у блістер із ПВХ, покритий вощеним папером. По 50 блістерів (1 мл ампули, 2 мл) або 225 блістерів (1 мл ампули) з інструкцією по застосуванню поміщають в картонну коробку. По 5 ампул (5 мл) поміщають у блістер із ПВХ, покритий вощеним папером. По 90 блістерів з інструкцією із застосування поміщають у картонну коробку. По 5 ампул (10 мл) поміщають у блістер із ПВХ, покритий вощеним папером. По 36 блістерів з інструкцією із застосування поміщають у картонну коробку. По 5 ампул (20 мл) поміщають у блістер із ПВХ, покритий вощеним папером. По 20 блістерів з інструкцією із застосування поміщають у картонну коробку.Опис лікарської формиПрозорий розчин янтарного кольору.Фармакотерапевтична групаНоотропний засіб.ФармакокінетикаСкладний склад Церебролізину, активна фракція якого складається із збалансованої та стабільної суміші біологічно активних олігопептидів, що мають сумарну поліфункціональну дію, не дозволяє провести звичайний фармакокінетичний аналіз окремих компонентів.ФармакодинамікаЦеребролізин містить низькомолекулярні біологічно активні нейропептиди, які проникають через гематоенцефалічний бар'єр і безпосередньо надходять до нервових клітин. Препарат має органоспецифічну мультимодальну дію на головний мозок, тобто. забезпечує метаболічну регуляцію, нейропротекцію, функціональну нейромодуляцію та нейротрофічну активність. а) метаболічна регуляція: церебролізин підвищує ефективність аеробного енергетичного метаболізму головного мозку, покращує внутрішньоклітинний синтез білка в старіючим головному мозку. б) нейропротекція: церебролізин захищає нейрони від ушкоджуючої дії лактацидозу, запобігає утворенню вільних радикалів, підвищує виживання та запобігає загибелі нейронів в умовах гіпоксії та ішемії, знижує ушкоджуючу нейротоксичну дію збудливих амінокислот (глутамату). в) нейротрофічна активність: церебролізин – єдиний ноотропний пептидергічний препарат з доведеною нейротрофічною активністю, аналогічною дії природних факторів нейронального росту (NGF), але виявляється в умовах периферичного введення. г) функціональна нейромодуляція: церебролізин позитивно впливає при порушеннях когнітивних функцій, на процеси запам'ятовування.Показання до застосуванняХвороба Альцгеймера, синдром деменції різного генезу, хронічна цереброваскулярна недостатність, ішемічний інсульт, травматичні ушкодження головного та спинного мозку; затримка розумового розвитку у дітей, гіперактивність та дефіцит уваги у дітей; у комплексній терапії – при ендогенній депресії, резистентній до антидепресантів.Протипоказання до застосуванняІндивідуальна непереносимість препарату; гостра ниркова недостатність; Епілептичний статус. З обережністю препарат призначають у І триместрі вагітності та в період лактації.Вагітність та лактаціяУ період вагітності та під час грудного вигодовування Церебролізин слід застосовувати лише після ретельного аналізу співвідношення позитивного ефекту лікування та ризику, пов'язаного з його проведенням. Результати експериментальних досліджень не дають підстав вважати, що Церебролізин має будь-яку тератогенну дію або токсично впливає на плід. Проте аналогічні клінічні дослідження не проводились.Побічна діяЧасті побічні ефекти – понад 1/100 – менше 1/10; рідкісні побічні ефекти – понад 1/1000 – менше 1/100; дуже рідкісні побічні ефекти – понад 1/10000 – менше 1/1000; вкрай рідкісні побічні ефекти менше 1/10000. При надмірно швидкому введенні в поодиноких випадках можливе відчуття жару, пітливість, запаморочення та (в поодиноких випадках) можливе прискорене серцебиття або аритмії. З боку шлунково-кишкового тракту: у поодиноких випадках спостерігалися втрата апетиту, диспепсія, діарея, запори, нудота та блювання. З боку ЦНС і периферичної нервової системи: у поодиноких випадках передбачуваний ефект активації супроводжувався збудженням (проявляється агресивною поведінкою, сплутаністю свідомості, безсонням). Є повідомлення про виникнення у поодиноких випадках ( З боку імунної системи: у вкрай поодиноких випадках відзначалися реакції підвищеної чутливості або алергічні реакції, що проявляються головним болем; больовими відчуттями у шиї, кінцівках, нижній частині спини; задишкою, ознобом та колаптоїдним станом. Місцеві реакції: у поодиноких випадках відзначається почервоніння шкіри, свербіж та печіння у місці ін'єкції. Інші: за результатами досліджень повідомлялося про вкрай рідкісні випадки гіпервентиляції, артеріальної гіпертонії, артеріальної гіпотонії, втоми, тремору, депресії, апатії, запаморочення та грипоподібних симптомів (кашля, нежить, інфекцій дихальних шляхів). Слід врахувати, що деякі небажані ефекти (збудження, артеріальна гіпертонія, артеріальна гіпотонія, млявість, тремор, депресія, апатія, запаморочення, головний біль, задишка, діарея, нудота) були виявлені в ході клінічних випробувань і виникали однаково як у пацієнтів, отримували Церебролізин, і у пацієнтів групи плацебо.Взаємодія з лікарськими засобамиЗ урахуванням фармакологічного профілю Церебролізину, слід приділити особливу увагу можливим адитивним ефектам при спільному призначенні з антидепресантами або інгібіторами МАО. У таких випадках рекомендується зменшити дозу антидепресанту. Не слід змішувати в одному розчині для інфузій Церебролізин та збалансовані розчини амінокислот. Церебролізин несумісний з розчинами, до складу яких входять ліпіди, та з розчинами, що змінюють рН середовища (5,0-8,0).Спосіб застосування та дозиЗастосовується парентерально. Дози та тривалість лікування залежать від характеру та тяжкості захворювання, а також від віку хворого. Можливе призначення одноразових доз, величина яких може досягати 50 мл, проте краще здійснення курсу лікування. Рекомендований оптимальний курс лікування є щоденними ін'єкціями протягом 10-20 днів. Гострі стани (ішемічний інсульт, черепномозкова травма, ускладнення нейрохірургічних операцій): від 10 мл до 50 мл. У резидуальному періоді мозкового інсульту та травматичного ушкодження головного та спинного мозку: від 5 мл до 50 мл. При психоорганічному синдромі та депресії: від 5 мл до 30 мл. При хворобі Альцгеймера, деменції судинного та поєднаного альцгеймерівсько-судинного генезу: від 5 мл до 30 мл. У нейропедіатричній практиці: 0,1-0,2 мл/кг ваги. Для підвищення ефективності лікування можуть бути проведені повторні курси, поки спостерігається поліпшення стану пацієнта внаслідок лікування. Після першого курсу періодичність призначення доз може бути знижена до 2 або 3 разів на тиждень. Церебролізин застосовують у вигляді ін'єкцій: внутрішньом'язово (до 5 мл) та внутрішньовенно (до 10 мл). Дози від 10 мл до 50 мл рекомендується вводити лише за допомогою повільних внутрішньовенних інфузій після розведення запропонованими стандартними розчинами для інфузій. Тривалість інфузії становить від 15 до 60 хвилин.ПередозуванняНе виявлено.Запобіжні заходи та особливі вказівкиПри надмірно швидкому виконанні ін'єкцій можливе відчуття жару, пітливість, запаморочення. Тому препарат слід вводити повільно. Перевірено та підтверджено сумісність препарату (протягом 24 годин при кімнатній температурі та наявності освітлення) з наступними стандартними розчинами для інфузій: 0,9% розчин натрію хлориду (9 мг NaCl/мл). Розчин Рінгера (Na+ - 153,98 ммоль/л; Са2+ - 2,74 ммоль/л; К+ - 4,02 ммоль/л; СГ - 163,48 ммоль/л). 5% розчин глюкози. Допускається одночасне призначення Церебролізину з вітамінами та препаратами, що покращують серцевий кровообіг, проте ці препарати не слід змішувати в одному шприці із Церебролізином. Використовувати лише прозорий розчин і лише одноразово. Вплив на здатність до керування автотранспортом та управління механізмами Клінічні випробування показали, що Церебролізин не впливає на здатність керувати транспортними засобами та використання механізмів.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаФосфатидилсерін; Фосфатидилхолін; Інозитол; Диметилгліцин Гідрохлорид; Гінкго білоба (екстракт); Вітамін В2(рібофлавін); Вітамін В6 (піридоксин); Вітамін Bj (тіамін); Вітамін В12 (ціанокобаламін); Фолієва кислота. Картонні коробки 2 блістери по 15 таблеток.Фармакотерапевтична групаНоотроп, ангіопротектор, коректор мікроциркуляції, антиагрегант.Властивості компонентівРегулює нервові процеси, у тому числі процеси розподілу та зростання нервових клітин. Активує метаболізм глюкози в головному мозку та підвищує стійкість нервових клітин до ішіємічного ушкодження. Фосфатидилсерин перешкоджає руйнуванню клітин головного мозку макрофагами, пригнічуючи їхню фагоцитарну активність, проходить через гематоенцефалічний бар'єр і надходить безпосередньо в мозкову тканину через кілька хвилин після прийому всередину. Стимулює синтез ацетилхоліну та активізує холінергічні процеси в головному мозку. Тим часом, зниження вироблення ацетилхоліну є одним із закономірних явищ при хворобі Альцгеймера та інших видах старечого недоумства. Вікове зниження розумових функцій відбувається паралельно зі зменшенням фосфатидилсерину в мозку. Покращує пам'ять, здатність до навчання, знімає пригнічений настрій,стимулює загальну активність, призводить до значних зрушень у запам'ятовуванні інформації, обсяг пам'яті. Екстракт Гінкго Білоба містить більше 40 інгредієнтів, основними з яких є флавоноїдні глікозиди (24%) і терпенові сполуки (6%). Екстракт Гінкго Білоба перешкоджає спазму артерій, зменшує проникність капілярів, нормалізуючи їх тонус, викликає чітке збільшення як мозкового, так і периферичного кровообігу в артеріальному, капілярному та венозному руслі; зменшує тенденції до небезпечної освіти згустків або тромбів у венах та артеріях. Маючи особливу спорідненість до ЦНС, надниркових залоз і щитовидної залози, екстракт ідеально підходить як засіб, що захищає серце,кровоносні судини і мозок від руйнівної дії вільних радикалів (на ряді експериментальних моделей показано, що екстракт інгібує вільні радикали та інактивує їх утворення, тобто має антиоксидантні властивості). На моделях експериментальної ішемії та гіпоксії встановлено, що екстракт збільшує споживання мозком кисню та глюкози, підвищує вміст АТФ у корі головного мозку, стимулює мозкову діяльність. Вітамін В2 (рибофлавін) багато в чому забезпечує функціонування центральної нервової системи; крім того, бере участь в обміні білків, жирів, вуглеводів; також рибофлавін дуже бере активну участь у клітинному диханні; при недостатності вітаміну В2, неможливе нормальне кровотворення. Вітамін В2 бере участь у захисній реакції організму при запальних процесах. Вітамін В6 (піридоксин) бере участь у білковому обміні; цей вітамін також впливає на біохімічні процеси у м'язах при їх скороченні. Вітамін В посилює імунітет і за його відсутності неможлива нормальна робота нервової системи. Вітамін В12 (ціанокобаламін) вкрай необхідний для зростання та поділу клітин; також цей вітамін бере участь у синтезі ДНК та РНК. При нестачі ціанокобаламіну в організмі неможливе нормальне кровотворення – зокрема порушується утворення еритроцитів та тромбоцитів. Вітамін В істотно впливає на обмін білків, жирів, вуглеводів, позитивно впливає на роботу печінки та центральної нервової системи. Фолієва кислота (вітамін В9) необхідний для зростання та розвитку кровоносної та імунної системи. Нестача фолієвої кислоти може спричинити мегалобластну анемію у дорослих. Фолієва кислота необхідна для зростання та розвитку молодих здорових клітин, тому її наявність особливо важлива у періоди швидкого розвитку організму. Процес реплікації ДНК потребує участі фолієвої кислоти. Порушення цього процесу збільшує ризик розвитку ракових пухлин. Насамперед від нестачі фолієвої кислоти страждає кістковий мозок, у якому відбувається активне розподіл клітин. Клітини-попередники червоних кров'яних тілець (еритроцитів), що утворюються в кістковому мозку, при дефіциті фолієвої кислоти збільшуються у розмірі, утворюючи так звані мегалобласти і призводять до мегалобластної анемії.ФармакодинамікаФосфатидилсерин є одним із високоефективних натуральних нейрометаболічних засобів. Фосфатидилсерин міститься у мембранах всіх клітин тіла, у своїй найбільші концентрації фосфатидилсерина спостерігаються у нервових клітинах. Він відіграє ключову фізіологічну роль у диференціюванні нейронів, процесах активації, регенерації, синтезу та вивільнення нейромедіаторів (ацетилхоліну та ін), русі іонів та проведенні біоелектричного струму.РекомендуєтьсяЯк біологічно активну добавку до їжі - додаткового джерела вітамінів В1, В2, В6, В12, фолієвої кислоти, джерела флавоноїдів, інозиту.Протипоказання до застосуванняГіперчутливість; дитячий вік до 8 років.Побічна діяДуже рідко диспепсичні розлади, біль голови, запаморочення, алергічні реакції.Спосіб застосування та дозиПри самостійному застосуванні споживачем рекомендується дотримуватися норм, зазначених на упаковці. Якщо препарат призначається лікарем, можлива зміна дозування. При порушеннях середнього ступеня по одній таблетці 1 раз на день, при порушеннях тяжкого ступеня по одній таблетці 2-3 рази на день внутрішньо, під час або після їди. Курс лікування 1-2 місяці.Запобіжні заходи та особливі вказівкиПеред застосуванням проконсультуйтеся зі спеціалістом.Умови відпустки з аптекБез рецептаВідео на цю тему
1 236,00 грн
0,00 грн
Склад, форма випуску та упаковка(на одну ампулу 2,2 мл (=2,2 г)): Активні компоненти: Cerebrum suis (церебрум суїс) D8 22 мкл, Embryo totalis suis (ембріо тоталіс суїс) D10 22 мкл, Hepar suis (гепар суїс) D10 22 мкл, Placenta totalis suis (плацента тоталіс суіс) D10 22 мкл мкл, Bothrops lanceolatus (ботропс ланцеолятус) D10 22 мкл, Ac2um 22 мкл Gelsemium sempervirens (гельсеміум семпервіренс) D4 22 мкл, Ruta graveolens (рута гравеоленс) D4 22 мкл, Arnica montana (арніка монтана) D28 22 мкл,Aesculus hippocastanum (ескулюс гіпокаштанум) D4 22 мкл, Manganum phosphoricum (манганум фосфорикум) D8 22 мкл, Magnesium phosphoricum (магнезіум фосфорикум) D10 22 мкл, Semecarpus anacardium 2 Medorrhinum-Nosode (медорринум-Нозоде) D13 22 мкл, Hyoscyamus niger (гіосціамус нігер) D6 22 мкл, Aconitum napellus (аконітум напеллус) D6 22 мкл, Anamirta cocculus (анамірта коккулюса D2 мкл; допоміжні речовини: хлорид натрію qs для встановлення ізотонії близько 9 мг/мл, вода для ін'єкцій до 2,2 мл.Medorrhinum-Nosode (медорринум-Нозоде) D13 22 мкл, Hyoscyamus niger (гіосціамус нігер) D6 22 мкл, Aconitum napellus (аконітум напеллус) D6 22 мкл, Anamirta cocculus (анамірта коккулюса D2 мкл; допоміжні речовини: хлорид натрію qs для встановлення ізотонії близько 9 мг/мл, вода для ін'єкцій до 2,2 мл.Medorrhinum-Nosode (медорринум-Нозоде) D13 22 мкл, Hyoscyamus niger (гіосціамус нігер) D6 22 мкл, Aconitum napellus (аконітум напеллус) D6 22 мкл, Anamirta cocculus (анамірта коккулюса D2 мкл; допоміжні речовини: хлорид натрію qs для встановлення ізотонії близько 9 мг/мл, вода для ін'єкцій до 2,2 мл.Опис лікарської формиБезбарвна прозора рідина без запаху.Фармакотерапевтична групаБагатокомпонентний гомеопатичний препарат, дія якого зумовлена компонентами, що входять до його складу.Показання до застосуванняЕнцефалопатія різного генезу (розлад пам'яті, уваги); стимуляція процесів регенерації та неспецифічного імунітету.Протипоказання до застосуванняПідвищена індивідуальна чутливість до компонентів препарату. Відома підвищена чутливість до хініну. Діти віком до 18 років у зв'язку з недостатністю клінічних даних.Вагітність та лактаціяЗастосування препарату можливе, якщо очікувана користь для матері перевищує потенційний ризик для плода та дитини. Потрібна консультація лікаря.Побічна діяМожливі алергічні реакції, зокрема шкірні алергічні реакції. За відомої індивідуальної чутливості до рослин сімейства складноцвітих можуть виникати реакції підвищеної чутливості (зокрема анафілактична реакція). Тимчасова поява почервоніння, припухлості та болю у місці ін'єкції. У дуже рідкісних випадках після прийому препаратів, що містять хінін, можуть спостерігатися шкірні алергічні реакції або гарячкові стани (реакції гіперчутливості). При появі побічних ефектів слід припинити прийом препарату та проконсультуватися з лікарем.Взаємодія з лікарськими засобамиПризначення комплексних гомеопатичних препаратів не виключає використання інших лікарських засобів, які застосовуються при цьому захворюванні.Спосіб застосування та дозиВнутрішньом'язово, внутрішньошкірно, підшкірно по 1 ампулі 1-3 рази на тиждень. Курс лікування – 4-6 тижнів. Можливі повторні курси лікування після погодження з лікарем.ПередозуванняВипадки передозування досі не були зареєстровані.Запобіжні заходи та особливі вказівкиПри прийомі гомеопатичних лікарських засобів можуть тимчасово загострюватись наявні симптоми (первинне погіршення). У цьому випадку слід припинити застосування препарату і звернутися до лікаря.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаКапсули - 1 капс. активна речовина: гліцерилфосфорілхолін гідрат (холіну альфосцерат) – 400 мг; допоміжні речовини: гліцерол (гліцирин), вода очищена; оболонка капсули: желатин медичний, гліцерол (гліцерин), метилпарагідроксибензоат (метилпарабен), пропілпарагідроксибензоат (пропілпарабен), барвник заліза оксид червоний, титану діоксид, вода очищена, сорбітол (сорбіт). Капсули 400 мг: по 10 або 14 капсул у контурне осередкове впакування. По 10 або 14 капсул у банку світлозахисного скла. Кожну банку або 1 або 2 контурні осередкові упаковки по 14 капсул, або 1 або 3 контурні осередкові упаковки по 10 капсул разом з інструкцією із застосування в пачку з картону.Опис лікарської формиКапсули м'які желатинові, довгастої форми, від червоного до коричневого кольору. Вміст капсул – масляниста, прозора, безбарвна або злегка забарвлена рідина.Фармакотерапевтична групаНоотропний засіб.ФармакокінетикаАбсорбція – 88%, легко проникає через гематоенцефалічний бар'єр (при пероральному прийомі концентрація у мозку – 45% від такої у плазмі). Виводиться переважно легкими, у вигляді діоксиду вуглецю (85%), а також нирками та через кишечник (15%).ФармакодинамікаЦентральний холіностимулятор, у складі якого міститься 40,5% метаболічно захищеного холіну (метаболічний захист сприяє виділенню холіну в головному мозку). При попаданні в організм розщеплюється під дією ферментів на холін та гліцерофосфат: холін бере участь у біосинтезі ацетилхоліну – одного з основних медіаторів нервового збудження; Гліцерофосфат є попередником фосфоліпідів (фосфатидилхоліну) нейронної мембрани. Забезпечує синтез ацетилхоліну та фосфатидилхоліну в нейрональних мембранах, покращує кровотік та посилює метаболічні процеси в центральній нервовій системі, активує ретикулярну формацію. Збільшує лінійну швидкість кровотоку за травматичного ураження мозку, сприяє нормалізації просторово-часових характеристик спонтанної біоелектричної активності мозку;надає позитивний вплив на пізнавальні та поведінкові реакції хворих із судинними захворюваннями головного мозку. Покращує функції мозку, впливаючи на патогенетичні фактори інволюційного психоорганічного синдрому, змінює фосфоліпідний склад мембран нейронів та знижує холінергічну активність. Дозозалежно стимулює виділення ацетилхоліну; беручи участь у синтезі фосфатидилхоліну (мембранного фосфоліпіду), покращує синаптичну передачу, пластичність нейрональних мембран, функцію рецепторів. Не впливає на репродуктивний цикл і не має тератогенної та мутагенної дії.Показання до застосуванняГострий та відновлювальний періоди важкої черепно-мозкової травми та ішемічного інсульту, відновлювальний період геморагічного інсульту, що протікають із осередковою півкульною симптоматикою або симптомами ураження стовбура мозку; хронічна недостатність мозкового кровообігу; когнітивні розлади (порушення розумової функції, пам'яті, сплутаність свідомості, дезорієнтація, зниження мотивації, ініціативності та здатності концентрації уваги) у тому числі при деменції та енцефалопатії; стареча псевдомеланхолія; психоорганічний синдром на тлі дегенеративних та інволюційних змін мозку.Протипоказання до застосуванняГіперчутливість, вагітність, грудне вигодовування.Побічна діяАлергічні реакції, нудота (внаслідок допамінергічної активації).Взаємодія з лікарськими засобамиНе виявлено.Спосіб застосування та дозиПри гострих станах: внутрішньом'язово або внутрішньовенно (повільно) по 1,0 г (1 ампула) на добу протягом 10-15 днів, потім переходять на прийом капсул внутрішньо по 0.8 г (2 капсули) вранці та 0.4 г (1 капсула) вдень протягом 6 місяців. При хронічних станах: внутрішньо по 0,4 г (1 капсула) 3 рази на добу, переважно до їди. Тривалість лікування становить 3-6 місяців.ПередозуванняСимптоми: диспептичні розлади. Лікування: промивання шлунка, прийом активованого вугілля, симптоматична терапія.Запобіжні заходи та особливі вказівкиПри виникненні нудоти після застосування препарату слід зменшити дозу. Церепро не впливає на швидкість психомоторних реакцій.Умови відпустки з аптекЗа рецептомВідео на цю тему
558,00 грн
0,00 грн
Склад, форма випуску та упаковкаРозчин – 1 амп.: діюча речовина: цитиколін натрію 522,5 мг (у перерахунку на цитиколін 500 мг); допоміжні речовини: натрію гідроксиду розчин 1 М або хлористоводневої кислоти розчин 1 М (до pH 6,5-7,1); вода для ін'єкцій до 4мл. Розчин для внутрішньовенного та внутрішньом'язового введення 125 мг/мл. По 4 мл ампули для лікарських засобів, виготовлені з медичного скла марок НС-1 або НС-3 або 1-го гідролітичного класу. По 3, 5 або 10 ампул в контурне осередкове впакування з полівінілхлоридної плівки. По 1 контурній комірковій упаковці по 3 ампули або по 1, 2 контурних коміркових упаковки по 5 ампул або по 1 контурній комірковій упаковці по 10 ампул разом з інструкцією по застосуванню поміщають в пачку з картону.Опис лікарської формиПрозорий безбарвний розчин (дозування 125 мг/мл).Фармакотерапевтична групаНоотропний засіб.ФармакокінетикаВсмоктування. Цитиколін добре абсорбується при внутрішньовенному та внутрішньом'язовому введенні. Метаболізм. При внутрішньовенному та внутрішньом'язовому введенні цитиколін метаболізується у печінці з утворенням холіну та цитидину. Після введення, концентрації холіну в плазмі істотно підвищуються. Розподіл. Цитиколін значною мірою розподіляється у структурах головного мозку, з швидким впровадженням фракцій холіну у структурні фосфоліпіди та фракції цитидину – у цитидинові нуклеотиди та нуклеїнові кислоти. Цитиколін проникає у головний мозок і активно вбудовується у клітинні, цитоплазматичні та мітохондріальні мембрани, утворюючи частину фракції структурних фосфоліпідів. Виведення. Тільки 15% введеної дози цитиколіну виводиться із організму людини; менше 3% - нирками і через кишечник і близько 12% - з видихається СО2. В екскреції цитиколін з сечею можна виділити 2 фази: перша фаза, що триває близько 36 годин, в ході якої швидкість виведення швидко знижується, і друга фаза, в ході якої швидкість екскреції знижується набагато повільніше. Те ж саме спостерігається у видихуваному СО2 - швидкість виведення швидко знижується приблизно через 15 годин, а потім знижується набагато повільніше.ФармакодинамікаЦитиколін, будучи попередником ключових ультраструктурних компонентів клітинної мембрани (переважно фосфоліпідів), володіє широким спектром дії - сприяє відновленню пошкоджених мембран клітин, інгібує дію фосфоліпаз, перешкоджає надмірному утворенню вільних радикалів, а також запобігає загибелі клітин, впливу на механізм. В гострому періоді інсульту цитиколін зменшує об'єм ураження тканини головного мозку, покращує холінергічну передачу. При черепно-мозковій травмі зменшує тривалість посттравматичної коми та вираженість неврологічних симптомів, крім цього, сприяє зменшенню тривалості відновлювального періоду. При хронічній гіпоксії головного мозку цитиколін ефективний у лікуванні когнітивних розладів, таких як погіршення пам'яті, безініціативність, складнощі, що виникають при виконанні повсякденних дій та самообслуговуванні. Підвищує рівень уваги та свідомості, а також зменшує прояв амнезії. Цитиколін ефективний у лікуванні чутливих та рухових неврологічних порушень дегенеративної та судинної етіології.Показання до застосуванняГострий період ішемічного інсульту (у складі комплексної терапії); відновлювальний період ішемічного та геморагічного інсультів; черепно-мозкова травма (ЧМТ), гострий (у складі комплексної терапії) та відновлювальний період; когнітивні та поведінкові порушення при дегенеративних та судинних захворюваннях головного мозку.Протипоказання до застосуванняНе слід призначати хворим з вираженою ваготонією (переважання тонусу парасимпатичної частини вегетативної нервової системи) та при гіперчутливості до будь-якого з компонентів препарату. У зв'язку з відсутністю достатніх клінічних даних не рекомендується застосовувати у дітей віком до 18 років.Вагітність та лактаціяДостатніх даних щодо застосування цитиколіну у вагітних жінок відсутні. Хоча у дослідженнях на тварин негативного впливу не виявлено, у період вагітності лікарський препарат Цересил® Канон призначають лише у випадках, коли очікувана користь для матері перевершує потенційний ризик для плода. При призначенні препарату Цересіл Канон в період лактації жінкам слід припинити грудне вигодовування, оскільки дані про виділення цитиколіну з жіночим молоком відсутні.Побічна діяЧастота несприятливих побічних реакцій: дуже рідкісні (менше 1/10 000, включаючи індивідуальні випадки) Алергічні реакції: висипання, свербіж шкіри, анафілактичний шок. Інші: почуття жару, набряки, задишка. З боку ЦНС та периферичної нервової системи: безсоння, головний біль, запаморочення, тремор, оніміння в паралізованих кінцівках, стимуляція парасимпатичної нервової системи. Порушення психіки: галюцинації, збудження. Серцево-судинна система: короткочасна зміна артеріального тиску. З боку травної системи: нудота, зниження апетиту, блювання, діарея; зміна активності печінкових ферментів. Якщо будь-які з побічних ефектів, що зазначені в інструкції, посилюються, або були помічені будь-які інші побічні ефекти, не зазначені в інструкції, слід повідомити про це лікаря.Взаємодія з лікарськими засобамиЦитиколін посилює ефекти леводопи. Не слід застосовувати одночасно з лікарськими засобами, що містять меклофеноксат.Спосіб застосування та дозиПрепарат призначають внутрішньовенно або внутрішньом'язово. внутрішньовенно препарат призначають у формі повільної внутрішньовенної ін'єкції (протягом 3-5 хв, залежно від призначеної дози) або краплинного внутрішньовенного вливання (40-60 крапель на хвилину). Внутрішньовенний шлях введення краще, ніж внутрішньом'язовий. При внутрішньом'язовому введенні слід уникати повторного введення препарату в те саме місце. Рекомендований режим дозування Гострий період ішемічного інсульту та черепно-мозкової травми (ЧМТ)\ 1000 мг кожні 12 год з першої доби після встановлення діагнозу, тривалість лікування не менше 6 тижнів. Через 3-5 днів після початку лікування (якщо не порушена функція ковтання) можливий перехід на пероральні форми препарату Цересіл Канон Відновлювальний період ішемічного та геморагічного інсультів, відновлювальний період ЧМТ, когнітивні та поведінкові порушення при дегенеративних та судинних захворюваннях головного мозку: 500-2000 мг на день. Дозування та тривалість лікування залежно від тяжкості симптомів захворювання. Можливе застосування пероральних форм препарату Цересіл Канон. При підозрі на внутрішньочерепну кровотечу, що триває, рекомендується не перевищувати дозу препарату Цересил® Канон 1000 мг на добу, препарат вводять внутрішньовенно краплинно зі швидкістю 30 крапель на хвилину. Літні пацієнти При призначенні препарату Цересіл Канон літнім пацієнтам корекція дози не потрібна. Розчин в ампулі призначений для одноразового застосування. Він має бути негайно використаний після розтину ампули. Препарат сумісний з усіма видами внутрішньовенних ізотонічних розчинів та розчинів декстрози.ПередозуванняЗ огляду на низьку токсичність препарату випадки передозування не описані.Запобіжні заходи та особливі вказівкиПрепарат Цересил Канон вводиться внутрішньовенно струминно повільно (3-5 хв залежно від дози). При внутрішньовенному краплинному введенні швидкість інфузії має бути 40-60 крапель на хвилину. При персистуючому внутрішньовенному крововиливі рекомендується не перевищувати дозу препарату Цересіл® Канон 1000 мг на добу, препарат вводять внутрішньовенно краплинно зі швидкістю 30 крапель на хвилину. Вплив на здатність до керування автотранспортом та управління механізмами У період лікування слід дотримуватися обережності при виконанні потенційно небезпечних видів діяльності, що вимагають особливої уваги та швидких реакцій (керування автомобілем та іншими транспортними засобами, робота з механізмами, що рухаються, робота диспетчера та оператора тощо).Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
700,00 грн
0,00 грн
Склад, форма випуску та упаковкаРозчин – 1 амп.: чинна речовина: цитиколін натрію 1045 мг (у перерахунку на цитиколін 1000 мг); допоміжні речовини: натрію гідроксиду розчин 1 М або хлористоводневої кислоти розчин 1 М (до pH 6,5-7,1); вода для ін'єкцій до 4мл. Розчин для внутрішньовенного та внутрішньом'язового введення 250 мг/мл. По 4 мл ампули для лікарських засобів, виготовлені з медичного скла марок НС-1 або НС-3 або 1-го гідролітичного класу. По 3, 5 або 10 ампул в контурне осередкове впакування з полівінілхлоридної плівки. По 1 контурній комірковій упаковці по 3 ампули або по 1, 2 контурних коміркових упаковки по 5 ампул або по 1 контурній комірковій упаковці по 10 ампул разом з інструкцією по застосуванню поміщають в пачку з картону.Опис лікарської формиПрозорий від безбарвного до зеленувато-жовтого кольору розчин (дозування 250 мг/мл).Фармакотерапевтична групаНоотропний засіб.ФармакокінетикаВсмоктування. Цитиколін добре абсорбується при внутрішньовенному та внутрішньом'язовому введенні. Метаболізм. При внутрішньовенному та внутрішньом'язовому введенні цитиколін метаболізується у печінці з утворенням холіну та цитидину. Після введення, концентрації холіну в плазмі істотно підвищуються. Розподіл. Цитиколін значною мірою розподіляється у структурах головного мозку, з швидким впровадженням фракцій холіну у структурні фосфоліпіди та фракції цитидину – у цитидинові нуклеотиди та нуклеїнові кислоти. Цитиколін проникає у головний мозок і активно вбудовується у клітинні, цитоплазматичні та мітохондріальні мембрани, утворюючи частину фракції структурних фосфоліпідів. Виведення. Тільки 15% введеної дози цитиколіну виводиться із організму людини; менше 3% - нирками і через кишечник і близько 12% - з видихається СО2. В екскреції цитиколін з сечею можна виділити 2 фази: перша фаза, що триває близько 36 годин, в ході якої швидкість виведення швидко знижується, і друга фаза, в ході якої швидкість екскреції знижується набагато повільніше. Те ж саме спостерігається у видихуваному СО2 - швидкість виведення швидко знижується приблизно через 15 годин, а потім знижується набагато повільніше.ФармакодинамікаЦитиколін, будучи попередником ключових ультраструктурних компонентів клітинної мембрани (переважно фосфоліпідів), володіє широким спектром дії - сприяє відновленню пошкоджених мембран клітин, інгібує дію фосфоліпаз, перешкоджає надмірному утворенню вільних радикалів, а також запобігає загибелі клітин, впливу на механізм. В гострому періоді інсульту цитиколін зменшує об'єм ураження тканини головного мозку, покращує холінергічну передачу. При черепно-мозковій травмі зменшує тривалість посттравматичної коми та вираженість неврологічних симптомів, крім цього, сприяє зменшенню тривалості відновлювального періоду. При хронічній гіпоксії головного мозку цитиколін ефективний у лікуванні когнітивних розладів, таких як погіршення пам'яті, безініціативність, складнощі, що виникають при виконанні повсякденних дій та самообслуговуванні. Підвищує рівень уваги та свідомості, а також зменшує прояв амнезії. Цитиколін ефективний у лікуванні чутливих та рухових неврологічних порушень дегенеративної та судинної етіології.Показання до застосуванняГострий період ішемічного інсульту (у складі комплексної терапії); відновлювальний період ішемічного та геморагічного інсультів; черепно-мозкова травма (ЧМТ), гострий (у складі комплексної терапії) та відновлювальний період; когнітивні та поведінкові порушення при дегенеративних та судинних захворюваннях головного мозку.Протипоказання до застосуванняНе слід призначати хворим з вираженою ваготонією (переважання тонусу парасимпатичної частини вегетативної нервової системи) та при гіперчутливості до будь-якого з компонентів препарату. У зв'язку з відсутністю достатніх клінічних даних не рекомендується застосовувати у дітей віком до 18 років.Вагітність та лактаціяДостатніх даних щодо застосування цитиколіну у вагітних жінок відсутні. Хоча у дослідженнях на тварин негативного впливу не виявлено, у період вагітності лікарський препарат Цересил® Канон призначають лише у випадках, коли очікувана користь для матері перевершує потенційний ризик для плода. При призначенні препарату Цересіл Канон в період лактації жінкам слід припинити грудне вигодовування, оскільки дані про виділення цитиколіну з жіночим молоком відсутні.Побічна діяЧастота несприятливих побічних реакцій: дуже рідкісні (менше 1/10 000, включаючи індивідуальні випадки) Алергічні реакції: висипання, свербіж шкіри, анафілактичний шок. Інші: почуття жару, набряки, задишка. З боку ЦНС та периферичної нервової системи: безсоння, головний біль, запаморочення, тремор, оніміння в паралізованих кінцівках, стимуляція парасимпатичної нервової системи. Порушення психіки: галюцинації, збудження. Серцево-судинна система: короткочасна зміна артеріального тиску. З боку травної системи: нудота, зниження апетиту, блювання, діарея; зміна активності печінкових ферментів. Якщо будь-які з побічних ефектів, що зазначені в інструкції, посилюються, або були помічені будь-які інші побічні ефекти, не зазначені в інструкції, слід повідомити про це лікаря.Взаємодія з лікарськими засобамиЦитиколін посилює ефекти леводопи. Не слід застосовувати одночасно з лікарськими засобами, що містять меклофеноксат.Спосіб застосування та дозиПрепарат призначають внутрішньовенно або внутрішньом'язово. внутрішньовенно препарат призначають у формі повільної внутрішньовенної ін'єкції (протягом 3-5 хв, залежно від призначеної дози) або краплинного внутрішньовенного вливання (40-60 крапель на хвилину). Внутрішньовенний шлях введення краще, ніж внутрішньом'язовий. При внутрішньом'язовому введенні слід уникати повторного введення препарату в те саме місце. Рекомендований режим дозування Гострий період ішемічного інсульту та черепно-мозкової травми (ЧМТ)\ 1000 мг кожні 12 год з першої доби після встановлення діагнозу, тривалість лікування не менше 6 тижнів. Через 3-5 днів після початку лікування (якщо не порушена функція ковтання) можливий перехід на пероральні форми препарату Цересіл Канон Відновлювальний період ішемічного та геморагічного інсультів, відновлювальний період ЧМТ, когнітивні та поведінкові порушення при дегенеративних та судинних захворюваннях головного мозку: 500-2000 мг на день. Дозування та тривалість лікування залежно від тяжкості симптомів захворювання. Можливе застосування пероральних форм препарату Цересіл Канон. При підозрі на внутрішньочерепну кровотечу, що триває, рекомендується не перевищувати дозу препарату Цересил® Канон 1000 мг на добу, препарат вводять внутрішньовенно краплинно зі швидкістю 30 крапель на хвилину. Літні пацієнти При призначенні препарату Цересіл Канон літнім пацієнтам корекція дози не потрібна. Розчин в ампулі призначений для одноразового застосування. Він має бути негайно використаний після розтину ампули. Препарат сумісний з усіма видами внутрішньовенних ізотонічних розчинів та розчинів декстрози.ПередозуванняЗ огляду на низьку токсичність препарату випадки передозування не описані.Запобіжні заходи та особливі вказівкиПрепарат Цересил Канон вводиться внутрішньовенно струминно повільно (3-5 хв залежно від дози). При внутрішньовенному краплинному введенні швидкість інфузії має бути 40-60 крапель на хвилину. При персистуючому внутрішньовенному крововиливі рекомендується не перевищувати дозу препарату Цересіл® Канон 1000 мг на добу, препарат вводять внутрішньовенно краплинно зі швидкістю 30 крапель на хвилину. Вплив на здатність до керування автотранспортом та управління механізмами У період лікування слід дотримуватися обережності при виконанні потенційно небезпечних видів діяльності, що вимагають особливої уваги та швидких реакцій (керування автомобілем та іншими транспортними засобами, робота з механізмами, що рухаються, робота диспетчера та оператора тощо).Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаКапсули - 1 капс. активна речовина: холіну альфосцерат (у перерахунку на 100% речовину) – 400 мг; допоміжні речовини: гліцерол – 50 мг, вода очищена – до отримання маси вмісту 590 мг; склад капсули: желатин, сорбітол, гліцерол, метилпарагідроксибензоат, пропілпарагідроксибензоат, титану діоксид, барвник заліза оксид жовтий, вода очищена. По 14 капсул в контурне осередкове впакування. По 1, 2, 3 або 4 контурні коміркові упаковки разом з інструкцією із застосування в пачці з картону.Опис лікарської формиКапсули м'які желатинові, овальної форми, жовтого або жовтого зі світло-коричневим відтінком кольору. Вміст капсул – масляниста прозора безбарвна або злегка забарвлена рідина.Фармакотерапевтична групаНоотропний засіб.ФармакокінетикаПри парентеральному прийомі (10 мг/кг) Церетон® переважно накопичується у мозку, легенях та печінці. Абсорбція – 88%, легко проникає через гематоенцефалічний бар'єр (при пероральному прийомі концентрація у мозку – 45% від такої у плазмі). Легкими екскретується 85% препарату у вигляді діоксиду вуглецю, решта (15%) виводиться нирками та через кишечник.ФармакодинамікаІзотропний засіб. Центральний холіностимулятор, у складі якого міститься 40,5% метаболічно захищеного холіну. Метаболічний захист сприяє виділенню холіну в | головному мозку. Забезпечує синтез ацетилхоліну та фосфатидилхоліну в нейрональних мембранах, покращує кровотік та посилює метаболічні процеси в центральній нервовій системі, активує ретикулярну формацію. Збільшує лінійну швидкість кровотоку на стороні травматичного ураження мозку, сприяє нормалізації просторово-часових характеристик: спонтанної біоелектричної активності мозку, регресові осередкових неврологічних симптомів та відновлення свідомості;надає позитивний вплив на пізнавальні та поведінкові реакції хворих із судинними захворюваннями головного мозку (дисциркуляторною енцефалопатією та залишковими явищами порушення мозкового кровообігу). Має профілактичну та коригуючу дію на патогенетичні фактори інволюційного психоорганічного синдрому, змінює фосфоліпідний склад мембран нейронів: бере участь у синтезі фосфатидилхоліну (мембранного фосфоліпіду), покращує пластичність нейрональних мембран. Стимулює дозозалежне виділення ацетилхоліну у фізіологічних умовах, покращує синаптичну передачу, функцію рецепторів. Не впливає на репродуктивний цикл і не має тератогенної, мутагенної дії.Має профілактичну та коригуючу дію на патогенетичні фактори інволюційного психоорганічного синдрому, змінює фосфоліпідний склад мембран нейронів: бере участь у синтезі фосфатидилхоліну (мембранного фосфоліпіду), покращує пластичність нейрональних мембран. Стимулює дозозалежне виділення ацетилхоліну у фізіологічних умовах, покращує синаптичну передачу, функцію рецепторів. Не впливає на репродуктивний цикл і не має тератогенної, мутагенної дії.Має профілактичну та коригуючу дію на патогенетичні фактори інволюційного психоорганічного синдрому, змінює фосфоліпідний склад мембран нейронів: бере участь у синтезі фосфатидилхоліну (мембранного фосфоліпіду), покращує пластичність нейрональних мембран. Стимулює дозозалежне виділення ацетилхоліну у фізіологічних умовах, покращує синаптичну передачу, функцію рецепторів. Не впливає на репродуктивний цикл і не має тератогенної, мутагенної дії.Не впливає на репродуктивний цикл і не має тератогенної, мутагенної дії.Не впливає на репродуктивний цикл і не має тератогенної, мутагенної дії.Показання до застосуванняВідновлювальний період важкої черепно-мозкової травми та ішемічного інсульту, відновлювальний період геморагічного інсульту, що протікають із осередковою півкульною симптоматикою або симптомами ураження стовбура мозку; психоорганічний синдром на тлі дегенеративних та інволюційних змін мозку; когнітивні розлади (порушення розумової функції, пам'яті, сплутаність свідомості, дезорієнтація, зниження мотивації, ініціативності та здатності до концентрації уваги), у тому числі при деменції та енцефалопатії; стареча псевдомеланхолія.Протипоказання до застосуванняПідвищена чутливість до препарату; гостра стадія геморагічного інсульту; вагітність; період грудного вигодовування; діти віком до 18 років (у зв'язку з відсутністю даних).Побічна діяМожлива поява нудоти (головним чином, як наслідок дофамінергічної активації). Не потребує відміни, достатньо тимчасового зниження дози препарату. Алергічні реакції.Взаємодія з лікарськими засобамиЗначного взаємодії коїться з іншими препаратами не виявлено.Спосіб застосування та дозиУ відновлювальному періоді черепно-мозкової травми, ішемічного або геморагічного інсульту Церетон призначають по 800 мг вранці та 400 мг вдень протягом 6 місяців. При хронічній цереброваскулярній недостатності та синдромах деменції Церетон призначають по 400 мг (1 капсула) 3 рази на добу, переважно після їди, протягом 3-6 місяців.ПередозуванняМоже спостерігатися нудота. Лікування: симптоматична терапія.Запобіжні заходи та особливі вказівкиЦеретон не впливає на швидкість психомоторних реакцій.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаСупозиторії – 1 супп.: Активна речовина: дііндолілметан 100 мг. Допоміжні речовини: жир твердий (Вітепсол Н-15) - 1.9795 г, кросповідон (колідон CL) 0.0200 г, барвник кармін червоний Е120 0.0005 г. 5 штук. - упаковки осередкові контурні (5) - пачки картонні.Опис лікарської формиСупозиторії вагінальні; від світло-рожевого до жовтувато-рожевого кольору, торпедоподібної форми.Фармакотерапевтична групаПрепарат Цервікон®-ДІМ як діюча речовина містить дііндолілметан, який є засобом, що стимулює апоптоз інфікованих вірусом папіломи людини (ВПЛ) та трансформованих клітин, а також стимулятором експресії рецепторів до γ-інтерферону. Тим самим, в основі терапевтичного ефекту дііндолілметану лежить його здатність прискорювати елімінацію інфікованих вірусом папіломи людини та трансформованих клітин та посилювати неспецифічну імунну відповідь на інфекцію. Крім того, дііндолілметан нормалізує метаболізм естрадіолу у ВПЛ-інфікованих клітинах, перешкоджаючи утворенню канцерогенного метаболіту естрогену (16α-гідроксіестрону), що стимулює експресію онкогенів ВПЛ. Пригнічуючи експресію онкогену Е7 вірусу папіломи людини,дііндолілметан блокує гормонозалежну патологічну проліферацію ВПЛ-інфікованих клітин.ФармакокінетикаПри інтравагінальному застосуванні дііндолілметан має високу місцеву біодоступність і при цьому практично не потрапляє в системний кровотік.Клінічна фармакологіяПротипухлинний засіб.Показання до застосуванняЛікування дисплазії (цервікальної інтраепітеліальної неоплазії) шийки матки (незалежно від результатів виявлення папіломавірусної інфекції методом ПЛР).Протипоказання до застосуванняІндивідуальна непереносимість будь-якого компонента препарату. ; Період вагітності та грудного вигодовування. ; Дитячий вік віком до 18 років.Вагітність та лактаціяПротипоказано застосування препарату при вагітності та в період грудного вигодовування.Побічна діяПрепарат добре переноситься пацієнтами. У деяких випадках можуть виникати перелічені нижче, зазвичай оборотні, небажані явища. Небажані явища, представлені нижче, перераховані в залежності від анатомо-фізіологічної класифікації та частоти народження. Частота виникнення побічних ефектів класифікується ВООЗ та має градації: дуже часто (≥1/10), часто (≥1/100 та <1/10), нечасто (≥1/1000 та <1/100), рідко (≥1/ 10000 та <1/1000), дуже рідко (<1/10000), не встановлено.Взаємодія з лікарськими засобамиЧи не вивчалося. У зв'язку з відсутністю системної фармакокінетики не очікується будь-якої взаємодії з лікарськими засобами системного застосування. Препарат не слід застосовувати одночасно з місцевими препаратами для інтравагінального застосування, що належать до групи антисептиків-окислювачів (перманганат калію, йод, перекис водню).Спосіб застосування та дозиІнтравагінально по 100 мг 2 рази на добу. Тривалість курсу лікування – 3-6 місяців. Тривалість лікування визначається динамікою клініко-лабораторних показників. ; Рекомендації щодо способу введення препарату: ; Препарат вводиться у піхву 2 рази на добу (вранці та ввечері) по 1 супозиторію. Перед введенням необхідно ретельно вимити руки. Супозиторій глибоко вводять у піхву в положенні лежачи. Після введення рекомендується користування гігієнічною прокладкою.Запобіжні заходи та особливі вказівкиПри лікуванні вагінальних інфекцій препарат не слід застосовувати під час менструації, лікування доцільно розпочинати після менструації. У період лікування рекомендується утримуватись від статевих контактів. Під час лікування рекомендується скористатися засобами контрацепції.Умови зберіганняУ холодильнику +2+8 градусівУмови відпустки з аптекЗа рецептомВідео на цю тему
Цетиризин-акрихин 10мг 20 шт таблетки покрытые пленочной оболочкой warsaw pharmaceutical works polfa
464,00 грн
366,00 грн
Склад, форма випуску та упаковкаПігулки - 1 таб. Активна речовина: цетиризину дигідрохлорид 10 мг. Допоміжні речовини: карбоксиметилкрохмаль натрію - 2 мг, крохмаль кукурудзяний - 20 мг, кремнію діоксид - 1.2 мг, лактози моногідрат - 31 мг, магнію стеарат - 2.5 мг, натрію лаурилсульфат - 0.3 мг, повідон - 4 мг, 9 мг. Склад оболонки: гіпромелоза – 3.4 мг, макрогол 6000 – 0.6 мг. 20 шт. - блістери (1) - пачки картонні.Опис лікарської формиТаблетки, покриті плівковою оболонкою від білого до кремового кольору, довгасті, двоопуклі, з ризиком на одному боці.Фармакотерапевтична групаБлокатори периферичних гістамінових H1-рецепторів. Чинить протиалергічну дію. Впливає на ранню гістамінозалежну стадію алергічних реакцій, зменшує міграцію еозинофілів, обмежує вивільнення медіаторів запалення на пізній, клітинній стадії алергічних реакцій. Попереджає розвиток та полегшує перебіг алергічних реакцій, надає протисвербіжну дію. Практично не чинить антихолінергічної та антисеротонінової дії. У терапевтичних дозах немає седативного ефекту. Дія препарату проявляється через 20 хв (50% пацієнтів), через 60 хв (95% пацієнтів) після прийому препарату і триває до 24 год.ФармакокінетикаВсмоктування Після прийому внутрішньо цетиризин швидко і добре всмоктується із ШКТ. C max у плазмі досягається через 30-60 хв. Прийом їжі не істотно впливає на величину абсорбції, проте в цьому випадку швидкість всмоктування незначно знижується. Розподіл Зв'язування із білками плазми становить 93%. Vd становить близько 0,5 л/кг. Не проникає через гематоенцефалічний бар'єр і всередину клітини. При застосуванні препарату у дозі 10 мг протягом 10 днів накопичення препарату не спостерігається. Метаболізм Цетиризин слабо метаболізується у печінці з утворенням неактивного метаболіту. Виведення Близько 70% прийнятої дози цетиризину виводиться нирками переважно у незміненому вигляді. Після одноразового прийому разової дози T1/2 становить близько 10 год. Фармакокінетика в особливих клінічних випадках Діти віком від 2 до 12 років T1/2 становить 5-6 год. При порушенні функції нирок (КК менше 11-31 мл/хв) та у пацієнтів, які перебувають на гемодіалізі (КК менше 7 мл/хв), T1/2 збільшується в 3 рази, кліренс зменшується на 70%. При хронічних захворюваннях та у пацієнтів похилого віку відзначається збільшення T1/2 на 50% та зменшення кліренсу на 40%.Клінічна фармакологіяБлокатор гістамінових Н1-рецепторів. Протиалергічний препарат.Показання до застосуванняСезонний та цілорічний алергічний риніт; алергічний кон'юнктивіт; поліноз (сінна лихоманка); кропив'янка (в т.ч. хронічна ідіопатична); сверблячі алергічні дерматози (в т.ч. атопічний дерматит, нейродерміт); набряк Квінке.Протипоказання до застосуванняДитячий вік віком до 6 років; вагітність; період лактації (грудне вигодовування); - підвищена чутливість до компонентів препарату. З обережністю слід призначати препарат при хронічній нирковій недостатності середнього та тяжкого ступеня (потрібна корекція режиму дозування), а також хворим похилого віку (можливе зниження клубочкової фільтрації).Вагітність та лактаціяЦетиризин-Акріхін не рекомендують застосовувати при вагітності. За необхідності застосування препарату в період лактації слід вирішити питання про припинення грудного вигодовування. Застосування у дітей Протипоказано: дитячий вік до 6 років.Побічна діяЗ боку травної системи: сухість у роті; в окремих випадках – диспепсія, біль у животі, метеоризм. З боку центральної нервової системи: в окремих випадках – головний біль, сонливість, запаморочення, збудження. Алергічні реакції: у поодиноких випадках – кропив'янка, ангіоневротичний набряк, задишка (пацієнт має бути попереджений про необхідність негайного припинення прийому препарату). Препарат загалом добре переноситься.Взаємодія з лікарськими засобамиПри одночасному застосуванні Цетиризин-Акріхін з теофіліном можливе збільшення частоти побічних ефектів.Спосіб застосування та дозиДорослим та дітям старше 12 років призначають 10 мг (1 таб.)/добу. Дітям віком від 6 до 12 років препарат призначають по 5 мг (1/2 таб.) 2 рази на добу вранці та ввечері або по 10 мг (1 таб.) 1 раз на добу. При нирковій недостатності дозу слід зменшити у 2 рази. При порушеннях функції печінки дозу підбирають індивідуально, особливо за одночасної ниркової недостатності. Пацієнтам похилого віку з нормальною функцією нирок корекція дози не потрібна. Препарат можна приймати незалежно від їди, переважно ввечері. Таблетки слід ковтати повністю, не розжовуючи, запиваючи невеликою кількістю води.ПередозуванняСимптоми: сонливість (при одноразовому прийомі препарату у дозі понад 50 мг); у дітей – занепокоєння, підвищена дратівливість; можливий антихолінергічний ефект (затримка сечовипускання, сухість у роті, запор). Лікування: промивання шлунка, прийом активованого вугілля; за необхідності проводять симптоматичну терапію. Гемодіаліз неефективний.Запобіжні заходи та особливі вказівкиЗ обережністю призначають препарат особам похилого віку та пацієнтам з порушеннями функції печінки та нирок. Пацієнта слід попередити про необхідність повідомляти лікаря про будь-які побічні ефекти на фоні прийому препарату. Пацієнта слід попередити про необхідність уникати одночасного застосування Аллертеку з іншими лікарськими засобами без призначення лікаря. Даних щодо взаємодії цетиризину з етанолом дотепер не отримано, незважаючи на це вживання алкоголю на тлі застосування препарату Цетиризин-Акріхін не рекомендується. Використання у педіатрії Препарат не призначають дітям віком до 6 років. Вплив на здатність до керування автотранспортом та управління механізмами З обережністю призначають препарат пацієнтам, які займаються потенційно небезпечними видами діяльності, що вимагають підвищеної уваги та швидкості психомоторних реакцій.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаКраплі - 1 мл: Діюча речовина: Цетиризину дигідрохлорид – 10,00 мг; допоміжні речовини: пропіленгліколь – 350,00 мг; гліцерол (гліцерин) – 250,00 мг; натрію ацетату тригідрат – 10,00 мг; натрію сахаринат – 10,00 мг; метилпарагідроксибензоат (метилпарабен) – 1,35 мг; оцтова кислота крижана – 0,53 мг; пропілпарагідроксибензоат (пропілпарабен) – 0,15 мг; вода очищена – до 1 мл.ХарактеристикаАнтигістамінний засіб 2 покоління. Застосовується для запобігання та зниження симптомів алергії. Діє швидко, ефект відзначається через 20 хвилин і зберігається більше доби.Фармакотерапевтична групаПротиалергічний засіб – блокатор Н1-гістамінових рецепторів.ФармакодинамікаЦетиризин є метаболітом гідроксизину, має антигістамінний ефект з протиалергічною дією. Цетиризин відноситься до групи конкурентних антагоністів гістаміну і блокує H1-гістамінові рецептори з невеликим впливом на інші рецептори і практично не має антихолінергічної та антисеротонінової дії. Цетиризин впливає на гістамінзалежну стадію алергічних реакцій негайної дії, а також зменшує міграцію еозинофілів та обмежує вивільнення медіаторів при алергічних реакціях уповільненого типу. Практично не проходить через гематоенцефалічний бар'єр і, отже, майже здатний досягти центральних рецепторів Н1.Показання до застосуванняПрепарат показаний дорослим та дітям з 6 місяців і старше для полегшення: назальних та очних симптомів цілорічного (персистуючого) та сезонного (інтермітуючого) алергічного риніту та алергічного кон'юнктивіту: сверблячки, чхання, закладеності носа, ринореї, сльозотечі, гіперемії кон'юнктиви; симптомів хронічної ідіопатичної кропив'янки. Застосування у дітей від 6 до 12 місяців можливе лише за призначенням лікаря та під суворим медичним контролем.Протипоказання до застосуванняПідвищена чутливість до цетиризину, гідроксизину або інших похідних піперазину, а також до будь-якого іншого компонента препарату; термінальна стадія ниркової недостатності (КК дитячий вік до 6 місяців (через обмеженість даних щодо ефективності та безпеки застосування препарату Цетиризин). З обережністю Хронічна ниркова недостатність (при КК > 10 мл/хв потрібна корекція режиму дозування); пацієнти похилого віку (при віковому зниженні клубочкової фільтрації); епілепсія та пацієнти з підвищеною судомною готовністю; пацієнти із сприятливими факторами до затримки сечі; дитячий вік до 1 року; при одночасному вживанні з алкоголем; період грудного вигодовування; вагітність.Вагітність та лактаціяВагітність Дані щодо застосування цетиризину під час вагітності обмежені (300-1000 результатів вагітності). Проте не виявлено випадків формування вад розвитку, ембріональної та неонатальної токсичності з чітким причинно-наслідковим зв'язком. Експериментальні дослідження на тваринах не виявили жодних прямих або непрямих несприятливих ефектів цетиризину на плід, що розвивається (у тому числі в постнатальному періоді), перебіг вагітності та постнатальний розвиток. При вагітності призначення цетиризину можливе після консультації з лікарем, якщо передбачувана користь для матері перевищує потенційний ризик для плода. Період грудного вигодовування Не слід застосовувати цетиризин під час грудного вигодовування, оскільки цетиризин екскретується з грудним молоком. У період грудного вигодовування застосовують після консультації з лікарем, якщо передбачувана користь матері перевищує потенційний ризик для дитини. Фертильність Доступні дані щодо впливу на фертильність людини обмежені, проте негативного впливу на фертильність у дослідженнях на тваринах не виявлено. Перед застосуванням препарату, якщо Ви вагітні, або припускаєте, що Ви могли бути вагітною, або плануєте вагітність, необхідно проконсультуватися з лікарем.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаКраплі - 1 мл: Діюча речовина: Цетиризину дигідрохлорид – 10,00 мг; допоміжні речовини: пропіленгліколь – 350,00 мг; гліцерол (гліцерин) – 250,00 мг; натрію ацетату тригідрат – 10,00 мг; натрію сахаринат – 10,00 мг; метилпарагідроксибензоат (метилпарабен) – 1,35 мг; оцтова кислота крижана – 0,53 мг; пропілпарагідроксибензоат (пропілпарабен) – 0,15 мг; вода очищена – до 1 мл.ХарактеристикаАнтигістамінний засіб 2 покоління. Застосовується для запобігання та зниження симптомів алергії. Діє швидко, ефект відзначається через 20 хвилин і зберігається більше доби.Фармакотерапевтична групаПротиалергічний засіб – блокатор Н1-гістамінових рецепторів.ФармакодинамікаЦетиризин є метаболітом гідроксизину, має антигістамінний ефект з протиалергічною дією. Цетиризин відноситься до групи конкурентних антагоністів гістаміну і блокує H1-гістамінові рецептори з невеликим впливом на інші рецептори і практично не має антихолінергічної та антисеротонінової дії. Цетиризин впливає на гістамінзалежну стадію алергічних реакцій негайної дії, а також зменшує міграцію еозинофілів та обмежує вивільнення медіаторів при алергічних реакціях уповільненого типу. Практично не проходить через гематоенцефалічний бар'єр і, отже, майже здатний досягти центральних рецепторів Н1.Показання до застосуванняПрепарат показаний дорослим та дітям з 6 місяців і старше для полегшення: назальних та очних симптомів цілорічного (персистуючого) та сезонного (інтермітуючого) алергічного риніту та алергічного кон'юнктивіту: сверблячки, чхання, закладеності носа, ринореї, сльозотечі, гіперемії кон'юнктиви; симптомів хронічної ідіопатичної кропив'янки. Застосування у дітей від 6 до 12 місяців можливе лише за призначенням лікаря та під суворим медичним контролем.Протипоказання до застосуванняПідвищена чутливість до цетиризину, гідроксизину або інших похідних піперазину, а також до будь-якого іншого компонента препарату; термінальна стадія ниркової недостатності (КК дитячий вік до 6 місяців (через обмеженість даних щодо ефективності та безпеки застосування препарату Цетиризин). З обережністю Хронічна ниркова недостатність (при КК > 10 мл/хв потрібна корекція режиму дозування); пацієнти похилого віку (при віковому зниженні клубочкової фільтрації); епілепсія та пацієнти з підвищеною судомною готовністю; пацієнти із сприятливими факторами до затримки сечі; дитячий вік до 1 року; при одночасному вживанні з алкоголем; період грудного вигодовування; вагітність.Вагітність та лактаціяВагітність Дані щодо застосування цетиризину під час вагітності обмежені (300-1000 результатів вагітності). Проте не виявлено випадків формування вад розвитку, ембріональної та неонатальної токсичності з чітким причинно-наслідковим зв'язком. Експериментальні дослідження на тваринах не виявили жодних прямих або непрямих несприятливих ефектів цетиризину на плід, що розвивається (у тому числі в постнатальному періоді), перебіг вагітності та постнатальний розвиток. При вагітності призначення цетиризину можливе після консультації з лікарем, якщо передбачувана користь для матері перевищує потенційний ризик для плода. Період грудного вигодовування Не слід застосовувати цетиризин під час грудного вигодовування, оскільки цетиризин екскретується з грудним молоком. У період грудного вигодовування застосовують після консультації з лікарем, якщо передбачувана користь матері перевищує потенційний ризик для дитини. Фертильність Доступні дані щодо впливу на фертильність людини обмежені, проте негативного впливу на фертильність у дослідженнях на тваринах не виявлено. Перед застосуванням препарату, якщо Ви вагітні, або припускаєте, що Ви могли бути вагітною, або плануєте вагітність, необхідно проконсультуватися з лікарем.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему