Вредные привычки Со скидкой
595,00 грн
552,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
413,00 грн
363,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
429,00 грн
395,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
429,00 грн
388,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
296,00 грн
248,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
294,00 грн
248,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
426,00 грн
395,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
433,00 грн
224,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
341,00 грн
163,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
392,00 грн
363,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
414,00 грн
381,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
651,00 грн
404,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
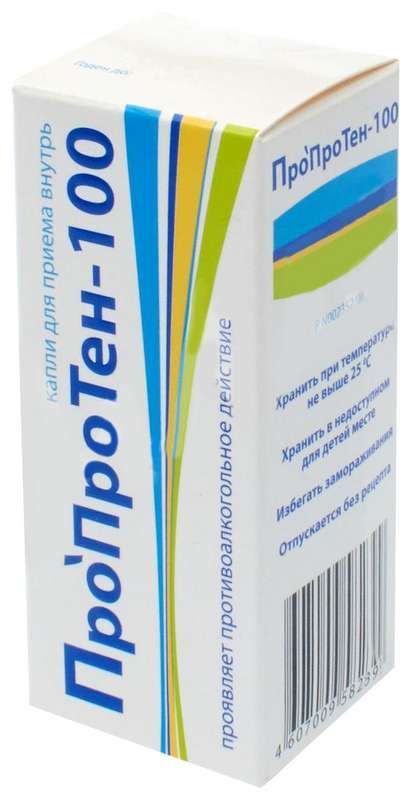
Склад, форма випуску та упаковкаКраплі - 100 р.: Активні речовини: Антитіла до мозковоспецифічного білка S-100 афінно очищені – 1,0 г*; Допоміжні речовини: спирт етиловий 95% 21,8г, вода очищена 77,2г. * Вводяться у вигляді водно-спиртової суміші з вмістом не більше 10-1991 нг/г активної форми діючої речовини. По 25 мл у флакони зі скла марки ОС, або у флакони з пофарбованого скла, закупорені полімерними пробками з дозуючим пристроєм (крапельницею) і кришками полімерними гвинтовими з контролем першого розтину. Кожен флакон разом з інструкцією з медичного застосування поміщають у пачку з картону.Опис лікарської формиБезбарвна прозора рідина із характерним спиртовим запахом.Фармакотерапевтична групаАлкоголізму засобу лікування.ФармакодинамікаПрепарат модифікує функціональну активність білка S-100, що здійснює в мозку поєднання інформаційних та метаболічних процесів. Сенситизує нейрональну мембрану, модулює синаптичну пластичність нейронів. Має модифікуючу дію на функціональний стан структур мозку, що беруть участь у формуванні алкогольної залежності: гіпоталамуса, гіпокампа та ін. При алкогольній залежності надає нормалізуючий вплив на систему позитивного емоційного підкріплення, що призводить до зниження частоти самостимуляції латерального гіпоталамуса. Знижує ниркову активність нейронів гіпокампу; зменшує кількість циркулюючих імунокомплексів у периферичній крові, що корелює зі зниженням споживання етанолу. Сприяє посиленню гальмівних впливів ГАМК у ЦНС. Експериментально встановлено,що препарат відновлює нейромедіаторний баланс та умовнорефлекторну діяльність. Підвищує стійкість мозку до гіпоксії та до токсичних впливів.Показання до застосуванняВиявляє протиалкогольну дію, зменшуючи потяг до алкоголю та знижуючи ймовірність рецидивів. Монотерапія алкогольного абстинентного синдрому легкого та середнього ступеня тяжкості. Препарат полегшує як психопатологічні порушення (занепокоєння, психічна напруга, безсоння, дратівливість, тривога, зниження настрою, інтенсивний потяг до спиртного), так і соматовегетативні розлади (слабкість, пітливість, головний біль, тремор, тахікардія, порушення травлення) алкогольного .Протипоказання до застосуванняПідвищена індивідуальна чутливість до компонентів препарату, вагітність та період лактації.Побічна діяМожливі реакції індивідуальної підвищеної чутливості до компонентів препарату.Взаємодія з лікарськими засобамиВипадків несумісності з іншими лікарськими засобами досі не виявлено.Спосіб застосування та дозиНа один прийом - 10 крапель у їдальні ложці води (не під час їди). У стані похмілля у перші 2 години препарат приймають по 10 крапель кожні 30 хвилин; у наступні 8 -10 годин – по 10 крапель на годину. У разі настання сну прийом поновлюють після пробудження. Надалі при поліпшенні стану препарат приймають по 10 крапель кожні 2-3 години (4-6 прийомів на добу) протягом 2-3 днів. При обтяженні симптомів алкогольної абстиненції необхідно приєднати лікарські засоби, які традиційно використовуються в детоксикації. Для профілактики рецидивів препарат приймають по 10 крапель 1-2 десь у добу протягом 2-3 місяців; після випадкового вживання алкоголю прийняти додатково 10 крапель препарату 2 рази – вдень та на ніч.ПередозуванняДо цього часу випадків передозування не спостерігалося.Умови відпустки з аптекБез рецептаВідео на цю тему
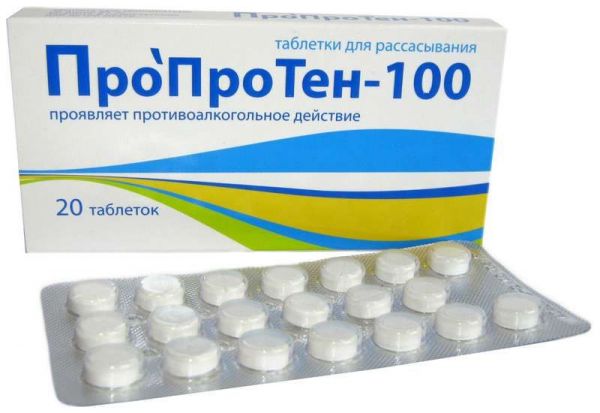
Склад, форма випуску та упаковкаПігулки - 1 таб. Активні речовини: Антитіла до мозковоспецифічного білка S-100 афінно очищені – 0,003 г*; Допоміжні речовини: лактози моногідрат 0,267 г, целюлоза мікрокристалічна 0,03 г, стеарат магнію 0,003 г. * Наносяться на лактозу у вигляді водно-спиртової суміші з вмістом не більше КГ1991 нг/г активної форми діючої речовини. По 20 таблеток у контурній комірковій упаковці з плівки полівінілхлоридної та алюмінієвої фольги. По 1, 2 або 5 контурних осередкових упаковок разом з інструкцією з медичного застосування поміщають у пачку з картону.Опис лікарської формиПігулки плоскоциліндричної форми, з ризиком та фаскою, від білого до майже білого кольору. На плоскій стороні з ризиком нанесено напис MATERIA MEDICA, на іншій плоскій стороні нанесено напис PROPROTEN 100.Фармакотерапевтична групаАлкоголізму засобу лікування.ФармакодинамікаПрепарат модифікує функціональну активність білка S-100, що здійснює в мозку поєднання інформаційних та метаболічних процесів. Сенситизує нейрональну мембрану, модулює синаптичну пластичність нейронів. Має модифікуючу дію на функціональний стан структур мозку, що беруть участь у формуванні алкогольної залежності: гіпоталамуса, гіпокампа та ін. При алкогольній залежності надає нормалізуючий вплив на систему позитивного емоційного підкріплення, що призводить до зниження частоти самостимуляції латерального гіпоталамуса. Знижує ниркову активність нейронів гіпокампу; зменшує кількість циркулюючих імунокомплексів у периферичній крові, що корелює зі зниженням споживання етанолу. Сприяє посиленню гальмівних впливів ГАМК у ЦНС. Експериментально встановлено,що препарат відновлює нейромедіаторний баланс та умовнорефлекторну діяльність. Підвищує стійкість мозку до гіпоксії та до токсичних впливів.Показання до застосуванняВиявляє протиалкогольну дію, зменшуючи потяг до алкоголю та знижуючи ймовірність рецидивів. Монотерапія алкогольного абстинентного синдрому легкого та середнього ступеня тяжкості. Препарат полегшує як психопатологічні порушення (занепокоєння, психічна напруга, безсоння, дратівливість, тривога, зниження настрою, інтенсивний потяг до спиртного), так і соматовегетативні розлади (слабкість, пітливість, головний біль, тремор, тахікардія, порушення травлення) алкогольного .Протипоказання до застосуванняПідвищена індивідуальна чутливість до компонентів препарату, вагітність та період лактації.Побічна діяМожливі реакції підвищеної індивідуальної чутливості до компонентів препарату.Взаємодія з лікарськими засобамиВипадків несумісності з іншими лікарськими засобами досі не виявлено.Спосіб застосування та дозиНа один прийом - 1 таблетку тримати в роті до повного розчинення - (не під час їди). У стані похмілля перші 2 години препарат приймають по 1 таблетці кожні 30 хвилин; наступні 8 -10 годин – по 1 таблетці на годину. У разі настання сну прийом поновлюють після пробудження. Надалі при поліпшенні стану препарат приймають по 1 таблетці кожні 2-3 години (4-6 таблеток на добу) протягом 2-3 днів. При обтяженні симптомів алкогольної абстиненції необхідно приєднати лікарські засоби, які традиційно використовуються в детоксикації. Для профілактики рецидивів препарат приймають по 1-2 таблетки на добу протягом 2-3 місяців; після випадкового вживання алкоголю прийняти додатково 2 таблетки препарату 2 рази – вдень та на ніч.ПередозуванняПри випадковому передозуванні можливі диспепсичні явища, зумовлені наповнювачами, що входять до складу препарату.Запобіжні заходи та особливі вказівкиДо складу препарату входить лактози моногідрат, у зв'язку з чим його не рекомендується призначати пацієнтам з вродженою галактоземією, синдромом мальабсорбції глюкози або при вродженій лактазній недостатності.Умови відпустки з аптекБез рецептаВідео на цю тему
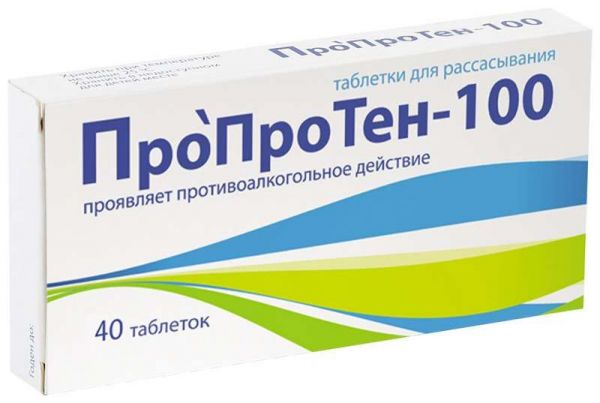
Склад, форма випуску та упаковкаПігулки - 1 таб. Активні речовини: Антитіла до мозковоспецифічного білка S-100 афінно очищені – 0,003 г*; Допоміжні речовини: лактози моногідрат 0,267 г, целюлоза мікрокристалічна 0,03 г, стеарат магнію 0,003 г. * Наносяться на лактозу у вигляді водно-спиртової суміші з вмістом не більше КГ1991 нг/г активної форми діючої речовини. По 20 таблеток у контурній комірковій упаковці з плівки полівінілхлоридної та алюмінієвої фольги. По 1, 2 або 5 контурних осередкових упаковок разом з інструкцією з медичного застосування поміщають у пачку з картону.Опис лікарської формиПігулки плоскоциліндричної форми, з ризиком та фаскою, від білого до майже білого кольору. На плоскій стороні з ризиком нанесено напис MATERIA MEDICA, на іншій плоскій стороні нанесено напис PROPROTEN 100.Фармакотерапевтична групаАлкоголізму засобу лікування.ФармакодинамікаПрепарат модифікує функціональну активність білка S-100, що здійснює в мозку поєднання інформаційних та метаболічних процесів. Сенситизує нейрональну мембрану, модулює синаптичну пластичність нейронів. Має модифікуючу дію на функціональний стан структур мозку, що беруть участь у формуванні алкогольної залежності: гіпоталамуса, гіпокампа та ін. При алкогольній залежності надає нормалізуючий вплив на систему позитивного емоційного підкріплення, що призводить до зниження частоти самостимуляції латерального гіпоталамуса. Знижує ниркову активність нейронів гіпокампу; зменшує кількість циркулюючих імунокомплексів у периферичній крові, що корелює зі зниженням споживання етанолу. Сприяє посиленню гальмівних впливів ГАМК у ЦНС. Експериментально встановлено,що препарат відновлює нейромедіаторний баланс та умовнорефлекторну діяльність. Підвищує стійкість мозку до гіпоксії та до токсичних впливів.Показання до застосуванняВиявляє протиалкогольну дію, зменшуючи потяг до алкоголю та знижуючи ймовірність рецидивів. Монотерапія алкогольного абстинентного синдрому легкого та середнього ступеня тяжкості. Препарат полегшує як психопатологічні порушення (занепокоєння, психічна напруга, безсоння, дратівливість, тривога, зниження настрою, інтенсивний потяг до спиртного), так і соматовегетативні розлади (слабкість, пітливість, головний біль, тремор, тахікардія, порушення травлення) алкогольного .Протипоказання до застосуванняПідвищена індивідуальна чутливість до компонентів препарату, вагітність та період лактації.Побічна діяМожливі реакції підвищеної індивідуальної чутливості до компонентів препарату.Взаємодія з лікарськими засобамиВипадків несумісності з іншими лікарськими засобами досі не виявлено.Спосіб застосування та дозиНа один прийом - 1 таблетку тримати в роті до повного розчинення - (не під час їди). У стані похмілля перші 2 години препарат приймають по 1 таблетці кожні 30 хвилин; наступні 8 -10 годин – по 1 таблетці на годину. У разі настання сну прийом поновлюють після пробудження. Надалі при поліпшенні стану препарат приймають по 1 таблетці кожні 2-3 години (4-6 таблеток на добу) протягом 2-3 днів. При обтяженні симптомів алкогольної абстиненції необхідно приєднати лікарські засоби, які традиційно використовуються в детоксикації. Для профілактики рецидивів препарат приймають по 1-2 таблетки на добу протягом 2-3 місяців; після випадкового вживання алкоголю прийняти додатково 2 таблетки препарату 2 рази – вдень та на ніч.ПередозуванняПри випадковому передозуванні можливі диспепсичні явища, зумовлені наповнювачами, що входять до складу препарату.Запобіжні заходи та особливі вказівкиДо складу препарату входить лактози моногідрат, у зв'язку з чим його не рекомендується призначати пацієнтам з вродженою галактоземією, синдромом мальабсорбції глюкози або при вродженій лактазній недостатності.Умови відпустки з аптекБез рецептаВідео на цю тему
ХарактеристикаНабір. Пластирі призначені для боротьби із тютюновою залежністю. Не містять нікотину. Основна активна речовина – сонікотинель. Діє у 2-х напрямках: знижує потяг до нікотину - надходячи в клітини, сонікотинель зв'язується з нікотиновими рецепторами, конкурентно замінюючи нікотин, тим самим знижує потребу організму в ньому; очищає організм від токсинів, що накопичилися - впливаючи на дихальні центри, сонікотинель забезпечує активний виведення токсинів з легенів, тим самим очищаючи організм. Розмір: 5 см х 7,5 смУмови відпустки з аптекБез рецептаВідео на цю тему
609,00 грн
187,00 грн
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
2 001,00 грн
404,00 грн
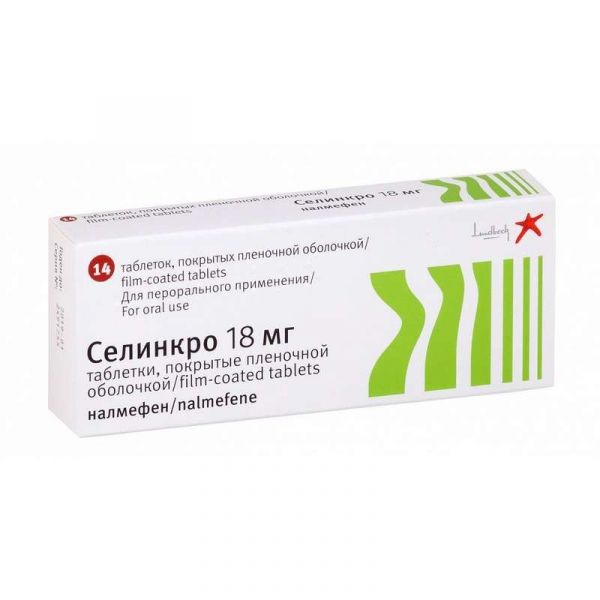
Склад, форма випуску та упаковкаТаблетки, покриті плівковою оболонкою - 1 табл. активна речовина: налмефен гідрохлориду дигідрат - 21,917 мг. (у перерахунку на налмефен гідрохлорид - 20 мг; на налмефен - 18,06 мг); допоміжні речовини: МКЦ – 61,4 мг; лактоза безводна – 60,683 мг; кросповідон (тип А) - 4,5 мг; магнію стеарат – 1,5 мг; оболонка плівкова: Opadry OY-S-28849 білий (гіпромелоза (5мПа·с), макрогол 400, титану діоксид (Е171)) - 4,5 мг. Пігулки, покриті плівковою оболонкою, 18 мг. По 7 чи 14 табл. у контурній комірковій упаковці (блістері) з ПВХ/ПВДХ та фольги алюмінієвої. 1 бл. по 7 табл.; 1 чи 2 бл. по 14 табл. поміщають у картонну пачку.Опис лікарської формиОвальні, двоопуклі, білі пігулки, покриті плівковою оболонкою, з тисненням «S» на одній стороні.Фармакотерапевтична групаАнтиалкогольне.ФармакокінетикаВсмоктування. Після однократної пероральної дози 18,06 мг налмефен швидко всмоктується. Cmax у плазмі крові – 16,5 нг/мл – досягається приблизно через 1,5 год. Експозиція (AUC) становить 131 нг·ч/мл. Абсолютна біодоступність налмефен після прийому внутрішньо становить 41%. Одночасний прийом з їжею з високим вмістом жирів збільшує загальну експозицію (AUC) на 30% і Cmax на 50%, при цьому Tmax у плазмі збільшується на 30 хв, що не вважається клінічно значущим. Розподіл. Зв'язування із білками плазми становить близько 30%. Здається Vd - близько 3200 л. За даними, отриманими в ході дослідження позитронно-емісійною томографією (ПЕТ), після одноразового та повторного прийому налмефену у добовій дозі 18,06 мг зв'язування 94-100% рецепторів досягається вже через 3 години, що передбачає, що налмефен легко проникає через гематоенцефалічний бар'єр. Біотрансформація. При прийомі внутрішньо налмефен піддається екстенсивному метаболізму до основного метаболіту налмефен-3-О-глюкуроніду, головним чином під дією ізоферменту UGT2B7 та меншою мірою за рахунок ізоферментів UGT1A3 та UGT1A8. Відносно невелика кількість налмефен метаболізується до норналмефен під дією ізоферменту CYP3A4/5 і налмефен-3-О-сульфату сульфуванням. Норналмефен у свою чергу перетворюється на норналмефен-3-О-глюкуронід і норналмефен-3-О-сульфат. Метаболіти не вносять значних внесків у фармакодинамічні ефекти, пов'язані з впливом на опіоїдні рецептори у людей, за винятком налмефен-3-О-сульфату, який має порівнянну з налмефеном активність. Однак концентрація налмефен-3-Осульфату становить менше 10% від концентрації налмефену. Тому малоймовірно,що цей метаболіт робить значний внесок у розвиток фармакологічних ефектів налмефену. Виведення. Зв'язування з глюкуронідами є основним механізмом, що визначає кліренс налмефену. Ниркова екскреція є основним шляхом виведення налмефену та його метаболітів. 54% виводиться із сечею у вигляді налмефен-3-О-глюкуроніду, сам же налмефен та інші його метаболіти визначаються у сечі у кількості, що не перевищує 3% кожен. Кліренс налмефену при внутрішньому прийомі становить 169 л/год. Кінцевий T1/2 дорівнює 12,5 год. Наведені дані про розподіл, метаболізм і виведення налмефену свідчать про його високий печінковий кліренс. Лінійність/нелінійність. Фармакокінетика налмефену має дозоннезалежний лінійний характер у діапазоні доз від 18,06 до 72,24 мг. У рівноважному стані порівняно з одноразовим прийомом налмефену спостерігається збільшення Cmax у 4,4 рази та загальної експозиції препарату (AUC0–τ) у 4,3 рази. Не виявлено значних відмінностей у фармакокінетиці налмефену залежно від статі, віку чи етнічної приналежності. Виявлено, що розмір тіла мінімально впливає на фармакокінетичні параметри налмефену (зі збільшенням розміру тіла кліренс зростає), але, ймовірно, ця відмінність не є клінічно значущою. Порушення функції нирок. В даний час немає даних щодо фармакокінетики налмефену при пероральному прийомі у пацієнтів з нирковою недостатністю. Введення 1 мг налмефену внутрішньовенно пацієнтам з тяжкою нирковою недостатністю призводило до збільшення експозиції налмефену (скоригована з урахуванням дози AUCinf) у 1,6 раза порівняно зі здоровими суб'єктами. T1/2 збільшувався до 26 год проти здоровими суб'єктами. Порушення функції печінки. При прийомі одноразової дози налмефену 18,06 мг у пацієнтів з легкою та помірною печінковою недостатністю спостерігалося збільшення експозиції налмефену порівняно зі здоровими суб'єктами. У пацієнтів з легкою печінковою недостатністю спостерігалося збільшення експозиції препарату в 1,5 рази та зниження кліренсу приблизно на 35%. У пацієнтів з помірною печінковою недостатністю експозиція зростала у 2,9 раза, Cmax у 1,7 раза, а кліренс знижувався приблизно на 60%. Зміни Tmax та T1/2 не мали клінічного значення в жодній групі пацієнтів. В даний час немає даних щодо фармакокінетики налмефену після перорального прийому у пацієнтів з тяжкою печінковою недостатністю. Літні пацієнти. Спеціальних досліджень фармакокінетики налмефену після перорального прийому у пацієнтів віком 65 років і більше не проводилося. У дослідженні з внутрішньовенним введенням налмефену не виявлено значних відмінностей фармакокінетики між віковими групами.ФармакодинамікаМеханізм дії Налмефен є модулятором опіоїдної системи з вираженою спорідненістю до μ-, δ- і κ-рецепторів. Дослідження in vitro показали, що налмефен є селективним лігандом опіоїдних рецепторів, виявляючи властивості антагоніста щодо μ- та δ-рецепторів та часткового агоніста щодо κ-рецепторів. Дослідження in vivo показали, що налмефен знижує споживання алкоголю, очевидно, модулюючи кортико-мезолімбічні функції. Дані, отримані з доклінічних досліджень, клінічних досліджень та літератури, не передбачають наявності у налмефена здатності викликати залежність або зловживання. Клінічна ефективність та безпека Ефективність налмефену у зниженні споживання алкоголю у пацієнтів із алкогольною залежністю оцінювалася у двох дослідженнях. З досліджень виключалися пацієнти з алкогольним делірієм в анамнезі, галюцинаціями, судомними нападами, серйозними психічними розладами, пацієнти із значним порушенням функцій печінки. Також виключалися пацієнти, у яких на момент скринінгу або рандомізації було виявлено виражені фізичні симптоми відміни алкоголю. Більшість пацієнтів (80%), включених у дослідження, на момент скринінгу мали високий або дуже високий рівень ризику розвитку шкідливих наслідків вживання алкоголю (згідно з визначенням ВООЗ, прийом >60 г/сут чистого алкоголю для чоловіків та >40 г/сут чистого алкоголю для жінок), з них 65% зберегли високий або дуже високий рівень ризику до моменту рандомізації. Обидва дослідження були рандомізованими подвійними сліпими плацебо-контрольованими дослідженнями в паралельних групах, і через 6 місяців лікування пацієнти, які отримували налмефен, були повторно рандомізовані, щоб отримувати або налмефен, або плацебо протягом 1 міс т.зв. run-out періоду. Ефективність налмефену також вивчалася в 1-річному рандомізованому подвійному сліпому плацебо-контрольованому дослідженні у паралельних групах. Загалом у цих дослідженнях було проліковано 1941 пацієнт, у тому числі 1144 пацієнта отримували налмефен у дозі 18 мг (за потреби). Під час першого візиту оцінювався клінічний статус пацієнта, соціальна ситуація та характер споживання алкоголю (за словами пацієнта). При рандомізації, яка проводилася через 1-2 тижні, повторно оцінювався рівень ризику розвитку шкідливих наслідків вживання алкоголю та призначалася терапія налмефеном у комплексі з психосоціальною інтервенцією (BRENDA), спрямованою на підтримку прихильності до лікування та зниження споживання алкоголю. Налмефен приймався за необхідності, що становить у середньому половину днів перебування у дослідженні. Ефективність налмефену оцінювалася за двома основними критеріями: зміна кількості днів важкого пияцтва (ДТП) на місяць за період між вихідним обстеженням та 6-м міс та зміна добової дози алкоголю (СДА) за період між вихідним обстеженням та 6-м міс. ДТП визначався як день, коли споживалося ≥60 г чистого алкоголю чоловіками та ≥40 г жінками. У період між вихідним візитом (скринінгом) та рандомізацією у деяких пацієнтів було відзначено значне зменшення ДТП та СДА, зумовлене нефармакологічними ефектами. У дослідженнях 1 (n=579) та 2 (n=655) 18 та 33% від загальної кількості пацієнтів, які брали участь у дослідженні, відповідно значно знизили споживання алкоголю в період між скринінгом і рандомізацією. Що стосується пацієнтів із спочатку високим і дуже високим ризиком розвитку шкідливих наслідків вживання алкоголю, то з них у 35% показники покращилися через нефармакологічні причини в період між скринінгом і рандомізацією. У цих пацієнтів на момент рандомізації кількість споживаного алкоголю була настільки невеликою, що можливості подальшого поліпшення були дуже обмеженими (вихідний рівень майже відповідав мінімальному). Пацієнти, що зберегли високий і дуже високий рівень ризику розвитку шкідливих наслідків вживання алкоголю між скринінгом та рандомізацією, ретроспективно склали цільову популяцію. У цій групі ефект лікування був значнішим, ніж у популяції загалом. Клінічна ефективність налмефену та достовірність даних аналізувалися у пацієнтів з високим та дуже високим ризиком розвитку шкідливих наслідків вживання алкоголю при скринінгу та рандомізації. Спочатку у таких пацієнтів спостерігалося в середньому 23 ДТП/міс (у 11% пацієнтів менше 14 ДТП/міс) при добовому споживанні 106 г чистого алкоголю. У більшості пацієнтів рівень алкогольної залежності, виміряний за шкалою алкогольної залежності, був низьким (0-13 балів у 55% пацієнтів) або проміжним (14-21 бал у 36% пацієнтів). Ретроспективний аналіз ефективності у пацієнтів з високим та дуже високим рівнем ризику розвитку шкідливих наслідків вживання алкоголю на момент рандомізації У Дослідженні 1 частка пацієнтів, що вибули з дослідження, була вищою у групі налмефену, ніж у групі плацебо (50 і 32% відповідно). Кількість ДТП при вихідному обстеженні становило 23 дні на місяць як у групі налмефену (n=171), так і у групі плацебо (n=167). Серед пацієнтів, які продовжили участь у дослідженні та у яких були отримані дані щодо ефективності через 6 міс, кількість ДТП склала 9 днів на місяць у групі налмефену (n=85) та 14 днів на місяць у групі плацебо (n=114). При вихідному обстеженні СДА склала 102 г у групі налмефену та 99 г у групі плацебо. Серед пацієнтів, які продовжили участь у дослідженні, та у яких були отримані дані щодо ефективності через 6 міс, СДА склала 40 г у групі налмефену та 57 г у групі плацебо. У Дослідженні 2 частка пацієнтів, що вибули з дослідження, була вищою у групі налмефену, ніж у групі плацебо (30 і 28% відповідно). При вихідному обстеженні кількість ДТП склала 23 дні на місяць у групі налмефену (n=148) та 22 дні на місяць у групі плацебо (n=155). Серед пацієнтів, які продовжили участь у дослідженні та у яких були отримані дані щодо ефективності через 6 міс, кількість ДТП склала 10 днів на місяць у групі налмефену (n=103) та 12 днів на місяць у групі плацебо (n=111). При вихідному обстеженні СДА склала 113 г у групі налмефену та 108 г у групі плацебо. Серед пацієнтів, які продовжили участь у дослідженні та у яких були отримані дані щодо ефективності через 6 міс, СДА склала 44 г у групі налмефену та 52 г у групі плацебо. Річне дослідження До дослідження було включено 665 пацієнтів, 52% з них мали високий або дуже високий ризик розвитку шкідливих наслідків вживання алкоголю на момент скринінгу, у свою чергу, 52% цих пацієнтів (27% від загальної популяції) зберегли високий або дуже високий рівень ризику до моменту рандомізації. У даній цільовій популяції серед пацієнтів, що достроково припинили лікування, більше пацієнтів було в групі налмефену (45%) порівняно з пацієнтами, що припинили лікування, у групі плацебо (31%). При вихідному обстеженні кількість ДТП склала 19 днів на місяць як у групі налмефену (n = 141), так і у групі плацебо (n = 42). Серед пацієнтів, які продовжили участь у дослідженні та у яких були отримані дані щодо ефективності через 1 рік, кількість ДТП склала 5 днів на місяць у групі налмефену (n=78) та 10 днів на місяць у групі плацебо (n=29).При вихідному обстеженні СДА становила 100 г у групі налмефену та 101 г у групі плацебо. Серед пацієнтів, які продовжили участь у дослідженні та у яких були отримані дані щодо ефективності через 1 рік, СДА склала 24 г у групі налмефену та 47 г у групі плацебо.Показання до застосуванняЗниження споживання алкоголю у дорослих пацієнтів з алкогольною залежністю, які мають високий ризик зловживання алкоголем, за відсутності фізичних проявів синдрому відміни або необхідності проведення негайної детоксикації. Селінкро рекомендовано застосовувати у поєднанні з тривалою психосоціальною підтримкою, спрямованою на збереження прихильності до лікування та зниження споживання алкоголю. Селінкро призначається після 2 тижнів спостереження за пацієнтом з високим ризиком зловживання алкоголем.Протипоказання до застосуваннягіперчутливість до налмефену чи будь-якого з компонентів препарату; спадкова непереносимість галактози, дефіцит лактази або глюкозо-галактозна мальабсорбція; застосування у пацієнтів, які нині приймають опіоїдні анальгетики; поточна чи недавня опіоїдна залежність; гострі симптоми відміни опіоїдів; підозра на недавній прийом опіоїдів; тяжка печінкова недостатність (класифікація по Чайлд-П'ю); тяжка ниркова недостатність (розрахована швидкість клубочкової фільтрації (рСКФ)) стан скасування алкоголю (включаючи галюцинації, судоми та алкогольний делірій) у недавньому минулому; вагітність; період грудного вигодовування; дитячий та підлітковий вік (до 18 років) (ефективність та безпека застосування не підтверджені). З обережністю: супутні психічні розлади у фазі декомпенсації (у зв'язку з відсутністю клінічних даних); судомні розлади в анамнезі, включаючи судоми, що розвиваються при скасуванні алкоголю; легка або помірна ниркова або печінкова недостатність, підвищений рівень АЛТ та АСТ (більш ніж у 3 рази перевищує ВГН); одночасне застосування потужних інгібіторів ізоферменту UGT2B7 протягом тривалого часу; літні пацієнти (≥65 років).Вагітність та лактаціяДані щодо застосування налмефену у вагітних жінок обмежені (менше 300 випадків наслідків вагітності). Дослідження у тварин виявили репродуктивну токсичність налмефену. Дослідження у тварин не виявили прямий шкідливий вплив налмефену щодо фертильності, вагітності, ембріо-фетального розвитку, пологів та постнатального розвитку. У дослідженні ембріо-фетальної токсичності у кроликів спостерігалося зниження маси плода та затримка осифікації (процесу формування кісткової тканини), будь-які інші серйозні порушення не були виявлені. Експозиція (AUC) при прийомі вищої нетоксичної дози (NOAEL/ВНТД) при цих небажаних ефектах була нижчою за експозицію при прийомі терапевтичної дози, рекомендованої для людини. Збільшення частоти появи мертвонароджених дитинчат і зменшення їх постнатальної виживання спостерігалося в дослідженнях пре-і постнатальної токсичності у щурів. Цей ефект вважався непрямим і пов'язаним із токсичністю у самок. Доклінічні дані не виявили особливої небезпеки налмефену для людини на підставі стандартних досліджень фармакологічної безпеки, токсичності при багаторазовому застосуванні, генотоксичності та канцерогенного потенціалу. Селінкро не рекомендується застосовувати під час вагітності. Доступні фармакодинамічні та токсикологічні дані у тварин показали здатність налмефену та метаболітів проникати у грудне молоко. Невідомо, чи налмефен проникає в грудне молоко людини. В даний час не можна виключити потенційний ризик для новонароджених/немовлят, тому Селінкро не рекомендується застосовувати під час грудного вигодовування. Фертильність. Дослідження на щурах не виявили впливу налмефену на фертильність, процес спарювання, вагітність або процес сперматогенезу.Побічна діяУ клінічних дослідженнях понад 3000 пацієнтів одержали лікування налмефеном. Загалом профіль безпеки виглядав подібним чином у всіх проведених дослідженнях. Найбільш поширеними небажаними реакціями були нудота, запаморочення, безсоння та біль голови. Більшість цих реакцій мала легкий і середній ступінь тяжкості і відзначалася лише на початку лікування. Сплутаність свідомості та, рідше, галюцинації та дисоціативні розлади також спостерігалися в ході клінічних досліджень. Більшість цих реакцій мала легкий і середній ступінь тяжкості і відзначалася лише на початку лікування (перший годинник або дні). Більшість подібних небажаних реакцій дозволяли при продовженні терапії та не відновлювалися при повторному застосуванні препарату. Ці розлади, що загалом мають короткочасний характер, можуть бути симптомами алкогольних психозів, алкогольного похмільного синдрому або коморбідних психічних розладів. Розрахунок частоти небажаних побічних реакцій проводився на підставі результатів трьох рандомізованих подвійних сліпих плацебо-контрольованих досліджень у пацієнтів з алкогольною залежністю (1144 пацієнти отримували Селінкро в режимі «за потребою» та 797 отримували плацебо в режимі «за потребою»). Частота визначається так: дуже часто (≥1/10), часто (від ≥1/100 до Органи та системи органів Частота Небажана реакція З боку обміну речовин та харчування Часто Зниження апетиту Порушення психіки Дуже часто Безсоння Часто Розлади сну Сплутаність свідомості Занепокоєння Зниження лібідо ( в т.ч. відсутність) Частота невідома Галюцинації ( в т.ч. слухові, тактильні, зорові та соматичні) Дисоціативні розлади З боку нервової системи Дуже часто Запаморочення Головний біль Часто Сонливість Тремор Розлади уваги Парестезія Гіпестезія З боку серця Часто Тахікардія Відчуття серцебиття З боку шлунково-кишкового тракту Дуже часто Нудота Часто Блювота Сухість в роті З боку шкіри та підшкірних тканин Часто Підвищене потовиділення З боку скелетно-м'язової та сполучної тканини Часто М'язові спазми Загальні розлади та порушення у місці введення Часто Стомлюваність Астенія нездужання Відчуття зміненості стану ( в т.ч. відчуття туману в голові, заціпеніння) Лабораторні та інструментальні дані Часто Зниження маси тіла Взаємодія з лікарськими засобамиДослідження взаємодії з іншими лікарськими засобами in vivo не проводились. Відповідно до даних досліджень in vitro, немає підстав припускати наявність клінічно значущої взаємодії між налмефеном або його метаболітами та лікарськими препаратами, що піддаються метаболізму за участю більшості ізоферментів CYP450 та UGT або мембранними переносниками. Одночасне застосування з препаратами, які є потужними інгібіторами ізоферменту UGT2B7 (наприклад, диклофенак, флуконазол, медроксипрогестерону ацетат, меклофенамова кислота), може значно підвищити експозицію налмефену. Рідкісне застосування цих лікарських препаратів одночасно з налмефеном навряд чи може призвести до клінічно значущих наслідків. У той же час, у разі тривалого одночасного застосування потужних інгібіторів ізоферменту UGT2B7 не можна виключати потенційно можливе підвищення експозиції налмефену.Відповідно одночасне застосування з індукторами UGT (наприклад, дексаметазон, фенобарбітал, рифампіцин, омепразол) може потенційно призвести до зниження концентрації налмефену в плазмі нижче терапевтичного рівня. У разі застосування налмефену одночасно з опіоїдними агоністами (наприклад, деякі протикашльові, протизастудні, протидіарейні засоби та опіоїдні анальгетики) може спостерігатися зниження їх терапевтичного ефекту. Не існує клінічно значущої фармакокінетичної взаємодії між налмефеном та алкоголем. Після застосування налмефену може спостерігатися незначне погіршення когнітивних та психомоторних функцій. Однак результат одночасного прийому налмефену та алкоголю не перевищував суму ефектів кожної речовини, що застосовувалася окремо. Одночасне застосування алкоголю та Селінкро не запобігає розвитку алкогольної інтоксикації.Спосіб застосування та дозиПід час первинного візиту до призначення Селінкро лікарю необхідно оцінити клінічний стан пацієнта та рівень споживання алкоголю (за його словами). У випадках, де потрібна додаткова інформація, пацієнту пропонується зареєструвати рівень споживання алкоголю приблизно протягом наступних 2 тижнів. Тим пацієнтам, у яких протягом цих двох тижнів зберігся порівняний з початковим рівень споживання алкоголю, Селінкро може бути призначений при повторному візиті. Селінкро рекомендовано застосовувати у поєднанні з психосоціальною підтримкою, спрямованою на збереження прихильності до лікування та зниження рівня споживання алкоголю. Селінкро не призначений для досягнення негайної помірності від алкоголю. Зниження споживання алкоголю є проміжною метою на шляху до повної помірності. Селінкро застосовується за потребою. Рішення про прийом препарату приймає сам пацієнт: у ті дні, коли, на його думку, висока ймовірність вживання алкоголю, за 1-2 години до передбачуваного моменту приймається 1 табл. Селінкро у дозі 18 мг. Якщо пацієнт почав вживати алкоголь, не прийнявши попередньо таблетку Селінкро, йому потрібно це зробити якнайшвидше. Максимальна добова доза Селінкро становить 1 табл. У ході клінічних досліджень максимальне покращення спостерігалося протягом перших 4 тижнів терапії. Відповідь пацієнта на лікування та доцільність продовження фармакотерапії необхідно оцінювати регулярно (наприклад, щомісяця). Лікар повинен постійно визначати прогрес пацієнта у зниженні споживання алкоголю, його загальний стан, відданість терапії та виникнення побічних ефектів. Тривалість клінічних досліджень Селінкро не перевищувала 12 місяців, тому його призначення на термін більше одного року має здійснюватися з обережністю. Спосіб застосування Всередину, незалежно від їди. Пігулки, покриті плівковою оболонкою, слід приймати повністю. Таблетки не слід ділити або іншим способом порушувати їхню цілісність, т.к. налмефен може спричинити подразнення у разі прямого контакту зі шкірою. Особливі групи пацієнтів Літні пацієнти (≥65 років). У даної групи пацієнтів корекція дози не потрібна. Порушення функції нирок. У пацієнтів з легкою та помірною нирковою недостатністю корекція дози не потрібна. Порушення функції печінки. У пацієнтів з легкою та помірною печінковою недостатністю корекція дози не потрібна. Діти та підлітки (до 18 років). Безпека та ефективність Селінкро у пацієнтів віком до 18 років не встановлена. Дані щодо цієї вікової групи відсутні.ПередозуванняУ дослідженні у пацієнтів з діагнозом патологічної пристрасті до азартних ігор налмефен застосовувався у дозах до 90 мг на добу протягом 16 тижнів. У дослідженні у пацієнтів з інтерстиціальним циститом 20 пацієнтів приймали налмефен у дозі 108 мг на добу протягом 2 років. Повідомлялося про випадок одноразового прийому налмефену в дозі 450 мг, який не супроводжувався зміною АТ, ЧСС, частотою дихальних рухів або температурою тіла. У цих випадках профіль безпеки налмефену відповідав описаному вище розділу «Побічні дії», однак досвід спостереження обмежений. Лікування: при передозуванні рекомендується симптоматична терапія та спостереження за станом пацієнта.Запобіжні заходи та особливі вказівкиСелінкро не призначений для досягнення негайної помірності від алкоголю. Зниження споживання алкоголю є проміжною метою на шляху до повної помірності. Застосування опіоїдів. В екстреній ситуації, коли пацієнту, який приймає Селінкро, необхідно введення опіоїдів, дози останніх, необхідні для досягнення бажаного ефекту, можуть перевищувати стандартні. При цьому слід уважно відстежувати симптоми пригнічення дихання, що є результатом введення опіоїдів та інші небажані реакції. Якщо для надання допомоги пацієнту в екстреній ситуації необхідне введення опіоїдів, їх дози слід підбирати індивідуально. У разі, коли потрібне застосування надто високих доз опіоїдів, слід ретельно спостерігати за станом пацієнта. Селінкро необхідно тимчасово відмінити за 1 тиждень до передбачуваного застосування опіоїдів, наприклад, у ході планового хірургічного втручання. Лікар, який призначає Селінкро, повинен рекомендувати пацієнтові повідомити медичних працівників про час останнього прийому препарату у випадках, коли стає необхідним застосування опіоїдів. Необхідно бути обережним у випадку, коли лікарські препарати, що містять опіоїди (наприклад протикашльові препарати та опіоїдні анальгетики), застосовуються у пацієнтів, які вже отримують терапію Селінкро. Налмефен протипоказаний у пацієнтів, які нині приймають опіоїдні аналгетики. Хвороби, що супруводжують Психічні розлади. У ході проведення клінічних досліджень повідомлялося про побічні реакції з боку психіки. Якщо у пацієнта виникають розлади психіки, не пов'язані з початком застосування Селінкро та/або вони не є тимчасовими, лікар повинен врахувати альтернативні причини виникнення цих симптомів та оцінити необхідність продовження терапії препаратом Селінкро. Селінкро не досліджувався у пацієнтів із нестабільним перебігом психічних захворювань. Слід призначати Селінкро з обережністю пацієнтам із супутніми психічними захворюваннями у фазі декомпенсації, у т.ч. пацієнтам із діагнозом «великий депресивний розлад». Судорожні розлади. Досвід застосування препарату у пацієнтів із судомними розладами в анамнезі, включаючи судоми, що розвиваються при відміні алкоголю, обмежений. Рекомендується бути обережним, якщо Селінкро застосовується з метою зменшення споживання алкоголю в цій групі пацієнтів. Порушення функції нирок чи печінки. Селінкро активно метаболізується в печінці та виводиться переважно із сечею. З цієї причини слід бути обережним при призначенні Селінкро пацієнтам з легкою або помірною нирковою або печінковою недостатністю. Слід бути обережними при призначенні Селінкро пацієнтам з підвищеним рівнем АЛТ і АСТ (більш ніж у 3 рази перевищують ВГН), т.к. дана категорія пацієнтів виключалася під час клінічних досліджень. Літні пацієнти (≥65 років). Клінічні дані щодо застосування Селінкро у пацієнтів з алкогольною залежністю у віці 65 років та старші обмежені. Слід бути обережними при призначенні Селінкро пацієнтам віком 65 років і старше. Інші. Слід бути обережними при одночасному застосуванні Селінкро з потужними інгібіторами ізоферменту UGT2B7. лактоза. Пацієнти з такими рідкісними спадковими проблемами, як непереносимість галактози, дефіцит лактази або глюкозо-галактозна мальабсорбція не повинні застосовувати цей препарат. Вплив на здатність керувати транспортними засобами та працювати з механізмами. Вплив налмефену на здатність керувати транспортними засобами та працювати з механізмами не вивчався. Селінкро може викликати небажані реакції, такі як нудота, запаморочення, безсоння та біль голови. Більшість цих реакцій мала легкий і середній ступінь тяжкості і відзначалася лише на початку лікування. Пацієнтам, які приймають Селінкро, не рекомендується керувати транспортними засобами та працювати з механізмами доти, доки не буде з'ясовано індивідуальну реакцію на препарат.Умови відпустки з аптекЗа рецептомВідео на цю тему
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
Состав, форма выпуска и упаковкаТаблетки, покрытые пленочной оболочкой - 1 табл.: активное вещество: цитизин - 1,5 мг; вспомогательные вещества: лактозы моногидрат — 28 мг; МКЦ — 67,5 мг; тальк — 2 мг; магния стеарат — 1 мг; оболонка плівкова: Опадрай II коричневий 8 F 26948 – 3 мг: полівініловий спирт частково гідролізований – 1,2 мг; титану діоксид (Е171) - 0,654 мг; макрогол 3350 - 0,606 мг; тальк – 0,444 мг; заліза оксид жовтий (Е172) – 0,062 мг, заліза оксид червоний (Е172) – 0,018 мг, заліза оксид чорний (Е172) – 0,016 мг. Пігулки, покриті плівковою оболонкою, 1,5 мг. У бл. із ПВХ-плівки/фольги алюмінієвої, 50 шт. 2 бл. у картонному вкладиші з календарем прийому в картонній пачці.Опис лікарської формиТаблетки: круглі, двоопуклі, покриті плівковою оболонкою світло-коричневого кольору. Вид на зламі – від білого до бежевого кольору.Фармакотерапевтична групаН-холіноміметичне.ФармакокінетикаФармакокінетичні дослідження на людях не проводились.ФармакодинамікаАлкалоїд цитизин, що є активною речовиною препарату, має н-холіноміметичну дію; збуджує ганглії вегетативної нервової системи, рефлекторно стимулює дихальний центр, викликає виділення адреналіну з мозкової речовини надниркових залоз, підвищує артеріальний тиск. При близькій схожості з механізмом дії нікотину, цитизин має набагато нижчу токсичність і більший терапевтичний індекс. Цитизин конкурентно пригнічує взаємодію нікотину з відповідними рецепторами, що веде до поступового зменшення та зникнення нікотинової залежності.Показання до застосуванняНікотинова залежність (для полегшення відмови від куріння). Фізична та психологічна залежність від нікотину вважається певним типом захворювання, що призводить до нездатності помірності від куріння, навіть при розумінні його негативних ефектів.Протипоказання до застосуваннягіперчутливість до активної або будь-якої з допоміжних речовин препарату; гострий інфаркт міокарда; нестабільна стенокардія; аритмія серця; нещодавно перенесене порушення мозкового кровообігу; атеросклероз; тяжка артеріальна гіпертензія; недостатність лактази, галактоземія, синдром мальабсорбції глюкози-галактози (до складу препарату входить лактоза); вагітність; період грудного вигодовування; вік до 18 та після 65 років. З обережністю: інші форми ішемічної хвороби серця (стабільна стенокардія, безсимптомна (тиха) ішемія міокарда, вазоспастична стенокардія, синдром "X" (мікросудинна стенокардія); серцева недостатність, підвищений АТ; захворювання судин головного мозку; облітеруючі артеріальні захворювання, гіпер шлунка, цукровий діабет, ниркова або печінкова недостатність, деякі форми шизофренії, наявність хромафінних пухлин надниркових залоз, гастроезофагеальна рефлюксна хвороба, особи з тривалим стажем куріння та особи старше 40-45 років.Вагітність та лактаціяТабекс не слід застосовувати жінкам під час вагітності та в період грудного вигодовування.Побічна діяПрепарат зазвичай добре переноситься, побічні явища, що спостерігаються, виражені слабо або помірно. Більшість із них з'являються на початку лікування та проходять самостійно. Найчастіше вони пов'язані з відмовою від тютюнопаління і виявляються запамороченням, головним болем та безсонням. У рекомендованих дозах препарат Табекс не викликає серйозних несприятливих ефектів. Можливі такі побічні дії З боку ССС: тахікардія, незначне підвищення артеріального тиску, відчуття серцебиття. З боку центральної нервової системи: головний біль, запаморочення, безсоння або сонливість, підвищена дратівливість. З боку дихальної системи: задишка. З боку шлунково-кишкового тракту: сухість у роті, нудота, біль у животі, запори, діарея, зміни смаку та апетиту. З боку скелетно-м'язової та сполучної тканини: біль у м'язах. З боку обміну речовин та харчування: зниження маси тіла, підвищене потовиділення. Інші: біль у грудній клітці.Взаємодія з лікарськими засобамиПісля припинення тютюнопаління можуть посилюватися побічні дії теофіліну, ропініролу, клозапіну та оланзапіну. При одночасному застосуванні препарату Табекс® з ацетилхоліном, карбахолом, галантаміном, піридостигміном, ривастигміном, дистигміном можливе посилення холіноміметичних побічних дій (слинотеча, сльозотеча, бронхіальна секреція з кашлем, терапія. підвищений тонус м'язів чи раптові скорочення м'язів). Застосування препарату Табекс одночасно з ловастатином, симвастатином, флувастатином, правастатином та ін. підвищує ризик появи болю в м'язах. Одночасне застосування препарату Табекс з гіпотензивними засобами (пропранолол та ін.) може послабити їхній ефект.Спосіб застосування та дозиВсередину повністю запиваючи достатньою кількістю рідини. Не слід перевищувати рекомендовані дози. Прийом препарату бажано розпочинати після встановлення пацієнта на повну відмову від куріння. Препарат слід застосовувати за наступною схемою: з 1 по 3 день - по 1 табл. 6 разів на день (кожні 2 години), поступово зменшуючи кількість викурених сигарет. Таблетку слід приймати між епізодами куріння для подовження інтервалів між викурюванням сигарет, щоб максимально знизити їхнє споживання. Інтервал прийому кожні 2 години повинен дотримуватися. Якщо результат незадовільний, лікування слід припинити і через 2-3 місяці можна почати його знову. При хорошому ефекті лікування продовжують за наступною схемою: з 4 по 12-й день - по 1 табл. кожні 2,5 год; з 13-го по 16-й день - по 1 табл. кожні 3 год; з 17-го по 20-й день – по 1 табл. кожні 5 год; з 21-го по 25-й день - по 1-2 табл. в день. Настійно рекомендується відмовитися від куріння не пізніше 5-го дня від початку лікування. Поєднання медикаментозної терапії із консультаціями, в т.ч. з заходами психологічної підтримки пацієнта, що достовірно підвищує ефективність лікування.ПередозуванняСимптоми: нудота, блювання, розширення зіниць, загальна слабкість, тахікардія, клонічні судоми, параліч дихання. Настають у разі, коли пацієнт не дотримується режиму дозування і приймає препарат у дозах, що у кілька разів перевищують терапевтичні. Лікування: промивання шлунка, призначення активованого вугілля, інфузійне введення водно-сольових розчинів, а також 5 або 10% розчину глюкози, призначення протисудомних засобів, кардіотоніків, дихальних аналептиків та інших симптоматичних засобів. Слід відстежувати роботу органів дихання, АТ та ЧСС.Запобіжні заходи та особливі вказівкиПрийом препарату слід розпочати лише тоді, коли пацієнт має серйозний намір відмовитись від куріння. Особам із тривалим стажем куріння та особам старше 40–45 років препарат Табекс слід застосовувати лише після консультації з лікарем. При застосуванні препарату не слід перевищувати рекомендованих доз. Лікування препаратом та продовження куріння може призвести до посилення побічних дій нікотину (нікотинова інтоксикація). Лікарський препарат містить допоміжну речовину лактозу. Пацієнтам з рідкісними спадковими проблемами непереносимості галактози, з лактазним дефіцитом (тип Лапп) або глюкозо-галактозною мальабсорбцією не слід застосовувати лікарський препарат. Вплив на здатність керувати транспортними засобами та працювати з механізмами. Хоча на тлі застосування препарату будь-якого негативного впливу на здатність керувати автотранспортом та роботу з механізмами не спостерігалося, проте внаслідок можливого виникнення сонливості та інших побічних реакцій слід бути обережним у перелічених ситуаціях.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Активна речовина: дисульфірам – 150 мг; Допоміжні речовини: крохмаль картопляний – 2,70 мг, целюлоза мікрокристалічна – 23,80 мг, кремнію діоксид колоїдний – 0,85 мг, кроскармелоза натрію – 0,85 мг, стеаринова кислота – 0,36 мг, магнію стеарат мг. По 10 таблеток у контурне осередкове пакування з плівки полівінілхлоридної та фольги алюмінієвої друкованої лакованої. По 3 або 5 контурних осередкових упаковок разом з інструкцією із застосування поміщають у пачку з картону.Опис лікарської формиКруглі, плоскоциліндричні пігулки білого або білого зі злегка жовтувато-зеленим відтінком кольору, з фаскою.Фармакотерапевтична групаЗасіб для лікування алкоголізму.ФармакокінетикаАбсорбція після перорального прийому – 70-90 %. Швидко метаболізується в печінці шляхом відновлення діетилдітіокарбамат, що виділяється у вигляді глюкуроніду нирками, або трансформується в діетиламін і сірковуглець, пропорція якого варіює від 4 до 53%. Останній виділяється через легені. Мінімальний вміст дисульфіраму в крові – близько 20 нг/мл.ФармакодинамікаДисульфірам інгібує фермент ацетальдегіддегідрогеназу, що бере участь у метаболізмі етанолу, що призводить до збільшення концентрації ацетальдегіду, що є метаболітом етанолу, в 5-10 разів. Ацетальдегід викликає ряд неприємних відчуттів: "припливи" крові до шкіри обличчя, нудоту, блювання, почуття нездужання, тахікардію, зниження артеріального тиску. В результаті відбувається вироблення умовно-рефлекторної реакції огиди до смаку та запаху спиртних напоїв. Сила реакцій, викликаних препаратом, пропорційна прийнятій дозі. Максимальний терапевтичний ефект досягається через 12 годин після перорального прийому та може тривати протягом 10-14 днів після припинення лікування. Чим триваліший курс терапії, тим більше виражені ефекти препарату.Показання до застосуванняДисульфірам використовується як допоміжна терапія хронічного алкоголізму у пацієнтів, які проходять лікування з приводу алкогольної залежності, які мають намір перебувати у стані утримання від алкоголю з метою досягнення найкращого ефекту підтримуючої та психотерапії. Дисульфірам не виліковує алкоголізм. При використанні як монотерапія, без відповідної мотивації та підтримуючого лікування не надає значного впливу на алкогольну поведінку в осіб з хронічним алкоголізмом.Протипоказання до застосуванняГіперчутливість, тиреотоксикоз, захворювання серцево-судинної системи (в т.ч., різко виражений кардіосклероз, атеросклероз мозкових судин, тяжке ураження міокарда, перед- та постінфарктні стани, аневризму аорти, оклюзія коронарних судин, артеріальна гіпертензія серцево-судинної системи в стадії декомпенсації), хронічна обструктивна хвороба легень, туберкульоз легень з кровохарканням, бронхіальна астма, виражена емфізема легень, ерозивні ураження слизової оболонки шлунково-кишкового тракту, виразкова хвороба шлунка та дванадцятипалої кишки ( кишкового тракту, хвороби нирок, печінкова недостатність, цукровий діабет, епілепсія, інфекційні захворювання центральної нервової системи, полінейропатія, неврит слухового та очного нервів,глаукоми, злоякісні пухлини, вагітність, період лактації. В окремих випадках при тривалому прийомі тетураму можуть спостерігатися гострі психози, що нагадують гострий алкогольний параноїд, гострий алкогольний галюциноз або алкогольний делірій. Можливий перехід галюцинаторного синдрому в параноїдний, параноїдний - в шизофреноподібний і т.д. Одночасний (або в недавньому минулому) прийом метронідазолу, паральдегіду, етанолу або етанолвмісних лікарських засобів та продуктів. Дитячий вік віком до 18 років. З обережністю: пацієнти старше 60 років, виразкова хвороба шлунка та дванадцятипалої кишки (в стадії ремісії), ендартеріїт, залишкові явища порушення мозкового кровообігу, психози на фоні прийому дисульфіраму в анамнезі.Вагітність та лактаціяПротипоказано застосовувати препарат при вагітності та в період годування груддю.Побічна дія"Металевий" присмак у роті, неприємний запах (обумовлений сірковуглецем) у хворих з колостомою, гепатит, неврит зорового нерва, периферичний неврит, поліневропатія нижніх кінцівок, нервово-психічні розлади, зниження пам'яті, дезорієнтація в часі та просторі, , шкірні алергічні реакції Побічні ефекти, зумовлені асоціацією дисульфіраметанол: колапс, аритмія, стенокардія, інфаркт міокарда, набряк мозку, крововилив у мозок.Взаємодія з лікарськими засобамиДисульфірам слід призначати з обережністю пацієнтам, які приймають фенітоїн та його похідні, оскільки одночасний прийом препаратів може призвести до інтоксикації фенітоїном. Перед призначенням дисульфіраму, хворим, які приймають фенітоїн, слід визначати базовий рівень фенітоїну в сироватці крові та надалі здійснювати контроль вмісту фенітоїну в крові з метою корекції дози препарату. Дисульфірам посилює ефект непрямих антикоагулянтів та збільшує ризик кровотеч. У разі одночасного призначення з пероральними антикоагулянтами необхідно здійснювати більш частий контроль вмісту протромбіну та корекцію доз антикоагулянтів. Необхідно також коригувати дозу дисульфіраму на початку та після закінчення курсу терапії, оскільки дисульфірам може подовжувати протромбіновий час. Ефекти дисульфіраму, зокрема. нейротоксичні,посилюють трициклічні антидепресанти (амітріптілін), метронідазол, ізоніазид. Метронідазол підвищує ризик розвитку порушень психіки, виникнення марення. При одночасному призначенні з ізоніазидом підвищується ризик виникнення порушень поведінки та координації рухів. При виявленні цих ознак прийом дисульфірів повинен бути припинений. Дисульфірам підвищує концентрацію в плазмі препаратів, що метаболізуються в печінці, внаслідок інгібування мікросомальних ферментів печінки. Посилює токсичні ефекти феназону, хлордіазепоксиду та діазепаму шляхом інгібування їх метаболізму. Аскорбінова кислота знижує реакцію на етанол.Спосіб застосування та дозиПеред початком лікування тривалість утримання від алкоголю повинна становити не менше 12 годин. Режим дозування на початку терапії Протягом 1 -2 перших тижнів лікування разова доза дисульфіраму повинна становити не більше 500 мг на добу. Препарат приймають вранці натще, перед сніданком. Зазвичай дисульфірам приймають у ранковий час, однак у разі появи седативного ефекту препарат може призначатися на ніч. Щоб мінімізувати або усунути седативний ефект, дозу можна скоригувати у бік зниження. Підтримуюча терапія Середня доза, що підтримує, становить 250 мг/с (діапазон від 125 до 500 мг), максимальна добова доза 500 мг. Тривалість терапії Щоденний регулярний прийом дисульфіраму повинен продовжуватися до повного одужання пацієнта, коли він може здійснювати самоконтроль над вживанням алкоголю. Прийом препарату має продовжуватись до досягнення стійкої ремісії.ПередозуванняСимптоми: сплутаність свідомості, колапс, коматозний стан, неврологічні ускладнення. Специфічного лікування передозування дисульфіраму немає. При тяжкій дисульфірам-алкогольній реакції тривалістю 1,5 год застосовують оксигенотерапію, вдихання карбогену (суміш 95 % кисню та 5 % вуглекислого газу), внутрішньовенно вводять високі дози аскорбінової кислоти (до 1 г), ефедрину сульфат та антигістамінний препарат. Необхідно моніторувати концентрацію калію в сироватці крові, особливо у випадках, якщо пацієнт приймає препарати наперстянки.Запобіжні заходи та особливі вказівкиПрепарат у жодному разі не можна приймати у стані алкогольної інтоксикації. Неприпустиме призначення препарату без попередження пацієнта. Родичі пацієнта повинні бути проінструктовані лікарем про особливості застосування препарату. Дисульфірам з особливою обережністю слід застосовувати при наступних супутніх захворюваннях: цукровий діабет, гіпотиреоз, епілепсія, хронічний та гострий нефрит, а також у пацієнтів віком від 65 років. Зареєстровані дані про гепатотоксичність препарату, включаючи печінкову недостатність, що потребує трансплантації печінки або смертельним наслідком. Тяжкі, а іноді летальні гепатити, спричинені терапією дисульфірамом, можуть розвинутись через багато місяців після завершення лікування препаратом. Пацієнта необхідно попередити про необхідність повідомляти лікаря про всі ранні симптоми прояву гепатиту, таких як швидка стомлюваність, слабкість, нездужання, зниження апетиту, нудота, блювання, жовтяниця, поява сечі темного кольору.Кожні 10-14 днів з початку терапії дисульфірамом пацієнту слід проводити контрольне дослідження параметрів функції печінки, включаючи загальний та біохімічний аналіз крові. Пацієнти, що приймають дисульфірам не повинні піддаватися впливу етилендіброміду та його пари. Результати досліджень на щурах продемонстрували, що інгаляційне введення етилендиброміду при застосуванні дисульфіраму підвищує розвиток пухлин та смертність у щурів. Аналогічних даних про дію пари діетилброміду на пацієнтів немає. Реакція взаємодії алкоголю та дисульфіраму: Пацієнт повинен бути поінформований про всі наслідки вживання алкоголю під час лікування дисульфірамом. Пацієнт повинен бути попереджений про неприпустимість таємного вживання алкоголю, а також алкоголю у складі харчових продуктів (соуси), лікарських препаратів (спиртсодержащіе лікарські засоби), парфумерії. Вживання алкоголю одночасно з дисульфірамом, навіть у невеликих кількостях викликає почервоніння обличчя, пульсацію в області голови та шиї, пульсуючий головний біль, утруднення дихання, нудоту, рвоту, пітливість, спрагу, біль за грудиною, почастішання серцебиття, задишку, слабкість, сплутаність і непритомність, виражене занепокоєння, запаморочення, порушення зору. У тяжких випадках може розвинутися пригнічення дихання, серцево-судинна недостатність, судоми та смерть. Інтенсивність реакції індивідуальна, але, як правило, пропорційна прийнятій внутрішньо кількості алкоголю і дисульфіраму. Початкові прояви реакції можуть спостерігатися у осіб з підвищеною чутливістю зі збільшенням концентрації алкоголю всього до 5-10 мг на 100 мл крові. Повний розвиток симптомів розвивається при концентрації алкоголю 50 мг на 100 мл. крові. При рівні алкоголю у крові від 125 мг до 150 мг на 100 мл відзначається непритомність. Тривалість реакції варіює від 30 - 60 хв до кількох годин; у тяжких випадках - до того часу, поки алкоголь визначається у крові. Вплив на здатність до керування автотранспортом та управління механізмами Препарат впливає здатність керувати транспортними засобами чи роботу з іншими механізмами.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Активна речовина: дисульфірам – 150 мг; Допоміжні речовини: крохмаль картопляний – 2,70 мг, целюлоза мікрокристалічна – 23,80 мг, кремнію діоксид колоїдний – 0,85 мг, кроскармелоза натрію – 0,85 мг, стеаринова кислота – 0,36 мг, магнію стеарат мг. По 10 таблеток у контурне осередкове пакування з плівки полівінілхлоридної та фольги алюмінієвої друкованої лакованої. По 3 або 5 контурних осередкових упаковок разом з інструкцією із застосування поміщають у пачку з картону.Опис лікарської формиКруглі, плоскоциліндричні пігулки білого або білого зі злегка жовтувато-зеленим відтінком кольору, з фаскою.Фармакотерапевтична групаЗасіб для лікування алкоголізму.ФармакокінетикаАбсорбція після перорального прийому – 70-90 %. Швидко метаболізується в печінці шляхом відновлення діетилдітіокарбамат, що виділяється у вигляді глюкуроніду нирками, або трансформується в діетиламін і сірковуглець, пропорція якого варіює від 4 до 53%. Останній виділяється через легені. Мінімальний вміст дисульфіраму в крові – близько 20 нг/мл.ФармакодинамікаДисульфірам інгібує фермент ацетальдегіддегідрогеназу, що бере участь у метаболізмі етанолу, що призводить до збільшення концентрації ацетальдегіду, що є метаболітом етанолу, в 5-10 разів. Ацетальдегід викликає ряд неприємних відчуттів: "припливи" крові до шкіри обличчя, нудоту, блювання, почуття нездужання, тахікардію, зниження артеріального тиску. В результаті відбувається вироблення умовно-рефлекторної реакції огиди до смаку та запаху спиртних напоїв. Сила реакцій, викликаних препаратом, пропорційна прийнятій дозі. Максимальний терапевтичний ефект досягається через 12 годин після перорального прийому та може тривати протягом 10-14 днів після припинення лікування. Чим триваліший курс терапії, тим більше виражені ефекти препарату.Показання до застосуванняДисульфірам використовується як допоміжна терапія хронічного алкоголізму у пацієнтів, які проходять лікування з приводу алкогольної залежності, які мають намір перебувати у стані утримання від алкоголю з метою досягнення найкращого ефекту підтримуючої та психотерапії. Дисульфірам не виліковує алкоголізм. При використанні як монотерапія, без відповідної мотивації та підтримуючого лікування не надає значного впливу на алкогольну поведінку в осіб з хронічним алкоголізмом.Протипоказання до застосуванняГіперчутливість, тиреотоксикоз, захворювання серцево-судинної системи (в т.ч., різко виражений кардіосклероз, атеросклероз мозкових судин, тяжке ураження міокарда, перед- та постінфарктні стани, аневризму аорти, оклюзія коронарних судин, артеріальна гіпертензія серцево-судинної системи в стадії декомпенсації), хронічна обструктивна хвороба легень, туберкульоз легень з кровохарканням, бронхіальна астма, виражена емфізема легень, ерозивні ураження слизової оболонки шлунково-кишкового тракту, виразкова хвороба шлунка та дванадцятипалої кишки ( кишкового тракту, хвороби нирок, печінкова недостатність, цукровий діабет, епілепсія, інфекційні захворювання центральної нервової системи, полінейропатія, неврит слухового та очного нервів,глаукоми, злоякісні пухлини, вагітність, період лактації. В окремих випадках при тривалому прийомі тетураму можуть спостерігатися гострі психози, що нагадують гострий алкогольний параноїд, гострий алкогольний галюциноз або алкогольний делірій. Можливий перехід галюцинаторного синдрому в параноїдний, параноїдний - в шизофреноподібний і т.д. Одночасний (або в недавньому минулому) прийом метронідазолу, паральдегіду, етанолу або етанолвмісних лікарських засобів та продуктів. Дитячий вік віком до 18 років. З обережністю: пацієнти старше 60 років, виразкова хвороба шлунка та дванадцятипалої кишки (в стадії ремісії), ендартеріїт, залишкові явища порушення мозкового кровообігу, психози на фоні прийому дисульфіраму в анамнезі.Вагітність та лактаціяПротипоказано застосовувати препарат при вагітності та в період годування груддю.Побічна дія"Металевий" присмак у роті, неприємний запах (обумовлений сірковуглецем) у хворих з колостомою, гепатит, неврит зорового нерва, периферичний неврит, поліневропатія нижніх кінцівок, нервово-психічні розлади, зниження пам'яті, дезорієнтація в часі та просторі, , шкірні алергічні реакції Побічні ефекти, зумовлені асоціацією дисульфіраметанол: колапс, аритмія, стенокардія, інфаркт міокарда, набряк мозку, крововилив у мозок.Взаємодія з лікарськими засобамиДисульфірам слід призначати з обережністю пацієнтам, які приймають фенітоїн та його похідні, оскільки одночасний прийом препаратів може призвести до інтоксикації фенітоїном. Перед призначенням дисульфіраму, хворим, які приймають фенітоїн, слід визначати базовий рівень фенітоїну в сироватці крові та надалі здійснювати контроль вмісту фенітоїну в крові з метою корекції дози препарату. Дисульфірам посилює ефект непрямих антикоагулянтів та збільшує ризик кровотеч. У разі одночасного призначення з пероральними антикоагулянтами необхідно здійснювати більш частий контроль вмісту протромбіну та корекцію доз антикоагулянтів. Необхідно також коригувати дозу дисульфіраму на початку та після закінчення курсу терапії, оскільки дисульфірам може подовжувати протромбіновий час. Ефекти дисульфіраму, зокрема. нейротоксичні,посилюють трициклічні антидепресанти (амітріптілін), метронідазол, ізоніазид. Метронідазол підвищує ризик розвитку порушень психіки, виникнення марення. При одночасному призначенні з ізоніазидом підвищується ризик виникнення порушень поведінки та координації рухів. При виявленні цих ознак прийом дисульфірів повинен бути припинений. Дисульфірам підвищує концентрацію в плазмі препаратів, що метаболізуються в печінці, внаслідок інгібування мікросомальних ферментів печінки. Посилює токсичні ефекти феназону, хлордіазепоксиду та діазепаму шляхом інгібування їх метаболізму. Аскорбінова кислота знижує реакцію на етанол.Спосіб застосування та дозиПеред початком лікування тривалість утримання від алкоголю повинна становити не менше 12 годин. Режим дозування на початку терапії Протягом 1 -2 перших тижнів лікування разова доза дисульфіраму повинна становити не більше 500 мг на добу. Препарат приймають вранці натще, перед сніданком. Зазвичай дисульфірам приймають у ранковий час, однак у разі появи седативного ефекту препарат може призначатися на ніч. Щоб мінімізувати або усунути седативний ефект, дозу можна скоригувати у бік зниження. Підтримуюча терапія Середня доза, що підтримує, становить 250 мг/с (діапазон від 125 до 500 мг), максимальна добова доза 500 мг. Тривалість терапії Щоденний регулярний прийом дисульфіраму повинен продовжуватися до повного одужання пацієнта, коли він може здійснювати самоконтроль над вживанням алкоголю. Прийом препарату має продовжуватись до досягнення стійкої ремісії.ПередозуванняСимптоми: сплутаність свідомості, колапс, коматозний стан, неврологічні ускладнення. Специфічного лікування передозування дисульфіраму немає. При тяжкій дисульфірам-алкогольній реакції тривалістю 1,5 год застосовують оксигенотерапію, вдихання карбогену (суміш 95 % кисню та 5 % вуглекислого газу), внутрішньовенно вводять високі дози аскорбінової кислоти (до 1 г), ефедрину сульфат та антигістамінний препарат. Необхідно моніторувати концентрацію калію в сироватці крові, особливо у випадках, якщо пацієнт приймає препарати наперстянки.Запобіжні заходи та особливі вказівкиПрепарат у жодному разі не можна приймати у стані алкогольної інтоксикації. Неприпустиме призначення препарату без попередження пацієнта. Родичі пацієнта повинні бути проінструктовані лікарем про особливості застосування препарату. Дисульфірам з особливою обережністю слід застосовувати при наступних супутніх захворюваннях: цукровий діабет, гіпотиреоз, епілепсія, хронічний та гострий нефрит, а також у пацієнтів віком від 65 років. Зареєстровані дані про гепатотоксичність препарату, включаючи печінкову недостатність, що потребує трансплантації печінки або смертельним наслідком. Тяжкі, а іноді летальні гепатити, спричинені терапією дисульфірамом, можуть розвинутись через багато місяців після завершення лікування препаратом. Пацієнта необхідно попередити про необхідність повідомляти лікаря про всі ранні симптоми прояву гепатиту, таких як швидка стомлюваність, слабкість, нездужання, зниження апетиту, нудота, блювання, жовтяниця, поява сечі темного кольору.Кожні 10-14 днів з початку терапії дисульфірамом пацієнту слід проводити контрольне дослідження параметрів функції печінки, включаючи загальний та біохімічний аналіз крові. Пацієнти, що приймають дисульфірам не повинні піддаватися впливу етилендіброміду та його пари. Результати досліджень на щурах продемонстрували, що інгаляційне введення етилендиброміду при застосуванні дисульфіраму підвищує розвиток пухлин та смертність у щурів. Аналогічних даних про дію пари діетилброміду на пацієнтів немає. Реакція взаємодії алкоголю та дисульфіраму: Пацієнт повинен бути поінформований про всі наслідки вживання алкоголю під час лікування дисульфірамом. Пацієнт повинен бути попереджений про неприпустимість таємного вживання алкоголю, а також алкоголю у складі харчових продуктів (соуси), лікарських препаратів (спиртсодержащіе лікарські засоби), парфумерії. Вживання алкоголю одночасно з дисульфірамом, навіть у невеликих кількостях викликає почервоніння обличчя, пульсацію в області голови та шиї, пульсуючий головний біль, утруднення дихання, нудоту, рвоту, пітливість, спрагу, біль за грудиною, почастішання серцебиття, задишку, слабкість, сплутаність і непритомність, виражене занепокоєння, запаморочення, порушення зору. У тяжких випадках може розвинутися пригнічення дихання, серцево-судинна недостатність, судоми та смерть. Інтенсивність реакції індивідуальна, але, як правило, пропорційна прийнятій внутрішньо кількості алкоголю і дисульфіраму. Початкові прояви реакції можуть спостерігатися у осіб з підвищеною чутливістю зі збільшенням концентрації алкоголю всього до 5-10 мг на 100 мл крові. Повний розвиток симптомів розвивається при концентрації алкоголю 50 мг на 100 мл. крові. При рівні алкоголю у крові від 125 мг до 150 мг на 100 мл відзначається непритомність. Тривалість реакції варіює від 30 - 60 хв до кількох годин; у тяжких випадках - до того часу, поки алкоголь визначається у крові. Вплив на здатність до керування автотранспортом та управління механізмами Препарат впливає здатність керувати транспортними засобами чи роботу з іншими механізмами.Умови відпустки з аптекЗа рецептомВідео на цю тему