Лекарства и БАД Со скидкой
Склад, форма випуску та упаковкаГлюкоза, аскорбінова кислота (вітамін С), мальтодекстрин (носій), стеаринова кислота, стеарат кальцію та дикосид кремнію аморфний (агенти антистежують), крохмаль кукурудзяний (носій), ароматизатори натуральні "Лимон", "Апельсин".ХарактеристикаАскорбінову кислоту, як аналог натурального вітаміну С, отримали швейцарські вчені в 1933 році, а назвали її так за здатність боротися з цингою, яку за старих часів називали «скорбут». Вітамін С рекомендується вживати як під час застуди, так і для профілактики різних вірусних інфекцій, тому прийом аскорбінової кислоти особливо актуальний в осінньо-зимовий період для підтримки організму. Згідно зі статистичними даними, оприлюдненими ВООЗ (Всесвітньою організацією охорони здоров'я), брак вітаміну С відчуває майже 95 % жителів нашої планети. А у 20–25% росіян рівень вітаміну С в організмі нижчий за норму навіть улітку. Вітамін С, життєво необхідний людині, не синтезується організмом самостійно. Саме тому важливо, щоб він надходив у достатній кількості із зовнішніх джерел. Його можна отримувати із продуктів харчування або біологічно активних добавок. Аскорбінова кислота (вітамін С) бере активну участь практично у всіх процесах життєдіяльності. Її дефіцит призводить до ослаблення імунної системи, тому людина частіше зазнає застудних захворювань.РекомендуєтьсяАскорбінову кислоту Евалар у формі жувальних таблеток з натуральним цитрусовим смаком можна приймати як додаткове джерело вітаміну С. Вона легко засвоюється організмом: речовина, розчиняючись вже в ротовій порожнині, швидше потрапляє в кров і проникає в клітини. Рекомендується не тільки дорослим, але й дітям з 3 років, вагітним і жінкам, що годують.Протипоказання до застосуванняІндивідуальна нестерпність компонентів.Спосіб застосування та дозиДорослим - по 1-3 таблетки на день під час їжі, дітям старше 3 років - по 1 таблетці на день, вагітним і жінкам, що годують, - по 3 таблетки на день протягом 10-15 днів, потім - по 1 таблетці на день. Тривалість прийому – 1 місяць.Запобіжні заходи та особливі вказівкиПеред застосуванням рекомендується проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаЖир борсука топлений.ХарактеристикаСприяє зниженню інтенсивності інфекційно-запального процесу при хронічному бронхіті, збільшує ефективність лікарської терапії позалікарняної пневмонії, має муколітичну дію, ефективний для профілактики (у комплексній терапії) запальних захворювань дихальних шляхів, надає загальнозміцнюючу дію.РекомендуєтьсяПростудні захворювання; бронхіти із астматичними компонентами; важкі та затяжні форми пневмонії; силікоз легень; туберкульоз легень; медикаментозна інтоксикація; захворювання шлунково-кишкового тракту; гастрит та виразка шлунка та дванадцятипалої кишки; атеросклероз; захворювання серцево-судинної системи; гіпертонічна хвороба; тромбофлебіт; порушення мозкового кровообігу; рахіт; дистрофія.Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність, годування груддю, захворювання печінки та жовчовивідних шляхів у стадії загострення.Спосіб застосування та дозиДорослим по 1 чайній ложці (3г) щодня під час їжі. Тривалість прийому – 1 місяць, можна повторювати 2-3 рази на рік.Запобіжні заходи та особливі вказівкиПеред застосуванням рекомендується проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
Дозування: 5% Форма випуску: крем для зовнішнього застосування Упаковка: туба Производитель: Фарметрикс ООО Завод-производитель: Фарметрикс ООО(Россия). . .
ХарактеристикаАскорбінова кислота відіграє важливу роль у регуляції окисно-відновних процесів, вуглеводного обміну, згортання крові, регенерації тканин, сприяє підвищенню опірності організму. Аскорбінова кислота (вітамін С) не утворюється в організмі людини, а надходить лише з їжею. При збалансованому та повноцінному харчуванні людина не відчуває дефіциту у вітаміні С.РекомендуєтьсяПрофілактика та лікування гіповітамінозу вітаміну С. При підвищеній потребі організму у вітаміні С: у період активного зростання у дітей, вагітності, грудного вигодовування, при підвищених фізичних та розумових навантаженнях, перевтомі, стресових станах, у період одужання після тривалих та тяжких захворювань.Протипоказання до застосуванняПідвищена чутливість до компонентів Аскорбінової кислоти. Не слід призначати великі дози хворим з підвищеною згортанням крові, тромбофлебітами та схильністю до тромбозів, а також при цукровому діабеті та станах, що супроводжуються підвищеним вмістом цукру в крові.Вагітність та лактаціяМінімальна щоденна потреба в аскорбіновій кислоті у ІІ-ІІІ триместрах вагітності – близько 60 мг. Мінімальна щоденна потреба у період грудного вигодовування – 80 мг. Дієта матері, що містить адекватну кількість аскорбінової кислоти, достатня для профілактики дефіциту вітаміну С у немовляти (рекомендується не перевищувати матері-годувальниці максимум щомісячної потреби в аскорбіновій кислоті).Побічна діяАлергічні реакції до компонентів препарату, подразнення слизової оболонки шлунково-кишкового тракту (нудота, блювання, діарея, спазми шлунка), при застосуванні у високих дозах – гіпероксалатурія та утворення сечового каміння з кальцію оксалату; пригнічення функції інсулярного апарату підшлункової залози (гіперглікемія, глюкозурія). Лабораторні показники: тромбоцитоз, гіперпротромбінемія, еритропенія, нейтрофільний лейкоцитоз, гіпокаліємія.Спосіб застосування та дозиАскорбінова кислота приймається внутрішньо після їжі. З профілактичною метою призначають: Дорослим – по 50-100 мг на добу; дітям 25 мг на добу. У період вагітності та лактації по 300 мг на добу. Протягом 10-15 днів, потім по 100 мг на добу. З лікувальною метою призначають: Дорослим – по 50-100 мг 3-5 разів на день; дітям по 50-100 мг 2-3 десь у день. Тривалість лікування залежить від характеру та перебігу захворювання та рекомендується лікарем.Запобіжні заходи та особливі вказівкиПеред застосуванням рекомендується проконсультуватися з лікарем.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
Дозировка: 5 % Форма выпуска: крем д/наружного применения Упаковка: туба Производитель: Фарметрикс ООО Завод-производитель: Фарметрикс ООО(Россия). . .
293,00 грн
268,00 грн
Дозування: 5% Форма випуску: крем для зовнішнього застосування Упаковка: туба Виробник: Фарметрікс ТОВ Завод-виробник: Фарметрікс ТОВ(Росія). . .
Склад, форма випуску та упаковкаВ 1 таблетці міститься: сорбіт (підсолоджувач), ксиліт (підсолоджувач), магнію стеарат (глазувач), холекальциферол (Вітамін D3). Містить підсолоджувачі. При надмірному вживанні може мати проносну дію.
Дозування: 1 мг Фасування: N10 Форма випуску: ліофілізат д/приготування розчину Упаковка: амп. Діюча речовина: Тирозил-D-аланіл-гліцил-фенілаланіл-лейцил-аргініну діацетат. .
Склад, форма випуску та упаковкаПігулки - 1 таб. Аскорбінова кислота (вітамін С) – 50 мг; Рутозид (Рутін) – 50 мг; Допоміжні компоненти: - До 330 мг; Сахароза (цукор – пісок) – 152,1 мг; Крохмаль картопляний – 68,6 мг; Тальк – 6,4 мг; Кальція стеарат – 2,9 мг. По 10 або 50 таблеток у контурні осередкові упаковки. По 5 контурних упаковок по 10 таблеток разом з інструкцією із застосування поміщають у пачку з картону. Контурні осередкові упаковки по 50 таблеток разом з інструкціями із застосування (за кількістю упаковок) поміщають у групову упаковку.Опис лікарської формиТаблетки від жовтого до жовтого із зеленуватим відтінком кольору з незначними вкрапленнями від зеленого до коричневого кольору, плоскоциліндричної форми з ризиком та фаскою.Фармакотерапевтична групаВітамін.ФармакодинамікаАскорбінова кислота бере участь у регуляції окисно-відновних реакцій, вуглеводного обміну, синтезі колагену. Рутозид усуває підвищену проникність капілярів, зміцнює судинну стінку.Показання до застосуванняГіпо- та авітаміноз аскорбінової кислоти та рутозиду. У складі комплексної терапії захворювань, що супроводжуються порушенням проникності судин: при варикозному розширенні вен, трофічних порушеннях та виразках шкіри, при хронічній венозній недостатності, геморагічному діатезі.Протипоказання до застосуванняПідвищена чутливість до компонентів препарату, дитячий вік, вагітність (I триместр). З обережністю: стани, що супроводжуються гіперкоагуляцією крові та схильністю до тромбозів, тромбофлебіт.Вагітність та лактаціяПри вагітності (II та III триместр) та в період лактації застосовують, якщо передбачувана користь для матері перевищує ризик для плода та дитини.Побічна діяАлергічні реакції, диспепсичні розлади, біль голови.Взаємодія з лікарськими засобамиАскорбінова кислота підвищує всмоктування лікарських засобів групи пеніциліну, заліза; знижує клінічний ефект гепарину та непрямих антикоагулянтів.Спосіб застосування та дозиВсередину, по 1 таблетці 2-3 рази на день під час або після їди. Курс лікування – 2-3 тижні.ПередозуванняЗастосування надмірних доз препарату може спричинити нудоту, блювання, пронос, біль голови. Лікування: симптоматичне, форсований діурез.Запобіжні заходи та особливі вказівкиВплив на здатність до керування автотранспортом та управління механізмами Не впливає на здатність до керування автотранспортним засобом та заняттям будь-якими потенційно небезпечними видами діяльності.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаЦукор, декстроза моногідрат, натрій двовуглекислий, лізоциму гідрохлорид, антистежуючий агент стеарат кальцію, антистежуючий агент діоксид кремнію, ароматизатор -ментол-, ароматизатор Холодок, ароматизатор Тутті-фрутті, загусник карбоксиметилцелюлоза, пантотенат кальцію, піридокси. Харчова цінність 1 таблетки (0,7 г): вміст вуглеводів – 0,6 г; енергетична цінність – 10 кДж/3 ккал.ХарактеристикаЕфективний для боротьби з дискомфортом у горлі, у т. ч. за перших ознак застуди (відчуття нездужання, після переохолодження, після перебування в закритому приміщенні з великою кількістю людей, у період вірусної активності). Ефективність таблеток досягається за рахунок унікального складу: з одного боку лізоцим – який допомагає організму боротися з вірусом та пом'якшувати запалення; з іншого - вітамінний комплекс В5 і В6, який допомагає відновити слизову оболонку і перешкоджає повторному розвитку запалення. Таблетки БАРСУКОР мають приємний смак та освіжають дихання, що також важливо при захворюваннях горла.РекомендуєтьсяЯк БАД до їжі - додаткового джерела вітамінів В5 та В6, що містить лізоцим.Протипоказання до застосуванняІндивідуальна нестерпність компонентів продукту.Спосіб застосування та дозиПісля їди, повільно розсмоктуючи таблетку в роті, не розжовуючи і не запиваючи. Тривалість прийому – до 10 днів. За потреби прийом БАД можна повторити.Запобіжні заходи та особливі вказівкиПеред застосуванням рекомендується проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Аскорбінова кислота - 50 мг, рутозид - 50 мг; Допоміжні речовини: сахароза (цукор білий) – 201,9 мг, крохмаль картопляний – 5,46 мг, крохмаль кукурудзяний – 13,54 мг, кальцію стеарат – 3,3 мг, тальк – 5,8 мг.Опис лікарської формикруглі, плоскоциліндричні таблетки світлого зеленувато-жовтого кольору з вкрапленнями, з плоскою поверхнею, з фаскою та ризиком.ХарактеристикаАскорутин-вітамін, що містить аскорбінову кислоту та рутозид. Аскорбінова кислота бере участь у регуляції окисно-відновних процесів, вуглеводного обміну, згортання крові, регенерації тканин, сприяє підвищенню опірності організму. Рутозид усуває підвищену проникність капілярів, зміцнює судинну стінку, зменшуючи її набряклість та запалення. Має антиагрегантну дію, що сприяє поліпшенню мікроциркуляції. Аскорутин застосовують у комплексній терапії при варикозному розширенні вен, трофічних порушеннях та виразках шкіри, при хронічній венозній недостатності та при геморагічному діатезі. Препарат випускається у формі пігулок. Таблетки можна приймати як під час, так і після їди. Відпускається без рецепта.Фармакотерапевтична групавітамінФармакодинамікаАскорбінова кислота бере участь у регуляції окисно-відновних процесів, вуглеводного обміну, згортання крові, регенерації тканин, сприяє підвищенню опірності організму. Рутозид (похідна рутина) усуває підвищену проникність капілярів, зміцнює судинну стінку, зменшуючи її набряклість та запалення. Має антиагрегантну дію, що сприяє поліпшенню мікроциркуляції.Показання до застосуванняГіпо- та авітаміноз аскорбінової кислоти та рутозиду. У складі комплексної терапії при варикозному розширенні вен, трофічних порушеннях та виразках шкіри, при хронічній венозній недостатності; при геморагічному діатезі.Протипоказання до застосування- Підвищена індивідуальна чутливість до компонентів препарату; вроджена непереносимість фруктози, глюкозогалактозна мальабсорбція, дефіцит сахарази/ізомальтази, дитячий вік. З обережністю: Стани, що супроводжуються гіперкоагуляцією крові та схильністю до тромбозів, тромбофлебіт, цукровий діабет. Якщо у Вас є одне з перелічених захворювань, перед прийомом препарату обов'язково проконсультуйтеся з лікарем.Вагітність та лактаціяЧерез вміст у препараті рутину його не слід застосовувати в І триместрі вагітності. При вживанні препарату при вагітності та в період грудного вигодовування необхідно дотримуватись дозування та тривалість курсу прийому, призначені лікарем.Побічна діяМожливі алергічні реакції (шкірні висипи), диспепсичні розлади, головний біль. Якщо будь-які вказані в інструкції побічні ефекти посилюються, або Ви помітили будь-які інші побічні ефекти, не вказані в інструкції, повідомте про це лікаря.Взаємодія з лікарськими засобамиАскорбінова кислота підвищує всмоктування лікарських засобів групи пеніциліну, заліза; знижує клінічний ефект гепарину та непрямих антикоагулянтів, що потребує корекції доз при їх одночасному застосуванні.Спосіб застосування та дозиВсередину по 1 таблетці 2-3 рази на добу під час або після їди. Курс лікування – 2-3 тижні.ПередозуванняЗастосування надмірних доз препарату може спричинити нудоту, блювання, діарею, головний біль. Лікування: симптоматичне, форсований діурез.Умови відпустки з аптекБез рецептаВідео на цю тему
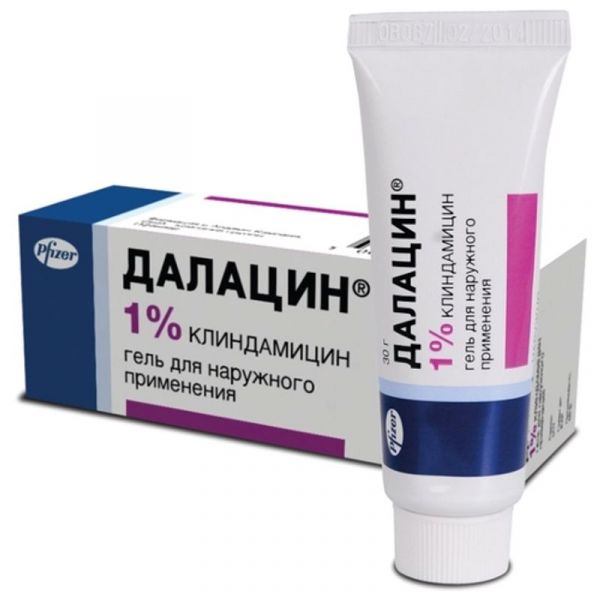
Склад, форма випуску та упаковкаСупозиторії вагінальні тверді, торпедоподібної форми, з гладкою поверхнею, білого або майже білого кольору. 1 супп.: Активна речовина: кліндаміцин (у формі фосфату) – 100 мг; Допоміжні речовини: твердий жир (Witepsol H-32, суміш тригліцеридів, дигліцеридів та моногліцеридів) – близько 2.4 г. 3 шт. - стрипи з ламінованої фольги; - пачки картонні. 3 шт. - стрипи з ламінованої фольги в комплекті з аплікатором - картонні пачки.Фармакотерапевтична групаАнтибіотик групи лінкозамідів для місцевого застосування. Кліндаміцину фосфат не активний in vitro, але швидко гідролізується in vivo з утворенням кліндаміцину, що має антибактеріальну активність. Кліндаміцин пригнічує синтез білків у мікробній клітині за рахунок взаємодії з 50S-субодиницею рибосом. В умовах in vitro до кліндаміцину чутливі такі мікроорганізми, що викликають бактеріальні вагінози: Gardnerella vaginalis, Mobiluncus spp., Mycoplasma hominis, Bacteroides spp., Peptostreptococcus spp.ФармакокінетикаВсмоктування Після застосування кліндаміцину інтравагінально в дозі 100 мг 1 раз на добу (у формі супозиторіїв) протягом 3 днів приблизно 30% (6-70%) введеної дози кліндаміцину всмоктується у системний кровотік, при цьому AUC становить 3.2 мкг/год/мл (0.42 -11 мкг/год/мл). Cmax у сироватці крові досягається приблизно через 5 год (1-10 год) після введення вагінального супозиторію і становить на 3-й день терапії в середньому 0.27 мкг/мл (0.03-0.67 мкг/мл). Системна дія кліндаміцину при введенні інтравагінально значно слабша, ніж при введенні в терапевтичних дозах внутрішньо або внутрішньовенно. Виведення У середньому Т1/2 становить 11 год (4-35 год). Фармакокінетика у спеціальних груп пацієнтів У клінічних дослідженнях кліндаміцину у формі вагінальних супозиторіїв брало участь недостатня кількість пацієнтів віком 65 років і старше, щоб можна було оцінити різницю у клінічній відповіді на терапію між зазначеною віковою групою та молодшими пацієнтами.Клінічна фармакологіяАнтибіотик для місцевого застосування у гінекології. мІнструкціяВведення супозиторіїв без аплікатора: Необхідно витягти супозиторій із фольги. У положенні лежачи на спині підтягнути коліна до грудей. Обережно ввести супозиторій у піхву за допомогою середнього пальця руки якнайглибше. Введення супозиторіїв за допомогою аплікатора: Пластиковий аплікатор, що міститься в упаковці з препаратом, призначений для полегшення введення супозиторію у піхву. Необхідно витягти супозиторій із фольги. Слід помістити плоский кінець супозиторію в отвір аплікатора. У положенні лежачи на спині підтягнути коліна до грудей. Тримаючи аплікатор горизонтально за ребристий кінець корпусу, обережно ввести його в піхву якнайглибше. Повільно натискаючи на поршень, ввести супозиторій у піхву. Слід обережно витягти аплікатор із піхви. Після кожного використання аплікатор слід вимити теплою водою з милом та дати йому повністю висохнути.Показання до застосуванняБактеріальний вагіноз.Протипоказання до застосуванняпідвищена чутливість до кліндаміцину, лінкоміцину або будь-якого компонента препарату; антибіотик-асоційований коліт в анамнезі; вік до 18 років (дані з безпеки та ефективності відсутні).Вагітність та лактаціяПри застосуванні кліндаміцину інтравагінально у ІІ або ІІІ триместрі вагітності збільшення частоти вроджених аномалій плода не відзначалося. Якщо Далацин® вагінальні супозиторії застосовується під час II або III триместрів вагітності (хоча офіційних досліджень із застосування супозиторіїв у вагітних жінок не проводилося), то несприятливий вплив на плід представляється малоймовірним. Застосування препарату у ІІ-ІІІ триместрі вагітності можливе, якщо потенційна користь для матері перевершує ризик для плода. Адекватних контрольованих досліджень із застосування препарату в І триместрі вагітності не проводилося, тому Далацин® вагінальні супозиторії можна призначати жінкам у I триместрі вагітності тільки за абсолютними показаннями, тобто. коли потенційна користь терапії препаратом перевищує потенційний ризик для плода. У дослідженнях на тваринах при введенні кліндаміцину підшкірно або внутрішньо будь-яких негативних впливів на плід не виявлено, за винятком випадків прийому препарату в дозах, токсичних для матері. Невідомо, чи виділяється кліндаміцин із грудним молоком після інтравагінального застосування. Кліндаміцин виявлений у грудному молоці після перорального або парентерального введення, тому в період грудного вигодовування слід або скасувати застосування препарату, або припинити грудне вигодовування з огляду на ступінь важливості застосування препарату для матері. Протипоказано застосування препарату віком до 18 років (дані щодо безпеки та ефективності відсутні).Побічна діяБезпеку застосування кліндаміцину у формі вагінальних супозиторіїв оцінювали у невагітних жінок. Таблиця. Небажані лікарські реакції Часто (від ≥1/100 до <1/10) Нечасто (від ≥ 1/1000 до <1/100) Частота невідома (неможливо оцінити на основі наявних даних) Інфекційні та паразитарні захворювання Грибкові інфекції, інфекції, спричинені грибами роду Candida З боку нервової системи Головний біль З боку травної системи Біль у животі, діарея, нудота Блювота Псевдомембранозний коліт З боку шкіри та підшкірних тканин Сверблячка шкіри Висип З боку кістково-м'язової системи Біль у боці З боку сечовидільної системи Пієлонефрит, дизурія З боку статевої системи Вульвовагінальний кандидоз, вульвовагінальний біль, вульвовагінальні розлади Вагінальні інфекції, виділення з піхви, порушення менструального циклу Загальні розлади та реакції у місці введення Біль у місці введення, свербіж (у місці введення), локалізовані набряк, біль, гіпертермія Взаємодія з лікарськими засобамиІснує перехресна резистентність між кліндаміцином та лінкоміцином. В умовах in vitro продемонстровано антагонізм між кліндаміцином та еритроміцином. Встановлено, що кліндаміцин порушує нейром'язову передачу і, отже, може посилювати дію міорелаксантів периферичної дії, тому препарат слід застосовувати з обережністю у пацієнтів, які отримують препарати цієї групи. Оскільки інформація щодо застосування з іншими препаратами для інтравагінального введення відсутня, спільне застосування препарату з іншими інтравагінальними засобами не рекомендується.Спосіб застосування та дозиДоза, що рекомендується, становить 1 супозиторій інтравагінально переважно перед сном протягом 3 днів поспіль.ПередозуванняПри інтравагінальному застосуванні супозиторіїв Далацин® можлива абсорбція кліндаміцину в кількостях, достатніх для розвитку системних реакцій. Випадкове потрапляння препарату в ШКТ може викликати системні ефекти, подібні до тих, що виникають після прийому внутрішньо кліндаміцину в терапевтичних дозах. До можливих системних побічних ефектів можна віднести діарею, геморагічну діарею, включаючи псевдомембранозний коліт. Лікування: проведення симптоматичної та підтримуючої терапії.Запобіжні заходи та особливі вказівкиДо призначення препарату за допомогою відповідних лабораторних методів слід виключити вульвовагініт, спричинений Trichomonas vaginalis, Chlamydia trachomatis, Neisseria gonorrhoeae, Candida albicans та вірусом Herpes simplex. Інтравагінальне застосування кліндаміцину може призвести до посиленого зростання нечутливих мікроорганізмів, особливо дріжджоподібних грибів. Застосування кліндаміцину (як і практично всіх антибіотиків) внутрішньо або парентерально пов'язане з розвитком важкої діареї та у ряді випадків псевдомембранозного коліту. При розвитку вираженої або тривалої діареї препарат слід відмінити та за необхідності провести відповідні діагностичні та лікувальні заходи. Пацієнток необхідно попередити, що під час терапії препаратом слід уникати статевих контактів, а також застосування інших засобів для інтравагінального введення (тампони, спринцювання). Препарат містить компоненти, які можуть зменшувати міцність виробів із латексу або каучуку (презервативи, протизаплідні вагінальні діафрагми). Тому використання подібних виробів під час лікування Далацином та протягом 72 годин після застосування не рекомендується. Не рекомендується застосування препарату Далацин супозиторії вагінальні в період менструації. Потрібно відкласти початок терапії до закінчення менструації. Вплив на здатність до керування автотранспортом та управління механізмами Препарат не впливає на здатність до керування транспортними засобами та заняття потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
1 092,00 грн
993,00 грн
Склад, форма випуску та упаковкаГель для зовнішнього застосування 1% у вигляді прозорої, безбарвної, в'язкої маси - 1 г: Активна речовина: кліндаміцин (у формі фосфату) – 10 мг; Допоміжні речовини: алантоїн – 2 мг, метилпарабен – 3 мг, пропіленгліколь – 50 мг, поліетиленгліколь – 100 мг, карбомер 934Р – 7.5 мг, натрію гідроксиду розчин 40% – qs, вода очищена – qs до 1 г. 30 г – туби (1) – пачки картонні.Фармакотерапевтична групаАнтибіотик групи лінкозамідів для місцевого застосування. Кліндаміцину фосфат не активний in vitro, але після нанесення на шкіру швидко гідролізується фосфатазами в протоках сальних залоз з утворенням кліндаміцину, що має антибактеріальну активність. Показана чутливість усіх досліджених штамів Propionibacterium acnes до кліндаміцину in vitro (МПК 0.4 мкг/мл). Після нанесення кліндаміцину на шкіру кількість вільних жирних кислот на поверхні шкіри зменшується приблизно з 14 до 2%.ФармакокінетикаПісля зовнішнього застосування 1% гелю кліндаміцину фосфату в сироватці крові та сечі визначаються дуже низькі концентрації кліндаміцину. Показано активність кліндаміцину в комедонах у пацієнтів із вульгарними вуграми. Середня концентрація антибіотика у вмісті комедону після нанесення розчину кліндаміцину в ізопропіловому спирті та воді (10 мг/мл) протягом 4 тижнів у середньому склала 597 мг/г вмісту комедон (0-1490 мг/г). Фармакокінетика у спеціальних груп пацієнтів При проведенні клінічних досліджень не було включено достатню кількість пацієнтів віком від 65 років, щоб можна було оцінити, чи є відмінності у фармакокінетиці у пацієнтів похилого віку порівняно з молодшими.Клінічна фармакологіяАнтибіотик для зовнішнього застосування.Показання до застосуванняВульгарні вугри.Протипоказання до застосуванняантибіотик-асоційований коліт в анамнезі; вік до 12 років (дані з безпеки та ефективності відсутні); підвищена чутливість до кліндаміцину чи лінкоміцину в анамнезі.Вагітність та лактаціяУ дослідженнях на тваринах при введенні кліндаміцину підшкірно або всередину погіршення фертильності, а також будь-яких негативних впливів на плід не виявлено, за винятком випадків застосування препарату в дозах, токсичних для матері. Результати досліджень на тваринах не завжди можна екстраполювати на людину. У клінічних дослідженнях при системному введенні препарату жінкам у ІІ та ІІІ триместрах вагітності не відзначали збільшення частоти вроджених аномалій плода. Досліджень застосування препарату у жінок у І триместрі вагітності не проводилося. Препарат слід призначати при вагітності тільки в тому випадку, якщо очікувана користь матері перевершує потенційний ризик для плода. Невідомо, чи виділяється кліндаміцин із грудним молоком після зовнішнього застосування. Кліндаміцин виявляється у грудному молоці після перорального або парентерального введення, тому в період лактації слід або відмінити препарат, або припинити грудне вигодовування з огляду на ступінь важливості застосування препарату для матері. Протипоказано застосування препарату у дітей віком до 12 років (дані щодо безпеки та ефективності відсутні).Побічна діяКласифікація частоти небажаних реакцій: дуже часто (≥1/10), часто (≥1/100 та Інфекційні та паразитарні захворювання: частота невідома – фолікуліт. З боку органу зору: частота невідома – біль у власних очах. З боку травної системи: часто – порушення травлення; частота невідома – біль у животі, псевдомембранозний коліт. З боку шкірних покривів: дуже часто – сухість шкіри, подразнення шкіри, кропив'янка; часто – себорея; частота невідома – контактний дерматит. Якщо будь-які з побічних ефектів, що зазначені в інструкції, посилюються або відзначаються будь-які інші побічні ефекти, не зазначені в інструкції, пацієнту слід негайно повідомити про це лікаря.Взаємодія з лікарськими засобамиІснує перехресна стійкість мікроорганізмів до кліндаміцину та лінкоміцину. Був відзначений антагонізм між кліндаміцином та еритроміцином. Встановлено, що кліндаміцин порушує нейром'язову передачу і, отже, може посилювати дію інших міорелаксантів периферичної дії, тому препарат слід застосовувати з обережністю у пацієнтів, які отримують препарати цієї групи.Спосіб застосування та дозиЗовнішньо. Тонкий шар гелю наносять на уражену ділянку чистої сухої шкіри 2 рази на добу. Для отримання задовільних результатів лікування слід продовжувати протягом 6-8 тижнів, а за необхідності можна продовжити до 6 місяців. Якщо після застосування препарату протягом кількох місяців ефективність терапії знижується, слід зробити перерву у лікуванні на 4 тижні.ПередозуванняСимптоми: при місцевому застосуванні кліндаміцин може всмоктуватись у кількостях, що викликають системні ефекти; до можливих системних побічних ефектів можна віднести діарею, геморагічну діарею, включаючи псевдомембранозний коліт. Лікування: проведення симптоматичної та підтримуючої терапії.Запобіжні заходи та особливі вказівкиСлід уникати попадання препарату на слизову оболонку очей та порожнини рота. Після нанесення гелю слід ретельно вимити руки. При випадковому контакті з чутливими поверхнями (очі, садна на шкірі, слизові оболонки) слід промити цю область прохолодною водою. Застосування кліндаміцину (як і інших антибіотиків) внутрішньо або парентерально у ряді випадків пов'язане з розвитком важкої діареї та псевдомембранозного коліту. При зовнішньому застосуванні кліндаміцину випадки виникнення діареї та коліту рідкісні, проте, слід виявляти обережність, і при розвитку вираженої чи тривалої діареї препарат слід відмінити та за необхідності провести відповідні діагностичні та лікувальні заходи. Зазвичай початок діареї, коліту та псевдомембранозного коліту відзначається протягом декількох тижнів після завершення пероральної та парентеральної терапії кліндаміцином. У разі важкої діареї слід вирішити питання щодо доцільності проведення колоноскопії. Призначення препаратів, що знижують моторику ШКТ, таких як опіоїдні аналгетики та дифеноксилат з атропіном,може продовжити та/або погіршити перебіг даного ускладнення. Було встановлено, що ванкоміцин ефективний щодо антибіотик-асоційованого псевдомембранозного коліту, спричиненого Clostridium difficile. Звичайна доза, розділена на 3-4 введення для дорослих, становить від 500 мг до 2 г ванкоміцину на добу протягом 7-10 днів. Вплив на здатність до керування автомобілем та керування механізмами Немає підстав вважати, що застосування препарату Далацин може впливати на здатність до керування автомобілем та управління механізмами.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаВагінальний крем білого кольору - 1 г.; Активна речовина: кліндаміцин (у формі фосфату) – 20 мг; Допоміжні речовини: сорбітан моностеарат - 20 мг, полісорбат 60 - 50 мг, пропіленгліколь - 50 мг, стеаринова кислота - 21.4 мг, цетостеариловий спирт - 32.1 мг, цетилпальмітат - 32.1 мг, олія мінеральна - 6, 0. очищена - qs 20 г - туби із поліетилену/алюмінієвої фольги (1) у комплекті з аплікаторами (3 шт.) - пачки картонні. 40 г - туби із поліетилену/алюмінієвої фольги (1) у комплекті з аплікаторами (7 шт.) - пачки картонні.Фармакотерапевтична групаАнтибіотик групи лінкозамідів для місцевого застосування. Кліндаміцину фосфат не активний in vitro, але швидко гідролізується in vivo з утворенням кліндаміцину, що має антибактеріальну активність. Кліндаміцин пригнічує синтез білка в мікробній клітині за рахунок взаємодії з 50S-субодиницею рибосом. In vitro до кліндаміцину чутливі такі мікроорганізми, що викликають бактеріальні вагінози: Gardnerella vaginalis, Mobiluncus spp., Mycoplasma hominis, Bacteroides spp., Peptostreptococcus spp.ФармакокінетикаВсмоктування Після інтравагінального застосування кліндаміцину в дозі 100 мг/добу одноразово протягом 7 днів Cmax кліндаміцину в плазмі крові досягається через 10 год (4-24 год) і становить 1-й день у середньому 18 нг/мл (4-47 нг/мл) ), а на 7 день - 25 нг/мл (6-61 нг/мл), при цьому системна абсорбція становить близько 4% (0.6-11%) від введеної дози. У жінок з бактеріальними вагінозами при аналогічному режимі дозування системної абсорбції піддається близько 4% кліндаміцину (з меншим розкидом 2-8%), Cmax досягається через 14 год (4-24 год) після введення і становить перший день в середньому 13 нг/мл (6-34 нг/мл), а на 7-й день – 16 нг/мл (7-26 нг/мл). Системна дія кліндаміцину при інтравагінальному застосуванні менш виражена, ніж при введенні внутрішньо або внутрішньовенно. Виведення T1/2 становить 1.5-2.6 год. Після повторного інтравагінального введення кліндаміцин майже не кумулює. Фармакокінетика у спеціальних груп пацієнтів У клінічних дослідженнях кліндаміцину 2% вагінального крему брало участь недостатня кількість пацієнтів у віці 65 років і старше, щоб можна було оцінити різницю в клінічній відповіді на терапію між зазначеною віковою групою і молодшими пацієнтами. У наявних повідомленнях з клінічного досвіду був відзначено різниці у відповіді літніх пацієнтів і молодших.Клінічна фармакологіяАнтибіотик для місцевого застосування у гінекології.ІнструкціяПравила використання препарату В упаковці з 20 г крему знаходиться 3 пластмасові аплікатори, а в упаковці з 40 г - 7 аплікаторів, призначених для правильного введення крему в піхву. Снять колпачок тюбика с кремом. Навинтить пластмассовый аппликатор на снабженное резьбой горлышко тюбика. Скатывая тюбик с противоположного конца, следует осторожно выдавить крем в аппликатор. Аппликатор заполнен, когда его поршень доходит до упора. Отвинтить аппликатор от тюбика и завернуть колпачок. В положении лежа на спине подтянуть колени к груди. Держа аппликатор горизонтально, следует осторожно ввести его во влагалище как можно глубже, не вызывая неприятных ощущений. Медленно нажимая на поршень до упора, ввести крем во влагалище. Осторожно извлечь аппликатор из влагалища и выбросить его.Показания к применениюБактериальный вагиноз.Противопоказания к применениюантибиотик-ассоциированный колит в анамнезе; возраст до 18 лет (данные по безопасности, эффективности отсутствуют); повышенная чувствительность к клиндамицину, линкомицину или любому компоненту препарата.Беременность и лактацияАдекватных и контролируемых исследований по применению препарата в I триместре беременности не проводилось. Применение Далацина в I триместре беременности возможно только по абсолютным показаниям, т.е. в том случае, если предполагаемая польза терапии препаратом для матери превосходит потенциальный риск для плода. В исследованиях на животных при введении клиндамицина п/к или внутрь каких-либо отрицательных влияний на плод не обнаружено, за исключением случаев приема препарата в дозах, токсичных для матери. При применении клиндамицина интравагинально во II и III триместрах беременности не отмечалось увеличения частоты врожденных аномалий плода. Аномальные роды имели место у 1.1% женщин по сравнению с 0.5% в группе плацебо, если Далацин® крем вагинальный применялся во II триместре в течение 7 дней. Применение препарата во II-III триместре беременности возможно, если потенциальная польза для матери превосходит риск для плода. Неизвестно, выделяется ли клиндамицин с грудным молоком после интравагинального применения. Клиндамицин обнаруживается в грудном молоке после приема внутрь или парентерального введения. Поэтому в период лактации следует либо отменить применение препарата, либо прекратить грудное вскармливание, учитывая степень важности применения препарата для матери. Протипоказано застосування препарату у дітей та підлітків віком до 18 років (дані з безпеки, ефективності відсутні).Побічна діяБезпеку вагінального крему кліндамнпіну оцінювали як у невагітних пацієнток, так і у пацієнток у період ІІ та ІІІ триместрів вагітності. Частота розвитку побічних реакцій така: дуже часто – ≥1/10; часто - ≥1/100, Інфекційні та паразитарні захворювання: часто – грибкові інфекції, що викликаються грибами роду Candida; нечасто – бактеріальні інфекції; частота невідома – кандидоз шкіри. З боку імунної системи: нечасто гіперчутливість. З боку ендокринної системи: частота невідома – гіпертиреоз. З боку нервової системи: часто головний біль, запаморочення, дисгевзія. З боку органу слуху та вестибулярного апарату: нечасто – вертиго. З боку дихальної системи: часто – інфекції верхніх дихальних шляхів; нечасто – носова кровотеча. З боку шлунково-кишкового тракту: часто – біль у животі, запор, діарея, нудота, блювання; нечасто - здуття живота, метеоризм, неприємний запах із рота; частота невідома - псевдомембранозний коліт *, шлунково-кишковий розлад, диспепсія. З боку шкіри та підшкірних тканин: часто - свербіж шкіри, висипання; нечасто - кропив'янка, еритема; частота невідома - макулопапульозний висип. З боку скелетно-м'язової системи та сполучної тканини: часто біль у спині. З боку нирок та сечовивідних шляхів: часто – інфекції сечовивідних шляхів, глюкозурія, протеїнурія; нечасто дизурія. Вагітність, післяпологові та перинатальні стани: часто – аномальні пологи. З боку статевих органів та молочної залози: дуже часто – вульвовагінальний кандидоз; часто - вульвовагініт, вульвовагінальні розлади, порушення менструального циклу, вульвовагінальний біль, метрорагія, виділення з піхви; нечасто – трихомонадний вульвовагініт, вагінальні інфекції, біль у тазі; частота невідома – ендометрит. Загальні розлади та реакції у місці введення: частота невідома – запалення, біль. Дані лабораторних та інструментальних досліджень: нечасто відхилення результатів мікробіологічних аналізів від норми.Взаємодія з лікарськими засобамиІснує перехресна резистентність між кліндаміцином та лінкоміцином. В умовах in vitro продемонстровано антагонізм між кліндаміцином та еритроміцином. Встановлено, що кліндаміцин порушує нейром'язову передачу і, отже, може посилювати дію міорелаксантів периферичної дії, тому препарат слід застосовувати з обережністю у пацієнтів, які отримують препарати цієї групи. Спільне застосування з іншими препаратами для інтравагінального введення не рекомендується.Спосіб застосування та дози1 повний аплікатор (5 г крему, приблизно 100 мг кліндаміцину) вводять у піхву переважно перед сном протягом 3 або 7 днів поспіль.ПередозуванняПри інтравагінальному застосуванні крему Далацин® можлива абсорбція кліндаміцину у кількостях, достатніх для розвитку системних реакцій. Випадкове потрапляння препарату в ШКТ також може викликати системні ефекти, подібні до тих, що виникають після прийому внутрішньо кліндаміцину в терапевтичних дозах. До можливих системних побічних ефектів можна віднести діарею, геморагічну діарею, включаючи псевдомембранозний коліт. Лікування: при необхідності проводять симптоматичну та підтримуючу терапію.Запобіжні заходи та особливі вказівкиДо призначення препарату за допомогою спеціальних лабораторних методів слід виключити наступні можливі збудники вульвовагініту: Trichomonas vaginalis, Chlamydia trachomatis, Neisseria gonorrhoeae, Candida albicans та вірус Herpes simplex. Інтравагінальне застосування Далацину може призвести до посиленого зростання нечутливих до препарату мікроорганізмів, особливо дріжджоподібних грибів. При застосуванні кліндаміцину (як і практично всіх антибіотиків) внутрішньо або інтравагінально можливий розвиток важкої діареї та у ряді випадків псевдомембранозного коліту. У зв'язку з цим у разі виникнення на тлі терапії Далацином вираженої або тривалої діареї слід відмінити препарат і при необхідності провести діагностичні та лікувальні заходи. Пацієнтка має бути поінформована про те, що під час застосування вагінального крему слід уникати статевих контактів, а також використання інших видів виробів, призначених для інтравагінального введення (наприклад, тампонів, спринцювання). Не рекомендується застосування препарату Далацин у період менструації. Потрібно відкласти початок терапії до закінчення менструації. Далацин містить компоненти, які можуть зменшувати міцність виробів з латексу або каучуку (презервативи, протизаплідні вагінальні діафрагми). Тому використання подібних виробів під час лікування Далацином та протягом 72 годин після застосування не рекомендується. Вплив на здатність до керування автотранспортом та управління механізмами Немає підстав вважати, що застосування препарату може впливати на здатність до керування автомобілем та управління механізмами.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаВагінальний крем білого кольору - 1 г.; Активна речовина: кліндаміцин (у формі фосфату) – 20 мг; Допоміжні речовини: сорбітан моностеарат - 20 мг, полісорбат 60 - 50 мг, пропіленгліколь - 50 мг, стеаринова кислота - 21.4 мг, цетостеариловий спирт - 32.1 мг, цетилпальмітат - 32.1 мг, олія мінеральна - 6, 0. очищена - qs 20 г - туби із поліетилену/алюмінієвої фольги (1) у комплекті з аплікаторами (3 шт.) - пачки картонні. 40 г - туби із поліетилену/алюмінієвої фольги (1) у комплекті з аплікаторами (7 шт.) - пачки картонні.Фармакотерапевтична групаАнтибіотик групи лінкозамідів для місцевого застосування. Кліндаміцину фосфат не активний in vitro, але швидко гідролізується in vivo з утворенням кліндаміцину, що має антибактеріальну активність. Кліндаміцин пригнічує синтез білка в мікробній клітині за рахунок взаємодії з 50S-субодиницею рибосом. In vitro до кліндаміцину чутливі такі мікроорганізми, що викликають бактеріальні вагінози: Gardnerella vaginalis, Mobiluncus spp., Mycoplasma hominis, Bacteroides spp., Peptostreptococcus spp.ФармакокінетикаВсмоктування Після інтравагінального застосування кліндаміцину в дозі 100 мг/добу одноразово протягом 7 днів Cmax кліндаміцину в плазмі крові досягається через 10 год (4-24 год) і становить 1-й день у середньому 18 нг/мл (4-47 нг/мл) ), а на 7 день - 25 нг/мл (6-61 нг/мл), при цьому системна абсорбція становить близько 4% (0.6-11%) від введеної дози. У жінок з бактеріальними вагінозами при аналогічному режимі дозування системної абсорбції піддається близько 4% кліндаміцину (з меншим розкидом 2-8%), Cmax досягається через 14 год (4-24 год) після введення і становить перший день в середньому 13 нг/мл (6-34 нг/мл), а на 7-й день – 16 нг/мл (7-26 нг/мл). Системна дія кліндаміцину при інтравагінальному застосуванні менш виражена, ніж при введенні внутрішньо або внутрішньовенно. Виведення T1/2 становить 1.5-2.6 год. Після повторного інтравагінального введення кліндаміцин майже не кумулює. Фармакокінетика у спеціальних груп пацієнтів У клінічних дослідженнях кліндаміцину 2% вагінального крему брало участь недостатня кількість пацієнтів у віці 65 років і старше, щоб можна було оцінити різницю в клінічній відповіді на терапію між зазначеною віковою групою і молодшими пацієнтами. У наявних повідомленнях з клінічного досвіду був відзначено різниці у відповіді літніх пацієнтів і молодших.Клінічна фармакологіяАнтибіотик для місцевого застосування у гінекології.ІнструкціяПравила використання препарату В упаковці з 20 г крему знаходиться 3 пластмасові аплікатори, а в упаковці з 40 г - 7 аплікаторів, призначених для правильного введення крему в піхву. Зняти ковпачок тюбика із кремом. Нагвинтити пластмасовий аплікатор на з різьбленням шийку тюбика. Скочуючи тюбик з протилежного кінця, слід обережно видавити крем в аплікатор. Аплікатор заповнений, коли поршень доходить до упору. Відкрутити аплікатор від тюбика і загорнути ковпачок. У положенні лежачи на спині підтягнути коліна до грудей. Тримаючи аплікатор горизонтально, слід обережно ввести його в піхву якнайглибше, не викликаючи неприємних відчуттів. Повільно натискаючи поршень до упору, ввести крем у піхву. Обережно витягти аплікатор із піхви та викинути його.Показання до застосуванняБактеріальний вагіноз.Протипоказання до застосуванняантибіотик-асоційований коліт в анамнезі; вік до 18 років (дані щодо безпеки, ефективності відсутні); підвищена чутливість до кліндаміцину, лінкоміцину або до будь-якого компонента препарату.Вагітність та лактаціяАдекватних та контрольованих досліджень щодо застосування препарату у І триместрі вагітності не проводилося. Застосування Далацина в І триместрі вагітності можливе лише з абсолютним показанням, тобто. у разі, якщо передбачувана користь терапії препаратом для матері перевищує потенційний ризик для плода. У дослідженнях на тваринах при введенні кліндаміцину підшкірно або внутрішньо будь-яких негативних впливів на плід не виявлено, за винятком випадків прийому препарату в дозах, токсичних для матері. При застосуванні кліндаміцину інтравагінально у ІІ та ІІІ триместрах вагітності не відзначалося збільшення частоти вроджених аномалій плода. Аномальні пологи мали місце у 1.1% жінок порівняно з 0.5% у групі плацебо, якщо Далацин® вагінальний крем застосовувався у II триместрі протягом 7 днів. Застосування препарату у ІІ-ІІІ триместрі вагітності можливе, якщо потенційна користь для матері перевершує ризик для плода. Невідомо, чи виділяється кліндаміцин із грудним молоком після інтравагінального застосування. Кліндаміцин виявляється у грудному молоці після прийому внутрішньо або парентерального введення. Тому в період лактації слід або скасувати застосування препарату, або припинити грудне вигодовування з огляду на ступінь важливості застосування препарату для матері. Протипоказано застосування препарату у дітей та підлітків віком до 18 років (дані з безпеки, ефективності відсутні).Побічна діяБезпеку вагінального крему кліндамнпіну оцінювали як у невагітних пацієнток, так і у пацієнток у період ІІ та ІІІ триместрів вагітності. Частота розвитку побічних реакцій така: дуже часто – ≥1/10; часто - ≥1/100, Інфекційні та паразитарні захворювання: часто – грибкові інфекції, що викликаються грибами роду Candida; нечасто – бактеріальні інфекції; частота невідома – кандидоз шкіри. З боку імунної системи: нечасто гіперчутливість. З боку ендокринної системи: частота невідома – гіпертиреоз. З боку нервової системи: часто головний біль, запаморочення, дисгевзія. З боку органу слуху та вестибулярного апарату: нечасто – вертиго. З боку дихальної системи: часто – інфекції верхніх дихальних шляхів; нечасто – носова кровотеча. З боку шлунково-кишкового тракту: часто – біль у животі, запор, діарея, нудота, блювання; нечасто - здуття живота, метеоризм, неприємний запах із рота; частота невідома - псевдомембранозний коліт *, шлунково-кишковий розлад, диспепсія. З боку шкіри та підшкірних тканин: часто - свербіж шкіри, висипання; нечасто - кропив'янка, еритема; частота невідома - макулопапульозний висип. З боку скелетно-м'язової системи та сполучної тканини: часто біль у спині. З боку нирок та сечовивідних шляхів: часто – інфекції сечовивідних шляхів, глюкозурія, протеїнурія; нечасто дизурія. Вагітність, післяпологові та перинатальні стани: часто – аномальні пологи. З боку статевих органів та молочної залози: дуже часто – вульвовагінальний кандидоз; часто - вульвовагініт, вульвовагінальні розлади, порушення менструального циклу, вульвовагінальний біль, метрорагія, виділення з піхви; нечасто – трихомонадний вульвовагініт, вагінальні інфекції, біль у тазі; частота невідома – ендометрит. Загальні розлади та реакції у місці введення: частота невідома – запалення, біль. Дані лабораторних та інструментальних досліджень: нечасто відхилення результатів мікробіологічних аналізів від норми.Взаємодія з лікарськими засобамиІснує перехресна резистентність між кліндаміцином та лінкоміцином. В умовах in vitro продемонстровано антагонізм між кліндаміцином та еритроміцином. Встановлено, що кліндаміцин порушує нейром'язову передачу і, отже, може посилювати дію міорелаксантів периферичної дії, тому препарат слід застосовувати з обережністю у пацієнтів, які отримують препарати цієї групи. Спільне застосування з іншими препаратами для інтравагінального введення не рекомендується.Спосіб застосування та дози1 повний аплікатор (5 г крему, приблизно 100 мг кліндаміцину) вводять у піхву переважно перед сном протягом 3 або 7 днів поспіль.ПередозуванняПри інтравагінальному застосуванні крему Далацин® можлива абсорбція кліндаміцину у кількостях, достатніх для розвитку системних реакцій. Випадкове потрапляння препарату в ШКТ також може викликати системні ефекти, подібні до тих, що виникають після прийому внутрішньо кліндаміцину в терапевтичних дозах. До можливих системних побічних ефектів можна віднести діарею, геморагічну діарею, включаючи псевдомембранозний коліт. Лікування: при необхідності проводять симптоматичну та підтримуючу терапію.Запобіжні заходи та особливі вказівкиДо призначення препарату за допомогою спеціальних лабораторних методів слід виключити наступні можливі збудники вульвовагініту: Trichomonas vaginalis, Chlamydia trachomatis, Neisseria gonorrhoeae, Candida albicans та вірус Herpes simplex. Інтравагінальне застосування Далацину може призвести до посиленого зростання нечутливих до препарату мікроорганізмів, особливо дріжджоподібних грибів. При застосуванні кліндаміцину (як і практично всіх антибіотиків) внутрішньо або інтравагінально можливий розвиток важкої діареї та у ряді випадків псевдомембранозного коліту. У зв'язку з цим у разі виникнення на тлі терапії Далацином вираженої або тривалої діареї слід відмінити препарат і при необхідності провести діагностичні та лікувальні заходи. Пацієнтка має бути поінформована про те, що під час застосування вагінального крему слід уникати статевих контактів, а також використання інших видів виробів, призначених для інтравагінального введення (наприклад, тампонів, спринцювання). Не рекомендується застосування препарату Далацин у період менструації. Потрібно відкласти початок терапії до закінчення менструації. Далацин містить компоненти, які можуть зменшувати міцність виробів з латексу або каучуку (презервативи, протизаплідні вагінальні діафрагми). Тому використання подібних виробів під час лікування Далацином та протягом 72 годин після застосування не рекомендується. Вплив на здатність до керування автотранспортом та управління механізмами Немає підстав вважати, що застосування препарату може впливати на здатність до керування автомобілем та управління механізмами.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
459,00 грн
417,00 грн
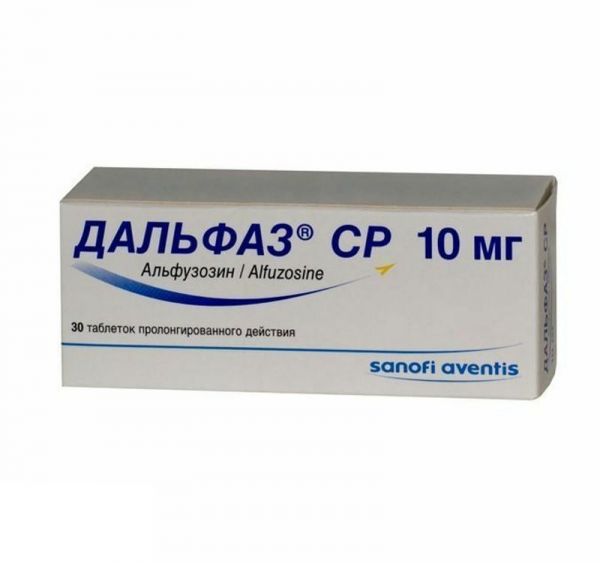
Склад, форма випуску та упаковкаПігулки - 1 таб. діюча речовина: альфузозіну гідрохлорид – 5,00 мг; допоміжні речовини: целюлоза мікрокристалічна – 42,00 мг; кальцію гідрофосфат дигідрат – 65,00 мг; рицинова олія гідрована - 19,6 мг; повідон - 7,0 мг; магнію стеарат – 1,4 мг; Плівкова оболонка: гіпромелоза – 4,158 мг; пропіленгліколь - 0,416 мг, титану діоксид (Е 171) - 0,416 мг; барвник заліза оксид червоний (Е 172) – 0,1765 мкг; барвник заліза оксид жовтий (Е 172)-9,8235 мкг. По 14 таблеток у блістер з алюмінієвої фольги та полівінілхлоридної плівки. По 4 блістери разом з інструкцією із застосування в картонну пачку.Опис лікарської формиКруглі, двоопуклі таблетки, вкриті оболонкою блідо-жовтого кольору.Фармакотерапевтична групаАльфа-1-адреноблокатор.ФармакокінетикаМаксимальна концентрація алфузозину в плазмі досягається приблизно через 3 години після прийому препарату внутрішньо. Період напіввиведення (з плазми) становить 8 год. Біодоступність порівняно з лікарською формою негайного вивільнення (алфузозин 2,5 мг) знижена приблизно на 15%. Їда не впливає на фармакокінетичний профіль препарату. Зв'язування із білками плазми крові близько 90%. Алфузозин піддається значному метаболізму в печінці, переважно, за допомогою ізоферменту CYP3A4. У сечі виявляється лише 11% незміненого алфузозину. Метаболіти алфузозину не мають фармакологічної активності. Більшість метаболітів виводиться через кишківник (75-90%). Фармакокінетика у спеціальних груп пацієнтів У пацієнтів старше 75 років може бути збільшена абсорбція препарату, і можуть досягатися вищі максимальні плазмові концентрації. У деяких пацієнтів можливе збільшення біодоступності препарату та зменшення обсягу розподілу. У цьому період напіввиведення не змінюється. У пацієнтів з тяжкими порушеннями функції печінки збільшується елімінаційний період напіввиведення та порівняно зі здоровими добровольцями зростає біодоступність препарату. У пацієнтів з порушеннями функції нирок, що вимагають або не потребують проведення гемодіалізу, у зв'язку із збільшенням вільної фракції препарату обсяг розподілу та кліренс алфузозину збільшуються. При хронічній серцевій недостатності фармакокінетичний профіль алфузозину не змінюється.ФармакодинамікаАлфузозин є похідним хіназоліну, активним при пероральному застосуванні. Він є селективним антагоністом постсинаптичних альфа1-адренорецепторів, розташованих у передміхуровій залозі, трикутнику сечового міхура та сечівнику. Клінічні прояви доброякісної гіпертрофії передміхурової залози виражаються в інфравезикальній обструкції сечовивідних шляхів, обумовленої як анатомічними (статичними), так і функціональними (динамічними) факторами. Функціональний компонент обструкції обумовлений збудженням альфа1-адренорецепторів, що призводить до скорочення гладкої мускулатури передміхурової залози, її оболонки, трикутника сечового міхура і передміхурової частини уретри, що призводить до збільшення опору відтоку сечі з сечового міхура і, мабуть, до вторинного небажаного. Внаслідок прямого впливу на гладку мускулатуру тканини передміхурової залози, пов'язаного з блокадою альфа1-адренорецепторів, алфузозин зменшує інфравезикальну обструкцію, тиск в уретрі та опір відтоку сечі під час сечовипускання. За рахунок цього алфузозин покращує відтік сечі та полегшує випорожнення сечового міхура. Ці сприятливі ефекти на уродінаміку ведуть до зменшення симптомів подразнення сечовивідних шляхів та симптомів, зумовлених порушеннями відтоку сечі у пацієнтів із доброякісною гіперплазією передміхурової залози. У пацієнтів з максимальною швидкістю відтоку сечі (Qmax) ≤15 мл/сек алфузозин, починаючи з першої дози, значно збільшує Qmax (в середньому на 30%). Крім того,у пацієнтів з доброякісною гіпертрофією передміхурової залози алфузозин значно знижує тиск у детрузорі сечового міхура і збільшує об'єм сечі, що викликає позиву до сечовипускання, а також значно знижує об'єм залишкової сечі. Ці ефекти призводять до зменшення обструктивних та ірритативних симптомів доброякісної гіпертрофії передміхурової залози. Препарат не надає несприятливого на сексуальну функцію. У зв'язку з селективністю дії алфузозину його вплив на альфа1-адренорецептори судин і, відповідно, на артеріальний тиск (АТ), у разі його застосування в терапевтичних дозах практично відсутній.Показання до застосуванняФункціональні порушення сечовипускання при доброякісній гіперплазії передміхурової залози.Протипоказання до застосуванняПідвищена чутливість до алфузозину та/або будь-якої з допоміжних речовин препарату. Ортостатична гіпотензія. Тяжкі порушення функції печінки (клас С за класифікацією Child-Pugh). Тяжкі порушення функції нирок (кліренс креатиніну Кишкова непрохідність (у зв'язку з наявністю у складі препарату касторової олії). Одночасний прийом інших альфа1-адреноблокаторів. Дитячий вік віком до 18 років. З обережністю: У пацієнтів, які приймають гіпотензивні препарати або нітрати (можливий розвиток ортостатичної гіпотензії, як протікає безсимптомно, так і симптоматичної, що супроводжується появою запаморочення, слабкості, холодного поту). У пацієнтів похилого віку (старше 75 років). У пацієнтів із вираженою гіпотензивною реакцією на інші альфа1-адреноблокатори в анамнезі. У пацієнтів із ортостатичною гіпотензією з клінічними проявами. У пацієнтів з ішемічною хворобою серця, стенокардія (можливість почастішання та обтяження нападів стенокардії). У пацієнтів з клінічною симптоматикою або без клінічної симптоматики ішемії головного мозку (у зв'язку з можливістю зниження АТ і посилення ішемії головного мозку). У пацієнтів з вродженим або набутим подовженням інтервалу QT або у пацієнтів, які приймають лікарські препарати, що збільшують тривалість інтервалу QT. З інгібіторами ізоферменту CYP3A4 (кетоконазол, ітраконазол, ритонавір) (можливе збільшення концентрації алфузозину в плазмі).Вагітність та лактаціяПрепарат Дальфаз ретард не призначений для застосування у жінок.Побічна діяНаведені нижче небажані реакції (HP) даються відповідно до наступних градацій частоти їх виникнення: дуже часто: (≥ 10%); часто: (≥1% - <10%); нечасто: (≥ 0,1% - Порушення з боку крові та лімфатичної системи - Невідома частота: тромбоцитопенія. Порушення з боку серця – Нечасто: тахікардія, відчуття серцебиття; Дуже рідко: можливе почастішання або обтяження нападів стенокардії; Невідома частота: фібриляція передсердь. Порушення з боку органу зору: - Нечасто: порушення зору; Невідома частота: інтраопераційний синдром млявої райдужної оболонки. Загальні розлади та порушення у місці введення - Часто: астенія, нездужання; Нечасто: набряки, біль у грудях. Порушення з боку шлунково-кишкового тракту: - Часто: нудота, біль у животі, діарея, сухість слизової оболонки порожнини рота; Невідома частота: блювання. Порушення з боку печінки та жовчовивідних шляхів - Невідома частота: гепатоцелюлярна жовтяниця, холестаз та пов'язані з ним захворювання печінки. Порушення з боку нервової системи - Часто: почуття нудоти/запаморочення, головний біль, вертиго; Нечасто: синкопальний стан, сонливість; Невідома частота: ішемічні порушення мозкового кровообігу у пацієнтів із вже наявною цереброваскулярною патологією. Порушення з боку статевих органів та молочної залози - Невідома частота: пріапізм. Порушення з боку дихальної системи, органів грудної клітки та середостіння - Нечасто: риніт. Порушення з боку шкіри та підшкірних тканин - Нечасто: висипання, свербіж; Дуже рідко: кропив'янка, ангіоневротичний набряк. Порушення з боку судин: - Часто: зниження артеріального тиску, включаючи ортостатичну гіпотензію; Нечасто: гіперемія покривів шкіри.Взаємодія з лікарськими засобамиПротипоказані комбінації З блокаторами альфа1-рецепторів (празозин, урапідил) – ризик розвитку тяжкої ортостатичної гіпотензії та посилення гіпотензивної дії. Взаємодії, які слід брати до уваги З гіпотензивними препаратами – посилення гіпотензивного ефекту та ризик розвитку ортостатичної гіпотензії (адитивна дія). З нітратами – збільшення ризику розвитку рефлекторної тахікардії та зниження АТ. Із засобами для інгаляційної та неінгаляційної загальної анестезії – можлива нестабільність АТ під час загальної анестезії. З інгібіторами ізоферменту CYP3A4 (кетоконазол, ітраконазол та ритонавір) – можливе підвищення концентрації алфузозину. При поєднанні алфузозину в дозі 10 мг на добу з курсовим застосуванням кетоконазолу в дозі 200 мг на добу протягом 7 днів Сmax та AUC алфузозину збільшувалися в 2,1 рази та 2,46 разів відповідно, а при його поєднанні з курсовим застосуванням кетоконазолу в дозі 400 мг на добу протягом 8 днів Сmax та AUC алфузозину збільшувалися у 2,3 рази та 3,0 рази відповідно.Спосіб застосування та дозиПрепарат призначений для вживання. Пігулки повинні прийматися повністю і запивати 1/2 склянкою води. Таблетки не можна роздавлювати, розжовувати, розмелювати або подрібнювати до порошкового стану, оскільки порушення структури таблетки може призвести до прискорення абсорбції діючої речовини, що сприятиме розвитку небажаних реакцій. Дорослі Рекомендована доза становить: по 1 таблетці препарату Дальфаз® ретард, 5 мг – двічі на день (вранці та ввечері). Пацієнти похилого віку та/або хворі з артеріальною гіпертензією, які отримують гіпотензивні засоби Як звичайний запобіжний засіб, при призначенні алфузозину цим категоріям пацієнтів рекомендується починати лікування з 1 таблетки препарату Дальфаз® ретард, 5 мг, увечері, підвищуючи дозу відповідно до клінічної відповіді, але не перевищувати дози: 1 таблетка двічі на день. Пацієнти з нирковою недостатністю При кліренсі креатиніну більше 30 мл/хв. корекції режиму дозування не потрібно. Хворі з печінковою недостатністю Слід враховувати подовження періоду напіввиведення препарату та можливість збільшення його біодоступності, тому лікування має починатися з дози 2,5 мг 1 раз на добу, яка може збільшуватись залежно від клінічної відповіді, але не повинна перевищувати 2,5 мг 2 рази на добу.ПередозуванняСимптоми. Надмірне зниження артеріального тиску, рефлекторна тахікардія. Лікування. У разі передозування пацієнт підлягає госпіталізації. При передозуванні пацієнт повинен перебувати в положенні "лежачи", і йому потрібне постійне моніторування артеріального тиску. При зниженні артеріального тиску рекомендується введення судинозвужувальних засобів і плазмозамінників (для збільшення обсягу циркулюючої крові). Після відновлення АТ необхідно продовжити контроль за АТ ще приблизно протягом доби. Алфузозин погано виводиться за допомогою гемодіалізу через високий рівень зв'язування з білками плазми.Запобіжні заходи та особливі вказівкиПротягом декількох годин після прийому алфузозину (як і після прийому будь-яких інших альфа1-адреноблокаторів) у деяких осіб, особливо у пацієнтів, які приймають гіпотензивні препарати, може розвинутись ортостатична гіпотензія з клінічною симптоматикою (запаморочення, різка слабкість, холодний піт) або без її. При розвитку цих явищ пацієнт повинен до повного зникнення перебувати у горизонтальному положенні. Ортостатична гіпотензія зазвичай буває скороминущою і спостерігається, як правило, на початку прийому препарату і зазвичай не вимагає відміни лікування. При постмаркетинговому застосуванні препарату у пацієнтів з факторами ризику зниження артеріального тиску (такими як захворювання серця або супутня терапія гіпотензивними препаратами) повідомлялося про виражене зниження артеріального тиску. Ризик надмірного зниження АТ і пов'язаних з ним небажаних реакцій може бути вищим у пацієнтів похилого віку. Перед початком лікування пацієнт повинен бути попереджений про можливість виникнення описаних реакцій. Слід дотримуватися обережності при застосуванні алфузозину у пацієнтів з ортостатичною гіпотензією з клінічною симптоматикою або у пацієнтів, які приймають гіпотензивні препарати або нітрати: необхідний ретельніший контроль за АТ, у тому числі при переході з горизонтального положення у вертикальне, особливо на початку лікування. Слід бути обережними при застосуванні алфузозину у пацієнтів з вираженою гіпотензивною реакцією у відповідь на прийом інших блокаторів альфа1-адренорецепторів в анамнезі. Пацієнтам з коронарною недостатністю при прийомі алфузозину необхідно продовжувати антиангінальну терапію. При відновленні або обтяженні стенокардії лікування алфузозином слід припинити. Слід бути обережними при застосуванні алфузозину у пацієнтів з вродженим або набутим подовженням інтервалу QT або у пацієнтів, які приймають лікарські препарати, здатні подовжувати інтервал QT. У зв'язку з тим, що після прийому алфузозину можливе зниження артеріального тиску, є ризик розвитку ішемічного порушення мозкового кровообігу у схильних до цього пацієнтів (як мають відповідні симптоми, так і у тих, у яких попередні цереброваскулярні розлади протікають безсимптомно). Під час проведення офтальмологічних операцій з приводу катаракти у деяких пацієнтів, які приймали або приймали раніше деякі альфа1-адреноблокатори, спостерігався розвиток інтраопераційного синдрому млявої райдужної оболонки (варіант синдрому вузької зіниці). Хоча ризик розвитку такого ускладнення при прийомі препарату Дальфаз® ретард є дуже низьким, перед проведенням операції з приводу катаракти хірург-офтальмолог повинен бути поінформований про те, що пацієнт приймає альфа1-адреноблокатори або приймав їх раніше, оскільки розвиток інтраопераційного синдрому млявої райдужної оболонки може збільшувати кількість ускладнень у своїй оперативному втручанні. Офтальмологи мають бути готовими до можливої зміни методики оперативного втручання Є повідомлення про випадки розвитку на тлі терапії альфа1-адреноблокаторами приапізму (тривалої хворобливої ерекції статевого члена, не пов'язаної із сексуальною активністю). Якщо терапія приапізму не була проведена негайно, це може призвести до пошкодження тканин статевого члена та необоротної втрати потенції. Пацієнтів слід інформувати про серйозність цього стану (див. розділ "Побічна дія") та необхідність негайного звернення за медичною допомогою у разі збереження ерекції протягом більше 4-х годин. Вплив на здатність до керування автотранспортом та управління механізмами Необхідно бути обережними при керуванні транспортними засобами та заняттями іншими потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій, оскільки препарат може викликати запаморочення та інші побічні ефекти, які можуть впливати на зазначені здібності.Умови відпустки з аптекЗа рецептом
Склад, форма випуску та упаковкаПігулки - 1 таб. Активні речовини: аскорбінова кислота – 50 мг, рутозид (рутин) – 50 мг; Допоміжні речовини: сахароза (цукор) – 147,1 мг, крохмаль картопляний – 76,2 мг, кальцію стеарату моногідрат (кальцію стеарат 1-водний) – 2,6 мг, тальк – 4,1 мг. По 10 таблеток у контурне осередкове пакування з плівки полівінілхлоридної та фольги алюмінієвої. По 50 пігулок у банку з полімерного матеріалу. Кожну банку з полімерного матеріалу або 5 контурних осередкових упаковок разом з інструкцією з медичного застосування поміщають у пачку з картону для споживчої тари.Опис лікарської формиТаблетки круглі плоскоциліндричної форми, з фаскою та ризиком, світлого зеленувато-жовтого кольору з дрібними вкрапленнями зеленого, коричневого та білого кольору.Фармакотерапевтична групаВітамін.ФармакодинамікаАскорбінова кислота бере участь у регуляції окисно-відновних реакцій, вуглеводного обміну, синтезі колагену. Рутозид усуває підвищену проникність капілярів, зміцнює судинну стінку.Показання до застосуванняПрофілактика та лікування гіпо- та авітамінозу С та Р. У складі комплексної терапії при варикозному розширенні вен, трофічних порушеннях та виразках шкіри, при хронічній венозній недостатності, геморагічному діатезі.Протипоказання до застосуванняГіперчутливість, дитячий вік, дефіцит сахарази/ізомальтази, непереносимість фруктози, глюкозо-галактозна мальабсорбція. З обережністю: Стани, що супроводжуються гіперкоагуляцією крові та схильністю до тромбозів, тромбофлебіт.Вагітність та лактаціяЧерез вміст у препараті рутину його не слід застосовувати у І триместрі вагітності. Мінімальна щоденна потреба в аскорбіновій кислоті у ІІ-ІІІ триместрах вагітності – близько 60 мг. Слід мати на увазі, що плід може адаптуватися до високих доз аскорбінової кислоти, яку приймає вагітна жінка, і потім у новонародженого можливий розвиток синдрому "скасування". Мінімальна щоденна потреба; період лактації – 80 мг. Дієта матері, що містить адекватну кількість аскорбінової кислоти, є достатньою для профілактики її дефіциту у немовляти. Теоретично існує небезпека для дитини при застосуванні матір'ю високих доз аскорбінової кислоти (рекомендується не перевищувати щоденної потреби в аскорбіновій кислоті, що годує матір'ю). При вживанні препарату необхідно в період вагітності та лактації дотримуватись дозування та тривалість курсу прийому, призначені лікарем.Побічна діяАлергічні реакції, диспепсичні розлади, біль голови.Взаємодія з лікарськими засобамиАскорбінова кислота підвищує всмоктування лікарських засобів групи пеніциліну, заліза; знижує клінічний ефект гепарину та непрямих антикоагулянтів.Спосіб застосування та дозиВсередину, по 1 таблетці 2-3 рази на день під час або після їди. Курс лікування-2-3 тижні. Для профілактики - по 1-2 таблетки на добу. Курс визначається індивідуально.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
1 016,00 грн
314,00 грн
Склад, форма випуску та упаковкаПігулки - 1 таб. Діюча речовина (другий шар): альфузозину гідрохлорид – 10,00 мг; Допоміжні речовини першого шару (зовнішній інкативний): гіпромелоза – 79,75 мг; рицинова олія гідрована - 13,50 мг; етилцелюлоза – 20-5,00 мг; барвник заліза оксид жовтий (Е172) – 0,25 мг; кремнію діоксид колоїдний водний – 0,50 мг; магнію стеарат – 1,00 мг; Допоміжні речовини другого шару (внутрішній активний): манітол – 10,00 мг; гіпромелоза -10,00 мг; целюлоза мікрокристалічна – 65,00 мг; повідон - 3,20 мг; кремнію діоксид колоїдний водний – 1,25 мг; магнію стеарат – 1,00 мг; Допоміжні речовини третього шару (зовнішній інкативний): гіпромелоза – 114,01 мг; рицинова олія гідрована - 27,90 мг; повідон - 4,72 мг; барвник заліза оксид жовтий (Е172) – 0,15 мг; кремнію діоксид колоїдний водний – 1,05 мг; магнію стеарат – 2,17 мг. По 10 або 30 таблеток у блістер ПВХ/Ал. По 1 або 3 блістери по 10 таблеток або по 1 блістеру по 30 таблеток разом з інструкцією із застосування в картонну пачку.Опис лікарської формиКруглі, двоопуклі тришарові таблетки: один білий шар між двома жовтими шарами з різною інтенсивністю фарбування. Допускаються вкраплення.Фармакотерапевтична групаАльфа1-адреноблокатор.ФармакокінетикаСереднє значення відносної біодоступності становить 104,4% порівняно із застосуванням алфузозину в дозі 7,5 мг у лікарській формі негайного вивільнення (2,5 мг 3 рази на добу) у здорових добровольців середнього віку. Максимальна концентрація алфузозину в плазмі досягається через 9 годин після прийому препарату порівняно з 1 годиною для форми негайного вивільнення. Період напіввиведення алфузозину становить 9,1 год. Дослідження показали, що біодоступність алфузозину збільшується при прийомі препарату після їди. Зв'язування з білками плазми становить близько 90%. Алфузозин піддається значному метаболізму в печінці, переважно, за допомогою ізоферменту CYP3A4. У сечі виявляється лише 11% незміненого алфузозину. Метаболіти алфузозину не мають фармакологічної активності. Більшість метаболітів виводиться через кишківник (75-90%). Фармакокінетика у спеціальних груп пацієнтів Порівняно зі здоровими добровольцями середнього віку, у пацієнтів похилого віку (старше 75 років) фармакокінетичні показники алфузозину не збільшуються. У порівнянні з особами з нормальною функцією нирок, середні значення максимальної концентрації у плазмі крові (Сmах) та площі під кривою "концентрація-час" (AUC) алфузозину у пацієнтів з нирковою недостатністю помірно збільшені, без зміни періоду напіввиведення (Т1/2). Ця зміна фармакокінетичного профілю алфузозину не має клінічного значення, тому не потрібна корекція дози у пацієнтів з легкою та помірною нирковою недостатністю (кліренс креатиніну >30 мл/хв). Фармакокінетичний профіль алфузозину не змінюється при хронічній серцевій недостатності.ФармакодинамікаАлфузозин є похідним хіназоліну, активним при пероральному застосуванні. Він є селективним антагоністом постсинаптичних альфа1-адренорецепторів, розташованих у передміхуровій залозі, трикутнику сечового міхура та сечівнику. Клінічні прояви доброякісної гіпертрофії передміхурової залози виражаються в інфравезикальній обструкції сечовивідних шляхів, обумовленої як анатомічними (статичними), так і функціональними (динамічними) факторами. Функціональний компонент обструкції обумовлений збудженням альфа1-адренорецепторів, що призводить до скорочення гладкої мускулатури передміхурової залози, її оболонки, трикутника сечового міхура і передміхурової частини уретри, що призводить до збільшення опору відтоку сечі з сечового міхура і, мабуть, до вторинного небажаного. Внаслідок прямого впливу на гладку мускулатуру тканини передміхурової залози, пов'язаного з блокадою альфа1-адренорецепторів, алфузозин зменшує інфравезикальну обструкцію, тиск в уретрі та опір відтоку сечі під час сечовипускання. За рахунок цього алфузозин покращує відтік сечі та полегшує випорожнення сечового міхура. Ці сприятливі ефекти на уродінаміку ведуть до зменшення симптомів подразнення сечовивідних шляхів та симптомів, зумовлених порушеннями відтоку сечі у пацієнтів із доброякісною гіперплазією передміхурової залози. У пацієнтів з максимальною швидкістю відтоку сечі (Qmax) ≤15 мл/сек алфузозин, починаючи з першої дози, значно збільшує Qmax (в середньому на 30%). Крім того,у пацієнтів з доброякісною гіпертрофією передміхурової залози алфузозин значно знижує тиск у детрузорі сечового міхура і збільшує об'єм сечі, що викликає позиву до сечовипускання, а також значно знижує об'єм залишкової сечі. Ці ефекти призводять до зменшення обструктивних та ірритативних симптомів доброякісної гіпертрофії передміхурової залози. Препарат не надає несприятливого на сексуальну функцію. У зв'язку з селективністю дії алфузозину його вплив на альфа1-адренорецептори судин і, відповідно, на артеріальний тиск (АТ), у разі його застосування в терапевтичних дозах практично відсутній.Показання до застосуванняЛікування функціональних симптомів доброякісної гіперплазії передміхурової залози. Як допоміжний засіб при використанні катетера при гострій затримці сечі, пов'язаної з доброякісною гіперплазією передміхурової залози.Протипоказання до застосуванняПідвищена чутливість до алфузозину та/або допоміжних речовин препарату. Ортостатична гіпотензія. Печінкова недостатність. Тяжка ниркова недостатність (кліренс креатиніну Кишкова непрохідність (у зв'язку із вмістом у препараті касторової олії). Одночасний прийом інших альфа1-адреноблокаторів. Дитячий вік віком до 18 років. З обережністю: У пацієнтів, які приймають гіпотензивні препарати або нітрати (можливий розвиток ортостатичної гіпотонії, як протікає безсимптомно, так і симптоматичної, що супроводжується запамороченням, слабкістю, холодним потом). У пацієнтів похилого віку (старше 75 років). У пацієнтів із вираженою гіпотензивною реакцією на інші альфа1-адреноблокатори в анамнезі. У пацієнтів із ортостатичною гіпотензією з клінічними проявами. У пацієнтів з ішемічну хворобу серця, стенокардії (можливе почастішання та обтяження нападів стенокардії). У пацієнтів з вродженим або набутим подовженням інтервалу QT або у пацієнтів, які приймають лікарські препарати, що збільшують тривалість інтервалу QT. У пацієнтів із ішемією головного мозку. З інгібіторами ізоферменту CYP3A4 (кетоконазол, ітраконазол, ритонавір) (можливе збільшення концентрації алфузозину в плазмі).Вагітність та лактаціяПрепарат Дальфаз СР не призначений для застосування у жінок.Побічна діяНаведені нижче небажані реакції (HP) даються відповідно до наступних градацій частоти їх виникнення: дуже часто: (≥ 10%); часто (≥1% - <10%); нечасто (≥0,1% - <1%); рідко (0,01% – 0,1%); дуже рідко ( Порушення з боку крові та лімфатичної системи - Невідома частота: тромбоцитопенія. Порушення з боку серця – Нечасто: тахікардія, відчуття серцебиття; Дуже рідко: можливе почастішання або обтяження нападів стенокардії; Невідома частота: фібриляція передсердь. Порушення з боку органу зору: - Нечасто: порушення зору; Невідома частота: інтраопераційний синдром млявої райдужної оболонки. Загальні розлади та порушення у місці введення - Часто: астенія, нездужання; Нечасто: набряки, біль у грудях. Порушення з боку шлунково-кишкового тракту: - Часто: нудота, біль у животі; Нечасто: діарея; Невідома частота: блювання. Порушення з боку печінки та жовчовивідних шляхів - Невідома частота: гепатоцелюлярна жовтяниця, холестаз та пов'язані з ним захворювання печінки. Порушення з боку нервової системи: - Часто: почуття нудоти/запаморочення, головний біль; Нечасто: синкопальний стан, вертиго, сонливість; Невідома частота: ішемічні порушення мозкового кровообігу у пацієнтів із вже наявною цереброваскулярною патологією. Порушення з боку статевих органів та молочної залози - Невідома частота: пріапізм. Порушення з боку дихальної системи, органів грудної клітки та середостіння - Нечасто: риніт. Порушення з боку шкіри та підшкірних тканин - Нечасто: висипання, свербіж; Дуже рідко: кропив'янка, ангіоневротичний набряк. Порушення з боку судин – Нечасто: зниження артеріального тиску, включаючи ортостатичну гіпотензію, гіперемія шкірних покривів.Взаємодія з лікарськими засобамиПротипоказані комбінації З блокаторами альфа1-рецепторів (празозин, урапідил): посилення гіпотензивного ефекту, ризик розвитку тяжкої ортостатичної гіпотензії. Взаємодії, які слід брати до уваги З гіпотензивними препаратами: посилення гіпотензивного ефекту та ризик розвитку ортостатичної гіпотензії (адитивна дія). З нітратами: збільшення ризику розвитку рефлекторної тахікардії та зниження АТ. Із засобами для інгаляційної та неінгаляційної загальної анестезії: можлива нестабільність АТ під час загальної анестезії. З інгібіторами ізоферменту CYP3A4 (кетоконазол, ітраконазол, ритонавір): можливе збільшення концентрації алфузозину в плазмі. При поєднанні алфузозину в дозі 10 мг на добу з курсовим застосуванням кетоконазолу в дозі 200 мг на добу протягом 7 днів Cmax та AUC алфузозину збільшуються в 2,1 рази та 2,46 разів, відповідно, а при його поєднанні з курсовим застосуванням кетоконазолу дозі 400 мг на добу протягом 8 днів Cmax та AUC алфузозину збільшуються у 2,3 рази та 3,0 рази відповідно.Спосіб застосування та дозиПрепарат призначений для вживання. Пацієнти повинні ковтати таблетку повністю. Забороняється подрібнювати, роздавлювати, розжовувати, розмелювати таблетку на порошок. Ці дії можуть призвести до неналежного вивільнення алфузозину з таблетки та його швидкої абсорбції, що збільшує ризик розвитку небажаних реакцій. Лікування функціональних симптомів доброякісної гіперплазії передміхурової залози Рекомендована доза становить: 1 таблетка (10 мг) щоденно після їди. Застосування як допоміжний засіб при використанні катетера при гострій затримці сечі, пов'язаної з доброякісною гіперплазією передміхурової залози Рекомендована доза – 1 таблетка (10 мг) на добу, після їди, починаючи з першого дня катетеризації. Препарат застосовують протягом 3-4 діб, тобто 2-3 дні під час знаходження катетера в уретрі та 1 день після його видалення.Запобіжні заходи та особливі вказівкиПротягом декількох годин після прийому алфузозину (як і після прийому будь-яких інших альфа1-адреноблокаторів) у деяких осіб, особливо у пацієнтів, які приймають гіпотензивні препарати, може розвинутись ортостатична гіпотензія з клінічною симптоматикою (запаморочення, різка слабкість, холодний піт) або без її. З появою цих явищ пацієнт повинен до повного зникнення перебувати у горизонтальному положенні. Ортостатична гіпотензія зазвичай буває скороминущою і спостерігається, як правило, на початку прийому препарату і зазвичай не вимагає відміни лікування. При постмаркетинговому застосуванні препарату у пацієнтів з факторами ризику зниження артеріального тиску (такими як захворювання серця або супутня терапія гіпотензивними препаратами) повідомлялося про виражене зниження артеріального тиску. Ризик надмірного зниження АТ і пов'язаних з ним небажаних реакцій може бути вищим у пацієнтів похилого віку. Перед початком лікування хворий має бути попереджений про можливість виникнення описаних вище реакцій. Слід дотримуватися обережності при застосуванні алфузозину у пацієнтів з ортостатичною гіпотензією з клінічною симптоматикою або у пацієнтів, які приймають гіпотензивні препарати або нітрати: необхідний ретельніший контроль за АТ, у тому числі при переході з горизонтального положення у вертикальне, особливо на початку лікування. Слід бути обережними при застосуванні алфузозину у пацієнтів з вираженою гіпотензивною реакцією у відповідь на прийом інших блокаторів альфа1-адренорецепторів в анамнезі. Пацієнтам з коронарною недостатністю при прийомі алфузозину необхідно продовжувати антиангінальну терапію. При відновленні або обтяженні стенокардії лікування алфузозином слід припинити. Слід бути обережними при застосуванні алфузозину у пацієнтів з вродженим або набутим подовженням інтервалу QT або у пацієнтів, які приймають лікарські препарати, здатні подовжувати інтервал QT. Під час проведення офтальмологічних операцій з приводу катаракти у деяких пацієнтів, які приймали або приймали раніше деякі альфа1-адреноблокатори, спостерігався розвиток інтраопераційного синдрому млявої райдужної оболонки (варіант синдрому вузької зіниці). Хоча ризик розвитку такого ускладнення при прийомі препарату Дальфаз® СР є дуже низьким, перед проведенням операції з приводу катаракти хірург-офтальмолог повинен бути поінформований про те, що пацієнт приймає альфа1-адреноблокатори або приймав їх раніше, оскільки розвиток інтраопераційного синдрому млявої райдужної оболонки може збільшувати кількість ускладнень у своїй оперативному втручанні. Офтальмологи мають бути готовими до можливої зміни методики оперативного втручання. Пацієнтів слід попередити, що забороняється подрібнювати, роздавлювати, розжовувати, розмелювати таблетку на порошок. Такі дії можуть призвести до надмірного вивільнення та абсорбції препарату, внаслідок чого можливий швидкий розвиток побічних ефектів, що особливо небезпечно у пацієнтів з цереброваскулярними розладами, що протікають з відповідними симптомами, а також у тих пацієнтів, у яких цереброваскулярні розлади протікають безсимптомно, оскільки пацієнтів при різкому зниженні артеріального тиску можливе посилення ішемії головного мозку. Є повідомлення про випадки розвитку на фоні терапії альфа г адреноблокатор приапізму (тривалої хворобливої ерекції статевого члена, не пов'язаної з сексуальною активністю). Якщо терапія приапізму не була проведена негайно, це може призвести до пошкодження тканин статевого члена та необоротної втрати потенції. Пацієнтів слід інформувати про серйозність цього стану та необхідність негайного звернення за медичною допомогою у разі збереження ерекції протягом більше 4-х годин. Вплив на здатність до керування автотранспортом та управління механізмами Необхідно бути обережними при керуванні транспортними засобами та заняттями іншими потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій, оскільки препарат може викликати запаморочення та інші побічні ефекти, які можуть впливати на зазначені здібності.Умови відпустки з аптекЗа рецептом
20 442,00 грн
303,00 грн
Склад, форма випуску та упаковкаРозчин - 0.8 мл: Діюча речовина: адалімумаб – 40,0 мг; Допоміжні речовини: динатрію гідрофосфату дигідрат – 1,224 мг, натрію дигідрофосфату дигідрат – 0,688 мг, полісорбат 80 – 0,8 мг, манітол – 9,6 мг; лимонної кислоти моногідрат – 1,044 мг; натрію цитрат – 0,244 мг; натрію хлорид – 4,932 мг; натрію гідроксид для корекції pH – до pH 5,2, вода для ін'єкцій – до 0,8 мл. Розчин для підшкірного введення 40 мг/0,8 мл. Препарат в одноразовому шприці По 0,8 мл препарату в одноразовому трикомпонентному стерильному шприці з нейтрального безбарвного скла I гідролітичного класу. По одному шприцю в блістері із ПВХ. По 1 або 2 блістери разом з інструкцією із застосування та 1 або 2 спиртовими серветками в картонній пачці. Препарат у флаконі По 0,8 мл препарату у флаконі, виготовленому з безбарвного нейтрального скла I гідролітичного класу, закупореному гумовою пробками з бутилкаучуку, ламінованим фторполімером, обжатий алюмінієвим ковпачком з пластиковою кришкою типу "flip-off". По 1 флакону поміщають у контурне осередкове впакування з плівки ПВХ. По 1 або 2 контурній комірковій упаковці разом з інструкцією із застосування та 1 або 2 спиртовими серветками в картонній пачці. Препарат в автоінжекторі По 0,8 мл препарату в одноразовому трикомпонентному стерильному шприці з безбарвного нейтрального скла I гідролітичного класу, розміщеному в автоінжекторі, що складається із захисного ковпачка, корпусу із прозорою зоною контролю, верхнього корпусу та кнопки активації. Внутрішній пристрій автоінжектора має циліндр, що захищає голку і поршень, який через систему механічного пуску з'єднаний з кнопкою активації. По 1 автоінжектору поміщають у контурне осередкове пакування з плівки ПВХ. По 1 або 2 контурній комірковій упаковці разом з інструкцією із застосування та 1 або 2 спиртовими серветками в картонній пачці.Опис лікарської формиОпалесцентний розчин світло-коричневого кольору.Фармакотерапевтична групаІмунодепресивний засіб.ФармакокінетикаВсмоктування Адалімумаб всмоктується і розподіляється повільно і досягає своєї максимальної сироваткової концентрації приблизно через 5 днів. Абсолютна біодоступність препарату при одноразовому підшкірному введенні 40 мг адалімумабу становить 64%. Розподіл та виведення Об'єм розподілу (Vd) при одноразовому внутрішньовенному введенні становить від 4,7 до 6,0 л, що вказує на практично однаковий розподіл адалімумабу в крові та позасудинних рідинах. Адалімумаб виводиться повільно, кліренс (С1) зазвичай не перевищує 12 мл/год. Період напіввиведення (T1/2) становить у середньому 2 тижні і варіює від 10 до 20 днів. Сl і T1/2 суттєво не змінюються при введенні доз 0.25-10 мг/кг, а T1/2 подібний при внутрішньовенному та підшкірному введенні адалімумабу. Концентрація адалімумабу в синовіальній рідині у пацієнтів з ревматоїдним артритом становить 31% - 96% від такої, у сироватці. Фармакокінетика адалімумабу у рівноважному стані Рівноважні концентрації адалімумабу при підшкірному введенні в дозі 40 мг один раз на два тижні у хворих на ревматоїдний артрит наприкінці інтервалу дозування становили близько 5 мкг/мл (без одночасного прийому метотрексату (МТХ)) та 8-9 мкг/мл (на фоні одночасного застосування). МТХ). При збільшенні дози адалімумабу в інтервалі 20 мг, 40 мг та 80 мг один раз на два тижні та один раз на тиждень підшкірно відмічено близьке до пропорційного збільшення сироваткових концентрацій адалімумабу наприкінці інтервалу дозування. При тривалому застосуванні (більше 2 років) кліренс адалімумабу не змінювався. При терапії адалімумабом (без метотрексату) у дозі 40 мг один раз на 2 тижні середня рівноважна мінімальна концентрація (Сmin) препарату у пацієнтів із псоріазом склала 5 мкг/мл. Відзначено тенденцію до зростання Сl адалімумабу при збільшенні маси тіла та наявності антитіл до адалімумабу. Для пацієнтів з хворобою Крона, зі стартовою дозою 160 мг на 0-му тижні та з подальшою дозою 80 мг на 2-му тижні, адалімумаб досягає своєї максимальної сироваткової концентрації (Сmах) (приблизно 12 мкг/мл) на 2-й та 4 -й тижні. У пацієнтів із хворобою Крона рівноважна концентрація (приблизно 7 мкг/мл) спостерігається на 24-му та 56-му тижнях підтримуючої терапії із застосуванням 40 мг адалімумабу один раз на 2 тижні. У пацієнтів з активним гнійним гідраденітом при введенні дози адалімумабу 160 мг на 0 тижні і потім 80 мг на 2 тижні було досягнуто максимальної концентрації адалімумабу в сироватці крові приблизно від 7 до 8 мкг/мл на 2 та 4 тижні. Середня мінімальна рівноважна концентрація з 12 до 36 тижнів склала близько 8-10 мкг/мл при лікуванні адалімумабом 40 мг один раз на тиждень. У пацієнтів з виразковим колітом, які отримували 160 мг адалімумабу вихідно та 80 мг через 2 тижні, концентрація препарату в плазмі становила приблизно 12 мкг/мл протягом індукційного періоду. Рівноважна концентрація становила приблизно 8 мкг/мл у пацієнтів, які отримували підтримуючу дозу 40 мг 1 раз на 2 тижні. У пацієнтів з увеїтом при введенні дози 80 мг на 0-му тижні, потім 40 мг через 1 тиждень і далі при продовженні терапії в дозі 40 мг 1 раз на 2 тижні рівноважна концентрація становила приблизно 8-10 мкг/мл. Діти Після введення 24 мг/м2 адалімумабу (максимум до 40 мг) підшкірно один раз на два тижні пацієнтам від 4 років до 17 років з ювенільним ідіопатичним артритом середня рівноважна концентрація адалімумабу (виміряна з 20-го тижня по 48-му) у сироватці крові. 5,6±5,6 мкг/мл (102% коефіцієнт варіації (CV)) при терапії адалімумабом без метотрексату та 10,9±5,2 мкг/мл (47,7% CV) із супутньою терапією метотрексатом. Середня рівноважна концентрація адалімумабу у сироватці крові у пацієнтів з масою тіла менше 30 кг, після введення адалімумабу у дозі 20 мг підшкірно один раз на два тижні, становила 6,8 мкг/мл при терапії адалімумабом без метотрексату та 10,9 мкг/мл. застосування у комбінації з метотрексатом. Середня рівноважна концентрація адалімумабу у сироватці крові у пацієнтів з масою тіла 30 кг і більше після введення адалімумабу у дозі 40 мг підшкірно один раз на два тижні становила 6,6 мкг/мл при терапії адалімумабом без метотрексату та 8,1 мкг/мл при застосуванні у комбінації з метотрексатом. У пацієнтів віком від 2 років до 4 років або від 4 років і старших з масою тіла менше 15 кг з ювенільним ідіопатичним артритом середня рівноважна концентрація становила 6,0±6,1 мкг/мл (101% CV) при терапії адалімумабом без метотрексу та 7,9±5,6 мкг/мл (71,2% CV) при застосуванні у комбінації з метотрексатом. У пацієнтів дитячого віку з хворобою Крона (середньотяжкого або тяжкого ступеня) після введення стартової дози адалімумабу 160/80 мг або 80/40 мг (залежно від маси тіла) на 0-му тижні та 2-му тижні, і далі із застосуванням підтримуючих доз 40/20 мг або 20/10 мг один раз на 2 тижні (залежно від маси тіла), середня концентрація адалімумабу в сироватці крові (з урахуванням стандартного відхилення) на 4-му тижні застосування становила 15,7±6,6 мкг /мл (у пацієнтів із масою тіла від 40 кг і більше) та 10,6 ± 6,1 мкг/мл (у пацієнтів із масою тіла менше 40 кг). Після введення 0,8 мг/кг (до 40 мг) підшкірно один раз на два тижні для лікування хронічного бляшкового псоріазу у дітей середня рівноважна концентрація адалімумабу становила близько 7,4±5,8 мкг/мл (79% CV). Експозиція адалімумабу у підлітків з 12 років з ГГ була спрогнозована, використовуючи моделювання та прогнозування на підставі наявних фармакокінетичних даних, отриманих у дослідженнях у пацієнтів дитячого віку з іншими захворюваннями (хронічний бляшковий псоріаз, ювенільний ідіопатичний артрит, хвороба Крона ). Рекомендована доза у підлітків становить 40 мг один раз на два тижні, таким чином, експозиція адалімумабу в сироватці крові очікується такою самою, що спостерігалася у дорослих пацієнтів, які отримували 40 мг адалімумабу 1 раз на тиждень. Особливі групи пацієнтів Літні пацієнти Вік надає мінімальний вплив на Сl адалімумабу. Підлога, раса Відмінностей у показниках фармакокінетики (з поправкою на масу тіла) у пацієнтів різної статі та расової приналежності не виявлено. Печінкова та ниркова недостатність Відомостей про фармакокінетику адалімумабу у хворих з порушенням функції печінки або нирок немає.ФармакодинамікаМеханізм дії Адалімумаб є рекомбінантним моноклональним антитілом, пептидна послідовність якого ідентична IgG1 людини. Адалімумаб селективно зв'язується з фактором некрозу пухлини альфа (ФНП-α) та нейтралізує його біологічні функції за рахунок блокади взаємодії з поверхневими клітинними р55 та р75 рецепторами до ФНП-α. ФНП-α - це природний цитокін, який бере участь у регуляції нормальної запальної та імунної відповіді. Підвищену концентрацію ФНП-α виявляють у синовіальній рідині у пацієнтів з ревматоїдним артритом (РА), псоріатичним артритом (ПсА) та анкілозуючим спондилітом (АС). ФНП-α відіграє важливу роль у розвитку патологічного запалення та руйнування суглобової тканини, характерних для цих захворювань. Підвищені концентрації ФНП-α також виявляються у псоріатичних бляшках. При бляшковому псоріазі лікування адалімумабом може призвести до зменшення товщини бляшок та інфільтрації запальними клітинами. Взаємозв'язок між цим клінічним ефектом адалімумабу та механізмом його дії не встановлений. Також адалімумаб модулює біологічні реакції у відповідь, які посилюються або регулюються ФНП-α, включаючи зміни рівнів молекул адгезії, що викликають міграцію лейкоцитів. Фармакодинаміка У пацієнтів з ревматоїдним артритом адалімумаб викликав швидке зниження концентрації острофазових показників запалення (С-реактивного білка (СРВ) та швидкості осідання еритроцитів) та сироваткової концентрації цитокінів (інтерлейкін-6). Зменшення концентрацій СРВ також спостерігалося у пацієнтів з ювенільним ідіопатичним артритом, хворобою Крона, виразковим колітом, активним гнійним гідраденітом. Крім того, відзначалося зниження сироваткової активності матриксних металопротеїназ (ММП-1 та ММП-3), що викликають ремоделювання тканин, що лежить в основі руйнування хрящової тканини.Показання до застосуванняДорослі Середньотяжкий та тяжкий активний ревматоїдний артрит (у режимі монотерапії або у комбінації з метотрексатом або іншими базовими протизапальними препаратами). У комбінації з метотрексатом адалімумаб знижує швидкість прогресування пошкодження суглобів (за даними рентгенографічного дослідження) та покращує функціональну активність. Активний псоріатичний артрит (у режимі монотерапії або комбінації з метотрексатом або іншими базовими протизапальними препаратами). Активний анкілозуючий спондиліт. Хвороба Крона (середньотяжкого чи тяжкого ступеня): при неадекватній відповіді на традиційну терапію, а також непереносимість або протипоказання до традиційної терапії; при неефективності (або зниженні ефективності) або непереносимості інфліксімабу. Хронічний бляшковий псоріаз (середньотяжкого та тяжкого ступеня), коли показана системна терапія. Виразковий коліт середньотяжкого та тяжкого ступеня, при неадекватній відповіді на традиційну терапію, включаючи кортикостероїди та/або б-меркаптопурин або азатіоприн, а також при непереносимості чи протипоказаннях до традиційної терапії. Неінфекційний увеїт (середній, задній) і панувеїт у дорослих при неадекватній відповіді на терапію кортикостероїдами, у ситуаціях, коли потрібне обмеження дози або відміна кортикостероїдів, а також коли терапія кортикостероїдами протипоказана. Аксіальний спондилоартрит без рентгенологічно підтвердженого анкілозуючого спондиліту, але за наявності об'єктивних ознак запалення за підвищеним рівнем СРБ та/або даними МРТ, за відсутності адекватної відповіді на лікування нестероїдними протизапальними препаратами або їх непереносимістю. Активний гнійний гідраденіт середнього або тяжкого ступеня тяжкості у дорослих пацієнтів за відсутності адекватної відповіді на стандартну системну терапію. Діти Ювенільний ідіопатичний артрит у пацієнтів віком від 2 років у режимі монотерапії або у комбінації з метотрексатом. Хвороба Крона (середньотяжкого та тяжкого ступеня) у пацієнтів 6 років і старше при неадекватній відповіді на традиційну терапію (включаючи повне ентеральне харчування та кортикостероїди та/або імуносупресори), а також непереносимість або протипоказання до традиційної терапії. Активний ентезит-асоційований артрит у пацієнтів віком від 6 років та старших за відсутності адекватної відповіді на терапію стандартними препаратами або їх непереносимості. Хронічний бляшковий псоріаз (тяжкого ступеня) у дітей з 4 років при неадекватній відповіді на місцеву терапію або фототерапію, а також у пацієнтів, яким місцева терапія та фототерапія протипоказана. Активний гнійний гідраденіт середнього або тяжкого ступеня тяжкості у дітей віком від 12 років за відсутності адекватної відповіді на стандартну системну терапію.Протипоказання до застосуванняГіперчутливість до адалімумабу або до будь-яких його допоміжних компонентів. Вагітність. Період грудного вигодовування. Дитячий вік до 18 років (крім пацієнтів від 2 років з ювенильним ідіопатичним артритом, пацієнтів від 6 років з хворобою Крона (середньотяжкого або тяжкого ступеня), пацієнтів від 6 років з активним ентезит-асоційованим артритом, пацієнтів від 4 років з хронічним бляшковим псори пацієнтів від 12 років з активним гнійним гідраденітом). Інфекційні захворювання, зокрема туберкульоз. Спільний прийом з антагоністами ПІБ або іншими генно-інженерними біологічними протиревматичними препаратами (наприклад, анакінра та абатацепт). З обережністю: Рецидивні інфекції в анамнезі. Носіння вірусу гепатиту Ст. Злоякісні новоутворення, зокрема в анамнезі. Серцева недостатність. Демієлінізуючі захворювання нервової системи, у тому числі в анамнезі. Пацієнти віком від 65 років.Вагітність та лактаціяУ дослідженнях на тваринах у дозах до 100 мг/кг ознак негативної дії адалімумабу на плід не виявлено. Однак у доказових контрольованих дослідженнях у вагітних жінок препарат не вивчався, тому застосування адалімумабу протипоказане під час вагітності. Жінкам репродуктивного віку слід уникати вагітності під час лікування адалімумабом. Відомостей про виведення адалімумабу з грудним молоком або його всмоктування після прийому внутрішньо немає. Багато людських імуноглобулінів проникають у грудне молоко. З огляду на ризик розвитку серйозних побічних реакцій у новонародженого, годування груддю не рекомендується в період лікування адалімумабом та протягом щонайменше п'яти місяців після останньої ін'єкції адалімумабу. Рішення про припинення годівлі або припинення лікування адалімумабом необхідно приймати, ґрунтуючись на важливості продовження терапії для матері. Пологи Вплив адалімумабу на родову діяльність та пологи невідомий.Побічна діяДані клінічних досліджень Приблизно у 13% пацієнтів очікується розвиток реакцій у місці введення препарату (одні з найпоширеніших побічних ефектів при введенні адалімумабу у контрольованих клінічних дослідженнях). Побічні реакції, можливо причинно пов'язані із застосуванням препарату, як клінічні, так і лабораторні, наведені із зазначенням частоти: дуже часто (≥1/10), часто (≥1/100, але Інфекції Дуже часто: інфекції дихальних шляхів (включаючи інфекції верхніх та нижніх дихальних шляхів, пневмонію, синусит, фарингіт, назофарингіт та герпес-вірусну пневмонію). Часто: генералізовані інфекції (включаючи сепсис, кандидоз і грип), інфекції шлунково-кишкового тракту (включаючи вірусний гастроентерит), інфекції шкіри та м'яких тканин (включаючи паронихій, целюліт, імпетиго, некротизуючий фасціїт та опоясуючий лишай) герпес, оральний герпес та ураження зубів), інфекції статевої сфери (включаючи вульвовагінальну мікотичну інфекцію), інфекції сечовивідного тракту (включаючи пієлонефрит), грибкові інфекції, інфекції суглобів. Нечасто: опортуністичні інфекції та туберкульоз (включаючи кокцидіоїдомікоз, гістоплазмоз та комплекс інфекцій, що викликаються Mycobacterium avium), неврологічні інфекції (включаючи вірусний менінгіт), інфекції ока, бактеріальні інфекції. Новоутворення Часто: доброякісні новоутворення, рак шкіри, крім меланоми (включаючи базально-клітинну карциному та лускато-клітинну карциному). Нечасто: лімфома, паренхіматозні новоутворення (включаючи рак молочної залози, новоутворення легені та щитовидної залози), меланома. З боку крові та лімфатичної системи Дуже часто: лейкопенія (включаючи нейтропенію та агранулоцитоз), анемія. Часто: тромбоцитопенія, лейкоцитоз. Нечасто: ідіопатична тромбоцитопенічна пурпура. Рідко: панцитопенія. З боку імунної системи Часто: реакції гіперчутливості, алергічні реакції (включаючи сезонну алергію). З боку обміну речовин Дуже часто: підвищення концентрації ліпідів. Часто: гіпокаліємія, підвищення концентрації сечової кислоти, аномальна концентрація натрію, гіпокальціємія, гіперглікемія, гіпофосфатемія, дегідратація. Порушення психіки Часто: зміни настрою (включаючи депресію), тривожні розлади, безсоння. З боку нервової системи Дуже часто: головний біль. Часто: парестезії (включаючи гіпестезію), мігрень, невралгія сідничного нерва, вестибулярне запаморочення. Нечасто: тремор, нейропатія. Рідко: розсіяний склероз. З боку органів чуття Часто: кон'юнктивіт, порушення зору, блефарит, набряк віку. Нечасто: диплопія, глухота, дзвін у вухах. З боку серцево-судинної системи Найчастіше: підвищення артеріального тиску, припливи, гематоми, тахікардія. Нечасто: аритмія, застійна серцева недостатність, артеріальна оклюзія, тромбофлебіт, аневризм аорти. Рідко: зупинка серця. З боку системи дихання Часто: кашель, астма, диспное. Нечасто: хронічна обструктивна хвороба легень, інтерстиціальні захворювання легень, пневмоніт. З боку системи травлення Дуже часто: нудота, блювання, біль у животі, підвищення активності печінкових ферментів. Часто: диспепсія, гастроезофагеальний рефлюкс, сухість у роті, шлунково-кишкові кровотечі. Нечасто: панкреатит, дисфагія, набряк обличчя, холецистит, холелітіаз, підвищення концентрації білірубіну, печінковий стеатоз. З боку шкіри та підшкірних тканин Дуже часто: висип (в т.ч. ексфоліативний). Часто: свербіж, кропив'янка, крововилив (в т.ч. пурпуру), дерматит (в т.ч. екзема), ламкість нігтів, гіпергідроз. Нечасто: нічна пітливість, рубці. З боку кістково-м'язової системи Дуже часто: кістково-м'язовий біль. Часто: м'язові спазми. Нечасто: рабдоміоліз, системний червоний вовчак. З боку сечостатевої системи Нерідко: гематурія, ниркова недостатність. Нечасто: ніктурія, еректильна дисфункція. Інші, включаючи реакції у місці введення Дуже часто: реакції у місці ін'єкції (включаючи еритему). Часто: біль у грудній клітці, набряки, погіршення загоєння ран. Нечасто: запалення. Лабораторні показники Часто: порушення в системі згортання крові (включаючи збільшення активованого часткового тромбопластинового часу), позитивні тести на аутоантитіла (включаючи антитіла до подвійної спіралі ДНК), збільшення концентрації лактатдегідрогенази. Клінічні випробування у дітей В основному, побічні реакції у дітей були однаковими за типом та частотою з тими, які спостерігалися у дорослих. Реакції у місці ін'єкції У базових дослідженнях у 12,9% пацієнтів, яким вводили адалімумаб, розвинулися реакції у місці введення (еритема та/або свербіж, кровотеча, біль, припухлість), у контрольній групі такі реакції розвинулися у 7,2% пацієнтів. Більшість реакцій у місці ін'єкцій оцінювалися як слабкі та не вимагали припинення прийому препарату. Інфекції У контрольованих дослідженнях рівень інфекційних ускладнень становив 1,51 на одного пацієнта на рік при лікуванні адалімумабом та 1,46 на одного пацієнта на рік у контрольній групі пацієнтів (дорослого та дитячого віку). Частота серйозних інфекційних ускладнень становила 0,04 на одного пацієнта на рік при лікуванні адалімумабом та 0,03 на одного пацієнта на рік у контрольній групі пацієнтів. Інфекційні ускладнення були здебільшого представлені інфекціями верхніх дихальних шляхів, назофарингітом, синуситом, бронхітом та інфекціями сечовидільного тракту. Більшість пацієнтів продовжували приймати адалімумаб після вирішення інфекції. У контрольованих відкритих дослідженнях адалімумабу повідомлялося про серйозні інфекції (включаючи рідкісні смертельні інфекції), зокрема про туберкульоз (включаючи міліарний та позалегеневий), легіонельоз та інвазивні опортуністичні інфекції (в т.ч. дисемінований гістоплазмоз і гемоплазму). Злоякісні новоутворення та лімфопроліферативні розлади У клінічних дослідженнях у 249 пацієнтів з ювенільним ідіопатичним артритом не спостерігалося злоякісних новоутворень під час спостереження протягом 655,6 пацієнтів. У клінічних дослідженнях у 192 пацієнтів дитячого віку із хворобою Крона не спостерігалося злоякісних новоутворень під час спостереження протягом 258,9 пацієнтів. Під час контрольованих етапів базових випробувань адалімумабу тривалістю щонайменше 12 тижнів у пацієнтів з ревматоїдним артритом, псоріатичним артритом, анкілозуючим спондилітом, аксіальним спондилоартритом, хворобою Крона, виразковим колітом, активним гномним , за винятком лімфоми та немеланомного раку шкіри, спостерігалися з частотою (95% довірчий інтервал) 6,8 (4,4-10,5) на 1000 пацієнто-років серед 5291 пацієнтів, які приймали адалімумаб, порівняно з 6,3 (3 ,4-11,8) на 1000 пацієнто-років серед 3444 пацієнтів контрольної групи (середня тривалість лікування становила 4,0 місяці при застосуванні адалімумабу та 3,8 місяця у контрольній групі пацієнтів). Частота (95% довірчий інтервал) раку шкіри, крім меланоми,становила 8,8 (6.0-13,0) на 1000 пацієнто-років серед пацієнтів, які приймали адалімумаб, та 3,2 (1,3-7,6) на 1000 пацієнто-років серед пацієнтів контрольної групи. Із загальної кількості випадків раку шкіри лускато-клітинні карциноми виникали з частотою (95% довірчий інтервал) 2,7 (1,4-5,4) на 1000 пацієнто-років серед пацієнтів, які приймали препарат адалімумаб, та 0,6 (0, 1-4,5) на 1000 пацієнто-років серед пацієнтів контрольної групи. Частота (95% довірчий інтервал) виникнення лімфом у пацієнтів, які застосовували адалімумаб, становила 0,7 (0,2-2,9) на 1000 пацієнто-років та 0,7 (0,1- 4,9) на 1000 пацієнто- років серед пацієнтів контрольної групи Частота, що спостерігається, злоякісних новоутворень, за винятком лімфом і немеланомного раку шкіри, становила близько 8,5 на 1000 пацієнто-років у контрольованих фазах клінічних досліджень, а також тривалих і завершених відкритих дослідженнях. Частота раку шкіри (крім меланоми), що спостерігається, становила близько 9,6 на 1000 пацієнто-років, спостерігається частота лімфоми - близько 1,3 на 1000 пацієнто-років. Середня тривалість цих досліджень становила близько 3,3 років і включала 6427 пацієнтів, які приймали адалімумаб щонайменше 1 рік або у яких розвинулося злоякісне новоутворення протягом 1 року від початку терапії, охоплюючи 26439,6 пацієнтів. Аутоантитіла На IV етапах дослідження ревматоїдного артриту проводився аналіз сироватки крові пацієнтів на аутоантитіла. У достовірних контрольованих випробуваннях повідомлялося, що у 11,9% пацієнтів, які приймали препарат адалімумаб, і у 8,1% пацієнтів, які приймали плацебо, та пацієнтів контрольної групи, які мали спочатку негативні титри антинуклеарних антитіл, позитивні титри з'явилися на 24 тижні. . У 2 з 3989 пацієнтів, які приймали адалімумаб у дослідженнях РА, ПсА та АС, розвинулися клінічні прояви вовчаково-подібного синдрому. Стан пацієнтів покращився після відміни лікування. У жодного з пацієнтів не розвинувся люпус-нефрит або симптоми ураження центральної нервової системи. Вплив тривалого застосування адалімумабу на розвиток аутоімунних захворювань залишається невивченим. Псоріаз: розвиток та погіршення Описуються випадки появи псоріазу, включаючи пустульозний псоріаз і долонопідошовний псоріаз, та випадки погіршення існуючого псоріазу при застосуванні всіх блокаторів ФНП, включаючи адалімумаб. Багато з цих пацієнтів приймали імунодепресанти (у тому числі МТХ, кортикостероїди) як супутнє лікування. Деяким із цих пацієнтів була потрібна госпіталізація. У більшості пацієнтів настало поліпшення стану після відміни блокаторів ФНП. У деяких пацієнтів наставав рецидив псоріазу після початку прийому різних блокаторів ФНП. Скасування адалімумабу має здійснюватися у тяжких випадках і тоді, коли немає поліпшення, або є погіршення у відповідь на місцеве лікування. Підвищення активності ферментів печінки У контрольованих дослідженнях адалімумабу III фази (40 мг п/к 1 раз на два тижні) у пацієнтів з ревматоїдним артритом та псоріатичним артритом з тривалістю контрольного періоду від 4 до 104 тижнів підвищення активності АЛТ≥3 ВГН було зареєстровано у 3,7% пацієнтів, отримували адалімумаб, та у 1,6% пацієнтів контрольної групи. У зв'язку з тим, що багато пацієнтів у цих дослідженнях також приймали лікарські препарати, які викликають підвищення активності ферментів печінки (наприклад, НПЗЗ, метотрексат), взаємозв'язок між адалімумабом та підвищенням активності ферментів печінки не зрозумілий. У контрольованих дослідженнях III фази адалімумабу (початкова доза 160 мг та 80 мг, або 80 мг та 40 мг у дні 1 та 15 відповідно, а потім 40 мг кожні два тижні) у пацієнтів із хворобою Крона з тривалістю контрольного періоду від 4 до 52 тижнів , підвищення активності АЛТ ≥3хВГН було зареєстровано у 0,9% пацієнтів, які отримували адалімумаб, та у 0,9% пацієнтів контрольної групи. У контрольованих дослідженнях III фази адалімумабу (початкова доза 160 мг та 80 мг у дні 1 та 15 відповідно, а потім 40 мг кожні два тижні) у пацієнтів з виразковим колітом з тривалістю контрольного періоду від 1 до 52 тижнів підвищення активності АЛТ≥3 ВГН було зареєстровано у 1,5% пацієнтів, які отримували адалімумаб, та у 1,0% пацієнтів контрольної групи. У контрольованих дослідженнях III фази адалімумабу (початкова доза 80 мг,потім 40 мг кожні два тижні) у пацієнтів з бляшковим псоріазом з тривалістю контрольного періоду від 12 до 24 тижнів підвищення активності АЛТ ≥3хВГН було зареєстровано у 1,8% пацієнтів, які отримували адалімумаб, та у 1,8% пацієнтів контрольної групи. У контрольованих дослідженнях III фази адалімумабу (40 мг 1 раз на два тижні) у пацієнтів з аксіальним спондилоартритом (анкілозуючий спондиліт та нерентгенологічний аксіальний спондилоартрит) з тривалістю контрольного періоду від 12 до 24 тижнів, підвищення активності АЛТ ≥3хВГН пацієнтів, які отримували адалімумаб, та у 0,8% пацієнтів контрольної групи. У контрольованих дослідженнях III фази адалімумабу у пацієнтів з ювенільним ідіопатичним артритом у віці від 4 до 17 років та у пацієнтів з ентезит-асоційованим артритом у віці від 6 до 17 років підвищення активності АЛТ ≥3хВГН було зареєстровано у 6,1% пацієнтів, , та у 1,3% пацієнтів контрольної групи. Більшість випадків підвищення активності АЛТ було зареєстровано при одночасному використанні метотрексату. У дослідженні ІІІ фази адалімумабу у пацієнтів з поліартикулярним ювенільним ідіопатичним артритом у віці від 2 до 4 років випадків підвищення активності АЛТ не зареєстровано. У дослідженні III фази адалімумабу у дітей із хворобою Крона, в якому оцінювалися ефективність та безпеку двох підтримуючих дозових схем (скоригованих на підставі маси тіла) після індукційної терапії, загальна тривалість періоду лікування в якому становила до 52 тижнів, підвищення активності АЛТ>3хВГН було зареєстровано у 2,6% (5/192) пацієнтів, з яких 4 пацієнти на момент початку дослідження отримували супутнє лікування імуносупресорами. У контрольованих дослідженнях адалімумабу (початкова доза 80 мг на тиждень 0, потім по 40 мг на тиждень, починаючи з тижня 1 у пацієнтів з увеїтом, максимальна тривалість яких склала 80 тижнів, із середньою експозицією 166,5 та 105,0 днів у групі пацієнтів , що отримували адалімумаб та у контрольній групі відповідно, спостерігалося підвищення АЛТ ≥3хВГН у 2,4% пацієнтів, які отримували адалімумаб, та у 2,4% пацієнтів у контрольній групі. При всіх показаннях у клінічних дослідженнях підвищення активності АЛТ у пацієнтів не супроводжувалося симптомами, і в більшості випадків мало минущий характер і дозволялося без припинення лікування. Тим не менш, у постмаркетинговому періоді застосування інгібіторів ФНП були отримані дуже рідкісні повідомлення про важкі печінкові реакції, включаючи печінкову недостатність у пацієнтів, які отримують антагоністи ФНП, у тому числі адалімумаб. Причинно-наслідковий зв'язок таких реакцій з лікуванням адалімумаб залишається неясним. Дані постреєстраційних досліджень адалімумабу Інфекції та інвазії: дивертикуліг. Доброякісні, злоякісні та некласифіковані новоутворення (включаючи кісти та поліпи): гепатоспленарна Т-клітинна лімфома, лейкемія, карцинома Меркеля (нейроендокринна шкірна карцинома). З боку імунної системи: анафілаксія, саркоїдоз. З боку нервової системи: демієлінізуючі захворювання (в т.ч. неврит зорового нерва, синдром Гійєна-Барре); цереброваскулярні розлади. Серцево-судинна система: легенева емболія, інфаркт міокарда. З боку дихальної системи: плевральний випіт, легеневий фіброз. З боку системи травлення: перфорація кишечника, реактивація вірусу гепатиту В, печінкова недостатність, гепатит. З боку шкіри та підшкірних тканин: шкірний васкуліт, синдром Стівенса-Джонсона, набряк Квінке (ангіоневротичний набряк), виникнення або погіршення псоріазу (включаючи долонно-підошовний пустульозний псоріаз), мультиформна еритема, алопеція. З боку кістково-м'язової системи та сполучної тканини: вовчаковоподібний синдром. Інші, включаючи реакції у місці введення: підвищення температури тіла.Взаємодія з лікарськими засобамиУ хворих на ревматоїдний артрит, які отримують метотрексат, немає необхідності в корекції дози препарату Далібра або метотрексату. Разом з тим, метотрексат при одноразовому та повторному застосуванні знижує кліренс адалімумабу на 29% та 44% відповідно. Взаємодія адалімумабу з іншими препаратами, крім метотрексату, у фармакокінетичних дослідженнях не вивчалась. У клінічних дослідженнях не відзначено ознак взаємодії адалімумабу з іншими базовими засобами (сульфасалазин, гідрохлорохін, лефлуномід та парентеральні препарати золота), глюкокортикостероїдами, саліцилатами, нестероїдними протизапальними препаратами та аналгетиками. Комбіноване застосування з азатіоприном/6-меркаптопурином У клінічних дослідженнях за участю дорослих із хворобою Крона збільшення частоти злоякісних новоутворень та серйозних побічних реакцій, пов'язаних з інфекціями, спостерігалося у групі пацієнтів, у яких застосовувалося комбіноване застосування адалімумабу з азатіоприном/6-меркаптопурином, порівняно з монотерапією адалімума. Одночасне застосування з генно-інженерними біологічними протиревматичними препаратами, у тому числі антагоністами ФНП Тяжкі інфекції спостерігалися в клінічних дослідженнях при одночасному застосуванні анакінри та іншого антагоніста ФНП, етанерцепту, при цьому не спостерігалося покращення клінічного ефекту порівняно із застосуванням етанерцепту у вигляді монотерапії. Виходячи з природи побічних реакцій, що спостерігаються при одночасному застосуванні етанерцепту та анакінри, можна припустити виникнення аналогічних токсичних ефектів при одночасному застосуванні анакінрів з іншими антагоністами ФНП. Таким чином, одночасне застосування препарату Далібра з анакінрою протипоказане. Одночасне застосування препарату Далібра з іншими біологічними базовими протиревматичними препаратами (наприклад, анакінрою, абатацептом) або іншими блокаторами ФНП пов'язане з підвищеним ризиком виникнення інфекцій та інших побічних реакцій, і тому протипоказане.Спосіб застосування та дозиПідшкірно. Лікування препаратом Далібра проводиться під контролем лікаря. Якщо лікар вважає це за можливе, то після відповідного навчання техніці підшкірних ін'єкцій хворі можуть самостійно вводити собі препарат. Препарат Далібра вводять підшкірно в область стегна або живота. Розчин слід оглянути перед введенням щодо наявності сторонніх частинок та зміни кольору. Адалімумаб не слід змішувати в одному шприці або флаконі з іншими лікарськими засобами. Розчин, що залишився, і використані матеріали слід утилізувати. Якщо чергова ін'єкція Далібра® була випадково пропущена, необхідно провести ін'єкцію відразу, як тільки це буде виявлено. Наступна ін'єкція має бути проведена відповідно до запланованого раніше графіка. Дорослі Ревматоїдний артрит (РА), псоріатичний артрит (ПсА) та анкілозуючий спондиліт (АС), аксіальний спондилоартрит без рентгенологічно підтвердженого анкілозуючого спондиліту (аксСпА) Рекомендована доза препарату Далібра® у дорослих з ревматоїдним артритом (РА), псоріатичним артритом (ПсА), анкілозуючим спондилітом (АС) та аксіальним спондилоартритом без рентгенологічно підтвердженого анкілозуючого спондиліту (аксСпА) становить 4. При призначенні препарату Далібра® терапія глюкокортикостероїдами, нестероїдними протизапальними препаратами (в т.ч. саліцилатами), анальгетиками (наркотичними та ненаркотичними), метотрексатом та іншими базовими протиревматичними препаратами може бути продовжена. У деяких хворих на ревматоїдний артрит, які не отримують метотрексат, додатковий ефект може бути досягнутий при збільшенні кратності застосування препарату Далібра до 40 мг один раз на тиждень. Хвороба Крона Рекомендований режим дозування препарату Далібра® для дорослих із хворобою Крона - 160 мг на 1 день (застосовується по чотири ін'єкції по 40 мг на день або по дві ін'єкції по 40 мг на день послідовно протягом двох днів), через 2 тижні (на 15-й день) – 80 мг, ще через 2 тижні (29-й день) починають застосовувати підтримуючу дозу – 40 мг один раз на 2 тижні. При призначенні препарату Далібра® терапія аміносаліцилатами, глюкокортикостероїдами та/або імуномодуляторами (наприклад, 6-меркаптопурин та азатіоприн) може бути продовжена. Пацієнти, які спостерігають зменшення відповіді на лікування, можуть отримати додатковий ефект від збільшення частоти введення препарату Далібра до 40 мг один раз на тиждень. Деякі пацієнти можуть не відповідати на терапію препаратом Далібра протягом перших чотирьох тижнів, проте лікування слід продовжити, т.к. позитивний ефект можна досягти протягом 12 тижнів. Рішення про припинення терапії може бути прийняте у випадку, якщо пацієнт не отримує ефект від лікування протягом цього періоду. Язвений коліт Початкова (індукційна) доза для дорослих із середньотяжким та тяжким ступенем виразкового коліту становить 160 мг вихідно (доза може бути введена у вигляді чотирьох ін'єкцій на один день або у вигляді двох ін'єкцій на добу протягом двох днів поспіль) та 80 мг через 2 тижні. Після індукційної дози рекомендована підтримуюча доза становить 40 мг, яка вводиться у вигляді регулярних підшкірних ін'єкцій з інтервалом у 2 тижні. Під час лікування препаратом Далібра® терапія аміносаліцилатами, кортикостероїдами та/або імуномодуляторами (наприклад, 6-меркаптопурином та азатіоприном) може бути продовжена. На тлі підтримуючого лікування препаратом Далібра® доза кортикостероїдів може знижуватися аж до повної відміни відповідно до наявних клінічних посібників з лікування виразкового коліту. Пацієнти, у яких спостерігається зменшення відповіді на лікування, можуть отримати додатковий ефект від збільшення частоти введення препарату Далібра до одного разу на тиждень. Наявні дані свідчать, що клінічний ефект зазвичай досягається протягом 2-8 тижнів лікування. Лікування препаратом Далібра слід продовжувати лише у пацієнтів, у яких спостерігається терапевтичний ефект протягом перших 8 тижнів терапії. Хронічний бляшковий псоріаз Початкова доза для дорослих становить 80 мг. Підтримуюча доза - по 40 мг один раз на два тижні, починаючи через тиждень після початкової дози. Якщо через 16 тижнів терапії у пацієнта не спостерігається адекватна відповідь на терапію, то частота застосування препарату Далібра може бути збільшена (40 мг 1 раз на тиждень). Протягом цього періоду слід проводити оцінку користі застосування та ризику небажаних явищ. Якщо адекватна відповідь досягнута при частоті застосування препарату Далібра 1 раз на тиждень, далі можна повернутися до звичайної підтримуючої дози (40 мг 1 раз на 2 тижні). Активний гнійний гідраденіт Рекомендований режим дозування для препарату Далібра® у дорослих пацієнтів з гнійним гідраденітом (ГГ) включає початкову дозу 160 мг на 1 день (можливе введення чотирьох ін'єкцій по 40 мг протягом однієї доби або двох ін'єкцій по 40 мг на добу протягом двох днів поспіль) і потім на 15 день (через два тижні) – 80 мг (введення двох ін'єкцій по 40 мг протягом однієї доби). Через два тижні (29 день) продовжують введення дози 40 мг один раз на тиждень. При необхідності може бути продовжено прийом антибіотиків під час лікування препаратом Далібра. У всіх дослідженнях адалімумабу пацієнти застосовували щодня зовнішні антисептики. Під час лікування препаратом Далібра пацієнтам рекомендується щодня промивати місця уражень ГГ місцевим антисептичним засобом. Слід ретельно переглянути продовження терапії у період понад 12 тижнів у пацієнтів, які не досягають покращень протягом даного періоду часу. При необхідності тимчасового припинення лікування прийом препарату Далібра 40 мг один раз на тиждень може бути відновлений. Слід періодично виконувати оцінку співвідношення користі та ризику продовження тривалого лікування. Увеїт Рекомендований режим дозування для препарату Далібра у дорослих пацієнтів з увеїтом включає початкову дозу 80 мг, потім по 40 мг 1 раз на два тижні, починаючи через тиждень після застосування початкової дози. Існує обмежений досвід початку терапії препаратом Далібра у режимі монотерапії. Лікування препаратом Далібра® може бути розпочато у комбінації з кортикостероїдами та/або іншими небіологічними імуномодулюючими засобами. Доза кортикостероїдів може бути поступово знижена до повної відміни відповідно до усталеної клінічної практики, початок зниження дози кортикостероїдів – через 2 тижні після початку лікування препаратом Далібра®. Діти Ювенільний ідіопатичний артрит Застосування адалімумабу у дітей віком до 2 років з ювенільним ідіопатичним артритом не вивчалося. При ювенільному ідіопатичному артриті у дітей віком від 2 до 12 років препарат Далібра® призначають у дозі 24 мг/м2 площі поверхні тіла, при цьому максимальна одноразова доза становить для дітей від 2 до 4 років – 20 мг; для дітей від 4 до 12 років – 40 мг. Препарат вводять підшкірно 1 раз на 2 тижні. Об'єм ін'єкції визначають виходячи із зростання та ваги пацієнта (див. Таблицю 1). Для пацієнтів, яким необхідне введення менше 40 мг препарату, необхідно використовувати препарат Далібра у флаконі. Таблиця 1. Дози препарату Далібра® (у флаконах) у мілілітрах виходячи із росту та ваги пацієнтів дитячого віку, які страждають на ювенільний ідіопатичний артрит Зріст Загальна маса тіла (кг) (см) 10 15 20 25 30 35 40 45 50 55 60 65 70 80 0,2 мл 0,3 мл 0,3 мл 0,3 мл - - - - - - - - - - - - - - - - - - (10 мг) (15 мг) (15 мг) (15 мг) - - - - - - - - - - - - - - - - - - 90 0,2 мл 0,3 мл 0,3 мл 0,4 мл 0,4 мл 0,4 мл - - - - - - - - - - - - - - (10 мг) (15 мг) (15 мг) (20 мг) (20 мг) (20 мг) - - - - - - - - - - - - - - 100 0,3 мл 0,3 мл 0,3 мл 0,4 мл 0,4 мл 0,4 мл 0,5 мл 0,5 мл - - - - - - - - - - (15 мг) (15 мг) (15 мг) (20 мг) (20 мг) (20 мг) (25 мг) (25 мг) - - - - - - - - - - 110 0,3 мл 0,3 мл 0,4 мл 0,4 мл 0,4 мл 0,5 мл 0,5 мл 0,5 мл 0,5 мл 0,6 мл 0,6 мл - - - - (15 мг) (15 мг) (20 мг) (20 мг) (20 мг) (25 мг) (25 мг) (25 мг) (25 мг) (30 мг) (30 мг) - - - - 120 0,3 мл 0,4 мл 0,4 мл 0,4 мл 0,5 мл 0,5 мл 0,5 мл 0,6 мл 0,6 мл 0,6 мл 0,6 мл 0,7 мл 0,7 мл (15 мг) (20 мг) (20 мг) (20 мг) (25 мг) (25 мг) (25 мг) (30 мг) (30 мг) (30 мг) (30 мг) (35 мг) (35 мг) 130 0,4 мл 0,4 мл 0,5 мл 0,5 мл 0,5 мл 0,6 мл 0,6 мл 0,6 мл 0,6 мл 0,7 мл 0,7 мл 0,7 мл (20 мг) (20 мг) (25 мг) (25 мг) (25 мг) (30 мг) (30 мг) (30 мг) (30 мг) (35 мг) (35 мг) (35 мг) 140 0,4 мл 0,4 мл 0,5 мл 0,5 мл 0,6 мл 0,6 мл 0,6 мл 0,7 мл 0,7 мл 0,7 мл 0,7 мл 0,8* мл (20 мг) (20 мг) (25 мг) (25 мг) (30 мг) (30 мг) (30 мг) (35 мг) (35 мг) (35 мг) (35 мг) (40 мг) 150 0,5 мл 0,5 мл 0,6 мл 0,6 мл 0,6 мл 0,7 мл 0,7 мл 0,7 мл 0,7 мл 0,8* мл 0,8* мл (25 мг) (25 мг) (30 мг) (30 мг) (30 мг) (35 мг) (35 мг) (35 мг) (35 мг) (40 мг) (40 мг) 160 0,5 мл 0,5 мл 0,6 мл 0,6 мл 0,7 мл 0,7 мл 0,7 мл 0,8* мл 0,8* мл 0,8* мл 0,8* мл (25 мг) (25 мг) (30 мг) (30 мг) (35 мг) (35 мг) (35 мг) (40 мг) (40 мг) (40 мг) (40 мг) 170 0,6 мл 0,6 мл 0,6 мл 0,7 мл 0,7 мл 0,8* мл 0,8* мл 0,8* мл 0,8* мл 0,8* мл (30 мг) (30 мг) (30 мг) (35 мг) (35 мг) (40 мг) (40 мг) (40 мг) (40 мг) (40 мг) 180 0,6 мл 0,7 мл 0,7 мл 0,8* мл 0,8* мл 0,8* мл 0,8* мл 0,8* мл 0,8* мл (30 мг) (35 мг) (35 мг) (40 мг) (40 мг) (40 мг) (40 мг) (40 мг) (40 мг) * - максимальна доза при одноразовому введенні становить 40 мг. Пацієнти, яким необхідна доза 40 мг, можуть використовувати препарат Далібра в шприцах або автоінжекторах. Підліткам від 13 років призначають по 40 мг один раз на 2 тижні незалежно від площі поверхні тіла. Клінічна відповідь зазвичай досягається протягом 12 тижнів лікування. Рішення про припинення терапії може бути прийнято у випадку, якщо пацієнт не отримує ефекту від лікування протягом цього періоду. Ентезит-асоційований артрит. Доза препарату Далібра® для пацієнтів з ентезит-асоційованим артритом, віком від 6 років і старше становить 24 мг/м2 площі поверхні тіла до максимальної одноразової дози 40 мг препарату Далібра® при підшкірному введенні один раз на два тижні. Вибір обсягу ін'єкції залежить від зростання та маси тіла пацієнтів. При використанні препарату Далібра у формі випуску "флакони" див. Таблицю 1 вище - режим дозування аналогічний режиму дозування при лікуванні ювенільного ідіопатичного артриту. Застосування адалімумабу у пацієнтів з ентезит-асоційованим артритом у віці до 6 років не вивчалося. Хвороба Крона Пацієнти з масою тіла менше 40 кг: 80 мг на 1-й день (застосовується по дві ін'єкції по 40 мг на день), через 2 тижні (на 15-й день) - 40 мг, ще через 2 тижні (29-й день) починають застосовувати підтримуючу дозу за наступною схемою - 20 мг один раз на 2 тижні (середньоважкий і важкий ступінь). Пацієнти з масою тіла 40 кг і більше: 160 мг на 1-й день (застосовується по чотири ін'єкції по 40 мг на день або по дві ін'єкції по 40 мг на день послідовно протягом двох днів), через 2 тижні (на 15-й день) - 80 мг, ще через 2 тижні (29-й день) починають застосовувати підтримуючу дозу за наступною схемою: хвороба Крона важкого ступеня – 40 мг один раз на 2 тижні; хвороба Крона середньотяжкого ступеня – 20 мг один раз на 2 тижні. Пацієнти, у яких спостерігається зменшення відповіді на лікування, можуть отримати додатковий ефект від збільшення частоти введення препарату Далібра до одного разу на тиждень. Клінічна відповідь зазвичай досягається протягом 12 тижнів лікування. Рішення про припинення терапії може бути прийняте у випадку, якщо пацієнт не отримує ефект від лікування протягом цього періоду. Застосування адалімумабу у дітей віком до 6 років із хворобою Крона не вивчалося. Хронічний бляшковий псоріаз Рекомендована доза препарату Далібра становить 0,8 мг/кг маси тіла (до 40 мг/доза) підшкірно 1 раз на тиждень (початок терапії – перші два введення препарату) і далі 1 раз на 2 тижні. Якщо пацієнт не відповідає на терапію протягом 16 тижнів терапії, необхідно ретельно розглянути питання необхідності продовження лікування. При повторній терапії хронічного бляшкового псоріазу у дітей препаратом Далібра необхідно слідувати такому ж режиму дозування. Немає даних про застосування адалімумабу у дітей віком до 4 років за цим показанням. Об'єм для ін'єкції вибирається, виходячи з маси тіла пацієнта. Для пацієнтів, яким необхідне введення менше 40 мг препарату, необхідно використовувати препарат Далібра у флаконі. Інструкцію з підготовки та проведення ін'єкції препарату Далібра® дивіться в інформаційному листку, вкладеному в картонну пачку.ПередозуванняМаксимальна доза адалімумабу, що переноситься, у людини не встановлена. Повторне застосування адалімумабу у дозах до 10 мг/кг не супроводжувалося токсичними ефектами, що вимагали зменшення дози. У разі передозування необхідно контролювати побічні реакції та негайно розпочинати адекватну симптоматичну терапію.Запобіжні заходи та особливі вказівкиЩоб покращити відстеження застосування біологічних лікарських препаратів, рекомендується записувати назву та серію препарату в медичній карті пацієнта. Інфекції Застосування препарату Далібра не слід починати у пацієнтів з активними інфекційними захворюваннями, що включають хронічні або осередкові інфекції, до усунення інфекції. У пацієнтів, у яких був контакт з туберкульозом, а також пацієнтів, які відвідували місця з високим рівнем захворюваності на туберкульоз або такими ендемічними мікозами, як гістоплазмоз, кокцидіоїдомікоз або бластомікоз, ризик та користь лікування адалімумабом повинні оцінюватися до початку терапії (див. . Як і у випадку з іншими антагоністами ФНП, пацієнти повинні бути ретельно обстежені з приводу інфекційних захворювань до, під час та після лікування адалімумабом. Пацієнти, у яких розвинулося інфекційне захворювання під час лікування адалімумабом, мають бути виявлені та повністю обстежені. Застосування адалімумабу повинно бути припинене, якщо у пацієнта розвивається серйозне інфекційне ускладнення або сепсис, при цьому відповідна антибактеріальна та протигрибкова терапія повинна проводитися до лікування інфекційного захворювання. З обережністю слід призначати адалімумаб пацієнтам з рецидивуючими інфекціями в анамнезі та за наявності умов, що призводять до інфекційних ускладнень. Туберкульоз Ризик розвитку активного туберкульозу або активації латентного туберкульозу при використанні всіх блокаторів ФНП, у тому числі адалімумабу. Частота реактивації туберкульозу була особливо вищою при дозах адалімумабу, що перевищували рекомендовані значення. До початку терапії адалімумабом усі пацієнти повинні бути обстежені на предмет активної, так і неактивної (латентної) туберкульозної інфекції. Ця оцінка повинна включати докладний анамнез захворювання, з урахуванням можливих контактів з хворими на активні форми туберкульозу та попередньої або поточної імуносупресивної терапії, а також необхідні скринінгові обстеження (в т.ч. рентгенографія органів грудної клітки, туберкуліновий тест). Лікування латентної туберкульозної інфекції має бути проведене до початку лікування препаратом Далібра®. Якщо діаметр папули після шкірної туберкулінової проби на приховану туберкульозну інфекцію більше 5 мм, то ця проба вважається позитивною, навіть якщо раніше проводилася вакцинація бацилою Calmette-Guerin (BCG або БЦЖ). Можливість наявності латентної туберкульозної інфекції повинна братися до уваги особливо у тих пацієнтів, які іммігрували з країни з високою захворюваністю на туберкульоз або подорожували в таку країну, або у тих, хто був у контакті з хворим на активну форму туберкульозу. Якщо діагностовано активний туберкульоз, не можна розпочинати терапію адалімумабом. Якщо діагностовано латентний туберкульоз, слід проводити превентивну терапію до початку лікування адалімумабом згідно з локальними рекомендаціями. Превентивна протитуберкульозна терапія до початку лікування адалімумабом також повинна призначатися тим пацієнтам, які схильні до факторів ризику туберкульозу, навіть при негативній туберкуліновій пробі. Рішення про проведення протитуберкульозної терапії у таких пацієнтів має прийматися лише з урахуванням ризику латентної туберкульозної інфекції та ризику, пов'язаного з проведенням протитуберкульозної терапії. Лікування призначається фтизіатром. Протитуберкульозне лікування пацієнтів з латентною туберкульозною інфекцією знижує ризик реактивації туберкульозу при лікуванні цих пацієнтів адалімумабом.Однак ризик розвитку активного туберкульозу або активації латентного туберкульозу існує навіть у пацієнтів, які пройшли скринінг та/або протитуберкульозну терапію, тому необхідно ретельне спостереження за пацієнтом у процесі терапії з метою своєчасного виявлення симптомів активного туберкульозу, особливо з огляду на те, що тести на латентну туберкульоз бувають хибно-негативними. Ризик помилково-негативних результатів внутрішньошкірних туберкулінових проб повинен братися до уваги особливо у хворих у тяжкому стані або імунокомпрометованих.що тести на латентну туберкульозну інфекцію часто бувають помилково-негативними. Ризик помилково-негативних результатів внутрішньошкірних туберкулінових проб повинен братися до уваги особливо у хворих у тяжкому стані або імунокомпрометованих.що тести на латентну туберкульозну інфекцію часто бувають помилково-негативними. Ризик помилково-негативних результатів внутрішньошкірних туберкулінових проб повинен братися до уваги особливо у хворих у тяжкому стані або імунокомпрометованих. Пацієнтів слід поінформувати про необхідність звернення до лікаря з появою симптомів (персистирующий кашель, втрата маси тіла, субфебрильна лихоманка), що вказують на розвиток туберкульозної інфекції. Інші опортуністичні інфекції У пацієнтів, які отримували адалімумаб, спостерігалися опортуністичні інфекції, включаючи грибкові інфекції. Ці інфекції вимагають своєчасної діагностики та адекватного лікування. Пацієнти, у яких виникає лихоманка, нездужання, втрата маси тіла, рясне потовиділення, кашель, задишка та/або інфільтрати в легенях на рентгенограмі, або інші виражені системні порушення з розвитком шокового стану, або без нього, повинні негайно звернутися до лікаря для проведення діагностичних заходів. У пацієнтів, які перебували в зонах, ендемічних за різними мікозами, слід передбачати розвиток грибкових інфекцій. Такі пацієнти перебувають у групі ризику розвитку гістоплазмозу або іншої грибкової інфекції, і лікарі, отже, повинні проводити емпіричну протигрибкову терапію до визначення патогену (-ів). Аналізи антиген-антитіло на гістоплазмоз можуть бути негативними у деяких пацієнтів з активною інфекцією. По можливості, рішення про призначення емпіричної протигрибкової терапії у таких пацієнтів має прийматися після консультації лікарем з кваліфікацією у діагностиці та лікуванні грибкових інфекцій, при цьому слід брати до уваги як ризик важкої грибкової інфекції, так і ризики, пов'язані з протигрибковою терапією. Пацієнтам, у яких розвинулася тяжка грибкова інфекція, рекомендується припинити прийом блокаторів ФНП до моменту лікування інфекції. Реактивація гепатиту В Застосування блокаторів ФНП пов'язане з ризиком реактивації вірусу гепатиту В (ВГВ) у пацієнтів, які є хронічними носіями цього вірусу. У деяких випадках реактивація ВГВ, що виникає у зв'язку з прийомом блокаторів ФНП, призводила до смерті. Більшість цих випадків виникала у пацієнтів, які приймають інші лікарські засоби, які пригнічували імунну систему, що також могло зробити свій внесок у реактивацію ВГВ. У пацієнтів із ризиком ВГВ інфекції має проводитися діагностика первинних симптомів ВГВ інфекції до початку терапії блокаторами ФНП. Слід з обережністю призначати блокатори ФНП тим пацієнтам, які є носіями ВГВ. Ті пацієнти, які є носіями ВГВ та потребують лікування блокаторами ФНП, повинні бути ретельно обстежені для виявлення ознак активної ВГВ інфекції під час терапії та через кілька місяців після закінчення терапії. Відсутні достовірні дані щодо безпеки або ефективності лікування носіїв ВГВ противірусними препаратами спільно з блокаторами ФНП для запобігання реактивації ВГВ. У пацієнтів, у яких розвивається реактивація ВГВ, застосування адалімумабу слід призупинити, і має бути розпочато ефективну противірусну терапію з відповідним підтримуючим лікуванням. Неврологічні ускладнення Застосування антагоністів ФНП, включаючи адалімумаб, пов'язане з рідкісними випадками виникнення або ускладнення клінічних проявів та/або рентгенологічних ознак демієлінізуючих захворювань ЦНС, включаючи розсіяний склероз та периферичні демієлінізуючі захворювання, включаючи синдром Гійєна-Барре. Слід з обережністю призначати адалімумаб пацієнтам з демієлінізуючими захворюваннями центральної та периферичної нервової системи поточними або в анамнезі. У разі розвитку описаних вище явищ слід розглянути можливість відміни препарату Далібра. Злоякісні новоутворення Існує більш високий ризик розвитку лімфоми у пацієнтів з ревматоїдним артритом, що характеризується тривалим тяжким запаленням, що ускладнює оцінку ступеня ризику. Під час тривалих відкритих випробувань адалімумаба середній рівень злоякісних утворень був подібний до того, який очікувався для загальної популяції даного віку, статі та раси. На підставі наявних даних не можна виключити можливий ризик розвитку лімфом або інших злоякісних новоутворень під час застосування блокаторів ФНП. Повідомлялося про злоякісні новоутворення, частина яких призводить до смерті, у дітей і дорослих, які отримували лікування блокаторами ФНП. Приблизно в половині випадків розвивалися лімфоми, як ходжкінські, так і неходжикнські. В інших випадках були представлені різні злоякісні новоутворення, включаючи рідкісні злоякісні новоутворення, пов'язані з імуносурпресією. Злоякісні новоутворення виникали загалом через 30 місяців терапії. Більшість пацієнтів отримували супутнє лікування імуносупресантами. Є рідкісні постмаркетингові повідомлення про гепатоспленарну Т-клітинну лімфому (ГСТКЛ), рідкісну агресивну лімфому, яка виникала у пацієнтів, які лікувалися адалімумабом, і нерідко призводила до летального результату. Більшість пацієнтів спочатку отримували терапію інфліксімабом, а також супутню терапію запальних захворювань товстого кишечника азатіоприном або 6-меркаптопурином. Причинно-наслідковий зв'язок ГСТКЛ із прийомом адалімумабу не доведено. Не проводилося досліджень, що включають пацієнтів з анамнезом злоякісних новоутворень, або в ході яких лікування адалімумабом тривало у пацієнтів з злоякісним новоутворенням, що розвинулося. Таким чином, слід виявляти додаткову обережність при застосуванні адалімумабу у таких пацієнтів. Всі пацієнти, і особливо ті, що раніше отримували тривалу терапію імуносуперсантами або ПУВА-терапію псоріазу, повинні обстежуватися на наявність не пов'язаного з меланомою раку шкіри, який розвинувся до або під час лікування адалімумабом. Випадки гострого або хронічного лейкозу описувалися у зв'язку з постмаркетинговим використанням блокаторів ФНП для лікування ревматоїдного артриту та інших показань. У пацієнтів з ревматоїдним артритом вищий ризик лейкемії (до дворазового), ніж у загальній популяції, навіть без терапії блокаторами ФНП. Алергія Серйозні алергічні реакції, пов'язані з прийомом адалімумабу, були рідкими під час клінічних випробувань. У постмаркетингових спостереженнях серйозні алергічні реакції, що включають анафілактичний шок, після прийому адалімумабу описувалися дуже рідко. Якщо виникає анафілактична реакція або інші серйозні алергічні реакції, слід негайно припинити введення адалімумабу та призначити відповідну протиалергічну терапію. Гематологічні ускладнення Були рідкісні повідомлення про розвиток панцітоієнія, включаючи апластичну анемію, при застосуванні блокаторів ФНП. Зрідка повідомлялося про побічні ефекти з боку системи крові, що включають значну цитопенію (у тому числі тромбоцитопенію, лейкопенію) під час лікування адалімумабом. Причинний зв'язок цих повідомлень із прийомом адалімумабу залишається незрозумілим. Всім пацієнтам слід рекомендувати негайно звертатися до лікаря, якщо у них розвиваються симптоми, що вказують на порушення з боку системи крові (у тому числі лихоманка, що персистує, гематоми, кровотечі, блідість) при лікуванні адалімумабом. При підтверджених значних гематологічних порушеннях лікування адалімумабом слід призупинити. Вакцинація Пацієнтам з ювенільним артритом рекомендується, але можливості пройти повну вакцинацію відповідно до поточного графіку імунізації до початку терапії препаратом Далібра®. Пацієнти, які приймають препарат Далібра, можуть бути вакциновані необхідними вакцинами, за винятком живих вакцин. Хронічна серцева недостатність (ХСП) Не проводилося досліджень застосування адалімумабу у пацієнтів із застійною серцевою недостатністю (ХСН), проте при клінічних випробуваннях іншого антагоніста ФНП спостерігався більш високий рівень пов'язаних із ХСН небажаних явищ, включаючи розвиток ХСН та прогресування ХСН. Випадки прогресування ХСН також описувалися у пацієнтів, які беруть адалімумаб. Слід з обережністю призначати адалімумаб пацієнтам із серцевою недостатністю та проводити ретельне спостереження за такими пацієнтами. Аутоімунні процеси Лікування адалімумабом може призводити до формування аутоантитіл. Вплив тривалого лікування в розвитку аутоімунних захворювань не вивчено. Якщо у пацієнта розвиваються симптоми, що передбачають вовчаковоподібний синдром внаслідок лікування адалімумабом, слід припинити використання препарату. Літні пацієнти Частота виникнення серйозних інфекцій серед пацієнтів старше 65 років, які приймали адалімумаб, була вищою, ніж у пацієнтів молодших 65 років. 9,5% від загальної кількості пацієнтів було старше 65 років і приблизно 2,0% було старше 75. Адалімумаб слід призначати з обережністю у літніх людей у зв'язку з високою ймовірністю виникнення інфекційних захворювань. Відмінності в ефективності цієї групи пацієнтів порівняно з молодшими пацієнтами не виявлено, коригування дози не потрібно. Діти Ефективність та безпека застосування адалімумабу у дітей показана тільки для лікування ідіопатичного ювенільного артриту у пацієнтів від 2 років та хвороби Крона (середньотяжкого та тяжкого ступеня) у пацієнтів від 6 років та старших. Можливість зберігання препарату Далібра® у шприцах за кімнатної температури При необхідності (наприклад, під час подорожі) адалімумаб допускається зберігати за кімнатної температури (до 25°С) у захищеному від світла місці не більше 14 днів. З моменту вилучення з холодильника шприц повинен бути використаний протягом 14 днів, якщо шприц після вилучення з холодильника не буде використаний протягом цього терміну, він повинен бути знищений. Для зручності рекомендується записати дату вилучення шприца з холодильника та термін, протягом якого слід використовувати препарат. Вплив на здатність до керування автотранспортом та управління механізмами Препарат Далібра може незначно впливати на здатність керувати транспортними засобами та іншими механізмами, оскільки на фоні застосування препарату можуть спостерігатися запаморочення та порушення зору.Умови зберіганняУ холодильнику +2+8 градусівУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаамлодипін + периндоприл таблетки на 1 таблетку 5 мг + 4 мг/10 мг + 4 мг/5 мг + 8 мг/10 мг + 8 мг речовини, що діють: Амлодипін безілат (амлодипін безілат) 6,935 мг/13,870 мг/6,935 мг/13,870 мг, еквівалентно амлодипіну 5 мг/10 мг/5 мг/10 мг Периндоприлу ербумін А субстанція – гранули 21,000 мг/21,000 мг/42,000 мг/42,000 мг, містить периндоприлу ербуміну 4 мг/4 мг/8 мг/8 мг Допоміжні речовини: Целюлоза мікрокристалічна, крохмаль прежелатинізований, карбоксиметилкрохмаль натрію, гідрокарбонат натрію, кремнію діоксид колоїдний, магнію стеаратОпис лікарської формиТаблетки 5 мг + 4 мг: Круглі, злегка двоопуклі таблетки з фаскою, від білого до майже білого кольору. Таблетки 10 мг + 4 мг: Капсулоподібні, двоопуклі таблетки з ризиком на одній стороні, від білого до майже білого кольору. Таблетки 5 мг + 8 мг: Круглі, двоопуклі таблетки з фаскою, від білого до майже білого кольору. Таблетки 10 мг + 8 мг: Круглі, двоопуклі таблетки з фаскою, з ризиком на одній стороні, від білого майже білого кольору.Фармакотерапевтична групагіпотензивний комбінований засіб (інгібітор ангіотензинперетворюючого ферменту [АПФ] + блокатор «повільних» кальцієвих каналів [БМКК])ФармакокінетикаВеличина абсорбції амлодипіну та периндоприлу при застосуванні комбінованого лікарського препарату Дальнева® суттєво не відрізняється від такої при застосуванні їх як монопрепарати. Амлодипін Після прийому внутрішньо амлодипін повільно абсорбується із шлунково-кишкового тракту (ЖКТ). Прийом їжі не впливає на біодоступність амлодипіну. Максимальна концентрація (Сmax) амлодипіну в плазмі досягається через 6-12 годин після прийому препарату внутрішньо. Абсолютна біодоступність становить 64-80%. Об'єм розподілу – приблизно 21 л/кг. У дослідженнях in vitro було показано, що близько 97,5% циркулюючого амлодипіну пов'язано з білками плазми. Кінцевий період напіввиведення (Т½) із плазми становить 35-50 годин, що дозволяє приймати препарат 1 раз на добу. Амлодипін метаболізується у печінці з утворенням неактивних метаболітів, при цьому 10% прийнятої дози амлодипіну виводиться у незміненому вигляді та 60% нирками – у вигляді метаболітів. Амлодипін не виводиться з організму за допомогою діалізу. Час досягнення Сmax(ТСmax) амлодипіну в плазмі крові не відрізняється у пацієнтів похилого віку та молодшого віку. У пацієнтів похилого віку відзначається уповільнення кліренсу амлодипіну, що призводить до збільшення площі під кривою «концентрація-час» (AUC). Збільшення AUC та Т½ у пацієнтів з ХСН відповідає передбачуваній величині для цієї вікової групи. У пацієнтів з порушенням функції нирок зміни концентрації амлодипіну в плазмі не корелюють зі ступенем ниркової недостатності. Можливе незначне подовження Т½. Дані щодо застосування амлодипіну пацієнтами з печінковою недостатністю обмежені. У пацієнтів з печінковою недостатністю спостерігається зниження кліренсу амлодипіну, що призводить до подовження Т½ та збільшення AUC приблизно на 40-60%. Периндоприл Після прийому периндоприл швидко всмоктується і досягає Сmaxв плазмі протягом 1 години. Т½ периндоприлу з плазми становить приблизно 1 годину. Периндоприл не має фармакологічної активності, є проліками. Приблизно 27% від загальної кількості, прийнятої внутрішньо периндоприлу, потрапляє в кровообіг у вигляді активного метаболіту – периндоприлату. Крім периндоприлату утворюються ще 5 метаболітів, які не мають фармакологічної активності. Сmax у плазмі крові досягається через 3-4 години після прийому внутрішньо. Прийом їжі зменшує біодоступність периндоприлу, тому препарат слід приймати 1 раз на добу, вранці, перед їдою. Існує лінійна залежність концентрації периндоприлу в плазмі від величини прийнятої всередину дози. Об'єм розподілу вільного периндоприлату становить приблизно 0,2 л/кг. Зв'язок периндоприлату з білками плазми (переважно з АПФ) становить 20% і залежить від його концентрації. Периндоприлат виводиться нирками, Т½ незв'язаної фракції становить приблизно 17 годин, тому рівноважний стан досягається протягом 4-х діб після прийому внутрішньо. Виведення периндоприлату сповільнене у пацієнтів похилого віку, а також у пацієнтів із серцевою та нирковою недостатністю (див. розділ «Спосіб застосування та дози»), тому спостереження за такими пацієнтами повинно включати регулярний контроль концентрації креатиніну та вмісту калію в плазмі крові. Діалізний кліренс периндоприлату становить 70 мл/хв. Фармакокінетика периндоприлу порушена у пацієнтів із цирозом печінки: його печінковий кліренс зменшується у 2 рази. Тим не менш, кількість периндоприлату, що утворюється, не зменшується, тому не потрібно корекції дози (див. розділи «Спосіб застосування та дози» та «Особливі вказівки»).ФармакодинамікаАмлодипін Амлодипін – БМКК, похідне дигідропіридину. Амлодипін пригнічує трансмембранний перехід іонів кальцію в кардіоміоцити та гладком'язові клітини судинної стінки. Антигіпертензивна дія амлодипіну обумовлена прямим розслаблюючим впливом на гладком'язові клітини судинної стінки. Детальний механізм, за допомогою якого амлодипін здійснює антиангінальну дію, не цілком встановлений, але відомо, що амлодипін зменшує загальне ішемічне навантаження за допомогою двох дій: викликає розширення периферичних артеріол, зменшуючи загальний периферичний судинний опір (ОПСС) (постнавантаження). Оскільки частота серцевих скорочень (ЧСС) у своїй не змінюється, потреба міокарда в кисні знижується; викликає розширення коронарних артерій та артеріол як у ішемізованій, так і в інтактній зонах. Їх дилатація збільшує надходження кисню до міокарда у пацієнтів з вазоспастичною стенокардією (стенокардія Принцметала або варіантна стенокардія). У пацієнтів з артеріальною гіпертензією (АГ) прийом амлодипіну 1 раз на добу забезпечує клінічно значуще зниження артеріального тиску (АТ) у положенні стоячи і лежачи протягом 24 годин. Антигіпертензивна дія розвивається повільно, у зв'язку з чим розвиток гострої гіпотензії нехарактерний. У пацієнтів зі стенокардією прийом амлодипіну 1 раз на добу збільшує загальний час фізичного навантаження, збільшує час до розвитку нападу стенокардії та до появи депресії сегмента ST на 1 мм, а також знижує частоту нападів стенокардії та споживання нітрогліцерину під язик. Амлодипін не чинить несприятливих метаболічних ефектів і не впливає на концентрацію ліпідів плазми. Препарат може застосовуватися у пацієнтів із супутньою бронхіальною астмою, цукровим діабетом та подагрою. Ішемічна хвороба серця (ІХС) Результати оцінки ефективності свідчать про те, що прийом амлодипіну характеризується меншою кількістю випадків госпіталізації щодо стенокардії та проведення процедур реваскуляризації у пацієнтів з ІХС. Периндоприл Периндоприл – інгібітор ферменту, що перетворює ангіотензин I на ангіотензин II. АПФ, або кініназа II, є екзопептидазою, яка здійснює як перетворення ангіотензину I на судинозвужувальну речовину ангіотензин II, так і розпад брадикініну, що має судинорозширювальну дію, до неактивного гептапептиду. Оскільки АПФ інактивує брадикінін, пригнічення АПФ супроводжується підвищенням активності як циркулюючої, так і тканинної калікреїн-кінінової системи, при цьому також активується система простагландинів. Периндоприл має терапевтичну дію завдяки активному метаболіту, периндоприлату. Інші метаболіти не мають інгібуючої дії на АПФ в умовах in vitro. Артеріальна гіпертензія Периндоприл є препаратом для лікування артеріальної гіпертензії будь-якого ступеня тяжкості. На тлі його застосування відзначається зниження як систолічного, так і діастолічного АТ у положенні «лежачи» та «стоячи». Периндоприл зменшує ОПСС, що призводить до зниження артеріального тиску та поліпшення периферичного кровотоку без зміни ЧСС. Як правило, прийом периндоприлу збільшує нирковий кровообіг, швидкість клубочкової фільтрації (СКФ) при цьому не змінюється. Антигіпертензивна дія препарату досягає максимуму через 4-6 годин після одноразового прийому внутрішньо та зберігається протягом 24 годин. Антигіпертензивна дія через 24 години після одноразового застосування внутрішньо становить близько 87-100% від максимального антигіпертензивного ефекту. Зниження АТ досягається досить швидко. Терапевтичний ефект настає через 1 місяць від початку терапії і не супроводжується тахіфілаксією. Припинення лікування не викликає ефекту "рикошету". Периндоприл має судинорозширювальну дію, сприяє відновленню еластичності великих артерій та структури судинної стінки дрібних артерій, а також зменшує гіпертрофію лівого шлуночка. Стабільна ІХС Ефективність застосування периндоприлу у пацієнтів (12218 пацієнтів віком від 18 років) зі стабільною ІХС без клінічних симптомів хронічної серцевої недостатності (ХСН) вивчалась у ході 4-річного дослідження. 90% учасників дослідження раніше перенесли гострий інфаркт міокарда та/або процедуру реваскуляризації. Більшість пацієнтів отримували крім досліджуваного препарату стандартну терапію, включаючи антиагреганти, гіполіпідемічні засоби та бета-адреноблокатори. Як основний критерій ефективності була обрана комбінована кінцева точка, що включає серцево-судинну смертність, нефатальний інфаркт міокарда та/або зупинку серця з успішною реанімацією. Терапія периндоприлом третбутиламіном у дозі 8 мг/добу 1 раз на день (еквівалентно 10 мг периндоприлу аргініну) призводила до суттєвого зниження абсолютного ризику щодо комбінованої кінцевої точки на 1,9 % у пацієнтів, які раніше перенесли інфаркт міокарда та/або процедуру реваскуляру. абсолютного ризику становило 2,2% порівняно з групою плацебо. Подвійна блокада ренін-ангіотензин-альдостеронової системи (РААС) Є дані клінічних досліджень комбінованої терапії із застосуванням інгібітору АПФ та антагоніста рецептора ангіотензину II (АРА II). Протипоказано застосування інгібіторів АПФ у поєднанні з АРА II у пацієнтів з діабетичною нефропатією. Є дані клінічного дослідження з вивчення позитивного впливу від додавання аліскірену до стандартної терапії інгібітором АПФ або АРА II у пацієнтів з цукровим діабетом 2 типу та/або хронічним захворюванням нирок, або кардіоваскулярним захворюванням, які мають поєднання цих захворювань. Дослідження було припинено достроково у зв'язку з зростанням ризику виникнення несприятливих результатів. Кардіоваскулярна смерть та інсульт відзначалися частіше у групі пацієнтів, які отримують аліскірен, порівняно з групою плацебо; також небажані явища та серйозні небажані явища особливого інтересу (гіперкаліємія, артеріальна гіпотензія та порушення функції нирок) реєструвалися частіше у групі аліскірену, ніж у групі плацебо. Амлодипін + периндоприл Ефективність при тривалому застосуванні амлодипіну в комбінації з периндоприлом і атенололу в комбінації з бендрофлуметіазидом у пацієнтів віком від 40 до 79 років з АГ та, щонайменше, з трьома з перелічених додаткових факторів ризику: гіпертрофія лівого шлуночка діабет 2 типу, атеросклероз периферичних артерій, раніше перенесений інсульт або транзиторна ішемічна атака, чоловіча стать, вік 55 років і старше, мікроальбумінурія або протеїнурія, куріння, загальний холестерин/холестерин ліпопротеїдів високої щільності ≥ 6, ранній розвиток ASCOT-BPLA. Основний критерій оцінки ефективності – комбінований показник частоти нефатального інфаркту міокарда (у тому числі безболевого) та летальних наслідків ІХС. Частота ускладнень, передбачених основним критерієм оцінки, у групі амлодипін/периндоприл була на 10% нижчою, ніж у групі атенолол/бендрофлуметіазид, проте ця відмінність не була статистично достовірною. У групі амлодипін/периндоприл відзначалося достовірне зниження частоти ускладнень, передбачених додатковими критеріями ефективності (крім фатальної та нефатальної серцевої недостатності).Показання до застосуванняАртеріальна гіпертензія та/або ішемічна хвороба серця: стабільна стенокардія напруги у пацієнтів, яким потрібна терапія периндоприлом та амлодипіном.Протипоказання до застосуванняПідвищена чутливість до периндоприлу або інших інгібіторів АПФ, амлодипіну та інших похідних дигідропіридину, а також допоміжних речовин, що входять до складу препарату. Ангіоневротичний набряк (набряк Квінке) в анамнезі (у тому числі на фоні прийому інших інгібіторів АПФ). Спадковий/ідіопатичний ангіоневротичний набряк. Одночасне застосування з аліскіреном та лікарськими препаратами, що містять аліскірен, у пацієнтів з цукровим діабетом та/або помірними або тяжкими порушеннями функції нирок (ШКФ < 60 мл/хв/1,73 м2 площі поверхні тіла) (див. розділи «Взаємодія з іншими лікарськими засобами) засобами" і "Фармакологічні властивості. Фармакодинаміка"). Одночасне застосування з АРА II у пацієнтів з діабетичною нефропатією (див. розділ «Особливі вказівки»). Одночасне застосування з інгібіторами нейтральної ендопептидази (наприклад, з препаратами, що містять сакубітрил) через високий ризик розвитку ангіоневротичного набряку. Екстракорпоральна терапія, що веде до контакту крові з негативно зарядженими поверхнями (див. розділ "Взаємодія з іншими лікарськими засобами"). Виражений двосторонній стеноз ниркових артерій або стеноз артерії єдиної нирки, що функціонує (див. розділ «Особливі вказівки»). Тяжка артеріальна гіпотензія (систолічний артеріальний тиск менше 90 мм рт. ст.). Шок (включно з кардіогенним). Обструкція вихідного тракту лівого шлуночка (наприклад, клінічно суттєвий стеноз аорти). Гемодинамічно нестабільна серцева недостатність після гострого інфаркту міокарда. Ниркова недостатність (кліренс креатиніну менше 60 мл/хв). Вагітність та період грудного вигодовування. Вік до 18 років (ефективність та безпека не встановлені). Стеноз ниркової артерії (у тому числі двосторонній), єдина функціонуюча нирка, печінкова недостатність, ниркова недостатність, системні захворювання сполучної тканини (у тому числі системний червоний вовчак, склеродермія), терапія імунодепресантами, алопуринолом, прокаїнамоз об'єм циркулюючої крові (ОЦК) (прийом діуретиків, безсольова дієта, блювання, діарея), атеросклероз, цереброваскулярні захворювання, ІХС з тяжким обструктивним ураженням коронарних артерій, гострий інфаркт міокарда (і період протягом 1 місяця після нього), нестабільна синусового вузла (виражена тахікардія, брадикардія), реноваскулярна гіпертензія, цукровий діабет, первинний гіперальдостеронізм, ХСН, одночасне застосування інгібіторів або індукторів ізоферменту CYP3A4,дантролену, естрамустину, калійзберігаючих діуретиків, препаратів калію, калійвмісних замінників харчової солі, препаратів літію, кларитроміцину, такролімусу, циклоспорину, гіперкаліємії, хірургічного втручання/загальна анестезія, пацієнтів похилого віку. гемодіалізу з використанням високопроточних мембран (наприклад, AN69®), десенсибілізуюча терапія, аферез ліпопротеїнів низької щільності (ЛПНЩ), аортальний стеноз/мітральний стеноз/гіпертрофічна обструктивна кардіоміопатія (ГОКМП), застосування у пацієнтів негроїдної раси NYHA класифікації.калійвмісних замінників харчової солі, препаратів літію, кларитроміцину, такролімусу, циклоспорину, гіперкаліємію, хірургічне втручання/загальна анестезія, пацієнти похилого віку, пригнічення кістковомозкового кровотворення, обтяжений алергологічний анамнез або ангіо ), десенсибілізуюча терапія, аферез ліпопротеїнів низької щільності (ЛПНГ), аортальний стеноз/мітральний стеноз/гіпертрофічна обструктивна кардіоміопатія (ГЗКМП), застосування у пацієнтів негроїдної раси, ХСН неішемічної етіології ІІІ-ІVфункціонального класу за клас.калійвмісних замінників харчової солі, препаратів літію, кларитроміцину, такролімусу, циклоспорину, гіперкаліємію, хірургічне втручання/загальна анестезія, пацієнти похилого віку, пригнічення кістковомозкового кровотворення, обтяжений алергологічний анамнез або ангіо ), десенсибілізуюча терапія, аферез ліпопротеїнів низької щільності (ЛПНГ), аортальний стеноз/мітральний стеноз/гіпертрофічна обструктивна кардіоміопатія (ГЗКМП), застосування у пацієнтів негроїдної раси, ХСН неішемічної етіології ІІІ-ІVфункціонального класу за клас.пригнічення кістковомозкового кровотворення, обтяжений алергологічний анамнез або ангіоневротичний набряк в анамнезі, проведення гемодіалізу з використанням високопроточних мембран (наприклад, AN69®), десенсибілізуюча терапія, аферез ліпопротеїнів низькій щільності (ЛПНДПіП) застосування у пацієнтів негроїдної раси, ХСН неішемічної етіології ІІІ-ІVфункціонального класу за класифікацією NYHA.пригнічення кістковомозкового кровотворення, обтяжений алергологічний анамнез або ангіоневротичний набряк в анамнезі, проведення гемодіалізу з використанням високопроточних мембран (наприклад, AN69®), десенсибілізуюча терапія, аферез ліпопротеїнів низькій щільності (ЛПНДПіП) застосування у пацієнтів негроїдної раси, ХСН неішемічної етіології ІІІ-ІVфункціонального класу за класифікацією NYHA.застосування у пацієнтів негроїдної раси, ХСН неішемічної етіології ІІІ-ІVфункціонального класу за класифікацією NYHA.застосування у пацієнтів негроїдної раси, ХСН неішемічної етіології ІІІ-ІVфункціонального класу за класифікацією NYHA.Вагітність та лактаціяПрепарат Дальнєва протипоказаний при вагітності. Препарат Дальнєва® не рекомендований для застосування у період грудного вигодовування. Необхідно оцінити значущість терапії для матері, щоб прийняти рішення про припинення грудного вигодовування або скасування препарату. Вагітність Амлодипін Безпека застосування амлодипіну при вагітності не встановлена. В експериментальних дослідженнях на тваринах фетотоксична та ембріотоксична дія препарату встановлена при застосуванні його у високих дозах. Застосування при вагітності можливе лише у разі відсутності безпечнішої альтернативи, і коли захворювання несе більший ризик для матері та плода. Периндоприл Застосування інгібіторів АПФ не рекомендовано до застосування у І триместрі вагітності (див. розділ «Особливі вказівки»). Застосування інгібіторів АПФ протипоказане у II та III триместрах вагітності (див. розділи «Протипоказання» та «Особливі вказівки»). На даний момент немає незаперечних епідеміологічних даних про тератогенний ризик при прийомі інгібіторів АПФ у І триместрі вагітності. Проте невелике збільшення ризику виникнення порушень розвитку плода виключити не можна. При плануванні вагітності слід відмінити препарат Дальнєва® та призначити інші гіпотензивні засоби, дозволені для застосування при вагітності. При встановленні вагітності слід негайно припинити терапію інгібіторами АПФ та, за необхідності, призначити іншу терапію. Відомо, що вплив інгібіторів АПФ на плід у ІІ та ІІІ триместрах вагітності може призводити до порушення його розвитку (зниження функції нирок, олігогідрамніон, уповільнення осифікації кісток черепа) та розвитку ускладнень у новонародженого (ниркова недостатність, артеріальна гіпотензія, гіперкаліємія). Якщо пацієнтка отримувала інгібітори АПФ у II або III триместрі вагітності, рекомендується провести ультразвукове дослідження для оцінки стану кісток черепа та функції нирок плода/дитини. Новонароджені, матері яких отримували інгібітори АПФ під час вагітності, повинні перебувати під ретельним медичним контролем через ризик розвитку артеріальної гіпотензії (див. розділи «Протипоказання» та «Особливі вказівки»). Період грудного вигодовування Амлодипін Амлодипін виділяється із грудним молоком. Частка материнської дози, отриманої немовлям, оцінили з міжквартильним діапазоном 3-7 %, але з більше 15 %. Про вплив амлодипіну на немовлят невідомо. Рішення про продовження/припинення терапії або грудного вигодовування слід приймати з огляду на користь від годування груддю для дитини та користь від прийому амлодипіну для матері. Периндоприл Внаслідок відсутності інформації, що стосується застосування периндоприлу в період годування груддю, прийом периндоприлу не рекомендований, краще дотримуватися в період годування груддю альтернативного лікування з більш вивченим профілем безпеки, особливо при вигодовуванні новонароджених або недоношених дітей. Лікарський препарат Дальнєва® не слід призначати дітям та підліткам віком до 18 років, оскільки відсутні дані про ефективність та безпеку застосування периндоприлу та амлодипіну у цих груп пацієнтів як у монотерапії, так і у складі комбінованої терапії.Побічна діяа. Резюме профілю безпеки Найчастіші небажані реакції при прийомі периндоприлу та амлодипіну у вигляді монотерапії: набряк, сонливість, запаморочення, головний біль (особливо на початку лікування), дисгевзія (перекручення смаку), парестезія, порушення зору (включаючи диплопію), дзвін у вухах, вертиго, відчуття серцебиття, «припливи» крові до шкіри обличчя, артеріальна гіпотензія (і симптоми, пов'язані з цим), задишка, кашель, біль у животі, нудота, блювання, диспепсія, зміна частоти та характеру стільця, діарея, запор, свербіж шкіри, висипання на шкірі , екзантема, припухлість у ділянці суглобів (припухлість у ділянці кісточок), спазми м'язів, підвищена стомлюваність, астенія. б. Перелік небажаних реакцій Наведені нижче небажані реакції, зазначені при проведенні клінічних досліджень та/або післяреєстраційному застосуванні в монотерапії периндоприлом та амлодипіном, наведені у вигляді наступної градації: дуже часто (≥ 1/10); часто (≥ 1/100, < 1/10); нечасто (≥ 1/1000, < 1/100); рідко (≥1/10000, <1/1000); дуже рідко (<1/10000); частота невідома (не може бути оцінена на основі наявних даних). Небажані реакції представлені у вигляді таблиці MedDRA Класи та системи органів Небажані реакції Частота Амлодипін Периндоприл Інфекційні та паразитарні захворювання Риніт Не часто Дуже рідко Порушення з боку крові та лімфатичної системи Еозинофілія - Не часто* Лейкопенія/нейтропенія (див. розділ «Особливі вказівки») Дуже рідко Дуже рідко Агранулоцитоз/панцитопенія (див. розділ «Особливі вказівки») - Дуже рідко Тромбоцитопенія (див. розділ «Особливі вказівки») Дуже рідко Дуже рідко Гемолітична анемія у пацієнтів з вродженою недостатністю глюкозо-6-фосфатдегідрогенази (див. розділ «Особливі вказівки») - Дуже рідко Порушення з боку імунної системи Гіперчутливість Дуже рідко Не часто Порушення з боку обміну речовин та харчування Гіперкаліємія, оборотна після відміни препарату (див. розділ «Особливі вказівки») - Не часто* Гіперглікемія Дуже рідко - Гіпонатріємія - Не часто* Гіпоглікемія (див. розділи «Взаємодія з іншими лікарськими засобами» та «Особливі вказівки») - Не часто* Порушення психіки Лабільність настрою (включаючи тривогу) Не часто Не часто Безсоння Не часто - Депресія Не часто - Порушення сну - Не часто Порушення з боку нервової системи Запаморочення (особливо на початку лікування) Часто Часто Головний біль (особливо на початку лікування) Часто Часто Сонливість (особливо на початку лікування) Часто Не часто* Дисгезія (перекручення смаку) Не часто Часто Парестезія Не часто Часто Непритомні стани Не часто Не часто* Сплутаність свідомості Рідко Дуже рідко Гіпестезія Не часто - Тремор Не часто - Гіпертонус Дуже рідко - Периферична нейропатія Дуже рідко - Інсульт, можливо, внаслідок надмірного зниження АТ у пацієнтів із групи високого ризику (див. розділ «Особливі вказівки») - Дуже рідко Екстрапірамідні порушення (екстрапірамідний синдром) Частота невідома - Порушення з боку органу зору Порушення зору Часто Часто Диплопія Часто - Порушення з боку органу слуху та лабіринтні порушення Дзвін у вухах Не часто Часто Вертіго - Часто Порушення з боку серця Відчуття серцебиття Часто Не часто* Тахікардія - Не часто* Стенокардія (див. розділ «Особливі вказівки») - Дуже рідко Інфаркт міокарда, можливий внаслідок надмірного зниження АТ у пацієнтів із групи високого ризику (див. розділ «Особливі вказівки») Дуже рідко Дуже рідко Аритмія (включаючи брадикардію, шлуночкову тахікардію та фібриляцію передсердь) Не часто Дуже рідко Порушення з боку судин «Припливи» крові до шкіри обличчя Часто - Артеріальна гіпотензія (і симптоми, пов'язані з артеріальною гіпотензією) Не часто Часто Васкуліт Дуже рідко Не часто* Синдром Рейно - Частота невідома Порушення з боку дихальної системи, органів грудної клітки та середостіння. Кашель Не часто Часто Задишка Часто Часто Бронхоспазм - Не часто Еозинофільна пневмонія - Дуже рідко Порушення з боку шлунково-кишкового тракту Біль в животі Часто Часто Нудота Часто Часто Блювота Не часто Часто Диспепсія Часто Часто Діарея Часто Часто Запор Часто Часто Зміна частоти та характеру стільця Часто - Сухість слизової оболонки ротової порожнини Не часто Не часто Гіперплазія ясен Дуже рідко - Панкреатит Дуже рідко Дуже рідко Гастрит Дуже рідко - Порушення з боку печінки та жовчовивідних шляхів Гепатит, жовтяниця Дуже рідко - Цитолітичний або холестатичний гепатит (див. розділ «Особливі вказівки») - Дуже рідко Підвищення активності «печінкових» ферментів у плазмі крові Дуже рідко (найчастіше у поєднанні з холестазом) Рідко Порушення з боку шкіри та підшкірних тканин Екзантема Не часто Часто Висипання на шкірі Не часто Часто Кожний зуд Не часто Часто Гіпергідроз Не часто Не часто Алопеція Не часто - Пурпура Не часто - Зміна кольору шкіри Не часто - Пухирчатка - Не часто* Ангіоневротичний набряк особи, кінцівок, губ, слизових оболонок, язика, голосових складок та/або гортані (див. розділ «Особливі вказівки») Дуже рідко Не часто Кропивниця (див. розділ «Особливі вказівки») Не часто Не часто Реакції фоточутливості Дуже рідко Не часто* Мультиформна еритема Дуже рідко Дуже рідко Набряк Квінке (ангіоневротичний набряк) Дуже рідко - Синдром Стівенса-Джонсона Дуже рідко - Ексфоліативний дерматит Дуже рідко - Загострення псоріазу - Рідко Токсичний епідермальний некроліз Частота невідома - Підвищене потовиділення Не часто Не часто Порушення з боку скелетном'язової та сполучної тканини Біль у спині Не часто - Припухлість у ділянці суглобів (припухлість у ділянці кісточок) Часто - М'язові спазми Часто Часто Артралгія Не часто Не часто* Міалгія Не часто Не часто* Порушення з боку нирок та сечовивідних шляхів Порушення сечовипускання, ніктурія, поллакіурія Не часто - Гостра ниркова недостатність - Дуже рідко Ниркова недостатність - Не часто Порушення з боку статевих органів та молочної залози еректильна дисфункція Не часто Не часто Гінекомастія Не часто - Загальні розлади та порушення у місці введення Набряки Дуже часто - Периферичні набряки - Не часто* Підвищена стомлюваність Часто - Астенія Часто Часто Біль у грудній клітці Не часто Не часто* нездужання Не часто Не часто* Біль Не часто - Лихоманка - Не часто* Лабораторні та інструментальні дані Збільшення маси тіла, зниження маси тіла Не часто - Підвищення концентрації сечовини у плазмі крові - Не часто* Підвищення концентрації креатиніну у плазмі крові - Не часто* Підвищення концентрації білірубіну у плазмі крові - Рідко Зниження гемоглобіну та гематокриту - Дуже рідко Травми, інтоксикації та ускладнення маніпуляцій Падіння - Не часто* *Оцінку частоти небажаних реакцій, виявлених за спонтанними повідомленнями, проведено на підставі даних результатів клінічних досліджень. Повідомлялося про розвиток синдрому неадекватної секреції антидіуретичного гормону (СНСАДГ) при одночасному застосуванні з іншими інгібіторами АПФ. СНСАДГ можна вважати дуже рідкісним можливим ускладненням, пов'язаним із лікуванням інгібіторами АПФ, у тому числі з периндоприлом.Взаємодія з лікарськими засобамиАмлодипін Нерекомендовані поєднання лікарських засобів Дантролен (внутрішньовенне введення) У лабораторних тварин були відзначені випадки фібриляції шлуночків із летальним кінцем та колапсом на фоні застосування верапамілу та внутрішньовенного введення дантролену, що супроводжувалися гіперкаліємією. Внаслідок ризику розвитку гіперкаліємії слід виключити одночасний прийом БМКК, у тому числі амлодипіну, у пацієнтів, що схильні до злоякісної гіпертермії, а також при лікуванні злоякісної гіпертермії. Поєднання лікарських засобів, що потребують особливої уваги Індуктори ізоферменту CYP3A4: при одночасному застосуванні з індукторами ізоферменту CYP3A4 концентрація амлодипіну в плазмі може змінюватися. Тому необхідно контролювати АТ та коригувати дозу як під час, так і після їх одночасного застосування, особливо у разі застосування з потужними індукторами ізоферменту CYP3A4 (наприклад, рифампіцин, препарати Звіробою продірявленого). Інгібітори ізоферменту CYP3A4: одночасний прийом амлодипіну та потужних, або помірних інгібіторів ізоферменту CYP3A4 (інгібітори протеази, протигрибкові препарати групи азолів, макроліди, наприклад, еритроміцин або кларитроміцин, при верапаміл або ди. Клінічні прояви зазначених фармакокінетичних відхилень можуть бути більш вираженими у пацієнтів похилого віку. У зв'язку з чим може знадобитися моніторинг клінічного стану та корекція дози. У пацієнтів, які приймають амлодипін одночасно з кларитроміцином, підвищений ризик розвитку гіпотензії. Слід проводити ретельне спостереження за станом пацієнтів, які приймають периндоприл одночасно з кларитроміцином. Поєднання лікарських засобів, що потребують уваги Амлодипін посилює антигіпертензивну дію гіпотензивних препаратів. Такролімус: існує ризик збільшення сироваткової концентрації такролімусу при одночасному застосуванні з амлодипіном. Щоб уникнути розвитку токсичних ефектів такролімусу при одночасному застосуванні цих препаратів потрібен моніторинг сироваткової концентрації такролімусу та корекція його дози за потреби. Циклоспорин: дослідження щодо вивчення взаємодії циклоспорину з амлодипіном у здорових добровольців або інших груп населення не проводилися, за винятком пацієнтів, які перенесли трансплантацію нирки, у яких відзначалася варіабельність підвищення найменших концентрацій циклоспорину в плазмі (в середньому від 0% до 40%). Слід розглянути можливість контролю сироваткової концентрації циклоспорину у пацієнтів після трансплантації нирки при одночасному застосуванні з амлодипіном. При необхідності доза циклоспорину має бути знижена. Симвастатин: при одночасному застосуванні кількох доз амлодипіну по 10 мг та симвастатину 80 мг було відзначено збільшення експозиції симвастатину на 77 % порівняно з ізольованим прийомом симвастатину. У пацієнтів, які приймають препарат Дальнєва у дозі 10 мг + 4 мг або 10 мг + 8 мг, слід обмежити прийом симвастатину до 20 мг на добу. Одночасний прийом амлодипіну та вживання грейпфрутів або грейпфрутового соку не рекомендується у зв'язку з можливим підвищенням біодоступності амлодипіну у деяких пацієнтів, що, в свою чергу, може призвести до посилення ефектів зниження АТ. Інгібітори тTOR(mammalianTargetofRapamycin – мета рапамицина ссавців): інгібітори mTOR, такі як сиролімус, темсіролімус і еверолімус, є субстрати ізоферменту CYP3A. Амлодипін є слабким інгібітором ізоферменту CYP3A. При одночасному застосуванні з інгібіторами mTOR амлодипін може підвищувати їхню експозицію. Кларитроміцин: Кларитроміцин є інгібітором ізоферменту CYP3A4. Існує підвищений ризик розвитку артеріальної гіпотензії у пацієнтів, які одночасно застосовують кларитроміцин з амлодипіном. Ретельне спостереження за пацієнтами рекомендується при одночасному застосуванні амлодипіну з кларитроміцином. Одночасне застосування бета-адреноблокаторів (бісопролол, метопролол) та альфа- та бета-адреноблокатора карведилолу при ХСН: підвищує ризик розвитку артеріальної гіпотензії та погіршення перебігу ХСН у пацієнтів з неконтрольованою або латентнопротікаючою ХСН (підсилення). Крім цього, бета-адреноблокатори можуть зменшити надмірну рефлекторну симпатичну серцеву активацію на тлі супутньої ХСН. При одночасному застосуванні амлодипін може підвищувати системну експозицію тасонерміну у плазмі. У таких випадках необхідний регулярний контроль концентрації тасонерміну в плазмі та корекція дози при необхідності. Інші комбінації лікарських засобів Препарати кальцію можуть зменшити ефект БМКК. При одночасному застосуванні БМКК з препаратами літію (для амлодипіну дані відсутні) можливе посилення прояву їхньої нейротоксичності (нудота, блювання, діарея, атаксія, тремор, шум у вухах). У ході клінічних досліджень лікарських взаємодій амлодипін не впливав на фармакокінетику аторвастатину, дигоксину, варфарину. Одноразовий прийом 100 мг силденафілу у пацієнтів з есенціальною гіпертензією не впливає на параметри фармакокінетики амлодипіну. Периндоприл Дані клінічних досліджень показують, що подвійна блокада РААС внаслідок одночасного застосування інгібіторів АПФ, АРА II або аліскірену призводить до збільшення частоти виникнення таких небажаних явищ, як артеріальна гіпотензія, гіперкаліємія та порушення функції нирок (включаючи гостру ниркову недостатність) порівняно з ситуаціями, коли застосовується лише один препарат, що впливає на РААС (див. розділи "Фармакологічні властивості. Фармакодинаміка", "Протипоказання", "Особливі вказівки"). Лікарські засоби, що викликають гіперкаліємію Деякі препарати можуть збільшувати ризик розвитку гіперкаліємії: аліскірен, солі калію, калійзберігаючі діуретики, інгібітори АПФ, АРА II, нестероїдні протизапальні препарати (НПЗП), гепарин, імунодепресанти, такі як циклоспорин або такролімус, триметоприм, ко-тримоксазол). Поєднання цих препаратів збільшує ризик розвитку гіперкаліємії. Циклоспорин: при одночасному застосуванні інгібіторів АПФ з циклоспорином можливий розвиток гіперкаліємії. Рекомендується контролювати вміст калію у сироватці крові. Гепарин: можливе підвищення вмісту калію у сироватці крові. Рекомендується контролювати вміст калію у сироватці крові. Одночасне застосування протипоказане Аліскірен та лікарські препарати, що містять аліскірен Одночасне застосування інгібіторів АПФ з лікарськими препаратами, що містять аліскірен, протипоказане у пацієнтів з цукровим діабетом та/або помірним або тяжким порушенням функції нирок (ШКФ менше 60 мл/хв/1,73 м(2) площі поверхні тіла) та не рекомендується у інших пацієнтів. (Див. розділ «Протипоказання»). Зростає ризик розвитку гіперкаліємії, погіршення функції нирок, серцево-судинної захворюваності та смертності. Екстракорпоральна терапія Екстракорпоральні методи лікування, що ведуть до контакту крові з негативно зарядженими поверхнями, такі як діаліз або гемофільтрація з використанням деяких високопроточних мембран (наприклад, поліакрилонітрилових), або аферез ЛПНГ з використанням декстрану сульфату, протипоказані через збільшення ризику розвитку тяжких анафілактоїд. розділ "Протипоказання"). Якщо пацієнту потрібна екстракорпоральна терапія, слід розглянути можливість використання іншого типу діалізної мембрани чи іншого класу гіпотензивних препаратів. Інгібітори нейтральної ендопептидази При одночасному застосуванні інгібіторів АПФ з лікарськими препаратами, що містять сакубітрил (інгібітор неприлізину), зростає ризик розвитку ангіоневротичного набряку, через що одночасне застосування зазначених препаратів протипоказане. Інгібітори АПФ слід призначати не раніше ніж через 36 годин після відміни препаратів, що містять сакубітрил. Протипоказано призначення препаратів, що містять сакубітрил, пацієнтам, які отримують інгібітори АПФ, а також протягом 36 годин після відміни інгібіторів АПФ. Нерекомендовані поєднання лікарських засобів Аліскірен та лікарські препарати, що містять аліскірен У пацієнтів, які не мають цукрового діабету або порушення функції нирок, можливе підвищення ризику гіперкаліємії, погіршення функції нирок та підвищення частоти серцево-судинної захворюваності та смертності. Одночасне призначення інгібіторів АПФ та АРА II За наявними літературними даними, у пацієнтів із встановленим діагнозом атеросклерозу, серцевою недостатністю або цукровим діабетом з ураженням органів-мішеней одночасний прийом інгібіторів АПФ та АРА II призводить до збільшення частоти розвитку артеріальної гіпотензії, непритомності, гіперкаліємії та погіршення функції нирок. порівняно із ситуаціями, коли застосовується лише один препарат, що впливає на РААС. Застосування подвійної блокади РААС (наприклад, одночасний прийом інгібіторів АПФ та АРА II) повинно бути обмежене поодинокими випадками із суворим контролем функції нирок, вмісту калію у плазмі крові та АТ (див. розділ «Особливі вказівки»). Естрамустін Одночасне застосування естрамустину з інгібіторами АПФ супроводжується підвищеним ризиком розвитку ангіоневротичного набряку. Ко-тримоксазол (триметоприм + сульфаметоксазол) При одночасному застосуванні з котримоксазолом (триметоприм + сульфаметоксазол) може підвищуватися ризик розвитку гіперкаліємії (див. розділ «Особливі вказівки»). Калійзберігаючі діуретики (наприклад, тріамтерен, амілорид) та солі калію Зазвичай вміст калію в плазмі залишається в межах норми, при цьому у деяких пацієнтів, які отримують інгібітори АПФ, може розвинутись гіперкаліємія. Застосування калійзберігаючих діуретиків (наприклад, спіронолактону, тріамтерену, еплеренону або амілориду), калійвмісних замінників кухонної солі, інших препаратів, що сприяють підвищенню вмісту калію в плазмі може призвести до значного збільшення вмісту калію в сироватці крові. Слід також бути обережними при одночасному призначенні периндоприлу з іншими препаратами, здатними збільшувати вміст калію в сироватці крові, такими як триметоприм і ко-тримоксазол (триметоприм + сульфаметоксазол), так як відомо, що триметоприм діє як калійзберігаючий діуретик, такий якТому одночасне застосування периндоприлу з вищезазначеними препаратами не рекомендується. Якщо, однак, одночасне застосування показано, слід застосовувати з дотриманням запобіжних заходів та регулярним контролем вмісту калію в сироватці крові. Препарати літію При одночасному застосуванні препаратів літію та інгібіторів АПФ може виникати оборотне підвищення вмісту літію у плазмі крові та пов'язані з цим токсичні ефекти (важкі нейротоксичні ефекти). Одночасне застосування периндоприлу та препаратів літію не рекомендується. За необхідності проведення такої терапії необхідний регулярний контроль вмісту літію в плазмі (див. розділ «Особливі вказівки»). Поєднання лікарських засобів, що потребують особливої уваги Гіпоглікемічні засоби (інсулін, похідні сульфонілсечовини) Згідно з даними, отриманими в епідеміологічних дослідженнях, інгібітори АПФ можуть посилювати гіпоглікемічний ефект інсуліну та похідних сульфонілсечовини з ризиком розвитку гіпоглікемії. Даний ефект найімовірніше можна спостерігати у перші тижні одночасного застосування та у пацієнтів з порушенням функції нирок. Калійнесберігаючі діуретики У пацієнтів, які отримують діуретики, особливо у пацієнтів з гіповолемією та/або зниженою концентрацією солей, на початку терапії периндоприлом може спостерігатися виражене зниження АТ, ризик розвитку якого можна зменшити шляхом відміни діуретичного засобу, заповненням втрати рідини або солей перед початком терапії периндоприлом, а також призначенням периндоприлу у низькій дозі з подальшим поступовим її збільшенням. При АГ у пацієнтів з гіповолемією або зниженим вмістом солей на фоні терапії діуретиками діуретики повинні бути або скасовані до початку застосування інгібітору АПФ (при цьому калійнесберігаючий діуретик може бути пізніше знову призначений), або інгібітор АПФ повинен бути призначений у низькій дозі з подальшим поступовим її збільшенням. . При застосуванні діуретиків у разі ХСН інгібітор АПФ повинен бути призначений у дуже низькій дозі, можливо, після зменшення дози одночасного калійнесберігаючого діуретика. У всіх випадках функція нирок (концентрація креатиніну в плазмі крові) повинна контролюватись у перші тижні застосування інгібіторів АПФ. Калійзберігаючі діуретики (застосування еплеренону, спіронолактону в дозах від 12,5 мг до 50 мг на добу та низьких доз інгібіторів АПФ) При лікуванні ХСН II-IV функціонального класу за класифікацією NYHA з фракцією викиду лівого шлуночка < 40 % у пацієнтів, які раніше отримували інгібітори АПФ та «петлеві» діуретики, існує ризик розвитку гіперкаліємії (з можливим летальним наслідком), особливо у разі недотримання рекомендацій щодо цієї комбінації. препаратів. Перед початком застосування цієї комбінації лікарських препаратів необхідно переконатися у відсутності гіперкаліємії та порушення функції нирок. Рекомендується регулярно контролювати концентрацію креатиніну та вміст калію в плазмі крові: щотижня у перший місяць лікування та щомісяця у подальшому. Рацекадотрил Повідомлялося про підвищений ризик розвитку ангіоневротичного набряку при одночасному застосуванні інгібіторів АПФ та рацекадотрилу (інгібітор енкефалінази). Тканинні активатори плазміногену В обсерваційних дослідженнях виявлено підвищену частоту розвитку ангіоневротичного набряку у пацієнтів, які приймали інгібітори АПФ після застосування алтеплази для тромболітичної терапії ішемічного інсульту. Інгібітори mTOR (наприклад, сиролімус, еверолімус, темсіролімус) У пацієнтів, які одночасно отримують терапію інгібіторами mTOR, підвищується ризик розвитку ангіоневротичного набряку (див. розділ «Особливі вказівки»). НПЗЗ, включаючи високі дози ацетилсаліцилової кислоти (≥ 3 г/добу) Одночасне застосування інгібіторів АПФ з нестероїдними протизапальними засобами (ацетилсаліцилова кислота в дозі, що має протизапальну дію, інгібітори циклооксигенази-2 [ЦОГ-2] і неселективні нестероїдні протизапальні засоби), може призвести до зниження антигіпертензивної дії інгібіторів АПФ. Одночасне застосування інгібіторів АПФ та НПЗЗ може призводити до погіршення функції нирок, включаючи розвиток гострої ниркової недостатності, та збільшення вмісту калію у сироватці крові, особливо у пацієнтів зі зниженою функцією нирок. Слід бути обережними при призначенні даної комбінації, особливо у пацієнтів похилого віку. Пацієнтам необхідно компенсувати втрату рідини та ретельно контролювати функцію нирок як на початку лікування, так і в процесі лікування. Поєднання лікарських засобів, що потребують уваги Інгібітори дипептидилпептидази IV (ДПП-IV) (гліптини), наприклад, лінагліптин, саксагліптин, сітагліптин, віллдагліптин Одночасне застосування з інгібіторами АПФ може збільшувати ризик розвитку ангіоневротичного набряку внаслідок пригнічення активності ДПП-IVгліптином. Симпатоміметики Можуть послаблювати антигіпертензивний ефект інгібіторів АПФ. Препарати золота При застосуванні інгібіторів АПФ, у тому числі периндоприлу, у пацієнтів, які отримують внутрішньовенно препарат золота (натрію ауротіомалат), були описані нітритоїдні реакції, з частотою виникнення «рідко» (симптомокомплекс, що включає гіперемію шкіри обличчя, нудоту, блювання, артеріальну гіпотензію). Алопуринол, імуносупресивні засоби, кортикостероїди (при системному застосуванні) та прокаїнамід Одночасне застосування з інгібіторами AПФ може супроводжуватися підвищеним ризиком розвитку лейкопенії, особливо у пацієнтів із наявними порушеннями функції нирок. Засоби для загальної анестезії Одночасне застосування інгібіторів АПФ та засобів для загальної анестезії може призводити до антигіпертензивного ефекту. Поєднання лікарських засобів, що потребують особливої уваги Баклофен Можливе посилення антигіпертензивної дії. Слід контролювати АТ та функцію нирок, за необхідності провести корекцію дози амлодипіну. Поєднання препаратів, що потребує уваги Гіпотензивні засоби (наприклад, бета-адреноблокатори) та вазодилататори Можливе посилення антигіпертензивного ефекту периндоприлу та амлодипіну. Слід бути обережними при одночасному застосуванні з нітрогліцерином, іншими нітратами або іншими вазодилататорами, оскільки при цьому можливе додаткове зниження АТ. Кортикостероїди (мінерало- та глюкокортикостероїди), тетракозактид Зниження антигіпертензивної дії (затримка рідини та іонів натрію внаслідок дії кортикостероїдів). Альфа-адреноблокатори (празозин, альфузозин, доксазозин, тамсулозин, теразозин) Посилення антигіпертензивної дії та підвищення ризику розвитку ортостатичної гіпотензії. Аміфостін Можливе посилення антигіпертензивного ефекту амлодипіну. Трициклічні антидепресанти/нейролептики/засоби для загальної анестезії Посилення антигіпертензивної дії та підвищення ризику розвитку ортостатичної гіпотензії.Спосіб застосування та дозиВсередину, по одній таблетці 1 раз на день, переважно вранці перед їдою. Доза лікарського препарату Дальнева® підбирається після раніше проведеного підбору доз окремих компонентів препарату: периндоприлу та амлодипіну у пацієнтів з артеріальною гіпертензією та стабільною стенокардією. При терапевтичній необхідності доза лікарського препарату Дальнева® може бути змінена на підставі індивідуального підбору доз окремих компонентів: амлодипін 5 мг + периндоприл 4 мг або амлодипін 10 мг + периндоприл 4 мг, або амлодипін 5 мг + периндоприл 8 мг, або амлодипін 10 мг . Максимальна добова доза: амлодипін – 10 мг + периндоприл – 8 мг.ПередозуванняІнформація про передозування препаратом Дальнева відсутня. Амлодипін Інформація про передозування амлодипіном обмежена. Симптоми: виражене зниження АТ з можливим розвитком рефлекторної тахікардії та надмірної периферичної вазодилатації (ризик розвитку вираженої та стійкої артеріальної гіпотензії, у т.ч. з розвитком шоку та летального результату). Лікування: промивання шлунка, призначення активованого вугілля (особливо в перші 2 години після передозування), підтримання функції серцево-судинної системи, підвищене положення нижніх кінцівок, контроль ОЦК та діурезу, симптоматична та підтримуюча терапія. Для відновлення тонусу судин – застосування судинозвужувальних засобів (за відсутності протипоказань до їх застосування), для усунення наслідків блокади кальцієвих каналів – внутрішньовенне введення розчину глюконату. Гемодіаліз неефективний. Периндоприл Дані передозування периндоприлом обмежені. Симптоми: виражене зниження артеріального тиску, шок, порушення водно-електролітного балансу, ниркова недостатність, гіпервентиляція легень, тахікардія, відчуття серцебиття, брадикардія, запаморочення, неспокій та кашель. Лікування: заходи невідкладної допомоги зводяться до виведення препарату з організму: промивання шлунка та/або призначення активованого вугілля з подальшим відновленням ОЦК. При вираженому зниженні артеріального тиску слід перевести пацієнта в положення «лежачи» на спині з піднятими ногами, за необхідності провести заходи для відновлення ОЦК (наприклад, внутрішньовенна інфузія 0,9 % розчину натрію хлориду). Також можливе внутрішньовенне введення катехоламінів. За допомогою гемодіалізу можна видалити периндоприл із системного кровотоку. При брадикардії, резистентної до терапії, може знадобитися імплантація електрокардіостимулятора. Необхідний динамічний контроль загального стану, концентрації креатиніну та вмісту електролітів у плазмі крові.Запобіжні заходи та особливі вказівкиОсобливі вказівки, що стосуються периндоприлу та амлодипіну, застосовні і до лікарського препарату Дальнєва®. Амлодипін Ефективність та безпека застосування амлодипіну при гіпертонічному кризі не встановлено. Серцева недостатність Лікування пацієнтів із серцевою недостатністю слід проводити з обережністю. При застосуванні амлодипіну у пацієнтів з ХСН III та IV функціонального класу за класифікацією NYHA можливий розвиток набряку легень. БМКК, включаючи амлодипін, необхідно з обережністю застосовувати у пацієнтів з ХСН у зв'язку з можливим збільшенням ризику розвитку небажаних явищ з боку серцево-судинної системи та смертності. Печінкова недостатність У пацієнтів з порушенням функції печінки Т(½) та AUCамлодипіну збільшуються. Рекомендації щодо дозування препарату не встановлені. Прийом амлодипіну необхідно почати з найнижчих доз і дотримуватися запобіжних заходів як на початку лікування, так і при збільшенні дози. Пацієнтам з тяжкою печінковою недостатністю підвищувати дозу слід поступово, забезпечуючи ретельний моніторинг клінічного стану. Пацієнти похилого віку У пацієнтів похилого віку збільшення дози слід проводити з обережністю (див. розділ «Спосіб застосування та дози» та «Фармакологічні властивості. Фармакокінетика»). Ниркова недостатність Пацієнти з нирковою недостатністю можуть приймати амлодипін у стандартних дозах. Зміни плазмових концентрацій амлодипіну не корелюють зі ступенем ниркової недостатності. Амлодипін не виводиться з організму за допомогою діалізу. Мітральний стеноз/аортальний стеноз/ГЗКМП Амлодипін протипоказаний пацієнтам із обструкцією вихідного тракту лівого шлуночка. Синдром «скасування» Незважаючи на відсутність у БМКК синдрому «скасування», припинення лікування препаратом Дальнєва бажано проводити поступово, зменшуючи дозу препарату. Амлодипін не запобігає розвитку синдрому «скасування» при різкому припиненні прийому бета-адреноблокаторів. Периферичні набряки Незначно або помірно виражені периферичні набряки були найчастішим небажаним явищем амлодипіну у клінічних дослідженнях. Частота виникнення периферичних набряків зростає зі збільшенням дози (при застосуванні амлодипіну у дозі 2,5 мг, 5 мг та 10 мг на добу набряки виникали відповідно у 1,8 %, 3 % та 10 % пацієнтів). Слід ретельно диференціювати периферичні набряки, пов'язані із застосуванням амлодипіну, від симптомів прогресування лівшлуночкової серцевої недостатності. Інше Необхідна підтримка гігієни зубів та спостереження у стоматолога (для запобігання болючості, кровоточивості та гіперплазії ясен). Периндоприл Підвищена чутливість/ангіоневротичний набряк (набряк Квінке) При застосуванні інгібіторів АПФ, у тому числі периндоприлу, в окремих випадках може спостерігатися розвиток ангіоневротичного набряку особи, губ, язика, голосових складок та/або гортані. Це може статися у будь-який період. При появі цих симптомів застосування препарату Дальнева® повинно бути негайно припинено, пацієнт повинен спостерігатися доти, доки ознаки набряку не зникнуть повністю. препарати. Ангіоневротичний набряк, що супроводжується набряком язика або гортані, може призвести до обструкції дихальних шляхів та летального результату.5 мл) та/або забезпечити прохідність дихальних шляхів. Пацієнт повинен перебувати під медичним наглядом до повного та стійкого зникнення симптомів. У пацієнтів, в анамнезі яких відзначався набряк Квінке, не пов'язаний із застосуванням інгібіторів АПФ, може бути підвищений ризик його розвитку на фоні застосування препаратів цієї групи (див. розділ "Протипоказання"). У поодиноких випадках на тлі терапії інгібіторами АПФ розвивається інтестинальний ангіоневротичний набряк (ангіоневротичний набряк кишечника). При цьому у пацієнтів відзначається біль у животі як ізольований симптом або у поєднанні з нудотою та блюванням, у деяких випадках без попереднього ангіоневротичного набряку обличчя та при нормальній сироватковій концентрації С1-естерази. Діагноз встановлюється за допомогою комп'ютерної томографії черевної порожнини, ультразвукового дослідження або на момент хірургічного втручання. Симптоми зникають після припинення інгібіторів АПФ. Тому у пацієнтів з болем у животі, які отримують інгібітори АПФ, при проведенні диференціального діагнозу необхідно враховувати можливість розвитку інтестинального ангіоневротичного набряку (див. розділ «Побічна дія»). При одночасному застосуванні інгібіторів АПФ з рацекадотрилом, інгібіторами mTOR (наприклад, темсиролімусом, еверолімусом, сиролімусом) або ДПП-IV (гліптинами, включаючи віллдагліптин) підвищується ризик розвитку ангіоневротичного набряку (наприклад, набряк верхніх дихальних шляхів). ) (див. розділ «Взаємодія з іншими лікарськими засобами»). Слід виявляти обережність на початку терапії рацекадотрилом, інгібіторами mTOR (наприклад, тимсиролімусом, еверолімусом, сиролімусом) або гліптинами, включаючи віллдагліптин, при одночасному застосуванні з інгібіторами АПФ. Анафілактоїдні реакції при проведенні процедур десенсибілізації Є окремі повідомлення про розвиток тривалих, що загрожують життю анафілактоїдних реакцій у пацієнтів, які отримують інгібітори АПФ під час десенсибілізуючої терапії отрутою перетинчастокрилих комах. У цих пацієнтів анафілактоїдної реакції вдавалося уникнути шляхом тимчасової відміни інгібіторів АПФ, а при випадковому прийомі препарату анафілактоїдна реакція виникала знову. Анафілактоїдні реакції при проведенні аферезу ЛПНЩ за допомогою декстрану сульфату У поодиноких випадках у пацієнтів, які отримують інгібітори АПФ, при проведенні аферезу ЛПНЩ з використанням декстрану сульфату можуть розвиватися анафілактоїдні реакції, що загрожують життю. Для запобігання анафілактоїдної реакції слід тимчасово припинити терапію інгібітором АПФ перед кожною процедурою аферезу ЛПНЩ з використанням декстрану сульфату. Нейтропенія/агранулоцитоз, тромбоцитопенія та анемія У пацієнтів, які приймають інгібітори АПФ, можливі випадки розвитку нейтропенії/агранулоцитозу, тромбоцитопенії та анемії. У пацієнтів з нормальною функцією нирок без інших обтяжливих факторів нейтропенія розвивається рідко. Особливою обережністю периндоприл слід застосовувати у пацієнтів із системними захворюваннями сполучної тканини, на фоні прийому імунодепресантів, алопуринолу або прокаїнаміду, особливо у пацієнтів з порушеною функцією нирок. У деяких пацієнтів виникали важкі інфекції, у ряді випадків стійкі до інтенсивної антибіотикотерапії. При призначенні периндоприлу таким пацієнтам рекомендується періодично контролювати кількість лейкоцитів у крові. Пацієнти повинні повідомляти лікаря про будь-які ознаки інфекційних захворювань (наприклад, біль у горлі, гарячка). Реноваскулярна гіпертензія У пацієнтів із двостороннім стенозом ниркових артерій або стенозом артерії єдиної функціонуючої нирки на фоні терапії інгібіторами АПФ зростає ризик розвитку артеріальної гіпотензії та ниркової недостатності. Прийом діуретиків може бути додатковим фактором ризику. Погіршення функції нирок може спостерігатися вже при незначній зміні концентрації креатиніну у сироватці, навіть у пацієнтів з одностороннім стенозом ниркової артерії. Подвійна блокада РААС Є дані, що свідчать про те, що одночасне застосування інгібіторів АПФ, АРА II або аліскірену підвищує ризик розвитку гіпотензії, гіперкаліємії та порушення функції нирок (включаючи гостру ниркову недостатність). Одночасне застосування інгібіторів АПФ з препаратами, що містять аліскірен, протипоказане у пацієнтів з цукровим діабетом та/або помірною або тяжкою нирковою недостатністю (ШКФ менше 60 мл/хв/1,73 м(2) площі поверхні тіла) та не рекомендується у інших пацієнтів. Якщо терапія за допомогою подвійної блокади РААС визнана абсолютно необхідною, її слід проводити лише під суворим медичним контролем та при регулярному контролі функції нирок, вмісту електролітів у плазмі крові та АТ.Протипоказане застосування інгібіторів АПФ одночасно з АРА II у пацієнтів з діабетичною нефропатією та не рекомендується у інших пацієнтів (див. розділ "Протипоказання"). Первинний гіперальдостеронізм Пацієнти з первинним гіперальдостеронізмом, як правило, не сприйнятливі до гіпотензивних препаратів, дія яких ґрунтується на інгібуванні РААС. Тому прийом препарату не рекомендовано. Артеріальна гіпотензія Інгібітори АПФ можуть викликати різке зниження артеріального тиску. Симптоматична гіпотензія рідко розвивається у пацієнтів без супутніх захворювань. Ризик вираженого зниження АТ підвищений у пацієнтів зі зниженим ОЦК, що може відзначатися на фоні терапії діуретиками, при дотриманні суворої дієти без солі, гемодіалізі, діареї та блюванні, а також у пацієнтів з тяжким ступенем АГ з високою активністю реніну (див. розділи «Взаємодія з іншими лікарськими засобами» та «Побічна дія»). У пацієнтів з підвищеним ризиком розвитку симптоматичної артеріальної гіпотензії необхідно ретельно контролювати АТ, функцію нирок та вміст калію у сироватці крові під час терапії лікарським препаратом Дальнєва®. Подібний підхід застосовується і у пацієнтів зі стенокардією та цереброваскулярними захворюваннями, у яких виражена артеріальна гіпотензія може призвести до інфаркту міокарда або порушення мозкового кровообігу. У разі розвитку артеріальної гіпотензії пацієнт повинен бути переведений у положення «лежачи» на спині з піднятими ногами. При необхідності слід заповнити ОЦК за допомогою внутрішньовенного введення 0,9% натрію розчину хлориду. Минуща артеріальна гіпотензія не є перешкодою для подальшого прийому препарату. Після відновлення ОЦК та АТ лікування може бути продовжено. Мітральний стеноз/аортальний стеноз/ГЗКМП Периндоприл, як і інші інгібітори АПФ, повинен обережно призначатися у пацієнтів з обструкцією вихідного тракту лівого шлуночка (аортальний стеноз, ГОКМП), а також у пацієнтів з мітральним стенозом. Амлодипін протипоказаний пацієнтам із обструкцією вихідного тракту лівого шлуночка. Порушення функції нирок Пацієнтам з нирковою недостатністю (КК менше 60 мл/хв) рекомендується індивідуальний підбір доз периндоприлу та амлодипіну (див. розділ «Спосіб застосування та дози»). Таким пацієнтам необхідний регулярний контроль вмісту калію та концентрації креатиніну у сироватці крові (див. розділ «Побічна дія»). У пацієнтів із двостороннім стенозом ниркової артерії або стенозом артерії єдиної нирки на фоні терапії інгібіторами АПФ можливе підвищення концентрацій сечовини та креатиніну у сироватці крові, що зазвичай відбувається при відміні терапії. Найчастіше цей ефект відзначається у пацієнтів із нирковою недостатністю. Додаткова наявність реноваскулярної гіпертензії зумовлює підвищений ризик розвитку тяжкої гіпотензії та ниркової недостатності у таких пацієнтів. У деяких пацієнтів з артеріальною гіпертензією без ознак ураження судин нирок можливе підвищення концентрацій сечовини та креатиніну в сироватці крові, особливо при одночасному призначенні периндоприлу з діуретиком, зазвичай незначне та минуще. Найчастіше цей ефект відзначається у пацієнтів із попереднім порушенням функції нирок. Порушення функції печінки У поодиноких випадках на фоні прийому інгібіторів АПФ виникає холестатична жовтяниця. При прогресуванні цього синдрому розвивається фульмінантний некроз печінки, іноді з летальним кінцем. Механізм розвитку цього синдрому незрозумілий. У разі появи жовтяниці або значного підвищення активності «печінкових» ферментів у плазмі крові на фоні прийому інгібіторів АПФ слід припинити прийом препарату (див. розділ «Побічна дія») та звернутися до лікаря. Етнічні відмінності У пацієнтів негроїдної раси частіше, ніж у інших рас, на фоні застосування інгібіторів АПФ розвивається ангіоневротичний набряк. Периндоприл, як і інші інгібітори АПФ, може мати менш виражену антигіпертензивну дію у пацієнтів негроїдної раси порівняно з представниками інших рас. Можливо, ця відмінність зумовлена тим, що у пацієнтів негроїдної раси з артеріальною гіпертензією частіше відзначається низька активність реніну плазми крові. Кашель На тлі терапії інгібітором АПФ може виникати сухий кашель. Кашель тривалий час зберігається на фоні прийому препаратів цієї групи і зникає після їх відміни. Це слід враховувати під час проведення диференціальної діагностики кашлю. Хірургічні втручання/загальна анестезія У пацієнтів, яким планується проведення великого оперативного втручання та/або застосування засобів для загальної анестезії, що викликають гіпотензію, застосування периндоприлу може блокувати утворення ангіотензину II на тлі компенсаторного вивільнення реніну. Лікування слід припинити за добу до хірургічного втручання. При розвитку артеріальної гіпотензії за вказаним механізмом слід підтримувати артеріальний тиск шляхом заповнення ОЦК. Гіперкаліємія Інгібітори АПФ можуть викликати гіперкаліємію, оскільки вони пригнічують вивільнення альдостерону. Цей ефект зазвичай незначний у пацієнтів із нормальною функцією нирок. Однак у пацієнтів з порушенням функції нирок та/або у пацієнтів, які одночасно приймають препарати, що містять калій (включаючи калійвмісні замінники кухонної солі), калійзберігаючі діуретики, триметоприм або ко-тримоксазол (фіксована комбінація триметоприму і сульфаметоксазолу), і особливо антагон можливий розвиток гіперкаліємії. Факторами ризику гіперкаліємії є ниркова недостатність, порушення функції нирок, вік старше 70 років, цукровий діабет, інтеркурентні стани (зокрема, дегідратація, гостра декомпенсація ХСН, метаболічний ацидоз), одночасне застосування калійзберігаючих діуретиків (наприклад,спіронолактон, еплеренон, тріамтерен або амілорид), препаратів калію або замінників калію кухонної солі або одночасне застосування інших препаратів, що сприяють підвищенню вмісту калію в плазмі крові (наприклад, гепарин, ко-тримоксазол). Гіперкаліємія може призвести до серйозних порушень серцевого ритму, іноді з летальним кінцем. Калійзберігаючі діуретики та АРА II слід застосовувати з обережністю у пацієнтів, які отримують інгібітори АПФ, та регулярно контролювати вміст калію у сироватці крові та функцію нирок (див. розділ «Взаємодія з іншими лікарськими засобами»).ко-тримоксазол). Гіперкаліємія може призвести до серйозних порушень серцевого ритму, іноді з летальним кінцем. Калійзберігаючі діуретики та АРА II слід застосовувати з обережністю у пацієнтів, які отримують інгібітори АПФ, та регулярно контролювати вміст калію у сироватці крові та функцію нирок (див. розділ «Взаємодія з іншими лікарськими засобами»).ко-тримоксазол). Гіперкаліємія може призвести до серйозних порушень серцевого ритму, іноді з летальним кінцем. Калійзберігаючі діуретики та АРА II слід застосовувати з обережністю у пацієнтів, які отримують інгібітори АПФ, та регулярно контролювати вміст калію у сироватці крові та функцію нирок (див. розділ «Взаємодія з іншими лікарськими засобами»). Пацієнти з цукровим діабетом При призначенні препарату пацієнтам з цукровим діабетом, які отримують гіпоглікемічні засоби для внутрішнього застосування або інсуліну, протягом першого місяця терапії необхідно ретельно контролювати концентрацію глюкози в крові (див. розділ «Взаємодія з іншими лікарськими засобами») Застосування препарату Дальнева у пацієнтів з гострим інфарктом міокарда не рекомендується через недостатній досвід клінічного застосування. Застосування при хронічних захворюваннях: Пацієнти з порушенням функції нирок Лікарський препарат Дальнєва може застосовуватися у пацієнтів з КК рівним або більше 60 мл/хв. Лікарський препарат Дальнєва протипоказаний до застосування у пацієнтів з КК менше 60 мл/хв. Таким пацієнтам рекомендується індивідуальний підбір доз периндоприлу та амлодипіну. Зміна концентрації амлодипіну в плазмі не корелює зі ступенем вираженості ниркової недостатності. Пацієнти похилого віку та пацієнти з порушенням функції печінки Необхідно зменшити початкову дозу препарату Дальнєва до найменшої дози амлодипіну (тобто до 1 таблетки амлодипін 5 мг + периндоприл 4 мг або амлодипін 5 мг + периндоприл 8 мг). Вплив на керування транспортними засобами: У зв'язку з можливістю виникнення запаморочення, сонливості та інших побічних ефектів на фоні застосування препарату Дальнева® необхідно дотримуватись обережності при керуванні транспортними засобами та роботі з іншими технічними пристроями, що потребують підвищеної концентрації уваги та швидкості психомоторних реакцій, особливо на початку лікування та збільшення дози.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаамлодипін + периндоприл таблетки на 1 таблетку 5 мг + 4 мг/10 мг + 4 мг/5 мг + 8 мг/10 мг + 8 мг речовини, що діють: Амлодипін безілат (амлодипін безілат) 6,935 мг/13,870 мг/6,935 мг/13,870 мг, еквівалентно амлодипіну 5 мг/10 мг/5 мг/10 мг Периндоприлу ербумін А субстанція – гранули 21,000 мг/21,000 мг/42,000 мг/42,000 мг, містить периндоприлу ербуміну 4 мг/4 мг/8 мг/8 мг Допоміжні речовини: Целюлоза мікрокристалічна, крохмаль прежелатинізований, карбоксиметилкрохмаль натрію, гідрокарбонат натрію, кремнію діоксид колоїдний, магнію стеаратОпис лікарської формиТаблетки 5 мг + 4 мг: Круглі, злегка двоопуклі таблетки з фаскою, від білого до майже білого кольору. Таблетки 10 мг + 4 мг: Капсулоподібні, двоопуклі таблетки з ризиком на одній стороні, від білого до майже білого кольору. Таблетки 5 мг + 8 мг: Круглі, двоопуклі таблетки з фаскою, від білого до майже білого кольору. Таблетки 10 мг + 8 мг: Круглі, двоопуклі таблетки з фаскою, з ризиком на одній стороні, від білого майже білого кольору.Фармакотерапевтична групагіпотензивний комбінований засіб (інгібітор ангіотензинперетворюючого ферменту [АПФ] + блокатор «повільних» кальцієвих каналів [БМКК])ФармакокінетикаВеличина абсорбції амлодипіну та периндоприлу при застосуванні комбінованого лікарського препарату Дальнева® суттєво не відрізняється від такої при застосуванні їх як монопрепарати. Амлодипін Після прийому внутрішньо амлодипін повільно абсорбується із шлунково-кишкового тракту (ЖКТ). Прийом їжі не впливає на біодоступність амлодипіну. Максимальна концентрація (Сmax) амлодипіну в плазмі досягається через 6-12 годин після прийому препарату внутрішньо. Абсолютна біодоступність становить 64-80%. Об'єм розподілу – приблизно 21 л/кг. У дослідженнях in vitro було показано, що близько 97,5% циркулюючого амлодипіну пов'язано з білками плазми. Кінцевий період напіввиведення (Т½) із плазми становить 35-50 годин, що дозволяє приймати препарат 1 раз на добу. Амлодипін метаболізується у печінці з утворенням неактивних метаболітів, при цьому 10% прийнятої дози амлодипіну виводиться у незміненому вигляді та 60% нирками – у вигляді метаболітів. Амлодипін не виводиться з організму за допомогою діалізу. Час досягнення Сmax(ТСmax) амлодипіну в плазмі крові не відрізняється у пацієнтів похилого віку та молодшого віку. У пацієнтів похилого віку відзначається уповільнення кліренсу амлодипіну, що призводить до збільшення площі під кривою «концентрація-час» (AUC). Збільшення AUC та Т½ у пацієнтів з ХСН відповідає передбачуваній величині для цієї вікової групи. У пацієнтів з порушенням функції нирок зміни концентрації амлодипіну в плазмі не корелюють зі ступенем ниркової недостатності. Можливе незначне подовження Т½. Дані щодо застосування амлодипіну пацієнтами з печінковою недостатністю обмежені. У пацієнтів з печінковою недостатністю спостерігається зниження кліренсу амлодипіну, що призводить до подовження Т½ та збільшення AUC приблизно на 40-60%. Периндоприл Після прийому периндоприл швидко всмоктується і досягає Сmaxв плазмі протягом 1 години. Т½ периндоприлу з плазми становить приблизно 1 годину. Периндоприл не має фармакологічної активності, є проліками. Приблизно 27% від загальної кількості, прийнятої внутрішньо периндоприлу, потрапляє в кровообіг у вигляді активного метаболіту – периндоприлату. Крім периндоприлату утворюються ще 5 метаболітів, які не мають фармакологічної активності. Сmax у плазмі крові досягається через 3-4 години після прийому внутрішньо. Прийом їжі зменшує біодоступність периндоприлу, тому препарат слід приймати 1 раз на добу, вранці, перед їдою. Існує лінійна залежність концентрації периндоприлу в плазмі від величини прийнятої всередину дози. Об'єм розподілу вільного периндоприлату становить приблизно 0,2 л/кг. Зв'язок периндоприлату з білками плазми (переважно з АПФ) становить 20% і залежить від його концентрації. Периндоприлат виводиться нирками, Т½ незв'язаної фракції становить приблизно 17 годин, тому рівноважний стан досягається протягом 4-х діб після прийому внутрішньо. Виведення периндоприлату сповільнене у пацієнтів похилого віку, а також у пацієнтів із серцевою та нирковою недостатністю (див. розділ «Спосіб застосування та дози»), тому спостереження за такими пацієнтами повинно включати регулярний контроль концентрації креатиніну та вмісту калію в плазмі крові. Діалізний кліренс периндоприлату становить 70 мл/хв. Фармакокінетика периндоприлу порушена у пацієнтів із цирозом печінки: його печінковий кліренс зменшується у 2 рази. Тим не менш, кількість периндоприлату, що утворюється, не зменшується, тому не потрібно корекції дози (див. розділи «Спосіб застосування та дози» та «Особливі вказівки»).ФармакодинамікаАмлодипін Амлодипін – БМКК, похідне дигідропіридину. Амлодипін пригнічує трансмембранний перехід іонів кальцію в кардіоміоцити та гладком'язові клітини судинної стінки. Антигіпертензивна дія амлодипіну обумовлена прямим розслаблюючим впливом на гладком'язові клітини судинної стінки. Детальний механізм, за допомогою якого амлодипін здійснює антиангінальну дію, не цілком встановлений, але відомо, що амлодипін зменшує загальне ішемічне навантаження за допомогою двох дій: викликає розширення периферичних артеріол, зменшуючи загальний периферичний судинний опір (ОПСС) (постнавантаження). Оскільки частота серцевих скорочень (ЧСС) у своїй не змінюється, потреба міокарда в кисні знижується; викликає розширення коронарних артерій та артеріол як у ішемізованій, так і в інтактній зонах. Їх дилатація збільшує надходження кисню до міокарда у пацієнтів з вазоспастичною стенокардією (стенокардія Принцметала або варіантна стенокардія). У пацієнтів з артеріальною гіпертензією (АГ) прийом амлодипіну 1 раз на добу забезпечує клінічно значуще зниження артеріального тиску (АТ) у положенні стоячи і лежачи протягом 24 годин. Антигіпертензивна дія розвивається повільно, у зв'язку з чим розвиток гострої гіпотензії нехарактерний. У пацієнтів зі стенокардією прийом амлодипіну 1 раз на добу збільшує загальний час фізичного навантаження, збільшує час до розвитку нападу стенокардії та до появи депресії сегмента ST на 1 мм, а також знижує частоту нападів стенокардії та споживання нітрогліцерину під язик. Амлодипін не чинить несприятливих метаболічних ефектів і не впливає на концентрацію ліпідів плазми. Препарат може застосовуватися у пацієнтів із супутньою бронхіальною астмою, цукровим діабетом та подагрою. Ішемічна хвороба серця (ІХС) Результати оцінки ефективності свідчать про те, що прийом амлодипіну характеризується меншою кількістю випадків госпіталізації щодо стенокардії та проведення процедур реваскуляризації у пацієнтів з ІХС. Периндоприл Периндоприл – інгібітор ферменту, що перетворює ангіотензин I на ангіотензин II. АПФ, або кініназа II, є екзопептидазою, яка здійснює як перетворення ангіотензину I на судинозвужувальну речовину ангіотензин II, так і розпад брадикініну, що має судинорозширювальну дію, до неактивного гептапептиду. Оскільки АПФ інактивує брадикінін, пригнічення АПФ супроводжується підвищенням активності як циркулюючої, так і тканинної калікреїн-кінінової системи, при цьому також активується система простагландинів. Периндоприл має терапевтичну дію завдяки активному метаболіту, периндоприлату. Інші метаболіти не мають інгібуючої дії на АПФ в умовах in vitro. Артеріальна гіпертензія Периндоприл є препаратом для лікування артеріальної гіпертензії будь-якого ступеня тяжкості. На тлі його застосування відзначається зниження як систолічного, так і діастолічного АТ у положенні «лежачи» та «стоячи». Периндоприл зменшує ОПСС, що призводить до зниження артеріального тиску та поліпшення периферичного кровотоку без зміни ЧСС. Як правило, прийом периндоприлу збільшує нирковий кровообіг, швидкість клубочкової фільтрації (СКФ) при цьому не змінюється. Антигіпертензивна дія препарату досягає максимуму через 4-6 годин після одноразового прийому внутрішньо та зберігається протягом 24 годин. Антигіпертензивна дія через 24 години після одноразового застосування внутрішньо становить близько 87-100% від максимального антигіпертензивного ефекту. Зниження АТ досягається досить швидко. Терапевтичний ефект настає через 1 місяць від початку терапії і не супроводжується тахіфілаксією. Припинення лікування не викликає ефекту "рикошету". Периндоприл має судинорозширювальну дію, сприяє відновленню еластичності великих артерій та структури судинної стінки дрібних артерій, а також зменшує гіпертрофію лівого шлуночка. Стабільна ІХС Ефективність застосування периндоприлу у пацієнтів (12218 пацієнтів віком від 18 років) зі стабільною ІХС без клінічних симптомів хронічної серцевої недостатності (ХСН) вивчалась у ході 4-річного дослідження. 90% учасників дослідження раніше перенесли гострий інфаркт міокарда та/або процедуру реваскуляризації. Більшість пацієнтів отримували крім досліджуваного препарату стандартну терапію, включаючи антиагреганти, гіполіпідемічні засоби та бета-адреноблокатори. Як основний критерій ефективності була обрана комбінована кінцева точка, що включає серцево-судинну смертність, нефатальний інфаркт міокарда та/або зупинку серця з успішною реанімацією. Терапія периндоприлом третбутиламіном у дозі 8 мг/добу 1 раз на день (еквівалентно 10 мг периндоприлу аргініну) призводила до суттєвого зниження абсолютного ризику щодо комбінованої кінцевої точки на 1,9 % у пацієнтів, які раніше перенесли інфаркт міокарда та/або процедуру реваскуляру. абсолютного ризику становило 2,2% порівняно з групою плацебо. Подвійна блокада ренін-ангіотензин-альдостеронової системи (РААС) Є дані клінічних досліджень комбінованої терапії із застосуванням інгібітору АПФ та антагоніста рецептора ангіотензину II (АРА II). Протипоказано застосування інгібіторів АПФ у поєднанні з АРА II у пацієнтів з діабетичною нефропатією. Є дані клінічного дослідження з вивчення позитивного впливу від додавання аліскірену до стандартної терапії інгібітором АПФ або АРА II у пацієнтів з цукровим діабетом 2 типу та/або хронічним захворюванням нирок, або кардіоваскулярним захворюванням, які мають поєднання цих захворювань. Дослідження було припинено достроково у зв'язку з зростанням ризику виникнення несприятливих результатів. Кардіоваскулярна смерть та інсульт відзначалися частіше у групі пацієнтів, які отримують аліскірен, порівняно з групою плацебо; також небажані явища та серйозні небажані явища особливого інтересу (гіперкаліємія, артеріальна гіпотензія та порушення функції нирок) реєструвалися частіше у групі аліскірену, ніж у групі плацебо. Амлодипін + периндоприл Ефективність при тривалому застосуванні амлодипіну в комбінації з периндоприлом і атенололу в комбінації з бендрофлуметіазидом у пацієнтів віком від 40 до 79 років з АГ та, щонайменше, з трьома з перелічених додаткових факторів ризику: гіпертрофія лівого шлуночка діабет 2 типу, атеросклероз периферичних артерій, раніше перенесений інсульт або транзиторна ішемічна атака, чоловіча стать, вік 55 років і старше, мікроальбумінурія або протеїнурія, куріння, загальний холестерин/холестерин ліпопротеїдів високої щільності ≥ 6, ранній розвиток ASCOT-BPLA. Основний критерій оцінки ефективності – комбінований показник частоти нефатального інфаркту міокарда (у тому числі безболевого) та летальних наслідків ІХС. Частота ускладнень, передбачених основним критерієм оцінки, у групі амлодипін/периндоприл була на 10% нижчою, ніж у групі атенолол/бендрофлуметіазид, проте ця відмінність не була статистично достовірною. У групі амлодипін/периндоприл відзначалося достовірне зниження частоти ускладнень, передбачених додатковими критеріями ефективності (крім фатальної та нефатальної серцевої недостатності).Показання до застосуванняАртеріальна гіпертензія та/або ішемічна хвороба серця: стабільна стенокардія напруги у пацієнтів, яким потрібна терапія периндоприлом та амлодипіном.Протипоказання до застосуванняПідвищена чутливість до периндоприлу або інших інгібіторів АПФ, амлодипіну та інших похідних дигідропіридину, а також допоміжних речовин, що входять до складу препарату. Ангіоневротичний набряк (набряк Квінке) в анамнезі (у тому числі на фоні прийому інших інгібіторів АПФ). Спадковий/ідіопатичний ангіоневротичний набряк. Одночасне застосування з аліскіреном та лікарськими препаратами, що містять аліскірен, у пацієнтів з цукровим діабетом та/або помірними або тяжкими порушеннями функції нирок (ШКФ < 60 мл/хв/1,73 м2 площі поверхні тіла) (див. розділи «Взаємодія з іншими лікарськими засобами) засобами" і "Фармакологічні властивості. Фармакодинаміка"). Одночасне застосування з АРА II у пацієнтів з діабетичною нефропатією (див. розділ «Особливі вказівки»). Одночасне застосування з інгібіторами нейтральної ендопептидази (наприклад, з препаратами, що містять сакубітрил) через високий ризик розвитку ангіоневротичного набряку. Екстракорпоральна терапія, що веде до контакту крові з негативно зарядженими поверхнями (див. розділ "Взаємодія з іншими лікарськими засобами"). Виражений двосторонній стеноз ниркових артерій або стеноз артерії єдиної нирки, що функціонує (див. розділ «Особливі вказівки»). Тяжка артеріальна гіпотензія (систолічний артеріальний тиск менше 90 мм рт. ст.). Шок (включно з кардіогенним). Обструкція вихідного тракту лівого шлуночка (наприклад, клінічно суттєвий стеноз аорти). Гемодинамічно нестабільна серцева недостатність після гострого інфаркту міокарда. Ниркова недостатність (кліренс креатиніну менше 60 мл/хв). Вагітність та період грудного вигодовування. Вік до 18 років (ефективність та безпека не встановлені). Стеноз ниркової артерії (у тому числі двосторонній), єдина функціонуюча нирка, печінкова недостатність, ниркова недостатність, системні захворювання сполучної тканини (у тому числі системний червоний вовчак, склеродермія), терапія імунодепресантами, алопуринолом, прокаїнамоз об'єм циркулюючої крові (ОЦК) (прийом діуретиків, безсольова дієта, блювання, діарея), атеросклероз, цереброваскулярні захворювання, ІХС з тяжким обструктивним ураженням коронарних артерій, гострий інфаркт міокарда (і період протягом 1 місяця після нього), нестабільна синусового вузла (виражена тахікардія, брадикардія), реноваскулярна гіпертензія, цукровий діабет, первинний гіперальдостеронізм, ХСН, одночасне застосування інгібіторів або індукторів ізоферменту CYP3A4,дантролену, естрамустину, калійзберігаючих діуретиків, препаратів калію, калійвмісних замінників харчової солі, препаратів літію, кларитроміцину, такролімусу, циклоспорину, гіперкаліємії, хірургічного втручання/загальна анестезія, пацієнтів похилого віку. гемодіалізу з використанням високопроточних мембран (наприклад, AN69®), десенсибілізуюча терапія, аферез ліпопротеїнів низької щільності (ЛПНЩ), аортальний стеноз/мітральний стеноз/гіпертрофічна обструктивна кардіоміопатія (ГОКМП), застосування у пацієнтів негроїдної раси NYHA класифікації.калійвмісних замінників харчової солі, препаратів літію, кларитроміцину, такролімусу, циклоспорину, гіперкаліємію, хірургічне втручання/загальна анестезія, пацієнти похилого віку, пригнічення кістковомозкового кровотворення, обтяжений алергологічний анамнез або ангіо ), десенсибілізуюча терапія, аферез ліпопротеїнів низької щільності (ЛПНГ), аортальний стеноз/мітральний стеноз/гіпертрофічна обструктивна кардіоміопатія (ГЗКМП), застосування у пацієнтів негроїдної раси, ХСН неішемічної етіології ІІІ-ІVфункціонального класу за клас.калійвмісних замінників харчової солі, препаратів літію, кларитроміцину, такролімусу, циклоспорину, гіперкаліємію, хірургічне втручання/загальна анестезія, пацієнти похилого віку, пригнічення кістковомозкового кровотворення, обтяжений алергологічний анамнез або ангіо ), десенсибілізуюча терапія, аферез ліпопротеїнів низької щільності (ЛПНГ), аортальний стеноз/мітральний стеноз/гіпертрофічна обструктивна кардіоміопатія (ГЗКМП), застосування у пацієнтів негроїдної раси, ХСН неішемічної етіології ІІІ-ІVфункціонального класу за клас.пригнічення кістковомозкового кровотворення, обтяжений алергологічний анамнез або ангіоневротичний набряк в анамнезі, проведення гемодіалізу з використанням високопроточних мембран (наприклад, AN69®), десенсибілізуюча терапія, аферез ліпопротеїнів низькій щільності (ЛПНДПіП) застосування у пацієнтів негроїдної раси, ХСН неішемічної етіології ІІІ-ІVфункціонального класу за класифікацією NYHA.пригнічення кістковомозкового кровотворення, обтяжений алергологічний анамнез або ангіоневротичний набряк в анамнезі, проведення гемодіалізу з використанням високопроточних мембран (наприклад, AN69®), десенсибілізуюча терапія, аферез ліпопротеїнів низькій щільності (ЛПНДПіП) застосування у пацієнтів негроїдної раси, ХСН неішемічної етіології ІІІ-ІVфункціонального класу за класифікацією NYHA.застосування у пацієнтів негроїдної раси, ХСН неішемічної етіології ІІІ-ІVфункціонального класу за класифікацією NYHA.застосування у пацієнтів негроїдної раси, ХСН неішемічної етіології ІІІ-ІVфункціонального класу за класифікацією NYHA.Вагітність та лактаціяПрепарат Дальнєва протипоказаний при вагітності. Препарат Дальнєва® не рекомендований для застосування у період грудного вигодовування. Необхідно оцінити значущість терапії для матері, щоб прийняти рішення про припинення грудного вигодовування або скасування препарату. Вагітність Амлодипін Безпека застосування амлодипіну при вагітності не встановлена. В експериментальних дослідженнях на тваринах фетотоксична та ембріотоксична дія препарату встановлена при застосуванні його у високих дозах. Застосування при вагітності можливе лише у разі відсутності безпечнішої альтернативи, і коли захворювання несе більший ризик для матері та плода. Периндоприл Застосування інгібіторів АПФ не рекомендовано до застосування у І триместрі вагітності (див. розділ «Особливі вказівки»). Застосування інгібіторів АПФ протипоказане у II та III триместрах вагітності (див. розділи «Протипоказання» та «Особливі вказівки»). На даний момент немає незаперечних епідеміологічних даних про тератогенний ризик при прийомі інгібіторів АПФ у І триместрі вагітності. Проте невелике збільшення ризику виникнення порушень розвитку плода виключити не можна. При плануванні вагітності слід відмінити препарат Дальнєва® та призначити інші гіпотензивні засоби, дозволені для застосування при вагітності. При встановленні вагітності слід негайно припинити терапію інгібіторами АПФ та, за необхідності, призначити іншу терапію. Відомо, що вплив інгібіторів АПФ на плід у ІІ та ІІІ триместрах вагітності може призводити до порушення його розвитку (зниження функції нирок, олігогідрамніон, уповільнення осифікації кісток черепа) та розвитку ускладнень у новонародженого (ниркова недостатність, артеріальна гіпотензія, гіперкаліємія). Якщо пацієнтка отримувала інгібітори АПФ у II або III триместрі вагітності, рекомендується провести ультразвукове дослідження для оцінки стану кісток черепа та функції нирок плода/дитини. Новонароджені, матері яких отримували інгібітори АПФ під час вагітності, повинні перебувати під ретельним медичним контролем через ризик розвитку артеріальної гіпотензії (див. розділи «Протипоказання» та «Особливі вказівки»). Період грудного вигодовування Амлодипін Амлодипін виділяється із грудним молоком. Частка материнської дози, отриманої немовлям, оцінили з міжквартильним діапазоном 3-7 %, але з більше 15 %. Про вплив амлодипіну на немовлят невідомо. Рішення про продовження/припинення терапії або грудного вигодовування слід приймати з огляду на користь від годування груддю для дитини та користь від прийому амлодипіну для матері. Периндоприл Внаслідок відсутності інформації, що стосується застосування периндоприлу в період годування груддю, прийом периндоприлу не рекомендований, краще дотримуватися в період годування груддю альтернативного лікування з більш вивченим профілем безпеки, особливо при вигодовуванні новонароджених або недоношених дітей. Лікарський препарат Дальнєва® не слід призначати дітям та підліткам віком до 18 років, оскільки відсутні дані про ефективність та безпеку застосування периндоприлу та амлодипіну у цих груп пацієнтів як у монотерапії, так і у складі комбінованої терапії.Побічна діяа. Резюме профілю безпеки Найчастіші небажані реакції при прийомі периндоприлу та амлодипіну у вигляді монотерапії: набряк, сонливість, запаморочення, головний біль (особливо на початку лікування), дисгевзія (перекручення смаку), парестезія, порушення зору (включаючи диплопію), дзвін у вухах, вертиго, відчуття серцебиття, «припливи» крові до шкіри обличчя, артеріальна гіпотензія (і симптоми, пов'язані з цим), задишка, кашель, біль у животі, нудота, блювання, диспепсія, зміна частоти та характеру стільця, діарея, запор, свербіж шкіри, висипання на шкірі , екзантема, припухлість у ділянці суглобів (припухлість у ділянці кісточок), спазми м'язів, підвищена стомлюваність, астенія. б. Перелік небажаних реакцій Наведені нижче небажані реакції, зазначені при проведенні клінічних досліджень та/або післяреєстраційному застосуванні в монотерапії периндоприлом та амлодипіном, наведені у вигляді наступної градації: дуже часто (≥ 1/10); часто (≥ 1/100, < 1/10); нечасто (≥ 1/1000, < 1/100); рідко (≥1/10000, <1/1000); дуже рідко (<1/10000); частота невідома (не може бути оцінена на основі наявних даних). Небажані реакції представлені у вигляді таблиці MedDRA Класи та системи органів Небажані реакції Частота Амлодипін Периндоприл Інфекційні та паразитарні захворювання Риніт Не часто Дуже рідко Порушення з боку крові та лімфатичної системи Еозинофілія - Не часто* Лейкопенія/нейтропенія (див. розділ «Особливі вказівки») Дуже рідко Дуже рідко Агранулоцитоз/панцитопенія (див. розділ «Особливі вказівки») - Дуже рідко Тромбоцитопенія (див. розділ «Особливі вказівки») Дуже рідко Дуже рідко Гемолітична анемія у пацієнтів з вродженою недостатністю глюкозо-6-фосфатдегідрогенази (див. розділ «Особливі вказівки») - Дуже рідко Порушення з боку імунної системи Гіперчутливість Дуже рідко Не часто Порушення з боку обміну речовин та харчування Гіперкаліємія, оборотна після відміни препарату (див. розділ «Особливі вказівки») - Не часто* Гіперглікемія Дуже рідко - Гіпонатріємія - Не часто* Гіпоглікемія (див. розділи «Взаємодія з іншими лікарськими засобами» та «Особливі вказівки») - Не часто* Порушення психіки Лабільність настрою (включаючи тривогу) Не часто Не часто Безсоння Не часто - Депресія Не часто - Порушення сну - Не часто Порушення з боку нервової системи Запаморочення (особливо на початку лікування) Часто Часто Головний біль (особливо на початку лікування) Часто Часто Сонливість (особливо на початку лікування) Часто Не часто* Дисгезія (перекручення смаку) Не часто Часто Парестезія Не часто Часто Непритомні стани Не часто Не часто* Сплутаність свідомості Рідко Дуже рідко Гіпестезія Не часто - Тремор Не часто - Гіпертонус Дуже рідко - Периферична нейропатія Дуже рідко - Інсульт, можливо, внаслідок надмірного зниження АТ у пацієнтів із групи високого ризику (див. розділ «Особливі вказівки») - Дуже рідко Екстрапірамідні порушення (екстрапірамідний синдром) Частота невідома - Порушення з боку органу зору Порушення зору Часто Часто Диплопія Часто - Порушення з боку органу слуху та лабіринтні порушення Дзвін у вухах Не часто Часто Вертіго - Часто Порушення з боку серця Відчуття серцебиття Часто Не часто* Тахікардія - Не часто* Стенокардія (див. розділ «Особливі вказівки») - Дуже рідко Інфаркт міокарда, можливий внаслідок надмірного зниження АТ у пацієнтів із групи високого ризику (див. розділ «Особливі вказівки») Дуже рідко Дуже рідко Аритмія (включаючи брадикардію, шлуночкову тахікардію та фібриляцію передсердь) Не часто Дуже рідко Порушення з боку судин «Припливи» крові до шкіри обличчя Часто - Артеріальна гіпотензія (і симптоми, пов'язані з артеріальною гіпотензією) Не часто Часто Васкуліт Дуже рідко Не часто* Синдром Рейно - Частота невідома Порушення з боку дихальної системи, органів грудної клітки та середостіння. Кашель Не часто Часто Задишка Часто Часто Бронхоспазм - Не часто Еозинофільна пневмонія - Дуже рідко Порушення з боку шлунково-кишкового тракту Біль в животі Часто Часто Нудота Часто Часто Блювота Не часто Часто Диспепсія Часто Часто Діарея Часто Часто Запор Часто Часто Зміна частоти та характеру стільця Часто - Сухість слизової оболонки ротової порожнини Не часто Не часто Гіперплазія ясен Дуже рідко - Панкреатит Дуже рідко Дуже рідко Гастрит Дуже рідко - Порушення з боку печінки та жовчовивідних шляхів Гепатит, жовтяниця Дуже рідко - Цитолітичний або холестатичний гепатит (див. розділ «Особливі вказівки») - Дуже рідко Підвищення активності «печінкових» ферментів у плазмі крові Дуже рідко (найчастіше у поєднанні з холестазом) Рідко Порушення з боку шкіри та підшкірних тканин Екзантема Не часто Часто Висипання на шкірі Не часто Часто Кожний зуд Не часто Часто Гіпергідроз Не часто Не часто Алопеція Не часто - Пурпура Не часто - Зміна кольору шкіри Не часто - Пухирчатка - Не часто* Ангіоневротичний набряк особи, кінцівок, губ, слизових оболонок, язика, голосових складок та/або гортані (див. розділ «Особливі вказівки») Дуже рідко Не часто Кропивниця (див. розділ «Особливі вказівки») Не часто Не часто Реакції фоточутливості Дуже рідко Не часто* Мультиформна еритема Дуже рідко Дуже рідко Набряк Квінке (ангіоневротичний набряк) Дуже рідко - Синдром Стівенса-Джонсона Дуже рідко - Ексфоліативний дерматит Дуже рідко - Загострення псоріазу - Рідко Токсичний епідермальний некроліз Частота невідома - Підвищене потовиділення Не часто Не часто Порушення з боку скелетном'язової та сполучної тканини Біль у спині Не часто - Припухлість у ділянці суглобів (припухлість у ділянці кісточок) Часто - М'язові спазми Часто Часто Артралгія Не часто Не часто* Міалгія Не часто Не часто* Порушення з боку нирок та сечовивідних шляхів Порушення сечовипускання, ніктурія, поллакіурія Не часто - Гостра ниркова недостатність - Дуже рідко Ниркова недостатність - Не часто Порушення з боку статевих органів та молочної залози еректильна дисфункція Не часто Не часто Гінекомастія Не часто - Загальні розлади та порушення у місці введення Набряки Дуже часто - Периферичні набряки - Не часто* Підвищена стомлюваність Часто - Астенія Часто Часто Біль у грудній клітці Не часто Не часто* нездужання Не часто Не часто* Біль Не часто - Лихоманка - Не часто* Лабораторні та інструментальні дані Збільшення маси тіла, зниження маси тіла Не часто - Підвищення концентрації сечовини у плазмі крові - Не часто* Підвищення концентрації креатиніну у плазмі крові - Не часто* Підвищення концентрації білірубіну у плазмі крові - Рідко Зниження гемоглобіну та гематокриту - Дуже рідко Травми, інтоксикації та ускладнення маніпуляцій Падіння - Не часто* *Оцінку частоти небажаних реакцій, виявлених за спонтанними повідомленнями, проведено на підставі даних результатів клінічних досліджень. Повідомлялося про розвиток синдрому неадекватної секреції антидіуретичного гормону (СНСАДГ) при одночасному застосуванні з іншими інгібіторами АПФ. СНСАДГ можна вважати дуже рідкісним можливим ускладненням, пов'язаним із лікуванням інгібіторами АПФ, у тому числі з периндоприлом.Взаємодія з лікарськими засобамиАмлодипін Нерекомендовані поєднання лікарських засобів Дантролен (внутрішньовенне введення) У лабораторних тварин були відзначені випадки фібриляції шлуночків із летальним кінцем та колапсом на фоні застосування верапамілу та внутрішньовенного введення дантролену, що супроводжувалися гіперкаліємією. Внаслідок ризику розвитку гіперкаліємії слід виключити одночасний прийом БМКК, у тому числі амлодипіну, у пацієнтів, що схильні до злоякісної гіпертермії, а також при лікуванні злоякісної гіпертермії. Поєднання лікарських засобів, що потребують особливої уваги Індуктори ізоферменту CYP3A4: при одночасному застосуванні з індукторами ізоферменту CYP3A4 концентрація амлодипіну в плазмі може змінюватися. Тому необхідно контролювати АТ та коригувати дозу як під час, так і після їх одночасного застосування, особливо у разі застосування з потужними індукторами ізоферменту CYP3A4 (наприклад, рифампіцин, препарати Звіробою продірявленого). Інгібітори ізоферменту CYP3A4: одночасний прийом амлодипіну та потужних, або помірних інгібіторів ізоферменту CYP3A4 (інгібітори протеази, протигрибкові препарати групи азолів, макроліди, наприклад, еритроміцин або кларитроміцин, при верапаміл або ди. Клінічні прояви зазначених фармакокінетичних відхилень можуть бути більш вираженими у пацієнтів похилого віку. У зв'язку з чим може знадобитися моніторинг клінічного стану та корекція дози. У пацієнтів, які приймають амлодипін одночасно з кларитроміцином, підвищений ризик розвитку гіпотензії. Слід проводити ретельне спостереження за станом пацієнтів, які приймають периндоприл одночасно з кларитроміцином. Поєднання лікарських засобів, що потребують уваги Амлодипін посилює антигіпертензивну дію гіпотензивних препаратів. Такролімус: існує ризик збільшення сироваткової концентрації такролімусу при одночасному застосуванні з амлодипіном. Щоб уникнути розвитку токсичних ефектів такролімусу при одночасному застосуванні цих препаратів потрібен моніторинг сироваткової концентрації такролімусу та корекція його дози за потреби. Циклоспорин: дослідження щодо вивчення взаємодії циклоспорину з амлодипіном у здорових добровольців або інших груп населення не проводилися, за винятком пацієнтів, які перенесли трансплантацію нирки, у яких відзначалася варіабельність підвищення найменших концентрацій циклоспорину в плазмі (в середньому від 0% до 40%). Слід розглянути можливість контролю сироваткової концентрації циклоспорину у пацієнтів після трансплантації нирки при одночасному застосуванні з амлодипіном. При необхідності доза циклоспорину має бути знижена. Симвастатин: при одночасному застосуванні кількох доз амлодипіну по 10 мг та симвастатину 80 мг було відзначено збільшення експозиції симвастатину на 77 % порівняно з ізольованим прийомом симвастатину. У пацієнтів, які приймають препарат Дальнєва у дозі 10 мг + 4 мг або 10 мг + 8 мг, слід обмежити прийом симвастатину до 20 мг на добу. Одночасний прийом амлодипіну та вживання грейпфрутів або грейпфрутового соку не рекомендується у зв'язку з можливим підвищенням біодоступності амлодипіну у деяких пацієнтів, що, в свою чергу, може призвести до посилення ефектів зниження АТ. Інгібітори тTOR(mammalianTargetofRapamycin – мета рапамицина ссавців): інгібітори mTOR, такі як сиролімус, темсіролімус і еверолімус, є субстрати ізоферменту CYP3A. Амлодипін є слабким інгібітором ізоферменту CYP3A. При одночасному застосуванні з інгібіторами mTOR амлодипін може підвищувати їхню експозицію. Кларитроміцин: Кларитроміцин є інгібітором ізоферменту CYP3A4. Існує підвищений ризик розвитку артеріальної гіпотензії у пацієнтів, які одночасно застосовують кларитроміцин з амлодипіном. Ретельне спостереження за пацієнтами рекомендується при одночасному застосуванні амлодипіну з кларитроміцином. Одночасне застосування бета-адреноблокаторів (бісопролол, метопролол) та альфа- та бета-адреноблокатора карведилолу при ХСН: підвищує ризик розвитку артеріальної гіпотензії та погіршення перебігу ХСН у пацієнтів з неконтрольованою або латентнопротікаючою ХСН (підсилення). Крім цього, бета-адреноблокатори можуть зменшити надмірну рефлекторну симпатичну серцеву активацію на тлі супутньої ХСН. При одночасному застосуванні амлодипін може підвищувати системну експозицію тасонерміну у плазмі. У таких випадках необхідний регулярний контроль концентрації тасонерміну в плазмі та корекція дози при необхідності. Інші комбінації лікарських засобів Препарати кальцію можуть зменшити ефект БМКК. При одночасному застосуванні БМКК з препаратами літію (для амлодипіну дані відсутні) можливе посилення прояву їхньої нейротоксичності (нудота, блювання, діарея, атаксія, тремор, шум у вухах). У ході клінічних досліджень лікарських взаємодій амлодипін не впливав на фармакокінетику аторвастатину, дигоксину, варфарину. Одноразовий прийом 100 мг силденафілу у пацієнтів з есенціальною гіпертензією не впливає на параметри фармакокінетики амлодипіну. Периндоприл Дані клінічних досліджень показують, що подвійна блокада РААС внаслідок одночасного застосування інгібіторів АПФ, АРА II або аліскірену призводить до збільшення частоти виникнення таких небажаних явищ, як артеріальна гіпотензія, гіперкаліємія та порушення функції нирок (включаючи гостру ниркову недостатність) порівняно з ситуаціями, коли застосовується лише один препарат, що впливає на РААС (див. розділи "Фармакологічні властивості. Фармакодинаміка", "Протипоказання", "Особливі вказівки"). Лікарські засоби, що викликають гіперкаліємію Деякі препарати можуть збільшувати ризик розвитку гіперкаліємії: аліскірен, солі калію, калійзберігаючі діуретики, інгібітори АПФ, АРА II, нестероїдні протизапальні препарати (НПЗП), гепарин, імунодепресанти, такі як циклоспорин або такролімус, триметоприм, ко-тримоксазол). Поєднання цих препаратів збільшує ризик розвитку гіперкаліємії. Циклоспорин: при одночасному застосуванні інгібіторів АПФ з циклоспорином можливий розвиток гіперкаліємії. Рекомендується контролювати вміст калію у сироватці крові. Гепарин: можливе підвищення вмісту калію у сироватці крові. Рекомендується контролювати вміст калію у сироватці крові. Одночасне застосування протипоказане Аліскірен та лікарські препарати, що містять аліскірен Одночасне застосування інгібіторів АПФ з лікарськими препаратами, що містять аліскірен, протипоказане у пацієнтів з цукровим діабетом та/або помірним або тяжким порушенням функції нирок (ШКФ менше 60 мл/хв/1,73 м(2) площі поверхні тіла) та не рекомендується у інших пацієнтів. (Див. розділ «Протипоказання»). Зростає ризик розвитку гіперкаліємії, погіршення функції нирок, серцево-судинної захворюваності та смертності. Екстракорпоральна терапія Екстракорпоральні методи лікування, що ведуть до контакту крові з негативно зарядженими поверхнями, такі як діаліз або гемофільтрація з використанням деяких високопроточних мембран (наприклад, поліакрилонітрилових), або аферез ЛПНГ з використанням декстрану сульфату, протипоказані через збільшення ризику розвитку тяжких анафілактоїд. розділ "Протипоказання"). Якщо пацієнту потрібна екстракорпоральна терапія, слід розглянути можливість використання іншого типу діалізної мембрани чи іншого класу гіпотензивних препаратів. Інгібітори нейтральної ендопептидази При одночасному застосуванні інгібіторів АПФ з лікарськими препаратами, що містять сакубітрил (інгібітор неприлізину), зростає ризик розвитку ангіоневротичного набряку, через що одночасне застосування зазначених препаратів протипоказане. Інгібітори АПФ слід призначати не раніше ніж через 36 годин після відміни препаратів, що містять сакубітрил. Протипоказано призначення препаратів, що містять сакубітрил, пацієнтам, які отримують інгібітори АПФ, а також протягом 36 годин після відміни інгібіторів АПФ. Нерекомендовані поєднання лікарських засобів Аліскірен та лікарські препарати, що містять аліскірен У пацієнтів, які не мають цукрового діабету або порушення функції нирок, можливе підвищення ризику гіперкаліємії, погіршення функції нирок та підвищення частоти серцево-судинної захворюваності та смертності. Одночасне призначення інгібіторів АПФ та АРА II За наявними літературними даними, у пацієнтів із встановленим діагнозом атеросклерозу, серцевою недостатністю або цукровим діабетом з ураженням органів-мішеней одночасний прийом інгібіторів АПФ та АРА II призводить до збільшення частоти розвитку артеріальної гіпотензії, непритомності, гіперкаліємії та погіршення функції нирок. порівняно із ситуаціями, коли застосовується лише один препарат, що впливає на РААС. Застосування подвійної блокади РААС (наприклад, одночасний прийом інгібіторів АПФ та АРА II) повинно бути обмежене поодинокими випадками із суворим контролем функції нирок, вмісту калію у плазмі крові та АТ (див. розділ «Особливі вказівки»). Естрамустін Одночасне застосування естрамустину з інгібіторами АПФ супроводжується підвищеним ризиком розвитку ангіоневротичного набряку. Ко-тримоксазол (триметоприм + сульфаметоксазол) При одночасному застосуванні з котримоксазолом (триметоприм + сульфаметоксазол) може підвищуватися ризик розвитку гіперкаліємії (див. розділ «Особливі вказівки»). Калійзберігаючі діуретики (наприклад, тріамтерен, амілорид) та солі калію Зазвичай вміст калію в плазмі залишається в межах норми, при цьому у деяких пацієнтів, які отримують інгібітори АПФ, може розвинутись гіперкаліємія. Застосування калійзберігаючих діуретиків (наприклад, спіронолактону, тріамтерену, еплеренону або амілориду), калійвмісних замінників кухонної солі, інших препаратів, що сприяють підвищенню вмісту калію в плазмі може призвести до значного збільшення вмісту калію в сироватці крові. Слід також бути обережними при одночасному призначенні периндоприлу з іншими препаратами, здатними збільшувати вміст калію в сироватці крові, такими як триметоприм і ко-тримоксазол (триметоприм + сульфаметоксазол), так як відомо, що триметоприм діє як калійзберігаючий діуретик, такий якТому одночасне застосування периндоприлу з вищезазначеними препаратами не рекомендується. Якщо, однак, одночасне застосування показано, слід застосовувати з дотриманням запобіжних заходів та регулярним контролем вмісту калію в сироватці крові. Препарати літію При одночасному застосуванні препаратів літію та інгібіторів АПФ може виникати оборотне підвищення вмісту літію у плазмі крові та пов'язані з цим токсичні ефекти (важкі нейротоксичні ефекти). Одночасне застосування периндоприлу та препаратів літію не рекомендується. За необхідності проведення такої терапії необхідний регулярний контроль вмісту літію в плазмі (див. розділ «Особливі вказівки»). Поєднання лікарських засобів, що потребують особливої уваги Гіпоглікемічні засоби (інсулін, похідні сульфонілсечовини) Згідно з даними, отриманими в епідеміологічних дослідженнях, інгібітори АПФ можуть посилювати гіпоглікемічний ефект інсуліну та похідних сульфонілсечовини з ризиком розвитку гіпоглікемії. Даний ефект найімовірніше можна спостерігати у перші тижні одночасного застосування та у пацієнтів з порушенням функції нирок. Калійнесберігаючі діуретики У пацієнтів, які отримують діуретики, особливо у пацієнтів з гіповолемією та/або зниженою концентрацією солей, на початку терапії периндоприлом може спостерігатися виражене зниження АТ, ризик розвитку якого можна зменшити шляхом відміни діуретичного засобу, заповненням втрати рідини або солей перед початком терапії периндоприлом, а також призначенням периндоприлу у низькій дозі з подальшим поступовим її збільшенням. При АГ у пацієнтів з гіповолемією або зниженим вмістом солей на фоні терапії діуретиками діуретики повинні бути або скасовані до початку застосування інгібітору АПФ (при цьому калійнесберігаючий діуретик може бути пізніше знову призначений), або інгібітор АПФ повинен бути призначений у низькій дозі з подальшим поступовим її збільшенням. . При застосуванні діуретиків у разі ХСН інгібітор АПФ повинен бути призначений у дуже низькій дозі, можливо, після зменшення дози одночасного калійнесберігаючого діуретика. У всіх випадках функція нирок (концентрація креатиніну в плазмі крові) повинна контролюватись у перші тижні застосування інгібіторів АПФ. Калійзберігаючі діуретики (застосування еплеренону, спіронолактону в дозах від 12,5 мг до 50 мг на добу та низьких доз інгібіторів АПФ) При лікуванні ХСН II-IV функціонального класу за класифікацією NYHA з фракцією викиду лівого шлуночка < 40 % у пацієнтів, які раніше отримували інгібітори АПФ та «петлеві» діуретики, існує ризик розвитку гіперкаліємії (з можливим летальним наслідком), особливо у разі недотримання рекомендацій щодо цієї комбінації. препаратів. Перед початком застосування цієї комбінації лікарських препаратів необхідно переконатися у відсутності гіперкаліємії та порушення функції нирок. Рекомендується регулярно контролювати концентрацію креатиніну та вміст калію в плазмі крові: щотижня у перший місяць лікування та щомісяця у подальшому. Рацекадотрил Повідомлялося про підвищений ризик розвитку ангіоневротичного набряку при одночасному застосуванні інгібіторів АПФ та рацекадотрилу (інгібітор енкефалінази). Тканинні активатори плазміногену В обсерваційних дослідженнях виявлено підвищену частоту розвитку ангіоневротичного набряку у пацієнтів, які приймали інгібітори АПФ після застосування алтеплази для тромболітичної терапії ішемічного інсульту. Інгібітори mTOR (наприклад, сиролімус, еверолімус, темсіролімус) У пацієнтів, які одночасно отримують терапію інгібіторами mTOR, підвищується ризик розвитку ангіоневротичного набряку (див. розділ «Особливі вказівки»). НПЗЗ, включаючи високі дози ацетилсаліцилової кислоти (≥ 3 г/добу) Одночасне застосування інгібіторів АПФ з нестероїдними протизапальними засобами (ацетилсаліцилова кислота в дозі, що має протизапальну дію, інгібітори циклооксигенази-2 [ЦОГ-2] і неселективні нестероїдні протизапальні засоби), може призвести до зниження антигіпертензивної дії інгібіторів АПФ. Одночасне застосування інгібіторів АПФ та НПЗЗ може призводити до погіршення функції нирок, включаючи розвиток гострої ниркової недостатності, та збільшення вмісту калію у сироватці крові, особливо у пацієнтів зі зниженою функцією нирок. Слід бути обережними при призначенні даної комбінації, особливо у пацієнтів похилого віку. Пацієнтам необхідно компенсувати втрату рідини та ретельно контролювати функцію нирок як на початку лікування, так і в процесі лікування. Поєднання лікарських засобів, що потребують уваги Інгібітори дипептидилпептидази IV (ДПП-IV) (гліптини), наприклад, лінагліптин, саксагліптин, сітагліптин, віллдагліптин Одночасне застосування з інгібіторами АПФ може збільшувати ризик розвитку ангіоневротичного набряку внаслідок пригнічення активності ДПП-IVгліптином. Симпатоміметики Можуть послаблювати антигіпертензивний ефект інгібіторів АПФ. Препарати золота При застосуванні інгібіторів АПФ, у тому числі периндоприлу, у пацієнтів, які отримують внутрішньовенно препарат золота (натрію ауротіомалат), були описані нітритоїдні реакції, з частотою виникнення «рідко» (симптомокомплекс, що включає гіперемію шкіри обличчя, нудоту, блювання, артеріальну гіпотензію). Алопуринол, імуносупресивні засоби, кортикостероїди (при системному застосуванні) та прокаїнамід Одночасне застосування з інгібіторами AПФ може супроводжуватися підвищеним ризиком розвитку лейкопенії, особливо у пацієнтів із наявними порушеннями функції нирок. Засоби для загальної анестезії Одночасне застосування інгібіторів АПФ та засобів для загальної анестезії може призводити до антигіпертензивного ефекту. Поєднання лікарських засобів, що потребують особливої уваги Баклофен Можливе посилення антигіпертензивної дії. Слід контролювати АТ та функцію нирок, за необхідності провести корекцію дози амлодипіну. Поєднання препаратів, що потребує уваги Гіпотензивні засоби (наприклад, бета-адреноблокатори) та вазодилататори Можливе посилення антигіпертензивного ефекту периндоприлу та амлодипіну. Слід бути обережними при одночасному застосуванні з нітрогліцерином, іншими нітратами або іншими вазодилататорами, оскільки при цьому можливе додаткове зниження АТ. Кортикостероїди (мінерало- та глюкокортикостероїди), тетракозактид Зниження антигіпертензивної дії (затримка рідини та іонів натрію внаслідок дії кортикостероїдів). Альфа-адреноблокатори (празозин, альфузозин, доксазозин, тамсулозин, теразозин) Посилення антигіпертензивної дії та підвищення ризику розвитку ортостатичної гіпотензії. Аміфостін Можливе посилення антигіпертензивного ефекту амлодипіну. Трициклічні антидепресанти/нейролептики/засоби для загальної анестезії Посилення антигіпертензивної дії та підвищення ризику розвитку ортостатичної гіпотензії.Спосіб застосування та дозиВсередину, по одній таблетці 1 раз на день, переважно вранці перед їдою. Доза лікарського препарату Дальнева® підбирається після раніше проведеного підбору доз окремих компонентів препарату: периндоприлу та амлодипіну у пацієнтів з артеріальною гіпертензією та стабільною стенокардією. При терапевтичній необхідності доза лікарського препарату Дальнева® може бути змінена на підставі індивідуального підбору доз окремих компонентів: амлодипін 5 мг + периндоприл 4 мг або амлодипін 10 мг + периндоприл 4 мг, або амлодипін 5 мг + периндоприл 8 мг, або амлодипін 10 мг . Максимальна добова доза: амлодипін – 10 мг + периндоприл – 8 мг.ПередозуванняІнформація про передозування препаратом Дальнева відсутня. Амлодипін Інформація про передозування амлодипіном обмежена. Симптоми: виражене зниження АТ з можливим розвитком рефлекторної тахікардії та надмірної периферичної вазодилатації (ризик розвитку вираженої та стійкої артеріальної гіпотензії, у т.ч. з розвитком шоку та летального результату). Лікування: промивання шлунка, призначення активованого вугілля (особливо в перші 2 години після передозування), підтримання функції серцево-судинної системи, підвищене положення нижніх кінцівок, контроль ОЦК та діурезу, симптоматична та підтримуюча терапія. Для відновлення тонусу судин – застосування судинозвужувальних засобів (за відсутності протипоказань до їх застосування), для усунення наслідків блокади кальцієвих каналів – внутрішньовенне введення розчину глюконату. Гемодіаліз неефективний. Периндоприл Дані передозування периндоприлом обмежені. Симптоми: виражене зниження артеріального тиску, шок, порушення водно-електролітного балансу, ниркова недостатність, гіпервентиляція легень, тахікардія, відчуття серцебиття, брадикардія, запаморочення, неспокій та кашель. Лікування: заходи невідкладної допомоги зводяться до виведення препарату з організму: промивання шлунка та/або призначення активованого вугілля з подальшим відновленням ОЦК. При вираженому зниженні артеріального тиску слід перевести пацієнта в положення «лежачи» на спині з піднятими ногами, за необхідності провести заходи для відновлення ОЦК (наприклад, внутрішньовенна інфузія 0,9 % розчину натрію хлориду). Також можливе внутрішньовенне введення катехоламінів. За допомогою гемодіалізу можна видалити периндоприл із системного кровотоку. При брадикардії, резистентної до терапії, може знадобитися імплантація електрокардіостимулятора. Необхідний динамічний контроль загального стану, концентрації креатиніну та вмісту електролітів у плазмі крові.Запобіжні заходи та особливі вказівкиОсобливі вказівки, що стосуються периндоприлу та амлодипіну, застосовні і до лікарського препарату Дальнєва®. Амлодипін Ефективність та безпека застосування амлодипіну при гіпертонічному кризі не встановлено. Серцева недостатність Лікування пацієнтів із серцевою недостатністю слід проводити з обережністю. При застосуванні амлодипіну у пацієнтів з ХСН III та IV функціонального класу за класифікацією NYHA можливий розвиток набряку легень. БМКК, включаючи амлодипін, необхідно з обережністю застосовувати у пацієнтів з ХСН у зв'язку з можливим збільшенням ризику розвитку небажаних явищ з боку серцево-судинної системи та смертності. Печінкова недостатність У пацієнтів з порушенням функції печінки Т(½) та AUCамлодипіну збільшуються. Рекомендації щодо дозування препарату не встановлені. Прийом амлодипіну необхідно почати з найнижчих доз і дотримуватися запобіжних заходів як на початку лікування, так і при збільшенні дози. Пацієнтам з тяжкою печінковою недостатністю підвищувати дозу слід поступово, забезпечуючи ретельний моніторинг клінічного стану. Пацієнти похилого віку У пацієнтів похилого віку збільшення дози слід проводити з обережністю (див. розділ «Спосіб застосування та дози» та «Фармакологічні властивості. Фармакокінетика»). Ниркова недостатність Пацієнти з нирковою недостатністю можуть приймати амлодипін у стандартних дозах. Зміни плазмових концентрацій амлодипіну не корелюють зі ступенем ниркової недостатності. Амлодипін не виводиться з організму за допомогою діалізу. Мітральний стеноз/аортальний стеноз/ГЗКМП Амлодипін протипоказаний пацієнтам із обструкцією вихідного тракту лівого шлуночка. Синдром «скасування» Незважаючи на відсутність у БМКК синдрому «скасування», припинення лікування препаратом Дальнєва бажано проводити поступово, зменшуючи дозу препарату. Амлодипін не запобігає розвитку синдрому «скасування» при різкому припиненні прийому бета-адреноблокаторів. Периферичні набряки Незначно або помірно виражені периферичні набряки були найчастішим небажаним явищем амлодипіну у клінічних дослідженнях. Частота виникнення периферичних набряків зростає зі збільшенням дози (при застосуванні амлодипіну у дозі 2,5 мг, 5 мг та 10 мг на добу набряки виникали відповідно у 1,8 %, 3 % та 10 % пацієнтів). Слід ретельно диференціювати периферичні набряки, пов'язані із застосуванням амлодипіну, від симптомів прогресування лівшлуночкової серцевої недостатності. Інше Необхідна підтримка гігієни зубів та спостереження у стоматолога (для запобігання болючості, кровоточивості та гіперплазії ясен). Периндоприл Підвищена чутливість/ангіоневротичний набряк (набряк Квінке) При застосуванні інгібіторів АПФ, у тому числі периндоприлу, в окремих випадках може спостерігатися розвиток ангіоневротичного набряку особи, губ, язика, голосових складок та/або гортані. Це може статися у будь-який період. При появі цих симптомів застосування препарату Дальнева® повинно бути негайно припинено, пацієнт повинен спостерігатися доти, доки ознаки набряку не зникнуть повністю. препарати. Ангіоневротичний набряк, що супроводжується набряком язика або гортані, може призвести до обструкції дихальних шляхів та летального результату.5 мл) та/або забезпечити прохідність дихальних шляхів. Пацієнт повинен перебувати під медичним наглядом до повного та стійкого зникнення симптомів. У пацієнтів, в анамнезі яких відзначався набряк Квінке, не пов'язаний із застосуванням інгібіторів АПФ, може бути підвищений ризик його розвитку на фоні застосування препаратів цієї групи (див. розділ "Протипоказання"). У поодиноких випадках на тлі терапії інгібіторами АПФ розвивається інтестинальний ангіоневротичний набряк (ангіоневротичний набряк кишечника). При цьому у пацієнтів відзначається біль у животі як ізольований симптом або у поєднанні з нудотою та блюванням, у деяких випадках без попереднього ангіоневротичного набряку обличчя та при нормальній сироватковій концентрації С1-естерази. Діагноз встановлюється за допомогою комп'ютерної томографії черевної порожнини, ультразвукового дослідження або на момент хірургічного втручання. Симптоми зникають після припинення інгібіторів АПФ. Тому у пацієнтів з болем у животі, які отримують інгібітори АПФ, при проведенні диференціального діагнозу необхідно враховувати можливість розвитку інтестинального ангіоневротичного набряку (див. розділ «Побічна дія»). При одночасному застосуванні інгібіторів АПФ з рацекадотрилом, інгібіторами mTOR (наприклад, темсиролімусом, еверолімусом, сиролімусом) або ДПП-IV (гліптинами, включаючи віллдагліптин) підвищується ризик розвитку ангіоневротичного набряку (наприклад, набряк верхніх дихальних шляхів). ) (див. розділ «Взаємодія з іншими лікарськими засобами»). Слід виявляти обережність на початку терапії рацекадотрилом, інгібіторами mTOR (наприклад, тимсиролімусом, еверолімусом, сиролімусом) або гліптинами, включаючи віллдагліптин, при одночасному застосуванні з інгібіторами АПФ. Анафілактоїдні реакції при проведенні процедур десенсибілізації Є окремі повідомлення про розвиток тривалих, що загрожують життю анафілактоїдних реакцій у пацієнтів, які отримують інгібітори АПФ під час десенсибілізуючої терапії отрутою перетинчастокрилих комах. У цих пацієнтів анафілактоїдної реакції вдавалося уникнути шляхом тимчасової відміни інгібіторів АПФ, а при випадковому прийомі препарату анафілактоїдна реакція виникала знову. Анафілактоїдні реакції при проведенні аферезу ЛПНЩ за допомогою декстрану сульфату У поодиноких випадках у пацієнтів, які отримують інгібітори АПФ, при проведенні аферезу ЛПНЩ з використанням декстрану сульфату можуть розвиватися анафілактоїдні реакції, що загрожують життю. Для запобігання анафілактоїдної реакції слід тимчасово припинити терапію інгібітором АПФ перед кожною процедурою аферезу ЛПНЩ з використанням декстрану сульфату. Нейтропенія/агранулоцитоз, тромбоцитопенія та анемія У пацієнтів, які приймають інгібітори АПФ, можливі випадки розвитку нейтропенії/агранулоцитозу, тромбоцитопенії та анемії. У пацієнтів з нормальною функцією нирок без інших обтяжливих факторів нейтропенія розвивається рідко. Особливою обережністю периндоприл слід застосовувати у пацієнтів із системними захворюваннями сполучної тканини, на фоні прийому імунодепресантів, алопуринолу або прокаїнаміду, особливо у пацієнтів з порушеною функцією нирок. У деяких пацієнтів виникали важкі інфекції, у ряді випадків стійкі до інтенсивної антибіотикотерапії. При призначенні периндоприлу таким пацієнтам рекомендується періодично контролювати кількість лейкоцитів у крові. Пацієнти повинні повідомляти лікаря про будь-які ознаки інфекційних захворювань (наприклад, біль у горлі, гарячка). Реноваскулярна гіпертензія У пацієнтів із двостороннім стенозом ниркових артерій або стенозом артерії єдиної функціонуючої нирки на фоні терапії інгібіторами АПФ зростає ризик розвитку артеріальної гіпотензії та ниркової недостатності. Прийом діуретиків може бути додатковим фактором ризику. Погіршення функції нирок може спостерігатися вже при незначній зміні концентрації креатиніну у сироватці, навіть у пацієнтів з одностороннім стенозом ниркової артерії. Подвійна блокада РААС Є дані, що свідчать про те, що одночасне застосування інгібіторів АПФ, АРА II або аліскірену підвищує ризик розвитку гіпотензії, гіперкаліємії та порушення функції нирок (включаючи гостру ниркову недостатність). Одночасне застосування інгібіторів АПФ з препаратами, що містять аліскірен, протипоказане у пацієнтів з цукровим діабетом та/або помірною або тяжкою нирковою недостатністю (ШКФ менше 60 мл/хв/1,73 м(2) площі поверхні тіла) та не рекомендується у інших пацієнтів. Якщо терапія за допомогою подвійної блокади РААС визнана абсолютно необхідною, її слід проводити лише під суворим медичним контролем та при регулярному контролі функції нирок, вмісту електролітів у плазмі крові та АТ.Протипоказане застосування інгібіторів АПФ одночасно з АРА II у пацієнтів з діабетичною нефропатією та не рекомендується у інших пацієнтів (див. розділ "Протипоказання"). Первинний гіперальдостеронізм Пацієнти з первинним гіперальдостеронізмом, як правило, не сприйнятливі до гіпотензивних препаратів, дія яких ґрунтується на інгібуванні РААС. Тому прийом препарату не рекомендовано. Артеріальна гіпотензія Інгібітори АПФ можуть викликати різке зниження артеріального тиску. Симптоматична гіпотензія рідко розвивається у пацієнтів без супутніх захворювань. Ризик вираженого зниження АТ підвищений у пацієнтів зі зниженим ОЦК, що може відзначатися на фоні терапії діуретиками, при дотриманні суворої дієти без солі, гемодіалізі, діареї та блюванні, а також у пацієнтів з тяжким ступенем АГ з високою активністю реніну (див. розділи «Взаємодія з іншими лікарськими засобами» та «Побічна дія»). У пацієнтів з підвищеним ризиком розвитку симптоматичної артеріальної гіпотензії необхідно ретельно контролювати АТ, функцію нирок та вміст калію у сироватці крові під час терапії лікарським препаратом Дальнєва®. Подібний підхід застосовується і у пацієнтів зі стенокардією та цереброваскулярними захворюваннями, у яких виражена артеріальна гіпотензія може призвести до інфаркту міокарда або порушення мозкового кровообігу. У разі розвитку артеріальної гіпотензії пацієнт повинен бути переведений у положення «лежачи» на спині з піднятими ногами. При необхідності слід заповнити ОЦК за допомогою внутрішньовенного введення 0,9% натрію розчину хлориду. Минуща артеріальна гіпотензія не є перешкодою для подальшого прийому препарату. Після відновлення ОЦК та АТ лікування може бути продовжено. Мітральний стеноз/аортальний стеноз/ГЗКМП Периндоприл, як і інші інгібітори АПФ, повинен обережно призначатися у пацієнтів з обструкцією вихідного тракту лівого шлуночка (аортальний стеноз, ГОКМП), а також у пацієнтів з мітральним стенозом. Амлодипін протипоказаний пацієнтам із обструкцією вихідного тракту лівого шлуночка. Порушення функції нирок Пацієнтам з нирковою недостатністю (КК менше 60 мл/хв) рекомендується індивідуальний підбір доз периндоприлу та амлодипіну (див. розділ «Спосіб застосування та дози»). Таким пацієнтам необхідний регулярний контроль вмісту калію та концентрації креатиніну у сироватці крові (див. розділ «Побічна дія»). У пацієнтів із двостороннім стенозом ниркової артерії або стенозом артерії єдиної нирки на фоні терапії інгібіторами АПФ можливе підвищення концентрацій сечовини та креатиніну у сироватці крові, що зазвичай відбувається при відміні терапії. Найчастіше цей ефект відзначається у пацієнтів із нирковою недостатністю. Додаткова наявність реноваскулярної гіпертензії зумовлює підвищений ризик розвитку тяжкої гіпотензії та ниркової недостатності у таких пацієнтів. У деяких пацієнтів з артеріальною гіпертензією без ознак ураження судин нирок можливе підвищення концентрацій сечовини та креатиніну в сироватці крові, особливо при одночасному призначенні периндоприлу з діуретиком, зазвичай незначне та минуще. Найчастіше цей ефект відзначається у пацієнтів із попереднім порушенням функції нирок. Порушення функції печінки У поодиноких випадках на фоні прийому інгібіторів АПФ виникає холестатична жовтяниця. При прогресуванні цього синдрому розвивається фульмінантний некроз печінки, іноді з летальним кінцем. Механізм розвитку цього синдрому незрозумілий. У разі появи жовтяниці або значного підвищення активності «печінкових» ферментів у плазмі крові на фоні прийому інгібіторів АПФ слід припинити прийом препарату (див. розділ «Побічна дія») та звернутися до лікаря. Етнічні відмінності У пацієнтів негроїдної раси частіше, ніж у інших рас, на фоні застосування інгібіторів АПФ розвивається ангіоневротичний набряк. Периндоприл, як і інші інгібітори АПФ, може мати менш виражену антигіпертензивну дію у пацієнтів негроїдної раси порівняно з представниками інших рас. Можливо, ця відмінність зумовлена тим, що у пацієнтів негроїдної раси з артеріальною гіпертензією частіше відзначається низька активність реніну плазми крові. Кашель На тлі терапії інгібітором АПФ може виникати сухий кашель. Кашель тривалий час зберігається на фоні прийому препаратів цієї групи і зникає після їх відміни. Це слід враховувати під час проведення диференціальної діагностики кашлю. Хірургічні втручання/загальна анестезія У пацієнтів, яким планується проведення великого оперативного втручання та/або застосування засобів для загальної анестезії, що викликають гіпотензію, застосування периндоприлу може блокувати утворення ангіотензину II на тлі компенсаторного вивільнення реніну. Лікування слід припинити за добу до хірургічного втручання. При розвитку артеріальної гіпотензії за вказаним механізмом слід підтримувати артеріальний тиск шляхом заповнення ОЦК. Гіперкаліємія Інгібітори АПФ можуть викликати гіперкаліємію, оскільки вони пригнічують вивільнення альдостерону. Цей ефект зазвичай незначний у пацієнтів із нормальною функцією нирок. Однак у пацієнтів з порушенням функції нирок та/або у пацієнтів, які одночасно приймають препарати, що містять калій (включаючи калійвмісні замінники кухонної солі), калійзберігаючі діуретики, триметоприм або ко-тримоксазол (фіксована комбінація триметоприму і сульфаметоксазолу), і особливо антагон можливий розвиток гіперкаліємії. Факторами ризику гіперкаліємії є ниркова недостатність, порушення функції нирок, вік старше 70 років, цукровий діабет, інтеркурентні стани (зокрема, дегідратація, гостра декомпенсація ХСН, метаболічний ацидоз), одночасне застосування калійзберігаючих діуретиків (наприклад,спіронолактон, еплеренон, тріамтерен або амілорид), препаратів калію або замінників калію кухонної солі або одночасне застосування інших препаратів, що сприяють підвищенню вмісту калію в плазмі крові (наприклад, гепарин, ко-тримоксазол). Гіперкаліємія може призвести до серйозних порушень серцевого ритму, іноді з летальним кінцем. Калійзберігаючі діуретики та АРА II слід застосовувати з обережністю у пацієнтів, які отримують інгібітори АПФ, та регулярно контролювати вміст калію у сироватці крові та функцію нирок (див. розділ «Взаємодія з іншими лікарськими засобами»).ко-тримоксазол). Гіперкаліємія може призвести до серйозних порушень серцевого ритму, іноді з летальним кінцем. Калійзберігаючі діуретики та АРА II слід застосовувати з обережністю у пацієнтів, які отримують інгібітори АПФ, та регулярно контролювати вміст калію у сироватці крові та функцію нирок (див. розділ «Взаємодія з іншими лікарськими засобами»).ко-тримоксазол). Гіперкаліємія може призвести до серйозних порушень серцевого ритму, іноді з летальним кінцем. Калійзберігаючі діуретики та АРА II слід застосовувати з обережністю у пацієнтів, які отримують інгібітори АПФ, та регулярно контролювати вміст калію у сироватці крові та функцію нирок (див. розділ «Взаємодія з іншими лікарськими засобами»). Пацієнти з цукровим діабетом При призначенні препарату пацієнтам з цукровим діабетом, які отримують гіпоглікемічні засоби для внутрішнього застосування або інсуліну, протягом першого місяця терапії необхідно ретельно контролювати концентрацію глюкози в крові (див. розділ «Взаємодія з іншими лікарськими засобами») Застосування препарату Дальнева у пацієнтів з гострим інфарктом міокарда не рекомендується через недостатній досвід клінічного застосування. Застосування при хронічних захворюваннях: Пацієнти з порушенням функції нирок Лікарський препарат Дальнєва може застосовуватися у пацієнтів з КК рівним або більше 60 мл/хв. Лікарський препарат Дальнєва протипоказаний до застосування у пацієнтів з КК менше 60 мл/хв. Таким пацієнтам рекомендується індивідуальний підбір доз периндоприлу та амлодипіну. Зміна концентрації амлодипіну в плазмі не корелює зі ступенем вираженості ниркової недостатності. Пацієнти похилого віку та пацієнти з порушенням функції печінки Необхідно зменшити початкову дозу препарату Дальнєва до найменшої дози амлодипіну (тобто до 1 таблетки амлодипін 5 мг + периндоприл 4 мг або амлодипін 5 мг + периндоприл 8 мг). Вплив на керування транспортними засобами: У зв'язку з можливістю виникнення запаморочення, сонливості та інших побічних ефектів на фоні застосування препарату Дальнева® необхідно дотримуватись обережності при керуванні транспортними засобами та роботі з іншими технічними пристроями, що потребують підвищеної концентрації уваги та швидкості психомоторних реакцій, особливо на початку лікування та збільшення дози.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаамлодипін + периндоприл таблетки на 1 таблетку 5 мг + 4 мг/10 мг + 4 мг/5 мг + 8 мг/10 мг + 8 мг речовини, що діють: Амлодипін безілат (амлодипін безілат) 6,935 мг/13,870 мг/6,935 мг/13,870 мг, еквівалентно амлодипіну 5 мг/10 мг/5 мг/10 мг Периндоприлу ербумін А субстанція – гранули 21,000 мг/21,000 мг/42,000 мг/42,000 мг, містить периндоприлу ербуміну 4 мг/4 мг/8 мг/8 мг Допоміжні речовини: Целюлоза мікрокристалічна, крохмаль прежелатинізований, карбоксиметилкрохмаль натрію, гідрокарбонат натрію, кремнію діоксид колоїдний, магнію стеаратОпис лікарської формиТаблетки 5 мг + 4 мг: Круглі, злегка двоопуклі таблетки з фаскою, від білого до майже білого кольору. Таблетки 10 мг + 4 мг: Капсулоподібні, двоопуклі таблетки з ризиком на одній стороні, від білого до майже білого кольору. Таблетки 5 мг + 8 мг: Круглі, двоопуклі таблетки з фаскою, від білого до майже білого кольору. Таблетки 10 мг + 8 мг: Круглі, двоопуклі таблетки з фаскою, з ризиком на одній стороні, від білого майже білого кольору.Фармакотерапевтична групагіпотензивний комбінований засіб (інгібітор ангіотензинперетворюючого ферменту [АПФ] + блокатор «повільних» кальцієвих каналів [БМКК])ФармакокінетикаВеличина абсорбції амлодипіну та периндоприлу при застосуванні комбінованого лікарського препарату Дальнева® суттєво не відрізняється від такої при застосуванні їх як монопрепарати. Амлодипін Після прийому внутрішньо амлодипін повільно абсорбується із шлунково-кишкового тракту (ЖКТ). Прийом їжі не впливає на біодоступність амлодипіну. Максимальна концентрація (Сmax) амлодипіну в плазмі досягається через 6-12 годин після прийому препарату внутрішньо. Абсолютна біодоступність становить 64-80%. Об'єм розподілу – приблизно 21 л/кг. У дослідженнях in vitro було показано, що близько 97,5% циркулюючого амлодипіну пов'язано з білками плазми. Кінцевий період напіввиведення (Т½) із плазми становить 35-50 годин, що дозволяє приймати препарат 1 раз на добу. Амлодипін метаболізується у печінці з утворенням неактивних метаболітів, при цьому 10% прийнятої дози амлодипіну виводиться у незміненому вигляді та 60% нирками – у вигляді метаболітів. Амлодипін не виводиться з організму за допомогою діалізу. Час досягнення Сmax(ТСmax) амлодипіну в плазмі крові не відрізняється у пацієнтів похилого віку та молодшого віку. У пацієнтів похилого віку відзначається уповільнення кліренсу амлодипіну, що призводить до збільшення площі під кривою «концентрація-час» (AUC). Збільшення AUC та Т½ у пацієнтів з ХСН відповідає передбачуваній величині для цієї вікової групи. У пацієнтів з порушенням функції нирок зміни концентрації амлодипіну в плазмі не корелюють зі ступенем ниркової недостатності. Можливе незначне подовження Т½. Дані щодо застосування амлодипіну пацієнтами з печінковою недостатністю обмежені. У пацієнтів з печінковою недостатністю спостерігається зниження кліренсу амлодипіну, що призводить до подовження Т½ та збільшення AUC приблизно на 40-60%. Периндоприл Після прийому периндоприл швидко всмоктується і досягає Сmaxв плазмі протягом 1 години. Т½ периндоприлу з плазми становить приблизно 1 годину. Периндоприл не має фармакологічної активності, є проліками. Приблизно 27% від загальної кількості, прийнятої внутрішньо периндоприлу, потрапляє в кровообіг у вигляді активного метаболіту – периндоприлату. Крім периндоприлату утворюються ще 5 метаболітів, які не мають фармакологічної активності. Сmax у плазмі крові досягається через 3-4 години після прийому внутрішньо. Прийом їжі зменшує біодоступність периндоприлу, тому препарат слід приймати 1 раз на добу, вранці, перед їдою. Існує лінійна залежність концентрації периндоприлу в плазмі від величини прийнятої всередину дози. Об'єм розподілу вільного периндоприлату становить приблизно 0,2 л/кг. Зв'язок периндоприлату з білками плазми (переважно з АПФ) становить 20% і залежить від його концентрації. Периндоприлат виводиться нирками, Т½ незв'язаної фракції становить приблизно 17 годин, тому рівноважний стан досягається протягом 4-х діб після прийому внутрішньо. Виведення периндоприлату сповільнене у пацієнтів похилого віку, а також у пацієнтів із серцевою та нирковою недостатністю (див. розділ «Спосіб застосування та дози»), тому спостереження за такими пацієнтами повинно включати регулярний контроль концентрації креатиніну та вмісту калію в плазмі крові. Діалізний кліренс периндоприлату становить 70 мл/хв. Фармакокінетика периндоприлу порушена у пацієнтів із цирозом печінки: його печінковий кліренс зменшується у 2 рази. Тим не менш, кількість периндоприлату, що утворюється, не зменшується, тому не потрібно корекції дози (див. розділи «Спосіб застосування та дози» та «Особливі вказівки»).ФармакодинамікаАмлодипін Амлодипін – БМКК, похідне дигідропіридину. Амлодипін пригнічує трансмембранний перехід іонів кальцію в кардіоміоцити та гладком'язові клітини судинної стінки. Антигіпертензивна дія амлодипіну обумовлена прямим розслаблюючим впливом на гладком'язові клітини судинної стінки. Детальний механізм, за допомогою якого амлодипін здійснює антиангінальну дію, не цілком встановлений, але відомо, що амлодипін зменшує загальне ішемічне навантаження за допомогою двох дій: викликає розширення периферичних артеріол, зменшуючи загальний периферичний судинний опір (ОПСС) (постнавантаження). Оскільки частота серцевих скорочень (ЧСС) у своїй не змінюється, потреба міокарда в кисні знижується; викликає розширення коронарних артерій та артеріол як у ішемізованій, так і в інтактній зонах. Їх дилатація збільшує надходження кисню до міокарда у пацієнтів з вазоспастичною стенокардією (стенокардія Принцметала або варіантна стенокардія). У пацієнтів з артеріальною гіпертензією (АГ) прийом амлодипіну 1 раз на добу забезпечує клінічно значуще зниження артеріального тиску (АТ) у положенні стоячи і лежачи протягом 24 годин. Антигіпертензивна дія розвивається повільно, у зв'язку з чим розвиток гострої гіпотензії нехарактерний. У пацієнтів зі стенокардією прийом амлодипіну 1 раз на добу збільшує загальний час фізичного навантаження, збільшує час до розвитку нападу стенокардії та до появи депресії сегмента ST на 1 мм, а також знижує частоту нападів стенокардії та споживання нітрогліцерину під язик. Амлодипін не чинить несприятливих метаболічних ефектів і не впливає на концентрацію ліпідів плазми. Препарат може застосовуватися у пацієнтів із супутньою бронхіальною астмою, цукровим діабетом та подагрою. Ішемічна хвороба серця (ІХС) Результати оцінки ефективності свідчать про те, що прийом амлодипіну характеризується меншою кількістю випадків госпіталізації щодо стенокардії та проведення процедур реваскуляризації у пацієнтів з ІХС. Периндоприл Периндоприл – інгібітор ферменту, що перетворює ангіотензин I на ангіотензин II. АПФ, або кініназа II, є екзопептидазою, яка здійснює як перетворення ангіотензину I на судинозвужувальну речовину ангіотензин II, так і розпад брадикініну, що має судинорозширювальну дію, до неактивного гептапептиду. Оскільки АПФ інактивує брадикінін, пригнічення АПФ супроводжується підвищенням активності як циркулюючої, так і тканинної калікреїн-кінінової системи, при цьому також активується система простагландинів. Периндоприл має терапевтичну дію завдяки активному метаболіту, периндоприлату. Інші метаболіти не мають інгібуючої дії на АПФ в умовах in vitro. Артеріальна гіпертензія Периндоприл є препаратом для лікування артеріальної гіпертензії будь-якого ступеня тяжкості. На тлі його застосування відзначається зниження як систолічного, так і діастолічного АТ у положенні «лежачи» та «стоячи». Периндоприл зменшує ОПСС, що призводить до зниження артеріального тиску та поліпшення периферичного кровотоку без зміни ЧСС. Як правило, прийом периндоприлу збільшує нирковий кровообіг, швидкість клубочкової фільтрації (СКФ) при цьому не змінюється. Антигіпертензивна дія препарату досягає максимуму через 4-6 годин після одноразового прийому внутрішньо та зберігається протягом 24 годин. Антигіпертензивна дія через 24 години після одноразового застосування внутрішньо становить близько 87-100% від максимального антигіпертензивного ефекту. Зниження АТ досягається досить швидко. Терапевтичний ефект настає через 1 місяць від початку терапії і не супроводжується тахіфілаксією. Припинення лікування не викликає ефекту "рикошету". Периндоприл має судинорозширювальну дію, сприяє відновленню еластичності великих артерій та структури судинної стінки дрібних артерій, а також зменшує гіпертрофію лівого шлуночка. Стабільна ІХС Ефективність застосування периндоприлу у пацієнтів (12218 пацієнтів віком від 18 років) зі стабільною ІХС без клінічних симптомів хронічної серцевої недостатності (ХСН) вивчалась у ході 4-річного дослідження. 90% учасників дослідження раніше перенесли гострий інфаркт міокарда та/або процедуру реваскуляризації. Більшість пацієнтів отримували крім досліджуваного препарату стандартну терапію, включаючи антиагреганти, гіполіпідемічні засоби та бета-адреноблокатори. Як основний критерій ефективності була обрана комбінована кінцева точка, що включає серцево-судинну смертність, нефатальний інфаркт міокарда та/або зупинку серця з успішною реанімацією. Терапія периндоприлом третбутиламіном у дозі 8 мг/добу 1 раз на день (еквівалентно 10 мг периндоприлу аргініну) призводила до суттєвого зниження абсолютного ризику щодо комбінованої кінцевої точки на 1,9 % у пацієнтів, які раніше перенесли інфаркт міокарда та/або процедуру реваскуляру. абсолютного ризику становило 2,2% порівняно з групою плацебо. Подвійна блокада ренін-ангіотензин-альдостеронової системи (РААС) Є дані клінічних досліджень комбінованої терапії із застосуванням інгібітору АПФ та антагоніста рецептора ангіотензину II (АРА II). Протипоказано застосування інгібіторів АПФ у поєднанні з АРА II у пацієнтів з діабетичною нефропатією. Є дані клінічного дослідження з вивчення позитивного впливу від додавання аліскірену до стандартної терапії інгібітором АПФ або АРА II у пацієнтів з цукровим діабетом 2 типу та/або хронічним захворюванням нирок, або кардіоваскулярним захворюванням, які мають поєднання цих захворювань. Дослідження було припинено достроково у зв'язку з зростанням ризику виникнення несприятливих результатів. Кардіоваскулярна смерть та інсульт відзначалися частіше у групі пацієнтів, які отримують аліскірен, порівняно з групою плацебо; також небажані явища та серйозні небажані явища особливого інтересу (гіперкаліємія, артеріальна гіпотензія та порушення функції нирок) реєструвалися частіше у групі аліскірену, ніж у групі плацебо. Амлодипін + периндоприл Ефективність при тривалому застосуванні амлодипіну в комбінації з периндоприлом і атенололу в комбінації з бендрофлуметіазидом у пацієнтів віком від 40 до 79 років з АГ та, щонайменше, з трьома з перелічених додаткових факторів ризику: гіпертрофія лівого шлуночка діабет 2 типу, атеросклероз периферичних артерій, раніше перенесений інсульт або транзиторна ішемічна атака, чоловіча стать, вік 55 років і старше, мікроальбумінурія або протеїнурія, куріння, загальний холестерин/холестерин ліпопротеїдів високої щільності ≥ 6, ранній розвиток ASCOT-BPLA. Основний критерій оцінки ефективності – комбінований показник частоти нефатального інфаркту міокарда (у тому числі безболевого) та летальних наслідків ІХС. Частота ускладнень, передбачених основним критерієм оцінки, у групі амлодипін/периндоприл була на 10% нижчою, ніж у групі атенолол/бендрофлуметіазид, проте ця відмінність не була статистично достовірною. У групі амлодипін/периндоприл відзначалося достовірне зниження частоти ускладнень, передбачених додатковими критеріями ефективності (крім фатальної та нефатальної серцевої недостатності).Показання до застосуванняАртеріальна гіпертензія та/або ішемічна хвороба серця: стабільна стенокардія напруги у пацієнтів, яким потрібна терапія периндоприлом та амлодипіном.Протипоказання до застосуванняПідвищена чутливість до периндоприлу або інших інгібіторів АПФ, амлодипіну та інших похідних дигідропіридину, а також допоміжних речовин, що входять до складу препарату. Ангіоневротичний набряк (набряк Квінке) в анамнезі (у тому числі на фоні прийому інших інгібіторів АПФ). Спадковий/ідіопатичний ангіоневротичний набряк. Одночасне застосування з аліскіреном та лікарськими препаратами, що містять аліскірен, у пацієнтів з цукровим діабетом та/або помірними або тяжкими порушеннями функції нирок (ШКФ < 60 мл/хв/1,73 м2 площі поверхні тіла) (див. розділи «Взаємодія з іншими лікарськими засобами) засобами" і "Фармакологічні властивості. Фармакодинаміка"). Одночасне застосування з АРА II у пацієнтів з діабетичною нефропатією (див. розділ «Особливі вказівки»). Одночасне застосування з інгібіторами нейтральної ендопептидази (наприклад, з препаратами, що містять сакубітрил) через високий ризик розвитку ангіоневротичного набряку. Екстракорпоральна терапія, що веде до контакту крові з негативно зарядженими поверхнями (див. розділ "Взаємодія з іншими лікарськими засобами"). Виражений двосторонній стеноз ниркових артерій або стеноз артерії єдиної нирки, що функціонує (див. розділ «Особливі вказівки»). Тяжка артеріальна гіпотензія (систолічний артеріальний тиск менше 90 мм рт. ст.). Шок (включно з кардіогенним). Обструкція вихідного тракту лівого шлуночка (наприклад, клінічно суттєвий стеноз аорти). Гемодинамічно нестабільна серцева недостатність після гострого інфаркту міокарда. Ниркова недостатність (кліренс креатиніну менше 60 мл/хв). Вагітність та період грудного вигодовування. Вік до 18 років (ефективність та безпека не встановлені). Стеноз ниркової артерії (у тому числі двосторонній), єдина функціонуюча нирка, печінкова недостатність, ниркова недостатність, системні захворювання сполучної тканини (у тому числі системний червоний вовчак, склеродермія), терапія імунодепресантами, алопуринолом, прокаїнамоз об'єм циркулюючої крові (ОЦК) (прийом діуретиків, безсольова дієта, блювання, діарея), атеросклероз, цереброваскулярні захворювання, ІХС з тяжким обструктивним ураженням коронарних артерій, гострий інфаркт міокарда (і період протягом 1 місяця після нього), нестабільна синусового вузла (виражена тахікардія, брадикардія), реноваскулярна гіпертензія, цукровий діабет, первинний гіперальдостеронізм, ХСН, одночасне застосування інгібіторів або індукторів ізоферменту CYP3A4,дантролену, естрамустину, калійзберігаючих діуретиків, препаратів калію, калійвмісних замінників харчової солі, препаратів літію, кларитроміцину, такролімусу, циклоспорину, гіперкаліємії, хірургічного втручання/загальна анестезія, пацієнтів похилого віку. гемодіалізу з використанням високопроточних мембран (наприклад, AN69®), десенсибілізуюча терапія, аферез ліпопротеїнів низької щільності (ЛПНЩ), аортальний стеноз/мітральний стеноз/гіпертрофічна обструктивна кардіоміопатія (ГОКМП), застосування у пацієнтів негроїдної раси NYHA класифікації.калійвмісних замінників харчової солі, препаратів літію, кларитроміцину, такролімусу, циклоспорину, гіперкаліємію, хірургічне втручання/загальна анестезія, пацієнти похилого віку, пригнічення кістковомозкового кровотворення, обтяжений алергологічний анамнез або ангіо ), десенсибілізуюча терапія, аферез ліпопротеїнів низької щільності (ЛПНГ), аортальний стеноз/мітральний стеноз/гіпертрофічна обструктивна кардіоміопатія (ГЗКМП), застосування у пацієнтів негроїдної раси, ХСН неішемічної етіології ІІІ-ІVфункціонального класу за клас.калійвмісних замінників харчової солі, препаратів літію, кларитроміцину, такролімусу, циклоспорину, гіперкаліємію, хірургічне втручання/загальна анестезія, пацієнти похилого віку, пригнічення кістковомозкового кровотворення, обтяжений алергологічний анамнез або ангіо ), десенсибілізуюча терапія, аферез ліпопротеїнів низької щільності (ЛПНГ), аортальний стеноз/мітральний стеноз/гіпертрофічна обструктивна кардіоміопатія (ГЗКМП), застосування у пацієнтів негроїдної раси, ХСН неішемічної етіології ІІІ-ІVфункціонального класу за клас.пригнічення кістковомозкового кровотворення, обтяжений алергологічний анамнез або ангіоневротичний набряк в анамнезі, проведення гемодіалізу з використанням високопроточних мембран (наприклад, AN69®), десенсибілізуюча терапія, аферез ліпопротеїнів низькій щільності (ЛПНДПіП) застосування у пацієнтів негроїдної раси, ХСН неішемічної етіології ІІІ-ІVфункціонального класу за класифікацією NYHA.пригнічення кістковомозкового кровотворення, обтяжений алергологічний анамнез або ангіоневротичний набряк в анамнезі, проведення гемодіалізу з використанням високопроточних мембран (наприклад, AN69®), десенсибілізуюча терапія, аферез ліпопротеїнів низькій щільності (ЛПНДПіП) застосування у пацієнтів негроїдної раси, ХСН неішемічної етіології ІІІ-ІVфункціонального класу за класифікацією NYHA.застосування у пацієнтів негроїдної раси, ХСН неішемічної етіології ІІІ-ІVфункціонального класу за класифікацією NYHA.застосування у пацієнтів негроїдної раси, ХСН неішемічної етіології ІІІ-ІVфункціонального класу за класифікацією NYHA.Вагітність та лактаціяПрепарат Дальнєва протипоказаний при вагітності. Препарат Дальнєва® не рекомендований для застосування у період грудного вигодовування. Необхідно оцінити значущість терапії для матері, щоб прийняти рішення про припинення грудного вигодовування або скасування препарату. Вагітність Амлодипін Безпека застосування амлодипіну при вагітності не встановлена. В експериментальних дослідженнях на тваринах фетотоксична та ембріотоксична дія препарату встановлена при застосуванні його у високих дозах. Застосування при вагітності можливе лише у разі відсутності безпечнішої альтернативи, і коли захворювання несе більший ризик для матері та плода. Периндоприл Застосування інгібіторів АПФ не рекомендовано до застосування у І триместрі вагітності (див. розділ «Особливі вказівки»). Застосування інгібіторів АПФ протипоказане у II та III триместрах вагітності (див. розділи «Протипоказання» та «Особливі вказівки»). На даний момент немає незаперечних епідеміологічних даних про тератогенний ризик при прийомі інгібіторів АПФ у І триместрі вагітності. Проте невелике збільшення ризику виникнення порушень розвитку плода виключити не можна. При плануванні вагітності слід відмінити препарат Дальнєва® та призначити інші гіпотензивні засоби, дозволені для застосування при вагітності. При встановленні вагітності слід негайно припинити терапію інгібіторами АПФ та, за необхідності, призначити іншу терапію. Відомо, що вплив інгібіторів АПФ на плід у ІІ та ІІІ триместрах вагітності може призводити до порушення його розвитку (зниження функції нирок, олігогідрамніон, уповільнення осифікації кісток черепа) та розвитку ускладнень у новонародженого (ниркова недостатність, артеріальна гіпотензія, гіперкаліємія). Якщо пацієнтка отримувала інгібітори АПФ у II або III триместрі вагітності, рекомендується провести ультразвукове дослідження для оцінки стану кісток черепа та функції нирок плода/дитини. Новонароджені, матері яких отримували інгібітори АПФ під час вагітності, повинні перебувати під ретельним медичним контролем через ризик розвитку артеріальної гіпотензії (див. розділи «Протипоказання» та «Особливі вказівки»). Період грудного вигодовування Амлодипін Амлодипін виділяється із грудним молоком. Частка материнської дози, отриманої немовлям, оцінили з міжквартильним діапазоном 3-7 %, але з більше 15 %. Про вплив амлодипіну на немовлят невідомо. Рішення про продовження/припинення терапії або грудного вигодовування слід приймати з огляду на користь від годування груддю для дитини та користь від прийому амлодипіну для матері. Периндоприл Внаслідок відсутності інформації, що стосується застосування периндоприлу в період годування груддю, прийом периндоприлу не рекомендований, краще дотримуватися в період годування груддю альтернативного лікування з більш вивченим профілем безпеки, особливо при вигодовуванні новонароджених або недоношених дітей. Лікарський препарат Дальнєва® не слід призначати дітям та підліткам віком до 18 років, оскільки відсутні дані про ефективність та безпеку застосування периндоприлу та амлодипіну у цих груп пацієнтів як у монотерапії, так і у складі комбінованої терапії.Побічна діяа. Резюме профілю безпеки Найчастіші небажані реакції при прийомі периндоприлу та амлодипіну у вигляді монотерапії: набряк, сонливість, запаморочення, головний біль (особливо на початку лікування), дисгевзія (перекручення смаку), парестезія, порушення зору (включаючи диплопію), дзвін у вухах, вертиго, відчуття серцебиття, «припливи» крові до шкіри обличчя, артеріальна гіпотензія (і симптоми, пов'язані з цим), задишка, кашель, біль у животі, нудота, блювання, диспепсія, зміна частоти та характеру стільця, діарея, запор, свербіж шкіри, висипання на шкірі , екзантема, припухлість у ділянці суглобів (припухлість у ділянці кісточок), спазми м'язів, підвищена стомлюваність, астенія. б. Перелік небажаних реакцій Наведені нижче небажані реакції, зазначені при проведенні клінічних досліджень та/або післяреєстраційному застосуванні в монотерапії периндоприлом та амлодипіном, наведені у вигляді наступної градації: дуже часто (≥ 1/10); часто (≥ 1/100, < 1/10); нечасто (≥ 1/1000, < 1/100); рідко (≥1/10000, <1/1000); дуже рідко (<1/10000); частота невідома (не може бути оцінена на основі наявних даних). Небажані реакції представлені у вигляді таблиці MedDRA Класи та системи органів Небажані реакції Частота Амлодипін Периндоприл Інфекційні та паразитарні захворювання Риніт Не часто Дуже рідко Порушення з боку крові та лімфатичної системи Еозинофілія - Не часто* Лейкопенія/нейтропенія (див. розділ «Особливі вказівки») Дуже рідко Дуже рідко Агранулоцитоз/панцитопенія (див. розділ «Особливі вказівки») - Дуже рідко Тромбоцитопенія (див. розділ «Особливі вказівки») Дуже рідко Дуже рідко Гемолітична анемія у пацієнтів з вродженою недостатністю глюкозо-6-фосфатдегідрогенази (див. розділ «Особливі вказівки») - Дуже рідко Порушення з боку імунної системи Гіперчутливість Дуже рідко Не часто Порушення з боку обміну речовин та харчування Гіперкаліємія, оборотна після відміни препарату (див. розділ «Особливі вказівки») - Не часто* Гіперглікемія Дуже рідко - Гіпонатріємія - Не часто* Гіпоглікемія (див. розділи «Взаємодія з іншими лікарськими засобами» та «Особливі вказівки») - Не часто* Порушення психіки Лабільність настрою (включаючи тривогу) Не часто Не часто Безсоння Не часто - Депресія Не часто - Порушення сну - Не часто Порушення з боку нервової системи Запаморочення (особливо на початку лікування) Часто Часто Головний біль (особливо на початку лікування) Часто Часто Сонливість (особливо на початку лікування) Часто Не часто* Дисгезія (перекручення смаку) Не часто Часто Парестезія Не часто Часто Непритомні стани Не часто Не часто* Сплутаність свідомості Рідко Дуже рідко Гіпестезія Не часто - Тремор Не часто - Гіпертонус Дуже рідко - Периферична нейропатія Дуже рідко - Інсульт, можливо, внаслідок надмірного зниження АТ у пацієнтів із групи високого ризику (див. розділ «Особливі вказівки») - Дуже рідко Екстрапірамідні порушення (екстрапірамідний синдром) Частота невідома - Порушення з боку органу зору Порушення зору Часто Часто Диплопія Часто - Порушення з боку органу слуху та лабіринтні порушення Дзвін у вухах Не часто Часто Вертіго - Часто Порушення з боку серця Відчуття серцебиття Часто Не часто* Тахікардія - Не часто* Стенокардія (див. розділ «Особливі вказівки») - Дуже рідко Інфаркт міокарда, можливий внаслідок надмірного зниження АТ у пацієнтів із групи високого ризику (див. розділ «Особливі вказівки») Дуже рідко Дуже рідко Аритмія (включаючи брадикардію, шлуночкову тахікардію та фібриляцію передсердь) Не часто Дуже рідко Порушення з боку судин «Припливи» крові до шкіри обличчя Часто - Артеріальна гіпотензія (і симптоми, пов'язані з артеріальною гіпотензією) Не часто Часто Васкуліт Дуже рідко Не часто* Синдром Рейно - Частота невідома Порушення з боку дихальної системи, органів грудної клітки та середостіння. Кашель Не часто Часто Задишка Часто Часто Бронхоспазм - Не часто Еозинофільна пневмонія - Дуже рідко Порушення з боку шлунково-кишкового тракту Біль в животі Часто Часто Нудота Часто Часто Блювота Не часто Часто Диспепсія Часто Часто Діарея Часто Часто Запор Часто Часто Зміна частоти та характеру стільця Часто - Сухість слизової оболонки ротової порожнини Не часто Не часто Гіперплазія ясен Дуже рідко - Панкреатит Дуже рідко Дуже рідко Гастрит Дуже рідко - Порушення з боку печінки та жовчовивідних шляхів Гепатит, жовтяниця Дуже рідко - Цитолітичний або холестатичний гепатит (див. розділ «Особливі вказівки») - Дуже рідко Підвищення активності «печінкових» ферментів у плазмі крові Дуже рідко (найчастіше у поєднанні з холестазом) Рідко Порушення з боку шкіри та підшкірних тканин Екзантема Не часто Часто Висипання на шкірі Не часто Часто Кожний зуд Не часто Часто Гіпергідроз Не часто Не часто Алопеція Не часто - Пурпура Не часто - Зміна кольору шкіри Не часто - Пухирчатка - Не часто* Ангіоневротичний набряк особи, кінцівок, губ, слизових оболонок, язика, голосових складок та/або гортані (див. розділ «Особливі вказівки») Дуже рідко Не часто Кропивниця (див. розділ «Особливі вказівки») Не часто Не часто Реакції фоточутливості Дуже рідко Не часто* Мультиформна еритема Дуже рідко Дуже рідко Набряк Квінке (ангіоневротичний набряк) Дуже рідко - Синдром Стівенса-Джонсона Дуже рідко - Ексфоліативний дерматит Дуже рідко - Загострення псоріазу - Рідко Токсичний епідермальний некроліз Частота невідома - Підвищене потовиділення Не часто Не часто Порушення з боку скелетном'язової та сполучної тканини Біль у спині Не часто - Припухлість у ділянці суглобів (припухлість у ділянці кісточок) Часто - М'язові спазми Часто Часто Артралгія Не часто Не часто* Міалгія Не часто Не часто* Порушення з боку нирок та сечовивідних шляхів Порушення сечовипускання, ніктурія, поллакіурія Не часто - Гостра ниркова недостатність - Дуже рідко Ниркова недостатність - Не часто Порушення з боку статевих органів та молочної залози еректильна дисфункція Не часто Не часто Гінекомастія Не часто - Загальні розлади та порушення у місці введення Набряки Дуже часто - Периферичні набряки - Не часто* Підвищена стомлюваність Часто - Астенія Часто Часто Біль у грудній клітці Не часто Не часто* нездужання Не часто Не часто* Біль Не часто - Лихоманка - Не часто* Лабораторні та інструментальні дані Збільшення маси тіла, зниження маси тіла Не часто - Підвищення концентрації сечовини у плазмі крові - Не часто* Підвищення концентрації креатиніну у плазмі крові - Не часто* Підвищення концентрації білірубіну у плазмі крові - Рідко Зниження гемоглобіну та гематокриту - Дуже рідко Травми, інтоксикації та ускладнення маніпуляцій Падіння - Не часто* *Оцінку частоти небажаних реакцій, виявлених за спонтанними повідомленнями, проведено на підставі даних результатів клінічних досліджень. Повідомлялося про розвиток синдрому неадекватної секреції антидіуретичного гормону (СНСАДГ) при одночасному застосуванні з іншими інгібіторами АПФ. СНСАДГ можна вважати дуже рідкісним можливим ускладненням, пов'язаним із лікуванням інгібіторами АПФ, у тому числі з периндоприлом.Взаємодія з лікарськими засобамиАмлодипін Нерекомендовані поєднання лікарських засобів Дантролен (внутрішньовенне введення) У лабораторних тварин були відзначені випадки фібриляції шлуночків із летальним кінцем та колапсом на фоні застосування верапамілу та внутрішньовенного введення дантролену, що супроводжувалися гіперкаліємією. Внаслідок ризику розвитку гіперкаліємії слід виключити одночасний прийом БМКК, у тому числі амлодипіну, у пацієнтів, що схильні до злоякісної гіпертермії, а також при лікуванні злоякісної гіпертермії. Поєднання лікарських засобів, що потребують особливої уваги Індуктори ізоферменту CYP3A4: при одночасному застосуванні з індукторами ізоферменту CYP3A4 концентрація амлодипіну в плазмі може змінюватися. Тому необхідно контролювати АТ та коригувати дозу як під час, так і після їх одночасного застосування, особливо у разі застосування з потужними індукторами ізоферменту CYP3A4 (наприклад, рифампіцин, препарати Звіробою продірявленого). Інгібітори ізоферменту CYP3A4: одночасний прийом амлодипіну та потужних, або помірних інгібіторів ізоферменту CYP3A4 (інгібітори протеази, протигрибкові препарати групи азолів, макроліди, наприклад, еритроміцин або кларитроміцин, при верапаміл або ди. Клінічні прояви зазначених фармакокінетичних відхилень можуть бути більш вираженими у пацієнтів похилого віку. У зв'язку з чим може знадобитися моніторинг клінічного стану та корекція дози. У пацієнтів, які приймають амлодипін одночасно з кларитроміцином, підвищений ризик розвитку гіпотензії. Слід проводити ретельне спостереження за станом пацієнтів, які приймають периндоприл одночасно з кларитроміцином. Поєднання лікарських засобів, що потребують уваги Амлодипін посилює антигіпертензивну дію гіпотензивних препаратів. Такролімус: існує ризик збільшення сироваткової концентрації такролімусу при одночасному застосуванні з амлодипіном. Щоб уникнути розвитку токсичних ефектів такролімусу при одночасному застосуванні цих препаратів потрібен моніторинг сироваткової концентрації такролімусу та корекція його дози за потреби. Циклоспорин: дослідження щодо вивчення взаємодії циклоспорину з амлодипіном у здорових добровольців або інших груп населення не проводилися, за винятком пацієнтів, які перенесли трансплантацію нирки, у яких відзначалася варіабельність підвищення найменших концентрацій циклоспорину в плазмі (в середньому від 0% до 40%). Слід розглянути можливість контролю сироваткової концентрації циклоспорину у пацієнтів після трансплантації нирки при одночасному застосуванні з амлодипіном. При необхідності доза циклоспорину має бути знижена. Симвастатин: при одночасному застосуванні кількох доз амлодипіну по 10 мг та симвастатину 80 мг було відзначено збільшення експозиції симвастатину на 77 % порівняно з ізольованим прийомом симвастатину. У пацієнтів, які приймають препарат Дальнєва у дозі 10 мг + 4 мг або 10 мг + 8 мг, слід обмежити прийом симвастатину до 20 мг на добу. Одночасний прийом амлодипіну та вживання грейпфрутів або грейпфрутового соку не рекомендується у зв'язку з можливим підвищенням біодоступності амлодипіну у деяких пацієнтів, що, в свою чергу, може призвести до посилення ефектів зниження АТ. Інгібітори тTOR(mammalianTargetofRapamycin – мета рапамицина ссавців): інгібітори mTOR, такі як сиролімус, темсіролімус і еверолімус, є субстрати ізоферменту CYP3A. Амлодипін є слабким інгібітором ізоферменту CYP3A. При одночасному застосуванні з інгібіторами mTOR амлодипін може підвищувати їхню експозицію. Кларитроміцин: Кларитроміцин є інгібітором ізоферменту CYP3A4. Існує підвищений ризик розвитку артеріальної гіпотензії у пацієнтів, які одночасно застосовують кларитроміцин з амлодипіном. Ретельне спостереження за пацієнтами рекомендується при одночасному застосуванні амлодипіну з кларитроміцином. Одночасне застосування бета-адреноблокаторів (бісопролол, метопролол) та альфа- та бета-адреноблокатора карведилолу при ХСН: підвищує ризик розвитку артеріальної гіпотензії та погіршення перебігу ХСН у пацієнтів з неконтрольованою або латентнопротікаючою ХСН (підсилення). Крім цього, бета-адреноблокатори можуть зменшити надмірну рефлекторну симпатичну серцеву активацію на тлі супутньої ХСН. При одночасному застосуванні амлодипін може підвищувати системну експозицію тасонерміну у плазмі. У таких випадках необхідний регулярний контроль концентрації тасонерміну в плазмі та корекція дози при необхідності. Інші комбінації лікарських засобів Препарати кальцію можуть зменшити ефект БМКК. При одночасному застосуванні БМКК з препаратами літію (для амлодипіну дані відсутні) можливе посилення прояву їхньої нейротоксичності (нудота, блювання, діарея, атаксія, тремор, шум у вухах). У ході клінічних досліджень лікарських взаємодій амлодипін не впливав на фармакокінетику аторвастатину, дигоксину, варфарину. Одноразовий прийом 100 мг силденафілу у пацієнтів з есенціальною гіпертензією не впливає на параметри фармакокінетики амлодипіну. Периндоприл Дані клінічних досліджень показують, що подвійна блокада РААС внаслідок одночасного застосування інгібіторів АПФ, АРА II або аліскірену призводить до збільшення частоти виникнення таких небажаних явищ, як артеріальна гіпотензія, гіперкаліємія та порушення функції нирок (включаючи гостру ниркову недостатність) порівняно з ситуаціями, коли застосовується лише один препарат, що впливає на РААС (див. розділи "Фармакологічні властивості. Фармакодинаміка", "Протипоказання", "Особливі вказівки"). Лікарські засоби, що викликають гіперкаліємію Деякі препарати можуть збільшувати ризик розвитку гіперкаліємії: аліскірен, солі калію, калійзберігаючі діуретики, інгібітори АПФ, АРА II, нестероїдні протизапальні препарати (НПЗП), гепарин, імунодепресанти, такі як циклоспорин або такролімус, триметоприм, ко-тримоксазол). Поєднання цих препаратів збільшує ризик розвитку гіперкаліємії. Циклоспорин: при одночасному застосуванні інгібіторів АПФ з циклоспорином можливий розвиток гіперкаліємії. Рекомендується контролювати вміст калію у сироватці крові. Гепарин: можливе підвищення вмісту калію у сироватці крові. Рекомендується контролювати вміст калію у сироватці крові. Одночасне застосування протипоказане Аліскірен та лікарські препарати, що містять аліскірен Одночасне застосування інгібіторів АПФ з лікарськими препаратами, що містять аліскірен, протипоказане у пацієнтів з цукровим діабетом та/або помірним або тяжким порушенням функції нирок (ШКФ менше 60 мл/хв/1,73 м(2) площі поверхні тіла) та не рекомендується у інших пацієнтів. (Див. розділ «Протипоказання»). Зростає ризик розвитку гіперкаліємії, погіршення функції нирок, серцево-судинної захворюваності та смертності. Екстракорпоральна терапія Екстракорпоральні методи лікування, що ведуть до контакту крові з негативно зарядженими поверхнями, такі як діаліз або гемофільтрація з використанням деяких високопроточних мембран (наприклад, поліакрилонітрилових), або аферез ЛПНГ з використанням декстрану сульфату, протипоказані через збільшення ризику розвитку тяжких анафілактоїд. розділ "Протипоказання"). Якщо пацієнту потрібна екстракорпоральна терапія, слід розглянути можливість використання іншого типу діалізної мембрани чи іншого класу гіпотензивних препаратів. Інгібітори нейтральної ендопептидази При одночасному застосуванні інгібіторів АПФ з лікарськими препаратами, що містять сакубітрил (інгібітор неприлізину), зростає ризик розвитку ангіоневротичного набряку, через що одночасне застосування зазначених препаратів протипоказане. Інгібітори АПФ слід призначати не раніше ніж через 36 годин після відміни препаратів, що містять сакубітрил. Протипоказано призначення препаратів, що містять сакубітрил, пацієнтам, які отримують інгібітори АПФ, а також протягом 36 годин після відміни інгібіторів АПФ. Нерекомендовані поєднання лікарських засобів Аліскірен та лікарські препарати, що містять аліскірен У пацієнтів, які не мають цукрового діабету або порушення функції нирок, можливе підвищення ризику гіперкаліємії, погіршення функції нирок та підвищення частоти серцево-судинної захворюваності та смертності. Одночасне призначення інгібіторів АПФ та АРА II За наявними літературними даними, у пацієнтів із встановленим діагнозом атеросклерозу, серцевою недостатністю або цукровим діабетом з ураженням органів-мішеней одночасний прийом інгібіторів АПФ та АРА II призводить до збільшення частоти розвитку артеріальної гіпотензії, непритомності, гіперкаліємії та погіршення функції нирок. порівняно із ситуаціями, коли застосовується лише один препарат, що впливає на РААС. Застосування подвійної блокади РААС (наприклад, одночасний прийом інгібіторів АПФ та АРА II) повинно бути обмежене поодинокими випадками із суворим контролем функції нирок, вмісту калію у плазмі крові та АТ (див. розділ «Особливі вказівки»). Естрамустін Одночасне застосування естрамустину з інгібіторами АПФ супроводжується підвищеним ризиком розвитку ангіоневротичного набряку. Ко-тримоксазол (триметоприм + сульфаметоксазол) При одночасному застосуванні з котримоксазолом (триметоприм + сульфаметоксазол) може підвищуватися ризик розвитку гіперкаліємії (див. розділ «Особливі вказівки»). Калійзберігаючі діуретики (наприклад, тріамтерен, амілорид) та солі калію Зазвичай вміст калію в плазмі залишається в межах норми, при цьому у деяких пацієнтів, які отримують інгібітори АПФ, може розвинутись гіперкаліємія. Застосування калійзберігаючих діуретиків (наприклад, спіронолактону, тріамтерену, еплеренону або амілориду), калійвмісних замінників кухонної солі, інших препаратів, що сприяють підвищенню вмісту калію в плазмі може призвести до значного збільшення вмісту калію в сироватці крові. Слід також бути обережними при одночасному призначенні периндоприлу з іншими препаратами, здатними збільшувати вміст калію в сироватці крові, такими як триметоприм і ко-тримоксазол (триметоприм + сульфаметоксазол), так як відомо, що триметоприм діє як калійзберігаючий діуретик, такий якТому одночасне застосування периндоприлу з вищезазначеними препаратами не рекомендується. Якщо, однак, одночасне застосування показано, слід застосовувати з дотриманням запобіжних заходів та регулярним контролем вмісту калію в сироватці крові. Препарати літію При одночасному застосуванні препаратів літію та інгібіторів АПФ може виникати оборотне підвищення вмісту літію у плазмі крові та пов'язані з цим токсичні ефекти (важкі нейротоксичні ефекти). Одночасне застосування периндоприлу та препаратів літію не рекомендується. За необхідності проведення такої терапії необхідний регулярний контроль вмісту літію в плазмі (див. розділ «Особливі вказівки»). Поєднання лікарських засобів, що потребують особливої уваги Гіпоглікемічні засоби (інсулін, похідні сульфонілсечовини) Згідно з даними, отриманими в епідеміологічних дослідженнях, інгібітори АПФ можуть посилювати гіпоглікемічний ефект інсуліну та похідних сульфонілсечовини з ризиком розвитку гіпоглікемії. Даний ефект найімовірніше можна спостерігати у перші тижні одночасного застосування та у пацієнтів з порушенням функції нирок. Калійнесберігаючі діуретики У пацієнтів, які отримують діуретики, особливо у пацієнтів з гіповолемією та/або зниженою концентрацією солей, на початку терапії периндоприлом може спостерігатися виражене зниження АТ, ризик розвитку якого можна зменшити шляхом відміни діуретичного засобу, заповненням втрати рідини або солей перед початком терапії периндоприлом, а також призначенням периндоприлу у низькій дозі з подальшим поступовим її збільшенням. При АГ у пацієнтів з гіповолемією або зниженим вмістом солей на фоні терапії діуретиками діуретики повинні бути або скасовані до початку застосування інгібітору АПФ (при цьому калійнесберігаючий діуретик може бути пізніше знову призначений), або інгібітор АПФ повинен бути призначений у низькій дозі з подальшим поступовим її збільшенням. . При застосуванні діуретиків у разі ХСН інгібітор АПФ повинен бути призначений у дуже низькій дозі, можливо, після зменшення дози одночасного калійнесберігаючого діуретика. У всіх випадках функція нирок (концентрація креатиніну в плазмі крові) повинна контролюватись у перші тижні застосування інгібіторів АПФ. Калійзберігаючі діуретики (застосування еплеренону, спіронолактону в дозах від 12,5 мг до 50 мг на добу та низьких доз інгібіторів АПФ) При лікуванні ХСН II-IV функціонального класу за класифікацією NYHA з фракцією викиду лівого шлуночка < 40 % у пацієнтів, які раніше отримували інгібітори АПФ та «петлеві» діуретики, існує ризик розвитку гіперкаліємії (з можливим летальним наслідком), особливо у разі недотримання рекомендацій щодо цієї комбінації. препаратів. Перед початком застосування цієї комбінації лікарських препаратів необхідно переконатися у відсутності гіперкаліємії та порушення функції нирок. Рекомендується регулярно контролювати концентрацію креатиніну та вміст калію в плазмі крові: щотижня у перший місяць лікування та щомісяця у подальшому. Рацекадотрил Повідомлялося про підвищений ризик розвитку ангіоневротичного набряку при одночасному застосуванні інгібіторів АПФ та рацекадотрилу (інгібітор енкефалінази). Тканинні активатори плазміногену В обсерваційних дослідженнях виявлено підвищену частоту розвитку ангіоневротичного набряку у пацієнтів, які приймали інгібітори АПФ після застосування алтеплази для тромболітичної терапії ішемічного інсульту. Інгібітори mTOR (наприклад, сиролімус, еверолімус, темсіролімус) У пацієнтів, які одночасно отримують терапію інгібіторами mTOR, підвищується ризик розвитку ангіоневротичного набряку (див. розділ «Особливі вказівки»). НПЗЗ, включаючи високі дози ацетилсаліцилової кислоти (≥ 3 г/добу) Одночасне застосування інгібіторів АПФ з нестероїдними протизапальними засобами (ацетилсаліцилова кислота в дозі, що має протизапальну дію, інгібітори циклооксигенази-2 [ЦОГ-2] і неселективні нестероїдні протизапальні засоби), може призвести до зниження антигіпертензивної дії інгібіторів АПФ. Одночасне застосування інгібіторів АПФ та НПЗЗ може призводити до погіршення функції нирок, включаючи розвиток гострої ниркової недостатності, та збільшення вмісту калію у сироватці крові, особливо у пацієнтів зі зниженою функцією нирок. Слід бути обережними при призначенні даної комбінації, особливо у пацієнтів похилого віку. Пацієнтам необхідно компенсувати втрату рідини та ретельно контролювати функцію нирок як на початку лікування, так і в процесі лікування. Поєднання лікарських засобів, що потребують уваги Інгібітори дипептидилпептидази IV (ДПП-IV) (гліптини), наприклад, лінагліптин, саксагліптин, сітагліптин, віллдагліптин Одночасне застосування з інгібіторами АПФ може збільшувати ризик розвитку ангіоневротичного набряку внаслідок пригнічення активності ДПП-IVгліптином. Симпатоміметики Можуть послаблювати антигіпертензивний ефект інгібіторів АПФ. Препарати золота При застосуванні інгібіторів АПФ, у тому числі периндоприлу, у пацієнтів, які отримують внутрішньовенно препарат золота (натрію ауротіомалат), були описані нітритоїдні реакції, з частотою виникнення «рідко» (симптомокомплекс, що включає гіперемію шкіри обличчя, нудоту, блювання, артеріальну гіпотензію). Алопуринол, імуносупресивні засоби, кортикостероїди (при системному застосуванні) та прокаїнамід Одночасне застосування з інгібіторами AПФ може супроводжуватися підвищеним ризиком розвитку лейкопенії, особливо у пацієнтів із наявними порушеннями функції нирок. Засоби для загальної анестезії Одночасне застосування інгібіторів АПФ та засобів для загальної анестезії може призводити до антигіпертензивного ефекту. Поєднання лікарських засобів, що потребують особливої уваги Баклофен Можливе посилення антигіпертензивної дії. Слід контролювати АТ та функцію нирок, за необхідності провести корекцію дози амлодипіну. Поєднання препаратів, що потребує уваги Гіпотензивні засоби (наприклад, бета-адреноблокатори) та вазодилататори Можливе посилення антигіпертензивного ефекту периндоприлу та амлодипіну. Слід бути обережними при одночасному застосуванні з нітрогліцерином, іншими нітратами або іншими вазодилататорами, оскільки при цьому можливе додаткове зниження АТ. Кортикостероїди (мінерало- та глюкокортикостероїди), тетракозактид Зниження антигіпертензивної дії (затримка рідини та іонів натрію внаслідок дії кортикостероїдів). Альфа-адреноблокатори (празозин, альфузозин, доксазозин, тамсулозин, теразозин) Посилення антигіпертензивної дії та підвищення ризику розвитку ортостатичної гіпотензії. Аміфостін Можливе посилення антигіпертензивного ефекту амлодипіну. Трициклічні антидепресанти/нейролептики/засоби для загальної анестезії Посилення антигіпертензивної дії та підвищення ризику розвитку ортостатичної гіпотензії.Спосіб застосування та дозиВсередину, по одній таблетці 1 раз на день, переважно вранці перед їдою. Доза лікарського препарату Дальнева® підбирається після раніше проведеного підбору доз окремих компонентів препарату: периндоприлу та амлодипіну у пацієнтів з артеріальною гіпертензією та стабільною стенокардією. При терапевтичній необхідності доза лікарського препарату Дальнева® може бути змінена на підставі індивідуального підбору доз окремих компонентів: амлодипін 5 мг + периндоприл 4 мг або амлодипін 10 мг + периндоприл 4 мг, або амлодипін 5 мг + периндоприл 8 мг, або амлодипін 10 мг . Максимальна добова доза: амлодипін – 10 мг + периндоприл – 8 мг.ПередозуванняІнформація про передозування препаратом Дальнева відсутня. Амлодипін Інформація про передозування амлодипіном обмежена. Симптоми: виражене зниження АТ з можливим розвитком рефлекторної тахікардії та надмірної периферичної вазодилатації (ризик розвитку вираженої та стійкої артеріальної гіпотензії, у т.ч. з розвитком шоку та летального результату). Лікування: промивання шлунка, призначення активованого вугілля (особливо в перші 2 години після передозування), підтримання функції серцево-судинної системи, підвищене положення нижніх кінцівок, контроль ОЦК та діурезу, симптоматична та підтримуюча терапія. Для відновлення тонусу судин – застосування судинозвужувальних засобів (за відсутності протипоказань до їх застосування), для усунення наслідків блокади кальцієвих каналів – внутрішньовенне введення розчину глюконату. Гемодіаліз неефективний. Периндоприл Дані передозування периндоприлом обмежені. Симптоми: виражене зниження артеріального тиску, шок, порушення водно-електролітного балансу, ниркова недостатність, гіпервентиляція легень, тахікардія, відчуття серцебиття, брадикардія, запаморочення, неспокій та кашель. Лікування: заходи невідкладної допомоги зводяться до виведення препарату з організму: промивання шлунка та/або призначення активованого вугілля з подальшим відновленням ОЦК. При вираженому зниженні артеріального тиску слід перевести пацієнта в положення «лежачи» на спині з піднятими ногами, за необхідності провести заходи для відновлення ОЦК (наприклад, внутрішньовенна інфузія 0,9 % розчину натрію хлориду). Також можливе внутрішньовенне введення катехоламінів. За допомогою гемодіалізу можна видалити периндоприл із системного кровотоку. При брадикардії, резистентної до терапії, може знадобитися імплантація електрокардіостимулятора. Необхідний динамічний контроль загального стану, концентрації креатиніну та вмісту електролітів у плазмі крові.Запобіжні заходи та особливі вказівкиОсобливі вказівки, що стосуються периндоприлу та амлодипіну, застосовні і до лікарського препарату Дальнєва®. Амлодипін Ефективність та безпека застосування амлодипіну при гіпертонічному кризі не встановлено. Серцева недостатність Лікування пацієнтів із серцевою недостатністю слід проводити з обережністю. При застосуванні амлодипіну у пацієнтів з ХСН III та IV функціонального класу за класифікацією NYHA можливий розвиток набряку легень. БМКК, включаючи амлодипін, необхідно з обережністю застосовувати у пацієнтів з ХСН у зв'язку з можливим збільшенням ризику розвитку небажаних явищ з боку серцево-судинної системи та смертності. Печінкова недостатність У пацієнтів з порушенням функції печінки Т(½) та AUCамлодипіну збільшуються. Рекомендації щодо дозування препарату не встановлені. Прийом амлодипіну необхідно почати з найнижчих доз і дотримуватися запобіжних заходів як на початку лікування, так і при збільшенні дози. Пацієнтам з тяжкою печінковою недостатністю підвищувати дозу слід поступово, забезпечуючи ретельний моніторинг клінічного стану. Пацієнти похилого віку У пацієнтів похилого віку збільшення дози слід проводити з обережністю (див. розділ «Спосіб застосування та дози» та «Фармакологічні властивості. Фармакокінетика»). Ниркова недостатність Пацієнти з нирковою недостатністю можуть приймати амлодипін у стандартних дозах. Зміни плазмових концентрацій амлодипіну не корелюють зі ступенем ниркової недостатності. Амлодипін не виводиться з організму за допомогою діалізу. Мітральний стеноз/аортальний стеноз/ГЗКМП Амлодипін протипоказаний пацієнтам із обструкцією вихідного тракту лівого шлуночка. Синдром «скасування» Незважаючи на відсутність у БМКК синдрому «скасування», припинення лікування препаратом Дальнєва бажано проводити поступово, зменшуючи дозу препарату. Амлодипін не запобігає розвитку синдрому «скасування» при різкому припиненні прийому бета-адреноблокаторів. Периферичні набряки Незначно або помірно виражені периферичні набряки були найчастішим небажаним явищем амлодипіну у клінічних дослідженнях. Частота виникнення периферичних набряків зростає зі збільшенням дози (при застосуванні амлодипіну у дозі 2,5 мг, 5 мг та 10 мг на добу набряки виникали відповідно у 1,8 %, 3 % та 10 % пацієнтів). Слід ретельно диференціювати периферичні набряки, пов'язані із застосуванням амлодипіну, від симптомів прогресування лівшлуночкової серцевої недостатності. Інше Необхідна підтримка гігієни зубів та спостереження у стоматолога (для запобігання болючості, кровоточивості та гіперплазії ясен). Периндоприл Підвищена чутливість/ангіоневротичний набряк (набряк Квінке) При застосуванні інгібіторів АПФ, у тому числі периндоприлу, в окремих випадках може спостерігатися розвиток ангіоневротичного набряку особи, губ, язика, голосових складок та/або гортані. Це може статися у будь-який період. При появі цих симптомів застосування препарату Дальнева® повинно бути негайно припинено, пацієнт повинен спостерігатися доти, доки ознаки набряку не зникнуть повністю. препарати. Ангіоневротичний набряк, що супроводжується набряком язика або гортані, може призвести до обструкції дихальних шляхів та летального результату.5 мл) та/або забезпечити прохідність дихальних шляхів. Пацієнт повинен перебувати під медичним наглядом до повного та стійкого зникнення симптомів. У пацієнтів, в анамнезі яких відзначався набряк Квінке, не пов'язаний із застосуванням інгібіторів АПФ, може бути підвищений ризик його розвитку на фоні застосування препаратів цієї групи (див. розділ "Протипоказання"). У поодиноких випадках на тлі терапії інгібіторами АПФ розвивається інтестинальний ангіоневротичний набряк (ангіоневротичний набряк кишечника). При цьому у пацієнтів відзначається біль у животі як ізольований симптом або у поєднанні з нудотою та блюванням, у деяких випадках без попереднього ангіоневротичного набряку обличчя та при нормальній сироватковій концентрації С1-естерази. Діагноз встановлюється за допомогою комп'ютерної томографії черевної порожнини, ультразвукового дослідження або на момент хірургічного втручання. Симптоми зникають після припинення інгібіторів АПФ. Тому у пацієнтів з болем у животі, які отримують інгібітори АПФ, при проведенні диференціального діагнозу необхідно враховувати можливість розвитку інтестинального ангіоневротичного набряку (див. розділ «Побічна дія»). При одночасному застосуванні інгібіторів АПФ з рацекадотрилом, інгібіторами mTOR (наприклад, темсиролімусом, еверолімусом, сиролімусом) або ДПП-IV (гліптинами, включаючи віллдагліптин) підвищується ризик розвитку ангіоневротичного набряку (наприклад, набряк верхніх дихальних шляхів). ) (див. розділ «Взаємодія з іншими лікарськими засобами»). Слід виявляти обережність на початку терапії рацекадотрилом, інгібіторами mTOR (наприклад, тимсиролімусом, еверолімусом, сиролімусом) або гліптинами, включаючи віллдагліптин, при одночасному застосуванні з інгібіторами АПФ. Анафілактоїдні реакції при проведенні процедур десенсибілізації Є окремі повідомлення про розвиток тривалих, що загрожують життю анафілактоїдних реакцій у пацієнтів, які отримують інгібітори АПФ під час десенсибілізуючої терапії отрутою перетинчастокрилих комах. У цих пацієнтів анафілактоїдної реакції вдавалося уникнути шляхом тимчасової відміни інгібіторів АПФ, а при випадковому прийомі препарату анафілактоїдна реакція виникала знову. Анафілактоїдні реакції при проведенні аферезу ЛПНЩ за допомогою декстрану сульфату У поодиноких випадках у пацієнтів, які отримують інгібітори АПФ, при проведенні аферезу ЛПНЩ з використанням декстрану сульфату можуть розвиватися анафілактоїдні реакції, що загрожують життю. Для запобігання анафілактоїдної реакції слід тимчасово припинити терапію інгібітором АПФ перед кожною процедурою аферезу ЛПНЩ з використанням декстрану сульфату. Нейтропенія/агранулоцитоз, тромбоцитопенія та анемія У пацієнтів, які приймають інгібітори АПФ, можливі випадки розвитку нейтропенії/агранулоцитозу, тромбоцитопенії та анемії. У пацієнтів з нормальною функцією нирок без інших обтяжливих факторів нейтропенія розвивається рідко. Особливою обережністю периндоприл слід застосовувати у пацієнтів із системними захворюваннями сполучної тканини, на фоні прийому імунодепресантів, алопуринолу або прокаїнаміду, особливо у пацієнтів з порушеною функцією нирок. У деяких пацієнтів виникали важкі інфекції, у ряді випадків стійкі до інтенсивної антибіотикотерапії. При призначенні периндоприлу таким пацієнтам рекомендується періодично контролювати кількість лейкоцитів у крові. Пацієнти повинні повідомляти лікаря про будь-які ознаки інфекційних захворювань (наприклад, біль у горлі, гарячка). Реноваскулярна гіпертензія У пацієнтів із двостороннім стенозом ниркових артерій або стенозом артерії єдиної функціонуючої нирки на фоні терапії інгібіторами АПФ зростає ризик розвитку артеріальної гіпотензії та ниркової недостатності. Прийом діуретиків може бути додатковим фактором ризику. Погіршення функції нирок може спостерігатися вже при незначній зміні концентрації креатиніну у сироватці, навіть у пацієнтів з одностороннім стенозом ниркової артерії. Подвійна блокада РААС Є дані, що свідчать про те, що одночасне застосування інгібіторів АПФ, АРА II або аліскірену підвищує ризик розвитку гіпотензії, гіперкаліємії та порушення функції нирок (включаючи гостру ниркову недостатність). Одночасне застосування інгібіторів АПФ з препаратами, що містять аліскірен, протипоказане у пацієнтів з цукровим діабетом та/або помірною або тяжкою нирковою недостатністю (ШКФ менше 60 мл/хв/1,73 м(2) площі поверхні тіла) та не рекомендується у інших пацієнтів. Якщо терапія за допомогою подвійної блокади РААС визнана абсолютно необхідною, її слід проводити лише під суворим медичним контролем та при регулярному контролі функції нирок, вмісту електролітів у плазмі крові та АТ.Протипоказане застосування інгібіторів АПФ одночасно з АРА II у пацієнтів з діабетичною нефропатією та не рекомендується у інших пацієнтів (див. розділ "Протипоказання"). Первинний гіперальдостеронізм Пацієнти з первинним гіперальдостеронізмом, як правило, не сприйнятливі до гіпотензивних препаратів, дія яких ґрунтується на інгібуванні РААС. Тому прийом препарату не рекомендовано. Артеріальна гіпотензія Інгібітори АПФ можуть викликати різке зниження артеріального тиску. Симптоматична гіпотензія рідко розвивається у пацієнтів без супутніх захворювань. Ризик вираженого зниження АТ підвищений у пацієнтів зі зниженим ОЦК, що може відзначатися на фоні терапії діуретиками, при дотриманні суворої дієти без солі, гемодіалізі, діареї та блюванні, а також у пацієнтів з тяжким ступенем АГ з високою активністю реніну (див. розділи «Взаємодія з іншими лікарськими засобами» та «Побічна дія»). У пацієнтів з підвищеним ризиком розвитку симптоматичної артеріальної гіпотензії необхідно ретельно контролювати АТ, функцію нирок та вміст калію у сироватці крові під час терапії лікарським препаратом Дальнєва®. Подібний підхід застосовується і у пацієнтів зі стенокардією та цереброваскулярними захворюваннями, у яких виражена артеріальна гіпотензія може призвести до інфаркту міокарда або порушення мозкового кровообігу. У разі розвитку артеріальної гіпотензії пацієнт повинен бути переведений у положення «лежачи» на спині з піднятими ногами. При необхідності слід заповнити ОЦК за допомогою внутрішньовенного введення 0,9% натрію розчину хлориду. Минуща артеріальна гіпотензія не є перешкодою для подальшого прийому препарату. Після відновлення ОЦК та АТ лікування може бути продовжено. Мітральний стеноз/аортальний стеноз/ГЗКМП Периндоприл, як і інші інгібітори АПФ, повинен обережно призначатися у пацієнтів з обструкцією вихідного тракту лівого шлуночка (аортальний стеноз, ГОКМП), а також у пацієнтів з мітральним стенозом. Амлодипін протипоказаний пацієнтам із обструкцією вихідного тракту лівого шлуночка. Порушення функції нирок Пацієнтам з нирковою недостатністю (КК менше 60 мл/хв) рекомендується індивідуальний підбір доз периндоприлу та амлодипіну (див. розділ «Спосіб застосування та дози»). Таким пацієнтам необхідний регулярний контроль вмісту калію та концентрації креатиніну у сироватці крові (див. розділ «Побічна дія»). У пацієнтів із двостороннім стенозом ниркової артерії або стенозом артерії єдиної нирки на фоні терапії інгібіторами АПФ можливе підвищення концентрацій сечовини та креатиніну у сироватці крові, що зазвичай відбувається при відміні терапії. Найчастіше цей ефект відзначається у пацієнтів із нирковою недостатністю. Додаткова наявність реноваскулярної гіпертензії зумовлює підвищений ризик розвитку тяжкої гіпотензії та ниркової недостатності у таких пацієнтів. У деяких пацієнтів з артеріальною гіпертензією без ознак ураження судин нирок можливе підвищення концентрацій сечовини та креатиніну в сироватці крові, особливо при одночасному призначенні периндоприлу з діуретиком, зазвичай незначне та минуще. Найчастіше цей ефект відзначається у пацієнтів із попереднім порушенням функції нирок. Порушення функції печінки У поодиноких випадках на фоні прийому інгібіторів АПФ виникає холестатична жовтяниця. При прогресуванні цього синдрому розвивається фульмінантний некроз печінки, іноді з летальним кінцем. Механізм розвитку цього синдрому незрозумілий. У разі появи жовтяниці або значного підвищення активності «печінкових» ферментів у плазмі крові на фоні прийому інгібіторів АПФ слід припинити прийом препарату (див. розділ «Побічна дія») та звернутися до лікаря. Етнічні відмінності У пацієнтів негроїдної раси частіше, ніж у інших рас, на фоні застосування інгібіторів АПФ розвивається ангіоневротичний набряк. Периндоприл, як і інші інгібітори АПФ, може мати менш виражену антигіпертензивну дію у пацієнтів негроїдної раси порівняно з представниками інших рас. Можливо, ця відмінність зумовлена тим, що у пацієнтів негроїдної раси з артеріальною гіпертензією частіше відзначається низька активність реніну плазми крові. Кашель На тлі терапії інгібітором АПФ може виникати сухий кашель. Кашель тривалий час зберігається на фоні прийому препаратів цієї групи і зникає після їх відміни. Це слід враховувати під час проведення диференціальної діагностики кашлю. Хірургічні втручання/загальна анестезія У пацієнтів, яким планується проведення великого оперативного втручання та/або застосування засобів для загальної анестезії, що викликають гіпотензію, застосування периндоприлу може блокувати утворення ангіотензину II на тлі компенсаторного вивільнення реніну. Лікування слід припинити за добу до хірургічного втручання. При розвитку артеріальної гіпотензії за вказаним механізмом слід підтримувати артеріальний тиск шляхом заповнення ОЦК. Гіперкаліємія Інгібітори АПФ можуть викликати гіперкаліємію, оскільки вони пригнічують вивільнення альдостерону. Цей ефект зазвичай незначний у пацієнтів із нормальною функцією нирок. Однак у пацієнтів з порушенням функції нирок та/або у пацієнтів, які одночасно приймають препарати, що містять калій (включаючи калійвмісні замінники кухонної солі), калійзберігаючі діуретики, триметоприм або ко-тримоксазол (фіксована комбінація триметоприму і сульфаметоксазолу), і особливо антагон можливий розвиток гіперкаліємії. Факторами ризику гіперкаліємії є ниркова недостатність, порушення функції нирок, вік старше 70 років, цукровий діабет, інтеркурентні стани (зокрема, дегідратація, гостра декомпенсація ХСН, метаболічний ацидоз), одночасне застосування калійзберігаючих діуретиків (наприклад,спіронолактон, еплеренон, тріамтерен або амілорид), препаратів калію або замінників калію кухонної солі або одночасне застосування інших препаратів, що сприяють підвищенню вмісту калію в плазмі крові (наприклад, гепарин, ко-тримоксазол). Гіперкаліємія може призвести до серйозних порушень серцевого ритму, іноді з летальним кінцем. Калійзберігаючі діуретики та АРА II слід застосовувати з обережністю у пацієнтів, які отримують інгібітори АПФ, та регулярно контролювати вміст калію у сироватці крові та функцію нирок (див. розділ «Взаємодія з іншими лікарськими засобами»).ко-тримоксазол). Гіперкаліємія може призвести до серйозних порушень серцевого ритму, іноді з летальним кінцем. Калійзберігаючі діуретики та АРА II слід застосовувати з обережністю у пацієнтів, які отримують інгібітори АПФ, та регулярно контролювати вміст калію у сироватці крові та функцію нирок (див. розділ «Взаємодія з іншими лікарськими засобами»).ко-тримоксазол). Гіперкаліємія може призвести до серйозних порушень серцевого ритму, іноді з летальним кінцем. Калійзберігаючі діуретики та АРА II слід застосовувати з обережністю у пацієнтів, які отримують інгібітори АПФ, та регулярно контролювати вміст калію у сироватці крові та функцію нирок (див. розділ «Взаємодія з іншими лікарськими засобами»). Пацієнти з цукровим діабетом При призначенні препарату пацієнтам з цукровим діабетом, які отримують гіпоглікемічні засоби для внутрішнього застосування або інсуліну, протягом першого місяця терапії необхідно ретельно контролювати концентрацію глюкози в крові (див. розділ «Взаємодія з іншими лікарськими засобами») Застосування препарату Дальнева у пацієнтів з гострим інфарктом міокарда не рекомендується через недостатній досвід клінічного застосування. Застосування при хронічних захворюваннях: Пацієнти з порушенням функції нирок Лікарський препарат Дальнєва може застосовуватися у пацієнтів з КК рівним або більше 60 мл/хв. Лікарський препарат Дальнєва протипоказаний до застосування у пацієнтів з КК менше 60 мл/хв. Таким пацієнтам рекомендується індивідуальний підбір доз периндоприлу та амлодипіну. Зміна концентрації амлодипіну в плазмі не корелює зі ступенем вираженості ниркової недостатності. Пацієнти похилого віку та пацієнти з порушенням функції печінки Необхідно зменшити початкову дозу препарату Дальнєва до найменшої дози амлодипіну (тобто до 1 таблетки амлодипін 5 мг + периндоприл 4 мг або амлодипін 5 мг + периндоприл 8 мг). Вплив на керування транспортними засобами: У зв'язку з можливістю виникнення запаморочення, сонливості та інших побічних ефектів на фоні застосування препарату Дальнева® необхідно дотримуватись обережності при керуванні транспортними засобами та роботі з іншими технічними пристроями, що потребують підвищеної концентрації уваги та швидкості психомоторних реакцій, особливо на початку лікування та збільшення дози.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаамлодипін + периндоприл таблетки на 1 таблетку 5 мг + 4 мг/10 мг + 4 мг/5 мг + 8 мг/10 мг + 8 мг речовини, що діють: Амлодипін безілат (амлодипін безілат) 6,935 мг/13,870 мг/6,935 мг/13,870 мг, еквівалентно амлодипіну 5 мг/10 мг/5 мг/10 мг Периндоприлу ербумін А субстанція – гранули 21,000 мг/21,000 мг/42,000 мг/42,000 мг, містить периндоприлу ербуміну 4 мг/4 мг/8 мг/8 мг Допоміжні речовини: Целюлоза мікрокристалічна, крохмаль прежелатинізований, карбоксиметилкрохмаль натрію, гідрокарбонат натрію, кремнію діоксид колоїдний, магнію стеаратОпис лікарської формиТаблетки 5 мг + 4 мг: Круглі, злегка двоопуклі таблетки з фаскою, від білого до майже білого кольору. Таблетки 10 мг + 4 мг: Капсулоподібні, двоопуклі таблетки з ризиком на одній стороні, від білого до майже білого кольору. Таблетки 5 мг + 8 мг: Круглі, двоопуклі таблетки з фаскою, від білого до майже білого кольору. Таблетки 10 мг + 8 мг: Круглі, двоопуклі таблетки з фаскою, з ризиком на одній стороні, від білого майже білого кольору.Фармакотерапевтична групагіпотензивний комбінований засіб (інгібітор ангіотензинперетворюючого ферменту [АПФ] + блокатор «повільних» кальцієвих каналів [БМКК])ФармакокінетикаВеличина абсорбції амлодипіну та периндоприлу при застосуванні комбінованого лікарського препарату Дальнева® суттєво не відрізняється від такої при застосуванні їх як монопрепарати. Амлодипін Після прийому внутрішньо амлодипін повільно абсорбується із шлунково-кишкового тракту (ЖКТ). Прийом їжі не впливає на біодоступність амлодипіну. Максимальна концентрація (Сmax) амлодипіну в плазмі досягається через 6-12 годин після прийому препарату внутрішньо. Абсолютна біодоступність становить 64-80%. Об'єм розподілу – приблизно 21 л/кг. У дослідженнях in vitro було показано, що близько 97,5% циркулюючого амлодипіну пов'язано з білками плазми. Кінцевий період напіввиведення (Т½) із плазми становить 35-50 годин, що дозволяє приймати препарат 1 раз на добу. Амлодипін метаболізується у печінці з утворенням неактивних метаболітів, при цьому 10% прийнятої дози амлодипіну виводиться у незміненому вигляді та 60% нирками – у вигляді метаболітів. Амлодипін не виводиться з організму за допомогою діалізу. Час досягнення Сmax(ТСmax) амлодипіну в плазмі крові не відрізняється у пацієнтів похилого віку та молодшого віку. У пацієнтів похилого віку відзначається уповільнення кліренсу амлодипіну, що призводить до збільшення площі під кривою «концентрація-час» (AUC). Збільшення AUC та Т½ у пацієнтів з ХСН відповідає передбачуваній величині для цієї вікової групи. У пацієнтів з порушенням функції нирок зміни концентрації амлодипіну в плазмі не корелюють зі ступенем ниркової недостатності. Можливе незначне подовження Т½. Дані щодо застосування амлодипіну пацієнтами з печінковою недостатністю обмежені. У пацієнтів з печінковою недостатністю спостерігається зниження кліренсу амлодипіну, що призводить до подовження Т½ та збільшення AUC приблизно на 40-60%. Периндоприл Після прийому периндоприл швидко всмоктується і досягає Сmaxв плазмі протягом 1 години. Т½ периндоприлу з плазми становить приблизно 1 годину. Периндоприл не має фармакологічної активності, є проліками. Приблизно 27% від загальної кількості, прийнятої внутрішньо периндоприлу, потрапляє в кровообіг у вигляді активного метаболіту – периндоприлату. Крім периндоприлату утворюються ще 5 метаболітів, які не мають фармакологічної активності. Сmax у плазмі крові досягається через 3-4 години після прийому внутрішньо. Прийом їжі зменшує біодоступність периндоприлу, тому препарат слід приймати 1 раз на добу, вранці, перед їдою. Існує лінійна залежність концентрації периндоприлу в плазмі від величини прийнятої всередину дози. Об'єм розподілу вільного периндоприлату становить приблизно 0,2 л/кг. Зв'язок периндоприлату з білками плазми (переважно з АПФ) становить 20% і залежить від його концентрації. Периндоприлат виводиться нирками, Т½ незв'язаної фракції становить приблизно 17 годин, тому рівноважний стан досягається протягом 4-х діб після прийому внутрішньо. Виведення периндоприлату сповільнене у пацієнтів похилого віку, а також у пацієнтів із серцевою та нирковою недостатністю (див. розділ «Спосіб застосування та дози»), тому спостереження за такими пацієнтами повинно включати регулярний контроль концентрації креатиніну та вмісту калію в плазмі крові. Діалізний кліренс периндоприлату становить 70 мл/хв. Фармакокінетика периндоприлу порушена у пацієнтів із цирозом печінки: його печінковий кліренс зменшується у 2 рази. Тим не менш, кількість периндоприлату, що утворюється, не зменшується, тому не потрібно корекції дози (див. розділи «Спосіб застосування та дози» та «Особливі вказівки»).ФармакодинамікаАмлодипін Амлодипін – БМКК, похідне дигідропіридину. Амлодипін пригнічує трансмембранний перехід іонів кальцію в кардіоміоцити та гладком'язові клітини судинної стінки. Антигіпертензивна дія амлодипіну обумовлена прямим розслаблюючим впливом на гладком'язові клітини судинної стінки. Детальний механізм, за допомогою якого амлодипін здійснює антиангінальну дію, не цілком встановлений, але відомо, що амлодипін зменшує загальне ішемічне навантаження за допомогою двох дій: викликає розширення периферичних артеріол, зменшуючи загальний периферичний судинний опір (ОПСС) (постнавантаження). Оскільки частота серцевих скорочень (ЧСС) у своїй не змінюється, потреба міокарда в кисні знижується; викликає розширення коронарних артерій та артеріол як у ішемізованій, так і в інтактній зонах. Їх дилатація збільшує надходження кисню до міокарда у пацієнтів з вазоспастичною стенокардією (стенокардія Принцметала або варіантна стенокардія). У пацієнтів з артеріальною гіпертензією (АГ) прийом амлодипіну 1 раз на добу забезпечує клінічно значуще зниження артеріального тиску (АТ) у положенні стоячи і лежачи протягом 24 годин. Антигіпертензивна дія розвивається повільно, у зв'язку з чим розвиток гострої гіпотензії нехарактерний. У пацієнтів зі стенокардією прийом амлодипіну 1 раз на добу збільшує загальний час фізичного навантаження, збільшує час до розвитку нападу стенокардії та до появи депресії сегмента ST на 1 мм, а також знижує частоту нападів стенокардії та споживання нітрогліцерину під язик. Амлодипін не чинить несприятливих метаболічних ефектів і не впливає на концентрацію ліпідів плазми. Препарат може застосовуватися у пацієнтів із супутньою бронхіальною астмою, цукровим діабетом та подагрою. Ішемічна хвороба серця (ІХС) Результати оцінки ефективності свідчать про те, що прийом амлодипіну характеризується меншою кількістю випадків госпіталізації щодо стенокардії та проведення процедур реваскуляризації у пацієнтів з ІХС. Периндоприл Периндоприл – інгібітор ферменту, що перетворює ангіотензин I на ангіотензин II. АПФ, або кініназа II, є екзопептидазою, яка здійснює як перетворення ангіотензину I на судинозвужувальну речовину ангіотензин II, так і розпад брадикініну, що має судинорозширювальну дію, до неактивного гептапептиду. Оскільки АПФ інактивує брадикінін, пригнічення АПФ супроводжується підвищенням активності як циркулюючої, так і тканинної калікреїн-кінінової системи, при цьому також активується система простагландинів. Периндоприл має терапевтичну дію завдяки активному метаболіту, периндоприлату. Інші метаболіти не мають інгібуючої дії на АПФ в умовах in vitro. Артеріальна гіпертензія Периндоприл є препаратом для лікування артеріальної гіпертензії будь-якого ступеня тяжкості. На тлі його застосування відзначається зниження як систолічного, так і діастолічного АТ у положенні «лежачи» та «стоячи». Периндоприл зменшує ОПСС, що призводить до зниження артеріального тиску та поліпшення периферичного кровотоку без зміни ЧСС. Як правило, прийом периндоприлу збільшує нирковий кровообіг, швидкість клубочкової фільтрації (СКФ) при цьому не змінюється. Антигіпертензивна дія препарату досягає максимуму через 4-6 годин після одноразового прийому внутрішньо та зберігається протягом 24 годин. Антигіпертензивна дія через 24 години після одноразового застосування внутрішньо становить близько 87-100% від максимального антигіпертензивного ефекту. Зниження АТ досягається досить швидко. Терапевтичний ефект настає через 1 місяць від початку терапії і не супроводжується тахіфілаксією. Припинення лікування не викликає ефекту "рикошету". Периндоприл має судинорозширювальну дію, сприяє відновленню еластичності великих артерій та структури судинної стінки дрібних артерій, а також зменшує гіпертрофію лівого шлуночка. Стабільна ІХС Ефективність застосування периндоприлу у пацієнтів (12218 пацієнтів віком від 18 років) зі стабільною ІХС без клінічних симптомів хронічної серцевої недостатності (ХСН) вивчалась у ході 4-річного дослідження. 90% учасників дослідження раніше перенесли гострий інфаркт міокарда та/або процедуру реваскуляризації. Більшість пацієнтів отримували крім досліджуваного препарату стандартну терапію, включаючи антиагреганти, гіполіпідемічні засоби та бета-адреноблокатори. Як основний критерій ефективності була обрана комбінована кінцева точка, що включає серцево-судинну смертність, нефатальний інфаркт міокарда та/або зупинку серця з успішною реанімацією. Терапія периндоприлом третбутиламіном у дозі 8 мг/добу 1 раз на день (еквівалентно 10 мг периндоприлу аргініну) призводила до суттєвого зниження абсолютного ризику щодо комбінованої кінцевої точки на 1,9 % у пацієнтів, які раніше перенесли інфаркт міокарда та/або процедуру реваскуляру. абсолютного ризику становило 2,2% порівняно з групою плацебо. Подвійна блокада ренін-ангіотензин-альдостеронової системи (РААС) Є дані клінічних досліджень комбінованої терапії із застосуванням інгібітору АПФ та антагоніста рецептора ангіотензину II (АРА II). Протипоказано застосування інгібіторів АПФ у поєднанні з АРА II у пацієнтів з діабетичною нефропатією. Є дані клінічного дослідження з вивчення позитивного впливу від додавання аліскірену до стандартної терапії інгібітором АПФ або АРА II у пацієнтів з цукровим діабетом 2 типу та/або хронічним захворюванням нирок, або кардіоваскулярним захворюванням, які мають поєднання цих захворювань. Дослідження було припинено достроково у зв'язку з зростанням ризику виникнення несприятливих результатів. Кардіоваскулярна смерть та інсульт відзначалися частіше у групі пацієнтів, які отримують аліскірен, порівняно з групою плацебо; також небажані явища та серйозні небажані явища особливого інтересу (гіперкаліємія, артеріальна гіпотензія та порушення функції нирок) реєструвалися частіше у групі аліскірену, ніж у групі плацебо. Амлодипін + периндоприл Ефективність при тривалому застосуванні амлодипіну в комбінації з периндоприлом і атенололу в комбінації з бендрофлуметіазидом у пацієнтів віком від 40 до 79 років з АГ та, щонайменше, з трьома з перелічених додаткових факторів ризику: гіпертрофія лівого шлуночка діабет 2 типу, атеросклероз периферичних артерій, раніше перенесений інсульт або транзиторна ішемічна атака, чоловіча стать, вік 55 років і старше, мікроальбумінурія або протеїнурія, куріння, загальний холестерин/холестерин ліпопротеїдів високої щільності ≥ 6, ранній розвиток ASCOT-BPLA. Основний критерій оцінки ефективності – комбінований показник частоти нефатального інфаркту міокарда (у тому числі безболевого) та летальних наслідків ІХС. Частота ускладнень, передбачених основним критерієм оцінки, у групі амлодипін/периндоприл була на 10% нижчою, ніж у групі атенолол/бендрофлуметіазид, проте ця відмінність не була статистично достовірною. У групі амлодипін/периндоприл відзначалося достовірне зниження частоти ускладнень, передбачених додатковими критеріями ефективності (крім фатальної та нефатальної серцевої недостатності).Показання до застосуванняАртеріальна гіпертензія та/або ішемічна хвороба серця: стабільна стенокардія напруги у пацієнтів, яким потрібна терапія периндоприлом та амлодипіном.Протипоказання до застосуванняПідвищена чутливість до периндоприлу або інших інгібіторів АПФ, амлодипіну та інших похідних дигідропіридину, а також допоміжних речовин, що входять до складу препарату. Ангіоневротичний набряк (набряк Квінке) в анамнезі (у тому числі на фоні прийому інших інгібіторів АПФ). Спадковий/ідіопатичний ангіоневротичний набряк. Одночасне застосування з аліскіреном та лікарськими препаратами, що містять аліскірен, у пацієнтів з цукровим діабетом та/або помірними або тяжкими порушеннями функції нирок (ШКФ < 60 мл/хв/1,73 м2 площі поверхні тіла) (див. розділи «Взаємодія з іншими лікарськими засобами) засобами" і "Фармакологічні властивості. Фармакодинаміка"). Одночасне застосування з АРА II у пацієнтів з діабетичною нефропатією (див. розділ «Особливі вказівки»). Одночасне застосування з інгібіторами нейтральної ендопептидази (наприклад, з препаратами, що містять сакубітрил) через високий ризик розвитку ангіоневротичного набряку. Екстракорпоральна терапія, що веде до контакту крові з негативно зарядженими поверхнями (див. розділ "Взаємодія з іншими лікарськими засобами"). Виражений двосторонній стеноз ниркових артерій або стеноз артерії єдиної нирки, що функціонує (див. розділ «Особливі вказівки»). Тяжка артеріальна гіпотензія (систолічний артеріальний тиск менше 90 мм рт. ст.). Шок (включно з кардіогенним). Обструкція вихідного тракту лівого шлуночка (наприклад, клінічно суттєвий стеноз аорти). Гемодинамічно нестабільна серцева недостатність після гострого інфаркту міокарда. Ниркова недостатність (кліренс креатиніну менше 60 мл/хв). Вагітність та період грудного вигодовування. Вік до 18 років (ефективність та безпека не встановлені). Стеноз ниркової артерії (у тому числі двосторонній), єдина функціонуюча нирка, печінкова недостатність, ниркова недостатність, системні захворювання сполучної тканини (у тому числі системний червоний вовчак, склеродермія), терапія імунодепресантами, алопуринолом, прокаїнамоз об'єм циркулюючої крові (ОЦК) (прийом діуретиків, безсольова дієта, блювання, діарея), атеросклероз, цереброваскулярні захворювання, ІХС з тяжким обструктивним ураженням коронарних артерій, гострий інфаркт міокарда (і період протягом 1 місяця після нього), нестабільна синусового вузла (виражена тахікардія, брадикардія), реноваскулярна гіпертензія, цукровий діабет, первинний гіперальдостеронізм, ХСН, одночасне застосування інгібіторів або індукторів ізоферменту CYP3A4,дантролену, естрамустину, калійзберігаючих діуретиків, препаратів калію, калійвмісних замінників харчової солі, препаратів літію, кларитроміцину, такролімусу, циклоспорину, гіперкаліємії, хірургічного втручання/загальна анестезія, пацієнтів похилого віку. гемодіалізу з використанням високопроточних мембран (наприклад, AN69®), десенсибілізуюча терапія, аферез ліпопротеїнів низької щільності (ЛПНЩ), аортальний стеноз/мітральний стеноз/гіпертрофічна обструктивна кардіоміопатія (ГОКМП), застосування у пацієнтів негроїдної раси NYHA класифікації.калійвмісних замінників харчової солі, препаратів літію, кларитроміцину, такролімусу, циклоспорину, гіперкаліємію, хірургічне втручання/загальна анестезія, пацієнти похилого віку, пригнічення кістковомозкового кровотворення, обтяжений алергологічний анамнез або ангіо ), десенсибілізуюча терапія, аферез ліпопротеїнів низької щільності (ЛПНГ), аортальний стеноз/мітральний стеноз/гіпертрофічна обструктивна кардіоміопатія (ГЗКМП), застосування у пацієнтів негроїдної раси, ХСН неішемічної етіології ІІІ-ІVфункціонального класу за клас.калійвмісних замінників харчової солі, препаратів літію, кларитроміцину, такролімусу, циклоспорину, гіперкаліємію, хірургічне втручання/загальна анестезія, пацієнти похилого віку, пригнічення кістковомозкового кровотворення, обтяжений алергологічний анамнез або ангіо ), десенсибілізуюча терапія, аферез ліпопротеїнів низької щільності (ЛПНГ), аортальний стеноз/мітральний стеноз/гіпертрофічна обструктивна кардіоміопатія (ГЗКМП), застосування у пацієнтів негроїдної раси, ХСН неішемічної етіології ІІІ-ІVфункціонального класу за клас.пригнічення кістковомозкового кровотворення, обтяжений алергологічний анамнез або ангіоневротичний набряк в анамнезі, проведення гемодіалізу з використанням високопроточних мембран (наприклад, AN69®), десенсибілізуюча терапія, аферез ліпопротеїнів низькій щільності (ЛПНДПіП) застосування у пацієнтів негроїдної раси, ХСН неішемічної етіології ІІІ-ІVфункціонального класу за класифікацією NYHA.пригнічення кістковомозкового кровотворення, обтяжений алергологічний анамнез або ангіоневротичний набряк в анамнезі, проведення гемодіалізу з використанням високопроточних мембран (наприклад, AN69®), десенсибілізуюча терапія, аферез ліпопротеїнів низькій щільності (ЛПНДПіП) застосування у пацієнтів негроїдної раси, ХСН неішемічної етіології ІІІ-ІVфункціонального класу за класифікацією NYHA.застосування у пацієнтів негроїдної раси, ХСН неішемічної етіології ІІІ-ІVфункціонального класу за класифікацією NYHA.застосування у пацієнтів негроїдної раси, ХСН неішемічної етіології ІІІ-ІVфункціонального класу за класифікацією NYHA.Вагітність та лактаціяПрепарат Дальнєва протипоказаний при вагітності. Препарат Дальнєва® не рекомендований для застосування у період грудного вигодовування. Необхідно оцінити значущість терапії для матері, щоб прийняти рішення про припинення грудного вигодовування або скасування препарату. Вагітність Амлодипін Безпека застосування амлодипіну при вагітності не встановлена. В експериментальних дослідженнях на тваринах фетотоксична та ембріотоксична дія препарату встановлена при застосуванні його у високих дозах. Застосування при вагітності можливе лише у разі відсутності безпечнішої альтернативи, і коли захворювання несе більший ризик для матері та плода. Периндоприл Застосування інгібіторів АПФ не рекомендовано до застосування у І триместрі вагітності (див. розділ «Особливі вказівки»). Застосування інгібіторів АПФ протипоказане у II та III триместрах вагітності (див. розділи «Протипоказання» та «Особливі вказівки»). На даний момент немає незаперечних епідеміологічних даних про тератогенний ризик при прийомі інгібіторів АПФ у І триместрі вагітності. Проте невелике збільшення ризику виникнення порушень розвитку плода виключити не можна. При плануванні вагітності слід відмінити препарат Дальнєва® та призначити інші гіпотензивні засоби, дозволені для застосування при вагітності. При встановленні вагітності слід негайно припинити терапію інгібіторами АПФ та, за необхідності, призначити іншу терапію. Відомо, що вплив інгібіторів АПФ на плід у ІІ та ІІІ триместрах вагітності може призводити до порушення його розвитку (зниження функції нирок, олігогідрамніон, уповільнення осифікації кісток черепа) та розвитку ускладнень у новонародженого (ниркова недостатність, артеріальна гіпотензія, гіперкаліємія). Якщо пацієнтка отримувала інгібітори АПФ у II або III триместрі вагітності, рекомендується провести ультразвукове дослідження для оцінки стану кісток черепа та функції нирок плода/дитини. Новонароджені, матері яких отримували інгібітори АПФ під час вагітності, повинні перебувати під ретельним медичним контролем через ризик розвитку артеріальної гіпотензії (див. розділи «Протипоказання» та «Особливі вказівки»). Період грудного вигодовування Амлодипін Амлодипін виділяється із грудним молоком. Частка материнської дози, отриманої немовлям, оцінили з міжквартильним діапазоном 3-7 %, але з більше 15 %. Про вплив амлодипіну на немовлят невідомо. Рішення про продовження/припинення терапії або грудного вигодовування слід приймати з огляду на користь від годування груддю для дитини та користь від прийому амлодипіну для матері. Периндоприл Внаслідок відсутності інформації, що стосується застосування периндоприлу в період годування груддю, прийом периндоприлу не рекомендований, краще дотримуватися в період годування груддю альтернативного лікування з більш вивченим профілем безпеки, особливо при вигодовуванні новонароджених або недоношених дітей. Лікарський препарат Дальнєва® не слід призначати дітям та підліткам віком до 18 років, оскільки відсутні дані про ефективність та безпеку застосування периндоприлу та амлодипіну у цих груп пацієнтів як у монотерапії, так і у складі комбінованої терапії.Побічна діяа. Резюме профілю безпеки Найчастіші небажані реакції при прийомі периндоприлу та амлодипіну у вигляді монотерапії: набряк, сонливість, запаморочення, головний біль (особливо на початку лікування), дисгевзія (перекручення смаку), парестезія, порушення зору (включаючи диплопію), дзвін у вухах, вертиго, відчуття серцебиття, «припливи» крові до шкіри обличчя, артеріальна гіпотензія (і симптоми, пов'язані з цим), задишка, кашель, біль у животі, нудота, блювання, диспепсія, зміна частоти та характеру стільця, діарея, запор, свербіж шкіри, висипання на шкірі , екзантема, припухлість у ділянці суглобів (припухлість у ділянці кісточок), спазми м'язів, підвищена стомлюваність, астенія. б. Перелік небажаних реакцій Наведені нижче небажані реакції, зазначені при проведенні клінічних досліджень та/або післяреєстраційному застосуванні в монотерапії периндоприлом та амлодипіном, наведені у вигляді наступної градації: дуже часто (≥ 1/10); часто (≥ 1/100, < 1/10); нечасто (≥ 1/1000, < 1/100); рідко (≥1/10000, <1/1000); дуже рідко (<1/10000); частота невідома (не може бути оцінена на основі наявних даних). Небажані реакції представлені у вигляді таблиці MedDRA Класи та системи органів Небажані реакції Частота Амлодипін Периндоприл Інфекційні та паразитарні захворювання Риніт Не часто Дуже рідко Порушення з боку крові та лімфатичної системи Еозинофілія - Не часто* Лейкопенія/нейтропенія (див. розділ «Особливі вказівки») Дуже рідко Дуже рідко Агранулоцитоз/панцитопенія (див. розділ «Особливі вказівки») - Дуже рідко Тромбоцитопенія (див. розділ «Особливі вказівки») Дуже рідко Дуже рідко Гемолітична анемія у пацієнтів з вродженою недостатністю глюкозо-6-фосфатдегідрогенази (див. розділ «Особливі вказівки») - Дуже рідко Порушення з боку імунної системи Гіперчутливість Дуже рідко Не часто Порушення з боку обміну речовин та харчування Гіперкаліємія, оборотна після відміни препарату (див. розділ «Особливі вказівки») - Не часто* Гіперглікемія Дуже рідко - Гіпонатріємія - Не часто* Гіпоглікемія (див. розділи «Взаємодія з іншими лікарськими засобами» та «Особливі вказівки») - Не часто* Порушення психіки Лабільність настрою (включаючи тривогу) Не часто Не часто Безсоння Не часто - Депресія Не часто - Порушення сну - Не часто Порушення з боку нервової системи Запаморочення (особливо на початку лікування) Часто Часто Головний біль (особливо на початку лікування) Часто Часто Сонливість (особливо на початку лікування) Часто Не часто* Дисгезія (перекручення смаку) Не часто Часто Парестезія Не часто Часто Непритомні стани Не часто Не часто* Сплутаність свідомості Рідко Дуже рідко Гіпестезія Не часто - Тремор Не часто - Гіпертонус Дуже рідко - Периферична нейропатія Дуже рідко - Інсульт, можливо, внаслідок надмірного зниження АТ у пацієнтів із групи високого ризику (див. розділ «Особливі вказівки») - Дуже рідко Екстрапірамідні порушення (екстрапірамідний синдром) Частота невідома - Порушення з боку органу зору Порушення зору Часто Часто Диплопія Часто - Порушення з боку органу слуху та лабіринтні порушення Дзвін у вухах Не часто Часто Вертіго - Часто Порушення з боку серця Відчуття серцебиття Часто Не часто* Тахікардія - Не часто* Стенокардія (див. розділ «Особливі вказівки») - Дуже рідко Інфаркт міокарда, можливий внаслідок надмірного зниження АТ у пацієнтів із групи високого ризику (див. розділ «Особливі вказівки») Дуже рідко Дуже рідко Аритмія (включаючи брадикардію, шлуночкову тахікардію та фібриляцію передсердь) Не часто Дуже рідко Порушення з боку судин «Припливи» крові до шкіри обличчя Часто - Артеріальна гіпотензія (і симптоми, пов'язані з артеріальною гіпотензією) Не часто Часто Васкуліт Дуже рідко Не часто* Синдром Рейно - Частота невідома Порушення з боку дихальної системи, органів грудної клітки та середостіння. Кашель Не часто Часто Задишка Часто Часто Бронхоспазм - Не часто Еозинофільна пневмонія - Дуже рідко Порушення з боку шлунково-кишкового тракту Біль в животі Часто Часто Нудота Часто Часто Блювота Не часто Часто Диспепсія Часто Часто Діарея Часто Часто Запор Часто Часто Зміна частоти та характеру стільця Часто - Сухість слизової оболонки ротової порожнини Не часто Не часто Гіперплазія ясен Дуже рідко - Панкреатит Дуже рідко Дуже рідко Гастрит Дуже рідко - Порушення з боку печінки та жовчовивідних шляхів Гепатит, жовтяниця Дуже рідко - Цитолітичний або холестатичний гепатит (див. розділ «Особливі вказівки») - Дуже рідко Підвищення активності «печінкових» ферментів у плазмі крові Дуже рідко (найчастіше у поєднанні з холестазом) Рідко Порушення з боку шкіри та підшкірних тканин Екзантема Не часто Часто Висипання на шкірі Не часто Часто Кожний зуд Не часто Часто Гіпергідроз Не часто Не часто Алопеція Не часто - Пурпура Не часто - Зміна кольору шкіри Не часто - Пухирчатка - Не часто* Ангіоневротичний набряк особи, кінцівок, губ, слизових оболонок, язика, голосових складок та/або гортані (див. розділ «Особливі вказівки») Дуже рідко Не часто Кропивниця (див. розділ «Особливі вказівки») Не часто Не часто Реакції фоточутливості Дуже рідко Не часто* Мультиформна еритема Дуже рідко Дуже рідко Набряк Квінке (ангіоневротичний набряк) Дуже рідко - Синдром Стівенса-Джонсона Дуже рідко - Ексфоліативний дерматит Дуже рідко - Загострення псоріазу - Рідко Токсичний епідермальний некроліз Частота невідома - Підвищене потовиділення Не часто Не часто Порушення з боку скелетном'язової та сполучної тканини Біль у спині Не часто - Припухлість у ділянці суглобів (припухлість у ділянці кісточок) Часто - М'язові спазми Часто Часто Артралгія Не часто Не часто* Міалгія Не часто Не часто* Порушення з боку нирок та сечовивідних шляхів Порушення сечовипускання, ніктурія, поллакіурія Не часто - Гостра ниркова недостатність - Дуже рідко Ниркова недостатність - Не часто Порушення з боку статевих органів та молочної залози еректильна дисфункція Не часто Не часто Гінекомастія Не часто - Загальні розлади та порушення у місці введення Набряки Дуже часто - Периферичні набряки - Не часто* Підвищена стомлюваність Часто - Астенія Часто Часто Біль у грудній клітці Не часто Не часто* нездужання Не часто Не часто* Біль Не часто - Лихоманка - Не часто* Лабораторні та інструментальні дані Збільшення маси тіла, зниження маси тіла Не часто - Підвищення концентрації сечовини у плазмі крові - Не часто* Підвищення концентрації креатиніну у плазмі крові - Не часто* Підвищення концентрації білірубіну у плазмі крові - Рідко Зниження гемоглобіну та гематокриту - Дуже рідко Травми, інтоксикації та ускладнення маніпуляцій Падіння - Не часто* *Оцінку частоти небажаних реакцій, виявлених за спонтанними повідомленнями, проведено на підставі даних результатів клінічних досліджень. Повідомлялося про розвиток синдрому неадекватної секреції антидіуретичного гормону (СНСАДГ) при одночасному застосуванні з іншими інгібіторами АПФ. СНСАДГ можна вважати дуже рідкісним можливим ускладненням, пов'язаним із лікуванням інгібіторами АПФ, у тому числі з периндоприлом.Взаємодія з лікарськими засобамиАмлодипін Нерекомендовані поєднання лікарських засобів Дантролен (внутрішньовенне введення) У лабораторних тварин були відзначені випадки фібриляції шлуночків із летальним кінцем та колапсом на фоні застосування верапамілу та внутрішньовенного введення дантролену, що супроводжувалися гіперкаліємією. Внаслідок ризику розвитку гіперкаліємії слід виключити одночасний прийом БМКК, у тому числі амлодипіну, у пацієнтів, що схильні до злоякісної гіпертермії, а також при лікуванні злоякісної гіпертермії. Поєднання лікарських засобів, що потребують особливої уваги Індуктори ізоферменту CYP3A4: при одночасному застосуванні з індукторами ізоферменту CYP3A4 концентрація амлодипіну в плазмі може змінюватися. Тому необхідно контролювати АТ та коригувати дозу як під час, так і після їх одночасного застосування, особливо у разі застосування з потужними індукторами ізоферменту CYP3A4 (наприклад, рифампіцин, препарати Звіробою продірявленого). Інгібітори ізоферменту CYP3A4: одночасний прийом амлодипіну та потужних, або помірних інгібіторів ізоферменту CYP3A4 (інгібітори протеази, протигрибкові препарати групи азолів, макроліди, наприклад, еритроміцин або кларитроміцин, при верапаміл або ди. Клінічні прояви зазначених фармакокінетичних відхилень можуть бути більш вираженими у пацієнтів похилого віку. У зв'язку з чим може знадобитися моніторинг клінічного стану та корекція дози. У пацієнтів, які приймають амлодипін одночасно з кларитроміцином, підвищений ризик розвитку гіпотензії. Слід проводити ретельне спостереження за станом пацієнтів, які приймають периндоприл одночасно з кларитроміцином. Поєднання лікарських засобів, що потребують уваги Амлодипін посилює антигіпертензивну дію гіпотензивних препаратів. Такролімус: існує ризик збільшення сироваткової концентрації такролімусу при одночасному застосуванні з амлодипіном. Щоб уникнути розвитку токсичних ефектів такролімусу при одночасному застосуванні цих препаратів потрібен моніторинг сироваткової концентрації такролімусу та корекція його дози за потреби. Циклоспорин: дослідження щодо вивчення взаємодії циклоспорину з амлодипіном у здорових добровольців або інших груп населення не проводилися, за винятком пацієнтів, які перенесли трансплантацію нирки, у яких відзначалася варіабельність підвищення найменших концентрацій циклоспорину в плазмі (в середньому від 0% до 40%). Слід розглянути можливість контролю сироваткової концентрації циклоспорину у пацієнтів після трансплантації нирки при одночасному застосуванні з амлодипіном. При необхідності доза циклоспорину має бути знижена. Симвастатин: при одночасному застосуванні кількох доз амлодипіну по 10 мг та симвастатину 80 мг було відзначено збільшення експозиції симвастатину на 77 % порівняно з ізольованим прийомом симвастатину. У пацієнтів, які приймають препарат Дальнєва у дозі 10 мг + 4 мг або 10 мг + 8 мг, слід обмежити прийом симвастатину до 20 мг на добу. Одночасний прийом амлодипіну та вживання грейпфрутів або грейпфрутового соку не рекомендується у зв'язку з можливим підвищенням біодоступності амлодипіну у деяких пацієнтів, що, в свою чергу, може призвести до посилення ефектів зниження АТ. Інгібітори тTOR(mammalianTargetofRapamycin – мета рапамицина ссавців): інгібітори mTOR, такі як сиролімус, темсіролімус і еверолімус, є субстрати ізоферменту CYP3A. Амлодипін є слабким інгібітором ізоферменту CYP3A. При одночасному застосуванні з інгібіторами mTOR амлодипін може підвищувати їхню експозицію. Кларитроміцин: Кларитроміцин є інгібітором ізоферменту CYP3A4. Існує підвищений ризик розвитку артеріальної гіпотензії у пацієнтів, які одночасно застосовують кларитроміцин з амлодипіном. Ретельне спостереження за пацієнтами рекомендується при одночасному застосуванні амлодипіну з кларитроміцином. Одночасне застосування бета-адреноблокаторів (бісопролол, метопролол) та альфа- та бета-адреноблокатора карведилолу при ХСН: підвищує ризик розвитку артеріальної гіпотензії та погіршення перебігу ХСН у пацієнтів з неконтрольованою або латентнопротікаючою ХСН (підсилення). Крім цього, бета-адреноблокатори можуть зменшити надмірну рефлекторну симпатичну серцеву активацію на тлі супутньої ХСН. При одночасному застосуванні амлодипін може підвищувати системну експозицію тасонерміну у плазмі. У таких випадках необхідний регулярний контроль концентрації тасонерміну в плазмі та корекція дози при необхідності. Інші комбінації лікарських засобів Препарати кальцію можуть зменшити ефект БМКК. При одночасному застосуванні БМКК з препаратами літію (для амлодипіну дані відсутні) можливе посилення прояву їхньої нейротоксичності (нудота, блювання, діарея, атаксія, тремор, шум у вухах). У ході клінічних досліджень лікарських взаємодій амлодипін не впливав на фармакокінетику аторвастатину, дигоксину, варфарину. Одноразовий прийом 100 мг силденафілу у пацієнтів з есенціальною гіпертензією не впливає на параметри фармакокінетики амлодипіну. Периндоприл Дані клінічних досліджень показують, що подвійна блокада РААС внаслідок одночасного застосування інгібіторів АПФ, АРА II або аліскірену призводить до збільшення частоти виникнення таких небажаних явищ, як артеріальна гіпотензія, гіперкаліємія та порушення функції нирок (включаючи гостру ниркову недостатність) порівняно з ситуаціями, коли застосовується лише один препарат, що впливає на РААС (див. розділи "Фармакологічні властивості. Фармакодинаміка", "Протипоказання", "Особливі вказівки"). Лікарські засоби, що викликають гіперкаліємію Деякі препарати можуть збільшувати ризик розвитку гіперкаліємії: аліскірен, солі калію, калійзберігаючі діуретики, інгібітори АПФ, АРА II, нестероїдні протизапальні препарати (НПЗП), гепарин, імунодепресанти, такі як циклоспорин або такролімус, триметоприм, ко-тримоксазол). Поєднання цих препаратів збільшує ризик розвитку гіперкаліємії. Циклоспорин: при одночасному застосуванні інгібіторів АПФ з циклоспорином можливий розвиток гіперкаліємії. Рекомендується контролювати вміст калію у сироватці крові. Гепарин: можливе підвищення вмісту калію у сироватці крові. Рекомендується контролювати вміст калію у сироватці крові. Одночасне застосування протипоказане Аліскірен та лікарські препарати, що містять аліскірен Одночасне застосування інгібіторів АПФ з лікарськими препаратами, що містять аліскірен, протипоказане у пацієнтів з цукровим діабетом та/або помірним або тяжким порушенням функції нирок (ШКФ менше 60 мл/хв/1,73 м(2) площі поверхні тіла) та не рекомендується у інших пацієнтів. (Див. розділ «Протипоказання»). Зростає ризик розвитку гіперкаліємії, погіршення функції нирок, серцево-судинної захворюваності та смертності. Екстракорпоральна терапія Екстракорпоральні методи лікування, що ведуть до контакту крові з негативно зарядженими поверхнями, такі як діаліз або гемофільтрація з використанням деяких високопроточних мембран (наприклад, поліакрилонітрилових), або аферез ЛПНГ з використанням декстрану сульфату, протипоказані через збільшення ризику розвитку тяжких анафілактоїд. розділ "Протипоказання"). Якщо пацієнту потрібна екстракорпоральна терапія, слід розглянути можливість використання іншого типу діалізної мембрани чи іншого класу гіпотензивних препаратів. Інгібітори нейтральної ендопептидази При одночасному застосуванні інгібіторів АПФ з лікарськими препаратами, що містять сакубітрил (інгібітор неприлізину), зростає ризик розвитку ангіоневротичного набряку, через що одночасне застосування зазначених препаратів протипоказане. Інгібітори АПФ слід призначати не раніше ніж через 36 годин після відміни препаратів, що містять сакубітрил. Протипоказано призначення препаратів, що містять сакубітрил, пацієнтам, які отримують інгібітори АПФ, а також протягом 36 годин після відміни інгібіторів АПФ. Нерекомендовані поєднання лікарських засобів Аліскірен та лікарські препарати, що містять аліскірен У пацієнтів, які не мають цукрового діабету або порушення функції нирок, можливе підвищення ризику гіперкаліємії, погіршення функції нирок та підвищення частоти серцево-судинної захворюваності та смертності. Одночасне призначення інгібіторів АПФ та АРА II За наявними літературними даними, у пацієнтів із встановленим діагнозом атеросклерозу, серцевою недостатністю або цукровим діабетом з ураженням органів-мішеней одночасний прийом інгібіторів АПФ та АРА II призводить до збільшення частоти розвитку артеріальної гіпотензії, непритомності, гіперкаліємії та погіршення функції нирок. порівняно із ситуаціями, коли застосовується лише один препарат, що впливає на РААС. Застосування подвійної блокади РААС (наприклад, одночасний прийом інгібіторів АПФ та АРА II) повинно бути обмежене поодинокими випадками із суворим контролем функції нирок, вмісту калію у плазмі крові та АТ (див. розділ «Особливі вказівки»). Естрамустін Одночасне застосування естрамустину з інгібіторами АПФ супроводжується підвищеним ризиком розвитку ангіоневротичного набряку. Ко-тримоксазол (триметоприм + сульфаметоксазол) При одночасному застосуванні з котримоксазолом (триметоприм + сульфаметоксазол) може підвищуватися ризик розвитку гіперкаліємії (див. розділ «Особливі вказівки»). Калійзберігаючі діуретики (наприклад, тріамтерен, амілорид) та солі калію Зазвичай вміст калію в плазмі залишається в межах норми, при цьому у деяких пацієнтів, які отримують інгібітори АПФ, може розвинутись гіперкаліємія. Застосування калійзберігаючих діуретиків (наприклад, спіронолактону, тріамтерену, еплеренону або амілориду), калійвмісних замінників кухонної солі, інших препаратів, що сприяють підвищенню вмісту калію в плазмі може призвести до значного збільшення вмісту калію в сироватці крові. Слід також бути обережними при одночасному призначенні периндоприлу з іншими препаратами, здатними збільшувати вміст калію в сироватці крові, такими як триметоприм і ко-тримоксазол (триметоприм + сульфаметоксазол), так як відомо, що триметоприм діє як калійзберігаючий діуретик, такий якТому одночасне застосування периндоприлу з вищезазначеними препаратами не рекомендується. Якщо, однак, одночасне застосування показано, слід застосовувати з дотриманням запобіжних заходів та регулярним контролем вмісту калію в сироватці крові. Препарати літію При одночасному застосуванні препаратів літію та інгібіторів АПФ може виникати оборотне підвищення вмісту літію у плазмі крові та пов'язані з цим токсичні ефекти (важкі нейротоксичні ефекти). Одночасне застосування периндоприлу та препаратів літію не рекомендується. За необхідності проведення такої терапії необхідний регулярний контроль вмісту літію в плазмі (див. розділ «Особливі вказівки»). Поєднання лікарських засобів, що потребують особливої уваги Гіпоглікемічні засоби (інсулін, похідні сульфонілсечовини) Згідно з даними, отриманими в епідеміологічних дослідженнях, інгібітори АПФ можуть посилювати гіпоглікемічний ефект інсуліну та похідних сульфонілсечовини з ризиком розвитку гіпоглікемії. Даний ефект найімовірніше можна спостерігати у перші тижні одночасного застосування та у пацієнтів з порушенням функції нирок. Калійнесберігаючі діуретики У пацієнтів, які отримують діуретики, особливо у пацієнтів з гіповолемією та/або зниженою концентрацією солей, на початку терапії периндоприлом може спостерігатися виражене зниження АТ, ризик розвитку якого можна зменшити шляхом відміни діуретичного засобу, заповненням втрати рідини або солей перед початком терапії периндоприлом, а також призначенням периндоприлу у низькій дозі з подальшим поступовим її збільшенням. При АГ у пацієнтів з гіповолемією або зниженим вмістом солей на фоні терапії діуретиками діуретики повинні бути або скасовані до початку застосування інгібітору АПФ (при цьому калійнесберігаючий діуретик може бути пізніше знову призначений), або інгібітор АПФ повинен бути призначений у низькій дозі з подальшим поступовим її збільшенням. . При застосуванні діуретиків у разі ХСН інгібітор АПФ повинен бути призначений у дуже низькій дозі, можливо, після зменшення дози одночасного калійнесберігаючого діуретика. У всіх випадках функція нирок (концентрація креатиніну в плазмі крові) повинна контролюватись у перші тижні застосування інгібіторів АПФ. Калійзберігаючі діуретики (застосування еплеренону, спіронолактону в дозах від 12,5 мг до 50 мг на добу та низьких доз інгібіторів АПФ) При лікуванні ХСН II-IV функціонального класу за класифікацією NYHA з фракцією викиду лівого шлуночка < 40 % у пацієнтів, які раніше отримували інгібітори АПФ та «петлеві» діуретики, існує ризик розвитку гіперкаліємії (з можливим летальним наслідком), особливо у разі недотримання рекомендацій щодо цієї комбінації. препаратів. Перед початком застосування цієї комбінації лікарських препаратів необхідно переконатися у відсутності гіперкаліємії та порушення функції нирок. Рекомендується регулярно контролювати концентрацію креатиніну та вміст калію в плазмі крові: щотижня у перший місяць лікування та щомісяця у подальшому. Рацекадотрил Повідомлялося про підвищений ризик розвитку ангіоневротичного набряку при одночасному застосуванні інгібіторів АПФ та рацекадотрилу (інгібітор енкефалінази). Тканинні активатори плазміногену В обсерваційних дослідженнях виявлено підвищену частоту розвитку ангіоневротичного набряку у пацієнтів, які приймали інгібітори АПФ після застосування алтеплази для тромболітичної терапії ішемічного інсульту. Інгібітори mTOR (наприклад, сиролімус, еверолімус, темсіролімус) У пацієнтів, які одночасно отримують терапію інгібіторами mTOR, підвищується ризик розвитку ангіоневротичного набряку (див. розділ «Особливі вказівки»). НПЗЗ, включаючи високі дози ацетилсаліцилової кислоти (≥ 3 г/добу) Одночасне застосування інгібіторів АПФ з нестероїдними протизапальними засобами (ацетилсаліцилова кислота в дозі, що має протизапальну дію, інгібітори циклооксигенази-2 [ЦОГ-2] і неселективні нестероїдні протизапальні засоби), може призвести до зниження антигіпертензивної дії інгібіторів АПФ. Одночасне застосування інгібіторів АПФ та НПЗЗ може призводити до погіршення функції нирок, включаючи розвиток гострої ниркової недостатності, та збільшення вмісту калію у сироватці крові, особливо у пацієнтів зі зниженою функцією нирок. Слід бути обережними при призначенні даної комбінації, особливо у пацієнтів похилого віку. Пацієнтам необхідно компенсувати втрату рідини та ретельно контролювати функцію нирок як на початку лікування, так і в процесі лікування. Поєднання лікарських засобів, що потребують уваги Інгібітори дипептидилпептидази IV (ДПП-IV) (гліптини), наприклад, лінагліптин, саксагліптин, сітагліптин, віллдагліптин Одночасне застосування з інгібіторами АПФ може збільшувати ризик розвитку ангіоневротичного набряку внаслідок пригнічення активності ДПП-IVгліптином. Симпатоміметики Можуть послаблювати антигіпертензивний ефект інгібіторів АПФ. Препарати золота При застосуванні інгібіторів АПФ, у тому числі периндоприлу, у пацієнтів, які отримують внутрішньовенно препарат золота (натрію ауротіомалат), були описані нітритоїдні реакції, з частотою виникнення «рідко» (симптомокомплекс, що включає гіперемію шкіри обличчя, нудоту, блювання, артеріальну гіпотензію). Алопуринол, імуносупресивні засоби, кортикостероїди (при системному застосуванні) та прокаїнамід Одночасне застосування з інгібіторами AПФ може супроводжуватися підвищеним ризиком розвитку лейкопенії, особливо у пацієнтів із наявними порушеннями функції нирок. Засоби для загальної анестезії Одночасне застосування інгібіторів АПФ та засобів для загальної анестезії може призводити до антигіпертензивного ефекту. Поєднання лікарських засобів, що потребують особливої уваги Баклофен Можливе посилення антигіпертензивної дії. Слід контролювати АТ та функцію нирок, за необхідності провести корекцію дози амлодипіну. Поєднання препаратів, що потребує уваги Гіпотензивні засоби (наприклад, бета-адреноблокатори) та вазодилататори Можливе посилення антигіпертензивного ефекту периндоприлу та амлодипіну. Слід бути обережними при одночасному застосуванні з нітрогліцерином, іншими нітратами або іншими вазодилататорами, оскільки при цьому можливе додаткове зниження АТ. Кортикостероїди (мінерало- та глюкокортикостероїди), тетракозактид Зниження антигіпертензивної дії (затримка рідини та іонів натрію внаслідок дії кортикостероїдів). Альфа-адреноблокатори (празозин, альфузозин, доксазозин, тамсулозин, теразозин) Посилення антигіпертензивної дії та підвищення ризику розвитку ортостатичної гіпотензії. Аміфостін Можливе посилення антигіпертензивного ефекту амлодипіну. Трициклічні антидепресанти/нейролептики/засоби для загальної анестезії Посилення антигіпертензивної дії та підвищення ризику розвитку ортостатичної гіпотензії.Спосіб застосування та дозиВсередину, по одній таблетці 1 раз на день, переважно вранці перед їдою. Доза лікарського препарату Дальнева® підбирається після раніше проведеного підбору доз окремих компонентів препарату: периндоприлу та амлодипіну у пацієнтів з артеріальною гіпертензією та стабільною стенокардією. При терапевтичній необхідності доза лікарського препарату Дальнева® може бути змінена на підставі індивідуального підбору доз окремих компонентів: амлодипін 5 мг + периндоприл 4 мг або амлодипін 10 мг + периндоприл 4 мг, або амлодипін 5 мг + периндоприл 8 мг, або амлодипін 10 мг . Максимальна добова доза: амлодипін – 10 мг + периндоприл – 8 мг.ПередозуванняІнформація про передозування препаратом Дальнева відсутня. Амлодипін Інформація про передозування амлодипіном обмежена. Симптоми: виражене зниження АТ з можливим розвитком рефлекторної тахікардії та надмірної периферичної вазодилатації (ризик розвитку вираженої та стійкої артеріальної гіпотензії, у т.ч. з розвитком шоку та летального результату). Лікування: промивання шлунка, призначення активованого вугілля (особливо в перші 2 години після передозування), підтримання функції серцево-судинної системи, підвищене положення нижніх кінцівок, контроль ОЦК та діурезу, симптоматична та підтримуюча терапія. Для відновлення тонусу судин – застосування судинозвужувальних засобів (за відсутності протипоказань до їх застосування), для усунення наслідків блокади кальцієвих каналів – внутрішньовенне введення розчину глюконату. Гемодіаліз неефективний. Периндоприл Дані передозування периндоприлом обмежені. Симптоми: виражене зниження артеріального тиску, шок, порушення водно-електролітного балансу, ниркова недостатність, гіпервентиляція легень, тахікардія, відчуття серцебиття, брадикардія, запаморочення, неспокій та кашель. Лікування: заходи невідкладної допомоги зводяться до виведення препарату з організму: промивання шлунка та/або призначення активованого вугілля з подальшим відновленням ОЦК. При вираженому зниженні артеріального тиску слід перевести пацієнта в положення «лежачи» на спині з піднятими ногами, за необхідності провести заходи для відновлення ОЦК (наприклад, внутрішньовенна інфузія 0,9 % розчину натрію хлориду). Також можливе внутрішньовенне введення катехоламінів. За допомогою гемодіалізу можна видалити периндоприл із системного кровотоку. При брадикардії, резистентної до терапії, може знадобитися імплантація електрокардіостимулятора. Необхідний динамічний контроль загального стану, концентрації креатиніну та вмісту електролітів у плазмі крові.Запобіжні заходи та особливі вказівкиОсобливі вказівки, що стосуються периндоприлу та амлодипіну, застосовні і до лікарського препарату Дальнєва®. Амлодипін Ефективність та безпека застосування амлодипіну при гіпертонічному кризі не встановлено. Серцева недостатність Лікування пацієнтів із серцевою недостатністю слід проводити з обережністю. При застосуванні амлодипіну у пацієнтів з ХСН III та IV функціонального класу за класифікацією NYHA можливий розвиток набряку легень. БМКК, включаючи амлодипін, необхідно з обережністю застосовувати у пацієнтів з ХСН у зв'язку з можливим збільшенням ризику розвитку небажаних явищ з боку серцево-судинної системи та смертності. Печінкова недостатність У пацієнтів з порушенням функції печінки Т(½) та AUCамлодипіну збільшуються. Рекомендації щодо дозування препарату не встановлені. Прийом амлодипіну необхідно почати з найнижчих доз і дотримуватися запобіжних заходів як на початку лікування, так і при збільшенні дози. Пацієнтам з тяжкою печінковою недостатністю підвищувати дозу слід поступово, забезпечуючи ретельний моніторинг клінічного стану. Пацієнти похилого віку У пацієнтів похилого віку збільшення дози слід проводити з обережністю (див. розділ «Спосіб застосування та дози» та «Фармакологічні властивості. Фармакокінетика»). Ниркова недостатність Пацієнти з нирковою недостатністю можуть приймати амлодипін у стандартних дозах. Зміни плазмових концентрацій амлодипіну не корелюють зі ступенем ниркової недостатності. Амлодипін не виводиться з організму за допомогою діалізу. Мітральний стеноз/аортальний стеноз/ГЗКМП Амлодипін протипоказаний пацієнтам із обструкцією вихідного тракту лівого шлуночка. Синдром «скасування» Незважаючи на відсутність у БМКК синдрому «скасування», припинення лікування препаратом Дальнєва бажано проводити поступово, зменшуючи дозу препарату. Амлодипін не запобігає розвитку синдрому «скасування» при різкому припиненні прийому бета-адреноблокаторів. Периферичні набряки Незначно або помірно виражені периферичні набряки були найчастішим небажаним явищем амлодипіну у клінічних дослідженнях. Частота виникнення периферичних набряків зростає зі збільшенням дози (при застосуванні амлодипіну у дозі 2,5 мг, 5 мг та 10 мг на добу набряки виникали відповідно у 1,8 %, 3 % та 10 % пацієнтів). Слід ретельно диференціювати периферичні набряки, пов'язані із застосуванням амлодипіну, від симптомів прогресування лівшлуночкової серцевої недостатності. Інше Необхідна підтримка гігієни зубів та спостереження у стоматолога (для запобігання болючості, кровоточивості та гіперплазії ясен). Периндоприл Підвищена чутливість/ангіоневротичний набряк (набряк Квінке) При застосуванні інгібіторів АПФ, у тому числі периндоприлу, в окремих випадках може спостерігатися розвиток ангіоневротичного набряку особи, губ, язика, голосових складок та/або гортані. Це може статися у будь-який період. При появі цих симптомів застосування препарату Дальнева® повинно бути негайно припинено, пацієнт повинен спостерігатися доти, доки ознаки набряку не зникнуть повністю. препарати. Ангіоневротичний набряк, що супроводжується набряком язика або гортані, може призвести до обструкції дихальних шляхів та летального результату.5 мл) та/або забезпечити прохідність дихальних шляхів. Пацієнт повинен перебувати під медичним наглядом до повного та стійкого зникнення симптомів. У пацієнтів, в анамнезі яких відзначався набряк Квінке, не пов'язаний із застосуванням інгібіторів АПФ, може бути підвищений ризик його розвитку на фоні застосування препаратів цієї групи (див. розділ "Протипоказання"). У поодиноких випадках на тлі терапії інгібіторами АПФ розвивається інтестинальний ангіоневротичний набряк (ангіоневротичний набряк кишечника). При цьому у пацієнтів відзначається біль у животі як ізольований симптом або у поєднанні з нудотою та блюванням, у деяких випадках без попереднього ангіоневротичного набряку обличчя та при нормальній сироватковій концентрації С1-естерази. Діагноз встановлюється за допомогою комп'ютерної томографії черевної порожнини, ультразвукового дослідження або на момент хірургічного втручання. Симптоми зникають після припинення інгібіторів АПФ. Тому у пацієнтів з болем у животі, які отримують інгібітори АПФ, при проведенні диференціального діагнозу необхідно враховувати можливість розвитку інтестинального ангіоневротичного набряку (див. розділ «Побічна дія»). При одночасному застосуванні інгібіторів АПФ з рацекадотрилом, інгібіторами mTOR (наприклад, темсиролімусом, еверолімусом, сиролімусом) або ДПП-IV (гліптинами, включаючи віллдагліптин) підвищується ризик розвитку ангіоневротичного набряку (наприклад, набряк верхніх дихальних шляхів). ) (див. розділ «Взаємодія з іншими лікарськими засобами»). Слід виявляти обережність на початку терапії рацекадотрилом, інгібіторами mTOR (наприклад, тимсиролімусом, еверолімусом, сиролімусом) або гліптинами, включаючи віллдагліптин, при одночасному застосуванні з інгібіторами АПФ. Анафілактоїдні реакції при проведенні процедур десенсибілізації Є окремі повідомлення про розвиток тривалих, що загрожують життю анафілактоїдних реакцій у пацієнтів, які отримують інгібітори АПФ під час десенсибілізуючої терапії отрутою перетинчастокрилих комах. У цих пацієнтів анафілактоїдної реакції вдавалося уникнути шляхом тимчасової відміни інгібіторів АПФ, а при випадковому прийомі препарату анафілактоїдна реакція виникала знову. Анафілактоїдні реакції при проведенні аферезу ЛПНЩ за допомогою декстрану сульфату У поодиноких випадках у пацієнтів, які отримують інгібітори АПФ, при проведенні аферезу ЛПНЩ з використанням декстрану сульфату можуть розвиватися анафілактоїдні реакції, що загрожують життю. Для запобігання анафілактоїдної реакції слід тимчасово припинити терапію інгібітором АПФ перед кожною процедурою аферезу ЛПНЩ з використанням декстрану сульфату. Нейтропенія/агранулоцитоз, тромбоцитопенія та анемія У пацієнтів, які приймають інгібітори АПФ, можливі випадки розвитку нейтропенії/агранулоцитозу, тромбоцитопенії та анемії. У пацієнтів з нормальною функцією нирок без інших обтяжливих факторів нейтропенія розвивається рідко. Особливою обережністю периндоприл слід застосовувати у пацієнтів із системними захворюваннями сполучної тканини, на фоні прийому імунодепресантів, алопуринолу або прокаїнаміду, особливо у пацієнтів з порушеною функцією нирок. У деяких пацієнтів виникали важкі інфекції, у ряді випадків стійкі до інтенсивної антибіотикотерапії. При призначенні периндоприлу таким пацієнтам рекомендується періодично контролювати кількість лейкоцитів у крові. Пацієнти повинні повідомляти лікаря про будь-які ознаки інфекційних захворювань (наприклад, біль у горлі, гарячка). Реноваскулярна гіпертензія У пацієнтів із двостороннім стенозом ниркових артерій або стенозом артерії єдиної функціонуючої нирки на фоні терапії інгібіторами АПФ зростає ризик розвитку артеріальної гіпотензії та ниркової недостатності. Прийом діуретиків може бути додатковим фактором ризику. Погіршення функції нирок може спостерігатися вже при незначній зміні концентрації креатиніну у сироватці, навіть у пацієнтів з одностороннім стенозом ниркової артерії. Подвійна блокада РААС Є дані, що свідчать про те, що одночасне застосування інгібіторів АПФ, АРА II або аліскірену підвищує ризик розвитку гіпотензії, гіперкаліємії та порушення функції нирок (включаючи гостру ниркову недостатність). Одночасне застосування інгібіторів АПФ з препаратами, що містять аліскірен, протипоказане у пацієнтів з цукровим діабетом та/або помірною або тяжкою нирковою недостатністю (ШКФ менше 60 мл/хв/1,73 м(2) площі поверхні тіла) та не рекомендується у інших пацієнтів. Якщо терапія за допомогою подвійної блокади РААС визнана абсолютно необхідною, її слід проводити лише під суворим медичним контролем та при регулярному контролі функції нирок, вмісту електролітів у плазмі крові та АТ.Протипоказане застосування інгібіторів АПФ одночасно з АРА II у пацієнтів з діабетичною нефропатією та не рекомендується у інших пацієнтів (див. розділ "Протипоказання"). Первинний гіперальдостеронізм Пацієнти з первинним гіперальдостеронізмом, як правило, не сприйнятливі до гіпотензивних препаратів, дія яких ґрунтується на інгібуванні РААС. Тому прийом препарату не рекомендовано. Артеріальна гіпотензія Інгібітори АПФ можуть викликати різке зниження артеріального тиску. Симптоматична гіпотензія рідко розвивається у пацієнтів без супутніх захворювань. Ризик вираженого зниження АТ підвищений у пацієнтів зі зниженим ОЦК, що може відзначатися на фоні терапії діуретиками, при дотриманні суворої дієти без солі, гемодіалізі, діареї та блюванні, а також у пацієнтів з тяжким ступенем АГ з високою активністю реніну (див. розділи «Взаємодія з іншими лікарськими засобами» та «Побічна дія»). У пацієнтів з підвищеним ризиком розвитку симптоматичної артеріальної гіпотензії необхідно ретельно контролювати АТ, функцію нирок та вміст калію у сироватці крові під час терапії лікарським препаратом Дальнєва®. Подібний підхід застосовується і у пацієнтів зі стенокардією та цереброваскулярними захворюваннями, у яких виражена артеріальна гіпотензія може призвести до інфаркту міокарда або порушення мозкового кровообігу. У разі розвитку артеріальної гіпотензії пацієнт повинен бути переведений у положення «лежачи» на спині з піднятими ногами. При необхідності слід заповнити ОЦК за допомогою внутрішньовенного введення 0,9% натрію розчину хлориду. Минуща артеріальна гіпотензія не є перешкодою для подальшого прийому препарату. Після відновлення ОЦК та АТ лікування може бути продовжено. Мітральний стеноз/аортальний стеноз/ГЗКМП Периндоприл, як і інші інгібітори АПФ, повинен обережно призначатися у пацієнтів з обструкцією вихідного тракту лівого шлуночка (аортальний стеноз, ГОКМП), а також у пацієнтів з мітральним стенозом. Амлодипін протипоказаний пацієнтам із обструкцією вихідного тракту лівого шлуночка. Порушення функції нирок Пацієнтам з нирковою недостатністю (КК менше 60 мл/хв) рекомендується індивідуальний підбір доз периндоприлу та амлодипіну (див. розділ «Спосіб застосування та дози»). Таким пацієнтам необхідний регулярний контроль вмісту калію та концентрації креатиніну у сироватці крові (див. розділ «Побічна дія»). У пацієнтів із двостороннім стенозом ниркової артерії або стенозом артерії єдиної нирки на фоні терапії інгібіторами АПФ можливе підвищення концентрацій сечовини та креатиніну у сироватці крові, що зазвичай відбувається при відміні терапії. Найчастіше цей ефект відзначається у пацієнтів із нирковою недостатністю. Додаткова наявність реноваскулярної гіпертензії зумовлює підвищений ризик розвитку тяжкої гіпотензії та ниркової недостатності у таких пацієнтів. У деяких пацієнтів з артеріальною гіпертензією без ознак ураження судин нирок можливе підвищення концентрацій сечовини та креатиніну в сироватці крові, особливо при одночасному призначенні периндоприлу з діуретиком, зазвичай незначне та минуще. Найчастіше цей ефект відзначається у пацієнтів із попереднім порушенням функції нирок. Порушення функції печінки У поодиноких випадках на фоні прийому інгібіторів АПФ виникає холестатична жовтяниця. При прогресуванні цього синдрому розвивається фульмінантний некроз печінки, іноді з летальним кінцем. Механізм розвитку цього синдрому незрозумілий. У разі появи жовтяниці або значного підвищення активності «печінкових» ферментів у плазмі крові на фоні прийому інгібіторів АПФ слід припинити прийом препарату (див. розділ «Побічна дія») та звернутися до лікаря. Етнічні відмінності У пацієнтів негроїдної раси частіше, ніж у інших рас, на фоні застосування інгібіторів АПФ розвивається ангіоневротичний набряк. Периндоприл, як і інші інгібітори АПФ, може мати менш виражену антигіпертензивну дію у пацієнтів негроїдної раси порівняно з представниками інших рас. Можливо, ця відмінність зумовлена тим, що у пацієнтів негроїдної раси з артеріальною гіпертензією частіше відзначається низька активність реніну плазми крові. Кашель На тлі терапії інгібітором АПФ може виникати сухий кашель. Кашель тривалий час зберігається на фоні прийому препаратів цієї групи і зникає після їх відміни. Це слід враховувати під час проведення диференціальної діагностики кашлю. Хірургічні втручання/загальна анестезія У пацієнтів, яким планується проведення великого оперативного втручання та/або застосування засобів для загальної анестезії, що викликають гіпотензію, застосування периндоприлу може блокувати утворення ангіотензину II на тлі компенсаторного вивільнення реніну. Лікування слід припинити за добу до хірургічного втручання. При розвитку артеріальної гіпотензії за вказаним механізмом слід підтримувати артеріальний тиск шляхом заповнення ОЦК. Гіперкаліємія Інгібітори АПФ можуть викликати гіперкаліємію, оскільки вони пригнічують вивільнення альдостерону. Цей ефект зазвичай незначний у пацієнтів із нормальною функцією нирок. Однак у пацієнтів з порушенням функції нирок та/або у пацієнтів, які одночасно приймають препарати, що містять калій (включаючи калійвмісні замінники кухонної солі), калійзберігаючі діуретики, триметоприм або ко-тримоксазол (фіксована комбінація триметоприму і сульфаметоксазолу), і особливо антагон можливий розвиток гіперкаліємії. Факторами ризику гіперкаліємії є ниркова недостатність, порушення функції нирок, вік старше 70 років, цукровий діабет, інтеркурентні стани (зокрема, дегідратація, гостра декомпенсація ХСН, метаболічний ацидоз), одночасне застосування калійзберігаючих діуретиків (наприклад,спіронолактон, еплеренон, тріамтерен або амілорид), препаратів калію або замінників калію кухонної солі або одночасне застосування інших препаратів, що сприяють підвищенню вмісту калію в плазмі крові (наприклад, гепарин, ко-тримоксазол). Гіперкаліємія може призвести до серйозних порушень серцевого ритму, іноді з летальним кінцем. Калійзберігаючі діуретики та АРА II слід застосовувати з обережністю у пацієнтів, які отримують інгібітори АПФ, та регулярно контролювати вміст калію у сироватці крові та функцію нирок (див. розділ «Взаємодія з іншими лікарськими засобами»).ко-тримоксазол). Гіперкаліємія може призвести до серйозних порушень серцевого ритму, іноді з летальним кінцем. Калійзберігаючі діуретики та АРА II слід застосовувати з обережністю у пацієнтів, які отримують інгібітори АПФ, та регулярно контролювати вміст калію у сироватці крові та функцію нирок (див. розділ «Взаємодія з іншими лікарськими засобами»).ко-тримоксазол). Гіперкаліємія може призвести до серйозних порушень серцевого ритму, іноді з летальним кінцем. Калійзберігаючі діуретики та АРА II слід застосовувати з обережністю у пацієнтів, які отримують інгібітори АПФ, та регулярно контролювати вміст калію у сироватці крові та функцію нирок (див. розділ «Взаємодія з іншими лікарськими засобами»). Пацієнти з цукровим діабетом При призначенні препарату пацієнтам з цукровим діабетом, які отримують гіпоглікемічні засоби для внутрішнього застосування або інсуліну, протягом першого місяця терапії необхідно ретельно контролювати концентрацію глюкози в крові (див. розділ «Взаємодія з іншими лікарськими засобами») Застосування препарату Дальнева у пацієнтів з гострим інфарктом міокарда не рекомендується через недостатній досвід клінічного застосування. Застосування при хронічних захворюваннях: Пацієнти з порушенням функції нирок Лікарський препарат Дальнєва може застосовуватися у пацієнтів з КК рівним або більше 60 мл/хв. Лікарський препарат Дальнєва протипоказаний до застосування у пацієнтів з КК менше 60 мл/хв. Таким пацієнтам рекомендується індивідуальний підбір доз периндоприлу та амлодипіну. Зміна концентрації амлодипіну в плазмі не корелює зі ступенем вираженості ниркової недостатності. Пацієнти похилого віку та пацієнти з порушенням функції печінки Необхідно зменшити початкову дозу препарату Дальнєва до найменшої дози амлодипіну (тобто до 1 таблетки амлодипін 5 мг + периндоприл 4 мг або амлодипін 5 мг + периндоприл 8 мг). Вплив на керування транспортними засобами: У зв'язку з можливістю виникнення запаморочення, сонливості та інших побічних ефектів на фоні застосування препарату Дальнева® необхідно дотримуватись обережності при керуванні транспортними засобами та роботі з іншими технічними пристроями, що потребують підвищеної концентрації уваги та швидкості психомоторних реакцій, особливо на початку лікування та збільшення дози.Умови відпустки з аптекЗа рецептомВідео на цю тему