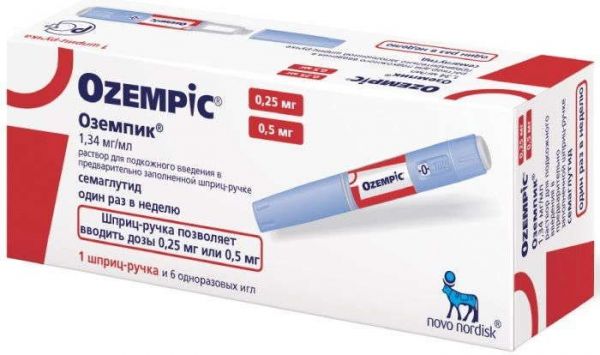
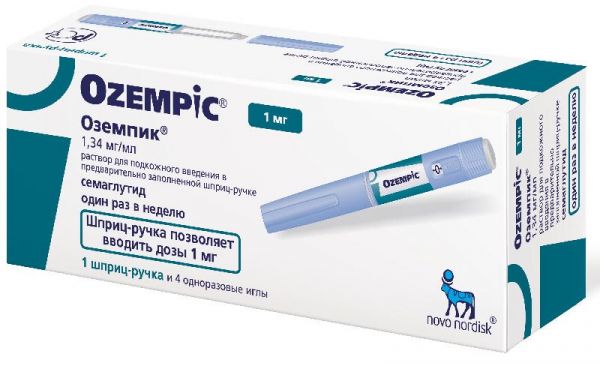
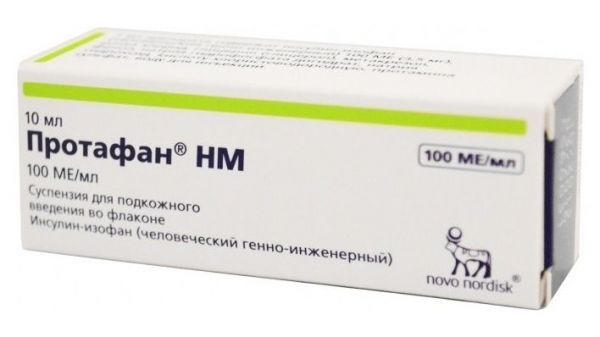
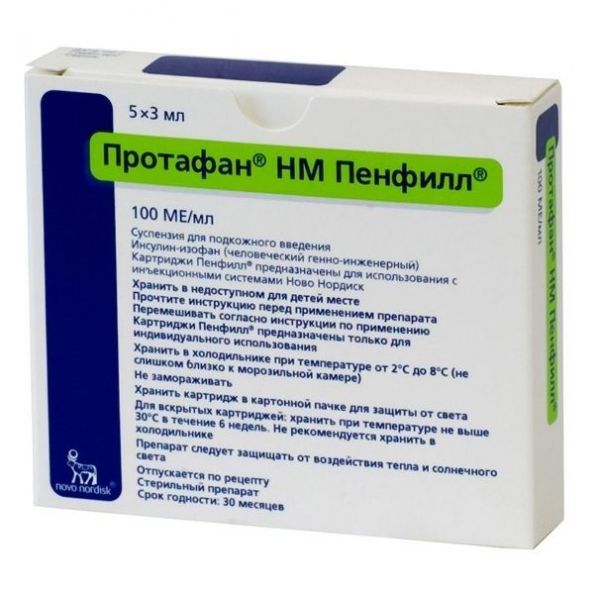
Инсулины Ново Нордиск А/С
Склад, форма випуску та упаковкаРозчин - 1 мл: активна речовина: інсулін розчинний (людський генноінженерний) 100 ME (3,5 мг); 1 ME відповідає 0,035 мг безводного людського інсуліну; допоміжні речовини: цинк 7 мкг (у вигляді цинку хлориду), гліцерин (гліцерол) 16 мг, метакрезол 3,0 мг, натрію гідроксид близько 2,6 мг та/або хлористоводнева кислота близько 1,7 мг (для коригування pН), вода для ін'єкцій до 1 мл. 1 флакон містить 10 мл препарату, що відповідає 1000ME. 1 шприц-ручка містить 3 мл препарату, що відповідає 300 МО. Розчин для ін'єкцій, 100 МО/мл. По 10 мл препарату у флакон зі скла 1 гідролітичного класу, закупорений пробкою з бромбутилової гуми/поліізопрену під алюмінієвою обкаткою та захисним пластмасовим ковпачком. По 1 флакону разом з інструкцією та застосування в картонну пачку. По 3 мл препарату в картриджі зі скла I гідролітичного класу, закупорені дисками з бромбутилової гуми/поліізопрену з одного боку та поршнями з бромбутилової гуми з іншого боку. Картридж запаяний у мультидозову одноразову поліпропіленову шприц-ручку для багаторазових ін'єкцій ФлексПен®. По 5 мультидозових одноразових шприц-ручок разом з інструкцією та застосуванням у картонну пачку.Опис лікарської формиПрозора, безбарвна рідина.Фармакотерапевтична групаГіпоглікемічний засіб – інсулін короткої дії.ФармакокінетикаПеріод напіввиведення інсуліну з кровотоку дорівнює всього кілька хвилин. Тривалість дії препаратів інсуліну здебільшого обумовлена швидкістю всмоктування, яка залежить від кількох факторів (наприклад, від дози інсуліну, способу та місця введення, товщини підшкірного жирового шару та типу цукрового діабету). Тому фармакокінетичні параметри інсуліну схильні до значних інтер- та інтраіндивідуальних коливань. Всмоктування Максимальна концентрація (Сmах) інсуліну в плазмі досягається протягом 1,5-2,5 годин після підшкірного введення. Розподіл Вираженого зв'язування з білками плазми не відзначається, за винятком циркулюючих антитіл до інсуліну (у разі їх наявності). Метаболізм Людський інсулін розщеплюється під дією інсуліназ або інсулінрозщеплювальних ферментів, а також, можливо, під дією протеїндисульфідізомерази. Передбачається, що в молекулі людського інсуліну є кілька ділянок розщеплення (гідролізу), проте жоден з метаболітів, що утворюються внаслідок розщеплення, не є активним. Виведення Період напіввиведення (Т1/2) визначається за швидкістю всмоктування з підшкірних тканин. Таким чином, Т1/2 швидше є мірою всмоктування, а не власне мірою виведення інсуліну з плазми (Т1/2 інсуліну з кровотоку дорівнює всього кілька хвилин). Дослідження показали, що Т1/2 становить близько 2-5 годин. Діти та підлітки Фармакокінетичний профіль препарату Актрапід НМ вивчали на нечисленній групі дітей з цукровим діабетом (18 осіб) у віці 6-12 років, а також підлітків (у віці 13-17 років). Хоча отримані дані вважаються обмеженими, але вони все ж таки показали, що фармакокінетичний профіль препарату Актрапид® НМ у дітей та підлітків подібний до дорослих. Разом з тим були виявлені відмінності між різними віковими групами за таким показником як Сmax, що ще раз наголошує на необхідності індивідуального підбору дози. Дані доклінічного дослідження безпеки У ході доклінічних досліджень, що включали фармакологічні дослідження безпеки, дослідження токсичності при повторному введенні дози, дослідження генотоксичності, канцерогенного потенціалу та токсичного впливу на репродуктивну сферу, специфічного ризику для людини не було виявлено.ФармакодинамікаАктрапид® НМ – препарат інсуліну короткої дії, вироблений методом біотехнології рекомбінантної ДНК з використанням штаму Saccharomyces cerevisiae. Зниження концентрації глюкози в крові відбувається за рахунок підвищення її внутрішньоклітинного транспорту після зв'язування інсуліну з інсуліновими рецепторами м'язової та жирової тканини та одночасного зниження швидкості продукції глюкози печінкою. Нормалізація концентрації глюкози в плазмі (до 4,4-6,1 ммоль/л) при внутрішньовенному введенні препарату Актрапид® НМ у пацієнтів відділення інтенсивної терапії, які перенесли серйозні хірургічні втручання (204 пацієнти з цукровим діабетом та 1344 пацієнти без цукрового діабету), та гіперглікемію (концентрацію глюкози в плазмі > 10 ммоль/л) дозволила знизити смертність на 42% (4,6% замість 8%). Дія препарату Актрапід НМ починається протягом півгодини після введення, а максимальний ефект проявляється протягом 1,5-3,5 годин, при цьому загальна тривалість дії становить близько 7-8 годин.ІнструкціяАктрапід® НМ призначений для підшкірних ін'єкцій. Щоразу змінюйте місце ін'єкції у межах анатомічної області. Це допоможе зменшити ризик утворення ущільнень та виразок у місці ін'єкції. Найкращими місцями для ін'єкцій є область передньої черевної стінки, сідниць, передньої поверхні стегна або плеча. Інсулін діятиме швидше, якщо він введений в ділянку передньої черевної стінки. В особливих випадках Актрапід НМ можна вводити внутрішньовенно, але такі процедури може проводити тільки медичний працівник. Як вводити препарат Актрапід НМ, якщо вводиться тільки Актрапід НМ або якщо необхідно змішати Актрапід НМ з інсуліном тривалої дії Переконайтеся, що ви використовуєте інсуліновий шприц, на якому нанесена шкала, що дозволяє відміряти дозу інсуліну в одиницях дії. Наберіть у шприц повітря у кількості, що відповідає потрібній дозі інсуліну. Виконуйте інструкції, які дав Вам лікар або медична сестра. Введіть інсулін під шкіру. Використовуйте ін'єкційну техніку, рекомендовану лікарем або медичною сестрою. Утримуйте голку під шкірою щонайменше 6 секунд, щоб переконатися, що доза інсуліну введена повністю.Показання до застосуванняЦукровий діабет, що потребує інсулінотерапії. Невідкладні стани у хворих на цукровий діабет, що супроводжуються порушенням глікемічного контролю.Протипоказання до застосуванняГіпоглікемія. Гіперчутливість до людського інсуліну або будь-якого компонента, що входить до складу даного препарату.Вагітність та лактаціяВагітність Обмежень застосування інсуліну в період вагітності не існує, оскільки інсулін не проникає через плацентарний бар'єр. Як гіпоглікемія, так і гіперглікемія, які можуть розвиватися у випадках недостатньо точно підібраної терапії, підвищують ризик виникнення вад розвитку плода та внутрішньоутробної загибелі плода. Вагітні жінки з цукровим діабетом протягом всієї вагітності повинні бути під наглядом, у них необхідно здійснювати посилений контроль концентрації глюкози в крові; такі ж рекомендації стосуються і жінок, які планують вагітність. Потреба в інсуліні зазвичай знижується у першому триместрі вагітності та поступово збільшується у другому та третьому триместрах. Після пологів потреба в інсуліні зазвичай швидко повертається до рівня, який відзначався до вагітності. Період грудного вигодовування Також не існує обмежень для застосування препарату Актрапід НМ у період грудного вигодовування. Проведення інсулінотерапії жінкам у період грудного вигодовування не становить небезпеки для дитини. Однак може знадобитися коригування режиму дозування препарату Актрапід НМ та/або дієти.Побічна діяНайпоширенішим побічним ефектом при застосуванні інсуліну є гіпоглікемія. У ході клінічних досліджень, а також у ході застосування препарату після його випуску на споживчий ринок було встановлено, що частота виникнення гіпоглікемії змінюється залежно від популяції пацієнтів, режиму дозування та контролю глікемії. На початковій стадії інсулінотерапії можуть виникати порушення рефракції, периферичні набряки та реакції в місцях введення препарату (що включають біль, почервоніння, кропив'янку, запалення, гематому, припухлість та свербіж у місці ін'єкції). Ці симптоми зазвичай мають тимчасовий характер. Швидке покращення контролю глікемії може призводити до стану "гострої больової нейропатії", яка зазвичай є оборотною. Інтенсифікація інсулінотерапії з різким покращенням контролю вуглеводного обміну може призвести до тимчасового погіршення стану діабетичної ретинопатії, водночас тривале покращення контролю глікемії знижує ризик прогресування діабетичної ретинопатії. Список побічних ефектів представлений у таблиці. Всі подані нижче побічні ефекти, засновані на даних, отриманих під час клінічних досліджень, розподілені по групах відповідно до частоти розвитку відповідно до McdDRA та систем органів. Частота розвитку побічних ефектів визначається як: дуже часто (≥ 1/10); часто (≥ 1/100 до Порушення з боку імунної системи: Нечасто - кропив'янка, висипання на шкірі; Дуже рідко – анафілактичні реакції. Порушення з боку обміну речовин та харчування: Дуже часто – гіпоглікемія. Порушення з боку нервової системи: Нечасто – периферична нейропатія ("гостра больова нейропатія"). Порушення з боку органу зору: Нечасто – порушення рефракції; Дуже рідко – діабетична ретинопатія. Порушення з боку шкіри та підшкірних тканин: Нечасто – ліподистрофія. Загальні розлади та порушення у місці введення: Нечасто - реакції у місцях введення; Нечасто – периферичні набряки. Опис окремих побічних реакцій: Анафілактичні реакції Відзначені дуже рідкісні реакції генералізованої гіперчутливості (у тому числі генералізована шкірна висипка, свербіж, підвищене потовиділення, шлунково-кишкові розлади, ангіоневротичний набряк, утруднення дихання, прискорене серцебиття, зниження артеріального тиску, а також непритомність/втрата свідомості, . Гіпоглікемія Гіпоглікемія є найчастішою побічною реакцією. Вона може розвинутись, якщо доза інсуліну надто висока по відношенню до потреби в інсуліні. Тяжка гіпоглікемія може призводити до втрати свідомості та/або судом, тимчасового або необоротного порушення функції головного мозку або навіть до смерті. Симптоми гіпоглікемії, як правило, розвиваються раптово. Вони можуть включати "холодний піт", блідість шкірних покривів, підвищену стомлюваність, нервозність або тремор, почуття тривоги, незвичайну втому або слабкість, порушення орієнтації, зниження концентрації уваги, сонливість, виражене почуття голоду, порушення зору, головний біль, нудоту та прискорене серцебиття . Ліподистрофія Повідомлялося про нечасті випадки розвитку ліподистрофії. Ліподистрофія може розвиватися у місці введення препарату.Взаємодія з лікарськими засобамиЄ низка лікарських засобів, які впливають потреба в інсуліні. Гипогликемическое действие инсулина усиливают пероральные гипогликемические препараты, ингибиторы моноаминоксидазы, ингибиторы ангиотензинпревращающего фермента, ингибиторы карбоангидразы, неселективные бета-адреноблокаторы, бромокриптин, сульфонамиды, анаболические стероиды, тетрациклины, клофибрат, кетоконазол, мебендазол, пиридоксин, теофиллин, циклофосфамид, фенфлурамин, препараты лития, салицилаты . Гіпоглікемічну дію інсуліну послаблюють пероральні гормональні контрацептивні засоби, глюкокортикостероїди, тиреоїдні гормони, тіазидні діуретики, гепарин, трициклічні антидепресанти, симпатоміметики, гормон росту (соматропін), даназол, клонідиннік, блокіні, Бета-адреноблокатори можуть маскувати симптоми гіпоглікемії та ускладнювати відновлення після гіпоглікемії. Октреотид/ланреотид може підвищувати, так і знижувати потребу організму в інсуліні. Етанол може посилювати або зменшувати гіпоглікемічний ефект інсуліну. Несумісність Актрапид® НМ можна додавати лише до тих сполук, з якими він, як відомо, сумісний. Деякі препарати (наприклад, препарати, що містять тіоли або сульфіти) при додаванні до розчину інсуліну можуть спричинити його деградацію.Спосіб застосування та дозиПрепарат призначений для підшкірного та внутрішньовенного введення. Доза препарату підбирається індивідуально з урахуванням потреб пацієнта. Зазвичай, потреба в інсуліні становить від 0,3 до 1 МО/кг/добу. Добова потреба в інсуліні може бути вищою у пацієнтів з інсулінорезистентністю (наприклад, у період статевого дозрівання, а також у пацієнтів з ожирінням), і нижче – у пацієнтів із залишковою ендогенною продукцією інсуліну. Препарат вводиться за 30 хвилин до їди або легкої закуски, що містить вуглеводи. Препарат Актрапід® НМ є інсуліном короткої дії та може застосовуватись у комбінації з інсулінами пролонгованої дії. Препарат Актрапид НМ зазвичай вводять підшкірно, в область передньої черевної стінки. Якщо це зручно, то ін'єкції можна робити також в область стегна, в сідничну область або область дельтовидного м'яза плеча. При введенні препарату в область передньої черевної стінки досягається швидке всмоктування, ніж при введенні до інших ділянок. Якщо ін'єкція виробляється у відтягнуту складку шкіри, ризик випадкового внутрішньом'язового введення препарату зводиться до мінімуму. Голка повинна залишатися під шкірою щонайменше 6 секунд, що гарантує повне введення дози. Необхідно постійно змінювати місця ін'єкцій у межах анатомічної області, щоб зменшити ризик розвитку ліподистрофії. Внутрішньом'язові ін'єкції також можливі, але лише за призначенням лікаря. Препарат Актрапид® НМ також можна вводити внутрішньовенно і такі процедури може проводити лише медичний працівник. Препарат Актрапид® НМ у флаконах можна використовувати лише разом із інсуліновими шприцами, на які нанесена шкала, що дозволяє відміряти дозу інсуліну в одиницях дії. Внутрішньовенне введення препарату Актрапид® НМ з картриджа або шприц-ручки дозволяється лише як виняток за відсутності флаконів. У цьому випадку слід набрати препарат Актрапід НМ в інсуліновий шприц без набору повітря або провести інфузію за допомогою системи для інфузій. Цю процедуру має проводити лише медичний працівник. Шприц-ручка ФлексПен® є попередньо заповненою шприц-ручкою, розробленою для використання з одноразовими голками НовоФайн® або НовоТвіст® довжиною до 8 мм. Шприц-ручка ФлексПен дозволяє вводити дозу від 1 до 60 ME з кроком 1 ME. Слід дотримуватися докладних рекомендацій щодо застосування та введення препарату (див. "Актрапид® НМ розчин для ін'єкцій у флаконах. Інструкція із застосування для пацієнтів" або "Актрапид® НМ розчин для ін'єкцій у шприц-ручках ФлексПен®. Інструкція із застосування для пацієнтів") . Корекція дози Супутні захворювання, особливо інфекційні та супроводжуються лихоманкою, зазвичай збільшують потребу організму в інсуліні. Корекція дози препарату може також бути потрібна при наявності у пацієнта супутніх захворювань нирок, печінки, порушенні функції надниркових залоз, гіпофізу або щитовидної залози. Необхідність корекції дози також може виникнути при зміні фізичного навантаження або звичайного режиму харчування пацієнта. Корекція дози може бути потрібна при переведенні пацієнта з одного виду інсуліну на інший.ПередозуванняПевної дози, необхідної для передозування інсуліну, не встановлено, однак гіпоглікемія може поступово розвиватися, якщо вводяться занадто високі дози інсуліну по відношенню до потреби пацієнта. Легку гіпоглікемію пацієнт може усунути сам, прийнявши всередину глюкозу або цукромісткі продукти харчування. Тому хворим на цукровий діабет рекомендується постійно носити з собою цукрозміщуючі продукти. У разі важкої гіпоглікемії, коли пацієнт непритомний, слід ввести від 0,5 мг до 1 мг глюкагону внутрішньом'язово або підшкірно (може вводити навчена людина), або внутрішньовенно розчин декстрози (глюкози) (може вводити тільки медичний працівник). Також необхідно внутрішньовенно ввести декстрозу у випадку, якщо через 10-15 хвилин після введення глюкагону пацієнт не приходить до тями. Після відновлення свідомості пацієнту рекомендується прийняти багату на вуглеводи їжу для профілактики рецидиву гіпоглікемії.Запобіжні заходи та особливі вказівкиНедостатня доза або припинення лікування, особливо при цукровому діабеті 1 типу, може призвести до розвитку гіперглікемії. Як правило, перші симптоми гіперглікемії з'являються поступово протягом декількох годин або днів. Симптомами гіперглікемії є почуття спраги, прискорене сечовипускання, нудота, блювання, сонливість, почервоніння та сухість шкіри, сухість у роті, втрата апетиту, а також поява запаху ацетону у повітрі, що видихається. Без відповідного лікування гіперглікемія у пацієнтів з цукровим діабетом 1 типу може призводити до діабетичного кетоацидозу - стану, що є потенційно летальним. Гіпоглікемія Гіпоглікемія може розвинутись, якщо введена занадто висока доза інсуліну щодо потреби пацієнта. Пропуск їжі або незаплановане інтенсивне фізичне навантаження можуть призвести до гіпоглікемії. Після компенсації вуглеводного обміну, наприклад, при інтенсифікованій інсулінотерапії, у пацієнтів можуть змінитися типові для них симптоми-провісники гіпоглікемії, про що хворі мають бути поінформовані. Звичайні симптоми-провісники можуть зникати при тривалому перебігу цукрового діабету. Переведення пацієнтів на інший тип інсуліну або інсулін іншої компанії-виробника повинен здійснюватися тільки під медичним контролем. При зміні концентрації виробника, типу, виду (людський інсулін, аналог людського інсуліну) та/або методу виготовлення може знадобитися зміна дози інсуліну. Пацієнтам, які переходять на лікування препаратом Актрапід НМ, може знадобитися зміна дози або збільшення частоти ін'єкцій порівняно з раніше застосовуваними препаратами інсуліну. Якщо при переведенні пацієнтів на лікування препаратом Актрапід НМ необхідна корекція дози, це можна зробити вже при введенні першої дози або в перші тижні або місяці терапії. Як і при лікуванні іншими препаратами інсуліну, можуть розвиватися реакції у місці введення, що проявляється болем, почервонінням, кропивницею, запаленням, гематомою, набряклістю та свербінням. Регулярна зміна місця ін'єкції в одній і тій же анатомічній ділянці допоможе зменшити симптоми або запобігти розвитку цих реакцій. Реакції зазвичай зникають протягом кількох днів до кількох тижнів. В окремих випадках може бути потрібна відміна препарату Актрапид® НМ через реакції в місцях введення. Перед поїздкою, пов'язаною зі зміною часових поясів, пацієнт повинен проконсультуватися зі своїм лікарем, оскільки зміна часового поясу означає, що пацієнт повинен вживати їжу та вводити інсулін в інший час. Використання препарату Актрапид® НМ для тривалих підшкірних інсулінових інфузій (ППІІ) не дозволяється через ризик преципітації у помпових катетерах. Одночасне застосування препаратів групи тіазолідиндіону та препаратів інсуліну. Повідомлялося про випадки розвитку хронічної серцевої недостатності при лікуванні пацієнтів тіазолідиндіонами у комбінації з препаратами інсуліну, особливо за наявності у таких пацієнтів факторів ризику хронічної серцевої недостатності. Слід враховувати цей факт при призначенні пацієнтам комбінованої терапії тіазолідиндіонами та препаратами інсуліну. При призначенні такої комбінованої терапії необхідно проводити медичні обстеження пацієнтів на предмет виявлення у них ознак та симптомів хронічної серцевої недостатності, збільшення маси тіла та наявності набряків. У разі погіршення у пацієнтів симптоматики серцевої недостатності лікування тіазолідиндіонами необхідно припинити. Запобіжні заходи при застосуванні Для внутрішньовенного введення застосовуються інфузійні системи, що містять препарат Актрапід НМ 100 МО/мл, у концентраціях від 0,05 МО/мл до 1 МО/мл людського інсуліну в інфузійних розчинах, таких як 0,9% розчин хлориду натрію, 5% та 10% розчини декстрози, що включають хлорид калію концентрації 40 ммоль/л. В системі для внутрішньовенного введення застосовуються інфузійні мішки, виготовлені з поліпропілену; ці розчини зберігають стабільність протягом 24 годин за кімнатної температури. Хоча ці розчини зберігають стабільність протягом певного часу, на початковому етапі відзначається абсорбція деякої кількості інсуліну матеріалом, з якого виготовлений мішок інфузійний. У ході інфузії необхідно здійснювати контроль концентрації глюкози в крові. Шприц-ручки слід використовувати лише у поєднанні із сумісними продуктами, що забезпечує безпеку та ефективність їх використання. Голки та препарат Актрапід® НМ у шприц-ручці ФлексПен® призначені лише для індивідуального використання. Забороняється повторне заповнення картриджа шприц-ручки. Не можна застосовувати препарат Актрапід НМ, якщо він був заморожений. Не можна застосовувати препарат Актрапид НМ, якщо він перестав бути прозорим і безбарвним. Препарат Актрапід НМ не можна використовувати в інсулінових насосах для тривалої підшкірної інфузії інсуліну. Поінформуйте пацієнта про необхідність викидати голку після кожної ін'єкції. В екстрених випадках (шпиталізація, несправність пристрою для введення інсуліну) препарат Актрапид® НМ для введення пацієнту можна витягти зі шприц-ручки ФлексПен® за допомогою інсулінового шприца U100. Інструкція з використання для пацієнтів Не можна використовувати Актрапід® НМ: В інсулінових насосах. Якщо у вас алергія (гіперчутливість) до людського інсуліну або будь-якого з компонентів, що входять до складу препарату Актрапід НМ. Якщо у Вас починається гіпоглікемія (низька концентрація глюкози у крові). Якщо захисний ковпачок відсутній або вдягнений нещільно. Кожен флакон має пластиковий захисний ковпачок. Якщо на новому флаконі захисний ковпачок пошкоджено, поверніть його в аптеку. Якщо були порушені умови зберігання препарату, або він був заморожений. Якщо інсулін перестав бути прозорим і безбарвним. Перед застосуванням Актрапід® НМ: Перевірте етикетку, щоб переконатися, що Ви використовуєте правильний тип інсуліну. Видаліть захисний ковпачок. Вплив на здатність до керування автотранспортом та управління механізмами Здатність пацієнтів до концентрації уваги та швидкість реакції можуть порушуватися під час гіпоглікемії, що може становити небезпеку в тих ситуаціях, коли ці здібності особливо необхідні (наприклад, при керуванні транспортними засобами або роботі з машинами та механізмами). Пацієнтам необхідно рекомендувати вживати заходів для запобігання розвитку гіпоглікемії при керуванні транспортними засобами. Це особливо важливо для пацієнтів з відсутністю або зниженням вираженості симптомів-провісників гіпоглікемії, що розвивається, або пацієнтів з частими епізодами гіпоглікемії. У цих випадках слід розглянути доцільність керування транспортними засобами та виконання подібних робіт.Умови зберіганняУ холодильнику +2+8 градусівУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаРозчин для ін'єкцій - 1 мл: активна речовина: інсулін розчинний (людський генно-інженерний) – 100 МО (1 МО відповідає 0,035 мг безводного людського інсуліну); допоміжні речовини: цинку хлорид - близько 7 мкг, гліцерол (гліцерин) - 16 мг, метакрезол - 3 мг, натрію гідроксид - близько 2.6 мг та/або хлористоводнева кислота - близько 1.7 мг (для коригування pH), вода д/і - до 1мл. Розчин для ін'єкцій, 100 МО/мл. У скляних картриджах Пенфіл по 3 мл; у блістері 5 картриджів; у пачці картонної 1 блістер.Опис лікарської формиРозчин для ін'єкцій прозорий, безбарвний.Фармакотерапевтична групаНейтральний людський монокомпонентний інсулін короткої дії.ФармакодинамікаВзаємодіє зі специфічним рецептором плазматичної мембрани та проникає в клітину, де активує фосфорилювання клітинних білків, стимулює глікогенсинтетазу, піруватдегідрогеназу, гексокіназу, інгібує ліпазу жирової тканини та ліпопротеїнліпазу. У комплексі зі специфічним рецептором полегшує проникнення глюкози в клітини, посилює її засвоєння тканинами та сприяє перетворенню на глікоген. Підвищує запас глікогену у м'язах, стимулює синтез пептидів.Клінічна фармакологіяЕфект розвивається через 30 хв після підшкірного введення, досягає максимуму через 1-3 год і триває 8 год.Показання до застосуванняЦукровий діабет І та ІІ типів.Протипоказання до застосуванняГіпоглікемія, інсулінома.Вагітність та лактаціяПри вагітності особливо важливо підтримувати хороший контроль глікемії у пацієнток із цукровим діабетом. При вагітності потреба в інсуліні зазвичай знижується в І триместрі та підвищується у ІІ та ІІІ триместрах. Хворим на цукровий діабет рекомендується інформувати лікаря про настання або планування вагітності. У хворих на цукровий діабет у період лактації (грудного вигодовування) може знадобитися корекція дози інсуліну, дієти або того й іншого. При дослідженнях генетичної токсичності в серіях in vitro та in vivo інсулін людини не чинив мутагенної дії.Побічна діяГіпоглікемія, порушення рефракції (зазвичай на початку терапії), алергічні реакції.Взаємодія з лікарськими засобамиІнгібітори МАО, неселективні бета-адреноблокатори, інгібітори АПФ, саліцилати, анаболічні стероїди, алкоголь – посилюють, пероральні контрацептиви, кортикостероїди, тиреоїдні гормони, тіазидні діуретики, симпатоміметичний.Спосіб застосування та дозиП/до, в/в. Доза препарату підбирається індивідуально з урахуванням потреб пацієнта. Зазвичай потреба в інсуліні становить від 0,3 до 1 МО/кг/добу. Добова потреба в інсуліні може бути вищою у пацієнтів з інсулінорезистентністю (наприклад, у період статевого дозрівання, а також у пацієнтів з ожирінням), і нижче – у пацієнтів із залишковою ендогенною продукцією інсуліну. Препарат вводиться за 30 хв до їди або легкої закуски, що містить вуглеводи. АктрапидНМ є інсуліном короткої дії та може використовуватися у комбінації з інсулінами пролонгованої дії. АктрапидНМ зазвичай вводять підшкірно, в область передньої черевної стінки. Якщо це зручно, то ін'єкції можна робити також в область стегна, в сідничну область або область дельтовидного м'яза плеча. При введенні препарату в область передньої черевної стінки досягається швидке всмоктування, ніж при введенні до інших ділянок. Якщо ін'єкція виробляється у відтягнуту складку шкіри, ризик випадкового внутрішньом'язового введення препарату зводиться до мінімуму. Голка повинна залишатися під шкірою не менше ніж 6 с, що гарантує повне введення дози. Необхідно постійно змінювати місця ін'єкцій у межах анатомічної області, щоб зменшити ризик розвитку ліподистрофії. В/м ін'єкції також можливі, але лише за призначенням лікаря. АктрапидНМ також можна вводити внутрішньовенно і такі процедури може проводити тільки медичний працівник. Внутрішньовенне введення препарату АктрапидНМ Пенфілліз картриджа дозволяється лише як виняток за відсутності флаконів. У цьому випадку слід набрати препарат в інсуліновий шприц без набору повітря або провести інфузію за допомогою системи інфузій. Ця процедура повинна проводитись лише лікарем. АктрапидНМ Пенфілл розроблений для використання з ін'єкційними системами для введення інсуліну компанії Ново Нордіськ та голками НовоФайнілі НовоТвіст. Слід дотримуватися детальних рекомендацій щодо використання та введення препарату. Корекція дози Супутні захворювання, особливо інфекційні та супроводжуються лихоманкою, зазвичай підвищують потребу організму в інсуліні. Корекція дози препарату може також бути потрібна при наявності у пацієнта супутніх захворювань нирок, печінки, порушенні функції надниркових залоз, гіпофізу або щитовидної залози. Необхідність корекції дози також може виникнути при зміні фізичного навантаження або звичайного режиму харчування пацієнта. Корекція дози може бути потрібна при переведенні пацієнта з одного виду інсуліну на інший.ПередозуванняСимптоми: розвиток гіпоглікемії (холодний піт, серцебиття, тремор, почуття голоду, збудженість, дратівливість, блідість, біль голови, сонливість, невпевненість рухів, порушення мови та зору, депресія). Тяжкі гіпоглікемії можуть призводити до тимчасового або постійного порушення функції мозку, коми та летального результату. Лікування: цукор або розчин глюкози всередину (якщо хворий у свідомості), підшкірно, внутрішньом'язово або внутрішньовенно - глюкагон або внутрішньовенно - глюкозу.Запобіжні заходи та особливі вказівкиСлід пам'ятати, що здатність до керування автомобілем після переведення хворих на людський інсулін може тимчасово знизитися. Препарат можна застосовувати, якщо він абсолютно прозорий та безбарвний. При використанні двох видів препаратів інсуліну в картриджах Пенфіл, потрібна шприц-ручка для кожного окремого типу інсуліну.Умови відпустки з аптекЗа рецептомВідео на цю тему
927,00 грн
201,00 грн
Умови зберіганняУ холодильнику +2+8 градусівУмови відпустки з аптекЗа рецептомВідео на цю тему.
1 142,00 грн
1 100,00 грн
Склад, форма випуску та упаковкаВ 1 мл препарату міститься: активна речовина: інсулін детемір – 100 ОД; допоміжні речовини: гліцерол, фенол, метакрезол, цинку ацетат, натрію гідрофосфату дигідрат, натрію хлорид, хлористоводнева кислота або натрію гідроксид, вода для ін'єкцій. Одна шприц-ручка містить 3 мл розчину, еквівалентного 300 ОД. Одна одиниця інсуліну детемир містить 0,142 мг безсольового інсуліну детемиру.
827,00 грн
196,00 грн
Дозировка: 100 МЕ/мл Фасовка: N5 Форма выпуска: суспензия д/п/кожного введения Упаковка: картр. в шпр. -ручк.
970,00 грн
172,00 грн
Склад, форма випуску та упаковкаРозчин для внутрішньовенного та підшкірного введення - 1 мл: активні речовини: інсулін аспарт - 100 ОД (100 ОД відповідає 3,5 мг безводного інсуліну аспарт); допоміжні речовини: гліцерол; фенол; метакрезол; цинку хлорид; динатрію фосфату дигідрат; натрію хлорид; натрію гідроксид; кислота хлористоводнева; вода для ін'єкцій. У шприц-ручках мультидозових по 3 мл; у блістері 5 штук; у пачці картонної 1 блістер.Опис лікарської формиПрозорий безбарвний розчин.Фармакотерапевтична групаГіпоглікемічний засіб, аналог людського інсуліну короткої дії.ФармакокінетикаПісля підшкірного введення інсуліну аспарт Tmax у плазмі крові в середньому в 2 рази менше, ніж після введення розчинного людського інсуліну. Сmax в середньому становить (492±256) пмоль/л і досягається через 40 хв після підшкірного введення дози 0,15 ОД/кг маси тіла пацієнтам з цукровим діабетом типу 1. Концентрація інсуліну повертається до вихідного рівня через 4-6 годин після запровадження препарату. Швидкість абсорбції дещо нижча у пацієнтів з діабетом типу 2, що призводить до нижчої максимальної концентрації (352±240 пмоль/л) і пізнішого Tmax (60 хв). Межиндивідуальна варіабельність по Tmax істотно нижче при використанні інсуліну аспарт у порівнянні з розчинним людським інсуліном, тоді як зазначена варіабельність Cmax для інсуліну аспарт більше. У пацієнтів похилого віку та пацієнтів з порушенням функції нирок або печінки дослідження фармакокінетики не проводилися. Фармакокінетика у дітей (6-12 років) та підлітків (13-17 років) з цукровим діабетом типу 1. Абсорбція інсуліну аспарту відбувається швидко в обох вікових групах з Tmax, аналогічним такому у дорослих. Однак є відмінності Cmax у двох вікових групах, що наголошує на важливості індивідуального дозування препарату.ФармакодинамікаНовоРапід® ФлексПен® — аналог людського інсуліну короткої дії, вироблений методом біотехнології рекомбінантної ДНК з використанням штаму Saccharomyces cerevisiae, в якому амінокислота проліну в положенні В28 заміщена на аспарагінову кислоту. Взаємодіє зі специфічним рецептором зовнішньої цитоплазматичної мембрани клітин та утворює інсулін-рецепторний комплекс, що стимулює внутрішньоклітинні процеси, у т.ч. синтез ряду ключових ферментів (гексокіназа, піруваткіназа, глікогенсинтетаза та ін.). Зниження вмісту глюкози в крові обумовлено підвищенням її внутрішньоклітинного транспорту, посиленням засвоєння тканинами, стимуляцією ліпогенезу, глікогеногенезу, зниженням швидкості продукції глюкози печінкою та ін. яка спостерігається у розчині звичайного інсуліну. У зв'язку з цим НовоРапід ФлексПен набагато швидше всмоктується з підшкірно-жирової клітковини і починає діяти набагато швидше, ніж розчинний людський інсулін. НовоРапід® ФлексПен® сильніше знижує рівень глюкози крові в перші 4 години після прийому їжі, ніж розчинний людський інсулін. Тривалість дії препарату НовоРапід® ФлексПен® після підшкірного введення коротша, ніж розчинний людський інсулін. Після підшкірного введення дія препарату починається протягом 10-20 хвилин після введення. Максимальний ефект спостерігається через 1-3 години після ін'єкції. Тривалість дії препарату становить 3-5 годин. Клінічні дослідження за участю пацієнтів із цукровим діабетом типу 1 продемонстрували зниження ризику нічної гіпоглікемії при використанні інсуліну аспарту порівняно з розчинним людським інсуліном. Ризик денної гіпоглікемії достовірно не підвищувався. Інсулін аспарт є еквіпотенційним розчинним людським інсуліном на підставі показників молярності. Дорослі. Клінічні дослідження за участю пацієнтів із цукровим діабетом типу 1 продемонстрували нижчий постпрандіальний рівень глюкози крові при введенні препарату НовоРапід у порівнянні з розчинним людським інсуліном. Діти та підлітки Використання препарату НовоРапід® у дітей показало схожі результати тривалого контролю глюкози порівняно з розчинним людським інсуліном. Клінічне дослідження з використанням розчинного людського інсуліну до їди та інсуліну аспарт після прийому їжі було проведено у маленьких дітей (26 пацієнтів віком від 2 до 6 років); фармакокінетичне/фармакодинамічне (ФК/ФД) дослідження з використанням одноразової дози було проведено у дітей (6-12 років) та підлітків (13-17 років). Фармакодинамічний профіль інсуліну аспарт у дітей був схожим на такий у дорослих пацієнтів. Вагітність Клінічні дослідження порівняльної безпеки та ефективності інсуліну аспарт та людського інсуліну при лікуванні вагітних жінок, які страждають на цукровий діабет типу 1 (322 обстежених вагітних, з них інсулін аспарт: 157; людський інсулін: 165) не виявили жодного негативного впливу на інсуліну аспарт плода/новонародженого. Додаткові клінічні дослідження 27 жінок з гестаційним діабетом, які отримують інсулін аспарт та людський інсулін (інсулін аспарт отримували 14 жінок, людський інсулін - 13) свідчать про сумісність профілів безпеки поряд зі значним поліпшенням контролю рівня глюкози після їди при лікуванні.Показання до застосуванняЦукровий діабет у дорослих, підлітків та дітей старше 2 років.Взаємодія з лікарськими засобамиГипогликемическое действие инсулина усиливают пероральные гипогликемические препараты, ингибиторы МАО, ингибиторы АПФ, ингибиторы карбоангидразы, неселективные бета-адреноблокаторы, бромокриптин, октреотид, сульфаниламиды, анаболические стероиды, тетрациклины, клофибрат, кетоконазол, мебендазол, пиридоксин, теофиллин, циклофосфамид, фенфлурамин, препараты лития, препарати, що містять етанол. Гіпоглікемічна дія інсуліну послаблюють пероральні контрацептиви, кортикостероїди, тиреоїдні гормони, тіазидні діуретики, гепарин, трициклічні антидепресанти, симпатоміметики, даназол, клонідин, блокатори кальцієвих каналів, діазоксид, морфін, фенітоїн. Під впливом резерпіну та саліцилатів можливе як ослаблення, так і посилення дії препарату. Фармацевтична взаємодія. ЛЗ, що містять тіоли або сульфіти, при додаванні до інсуліну спричиняють його руйнування.Спосіб застосування та дозиНовоРапід® ФлексПен® є швидкодіючим аналогом інсуліну. Доза НовоРапід® ФлексПен® визначається лікарем індивідуально відповідно до потреб пацієнта. Зазвичай препарат використовують у поєднанні з препаратами інсуліну середньої тривалості або тривалої дії, які вводять щонайменше 1 раз на добу. Для досягнення оптимального контролю глікемії рекомендується регулярно вимірювати концентрацію глюкози у крові та коригувати дозу інсуліну. Зазвичай індивідуальна добова потреба в інсуліні у дорослих та дітей становить від 0,5 до 1 ОД/кг маси тіла. При введенні препарату перед їдою, потреба в інсуліні може забезпечуватися препаратом НовоРапід® ФлексПен® на 50-70%, потреба в інсуліні, що залишилася, забезпечується інсуліном продовженої дії. Підвищення фізичної активності пацієнта, зміна звичного харчування або супутні захворювання можуть призвести до корекції дози. НовоРапід® ФлексПен® має більш швидкий початок та меншу тривалість дії, ніж розчинний людський інсулін. Завдяки швидшому початку дії, НовоРапід® ФлексПен® слід вводити, як правило, безпосередньо перед їдою, при необхідності можна вводити невдовзі після їди. Завдяки меншій тривалості дії порівняно з людським інсуліном, ризик розвитку нічних гіпоглікемій у пацієнтів, які отримують НовоРапід® ФлексПен®, є нижчим. Особливі групи пацієнтів Як і при застосуванні інших інсулінів, у літніх пацієнтів та пацієнтів з нирковою або печінковою недостатністю слід ретельніше контролювати концентрацію глюкози в крові та коригувати дозу інсуліну аспарт індивідуально. Діти та підлітки Застосовувати НовоРапід® ФлексПен® замість розчинного людського інсуліну у дітей краще в тому випадку, коли необхідно швидке початок дії препарату, наприклад, коли дитині важко дотримуватися необхідного інтервалу часу між ін'єкцією та прийомом їжі. Переведення з інших препаратів інсуліну При переведенні пацієнта з інших препаратів інсуліну на НовоРапід® ФлексПен®, може знадобитися корекція дози НовоРапід® ФлексПен® та базального інсуліну. НовоРапід® ФлексПен® вводиться підшкірно в область передньої черевної стінки, стегно, плече, дельтоподібну або сідничну ділянку. Місця ін'єкцій у межах однієї ділянки тіла потрібно регулярно змінювати для зменшення ризику розвитку ліподистрофії. Як і при застосуванні всіх препаратів інсуліну, підшкірне введення у передню черевну стінку забезпечує більш швидке всмоктування порівняно з введенням до інших місць. Тривалість дії залежить від дози, місця введення, інтенсивності кровотоку, температури та рівня фізичної активності. Проте швидке початок дії проти розчинним людським інсуліном зберігається незалежно від локалізації місця ін'єкції. НовоРапід® може використовуватися для тривалих підшкірних інсулінових інфузій (ППІІ) в інсулінових насосах, розроблених для інфузій інсуліну. ППІІ слід проводити в передню черевну стінку. Місця інфузій слід періодично змінювати. При використанні інсулінового насоса для інфузій НовоРапід не слід змішувати з іншими типами інсулінів. Пацієнти, які використовують ППІІ, повинні бути повністю навчені користування насосом, відповідним резервуаром та системою трубок для насоса. Інфузійний набір (трубка та катетер) слід замінювати відповідно до посібника користувача, що додається до інфузійного набору. Пацієнти, які отримують НовоРапід® за допомогою ППІІ, повинні мати додатковий інсулін на випадок поломки інфузійної системи. Внутрішньовенне введення При необхідності НовоРапід® може вводитися внутрішньовенно, але тільки кваліфікованим медичним персоналом. Для внутрішньовенного введення використовуються інфузійні системи з препаратом НовоРапід® 100 ОД/мл із концентрацією від 0,05 ОД/мл до 1 ОД/мл інсуліну аспарт у 0,9% розчині хлориду натрію; 5% розчин декстрози або 10% розчин декстрози, що містить 40 ммоль/л хлориду калію, з використанням поліпропіленових контейнерів для інфузій. Дані розчини стабільні за кімнатної температури протягом 24 годин. Незважаючи на стабільність протягом певного часу, певна кількість інсуліну спочатку абсорбується матеріалом інфузійної системи. Під час інфузій інсуліну слід постійно контролювати концентрацію глюкози крові.ПередозуванняСимптоми: можливий розвиток гіпоглікемії. Лікування: легку гіпоглікемію пацієнт може усунути сам, прийнявши внутрішньо глюкозу, цукор або багаті на вуглеводи продукти харчування. Тому хворим на цукровий діабет рекомендується постійно носити із собою цукор, солодощі, печиво або солодкий фруктовий сік. У тяжких випадках, при втраті пацієнтом свідомості, внутрішньовенно вводять 40% розчин декстрози (глюкози); в/м або п/к - глюкагон (0,5-1 мг). Після відновлення свідомості пацієнту рекомендують прийняти їжу, багату на вуглеводи, для запобігання повторному розвитку гіпоглікемії.Умови відпустки з аптекЗа рецептомВідео на цю тему
448,00 грн
160,00 грн
Склад, форма випуску та упаковкаРозчин - 1 мл: речовина, що діє: семаглутид 1,34 мг; допоміжні речовини: динатрію гідрофосфат дигідрат, пропіленгліколь, фенол, хлористоводнева кислота (для корекції pH), гідроксид натрію (для корекції pH), вода для ін'єкцій. В одній попередньо заповненій шприц-ручці об'ємом 1,5 мл міститься 2 мг семаглутиду. Розчин для підшкірного введення 1,34 мг/мл. По 1,5 мл препарату в картриджі зі скла, закупорені поршнями з хлорбутилової гуми з одного боку та алюмінієвими ковпачками з дисками з бромбутилової гуми/поліізопрену, з іншого боку. Картридж вбудований в мультидозову одноразову шприц-ручку для багаторазових ін'єкцій з поліпропілену, поліоксиметилену, полікарбонату та акрилонітрил бутадієн стиролу. 1 шприц-ручка разом з інструкцією із застосування та 6 одноразовими голками НовоФайн® Плюс у картонну пачку.Опис лікарської формиПрозорий, безбарвний чи майже безбарвний розчин.Фармакотерапевтична групаГіпоглікемічний засіб – аналог глюкагоноподібного пептиду-1.ФармакокінетикаПрепарат підходить для введення 1 раз на тиждень, тому що період напіввиведення семаглутиду дорівнює приблизно 1 тижню. Абсорбція Час досягнення максимальної концентрації (Сmах) у плазмі становить від 1 до 3 днів після введення дози препарату. Рівноважна концентрація препарату (AUCt/24) досягалася через 4-5 тижнів одноразового щотижневого застосування препарату. Після підшкірного введення семаглутиду в дозах 0,5 мг та 1 мг середні показники його рівноважної концентрації у пацієнтів із ЦД2 склали близько 16 нмоль/л та 30 нмоль/л відповідно. Експозиція для доз семаглутиду 0,5 мг та 1 мг збільшується пропорційно до введеної дози. При підшкірному введенні семаглутиду в передню черевну стінку, стегно або плече досягається подібна експозиція. Абсолютна біодоступність семаглутиду після підшкірного введення склала 89%. Розподіл Середній обсяг розподілу семаглутиду в тканинах після підшкірного введення пацієнтам з ЦД2 становив приблизно 12,5 л. Семаглутид значною мірою зв'язувався з альбуміном плазми (>99%). Метаболізм Семаглутид метаболізується за допомогою протеолітичного розщеплення пептидної основи білка та подальшого бета-окислення жирної кислоти бічного ланцюга. Виведення Шлунково-кишковий тракт (ЖКТ) та нирки є основними шляхами виведення семаглутиду та його метаболітів. 2/3 введеної дози семаглутиду виводиться нирками 1/3 - через кишечник. Приблизно 3% введеної дози виводиться нирками у вигляді незміненого семаглутиду. У пацієнтів із ЦД2 кліренс семаглутиду становив близько 0,05 л/год. З елімінаційним періодом напіввиведення приблизно 1 тиждень семаглутид буде присутній у загальному кровотоку протягом 5 тижнів після введення останньої дози препарату. Особливі групи пацієнтів Не потрібна корекція дози семаглутиду залежно від віку, статі, расової та етнічної приналежності, маси тіла, наявності ниркової або печінкової недостатності. Вік На підставі даних, отриманих в ході КІ 3а фази, що включали пацієнтів віком від 20 до 86 років, показано, що вік не впливав на фармакокінетику семаглутиду. Підлога Підлога не впливала на фармакокінетику семаглутиду. Раса Расова група (біла, чорна або афроамериканська, азіатська) не впливала на фармакокінетику семаглутиду. Етнічна приналежність Етнічна приналежність (латиноамериканська) не впливала на фармакокінетику семаглутиду. Маса тіла Маса тіла впливала на експозицію семаглутіду. Вища маса тіла призводить до нижчої експозиції. Дози семаглутиду рівні 0,5 і 1 мг забезпечують достатню експозицію препарату в діапазоні маси тіла від 40 до 198 кг. Ниркова недостатність Ниркова недостатність не справила клінічно значущого ефекту на фармакокінетику семаглутиду. Це було показано у пацієнтів з різним ступенем ниркової недостатності (легкої, середньої, тяжкої або у пацієнтів, які перебувають на діалізі) порівняно з пацієнтами з нормальною функцією нирок у дослідженні одноразової дози семаглутиду, що дорівнює 0,5 мг. Це також було показано на підставі даних КІ 3а фази для пацієнтів з ЦД2 та нирковою недостатністю, хоча досвід застосування у пацієнтів з термінальною стадією захворювання нирок був обмежений. Печінкова недостатність Печінкова недостатність не впливала на експозицію семаглутиду. Фармакокінетичні властивості семаглутиду оцінювалися під час дослідження! одноразової дози семаглутиду, що дорівнює 0,5 мг у пацієнтів з різним ступенем печінкової недостатності (легкої, середньої, тяжкої) порівняно з пацієнтами з нормальною функцією печінки. Діти та підлітки Досліджень семаглутиду у дітей та підлітків до 18 років не проводили.ФармакодинамікаСемаглутид є агоністом рецепторів ГПП-1 (ГПП-1Р), виробленим методом біотехнології рекомбінантної ДНК з використанням штаму Saccharomyces cerevisiae з подальшим очищенням. Семаглутид є аналогом ГПП-1, що має 94% гомологічності з людським ГПП-1. Семаглутид діє як агоніст ГПП-1Р, який селективно зв'язується та активує ГПП-1Р. ГПП-1Р є мішенню для нативного ГПП-1. ГПП-1 є фізіологічним гормоном, який надає відразу кілька ефектів на регуляцію концентрації глюкози та апетит, а також на серцево-судинну систему (ССС). Вплив на концентрацію глюкози та апетит специфічно опосередкований ГПП-1Р, розташованими в підшлунковій залозі та головному мозку. Фармакологічні концентрації семаглутиду знижують концентрацію глюкози крові та масу тіла за допомогою поєднання ефектів, описаних нижче. ГПП-1Р представлені також у специфічних областях серця, судин, імунної системи та нирок, де їх активація може надавати серцево-судинні (СС) та мікроциркуляторні ефекти. На відміну від нативного ГПП-1, продовжений період напіввиведення семаглутиду (близько 1 тижня) дозволяє застосовувати його підшкірно (п/к) 1 раз на тиждень. Зв'язування з альбуміном є основним механізмом тривалої дії семаглутиду, що призводить до зниження виведення його нирками та захищає від метаболічного розпаду. Крім того, семаглутид стабільний щодо розщеплення ферментом дипептидилпептидазой-4. Семаглутид знижує концентрацію глюкози крові за допомогою глюкозозалежної стимуляції секреції інсуліну та пригнічення секреції глюкагону. Таким чином, при підвищенні концентрації глюкози крові відбувається стимуляція секреції інсуліну та пригнічення секреції глюкагону. Механізм зниження рівня глікемії включає також невелику затримку випорожнення шлунка у ранній постпрандіальній фазі. Під час гіпоглікемії семаглутид зменшує секрецію інсуліну та не знижує секрецію глюкагону. Семаглутид знижує загальну масу тіла та масу жирової тканини, зменшуючи споживання енергії. Даний механізм зачіпає загальне зниження апетиту, включаючи посилення сигналів насичення та ослаблення сигналів голоду, а також покращення контролю споживання їжі та зниження тяги до їжі. Знижується також інсулінорезистентність, можливо, рахунок зменшення маси тіла. Крім цього, семаглутид знижує перевагу до їди з високим вмістом жирів. У дослідженнях на тваринах було показано, що семаглутид поглинається специфічними областями головного мозку та посилює ключові сигнали насичення та послаблює ключові сигнали голоду. Впливаючи на ізольовані ділянки тканин головного мозку, семаглутид активує нейрони, пов'язані з почуттям ситості, і пригнічує нейрони, пов'язані з почуттям голоду. У клінічних дослідженнях (КІ) семаглутид надавав позитивний вплив на ліпіди плазми, знижував систолічний артеріальний тиск (АТ) і зменшував запалення. У дослідженнях на тваринах семаглутид пригнічує розвиток атеросклерозу, попереджаючи подальший розвиток аортальних бляшок та зменшуючи запалення у бляшках. Фармакодинаміка Всі фармакодинамічні дослідження були проведені після 12 тижнів терапії (включаючи період збільшення дози) у рівноважній концентрації семаглутиду 1 мг 1 раз на тиждень. Рівень глікемії натще і постпрандіальний рівень глікемії Семаглутид знижує концентрацію глюкози натще і концентрацію постпрандіальної глюкози. У порівнянні з плацебо терапія семаглутидом 1 мг у пацієнтів з цукровим діабетом 2 типу (ЦД2) призвела до зниження концентрації глюкози з точки зору абсолютної зміни від вихідного значення (ммоль/л) та відносного зниження порівняно з плацебо (%) щодо: концентрації глюкози натще (1,6 ммоль/л; 22%); концентрації глюкози через 2 години після їди (4,1 ммоль/л; 37%); середньої добової концентрації глюкози (1,7 ммоль/л; 22%) та постпрандіальних піків концентрації глюкози за 3 прийоми їжі (0,6-1,1 ммоль/л). Семаглутид знижував концентрацію глюкози натще після введення першої дози. Функція бета-клітин підшлункової залози та секреція інсуліну Семаглутид покращує функцію бета-клітин підшлункової залози. Після внутрішньовенного струменевого введення глюкози пацієнтам з ЦД2 семаглутид у порівнянні з плацебо покращував першу та другу фазу інсулінової відповіді з трикратним та двократним підвищенням, відповідно, і збільшував максимальну секреторну активність бета-клітин підшлункової залози після тесту стимуляції аргін. Крім того, порівняно з плацебо-терапія семаглутидом збільшує концентрації інсуліну натще. Секреція глюкагону Семаглутид знижує концентрацію глюкагону натще і постпрандіальну концентрацію глюкагону. У пацієнтів із ЦД2 семаглутид призводить до відносного зниження концентрації глюкагону порівняно з плацебо: концентрації глюкагону натще (8-21%), постпрандіальної глюкагонової відповіді (14-15%) та середньої добової концентрації глюкагону (12%). Глюкозозалежна секреція інсуліну та глюкозозалежна секреція глюкагону Семаглутид знижував високу концентрацію глюкози в крові, стимулюючи секрецію інсуліну та знижуючи секрецію глюкагону глюкозозалежним способом. Швидкість секреції інсуліну після введення семаглутиду пацієнтам із ЦД2 була порівнянна з такою у здорових добровольців. Під час індукованої гіпоглікемії семаглутид у порівнянні з плацебо не змінював контррегуляторну відповідь підвищення концентрації глюкагону. а також не посилював зниження концентрації С-пептиду у пацієнтів із ЦД2. Випорожнення шлунка Семаглутид викликав невелику затримку раннього постпрандіального спорожнення шлунка, тим самим знижуючи швидкість надходження постпрандіати глюкози в кров. Маса тіла та склад тіла Спостерігалося більше зниження маси тіла при застосуванні семаглутиду порівняно з вивченими препаратами порівняння (плацебо, ситагліптином, ексенатидом уповільненого вивільнення (ЗВ), дулаглутидом та інсуліном гларгін) (див. розділ "Клінічна ефективність та безпека"). Втрата маси тіла при застосуванні семаглутиду відбувалася переважно рахунок втрати жирової тканини, що перевищує втрату м'язової маси в 3 разу. Апетит, споживання калорій та вибір продуктів харчування У порівнянні з плацебо, семаглутид знизив споживання калорій на 18-35% під час трьох послідовних прийомів їжі ad libitum. Цьому сприяли стимульовані семаглутидом придушення апетиту як натще, так і після прийому їжі, покращений контроль споживання їжі, ослаблення потягу до їжі, особливо з високим вмістом жирів. Ліпіди натще і постпрандіальні ліпіди У порівнянні з плацебо семаглутид знижував концентрації тригліцеридів та холестерину ліпопротеїнів дуже низької щільності (ЛПДНЩ) натще на 12% та 21%, відповідно. Постпрандіальне збільшення концентрації тригліцеридів та холестерину ЛПДНЩ у відповідь на прийом їжі з високим вмістом жирів знизилося більш ніж на 40%. Електрофізіологія серця (ЕФС) Дія семаглутиду на процес реполяризації у серці була протестована у дослідженні ЕФС. Застосування семаглутиду в дозах, що перевищують терапевтичні (у рівноважній концентрації до 1,5 мг), не призводило до подовження скоригованого інтервалу QT. Клінічна ефективність та безпека Як покращення глікемічного контролю, так і зниження СС захворюваності та смертності є невід'ємною частиною лікування ЦД2. Ефективність та безпека препарату Оземпік® у дозах 0,5 мг та 1 мг оцінювалися у шести рандомізованих контрольованих КІ 3а фази. З них п'ять КІ як основна мета оцінювали ефективність глікемічного контролю, в той час як одне КВ оцінювало в якості основної мети СС результат. На додаток було проведено два КІ препарату Оземпік® 3 фази за участю японських пацієнтів. Терапія препаратом Оземпік® продемонструвала стійкі, статистично переважаючі та клінічно значущі покращення показника HbA1c та зниження маси тіла на строк до 2 років порівняно з плацебо та лікуванням з активним контролем (ситагліптином, інсуліном гларгін, ексенатидом 3В та дулаглу). Вік, стать, раса, етнічна приналежність, вихідні значення індексу маси тіла (ІМТ) та маси тіла (кг), тривалість цукрового діабету (ЦД) та ниркова недостатність не вплинули на ефективність препарату Оземпік®. Монотерапія Монотерапія препаратом Оземпік® у дозах 0,5 мг та 1 мг 1 раз на тиждень протягом 30 тижнів порівняно з плацебо призвела до статистично більш значущого зниження показників HbA1c (-1,5%, -1,6% проти 0%, відповідно ), глюкози плазми натще (ГПН) (-2,5 ммоль/л, -2,3 ммоль/л проти -0,6 ммоль/л, відповідно) та маси тіла (-3,7 кг, -4,5 кг проти -1,0 кг відповідно). Препарат Оземпік® у порівнянні з ситагліптином, обидва в комбінації з 1-2 пероральними гіпоглікемічними препаратами (ПГГП) (метформіном та/або препаратами тіазолідиндіону) Терапія препаратом Оземпік® 0,5 мг та 1 мг 1 раз на тиждень протягом 56 тижнів порівняно з ситагліптином призвела до стійкого та статистично більшого зниження показників HbA1c (-1,3%, -1,6% проти -0,5 %, відповідно), ДПН (-2,1 ммоль/л, -2,6 ммоль/л проти -1,1 ммоль/л, відповідно) та маси тіла (-4,3 кг, -6,1 кг проти - 1,9 кг відповідно). Терапія препаратом Оземпік® 0,5 мг та 1 мг порівняно з ситагліптином значно знижувала систолічний АТ від вихідного значення 132,6 мм рт.ст. (-5,1 мм рт.ст., -5,6 мм рт.ст. проти -2,3 мм рт.ст. відповідно). Змін діастолічного артеріального тиску не відбувалося. Препарат Оземпік® у порівнянні з дулаглутидом, обидва у комбінації з метформіном Терапія препаратом Оземпік® 0,5 мг порівняно з дулаглутидом 0,75 мг, обидва 1 раз на тиждень протягом 40 тижнів, призвела до стійкого та статистично переважаючого зниження показників HbA1c (-1,5% проти -1,1%), ДПН (-2,2 ммоль/л проти -1,9 ммоль/л) та маси тіла (-4,6 кг проти -2,3 кг), відповідно. Терапія препаратом Оземпік® 1 мг у порівнянні з дулаглутидом 1,5 мг обидва 1 раз на тиждень протягом 40 тижнів, призвела до стійкого та статистично переважаючого зниження показників HbA1c (-l,8% проти -1,4%), ДПН (- 2,8 ммоль/л проти -2,2 ммоль/л) та маси тіла (-6,5 кг проти -3,0 кг), відповідно. Препарат Оземпік® в порівнянні з ексенатидом 3В, обидва в комбінації з метформіном або метформіном спільно з похідним сульфонілсечовини Терапія препаратом Оземпік® 1 мг 1 раз: на тиждень протягом 56 тижнів порівняно з ексенатидом 3В 2,0 мг призвела до стійкого та статистично більшого зниження показників HbA1c (-1,5% проти -0,9%), ДПН ( -2,8 ммоль/л проти -2,0 ммоль/л) та маси тіла (-5,6 кг проти -1,9 кг), відповідно. Препарат Оземпік® у порівнянні з інсуліном гларгін, обидва в комбінації з 1-2 ПГГП (монотерапія метформіном або метформін з похідним сульфонілсечовини) Терапія препаратом Оземпік у дозах 0,5 мг та 1 мг 1 раз на тиждень порівняно з інсуліном гларгін протягом 30 тижнів призвела до статистично більш значущого зниження показників HbA1c (-l,2%, -1,6% проти -0, 8%, відповідно) та маси тіла (-3,5 кг, -5,2 кг проти +1,2 кг, відповідно). Зниження показника ГНН було статистично більш значущим для препарату Оземпік 1 мг порівняно з інсуліном гларгін (-2,7 ммоль/л проти -2,1 ммоль/л). Не спостерігалося статистично більш значуще зниження показника ГНН для препарату Оземпік 0,5 мг (-2,0 ммоль/л проти -2,1 ммоль/л). Частка пацієнтів, у яких спостерігалися важкі чи підтверджені ( Більше пацієнтів досягли показника HbA1c Препарат Оземпік® у порівнянні з плацебо, обидва у комбінації з базальним інсуліном Терапія препаратом Оземпік у дозах 0,5 мг та 1 мг порівняно з плацебо протягом 30 тижнів призвела до статистично більш значущого зниження показників HbA1c (-1,4%, -1,8% проти -0,1%, відповідно) , ДПН (-1,6 ммоль/л, -2,4 ммоль/л проти -0,5 ммоль/л, відповідно) та маси тіла (-3,7 кг, -6,4 кг проти -1,4 кг відповідно). Частота важких або підтверджених епізодів гіпоглікемії істотно не відрізнялася при застосуванні препарату Оземпік і плацебо. Частка пацієнтів з показником HbA1c≤8% на скринінгу, що повідомили про важкі або підтверджені (8% на скринінгу). Комбінація з монотерапією похідним сульфонілсечовини На 30-му тижні КІ була проведена оцінка підгрупи з 123 пацієнтів, які перебувають на монотерапії похідним сульфонілсечовини. На 30-му тижні показник HbA1c знизився на 1,6% і на 1,5% при застосуванні препарату Оземпік у дозах 0,5 мг та 1 мг, відповідно, і збільшився на 0,1% при застосуванні плацебо. Комбінація із попередньо змішаним інсуліном ± 1-2 ПГГП На 30-му тижні КІ була проведена оцінка підгрупи з 867 пацієнтів, які перебувають на терапії попередньо змішаним інсуліном (у комбінації або без 2-х ПГГП). На 30-му тижні показник HbA1c знизився на 1,3% та на 1,8% при застосуванні препарату Оземпік у дозах 0,5 мг та 1 мг, відповідно, та знизився на 0,4% при застосуванні плацебо. Співвідношення пацієнтів, які досягли цільового зниження показника HbA1c До 79% пацієнтів досягли цілей лікування щодо зниження показника HbA1c Частка пацієнтів, які досягли показника HbA1c менше 7% без важких або підтверджених епізодів гіпоглікемії та без набору ваги, була значно більшою при застосуванні препарату Оземпік у дозах 0,5 мг та 1 мг (до 66% та 74%, відповідно) порівняно з пацієнтами, які отримували ситагліптин (27%), ексенатид 3В (29%), інсулін гларгін (16%), дулаглутид 0,75 мг (44%) та дулаглутид 1,5 мг (58%). Маса тіла Монотерапія препаратом Оземпік® 1 мг або терапія в комбінації з 1-2 лікарськими препаратами призводила до статистично більшого зниження маси тіла (втрата становила до 6,5 кг) порівняно з терапією плацебо, сітагліптином, ексенатидом 3В, інсуліном гларгін або дулаглу. Зниження маси тіла було стійким терміном до 2-х років. Після одного року терапії втрати маси ≥ 5% та ≥ 10% досягла більша кількість пацієнтів, які отримували препарат Оземпік® 0,5 мг (46% та 13%) та 1 мг (до 62% та 24%), порівняно з пацієнтами, активними препаратами, що перебували на терапії, порівняння ситагліптином і ексенатидом ЗВ (до 18% і до 4%). У КІ тривалістю 40 тижнів втрати маси ≥ 5% і ≥ 10% досягли більшої кількості пацієнтів, які отримували препарат Оземпік® 0,5 мг (44% і 14%), порівняно з пацієнтами, які отримували дулаглутид 0,75 мг (23% і 3%). Втрати маси ≥ 5% та ≥ 10% досягли більшої кількості пацієнтів, які отримували препарат Оземпік® 1 мг (до 63% та 27%), порівняно з пацієнтами, які отримували дулаглутид 1,5 мг (30% та 8%). У СС КІ втрати маси тіла ≥ 5% та ≥ 10% досягли більшої кількості пацієнтів, які отримували препарат Оземпік® 0,5 мг (36% та 13%) та 1 мг (47% та 20%), порівняно з пацієнтами, отримували плацебо 0,5 мг (18% та 6%) та 1 мг (19% та 7%). ДПН та постпрандіальне збільшення концентрації глюкози Під час усіх трьох щоденних прийомів їжі препарат Оземпік® 0,5 мг та 1 мг показав значне зниження концентрації ГНН до 2,8 ммоль/л та зниження постпрандіального приросту концентрації глюкози до 1,2 ммоль/л (різниця між значеннями до та після їжі). , отримана після трьох прийомів їжі). Функція бета-клітин підшлункової залози та інсулінорезистентність В ході терапії препаратом Оземпік® 0,5 мг та 1 мг відбулося покращення функції бета-клітин підшлункової залози та зменшення інсулінорезистентності, що підтверджується оцінкою гомеостатичних моделей функції бета-клітин підшлункової залози (НОМА-В) та інсулінорезистентності (HO). Ліпіди Під час КІ препарату Оземпік® спостерігалося покращення профілю ліпідів крові натще, переважно у групі, яка отримувала дозу 1 мг. Оцінка впливу на ССС 3297 пацієнтів з ЦД2 та високим СС ризиком були рандомізовані у подвійне сліпе КІ тривалістю 104 тижні на отримання препарату Оземпік® 0,5 мг або 1 мг 1 раз на тиждень або плацебо 0,5 мг або 1 мг на додаток до стандартної терапії СС захворювань у протягом наступних двох років. Терапія препаратом Оземпік привела до зниження на 26% ризику первинного комбінованого результату, що включає смерть через СС патології, інфаркт міокарда (ІМ) без смертельного результату та інсульт без смертельного результату. Насамперед це було зумовлено значним зменшенням частоти інсульту без смертельного результату (39%) та незначним зменшенням частоти ІМ без смертельного результату (26%), але без змін у частоті смерті через СС патології. Значно знизився ризик реваскуляризації міокарда або периферичних артерій, тоді як ризик нестабільної стенокардії, яка потребує госпіталізації, та ризик госпіталізації через серцеву недостатність знизилися незначно. Мікроциркуляторні результати включали 158 нових або погіршилися випадків нефропатії. Відносний ризик щодо часу до виникнення нефропатії (нові випадки розвитку персистуючої макроальбумінурії, персистуюче подвоєння сироваткової концентрації креатиніну, необхідність постійної замісної ниркової терапії та смерть через хворобу нирок) становив 0,64. На додаток до стандартної терапії СС захворювань, терапія препаралгом Оземпік® у дозах 0,5 мг та 1 мг порівняно з плацебо 0,5 мг та I мг протягом 104 тижнів призвела до значного та стійкого зниження від вихідних значень показника HbA1c (-1,1 % та -1,4% проти -0,4% та -0,4%, відповідно). Артеріальний тиск Спостерігалося значне зниження середнього систолічного АТ при застосуванні препарату Оземпік® 0,5 мг (3,5-5,1 мм рт.ст.) та Оземпік® 1 мг (5,4-7,3 мм рт.ст.) у комбінації з ПГГП чи базальним інсуліном. Не було значної різниці за показниками діастолічного АТ між препаратом Оземпік® та препаратами порівняння.Показання до застосуванняПрепарат Оземпік® показаний для застосування у дорослих пацієнтів з цукровим діабетом 2 типу на фоні дієти та фізичних вправ для покращення глікемічного контролю як: монотерапії; комбінованої терапії з іншими пероральними гіпоглікемічними препаратами (ПГГП) - метформіном, метформіном та похідним сульфонілсечовини, метформіном та/або тіазолідиндіоном, у пацієнтів, які не досягли адекватного глікемічного контролю при проведенні попередньої терапії; комбінованої терапії з інсуліном у пацієнтів, які не досягли адекватного глікемічного контролю на терапії препаратом Оземпік® та метформіном. Препарат Оземпік® показаний для зниження ризику розвитку великих серцево-судинних подій* у пацієнтів з цукровим діабетом 2 типу та високим серцево-судинним ризиком як доповнення до стандартного лікування серцево-судинних захворювань (на підставі аналізу часу настання першої великої серцево-судинної події) . *великі серцево-судинні події включають: смерть через серцево-судинну патологію, інфаркт міокарда без смертельного результату, інсульт без смертельного результату.Протипоказання до застосуванняГіперчутливість до семаглутиду або будь-якої з допоміжних речовин препарату; медулярний рак щитовидної залози в анамнезі, у тому числі у сімейному; множинна ендокринна неоплазія (МЕН) 2 типи; цукровий діабет 1 типу (ЦД1); діабетичний кетоацидоз. Протипоказано застосування препарату Оземпік® у наступних груп пацієнтів та при наступних станах/захворюваннях у зв'язку з відсутністю даних щодо ефективності та безпеки та обмеженим досвідом застосування: вагітність та період грудного вигодовування; вік до 18 років; печінкова недостатність важкого ступеня; термінальна стадія ниркової недостатності (кліренс креатиніну (КК)) хронічна серцева недостатність (ХСН) IV функціонального класу (відповідно до класифікації NYHA (Нью-Йоркська кардіологічна асоціація)). З обережністю: Препарат Оземпік® рекомендується застосовувати з обережністю у пацієнтів із нирковою недостатністю та у пацієнтів з наявністю панкреатиту в анамнезі.Вагітність та лактаціяВагітність Дослідження на тваринах продемонстрували репродуктивну токсичність препарату. Дані щодо застосування семаглутиду у вагітних жінок обмежені. Протипоказано застосовувати семаглутид під час вагітності. Жінкам із збереженим репродуктивним потенціалом рекомендується використовувати контрацепцію під час терапії семаглутидом. Якщо пацієнтка готується до вагітності або вагітність вже настала, терапію семаглутидом необхідно припинити. Через тривалий період напіввиведення терапію семаглутидом необхідно припинити щонайменше за 2 місяці до запланованого настання вагітності. Період грудного вигодовування У лактуючих щурів семаглутид проникав у молоко. Не можна виключити ризик для дитини, яка перебуває на грудному вигодовуванні. Протипоказано застосовувати семаглутид у період грудного вигодовування.Побічна діяНайчастіше реєстрованими небажаними реакціями (HP) під час КІ були порушення з боку шлунково-кишкового тракту, включаючи нудоту, діарею та блювання. В цілому, дані реакції були легким або середнім ступенем тяжкості і короткостроковими. HP розподілені за системно-органними класами відповідно до MedDRA із зазначенням частоти їх виникнення згідно з рекомендаціями ВООЗ: дуже часто (≥ 1/10); часто (≥ 1/100 до < 1/10); нечасто (≥ 1/1000 до < 1/100); рідко (≥ 1/10 000 до < 1/1000) та дуже рідко (< 1/10 000). У кожній групі частоти розвитку HP представлені зниження рівня серйозності. Таблиця 1 HP, виявлені при проведенні КІ 3 фази Система органів MedDRA Дуже часто Часто Не часто Рідко Порушення з боку імунної системи Анафілактичні реакції Порушення з боку обміну речовин та харчування Гіпоглікемія при спільному застосуванні з інсуліном або похідним сульфонілсечовини Гіпоглікемія при спільному застосуванні з іншими ПГГП; Зниження апетиту Порушення з боку нервової системи Запаморочення Дисгевзія Порушення з боку органу зору Ускладнення діабетичної ретинопатії Порушення з боку серця Збільшення частоти серцевих скорочень (ЧСС) Порушення з боку шлунково-кишкового тракту Нудота; Діарея Блювота; Біль в животі; Здуття живота; Запор; Диспепсія; Гастрит; Гастроезофагеальна рефлюксна хвороба; Відрижка; Метеоризм Порушення з боку печінки та жовчовивідних шляхів Холелітіаз Загальні розлади та порушення у місці введення Стомлюваність Реакції у місці введення Лабораторні та інструментальні дані Підвищення активності ліпази; Підвищення активності амілази; Зниження маси тіла aГіпоглікемія, визначена як важка (що вимагає допомоги іншої людини) або симптоматична у поєднанні з концентрацією глюкози у плазмі крові Ускладнення діабетичної ретинопатії - це поєднання з необхідності в фотокоагуляції сітківки ока, необхідності в інтравітреальному введенні препаратів, крововиливу в склоподібне тіло, розвитку сліпоти, пов'язаної з ЦД. Частота заснована на дослідженні результатів СС. 2-річне дослідження СС результатів та безпеки У популяції пацієнтів з високим ризиком розвитку СС захворювань профіль HP був аналогічним такому в інших КІ 3а фази. Опис окремих HP Гіпоглікемія Під час монотерапії препаратом Оземпік не спостерігалося епізодів важкої гіпоглікемії. Гіпоглікемія тяжкого ступеня, в основному, спостерігалася при застосуванні препарату Оземпік у комбінації з похідним сульфонілсечовини або інсуліном. Спостерігалося кілька епізодів тяжкої гіпоглікемії при застосуванні препарату Оземпік у комбінації з іншими, за винятком похідної сульфонілсечовини, ПГГП. HP з боку ШКТ Під час терапії препаратом Оземпік у дозах 0,5 мг та 1 мг у пацієнтів відзначалася нудота, діарея та блювання. Більшість реакцій були від легкого до середнього ступеня важкості та короткостроковими. HP стали причиною передчасного вибуття з КІ 3,9% та 5,9% пацієнтів відповідно. Найчастіше про HP повідомлялося у перші місяці терапії. Ускладнення діабетичної ретинопатії У 2-річному КІ, в якому брали участь пацієнти з ЦД2 та високим СС ризиком, тривалим перебігом ЦД та неадекватним контролем глікемії, підтверджені випадки ускладнень діабетичної ретинопатії розвивалися у більшої кількості пацієнтів, які отримували препарат Оземпік® (3,0%), порівняно з пацієнтами, які отримували плацебо (1,8%). У пацієнтів з анамнезом діабетичної ретинопатії на початку КІ зростання абсолютного ризику розвитку ускладнень було вищим. У пацієнтів з відсутністю підтвердженого анамнезу діабетичної ретинопатії кількість подій була однакова при застосуванні препарату Оземпік® та гошцебо. У КІ тривалістю до І року частота HP, пов'язаних з діабетичною ретинопатією, була однаковою у групі препарату Оземпік® та препаратів порівняння. Припинення лікування через HP Частота припинення лікування через HP склала 8,7% для пацієнтів, які отримували препарат Оземпік® 1 мг. Найбільш частими HP, що призводили до припинення лікування, були порушення з боку шлунково-кишкового тракту. Реакції у місці введення Повідомлялося про реакції в місці введення (таких як висип у місці введення, почервоніння) у 0,6% і 0,5% пацієнтів, які отримували семаглутид 0,5 мг і 1 мг, відповідно. Ці реакції мали, зазвичай, легкий характер. Імуногенність Внаслідок потенційних імуногенних властивостей білкових та пептидних лікарських препаратів у пацієнтів можуть з'явитися антитіла до семаглутиду після терапії препаратом Оземпік®. В кінці КІ частка пацієнтів, у яких були виявлені антитіла до семаглутиду в будь-який момент часу, була низькою (1-2%) і в жодного пацієнта не було виявлено нейтралізуючих антитіл до семаглутиду або антитіл з нейтралізуючим ендогенним ГПП-1 ефектом.Спосіб застосування та дозиПрепарат Оземпік® застосовують 1 раз на тиждень у будь-який час, незалежно від їди. Препарат Оземпік® вводять підшкірно в живіт, стегно або плече. Місце ін'єкції може змінюватись без корекції дози. Препарат Оземпік® не можна вводити внутрішньовенно та внутрішньом'язово. Подальша інформація щодо способу застосування міститься в інструкції-вкладиші. При необхідності день щотижневого введення можна змінювати за умови, що інтервал часу між двома ін'єкціями становить не менше 3-х днів (72 годин). Дози Початкова доза препарату Оземпік становить 0,25 мг 1 раз на тиждень. Після 4 тижнів застосування дозу слід збільшити до 0,5 мг 1 раз на тиждень. Для подальшого поліпшення глікемічного контролю після мінімуму 4 тижнів застосування препарату в дозі 0,5 мг 1 раз на тиждень, дозу можна збільшити до 1 мг 1 раз на тиждень. Доза препарату Оземпік 0,25 мг не є терапевтичною. Препарат Оземпік може застосовуватися у вигляді монотерапії або в комбінації з одним або більше гіпоглікемічними препаратами. При додаванні препарату Оземпік до попередньої терапії метформіном та/або тіазолідиндіоном терапію метформіном та/або тіазолідиндіоном можна продовжити в колишніх дозах. При додаванні препарату Оземпік® до терапії похідним сульфонілсечовини або інсуліном слід передбачити зниження дози похідного сульфонілсечовини або інсуліну з метою зниження ризику виникнення гіпоглікемій. Застосування препарату Оземпік не вимагає проведення самоконтролю концентрації глюкози крові. При застосуванні препарату Оземпік у комбінації з похідним сульфонілсечовини або інсуліном, такий самоконтроль концентрації глюкози крові може знадобитися для корекції дози похідного сульфонілсечовини або інсуліну. Пропущена доза У разі пропуску дози препарат Оземпік® слід ввести якнайшвидше протягом 5 днів з моменту запланованого введення дози. Якщо тривалість пропуску становить понад 5 днів, пропущену дозу не слід вводити. Наступну дозу препарату Оземпік слід ввести у звичайний запланований день. У кожному разі, пацієнти можуть відновити їх звичайний одноразовий щотижневий графік введення. Застосування препарату в спеціальних клінічних групах пацієнтів Пацієнти похилого віку (≥65 років) Не потрібна корекція дози залежно від віку. Досвід застосування семаглутиду у пацієнтів віком 75 років та старший обмежений. Пацієнти з печінковою недостатністю Не потрібна корекція дози у пацієнтів з печінковою недостатністю. Досвід застосування семаглутиду у пацієнтів, з печінковою недостатністю тяжкого ступеня обмежений; застосування препарату Оземпік у таких пацієнтів протипоказане. Пацієнти з нирковою недостатністю Не потрібна корекція дози у пацієнтів з нирковою недостатністю. Досвід застосування препарату у пацієнтів із термінальною стадією ниркової недостатності відсутній; застосування препарату Оземпік у таких пацієнтів протипоказане. Діти та підлітки Застосування препарату Оземпік® у дітей та підлітків віком до 18 років протипоказане через відсутність даних щодо безпеки та ефективності. Дослідження семаглутиду in vitro показали дуже невелику можливість інгібування або індукції ферментів системи цитохрому Р450 (CYP) та інгібування транспортерів лікарських препаратів. Затримка спорожнення шлунка при застосуванні семаглутиду може впливати на всмоктування супутніх пероральних лікарських засобів. Семаглутид слід застосовувати з обережністю у пацієнтів, які отримують пероральні лікарські препарати, для яких необхідна швидка абсорбція шлунково-кишкового тракту. Парацетамол Оцінюючи фармакокінетики парацетамолу під час тесту стандартизованого прийому їжі було виявлено, що семаглутид затримує спорожнення шлунка. При одночасному застосуванні семаглутиду в дозі 1 мг AUC0-60 хв та Сmах парацетамолу знизилися на 27% та 23% відповідно. Загальна експозиція парацетамолу (AUC0-5год) не змінювалася. При одночасному прийомі семаглутиду та парацетамолу корекція дози останнього не потрібна. Пероральні гормональні контрацептивні засоби Не передбачається, що семаглутид знижує ефективність пероральних гормональних контрацептивних засобів. При одночасному застосуванні комбінованого перорального гормонального контрацептивного препарату (0,03 мг етинілестрадіолу/0,15 мг левоноргестрелу) та семаглутиду останній не впливав на клінічно значущий вплив на загальну експозицію етинілестрадіолу та левоноргестрелу. Експозиція етинілестрадіолу не була порушена; спостерігалося збільшення на 20% експозиції левоноргестрелу у рівноважному стані. Сахах не змінилася для жодного з компонентів. Аторвастатин Семаглутид не змінював системну експозицію аторвастатину після застосування одноразової дози аторвастатину (40 мг). Стих аторвастатину знизився на 38%. Ця зміна була розцінена як клінічно незначна. Дігоксин Семаглутид не змінював системну експозицію або Сmах дигоксину після застосування одноразової дози дигоксину (0,5 мг). Метформін Семаглутид не змінював системну експозицію або Сmах метформіну після застосування метформіну в дозі 500 мг 2 рази на день протягом 3,5 днів. Варфарін Семаглутид не змінював системну експозицію або Сmах R- та S-ізомерів варфарину після застосування одноразової дози варфарину (25 мг). На підставі визначення міжнародного нормалізованого відношення (МНО) клінічно значущих змін фармакодинамічних ефектів варфарину також не спостерігалося. Несумісність Речовини, додані до препарату Оземпік®, можуть спричинити деградацію семаглутиду. Препарат Оземпік® не можна змішувати з іншими лікарськими засобами, зокрема з інфузійними розчинами.ПередозуванняУ ході КІ повідомлялося про передозування до 4 мг в одноразовій дозі та до 4 мг на тиждень. Найчастішою HP, про яку повідомлялося, була нудота. Усі пацієнти одужали без ускладнень. Специфічного антидоту при передозуванні препарату Оземпік не існує. У разі передозування рекомендується проведення відповідної симптоматичної терапії. Враховуючи тривалий період виведення препарату (приблизно 1 тиждень), може знадобитися тривалий період спостереження та лікування симптомів передозування.Запобіжні заходи та особливі вказівкиЗастосування препарату Оземпік протипоказано у пацієнтів з ЦД1 або для лікування діабетичного кетоацидозу. Препарат Оземпік не замінює інсулін. Реакції з боку шлунково-кишкового тракту Застосування агоністів ГПП-1Р може бути асоційоване з HP з боку шлунково-кишкового тракту. Це слід враховувати при лікуванні пацієнтів з нирковою недостатністю, оскільки нудота, блювання та діарея можуть призвести до дегідратації та погіршення функції нирок. Гострий панкреатит При застосуванні агоністів ГПП-1Р спостерігалися випадки розвитку гострого панкреатиту. Пацієнти повинні бути поінформовані про характерні симптоми гострого панкреатиту. При підозрі на панкреатит терапія препаратом Оземпік повинна бути припинена; у разі підтвердження гострого панкреатиту терапію препаратом Оземпік® відновлювати не слід. Слід бути обережними у пацієнтів з панкреатитом в анамнезі. За відсутності інших ознак та симптомів гострого панкреатиту підвищення активності ферментів підшлункової залози не є прогностичним фактором розвитку гострого панкреатиту. Гіпоглікемія Пацієнти, які отримують препарат Оземпік у комбінації з похідним сульфонілсечовини або інсуліном, можуть мати підвищений ризик розвитку гіпоглікемії. На початку лікування препаратом Оземпік® ризик розвитку гіпоглікемії можна знизити, зменшивши дозу похідного сульфонілсечовини або інсуліну. Діабетична ретинопатія Спостерігалося підвищення ризику ускладнень діабетичної ретинопатії у пацієнтів з наявністю діабетичної ретинопатії, які отримують терапію інсуліном та семаглутидом (див. розділ "Побічна дія"). Слід бути обережними при застосуванні семаглутиду у пацієнтів з діабетичною ретинопатією, які отримують інсулінотерапію. Такі пацієнти повинні перебувати під постійним наглядом та отримувати лікування відповідно до клінічних рекомендацій. Швидке покращення глікемічного контролю було асоційоване з тимчасовим погіршенням стану діабетичної ретинопатії, проте не можна виключати й інші причини. Серцева недостатність Відсутній досвід застосування препарату Оземпік у пацієнтів з ХСН IV функціонального класу відповідно до класифікації NYHA. Застосування препарату у пацієнтів протипоказане. Захворювання щитовидної залози У післяреєстраційному періоді застосування іншого аналога ГПП-1, ліраглутиду, були відмічені випадки медулярного раку щитовидної залози (МРЩЗ). Наявних даних недостатньо для встановлення або виключення причинно-наслідкового зв'язку виникнення МРЩЗ із застосуванням аналогів ГПП-1. Необхідно проінформувати пацієнта про ризик МРЩЗ та про симптоми пухлини щитовидної залози (появи ущільнення в області шиї, дисфагії, задишки, непрохідної захриплості голосу). Значне підвищення концентрації кальцитоніну в плазмі може вказувати на МРЖЩ (у пацієнтів з МРЖЩ значення концентрації кальцитоніну в плазмі крові зазвичай >50 нг/л). При виявленні підвищення концентрації кальцитону в плазмі слід провести подальше обстеження пацієнта. Пацієнти з вузлами у щитовидній залозі,виявленими при медичному огляді або при проведенні УЗД щитовидної залози також повинні бути додатково обстежені. Застосування семаглутиду у пацієнтів із особистим або сімейним анамнезом МРЩЗ або з синдромом МЕН типу 2 протипоказане. Доклінічні дані щодо безпеки Доклінічні дані, засновані на дослідженнях фармакологічної безпеки, токсичності повторних доз та генотоксичності, не виявили жодної небезпеки для людини. У 2-річних дослідженнях канцерогенності у щурів та мишей при клінічно значущих концентраціях семаглутид спричинив розвиток пухлин С-клітин щитовидної залози без смертельного результату. Пухлини С-клітин щитовидної залози без смертельного результату, які спостерігаються у щурів, характерні для групи аналогів ГПП-1. Вважається, що щодо людей цей ризик є низьким, але може бути повністю виключений. Фертильність Дія семаглутиду на фертильність у людей невідома. Семаглутід не впливав на фертильність самців щурів. Серед самок щурів збільшення естрального циклу та незначне зниження кількості овуляцій спостерігалося при дозах, що супроводжувалися зниженням маси тіла самки. Посібник із використання Попередньо заповнена шприц-ручка Оземпік® поставляється у двох видах: Оземпік® 0.25 мг/доза або 0,5 мг/доза розчин для підшкірного введення у попередньо заповненій шприц-ручці дозволяє вводити дози 0,25 мг або 0,5 мг. Дана шприц-ручка призначена для підвищення дози та підтримання терапевтичної дози 0,5 мг. Одна шприц-ручка містить 15 мл розчину. Оземпік® 1 мг/доза розчин для підшкірного введення у попередньо заповненій шприц-ручці дозволяє вводити дози лише 1 мг. Дана шприц-ручка призначена лише для підтримки терапевтичної дози 1 мг. Одна шприц-ручка містить 3 мл розчину. В упаковку препарату Оземпік включені голки НовоФайн Плюс. Пацієнту слід рекомендувати викидати ін'єкційну голку після кожної ін'єкції відповідно до місцевих вимог. Шприц-ручка Оземпік призначена тільки для індивідуального використання. Препарат Оземпік® не можна застосовувати, якщо він виглядає інакше, ніж прозорий безбарвний або майже безбарвний розчин. Препарат Оземпік® не можна застосовувати, якщо він був заморожений. Препарат Оземпік можна вводити за допомогою голок довжиною до 8 мм. Шприц-ручка призначена для використання із одноразовими ін'єкційними голками НовоФайн®. Завжди після кожної ін'єкції видаляйте голку та зберігайте шприц-ручку Оземпік з від'єднаною голкою. Це допоможе запобігти закупорці голок, забруднення, зараження, витікання розчину та введення неправильної дози препарату. Інструкція для пацієнтів із застосування препарату Оземпік® 0,25 мг/доза або 0,5 мг/доза розчин для підшкірного введення у попередньо заповненій шприц-ручці Уважно прочитайте цю інструкцію перед застосуванням попередньо заповненої шприц-ручки Оземпік®. Використовуйте шприц-ручку лише після того, як Ви навчитеся нею користуватися під керівництвом лікаря або медсестри. Почніть з перевірки шприц-ручки, щоб переконатися, що міститься препарат Оземпік® 0,25 мг/доза або 0,5 мг/доза, потім подивіться на подані нижче ілюстрації, щоб ознайомитися з різними частинами шприц-ручки та голки. Якщо Ви слабозорі або у Вас є серйозні проблеми із зором, і Ви не можете розрізнити цифри на лічильнику дози, не використовуйте шприц-ручку без сторонньої допомоги. Допомогти вам може людина з добрим зором, навчена використанню попередньо заповненої шприц-ручки з препаратом Оземпік®. Ця шприц-ручка є попередньо заповненою шприц-ручкою. Вона містить 2 мг семаглутиду та дозволяє вибрати дози 0,25 мг або 0,5 мг. Шприц-ручка розроблена для використання з одноразовими голками НовоФайн довжиною до 8 мм. Голки НовоФайн Плюс включені в упаковку. Важлива інформація Зверніть особливу увагу на інформацію, зазначену такими значками, це дуже важливо для безпечного використання шприц-ручки. 1. Підготовка шприц-ручки з новою голкою для використання Перевірте назву та колірний код на етикетці шприц-ручки, щоб переконатися, що вона містить препарат Оземпік® 0,25 мг/доза або 0,5 мг/доза. Це особливо важливо, якщо Ви використовуєте більше одного ін'єкційного препарату. Зніміть ковпачок із шприц-ручки. Переконайтеся, що розчин у шприц-ручці є прозорим і безбарвним. Подивіться у віконце шприц-ручки. Якщо розчин каламутний і безбарвний, не використовуйте шприц ручку. Візьміть нову голку та видаліть захисну наклейку. Якщо захисна наклейка пошкоджена, не використовуйте голку, оскільки стерильність у цьому випадку не гарантується. Надягніть голку на шприц-ручку і поверніть її, щоб голка щільно трималася на шприц-ручці. Зніміть зовнішній ковпачок голки, але не викидайте його. Він знадобиться після завершення ін'єкції, щоб безпечно зняти голку зі шприц-ручки. Зніміть та викиньте внутрішній ковпачок голки. Якщо Ви спробуєте надіти внутрішній ковпачок назад на голку, Ви можете випадково вколотись голкою. На кінці голки може виникнути крапля розчину. Це нормальне явище, однак, Ви все одно повинні перевірити надходження препарату, якщо Ви використовуєте нову шприц-ручку вперше. Не приєднуйте нову голку доти, доки Ви не будете готові зробити ін'єкцію. Завжди використовуйте нову голку для кожної ін'єкції. Це може запобігти закупорці голок, забруднення, інфікування та введення неправильної дози препарату. Ніколи не використовуйте голку, якщо вона погнута чи пошкоджена. 2. Перевірка надходження препарату Перед першою ін'єкцією за допомогою кожної нової шприц-ручки перевірте надходження препарату. Якщо шприц-ручка вже є у використанні, перейдіть до операції 3 "Встановлення дози". Повертайте селектор дози, доки лічильник дози не порівняється із символом перевірки надходження препарату. Тримайте шприц-ручку голкою вгору. Натисніть пускову кнопку і утримуйте її в цьому положенні, доки лічильник дози не повернеться до "0". "0" повинен стояти навпроти вказівника дози. На кінці голки має з'явитися крапля розчину. На кінці голки може залишатися невелика крапля, але вона не буде введена при ін'єкції. Якщо крапля розчину на кінці голки не з'явилася, повторіть операцію "2" "Перевірка надходження препарату", але не більше 6 разів. Якщо крапля розчину так і не з'явилася, поміняйте голку та повторіть операцію "2" "Перевірка надходження препарату" ще раз. Якщо крапля розчину так і не з'явилася, утилізуйте шприц-ручку та використовуйте нову. Завжди перед використанням нової шприц-ручки вперше переконайтеся, що на кінці голки з'явилася крапля розчину. Це гарантує надходження препарату. Якщо крапля розчину не з'явилася, препарат не буде введений, навіть якщо лічильник дози рухатиметься. Це може вказувати на те, що голка закупорена або пошкоджена. Якщо Ви не перевірите надходження препарату перед першою ін'єкцією за допомогою кожної нової шприц-ручки, Ви можете не ввести необхідну дозу та очікуваного ефекту препарату Оземпік® не буде досягнуто. 3. Встановлення дози Повертайте селектор дози доти, доки він не покаже необхідну Вам дозу (0,25 мг або 0,5 мг). Якщо доза була вибрана неправильно, Ви можете повертати селектор дози вперед або назад, доки не буде встановлена правильна доза. Максимальна доза, яку можна встановити становить 0,5 мг. Селектор дози змінює дозу. Тільки лічильник дози та покажчик дози покажуть кількість мг препарату у вибраній Вами дозі. Ви можете вибрати до 0,5 мг препарату на дозу. Якщо шприц-ручка містить менше 0,5 мг, лічильник дози зупиниться перш, ніж з'явиться "0,5". При кожному повороті селектора дози лунають клацання, звук клацань залежить від того, в яку сторону обертається селектор дози: вперед, назад або якщо набрана доза перевищує кількість мг препарату, що залишилися в шприц-ручці. Не рахуйте клацання шприц-ручки. Завжди перед кожною ін'єкцією перевіряйте скільки мг препарату Ви набрали але лічильнику дози та вказівнику дози. Не рахуйте клацання шприц-ручки. За допомогою селектора дози слід вибирати лише дози 0,25 мг або 0,5 мг. Вибрана доза повинна бути точно напроти вказівника дози - таке положення гарантує, що Ви отримаєте правильну дозу препарату. Скільки препарату залишилось Щоб визначити, скільки препарату залишилося, використовуйте лічильник дози: Повертайте селектор дози до зупинки лічильника. Якщо він показує "0,5", у шприц-ручці залишилося щонайменше 0,5 мг препарату. Якщо лічильник дози зупинився до того, як з'явилося "0,5", це означає, що в шприц-ручці залишилася недостатня кількість препарату, щоб ввести повну дозу 0,5 мг. Якщо в шприц-ручці залишилася недостатня кількість препарату для введення повної дози, не використовуйте шприц-ручку. Використовуйте нову шприц-ручку Оземпік®. 4. Введення препарату Введіть голку під шкіру, використовуючи техніку ін'єкцій, рекомендовану лікарем або медсестрою. Переконайтеся, що лічильник дози знаходиться у полі вашого зору. Не торкайтеся лічильника дози пальцями - це може перервати ін'єкцію. Натисніть пускову кнопку до упору та утримуйте її в цьому положенні, доки лічильник дози не покаже "0". "0" повинен знаходитися напроти вказівника дози. При цьому Ви можете почути чи відчути клацання. Утримуйте голку під шкірою після того, як лічильник дози повернувся до "0" і повільно рахуйте до 6. Якщо ви витягнете голку з-під шкіри раніше, ви можете побачити, як препарат випливає з голки. У цьому випадку буде введено неповну дозу препарату. Вийміть голку з-під шкіри. Якщо в місці ін'єкції з'явилася кров, притисніть до місця уколу ватний тампон. Не масажуйте місце уколу. Після завершення ін'єкції можна побачити краплю розчину на кінці голки. Це нормально і не впливає на дозу, яку Ви ввели. Завжди звіряйтеся зі показаннями лічильника дози, щоб знати, яку кількість мг препарату ви ввели. Утримуйте пускову кнопку, доки лічильник дози не покаже "0". Як виявити закупорку або пошкодження голки Якщо після тривалого натискання на пускову кнопку на лічильнику дози не з'являється "0", це може означати закупорку або пошкодження голки. У цьому випадку Ви не отримали препарат, навіть якщо лічильник дози змінив положення вихідної дози, яку Ви встановили. Що робити із закупореною голкою Замініть голку як описано в операції 5 "Після завершення ін'єкції" і повторіть всі кроки, починаючи з операції 1 "Підготовка шприц-ручки з новою голкою до використання". Переконайтеся, що встановили необхідну Вам дозу. Ніколи не торкайтеся лічильника дози під час введення препарату. Це може перервати ін'єкцію. 5. Після завершення ін'єкції Поклавши зовнішній ковпачок голки на плоску поверхню, введіть кінець голки всередину ковпачка, не торкаючись його голки. Коли голка увійде в ковпачок, обережно надягніть зовнішній ковпачок на голку. Відкрутіть голку і викиньте її, дотримуючись запобіжних заходів. Після кожного використання надягайте на шприц-ручку ковпачок, щоб захистити розчин, що міститься в ній, від впливу світла. Завжди після кожної ін'єкції викидайте голку, щоб забезпечити комфортну ін'єкцію та уникнути закупорки голок. Якщо голка закупорена, Ви не введете препарат. Викидайте порожню шприц-ручку з від'єднаною голкою відповідно до рекомендацій лікаря, медсестра, фармацевта або місцевих вимог. Ніколи не намагайтеся надіти внутрішній ковпачок назад на голку. Ви можете вколотись. Після кожної ін'єкції завжди одразу видаляйте голку зі шприц-ручки. Це може запобігти закупорці голок, забруднення, інфікування, витікання розчину та введення неправильної дози препарату. Додаткова важлива інформація Завжди зберігайте шприц-ручку та голки до неї в недоступному для всіх, особливо для дітей, місці. Ніколи не передавайте свою шприц-ручку та голки до неї іншим особам. Особи, що здійснюють догляд за хворим, повинні звертатися з використаними голками з особливою обережністю, щоб запобігти уколам голки та перехресному інфікуванню. Догляд за шприц-ручкою Акуратно поводьтеся зі шприц-ручкою. Недбале поводження або неправильне використання можуть призвести до введення неправильної дози препарату, наслідком чого можуть стати висока концентрація глюкози крові або дискомфорт у ділянці живота (нудота або блювання). Не залишайте шприц-ручку в автомобілі або іншому місці, де вона може піддаватися впливу занадто високих або занадто низьких температур. Не застосовуйте препарат Оземпік, якщо він був заморожений. У цьому випадку концентрація глюкози крові може стати занадто високою або Ви можете відчути дискомфорт у ділянці живота, такий, як нудота або блювота. Не застосовуйте препарат Оземпік®, якщо він зазнав прямих сонячних променів. У цьому випадку концентрація глюкози може стати занадто високою. Захищайте шприц-ручку від попадання на неї пилу, забруднень та рідини. Не мийте шприц-ручку, не занурюйте її в рідину і не змащуйте її. При необхідності шприц-ручку можна очищати вологою тканиною, змоченою м'яким миючим засобом. Не можна кидати або вдаряти шприц-ручку об тверду поверхню. Якщо Ви впустили шприц-ручку або сумніваєтеся у її справності, приєднайте нову голку та перевірте надходження препарату перед тим, як зробити ін'єкцію. Не намагайтеся повторно заповнити шприц-ручку. Порожню шприц-ручку слід викинути. Не намагайтеся самостійно полагодити шприц-ручку або розібрати її на частини. Інструкція для пацієнтів із застосування препарату Оземпік® 1 мг/доза розчин для підшкірного введення у попередньо заповненій шприц-ручці Уважно прочитайте цю інструкцію перед застосуванням попередньо заповненої шприц-ручки Оземпік®. Використовуйте шприц-ручку лише після того, як Ви навчитеся нею користуватися під керівництвом лікаря або медсестри. Почніть з перевірки шприц-ручки, щоб переконатися, що міститься препарат Оземпік® 1 мг/доза, потім подивіться на подані нижче ілюстрації, щоб ознайомитися з різними частинами шприц-ручки та голки. Якщо Ви слабозорі або у Вас є серйозні проблеми із зором, і Ви не можете розрізнити цифри на лічильнику дози, не використовуйте шприц-ручку без сторонньої допомоги. Допомогти вам може людина з добрим зором, навчена використанню попередньо заповненої шприц-ручки з препаратом Оземпік®. Ця шприц-ручка є попередньо заповненою шприц-ручкою. Вона містить 4 мг семаглутиду і дозволяє вибрати лише дозу 1 мг. Шприц-ручка розроблена для використання з одноразовими голками НовоФайн довжиною до 8 мм. Голки НовоФайн Плюс включені в упаковку. Важлива інформація Зверніть особливу увагу на інформацію, зазначену такими значками, це дуже важливо для безпечного використання шприц-ручки. 1. Підготовка шприц-ручки з новою голкою для використання Перевірте назву та колірний код на етикетці шприц-ручки, щоб переконатися, що міститься препарат Оземпік® 1 мг/доза. Це особливо важливо, якщо Ви використовуєте більше одного ін'єкційного препарату. Зніміть ковпачок із шприц-ручки. Переконайтеся, що розчин у шприц-ручці є прозорим і безбарвним. Подивіться у віконце шприц-ручки. Якщо розчин каламутний і безбарвний, не використовуйте шприц ручку. Візьміть нову голку та видаліть захисну наклейку. Якщо захисна наклейка пошкоджена, не використовуйте голку, оскільки стерильність у цьому випадку не гарантується. Надягніть голку на шприц-ручку і поверніть її, щоб голка щільно трималася на шприц-ручці. Зніміть зовнішній ковпачок голки, але не викидайте його. Він знадобиться після завершення ін'єкції, щоб безпечно зняти голку зі шприц-ручки. Зніміть та викиньте внутрішній ковпачок голки. Якщо Ви спробуєте надіти внутрішній ковпачок назад на голку, Ви можете випадково вколотись голкою. На кінці голки може виникнути крапля розчину. Це нормальне явище, однак Ви все одно повинні перевірити надходження препарату, якщо Ви використовуєте нову шприц-ручку вперше. Не приєднуйте нову голку доти, доки Ви не будете готові зробити ін'єкцію. Завжди використовуйте нову голку для кожної ін'єкції. Це може запобігти закупорці голок, забруднення, інфікування та введення неправильної дози препарату. Ніколи не використовуйте голку, якщо вона погнута чи пошкоджена. 2. Перевірка надходження препарату Перед першою ін'єкцією за допомогою кожної нової шприц-ручки перевірте надходження препарату. Якщо шприц-ручка вже є у використанні, перейдіть до операції 3 "Встановлення дози". - Повертайте селектор дози, доки лічильник дози не порівняється із символом перевірки надходження препарату (рис. А). - Тримайте шприц-ручку голкою вгору. Натисніть пускову кнопку та утримуйте її в цьому положенні, доки лічильник дози не повернеться до "0" (мал. В). "О" має стояти навпроти вказівника дози. На кінці голки має з'явитися крапля розчину. На кінці голки може залишатися невелика крапля, але вона не буде введена при ін'єкції. Якщо крапля розчину на кінці голки не з'явилася, повторіть операцію "2" "Перевірка надходження препарату", але не більше 6 разів. Якщо крапля розчину так і не з'явилася, поміняйте голку та повторіть операцію "2" "Перевірка надходження препарату" ще раз. Якщо крапля розчину так і не з'явилася, утилізуйте шприц-ручку та використовуйте нову. Завжди перед використанням нової шприц-ручки вперше переконайтеся, що на кінці голки з'явилася крапля розчину. Це гарантує надходження препарату. Якщо крапля розчину не з'явилася, препарат не буде введений, навіть якщо лічильник дози рухатиметься. Це може вказувати на те, що голка закупорена або пошкоджена. Якщо Ви не перевірите надходження препарату перед першою ін'єкцією за допомогою кожної нової шприц-ручки, Ви можете не ввести необхідну дозу та очікуваного ефекту препарату Оземпік® не буде досягнуто. 3. Встановлення дози Поверніть селектор дози, щоб вибрати дозу 1 мг. Продовжуйте повертати, доки лічильник дози не зупиниться і не покаже "1". Тільки лічильник дози та покажчик дози покажуть, що було обрано 1 мг. Ви можете вибрати лише 1 мг препарату на дозу. Якщо шприц-ручка містить менше 1 мг, лічильник дози зупиниться перш, ніж з'явиться "1". При кожному повороті селектора дози лунають клацання, звук клацань залежить від того, в яку сторону обертається селектор дози: вперед, назад або якщо Ви намагаєтесь набрати дозу більше 1 мг. Не рахуйте клацання шприц-ручки. Завжди перед кожною ін'єкцією за лічильником дози та вказівником дози перевіряйте, що набрано 1 мг. Не рахуйте клацання шприц-ручки. За допомогою селектора дози слід вибирати лише дозу 1 мг. Доза 1 мг повинна бути точно проти вказівника дози – таке положення гарантує, що Ви отримаєте правильну дозу препарату. Скільки препарату залишилось Щоб визначити, скільки препарату залишилося, використовуйте лічильник дози: Повертайте селектор дози до зупинки лічильника. Якщо він показує "1", у шприц-ручці залишилося щонайменше 1 мг препарату. Якщо лічильник дози зупинився до того, як з'явилася цифра "1", це означає, що в шприц-ручці залишилася недостатня кількість препарату, щоб ввести повну дозу 1 мг. Якщо в шприц-ручці залишилася недостатня кількість препарату для введення повної дози, не використовуйте шприц-ручку. Використовуйте нову шприц-ручку Оземпік®. 4. Введення препарату Введіть голку під шкіру, використовуючи техніку ін'єкцій, рекомендовану лікарем або медсестрою. Переконайтеся, що лічильник дози знаходиться у полі вашого зору. Не торкайтеся лічильника дози пальцями - це може перервати ін'єкцію. Натисніть пускову кнопку до упору та утримуйте її в цьому положенні, доки лічильник дози не покаже "О". "О" повинен бути точно навпроти вказівника дози. При цьому Ви можете почути чи відчути клацання. Утримуйте голку під шкірою після того, як лічильник дози повернувся до "0" і повільно рахуйте до 6. Якщо ви витягнете голку з-під шкіри раніше, ви можете побачити, як препарат випливає з голки. У цьому випадку буде введено неповну дозу препарату. Вийміть голку з-під шкіри. Якщо в місці ін'єкції з'явилася кров, притисніть до місця уколу ватний тампон. Не масажуйте місце уколу. Після завершення ін'єкції можна побачити краплю розчину на кінці голки. Це нормально і не впливає на дозу, яку Ви ввели. Завжди звіряйтеся зі показаннями лічильника дози, щоб знати, яку кількість мг препарату ви ввели. Утримуйте пускову кнопку, доки лічильник дози не покаже "О". Як виявити закупорку або пошкодження голки Якщо після тривалого натискання на пускову кнопку на лічильнику дози не з'являється "О", це може означати закупорку або пошкодження голки. У цьому випадку Ви не отримали препарат, навіть якщо лічильник дози змінив положення вихідної дози, яку Ви встановили. Що робити із закупореною голкою Замініть голку як описано в операції 5 "Після завершення ін'єкції" і повторіть всі кроки, починаючи з операції 1 "Підготовка шприц-ручки з новою голкою до використання". Переконайтеся, що встановили необхідну Вам дозу. Ніколи не торкайтеся лічильника дози під час введення препарату. Це може перервати ін'єкцію. 5. Після завершення ін'єкції Поклавши зовнішній ковпачок голки на плоску поверхню, введіть кінець голки всередину ковпачка, не торкаючись його голки. Коли голка увійде в ковпачок, обережно надягніть зовнішній ковпачок на голку. Відкрутіть голку і викиньте її, дотримуючись запобіжних заходів. - Після кожного використання надягайте на шприц-ручку ковпачок, щоб захистити розчин, що міститься в ній, від впливу світла. Завжди після кожної ін'єкції викидайте голку, щоб забезпечити комфортну ін'єкцію та уникнути закупорки голок. Якщо голка закупорена, Ви не введете препарат. Викидайте порожню шприц-ручку з від'єднаною голкою відповідно до рекомендацій лікаря, медсестра, фармацевта або місцевих вимог. Ніколи не намагайтеся надіти внутрішній ковпачок назад на голку. Ви можете вколотись. Після кожної ін'єкції завжди одразу видаляйте голку зі шприц-ручки. Це може запобігти закупорці голок, забруднення, інфікування, витікання розчину та введення неправильної дози препарату. Додаткова важлива інформація Завжди зберігайте шприц-ручку та голки до неї в недоступному для всіх, особливо для дітей, місці. Ніколи не передавайте свою шприц-ручку та голки до неї іншим особам. Особи, що здійснюють догляд за хворим, повинні звертатися з використаними голками з особливою обережністю, щоб запобігти уколам голки та перехресному інфікуванню. Догляд за шприц-ручкою Акуратно поводьтеся зі шприц-ручкою. Недбале поводження або неправильне використання можуть призвести до введення неправильної дози препарату, наслідком чого можуть стати висока концентрація глюкози крові або дискомфорт у ділянці живота (нудота або блювання). Не залишайте шприц-ручку в автомобілі або іншому місці, де вона може піддаватися впливу занадто високих або занадто низьких температур. Не застосовуйте препарат Оземпік, якщо він був заморожений. У цьому випадку концентрація глюкози крові може стати занадто високою або Ви можете відчути дискомфорт у ділянці живота, такий, як нудота або блювота. Не застосовуйте препарат Оземпік®, якщо він зазнав прямих сонячних променів. У цьому випадку концентрація глюкози може стати занадто високою. Захищайте шприц-ручку від попадання на неї пилу, забруднень та рідини. Не мийте шприц-ручку, не занурюйте її в рідину і не змащуйте її. При необхідності шприц-ручку можна очищати вологою тканиною, змоченою м'яким миючим засобом. Не можна кидати або вдаряти шприц-ручку об тверду поверхню. Якщо Ви впустили шприц-ручку або сумніваєтеся у її справності, приєднайте нову голку та перевірте надходження препарату перед тим, як зробити ін'єкцію. Не намагайтеся повторно заповнити шприц-ручку. Порожню шприц-ручку слід викинути. Не намагайтеся самостійно полагодити шприц-ручку або розібрати її на частини. Вплив на здатність до керування автотранспортом та управління механізмами Препарат Оземпик® не влияет или незначительно влияет на способность управлять транспортными средствами или работу с механизмами. Пациенты должны быть предупреждены о том, что им следует соблюдать меры предосторожности во избежание развития у них гипогликемии во время управления транспортными средствами и при работе с механизмами, особенно при применении препарата Оземпик® в комбинации с производным сульфонилмочевины или инсулином.Условия храненияВ холодильнике +2 +8 градусУсловия отпуска из аптекПо рецептуВідео на цю тему
449,00 грн
232,00 грн
Склад, форма випуску та упаковкаРозчин - 1 мл: речовина, що діє: семаглутид 1,34 мг; допоміжні речовини: динатрію гідрофосфат дигідрат, пропіленгліколь, фенол, хлористоводнева кислота (для корекції pH), гідроксид натрію (для корекції pH), вода для ін'єкцій. В одній попередньо заповненій шприц-ручці об'ємом 1,5 мл міститься 2 мг семаглутиду. Розчин для підшкірного введення 1,34 мг/мл. По 1,5 мл препарату в картриджі зі скла, закупорені поршнями з хлорбутилової гуми з одного боку та алюмінієвими ковпачками з дисками з бромбутилової гуми/поліізопрену, з іншого боку. Картридж вбудований в мультидозову одноразову шприц-ручку для багаторазових ін'єкцій з поліпропілену, поліоксиметилену, полікарбонату та акрилонітрил бутадієн стиролу. 1 шприц-ручка разом з інструкцією із застосування та 6 одноразовими голками НовоФайн® Плюс у картонну пачку.Опис лікарської формиПрозорий, безбарвний чи майже безбарвний розчин.Фармакотерапевтична групаГіпоглікемічний засіб – аналог глюкагоноподібного пептиду-1.ФармакокінетикаПрепарат підходить для введення 1 раз на тиждень, тому що період напіввиведення семаглутиду дорівнює приблизно 1 тижню. Абсорбція Час досягнення максимальної концентрації (Сmах) у плазмі становить від 1 до 3 днів після введення дози препарату. Рівноважна концентрація препарату (AUCt/24) досягалася через 4-5 тижнів одноразового щотижневого застосування препарату. Після підшкірного введення семаглутиду в дозах 0,5 мг та 1 мг середні показники його рівноважної концентрації у пацієнтів із ЦД2 склали близько 16 нмоль/л та 30 нмоль/л відповідно. Експозиція для доз семаглутиду 0,5 мг та 1 мг збільшується пропорційно до введеної дози. При підшкірному введенні семаглутиду в передню черевну стінку, стегно або плече досягається подібна експозиція. Абсолютна біодоступність семаглутиду після підшкірного введення склала 89%. Розподіл Середній обсяг розподілу семаглутиду в тканинах після підшкірного введення пацієнтам з ЦД2 становив приблизно 12,5 л. Семаглутид значною мірою зв'язувався з альбуміном плазми (>99%). Метаболізм Семаглутид метаболізується за допомогою протеолітичного розщеплення пептидної основи білка та подальшого бета-окислення жирної кислоти бічного ланцюга. Виведення Шлунково-кишковий тракт (ЖКТ) та нирки є основними шляхами виведення семаглутиду та його метаболітів. 2/3 введеної дози семаглутиду виводиться нирками 1/3 - через кишечник. Приблизно 3% введеної дози виводиться нирками у вигляді незміненого семаглутиду. У пацієнтів із ЦД2 кліренс семаглутиду становив близько 0,05 л/год. З елімінаційним періодом напіввиведення приблизно 1 тиждень семаглутид буде присутній у загальному кровотоку протягом 5 тижнів після введення останньої дози препарату. Особливі групи пацієнтів Не потрібна корекція дози семаглутиду залежно від віку, статі, расової та етнічної приналежності, маси тіла, наявності ниркової або печінкової недостатності. Вік На підставі даних, отриманих в ході КІ 3а фази, що включали пацієнтів віком від 20 до 86 років, показано, що вік не впливав на фармакокінетику семаглутиду. Підлога Підлога не впливала на фармакокінетику семаглутиду. Раса Расова група (біла, чорна або афроамериканська, азіатська) не впливала на фармакокінетику семаглутиду. Етнічна приналежність Етнічна приналежність (латиноамериканська) не впливала на фармакокінетику семаглутиду. Маса тіла Маса тіла впливала на експозицію семаглутіду. Вища маса тіла призводить до нижчої експозиції. Дози семаглутиду рівні 0,5 і 1 мг забезпечують достатню експозицію препарату в діапазоні маси тіла від 40 до 198 кг. Ниркова недостатність Ниркова недостатність не справила клінічно значущого ефекту на фармакокінетику семаглутиду. Це було показано у пацієнтів з різним ступенем ниркової недостатності (легкої, середньої, тяжкої або у пацієнтів, які перебувають на діалізі) порівняно з пацієнтами з нормальною функцією нирок у дослідженні одноразової дози семаглутиду, що дорівнює 0,5 мг. Це також було показано на підставі даних КІ 3а фази для пацієнтів з ЦД2 та нирковою недостатністю, хоча досвід застосування у пацієнтів з термінальною стадією захворювання нирок був обмежений. Печінкова недостатність Печінкова недостатність не впливала на експозицію семаглутиду. Фармакокінетичні властивості семаглутиду оцінювалися під час дослідження! одноразової дози семаглутиду, що дорівнює 0,5 мг у пацієнтів з різним ступенем печінкової недостатності (легкої, середньої, тяжкої) порівняно з пацієнтами з нормальною функцією печінки. Діти та підлітки Досліджень семаглутиду у дітей та підлітків до 18 років не проводили.ФармакодинамікаСемаглутид є агоністом рецепторів ГПП-1 (ГПП-1Р), виробленим методом біотехнології рекомбінантної ДНК з використанням штаму Saccharomyces cerevisiae з подальшим очищенням. Семаглутид є аналогом ГПП-1, що має 94% гомологічності з людським ГПП-1. Семаглутид діє як агоніст ГПП-1Р, який селективно зв'язується та активує ГПП-1Р. ГПП-1Р є мішенню для нативного ГПП-1. ГПП-1 є фізіологічним гормоном, який надає відразу кілька ефектів на регуляцію концентрації глюкози та апетит, а також на серцево-судинну систему (ССС). Вплив на концентрацію глюкози та апетит специфічно опосередкований ГПП-1Р, розташованими в підшлунковій залозі та головному мозку. Фармакологічні концентрації семаглутиду знижують концентрацію глюкози крові та масу тіла за допомогою поєднання ефектів, описаних нижче. ГПП-1Р представлені також у специфічних областях серця, судин, імунної системи та нирок, де їх активація може надавати серцево-судинні (СС) та мікроциркуляторні ефекти. На відміну від нативного ГПП-1, продовжений період напіввиведення семаглутиду (близько 1 тижня) дозволяє застосовувати його підшкірно (п/к) 1 раз на тиждень. Зв'язування з альбуміном є основним механізмом тривалої дії семаглутиду, що призводить до зниження виведення його нирками та захищає від метаболічного розпаду. Крім того, семаглутид стабільний щодо розщеплення ферментом дипептидилпептидазой-4. Семаглутид знижує концентрацію глюкози крові за допомогою глюкозозалежної стимуляції секреції інсуліну та пригнічення секреції глюкагону. Таким чином, при підвищенні концентрації глюкози крові відбувається стимуляція секреції інсуліну та пригнічення секреції глюкагону. Механізм зниження рівня глікемії включає також невелику затримку випорожнення шлунка у ранній постпрандіальній фазі. Під час гіпоглікемії семаглутид зменшує секрецію інсуліну та не знижує секрецію глюкагону. Семаглутид знижує загальну масу тіла та масу жирової тканини, зменшуючи споживання енергії. Даний механізм зачіпає загальне зниження апетиту, включаючи посилення сигналів насичення та ослаблення сигналів голоду, а також покращення контролю споживання їжі та зниження тяги до їжі. Знижується також інсулінорезистентність, можливо, рахунок зменшення маси тіла. Крім цього, семаглутид знижує перевагу до їди з високим вмістом жирів. У дослідженнях на тваринах було показано, що семаглутид поглинається специфічними областями головного мозку та посилює ключові сигнали насичення та послаблює ключові сигнали голоду. Впливаючи на ізольовані ділянки тканин головного мозку, семаглутид активує нейрони, пов'язані з почуттям ситості, і пригнічує нейрони, пов'язані з почуттям голоду. У клінічних дослідженнях (КІ) семаглутид надавав позитивний вплив на ліпіди плазми, знижував систолічний артеріальний тиск (АТ) і зменшував запалення. У дослідженнях на тваринах семаглутид пригнічує розвиток атеросклерозу, попереджаючи подальший розвиток аортальних бляшок та зменшуючи запалення у бляшках. Фармакодинаміка Всі фармакодинамічні дослідження були проведені після 12 тижнів терапії (включаючи період збільшення дози) у рівноважній концентрації семаглутиду 1 мг 1 раз на тиждень. Рівень глікемії натще і постпрандіальний рівень глікемії Семаглутид знижує концентрацію глюкози натще і концентрацію постпрандіальної глюкози. У порівнянні з плацебо терапія семаглутидом 1 мг у пацієнтів з цукровим діабетом 2 типу (ЦД2) призвела до зниження концентрації глюкози з точки зору абсолютної зміни від вихідного значення (ммоль/л) та відносного зниження порівняно з плацебо (%) щодо: концентрації глюкози натще (1,6 ммоль/л; 22%); концентрації глюкози через 2 години після їди (4,1 ммоль/л; 37%); середньої добової концентрації глюкози (1,7 ммоль/л; 22%) та постпрандіальних піків концентрації глюкози за 3 прийоми їжі (0,6-1,1 ммоль/л). Семаглутид знижував концентрацію глюкози натще після введення першої дози. Функція бета-клітин підшлункової залози та секреція інсуліну Семаглутид покращує функцію бета-клітин підшлункової залози. Після внутрішньовенного струменевого введення глюкози пацієнтам з ЦД2 семаглутид у порівнянні з плацебо покращував першу та другу фазу інсулінової відповіді з трикратним та двократним підвищенням, відповідно, і збільшував максимальну секреторну активність бета-клітин підшлункової залози після тесту стимуляції аргін. Крім того, порівняно з плацебо-терапія семаглутидом збільшує концентрації інсуліну натще. Секреція глюкагону Семаглутид знижує концентрацію глюкагону натще і постпрандіальну концентрацію глюкагону. У пацієнтів із ЦД2 семаглутид призводить до відносного зниження концентрації глюкагону порівняно з плацебо: концентрації глюкагону натще (8-21%), постпрандіальної глюкагонової відповіді (14-15%) та середньої добової концентрації глюкагону (12%). Глюкозозалежна секреція інсуліну та глюкозозалежна секреція глюкагону Семаглутид знижував високу концентрацію глюкози в крові, стимулюючи секрецію інсуліну та знижуючи секрецію глюкагону глюкозозалежним способом. Швидкість секреції інсуліну після введення семаглутиду пацієнтам із ЦД2 була порівнянна з такою у здорових добровольців. Під час індукованої гіпоглікемії семаглутид у порівнянні з плацебо не змінював контррегуляторну відповідь підвищення концентрації глюкагону. а також не посилював зниження концентрації С-пептиду у пацієнтів із ЦД2. Випорожнення шлунка Семаглутид викликав невелику затримку раннього постпрандіального спорожнення шлунка, тим самим знижуючи швидкість надходження постпрандіати глюкози в кров. Маса тіла та склад тіла Спостерігалося більше зниження маси тіла при застосуванні семаглутиду порівняно з вивченими препаратами порівняння (плацебо, ситагліптином, ексенатидом уповільненого вивільнення (ЗВ), дулаглутидом та інсуліном гларгін) (див. розділ "Клінічна ефективність та безпека"). Втрата маси тіла при застосуванні семаглутиду відбувалася переважно рахунок втрати жирової тканини, що перевищує втрату м'язової маси в 3 разу. Апетит, споживання калорій та вибір продуктів харчування У порівнянні з плацебо, семаглутид знизив споживання калорій на 18-35% під час трьох послідовних прийомів їжі ad libitum. Цьому сприяли стимульовані семаглутидом придушення апетиту як натще, так і після прийому їжі, покращений контроль споживання їжі, ослаблення потягу до їжі, особливо з високим вмістом жирів. Ліпіди натще і постпрандіальні ліпіди У порівнянні з плацебо семаглутид знижував концентрації тригліцеридів та холестерину ліпопротеїнів дуже низької щільності (ЛПДНЩ) натще на 12% та 21%, відповідно. Постпрандіальне збільшення концентрації тригліцеридів та холестерину ЛПДНЩ у відповідь на прийом їжі з високим вмістом жирів знизилося більш ніж на 40%. Електрофізіологія серця (ЕФС) Дія семаглутиду на процес реполяризації у серці була протестована у дослідженні ЕФС. Застосування семаглутиду в дозах, що перевищують терапевтичні (у рівноважній концентрації до 1,5 мг), не призводило до подовження скоригованого інтервалу QT. Клінічна ефективність та безпека Як покращення глікемічного контролю, так і зниження СС захворюваності та смертності є невід'ємною частиною лікування ЦД2. Ефективність та безпека препарату Оземпік® у дозах 0,5 мг та 1 мг оцінювалися у шести рандомізованих контрольованих КІ 3а фази. З них п'ять КІ як основна мета оцінювали ефективність глікемічного контролю, в той час як одне КВ оцінювало в якості основної мети СС результат. На додаток було проведено два КІ препарату Оземпік® 3 фази за участю японських пацієнтів. Терапія препаратом Оземпік® продемонструвала стійкі, статистично переважаючі та клінічно значущі покращення показника HbA1c та зниження маси тіла на строк до 2 років порівняно з плацебо та лікуванням з активним контролем (ситагліптином, інсуліном гларгін, ексенатидом 3В та дулаглу). Вік, стать, раса, етнічна приналежність, вихідні значення індексу маси тіла (ІМТ) та маси тіла (кг), тривалість цукрового діабету (ЦД) та ниркова недостатність не вплинули на ефективність препарату Оземпік®. Монотерапія Монотерапія препаратом Оземпік® у дозах 0,5 мг та 1 мг 1 раз на тиждень протягом 30 тижнів порівняно з плацебо призвела до статистично більш значущого зниження показників HbA1c (-1,5%, -1,6% проти 0%, відповідно ), глюкози плазми натще (ГПН) (-2,5 ммоль/л, -2,3 ммоль/л проти -0,6 ммоль/л, відповідно) та маси тіла (-3,7 кг, -4,5 кг проти -1,0 кг відповідно). Препарат Оземпік® у порівнянні з ситагліптином, обидва в комбінації з 1-2 пероральними гіпоглікемічними препаратами (ПГГП) (метформіном та/або препаратами тіазолідиндіону) Терапія препаратом Оземпік® 0,5 мг та 1 мг 1 раз на тиждень протягом 56 тижнів порівняно з ситагліптином призвела до стійкого та статистично більшого зниження показників HbA1c (-1,3%, -1,6% проти -0,5 %, відповідно), ДПН (-2,1 ммоль/л, -2,6 ммоль/л проти -1,1 ммоль/л, відповідно) та маси тіла (-4,3 кг, -6,1 кг проти - 1,9 кг відповідно). Терапія препаратом Оземпік® 0,5 мг та 1 мг порівняно з ситагліптином значно знижувала систолічний АТ від вихідного значення 132,6 мм рт.ст. (-5,1 мм рт.ст., -5,6 мм рт.ст. проти -2,3 мм рт.ст. відповідно). Змін діастолічного артеріального тиску не відбувалося. Препарат Оземпік® у порівнянні з дулаглутидом, обидва у комбінації з метформіном Терапія препаратом Оземпік® 0,5 мг порівняно з дулаглутидом 0,75 мг, обидва 1 раз на тиждень протягом 40 тижнів, призвела до стійкого та статистично переважаючого зниження показників HbA1c (-1,5% проти -1,1%), ДПН (-2,2 ммоль/л проти -1,9 ммоль/л) та маси тіла (-4,6 кг проти -2,3 кг), відповідно. Терапія препаратом Оземпік® 1 мг у порівнянні з дулаглутидом 1,5 мг обидва 1 раз на тиждень протягом 40 тижнів, призвела до стійкого та статистично переважаючого зниження показників HbA1c (-l,8% проти -1,4%), ДПН (- 2,8 ммоль/л проти -2,2 ммоль/л) та маси тіла (-6,5 кг проти -3,0 кг), відповідно. Препарат Оземпік® в порівнянні з ексенатидом 3В, обидва в комбінації з метформіном або метформіном спільно з похідним сульфонілсечовини Терапія препаратом Оземпік® 1 мг 1 раз: на тиждень протягом 56 тижнів порівняно з ексенатидом 3В 2,0 мг призвела до стійкого та статистично більшого зниження показників HbA1c (-1,5% проти -0,9%), ДПН ( -2,8 ммоль/л проти -2,0 ммоль/л) та маси тіла (-5,6 кг проти -1,9 кг), відповідно. Препарат Оземпік® у порівнянні з інсуліном гларгін, обидва в комбінації з 1-2 ПГГП (монотерапія метформіном або метформін з похідним сульфонілсечовини) Терапія препаратом Оземпік у дозах 0,5 мг та 1 мг 1 раз на тиждень порівняно з інсуліном гларгін протягом 30 тижнів призвела до статистично більш значущого зниження показників HbA1c (-l,2%, -1,6% проти -0, 8%, відповідно) та маси тіла (-3,5 кг, -5,2 кг проти +1,2 кг, відповідно). Зниження показника ГНН було статистично більш значущим для препарату Оземпік 1 мг порівняно з інсуліном гларгін (-2,7 ммоль/л проти -2,1 ммоль/л). Не спостерігалося статистично більш значуще зниження показника ГНН для препарату Оземпік 0,5 мг (-2,0 ммоль/л проти -2,1 ммоль/л). Частка пацієнтів, у яких спостерігалися важкі чи підтверджені ( Більше пацієнтів досягли показника HbA1c Препарат Оземпік® у порівнянні з плацебо, обидва у комбінації з базальним інсуліном Терапія препаратом Оземпік у дозах 0,5 мг та 1 мг порівняно з плацебо протягом 30 тижнів призвела до статистично більш значущого зниження показників HbA1c (-1,4%, -1,8% проти -0,1%, відповідно) , ДПН (-1,6 ммоль/л, -2,4 ммоль/л проти -0,5 ммоль/л, відповідно) та маси тіла (-3,7 кг, -6,4 кг проти -1,4 кг відповідно). Частота важких або підтверджених епізодів гіпоглікемії істотно не відрізнялася при застосуванні препарату Оземпік і плацебо. Частка пацієнтів з показником HbA1c≤8% на скринінгу, що повідомили про важкі або підтверджені (8% на скринінгу). Комбінація з монотерапією похідним сульфонілсечовини На 30-му тижні КІ була проведена оцінка підгрупи з 123 пацієнтів, які перебувають на монотерапії похідним сульфонілсечовини. На 30-му тижні показник HbA1c знизився на 1,6% і на 1,5% при застосуванні препарату Оземпік у дозах 0,5 мг та 1 мг, відповідно, і збільшився на 0,1% при застосуванні плацебо. Комбінація із попередньо змішаним інсуліном ± 1-2 ПГГП На 30-му тижні КІ була проведена оцінка підгрупи з 867 пацієнтів, які перебувають на терапії попередньо змішаним інсуліном (у комбінації або без 2-х ПГГП). На 30-му тижні показник HbA1c знизився на 1,3% та на 1,8% при застосуванні препарату Оземпік у дозах 0,5 мг та 1 мг, відповідно, та знизився на 0,4% при застосуванні плацебо. Співвідношення пацієнтів, які досягли цільового зниження показника HbA1c До 79% пацієнтів досягли цілей лікування щодо зниження показника HbA1c Частка пацієнтів, які досягли показника HbA1c менше 7% без важких або підтверджених епізодів гіпоглікемії та без набору ваги, була значно більшою при застосуванні препарату Оземпік у дозах 0,5 мг та 1 мг (до 66% та 74%, відповідно) порівняно з пацієнтами, які отримували ситагліптин (27%), ексенатид 3В (29%), інсулін гларгін (16%), дулаглутид 0,75 мг (44%) та дулаглутид 1,5 мг (58%). Маса тіла Монотерапія препаратом Оземпік® 1 мг або терапія в комбінації з 1-2 лікарськими препаратами призводила до статистично більшого зниження маси тіла (втрата становила до 6,5 кг) порівняно з терапією плацебо, сітагліптином, ексенатидом 3В, інсуліном гларгін або дулаглу. Зниження маси тіла було стійким терміном до 2-х років. Після одного року терапії втрати маси ≥ 5% та ≥ 10% досягла більша кількість пацієнтів, які отримували препарат Оземпік® 0,5 мг (46% та 13%) та 1 мг (до 62% та 24%), порівняно з пацієнтами, активними препаратами, що перебували на терапії, порівняння ситагліптином і ексенатидом ЗВ (до 18% і до 4%). У КІ тривалістю 40 тижнів втрати маси ≥ 5% і ≥ 10% досягли більшої кількості пацієнтів, які отримували препарат Оземпік® 0,5 мг (44% і 14%), порівняно з пацієнтами, які отримували дулаглутид 0,75 мг (23% і 3%). Втрати маси ≥ 5% та ≥ 10% досягли більшої кількості пацієнтів, які отримували препарат Оземпік® 1 мг (до 63% та 27%), порівняно з пацієнтами, які отримували дулаглутид 1,5 мг (30% та 8%). У СС КІ втрати маси тіла ≥ 5% та ≥ 10% досягли більшої кількості пацієнтів, які отримували препарат Оземпік® 0,5 мг (36% та 13%) та 1 мг (47% та 20%), порівняно з пацієнтами, отримували плацебо 0,5 мг (18% та 6%) та 1 мг (19% та 7%). ДПН та постпрандіальне збільшення концентрації глюкози Під час усіх трьох щоденних прийомів їжі препарат Оземпік® 0,5 мг та 1 мг показав значне зниження концентрації ГНН до 2,8 ммоль/л та зниження постпрандіального приросту концентрації глюкози до 1,2 ммоль/л (різниця між значеннями до та після їжі). , отримана після трьох прийомів їжі). Функція бета-клітин підшлункової залози та інсулінорезистентність В ході терапії препаратом Оземпік® 0,5 мг та 1 мг відбулося покращення функції бета-клітин підшлункової залози та зменшення інсулінорезистентності, що підтверджується оцінкою гомеостатичних моделей функції бета-клітин підшлункової залози (НОМА-В) та інсулінорезистентності (HO). Ліпіди Під час КІ препарату Оземпік® спостерігалося покращення профілю ліпідів крові натще, переважно у групі, яка отримувала дозу 1 мг. Оцінка впливу на ССС 3297 пацієнтів з ЦД2 та високим СС ризиком були рандомізовані у подвійне сліпе КІ тривалістю 104 тижні на отримання препарату Оземпік® 0,5 мг або 1 мг 1 раз на тиждень або плацебо 0,5 мг або 1 мг на додаток до стандартної терапії СС захворювань у протягом наступних двох років. Терапія препаратом Оземпік привела до зниження на 26% ризику первинного комбінованого результату, що включає смерть через СС патології, інфаркт міокарда (ІМ) без смертельного результату та інсульт без смертельного результату. Насамперед це було зумовлено значним зменшенням частоти інсульту без смертельного результату (39%) та незначним зменшенням частоти ІМ без смертельного результату (26%), але без змін у частоті смерті через СС патології. Значно знизився ризик реваскуляризації міокарда або периферичних артерій, тоді як ризик нестабільної стенокардії, яка потребує госпіталізації, та ризик госпіталізації через серцеву недостатність знизилися незначно. Мікроциркуляторні результати включали 158 нових або погіршилися випадків нефропатії. Відносний ризик щодо часу до виникнення нефропатії (нові випадки розвитку персистуючої макроальбумінурії, персистуюче подвоєння сироваткової концентрації креатиніну, необхідність постійної замісної ниркової терапії та смерть через хворобу нирок) становив 0,64. На додаток до стандартної терапії СС захворювань, терапія препаралгом Оземпік® у дозах 0,5 мг та 1 мг порівняно з плацебо 0,5 мг та I мг протягом 104 тижнів призвела до значного та стійкого зниження від вихідних значень показника HbA1c (-1,1 % та -1,4% проти -0,4% та -0,4%, відповідно). Артеріальний тиск Спостерігалося значне зниження середнього систолічного АТ при застосуванні препарату Оземпік® 0,5 мг (3,5-5,1 мм рт.ст.) та Оземпік® 1 мг (5,4-7,3 мм рт.ст.) у комбінації з ПГГП чи базальним інсуліном. Не було значної різниці за показниками діастолічного АТ між препаратом Оземпік® та препаратами порівняння.Показання до застосуванняПрепарат Оземпік® показаний для застосування у дорослих пацієнтів з цукровим діабетом 2 типу на фоні дієти та фізичних вправ для покращення глікемічного контролю як: монотерапії; комбінованої терапії з іншими пероральними гіпоглікемічними препаратами (ПГГП) - метформіном, метформіном та похідним сульфонілсечовини, метформіном та/або тіазолідиндіоном, у пацієнтів, які не досягли адекватного глікемічного контролю при проведенні попередньої терапії; комбінованої терапії з інсуліном у пацієнтів, які не досягли адекватного глікемічного контролю на терапії препаратом Оземпік® та метформіном. Препарат Оземпік® показаний для зниження ризику розвитку великих серцево-судинних подій* у пацієнтів з цукровим діабетом 2 типу та високим серцево-судинним ризиком як доповнення до стандартного лікування серцево-судинних захворювань (на підставі аналізу часу настання першої великої серцево-судинної події) . *великі серцево-судинні події включають: смерть через серцево-судинну патологію, інфаркт міокарда без смертельного результату, інсульт без смертельного результату.Протипоказання до застосуванняГіперчутливість до семаглутиду або будь-якої з допоміжних речовин препарату; медулярний рак щитовидної залози в анамнезі, у тому числі у сімейному; множинна ендокринна неоплазія (МЕН) 2 типи; цукровий діабет 1 типу (ЦД1); діабетичний кетоацидоз. Протипоказано застосування препарату Оземпік® у наступних груп пацієнтів та при наступних станах/захворюваннях у зв'язку з відсутністю даних щодо ефективності та безпеки та обмеженим досвідом застосування: вагітність та період грудного вигодовування; вік до 18 років; печінкова недостатність важкого ступеня; термінальна стадія ниркової недостатності (кліренс креатиніну (КК)) хронічна серцева недостатність (ХСН) IV функціонального класу (відповідно до класифікації NYHA (Нью-Йоркська кардіологічна асоціація)). З обережністю: Препарат Оземпік® рекомендується застосовувати з обережністю у пацієнтів із нирковою недостатністю та у пацієнтів з наявністю панкреатиту в анамнезі.Вагітність та лактаціяВагітність Дослідження на тваринах продемонстрували репродуктивну токсичність препарату. Дані щодо застосування семаглутиду у вагітних жінок обмежені. Протипоказано застосовувати семаглутид під час вагітності. Жінкам із збереженим репродуктивним потенціалом рекомендується використовувати контрацепцію під час терапії семаглутидом. Якщо пацієнтка готується до вагітності або вагітність вже настала, терапію семаглутидом необхідно припинити. Через тривалий період напіввиведення терапію семаглутидом необхідно припинити щонайменше за 2 місяці до запланованого настання вагітності. Період грудного вигодовування У лактуючих щурів семаглутид проникав у молоко. Не можна виключити ризик для дитини, яка перебуває на грудному вигодовуванні. Протипоказано застосовувати семаглутид у період грудного вигодовування.Побічна діяНайчастіше реєстрованими небажаними реакціями (HP) під час КІ були порушення з боку шлунково-кишкового тракту, включаючи нудоту, діарею та блювання. В цілому, дані реакції були легким або середнім ступенем тяжкості і короткостроковими. HP розподілені за системно-органними класами відповідно до MedDRA із зазначенням частоти їх виникнення згідно з рекомендаціями ВООЗ: дуже часто (≥ 1/10); часто (≥ 1/100 до < 1/10); нечасто (≥ 1/1000 до < 1/100); рідко (≥ 1/10 000 до < 1/1000) та дуже рідко (< 1/10 000). У кожній групі частоти розвитку HP представлені зниження рівня серйозності. Таблиця 1 HP, виявлені при проведенні КІ 3 фази Система органів MedDRA Дуже часто Часто Не часто Рідко Порушення з боку імунної системи Анафілактичні реакції Порушення з боку обміну речовин та харчування Гіпоглікемія при спільному застосуванні з інсуліном або похідним сульфонілсечовини Гіпоглікемія при спільному застосуванні з іншими ПГГП; Зниження апетиту Порушення з боку нервової системи Запаморочення Дисгевзія Порушення з боку органу зору Ускладнення діабетичної ретинопатії Порушення з боку серця Збільшення частоти серцевих скорочень (ЧСС) Порушення з боку шлунково-кишкового тракту Нудота; Діарея Блювота; Біль в животі; Здуття живота; Запор; Диспепсія; Гастрит; Гастроезофагеальна рефлюксна хвороба; Відрижка; Метеоризм Порушення з боку печінки та жовчовивідних шляхів Холелітіаз Загальні розлади та порушення у місці введення Стомлюваність Реакції у місці введення Лабораторні та інструментальні дані Підвищення активності ліпази; Підвищення активності амілази; Зниження маси тіла aГіпоглікемія, визначена як важка (що вимагає допомоги іншої людини) або симптоматична у поєднанні з концентрацією глюкози у плазмі крові Ускладнення діабетичної ретинопатії - це поєднання з необхідності в фотокоагуляції сітківки ока, необхідності в інтравітреальному введенні препаратів, крововиливу в склоподібне тіло, розвитку сліпоти, пов'язаної з ЦД. Частота заснована на дослідженні результатів СС. 2-річне дослідження СС результатів та безпеки У популяції пацієнтів з високим ризиком розвитку СС захворювань профіль HP був аналогічним такому в інших КІ 3а фази. Опис окремих HP Гіпоглікемія Під час монотерапії препаратом Оземпік не спостерігалося епізодів важкої гіпоглікемії. Гіпоглікемія тяжкого ступеня, в основному, спостерігалася при застосуванні препарату Оземпік у комбінації з похідним сульфонілсечовини або інсуліном. Спостерігалося кілька епізодів тяжкої гіпоглікемії при застосуванні препарату Оземпік у комбінації з іншими, за винятком похідної сульфонілсечовини, ПГГП. HP з боку ШКТ Під час терапії препаратом Оземпік у дозах 0,5 мг та 1 мг у пацієнтів відзначалася нудота, діарея та блювання. Більшість реакцій були від легкого до середнього ступеня важкості та короткостроковими. HP стали причиною передчасного вибуття з КІ 3,9% та 5,9% пацієнтів відповідно. Найчастіше про HP повідомлялося у перші місяці терапії. Ускладнення діабетичної ретинопатії У 2-річному КІ, в якому брали участь пацієнти з ЦД2 та високим СС ризиком, тривалим перебігом ЦД та неадекватним контролем глікемії, підтверджені випадки ускладнень діабетичної ретинопатії розвивалися у більшої кількості пацієнтів, які отримували препарат Оземпік® (3,0%), порівняно з пацієнтами, які отримували плацебо (1,8%). У пацієнтів з анамнезом діабетичної ретинопатії на початку КІ зростання абсолютного ризику розвитку ускладнень було вищим. У пацієнтів з відсутністю підтвердженого анамнезу діабетичної ретинопатії кількість подій була однакова при застосуванні препарату Оземпік® та гошцебо. У КІ тривалістю до І року частота HP, пов'язаних з діабетичною ретинопатією, була однаковою у групі препарату Оземпік® та препаратів порівняння. Припинення лікування через HP Частота припинення лікування через HP склала 8,7% для пацієнтів, які отримували препарат Оземпік® 1 мг. Найбільш частими HP, що призводили до припинення лікування, були порушення з боку шлунково-кишкового тракту. Реакції у місці введення Повідомлялося про реакції в місці введення (таких як висип у місці введення, почервоніння) у 0,6% і 0,5% пацієнтів, які отримували семаглутид 0,5 мг і 1 мг, відповідно. Ці реакції мали, зазвичай, легкий характер. Імуногенність Внаслідок потенційних імуногенних властивостей білкових та пептидних лікарських препаратів у пацієнтів можуть з'явитися антитіла до семаглутиду після терапії препаратом Оземпік®. В кінці КІ частка пацієнтів, у яких були виявлені антитіла до семаглутиду в будь-який момент часу, була низькою (1-2%) і в жодного пацієнта не було виявлено нейтралізуючих антитіл до семаглутиду або антитіл з нейтралізуючим ендогенним ГПП-1 ефектом.Спосіб застосування та дозиПрепарат Оземпік® застосовують 1 раз на тиждень у будь-який час, незалежно від їди. Препарат Оземпік® вводять підшкірно в живіт, стегно або плече. Місце ін'єкції може змінюватись без корекції дози. Препарат Оземпік® не можна вводити внутрішньовенно та внутрішньом'язово. Подальша інформація щодо способу застосування міститься в інструкції-вкладиші. При необхідності день щотижневого введення можна змінювати за умови, що інтервал часу між двома ін'єкціями становить не менше 3-х днів (72 годин). Дози Початкова доза препарату Оземпік становить 0,25 мг 1 раз на тиждень. Після 4 тижнів застосування дозу слід збільшити до 0,5 мг 1 раз на тиждень. Для подальшого поліпшення глікемічного контролю після мінімуму 4 тижнів застосування препарату в дозі 0,5 мг 1 раз на тиждень, дозу можна збільшити до 1 мг 1 раз на тиждень. Доза препарату Оземпік 0,25 мг не є терапевтичною. Препарат Оземпік може застосовуватися у вигляді монотерапії або в комбінації з одним або більше гіпоглікемічними препаратами. При додаванні препарату Оземпік до попередньої терапії метформіном та/або тіазолідиндіоном терапію метформіном та/або тіазолідиндіоном можна продовжити в колишніх дозах. При додаванні препарату Оземпік® до терапії похідним сульфонілсечовини або інсуліном слід передбачити зниження дози похідного сульфонілсечовини або інсуліну з метою зниження ризику виникнення гіпоглікемій. Застосування препарату Оземпік не вимагає проведення самоконтролю концентрації глюкози крові. При застосуванні препарату Оземпік у комбінації з похідним сульфонілсечовини або інсуліном, такий самоконтроль концентрації глюкози крові може знадобитися для корекції дози похідного сульфонілсечовини або інсуліну. Пропущена доза У разі пропуску дози препарат Оземпік® слід ввести якнайшвидше протягом 5 днів з моменту запланованого введення дози. Якщо тривалість пропуску становить понад 5 днів, пропущену дозу не слід вводити. Наступну дозу препарату Оземпік слід ввести у звичайний запланований день. У кожному разі, пацієнти можуть відновити їх звичайний одноразовий щотижневий графік введення. Застосування препарату в спеціальних клінічних групах пацієнтів Пацієнти похилого віку (≥65 років) Не потрібна корекція дози залежно від віку. Досвід застосування семаглутиду у пацієнтів віком 75 років та старший обмежений. Пацієнти з печінковою недостатністю Не потрібна корекція дози у пацієнтів з печінковою недостатністю. Досвід застосування семаглутиду у пацієнтів, з печінковою недостатністю тяжкого ступеня обмежений; застосування препарату Оземпік у таких пацієнтів протипоказане. Пацієнти з нирковою недостатністю Не потрібна корекція дози у пацієнтів з нирковою недостатністю. Досвід застосування препарату у пацієнтів із термінальною стадією ниркової недостатності відсутній; застосування препарату Оземпік у таких пацієнтів протипоказане. Діти та підлітки Застосування препарату Оземпік® у дітей та підлітків віком до 18 років протипоказане через відсутність даних щодо безпеки та ефективності. Дослідження семаглутиду in vitro показали дуже невелику можливість інгібування або індукції ферментів системи цитохрому Р450 (CYP) та інгібування транспортерів лікарських препаратів. Затримка спорожнення шлунка при застосуванні семаглутиду може впливати на всмоктування супутніх пероральних лікарських засобів. Семаглутид слід застосовувати з обережністю у пацієнтів, які отримують пероральні лікарські препарати, для яких необхідна швидка абсорбція шлунково-кишкового тракту. Парацетамол Оцінюючи фармакокінетики парацетамолу під час тесту стандартизованого прийому їжі було виявлено, що семаглутид затримує спорожнення шлунка. При одночасному застосуванні семаглутиду в дозі 1 мг AUC0-60 хв та Сmах парацетамолу знизилися на 27% та 23% відповідно. Загальна експозиція парацетамолу (AUC0-5год) не змінювалася. При одночасному прийомі семаглутиду та парацетамолу корекція дози останнього не потрібна. Пероральні гормональні контрацептивні засоби Не передбачається, що семаглутид знижує ефективність пероральних гормональних контрацептивних засобів. При одночасному застосуванні комбінованого перорального гормонального контрацептивного препарату (0,03 мг етинілестрадіолу/0,15 мг левоноргестрелу) та семаглутиду останній не впливав на клінічно значущий вплив на загальну експозицію етинілестрадіолу та левоноргестрелу. Експозиція етинілестрадіолу не була порушена; спостерігалося збільшення на 20% експозиції левоноргестрелу у рівноважному стані. Сахах не змінилася для жодного з компонентів. Аторвастатин Семаглутид не змінював системну експозицію аторвастатину після застосування одноразової дози аторвастатину (40 мг). Стих аторвастатину знизився на 38%. Ця зміна була розцінена як клінічно незначна. Дігоксин Семаглутид не змінював системну експозицію або Сmах дигоксину після застосування одноразової дози дигоксину (0,5 мг). Метформін Семаглутид не змінював системну експозицію або Сmах метформіну після застосування метформіну в дозі 500 мг 2 рази на день протягом 3,5 днів. Варфарін Семаглутид не змінював системну експозицію або Сmах R- та S-ізомерів варфарину після застосування одноразової дози варфарину (25 мг). На підставі визначення міжнародного нормалізованого відношення (МНО) клінічно значущих змін фармакодинамічних ефектів варфарину також не спостерігалося. Несумісність Речовини, додані до препарату Оземпік®, можуть спричинити деградацію семаглутиду. Препарат Оземпік® не можна змішувати з іншими лікарськими засобами, зокрема з інфузійними розчинами.ПередозуванняУ ході КІ повідомлялося про передозування до 4 мг в одноразовій дозі та до 4 мг на тиждень. Найчастішою HP, про яку повідомлялося, була нудота. Усі пацієнти одужали без ускладнень. Специфічного антидоту при передозуванні препарату Оземпік не існує. У разі передозування рекомендується проведення відповідної симптоматичної терапії. Враховуючи тривалий період виведення препарату (приблизно 1 тиждень), може знадобитися тривалий період спостереження та лікування симптомів передозування.Запобіжні заходи та особливі вказівкиЗастосування препарату Оземпік протипоказано у пацієнтів з ЦД1 або для лікування діабетичного кетоацидозу. Препарат Оземпік не замінює інсулін. Реакції з боку шлунково-кишкового тракту Застосування агоністів ГПП-1Р може бути асоційоване з HP з боку шлунково-кишкового тракту. Це слід враховувати при лікуванні пацієнтів з нирковою недостатністю, оскільки нудота, блювання та діарея можуть призвести до дегідратації та погіршення функції нирок. Гострий панкреатит При застосуванні агоністів ГПП-1Р спостерігалися випадки розвитку гострого панкреатиту. Пацієнти повинні бути поінформовані про характерні симптоми гострого панкреатиту. При підозрі на панкреатит терапія препаратом Оземпік повинна бути припинена; у разі підтвердження гострого панкреатиту терапію препаратом Оземпік® відновлювати не слід. Слід бути обережними у пацієнтів з панкреатитом в анамнезі. За відсутності інших ознак та симптомів гострого панкреатиту підвищення активності ферментів підшлункової залози не є прогностичним фактором розвитку гострого панкреатиту. Гіпоглікемія Пацієнти, які отримують препарат Оземпік у комбінації з похідним сульфонілсечовини або інсуліном, можуть мати підвищений ризик розвитку гіпоглікемії. На початку лікування препаратом Оземпік® ризик розвитку гіпоглікемії можна знизити, зменшивши дозу похідного сульфонілсечовини або інсуліну. Діабетична ретинопатія Спостерігалося підвищення ризику ускладнень діабетичної ретинопатії у пацієнтів з наявністю діабетичної ретинопатії, які отримують терапію інсуліном та семаглутидом (див. розділ "Побічна дія"). Слід бути обережними при застосуванні семаглутиду у пацієнтів з діабетичною ретинопатією, які отримують інсулінотерапію. Такі пацієнти повинні перебувати під постійним наглядом та отримувати лікування відповідно до клінічних рекомендацій. Швидке покращення глікемічного контролю було асоційоване з тимчасовим погіршенням стану діабетичної ретинопатії, проте не можна виключати й інші причини. Серцева недостатність Відсутній досвід застосування препарату Оземпік у пацієнтів з ХСН IV функціонального класу відповідно до класифікації NYHA. Застосування препарату у пацієнтів протипоказане. Захворювання щитовидної залози У післяреєстраційному періоді застосування іншого аналога ГПП-1, ліраглутиду, були відмічені випадки медулярного раку щитовидної залози (МРЩЗ). Наявних даних недостатньо для встановлення або виключення причинно-наслідкового зв'язку виникнення МРЩЗ із застосуванням аналогів ГПП-1. Необхідно проінформувати пацієнта про ризик МРЩЗ та про симптоми пухлини щитовидної залози (появи ущільнення в області шиї, дисфагії, задишки, непрохідної захриплості голосу). Значне підвищення концентрації кальцитоніну в плазмі може вказувати на МРЖЩ (у пацієнтів з МРЖЩ значення концентрації кальцитоніну в плазмі крові зазвичай >50 нг/л). При виявленні підвищення концентрації кальцитону в плазмі слід провести подальше обстеження пацієнта. Пацієнти з вузлами у щитовидній залозі,виявленими при медичному огляді або при проведенні УЗД щитовидної залози також повинні бути додатково обстежені. Застосування семаглутиду у пацієнтів із особистим або сімейним анамнезом МРЩЗ або з синдромом МЕН типу 2 протипоказане. Доклінічні дані щодо безпеки Доклінічні дані, засновані на дослідженнях фармакологічної безпеки, токсичності повторних доз та генотоксичності, не виявили жодної небезпеки для людини. У 2-річних дослідженнях канцерогенності у щурів та мишей при клінічно значущих концентраціях семаглутид спричинив розвиток пухлин С-клітин щитовидної залози без смертельного результату. Пухлини С-клітин щитовидної залози без смертельного результату, які спостерігаються у щурів, характерні для групи аналогів ГПП-1. Вважається, що щодо людей цей ризик є низьким, але може бути повністю виключений. Фертильність Дія семаглутиду на фертильність у людей невідома. Семаглутід не впливав на фертильність самців щурів. Серед самок щурів збільшення естрального циклу та незначне зниження кількості овуляцій спостерігалося при дозах, що супроводжувалися зниженням маси тіла самки. Посібник із використання Попередньо заповнена шприц-ручка Оземпік® поставляється у двох видах: Оземпік® 0.25 мг/доза або 0,5 мг/доза розчин для підшкірного введення у попередньо заповненій шприц-ручці дозволяє вводити дози 0,25 мг або 0,5 мг. Дана шприц-ручка призначена для підвищення дози та підтримання терапевтичної дози 0,5 мг. Одна шприц-ручка містить 15 мл розчину. Оземпік® 1 мг/доза розчин для підшкірного введення у попередньо заповненій шприц-ручці дозволяє вводити дози лише 1 мг. Дана шприц-ручка призначена лише для підтримки терапевтичної дози 1 мг. Одна шприц-ручка містить 3 мл розчину. В упаковку препарату Оземпік включені голки НовоФайн Плюс. Пацієнту слід рекомендувати викидати ін'єкційну голку після кожної ін'єкції відповідно до місцевих вимог. Шприц-ручка Оземпік призначена тільки для індивідуального використання. Препарат Оземпік® не можна застосовувати, якщо він виглядає інакше, ніж прозорий безбарвний або майже безбарвний розчин. Препарат Оземпік® не можна застосовувати, якщо він був заморожений. Препарат Оземпік можна вводити за допомогою голок довжиною до 8 мм. Шприц-ручка призначена для використання із одноразовими ін'єкційними голками НовоФайн®. Завжди після кожної ін'єкції видаляйте голку та зберігайте шприц-ручку Оземпік з від'єднаною голкою. Це допоможе запобігти закупорці голок, забруднення, зараження, витікання розчину та введення неправильної дози препарату. Інструкція для пацієнтів із застосування препарату Оземпік® 0,25 мг/доза або 0,5 мг/доза розчин для підшкірного введення у попередньо заповненій шприц-ручці Уважно прочитайте цю інструкцію перед застосуванням попередньо заповненої шприц-ручки Оземпік®. Використовуйте шприц-ручку лише після того, як Ви навчитеся нею користуватися під керівництвом лікаря або медсестри. Почніть з перевірки шприц-ручки, щоб переконатися, що міститься препарат Оземпік® 0,25 мг/доза або 0,5 мг/доза, потім подивіться на подані нижче ілюстрації, щоб ознайомитися з різними частинами шприц-ручки та голки. Якщо Ви слабозорі або у Вас є серйозні проблеми із зором, і Ви не можете розрізнити цифри на лічильнику дози, не використовуйте шприц-ручку без сторонньої допомоги. Допомогти вам може людина з добрим зором, навчена використанню попередньо заповненої шприц-ручки з препаратом Оземпік®. Ця шприц-ручка є попередньо заповненою шприц-ручкою. Вона містить 2 мг семаглутиду та дозволяє вибрати дози 0,25 мг або 0,5 мг. Шприц-ручка розроблена для використання з одноразовими голками НовоФайн довжиною до 8 мм. Голки НовоФайн Плюс включені в упаковку. Важлива інформація Зверніть особливу увагу на інформацію, зазначену такими значками, це дуже важливо для безпечного використання шприц-ручки. 1. Підготовка шприц-ручки з новою голкою для використання Перевірте назву та колірний код на етикетці шприц-ручки, щоб переконатися, що вона містить препарат Оземпік® 0,25 мг/доза або 0,5 мг/доза. Це особливо важливо, якщо Ви використовуєте більше одного ін'єкційного препарату. Зніміть ковпачок із шприц-ручки. Переконайтеся, що розчин у шприц-ручці є прозорим і безбарвним. Подивіться у віконце шприц-ручки. Якщо розчин каламутний і безбарвний, не використовуйте шприц ручку. Візьміть нову голку та видаліть захисну наклейку. Якщо захисна наклейка пошкоджена, не використовуйте голку, оскільки стерильність у цьому випадку не гарантується. Надягніть голку на шприц-ручку і поверніть її, щоб голка щільно трималася на шприц-ручці. Зніміть зовнішній ковпачок голки, але не викидайте його. Він знадобиться після завершення ін'єкції, щоб безпечно зняти голку зі шприц-ручки. Зніміть та викиньте внутрішній ковпачок голки. Якщо Ви спробуєте надіти внутрішній ковпачок назад на голку, Ви можете випадково вколотись голкою. На кінці голки може виникнути крапля розчину. Це нормальне явище, однак, Ви все одно повинні перевірити надходження препарату, якщо Ви використовуєте нову шприц-ручку вперше. Не приєднуйте нову голку доти, доки Ви не будете готові зробити ін'єкцію. Завжди використовуйте нову голку для кожної ін'єкції. Це може запобігти закупорці голок, забруднення, інфікування та введення неправильної дози препарату. Ніколи не використовуйте голку, якщо вона погнута чи пошкоджена. 2. Перевірка надходження препарату Перед першою ін'єкцією за допомогою кожної нової шприц-ручки перевірте надходження препарату. Якщо шприц-ручка вже є у використанні, перейдіть до операції 3 "Встановлення дози". Повертайте селектор дози, доки лічильник дози не порівняється із символом перевірки надходження препарату. Тримайте шприц-ручку голкою вгору. Натисніть пускову кнопку і утримуйте її в цьому положенні, доки лічильник дози не повернеться до "0". "0" повинен стояти навпроти вказівника дози. На кінці голки має з'явитися крапля розчину. На кінці голки може залишатися невелика крапля, але вона не буде введена при ін'єкції. Якщо крапля розчину на кінці голки не з'явилася, повторіть операцію "2" "Перевірка надходження препарату", але не більше 6 разів. Якщо крапля розчину так і не з'явилася, поміняйте голку та повторіть операцію "2" "Перевірка надходження препарату" ще раз. Якщо крапля розчину так і не з'явилася, утилізуйте шприц-ручку та використовуйте нову. Завжди перед використанням нової шприц-ручки вперше переконайтеся, що на кінці голки з'явилася крапля розчину. Це гарантує надходження препарату. Якщо крапля розчину не з'явилася, препарат не буде введений, навіть якщо лічильник дози рухатиметься. Це може вказувати на те, що голка закупорена або пошкоджена. Якщо Ви не перевірите надходження препарату перед першою ін'єкцією за допомогою кожної нової шприц-ручки, Ви можете не ввести необхідну дозу та очікуваного ефекту препарату Оземпік® не буде досягнуто. 3. Встановлення дози Повертайте селектор дози доти, доки він не покаже необхідну Вам дозу (0,25 мг або 0,5 мг). Якщо доза була вибрана неправильно, Ви можете повертати селектор дози вперед або назад, доки не буде встановлена правильна доза. Максимальна доза, яку можна встановити становить 0,5 мг. Селектор дози змінює дозу. Тільки лічильник дози та покажчик дози покажуть кількість мг препарату у вибраній Вами дозі. Ви можете вибрати до 0,5 мг препарату на дозу. Якщо шприц-ручка містить менше 0,5 мг, лічильник дози зупиниться перш, ніж з'явиться "0,5". При кожному повороті селектора дози лунають клацання, звук клацань залежить від того, в яку сторону обертається селектор дози: вперед, назад або якщо набрана доза перевищує кількість мг препарату, що залишилися в шприц-ручці. Не рахуйте клацання шприц-ручки. Завжди перед кожною ін'єкцією перевіряйте скільки мг препарату Ви набрали але лічильнику дози та вказівнику дози. Не рахуйте клацання шприц-ручки. За допомогою селектора дози слід вибирати лише дози 0,25 мг або 0,5 мг. Вибрана доза повинна бути точно напроти вказівника дози - таке положення гарантує, що Ви отримаєте правильну дозу препарату. Скільки препарату залишилось Щоб визначити, скільки препарату залишилося, використовуйте лічильник дози: Повертайте селектор дози до зупинки лічильника. Якщо він показує "0,5", у шприц-ручці залишилося щонайменше 0,5 мг препарату. Якщо лічильник дози зупинився до того, як з'явилося "0,5", це означає, що в шприц-ручці залишилася недостатня кількість препарату, щоб ввести повну дозу 0,5 мг. Якщо в шприц-ручці залишилася недостатня кількість препарату для введення повної дози, не використовуйте шприц-ручку. Використовуйте нову шприц-ручку Оземпік®. 4. Введення препарату Введіть голку під шкіру, використовуючи техніку ін'єкцій, рекомендовану лікарем або медсестрою. Переконайтеся, що лічильник дози знаходиться у полі вашого зору. Не торкайтеся лічильника дози пальцями - це може перервати ін'єкцію. Натисніть пускову кнопку до упору та утримуйте її в цьому положенні, доки лічильник дози не покаже "0". "0" повинен знаходитися напроти вказівника дози. При цьому Ви можете почути чи відчути клацання. Утримуйте голку під шкірою після того, як лічильник дози повернувся до "0" і повільно рахуйте до 6. Якщо ви витягнете голку з-під шкіри раніше, ви можете побачити, як препарат випливає з голки. У цьому випадку буде введено неповну дозу препарату. Вийміть голку з-під шкіри. Якщо в місці ін'єкції з'явилася кров, притисніть до місця уколу ватний тампон. Не масажуйте місце уколу. Після завершення ін'єкції можна побачити краплю розчину на кінці голки. Це нормально і не впливає на дозу, яку Ви ввели. Завжди звіряйтеся зі показаннями лічильника дози, щоб знати, яку кількість мг препарату ви ввели. Утримуйте пускову кнопку, доки лічильник дози не покаже "0". Як виявити закупорку або пошкодження голки Якщо після тривалого натискання на пускову кнопку на лічильнику дози не з'являється "0", це може означати закупорку або пошкодження голки. У цьому випадку Ви не отримали препарат, навіть якщо лічильник дози змінив положення вихідної дози, яку Ви встановили. Що робити із закупореною голкою Замініть голку як описано в операції 5 "Після завершення ін'єкції" і повторіть всі кроки, починаючи з операції 1 "Підготовка шприц-ручки з новою голкою до використання". Переконайтеся, що встановили необхідну Вам дозу. Ніколи не торкайтеся лічильника дози під час введення препарату. Це може перервати ін'єкцію. 5. Після завершення ін'єкції Поклавши зовнішній ковпачок голки на плоску поверхню, введіть кінець голки всередину ковпачка, не торкаючись його голки. Коли голка увійде в ковпачок, обережно надягніть зовнішній ковпачок на голку. Відкрутіть голку і викиньте її, дотримуючись запобіжних заходів. Після кожного використання надягайте на шприц-ручку ковпачок, щоб захистити розчин, що міститься в ній, від впливу світла. Завжди після кожної ін'єкції викидайте голку, щоб забезпечити комфортну ін'єкцію та уникнути закупорки голок. Якщо голка закупорена, Ви не введете препарат. Викидайте порожню шприц-ручку з від'єднаною голкою відповідно до рекомендацій лікаря, медсестра, фармацевта або місцевих вимог. Ніколи не намагайтеся надіти внутрішній ковпачок назад на голку. Ви можете вколотись. Після кожної ін'єкції завжди одразу видаляйте голку зі шприц-ручки. Це може запобігти закупорці голок, забруднення, інфікування, витікання розчину та введення неправильної дози препарату. Додаткова важлива інформація Завжди зберігайте шприц-ручку та голки до неї в недоступному для всіх, особливо для дітей, місці. Ніколи не передавайте свою шприц-ручку та голки до неї іншим особам. Особи, що здійснюють догляд за хворим, повинні звертатися з використаними голками з особливою обережністю, щоб запобігти уколам голки та перехресному інфікуванню. Догляд за шприц-ручкою Акуратно поводьтеся зі шприц-ручкою. Недбале поводження або неправильне використання можуть призвести до введення неправильної дози препарату, наслідком чого можуть стати висока концентрація глюкози крові або дискомфорт у ділянці живота (нудота або блювання). Не залишайте шприц-ручку в автомобілі або іншому місці, де вона може піддаватися впливу занадто високих або занадто низьких температур. Не застосовуйте препарат Оземпік, якщо він був заморожений. У цьому випадку концентрація глюкози крові може стати занадто високою або Ви можете відчути дискомфорт у ділянці живота, такий, як нудота або блювота. Не застосовуйте препарат Оземпік®, якщо він зазнав прямих сонячних променів. У цьому випадку концентрація глюкози може стати занадто високою. Захищайте шприц-ручку від попадання на неї пилу, забруднень та рідини. Не мийте шприц-ручку, не занурюйте її в рідину і не змащуйте її. При необхідності шприц-ручку можна очищати вологою тканиною, змоченою м'яким миючим засобом. Не можна кидати або вдаряти шприц-ручку об тверду поверхню. Якщо Ви впустили шприц-ручку або сумніваєтеся у її справності, приєднайте нову голку та перевірте надходження препарату перед тим, як зробити ін'єкцію. Не намагайтеся повторно заповнити шприц-ручку. Порожню шприц-ручку слід викинути. Не намагайтеся самостійно полагодити шприц-ручку або розібрати її на частини. Інструкція для пацієнтів із застосування препарату Оземпік® 1 мг/доза розчин для підшкірного введення у попередньо заповненій шприц-ручці Уважно прочитайте цю інструкцію перед застосуванням попередньо заповненої шприц-ручки Оземпік®. Використовуйте шприц-ручку лише після того, як Ви навчитеся нею користуватися під керівництвом лікаря або медсестри. Почніть з перевірки шприц-ручки, щоб переконатися, що міститься препарат Оземпік® 1 мг/доза, потім подивіться на подані нижче ілюстрації, щоб ознайомитися з різними частинами шприц-ручки та голки. Якщо Ви слабозорі або у Вас є серйозні проблеми із зором, і Ви не можете розрізнити цифри на лічильнику дози, не використовуйте шприц-ручку без сторонньої допомоги. Допомогти вам може людина з добрим зором, навчена використанню попередньо заповненої шприц-ручки з препаратом Оземпік®. Ця шприц-ручка є попередньо заповненою шприц-ручкою. Вона містить 4 мг семаглутиду і дозволяє вибрати лише дозу 1 мг. Шприц-ручка розроблена для використання з одноразовими голками НовоФайн довжиною до 8 мм. Голки НовоФайн Плюс включені в упаковку. Важлива інформація Зверніть особливу увагу на інформацію, зазначену такими значками, це дуже важливо для безпечного використання шприц-ручки. 1. Підготовка шприц-ручки з новою голкою для використання Перевірте назву та колірний код на етикетці шприц-ручки, щоб переконатися, що міститься препарат Оземпік® 1 мг/доза. Це особливо важливо, якщо Ви використовуєте більше одного ін'єкційного препарату. Зніміть ковпачок із шприц-ручки. Переконайтеся, що розчин у шприц-ручці є прозорим і безбарвним. Подивіться у віконце шприц-ручки. Якщо розчин каламутний і безбарвний, не використовуйте шприц ручку. Візьміть нову голку та видаліть захисну наклейку. Якщо захисна наклейка пошкоджена, не використовуйте голку, оскільки стерильність у цьому випадку не гарантується. Надягніть голку на шприц-ручку і поверніть її, щоб голка щільно трималася на шприц-ручці. Зніміть зовнішній ковпачок голки, але не викидайте його. Він знадобиться після завершення ін'єкції, щоб безпечно зняти голку зі шприц-ручки. Зніміть та викиньте внутрішній ковпачок голки. Якщо Ви спробуєте надіти внутрішній ковпачок назад на голку, Ви можете випадково вколотись голкою. На кінці голки може виникнути крапля розчину. Це нормальне явище, однак Ви все одно повинні перевірити надходження препарату, якщо Ви використовуєте нову шприц-ручку вперше. Не приєднуйте нову голку доти, доки Ви не будете готові зробити ін'єкцію. Завжди використовуйте нову голку для кожної ін'єкції. Це може запобігти закупорці голок, забруднення, інфікування та введення неправильної дози препарату. Ніколи не використовуйте голку, якщо вона погнута чи пошкоджена. 2. Перевірка надходження препарату Перед першою ін'єкцією за допомогою кожної нової шприц-ручки перевірте надходження препарату. Якщо шприц-ручка вже є у використанні, перейдіть до операції 3 "Встановлення дози". - Повертайте селектор дози, доки лічильник дози не порівняється із символом перевірки надходження препарату (рис. А). - Тримайте шприц-ручку голкою вгору. Натисніть пускову кнопку та утримуйте її в цьому положенні, доки лічильник дози не повернеться до "0" (мал. В). "О" має стояти навпроти вказівника дози. На кінці голки має з'явитися крапля розчину. На кінці голки може залишатися невелика крапля, але вона не буде введена при ін'єкції. Якщо крапля розчину на кінці голки не з'явилася, повторіть операцію "2" "Перевірка надходження препарату", але не більше 6 разів. Якщо крапля розчину так і не з'явилася, поміняйте голку та повторіть операцію "2" "Перевірка надходження препарату" ще раз. Якщо крапля розчину так і не з'явилася, утилізуйте шприц-ручку та використовуйте нову. Завжди перед використанням нової шприц-ручки вперше переконайтеся, що на кінці голки з'явилася крапля розчину. Це гарантує надходження препарату. Якщо крапля розчину не з'явилася, препарат не буде введений, навіть якщо лічильник дози рухатиметься. Це може вказувати на те, що голка закупорена або пошкоджена. Якщо Ви не перевірите надходження препарату перед першою ін'єкцією за допомогою кожної нової шприц-ручки, Ви можете не ввести необхідну дозу та очікуваного ефекту препарату Оземпік® не буде досягнуто. 3. Встановлення дози Поверніть селектор дози, щоб вибрати дозу 1 мг. Продовжуйте повертати, доки лічильник дози не зупиниться і не покаже "1". Тільки лічильник дози та покажчик дози покажуть, що було обрано 1 мг. Ви можете вибрати лише 1 мг препарату на дозу. Якщо шприц-ручка містить менше 1 мг, лічильник дози зупиниться перш, ніж з'явиться "1". При кожному повороті селектора дози лунають клацання, звук клацань залежить від того, в яку сторону обертається селектор дози: вперед, назад або якщо Ви намагаєтесь набрати дозу більше 1 мг. Не рахуйте клацання шприц-ручки. Завжди перед кожною ін'єкцією за лічильником дози та вказівником дози перевіряйте, що набрано 1 мг. Не рахуйте клацання шприц-ручки. За допомогою селектора дози слід вибирати лише дозу 1 мг. Доза 1 мг повинна бути точно проти вказівника дози – таке положення гарантує, що Ви отримаєте правильну дозу препарату. Скільки препарату залишилось Щоб визначити, скільки препарату залишилося, використовуйте лічильник дози: Повертайте селектор дози до зупинки лічильника. Якщо він показує "1", у шприц-ручці залишилося щонайменше 1 мг препарату. Якщо лічильник дози зупинився до того, як з'явилася цифра "1", це означає, що в шприц-ручці залишилася недостатня кількість препарату, щоб ввести повну дозу 1 мг. Якщо в шприц-ручці залишилася недостатня кількість препарату для введення повної дози, не використовуйте шприц-ручку. Використовуйте нову шприц-ручку Оземпік®. 4. Введення препарату Введіть голку під шкіру, використовуючи техніку ін'єкцій, рекомендовану лікарем або медсестрою. Переконайтеся, що лічильник дози знаходиться у полі вашого зору. Не торкайтеся лічильника дози пальцями - це може перервати ін'єкцію. Натисніть пускову кнопку до упору та утримуйте її в цьому положенні, доки лічильник дози не покаже "О". "О" повинен бути точно навпроти вказівника дози. При цьому Ви можете почути чи відчути клацання. Утримуйте голку під шкірою після того, як лічильник дози повернувся до "0" і повільно рахуйте до 6. Якщо ви витягнете голку з-під шкіри раніше, ви можете побачити, як препарат випливає з голки. У цьому випадку буде введено неповну дозу препарату. Вийміть голку з-під шкіри. Якщо в місці ін'єкції з'явилася кров, притисніть до місця уколу ватний тампон. Не масажуйте місце уколу. Після завершення ін'єкції можна побачити краплю розчину на кінці голки. Це нормально і не впливає на дозу, яку Ви ввели. Завжди звіряйтеся зі показаннями лічильника дози, щоб знати, яку кількість мг препарату ви ввели. Утримуйте пускову кнопку, доки лічильник дози не покаже "О". Як виявити закупорку або пошкодження голки Якщо після тривалого натискання на пускову кнопку на лічильнику дози не з'являється "О", це може означати закупорку або пошкодження голки. У цьому випадку Ви не отримали препарат, навіть якщо лічильник дози змінив положення вихідної дози, яку Ви встановили. Що робити із закупореною голкою Замініть голку як описано в операції 5 "Після завершення ін'єкції" і повторіть всі кроки, починаючи з операції 1 "Підготовка шприц-ручки з новою голкою до використання". Переконайтеся, що встановили необхідну Вам дозу. Ніколи не торкайтеся лічильника дози під час введення препарату. Це може перервати ін'єкцію. 5. Після завершення ін'єкції Поклавши зовнішній ковпачок голки на плоску поверхню, введіть кінець голки всередину ковпачка, не торкаючись його голки. Коли голка увійде в ковпачок, обережно надягніть зовнішній ковпачок на голку. Відкрутіть голку і викиньте її, дотримуючись запобіжних заходів. - Після кожного використання надягайте на шприц-ручку ковпачок, щоб захистити розчин, що міститься в ній, від впливу світла. Завжди після кожної ін'єкції викидайте голку, щоб забезпечити комфортну ін'єкцію та уникнути закупорки голок. Якщо голка закупорена, Ви не введете препарат. Викидайте порожню шприц-ручку з від'єднаною голкою відповідно до рекомендацій лікаря, медсестра, фармацевта або місцевих вимог. Ніколи не намагайтеся надіти внутрішній ковпачок назад на голку. Ви можете вколотись. Після кожної ін'єкції завжди одразу видаляйте голку зі шприц-ручки. Це може запобігти закупорці голок, забруднення, інфікування, витікання розчину та введення неправильної дози препарату. Додаткова важлива інформація Завжди зберігайте шприц-ручку та голки до неї в недоступному для всіх, особливо для дітей, місці. Ніколи не передавайте свою шприц-ручку та голки до неї іншим особам. Особи, що здійснюють догляд за хворим, повинні звертатися з використаними голками з особливою обережністю, щоб запобігти уколам голки та перехресному інфікуванню. Догляд за шприц-ручкою Акуратно поводьтеся зі шприц-ручкою. Недбале поводження або неправильне використання можуть призвести до введення неправильної дози препарату, наслідком чого можуть стати висока концентрація глюкози крові або дискомфорт у ділянці живота (нудота або блювання). Не залишайте шприц-ручку в автомобілі або іншому місці, де вона може піддаватися впливу занадто високих або занадто низьких температур. Не застосовуйте препарат Оземпік, якщо він був заморожений. У цьому випадку концентрація глюкози крові може стати занадто високою або Ви можете відчути дискомфорт у ділянці живота, такий, як нудота або блювота. Не застосовуйте препарат Оземпік®, якщо він зазнав прямих сонячних променів. У цьому випадку концентрація глюкози може стати занадто високою. Захищайте шприц-ручку від попадання на неї пилу, забруднень та рідини. Не мийте шприц-ручку, не занурюйте її в рідину і не змащуйте її. При необхідності шприц-ручку можна очищати вологою тканиною, змоченою м'яким миючим засобом. Не можна кидати або вдаряти шприц-ручку об тверду поверхню. Якщо Ви впустили шприц-ручку або сумніваєтеся у її справності, приєднайте нову голку та перевірте надходження препарату перед тим, як зробити ін'єкцію. Не намагайтеся повторно заповнити шприц-ручку. Порожню шприц-ручку слід викинути. Не намагайтеся самостійно полагодити шприц-ручку або розібрати її на частини. Вплив на здатність до керування автотранспортом та управління механізмами Препарат Оземпик® не влияет или незначительно влияет на способность управлять транспортными средствами или работу с механизмами. Пациенты должны быть предупреждены о том, что им следует соблюдать меры предосторожности во избежание развития у них гипогликемии во время управления транспортными средствами и при работе с механизмами, особенно при применении препарата Оземпик® в комбинации с производным сульфонилмочевины или инсулином.Условия храненияВ холодильнике +2 +8 градусУсловия отпуска из аптекПо рецептуВідео на цю тему
Склад, форма випуску та упаковкаСуспензія - 1 мл: активна речовина: інсулін-ізофан (людський генно-інженерний) 100 МВ (3,5 мг) (1 ME відповідає 0,035 мг безводного людського інсуліну); допоміжні речовини: цинк 18 мкг (у вигляді цинку хлориду), гліцерин (гліцерол) 16 мг, метакрезол 1,5 мг, фенол 0,65 мг, натрію гідрофосфату дигідрат 2,4 мг, протаміну сульфат близько 0,35 мг, натрію гідр близько 0,4 мг та/або хлористоводнева кислота близько 1,7 мг (для коригування pH), вода для ін'єкцій до 1,0 мл. 1 флакон містить 10 мл препарату, що відповідає 1000ME. 1 шприц-ручка містить 3 мл препарату, що відповідає 300 МО. 1) По 10 мл препарату у флакон зі скла 1 гідролітичного класу, закупорений пробкою з бромбутилової гуми/поліізопрену під алюмінієвою обкаткою та захисним пластмасовим ковпачком. По 1 флакону разом з інструкцією із застосування в картонну пачку. 2) По 3 мл препарату в картриджі зі скла I гідролітичного класу, закупорені дисками з бромбутилової гуми/поліізопрену з одного боку та поршнями з бромбутилової гуми з іншого боку. У картридж поміщена скляна кулька, що полегшує ресуспендування. Картридж запаяний у мультидозову одноразову поліпропіленову шприц-ручку для багаторазових ін'єкцій ФлексПен®. По 5 мультидозових одноразових шприц-ручок разом із інструкцією із застосування в картонну пачку.Опис лікарської формиСуспензія білого кольору, що при стоянні розшаровується, утворюючи білий осад та безбарвну або майже безбарвну надосадову рідину. При перемішуванні препарату за методикою, описаною в інструкції з медичного застосування, осад повинен ресуспендуватись.Фармакотерапевтична групаГіпоглікемічний засіб – інсулін середньої тривалості дії.ФармакокінетикаПеріод напіввиведення інсуліну з кровотоку дорівнює всього кілька хвилин. Тривалість дії препаратів інсуліну в основному обумовлена швидкістю всмоктування, яка залежить від кількох факторів (наприклад, від дози інсуліну, способу та місця введення, товщини підшкірного жирового шару та типу цукрового діабету). Тому фармакокінетичні параметри інсуліну схильні до значних інтер- та інтраіндивідуальних коливань. Всмоктування Максимальна концентрація (Сmах) інсуліну в плазмі досягається протягом 2-18 годин після підшкірного введення. Розподіл Вираженого зв'язування з білками плазми не відзначається, за винятком циркулюючих антитіл до інсуліну (у разі їх наявності). Метаболізм Людський інсулін розщеплюється під дією інсулінової протеази або інсулін-розщеплювальних ферментів, а також, можливо, під дією протеїндисульфідізомерази. Передбачається, що у молекулі людського інсуліну є кілька ділянок розщеплення (гідролізу); однак жоден із метаболітів, що утворюються внаслідок розщеплення, не є активним. Виведення Період напіввиведення (Т1/2) визначається за швидкістю всмоктування з підшкірних тканин. Таким чином, Т1/2 швидше є мірою всмоктування, а не власне мірою виведення інсуліну з плазми (Т1/2 інсуліну з кровотоку дорівнює всього кілька хвилин). Дослідження показали, що Т1/2 становить близько 5-10 годин. Доклінічні дані щодо безпеки У ході доклінічних досліджень, що включали фармакологічні дослідження безпеки, дослідження токсичності при повторному введенні дози, дослідження генотоксичності, канцерогенного потенціалу та токсичного впливу на репродуктивну сферу, специфічного ризику для людини не було виявлено.ФармакодинамікаПротафан НМ - препарат людського інсуліну середньої тривалості дії, вироблений методом біотехнології рекомбінантної ДНК з використанням штаму Saccharomyces cerevisiae. Зниження концентрації глюкози в крові відбувається за рахунок підвищення її внутрішньоклітинного транспорту після зв'язування інсуліну з інсуліновими рецепторами м'язової та жирової тканини та одночасного зниження швидкості продукції глюкози печінкою. Дія препарату починається протягом 11/2 години після введення, максимальний ефект проявляється протягом 4-12 годин, при цьому загальна тривалість дії становить близько 24 годин.Показання до застосуванняЦукровий діабет, що потребує інсулінотерапії.Протипоказання до застосуванняГіпоглікемія. Гіперчутливість до людського інсуліну або будь-якого компонента, що входить до складу даного препарату.Вагітність та лактаціяВагітність Обмежень застосування інсуліну під час вагітності не існує, оскільки інсулін не проникає через плацентарний бар'єр. Як гіпоглікемія, так і гіперглікемія, які можуть розвиватися у випадках недостатньо точно підібраної терапії, підвищують ризик виникнення вад розвитку плода та внутрішньоутробної загибелі плода. Вагітні жінки з цукровим діабетом протягом всієї вагітності повинні бути під наглядом, у них необхідно здійснювати посилений контроль концентрації глюкози в крові; такі ж рекомендації стосуються і жінок, які планують вагітність. Потреба в інсуліні зазвичай знижується у першому триместрі вагітності та поступово збільшується у другому та третьому триместрах. Після пологів потреба в інсуліні зазвичай швидко повертається до рівня, який відзначався до вагітності. Період грудного вигодовування Також не існує обмежень для застосування препарату Протафан НМ у період грудного вигодовування. Проведення інсулінотерапії жінкам у період грудного вигодовування не становить небезпеки для дитини. Однак може знадобитися корекція режиму дозування препарату Протафан НМ та/або дієти.Побічна діяНайпоширенішим небажаним явищем при застосуванні інсуліну є гіпоглікемія. У ході клінічних досліджень, а також у ході застосування препарату після його випуску на споживчий ринок було встановлено, що частота виникнення гіпоглікемії змінюється залежно від популяції пацієнтів, режиму дозування препарату та контролю за глікемією. На початковій стадії інсулінотерапії можуть виникати порушення рефракції, периферичні набряки та реакції у місці введення препарату (що включають біль, почервоніння, кропив'янку, запалення, гематому, припухлість та свербіж у місці ін'єкції). Ці симптоми зазвичай носять тимчасовий характер, швидке поліпшення контролю глікемії може призводити до стану "гострої больової нейропатії", яка зазвичай є оборотною. Інтенсифікація інсулінотерапії з різким покращенням контролю вуглеводного обміну може призвести до тимчасового погіршення стану діабетичної ретинопатії, водночас тривале покращення контролю глікемії знижує ризик прогресування діабетичної ретинопатії. Список побічних явищ представлений у таблиці. Всі подані нижче побічні ефекти, засновані на даних, отриманих у ході клінічних досліджень, розподілені по групам відповідно до частоти розвитку відповідно до MedDRA та систем органів. Частота розвитку побічних ефектів визначається як: дуже часто (≥1/10); часто (≥1/100 до Порушення з боку імунної системи: Нечасто - кропив'янка, висипання на шкірі; Дуже рідко – анафілактичні реакції*. Порушення з боку обміну речовин та харчування: Дуже часто – гіпоглікемія*. Порушення з боку нервової системи: Дуже рідко – периферична нейропатія ("гостра больова нейропатія"). Порушення з боку органу зору: Дуже рідко – порушення рефракції; Нечасто – діабетична ретинопатія. Порушення з боку шкіри та підшкірних тканин: Нечасто – ліподистрофія*. Загальні розлади та порушення у місці введення: Нечасто - реакції у місці введення; Нечасто – периферичні набряки. *Див. "Опис окремих побічних реакцій" Опис окремих побічних реакцій Анафілактичні реакції Відзначені дуже рідкісні реакції генералізованої гіперчутливості, у тому числі генералізована шкірна висипка, свербіж, підвищене потовиділення, шлунково-кишкові розлади, ангіоневротичний набряк, утруднення дихання, прискорене серцебиття, зниження артеріального тиску, а також непритомність/втрата свідомості, . Гіпоглікемія Гіпоглікемія є найчастішим побічним явищем. Вона може розвинутись, якщо доза інсуліну надто висока по відношенню до потреби в інсуліні. Тяжка гіпоглікемія може призводити до втрати свідомості та/або судом, тимчасового або необоротного порушення функції головного мозку або навіть до смерті. Симптоми гіпоглікемії, як правило, розвиваються раптово. Вони можуть включати "холодний піт", блідість шкірних покривів, підвищену стомлюваність, нервозність або тремор, почуття тривоги, незвичайну втому або слабкість, порушення орієнтації, зниження концентрації уваги, сонливість, виражене почуття голоду, порушення зору, головний біль, нудоту та прискорене серцебиття . Ліподистрофія Повідомлялося про нечасті випадки розвитку ліподистрофії. Ліподистрофія може розвиватися у місці введення препарату.Взаємодія з лікарськими засобамиЄ ряд лікарських засобів, які впливають потребу в інсуліні. Гипогликемическое действие инсулина усиливают пероральные гипогликемические препараты, ингибиторы моноаминоксидазы, ингибиторы ангиотензинпревращающего фермента, ингибиторы карбоангидразы, неселективные бета-адреноблокаторы, бромокриптин, сульфонамиды, анаболические стероиды, тетрациклины, клофибрат, кетоконазол, мебендазол, пиридоксин, теофиллин, циклофосфамид, фенфлурамин, препараты лития, салицилаты . Гіпоглікемічну дію інсуліну послаблюють пероральні гормональні контрацептивні засоби, глюкокортикостероїди, тиреоїдні гормони, тіазидні діуретики, гепарин, трициклічні антидепресанти, симпатоміметики, соматропін, даназол, клонідин, блокатори, медлен, Бета-адреноблокатори можуть маскувати симптоми гіпоглікемії та уповільнювати відновлення після гіпоглікемії. Октреотид/ланреотид може підвищувати, так і знижувати потребу організму в інсуліні. Алкоголь може посилювати чи зменшувати гіпоглікемічний ефект інсуліну. Несумісність Суспензії інсуліну не можна додавати до розчинів для інфузій.Спосіб застосування та дозиПрепарат призначений для підшкірного введення. Суспензії інсуліну не можна вводити внутрішньовенно. Препарат Протафан НМ може застосовуватися як у монотерапії, так і в комбінації з інсуліном швидкої або короткої дії. Доза препарату підбирається індивідуально з урахуванням потреб пацієнта. Зазвичай потреба в інсуліні становить від 0,3 до 1 МО/кг/добу. залишковою ендогенною продукцією інсуліну Препарат Протафан НМ зазвичай вводять підшкірно, в область стегна. Якщо це зручно, то ін'єкції можна робити також у передню черевну стінку, сідничну область або область дельтовидного м'яза плеча. При введенні препарату в область стегна відзначається повільніше всмоктування, ніж при введенні до інших областей. Якщо ін'єкція виробляється у відтягнуту шкірну складку, ризик випадкового внутрішньом'язового введення препарату зводиться до мінімуму. Голка повинна залишатися під шкірою щонайменше 6 секунд, що гарантує повне введення дози. Необхідно постійно змінювати місця ін'єкцій у межах анатомічної області, щоб запобігти розвитку ліподистрофій. Препарат Протафан® НМ на флаконах може застосовуватися тільки разом з інсуліновими шприцами, на які нанесена шкала, що дозволяє відміряти дозу інсуліну в одиницях дії. Шприц-ручка ФлексПен® є попередньо заповненою шприц-ручкою, розробленою для використання з одноразовими ін'єкційними голками НовоФайн® або НовоТвіст® довжиною до 8 мм. Шприц-ручка ФлексПен дозволяє вводити дозу інсуліну в межах від 1 до 60 одиниць з кроком в 1 одиницю. Слід дотримуватися докладних рекомендацій щодо застосування та введення препарату. Корекція дози Супутні захворювання, особливо інфекційні та супроводжуються лихоманкою, зазвичай підвищують потребу організму в інсуліні. Корекція дози препарату може також бути потрібна при наявності у пацієнта супутніх захворювань нирок, печінки, порушенні функції надниркових залоз, гіпофізу або щитовидної залози. Необхідність корекції дози також може виникнути при зміні фізичного навантаження або звичайного режиму харчування пацієнта. Корекція дози може бути потрібна при переведенні пацієнта з одного виду інсуліну на інший.ПередозуванняПевної дози, необхідної для передозування інсуліну, не встановлено, однак гіпоглікемія може поступово розвиватися, якщо вводяться занадто високі дози інсуліну по відношенню до потреби пацієнта. Легку гіпоглікемію пацієнт може усунути сам. прийнявши всередину глюкозу або цукромісткі продукти харчування. Тому хворим на цукровий діабет рекомендується постійно носити з собою цукрозміщуючі продукти. У разі важкої гіпоглікемії, коли пацієнт непритомний, слід ввести від 0,5 мг до 1 мг глюкагону внутрішньом'язово або підшкірно (може вводити навчена людина), або внутрішньовенно розчин декстрози (глюкози) (може вводити тільки медичний працівник). Також необхідно внутрішньовенно ввести декстрозу у випадку, якщо через 10-15 хв після введення глюкагону пацієнт не приходить до тями. Після відновлення свідомості пацієнту рекомендується прийняти багату на вуглеводи їжу для профілактики рецидиву гіпоглікемії.Запобіжні заходи та особливі вказівкиНедостатня доза або припинення лікування, особливо при цукровому діабеті 1 типу, може призвести до розвитку гіперглікемії. Як правило, перші симптоми гіперглікемії з'являються поступово протягом декількох годин або днів. Симптомами гіперглікемії є почуття спраги, прискорене сечовипускання, нудота, блювання, сонливість, почервоніння та сухість шкіри, сухість у роті, втрата апетиту, а також поява запаху ацетону у повітрі, що видихається. Віз відповідного лікування гіперглікемія у пацієнтів з цукровим діабетом 1 типу може призводити до діабетичного кетоацидозу - стану, що є потенційно летальним. Гіпоглікемія Гіпоглікемія може розвинутись, якщо введена занадто висока доза інсуліну, але стосовно потреби пацієнта. Пропуск їжі або незаплановане інтенсивне фізичне навантаження можуть призвести до гіпоглікемії. Після компенсації вуглеводного обміну, наприклад, при інтенсифікованій інсулінотерапії, у пацієнтів можуть змінитися типові для них симптоми-провісники гіпоглікемії, про що хворі мають бути поінформовані. Звичайні симптоми-провісники можуть зникати при тривалому перебігу цукрового діабету. Переведення пацієнтів на інший тип інсуліну або інсулін іншої компанії-виробника повинен здійснюватися тільки під медичним контролем. При зміні концентрації виробника, типу, виду (людський інсулін, аналог людського інсуліну) та/або методу виготовлення може знадобитися зміна дози інсуліну. Пацієнтам, які переходять на лікування препаратом Протафан® НМ, може знадобитися зміна дози або збільшення частоти ін'єкцій порівняно з препаратами інсуліну, що застосовувалися раніше. Якщо при переведенні пацієнтів на лікування препаратом Протафан НМ необхідна корекція дози, це можна зробити вже при введенні першої дози або в перші тижні або місяці терапії. Як і при лікуванні іншими препаратами інсуліну, можуть розвиватися реакції у місці введення, що проявляється болем, почервонінням, кропивницею, запаленням, гематомою, набряклістю та свербінням. Регулярна зміна місці ін'єкції в одній і топ же анатомічній області допоможе зменшити симптоми або запобігти розвитку цих реакцій. Реакції зазвичай зникають протягом кількох днів до кількох тижнів. У поодиноких випадках може знадобитися відміна препарату Протафан НМ через реакції в місці введення. Перед поїздкою, пов'язаною зі зміною часових поясів, пацієнт повинен проконсультуватися зі своїм лікарем, оскільки зміна часового поясу означає, що пацієнт повинен вживати їжу та вводити інсулін в інший час. Суспензії інсуліну не можна застосовувати в інсулінових насосах. Одночасне застосування препаратів групи тіазолідиндіону та препаратів інсуліну. Повідомлялося про випадки розвитку хронічної серцевої недостатності при лікуванні пацієнтів тіазолідиндіонами у комбінації з препаратами інсуліну, особливо за наявності у таких пацієнтів факторів ризику хронічної серцевої недостатності. Слід враховувати цей факт при призначенні пацієнтам комбінованої терапії тіазолідиндіонами та препаратами інсуліну. При призначенні такої комбінованої терапії необхідно проводити медичні обстеження пацієнтів щодо виявлення у них ознак і симптомів хронічної серцевої недостатності, збільшення маси тіла та наявності периферичних набряків. У разі погіршення у пацієнтів симптоматики серцевої недостатності лікування тіазолідиндіонами необхідно припинити. Запобіжні заходи при застосуванні Шприц-ручки слід використовувати лише у поєднанні із сумісними продуктами, що забезпечує безпеку та ефективність їх використання. Препарат Протафан® НМ у шприц-ручці ФлексПен® та голки призначені лише для індивідуального використання. Не допускається повторне заповнення картриджа шприц-ручки. Не можна застосовувати препарат Протафан НМ, якщо він був заморожений. Перед першим застосуванням необхідно вийняти препарат Протафан НМ з холодильника і дати йому досягти кімнатної температури для полегшення перемішування суспензії. Суспензію інсуліну не можна застосовувати, якщо вона після перемішування не стає однорідно білою і каламутною. Поінформуйте пацієнта про необхідність викидати голку після кожної ін'єкції. Інструкція із застосування для пацієнтів Не можна використовувати Протафан® НМ: В інсулінових насосах. Якщо у Вас алергія (гіперчутливість) до людського інсуліну або будь-якого компонента, що входять до складу препарату Протафан® НМ. Якщо у вас починається гіпоглікемія (низька концентрація цукру в крові). Якщо захисний ковпачок відсутній або вдягнений нещільно. Кожен флакон має пластиковий захисний ковпачок. Якщо на новому флаконі захисний ковпачок пошкоджено, поверніть його в аптеку. Якщо були порушені умови зберігання препарату, або він був заморожений. Якщо інсулін не стає однорідно білим та каламутним після перемішування. Перед застосуванням Протафан® НМ: Перевірте етикетку, щоб переконатися, що Ви використовуєте правильний тип інсуліну. Видаліть захисний ковпачок. Як застосовувати препарат Протафан НМ Препарат Протафан НМ призначений для підшкірного введення. Ніколи не вводьте інсулін внутрішньовенно чи внутрішньом'язово. Завжди змінюйте місця ін'єкцій у межах анатомічної області, щоб зменшити ризик утворення ущільнень та виразок у місці ін'єкції. Найкращими місцями для ін'єкцій є область сідниць, передньої поверхні стегна або плеча. Як вводити препарат Протафан НМ, якщо вводиться тільки Протафан НМ або якщо необхідно змішати Протафан НМ з інсуліном короткої дії: Переконайтеся, що ви використовуєте інсуліновий шприц, на який нанесена шкала, що дозволяє відміряти дозу в одиницях дії. Наберіть у шприц повітря у кількості, що відповідає потрібній дозі інсуліну. Виконуйте інструкції, які дав Вам лікар або медична сестра. Безпосередньо перед набором дози покатайте флакон між долонями до того часу, поки інсулін стане рівномірно білим і каламутним. Ресуспендування полегшується, якщо препарат має кімнатну температуру. Введіть інсулін під шкіру. Використовуйте техніку ін'єкції, рекомендовану лікарем або медичною сестрою. Утримуйте голку під шкірою щонайменше 6 секунд, щоб переконатися, що доза інсуліну введена повністю. Протафан® НМ суспензія для підшкірного введення у шприц-ручках ФлексПен® Інструкція із застосування для пацієнтів Уважно прочитайте цю інструкцію перед застосуванням препарату Протафан® НМ у шприц-ручці ФлексПен®. Шприц-ручка ФлексПен - це попередньо заповнена інсулінова шприц-ручка з дозатором. Ви можете вибрати дозу від 1 до 60 одиниць із кроком в 1 одиницю. Шприц-ручка ФлексПен® розроблена для використання з одноразовими голками НовоФайн або НовоТвіст® завдовжки до 8 мм. В якості запобіжного заходу завжди носіть із собою запасну систему для введення інсуліну на випадок втрати або пошкодження Вашої шприц-ручки ФлексПен® з препаратом Протафан® НМ. Зберігання та догляд Шприц-ручка ФлексПен® розроблена для ефективного та безпечного використання та потребує акуратного поводження. У разі падіння або сильного механічного впливу, можливе пошкодження шприц-ручки та витікання інсуліну. Зовні шприц-ручку ФлексПен можна очищати ватним тампоном. Не мийте, не занурюйте в рідину та не змащуйте шприц-ручку, т.к. це може зашкодити механізм. Забороняється повторне заповнення шприц-ручки ФлексПен®. Підготовка шприц-ручки ФлексПен з препаратом Протафан HМ до роботи Перевірте етикетку, щоб переконатися, що шприц-ручка ФлексПен з препаратом Протафан НМ містить необхідний тип інсуліну. Перемішайте інсулін перед першою ін'єкцією за допомогою нової шприц-ручки ФлексПен®. Щоб полегшити перемішування, дайте препарату нагрітися до кімнатної температури. Зніміть ковпачок із шприц-ручки. Підніміть і опустіть шприц-ручку вгору і вниз 20 разів, як показано на малюнку, щоб скляна кулька переміщалася від одного кінця картриджа до іншого. Повторюйте зазначені маніпуляції, поки вміст картриджа не буде рівномірно білим і каламутним. Перед кожною наступною ін'єкцією перемішуйте вміст, піднімаючи та опускаючи шприц-ручку вгору та вниз мінімум 10 разів, поки вміст картриджа не стане рівномірно білим та каламутним. Після перемішування одразу зробіть ін'єкцію. Завжди перевіряйте, щоб у картриджі залишалося щонайменше 12 одиниць інсуліну для забезпечення рівномірного перемішування. Якщо залишилося менше 12 одиниць – використовуйте нову шприц-ручку ФлексПен® із препаратом Протафан® HМ. Приєднання голки Видаліть захисну наклейку з одноразової голки. Акуратно та щільно накрутіть голку на шприц-ручку ФлексПен®. Зніміть зовнішній ковпачок голки, але не викидайте його. Зніміть та викиньте внутрішнім ковпачок голки. Завжди використовуйте нову голку для кожної ін'єкції, щоб запобігти зараженню. Будьте обережні, не погніть та не пошкодіть голку перед використанням. Щоб уникнути випадкових уколів, ніколи не надягайте внутрішній ковпачок назад на голку. Перевірка надходження інсуліну У процесі використання шприц-ручки перед кожною ін'єкцією в картриджі може накопичуватися невелика кількість повітря. Для запобігання попаданню бульбашки повітря та забезпечення введення правильної дози препарату. Наберіть 2 ОД препарату поворотом дози селектора. Тримаючи шприц-ручку ФлексПен® голкою вгору, кілька разів трохи постукайте по картриджу кінчиком пальця, щоб бульбашки повітря перемістилися у верхню частину картриджа. Утримуючи шприц-ручку голкою вгору, натисніть кнопку пуску до упору. Селектор доти повернеться до нуля. На кінці голки має з'явитися крапля інсуліну. Якщо цього не сталося, замініть голку та повторіть процедуру, але не більше 6 разів. Якщо крапля інсуліну не з'явилася, це означає, що шприц-ручка несправна і її не можна використовувати. Встановлення дози Переконайтеся, що селектор дози встановлено у положення "0". Поворотом селектора дози встановіть кількість одиниць, необхідних ін'єкції. Дозу можна регулювати обертанням селектора дози в будь-якому напрямку, доки правильна доза не буде встановлена навпроти вказівника дози. Щоб уникнути викиду дози інсуліну, будьте обережні при обертанні селектора дози, щоб випадково не натиснути на пускову кнопку. Неможливо встановити дозу, яка перевищує кількість одиниць, що залишилися в картриджі. Не можна використовувати шкалу залишку інсуліну для відмірювання дози інсуліну. Введення інсуліну Введіть голку під шкіру. Використовуйте техніку ін'єкції, рекомендовану лікарем. Щоб зробити ін'єкцію, натисніть пускову кнопку до упору, доки напроти вказівника дози не з'явиться "0". Будьте уважні: при введенні препарату слід натискати лише на кнопку пуску. При повороті дози селектора препарат не буде введений. Витягаючи голку з-під шкіри, утримуйте пускову кнопку повністю натиснутою. Після ін'єкції залишайте голку під шкірою щонайменше 6 секунд. Це забезпечить повну дозу інсуліну. Направте голку у зовнішній ковпачок голки, не чіпаючи ковпачок. Коли голка повністю увійде всередину, надягніть ковпачок і відкрутіть голку. Викиньте голку, дотримуючись запобіжних заходів, і закрийте шприц-ручку ковпачком. Видаляйте голку після кожної ін'єкції та ніколи не зберігайте шприц-ручку ФлексПен® із приєднаною голкою. В іншому випадку можливе витікання рідини зі шприц-ручки, що може призвести до неправильного дозування. Особи, які здійснюють догляд за хворим, повинні поводитися з використаними голками з особливою обережністю, щоб уникнути випадкових уколів. Викидайте використану шприц-ручку ФлексПен з від'єднаною голкою. Шприц-ручка ФлексПен® із препаратом Протафан® НМ та голки призначені лише для індивідуального використання, не можна передавати їх іншим особам. Вплив на здатність до керування автотранспортом та управління механізмами Здатність пацієнтів до концентрації уваги та швидкість реакції можуть порушуватися під час гіпоглікемії, що може становити небезпеку в тих ситуаціях, коли ці здібності особливо необхідні (наприклад, при керуванні транспортними засобами або роботі з машинами та механізмами). Пацієнтам необхідно рекомендувати вживати заходів для запобігання розвитку гіпоглікемії при керуванні транспортними засобами. Це особливо важливо для пацієнтів з відсутністю або зниженням вираженості симптомів-провісників гіпоглікемії, що розвивається або страждають частими епізодами гіпоглікемії. У цих випадках слід розглянути доцільність керування транспортними засобами та виконання подібних робіт.Умови відпустки з аптекЗа рецептомВідео на цю тему
482,00 грн
297,00 грн
Склад, форма випуску та упаковкаСуспензія для підшкірного введення - 1 мл: Активні речовини: інсулін-ізофан (людський генно-інженерний) – 100 МО (1 МО відповідає 35 мкг безводного людського інсуліну); Допоміжні речовини: цинку хлорид – 33 мкг, гліцерол – 16 мг, метакрезол – 1.5 мг, фенол – 0.65 мг, натрію гідрофосфату дигідрат – 2.4 мг, протаміну сульфат – близько 0.35 мг, натрію гідроксид – до 0. близько 1.7 мг (для коригування pH), вода д/і – до 1 мл. 3 мл – картриджі безбарвного скла (5) – блістери (1) – пачки картонні.Опис лікарської формиСуспензія для підшкірного введення білого кольору, при стоянні розшаровується, утворюючи білий осад і безбарвну або майже безбарвну надосадову рідину; при перемішуванні осад повинен ресуспендуватись.Фармакотерапевтична групаІнсулін людини середньої тривалості дії.ФармакокінетикаПовнота всмоктування та початок ефекту інсуліну залежить від місця введення (живот, стегно, сідниці), дози (об'єму інсуліну, що вводиться), концентрації інсуліну в препараті. Розподіляється по тканинах нерівномірно; не проникає через плацентарний бар'єр та у грудне молоко. Руйнується інсуліназою в основному в печінці та нирках. Виводиться нирками (30-80%).ФармакодинамікаІнсулін людський середньої тривалості дії, отриманий із застосуванням технології рекомбінантної ДНК. Взаємодіє зі специфічним рецептором зовнішньої цитоплазматичної мембрани клітин та утворює інсулін-рецепторний комплекс, що стимулює внутрішньоклітинні процеси, у т.ч. синтез ряду ключових ферментів (гексокіназа, піруваткіназа, глікогенсинтетаза). Зниження вмісту глюкози в крові обумовлено підвищенням її внутрішньоклітинного транспорту, посиленням поглинання та засвоєння тканинами, стимуляцією ліпогенезу, глікогеногенезу, зниженням швидкості продукції глюкози печінкою. Тривалість дії препаратів інсуліну в основному обумовлена швидкістю всмоктування, яка залежить від декількох факторів (наприклад, від дози, способу та місця введення), у зв'язку з чим профіль дії інсуліну схильний до значних коливань, як у різних людей, так і в одного і того ж людини. У середньому, після підшкірного введення даний інсулін починає діяти через 1.5 год, максимальний ефект розвивається в проміжку між 4 год і 12 год, тривалість дії - до 24 год.Показання до застосуванняЦукровий діабет 1 типу; цукровий діабет 2 типу: стадія резистентності до пероральних гіпоглікемічних засобів, часткова резистентність до цих препаратів (при проведенні комбінованої терапії), інтеркурентні захворювання; цукровий діабет 2 типи у вагітних.Протипоказання до застосуванняГіпоглікемія, підвищена індивідуальна чутливість до інсуліну.Вагітність та лактаціяОбмежень лікування цукрового діабету інсуліном при вагітності немає, т.к. інсулін не проникає крізь плацентарний бар'єр. При плануванні вагітності та під час неї необхідно інтенсифікувати лікування цукрового діабету. Потреба в інсуліні зазвичай знижується в І триместрі вагітності і поступово підвищується у ІІ та ІІІ триместрах. Під час пологів і після них потреба в інсуліні може різко знизитися. Незабаром після пологів потреба в інсуліні швидко повертається до рівня, який був до вагітності.Побічна діяПобічна дія, зумовлена впливом на вуглеводний обмін: гіпоглікемічні стани (блідість шкірних покривів, посилення потовиділення, відчуття серцебиття, тремор, почуття голоду, збудження, парестезії слизової оболонки порожнини рота, головний біль, запаморочення, зниження гостроти зору). Виражена гіпоглікемія може призвести до розвитку гіпоглікемічної коми. Алергічні реакції: шкірний висип, набряк Квінке, анафілактичний шок. Місцеві реакції: гіперемія, набряк та свербіж у місці ін'єкції, при тривалому застосуванні – ліподистрофія у місці ін'єкції. Інші: набряки, минуще зниження гостроти зору (зазвичай на початку терапії).Взаємодія з лікарськими засобамиГипогликемическое действие инсулина усиливают пероральные гипогликемические препараты, ингибиторы МАО, ингибиторы АПФ, ингибиторы карбоангидразы, неселективные бета-адреноблокаторы, бромокриптин, октреотид, сульфаниламиды, анаболические стероиды, тетрациклины, клофибрат, кетоконазол, мебендазол, пиридоксин, теофиллин, циклофосфамид, фенфлурамин, препараты лития, препарати, що містять етанол. Гіпоглікемічна дія інсуліну послаблюють глюкагон, соматропін, естрогени, пероральні контрацептиви; , діазоксид, морфін, фенітоїн, нікотин. Під впливом резерпіну та саліцилатів можливе як ослаблення, так і посилення дії інсуліну. Знижує толерантність до етанолу.Спосіб застосування та дозиСпосіб застосування та режим дозування конкретного препарату залежать від форми випуску та інших факторів. Оптимальний режим дозування визначає лікар. Слід суворо дотримуватися відповідності лікарської форми конкретного препарату, що використовується, показанням до застосування і режиму дозування. Тільки для підшкірного введення. Доза препарату визначається лікарем індивідуально у кожному конкретному випадку, на підставі концентрації глюкози у крові. У середньому добова доза коливається від 0,5 до 1 МО/кг маси тіла (залежить від індивідуальних особливостей пацієнта та концентрації глюкози крові).Запобіжні заходи та особливі вказівкиЗ огляду на терапії інсуліном необхідний постійний контроль концентрації глюкози у крові. Причинами гіпоглікемії крім передозування інсуліну можуть бути: заміна препарату, пропуск прийому їжі, блювання, діарея, збільшення фізичної активності, захворювання, що знижують потребу в інсуліні (порушення функції печінки та нирок, гіпофункція кори надниркових залоз, гіпофіза або щитовидної залози), а також взаємодія з іншими лікарськими засобами. Неправильне дозування або перерви у введенні інсуліну, особливо у пацієнтів з цукровим діабетом 1 типу, можуть призвести до гіперглікемії. Зазвичай перші симптоми гіперглікемії поступово розвиваються протягом декількох годин або днів. Вони включають появу спраги, прискорене сечовипускання, нудоту, блювання, запаморочення, почервоніння і сухість шкіри, сухість у роті, втрату апетиту, запах ацетону в повітрі, що видихається. Якщо не проводити лікування, гіперглікемія при цукровому діабеті 1 типу може призвести до розвитку небезпечного для життя діабетичного кетоацидозу. Дозу інсуліну необхідно коригувати при порушенні функції щитовидної залози, хворобі Аддісона, гіпопітуїтаризмі, порушеннях функції печінки та нирок та при цукровому діабеті у пацієнтів старше 65 років. Зважаючи на підвищений ризик кардіальних та церебральних ускладнень гіпоглікемії, препарат інсуліну слід застосовувати препарат з обережністю у пацієнтів з вираженим стенозом коронарних та мозкових артерій. З обережністю у пацієнтів з проліферативною ретинопатією, що особливо не отримують лікування фотокоагуляцією (лазерною коагуляцією) у зв'язку з ризиком виникнення амаврозу (повної сліпоти). Якщо пацієнт збільшує інтенсивність фізичної активності або змінює звичну дієту, може знадобитися корекція дози інсуліну. Супутні захворювання, особливо інфекції та стани, що супроводжуються лихоманкою, збільшують потребу в інсуліні. Переведення пацієнта на новий тип інсуліну або препарат інсуліну іншого виробника необхідно проводити під контролем лікаря. При застосуванні препаратів інсуліну в комбінації з препаратами групи тіазолідиндіону у пацієнтів з цукровим діабетом 2 типу може виникати затримка рідини в організмі, внаслідок чого підвищується ризик розвитку та прогресування хронічної серцевої недостатності, особливо у пацієнтів із захворюваннями серцево-судинної системи та наявністю факторів ризику хронічної. серцевої недостатності. Пацієнтів, які отримують таку терапію, слід регулярно обстежувати з метою виявлення ознак серцевої недостатності. У разі виникнення серцевої недостатності терапію слід здійснювати відповідно до поточних стандартів лікування. При цьому необхідно розглянути можливість відміни або зниження дози тіазолідиндіону.Умови відпустки з аптекЗа рецептомВідео на цю тему
1 514,00 грн
1 486,00 грн
Склад, форма випуску та упаковкаРозчин - 1 мл: Активна речовина: інсулін деглудек/інсулін аспарт (у співвідношенні 70/30) 100 ОД*, що еквівалентно інсуліну деглудек 2.56 мг (70 ОД), інсуліну аспарт 1.05 мг (30 ОД); Допоміжні речовини: гліцерол - 19 мг, фенол - 1.5 мг, метакрезол - 1.72 мг, цинк - 27.4 мкг (у вигляді цинку ацетату - 92 мкг), натрію хлорид - 0.58 мг, хлористоводнева кислота або натрію ** , вода д/і – до 1 мл. 3 мл (300 ОД) – картриджі скляні (1) – шприц-ручки мультидозові одноразові для багаторазових ін'єкцій (5) – пачки картонні.Опис лікарської формиРозчин для підшкірного введення прозорий, безбарвний.Фармакотерапевтична групаПрепарат містить легко засвоюваний аналог надтривалого людського інсуліну (деглудек) та швидкого (аспарт). Речовина виходить за допомогою біотехнологічних методів із застосуванням штамів мікроорганізмів цукроміцетів. Ці інсулінові види зв'язуються з рецепторами природного інсуліну, що виробляється в організмі, і мають необхідний медичний ефект. Цукропонижувальна дія забезпечується інтенсифікацією процесу зв'язування глюкози та падінням інтенсивності утворення цього гормону в тканинах печінки. Ліки зв'язується з рецепторами природного інсуліну, що виробляється в організмі, та надають необхідний медичний ефект. Деглудек після п/в формує засвоювані сполуки депо підшкірної клітковини, звідки він повільно поширюється в кров. Цим пояснюється плоский профіль дії інсуліну та його довга дія. Аспарт починає діяти швидко. Загальна тривалість дії 1 дози – більше 24 годин.ФармакокінетикаАбсорбція. Після підшкірної ін'єкції відбувається утворення стабільних розчинних мультигекеамерів інсуліну деглудек. які створюють депо інсуліну в підшкірно-жировій тканині і при цьому не перешкоджає швидкому вивільненню мономерів інсуліну аспарт у кров'яне русло. Мультигексамери поступово дисоціюють, вивільняючи мономери інсуліну деглудек, у результаті відбувається повільне безперервне надходження препарату в кров. Рівноважна концентрація компонента надтривалої дії (інсуліну деглудек) у плазмі досягається через 2-3 дні після введення препарату Райзодег. Добре відомі показники швидкої абсорбції інсуліну аспарт зберігаються у препараті Райзодег. Фармакокінетичний профіль інсуліну аспарт проявляється через 14 хвилин після ін'єкції, максимальна концентрація спостерігається через 72 хвилини. Розподіл. Спорідненість інсуліну деглудек до сироваткового альбуміну відповідає сполучній здатності білка плазми більше 99% у плазмі крові людини. У інсуліну аспарт зв'язує здатність білка плазми нижче (менше 10%), як і у людського інсуліну. Метаболізм. Розпад інсуліну деглудек і інсуліну аспарт подібний до такого людського інсуліну, всі метаболіти, що утворюються, є неактивними. Виведення. Період напіввиведення препарату Райзодег після підшкірної ін'єкції визначається швидкістю його всмоктування із підшкірної тканини. Період напіввиведення інсуліну деглудек становить приблизно 25 годин та не залежить від дози. Лінійність. Сумарна дія препарату Райзодег пропорційно введеній дозі базального компонента (інсуліну деглудек) та прандіального компонента (інсуліну аспарт) при цукровому діабеті 1 та 2 типу. Спеціальні групи пацієнтів. Не виявлено різниці у фармакокіпстичних властивостях препарату Райзодег залежно від статі пацієнтів. Пацієнти похилого віку, пацієнти різних етнічних груп, пацієнти з порушенням ниркової функції або печінки. Не виявлено клінічно значимих відмінностей у фармакокінетиці препарату Райзодег між літніми та молодими пацієнтами, між пацієнтами різних етнічних груп, між пацієнтами з порушеннями функції нирок та печінки та здоровими пацієнтами.Показання до застосуванняЦукровий діабет у дорослих.Протипоказання до застосуванняПідвищена індивідуальна чутливість до активних речовин або до будь-якого з допоміжних компонентів препарату.Вагітність та лактаціяЗастосування препарату Райзодег ФлексТач у період вагітності протипоказане, оскільки клінічний досвід його застосування під час вагітності відсутнє. Дослідження репродуктивної функції у тварин не виявили відмінностей між інсуліном деглудек та людським інсуліном за показниками ембріотоксичності та тератогенності. Застосування препарату Райзодег ФлексТач у період грудного вигодовування протипоказане, оскільки клінічний досвід його застосування у жінок, які годують, відсутня. Дослідження на тваринах показали, що у щурів інсулін деглудек виділяється з грудним молоком, концентрація препарату у грудному молоці нижча, ніж у плазмі крові. Невідомо, чи виділяється інсулін деглудек із грудним молоком жінок. Протипоказано дітям віком до 18 років.Побічна діяЗ боку шкірних покривів. Іноді підшкірна ін'єкція призводить до розвитку ліподистрофії. Її вдається уникнути, якщо постійно змінювати місце уколу. Іноді у місці введення з'являється гематома, крововилив, біль, припухлість, набряк, почервоніння, подразнення та ущільнення шкіри. Вони швидко минають без лікування. З боку імунної системи. Можлива поява кропив'янки. З боку обміну речовин. Гіпоглікемія проявляється, якщо доза інсуліну виявилася вищою за потрібну. Різке зниження глюкози призводить до втрати свідомості, судом та дисфункції мозку. Симптоми цього стану швидко розвиваються: підвищене потовиділення, слабкість, дратівливість, збліднення, втома, сонливість, почуття голоду, діарея. Нерідко посилюється серцебиття і порушується зір. Алергії. Набряк язика, губ, тяжкість у шлунку, свербіж шкіри, пронос. Ці реакції тимчасові та при продовженні лікування повільно зникають.Взаємодія з лікарськими засобамиЗнижують інсулінову потребу комбінації з: пероральними медикаментами для боротьби з гіперглікемією; агоністами ГПП-1; інгібіторами МАО та АПФ; бета-адреноблокаторами; препаратами саліцилової кислоти; анаболіками; сульфаніламідними засобами. Збільшують потребу: ОК; медикаменти збільшення диуреза; кортикостероїди; аналоги тиреоїдних гормонів; соматотропін; даназол.Спосіб застосування та дозиПочаткова доза при діабеті 2 типу – 10 ОД. Надалі вона підбирається з урахуванням стану пацієнта. При інсулінозалежному діабеті початкова доза - до 70% загальної потреби. Препарат вводиться підшкірно перед основними прийомами їжі.ПередозуванняУ разі підвищення дози виникає гіпоглікемія. Точної дози, коли вона може виникати, немає. Легка форма усувається самостійно: досить використати невелику кількість солодкого. Пацієнтам рекомендується мати при собі цукор. Якщо людина непритомна, їй призначається глюкагон у м'яз або під шкіру. В/в робить лише медпрацівник. Глюкагон вводиться до виведення людини із несвідомого стану.Умови відпустки з аптекЗа рецептомВідео на цю тему
1 053,00 грн
1 010,00 грн
Склад, форма випуску та упаковкаРозчин для підшкірного введення – 1 мл: активна речовина: інсулін деглудек – 100 ОД (3,66 мг)/200 ОД (7,32 мг); допоміжні речовини: гліцерол – 19,6/19,6 мг; фенол - 1,5/1,5 мг; метакрезол - 1,72/1,72 мг; цинк – 32,7/71,9 мкг (у вигляді цинку ацетату – 109,7/241,4 мкг); кислота хлористоводнева/натрію гідроксид (для корекції рН); вода для ін'єкцій – до 1/1 мл; рН розчину 7,6/7,6; 1 шприц-ручка містить 3/3 мл розчину, еквівалентного 300/600 ОД. Шприц-ручка дозволяє ввести до 80/160 ОД за одну ін'єкцію з кроком 1/2 ОД; 1 ОД інсуліну деглудек містить 0,0366 мг безводного безсольового інсуліну деглудек; 1 ОД інсуліну деглудек відповідає 1 ME людського інсуліну, 1 ОД інсуліну детемир або інсуліну гларгіну. Розчин для підшкірного введення, 100 ОД/мл, 200 ОД/мл у попередньо заповнених шприц-ручках ФлексТач®. По 3 мл у картриджах зі скла I гідролітичного класу, закупорених пробками з дисками з галобутилової гуми/поліізопрену з одного боку та поршнями з галобутилової гуми з іншого боку. Картридж запаяний у мультидозову одноразову поліпропіленову шприц-ручку для багаторазових ін'єкцій. Для дозування 100 ОД/мл: по 5 одноразових мультидозових шприц-ручок поміщають у картонну пачку. Для дозування 200 ОД/мл: по 3 одноразових мультидозових шприц-ручки поміщають у картонну пачку.Опис лікарської формиПрозорий безбарвний розчин.Фармакотерапевтична групаГіпоглікемічний.ФармакокінетикаАбсорбція. Надтривала дія інсуліну деглудек обумовлена спеціально створеною структурою його молекули. Після підшкірної ін'єкції відбувається утворення розчинних стабільних мультигексамерів, які створюють депо інсуліну в підшкірно-жировій тканині. Мультигексамери поступово дисоціюють, вивільняючи мономери інсуліну деглудек, внаслідок чого відбувається повільне та пролонговане надходження препарату в кров. Css препарату Тресіба® у плазмі крові досягається через 2-3 дні після введення препарату. Дія інсуліну деглудек протягом 24 годин при його щоденному введенні один раз на добу рівномірно розподіляється між першим і другим 12-годинними інтервалами (AUCGIR0–12h.SS/AUCGIR.t.SS=0,5). Розподіл. Зв'язок інсуліну деглудек з білками плазми (альбумін) становить >99%. Метаболізм. Розпад інсуліну деглудек подібний до такого людського інсуліну; всі метаболіти, що утворюються, є неактивними. Виведення. T1/2 після підшкірної ін'єкції препарату Тресиба® ФлексТач® визначається швидкістю його всмоктування з підшкірної тканини. T1/2 препарату Тресіба® ФлексТач® становить приблизно 25 годин і не залежить від дози. Лінійність. При підшкірному введенні сумарні концентрації в плазмі були пропорційні введеній дозі в діапазоні терапевтичних доз. При безпосередньому зіставленні обох форм випуску препарату Тресиба® ФлексТач® — 100 та 200 ОД/мл отримані дані про відповідність їх біоеквівалентності встановленим вимогам (на основі отриманих даних за AUCIDeg.τ.SS та Cmax.IDeg.SS) Особливі групи пацієнтів Не виявлено відмінностей у фармакокінетичних властивостях препарату Тресіба® ФлексТач® залежно від статі пацієнтів. Пацієнти похилого віку, пацієнти різних етнічних груп, пацієнти з порушенням ниркової функції або печінки. Не виявлено клінічно значущих відмінностей у фармакокінетиці інсуліну деглудек між літніми та молодими пацієнтами, між пацієнтами різних етнічних груп, між пацієнтами з порушеннями функції нирок, печінки та здоровими пацієнтами. Діти та підлітки. Фармакокінетичні властивості інсуліну деглудек у дітей (від 1 до 11 років) та підлітків (від 12 до 18 років) у рівноважному стані були зіставні з такими, що спостерігаються у дорослих пацієнтів з цукровим діабетом типу 1. Однак після одноразового застосування загальна експозиція у дітей та підлітків була вищою, ніж у дорослих пацієнтів з цукровим діабетом типу 1. Дані доклінічних досліджень безпеки. Доклінічні дані, засновані на дослідженнях фармакологічної безпеки, токсичності повторних доз, канцерогенного потенціалу, токсичного впливу на репродуктивну функцію, не виявили будь-якої небезпеки інсуліну деглудек для людини. Співвідношення метаболічної та мітогенної активностей інсуліну деглудек є аналогічним до такого людського інсуліну.ФармакодинамікаПрепарат Тресіба® ФлексТач® — аналог людського інсуліну надтривалої дії, який виробляється методом біотехнології рекомбінантної ДНК з використанням штаму Saccharomyces cerevisiae. Механізм дії. Інсулін деглудек специфічним чином зв'язується з рецептором людського ендогенного інсуліну та взаємодіючи з ним, реалізує свій фармакологічний ефект аналогічно до ефекту людського інсуліну. Гіпоглікемічна дія інсуліну деглудек обумовлена підвищенням утилізації глюкози тканинами після зв'язування інсуліну з рецепторами м'язових та жирових клітин та одночасним зниженням швидкості продукції глюкози печінкою. Препарат Тресіба® ФлексТач® є базальним аналогом людського інсуліну надтривалої дії; після п/к ін'єкції він формує розчинні мультигексамери в підшкірному депо, звідки відбувається безперервне та пролонговане всмоктування інсуліну деглудек у судинне русло, що забезпечує наддовгий, плоский профіль дії та стабільний гіпоглікемічний ефект препарату. Протягом 24-годинного періоду моніторингу гіпоглікемічної дії препарату у пацієнтів, яким доза інсуліну деглудек вводилася один раз на добу, препарат Тресіба® ФлексТач®, на відміну від інсуліну гларгін, продемонстрував рівномірний Vd між дією у перший та другий 12-годинні періоди (AUCGIR0 -12h.SS/AUCGIRtotal.SS = 0,5). 24-годинний середній профіль швидкості інфузії глюкози Css інсуліну деглудек 100 ОД/мл 0,6 ОД/кг (дослідження 1987) Тривалість дії препарату Тресіба® ФлексТач® становить понад 42 години в межах терапевтичного діапазону доз. Css препарату в плазмі досягається через 2-3 дні після введення препарату. Інсулін деглудек у стані Css демонструє достовірно меншу (у 4 рази) порівняно з інсуліном гларгін варіабельність щоденних профілів гіпоглікемічної дії, яка оцінюється за значенням коефіцієнта варіабельності (CV) для дослідження гіпоглікемічної дії препарату протягом одного інтервалу дозування (UC). та в межах тимчасового періоду від 2 до 24 год (AUCGIR2–24h.SS). Доведено лінійний взаємозв'язок між підвищенням дози препарату Тресиба® ФлексТач® та його загальною гіпоглікемічною дією. Обидві форми випуску препарату Тресиба® ФлексТач® — 100 та 200 ОД/мл демонструють порівняний загальний гіпоглікемічний ефект при введенні кожної з двох дозувань препарату в однаковій сумарній дозі. У дослідженнях не виявлено клінічно достовірної різниці у фармакодинаміці препарату Тресиба® між пацієнтами похилого віку та дорослими пацієнтами молодого віку. Клінічна ефективність та безпека Проведено 11 міжнародних рандомізованих відкритих клінічних досліджень Treat-to-Target (стратегія «лікувати до мети») тривалістю 26 та 52 тижнів, що проводяться у паралельних групах, які включали загалом 4275 пацієнтів (1102 пацієнти з цукровим діабетом типу 1 та 3 цукровим діабетом типу 2), які отримували препарат Тресіба®. Ефективність препарату Тресіба® вивчалася у пацієнтів з цукровим діабетом типу 1, які не отримували до цього інсулін, та цукровим діабетом типу 2, які отримували інсулінотерапію, у фіксованому або гнучкому режимі дозування препарату Тресіба®. Доведено відсутність переваги препаратів порівняння (інсулін детемір та інсулін гларгін) над препаратом Тресіба® щодо зниження показника HbА1с з моменту включення до кінця дослідження. Винятком з'явився препарат ситагліптин, в ході порівняння з яким препарат Тресіба продемонстрував свою статистично значущу перевагу щодо зниження показника HbА1с. Результати клінічного дослідження (стратегія «лікувати до мети») з ініціювання інсулінотерапії у пацієнтів з цукровим діабетом типу 2 продемонстрували зниження на 36% частоти розвитку епізодів підтвердженої нічної гіпоглікемії (визначених як епізоди гіпоглікемії, що виникли в період часу доби між нулем год. , підтверджені результатом вимірювання концентрації глюкози у плазмі крові Результати проспективного мета-аналізу даних, отриманих у ході семи спланованих за принципом «лікувати до мети» клінічних досліджень за участю пацієнтів з цукровим діабетом типів 1 та 2, продемонстрували переваги терапії препаратом Тресіба® щодо нижчої, порівняно з терапією інсуліном гларгін, частоти розвитку у пацієнтів епізодів підтвердженої гіпоглікемії та епізодів підтвердженої нічної гіпоглікемії. Зниження частоти епізодів гіпоглікемії на фоні лікування препаратом Тресіба® було досягнуто при нижчому середньому показнику глюкози плазми крові натще, ніж при лікуванні інсуліном гларгін. Не виявлено клінічно значуще утворення антитіл до інсуліну після лікування препаратом Тресіба® ФлексТач® протягом тривалого періоду часу. У 104-тижневому клінічному дослідженні у 57% пацієнтів з цукровим діабетом типу 2, які отримували лікування препаратом Тресіба® у комбінації з метформіном, було досягнуто цільового показника HbА1с. Додавання ліраглутиду призвело до статистично значущого зниження показника HbА1с (−0,73% при застосуванні ліраглутиду порівняно з −0,4% при застосуванні препарату порівняння, розраховані середні значення) та маси тіла (−3,03 кг у порівнянні з 0, 72 кг (розраховані середні значення). Частота епізодів гіпоглікемії (на один пацієнто-рік експозиції) була статистично значуще нижче при додаванні ліраглутиду порівняно з додаванням одноразової дози інсуліну аспарт (1 у порівнянні з 8,15; відношення: 0,13; 95% ДІ: від 0,08 до 0,21). Діти та підлітки. Ефективність та безпека препарату Тресіба® були вивчені у рандомізованому (1:1) контрольованому клінічному дослідженні у дітей та підлітків із цукровим діабетом типу 1 тривалістю 26 тижнів (n=350) з наступним 26-тижневим періодом продовження (n=280). До групи препарату Тресіба® було включено 43 дитини віком від 1 до 5 років, 70 дітей віком від 6 до 11 років та 61 підліток у віці від 12 до 17 років. При застосуванні препарату Тресиба® один раз на добу було показано подібне зниження показника HbA1с на 52-й тиж і більше виражене зниження показника глюкози в плазмі крові натще (ГПН) щодо вихідних значень порівняно із застосуванням препарату порівняння (інсулін детемир один або два рази) добу).Цей результат був досягнутий при застосуванні препарату Тресіба® у добовій дозі на 30% менше від такого інсуліну детемир. Частота (яви на один пацієнто-рік експозиції) епізодів важкої гіпоглікемії (визначення міжнародного товариства з вивчення цукрового діабету у дітей та підлітків (ISPAD); 0,51 у порівнянні з 0,33), підтвердженої гіпоглікемії (57,71 у порівнянні з 54 ,05) та нічний підтвердженої гіпоглікемії (6,03 у порівнянні з 7,6) була порівнянною при застосуванні препарату Тресіба® та інсуліну детемир. В обох групах лікування у дітей віком від 6 до 11 років частота епізодів підтвердженої гіпоглікемії була вищою, ніж в інших вікових групах. Спостерігалася вища частота епізодів тяжкої гіпоглікемії у дітей віком від 6 до 11 років у групі препарату Тресіба®.Частота епізодів гіперглікемії з кетозом була суттєво нижчою при застосуванні препарату Тресіба® у порівнянні з лікуванням інсуліном детемиром – 0,68 та 1,09 відповідно. Частота виникнення, тип і рівень тяжкості небажаних реакцій у популяції пацієнтів дитячого віку не відрізняються від таких у загальній популяції пацієнтів з цукровим діабетом. Вироблення антитіл зустрічалося рідко і мало клінічного значення. Дані щодо ефективності та безпеки, отримані у підлітків з цукровим діабетом типу 2, були екстраполовані на підставі даних, отриманих у підлітків та дорослих пацієнтів з цукровим діабетом типу 1 та дорослих пацієнтів з цукровим діабетом типу 2. Отримані результати дозволяють рекомендувати препарат Тресіба® для лікування підлітків із цукровим діабетом типу 2.68 та 1,09 відповідно. Частота виникнення, тип і рівень тяжкості небажаних реакцій у популяції пацієнтів дитячого віку не відрізняються від таких у загальній популяції пацієнтів з цукровим діабетом. Вироблення антитіл зустрічалося рідко і мало клінічного значення. Дані щодо ефективності та безпеки, отримані у підлітків з цукровим діабетом типу 2, були екстраполовані на підставі даних, отриманих у підлітків та дорослих пацієнтів з цукровим діабетом типу 1 та дорослих пацієнтів з цукровим діабетом типу 2. Отримані результати дозволяють рекомендувати препарат Тресіба® для лікування підлітків із цукровим діабетом типу 2.68 та 1,09 відповідно. Частота виникнення, тип і рівень тяжкості небажаних реакцій у популяції пацієнтів дитячого віку не відрізняються від таких у загальній популяції пацієнтів з цукровим діабетом. Вироблення антитіл зустрічалося рідко і мало клінічного значення. Дані щодо ефективності та безпеки, отримані у підлітків з цукровим діабетом типу 2, були екстраполовані на підставі даних, отриманих у підлітків та дорослих пацієнтів з цукровим діабетом типу 1 та дорослих пацієнтів з цукровим діабетом типу 2. Отримані результати дозволяють рекомендувати препарат Тресіба® для лікування підлітків із цукровим діабетом типу 2.Вироблення антитіл зустрічалося рідко і мало клінічного значення. Дані щодо ефективності та безпеки, отримані у підлітків з цукровим діабетом типу 2, були екстраполовані на підставі даних, отриманих у підлітків та дорослих пацієнтів з цукровим діабетом типу 1 та дорослих пацієнтів з цукровим діабетом типу 2. Отримані результати дозволяють рекомендувати препарат Тресіба® для лікування підлітків із цукровим діабетом типу 2.Вироблення антитіл зустрічалося рідко і мало клінічного значення. Дані щодо ефективності та безпеки, отримані у підлітків з цукровим діабетом типу 2, були екстраполовані на підставі даних, отриманих у підлітків та дорослих пацієнтів з цукровим діабетом типу 1 та дорослих пацієнтів з цукровим діабетом типу 2. Отримані результати дозволяють рекомендувати препарат Тресіба® для лікування підлітків із цукровим діабетом типу 2.Отримані результати дозволяють рекомендувати препарат Тресіба для лікування підлітків з цукровим діабетом типу 2.Отримані результати дозволяють рекомендувати препарат Тресіба для лікування підлітків з цукровим діабетом типу 2.Показання до застосуванняЦукровий діабет у дорослих, підлітків та дітей старше 1 року.Протипоказання до застосуванняпідвищена індивідуальна чутливість до активної речовини або до будь-якого з допоміжних компонентів препарату; період вагітності, період грудного вигодовування (клінічний досвід застосування препарату у жінок під час вагітності та грудного вигодовування відсутній); дитячий вік до 1 року, т.к. клінічні дослідження в дітей віком до 1 року не проводилися.Вагітність та лактаціяЗастосування препарату Тресіба® ФлексТач® у період вагітності протипоказане, тому що. клінічного досвіду його застосування під час вагітності відсутня. Дослідження репродуктивної функції у тварин не виявили відмінностей між інсуліном деглудек та людським інсуліном за показниками ембріотоксичності та тератогенності. Застосування препарату Тресіба® ФлексТач® у період грудного вигодовування протипоказане, тому що симптоми інфекції не рекомендуються. клінічний досвід його застосування у жінок, що годують, відсутній. Дослідження на тваринах показали, що у щурів інсулін деглудек виділяється з грудним молоком, концентрація препарату у грудному молоці нижча, ніж у плазмі крові. Невідомо, чи виділяється інсулін деглудек із грудним молоком жінок. Не очікується поява метаболічних ефектів у новонароджених дітей та дітей, які перебувають на грудному вигодовуванні. Фертильність. У дослідженнях на тваринах не виявлено несприятливий вплив інсуліну деглудек на фертильність.Побічна діяНайчастішим побічним ефектом, про який повідомлялося під час лікування інсуліном деглудек, є гіпоглікемія. Всі побічні ефекти, що представлені нижче, засновані на даних, отриманих в ході клінічних досліджень, розподілені по групам відповідно до MedDRA та систем органів. Частота розвитку побічних ефектів визначається як: дуже часто (≥1/10); часто (≥1/100 до З боку імунної системи: рідко – реакції гіперчутливості, кропив'янка. З боку обміну речовин та харчування: дуже часто – гіпоглікемія. З боку шкіри та підшкірних тканин: нечасто – ліподистрофія. Загальні розлади та порушення у місці введення: часто — реакції у місці введення; нечасто - периферичні набряки. Опис окремих побічних реакцій Порушення імунної системи. При застосуванні препаратів інсуліну можливий розвиток алергічних реакцій. Алергічні реакції негайного типу на препарат інсуліну або допоміжні компоненти, що входять до його складу, можуть потенційно загрожувати життю пацієнта. При застосуванні препарату Тресіба® ФлексТач® реакції гіперчутливості (в т.ч. набряк язика або губ, діарея, нудота, відчуття втоми та свербіж шкіри) та кропив'янка були відмічені рідко. Гіпоглікемія. Може розвинутись, якщо доза інсуліну надто висока по відношенню до потреби пацієнта в інсуліні. Тяжка гіпоглікемія може призводити до втрати свідомості та/або судом, тимчасового або незворотного порушення функції головного мозку аж до летального результату. Симптоми гіпоглікемії, як правило, розвиваються раптово. Вони включають: холодний піт, блідість шкірних покривів, підвищену стомлюваність, нервозність або тремор, почуття тривоги, незвичайну втому або слабкість, порушення орієнтації, зниження концентрації уваги, сонливість, виражене почуття голоду, порушення зору, головний біль, нудоту, відчуття серцебиття. Ліподистрофія (в т.ч. ліпогіпертрофія, ліпоатрофія) може розвиватися у місці ін'єкції. Дотримання правил зміни місця ін'єкції межах однієї анатомічної області допомагає скоротити ризик розвитку цієї побічної реакції. Реакції у місці введення. У пацієнтів, які отримували препарат Тресіба® ФлексТач®, відзначалися реакції у місці введення препарату (гематома, біль, місцевий крововилив, еритема, вузлики сполучної тканини, припухлість, зміна забарвлення шкіри, свербіж, подразнення та ущільнення у місці ін'єкції). Більшість реакцій у місці введення незначні і мають тимчасовий характер і зазвичай зникають при продовженні лікування. Діти та підлітки. Препарат Тресиба® застосовували у дітей та підлітків віком до 18 років для дослідження фармакокінетичних властивостей. У довгостроковому дослідженні у дітей віком від 1 до 18 років було продемонстровано безпеку та ефективність. Частота виникнення, тип і рівень тяжкості небажаних реакцій у популяції пацієнтів дитячого віку не відрізняються від таких у загальній популяції пацієнтів з цукровим діабетом. Особливі групи пацієнтів У ході клінічних досліджень жодних відмінностей щодо частоти, типу або тяжкості побічних реакцій між пацієнтами похилого віку та пацієнтами з порушенням функції нирок або печінки та загальною популяцією пацієнтів не виявлено.Взаємодія з лікарськими засобамиЄ ряд ЛЗ, які впливають потреба в інсуліні. Потребу інсуліну можуть зменшувати: пероральні гіпоглікемічні препарати, агоністи рецепторів ГПП-1, інгібітори МАО, неселективні бета-адреноблокатори, інгібітори АПФ, саліцилати, анаболічні стероїди та сульфонаміди. Потреба в інсуліні можуть збільшувати: пероральні гормональні контрацептивні засоби, тіазидні діуретики, кортикостероїди, тиреоїдні гормони, симпатоміметики, соматропін і даназол. Бета-адреноблокатори можуть маскувати симптоми гіпоглікемії. Октреотид/ланреотид може підвищувати, так і знижувати потребу організму в інсуліні. Етанол (алкоголь) може посилювати, так і зменшувати гіпоглікемічний ефект інсуліну. Несумісність. Деякі лікарські речовини при додаванні до препарату Тресіба® ФлексТач® можуть спричинити його руйнування. Препарат Тресиба® ФлексТач® не можна додавати до інфузійних розчинів. Не можна змішувати препарат Тресіба® ФлексТач® з іншими лікарськими засобами.Спосіб застосування та дозиП/к, 1 раз на день у будь-який час доби, але краще вводити препарат в один і той же час щодня. Препарат Тресіба® ФлексТач® є аналогом інсуліну надтривалої дії. У пацієнтів з цукровим діабетом типу 2 препарат Тресіба® ФлексТач® може застосовуватися як у вигляді монотерапії, так і у комбінації з ПГГП, агоністами рецепторів ГПП-1 або болюсним інсуліном (див. «Фармакодинаміка»). Пацієнтам з цукровим діабетом типу 1 призначають препарат Тресіба® ФлексТач® у поєднанні з інсуліном короткої/ультракороткої дії, для покриття потреби у прандіальному інсуліні. Доза препарату Тресиба® ФлексТач® повинна визначатися індивідуально відповідно до потреб пацієнта. Для оптимізації контролю глікемії рекомендується проводити корекцію дози препарату на підставі показників глюкози у плазмі натще. Як і при застосуванні будь-яких препаратів інсуліну, корекція дози препарату Тресиба® ФлексТач® може бути також необхідною при посиленні фізичної активності пацієнта, зміні його звичайної дієти або при супутньому захворюванні. Початкова доза препарату Тресіба® ФлексТач® Пацієнти з цукровим діабетом типу 2. Початкова щоденна доза препарату Тресиба® ФлексТач® становить 10 ОД, з наступним підбором індивідуальної дози препарату. Пацієнти з цукровим діабетом типу 1. Препарат Тресіба® ФлексТач® призначають один раз на добу у поєднанні з прандіальним інсуліном, який вводять разом з їдою, з наступним підбором індивідуальної дози препарату. Переведення з інших препаратів інсуліну Рекомендується ретельний контроль концентрації глюкози в крові під час перекладу та у перші тижні призначення нового препарату. Можливо, потрібна корекція супутньої гіпоглікемічної терапії (дози та часу введення препаратів інсуліну короткої та ультракороткої дії або інших одночасно застосовуваних гіпоглікемічних препаратів). Пацієнти з цукровим діабетом типу 2. При переведенні на препарат Тресіба® ФлексТач® пацієнтів з цукровим діабетом типу 2, які перебувають на базальному або базис-болюсному режимі інсулінотерапії, або режимі терапії готовими сумішами інсуліну/самостійно змішаними інсулінами®® розраховувати на підставі дози базального інсуліну, яку пацієнт отримував до його переведення на новий тип інсуліну, за принципом «одиниця на одиницю», а потім коригувати відповідно до індивідуальних потреб пацієнта. Пацієнти з цукровим діабетом типу 1. У більшості пацієнтів з цукровим діабетом типу 1 при переході з будь-якого базального інсуліну на препарат Тресіба® ФлексТач® використовується принцип «одиниця на одиницю» на підставі дози базального інсуліну, яку пацієнт отримував до переходу, потім дозу коригують у відповідно до його індивідуальних потреб. У пацієнтів із цукровим діабетом типу 1, які на момент переведення на терапію препаратом Тресіба® ФлексТач® перебували на інсулінотерапії базальним інсуліном у режимі дворазового щоденного введення, або у пацієнтів із показником HbA1c Застосування препарату Тресіба® у комбінації з агоністами рецепторів ГПП-1 у пацієнтів з цукровим діабетом типу 2. При додаванні препарату Тресіба® для лікування агоністами рецепторів ГПП-1 рекомендована початкова добова доза дорівнює 10 ОД з наступною індивідуальною корекцією дози. При додаванні агоністів рецепторів ГПП-1 до лікування препаратом Тресіба® рекомендується знизити дозу препарату Тресіба® на 20% для мінімізації ризику розвитку гіпоглікемії. Згодом дозу слід скоригувати. Гнучкий режим дозування Виходячи з потреб пацієнта, препарат Тресіба® ФлексТач® дозволяє змінювати час його введення. При цьому інтервал між ін'єкціями повинен бути не менше 8 годин. Тим пацієнтам, які забувають вчасно ввести дозу інсуліну, рекомендується ввести дозу, як тільки вони виявили, а потім повернутися до свого звичного часу щоденного одноразового введення препарату. Препарат Тресіба® ФлексТач® 100 та 200 ОД/мл. Препарат Тресіба® ФлексТач® представлений у двох дозах. Для обох дозування набір необхідної дози препарату здійснюють в одиницях. Однак, крок дози відрізняється між двома дозуваннями препарату Тресиба® ФлексТач®. Тресиба® ФлексТач®, 100 ОД/мл дозволяє вводити дози від 1 до 80 ОД із кроком 1 ОД в одній ін'єкції. Тресиба® ФлексТач®, 200 ОД/мл дозволяє вводити дози від 2 до 160 ОД з кроком 2 ОД в одній ін'єкції. Доза інсуліну міститься у вдвічі меншому обсязі розчину порівняно з препаратами базальних інсулінів 100 ОД/мл. Лічильник дози показує кількість одиниць незалежно від дозування; не потрібно проводити перерахунок дози при переведенні пацієнтів на нове дозування. Особливі групи пацієнтів Пацієнти похилого віку (старше 65 років). Препарат Тресиба® ФлексТач® може застосовуватися у пацієнтів похилого віку. Слід ретельно контролювати концентрацію глюкози крові та коригувати дозу інсуліну індивідуально. Недостатність функції нирок та печінки. Препарат Тресіба® ФлексТач® може застосовуватись у пацієнтів з недостатністю функції нирок та печінки. Слід ретельно контролювати концентрацію глюкози крові та коригувати дозу інсуліну індивідуально. Діти та підлітки. Препарат Тресіба® можна застосовувати для лікування підлітків та дітей старше 1 року. При переході з базального інсуліну на препарат Тресіба слід у кожному окремому випадку розглянути необхідність зниження дози базального та болюсного інсуліну для мінімізації ризику розвитку гіпоглікемії. Спосіб застосування Препарат Тресіба® ФлексТач® призначений тільки для підшкірного введення. Препарат Тресиба® ФлексТач® не можна вводити внутрішньовенно, т.к. це може призвести до розвитку тяжкої гіпоглікемії. Препарат Тресиба® ФлексТач® не можна вводити внутрішньом'язово, т.к. у цьому випадку всмоктування препарату змінюється. Препарат Тресиба® ФлексТач® не можна використовувати в інсулінових насосах. Препарат Тресиба® ФлексТач® вводиться підшкірно в область стегна, передньої черевної стінки або в область плеча. Слід постійно змінювати місця ін'єкцій у межах однієї анатомічної області, щоб зменшити ризик розвитку ліподистрофії. Препарат Тресіба® ФлексТач® є попередньо заповненою шприц-ручкою, розробленою для використання з одноразовими ін'єкційними голками НовоФайн® або НовоТвіст®. Вказівки щодо застосування препарату ФлексТач® – попередньо заповнена шприц-ручка розроблена для використання з голками НовоФайн® або НовоТвіст® довжиною до 8 мм. Тресиба® ФлексТач®, 100 ОД/мл дозволяє вводити дози від 1 до 80 ОД з кроком 1 ОД. Тресиба® ФлексТач® 200 ОД/мл дозволяє вводити дози від 2 до 160 ОД з кроком 2 ОД. Необхідно суворо дотримуватися вказівок, що містяться в доданій Інструкції із застосування шприц-ручки ФлексТач®. Препарат Тресіба® ФлексТач® та голки призначені лише для індивідуального використання. Забороняється повторне заповнення картриджа шприц-ручки. Не можна застосовувати препарат, якщо розчин перестав бути прозорим та безбарвним. Не можна застосовувати препарат, якщо він був заморожений. Слід викидати голку після кожної ін'єкції. Дотримуватись місцевих вимог до утилізації використаних медичних матеріалів. Необхідно уважно прочитати цю інструкцію перед застосуванням попередньо заповненої шприц-ручки Тресіба® ФлексТач®. Якщо пацієнт не ретельно дотримуватиметься інструкції, він може ввести недостатню або занадто велику дозу інсуліну, що може призвести до занадто високої або занадто низької концентрації глюкози крові. Використовувати шприц-ручку слід лише після того, як пацієнт навчиться нею користуватися під керівництвом лікаря чи медсестри. Необхідно спочатку перевірити маркування на етикетці шприц-ручки, щоб переконатися, що вона містить препарат Тресиба® ФлексТач® 100 ОД/мл/Тресиба® ФлексТач® 200 ОД/мл, а потім уважно вивчити подані нижче ілюстрації, на яких показані деталі та голки. Якщо пацієнт слабкозорий або має серйозні проблеми із зором, і він не може розрізнити цифри на лічильнику дози, не слід використовувати шприц-ручку без сторонньої допомоги. Допомогти такому пацієнту може людина без порушень зору, навчена правильному використанню попередньо заповненої шприц-ручки ФлексТач®. Тресиба® ФлексТач® 100 ОД/мл — попередньо заповнена шприц-ручка, що містить 300 ОД інсуліну деглудек. Максимальна доза, яку пацієнт може встановити, становить 80 ОД з кроком 1 ОД. Тресиба® ФлексТач® 200 ОД/мл – попередньо заповнена шприц-ручка, що містить 600 ОД інсуліну деглудек. Максимальна доза, яку пацієнт може встановити, становить 160 ОД з кроком 2 ОД. Шприц-ручка розроблена для використання з одноразовими голками НовоФайн або НовоТвіст довжиною до 8 мм. Голки не входять до упаковки. Важлива інформація. Звернути увагу на інформацію, зазначену як важливу, це дуже важливо для правильного використання шприц-ручки. I. Підготовка шприц-ручки до використання Перевірити назву та дозування на етикетці шприц-ручки, щоб переконатися, що в ній міститься препарат Тресіба® ФлексТач® 100 ОД/мл/Тресіба® ФлексТач® 200 ОД/мл. Це особливо важливо, якщо пацієнт застосовує інсуліни різного типу. Якщо він помилково введе інший тип інсуліну, концентрація глюкози в крові може бути надто високою або надто низькою. А. Зняти ковпачок із шприц-ручки В. Переконайтеся, що препарат інсуліну в шприц-ручці є прозорим і безбарвним. Подивитися в віконце шкали залишку інсуліну. Якщо препарат каламутний, шприц-ручку не можна використовувати. С. Взяти нову одноразову голку та видалити захисну наклейку D. Надіти голку на шприц-ручку і повернути її, щоб голка щільно трималася на шприц-ручці. Е. Зняти зовнішній ковпачок голки, але не викидати його. Він знадобиться після завершення ін'єкції, щоб правильно зняти голку зі шприц-ручки. F. Зняти та викинути внутрішній ковпачок голки. Якщо пацієнт спробує надягти внутрішній ковпачок назад на голку, він може випадково вколотись. На кінці голки може виникнути крапля інсуліну. Це нормальне явище, проте пацієнт все одно має перевірити надходження інсуліну. Важлива інформація. Для кожної ін'єкції слід використовувати нову голку. Це зменшує ризик зараження, інфікування, витікання інсуліну, закупорки голки та запровадження неправильної дози препарату. Важлива інформація. Ніколи не використовувати голку, якщо вона погнута чи пошкоджена. ІІ. Перевірка надходження інсуліну G. Перед кожною ін'єкцією слід перевіряти надходження інсуліну. Це допоможе пацієнту переконатись, що доза інсуліну введена повністю. Набрати 2 ОД препарату поворотом дози селектора. Переконатись, що лічильник дози показує «2». H. Тримаючи шприц-ручку голкою вгору, кілька разів злегка постукати верхньою частиною шприц-ручки кінчиком пальця, щоб бульбашки повітря перемістилися вгору. I. Натисніть пускову кнопку та утримуйте її в цьому положенні, доки лічильник дози не повернеться до «0». "0" повинен стояти навпроти вказівника дози. На кінці голки має з'явитися крапля інсуліну. На кінці голки може залишатися маленька бульбашка повітря, але вона не буде введена при ін'єкції. Якщо крапля інсуліну на кінці голки не з'явилася, повторити операції IIG-II I, але не більше 6 разів. Якщо крапля інсуліну не з'явилася, змінити голку і ще раз повторити операції IIG–II I. Якщо крапля інсуліну на кінці голки так і не з'явилася, не застосовуйте цю шприц-ручку. Використовуйте нову шприц-ручку. Важлива інформація. Перед кожною ін'єкцією слід переконатися, що на кінці голки з'явилася крапля інсуліну. Це гарантує надходження інсуліну. Якщо крапля інсуліну не з'явилася, доза не буде введена, навіть якщо лічильник дози рухатиметься. Це може вказувати на те, що голка закупорена або пошкоджена. Важлива інформація. Перед кожною ін'єкцією необхідно перевіряти надходження інсуліну. Якщо пацієнт не перевірятиме надходження інсуліну, він може ввести недостатню дозу інсуліну або не ввести його зовсім, що може призвести до занадто високої концентрації глюкози крові. ІІІ. Встановлення дози J. Перед початком ін'єкції слід переконатися, що лічильник дози встановлено в положення «0». "0" повинен стояти навпроти вказівника дози. Повертанням селектора дози встановити необхідну дозу, призначену лікарем. Максимальна доза, яку пацієнт може встановити, становить 80 або 160 ОД (для препарату Тресіба® ФлексТач® 100 ОД/мл та Тресіба® ФлексТач® 200 ОД/мл відповідно). Якщо встановлено неправильну дозу, пацієнт може повернути селектор дози вперед або назад, доки не встановить правильну дозу. Селектор дози визначає кількість одиниць. Тільки лічильник дози та покажчик дози показують кількість одиниць інсуліну в набраній дозі. Максимальна доза, яку пацієнт може встановити, становить 80 або 160 ОД (для препарату Тресіба® ФлексТач® 100 ОД/мл та Тресіба® ФлексТач® 200 ОД/мл відповідно). Якщо залишок інсуліну в шприц-ручці менший за 80 або 160 ОД (для препарату Тресіба® ФлексТач® 100 ОД/мл та Тресіба® ФлексТач® 200 ОД/мл відповідно), лічильник дози зупиниться на кількості одиниць інсуліну, яка залишилася у шприц-ручці. При кожному повороті селектора дози лунають клацання, звук клацань залежить від того, у який бік обертається селектор дози (вперед, назад або якщо набрана доза перевищує кількість одиниць інсуліну, що залишилися в шприц-ручці). Не слід рахувати ці клацання. Важлива інформація. Перед кожною ін'єкцією необхідно перевіряти, скільки одиниць інсуліну пацієнт набрав за лічильником дози та вказівником дози. Не рахувати клацання шприц-ручки. Якщо пацієнт встановить та введе неправильну дозу, концентрація глюкози в крові може стати занадто високою або занадто низькою. Шкала залишку інсуліну показує приблизну кількість інсуліну, що залишився в шприц-ручці, тому її не можна використовувати для відмірювання дози інсуліну IV. Введення інсуліну Ввести голку під шкіру, використовуючи техніку ін'єкцій, рекомендовану лікарем або медсестрою. Переконайтеся, що лічильник дози знаходиться в полі зору пацієнта. Не слід торкатися лічильника дози пальцями. Це може перервати ін'єкцію. Натиснути пускову кнопку до упору та утримувати її в цьому положенні, доки лічильник дози не покаже «0». «0» повинен знаходитися напроти вказівника дози, при цьому пацієнт може почути або відчути клацання. Після ін'єкції залишити голку під шкірою не менше ніж 6 с, щоб переконатися, що відбулося введення повної дози інсуліну. L. Витягти голку з-під шкіри, потягнувши шприц-ручку вгору. Якщо в місці ін'єкції з'явилася кров, притиснути до місця уколу ватний тампон. Не масажувати місце уколу. Після ін'єкції пацієнт може побачити краплю інсуліну на кінці голки. Це нормально та не впливає на дозу препарату, яка введена. Важлива інформація. Завжди звірятися зі показаннями лічильника дози, щоб знати, скільки одиниць інсуліну введено. Лічильник дози покаже точну кількість одиниць. Не рахувати кількість клацань шприц-ручки. Після ін'єкції утримувати пускову кнопку, доки лічильник дози не повернеться до «0». Якщо лічильник дози зупинився до того, як показав "0", повна доза інсуліну не була введена, що може призвести до надто високої концентрації глюкози у крові. V. Після завершення ін'єкції M. Покласти зовнішній ковпачок голки на плоску поверхню, ввести кінець голки всередину ковпачка, не торкаючись його голки. N. Коли голка увійде в ковпачок, обережно вдягнути ковпачок на голку. Відгвинтити голку і викинути її, дотримуючись запобіжних заходів. О. Після кожної ін'єкції надягати на шприц-ручку ковпачок, щоб захистити інсулін, що міститься в ній, від впливу світла. Викидати голку після кожної ін'єкції. Це зменшує ризик зараження, інфікування, витікання інсуліну, закупорки голки та запровадження неправильної дози препарату. Якщо голка буде закупорена, пацієнт зможе ввести собі інсулін. Викидати використану шприц-ручку з від'єднаною голкою, відповідно до рекомендацій, даних лікарем, медсестрою, фармацевтом або відповідно до місцевих вимог. Важлива інформація. Ніколи не намагайтеся надягти внутрішній ковпачок назад на голку. Пацієнт може вколотись. Важлива інформація. Після кожної ін'єкції завжди видаляти голку та зберігати шприц-ручку з від'єднаною голкою. Це зменшує ризик зараження, інфікування, витікання інсуліну, закупорки голки та запровадження неправильної дози препарату. VI. Скільки інсуліну лишилося? P. Шкала залишку інсуліну показує приблизну кількість інсуліну, що залишилася у шприц-ручці. R. Щоб точно дізнатися, скільки інсуліну залишилося в шприц-ручці, необхідно використовувати лічильник дози: обертати селектор дози, доки лічильник дози не зупиниться. Якщо лічильник дози показує цифру 80 або 160 (для препарату Тресіба® ФлексТач® 100 ОД/мл та Тресіба® ФлексТач® 200 ОД/мл відповідно), це означає, що в шприц-ручці залишилося як мінімум 80 або 160 ОД інсуліну (для препарату Тресіба® ФлексТач® 100 ОД/мл та Тресіба® ФлексТач® 200 ОД/мл відповідно). Якщо лічильник дози показує менше 80 або 160 (для препарату Тресіба® ФлексТач® 100 ОД/мл та Тресіба® ФлексТач® 200 ОД/мл відповідно), це означає, що в шприц-ручці залишилася саме та кількість одиниць інсуліну, яка відобразилася на лічильнику дози. Повертати селектор дози у зворотному напрямку, доки лічильник дози не покаже «0». Якщо інсуліну, що залишився в шприц-ручці, не вистачає для введення повної дози, можна ввести необхідну дозу за дві ін'єкції за допомогою двох шприц-ручок. Важлива інформація Необхідно бути дуже уважним для обчислення залишку необхідної дози інсуліну. Якщо у пацієнта є сумніви, краще ввести повну дозу інсуліну за допомогою нової шприц-ручки. Якщо пацієнт помилиться в розрахунках, він може ввести недостатню дозу або надто велику дозу інсуліну, що може призвести до того, що концентрація глюкози може стати занадто високою або низькою. Завжди слід носити шприц-ручку із собою. Завжди слід носити із собою запасну шприц-ручку та нові голки на випадок їхньої втрати або пошкодження. Зберігати шприц-ручку та голки в недоступному для всіх, особливо для дітей, місці. Ніколи не передавати власну шприц-ручку пацієнта та голки до неї іншим особам. Це може призвести до перехресного інфікування. Ніколи не передавати власну шприц-ручку пацієнта та голки до неї іншим особам. Препарат може завдати шкоди здоров'ю. Особи, які здійснюють догляд за хворим, повинні звертатися з використаними голками з особливою обережністю, щоб зменшити ризик уколів голкою та перехресного інфікування. Догляд за шприц-ручкою Акуратно поводитися зі шприц-ручкою. Недбале або неправильне поводження може спричинити неправильне дозування, що може призвести до надто високої або надто низької концентрації глюкози. Не залишайте шприц-ручку в автомобілі або будь-якому іншому місці, де вона може піддаватися впливу надто високих або надто низьких температур. Захищати шприц-ручку від попадання на неї пилу, забруднень та всіх видів рідин. Не мити шприц-ручку, не занурювати її в рідину і не змащувати. При необхідності шприц-ручку можна очищати вологою тканиною, змоченою м'яким миючим засобом. Не можна кидати або вдаряти шприц-ручку об тверду поверхню. Якщо пацієнт упустив шприц-ручку або сумнівається у її справності, приєднати нову голку та перевірити надходження інсуліну перед тим, як зробити ін'єкцію. Не намагайтеся повторно заповнити шприц-ручку. Порожню шприц-ручку слід викинути. Не намагатися самостійно полагодити шприц-ручку або розібрати її на частини.ПередозуванняСимптоми: певної дози, необхідної для передозування інсуліну не встановлено, проте гіпоглікемія може поступово розвиватися, якщо була введена занадто висока порівняно з потребою пацієнта доза препарату. Лікування: легку гіпоглікемію пацієнт може усунути сам, прийнявши всередину глюкозу або цукромісткі продукти. Тому пацієнтам з цукровим діабетом рекомендується постійно носити із собою цукрозміщуючі продукти. У разі важкої гіпоглікемії, коли пацієнт непритомний, йому слід ввести глюкагон (від 0,5 до 1 мг) внутрішньом'язово або підшкірно (може вводити навчена людина), або внутрішньовенний розчин декстрози (глюкози) (може вводити лише медичний працівник). Також необхідно внутрішньовенно вводити декстрозу у випадку, якщо через 10-15 хв після введення глюкагону пацієнт не приходить до тями. Після відновлення свідомості пацієнту рекомендується прийняти їжу, багату на вуглеводи, для профілактики рецидиву гіпоглікемії.Запобіжні заходи та особливі вказівкиГіпоглікемія. При пропуску їжі або незапланованому інтенсивному фізичному навантаженні у хворого може розвинутися гіпоглікемія. Гіпоглікемія також може розвинутись, якщо введена занадто висока до потреби пацієнта доза інсуліну. У дітей слід бути обережними при доборі доз інсуліну (особливо при базально-болюсному режимі) з урахуванням споживання їжі та фізичної активності для мінімізації ризику розвитку гіпоглікемії. Після компенсації вуглеводного обміну (наприклад, при інтенсифікованій інсулінотерапії), у пацієнтів можуть змінитися типові для них симптоми-провісники гіпоглікемії, про що пацієнти повинні бути поінформовані. Звичайні симптоми-провісники можуть зникати при тривалому перебігу цукрового діабету. Супутні захворювання, особливо інфекційні та супроводжуються лихоманкою, зазвичай підвищують потребу організму в інсуліні. Корекція дози препарату може також бути потрібна при наявності у пацієнта супутніх захворювань нирок, печінки або порушень функції надниркових залоз, гіпофізу або щитовидної залози. Як і при застосуванні інших препаратів базального інсуліну, відновлення після гіпоглікемії при застосуванні препарату Тресіба ФлексТач може затримуватися. Гіперглікемія. Недостатня доза препарату або припинення лікування може спричинити розвиток гіперглікемії або діабетичного кетоацидозу. Крім того, супутні захворювання, особливо інфекційні, можуть сприяти розвитку гіперглікемічних станів і відповідно підвищують потребу організму в інсуліні. Як правило, перші симптоми гіперглікемії з'являються поступово протягом декількох годин або днів. До цих симптомів відносяться спрага, прискорене сечовиділення, нудота, блювання, сонливість, почервоніння і сухість шкіри, сухість у роті, втрата апетиту, запах ацетону в повітрі, що видихається. При цукровому діабеті типу 1 без відповідного лікування гіперглікемія призводить до розвитку діабетичного кетоацидозу та може призвести до смерті. Для лікування тяжкої гіперглікемії рекомендується вводити швидкодіючий інсулін. Переклад хворого з інших інсуліну. Переведення хворого на новий тип або препарат інсуліну нової марки або іншого виробника має відбуватися під суворим контролем. При перекладі може бути потрібна корекція дози. Одночасне застосування препаратів групи тіазолідиндіону та препаратів інсуліну. Повідомлялося про випадки розвитку ХСН при лікуванні пацієнтів тіазолідиндіонами у комбінації з препаратами інсуліну, особливо за наявності у таких пацієнтів факторів ризику розвитку ХСН. Слід враховувати цей факт при призначенні пацієнтам комбінованої терапії тіазолідиндіонами та препаратом Тресіба® ФлексТач®. При призначенні такої комбінованої терапії необхідно проводити медичні обстеження пацієнтів щодо виявлення у них ознак і симптомів ХСН, збільшення маси тіла та наявності периферичних набряків. У разі погіршення у пацієнтів симптоматики серцевої недостатності лікування тіазолідиндіонами необхідно припинити. Порушення органу зору. Інтенсифікація інсулінотерапії з різким покращенням контролю вуглеводного обміну може призвести до тимчасового погіршення стану діабетичної ретинопатії, водночас тривале покращення контролю глікемії знижує ризик прогресування діабетичної ретинопатії. Запобігання випадковому переплутуванню препаратів інсуліну. Слід проінструктувати пацієнта про необхідність перед кожною ін'єкцією перевіряти маркування на етикетці, щоб уникнути випадкового введення іншої дози або іншого інсуліну. Перед кожною ін'єкцією пацієнтам слід перевіряти на лічильнику дози кількість одиниць, набраних у шприц-ручку. Таким чином, лише пацієнти, які можуть чітко розрізняти цифри на лічильнику дози, можуть самостійно вводити інсулін. Необхідно поінформувати незрячих пацієнтів або людей з ослабленим зором про те, що їм завжди необхідна допомога осіб, які не мають проблем із зором та навчені роботи зі шприц-ручкою. Антитіла до інсуліну При застосуванні інсуліну можливе утворення антитіл. В окремих випадках при утворенні антитіл може знадобитися корекція дози інсуліну для запобігання випадків гіперглікемії або гіпоглікемії. Вплив на здатність керувати транспортними засобами та механізмами. Здатність пацієнтів до концентрації уваги та швидкість реакції можуть порушуватися під час гіпоглікемії, що може становити небезпеку в тих ситуаціях, коли ця здатність особливо необхідна (наприклад, при керуванні транспортними засобами або механізмами). Пацієнтам необхідно рекомендувати вживати заходів для запобігання розвитку гіпоглікемії при керуванні транспортними засобами. Це особливо важливо для пацієнтів з відсутністю або зниженням вираженості симптомів-провісників гіпоглікемії, що розвивається, або частими епізодами гіпоглікемії. У цих випадках слід розглянути доцільність керування транспортним засобом.Умови відпустки з аптекЗа рецептомВідео на цю тему