Гипогликемические средства Ново Нордиск А/С
474,00 грн
441,00 грн
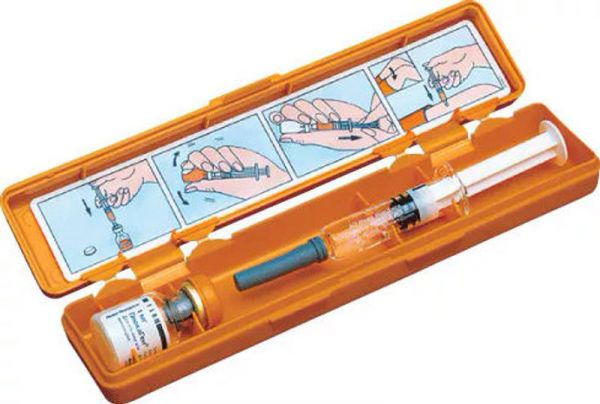
Склад, форма випуску та упаковкаЛіофілізат: Активна речовина: глюкагону гідрохлорид генно-інженерний – 1 мг (відповідає 1 ME); Допоміжні речовини: лактози, гідрогідрат, вода для ін'єкцій. До складу можуть також входити хлористоводнева кислота і/або натрію гідроксид, що використовуються при виробництві препарату для підбору pH. 1 мг ліофілізату у флаконах у комплекті з розчинником у одноразових шприцах по 1 мл. 1 флакон з ліофілізованим порошком (ліофілізатом) та 1 шприц з розчинником у пластиковому пеналі.Опис лікарської формиЛіофілізований порошок або пориста біла маса. При розчиненні в розчиннику, що додається, протягом 1 хв утворюється прозорий безбарвний розчин.Фармакотерапевтична групаГіпоглікемії засіб лікування.ФармакокінетикаШвидкість метаболічного кліренсу глюкагону у людини становить приблизно 10 мл/кг/хв. Глюкагон метаболізується ферментативним шляхом у плазмі крові та в органах, в яких він розподілений. Основні місця метаболізму глюкагону – печінка та нирки, внесок кожного органу в загальну швидкість метаболічного кліренсу становить приблизно 30%. Період напіввиведення глюкагону становить 3-6 хвилин.ФармакодинамікаГлюкаГен® 1 мг ГіпоКіт містить генно-інженерний людський глюкагон - білково-пептидний гормон, фізіологічний антагоніст інсуліну, що бере участь у регуляції вуглеводного обміну. Глюкагон посилює розщеплення глікогену в печінці до глюкозо-6-фосфату (глюкогеноліз), внаслідок чого підвищується концентрація глюкози у крові. Глюкагон неефективний при лікуванні пацієнтів, у печінці яких запаси глікогену виснажені. З цієї причини глюкагон малоефективний або неефективний зовсім при лікуванні пацієнтів натще або пацієнтів з недостатністю надниркових залоз, хронічною гіпоглікемією або гіпоглікемією, викликаної прийомом алкоголю. На відміну від адреналіну, глюкагон не впливає на м'язову фосфорилазу і тому не може сприяти перенесенню вуглеводів з більш багатих на запаси глікогену скелетних м'язів. Глюкагон стимулює виділення катехоламінів. За наявності феохромоцитоми глюкагон може спровокувати виділення пухлиною великої кількості катехоламінів, які спричиняють різке підвищення артеріального тиску. Глюкагон знижує скорочувальну здатність гладкої мускулатури шлунково-кишкового тракту. Дія препарату починається через 1 хвилину після внутрішньовенної ін'єкції, тривалість дії препарату становить 5-20 хвилин залежно від дози та органу. Дія препарату починається через 5-15 хвилин після внутрішньом'язової ін'єкції та триває від 10 до 40 хвилин залежно від дози та органу. При лікуванні тяжкої гіпоглікемії дія глюкагону на вміст глюкози у крові зазвичай спостерігається протягом 10 хвилин.Показання до застосуванняТяжкі гіпоглікемічні стани (низький вміст глюкози в крові), що виникають у хворих на цукровий діабет після ін'єкції інсуліну або прийому таблетованих гіпоглікемічних препаратів. Для пригнічення: Пригнічення моторики органів шлунково-кишкового тракту при проведенні обстеження методами ендоскопії та радіографії.Протипоказання до застосуванняПідвищена індивідуальна чутливість до глюкагону або до будь-якого іншого компонента препарату; гіперглікемія; феохромоцитома.Вагітність та лактаціяГлюкагон не проходить через плацентарний людський бар'єр. Наявні дані про використання глюкагону у вагітних жінок з цукровим діабетом свідчать про відсутність несприятливого впливу як протягом вагітності, так і на здоров'я плода і новонародженого. Глюкагон дуже швидко виводиться з кровотоку (в основному через печінку, Т1/2 = 3-6 хв), таким чином кількість глюкагону, що виділяється з молоком матері після застосування препарату з приводу важкої гіпоглікемії, надзвичайно мала. Оскільки глюкагон руйнується в травному тракті і, отже, не всмоктується у незміненому вигляді, він не має жодного метаболічного впливу на дитину.Побічна діяЧастота виникнення побічних реакцій, пов'язаних із застосуванням препарату ГлюкаГен® 1 мг ГіпоКіт як у клінічних дослідженнях, так і під час постмаркетингового спостереження, представлена нижче. Побічні реакції, які не спостерігалися в ході клінічних досліджень, але про які надходили спонтанні повідомлення, представлені як дуже рідкісні. Повідомлення про побічні реакції при постмаркетинговому використанні дуже рідкісні. Однак для постмаркетингових досліджень характерні занижені дані побічних реакцій, що слід враховувати при інтерпретації результатів про кількість цих реакцій. Кількість епізодів використання препарату оцінюється як 46,9 мільйона за 16 років. Частота побічних реакцій визначалася так: дуже рідко (≤ 1/10000); рідко (>1/10000, ≤ 1/1000); нечасто (>1/1000, ≤ 1/100); часто (>1/100, ≤ 1/10). Порушення з боку імунної системи - дуже рідко: підвищена чутливість, включаючи анафілактичний шок. Порушення з боку шлунково-кишкового тракту: - Часто: нудота; Нечасто: блювання; Рідко: біль у животі. Крім зазначених вище, при діагностичному застосуванні спостерігалися такі побічні реакції: З боку обміну речовин – Нечасто: гіпоглікемія; Дуже рідко: гіпоглікемічна кома. Після діагностичних процедур вона може бути виражена сильніше у пацієнтів натще. З боку серцево-судинної системи – дуже рідко: брадикардія, тахікардія, зниження артеріального тиску (АТ), підвищення АТ. Побічні ефекти з боку серцево-судинної системи спостерігалися тільки в тих випадках, коли ГлюкаГен® 1 мг ГіпоКіт використовувався як допоміжний засіб для проведення ендоскопічних або радіографічних процедур.Взаємодія з лікарськими засобамиНа тлі бета-адреноблокаторів введення препарату ГлюкаГен® 1 мг ГіпоКіт може призвести до вираженої тахікардії та підвищення артеріального тиску. Інсулін: Дія глюкагону протилежне дії інсуліну (інсулін антагоніст глюкагону). Індометацин: при сумісному застосуванні глюкагон може втратити здатність підвищувати вміст глюкози в крові та навіть викликати гіпоглікемію. Варфарин: при сумісному застосуванні глюкагон може посилити дію антикоагулянту варфарину.Спосіб застосування та дозиДля терапії тяжких гіпоглікемічних станів Для приготування ін'єкційного розчину 1 мг (1 ME) ліофілізату розчиняють у 1 мл розчинника. Дорослим та дітям з масою тіла понад 25 кг або старше 6-8 років вводять 1 мг (1 мл, відмітка на шприці 1/1). Дітям з масою тіла менше 25 кг або молодше 6-8 років вводять 0,5 мг (0,5 мл, відмітка на шприці 1/2) підшкірно або внутрішньом'язово. Пацієнт зазвичай приходить до тями протягом 10 хвилин після введення препарату. Після того, як пацієнт прийде до тями, йому необхідно дати їжу, багату на вуглеводи, для запобігання повторному розвитку гіпоглікемії та відновлення глікогену в печінці. Якщо протягом 10 хвилин хворий не прийде до тями, йому необхідно ввести внутрішньовенно декстрозу. Усім пацієнтам із тяжкою формою гіпоглікемії необхідна медична допомога. Для діагностики (пригнічення скорочувальної здатності органів шлунково-кишкового тракту) ГлюкаГен® 1 мг ГіпоКіт повинен вводитися лише медичним персоналом. Після внутрішньовенного введення 0,2-0,5 мг дія препарату починається протягом 1 хвилини і триває від 5 до 20 хвилин, залежно від обстежуваного органу. Після внутрішньом'язового введення 1-2 мг дія препарату починається через 5-15 хвилин і продовжується 10-40 хвилин залежно від обстежуваного органу. Після завершення процедури пацієнту треба дати багаті вуглеводами продукти, якщо це сумісне з діагностичною процедурою, що застосовується. Залежно від методу діагностики та способу введення, доза препарату становить 0,2-2 мг. Звичайна діагностична доза, що використовується для розслаблення м'язів шлунка, цибулини дванадцятипалої кишки, дванадцятипалої кишки та тонкої кишки, становить 0,2-0,5 мг при внутрішньовенному введенні та 1 мг при внутрішньом'язовому введенні. Доза для розслаблення м'язів прямої кишки становить 0,5-0,75 мг при внутрішньовенному введенні та 1-2 мг при внутрішньом'язовому введенні. Приготування розчину для ін'єкції Зняти пластиковий ковпачок з флакона та захисний наконечник голки зі шприца. Проколоти голкою гумовий корок флакона, що містить ГлюкаГен®, і ввести у флакон всю рідину, що знаходиться в шприці. Не виймаючи голки з флакона, обережно струшувати флакон до повного розчинення препарату ГлюкаГен® та утворення прозорого розчину. Потрібно переконатися, що поршень повністю засунутий уперед. Набрати весь розчин у шприц. Слід слідкувати за тим, щоб поршень не вийшов із шприца. Випустити із шприца повітря та зробити ін'єкцію. Утилізуйте залишки невикористаного препарату та упаковки відповідно до місцевих вимог.ПередозуванняПри передозуванні препарату ГлюкаГен® 1 мг ГіпоКіт можлива поява нудоти, блювання, діареї, гіпокаліємії, тахікардії, підвищення артеріального тиску. Лікування симптоматичне. Необхідний постійний контроль рівня калію та, при необхідності, його корекція. Застосування форсованого діурезу та гемодіалізу малоефективне. У разі появи блювоти – регідратація та поповнення втрат калію.Запобіжні заходи та особливі вказівкиПри терапії тяжких гіпоглікемічних станів Після того, як пацієнт прийшов до тями, для запобігання повторному розвитку гіпоглікемії йому слід дати багаті вуглеводами продукти для відновлення запасів глікогену в печінці. Діагностичне застосування Пацієнти, які отримували глюкагон у зв'язку з діагностичними процедурами, можуть відчути дискомфорт, якщо процедури проводилися натще. Є повідомлення про випадки нудоти, гіпоглікемії та зміни АТ у цих ситуаціях. Після завершення діагностичної процедури голодуючим пацієнтам слід дати багатий вуглеводами продукт, якщо це сумісне з діагностичною процедурою, що застосовувалася. Якщо голодування необхідно після обстеження або у разі тяжкої гіпоглікемії, може знадобитися внутрішньовенне введення декстрози (глюкози). Глюкагон є антагоністом інсуліну, і слід бути обережним при застосуванні препарату ГлюкаГен® 1 мг ГіпоКіт у хворих з інсуліномою, а також з глюкагономою. Також слід бути обережним при застосуванні препарату ГлюкаГен® 1 мг ГіпоКіт як допоміжний засіб при проведенні ендоскопічних або радіографічних процедур у пацієнтів з цукровим діабетом або у літніх пацієнтів з патологією серцево-судинної системи. ГлюкаГен® 1 мг ГіпоКіт не слід вводити у вигляді внутрішньовенної інфузії. Флакон з препаратом ГлюкаГен® має пластиковий ковпачок, який слід зняти перед приготуванням розчину. Не можна використовувати приготований розчин, якщо має гелеподібну консистенцію або містить нерозчинені частинки. Вплив на здатність до керування автотранспортом та управління механізмами Дослідження впливу препарату на здатність керувати автомобілем або працювати з механізмами не проводилися. Оскільки є повідомлення про випадки гіпоглікемії після проведення діагностичних процедур, слід уникати керування транспортними засобами доти, доки пацієнт не з'їсть їжу, що містить вуглеводи.Умови відпустки з аптекЗа рецептомВідео на цю тему
6 695,00 грн
363,00 грн
Умови зберіганняУ холодильнику +2+8 градусівУмови відпустки з аптекЗа рецептомВідео на цю тему.
10 336,00 грн
133,00 грн
Склад, форма випуску та упаковкаРозчин для підшкірного введення – 1 мл: активна речовина: ліраглутид – 6 мг (в одній попередньо заповненій шприц-ручці міститься 3 мл розчину, що відповідає 18 мг ліраглутиду); допоміжні речовини: натрію гідрофосфату дигідрат – 1,42 мг; фенол - 5,5 мг; пропіленгліколь - 14 мг; кислота хлористоводнева/натрію гідроксид (для корекції рН); вода для ін'єкцій – до 1 мл. Розчин для підшкірного введення 6 мг/мл. По 3 мл у картриджі зі скла I гідролітичного класу, закупорені дисками з бромбутилової гуми/поліізопрену з одного боку та поршнями з бромбутилової гуми з іншого. Картридж запаяний у пластикову мультидозову одноразову шприц-ручку для багаторазових ін'єкцій. По 5 мультидозових одноразових шприц-ручок у картонну пачку.Опис лікарської формиПрозорий, безбарвний чи майже безбарвний розчин.Фармакотерапевтична групаЗнижувальне масу тіла.ФармакокінетикаВсмоктування. Всмоктування ліраглутиду після підшкірного введення відбувається повільно, час досягнення Tmax – близько 11 години після введення. У пацієнтів з ожирінням (ІМТ 30-40 кг/м2) після введення ліраглутиду в дозі 3 мг середня рівноважна концентрація ліраглутиду (AUCτ/24) досягає приблизно 31 нмоль/л. У діапазоні доз від 0,6 до 3 мг експозиція ліраглутиду збільшується пропорційно дозі. Абсолютна біодоступність ліраглутиду після підшкірного введення становить приблизно 55%. Розподіл. Середній здається Vd після підшкірного введення ліраглутиду в дозі 3 мг становить 20-25 л (у осіб з масою тіла близько 100 кг). Ліраглутид значною мірою пов'язується з білками плазми (>98%). Метаболізм. Протягом 24 годин після введення здоровим добровольцям одноразової дози [3Н]-ліраглутиду головним компонентом у плазмі залишався незмінений ліраглутид. Було виявлено 2 метаболіти (≤9 і ≤5% від рівня загальної радіоактивності у плазмі крові). Виведення. Ліраглутид метаболізується ендогенно подібно до великих білків без участі будь-якого специфічного органу як основного шляху виведення. Після введення дози [3Н]-ліраглутиду незмінений ліраглутид не визначався у сечі або калі. Лише незначна частина введеної радіоактивності у вигляді метаболітів ліраглутиду виводилася нирками або через кишечник (6 та 5% відповідно). Радіоактивні речовини виділяються нирками або через кишечник, в основному, протягом перших 6-8 днів і є 3 метаболітами. Середній кліренс після підшкірного введення ліраглутиду становить приблизно 0,9-1,4 л/год, T1/2 становить приблизно 13 год. Особливі групи пацієнтів Літній вік. Корекція дози з урахуванням віку не потрібна. Згідно з результатами популяційного фармакокінетичного аналізу у пацієнтів з ожирінням або надмірною масою тіла у віці 18-82 років, вік не надавав клінічно значущого впливу на фармакокінетику ліраглутиду при підшкірному введенні в дозі 3 мг. Підлога. На основі даних популяційного фармакокінетичного аналізу, у жінок скоригований за масою тіла кліренс ліраглутиду після підшкірного введення в дозі 3 мг на 24% менше, ніж у чоловіків. На підставі даних відповідної реакції на вплив препарату, корекція дози з урахуванням статі не потрібна. Етнічна приналежність. Згідно з результатами популяційного фармакокінетичного аналізу, в який були включені дані досліджень у пацієнтів з ожирінням або надмірною масою тіла європеоїдної, негроїдної, азіатської та латиноамериканської расових груп, етнічна приналежність не впливала на фармакокінетику ліраглутиду. Маса тіла. Експозиція ліраглутиду зменшується зі збільшенням вихідної маси тіла. Застосування ліраглутиду в дозі 3 мг щодня забезпечує адекватну експозицію в діапазоні маси тіла 60-234 кг, згідно з оцінкою реакції у відповідь на системну експозицію препарату в клінічних дослідженнях. Експозицію ліраглутиду у пацієнтів із масою тіла більше 234 кг не вивчали. Порушення функції печінки. Фармакокінетику ліраглутиду оцінювали у пацієнтів з різним ступенем порушення функції печінки у дослідженні одноразової дози (0,75 мг). Експозиція ліраглутиду була на 23 і 13% менша у пацієнтів з порушенням функції печінки легкого або середнього ступеня тяжкості відповідно порівняно зі здоровими добровольцями. Експозиція була значно меншою (на 44%) у пацієнтів з порушенням функції печінки тяжкого ступеня (>9 балів за класифікацією Child Pugh). Ниркова недостатність. У дослідженні одноразової дози (0,75 мг) експозиція ліраглутиду була меншою у пацієнтів із нирковою недостатністю порівняно з особами з нормальною функцією нирок. Експозиція ліраглутиду була меншою на 33, 14, 27 та 26%, відповідно, у пацієнтів з нирковою недостатністю легкої (Cl креатиніну 50–80 мл/хв), середнього (30–50 мл/хв), тяжкого ступеня (<30 мл/ хв) і у пацієнтів з термінальною стадією ниркової недостатності, які потребують гемодіалізу. Діти. Клінічні дослідження ефективності та безпеки препарату Саксенда® у дітей не проводились.ФармакодинамікаМеханізм дії Діюча речовина препарату Саксенда® — ліраглутид — є аналогом людського глюкагоноподібного пептиду-1 (ГПП-1), вироблений методом біотехнології рекомбінантної ДНК з використанням штаму Saccharomyces cerevisiae, що має 97% гомологічності амінокислотної 1 Ліраглутид зв'язується та активує рецептор ГПП-1 (ГПП-1Р). Ліраглутид стійкий до метаболічного розпаду, його T1/2 з плазми після підшкірного введення становить 13 год. Фармакокінетичний профіль ліраглутиду, що дозволяє вводити його пацієнтам 1 раз на добу, є результатом самоасоціації, внаслідок якої відбувається уповільнене всмоктування препарату; зв'язування із білками плазми; а також стійкості до дипептидилпептидази-4 (ДПП-4) та нейтральної ендопептидази (НЕП). ГПП-1 є фізіологічним регулятором апетиту та споживання їжі. ГПП-1Р виявлено у кількох областях головного мозку, задіяних у регулюванні апетиту. У дослідженнях на тваринах введення ліраглутиду призводило до його захоплення в специфічних галузях головного мозку, включаючи гіпоталамус, де ліраглутид за допомогою специфічної активації ГПП-1Р посилював сигнали про насичення та послаблював сигнали про голод, тим самим призводячи до зменшення маси тіла. Ліраглутид зменшує масу тіла у людини переважно через зменшення маси жирової тканини. Зменшення маси тіла відбувається за рахунок зменшення споживання їжі. Ліраглутид не збільшує 24-годинну витрату енергії. Ліраглутид регулює апетит за допомогою посилення почуття наповнення шлунка та насичення, одночасно послаблюючи почуття голоду та зменшуючи передбачуване споживання їжі. Ліраглутид стимулює секрецію інсуліну і зменшує невиправдано високу секрецію глюкагону глюкозозалежним чином, а також покращує функцію бета-клітин підшлункової залози, що призводить до зниження концентрації глюкози натще і після їди. Механізм зниження концентрації глюкози також включає невелику затримку випорожнення шлунка. У довгострокових клінічних дослідженнях за участю пацієнтів із надмірною масою тіла або ожирінням застосування препарату Саксенда® у поєднанні з низькокалорійною дієтою та посиленою фізичною активністю призводило до значного зниження маси тіла. Вплив на апетит, споживання калорій, витрата енергії, спорожнення шлунка та концентрацію глюкози натще і після їди Фармакодинамічні ефекти ліраглутиду вивчали у 5-тижневому дослідженні за участю 49 пацієнтів з ожирінням (ІМТ — 30–40 кг/м2) без цукрового діабету. Апетит, споживання калорій та витрата енергії Вважається, що зниження маси тіла при застосуванні препарату Саксенда пов'язане з регулюванням апетиту та кількості споживаних калорій. Апетит оцінювали перед та протягом 5 год після стандартного сніданку; необмежене споживання їжі оцінювали під час наступного обіду. Препарат Саксенда® збільшував почуття насичення та наповнення шлунка після їди та зменшував почуття голоду та оцінну кількість передбачуваного споживання їжі, а також зменшував необмежене споживання їжі порівняно з плацебо. При оцінці за допомогою респіраторної камери не відзначалося пов'язаного з терапією збільшення 24-годинної витрати енергії. Випорожнення шлунка Застосування препарату Саксенда® призводило до невеликої затримки спорожнення шлунка протягом першої години після їди, внаслідок чого зменшувалася швидкість підвищення концентрації, а також загальна концентрація глюкози крові після їди. Концентрація глюкози, інсуліну та глюкагону натще та після їди Концентрацію глюкози, інсуліну і глюкагону натще і після їди оцінювали перед і протягом 5 годин після стандартизованого їди. Порівняно з плацебо препарат Саксенда® зменшував концентрацію глюкози крові натще і після їди (AUC0–60 хв) протягом першої години після їди, а також зменшував 5-годинну AUC глюкози та наростаючу концентрацію глюкози (AUC0–300 хв). Крім того, препарат Саксенда® зменшував постпрандіальну концентрацію глюкагону (AUC0–300 хв) та інсуліну (AUC0–60 хв) та наростаючу концентрацію інсуліну (iAUC0–60 хв) після їди порівняно з плацебо. Концентрацію натще і наростаючу концентрацію глюкози та інсуліну також оцінювали під час перорального тесту толерантності до глюкози або без порушення толерантності до глюкози. Порівняно з плацебо препарат Саксенда® зменшував концентрацію натще і наростаючу концентрацію глюкози. Ефект був більш вираженим у пацієнтів із порушенням толерантності до глюкози. Крім того, препарат Саксенда зменшував концентрацію натще і збільшував наростаючу концентрацію інсуліну порівняно з плацебо. Вплив на концентрацію натще і наростаючу концентрацію глюкози у пацієнтів з цукровим діабетом типу 2 з надмірною масою тіла або ожирінням Препарат Саксенда® знижував концентрацію глюкози натще і середню наростаючу постпрандіальну концентрацію глюкози (через 90 хв після їди, середнє значення для 3-х прийомів їжі на добу) порівняно з плацебо. Функція бета-клітин підшлункової залози У клінічних дослідженнях тривалістю до одного року із застосуванням препарату Саксенда® у пацієнтів з надмірною масою тіла або ожирінням та з цукровим діабетом або без такого було продемонстровано покращення та збереження функції бета-клітин підшлункової залози при використанні таких методів вимірювання, як гомеостатична модель оцінки функції бета -клітин (НОМА-В) та співвідношення концентрацій проінсуліну та інсуліну. Клінічна ефективність та безпека Ефективність та безпека застосування препарату Саксенда® для тривалої корекції маси тіла у поєднанні з низькокалорійною дієтою та посиленням фізичної активності була вивчена у 4 рандомізованих подвійних сліпих плацебо-контрольованих дослідженнях (3 дослідження тривалістю 56 тижнів та 1 дослідження тривалістю 32 тижнів). Дослідження включали загалом 5358 пацієнтів 4 різних популяцій: 1) пацієнти з ожирінням або надмірною масою тіла, а також з одним із наступних станів/захворювань: порушення толерантності до глюкози, артеріальна гіпертензія, дисліпідемія; 2) пацієнти з ожирінням або надмірною масою тіла з недостатньо контрольованим цукровим діабетом типу 2 (значення HbА1c у діапазоні 7-10%), до початку дослідження для корекції HbА1c у цих пацієнтів застосовували: дієту та фізичні вправи, метформін,препарати сульфонілсечовини, глітазону окремо або у будь-яких комбінаціях; 3) пацієнти з ожирінням з обструктивним апное середнього або тяжкого ступеня; 4) пацієнти з ожирінням або надмірною масою тіла та супутньою артеріальною гіпертензією або дисліпідемією, які досягли зниження маси тіла не менше ніж на 5% за допомогою низькокалорійної дієти. Маса тіла Більше виражене зниження маси тіла було досягнуто у пацієнтів з ожирінням/надлишковою масою тіла, які отримували препарат Саксенда®, у порівнянні з пацієнтами, які отримували плацебо, у всіх досліджених групах, у т.ч. з наявністю або відсутністю порушення толерантності до глюкози, цукровим діабетом типу 2 та обструктивним апное середнього або тяжкого ступеня. У дослідженні 1 (пацієнти з ожирінням та надмірною масою тіла, з наявністю або відсутністю порушення толерантності до глюкози) зниження маси тіла становило 8% у пацієнтів, які отримували препарат Саксенда у порівнянні з 2,6% у групі плацебо. У дослідженні 2 (пацієнти з ожирінням та надмірною масою тіла з цукровим діабетом типу 2) зниження маси тіла склало 5,9% у пацієнтів, які отримували препарат Саксенда®, порівняно з 2% у групі плацебо. У дослідженні 3 (пацієнти з ожирінням та надмірною масою тіла з обструктивним апное середнього або тяжкого ступеня) зниження маси тіла склало 5,7% у пацієнтів, які отримували препарат Саксенда®, порівняно з 1,6% у групі плацебо. У дослідженні 4 (пацієнти з ожирінням та надмірною масою тіла після попередньої втрати маси тіла не менше ніж 5%) подальше зниження маси тіла становило 6,3% у пацієнтів, які отримували препарат Саксенда®, порівняно з 0,2% у групі плацебо. У дослідженні 4 більша кількість пацієнтів зберегла втрату маси тіла, яка була досягнута до початку лікування препаратом Саксенда® у порівнянні з плацебо (81,4 та 48,9% відповідно). Крім того, у всіх досліджених популяціях більша частина пацієнтів, які отримували препарат Саксенда®, досягли зниження маси тіла не менше ніж на 5% і більш ніж на 10% порівняно з пацієнтами, які отримували плацебо. У дослідженні 1 (пацієнти з ожирінням та надмірною масою тіла з наявністю або відсутністю порушення толерантності до глюкози) зниження маси тіла не менше ніж 5% на 56-й нед терапії відмічено у 63,5% пацієнтів, які отримували препарат Саксенда®, порівняно з 26,6% у групі плацебо. Співвідношення пацієнтів, у яких зниження маси тіла на 56 тижнів терапії досягло більш ніж 10%, становить 32,8% у групі пацієнтів, які отримували препарат Саксенда®, порівняно з 10,1% у групі плацебо. Загалом зниження маси тіла відбулося у приблизно 92% пацієнтів, які отримували препарат Саксенда®, порівняно з приблизно 65% у групі плацебо. Зниження маси тіла після 12 тижнів терапії препаратом Саксенда® Пацієнти з ранньою відповіддю на терапію були визначені як пацієнти, у яких було досягнуто зниження маси тіла не менше ніж на 5% після 12 тижнів терапії (4 тижні збільшення дози та 12 тижнів терапії в дозі 3 мг). У двох дослідженнях (пацієнти з ожирінням або надмірною масою тіла без та з цукровим діабетом типу 2) у 67,5 та 50,4% пацієнтів було досягнуто зниження маси тіла не менше ніж на 5% після 12 тижнів терапії. При продовженні терапії препаратом Саксенда® (до 1 року) 86,2% з цих пацієнтів досягли зниження маси тіла не менше ніж на 5% та 51% – не менше ніж на 10%. Середнє зниження маси тіла цих пацієнтів, які завершили дослідження, становило 11,2% проти вихідним значенням. У пацієнтів, які досягли зниження маси тіла менш ніж на 5% після 12 тижнів терапії в дозі 3 мг і завершили дослідження (1 рік), середнє зниження маси тіла становило 3,8%. Контроль глікемії Терапія препаратом Саксенда® суттєво покращувала глікемічні показники в субпопуляціях з нормоглікемією, порушенням толерантності до глюкози (середнє зниження HbА1с – 0,3%) та цукровим діабетом типу 2 (середнє зниження HbA1c – 1,3%) порівняно з плацебо - 0,1 та 0,4% відповідно). У дослідженні за участю пацієнтів з порушенням толерантності до глюкози цукровий діабет типу 2 розвинувся у меншої кількості пацієнтів, які отримували препарат Саксенда®, порівняно з групою плацебо (0,2 та 1,1% відповідно). У більшої кількості пацієнтів із порушенням толерантності до глюкози спостерігався зворотний розвиток цього стану порівняно з групою плацебо (69,2 та 32,7% відповідно). У дослідженні за участю пацієнтів із цукровим діабетом типу 2 69,2 та 56,5% пацієнтів, які отримували препарат Саксенда®, досягли цільового значення HbА1с Кардіометаболічні параметри У дослідженні за участю пацієнтів з ожирінням або надмірною масою тіла з або без порушення толерантності до глюкози при застосуванні препарату Саксенда® спостерігалося суттєве зниження сАД (на 4,3 проти 1,5 пункту), дАД (на 2,7 проти 1,8 пункту) ), кола талії (на 8,2 проти 4 см) та значна зміна концентрації ліпідів натще (зниження загального Хс на 3,2 проти 0,9%; зниження ЛПНГ на 3,1 проти 0,7%; збільшення ЛПВП на 2, 3 проти 0,5%, зниження тригліцеридів на 13,6 проти 4,8% порівняно з плацебо. Індекс апное-гіпное При застосуванні препарату Саксенда® спостерігалося суттєве зниження порівняно з плацебо тяжкості обструктивного апное, що оцінювалось зі зменшення індексу апное-гіпное (ІАГ) на 12,2 та 6,1 випадків на годину відповідно. Імуногенність З урахуванням потенційних імуногенних властивостей білкових та пептидних лікарських препаратів у пацієнтів можуть з'явитися антитіла до ліраглутиду після терапії препаратом Саксенда®. У клінічних дослідженнях у 2,5% пацієнтів, які отримували препарат Саксенда, з'явилися антитіла до ліраглутиду. Утворення антитіл не спричинило зниження ефективності препарату Саксенда®. Оцінка серцево-судинних явищ Значні небажані серцево-судинні явища (МАСЕ) були оцінені групою зовнішніх незалежних експертів та визначені як несмертельний інфаркт міокарда, несмертельний інсульт та смерть через серцево-судинну патологію. У всіх довгострокових клінічних дослідженнях із застосуванням препарату Саксенда® було відмічено 6 МАСЕ у пацієнтів, які отримували препарат Саксенда®, та 10 МАСЕ – у отримували плацебо. Відношення ризиків та 95% ДІ при порівнянні препарату Саксенда® та плацебо склало 0,31 [0,1; 0,92]. У клінічних дослідженнях 3-ї фази спостерігалося збільшення ЧСС у середньому на 2,5 уд/хв (від 1,6 до 3,6 уд/хв в окремих дослідженнях) у пацієнтів, які отримували препарат Саксенда®. Найбільше збільшення ЧСС спостерігалося після 6 тижнів терапії. Це збільшення було оборотним і зникало після припинення терапії ліраглутидом. Результати оцінки пацієнтів Препарат Саксенда® у порівнянні з плацебо покращував оцінки, що визначаються пацієнтами, за окремими показниками. Було відзначено значне поліпшення загальної оцінки спрощеного опитувальника впливу маси тіла на якість життя (IWQoL-Lite) і всіх шкал опитувальника для оцінки якості життя SF-36, що вказує на позитивний вплив на фізичний та психологічний компонент якості життя. Доклінічні дані щодо безпеки Доклінічні дані, засновані на дослідженнях фармакологічної безпеки, токсичності повторних доз та генотоксичності, не виявили жодної небезпеки для людини. У 2-річних дослідженнях канцерогенності у щурів та мишей були виявлені пухлини С-клітин щитовидної залози, які не призводили до летального результату. Нетоксична доза (NOAEL) у щурів не встановлена. У мавп, які отримували терапію протягом 20 місяців, розвиток цих пухлин не спостерігалося. Результати, отримані в ході досліджень на гризунах, обумовлені тим, що гризуни виявляють особливу чутливість щодо опосередкованого рецептором ГПП-1 не специфічного генотоксичного механізму. Значимість даних для людини є низькою, проте не може бути повністю виключена. Поява інших новоутворень, пов'язаних із терапією, відзначено не було. У дослідженнях на тваринах не виявлено прямого несприятливого ефекту препарату на фертильність, але було відзначено незначне збільшення частоти ранньої ембріональної смерті при застосуванні найвищих доз препарату. Введення ліраглутиду в середині гестаційного періоду викликало зменшення маси тіла матері та зростання плода з невивченим до кінця впливом на ребра у щурів, а у кролів – відхилення у будові скелета. Зростання новонароджених у щурів було знижено під час терапії ліраглутидом, і це зниження зберігалося після закінчення грудного вигодовування у групі, яка отримувала високі дози препарату. Невідомо, чим зумовлено таке зниження зростання новонароджених особин щурів - зниженням споживання калорій материнськими особинами або прямим впливом ГПП-1 на плід/новонароджених.Показання до застосуванняЯк доповнення до низькокалорійної дієти та посиленого фізичного навантаження для тривалого застосування з метою корекції маси тіла у дорослих пацієнтів з ІМТ: ≥30 кг/м2 (ожиріння) або ≥27 кг/м2 таПротипоказання до застосуванняпідвищена чутливість до ліраглутиду або до будь-якого з допоміжних компонентів препарату; медулярний рак щитовидної залози в анамнезі, зокрема. у сімейному; множинна ендокринна неоплазія ІІ типу; тяжка депресія, суїцидальні думки або поведінка, у т.ч. в анамнезі; порушення функції нирок тяжкого ступеня; порушення функції печінки тяжкого ступеня; серцева недостатність III–IV функціонального класу (відповідно до класифікації NYHA); одночасне застосування інших препаратів для корекції маси тіла; одночасне застосування з інсуліном; вторинне ожиріння на фоні ендокринологічних захворювань або розладів харчової поведінки, або на фоні застосування лікарських засобів, які можуть призвести до збільшення маси тіла; запальні захворювання кишечника та діабетичний парез шлунка (досвід застосування препарату Саксенда® у пацієнтів обмежений). Застосування ліраглутиду у таких пацієнтів не рекомендується, оскільки воно пов'язане з транзиторними небажаними реакціями з боку шлунково-кишкового тракту, включаючи нудоту, блювання та діарею; період вагітності; період грудного вигодовування; дитячий вік до 18 років. З обережністю: у пацієнтів з хронічною серцевою недостатністю класу I–II відповідно до класифікації NYHA, порушення функції печінки легкого або середнього ступеня тяжкості, панкреатиту в анамнезі, захворювань щитовидної залози; у пацієнтів віком ≥75 років.Вагітність та лактаціяДані щодо застосування препарату Саксенда у вагітних жінок обмежені. У дослідженнях на тваринах була продемонстрована репродуктивна токсичність (див. Доклінічні дані з безпеки). Потенційний ризик для людини невідомий. Застосування препарату Саксенда у період вагітності протипоказане. При плануванні або настанні вагітності терапію препаратом Саксенда необхідно припинити. Невідомо, чи ліраглутид проникає в грудне молоко людини. У дослідженнях на тваринах було продемонстровано, що проникнення ліраглутиду та структурно близьких метаболітів у грудне молоко є низьким. У доклінічних дослідженнях було продемонстровано пов'язане з терапією уповільнення зростання новонароджених щурів, які перебувають на грудному вигодовуванні. У зв'язку з відсутністю досвіду застосування препарат Саксенда протипоказаний під час грудного вигодовування.Побічна діяПрограма клінічних досліджень препарату Саксенда® складається з 5 завершених клінічних досліджень, у яких взяли участь 5813 пацієнтів з ожирінням або надмірною масою тіла і, як мінімум, з одним пов'язаним з надлишковою масою тіла супутнім захворюванням. В цілому, порушення з боку шлунково-кишкового тракту були найпоширенішими побічними ефектами під час терапії препаратом Саксенда®. Нижче наведено перелік небажаних реакцій, зареєстрованих у ході клінічних досліджень. Небажані реакції розподілені по групам відповідно до систем органів MedDRA та частоти. Частота визначена так: дуже часто (≥1/10); часто (≥1/100 до З боку шлунково-кишкового тракту: дуже часто – нудота, блювання, діарея, запор; часто - сухість у роті, диспепсія, гастрит, гастроезофагеальний рефлюкс, біль у верхніх відділах живота, метеоризм, відрижка, здуття живота; нечасто – панкреатит. З боку імунної системи: рідко – анафілактичні реакції. З боку обміну речовин та харчування: часто – гіпоглікемія; нечасто – дегідратація. Порушення психіки: часто безсоння. З боку нервової системи: часто запаморочення, дисгевзія. Серце: нечасто – тахікардія. З боку печінки та жовчовивідних шляхів: часто – холелітіаз; нечасто – холецистит. З боку шкіри та підшкірних тканин: нечасто – кропив'янка. З боку нирок та сечовивідних шляхів: рідко – гостра ниркова недостатність, порушення функції нирок. Загальні розлади та порушення у місці введення: часто - реакції у місці введення, астенія, стомлюваність; нечасто – нездужання. Опис окремих небажаних реакцій Гіпоглікемія у пацієнтів без цукрового діабету типу 2. У клінічних дослідженнях за участю пацієнтів з надмірною масою тіла або ожирінням без цукрового діабету типу 2, які отримували терапію препаратом Саксенда® у поєднанні з дієтою та фізичними навантаженнями, тяжких гіпоглікемій (вимагають надання допомоги третьою особою) не було. Про симптоми гіпоглікемії повідомляли 1,6% пацієнтів, які отримували препарат Саксенда®, та 1,1% пацієнтів, які отримували плацебо; однак ці випадки не були підтверджені вимірюванням концентрації глюкози крові. Найчастіше відзначалася легка гіпоглікемія. Гіпоглікемія у пацієнтів з цукровим діабетом типу 2. У клінічному дослідженні за участю пацієнтів з надмірною масою тіла або ожирінням та цукровим діабетом типу 2, які отримували терапію препаратом Саксенда® у поєднанні з дієтою та фізичними навантаженнями, випадки тяжкої гіпоглікемії (вимагають надання допомоги) були відзначені у 0,7% пацієнтів, які отримували препарат Саксенда®, і лише у пацієнтів, які одночасно отримували терапію похідними сульфонілсечовини. Також у цій групі пацієнтів підтверджена гіпоглікемія (концентрація глюкози ≤3,9 ммоль/л у поєднанні з симптомами) була відзначена у 43,6% пацієнтів, які отримували препарат Саксенда®, та 27,3% пацієнтів, які отримували плацебо. Серед пацієнтів, які не отримували одночасно сульфонілсечовини, підтверджена гіпоглікемія була відзначена у 15,7% пацієнтів, які отримували препарат Саксенда®,та у 7,6% пацієнтів, які отримували плацебо. Небажані реакції з боку шлунково-кишкового тракту. Більшість реакцій з боку шлунково-кишкового тракту були легким або середнім ступенем тяжкості, минущими і, в більшості випадків, не призводили до припинення терапії. Реакції зазвичай виникали у перші тижні терапії, та їх прояви поступово зменшувалися протягом кількох днів чи тижнів під час продовження терапії. У пацієнтів віком ≥65 років можуть спостерігатися більш виражені прояви небажаних реакцій з боку шлунково-кишкового тракту під час терапії препаратом Саксенда®. У пацієнтів з порушенням функції нирок легкого або середнього ступеня тяжкості (Cl креатиніну ≥30 мл/хв) можуть спостерігатися більш виражені прояви небажаних реакцій з боку шлунково-кишкового тракту під час терапії препаратом Саксенда®. Алергічні реакції. Було відмічено кілька випадків анафілактичних реакцій з такими симптомами, як артеріальна гіпотензія, серцебиття, задишка або периферичні набряки. Анафілактичні реакції потенційно можуть бути загрозливими для життя. Реакції у місці введення. У пацієнтів, які отримували препарат Саксенда, були описані реакції в місці введення. Ці реакції, як правило, були легким, носили транзиторний характер і в більшості випадків зникали при продовженні терапії. Тахікардія. У клінічних дослідженнях тахікардія була відзначена у 0,6% пацієнтів, які отримували препарат Саксенда®, та у 0,1% пацієнтів, які отримували плацебо. Більшість явищ були легким або середнім ступенем тяжкості. Явлення були поодинокими і здебільшого проходили при продовженні терапії препаратом Саксенда®.Взаємодія з лікарськими засобамиОцінка лікарської взаємодії in vitro. Була продемонстрована дуже низька здатність ліраглутиду до фармакокінетичних взаємодій з іншими діючими речовинами, зумовленим метаболізмом у системі цитохрому Р450 (CYP) та зв'язуванням із білками плазми крові. Оцінка лікарської взаємодії in vivo. Невелика затримка спорожнення шлунка при застосуванні ліраглутиду може впливати на всмоктування препаратів, що одночасно застосовуються для прийому внутрішньо. У дослідженнях взаємодії не було продемонстровано якесь клінічно значуще уповільнення всмоктування, тому корекція дози препаратів не потрібна. Дослідження взаємодії проводили із застосуванням ліраглутиду у дозі 1,8 мг. Вплив на швидкість спорожнення шлунка був однаковим при застосуванні ліраглутиду у дозі 1,8 мг та 3 мг (AUC0–300 хв парацетамолу). У кількох пацієнтів, які отримували ліраглутид, було відмічено щонайменше один епізод важкої діареї. Діарея може впливати на всмоктування одночасно застосовуваних лікарських препаратів для внутрішнього застосування. Варфарин та інші похідні кумарину. Досліджень взаємодії не проводили. Клінічно значуща взаємодія з діючими речовинами з низькою розчинністю або з вузьким терапевтичним індексом, таким як варфарин, не може бути виключена. Після початку лікування препаратом Саксенда® у пацієнтів, які отримують варфарин або інші похідні кумарину, рекомендується більш частий контроль MHO. Парацетамол (ацетамінофен). Ліраглутид не змінював загальну експозицію парацетамолу після одноразової дози 1000 мг. Cmax парацетамолу було знижено на 31%, а медіана Tmax збільшено на 15 хв. Корекція дози при супутньому застосуванні парацетамолу не потрібна. Аторвастатин. Ліраглутид не змінював загальну експозицію аторвастатину після застосування одноразової дози аторвастатину 40 мг. Тому корекція дози аторвастатину при застосуванні у поєднанні з ліраглутидом не потрібна. Cmax аторвастатину була знижена на 38%, а медіана Tmax збільшена з 1 до 3 годин при застосуванні ліраглутиду. Гризеофульвін. Ліраглутид не змінював загальну експозицію гризеофульвіну після застосування одноразової дози гризеофульвіну 500 мг. Cmax гризеофульвіну було збільшено на 37%, а медіана Tmax не змінилася. Корекція дози гризеофульвіну та інших сполук з низькою розчинністю та високою проникною здатністю не потрібна. Дігоксин. Застосування одноразової дози дигоксину 1 мг у поєднанні з ліраглутидом призвело до зменшення AUC дигоксину на 16%, зменшення Cmax на 31%. Медіана Tmax збільшилася з 1 до 1,5 год. З урахуванням даних результатів корекція дози дигоксину не потрібна. Лізіноприл. Застосування одноразової дози лізиноприлу 20 мг у поєднанні з ліраглутидом призвело до зменшення AUC лізиноприлу на 15%, зменшення Cmax на 27%. Медіана Tmax лізиноприлу збільшилася з 6 до 8 год. З урахуванням даних результатів корекція дози лізиноприлу не потрібна. Пероральні гормональні контрацептивні засоби. Ліраглутид призводив до зменшення Cmax етинілестрадіолу та левоноргестрелу на 12 і 13% відповідно після застосування одноразової дози перорального гормонального контрацептивного препарату. Tmax обох лікарських речовин на фоні застосування ліраглутиду збільшувався на 1,5 год. Таким чином, не очікується вплив на контрацептивний ефект при сумісному застосуванні з ліраглутидом. Несумісність. Лікарські речовини, додані до препарату Саксенда можуть викликати руйнування ліраглутиду. У зв'язку з відсутністю досліджень сумісності цей лікарський препарат не можна змішувати з іншими лікарськими засобами.Спосіб застосування та дозиП/к. Препарат не можна вводити внутрішньовенно або внутрішньом'язово. Препарат Саксенда® вводять один раз на добу будь-коли, незалежно від їди. Його слід вводити в ділянку живота, стегна чи плеча. Місце та час ін'єкції може бути змінено без корекції дози. Тим не менш, бажано робити ін'єкції приблизно в той самий час доби після вибору найбільш зручного часу. Дози. Початкова доза становить 0,6 мг на добу. Дозу збільшують до 3 мг на добу, додаючи по 0,6 мг з інтервалами не менше 1 тиж для поліпшення шлунково-кишкової переносимості (див. таблицю). Якщо зі збільшенням дози нова погано переноситься пацієнтом протягом 2 тижнів поспіль, слід розглянути питання припинення терапії. Застосування препарату у добовій дозі більше 3 мг не рекомендується. Показники Доза, мг Тижня Збільшення дози протягом 4 тижнів 0,6 1-а 1,2 2-а 1,8 3-тя 2,4 4-та Терапевтична доза 3 Терапію препаратом Саксенда слід припинити, якщо після 12 тижнів застосування препарату в дозі 3 мг на добу втрата в масі тіла склала менше 5% від вихідного значення. Необхідність продовження терапії слід щорічно переглядати. Пропущена доза. Якщо після звичайного часу введення дози пройшло менше 12 годин, пацієнт повинен ввести нову якнайшвидше. Якщо до звичайного часу введення наступної дози залишилося менше 12 годин, пацієнт не повинен вводити пропущену, а відновити введення препарату з наступної запланованої дози. Не слід вводити додаткову або підвищену дозу для компенсації пропущеної. Пацієнти з цукровим діабетом типу 2. Препарат Саксенда не слід застосовувати в комбінації з іншими агоністами рецепторів ГПП-1. На початку терапії препаратом Саксенда® рекомендується зменшити дози одночасно застосовуваних секретагогів інсуліну (таких як препарати сульфонілсечовини) для зменшення ризику розвитку гіпоглікемії. Особливі групи пацієнтів Пацієнти похилого віку (≥65 років). Корекція дози з урахуванням віку не потрібна. Досвід застосування препарату у пацієнтів віком ≥75 років обмежений, застосовувати препарат у таких пацієнтів потрібно з обережністю. Ниркова недостатність. У пацієнтів з порушенням функції нирок легкого або середнього ступеня (Cl креатиніну ≥30 мл/хв) корекція дози не потрібна. Є обмежений досвід застосування препарату Саксенда у пацієнтів з порушенням функції нирок тяжкого ступеня (Cl креатиніну Порушення функції печінки. У пацієнтів з порушенням функції печінки легкого або середнього ступеня тяжкості дози не потрібно. У пацієнтів з порушенням функції печінки легкого або середнього ступеня тяжкості препарат слід застосовувати з обережністю. Застосування препарату Саксенда у пацієнтів з порушенням функції печінки тяжкого ступеня протипоказано. Діти. Застосування препарату Саксенда® у дітей та підлітків віком до 18 років протипоказане через відсутність даних щодо безпеки та ефективності. Перед використанням попередньо заповненої шприц-ручки з препаратом Саксенда слід уважно прочитати цю інструкцію. Використовувати шприц-ручку лише після того, як пацієнт навчився нею користуватися під керівництвом лікаря чи медсестри. Перевірити маркування на етикетці шприц-ручки, щоб переконатися, що вона містить препарат Саксенда® 6 мг/мл, а потім уважно вивчити наведені нижче ілюстрації, на яких показано деталі шприц-ручки та голки. Якщо пацієнт слабкозорий або має серйозні проблеми із зором, і він не може розрізнити цифри на лічильнику дози, не використовувати шприц-ручку без сторонньої допомоги. Допомогти може людина без порушень зору, навчена правильному використанню попередньо заповненої шприц-ручки із препаратом Саксенда®. Попередньо заповнена шприц-ручка містить 18 мг ліраглутиду та дозволяє вибрати дозу 0,6 мг, 1,2 мг, 1,8 мг, 2,4 мг та 3,0 мг. Шприц-ручка Саксенда® розроблена для використання з одноразовими голками НовоФайн® або НовоТвіст® довжиною до 8 мм. Голки не входять до упаковки. Важлива інформація. Звернути увагу на інформацію, зазначену як важливу, це необхідно для безпечного використання шприц-ручки. Попередньо заповнена шприц-ручка із препаратом Саксенда® та голка. I. Підготовка шприц-ручки з голкою для використання Перевірити назву та колірний код на етикетці шприц-ручки, щоб переконатися, що міститься препарат Саксенда®. Це особливо важливо, якщо пацієнт застосовує різні ін'єкційні препарати. Застосування неправильного препарату може бути шкідливим для здоров'я. Зняти ковпачок із шприц-ручки. Переконатись, що розчин у шприц-ручці прозорий та безбарвний. Подивитися у вікно шкали залишку. Якщо препарат каламутний, шприц-ручку не можна використовувати. Взяти нову одноразову голку та видалити захисну наклейку. Одягти голку на шприц-ручку і повернути її, щоб голка щільно трималася на шприц-ручці. Зняти зовнішній ковпачок голки, але не викидати його. Він знадобиться після завершення ін'єкції, щоб безпечно зняти голку. Зняти та викинути внутрішній ковпачок голки. Якщо пацієнт спробує надягти внутрішній ковпачок назад на голку, він може вколотися. На кінці голки може виникнути крапля розчину. Це нормальне явище, проте пацієнт все одно повинен перевірити надходження препарату, якщо використовується нова шприц-ручка вперше. Не слід приєднувати нову голку до того часу, поки пацієнт нічого очікувати готовий зробити ін'єкцію. Важлива інформація. Завжди використовувати нову голку для кожної ін'єкції, щоб уникнути закупорки голки, зараження, інфікування та введення неправильної дози препарату. Ніколи не використовувати голку, якщо вона погнута чи пошкоджена. ІІ. Перевірка надходження препарату Перед першою ін'єкцією за допомогою нової шприц-ручки перевірити надходження препарату. Якщо шприц-ручка вже є у використанні, то перейти до операції III «Встановлення дози». Повертати селектор дози доти, доки в індикаторному вікні символ перевірки надходження препарату (vvw) не порівняється з вказівником дози. Тримати шприц-ручку голкою вгору. Натиснути пускову кнопку та утримувати її в цьому положенні, доки лічильник дози не повернеться до нуля. "0" повинен стояти навпроти вказівника дози. На кінці голки має з'явитися крапля розчину. На кінці голки може залишатися невелика крапля, але вона не буде введена при ін'єкції. Якщо крапля розчину на кінці голки не з'явилася, необхідно повторити операцію ІІ "Перевірка надходження препарату", але не більше 6 разів. Якщо крапля розчину не з'явилася, слід поміняти голку та повторити цю операцію. Якщо крапля розчину препарату Саксенда так і не з'явилася, слід утилізувати шприц-ручку та використовувати нову. Важлива інформація. Перед використанням нової шприц-ручки вперше необхідно переконатися, що на кінці голки з'явилася крапля розчину. Це гарантує надходження препарату. Якщо крапля розчину не з'явилася, препарат не буде введений, навіть якщо лічильник дозування рухатиметься. Це може вказувати на те, що голка закупорена або пошкоджена. Якщо пацієнт не перевірить надходження препарату перед першою ін'єкцією за допомогою нової шприц-ручки, він може не ввести необхідну дозу і очікуваний ефект препарату Саксенда не буде досягнутий. ІІІ. Встановлення дози Повертати селектор дози, щоб набрати необхідну пацієнтові дозу (0,6 мг, 1,2 мг, 1,8 мг, 2,4 мг або 3 мг). Якщо дозу було встановлено неправильно, повертайте селектор дози вперед або назад, доки не буде встановлено правильну дозу. Максимальна доза, яку можна встановити становить 3 мг. Селектор дози дає змогу змінити дозу. Тільки лічильник дози та покажчик дози покажуть кількість мг препарату у вибраній пацієнтом дозі. Пацієнт може набрати до 3 мг на дозу. Якщо у шприц-ручці, що використовується, міститься менше 3 мг, лічильник дози зупиниться перш, ніж у віконці з'явиться 3. При кожному повороті селектора дози лунають клацання, звук клацань залежить від того, в яку сторону обертається селектор дози (вперед, назад або якщо набрана доза перевищує кількість мг препарату, що залишилася в шприц-ручці). Не слід рахувати ці клацання. Важлива інформація. Перед кожною ін'єкцією перевіряти, скільки препарату пацієнт набрав за лічильником і вказівником дози. Не слід рахувати клацання шприц-ручки. Шкала залишку показує приблизну кількість розчину, що залишився в шприц-ручці, тому її не можна використовувати для відмірювання дози препарату. Не намагатись вибрати інші дози, крім доз 0,6; 1,2; 1,8; 2,4 або 3 мг. Цифри в індикаторному вікні повинні знаходитись навпроти вказівника дозування - таке положення гарантує, що пацієнт отримає правильну дозу препарату. Скільки препарату лишилося? Шкала залишку показує приблизну кількість препарату, що залишився в шприц-ручці Щоб точно визначити скільки препарату залишилося, використовувати лічильник дози. Повертати селектор дози до зупинки лічильника. Якщо він показує «3», у шприц-ручці залишилося щонайменше 3 мг препарату. Якщо лічильник дози показує менше "3", це означає, що в шприц-ручці залишилася недостатня кількість препарату, щоб ввести повну дозу 3 мг. Якщо необхідно ввести більше препарату, ніж залишилося в шприц-ручці Тільки якщо пацієнта навчили лікаря або медсестру, він може розділити дозу препарату між двома шприц-ручками. Використовувати калькулятор, щоб спланувати дози, як рекомендовано лікарем або медсестрою. Важлива інформація. Необхідно бути дуже уважним, щоб розрахувати дозу. Якщо немає впевненості, як правильно розділити дозу при використанні двох шприц-ручок, слід встановити та ввести повну дозу за допомогою нової шприц-ручки. IV. Введення препарату Ввести голку під шкіру, використовуючи техніку ін'єкцій, рекомендовану лікарем або медсестрою. Переконайтеся, що лічильник дози знаходиться в полі зору пацієнта. Не торкатися лічильника дози пальцями - це може перервати ін'єкцію. Натиснути пускову кнопку до упору та утримувати її в цьому положенні, доки лічильник дози не покаже «0». "0" повинен знаходитися точно напроти вказівника дози. При цьому пацієнт може почути чи відчути клацання. Утримувати голку під шкірою після того, як лічильник дози повернувся до нульової позначки, і повільно рахувати до 6. Якщо пацієнт витягне голку з-під шкіри раніше, він побачить, як препарат випливає з голки. У цьому випадку буде введено неповну дозу препарату. Витягти голку з-під шкіри. Якщо в місці ін'єкції з'явилася кров, притиснути до місця уколу ватний тампон. Не масажувати місце уколу. Після завершення ін'єкції можна побачити краплю розчину на кінці голки. Це нормально та не впливає на дозу препарату, яка була введена. Важлива інформація. Завжди звірятися з показаннями лічильника дози, щоб знати, скільки препарату Саксенда® введено. Утримувати пускову кнопку, доки лічильник дози не покаже «0». Як виявити закупорку чи пошкодження голки? Якщо після довгого натискання на пускову кнопку на лічильнику дози не з'являється "0", це може означати закупорку або пошкодження голки. Це означає, що пацієнт не отримав препарат, навіть якщо лічильник доз змінив положення вихідної дози, яку пацієнт встановив. Що робити із закупореною голкою? Зняти голку як описано в операції V «Після завершення ін'єкції» та повторити всі кроки, починаючи з операції I «Підготовка шприц-ручки та нової голки». Слід переконатися, що встановлено необхідну пацієнтові дозу. Ніколи не торкатися лічильника дози під час введення препарату. Це може перервати ін'єкцію. V. Після завершення ін'єкції Поклавши зовнішній ковпачок голки на плоску поверхню, ввести кінець голки всередину ковпачка, не торкаючись його голки. Коли голка увійде в ковпачок, обережно вдягнути ковпачок на голку. Відгвинтити голку і викинути її, дотримуючись запобіжних заходів, згідно з інструкцією лікаря або медсестри. Після кожної ін'єкції надягати на шприц-ручку ковпачок, щоб захистити розчин, що міститься в ній, від впливу світла. Завжди необхідно викидати голку після кожної ін'єкції, щоб забезпечити комфортну ін'єкцію та уникнути закупорки голок. Якщо голка буде закупорена, пацієнт не зможе запровадити препарат. Викидати порожню шприц-ручку з від'єднаною голкою, відповідно до рекомендацій, даних лікарем, медсестрою, фармацевтом або відповідно до місцевих вимог. Важлива інформація. Щоб уникнути випадкових уколів голкою, ніколи не намагайтеся надягти внутрішній ковпачок назад на голку. Завжди видаляти голку зі шприц-ручки після кожної ін'єкції. Це дозволить уникнути закупорки голки, зараження, інфікування, витікання розчину та запровадження неправильної дози препарату. Зберігати шприц-ручку та голки в недоступному для всіх, особливо для дітей місці. Ніколи не передавати свою шприц-ручку з препаратом та голки до неї іншим особам. Особи, які здійснюють догляд за хворим, повинні звертатися з використаними голками з особливою обережністю, щоб уникнути випадкових уколів та перехресного інфікування. Догляд за шприц-ручкою Не залишати шприц-ручку в автомобілі або будь-якому іншому місці, де вона може піддаватися впливу надто високих або надто низьких температур. Не застосовувати препарат Саксенда, якщо він був заморожений. У цьому випадку очікуваного ефекту від застосування препарату не буде досягнуто. Захищати шприц-ручку від попадання на неї пилу, забруднень та всіх видів рідин. Не мити шприц-ручку, не занурювати її в рідину і не змащувати. При необхідності шприц-ручку можна очищати вологою тканиною, змоченою м'яким миючим засобом. Не можна кидати або вдаряти шприц-ручку об тверду поверхню. Якщо пацієнт упустив шприц-ручку або сумнівається у її справності, слід приєднати нову голку та перевірити надходження препарату перед тим, як зробити ін'єкцію. Не допускається повторне наповнення шприц-ручки. Порожню шприц-ручку слід одразу викинути. Не намагатися самостійно полагодити шприц-ручку або розібрати її на частини.ПередозуванняЗа даними клінічних досліджень та післяреєстраційного застосування ліраглутиду, були зареєстровані випадки передозування (вводилася доза 72 мг, що у 24 рази більше за рекомендовану для корекції маси тіла). Також зареєстровано один випадок, коли вводилася шестиразова доза (18 мг на добу) протягом 7 місяців. Симптоми: ці випадки передозування супроводжувалися сильною нудотою, блюванням та діареєю, але у всіх випадках стан пацієнтів відновився без ускладнень. У жодному разі був відзначено важкої гіпоглікемії. Лікування: проведення відповідної симптоматичної терапії.Запобіжні заходи та особливі вказівкиУ пацієнтів з цукровим діабетом не можна застосовувати препарат Саксенда як заміну інсуліну. Серцево-судинна недостатність. Досвід застосування у пацієнтів із ХСН класу I–II відповідно до класифікації NYHA обмежений, тому препарат Саксенда® слід застосовувати з обережністю. панкреатит. Застосування агоністів рецепторів ГПП-1 асоціювалося із ризиком розвитку гострого панкреатиту. Повідомлялося про декілька випадків розвитку гострого панкреатиту при застосуванні ліраглутиду. Пацієнти повинні бути поінформовані про характерні симптоми гострого панкреатиту. У разі підозри на розвиток панкреатиту застосування препарату Саксенда слід припинити; у разі підтвердження гострого панкреатиту терапію відновлювати не слід. Слід бути обережними при застосуванні препарату у пацієнтів з панкреатитом в анамнезі. Холелітіаз та холецистит. У клінічних дослідженнях була відзначена більш висока частота розвитку холелітіазу та холециститу у пацієнтів, які отримували препарат Саксенда®, порівняно з пацієнтами, які отримували плацебо. Це може бути частково пояснено тим, що зниження маси тіла може збільшити ризик розвитку холелітіазу та, отже, холециститу. Холелітіаз та холецистит можуть призвести до госпіталізації та холецистектомії. Пацієнти повинні бути поінформовані про характерні симптоми холелітіазу та холециститу. Захворювання щитовидної залози. У ході клінічних досліджень за участю пацієнтів з цукровим діабетом типу 2 були відмічені небажані явища з боку щитовидної залози, включаючи збільшення концентрації кальцитоніну в сироватці крові, зоб та новоутворення щитовидної залози, особливо у пацієнтів, які вже мають захворювання щитовидної залози. У пацієнтів із захворюваннями щитовидної залози препарат Саксенда слід застосовувати з обережністю. У постмаркетинговому періоді у пацієнтів, які отримували ліраглутид, було виявлено випадки медулярного раку щитовидної залози. Наявних даних недостатньо для встановлення або виключення причинно-наслідкового зв'язку виникнення медулярного раку щитовидної залози із застосуванням ліраглутиду у людини. Препарат Саксенда протипоказаний до застосування у пацієнтів з медулярним раком щитовидної залози в анамнезі, в т.ч. сімейному, та множинній ендокринній неоплазії II типу. Необхідно проінформувати пацієнта про ризик медулярного раку щитовидної залози та про симптоми пухлини щитовидної залози (ущільнення в ділянці шиї, дисфагія, задишка, непрохідна захриплість голосу). Поточний контроль концентрації кальцитоніну в сироватці крові або УЗД щитовидної залози не має суттєвого значення для раннього виявлення медулярного раку щитовидної залози у пацієнтів, які застосовують препарат Саксенда®. Значне підвищення концентрації кальцитоніну в сироватці може свідчити про наявність медулярного раку щитовидної залози, пацієнти з медулярним раком щитовидної залози зазвичай мають концентрацію кальцитоніну більше 50 нг/л. При виявленні підвищення концентрації кальцитоніну в сироватці необхідно провести подальше обстеження пацієнта. Пацієнти з вузлами щитовидної залози, які були виявлені при медогляді або УЗД щитовидної залози, також повинні бути додатково обстежені. ЧСС. У клінічних дослідженнях відзначалося збільшення ЧСС. Клінічна значущість збільшення ЧСС при застосуванні препарату Саксенда®, особливо у пацієнтів із серцевими та цереброваскулярними захворюваннями, залишається неясною через обмежений досвід застосування препарату у цих пацієнтів. Слід проводити контроль ЧСС з інтервалами, що відповідають звичайній клінічній практиці. Пацієнтів слід проінформувати про симптоми тахікардії (відчуття серцебиття або відчуття прискореного серцебиття у спокої). У пацієнтів із клінічно значущою постійною тахікардією у стані спокою слід припинити терапію препаратом Саксенда®. Зневоднення. Ознаки та симптоми зневоднення, включаючи порушення функції нирок та гостру ниркову недостатність, були відзначені у пацієнтів, які отримували агоністи рецепторів ГПП-1. Пацієнти, які отримують препарат Саксенда®, повинні бути поінформовані про потенційний ризик зневоднення, пов'язаного з побічними ефектами з боку шлунково-кишкового тракту, та про необхідність профілактики гіповолемії. Гіпоглікемія у пацієнтів з надмірною масою тіла або ожирінням та цукровим діабетом типу 2. Ризик розвитку гіпоглікемії може бути вищим у пацієнтів з цукровим діабетом типу 2, які отримують препарат Саксенда® у комбінації з похідними сульфонілсечовини. Цей ризик може бути зменшений шляхом зниження дози похідної сульфонілсечовини. Додавання препарату Саксенда до терапії у пацієнтів, які отримують інсулін, не оцінювали. Суїцидальні думки та поведінка. У ході клінічних досліджень 6 (0,2%) з 3384 пацієнтів, які отримували препарат Саксенда®, повідомили про появу суїцидальних думок, один із пацієнтів зробив спробу суїциду. У пацієнтів (1941 особа), які отримували плацебо, це не було відзначено. Пацієнтів необхідно контролювати щодо появи або погіршення депресії, суїцидальних думок або поведінки та/або будь-яких несподіваних змін у настрої або поведінці. У пацієнтів із суїцидальними думками або поведінкою застосування препарату Саксенда слід припинити. Протипоказано застосовувати препарат Саксенда у пацієнтів із суїцидальними спробами або активними суїцидальними думками в анамнезі. Рак грудей. У ході клінічних досліджень повідомлялося про підтверджений рак грудей у 14 (0,6%) з 2379 жінок, які отримували препарат Саксенда®, порівняно з 3 (0,2%) з 1300 жінок, які отримували плацебо, включаючи інвазивний рак (11 випадків у жінок, які отримували препарат Саксенда®, та 3 випадки у жінок, які отримували плацебо) та внутрішньопротокова карцинома in situ (3 випадки у жінок, які отримували препарат Саксенда®, та 1 випадок у жінки, яка отримувала плацебо). Більшість випадків раку були естроген-і прогестеронзалежними. Неможливо визначити, чи були ці випадки пов'язані із застосуванням препарату Саксенда через їхню невелику кількість. Крім того, немає достатніх даних, щоб визначити, чи Саксенда® впливає на вже існуючі новоутворення молочної залози. Папілярний рак щитовидної залози. У ході клінічних досліджень повідомлялося про підтверджену папілярну карциному щитовидної залози у 7 (0,2%) з 3291 пацієнтів, які отримували препарат Саксенда®, порівняно з відсутністю її у групі пацієнтів, які отримували плацебо (1843 пацієнти). З усіх випадків 4 карциноми були менше 1 см у найбільшому діаметрі та 4 були діагностовані за результатами гістології після проведеної за медичними показаннями тиреоїдектомії. Неоплазії ободової та прямої кишки. У ході клінічних досліджень повідомлялося про підтверджені доброякісні неоплазії ободової та прямої кишки (переважно аденомах ободової кишки) у 17 (0,5%) з 3291 пацієнтів, які отримували препарат Саксенда®, порівняно з 4 (0,2%) з 1843 пацієнтів, отримували плацебо. Було зареєстровано два підтверджені випадки злоякісної карциноми ободової та прямої кишки (0,1%) у пацієнтів, які отримували препарат Саксенда®, та жодного у пацієнтів, які отримували плацебо. Порушення серцевої провідності. У ході клінічних досліджень у 11 (0,3%) з 3384 пацієнтів, які отримували препарат Саксенда®, повідомлялося про розвиток порушень серцевої провідності, таких як AV блокада 1-го ступеня, блокада правої ніжки пучка Гіса або блокада лівої ніжки пучка Гіса. У пацієнтів (1941 особа), які отримували плацебо, про розвиток порушень серцевої провідності не повідомлялося. Фертильність. За винятком незначного зменшення кількості живих зародків, результати досліджень тварин не вказують на наявність несприятливого впливу на фертильність. Посібник із застосування. Препарат Саксенда® не можна застосовувати, якщо він виглядає інакше, ніж прозора та безбарвна або майже безбарвна рідина. Препарат Саксенда не можна застосовувати, якщо він був заморожений. Препарат Саксенда можна вводити за допомогою голок довжиною до 8 мм. Шприц-ручка призначена для використання з одноразовими голками НовоФайн або НовоТвіст. Ін'єкційні голки не включені в упаковку. Пацієнт повинен бути проінформований про те, що використану голку слід викидати після кожної ін'єкції, а також про те, що не можна зберігати шприц-ручку із приєднаною голкою. Такий захід дозволить запобігти блокуванню голок, забруднення, інфікування та витікання препарату зі шприц-ручки та гарантує точність дозування. Вплив на здатність керувати транспортними засобами та механізмами. Препарат Саксенда не впливає або незначно впливає на здатність керувати транспортними засобами та механізмами. У зв'язку з ризиком розвитку гіпоглікемії при застосуванні препарату, особливо при комбінованому застосуванні з препаратами сульфонілсечовини у пацієнтів з цукровим діабетом типу 2, слід бути обережними при керуванні транспортними засобами та механізмами.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаРозчин - 1 мл: активна речовина: ліраглутид 6 мг (в одній попередньо заповненій шприц-ручці об'ємом 3 мл міститься 18 мг ліраглутиду); допоміжні речовини: натрію гідрофосфату дигідрат 1,42 мг, пропіленгліколь 14,0 мг, фенол 5,5 мг, кислота хлористоводнева/натрію гідроксид qs, вода для ін'єкцій до 1 мл. По 3 мл у картриджі зі скла 1 гідролітичного класу, закупорений диском з бромбутилової гуми/поліізопрену з одного боку та поршнем з бромбутилової гуми з іншого. Картридж запаяний в одноразову пластикову шприц-ручку для багаторазових ін'єкцій. По 1, 2 або 3 пластикові одноразові шприц-ручки для багаторазових ін'єкцій разом з інструкцією із застосування в картонній пачці. Кожна шприц-ручка (3 мл) містить 30 доз по 0,6 мг, 15 доз по 1,2 мг або 10 доз по 1,8 мг ліраглутиду.Опис лікарської формиБезбарвний чи майже безбарвний, прозорий розчин.Фармакотерапевтична групаГіпоглікемічний засіб - глюкагоноподібний поліпептид рецепторів агоніст.ФармакокінетикаАбсорбція Всмоктування ліраглутиду після підшкірного введення відбувається повільно, час досягнення максимальної концентрації у плазмі – 8-12 годин після введення дози препарату. Максимальна концентрація (Сmах) ліраглутиду у плазмі після підшкірної ін'єкції в одноразовій дозі 0,6 мг становить 9,4 нмоль/л. При введенні ліраглутиду в дозі 1,8 мг середній показник рівноважної концентрації в плазмі (AUCt/24) досягає приблизно 34 нмоль/л. Експозиція ліраглутиду посилюється пропорційно до дози. Після введення ліраглутиду в одноразовій дозі внутрішньо-індивідуальний коефіцієнт варіації площі під кривою "концентрація-час" AUC становить 11%. Абсолютна біодоступність ліраглутиду після підшкірного введення становить приблизно 55%. Розподіл Здається обсяг розподілу ліраглутиду в тканинах після підшкірного введення становить 11-17 л. Середній обсяг розподілу ліраглутиду після внутрішньовенного введення становить 0,07 л/кг. Ліраглутид значною мірою пов'язується з білками плазми (> 98%). Метаболізм Протягом 24 годин після введення здоровим добровольцям одноразової дози міченого радіоактивним ізотопом [3Н]-ліраглутиду головним компонентом плазми залишався незмінений ліраглутид. Було виявлено два метаболіти у плазмі (≤ 9% та ≤ 5% від рівня загальної радіоактивності у плазмі крові). Ліраглутид метаболізується ендогенно подібно до великих білків, без залучення будь-якого специфічного органу як шлях виведення. Виведення Після введення дози [3Н]-ліраглутиду незмінений ліраглутид не визначався в сечі або калі. Лише незначна частина введеної радіоактивності у вигляді пов'язаних з ліраглутидом метаболітів (6% та 5% відповідно) виводилася нирками або через кишечник. Радіоактивні речовини нирками або через кишечник виводяться, в основному, протягом перших 6-8 днів після введення дози препарату, і є три метаболіти. Середній кліренс з організму після підшкірного введення ліраглутиду в одноразовій дозі становить приблизно 1,2 л/год із елімінаційним періодом напіввиведення приблизно 13 годин. Особливі групи пацієнтів Літній вік: Дані фармакокінетичних досліджень у групі здорових добровольців та аналіз фармакокінетичних даних, отриманих у популяції пацієнтів (від 18 до 80 років), свідчать про те, що вік не має клінічно значущого впливу на фармакокінетичні властивості ліраглутиду. Стать: Популяційний фармакокінетичний аналіз даних, отриманих при дослідженні дії ліраглутиду у пацієнтів жіночої та чоловічої статі, та дані фармакокінетичних досліджень у групі здорових добровольців свідчать про те, що стать не має клінічно значущого ефекту на фармакокінетичні властивості ліраглутиду. Етнічна приналежність: Популяційний фармакокінетичний аналіз даних, отриманих при дослідженні дії ліраглутиду у суб'єктів білої, чорної, азіатської та латиноамериканської расових груп, свідчить про те, що етнічна приналежність не має клінічно значущого ефекту на фармако. Ожиріння: Популяційний фармакокінетичний аналіз даних свідчить про те, що індекс маси тіла (ІМТ) не має клінічно значущого впливу на фармакокінетичні властивості ліраглутиду. Печінкова недостатність: Фармакокінетичні властивості ліраглутиду досліджувалися в ході клінічного дослідження одноразової дози препарату у суб'єктів з різним ступенем печінкової недостатності. У дослідження були включені пацієнти з печінковою недостатністю легкого ступеня (за класифікацією Child Pugh тяжкість захворювання 5-6 балів) та тяжкою печінковою недостатністю (за класифікацією Child Pugh тяжкість захворювання > 9 балів). Експозиція ліраглутиду у групі пацієнтів з порушеннями функції печінки була не вищою, ніж така у групі здорових суб'єктів, що вказує на те, що печінкова недостатність не має клінічно значущого ефекту на фармакокінетику ліраглутиду. Ниркова недостатність: Фармакокінетика ліраглутиду вивчалася у пацієнтів із різним ступенем ниркової недостатності у дослідженні одноразової дози. До цього дослідження були включені суб'єкти з різним ступенем ниркової недостатності: від легкої (оцінка кліренсу креатиніну 50-80 мл/хв) до важкої (оцінка кліренсу креатиніну Діти: Дослідження Віктозу у дітей не проводилося. Дані доклінічного дослідження безпеки Доклінічні дані, засновані на дослідженнях фармакологічної безпеки, токсичності повторних доз та генотоксичності, не виявили жодної небезпеки для людини. У дворічних дослідженнях канцерогенності були виявлені пухлини С-клітин щитовидної залози у щурів та мишей, які не призводили до летального результату. Нетоксична доза (NOAEL) у щурів не встановлена. Поява подібних пухлин у мавп, які отримували терапію ліраглутидом протягом 20 місяців, не спостерігалося. Результати, отримані в ході досліджень на гризунах, пов'язані з тим, що гризуни виявляють особливу чутливість щодо опосередкованого рецептором ГПП-1 не специфічного генотоксичного механізму. Значимість даних для людини є низькою, проте не може бути повністю виключена. Появи будь-яких інших новоутворень, пов'язаних із терапією, відзначено не було. У дослідженнях тварин не виявлено прямого несприятливого ефекту препарату на фертильність, але відзначено незначне збільшення частоти ранньої ембріональної смерті при лікуванні найвищою дозою препарату. Введення препарату Віктоза® щурам у середині періоду вагітності викликало у них зменшення маси тіла матері та зростання ембріона з не вивченим до кінця ефектом на ребра, а в групі кроликів – відхилення у скелетній структурі. Зростання новонароджених особин у групі щурів під час терапії препаратом Віктоза® знизилося, і це зниження стійко зберігалося в період після закінчення грудного вигодовування у групі моделей, які отримували високі дози ліраглутиду. Невідомо, чи цей ефект зумовлений зниженням споживання калорій внаслідок прямого впливу ГПП-1.ФармакодинамікаМеханізм дії Ліраглутид є аналогом людського глюкагоноподібного пептиду-1 (ГПП-1), вироблений методом біотехнології рекомбінантної ДНК з використанням штаму Saccharomyces cerevisiae, що має 97% гомологічності з людським ГПП-1, який зв'язується і активує рецептори ГПП. Рецептор ГПП-1 служить мішенню для нативного ГПП-1 – ендогенного гормону інкретину, що викликає стимуляцію глюкозозалежної секреції інсуліну в бета-клітинах підшлункової залози. На відміну від нативного ГПП-1, фармакокінетичний та фармакодинамічний профілі ліраглутиду дозволяють вводити його пацієнтам один раз на добу. Профіль тривалої дії ліраглутиду при підшкірній ін'єкції забезпечується трьома механізмами: самоасоціацією, в результаті якої відбувається уповільнене всмоктування препарату, зв'язуванням з альбуміном і вищим рівнем ферментативної стабільності по відношенню до дипептидилпептидази-4 (ДПП-4) і ферменту рахунок чого забезпечується тривалий період напіввиведення препарату із плазми. Дія ліраглутиду здійснюється за рахунок взаємодії зі специфічними рецепторами ГПП-1, внаслідок чого підвищується концентрація циклічного аденозинмонофосфату (цАМФ). Під дією ліраглутиду відбувається глюкозозалежна стимуляція секреції інсуліну та покращення функції бета-клітин підшлункової залози. У той же час під дією ліраглутиду відбувається глюкозозалежне пригнічення зайво високої секреції глюкагону.Таким чином, при підвищенні концентрації глюкози крові відбувається стимуляція секреції інсуліну та пригнічення секреції глюкагону. З іншого боку, під час гіпоглікемії ліраглутид знижує секрецію інсуліну, але не пригнічує секрецію глюкагону. Механізм зниження рівня глікемії включає також невелику затримку випорожнення шлунка. Ліраглутид знижує масу тіла та зменшує жирову масу тіла за допомогою механізмів, що викликають зменшення почуття голоду та зниження витрати енергії. ГПП-1 є фізіологічним регулятором апетиту та споживання калорій, а рецептори ГПП-1 розташовані у кількох областях головного мозку, що беруть участь у процесах регуляції апетиту. У дослідженнях на тваринах периферичне введення ліраглутиду призводило до захоплення препарату в специфічних галузях головного мозку, включаючи гіпоталамус, де ліраглутид за допомогою специфічної активації рецепторів ГПП-1 посилював сигнали насичення та послаблював сигнали голоду, що призводило до зменшення маси тіла. Дослідження на експериментальних тваринних моделях з предіабетом показали, що ліраглутид уповільнює розвиток цукрового діабету. Діагностика in vitro показала, що ліраглутид є потужним фактором специфічної стимуляції проліферації бета-клітин підшлункової залози та попереджає загибель бета-клітин (апоптоз), що індукується цитокінами та вільними жирними кислотами. In vivo ліраглутид підвищує біосинтез інсуліну та збільшує масу бета-клітин у експериментальних тваринних моделей із цукровим діабетом. Коли концентрація глюкози нормалізується, ліраглутид перестає збільшувати масу бета-клітин підшлункової залози. Фармакодинаміка Препарат Віктоза® має тривалу 24-годинну дію та покращує глікемічний контроль шляхом зниження концентрації глюкози крові натще та після їжі у пацієнтів з цукровим діабетом 2 типу. Глюкозозалежна секреція інсуліну При зростанні концентрації глюкози у крові препарат Віктоза® збільшує секрецію інсуліну. При застосуванні поетапної інфузії глюкози секреція інсуліну після введення одноразової дози препарату Віктоза® пацієнтам із цукровим діабетом 2 типу зростає до рівня, який можна порівняти з таким у здорових суб'єктів. Функція бета-клітин підшлункової залози Препарат Віктоза® покращував функцію бета-клітин підшлункової залози, що підтверджується першою та другою фазою інсулінової відповіді та максимальною секреторною активністю бета-клітин. Фармакодинамічні дослідження пацієнтів з цукровим діабетом 2 типу показали відновлення першої фази секреції інсуліну (внутрішньовенне введення інсуліну), покращення другої фази секреції інсуліну (гіперглікемічний клемп-тест) та максимальну секреторну активність інсуліну (тест стимуляції аргініном). У ході 52-тижневої терапії препаратом Віктоза відбулося поліпшення функції бета-клітин підшлункової залози, що підтверджується оцінкою гомеостатичної моделі функції бета-клітин підшлункової залози (НОМА-індекс) та співвідношенням інсуліну до проінсуліну. Секреція глюкагону Препарат Віктоза®, стимулюючи секрецію інсуліну та пригнічуючи секрецію глюкагону, зменшує концентрацію глюкози у крові. Препарат Віктоза не пригнічує глюкагонову відповідь на низьку концентрацію глюкози. Крім того, на тлі препарату Віктоза® спостерігалося нижче вироблення ендогенної глюкози. Випорожнення шлунка Препарат Віктоза викликає невелику затримку спорожнення шлунка, що призводить до зниження швидкості надходження постпрандиальної глюкози в кров. Маса тіла, склад тіла та витрата енергії У суб'єктів із підвищеною масою тіла, включених у довгострокові клінічні дослідження препарату Віктоза, останній викликав значне зниження маси тіла. Сканування за допомогою методів комп'ютерної томографії (КТ) та двоенергетичної рентгенівської абсорбціометрії (ДЕРА) показало, що втрата маси тіла відбулася насамперед через втрату жирової тканини пацієнтів. Ці результати пояснюються тим, що під час терапії препаратом Віктоза® у пацієнтів знижуються відчуття голоду та витрати енергії. Електрофізіологія серця (ЕФС) Дія препарату Віктоза на процес реполяризації в серці була протестована у дослідженні ЕФС. Застосування Віктозу в рівноважній концентрації в щоденній дозі до 1,8 мг не продукує подовження скоригованого інтервалу QT. Клінічна ефективність 3992 пацієнти з цукровим діабетом 2 типу були рандомізовані у 5 подвійних сліпих клінічних дослідженнях безпеки та ефективності, здійснених з метою оцінки впливу Віктозу на глікемічний контроль. Терапія препаратом Віктоза викликала клінічно та статистично значуще поліпшення показника НbА1С, концентрації глюкози натще та постпрандіальної глюкози порівняно з плацебо. Ці дослідження включали 3978 пацієнтів, що отримали терапію (2501 пацієнт отримував терапію препаратом Віктоза®), 53,7% чоловіків і 46,3% жінок, у 797 пацієнтів (508 отримали терапію препаратом Віктоза®) вік склав ≥ 65 років, у 113 пацієнтів ( 66 дістали терапію препаратом Віктоза®) вік становив ≥ 75 років. Глікемічний контроль Препарат Віктоза у вигляді монотерапії протягом 52 тижнів викликав статистично значуще (р У пацієнтів з НbА1С вище 9,5% у вихідній точці дослідження цей показник знизився на 2,1% на тлі монотерапії препаратом Віктоза®, тоді як у пацієнтів, які беруть участь у клінічних дослідженнях комбінованого застосування препарату Віктоза®, середній показник НbА1С знизився на 1,1-2,5%. Препарат Віктоза протягом 26-тижневої комбінованої терапії з метформіном, препаратами сульфонілсечовини або метформіном та тіазолідиндіоном викликав статистично значуще (р У пацієнтів, які не досягли адекватного глікемічного контролю на терапії препаратом Віктоза® та метформіном, додавання інсуліну детемир забезпечило більшу ефективність порівняно з терапією препаратом Віктоза® та метформіном після 26 тижнів лікування (зниження показника НbА1С на 0,52%). Було доведено, що ефективність препарату Віктоза в дозі 0,6 мг у комбінації з препаратами сульфонілсечовини або метформіном перевищує плацебо, але водночас нижча порівняно з дозами 1,2 мг та 1,8 мг. Співвідношення пацієнтів, які досягли зниження показника НbА1С На тлі монотерапії препаратом Віктоза протягом 52-тижневого дослідження кількість пацієнтів, які досягли показника НbА1С У групах пацієнтів, які не досягли адекватного глікемічного контролю на терапії препаратом Віктоза® та метформіном, відсоткове співвідношення пацієнтів, які досягли цільового показника НbА1С ( У ході 26-тижневого дослідження комбінованого застосування препарату Віктоза вдалося досягти показника НbА1С Застосування у пацієнтів із порушенням функції нирок У подвійному сліпому дослідженні ефективності та безпеки препарату Віктоза® 1,8 мг порівняно з плацебо як доповнення до інсуліну та/або пероральним цукрознижувальним препаратам у пацієнтів з цукровим діабетом 2 типу та порушенням функції нирок помірного ступеня препарат Віктоза® був більш ефективним у зниженні. рівня НbА1С через 26 тижнів (-1,05% у порівнянні з -0,38%, р Рівень глікемії натще Концентрація глюкози натще знизилася на 13-43,5 мг% (0,72-2,42 ммоль/л) на фоні застосування препарату Віктоза як у вигляді монотерапії, так і в комбінації з одним або двома пероральними гіпоглікемічними препаратами. Це зниження спостерігалося протягом перших двох тижнів лікування. Постпрандіальний рівень глікемії При застосуванні препарату Віктоза спостерігалося зниження концентрації постпрандіальної глюкози після кожного з трьох щоденних прийомів їжі на 31-49 мг% (1,68-2,71 ммоль/л). Маса тіла 52-тижнева монотерапія препаратом Віктора® асоціювалася зі стійким зниженням маси тіла. Протягом усього періоду клінічного дослідження стійке зниження маси тіла також асоціювалося із застосуванням препарату Віктоза у комбінації з метформіном та у поєднанні з комбінацією метформіну з похідними сульфонілсечовини або комбінацією метформіну з тіазолідиндіоном. Зниження маси тіла у пацієнтів, які отримують препарат Віктоза у комбінації з метформіном, також спостерігалося після додавання інсуліну детемир. Найбільше зниження маси тіла спостерігалося у пацієнтів, які мали у вихідній точці дослідження підвищений індекс маси тіла (ІМТ). Монотерапія препаратом Віктоза протягом 52 тижнів викликала зменшення середнього обсягу талії на 3,0-3,6 см. Зниження маси тіла спостерігалося у всіх пацієнтів, які отримували терапію препаратом Віктоза, незалежно від того, відчували вони чи ні побічну реакцію у вигляді нудоти. Препарат Віктоза у складі комбінованої терапії з метформіном знизив обсяг підшкірно-жирової клітковини на 13 - 17%. Неалкогольний стеатогепатоз Препарат Віктоза зменшує вираженість стеатогепатозу у пацієнтів з цукровим діабетом 2 типу. Імуногенність Враховуючи можливість імуногенного впливу білкових та пептидних лікарських препаратів, застосування Віктозу у пацієнтів може призвести до утворення антитіл до ліраглутиду. Утворення антитіл відзначається у середньому у 8,6% пацієнтів. Утворення антитіл не призводить до зниження ефективності препарату Віктоза. Оцінка впливу на серцево-судинну систему Довгострокові клінічні дослідження показали, що Віктоза® знижує показники систолічного артеріального тиску в середньому на 2,3-6,7 мм рт.ст. у перші два тижні лікування. Препарат Віктоза® знижував частоту розвитку метаболічного синдрому відповідно до визначення III доповіді групи експертів з лікування дорослих (АТРIII). Зниження артеріального тиску систоли відбувалося до зниження маси тіла. У ретроспективному аналізі серйозних небажаних явищ з боку серцево-судинної системи (смерть через серцево-судинну патологію, інфаркт міокарда, інсульт) за даними всіх довгострокових досліджень та досліджень середньої тривалості II та III фази (тривалістю від 26 до 100 тижнів), включають пацієнтів (3651 пацієнт отримував препарат Віктоза®), було продемонстровано відсутність збільшення серцево-судинного ризику (відношення коефіцієнтів захворюваності 0,75 (95% ДІ 0,35; 1,63) щодо комбінованої кінцевої точки при застосуванні препарату Віктоза® порівняно з усіма препаратами порівняння (метформін, глімепірид, росиглітазон, інсулін гларгін, плацебо)).Пацієнти з високим серцево-судинним ризиком були виключені з досліджень і частота серйозних серцево-судинних явищ у дослідженнях була низькою (6,02 на 1000 пацієнтів у пацієнтів, які отримували препарат Віктоза® і 10,45 у пацієнтів, які отримували всі препарати порівняння), що перешкоджає одержанню однозначних висновків. Інші клінічні дані У відкритому дослідженні, в якому проводили порівняння ефективності та безпеки препарату Віктоза® у дозі 1,8 мг та ліксисенатиду у дозі 20 мкг у 404 пацієнтів з незадовільним контролем глікемії на тлі терапії метформіном (середнє значення НbА1С 8,4%). ефективно знижував рівень НbА1С порівняно з ліксісенатидом через 26 тижнів терапії (-1,83% порівняно з -1,21%, р У порівняльному дослідженні ефективності та безпеки препарату Віктоза (у дозах 1,2 мг та 1,8 мг) та інгібітору дипептидилпептидази-4 ситагліптину в дозі 100 мг у пацієнтів, які не досягли адекватного контролю на терапії метформіном, після 26 тижнів лікування доведено найкраще зниження. показника НbА1С при застосуванні препарату Віктоза® в обох дозах порівняно з ситагліптином (- 1,24%, - 1,50% порівняно з - 0,90%, р У порівняльному дослідженні ефективності та безпеки препарату Віктоза® (у дозі 1,8 мг) та ексенатиду (у дозі 10 мкг двічі на день) у пацієнтів, які не досягли адекватного контролю на терапії метформіном та/або похідними сульфонілсечовини, після 26 тижнів застосування препарату Віктоза® відзначено більше зниження показника НbА1С порівняно з ексенатидом (- 1,12% порівняно з - 0,79%, р Терапія препаратом Віктоза протягом 52 тижнів покращила інсуліночутливість порівняно з такою у препаратів сульфонілсечовини, що було виявлено за допомогою гомеостатичної моделі оцінки інсулінорезистентності HOMA-IR.Показання до застосуванняПрепарат Віктоза® показаний для застосування один раз на день у дорослих пацієнтів з цукровим діабетом 2 типу на тлі дієти та фізичних вправ для досягнення глікемічного контролю як: монотерапії; Комбінованої терапії з одним або декількома пероральними гіпоглікемічними препаратами (з метформіном, похідними сульфонілсечовини або тіазолідиндіонами) у пацієнтів, які не досягли адекватного глікемічного контролю на попередній терапії; Комбінована терапія з базальним інсуліном у пацієнтів, які не досягли адекватного глікемічного контролю на терапії препаратом Віктоза® та метформіном.Протипоказання до застосуванняПідвищена чутливість до активної речовини або до інших компонентів, що входять до складу препарату; медулярний рак щитовидної залози в анамнезі, у тому числі у сімейному; множинна ендокринна неоплазія 2 типи. Протипоказано застосування препарату Віктоза у наступних груп пацієнтів та при наступних станах/захворюваннях у зв'язку з відсутністю даних щодо ефективності та безпеки: цукровий діабет 1 типу; діабетичний кетоацидоз; вагітність та період грудного вигодовування; тяжкі порушення функції нирок; порушення функції печінки; хронічна серцева недостатність III-IV функціонального класу (відповідно до класифікації NYHA (Нью-Йоркська кардіологічна асоціація)); запальні захворювання кишок; діабетичний гастропарез; дитячий вік до 18 років З обережністю: У зв'язку з обмеженим досвідом застосування рекомендується застосовувати з обережністю у пацієнтів із хронічною серцевою недостатністю І-ІІ функціонального класу (відповідно до класифікації NYHA); у віці 75 років та старше; при захворюваннях щитовидної залозиВагітність та лактаціяВагітність Адекватні дані щодо застосування препарату Віктоза у вагітних жінок відсутні. Дослідження на тваринах продемонстрували репродуктивну токсичність препарату. Потенційний ризик для людей невідомий. Протипоказано застосовувати препарат Віктоза під час вагітності, замість нього рекомендується проводити лікування інсуліном. Якщо пацієнтка готується до вагітності, або вагітність вже настала, терапію препаратом Віктоза необхідно негайно припинити. Період грудного вигодовування Невідомо, чи ліраглутид проникає в грудне молоко жінок. Дослідження на тваринах показали, що проникнення ліраглутиду та метаболітів близького структурного зв'язку у грудне молоко є низьким. Досвід застосування препарату Віктоза® у жінок, що годують, відсутній; застосування препарату у період грудного вигодовування протипоказане.Побічна діяНайчастіше реєстрованими небажаними реакціями під час клінічних досліджень були порушення з боку шлунково-кишкового тракту: нудоту та діарею реєстрували дуже часто, а блювоту, запор, біль у животі та диспепсію – часто. На початку терапії препаратом Віктоза ці небажані явища з боку шлунково-кишкового тракту можуть виникати частіше; ці реакції зазвичай слабшають протягом кількох днів чи тижнів на фоні продовження терапії. Головний біль та інфекції верхніх дихальних шляхів також реєстрували часто. Крім того, гіпоглікемію реєстрували часто і дуже часто при застосуванні препарату Віктоза у комбінації з похідними сульфонілсечовини. Виражену гіпоглікемію переважно відзначали при комбінованій терапії з похідними сульфонілсечовини. У Таблиці 1 представлений перелік небажаних реакцій, зазначених у довгострокових контрольованих дослідженнях III фази та спонтанних (постреєстраційних) повідомленнях. Частота для пов'язаних спонтанних (постреєстраційних) повідомлень була розрахована на підставі їхньої частоти в клінічних дослідженнях II 1а фази. Небажані реакції розподілені за групами відповідно до систем органів MedDRA та частоти. Частота визначена так: дуже часто (≥ 1/10); часто (≥ 1/100 до < 1/10); нечасто (≥ 1/1000 до < 1/100); рідко (≥ 1/10000 до < 1/1000); дуже рідко (<1/10 000). Таблиця 1. Побічні реакції, виявлені в ході довгострокових плацебо-контрольованих клінічних досліджень ІІІ фази та спонтанних (постмаркетингових) повідомлень Система органів Дуже часто Часто Не часто Рідко Дуже рідко Інфекції та інвазії Інфекція верхніх дихальних шляхів Порушення імунної системи Анафілактичні реакції Порушення метаболізму та харчування Гіпоглікемія* Анорексія Зниження апетиту Дегідратація# Порушення з боку нервової системи Головний біль Порушення з боку серця Збільшення частоти серцевих скорочень Порушення з боку шлунково-кишкового тракту Нудота Діарея Блювота Диспепсія Болі у верхній частині живота Запор Гастрит Метеоризм Здуття живота Гастроезофагеальна рефлюксна хвороба Відрижка Панкреатит (включаючи панкреонекроз) Порушення з боку шкіри та підшкірних тканин Висип Кропивниця Сверблячка Порушення з боку нирок та сечовивідних шляхів Порушення функції нирок Гостра ниркова недостатність Загальні розлади та реакції у місці введення Реакції у місці введення нездужання N = 2501 пацієнти, які отримували терапію препаратом Віктоза® *Явлення зустрічається дуже часто при застосуванні у комбінації з інсуліном. Опис окремих побічних реакцій Гіпоглікемія Більшість епізодів підтвердженої гіпоглікемії, зареєстрованих у ході клінічних досліджень, були легкими. Під час клінічних досліджень при застосуванні препарату Віктоза у вигляді монотерапії не відмічено випадків виникнення тяжкої гіпоглікемії. Тяжкі гіпоглікемії можуть виникати нечасто і, головним чином, спостерігаються при застосуванні препарату Віктоза у комбінації з похідними сульфонілсечовини (0,02 випадки/пацієнта на рік). При застосуванні препарату Віктоза у поєднанні з іншими пероральними гіпоглікемічними препаратами (не похідними сульфонілсечовини) спостерігалися окремі випадки гіпоглікемії (0,001 випадків/пацієнта на рік). При терапії препаратом Віктоза у дозі 1,8 мг у поєднанні з інсуліном детемиром та метформіном не було відзначено випадків тяжких гіпоглікемій. Частота випадків легкої гіпоглікемії склала 0,228 випадки/пацієнта на рік. У групах пацієнтів, які отримували терапію ліраглутидом 1,8 мг та метформіном, частота випадків легкої гіпоглікемії склала 0,034 та 0,115 випадку/пацієнта на рік відповідно. Побічні реакції з боку шлунково-кишкового тракту У більшості випадків нудота мала легкий або помірний характер, була скороминущою і рідко призводила до скасування терапії. Відсоток пацієнтів із побічними реакціями у вигляді нудоти (по тижнях) у довгостроковому клінічному дослідженні наведено на Рис.3. 20,7% пацієнтів, які отримували препарат Віктоза у комбінації з метформіном, перенесли мінімум один епізод нудоти, а 12,6% - принаймні один епізод діареї. При застосуванні препарату Віктоза у комбінації з похідними сульфонілсечовини у 9,1% пацієнтів відмічено мінімум один епізод нудоти, і у 7,9% – принаймні, по одному випадку розвитку діареї. У ході довгострокових контрольованих клінічних досліджень (26 тижнів або більше) частота припинення участі пацієнтів у дослідженні через розвиток побічних ефектів склала 7,8% у групі пацієнтів, які отримували препарат Віктоза®, та 3,4% у групі пацієнтів, які отримували препарати порівняння. . Найбільш частими побічними реакціями, які призводили до відміни препарату Віктоза, були нудота (2,8% пацієнтів) та блювання (1,5%). У пацієнтів старше 70 років частота розвитку побічних реакцій з боку шлунково-кишкового тракту при застосуванні препарату Віктоза може бути вищою. При застосуванні препарату Віктоза у пацієнтів з легким та середнім ступенем ниркової недостатності (кліренс креатиніну 60-90 мл/хв і 30-59 мл/хв відповідно) частота побічних реакцій з боку шлунково-кишкового тракту може бути вищою. Реакції у місці введення У ході довгострокових (26 тижнів або більше) контрольованих досліджень приблизно у 2% пацієнтів, які отримували Віктозу, відзначалися реакції в місці введення препарату. Ці реакції мали, зазвичай, легкий характер. Панкреатит Повідомлялося про кілька випадків розвитку гострого панкреатиту. Алергічні реакції У післяреєстраційному періоді повідомлялося про виникнення алергічних реакцій, таких як кропив'янка, висипання та свербіж. У післяреєстраційному періоді при застосуванні препарату Віктоза описано кілька випадків анафілактичних реакцій, що супроводжуються такими симптомами як артеріальна гіпотонія, прискорене серцебиття, задишка, периферичні набряки. Збільшення частоти серцевих скорочень Повідомлялося про випадки збільшення частоти серцевих скорочень при застосуванні Віктозу. У довгострокових клінічних дослідженнях при застосуванні препарату Віктоза середнє збільшення частоти серцевих скорочень від вихідного рівня становило від 2 до 3 ударів на хвилину. Довгострокові клінічні наслідки були встановлені.Взаємодія з лікарськими засобамиОцінка взаємодії лікарських засобів in vitro Препарат Віктоза показав дуже низьку здатність до лікарської фармакокінетичної взаємодії, зумовленої метаболізмом у системі цитохрому Р-450 (СУР), а також зв'язуванням з білками плазми. Оцінка взаємодії лікарських засобів in vivo Невелика затримка спорожнення шлунка при застосуванні Віктозу може впливати на всмоктування супутніх пероральних лікарських препаратів. Дослідження лікарської взаємодії не показали будь-якого клінічно значущого уповільнення всмоктування цих препаратів, тому корекція дози не потрібна. У кількох пацієнтів, які отримували лікування препаратом Віктоза, відзначалося мінімум але одному епізоду гострої діареї. Діарея може впливати на всмоктування пероральних лікарських засобів, що застосовуються одночасно з препаратом Віктоза. Варфарин та інші похідні кумарину Дослідження щодо взаємодії не проводилися. Не може бути виключено клінічно значущу взаємодію з діючими речовинами з низькою розчинністю або вузьким терапевтичним індексом, таким як варфарин. На початку лікування препаратом Віктоза у пацієнтів, які отримують варфарин або інші похідні кумарину, рекомендується частіше проводити моніторинг Міжнародного нормалізованого відношення (МНО). Парацетамол Одноразове застосування парацетамолу в дозі 1000 мг на фоні застосування Віктозу не викликає зміну системної експозиції. Смах парацетамолу в плазмі знизився на 31%, а середній час досягнення максимальної концентрації в плазмі крові tmax збільшився на 15 хвилин. При одночасному прийомі Віктозу і парацетамолу корекції дози останнього не потрібно. Аторвастатин Одноразове застосування аторвастатину в дозі 40 мг на фоні застосування Віктозу не викликає зміну системної експозиції. Таким чином, на фоні прийому Віктозу корекції дози аторвастатину не потрібно. Смах аторвастатину в плазмі знизився на 38%, а середнє значення tmax у плазмі на фоні прийому препарату Віктоза® збільшилося з 1 до 3 годин. Гризеофульвін Одноразове застосування гризеофульвіну в дозі 500 мг на фоні застосування Віктозу не викликає зміну системної експозиції. Смах гризеофульвіну зросла на 37%, тоді як середнє значення tmax у плазмі не змінилося. Корекції дози гризеофульвіну та інших лікарських засобів, що мають низьку розчинність та високу проникність, не потрібні. Дігоксин При одноразовому введенні дигоксину в дозі 1 мг та препарату Віктоза відзначалося зменшення площі під кривою AUC дигоксину на 16%; Сах дигоксину знизилася на 31%. Середнє значення tmax дигоксину у плазмі збільшилося з 1 до 1,5 години. Виходячи з отриманих результатів корекції дози дигоксину не потрібно. Лізіноприл Одноразове застосування лізиноприлу в дозі 20 мг на фоні застосування Віктозу призвело до зменшення площі під кривою AUC лізиноприлу на 15%; Стах лізиноприлу знизилася на 27%. Середнє значення tmax лізиноприлу в плазмі на фоні прийому Віктозу збільшилося з 6 до 8 годин. Виходячи з отриманих результатів корекції дози лізиноприлу не потрібно. Пероральні контрацептиви Схах етинілестрадіолу та левоноргестрелу після їх одноразового застосування на фоні терапії препаратом Віктоза® знизилася на 12% та 13%, відповідно. Застосування обох препаратів разом із Віктозом супроводжувалося збільшенням tmax цих лікарських засобів на 1,5 години. Клінічно значущого ефекту на системну експозицію етинілестрадіолу та левоноргестрелу в організмі ліраглутид не має. Таким чином, очікуваний контрацептивний ефект обох лікарських засобів на тлі терапії препаратом Віктоза не змінюється. Інсулін Не було виявлено фармакокінетичної або фармакодинамічної взаємодії препарату Віктоза® з інсуліном детеміром при одноразовому застосуванні інсуліну детеміру у дозі 0,5 ОД/кг з препаратом Віктоза® у дозі 1,8 мг у пацієнтів з цукровим діабетом 2 типу. Несумісність Речовини, додані до препарату Віктоза, можуть спричинити деградацію ліраглутиду. Препарат Віктозу не можна змішувати з іншими лікарськими засобами, у тому числі з інфузійними розчинами.Спосіб застосування та дозиПрепарат Віктоза® застосовують один раз на добу будь-коли, незалежно від прийому їжі, його можна вводити у вигляді підшкірної ін'єкції в живіт, стегно або плече. Місце та час ін'єкції можуть змінюватись без корекції дози. Однак краще вводити препарат приблизно в той самий час доби, в найбільш зручний для пацієнта час. Подальшу інформацію щодо способу застосування препарату Віктоза® міститься в розділі "Посібник із використання". Препарат Віктоза® не можна вводити внутрішньовенно та внутрішньом'язово. Дози Для поліпшення шлунково-кишкової переносимості початкова доза становить 0,6 мг ліраглутиду на день. Після застосування препарату протягом щонайменше одного тижня дозу слід збільшити до 1,2 мг. Є дані про те, що у деяких пацієнтів ефективність лікування зростає зі збільшенням дози препарату з 1,2 до 1,8 мг. З метою досягнення найкращого глікемічного контролю у хворого та з урахуванням клінічної ефективності дозу препарату Віктоза можна збільшити до 1,8 мг після застосування його у дозі 1,2 мг протягом мінімум одного тижня. Застосування препарату у щоденній дозі вище 1,8 мг не рекомендується. Препарат Віктоза можна застосовувати додатково до існуючої терапії метформіном або комбінованої терапії метформіном з тіазолідиндіоном. Терапію метформіном та тіазолідиндіоном можна продовжити у колишніх дозах. Препарат Віктоза® можна додавати до терапії похідними сульфонілсечовини або до комбінованої терапії метформіном з похідними сульфонілсечовини. При додаванні препарату Віктоза до терапії похідними сульфонілсечовини слід враховувати зниження дози похідних сульфонілсечовини з метою мінімізації ризику виникнення небажаних гіпоглікемій. При додаванні препарату Віктоза до терапії базальним інсуліном слід враховувати зниження дози інсуліну з метою мінімізації ризику виникнення гіпоглікемії. Для корекції дози Віктозу не потрібно проведення самоконтролю глюкози крові. Однак, на початку терапії препаратом Віктоза® у комбінації з похідними сульфонілсечовини або базальним інсуліном, такий самоконтроль глюкози крові може знадобитися для корекції дози похідних сульфонілсечовини або базального інсуліну. Пропущена доза У разі пропуску дози препарат Віктоза слід ввести якнайшвидше в межах 12 годин з моменту запланованого введення дози. Якщо тривалість пропуску становить понад 12 годин, препарат Віктоза слід ввести наступного дня у запланований час. Не слід вводити наступного дня додаткову або збільшену дозу Віктозу для компенсації пропущеної дози. Особливі групи пацієнтів Літній вік (> 65 років): Не потрібна корекція дози залежно від віку. Є обмежений досвід застосування препарату у пацієнтів віком 75 років та старших. Пацієнти з нирковою недостатністю Не потрібна корекція дози у пацієнтів з нирковою недостатністю легкого або середнього ступеня тяжкості (кліренс креатиніну 60-90 мл/хв і 30-59 мл/хв відповідно). Досвід застосування препарату у пацієнтів з тяжкою нирковою недостатністю (кліренс креатиніну нижче 30 мл/хв) відсутній. В даний час застосування Віктозу у пацієнтів з тяжкими порушеннями функції нирок, у тому числі у пацієнтів з термінальною стадією ниркової недостатності, протипоказано. Пацієнти з печінковою недостатністю В даний час є обмежений досвід застосування препарату Віктоза у пацієнтів з печінковою недостатністю, тому протипоказано застосовувати його у пацієнтів з печінковою недостатністю легкого, помірного або тяжкого ступеня. Діти та підлітки Застосування препарату Віктоза у дітей та підлітків віком до 18 років протипоказане у зв'язку з відсутністю даних щодо безпеки та ефективності.ПередозуванняЗа даними клінічних досліджень та післяреєстраційного застосування ліраглутиду були зареєстровані випадки передозування зі збільшенням дози до 40 разів, що перевищує рекомендовану дозу (72 мг). Було відмічено один випадок передозування з перевищенням дози в 10 разів (18 мг щодня) протягом 7 місяців. Як правило, пацієнти відзначали важку нудоту, блювоту та діарею, але одужували без залишкових явищ. Ніхто з пацієнтів був відзначено гіпоглікемії важкого ступеня. У разі передозування препарату Віктоза рекомендується проведення відповідної симптоматичної терапії.Запобіжні заходи та особливі вказівкиЗастосування препарату Віктоза протипоказане у пацієнтів з цукровим діабетом 1 типу або для лікування діабетичного кетоацидозу. Препарат Віктоза не замінює інсулін. Досвід застосування Віктозу у пацієнтів з хронічною серцевою недостатністю I-II функціональних класів відповідно до функціональної класифікації хронічної серцевої недостатності NYHA обмежений, тому у цих пацієнтів препарат слід застосовувати з обережністю. Відсутній досвід застосування препарату Віктоза у пацієнтів з хронічною серцевою недостатністю III-IV функціональних класів відповідно до класифікації хронічної серцевої недостатності NYHA. Застосування препарату Віктоза у таких пацієнтів протипоказане. Досвід застосування препарату Віктоза у пацієнтів із запальними захворюваннями кишечника та діабетичним гастропарезом обмежений. Застосування препарату Віктоза у цих групах пацієнтів протипоказане, т.к. асоціюється з розвитком минулих побічних реакцій з боку шлунково-кишкового тракту, таких як нудота, блювання та діарея. Гострий панкреатит Застосування агоністів ГПП-1 асоціювалося із ризиком розвитку гострого панкреатиту. Повідомлялося про розвиток гострого панкреатиту в ході клінічних досліджень та післяреєстраційному періоді. Пацієнти повинні бути поінформовані про характерні симптоми гострого панкреатиту. При підозрі на панкреатит терапія препаратом Віктоза повинна бути негайно припинена; у разі підтвердження гострого панкреатиту терапію препаратом Віктоза відновлювати не слід. Слід бути обережними при застосуванні препарату у пацієнтів з панкреатитом в анамнезі. Захворювання щитовидної залози У ході клінічних досліджень препарату Віктоза у окремих пацієнтів (зокрема, у пацієнтів, які вже мають захворювання щитовидної залози) повідомлялося про побічні явища з боку щитовидної залози, включаючи підвищення концентрації кальцитоніну в сироватці крові, зоб та новоутворення щитовидної залози, у зв'язку з цим препарат Віктоза® у таких пацієнтів слід застосовувати з обережністю (див. розділ "З обережністю"). У постмаркетинговому періоді у пацієнтів, які отримували ліраглутид, було виявлено випадки медулярного раку щитовидної залози. Наявних даних недостатньо для встановлення або виключення причинно-наслідкового зв'язку виникнення медулярного раку щитовидної залози із застосуванням ліраглутиду у людини. Необхідно проінформувати пацієнта про ризик медулярного раку щитовидної залози та про симптоми пухлини щитовидної залози (ущільнення в ділянці шиї, дисфагія, задишка, непрохідна захриплість голосу). Гіпоглікемія Пацієнти, які отримують препарат Віктоза у комбінації з похідними сульфонілсечовини або базальним інсуліном, мають підвищений ризик розвитку гіпоглікемії. Ризик розвитку гіпоглікемії можна знизити, зменшивши дозу похідних сульфонілсечовини або базального інсуліну. Дегідратація У ході проведення клінічних досліджень повідомлялося про появу ознак та симптомів дегідратації та ниркової недостатності у пацієнтів, які приймали препарат Віктоза. Пацієнти, які отримують препарат Віктоза®, повинні бути попереджені про можливий ризик зневоднення у зв'язку з побічними ефектами з боку шлунково-кишкового тракту та необхідність дотримання ними запобіжних заходів, щоб уникнути розвитку гіповолемії. Фертильність За винятком невеликого зменшення кількості живих імплантатів, у дослідженнях на тваринах не було отримано свідчень несприятливого впливу на фертильність. Посібник із використання Шприц-ручка Віктоза призначена тільки для індивідуального використання. Препарат Віктоза® не можна використовувати, якщо він виглядає інакше, ніж прозора та безбарвна або майже безбарвна рідина. Препарат Віктоза® не можна використовувати, якщо він заморозив. Препарат Віктоза можна вводити за допомогою голок довжиною до 8 мм і товщиною до 32G. Шприц-ручка призначена для використання в комбінації з одноразовими ін'єкційними голками НовоФайн або НовоТвіст. Ін'єкційні голки не включені в упаковку. Пацієнт повинен бути проінформований про те, що використану голку слід викидати після кожної ін'єкції, а також про те, що не можна зберігати шприц-ручку із приєднаною голкою. Такий захід дозволить запобігти забрудненню, інфікуванню та витоку препарату зі шприц-ручки та гарантує точність дозування. Вплив на здатність до керування автотранспортом та управління механізмами Досліджень впливу препарату Віктоза на здатність керувати транспортними засобами та роботу з механізмами не проводилося. Малоймовірно, що препарат Віктоза може впливати на здатність керувати транспортними засобами або роботу з механізмами. Пацієнти повинні бути попереджені про те, що їм слід дотримуватися запобіжних заходів, щоб уникнути розвитку у них гіпоглікемії під час керування транспортними засобами та при роботі з механізмами, особливо при застосуванні препарату Віктоза у комбінації з похідними сульфонілсечовини або базальним інсуліном.Умови відпустки з аптекЗа рецептомВідео на цю тему