Все товары
Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему.
Фармакотерапевтична групаКоронародилатируючий засіб рефлекторної дії.ФармакокінетикаПри під'язиковому прийомі терапевтичний ефект в середньому настає через 5 хвилин, при цьому до 70% вивільняється протягом 3 хвилин.ФармакодинамікаМає заспокійливу дію на центральну нервову систему, а також помірну рефлекторну судинорозширювальну дію, обумовлену подразненням чутливих нервових закінчень. Стимулює вироблення та вивільнення енкефалінів, ендорфінів та інших пептидів, гістаміну, кінінів (за рахунок подразнення рецепторів слизової оболонки), які беруть активну участь у регуляції проникності судин, формуванні больових відчуттів.Показання до застосуванняФункціональні кардіалгії, напади стенокардії ангіоневротичного характеру, легені, нетривалі напади стенокардії при ішемічній хворобі серця, неврозах, істерії, а також як протиблювотний засіб при морській та повітряній хворобі.Протипоказання до застосуванняПідвищена чутливість до компонентів препарату, цукровий діабет, порушення толерантності до вуглеводів.Побічна діяПри тривалому прийомі іноді можуть спостерігатися легка нудота, сльозотеча, запаморочення. Ці явища зазвичай відбуваються самостійно.Спосіб застосування та дозиВалідол з глюкозою призначають під язик. Таблетку слід тримати у роті під язиком до повного розчинення. Приймають по 1 таблетці 2-3 десь у день. Добова кратність та тривалість прийому визначається залежно від ефективності лікування. При недостатньо вираженому ефекті або, коли в окремих хворих протягом 5 хвилин після прийому препарату ефект не спостерігається, необхідно звернутися до лікаря для призначення іншої терапії.Умови зберіганняУ прохолодному місці +8+15 градусУмови відпустки з аптекБез рецептаВідео на цю тему
Дозування: 60 мг Фасування: N20 Форма випуску таб. під'язичні Упакування: упак. Діюча речовина: Левоментола розчин у ментил ізовалераті+[Декстроза].
Склад, форма випуску та упаковкаПігулки - 1 таб. активна речовина: левоментолу розчин у ментил ізовалераті (валідол) - 0,060 г; допоміжні речовини: сахароза (цукор) – 1,157 г; кальцію стеарат – 0,006 г.Опис лікарської формиКруглі плоскоциліндричні пігулки з фаскою та ризиком, білого або білого з жовтуватим відтінком кольору з характерним запахом ментолу. Допускаються сірі вкраплення.ФармакокінетикаПри прийомі під язик терапевтичний ефект настає в середньому через 5 хвилин, при цьому до 70% препарату вивільняється протягом 3 хвилин.ФармакодинамікаЧинить седативну дію, має помірну рефлекторну судиннорозширювальну дію, обумовлену подразненням чутливих нервових закінчень. Стимулює вироблення та вивільнення енкефалінів, ендорфінів та інших пептидів, кінінів (за рахунок подразнення рецепторів слизової оболонки), які беруть активну участь у регуляції проникності судин, формування больових відчуттів.Показання до застосуванняФункціональні кардіалгії, синдром «захитування» (нудота, блювання при морській та повітряній хворобі).Протипоказання до застосуванняПідвищена чутливість до компонентів препарату. Дефіцит сахарози/ізомальтози, непереносимість фруктози, глюкозо-галактозна мальабсорбція (бо препарат містить сахарозу). З обережністю: Слід призначати з обережністю хворим на цукровий діабет (препарат містить сахарозу).Вагітність та лактаціяУ період вагітності та годування груддю Валідол призначають лише в тому випадку, якщо очікуваний терапевтичний ефект для матері перевищує можливий негативний вплив препарату на плід та немовля.Побічна діяПри тривалому прийомі валідолу може спостерігатися легка нудота, сльозотеча, запаморочення. Ці явища зазвичай відбуваються самостійно.Взаємодія з лікарськими засобамиПри сумісному застосуванні з іншими лікарськими засобами, що пригнічують центральну нервову систему, посилює дію останніх. Одночасне застосування препарату з нітратами зменшує головний біль, який виникає при їх застосуванні.Спосіб застосування та дозиВалідол призначають під язик. Таблетку слід тримати у роті під язиком до повного розсмоктування. Приймають по 1 таблетці 2-3 десь у день. Добова кратність та тривалість прийому валідолу визначається залежно від ефективності лікування. При недостатньо вираженому ефекті або, коли в окремих хворих протягом 5 хвилин після прийому препарату ефект не спостерігається, необхідно звернутися до лікаря для призначення іншої терапії.ПередозуванняГоловний біль, нудота, збуджений стан, зниження артеріального тиску, гноблення центральної нервової системи. У разі передозування необхідно відмінити препарат та призначити симптоматичну терапію.Запобіжні заходи та особливі вказівки1 таблетка містить хлібних одиниць – 0,096-0,116 ХЕ (0,106 ХЕ).Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. діючі речовини: левоментолу розчин у ментил ізовалераті (валідол) – 60,0 мг, декстрози моногідрат (глюкози моногідрат) – 188,0 мг; Допоміжні речовини: сахароза (цукор білий) – 546,0 мг, кальцію стеарат – 6,0 мг.Опис лікарської формиКруглі, плоскоциліндричні пігулки білого з жовтуватим відтінком кольору, із сіруватими вкрапленнями, з характерним запахом ментолу.ХарактеристикаВалідол з глюкозою - коронародилатируючий засіб рефлекторної дії. Має заспокійливу дію на центральну нервову систему, а також помірну рефлекторну судинорозширювальну дію, обумовлену подразненням чутливих нервових закінчень. Стимулює вироблення та вивільнення енкефалінів, ендорфінів та інших пептидів, гістаміну, кінінів, які беруть активну участь у регуляції проникності судин, формуванні больових відчуттів. Застосовується при функціональній кардіалгії, неврозах, а також як протиблювотний засіб при морській та повітряній хворобі. Випускається у формі під'язикових таблеток по 6 або 10 таблеток в контурну осередкову упаковку. Відпускається без рецепта.Фармакотерапевтична групакоронародилатируючий засіб рефлекторної дії.ФармакокінетикаПри сублінгвальному (під'язичному) застосуванні левоментол абсорбується зі слизової оболонки ротової порожнини; після всмоктування метаболізується у печінці, виводиться нирками у вигляді глюкуронідів. Декстрози моногідрат повністю засвоюється організмом, нирками не виводиться (поява у сечі є патологічною ознакою).ФармакодинамікаВалідол має заспокійливу дію на центральну нервову систему, а також помірну рефлекторну судинорозширювальну дію, обумовлену подразненням чутливих нервових закінчень. Стимулює вироблення та вивільнення енкефалінів, ендорфінів та інших пептидів, гістаміну, кінінів (за рахунок подразнення рецепторів слизової оболонки ротової порожнини), які беруть активну участь у регуляції проникності судин, формуванні больових відчуттів. При сублінгвальному (під'язичному) прийомі терапевтичний ефект в середньому настає через 5 хвилин, при цьому до 70% вивільняється протягом 3 хвилин. Декстрози моногідрат, надходячи в тканини, фосфорилюється, перетворюючись на глюкозо-6-фосфат, який бере активну участь у різних процесах обміну речовин в організмі і в метаболічних процесах.Показання до застосуванняФункціональна кардіалгія, неврози, а також як протиблювотний засіб при морській та повітряній хворобі.Протипоказання до застосуванняПідвищена чутливість до компонентів препарату, дефіцит сахарази/ізомальтази, непереносимість фруктози, глюкозо-галактозна мальабсорбція, вік до 18 років (відсутні дані щодо ефективності та безпеки застосування препарату у дітей). З обережністю Слід призначати з обережністю пацієнтам із цукровим діабетом (препарат містить цукор).Вагітність та лактаціяЗастосування препарату при вагітності та в період грудного вигодовування можливе у випадку, якщо передбачувана користь для матері перевищує потенційний ризик для плода та дитини. Потрібно проконсультуватися з лікарем.Побічна діяМожуть спостерігатися нудота, сльозотеча, запаморочення. При відміні препарату ці побічні ефекти проходять самостійно. Можливий розвиток алергічних реакцій (шкірний висип, свербіж, ангіоневротичний набряк). Якщо будь-які з побічних ефектів, що вказані в інструкції, посилюються, або Ви помітили інші побічні ефекти, не вказані в інструкції, повідомте про це лікаря.Взаємодія з лікарськими засобамиПри одночасному застосуванні з іншими лікарськими засобами, що пригнічують центральну нервову систему, посилює дію останніх. Одночасне застосування препарату з нітратами зменшує головний біль, який виникає при їх застосуванні.Спосіб застосування та дозиПрепарат призначають дорослим по 1 таблетці під язик до повного розсмоктування. Приймають по 1 таблетці 2-3 рази на день. Кратність та тривалість прийому препарату визначається залежно від ефективності лікування. За відсутності або недостатньої виразності терапевтичного ефекту протягом 5-10 хвилин після прийому препарату необхідно звернутися до лікаря для призначення іншої терапії.ПередозуванняСимптоми: біль голови, нудота, стан збудження, порушення серцевої діяльності, різке зниження артеріального тиску, пригнічення центральної нервової системи. Лікування: відміна препарату, симптоматична терапія.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Діючі речовини: левоментолу розчин у ментилізовалераті (валідол) - 60,0 мг; декстрози моногідрат (глюкози моногідрат) – 188,0 мг; Допоміжні речовини: Сахароза (цукор білий) – 548,0 мг; Кальція стеарат – 4,0 мг. По 6 або 10 таблеток у контурне осередкове пакування з плівки полівінілхлоридної та фольги алюмінієвої друкованої лакованої. По 1, 2, 3, 5 контурних осередкових упаковок разом з інструкцією із застосування поміщають у пачку з картону. 200, 300, 400, 500, 600 контурних осередкових упаковок з рівною кількістю інструкцій з медичного застосування поміщають у картонну коробку (для стаціонарів).Опис лікарської формиКруглі плоскі пігулки з фаскою та ризиком, білого або білого з жовтуватим відтінком кольору з сіруватими вкрапленнями, з характерним запахом ментолу.Фармакотерапевтична групаКоронародилатируючий засіб рефлекторної дії.ФармакокінетикаПри під'язиковому застосуванні левоментол абсорбується зі слизової оболонки порожнини рота, метаболізується у печінці та виводиться нирками у вигляді глюкуронідів.ФармакодинамікаЧинить седативну дію, має помірну рефлекторну судиннорозширювальну дію, обумовлену подразненням чутливих нервових закінчень. Стимулює вироблення та вивільнення енкефалінів, ендорфінів та інших пептидів, гістаміну, кінінів (за рахунок подразнення рецепторів слизової оболонки), які беруть активну участь у регуляції проникності судин, формуванні больових відчуттів. При під'язиковому прийомі терапевтичний ефект у середньому настає через 5 хв, при цьому 70% діючої речовини вивільняється протягом 3 хвилин. Декстрози моногідрат, надходячи в тканини фосфорилюється, перетворюючись на глюкозо-6-фосфат, який бере активну участь у різних процесах обміну речовин в організмі та в метаболічних процесах.Показання до застосуванняФункціональна кардіалгія, неврози, а також як протиблювотний засіб при морській та повітряній хворобі.Протипоказання до застосуванняПідвищена чутливість до компонентів препарату віком до 18 років. Дефіцит сахарази/ізомальтази, непереносимість фруктози, глюкозо-галактозна мальабсорбція (бо препарат містить сахарозу і глюкозу). З обережністю: цукровий діабет (препарат містить сахарозу та глюкозу). Якщо Ви маєте одне з перелічених вище захворювань, перед застосуванням препарату необхідно проконсультуватися з лікарем.Вагітність та лактаціяПризначення препарату під час вагітності та в період грудного вигодовування можливе лише у тому випадку, коли передбачувана користь для матері перевищує потенційний ризик для плода та/або дитини.Побічна діяМожливі: нудота, сльозотеча, запаморочення. При відміні препарату ці побічні явища зазвичай відбуваються самостійно. Можливий розвиток алергічних реакцій (шкірний висип, свербіж шкіри, ангіоневротичний набряк). Якщо будь-які побічні ефекти посилюються, або Ви помітили будь-які інші побічні ефекти, не зазначені в інструкції, повідомте про це лікаря.Взаємодія з лікарськими засобамиПри одночасному застосуванні з лікарськими засобами, що пригнічують центральну нервову систему, посилює дію останніх. Одночасне застосування препарату Валідол із глюкозою з нітратами зменшує головний біль, який виникає при їх застосуванні. Якщо Ви застосовуєте вищезгадані або інші лікарські препарати (у тому числі безрецептурні) перед застосуванням Валідолу з глюкозою проконсультуйтеся з лікарем.Спосіб застосування та дозиПрепарат Валідол з глюкозою призначають дорослим по 1 таблетці під язик до повного розсмоктування. Приймають по 1 таблетці 2-3 рази на день. Кратність та тривалість прийому визначається залежно від ефективності лікування. За відсутності або недостатньої виразності терапевтичного ефекту протягом 5-10 хвилин після прийому необхідно звернутися до лікаря для призначення іншої терапії.ПередозуванняСимптоми: біль голови, нудота, збуджений стан, порушення діяльності серця, різке зниження артеріального тиску, пригнічення центральної нервової системи. Лікування: відміна препарату. Симптоматична терапія. При передозуванні препарату слід звернутися до лікаря.Запобіжні заходи та особливі вказівкиСлід призначати з обережністю пацієнтам із цукровим діабетом, т.к. одна таблетка препарату Валідол із глюкозою містить 0,09 ХЕ (хлібних одиниць). Не рекомендується одночасне вживання алкоголю. Слід не перевищувати максимальних термінів та рекомендованих доз при самостійному застосуванні препарату. Необхідно звернутися до лікаря у разі відсутності зменшення або при обтяженні симптомів захворювання. Вплив на здатність до керування автотранспортом та управління механізмами При прийомі препарату Валідол з глюкозою необхідно дотримуватись обережності при керуванні транспортними засобами та зайнятті іншими потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. активні речовини: левоментолу розчин у ментил ізовалераті [валідол] 0,060 г; декстрози моногідрат [глюкози моногідрат] (у перерахунку на безводну речовину) 0,171 г; допоміжні речовини: повідон – 0,049 г, крохмаль картопляний – 0,023 г, сахароза [цукор] – 0,489 г, кальцію стеарат – 0,008 г до отримання таблетки масою 0,8 г. По 6, 10 таблеток в контурне осередкове пакування з плівки полівінілхлоридної та фольги алюмінієвої друкованої лакованої. По 10, 20, 30, 40, 50, 60 таблеток у банки полімерні. Кожну банку або 1, 2, 3, 4, 5 контурних осередкових упаковок з інструкцією із застосування поміщають у картонну пачку.Опис лікарської формиТаблетки білого або білого з сіруватими вкрапленнями кольору, з характерним запахом ментолу, круглі, плоскоциліндричні, з ризиком та фаскою.Фармакотерапевтична групаКоронародилатируючий засіб рефлекторної дії.ФармакокінетикаПри під'язичному застосуванні абсорбується зі слизової оболонки ротової порожнини, метаболізується в печінці, виводиться нирками у вигляді глюкуронідів.ФармакодинамікаВалідол має заспокійливу дію на центральну нервову систему, а також помірну рефлекторну судинорозширювальну дію, обумовлену подразненням чутливих нервових закінчень. Стимулює вироблення та вивільнення енкефалінів, ендорфінів та інших пептидів, гістаміну, кінінів (за рахунок подразнення рецепторів слизової оболонки), які беруть активну участь у регуляції проникності судин, формуванні больових відчуттів. При сублінгвальному прийомі терапевтичний ефект у середньому настає через 5 хв, причому до 70 % препарату вивільняється протягом 3 хв. Декстроза бере участь у різних процесах обміну речовин в організмі, зокрема посилює окисно-відновні процеси.Показання до застосуванняФункціональна кардіалгія, невроз, синдром "захитування" (нудота, блювання при морській та повітряній хворобі).Протипоказання до застосуванняПідвищена чутливість до компонентів препарату, дефіцит цукрози/ізомальтози, непереносимість фруктози, глюкозо-галактозна мальабсорбція. Вік до 18 років (відсутні дані щодо безпеки та ефективності застосування у дітей). З обережністю: цукровий діабет.Вагітність та лактаціяМожливе застосування препарату у періоди вагітності. Слід утриматися від застосування препарату під час грудного вигодовування.Побічна діяПри тривалому прийомі іноді можуть спостерігатися легка нудота, сльозотеча, запаморочення. Ці явища зазвичай відбуваються самостійно. Якщо будь-які вказані в інструкції побічні ефекти посилюються, або Ви помітили будь-які інші побічні ефекти, не зазначені в інструкції, повідомте про це лікаря.Взаємодія з лікарськими засобамиПри сумісному застосуванні з нейротропними засобами пригнічувального типу дії посилює пригнічуючу дію останніх на центральну нервову систему. Одночасне застосування Валідолу з глюкозою з нітратами зменшує біль голови, який виникає при їх застосуванні.Спосіб застосування та дозиВалідол з глюкозою призначають під язик. Таблетку слід тримати у роті під язиком до повного розчинення. Приймають по 1 таблетці 2-3 десь у день. При недостатньо вираженому ефекті або, коли в окремих хворих протягом 5 хвилин після прийому препарату ефект не спостерігається, необхідно звернутися до лікаря для призначення іншої терапії.ПередозуванняСимптоми: біль голови, нудота, збудження, порушення діяльності серця (зміна частоти скорочень серця), зниження артеріального тиску, пригнічення центральної нервової системи. Лікування: відмінити препарат. Симптоматична терапія.Запобіжні заходи та особливі вказівкиДо складу препарату входять вуглеводи – декстроза, сахароза (1 таблетка містить 0,058 ХЕ вуглеводів), що слід враховувати хворим на цукровий діабет. Вплив на здатність до керування автотранспортом та управління механізмами При прийомі внутрішньо слід бути обережними при керуванні транспортними засобами та іншими механізмами, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Активна речовина: левоментолу розчин у ментил ізовалераті (валідол) 60 мг. Допоміжні речовини: ізомальт – 670 мг, кремнію діоксид колоїдний – 12.5 мг, кальцію стеарат – 7.5 мг. 10 шт. - упаковки осередкові контурні (1) - пачки картонні.Опис лікарської формиПігулки під'язичні; білого або білого з сіруватими вкрапленнями кольору, круглі, плоскоциліндричної форми, з двосторонньою фаскою та ризиком на одному боці, з характерним запахом ментолу.Фармакотерапевтична групаЧинить седативну дію, має помірну рефлекторну судиннорозширювальну дію, обумовлену подразненням чутливих нервових закінчень. Стимулює вироблення та звільнення енкефалінів, ендорфінів та інших пептидів, гістаміну, кінінів (за рахунок подразнення рецепторів слизової оболонки), які беруть активну участь у регуляції проникності судин, формуванні больових відчуттів. При сублінгвальному прийомі терапевтичний ефект у середньому настає через 5 хв, причому до 70% препарату вивільняється протягом 3 хв.Клінічна фармакологіяПрепарат з рефлекторною судинорозширювальною дією.Показання до застосуванняКардіалгія; стенокардія; синдром "захитування" (нудота, блювання при морській та повітряній хворобі); істерія; невроз; біль голови на тлі прийому нітратів.Протипоказання до застосуванняГіперчутливість.Побічна діяНудота, сльозотеча, запаморочення.Спосіб застосування та дозиТаблетки – сублінгвально, по 1 таб. 2-3 рази на добу. Кратність та тривалість прийому визначається залежно від ефективності лікування. За відсутності або недостатньої виразності терапевтичного ефекту протягом найближчих 5-10 хв після прийому необхідне призначення іншої терапії.Запобіжні заходи та особливі вказівкиСлід призначати з обережністю хворим на цукровий діабет (для лікарських форм, що містять цукор).Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
277,00 грн
233,00 грн
Склад, форма випуску та упаковкаКраплі для прийому внутрішньо - 1 мл (22 краплі): активна речовина: доксиламіну сукцинат – 25 мг; допоміжні речовини: етанол 96% - 450 мг; м'ятна олія - 1,4 мг; вода очищена – 449,7 мг. Краплі для вживання, 25 мг/мл. У флаконах-крапельницях коричневого скла, 20 чи 50 мл. Кожен флакон-крапельниця у картонній пачці.Опис лікарської формиКраплі: прозора безбарвна рідина із м'ятним запахом.Фармакотерапевтична групаАнтигістамінне, снодійне, седативне.ФармакокінетикаДоксиламін швидко та практично повністю всмоктується після перорального застосування. Cmax у сироватці крові виявляється через 2-2,4 години після прийому в дозі 25 мг і становить 99 нг/мл. Доксиламін метаболізується переважно у печінці. Основними метаболітами є N-десметил доксиламін, N,N-дидесметил доксиламін та їх N-ацетил-кон'югати. Добре проникає через гістогематичні бар'єри, включаючи гематоенцефалічний бар'єр. T1/2 коливається в межах від 10,1 до 12 год. Основна частина дози (близько 60%) виводиться у незміненому вигляді із сечею, частково – через кишечник.ФармакодинамікаБлокатор Н1-гістамінових рецепторів із групи етаноламінів. Препарат має снодійну, седативну, антигістамінну та м-холіноблокуючу дію. Скорочує час засинання, підвищує тривалість та якість сну, не змінюючи фази сну. Дія починається протягом 30 хв після прийому доксиламіну, його тривалість – 3-6 год.Показання до застосуванняСимптоматичне лікування порушень сну (утруднення засипання та нічні пробудження), що періодично виникають, у пацієнтів старше 18 років. Не всі розлади сну вимагають медикаментозної терапії. Часто розлади сну обумовлені погіршенням стану здоров'я або психічними розладами та можуть бути усунені іншими заходами або безпосереднім лікуванням основного захворювання. Тому не слід проводити лікування хронічних порушень сну (утруднення засипання та нічні пробудження) препаратом Валокордин®-Доксиламін протягом тривалого часу без консультацій з лікарем; у разі рекомендується звернутися до лікаря.Протипоказання до застосуванняпідвищена чутливість до доксиламіну, будь-якого компонента препарату, а також інших антигістамінних препаратів; гострий астматичний напад; закритокутова глаукома; уроджений синдром подовженого інтервалу QT; феохромоцитома; гіперплазія передміхурової залози з порушенням відтоку сечі; гострі отруєння алкоголем та снодійними препаратами, наркотичними анальгетиками, нейролептиками, транквілізаторами, антидепресантами, препаратами літію; епілепсія; одночасний прийом інгібіторів МАО; бронхіальна астма або інші респіраторні захворювання, що характеризуються підвищеною чутливістю дихальних шляхів. Не слід застосовувати Валокордин®-Доксиламін, оскільки в ньому міститься м'ятна олія, вдихання якої може спричинити бронхоспазм; період грудного вигодовування; вік до 18 років. З обережністю: вагітність; печінкова недостатність; алкоголізм; серцева недостатність; артеріальна гіпертензія; бронхоспазм в анамнезі; хронічна задишка; шлунково-стравохідний рефлюкс; пілоростеноз, ахалазія кардії; вік старше 65 років (можливість розвитку запаморочень, небезпека втрати рівноваги та падіння при нічних пробудженнях, а також у зв'язку з можливим збільшенням T1/2 доксиламіну). Валокордин®-Доксиламін необхідно з особливою обережністю призначати пацієнтам з локальним пошкодженням кори головного мозку та судомними нападами в анамнезі, оскільки навіть невеликі дози препарату можуть спровокувати тяжкі напади епілепсії. Рекомендується проводити ЕЕГ. Протисудомна терапія не повинна перериватися під час застосування препарату Валокордин-Доксиламін.Вагітність та лактаціяЕксперименти на тваринах не виявили жодних даних про наявність тератогенних властивостей у доксиламіну, а також зниження фертильності на його фоні. Епідеміологічні дослідження лікарських засобів, що містять доксиламіну сукцинат, не показали розвитку тератогенних ефектів у людей. Тим не менш, Валокордин®-Доксиламін може застосовуватися під час вагітності, тільки коли передбачувана користь для матері перевищує можливий ризик для плода. Годування груддю під час лікування препаратом Валокордин®-Доксиламін має бути припинено, оскільки речовина, що діє, проникає в грудне молоко.Побічна діяЧастота потенційних небажаних реакцій класифікована так: дуже часто (≥1/10); часто (≥1/100 до З боку крові та лімфатичної системи: у виняткових випадках при лікуванні блокаторами H1-гістамінових рецепторів повідомлялося про розвиток лейкопенії, тромбоцитопенії, гемолітичної анемії; дуже рідко – повідомлялося про випадки апластичної анемії та агранулоцитозу. З боку ендокринної системи: у пацієнтів з феохромоцитомою застосування блокаторів H1-гістамінових рецепторів може спричинити підвищення викиду катехоламінів. Психічні розлади: до небажаних реакцій, що залежать від індивідуальної сприйнятливості та прийнятої дози, відносяться зниження швидкості психомоторних реакцій, зниження концентрації уваги, депресія; крім того, можливе виникнення парадоксальних реакцій - занепокоєння, ажитація, тривога, безсоння, нічні кошмари, сплутаність свідомості, галюцинації, тремор. Після тривалого щоденного застосування різке скасування терапії може призвести до рикошетного безсоння. Лікарська залежність. Подібно до інших снодійних засобів, доксиламін може викликати фізичну та психічну залежність. Ризик залежності підвищується із збільшенням дози та тривалості лікування, а також у пацієнтів із алкогольною, наркотичною залежністю (в т.ч. в анамнезі). Рикошетне безсоння. Навіть після коротких курсів прийому доксиламіну, його скасування може призвести до рецидиву безсоння. Тому припиняти лікування слід поступово знижуючи дозу. Антероградна амнезія. Навіть у терапевтичних дозах доксиламін може спричинити антероградну амнезію, особливо протягом першої години після його прийому. Ризик зростає зі збільшенням дози, проте може бути знижений завдяки безперервному сну достатньої тривалості (7-8 годин). З боку нервової системи: запаморочення, сонливість, біль голови; рідко – можливі судоми. Порушення акомодації, підвищення ВГД. З боку органу слуху та рівноваги: шум у вухах. З боку ССС: тахікардія, аритмія, зниження або підвищення артеріального тиску, декомпенсована серцева недостатність. У кількох випадках виявляли зміни на ЕКГ. З боку органів дихання, грудної клітки та середостіння: згущення бронхіального секрету, бронхіальна обструкція, бронхоспазм, що може призвести до порушення функції легень. З боку шлунково-кишкового тракту: автономні небажані реакції, такі як сухість у роті та запор; можуть виникнути нудота, блювання, діарея, зниження або підвищення апетиту, біль у епігастрії; дуже рідко – загрозлива для життя паралітична кишкова непрохідність. З боку печінки та жовчовивідних шляхів: на фоні антигістамінної терапії повідомлялося про порушення функції печінки (холестатична жовтяниця). З боку шкіри та підшкірної клітковини: шкірні алергічні реакції, фотосенсибілізація, порушення терморегуляції. З боку кістково-м'язової системи та сполучної тканини: м'язова слабкість. З боку нирок та сечовивідних шляхів: порушення сечовипускання. Загальні розлади та розлади у місці введення: закладеність носа, втома, млявість. Ретельний індивідуальний підбір добової дози дозволяє знизити частоту та тяжкість небажаних реакцій. Ризик виникнення небажаних реакцій вищий у пацієнтів похилого віку, що може збільшувати у них ризик падінь. Розвиток звикання: регулярне застосування може спричинити зниження ефективності (звикання).Взаємодія з лікарськими засобамиПри одночасному застосуванні препарату Валокордин®-Доксиламін з антидепресантами, барбітуратами, бензодіазепінами, анксіолітиками, седативними препаратами, наркотичними анальгетиками, кодеїновмісними анальгетиками та протикашльовими препаратами, нейролептиками, іншими блокаторами Н1-гістамінів. , талідомідом, баклофеном, пізотифеном посилюється пригнічуюча дія на ЦНС. Застосування доксиламіну призводить до значного збільшення активності CYP2B, а також помірної індукції CYP3A та CYP2A. Не можна виключити можливість взаємодії з лікарськими препаратами, що метаболізуються за участю цих ферментів, наприклад, антиаритмічними засобами, інгібіторами протеази, нейролептиками, бета-адреноблокаторами, імунодепресантами та протиепілептичними препаратами. Оскільки етанол посилює седативну дію більшості блокаторів Н1-гістамінових рецепторів, необхідно уникати одночасного застосування препарату Валокордин®-Доксиламін та лікарських препаратів, що містять етанол, а також вживання алкогольних напоїв. При одночасному застосуванні з препаратами, що володіють м-холіноблокуючою активністю (атропін і атропінсодержащіе спазмолітики, трициклічні антидепресанти, інгібітори МАО, протипаркінсонічні препарати, дизопірамід, фенотіазинові нейролептики), може бути непередбачувано збільшений і пролонгований. реакцій, як затримка сечі, запори, паралітична кишкова непрохідність, сухість у роті, підвищення ВГД. Крім того, комбіноване застосування доксиламіну з інгібіторами МАО може спричинити розвиток артеріальної гіпотензії, пригнічення ЦНС та функції дихання. Прийом антигістамінних препаратів може замаскувати початкові ознаки ураження внутрішнього вуха (дзвін у вухах, запаморочення, затьмарення свідомості), що викликається одночасним прийомом ототоксичних препаратів (такі як аміноглікозиди, саліцилати, сечогінні засоби). У період лікування доксиламіну сукцинатом результати шкірних проб можуть бути помилково негативними. Пацієнтам, які приймають доксиламіну сукцинат, не можна усувати артеріальну гіпотензію епінефрином (адреналін) (можливе парадоксальне посилення вираженості гіпотензії). При шокових станах слід застосовувати норепінефрін (норадреналіну). При одночасному застосуванні з фотосенсибілізуючими лікарськими препаратами може спостерігатися адитивний фотосенсибілізуючий ефект.Спосіб застосування та дозиВсередину з 100-150 мл рідини (вода) за 30 хв - 1 год до бажаного часу настання сну. Якщо лікар не призначений інакше, то разова доза препарату Валокордин®-Доксиламін для пацієнтів старше 18 років становить 22 краплі (відповідає 25 мг доксиламіну сукцинату). При недостатній ефективності терапії доза може бути збільшена до максимальної – 44 краплі (50 мг). Не можна перевищувати максимальну добову дозу. Після прийому препарату Валокордин®-Доксиламін необхідно забезпечити достатню тривалість сну, що дозволить уникнути порушення психомоторних реакцій уранці. При гострих порушеннях сну наскільки можна обмежитися одноразовим застосуванням. Щоб перевірити необхідність продовження лікування при регулярних порушеннях сну, рекомендується не пізніше ніж через 14 днів після початку щоденного застосування перейти до поступового зниження дози. Зазвичай тривалість лікування становить 2-5 днів, максимальна тривалість лікування доксиламіном – 14 днів. Особливі групи пацієнтів Пацієнти з нирковою та/або печінковою недостатністю, а також пацієнти віком від 65 років можуть бути більш сприйнятливими до дії доксиламіну, у зв'язку з чим рекомендується зниження його дози.ПередозуванняСимптоми: денна сонливість, розширення зіниць, парез акомодації, сухість у роті, почервоніння шкіри обличчя та шиї, підвищення температури тіла, синусова тахікардія, розлад свідомості, галюцинації, зниження настрою, підвищена тривожність, порушення координації рухів, тремор , кома. Мимовільні рухи іноді є провісниками судом, що може свідчити про тяжкий ступінь отруєння. Навіть за відсутності судом отруєння доксиламіном можуть спричинити розвиток рабдоміолізу, який часто супроводжується розвитком тяжкої ниркової недостатності. У таких випадках показано стандартну терапію з постійним контролем активності КФК. Є повідомлення про випадок, коли в результаті прийому пацієнтом 500 мг доксиламіну (через стійке безсоння) розвинувся гострий панкреатит та гостра ниркова недостатність. З появою симптомів отруєння слід негайно звернутися до лікаря. Лікування: симптоматична (в т.ч. м-холіноміметики та протисудомні ЛЗ) та підтримуюча терапія (в т.ч. ШВЛ). Як засіб першої допомоги показаний прийом активованого вугілля (дорослим – 50 г, дітям при випадковому передозуванні – 1 г/кг). При внутрішньому прийомі великої кількості препарату - призначення промивання шлунка або індукція блювоти. Аналептики протипоказані, оскільки через можливе зниження судомного порогу, спричинене прийомом препарату Валокордин®-Доксиламін, підвищується ризик виникнення судомного синдрому. При артеріальній гіпотензії не призначають альфа- та бета-адреностимулятори, у т.ч. епінефрін (адреналін), через можливість парадоксального посилення виразності гіпотензії. Доцільним є призначення норепінефрину (норадреналін). Необхідно уникати використання препаратів з бета-адреностимулюючою дією,оскільки вони можуть посилити вазодилатацію. При тяжкому отруєнні (втрата свідомості, серцева аритмія) або виникненні антихолінергічного синдрому (при забезпеченні моніторування ЕКГ) можна застосувати антидот - фізіостигміну саліцилат. При епілептичних нападах, що повторюються, призначають протисудомні препарати. Через підвищений ризик розвитку пригнічення дихання їх призначення можливе лише у випадках, коли є можливість проводити ШВЛ. Ефективність гемодіалізу, гемофільтрації та перитонеального діалізу при передозуванні доксиламіну не вивчена, проте ці методи навряд чи будуть ефективні у зв'язку з великим Vd препаратом. Ефективність форсованого діурезу не встановлено.серцева аритмія) або виникнення антихолінергічного синдрому (при забезпеченні моніторування ЕКГ) можна застосувати антидот - фізостигміну саліцилат. При епілептичних нападах, що повторюються, призначають протисудомні препарати. Через підвищений ризик розвитку пригнічення дихання їх призначення можливе лише у випадках, коли є можливість проводити ШВЛ. Ефективність гемодіалізу, гемофільтрації та перитонеального діалізу при передозуванні доксиламіну не вивчена, проте ці методи навряд чи будуть ефективні у зв'язку з великим Vd препаратом. Ефективність форсованого діурезу не встановлено.серцева аритмія) або виникнення антихолінергічного синдрому (при забезпеченні моніторування ЕКГ) можна застосувати антидот - фізостигміну саліцилат. При епілептичних нападах, що повторюються, призначають протисудомні препарати. Через підвищений ризик розвитку пригнічення дихання їх призначення можливе лише у випадках, коли є можливість проводити ШВЛ. Ефективність гемодіалізу, гемофільтрації та перитонеального діалізу при передозуванні доксиламіну не вивчена, проте ці методи навряд чи будуть ефективні у зв'язку з великим Vd препаратом. Ефективність форсованого діурезу не встановлено.коли є можливість проводити ШВЛ. Ефективність гемодіалізу, гемофільтрації та перитонеального діалізу при передозуванні доксиламіну не вивчена, проте ці методи навряд чи будуть ефективні у зв'язку з великим Vd препаратом. Ефективність форсованого діурезу не встановлено.коли є можливість проводити ШВЛ. Ефективність гемодіалізу, гемофільтрації та перитонеального діалізу при передозуванні доксиламіну не вивчена, проте ці методи навряд чи будуть ефективні у зв'язку з великим Vd препаратом. Ефективність форсованого діурезу не встановлено.Запобіжні заходи та особливі вказівкиВалокордин®-Доксиламін містить 55 об.% етанолу (до 900 мг на дозу (22 краплі), відповідає 21,87 мл пива або 9,11 мл вина), що може становити небезпеку для людей із захворюваннями печінки, алкоголізмом, епілепсією, а також для вагітних жінок. Після прийому препарату слід забезпечити достатній час для сну (профілактика уповільненої психомоторної реакції після пробудження). Як усі снодійні та седативні препарати, доксиламіну сукцинат може посилювати перебіг синдрому нічного апное – збільшувати число та тривалість нападів раптової зупинки дихання уві сні. Під час лікування антигістамінними препаратами потрібний регулярний контроль функції серця, т.к. є повідомлення про зміни ЕКГ, зокрема зміни фази реполяризації. Це особливо важливо для пацієнтів похилого віку та хворих із серцевою недостатністю. Особливу обережність слід виявляти при лікуванні пацієнтів з артеріальною гіпертензією, оскільки антигістамінні препарати можуть підвищувати артеріальний тиск. Вплив на здатність керувати транспортними засобами та робочими механізмами. Даний лікарський препарат (навіть при його належному вживанні) може негативно впливати на здатність активної участі в дорожньому русі або керування іншими механізмами. Особливо при одночасному вживанні лікарського препарату та алкоголю. Тому слід уникати керування автомобілем, обслуговування інших механізмів та будь-якої діяльності в умовах підвищеного ризику, принаймні протягом першої фази лікування. Лікар приймає рішення в кожному конкретному випадку з урахуванням індивідуальної швидкості реакції, призначеної дозування.Умови відпустки з аптекЗа рецептомВідео на цю тему
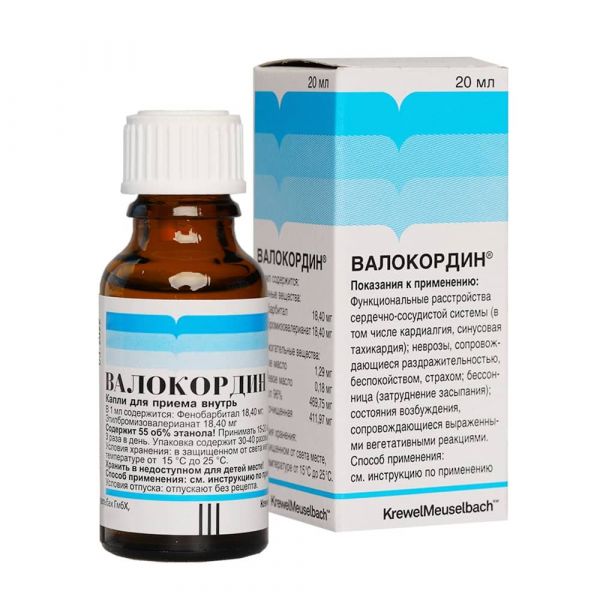
Склад, форма випуску та упаковкаКраплі - 1 мл: Активні речовини: Фенобарбітал – 18,40 мг; Етилбромізовалеріанат - 18,40 мг; Допоміжні речовини: М'ята - 1,29 мг; Хмелева олія – 0,18 мг; Етанол 96% – 469,75 мг; Вода очищена – 411,97 мг. По 20 мл, 50 мл у флакони коричневого скла з крапельницею. Кожен флакон-крапельницю разом з інструкцією із застосування поміщають у картонну пачку.Опис лікарської формиПрозора безбарвна рідина з ароматним запахом.Фармакотерапевтична групаСедативний засіб.ФармакодинамікаВалокордин® – комбінований лікарський засіб, терапевтична дія якого зумовлена фармакологічними властивостями компонентів, що входять до його складу. Фенобарбітал має седативний і м'який снодійний ефект. Сприяє зниженню збудження центральної нервової системи та полегшує настання природного сну. Етилбромізовалеріанат має седативну, снодійну та спазмолітичну дію.Показання до застосуванняФункціональні розлади серцево-судинної системи (у тому числі кардіалгія, синусова тахікардія); неврози, що супроводжуються дратівливістю, занепокоєнням, страхом; безсоння (утруднення засипання); стани збудження, що супроводжуються вираженими вегетативними реакціями.Протипоказання до застосуванняПідвищена чутливість до будь-якого компонента препарату; виражені порушення функції нирок та/або печінки; вагітність, період лактації; дитячий вік до 18 років. З обережністю: захворювання печінки, алкоголізм, черепно-мозкова травма, захворювання мозку т.к. препарат містить етанол.Побічна діяВалокордин®, як правило, добре переноситься навіть при тривалому застосуванні. В окремих випадках, в денний час може спостерігатися сонливість і легке запаморочення. При тривалому застосуванні великих доз можливий розвиток хронічного отруєння бромом, проявами якого бувають депресивний настрій, апатія, риніт, кон'юнктивіт, геморагічний діатез, порушення координації рухів. Рідко при підвищеній чутливості можуть виникнути шкірні реакції. При прояві будь-яких побічних (незвичайних) ефектів, не відображених в інструкції, необхідно повідомити про них лікаря.Взаємодія з лікарськими засобамиПри одночасному застосуванні Валокордіну з седативними засобами – посилення ефекту. Одночасне застосування з нейролептиками та транквілізаторами посилює, а зі стимуляторами центральної нервової системи – послаблює дію кожного з компонентів препарату. Алкоголь посилює ефекти Валокордіну і може підвищувати його токсичність. Наявність у складі Валокордина® фенобарбіталу може індукувати мікросомальні ферменти печінки, і це робить небажаним його одночасне застосування з препаратами, які метаболізуються в печінці, оскільки їх концентрація та, відповідно, ефективність буде змінюватися внаслідок більш прискореного метаболізму (непрямі антикоагулянти, антибіотики та сульф ін) Фенобарбітал послаблює дію похідних кумарину, глюкокортикостероїдів, гризеофульвіну, пероральних контрацептивних засобів.Спосіб застосування та дозиВалокордин приймають внутрішньо, до їди, з невеликою кількістю рідини. Доза встановлюється індивідуально. Дорослим призначають зазвичай по 15-20 крапель 3 десь у день. При порушенні засипання дозу можна збільшити до 30 крапель. Тривалість застосування препарату визначається індивідуально лікарем.ПередозуванняСимптоми: При легкій та середньотяжкій інтоксикації спостерігається сонливість, запаморочення, психомоторні порушення. У тяжких випадках – кома, зниження артеріального тиску, порушення дихання, тахікардія, судинний колапс, зниження периферичних рефлексів. Лікування: Промити шлунок, прийняти активоване вугілля та терміново викликати лікаря.Запобіжні заходи та особливі вказівкиПри необхідності призначення препарату під час лактації слід вирішити питання про припинення грудного вигодовування. Препарат містить 55 об'ємних % етанолу (абсолютний вміст етанолу в максимальній разовій дозі (30 крапель) становить 0,469 грам) та фенобарбітал, тому Валокордин® навіть при правильному застосуванні може послаблювати здатність хворих швидко реагувати у певних ситуаціях, як, наприклад, при перебування на вулиці або під час обслуговування машин. Це особливо виражається при одночасному прийомі алкоголю. При тривалому застосуванні препарату можливе формування лікарської залежності; можливе накопичення брому в організмі та розвиток отруєння ним.Умови відпустки з аптекБез рецептаВідео на цю тему
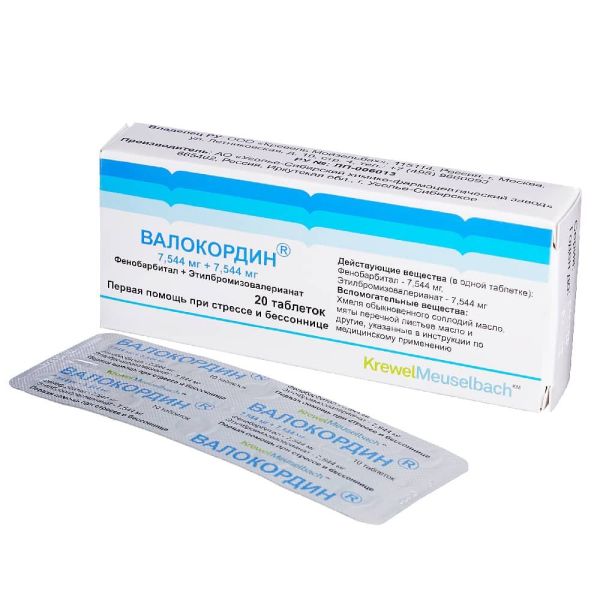
Склад, форма випуску та упаковкаПігулки - 1 таб. діючі речовини: фенобарбітал – 7,544 мг; етилбромізовалеріанат – 7,544 мг; допоміжні речовини: м'яти перцевої листя олія - 0,529 мг; хмелю звичайного супліддя олія - 0,074 мг; бета-циклодекстрин у перерахунку на суху речовину – 55,550 мг; крохмаль картопляний – 13,589 мг; лактози моногідрат – 43,770 мг; целюлоза мікрокристалічна тип 101 - 10,500 мг; кальцію стеарат – 0,900 мг. Пігулки 7,544 мг + 7,544 мг. По 10 таблеток у контурне осередкове впакування. По 1, 2, 3, 5 контурних осередкових упаковок разом з інструкцією із застосування поміщають у пачку з картону.Опис лікарської формиКруглі плоскі таблетки з фаскою білого або майже білого кольору з вкрапленнями з видавленим маркуванням V на одній стороні, з іншого боку гладкі.Фармакотерапевтична групаСедативний засіб.ФармакокінетикаДані щодо фармакокінетики етилбромізовалеріянату відсутні. При внутрішньому прийомі фенобарбітал всмоктується повільно, повністю. Максимальна концентрація у плазмі визначається через 1-2 години, зв'язок з білками плазми – 50 %, у новонароджених – 30-40 %. Метабілізується у печінці, індукує мікросомальні ферменти печінки ізоферментами CYP3A4, CYP3A5, CYP3A7 (швидкість ферментативних реакцій зростає у 10-12 разів). Кумулюється в організмі. Період напіввиведення становить 2 – 4 дні. Виводиться нирками як глюкуроніду, близько 25 % - у постійному вигляді. Проникає у грудне молоко та через плацентарний бар'єр.ФармакодинамікаКомбінований препарат, дія якого зумовлена фармакологічними властивостями компонентів, що входять до його складу. Чинить седативну та спазмолітичну дію. Фенобарбітал має седативну (у низьких дозах), снодійну, міорелаксуючу та спазмолітичну дію. Сприяє зниженню збудження центральної нервової системи та полегшує настання сну, посилює седативну дію іншої діючої речовини. Етилбромізовалеріанат має седативну (подібно ефекту валеріани) і спазмолітичну дію, переважно рецепторів порожнини рота і носоглотки, обумовленим подразненням, зниженням рефлекторної збудливості в центральних відділах нервової системи та посиленням гальмування в нейронах кори та підкіркових структур. прямою місцевою спазмолітичною дією на гладку мускулатуру.Показання до застосуванняЯк симптоматичний заспокійливий засіб при функціональних розладах серцево-судинної системи, при неврозоподібних станах, що супроводжуються підвищеною дратівливістю, порушенням засинання, тахікардії, станом збудження з вираженими вегетативними проявами.Протипоказання до застосуванняПідвищена чутливість до компонентів препарату, гостра печінкова порфірія, спадкова непереносимість лактози, глюкозо-галактозна мальабсорбція, вік до 18 років (ефективність та безпека не встановлені), тяжкі порушення функції нирок та/або печінки, вагітність та період грудного вигодовування. З обережністю Порушення функції нирок та/або печінки; одночасне застосування з препаратами, що метаболізуються у печінці. Якщо у Вас є одне з перелічених захворювань/станів, перед прийомом препарату обов'язково проконсультуйтеся з лікарем.Вагітність та лактаціяЗастосування препарату при вагітності та в період грудного вигодовування протипоказане, оскільки фенобарбітал проникає через плаценту і має тератогенну дію, негативно впливає на формування та подальше функціонування центральної нервової системи плода та новонародженого. Фенобарбітал проникає у грудне молоко. Можливий розвиток фізичної залежності у новонароджених. При необхідності застосування препарату в період лактації грудне вигодовування необхідно припинити.Побічна діяСонливість, запаморочення, уповільнення серцевого ритму, зниження здатності концентрації уваги, алергічні реакції. Можуть виникати порушення шлунково-кишкового тракту. Зазначені явища відбуваються при зниженні дози препарату. При тривалому застосуванні препарату можливий розвиток лікарської залежності, звикання, синдрому «скасування», а також накопичення брому в організмі та розвиток бромізму (депресивний настрій, апатія, риніт, кон'юнктивіт, геморагічний діатез, порушення координації рухів). Дуже рідко можуть виникати реакції підвищеної чутливості (задишка, набряк Квінке, важкі небажані шкірні реакції). Були отримані повідомлення: про знижену мінеральну щільність кісткової тканини; про розвиток остеопенії та остеопорозу; про переломи у пацієнтів, які тривалий час приймали фенобарбітал. Механізм впливу фенобарбіталу на метаболізм кісткової тканини не виявлено. Якщо у Вас є побічні ефекти, зазначені в інструкції із застосування; або вони посилюються; або Ви помітили будь-які інші побічні ефекти, які не вказані в інструкції, необхідно повідомити про це лікаря.Взаємодія з лікарськими засобамиЛікарські засоби, що пригнічують центральну нервову систему, посилюють дію препарату. Етанол посилює дію препарату. Фенобарбітал (індуктор мікросомального окиснення) може знижувати ефективність лікарських засобів, що метаболізуються в печінці (у тому числі похідних кумарину, ламотриджину, гормонів щитовидної залози, доксицикліну, хлорамфеніколу, протигрибкових препаратів (азольного типу), антибіотиків, органо . Препарат може збільшувати токсичність метотрексату. Дія препарату посилюється на фоні застосування вальпроєвої кислоти. Якщо Ви застосовуєте вищезгадані або інші лікарські препарати (у тому числі безрецептурні) перед застосуванням препарату Валокордин проконсультуйтеся з лікарем.Спосіб застосування та дозиВсередину, перед їдою, запивати достатньою кількістю води. Дорослим по 1-2 таблетки 2 рази на добу. При тахікардії разова доза може бути збільшена до 3 таблеток. Максимальна добова доза становить 6 таблеток. Дозування та тривалість застосування препарату встановлюється лікарем індивідуально для кожного хворого. За потреби, будь ласка, проконсультуйтеся з лікарем.ПередозуванняСимптоми: Пригнічення центральної нервової системи, ністагм, атаксія, зниження артеріального тиску, збудження, запаморочення, слабкість, хронічна інтоксикація бромом (депресія, апатія, риніт, кон'юнктивіт, геморагічний діатез, порушення координації рухів). У тяжких випадках – кома, що супроводжується гіпоксією тканин, порушення дихання, тахікардія, аритмія, судинний колапс, зниження периферичних рефлексів. Лікування: припинення прийому препарату, промивання шлунка та симптоматична терапія. При пригніченні центральної нервової системи – кофеїн, нікетамід. Специфічного антидоту немає.Запобіжні заходи та особливі вказівкиПеред застосуванням препарату слід проконсультуватися з лікарем. Досвід застосування препарату у дітей віком до 18 років відсутній. При неконтрольованому застосуванні препарату можливе виникнення лікарської залежності. Під час застосування препарату не слід вживати алкоголю. Вплив на здатність до керування автотранспортом та управління механізмами При застосуванні препарату слід уникати потенційно небезпечних видів діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій (у тому числі керування транспортними засобами, робота з рушійними механізмами).Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаКраплі - 1 мл: Активні речовини: етилбромізовалеріанат – 20 мг; фенобарбітал – 20 мг; Допоміжні речовини: олія м'яти перцевої – 1.4 мг, олія материнки – 0.2 мг, етанол (спирт етиловий) 95% – 520 мг, вода очищена – до 1 мг.Опис лікарської формиКраплі для вживання у вигляді прозорої, безбарвної рідини з характерним запахом.Фармакотерапевтична групаСедативний засіб.ФармакодинамікаКомбінований препарат, дія якого обумовлена властивостями речовин, що входять до його складу. Чинить седативну та спазмолітичну дію. Полегшує настання природного сну. Фенобарбітал має вазодилатуючу, снодійну (у відповідних дозах) та легку гіпотензивну дію, посилює седативний вплив інших компонентів. Етиловий ефір α-бромізовалеріанової кислоти має седативну (подібно до ефекту валеріани) і спазмолітичну дію. Масло м'яти перцевої, що входить до складу деяких комбінованих препаратів як допоміжний компонент, має рефлекторну вазодилатуючу та спазмолітичну дію. До складу деяких препаратів як допоміжні компоненти входять масло шишок хмелю або масло материнки.Показання до застосуванняЯк седативний і судинорозширювальний засіб при безсонні (порушення засипання); кардіалгії; синусової тахікардії; невротичні стани; вегетативної лабільності; дратівливості; іпохондричний синдром; артеріальної гіпертензії (ранні стадії) Як спазмолітичний засіб при спазмах мускулатури органів ШКТ (кишкова та жовчна колька).Протипоказання до застосуванняПечінкова та/або ниркова недостатність тяжкого ступеня; період лактації; - підвищена чутливість до компонентів препарату. З обережністю: вагітність.Вагітність та лактаціяЗ обережністю слід застосовувати при вагітності. За необхідності застосування в період лактації слід вирішити питання про припинення грудного вигодовування.Побічна діяМожливе: сонливість, запаморочення, зниження здатності до концентрації уваги, алергічні реакції. При тривалому застосуванні: розвиток хронічного отруєння бромом (депресія, апатія, риніт, кон'юнктивіт, геморагічний діатез, порушення координації рухів); Лікарська залежність.Взаємодія з лікарськими засобамиСедативні засоби – посилення ефекту. Метотрексат – можливе підвищення токсичності метотрексату. Нейролептики та анксіолітики – можливе посилення дії препарату. Стимулятори ЦНС – ослаблення дії кожного з компонентів препарату. Етанол - посилення ефектів препарату та підвищення його токсичності. Антибіотики, сульфаніламіди – зниження антибактеріальної активності за рахунок наявності у складі препарату фенобарбіталу. Гризеофульвін – зниження ступеня абсорбції та, як наслідок, ослаблення протигрибкової дії (за рахунок наявності у складі препарату фенобарбіталу). Непрямі антикоагулянти, глюкокортикостероїди, доксициклін, естрогени та інші лікарські засоби, що метаболізуються в печінці шляхом окислення - зниження ефективності, т.к. фенобарбітал прискорює їхнє руйнування.Спосіб застосування та дозиПриймають внутрішньо перед прийомом їжі, попередньо розчинивши в невеликій кількості (30-50 мл) води. Дорослим – по 15-30 крапель 2-3 рази на добу. Разова доза за необхідності (наприклад, при тахікардії) може бути збільшена до 40-50 крапель. Дітям - по 3-15 крапель на добу (залежно від віку та клінічної картини захворювання). Тривалість застосування встановлюється лікарем індивідуально.Запобіжні заходи та особливі вказівкиВплив на здатність до керування автотранспортом та управління механізмами У період лікування необхідно дотримуватися обережності при керуванні автотранспортом та зайнятті іншими потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекБез рецептаВідео на цю тему
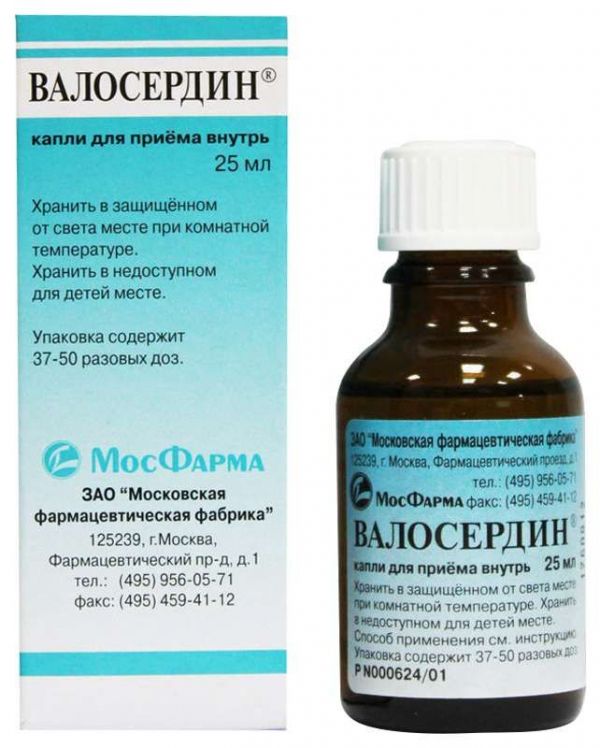
Склад, форма випуску та упаковкаКраплі - 100 р.: Активні речовини: Фенобарбітал – 2,00 г; Етилбромізовалеріанат (Етиловий ефір -бромізовалеріанової кислоти) - 2,00 г; Допоміжні речовини: М'яти перцевої олії - 0,14 г; Іспанська хмелева олія (материни олія) - 0,02 г; Етанол (етиловий спирт) 95% – 52,80 г; Вода очищена – 43,04 г. По 15 мл, 25 мл і 50 мл у флакони-крапельниці оранжевого скла або у флакони скляні з коричневого скла з гвинтовою горловиною, закупорені полімерними пробками-крапельницями і кришками полімерними нагвинчуються або кришками з крапельницею. Кожен флакон-крапельницю або флакон разом з інструкцією із застосування поміщають у пачку з картону.Опис лікарської формиПрозора безбарвна рідина із специфічним ароматичним запахом.Фармакотерапевтична групаСедативний засіб.ФармакодинамікаКомбінований лікарський засіб, терапевтична дія якого зумовлена фармакологічними властивостями компонентів, що входять до його складу. Чинить седативну та спазмолітичну дію. Фенобарбітал має седативний і м'який снодійний ефект. Сприяє зниженню збудження центральної нервової системи та полегшує настання природного сну, посилюючи седативний вплив інших компонентів. Етилбромізовалеріанат має також седативну (подібно до ефекту валеріани) і спазмолітичну дію.Показання до застосуванняВалосердин® призначають як заспокійливий і судинно-розширювальний засіб при функціональних розладах серцево-судинної системи, при неврозоподібних станах, що супроводжуються підвищеною дратівливістю, порушеним засипанням, тахікардією, станом збудження з вираженими вегетативними проявами; як спазмолітичний засіб - при спазмах кишечника.Протипоказання до застосуванняПідвищена чутливість до компонентів препарату; виражені порушення функції нирок та печінки, вагітність, період грудного вигодовування, порфірія, дитячий вік до 18 років. У зв'язку із вмістом абсолютного етилового спирту більше 3,0 г у добовій дозі Валосердин протипоказаний пацієнтам із захворюваннями печінки, алкоголізмом, черепно-мозковою травмою та захворюваннями головного мозку.Побічна діяВалосердин®, як правило, добре переноситься навіть при тривалому застосуванні. В окремих випадках, в денний час може спостерігатися сонливість і легке запаморочення. При тривалому застосуванні великих доз можливий розвиток хронічного отруєння бромом, проявами якого бувають депресивний настрій, апатія, риніт, кон'юнктивіт, геморагічний діатез, порушення координації рухів. При прояві будь-яких побічних (незвичайних) ефектів, не відображених в інструкції із застосування, необхідно повідомити про них лікаря.Взаємодія з лікарськими засобамиПри одночасному застосуванні Валосердіну з седативними засобами – посилення ефекту. Одночасне застосування з нейролептиками та транквілізаторами посилює, а зі стимуляторами центральної нервової системи – послаблює дію кожного з компонентів препарату. Алкоголь посилює ефекти Валосердіну і може підвищувати його токсичність. Наявність у складі фенобарбіталу може індукувати ферменти печінки, і це робить небажаним його одночасне застосування з препаратами, які метаболізуються в печінці, оскільки їх концентрація, а відповідно ефективність знижуватиметься внаслідок більш прискореного метаболізму (непрямі антикоагулянти, антибіотики, сульфаніламіди та ін.). Фенобарбітал послаблює дію похідних кумарину, глюкокортикостероїдів, гризеофульвіну, контрацептивних засобів для внутрішнього прийому. Валосердин може підвищувати токсичність метотрексату.Спосіб застосування та дозиДо їжі, попередньо розчинивши в невеликій кількості (30-50 мл) води. Дорослим призначають зазвичай по 15-20 крапель 3 десь у день. При тахікардії можливе збільшення разової дози до 40-50 крапель. Тривалість застосування препарату визначається індивідуально лікарем.ПередозуванняСимптоми: при легкій та середньотяжкій інтоксикації спостерігається сонливість, запаморочення, психомоторні порушення. У тяжких випадках – кома, зниження артеріального тиску, порушення дихання, тахікардія, судинний колапс, зниження периферичних рефлексів. Лікування: промити шлунок, прийняти активоване вугілля та викликати лікаря.Запобіжні заходи та особливі вказівкиПеред початком застосування препарату слід проконсультуватися з лікарем. При необхідності призначення препарату в період грудного вигодовування слід вирішити питання про припинення грудного вигодовування. При тривалому застосуванні препарату можливе формування лікарської залежності; можливе накопичення брому в організмі та розвиток отруєння ним. Препарат містить не менше 52 об'ємних процентів етанолу. Максимальна разова доза містить 1,03 г абсолютного етилового спирту; максимальна добова доза містить 3,09 г абсолютного етилового спирту. Вплив на здатність до керування автотранспортом та управління механізмами При застосуванні препарату не рекомендується виконання потенційно небезпечних видів діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій (у тому числі, керування транспортними засобами, робота з механізмами, що рухаються).Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаКраплі - 100 мл: Активні речовини: фенобарбітал 2 г, етилбромізовалеріанат (етиловий ефір α-бромізовалеріанової кислоти) 2 г. Допоміжні речовини: олія м'яти перцевої - 0.14 г, олія іспанська хмелева (масло материнки) - 0.02 г, етанол 95% - 52.8 г, вода очищена - 43.04 г. 25 мл - флакони-крапельниці темного скла (1) - пачки картонні.Опис лікарської формиКраплі для прийому внутрішньо; у вигляді прозорої, безбарвної рідини зі слабким ароматичним запахом.Фармакотерапевтична групаКомбінований препарат, терапевтична дія якого зумовлена фармакологічними властивостями компонентів, що входять до його складу. Чинить седативну та спазмолітичну дію. Фенобарбітал ; володіє седативним і м'яким снодійним ефектами. Сприяє зниженню збудження ЦНС та полегшує настання природного сну, посилюючи седативний вплив інших компонентів. Етилбромізовалеріанат ;надає також седативну (подібно ефекту валеріани) і спазмолітичну дію.ФармакокінетикаДані про фармакокінетику не надано.Клінічна фармакологіяФітопрепарат із седативною та спазмолітичною дією.Показання до застосуванняЯк заспокійливий і судинорозширювальний засіб при: функціональних розладах серцево-судинної системи; при неврозоподібних станах, що супроводжуються підвищеною дратівливістю; порушеному засипанні; тахікардії; стан збудження з вираженими вегетативними проявами як спазмолітичний засіб при спазмах кишечника.Протипоказання до застосуванняПідвищена чутливість до компонентів препарату; виражені порушення функції нирок та/або печінки; вагітність; період грудного вигодовування; порфірія; вік до 18 років. У зв'язку із вмістом абсолютного етилового спирту більше 3 г у добовій дозі Валосердин® протипоказаний пацієнтам із захворюваннями печінки, алкоголізмом, черепно-мозковою травмою та іншими захворюваннями головного мозку.Вагітність та лактаціяПротипоказане застосування препарату при вагітності та в період лактації. При необхідності призначення препарату в період грудного вигодовування слід вирішити питання про припинення грудного вигодовування. Застосування у дітей Протипоказано застосування препарату до 18 років.Побічна діяВалосердин®, як правило, добре переноситься навіть при тривалому застосуванні. В окремих випадках, в денні години може спостерігатися сонливість і легке запаморочення. При тривалому застосуванні у великих дозах можливий розвиток хронічного отруєння бромом, проявами якого бувають: депресивний настрій, апатія, риніт, кон'юнктивіт, геморагічний діатез, порушення координації рухів. При прояві будь-яких побічних (незвичайних) ефектів, не відображених в інструкції із застосування, пацієнту необхідно повідомити про них лікаря.Взаємодія з лікарськими засобамиПри одночасному застосуванні препарату Валосердин з седативними засобами – посилення ефекту. Одночасне застосування з нейролептиками та транквілізаторами посилює, а зі стимуляторами ЦНС – послаблює дію кожного з компонентів препарату. Етанол посилює ефекти Валосердіну і може підвищувати його токсичність. Наявність у складі фенобарбіталу може індукувати ферменти печінки, і це робить небажаним одночасне застосування з препаратами, що метаболізуються у печінці, оскільки їх концентрація, а відповідно ефективність буде знижуватися внаслідок більш прискореного метаболізму (непрямі антикоагулянти, антибіотики, сульфаніламіди та інші). Фенобарбітал послаблює дію похідних кумарину, кортикостероїдів, гризеофульвіну, контрацептивних засобів для прийому внутрішньо. Валосердин® може підвищувати токсичність метотрексату.Спосіб застосування та дозиЯк усп Препарат приймають внутрішньо, до їди, попередньо розчинивши у невеликій кількості (30-50 мл) води. Дорослим; призначають зазвичай по 15-20 крапель 3 рази на добу. При тахікардії можливе збільшення разової дози до 40-50 крапель. Тривалість застосування препарату визначається індивідуально лікарем. ського засобу при спазмах кишківника.ПередозуванняСимптоми: ;при легкій та середньотяжкій інтоксикації спостерігається сонливість, запаморочення, психомоторні порушення. У тяжких випадках – кома, зниження артеріального тиску, порушення дихання, тахікардія, судинний колапс, зниження периферичних рефлексів. Лікування: промити шлунок, прийняти активоване вугілля і викликати лікаря.Запобіжні заходи та особливі вказівкиПеред початком застосування препарату необхідно проконсультуватися з лікарем. При тривалому застосуванні препарату можливе формування лікарської залежності; можливе накопичення брому в організмі та розвиток отруєння ним. Препарат містить не менше 52 об.% етанолу. Максимальна разова доза містить 1.03 г абсолютного етилового спирту; максимальна добова доза містить 3,09 г абсолютного етилового спирту. Вплив на здатність до керування автотранспортом та управління механізмами При застосуванні препарату не рекомендується виконання потенційно небезпечних видів діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій (в т.ч. керування транспортними засобами, робота з механізмами, що рухаються).Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. вальпроат натрію 200/333 мг і вальпроєва кислота 87/145 мг [екв. вальпроату натрію 300,27/500,11 мг]; Допоміжні речовини: кремнію діоксид колоїдний 2,4/4 мг, гіпромелоза 105,4/176 мг, етилцелюлоза (20 cps) 7,2/12 мг, кремнію діоксиду гідрат 30/50 мг, натрію сахаринат 6/10 мг; Плівкова оболонка I: гіпромелоза 3,79/5,03 мг, гліцерол 1,48/1,96 мг, титану діоксид 0,23/0,31 мг; Плівкова оболонка II: гіпромелоза 1,15/1,72 мг, бутилметакрилату диметиламіноетилметакрилату та метилметакрилату сополімер [1:2:1] 2,59/3,82 мг, метилметакрилату та етилакрилату сополімер [2:1] 1,42/2, 12 мг, макрогол-1500 0,87/1,28 мг, тальк 0,23/3,52 мг, титану діоксид 0,24/0,24 мг. По 10 таблеток у стрип із алюмінієвої фольги. По 3, 5 або 10 стрипів разом з інструкцією із застосування в картонну пачку.Опис лікарської формиБіла, кругла, двоопукла таблетка, покрита плівковою оболонкою; вид на зламі: зовнішнє кільце оболонки, а також ядро таблетки білого кольору.Фармакотерапевтична групаПротиепілептичний засіб.ФармакокінетикаБіодоступність препарату – близько 100%. Розподіляється переважно в кров та позаклітинну рідину. Вальпроєва кислота проникає в спинномозкову рідину та через гематоенцефалічний бар'єр. Період напіввиведення становить 15-17 годин. Терапевтична ефективність проявляється при концентрації у плазмі крові від 40 до 100 мг/л. При рівнях понад 200 мг/л потрібне зниження дози. Рівноважна концентрація у плазмі досягається через 3-4 дні прийому. Зв'язок із білками плазми - 90-95% (при концентрації у плазмі до 50 мг/л), при концентрації 50-100 мг/л знижується до 80-85%; при уремії, гіпопротеїнемії та цирозі печінки зв'язування з білками плазми також знижено. Виводиться в основному із сечею у вигляді глюкуроніду та шляхом бета-окислення у кон'югованому вигляді. Вальпроєва кислота є індуктором ферментів метаболічної системи цитохрому Р450. На відміну від більшості інших протиепілептичних препаратів, не впливає на рівень як власної біотрансформації, так і на біотрансформацію інших речовин, таких як естрогени, прогестагени та антагоністи вітаміну К. Пролонгована форма характеризується відсутністю часу затримки всмоктування, пролонгованої абсорбцією, ідентичною біодоступністю, нижчою (на 25%), але відносно стабільнішою концентрацією в плазмі між 4 і 14 год після прийому, більш лінійною кореляцією між дозою та концентрацією препарату в плазмі.ФармакодинамікаПротиепілептичний препарат, має центральну міорелаксуючу та седативну дію. Виявляє протиепілептичну активність при різних типах епілепсії. Основний механізм дії, мабуть, пов'язаний із впливом вальпроєвої кислоти на ГАМК-ергічну систему: препарат підвищує вміст ГАМК у центральній нервовій системі (ЦНС) та активує ГАМК-ергічну передачу. Терапевтична ефективність починається з мінімальної концентрації 40-50 мг/л та може досягати 100 мг/л. При концентрації понад 200 мг/л необхідне зменшення дози.Показання до застосуванняУ дорослих як монотерапія або в комбінації з іншими протиепілептичними засобами: лікування генералізованих епілептичних нападів (клонічні, тонічні, тоніко-клонічні, абсанси, міоклонічні, атонічні); синдром Леннокса-Гасто; лікування парціальних, епілептичних нападів (парціальні напади із вторинною генералізацією або без неї); лікування та профілактика біполярних афективних розладів. У дітей як монотерапія або в комбінації з іншими протиепілептичними засобами: лікування генералізованих епілептичних нападів (клонічні, тонічні, тоніко-клонічні, абсанси, міоклонічні, атонічні); синдром Леннокса-Гасто; лікування парціальних епілептичних нападів (парціальні напади із вторинною генералізацією або без неї).Протипоказання до застосуванняПідвищена чутливість до вальпроєвої кислоти або інших компонентів препарату; гострий гепатит; хронічний гепатит; захворювання печінки в анамнезі, порфірія; комбінація з мефлохіном; комбінація зі звіробою продірявленим; дитячий вік до 3 років; не рекомендується застосовувати у комбінації з ламотриджином. З обережністю: пригнічення кістковомозкового кровотворення (лейкопенія, тромбоцитопенія, анемія), органічні захворювання головного мозку, захворювання печінки та підшлункової залози в анамнезі, гіпопротеїнемія, розумова відсталість у дітей, вроджені ферментопатії, ниркова недостатність.Вагітність та лактаціяУ дослідженнях на тваринах доведено тератогенну дію. За наявними даними у людини вальпроєва кислота переважно спричиняє порушення розвитку нервової трубки: мієломенінгоцеле, ущелина хребта (1-2%). Описано випадки лицьової дисморфії та вад розвитку кінцівок (особливо вкорочення кінцівок), а також вади розвитку серцево-судинної системи. Ризик вад розвитку вище при комбінованій протиепілептичній терапії, ніж при монотерапії вальпроєвою кислотою. Враховуючи вищевикладене, при вагітності застосування препарату можливе лише в тому випадку, коли ймовірна користь для матері перевершує потенційний ризик для плода. У період вагітності не слід переривати протиепілептичне лікування вальпроєвою кислотою, якщо воно є ефективним. У разі рекомендується монотерапія; мінімальну ефективну добову дозу слід розділити на два прийоми. На додаток до протиепілептичної терапії можуть бути додані препарати фолієвої кислоти (доза 5 мг/суг), т.к. вони дозволяють мінімізувати ризик виникнення вад розвитку нервової трубки. Вальпроєва кислота може викликати геморагічний синдром у новонароджених, що, мабуть, пов'язане з гіпофібриногенемією. Були відзначені випадки розвитку афібриногенемії з летальним кінцем. Вальпроєва кислота виділяється з грудним молоком у концентраціях від 1% до 10%. Рекомендується припинити грудне вигодовування на час прийому препарату.Побічна діяЗ боку центральної нервової системи: Атаксія; випадки когнітивних порушень із прогресуючим настанням аж до розвитку повної картини синдрому деменції (оборотні протягом декількох тижнів або місяців після відміни препарату); стану сплутаності свідомості чи конвульсій; ступор або летаргія, що іноді призводила до минущої коми (енцефалопатія); оборотний паркінсонізм; головний біль, запаморочення, легкий постуральний тремор і сонливість, зміни поведінки, настрою чи психічного стану (депресія, почуття втоми, галюцинації, агресивність, гіперактивний стан, психози, незвичайне збудження, рухове занепокоєння чи дратівливість), дизартрія. З боку травної системи: часто на початку лікування – гастроінтестинальні порушення (нудота, блювання, гастралгія, зниження апетиту або підвищення апетиту, діарея), які зазвичай проходять протягом кількох днів без відміни препарату; порушення функції печінки; панкреатит, аж до тяжких уражень із летальним кінцем (у перші 6 місяців лікування, частіше на 2-12 тижні). З боку органів кровотворення та системи гемостазу: пригнічення кістковомозкового кровотворення (анемія, лейкопенія або панцитопенія); тромбоцитопенія, зниження вмісту фібриногену та агрегації тромбоцитів, що призводять до розвитку гіпокоагуляції (супроводжується подовженням часу кровотечі, петехіальними крововиливами, синцями, гематомами, кровоточивістю та ін.). З боку сечовивідної системи: енурез; випадки оборотного синдрому Фанконі (неясного генезу). З боку ендокринної системи дисменорея, вторинна аменорея, збільшення молочних залоз, галакторея. Алергічні реакції: висипання на шкірі, кропив'янка, васкуліт; ангіоневротичний набряк, фотосенсибілізація, випадки токсичного епідермального некролізу, синдром Стівенса-Джонсона, багатоформної еритеми. Лабораторні показники: ізольована та помірна гіперамоніємія без змін в аналізах функцій печінки, особливо при політерапії (скасування препарату не потрібно); можлива гіперамоніємія, пов'язана з неврологічними симптомами (потрібне подальше обстеження); можливе підвищення активності "печінкових" трансаміназ; зниження рівня фібриногену або збільшення часу кровотечі, зазвичай без клінічних проявів і особливо при високих дозах (вальпроєва кислота має інгібуючу дію на другу стадію агрегації тромбоцитів); гіпонатріємія. Інші: тератогенний ризик; диплопія, ністагм, миготіння "мушок" перед очима, алопеція; оборотна або необоротна втрата слуху; периферичні набряки; збільшення маси тіла (оскільки збільшення маси тіла є фактором ризику синдрому полікістозу яєчників, рекомендується ретельний контроль за станом таких пацієнтів); Порушення менструального циклу, аменорея.Взаємодія з лікарськими засобамиПротипоказані комбінації Мефлохін: ризик епілептичних нападів у хворих на епілепсію у зв'язку з посиленням метаболізму вальпроєвої кислоти та конвульсантним мефлохіном. Звіробій продірявлений: небезпека зниження концентрації вальпроєвої кислоти у плазмі крові. Нерекомендовані комбінації Ламотриджин: підвищений ризик тяжких реакцій шкіри аж до розвитку токсичного епідермального некролізу. Крім того, підвищення концентрації ламотриджину в плазмі (його метаболізм у печінці сповільнюється вальпроєвою кислотою). Якщо комбінація необхідна, потрібний ретельний клінічний та лабораторний контроль. Комбінації, що вимагають особливих застережень Карбамазепін: підвищення концентрації активного метаболіту карбамазепіну у плазмі з ознаками передозування. Крім того, зниження концентрації вальпроєвої кислоти у плазмі, пов'язане з посиленням метаболізму вальпроєвої кислоти у печінці під дією карбамазепіну. Рекомендується: клінічне спостереження, визначення концентрацій препаратів у плазмі та, можливо, корекція їх дози, особливо на початку лікування. Карбапенеми, монобактами: меропенем, паніпенем, та, за екстраполяцією, азтреонами та іміпенем: підвищенням ризику появи судом у зв'язку зі зниженням концентрації вальпроєвої кислоти в плазмі крові. Рекомендується: клінічне спостереження, визначення концентрацій препаратів у плазмі крові, може знадобитися корекція дози вальпроєвої кислоти під час лікування антибактеріальним засобом та після його відміни. Фелбамат: підвищення концентрації вальпроєвої кислоти у плазмі з ризиком передозування. Рекомендується: клінічний та лабораторний контроль та, можливо, перегляд дози вальпроєвої кислоти в ході лікування фелбаматом та після його відміни). Фенобарбітал, примідон: підвищення концентрації фенобарбіталу та примідону у плазмі з ознаками передозування, зазвичай у дітей. Крім того, зниження концентрації вальпроєвої кислоти у плазмі, пов'язане з посиленням її печінкового метаболізму під впливом фенобарбіталу або примідону. Рекомендується: клінічний моніторинг протягом перших 15 днів комбінованого лікування з негайним зменшенням дози фенобарбіталу або примідону з появою перших ознак седації, визначення концентрацій обох протисудомних препаратів у крові. Фенітоїн: зміна концентрації фенітоїну в плазмі, небезпека зниження концентрації вальпроєвої кислоти, пов'язаного з посиленням метаболізму вальпроєвої кислоти у печінці під впливом фенітоїну. Рекомендується: клінічний моніторинг із визначенням концентрацій обох протиепілептичних препаратів у плазмі та при необхідності – корекція їх доз. Топірамат: ризик розвитку гіперамоніємії або енцефалопатії. Рекомендується: клінічний та лабораторний контроль протягом першого місяця лікування та у разі виникнення симптомів амоніємії. Нейролептики, інгібітори моноаміноксидази (МАО), антидепресанти, бензодіазепіни: вальпроєва кислота потенціює дію психотропних препаратів, таких як нейролептики, інгібітори МАО, антидепресанти, бензодіазепіни. Рекомендується: клінічний моніторинг та при необхідності корекція дози препарату. Циметидин та еритроміцин: підвищується концентрація вальпроєвої кислоти у плазмі крові. Зідовудін: вальпроєва кислота може підвищувати концентрацію зидовудину в плазмі, що призводить до підвищення токсичності зидовудину. Комбінації, які слід брати до уваги Німодипін (перорально і, за екстраполяцією, парентерально): посилення гіпотензивного ефекту німодипіну внаслідок зменшення його метаболізму під впливом вальпроєвої кислоти та підвищення концентрації у плазмі крові. Ацетилсаліцилова кислота: посилення ефектів вальпроєвої кислоти внаслідок підвищення її концентрації у плазмі крові. При одночасному застосуванні з антикоагулянтами антагоністів вітаміну К потрібний ретельний моніторинг протромбінового індексу. Інші форми взаємодій Вальпроєва кислота не має фермент-індукувального ефекту і тому не впливає на ефективність гормональних контрацептивів, що містять комбінації естрогену та прогестерону.Спосіб застосування та дозиВальпарин ХР призначений для прийому внутрішньо. Добову дозу рекомендується приймати в один або два прийоми, переважно під час їди. Застосування 1 прийом можливе при добре контрольованій епілепсії. Таблетки приймають не роздавлюючи і не розжовуючи, запиваючи невеликою кількістю води. Початкова доза при монотерапії для дорослих та дітей з масою тіла понад 25 кг: 5-15 мг/кг/добу; потім цю дозу поступово підвищують на 5-10 Мг/кг/тиж. Максимальна доза - 30 мг/кг/добу (може бути збільшена за можливості організації контролю за концентрацією в плазмі до 60 мг/кг/добу). При комбінованій терапії у дорослих: 10-30 мг/кг/добу з подальшим підвищенням дози на 5-10 мг/кг/тиж. Дітям при масі тіла менше 25 кг: середня добова доза при монотерапії – 15-45 мг/кг, максимальна – 50 мг/кг. При комбінованій терапії – 30-100 мг/кг/добу. У пацієнтів похилого віку дозу слід встановлювати відповідно до їх клінічного стану. Добова доза визначається залежно від віку та маси тіла пацієнта, а також з урахуванням індивідуальної чутливості до вальпроєвої кислоти. Встановлено хорошу кореляцію між добовою дозою, концентрацією препарату у сироватці та терапевтичним ефектом: дозу слід встановлювати на основі клінічної відповіді. Визначення рівня вальпроєвої кислоти в плазмі можна розглядати як доповнення до клінічного спостереження, коли епілепсія не піддається контролю, або є підозра на побічні ефекти. Діапазон концентрацій, у яких спостерігається клінічний ефект, зазвичай становить 40-100 мг/л (300-700 мкмоль/л). При переході з таблеток негайного вивільнення вальпроєвої кислоти, які забезпечували необхідний контроль над захворюванням, на форму пролонгованої дії (Вальпарин ХР) слід зберігати добову дозу: Заміну інших протиепілептичних препаратів на Вальпарин ХР слід проводити поступово, досягаючи оптимальної дози вальпроєвої кислоти приблизно протягом 2 тижнів. При цьому, залежно від стану пацієнта, зменшується доза попереднього препарату. Для пацієнтів, які не приймають інші протиепілептичні препарати, дози слід збільшувати через 2-3 дні для того, щоб досягти оптимальної дози приблизно протягом тижня. При необхідності комбінації з іншими протиепілептичними засобами слід вводити поступово.ПередозуванняСимптоми: грудка з м'язовою гіпотонією, гіпорефлексією, міозом, пригніченням дихання, метаболічним ацидозом; описано випадки внутрішньочерепної гіпертензії, пов'язаної з набряком мозку. Лікування: у стаціонарі – промивання шлунка, якщо після прийому препарату пройшло не більше 10-12 год; спостереження за станом серцево-судинної та дихальної систем та підтримання ефективного діурезу. У дуже тяжких випадках проводять діаліз. Як правило, прогноз сприятливий, проте було описано кілька випадків детального результату.Запобіжні заходи та особливі вказівкиДо початку лікування та протягом перших 6 місяців терапії потрібен періодичний контроль функції печінки, особливо у пацієнтів групи ризику. Серед класичних тестів найбільш важливими є тести, що відображають синтез білка в печінці, і особливо - протромбіновий індекс. При значному зниженні концентрації протромбіну, вираженому зменшенні вмісту фібриногену, факторів згортання крові, підвищенні концентрації білірубіну та активності трансаміназ, лікування препаратом Вальпарин ХР слід призупинити. Якщо пацієнт отримує одночасно саліцилати, їх слід також негайно скасувати, оскільки саліцилати і вальпроєва кислота мають спільні шляхи метаболізму. Ризик розвитку побічних ефектів з боку печінки підвищений під час проведення комбінованої протисудомної терапії, а також у дітей. Рання діагностика базується переважно на клінічному обстеженні. Зокрема, слід брати до уваги два фактори, які можуть передувати жовтяниці, особливо у пацієнтів, які становлять групу ризику: неспецифічні загальні симптоми, які зазвичай з'являються раптово, такі як астенія, анорексія, крайня втома, сонливість, іноді супроводжуються повторюваною блювотою і болями в животі; рецидив епілептичних нападів на фоні протиепілептичної терапії Слід попередити пацієнта, а якщо це дитина, то її сім'ю, про необхідність негайно повідомити лікаря про виникнення зазначених симптомів. Крім клінічного обстеження у разі слід негайно провести аналіз функції печінки. У поодиноких випадках відзначалися важкі форми панкреатиту, іноді - з летальним кінцем. Ці випадки спостерігали незалежно від віку пацієнта та тривалості лікування, хоча ризик розвитку панкреатиту знижувався зі збільшенням віку хворих. Недостатність функції печінки при панкреатиті підвищує ризик смерті. Слід наголосити, що при лікуванні як препаратом Вальпарин ХР, так і іншими протиепілептичними препаратами, може спостерігатися невелике ізольоване та тимчасове підвищення активності трансаміназ, особливо на початку лікування, за відсутності будь-яких клінічних симптомів. У цьому випадку рекомендується провести більш повне обстеження (що включає, зокрема, визначення протромбінового індексу) для того, щоб при необхідності переглянути дозу та повторити аналізи в залежності від зміни параметрів. Перед початком терапії, перед хірургічним втручанням, у разі виникнення гематом або спонтанних кровотеч необхідний загальний аналіз крові (включаючи визначення кількості тромбоцитів, часу кровотечі та показників коагулограми). При виникненні на фоні лікування симптоматики "гострого" живота та таких шлунково-кишкових симптомів, як нудота, блювання та/або анорексія необхідно визначити активність амілази в крові для виключення гострого панкреатиту. При підвищеній активності ферментів підшлункової залози препарат слід відмінити, вживаючи альтернативних терапевтичних заходів. При застосуванні Вальпарину ХР у пацієнтів з нирковою недостатністю рекомендується враховувати підвищену концентрацію вільної форми вальпроєвої кислоти у плазмі крові та знизити дозу. При необхідності призначення препарату пацієнтам із системним червоним вовчаком та іншими захворюваннями імунної системи слід оцінити очікуваний лікувальний ефект та можливий ризик терапії, оскільки при застосуванні Вальпарину® ХР у рідкісних випадках відзначалися порушення імунної системи. Не рекомендується призначати препарат пацієнтам із дефіцитом ферментів карбамідного циклу. У таких хворих було описано кілька випадків гіперамоніємії, що супроводжується ступором та/або комою. Під час лікування не допускається прийом напоїв, які містять етанол. Пацієнтів необхідно попередити про ризик збільшення маси тіла на початку лікування та рекомендувати дотримання дієти для мінімізації такого впливу. Вплив на здатність до керування автотранспортом та управління механізмами У період лікування пацієнтам необхідно дотримуватися обережності при керуванні автотранспортом та іншою діяльністю, що потребує високої концентрації уваги та швидкості психомоторних реакцій.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. вальпроат натрію 200/333 мг і вальпроєва кислота 87/145 мг [екв. вальпроату натрію 300,27/500,11 мг]; Допоміжні речовини: кремнію діоксид колоїдний 2,4/4 мг, гіпромелоза 105,4/176 мг, етилцелюлоза (20 cps) 7,2/12 мг, кремнію діоксиду гідрат 30/50 мг, натрію сахаринат 6/10 мг; Плівкова оболонка I: гіпромелоза 3,79/5,03 мг, гліцерол 1,48/1,96 мг, титану діоксид 0,23/0,31 мг; Плівкова оболонка II: гіпромелоза 1,15/1,72 мг, бутилметакрилату диметиламіноетилметакрилату та метилметакрилату сополімер [1:2:1] 2,59/3,82 мг, метилметакрилату та етилакрилату сополімер [2:1] 1,42/2, 12 мг, макрогол-1500 0,87/1,28 мг, тальк 0,23/3,52 мг, титану діоксид 0,24/0,24 мг. По 10 таблеток у стрип із алюмінієвої фольги. По 3, 5 або 10 стрипів разом з інструкцією із застосування в картонну пачку.Опис лікарської формиБіла, кругла, двоопукла таблетка, покрита плівковою оболонкою; вид на зламі: зовнішнє кільце оболонки, а також ядро таблетки білого кольору.Фармакотерапевтична групаПротиепілептичний засіб.ФармакокінетикаБіодоступність препарату – близько 100%. Розподіляється переважно в кров та позаклітинну рідину. Вальпроєва кислота проникає в спинномозкову рідину та через гематоенцефалічний бар'єр. Період напіввиведення становить 15-17 годин. Терапевтична ефективність проявляється при концентрації у плазмі крові від 40 до 100 мг/л. При рівнях понад 200 мг/л потрібне зниження дози. Рівноважна концентрація у плазмі досягається через 3-4 дні прийому. Зв'язок із білками плазми - 90-95% (при концентрації у плазмі до 50 мг/л), при концентрації 50-100 мг/л знижується до 80-85%; при уремії, гіпопротеїнемії та цирозі печінки зв'язування з білками плазми також знижено. Виводиться в основному із сечею у вигляді глюкуроніду та шляхом бета-окислення у кон'югованому вигляді. Вальпроєва кислота є індуктором ферментів метаболічної системи цитохрому Р450. На відміну від більшості інших протиепілептичних препаратів, не впливає на рівень як власної біотрансформації, так і на біотрансформацію інших речовин, таких як естрогени, прогестагени та антагоністи вітаміну К. Пролонгована форма характеризується відсутністю часу затримки всмоктування, пролонгованої абсорбцією, ідентичною біодоступністю, нижчою (на 25%), але відносно стабільнішою концентрацією в плазмі між 4 і 14 год після прийому, більш лінійною кореляцією між дозою та концентрацією препарату в плазмі.ФармакодинамікаПротиепілептичний препарат, має центральну міорелаксуючу та седативну дію. Виявляє протиепілептичну активність при різних типах епілепсії. Основний механізм дії, мабуть, пов'язаний із впливом вальпроєвої кислоти на ГАМК-ергічну систему: препарат підвищує вміст ГАМК у центральній нервовій системі (ЦНС) та активує ГАМК-ергічну передачу. Терапевтична ефективність починається з мінімальної концентрації 40-50 мг/л та може досягати 100 мг/л. При концентрації понад 200 мг/л необхідне зменшення дози.Показання до застосуванняУ дорослих як монотерапія або в комбінації з іншими протиепілептичними засобами: лікування генералізованих епілептичних нападів (клонічні, тонічні, тоніко-клонічні, абсанси, міоклонічні, атонічні); синдром Леннокса-Гасто; лікування парціальних, епілептичних нападів (парціальні напади із вторинною генералізацією або без неї); лікування та профілактика біполярних афективних розладів. У дітей як монотерапія або в комбінації з іншими протиепілептичними засобами: лікування генералізованих епілептичних нападів (клонічні, тонічні, тоніко-клонічні, абсанси, міоклонічні, атонічні); синдром Леннокса-Гасто; лікування парціальних епілептичних нападів (парціальні напади із вторинною генералізацією або без неї).Протипоказання до застосуванняПідвищена чутливість до вальпроєвої кислоти або інших компонентів препарату; гострий гепатит; хронічний гепатит; захворювання печінки в анамнезі, порфірія; комбінація з мефлохіном; комбінація зі звіробою продірявленим; дитячий вік до 3 років; не рекомендується застосовувати у комбінації з ламотриджином. З обережністю: пригнічення кістковомозкового кровотворення (лейкопенія, тромбоцитопенія, анемія), органічні захворювання головного мозку, захворювання печінки та підшлункової залози в анамнезі, гіпопротеїнемія, розумова відсталість у дітей, вроджені ферментопатії, ниркова недостатність.Вагітність та лактаціяУ дослідженнях на тваринах доведено тератогенну дію. За наявними даними у людини вальпроєва кислота переважно спричиняє порушення розвитку нервової трубки: мієломенінгоцеле, ущелина хребта (1-2%). Описано випадки лицьової дисморфії та вад розвитку кінцівок (особливо вкорочення кінцівок), а також вади розвитку серцево-судинної системи. Ризик вад розвитку вище при комбінованій протиепілептичній терапії, ніж при монотерапії вальпроєвою кислотою. Враховуючи вищевикладене, при вагітності застосування препарату можливе лише в тому випадку, коли ймовірна користь для матері перевершує потенційний ризик для плода. У період вагітності не слід переривати протиепілептичне лікування вальпроєвою кислотою, якщо воно є ефективним. У разі рекомендується монотерапія; мінімальну ефективну добову дозу слід розділити на два прийоми. На додаток до протиепілептичної терапії можуть бути додані препарати фолієвої кислоти (доза 5 мг/суг), т.к. вони дозволяють мінімізувати ризик виникнення вад розвитку нервової трубки. Вальпроєва кислота може викликати геморагічний синдром у новонароджених, що, мабуть, пов'язане з гіпофібриногенемією. Були відзначені випадки розвитку афібриногенемії з летальним кінцем. Вальпроєва кислота виділяється з грудним молоком у концентраціях від 1% до 10%. Рекомендується припинити грудне вигодовування на час прийому препарату.Побічна діяЗ боку центральної нервової системи: Атаксія; випадки когнітивних порушень із прогресуючим настанням аж до розвитку повної картини синдрому деменції (оборотні протягом декількох тижнів або місяців після відміни препарату); стану сплутаності свідомості чи конвульсій; ступор або летаргія, що іноді призводила до минущої коми (енцефалопатія); оборотний паркінсонізм; головний біль, запаморочення, легкий постуральний тремор і сонливість, зміни поведінки, настрою чи психічного стану (депресія, почуття втоми, галюцинації, агресивність, гіперактивний стан, психози, незвичайне збудження, рухове занепокоєння чи дратівливість), дизартрія. З боку травної системи: часто на початку лікування – гастроінтестинальні порушення (нудота, блювання, гастралгія, зниження апетиту або підвищення апетиту, діарея), які зазвичай проходять протягом кількох днів без відміни препарату; порушення функції печінки; панкреатит, аж до тяжких уражень із летальним кінцем (у перші 6 місяців лікування, частіше на 2-12 тижні). З боку органів кровотворення та системи гемостазу: пригнічення кістковомозкового кровотворення (анемія, лейкопенія або панцитопенія); тромбоцитопенія, зниження вмісту фібриногену та агрегації тромбоцитів, що призводять до розвитку гіпокоагуляції (супроводжується подовженням часу кровотечі, петехіальними крововиливами, синцями, гематомами, кровоточивістю та ін.). З боку сечовивідної системи: енурез; випадки оборотного синдрому Фанконі (неясного генезу). З боку ендокринної системи дисменорея, вторинна аменорея, збільшення молочних залоз, галакторея. Алергічні реакції: висипання на шкірі, кропив'янка, васкуліт; ангіоневротичний набряк, фотосенсибілізація, випадки токсичного епідермального некролізу, синдром Стівенса-Джонсона, багатоформної еритеми. Лабораторні показники: ізольована та помірна гіперамоніємія без змін в аналізах функцій печінки, особливо при політерапії (скасування препарату не потрібно); можлива гіперамоніємія, пов'язана з неврологічними симптомами (потрібне подальше обстеження); можливе підвищення активності "печінкових" трансаміназ; зниження рівня фібриногену або збільшення часу кровотечі, зазвичай без клінічних проявів і особливо при високих дозах (вальпроєва кислота має інгібуючу дію на другу стадію агрегації тромбоцитів); гіпонатріємія. Інші: тератогенний ризик; диплопія, ністагм, миготіння "мушок" перед очима, алопеція; оборотна або необоротна втрата слуху; периферичні набряки; збільшення маси тіла (оскільки збільшення маси тіла є фактором ризику синдрому полікістозу яєчників, рекомендується ретельний контроль за станом таких пацієнтів); Порушення менструального циклу, аменорея.Взаємодія з лікарськими засобамиПротипоказані комбінації Мефлохін: ризик епілептичних нападів у хворих на епілепсію у зв'язку з посиленням метаболізму вальпроєвої кислоти та конвульсантним мефлохіном. Звіробій продірявлений: небезпека зниження концентрації вальпроєвої кислоти у плазмі крові. Нерекомендовані комбінації Ламотриджин: підвищений ризик тяжких реакцій шкіри аж до розвитку токсичного епідермального некролізу. Крім того, підвищення концентрації ламотриджину в плазмі (його метаболізм у печінці сповільнюється вальпроєвою кислотою). Якщо комбінація необхідна, потрібний ретельний клінічний та лабораторний контроль. Комбінації, що вимагають особливих застережень Карбамазепін: підвищення концентрації активного метаболіту карбамазепіну у плазмі з ознаками передозування. Крім того, зниження концентрації вальпроєвої кислоти у плазмі, пов'язане з посиленням метаболізму вальпроєвої кислоти у печінці під дією карбамазепіну. Рекомендується: клінічне спостереження, визначення концентрацій препаратів у плазмі та, можливо, корекція їх дози, особливо на початку лікування. Карбапенеми, монобактами: меропенем, паніпенем, та, за екстраполяцією, азтреонами та іміпенем: підвищенням ризику появи судом у зв'язку зі зниженням концентрації вальпроєвої кислоти в плазмі крові. Рекомендується: клінічне спостереження, визначення концентрацій препаратів у плазмі крові, може знадобитися корекція дози вальпроєвої кислоти під час лікування антибактеріальним засобом та після його відміни. Фелбамат: підвищення концентрації вальпроєвої кислоти у плазмі з ризиком передозування. Рекомендується: клінічний та лабораторний контроль та, можливо, перегляд дози вальпроєвої кислоти в ході лікування фелбаматом та після його відміни). Фенобарбітал, примідон: підвищення концентрації фенобарбіталу та примідону у плазмі з ознаками передозування, зазвичай у дітей. Крім того, зниження концентрації вальпроєвої кислоти у плазмі, пов'язане з посиленням її печінкового метаболізму під впливом фенобарбіталу або примідону. Рекомендується: клінічний моніторинг протягом перших 15 днів комбінованого лікування з негайним зменшенням дози фенобарбіталу або примідону з появою перших ознак седації, визначення концентрацій обох протисудомних препаратів у крові. Фенітоїн: зміна концентрації фенітоїну в плазмі, небезпека зниження концентрації вальпроєвої кислоти, пов'язаного з посиленням метаболізму вальпроєвої кислоти у печінці під впливом фенітоїну. Рекомендується: клінічний моніторинг із визначенням концентрацій обох протиепілептичних препаратів у плазмі та при необхідності – корекція їх доз. Топірамат: ризик розвитку гіперамоніємії або енцефалопатії. Рекомендується: клінічний та лабораторний контроль протягом першого місяця лікування та у разі виникнення симптомів амоніємії. Нейролептики, інгібітори моноаміноксидази (МАО), антидепресанти, бензодіазепіни: вальпроєва кислота потенціює дію психотропних препаратів, таких як нейролептики, інгібітори МАО, антидепресанти, бензодіазепіни. Рекомендується: клінічний моніторинг та при необхідності корекція дози препарату. Циметидин та еритроміцин: підвищується концентрація вальпроєвої кислоти у плазмі крові. Зідовудін: вальпроєва кислота може підвищувати концентрацію зидовудину в плазмі, що призводить до підвищення токсичності зидовудину. Комбінації, які слід брати до уваги Німодипін (перорально і, за екстраполяцією, парентерально): посилення гіпотензивного ефекту німодипіну внаслідок зменшення його метаболізму під впливом вальпроєвої кислоти та підвищення концентрації у плазмі крові. Ацетилсаліцилова кислота: посилення ефектів вальпроєвої кислоти внаслідок підвищення її концентрації у плазмі крові. При одночасному застосуванні з антикоагулянтами антагоністів вітаміну К потрібний ретельний моніторинг протромбінового індексу. Інші форми взаємодій Вальпроєва кислота не має фермент-індукувального ефекту і тому не впливає на ефективність гормональних контрацептивів, що містять комбінації естрогену та прогестерону.Спосіб застосування та дозиВальпарин ХР призначений для прийому внутрішньо. Добову дозу рекомендується приймати в один або два прийоми, переважно під час їди. Застосування 1 прийом можливе при добре контрольованій епілепсії. Таблетки приймають не роздавлюючи і не розжовуючи, запиваючи невеликою кількістю води. Початкова доза при монотерапії для дорослих та дітей з масою тіла понад 25 кг: 5-15 мг/кг/добу; потім цю дозу поступово підвищують на 5-10 Мг/кг/тиж. Максимальна доза - 30 мг/кг/добу (може бути збільшена за можливості організації контролю за концентрацією в плазмі до 60 мг/кг/добу). При комбінованій терапії у дорослих: 10-30 мг/кг/добу з подальшим підвищенням дози на 5-10 мг/кг/тиж. Дітям при масі тіла менше 25 кг: середня добова доза при монотерапії – 15-45 мг/кг, максимальна – 50 мг/кг. При комбінованій терапії – 30-100 мг/кг/добу. У пацієнтів похилого віку дозу слід встановлювати відповідно до їх клінічного стану. Добова доза визначається залежно від віку та маси тіла пацієнта, а також з урахуванням індивідуальної чутливості до вальпроєвої кислоти. Встановлено хорошу кореляцію між добовою дозою, концентрацією препарату у сироватці та терапевтичним ефектом: дозу слід встановлювати на основі клінічної відповіді. Визначення рівня вальпроєвої кислоти в плазмі можна розглядати як доповнення до клінічного спостереження, коли епілепсія не піддається контролю, або є підозра на побічні ефекти. Діапазон концентрацій, у яких спостерігається клінічний ефект, зазвичай становить 40-100 мг/л (300-700 мкмоль/л). При переході з таблеток негайного вивільнення вальпроєвої кислоти, які забезпечували необхідний контроль над захворюванням, на форму пролонгованої дії (Вальпарин ХР) слід зберігати добову дозу: Заміну інших протиепілептичних препаратів на Вальпарин ХР слід проводити поступово, досягаючи оптимальної дози вальпроєвої кислоти приблизно протягом 2 тижнів. При цьому, залежно від стану пацієнта, зменшується доза попереднього препарату. Для пацієнтів, які не приймають інші протиепілептичні препарати, дози слід збільшувати через 2-3 дні для того, щоб досягти оптимальної дози приблизно протягом тижня. При необхідності комбінації з іншими протиепілептичними засобами слід вводити поступово.ПередозуванняСимптоми: грудка з м'язовою гіпотонією, гіпорефлексією, міозом, пригніченням дихання, метаболічним ацидозом; описано випадки внутрішньочерепної гіпертензії, пов'язаної з набряком мозку. Лікування: у стаціонарі – промивання шлунка, якщо після прийому препарату пройшло не більше 10-12 год; спостереження за станом серцево-судинної та дихальної систем та підтримання ефективного діурезу. У дуже тяжких випадках проводять діаліз. Як правило, прогноз сприятливий, проте було описано кілька випадків детального результату.Запобіжні заходи та особливі вказівкиДо початку лікування та протягом перших 6 місяців терапії потрібен періодичний контроль функції печінки, особливо у пацієнтів групи ризику. Серед класичних тестів найбільш важливими є тести, що відображають синтез білка в печінці, і особливо - протромбіновий індекс. При значному зниженні концентрації протромбіну, вираженому зменшенні вмісту фібриногену, факторів згортання крові, підвищенні концентрації білірубіну та активності трансаміназ, лікування препаратом Вальпарин ХР слід призупинити. Якщо пацієнт отримує одночасно саліцилати, їх слід також негайно скасувати, оскільки саліцилати і вальпроєва кислота мають спільні шляхи метаболізму. Ризик розвитку побічних ефектів з боку печінки підвищений під час проведення комбінованої протисудомної терапії, а також у дітей. Рання діагностика базується переважно на клінічному обстеженні. Зокрема, слід брати до уваги два фактори, які можуть передувати жовтяниці, особливо у пацієнтів, які становлять групу ризику: неспецифічні загальні симптоми, які зазвичай з'являються раптово, такі як астенія, анорексія, крайня втома, сонливість, іноді супроводжуються повторюваною блювотою і болями в животі; рецидив епілептичних нападів на фоні протиепілептичної терапії Слід попередити пацієнта, а якщо це дитина, то її сім'ю, про необхідність негайно повідомити лікаря про виникнення зазначених симптомів. Крім клінічного обстеження у разі слід негайно провести аналіз функції печінки. У поодиноких випадках відзначалися важкі форми панкреатиту, іноді - з летальним кінцем. Ці випадки спостерігали незалежно від віку пацієнта та тривалості лікування, хоча ризик розвитку панкреатиту знижувався зі збільшенням віку хворих. Недостатність функції печінки при панкреатиті підвищує ризик смерті. Слід наголосити, що при лікуванні як препаратом Вальпарин ХР, так і іншими протиепілептичними препаратами, може спостерігатися невелике ізольоване та тимчасове підвищення активності трансаміназ, особливо на початку лікування, за відсутності будь-яких клінічних симптомів. У цьому випадку рекомендується провести більш повне обстеження (що включає, зокрема, визначення протромбінового індексу) для того, щоб при необхідності переглянути дозу та повторити аналізи в залежності від зміни параметрів. Перед початком терапії, перед хірургічним втручанням, у разі виникнення гематом або спонтанних кровотеч необхідний загальний аналіз крові (включаючи визначення кількості тромбоцитів, часу кровотечі та показників коагулограми). При виникненні на фоні лікування симптоматики "гострого" живота та таких шлунково-кишкових симптомів, як нудота, блювання та/або анорексія необхідно визначити активність амілази в крові для виключення гострого панкреатиту. При підвищеній активності ферментів підшлункової залози препарат слід відмінити, вживаючи альтернативних терапевтичних заходів. При застосуванні Вальпарину ХР у пацієнтів з нирковою недостатністю рекомендується враховувати підвищену концентрацію вільної форми вальпроєвої кислоти у плазмі крові та знизити дозу. При необхідності призначення препарату пацієнтам із системним червоним вовчаком та іншими захворюваннями імунної системи слід оцінити очікуваний лікувальний ефект та можливий ризик терапії, оскільки при застосуванні Вальпарину® ХР у рідкісних випадках відзначалися порушення імунної системи. Не рекомендується призначати препарат пацієнтам із дефіцитом ферментів карбамідного циклу. У таких хворих було описано кілька випадків гіперамоніємії, що супроводжується ступором та/або комою. Під час лікування не допускається прийом напоїв, які містять етанол. Пацієнтів необхідно попередити про ризик збільшення маси тіла на початку лікування та рекомендувати дотримання дієти для мінімізації такого впливу. Вплив на здатність до керування автотранспортом та управління механізмами У період лікування пацієнтам необхідно дотримуватися обережності при керуванні автотранспортом та іншою діяльністю, що потребує високої концентрації уваги та швидкості психомоторних реакцій.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Активні речовини: вальпроат натрію 333 мг, вальпроєва кислота 145 мг, що відповідає загальному вмісту натрію вальпроату 500 мг. Допоміжні речовини: кремнію діоксид колоїдний, гідроксипропілметилцелюлоза, етилцелюлоза, кремнію діоксиду гідрат, натрію сахарин, гліцерин, титану діоксид, евдрагіт Е-100, евдрагіт NE-30D, поліетиленгліколь 1500, тальк. 10 шт. - Стрипи (10) - Пачки картонні.Опис лікарської формиТаблетки пролонгованої дії, покриті оболонкою; білого кольору, довгасті, з насічкою на обох сторонах.Фармакотерапевтична групаПротисудомний препарат. Натрію вальпроат підвищує вміст гамма-амінобутирової кислоти (GABA) у головному мозку, що відповідно збільшує вміст GABA у постсинаптичних нейронах. Крім того, вальпроат натрію впливає на перенесення іонів калію через мембрани нейронів. В результаті відбувається придушення розвитку, а також поширення епілептичного збудження нейронів. Натрію вальпроат має протисудомну активність при різних типах епілепсії у людей. Препарат не має виражених снодійних і седативних ефектів, а також не чинить гнітючої дії на дихальний центр. Натрію вальпроат не має негативної дії на АТ, ЧСС, функцію нирок та температуру тіла.ФармакокінетикаВсмоктування Після прийому внутрішньо таблеток з контрольованим вивільненням Cmax; у плазмі досягається протягом 2-8 годин. Біодоступність препарату - близько 100%. Терапевтична ефективність проявляється при концентрації вальпроєвої кислоти у плазмі крові 40-100 мг/л. У той же час фармакологічний та терапевтичний ефекти даного препарату з контрольованим вивільненням не завжди залежать від його концентрації у плазмі. Розподіл Зв'язування з білками плазми становить 80-90%. Vd; становить 0.2 л/кг. Метаболізм та виведення Метаболізується у печінці та виводиться із сечею. Пресистемний метаболізм не відзначається. T1/2; становить приблизно 8-20 год. Фармакокінетика в особливих клінічних випадках У дітей T1/2; зменшується.Клінічна фармакологіяПротисудомний препарат.Показання до застосуванняЛікування генералізованої або парціальної епілепсії, особливо при наступних типах нападів: абсанси; міоклонічні; тоніко-клонічні; атонічні. Парціальна епілепсія: прості або комбіновані напади; вторинні генералізовані напади. Специфічні синдроми (Веста, Леннокса-Гасто).Протипоказання до застосуванняТяжкі порушення функції підшлункової залози; гострий або хронічний гепатит, випадки активного гепатиту в сімейному анамнезі (насамперед лікарського генезу); порфірія; тромбоцитопенія; вагітність; лактація (грудне вигодовування); дитячий вік до 3 років; підвищена чутливість до вальпроєвої кислоти та інших компонентів препарату.Вагітність та лактаціяПризначення препарату при вагітності можливе лише у випадку, коли ймовірна користь для матері перевищує потенційний ризик для плода. У разі прийому препарату при вагітності обов'язковим є проведення спеціалізованого передпологового спостереження за плодом. Застосування препарату під час грудного вигодовування не рекомендується. Застосування у дітей Препарат протипоказаний дітям віком до 3 років. Для дітей з масою тіла більше 20 кг початкова доза - 400 мг на добу. Дозу слід підвищувати поступово до досягнення оптимальних значень - зазвичай 20-30 мг/кг/сут на 1 або 2 прийоми. У дітей масою тіла до 20 кг не слід застосовувати Вальпарин ХР.Побічна діяЗ боку системи травлення: рідко - нудота, блювання, діарея та/або запор, гепатит, панкреатит. Алергічні реакції: рідко - шкірний висип, свербіж, фотосенсибілізація, мультиформна еритема, синдром Стівенса-Джонсона. З боку ЦНС: рідко - атаксія, тремор, порушення свідомості, кома. З боку статевої системи: рідко - порушення менструального циклу, вторинна аменорея. З боку системи кровотворення: рідко - анемія, тромбоцитопенія, нейтропенія, лейкопенія, зниження вмісту фібриногену, гальмування агрегації тромбоцитів. Інші: ;2-12% - випадання волосся; рідко – збільшення маси тіла, гіперамоніємія, креатинінемія.Взаємодія з лікарськими засобамиНатрію вальпроат посилює дію антипсихотичних препаратів, протисудомних засобів та антидепресантів. На відміну від інших протисудомних препаратів, вальпроат натрію не викликає індукції печінкових ферментів, тому не знижує ефективності пероральних контрацептивів. При сумісному застосуванні натрію вальпроату та варфарину знижується відсоток зв'язування з білками плазми крові останнього. Натрію вальпроат змінює плазмові концентрації фенітоїну та ламотригіну. У поєднанні з антикоагулянтами та похідними ацетилсаліцилової кислоти посилюється антиагрегантна дія.Спосіб застосування та дозиРежим дозування підбирають індивідуально залежно від віку та маси тіла пацієнта. Для дорослих початкова доза становить 600 мг на добу з подальшим збільшенням дози на 200 мг кожні 3 дні до досягнення оптимального ефекту. Кратність прийому – 1-2 рази на добу. Максимально рекомендована доза 1-2 г на добу. Таблетки слід ковтати повністю, запиваючи невеликою кількістю води. У; пацієнтів похилого віку; режим дозування Вальпарину ХР подібний до режиму дозування у дорослих і підбирається індивідуально. Для дітей з масою тіла більше 20 кг початкова доза - 400 мг на добу. Дозу слід підвищувати поступово до досягнення оптимальних значень - зазвичай 20-30 мг/кг/сут на 1 або 2 прийоми. У дітей масою тіла до 20 кг не слід застосовувати Вальпарин ХР.ПередозуванняПовідомлялося про поодинокі випадки випадкового або навмисного передозування препарату. Симптоми: нудота, блювання, запаморочення, діарея, пригнічення дихання, гіпорефлексія, коматозний стан. Лікування: ; промивання шлунка, прийом активованого вугілля. При необхідності – стаціонарне лікування з проведенням симптоматичної терапії, гемодіалізу.Запобіжні заходи та особливі вказівкиНеобхідне регулярне проведення контролю активності трансаміназ, вмісту білірубіну, тромбоцитів крові, амілази (кожні 3 місяці). Вальпроєва кислота пригнічує агрегацію тромбоцитів, що підвищує ризик збільшення часу зсідання крові при кровотечах. Слід враховувати можливість розвитку ускладнень, пов'язаних із кровотечею у післяопераційному періоді у пацієнтів, які отримують натрію вальпроат. При тривалому прийомі натрію вальпроату можливий розвиток спонтанних гематом та кровотеч. У такому разі слід негайно припинити прийом препарату. Натрію вальпроат може спричинити лікарський панкреатит та порушення функції печінки (зазвичай у перші 6 місяців застосування). У зв'язку з цим необхідно протягом перших 23 місяців лікування контролювати стан підшлункової залози, проводити печінкові проби, стежити за рівнем протромбіну. Порушення функції печінки, печінкова недостатність на фоні терапії натрію вальпроатом іноді спостерігаються у дітей з епілепсією та поєднаними метаболічними та дегенеративними захворюваннями, органічною патологією мозкової тканини та уповільненим розумовим розвитком. При виникненні таких симптомів, як виражена слабкість, летаргійний стан, набряклість, блювання та жовтяниця, слід негайно припинити застосування препарату. Вплив на здатність до керування автотранспортом та управління механізмами Пацієнту слід дотримуватися обережності під час роботи з механізмами, т.к. препарат знижує здатність до концентрації уваги.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Активні речовини: вальпроат натрію 333 мг, вальпроєва кислота 145 мг, що відповідає загальному вмісту натрію вальпроату 500 мг. Допоміжні речовини: кремнію діоксид колоїдний, гідроксипропілметилцелюлоза, етилцелюлоза, кремнію діоксиду гідрат, натрію сахарин, гліцерин, титану діоксид, евдрагіт Е-100, евдрагіт NE-30D, поліетиленгліколь 1500, тальк. 10 шт. - стрипи (3) - пачки картонні.Опис лікарської формиТаблетки пролонгованої дії, покриті оболонкою; білого кольору, довгасті, з насічкою на обох сторонах.Фармакотерапевтична групаПротисудомний препарат. Натрію вальпроат підвищує вміст гамма-амінобутирової кислоти (GABA) у головному мозку, що відповідно збільшує вміст GABA у постсинаптичних нейронах. Крім того, вальпроат натрію впливає на перенесення іонів калію через мембрани нейронів. В результаті відбувається придушення розвитку, а також поширення епілептичного збудження нейронів. Натрію вальпроат має протисудомну активність при різних типах епілепсії у людей. Препарат не має виражених снодійних і седативних ефектів, а також не чинить гнітючої дії на дихальний центр. Натрію вальпроат не має негативної дії на АТ, ЧСС, функцію нирок та температуру тіла.ФармакокінетикаВсмоктування Після прийому внутрішньо таблеток з контрольованим вивільненням Cmax; у плазмі досягається протягом 2-8 годин. Біодоступність препарату - близько 100%. Терапевтична ефективність проявляється при концентрації вальпроєвої кислоти у плазмі крові 40-100 мг/л. У той же час фармакологічний та терапевтичний ефекти даного препарату з контрольованим вивільненням не завжди залежать від його концентрації у плазмі. Розподіл Зв'язування з білками плазми становить 80-90%. Vd; становить 0.2 л/кг. Метаболізм та виведення Метаболізується у печінці та виводиться із сечею. Пресистемний метаболізм не відзначається. T1/2; становить приблизно 8-20 год. Фармакокінетика в особливих клінічних випадках У дітей T1/2; зменшується.Клінічна фармакологіяПротисудомний препарат.Показання до застосуванняЛікування генералізованої або парціальної епілепсії, особливо при наступних типах нападів: абсанси; міоклонічні; тоніко-клонічні; атонічні. Парціальна епілепсія: прості або комбіновані напади; вторинні генералізовані напади. Специфічні синдроми (Веста, Леннокса-Гасто).Протипоказання до застосуванняТяжкі порушення функції підшлункової залози; гострий або хронічний гепатит, випадки активного гепатиту в сімейному анамнезі (насамперед лікарського генезу); порфірія; тромбоцитопенія; вагітність; лактація (грудне вигодовування); дитячий вік до 3 років; підвищена чутливість до вальпроєвої кислоти та інших компонентів препарату.Вагітність та лактаціяПризначення препарату при вагітності можливе лише у випадку, коли ймовірна користь для матері перевищує потенційний ризик для плода. У разі прийому препарату при вагітності обов'язковим є проведення спеціалізованого передпологового спостереження за плодом. Застосування препарату під час грудного вигодовування не рекомендується. Застосування у дітей Препарат протипоказаний дітям віком до 3 років. Для дітей з масою тіла більше 20 кг початкова доза - 400 мг на добу. Дозу слід підвищувати поступово до досягнення оптимальних значень - зазвичай 20-30 мг/кг/сут на 1 або 2 прийоми. У дітей масою тіла до 20 кг не слід застосовувати Вальпарин ХР.Побічна діяЗ боку системи травлення: рідко - нудота, блювання, діарея та/або запор, гепатит, панкреатит. Алергічні реакції: рідко - шкірний висип, свербіж, фотосенсибілізація, мультиформна еритема, синдром Стівенса-Джонсона. З боку ЦНС: рідко - атаксія, тремор, порушення свідомості, кома. З боку статевої системи: рідко - порушення менструального циклу, вторинна аменорея. З боку системи кровотворення: рідко - анемія, тромбоцитопенія, нейтропенія, лейкопенія, зниження вмісту фібриногену, гальмування агрегації тромбоцитів. Інші: ;2-12% - випадання волосся; рідко – збільшення маси тіла, гіперамоніємія, креатинінемія.Взаємодія з лікарськими засобамиНатрію вальпроат посилює дію антипсихотичних препаратів, протисудомних засобів та антидепресантів. На відміну від інших протисудомних препаратів, вальпроат натрію не викликає індукції печінкових ферментів, тому не знижує ефективності пероральних контрацептивів. При сумісному застосуванні натрію вальпроату та варфарину знижується відсоток зв'язування з білками плазми крові останнього. Натрію вальпроат змінює плазмові концентрації фенітоїну та ламотригіну. У поєднанні з антикоагулянтами та похідними ацетилсаліцилової кислоти посилюється антиагрегантна дія.Спосіб застосування та дозиРежим дозування підбирають індивідуально залежно від віку та маси тіла пацієнта. Для дорослих початкова доза становить 600 мг на добу з подальшим збільшенням дози на 200 мг кожні 3 дні до досягнення оптимального ефекту. Кратність прийому – 1-2 рази на добу. Максимально рекомендована доза 1-2 г на добу. Таблетки слід ковтати повністю, запиваючи невеликою кількістю води. У; пацієнтів похилого віку; режим дозування Вальпарину ХР подібний до режиму дозування у дорослих і підбирається індивідуально. Для дітей з масою тіла більше 20 кг початкова доза - 400 мг на добу. Дозу слід підвищувати поступово до досягнення оптимальних значень - зазвичай 20-30 мг/кг/сут на 1 або 2 прийоми. У дітей масою тіла до 20 кг не слід застосовувати Вальпарин ХР.ПередозуванняПовідомлялося про поодинокі випадки випадкового або навмисного передозування препарату. Симптоми: нудота, блювання, запаморочення, діарея, пригнічення дихання, гіпорефлексія, коматозний стан. Лікування: ; промивання шлунка, прийом активованого вугілля. При необхідності – стаціонарне лікування з проведенням симптоматичної терапії, гемодіалізу.Запобіжні заходи та особливі вказівкиНеобхідне регулярне проведення контролю активності трансаміназ, вмісту білірубіну, тромбоцитів крові, амілази (кожні 3 місяці). Вальпроєва кислота пригнічує агрегацію тромбоцитів, що підвищує ризик збільшення часу зсідання крові при кровотечах. Слід враховувати можливість розвитку ускладнень, пов'язаних із кровотечею у післяопераційному періоді у пацієнтів, які отримують натрію вальпроат. При тривалому прийомі натрію вальпроату можливий розвиток спонтанних гематом та кровотеч. У такому разі слід негайно припинити прийом препарату. Натрію вальпроат може спричинити лікарський панкреатит та порушення функції печінки (зазвичай у перші 6 місяців застосування). У зв'язку з цим необхідно протягом перших 23 місяців лікування контролювати стан підшлункової залози, проводити печінкові проби, стежити за рівнем протромбіну. Порушення функції печінки, печінкова недостатність на фоні терапії натрію вальпроатом іноді спостерігаються у дітей з епілепсією та поєднаними метаболічними та дегенеративними захворюваннями, органічною патологією мозкової тканини та уповільненим розумовим розвитком. При виникненні таких симптомів, як виражена слабкість, летаргійний стан, набряклість, блювання та жовтяниця, слід негайно припинити застосування препарату. Вплив на здатність до керування автотранспортом та управління механізмами Пацієнту слід дотримуватися обережності під час роботи з механізмами, т.к. препарат знижує здатність до концентрації уваги.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Діюча речовина: валсартан 160 мг; допоміжні речовини: лактози моногідрат 60,00 мг, целюлоза мікрокристалічна 82,00 мг, повідон-К25 3,00 мг, кроскармелоза натрію 4,00 мг, кремнію діоксид колоїдний 2,00 мг, магнію стеарат 9,00 мг; Оболонка плівкова: гіпромелоза 6ср 5,52 мг, титану діоксид (Е171) 1,36 мг, барвник заліза оксид жовтий (Е172) 0,50 мг, барвник заліза оксид червоний (Е172) 0,02 мг, макрогол-4000 0,6 мг. По 7, 10, 14 або 15 таблеток у блістері (контурному осередковому впакуванні) з комбінованого матеріалу ПВХ/ПЕ/ПВДХ - алюмінієвої фольги. По 2, 4, 8, 12, 14 або 20 блістерів (контурних осередкових упаковок) (по 7 таблеток), або по 2, 3, 6 або 9 блістерів (контурних осередкових упаковок) (по 10 таблеток), або по 1,2 , 4, 6, 7 або 10 блістерів (контурних осередкових упаковок) (по 14 таблеток), або по 2, 4 або 6 блістерів (контурних осередкових упаковок) (по 15 таблеток) разом з інструкцією по застосуванню поміщають в картонну пачку.Опис лікарської формиОвальні, двоопуклі таблетки з ризиком на одній стороні, покриті плівковою оболонкою коричнево-жовтого кольору. Вид на зламі: біла шорстка маса з плівковою оболонкою коричнево-жовтого кольору.Фармакотерапевтична групаАнгіотензин II рецепторів антагоніст.ФармакокінетикаВсмоктування. Після прийому валсартану внутрішньо Cmax у плазмі досягається протягом 2-4 годин. Середня абсолютна біодоступність становить 23%. При застосуванні валсартану з їжею AUC та Cmax у плазмі крові зменшуються на 40 та 50% відповідно. Тим не менш, через 8 годин після прийому препарату плазмові концентрації валсартану, прийнятого натще і з їжею, однакові. Зменшення AUC не супроводжується клінічно значущим зниженням терапевтичного ефекту валсартану, тому препарат Вальсакор можна приймати незалежно від часу їди. Розподіл. Vd валсартану в період рівноважного стану після внутрішньовенного введення становив близько 17 л, що вказує на відсутність вираженого розподілу валсартану в тканинах. Валсартан активно зв'язується з білками плазми (94-97%), переважно з альбуміном. Метаболізм. Валсартан не піддається суттєвій біотрансформації, лише близько 20% дози, прийнятої внутрішньо, виводиться у вигляді метаболітів. Гідроксильний метаболіт визначається в плазмі у низьких концентраціях (менше 10% від AUC валсартану). Цей метаболіт не має фармакологічної активності. Виведення. Валсартан виводиться двофазно: α-фаза з T1/2α менше 1 год і β-фаза з T1/2β — близько 9 год. Валсартан виводиться, в основному, у незміненому вигляді через кишечник (близько 83%) та нирками (близько 13%) . Після внутрішньовенного введення плазмовий кліренс валсартану становить близько 2 л/год, нирковий кліренс – 0,62 л/год (близько 30% від загального кліренсу). T1/2 валсартану становить 6 год. Фармакокінетика спеціальних груп пацієнтів Пацієнти з ХСН. У пацієнтів з ХСН час досягнення Cmax та T1/2 подібні до аналогічних показників у здорових добровольців. Підвищення AUC та Cmax прямо пропорційно збільшенню дози валсартану (з 40 до 160 мг 2 рази на добу). Чинник кумуляції становить, у середньому, 1,7. При внутрішньому прийомі кліренс валсартану становить близько 4,5 л/год. Вік пацієнтів із ХСН не впливав на кліренс валсартану. Пацієнти похилого віку (старше 65 років). У деяких пацієнтів старше 65 років біодоступність валсартану була вищою за таку у пацієнтів молодого віку, що не має клінічного значення. Пацієнти із порушеннями функції нирок. Нирковий кліренс валсартану становить лише 30% від загального кліренсу, тому кореляції між функцією нирок та системною біодоступністю валсартану немає. Корекція дози у пацієнтів з порушенням функції нирок (Cl креатиніну більше 10 мл/хв) не потрібна. Безпека валсартану у пацієнтів з Cl креатиніну менше 10 мл/хв та пацієнтів, які перебувають на гемодіалізі, не встановлена, тому у таких пацієнтів препарат слід застосовувати з обережністю. Оскільки ступінь зв'язування валсартану з білками плазми висока, його виведення при гемодіалізі малоймовірне. Пацієнти із порушеннями функції печінки. Близько 70% дози валсартану, що всмокталася, виводиться через кишечник, переважно в незміненому вигляді. Валсартан значною мірою не піддається метаболізму. У пацієнтів з легким або помірним порушенням функції печінки відзначалося підвищення AUC валсартану в 2 рази, порівняно з такою, у здорових добровольців. Однак не спостерігається кореляція значень AUC валсартану зі ступенем порушення функції печінки. Застосування валсартану у пацієнтів із тяжким порушенням функції печінки не вивчалось. Пацієнти віком від 6 до 18 років. Фармакокінетика валсартану у дітей та підлітків від 6 до 18 років не відрізняється від фармакокінетики валсартану у пацієнтів віком від 18 років.ФармакодинамікаВалсартан є селективним антагоністом рецепторів ангіотензину II (типу AT1) для внутрішнього прийому, небілкової природи. Вибірково блокує рецептори АТ1. Наслідком блокади АТ1-рецепторів є підвищення концентрації плазми ангіотензину II, який може стимулювати незаблоковані АТ2-рецептори, що врівноважує вазопресорні ефекти, пов'язані з порушенням АТ1-рецепторів. Валсартан не має агоністичної активності щодо АТ1-рецепторів. Його спорідненість до АТ1-рецепторів приблизно в 20000 разів вища, ніж до АТ2-рецепторів. Валсартан не інгібує АПФ, відомий також під назвою кінінази II, який перетворює ангіотензин I на ангіотензин II і руйнує брадикінін. У зв'язку з відсутністю впливу на АПФ не потенціюються ефекти брадикініну та субстанції Р. Частота розвитку сухого кашлю нижче у пацієнтів, які отримували антагоністи рецепторів ангіотензину II (АРА II), порівняно з пацієнтами, які отримували інгібітор АПФ. Валсартан не вступає у взаємодію та не блокує рецептори інших гормонів або іонні канали, що беруть участь у регуляції функцій ССС. Застосування при артеріальній гіпертензії у пацієнтів віком від 18 років. При лікуванні артеріальної гіпертензії (АГ) валсартан знижує артеріальний тиск, не впливаючи на ЧСС. Після прийому внутрішньо разової дози валсартану антигіпертензивний ефект розвивається протягом 2 годин, а максимальне зниження артеріального тиску досягається протягом 4-6 годин. Антигіпертензивний ефект валсартану зберігається протягом 24 годин після його застосування. При постійному застосуванні валсартану максимальне зниження артеріального тиску, незалежно від дози, досягається через 2-4 тижні і підтримується на досягнутому рівні під час тривалої терапії. Одночасне застосування з гідрохлортіазидом дозволяє досягти значного додаткового зниження артеріального тиску. Раптова відміна валсартану не супроводжується різким підвищенням артеріального тиску або іншими небажаними клінічними наслідками (тобто синдром відміни не розвивається). У пацієнтів з артеріальною гіпертензією, цукровим діабетом (ЦД) типу 2 та нефропатією, які приймають валсартан у дозі 160–320 мг на добу, відзначається значне зниження протеїнурії (36–44%). Застосування після гострого інфаркту міокарда (ІМ) у пацієнтів віком від 18 років. При застосуванні валсартану протягом 2 років, з початком прийому від 12 год до 10 днів після розвитку ІМ (ускладненого лівошлуночковою недостатністю та/або систолічною дисфункцією лівого шлуночка) знижуються показники загальної смертності, серцево-судинної смертності та подовжується час до першої госпіталізації. перебігу ХСН, повторного ІМ, раптової зупинки серця та інсульту (без летального результату). ХСН у пацієнтів віком від 18 років При застосуванні валсартану (в середній добовій дозі 254 мг) протягом 2 років у пацієнтів з ХСН II–IV функціонального класу за класифікацією NYHA з фракцією викиду лівого шлуночка (ФВЛШ) менше 40% та внутрішнім діастолічним діаметром ЛШ понад 2,9 см/м2 , що отримують стандартну терапію (інгібітори АПФ, діуретики, дигоксин, бета-адреноблокатори), було відзначено достовірне зниження ризику госпіталізації з приводу загострення перебігу ХСН, уповільнення прогресування ХСН, поліпшення функціонального класу ХСН за класифікацією NYHA, збільшення недостатність та поліпшення якості життя в порівнянні з плацебо. Застосування у пацієнтів старше 18 років з АГ та порушенням толерантності до глюкози При застосуванні валсартану та зміні способу життя відзначалося статистично достовірне зниження ризику розвитку ЦД у пацієнтів з артеріальною гіпертензією та порушенням толерантності до глюкози. Валсартан не впливав на частоту летальних наслідків внаслідок серцево-судинних подій, ІМ та транзиторних ішемічних атак без летального результату, на частоту госпіталізацій унаслідок загострення перебігу ХСН або нестабільної стенокардії, артеріальної реваскуляризації у даної категорії пацієнтів, що відрізняються за віком, статтю та расовою. приладдя. У пацієнтів, які отримують валсартан, ризик розвитку мікроальбумінурії був достовірно нижчим, ніж у пацієнтів, які не одержують цієї терапії. Рекомендована початкова доза валсартану у пацієнтів з артеріальною гіпертензією та порушенням толерантності до глюкози становить 80 мг 1 раз на добу. За потреби доза може бути збільшена до 160 мг. Застосування у дітей та підлітків від 6 до 18 років при АГ У дітей та підлітків від 6 до 18 років валсартан забезпечує дозозалежне плавне зниження артеріального тиску. При застосуванні валсартану максимальне зниження АТ незалежно від прийнятої внутрішньо дози досягається протягом 2 тижнів і підтримується на досягнутому рівні в ході тривалої терапії.Показання до застосуванняПацієнти старше 18 років артеріальна гіпертензія. хронічна серцева недостатність (II–IV функціональний клас за класифікацією NYHA) у складі комплексної терапії (на фоні стандартної терапії) у пацієнтів, які не одержують інгібітори АПФ; підвищення виживання пацієнтів після перенесеного гострого ІМ, ускладненого лівошлуночковою недостатністю та/або систолічною дисфункцією лівого шлуночка (ЛШ), за наявності стабільних показників гемодинаміки. Пацієнти від 6 до 18 років артеріальна гіпертензія у дітей та підлітків від 6 до 18 років.Протипоказання до застосуванняпідвищена чутливість до валсартану або інших компонентів препарату; тяжкі порушення функції печінки (більше 9 балів за шкалою Чайлд-П'ю), біліарний цироз та холестаз; одночасне застосування з аліскіреном у пацієнтів з цукровим діабетом або помірними та тяжкими порушеннями функції нирок (Cl креатиніну менше 60 мл/хв); дефіцит лактази, непереносимість лактози, синдром глюкозо-галактозної мальабсорбції, оскільки до складу препарату Вальсакор входить лактоза; вагітність; період грудного вигодовування; вік до 6 років – за показанням артеріальна гіпертензія, до 18 років – за іншими показаннями. З обережністю: гіперкаліємія; одночасне застосування калійзберігаючих діуретиків; препаратів калію; калійвмісних харчових добавок або інших препаратів, здатних підвищувати вміст калію в плазмі (наприклад, гепарин); легкі та помірні порушення функції печінки небіліарного генезу без явищ холестазу; тяжкі порушення функції нирок (Cl креатиніну менше 10 мл/хв – немає клінічних даних); порушення функції нирок у пацієнтів від 6 до 18 років (Cl креатиніну менше 30 мл/хв), в т.ч. що знаходяться на гемодіалізі, гіпонатріємія, дотримання дієти з обмеженням споживання кухонної солі, стани, що супроводжуються зниженням ОЦК (в т.ч. діарея, блювання); двосторонній стеноз ниркових артерій чи стеноз артерії єдиної нирки; стан після трансплантації нирки; первинний гіперальдостеронізм,у пацієнтів із хронічною серцевою недостатністю III–IV функціонального класу (за NYNA); функція нирок яких залежить стану РААС; стеноз аортального та/або мітрального клапана; гіпертрофічна обструктивна кардіоміопатія (ГЗКМП), у пацієнтів зі спадковим ангіоневротичним набряком або ангіоневротичним набряком на фоні попередньої терапії АРА II або інгібіторами АПФ. Не рекомендується застосовувати АРА II, включаючи валсартан, одночасно з інгібіторами АПФ, оскільки їх одночасне застосування не має переваг перед монотерапією валсартаном або інгібітором АПФ щодо показників загальної смертності.Вагітність та лактаціяЗастосування АРА II у І триместрі вагітності не рекомендується. Застосування АРА II протипоказане у II–III триместрах вагітності, оскільки застосування у II–III триместрах вагітності може спричинити фетотоксичні ефекти (зниження функції нирок, маловоддя, уповільнення окостеніння кісток черепа плода) та неонатальні токсичні ефекти (ниркову недостатність, артеріальну гіпотензію, гіперкалієм). Якщо все ж таки застосовували препарат у II–III триместрах вагітності, то необхідно провести УЗД нирок та кісток черепа плода. При плануванні вагітності рекомендується перевести пацієнтку на альтернативну гіпотензивну терапію з урахуванням профілю безпеки. При підтвердженні вагітності препарат Вальсакор необхідно відмінити якомога раніше. Новонароджені, матері яких отримували АРА II під час вагітності, потребують медичного спостереження, т.к. Існує ризик розвитку артеріальної гіпотензії. Немає даних про виділення валсартану у грудне молоко. Тому слід вирішити питання про припинення годування груддю або скасування терапії валсартаном та переведення на альтернативну гіпотензивну терапію з урахуванням профілю безпеки.Побічна діяКласифікація частоти розвитку побічних ефектів Всесвітньої організації охорони здоров'я: дуже часто — ≥1/10; часто – від ≥1/100 до <1/10; нечасто – від ≥1/1000 до <1/100; рідко – від ≥1/10000 до <1/1000; дуже рідко - <1/10000; частота невідома - не може бути оцінена на основі наявних даних. Профіль безпеки валсартану у пацієнтів з АГ віком від 6 до 18 років не відрізняється від профілю безпеки валсартану у пацієнтів з АГ віком від 18 років. Артеріальна гіпертензія З боку крові та лімфатичної системи: частота невідома – зниження гемоглобіну, зниження гематокриту, нейтропенія, тромбоцитопенія. З боку імунної системи: частота невідома – реакції підвищеної чутливості, включаючи сироваткову хворобу. З боку обміну речовин та харчування: частота невідома – підвищення вмісту калію у сироватці крові, гіпонатріємія. З боку органу слуху та лабіринтні порушення: нечасто – вертиго. З боку судин: частота невідома – васкуліт. З боку дихальної системи, органів грудної клітки та середостіння: нечасто – кашель. З боку шлунково-кишкового тракту: нечасто – біль у животі. З боку печінки та жовчовивідних шляхів: частота невідома – порушення функції печінки, включаючи підвищення концентрації білірубіну у плазмі крові. З боку шкіри та підшкірних тканин: частота невідома — ангіоневротичний набряк, висипання на шкірі, свербіж шкіри, бульозний дерматит. З боку скелетно-м'язової та сполучної тканини: частота невідома – міалгія. З боку нирок та сечовивідних шляхів: частота невідома – порушення функції нирок та ниркова недостатність, підвищення концентрації креатиніну у сироватці крові. Загальні розлади та порушення у місці введення: нечасто – підвищена стомлюваність. У ході клінічних досліджень у пацієнтів з АГ спостерігалися такі небажані явища, причинно-наслідковий зв'язок яких з прийомом валсартану не встановлений: артралгія, астенія, біль у спині, діарея, запаморочення, безсоння, зниження лібідо, нудота, периферичні набряки, фарингіт, рин синусит, інфекції верхніх дихальних шляхів Після перенесеного гострого ІМ та/або при хронічній серцевій недостатності (II–IV функціональний клас за класифікацією NYHA) З боку крові та лімфатичної системи: частота невідома – тромбоцитопенія. З боку імунної системи: частота невідома – реакції підвищеної чутливості, включаючи сироваткову хворобу. З боку обміну речовин та харчування: нечасто – гіперкаліємія; частота невідома – підвищення вмісту калію в сироватці крові, гіпонатріємія. З боку нервової системи: часто – запаморочення, постуральне запаморочення; нечасто - непритомність, головний біль. З боку органу слуху та лабіринтні порушення: нечасто – вертиго. З боку серця: нечасто посилення симптомів ХСН. З боку судин: часто – виражене зниження артеріального тиску, ортостатична гіпотензія; частота невідома – васкуліт. З боку дихальної системи, органів грудної клітки та середостіння: нечасто – кашель. З боку шлунково-кишкового тракту: нечасто – нудота, діарея. З боку печінки та жовчовивідних шляхів: частота невідома – порушення функції печінки. З боку шкіри та підшкірних тканин: нечасто – ангіоневротичний набряк; частота невідома – шкірний висип, свербіж шкіри, бульозний дерматит. З боку скелетно-м'язової та сполучної тканини: рідко – рабдоміоліз; частота невідома – міалгія. З боку нирок та сечовивідних шляхів: часто – порушення функції нирок та ниркова недостатність; нечасто – гостра ниркова недостатність, підвищення концентрації креатиніну у сироватці крові; частота невідома – підвищення вмісту азоту сечовини у плазмі крові. Загальні розлади та порушення у місці введення: нечасто – астенія, підвищена стомлюваність.Взаємодія з лікарськими засобамиОдночасне застосування протипоказане Одночасне застосування АРА II, включаючи валсартан, або інгібіторів АПФ з аліскіреном, протипоказане у пацієнтів з ЦД або помірними та тяжкими порушеннями функції нирок (Cl креатиніну менше 60 мл/хв). Одночасне застосування не рекомендується Літій. Одночасне застосування препаратами літію не рекомендується, т.к. можливе оборотне збільшення концентрації літію в плазмі крові та посилення його токсичної дії. Ризик токсичних проявів, пов'язаних із застосуванням препаратів літію, може додатково збільшуватися при одночасному застосуванні з Вальсакором та діуретиками. При необхідності одночасного застосування з препаратами літію слід ретельно контролювати концентрацію літію у плазмі крові. Калійзберігаючі діуретики (спіронолактон, еплеренон, тріамтерен, амілорид), препарати калію, калійвмісні харчові добавки та інші лікарські засоби та речовини, які можуть спричинити гіперкаліємію (наприклад, гепарин). При необхідності одночасного застосування з препаратами, що впливають вміст калію, рекомендується контролювати вміст калію в плазмі крові. Одночасне застосування з обережністю Подвійна блокада РААС. У деяких пацієнтів подвійна блокада РААС супроводжувалася розвитком артеріальної гіпотензії, непритомності, гіперкаліємії та порушенням функції нирок (включаючи гостру ниркову недостатність (ОПН)). АПФ або аліскірен. НПЗЗ, в т.ч. селективні інгібітори ЦОГ-2, ацетилсаліцилова кислота в дозі більше 3 г на добу та неселективні НПЗЗ. При одночасному застосуванні з валсартаном можливе зменшення антигіпертензивного ефекту, збільшення ризику розвитку порушень функції нирок та підвищення вмісту калію у плазмі. До початку комбінованої терапії рекомендується оцінити функцію нирок, а також корекцію порушень водно-електролітного балансу. Білки-переносники. Дослідження in vitro на культурах печінки показали, що валсартан є субстратом для білків-переносників OATP1B1/OATP1B3 та MRP2. Одночасне застосування валсартану з інгібіторами білка-переносника OATP1B1/OATP1B3 (рифампіцин, циклоспорин) або MRP2 (ритонавір) може збільшити системну експозицію валсартану (Cmax та AUC). Необхідно бути обережними на початку одночасного застосування з вищевказаними препаратами або після їх відміни. Відсутність лікарської взаємодії Не виявлено клінічно значущих взаємодій з наступними ЛЗ: циметидин, варфарин, фуросемід, дигоксин, атенолол, індометацин, гідрохлортіазид, амлодипін та глібенкламід. Пацієнти віком від 6 до 18 років. У дітей та підлітків АГ часто пов'язана з порушенням функції нирок. Одночасне застосування валсартану з іншими ЛЗ, що впливають на РААС, може спричинити підвищення вмісту калію в плазмі у таких пацієнтів. Необхідно бути обережними при одночасному застосуванні вищезгаданої комбінації та регулярно контролювати функцію нирок та вміст калію в плазмі крові у даної групи пацієнтів.Спосіб застосування та дозиВсередину, незалежно від часу їди. Пацієнти старше 18 років Артеріальна гіпертензія. Рекомендована початкова доза препарату Вальсакор становить 80 мг 1 раз на добу, незалежно від расової приналежності, віку та статі пацієнта. Антигіпертензивний ефект розвивається протягом 2 тижнів і досягає свого максимуму через 4 тижні. Пацієнтам, у яких не вдалося досягти адекватного контролю АТ, добова доза валсартану може бути поступово збільшена до максимальної добової дози 320 мг. З метою додаткового зниження АТ можливе застосування діуретичних засобів (гідрохлортіазид), а також одночасне застосування інших гіпотензивних засобів. ХСН. Рекомендована початкова доза препарату Вальсакор становить 40 мг 2 рази на добу. Дозу препарату слід поступово збільшувати протягом щонайменше 2 тижнів до 80 мг 2 рази на добу, а при хорошій переносимості – до 160 мг 2 рази на добу. Максимальна добова доза становить 320 мг на два прийоми. При цьому може знадобитися зниження дози діуретиків, що одночасно приймаються. Можливе одночасне застосування з іншими лікарськими засобами, призначеними для лікування ХСН. Проте одночасна терапія препаратами трьох класів: валсартаном, інгібіторами АПФ та бета-адреноблокаторами не рекомендується. Оцінка стану пацієнтів із ХСН повинна включати контроль функції нирок. Застосування після перенесеного гострого ІМ. Лікування слід розпочинати вже через 12 годин після розвитку гострого ІМ за наявності стабільних показників гемодинаміки. Після застосування початкової дози 20 мг 2 рази на добу (1/2табл. 40 мг), дозу препарату Вальсакор можна поступово збільшити методом титрування до: 40, 80 та 160 мг 2 рази на добу протягом декількох тижнів. Максимальна добова доза становить 320 мг на 2 прийоми. Рекомендується збільшення дози до 80 мг 2 рази на добу до кінця 2-го тижня, а максимальна цільова доза 160 мг 2 рази на добу може бути досягнута до кінця 3-го місяця терапії препаратом Вальсакор®. Досягнення цільової дози залежить від переносимості валсартану під час титрування доз. При розвитку надмірного зниження артеріального тиску, що супроводжується клінічними проявами, або порушенням функції нирок, слід зменшити дозу препарату. Можливе одночасне застосування з іншими ЛЗ, у т.ч. тромболітичними засобами, ацетилсаліцилової кислотою як антиагрегантний засіб, бета-адреноблокаторами та інгібіторами ГМГ-КоА-редуктази (статинами). Одночасне застосування з інгібіторами АПФ не рекомендується. Оцінка стану пацієнтів після перенесеного гострого ІМ має включати контроль функції нирок. Пацієнти від 6 до 18 років АГ. Рекомендована початкова доза препарату Вальсакор® у дітей та підлітків від 6 до 18 років становить 40 мг при масі тіла дитини менше 35 кг та 80 мг при масі тіла дитини понад 35 кг. Рекомендується корекція дози з урахуванням зниження артеріального тиску. Максимальні рекомендовані добові дози відображені нижче. При масі тіла ≥8 та <35 кг максимальна рекомендована добова доза становить 80 мг; від 35 до <80 кг – 160 мг; від ≥80 до ≤160 кг – 320 мг. Застосування вищих доз не рекомендовано. ХСН та перенесений ІМ. Препарат Вальсакор® не рекомендований для лікування ХСН та перенесеного гострого ІМ у пацієнтів віком до 18 років. Пацієнти похилого віку. Корекція дози препарату у пацієнтів віком від 65 років не потрібна. Порушення функції нирок. Корекція дози у пацієнтів із Cl креатиніну більше 10 мл/хв не потрібна. Одночасне застосування препарату Вальсакор з аліскіреном у пацієнтів з помірними та тяжкими порушеннями функції нирок (Cl креатиніну менше 60 мл/хв) протипоказане. Порушення функції печінки. У пацієнтів з легким або помірним порушенням функції печінки небіліарного генезу без холестазу препарат слід застосовувати з обережністю, добова доза не повинна перевищувати 80 мг. Пацієнти із цукровим діабетом. Одночасне застосування препарату Вальсакор з аліскіреном у пацієнтів із ЦД протипоказане.ПередозуванняСимптоми: основним очікуваним проявом передозування валсартану є виражене зниження артеріального тиску, яке може призвести до порушення свідомості, колапсу та/або шоку. Лікування: симптоматичне, рекомендується викликати блювання та промити шлунок. При розвитку вираженого зниження артеріального тиску необхідно перевести пацієнта в положення лежачи на спині з піднятими вгору ногами, внутрішньовенно ввести 0,9% розчин натрію хлориду. Рекомендується регулярний контроль діяльності серця та дихальної системи, ОЦК та кількості сечі, що виділяється. Гемодіаліз неефективний.Запобіжні заходи та особливі вказівкиГіперкаліємія. При одночасному застосуванні калійзберігаючих діуретиків (спіронолактон, еплеренон, тріамтерен, амілорид), препаратів калію, калійвмісних замінників солі або інших препаратів, здатних підвищувати вміст калію в плазмі крові (наприклад, гепарин), слід бути обережним. Необхідно регулярно контролювати вміст калію у плазмі крові. Порушення функції нирок. У пацієнтів з порушенням функції нирок не потрібна зміна доз препарату. Т.к. відсутні дані про застосування препарату при тяжкій нирковій недостатності (Cl креатиніну менше 10 мл/хв або 0,167 мл/с) та у пацієнтів, які перебувають на гемодіалізі, у таких випадках препарат рекомендується застосовувати з обережністю. Одночасне застосування валсартану з аліскіреном у пацієнтів з помірними та тяжкими порушеннями функції нирок (Cl креатиніну менше 60 мл/хв) протипоказано. Порушення функції печінки. У пацієнтів з легкими та помірними порушеннями функції печінки без явищ холестазу препарат Вальсакор слід застосовувати з обережністю. Пацієнти з гіпонатріємією та/або дегідратацією. У пацієнтів з вираженою гіпонатріємією та/або дегідратацією, наприклад внаслідок прийому великих доз діуретиків, у поодиноких випадках на початку терапії препаратом Вальсакор може розвинутись артеріальна гіпотензія з клінічними проявами. Перед початком лікування рекомендовано відновити вміст натрію та/або ОЦК, зокрема шляхом зменшення доз діуретиків. Стеноз ниркової артерії. Застосування валсартану коротким курсом у пацієнтів з реноваскулярною гіпертензією, що розвинулася вдруге внаслідок стенозу артерії єдиної нирки, не спричиняє суттєвих змін показників ниркової гемодинаміки, концентрації креатиніну або азоту сечовини у сироватці крові. Однак, враховуючи, що інші ЛЗ, що впливають на РААС, можуть викликати підвищення концентрації сечовини та креатиніну у сироватці крові у пацієнтів із двостороннім стенозом ниркових артерій або стенозом артерії єдиної нирки, необхідно регулярно контролювати концентрації креатиніну та залишкового азоту сечовини у сироватці крові. Стан після перенесеної трансплантації нирки. Безпека застосування препарату Вальсакор у пацієнтів, які недавно перенесли трансплантацію нирки, не встановлена. Первинний гіперальдостеронізм. Пацієнти з первинним гіперальдостеронізмом є резистентними до гіпотензивних препаратів, що впливають на РААС, тому таким пацієнтам застосування препарату Вальсакор® не рекомендується. Стеноз аортального та/або мітрального клапанів, ГЗКМП. Препарат Вальсакор® необхідно з обережністю застосовувати у пацієнтів з гемодинамічно значущим стенозом аортального та/або мітрального клапанів або ГОКМП. Період після перенесеного ІМ. Одночасне застосування з АПФ інгібіторами не рекомендується, т.к. не має додаткових клінічних переваг перед монотерапією та збільшує ризик розвитку небажаних явищ. Застосування валсартану у пацієнтів після перенесеного ІМ часто призводить до невеликого зниження артеріального тиску, проте припинення терапії через артеріальну гіпотензію зазвичай не потрібне, якщо виконувати рекомендації щодо дозування препарату. Терапію препаратом Вальсакор слід починати обережно. Оцінка стану хворих після гострого інфаркту міокарда повинна включати контроль функції нирок. Можливе одночасне застосування при гострому ІМ з іншими ЛЗ: тромболітики, ацетилсаліцилова кислота, бета-адреноблокатори та інгібітори ГМГ-КоА-редуктази (статини). ХСН. У пацієнтів з ХСН не рекомендується одночасне застосування трьох класів препаратів: інгібіторів АПФ, бета-адреноблокаторів та валсартану, т.к. ця терапія не давала додаткового клінічного ефекту, у своїй збільшувався ризик розвитку небажаних явищ. Застосування у пацієнтів з ХСН зазвичай супроводжується зниженням артеріального тиску, проте при дотриманні рекомендацій щодо добору доз лікування рідко вимагає відміни через артеріальну гіпотензію. Терапію препаратом Вальсакор у пацієнтів з ХСН слід починати з обережністю. Внаслідок придушення активності РААС у деяких пацієнтів (наприклад, у пацієнтів з ХСН III–IV функціонального класу за класифікацією NYNA, функція нирок яких залежить від стану РААС) на тлі терапії інгібіторами АПФ можлива зміна функції нирок: розвиток олігурії та/або прогресуючої азотемії,а в поодиноких випадках - ГНН та/або летальний результат. Препарат Вальсакор® блокує рецептори ангіотензину ІІ, тому у пацієнтів з ХСН потрібний регулярний контроль функції нирок. Ангіоневротичний набряк в анамнезі. Серед пацієнтів з ангіоневротичним набряком на фоні терапії препаратом Вальсакор® спостерігалися випадки розвитку ангіоневротичного набряку в анамнезі, у т.ч. та на інгібітори АПФ. При розвитку ангіоневротичного набряку слід негайно відмінити препарат та виключити можливість повторного застосування. Спеціальна інформація щодо допоміжних речовин Препарат Вальсакор містить лактозу, тому не слід застосовувати при наступних станах: непереносимість лактози, дефіцит лактази, синдром глюкозо-галактозної мальабсорбції. Вплив на здатність виконання потенційно небезпечних видів діяльності, що вимагають особливої уваги та швидких реакцій (наприклад управління автотранспортом, робота з механізмами, що рухаються). У зв'язку з можливістю виникнення запаморочення або слабкості на фоні застосування препарату Вальсакор® необхідно бути обережним при керуванні транспортними засобами та зайнятті потенційно небезпечними видами діяльності.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Діюча речовина: валсартан 160 мг; допоміжні речовини: лактози моногідрат 60,00 мг, целюлоза мікрокристалічна 82,00 мг, повідон-К25 3,00 мг, кроскармелоза натрію 4,00 мг, кремнію діоксид колоїдний 2,00 мг, магнію стеарат 9,00 мг; Оболонка плівкова: гіпромелоза 6ср 5,52 мг, титану діоксид (Е171) 1,36 мг, барвник заліза оксид жовтий (Е172) 0,50 мг, барвник заліза оксид червоний (Е172) 0,02 мг, макрогол-4000 0,6 мг. По 7, 10, 14 або 15 таблеток у блістері (контурному осередковому впакуванні) з комбінованого матеріалу ПВХ/ПЕ/ПВДХ - алюмінієвої фольги. По 2, 4, 8, 12, 14 або 20 блістерів (контурних осередкових упаковок) (по 7 таблеток), або по 2, 3, 6 або 9 блістерів (контурних осередкових упаковок) (по 10 таблеток), або по 1,2 , 4, 6, 7 або 10 блістерів (контурних осередкових упаковок) (по 14 таблеток), або по 2, 4 або 6 блістерів (контурних осередкових упаковок) (по 15 таблеток) разом з інструкцією по застосуванню поміщають в картонну пачку.Опис лікарської формиОвальні, двоопуклі таблетки з ризиком на одній стороні, покриті плівковою оболонкою коричнево-жовтого кольору. Вид на зламі: біла шорстка маса з плівковою оболонкою коричнево-жовтого кольору.Фармакотерапевтична групаАнгіотензин II рецепторів антагоніст.ФармакокінетикаВсмоктування. Після прийому валсартану внутрішньо Cmax у плазмі досягається протягом 2-4 годин. Середня абсолютна біодоступність становить 23%. При застосуванні валсартану з їжею AUC та Cmax у плазмі крові зменшуються на 40 та 50% відповідно. Тим не менш, через 8 годин після прийому препарату плазмові концентрації валсартану, прийнятого натще і з їжею, однакові. Зменшення AUC не супроводжується клінічно значущим зниженням терапевтичного ефекту валсартану, тому препарат Вальсакор можна приймати незалежно від часу їди. Розподіл. Vd валсартану в період рівноважного стану після внутрішньовенного введення становив близько 17 л, що вказує на відсутність вираженого розподілу валсартану в тканинах. Валсартан активно зв'язується з білками плазми (94-97%), переважно з альбуміном. Метаболізм. Валсартан не піддається суттєвій біотрансформації, лише близько 20% дози, прийнятої внутрішньо, виводиться у вигляді метаболітів. Гідроксильний метаболіт визначається в плазмі у низьких концентраціях (менше 10% від AUC валсартану). Цей метаболіт не має фармакологічної активності. Виведення. Валсартан виводиться двофазно: α-фаза з T1/2α менше 1 год і β-фаза з T1/2β — близько 9 год. Валсартан виводиться, в основному, у незміненому вигляді через кишечник (близько 83%) та нирками (близько 13%) . Після внутрішньовенного введення плазмовий кліренс валсартану становить близько 2 л/год, нирковий кліренс – 0,62 л/год (близько 30% від загального кліренсу). T1/2 валсартану становить 6 год. Фармакокінетика спеціальних груп пацієнтів Пацієнти з ХСН. У пацієнтів з ХСН час досягнення Cmax та T1/2 подібні до аналогічних показників у здорових добровольців. Підвищення AUC та Cmax прямо пропорційно збільшенню дози валсартану (з 40 до 160 мг 2 рази на добу). Чинник кумуляції становить, у середньому, 1,7. При внутрішньому прийомі кліренс валсартану становить близько 4,5 л/год. Вік пацієнтів із ХСН не впливав на кліренс валсартану. Пацієнти похилого віку (старше 65 років). У деяких пацієнтів старше 65 років біодоступність валсартану була вищою за таку у пацієнтів молодого віку, що не має клінічного значення. Пацієнти із порушеннями функції нирок. Нирковий кліренс валсартану становить лише 30% від загального кліренсу, тому кореляції між функцією нирок та системною біодоступністю валсартану немає. Корекція дози у пацієнтів з порушенням функції нирок (Cl креатиніну більше 10 мл/хв) не потрібна. Безпека валсартану у пацієнтів з Cl креатиніну менше 10 мл/хв та пацієнтів, які перебувають на гемодіалізі, не встановлена, тому у таких пацієнтів препарат слід застосовувати з обережністю. Оскільки ступінь зв'язування валсартану з білками плазми висока, його виведення при гемодіалізі малоймовірне. Пацієнти із порушеннями функції печінки. Близько 70% дози валсартану, що всмокталася, виводиться через кишечник, переважно в незміненому вигляді. Валсартан значною мірою не піддається метаболізму. У пацієнтів з легким або помірним порушенням функції печінки відзначалося підвищення AUC валсартану в 2 рази, порівняно з такою, у здорових добровольців. Однак не спостерігається кореляція значень AUC валсартану зі ступенем порушення функції печінки. Застосування валсартану у пацієнтів із тяжким порушенням функції печінки не вивчалось. Пацієнти віком від 6 до 18 років. Фармакокінетика валсартану у дітей та підлітків від 6 до 18 років не відрізняється від фармакокінетики валсартану у пацієнтів віком від 18 років.ФармакодинамікаВалсартан є селективним антагоністом рецепторів ангіотензину II (типу AT1) для внутрішнього прийому, небілкової природи. Вибірково блокує рецептори АТ1. Наслідком блокади АТ1-рецепторів є підвищення концентрації плазми ангіотензину II, який може стимулювати незаблоковані АТ2-рецептори, що врівноважує вазопресорні ефекти, пов'язані з порушенням АТ1-рецепторів. Валсартан не має агоністичної активності щодо АТ1-рецепторів. Його спорідненість до АТ1-рецепторів приблизно в 20000 разів вища, ніж до АТ2-рецепторів. Валсартан не інгібує АПФ, відомий також під назвою кінінази II, який перетворює ангіотензин I на ангіотензин II і руйнує брадикінін. У зв'язку з відсутністю впливу на АПФ не потенціюються ефекти брадикініну та субстанції Р. Частота розвитку сухого кашлю нижче у пацієнтів, які отримували антагоністи рецепторів ангіотензину II (АРА II), порівняно з пацієнтами, які отримували інгібітор АПФ. Валсартан не вступає у взаємодію та не блокує рецептори інших гормонів або іонні канали, що беруть участь у регуляції функцій ССС. Застосування при артеріальній гіпертензії у пацієнтів віком від 18 років. При лікуванні артеріальної гіпертензії (АГ) валсартан знижує артеріальний тиск, не впливаючи на ЧСС. Після прийому внутрішньо разової дози валсартану антигіпертензивний ефект розвивається протягом 2 годин, а максимальне зниження артеріального тиску досягається протягом 4-6 годин. Антигіпертензивний ефект валсартану зберігається протягом 24 годин після його застосування. При постійному застосуванні валсартану максимальне зниження артеріального тиску, незалежно від дози, досягається через 2-4 тижні і підтримується на досягнутому рівні під час тривалої терапії. Одночасне застосування з гідрохлортіазидом дозволяє досягти значного додаткового зниження артеріального тиску. Раптова відміна валсартану не супроводжується різким підвищенням артеріального тиску або іншими небажаними клінічними наслідками (тобто синдром відміни не розвивається). У пацієнтів з артеріальною гіпертензією, цукровим діабетом (ЦД) типу 2 та нефропатією, які приймають валсартан у дозі 160–320 мг на добу, відзначається значне зниження протеїнурії (36–44%). Застосування після гострого інфаркту міокарда (ІМ) у пацієнтів віком від 18 років. При застосуванні валсартану протягом 2 років, з початком прийому від 12 год до 10 днів після розвитку ІМ (ускладненого лівошлуночковою недостатністю та/або систолічною дисфункцією лівого шлуночка) знижуються показники загальної смертності, серцево-судинної смертності та подовжується час до першої госпіталізації. перебігу ХСН, повторного ІМ, раптової зупинки серця та інсульту (без летального результату). ХСН у пацієнтів віком від 18 років При застосуванні валсартану (в середній добовій дозі 254 мг) протягом 2 років у пацієнтів з ХСН II–IV функціонального класу за класифікацією NYHA з фракцією викиду лівого шлуночка (ФВЛШ) менше 40% та внутрішнім діастолічним діаметром ЛШ понад 2,9 см/м2 , що отримують стандартну терапію (інгібітори АПФ, діуретики, дигоксин, бета-адреноблокатори), було відзначено достовірне зниження ризику госпіталізації з приводу загострення перебігу ХСН, уповільнення прогресування ХСН, поліпшення функціонального класу ХСН за класифікацією NYHA, збільшення недостатність та поліпшення якості життя в порівнянні з плацебо. Застосування у пацієнтів старше 18 років з АГ та порушенням толерантності до глюкози При застосуванні валсартану та зміні способу життя відзначалося статистично достовірне зниження ризику розвитку ЦД у пацієнтів з артеріальною гіпертензією та порушенням толерантності до глюкози. Валсартан не впливав на частоту летальних випадків внаслідок серцево-судинних подій, ІМ та транзиторних ішемічних атак без летального результату, на частоту госпіталізацій через загострення перебігу ХСН або нестабільної стенокардії, артеріальної реваскуляризації у даної категорії пацієнтів, що відрізняються за віком, статтю та расовою. приладдя. У пацієнтів, які отримують валсартан, ризик розвитку мікроальбумінурії був достовірно нижчим, ніж у пацієнтів, які не одержують цієї терапії. Рекомендована початкова доза валсартану у пацієнтів з артеріальною гіпертензією та порушенням толерантності до глюкози становить 80 мг 1 раз на добу. За потреби доза може бути збільшена до 160 мг. Застосування у дітей та підлітків від 6 до 18 років при АГ У дітей та підлітків від 6 до 18 років валсартан забезпечує дозозалежне плавне зниження артеріального тиску. При застосуванні валсартану максимальне зниження АТ незалежно від прийнятої внутрішньо дози досягається протягом 2 тижнів і підтримується на досягнутому рівні в ході тривалої терапії.Показання до застосуванняПацієнти старше 18 років артеріальна гіпертензія. хронічна серцева недостатність (II–IV функціональний клас за класифікацією NYHA) у складі комплексної терапії (на фоні стандартної терапії) у пацієнтів, які не одержують інгібітори АПФ; підвищення виживання пацієнтів після перенесеного гострого ІМ, ускладненого лівошлуночковою недостатністю та/або систолічною дисфункцією лівого шлуночка (ЛШ), за наявності стабільних показників гемодинаміки. Пацієнти від 6 до 18 років артеріальна гіпертензія у дітей та підлітків від 6 до 18 років.Протипоказання до застосуванняпідвищена чутливість до валсартану або інших компонентів препарату; тяжкі порушення функції печінки (більше 9 балів за шкалою Чайлд-П'ю), біліарний цироз та холестаз; одночасне застосування з аліскіреном у пацієнтів з цукровим діабетом або помірними та тяжкими порушеннями функції нирок (Cl креатиніну менше 60 мл/хв); дефіцит лактази, непереносимість лактози, синдром глюкозо-галактозної мальабсорбції, оскільки до складу препарату Вальсакор входить лактоза; вагітність; період грудного вигодовування; вік до 6 років – за показанням артеріальна гіпертензія, до 18 років – за іншими показаннями. З обережністю: гіперкаліємія; одночасне застосування калійзберігаючих діуретиків; препаратів калію; калійвмісних харчових добавок або інших препаратів, здатних підвищувати вміст калію в плазмі (наприклад, гепарин); легкі та помірні порушення функції печінки небіліарного генезу без явищ холестазу; тяжкі порушення функції нирок (Cl креатиніну менше 10 мл/хв – немає клінічних даних); порушення функції нирок у пацієнтів від 6 до 18 років (Cl креатиніну менше 30 мл/хв), в т.ч. що знаходяться на гемодіалізі, гіпонатріємія, дотримання дієти з обмеженням споживання кухонної солі, стани, що супроводжуються зниженням ОЦК (в т.ч. діарея, блювання); двосторонній стеноз ниркових артерій чи стеноз артерії єдиної нирки; стан після трансплантації нирки; первинний гіперальдостеронізм,у пацієнтів із хронічною серцевою недостатністю III–IV функціонального класу (за NYNA); функція нирок яких залежить стану РААС; стеноз аортального та/або мітрального клапана; гіпертрофічна обструктивна кардіоміопатія (ГЗКМП), у пацієнтів зі спадковим ангіоневротичним набряком або ангіоневротичним набряком на фоні попередньої терапії АРА II або інгібіторами АПФ. Не рекомендується застосовувати АРА II, включаючи валсартан, одночасно з інгібіторами АПФ, оскільки їх одночасне застосування не має переваг перед монотерапією валсартаном або інгібітором АПФ щодо показників загальної смертності.Вагітність та лактаціяЗастосування АРА II у І триместрі вагітності не рекомендується. Застосування АРА II протипоказане у II–III триместрах вагітності, оскільки застосування у II–III триместрах вагітності може спричинити фетотоксичні ефекти (зниження функції нирок, маловоддя, уповільнення окостеніння кісток черепа плода) та неонатальні токсичні ефекти (ниркову недостатність, артеріальну гіпотензію, гіперкалієм). Якщо все ж таки застосовували препарат у II–III триместрах вагітності, то необхідно провести УЗД нирок та кісток черепа плода. При плануванні вагітності рекомендується перевести пацієнтку на альтернативну гіпотензивну терапію з урахуванням профілю безпеки. При підтвердженні вагітності препарат Вальсакор необхідно відмінити якомога раніше. Новонароджені, матері яких отримували АРА II під час вагітності, потребують медичного спостереження, т.к. Існує ризик розвитку артеріальної гіпотензії. Немає даних про виділення валсартану у грудне молоко. Тому слід вирішити питання про припинення годування груддю або скасування терапії валсартаном та переведення на альтернативну гіпотензивну терапію з урахуванням профілю безпеки.Побічна діяКласифікація частоти розвитку побічних ефектів Всесвітньої організації охорони здоров'я: дуже часто — ≥1/10; часто – від ≥1/100 до <1/10; нечасто – від ≥1/1000 до <1/100; рідко – від ≥1/10000 до <1/1000; дуже рідко - <1/10000; частота невідома - не може бути оцінена на основі наявних даних. Профіль безпеки валсартану у пацієнтів з АГ віком від 6 до 18 років не відрізняється від профілю безпеки валсартану у пацієнтів з АГ віком від 18 років. Артеріальна гіпертензія З боку крові та лімфатичної системи: частота невідома – зниження гемоглобіну, зниження гематокриту, нейтропенія, тромбоцитопенія. З боку імунної системи: частота невідома – реакції підвищеної чутливості, включаючи сироваткову хворобу. З боку обміну речовин та харчування: частота невідома – підвищення вмісту калію у сироватці крові, гіпонатріємія. З боку органу слуху та лабіринтні порушення: нечасто – вертиго. З боку судин: частота невідома – васкуліт. З боку дихальної системи, органів грудної клітки та середостіння: нечасто – кашель. З боку шлунково-кишкового тракту: нечасто – біль у животі. З боку печінки та жовчовивідних шляхів: частота невідома – порушення функції печінки, включаючи підвищення концентрації білірубіну у плазмі крові. З боку шкіри та підшкірних тканин: частота невідома — ангіоневротичний набряк, висипання на шкірі, свербіж шкіри, бульозний дерматит. З боку скелетно-м'язової та сполучної тканини: частота невідома – міалгія. З боку нирок та сечовивідних шляхів: частота невідома – порушення функції нирок та ниркова недостатність, підвищення концентрації креатиніну у сироватці крові. Загальні розлади та порушення у місці введення: нечасто – підвищена стомлюваність. У ході клінічних досліджень у пацієнтів з АГ спостерігалися такі небажані явища, причинно-наслідковий зв'язок яких з прийомом валсартану не встановлений: артралгія, астенія, біль у спині, діарея, запаморочення, безсоння, зниження лібідо, нудота, периферичні набряки, фарингіт, рин синусит, інфекції верхніх дихальних шляхів Після перенесеного гострого ІМ та/або при хронічній серцевій недостатності (II–IV функціональний клас за класифікацією NYHA) З боку крові та лімфатичної системи: частота невідома – тромбоцитопенія. З боку імунної системи: частота невідома – реакції підвищеної чутливості, включаючи сироваткову хворобу. З боку обміну речовин та харчування: нечасто – гіперкаліємія; частота невідома – підвищення вмісту калію в сироватці крові, гіпонатріємія. З боку нервової системи: часто – запаморочення, постуральне запаморочення; нечасто - непритомність, головний біль. З боку органу слуху та лабіринтні порушення: нечасто – вертиго. З боку серця: нечасто посилення симптомів ХСН. З боку судин: часто – виражене зниження артеріального тиску, ортостатична гіпотензія; частота невідома – васкуліт. З боку дихальної системи, органів грудної клітки та середостіння: нечасто – кашель. З боку шлунково-кишкового тракту: нечасто – нудота, діарея. З боку печінки та жовчовивідних шляхів: частота невідома – порушення функції печінки. З боку шкіри та підшкірних тканин: нечасто – ангіоневротичний набряк; частота невідома – шкірний висип, свербіж шкіри, бульозний дерматит. З боку скелетно-м'язової та сполучної тканини: рідко – рабдоміоліз; частота невідома – міалгія. З боку нирок та сечовивідних шляхів: часто – порушення функції нирок та ниркова недостатність; нечасто – гостра ниркова недостатність, підвищення концентрації креатиніну у сироватці крові; частота невідома – підвищення вмісту азоту сечовини у плазмі крові. Загальні розлади та порушення у місці введення: нечасто – астенія, підвищена стомлюваність.Взаємодія з лікарськими засобамиОдночасне застосування протипоказане Одночасне застосування АРА II, включаючи валсартан, або інгібіторів АПФ з аліскіреном, протипоказане у пацієнтів з ЦД або помірними та тяжкими порушеннями функції нирок (Cl креатиніну менше 60 мл/хв). Одночасне застосування не рекомендується Літій. Одночасне застосування препаратами літію не рекомендується, т.к. можливе оборотне збільшення концентрації літію в плазмі крові та посилення його токсичної дії. Ризик токсичних проявів, пов'язаних із застосуванням препаратів літію, може додатково збільшуватися при одночасному застосуванні з Вальсакором та діуретиками. При необхідності одночасного застосування з препаратами літію слід ретельно контролювати концентрацію літію у плазмі крові. Калійзберігаючі діуретики (спіронолактон, еплеренон, тріамтерен, амілорид), препарати калію, калійвмісні харчові добавки та інші лікарські засоби та речовини, які можуть спричинити гіперкаліємію (наприклад, гепарин). При необхідності одночасного застосування з препаратами, що впливають вміст калію, рекомендується контролювати вміст калію в плазмі крові. Одночасне застосування з обережністю Подвійна блокада РААС. У деяких пацієнтів подвійна блокада РААС супроводжувалася розвитком артеріальної гіпотензії, непритомності, гіперкаліємії та порушенням функції нирок (включаючи гостру ниркову недостатність (ОПН)). АПФ або аліскірен. НПЗЗ, в т.ч. селективні інгібітори ЦОГ-2, ацетилсаліцилова кислота в дозі більше 3 г на добу та неселективні НПЗЗ. При одночасному застосуванні з валсартаном можливе зменшення антигіпертензивного ефекту, збільшення ризику розвитку порушень функції нирок та підвищення вмісту калію у плазмі. До початку комбінованої терапії рекомендується оцінити функцію нирок, а також корекцію порушень водно-електролітного балансу. Білки-переносники. Дослідження in vitro на культурах печінки показали, що валсартан є субстратом для білків-переносників OATP1B1/OATP1B3 та MRP2. Одночасне застосування валсартану з інгібіторами білка-переносника OATP1B1/OATP1B3 (рифампіцин, циклоспорин) або MRP2 (ритонавір) може збільшити системну експозицію валсартану (Cmax та AUC). Необхідно бути обережними на початку одночасного застосування з вищевказаними препаратами або після їх відміни. Відсутність лікарської взаємодії Не виявлено клінічно значущих взаємодій з наступними ЛЗ: циметидин, варфарин, фуросемід, дигоксин, атенолол, індометацин, гідрохлортіазид, амлодипін та глібенкламід. Пацієнти віком від 6 до 18 років. У дітей та підлітків АГ часто пов'язана з порушенням функції нирок. Одночасне застосування валсартану з іншими ЛЗ, що впливають на РААС, може спричинити підвищення вмісту калію в плазмі у таких пацієнтів. Необхідно бути обережними при одночасному застосуванні вищезгаданої комбінації та регулярно контролювати функцію нирок та вміст калію в плазмі крові у даної групи пацієнтів.Спосіб застосування та дозиВсередину, незалежно від часу їди. Пацієнти старше 18 років Артеріальна гіпертензія. Рекомендована початкова доза препарату Вальсакор становить 80 мг 1 раз на добу, незалежно від расової приналежності, віку та статі пацієнта. Антигіпертензивний ефект розвивається протягом 2 тижнів і досягає свого максимуму через 4 тижні. Пацієнтам, у яких не вдалося досягти адекватного контролю АТ, добова доза валсартану може бути поступово збільшена до максимальної добової дози 320 мг. З метою додаткового зниження АТ можливе застосування діуретичних засобів (гідрохлортіазид), а також одночасне застосування інших гіпотензивних засобів. ХСН. Рекомендована початкова доза препарату Вальсакор становить 40 мг 2 рази на добу. Дозу препарату слід поступово збільшувати протягом щонайменше 2 тижнів до 80 мг 2 рази на добу, а при хорошій переносимості – до 160 мг 2 рази на добу. Максимальна добова доза становить 320 мг на два прийоми. При цьому може знадобитися зниження дози діуретиків, що одночасно приймаються. Можливе одночасне застосування з іншими лікарськими засобами, призначеними для лікування ХСН. Проте одночасна терапія препаратами трьох класів: валсартаном, інгібіторами АПФ та бета-адреноблокаторами не рекомендується. Оцінка стану пацієнтів із ХСН повинна включати контроль функції нирок. Застосування після перенесеного гострого ІМ. Лікування слід розпочинати вже через 12 годин після розвитку гострого ІМ за наявності стабільних показників гемодинаміки. Після застосування початкової дози 20 мг 2 рази на добу (1/2табл. 40 мг), дозу препарату Вальсакор можна поступово збільшити методом титрування до: 40, 80 та 160 мг 2 рази на добу протягом декількох тижнів. Максимальна добова доза становить 320 мг на 2 прийоми. Рекомендується збільшення дози до 80 мг 2 рази на добу до кінця 2-го тижня, а максимальна цільова доза 160 мг 2 рази на добу може бути досягнута до кінця 3-го місяця терапії препаратом Вальсакор®. Досягнення цільової дози залежить від переносимості валсартану під час титрування доз. При розвитку надмірного зниження артеріального тиску, що супроводжується клінічними проявами, або порушенням функції нирок, слід зменшити дозу препарату. Можливе одночасне застосування з іншими ЛЗ, у т.ч. тромболітичними засобами, ацетилсаліцилової кислотою як антиагрегантний засіб, бета-адреноблокаторами та інгібіторами ГМГ-КоА-редуктази (статинами). Одночасне застосування з інгібіторами АПФ не рекомендується. Оцінка стану пацієнтів після перенесеного гострого ІМ має включати контроль функції нирок. Пацієнти від 6 до 18 років АГ. Рекомендована початкова доза препарату Вальсакор® у дітей та підлітків від 6 до 18 років становить 40 мг при масі тіла дитини менше 35 кг та 80 мг при масі тіла дитини понад 35 кг. Рекомендується корекція дози з урахуванням зниження артеріального тиску. Максимальні рекомендовані добові дози відображені нижче. При масі тіла ≥8 та <35 кг максимальна рекомендована добова доза становить 80 мг; від 35 до <80 кг – 160 мг; від ≥80 до ≤160 кг – 320 мг. Застосування вищих доз не рекомендовано. ХСН та перенесений ІМ. Препарат Вальсакор® не рекомендований для лікування ХСН та перенесеного гострого ІМ у пацієнтів віком до 18 років. Пацієнти похилого віку. Корекція дози препарату у пацієнтів віком від 65 років не потрібна. Порушення функції нирок. Корекція дози у пацієнтів із Cl креатиніну більше 10 мл/хв не потрібна. Одночасне застосування препарату Вальсакор з аліскіреном у пацієнтів з помірними та тяжкими порушеннями функції нирок (Cl креатиніну менше 60 мл/хв) протипоказане. Порушення функції печінки. У пацієнтів з легким або помірним порушенням функції печінки небіліарного генезу без холестазу препарат слід застосовувати з обережністю, добова доза не повинна перевищувати 80 мг. Пацієнти із цукровим діабетом. Одночасне застосування препарату Вальсакор з аліскіреном у пацієнтів із ЦД протипоказане.ПередозуванняСимптоми: основним очікуваним проявом передозування валсартану є виражене зниження артеріального тиску, яке може призвести до порушення свідомості, колапсу та/або шоку. Лікування: симптоматичне, рекомендується викликати блювання та промити шлунок. При розвитку вираженого зниження артеріального тиску необхідно перевести пацієнта в положення лежачи на спині з піднятими вгору ногами, внутрішньовенно ввести 0,9% розчин натрію хлориду. Рекомендується регулярний контроль діяльності серця та дихальної системи, ОЦК та кількості сечі, що виділяється. Гемодіаліз неефективний.Запобіжні заходи та особливі вказівкиГіперкаліємія. При одночасному застосуванні калійзберігаючих діуретиків (спіронолактон, еплеренон, тріамтерен, амілорид), препаратів калію, калійвмісних замінників солі або інших препаратів, здатних підвищувати вміст калію в плазмі крові (наприклад, гепарин), слід бути обережним. Необхідно регулярно контролювати вміст калію у плазмі крові. Порушення функції нирок. У пацієнтів з порушенням функції нирок не потрібна зміна доз препарату. Т.к. відсутні дані про застосування препарату при тяжкій нирковій недостатності (Cl креатиніну менше 10 мл/хв або 0,167 мл/с) та у пацієнтів, які перебувають на гемодіалізі, у таких випадках препарат рекомендується застосовувати з обережністю. Одночасне застосування валсартану з аліскіреном у пацієнтів з помірними та тяжкими порушеннями функції нирок (Cl креатиніну менше 60 мл/хв) протипоказано. Порушення функції печінки. У пацієнтів з легкими та помірними порушеннями функції печінки без явищ холестазу препарат Вальсакор слід застосовувати з обережністю. Пацієнти з гіпонатріємією та/або дегідратацією. У пацієнтів з вираженою гіпонатріємією та/або дегідратацією, наприклад внаслідок прийому великих доз діуретиків, у поодиноких випадках на початку терапії препаратом Вальсакор може розвинутись артеріальна гіпотензія з клінічними проявами. Перед початком лікування рекомендовано відновити вміст натрію та/або ОЦК, зокрема шляхом зменшення доз діуретиків. Стеноз ниркової артерії. Застосування валсартану коротким курсом у пацієнтів з реноваскулярною гіпертензією, що розвинулася вдруге внаслідок стенозу артерії єдиної нирки, не спричиняє суттєвих змін показників ниркової гемодинаміки, концентрації креатиніну або азоту сечовини у сироватці крові. Однак, враховуючи, що інші ЛЗ, що впливають на РААС, можуть викликати підвищення концентрації сечовини та креатиніну у сироватці крові у пацієнтів із двостороннім стенозом ниркових артерій або стенозом артерії єдиної нирки, необхідно регулярно контролювати концентрації креатиніну та залишкового азоту сечовини у сироватці крові. Стан після перенесеної трансплантації нирки. Безпека застосування препарату Вальсакор у пацієнтів, які недавно перенесли трансплантацію нирки, не встановлена. Первинний гіперальдостеронізм. Пацієнти з первинним гіперальдостеронізмом є резистентними до гіпотензивних препаратів, що впливають на РААС, тому таким пацієнтам застосування препарату Вальсакор® не рекомендується. Стеноз аортального та/або мітрального клапанів, ГЗКМП. Препарат Вальсакор® необхідно з обережністю застосовувати у пацієнтів з гемодинамічно значущим стенозом аортального та/або мітрального клапанів або ГОКМП. Період після перенесеного ІМ. Одночасне застосування з АПФ інгібіторами не рекомендується, т.к. не має додаткових клінічних переваг перед монотерапією та збільшує ризик розвитку небажаних явищ. Застосування валсартану у пацієнтів після перенесеного ІМ часто призводить до невеликого зниження артеріального тиску, проте припинення терапії через артеріальну гіпотензію зазвичай не потрібне, якщо виконувати рекомендації щодо дозування препарату. Терапію препаратом Вальсакор слід починати обережно. Оцінка стану хворих після гострого інфаркту міокарда повинна включати контроль функції нирок. Можливе одночасне застосування при гострому ІМ з іншими ЛЗ: тромболітики, ацетилсаліцилова кислота, бета-адреноблокатори та інгібітори ГМГ-КоА-редуктази (статини). ХСН. У пацієнтів з ХСН не рекомендується одночасне застосування трьох класів препаратів: інгібіторів АПФ, бета-адреноблокаторів та валсартану, т.к. ця терапія не давала додаткового клінічного ефекту, у своїй збільшувався ризик розвитку небажаних явищ. Застосування у пацієнтів з ХСН зазвичай супроводжується зниженням артеріального тиску, проте при дотриманні рекомендацій щодо добору доз лікування рідко вимагає відміни через артеріальну гіпотензію. Терапію препаратом Вальсакор у пацієнтів з ХСН слід починати з обережністю. Внаслідок придушення активності РААС у деяких пацієнтів (наприклад, у пацієнтів з ХСН III–IV функціонального класу за класифікацією NYNA, функція нирок яких залежить від стану РААС) на тлі терапії інгібіторами АПФ можлива зміна функції нирок: розвиток олігурії та/або прогресуючої азотемії,а в поодиноких випадках - ГНН та/або летальний результат. Препарат Вальсакор® блокує рецептори ангіотензину ІІ, тому у пацієнтів з ХСН потрібний регулярний контроль функції нирок. Ангіоневротичний набряк в анамнезі. Серед пацієнтів з ангіоневротичним набряком на фоні терапії препаратом Вальсакор® спостерігалися випадки розвитку ангіоневротичного набряку в анамнезі, у т.ч. та на інгібітори АПФ. При розвитку ангіоневротичного набряку слід негайно відмінити препарат та виключити можливість повторного застосування. Спеціальна інформація щодо допоміжних речовин Препарат Вальсакор містить лактозу, тому не слід застосовувати при наступних станах: непереносимість лактози, дефіцит лактази, синдром глюкозо-галактозної мальабсорбції. Вплив на здатність виконання потенційно небезпечних видів діяльності, що вимагають особливої уваги та швидких реакцій (наприклад управління автотранспортом, робота з механізмами, що рухаються). У зв'язку з можливістю виникнення запаморочення або слабкості на фоні застосування препарату Вальсакор® необхідно бути обережним при керуванні транспортними засобами та зайнятті потенційно небезпечними видами діяльності.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
450,00 грн
246,00 грн
Склад, форма випуску та упаковкаПігулки - 1 таб. Діюча речовина: валсартан 320 мг; допоміжні речовини: лактози моногідрат 120,00 мг, целюлоза мікрокристалічна 164,00 мг, повідон 6,00 мг, кроскармелоза натрію 8,00 мг, кремнію діоксид колоїдний 4,00 мг, магнію стеарат 18,00 мг; Оболонка плівкова: гіпромелоза 11,20 мг, титану діоксид (Е171) 2,40 мг, барвник заліза оксид жовтий (Е172) 1,00 мг, барвник заліза оксид червоний (Е172) 0,20 мг, макрогол-4000 1,20 мг . По 10, 14 або 15 таблеток у блістері з комбінованого матеріалу ПВХ/ПЕ/ПВДХ – алюмінієвої фольги. По 2, 3 або 14 блістерів (по 10 таблеток), або по 1, 2, 4, 7 або 10 блістерів (по 14 таблеток), або по 2 блістери (по 15 таблеток) разом з інструкцією по застосуванню поміщають у картонну пачку.Опис лікарської формиОвальні, двоопуклі таблетки з ризиком на одній стороні, покриті плівковою оболонкою світло-коричневого кольору.Фармакотерапевтична групаАнгіотензин II рецепторів антагоніст.ФармакокінетикаВсмоктування. Після прийому валсартану внутрішньо Cmax у плазмі досягається протягом 2-4 годин. Середня абсолютна біодоступність становить 23%. При застосуванні валсартану з їжею AUC та Cmax у плазмі крові зменшуються на 40 та 50% відповідно. Тим не менш, через 8 годин після прийому препарату плазмові концентрації валсартану, прийнятого натще і з їжею, однакові. Зменшення AUC не супроводжується клінічно значущим зниженням терапевтичного ефекту валсартану, тому препарат Вальсакор можна приймати незалежно від часу їди. Розподіл. Vd валсартану в період рівноважного стану після внутрішньовенного введення становив близько 17 л, що вказує на відсутність вираженого розподілу валсартану в тканинах. Валсартан активно зв'язується з білками плазми (94-97%), переважно з альбуміном. Метаболізм. Валсартан не піддається суттєвій біотрансформації, лише близько 20% дози, прийнятої внутрішньо, виводиться у вигляді метаболітів. Гідроксильний метаболіт визначається в плазмі у низьких концентраціях (менше 10% від AUC валсартану). Цей метаболіт не має фармакологічної активності. Виведення. Валсартан виводиться двофазно: α-фаза з T1/2α менше 1 год і β-фаза з T1/2β — близько 9 год. Валсартан виводиться, в основному, у незміненому вигляді через кишечник (близько 83%) та нирками (близько 13%) . Після внутрішньовенного введення плазмовий кліренс валсартану становить близько 2 л/год, нирковий кліренс – 0,62 л/год (близько 30% від загального кліренсу). T1/2 валсартану становить 6 год. Фармакокінетика спеціальних груп пацієнтів Пацієнти з ХСН. У пацієнтів з ХСН час досягнення Cmax та T1/2 подібні до аналогічних показників у здорових добровольців. Підвищення AUC та Cmax прямо пропорційно збільшенню дози валсартану (з 40 до 160 мг 2 рази на добу). Чинник кумуляції становить, у середньому, 1,7. При внутрішньому прийомі кліренс валсартану становить близько 4,5 л/год. Вік пацієнтів із ХСН не впливав на кліренс валсартану. Пацієнти похилого віку (старше 65 років). У деяких пацієнтів старше 65 років біодоступність валсартану була вищою за таку у пацієнтів молодого віку, що не має клінічного значення. Пацієнти із порушеннями функції нирок. Нирковий кліренс валсартану становить лише 30% від загального кліренсу, тому кореляції між функцією нирок та системною біодоступністю валсартану немає. Корекція дози у пацієнтів з порушенням функції нирок (Cl креатиніну більше 10 мл/хв) не потрібна. Безпека валсартану у пацієнтів з Cl креатиніну менше 10 мл/хв та пацієнтів, які перебувають на гемодіалізі, не встановлена, тому у таких пацієнтів препарат слід застосовувати з обережністю. Оскільки ступінь зв'язування валсартану з білками плазми висока, його виведення при гемодіалізі малоймовірне. Пацієнти із порушеннями функції печінки. Близько 70% дози валсартану, що всмокталася, виводиться через кишечник, переважно в незміненому вигляді. Валсартан значною мірою не піддається метаболізму. У пацієнтів з легким або помірним порушенням функції печінки відзначалося підвищення AUC валсартану в 2 рази, порівняно з такою, у здорових добровольців. Однак не спостерігається кореляція значень AUC валсартану зі ступенем порушення функції печінки. Застосування валсартану у пацієнтів із тяжким порушенням функції печінки не вивчалось. Пацієнти віком від 6 до 18 років. Фармакокінетика валсартану у дітей та підлітків від 6 до 18 років не відрізняється від фармакокінетики валсартану у пацієнтів віком від 18 років.ФармакодинамікаВалсартан є селективним антагоністом рецепторів ангіотензину II (типу AT1) для внутрішнього прийому, небілкової природи. Вибірково блокує рецептори АТ1. Наслідком блокади АТ1-рецепторів є підвищення концентрації плазми ангіотензину II, який може стимулювати незаблоковані АТ2-рецептори, що врівноважує вазопресорні ефекти, пов'язані з порушенням АТ1-рецепторів. Валсартан не має агоністичної активності щодо АТ1-рецепторів. Його спорідненість до АТ1-рецепторів приблизно в 20000 разів вища, ніж до АТ2-рецепторів. Валсартан не інгібує АПФ, відомий також під назвою кінінази II, який перетворює ангіотензин I на ангіотензин II і руйнує брадикінін. У зв'язку з відсутністю впливу на АПФ не потенціюються ефекти брадикініну та субстанції Р. Частота розвитку сухого кашлю нижче у пацієнтів, які отримували антагоністи рецепторів ангіотензину II (АРА II), порівняно з пацієнтами, які отримували інгібітор АПФ. Валсартан не вступає у взаємодію та не блокує рецептори інших гормонів або іонні канали, що беруть участь у регуляції функцій ССС. Застосування при артеріальній гіпертензії у пацієнтів віком від 18 років. При лікуванні артеріальної гіпертензії (АГ) валсартан знижує артеріальний тиск, не впливаючи на ЧСС. Після прийому внутрішньо разової дози валсартану антигіпертензивний ефект розвивається протягом 2 годин, а максимальне зниження артеріального тиску досягається протягом 4-6 годин. Антигіпертензивний ефект валсартану зберігається протягом 24 годин після його застосування. При постійному застосуванні валсартану максимальне зниження артеріального тиску, незалежно від дози, досягається через 2-4 тижні і підтримується на досягнутому рівні під час тривалої терапії. Одночасне застосування з гідрохлортіазидом дозволяє досягти значного додаткового зниження артеріального тиску. Раптова відміна валсартану не супроводжується різким підвищенням артеріального тиску або іншими небажаними клінічними наслідками (тобто синдром відміни не розвивається). У пацієнтів з артеріальною гіпертензією, цукровим діабетом (ЦД) типу 2 та нефропатією, які приймають валсартан у дозі 160–320 мг на добу, відзначається значне зниження протеїнурії (36–44%). Застосування після гострого інфаркту міокарда (ІМ) у пацієнтів віком від 18 років. При застосуванні валсартану протягом 2 років, з початком прийому від 12 год до 10 днів після розвитку ІМ (ускладненого лівошлуночковою недостатністю та/або систолічною дисфункцією лівого шлуночка) знижуються показники загальної смертності, серцево-судинної смертності та подовжується час до першої госпіталізації. перебігу ХСН, повторного ІМ, раптової зупинки серця та інсульту (без летального результату). ХСН у пацієнтів віком від 18 років При застосуванні валсартану (в середній добовій дозі 254 мг) протягом 2 років у пацієнтів з ХСН II–IV функціонального класу за класифікацією NYHA з фракцією викиду лівого шлуночка (ФВЛШ) менше 40% та внутрішнім діастолічним діаметром ЛШ понад 2,9 см/м2 , що отримують стандартну терапію (інгібітори АПФ, діуретики, дигоксин, бета-адреноблокатори), було відзначено достовірне зниження ризику госпіталізації з приводу загострення перебігу ХСН, уповільнення прогресування ХСН, поліпшення функціонального класу ХСН за класифікацією NYHA, збільшення недостатність та поліпшення якості життя в порівнянні з плацебо. Застосування у пацієнтів старше 18 років з АГ та порушенням толерантності до глюкози При застосуванні валсартану та зміні способу життя відзначалося статистично достовірне зниження ризику розвитку ЦД у пацієнтів з артеріальною гіпертензією та порушенням толерантності до глюкози. Валсартан не впливав на частоту летальних випадків внаслідок серцево-судинних подій, ІМ та транзиторних ішемічних атак без летального результату, на частоту госпіталізацій через загострення перебігу ХСН або нестабільної стенокардії, артеріальної реваскуляризації у даної категорії пацієнтів, що відрізняються за віком, статтю та расовою. приладдя. У пацієнтів, які отримують валсартан, ризик розвитку мікроальбумінурії був достовірно нижчим, ніж у пацієнтів, які не одержують цієї терапії. Рекомендована початкова доза валсартану у пацієнтів з артеріальною гіпертензією та порушенням толерантності до глюкози становить 80 мг 1 раз на добу. За потреби доза може бути збільшена до 160 мг. Застосування у дітей та підлітків від 6 до 18 років при АГ У дітей та підлітків від 6 до 18 років валсартан забезпечує дозозалежне плавне зниження артеріального тиску. При застосуванні валсартану максимальне зниження АТ незалежно від прийнятої внутрішньо дози досягається протягом 2 тижнів і підтримується на досягнутому рівні в ході тривалої терапії.Показання до застосуванняПацієнти старше 18 років артеріальна гіпертензія. хронічна серцева недостатність (II–IV функціональний клас за класифікацією NYHA) у складі комплексної терапії (на фоні стандартної терапії) у пацієнтів, які не одержують інгібітори АПФ; підвищення виживання пацієнтів після перенесеного гострого ІМ, ускладненого лівошлуночковою недостатністю та/або систолічною дисфункцією лівого шлуночка (ЛШ), за наявності стабільних показників гемодинаміки. Пацієнти від 6 до 18 років артеріальна гіпертензія у дітей та підлітків від 6 до 18 років.Протипоказання до застосуванняпідвищена чутливість до валсартану або інших компонентів препарату; тяжкі порушення функції печінки (більше 9 балів за шкалою Чайлд-П'ю), біліарний цироз та холестаз; одночасне застосування з аліскіреном у пацієнтів з цукровим діабетом або помірними та тяжкими порушеннями функції нирок (Cl креатиніну менше 60 мл/хв); дефіцит лактази, непереносимість лактози, синдром глюкозо-галактозної мальабсорбції, оскільки до складу препарату Вальсакор входить лактоза; вагітність; період грудного вигодовування; вік до 6 років – за показанням артеріальна гіпертензія, до 18 років – за іншими показаннями. З обережністю: гіперкаліємія; одночасне застосування калійзберігаючих діуретиків; препаратів калію; калійвмісних харчових добавок або інших препаратів, здатних підвищувати вміст калію в плазмі (наприклад, гепарин); легкі та помірні порушення функції печінки небіліарного генезу без явищ холестазу; тяжкі порушення функції нирок (Cl креатиніну менше 10 мл/хв – немає клінічних даних); порушення функції нирок у пацієнтів від 6 до 18 років (Cl креатиніну менше 30 мл/хв), в т.ч. що знаходяться на гемодіалізі, гіпонатріємія, дотримання дієти з обмеженням споживання кухонної солі, стани, що супроводжуються зниженням ОЦК (в т.ч. діарея, блювання); двосторонній стеноз ниркових артерій чи стеноз артерії єдиної нирки; стан після трансплантації нирки; первинний гіперальдостеронізм,у пацієнтів із хронічною серцевою недостатністю III–IV функціонального класу (за NYNA); функція нирок яких залежить стану РААС; стеноз аортального та/або мітрального клапана; гіпертрофічна обструктивна кардіоміопатія (ГЗКМП), у пацієнтів зі спадковим ангіоневротичним набряком або ангіоневротичним набряком на фоні попередньої терапії АРА II або інгібіторами АПФ. Не рекомендується застосовувати АРА II, включаючи валсартан, одночасно з інгібіторами АПФ, оскільки їх одночасне застосування не має переваг перед монотерапією валсартаном або інгібітором АПФ щодо показників загальної смертності.Вагітність та лактаціяЗастосування АРА II у І триместрі вагітності не рекомендується. Застосування АРА II протипоказане у II–III триместрах вагітності, оскільки застосування у II–III триместрах вагітності може спричинити фетотоксичні ефекти (зниження функції нирок, маловоддя, уповільнення окостеніння кісток черепа плода) та неонатальні токсичні ефекти (ниркову недостатність, артеріальну гіпотензію, гіперкалієм). Якщо все ж таки застосовували препарат у II–III триместрах вагітності, то необхідно провести УЗД нирок та кісток черепа плода. При плануванні вагітності рекомендується перевести пацієнтку на альтернативну гіпотензивну терапію з урахуванням профілю безпеки. При підтвердженні вагітності препарат Вальсакор необхідно відмінити якомога раніше. Новонароджені, матері яких отримували АРА II під час вагітності, потребують медичного спостереження, т.к. Існує ризик розвитку артеріальної гіпотензії. Немає даних про виділення валсартану у грудне молоко. Тому слід вирішити питання про припинення годування груддю або скасування терапії валсартаном та переведення на альтернативну гіпотензивну терапію з урахуванням профілю безпеки.Побічна діяКласифікація частоти розвитку побічних ефектів Всесвітньої організації охорони здоров'я: дуже часто — ≥1/10; часто – від ≥1/100 до <1/10; нечасто – від ≥1/1000 до <1/100; рідко – від ≥1/10000 до <1/1000; дуже рідко - <1/10000; частота невідома - не може бути оцінена на основі наявних даних. Профіль безпеки валсартану у пацієнтів з АГ віком від 6 до 18 років не відрізняється від профілю безпеки валсартану у пацієнтів з АГ віком від 18 років. Артеріальна гіпертензія З боку крові та лімфатичної системи: частота невідома – зниження гемоглобіну, зниження гематокриту, нейтропенія, тромбоцитопенія. З боку імунної системи: частота невідома – реакції підвищеної чутливості, включаючи сироваткову хворобу. З боку обміну речовин та харчування: частота невідома – підвищення вмісту калію у сироватці крові, гіпонатріємія. З боку органу слуху та лабіринтні порушення: нечасто – вертиго. З боку судин: частота невідома – васкуліт. З боку дихальної системи, органів грудної клітки та середостіння: нечасто – кашель. З боку шлунково-кишкового тракту: нечасто – біль у животі. З боку печінки та жовчовивідних шляхів: частота невідома – порушення функції печінки, включаючи підвищення концентрації білірубіну у плазмі крові. З боку шкіри та підшкірних тканин: частота невідома — ангіоневротичний набряк, висипання на шкірі, свербіж шкіри, бульозний дерматит. З боку скелетно-м'язової та сполучної тканини: частота невідома – міалгія. З боку нирок та сечовивідних шляхів: частота невідома – порушення функції нирок та ниркова недостатність, підвищення концентрації креатиніну у сироватці крові. Загальні розлади та порушення у місці введення: нечасто – підвищена стомлюваність. У ході клінічних досліджень у пацієнтів з АГ спостерігалися такі небажані явища, причинно-наслідковий зв'язок яких з прийомом валсартану не встановлений: артралгія, астенія, біль у спині, діарея, запаморочення, безсоння, зниження лібідо, нудота, периферичні набряки, фарингіт, рин синусит, інфекції верхніх дихальних шляхів Після перенесеного гострого ІМ та/або при хронічній серцевій недостатності (II–IV функціональний клас за класифікацією NYHA) З боку крові та лімфатичної системи: частота невідома – тромбоцитопенія. З боку імунної системи: частота невідома – реакції підвищеної чутливості, включаючи сироваткову хворобу. З боку обміну речовин та харчування: нечасто – гіперкаліємія; частота невідома – підвищення вмісту калію в сироватці крові, гіпонатріємія. З боку нервової системи: часто – запаморочення, постуральне запаморочення; нечасто - непритомність, головний біль. З боку органу слуху та лабіринтні порушення: нечасто – вертиго. З боку серця: нечасто посилення симптомів ХСН. З боку судин: часто – виражене зниження артеріального тиску, ортостатична гіпотензія; частота невідома – васкуліт. З боку дихальної системи, органів грудної клітки та середостіння: нечасто – кашель. З боку шлунково-кишкового тракту: нечасто – нудота, діарея. З боку печінки та жовчовивідних шляхів: частота невідома – порушення функції печінки. З боку шкіри та підшкірних тканин: нечасто – ангіоневротичний набряк; частота невідома – шкірний висип, свербіж шкіри, бульозний дерматит. З боку скелетно-м'язової та сполучної тканини: рідко – рабдоміоліз; частота невідома – міалгія. З боку нирок та сечовивідних шляхів: часто – порушення функції нирок та ниркова недостатність; нечасто – гостра ниркова недостатність, підвищення концентрації креатиніну у сироватці крові; частота невідома – підвищення вмісту азоту сечовини у плазмі крові. Загальні розлади та порушення у місці введення: нечасто – астенія, підвищена стомлюваність.Взаємодія з лікарськими засобамиОдночасне застосування протипоказане Одночасне застосування АРА II, включаючи валсартан, або інгібіторів АПФ з аліскіреном, протипоказане у пацієнтів з ЦД або помірними та тяжкими порушеннями функції нирок (Cl креатиніну менше 60 мл/хв). Одночасне застосування не рекомендується Літій. Одночасне застосування препаратами літію не рекомендується, т.к. можливе оборотне збільшення концентрації літію в плазмі крові та посилення його токсичної дії. Ризик токсичних проявів, пов'язаних із застосуванням препаратів літію, може додатково збільшуватися при одночасному застосуванні з Вальсакором та діуретиками. При необхідності одночасного застосування з препаратами літію слід ретельно контролювати концентрацію літію у плазмі крові. Калійзберігаючі діуретики (спіронолактон, еплеренон, тріамтерен, амілорид), препарати калію, калійвмісні харчові добавки та інші лікарські засоби та речовини, які можуть спричинити гіперкаліємію (наприклад, гепарин). За необхідності одночасного застосування з препаратами, що впливають на вміст калію, рекомендується контролювати вміст калію у плазмі. Одночасне застосування з обережністю Подвійна блокада РААС. У деяких пацієнтів подвійна блокада РААС супроводжувалася розвитком артеріальної гіпотензії, непритомності, гіперкаліємії та порушенням функції нирок (включаючи гостру ниркову недостатність (ОПН)). АПФ або аліскірен. НПЗЗ, в т.ч. селективні інгібітори ЦОГ-2, ацетилсаліцилова кислота в дозі більше 3 г на добу та неселективні НПЗЗ. При одночасному застосуванні з валсартаном можливе зменшення антигіпертензивного ефекту, збільшення ризику розвитку порушень функції нирок та підвищення вмісту калію у плазмі. До початку комбінованої терапії рекомендується оцінити функцію нирок, а також корекцію порушень водно-електролітного балансу. Білки-переносники. Дослідження in vitro на культурах печінки показали, що валсартан є субстратом для білків-переносників OATP1B1/OATP1B3 та MRP2. Одночасне застосування валсартану з інгібіторами білка-переносника OATP1B1/OATP1B3 (рифампіцин, циклоспорин) або MRP2 (ритонавір) може збільшити системну експозицію валсартану (Cmax та AUC). Необхідно бути обережними на початку одночасного застосування з вищевказаними препаратами або після їх відміни. Відсутність лікарської взаємодії Не виявлено клінічно значущих взаємодій з наступними ЛЗ: циметидин, варфарин, фуросемід, дигоксин, атенолол, індометацин, гідрохлортіазид, амлодипін та глібенкламід. Пацієнти віком від 6 до 18 років. У дітей та підлітків АГ часто пов'язана з порушенням функції нирок. Одночасне застосування валсартану з іншими ЛЗ, що впливають на РААС, може спричинити підвищення вмісту калію в плазмі у таких пацієнтів. Необхідно бути обережними при одночасному застосуванні вищезгаданої комбінації та регулярно контролювати функцію нирок та вміст калію в плазмі крові у даної групи пацієнтів.Спосіб застосування та дозиВсередину, незалежно від часу їди. Пацієнти старше 18 років Артеріальна гіпертензія. Рекомендована початкова доза препарату Вальсакор становить 80 мг 1 раз на добу, незалежно від расової приналежності, віку та статі пацієнта. Антигіпертензивний ефект розвивається протягом 2 тижнів і досягає свого максимуму через 4 тижні. Пацієнтам, у яких не вдалося досягти адекватного контролю АТ, добова доза валсартану може бути поступово збільшена до максимальної добової дози 320 мг. З метою додаткового зниження АТ можливе застосування діуретичних засобів (гідрохлортіазид), а також одночасне застосування інших гіпотензивних засобів. ХСН. Рекомендована початкова доза препарату Вальсакор становить 40 мг 2 рази на добу. Дозу препарату слід поступово збільшувати протягом щонайменше 2 тижнів до 80 мг 2 рази на добу, а при хорошій переносимості – до 160 мг 2 рази на добу. Максимальна добова доза становить 320 мг на два прийоми. При цьому може знадобитися зниження дози діуретиків, що одночасно приймаються. Можливе одночасне застосування з іншими лікарськими засобами, призначеними для лікування ХСН. Проте одночасна терапія препаратами трьох класів: валсартаном, інгібіторами АПФ та бета-адреноблокаторами не рекомендується. Оцінка стану пацієнтів із ХСН повинна включати контроль функції нирок. Застосування після перенесеного гострого ІМ. Лікування слід розпочинати вже через 12 годин після розвитку гострого ІМ за наявності стабільних показників гемодинаміки. Після застосування початкової дози 20 мг 2 рази на добу (1/2табл. 40 мг), дозу препарату Вальсакор можна поступово збільшити методом титрування до: 40, 80 та 160 мг 2 рази на добу протягом декількох тижнів. Максимальна добова доза становить 320 мг на 2 прийоми. Рекомендується збільшення дози до 80 мг 2 рази на добу до кінця 2-го тижня, а максимальна цільова доза 160 мг 2 рази на добу може бути досягнута до кінця 3-го місяця терапії препаратом Вальсакор®. Досягнення цільової дози залежить від переносимості валсартану під час титрування доз. При розвитку надмірного зниження артеріального тиску, що супроводжується клінічними проявами, або порушенням функції нирок, слід зменшити дозу препарату. Можливе одночасне застосування з іншими ЛЗ, у т.ч. тромболітичними засобами, ацетилсаліцилової кислотою як антиагрегантний засіб, бета-адреноблокаторами та інгібіторами ГМГ-КоА-редуктази (статинами). Одночасне застосування з інгібіторами АПФ не рекомендується. Оцінка стану пацієнтів після перенесеного гострого ІМ має включати контроль функції нирок. Пацієнти від 6 до 18 років АГ. Рекомендована початкова доза препарату Вальсакор® у дітей та підлітків від 6 до 18 років становить 40 мг при масі тіла дитини менше 35 кг та 80 мг при масі тіла дитини понад 35 кг. Рекомендується корекція дози з урахуванням зниження артеріального тиску. Максимальні рекомендовані добові дози відображені нижче. При масі тіла ≥8 та <35 кг максимальна рекомендована добова доза становить 80 мг; від 35 до <80 кг – 160 мг; від ≥80 до ≤160 кг – 320 мг. Застосування вищих доз не рекомендовано. ХСН та перенесений ІМ. Препарат Вальсакор® не рекомендований для лікування ХСН та перенесеного гострого ІМ у пацієнтів віком до 18 років. Пацієнти похилого віку. Корекція дози препарату у пацієнтів віком від 65 років не потрібна. Порушення функції нирок. Корекція дози у пацієнтів із Cl креатиніну більше 10 мл/хв не потрібна. Одночасне застосування препарату Вальсакор з аліскіреном у пацієнтів з помірними та тяжкими порушеннями функції нирок (Cl креатиніну менше 60 мл/хв) протипоказане. Порушення функції печінки. У пацієнтів з легким або помірним порушенням функції печінки небіліарного генезу без холестазу препарат слід застосовувати з обережністю, добова доза не повинна перевищувати 80 мг. Пацієнти із цукровим діабетом. Одночасне застосування препарату Вальсакор з аліскіреном у пацієнтів із ЦД протипоказане.ПередозуванняСимптоми: основним очікуваним проявом передозування валсартану є виражене зниження артеріального тиску, яке може призвести до порушення свідомості, колапсу та/або шоку. Лікування: симптоматичне, рекомендується викликати блювання та промити шлунок. При розвитку вираженого зниження артеріального тиску необхідно перевести пацієнта в положення лежачи на спині з піднятими вгору ногами, внутрішньовенно ввести 0,9% розчин натрію хлориду. Рекомендується регулярний контроль діяльності серця та дихальної системи, ОЦК та кількості сечі, що виділяється. Гемодіаліз неефективний.Запобіжні заходи та особливі вказівкиГіперкаліємія. При одночасному застосуванні калійзберігаючих діуретиків (спіронолактон, еплеренон, тріамтерен, амілорид), препаратів калію, калійвмісних замінників солі або інших препаратів, здатних підвищувати вміст калію в плазмі крові (наприклад, гепарин), слід бути обережним. Необхідно регулярно контролювати вміст калію у плазмі крові. Порушення функції нирок. У пацієнтів з порушенням функції нирок не потрібна зміна доз препарату. Т.к. відсутні дані про застосування препарату при тяжкій нирковій недостатності (Cl креатиніну менше 10 мл/хв або 0,167 мл/с) та у пацієнтів, які перебувають на гемодіалізі, у таких випадках препарат рекомендується застосовувати з обережністю. Одночасне застосування валсартану з аліскіреном у пацієнтів з помірними та тяжкими порушеннями функції нирок (Cl креатиніну менше 60 мл/хв) протипоказано. Порушення функції печінки. У пацієнтів з легкими та помірними порушеннями функції печінки без явищ холестазу препарат Вальсакор слід застосовувати з обережністю. Пацієнти з гіпонатріємією та/або дегідратацією. У пацієнтів з вираженою гіпонатріємією та/або дегідратацією, наприклад внаслідок прийому великих доз діуретиків, у поодиноких випадках на початку терапії препаратом Вальсакор може розвинутись артеріальна гіпотензія з клінічними проявами. Перед початком лікування рекомендовано відновити вміст натрію та/або ОЦК, зокрема шляхом зменшення доз діуретиків. Стеноз ниркової артерії. Застосування валсартану коротким курсом у пацієнтів з реноваскулярною гіпертензією, що розвинулася вдруге внаслідок стенозу артерії єдиної нирки, не спричиняє суттєвих змін показників ниркової гемодинаміки, концентрації креатиніну або азоту сечовини у сироватці крові. Однак, враховуючи, що інші ЛЗ, що впливають на РААС, можуть викликати підвищення концентрації сечовини та креатиніну у сироватці крові у пацієнтів із двостороннім стенозом ниркових артерій або стенозом артерії єдиної нирки, необхідно регулярно контролювати концентрації креатиніну та залишкового азоту сечовини у сироватці крові. Стан після перенесеної трансплантації нирки. Безпека застосування препарату Вальсакор у пацієнтів, які недавно перенесли трансплантацію нирки, не встановлена. Первинний гіперальдостеронізм. Пацієнти з первинним гіперальдостеронізмом є резистентними до гіпотензивних препаратів, що впливають на РААС, тому таким пацієнтам застосування препарату Вальсакор® не рекомендується. Стеноз аортального та/або мітрального клапанів, ГЗКМП. Препарат Вальсакор® необхідно з обережністю застосовувати у пацієнтів з гемодинамічно значущим стенозом аортального та/або мітрального клапанів або ГОКМП. Період після перенесеного ІМ. Одночасне застосування з АПФ інгібіторами не рекомендується, т.к. не має додаткових клінічних переваг перед монотерапією та збільшує ризик розвитку небажаних явищ. Застосування валсартану у пацієнтів після перенесеного ІМ часто призводить до невеликого зниження артеріального тиску, проте припинення терапії через артеріальну гіпотензію зазвичай не потрібне, якщо виконувати рекомендації щодо дозування препарату. Терапію препаратом Вальсакор слід починати обережно. Оцінка стану хворих після гострого інфаркту міокарда повинна включати контроль функції нирок. Можливе одночасне застосування при гострому ІМ з іншими ЛЗ: тромболітики, ацетилсаліцилова кислота, бета-адреноблокатори та інгібітори ГМГ-КоА-редуктази (статини). ХСН. У пацієнтів з ХСН не рекомендується одночасне застосування трьох класів препаратів: інгібіторів АПФ, бета-адреноблокаторів та валсартану, т.к. ця терапія не давала додаткового клінічного ефекту, у своїй збільшувався ризик розвитку небажаних явищ. Застосування у пацієнтів з ХСН зазвичай супроводжується зниженням артеріального тиску, проте при дотриманні рекомендацій щодо добору доз лікування рідко вимагає відміни через артеріальну гіпотензію. Терапію препаратом Вальсакор у пацієнтів з ХСН слід починати з обережністю. Внаслідок придушення активності РААС у деяких пацієнтів (наприклад, у пацієнтів з ХСН III–IV функціонального класу за класифікацією NYNA, функція нирок яких залежить від стану РААС) на тлі терапії інгібіторами АПФ можлива зміна функції нирок: розвиток олігурії та/або прогресуючої азотемії,а в поодиноких випадках - ГНН та/або летальний результат. Препарат Вальсакор® блокує рецептори ангіотензину ІІ, тому у пацієнтів з ХСН потрібний регулярний контроль функції нирок. Ангіоневротичний набряк в анамнезі. Серед пацієнтів з ангіоневротичним набряком на фоні терапії препаратом Вальсакор® спостерігалися випадки розвитку ангіоневротичного набряку в анамнезі, у т.ч. та на інгібітори АПФ. При розвитку ангіоневротичного набряку слід негайно відмінити препарат та виключити можливість повторного застосування. Спеціальна інформація щодо допоміжних речовин Препарат Вальсакор містить лактозу, тому не слід застосовувати при наступних станах: непереносимість лактози, дефіцит лактази, синдром глюкозо-галактозної мальабсорбції. Вплив на здатність виконання потенційно небезпечних видів діяльності, що вимагають особливої уваги та швидких реакцій (наприклад управління автотранспортом, робота з механізмами, що рухаються). У зв'язку з можливістю виникнення запаморочення або слабкості на фоні застосування препарату Вальсакор® необхідно бути обережним при керуванні транспортними засобами та зайнятті потенційно небезпечними видами діяльності.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Діюча речовина: валсартан 320 мг; допоміжні речовини: лактози моногідрат 120,00 мг, целюлоза мікрокристалічна 164,00 мг, повідон 6,00 мг, кроскармелоза натрію 8,00 мг, кремнію діоксид колоїдний 4,00 мг, магнію стеарат 18,00 мг; Оболонка плівкова: гіпромелоза 11,20 мг, титану діоксид (Е171) 2,40 мг, барвник заліза оксид жовтий (Е172) 1,00 мг, барвник заліза оксид червоний (Е172) 0,20 мг, макрогол-4000 1,20 мг . По 10, 14 або 15 таблеток у блістері з комбінованого матеріалу ПВХ/ПЕ/ПВДХ – алюмінієвої фольги. По 2, 3 або 14 блістерів (по 10 таблеток), або по 1, 2, 4, 7 або 10 блістерів (по 14 таблеток), або по 2 блістери (по 15 таблеток) разом з інструкцією по застосуванню поміщають у картонну пачку.Опис лікарської формиОвальні, двоопуклі таблетки з ризиком на одній стороні, покриті плівковою оболонкою світло-коричневого кольору.Фармакотерапевтична групаАнгіотензин II рецепторів антагоніст.ФармакокінетикаВсмоктування. Після прийому валсартану внутрішньо Cmax у плазмі досягається протягом 2-4 годин. Середня абсолютна біодоступність становить 23%. При застосуванні валсартану з їжею AUC та Cmax у плазмі крові зменшуються на 40 та 50% відповідно. Тим не менш, через 8 годин після прийому препарату плазмові концентрації валсартану, прийнятого натще і з їжею, однакові. Зменшення AUC не супроводжується клінічно значущим зниженням терапевтичного ефекту валсартану, тому препарат Вальсакор можна приймати незалежно від часу їди. Розподіл. Vd валсартану в період рівноважного стану після внутрішньовенного введення становив близько 17 л, що вказує на відсутність вираженого розподілу валсартану в тканинах. Валсартан активно зв'язується з білками плазми (94-97%), переважно з альбуміном. Метаболізм. Валсартан не піддається суттєвій біотрансформації, лише близько 20% дози, прийнятої внутрішньо, виводиться у вигляді метаболітів. Гідроксильний метаболіт визначається в плазмі у низьких концентраціях (менше 10% від AUC валсартану). Цей метаболіт не має фармакологічної активності. Виведення. Валсартан виводиться двофазно: α-фаза з T1/2α менше 1 год і β-фаза з T1/2β — близько 9 год. Валсартан виводиться, в основному, у незміненому вигляді через кишечник (близько 83%) та нирками (близько 13%) . Після внутрішньовенного введення плазмовий кліренс валсартану становить близько 2 л/год, нирковий кліренс – 0,62 л/год (близько 30% від загального кліренсу). T1/2 валсартану становить 6 год. Фармакокінетика спеціальних груп пацієнтів Пацієнти з ХСН. У пацієнтів з ХСН час досягнення Cmax та T1/2 подібні до аналогічних показників у здорових добровольців. Підвищення AUC та Cmax прямо пропорційно збільшенню дози валсартану (з 40 до 160 мг 2 рази на добу). Чинник кумуляції становить, у середньому, 1,7. При внутрішньому прийомі кліренс валсартану становить близько 4,5 л/год. Вік пацієнтів із ХСН не впливав на кліренс валсартану. Пацієнти похилого віку (старше 65 років). У деяких пацієнтів старше 65 років біодоступність валсартану була вищою за таку у пацієнтів молодого віку, що не має клінічного значення. Пацієнти із порушеннями функції нирок. Нирковий кліренс валсартану становить лише 30% від загального кліренсу, тому кореляції між функцією нирок та системною біодоступністю валсартану немає. Корекція дози у пацієнтів з порушенням функції нирок (Cl креатиніну більше 10 мл/хв) не потрібна. Безпека валсартану у пацієнтів з Cl креатиніну менше 10 мл/хв та пацієнтів, які перебувають на гемодіалізі, не встановлена, тому у таких пацієнтів препарат слід застосовувати з обережністю. Оскільки ступінь зв'язування валсартану з білками плазми висока, його виведення при гемодіалізі малоймовірне. Пацієнти із порушеннями функції печінки. Близько 70% дози валсартану, що всмокталася, виводиться через кишечник, переважно в незміненому вигляді. Валсартан значною мірою не піддається метаболізму. У пацієнтів з легким або помірним порушенням функції печінки відзначалося підвищення AUC валсартану в 2 рази, порівняно з такою, у здорових добровольців. Однак не спостерігається кореляція значень AUC валсартану зі ступенем порушення функції печінки. Застосування валсартану у пацієнтів із тяжким порушенням функції печінки не вивчалось. Пацієнти віком від 6 до 18 років. Фармакокінетика валсартану у дітей та підлітків від 6 до 18 років не відрізняється від фармакокінетики валсартану у пацієнтів віком від 18 років.ФармакодинамікаВалсартан є селективним антагоністом рецепторів ангіотензину II (типу AT1) для внутрішнього прийому, небілкової природи. Вибірково блокує рецептори АТ1. Наслідком блокади АТ1-рецепторів є підвищення концентрації плазми ангіотензину II, який може стимулювати незаблоковані АТ2-рецептори, що врівноважує вазопресорні ефекти, пов'язані з порушенням АТ1-рецепторів. Валсартан не має агоністичної активності щодо АТ1-рецепторів. Його спорідненість до АТ1-рецепторів приблизно в 20000 разів вища, ніж до АТ2-рецепторів. Валсартан не інгібує АПФ, відомий також під назвою кінінази II, який перетворює ангіотензин I на ангіотензин II і руйнує брадикінін. У зв'язку з відсутністю впливу на АПФ не потенціюються ефекти брадикініну та субстанції Р. Частота розвитку сухого кашлю нижче у пацієнтів, які отримували антагоністи рецепторів ангіотензину II (АРА II), порівняно з пацієнтами, які отримували інгібітор АПФ. Валсартан не вступає у взаємодію та не блокує рецептори інших гормонів або іонні канали, що беруть участь у регуляції функцій ССС. Застосування при артеріальній гіпертензії у пацієнтів віком від 18 років. При лікуванні артеріальної гіпертензії (АГ) валсартан знижує артеріальний тиск, не впливаючи на ЧСС. Після прийому внутрішньо разової дози валсартану антигіпертензивний ефект розвивається протягом 2 годин, а максимальне зниження артеріального тиску досягається протягом 4-6 годин. Антигіпертензивний ефект валсартану зберігається протягом 24 годин після його застосування. При постійному застосуванні валсартану максимальне зниження артеріального тиску, незалежно від дози, досягається через 2-4 тижні і підтримується на досягнутому рівні під час тривалої терапії. Одночасне застосування з гідрохлортіазидом дозволяє досягти значного додаткового зниження артеріального тиску. Раптова відміна валсартану не супроводжується різким підвищенням артеріального тиску або іншими небажаними клінічними наслідками (тобто синдром відміни не розвивається). У пацієнтів з артеріальною гіпертензією, цукровим діабетом (ЦД) типу 2 та нефропатією, які приймають валсартан у дозі 160–320 мг на добу, відзначається значне зниження протеїнурії (36–44%). Застосування після гострого інфаркту міокарда (ІМ) у пацієнтів віком від 18 років. При застосуванні валсартану протягом 2 років, з початком прийому від 12 год до 10 днів після розвитку ІМ (ускладненого лівошлуночковою недостатністю та/або систолічною дисфункцією лівого шлуночка) знижуються показники загальної смертності, серцево-судинної смертності та подовжується час до першої госпіталізації. перебігу ХСН, повторного ІМ, раптової зупинки серця та інсульту (без летального результату). ХСН у пацієнтів віком від 18 років При застосуванні валсартану (в середній добовій дозі 254 мг) протягом 2 років у пацієнтів з ХСН II–IV функціонального класу за класифікацією NYHA з фракцією викиду лівого шлуночка (ФВЛШ) менше 40% та внутрішнім діастолічним діаметром ЛШ понад 2,9 см/м2 , що отримують стандартну терапію (інгібітори АПФ, діуретики, дигоксин, бета-адреноблокатори), було відзначено достовірне зниження ризику госпіталізації з приводу загострення перебігу ХСН, уповільнення прогресування ХСН, поліпшення функціонального класу ХСН за класифікацією NYHA, збільшення недостатність та поліпшення якості життя в порівнянні з плацебо. Застосування у пацієнтів старше 18 років з АГ та порушенням толерантності до глюкози При застосуванні валсартану та зміні способу життя відзначалося статистично достовірне зниження ризику розвитку ЦД у пацієнтів з артеріальною гіпертензією та порушенням толерантності до глюкози. Валсартан не впливав на частоту летальних випадків внаслідок серцево-судинних подій, ІМ та транзиторних ішемічних атак без летального результату, на частоту госпіталізацій через загострення перебігу ХСН або нестабільної стенокардії, артеріальної реваскуляризації у даної категорії пацієнтів, що відрізняються за віком, статтю та расовою. приладдя. У пацієнтів, які отримують валсартан, ризик розвитку мікроальбумінурії був достовірно нижчим, ніж у пацієнтів, які не одержують цієї терапії. Рекомендована початкова доза валсартану у пацієнтів з артеріальною гіпертензією та порушенням толерантності до глюкози становить 80 мг 1 раз на добу. За потреби доза може бути збільшена до 160 мг. Застосування у дітей та підлітків від 6 до 18 років при АГ У дітей та підлітків від 6 до 18 років валсартан забезпечує дозозалежне плавне зниження артеріального тиску. При застосуванні валсартану максимальне зниження АТ незалежно від прийнятої внутрішньо дози досягається протягом 2 тижнів і підтримується на досягнутому рівні в ході тривалої терапії.Показання до застосуванняПацієнти старше 18 років артеріальна гіпертензія. хронічна серцева недостатність (II–IV функціональний клас за класифікацією NYHA) у складі комплексної терапії (на фоні стандартної терапії) у пацієнтів, які не одержують інгібітори АПФ; підвищення виживання пацієнтів після перенесеного гострого ІМ, ускладненого лівошлуночковою недостатністю та/або систолічною дисфункцією лівого шлуночка (ЛШ), за наявності стабільних показників гемодинаміки. Пацієнти від 6 до 18 років артеріальна гіпертензія у дітей та підлітків від 6 до 18 років.Протипоказання до застосуванняпідвищена чутливість до валсартану або інших компонентів препарату; тяжкі порушення функції печінки (більше 9 балів за шкалою Чайлд-П'ю), біліарний цироз та холестаз; одночасне застосування з аліскіреном у пацієнтів з цукровим діабетом або помірними та тяжкими порушеннями функції нирок (Cl креатиніну менше 60 мл/хв); дефіцит лактази, непереносимість лактози, синдром глюкозо-галактозної мальабсорбції, оскільки до складу препарату Вальсакор входить лактоза; вагітність; період грудного вигодовування; вік до 6 років – за показанням артеріальна гіпертензія, до 18 років – за іншими показаннями. З обережністю: гіперкаліємія; одночасне застосування калійзберігаючих діуретиків; препаратів калію; калійвмісних харчових добавок або інших препаратів, здатних підвищувати вміст калію в плазмі (наприклад, гепарин); легкі та помірні порушення функції печінки небіліарного генезу без явищ холестазу; тяжкі порушення функції нирок (Cl креатиніну менше 10 мл/хв – немає клінічних даних); порушення функції нирок у пацієнтів від 6 до 18 років (Cl креатиніну менше 30 мл/хв), в т.ч. що знаходяться на гемодіалізі, гіпонатріємія, дотримання дієти з обмеженням споживання кухонної солі, стани, що супроводжуються зниженням ОЦК (в т.ч. діарея, блювання); двосторонній стеноз ниркових артерій чи стеноз артерії єдиної нирки; стан після трансплантації нирки; первинний гіперальдостеронізм,у пацієнтів із хронічною серцевою недостатністю III–IV функціонального класу (за NYNA); функція нирок яких залежить стану РААС; стеноз аортального та/або мітрального клапана; гіпертрофічна обструктивна кардіоміопатія (ГЗКМП), у пацієнтів зі спадковим ангіоневротичним набряком або ангіоневротичним набряком на фоні попередньої терапії АРА II або інгібіторами АПФ. Не рекомендується застосовувати АРА II, включаючи валсартан, одночасно з інгібіторами АПФ, оскільки їх одночасне застосування не має переваг перед монотерапією валсартаном або інгібітором АПФ щодо показників загальної смертності.Вагітність та лактаціяЗастосування АРА II у І триместрі вагітності не рекомендується. Застосування АРА II протипоказане у II–III триместрах вагітності, оскільки застосування у II–III триместрах вагітності може спричинити фетотоксичні ефекти (зниження функції нирок, маловоддя, уповільнення окостеніння кісток черепа плода) та неонатальні токсичні ефекти (ниркову недостатність, артеріальну гіпотензію, гіперкалієм). Якщо все ж таки застосовували препарат у II–III триместрах вагітності, то необхідно провести УЗД нирок та кісток черепа плода. При плануванні вагітності рекомендується перевести пацієнтку на альтернативну гіпотензивну терапію з урахуванням профілю безпеки. При підтвердженні вагітності препарат Вальсакор необхідно відмінити якомога раніше. Новонароджені, матері яких отримували АРА II під час вагітності, потребують медичного спостереження, т.к. Існує ризик розвитку артеріальної гіпотензії. Немає даних про виділення валсартану у грудне молоко. Тому слід вирішити питання про припинення годування груддю або скасування терапії валсартаном та переведення на альтернативну гіпотензивну терапію з урахуванням профілю безпеки.Побічна діяКласифікація частоти розвитку побічних ефектів Всесвітньої організації охорони здоров'я: дуже часто — ≥1/10; часто – від ≥1/100 до <1/10; нечасто – від ≥1/1000 до <1/100; рідко – від ≥1/10000 до <1/1000; дуже рідко - <1/10000; частота невідома - не може бути оцінена на основі наявних даних. Профіль безпеки валсартану у пацієнтів з АГ віком від 6 до 18 років не відрізняється від профілю безпеки валсартану у пацієнтів з АГ віком від 18 років. Артеріальна гіпертензія З боку крові та лімфатичної системи: частота невідома – зниження гемоглобіну, зниження гематокриту, нейтропенія, тромбоцитопенія. З боку імунної системи: частота невідома – реакції підвищеної чутливості, включаючи сироваткову хворобу. З боку обміну речовин та харчування: частота невідома – підвищення вмісту калію у сироватці крові, гіпонатріємія. З боку органу слуху та лабіринтні порушення: нечасто – вертиго. З боку судин: частота невідома – васкуліт. З боку дихальної системи, органів грудної клітки та середостіння: нечасто – кашель. З боку шлунково-кишкового тракту: нечасто – біль у животі. З боку печінки та жовчовивідних шляхів: частота невідома – порушення функції печінки, включаючи підвищення концентрації білірубіну у плазмі крові. З боку шкіри та підшкірних тканин: частота невідома — ангіоневротичний набряк, висипання на шкірі, свербіж шкіри, бульозний дерматит. З боку скелетно-м'язової та сполучної тканини: частота невідома – міалгія. З боку нирок та сечовивідних шляхів: частота невідома – порушення функції нирок та ниркова недостатність, підвищення концентрації креатиніну у сироватці крові. Загальні розлади та порушення у місці введення: нечасто – підвищена стомлюваність. У ході клінічних досліджень у пацієнтів з АГ спостерігалися такі небажані явища, причинно-наслідковий зв'язок яких з прийомом валсартану не встановлений: артралгія, астенія, біль у спині, діарея, запаморочення, безсоння, зниження лібідо, нудота, периферичні набряки, фарингіт, рин синусит, інфекції верхніх дихальних шляхів Після перенесеного гострого ІМ та/або при хронічній серцевій недостатності (II–IV функціональний клас за класифікацією NYHA) З боку крові та лімфатичної системи: частота невідома – тромбоцитопенія. З боку імунної системи: частота невідома – реакції підвищеної чутливості, включаючи сироваткову хворобу. З боку обміну речовин та харчування: нечасто – гіперкаліємія; частота невідома – підвищення вмісту калію в сироватці крові, гіпонатріємія. З боку нервової системи: часто – запаморочення, постуральне запаморочення; нечасто - непритомність, головний біль. З боку органу слуху та лабіринтні порушення: нечасто – вертиго. З боку серця: нечасто посилення симптомів ХСН. З боку судин: часто – виражене зниження артеріального тиску, ортостатична гіпотензія; частота невідома – васкуліт. З боку дихальної системи, органів грудної клітки та середостіння: нечасто – кашель. З боку шлунково-кишкового тракту: нечасто – нудота, діарея. З боку печінки та жовчовивідних шляхів: частота невідома – порушення функції печінки. З боку шкіри та підшкірних тканин: нечасто – ангіоневротичний набряк; частота невідома – шкірний висип, свербіж шкіри, бульозний дерматит. З боку скелетно-м'язової та сполучної тканини: рідко – рабдоміоліз; частота невідома – міалгія. З боку нирок та сечовивідних шляхів: часто – порушення функції нирок та ниркова недостатність; нечасто – гостра ниркова недостатність, підвищення концентрації креатиніну у сироватці крові; частота невідома – підвищення вмісту азоту сечовини у плазмі крові. Загальні розлади та порушення у місці введення: нечасто – астенія, підвищена стомлюваність.Взаємодія з лікарськими засобамиОдночасне застосування протипоказане Одночасне застосування АРА II, включаючи валсартан, або інгібіторів АПФ з аліскіреном, протипоказане у пацієнтів з ЦД або помірними та тяжкими порушеннями функції нирок (Cl креатиніну менше 60 мл/хв). Одночасне застосування не рекомендується Літій. Одночасне застосування препаратами літію не рекомендується, т.к. можливе оборотне збільшення концентрації літію в плазмі крові та посилення його токсичної дії. Ризик токсичних проявів, пов'язаних із застосуванням препаратів літію, може додатково збільшуватися при одночасному застосуванні з Вальсакором та діуретиками. При необхідності одночасного застосування з препаратами літію слід ретельно контролювати концентрацію літію у плазмі крові. Калійзберігаючі діуретики (спіронолактон, еплеренон, тріамтерен, амілорид), препарати калію, калійвмісні харчові добавки та інші лікарські засоби та речовини, які можуть спричинити гіперкаліємію (наприклад, гепарин). При необхідності одночасного застосування з препаратами, що впливають вміст калію, рекомендується контролювати вміст калію в плазмі крові. Одночасне застосування з обережністю Подвійна блокада РААС. У деяких пацієнтів подвійна блокада РААС супроводжувалася розвитком артеріальної гіпотензії, непритомності, гіперкаліємії та порушенням функції нирок (включаючи гостру ниркову недостатність (ОПН)). АПФ або аліскірен. НПЗЗ, в т.ч. селективні інгібітори ЦОГ-2, ацетилсаліцилова кислота в дозі більше 3 г на добу та неселективні НПЗЗ. При одночасному застосуванні з валсартаном можливе зменшення антигіпертензивного ефекту, збільшення ризику розвитку порушень функції нирок та підвищення вмісту калію у плазмі. До початку комбінованої терапії рекомендується оцінити функцію нирок, а також корекцію порушень водно-електролітного балансу. Білки-переносники. Дослідження in vitro на культурах печінки показали, що валсартан є субстратом для білків-переносників OATP1B1/OATP1B3 та MRP2. Одночасне застосування валсартану з інгібіторами білка-переносника OATP1B1/OATP1B3 (рифампіцин, циклоспорин) або MRP2 (ритонавір) може збільшити системну експозицію валсартану (Cmax та AUC). Необхідно бути обережними на початку одночасного застосування з вищевказаними препаратами або після їх відміни. Відсутність лікарської взаємодії Не виявлено клінічно значущих взаємодій з наступними ЛЗ: циметидин, варфарин, фуросемід, дигоксин, атенолол, індометацин, гідрохлортіазид, амлодипін та глібенкламід. Пацієнти віком від 6 до 18 років. У дітей та підлітків АГ часто пов'язана з порушенням функції нирок. Одночасне застосування валсартану з іншими ЛЗ, що впливають на РААС, може спричинити підвищення вмісту калію в плазмі у таких пацієнтів. Необхідно бути обережними при одночасному застосуванні вищезгаданої комбінації та регулярно контролювати функцію нирок та вміст калію в плазмі крові у даної групи пацієнтів.Спосіб застосування та дозиВсередину, незалежно від часу їди. Пацієнти старше 18 років Артеріальна гіпертензія. Рекомендована початкова доза препарату Вальсакор становить 80 мг 1 раз на добу, незалежно від расової приналежності, віку та статі пацієнта. Антигіпертензивний ефект розвивається протягом 2 тижнів і досягає свого максимуму через 4 тижні. Пацієнтам, у яких не вдалося досягти адекватного контролю АТ, добова доза валсартану може бути поступово збільшена до максимальної добової дози 320 мг. З метою додаткового зниження АТ можливе застосування діуретичних засобів (гідрохлортіазид), а також одночасне застосування інших гіпотензивних засобів. ХСН. Рекомендована початкова доза препарату Вальсакор становить 40 мг 2 рази на добу. Дозу препарату слід поступово збільшувати протягом щонайменше 2 тижнів до 80 мг 2 рази на добу, а при хорошій переносимості – до 160 мг 2 рази на добу. Максимальна добова доза становить 320 мг на два прийоми. При цьому може знадобитися зниження дози діуретиків, що одночасно приймаються. Можливе одночасне застосування з іншими лікарськими засобами, призначеними для лікування ХСН. Проте одночасна терапія препаратами трьох класів: валсартаном, інгібіторами АПФ та бета-адреноблокаторами не рекомендується. Оцінка стану пацієнтів із ХСН повинна включати контроль функції нирок. Застосування після перенесеного гострого ІМ. Лікування слід розпочинати вже через 12 годин після розвитку гострого ІМ за наявності стабільних показників гемодинаміки. Після застосування початкової дози 20 мг 2 рази на добу (1/2табл. 40 мг), дозу препарату Вальсакор можна поступово збільшити методом титрування до: 40, 80 та 160 мг 2 рази на добу протягом декількох тижнів. Максимальна добова доза становить 320 мг на 2 прийоми. Рекомендується збільшення дози до 80 мг 2 рази на добу до кінця 2-го тижня, а максимальна цільова доза 160 мг 2 рази на добу може бути досягнута до кінця 3-го місяця терапії препаратом Вальсакор®. Досягнення цільової дози залежить від переносимості валсартану під час титрування доз. При розвитку надмірного зниження артеріального тиску, що супроводжується клінічними проявами, або порушенням функції нирок, слід зменшити дозу препарату. Можливе одночасне застосування з іншими ЛЗ, у т.ч. тромболітичними засобами, ацетилсаліцилової кислотою як антиагрегантний засіб, бета-адреноблокаторами та інгібіторами ГМГ-КоА-редуктази (статинами). Одночасне застосування з інгібіторами АПФ не рекомендується. Оцінка стану пацієнтів після перенесеного гострого ІМ має включати контроль функції нирок. Пацієнти від 6 до 18 років АГ. Рекомендована початкова доза препарату Вальсакор® у дітей та підлітків від 6 до 18 років становить 40 мг при масі тіла дитини менше 35 кг та 80 мг при масі тіла дитини понад 35 кг. Рекомендується корекція дози з урахуванням зниження артеріального тиску. Максимальні рекомендовані добові дози відображені нижче. При масі тіла ≥8 та <35 кг максимальна рекомендована добова доза становить 80 мг; від 35 до <80 кг – 160 мг; від ≥80 до ≤160 кг – 320 мг. Застосування вищих доз не рекомендовано. ХСН та перенесений ІМ. Препарат Вальсакор® не рекомендований для лікування ХСН та перенесеного гострого ІМ у пацієнтів віком до 18 років. Пацієнти похилого віку. Корекція дози препарату у пацієнтів віком від 65 років не потрібна. Порушення функції нирок. Корекція дози у пацієнтів із Cl креатиніну більше 10 мл/хв не потрібна. Одночасне застосування препарату Вальсакор з аліскіреном у пацієнтів з помірними та тяжкими порушеннями функції нирок (Cl креатиніну менше 60 мл/хв) протипоказане. Порушення функції печінки. У пацієнтів з легким або помірним порушенням функції печінки небіліарного генезу без холестазу препарат слід застосовувати з обережністю, добова доза не повинна перевищувати 80 мг. Пацієнти із цукровим діабетом. Одночасне застосування препарату Вальсакор з аліскіреном у пацієнтів із ЦД протипоказане.ПередозуванняСимптоми: основним очікуваним проявом передозування валсартану є виражене зниження артеріального тиску, яке може призвести до порушення свідомості, колапсу та/або шоку. Лікування: симптоматичне, рекомендується викликати блювання та промити шлунок. При розвитку вираженого зниження артеріального тиску необхідно перевести пацієнта в положення лежачи на спині з піднятими вгору ногами, внутрішньовенно ввести 0,9% розчин натрію хлориду. Рекомендується регулярний контроль діяльності серця та дихальної системи, ОЦК та кількості сечі, що виділяється. Гемодіаліз неефективний.Запобіжні заходи та особливі вказівкиГіперкаліємія. При одночасному застосуванні калійзберігаючих діуретиків (спіронолактон, еплеренон, тріамтерен, амілорид), препаратів калію, калійвмісних замінників солі або інших препаратів, здатних підвищувати вміст калію в плазмі крові (наприклад, гепарин), слід бути обережним. Необхідно регулярно контролювати вміст калію у плазмі крові. Порушення функції нирок. У пацієнтів з порушенням функції нирок не потрібна зміна доз препарату. Т.к. відсутні дані про застосування препарату при тяжкій нирковій недостатності (Cl креатиніну менше 10 мл/хв або 0,167 мл/с) та у пацієнтів, які перебувають на гемодіалізі, у таких випадках препарат рекомендується застосовувати з обережністю. Одночасне застосування валсартану з аліскіреном у пацієнтів з помірними та тяжкими порушеннями функції нирок (Cl креатиніну менше 60 мл/хв) протипоказано. Порушення функції печінки. У пацієнтів з легкими та помірними порушеннями функції печінки без явищ холестазу препарат Вальсакор слід застосовувати з обережністю. Пацієнти з гіпонатріємією та/або дегідратацією. У пацієнтів з вираженою гіпонатріємією та/або дегідратацією, наприклад внаслідок прийому великих доз діуретиків, у поодиноких випадках на початку терапії препаратом Вальсакор може розвинутись артеріальна гіпотензія з клінічними проявами. Перед початком лікування рекомендовано відновити вміст натрію та/або ОЦК, зокрема шляхом зменшення доз діуретиків. Стеноз ниркової артерії. Застосування валсартану коротким курсом у пацієнтів з реноваскулярною гіпертензією, що розвинулася вдруге внаслідок стенозу артерії єдиної нирки, не спричиняє суттєвих змін показників ниркової гемодинаміки, концентрації креатиніну або азоту сечовини у сироватці крові. Однак, враховуючи, що інші ЛЗ, що впливають на РААС, можуть викликати підвищення концентрації сечовини та креатиніну у сироватці крові у пацієнтів із двостороннім стенозом ниркових артерій або стенозом артерії єдиної нирки, необхідно регулярно контролювати концентрації креатиніну та залишкового азоту сечовини у сироватці крові. Стан після перенесеної трансплантації нирки. Безпека застосування препарату Вальсакор у пацієнтів, які недавно перенесли трансплантацію нирки, не встановлена. Первинний гіперальдостеронізм. Пацієнти з первинним гіперальдостеронізмом є резистентними до гіпотензивних препаратів, що впливають на РААС, тому таким пацієнтам застосування препарату Вальсакор® не рекомендується. Стеноз аортального та/або мітрального клапанів, ГЗКМП. Препарат Вальсакор® необхідно з обережністю застосовувати у пацієнтів з гемодинамічно значущим стенозом аортального та/або мітрального клапанів або ГОКМП. Період після перенесеного ІМ. Одночасне застосування з АПФ інгібіторами не рекомендується, т.к. не має додаткових клінічних переваг перед монотерапією та збільшує ризик розвитку небажаних явищ. Застосування валсартану у пацієнтів після перенесеного ІМ часто призводить до невеликого зниження артеріального тиску, проте припинення терапії через артеріальну гіпотензію зазвичай не потрібне, якщо виконувати рекомендації щодо дозування препарату. Терапію препаратом Вальсакор слід починати обережно. Оцінка стану хворих після гострого інфаркту міокарда повинна включати контроль функції нирок. Можливе одночасне застосування при гострому ІМ з іншими ЛЗ: тромболітики, ацетилсаліцилова кислота, бета-адреноблокатори та інгібітори ГМГ-КоА-редуктази (статини). ХСН. У пацієнтів з ХСН не рекомендується одночасне застосування трьох класів препаратів: інгібіторів АПФ, бета-адреноблокаторів та валсартану, т.к. ця терапія не давала додаткового клінічного ефекту, у своїй збільшувався ризик розвитку небажаних явищ. Застосування у пацієнтів з ХСН зазвичай супроводжується зниженням артеріального тиску, проте при дотриманні рекомендацій щодо добору доз лікування рідко вимагає відміни через артеріальну гіпотензію. Терапію препаратом Вальсакор у пацієнтів з ХСН слід починати з обережністю. Внаслідок придушення активності РААС у деяких пацієнтів (наприклад, у пацієнтів з ХСН III–IV функціонального класу за класифікацією NYNA, функція нирок яких залежить від стану РААС) на тлі терапії інгібіторами АПФ можлива зміна функції нирок: розвиток олігурії та/або прогресуючої азотемії,а в поодиноких випадках - ГНН та/або летальний результат. Препарат Вальсакор® блокує рецептори ангіотензину ІІ, тому у пацієнтів з ХСН потрібний регулярний контроль функції нирок. Ангіоневротичний набряк в анамнезі. Серед пацієнтів з ангіоневротичним набряком на фоні терапії препаратом Вальсакор® спостерігалися випадки розвитку ангіоневротичного набряку в анамнезі, у т.ч. та на інгібітори АПФ. При розвитку ангіоневротичного набряку слід негайно відмінити препарат та виключити можливість повторного застосування. Спеціальна інформація щодо допоміжних речовин Препарат Вальсакор містить лактозу, тому не слід застосовувати при наступних станах: непереносимість лактози, дефіцит лактази, синдром глюкозо-галактозної мальабсорбції. Вплив на здатність виконання потенційно небезпечних видів діяльності, що вимагають особливої уваги та швидких реакцій (наприклад управління автотранспортом, робота з механізмами, що рухаються). У зв'язку з можливістю виникнення запаморочення або слабкості на фоні застосування препарату Вальсакор® необхідно бути обережним при керуванні транспортними засобами та зайнятті потенційно небезпечними видами діяльності.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Діюча речовина: валсартан 80 мг; допоміжні речовини: лактози моногідрат 30,00 мг, целюлоза мікрокристалічна 41,00 мг, повідон-К25 1,50 мг, кроскармелоза натрію 2,00 мг, кремнію діоксид колоїдний 1,00 мг, магнію стеарат 4,50 мг; Оболонка плівкова: гіпромелоза 6ср 3,00 мг, титану діоксид (Е171) 0,68 мг, барвник заліза оксид червоний (Е172) 0,02 мг, макрогол-4000 0,30 мг. По 7, 10, 14 або 15 таблеток у блістері (контурному осередковому впакуванні) з комбінованого матеріалу ПВХ/ПЕ/ПВДХ - алюмінієвої фольги. По 2, 4, 8, 12, 14 або 20 блістерів (контурних осередкових упаковок) (по 7 таблеток), або по 2, 3, 6 або 9 блістерів (контурних осередкових упаковок) (по 10 таблеток), або по 1,2 , 4, 6, 7 або 10 блістерів (контурних осередкових упаковок) (по 14 таблеток), або по 2, 4 або 6 блістерів (контурних осередкових упаковок) (по 15 таблеток) разом з інструкцією по застосуванню поміщають в картонну пачку.Опис лікарської формиКруглі, двоопуклі таблетки з ризиком на одній стороні, покриті плівковою оболонкою рожевого кольору. Вид на зламі: біла шорстка маса з плівковою оболонкою рожевого кольору.Фармакотерапевтична групаАнгіотензин II рецепторів антагоніст.ФармакокінетикаВсмоктування. Після прийому валсартану внутрішньо Cmax у плазмі досягається протягом 2-4 годин. Середня абсолютна біодоступність становить 23%. При застосуванні валсартану з їжею AUC та Cmax у плазмі крові зменшуються на 40 та 50% відповідно. Тим не менш, через 8 годин після прийому препарату плазмові концентрації валсартану, прийнятого натще і з їжею, однакові. Зменшення AUC не супроводжується клінічно значущим зниженням терапевтичного ефекту валсартану, тому препарат Вальсакор можна приймати незалежно від часу їди. Розподіл. Vd валсартану в період рівноважного стану після внутрішньовенного введення становив близько 17 л, що вказує на відсутність вираженого розподілу валсартану в тканинах. Валсартан активно зв'язується з білками плазми (94-97%), переважно з альбуміном. Метаболізм. Валсартан не піддається суттєвій біотрансформації, лише близько 20% дози, прийнятої внутрішньо, виводиться у вигляді метаболітів. Гідроксильний метаболіт визначається в плазмі у низьких концентраціях (менше 10% від AUC валсартану). Цей метаболіт не має фармакологічної активності. Виведення. Валсартан виводиться двофазно: α-фаза з T1/2α менше 1 год і β-фаза з T1/2β — близько 9 год. Валсартан виводиться, в основному, у незміненому вигляді через кишечник (близько 83%) та нирками (близько 13%) . Після внутрішньовенного введення плазмовий кліренс валсартану становить близько 2 л/год, нирковий кліренс – 0,62 л/год (близько 30% від загального кліренсу). T1/2 валсартану становить 6 год. Фармакокінетика спеціальних груп пацієнтів Пацієнти з ХСН. У пацієнтів з ХСН час досягнення Cmax та T1/2 подібні до аналогічних показників у здорових добровольців. Підвищення AUC та Cmax прямо пропорційно збільшенню дози валсартану (з 40 до 160 мг 2 рази на добу). Чинник кумуляції становить, у середньому, 1,7. При внутрішньому прийомі кліренс валсартану становить близько 4,5 л/год. Вік пацієнтів із ХСН не впливав на кліренс валсартану. Пацієнти похилого віку (старше 65 років). У деяких пацієнтів старше 65 років біодоступність валсартану була вищою за таку у пацієнтів молодого віку, що не має клінічного значення. Пацієнти із порушеннями функції нирок. Нирковий кліренс валсартану становить лише 30% від загального кліренсу, тому кореляції між функцією нирок та системною біодоступністю валсартану немає. Корекція дози у пацієнтів з порушенням функції нирок (Cl креатиніну більше 10 мл/хв) не потрібна. Безпека валсартану у пацієнтів з Cl креатиніну менше 10 мл/хв та пацієнтів, які перебувають на гемодіалізі, не встановлена, тому у таких пацієнтів препарат слід застосовувати з обережністю. Оскільки ступінь зв'язування валсартану з білками плазми висока, його виведення при гемодіалізі малоймовірне. Пацієнти із порушеннями функції печінки. Близько 70% дози валсартану, що всмокталася, виводиться через кишечник, переважно в незміненому вигляді. Валсартан значною мірою не піддається метаболізму. У пацієнтів з легким або помірним порушенням функції печінки відзначалося підвищення AUC валсартану в 2 рази, порівняно з такою, у здорових добровольців. Однак не спостерігається кореляція значень AUC валсартану зі ступенем порушення функції печінки. Застосування валсартану у пацієнтів із тяжким порушенням функції печінки не вивчалось. Пацієнти віком від 6 до 18 років. Фармакокінетика валсартану у дітей та підлітків від 6 до 18 років не відрізняється від фармакокінетики валсартану у пацієнтів віком від 18 років.ФармакодинамікаВалсартан є селективним антагоністом рецепторів ангіотензину II (типу AT1) для внутрішнього прийому, небілкової природи. Вибірково блокує рецептори АТ1. Наслідком блокади АТ1-рецепторів є підвищення концентрації плазми ангіотензину II, який може стимулювати незаблоковані АТ2-рецептори, що врівноважує вазопресорні ефекти, пов'язані з порушенням АТ1-рецепторів. Валсартан не має агоністичної активності щодо АТ1-рецепторів. Його спорідненість до АТ1-рецепторів приблизно в 20000 разів вища, ніж до АТ2-рецепторів. Валсартан не інгібує АПФ, відомий також під назвою кінінази II, який перетворює ангіотензин I на ангіотензин II і руйнує брадикінін. У зв'язку з відсутністю впливу на АПФ не потенціюються ефекти брадикініну та субстанції Р. Частота розвитку сухого кашлю нижче у пацієнтів, які отримували антагоністи рецепторів ангіотензину II (АРА II), порівняно з пацієнтами, які отримували інгібітор АПФ. Валсартан не вступає у взаємодію та не блокує рецептори інших гормонів або іонні канали, що беруть участь у регуляції функцій ССС. Застосування при артеріальній гіпертензії у пацієнтів віком від 18 років. При лікуванні артеріальної гіпертензії (АГ) валсартан знижує артеріальний тиск, не впливаючи на ЧСС. Після прийому внутрішньо разової дози валсартану антигіпертензивний ефект розвивається протягом 2 годин, а максимальне зниження артеріального тиску досягається протягом 4-6 годин. Антигіпертензивний ефект валсартану зберігається протягом 24 годин після його застосування. При постійному застосуванні валсартану максимальне зниження артеріального тиску, незалежно від дози, досягається через 2-4 тижні і підтримується на досягнутому рівні під час тривалої терапії. Одночасне застосування з гідрохлортіазидом дозволяє досягти значного додаткового зниження артеріального тиску. Раптова відміна валсартану не супроводжується різким підвищенням артеріального тиску або іншими небажаними клінічними наслідками (тобто синдром відміни не розвивається). У пацієнтів з артеріальною гіпертензією, цукровим діабетом (ЦД) типу 2 та нефропатією, які приймають валсартан у дозі 160–320 мг на добу, відзначається значне зниження протеїнурії (36–44%). Застосування після гострого інфаркту міокарда (ІМ) у пацієнтів віком від 18 років. При застосуванні валсартану протягом 2 років, з початком прийому від 12 год до 10 днів після розвитку ІМ (ускладненого лівошлуночковою недостатністю та/або систолічною дисфункцією лівого шлуночка) знижуються показники загальної смертності, серцево-судинної смертності та подовжується час до першої госпіталізації. перебігу ХСН, повторного ІМ, раптової зупинки серця та інсульту (без летального результату). ХСН у пацієнтів віком від 18 років При застосуванні валсартану (в середній добовій дозі 254 мг) протягом 2 років у пацієнтів з ХСН II–IV функціонального класу за класифікацією NYHA з фракцією викиду лівого шлуночка (ФВЛШ) менше 40% та внутрішнім діастолічним діаметром ЛШ понад 2,9 см/м2 , що отримують стандартну терапію (інгібітори АПФ, діуретики, дигоксин, бета-адреноблокатори), було відзначено достовірне зниження ризику госпіталізації з приводу загострення перебігу ХСН, уповільнення прогресування ХСН, поліпшення функціонального класу ХСН за класифікацією NYHA, збільшення недостатність та поліпшення якості життя в порівнянні з плацебо. Застосування у пацієнтів старше 18 років з АГ та порушенням толерантності до глюкози При застосуванні валсартану та зміні способу життя відзначалося статистично достовірне зниження ризику розвитку ЦД у пацієнтів з артеріальною гіпертензією та порушенням толерантності до глюкози. Валсартан не впливав на частоту летальних випадків внаслідок серцево-судинних подій, ІМ та транзиторних ішемічних атак без летального результату, на частоту госпіталізацій через загострення перебігу ХСН або нестабільної стенокардії, артеріальної реваскуляризації у даної категорії пацієнтів, що відрізняються за віком, статтю та расовою. приладдя. У пацієнтів, які отримують валсартан, ризик розвитку мікроальбумінурії був достовірно нижчим, ніж у пацієнтів, які не одержують цієї терапії. Рекомендована початкова доза валсартану у пацієнтів з артеріальною гіпертензією та порушенням толерантності до глюкози становить 80 мг 1 раз на добу. За потреби доза може бути збільшена до 160 мг. Застосування у дітей та підлітків від 6 до 18 років при АГ У дітей та підлітків від 6 до 18 років валсартан забезпечує дозозалежне плавне зниження артеріального тиску. При застосуванні валсартану максимальне зниження АТ незалежно від прийнятої внутрішньо дози досягається протягом 2 тижнів і підтримується на досягнутому рівні в ході тривалої терапії.Показання до застосуванняПацієнти старше 18 років артеріальна гіпертензія. хронічна серцева недостатність (II–IV функціональний клас за класифікацією NYHA) у складі комплексної терапії (на фоні стандартної терапії) у пацієнтів, які не одержують інгібітори АПФ; підвищення виживання пацієнтів після перенесеного гострого ІМ, ускладненого лівошлуночковою недостатністю та/або систолічною дисфункцією лівого шлуночка (ЛШ), за наявності стабільних показників гемодинаміки. Пацієнти від 6 до 18 років артеріальна гіпертензія у дітей та підлітків від 6 до 18 років.Протипоказання до застосуванняпідвищена чутливість до валсартану або інших компонентів препарату; тяжкі порушення функції печінки (більше 9 балів за шкалою Чайлд-П'ю), біліарний цироз та холестаз; одночасне застосування з аліскіреном у пацієнтів з цукровим діабетом або помірними та тяжкими порушеннями функції нирок (Cl креатиніну менше 60 мл/хв); дефіцит лактази, непереносимість лактози, синдром глюкозо-галактозної мальабсорбції, оскільки до складу препарату Вальсакор входить лактоза; вагітність; період грудного вигодовування; вік до 6 років – за показанням артеріальна гіпертензія, до 18 років – за іншими показаннями. З обережністю: гіперкаліємія; одночасне застосування калійзберігаючих діуретиків; препаратів калію; калійвмісних харчових добавок або інших препаратів, здатних підвищувати вміст калію в плазмі (наприклад, гепарин); легкі та помірні порушення функції печінки небіліарного генезу без явищ холестазу; тяжкі порушення функції нирок (Cl креатиніну менше 10 мл/хв – немає клінічних даних); порушення функції нирок у пацієнтів від 6 до 18 років (Cl креатиніну менше 30 мл/хв), в т.ч. що знаходяться на гемодіалізі, гіпонатріємія, дотримання дієти з обмеженням споживання кухонної солі, стани, що супроводжуються зниженням ОЦК (в т.ч. діарея, блювання); двосторонній стеноз ниркових артерій чи стеноз артерії єдиної нирки; стан після трансплантації нирки; первинний гіперальдостеронізм,у пацієнтів із хронічною серцевою недостатністю III–IV функціонального класу (за NYNA); функція нирок яких залежить стану РААС; стеноз аортального та/або мітрального клапана; гіпертрофічна обструктивна кардіоміопатія (ГЗКМП), у пацієнтів зі спадковим ангіоневротичним набряком або ангіоневротичним набряком на фоні попередньої терапії АРА II або інгібіторами АПФ. Не рекомендується застосовувати АРА II, включаючи валсартан, одночасно з інгібіторами АПФ, оскільки їх одночасне застосування не має переваг перед монотерапією валсартаном або інгібітором АПФ щодо показників загальної смертності.Вагітність та лактаціяЗастосування АРА II у І триместрі вагітності не рекомендується. Застосування АРА II протипоказане у II–III триместрах вагітності, оскільки застосування у II–III триместрах вагітності може спричинити фетотоксичні ефекти (зниження функції нирок, маловоддя, уповільнення окостеніння кісток черепа плода) та неонатальні токсичні ефекти (ниркову недостатність, артеріальну гіпотензію, гіперкалієм). Якщо все ж таки застосовували препарат у II–III триместрах вагітності, то необхідно провести УЗД нирок та кісток черепа плода. При плануванні вагітності рекомендується перевести пацієнтку на альтернативну гіпотензивну терапію з урахуванням профілю безпеки. При підтвердженні вагітності препарат Вальсакор необхідно відмінити якомога раніше. Новонароджені, матері яких отримували АРА II під час вагітності, потребують медичного спостереження, т.к. Існує ризик розвитку артеріальної гіпотензії. Немає даних про виділення валсартану у грудне молоко. Тому слід вирішити питання про припинення годування груддю або скасування терапії валсартаном та переведення на альтернативну гіпотензивну терапію з урахуванням профілю безпеки.Побічна діяКласифікація частоти розвитку побічних ефектів Всесвітньої організації охорони здоров'я: дуже часто — ≥1/10; часто – від ≥1/100 до <1/10; нечасто – від ≥1/1000 до <1/100; рідко – від ≥1/10000 до <1/1000; дуже рідко - <1/10000; частота невідома - не може бути оцінена на основі наявних даних. Профіль безпеки валсартану у пацієнтів з АГ віком від 6 до 18 років не відрізняється від профілю безпеки валсартану у пацієнтів з АГ віком від 18 років. Артеріальна гіпертензія З боку крові та лімфатичної системи: частота невідома – зниження гемоглобіну, зниження гематокриту, нейтропенія, тромбоцитопенія. З боку імунної системи: частота невідома – реакції підвищеної чутливості, включаючи сироваткову хворобу. З боку обміну речовин та харчування: частота невідома – підвищення вмісту калію у сироватці крові, гіпонатріємія. З боку органу слуху та лабіринтні порушення: нечасто – вертиго. З боку судин: частота невідома – васкуліт. З боку дихальної системи, органів грудної клітки та середостіння: нечасто – кашель. З боку шлунково-кишкового тракту: нечасто – біль у животі. З боку печінки та жовчовивідних шляхів: частота невідома – порушення функції печінки, включаючи підвищення концентрації білірубіну у плазмі крові. З боку шкіри та підшкірних тканин: частота невідома — ангіоневротичний набряк, висипання на шкірі, свербіж шкіри, бульозний дерматит. З боку скелетно-м'язової та сполучної тканини: частота невідома – міалгія. З боку нирок та сечовивідних шляхів: частота невідома – порушення функції нирок та ниркова недостатність, підвищення концентрації креатиніну у сироватці крові. Загальні розлади та порушення у місці введення: нечасто – підвищена стомлюваність. У ході клінічних досліджень у пацієнтів з АГ спостерігалися такі небажані явища, причинно-наслідковий зв'язок яких з прийомом валсартану не встановлений: артралгія, астенія, біль у спині, діарея, запаморочення, безсоння, зниження лібідо, нудота, периферичні набряки, фарингіт, рин синусит, інфекції верхніх дихальних шляхів Після перенесеного гострого ІМ та/або при хронічній серцевій недостатності (II–IV функціональний клас за класифікацією NYHA) З боку крові та лімфатичної системи: частота невідома – тромбоцитопенія. З боку імунної системи: частота невідома – реакції підвищеної чутливості, включаючи сироваткову хворобу. З боку обміну речовин та харчування: нечасто – гіперкаліємія; частота невідома – підвищення вмісту калію в сироватці крові, гіпонатріємія. З боку нервової системи: часто – запаморочення, постуральне запаморочення; нечасто - непритомність, головний біль. З боку органу слуху та лабіринтні порушення: нечасто – вертиго. З боку серця: нечасто посилення симптомів ХСН. З боку судин: часто – виражене зниження артеріального тиску, ортостатична гіпотензія; частота невідома – васкуліт. З боку дихальної системи, органів грудної клітки та середостіння: нечасто – кашель. З боку шлунково-кишкового тракту: нечасто – нудота, діарея. З боку печінки та жовчовивідних шляхів: частота невідома – порушення функції печінки. З боку шкіри та підшкірних тканин: нечасто – ангіоневротичний набряк; частота невідома – шкірний висип, свербіж шкіри, бульозний дерматит. З боку скелетно-м'язової та сполучної тканини: рідко – рабдоміоліз; частота невідома – міалгія. З боку нирок та сечовивідних шляхів: часто – порушення функції нирок та ниркова недостатність; нечасто – гостра ниркова недостатність, підвищення концентрації креатиніну у сироватці крові; частота невідома – підвищення вмісту азоту сечовини у плазмі крові. Загальні розлади та порушення у місці введення: нечасто – астенія, підвищена стомлюваність.Взаємодія з лікарськими засобамиОдночасне застосування протипоказане Одночасне застосування АРА II, включаючи валсартан, або інгібіторів АПФ з аліскіреном, протипоказане у пацієнтів з ЦД або помірними та тяжкими порушеннями функції нирок (Cl креатиніну менше 60 мл/хв). Одночасне застосування не рекомендується Літій. Одночасне застосування препаратами літію не рекомендується, т.к. можливе оборотне збільшення концентрації літію в плазмі крові та посилення його токсичної дії. Ризик токсичних проявів, пов'язаних із застосуванням препаратів літію, може додатково збільшуватися при одночасному застосуванні з Вальсакором та діуретиками. При необхідності одночасного застосування з препаратами літію слід ретельно контролювати концентрацію літію у плазмі крові. Калійзберігаючі діуретики (спіронолактон, еплеренон, тріамтерен, амілорид), препарати калію, калійвмісні харчові добавки та інші лікарські засоби та речовини, які можуть спричинити гіперкаліємію (наприклад, гепарин). При необхідності одночасного застосування з препаратами, що впливають вміст калію, рекомендується контролювати вміст калію в плазмі крові. Одночасне застосування з обережністю Подвійна блокада РААС. У деяких пацієнтів подвійна блокада РААС супроводжувалася розвитком артеріальної гіпотензії, непритомності, гіперкаліємії та порушенням функції нирок (включаючи гостру ниркову недостатність (ОПН)). АПФ або аліскірен. НПЗЗ, в т.ч. селективні інгібітори ЦОГ-2, ацетилсаліцилова кислота в дозі більше 3 г на добу та неселективні НПЗЗ. При одночасному застосуванні з валсартаном можливе зменшення антигіпертензивного ефекту, збільшення ризику розвитку порушень функції нирок та підвищення вмісту калію у плазмі. До початку комбінованої терапії рекомендується оцінити функцію нирок, а також корекцію порушень водно-електролітного балансу. Білки-переносники. Дослідження in vitro на культурах печінки показали, що валсартан є субстратом для білків-переносників OATP1B1/OATP1B3 та MRP2. Одночасне застосування валсартану з інгібіторами білка-переносника OATP1B1/OATP1B3 (рифампіцин, циклоспорин) або MRP2 (ритонавір) може збільшити системну експозицію валсартану (Cmax та AUC). Необхідно бути обережними на початку одночасного застосування з вищевказаними препаратами або після їх відміни. Відсутність лікарської взаємодії Не виявлено клінічно значущих взаємодій з наступними ЛЗ: циметидин, варфарин, фуросемід, дигоксин, атенолол, індометацин, гідрохлортіазид, амлодипін та глібенкламід. Пацієнти віком від 6 до 18 років. У дітей та підлітків АГ часто пов'язана з порушенням функції нирок. Одночасне застосування валсартану з іншими ЛЗ, що впливають на РААС, може спричинити підвищення вмісту калію в плазмі у таких пацієнтів. Необхідно бути обережними при одночасному застосуванні вищезгаданої комбінації та регулярно контролювати функцію нирок та вміст калію в плазмі крові у даної групи пацієнтів.Спосіб застосування та дозиВсередину, незалежно від часу їди. Пацієнти старше 18 років Артеріальна гіпертензія. Рекомендована початкова доза препарату Вальсакор становить 80 мг 1 раз на добу, незалежно від расової приналежності, віку та статі пацієнта. Антигіпертензивний ефект розвивається протягом 2 тижнів і досягає свого максимуму через 4 тижні. Пацієнтам, у яких не вдалося досягти адекватного контролю АТ, добова доза валсартану може бути поступово збільшена до максимальної добової дози 320 мг. З метою додаткового зниження АТ можливе застосування діуретичних засобів (гідрохлортіазид), а також одночасне застосування інших гіпотензивних засобів. ХСН. Рекомендована початкова доза препарату Вальсакор становить 40 мг 2 рази на добу. Дозу препарату слід поступово збільшувати протягом щонайменше 2 тижнів до 80 мг 2 рази на добу, а при хорошій переносимості – до 160 мг 2 рази на добу. Максимальна добова доза становить 320 мг на два прийоми. При цьому може знадобитися зниження дози діуретиків, що одночасно приймаються. Можливе одночасне застосування з іншими лікарськими засобами, призначеними для лікування ХСН. Проте одночасна терапія препаратами трьох класів: валсартаном, інгібіторами АПФ та бета-адреноблокаторами не рекомендується. Оцінка стану пацієнтів із ХСН повинна включати контроль функції нирок. Застосування після перенесеного гострого ІМ. Лікування слід розпочинати вже через 12 годин після розвитку гострого ІМ за наявності стабільних показників гемодинаміки. Після застосування початкової дози 20 мг 2 рази на добу (1/2табл. 40 мг), дозу препарату Вальсакор можна поступово збільшити методом титрування до: 40, 80 та 160 мг 2 рази на добу протягом декількох тижнів. Максимальна добова доза становить 320 мг на 2 прийоми. Рекомендується збільшення дози до 80 мг 2 рази на добу до кінця 2-го тижня, а максимальна цільова доза 160 мг 2 рази на добу може бути досягнута до кінця 3-го місяця терапії препаратом Вальсакор®. Досягнення цільової дози залежить від переносимості валсартану під час титрування доз. При розвитку надмірного зниження артеріального тиску, що супроводжується клінічними проявами, або порушенням функції нирок, слід зменшити дозу препарату. Можливе одночасне застосування з іншими ЛЗ, у т.ч. тромболітичними засобами, ацетилсаліцилової кислотою як антиагрегантний засіб, бета-адреноблокаторами та інгібіторами ГМГ-КоА-редуктази (статинами). Одночасне застосування з інгібіторами АПФ не рекомендується. Оцінка стану пацієнтів після перенесеного гострого ІМ має включати контроль функції нирок. Пацієнти від 6 до 18 років АГ. Рекомендована початкова доза препарату Вальсакор® у дітей та підлітків від 6 до 18 років становить 40 мг при масі тіла дитини менше 35 кг та 80 мг при масі тіла дитини понад 35 кг. Рекомендується корекція дози з урахуванням зниження артеріального тиску. Максимальні рекомендовані добові дози відображені нижче. При масі тіла ≥8 та <35 кг максимальна рекомендована добова доза становить 80 мг; від 35 до <80 кг – 160 мг; від ≥80 до ≤160 кг – 320 мг. Застосування вищих доз не рекомендовано. ХСН та перенесений ІМ. Препарат Вальсакор® не рекомендований для лікування ХСН та перенесеного гострого ІМ у пацієнтів віком до 18 років. Пацієнти похилого віку. Корекція дози препарату у пацієнтів віком від 65 років не потрібна. Порушення функції нирок. Корекція дози у пацієнтів із Cl креатиніну більше 10 мл/хв не потрібна. Одночасне застосування препарату Вальсакор з аліскіреном у пацієнтів з помірними та тяжкими порушеннями функції нирок (Cl креатиніну менше 60 мл/хв) протипоказане. Порушення функції печінки. У пацієнтів з легким або помірним порушенням функції печінки небіліарного генезу без холестазу препарат слід застосовувати з обережністю, добова доза не повинна перевищувати 80 мг. Пацієнти із цукровим діабетом. Одночасне застосування препарату Вальсакор з аліскіреном у пацієнтів із ЦД протипоказане.ПередозуванняСимптоми: основним очікуваним проявом передозування валсартану є виражене зниження артеріального тиску, яке може призвести до порушення свідомості, колапсу та/або шоку. Лікування: симптоматичне, рекомендується викликати блювання та промити шлунок. При розвитку вираженого зниження артеріального тиску необхідно перевести пацієнта в положення лежачи на спині з піднятими вгору ногами, внутрішньовенно ввести 0,9% розчин натрію хлориду. Рекомендується регулярний контроль діяльності серця та дихальної системи, ОЦК та кількості сечі, що виділяється. Гемодіаліз неефективний.Запобіжні заходи та особливі вказівкиГіперкаліємія. При одночасному застосуванні калійзберігаючих діуретиків (спіронолактон, еплеренон, тріамтерен, амілорид), препаратів калію, калійвмісних замінників солі або інших препаратів, здатних підвищувати вміст калію в плазмі крові (наприклад, гепарин), слід бути обережним. Необхідно регулярно контролювати вміст калію у плазмі крові. Порушення функції нирок. У пацієнтів з порушенням функції нирок не потрібна зміна доз препарату. Т.к. відсутні дані про застосування препарату при тяжкій нирковій недостатності (Cl креатиніну менше 10 мл/хв або 0,167 мл/с) та у пацієнтів, які перебувають на гемодіалізі, у таких випадках препарат рекомендується застосовувати з обережністю. Одночасне застосування валсартану з аліскіреном у пацієнтів з помірними та тяжкими порушеннями функції нирок (Cl креатиніну менше 60 мл/хв) протипоказано. Порушення функції печінки. У пацієнтів з легкими та помірними порушеннями функції печінки без явищ холестазу препарат Вальсакор слід застосовувати з обережністю. Пацієнти з гіпонатріємією та/або дегідратацією. У пацієнтів з вираженою гіпонатріємією та/або дегідратацією, наприклад внаслідок прийому великих доз діуретиків, у поодиноких випадках на початку терапії препаратом Вальсакор може розвинутись артеріальна гіпотензія з клінічними проявами. Перед початком лікування рекомендовано відновити вміст натрію та/або ОЦК, зокрема шляхом зменшення доз діуретиків. Стеноз ниркової артерії. Застосування валсартану коротким курсом у пацієнтів з реноваскулярною гіпертензією, що розвинулася вдруге внаслідок стенозу артерії єдиної нирки, не спричиняє суттєвих змін показників ниркової гемодинаміки, концентрації креатиніну або азоту сечовини у сироватці крові. Однак, враховуючи, що інші ЛЗ, що впливають на РААС, можуть викликати підвищення концентрації сечовини та креатиніну у сироватці крові у пацієнтів із двостороннім стенозом ниркових артерій або стенозом артерії єдиної нирки, необхідно регулярно контролювати концентрації креатиніну та залишкового азоту сечовини у сироватці крові. Стан після перенесеної трансплантації нирки. Безпека застосування препарату Вальсакор у пацієнтів, які недавно перенесли трансплантацію нирки, не встановлена. Первинний гіперальдостеронізм. Пацієнти з первинним гіперальдостеронізмом є резистентними до гіпотензивних препаратів, що впливають на РААС, тому таким пацієнтам застосування препарату Вальсакор® не рекомендується. Стеноз аортального та/або мітрального клапанів, ГЗКМП. Препарат Вальсакор® необхідно з обережністю застосовувати у пацієнтів з гемодинамічно значущим стенозом аортального та/або мітрального клапанів або ГОКМП. Період після перенесеного ІМ. Одночасне застосування з АПФ інгібіторами не рекомендується, т.к. не має додаткових клінічних переваг перед монотерапією та збільшує ризик розвитку небажаних явищ. Застосування валсартану у пацієнтів після перенесеного ІМ часто призводить до невеликого зниження артеріального тиску, проте припинення терапії через артеріальну гіпотензію зазвичай не потрібне, якщо виконувати рекомендації щодо дозування препарату. Терапію препаратом Вальсакор слід починати обережно. Оцінка стану хворих після гострого інфаркту міокарда повинна включати контроль функції нирок. Можливе одночасне застосування при гострому ІМ з іншими ЛЗ: тромболітики, ацетилсаліцилова кислота, бета-адреноблокатори та інгібітори ГМГ-КоА-редуктази (статини). ХСН. У пацієнтів з ХСН не рекомендується одночасне застосування трьох класів препаратів: інгібіторів АПФ, бета-адреноблокаторів та валсартану, т.к. ця терапія не давала додаткового клінічного ефекту, у своїй збільшувався ризик розвитку небажаних явищ. Застосування у пацієнтів з ХСН зазвичай супроводжується зниженням артеріального тиску, проте при дотриманні рекомендацій щодо добору доз лікування рідко вимагає відміни через артеріальну гіпотензію. Терапію препаратом Вальсакор у пацієнтів з ХСН слід починати з обережністю. Внаслідок придушення активності РААС у деяких пацієнтів (наприклад, у пацієнтів з ХСН III–IV функціонального класу за класифікацією NYNA, функція нирок яких залежить від стану РААС) на тлі терапії інгібіторами АПФ можлива зміна функції нирок: розвиток олігурії та/або прогресуючої азотемії,а в поодиноких випадках - ГНН та/або летальний результат. Препарат Вальсакор® блокує рецептори ангіотензину ІІ, тому у пацієнтів з ХСН потрібний регулярний контроль функції нирок. Ангіоневротичний набряк в анамнезі. Серед пацієнтів з ангіоневротичним набряком на фоні терапії препаратом Вальсакор® спостерігалися випадки розвитку ангіоневротичного набряку в анамнезі, у т.ч. та на інгібітори АПФ. При розвитку ангіоневротичного набряку слід негайно відмінити препарат та виключити можливість повторного застосування. Спеціальна інформація щодо допоміжних речовин Препарат Вальсакор містить лактозу, тому не слід застосовувати при наступних станах: непереносимість лактози, дефіцит лактази, синдром глюкозо-галактозної мальабсорбції. Вплив на здатність виконання потенційно небезпечних видів діяльності, що вимагають особливої уваги та швидких реакцій (наприклад управління автотранспортом, робота з механізмами, що рухаються). У зв'язку з можливістю виникнення запаморочення або слабкості на фоні застосування препарату Вальсакор® необхідно бути обережним при керуванні транспортними засобами та зайнятті потенційно небезпечними видами діяльності.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Діюча речовина: валсартан 80 мг; допоміжні речовини: лактози моногідрат 30,00 мг, целюлоза мікрокристалічна 41,00 мг, повідон-К25 1,50 мг, кроскармелоза натрію 2,00 мг, кремнію діоксид колоїдний 1,00 мг, магнію стеарат 4,50 мг; Оболонка плівкова: гіпромелоза 6ср 3,00 мг, титану діоксид (Е171) 0,68 мг, барвник заліза оксид червоний (Е172) 0,02 мг, макрогол-4000 0,30 мг. По 7, 10, 14 або 15 таблеток у блістері (контурному осередковому впакуванні) з комбінованого матеріалу ПВХ/ПЕ/ПВДХ - алюмінієвої фольги. По 2, 4, 8, 12, 14 або 20 блістерів (контурних осередкових упаковок) (по 7 таблеток), або по 2, 3, 6 або 9 блістерів (контурних осередкових упаковок) (по 10 таблеток), або по 1,2 , 4, 6, 7 або 10 блістерів (контурних осередкових упаковок) (по 14 таблеток), або по 2, 4 або 6 блістерів (контурних осередкових упаковок) (по 15 таблеток) разом з інструкцією по застосуванню поміщають в картонну пачку.Опис лікарської формиКруглі, двоопуклі таблетки з ризиком на одній стороні, покриті плівковою оболонкою рожевого кольору. Вид на зламі: біла шорстка маса з плівковою оболонкою рожевого кольору.Фармакотерапевтична групаАнгіотензин II рецепторів антагоніст.ФармакокінетикаВсмоктування. Після прийому валсартану внутрішньо Cmax у плазмі досягається протягом 2-4 годин. Середня абсолютна біодоступність становить 23%. При застосуванні валсартану з їжею AUC та Cmax у плазмі крові зменшуються на 40 та 50% відповідно. Тим не менш, через 8 годин після прийому препарату плазмові концентрації валсартану, прийнятого натще і з їжею, однакові. Зменшення AUC не супроводжується клінічно значущим зниженням терапевтичного ефекту валсартану, тому препарат Вальсакор можна приймати незалежно від часу їди. Розподіл. Vd валсартану в період рівноважного стану після внутрішньовенного введення становив близько 17 л, що вказує на відсутність вираженого розподілу валсартану в тканинах. Валсартан активно зв'язується з білками плазми (94-97%), переважно з альбуміном. Метаболізм. Валсартан не піддається суттєвій біотрансформації, лише близько 20% дози, прийнятої внутрішньо, виводиться у вигляді метаболітів. Гідроксильний метаболіт визначається в плазмі у низьких концентраціях (менше 10% від AUC валсартану). Цей метаболіт не має фармакологічної активності. Виведення. Валсартан виводиться двофазно: α-фаза з T1/2α менше 1 год і β-фаза з T1/2β — близько 9 год. Валсартан виводиться, в основному, у незміненому вигляді через кишечник (близько 83%) та нирками (близько 13%) . Після внутрішньовенного введення плазмовий кліренс валсартану становить близько 2 л/год, нирковий кліренс – 0,62 л/год (близько 30% від загального кліренсу). T1/2 валсартану становить 6 год. Фармакокінетика спеціальних груп пацієнтів Пацієнти з ХСН. У пацієнтів з ХСН час досягнення Cmax та T1/2 подібні до аналогічних показників у здорових добровольців. Підвищення AUC та Cmax прямо пропорційно збільшенню дози валсартану (з 40 до 160 мг 2 рази на добу). Чинник кумуляції становить, у середньому, 1,7. При внутрішньому прийомі кліренс валсартану становить близько 4,5 л/год. Вік пацієнтів із ХСН не впливав на кліренс валсартану. Пацієнти похилого віку (старше 65 років). У деяких пацієнтів старше 65 років біодоступність валсартану була вищою за таку у пацієнтів молодого віку, що не має клінічного значення. Пацієнти із порушеннями функції нирок. Нирковий кліренс валсартану становить лише 30% від загального кліренсу, тому кореляції між функцією нирок та системною біодоступністю валсартану немає. Корекція дози у пацієнтів з порушенням функції нирок (Cl креатиніну більше 10 мл/хв) не потрібна. Безпека валсартану у пацієнтів з Cl креатиніну менше 10 мл/хв та пацієнтів, які перебувають на гемодіалізі, не встановлена, тому у таких пацієнтів препарат слід застосовувати з обережністю. Оскільки ступінь зв'язування валсартану з білками плазми висока, його виведення при гемодіалізі малоймовірне. Пацієнти із порушеннями функції печінки. Близько 70% дози валсартану, що всмокталася, виводиться через кишечник, переважно в незміненому вигляді. Валсартан значною мірою не піддається метаболізму. У пацієнтів з легким або помірним порушенням функції печінки відзначалося підвищення AUC валсартану в 2 рази, порівняно з такою, у здорових добровольців. Однак не спостерігається кореляція значень AUC валсартану зі ступенем порушення функції печінки. Застосування валсартану у пацієнтів із тяжким порушенням функції печінки не вивчалось. Пацієнти віком від 6 до 18 років. Фармакокінетика валсартану у дітей та підлітків від 6 до 18 років не відрізняється від фармакокінетики валсартану у пацієнтів віком від 18 років.ФармакодинамікаВалсартан є селективним антагоністом рецепторів ангіотензину II (типу AT1) для внутрішнього прийому, небілкової природи. Вибірково блокує рецептори АТ1. Наслідком блокади АТ1-рецепторів є підвищення концентрації плазми ангіотензину II, який може стимулювати незаблоковані АТ2-рецептори, що врівноважує вазопресорні ефекти, пов'язані з порушенням АТ1-рецепторів. Валсартан не має агоністичної активності щодо АТ1-рецепторів. Його спорідненість до АТ1-рецепторів приблизно в 20000 разів вища, ніж до АТ2-рецепторів. Валсартан не інгібує АПФ, відомий також під назвою кінінази II, який перетворює ангіотензин I на ангіотензин II і руйнує брадикінін. У зв'язку з відсутністю впливу на АПФ не потенціюються ефекти брадикініну та субстанції Р. Частота розвитку сухого кашлю нижче у пацієнтів, які отримували антагоністи рецепторів ангіотензину II (АРА II), порівняно з пацієнтами, які отримували інгібітор АПФ. Валсартан не вступає у взаємодію та не блокує рецептори інших гормонів або іонні канали, що беруть участь у регуляції функцій ССС. Застосування при артеріальній гіпертензії у пацієнтів віком від 18 років. При лікуванні артеріальної гіпертензії (АГ) валсартан знижує артеріальний тиск, не впливаючи на ЧСС. Після прийому внутрішньо разової дози валсартану антигіпертензивний ефект розвивається протягом 2 годин, а максимальне зниження артеріального тиску досягається протягом 4-6 годин. Антигіпертензивний ефект валсартану зберігається протягом 24 годин після його застосування. При постійному застосуванні валсартану максимальне зниження артеріального тиску, незалежно від дози, досягається через 2-4 тижні і підтримується на досягнутому рівні під час тривалої терапії. Одночасне застосування з гідрохлортіазидом дозволяє досягти значного додаткового зниження артеріального тиску. Раптова відміна валсартану не супроводжується різким підвищенням артеріального тиску або іншими небажаними клінічними наслідками (тобто синдром відміни не розвивається). У пацієнтів з артеріальною гіпертензією, цукровим діабетом (ЦД) типу 2 та нефропатією, які приймають валсартан у дозі 160–320 мг на добу, відзначається значне зниження протеїнурії (36–44%). Застосування після гострого інфаркту міокарда (ІМ) у пацієнтів віком від 18 років. При застосуванні валсартану протягом 2 років, з початком прийому від 12 год до 10 днів після розвитку ІМ (ускладненого лівошлуночковою недостатністю та/або систолічною дисфункцією лівого шлуночка) знижуються показники загальної смертності, серцево-судинної смертності та подовжується час до першої госпіталізації. перебігу ХСН, повторного ІМ, раптової зупинки серця та інсульту (без летального результату). ХСН у пацієнтів віком від 18 років При застосуванні валсартану (в середній добовій дозі 254 мг) протягом 2 років у пацієнтів з ХСН II–IV функціонального класу за класифікацією NYHA з фракцією викиду лівого шлуночка (ФВЛШ) менше 40% та внутрішнім діастолічним діаметром ЛШ понад 2,9 см/м2 , що отримують стандартну терапію (інгібітори АПФ, діуретики, дигоксин, бета-адреноблокатори), було відзначено достовірне зниження ризику госпіталізації з приводу загострення перебігу ХСН, уповільнення прогресування ХСН, поліпшення функціонального класу ХСН за класифікацією NYHA, збільшення недостатність та поліпшення якості життя в порівнянні з плацебо. Застосування у пацієнтів старше 18 років з АГ та порушенням толерантності до глюкози При застосуванні валсартану та зміні способу життя відзначалося статистично достовірне зниження ризику розвитку ЦД у пацієнтів з артеріальною гіпертензією та порушенням толерантності до глюкози. Валсартан не впливав на частоту летальних випадків внаслідок серцево-судинних подій, ІМ та транзиторних ішемічних атак без летального результату, на частоту госпіталізацій через загострення перебігу ХСН або нестабільної стенокардії, артеріальної реваскуляризації у даної категорії пацієнтів, що відрізняються за віком, статтю та расовою. приладдя. У пацієнтів, які отримують валсартан, ризик розвитку мікроальбумінурії був достовірно нижчим, ніж у пацієнтів, які не одержують цієї терапії. Рекомендована початкова доза валсартану у пацієнтів з артеріальною гіпертензією та порушенням толерантності до глюкози становить 80 мг 1 раз на добу. За потреби доза може бути збільшена до 160 мг. Застосування у дітей та підлітків від 6 до 18 років при АГ У дітей та підлітків від 6 до 18 років валсартан забезпечує дозозалежне плавне зниження артеріального тиску. При застосуванні валсартану максимальне зниження АТ незалежно від прийнятої внутрішньо дози досягається протягом 2 тижнів і підтримується на досягнутому рівні в ході тривалої терапії.Показання до застосуванняПацієнти старше 18 років артеріальна гіпертензія. хронічна серцева недостатність (II–IV функціональний клас за класифікацією NYHA) у складі комплексної терапії (на фоні стандартної терапії) у пацієнтів, які не одержують інгібітори АПФ; підвищення виживання пацієнтів після перенесеного гострого ІМ, ускладненого лівошлуночковою недостатністю та/або систолічною дисфункцією лівого шлуночка (ЛШ), за наявності стабільних показників гемодинаміки. Пацієнти від 6 до 18 років артеріальна гіпертензія у дітей та підлітків від 6 до 18 років.Протипоказання до застосуванняпідвищена чутливість до валсартану або інших компонентів препарату; тяжкі порушення функції печінки (більше 9 балів за шкалою Чайлд-П'ю), біліарний цироз та холестаз; одночасне застосування з аліскіреном у пацієнтів з цукровим діабетом або помірними та тяжкими порушеннями функції нирок (Cl креатиніну менше 60 мл/хв); дефіцит лактази, непереносимість лактози, синдром глюкозо-галактозної мальабсорбції, оскільки до складу препарату Вальсакор входить лактоза; вагітність; період грудного вигодовування; вік до 6 років – за показанням артеріальна гіпертензія, до 18 років – за іншими показаннями. З обережністю: гіперкаліємія; одночасне застосування калійзберігаючих діуретиків; препаратів калію; калійвмісних харчових добавок або інших препаратів, здатних підвищувати вміст калію в плазмі (наприклад, гепарин); легкі та помірні порушення функції печінки небіліарного генезу без явищ холестазу; тяжкі порушення функції нирок (Cl креатиніну менше 10 мл/хв – немає клінічних даних); порушення функції нирок у пацієнтів від 6 до 18 років (Cl креатиніну менше 30 мл/хв), в т.ч. що знаходяться на гемодіалізі, гіпонатріємія, дотримання дієти з обмеженням споживання кухонної солі, стани, що супроводжуються зниженням ОЦК (в т.ч. діарея, блювання); двосторонній стеноз ниркових артерій чи стеноз артерії єдиної нирки; стан після трансплантації нирки; первинний гіперальдостеронізм,у пацієнтів із хронічною серцевою недостатністю III–IV функціонального класу (за NYNA); функція нирок яких залежить стану РААС; стеноз аортального та/або мітрального клапана; гіпертрофічна обструктивна кардіоміопатія (ГЗКМП), у пацієнтів зі спадковим ангіоневротичним набряком або ангіоневротичним набряком на фоні попередньої терапії АРА II або інгібіторами АПФ. Не рекомендується застосовувати АРА II, включаючи валсартан, одночасно з інгібіторами АПФ, оскільки їх одночасне застосування не має переваг перед монотерапією валсартаном або інгібітором АПФ щодо показників загальної смертності.Вагітність та лактаціяЗастосування АРА II у І триместрі вагітності не рекомендується. Застосування АРА II протипоказане у II–III триместрах вагітності, оскільки застосування у II–III триместрах вагітності може спричинити фетотоксичні ефекти (зниження функції нирок, маловоддя, уповільнення окостеніння кісток черепа плода) та неонатальні токсичні ефекти (ниркову недостатність, артеріальну гіпотензію, гіперкалієм). Якщо все ж таки застосовували препарат у II–III триместрах вагітності, то необхідно провести УЗД нирок та кісток черепа плода. При плануванні вагітності рекомендується перевести пацієнтку на альтернативну гіпотензивну терапію з урахуванням профілю безпеки. При підтвердженні вагітності препарат Вальсакор необхідно відмінити якомога раніше. Новонароджені, матері яких отримували АРА II під час вагітності, потребують медичного спостереження, т.к. Існує ризик розвитку артеріальної гіпотензії. Немає даних про виділення валсартану у грудне молоко. Тому слід вирішити питання про припинення годування груддю або скасування терапії валсартаном та переведення на альтернативну гіпотензивну терапію з урахуванням профілю безпеки.Побічна діяКласифікація частоти розвитку побічних ефектів Всесвітньої організації охорони здоров'я: дуже часто — ≥1/10; часто – від ≥1/100 до <1/10; нечасто – від ≥1/1000 до <1/100; рідко – від ≥1/10000 до <1/1000; дуже рідко - <1/10000; частота невідома - не може бути оцінена на основі наявних даних. Профіль безпеки валсартану у пацієнтів з АГ віком від 6 до 18 років не відрізняється від профілю безпеки валсартану у пацієнтів з АГ віком від 18 років. Артеріальна гіпертензія З боку крові та лімфатичної системи: частота невідома – зниження гемоглобіну, зниження гематокриту, нейтропенія, тромбоцитопенія. З боку імунної системи: частота невідома – реакції підвищеної чутливості, включаючи сироваткову хворобу. З боку обміну речовин та харчування: частота невідома – підвищення вмісту калію у сироватці крові, гіпонатріємія. З боку органу слуху та лабіринтні порушення: нечасто – вертиго. З боку судин: частота невідома – васкуліт. З боку дихальної системи, органів грудної клітки та середостіння: нечасто – кашель. З боку шлунково-кишкового тракту: нечасто – біль у животі. З боку печінки та жовчовивідних шляхів: частота невідома – порушення функції печінки, включаючи підвищення концентрації білірубіну у плазмі крові. З боку шкіри та підшкірних тканин: частота невідома — ангіоневротичний набряк, висипання на шкірі, свербіж шкіри, бульозний дерматит. З боку скелетно-м'язової та сполучної тканини: частота невідома – міалгія. З боку нирок та сечовивідних шляхів: частота невідома – порушення функції нирок та ниркова недостатність, підвищення концентрації креатиніну у сироватці крові. Загальні розлади та порушення у місці введення: нечасто – підвищена стомлюваність. У ході клінічних досліджень у пацієнтів з АГ спостерігалися такі небажані явища, причинно-наслідковий зв'язок яких з прийомом валсартану не встановлений: артралгія, астенія, біль у спині, діарея, запаморочення, безсоння, зниження лібідо, нудота, периферичні набряки, фарингіт, рин синусит, інфекції верхніх дихальних шляхів Після перенесеного гострого ІМ та/або при хронічній серцевій недостатності (II–IV функціональний клас за класифікацією NYHA) З боку крові та лімфатичної системи: частота невідома – тромбоцитопенія. З боку імунної системи: частота невідома – реакції підвищеної чутливості, включаючи сироваткову хворобу. З боку обміну речовин та харчування: нечасто – гіперкаліємія; частота невідома – підвищення вмісту калію в сироватці крові, гіпонатріємія. З боку нервової системи: часто – запаморочення, постуральне запаморочення; нечасто - непритомність, головний біль. З боку органу слуху та лабіринтні порушення: нечасто – вертиго. З боку серця: нечасто посилення симптомів ХСН. З боку судин: часто – виражене зниження артеріального тиску, ортостатична гіпотензія; частота невідома – васкуліт. З боку дихальної системи, органів грудної клітки та середостіння: нечасто – кашель. З боку шлунково-кишкового тракту: нечасто – нудота, діарея. З боку печінки та жовчовивідних шляхів: частота невідома – порушення функції печінки. З боку шкіри та підшкірних тканин: нечасто – ангіоневротичний набряк; частота невідома – шкірний висип, свербіж шкіри, бульозний дерматит. З боку скелетно-м'язової та сполучної тканини: рідко – рабдоміоліз; частота невідома – міалгія. З боку нирок та сечовивідних шляхів: часто – порушення функції нирок та ниркова недостатність; нечасто – гостра ниркова недостатність, підвищення концентрації креатиніну у сироватці крові; частота невідома – підвищення вмісту азоту сечовини у плазмі крові. Загальні розлади та порушення у місці введення: нечасто – астенія, підвищена стомлюваність.Взаємодія з лікарськими засобамиОдночасне застосування протипоказане Одночасне застосування АРА II, включаючи валсартан, або інгібіторів АПФ з аліскіреном, протипоказане у пацієнтів з ЦД або помірними та тяжкими порушеннями функції нирок (Cl креатиніну менше 60 мл/хв). Одночасне застосування не рекомендується Літій. Одночасне застосування препаратами літію не рекомендується, т.к. можливе оборотне збільшення концентрації літію в плазмі крові та посилення його токсичної дії. Ризик токсичних проявів, пов'язаних із застосуванням препаратів літію, може додатково збільшуватися при одночасному застосуванні з Вальсакором та діуретиками. При необхідності одночасного застосування з препаратами літію слід ретельно контролювати концентрацію літію у плазмі крові. Калійзберігаючі діуретики (спіронолактон, еплеренон, тріамтерен, амілорид), препарати калію, калійвмісні харчові добавки та інші лікарські засоби та речовини, які можуть спричинити гіперкаліємію (наприклад, гепарин). При необхідності одночасного застосування з препаратами, що впливають вміст калію, рекомендується контролювати вміст калію в плазмі крові. Одночасне застосування з обережністю Подвійна блокада РААС. У деяких пацієнтів подвійна блокада РААС супроводжувалася розвитком артеріальної гіпотензії, непритомності, гіперкаліємії та порушенням функції нирок (включаючи гостру ниркову недостатність (ОПН)). АПФ або аліскірен. НПЗЗ, в т.ч. селективні інгібітори ЦОГ-2, ацетилсаліцилова кислота в дозі більше 3 г на добу та неселективні НПЗЗ. При одночасному застосуванні з валсартаном можливе зменшення антигіпертензивного ефекту, збільшення ризику розвитку порушень функції нирок та підвищення вмісту калію у плазмі. До початку комбінованої терапії рекомендується оцінити функцію нирок, а також корекцію порушень водно-електролітного балансу. Білки-переносники. Дослідження in vitro на культурах печінки показали, що валсартан є субстратом для білків-переносників OATP1B1/OATP1B3 та MRP2. Одночасне застосування валсартану з інгібіторами білка-переносника OATP1B1/OATP1B3 (рифампіцин, циклоспорин) або MRP2 (ритонавір) може збільшити системну експозицію валсартану (Cmax та AUC). Необхідно бути обережними на початку одночасного застосування з вищевказаними препаратами або після їх відміни. Відсутність лікарської взаємодії Не виявлено клінічно значущих взаємодій з наступними ЛЗ: циметидин, варфарин, фуросемід, дигоксин, атенолол, індометацин, гідрохлортіазид, амлодипін та глібенкламід. Пацієнти віком від 6 до 18 років. У дітей та підлітків АГ часто пов'язана з порушенням функції нирок. Одночасне застосування валсартану з іншими ЛЗ, що впливають на РААС, може спричинити підвищення вмісту калію в плазмі у таких пацієнтів. Необхідно бути обережними при одночасному застосуванні вищезгаданої комбінації та регулярно контролювати функцію нирок та вміст калію в плазмі крові у даної групи пацієнтів.Спосіб застосування та дозиВсередину, незалежно від часу їди. Пацієнти старше 18 років Артеріальна гіпертензія. Рекомендована початкова доза препарату Вальсакор становить 80 мг 1 раз на добу, незалежно від расової приналежності, віку та статі пацієнта. Антигіпертензивний ефект розвивається протягом 2 тижнів і досягає свого максимуму через 4 тижні. Пацієнтам, у яких не вдалося досягти адекватного контролю АТ, добова доза валсартану може бути поступово збільшена до максимальної добової дози 320 мг. З метою додаткового зниження АТ можливе застосування діуретичних засобів (гідрохлортіазид), а також одночасне застосування інших гіпотензивних засобів. ХСН. Рекомендована початкова доза препарату Вальсакор становить 40 мг 2 рази на добу. Дозу препарату слід поступово збільшувати протягом щонайменше 2 тижнів до 80 мг 2 рази на добу, а при хорошій переносимості – до 160 мг 2 рази на добу. Максимальна добова доза становить 320 мг на два прийоми. При цьому може знадобитися зниження дози діуретиків, що одночасно приймаються. Можливе одночасне застосування з іншими лікарськими засобами, призначеними для лікування ХСН. Проте одночасна терапія препаратами трьох класів: валсартаном, інгібіторами АПФ та бета-адреноблокаторами не рекомендується. Оцінка стану пацієнтів із ХСН повинна включати контроль функції нирок. Застосування після перенесеного гострого ІМ. Лікування слід розпочинати вже через 12 годин після розвитку гострого ІМ за наявності стабільних показників гемодинаміки. Після застосування початкової дози 20 мг 2 рази на добу (1/2табл. 40 мг), дозу препарату Вальсакор можна поступово збільшити методом титрування до: 40, 80 та 160 мг 2 рази на добу протягом декількох тижнів. Максимальна добова доза становить 320 мг на 2 прийоми. Рекомендується збільшення дози до 80 мг 2 рази на добу до кінця 2-го тижня, а максимальна цільова доза 160 мг 2 рази на добу може бути досягнута до кінця 3-го місяця терапії препаратом Вальсакор®. Досягнення цільової дози залежить від переносимості валсартану під час титрування доз. При розвитку надмірного зниження артеріального тиску, що супроводжується клінічними проявами, або порушенням функції нирок, слід зменшити дозу препарату. Можливе одночасне застосування з іншими ЛЗ, у т.ч. тромболітичними засобами, ацетилсаліцилової кислотою як антиагрегантний засіб, бета-адреноблокаторами та інгібіторами ГМГ-КоА-редуктази (статинами). Одночасне застосування з інгібіторами АПФ не рекомендується. Оцінка стану пацієнтів після перенесеного гострого ІМ має включати контроль функції нирок. Пацієнти від 6 до 18 років АГ. Рекомендована початкова доза препарату Вальсакор® у дітей та підлітків від 6 до 18 років становить 40 мг при масі тіла дитини менше 35 кг та 80 мг при масі тіла дитини понад 35 кг. Рекомендується корекція дози з урахуванням зниження артеріального тиску. Максимальні рекомендовані добові дози відображені нижче. При масі тіла ≥8 та <35 кг максимальна рекомендована добова доза становить 80 мг; від 35 до <80 кг – 160 мг; від ≥80 до ≤160 кг – 320 мг. Застосування вищих доз не рекомендовано. ХСН та перенесений ІМ. Препарат Вальсакор® не рекомендований для лікування ХСН та перенесеного гострого ІМ у пацієнтів віком до 18 років. Пацієнти похилого віку. Корекція дози препарату у пацієнтів віком від 65 років не потрібна. Порушення функції нирок. Корекція дози у пацієнтів із Cl креатиніну більше 10 мл/хв не потрібна. Одночасне застосування препарату Вальсакор з аліскіреном у пацієнтів з помірними та тяжкими порушеннями функції нирок (Cl креатиніну менше 60 мл/хв) протипоказане. Порушення функції печінки. У пацієнтів з легким або помірним порушенням функції печінки небіліарного генезу без холестазу препарат слід застосовувати з обережністю, добова доза не повинна перевищувати 80 мг. Пацієнти із цукровим діабетом. Одночасне застосування препарату Вальсакор з аліскіреном у пацієнтів із ЦД протипоказане.ПередозуванняСимптоми: основним очікуваним проявом передозування валсартану є виражене зниження артеріального тиску, яке може призвести до порушення свідомості, колапсу та/або шоку. Лікування: симптоматичне, рекомендується викликати блювання та промити шлунок. При розвитку вираженого зниження артеріального тиску необхідно перевести пацієнта в положення лежачи на спині з піднятими вгору ногами, внутрішньовенно ввести 0,9% розчин натрію хлориду. Рекомендується регулярний контроль діяльності серця та дихальної системи, ОЦК та кількості сечі, що виділяється. Гемодіаліз неефективний.Запобіжні заходи та особливі вказівкиГіперкаліємія. При одночасному застосуванні калійзберігаючих діуретиків (спіронолактон, еплеренон, тріамтерен, амілорид), препаратів калію, калійвмісних замінників солі або інших препаратів, здатних підвищувати вміст калію в плазмі крові (наприклад, гепарин), слід бути обережним. Необхідно регулярно контролювати вміст калію у плазмі крові. Порушення функції нирок. У пацієнтів з порушенням функції нирок не потрібна зміна доз препарату. Т.к. відсутні дані про застосування препарату при тяжкій нирковій недостатності (Cl креатиніну менше 10 мл/хв або 0,167 мл/с) та у пацієнтів, які перебувають на гемодіалізі, у таких випадках препарат рекомендується застосовувати з обережністю. Одночасне застосування валсартану з аліскіреном у пацієнтів з помірними та тяжкими порушеннями функції нирок (Cl креатиніну менше 60 мл/хв) протипоказано. Порушення функції печінки. У пацієнтів з легкими та помірними порушеннями функції печінки без явищ холестазу препарат Вальсакор слід застосовувати з обережністю. Пацієнти з гіпонатріємією та/або дегідратацією. У пацієнтів з вираженою гіпонатріємією та/або дегідратацією, наприклад внаслідок прийому великих доз діуретиків, у поодиноких випадках на початку терапії препаратом Вальсакор може розвинутись артеріальна гіпотензія з клінічними проявами. Перед початком лікування рекомендовано відновити вміст натрію та/або ОЦК, зокрема шляхом зменшення доз діуретиків. Стеноз ниркової артерії. Застосування валсартану коротким курсом у пацієнтів з реноваскулярною гіпертензією, що розвинулася вдруге внаслідок стенозу артерії єдиної нирки, не спричиняє суттєвих змін показників ниркової гемодинаміки, концентрації креатиніну або азоту сечовини у сироватці крові. Однак, враховуючи, що інші ЛЗ, що впливають на РААС, можуть викликати підвищення концентрації сечовини та креатиніну у сироватці крові у пацієнтів із двостороннім стенозом ниркових артерій або стенозом артерії єдиної нирки, необхідно регулярно контролювати концентрації креатиніну та залишкового азоту сечовини у сироватці крові. Стан після перенесеної трансплантації нирки. Безпека застосування препарату Вальсакор у пацієнтів, які недавно перенесли трансплантацію нирки, не встановлена. Первинний гіперальдостеронізм. Пацієнти з первинним гіперальдостеронізмом є резистентними до гіпотензивних препаратів, що впливають на РААС, тому таким пацієнтам застосування препарату Вальсакор® не рекомендується. Стеноз аортального та/або мітрального клапанів, ГЗКМП. Препарат Вальсакор® необхідно з обережністю застосовувати у пацієнтів з гемодинамічно значущим стенозом аортального та/або мітрального клапанів або ГОКМП. Період після перенесеного ІМ. Одночасне застосування з АПФ інгібіторами не рекомендується, т.к. не має додаткових клінічних переваг перед монотерапією та збільшує ризик розвитку небажаних явищ. Застосування валсартану у пацієнтів після перенесеного ІМ часто призводить до невеликого зниження артеріального тиску, проте припинення терапії через артеріальну гіпотензію зазвичай не потрібне, якщо виконувати рекомендації щодо дозування препарату. Терапію препаратом Вальсакор слід починати обережно. Оцінка стану хворих після гострого інфаркту міокарда повинна включати контроль функції нирок. Можливе одночасне застосування при гострому ІМ з іншими ЛЗ: тромболітики, ацетилсаліцилова кислота, бета-адреноблокатори та інгібітори ГМГ-КоА-редуктази (статини). ХСН. У пацієнтів з ХСН не рекомендується одночасне застосування трьох класів препаратів: інгібіторів АПФ, бета-адреноблокаторів та валсартану, т.к. ця терапія не давала додаткового клінічного ефекту, у своїй збільшувався ризик розвитку небажаних явищ. Застосування у пацієнтів з ХСН зазвичай супроводжується зниженням артеріального тиску, проте при дотриманні рекомендацій щодо добору доз лікування рідко вимагає відміни через артеріальну гіпотензію. Терапію препаратом Вальсакор у пацієнтів з ХСН слід починати з обережністю. Внаслідок придушення активності РААС у деяких пацієнтів (наприклад, у пацієнтів з ХСН III–IV функціонального класу за класифікацією NYNA, функція нирок яких залежить від стану РААС) на тлі терапії інгібіторами АПФ можлива зміна функції нирок: розвиток олігурії та/або прогресуючої азотемії,а в поодиноких випадках - ГНН та/або летальний результат. Препарат Вальсакор® блокує рецептори ангіотензину ІІ, тому у пацієнтів з ХСН потрібний регулярний контроль функції нирок. Ангіоневротичний набряк в анамнезі. Серед пацієнтів з ангіоневротичним набряком на фоні терапії препаратом Вальсакор® спостерігалися випадки розвитку ангіоневротичного набряку в анамнезі, у т.ч. та на інгібітори АПФ. При розвитку ангіоневротичного набряку слід негайно відмінити препарат та виключити можливість повторного застосування. Спеціальна інформація щодо допоміжних речовин Препарат Вальсакор містить лактозу, тому не слід застосовувати при наступних станах: непереносимість лактози, дефіцит лактази, синдром глюкозо-галактозної мальабсорбції. Вплив на здатність виконання потенційно небезпечних видів діяльності, що вимагають особливої уваги та швидких реакцій (наприклад управління автотранспортом, робота з механізмами, що рухаються). У зв'язку з можливістю виникнення запаморочення або слабкості на фоні застосування препарату Вальсакор® необхідно бути обережним при керуванні транспортними засобами та зайнятті потенційно небезпечними видами діяльності.Умови зберіганняПри кімнатній температуріУмови відпустки з аптекЗа рецептомВідео на цю тему