Все товары
Склад, форма випуску та упаковкаДжимнеми екстракт, грифон екстракт, піридоксину гідрохлорид (вітамін B6), хрому піколінат, целюлоза мікрокристалічна (носій), магнію стеарат (агент антистежуючий).ХарактеристикаДля того, щоб зменшити кількість калорій, досить просто відмовитися від зайвої, особливо від калорійної – борошняної та солодкої – їжі. Якщо складно обмежувати себе одним зусиллям волі, то впоратись із переїданням допоможе засіб Турбослім Нейрослім. Його головна головна особливість у тому, що на відміну від інших засобів, він впливає на психологічну причину підвищеного апетиту. У складі Турбослім Нейро – унікальне поєднання 1 екстрактів джимнеми та грифонії, посилене хромом. Турбослім Нейро допомагає зменшити кількість калорій: він сприяє зниженню апетиту та усуненню переїдань, тому що підвищує рівень серотоніну – "гормону щастя" і знижує потяг до солодкого та борошняного.Властивості компонентівГриффонія - природне джерело триптофану, з якого в нашому організмі утворюється серотонін - "гормон щастя". Рецептори центру насичення є серотоніновими, отже при нормальному рівні серотоніну відбувається їх активація: апетит знижується, а насичення настає швидше. Крім того, саме серотонін забезпечує піднятий настрій та емоційний комфорт і робить це анітрохи не гірше, ніж шматочок смачного жирного торта. Джимнема – одна з головних рослин, що застосовуються у світі для підтримки нормальної роботи підшлункової залози та вироблення інсуліну. Слово "джимнема" перекладається як "руйнівник цукру". Вона уповільнює всмоктування цукру з їжі, знижує його рівень, але до нормальних показників. Хром необхідний для вуглеводного та ліпідного (жирового) обміну, він підтримує нормальний рівень глюкози в крові, що знижує почуття голоду та потяг до солодкого та борошняного.Протипоказання до застосуванняІндивідуальна непереносимість компонентів БАД, вагітність, годування груддю.Спосіб застосування та дозиПриймати дорослим по 2 капсули на день під час або після їди, запиваючи достатньою кількістю води. Рекомендується приймати у першій половині дня. Тривалість прийому – 1 місяць. За потреби прийом можна продовжити.Запобіжні заходи та особливі вказівкиПеред застосуванням рекомендується проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаІнулін, худий екстракт, L-карнітин, піколінат хрому.ХарактеристикаУправління апетитом — найкращий спосіб схуднути та контролювати свою вагу надалі. Мало кому вдається контролювати апетит зусиллям волі. Під час дієти завжди хочеться щось з'їсти. «Турбослім Контроль апетиту» з екстрактом худої гордонії (південно-африканський кактус) пригнічує почуття голоду. Відомо, що особливої шкоди фігурі завдають пізні вечері. Варто відмовитися від перекушування після шостої вечора — і вага починає знижуватися. «Турбослім Контроль апетиту» допомагає цього досягти! Зручна форма випуску - жувальні таблетки - дозволяє легко контролювати апетит протягом дня і ввечері, дотримуватися дієти без зривів, тому що відсутня їхня основна причина - почуття голоду. «Турбослім Контроль апетиту» не містить проносних компонентів, тому його можна включати в будь-яку програму схуднення та застосовувати у комплексі з будь-якими іншими засобами лінії «Турбослім». Жувальні таблетки не вимагають запивання водою і їх легко використовувати в будь-якій ситуації. Для кращого ефекту бажано тримати таблетку в роті якнайдовше. Впливаючи безпосередньо на смакові рецептори, вона втричі швидше пригнічує почуття голоду проти капсулами. "Турбослім Контроль апетиту" - маленька пігулка від великого апетиту!Дія на організмМістить екстракт худи гордонії (південно-африканський кактус), який ефективно пригнічує почуття голоду. Допомагає відмовитись від щільних вечерь, впоратися з вечірнім апетитом. Впливаючи безпосередньо на смакові рецептори, жувальні таблетки втричі швидше пригнічують почуття голоду проти капсулами. Не містить проносних компонентів, може використовуватися в будь-якій програмі схуднення, у тому числі у комплексі з будь-якими іншими засобами Турбосліму. Зручна форма випуску — жувальні таблетки, що не потребують запивання водою, — дозволяє застосовувати препарат у будь-якій ситуації.Протипоказання до застосуванняОсобам з індивідуальною непереносимістю компонентів, вагітним, які годують груддю. Перед застосуванням слід проконсультуватися з лікарем.Спосіб застосування та дозиДорослим по 1 таблетці перед кожним їдою, повільно розжовуючи до повного розчинення. Рекомендується регулярний прийом. Таблетки світло-бежевого кольору із дрібними вкрапленнями. Колір таблеток в одній упаковці може відрізнятися за тоном через гігроскопічність екстракту худи, що вважається нормою і не погіршує якість. Після розтину упаковки не рекомендується зберігати таблетки при підвищеній вологості повітря.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковка1 капсула (добовий прийом) містить хрому піколінат 1,819 мг, у тому числі хром 200 мкг.ХарактеристикаВи вирішили схуднути та вибрали дієту. Проте вже за кілька днів ваше бажання помітно послабшало? Почалися поблажки у вигляді цукерок, морозива, посилилася потяг до солодкого, погіршився настрій, і в результаті ви вирішили відкласти схуднення до «наступного понеділка»? Як показує практика, лише невеликий відсоток людей здатний витримати дієту тривалий час. Однак, насправді, щоб скинути зайву вагу, зовсім не потрібно виснажувати себе голодом і вводити жорсткі обмеження в харчуванні. Досить навчитися легко контролювати свій апетит і не переїдати більше норми. Як вирішити цю проблему природним способом? Встановлено, що проблеми з дотриманням дієти часто пов'язані з рівнем цукру (глюкози) в крові. А метаболізм глюкози, у свою чергу, багато в чому залежить від участі в ньому мікроелементу хрому: разом із інсуліном він допомагає організму засвоювати цукор. Додатковий прийом хрому сприяє підтримці в нормі рівня цукру в крові. Турбослім Піколінат хрому містить хром у легко засвоюваній органічній формі. Кожна капсула містить оптимальне дозування, заповнюючи нестачу хрому в організмі. Хром є життєво важливим мікроелементом, який грає колосальну роль нашому організмі. Біологічна роль хрому насамперед пов'язана з його участю в регуляції вуглеводного та ліпідного (жирового) обмінів, і, насамперед, з підтриманням нормальної толерантності до глюкози. Хром здатний посилювати дію інсуліну. Він підтримує здорову чутливість клітинних рецепторів тканин до інсуліну. Хром впливає проникність клітинних мембран для глюкози. Завдяки участі у процесах підтримання нормального рівня глюкози у крові, він допомагає дотримуватися здорового харчування. З віком вміст хрому в організмі, на відміну інших мікроелементів, прогресивно знижується. При цьому концентрація хрому в харчових продуктах є досить низькою. Вміст хрому зменшується через надмірне очищення продуктів. Так, при обробці цільного зерна з отриманням білої муки втрачається майже 80% хрому. З неочищеного цукру після перетворення його на білий гранульований пісок йде 98% хрому. До дефіциту хрому також призводить і споживання великої кількості легкозасвоюваних вуглеводів. Низькі рівні хрому в організмі викликають різкі коливання вмісту цукру в крові та можуть спровокувати стійке збільшення його рівня. Ознаки низької кількості хрому включають дратівливість, проблеми із запам'ятовуванням, сильну спрагу. У нормі людина повинна одержувати з їжею до 200 мкг хрому на добу.Дія на організмЗменшення тяги до солодкого та борошняного; Підтримка у нормі рівня цукру на крові; Зниження почуття голоду.Протипоказання до застосуванняОсобам з індивідуальною непереносимістю компонентів, вагітним, які годують груддю. Перед застосуванням слід проконсультуватися з лікарем.Спосіб застосування та дозиДорослим по 1 капсулі 1 раз на день після їди. Тривалість прийому – 1 місяць. За потреби прийом можна продовжувати.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаКапсули ВТРО: гуарани екстракт, червоних морських водоростей екстракт, кальцію карбонат, червоного виноградного листя екстракт, кислота аскорбінова. Капсули ДЕНЬ: гарцинії екстракт, квіток опунції екстракт, фенхелю екстракт, кукурудзяний рилець екстракт, сенни екстракт, хрому піколінат. Капсули ВЕЧІР: гарцинії екстракт, меліси екстракт, фукус екстракт, сенни екстракт, L-карнітин, хрому піколінат. Саші: олігофруктоза, лимонний сік, квіток опунції екстракт, артишок екстракт, зеленого чаю екстракт, фенхелю екстракт.Опис лікарської форми6 капсул "ранок" білого кольору по 0,375 г, 6 капсул "день" рожевого кольору по 0,34 г, 6 капсул "вечір" синього кольору по 0,34 г, 3 саші по 6,7 г.ХарактеристикаБувають у житті моменти, коли терміново треба схуднути. Дні народження, Новий рік, Восьме березня, весілля, нарешті! Особливо складно, коли у вас лише 3 дні! І, звичайно, здорово, якщо у цій складній справі у вас є помічник. Натуральний комплекс «Турбослім Експрес-Схуднення» - це єдиний комплекс для схуднення, який допоможе вам за 3 дні скинути до 3 кг і зменшити обсяг талії максимум до 3-3,5 см. Секрет – у складному поєднанні великої кількості компонентів, які запускають процес прискореного схуднення. Як професійні дієтологи, вони допоможуть вам упоратися з апетитом; як умілі масажисти, позбавлять набряків* і зайвої рідини в організмі; як досвідчені тренери, змусять посилено спалювати жир та допоможуть підвищити тонус м'язів та судин. А ще «Турбослім Експрес-схуднення» добре очищає організм. І вже через 3 дні ваше відображення в дзеркалі знову радуватиме вас своїми стрункими обрисами! * Якщо набряки не є наслідком захворювань. «Турбослім Експрес-схуднення» включає найсильніші натуральні компоненти для боротьби з зайвою вагою, які в комплексі посилюють ефективність один одного. А для досягнення ще більшого результату діючі речовини розділені на 3 капсули для прийому в різний час дня з урахуванням особливостей роботи організму в різний час доби.Дія на організмЗавдяки складному поєднанню великої кількості компонентів запускає процес прискореного схуднення: сприяє спалюванню жирів, придушенню почуття голоду, виведенню зайвої рідини, активному очищенню організму. Ранкові капсули «включають» процеси спалювання жиру та виведення рідини, підвищують тонус організму. Денні капсули сприяють придушенню апетиту, прискорюють переробку жирів та вуглеводів в енергію для активного життя, нормалізують роботу кишківника. Вечірні капсули допомагають легше заснути, активізують процеси нічного схуднення та очищення організму. Напій для прийому протягом дня посилює дренаж, сприяє нормалізації мікрофлори кишечника, знижує стомлюваність.Протипоказання до застосуванняОсобам з індивідуальною непереносимістю компонентів, вагітним, які годують груддю. Перед застосуванням слід проконсультуватися з лікарем.Спосіб застосування та дозиДорослим: 2 капсули білого кольору вранці під час сніданку, 2 капсули рожевого кольору вдень під час обіду, 2 капсули синього кольору ввечері під час вечері. 1 саше для приготування напою розчинити в 1 л питної води кімнатної температури приймати протягом усього дня. Тривалість прийому – 3 дні.Умови відпустки з аптекБез рецептаВідео на цю тему
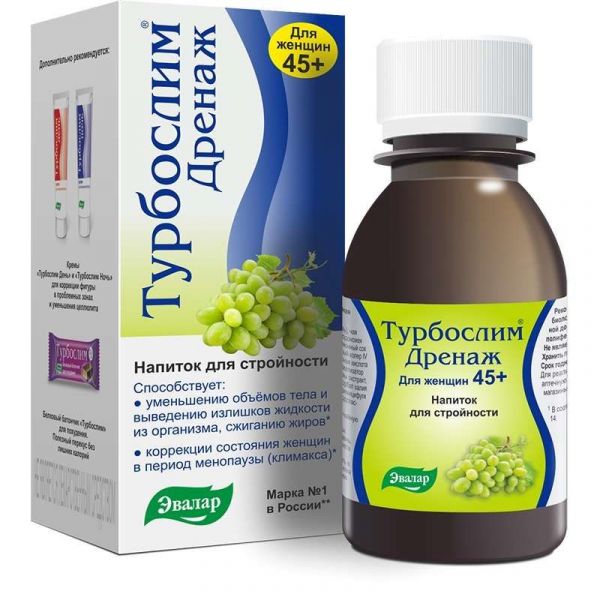
Склад, форма випуску та упаковкаМінеральний комплекс з морської солі, екстракт зеленого чаю, екстракт плодоніжок вишні, лимонний сік порошкоподібний, екстракт сенни, L-карнітин, соковмісна основа «Грейпфрут», екстракт фенхелю, екстракт циміцифуги, екстракт артишоку, екстракт вівса.Характеристика«Турбослім Дренаж для жінок 45+» розроблений спеціально для жінок 45 років і старше, чий гормональний баланс та пов'язаний з ним мінеральний обмін нестійкі. Напій «Турбослім Дренаж для жінок 45+» з приємним смаком дозволяє худнути із задоволенням та користю для здоров'я! «Турбослім Дренаж для жінок 45+» має сечогінну дію, посилює лімфовідтік, тонізує, активізує роботу систем виділення та очищення. Все це дозволяє легко «вигнати» зайву рідину з організму, зменшити обсяги тіла, впливати на жирові клітини, зменшити виразність целюліту.Дія на організмРозроблено спеціально для жінок 45 років і старших, чий гормональний баланс і пов'язаний з ним мінеральний обмін нестійкі. Активно бореться із затримкою рідини в організмі, зменшує набряки, надаючи сечогінну дію, посилюючи лімфострум. Допомагає зменшити обсяги тіла, звільнити жирові клітини, знизити вираженість целюліту. Тонізує організм, активізує роботу систем виділення та очищення. Крім дренажного ефекту, має загальну омолоджуючу дію на організм жінки, завдяки наявності в його складі фітоестрогенів - екстракту циміцифуги.Протипоказання до застосуванняОсобам з індивідуальною непереносимістю компонентів, вагітним, які годують груддю. Перед застосуванням слід проконсультуватися з лікарем.Спосіб застосування та дозиДорослим 1 чайну ложку (5 мл) концентрату напою розчинити в 1 склянці (250 мл) води. Приймати 4 склянки на день. Допускається денну дозу концентрату напою – 4 чайні ложки (20 мл) – розчинити в 1 літрі води та приймати протягом дня. Тривалість прийому – 10 днів з регулярним повтором не менше 4 разів на рік. Можливе помутніння та поява осаду є властивим для рослинних компонентів, що входять до складу напою, не впливає на якість та не знижує ефективність. Перед приготуванням напою флакон із концентратом необхідно збовтувати.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаВода, гліцерин (загусник), фруктоза, вишні плодоніжок екстракт, виноградного листя екстракт, лимонна кислота (регулятор кислотності), вівса екстракт, лимонний сік порошкоподібний, сенни екстракт, артишока екстракт, гуарани екстракт, фенхелю екстракт, чая виноград), сукралоза (підсолоджувач), натрію бензоат та калію сорбат (консерванти).ХарактеристикаНапій «Турбослім Дренаж» активно бореться із затримкою рідини в організмі завдяки поєднанню відразу кількох ефектів. Він одночасно працює як сечогінний засіб, посилює лімфострум, активізує роботу системи виділення та очищення. Все це дозволяє легко «вигнати» зайву рідину, зменшити обсяги тіла та «звільнити» жирові клітини для легшого схуднення. «Турбослім Дренаж» нормалізує жировий обмін, зменшує набряки*, очищує та тонізує організм. А значить, ви не тільки позбудетеся зайвої рідини, але й без проблем впораєтеся з жиром.Дія на організмАктивно бореться із затримкою рідини в організмі, зменшує набряки*, діючи відразу в декількох напрямках: має сечогінну дію, посилює лімфострум, активізує роботу системи виділення та очищення. Допомагає звільнити жирові клітини, зменшити обсяги тіла, знизити вираженість целюліту. Нормалізує жировий обмін. Очищає організм від токсинів та шлаків. Тонізує, надає енергії.Протипоказання до застосуванняОсобам з індивідуальною непереносимістю компонентів, вагітним, які годують груддю. Перед застосуванням слід проконсультуватися з лікарем.Спосіб застосування та дози2 чайні ложки (10 мл) БАД розчинити в 1 літрі питної води кімнатної температури, приймати протягом дня. Допускається розчиняти 2,5 мл (0,5 чайні ложки) БАД в 1 склянці (250 мл) питної води та приймати 4 склянки на день.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаL-карнітин тартрат, гуарани екстракт, плодоніжок вишні екстракт, інулін, хром піколінат.ХарактеристикаЖінки, які стежать за собою, хочуть постійно контролювати свою вагу. Але, як правило, у боротьбі за ідеальну фігуру багато часу йде марно, адже значна частина нашого життя минає уві сні. Саме тому в серію «Турбослім» увійшов комплекс, що не має аналогів, для схуднення 24 години на добу, що враховує хронобіологію людини. З препаратами «Турбослім День посилена формула» та «Турбослім Ніч посилена формула» ви зможете худнути не лише вдень, а й уночі! «Турбослім День посилена формула» містить підвищене дозування натуральних екстрактів та біологічно активних субстанцій, виготовлених із застосуванням сучасних технологій. Завдяки збалансованому складу та ефективності діючих компонентів, «Турбослім День посилена формула» працює одразу в декількох напрямках: надає дренажне та протинабрякову дію, активізує обмінні процеси, стимулює спалювання жирів, сприяє зниженню апетиту та зменшенню потягу до солодкого. Таким чином досягається природне схуднення без строгих дієт та високих фізичних навантажень.Дія на організмМістить підвищену дозу натуральних екстрактів та біологічно активних субстанцій, підібраних з урахуванням особливостей роботи організму в денний час. Активізує обмін речовин, уповільнення якого є однією з найпоширеніших причин набору зайвих кілограмів. Стимулює спалювання жирів, перетворюючи їх на енергію для активного життя. Сприяє зниженню апетиту, зменшує потяг до солодкого протягом дня. Оптимально працює у поєднанні з препаратом Турбослім Ніч посилена формула, що дозволяє худнути не лише вдень, а й уночі.Протипоказання до застосуванняПри індивідуальній непереносимості компонентів, вагітності, годуванні груддю. Перед застосуванням рекомендується проконсультуватися з лікарем.Спосіб застосування та дозиДорослим по 2 капсули вранці під час їжі. Тривалість прийому – не менше 1 місяця. За потреби прийом можна повторити.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаХітозан, екстракт насіння квасолі, екстракт гарцинії, екстракт фенхелю, піколінат хрому.ХарактеристикаНе завжди є можливість змінити звичний раціон харчування, далеко не у всіх вистачає сили волі відмовитися від висококалорійних смаколиків. "Турбослім Блокатор калорій" дає таку можливість - позбавлятися зайвих кілограмів, не змінюючи звичного раціону харчування. «Турбослім Блокатор калорій» блокує всмоктування та засвоєння зайвих калорій, що надходять із їжею. Формула препарату дозволяє блокувати засвоєння як вуглеводів, а й жирів. У результаті ви отримуєте менше калорій і не мучаєтеся докорами сумління через шматочок тортика! Також «Турбослім Блокатор калорій» пригнічує апетит та бажання поласувати солодким. Тому наступного разу тортика вам просто не захочеться. А зайві кілограми підуть ще швидше!Дія на організмДає можливість позбавлятися зайвих кілограмів, не змінюючи звичного раціону харчування. Блокує засвоєння як вуглеводів, а й жирів, знижуючи калорійність раціону. Пригнічує апетит і потяг до солодкого.Протипоказання до застосуванняОсобам з індивідуальною непереносимістю компонентів, вагітним, які годують груддю. Перед застосуванням рекомендується проконсультуватися з лікарем.Спосіб застосування та дозиДорослим та дітям старше 14 років по 1 таблетці з кожним прийомом їжі. Тривалість прийому щонайменше 20 днів. Допускається регулярний прийом із 10-денною перервою.Умови відпустки з аптекБез рецептаВідео на цю тему
451,00 грн
422,00 грн
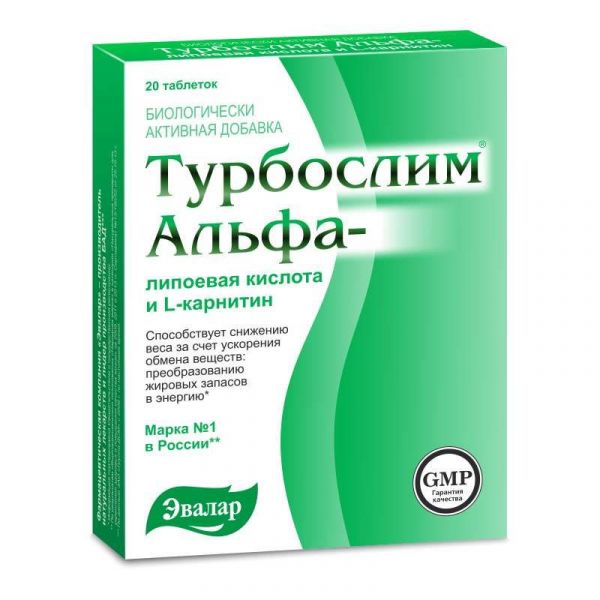
Склад, форма випуску та упаковкаL-карнітин, альфа-ліпоєва кислота, вітамін В5, вітамін В6, вітамін В2, вітамін В1.ХарактеристикаОбмін речовин (метаболізм) уповільнюється при неправильному харчуванні, малорухливому способі життя, а також із віком. Саме тому після 40 років утримувати вагу в нормі стає дедалі важче. Але швидкість метаболізму можна змінити та підтримувати її на «молодому» рівні! У світовій практиці для цілеспрямованого прискорення обмінних процесів використовують вітаміноподібні речовини - альфа-ліпоєву кислоту в комбінації з L-карнітином. Для багатьох це стало справжнім проривом у схудненні. Адже саме недолік альфа-ліпоєвої кислоти та L-карнітину часто стає причиною зайвої ваги та ожиріння. Поєднання цих речовин у препараті «Турбослім Альфа-ліпоєва кислота та L-карнітин» відчутно активізує обмінні процеси в організмі, сприяє розщепленню жирів та вуглеводів та переробці їх в енергію. Це актуально як прискорення процесу схуднення, так закріплення отриманого результату. Комбінація альфа-ліпоєвої кислоти, L-карнітину та вітамінів групи В у препараті є максимально збалансованою та сприяє ефективному прискоренню обміну речовин.Властивості компонентівМістить альфа-ліпоєву кислоту в комбінації з L-карнітином - поєднання речовин, яке широко використовує у світовій практиці для цілеспрямованого прискорення обмінних процесів. Сприяє розщепленню жирів та вуглеводів та переробці їх в енергію для активного життя. Допомагає не лише схуднути, а й утримати результат. Альфа - ліпоєва кислота, L-карнітин та вітаміни групи у складі препарату максимально збалансовані для досягнення найкращого результату.РекомендуєтьсяЦей препарат для вас, якщо ви: Ведете активний спосіб життя; Займаєтесь фітнесом; Бажаєте збільшити ефективність фізичних навантажень та прискорити схуднення.Протипоказання до застосуванняОсобам з індивідуальною непереносимістю компонентів, вагітним, які годують груддю. Перед застосуванням слід проконсультуватися з лікарем.Спосіб застосування та дозиДорослим по 2 таблетки 1 раз на день до їди. Тривалість прийому не менше ніж 1 місяць. За потреби прийом можна повторити.Умови відпустки з аптекБез рецептаВідео на цю тему
319,00 грн
271,00 грн
Склад, форма випуску та упаковкаL-карнітин, альфа-ліпоєва кислота, вітамін В5, вітамін В6, вітамін В2, вітамін В1.ХарактеристикаОбмін речовин (метаболізм) уповільнюється при неправильному харчуванні, малорухливому способі життя, а також із віком. Саме тому після 40 років утримувати вагу в нормі стає дедалі важче. Але швидкість метаболізму можна змінити та підтримувати її на «молодому» рівні! У світовій практиці для цілеспрямованого прискорення обмінних процесів використовують вітаміноподібні речовини - альфа-ліпоєву кислоту в комбінації з L-карнітином. Для багатьох це стало справжнім проривом у схудненні. Адже саме недолік альфа-ліпоєвої кислоти та L-карнітину часто стає причиною зайвої ваги та ожиріння. Поєднання цих речовин у препараті «Турбослім Альфа-ліпоєва кислота та L-карнітин» відчутно активізує обмінні процеси в організмі, сприяє розщепленню жирів та вуглеводів та переробці їх в енергію. Це актуально як прискорення процесу схуднення, так закріплення отриманого результату. Комбінація альфа-ліпоєвої кислоти, L-карнітину та вітамінів групи В у препараті є максимально збалансованою та сприяє ефективному прискоренню обміну речовин.Властивості компонентівМістить альфа-ліпоєву кислоту в комбінації з L-карнітином - поєднання речовин, яке широко використовує у світовій практиці для цілеспрямованого прискорення обмінних процесів. Сприяє розщепленню жирів та вуглеводів та переробці їх в енергію для активного життя. Допомагає не лише схуднути, а й утримати результат. Альфа - ліпоєва кислота, L-карнітин та вітаміни групи у складі препарату максимально збалансовані для досягнення найкращого результату.РекомендуєтьсяЦей препарат для вас, якщо ви: Ведете активний спосіб життя; Займаєтесь фітнесом; Бажаєте збільшити ефективність фізичних навантажень та прискорити схуднення.Протипоказання до застосуванняОсобам з індивідуальною непереносимістю компонентів, вагітним, які годують груддю. Перед застосуванням слід проконсультуватися з лікарем.Спосіб застосування та дозиДорослим по 2 таблетки 1 раз на день до їди. Тривалість прийому не менше ніж 1 місяць. За потреби прийом можна повторити.Умови відпустки з аптекБез рецептаВідео на цю тему
246,00 грн
210,00 грн
Фасовка: N20 Форма выпуска: таб. жевательные Упаковка: упак. Производитель: Грин Сайд Завод-производитель: Грин Сайд ООО(Россия).
Склад, форма випуску та упаковкаМікрокристалічна целюлоза (Е460, носій), желатин (капсула), йод (йодат калію)ХарактеристикаЯк біологічно активної добавки до їжі - додаткового джерела йоду. Йод за своїм значенням для життєдіяльності організму відноситься до істинних мікроелементів. Основне фізіологічне значення йоду визначається його участю функції щитовидної залози. Йод, що надходить у щитовидну залозу, піддається окисленню і включається в процес біосинтезу тиреоїдних гормонів. При призначенні внутрішньо йод вибірково накопичуючись у тканині щитовидної залози впливає на функцію щитовидної залози, бере участь у синтезі гормону тироксину, посилює процеси дисиміляції, сприятливо діє на ліпідний та білковий обмін. При недостатньому вмісті йоду у воді та харчових продуктах синтез тироксину порушується і для відновлення нормальної гормональної функції щитовидної залози необхідне введення йоду та його препаратів.що доводить застосування препаратів йоду для профілактики ендемічного зоба.РекомендуєтьсяЯк біологічно активна добавка до їжі - додаткового джерела йоду.Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність, годування груддю, особам, яким протипоказані препарати йоду, особам із захворюваннями щитовидної залози.Спосіб застосування та дозиДорослим по 1 капсулі 2 десь у день, дітям старше 14 років по 1 капсулі 1 десь у день під час їжі. Тривалість прийому: 1 місяць. Можливі повторні прийоми протягом року.Запобіжні заходи та особливі вказівкиПеред застосуванням слід проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаМікрокристалічна целюлоза (Е460, наповнювач), желатин (капсула), цинк (цинку цитрат)ХарактеристикаЯк біологічно активної добавки до їжі - додаткового джерела цинку. Цинк необхідний для нормального зростання шкіри, волосся і нігтів, а також при загоєнні ран, оскільки він відіграє важливу роль у синтезі білків організму та при копіюванні генетичного матеріалу. Цинк необхідний здорової імунної системи. Цинк діє як необхідний кофактор більш ніж у дюжині хімічних реакцій, надзвичайно важливих для людського здоров'я, один із ферментів – гастин – дає нам можливість відчувати смак. Цинк діє як детоксикатор при видаленні надлишку двоокису вуглецю з організму та при детоксикації алкоголю. Цинк впливає на активність статевих та гонадотропних гормонів гіпофізу. Цинк також збільшує активність ферментів: фосфатаз кишкової та кісткової, що каталізують гідроліз.Тісний зв'язок цинку з гормонами та ферментами пояснює його вплив на вуглеводний, жировий та білковий обмін речовин, на окисно-відновні процеси, на синтетичну здатність печінки. Вважається, що цинк має ліпотропний ефект, тобто. сприяє підвищенню інтенсивності розпаду жирів, що проявляється зменшенням вмісту жиру у печінці.РекомендуєтьсяЯк біологічно активна добавка до їжі - додаткового джерела цинку.Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність, годування груддю.Спосіб застосування та дозиДорослим по 1 капсулі 1-2 десь у день, дітям старше 14 років по 1 капсулі 1 десь у день під час їжі. Тривалість прийому: 1 місяць. Можливі повторні прийоми протягом року.Запобіжні заходи та особливі вказівкиПеред застосуванням слід проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаМікрокристалічна целюлоза (Е460, наповнювач), желатин (капсула), "Селексен" (селеномісткий компонент)ХарактеристикаЯк біологічно активної добавки до їжі - додаткового джерела селену. Селен є есенціальним мікроелементом для людини і тварин. Він є одним з біологічно важливих мікроелементів, присутніх в організмі людини та що беруть участь у метаболічних, біофізичних та енергетичних реакціях організму, що забезпечують життєздатність та функції клітин, тканин, органів та організму в цілому. Особливо важливою є роль селену для функціональної активності таких органів як серце, печінка, нирки та ін. Біологічні функції селену величезні. Антиоксидантні властивості селену визначають перспективність використання препаратів мікроелементу при оксидантному стресі. Селен стимулює імунітет. Як антиокислювач має захисний вплив на цитоплазматичні мембрани, не допускаючи їх зміни. Поряд з кобальтом та магнієм,є фактором, що протидіє порушенням хромосомного апарату. Бере участь у виробленні еритроцитів. Чинить захисну дію на імунну систему, запобігаючи формуванню вільних радикалів, які надають ушкоджуючу дію на організм.РекомендуєтьсяЯк біологічно активна добавка до їжі - додаткового джерела селену.Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність, годування груддю.Спосіб застосування та дозиДорослим по 1 капсулі 1-2 десь у день під час їжі. Тривалість прийому: 1 місяць. Можливі повторні прийоми протягом року.Запобіжні заходи та особливі вказівкиПеред застосуванням слід проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
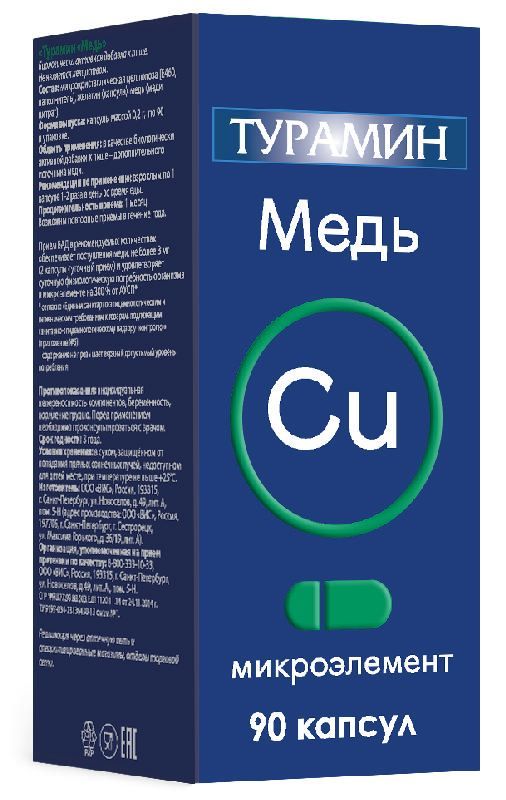
Склад, форма випуску та упаковкаМікрокристалічна целюлоза (Е460, наповнювач), желатин (капсула), мідь (міді цитрат)ХарактеристикаЯк біологічно активної добавки до їжі - додаткового джерела міді. Мед - один з найважливіших незамінних мікроелементів. Мідь бере участь у біохімічних процесах як складова частина електроносних білків, що здійснюють реакції окиснення органічних субстратів молекулярним киснем. Цією роллю вона має своїм особливим властивістю як перехідного металу. Вона входить до складу церулоплазміну, який забезпечує окислення заліза та біогенних амінів, до складу супероксиддисмутази, яка є найсильнішим антиоксидантом, цитохром-з-оксидази, завдяки якій бере участь у процесі дихання, а також бере участь у гідроксилюванні та окисленні дофаміну, тирозину, лізину, кислоти, гістаміну, адреналіну та низки фенолів. Мідь бере участь у кровотворенні та у великій кількості реакцій обміну речовин, як компонент солей оксидоредуктаз,у процесах формування еластину, утворення енергії, прискорює одужання, впливає на фарбування шкіри та смакову чутливість. Цей мінерал необхідний підтримки здорового стану нервової системи та суглобів.РекомендуєтьсяЯк біологічно активну добавку до їжі – додаткового джерела міді.Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність, годування груддю.Спосіб застосування та дозиДорослим по 1 капсулі 1-2 десь у день під час їжі. Тривалість прийому: 1 місяць. Можливі повторні прийоми протягом року.Запобіжні заходи та особливі вказівкиПеред застосуванням слід проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаЖелатин (капсула), мікрокристалічна целюлоза (Е460, наповнювач), марганець (марганцю глюконат)ХарактеристикаЯк біологічно активної добавки до їжі - додаткового джерела марганцю. Марганець - есенціальний мікроелемент, що бере участь у регуляції нейрохімічних процесів у центральній нервовій системі. Марганець відіграє у метаболізмі клітини. Марганець необхідний для зростання, відтворення, загоєння ран, ефективної роботи мозку та правильного метаболізму цукрів, інсуліну та холестерину. Марганець є одним із життєво необхідних мікроелементів і бере участь у регуляції найважливіших процесів в організмі людини: входить до складу кількох ферментних систем, є активатором окисно-відновних процесів, активно впливає на обмін білків, вуглеводів та жирів, бере участь в утворенні кісток та хрящів, зміцнює тканини артерій, роблячи їх більш стійкими до утворення склеротичних бляшок,має виражену антиоксидантну активність, необхідний для утворення гемоглобіну та еритроцитів, бере участь в обміні вітамінів С, Е, холіну та вітамінів групи В, необхідний для правильного травлення та засвоєння їжі, важливий для роботи центральної нервової системи, покращує м'язові рефлекси та пам'ять, стимулює процеси зростання , захищає кістковий скелет від наслідків травм, а суглоби – від тертя, впливає на імунний захист організму.впливає на імунний захист організму.впливає на імунний захист організму.РекомендуєтьсяЯк біологічно активна добавка до їжі - додаткового джерела марганцю.Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність, годування груддю.Спосіб застосування та дозиДорослим по 1 капсулі 1-2 десь у день, дітям старше 14 років по 1 капсулі 1 десь у день під час їжі. Тривалість прийому: 1 місяць. Можливі повторні прийоми протягом року.Запобіжні заходи та особливі вказівкиПеред застосуванням слід проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаМагній (магнію цитрат), желатин (капсула), мікрокристалічна целюлоза (Е460, наповнювач)ХарактеристикаЯк біологічно активної добавки до їжі - додаткового джерела магнію. Магній бере участь у багатьох процесах, що відбуваються в організмі - у виробленні енергії, засвоєнні глюкози, передачі нервового сигналу, синтезі білків, побудові кісткової тканини, регуляції розслаблення та напруги судин та м'язів. Він надає заспокійливу дію, знижуючи збудливість нервової системи та посилюючи процеси гальмування в корі головного мозку, виступає як протиалергічний та протизапальний фактор, захищає організм від інфекції, беручи участь у виробленні антитіл, відіграє значну роль у процесах згортання крові, регуляції роботи кишечника, сеч передміхурової залози. Магній один з найважливіших мінералів, будучи основним внутрішньоклітинним елементом, активізує ферменти, що регулюють вуглеводний обмін, стимулює утворення білків,регулює зберігання та вивільнення енергії в АТФ, знижує збудження у нервових клітинах, розслаблює серцевий м'яз. Магній торкається майже всіх аспектів нашого здоров'я.РекомендуєтьсяЯк біологічно активну добавку до їжі - додаткового джерела магнію.Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність, годування груддю.Спосіб застосування та дозиДорослим по 2 капсули 3-4 десь у день, дітям старше 14 років по 1 капсулі 4 десь у день під час їжі. Тривалість прийому: 1 місяць. Можливі повторні прийоми протягом року.Запобіжні заходи та особливі вказівкиПеред застосуванням слід проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
Склад, форма випуску та упаковкаМікрокристалічна целюлоза (Е460, наповнювач), желатин (капсула), хром (хром піколінат)ХарактеристикаЯк біологічно активної добавки до їжі - додаткового джерела хрому. Хром є необхідним елементом організму, що відповідає за регуляцію цукру в крові. Він впливає на стан клітинних тканин, на діяльність серцевого м'яза, посилює відновлювальні функції організму, важливий для гормонального обміну. Через погану екологічну обстановку і стресів вміст хрому в організмі зменшується. Нестача хрому в організмі призводить до порушення вуглеводного обміну, виникнення цукрового діабету, розвитку депресій, головного болю, сприяє збільшенню ваги. З віком засвоюваність хрому порушується і тому 90% людей відчувають його нестачу. Хром також вважається фактором довголіття.Це пов'язано з його позитивним впливом на функцію дегідроепіандростерону (ДГЕА) – важливого ендогенного гормону молодості – а також із захистом білків від гліколізу, зокрема, сполучної тканини. Високий рівень інсуліну гальмує дію вироблюваного організмом ДГЭА, а результаті організм людей, " залежних від солодкого " , виявляє тенденцію до прискореного старіння. Враховуючи, що з віком рівень ДГЕА знижується, люди похилого віку повинні періодично доповнювати свій раціон "біологічно активним" хромом, щоб підтримати функцію мозку, активність імунної системи та м'язовий тонус.Враховуючи, що з віком рівень ДГЕА знижується, люди похилого віку повинні періодично доповнювати свій раціон "біологічно активним" хромом, щоб підтримати функцію мозку, активність імунної системи та м'язовий тонус.Враховуючи, що з віком рівень ДГЕА знижується, люди похилого віку повинні періодично доповнювати свій раціон "біологічно активним" хромом, щоб підтримати функцію мозку, активність імунної системи та м'язовий тонус.РекомендуєтьсяЯк біологічно активна добавка до їжі - додаткового джерела хрому.Протипоказання до застосуванняІндивідуальна непереносимість компонентів, вагітність, годування груддю.Спосіб застосування та дозиДорослим та дітям старше 14 років по 1 капсулі на день, запиваючи невеликою кількістю води, під час їжі. Тривалість прийому: 1 місяць. Можливі повторні прийоми протягом року.Запобіжні заходи та особливі вказівкиПеред застосуванням слід проконсультуватися з лікарем.Умови відпустки з аптекБез рецептаВідео на цю тему
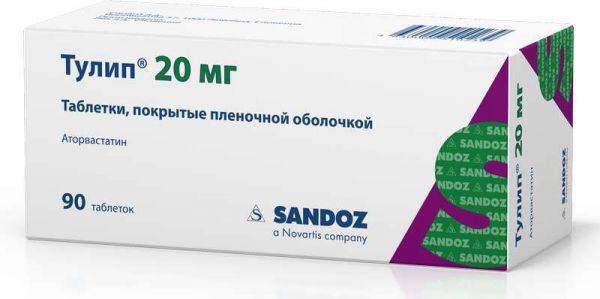
Склад, форма випуску та упаковкаПігулки - 1 таб. Активна речовина: аторвастатин кальцію – 41.43 мг (відповідає вмісту аторвастатину – 40 мг); Допоміжні речовини: целюлоза мікрокристалічна - 284.97 мг, лактози моногідрат - 69.6 мг, кроскармелоза натрію - 38.4 мг, гіпоролоза - 4 мг, полісорбат 80 - 5.2 мг, магнію оксид важкий - 52 мг, магнію 2 . мг; Склад оболонки: гіпромелоза – 5.952 мг, гіпоролоза – 1.488 мг, титану діоксид – 2.736 мг, макрогол 6000 – 1.2 мг, тальк – 0.6 мг, заліза оксид жовтий (Е172) – 0.024 мг. По 10 таблеток А1/А1 блістер. По 3, 6 або 9 блістерів поміщають у картонну пачку разом із інструкцією з медичного застосування.Опис лікарської формиТаблетки, покриті плівковою оболонкою білого кольору з жовтувато-коричневим відтінком, круглі, двоопуклі, з гравіюванням "HLA 40" - на одній стороні; вид на зламі: таблетки білого кольору.Фармакотерапевтична групаГіполіпідемічний препарат.ФармакокінетикаВсмоктування та розподіл Абсорбція висока. Cmax у плазмі після прийому внутрішньо досягається через 1-2 год. Прийом їжі дещо знижує швидкість і ступінь абсорбції препарату (на 25% і 9% відповідно), проте зниження Хс-ЛПНГ подібне до такого при застосуванні аторвастатину без одночасного прийому їжі. Після прийому внутрішньо аторвастатину у вечірній час концентрація його в плазмі нижче (Cmax і AUC приблизно на 30%), ніж після прийому в ранковий час, тоді як зниження концентрації Хс-ЛПНГ не залежить від часу доби прийому препарату. Виявлено лінійну залежність між ступенем всмоктування та дозою препарату. Біодоступність становить 12-14%, системна біодоступність інгібуючої активності щодо ГМГ-КоА-редуктази – близько 30%. Низька системна біодоступність обумовлена пресистемним метаболізмом у шлунково-кишковому тракті та ефектом "першого проходження" через печінку. Середній Vd – 381 л, зв'язування з білками плазми крові – 98%. Відношення концентрації аторвастатину в еритроцитах/плазмі становить близько 0.25, що вказує на погане проникнення аторвастатину в еритроцити. Метаболізм та виведення Аторвастатин метаболізується переважно у печінці під дією ізоферментів CYP3A4, CYP3A5 та CYP3A7 з утворенням фармакологічно активних метаболітів (орто- та парагідроксильованих похідних, продуктів бета-окислення). In vitro орто- та парагідроксильовані метаболіти мають інгібуючу дію на ГМГ-КоА-редуктазу, порівнянну з дією аторвастатину. Інгібуючий ефект препарату щодо ГМГ-КоА-редуктази приблизно на 70% визначається активністю циркулюючих метаболітів, який зберігається приблизно протягом 20-30 годин завдяки їх наявності. Результати досліджень in vitro дають підставу припустити, що ізофермент печінки CYP3A4 відіграє важливу роль у метаболізмі аторвастатину. Це підтверджується підвищенням концентрації аторвастатину в плазмі при одночасному прийомі еритроміцину, який є інгібітором цього ізоферменту. Дослідження in vitro також показали, що аторвастатин є слабким інгібітором ізоферменту CYP3A4. Виводиться в основному через кишечник після печінкового та/або позапечінкового метаболізму (препарат не піддається вираженій кишково-печінковій рециркуляції). T1/2 - 14 год. T1/2 інгібуючої активності ГМГ-КоА-редуктази становить 20-30 год. Менше 2% від прийнятої внутрішньо дози визначається сечі. Не виводиться в ході гемодіалізу через інтенсивне зв'язування з білками плазми. Фармакокінетика в особливих клінічних випадках У жінок Cmax вище на 20%, AUC – нижче на 10%, ніж у чоловіків, що не має клінічного значення. У пацієнтів з алкогольним цирозом (клас В за шкалою Чайлд-П'ю) печінки Cmax у 16 разів, а AUC – в 11 разів вище за норму. Cmax та AUC у літніх пацієнтів (≥65 років) на 40% та 30% відповідно вище, ніж у пацієнтів молодого віку, однак це не впливає на ступінь зниження холестерину ЛПНЩ. Порушення функції нирок не впливає на концентрацію препарату в плазмі ступінь зниження холестерину ЛПНГ.ФармакодинамікаАторвастатин є селективним конкурентним інгібітором ГМГ-КоА-редуктази - ферменту, що перетворює 3-гідрокси-3-метилглутарил коензим А в мевалонову кислоту, що є попередником стеролів, включаючи холестерин. Тригліцериди (ТГ) і холестерин (Хс) включаються до складу ліпопротеїнів дуже низької щільності (ЛПДНЩ) при синтезі в печінці, надходять у плазму крові та транспортуються в периферичні тканини. Ліпопротеїни низької щільності (ЛПНЩ) утворюються з ЛПДНЩ у ході взаємодії з рецепторами ЛПНЩ. Дослідження показали, що підвищення концентрацій загального Хс, ЛПНГ та аполіпопротеїну В (апо-В) у плазмі крові сприяє розвитку атеросклерозу та входять до групи факторів ризику виникнення серцево-судинних захворювань, у той час як збільшення концентрації ліпопротеїнів високої щільності (ЛПВЩ) знижує ризик розвитку серцево-судинних захворювань Аторвастатин знижує концентрацію Хс та ліпопротеїнів у плазмі крові за рахунок пригнічення ГМГ-КоА-редуктази, синтезу холестерину в печінці та збільшення числа "печінкових" рецепторів ЛПНГ на поверхні клітин, що призводить до посилення захоплення та катаболізму ЛПНГ (за даними доклінічних досліджень). Аторвастатин знижує синтез та концентрацію Хс-ЛПНГ, загального Хс, апо-В у пацієнтів з гомозиготною та гетерозиготною сімейною гіперхолестеринемією, первинною гіперхолестеринемією та змішаною гіперліпідемією. Викликає також зниження концентрації холестерину-ЛПОНП та ТГ та підвищення концентрації холестерину-ЛПВЩ та аполіпопротеїну А-1 (апо-А). У пацієнтів з дисбеталіпопротеїнемією знижує концентрацію ліпопротеїнів проміжної щільності ХС-ЛПСШ. Аторвастатин у дозах 10 мг та 20 мг знижує концентрацію загального Хс на 29% та 33%, ЛПНГ – на 39% та 43%, апо-В – на 32% та 35% та ТГ – на 14% та 26% відповідно; викликає підвищення концентрації холестерину-ЛПЗЗ та апо-А. Аторвастатин у дозах 40 мг знижує концентрацію загального Хс на 37%, ЛПНГ – на 50%, апо-В – на 42% та ТГ – на 29%; викликає підвищення концентрації Хс-ЛПЗЗ та апо-А. Дозозалежно знижує концентрацію ЛПНГ у хворих на гомозиготну сімейну гіперхолестеринемію, резистентну до терапії іншими гіполіпідемічними засобами. Не надає канцерогенної та мутагенної дії. Терапевтичний ефект розвивається через 2 тижні після початку терапії, досягає максимуму через 4 тижні та зберігається протягом усього періоду лікування.Показання до застосуванняу поєднанні з гіпохолестеринемічною дієтою для зниження підвищених концентрацій загального Хс, Хс-ЛПНЩ, апо-В і ТГ та підвищення концентрації Хс-ЛПВЩ у хворих з первинною гіперхолестеринемією, гетерозиготною сімейною та несемейною гіперхолестеринемією та комбінованою (змішаною) гіперліпі класифікації Фредріксона), коли дієтотерапія та інші нефармакологічні методи лікування виявляються недостатньо ефективними; для зниження концентрації загального Хс та Хс-ЛПНГ у хворих з гомозиготною сімейною гіперхолестеринемією, коли дієтотерапія та інші нефармакологічні методи лікування виявляються недостатньо ефективними; первинна профілактика серцево-судинних ускладнень у пацієнтів без клінічних ознак ІХС, але які мають кілька факторів ризику її розвитку: вік старше 55 років, нікотинова залежність, артеріальна гіпертензія, цукровий діабет, ретинопатія, альбумінурія, низькі концентрації Хс-ЛПВП в плазмі , в т.ч. на фоні дисліпідемії; вторинна профілактика серцево-судинних ускладнень у пацієнтів з ІХС з метою зниження сумарного показника смертності, інфаркту міокарда, інсульту, повторної госпіталізації щодо стенокардії та необхідності реваскуляризації.Протипоказання до застосуваннязахворювання печінки на активній стадії або підвищення активності печінкових трансаміназ у плазмі крові (більш ніж у 3 рази порівняно з ВГН) неясного генезу; вагітність; період лактації; вік до 18 років (ефективність та безпека не встановлені); дефіцит лактази, непереносимість лактози, синдром глюкозо-галактозної мальабсорбції (оскільки у складі міститься лактоза); підвищена чутливість до аторвастатину та інших допоміжних компонентів препарату. З обережністю слід призначати препарат при зловживанні алкоголем, захворюваннях печінки в анамнезі, захворюваннях м'язової системи (в анамнезі від застосування інших представників групи інгібіторів ГМГ-КоА-редуктази), тяжких порушеннях електролітного балансу, ендокринних (гіпертиреоз) та метаболічних порушеннях, діабеті, тяжких гострих інфекціях (сепсис), неконтрольованій епілепсії, великих хірургічних втручаннях, травмах, агресивній ліпідзнижувальній терапії (аторвастатин у дозі 80 мг) при вторинній профілактиці інсульту у пацієнтів з геморагічним абонсультом.Вагітність та лактаціяПрепарат Туліп протипоказаний до застосування під час вагітності. Оскільки холестерин та речовини, що синтезуються з холестерину, важливі для розвитку плода, потенційний ризик інгібування ГМГ-КоА-редуктази перевищує користь від застосування препарату під час вагітності. У разі діагностування вагітності в процесі терапії препаратом Туліп®, його прийом слід припинити якнайшвидше, а пацієнтку необхідно попередити про потенційний ризик для плода. Препарат Туліп® можна застосовувати у жінок репродуктивного віку лише в тому випадку, якщо ймовірність вагітності у них дуже низька, а пацієнтка поінформована про можливий ризик для плода під час лікування. Жінки репродуктивного віку під час лікування препаратом Туліп повинні застосовувати надійні методи контрацепції. Аторвастатин виділяється з грудним молоком, тому протипоказаний до застосування у період грудного вигодовування. При необхідності застосування препарату Туліп® у період лактації грудне вигодовування слід припинити. Протипоказаний у дитячому та підлітковому віці до 18 років (ефективність та безпека не встановлені).Побічна діяЗа даними ВООЗ небажані ефекти класифіковані відповідно до їх частоти розвитку наступним чином: часто (більше 1/100, менше 1/10), нечасто (більше 1/1000, менше 1/100), рідко (більше 1/10 000, менше 1/1000) та дуже рідко (менше 1/10 000), включаючи окремі повідомлення; частота невідома - за наявними даними встановити частоту виникнення неможливо. З боку імунної системи: часто – алергічні реакції; дуже рідко – анафілаксія. З боку нервової системи: часто – головний біль; нечасто - запаморочення, порушення сну, включаючи безсоння та кошмарні сновидіння, астенічний синдром, слабкість, парестезія, гіпестезія, порушення смакової чутливості, втрата або зниження пам'яті; рідко – периферична невропатія. З боку органів чуття: нечасто - шум у вухах, нечіткість зору; рідко – порушення зору; дуже рідко – втрата слуху. З боку травної системи: часто – запор, метеоризм, диспепсія, нудота, діарея; нечасто – анорексія, блювання, панкреатит, гепатит, біль у животі, відрижка; рідко – холестатична жовтяниця (в т.ч. обструктивна); дуже рідко – печінкова недостатність. З боку кістково-м'язової системи: часто – міалгія, артралгія, припухлість суглобів, біль у суглобах, біль у спині, м'язовий спазм; нечасто – біль у м'язах шиї, м'язова слабкість; рідко – міопатія, міозит, рабдоміоліз, тендинопатія (іноді ускладнена розривом сухожилля); частота невідома – імуноопосередкована некротизуюча міопатія. З боку шкіри та підшкірних тканин: нечасто – кропив'янка, висипання на шкірі та свербіж, алопеція; рідко – ангіоневротичний набряк, бульозний висип, багатоформна ексудативна еритема (в т.ч. синдром Стівенса-Джонсона), токсичний епідермальний некроліз (синдром Лайєлла). З боку обміну речовин: часто – гіперглікемія; нечасто – гіпоглікемія. З боку системи кровотворення: нечасто – тромбоцитопенія. З боку дихальної системи: часто – назофарингіт, біль у горлі, носова кровотеча. Лабораторні показники: часто – підвищення активності сироваткової КФК, підвищення активності печінкових трансаміназ; нечасто – лейкоцитурія; частота невідома – підвищення концентрації глікозильованого гемоглобіну. Інші: нечасто – підвищена втома, порушення потенції, вторинна ниркова недостатність, підвищення температури тіла, біль у грудях, периферичні набряки, збільшення маси тіла; дуже рідко – гінекомастія, цукровий діабет. Є окремі повідомлення про розвиток атонічного фасціїту (зв'язок із застосуванням аторвастатину точно не встановлено); частота невідома – депресія, інтерстиціальне захворювання легень (особливо при тривалій терапії), сексуальна дисфункція.Взаємодія з лікарськими засобамиРизик міопатії під час лікування інгібіторами ГМГ-КоА-редуктази підвищується при одночасному застосуванні з циклоспорином, еритроміцином, кларитроміцином, імунодепресивними, протигрибковими препаратами (похідними азолу) внаслідок можливого підвищення концентрації аторвастатину у сироватці крові. При одночасному застосуванні з інгібіторами ВІЛ-протеаз – індинавір, ритонавір – збільшується ризик розвитку міопатії. Подібна взаємодія можлива при одночасному застосуванні аторвастатину з фібратами та нікотиновою кислотою у ліпідзнижуючих дозах (більше 1 г/добу). Інгібітори ізоферменту CYP3A4 Оскільки аторвастатин метаболізується за допомогою ізоферменту CYP3A4, спільне застосування препарату Туліп з інгібіторами цього ізоферменту може призводити до збільшення концентрації аторвастатину в плазмі. Ступінь взаємодії та ефект збільшення концентрації аторвастатину визначаються варіабельністю впливу на ізофермент CYP3A4. Інгібітори транспортного білка ОАТР1В1 Аторвастатин та його метаболіти є субстратами транспортного білка ОАТР1В1. Інгібітори ОАТР1В1 (наприклад, циклоспорин) можуть збільшувати біодоступність аторвастатину. Так, застосування аторвастатину в дозі 10 мг та циклоспорину в дозі 5.2 мг/кг/добу призводить до збільшення концентрації аторвастатину у плазмі крові у 7.7 рази. Еритроміцин/кларитроміцин При одночасному застосуванні аторвастатину 10 мг та еритроміцину (по 500 мг 4 рази на добу) або кларитроміцину (по 500 мг 2 рази на добу), які інгібують ізофермент цитохрому CYP3A4, спостерігається підвищення концентрації аторвастатину в плазмі крові (на 40% еритроміцином та на 56% – при застосуванні з кларитроміцином). Інгібітори протеаз Одночасне застосування аторвастатину з інгібіторами протеаз, відомими як інгібітори ізоферменту цитохрому CYP3A4, супроводжується збільшенням концентрації аторвастатину в плазмі крові (при одночасному застосуванні з еритроміцином – Cmax аторвастатину збільшується на 40%). Ділтіазем Спільне застосування аторвастатину в дозі 40 мг з дилтіаземом у дозі 240 мг призводить до збільшення концентрації аторвастатину в плазмі. Ціметідин Клінічно значущої взаємодії аторвастатину з циметидином не виявлено. Ітраконазол Одночасне застосування аторвастатину у дозах від 20 мг до 40 мг та ітраконазолу у дозі 200 мг призводить до 3-кратного збільшення значення AUC аторвастатину. Грейпфрутовий сік Оскільки грейпфрутовий сік містить один або більше компонентів, які пригнічують ізофермент CYP3A4, його надмірне вживання (більше 1.2 л на день протягом 5 днів) може спричинити збільшення концентрації аторвастатину в плазмі крові. Індуктори ізоферменту CYP3A4 Спільне застосування аторвастатину з індукторами ізоферменту СУРЗА4 (наприклад, ефавіренз або рифампіцин) може призвести до зниження концентрації аторвастатину в плазмі крові. Внаслідок двоїстого механізму взаємодії з рифампіцином (індуктором ізоферменту CYP3A4 та інгібітором транспортного білка гепатоцитів ОАТР1В1), не рекомендується одночасне застосування аторвастатину та рифампіцину, оскільки відстрочений прийом аторвастатину після прийому рифам. Антациди При одночасному застосуванні внутрішньо аторвастатину та суспензії, що містить магнію та алюмінію гідроксиди, концентрація аторвастатину в плазмі знижується приблизно на 35%, проте ступінь зниження концентрації Хс-ЛПНЩ при цьому не змінюється. Феназон Аторвастатин не впливає на фармакокінетику феназону, тому взаємодія з іншими препаратами, що метаболізуються тими самими ізоферментами, не очікується. Колестипол Гіполіпідемічний ефект комбінації з колестиполом перевищує такий для кожного препарату окремо, незважаючи на зниження концентрації аторвастатину на 25% при його одночасному застосуванні з колестиполом. Фузидова кислота Досліджень щодо взаємодії аторвастатину та фузидової кислоти не проводилося. Як і у випадку з іншими статинами, у постмаркетингових дослідженнях спільного застосування аторвастатину та фузидової кислоти повідомлялося про побічні дії на м'язи, включаючи рабдоміоліз. Механізм взаємодії невідомий. Такі пацієнти вимагають ретельного спостереження та, можливо, тимчасової відміни прийому аторвастатину. Колхіцін Хоча дослідження взаємодії аторвастатину та колхіцину не проводилися, повідомлялося про випадки міопатії при спільному застосуванні з колхіцином, і при одночасному призначенні аторвастатину та колхіцину слід дотримуватися обережності. Дігоксин При повторному застосуванні дигоксину та аторвастатину у дозі 10 мг Css дигоксину у плазмі крові не змінюються. Однак при застосуванні дигоксину в комбінації з аторвастатином у дозі 80 мг на добу концентрація дигоксину в плазмі збільшується приблизно на 20%. Пацієнтам, які приймають дигоксин у поєднанні з аторвастатином, потрібен контроль концентрації дигоксину у плазмі. Азітроміцин При одночасному застосуванні аторвастатину в дозі 10 мг 1 раз на добу та азитроміцину в дозі 500 мг 1 раз на добу концентрація аторвастатину в плазмі крові не змінюється. Пероральні контрацептиви При одночасному застосуванні аторвастатину та перорального контрацептиву, що містить норетистерон та етинілестрадіол, спостерігається значне підвищення AUC норетистерону та етинілестрадіолу приблизно на 30% та 20%, відповідно, що слід враховувати при виборі перорального контрацептиву. Терфенадін Аторвастатин при одночасному застосуванні з терфенадином не має клінічно значущого впливу на фармакокінетику терфенадину. Варфарін У пацієнтів, які тривало приймають варфарин, аторвастатин у дозі 80 мг на добу дещо скорочує протромбіновий час у перші дні спільного застосування. Цей ефект зникає після 15 днів одночасного застосування цих препаратів. Хоча про випадки клінічно значущих змін антикоагулянтного ефекту повідомлялося дуже рідко, слід визначати протромбіновий час у пацієнтів, які приймають кумаринові антикоагулянти, перед початком та досить часто на початку лікування аторвастатином, щоб переконатися у відсутності значних змін протромбінового часу. Як тільки буде зареєстровано стабільний протромбіновий час, він може перевірятися з інтервалами, звичайними для пацієнтів, які приймають кумаринові антикоагулянти. У разі зміни дози або припинення лікування ці заходи слід повторити.Не спостерігалося зв'язку між застосуванням аторвастатину та кровотечами або зміною протромбінового часу у пацієнтів, які не приймають антикоагулянти. Амлодипін При одночасному застосуванні аторвастатину у дозі 80 мг та амлодипіну у дозі 10 мг фармакокінетика аторвастатину у рівноважному стані не змінюється. Інші гіполіпідемічні препарати При одночасному застосуванні аторвастатину з іншими гіполіпідемічними препаратами (наприклад, езетимиб, гемфіброзил, похідне фіброєвої кислоти) у ліпід-знижувальних дозах збільшується ризик розвитку рабдоміолізу. Інша супутня терапія При сумісному застосуванні аторвастатину з гіпотензивними засобами та естрогенами (як замісна терапія) – клінічно значущої взаємодії не виявлено.Спосіб застосування та дозиПеред початком застосування препарату Туліп® пацієнту необхідно рекомендувати стандартну гіпохолестеринемічну дієту, яку він повинен продовжувати дотримуватись протягом усього періоду терапії препаратом. Препарат приймають внутрішньо незалежно від часу їди. Доза препарату Туліп® варіює в межах від 10 мг до 80 мг на добу, і підбирається з урахуванням вихідних концентрацій Хс-ЛПНГ, мети терапії та індивідуальної терапевтичної відповіді на терапію. Для більшості пацієнтів початкова доза становить 10 мг 1 раз на добу. На початку лікування, через 2-4 тижні терапії та/або після підвищення дози препарату Туліп® необхідно контролювати концентрації ліпідів у плазмі крові та за необхідності коригувати дозу препарату. Максимальна добова доза – 80 мг на добу. Первинна (гетерозиготна спадкова та полігенна) гіперхолестеринемія (тип IIа) та змішана гіперліпідемія (тип IIb) У більшості випадків буває достатньо застосування препарату Туліп у дозі 10 мг 1 раз на добу (можливе застосування аторвастатину у таблетках по 10 та 20 мг). При необхідності можливе поступове збільшення дози до 80 мг (2 таб. по 40 мг) залежно від реакції пацієнта з інтервалом 2-4 тижні, оскільки терапевтичний ефект відзначається через 2 тижні, а максимальний терапевтичний ефект – через 4 тижні. При тривалому лікуванні цей ефект зберігається. Гомозиготна спадкова гіперхолестеринемія Препарат Туліп® у більшості випадків застосовують у дозі 80 мг (2 таб. по 40 мг) 1 раз на добу. Попередження розвитку серцево-судинних захворювань Туліп® застосовують у дозі 10 мг 1 раз на добу. Якщо не досягнуто оптимальної концентрації ЛПНЩ у плазмі, можливе збільшення дози препарату до 80 мг на добу залежно від реакції пацієнта з інтервалом 2-4 тижні. Корекція дози препарату Туліп у пацієнтів з порушенням функції нирок та у пацієнтів похилого віку не потрібна. У пацієнтів з порушенням функції печінки сповільнюється виведення аторвастатину з організму, тому рекомендується застосовувати його з обережністю при постійному контролі активності печінкових трансаміназ: ACT та АЛТ. Якщо підвищення активності ACT або АЛТ, що спостерігається, більш ніж у 3 рази в порівнянні з ВГН зберігається, рекомендується зниження дози або відміна препарату Туліп®.ПередозуванняЛікування: специфічного антидоту для лікування передозування немає. У разі передозування слід проводити симптоматичне лікування. Гемодіаліз не ефективний (оскільки препарат значно пов'язується з білками плазми).Запобіжні заходи та особливі вказівкиВплив на печінку Як і при застосуванні інших інгібіторів ГМГ-Ко-редуктази (статинів), при терапії препаратом Туліп® можливе помірне (більш ніж у 3 рази порівняно з ВГН) підвищення сироваткової активності печінкових трансаміназ: ACT та АЛТ. До початку терапії, через 6 тижнів та 12 тижнів після початку прийому препарату Туліп або після збільшення його дози, необхідно контролювати показники функції печінки (ACT, АЛТ). Функцію печінки слід контролювати також у разі появи клінічних ознак ураження печінки. У разі підвищення активності ACT та АЛТ, їх активність слід контролювати доти, доки вона не нормалізується. Туліп® слід застосовувати з обережністю у пацієнтів, які зловживають алкоголем та/або мають захворювання печінки в анамнезі. Захворювання печінки в активній стадії або підвищення активності печінкових трансаміназ плазми неясного генезу є протипоказанням для застосування препарату Туліп®. Профілактика інсульту за допомогою інтенсивної ліпідзнижувальної терапії (SPARCL) При ретроспективному аналізі різних підвидів інсульту у осіб, які не страждають на ІХС, які недавно перенесли інсульт або транзиторну ішемічну атаку (ТІА), був виявлений більш високий ризик геморагічного інсульту у пацієнтів, які приймають аторвастатин у дозі 80 мг порівняно з плацебо. Особливо високий ризик відзначався у пацієнтів, які перенесли геморагічний інсульт або лакунарний інфаркт на момент початку дослідження. Для пацієнтів, які перенесли геморагічний інсульт або лакунарний інфаркт і приймають аторвастатин у дозі 80 мг, співвідношення ризик/користування є неоднозначним, і слід уважно оцінювати потенційний ризик розвитку геморагічного інсульту перед початком лікування. Дія на скелетні м'язи При застосуванні препарату Туліп можливий розвиток міалгії. Діагноз міопатії (біль і слабкість у м'язах у поєднанні з підвищенням активності КФК більш ніж у 10 разів порівняно з ВГН) можна припустити у пацієнтів з дифузною міалгією, хворобливістю або слабкістю м'язів та/або вираженим підвищенням активності КФК. Терапію препаратом Туліп слід припинити у разі вираженого підвищення активності КФК або за наявності підтвердженої або передбачуваної міопатії. При застосуванні інших інгібіторів ГМГ-Ко-редуктази (статинів) можливе підвищення ризику міопатії при одночасному застосуванні з циклоспорином, фібратами, еритроміцином, нікотиновою кислотою у ліпід-знижувальних дозах (більше 1 г/добу) або протигрибкових препаратів групи азолів. Застосовуючи препарат Туліп® у комбінації з фібратами, еритроміцином, імунодепресантами, протигрибковими препаратами групи азолів або нікотиновою кислотою у ліпідзнижуючих дозах (більше 1 г/добу), необхідно зважити очікувану користь та ризик лікування Туліп®. Дуже рідко повідомлялося про випадки імуноопосередкованої некротизуючої міопатії під час або після лікування статинами, включаючи аторвастатин. Імуноопосередкована некротизуюча міопатія клінічно характеризується м'язовою слабкістю у верхніх відділах кінцівок та підвищенням концентрації КФК плазми крові, що зберігаються незважаючи на припинення лікування статинами. У разі потреби комбінованої терапії слід розглянути можливість застосування зазначених препаратів у нижчих початкових та підтримуючих дозах. Рекомендується періодичний контроль за активністю КФК. Спільне застосування аторвастатину та фузидової кислоти не рекомендується, отже слід розглянути тимчасове припинення терапії аторвастатином під час застосування фузидової кислоти. Пацієнтів слід попередити про те, що необхідно негайно звернутися до лікаря при появі незрозумілого болю або м'язової слабкості, особливо, якщо вони супроводжуються нездужанням або лихоманкою. При застосуванні препарату Туліп, як і інших інгібіторів ГМГ-Ко-редуктази (статинів), описані рідкісні випадки рабдоміолізу з гострою нирковою недостатністю, зумовленою міоглобінурією. При появі симптомів можливої міопатії або наявності фактора ризику розвитку ниркової недостатності на тлі рабдоміолізу (наприклад, тяжка гостра інфекція, артеріальна гіпотензія, широке хірургічне втручання, травми, серйозні метаболічні, електролітні та ендокринні порушення та неконтрольовані судоми). скасувати. Інтерстиційна хвороба легень Повідомлялося про рідкісні випадки розвитку інтерстиціальної хвороби легень при застосуванні деяких статинів, особливо при тривалій терапії. Клінічні прояви включають задишку, непродуктивний кашель та погіршення загального здоров'я (підвищена стомлюваність, зниження маси тіла та лихоманка). У разі підозри на інтерстиціальну хворобу легенів, що розвивалася, лікування статинами слід припинити. Цукровий діабет Дані деяких досліджень свідчать про те, що застосування статинів як класу може призводити до підвищення концентрації глюкози в крові, а у деяких пацієнтів з підвищеним ризиком розвитку діабету в майбутньому може викликати гіперглікемію, при якій необхідна стандартна антидіабетична терапія. Однак такий ризик є незначним у порівнянні зі зниженням судинного ризику при прийомі статинів, і, отже, не може бути причиною скасування лікування статинами. Пацієнти в групі ризику (з концентрацією глюкози натще 5.6-6.9 ммоль/л, ІМТ >30 кг/м2, підвищеним рівнем тригліцеридів, підвищеним АТ) повинні бути під контролем як клінічним, так і біохімічним відповідно до національних стандартів надання медичної допомоги . Вплив на здатність до керування автотранспортом та управління механізмами У період лікування препаратом Туліп® необхідно дотримуватись обережності при керуванні транспортними засобами та зайнятті іншими потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Активна речовина: аторвастатин (у формі аторвастатину кальцію) – 20 мг; Допоміжні речовини: лактози моногідрат - 34.8 мг, кроскармеллозу натрію - 19.2 мг, гіпоролозу - 2 мг, полісорбат 80 - 2.6 мг, магнію оксид важкий - 26 мг, кремнію діоксид колоїдний - 1.2 мг, магнію стеарат - 1 250 мг; Склад оболонки: гіпромелоза – 2.976 мг, гіпоролоза – 0.744 мг, титану діоксид (Е171) – 1.368 мг, макрогол 6000 – 0.6 мг, тальк – 0.3 мг, заліза оксид жовтий (Е172) – 0.01. По 10 таблеток поміщають у блістер А1/А1 фольги. По 3, 6 або 9 блістерів поміщають у картонну пачку разом із інструкцією з медичного застосування.Опис лікарської формиТаблетки, покриті плівковою оболонкою світло-жовтого кольору, круглі, двоопуклі, з гравіюванням "HLA 20" на одній стороні; вид на зламі: таблетки білого кольору.Фармакотерапевтична групаГіполіпідемічний препарат.ФармакокінетикаВсмоктування та розподіл Абсорбція висока. Cmax у плазмі після прийому внутрішньо досягається через 1-2 год. Прийом їжі дещо знижує швидкість і ступінь абсорбції препарату (на 25% і 9% відповідно), проте зниження Хс-ЛПНГ подібне до такого при застосуванні аторвастатину без одночасного прийому їжі. Після прийому внутрішньо аторвастатину у вечірній час концентрація його в плазмі нижче (Cmax і AUC приблизно на 30%), ніж після прийому в ранковий час, тоді як зниження концентрації Хс-ЛПНГ не залежить від часу доби прийому препарату. Виявлено лінійну залежність між ступенем всмоктування та дозою препарату. Біодоступність становить 12-14%, системна біодоступність інгібуючої активності щодо ГМГ-КоА-редуктази – близько 30%. Низька системна біодоступність обумовлена пресистемним метаболізмом у шлунково-кишковому тракті та ефектом "першого проходження" через печінку. Середній Vd – 381 л, зв'язування з білками плазми крові – 98%. Відношення концентрації аторвастатину в еритроцитах/плазмі становить близько 0.25, що вказує на погане проникнення аторвастатину в еритроцити. Метаболізм та виведення Аторвастатин метаболізується переважно у печінці під дією ізоферментів CYP3A4, CYP3A5 та CYP3A7 з утворенням фармакологічно активних метаболітів (орто- та парагідроксильованих похідних, продуктів бета-окислення). In vitro орто- та парагідроксильовані метаболіти мають інгібуючу дію на ГМГ-КоА-редуктазу, порівнянну з дією аторвастатину. Інгібуючий ефект препарату щодо ГМГ-КоА-редуктази приблизно на 70% визначається активністю циркулюючих метаболітів, який зберігається приблизно протягом 20-30 годин завдяки їх наявності. Результати досліджень in vitro дають підставу припустити, що ізофермент печінки CYP3A4 відіграє важливу роль у метаболізмі аторвастатину. Це підтверджується підвищенням концентрації аторвастатину в плазмі при одночасному прийомі еритроміцину, який є інгібітором цього ізоферменту. Дослідження in vitro також показали, що аторвастатин є слабким інгібітором ізоферменту CYP3A4. Виводиться в основному через кишечник після печінкового та/або позапечінкового метаболізму (препарат не піддається вираженій кишково-печінковій рециркуляції). T1/2 - 14 год. T1/2 інгібуючої активності ГМГ-КоА-редуктази становить 20-30 год. Менше 2% від прийнятої внутрішньо дози визначається сечі. Не виводиться в ході гемодіалізу через інтенсивне зв'язування з білками плазми. Фармакокінетика в особливих клінічних випадках У жінок Cmax вище на 20%, AUC – нижче на 10%, ніж у чоловіків, що не має клінічного значення. У пацієнтів з алкогольним цирозом (клас В за шкалою Чайлд-П'ю) печінки Cmax у 16 разів, а AUC – в 11 разів вище за норму. Cmax та AUC у літніх пацієнтів (≥65 років) на 40% та 30% відповідно вище, ніж у пацієнтів молодого віку, однак це не впливає на ступінь зниження холестерину ЛПНЩ. Порушення функції нирок не впливає на концентрацію препарату в плазмі ступінь зниження холестерину ЛПНГ.ФармакодинамікаАторвастатин є селективним конкурентним інгібітором ГМГ-КоА-редуктази - ферменту, що перетворює 3-гідрокси-3-метилглутарил коензим А в мевалонову кислоту, що є попередником стеролів, включаючи холестерин. Тригліцериди (ТГ) і холестерин (Хс) включаються до складу ліпопротеїнів дуже низької щільності (ЛПДНЩ) при синтезі в печінці, надходять у плазму крові та транспортуються в периферичні тканини. Ліпопротеїни низької щільності (ЛПНЩ) утворюються з ЛПДНЩ у ході взаємодії з рецепторами ЛПНЩ. Дослідження показали, що підвищення концентрацій загального Хс, ЛПНГ та аполіпопротеїну В (апо-В) у плазмі крові сприяє розвитку атеросклерозу та входять до групи факторів ризику виникнення серцево-судинних захворювань, у той час як збільшення концентрації ліпопротеїнів високої щільності (ЛПВЩ) знижує ризик розвитку серцево-судинних захворювань Аторвастатин знижує концентрацію Хс та ліпопротеїнів у плазмі крові за рахунок пригнічення ГМГ-КоА-редуктази, синтезу холестерину в печінці та збільшення числа "печінкових" рецепторів ЛПНГ на поверхні клітин, що призводить до посилення захоплення та катаболізму ЛПНГ (за даними доклінічних досліджень). Аторвастатин знижує синтез та концентрацію Хс-ЛПНГ, загального Хс, апо-В у пацієнтів з гомозиготною та гетерозиготною сімейною гіперхолестеринемією, первинною гіперхолестеринемією та змішаною гіперліпідемією. Викликає також зниження концентрації холестерину-ЛПОНП та ТГ та підвищення концентрації холестерину-ЛПВЩ та аполіпопротеїну А-1 (апо-А). У пацієнтів з дисбеталіпопротеїнемією знижує концентрацію ліпопротеїнів проміжної щільності ХС-ЛПСШ. Аторвастатин у дозах 10 мг та 20 мг знижує концентрацію загального Хс на 29% та 33%, ЛПНГ – на 39% та 43%, апо-В – на 32% та 35% та ТГ – на 14% та 26% відповідно; викликає підвищення концентрації холестерину-ЛПЗЗ та апо-А. Аторвастатин у дозах 40 мг знижує концентрацію загального Хс на 37%, ЛПНГ – на 50%, апо-В – на 42% та ТГ – на 29%; викликає підвищення концентрації Хс-ЛПЗЗ та апо-А. Дозозалежно знижує концентрацію ЛПНГ у хворих на гомозиготну сімейну гіперхолестеринемію, резистентну до терапії іншими гіполіпідемічними засобами. Не надає канцерогенної та мутагенної дії. Терапевтичний ефект розвивається через 2 тижні після початку терапії, досягає максимуму через 4 тижні та зберігається протягом усього періоду лікування.Показання до застосуванняу поєднанні з гіпохолестеринемічною дієтою для зниження підвищених концентрацій загального Хс, Хс-ЛПНЩ, апо-В і ТГ та підвищення концентрації Хс-ЛПВЩ у хворих з первинною гіперхолестеринемією, гетерозиготною сімейною та несемейною гіперхолестеринемією та комбінованою (змішаною) гіперліпі класифікації Фредріксона), коли дієтотерапія та інші нефармакологічні методи лікування виявляються недостатньо ефективними; для зниження концентрації загального Хс та Хс-ЛПНГ у хворих з гомозиготною сімейною гіперхолестеринемією, коли дієтотерапія та інші нефармакологічні методи лікування виявляються недостатньо ефективними; первинна профілактика серцево-судинних ускладнень у пацієнтів без клінічних ознак ІХС, але які мають кілька факторів ризику її розвитку: вік старше 55 років, нікотинова залежність, артеріальна гіпертензія, цукровий діабет, ретинопатія, альбумінурія, низькі концентрації Хс-ЛПВП в плазмі , в т.ч. на фоні дисліпідемії; вторинна профілактика серцево-судинних ускладнень у пацієнтів з ІХС з метою зниження сумарного показника смертності, інфаркту міокарда, інсульту, повторної госпіталізації щодо стенокардії та необхідності реваскуляризації.Протипоказання до застосуваннязахворювання печінки на активній стадії або підвищення активності печінкових трансаміназ у плазмі крові (більш ніж у 3 рази порівняно з ВГН) неясного генезу; вагітність; період лактації; вік до 18 років (ефективність та безпека не встановлені); дефіцит лактази, непереносимість лактози, синдром глюкозо-галактозної мальабсорбції (оскільки у складі міститься лактоза); підвищена чутливість до аторвастатину та інших допоміжних компонентів препарату. З обережністю слід призначати препарат при зловживанні алкоголем, захворюваннях печінки в анамнезі, захворюваннях м'язової системи (в анамнезі від застосування інших представників групи інгібіторів ГМГ-КоА-редуктази), тяжких порушеннях електролітного балансу, ендокринних (гіпертиреоз) та метаболічних порушеннях, діабеті, тяжких гострих інфекціях (сепсис), неконтрольованій епілепсії, великих хірургічних втручаннях, травмах, агресивній ліпідзнижувальній терапії (аторвастатин у дозі 80 мг) при вторинній профілактиці інсульту у пацієнтів з геморагічним абонсультом.Вагітність та лактаціяПрепарат Туліп протипоказаний до застосування під час вагітності. Оскільки холестерин та речовини, що синтезуються з холестерину, важливі для розвитку плода, потенційний ризик інгібування ГМГ-КоА-редуктази перевищує користь від застосування препарату під час вагітності. У разі діагностування вагітності в процесі терапії препаратом Туліп®, його прийом слід припинити якнайшвидше, а пацієнтку необхідно попередити про потенційний ризик для плода. Препарат Туліп® можна застосовувати у жінок репродуктивного віку лише в тому випадку, якщо ймовірність вагітності у них дуже низька, а пацієнтка поінформована про можливий ризик для плода під час лікування. Жінки репродуктивного віку під час лікування препаратом Туліп повинні застосовувати надійні методи контрацепції. Аторвастатин виділяється з грудним молоком, тому протипоказаний до застосування у період грудного вигодовування. При необхідності застосування препарату Туліп® у період лактації грудне вигодовування слід припинити. Протипоказаний у дитячому та підлітковому віці до 18 років (ефективність та безпека не встановлені).Побічна діяЗа даними ВООЗ небажані ефекти класифіковані відповідно до їх частоти розвитку наступним чином: часто (більше 1/100, менше 1/10), нечасто (більше 1/1000, менше 1/100), рідко (більше 1/10 000, менше 1/1000) та дуже рідко (менше 1/10 000), включаючи окремі повідомлення; частота невідома - за наявними даними встановити частоту виникнення неможливо. З боку імунної системи: часто – алергічні реакції; дуже рідко – анафілаксія. З боку нервової системи: часто – головний біль; нечасто - запаморочення, порушення сну, включаючи безсоння та кошмарні сновидіння, астенічний синдром, слабкість, парестезія, гіпестезія, порушення смакової чутливості, втрата або зниження пам'яті; рідко – периферична невропатія. З боку органів чуття: нечасто - шум у вухах, нечіткість зору; рідко – порушення зору; дуже рідко – втрата слуху. З боку травної системи: часто – запор, метеоризм, диспепсія, нудота, діарея; нечасто – анорексія, блювання, панкреатит, гепатит, біль у животі, відрижка; рідко – холестатична жовтяниця (в т.ч. обструктивна); дуже рідко – печінкова недостатність. З боку кістково-м'язової системи: часто – міалгія, артралгія, припухлість суглобів, біль у суглобах, біль у спині, м'язовий спазм; нечасто – біль у м'язах шиї, м'язова слабкість; рідко – міопатія, міозит, рабдоміоліз, тендинопатія (іноді ускладнена розривом сухожилля); частота невідома – імуноопосередкована некротизуюча міопатія. З боку шкіри та підшкірних тканин: нечасто – кропив'янка, висипання на шкірі та свербіж, алопеція; рідко – ангіоневротичний набряк, бульозний висип, багатоформна ексудативна еритема (в т.ч. синдром Стівенса-Джонсона), токсичний епідермальний некроліз (синдром Лайєлла). З боку обміну речовин: часто – гіперглікемія; нечасто – гіпоглікемія. З боку системи кровотворення: нечасто – тромбоцитопенія. З боку дихальної системи: часто – назофарингіт, біль у горлі, носова кровотеча. Лабораторні показники: часто – підвищення активності сироваткової КФК, підвищення активності печінкових трансаміназ; нечасто – лейкоцитурія; частота невідома – підвищення концентрації глікозильованого гемоглобіну. Інші: нечасто – підвищена втома, порушення потенції, вторинна ниркова недостатність, підвищення температури тіла, біль у грудях, периферичні набряки, збільшення маси тіла; дуже рідко – гінекомастія, цукровий діабет. Є окремі повідомлення про розвиток атонічного фасціїту (зв'язок із застосуванням аторвастатину точно не встановлено); частота невідома – депресія, інтерстиціальне захворювання легень (особливо при тривалій терапії), сексуальна дисфункція.Взаємодія з лікарськими засобамиРизик міопатії під час лікування інгібіторами ГМГ-КоА-редуктази підвищується при одночасному застосуванні з циклоспорином, еритроміцином, кларитроміцином, імунодепресивними, протигрибковими препаратами (похідними азолу) внаслідок можливого підвищення концентрації аторвастатину у сироватці крові. При одночасному застосуванні з інгібіторами ВІЛ-протеаз – індинавір, ритонавір – збільшується ризик розвитку міопатії. Подібна взаємодія можлива при одночасному застосуванні аторвастатину з фібратами та нікотиновою кислотою у ліпідзнижуючих дозах (більше 1 г/добу). Інгібітори ізоферменту CYP3A4 Оскільки аторвастатин метаболізується за допомогою ізоферменту CYP3A4, спільне застосування препарату Туліп з інгібіторами цього ізоферменту може призводити до збільшення концентрації аторвастатину в плазмі. Ступінь взаємодії та ефект збільшення концентрації аторвастатину визначаються варіабельністю впливу на ізофермент CYP3A4. Інгібітори транспортного білка ОАТР1В1 Аторвастатин та його метаболіти є субстратами транспортного білка ОАТР1В1. Інгібітори ОАТР1В1 (наприклад, циклоспорин) можуть збільшувати біодоступність аторвастатину. Так, застосування аторвастатину в дозі 10 мг та циклоспорину в дозі 5.2 мг/кг/добу призводить до збільшення концентрації аторвастатину у плазмі крові у 7.7 рази. Еритроміцин/кларитроміцин При одночасному застосуванні аторвастатину 10 мг та еритроміцину (по 500 мг 4 рази на добу) або кларитроміцину (по 500 мг 2 рази на добу), які інгібують ізофермент цитохрому CYP3A4, спостерігається підвищення концентрації аторвастатину в плазмі крові (на 40% еритроміцином та на 56% – при застосуванні з кларитроміцином). Інгібітори протеаз Одночасне застосування аторвастатину з інгібіторами протеаз, відомими як інгібітори ізоферменту цитохрому CYP3A4, супроводжується збільшенням концентрації аторвастатину в плазмі крові (при одночасному застосуванні з еритроміцином – Cmax аторвастатину збільшується на 40%). Ділтіазем Спільне застосування аторвастатину в дозі 40 мг з дилтіаземом у дозі 240 мг призводить до збільшення концентрації аторвастатину в плазмі. Ціметідин Клінічно значущої взаємодії аторвастатину з циметидином не виявлено. Ітраконазол Одночасне застосування аторвастатину у дозах від 20 мг до 40 мг та ітраконазолу у дозі 200 мг призводить до 3-кратного збільшення значення AUC аторвастатину. Грейпфрутовий сік Оскільки грейпфрутовий сік містить один або більше компонентів, які пригнічують ізофермент CYP3A4, його надмірне вживання (більше 1.2 л на день протягом 5 днів) може спричинити збільшення концентрації аторвастатину в плазмі крові. Індуктори ізоферменту CYP3A4 Спільне застосування аторвастатину з індукторами ізоферменту СУРЗА4 (наприклад, ефавіренз або рифампіцин) може призвести до зниження концентрації аторвастатину в плазмі крові. Внаслідок двоїстого механізму взаємодії з рифампіцином (індуктором ізоферменту CYP3A4 та інгібітором транспортного білка гепатоцитів ОАТР1В1), не рекомендується одночасне застосування аторвастатину та рифампіцину, оскільки відстрочений прийом аторвастатину після прийому рифам. Антациди При одночасному застосуванні внутрішньо аторвастатину та суспензії, що містить магнію та алюмінію гідроксиди, концентрація аторвастатину в плазмі знижується приблизно на 35%, проте ступінь зниження концентрації Хс-ЛПНЩ при цьому не змінюється. Феназон Аторвастатин не впливає на фармакокінетику феназону, тому взаємодія з іншими препаратами, що метаболізуються тими самими ізоферментами, не очікується. Колестипол Гіполіпідемічний ефект комбінації з колестиполом перевищує такий для кожного препарату окремо, незважаючи на зниження концентрації аторвастатину на 25% при його одночасному застосуванні з колестиполом. Фузидова кислота Досліджень щодо взаємодії аторвастатину та фузидової кислоти не проводилося. Як і у випадку з іншими статинами, у постмаркетингових дослідженнях спільного застосування аторвастатину та фузидової кислоти повідомлялося про побічні дії на м'язи, включаючи рабдоміоліз. Механізм взаємодії невідомий. Такі пацієнти вимагають ретельного спостереження та, можливо, тимчасової відміни прийому аторвастатину. Колхіцін Хоча дослідження взаємодії аторвастатину та колхіцину не проводилися, повідомлялося про випадки міопатії при спільному застосуванні з колхіцином, і при одночасному призначенні аторвастатину та колхіцину слід дотримуватися обережності. Дігоксин При повторному застосуванні дигоксину та аторвастатину у дозі 10 мг Css дигоксину у плазмі крові не змінюються. Однак при застосуванні дигоксину в комбінації з аторвастатином у дозі 80 мг на добу концентрація дигоксину в плазмі збільшується приблизно на 20%. Пацієнтам, які приймають дигоксин у поєднанні з аторвастатином, потрібен контроль концентрації дигоксину у плазмі. Азітроміцин При одночасному застосуванні аторвастатину в дозі 10 мг 1 раз на добу та азитроміцину в дозі 500 мг 1 раз на добу концентрація аторвастатину в плазмі крові не змінюється. Пероральні контрацептиви При одночасному застосуванні аторвастатину та перорального контрацептиву, що містить норетистерон та етинілестрадіол, спостерігається значне підвищення AUC норетистерону та етинілестрадіолу приблизно на 30% та 20%, відповідно, що слід враховувати при виборі перорального контрацептиву. Терфенадін Аторвастатин при одночасному застосуванні з терфенадином не має клінічно значущого впливу на фармакокінетику терфенадину. Варфарін У пацієнтів, які тривало приймають варфарин, аторвастатин у дозі 80 мг на добу дещо скорочує протромбіновий час у перші дні спільного застосування. Цей ефект зникає після 15 днів одночасного застосування цих препаратів. Хоча про випадки клінічно значущих змін антикоагулянтного ефекту повідомлялося дуже рідко, слід визначати протромбіновий час у пацієнтів, які приймають кумаринові антикоагулянти, перед початком та досить часто на початку лікування аторвастатином, щоб переконатися у відсутності значних змін протромбінового часу. Як тільки буде зареєстровано стабільний протромбіновий час, він може перевірятися з інтервалами, звичайними для пацієнтів, які приймають кумаринові антикоагулянти. У разі зміни дози або припинення лікування ці заходи слід повторити.Не спостерігалося зв'язку між застосуванням аторвастатину та кровотечами або зміною протромбінового часу у пацієнтів, які не приймають антикоагулянти. Амлодипін При одночасному застосуванні аторвастатину у дозі 80 мг та амлодипіну у дозі 10 мг фармакокінетика аторвастатину у рівноважному стані не змінюється. Інші гіполіпідемічні препарати При одночасному застосуванні аторвастатину з іншими гіполіпідемічними препаратами (наприклад, езетимиб, гемфіброзил, похідне фіброєвої кислоти) у ліпід-знижувальних дозах збільшується ризик розвитку рабдоміолізу. Інша супутня терапія При сумісному застосуванні аторвастатину з гіпотензивними засобами та естрогенами (як замісна терапія) – клінічно значущої взаємодії не виявлено.Спосіб застосування та дозиПеред початком застосування препарату Туліп® пацієнту необхідно рекомендувати стандартну гіпохолестеринемічну дієту, яку він повинен продовжувати дотримуватись протягом усього періоду терапії препаратом. Препарат приймають внутрішньо незалежно від часу їди. Доза препарату Туліп® варіює в межах від 10 мг до 80 мг на добу, і підбирається з урахуванням вихідних концентрацій Хс-ЛПНГ, мети терапії та індивідуальної терапевтичної відповіді на терапію. Для більшості пацієнтів початкова доза становить 10 мг 1 раз на добу. На початку лікування, через 2-4 тижні терапії та/або після підвищення дози препарату Туліп® необхідно контролювати концентрації ліпідів у плазмі крові та за необхідності коригувати дозу препарату. Максимальна добова доза – 80 мг на добу. Первинна (гетерозиготна спадкова та полігенна) гіперхолестеринемія (тип IIа) та змішана гіперліпідемія (тип IIb) У більшості випадків буває достатньо застосування препарату Туліп у дозі 10 мг 1 раз на добу (можливе застосування аторвастатину у таблетках по 10 та 20 мг). При необхідності можливе поступове збільшення дози до 80 мг (2 таб. по 40 мг) залежно від реакції пацієнта з інтервалом 2-4 тижні, оскільки терапевтичний ефект відзначається через 2 тижні, а максимальний терапевтичний ефект – через 4 тижні. При тривалому лікуванні цей ефект зберігається. Гомозиготна спадкова гіперхолестеринемія Препарат Туліп® у більшості випадків застосовують у дозі 80 мг (2 таб. по 40 мг) 1 раз на добу. Попередження розвитку серцево-судинних захворювань Туліп® застосовують у дозі 10 мг 1 раз на добу. Якщо не досягнуто оптимальної концентрації ЛПНЩ у плазмі, можливе збільшення дози препарату до 80 мг на добу залежно від реакції пацієнта з інтервалом 2-4 тижні. Корекція дози препарату Туліп у пацієнтів з порушенням функції нирок та у пацієнтів похилого віку не потрібна. У пацієнтів з порушенням функції печінки сповільнюється виведення аторвастатину з організму, тому рекомендується застосовувати його з обережністю при постійному контролі активності печінкових трансаміназ: ACT та АЛТ. Якщо підвищення активності ACT або АЛТ, що спостерігається, більш ніж у 3 рази в порівнянні з ВГН зберігається, рекомендується зниження дози або відміна препарату Туліп®.ПередозуванняЛікування: специфічного антидоту для лікування передозування немає. У разі передозування слід проводити симптоматичне лікування. Гемодіаліз не ефективний (оскільки препарат значно пов'язується з білками плазми).Запобіжні заходи та особливі вказівкиВплив на печінку Як і при застосуванні інших інгібіторів ГМГ-Ко-редуктази (статинів), при терапії препаратом Туліп® можливе помірне (більш ніж у 3 рази порівняно з ВГН) підвищення сироваткової активності печінкових трансаміназ: ACT та АЛТ. До початку терапії, через 6 тижнів та 12 тижнів після початку прийому препарату Туліп або після збільшення його дози, необхідно контролювати показники функції печінки (ACT, АЛТ). Функцію печінки слід контролювати також у разі появи клінічних ознак ураження печінки. У разі підвищення активності ACT та АЛТ, їх активність слід контролювати доти, доки вона не нормалізується. Туліп® слід застосовувати з обережністю у пацієнтів, які зловживають алкоголем та/або мають захворювання печінки в анамнезі. Захворювання печінки в активній стадії або підвищення активності печінкових трансаміназ плазми неясного генезу є протипоказанням для застосування препарату Туліп®. Профілактика інсульту за допомогою інтенсивної ліпідзнижувальної терапії (SPARCL) При ретроспективному аналізі різних підвидів інсульту у осіб, які не страждають на ІХС, які недавно перенесли інсульт або транзиторну ішемічну атаку (ТІА), був виявлений більш високий ризик геморагічного інсульту у пацієнтів, які приймають аторвастатин у дозі 80 мг порівняно з плацебо. Особливо високий ризик відзначався у пацієнтів, які перенесли геморагічний інсульт або лакунарний інфаркт на момент початку дослідження. Для пацієнтів, які перенесли геморагічний інсульт або лакунарний інфаркт і приймають аторвастатин у дозі 80 мг, співвідношення ризик/користування є неоднозначним, і слід уважно оцінювати потенційний ризик розвитку геморагічного інсульту перед початком лікування. Дія на скелетні м'язи При застосуванні препарату Туліп можливий розвиток міалгії. Діагноз міопатії (біль і слабкість у м'язах у поєднанні з підвищенням активності КФК більш ніж у 10 разів порівняно з ВГН) можна припустити у пацієнтів з дифузною міалгією, хворобливістю або слабкістю м'язів та/або вираженим підвищенням активності КФК. Терапію препаратом Туліп слід припинити у разі вираженого підвищення активності КФК або за наявності підтвердженої або передбачуваної міопатії. При застосуванні інших інгібіторів ГМГ-Ко-редуктази (статинів) можливе підвищення ризику міопатії при одночасному застосуванні з циклоспорином, фібратами, еритроміцином, нікотиновою кислотою у ліпід-знижувальних дозах (більше 1 г/добу) або протигрибкових препаратів групи азолів. Застосовуючи препарат Туліп® у комбінації з фібратами, еритроміцином, імунодепресантами, протигрибковими препаратами групи азолів або нікотиновою кислотою у ліпідзнижуючих дозах (більше 1 г/добу), необхідно зважити очікувану користь та ризик лікування Туліп®. Дуже рідко повідомлялося про випадки імуноопосередкованої некротизуючої міопатії під час або після лікування статинами, включаючи аторвастатин. Імуноопосередкована некротизуюча міопатія клінічно характеризується м'язовою слабкістю у верхніх відділах кінцівок та підвищенням концентрації КФК плазми крові, що зберігаються незважаючи на припинення лікування статинами. У разі потреби комбінованої терапії слід розглянути можливість застосування зазначених препаратів у нижчих початкових та підтримуючих дозах. Рекомендується періодичний контроль за активністю КФК. Спільне застосування аторвастатину та фузидової кислоти не рекомендується, отже слід розглянути тимчасове припинення терапії аторвастатином під час застосування фузидової кислоти. Пацієнтів слід попередити про те, що необхідно негайно звернутися до лікаря при появі незрозумілого болю або м'язової слабкості, особливо, якщо вони супроводжуються нездужанням або лихоманкою. При застосуванні препарату Туліп, як і інших інгібіторів ГМГ-Ко-редуктази (статинів), описані рідкісні випадки рабдоміолізу з гострою нирковою недостатністю, зумовленою міоглобінурією. При появі симптомів можливої міопатії або наявності фактора ризику розвитку ниркової недостатності на тлі рабдоміолізу (наприклад, тяжка гостра інфекція, артеріальна гіпотензія, широке хірургічне втручання, травми, серйозні метаболічні, електролітні та ендокринні порушення та неконтрольовані судоми). скасувати. Інтерстиційна хвороба легень Повідомлялося про рідкісні випадки розвитку інтерстиціальної хвороби легень при застосуванні деяких статинів, особливо при тривалій терапії. Клінічні прояви включають задишку, непродуктивний кашель та погіршення загального здоров'я (підвищена стомлюваність, зниження маси тіла та лихоманка). У разі підозри на інтерстиціальну хворобу легенів, що розвивалася, лікування статинами слід припинити. Цукровий діабет Дані деяких досліджень свідчать про те, що застосування статинів як класу може призводити до підвищення концентрації глюкози в крові, а у деяких пацієнтів з підвищеним ризиком розвитку діабету в майбутньому може викликати гіперглікемію, при якій необхідна стандартна антидіабетична терапія. Однак такий ризик є незначним у порівнянні зі зниженням судинного ризику при прийомі статинів, і, отже, не може бути причиною скасування лікування статинами. Пацієнти в групі ризику (з концентрацією глюкози натще 5.6-6.9 ммоль/л, ІМТ >30 кг/м2, підвищеним рівнем тригліцеридів, підвищеним АТ) повинні бути під контролем як клінічним, так і біохімічним відповідно до національних стандартів надання медичної допомоги . Вплив на здатність до керування автотранспортом та управління механізмами У період лікування препаратом Туліп® необхідно дотримуватись обережності при керуванні транспортними засобами та зайнятті іншими потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Активна речовина: аторвастатин (у формі аторвастатину кальцію) – 20 мг; Допоміжні речовини: лактози моногідрат - 34.8 мг, кроскармеллозу натрію - 19.2 мг, гіпоролозу - 2 мг, полісорбат 80 - 2.6 мг, магнію оксид важкий - 26 мг, кремнію діоксид колоїдний - 1.2 мг, магнію стеарат - 1 250 мг; Склад оболонки: гіпромелоза – 2.976 мг, гіпоролоза – 0.744 мг, титану діоксид (Е171) – 1.368 мг, макрогол 6000 – 0.6 мг, тальк – 0.3 мг, заліза оксид жовтий (Е172) – 0.01. По 10 таблеток поміщають у блістер А1/А1 фольги. По 3, 6 або 9 блістерів поміщають у картонну пачку разом із інструкцією з медичного застосування.Опис лікарської формиТаблетки, покриті плівковою оболонкою світло-жовтого кольору, круглі, двоопуклі, з гравіюванням "HLA 20" на одній стороні; вид на зламі: таблетки білого кольору.Фармакотерапевтична групаГіполіпідемічний препарат.ФармакокінетикаВсмоктування та розподіл Абсорбція висока. Cmax у плазмі після прийому внутрішньо досягається через 1-2 год. Прийом їжі дещо знижує швидкість і ступінь абсорбції препарату (на 25% і 9% відповідно), проте зниження Хс-ЛПНГ подібне до такого при застосуванні аторвастатину без одночасного прийому їжі. Після прийому внутрішньо аторвастатину у вечірній час концентрація його в плазмі нижче (Cmax і AUC приблизно на 30%), ніж після прийому в ранковий час, тоді як зниження концентрації Хс-ЛПНГ не залежить від часу доби прийому препарату. Виявлено лінійну залежність між ступенем всмоктування та дозою препарату. Біодоступність становить 12-14%, системна біодоступність інгібуючої активності щодо ГМГ-КоА-редуктази – близько 30%. Низька системна біодоступність обумовлена пресистемним метаболізмом у шлунково-кишковому тракті та ефектом "першого проходження" через печінку. Середній Vd – 381 л, зв'язування з білками плазми крові – 98%. Відношення концентрації аторвастатину в еритроцитах/плазмі становить близько 0.25, що вказує на погане проникнення аторвастатину в еритроцити. Метаболізм та виведення Аторвастатин метаболізується переважно у печінці під дією ізоферментів CYP3A4, CYP3A5 та CYP3A7 з утворенням фармакологічно активних метаболітів (орто- та парагідроксильованих похідних, продуктів бета-окислення). In vitro орто- та парагідроксильовані метаболіти мають інгібуючу дію на ГМГ-КоА-редуктазу, порівнянну з дією аторвастатину. Інгібуючий ефект препарату щодо ГМГ-КоА-редуктази приблизно на 70% визначається активністю циркулюючих метаболітів, який зберігається приблизно протягом 20-30 годин завдяки їх наявності. Результати досліджень in vitro дають підставу припустити, що ізофермент печінки CYP3A4 відіграє важливу роль у метаболізмі аторвастатину. Це підтверджується підвищенням концентрації аторвастатину в плазмі при одночасному прийомі еритроміцину, який є інгібітором цього ізоферменту. Дослідження in vitro також показали, що аторвастатин є слабким інгібітором ізоферменту CYP3A4. Виводиться в основному через кишечник після печінкового та/або позапечінкового метаболізму (препарат не піддається вираженій кишково-печінковій рециркуляції). T1/2 - 14 год. T1/2 інгібуючої активності ГМГ-КоА-редуктази становить 20-30 год. Менше 2% від прийнятої внутрішньо дози визначається сечі. Не виводиться в ході гемодіалізу через інтенсивне зв'язування з білками плазми. Фармакокінетика в особливих клінічних випадках У жінок Cmax вище на 20%, AUC – нижче на 10%, ніж у чоловіків, що не має клінічного значення. У пацієнтів з алкогольним цирозом (клас В за шкалою Чайлд-П'ю) печінки Cmax у 16 разів, а AUC – в 11 разів вище за норму. Cmax та AUC у літніх пацієнтів (≥65 років) на 40% та 30% відповідно вище, ніж у пацієнтів молодого віку, однак це не впливає на ступінь зниження холестерину ЛПНЩ. Порушення функції нирок не впливає на концентрацію препарату в плазмі ступінь зниження холестерину ЛПНГ.ФармакодинамікаАторвастатин є селективним конкурентним інгібітором ГМГ-КоА-редуктази - ферменту, що перетворює 3-гідрокси-3-метилглутарил коензим А в мевалонову кислоту, що є попередником стеролів, включаючи холестерин. Тригліцериди (ТГ) і холестерин (Хс) включаються до складу ліпопротеїнів дуже низької щільності (ЛПДНЩ) при синтезі в печінці, надходять у плазму крові та транспортуються в периферичні тканини. Ліпопротеїни низької щільності (ЛПНЩ) утворюються з ЛПДНЩ у ході взаємодії з рецепторами ЛПНЩ. Дослідження показали, що підвищення концентрацій загального Хс, ЛПНГ та аполіпопротеїну В (апо-В) у плазмі крові сприяє розвитку атеросклерозу та входять до групи факторів ризику виникнення серцево-судинних захворювань, у той час як збільшення концентрації ліпопротеїнів високої щільності (ЛПВЩ) знижує ризик розвитку серцево-судинних захворювань Аторвастатин знижує концентрацію Хс та ліпопротеїнів у плазмі крові за рахунок пригнічення ГМГ-КоА-редуктази, синтезу холестерину в печінці та збільшення числа "печінкових" рецепторів ЛПНГ на поверхні клітин, що призводить до посилення захоплення та катаболізму ЛПНГ (за даними доклінічних досліджень). Аторвастатин знижує синтез та концентрацію Хс-ЛПНГ, загального Хс, апо-В у пацієнтів з гомозиготною та гетерозиготною сімейною гіперхолестеринемією, первинною гіперхолестеринемією та змішаною гіперліпідемією. Викликає також зниження концентрації холестерину-ЛПОНП та ТГ та підвищення концентрації холестерину-ЛПВЩ та аполіпопротеїну А-1 (апо-А). У пацієнтів з дисбеталіпопротеїнемією знижує концентрацію ліпопротеїнів проміжної щільності ХС-ЛПСШ. Аторвастатин у дозах 10 мг та 20 мг знижує концентрацію загального Хс на 29% та 33%, ЛПНГ – на 39% та 43%, апо-В – на 32% та 35% та ТГ – на 14% та 26% відповідно; викликає підвищення концентрації холестерину-ЛПЗЗ та апо-А. Аторвастатин у дозах 40 мг знижує концентрацію загального Хс на 37%, ЛПНГ – на 50%, апо-В – на 42% та ТГ – на 29%; викликає підвищення концентрації Хс-ЛПЗЗ та апо-А. Дозозалежно знижує концентрацію ЛПНГ у хворих на гомозиготну сімейну гіперхолестеринемію, резистентну до терапії іншими гіполіпідемічними засобами. Не надає канцерогенної та мутагенної дії. Терапевтичний ефект розвивається через 2 тижні після початку терапії, досягає максимуму через 4 тижні та зберігається протягом усього періоду лікування.Показання до застосуванняу поєднанні з гіпохолестеринемічною дієтою для зниження підвищених концентрацій загального Хс, Хс-ЛПНЩ, апо-В і ТГ та підвищення концентрації Хс-ЛПВЩ у хворих з первинною гіперхолестеринемією, гетерозиготною сімейною та несемейною гіперхолестеринемією та комбінованою (змішаною) гіперліпі класифікації Фредріксона), коли дієтотерапія та інші нефармакологічні методи лікування виявляються недостатньо ефективними; для зниження концентрації загального Хс та Хс-ЛПНГ у хворих з гомозиготною сімейною гіперхолестеринемією, коли дієтотерапія та інші нефармакологічні методи лікування виявляються недостатньо ефективними; первинна профілактика серцево-судинних ускладнень у пацієнтів без клінічних ознак ІХС, але які мають кілька факторів ризику її розвитку: вік старше 55 років, нікотинова залежність, артеріальна гіпертензія, цукровий діабет, ретинопатія, альбумінурія, низькі концентрації Хс-ЛПВП в плазмі , в т.ч. на фоні дисліпідемії; вторинна профілактика серцево-судинних ускладнень у пацієнтів з ІХС з метою зниження сумарного показника смертності, інфаркту міокарда, інсульту, повторної госпіталізації щодо стенокардії та необхідності реваскуляризації.Протипоказання до застосуваннязахворювання печінки на активній стадії або підвищення активності печінкових трансаміназ у плазмі крові (більш ніж у 3 рази порівняно з ВГН) неясного генезу; вагітність; період лактації; вік до 18 років (ефективність та безпека не встановлені); дефіцит лактази, непереносимість лактози, синдром глюкозо-галактозної мальабсорбції (оскільки у складі міститься лактоза); підвищена чутливість до аторвастатину та інших допоміжних компонентів препарату. З обережністю слід призначати препарат при зловживанні алкоголем, захворюваннях печінки в анамнезі, захворюваннях м'язової системи (в анамнезі від застосування інших представників групи інгібіторів ГМГ-КоА-редуктази), тяжких порушеннях електролітного балансу, ендокринних (гіпертиреоз) та метаболічних порушеннях, діабеті, тяжких гострих інфекціях (сепсис), неконтрольованій епілепсії, великих хірургічних втручаннях, травмах, агресивній ліпідзнижувальній терапії (аторвастатин у дозі 80 мг) при вторинній профілактиці інсульту у пацієнтів з геморагічним абонсультом.Вагітність та лактаціяПрепарат Туліп протипоказаний до застосування під час вагітності. Оскільки холестерин та речовини, що синтезуються з холестерину, важливі для розвитку плода, потенційний ризик інгібування ГМГ-КоА-редуктази перевищує користь від застосування препарату під час вагітності. У разі діагностування вагітності в процесі терапії препаратом Туліп®, його прийом слід припинити якнайшвидше, а пацієнтку необхідно попередити про потенційний ризик для плода. Препарат Туліп® можна застосовувати у жінок репродуктивного віку лише в тому випадку, якщо ймовірність вагітності у них дуже низька, а пацієнтка поінформована про можливий ризик для плода під час лікування. Жінки репродуктивного віку під час лікування препаратом Туліп повинні застосовувати надійні методи контрацепції. Аторвастатин виділяється з грудним молоком, тому протипоказаний до застосування у період грудного вигодовування. При необхідності застосування препарату Туліп® у період лактації грудне вигодовування слід припинити. Протипоказаний у дитячому та підлітковому віці до 18 років (ефективність та безпека не встановлені).Побічна діяЗа даними ВООЗ небажані ефекти класифіковані відповідно до їх частоти розвитку наступним чином: часто (більше 1/100, менше 1/10), нечасто (більше 1/1000, менше 1/100), рідко (більше 1/10 000, менше 1/1000) та дуже рідко (менше 1/10 000), включаючи окремі повідомлення; частота невідома - за наявними даними встановити частоту виникнення неможливо. З боку імунної системи: часто – алергічні реакції; дуже рідко – анафілаксія. З боку нервової системи: часто – головний біль; нечасто - запаморочення, порушення сну, включаючи безсоння та кошмарні сновидіння, астенічний синдром, слабкість, парестезія, гіпестезія, порушення смакової чутливості, втрата або зниження пам'яті; рідко – периферична невропатія. З боку органів чуття: нечасто - шум у вухах, нечіткість зору; рідко – порушення зору; дуже рідко – втрата слуху. З боку травної системи: часто – запор, метеоризм, диспепсія, нудота, діарея; нечасто – анорексія, блювання, панкреатит, гепатит, біль у животі, відрижка; рідко – холестатична жовтяниця (в т.ч. обструктивна); дуже рідко – печінкова недостатність. З боку кістково-м'язової системи: часто – міалгія, артралгія, припухлість суглобів, біль у суглобах, біль у спині, м'язовий спазм; нечасто – біль у м'язах шиї, м'язова слабкість; рідко – міопатія, міозит, рабдоміоліз, тендинопатія (іноді ускладнена розривом сухожилля); частота невідома – імуноопосередкована некротизуюча міопатія. З боку шкіри та підшкірних тканин: нечасто – кропив'янка, висипання на шкірі та свербіж, алопеція; рідко – ангіоневротичний набряк, бульозний висип, багатоформна ексудативна еритема (в т.ч. синдром Стівенса-Джонсона), токсичний епідермальний некроліз (синдром Лайєлла). З боку обміну речовин: часто – гіперглікемія; нечасто – гіпоглікемія. З боку системи кровотворення: нечасто – тромбоцитопенія. З боку дихальної системи: часто – назофарингіт, біль у горлі, носова кровотеча. Лабораторні показники: часто – підвищення активності сироваткової КФК, підвищення активності печінкових трансаміназ; нечасто – лейкоцитурія; частота невідома – підвищення концентрації глікозильованого гемоглобіну. Інші: нечасто – підвищена втома, порушення потенції, вторинна ниркова недостатність, підвищення температури тіла, біль у грудях, периферичні набряки, збільшення маси тіла; дуже рідко – гінекомастія, цукровий діабет. Є окремі повідомлення про розвиток атонічного фасціїту (зв'язок із застосуванням аторвастатину точно не встановлено); частота невідома – депресія, інтерстиціальне захворювання легень (особливо при тривалій терапії), сексуальна дисфункція.Взаємодія з лікарськими засобамиРизик міопатії під час лікування інгібіторами ГМГ-КоА-редуктази підвищується при одночасному застосуванні з циклоспорином, еритроміцином, кларитроміцином, імунодепресивними, протигрибковими препаратами (похідними азолу) внаслідок можливого підвищення концентрації аторвастатину у сироватці крові. При одночасному застосуванні з інгібіторами ВІЛ-протеаз – індинавір, ритонавір – збільшується ризик розвитку міопатії. Подібна взаємодія можлива при одночасному застосуванні аторвастатину з фібратами та нікотиновою кислотою у ліпідзнижуючих дозах (більше 1 г/добу). Інгібітори ізоферменту CYP3A4 Оскільки аторвастатин метаболізується за допомогою ізоферменту CYP3A4, спільне застосування препарату Туліп з інгібіторами цього ізоферменту може призводити до збільшення концентрації аторвастатину в плазмі. Ступінь взаємодії та ефект збільшення концентрації аторвастатину визначаються варіабельністю впливу на ізофермент CYP3A4. Інгібітори транспортного білка ОАТР1В1 Аторвастатин та його метаболіти є субстратами транспортного білка ОАТР1В1. Інгібітори ОАТР1В1 (наприклад, циклоспорин) можуть збільшувати біодоступність аторвастатину. Так, застосування аторвастатину в дозі 10 мг та циклоспорину в дозі 5.2 мг/кг/добу призводить до збільшення концентрації аторвастатину у плазмі крові у 7.7 рази. Еритроміцин/кларитроміцин При одночасному застосуванні аторвастатину 10 мг та еритроміцину (по 500 мг 4 рази на добу) або кларитроміцину (по 500 мг 2 рази на добу), які інгібують ізофермент цитохрому CYP3A4, спостерігається підвищення концентрації аторвастатину в плазмі крові (на 40% еритроміцином та на 56% – при застосуванні з кларитроміцином). Інгібітори протеаз Одночасне застосування аторвастатину з інгібіторами протеаз, відомими як інгібітори ізоферменту цитохрому CYP3A4, супроводжується збільшенням концентрації аторвастатину в плазмі крові (при одночасному застосуванні з еритроміцином – Cmax аторвастатину збільшується на 40%). Ділтіазем Спільне застосування аторвастатину в дозі 40 мг з дилтіаземом у дозі 240 мг призводить до збільшення концентрації аторвастатину в плазмі. Ціметідин Клінічно значущої взаємодії аторвастатину з циметидином не виявлено. Ітраконазол Одночасне застосування аторвастатину у дозах від 20 мг до 40 мг та ітраконазолу у дозі 200 мг призводить до 3-кратного збільшення значення AUC аторвастатину. Грейпфрутовий сік Оскільки грейпфрутовий сік містить один або більше компонентів, які пригнічують ізофермент CYP3A4, його надмірне вживання (більше 1.2 л на день протягом 5 днів) може спричинити збільшення концентрації аторвастатину в плазмі крові. Індуктори ізоферменту CYP3A4 Спільне застосування аторвастатину з індукторами ізоферменту СУРЗА4 (наприклад, ефавіренз або рифампіцин) може призвести до зниження концентрації аторвастатину в плазмі крові. Внаслідок двоїстого механізму взаємодії з рифампіцином (індуктором ізоферменту CYP3A4 та інгібітором транспортного білка гепатоцитів ОАТР1В1), не рекомендується одночасне застосування аторвастатину та рифампіцину, оскільки відстрочений прийом аторвастатину після прийому рифам. Антациди При одночасному застосуванні внутрішньо аторвастатину та суспензії, що містить магнію та алюмінію гідроксиди, концентрація аторвастатину в плазмі знижується приблизно на 35%, проте ступінь зниження концентрації Хс-ЛПНЩ при цьому не змінюється. Феназон Аторвастатин не впливає на фармакокінетику феназону, тому взаємодія з іншими препаратами, що метаболізуються тими самими ізоферментами, не очікується. Колестипол Гіполіпідемічний ефект комбінації з колестиполом перевищує такий для кожного препарату окремо, незважаючи на зниження концентрації аторвастатину на 25% при його одночасному застосуванні з колестиполом. Фузидова кислота Досліджень щодо взаємодії аторвастатину та фузидової кислоти не проводилося. Як і у випадку з іншими статинами, у постмаркетингових дослідженнях спільного застосування аторвастатину та фузидової кислоти повідомлялося про побічні дії на м'язи, включаючи рабдоміоліз. Механізм взаємодії невідомий. Такі пацієнти вимагають ретельного спостереження та, можливо, тимчасової відміни прийому аторвастатину. Колхіцін Хоча дослідження взаємодії аторвастатину та колхіцину не проводилися, повідомлялося про випадки міопатії при спільному застосуванні з колхіцином, і при одночасному призначенні аторвастатину та колхіцину слід дотримуватися обережності. Дігоксин При повторному застосуванні дигоксину та аторвастатину у дозі 10 мг Css дигоксину у плазмі крові не змінюються. Однак при застосуванні дигоксину в комбінації з аторвастатином у дозі 80 мг на добу концентрація дигоксину в плазмі збільшується приблизно на 20%. Пацієнтам, які приймають дигоксин у поєднанні з аторвастатином, потрібен контроль концентрації дигоксину у плазмі. Азітроміцин При одночасному застосуванні аторвастатину в дозі 10 мг 1 раз на добу та азитроміцину в дозі 500 мг 1 раз на добу концентрація аторвастатину в плазмі крові не змінюється. Пероральні контрацептиви При одночасному застосуванні аторвастатину та перорального контрацептиву, що містить норетистерон та етинілестрадіол, спостерігається значне підвищення AUC норетистерону та етинілестрадіолу приблизно на 30% та 20%, відповідно, що слід враховувати при виборі перорального контрацептиву. Терфенадін Аторвастатин при одночасному застосуванні з терфенадином не має клінічно значущого впливу на фармакокінетику терфенадину. Варфарін У пацієнтів, які тривало приймають варфарин, аторвастатин у дозі 80 мг на добу дещо скорочує протромбіновий час у перші дні спільного застосування. Цей ефект зникає після 15 днів одночасного застосування цих препаратів. Хоча про випадки клінічно значущих змін антикоагулянтного ефекту повідомлялося дуже рідко, слід визначати протромбіновий час у пацієнтів, які приймають кумаринові антикоагулянти, перед початком та досить часто на початку лікування аторвастатином, щоб переконатися у відсутності значних змін протромбінового часу. Як тільки буде зареєстровано стабільний протромбіновий час, він може перевірятися з інтервалами, звичайними для пацієнтів, які приймають кумаринові антикоагулянти. У разі зміни дози або припинення лікування ці заходи слід повторити.Не спостерігалося зв'язку між застосуванням аторвастатину та кровотечами або зміною протромбінового часу у пацієнтів, які не приймають антикоагулянти. Амлодипін При одночасному застосуванні аторвастатину у дозі 80 мг та амлодипіну у дозі 10 мг фармакокінетика аторвастатину у рівноважному стані не змінюється. Інші гіполіпідемічні препарати При одночасному застосуванні аторвастатину з іншими гіполіпідемічними препаратами (наприклад, езетимиб, гемфіброзил, похідне фіброєвої кислоти) у ліпід-знижувальних дозах збільшується ризик розвитку рабдоміолізу. Інша супутня терапія При сумісному застосуванні аторвастатину з гіпотензивними засобами та естрогенами (як замісна терапія) – клінічно значущої взаємодії не виявлено.Спосіб застосування та дозиПеред початком застосування препарату Туліп® пацієнту необхідно рекомендувати стандартну гіпохолестеринемічну дієту, яку він повинен продовжувати дотримуватись протягом усього періоду терапії препаратом. Препарат приймають внутрішньо незалежно від часу їди. Доза препарату Туліп® варіює в межах від 10 мг до 80 мг на добу, і підбирається з урахуванням вихідних концентрацій Хс-ЛПНГ, мети терапії та індивідуальної терапевтичної відповіді на терапію. Для більшості пацієнтів початкова доза становить 10 мг 1 раз на добу. На початку лікування, через 2-4 тижні терапії та/або після підвищення дози препарату Туліп® необхідно контролювати концентрації ліпідів у плазмі крові та за необхідності коригувати дозу препарату. Максимальна добова доза – 80 мг на добу. Первинна (гетерозиготна спадкова та полігенна) гіперхолестеринемія (тип IIа) та змішана гіперліпідемія (тип IIb) У більшості випадків буває достатньо застосування препарату Туліп у дозі 10 мг 1 раз на добу (можливе застосування аторвастатину у таблетках по 10 та 20 мг). При необхідності можливе поступове збільшення дози до 80 мг (2 таб. по 40 мг) залежно від реакції пацієнта з інтервалом 2-4 тижні, оскільки терапевтичний ефект відзначається через 2 тижні, а максимальний терапевтичний ефект – через 4 тижні. При тривалому лікуванні цей ефект зберігається. Гомозиготна спадкова гіперхолестеринемія Препарат Туліп® у більшості випадків застосовують у дозі 80 мг (2 таб. по 40 мг) 1 раз на добу. Попередження розвитку серцево-судинних захворювань Туліп® застосовують у дозі 10 мг 1 раз на добу. Якщо не досягнуто оптимальної концентрації ЛПНЩ у плазмі, можливе збільшення дози препарату до 80 мг на добу залежно від реакції пацієнта з інтервалом 2-4 тижні. Корекція дози препарату Туліп у пацієнтів з порушенням функції нирок та у пацієнтів похилого віку не потрібна. У пацієнтів з порушенням функції печінки сповільнюється виведення аторвастатину з організму, тому рекомендується застосовувати його з обережністю при постійному контролі активності печінкових трансаміназ: ACT та АЛТ. Якщо підвищення активності ACT або АЛТ, що спостерігається, більш ніж у 3 рази в порівнянні з ВГН зберігається, рекомендується зниження дози або відміна препарату Туліп®.ПередозуванняЛікування: специфічного антидоту для лікування передозування немає. У разі передозування слід проводити симптоматичне лікування. Гемодіаліз не ефективний (оскільки препарат значно пов'язується з білками плазми).Запобіжні заходи та особливі вказівкиВплив на печінку Як і при застосуванні інших інгібіторів ГМГ-Ко-редуктази (статинів), при терапії препаратом Туліп® можливе помірне (більш ніж у 3 рази порівняно з ВГН) підвищення сироваткової активності печінкових трансаміназ: ACT та АЛТ. До початку терапії, через 6 тижнів та 12 тижнів після початку прийому препарату Туліп або після збільшення його дози, необхідно контролювати показники функції печінки (ACT, АЛТ). Функцію печінки слід контролювати також у разі появи клінічних ознак ураження печінки. У разі підвищення активності ACT та АЛТ, їх активність слід контролювати доти, доки вона не нормалізується. Туліп® слід застосовувати з обережністю у пацієнтів, які зловживають алкоголем та/або мають захворювання печінки в анамнезі. Захворювання печінки в активній стадії або підвищення активності печінкових трансаміназ плазми неясного генезу є протипоказанням для застосування препарату Туліп®. Профілактика інсульту за допомогою інтенсивної ліпідзнижувальної терапії (SPARCL) При ретроспективному аналізі різних підвидів інсульту у осіб, які не страждають на ІХС, які недавно перенесли інсульт або транзиторну ішемічну атаку (ТІА), був виявлений більш високий ризик геморагічного інсульту у пацієнтів, які приймають аторвастатин у дозі 80 мг порівняно з плацебо. Особливо високий ризик відзначався у пацієнтів, які перенесли геморагічний інсульт або лакунарний інфаркт на момент початку дослідження. Для пацієнтів, які перенесли геморагічний інсульт або лакунарний інфаркт і приймають аторвастатин у дозі 80 мг, співвідношення ризик/користування є неоднозначним, і слід уважно оцінювати потенційний ризик розвитку геморагічного інсульту перед початком лікування. Дія на скелетні м'язи При застосуванні препарату Туліп можливий розвиток міалгії. Діагноз міопатії (біль і слабкість у м'язах у поєднанні з підвищенням активності КФК більш ніж у 10 разів порівняно з ВГН) можна припустити у пацієнтів з дифузною міалгією, хворобливістю або слабкістю м'язів та/або вираженим підвищенням активності КФК. Терапію препаратом Туліп слід припинити у разі вираженого підвищення активності КФК або за наявності підтвердженої або передбачуваної міопатії. При застосуванні інших інгібіторів ГМГ-Ко-редуктази (статинів) можливе підвищення ризику міопатії при одночасному застосуванні з циклоспорином, фібратами, еритроміцином, нікотиновою кислотою у ліпід-знижувальних дозах (більше 1 г/добу) або протигрибкових препаратів групи азолів. Застосовуючи препарат Туліп® у комбінації з фібратами, еритроміцином, імунодепресантами, протигрибковими препаратами групи азолів або нікотиновою кислотою у ліпідзнижуючих дозах (більше 1 г/добу), необхідно зважити очікувану користь та ризик лікування Туліп®. Дуже рідко повідомлялося про випадки імуноопосередкованої некротизуючої міопатії під час або після лікування статинами, включаючи аторвастатин. Імуноопосередкована некротизуюча міопатія клінічно характеризується м'язовою слабкістю у верхніх відділах кінцівок та підвищенням концентрації КФК плазми крові, що зберігаються незважаючи на припинення лікування статинами. У разі потреби комбінованої терапії слід розглянути можливість застосування зазначених препаратів у нижчих початкових та підтримуючих дозах. Рекомендується періодичний контроль за активністю КФК. Спільне застосування аторвастатину та фузидової кислоти не рекомендується, отже слід розглянути тимчасове припинення терапії аторвастатином під час застосування фузидової кислоти. Пацієнтів слід попередити про те, що необхідно негайно звернутися до лікаря при появі незрозумілого болю або м'язової слабкості, особливо, якщо вони супроводжуються нездужанням або лихоманкою. При застосуванні препарату Туліп, як і інших інгібіторів ГМГ-Ко-редуктази (статинів), описані рідкісні випадки рабдоміолізу з гострою нирковою недостатністю, зумовленою міоглобінурією. При появі симптомів можливої міопатії або наявності фактора ризику розвитку ниркової недостатності на тлі рабдоміолізу (наприклад, тяжка гостра інфекція, артеріальна гіпотензія, широке хірургічне втручання, травми, серйозні метаболічні, електролітні та ендокринні порушення та неконтрольовані судоми). скасувати. Інтерстиційна хвороба легень Повідомлялося про рідкісні випадки розвитку інтерстиціальної хвороби легень при застосуванні деяких статинів, особливо при тривалій терапії. Клінічні прояви включають задишку, непродуктивний кашель та погіршення загального здоров'я (підвищена стомлюваність, зниження маси тіла та лихоманка). У разі підозри на інтерстиціальну хворобу легенів, що розвивалася, лікування статинами слід припинити. Цукровий діабет Дані деяких досліджень свідчать про те, що застосування статинів як класу може призводити до підвищення концентрації глюкози в крові, а у деяких пацієнтів з підвищеним ризиком розвитку діабету в майбутньому може викликати гіперглікемію, при якій необхідна стандартна антидіабетична терапія. Однак такий ризик є незначним у порівнянні зі зниженням судинного ризику при прийомі статинів, і, отже, не може бути причиною скасування лікування статинами. Пацієнти в групі ризику (з концентрацією глюкози натще 5.6-6.9 ммоль/л, ІМТ >30 кг/м2, підвищеним рівнем тригліцеридів, підвищеним АТ) повинні бути під контролем як клінічним, так і біохімічним відповідно до національних стандартів надання медичної допомоги . Вплив на здатність до керування автотранспортом та управління механізмами У період лікування препаратом Туліп® необхідно дотримуватись обережності при керуванні транспортними засобами та зайнятті іншими потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Активна речовина: аторвастатин (у формі аторвастатину кальцію) – 10 мг; Допоміжні речовини: лактози моногідрат - 34.8 мг, кроскармеллозу натрію - 19.2 мг, гіпоролозу - 2 мг, полісорбат 80 - 2.6 мг, магнію оксид важкий - 26 мг, кремнію діоксид колоїдний - 1.2 мг, магнію стеарат - 1 250 мг; Склад оболонки: гіпромелоза – 2.976 мг, гіпоролоза – 0.744 мг, титану діоксид (Е171) – 1.38 мг, макрогол 6000 – 0.6 мг, тальк – 0.3 мг. По 10 таблеток поміщають у блістер А1/А1 фольги. По 3, 6 або 9 блістерів поміщають у картонну пачку разом із інструкцією з медичного застосування.Опис лікарської формиТаблетки, покриті плівковою оболонкою білого або майже білого кольору, круглі, двоопуклі, з гравіюванням "HLA 10" на одній стороні; вид на зламі: таблетки білого кольору.Фармакотерапевтична групаГіполіпідемічний препарат.ФармакокінетикаВсмоктування та розподіл Абсорбція висока. Cmax у плазмі після прийому внутрішньо досягається через 1-2 год. Прийом їжі дещо знижує швидкість і ступінь абсорбції препарату (на 25% і 9% відповідно), проте зниження Хс-ЛПНГ подібне до такого при застосуванні аторвастатину без одночасного прийому їжі. Після прийому внутрішньо аторвастатину у вечірній час концентрація його в плазмі нижче (Cmax і AUC приблизно на 30%), ніж після прийому в ранковий час, тоді як зниження концентрації Хс-ЛПНГ не залежить від часу доби прийому препарату. Виявлено лінійну залежність між ступенем всмоктування та дозою препарату. Біодоступність становить 12-14%, системна біодоступність інгібуючої активності щодо ГМГ-КоА-редуктази – близько 30%. Низька системна біодоступність обумовлена пресистемним метаболізмом у шлунково-кишковому тракті та ефектом "першого проходження" через печінку. Середній Vd – 381 л, зв'язування з білками плазми крові – 98%. Відношення концентрації аторвастатину в еритроцитах/плазмі становить близько 0.25, що вказує на погане проникнення аторвастатину в еритроцити. Метаболізм та виведення Аторвастатин метаболізується переважно у печінці під дією ізоферментів CYP3A4, CYP3A5 та CYP3A7 з утворенням фармакологічно активних метаболітів (орто- та парагідроксильованих похідних, продуктів бета-окислення). In vitro орто- та парагідроксильовані метаболіти мають інгібуючу дію на ГМГ-КоА-редуктазу, порівнянну з дією аторвастатину. Інгібуючий ефект препарату щодо ГМГ-КоА-редуктази приблизно на 70% визначається активністю циркулюючих метаболітів, який зберігається приблизно протягом 20-30 годин завдяки їх наявності. Результати досліджень in vitro дають підставу припустити, що ізофермент печінки CYP3A4 відіграє важливу роль у метаболізмі аторвастатину. Це підтверджується підвищенням концентрації аторвастатину в плазмі при одночасному прийомі еритроміцину, який є інгібітором цього ізоферменту. Дослідження in vitro також показали, що аторвастатин є слабким інгібітором ізоферменту CYP3A4. Виводиться в основному через кишечник після печінкового та/або позапечінкового метаболізму (препарат не піддається вираженій кишково-печінковій рециркуляції). T1/2 - 14 год. T1/2 інгібуючої активності ГМГ-КоА-редуктази становить 20-30 год. Менше 2% від прийнятої внутрішньо дози визначається сечі. Не виводиться в ході гемодіалізу через інтенсивне зв'язування з білками плазми. Фармакокінетика в особливих клінічних випадках У жінок Cmax вище на 20%, AUC – нижче на 10%, ніж у чоловіків, що не має клінічного значення. У пацієнтів з алкогольним цирозом (клас В за шкалою Чайлд-П'ю) печінки Cmax у 16 разів, а AUC – в 11 разів вище за норму. Cmax та AUC у літніх пацієнтів (≥65 років) на 40% та 30% відповідно вище, ніж у пацієнтів молодого віку, однак це не впливає на ступінь зниження холестерину ЛПНЩ. Порушення функції нирок не впливає на концентрацію препарату в плазмі ступінь зниження холестерину ЛПНГ.ФармакодинамікаАторвастатин є селективним конкурентним інгібітором ГМГ-КоА-редуктази - ферменту, що перетворює 3-гідрокси-3-метилглутарил коензим А в мевалонову кислоту, що є попередником стеролів, включаючи холестерин. Тригліцериди (ТГ) і холестерин (Хс) включаються до складу ліпопротеїнів дуже низької щільності (ЛПДНЩ) при синтезі в печінці, надходять у плазму крові та транспортуються в периферичні тканини. Ліпопротеїни низької щільності (ЛПНЩ) утворюються з ЛПДНЩ у ході взаємодії з рецепторами ЛПНЩ. Дослідження показали, що підвищення концентрацій загального Хс, ЛПНГ та аполіпопротеїну В (апо-В) у плазмі крові сприяє розвитку атеросклерозу та входять до групи факторів ризику виникнення серцево-судинних захворювань, у той час як збільшення концентрації ліпопротеїнів високої щільності (ЛПВЩ) знижує ризик розвитку серцево-судинних захворювань Аторвастатин знижує концентрацію Хс та ліпопротеїнів у плазмі крові за рахунок пригнічення ГМГ-КоА-редуктази, синтезу холестерину в печінці та збільшення числа "печінкових" рецепторів ЛПНГ на поверхні клітин, що призводить до посилення захоплення та катаболізму ЛПНГ (за даними доклінічних досліджень). Аторвастатин знижує синтез та концентрацію Хс-ЛПНГ, загального Хс, апо-В у пацієнтів з гомозиготною та гетерозиготною сімейною гіперхолестеринемією, первинною гіперхолестеринемією та змішаною гіперліпідемією. Викликає також зниження концентрації холестерину-ЛПОНП та ТГ та підвищення концентрації холестерину-ЛПВЩ та аполіпопротеїну А-1 (апо-А). У пацієнтів з дисбеталіпопротеїнемією знижує концентрацію ліпопротеїнів проміжної щільності ХС-ЛПСШ. Аторвастатин у дозах 10 мг та 20 мг знижує концентрацію загального Хс на 29% та 33%, ЛПНГ – на 39% та 43%, апо-В – на 32% та 35% та ТГ – на 14% та 26% відповідно; викликає підвищення концентрації холестерину-ЛПЗЗ та апо-А. Аторвастатин у дозах 40 мг знижує концентрацію загального Хс на 37%, ЛПНГ – на 50%, апо-В – на 42% та ТГ – на 29%; викликає підвищення концентрації Хс-ЛПЗЗ та апо-А. Дозозалежно знижує концентрацію ЛПНГ у хворих на гомозиготну сімейну гіперхолестеринемію, резистентну до терапії іншими гіполіпідемічними засобами. Не надає канцерогенної та мутагенної дії. Терапевтичний ефект розвивається через 2 тижні після початку терапії, досягає максимуму через 4 тижні та зберігається протягом усього періоду лікування.Показання до застосуванняу поєднанні з гіпохолестеринемічною дієтою для зниження підвищених концентрацій загального Хс, Хс-ЛПНЩ, апо-В і ТГ та підвищення концентрації Хс-ЛПВЩ у хворих з первинною гіперхолестеринемією, гетерозиготною сімейною та несемейною гіперхолестеринемією та комбінованою (змішаною) гіперліпі класифікації Фредріксона), коли дієтотерапія та інші нефармакологічні методи лікування виявляються недостатньо ефективними; для зниження концентрації загального Хс та Хс-ЛПНГ у хворих з гомозиготною сімейною гіперхолестеринемією, коли дієтотерапія та інші нефармакологічні методи лікування виявляються недостатньо ефективними; первинна профілактика серцево-судинних ускладнень у пацієнтів без клінічних ознак ІХС, але які мають кілька факторів ризику її розвитку: вік старше 55 років, нікотинова залежність, артеріальна гіпертензія, цукровий діабет, ретинопатія, альбумінурія, низькі концентрації Хс-ЛПВП в плазмі , в т.ч. на фоні дисліпідемії; вторинна профілактика серцево-судинних ускладнень у пацієнтів з ІХС з метою зниження сумарного показника смертності, інфаркту міокарда, інсульту, повторної госпіталізації щодо стенокардії та необхідності реваскуляризації.Протипоказання до застосуваннязахворювання печінки на активній стадії або підвищення активності печінкових трансаміназ у плазмі крові (більш ніж у 3 рази порівняно з ВГН) неясного генезу; вагітність; період лактації; вік до 18 років (ефективність та безпека не встановлені); дефіцит лактази, непереносимість лактози, синдром глюкозо-галактозної мальабсорбції (оскільки у складі міститься лактоза); підвищена чутливість до аторвастатину та інших допоміжних компонентів препарату. З обережністю слід призначати препарат при зловживанні алкоголем, захворюваннях печінки в анамнезі, захворюваннях м'язової системи (в анамнезі від застосування інших представників групи інгібіторів ГМГ-КоА-редуктази), тяжких порушеннях електролітного балансу, ендокринних (гіпертиреоз) та метаболічних порушеннях, діабеті, тяжких гострих інфекціях (сепсис), неконтрольованій епілепсії, великих хірургічних втручаннях, травмах, агресивній ліпідзнижувальній терапії (аторвастатин у дозі 80 мг) при вторинній профілактиці інсульту у пацієнтів з геморагічним абонсультом.Вагітність та лактаціяПрепарат Туліп протипоказаний до застосування під час вагітності. Оскільки холестерин та речовини, що синтезуються з холестерину, важливі для розвитку плода, потенційний ризик інгібування ГМГ-КоА-редуктази перевищує користь від застосування препарату під час вагітності. У разі діагностування вагітності в процесі терапії препаратом Туліп®, його прийом слід припинити якнайшвидше, а пацієнтку необхідно попередити про потенційний ризик для плода. Препарат Туліп® можна застосовувати у жінок репродуктивного віку лише в тому випадку, якщо ймовірність вагітності у них дуже низька, а пацієнтка поінформована про можливий ризик для плода під час лікування. Жінки репродуктивного віку під час лікування препаратом Туліп повинні застосовувати надійні методи контрацепції. Аторвастатин виділяється з грудним молоком, тому протипоказаний до застосування у період грудного вигодовування. При необхідності застосування препарату Туліп® у період лактації грудне вигодовування слід припинити. Протипоказаний у дитячому та підлітковому віці до 18 років (ефективність та безпека не встановлені).Побічна діяЗа даними ВООЗ небажані ефекти класифіковані відповідно до їх частоти розвитку наступним чином: часто (більше 1/100, менше 1/10), нечасто (більше 1/1000, менше 1/100), рідко (більше 1/10 000, менше 1/1000) та дуже рідко (менше 1/10 000), включаючи окремі повідомлення; частота невідома - за наявними даними встановити частоту виникнення неможливо. З боку імунної системи: часто – алергічні реакції; дуже рідко – анафілаксія. З боку нервової системи: часто – головний біль; нечасто - запаморочення, порушення сну, включаючи безсоння та кошмарні сновидіння, астенічний синдром, слабкість, парестезія, гіпестезія, порушення смакової чутливості, втрата або зниження пам'яті; рідко – периферична невропатія. З боку органів чуття: нечасто - шум у вухах, нечіткість зору; рідко – порушення зору; дуже рідко – втрата слуху. З боку травної системи: часто – запор, метеоризм, диспепсія, нудота, діарея; нечасто – анорексія, блювання, панкреатит, гепатит, біль у животі, відрижка; рідко – холестатична жовтяниця (в т.ч. обструктивна); дуже рідко – печінкова недостатність. З боку кістково-м'язової системи: часто – міалгія, артралгія, припухлість суглобів, біль у суглобах, біль у спині, м'язовий спазм; нечасто – біль у м'язах шиї, м'язова слабкість; рідко – міопатія, міозит, рабдоміоліз, тендинопатія (іноді ускладнена розривом сухожилля); частота невідома – імуноопосередкована некротизуюча міопатія. З боку шкіри та підшкірних тканин: нечасто – кропив'янка, висипання на шкірі та свербіж, алопеція; рідко – ангіоневротичний набряк, бульозний висип, багатоформна ексудативна еритема (в т.ч. синдром Стівенса-Джонсона), токсичний епідермальний некроліз (синдром Лайєлла). З боку обміну речовин: часто – гіперглікемія; нечасто – гіпоглікемія. З боку системи кровотворення: нечасто – тромбоцитопенія. З боку дихальної системи: часто – назофарингіт, біль у горлі, носова кровотеча. Лабораторні показники: часто – підвищення активності сироваткової КФК, підвищення активності печінкових трансаміназ; нечасто – лейкоцитурія; частота невідома – підвищення концентрації глікозильованого гемоглобіну. Інші: нечасто – підвищена втома, порушення потенції, вторинна ниркова недостатність, підвищення температури тіла, біль у грудях, периферичні набряки, збільшення маси тіла; дуже рідко – гінекомастія, цукровий діабет. Є окремі повідомлення про розвиток атонічного фасціїту (зв'язок із застосуванням аторвастатину точно не встановлено); частота невідома – депресія, інтерстиціальне захворювання легень (особливо при тривалій терапії), сексуальна дисфункція.Взаємодія з лікарськими засобамиРизик міопатії під час лікування інгібіторами ГМГ-КоА-редуктази підвищується при одночасному застосуванні з циклоспорином, еритроміцином, кларитроміцином, імунодепресивними, протигрибковими препаратами (похідними азолу) внаслідок можливого підвищення концентрації аторвастатину у сироватці крові. При одночасному застосуванні з інгібіторами ВІЛ-протеаз – індинавір, ритонавір – збільшується ризик розвитку міопатії. Подібна взаємодія можлива при одночасному застосуванні аторвастатину з фібратами та нікотиновою кислотою у ліпідзнижуючих дозах (більше 1 г/добу). Інгібітори ізоферменту CYP3A4 Оскільки аторвастатин метаболізується за допомогою ізоферменту CYP3A4, спільне застосування препарату Туліп з інгібіторами цього ізоферменту може призводити до збільшення концентрації аторвастатину в плазмі. Ступінь взаємодії та ефект збільшення концентрації аторвастатину визначаються варіабельністю впливу на ізофермент CYP3A4. Інгібітори транспортного білка ОАТР1В1 Аторвастатин та його метаболіти є субстратами транспортного білка ОАТР1В1. Інгібітори ОАТР1В1 (наприклад, циклоспорин) можуть збільшувати біодоступність аторвастатину. Так, застосування аторвастатину в дозі 10 мг та циклоспорину в дозі 5.2 мг/кг/добу призводить до збільшення концентрації аторвастатину у плазмі крові у 7.7 рази. Еритроміцин/кларитроміцин При одночасному застосуванні аторвастатину 10 мг та еритроміцину (по 500 мг 4 рази на добу) або кларитроміцину (по 500 мг 2 рази на добу), які інгібують ізофермент цитохрому CYP3A4, спостерігається підвищення концентрації аторвастатину в плазмі крові (на 40% еритроміцином та на 56% – при застосуванні з кларитроміцином). Інгібітори протеаз Одночасне застосування аторвастатину з інгібіторами протеаз, відомими як інгібітори ізоферменту цитохрому CYP3A4, супроводжується збільшенням концентрації аторвастатину в плазмі крові (при одночасному застосуванні з еритроміцином – Cmax аторвастатину збільшується на 40%). Ділтіазем Спільне застосування аторвастатину в дозі 40 мг з дилтіаземом у дозі 240 мг призводить до збільшення концентрації аторвастатину в плазмі. Ціметідин Клінічно значущої взаємодії аторвастатину з циметидином не виявлено. Ітраконазол Одночасне застосування аторвастатину у дозах від 20 мг до 40 мг та ітраконазолу у дозі 200 мг призводить до 3-кратного збільшення значення AUC аторвастатину. Грейпфрутовий сік Оскільки грейпфрутовий сік містить один або більше компонентів, які пригнічують ізофермент CYP3A4, його надмірне вживання (більше 1.2 л на день протягом 5 днів) може спричинити збільшення концентрації аторвастатину в плазмі крові. Індуктори ізоферменту CYP3A4 Спільне застосування аторвастатину з індукторами ізоферменту СУРЗА4 (наприклад, ефавіренз або рифампіцин) може призвести до зниження концентрації аторвастатину в плазмі крові. Внаслідок двоїстого механізму взаємодії з рифампіцином (індуктором ізоферменту CYP3A4 та інгібітором транспортного білка гепатоцитів ОАТР1В1), не рекомендується одночасне застосування аторвастатину та рифампіцину, оскільки відстрочений прийом аторвастатину після прийому рифам. Антациди При одночасному застосуванні внутрішньо аторвастатину та суспензії, що містить магнію та алюмінію гідроксиди, концентрація аторвастатину в плазмі знижується приблизно на 35%, проте ступінь зниження концентрації Хс-ЛПНЩ при цьому не змінюється. Феназон Аторвастатин не впливає на фармакокінетику феназону, тому взаємодія з іншими препаратами, що метаболізуються тими самими ізоферментами, не очікується. Колестипол Гіполіпідемічний ефект комбінації з колестиполом перевищує такий для кожного препарату окремо, незважаючи на зниження концентрації аторвастатину на 25% при його одночасному застосуванні з колестиполом. Фузидова кислота Досліджень щодо взаємодії аторвастатину та фузидової кислоти не проводилося. Як і у випадку з іншими статинами, у постмаркетингових дослідженнях спільного застосування аторвастатину та фузидової кислоти повідомлялося про побічні дії на м'язи, включаючи рабдоміоліз. Механізм взаємодії невідомий. Такі пацієнти вимагають ретельного спостереження та, можливо, тимчасової відміни прийому аторвастатину. Колхіцін Хоча дослідження взаємодії аторвастатину та колхіцину не проводилися, повідомлялося про випадки міопатії при спільному застосуванні з колхіцином, і при одночасному призначенні аторвастатину та колхіцину слід дотримуватися обережності. Дігоксин При повторному застосуванні дигоксину та аторвастатину у дозі 10 мг Css дигоксину у плазмі крові не змінюються. Однак при застосуванні дигоксину в комбінації з аторвастатином у дозі 80 мг на добу концентрація дигоксину в плазмі збільшується приблизно на 20%. Пацієнтам, які приймають дигоксин у поєднанні з аторвастатином, потрібен контроль концентрації дигоксину у плазмі. Азітроміцин При одночасному застосуванні аторвастатину в дозі 10 мг 1 раз на добу та азитроміцину в дозі 500 мг 1 раз на добу концентрація аторвастатину в плазмі крові не змінюється. Пероральні контрацептиви При одночасному застосуванні аторвастатину та перорального контрацептиву, що містить норетистерон та етинілестрадіол, спостерігається значне підвищення AUC норетистерону та етинілестрадіолу приблизно на 30% та 20%, відповідно, що слід враховувати при виборі перорального контрацептиву. Терфенадін Аторвастатин при одночасному застосуванні з терфенадином не має клінічно значущого впливу на фармакокінетику терфенадину. Варфарін У пацієнтів, які тривало приймають варфарин, аторвастатин у дозі 80 мг на добу дещо скорочує протромбіновий час у перші дні спільного застосування. Цей ефект зникає після 15 днів одночасного застосування цих препаратів. Хоча про випадки клінічно значущих змін антикоагулянтного ефекту повідомлялося дуже рідко, слід визначати протромбіновий час у пацієнтів, які приймають кумаринові антикоагулянти, перед початком та досить часто на початку лікування аторвастатином, щоб переконатися у відсутності значних змін протромбінового часу. Як тільки буде зареєстровано стабільний протромбіновий час, він може перевірятися з інтервалами, звичайними для пацієнтів, які приймають кумаринові антикоагулянти. У разі зміни дози або припинення лікування ці заходи слід повторити.Не спостерігалося зв'язку між застосуванням аторвастатину та кровотечами або зміною протромбінового часу у пацієнтів, які не приймають антикоагулянти. Амлодипін При одночасному застосуванні аторвастатину у дозі 80 мг та амлодипіну у дозі 10 мг фармакокінетика аторвастатину у рівноважному стані не змінюється. Інші гіполіпідемічні препарати При одночасному застосуванні аторвастатину з іншими гіполіпідемічними препаратами (наприклад, езетимиб, гемфіброзил, похідне фіброєвої кислоти) у ліпід-знижувальних дозах збільшується ризик розвитку рабдоміолізу. Інша супутня терапія При сумісному застосуванні аторвастатину з гіпотензивними засобами та естрогенами (як замісна терапія) – клінічно значущої взаємодії не виявлено.Спосіб застосування та дозиПеред початком застосування препарату Туліп® пацієнту необхідно рекомендувати стандартну гіпохолестеринемічну дієту, яку він повинен продовжувати дотримуватись протягом усього періоду терапії препаратом. Препарат приймають внутрішньо незалежно від часу їди. Доза препарату Туліп® варіює в межах від 10 мг до 80 мг на добу, і підбирається з урахуванням вихідних концентрацій Хс-ЛПНГ, мети терапії та індивідуальної терапевтичної відповіді на терапію. Для більшості пацієнтів початкова доза становить 10 мг 1 раз на добу. На початку лікування, через 2-4 тижні терапії та/або після підвищення дози препарату Туліп® необхідно контролювати концентрації ліпідів у плазмі крові та за необхідності коригувати дозу препарату. Максимальна добова доза – 80 мг на добу. Первинна (гетерозиготна спадкова та полігенна) гіперхолестеринемія (тип IIа) та змішана гіперліпідемія (тип IIb) У більшості випадків буває достатньо застосування препарату Туліп у дозі 10 мг 1 раз на добу (можливе застосування аторвастатину у таблетках по 10 та 20 мг). При необхідності можливе поступове збільшення дози до 80 мг (2 таб. по 40 мг) залежно від реакції пацієнта з інтервалом 2-4 тижні, оскільки терапевтичний ефект відзначається через 2 тижні, а максимальний терапевтичний ефект – через 4 тижні. При тривалому лікуванні цей ефект зберігається. Гомозиготна спадкова гіперхолестеринемія Препарат Туліп® у більшості випадків застосовують у дозі 80 мг (2 таб. по 40 мг) 1 раз на добу. Попередження розвитку серцево-судинних захворювань Туліп® застосовують у дозі 10 мг 1 раз на добу. Якщо не досягнуто оптимальної концентрації ЛПНЩ у плазмі, можливе збільшення дози препарату до 80 мг на добу залежно від реакції пацієнта з інтервалом 2-4 тижні. Корекція дози препарату Туліп у пацієнтів з порушенням функції нирок та у пацієнтів похилого віку не потрібна. У пацієнтів з порушенням функції печінки сповільнюється виведення аторвастатину з організму, тому рекомендується застосовувати його з обережністю при постійному контролі активності печінкових трансаміназ: ACT та АЛТ. Якщо підвищення активності ACT або АЛТ, що спостерігається, більш ніж у 3 рази в порівнянні з ВГН зберігається, рекомендується зниження дози або відміна препарату Туліп®.ПередозуванняЛікування: специфічного антидоту для лікування передозування немає. У разі передозування слід проводити симптоматичне лікування. Гемодіаліз не ефективний (оскільки препарат значно пов'язується з білками плазми).Запобіжні заходи та особливі вказівкиВплив на печінку Як і при застосуванні інших інгібіторів ГМГ-Ко-редуктази (статинів), при терапії препаратом Туліп® можливе помірне (більш ніж у 3 рази порівняно з ВГН) підвищення сироваткової активності печінкових трансаміназ: ACT та АЛТ. До початку терапії, через 6 тижнів та 12 тижнів після початку прийому препарату Туліп або після збільшення його дози, необхідно контролювати показники функції печінки (ACT, АЛТ). Функцію печінки слід контролювати також у разі появи клінічних ознак ураження печінки. У разі підвищення активності ACT та АЛТ, їх активність слід контролювати доти, доки вона не нормалізується. Туліп® слід застосовувати з обережністю у пацієнтів, які зловживають алкоголем та/або мають захворювання печінки в анамнезі. Захворювання печінки в активній стадії або підвищення активності печінкових трансаміназ плазми неясного генезу є протипоказанням для застосування препарату Туліп®. Профілактика інсульту за допомогою інтенсивної ліпідзнижувальної терапії (SPARCL) При ретроспективному аналізі різних підвидів інсульту у осіб, які не страждають на ІХС, які недавно перенесли інсульт або транзиторну ішемічну атаку (ТІА), був виявлений більш високий ризик геморагічного інсульту у пацієнтів, які приймають аторвастатин у дозі 80 мг порівняно з плацебо. Особливо високий ризик відзначався у пацієнтів, які перенесли геморагічний інсульт або лакунарний інфаркт на момент початку дослідження. Для пацієнтів, які перенесли геморагічний інсульт або лакунарний інфаркт і приймають аторвастатин у дозі 80 мг, співвідношення ризик/користування є неоднозначним, і слід уважно оцінювати потенційний ризик розвитку геморагічного інсульту перед початком лікування. Дія на скелетні м'язи При застосуванні препарату Туліп можливий розвиток міалгії. Діагноз міопатії (біль і слабкість у м'язах у поєднанні з підвищенням активності КФК більш ніж у 10 разів порівняно з ВГН) можна припустити у пацієнтів з дифузною міалгією, хворобливістю або слабкістю м'язів та/або вираженим підвищенням активності КФК. Терапію препаратом Туліп слід припинити у разі вираженого підвищення активності КФК або за наявності підтвердженої або передбачуваної міопатії. При застосуванні інших інгібіторів ГМГ-Ко-редуктази (статинів) можливе підвищення ризику міопатії при одночасному застосуванні з циклоспорином, фібратами, еритроміцином, нікотиновою кислотою у ліпід-знижувальних дозах (більше 1 г/добу) або протигрибкових препаратів групи азолів. Застосовуючи препарат Туліп® у комбінації з фібратами, еритроміцином, імунодепресантами, протигрибковими препаратами групи азолів або нікотиновою кислотою у ліпідзнижуючих дозах (більше 1 г/добу), необхідно зважити очікувану користь та ризик лікування Туліп®. Дуже рідко повідомлялося про випадки імуноопосередкованої некротизуючої міопатії під час або після лікування статинами, включаючи аторвастатин. Імуноопосередкована некротизуюча міопатія клінічно характеризується м'язовою слабкістю у верхніх відділах кінцівок та підвищенням концентрації КФК плазми крові, що зберігаються незважаючи на припинення лікування статинами. У разі потреби комбінованої терапії слід розглянути можливість застосування зазначених препаратів у нижчих початкових та підтримуючих дозах. Рекомендується періодичний контроль за активністю КФК. Спільне застосування аторвастатину та фузидової кислоти не рекомендується, отже слід розглянути тимчасове припинення терапії аторвастатином під час застосування фузидової кислоти. Пацієнтів слід попередити про те, що необхідно негайно звернутися до лікаря при появі незрозумілого болю або м'язової слабкості, особливо, якщо вони супроводжуються нездужанням або лихоманкою. При застосуванні препарату Туліп, як і інших інгібіторів ГМГ-Ко-редуктази (статинів), описані рідкісні випадки рабдоміолізу з гострою нирковою недостатністю, зумовленою міоглобінурією. При появі симптомів можливої міопатії або наявності фактора ризику розвитку ниркової недостатності на тлі рабдоміолізу (наприклад, тяжка гостра інфекція, артеріальна гіпотензія, широке хірургічне втручання, травми, серйозні метаболічні, електролітні та ендокринні порушення та неконтрольовані судоми). скасувати. Інтерстиційна хвороба легень Повідомлялося про рідкісні випадки розвитку інтерстиціальної хвороби легень при застосуванні деяких статинів, особливо при тривалій терапії. Клінічні прояви включають задишку, непродуктивний кашель та погіршення загального здоров'я (підвищена стомлюваність, зниження маси тіла та лихоманка). У разі підозри на інтерстиціальну хворобу легенів, що розвивалася, лікування статинами слід припинити. Цукровий діабет Дані деяких досліджень свідчать про те, що застосування статинів як класу може призводити до підвищення концентрації глюкози в крові, а у деяких пацієнтів з підвищеним ризиком розвитку діабету в майбутньому може викликати гіперглікемію, при якій необхідна стандартна антидіабетична терапія. Однак такий ризик є незначним у порівнянні зі зниженням судинного ризику при прийомі статинів, і, отже, не може бути причиною скасування лікування статинами. Пацієнти в групі ризику (з концентрацією глюкози натще 5.6-6.9 ммоль/л, ІМТ >30 кг/м2, підвищеним рівнем тригліцеридів, підвищеним АТ) повинні бути під контролем як клінічним, так і біохімічним відповідно до національних стандартів надання медичної допомоги . Вплив на здатність до керування автотранспортом та управління механізмами У період лікування препаратом Туліп® необхідно дотримуватись обережності при керуванні транспортними засобами та зайнятті іншими потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови відпустки з аптекЗа рецептомВідео на цю тему
Склад, форма випуску та упаковкаПігулки - 1 таб. Активна речовина: аторвастатин (у формі аторвастатину кальцію) – 10 мг; Допоміжні речовини: лактози моногідрат - 34.8 мг, кроскармеллозу натрію - 19.2 мг, гіпоролозу - 2 мг, полісорбат 80 - 2.6 мг, магнію оксид важкий - 26 мг, кремнію діоксид колоїдний - 1.2 мг, магнію стеарат - 1 250 мг; Склад оболонки: гіпромелоза – 2.976 мг, гіпоролоза – 0.744 мг, титану діоксид (Е171) – 1.38 мг, макрогол 6000 – 0.6 мг, тальк – 0.3 мг. По 10 таблеток поміщають у блістер А1/А1 фольги. По 3, 6 або 9 блістерів поміщають у картонну пачку разом із інструкцією з медичного застосування.Опис лікарської формиТаблетки, покриті плівковою оболонкою білого або майже білого кольору, круглі, двоопуклі, з гравіюванням "HLA 10" на одній стороні; вид на зламі: таблетки білого кольору.Фармакотерапевтична групаГіполіпідемічний препарат.ФармакокінетикаВсмоктування та розподіл Абсорбція висока. Cmax у плазмі після прийому внутрішньо досягається через 1-2 год. Прийом їжі дещо знижує швидкість і ступінь абсорбції препарату (на 25% і 9% відповідно), проте зниження Хс-ЛПНГ подібне до такого при застосуванні аторвастатину без одночасного прийому їжі. Після прийому внутрішньо аторвастатину у вечірній час концентрація його в плазмі нижче (Cmax і AUC приблизно на 30%), ніж після прийому в ранковий час, тоді як зниження концентрації Хс-ЛПНГ не залежить від часу доби прийому препарату. Виявлено лінійну залежність між ступенем всмоктування та дозою препарату. Біодоступність становить 12-14%, системна біодоступність інгібуючої активності щодо ГМГ-КоА-редуктази – близько 30%. Низька системна біодоступність обумовлена пресистемним метаболізмом у шлунково-кишковому тракті та ефектом "першого проходження" через печінку. Середній Vd – 381 л, зв'язування з білками плазми крові – 98%. Відношення концентрації аторвастатину в еритроцитах/плазмі становить близько 0.25, що вказує на погане проникнення аторвастатину в еритроцити. Метаболізм та виведення Аторвастатин метаболізується переважно у печінці під дією ізоферментів CYP3A4, CYP3A5 та CYP3A7 з утворенням фармакологічно активних метаболітів (орто- та парагідроксильованих похідних, продуктів бета-окислення). In vitro орто- та парагідроксильовані метаболіти мають інгібуючу дію на ГМГ-КоА-редуктазу, порівнянну з дією аторвастатину. Інгібуючий ефект препарату щодо ГМГ-КоА-редуктази приблизно на 70% визначається активністю циркулюючих метаболітів, який зберігається приблизно протягом 20-30 годин завдяки їх наявності. Результати досліджень in vitro дають підставу припустити, що ізофермент печінки CYP3A4 відіграє важливу роль у метаболізмі аторвастатину. Це підтверджується підвищенням концентрації аторвастатину в плазмі при одночасному прийомі еритроміцину, який є інгібітором цього ізоферменту. Дослідження in vitro також показали, що аторвастатин є слабким інгібітором ізоферменту CYP3A4. Виводиться в основному через кишечник після печінкового та/або позапечінкового метаболізму (препарат не піддається вираженій кишково-печінковій рециркуляції). T1/2 - 14 год. T1/2 інгібуючої активності ГМГ-КоА-редуктази становить 20-30 год. Менше 2% від прийнятої внутрішньо дози визначається сечі. Не виводиться в ході гемодіалізу через інтенсивне зв'язування з білками плазми. Фармакокінетика в особливих клінічних випадках У жінок Cmax вище на 20%, AUC – нижче на 10%, ніж у чоловіків, що не має клінічного значення. У пацієнтів з алкогольним цирозом (клас В за шкалою Чайлд-П'ю) печінки Cmax у 16 разів, а AUC – в 11 разів вище за норму. Cmax та AUC у літніх пацієнтів (≥65 років) на 40% та 30% відповідно вище, ніж у пацієнтів молодого віку, однак це не впливає на ступінь зниження холестерину ЛПНЩ. Порушення функції нирок не впливає на концентрацію препарату в плазмі ступінь зниження холестерину ЛПНГ.ФармакодинамікаАторвастатин є селективним конкурентним інгібітором ГМГ-КоА-редуктази - ферменту, що перетворює 3-гідрокси-3-метилглутарил коензим А в мевалонову кислоту, що є попередником стеролів, включаючи холестерин. Тригліцериди (ТГ) і холестерин (Хс) включаються до складу ліпопротеїнів дуже низької щільності (ЛПДНЩ) при синтезі в печінці, надходять у плазму крові та транспортуються в периферичні тканини. Ліпопротеїни низької щільності (ЛПНЩ) утворюються з ЛПДНЩ у ході взаємодії з рецепторами ЛПНЩ. Дослідження показали, що підвищення концентрацій загального Хс, ЛПНГ та аполіпопротеїну В (апо-В) у плазмі крові сприяє розвитку атеросклерозу та входять до групи факторів ризику виникнення серцево-судинних захворювань, у той час як збільшення концентрації ліпопротеїнів високої щільності (ЛПВЩ) знижує ризик розвитку серцево-судинних захворювань Аторвастатин знижує концентрацію Хс та ліпопротеїнів у плазмі крові за рахунок пригнічення ГМГ-КоА-редуктази, синтезу холестерину в печінці та збільшення числа "печінкових" рецепторів ЛПНГ на поверхні клітин, що призводить до посилення захоплення та катаболізму ЛПНГ (за даними доклінічних досліджень). Аторвастатин знижує синтез та концентрацію Хс-ЛПНГ, загального Хс, апо-В у пацієнтів з гомозиготною та гетерозиготною сімейною гіперхолестеринемією, первинною гіперхолестеринемією та змішаною гіперліпідемією. Викликає також зниження концентрації холестерину-ЛПОНП та ТГ та підвищення концентрації холестерину-ЛПВЩ та аполіпопротеїну А-1 (апо-А). У пацієнтів з дисбеталіпопротеїнемією знижує концентрацію ліпопротеїнів проміжної щільності ХС-ЛПСШ. Аторвастатин у дозах 10 мг та 20 мг знижує концентрацію загального Хс на 29% та 33%, ЛПНГ – на 39% та 43%, апо-В – на 32% та 35% та ТГ – на 14% та 26% відповідно; викликає підвищення концентрації холестерину-ЛПЗЗ та апо-А. Аторвастатин у дозах 40 мг знижує концентрацію загального Хс на 37%, ЛПНГ – на 50%, апо-В – на 42% та ТГ – на 29%; викликає підвищення концентрації Хс-ЛПЗЗ та апо-А. Дозозалежно знижує концентрацію ЛПНГ у хворих на гомозиготну сімейну гіперхолестеринемію, резистентну до терапії іншими гіполіпідемічними засобами. Не надає канцерогенної та мутагенної дії. Терапевтичний ефект розвивається через 2 тижні після початку терапії, досягає максимуму через 4 тижні та зберігається протягом усього періоду лікування.Показання до застосуванняу поєднанні з гіпохолестеринемічною дієтою для зниження підвищених концентрацій загального Хс, Хс-ЛПНЩ, апо-В і ТГ та підвищення концентрації Хс-ЛПВЩ у хворих з первинною гіперхолестеринемією, гетерозиготною сімейною та несемейною гіперхолестеринемією та комбінованою (змішаною) гіперліпі класифікації Фредріксона), коли дієтотерапія та інші нефармакологічні методи лікування виявляються недостатньо ефективними; для зниження концентрації загального Хс та Хс-ЛПНГ у хворих з гомозиготною сімейною гіперхолестеринемією, коли дієтотерапія та інші нефармакологічні методи лікування виявляються недостатньо ефективними; первинна профілактика серцево-судинних ускладнень у пацієнтів без клінічних ознак ІХС, але які мають кілька факторів ризику її розвитку: вік старше 55 років, нікотинова залежність, артеріальна гіпертензія, цукровий діабет, ретинопатія, альбумінурія, низькі концентрації Хс-ЛПВП в плазмі , в т.ч. на фоні дисліпідемії; вторинна профілактика серцево-судинних ускладнень у пацієнтів з ІХС з метою зниження сумарного показника смертності, інфаркту міокарда, інсульту, повторної госпіталізації щодо стенокардії та необхідності реваскуляризації.Протипоказання до застосуваннязахворювання печінки на активній стадії або підвищення активності печінкових трансаміназ у плазмі крові (більш ніж у 3 рази порівняно з ВГН) неясного генезу; вагітність; період лактації; вік до 18 років (ефективність та безпека не встановлені); дефіцит лактази, непереносимість лактози, синдром глюкозо-галактозної мальабсорбції (оскільки у складі міститься лактоза); підвищена чутливість до аторвастатину та інших допоміжних компонентів препарату. З обережністю слід призначати препарат при зловживанні алкоголем, захворюваннях печінки в анамнезі, захворюваннях м'язової системи (в анамнезі від застосування інших представників групи інгібіторів ГМГ-КоА-редуктази), тяжких порушеннях електролітного балансу, ендокринних (гіпертиреоз) та метаболічних порушеннях, діабеті, тяжких гострих інфекціях (сепсис), неконтрольованій епілепсії, великих хірургічних втручаннях, травмах, агресивній ліпідзнижувальній терапії (аторвастатин у дозі 80 мг) при вторинній профілактиці інсульту у пацієнтів з геморагічним абонсультом.Вагітність та лактаціяПрепарат Туліп протипоказаний до застосування під час вагітності. Оскільки холестерин та речовини, що синтезуються з холестерину, важливі для розвитку плода, потенційний ризик інгібування ГМГ-КоА-редуктази перевищує користь від застосування препарату під час вагітності. У разі діагностування вагітності в процесі терапії препаратом Туліп®, його прийом слід припинити якнайшвидше, а пацієнтку необхідно попередити про потенційний ризик для плода. Препарат Туліп® можна застосовувати у жінок репродуктивного віку лише в тому випадку, якщо ймовірність вагітності у них дуже низька, а пацієнтка поінформована про можливий ризик для плода під час лікування. Жінки репродуктивного віку під час лікування препаратом Туліп повинні застосовувати надійні методи контрацепції. Аторвастатин виділяється з грудним молоком, тому протипоказаний до застосування у період грудного вигодовування. При необхідності застосування препарату Туліп® у період лактації грудне вигодовування слід припинити. Протипоказаний у дитячому та підлітковому віці до 18 років (ефективність та безпека не встановлені).Побічна діяЗа даними ВООЗ небажані ефекти класифіковані відповідно до їх частоти розвитку наступним чином: часто (більше 1/100, менше 1/10), нечасто (більше 1/1000, менше 1/100), рідко (більше 1/10 000, менше 1/1000) та дуже рідко (менше 1/10 000), включаючи окремі повідомлення; частота невідома - за наявними даними встановити частоту виникнення неможливо. З боку імунної системи: часто – алергічні реакції; дуже рідко – анафілаксія. З боку нервової системи: часто – головний біль; нечасто - запаморочення, порушення сну, включаючи безсоння та кошмарні сновидіння, астенічний синдром, слабкість, парестезія, гіпестезія, порушення смакової чутливості, втрата або зниження пам'яті; рідко – периферична невропатія. З боку органів чуття: нечасто - шум у вухах, нечіткість зору; рідко – порушення зору; дуже рідко – втрата слуху. З боку травної системи: часто – запор, метеоризм, диспепсія, нудота, діарея; нечасто – анорексія, блювання, панкреатит, гепатит, біль у животі, відрижка; рідко – холестатична жовтяниця (в т.ч. обструктивна); дуже рідко – печінкова недостатність. З боку кістково-м'язової системи: часто – міалгія, артралгія, припухлість суглобів, біль у суглобах, біль у спині, м'язовий спазм; нечасто – біль у м'язах шиї, м'язова слабкість; рідко – міопатія, міозит, рабдоміоліз, тендинопатія (іноді ускладнена розривом сухожилля); частота невідома – імуноопосередкована некротизуюча міопатія. З боку шкіри та підшкірних тканин: нечасто – кропив'янка, висипання на шкірі та свербіж, алопеція; рідко – ангіоневротичний набряк, бульозний висип, багатоформна ексудативна еритема (в т.ч. синдром Стівенса-Джонсона), токсичний епідермальний некроліз (синдром Лайєлла). З боку обміну речовин: часто – гіперглікемія; нечасто – гіпоглікемія. З боку системи кровотворення: нечасто – тромбоцитопенія. З боку дихальної системи: часто – назофарингіт, біль у горлі, носова кровотеча. Лабораторні показники: часто – підвищення активності сироваткової КФК, підвищення активності печінкових трансаміназ; нечасто – лейкоцитурія; частота невідома – підвищення концентрації глікозильованого гемоглобіну. Інші: нечасто – підвищена втома, порушення потенції, вторинна ниркова недостатність, підвищення температури тіла, біль у грудях, периферичні набряки, збільшення маси тіла; дуже рідко – гінекомастія, цукровий діабет. Є окремі повідомлення про розвиток атонічного фасціїту (зв'язок із застосуванням аторвастатину точно не встановлено); частота невідома – депресія, інтерстиціальне захворювання легень (особливо при тривалій терапії), сексуальна дисфункція.Взаємодія з лікарськими засобамиРизик міопатії під час лікування інгібіторами ГМГ-КоА-редуктази підвищується при одночасному застосуванні з циклоспорином, еритроміцином, кларитроміцином, імунодепресивними, протигрибковими препаратами (похідними азолу) внаслідок можливого підвищення концентрації аторвастатину у сироватці крові. При одночасному застосуванні з інгібіторами ВІЛ-протеаз – індинавір, ритонавір – збільшується ризик розвитку міопатії. Подібна взаємодія можлива при одночасному застосуванні аторвастатину з фібратами та нікотиновою кислотою у ліпідзнижуючих дозах (більше 1 г/добу). Інгібітори ізоферменту CYP3A4 Оскільки аторвастатин метаболізується за допомогою ізоферменту CYP3A4, спільне застосування препарату Туліп з інгібіторами цього ізоферменту може призводити до збільшення концентрації аторвастатину в плазмі. Ступінь взаємодії та ефект збільшення концентрації аторвастатину визначаються варіабельністю впливу на ізофермент CYP3A4. Інгібітори транспортного білка ОАТР1В1 Аторвастатин та його метаболіти є субстратами транспортного білка ОАТР1В1. Інгібітори ОАТР1В1 (наприклад, циклоспорин) можуть збільшувати біодоступність аторвастатину. Так, застосування аторвастатину в дозі 10 мг та циклоспорину в дозі 5.2 мг/кг/добу призводить до збільшення концентрації аторвастатину у плазмі крові у 7.7 рази. Еритроміцин/кларитроміцин При одночасному застосуванні аторвастатину 10 мг та еритроміцину (по 500 мг 4 рази на добу) або кларитроміцину (по 500 мг 2 рази на добу), які інгібують ізофермент цитохрому CYP3A4, спостерігається підвищення концентрації аторвастатину в плазмі крові (на 40% еритроміцином та на 56% – при застосуванні з кларитроміцином). Інгібітори протеаз Одночасне застосування аторвастатину з інгібіторами протеаз, відомими як інгібітори ізоферменту цитохрому CYP3A4, супроводжується збільшенням концентрації аторвастатину в плазмі крові (при одночасному застосуванні з еритроміцином – Cmax аторвастатину збільшується на 40%). Ділтіазем Спільне застосування аторвастатину в дозі 40 мг з дилтіаземом у дозі 240 мг призводить до збільшення концентрації аторвастатину в плазмі. Ціметідин Клінічно значущої взаємодії аторвастатину з циметидином не виявлено. Ітраконазол Одночасне застосування аторвастатину у дозах від 20 мг до 40 мг та ітраконазолу у дозі 200 мг призводить до 3-кратного збільшення значення AUC аторвастатину. Грейпфрутовий сік Оскільки грейпфрутовий сік містить один або більше компонентів, які пригнічують ізофермент CYP3A4, його надмірне вживання (більше 1.2 л на день протягом 5 днів) може спричинити збільшення концентрації аторвастатину в плазмі крові. Індуктори ізоферменту CYP3A4 Спільне застосування аторвастатину з індукторами ізоферменту СУРЗА4 (наприклад, ефавіренз або рифампіцин) може призвести до зниження концентрації аторвастатину в плазмі крові. Внаслідок двоїстого механізму взаємодії з рифампіцином (індуктором ізоферменту CYP3A4 та інгібітором транспортного білка гепатоцитів ОАТР1В1), не рекомендується одночасне застосування аторвастатину та рифампіцину, оскільки відстрочений прийом аторвастатину після прийому рифам. Антациди При одночасному застосуванні внутрішньо аторвастатину та суспензії, що містить магнію та алюмінію гідроксиди, концентрація аторвастатину в плазмі знижується приблизно на 35%, проте ступінь зниження концентрації Хс-ЛПНЩ при цьому не змінюється. Феназон Аторвастатин не впливає на фармакокінетику феназону, тому взаємодія з іншими препаратами, що метаболізуються тими самими ізоферментами, не очікується. Колестипол Гіполіпідемічний ефект комбінації з колестиполом перевищує такий для кожного препарату окремо, незважаючи на зниження концентрації аторвастатину на 25% при його одночасному застосуванні з колестиполом. Фузидова кислота Досліджень щодо взаємодії аторвастатину та фузидової кислоти не проводилося. Як і у випадку з іншими статинами, у постмаркетингових дослідженнях спільного застосування аторвастатину та фузидової кислоти повідомлялося про побічні дії на м'язи, включаючи рабдоміоліз. Механізм взаємодії невідомий. Такі пацієнти вимагають ретельного спостереження та, можливо, тимчасової відміни прийому аторвастатину. Колхіцін Хоча дослідження взаємодії аторвастатину та колхіцину не проводилися, повідомлялося про випадки міопатії при спільному застосуванні з колхіцином, і при одночасному призначенні аторвастатину та колхіцину слід дотримуватися обережності. Дігоксин При повторному застосуванні дигоксину та аторвастатину у дозі 10 мг Css дигоксину у плазмі крові не змінюються. Однак при застосуванні дигоксину в комбінації з аторвастатином у дозі 80 мг на добу концентрація дигоксину в плазмі збільшується приблизно на 20%. Пацієнтам, які приймають дигоксин у поєднанні з аторвастатином, потрібен контроль концентрації дигоксину у плазмі. Азітроміцин При одночасному застосуванні аторвастатину в дозі 10 мг 1 раз на добу та азитроміцину в дозі 500 мг 1 раз на добу концентрація аторвастатину в плазмі крові не змінюється. Пероральні контрацептиви При одночасному застосуванні аторвастатину та перорального контрацептиву, що містить норетистерон та етинілестрадіол, спостерігається значне підвищення AUC норетистерону та етинілестрадіолу приблизно на 30% та 20%, відповідно, що слід враховувати при виборі перорального контрацептиву. Терфенадін Аторвастатин при одночасному застосуванні з терфенадином не має клінічно значущого впливу на фармакокінетику терфенадину. Варфарін У пацієнтів, які тривало приймають варфарин, аторвастатин у дозі 80 мг на добу дещо скорочує протромбіновий час у перші дні спільного застосування. Цей ефект зникає після 15 днів одночасного застосування цих препаратів. Хоча про випадки клінічно значущих змін антикоагулянтного ефекту повідомлялося дуже рідко, слід визначати протромбіновий час у пацієнтів, які приймають кумаринові антикоагулянти, перед початком та досить часто на початку лікування аторвастатином, щоб переконатися у відсутності значних змін протромбінового часу. Як тільки буде зареєстровано стабільний протромбіновий час, він може перевірятися з інтервалами, звичайними для пацієнтів, які приймають кумаринові антикоагулянти. У разі зміни дози або припинення лікування ці заходи слід повторити.Не спостерігалося зв'язку між застосуванням аторвастатину та кровотечами або зміною протромбінового часу у пацієнтів, які не приймають антикоагулянти. Амлодипін При одночасному застосуванні аторвастатину у дозі 80 мг та амлодипіну у дозі 10 мг фармакокінетика аторвастатину у рівноважному стані не змінюється. Інші гіполіпідемічні препарати При одночасному застосуванні аторвастатину з іншими гіполіпідемічними препаратами (наприклад, езетимиб, гемфіброзил, похідне фіброєвої кислоти) у ліпід-знижувальних дозах збільшується ризик розвитку рабдоміолізу. Інша супутня терапія При сумісному застосуванні аторвастатину з гіпотензивними засобами та естрогенами (як замісна терапія) – клінічно значущої взаємодії не виявлено.Спосіб застосування та дозиПеред початком застосування препарату Туліп® пацієнту необхідно рекомендувати стандартну гіпохолестеринемічну дієту, яку він повинен продовжувати дотримуватись протягом усього періоду терапії препаратом. Препарат приймають внутрішньо незалежно від часу їди. Доза препарату Туліп® варіює в межах від 10 мг до 80 мг на добу, і підбирається з урахуванням вихідних концентрацій Хс-ЛПНГ, мети терапії та індивідуальної терапевтичної відповіді на терапію. Для більшості пацієнтів початкова доза становить 10 мг 1 раз на добу. На початку лікування, через 2-4 тижні терапії та/або після підвищення дози препарату Туліп® необхідно контролювати концентрації ліпідів у плазмі крові та за необхідності коригувати дозу препарату. Максимальна добова доза – 80 мг на добу. Первинна (гетерозиготна спадкова та полігенна) гіперхолестеринемія (тип IIа) та змішана гіперліпідемія (тип IIb) У більшості випадків буває достатньо застосування препарату Туліп у дозі 10 мг 1 раз на добу (можливе застосування аторвастатину у таблетках по 10 та 20 мг). При необхідності можливе поступове збільшення дози до 80 мг (2 таб. по 40 мг) залежно від реакції пацієнта з інтервалом 2-4 тижні, оскільки терапевтичний ефект відзначається через 2 тижні, а максимальний терапевтичний ефект – через 4 тижні. При тривалому лікуванні цей ефект зберігається. Гомозиготна спадкова гіперхолестеринемія Препарат Туліп® у більшості випадків застосовують у дозі 80 мг (2 таб. по 40 мг) 1 раз на добу. Попередження розвитку серцево-судинних захворювань Туліп® застосовують у дозі 10 мг 1 раз на добу. Якщо не досягнуто оптимальної концентрації ЛПНЩ у плазмі, можливе збільшення дози препарату до 80 мг на добу залежно від реакції пацієнта з інтервалом 2-4 тижні. Корекція дози препарату Туліп у пацієнтів з порушенням функції нирок та у пацієнтів похилого віку не потрібна. У пацієнтів з порушенням функції печінки сповільнюється виведення аторвастатину з організму, тому рекомендується застосовувати його з обережністю при постійному контролі активності печінкових трансаміназ: ACT та АЛТ. Якщо підвищення активності ACT або АЛТ, що спостерігається, більш ніж у 3 рази в порівнянні з ВГН зберігається, рекомендується зниження дози або відміна препарату Туліп®.ПередозуванняЛікування: специфічного антидоту для лікування передозування немає. У разі передозування слід проводити симптоматичне лікування. Гемодіаліз не ефективний (оскільки препарат значно пов'язується з білками плазми).Запобіжні заходи та особливі вказівкиВплив на печінку Як і при застосуванні інших інгібіторів ГМГ-Ко-редуктази (статинів), при терапії препаратом Туліп® можливе помірне (більш ніж у 3 рази порівняно з ВГН) підвищення сироваткової активності печінкових трансаміназ: ACT та АЛТ. До початку терапії, через 6 тижнів та 12 тижнів після початку прийому препарату Туліп або після збільшення його дози, необхідно контролювати показники функції печінки (ACT, АЛТ). Функцію печінки слід контролювати також у разі появи клінічних ознак ураження печінки. У разі підвищення активності ACT та АЛТ, їх активність слід контролювати доти, доки вона не нормалізується. Туліп® слід застосовувати з обережністю у пацієнтів, які зловживають алкоголем та/або мають захворювання печінки в анамнезі. Захворювання печінки в активній стадії або підвищення активності печінкових трансаміназ плазми неясного генезу є протипоказанням для застосування препарату Туліп®. Профілактика інсульту за допомогою інтенсивної ліпідзнижувальної терапії (SPARCL) При ретроспективному аналізі різних підвидів інсульту у осіб, які не страждають на ІХС, які недавно перенесли інсульт або транзиторну ішемічну атаку (ТІА), був виявлений більш високий ризик геморагічного інсульту у пацієнтів, які приймають аторвастатин у дозі 80 мг порівняно з плацебо. Особливо високий ризик відзначався у пацієнтів, які перенесли геморагічний інсульт або лакунарний інфаркт на момент початку дослідження. Для пацієнтів, які перенесли геморагічний інсульт або лакунарний інфаркт і приймають аторвастатин у дозі 80 мг, співвідношення ризик/користування є неоднозначним, і слід уважно оцінювати потенційний ризик розвитку геморагічного інсульту перед початком лікування. Дія на скелетні м'язи При застосуванні препарату Туліп можливий розвиток міалгії. Діагноз міопатії (біль і слабкість у м'язах у поєднанні з підвищенням активності КФК більш ніж у 10 разів порівняно з ВГН) можна припустити у пацієнтів з дифузною міалгією, хворобливістю або слабкістю м'язів та/або вираженим підвищенням активності КФК. Терапію препаратом Туліп слід припинити у разі вираженого підвищення активності КФК або за наявності підтвердженої або передбачуваної міопатії. При застосуванні інших інгібіторів ГМГ-Ко-редуктази (статинів) можливе підвищення ризику міопатії при одночасному застосуванні з циклоспорином, фібратами, еритроміцином, нікотиновою кислотою у ліпід-знижувальних дозах (більше 1 г/добу) або протигрибкових препаратів групи азолів. Застосовуючи препарат Туліп® у комбінації з фібратами, еритроміцином, імунодепресантами, протигрибковими препаратами групи азолів або нікотиновою кислотою у ліпідзнижуючих дозах (більше 1 г/добу), необхідно зважити очікувану користь та ризик лікування Туліп®. Дуже рідко повідомлялося про випадки імуноопосередкованої некротизуючої міопатії під час або після лікування статинами, включаючи аторвастатин. Імуноопосередкована некротизуюча міопатія клінічно характеризується м'язовою слабкістю у верхніх відділах кінцівок та підвищенням концентрації КФК плазми крові, що зберігаються незважаючи на припинення лікування статинами. У разі потреби комбінованої терапії слід розглянути можливість застосування зазначених препаратів у нижчих початкових та підтримуючих дозах. Рекомендується періодичний контроль за активністю КФК. Спільне застосування аторвастатину та фузидової кислоти не рекомендується, отже слід розглянути тимчасове припинення терапії аторвастатином під час застосування фузидової кислоти. Пацієнтів слід попередити про те, що необхідно негайно звернутися до лікаря при появі незрозумілого болю або м'язової слабкості, особливо, якщо вони супроводжуються нездужанням або лихоманкою. При застосуванні препарату Туліп, як і інших інгібіторів ГМГ-Ко-редуктази (статинів), описані рідкісні випадки рабдоміолізу з гострою нирковою недостатністю, зумовленою міоглобінурією. При появі симптомів можливої міопатії або наявності фактора ризику розвитку ниркової недостатності на тлі рабдоміолізу (наприклад, тяжка гостра інфекція, артеріальна гіпотензія, широке хірургічне втручання, травми, серйозні метаболічні, електролітні та ендокринні порушення та неконтрольовані судоми). скасувати. Інтерстиційна хвороба легень Повідомлялося про рідкісні випадки розвитку інтерстиціальної хвороби легень при застосуванні деяких статинів, особливо при тривалій терапії. Клінічні прояви включають задишку, непродуктивний кашель та погіршення загального здоров'я (підвищена стомлюваність, зниження маси тіла та лихоманка). У разі підозри на інтерстиціальну хворобу легенів, що розвивалася, лікування статинами слід припинити. Цукровий діабет Дані деяких досліджень свідчать про те, що застосування статинів як класу може призводити до підвищення концентрації глюкози в крові, а у деяких пацієнтів з підвищеним ризиком розвитку діабету в майбутньому може викликати гіперглікемію, при якій необхідна стандартна антидіабетична терапія. Однак такий ризик є незначним у порівнянні зі зниженням судинного ризику при прийомі статинів, і, отже, не може бути причиною скасування лікування статинами. Пацієнти в групі ризику (з концентрацією глюкози натще 5.6-6.9 ммоль/л, ІМТ >30 кг/м2, підвищеним рівнем тригліцеридів, підвищеним АТ) повинні бути під контролем як клінічним, так і біохімічним відповідно до національних стандартів надання медичної допомоги . Вплив на здатність до керування автотранспортом та управління механізмами У період лікування препаратом Туліп® необхідно дотримуватись обережності при керуванні транспортними засобами та зайнятті іншими потенційно небезпечними видами діяльності, що вимагають підвищеної концентрації уваги та швидкості психомоторних реакцій.Умови відпустки з аптекЗа рецептомВідео на цю тему
2 065,00 грн
2 037,00 грн
Склад, форма випуску та упаковкаРозчин для підшкірного введення - 1 мл: Активні речовини: інсулін гларгін – 300 ОД (10.91 мг); Допоміжні речовини: метакрезол (м-крезол) - 2.7 мг, цинку хлорид - 0.19 мг (відповідає 0.9 мг цинку), гліцерол (85%) - 20 мг, натрію гідроксид - до pH 4.0, хлористоводнева кислота - до pH 40, /і - до 1 мл. 1.5 мл - картриджі з безбарвного скла (тип I), вмонтовані в одноразові шприц-ручки СолоСтар, пачки картонні.Опис лікарської формиРозчин для підшкірного введення прозорий, безбарвний або майже безбарвний.Фармакотерапевтична групаАналог людського інсуліну тривалої дії.ФармакокінетикаВсмоктування та розподіл Після п/к ін'єкції препарату Туджео СолоСтар® здоровим добровольцям та пацієнтам з цукровим діабетом сироваткова концентрація інсуліну вказує на набагато повільнішу та тривалішу абсорбцію, що призводить до створення більш пологої кривої "концентрація-час" протягом до 36 год, порівняно з інсуліном гларгіном 100 ОД/мл. Крива "концентрація-час" препарату Туджео СолоСтар® відповідала кривою його фармакодинамічної активності. Css у межах терапевтичного діапазону концентрацій досягалася через 3-4 дні щоденного застосування препарату Туджео СолоСтар®. Після п/к ін'єкції препарату Туджео СолоСтар® варіабельність у одного і того ж пацієнта, що визначається як коефіцієнт варіації системної експозиції інсуліну протягом 24 годин у рівноважному стані, була низькою (17.4%). Метаболізм У людини після підшкірного введення препарату Туджео СолоСтар® інсулін гларгін швидко метаболізується з боку карбоксильного кінця (С-кінця) β-ланцюга з утворенням двох активних метаболітів М1 (21A-Gly-інсуліну) та М2 (21А-Gly-des-30В) -Thr-інсуліну). Переважно у плазмі крові циркулює метаболіт M1. Системна експозиція метаболіту M1 збільшується зі збільшенням дози препарату Туджео СолоСтар®. Зіставлення даних фармакокінетики та фармакодинаміки показали, що дія препарату в основному здійснюється за рахунок системної експозиції метаболіту M1. Переважна більшість пацієнтів не вдавалося виявити інсулін гларгін і метаболіт М2 у системному кровотоку. У випадках, коли все-таки вдавалося виявити в крові інсулін гларгін та метаболіт М2, їх концентрації не залежали від введеної дози та лікарської форми інсуліну гларгіну. Виведення Т1/2 метаболіту M1, що кількісно переважає метаболіт препарату Туджео СолоСтар®, після п/к ін'єкції препарату становить 18-19 год, незалежно від дози. Фармакокінетика у спеціальних груп пацієнтів Інформація про вплив раси та статі на фармакокінетику інсуліну гларгіну відсутня. Вплив віку на фармакокінетику препарату Туджео СолоСтар® зараз не вивчений. У пацієнтів похилого віку з цукровим діабетом, щоб уникнути гіпоглікемічних реакцій, початкова доза і підтримуюча доза повинні бути нижчими, а збільшення дози слід проводити повільніше. У пацієнтів дитячого віку фармакокінетика препарату Туджео СолоСтар® зараз не вивчена. Вплив ниркової та печінкової недостатності на фармакокінетику препарату Туджео СолоСтар® зараз не вивчений. Однак у деяких дослідженнях, проведених з людським інсуліном, було показано підвищення концентрацій інсуліну у пацієнтів з нирковою та печінковою недостатністю. Рекомендується ретельний моніторинг концентрації глюкози у крові та індивідуальна корекція дози інсуліну.ФармакодинамікаНайбільш важливою дією інсуліну, у т.ч. Інсуліну гларгіну, є регуляція метаболізму глюкози. Інсулін та його аналоги знижують концентрацію глюкози в крові, стимулюючи поглинання глюкози периферичними тканинами (особливо скелетною мускулатурою та жировою тканиною) та інгібуючи утворення глюкози в печінці. Інсулін пригнічує ліполіз в адипоцитах та інгібує протеоліз, збільшуючи при цьому синтез білка. Фармакодинамічні характеристики Інсулін гларгін є аналогом людського інсуліну, отриманим методом рекомбінації ДНК бактерій виду Escherichia coli (штами К12), що використовуються як штам-продуцент. Він має низьку розчинність у нейтральному середовищі. При pH 4 (у кислому середовищі) інсулін гларгін повністю розчинний. Після введення в підшкірно-жирову клітковину кисла реакція розчину нейтралізується, що призводить до утворення мікропреципітатів, у тому числі постійно вивільняються невеликі кількості інсуліну гларгіну. Початок дії введеного підшкірного інсуліну гларгіну 100 ОД/мл був більш повільним, порівняно з людським інсуліном ізофан, крива його дії була гладкою і позбавленою піків, тривалість дії була пролонгованою (дані еуглікемічних кламп-досліджень, проведених у здорових добро цукровим діабетом 1 типу). Гіпоглікемічна дія препарату Туджео СолоСтар® після його підшкірного введення, порівняно з таким при підшкірному введенні інсуліну гларгіну 100 ОД/мл, була більш постійною за величиною і більш пролонгованою (дані 36-годинного перехресного еуглікемічного кламп-дослідження, 18 пацієнтів із цукровим діабетом 1 типу). Дія препарату Туджео СолоСтар® тривала більше 24 годин (до 36 годин) при підшкірному введенні в клінічно значущих дозах. Пролонгована гіпоглікемічна дія препарату Туджео СолоСтар®, що триває більше 24 годин, дозволяє, при необхідності, змінювати час введення препарату в межах 3 годин або 3 години після звичайного для пацієнта часу проведення ін'єкції. Відмінності у кривих гіпоглікемічної дії препарату Туджео СолоСтар® та інсуліну гларгіну 100 ОД/мл пов'язані зі зміною вивільнення інсуліну гларгіну з преципітату. Для одного і того ж кількості одиниць інсуліну гларгіну об'єм препарату Туджео СолоСтар® становить одну третину від такого при введенні інсуліну гларгіну 100 ОД/мл. Це призводить до зменшення площі поверхні преципітату, що забезпечує більш поступове вивільнення інсуліну гларгіну з преципітату препарату Туджео СолоСтар® порівняно з преципітатом інсуліну гларгіну 100 ОД/мл. При внутрішньовенному введенні однакових доз інсуліну гларгіну та людського інсуліну їх гіпоглікемічна дія була однаковою. Зв'язок з інсуліновими рецепторами: інсулін гларгін метаболізується до двох активних метаболітів M1 та M2. Дослідження in vitro показали, що афінність інсуліну гларгіну та його метаболітів M1 та M2 до рецепторів інсуліну людини подібна до такої у людського інсуліну. Зв'язок з рецепторами інсуліноподібного фактора росту 1 (ІФР-1): афінність інсуліну гларгіну до рецептора ІФР-1 приблизно в 5-8 разів вища, ніж у людського інсуліну (але приблизно в 70-80 разів нижче, ніж у ІФР-1), водночас, у порівнянні з людським інсуліном, метаболіти інсуліну гларгіну M1 та M2 мають дещо меншу афінність до рецептора ІФР-1 порівняно з людським інсуліном. Загальна терапевтична концентрація інсуліну (концентрація інсуліну гларгіну та його метаболітів), що визначається у пацієнтів з цукровим діабетом 1 типу, була помітно нижчою від концентрації, необхідної для напівмаксимального зв'язування з рецепторами ІФР-1 та подальшої активації мітогенно-проліферативного шляху, що запускається через 1 . Фізіологічні концентрації ендогенного ІФР-1 можуть активувати мітогенно-проліферативний шлях, однак терапевтичні концентрації інсуліну, що визначаються при інсулінотерапії, включаючи лікування препаратом Туджео СолоСтар®, значно нижчі від фармакологічних концентрацій, необхідних для активації мітогенно-проліферативного шляху. Результати, отримані у всіх клінічних дослідженнях препарату Туджео СолоСтар®, проведених за участю 546 пацієнтів з цукровим діабетом 1 типу та 2474 пацієнтів з цукровим діабетом 2 типу, показали, що зниження значень показника глікозильованого гемоглобіну (HbA1c) вихідними значеннями до кінця досліджень було не менше такого при лікуванні інсуліном гларгіном 100 ОД/мл. Відсоток пацієнтів, які досягли цільового значення HbA1c (нижче 7%), був порівнянним в обох групах лікування. Зниження концентрацій глюкози в плазмі крові до кінця дослідження з препаратом Туджео СолоСтар® та інсуліном гларгіном 100 ОД/мл було однаковим, але при цьому при лікуванні препаратом Туджео СолоСтар® це зниження було більш поступовим у період добору дози. Глікемічний контроль, включаючи покращення показника HbA1c, при введенні препарату Туджео СолоСтар® вранці або ввечері був порівнянним, а зміна часу введення препарату в межах 3 години до або 3 години після звичайного для пацієнта часу введення препарату не впливало на його ефективність. У пацієнтів, які отримували лікування препаратом Туджео СолоСтар®, до кінця 6-місячного періоду лікування спостерігалася зміна маси тіла, в середньому менш ніж на 1 кг. Поліпшення показника НbА1с не залежало від статі, етнічної приналежності, віку, тривалості захворювання на цукровий діабет (менше 10 років і ≥10 років), значення показника HbA1c у результаті (менше 8% або ≥8%) або ІМТ у результаті. У пацієнтів з цукровим діабетом 2 типу результати клінічних досліджень продемонстрували меншу частоту розвитку тяжкої та/або підтвердженої гіпоглікемії, а також документованої гіпоглікемії, що протікає з клінічною симптоматикою, при лікуванні препаратом Туджео СолоСтар®, порівняно з лікуванням інсуліном гларгіном 100. Перевага препарату Туджео СолоСтар® перед інсуліном гларгіном 100 ОД/мл щодо зниження ризику розвитку тяжкої та/або підтвердженої нічної гіпоглікемії була показана у пацієнтів, які раніше отримували пероральні гіпоглікемічні препарати (23% зниження ризику) або інсулін під час їди. ) протягом періоду від 9-го тижня до кінця дослідження порівняно з лікуванням інсуліном гларгіном 100 ОД/мл. У групі пацієнтів, які отримували лікування препаратом Туджео СолоСтар®, порівняно з пацієнтами, які отримували лікування інсуліном гларгіном 100 ОД/мл, зниження ризику розвитку гіпоглікемії спостерігалося як у пацієнтів, які раніше отримували інсулінотерапію, так і у пацієнтів, які раніше не отримували інсулін; зниження ризику було більшим протягом перших 8 тижнів лікування (початковий період лікування) і не залежало від віку, статі, расової приналежності, ІМТ та тривалості захворювання на цукровий діабет (менше 10 років та ≥10 років). У пацієнтів з цукровим діабетом 1 типу частота розвитку гіпоглікемії на фоні лікування препаратом Туджео СолоСтар® була подібною до пацієнтів, які отримували лікування інсуліном гларгіном 100 ОД/мл. Однак частота розвитку нічної гіпоглікемії (для всіх категорій гіпоглікемії) під час початкового періоду лікування була нижчою у пацієнтів, які отримували лікування препаратом Туджео СолоСтар®, порівняно з пацієнтами, які отримували лікування інсуліном гларгіном 100 ОД/мл. У клінічних дослідженнях одноразове протягом доби введення препарату Туджео СолоСтар® увечері, з фіксованим графіком введення (одночасно) або гнучким графіком введення (як мінімум, 2 рази на тиждень введення препарату проводилося за 3 години до або через 3 години після звичайного). часу введення, внаслідок чого інтервали між введеннями скорочувалися до 18 год і подовжувалися до 30 год) надавав однаковий вплив на показник HbA1c, концентрацію глюкози плазми крові натще (ГПН) та середнє значення передін'єкційної концентрації глюкози в плазмі крові при самовизначенні. Крім того, при застосуванні препарату Туджео СолоСтар з фіксованим або гнучким графіком часу введення не спостерігалося жодних відмінностей у частоті розвитку гіпоглікемії у будь-який час доби чи нічної гіпоглікемії. Результати досліджень порівняно препарату Туджео СолоСтар® та інсуліну гларгіну 100 ОД/мл не вказали на наявність будь-яких відмінностей, пов'язаних з утворенням антитіл до інсуліну, в ефективності, безпеці або дозі базального інсуліну між пацієнтами, які отримували лікування препаратами Туджео СолоСтар® та інсу гларгін 100 ОД/мл. Дослідження ORIGIN (Outcome Reduction with Initial Glargine INtervention) - міжнародне, багатоцентрове, рандомізоване дослідження, було проведено у 12 537 пацієнтів з порушеною глікемією натще (НГН), порушеною толерантністю до глюкози (НТГ) або ранньою стадією серного судинним захворюванням. Учасники дослідження були випадково розподілені для отримання інсуліну гларгіну 100 ОД/мл (n=6264), який титрувався до досягнення концентрації глюкози в плазмі крові натще ≤5.3 ммоль, або стандартного лікування (n=6273). Медіана періоду спостереження становила приблизно 6.2 роки. Медіана вихідних значень HbA1c становила 6.4%. Медіана значень показника HbA1c під час лікування знаходилась у діапазоні 5.9-6.4% у групі інсуліну гларгіну та 6.2-6.6% у групі стандартного лікування протягом усього періоду спостереження. Дослідження ORIGIN показало, що лікування інсуліном гларгіном 100 ОД/мл, в порівнянні зі стандартною гіпоглікемічною терапією, не змінювало ризик розвитку серцево-судинних ускладнень (серцево-судинної смерті, нефатального інфаркту міокарда або нефатального інсульту). або периферичних артерій) або ризик госпіталізації з приводу розвитку серцевої недостатності, ризик мікросудинних ускладнень (комбінований показник мікросудинних ускладнень: проведення лазерної фотокоагуляції або вітректомії, втрата зору у зв'язку з діабетичною ретинопатією, прогресування альбумінурії, або концентрація в проведення діалізної терапії). У дослідженні з оцінки впливу інсуліну гларгіну 100 ОД/мл на розвиток діабетичної ретинопатії при п'ятирічному спостереженні за пацієнтами з цукровим діабетом 2 типу не спостерігалося достовірних відмінностей у прогресуванні діабетичної ретинопатії при лікуванні інсуліном гларгіном 100 ОД/м. Особливі групи пацієнтів Статева та расова приналежність. Не спостерігалося відмінностей у ефективності та безпеці препарату Туджео СолоСтар® та інсуліну гларгіну 100 ОД/мл залежно від статі та раси пацієнтів. Пацієнти похилого віку. У контрольованих клінічних дослідженнях 716 пацієнтів (23% популяції для оцінки безпеки) з цукровим діабетом 1 та 2 типу були у віці ≥65 років та 97 пацієнтів (3%) були у віці ≥75 років. Загалом не спостерігалося відмінностей у ефективності та безпеці між цими пацієнтами та пацієнтами молодшого віку. У пацієнтів похилого віку з цукровим діабетом, щоб уникнути гіпоглікемічних реакцій, початкова доза та підтримуюча доза повинні бути нижчими, а збільшення дози слід проводити повільніше. У пацієнтів похилого віку можуть бути проблеми при розпізнаванні гіпоглікемії. Рекомендується ретельний моніторинг концентрації глюкози у крові, доза інсуліну має коригуватися індивідуально. Пацієнти з нирковою недостатністю. У контрольованих клінічних дослідженнях підгруповий аналіз, заснований на функціональному стані нирок (визначеному у результаті СКФ Пацієнти з ожирінням. У клінічних дослідженнях підгруповий аналіз на підставі ІМТ (до 63 кг/м2) показав відсутність відмінностей у ефективності та безпеці між препаратом Туджео СолоСтар® та інсуліном гларгіном 100 ОД/мл. Пацієнти дитячого віку. Даних щодо застосування препарату Туджео СолоСтар® у дітей немає.ІнструкціяПрепарат Туджео СолоСтар® вводиться в підшкірно-жирову клітковину живота, плечей чи стегон. Місця ін'єкцій слід чергувати з кожною новою ін'єкцією в межах рекомендованих областей для введення препарату. Препарат Туджео СолоСтар® не призначений для внутрішньовенного введення. Пролонгована дія інсуліну гларгіну спостерігається лише при його введенні у підшкірно-жирову клітковину. В/в введення звичайної підшкірної дози може спричинити важку гіпоглікемію. Препарат Туджео СолоСтар® не призначений для введення за допомогою інсулінової інфузійної помпи. Препарат Туджео СолоСтар є прозорим розчином, а не суспензією, тому ресуспендування перед застосуванням не потрібно. За допомогою шприц-ручки Туджео СолоСтар можна вводити дози від 1 до 80 одиниць на ін'єкцію з кроком збільшення дози в 1 одиницю. Лічильник доз шприц-ручки Туджео СолоСтар® показує кількість одиниць препарату Туджео СолоСтар®, яку буде введено. Шприц-ручка Туджео СолоСтар® була спеціально розроблена для препарату Туджео СолоСтар®, тому не потрібно жодного додаткового перерахунку доз. Препарат Туджео СолоСтар® ніколи не повинен витягуватися з картриджа шприц-ручки в шприц. Повторно використовувати голки не можна. Перед кожною ін'єкцією слід приєднувати нову стерильну голку. Повторне використання голок збільшує ризик їх закупорювання, що може призводити до введення меншої дози або передозування. Крім того, використання нової стерильної голки для кожної ін'єкції мінімізує ризик її контамінації та інфікування. У разі закупорки голки пацієнт повинен дотримуватися інструкцій, зазначених у Етапі 3 розділу "Правила використання та поводження з попередньо заповненою шприц-ручкою Туджео СолоСтар®" (. Щоб уникнути можливої передачі захворювань, що передаються через кров, інсулінові шприц-ручки не повинні використовуватися більш ніж одним пацієнтом, навіть за умови заміни голки. Для того, щоб виключити можливість помилкового (випадкового) введення іншого виду інсуліну замість препарату Туджео СолоСтар® слід завжди перед кожною ін'єкцією перевіряти етикетку на шприц-ручці (на етикетці шприц-ручки Туджео СолоСтар® концентрація "300 ОД/мл" виділена медово- фоном). Правила використання та поводження з попередньо заповненою шприц-ручкою Туджео СолоСтар® Шприц-ручка Туджео СолоСтар містить інсулін гларгін в концентрації 300 ОД/мл. Не слід використовувати голки повторно. При повторному використанні голки через те, що голка може закупоритися, пацієнт може не отримати потрібну дозу (введення меншої дози) або отримати занадто велику дозу (передозування). Не слід використовувати шприц для вилучення інсуліну зі шприц-ручки. У такому разі пацієнт може отримати надто велику дозу інсуліну. Шкала на більшості інсулінових шприців призначена лише для неконцентрованих інсулінів. Важлива інформація Не слід користуватися однією шприц-ручкою одночасно з іншими людьми, навіть за умови заміни голки. Пацієнт може отримати серйозну інфекцію від інших людей або передати їм серйозну інфекцію через кров. Не слід користуватися шприц-ручкою, якщо вона пошкоджена чи ні впевненість у тому, що вона справна. Слід завжди проводити тест на безпеку. Необхідно завжди мати при собі запасну шприц-ручку та запасні голки на випадок, якщо вони загубляться або стануть несправними. Перед використанням шприц-ручки пацієнт повинен уточнити у медичного працівника, як правильно проводити підшкірну ін'єкцію. У разі наявності у пацієнта проблем із зором може бути потрібна допомога інших осіб, здатних дотримуватися всіх рекомендацій даної інструкції щодо використання шприц-ручки Туджео СолоСтар®. Перед використанням шприц-ручки слід прочитати всю інструкцію. Якщо не дотримуватись всіх рекомендацій, можна отримати занадто багато або занадто мало інсуліну. Додатково потрібні: нова стерильна голка (див. Крок 2), змочена спиртом серветка, резистентний до проколів контейнер для використаних голок та шприців. Крок 1: Перевірка шприц-ручки Вийняти нову шприц-ручку з холодильника щонайменше за 1 год до проведення ін'єкції. Введення холодного інсуліну є болючим. А. Перевірити назву інсуліну та термін придатності на етикетці шприц-ручки. Ніколи не використовувати шприц-ручку після закінчення терміну придатності. В. Зняти ковпачок із шприц-ручки. Перевірити прозорість інсуліну. Не слід використовувати шприц-ручку, якщо інсулін каламутний, має забарвлення або містить сторонні частки. D. Протерти гумову мембрану за допомогою змоченої етиловим спиртом серветки. Якщо є інші шприц-ручки, особливо важливо переконатись у тому, що вибрано правильний препарат. Крок 2: Приєднання нової голки Завжди слід використовувати нову стерильну голку для кожної ін'єкції. Це допоможе запобігти закупорці голки, контамінації та інфекції. Необхідно використовувати голки BD Мікро-Файн® Плюс. A. Взяти нову голку та видалити захисне покриття. B. Утримуючи голку прямо перед шприц-ручкою, прикрутіть її на шприц-ручку до упору. Не слід застосовувати надмірні зусилля при прикручуванні голки. C. Зніміть зовнішній ковпачок голки. Необхідно зберегти його для використання надалі. D. Зняти внутрішній ковпачок з голки та викинути його. Необхідно бути обережними при поводженні з голками - це запобігає пошкодженню голок і перехресному інфікуванню. Крок 3: Проведення тесту на безпеку Обов'язково перед кожною ін'єкцією проводити тест на безпеку для перевірки правильності роботи шприц-ручки та виключення непрохідності голки, а також щоб бути впевненим, що буде введена правильна доза інсуліну. A. Набрати 3 ОД, обертаючи селектор дози, доки покажчик дози не опиниться між цифрами 2 і 4. B. Натиснути до упору на кнопку введення дози. Якщо крапля інсуліну з'являється на кінчику голки, це говорить про те, що шприц-ручка працює правильно. Якщо інсулін не відображається на кінчику голки: може знадобитися повторення цього кроку до 3 разів, перед тим, як з'явиться інсулін. Якщо інсулін не з'являється на кінчику голки та після третього повтору цього кроку, можливо голка непрохідна; тоді слід замінити голку (див. Крок 6 та Крок 2) і потім повторити тест на безпеку (Крок 3); не слід використовувати шприц-ручку, якщо інсулін все ж таки не показується на кінчику голки. Необхідно використати нову шприц-ручку; ніколи не слід використовувати шприц для вилучення інсуліну зі шприц-ручки Туджео СолоСтар®. Можлива поява бульбашок повітря в інсуліні. Це нормально, вони не завдадуть шкоди. Крок 4: Набір дози Ніколи не слід набирати дозу та натискати кнопку введення дози без приєднаної голки. Це може пошкодити шприц-ручку. A. Необхідно переконатися, що голка приєднана та доза встановлена на "0". B. Повертати селектор дози, доки покажчик дози не опиниться на одній лінії з потрібною дозою. якщо селектор дози був провернути далі необхідної дози, можна повернути його назад; якщо в шприц-ручці немає достатньої кількості одиниць для потрібної дози, можна ввести її у двох ін'єкціях, використовуючи для другої ін'єкції нову шприц-ручку або відразу використовувати нову шприц-ручку для всієї дози. Як читати показання вікна індикатора дози: парні числа (кількості одиниць) відображаються напроти вказівника дози; непарні числа (кількості одиниць) відображаються на лінії між парними числами. Одиниці інсуліну в шприц-ручці: у шприц-ручці міститься загалом 450 одиниць інсуліну. Можна набирати дози від 1 до 80 одиниць із кроком 1 одиницю. Кожна шприц-ручка містить більше однієї дози; можна приблизно визначити кількість одиниць інсуліну, що залишилися, за розташуванням поршня на шкалі інсуліну. Крок 5: Введення дози Якщо виникають труднощі при натисканні на кнопку введення дози, слід застосовувати силу, т.к. це може пошкодити шприц-ручку. Див. розділ нижче, де описані необхідні дії у цій ситуації. A. Вибрати місце для ін'єкції. B. Ввести голку в шкіру, як показано медичним працівником. Не торкайтеся кнопки введення дози. C. Покласти великий палець на кнопку введення дози. Потім натиснути до упору та утримувати в цьому положенні. Не натискати кнопку під кутом - великий палець може блокувати провертання селектора дози. D. Продовжувати натискати кнопку введення дози, і, коли у вікні дози з'явиться "0", повільно дорахувати до п'яти. Це гарантуватиме введення повної дози. E. Після утримання кнопки введення дози та рахунку до п'яти відпустити кнопку введення дози. Потім витягти голку зі шкіри. Якщо виникають труднощі при натисканні на кнопку введення дози, слід змінити голку (див. Крок 6 та Крок 2), а потім провести тест на безпеку (див. Крок 3). Якщо все одно зберігаються труднощі при натисканні на кнопку введення дози, слід взяти нову шприц-ручку. Крок 6: Видалення голки Слід бути обережними при поводженні з голками - це запобігає пошкодженню голки та перехресній інфекції. Ніколи не слід знову надягати на голку внутрішній ковпачок голки. A. Взяти широкий кінець зовнішнього ковпачка голки двома пальцями. Утримуючи голку прямо, ввести в зовнішній ковпачок голки. Потім щільно притиснути ковпачок. Якщо голка вводиться в ковпачок під кутом вона може його проткнути. B. Міцно охопити широку частину зовнішнього ковпачка голки. Прокрутити шприц-ручку кілька разів іншою рукою, щоб зняти голку. Якщо не вдалося зняти голку з першого разу, повторіть спробу. C. Викинути використану голку в щільний (стійкий до проколів) контейнер, який слід ретельно закривати, а після заповнення утилізувати відповідно до вказівок медичного працівника. D. Закрити шприц-ручку її ковпачком. Не слід поміщати шприц-ручку в холодильник. Термін використання Слід використовувати шприц-ручку протягом 4 тижнів після першого застосування. Зберігання шприц-ручки Перед першим використанням: зберігати нові шприц-ручки у холодильнику при температурі 2-8°C; шприц-ручки не можна заморожувати; Після першого використання: зберігати шприц-ручку за температури нижче 30°C; ніколи не поміщати шприц-ручку назад у холодильник; ніколи не зберігати шприц-ручку з приєднаною голкою; зберігати шприц-ручку, закритою ковпачком. Поводження зі шприц-ручкою Туджео СолоСтар® Слід з обережністю звертатися зі шприц-ручкою: не упускати шприц-ручку або уникати її удару об тверді поверхні; при підозрі на пошкодження шприц-ручки не намагатися полагодити її, слід використовувати нову шприц-ручку. Захищати шприц-ручку від попадання пилу та бруду: можна очищати зовнішню поверхню шприц-ручки, протираючи її вологою тканиною; не замочувати, не мити і не змащувати шприц-ручку – це може зашкодити її. Утилізація шприц-ручки зняти голку перед тим, як викинути шприц-ручку; утилізувати використані шприц-ручки відповідно до вказівок медичного працівника.Показання до застосуванняЦукровий діабет у дорослих, що потребує лікування інсуліном.Протипоказання до застосуванняВік до 18 років (у зв'язку з відсутністю клінічних даних, що підтверджують ефективність та безпеку застосування препарату у дітей та підлітків); підвищена чутливість до інсуліну гларгіну або будь-якої з допоміжних речовин препарату. З обережністю слід призначати препарат при вагітності (можливість зміни потреби в інсуліні протягом вагітності та після пологів); пацієнтам похилого віку; пацієнтам з некомпенсованими ендокринними порушеннями (такими як гіпотиреоз, недостатність аденогіпофіза та кори надниркових залоз); при захворюваннях, що супроводжуються блюванням або діареєю; виражений стеноз коронарних артерій або судин головного мозку; проліферативної ретинопатії (особливо якщо у пацієнтів не проводилася фотокоагуляція; ниркової недостатності; тяжкої печінкової недостатності.Вагітність та лактаціяПацієнтки з цукровим діабетом повинні інформувати лікаря про справжню або заплановану вагітність. Не проводилося рандомізованих контрольованих клінічних досліджень щодо застосування препарату Туджео СолоСтар у вагітних жінок. Велика кількість спостережень (більше 1000 результатів вагітностей при ретроспективному та проспективному спостереженні) при посмаркетинговій застосуванні інсуліну гларгіну 100 ОД/мл показали відсутність у нього будь-яких специфічних ефектів протягом та результат вагітності, стан плода або здоров'я новонародженого. Крім того, з метою оцінки безпеки застосування інсуліну гларгіну та інсуліну ізофан у вагітних жінок з раніше наявним або гестаційним цукровим діабетом, був проведений мета-аналіз восьми спостережних клінічних досліджень, що включав жінок, у яких під час вагітності застосовувався інсулін гларгін 100 ОД/мл ( n=331) та інсулін ізофан (n=371). Цей мета-аналіз не виявив істотних відмінностей щодо безпеки щодо здоров'я матерів або новонароджених, при застосуванні інсуліну гларгіну та інсуліну ізофан під час вагітності. У дослідженнях на тварин не було отримано прямих або непрямих даних про ембріотоксичну або фетотоксичну дію інсуліну гларгіну 100 ОД/мл при його застосуванні в дозах, що у 6-40 разів перевищують рекомендовані дози у людини. Для пацієнток з раніше наявним або гестаційним цукровим діабетом важливо протягом всієї вагітності підтримувати адекватну регуляцію метаболічних процесів, щоб запобігти появі небажаних наслідків, пов'язаних з гіперглікемією. У разі необхідності може бути розглянуто питання про застосування Туджео СолоСтар® при вагітності. Потреба в інсуліні може знижуватися в І триместрі вагітності та, в цілому, збільшуватися протягом ІІ та ІІІ триместрів. Безпосередньо після пологів потреба в інсуліні швидко зменшується (зростає ризик розвитку гіпоглікемії). У умовах істотне значення має ретельний контроль концентрації глюкози у крові. Пацієнткам у період грудного вигодовування може знадобитися корекція режиму дозування інсуліну та дієти. Протипоказано застосування препарату у пацієнтів віком до 18 років (у зв'язку з відсутністю клінічних даних, що підтверджують ефективність та безпеку застосування препарату у дітей та підлітків).Побічна діяНаведені нижче небажані реакції спостерігалися під час клінічних досліджень, проведених із препаратом Туджео СолоСтар® та під час клінічного застосування інсуліну гларгіну 100 ОД/мл. Ці небажані реакції представлені за системами органів (відповідно до класифікації MedDRA) відповідно до рекомендованих ВООЗ наступних градацій частоти виникнення: дуже часто (≥10%); часто (≥1%; менше 10%); нечасто (≥0.1%; менше 1%); рідко (≥0.01%; менше 0.1%); дуже рідко (менше 0.01%), частота невідома (визначити частоту народження небажаних реакцій за наявними даними неможливо). З боку обміну речовин Гіпоглікемія - небажана реакція, що найчастіше зустрічається при інсулінотерапії, може виникнути, якщо доза інсуліну виявляється занадто високою, в порівнянні з потребою в ньому. Як і при застосуванні інших інсулінів, епізоди важкої гіпоглікемії, що особливо повторюються, можуть призводити до неврологічним порушенням. Епізоди тривалої та вираженої гіпоглікемії можуть загрожувати життю пацієнтів. У багатьох пацієнтів ознаками і симптомами нейроглікопенії (почуття втоми, неадекватна стомлюваність або слабкість, зниження здатності до концентрації уваги, сонливість, зорові розлади, головний біль, нудота, сплутаність свідомості або його втрата, судомний синдром) передують ознаки адренергічної контррегуляції (активації системи у відповідь на гіпоглікемію): почуття голоду, дратівливість, нервове збудження або тремор, занепокоєння, блідість шкірних покривів, "холодний" піт, тахікардія, виражене серцебиття. Зазвичай, що швидше розвивається гипогликемия, і що вона важче, то сильніше виражені симптоми адренергической контррегуляції. З боку органу зору Значне поліпшення глікемічного контролю може спричинити тимчасове погіршення зору внаслідок тимчасового порушення тургору та коефіцієнта заломлення кришталика ока. Тривале покращення глікемічного контролю знижує ризик прогресування діабетичної ретинопатії. Однак, як і за будь-яких схем призначення інсуліну, інтенсифікація інсулінової терапії з різким поліпшенням глікемічного контролю може асоціюватися з тимчасовим обтяженням перебігу діабетичної ретинопатії. У пацієнтів з проліферативною ретинопатією, які особливо не отримують лікування фотокоагуляцією, епізоди важкої гіпоглікемії можуть призводити до скороминущої втрати зору. З боку шкіри та підшкірних тканин Як і при лікуванні будь-якими іншими препаратами інсуліну, на місці ін'єкцій може розвиватися ліподистрофія, здатна уповільнити місцеву абсорбцію інсуліну. При застосуванні схем інсулінотерапії, що включає інсулін гларгін, ліподистрофія спостерігалася у 1-2% пацієнтів, а ліпоатрофія спостерігалася нечасто. Постійна зміна місць ін'єкцій у межах областей тіла, рекомендованих для підшкірного введення інсуліну, може сприяти зменшенню вираженості цієї реакції або запобігти її розвитку. З боку кістково-м'язової системи: дуже рідко – міалгія. Реакції у місці введення Як при будь-якій інсулінотерапії, такі реакції включають почервоніння шкіри, біль, свербіж, кропив'янку, висип, набряк та запалення. У клінічних дослідженнях, що проводилися з препаратом Туджео СолоСтар® у дорослих пацієнтів, частота всіх реакцій у місці введення у пацієнтів, які отримували лікування препаратом Туджео СолоСтар® (2.5%), була подібна до такої у пацієнтів, які отримували лікування інсуліном гларгіном 100 ОД/мл (2.8). %). Більшість незначних реакцій у місці введення інсулінів зазвичай проходить протягом кількох днів або кількох тижнів. З боку імунної системи Алергічні реакції негайного типу інсулін розвиваються рідко. Такі реакції на інсулін (включаючи інсулін гларгін) або допоміжні речовини можуть, наприклад, супроводжуватися генералізованими шкірними реакціями, ангіоневротичним набряком (набряком Квінке), бронхоспазмом, зниженням артеріального тиску та шоком і становити загрозу для життя пацієнта. Застосування інсуліну може спричинити утворення антитіл до нього. У клінічних дослідженнях порівняно з препаратом Туджео СолоСтар® та інсуліну гларгіну 100 ОД/мл утворення антитіл до інсуліну в обох групах лікування спостерігалося з однаковою частотою. Як і при застосуванні інших інсулінів, в окремих випадках наявність таких антитіл до інсуліну може вимагати зміни дози інсуліну з метою усунення тенденції до розвитку гіпоглікемії або гіперглікемії. У поодиноких випадках інсулін може спричинити затримку натрію та виникнення набряків, особливо при покращенні раніше недостатнього метаболічного контролю при інтенсифікації інсулінотерапії. Діти Профіль безпеки для дітей та підлітків віком до 18 років на даний момент не встановлений.Взаємодія з лікарськими засобамиРяд лікарських засобів впливає на метаболізм глюкози, внаслідок чого при їх одночасному застосуванні з інсулінами може знадобитися корекція дози інсуліну та особливо ретельне спостереження. Пероральні гіпоглікемічні засоби, інгібітори АПФ, саліцилати, дизопірамід; фібрати, флуоксетин, інгібітори MAO, пентоксифілін, пропоксифен, сульфаніламідні антибіотики можуть збільшити гіпоглікемічну дію інсуліну та схильність до розвитку гіпоглікемії. Одночасне застосування цих лікарських засобів з інсуліном гларгіном може вимагати корекції дози інсуліну. ГКС, даназол, діазоксид, діуретики, симпатоміметики (такі як адреналін, сальбутамол, тербуталін); глюкагон, ізоніазид, похідні фенотіазину, соматотропний гормон, гормони щитовидної залози, естрогени та гестагени (наприклад, у гормональних контрацептивах), інгібітори протеаз та атипові нейролептики (наприклад, оланзапін та клозапін) можуть послабити гіпоглікемію. Одночасне застосування цих лікарських засобів з інсуліном гларгіном може вимагати корекції дози інсуліну. Бета-адреноблокатори, клонідин, солі літію та етанол можуть спричинити як посилення, так і ослаблення гіпоглікемічної дії інсуліну. Пентамідин при поєднанні з інсуліном може спричиняти гіпоглікемію, яка іноді змінюється гіперглікемією. Під впливом симпатоміметичних засобів, таких як бета-адреноблокатори, клонідин, гуанетидин і резерпін, можуть зменшуватися або відсутні ознаки адренергічної контррегуляції (активації симпатичної нервової системи у відповідь на розвиток гіпоглікемії). При застосуванні піоглітазону в комбінації з інсуліном повідомлялося про випадки серцевої недостатності, особливо у пацієнтів з ризиком серцевої недостатності. При появі або обтяженні кардіальних симптомів застосування піоглітазону слід припинити.Спосіб застосування та дозиОдиниці препарату Туджео СолоСтар® (інсуліну гларгіну 300 ОД/мл) відносяться лише до препарату Туджео СолоСтар® та не еквівалентні іншим одиницям, що виражають силу дії інших аналогів інсуліну. Препарат Туджео СолоСтар® слід вводити підшкірно 1 раз на добу в будь-який час дня, переважно в один і той же час. Препарат Туджео СолоСтар® при одноразовому введенні протягом доби дозволяє мати гнучкий графік проведення ін'єкцій: за необхідності пацієнти можуть проводити ін'єкцію протягом 3 годин до або 3 години після звичайного для них часу її проведення. Цільові значення концентрації глюкози в крові, дози та час прийому/введення гіпоглікемічних препаратів повинні визначатися та коригуватися індивідуально. Корекція дози також може бути потрібна, наприклад, при зміні маси тіла пацієнта, його способу життя, зміні часу введення інсуліну або при інших станах, які можуть збільшити схильність до розвитку гіпо-або гіперглікемії. Будь-які зміни дози інсуліну повинні проводитися з обережністю та лише під медичним наглядом. Препарат Туджео СолоСтар не є інсуліном вибору для лікування діабетичного кетоацидозу. У цьому випадку перевагу слід віддавати внутрішньовенному введенню інсуліну короткої дії. У всіх пацієнтів із цукровим діабетом рекомендується проводити моніторинг концентрації глюкози у крові. Пацієнти з цукровим діабетом 1 типу Препарат Туджео СолоСтар® повинен застосовуватися 1 раз на добу у поєднанні з інсуліном, що вводиться під час їди, та потребує індивідуальної корекції дози. Пацієнти з цукровим діабетом 2 типи Початкова доза, що рекомендується, становить 0.2 ОД/кг маси тіла 1 раз на добу з подальшою індивідуальною корекцією дози. Перехід із введення інсуліну гларгіну 100 ОД/мл на препарат Туджео СолоСтар® і, навпаки, з препарату Туджео СолоСтар® на інсулін гларгін 100 ОД/мл Інсулін гларгін 100 ОД/мл та препарат Туджео СолоСтар® не біоеквівалентні та безпосередньо не взаємозамінні. Перехід з інсуліну гларгіну 100 ОД/мл на препарат Туджео СолоСтар® може бути проведений з розрахунку одиниця на одиницю, але для досягнення цільового діапазону концентрацій глюкози в плазмі крові може знадобитися більша доза препарату Туджео СолоСтар®. При переході з застосування препарату Туджео СолоСтар на інсулін гларгін 100 ОД/мл для зниження ризику розвитку гіпоглікемії доза повинна бути зменшена (приблизно на 20%) з подальшою корекцією дози за потреби. Рекомендується проведення ретельного метаболічного моніторингу під час та протягом перших тижнів після переходу з одного з цих препаратів на інший. Перехід з інших базальних інсулінів на препарат Туджео СолоСтар® При переході зі схеми лікування з інсулінами проміжної та тривалої тривалості дії на схему лікування з препаратом Туджео СолоСтар® може знадобитися зміна дози базального інсуліну та корекція одночасно проведеної гіпоглікемічної терапії (зміна доз та часу введення інсулінів короткої дії або швидкодіючих аналогів. препаратів). Перехід з одноразового протягом доби введення базальних інсулінів на одноразове протягом доби введення препарату Туджео СолоСтар® може проводитися з розрахунку одиниця на одиницю дози базального інсуліну, що раніше вводиться. При переході з дворазового протягом доби введення базальних інсулінів на одноразове введення препарату Туджео СолоСтар® рекомендована початкова доза препарату Туджео СолоСтар® становить 80% від загальної добової дози базального інсуліну, лікування яким припиняється. Пацієнти з високими дозами інсуліну, через наявність у них антитіл до людського інсуліну, можуть мати покращену реакцію на препарат Туджео СолоСтар®. Під час переходу на препарат Туджео СолоСтар® та протягом декількох тижнів після нього рекомендується проведення ретельного метаболічного моніторингу. З поліпшенням метаболічного контролю і збільшення чутливості до інсуліну, що виникає в результаті цього, може знадобитися додаткова корекція режиму дозування. Корекція режиму дозування може також бути потрібна, наприклад, при зміні маси тіла або способу життя пацієнта, при зміні часу введення дози інсуліну або при виникненні інших станів, які підвищують схильність до розвитку гіпо- та гіперглікемії. Перехід із введення препарату Туджео СолоСтар® на інші базальні інсуліни Під час переходу з введення препарату Туджео СолоСтар на застосування інших базальних інсулінів і протягом декількох тижнів після нього рекомендується медичне спостереження та ретельний метаболічний моніторинг. Рекомендується звернутися до інструкції щодо застосування лікарського препарату, на який переводиться пацієнт. Змішування та розведення Препарат Туджео СолоСтар® не можна змішувати з іншим інсуліном. Змішування призводить до зміни профілю дії препарату Туджео СолоСтар® у часі та викликає преципітацію. Препарат Туджео СолоСтар® не можна розводити. Розведення може призвести до зміни профілю дії препарату Туджео СолоСтар® у часі. Особливі групи пацієнтів Безпека та ефективність препарату Туджео СолоСтар® у дітей та підлітків віком до 18 років наразі не встановлена. Препарат Туджео СолоСтар® можна застосовувати у пацієнтів похилого віку. Рекомендується ретельний моніторинг концентрації глюкози у крові, дозу інсуліну слід підбирати індивідуально. У пацієнтів похилого віку прогресивне погіршення функції нирок може спричинити постійне зниження потреби в інсуліні. Препарат Туджео СолоСтар® можна застосовувати у пацієнтів з нирковою недостатністю. Рекомендується ретельний моніторинг концентрації глюкози у крові, дозу інсуліну слід підбирати індивідуально. У пацієнтів з нирковою недостатністю потреба в інсуліні може зменшуватися через уповільнення метаболізму інсуліну. Препарат Туджео СолоСтар® можна застосовувати у пацієнтів із печінковою недостатністю. Рекомендується ретельний моніторинг концентрації глюкози у крові, дозу інсуліну слід підбирати індивідуально. У пацієнтів із печінковою недостатністю потреба в інсуліні може зменшуватися внаслідок зменшення глюконеогенезу та уповільнення метаболізму інсуліну.ПередозуванняСимптоми: передозування інсуліну (надлишок інсуліну щодо споживання їжі, енерговитрат або того й іншого разом) може призводити до важкого та іноді тривалого та загрозливого життя хворого на гіпоглікемію. Лікування: епізоди гіпоглікемії середньої тяжкості зазвичай купуються шляхом прийому внутрішньо швидкозасвоюваних вуглеводів. Може виникнути потреба зміни схеми дозування препарату, режиму харчування або фізичної активності. Епізоди тяжчої гіпоглікемії, що виявляються комою, судомами або неврологічними розладами, можуть бути куповані внутрішньом'язово або підшкірно введенням глюкагону або внутрішньовенним введенням концентрованого розчину декстрози (глюкози). Може знадобитися тривалий прийом вуглеводів та нагляд фахівця, т.к. після видимого клінічного покращення можливий рецидив гіпоглікемії.Запобіжні заходи та особливі вказівкиПацієнти повинні мати навички самостійного контролю цукрового діабету, включаючи моніторинг концентрації глюкози в крові, а також дотримуватися правильної техніки проведення підшкірних ін'єкцій та вміти усунути гіпоглікемію та гіперглікемію. Інсулінотерапія вимагає постійної настороженості щодо можливості розвитку гіперглікемії чи гіпоглікемії. У разі недостатнього контролю концентрації глюкози в крові, а також за наявності тенденції до розвитку гіпо- або гіперглікемії, перш ніж приступати до корекції режиму дозування, слід перевірити точність виконання запропонованої схеми лікування, дотримання вказівок щодо місць введення препарату, правильність техніки проведення підшкірно. ін'єкцій та поводження зі шприц-ручкою СолоСтар®, а також враховувати можливість усіх інших факторів, здатних викликати такий стан. Гіпоглікемія Час розвитку гіпоглікемії залежить від профілю дії інсулінів і може, таким чином, змінюватися при зміні схеми лікування. Слід дотримуватись особливої обережності та проводити ретельний моніторинг концентрації глюкози в крові при застосуванні препарату у пацієнтів, у яких епізоди гіпоглікемії можуть мати особливе клінічне значення, таких як пацієнти з вираженим стенозом коронарних артерій або судин головного мозку (ризик розвитку кардіальних та церебральних ускладнень). а також пацієнтам з проліферативною ретинопатією, особливо, якщо вони не отримують лікування фотокоагуляцією (ризик скороминущої втрати зору за гіпоглікемією). Як і при застосуванні будь-яких інсулінів, при деяких станах симптоми-провісники гіпоглікемії можуть змінюватися, ставати менш вираженими або відсутніми. До них відносяться: помітне покращення глікемічного контролю; поступовий розвиток гіпоглікемії; літній вік; наявність вегетативної невропатії; тривалий анамнез цукрового діабету; наявність психічних розладів; одночасне застосування інсуліну гларгіну з деякими іншими лікарськими засобами. Такі ситуації можуть призводити до розвитку тяжкої гіпоглікемії (з можливою втратою свідомості) до того, як пацієнт усвідомлює, що розвивається гіпоглікемія. Слід брати до уваги те, що пролонгована дія препарату Туджео СолоСтар® при його підшкірному введенні може відстрочити вихід пацієнта зі стану гіпоглікемії. У разі якщо відзначаються нормальні або знижені показники глікозильованого гемоглобіну, необхідно враховувати можливість розвитку нерозпізнаних епізодів гіпоглікемії, що повторюються (особливо в нічний час). Дотримання пацієнтами схеми дозування та режиму харчування, правильне введення інсуліну та знання симптомів-провісників гіпоглікемії сприяють суттєвому зниженню ризику розвитку гіпоглікемії. Фактори, що підвищують схильність до гіпоглікемії, за наявності яких потрібне особливо ретельне спостереження та корекція дози інсуліну: зміна місця запровадження інсуліну; підвищення чутливості до інсуліну (наприклад, усунення стресових факторів); незвична, підвищена чи тривала фізична активність; інтеркурентні захворювання, що супроводжуються блюванням, діареєю; недостатній прийом їжі; споживання алкоголю; деякі некомпенсовані ендокринні порушення (такі як гіпотиреоз, недостатність передньої частки гіпофіза або недостатність кори надниркових залоз); одночасне застосування інсуліну гларгіну з деякими іншими лікарськими засобами. У пацієнтів із нирковою недостатністю потреба в інсуліні може зменшуватись за рахунок уповільнення метаболізму інсуліну. У пацієнтів похилого віку прогресуюче погіршення функції нирок може призвести до сталого зниження потреби в інсуліні. У пацієнтів з тяжкою печінковою недостатністю потреба в інсуліні може бути зменшена через зниження здатності до глюконеогенезу та уповільнення метаболізму інсуліну. Гіпоглікемія, в цілому, може бути усунена негайним прийомом вуглеводів, що швидко засвоюються. Оскільки початкові дії з корекції гіпоглікемії повинні проводитися негайно, пацієнтам слід завжди мати з собою, як мінімум, 20 г вуглеводів, що швидко засвоюються. Інтеркурентні захворювання При інтеркурентних захворюваннях потрібний інтенсивніший контроль концентрації глюкози в крові. У багатьох випадках показано проведення аналізу на наявність кетонових тіл у сечі, також часто потрібна корекція режиму дозування інсуліну. У разі виникнення інтеркурентного захворювання потреба в інсуліні часто підвищується. Пацієнти з цукровим діабетом 1 типу повинні продовжувати отримувати вуглеводи на регулярній основі, навіть якщо вони здатні вживати їжу лише невеликими порціями або взагалі не вживають їжу, або у разі розвитку блювоти; Пацієнти з цукровим діабетом 1 типу ніколи не повинні повністю пропускати введення інсуліну. Комбінація інсуліну гларгіну з піоглітазоном При застосуванні піоглітазону в комбінації інсуліном повідомлялося про випадки розвитку серцевої недостатності, особливо у пацієнтів із ризиком серцевої недостатності. Цю інформацію слід брати до уваги при розгляді питання застосування комбінації піоглітазону з препаратом Туджео СолоСтар®. При застосуванні такої комбінації пацієнти повинні спостерігатися щодо появи ознак і симптомів серцевої недостатності, таких як збільшення маси тіла, поява набряків. При появі або обтяженні кардіальних симптомів застосування піоглітазону слід припинити. Запобігання помилкам при введенні препаратів інсуліну Щоб не переплутати препарат Туджео СолоСтар з іншими інсулінами, необхідно завжди перевіряти маркування на шприц-ручці перед кожною ін'єкцією. Повідомлялося про випадки, коли випадково помилково вводилися інші інсуліни, зокрема інсуліни короткої дії, замість інсулінів, що довго діють. Щоб уникнути помилок дозування та можливого передозування, пацієнти ніколи не повинні використовувати шприц для вилучення препарату Туджео із шприца-ручки СолоСтар®. Як і при застосуванні інших інсулінових шприц-ручок, пацієнти повинні візуально перевіряти кількість набраних одиниць дози у вікні індикатора дози на шприц-ручці. Сліпі або слабозорі пацієнти повинні отримувати допомогу від інших осіб з добрим зором і тих, хто вміє користуватися шприц-ручкою Туджео СолоСтар®. Вплив на здатність до керування автотранспортом та управління механізмами Здатність пацієнтів до концентрації уваги та швидкість психомоторних реакцій можуть бути порушені, наприклад, внаслідок розвитку гіпоглікемії або гіперглікемії, а також внаслідок порушення зору. Це може становити ризик у ситуаціях, коли зазначені здібності особливо важливі (наприклад, керування автомобілем або робота з іншими механізмами). Пацієнтам рекомендується дотримуватися запобіжних заходів, щоб уникнути розвитку гіпоглікемії під час керування транспортними засобами. Це особливо важливо для тих з них, у кого слабко виражені або відсутні симптоми, що є провісниками гіпоглікемії, що розвивається, або для пацієнтів з часто виникаючими епізодами гіпоглікемії. Ці особливості пацієнта слід враховувати під час вирішення питання про можливість керування ним транспортними засобами.Умови зберіганняУ холодильнику +2+8 градусівУмови відпустки з аптекЗа рецептомВідео на цю тему